간시클로비르
Ganciclovir | |
 | |
| 임상자료 | |
|---|---|
| 발음 | /ɡænˈsaɪkləvɪər/ |
| 상명 | 키토베네 |
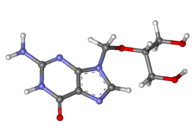
| 기타 이름 | gancyclovir; DHPG; 9-(1,3-dihydroxy-2-propoxymethyl)guanine |
| AHFS/Drugs.com | 모노그래프 |
| 메드라인플러스 | a605011 |
| 라이센스 데이터 | |
| 임신 범주 |
|
| 경로: 행정 | 정맥주사, 구강주사, 인트라비트리얼 |
| ATC 코드 | |
| 법적현황 | |
| 법적현황 | |
| 약동학 데이터 | |
| 생체이용가능성 | 5%(도덕) |
| 신진대사 | 구아닐레이트 키나아제(CMV UL97 유전자 제품) |
| 제거 반감기 | 2.5~5시간 |
| 배설 | 신장 |
| 식별자 | |
| |
| CAS 번호 | |
| 펍켐 CID | |
| 드러그뱅크 | |
| 켐스파이더 | |
| 유니 | |
| 케그 | |
| 체비 | |
| 켐벨 | |
| CompTox 대시보드 (EPA) | |
| ECHA InfoCard | 100.155.403 |
| 화학 및 물리적 데이터 | |
| 공식 | C9H13N5O4 |
| 어금질량 | 255.234 g·180−1 |
| 3D 모델(JSmol) | |
| 녹는점 | 250°C(482°F) (결국) |
| |
| |
| (iii) | |
그중 시토베네라는 상표명으로 판매되는 간키클로비르는 시토메갈로바이러스(CMV) 감염 치료에 사용되는 항바이러스제다.
간시클로비르는 1980년에 특허를 받았으며 1988년에 의료용으로 승인되었다.[1]
의료용
간시클로비르는 다음을 위해 표시된다.[2]
- 중증 면역억제자의 시력을 위협하는 CMV망막염
- 골수 이식수혜자의 CMV 폐염
- 골수 및 고형 장기이식 수혜자의 CMV 질환 예방
- AIDS(내부 임플란트) 환자에서 CMV 망막염 확진
또한 HIV/AIDS의 급성 CMV 대장염과 면역억제 환자의 CMV 폐렴염에도 사용된다.[medical citation needed]
간시클로비르는 또한 휴먼 헤르페스바이러스 6 감염을 치료하는 데 어느 정도 성공했다.[3]
간시클로비르는 또한 대상포진 바이러스 상피막염에 효과적인 치료제인 것으로 밝혀졌다.[4]
역효과
간시클로비르는 일반적으로 다양한 심각한 혈액학적 부작용과 관련이 있다.일반적인 부작용 약물 반응(환자의 ≥1%)은 과립세포세증, 중성미자, 빈혈, 혈소판감소증, 발열, 구토, 과립, 설사, 복통, 거식증, 간 효소 상승, 두통, 혼란, 환각, 발작, 발작, 발작, 가려움증, 증가 등이다.아스데이드 혈청 크레아티닌과 혈액 [2]요소 농도
독성
간시클로비르는 잠재적인 인간 발암물질, 테라토겐, 돌연변이 물질로 간주된다.또한 정조세포의 억제를 유발할 가능성이 있는 것으로 간주된다.따라서, 그것은 현명하게 사용되고 임상 환경에서 세포독성 약물로 취급된다.[2][5]
작용기전
간시클로비르는 2′-데옥시-과노신의 합성 아날로그다.감염 시 CMV(사이토메갈로바이러스) 유전자 UL97로 인코딩된 바이러스 키나아제에 의해 간시클로비르 모노인산염에 최초로 인산염화된다.그 후 세포키나제는 무감염 세포보다 CMV 또는 헤르페스 심플렉스 바이러스(HSV) 감염 세포에 10배 더 큰 농도로 존재하는 간시클로비르 디프인산염과 간시클로비르 삼인산염의 형성을 촉진한다.
간시클로비르 삼인산염은 디옥시구아노신 삼인산염(dGTP)이 DNA에 통합되는 경쟁 억제제로 세포 DNA 중합효소보다 바이러스성 DNA 중합효소를 우선 억제한다.또한, 간시클로비르 삼인산염은 체인 연장에 좋지 않은 기질 역할을 하므로 제2의 경로에 의한 바이러스 DNA 합성을 방해한다.
약동학
구강 형태의 흡수는 매우 제한적이다. 약 5%의 단식, 약 8%의 음식 섭취.혈장 수준의 약 50%의 중추신경계 농도를 달성한다.혈장 간시클로비르의 약 90%는 소변에서 변하지 않고 제거되며, 신기능에 따라 2~6시간의 반감기가 발생한다(말기 신장질환에서는 제거가 24시간 이상 걸린다).
관리
급성 감염은 다음 두 단계로 처리된다.
- 유도 단계, 14-21일 동안 12시간마다 정맥주사 5mg, 정맥주사 1시간 주입으로 주어지는 정맥주사량
- 유지관리 단계, 매일 정맥 주사로 kg당 5mg
안정병은 하루에 세 번 1000mg의 구강으로 치료한다.인체면역결핍바이러스(HIV)에 감염된 환자나 장기이식을 한 환자 등 고위험 환자에서도 유사한 투약을 통해 질병을 예방한다.
간시클로비르는 또한 CMV 망막염 치료(HIV 감염과 연관됨)로서 눈의 유리 유머에 삽입하기 위한 슬로우 릴리스 공식으로도 이용할 수 있다.
간시클로비르의 국소 안과 젤 제제는 최근[when?] 급성 헤르페스 단순 각막염 치료를 위해 승인되었다.[citation needed]
참고 항목
발간시클로비르, 간시클로비르의 프로드러
참조
- ^ Fischer J, Ganellin CR (2006). Analogue-based Drug Discovery. John Wiley & Sons. p. 504. ISBN 9783527607495.
- ^ a b c 로시 S, 편집자.2006년 오스트레일리아의약학 핸드북.애들레이드:오스트레일리아의약학 핸드북, 2006.ISBN 0-97577919-2-3
- ^ Nakano (2009). "Detection and identification of U69 gene mutations encoded by ganciclovir-resistant human herpesvirus 6 using denaturing high-performance liquid chromatography".
{{cite journal}}:Cite 저널은 필요로 한다.journal=(도움말) - ^ Wilhelmus KR (January 2015). "Antiviral treatment and other therapeutic interventions for herpes simplex virus epithelial keratitis". The Cochrane Database of Systematic Reviews. 1: CD002898. doi:10.1002/14651858.CD002898.pub5. PMC 4443501. PMID 25879115.
- ^ Roche Products Pty Ltd.Cymevene(호주 승인 제품 정보).Die Why (NSW): Roche; 2005.
추가 읽기
- Noble S, Faulds D (July 1998). "Ganciclovir. An update of its use in the prevention of cytomegalovirus infection and disease in transplant recipients". Drugs. 56 (1): 115–46. doi:10.2165/00003495-199856010-00012. PMID 9664203.
- Spector SA (1999). "Oral ganciclovir". Antiviral Chemotherapy 5. Advances in Experimental Medicine and Biology. Vol. 458. pp. 121–7. doi:10.1007/978-1-4615-4743-3_11. ISBN 978-1-4613-7150-2. PMID 10549384.
- Couchoud-Heyer C (July 2007). "WITHDRAWN: Cytomegalovirus prophylaxis with antiviral agents for solid organ transplantation". The Cochrane Database of Systematic Reviews (4): CD001320. doi:10.1002/14651858.cd001320.pub2. PMID 17636667.
외부 링크
- "Ganciclovir". Drug Information Portal. U.S. National Library of Medicine.
- "Ganciclovir sodium". Drug Information Portal. U.S. National Library of Medicine.


