Lisina
| Lisina Alerta sobre risco à saúde | |
|---|---|
|
|
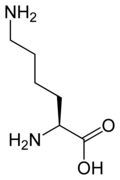
| Nome IUPAC | ácido 2,6-diaminohexanóico |
| Identificadores | |
| Número CAS | ,(enantiômero L 923-27-3 (enantiômero D) 70-54-2 (racêmico) 657-27-2 (monocloridrato) |
| PubChem | |
| ChemSpider | |
| SMILES |
|
| Propriedades | |
| Fórmula química | C6H14N2O2 |
| Massa molar | 146.18 g mol-1 |
| Ponto de fusão |
224–225 °C (base livre, enantiômero, decompõe-se)[1] |
| Acidez (pKa) | pKCOOH : 2,20[1] pKα-NH3+ : 8,90[1] pKε-NH3+ : 10,28[1] |
| Compostos relacionados | |
| Alfa-aminoácidos relacionados | Ornitina (C5) Norleucina (ácido 2-amino-hexanoico) Hidroxilisina (5-hidroxi-lisina) Ácido diaminopimélico (epsilon-carboxi-lisina) |
| Compostos relacionados | Ácido aminocaproico (ácido 6-amino-hexanoico) |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
A Lisina é um aminoácido polar básico, codificado pelos códons AAA e AAG. Altamente solúvel em água, foi descoberta em 1889 por Edmund Drechsel, que a isolou pela primeira vez a partir da caseína.[4] Sua estrutura foi elucidada três anos depois. Em humanos, o aminoácido lisina é exclusivamente cetogênico.
Ela apresenta uma cadeia lateral carregada positivamente em pH fisiológico, por ser um aminoácido com cadeia lateral butilamônica. Devido a esta característica a lisina possui três valores de constante de dissociação (pKs). Estes diferentes valores são correspondentes a ionização do grupo carboxila da cadeia principal (pK = 2,16), assim como a ionização do grupo amina da cadeia principal (pK = 9,06) e da cadeia lateral (pK = 10,54).[5]
A degradação do aminoácido lisina em mamíferos ocorre através de duas vias catabólicas: a via de sacaropina e a via do ácido pipecólico. Ambas as vias geram acetil-CoA, importante componente do Ciclo de Krebs.[6][7]
Em circunstâncias normais, um ser humano consome quantidade suficiente de lisina através da alimentação. A falta desse aminoácido pode ocasionar crescimento lento, fadiga, náusea, tontura, perda de apetite e distúrbios reprodutivos. É encontrada principalmente em alimentos ricos em proteínas como: carnes, frutos do mar, produtos à base de soja, leite e derivados. Em menor concentração, é encontrada em verduras e legumes. O excesso de lisina no organismo pode resultar em diarreia, dor de estômago, aumento do colesterol, danos hepáticos e renais.[8][9]
O aminoácido lisina começou a ser adicionado na ração de animais de abate na segunda metade do século passado. Para alguns animais, como porcos, é um aminoácido limitante. A suplementação com lisina proporciona a utilização de rações com componentes mais baratos, porém mantém boas taxas de proteínas e crescimento para os animais. Estima-se que a produção anual do aminoácido ultrapasse 600.000 toneladas.[10]
Efeitos e atuação
[editar | editar código-fonte]Vários estudos já foram realizados para esclarecer o papel da lisina no organismo e no tratamento de vários problemas de saúde. Alguns desses estudos se contradizem e não há um consenso sobre o papel desse aminoácido em algumas situações.
- Diminui a replicação viral do vírus da herpes.[11]
- Possível eficácia no tratamento da osteoporose, por aumentar a absorção de cálcio pelo intestino e reduzir sua eliminação pelos rins.[12]
- Auxilia no reparo muscular.[carece de fontes]
- A lisina é necessária para a sintetização da carnitina, uma amina quaternária que tem função fundamental na geração de energia pela célula.[17]
- Estudos preliminares apontam que o sal de lisina do bendazac pode ter efeito positivo no tratamento de catarata.[18]
- Sob a ação da vitamina C, a lisina é convertida em hidroxilisina, componente do colágeno. A lisina também está relacionada à produção de elastina.[21]
- O aminoácido lisina participa do processo químico responsável pela visão humana, por consequência, a falta desse aminoácido pode acarretar problemas visuais.[carece de fontes]
Referências
- ↑ a b c d e Thieme Römpp Online, abgerufen am 19. Juli 2011.
- ↑ The Merck Index. An Encyclopaedia of Chemicals, Drugs and Biologicals. 14. Auflage, 2006, S. 698, ISBN 978-0-911910-00-1.
- ↑ a b Organic Syntheses, Coll. Vol. 2, p.374 (1943); Vol. 19, p.61 (1939). pdf
- ↑ «Lysine». aminoacidsguide.com. Consultado em 20 de Fevereiro de 2016
- ↑ Voet, Donald; Voet, Judith G. (1 de janeiro de 2013). Bioquímica - 4ed. [S.l.]: Artmed Editora. ISBN 9788582710050
- ↑ «Lysine metabolism in mammalian brain: an update on the importance of recent discoveries.». ncbi.nlm.nih.gov. Consultado em 20 de Fevereiro de 2016
- ↑ Paulo Arruda. «AO papel da via da sacaropina em diversos modelos biológicos». bv.fapesp.b. Consultado em 20 de Fevereiro de 2016
- ↑ «L-lysine and L-arginine amino acid ratios in food diet». .traditionaloven. Consultado em 20 de Fevereiro de 2016
- ↑ «Lysine». University of Maryland Medical Center. Consultado em 20 de Fevereiro de 2016
- ↑ Yasuhiko Toride. «Lysine and other amino acids for feed: production and contribution to protein utilization in animal feeding - Yasuhiko Toride». .fao.org. Consultado em 20 de Fevereiro de 2016
- ↑ «L-Lisina». entendaoherpes.com.br. Consultado em 20 de Fevereiro de 2016. Arquivado do original em 6 de março de 2016
- ↑ Tatiana Zanin. «Alimentos ricos em Lisina». tuasaude.com. Consultado em 20 de Fevereiro de 2016
- ↑ Miro Smriga et al. «Lysine fortification reduces anxiety and lessens stress in family members in economically weak communities in Northwest Syria». pnas.org. Consultado em 20 de Fevereiro de 2016
- ↑ Miro Smriga e Kunio Torii. «L-Lysine acts like a partial serotonin receptor 4 antagonist and inhibits serotonin-mediated intestinal pathologies and anxiety in rats». pnas.org. Consultado em 20 de Fevereiro de 2016
- ↑ Kimberly Pryor e Ward Dean. «Growth Hormone: Amino Acids as GH Secretagogues». vrp.com. Consultado em 20 de Fevereiro de 2016
- ↑ A. Isidori et al. «GROWTH HORMONE AND AMINO ACIDS» (PDF). nutrimaxorganic.com. Consultado em 20 de Fevereiro de 2016
- ↑ Christianne de Faria Coelho et al. «Aplicações clínicas da suplementação de L-carnitina». scielo.br. Consultado em 20 de Fevereiro de 2016
- ↑ Balfour JA e Clissold SP. «Bendazac lysine. A review of its pharmacological properties and therapeutic potential in the management of cataracts.». ncbi.nlm.nih.gov. Consultado em 20 de Fevereiro de 2016
- ↑ Adrian F. Gombart. «The end of the line for neutrophils». bloodjournal. Consultado em 20 de Fevereiro de 2016
- ↑ Azzarà A et al. «Effects of lysine-arginine association on immune functions in patients with recurrent infections.». Pncbi.nlm.nih.gov. Consultado em 3 de março de 2014
- ↑ Jim English e Hyla Cass. «The Collagen Connection». nutritionreview.org. Consultado em 20 de Fevereiro de 2016
