RU2377301C2 - ОЛИГОМЕРНОЕ СОЕДИНЕНИЕ, ПОНИЖАЮЩЕЕ ЭКСПРЕССИЮ ЧЕЛОВЕЧЕСКОГО ГЕНА Bcl-2, КОНЪЮГАТ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ПРИМЕНЕНИЕ ОЛИГОМЕРНОГО СОЕДИНЕНИЯ ДЛЯ ЛЕЧЕНИЯ РАКА - Google Patents
ОЛИГОМЕРНОЕ СОЕДИНЕНИЕ, ПОНИЖАЮЩЕЕ ЭКСПРЕССИЮ ЧЕЛОВЕЧЕСКОГО ГЕНА Bcl-2, КОНЪЮГАТ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ПРИМЕНЕНИЕ ОЛИГОМЕРНОГО СОЕДИНЕНИЯ ДЛЯ ЛЕЧЕНИЯ РАКА Download PDFInfo
- Publication number
- RU2377301C2 RU2377301C2 RU2006126643/13A RU2006126643A RU2377301C2 RU 2377301 C2 RU2377301 C2 RU 2377301C2 RU 2006126643/13 A RU2006126643/13 A RU 2006126643/13A RU 2006126643 A RU2006126643 A RU 2006126643A RU 2377301 C2 RU2377301 C2 RU 2377301C2
- Authority
- RU
- Russia
- Prior art keywords
- lna
- dna
- seq
- rna
- binding domain
- Prior art date
Links
- 0 B[C@@]1C(*C2)[C@](*)C2(C[Zn])*1 Chemical compound B[C@@]1C(*C2)[C@](*)C2(C[Zn])*1 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/113—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/113—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing
- C12N15/1135—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing against oncogenes or tumor suppressor genes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H21/00—Compounds containing two or more mononucleotide units having separate phosphate or polyphosphate groups linked by saccharide radicals of nucleoside groups, e.g. nucleic acids
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/31—Chemical structure of the backbone
- C12N2310/315—Phosphorothioates
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/32—Chemical structure of the sugar
- C12N2310/323—Chemical structure of the sugar modified ring structure
- C12N2310/3231—Chemical structure of the sugar modified ring structure having an additional ring, e.g. LNA, ENA
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Chemical & Material Sciences (AREA)
- Genetics & Genomics (AREA)
- Organic Chemistry (AREA)
- Molecular Biology (AREA)
- Biomedical Technology (AREA)
- Biotechnology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Health & Medical Sciences (AREA)
- General Engineering & Computer Science (AREA)
- Wood Science & Technology (AREA)
- Biochemistry (AREA)
- Zoology (AREA)
- Physics & Mathematics (AREA)
- Microbiology (AREA)
- Plant Pathology (AREA)
- Biophysics (AREA)
- Oncology (AREA)
- Pharmacology & Pharmacy (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Animal Behavior & Ethology (AREA)
- Medicinal Chemistry (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Compositions Of Macromolecular Compounds (AREA)
Abstract
Изобретение относится к области биотехнологии, конкретно к олигомерному соединению, длиной 10-30 нуклеиновых оснований, и может быть использовано в медицине. Олигомерное соединение представляет собой мишень-связывающий домен, комплементарный отрезку из 10-18 последовательных нуклеотидов области от положения основания 1459 (5') до 1476 (3') мРНК человеческого Bcl-2 (HUMBcl2A (номер доступа М13994) в базе данных GenBank), кроме максимум одного ошибочного спаривания с указанным участком мРНК человеческого Bcl-2, где указанный связывающийся с мишенью домен имеет формулу: 5'-[(ДНК/РНК)0-1-(LNA/LNA*)2-7-(ДНК/РНК/LNA*)4-14-(LNA/LNA*)2-7-(WK/PHK)0-1]-3'. Изобретение позволяет получить олигомерное соединение, которое эффективно понижает экспрессию человеческого гена Bcl-2. 4 н. и 21 з.п. ф-лы, 20 ил., 3 табл.
Description
Настоящее изобретение относится к олигомерному соединению с улучшенными свойствами и к способам модуляции экспрессии гена Bcl-2 у человека. В частности, настоящее изобретение относится к олигомерным соединениям, имеющим длину 10-30 нуклеиновых оснований, и содержащим домен, связывающийся с мишенью, который специфически гибридизуется с областью от положения основания 1459 (5') до 1476 (3') мРНК человеческого Bcl-2, где указанный связывающийся с мишенью домен содержит, по меньшей мере, два нуклеотида LNA или нуклеотидных аналога LNA, связанных посредством фосфортиоатной группы (-О-Р(O,S)-O-).
Кроме того, настоящее изобретение относится к антисмысловым олигомерным соединениям, направленным против мРНК человеческого Bcl-2, и способным модулировать биосинтез человеческого белка Bcl-2. Настоящее изобретение также относится к фармацевтической композиции, содержащей такие олигомерные соединения, к ее применению и к способам лечения и диагностики с применением таких олигомерных соединений.
Предшествующий уровень техники
Человеческий Bcl-2 представляет собой белок, который тесно ассоциируется с механизмом запрограммированной клеточной гибели (апоптозом). Апоптоз представляет собой активный, жестко регулируемый физиологический процесс, участвующий в развитии клеток, в метаболизме клеток, в функциональном цикле нормальных клеток и в индуцированной гормонами атрофии ткани. Отсутствие запрограммированной клеточной гибели играет важную роль в развитии рака и других гиперпролиферативных заболеваний, таких как рестеноз, фиброз, псориаз или аллергические заболевания некоторых типов, в частности, в прогрессировании развития опухоли, и, что самое важное, может создавать проблемы, связанные с резистентностью к противоопухолевым курсам лечения, в частности курсам лечения стандартными химиотерапевтическими соединениями. В отличие от большинства нормальных тканей, в злокачественных опухолях, таких как мелкоклеточный рак легких (SCLC) и не-мелкоклеточный рак легких (NSCLC), часто ко-эпрессируется Вcl-2.
В заявке WO 95/08350 описаны антисмысловые олигомеры и способы с использованием этих олигомеров для предотвращения роста раковых клеток, экспрессирующих ген Bcl-2.
В публикации Klasa et al., Antisense & Nucleic Acid Drug Development 12:1993-213 (2002) (обзор) обсуждаются биологические эффекты соединения облимерсен-натрия (G3139) и его потенциальная эффективность как антисмыслового лекарственного средства. Указанное соединение имеет структуру 5'-d(P-тио)TCT-CCC-AGC-GTG-CGC-CAT-3'. Организация Genta Incorporated сделала заявление в Департамент по контролю за качеством пищевых продуктов, медикаментов и косметических средств о разрешении использования нового лекарственного средства (NDA) “облимерсен-натрий (G3139) + дакарбазин (DTIC)”. Во многих Научно-исследовательских центрах были проведены рандомизированные испытания на фазе 3 по использованию облимерсен-натрия (G3139) + дакарбазина (DTIC) и одного DTIC как химиотерапию первого ряда, проводимую через каждые три недели для лечения меланомы с метастазами. В мае 2004 г. было сделано сообщение о том, что данное исследование не давало положительного результата в отношении выживаемости пациентов после лечения G3139 + DTIC. Комбинация лекарственных средств ассоциировалась с повышенной токсичностью и с прерыванием курса лечения из-за побочных эффектов (AE) у пациентов, а именно, 69 (18,6%) пациентов прервали курс лечения препаратом G3139 из-за побочных эффектов, и 39 пациентов (10,8%) прервали курс лечения препаратом DTIC. Серьезные побочные эффекты (СПЭ) наблюдались у 40% пациентов, проходивших курс лечения препаратом G3139, и только у 27% пациентов, проходивших курс лечения препаратом DТIC. Поскольку доза DТIC в двух комбинациях была идентичной, то увеличение токсичности, вероятно, было обусловлено добавлением G3139. При этом, уровень выживаемости не увеличивался, а токсичность повышалась. Поэтому от применения этого нового лекарственного средства (NDA) пришлось отказаться. Однако, конечный результат второго анализа, проведенного спонсором, показал статистически значимое увеличение выживаемости пациентов без прогрессирования у них заболевания в среднем от 49 дней, при лечении препаратом DТIC, и до 74 дней при лечении комбинацией лекарственных средств, с разницей 25 дней (р=0,0003, НR=0,73). Кроме того, спонсор сообщил о значительном различии в показателях отклика, который в случае приема лишь одного DТIC составлял 6,8%, а в случае применение комбинации, составлял 11,7% (р=0,019). Тот факт, что облимерсен-натрий давал удовлетворительный конечный результат во втором исследовании, указывает на то, что он должен быть эффективным соединением для лечения меланомы с метастазами. Повышенная токсичность, выбор первичных конечных результатов и программы общих клинических испытаний являются теми факторами, которые могут приводить к неблагоприятному исходу лечения.
LNA-содержащие олигонуклеотиды, нацеленные на 6 первых кодонов мРНК человеческого Bcl-2, были исследованы в публикации Ph.D., диссертации, защищенной Jan Stenvang Jepsen (Май, 2003, Копенгагенский Университет). Полностью модифицированные последовательности LNA-фосфодиэфира (РО), фосфордиэфирные хэдмеры (LNA/PO у 5'-конца и ДНК/PS-фосфортиоат у 3'-конца), полностью фосфордиэфирные гэпмеры (размеры гэпа 8, 10, 12, 14) и гэпмеры с исключительным тиолированием в гэпе (размеры гэпа 8, 10, 12, 14) анализировали на in vitro поглощение различными трансфицирующими агентами, и на ингибирование белка Bcl-2. Исследование поглощения проводили в клетках МСF-7, и результаты анализировали с помощью микроскопии и проточной цитометрии. Для всех РО- и РО/PS-содержащих конструкций была достигнута одинаково эффективная доставка. Хотя было проведено исследование различных LNA-содержащих олигонуклеотидов и конструкций, однако в работе Stenvang Jepsen не сообщается и не высказывается каких-либо предположений о LNA-содержащих олигонуклеотидных гэпмерах, в которых значительное число нуклеотидных связей в мишень-связывающем домене, включая LNA-концы, представляют собой фосфортиоатные группы (-О-Р(О,S)-О-), вероятно, обусловлено тем известным фактом, что фосфортиолирование должно приводить к снижению аффинности, и потому, оно должно приводить к нестабильности.
В публикации Frieden et al., Nucleic Acid Research, 2003, Vol. 31, № 21, 6365-6373 и в WO 2004/046160 A2 приводятся различные обсуждения, касающиеся конструирования антисмысловых олигонуклеотидов, проводимого в in vitro экспериментах.
В публикации Fluiter et al., Nucleic Acid Research, 2003, Vol. 3, 953-962 описаны исследования по in vivo ингибированию роста опухоли и биологического распределения антисмысловых LNA-олигонуклеотидов.
Описание сущности изобретения
Исходя из вышеописанного, и в частности, принимая во внимание проблемы, связанные с эффективностью применения соединения облимерсен-натрия, очевидно, что необходимость в улучшении свойств олигомерного соединения, ингибирующего Bcl-2, остается актуальной. Такое соединение, предпочтительно, должно иметь подходящий in vivo профиль распределения в тканях и ингибирования Bcl-2, а следовательно, и более высокую терапевтическую эффективность при лечении различных Bcl-2-ассоциированных состояний, в частности рака.
В этой связи следует сказать, что авторами настоящего изобретения было обнаружено, что некоторые новые LNA-олигомерные соединения типа гэпмера обладают биологическим действием, которое сравнимо или превышает действие облимерсен-натрия, и, при исследовании этого средства в фармакологически релевантных дозах не было обнаружено побочных эффектов.
Более конкретно, авторами настоящего изобретения было обнаружено, что олигомерные соединения, имеющие длину 10-30 нуклеиновых оснований и содержащие домен, связывающийся с мишенью, который специфически гибридизуется с областью от положения основания 1459 (5') до 1476 (3') мРНК человеческого Bcl-2, где указанный связывающийся с мишенью домен имеет формулу:
5'-[(ДНК/РНК)0-1-(LNA/LNA*)2-7-(ДНК/РНК/LNA*)4-14-(LNA/LNA*)2-7-
(ДНК/РНК)0-1]-3',
где “LNA” означает нуклеотид LNA, и “LNA*” означает аналог нуклеотида LNA; и где указанный мишень-связывающий домен содержит, по меньшей мере, два нуклеотида LNA или нуклеотидного аналога LNA, связанных фосфортиоатной группой, и обладают представляющими интерес биологическими свойствами.
Краткое описание графического материала
На фиг.1 проиллюстрировано ингибирование Bcl-2 в клетках 15PC3, трансфицированных олигомерными соединениями LNA, и проанализированных с помощью Вестерн-блот-анализа. Последовательности SEQ ID NO:2, 4, 15, 21 и 24 (см. таблицу 1) оказались более сильными ингибиторами Bcl-2, как было измерено на уровне белка, по сравнению с облимерсен-натрием, то есть соединением, имеющим последовательность SEQ ID NO:56 (эталон). Белок сурвивин служил в качестве контроля.
На фиг.2А проиллюстрировано ингибирование Bcl-2 в клетках 15PC3, трансфицированных олигомерными соединениями LNA, проанализированных с помощью Вестерн-блот-анализа и визуализированных с помощью хемилюминесцентной системы детекции. Последовательность SEQ ID NO:2 оказалась более эффективной, чем SEQ ID NO:56 (эталон). Белок сурвивин служил в качестве контроля.
На фиг.2В представлен Вестерн-блот-анализ. Клетки 518А2 были подвергнуты липофекции 5 нМ SEQ ID NO:56 (эталон), SEQ ID NO:8 и SEQ ID NO:15, соответственно. Белок анализировали через 48 часов. Последовательность SEQ ID NO:15 сохраняла активность на протяжении всего этого времени. На графике представлены данные, нормализованные к тубулину.
На фиг.2С представлен Вестерн-блот-анализ. Клетки 518А2 были подвергнуты липофекции 5 нМ SEQ ID NO:56, SEQ ID NO:8, SEQ ID NO:15 и SEQ ID NO:35, соответственно, которая представляет собой n-1-вариант 15-мера SEQ ID NO:15. Белок анализировали через 48 часов. Последовательность SEQ ID NO:35 была такой же эффективной, как и последовательность SEQ ID NO:15. Данные были нормализованы к тубулину.
На фиг.3А проиллюстрировано индуцирование апоптоза, измеренное по активности каспазы 3/7, LNA-содержащим соединением в клетках 518А2, через 24, 48 и 72 ч. LNA-олигомеры SEQ ID NO:2, 4, 12, 15, 21, 24 и 57 индуцировали апоптоз более эффективно, чем SEQ ID NO:56 (эталон) и соответствующее метилированное соединение цитозина, обозначаемое SEQ ID NO:59. Более низкие уровни каспазы 3/7 в более поздние промежутки времени (например, через 72 часа) обусловлены клеточной гибелью в результате апоптоза при более ранней активации каспазы 3/7. Таким образом, максимальная активация была достигнута еще до проведения мониторинга.
На фигуре 3В проиллюстрировано индуцирование апоптоза, измеренное по активности каспазы 3/7, LNA-содержащим соединением в клетках 518А2, через 13, 24, 48 и 72 ч. LNA-олигомеры SEQ ID NO:8, 9, 15 и 16 индуцировали апоптоз более эффективно, по сравнению с SEQ ID NO:58, то есть контрольным олигонуклеотидом с противоположной полярностью, также содержащим LNA.
На фиг.3С проиллюстрировано индуцирование поздней фазы клеточного апоптоза, измеренное с помощью проточного цитометрического анализа с использованием аннексина V-FITC. Клетки НеLa, обработанные олигомерным соединением LNA SEQ ID NO:15, были классифицированы как клетки “с более поздним апоптозом” или “поврежденные” клетки по сравнению с ложнообработанными клетками и клетками, обработанными SEQ ID NO:56 (эталон).
На фиг.3D проиллюстрирована обработка клеток 5 нМ и 12,5 нМ SEQ ID NO:8 и SEQ ID NO:15, которая приводит к индуцированию апоптоза на ранней и поздней стадии, измеренному с помощью проточного цитометрического анализа с использованием аннексина V-FITC, по сравнению с ложнообработанными клетками.
На фиг.4 проиллюстрировано ингибирование Bcl-2 в пролиферирующихcя раковых клетках (анализ MTS), клетках 518А2, измеренное через 48 часов после обработки LNA-олигомерным соединением, ингибирующим Bcl-2. Все соединения SEQ ID NO:2, 4, 12, 15, 21, 24 и 57 были более сильными ингибиторами пролиферации по сравнению с соединением SEQ ID NO:56 (эталон) и соответствующим метилированным соединением цитозина SEQ ID NO:59 (эталон). Данные были скорректированы на ложнообработанный контроль. Эксперимент 1 и эксперимент 2 представляют собой два отдельных эксперимента.
На фиг.5 проиллюстрировано ингибирование Bcl-2 в пролиферирующих раковых клетках, клетках 518А2, измеренное во время действия 0-48 часов после обработки олигомерным соединением LNA, ингибирующим Bcl-2. Все соединения SEQ ID NO:2, 4, 12, 15, 21, 24 и 57 являются более сильными ингибиторами пролиферации по сравнению с соединением SEQ ID NO:56 (эталон) и соответствующим метилированным соединением цитозина SEQ ID NO:59 (эталон). Данные были скорректированы на ложнообработанный контроль.
На фиг.6 представлен Вестерн-блот-анализ. Клетки 518А2 были подвергнуты липофекции 10 нМ SEQ ID NO:56 (эталон) и SEQ ID NO:15, соответственно. Белок анализировали через 24 часа, 48 часов и 72 часа. Последовательность SEQ ID NO:15 сохраняла активность на протяжении всего этого времени. Через 24 часа белок Bcl-2 еще наблюдался благодаря своему продолжительному времени полужизни.
На фиг.7А проиллюстрировано эффективное in vivo уменьшение объема опухоли под действием соединения SEQ ID NO:15 по сравнению с соединением SEQ ID NO:56 (эталон) в предстательной железе бестимусных (“голых”) мышей с моделью ксенотрансплантата PC3. Соединения вводили внутрибрюшинно в дозе в течение 14 дней. Митомицин С, вводимый внутрибрюшинно в дозе 2 мг/кг в течение 14 дней, использовали в качестве позитивного контроля. Мониторинг роста опухоли проводили еще 8 дней после обработки.
На фиг.7В показано, что при введении соединения SEQ ID NO:15 в предстательную железу бестимусных (“голых”) мышей с моделью ксенотрансплантата PC3, какой-либо значимой потери веса у этих мышей не наблюдалось. SEQ ID NO:56 (эталон) в дозе 10 мг/кг и митомицин С, используемый в качестве позитивного контроля и вводимый в дозе 2 мг/кг, давал аналогичный эффект.
На фиг.7С проиллюстрировано эффективное in vivo уменьшение объема опухоли под действием SEQ ID NO:8 по сравнению с физиологическим раствором, используемым в качестве контроля, в модели ксенотрансплантата PC3 предстательной железы у бестимусных (“голых”) мышей. Соединения вводили внутрибрюшинно в дозе 10 мг/кг в течение 14 дней (дни 5-19).
На фиг.7D проиллюстрировано эффективное in vivo уменьшение объема опухоли под действием SEQ ID NO:15, вводимого в предстательную железу бестимусных (“голых”) мышей с моделью ксенотрансплантата PC3 ежедневно в дни 7-15 или в дни 8, 11, 13, 15, 18, 20, по сравнению с контрольным физиологическим раствором в модели ксенотрансплантата PC3 предстательной железы у бестимусных (“голых”) мышей. Соединения вводили внутрибрюшинно в дозе 10 мг/кг в течение 14 дней. Мониторинг роста опухоли проводили еще 8 дней после обработки.
На фиг.8А проиллюстрировано сравнимое in vivo уменьшение массы опухоли (граммы) после внутрибрюшинного введения SEQ ID NO:15 в дозе 1,75 мг/кг в течение 14 дней мышам SCID с моделью 518А2 ксенотрансплантата меланомы по сравнению с уменьшением массы опухоли после введения соединения SEQ ID NO:56 (эталон) в дозе, которая в 4 раза превышала дозу соединения SEQ ID NO:15.
На фиг.8В представлены результаты эксперимента, проиллюстрированного на фиг.8А, за исключением того, что эти результаты представлены, не в граммах, а в % уменьшения массы опухоли.
На фиг.9 проиллюстрировано сравнимое in vivo уменьшение объема опухоли после внутрибрюшинного введения SEQ ID NO:15 в дозе 1,75 мг/кг в течение 14 дней мышам SCID с моделью ксенотрансплантата меланомы 518А2 по сравнению с уменьшением объема опухоли после введения соединения SEQ ID NO:56 (эталон) в дозе, которая в 4 раза превышала дозу соединения SEQ ID NO:15.
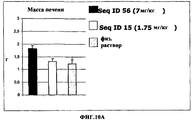
На фиг.10А проиллюстрировано отсутствие увеличения размера печени после внутрибрюшинного введения SEQ ID NO:15 в дозе 1,75 мг/кг в течение 14 дней мышам SCID с моделью ксенотрансплантата меланомы 518А2 по сравнению с эффектом, достигаемом после введения физиологического раствора, используемого в качестве контроля. Соединение SEQ ID NO:56 (эталон), вводимое в дозе 7 мг/кг, приводило к увеличению размера печени.
На фиг.10В проиллюстрировано отсутствие увеличения размера селезенки после внутрибрюшинного введения SEQ ID NO:15 в дозе 1,75 мг/кг в течение 14 дней мышам SCID с моделью ксенотрансплантата меланомы 518А2 по сравнению с эффектом, достигаемом при введении физиологического раствора, используемого в качестве контроля. Соединение SEQ ID NO:56 (эталон), вводимое в дозе 7 мг/кг, приводило к увеличению размера селезенки. Это указывает на то, что соединение SEQ ID NO:15 в активной дозе обладает более низкой токсичностью, чем соединение SEQ ID NO:56 (эталон).
На фиг.10С показано, что обработка не приводит к уменьшению массы тела мыши при внутрибрюшинном введении SEQ ID NO:15 в дозе 1,75 мг/кг в течение 14 дней мышам SCID с моделью ксенотрансплантата меланомы 518А2 по сравнению с эффектом, достигаемым при введении физиологического раствора, используемого в качестве контроля, и SEQ ID NO:56 (эталон), вводимого в дозе 7 мг/кг. Это указывает на то, что соединение SEQ ID NO:15 в активной дозе обладает более низкой токсичностью, чем соединение SEQ ID NO:56 (эталон).
На фиг.11 показано значительное уменьшение in vivo массы опухоли у мышей SCID с моделью ксенотрансплантата меланомы 518А2 при внутрибрюшинном введении SEQ ID NO:8 в дозе 7 мг/кг в течение 14 дней по сравнению с эффектом, достигаемом при введении соединения SEQ ID NO:56 (эталон) в той же самой дозе. SEQ ID NO:8 обнаруживает такую же противоопухолевую активность при введении в дозе в 7 раз более низкой дозе, чем SEQ ID NO:56 (эталон).
На фиг.12А проиллюстрирована повышенная стабильность SEQ ID NO:15, 16 и 20 в плазме крыс (самцов крыс NtacSD, Li-гепарин (Taconic, M&B)) по сравнению с соединением SEQ ID NO:56 (эталон). Олигонуклеотиды инкубировали при концентрациях 20 мкМ при 37°С в течение 0, 4, 24 и 48 часов, соответственно. Фрагментом расщепления, присутствующим в образце, является лишь олигонуклеотид, соответствующий n-1 (15-мер), в котором у 3'-конца отсутствует остаток ДНК. Каких-либо других фрагментов расщепления, даже после проведения 48-часового гидролиза, не обнаруживалось.
На фиг.12В показано, что SEQ ID NO: 8 и 9 обладают высокой стабильностью в плазме крыс по сравнению со стабильностью SEQ ID NO:56 (эталон). Олигонуклеотиды инкубировали при концентрациях 20 мкМ при 37°С в течение 0, 4, 24 и 48 часов, соответственно. Фрагментом расщепления, присутствующим в образце, является лишь олигонуклеотид, соответствующий n-1 (15-мер), в котором, у 3'-конца отсутствует остаток ДНК. Каких-либо других фрагментов расщепления, даже после проведения 48-часового гидролиза, не обнаруживалось.
На фиг.13 показаны уровни SEQ ID NO:15 в печени и в почках мышей NMRI после внутривенного введения разовой дозы (25 мг/кг). Было установлено, что время полужизни (Т1/2) активного соединения SEQ ID NO:15 как в печени, так и в почках составляет примерно 3 дня. Это указывает на то, что схемы введения оптимальных биологических доз SEQ ID NO:15 могут быть составлены с меньшей частотой, чем непрерывное вливание и введение суточной дозы.
Описание изобретения
Как было упомянуто выше, авторами настоящего изобретения было обнаружено, что олигомерные соединения, имеющие длину 10-30 нуклеиновых оснований, и содержащие домен, связывающийся с мишенью, который специфически гибридизуется с областью от положения основания 1459 (5') до 1476 (3') мРНК человеческого Bcl-2, где указанный связывающийся с мишенью домен имеет формулу:
5'-[(ДНК/РНК)0-1-(LNA/LNA*)2-7-(ДНК/РНК/LNA*)4-14-(LNA/LNA*)2-7-
ДНК/РНК)0-1]-3',
где “LNA” означает нуклеотид LNA, а “LNA*” означает аналог нуклеотида LNA; и где указанный мишень-связывающий домен содержит, по меньшей мере, два нуклеотида LNA или аналога нуклеотида LNA, связанных фосфортиоатной группой, и обладает представляющими интерес биологическими свойствами.
В общих чертах, описанные здесь олигомерные соединения, очевидно, обладают улучшенными свойствами по сравнению со свойствами известных олигомерных соединений. Термин “улучшенные свойства” следует понимать как один или несколько параметров, благодаря которым олигомерные соединения обладают общей эффективностью, которая превышает или равна эффективности их фосфотиоатных аналогов.
Примерами таких улучшенных параметров являются более длительный срок хранения лекарственного средства, более высокая константа связывания с мишенью (промежуточным комплементом в олигомерном соединении или мРНК-мишень), хорошая резистентность к внеклеточным и внутриклеточным нуклеазам, более высокая эффективность в данном механизме действия, лучший фенотипический ответ, более продолжительное действие, более высокий уровень хемосенситизации и более удобное применение лекарственного средства пациентом. Примерами параметров, сообщающих такую же эффективность, являются легкость получения лекарственных средств, легкость приготовления фармацевтических композиций, распределение в тканях и хороший профиль безопасности.
В целом, описанные здесь олигомерные соединения имеют величины IC50 в очень низком наномолярном интервале (5 нМ) в отношении ингибирования мРНК Bcl-2, в отношении ингибирования белка (отношение Bcl-2/Вах изменяется от 1 нМ) и ингибирования пролиферации клеток. Эти величины значительно превышают величины, наблюдаемые для облимерсена и для соединений Jepsen (при 400 нМ могут наблюдаться значительные уровни ингибирования). Кроме того, клеточная гибель значительно коррелирует с индуцированием апоптоза, и было показано, что эти уровни индуцирования апоптоза значительно превышают уровни индуцирования, обеспечиваемые облимерсеном. Кроме того, описанные здесь олигомерные соединения обнаруживают значительно более высокую стабильность в плазме крыс и более длительное время полужизни в ткани по сравнению с облимерсеном. Повторный противоопухолевый ответ наблюдался в предстательной железе и в модели меланомы, даже при дозе 1 мг/кг/день. Кроме того, противоопухолевый ответ также наблюдался при менее частом введении доз указанного соединения по сравнению с обычной дозой, описанной в литературе для облимерсена. При этом каких-либо побочных эффектов при фармакологически релевантных дозах, таких как увеличение ASAT, ALAT, не наблюдалось. Результаты, полученные авторами настоящего изобретения, превосходили результаты, полученные для конструкций Jepsen, для которых не были проанализированы функциональный ответ, стабильность, время полужизни в ткани, in vivo ответ, клинические биохимические параметры или биологическое распределение.
Упоминаемая здесь последовательность человеческой мРНК Bcl-2 имеется в базе данных Genbank под названием HUMBcl2A и под регистрационным номером М13994. В контексте описания настоящей заявки, нумерация нуклеиновых кислот, в частности последовательностей мРНК или соответствующих кДНК, соответствует нумерации человеческой мРНК Bcl-2, имеющейся в указанной базе данных под указанным регистрационным номером. Соответствующая последовательность кДНК может быть выведена из последовательности мРНК, в частности, путем замены любого основания Т указанной последовательности кДНК основанием U в последовательности мРНК, и наоборот.
Олигомерные соединения
Олигомерные соединения характеризуются тем, что они в своем мишень-связывающем домене содержат, по меньшей мере, два нуклеотида LNA или нуклеотидных аналога LNA, связанных фосфортиоатной группой.
Используемый здесь термин “мишень-связывающий домен” означает домен олигомерного соединения (или даже само олигомерное соединение), который связывается с конкретной последовательностью-мишенью, а именно, с областью от положения основания 1459 (5') до 1476 (3') мРНК человеческого Bcl-2.
В одном из вариантов изобретения мишень-связывающий домен содержит, по меньшей мере, два нуклеотида LNA, связанных фосфортиоатной группой (-О-Р(О,S)-О-).
В другом варианте изобретения мишень-связывающий домен содержит, по меньшей мере, два нуклеотидных аналога LNA, связанных фосфортиоатной группой (-О-Р(О,S)-О-).
Используемый здесь термин “олигомерные соединения” означает LNA-олигонуклеотиды, т.е., рибонуклеиновую кислоту (РНК) или дезоксирибонуклеиновую кислоту (ДНК), модифицированную путем замены одного или нескольких (или всех) присутствующих в них нуклеотидов нуклеотидами LNA или нуклеотидными аналогами LNA, в частности, по меньшей мере, двумя нуклеотидами LNA, при этом возможна и другая замена нуклеотидов нуклеотидными аналогами LNA и производными/аналогами этих нуклеотидов.
Термин “олигонуклеотид” включает олигонуклеотиды, состоящие из природных нуклеиновых оснований, сахаров и межнуклеозидных (каркасных) связей, а также олигонуклеотиды, имеющие неприродные части с аналогичными функциями или с конкретными улучшенными функциями.
Олигомерные соединения, используемые в контексте описания изобретения, имеют длину в 10-30 нуклеиновых оснований, например 10-25, а именно 10-20, например 10-18, или 10-16 или 15-17 нуклеиновых оснований.
Используемый здесь термин “длина нуклеинового основания” означает число нуклеиновых оснований после их гибридизации с линейной комплементарной молекулой нуклеиновой кислоты, т.е., общее число нуклеиновых оснований комплементарной нуклеиновой кислоты в области, с которой гибридизовано указанное олигомерное соединение. Таким образом, длина олигомерного соединения включает любые промежуточные нуклеотиды, где отсутствует нуклеиновое основание.
В одном из основных вариантов изобретения олигомерные соединения (LNA-олигонуклеотиды) согласно изобретению включают, по меньшей мере, два нуклеотида LNA.
В другом варианте изобретения олигомерные соединения (LNA-олигонуклеотиды) согласно изобретению включают, по меньшей мере, два нуклеотидных аналога LNA, и возможно, один или несколько нуклеотидов LNA.
Термин “по меньшей мере, два” включает целое число, превышающее или равное 2, такое как 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17 и т.д.
Термин “по меньшей мере, один” включает целое число, превышающее или равное 1, такое как 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17 и т.д.
Артикль “а”, используемый по отношению к нуклеозиду, нуклеозидному аналогу, SEQ ID NO: и т.п. означает “один или более”. В частности, выражение “компонент (такой как нуклеозид, нуклеозидный аналог, SEQ ID NO: или т.п.), выбранный из группы, состоящей из…” означает, что могут быть выбраны один или несколько из указанных компонентов. Таким образом, выражение типа “компонент, выбранный из группы, состоящей из А, В и С”, включает все комбинации А, В и С, то есть, А, В, С, А+В, А+С, В+С и А+В+С.
Термин “LNA” (блокированная нуклеиновая кислота) (или “олигонуклеотид LNA”) означает олигонуклеотид, содержащий один или более бициклических нуклеозидных аналогов, что также относится к нуклеотидам LNA и нуклеотидным аналогам LNA.
Олигонуклеотиды LNA, нуклеотиды LNA и нуклеотидные аналоги LNA в общих чертах описаны в WO 99/14226 и в следующих заявках, WO 00/56746, WO 00/56748, WO 00/66604, WO 00/125248, WO 02/28875, WO 2002/094250 и РСТ/DK02/00488, каждая из которых включена в настоящее описание посредством ссылки.
В контексте настоящей заявки и формулы изобретения авторы настоящего изобретения считают, что термины “нуклеотиды LNA” и “нуклеотидные аналоги LNA” отличаются друг от друга. Термин “нуклеотид LNA” означает нуклеотид формулы I:
Такие нуклеотиды LNA часто обозначаются "p-D-окси-LNA".
В формуле 1 В означает нуклеиновое основание. Нуклеиновые основания включают природные нуклеиновые основания, а также неприродные нуклеиновые основания. Репрезентативными нуклеиновыми основаниями являются нуклеиновые основания, выбранные из аденина, цитозина, 5-метилцитозина, изоцитозина, псевдоизоцитозина, гуанина, тимина, урацила, 5-бромурацила, 5-пропинилурацила, 5-пропинил-6-фторурацила, 5-метилтиазолурацила, 6-аминопурина, 2-аминопурина, инозина, диаминопурина, 7-пропин-7-деазааденина, 7-пропин-7-деазагуанина и 2-хлор-6-аминопурина. Предпочтительными примерами В являются аденин, цитозин, 5-метилцитозин, изоцитозин, псевдоизоцитозин, гуанин, тимин, урацил, 5-бромурацил, 5-пропинилурацил, 6-аминопурин, 2-аминопурин, инозин, диаминопурин и 2-хлор-6-аминопурин.
В формуле 1, Z* выбран из межнуклеозидной связи и концевой группы, а Z выбран из связи с межнуклеозидной связью предшествующего нуклеотида/нуклеозида и концевой группы, разумеется, при условии, что только один из Z и Z* может быть концевой группой.
Межнуклеозидная связь, как возможное значение Z*, означает межнуклеозидную связь с последующим нуклеотидом/нуклеозидом. Примерами межнуклеозидных линкеров являются -O-Р(O)2-O-, -O- Р(О,S)-О-, -О-Р(S)2-О-, -S-Р(О)2-О-, -S-Р(О,S)-О-, -S-Р(S)2-О-, -О-Р(О)2-S-, -О-Р(О,S)-S-, -S-Р(О)2-S-, О-РО(RН)-О-, O-PO(OСН3)-О-, -О-РО(NRН)-О-, -О-РО(ОСН2СН2S-R)-O-, -О-РО(ВH3)-О-, -О-РО(NHRН)-О-, -О-Р(О)2-NRН-, NRН-Р(О)2-О-, -NRН-СО-О-, -NRН-СО-NRН-, -О-СО-О-, -О-СО-NRН-, NRН-СО-СН2-, -О-СН2-СО-NRН-, -О-СН2-СН2-NRН-, -СО-NRН-СН2-, -СН2-NRН-СО-, -О-СН2-СН2-S-, -S-СН2-СН2-О-, -S-СН2-СН2-S-, -СН2-SО2-СН2-, -СН2-СО-NRН-,
-О-СН2-СН2-NRН-СО-, -СН2-NСН3-О-СН2-, где RН выбран из водорода и С1-4алкила. Предпочтительными межнуклеозидными связями являются -О-Р(О)2-О-, -О-Р(О,S)-О-, -О-Р(S)2-О-, -S-Р(О)2-О-, -S-P(O,S)-O-, -S-Р(S)2-О-, -О-Р(О)2-S-, -О-P(O,S)-S- и
-S-Р(О)2-S-. Отличительным признаком настоящего изобретения является то, что два нуклеотида LNA связаны посредством -О-Р(О,S)-О- (фосфортиоатной) группы, т.е., межнуклеозидной связью предпочтительно является фосфортиоатная группа.
В контексте настоящего изобретения термин “С1-4алкил” означает прямую или разветвленную насыщенную углеводородную цепь, имеющую от одного до четырех атомов углерода, такую как метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил и трет-бутил.
Если нуклеотид LNA представляет собой 5'-концевой нуклеотид олигомерного соединения, то Z* означает концевую группу, а если нуклеотид LNA представляет собой 3'-концевой нуклеотид олигомерного соединения, то Z означает концевую группу. Такие концевые группы обычно выбирают из водорода, азидо, галогена, циано, нитро, гидрокси, Prot-O, Асt-О, меркапто, Prot-S, Асt-S, С1-6алкилтио, амино, Prot-N(RН)-, Асt-N(RН)-, моно или ди(С1-6алкил)амино, необязательно замещенного
С1-6алкокси, необязательно замещенного С1-6алкила, необязательно замещенного С2-6алкенила, необязательно замещенного С2-6алкенилокси, необязательно замещенного С2-6алкинила, необязательно замещенного С2-6алкинилокси, монофосфата, монотиофосфата, дифосфата, дитиофосфата, трифосфата, тритиофосфата, ДНК-интекаляторов, фотохимически активных групп, термохимически активных групп, хелатообразующих групп, репортерных групп, лигандов, карбокси, сульфоно, гидроксиметила, Prot-О-СН2, Асt-О-СН2, аминометила, Prot-N(RН)-СН2, Асt-N(RН)-СН2, карбоксиметила и сульфонометила, где Prot представляет собой защитную группу для -ОН, -SН и -NН(RН), соответственно, Асt представляет собой активирующую группу для -ОН, -SН и -NН(RН), соответственно, а RН выбран из водорода и С1-6алкила. Предпочтительными примерами концевых групп являются водород, азидо, галоген, циано, нитро, гидрокси, Prot-O, Асt-О, меркапто, Prot-S, Асt-S, С1-6алкилтио, амино, Prot-N(RН)-, Асt-N(RН)-, моно или ди(С1-6алкил)амино, необязательно замещенный С1-6алкокси, необязательно замещенный С1-6алкил, необязательно замещенный монофосфат, монотиофосфат, дифосфат, дитиофосфат, трифосфат и тритиофосфат, где Prot представляет собой защитную группу для -ОН, -SН и -NН(RН), соответственно, Асt представляет собой активирующую группу для -ОН, -SН и -NН(RН), соответственно, а RН выбран из водорода и С1-6алкила.
Защитные группы (Prot) заместителей гидрокси (и серы) включают замещенный тритил, такой как 4,4'-диметокситритилокси (DМТ), 4-монометокситритилокси (ММТ) и тритилокси, необязательно замещенный 9-(9-фенил)ксантенилокси (пиксил), необязательно замещенный метокситетрагидропиранилокси (mthp), силилокси, такой как триметилсилилокси (ТМS), триизопропилсилилокси (TIPS), трет-бутилдиметилсилилокси (TBDMS), триэтилсилилокси и фенилдиметилсилилокси, трет-бутиловые эфиры, ацетали (включающие две гидроксигруппы), ацилокси, такой как ацетил или замещенные галогеном ацетилы, например хлорацетилокси или фторацетилокси, изобутирилокси, пивалоилокси, бензоилокси и замещенные бензоилы, метоксиметилокси (МОМ) и бензиловые эфиры или замещенные бензиловые эфиры, такие как 2,6-дихлорбензилокси (2,6-Cl2Bzl). Предпочтительные защитные группы заместителей гидрокси (и серы) включают замещенный тритил, такой как 4,4'-диметокситритилокси (DMT), 4-монометокситритилокси (ММТ), необязательно замещенный 9-(9-фенил)ксантенилокси (пиксил), необязательно замещенный метокситетрагидропиранилокси (mthp), силилокси, такой как триметилсилилокси (TMS), триизопропилсилилокси (TIPS), трет-бутилдиметилсилилокси (TBDMS), триэтилсилилокси и фенилдиметилсилилокси, трет-бутиловые эфиры, ацетали (включающие две гидроксигруппы) и ацилокси, такой как ацетил.
Репрезентативными примерами защитных групп амидо- и амидогрупп являются флуоренилметоксикарбониламино (Fmoc), трет-бутилоксикарбониламино (ВОС), трифторацетиламино, аллилоксикарбониламино (alloc, AOC), Z-бензилоксикарбониламино (Cbz), замещенные бензилоксикарбониламины, такие как 2-хлорбензилоксикарбониламино (2-CIZ), монометокситритиламино (ММТ), диметокситритиламино (DMT), фталоиламино и 9-(9-фенил)ксантениламино (пиксил). Предпочтительными примерами являются флуоренилметоксикарбониламино (Fmoc), трет-бутилоксикарбониламино (ВОС), трифторацетиламино, аллилоксикарбониламино (alloc, AOC), монометокситритиламино (ММТ), диметокситритиламино (DMT), фталоиламино.
Группа “Act” представляет собой активирующую группу для -ОН, -SH и -NH(RН), соответственно, для присоединения других нуклеотидов, твердофазных носителей, белков и т.п. В вышеуказанных вариантах изобретения, Act означает активирующую группу. Такие активирующие группы, например, выбирают из необязательно замещенного О-фосфорамидита, необязательно замещенного О-фосфотриэфира, необязательно замещенного О-фосфодиэфира, необязательно замещенного Н-фосфоната и необязательно замещенного О-фосфоната. В контексте настоящего изобретения, термин “фосфорамидит” означает группу формулы -Р(ОRх)-N(Ry)2, где Rх означает необязательно замещенную алкильную группу, например, метил, 2-цианоэтил или бензил, а каждый из Ry означает необязательно замещенные алкильные группы, например этил или изопропил, либо группа -N(Ry)2 образует морфолиногруппу (-N(СН2СН2)2О). Rх предпочтительно означает 2-цианоэтил, а два
Ry, предпочтительно, являются идентичными и означают изопропил. Так, например, особенно подходящим фосфорамидитом является N,N-диизопропил-О-(2-цианоэтил)фосфорамидит.
Как упоминалось выше, олигомерные соединения включают нуклеотиды LNA, возможно, в комбинации с нуклеотидами, которые не являются нуклеотидами LNA. Такими нуклеотидами являются дезоксирибонуклеотиды (нуклеотиды ДНК), рибонуклеотиды (нуклеотиды РНК), нуклеотидные производные, нуклеотидные аналоги LNA, нуклеотидные аналоги (соединения, отличающиеся от LNA) и компоненты РNA и т.п.
Нуклеотидные аналоги и нуклеотидные производные описаны, например, в публикациях Freier & Altmann (Nucl. Acid. Res., 1997, 25, 4429-4443) и Uhlmann (Curr. Opinion in Drug & Development (2000, 3(2):293-213). На схеме 1 проиллюстрированы их выбранные примеры:
Схема 1
Термин “нуклеотидный аналог LNA” означает бициклические нуклеотидные аналоги, которые в общих чертах описаны в WO 99/14226 и в следующих заявках, WO 00/56746, WO 00/56748, WO 00/66604, WO 00/125248, WO 02/28875, WO 2002/094250 и WO 2003/006475 (РСТ/DK02/00488)(см. выше), за исключением, однако, уже описанных “нуклеотидов LNA”.
Примеры конкретной группы предпочтительных нуклеотидных аналогов LNA представлены формулой 2:
Формула 2 (нуклеотидный аналог LNA)
В формуле 2, Х и Y независимо выбраны из -О-, -S-, -N(Н)-, -N(R)-, -СН2- или -СН- (если они являются частью двойной связи), -СН2-О-, -СН2-S-, -СН2-N(Н)-, -СН2-N(R)-, -СН2-СН2- или -СН2-СН- (если они являются частью двойной связи), -СН=СН-, где R выбран из водорода и С1-4алкила. Ассиметирические группы могут присутствовать в любой ориентации. В предпочтительных вариантах изобретения, Х представляет собой кислород, а Y выбран из -О-, -S-, -N(Н)- и -N(R)-, но, при этом, не включаются “нуклеотиды LNA” (Х=О и Y=О).
Олигомерное соединение согласно изобретению может также содержать группы Z и Z*, определенные для нуклеотидов LNA.
В формуле 2 четыре хиральных центра показаны в фиксированной конфигурации. Однако настоящее изобретение также включает соединения общей формулы 2, в которых хиральные центры присутствуют в различных конфигурациях. Таким образом, каждый хиральный центр в формуле 2 может присутствовать в R- или S-конфигурации. Определения R (праворащающего изомера)(rectus) и S (левовращающего изомера) (sinister) описаны в Рекомендациях IUPAC 1974, в разделе Е, озаглавленном “Фундаментальная стереохимия”: Эти правила можно найти в публикации Pure Appl. Chem. 45, 13-30 (1976) и “Nomenclature of organic Chemistry” Pergamon, New York, 1979.
Конкретные примеры “нуклеотидных аналогов LNA” представлены формулами I, II, III, IV, V и VI:
Одним из примеров является нуклеотид “тио-LNA”, то есть нуклеотидный аналог LNA, в котором, по меньшей мере, один из Х в формулах I, III, IV или VI выбран из -S- или -СН2-S-. Такой тио-LNA может присутствовать в бета-D-конфигурации (I и IV) и в альфа-L-конфигурации (III и VI), соответственно.
Другим примером является нуклеотид “амино-LNA”, то есть нуклеотидный аналог LNA, в котором, по меньшей мере, один из Х в формулах I, III, IV или VI выбран из -N(Н)-, -N(R)-, -СН2-N(Н)-, -СН2-N(R)-, где R выбран из водорода и С1-4алкила. Такой амино-LNA может присутствовать в бета-D-конфигурации (I и IV) и в альфа-L-конфигурации (III и VI), соответственно.
Еще одним примером является нуклеотид “ена-LNA”, то есть нуклеотидный аналог LNA, в котором, по меньшей мере, один из Х в формулах II или V представляет собой -СН2-О-.
β-D-окси-LNA α-L-окси-LNA
В еще одном варианте изобретения олигомерное соединение содержит нуклеотид “альфа-L-LNA” (то есть, “α-L-LNA”), то есть нуклеотидный аналог LNA, представленный формулами III и VI.
Следует отметить, что нуклеотидные аналоги LNA, если они присутствуют, предпочтительно, выбраны из β-D-амино-LNA, β-D-тио-LNA и α-L-окси-LNA, в частности, все нуклеотидные аналоги LNA, если они присутствуют, представляют собой α-L-окси-LNA.
Как было упомянуто выше, настоящее изобретение, в частности, относится к олигомерному соединению, имеющему длину в 10-30 нуклеиновых оснований, и содержащему домен, связывающийся с мишенью, который специфически гибридизуется с областью от положения основания 1459 (5') до 1476 (3') мРНК человеческого Bcl-2, где указанный связывающийся с мишенью домен имеет формулу:
5'-[(ДНК/РНК)0-1-(LNA/LNA*)2-7-(ДНК/РНК/LNA*)4-14-(LNA/LNA*)2-7-
ДНК/РНК)0-1]-3',
где “LNA” означает нуклеотид LNA, а “LNA*” означает нуклеотидный аналог LNA; и где указанный мишень-связывающий домен содержит, по меньшей мере, два нуклеотида LNA или нуклеотидных аналога LNA, связанных фосфортиоатной группой, (-О-Р(О,S)-О-).
Таким образом, олигомерные соединения имеют длину в 10-30 нуклеиновых оснований, например 10-25, а именно 10-20, например 10-18 или 10-16 нуклеиновых оснований. “Мишень-связывающий домен” этих соединений имеет длину до 18 нуклеиновых оснований/нуклеотидов, поскольку он не может быть больше области, с которой он “специфически гибридизуется”. Однако в этой связи следует отметить, что мишень-связывающий домен необязательно должен иметь длину 18 нуклеиновых оснований, даже если такое олигомерное соединение имеет длину в 18 нуклеиновых оснований или более. Так, например, олигомерное соединение может иметь длину в 20 нуклеиновых оснований, а мишень-связывающий домен может иметь длину 18, 17 или 16 нуклеиновых оснований и т.п. (следует отметить, что любые нуклеотиды олигомерного соединения, которые не являются частью мишень-связывающего домена, могут связываться с любыми нуклеиновых основаниями, смежными со специфической областью мРНК-мишени). Однако желательно, чтобы мишень-связывающий домен представлял собой основную часть олигомерного соединения. Наиболее предпочтительно, чтобы мишень-связывающий домен составлял 90%-100% от длины олигомерного соединения, которая не превышает 18 нуклеотидов, то есть если олигомерное соединение имеет длину до 18 нуклеотидов, то мишень-связывающий домен будет составлять 90%-100% от его длины, а если олигомерное соединение имеет длину до 19 или более нуклеотидов, то длина мишень-связывающего домена будет составлять 16-18 нуклеотидов (то есть 90%-100% от 18 нуклеотидов). Более предпочтительно, чтобы мишень-связывающий домен составлял все олигомерное соединение.
Используемый здесь термин “гибридизация” означает присоединение посредством водородных связей, которыми могут быть водородные связи Уотсона-Крика, связи Хугстена, обратные водородные связи Хугстена и т.п., расположенные между комплементарными нуклеозидами или нуклеиновыми основаниями. Приблизительно пятьдесят лет назад Уотсон и Крик сообщали, что дезоксирибонуклеиновая кислота (ДНК) состоит из двух цепей, которые связаны друг с другом в спиральной конфигурации водородными связями, образованными между противоположными комплементарными основаниями в двух цепях. Четырьмя нуклеиновыми основаниями, обычно присутствующими в ДНК, являются гуанин (G), аденин (А), тимин (Т) и цитозин (С), из которых основание G образует пару с С, а основание А образует пару с Т. В РНК основание тимин заменено основанием урацилом (U), которое, по аналогии с основанием Т, образует пару с А. Химические группы в нуклеиновых основаниях, которые участвуют в образовании стандартного дуплекса, находятся в плоскости Уотсона-Крика. Спустя два года, Хугстен сообщал, что пуриновые нуклеиновые основания (G и А), помимо того, что они находятся в плоскости Уотсона-Крика, имеют также плоскость Хугстена, которая может быть обнаружена с внешней стороны дуплекса и используется для связывания с пиримидиновыми олигонуклеотидами посредством водородных связей, образуя, тем самым, тройную спиральную структуру.
Термин “специфически гибридизуемый” означает, что рассматриваемое олигомерное соединение обладает способностью достаточно сильно и специфически связываться с мРНК-мишенью, в результате чего достигается нужное подавление нормальной функции мРНК-мишени, но, при этом, функция мРНК, не являющаяся мишенью, остается неизменной. Релевантная гибридизация, а следовательно, и подавление данной функции обычно происходит в физиологических условиях, то есть, при температуре примерно 37оС. Однако это не исключает того, что в мишень-связывающем домене не будут присутствовать одно или два ошибочных спаривания. При этом, предпочтительно, чтобы мишень-связывающий домен не имел таких ошибочных спариваний, или имел, по меньшей мере, одно такое ошибочное спаривание (подробное описание см. ниже).
Используемый здесь термин “мРНК-мишень” означает мРНК человеческого Bcl-2, кодирующую человеческий белок Bcl-2.
Используемый здесь термин “модуляция” означает снижение (например, ингибирование) уровня экспрессии человеческого гена Bcl-2 посредством связывания олигомерного соединения с мРНК человеческого Bcl-2, кодирующей белок bcl-2.
“Специфическая гибридизация” достигается путем связывания мишень-связывающего домена со специфической областью мРНК-мишени. При этом следует отметить, что мишень-связывающий домен не должен обязательно связываться с полноразмерной областью мРНК-мишени, состоящей из 18 нуклеиновых оснований, в частности, в том случае, если олигомерное соединение, а следовательно, и мишень-связывающий домен имеет длину менее чем 18 нуклеиновых оснований. Однако, предпочтительно, мишень-связывающий домен связывается с фрагментом, имеющим, по меньшей мере, 10 нуклеиновых оснований, таким как фрагмент, имеющий 10-18 или 10-17, или 10-16, или 10-15, или 10-14 нуклеиновых оснований конкретной области мРНК-мишени.
В общих чертах, предпочтительно, чтобы значительное число нуклеотидных связей (более точно, связей между нуклеозидами, то есть, межнуклеозидных связей) в мишень-связывающем домене представляло собой фосфортиоатные группы (-О-Р(О,S)-О-). Более предпочтительно, чтобы, по меньшей мере, 70%, например, по меньшей мере, 80% или, по меньшей мере, 87% или, по меньшей мере, 93% нуклеотидных связей составляли фосфортиоатные группы (-О-Р(О,S)-О-). В конкретном варианте изобретения все нуклеотидные связи представляют собой фосфортиоатные группы. В частности, все нуклеотидные связи в олигомерном соединении представляют собой фосфортиоатные группы.
Во многих вариантах изобретения, по меньшей мере, 3, например, по меньшей мере, 4, по меньшей мере, 5 или даже, по меньшей мере, 6, по меньшей мере, 7 или по меньшей мере, 8 нуклеиновых оснований в указанном мишень-связывающем домене представляют собой нуклеиновые основания LNA.
В других вариантах изобретения, по меньшей мере, 3, например, по меньшей мере, 4, по меньшей мере, 5 или даже, по меньшей мере, 6, по меньшей мере, 7 или по меньшей мере, 8 нуклеиновых оснований в указанном мишень-связывающем домене представляют собой нуклеиновые основания нуклеотидного аналога LNA.
В предпочтительных вариантах изобретения, в которых рассматриваются многие конкретные последовательности, представленные в таблице 1, 10-50% нуклеиновых оснований в мишень-связывающем домене составляют нуклеиновые основания LNA нуклеотидов.
В некоторых предпочтительных вариантах два 5'-концевых нуклеиновых основания в указанном мишень-связывающем домене представляют собой нуклеиновые основания LNA нуклеотида.
В других предпочтительных вариантах два 5'-концевых нуклеиновых основания в указанном мишень-связывающем домене представляют собой нуклеиновые основания нуклеотида ДНК или РНК, за которыми следуют нуклеиновые основания нуклеотида LNA, в частности нуклеотид ДНК или РНК, за которым следует два нуклеиновых основания LNA.
В других предпочтительных вариантах 3'-концевое нуклеиновое основание в указанном мишень-связывающем домене представляет собой нуклеиновое основание нуклеотида ДНК или РНК.
В одном из этих вариантов два 3'-концевых нуклеиновых основания в указанном мишень-связывающем домене представляют собой нуклеиновые основания нуклеотида ДНК или РНК, за которыми следуют нуклеиновые основания нуклеотида LNA.
В других предпочтительных вариантах изобретения два 3'-концевых нуклеиновых основания в указанном мишень-связывающем домене представляют собой нуклеиновые основания нуклеотидов LNA.
Олигомерные соединения имеют мишень-связывающий домен, содержащий гэпмерную структуру, например структуру LNA/(не-LNA)/LNA-гэпмера. Конкретными вариантами гэпмерной структуры, определенной выше, являются мишень-связывающие домены, имеющие формулы, выбранные из:
5'-[(LNA/LNA*)2-7-(ДНК/РНК/LNA*)4-14-LNA/LNA*2-7]-3';
5'-[(LNA/LNA*)2-7-(ДНК/РНК/LNA*)4-14-LNA/LNA*2-7-(ДНК/РНК)]-3';
5'-[(ДНК/РНК)-(LNA/LNA*)2-7-(ДНК/РНК/LNA*)4-14-LNA/LNA*2-7]-3' и
5'-[(ДНК/РНК)-(LNA/LNA*)2-7-(ДНК/РНК/LNA*)4-14-LNA/LNA*2-7-(ДНК/РНК)]-3'.
Очевидно, что вышеупомянутые гэпмеры четырех типов будут образовывать активные соединения одного и того же типа, а именно гэпмер типа 5'-[(LNA/LNA*)2-7-(ДНК/РНК/LNA*)4-14-LNA/LNA*2-7]-3', после отщепления 5'- или 3'-ДНК-части экзонуклеазами, см. пример 15. Следовательно, поскольку SEQ ID NO:15 представляет собой особенно предпочтительный гэпмер (и дискретное соединение), то из этого следует, что такой же интерес должна представлять SEQ ID NO:29. Аналогичным образом, поскольку SEQ ID NO:8 представляет собой особенно предпочтительный гэпмер (и дискретное соединение), то из этого следует, что такой же интерес должна представлять SEQ ID NO:35.
Конкретным вариантом является соединение, в котором мишень-связывающий домен имеет формулу 5'-[(LNA/LNA*)2-7-(ДНК/РНК/LNA*)4-14-LNA/LNA*2-7-(ДНК/РНК)]-3', такую как 5'-[(LNA/LNA*)2-5-(ДНК/РНК/LNA*)7-12-LNA/LNA*2-5-(ДНК/РНК)]-3', в частности 5'-[(LNA/LNA*)2-4-(ДНК/РНК/LNA*)10-12-LNA/LNA*2-4-(ДНК/РНК)]-3'.
Термин “(LNA/LNA*)” означает, что рассматриваемый сегмент (то есть сегмент, содержащий 2-7 нуклеотидов) может включать нуклеотиды LNA, нуклеотидные аналоги LNA, либо то и другое. Аналогичным образом, сегмент “(ДНК/РНК/LNA*)” может включать дезоксирибонуклеотиды (нуклеотиды ДНК), рибонуклеотиды (нуклеотиды РНК) и нуклеотидные аналоги LNA, а также их комбинации. Сегмент “(ДНК/РНК)” может включать дезоксирибонуклеотиды (нуклеотиды ДНК) и рибонуклеотиды (нуклеотиды РНК) или то и другое.
Очевидно, что субсегмент -(ДНК/РНК/LNA*)4-14- должен обладать способностью к рекрутингу РНКазы Н, а поэтому такой субсегмент должен, предпочтительно, состоять из нуклеотидов ДНК или из нуклеотидных аналогов LNA в форме нуклеотидов α-L-LNA, в частности, из нуклеотидов ДНК. Хотя было определено, что субсегмент имеет длину от 4 до 14 нуклеиновых оснований, однако очевидно, что его длина в пределах от 7 до 12 нуклеиновых оснований, например, от 10 до 12 нуклеиновых оснований, в частности 11 нуклеиновых оснований, позволяет получить особенно ценные гэпмеры, см. таблицу 1.
Таким образом, более конкретным вариантом является вариант, в котором мишень-связывающий домен имеет формулу 5'-[(LNA/LNA*)2-7-(ДНК/α-L-LNA)5-14-LNA/LNA*2-7-(ДНК/РНК)]-3', такую как 5'-[(LNA/LNA*)2-5-(ДНК/α-L-LNA)7-12-LNA/LNA*2-5-(ДНК/РНК)]-3', в частности 5'-[(LNA/LNA*)2-4-(ДНК/α-L-LNA)10-12-LNA/LNA*2-4-(ДНК/РНК)]-3'.
Особый интерес также представляет вариант, в котором мишень-связывающий домен имеет формулу 5'-[LNA2-7-(ДНК)4-14-LNA2-7-(ДНК/РНК)]-3', такую как 5'-[LNA2-5-(ДНК)7-12-LNA2-5-(ДНК/РНК)]-3', в частности 5'-[LNA2-4-(ДНК)10-12-LNA2-4-(ДНК/РНК)]-3'. Еще больший интерес представляет вариант, в котором мишень-связывающий домен имеет формулу 5'-[LNA2-7-(ДНК)5-14-LNA2-7-(РНК)]-3', или 5'-[LNA2-7-(ДНК)5-14-LNA2-7-(ДНК)]-3', или 5'-[LNA2-7-(ДНК/α-L-LNA)5-14-LNA2-7-(РНК)]-3', или 5'-[LNA2-7-(ДНК/α-L-LNA)5-14-LNA2-7-(ДНК)]-3', такую как 5'-[LNA2-5-(ДНК)7-12-
LNA2-5-(РНК)]-3', или 5'-[LNA2-5-(ДНК)7-12-LNA2-5-(ДНК)]-3', или 5'-[LNA2-5-(ДНК/α-L-LNA)7-12-LNA2-5-(РНК)]-3', или 5'-[LNA2-5-(ДНК/α-L-LNA)7-12-LNA2-5-(ДНК)]-3', в частности 5'-[LNA2-4-(ДНК)10-12-LNA2-4-(РНК)]-3', или 5'-[LNA2-4-(ДНК)10-12-LNA2-4-(ДНК)]-3', или 5'-[LNA2-4-(ДНК/α-L-LNA)10-12-LNA2-4-(РНК)]-3' или 5'-[LNA2-4-(ДНК/α-L-LNA)10-12-LNA2-4-(ДНК)]-3'.
В другом варианте изобретения мишень-связывающий домен имеет формулу 5'-[(ДНК/РНК)-(LNA/LNA*)2-7-(ДНК/РНК/LNA*)4-14-LNA/LNA*2-7-(ДНК/РНК)]-3', в частности формулу 5'-[(ДНК/РНК)-LNA2-7-(ДНК)4-14-(LNA)2-7-(ДНК/РНК)]-3', например 5'-[(ДНК/РНК)-(LNA/LNA*)2-5-(ДНК/РНК/LNA*)7-12-LNA/LNA*2-5-(ДНК/РНК)]-3', в частност, формулу 5'-[(ДНК/РНК)-LNA2-5-(ДНК)7-12-LNA2-5-(ДНК/РНК)]-3', или 5'-[(ДНК/РНК)-(LNA/LNA*)2-4-(ДНК/РНК/LNA*)10-12-(LNA/LNA*)2-4-(ДНК/РНК)]-3', в частности формулу 5'-[(ДНК/РНК)-LNA2-4-(ДНК)10-12-LNA2-4-(ДНК/РНК)]-3'. Еще одним вариантом, представляющим особый интерес, является вариант, в котором мишень-связывающий домен имеет формулу
5'-[(ДНК)-LNA2-7-(ДНК)5-14-LNA2-7-(РНК)]-3', или 5'-[(ДНК)-LNA2-7-(ДНК)5-14-
LNA2-7-(ДНК)]-3', или 5'-[(ДНК)-LNA2-7-(ДНК/α-L-LNA)5-14-LNA2-7-(ДНК)]-3',
или 5'-[(ДНК)-LNA2-7-(ДНК/α-L-LNA)5-14-LNA2-7-(ДНК)]-3', или 5'-[(РНК)-LNA2-7-
(ДНК)5-14-LNA2-7-(РНК)]-3', или 5'-[(РНК)-LNA2-7-(ДНК)5-14-LNA2-7-(ДНК)]-3',
или 5'-[(РНК)-LNA2-7-(ДНК/α-L-LNA)5-14-LNA2-7-(РНК)]-3', или 5'-[(РНК)-LNA2-7-(ДНК/α-L-
LNA)5-14-LNA2-7-(ДНК)]-3', такую как 5'-[(ДНК)-LNA2-5-(ДНК)7-12-LNA2-5-(РНК)]-3',
или 5'-[(ДНК)-LNA2-5-(ДНК)7-12-LNA2-5-(ДНК)]-3', или 5'-[(ДНК)-LNA2-5-(ДНК/α-L-
LNA)7-12-LNA2-5-(РНК)]-3', или 5'-[(ДНК)-LNA2-5-(ДНК/α-L-LNA)7-12-LNA2-5-(ДНК)]-3',
или 5'-[(РНК)-LNA2-5-(ДНК)7-12-LNA2-5-(РНК)]-3',
или 5'-[(РНК)-LNA2-5-(ДНК)7-12-LNA2-5-(ДНК)]-3', или 5'-[(РНК)-LNA2-5-(ДНК/α-L-
LNA)7-12-LNA2-5-(РНК)]-3', или 5'-[(РНК)-LNA2-5-(ДНК/α-L-LNA)7-12-LNA2-5-(ДНК)]-3',
в частности 5'-[(ДНК)-LNA2-4-(ДНК)10-12-LNA2-4-(РНК)]-3',
или 5'-[(ДНК)-LNA2-4-(ДНК)10-12-LNA2-4-(ДНК)]-3', или 5'-[(ДНК)-LNA2-4-(ДНК/α-L-
LNA)10-12-LNA2-4-(РНК)]-3', или 5'-[(ДНК)-LNA2-4-(ДНК/α-L-LNA)10-12-LNA2-4-(
ДНК)]-3', или 5'-[(РНК)-LNA2-4-(ДНК)10-12-LNA2-4-(РНК)]-3', или 5'-[(РНК)-LNA2-4-(ДНК)10-12-LNA2-4-(ДНК)]-3', или
5'-[(РНК)-LNA2-4-(ДНК/α-L-LNA)10-12-LNA2-4-(РНК)]-3', или
5'-[(РНК)-LNA2-4-(ДНК/α-L-LNA)10-12-LNA2-4-(ДНК)]-3'.
В другом варианте изобретения мишень-связывающий домен имеет формулу 5'-[(ДНК/РНК)-(LNA/LNA*)2-7-(ДНК/РНК/LNA*)4-14-LNA/LNA*2-7]-3', в частности формулу 5'-[(ДНК/РНК)-LNA2-7-(ДНК)4-14-LNA2-7]-3', такую как 5'-[(ДНК/РНК)-(LNA/LNA*)2-5-(ДНК/РНК/LNA*)7-12-LNA/LNA*2-5]-3', в частности формулу 5'-[(ДНК/РНК)-LNA2-5-(ДНК)7-12-LNA2-5]-3' или 5'-[(ДНК/РНК)-(LNA/LNA*)2-4-(ДНК/РНК/LNA*)10-12-LNA/LNA*2-4]-3', в частности формулу 5'-[(ДНК/РНК)-LNA2-4-(ДНК)10-12-LNA2-4]-3'. Еще одним вариантом, представляющим особый интерес, является вариант, в котором мишень-связывающий домен имеет формулу 5'-[(ДНК)-LNA2-7-(ДНК)5-14-LNA2-7]-3', или
5'-[(ДНК)-LNA2-7-(ДНК/α-L-LNA)5-14-LNA2-7]-3', или 5'-[(РНК)-LNA2-7-(ДНК)5-14-LNA2-7]-
3', или 5'-[(РНК)-LNA2-7-(ДНК/α-L-LNA)5-14-LNA2-7]-3', например, такую
как 5'-[(ДНК)-LNA2-5-(ДНК)7-12-LNA2-5]-3', или
5'-[(ДНК)-LNA2-5-(ДНК/α-L-LNA)7-12-LNA2-5]-3', или 5'-[(РНК)-LNA2-5-(ДНК)7-12-
LNA2-5]-3', или 5'-[(РНК)-LNA2-5-(ДНК/α-L-LNA)7-12-LNA2-5]-3', в частности
5'-[(ДНК)-LNA2-4-(ДНК)10-12-LNA2-4-(РНК)]-3', или
5'-[(ДНК)-LNA2-4-(ДНК/α-L-LNA)10-12-LNA2-4]-3', или
5'-[(РНК)-LNA2-4-(ДНК)10-12-LNA2-4]-3', или
5'-[(РНК)-LNA2-4-(ДНК/α-L-LNA)10-12-LNA2-4]-3'.
В еще одном варианте изобретения мишень-связывающий домен имеет формулу 5'-[(LNA/LNA*)2-7-(ДНК/РНК/LNA*)4-14-LNA/LNA*2-7]-3', в частности формулу
5'-[LNA2-7-(ДНК)4-14-(LNA)2-7]-3', такую как
5'-[(LNA/LNA*)2-5-(ДНК/РНК/LNA*)7-12-(LNA/LNA*)2-5]-3',
в частности формулу 5'-[LNA2-5-(ДНК)7-12-LNA2-5]-3', или
5'-[(LNA/LNA*)2-4-(ДНК/РНК/LNA*)10-12-LNA/LNA*2-4]-3',
в частности формулу 5'-[LNA2-4-(ДНК)10-12-LNA2-4]-3'. Еще одним вариантом, представляющим особый интерес, является вариант, в котором мишень-связывающий домен имеет формулу
5'-[LNA2-7-(ДНК)5-14-LNA2-7)]-3', или 5'-[LNA2-7-(ДНК/α-L-LNA)5-14-LNA2-7]-3',
такую как 5'-[LNA2-5-(ДНК)7-12-LNA2-5]-3' или
5'-[LNA2-5-(ДНК/α-L-LNA)7-12-LNA2-5]-3', в частности
5'-[LNA2-4-(ДНК)10-12-LNA2-4]-3', или
5'-[LNA2-4-(ДНК/α-L-LNA)10-12-LNA2-4]-3'.
В некоторых вариантах изобретения олигомерные соединения также содержат нуклеотидные аналоги LNA (обозначаемые здесь “LNA*”). В частности, 10-100% или 0-90%, например, 10-50% нуклеиновых оснований в мишень-связывающем домене представляют собой нуклеиновые основания нуклеотидных аналогов LNA (LNA*).
В одном из вариантов, указанный мишень-связывающий домен имеет формулу
5'-[(LNA*)2-7-(ДНК/РНК/LNA*)4-14-LNA*2-7-(ДНК/РНК)]-3', в частности
5'-[LNA*2-7-(ДНК)4-14-LNA*2-7-(ДНК/РНК)]-3', такую как
5'-[(LNA*)2-5-(ДНК/РНК/LNA*)7-12-LNA*2-5-(ДНК/РНК)]-3', в частности,
5'-[LNA*2-5-(ДНК)7-12-LNA*2-5-(ДНК/РНК)]-3', или
5'-[(LNA*)2-4-(ДНК/РНК/LNA*)10-12-LNA*2-4-(ДНК/РНК)]-3', в частности,
5'-[LNA*2-4-(ДНК)10-12-LNA*2-4-(ДНК/РНК)]-3'.
Как упомянуто выше, олигомерное соединение должно специфически гибридизоваться с конкретной областью мРНК-мишени. Более конкретно, мишень-связывающий домен является комплементарным части области от положения основания 1459 (5') до 1476 (3') мРНК человеческого Bcl-2, с которой он специфически гибридизуется, возможно, за исключением 1-2 не-комплементарных оснований.
В контексте настоящего изобретения, термин “комплементарный” относится к способности точного спаривания между нуклеотидами релевантной области мРНК-мишени и нуклеотидами мишень-связывающих доменов. Так, например, если нуклеотид в определенном положении мРНК-мишени способен образовывать водородные связи с нуклеотидом мишень-связывающего домена, то считается, что указанные мРНК-мишень и мишень-связывающий домен комплементарны друг другу в данном положении. (И снова следует отметить, что исходя из вышесказанного, мишень-связывающим доменом является домен, соответствующий конкретной области мРНК человеческого Bcl-2 или его более короткому фрагменту). Само собой разумеется, что термин “некомплементарные нуклеиновые основания” означает основание конкретного нуклеотида, не являющееся “комплементарным”.
В одном из вариантов изобретения мишень-связывающий домен является комплементарным части области от положения основания 1459 (5') до 1476 (3') мРНК человеческого Bcl-2, с которой он специфически гибридизуется.
В этом варианте изобретения, примерами предпочтительных соединений являются соединения, которые включают мишень-связывающий домен, выбранный из группы, состоящей из SEQ ID NO: 1, 2, 3, 4, 5, 6, 7, 8 (и 35), 12, 13, 14, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51 и 52, в частности, SEQ ID NO:8 (и 35). В одном из вариантов указанным мишень-связывающим доменом является SEQ ID NO:8. В другом варианте изобретения указанным мишень-связывающим доменом является SEQ ID NO:35.
Более предпочтительными соединениями являются соединения, выбранные из группы, состоящей из SEQ ID NO: 1, 2, 3, 4, 5, 6, 7, 8 (и 35), 12, 13, 14, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51 и 52, в частности SEQ ID NO:8 (и 35). В одном из вариантов указанным соединением является SEQ ID NO:8. В другом варианте изобретения указанным соединением является SEQ ID NO:35.
В другом варианте изобретения мишень-связывающий домен является комплементарным части области от положения основания 1459 (5') до 1476 (3') мРНК человеческого Bcl-2, с которой он специфически гибридизуется, за исключением 1-2 некомплементарных нуклеиновых оснований, в частности за исключением 1 некомплементарного нуклеинового основания. Так, например, допускается присутствие 1-2 ошибочных спариваний (некомплементарных нуклеиновых оснований), однако в большинстве случаев вводится только одно ошибочное спаривание. Такие ошибочные спаривания чаще всего присутствуют в сегментах ДНК/РНК/LNA* олигомерного соединения, например в сегменте ДНК/РНК/LNA* соединения, имеющего мишень-связывающий домен, содержащий сегмент формулы
5'-[(LNA/LNA*)2-7-(ДНК/РНК/LNA*)4-14-LNA/LNA*2-7-(ДНК/РНК)]-3'.
В одном из вариантов изобретения мишень-связывающий домен содержит подпоследовательность GCGXGCGC, где Х не является Т (тимином). В частности, Х представляет собой С (цитозин), или Х представляет собой А (аденин), или Х представляет собой G (гуанин).
В другом варианте изобретения мишень-связывающий домен содержит подпоследовательность СССАXCGТ, где Х не является G (гуанином). В частности, Х представляет собой А (аденин), или Х представляет собой Т (тимин), или Х представляет собой С (цитозин).
В еще одном варианте изобретения мишень-связывающий домен содержит подпоследовательность САGXGТG, где Х не является С (цитозином). В частности, Х представляет собой А (аденин), или Х представляет собой Т (тимин), или Х представляет собой G (гуанин).
В другом варианте изобретения мишень-связывающий домен содержит подпоследовательность АGCXТGC, где Х не является G (гуанином). В частности, Х представляет собой А (аденин), или Х представляет собой Т (тимин), или Х представляет собой С (цитозин).
Примерами предпочтительных соединений этого варианта являются соединения, которые включают мишень-связывающий домен, выбранный из группы, состоящей из SEQ ID NO:15 (и 29), 17, 18, 19, 21, 22, 23, 24, 25, 26, 27, 28, 53, 54 и 55, в частности SEQ ID NO:15 (и 29). В одном из вариантов, указанным мишень-связывающим доменом является SEQ ID NO:15. В другом варианте изобретения, указанным мишень-связывающим доменом является SEQ ID NO:29.
Более предпочтительными соединениями являются соединения, выбранные из группы, состоящей из SEQ ID NO: 15 (и 29), 17, 18, 19, 21, 22, 23, 24, 25, 26, 27, 28, 53, 54 и 55, в частности SEQ ID NO:15 (и 29). В одном из вариантов указанным соединением является SEQ ID NO:15. В другом варианте изобретения указанным соединением является SEQ ID NO:29.
Следует отметить, что в соответствии с вышесказанным очевидно, что каждое из олигомерных соединений SEQ ID NO:8 (а также 35) и олигомерных соединений SEQ ID NO:15 (а также 29) имеет значительные преимущества по сравнению с соединением облимерсен-натрия (SEQ ID NO:56; эталон) в отношении желательных биологических эффектов, см. примеры.
Авторами настоящего изобретения, inter alia, было проиллюстрировано in vivo значительное снижение массы опухоли у крыс SCID с моделью ксенотрансплатата меланомы 518А2 при введении внутрибрюшинно 7 мг/кг соединения SEQ ID NO:8 в течение 14 дней по сравнению с такой же дозой соединения SEQ ID NO:56 (эталон), см. фиг.11. Соединение SEQ ID NO: 8 обладает такой же противоопухолевой активностью, как и соединение SEQ ID NO:56 (эталон), но при его введении в 7 раз меньшей дозе.
На фиг.13 показаны уровни соединения SEQ ID NO:15 в печени и в почках крыс NМRI после введения внутривенно одной дозы (25 мг/кг) этого соединения. Было обнаружено, что время полужизни (Т1/2) активного соединения SEQ ID NO:15 в печени и в почках составляет приблизительно 3 дня. Это означает, что такая схема введения оптимальных биологических доз SEQ ID NO:15 может проводиться с меньшей частотой, чем непрерывное вливание и ежедневно вводимая доза.
Авторами настоящего изобретения было также продемонстрировано эффективное in vivo снижение объема опухоли с использованием соединения SEQ ID NO:15, ежедневно вводимого в предстательную железу бестимусной “голой” мыши с моделью ксенотрансплатата РС3 в дни 7-15 или в дни 8, 11, 13, 15, 18, 20, по сравнению с физиологическим раствором (контролем), см. фигуру 7D. Эти соединения вводили внутрибрюшинно в дозе 10 мг/кг в течение 14 дней. Мониторинг роста опухоли проводили еще 8 дней после обработки.
Следует отметить, что олигомерные соединения согласно изобретению имеют подходящий in vivo профиль распределения и ингибирования Bcl-2, а поэтому являются терапевтически эффективными для лечения различных Bcl-2-ассоциированных состояний, в частности рака.
Получение олигомерных соединений
Олигомерные соединения согласно изобретению могут быть получены как описано в примерах 1 и 2 и в WO 99/14226, WO 00/56746, WO 00/56748, WO 00/66604, WO 00/125248, WO 02/28875, WO 2002/094250 и РСТ/DK02/00488, а также в публикациях Herdewijn P., Oligonucleotide Synthesis, Methods and Applications, pp. 127-145, Humana Press, Totowa, New Jersey, 2005. Таким образом, олигомерные соединения согласно изобретению могут быть получены методами полимеризации, применяемыми в химии нуклеиновых кислот и хорошо известными среднему специалисту в области органической химии. Обычно используется фосфорамидитный метод со стандартными циклами олигомеризации (S.L. Beaucage & R.P. Iyer, Tetrahedron, 1993, 49, 6123; S.L. Beaucage and R.P. Iyer, Tetrahedron, 1992, 48, 2223), но могут также применяться методы Н-фосфонатной химии и фосфотриэфирной химии.
Для получения некоторых мономеров согласно изобретению требуется более длительное время реакции сочетания, и/или проведение повторных реакций сочетания со свежими реагентами, и/или использование реагентов сочетания в высокой концентрации.
Фосфорамидиты, используемые в постадийных реакциях сочетания, дают удовлетворительный выход >95%. Тиолирование фосфата проводят путем замены нормального окислителя, например смеси иод/пиридин/H2O, используемой для синтеза фосфордиэфирных олигомеров, таким окислителем, как реагент АDТТ (гидрид ксантана (0,01М в смеси ацетонитрил:пиридин, 9:1, об/об)), при этом, могут быть также использованы и другие реагенты тиолирования, такие как реагент Бокажа. Фосфортиоатные олигомеры LNA были эффективно синтезированы посредством постадийных реакций сочетания с выходом ≥ 98%.
β-D-амино-LNA-, β-D-тио-LNA-олигонуклеотиды, α-L-LNA и β-D-метиламино-LNA-олигонуклеотиды были также эффективно синтезированы фосфорамидитными методами посредством постадийных реакций сочетания с выходом ≥ 98%.
Очистку олигомерных соединений LNA проводили на обращенно-фазовой колонке со сменными патронами и/или с помощью обращенно-фазовой ВЭЖХ и/или путем преципитации из этанола или бутанола. Для подтверждения очистки синтезированных олигонуклеотидов проводили электрофорез в капиллярном геле, обращенно-фазовую ВЭЖХ, MALDI-MS и ESI-MS. Кроме того, представляющими особый интерес материалами для синтеза LNA-содержащих олигомерных соединений, в которых нуклеотид LNA присутствует у 3'-конца, являются твердые носители, на которых иммобилизованы необязательно защищенные нуклеиновые основания и, необязательно, LNA с защищенной 5'-ОН. В этом случае твердый носитель, предпочтительно, представляет собой СРG (стекло с регулируемым размером пор), например готовый материал (коммерчески доступный) из СРG или полистирола, который имеет 3'-функционализированное, необязательно защищенное нуклеиновое основание и необязательно 5'-ОН-защищенное основание LNA, связанные с этим материалом в условиях, рекомендованных поставщиком данного конкретного материала.
Соли
Олигомерное соединение согласно изобретению может быть использовано в виде различных фармацевтически приемлемых солей. Используемый здесь термин “соли” означает соли, которые сохраняют нужную биологическую активность идентифицированных здесь соединений и обладают минимальным нежелательным токсическим действием. Неограничивающими примерами таких солей являются соли, которые могут быть образованы органической аминокислотой, и основно-аддитивные соли, которые могут быть образованы катионами металлов, такими как цинк, кальций, висмут, барий, магний, алюминий, медь, кобальт, никель, кадмий, натрий, калий и т.п., или катионом аммиака, N,N-дибензилэтилендиамина, D-глюкозамина, тетраэтиламмония или этилендиамина; или (с) соли, образованные комбинациями (а) и (b), например таннат цинка или т.п.
Такие соли образуются, например, из соединений согласно изобретению, которые имеют кислотную группу, например карбоксильную группу, фосфодиэфирную группу или фосфортиоатную группу, и такими солями являются, например, соли подходящих оснований. Такими солями являются, например, соли нетоксичных металлов, которые образуются из металлов групп Iа, Ib, IIа и IIb Периодической системы элементов, в частности соли подходящих щелочных металлов, например, соли лития, натрия или калия, или соли щелочноземельных металлов, например соли магния или кальция. Такими солями являются, кроме того, соли цинка и аммония, а также соли, образованные подходящими органическими аминами, такими как незамещенные или гидрокси-замещенные моно-, ди- или триалкиламины, в частности моно-, ди- или триалкиламины, или соли, образованные четвертичными аммониевыми соединениями, например N-метил-N-этиламином, диэтиламином, триэтиламином, моно-, бис- или трис-(2-гидрокси-низший алкил)аминами, такими как моно-, бис- или трис-(2-гидроксиэтил)амин, 2-гидрокси-трет-бутиламин или трис(гидроксиметил)метиламин, N,N-ди-низший алкил-N-(гидрокси-низший алкил)амины, такие как N,N-диметил-N-(2-гидроксиэтил)амин или три-(2-гидроксиэтил)амин, или N-метил-D-глюкамин, или четвертичными аммониевыми соединениями, такие как соли тетрабутиламмония. Предпочтительными являются соли лития, натрия, магния, цинка или калия, а особенно предпочтительными являются соли натрия.
Соединения согласно изобретению, имеющие основную группу, например аминогруппу или иминогруппу, могут образовывать кислотно-аддитивные соли, например, соли, образованные неорганическими кислотами, например галогенводородной кислотой, такой как соляная кислота, серная кислота или фосфорная кислота, или органическими карбоновыми кислотами, сульфоновыми кислотами, сульфокислотами или фосфокислотами или N-замещенной сульфаминовой кислотой, например уксусной кислотой, пропионовой кислотой, гликолевой кислотой, янтарной кислотой, малеиновой кислотой, гидроксималеиновой кислотой, метилмалеиновой кислотой, фумаровой кислотой, яблочной кислотой, винной кислотой, глюконовой кислотой, глукаровой кислотой, глюкуроновой кислотой, лимонной кислотой, бензойной кислотой, коричной кислотой, миндальной кислотой, салициловой кислотой, 4-аминосалициловой кислотой, 2-феноксибензойной кислотой, 2-ацетоксибензойной кислотой, эмбоновой кислотой, никотиновой кислотой или изоникотиновой кислотой, и, кроме того, аминокислотами, например α-аминокислотой, а также метансульфоновой кислотой, этансульфоновой кислотой, 2-гидроксиметансульфоновой кислотой, этан-1,2-дисульфоновой кислотой, бензолдисульфоновой кислотой, 4-метилбензолсульфоновой кислотой, нафталинсульфоновой кислотой, 2- или 3-фосфоглицератом, фосфатом глюкозы или N-циклогексилсульфаминовой кислотой (с образованием цикламатов) или другими кислотными органическими соединениями, такими как аскорбиновая кислота.
Соединения согласно изобретению, которые имеют кислотные и основные группы, могут также образовывать внутренние соли. Фармацевтически неприемлемые соли, например пикраты или перхлораты, могут быть использованы для выделения и очистки.
Для терапевтических целей применяются только фармацевтически приемлемые соли, которые являются нетоксичными при их “корректном” использовании, а поэтому эти соли являются предпочтительными.
Конъюгаты
В другом своем аспекте, настоящее изобретение относится к конъюгату, содержащему определенное здесь соединение, имеющее, по меньшей мере, одну не-нуклеотидную или не-полинуклеотидную молекулу, ковалентно связанную с указанным соединением.
В контексте настоящего изобретения термин “конъюгат” означает гетерогенную молекулу, образованную посредством ковалентного связывания описанного здесь олигомерного соединения (т.е., соединения, содержащего последовательность нуклеозидов или нуклеозидных аналогов) с одной или несколькими не-нуклеотидными или не-полинуклеотидными молекулами.
Таким образом, олигомерные соединения могут быть, например, конъюгированы или они могут образовывать химеры с не-нуклеотидными или с не-полинуклеотидными молекулами, включая связанные с пептидом нуклеиновые кислоты (PNA), белки (например, антитела против белка-мишени), макромолекулы, низкомолекулярные лекарственные средства, цепи жирных кислот, сахарные остатки, гликопротеины, полимеры (например, полиэтиленгликоль), группы, образующие мицеллы, антитела, углеводы, связывающиеся с рецептором белки, стероиды, такие как холестерин, полипептиды, интеркалирующие агенты, такие как производное акридина, длинноцепочечный спирт, дендример, фосфолипид и другие липофильные группы или их комбинации и т.п., а также указанные олигомерные соединения могут иметь упорядоченную димерную или дендритную структуры. Соединения или конъюгаты согласно изобретению могут быть также конъюгированы или дополнительно конъюгированы с активными лекарственными средствами, например с аспирином, ибупрофеном, сульфасодержащим лекарственным средством, средством против диабета, антибактериальным средством, химиотерапевтическим соединением или антибиотиком.
Такое конъюгирование обладает тем преимуществом, что оно сообщает олигомерным соединениям согласно изобретению нужные фармакокинетические свойства. В частности, конъюгирование, проводимое таким методом, приводит к усилению поглощения лекарственного средства клетками.
В одном из вариантов изобретения олигомерное соединение согласно изобретению присоединяют к лигандам так, чтобы образовывался конъюгат, где указанные лиганды способствуют усилению поглощения указанного конъюгата клетками по сравнению с антисмысловыми олигонуклеотидами. Такое конъюгирование может происходить в концевых положениях 5'/3'-ОН, и лиганды могут также присоединяться у сахаров и/или у оснований. Примерами конъюгатов/лигандов являются молекулы холестерина (Soutschek et al., Nature, 432, 173-178 (2004)), дуплексные интеркаляторы, такие как акридин, поли-L-лизин, “кэппированные по концам” одной или несколькими нуклеазо-резистентными линкерными группами, такими как фосформонотиоат, трансфериновые комплексы (Wagner et al., Proc. Natl. Acad. Sci., USA, 87, 3410-3414 (1990)), производные фолата (Low et al., патент США № 5108921. См. также Leamon et al., Proc. Natl. Acad. Sci. 88, 5572 (1991)) и т.п.
Пролекарства
В некоторых вариантах изобретения олигомерное соединение может присутствовать в форме пролекарства. Олигонуклеотиды являются, по существу, отрицательно заряженными ионами. Благодаря липофильной природе клеточных мембран уровень поглощения олигонуклеотидов клетками ниже, чем уровень поглощения нейтральных или липофильных эквивалентов. Такая проблема, связанная с полярностью, может быть решена методом с использованием пролекарства (см. например, Crooke R.M. (1998) in Crooke S.T., Antisense Research & Application. Springer-Verlag, Berlin, Germany, vol. 131, pp.103-140). В этом методе олигомерные соединения получают в защищенной форме, так, чтобы они были нейтральными при их введении. Эти защитные группы получают так, чтобы они могли быть затем удалены в случае поглощения этих олигомерных соединений клетками. Примерами таких защитных групп являются S-ацетилтиоэтил (SАТЕ) или S-пивалоилтиоэтил (трет-бутил-SАТЕ). Эти защитные группы являются нуклеазо-резистентными и подвергаются внутриклеточному селективному удалению.
Терапевтический метод
Специалистам известно, что LNA-олигомерные соединения согласно изобретению могут быть использованы для лечения Bcl-2-ассоциированных заболеваний многими различными методами, которые входят в объем настоящего изобретения.
Так, например, олигомерные соединения LNA могут быть сконструированы как антисмысловые ингибиторы, которые представляют собой одноцепочечные нуклеиновые кислоты и которые предупреждают развитие заболевания, вызываемого белком, путем их введения на уровне мРНК. Кроме того, они могут быть сконструированы в качестве олигонуклеотидов-иммумодуляторов (IMO), рибозимов или олигозимов, представляющих собой антисмысловые олигонуклеотиды, которые, помимо мишень-связывающего(их) домена(ов), содержат каталитическую активность, которая разрушает мРНК-мишень (рибозимы), или содержат внешнюю вспомогательную последовательность (ЕGS), способствующую рекрутингу эндогенного фермента (РНКазы Р), который разрушает мРНК-мишень (олигозимы).
Аналогичным образом олигомерные соединения LNA могут быть сконструированы в виде оцРНК, которые представляют собой небольшие двухцепочечные молекулы РНК, используемые клетками для создания молчащих специфических эндогенных или экзогенных генов посредством еще очень плохо изученного механизма, напоминающего действие антисмысловых последовательностей.
Олигомерные соединения могут быть также сконструированы в виде аптамеров (и их вариантов, называемых оптическими изомерами), представляющих собой нуклеиновые кислоты, которые благодаря своим внутримолекулярным водородным связям образуют трехмерные структуры, позволяющие этим нуклеиновым кислотам связываться с биологическими мишенями с высокой аффинностью и специфичностью и блокировать такие мишени. Кроме того, олигомерные соединения LNA могут быть сконструированы в виде “ловушек”, которые представляют собой небольшие двухцепочечные нуклеиновые кислоты, способствующие предотвращению трансактивации генов-мишеней клеточными факторами транскрипции путем селективного блокирования их ДНК-связывающего сайта.
Кроме того, олигомерные соединения LNA могут быть также сконструированы в виде химерапластов, которые представляют собой небольшие одноцепочечные нуклеиновые кислоты, способные специфически спариваться с последовательностью гена-мишени и модифицировать эту последовательность. Поэтому LNA-содержащие олигомерные соединения, вводимые таким методом, могут быть, в частности, использованы для лечения Bcl-2-ассоциированных заболеваний, вызываемых мутацией гена Bcl-2.
И наконец, олигомерные соединения LNA могут быть сконструированы в виде ТFO (триплекс-образующих олигонуклеотидов), которые представляют собой нуклеиновые кислоты, связывающиеся с двухцепочечной ДНК и предотвращающие продуцирование белков, вызывающих данное заболевание, на уровне транскрипции РНК.
В соответствии с вышеописанными методами, благодаря которым олигомерное соединение LNA приобретает терапевтическую активность, мишенью согласно изобретению является мРНК Bcl-2.
Олигомерное соединение LNA соединения гибридизуется с частью мРНК человеческого Bcl-2, которая содержит сайт инициации трансляции, то есть область от положения основания 1459 (5') до 1476 (3') мРНК человеческой мРНК, кодирующей белок Bcl-2.
Для специалистов в данной области очевидно, что предпочтительными олигомерными соединениями LNA являются соединения, гибридизующиеся с частью мРНК Bcl-2, последовательность которой обычно отсутствует в транскриптах неродственных генов, в результате чего обеспечивается специфичность лечения.
Олигомерные соединения согласно изобретению конструируют так, чтобы они были в достаточной степени комплементарны данной мишени и обладали нужным клиническим ответом, например, такое олигомерное соединение должно связываться с его мишенью с активностью и специфичностью, достаточными для достижения нужного эффекта. В одном из вариантов изобретения указанное олигомерное соединение LNA конструируют так, чтобы оно также модулировало другие специфические нуклеиновые кислоты, которые не кодируют человеческий белок Bcl-2.
При этом, предпочтительно, чтобы олигомерные соединения согласно изобретению были сконструированы так, чтобы можно было избежать внутри- и межмолекулярной гибридизации олигонуклеотидов.
Антисмысловые лекарственные средства
В одном из вариантов изобретения олигомерные соединения LNA получают в виде подходящих антисмысловых лекарственных средств. Для создания эффективного и безопасного антисмыслового лекарственного средства требуется тонкая корректировка различных параметров, таких как активность/эффективноть, аффинность/специфичность, стабильность в биологических жидкостях, поглощение клетками, механизм действия, фармакокинетические свойства и токсичность.
Аффинность и специфичность: LNA с оксиметиленовой 2'-О,4'-С-связью (β-D-окси-LNA) обладает беспрецедентной способностью связываться с последовательностями ДНК- и РНК-мишеней. Аналогичным образом, производные LNA, такие как амино-, тио- и α-L-окси-LNA, обнаруживают беспрецедентную способность к аффинному связыванию с комплементарной РНК и ДНК, а в случае тио-LNA его аффинность связывания с РНК даже превышает аффинность связывания β-D-окси-LNA.
Помимо своих замечательных гибридизационных свойств нуклеотиды LNA, будучи смешанными, могут действовать в кооперации с нуклеотидами ДНК и РНК, а также с другими аналогами нуклеиновых кислот, такими как 2'-О-алкил-модифицированные мономеры РНК. Олигонуклеотиды согласно изобретению, сами по себе, могут полностью состоять из нуклеотидов β-D-окси-LNA, либо они могут состоять из β-D-окси-LNA в любой комбинации с нуклеотидами ДНК, РНК или с современными аналогами нуклеиновых кислот, которые включают такие производные LNA, как, например, амино-LNA, тио-LNA и α-L-окси-LNA. Исключительно высокая аффинность связывания LNA с последовательностями ДНК- или РНК-мишеней и его способность свободно смешиваться с ДНК, РНК и с различными современными аналогами нуклеиновых кислот в соответствии с настоящим изобретением имеет важное значение для разработки эффективных и безопасных антисмысловых соединений. Кроме того, олигонуклеотиды, содержащие LNA, обладают превосходной растворимостью в воде.
Во-первых, в одном из вариантов изобретения предусматривается значительное укорочение обычной длины антисмысловых олигонуклеотидов (от 20-25-меров, например до 12-16-меров) без снижения аффинности, требуемой для осуществления фармакологической активности. Поскольку внутренняя специфичность олигонуклеотида обратно пропорциональна его длине, то такое укорочение будет приводить к значительному увеличению специфичности антисмыслового соединения к его РНК-мишени. Благодаря тому, что последовательность человеческого генома является доступной и информация о его генах быстро накапливается, один из вариантов изобретения относится к идентификации самых коротких, возможно даже уникальных последовательностей в мРНК-мишени.
В другом варианте изобретения использование LNA для снижения размера антисмысловых олигонуклеотидов позволяет значительно сократить время и стоимость их получения, что дает основу для разработки коммерчески конкурентной антисмысловой терапии для лечения различных заболеваний.
В другом варианте изобретения исключительно высокая аффинность LNA может быть использована для значительного усиления способности олигомерного соединения гибридизоваться с его мРНК-мишенью in vivo, что позволяет значительно сократить время и усилия, необходимые для идентификации активного соединения, по сравнению с теми случаями, когда используются химические соединения.
В другом варианте изобретения, исключительно высокая аффинность LNA может быть использована для повышения эффективности антисмысловых олигонуклеотидов, что позволит получить соединения с более благоприятными “терапевтическими окнами”, чем соединения, используемые в настоящее время в клинических испытаниях.
Олигонуклеотиды согласно изобретению, если они сконструированы в виде антисмысловых ингибиторов, специфически и селективно связываются с нуклеиновой кислотой-мишенью и модулируют экспрессию ее когнатного белка. Такая модуляция, предпочтительно, приводит, по меньшей мере, к 10%- или 20%-ному, более предпочтительно, по меньшей мере, 30%-, 40%-, 50%-, 60%-, 70%-, 80%- или 90%-ному ингибированию экспрессии по сравнению с нормальным уровнем экспрессии.
Стабильность в биологических жидкостях. Один из вариантов изобретения включает введение нуклеотидов LNA в стандартный ДНК- или РНК-олигонуклеотид для повышения стабильности полученного олигомерного соединения в биологических жидкостях, например, посредством увеличения резистентности к нуклеазам (эндонуклеазам и экзонуклеазам). Степень стабильности зависит от числа используемых нуклеотидов LNA, их положения в олигонуклеотиде и типа используемых нуклеотидов LNA. По сравнению с ДНК и фосфортиоатами способность к стабилизации олигонуклеотидов, обеспечивающая предотвращение их нуклеолитической деградации, может быть выражена в следующем порядке: ДНК << фосфортиоаты ~ окси-LNA<α-L-LNA <амино-LNA<тио-LNA.
Принимая во внимание тот факт, что LNA является совместимой с синтезом стандартной ДНК и может легко смешиваться с многими известными в настоящее время аналогами нуклеиновых кислот, резистентность LNA-олигомерных соединений согласно изобретению к нуклеазе может быть еще более усилена либо путем включения других аналогов, обладающих повышенной стабильностью к нуклеазе, либо путем введения резистентных к нуклеазе межнуклеозидных связей, например фосформонотиоатных, фосфордитиоатных и метилфосфонатных связей и т.п.
Механизм действия: Антисмысловые соединения согласно изобретению могут осуществлять свое терапевтическое действие посредством различных механизмов и способны действовать в соответствии с несколькими механизмами в одном и том же соединении. В одном сценарии связывание олигонуклеотида с его мишенью (пре-мРНК или мРНК) действует по механизму предотвращения связывания других факторов (белков, других нуклеиновых кислот и т.п.), необходимых для правильного функционирования мишени, то есть действует посредством стерического затруднения. Так, например, антисмысловой олигонуклеотид может связываться с мотивами последовательностей либо в пре-мРНК, либо в мРНК, что очень важно для распознавания и связывания транс-действующих факторов, участвующих в сплайсинге, полиаденилировании, клеточном транспорте, посттрансляционных модификациях нуклеозидов в РНК, “кэпировании” по 5'-концу, трансляции и т.п. В случае сплайсинга пре-мРНК взаимодействие между олигонуклеотидом и его мишенью может приводить к подавлению экспрессии нежелательного белка, генерированию альтернативно сплайсированной мРНК, кодирующей нужный белок или к тому и другому.
В другом варианте изобретения, связывание олигонуклеотида с его мишенью приводит к прекращению процесса трансляции путем физического блокирования механизма действия рибосомы, то есть прекращения трансляции.
В еще одном варианте изобретения связывание олигонуклеотида с его мишенью подавляет способность РНК образовывать вторичные структуры и структуры высшего порядка, которые играют важную роль в ее правильном функционировании, то есть препятствует образованию соответствующей структуры. Так, например, данный олигонуклеотид может препятствовать образованию структуры “стебель-петля”, которая играет решающую роль в различных функциях, таких как придание РНК дополнительной стабильности или образование главных мотивов распознавания для различных белков.
В другом варианте изобретения связывание указанных олигонуклеотидов приводит к инактивации мишени для других процессов клеточного метаболизма путем рекрутинга клеточных ферментов, разлагающих мРНК. Так, например, олигонуклеотид может включать сегмент из нуклеозидов, обладающий способностью осуществлять рекрутинг рибонуклеазы Н (РНКазы Н), которая отщепляет РНК-часть от дуплекса ДНК/РНК. Аналогичным образом, олигонуклеотид может содержать сегмент, который обеспечивает рекрутинг двухцепочечных РНКаз, таких как, например, РНКаза III, или он может содержать внешнюю вспомогательную последовательность (EGS), которая обеспечивает рекрутинг эндогенного фермента (РНКазы Р), разлагающего мРНК-мишень. Кроме того, последовательность олигонуклеотида может содержать мотив, который обладает РНКазной каталитической активностью, либо его часть может быть присоединена к олигонуклеотидам, которые, при их непосредственном приближении к мишени в результате гибридизации, сообщают этой мишени неспособность к дальнейшей метаболической активности.
Следует отметить, что хотя было установлено, что размер “гэпов” гэпмера, то есть, субсегмента, составляет от 4 до 14 нуклеиновых оснований, однако, очевидно, что особенно подходящими являются гэпмеры размером от 8 до 13 нуклеиновых оснований, например, от 10 до 12 нуклеиновых оснований, в частности 11 нуклеиновых оснований, см. таблицу 1.
Фармакокинетические свойства
Клиническая эффективность антисмысловых олигонуклеотидов зависит от их фармакокинетических свойств, например абсорбции, распределения, поглощения клетками, метаболизма и экскреции. В свою очередь, на эти параметры в значительной степени влияет химическая структура, а также размер и трехмерная структура олигонуклеотидов.
Как было упомянуто выше, LNA согласно изобретению не является уникальной и существует несколько родственных ей химических соединений, которые отличаются по своей химической структуре, но, при этом, все они обладают превосходной аффинностью по отношению к комплементарной ДНК и РНК. Таким образом, семейство химических соединений LNA является исключительно подходящим для продуцирования олигонуклеотидов согласно изобретению с нужными фармакокинетическими свойствами, которые получают либо с использованием LNA с высокой аффинностью для модуляции размера активных соединений, либо с использованием различных химических соединений LNA для модуляции точного молекулярного состава активных соединений. В последнем случае использование, например, амино-LNA, а не окси-LNA будет приводить к изменению общего заряда олигомерного соединения и будет влиять на характер поглощения и распределения. Аналогичным образом, использование тио-LNA вместо окси-LNA будет приводить к увеличению липофильности олигонуклеотида, что будет влиять на его способность проходить через липофильные барьеры, такие как, например, клеточная мембрана.
Модуляция фармакокинетических свойств LNA-олигонуклеотида согласно изобретению может быть также достигнута путем присоединения других различных молекул. Так, например, способность олигонуклеотидов проходить через клеточную мембрану может быть усилена путем присоединения, например, липидных молекул, таких как холестериновая молекула, тиоэфир, алифатическая цепь, фосфолипид или полиамин, к указанному олигонуклеотиду. Аналогичным образом, поглощение LNA-олигонуклеотидов клетками может быть усилено путем конъюгирования молекул с олигонуклеотидом, который взаимодействует с молекулами в мембране, и который опосредует транспорт в цитоплазму.
Фармакодинамические свойства
В соответствии с настоящим изобретением фармакодинамические свойства могут быть усилены введением групп, которые улучшают поглощение олигомеров, повышают биологическую стабильность, например, усиливают резистентность олигомеров к деградации, и/или увеличивают специфичность и аффинность гибридизации олигонуклеотидов с последовательностью-мишенью, например с последовательностью мРНК.
Токсикология
Существуют, в основном, два типа токсичности, ассоциированной с антисмысловыми олигомерами: последовательность-зависимая токсичность, вызываемая мишень-связывающим доменом, и последовательность-независимая токсичность, ассоциированная с соединениями определенного класса. За исключением токсичности, связанной с иммуностимуляцией нативными последовательностями-мотивами СрG, токсичность, которая была наиболее явно выражена при продуцировании антисмысловых олигонуклеотидов, не зависит от последовательности, например, она зависит от химической природы олигонуклеотида, а также от дозы, способа, частоты и продолжительности введения. Олигонуклеотиды фосфортиоатного класса были особенно хорошо охарактеризованы, и было обнаружено, что они продуцируют ряд побочных эффектов, таких как активация комплемента, продолжительное парциальное тромбопластиновое время (РТТ), тромбоцитопения, гепатотоксичность (увеличение ферментов печени), спленомегалия и гиперплазия ретикулоэндотелиальных клеток.
Как было упомянуто выше, химические соединения семейства LNA обладают исключительно высокой аффинностью, очень высокой биологической стабильностью и способностью модулировать точный молекулярный состав олигонуклеотида. В одном из вариантов изобретения LNA-содержащие соединения позволяют получить олигонуклеотиды, которые обладают высокой эффективностью и, при этом, имеют небольшое количество (если вообще имеют) фосфортиоатных связей, а поэтому они, вероятно, обладают лучшей эффективностью и являются более безопасными, чем современные антисмысловые соединения.
Фармацевтическая композиция
В соответствии с вышесказанным следует отметить, что настоящее изобретение также относится к фармацевтической композиции, содержащей описанные здесь олигомерные соединения или конъюгат и фармацевтически приемлемый носитель.
Рекомендации к получению фармацевтических композиций можно найти в руководстве “Remington: The Science and Practice of Pharmacy”, Alfonso R. Gennaro, и в нижеследующем описании.
Фармацевтически приемлемые носители, такие как связывающие агенты и адъюванты, являются частью такой фармацевтической композиции. Капсулы, таблетки, драже и т.п. могут содержать, например, следующие соединения: микрокристаллическую целлюлозу, камедь или желатин в качестве связывающих агентов; крахмал или лактозу в качестве наполнителей; стеараты в качестве замасливателей и различные подсластители или ароматизаторы. В случае капсул, унифицированная лекарственная форма может содержать жидкий носитель, такой как жирные масла. Аналогичным образом, частью такой унифицированной лекарственной формы может быть сахарное или энтеросолюбильное покрытие. Фармацевтическая композиция может также представлять собой эмульсии, состоящие из активных фармацевтических ингредиентов (включая олигомерное соединение) и липида, образующего мицеллярную эмульсию.
Олигомерное соединение согласно изобретению может быть смешано с любым материалом, который не оказывает нежелательного действия, или с материалом, который обладает дополнительным желательным действием. Такими материалами могут быть и другие лекарственные средства, включая другие нуклеозидные соединения.
Лекарственная композиция для внутривенного, подкожного или местного введения может включать стерильный разбавитель, буферы, регуляторы тоничности и антибактериальные средства. Активное соединение может быть приготовлено в комбинации с носителями, которые обеспечивают защиту против деградации или быстрого выведения из организма, включая имплантаты или микрокапсулы с регулируемым высвобождением. Для внутривенного введения предпочтительными носителями являются физиологический раствор или забуференный фосфатом физиологический раствор.
Олигомерное соединение, предпочтительно, включают в унифицированную лекарственную композицию, например, в фармацевтически приемлемый носитель или разбавитель в количестве, достаточном для доставки пациенту терапевтически эффективного количества препарата, не вызывающего серьезных побочных эффектов у пациента, проходящего курс лечения.
В предпочтительных вариантах фармацевтических композиций олигомерное соединение приготавливают в водном носителе, в частности в водном носителе, содержащем буфер для поддержания рН в пределах 4,0-8,5 и имеющем ионную силу 20-2000 мМ.
Термин “водный носитель” означает, что рассматриваемая фармацевтическая композиция имеет жидкую форму, и что водный носитель, преимущественно состоит из воды, то есть, этот водный носитель, по меньшей мере, на 80% (мас./мас.) или, по меньшей мере, на 90% (мас./мас.) или даже, по меньшей мере, на 95% (мас./мас.) состоит из воды. Могут быть также использованы и другие жидкие ингредиенты, например этанол, ДМСО, этиленгликоль и т.п.
Водный носитель, предпочтительно, содержит буфер для поддержания рН в пределах 4,0-8,5. При этом, предпочтительно, чтобы буфер поддерживал рН в пределах 5,0-8,0, например в пределах 6,0-7,5.
Важными свойствами фармацевтической композиции также являются ионная сила/тоничность. Так, например, обычно, жидкая фармацевтическая композиция имеет ионную силу в пределах 20-2000 нМ, например в пределах 50-1500 нМ или в пределах 100-1000 мМ.
В одном из вариантов изобретения жидкая фармацевтическая композиция содержит определенное здесь олигомерное соединение в водном носителе, где указанный водный носитель содержит буфер для поддержания рН в пределах 4,0-8,5 и имеет ионную силу 20-2000 мМ.
В другом варианте изобретения жидкая фармацевтическая композиция содержит конъюгат в водном носителе, где указанный конъюгат состоит из определенного здесь олигомерного соединения, и, по меньшей мере, одного не-нуклеотидного/не-полинуклеотидного фрагмента, ковалентно связанного с указанным олигомерным соединением, а указанный водный носитель содержит буфер для поддержания рН в пределах 4,0-8,5 и имеет ионную силу 20-2000 мМ.
В двух вариантах изобретения мишень-связывающий домен олигомерного соединения предпочтительно выбран из группы, состоящей из соединений SEQ ID NO:1, 2, 3, 4, 5, 6, 7, 8 (и 35), 12, 13, 14, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51 и 52, в частности, мишень-связывающим доменом является SEQ ID NO:8 (и 35), либо указанный мишень-связывающий домен олигомерного соединения, предпочтительно, выбран из группы, состоящей из SEQ ID NO: 15 (и 29), 17, 18, 19, 21, 22, 23, 24, 25, 26, 27, 28, 53, 54 и 55, в частности, мишень-связывающим доменом является SEQ ID NO:15 (и 29).
Как указывалось выше, особенно предпочтительно, если данное соединение выбрано из группы, состоящей из соединений SEQ ID NO:1, 2, 3, 4, 5, 6, 7, 8 (и 35), 12, 13, 14, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51 и 52, в частности SEQ ID NO:8 (и 35), либо, если данное соединение выбрано из группы, состоящей из соединений SEQ ID NO: 15 (и 29), 17, 18, 19, 21, 22, 23, 24, 25, 26, 27, 28, 53, 54 и 55, в частности SEQ ID NO:15 (и 29).
В другом варианте изобретения, фармацевтическая композиция также содержит дополнительный агент, выбранный из группы, состоящей из химиотерапевтических соединений, противовоспалительных соединений, противовирусных соединений, цитостатических соединений, антиангиогенных соединений, антипролиферативных соединений, про-апоптатических соединений, модуляторов передачи сигнала и ингибиторов киназы.
В варианте, представляющем особый интерес, таким дополнительным агентом является, по меньшей мере, одно химиотерапевтическое соединение. Подходящими примерами таких химиотерапевтических соединений являются соединения, выбранные из группы, состоящей из адренокортикостероидов, таких как преднизон, дексаметазон или декадрон; альтретамина (гексалена, гексаметилмеламина (НММ)); амифостина (этиола); аминоглютетимида (цитадрена); амсакрина (М-AMSA); анастрозола (аримидекса); андрогенов, таких как тестостерон; аспарагиназы (эльспара); кальметт-гурина бацилл; бикалутамида (казодекса); блеомицина (бленоксана); бусульфана (милерана); карбоплатина (параплатина); кармустина (BCNU, BiCNU); хлорамбуцила (лейкерана); хлордезоксиаденозина (2-CDA, кладрибина, лейстатина); цисплатина (платинола); арабинозида цитозина (цитарабина); дакарбазина (DТIC); дактиномицина (актиномицина-D, космегена); даунорубицина (церубидина); доцетаксела (таксотера); доксорубицина (адриомицина); эпирубицина; эстрамустина (эмцита); эстрогенов, таких как диэтилстильбестрол (DES); этопозида (VP-16, Вепезида, этопофоса); флударабина (флудары); флутамида (эйлексина); 5-FUDR (флоксуридина); 5-фторурацила (5-FU); гемцитабина (гемзара); гозерелина (зодалекса); герцептина (трастузумаба); гидроксимочевины (гидреи); идарубицина (идамицина); ифосфамида; IL-2 (пролейкина, альдеслейкина); интерферона-альфа (интрона А, роферона А); иринотекана (камптозара); лейпролида (лупрона); левамизола (эргамизола); ломустина (CCNU); мехлоратамина (мустаргена, азотного аналога горчичного газа); мелфалана (алкерана); меркаптопурина (пуринетола, 6-MP); метотрексата (мексата); митомицина-С (мутамуцина); митоксантрона (новантрона); остреотида (сандостатина); пентостатина (2-дезоксикоформицина, нипента); пликамицина (митрамицина, митрацина); пророкарбазина (матулана); стрептозоцина; тамоксифена (нолвадекса); таксола (паклитаксела); тенипозида (вумона, VM-26); тиотепы; топотекана (гикамтина); третиноина (везаноида, ретиноевой кислоты, которые присутствуют в транс-ориентации); винбластина (валбана); винкристина (онковина) и винорелбина (навелбина). В одном из вариантов изобретения, указанное химиотерапевтическое соединение выбрано из флударабина и таксанов, таких как таксол, паклитаксел и доцетаксел, в частности, флударабина.
В одном из своих вариантов настоящее изобретение относится к фармацевтическим композициям, содержащим (а) одно или несколько олигомерных соединений и (b) одно или несколько других химиотерапевтических соединений, которые действуют по не-антисмысловому механизму. При использовании соединений согласно изобретению такие химиотерапевтические соединения могут быть введены отдельно (например, митрамицин и олигонуклеотид), последовательно (например, митрамицин и олигонуклеотид в течение определенного периода времени, а затем другой агент и олигонуклеотид) или в комбинации с одним или несколькими другими такими химиотерапевтическими соединениями или в комбинации с лучевой терапией. Все химиотерапевтические соединения, известные специалистам в данной области, включая упомянутые выше соединения, вводят в комбинации с соединением согласно изобретению.
В одном из своих вариантов настоящее изобретение относится к фармацевтическим композициям, содержащим (а) одно или несколько олигомерных соединений и (b) одно или несколько соединений антител. К этой комбинации могут быть также добавлены одно или несколько химиотерапевтических соединений.
В одном из предпочтительных вариантов изобретения указанную фармацевтическую композицию вводят в комбинации с соединением, выбранным из соединений флударабина и таксана.
Термин “таксановое соединение” охватывает паклитаксел (Таксол®), производные паклитаксела, доцетаксел, таксотер, модифицированные таксаны и аналоги таксоидов. Паклитаксел (таксол®) представляет собой дитерпен, выделенный из коры Американского (тихоокеанского) тиса, Taxus brevifolia и принадлежит к репрезентативному классу терапевтических средств, имеющих систему таксановых колец. Паклитаксел и его аналоги были получены путем частичного синтеза из 10-деацетилбаккатина-III, т.е. предшественника, выделенного из иголок и побегов тиса, а также путем полного синтеза. См. Holton et al., J. Am. Chem. Soc. 116:1597-1601 (1994) и Nicolaou et al., Nature 367:630 (1994). Клинические испытания паклитаксела продемонстрировали его эффективность при лечении некоторых опухолей человека. См. McGuire et al., Ann. Int. Med. 111:237-279 (1989); Holmes et al., J. Natl. Cancer. Inst. 83:1797-1805 (1991); Kohn et al., J. Natl. Cancer Inst. 86:18-24 (1994); и Kohn et al., American Society for Clinical Oncology 12 (1993). Модифицированный таксан или таксоидные аналоги представляют собой соединения, имеющие таксановое кольцо, несущее модифицированные боковые цепи. Ряд этих аналогов, по сравнению с природным паклитакселом, обладает улучшенными свойствами, такими как более высокая растворимость в воде и стабильность. Эти аналоги известны специалистам в данной области и описаны, например, в патентах США №№ 5278324, 5272171, 5254580, 5250683, 5248796 и 5227400, каждый из которых вводится в настоящее описание посредством ссылки. Паклитаксел и таксотер могут быть получены методами, описанными в заявках WO 93/18210, EP 0253739, EP0253739 и в WO 92/09589, каждая из которых вводится в настоящее описание посредством ссылки. В конкретных вариантах изобретения таксановым соединением является паклитаксел или таксотер.
Массовое отношение химиотерапевтического(их) соединения(ий) (например, соединений флударабина и/или таксана) и олигомерного соединения в указанной композиции обычно составляет в пределах от 50:1 до 1:25, например, от 25:1 до 1:25, или в пределах от 10:1 до 1:25, или в пределах от 1:1 до 1:25, или в пределах от 50:1 до 1:10, или в пределах от 1:1 до 1:50, или в пределах от 25:1 до 1:10.
В одном из вариантов изобретения фармацевтическая композиция содержит, по меньшей мере, одно химиотерапевтическое соединение (например, соединение флударабина и/или таксана) и определенное здесь олигомерное соединение в фармацевтически приемлемом носителе, где массовое отношение химиотерапевтического(их) соединения(ий) и олигомерного соединения в указанной композиции составляет в пределах от 50:1 до 1:25.
В другом варианте изобретения фармацевтическая композиция содержит, по меньшей мере, одно химиотерапевтическое соединение (например, соединение флударабина и/или таксана) и конъюгат в фармацевтически приемлемом носителе, где указанный конъюгат состоит из определенного здесь олигомерного соединения и, по меньшей мере, одного не-нуклеотидного/не-полинуклеотидного фрагмента, ковалентно связанного с указанным олигомерным соединением, и где массовое отношение химиотерапевтического(их) соединения(й) и олигомерного соединения как части конъюгата в указанной композиции составляет в пределах от 50:1 до 1:25. В одном из вариантов описанного варианта изобретения, указанная, по меньшей мере, один не-нуклеотидный/не-полинуклеотидный фрагмент включает химиотерапевтическое соединение (например, соединение флударабина или таксана).
В двух вариантах изобретения мишень-связывающий домен олигомерного соединения предпочтительно выбран из группы, состоящей из соединений SEQ ID NO:1, 2, 3, 4, 5, 6, 7, 8 (и 35), 12, 13, 14, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51 и 52, в частности, мишень-связывающим доменом является SEQ ID NO:8 (и 35), либо указанный мишень-связывающий домен олигомерного соединения, предпочтительно, выбран из группы, состоящей из SEQ ID NO: 15 (и 29), 17, 18, 19, 21, 22, 23, 24, 25, 26, 27, 28, 53, 54 и 55, в частности, мишень-связывающим доменом является SEQ ID NO:15 (и 29).
Как указывалось выше, особенно предпочтительно, если данное соединение выбрано из группы, состоящей из SEQ ID NO:1, 2, 3, 4, 5, 6, 7, 8 (и 35), 12, 13, 14, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51 и 52, в частности SEQ ID NO:8 (и 35), либо, если данное соединение выбрано из группы, состоящей из SEQ ID NO: 15 (и 29), 17, 18, 19, 21, 22, 23, 24, 25, 26, 27, 28, 53, 54 и 55, в частности SEQ ID NO:15 (и 29).
Олигомерные соединения согласно изобретению могут быть также конъюгированы с активными лекарственными средствами, например с аспирином, ибупрофеном, сульфасодержащим лекарственным средством, средством против диабета, антибактериальным средством или антибиотиком.
Противовоспалительные средства, включая, но не ограничиваясь ими, нестероидные противовоспалительные средства и кортикостероиды, противовирусные лекарственные средства и иммуномодулирующие лекарственные средства могут быть также объединены в композиции согласно изобретению. Два или более объединенных соединения могут быть использованы в комбинации друг с другом или по отдельности.
В другом варианте изобретения фармацевтические композиции согласно изобретению могут содержать одно или несколько олигомерных соединений, направленных на Bcl-2, и одно или несколько дополнительных антисмысловых соединений, направленных на вторую нуклеиновую кислоту-мишень. Два или более объединенных соединения могут быть использованы в комбинации друг с другом или по отдельности.
Кроме того, лекарственные средства, содержащие указанные олигомерные соединения, могут быть использованы в комбинации с лучевой терапией и т.п.
Предпочтительные фармацевтические композиции
В одном из вариантов изобретения фармацевтическая композиция согласно изобретению представляет собой жидкую фармацевтическую композицию, содержащую олигомерное соединение, состоящее из 10-30 нуклеиновых оснований, в водном носителе, где указанное олигомерное соединение содержит домен, связывающийся с мишенью, который специфически гибридизуется с областью от положения основания 1459 (5') до 1476 (3') мРНК человеческого Bcl-2, где указанный связывающийся с мишенью домен имеет формулу:
5'-[(ДНК/РНК)0-1-(LNA/LNA*)2-7-(ДНК/РНК/LNA*)4-14-(LNA/LNA*)2-7-
ДНК/РНК)0-1]-3', где:
“LNA” означает нуклеотид LNA, а “LNA*” означает нуклеотидный аналог LNA;
указанный мишень-связывающий домен содержит, по меньшей мере, два нуклеотида LNA или нуклеотидных аналога LNA, связанных фосфортиоатной группой (-О-Р(О,S)-О-); и
указанный водный носитель содержит буфер для поддержания рН в пределах 4,0-8,5 и имеет ионную силу 20-2000 мМ.
В другом варианте изобретения фармацевтическая композиция согласно изобретению представляет собой жидкую фармацевтическую композицию, содержащую конъюгат в водном носителе, где указанный конъюгат состоит из олигомерного соединения, имеющего длину 10-30 нуклеиновых оснований, и, по меньшей мере, одного не-нуклеотидного/не-полинуклеотидного фрагмента, ковалентно связанного с указанным соединением, и где указанное олигомерное соединение содержит домен, связывающийся с мишенью, который специфически гибридизуется с областью от положения основания 1459 (5') до 1476 (3') мРНК человеческого Bcl-2, где указанный связывающийся с мишенью домен имеет формулу:
5'-[(ДНК/РНК)0-1-(LNA/LNA*)2-7-(ДНК/РНК/LNA*)4-14-(LNA/LNA*)2-7-
(ДНК/РНК)0-1]-3', где:
“LNA” означает нуклеотид LNA, а “LNA*” означает нуклеотидный аналог LNA;
указанный мишень-связывающий домен содержит, по меньшей мере, два нуклеотида LNA или нуклеотидных аналога LNA, связанных фосфортиоатной группой (-О-Р(О,S)-О-); и
указанный водный носитель содержит буфер для поддержания рН в пределах 4,0-8,5 и имеет ионную силу 20-2000 мМ.
Кроме того, такая композиция предпочтительно содержит, по меньшей мере, одно химиотерапевтическое соединение (например, соединение флударабина и/или таксана). Как было упомянуто выше, массовое отношение химиотерапевтического(их) соединения(ий) и LNA-олигонуклеотида как части конъюгата в указанной композиции обычно составляет в пределах от 50:1 до 1:25.
В другом варианте изобретения фармацевтическая композиция согласно изобретению представляет собой фармацевтическую композицию, содержащую, по меньшей мере, одно химиотерапевтическое соединение (например, соединение флударабина и/или таксана) и олигомерное соединение, состоящее из 10-30 нуклеиновых оснований, в водном носителе, где указанное олигомерное соединение содержит домен, связывающийся с мишенью, который специфически гибридизуется с областью от положения основания 1459 (5') до 1476 (3') мРНК человеческого Bcl-2, где указанный связывающийся с мишенью домен имеет формулу:
5'-[(ДНК/РНК)0-1-(LNA/LNA*)2-7-(ДНК/РНК/LNA*)4-14-(LNA/LNA*)2-7-
(ДНК/РНК)0-1]-3', где:
“LNA” означает нуклеотид LNA, а “LNA*” означает нуклеотидный аналог LNA;
указанный мишень-связывающий домен содержит, по меньшей мере, два нуклеотида LNA или нуклеотидных аналога LNA, связанных фосфортиоатной группой (-О-Р(О,S)-О-); и
указанное массовое отношение химиотерапевтического(их) соединения(ий) и LNA-олигонуклеотида в указанной композиции составляет в пределах от 50:1 до 1:25.
В еще одном варианте изобретения, фармацевтическая композиция согласно изобретению представляет собой фармацевтическую композицию, содержащую, по меньшей мере, одно химиотерапевтическое соединение (например, соединение флударабина и/или таксана) и конъюгат в фармацевтически приемлемом носителе, где указанный конъюгат состоит из олигомерного соединения, имеющего длину 10-30 нуклеиновых оснований, и, по меньшей мере, одного не-нуклеотидного/не-полинуклеотидного фрагмента, ковалентно связанного с указанным соединением, где указанное олигомерное соединение содержит домен, связывающийся с мишенью, который специфически гибридизуется с областью от положения основания 1459 (5') до основания 1476 (3') мРНК человеческого Bcl-2, где указанный связывающийся с мишенью домен имеет формулу:
5'-[(ДНК/РНК)0-1-(LNA/LNA*)2-7-(ДНК/РНК/LNA*)4-14-(LNA/LNA*)2-7-
(ДНК/РНК)0-1]-3', где:
“LNA” означает нуклеотид LNA, а “LNA*” означает нуклеотидный аналог LNA;
указанный мишень-связывающий домен содержит, по меньшей мере, два нуклеотида LNA или нуклеотидных аналога LNA, связанных фосфортиоатной группой (-О-Р(О,S)-О-); и
указанное массовое отношение химиотерапевтического(их) соединения(ий) и LNA-олигонуклеотида как части конъюгата в указанной композиции составляет в пределах от 50:1 до 1:25.
Показания
Bcl-2 участвует в различных основных биологических механизмах, включая пролиферацию эритроцитов, пролиферацию клеток, ионный метаболизм, метаболизм глюкозы и энергетический обмен, регуляцию рН и матриксный метаболизм. Способы согласно изобретению предпочтительно применяются для лечения, поддерживающей терапии или профилактики раковых заболеваний, в частности, для лечения рака, ассоциированного с экспрессией Bcl-2, такого как рак молочной железы, толстой кишки, предстательной железы, поджелудочной железы, легких, печени, щитовидной железы, почек, головного мозга, яичек, желудка, тонкой кишки, кишечника, спинного мозга, синусов, мочевого пузыря, мочевых путей, яичника, головы и шеи, крови, кожи, желудочно-кишечного тракта или костей.
Настоящее изобретение относится к способу предупреждения, поддерживающей терапии или лечения раковых заболеваний, включающему введение терапевтически эффективного количества Bcl-2-модулирующего олигомерного соединения человеку. Настоящее изобретение также включает введение Bcl-2-модулирующего олигомерного соединения в течение короткого промежутка времени. Обычно не-раковые клетки делятся с частотой, характерной для клеток данного конкретного типа. Если клетка трансформируется в раковую клетку, то это приводит к неконтролируемой пролиферации клеток и к снижению уровня клеточной гибели, а поэтому, беспорядочное деление или нерегулируемый рост клеток является признаком раковых клеток. Примерами раковых заболеваний различных типов являются, но не ограничиваются ими, лимфомы и лейкозы (например, не-ходжкинская лимфома, лимфома Ходжкина, острый лейкоз, такой как острый лимфоцитарный лейкоз, острый миелоцитарный лейкоз, хронический миелоидный лейкоз, хронический лимфоцитарный лейкоз, множественная миелома), карцинома толстой кишки, карцинома прямой кишки, рак поджелудочной железы, рак молочной железы, рак яичника, рак предстательной железы, почечно-клеточная карцинома, гепатома, карцинома желчных путей, хориокарцинома, рак шейки матки, рак яичек, карцинома легких, карцинома мочевого пузыря, меланома, рак головы и шеи, рак головного мозга, рак неизвестной первичной локализации, неоплазмы, рак периферической нервной системы, рак центральной нервной системы, опухоли различных видов (например, фибросаркома, миксосаркома, липосаркома, хондросаркома, остеогенная саркома, хордома, ангиосаркома, эндотелиосаркома, лимфангиосаркома, лимфангиоэндотелиосаркома, синовиома, мезотелиома, опухоль Юинга, лейомиосаркома, рабдомиосаркома, плоскоклеточная карцинома, базально-клеточная карцинома, аденокарцинома, карцинома потовых желез, карцинома сальных желез, папиллярная карцинома, папиллярная аденокарцинома, цистаденокарцинома, медуллярная карцинома, бронхогенная карцинома, семинома, эмбриональная карцинома, опухоль Вильмса, мелкоклеточная карцинома легких, эпителиальная карцинома, глиома, астроцитома, медуллобластома, краниофарингиома, эпендимома, пинеалома, гемангиобластома, неврома слухового нерва, олигодендроглиома, менингиома, нейробластома и ретинобластома), болезнь тяжелых цепей, метастазы или любое заболевание или расстройство, характеризующееся неконтролируемым или аномальным ростом клеток.
Не-ходжкинскими лимфомами согласно изобретению являются, но не ограничиваются ими, лимфома клеток-предшественников, такая как лимфобластная лимфома (Т-клеточная и В-клеточная); неоплазмы периферических В-клеток, такие как хронический В-лимфоцитарный лейкоз и мелкоклеточная лимфоцитарная лимфома, В-пролимфоцитарный лейкоз, лимфоплазмоцитарная лимфома, лимфома клеток мантии, фолликулярная лимфома, В-клеточная лимфома экстралимфатической маргинальной зоны типа МАLT, В-клеточная лимфома лимфатической маргинальной зоны, В-клеточная лимфома селезеночной маргинальной зоны, ретикулоэндотелиоз, диффузная крупноклеточная лимфома, лимфома Беркитта, включая лимфому типа лимфомы Беркитта, плазмацитома и миелома плазматических клеток; неоплазмы периферических Т- и NK-клеток, такие как Т-клеточный пролимфоцитарный лейкоз, Т-клеточный гранулярный лимфоцитарный лейкоз, агрессивный NK-клеточный лейкоз, грибовидный микоз и синдром Сезари, периферическая Т-клеточная лимфома, ангиоиммунобластная Т-клеточная лимфома, экстралимфатическая NK/Т-клеточная лимфома (назальная и назального типа), Т-клеточная лимфома типа энтеропатии, Т-клеточная лимфома спленоцитов печени γδ, подкожная панникулит-подобная Т-клеточная лимфома, анапласитическая крупноклеточная лимфома (Т/“нуль”-клеточная и первичная системная), анапластическая крупноклеточная лимфома (Т/“нуль”-клеточная, первичная кожная) и лимфома и лейкоз зрелых Т-клеток (HTLV1+).
В настоящее время считается, что типами рака, для которых могут быть достигнуты особенно хорошие клинические результаты, являются острый миелоидный лейкоз, хронический лимфоцитарный лейкоз и не-ходжкинские лимфомы, в частности фолликулярная лимфома и диффузная крупноклеточная В-лимфома.
Термин “карцинома” означает злокачественную опухоль эпителиального происхождения. Эпителиальная ткань покрывает или выстилает поверхности организма как внутри, так и снаружи. Примерами эпителиальных тканей являются кожа, слизистая и серозная оболочка, которая выстилает полости в организме и внутренние органы, такие как тонкий кишечник, мочевой пузырь, матка и т.п. Эпителий может также распространяться в более глубокие слои ткани с образованием желез, таких как железы, секретирующие слизь.
Термин “карцинома” означает злокачественную опухоль, развивающуюся из соединительной ткани, такой как хрящ, жир, мышцы, сухожилия и кости.
Используемый здесь термин “глиома” означает злокачественную опухоль, происходящую из глиальных клеток.
Применение
Олигомерные соединения согласно изобретению могут быть использованы в качестве терапевтических средств, средств для поддерживающей терапии и профилактических средств. В исследованиях, антисмысловые олигомерные соединения могут быть использованы для специфического ингибирования синтеза белка Bcl-2 в клетках и у экспериментальных животных, что, тем самым, облегчает проведение функционального анализа мишени или оценку ее пригодности как мишени для терапевтического воздействия. В терапевтических целях животному или человеку (в частности, человеку) с подозрением на заболевание или расстройство, которое может быть подвергнуто лечению путем модуляции экспрессии Bcl-2, вводят антисмысловые соединения согласно изобретению. Настоящее изобретение также относится к способам лечения животного, в частности мыши и крысы, и лечения человека с подозрением на заболевание или состояние или с предрасположенностью к заболеванию или состоянию, ассоциированному с экспрессией Bcl-2, путем введения терапевтически или профилактически эффективного количества одного или нескольких антисмысловых соединений или композиций согласно изобретению.
Настоящее изобретение также относится к способу модуляции экспрессии Bcl-2 в клетках или в тканях, где указанный способ включает контактирование указанных клеток или тканей с определенным здесь олигомерным соединением или конъюгатом, в частности, с определенной здесь фармацевтической композицией, где указанное контактирование приводит к модуляции экспрессии Bcl-2.
Кроме того, настоящее изобретение относится к способу модуляции экспрессии гена, ответственного за развитие ракового заболевания, где указанный способ включает контактирование гена или РНК данного гена с определенным здесь олигомерным соединением или конъюгатом, в частности, с определенной здесь фармацевтической композицией, где указанное контактирование приводит к модуляции экспрессии генов. Таким геном, предпочтительно, является человеческий ген Bcl-2.
В другом своем аспекте настоящее изобретение относится к способу индуцирования клеточного апоптоза, включающему контактирование клетки или РНК данной клетки с определенным здесь олигомерным соединением или конъюгатом, в частности с определенной здесь фармацевтической композицией, где указанное контактирование приводит к индуцированию апоптоза клеток. Индуцирование апоптоза может происходить in vitro или in vivo. Такое индуцирование апоптоза может быть стимулировано в клеточном анализе или в образце ткани или в организме млекопитающего.
В другом своем аспекте настоящее изобретение относится к способу предотвращения или снижения пролиферации клеток, включающему контактирование клетки или РНК данной клетки с определенным здесь олигомерным соединением или конъюгатом, в частности с определенной здесь фармацевтической композицией, где указанное контактирование приводит к предотвращению или к снижению пролиферации клеток. Предотвращение или снижение пролиферации может происходить in vitro или in vivo. Такое предотвращение может быть достигнуто в клеточном анализе или в образце ткани или в организме млекопитающего.
Кроме того, настоящее изобретение относится к способу лечения млекопитающего, страдающего раковым заболеванием или восприимчивого к такому заболеванию, где указанный способ включает введение данному млекопитающему терапевтически эффективного количества определенного здесь олигомерного соединения или конъюгата, в частности определенной здесь фармацевтической композиции.
В одном из вариантов изобретения указанное лечение осуществляют в комбинации с введением дополнительного средства, выбранного из группы, состоящей из химиотерапевтических соединений, противовоспалительных соединений, противовирусных соединений, цитостатических соединений, антиангиогенных соединений, антипролиферативных соединений, про-апоптотических соединений, модуляторов передачи сигнала, антитела и ингибиторов киназы. В конкретном варианте изобретения, указанным дополнительным средством является, по меньшей мере, одно химиотерапевтическое средство, в частности одно или несколько вышеупомянутых специфических химиотерапевтических средств.
Настоящее изобретение также относится к способу лечения млекопитающего, страдающего заболеванием, вызываемым ангиогенезом, или восприимчивого к такому заболеванию, где указанный способ включает введение данному млекопитающему терапевтически эффективного количества определенного здесь олигомерного соединения или конъюгата, в частности определенной здесь фармацевтической композиции.
Кроме того, настоящее изобретение относится к олигомерным соединениям, определенным здесь как соединения, используемые в качестве лекарственного средства. Более конкретно, настоящее изобретение относится к использованию определенного здесь олигомерного соединения в целях приготовления лекарственного средства для лечения ракового заболевания. Указанное лекарственное средство, предпочтительно, приготавливают в форме определенной выше фармацевтической композиции.
Таким образом, в другом своем аспекте, настоящее изобретение относится к использованию определенного здесь олигомерного соединения в целях приготовления фармацевтической композиции для лечения млекопитающего, в частности человека, страдающего раковым заболеванием или восприимчивого к такому заболеванию.
В еще одном своем аспекте настоящее изобретение относится к способу лечения млекопитающего, в частности человека, страдающего раковым заболеванием или восприимчивого к такому заболеванию, где указанный способ включает стадию введения данному млекопитающему одной или нескольких терапевтически эффективных доз первой фармацевтической композиции, содержащей определенное здесь олигомерное соединение.
В еще одном своем аспекте, настоящее изобретение относится к способу лечения млекопитающего, в частности, человека, страдающего раковым заболеванием или восприимчивого к такому заболеванию, где указанный способ включает стадию введения данному млекопитающему одной или нескольких терапевтически эффективных доз первой фармацевтической композиции, содержащей конъюгат, где указанный конъюгат состоит из определенного здесь олигомерного соединения и, по меньшей мере, одного не-нуклеотидного/не-полинуклеотидного фрагмента, ковалентно связанного с указанным олигомерным соединением.
Одним из вариантов двух последних аспектов является вариант, в котором одно или несколько химиотерапевтических соединений (например, соединение флударабина и/или таксана) вводят в комбинации с LNA-олигонуклеотидом, в частности, в котором указанное(ые) химиотерапевтическое(ие) соединение(я) присутствует(ют) в первой фармацевтической композиции, содержащей указанный LNA-олигонуклеотид.
Другим вариантом из двух последних аспектов является вариант, в котором одно или несколько химиотерапевтических соединений (например, соединение флударабина и/или таксана) присутствует во второй фармацевтической композиции, не содержащей LNA-олигонуклеотида. В этом случае первая фармацевтическая композиция и вторая фармацевтическая композиция могут быть введены одновременно или последовательно.
В более общем варианте указанное лекарственное средство может также содержать дополнительное средство, выбранное из группы, состоящей из химиотерапевтических соединений, противовоспалительных соединений, противовирусных соединений, цитостатических соединений, антиангиогенных соединений, антипролиферативных соединений, про-апоптотических соединений, модуляторов передачи сигнала и ингибиторов киназы. В конкретном варианте изобретения указанным дополнительным средством является, по меньшей мере, одно химиотерапевтическое соединение, в частности одно или несколько вышеупомянутых специфических химиотерапевтических соединений.
Описанными выше раковыми заболеваниями являются, в частности, рак легких, молочной железы, толстой кишки, предстательной железы, поджелудочной железы, печени, щитовидной железы, почек, головного мозга, яичек, желудка, тонкой кишки, кишечника, спинного мозга, синусов, мочевого пузыря, мочевых путей, яичника, головы и шеи, крови или кожи, как подробно описано выше.
Кроме того, настоящее изобретение относится к комплексу, содержащему соединение, гибридизованное с рибонуклеиновой кислотой, кодирующей человеческий белок Bcl-2, где указанным соединением является определенное выше олигомерное соединение или конъюгат. Такие комплексы могут образовываться в результате обработки мишени, то есть, рибонуклеиновой кислоты, кодирующей человеческий белок Bcl-2, определенным здесь олигомерным соединением или конъюгатом.
Введение
Фармацевтические композиции согласно изобретению могут быть введены различными методами в зависимости от того, является ли данное лечение местным или системным, и в зависимости от участка организма, подвергаемого лечению. Введение может быть (а) пероральным, (b) пульмональным, например, путем ингаляции или инсуффляции порошков или аэрозолей, включая введение с помощью ингалятора; интратрахеальным и интраназальным; (с) местным, включая эпидермальное введение, чрезкожное введение, офтальмическое введение и введение в слизистые оболочки, включая вагинальное и ректальное введение; или (d) парентеральным, включая внутривенное, внутриартериальное, подкожное, внутрибрюшинное или внутримышечное введение или вливание; или интракраниальным, например, интратекальным или интравентрикулярным введением. В одном из вариантов изобретения олигомерное соединение вводят внутривенно, внутрибрюшинно, перорально, местно или в виде инъекции ударной дозы или непосредственно в нужный орган.
Фармацевтическими композициями и препаратами для местного применения могут быть чрезкожные пластыри, мази, лосьоны, кремы, гели, капли, спреи, суппозитории, жидкости и порошки. При этом необходимыми или желательными могут быть стандартные фармацевтические носители, водные порошкообразные или масляные основы, загустители и т.п. Могут быть также использованы презервативы, перчатки и т.п., покрытые этими композициями. Предпочтительными препаратами для местного применения являются препараты, в которых олигонуклеотиды согласно изобретению присутствуют в смеси со средством для местного введения, таким как липиды, липосомы, жирные кислоты, сложные эфиры сложных кислот, стероиды, хелатообразующие агенты и поверхностно-активные вещества. Композициями и препаратами для перорального введения являются, но не ограничиваются ими, порошки или гранулы, микрочастицы, наночастицы, суспензии или растворы в воде или в безводных средах, капсулы, гелевые капсулы, саше, таблетки или минитаблетки. Композиции и препараты для парентерального, интратекального или интравентрикулярного введения могут включать стерильные водные растворы, которые могут также содержать буферы, разбавители и другие подходящие добавки, такие как, но не ограничивающиеся ими, усилители пенетрации, соединения-носители и другие фармацевтически приемлемые носители или наполнители.
Доставка
Фармацевтическми композициями согласно изобретению являются, но не ограничиваются ими, растворы, эмульсии и композиции, содержащие липосомы. Эти композиции могут быть получены из различных компонентов, которыми являются, но не ограничиваются ими, предварительно приготовленные жидкости, самоэмульгирующиеся твердые вещества и самоэмульгирующиеся полутвердые вещества. Доставка лекарственного средства в опухолевую ткань может быть улучшена с помощью носителей, включая, но не ограничиваясь ими, катионные липосомы, циклодекстрины, производные порфирина, дендримеры с разветвленной цепью, полиэтилениминовые полимеры, наночастицы и микросферы (Dass C.R., J.Pharm. Pharmacol. 2002; 54(1):3-27).
Фармацевтические композиции согласно изобретению, которые обычно приготавливают в виде унифицированной лекарственной формы, могут быть получены стандартными методами, хорошо известными специалистам-фармацевтам. Такие методы включают стадию объединения активных ингредиентов с фармацевтическим(и) носителем(ями) или наполнителем(ями). В общих чертах, такие композиции получают путем однородного и тщательного смешивания активных ингредиентов с жидкими носителями или с тонкодисперсными твердыми носителями, либо с теми и другими, а затем, если это необходимо, формования полученного продукта.
Композиции согласно изобретению могут быть приготовлены в виде любой из многих возможных лекарственных форм, таких как, но не ограничивающихся ими, таблетки, капсулы, гелевые капсулы, жидкие сиропы, мягкие гели и суппозитории. Композиции согласно изобретению могут быть также приготовлены в виде суспензий в водных, безводных или смешанных средах. Водные суспензии могут также содержать вещества, повышающие вязкость данной суспензии, включая, например, натрийсодержащую карбоксиметилцеллюлозу, сорбит и/или декстран. Такая суспензия может также содержать стабилизаторы.
Дозы
Доза зависит от тяжести данного патологического состояния, и его восприимчивости к подвергаемому лечению, и курс лечения может продолжаться от нескольких дней до нескольких месяцев, либо до тех пор, пока лечение не будет давать определенный результат или пока не будет наблюдаться ослабление симптомов данного патологического состояния. Оптимальные схемы введения доз будут зависеть, например, от выбранной комбинированной терапии, от типа заболевания или патологического состояния и от результатов предварительных клинических испытаний.
Оптимальные дозы могут варьироваться в зависимости от относительной эффективности отдельных олигонуклеотидов. В основном эти дозы могут быть определены исходя из величин EC50, которые, как было установлено, являются эффективными in vitro и in vivo у животных с моделью заболевания. В общих чертах, доза составляет от 0,01 мкг до 1 г на кг массы тела и может быть введена один раз или несколько раз в день, в неделю, в месяц или в год, или даже один раз каждые 2 года - 10 лет, либо она может быть введена путем непрерывного вливания в течение периода времени от одного часа до нескольких месяцев. Частота введения дозы может быть оценена исходя из результатов измерения времени присутствия и концентрации лекарственного средства в физиологических жидкостях или тканях. После успешного лечения для пациента может оказаться желательным проведение поддерживающей терапии в целях предупреждения рецидива данного патологического состояния.
Не ограничиваясь какой-либо конкретной теорией, авторы настоящего изобретения считают, что комбинированный эффект (а возможно и синергический эффект) химиотерапевтического соединения и олигомерного соединения согласно изобретению позволит снизить дозу химиотерапевтического соединения или олигомерного соединения или того и другого.
Набор
В другом своем аспекте настоящее изобретение относится к набору, включающему:
(а) первый компонент, содержащий одну или несколько доз раствора для инъекций, включающего определенное здесь олигомерное соединение, и
(b) второй компонент, содержащий одну или несколько доз раствора для инъекций, включающего одно или несколько химиотерапевтических соединений (например, соединений флударабина и/или таксана));
где массовое отношение, по меньшей мере, одного соединения таксана и, по меньшей мере, одного LNA-олигонуклеотида в указанной композиции составляет в пределах от 50:1 до 1:25.
Указанные растворы для инъекций, включающие дозы олигомерного соединения, предпочтительно, представляют собой описанные выше фармацевтические композиции.
ПРИМЕРЫ
Пример 1: Синтез мономеров
Структурные элементы, содержащие LNA-мономер, и их производные были получены в соответствии с известными процедурами и процедурами, описанными в нижеследующих работах:
WO 03/095467 A1
D. S. Pedersen, C. Rosenbohm, T. Koch (2002) Preparation of LNA Phosphoramidites, Synthesis 6, 802-808.
M. D. Sоrensen, L. Kvаеrnо, T. Bryld, A. E. Hаkansson, B. Verbeure, G. Gaubert, P. Herdewijn, J. Wengel (2002) α-L-ribo-configured Locked Nucleic Acid (α-l-LNA): Synthesis and Properties, J. Am. Chem. Soc., 124, 2164-2176.
S. K. Singh, R. Kumar, J. Wengel (1998) Synthesis of Novel Bicyclo[2.2.1]Ribonucleosides: 2'-Amino- and 2'-Thio-LNA Monomeric Nucleosides, J. Org. Chem. 1998, 63, 6078-6079.
C. Rosenbohm, S. M. Christensen, M. D. Sоrensen, D. S. Pedersen, L. E. Larsen, J. Wengel, T. Koch (2003) Synthesis of 2'-amino-LNA: a new strategy, Org. Biomol. Chem. 1, 655-663.
D. S. Pedersen, T. Koch (2003) Analogues of LNA (Locked Nucleic Acid). Synthesis of the 2'-Thio-LNA Thymine and 5-Methyl Cytosine Phosphoramidites, Synthesis, accepted.
Пример 2: Синтез олигонуклеотидов
Лабораторный синтез олигонуклеотидов
Олигонуклеотиды синтезировали фосфорамидитным методом на синтезаторе 8900/МОSS Expedite (Multiple Oligonucleotide Synthesis System) в масштабе 1 мкмоль или 15 мкмоль. Для крупномасштабного синтеза использовали устройство Аkta Oligo Pilot. По окончании синтеза (DМТ-on), олигонуклеотиды отщепляли от твердого носителя с использованием водного аммиака в течение 1-2 ч при комнатной температуре, а затем подвергали реакции деблокирования в течение 4 часов при 65°С. Олигонуклеотиды очищали с помощью обращенно-фазовой ВЭЖХ (ОФ-ВЭЖХ). После удаления группы DМТ, олигонуклеотиды охарактеризовывали с помощью AE-ВЭЖХ, ОФ-ВЭЖХ и СGE, а молекулярную массу дополнительно подтверждали с помощью ESI-MS. Более подробное описание см. ниже.
Получение конъюгата “LNA-твердый носитель”
Получение неполного сукцинилового эфира LNA
5'-O-Dmt-3'-гидрокси-LNA-мономер (500 мг), ангидрид янтарной кислоты (1,2 экв.) и DMAP (1,2 экв.) растворяли в ДХМ (35 мл). Реакционную смесь перемешивали при комнатной температуре в течение ночи. После экстрагирования NaH2PO4, 0,1 М рН 5,5 (2×) и насыщенным раствором соли (1×), органический слой дополнительно сушили безводным Na2SO4, фильтровали и упаривали. Производное неполного сложного эфира получали с выходом 95% и использовали без дополнительной очистки.
Получение конъюгата “LNA-носитель”
Производное неполного сложного эфира (90 мкмоль), полученное как описано выше, растворяли в минимальном количестве ДМФ, добавляли DIEA и РуВОР (90 мкмоль) и смешивали в течение 1 минуты. Эту предварительно активированную смесь объединяли с LCAA-CPG (500 A, размер 80-120 меш, 300 мг) в синтезаторе с ручным управлением и перемешивали. После выдерживания в течение 1,5 часа при комнатной температуре носитель отфильтровывали и промывали ДМФ, ДХМ и МеОН. После сушки, загрузка, как было определено, составляла 57 мкмоль/г (см. Tom Brown, Dorcas J.S. Brown. Modern machine-aided methods of oligodeoxyribonucleotide synthesis. In: F. Eckstein, editor. Oligonucleotides and Analogues A Practical Approach. Oxford: IRL Press, 1991:13-14).
Удлинение олигонуклеотида
Реакцию сочетания фосфорамидитов (А(bz), G(ibu), 5-метил-С(bz)) или Т-β-цианоэтилфосфорамидита) проводили с использованием раствора 0,1М 5'-О-DMT-защищенного амидита в ацетонитриле и DCI (4,5-дицианоимидазола) в ацетонитриле (0,25 М) в качестве активатора. Тиолирование проводили с использованием гидрида ксантана (0,01 М в смеси ацетонитрил:пиридин 10%). Остальными реагентами являются реагенты, которые обычно используются для синтеза олигонуклеотидов. Протокол, осуществляемый в соответствии с рекомендациями поставщиков, был соответствующим образом оптимизирован.
Очистка с помощью ОФ-ВЭЖХ
| Колонка: | Xterra RP18 |
| Скорость потока: | 3 мл/мин |
| Буфер: | 0,1 ацетат аммония, рН 8, и ацетонитрил |
Сокращения:
| DМТ: | Диметокситритил |
| DСI: | 4,5-дицианоимидазол |
| DMAР: | 4-диметиламинопиридин |
| DСМ (ДХМ): | Дихлорметан |
| DМF (ДМФ): | Диметилформамид |
| ТHF(ТГФ): | Тетрагидрофуран |
| DIEA: | N,N-диизопропилэтиламин |
| PyBOP: | Гексафторфосфат бензотриазол-1-ил-окси-трис-пирролидинофосфония |
| Bz: | Бензоил |
| Ibu: | Изобутирил |
Крупномасштабный синтез олигонуклеотидов:
При проведении крупномасштабного синтеза, олигонуклеотиды синтезировали фосфорамидитным методом на экспериментальном устройстве для синтеза олигонуклеотидов Аkta Oligo Pilot в масштабе от 200 мкмоль до 1 ммоль. Затем DМТ-OFF-синтез олигонуклеотидов и последующую DЕА-обработку также проводили на синтезаторе. Отщепление олигонуклеотида от твердого носителя и удаление защитных групп осуществляли путем обработки водным аммиаком в течение 12 часов при 55°С. После этого олигонуклеотиды очищали с помощью ионообменной (IEX) хроматографии на Аkta Pilot. Олигонуклеотиды обессоливали на среде с сефадексомТМ G-25, а затем лиофилизовали. Полученные олигонуклеотиды характеризовали с помощью IEX-ВЭЖХ, CGE и ESI-MS.
Реакцию сочетания ДНК-фосфорамидитов (А(bz), С(bz), G(ibu) и (Т)) и LNA-фосфорамидитов (С(bz) и (Т)) проводили с использованием 0,2М раствора амидита в ацетонитриле и 0,75М DCI (4,5-дицианоимидазола) в качестве активатора. Тиолирование проводили с использованием гидрида ксантана (0,0175 М в смеси ацетонитрил:пиридин 20%). Остальными реагентами являются реагенты, которые обычно используются для синтеза олигонуклеотидов.
Пример 3: Конструирование олигомерного соединения
В описании настоящей заявки, олигомерные соединения обозначаются номером их последовательности, например “SEQ ID NO:15”. Соединение “SEQ ID NO:56” также называется облимерсен-натрием и используется здесь как контрольное соединение.
|
Таблица 1
Олигомерные соединения согласно изобретению |
||
| SEQ ID NO: | Последовательность | Структура |
| Комплементарные 18-меры | ||
| 1 | TsCstscscscsasgscsgstsgscsgscsCsAst | гэп 13 |
| 2 | TsCsTscscscsasgscsgstsgscsgsCsCsAst | гэп 11 |
| 3 | TsCsTsCscscsasgscsgstsgscsGsCsCsAst | гэп 9 |
| 4 | tsCsTsCscscsasgscsgstsgscsgsCsCsAst | гэп 10 |
| 5 | TsCsTscscscsasgscsgstsgscsgsCsCsAsT | гэп 11 |
| 6 | Tα sCα sTα scscscsasgscsgstsgscsgsCα sCα sAα st | гэп 11 |
| 7 | tsCα sTα sCα scscsasgscsgstsgscsgsCα sCα sAα st | гэп 10 |
| Комплементарные 16-меры | ||
| 8 | CsTscscscsasgscsgstsgscsgsCsCsa | гэп 11 |
| 9 | Cα sTα scscscsasgscsgstsgscsgsCα sCα sa | гэп 11, α-L-LNA |
| 10 | CsTscscscsasgscsgstsgscsgsCsCsA | LNA 3'-конец |
| 11 | CsTscscscsasgscsgstsgscsgscsCsA | LNA 3'-конец |
| 12 | CsTsCscscsasgscsgstsgscsGsCsCsa | гэп 9 |
| 13 | CsTsCsCscsasgscsgstsgsCsGsCsCsa | гэп 7 |
| 14 | CsTsCscscsasgscsgstsgscsGsCsCsA | гэп 9 |
| cstscscscsasMscsgstsgscsgscscsa, 16-меры | ||
| 15 | CsTscscscsasascsgstsgscsgsCsCsa | гэп 11 |
| 16 | Cα sTα scscscsasascsgstsgscsgsCα sCα sa | гэп 11, α-L-LNA |
| 17 | CsTsCscscsasascsgstsgscsGsCsCsa | гэп 9 |
| 18 | CsTsCscscsastscsgstsgscsGsCsCsa | гэп 9 |
| 19 | CsTsCsCscsasascsgstsgsCsGsCsCsa | гэп 7 |
| 20 | CsTscscscsasascsgstsgscsGsCsCsa | гэп 10 |
| cstscscscsasgscsgsMsgscsgscscsa, 16-меры | ||
| 21 | CsTscscscsasgscsgscsgscsgsCsCsa | гэп 11 |
| 22 | CsTsCscscsasgscsgscsgscsGsCsCsa | гэп 9 |
| 23 | CsTsCsCscsasgscsgscsgsCsGsCsCsa | гэп 7 |
| 24 | CsTscscscsasgscsgsasgscsgsCsCsa | гэп 11 |
| 25 | CsTscscscsasgscsgsgsgscsgsCsCsa | гэп 11 |
| tscstscscscsasgsMsgstsgscsgscscsa,t, 18-меры | ||
| 26 | TCsTscscscsasgsasgstsgscsgsCsCsAst | гэп 11 |
| 27 | TCsTscscscsasgstsgstsgscsgsCsCsAst | гэп 11 |
| 28 | TCsTscscscsasgsgsgstsgscsgsCsCsAst | гэп 11 |
| Стандарты | ||
| 29 | CsTscscscsasascsgstsgscsgsCsC | N-1, 3'-конец |
| 30 | CsTscscscsasascsgstsgscsgsC | N-2, 3'-конец (контроль) |
| 31 | CsTscscscsasascsgstsgscsgs | N-3, 3'-конец (контроль) |
| 32 | TscscscsasascsgstsgscsgsCsCsa | N-1, 5'-конец (контроль) |
| 33 | cscscsasascsgstsgscsgsCsCsa | N-2, 5'-конец (контроль) |
| 34 | cscsasascsgstsgscsgsCsCsa | N-3, 5'-конец (контроль) |
| 35 | CsTscscscsasgscsgstsgscsgsCsC | N-1, 3'-конец |
| 36 | CsTscscscsasgscsgstsgscsgsC | N-2, 3'-конец (контроль) |
| 37 | CsTscscscsasgscsgstsgscsgs | N-3, 3'-конец (контроль) |
| 38 | TscscscsasgscsgstsgscsgsCsCsa | N-1, 5'-конец (контроль) |
| 39 | cscscsasgscsgstsgscsgsCsCsa | N-2, 5'-конец (контроль) |
| 40 | cscsasgscsgstsgscsgsCsCsa | N-3, 5'-конец (контроль) |
| 41 | CsTscscscsasgscsgstsgscsgscsCsAst | гэп 12 |
| 42 | CsTsCscscsasgscsgstsgscsgsCsCsAst | гэп 10 |
| 43 | CsTsCsCscsasgscsgstsgscsGsCsCsAst | гэп 8 |
| 44 | TsCstscscscsasgscsgstsgscsgsCsCsa | гэп 12 |
| 45 | TsCsTscscscsasgscsgstsgscsGsCsCsa | гэп 10 |
| 46 | TsCsTsCscscsasgscsgstsgsCsGsCsCsa | гэп 8 |
| 47 | TsCstscscscsasgscsgstsgscsGsCsc | гэп 11 |
| 48 | TsCsTscscscsasgscsgstsgsCsGsCsc | гэп 9 |
| 49 | TsCsTsCscscsasgscsgstsGsCsGsCsc | гэп 7 |
| 50 | TsCscscsasgscsgstsgscsgscsCsAst | гэп 11 |
| 51 | TsCsCscsasgscsgstsgscsgsCsCsAst | гэп 9 |
| 52 | TsCsCsCsasgscsgstsgscsGsCsCsAst | гэп 7 |
| 53 | TCsTscscscsasgscsastsgscsgsCsCsAst | гэп 11 |
| 54 | TCsTscscscsasgscststsgscsgsCsCsAst | гэп 11 |
| 55 | TCsTscscscsasgscscstsgscsgsCsCsAst | гэп 11 |
| 56 | tscstscscscsasgscsgstsgscsgscscsast | Контроль |
| 57 | TsCsTscscscsasgscsastsgstsgsCsCsAst | 2 ошибочных спаривания |
| 58 | AsCscsgscsgstsgscsgsascscsCsTsc | Контроль; обратная полярность |
| 59 | ts mcsts mcs mcs mcsasgs mcsgstsgs mcsgs mcs mcsast | Контроль |
| 60 | CsTscscscsasascm sgstsgscm sgsCsCsa | гэп 11 |
| 61 | CsTs mcs mcs mcsasas mcsgstsgs mcsgsCsCsa | гэп 11 |
| Праймеры | ||
| 62 | catgtgtgtggagagcgtcaa | |
| 63 | gccggttcaggtactcagtca | |
| 64 | FAM-cctggtggacaacatcgccctgt-TAMRA | |
В таблице 1 заглавные буквы означают нуклеотиды LNA, надстрочный индекс “α“ означает, что нуклеотидом LNA является нуклеотид альфа-L-LNA (то есть, нуклеотидный аналог LNA), а подстрочный индекс “S” означает, что соседние нуклеотиды связаны с фосфортиоатной группой. Все LNA-С-мономеры представляют собой метил-С.
Пример 4: in vitro-модель: культуровование клеток
Влияние антисмысловых соединений на экспрессию нуклеиновой кислоты-мишени может быть проанализировано в любых клетках различных типов при условии, что такая нуклеиновая кислота-мишень присутствует на измеримых уровнях. Мишень может быть экспрессирована эндогенно или путем временной или стабильной трансфекции нуклеиновой кислоты, содержащей указанную нуклеиновую кислоту.
Уровень экспрессии нуклеиновой кислоты-мишени может быть рутинно определен с помощью, например, Нозерн-блот-анализов, количественной ПЦР, анализов путем защиты от рибонуклеазы или другими количественными методами. Ниже представлены лишь некоторые типы клеток, использованных в этих целях, однако могут быть использованы и клетки других типов, при условии, что в клетке выбранного типа будет экспрессироваться данная мишень.
Клетки культивировали в соответствующей среде, описанной ниже, и поддерживали при 37оС в условиях влажности 95-98% и в присутствии 5% СО2. Клетки обычно пересевали 2-3 раза в неделю.
15РС3: Клеточная линия рака человеческой предстательной железы 15РС3 была любезно предоставлена Dr. F. Baas, Neurozintuigen Laboratory, AMC, The Netherlands, и эту клеточную линию культивировали в DMEM (Sigma) + 10% фетальная бычья сыворотка (FBS) + глутамакс I + гентамицин.
РС3: Клеточная линия рака человеческой предстательной железы РС3 была закуплена у АТСС и культивирована в среде Куна F12, содержащей глутамин (Gibco) + 10% FBS + гентамицин.
518А2: Клеточная линия человеческой меланомы 518А2 была любезно предоставлена Dr. B. Jansen, Section of experimental Oncology, Molecular Pharmacology, Department of Clinical Pharmacology, University of Vienna, и эту клеточную линию культивировали в DMEM (Sigma) + 10% фетальная бычья сыворотка (FBS) + глутамакс I + гентамицин.
Пример 5: In vitro-модель: обработка антисмысловым олигонуклеотидом
Клетки обрабатывали олигонуклеотидом с использованием катионного липосомного препарата липофектамина 2000 (Gibco) в качестве носителя для трансфекции.
Эти клетки высевали в 12-луночные планшеты для культивирования клеток (NUNC) и обрабатывали при конфлюэнтности 80-90%. Концентрации используемого олигомера составляли от 0,2 нМ до конечной концентрации 100 нМ. Комплексы “олигомер-липид” получали, в основном, как описано Dеаn et al. (Journal of Biological Chemistry 1994, 269, 16416-16424) с использованием бессывороточной среды ОрtiMEM (Gibco) и липида в конечной концентрации 10 мкг/мл липофектамина 2000 в общем объеме 500 мкл.
Клетки трансфицировали путем инкубирования при 37оС в течение 4 часов. Затем среду для трансфекции удаляли и клетки промывали, после чего в них добавляли среду, содержащую сыворотку. Эти клетки культивировали в течение различных периодов времени в пределах от 0 до 72 часов.
Пример 6: In vitro-модель: экстракция РНК и синтез кДНК
Выделение полноразмерной РНК
Полноразмерную РНК выделяли либо с использованием мини-набора RNeasy (Qiagen саt № 74104), либо с использованием реагента тризола (Life Technologies саt № 15596). Для выделения РНК из клеточных линий, предпочтительным методом является метод с использованием набора RNeasy, а для выделения образцов ткани, предпочтительными методом является метод с использованием тризола.
Полноразмерную РНК выделяли из клеточных линий с использованием роботизированного устройства Qiagen RNA OРF Robot - BIO Robot 3000 в соответствии с протоколом, рекомендованным производителем.
Образцы тканей гомогенизировали и полноразмерную РНК выделяли с использованием реагента тризола в соответствии с протоколом, рекомендованным производителем.
Синтез первой цепи
Синтез первой цепи проводили с использованием набора, содержащего обратную транскриптазу OmniScript Reverse Transcriptase kit (саt #205113, Qiagen) в соответствии с инструкциями производителя.
Для каждого образца, 0,5 мкг полноразмерной РНК доводили до 12 мкл с использованием H2O, не содержащей РНКазы, и смешивали с 2 мкл poly(dT)12-18(2,5 мкг/мл)(Life Technologies, GibcoВRL, Roskilde, DK), 2 мкл dNTP-смеси (2 мМ каждого dNTP), 2 мкл 10×буфера RТ, 1 мкл ингибитора РНКазы RNAguardТМ (33,3 ед/мл) (саt #27-0816-01, Amersham Pharmacia Biotech, Ноrsholm, DK) и 1 мкл обратной транскриптазы OmniScript (4 ед/мкл), а затем инкубировали при 37оС в течение 60 минут и фермент подвергали термоинактивации при 93°С в течение 5 минут.
Пример 7: In vitro-модель: анализ на ингибирование олигонуклеотидами экспрессии Bcl-2, проводимый с помощью ПЦР в режиме реального времени
Модуляция экспрессии Bcl-2 антисмысловыми олигонуклеотидами может быть проанализирована различными методами, известными специалистам. Так, например, уровни мРНК Bcl-2 могут быть количественно оценены с помощью, например, Вестерн-блот-анализа или количественной ПЦР. В настоящем изобретении предпочтительной является количественная ПЦР в режиме реального времени. Анализ РНК может быть проведен исходя из полноразмерной клеточной РНК или мРНК.
Методы выделения РНК и анализ РНК, такой как Вестерн-блот-анализ, являются рутинными и описаны, например, в публикации Current Protocols in Molecular Biology, John Wiley and Sons.
Количественный анализ в режиме реального времени (ПЦР) обычно проводят с использованием коммерчески доступной ПЦР-системы детекции в режиме реального времени iQ Multi-Color, поставляемой BioRad Laboratories.
Анализ уровней мРНК Bcl-2, проводимый с помощью количественной ПЦР в режиме реального времени
Количественный анализ уровней мРНК проводили с помощью количественной ПЦР с использованием ПЦР-системы детекции iQ Multi-Color Real Time PCR Detection System (BioRad) в соответствии с инструкциями производителя.
Количественная ПЦР в режиме реального времени представляет собой хорошо известный метод и описана, например, Heid et al., Real time quantitative PCR, Genome Research (1996), 6:986-994.
Смесь для проведения количественной ПЦР (Platinum Quantitative PCR SuperMix UDG 2× PCR Master) получали от Invitrogen, cat.# 11730. Праймеры и зонды TaqMan® получали от фирмы MWG-Biotech AG, Ebersberg, Germany.
Зонды и праймеры для человеческого Bcl-2 конструировали для гибридизации с последовательностью человеческого Bcl-2 с использованием опубликованных данных для этой последовательности.
Для человеческого Bcl-2 использовали следующие ПЦР-праймеры:
прямой праймер: 5'-catgtgtgtggagagcgtcaa-3' (конечная концентрация в анализе: 0,6 мкМ)(SEQ ID NO:62)
обратный праймер: 5'-gccggttcaggtactcagtca-3'(конечная концентрация в анализе: 0,6 мкМ)(SEQ ID NO:63), и ПЦР-зонд: 5'-FАМ-cctggtggacaacatcgccctgt-TAMRA 3'(конечная концентрация в анализе: 0,1 мкМ)(SEQ ID NO:64).
Количество мРНК глицеральдегид-3-фосфат-дегидрогеназы (GAPDH) использовали в качестве эндогенного контроля для нормализации любой дисперсии между препаратами образцов.
Содержание мРНК GAPDH в человеческом образце оценивали с использованием аналитического реагента человеческого GAPDH ABI Prism Pre-Developed TaqMan Assay Reagent (Apрlied Biosystems cat. № 4310884Е) в соответствии с инструкциями производителя.
ПЦР в режиме реального времени
кДНК, полученную в результате синтеза первой цепи, проведенного как описано выше, 2-20-кратно разводили и анализировали с помощью количественной ПЦР, проводимой в режиме реального времени. Праймеры и зонды смешивали с 2 х Platinum Quantitative PCR SuperMix UDG (cat.# 11730, Invitrogen) и добавляли к 3,3 мкл кДНК до конечного объема 25 мкл. Каждый образец анализировали с тремя повторениями. Анализ с 2-кратным разведением кДНК, которую получали из материала, выделенного из клеточной линии, экспрессирующей нужную РНК, осуществляли путем построения стандартных кривых для анализов. Для не-матричного контроля, вместо кДНК использовали стерильную H2O. ПЦР осуществляли в следующем режиме: 50°С, 2 минуты; 95°С, 10 минут, а затем 40 циклов: 95°С, 15 секунд, 60°С, 1 минута.
Относительные количества последовательности мРНК-мишени определяли исходя из вычисленного порогового цикла с использованием программы для детекции iCycler iQ Real Time PCR Detection System (см. таблица 3).
Пример 8: In vitro анализ: вестерн-блот-анализ уровней белка Bcl-2
Уровни белка Bcl-2 количественно оценивали различными хорошо известными методами, такими как иммунопреципитация, Вестерн-блот-анализ (иммуноблоттинг), ELISA, РИА (радиоиммуноанализ) или клеточный сортинг с активацией флуоресценции (FAСS) и т.п. Антитела против Bcl-2 могут быть идентифицированы и получены из различных источников, таких как Upstate Вiotechnologies (Lake Placid, USA), Novus Biological (Littleton, Colorado), Santa Cruz Biotechnology (Santa Cruz, California), DAKO (Glostrup, Denmark), либо они могут быть получены стандартными методами продуцирования антител.
Вестерн-блоттинг:
Влияние олигонуклеотидов Bcl-2 на уровни белка Bcl-2 in vitro определяли с помощью Вестерн-блот-анализа.
Клетки трансфицировали как описано в примере 5. Через 0-72 часа после трансфекции, клетки собирали и подвергали лизису в буфере, содержащем 2,5% ДСН, 5 мМ DТТ и 6М мочевину, в который были добавлены таблетки смеси ингибиторов протеазы (Roche). Концентрацию общего белка измеряли с использованием реагента Брэдфорда. 150 мкг общего белка подвергали электрофорезу в 12% бис-трис-гелях в буфере МОРS и блотировали на ПВДФ-мембранах в соответствии с рекомендациями производителя (Invitrogen). После инкубирования в течение ночи в блокирующем буфере (Invitrogen), мембраны инкубировали в течение двух часов с моноклональным антителом против bcl-2 (DАКО) и антителом против сурвивина (Novus Вiological 500-205, клон 60.11) или против тубулина (NeoMarkers), а затем инкубировали в течение одного часа со “вторыми” антителами. Для визуализации Bcl-2, сурвивина или тубулина использовали набор для хромогенной иммунодетекции (Invitrogen). Альтернативно, мембрану инкубировали с ПХ-конъюгированными мышиными иммуноглобулинами (DАКО), а затем инкубировали с реагентом ЕСL+ Plus (Amersham) и визуализировали с использованием системы детекции хемилюминесценции VersaDoc. См. фиг.1, 2А, 2В и 2С. На фиг.6 проиллюстрирована продолжительность воздействия SEQ ID NO:15 на белок Bcl-2. В таблице 2 представлены величины хемилюминесценции для геля при концентрации соединений 10 нМ и 100 нМ (гель не указан). На фиг.2А показан гель из аналогичного эксперимента, но с другими дозами (1 нМ и 5 нМ).
| Таблица 2 | |
| Олигомерное соединение и концентрация | Количество Bcl-2 (%), нормализованное на SEQ ID NO:56, 10 нМ |
| SEQ ID NO:56 (эталон), 10 нМ | 100 |
| SEQ ID NO:56 (эталон), 100 нМ | 72 |
| SEQ ID NO:2, 10 нМ | 33 |
| SEQ ID NO:2, 100 нМ | 4 |
Пример 9: In vitro-анализ: ингибирование экспрессии человеческого Bcl-2 антисмысловыми олигонуклеотидами
В соответствии с настоящим изобретением была сконструирована серия олигонуклеотидов для их гибридизации со специфической областью мРНК человеческого Bcl-2, то есть с областью, расположенной возле кодона инициации трансляции. Олигонуклеотиды с различной структурой и длиной представлены в таблице 1. Олигомерные соединения оценивали на их потенциальный дефицит Bcl-2 в 15PC3 и 518А2 посредством трансфекции в эти клеточные линии. Мониторинг стабильности транскрипта Bcl-2 проводили с помощью ПЦР в режиме реального времени и полученные данные нормализовали на уровень стабильности транскрипта GAPDH. В таблице 3 приводится сравнение эффективности ряда соединений с эффективностью SEQ ID NO:56 (облимерсен-натрия; полностью модифицированного фосфортиоата; контроль).
| Таблица 3 Уровень экспрессии мРНК Bcl-2 определяли с помощью ПЦР в режиме реального времени. Клетки 15PC3 или 518А2 трансфицировали указанной концентрацией олигомерного соединения, и после 24-часового инкубирования, РНК экстрагировали. Результаты ингибирования приводятся по сравнению с обработанным контролем |
||||||
| Клеточная линия | 15PC3 | 518А2 | ||||
| SEQ ID NO: | Концентрация (нМ) | |||||
| 1 | 5 | 25 | 1 | 5 | 25 | |
| 56 (эталон) | 0% | 70% | 88% | 42% | 66% | |
| 59 (эталон) | 29% | 70% | 90% | |||
| 1 | 72% | 87% | 91% | |||
| 2 | 74% | 92% | 89% | 72% | 89% | |
| 3 | 34% | 45% | 84% | |||
| 4 | 53% | 82% | 90% | 78% | 90% | |
| 8 | 61% | 80% | ND | 44% | 60% | 82% |
| 12 | 62% | 92% | 91% | 78% | 92% | |
| 13 | 36% | ND | 60% | % | ||
| 15 | 24% | 79% | 89% | 72% | 84% | |
| 18 | 0% | 71% | 88% | |||
| 19 | 0% | 0% | 37% | |||
| 21 | 23% | 80% | 89% | 74% | 86% | |
| 23 | 45% | 62% | 70% | |||
| 24 | 39% | 85% | 92% | 70% | 82% | |
| 57 | 0% | 37% | 91% | 61% | 81% | |
| 16 | 18% | 36% | 68% | |||
| 9 | 26% | ND | 78% | |||
ND-не определяли
Пример 10: Индуцирование апоптоза антисмысловыми LNA-олигомерными соединениями
Клетки высевали до плотности 12000 клеток на лунку в белые 96-луночные планшеты (Nunc 136101) в DMEM за день до трансфекции. На следующий день, клетки один раз промывали в предварительно нагретой среде OptiMEM с последующим добавлением 72 мкл среды OptiMEM, содержащей 5 мкг/мл липофектамина 2000 (Invitrogen). Клетки инкубировали в течение 7 минут, а затем добавляли 18 мкл олигонуклеотидов, разведенных в OptiMEM. Конечная концентрация олигонуклеотида составляла от 0,2 нМ до 25 нМ. После обработки в течение 4 часов, клетки промывали в OptiMEM и добавляли 50 мкл среды DMEM, содержащей сыворотку. После обработки олигомерным соединением, клетки оставляли для восстановления на указанный период времени, а затем их удаляли из CO2-инкубатора и уравновешивали до комнатной температуры в течение 15 минут. К этим клеткам в 96-луночном планшете непосредственно добавляли равный объем смеси в высокой степени чувствительной каспазы 3/реагента 7-GloТМ (Promega), и по истечении лаг-периода = 1 мин, планшеты инкубировали в течение 60 минут, а затем регистрировали люминесценцию (люциферазную активность) на приборе Luminoskan Ascent, поставляемом Thermo Labsystems. Люциферазную активность измеряли в относительных световых единицах в секунду (ОСЕ/с). Данные обрабатывали с помощью компьютерной программы Ascent 2,6 и строили графики в программе Excel (см. фиг.3А и 3В).
Проточный цитометрический анализ с использованием аннексина V-FITC: 0,4×106 клеток НеLa высевали в колбы Т25 за день до трансфекции. В день трансфекции клетки один раз промывали при 37оС в среде OptiMEM с последующим добавлением 2,8 мл среды OptiMEM, содержащей 5 мкг/мл липофектамина 2000 (Invitrogen). Клетки инкубировали в течение 7 минут, а затем добавляли 700 мкл олигонуклеотидов, разведенных в среде OptiMEM до конечной концентрации олигонуклеотидов 5 нМ или 25 нМ. Клетки, трансфицированные без олигонуклеотида, служили в качестве контроля. После обработки в течение 4 часов, клетки промывали в OptiMEM и добавляли 3 мл культуральной среды. После обработки клеток олигонуклеотидами эти клетки оставляли для восстановления на 48 часов, а затем их собирали (путем соскабливания) и два раза промывали в PBS. 0,2×106 клеток инкубировали с 5 мкл аннексина V-FITC и 10 мкл иодида пропидия (РI - 10 мг/мл) и инкубировали в течение 15 минут при комнатной температуре в темноте.
Трансфицированные клетки инкубировали с очищенным рекомбинантным аннексином V, в результате чего блокировалось связывание с аннексином V, а затем добавление аннексина V-FITC применяли для иллюстрации специфичности и селективности окрашивания. Кроме того, в качестве позитивного контроля использовали клетки НеLa (0,5 мкг/мл), индуцированные TRAIL (Аро2L) (данные не приводятся). (см. фиг.3С и 3D).
Пример 11: Ингибирование Bcl-2 в пролиферирующихся раковых клетках под действием антисмысловых олигонуклеотидов
Клетки высевали до плотности 12000 клеток на лунку в белые 96-луночные планшеты (Nunc 136101) в DMEM за день до трансфекции. На следующий день клетки один раз промывали в предварительно нагретой среде OptiMEM с последующим добавлением 72 мкл OptiMEM, содержащей 5 мкг/мл липофектамина 2000 (Invitrogen). Клетки инкубировали в течение 7 минут, а затем добавляли 18 мкл олигонуклеотидов, разведенных в OptiMEM. Конечная концентрация олигонуклеотида составляла от 5 нМ до 100 нМ. После обработки в течение 4 часов клетки промывали в OptiMEM и добавляли 100 мкл DMEM, содержащей сыворотку. После обработки олигомерным соединением клетки оставляли для восстановления на указанный период времени и жизнеспособные клетки оценивали путем добавления 20 мкл тетразолиевого соединения [3-(4,5-диметил-2-ил)-5-(3-карбоксиметоксифенил)-2-(4-сульфофенил)-2Н-тетразолия, внутренней соли; MTS] и реагента, образующего электронные связи (этосульфата феназина; PES)(анализ на пролиферацию клеток в одном растворе CellTiter 96®
AQueous, Promega) на 100 мкл DMEM. Жизнеспособные клетки оценивали при 490 нм на устройстве Powerwave (Biotek Instruments). Затем строили график (ΔOD/ч) скорости роста в зависимости от концентрации олигомерного соединения (см. фиг.4 и 5).
Пример 12: In vivo-модель: ингибирование роста опухолевых клеток in vivo в модели человеческого ксенотрансплантата PC-3 после системной обработки антисмысловыми олигонуклеотидами
Бестимусных голых самок мышей Balb/с в возрасте 6 недель закупали у М&B, Denmark и оставляли для акклиматизации, по меньшей мере, за одну неделю до начала проведения экспериментов. Человеческие раковые клетки, обычно 3×106 клеток, суспендированных в 300 мкл Matrigel (BD Bioscience), подкожно инъецировали мышам в бок. В случае моделей с двойным ксенотрансплантатом, имплантировали две опухоли, по одной в каждый бок. При устойчивом росте опухоли, через 5-12 дней после инъекции опухолевых клеток, внутрибрюшинно вводили различные антисмысловые олигонуклеотиды в количестве от 0,01 до 20 мг/кг/день в течение 30 дней ежедневно, два раза в день, через два или три дня или еженедельно. Контрольным животным вводили только физиологический раствор в то же самое время и тем же самым способом. В каждую экспериментальную группу включали, по меньшей мере, 5 мышей. Противоопухолевую активность оценивали по ингибированию клеточного роста, измеренному по объему опухоли. Рост опухоли регулярно оценивали путем измерения 2 перпендикулярных диаметров опухоли. Объем опухоли вычисляли по формуле, указанной в работе Teicher B.A., Tumour Models in Cancer Research. Humana Press, NJ, USA 2002, p.596, а именно: объем опухоли (мм3)=L×W2×0,5), где L означает больший диаметр, а W означает диаметр опухоли, перпендикулярный L. По окончании обработки животных умерщвляли и измеряли массу опухоли. Средний объем и массу опухоли животных в соответствующей группе сравнивали с использованием критерия Манна-Уитни. Все анализы проводили с помощью программы SPSS, version 11,0 для Window. См. фиг.7А, 7В, 7С и 7D.
Пример 13: In vivo-анализ: ингибирование Bcl-2 в опухолевых клетках in vivo в модели человеческого ксенотрансплантата PC-3 после системной обработки антисмысловыми олигонуклеотидами
Бестимусных голых самок мышей Balb/с в возрасте 6 недель закупали у М&B, Denmark и оставляли для акклиматизации, по меньшей мере, за одну неделю до начала проведения экспериментов. Человеческие раковые клетки, обычно 3×106 клеток, суспендированных в 300 мкл Matrigel (BD Bioscience), подкожно инъецировали мышам в бок. Для создания моделей с двойным ксенотрансплантатом имплантировали две опухоли, по одной в каждый бок. При устойчивом росте опухоли, обычно, через 5-12 дней после инъекции опухолевых клеток, внутривенно или внутрибрюшинно вводили различные антисмысловые олигонуклеотиды в количестве от 0,01 до 20 мг/кг/день в течение 30 дней ежедневно, два раза в день, через два или три дня или еженедельно. Контрольным животным вводили только физиологический раствор в то же самое время и тем же самым способом. В каждую экспериментальную группу включали, по меньшей мере, 5 мышей. По окончании обработки мышей анестезировали и опухоли вырезали, а затем сразу замораживали в жидком азоте.
Для того чтобы определить, обладают ли антисмысловые олигонуклеотиды ингибирующим действием на уровни белка, проводили Вестерн-блот-анализ. Опухоли гомогенизировали в буфере для лизиса (то есть, 20 мМ Трис-HCl [рН 7,5]; 2% тритона Х-100; 1/100 объема смеси ингибиторов протеазы серии III (Calbiochem); 1/100 объема смеси ингибиторов протеазы серии II (Calbiochem) при 4°С с использованием роторного гомогенизатора. На 100 мг опухолевой ткани использовали 500 мкл буфера для лизиса. Опухолевые лизаты для мышей каждой группы объединяли и центрифугировали при 13000×g в течение 5 минут при 4°С для удаления дебриса ткани. Концентрации белка в опухолевых экстрактах определяли с использованием набора, содержащего реагент для анализа белка ВСА (Pierce, Rockford).
Экстракты белка (50-100 мкг) фракционировали с помощью электрофореза в ДСН-ПААГ в градиентном 4-20%-геле и переносили на ПВДФ-мембраны, а затем визуализировали путем окрашивания аминовым черным. Экспрессию Bcl-2 детектировали с использованием антитела sc-509 против человеческого Bcl-2 (Santa Cruz Biotechnology, Inc. Santa Cruz, CA, US) или антитела против человеческого Bcl-2 (клон 101, Zymed), а затем с использованием конъюгированного с пероксидазой хрена антитела против козьих IgG (DAKO). Иммунореактивность детектировали с помощью реагента ЕСL Plus (Amersham Biotech) и количественно оценивали с помощью оптической системы VersaDoc 5000 (Bio-Rad).
Пример 14: In vivo-испытание Bcl-2-ингибирующего LNA-олигомерного соединения, проводимое по сравнению с современным клинически протестированным средством облимерсен-натрием (SEQ ID NO:56) на мышах SCID с моделью ксенотрансплантата человеческой меланомы 518А2
Самок мышей scid/scid (SCID) С.В.-17 в возрасте 4-6 недель, не содержащих патогенов и обследованных на отсутствие повреждений на теле, получали от фирмы Harlan & Winkelmann (Borchen, Germany). Животных помещали в микроизоляционные клетки на полки шкафа с ламинарным потоком и этим животным давали обработанную в автоклаве пищу и воду ad libitum. Мышам SCID в левый нижний бок подкожно (s.c.) инъецировали 1,5×107 клеток человеческой меланомы 518 А2, ресуспендироанных в 200 мкл PBS. Через 10 дней у всех мышей развивались пальпируемые подкожные опухоли, и этих мышей произвольно распределяли по группам обработки или контроля и начинали обработку. Для непрерывного s.c. введения мышей анестезировали и в параспинальный карман подкожно имплантировали миниосмотические насосы (Alzet 2002, Alza, Moutain View, CA, USA), наполненные олигонуклеотидами в физиологическом растворе или физиологическим раствором, используемым в качестве носителя-контроля.
Противоопухолевая активность. SEQ ID NO:56 (эталон) вводили с помощью миниосмотических насосов s.c. в течение 14 дней в стандартной дозе 7 мг/кг/день по стандартной схеме. LNA-олигомерное соединение SEQ ID NO:15 вводили s.c. в дозах 7, 3,5 и 1,75 мг/кг путем непрерывного вливания в течение 14 дней. Животных, обработанных физиологическим раствором, использовали в качестве контроля.
Главными определяемыми параметрами были рост опухоли в течение определенного периода времени, измеряемый с помощью штангенциркуля, и масса опухоли, измеряемая по окончании экспериментов.
На фиг.8А, 8В, 9, 10А, 10В и 10С представлены данные для SEQ ID NO:15 при 1,75 мг/кг. Увеличение концентрации (7 и 3,5 мг/кг) не приводило к дальнейшему снижению массы или объема опухоли, что указывает на то, что соединение SEQ ID NO:15 имеет кривую доза-ответ при более низких концентрациях.
На фиг.11 представлены данные для SEQ ID NO:8 при 1 и 7 мг/кг, и данные для SEQ ID NO:15 и SEQ ID NO:56 при 7 мг/кг. Введение соединения SEQ ID NO:8 и контрольных соединений давало аналогичную картину, и какой-либо потери массы тела за период проведения эксперимента не наблюдалось.
Пример 15: Стабильность SEQ ID NO:15 и SEQ ID NO:8 в плазме крыс
Стабильность соединения SEQ ID NO:15 в плазме крыс (самцов NtacSD, Li-гепарин (Taconic, M&B)) после его введения в концентрации 20 мкМ при 37оС оценивали в различные периоды времени: 0, 4, 24 и 48 часов после введения. SEQ ID NO:56 соответствует SEQ ID NO:56 (эталон). Были также протестированы и другие олигонуклеотиды SEQ ID NO:20 и 16. Олигонуклеотиды, соответствующие n-1, n-2 и n-3 SEQ ID NO:15 (с 3'-конца), служили в качестве контроля, который позволял идентифицировать возможные фрагменты, образующиеся после гидролиза SEQ ID NO:15. Был также включен коммерчески доступный “лэддер” (10- и 20-мер были видимыми на ДСН-ПААГ-геле) (см. фиг.12А).
Стабильность соединения SEQ ID NO:8 в плазме крыс (самцов NtacSD, Li-гепарин (Taconic, M&B)) после его введения его в концентрации 20 мкМ при 37оС оценивали в различные периоды времени: 0, 4, 24 и 48 часов после введения. SEQ ID NO:56 соответствует SEQ ID NO:56 (эталон). Был также протестирован и другой олигонуклеотид SEQ ID NO:9. Олигонуклеотиды, соответствующие n-1, n-2 и n-3 SEQ ID NO:8 (с 3'-конца), служили в качестве контроля, который позволял идентифицировать возможные фрагменты, образующиеся после гидролиза SEQ ID NO:8. Был также включен коммерчески доступный “лэддер” (10- и 20-мер были видимыми на ДСН-ПААГ-геле) (см. фиг.12В).
Олигомерные соединения, например SEQ ID NO:8 и SEQ ID NO:15, синтезировали как олигонуклеотиды с ДНК, которая в 3'-положении связана со смежной LNA фосфортиоатной связью. 3'-ДНК-часть может быть отщеплена экзонуклеазами. Продуктом отщепления является укороченное на 1 нуклеотид (N-1) олигомерное соединение (SEQ ID NO:35), которое, по сравнению с полноразмерной родительской молекулой, имело, в основном, повышенную резистентность к расщеплению нуклеазой. N-1-соединения (например, SEQ ID NO:35) полностью сохраняли активность, например, SEQ ID NO:8 (см. фиг.2С).
Пример 16: Анализ времени полужизни SEQ ID NO:15 в ткани печени и почек
90 самок мышей NМRI (прибл. 30 г) распределяли по группам из 5 животных, и этим животным внутривенно вводили 25 мг/кг SРС 2996 (10 мл/кг, 2,5 мг/мл) в течение 30 сек. Контрольной группе вводили дозу 0,9% физиологического раствора. Затем для животных этих групп регистрировали данные через 30 минут, 6 ч, 24 ч, 48 ч, 72 ч и 96 ч после инъекции. После этого брали образцы тканей и приготавливали в виде РНК-препарата.
Экстракция олигонуклеотида из ткани
Приблизительно 100 мг ткани механически гомогенизировали в 500 мкл буфера для экстракции (0,5% Igepal СА-630, 25 мМ трис, рН 8,0, 25 мМ EDTA, 100 мМ NаСl, содержащем 1 мг/мл РНКазы А) и инкубировали в течение ночи при 37оС. В 500 мл образца добавляли контрольный олигонуклеотид и экстрагировали путем добавления 1 мл смеси фенол-изоамил-хлороформ (25:1:24 (об/об/об)). Водную фазу переносили в новую пробирку и снова экстрагировали. Если это необходимо, то экстракт лиофилизовали.
IEX-ВЭЖХ-анализ олигонуклеотида, экстрагированного из образцов тканей
Образец объемом в 50 мкл выделяли на колонке DNAPac РА-100 (2×50 мм, Dionex), снабженной предохранительной колонкой DNAPac РА-100 (2×50 мм, Dionex). Эти колонки нагревали до 40°С. Скорость потока составляла 0,25 мл/мин, а детекцию осуществляли на длине волны 260 нм. Градиент подвижных фаз А: трис (20 мМ), EDTA (1 мМ) и перхлорат натрия (10 мМ), рН 7,6; В: трис (20 мМ), EDTA (1 мМ) и перхлорат натрия (1 М), рН 7,6 (0-13 мин, А: 20%, В: 20%; 14-18 мин, А: 40%, В: 60%; 22-28 мин, А: 0%, В: 1000%; 33-38 мин, А: 80%, В: 20%).
На фиг.13 показано время полужизни SEQ ID NO:15 в ткани печени и почек у мышей NМRI после внутривенного введения одной дозы (25 мг/кг).
Claims (30)
1. Олигомерное соединение, имеющее длину 10-30 нуклеиновых оснований, которое понижает экспрессию человеческого гена Вс1-2, которое представляет собой мишень-связывающий домен, комплементарный отрезку из 10-18 последовательных нуклеотидов области от положения основания 1459 (5') до 1476 (3') мРНК человеческого Вс1-2 (HUMBcl2A (номер доступа M13994) в базе данных GenBank), кроме максимум одного ошибочного спаривания с указанным участком мРНК человеческого Вс1-2, где указанный связывающийся с мишенью домен имеет формулу
5'-[(ДНК/РНК)0-1-(LNA/LNA*)2-7-(ДНК/РНК/LNA*)4-14- (LNA/LNA*)2-7-(ДНК/PHK)0-1]-3',
где LNA означает нуклеотид LNA формулы 1
где В составляет нуклеиновое основание, Z* выбран из межнуклеозидной связи и концевой группы, а Z выбран из связи с межнуклеозидной связью предшествующего нуклеотида/нуклеозида и концевой группы, и LNA* означает нуклеотидный аналог LNA формулы 2
где X и Y независимо выбраны из -O-, -S-, -N(H)-, -N(R)-, -СН2- или - СН- (если они являются частью двойной связи), -СН2-O-, -СН2-S-, -CH2-N(H)-, -CH2-N(R)-, -СН2-СН2- или -СН2-СН- (если они являются частью двойной связи), -СН=СН-, где R выбран из водорода и C1-4-алкила; где, когда один из Z или Y представляет собой кислород, Z и Y различны; и где асимметрические группы могут присутствовать в любой ориентации; и где В составляет нуклеиновое основание, Z* выбран из межнуклеозидной связи и концевой группы, а Z выбран из связи с межнуклеозидной связью предшествующего нуклеотида/нуклеозида и концевой группы; где указанный мишень-связывающий домен содержит, по меньшей мере, два нуклеотида LNA или нуклеотидных аналога LNA, связанных фосфортиоатной группой (-O-P(O,S)-O-); и где область от положения основания 1459 (5') до 1476 (3') мРНК человеческого Bcl-2 (HUMBcl2A (номер доступа M13994) в базе данных GenBank) имеет следующую последовательность: АТGGСGСАСGСТGGGАGА.
5'-[(ДНК/РНК)0-1-(LNA/LNA*)2-7-(ДНК/РНК/LNA*)4-14- (LNA/LNA*)2-7-(ДНК/PHK)0-1]-3',
где LNA означает нуклеотид LNA формулы 1
где В составляет нуклеиновое основание, Z* выбран из межнуклеозидной связи и концевой группы, а Z выбран из связи с межнуклеозидной связью предшествующего нуклеотида/нуклеозида и концевой группы, и LNA* означает нуклеотидный аналог LNA формулы 2
где X и Y независимо выбраны из -O-, -S-, -N(H)-, -N(R)-, -СН2- или - СН- (если они являются частью двойной связи), -СН2-O-, -СН2-S-, -CH2-N(H)-, -CH2-N(R)-, -СН2-СН2- или -СН2-СН- (если они являются частью двойной связи), -СН=СН-, где R выбран из водорода и C1-4-алкила; где, когда один из Z или Y представляет собой кислород, Z и Y различны; и где асимметрические группы могут присутствовать в любой ориентации; и где В составляет нуклеиновое основание, Z* выбран из межнуклеозидной связи и концевой группы, а Z выбран из связи с межнуклеозидной связью предшествующего нуклеотида/нуклеозида и концевой группы; где указанный мишень-связывающий домен содержит, по меньшей мере, два нуклеотида LNA или нуклеотидных аналога LNA, связанных фосфортиоатной группой (-O-P(O,S)-O-); и где область от положения основания 1459 (5') до 1476 (3') мРНК человеческого Bcl-2 (HUMBcl2A (номер доступа M13994) в базе данных GenBank) имеет следующую последовательность: АТGGСGСАСGСТGGGАGА.
2. Соединение по п.1, где, по меньшей мере, 70% нуклеотидных связей в мишень-связывающем домене представляют собой фосфортиоатные группы (-O-P(O,S)-O-).
3. Соединение по п.2, где все нуклеотидные связи в олигомерном соединении представляют собой фосфортиоатные группы.
4. Соединение по п.1, где 10-50% нуклеиновых оснований в мишень-связывающем домене представляют собой нуклеиновые основания LNA нуклеотидов.
5. Соединение по любому из предыдущих пунктов, где мишень -связывающий домен имеет формулу 5'-[LNA2-7-(ДНК)4-14-LNA2-7-(ДНК/РНК)]-3'.
6. Соединение по любому из пп.1-4, где мишень-связывающий домен имеет формулу 5'-[(ДНК/РНК)-LNA2-7-(ДНК)4-14-LNA2-7-(ДНК/РНК)]-3'.
7. Соединение по любому из пп.1-4, где мишень-связывающий домен имеет формулу 5'-[(ДНК/РНК)-LNA2-7-(ДНК)4-14-LNA2-7-3'.
8. Соединение по любому из пп.1-4, где мишень-связывающий домен имеет формулу 5'-[LNA2-7-(ДНК)4-14-LNA2-7]-3'.
9. Соединение по любому из пп.1-4, где 10-50% нуклеиновых оснований в мишень-связывающем домене представляют собой нуклеиновые основания нуклеотидного аналога LNA (LNA*).
10. Соединение по любому из пп.1-4, где мишень-связывающий домен комплементарен части области от положения основания 1459 (5') до 1476 (3') мРНК человеческого Bcl-2 (HUMBcl2A (номер доступа Ml3994) в базе данных GenBank).
11. Соединение по п.10, где мишень-связывающий домен выбран из группы, состоящей из SEQ ID NO:1, 2, 3, 4, 5, 6, 7, 8, 12, 13, 14, 35, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51 и 52.
12. Соединение по п.11, где мишень-связывающий домен представляет собой SEQ ID NO:8.
13. Соединение по п.12, где мишень-связывающий домен представляет собой SEQ ID NO:35.
14. Соединение по любому из пп.1-4, где мишень-связывающий домен комплементарен части области от положения основания 1459 (5') до 1476 (3') мРНК человеческого Bcl-2 (HUMBcl2A (номер доступа M13994) в базе данных GenBank), с которой он специфически гибридизуется, за исключением 1 некомплементарного нуклеинового основания.
15. Соединение по п.14, где мишень-связывающий домен содержит подпоследовательность CCCAXCGT, где Х не является G (гуанином).
16. Соединение по п.15, где мишень-связывающий домен выбран из группы, состоящей из SEQ ID NO:15, 17, 18, 19, 21, 22, 23, 24, 25, 26, 27, 28, 29, 53, 54 и 55.
17. Соединение по п.16, где мишень-связывающим доменом является SEQ ID NO:15.
18. Соединение по п.16, где мишень-связывающим доменом является SEQ ID NO:29.
19. Соединение по п,1, где мишень-связывающий домен составляет полное олигомерное соединение.
20. Соединение по п.19, которое состоит из SEQ ID NO:15.
21. Соединение по п.1, которое состоит из последовательности CsTsCsCsCsasasCsgstsgsCsgsCsCsa, где заглавные буквы означают нуклеотиды LNA, строчные буквы означают нуклеотиды ДНК, подстрочный индекс «s» означает, что соседние нуклеотиды связаны фосфортиоатной группой, и где все LNA-C-мономеры представляют собой метил-С.
22. Соединение по п.1, где нуклеотиды LNA представляют собой нуклеотиды бета-D-окси-LNA.
23. Конъюгат, содержащий олигомерное соединение по любому из пп.1-22, и, по меньшей мере, один ненуклеотидный/неполинуклеотидный фрагмент, ковалентно связанный с указанным соединением, где ненуклеотидный/неполинуклеотидный фрагмент представляет собой лиганд, предназначенный для усиления поглощения конъюгата клетками по сравнению с антисмысловыми олигонуклеотидами.
24. Фармацевтическая композиция для лечения рака, содержащая олигомерное соединение по любому из пп.1-22 и фармацевтически приемлемый носитель.
25. Применение олигомерного соединения по любому из пп.1-22 для получения лекарственного средства для лечения ракового заболевания.
Приоритет по пунктам и признакам:
Приоритет по пунктам и признакам:
23.12.2003 по пп.1 (все, кроме 5'-концевого нуклеотида РНК/ДНК), 2-5, 9-10, 11 (в части SEQ ID NO:1-4, 8, 12, 13), 12, 14-15, 16 (в части SEQ ID NO:15, 17, 18, 19, 21-28), 17-22, 23 (все, кроме ненуклеотидного/неполинуклеотидного фрагмента), 24, 25.
31.03.2004 по пп.1 (в части 5'-концевого нуклеотида РНК/ДНК), 6-8, 23 (в части ненуклеотидного/неполинуклеотидного фрагмента).
07.07.2004 по пп.11 (в части SEQ ID NO:6, 7).
22.10.2004 по пп.11 (в части SEQ ID NO:9), 16 (в части SEQ ID NO:16).
23.12.2004 по пп.13, 16 (в части SEQ ID NO:20, 29, 53-55).
Applications Claiming Priority (16)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US53284403P | 2003-12-23 | 2003-12-23 | |
| DKPA200301929 | 2003-12-23 | ||
| DKPA200301929 | 2003-12-23 | ||
| US60/532,844 | 2003-12-23 | ||
| US55839204P | 2004-03-31 | 2004-03-31 | |
| DKPA200400517 | 2004-03-31 | ||
| US60/558,392 | 2004-03-31 | ||
| DKPA200400517 | 2004-03-31 | ||
| US58634004P | 2004-07-07 | 2004-07-07 | |
| DKPA200401069 | 2004-07-07 | ||
| DKPA200401069 | 2004-07-07 | ||
| US60/586,340 | 2004-07-07 | ||
| US62159404P | 2004-10-22 | 2004-10-22 | |
| DKPA200401629 | 2004-10-22 | ||
| US60/621,594 | 2004-10-22 | ||
| DKPA200401629 | 2004-10-22 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2006126643A RU2006126643A (ru) | 2008-01-27 |
| RU2377301C2 true RU2377301C2 (ru) | 2009-12-27 |
Family
ID=42727309
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2006126643/13A RU2377301C2 (ru) | 2003-12-23 | 2004-12-23 | ОЛИГОМЕРНОЕ СОЕДИНЕНИЕ, ПОНИЖАЮЩЕЕ ЭКСПРЕССИЮ ЧЕЛОВЕЧЕСКОГО ГЕНА Bcl-2, КОНЪЮГАТ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ПРИМЕНЕНИЕ ОЛИГОМЕРНОГО СОЕДИНЕНИЯ ДЛЯ ЛЕЧЕНИЯ РАКА |
Country Status (16)
| Country | Link |
|---|---|
| US (1) | US7622453B2 (ru) |
| EP (1) | EP1706489B9 (ru) |
| JP (1) | JP4642775B2 (ru) |
| KR (1) | KR20070006709A (ru) |
| CN (1) | CN100569945C (ru) |
| AT (1) | ATE467679T1 (ru) |
| AU (1) | AU2004303464B2 (ru) |
| BR (1) | BRPI0418104A (ru) |
| CA (1) | CA2550258A1 (ru) |
| DE (1) | DE602004027163D1 (ru) |
| DK (1) | DK1706489T3 (ru) |
| ES (1) | ES2344566T3 (ru) |
| IL (1) | IL176320A0 (ru) |
| NZ (1) | NZ548254A (ru) |
| RU (1) | RU2377301C2 (ru) |
| WO (1) | WO2005061710A1 (ru) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2649367C2 (ru) * | 2013-01-30 | 2018-04-02 | Ф. Хоффманн-Ля Рош Аг | Конъюгаты углевода и lna-олигонуклеотида |
Families Citing this family (121)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DK2284269T3 (en) | 2002-11-18 | 2017-10-23 | Roche Innovation Ct Copenhagen As | Antisense design |
| US7399853B2 (en) | 2003-04-28 | 2008-07-15 | Isis Pharmaceuticals | Modulation of glucagon receptor expression |
| US7807647B2 (en) * | 2004-06-01 | 2010-10-05 | Pronai Therapeutics, Inc. | Methods and compositions for cancer therapy |
| US8815599B2 (en) * | 2004-06-01 | 2014-08-26 | Pronai Therapeutics, Inc. | Methods and compositions for the inhibition of gene expression |
| US20050287667A1 (en) * | 2004-06-01 | 2005-12-29 | Pronai Therapeutics, Inc. | Methods and compositions for the inhibition of gene expression |
| WO2007035759A1 (en) * | 2005-09-19 | 2007-03-29 | Johnson & Johnson Pharmaceutical Research & Development L.L.C. | Modulation of glucocorticoid receptor expression |
| KR20080074101A (ko) * | 2005-09-19 | 2008-08-12 | 존슨 앤드 존슨 파머슈티컬 리서치 앤드 디벨로프먼트 엘엘씨 | 글루카곤 수용체 발현의 조절 |
| WO2007064853A2 (en) * | 2005-12-01 | 2007-06-07 | Pronai Therapeutics, Inc. | Locked nucleic acid oligonucleotides |
| EP1957044B1 (en) | 2005-12-01 | 2013-03-13 | Pronai Therapeutics, Inc. | Amphoteric liposome formulation |
| EP1971371B1 (en) | 2005-12-01 | 2015-08-05 | Pronai Therapeutics, Inc. | Cancer therapies and pharmaceutical compositions used therein |
| WO2007087113A2 (en) | 2005-12-28 | 2007-08-02 | The Scripps Research Institute | Natural antisense and non-coding rna transcripts as drug targets |
| AU2012216487B2 (en) * | 2006-04-03 | 2015-05-14 | Roche Innovation Center Copenhagen A/S | Pharmaceutical composition comprising anti-miRNA antisense oligonucleotides |
| EA201100811A1 (ru) * | 2006-04-03 | 2012-06-29 | Сантарис Фарма А/С | Фармацевтическая композиция |
| WO2007112753A2 (en) * | 2006-04-03 | 2007-10-11 | Santaris Pharma A/S | Pharmaceutical composition comprising anti-mirna antisense oligonucleotides |
| WO2007136988A2 (en) * | 2006-05-05 | 2007-11-29 | Isis Pharmaceuticals, Inc. | Compounds and methods for modulating expression of gccr |
| US20090023221A1 (en) * | 2006-05-19 | 2009-01-22 | Exigon A/S | Oligonucleotide probes useful for detection and analysis of microrna precursors |
| EP2410053B2 (en) * | 2006-10-18 | 2020-07-15 | Ionis Pharmaceuticals, Inc. | Antisense compounds |
| WO2008113830A1 (en) | 2007-03-22 | 2008-09-25 | Santaris Pharma A/S | Rna antagonist compounds for the inhibition of apo-b100 expression |
| US8580756B2 (en) | 2007-03-22 | 2013-11-12 | Santaris Pharma A/S | Short oligomer antagonist compounds for the modulation of target mRNA |
| DK2548962T3 (en) | 2007-09-19 | 2016-04-11 | Applied Biosystems Llc | Sirna sequence-independent modification formats to reduce off-target phenotype effects in RNAI and stabilized forms thereof |
| ES2689508T3 (es) | 2007-10-04 | 2018-11-14 | Roche Innovation Center Copenhagen A/S | Micromir |
| UA100253C2 (ru) * | 2007-11-26 | 2012-12-10 | Сантаріс Фарма А/С | Lna-антагонисты андрогенного рецептора |
| WO2009071681A2 (en) * | 2007-12-07 | 2009-06-11 | Santaris Pharma A/S | Rna antagonist compounds for the modulation of bcl-2 |
| US8361980B2 (en) | 2008-03-07 | 2013-01-29 | Santaris Pharma A/S | Pharmaceutical compositions for treatment of microRNA related diseases |
| EP2315832B1 (en) | 2008-08-01 | 2015-04-08 | Roche Innovation Center Copenhagen A/S | Micro-rna mediated modulation of colony stimulating factors |
| CA2739464C (en) | 2008-10-03 | 2020-03-31 | Opko Curna, Llc | Treatment of apolipoprotein-a1 related diseases by inhibition of natural antisense transcript to apolipoprotein-a1 |
| US20110218155A1 (en) * | 2008-10-10 | 2011-09-08 | Dana-Farber Cancer Institute, Inc. | Chemical modulators of pro-apoptotic bax and bcl-2 polypeptides |
| WO2010043582A1 (en) * | 2008-10-17 | 2010-04-22 | Santaris Pharma A/S | Method for the treatment of cancer |
| KR101866152B1 (ko) | 2008-12-04 | 2018-06-08 | 큐알엔에이, 인크. | 종양 억제 유전자에 대한 천연 안티센스 전사체의 억제에 의해 종양 억제 유전자 관련된 질환의 치료 |
| WO2010065671A2 (en) | 2008-12-04 | 2010-06-10 | Curna, Inc. | Treatment of vascular endothelial growth factor (vegf) related diseases by inhibition of natural antisense transcript to vegf |
| CN102317458B (zh) | 2008-12-04 | 2018-01-02 | 库尔纳公司 | 通过红细胞生成素(epo)天然反义转录物的抑制对epo相关疾病的治疗 |
| EP3009150B1 (en) | 2009-02-12 | 2019-11-13 | CuRNA, Inc. | Treatment of brain derived neurotrophic factor (bdnf) related diseases by inhibition of natural antisense transcript to bdnf |
| US9464287B2 (en) | 2009-03-16 | 2016-10-11 | Curna, Inc. | Treatment of nuclear factor (erythroid-derived 2)-like 2 (NRF2) related diseases by inhibition of natural antisense transcript to NRF2 |
| EP2408920B1 (en) | 2009-03-17 | 2017-03-08 | CuRNA, Inc. | Treatment of delta-like 1 homolog (dlk1) related diseases by inhibition of natural antisense transcript to dlk1 |
| JP5773535B2 (ja) | 2009-04-24 | 2015-09-02 | ロシュ・イノベーション・センター・コペンハーゲン・アクティーゼルスカブRoche Innovation Center Copenhagen A/S | インターフェロンに非応答性のhcv患者の治療のための医薬組成物 |
| CA2761142C (en) | 2009-05-06 | 2021-06-08 | Opko Curna, Llc | Treatment of tristetraproline (ttp) related diseases by inhibition of natural antisense transcript to ttp |
| EP2427553A4 (en) | 2009-05-06 | 2012-11-07 | Opko Curna Llc | TREATMENT OF LIPID TRANSPORT AND METABOLISM-RELATED DISEASES BY INHIBITING THE NATURAL ANTISENSE TRANSCRIPT AGAINST A LIPID TRANSPORT AND METABOLIC TREATMENT |
| CA3185821A1 (en) | 2009-05-08 | 2010-11-11 | Curna, Inc. | Treatment of dystrophin family related diseases by inhibition of natural antisense transcript to dmd family |
| NO2432881T3 (ru) | 2009-05-18 | 2018-04-14 | ||
| US8895527B2 (en) | 2009-05-22 | 2014-11-25 | Curna, Inc. | Treatment of transcription factor E3 (TFE3) and insulin receptor substrate 2(IRS2) related diseases by inhibition of natural antisense transcript to TFE3 |
| ES2618576T3 (es) | 2009-05-28 | 2017-06-21 | Curna, Inc. | Tratamiento de enfermedades relacionadas con un gen antivírico mediante la inhibición de una transcripción antisentido natural a un gen antivírico |
| CA2765509C (en) | 2009-06-16 | 2021-08-17 | Joseph Collard | Treatment of paraoxonase 1 (pon1) related diseases by inhibition of natural antisense transcript to pon1 |
| KR101801404B1 (ko) | 2009-06-16 | 2017-12-20 | 큐알엔에이, 인크. | 콜라겐 유전자에 대한 천연 안티센스 전사체의 억제에 의한 콜라겐 유전자 관련된 질환의 치료 |
| ES2618894T3 (es) | 2009-06-24 | 2017-06-22 | Curna, Inc. | Tratamiento de enfermedades relacionadas con el receptor del factor de necrosis tumoral 2 (tnfr2) por inhibición del transcrito natural antisentido para tnfr2 |
| CA2765815A1 (en) | 2009-06-26 | 2010-12-29 | Opko Curna, Llc | Treatment of down syndrome gene related diseases by inhibition of natural antisense transcript to a down syndrome gene |
| EP2456870A1 (en) | 2009-07-21 | 2012-05-30 | Santaris Pharma A/S | Antisense oligomers targeting pcsk9 |
| CA2768947C (en) | 2009-07-24 | 2018-06-19 | Opko Curna, Llc | Treatment of sirtuin (sirt) related diseases by inhibition of natural antisense transcript to a sirtuin (sirt) |
| EP2462229B1 (en) | 2009-08-05 | 2016-05-11 | CuRNA, Inc. | Treatment of insulin gene (ins) related diseases by inhibition of natural antisense transcript to an insulin gene (ins) |
| KR101827015B1 (ko) | 2009-08-11 | 2018-02-07 | 큐알엔에이, 인크. | 아디포넥틴(adipoq)에 대한 천연 안티센스 전사체의 억제에 의한 아디포넥틴(adipoq) 관련된 질환의 치료 |
| WO2011022606A2 (en) | 2009-08-21 | 2011-02-24 | Curna, Inc. | Treatment of 'c terminus of hsp70-interacting protein' (chip) related diseases by inhibition of natural antisense transcript to chip |
| WO2011031482A2 (en) | 2009-08-25 | 2011-03-17 | Curna, Inc. | Treatment of 'iq motif containing gtpase activating protein' (iqgap) related diseases by inhibition of natural antisense transcript to iqgap |
| ES2664591T3 (es) | 2009-09-25 | 2018-04-20 | Curna, Inc. | Tratamiento de enfermedades relacionadas con la filagrina (flg) mediante la modulación de la expresión y actividad del gen FLG |
| EP2513310B1 (en) | 2009-12-16 | 2017-11-01 | CuRNA, Inc. | Treatment of membrane bound transcription factor peptidase, site 1 (mbtps1) related diseases by inhibition of natural antisense transcript to mbtps1 |
| KR101891352B1 (ko) | 2009-12-23 | 2018-08-24 | 큐알엔에이, 인크. | 간세포 성장 인자(hgf)에 대한 천연 안티센스 전사체의 억제에 의한 hgf 관련 질환의 치료 |
| CA2782375C (en) | 2009-12-23 | 2023-10-31 | Opko Curna, Llc | Treatment of uncoupling protein 2 (ucp2) related diseases by inhibition of natural antisense transcript to ucp2 |
| EP2519633B1 (en) | 2009-12-29 | 2017-10-25 | CuRNA, Inc. | Treatment of nuclear respiratory factor 1 (nrf1) related diseases by inhibition of natural antisense transcript to nrf1 |
| RU2611186C2 (ru) | 2009-12-29 | 2017-02-21 | Курна, Инк. | ЛЕЧЕНИЕ ЗАБОЛЕВАНИЙ, СВЯЗАННЫХ С ОПУХОЛЕВЫМ БЕЛКОМ 63 (р63), ПУТЕМ ИНГИБИРОВАНИЯ ПРИРОДНОГО АНТИСМЫСЛОВОГО ТРАНСКРИПТА К р63 |
| RU2016115782A (ru) | 2009-12-31 | 2018-11-28 | Курна, Инк. | Лечение заболеваний, связанных с субстратом рецептора инсулина 2 (irs2), путем ингибирования природного антисмыслового транскрипта к irs2 и транскрипционному фактору е3 (tfe3) |
| DK2521784T3 (en) | 2010-01-04 | 2018-03-12 | Curna Inc | TREATMENT OF INTERFERON REGULATORY FACTOR 8- (IRF8) RELATED DISEASES BY INHIBITION OF NATURAL ANTISENCE TRANSCRIPT TO IRF8 |
| CN102822342B (zh) | 2010-01-06 | 2017-05-10 | 库尔纳公司 | 通过抑制胰腺发育基因的天然反义转录物而治疗胰腺发育基因相关疾病 |
| ES2664866T3 (es) | 2010-01-11 | 2018-04-23 | Curna, Inc. | Tratamiento de enfermedades relacionadas con la globulina fijadora de hormonas sexuales (shbg) mediante inhibición del transcrito antisentido natural a shbg |
| CN102782135A (zh) | 2010-01-25 | 2012-11-14 | 库尔纳公司 | 通过抑制rna酶h1的天然反义转录物而治疗rna酶h1相关疾病 |
| CN102844435B (zh) | 2010-02-22 | 2017-05-10 | 库尔纳公司 | 通过抑制吡咯啉‑5‑羧酸还原酶1(pycr1)的天然反义转录物而治疗pycr1相关疾病 |
| KR101877065B1 (ko) | 2010-04-02 | 2018-07-10 | 큐알엔에이, 인크. | 집락 자극 인자 3 (csf3)에 대한 자연 안티센스 전사체의 저해에 의한 집락 자극 인자 3 (csf3) 관련된 질환의 치료 |
| CA2795281A1 (en) | 2010-04-09 | 2011-10-13 | Curna, Inc. | Treatment of fibroblast growth factor 21 (fgf21) related diseases by inhibition of natural antisense transcript to fgf21 |
| EP2957636B1 (en) | 2010-05-03 | 2020-04-01 | CuRNA, Inc. | Treatment of sirtuin 3 (sirt3) related diseases by inhibition of natural antisense transcript to sirt3 |
| TWI586356B (zh) | 2010-05-14 | 2017-06-11 | 可娜公司 | 藉由抑制par4天然反股轉錄本治療par4相關疾病 |
| NO2576784T3 (ru) | 2010-05-26 | 2018-04-14 | ||
| CA2799207C (en) | 2010-05-26 | 2019-03-26 | Curna, Inc. | Treatment of atonal homolog 1 (atoh1) related diseases by inhibition of natural antisense transcript to atoh1 |
| ES2863526T3 (es) | 2010-06-23 | 2021-10-11 | Curna Inc | Tratamiento de enfermedades relacionadas con la subunidad alfa del canal de sodio (SCNA), controlado por voltaje, mediante inhibición de la transcripción antisentido natural a SCNA |
| WO2012009402A2 (en) | 2010-07-14 | 2012-01-19 | Opko Curna Llc | Treatment of discs large homolog (dlg) related diseases by inhibition of natural antisense transcript to dlg |
| RU2624048C2 (ru) | 2010-10-06 | 2017-06-30 | Курна, Инк. | Лечение заболеваний, связанных с геном сиалидазы 4 (neu4), путем ингибирования природного антисмыслового транскрипта гена neu4 |
| JP6049623B2 (ja) | 2010-10-22 | 2016-12-21 | カッパーアールエヌエー,インコーポレイテッド | α‐L‐イズロニダーゼ(IDUA)への天然アンチセンス転写物の阻害によるIDUA関連疾患の治療 |
| WO2012068340A2 (en) | 2010-11-18 | 2012-05-24 | Opko Curna Llc | Antagonat compositions and methods of use |
| CN103459599B (zh) | 2010-11-23 | 2017-06-16 | 库尔纳公司 | 通过抑制nanog的天然反义转录物而治疗nanog相关疾病 |
| EP3467109A1 (en) | 2011-02-08 | 2019-04-10 | Ionis Pharmaceuticals, Inc. | Oligomeric compounds comprising bicyclic nucleotides and uses thereof |
| RU2620980C2 (ru) | 2011-06-09 | 2017-05-30 | Курна, Инк. | Лечение заболеваний, связанных с фратаксином (fxn), путем ингибирования природного антисмыслового транскрипта fxn |
| WO2013022990A1 (en) | 2011-08-11 | 2013-02-14 | Isis Pharmaceuticals, Inc. | Selective antisense compounds and uses thereof |
| EP2753317B1 (en) | 2011-09-06 | 2020-02-26 | CuRNA, Inc. | TREATMENT OF DISEASES RELATED TO ALPHA SUBUNITS OF SODIUM CHANNELS, VOLTAGE-GATED (SCNxA) WITH SMALL MOLECULES |
| WO2013040429A1 (en) | 2011-09-14 | 2013-03-21 | Rana Therapeutics Inc. | Multimeric oligonucleotide compounds |
| CN108410868A (zh) | 2011-09-20 | 2018-08-17 | Ionis制药公司 | Gcgr表达的反义调节 |
| AU2012322788B2 (en) | 2011-10-11 | 2018-01-04 | The Brigham And Women's Hospital, Inc. | Micrornas in neurodegenerative disorders |
| BR112014009790A2 (pt) | 2011-10-25 | 2018-05-15 | Isis Pharmaceuticals Inc | composto para modulação antisense da expressão de gccr, seu uso e composição |
| CA2855362A1 (en) * | 2011-11-11 | 2013-05-16 | Santaris Pharma A/S | Compounds for the modulation of beta-catenin expression and uses thereof |
| CN104583405A (zh) | 2012-03-15 | 2015-04-29 | 科纳公司 | 通过抑制脑源神经营养因子(bdnf)的天然反义转录物治疗bdnf相关疾病 |
| EP3336189A1 (en) | 2012-04-20 | 2018-06-20 | Ionis Pharmaceuticals, Inc. | Oligomeric compounds comprising bicyclic nucleotides and uses thereof |
| CA2873779A1 (en) | 2012-05-16 | 2013-11-21 | Rana Therapeutics Inc. | Compositions and methods for modulating mecp2 expression |
| CA2873797A1 (en) | 2012-05-16 | 2013-11-21 | Rana Therapeutics Inc. | Compositions and methods for modulating utrn expression |
| BR112014028631A2 (pt) | 2012-05-16 | 2017-10-17 | Rana Therapeutics Inc | composições e métodos para modulação da expressão da família de genes da hemoglobina |
| US10837014B2 (en) | 2012-05-16 | 2020-11-17 | Translate Bio Ma, Inc. | Compositions and methods for modulating SMN gene family expression |
| CN104540947A (zh) | 2012-05-16 | 2015-04-22 | Rana医疗有限公司 | 用于调节smn基因家族表达的组合物和方法 |
| JP2015523853A (ja) | 2012-05-16 | 2015-08-20 | ラナ セラピューティクス インコーポレイテッド | Atp2a2発現を調節するための組成物及び方法 |
| CN102827056B (zh) * | 2012-09-03 | 2014-07-23 | 华东理工大学 | N-芳基取代吡咯烷酮衍生物及其用途 |
| US20150247141A1 (en) | 2012-09-14 | 2015-09-03 | Rana Therapeutics, Inc. | Multimeric oligonucleotide compounds |
| AU2013324716B2 (en) | 2012-09-26 | 2019-06-13 | Guandong Mijinjia Biotechnology Co., Ltd | Oligomers with improved off-target profile |
| WO2014059353A2 (en) | 2012-10-11 | 2014-04-17 | Isis Pharmaceuticals, Inc. | Oligomeric compounds comprising bicyclic nucleosides and uses thereof |
| US20150299803A1 (en) | 2012-11-05 | 2015-10-22 | Pronai Therapeutics, Inc. | Methods of Using Biomarkers for the Treatment of Cancer by Modulation of BCL2 Expression |
| DK2920304T3 (da) | 2012-11-15 | 2019-05-13 | Roche Innovation Ct Copenhagen As | Oligonukleotidkonjugater |
| JP6492053B2 (ja) | 2013-03-27 | 2019-03-27 | イサルナ セラピューティクス ゲゼルシャフト ミット ベシュレンクテル ハフツング | 修飾tgf−ベータオリゴヌクレオチド |
| JP2016518842A (ja) | 2013-05-01 | 2016-06-30 | レグルス セラピューティクス インコーポレイテッド | マイクロRNA化合物およびmiR−122をモジュレートする方法 |
| CA2909868C (en) | 2013-05-01 | 2021-10-19 | Regulus Therapeutics Inc. | Compounds and methods for enhanced cellular uptake |
| RS59986B1 (sr) | 2013-06-27 | 2020-03-31 | Roche Innovation Ct Copenhagen As | Antisens oligomeri i konjugati koji ciljno deluju na pcsk9 |
| CA2921457A1 (en) * | 2013-08-16 | 2015-02-19 | Rana Therapeutics, Inc. | Heterochromatin forming non-coding rnas |
| WO2015075166A1 (en) | 2013-11-22 | 2015-05-28 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Methods and pharmaceutical compositions for treatment of a bacterial infection |
| EP3099798B1 (en) | 2014-01-29 | 2018-06-27 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Oligonucleotides and methods for inhibiting or reducing bacterial biofilms |
| DK3341479T3 (da) * | 2015-08-24 | 2020-02-24 | Roche Innovation Ct Copenhagen As | LNA-G-Proces |
| WO2017067970A1 (en) | 2015-10-22 | 2017-04-27 | Roche Innovation Center Copenhagen A/S | In vitro toxicity screening assay |
| CN107574243B (zh) * | 2016-06-30 | 2021-06-29 | 博奥生物集团有限公司 | 分子标志物、内参基因及其应用、检测试剂盒以及检测模型的构建方法 |
| US11666595B2 (en) | 2016-10-07 | 2023-06-06 | Secarna Pharmaceuticals Gmbh & Co. Kg | Antisense oligonucleotides for inhibition of PD-L1 expression and treating cancer |
| JP7198768B2 (ja) * | 2017-03-29 | 2023-01-04 | ロシュ イノベーション センター コペンハーゲン エーエス | UnyLinker迅速切断方法 |
| JP7313696B2 (ja) * | 2017-08-18 | 2023-07-25 | ヨーロピアン モレキュラー バイオロジー ラボラトリー | 増強されたRNAインタラクトーム捕捉(eRIC) |
| EP3697904A1 (en) | 2017-10-17 | 2020-08-26 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Combination treatment for cystic fibrosis |
| US12005120B2 (en) | 2018-05-08 | 2024-06-11 | Regulus Therapeutics Inc. | Galnac conjugated modified oligonucleotides as miR-122 inhibitor having HCV antiviral activity with reduced hyperbilirubinemia side-effect |
| EP3997225A1 (en) | 2019-07-10 | 2022-05-18 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Methods for the treatment of epilepsy |
| WO2021074657A1 (en) | 2019-10-17 | 2021-04-22 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Combination treatment for cystic fibrosis |
| EP4061943A1 (en) | 2019-11-19 | 2022-09-28 | Institut National de la Santé et de la Recherche Médicale (INSERM) | Antisense oligonucleotides and their use for the treatment of cancer |
| IL299708A (en) * | 2020-07-09 | 2023-03-01 | Hoffmann La Roche | A process for the preparation of oligonucleotides using a modified oxidation protocol |
| EP4179091A1 (en) | 2020-07-10 | 2023-05-17 | Institut National De La Sante Et De La Recherche Medicale - Inserm | Methods and compositions for treating epilepsy |
| WO2023152369A1 (en) | 2022-02-14 | 2023-08-17 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Nucleic acid mir-9 inhibitor for the treatment of cystic fibrosis |
| WO2024017990A1 (en) | 2022-07-21 | 2024-01-25 | Institut National de la Santé et de la Recherche Médicale | Methods and compositions for treating chronic pain disorders |
| WO2024146935A1 (en) | 2023-01-06 | 2024-07-11 | Institut National de la Santé et de la Recherche Médicale | Intravenous administration of antisense oligonucleotides for the treatment of pain |
Family Cites Families (26)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2601676B1 (fr) | 1986-07-17 | 1988-09-23 | Rhone Poulenc Sante | Procede de preparation du taxol et du desacetyl-10 taxol |
| US5831066A (en) * | 1988-12-22 | 1998-11-03 | The Trustees Of The University Of Pennsylvania | Regulation of bcl-2 gene expression |
| US5108921A (en) | 1989-04-03 | 1992-04-28 | Purdue Research Foundation | Method for enhanced transmembrane transport of exogenous molecules |
| US5278324A (en) | 1990-08-28 | 1994-01-11 | Virginia Tech Intellectual Properties, Inc. | Water soluble derivatives of taxol |
| MX9102128A (es) | 1990-11-23 | 1992-07-08 | Rhone Poulenc Rorer Sa | Derivados de taxano,procedimiento para su preparacion y composicion farmaceutica que los contiene |
| US5250683A (en) | 1991-09-23 | 1993-10-05 | Florida State University | Certain substituted taxanes and pharmaceutical compositions containing them |
| US5227400A (en) | 1991-09-23 | 1993-07-13 | Florida State University | Furyl and thienyl substituted taxanes and pharmaceutical compositions containing them |
| US5272171A (en) | 1992-02-13 | 1993-12-21 | Bristol-Myers Squibb Company | Phosphonooxy and carbonate derivatives of taxol |
| FR2688518B1 (fr) | 1992-03-13 | 1994-05-06 | Rhone Poulenc Rorer Sa | Procede de preparation de derives du taxane. |
| US5248796A (en) | 1992-06-18 | 1993-09-28 | Bristol-Myers Squibb Company | Taxol derivatives |
| US5254580A (en) | 1993-01-19 | 1993-10-19 | Bristol-Myers Squibb Company | 7,8-cyclopropataxanes |
| PT1584682E (pt) | 1993-09-20 | 2009-08-03 | Univ Pennsylvania | Regulação da expressão do gene bcl-2 |
| US6133246A (en) * | 1997-08-13 | 2000-10-17 | Isis Pharmaceuticals Inc. | Antisense oligonucleotide compositions and methods for the modulation of JNK proteins |
| AU9063398A (en) | 1997-09-12 | 1999-04-05 | Exiqon A/S | Oligonucleotide analogues |
| US6794499B2 (en) * | 1997-09-12 | 2004-09-21 | Exiqon A/S | Oligonucleotide analogues |
| DE69840600D1 (de) | 1997-09-16 | 2009-04-09 | Univ Oregon Health & Science | Rekombinante mhc-moleküle welche nützlich sind für die manipulation von antigen-spezifischen t-zellen |
| JP2002540118A (ja) | 1999-03-18 | 2002-11-26 | エクシコン エ/エス | キシロ−lna類似体 |
| DK1163250T3 (da) * | 1999-03-24 | 2006-11-13 | Exiqon As | Forbedret syntese af [2.2.1]bicyclonukleosider |
| ES2283298T3 (es) | 1999-05-04 | 2007-11-01 | Santaris Pharma A/S | Analogos de l-ribo-lna. |
| WO2001025248A2 (en) | 1999-10-04 | 2001-04-12 | Exiqon A/S | Design of high affinity rnase h recruiting oligonucleotide |
| JP4413493B2 (ja) | 2000-10-04 | 2010-02-10 | サンタリス ファーマ アー/エス | プリンlna類似体の改善された合成方法 |
| AU2002317437A1 (en) | 2001-05-18 | 2002-12-03 | Cureon A/S | Therapeutic uses of lna-modified oligonucleotides in infectious diseases |
| DK1409497T3 (da) | 2001-07-12 | 2005-05-30 | Santaris Pharma As | Fremgangsmåde til fremstilling af LNA-phosphoramiditer |
| CA2463595A1 (en) | 2002-02-20 | 2003-08-28 | Sirna Therapeutics, Inc. | Rna interference mediated inhibition of bcl2 gene expression using short interfering nucleic acid (sina) |
| CA2484526C (en) | 2002-05-08 | 2009-10-13 | Santaris Pharma A/S | Synthesis of locked nucleic acid derivatives |
| DK2284269T3 (en) | 2002-11-18 | 2017-10-23 | Roche Innovation Ct Copenhagen As | Antisense design |
-
2004
- 2004-12-23 RU RU2006126643/13A patent/RU2377301C2/ru not_active IP Right Cessation
- 2004-12-23 AT AT04803067T patent/ATE467679T1/de not_active IP Right Cessation
- 2004-12-23 BR BRPI0418104-2A patent/BRPI0418104A/pt not_active IP Right Cessation
- 2004-12-23 ES ES04803067T patent/ES2344566T3/es active Active
- 2004-12-23 EP EP04803067A patent/EP1706489B9/en not_active Not-in-force
- 2004-12-23 JP JP2006545924A patent/JP4642775B2/ja not_active Expired - Fee Related
- 2004-12-23 CN CNB2004800418197A patent/CN100569945C/zh not_active Expired - Fee Related
- 2004-12-23 WO PCT/DK2004/000917 patent/WO2005061710A1/en active Application Filing
- 2004-12-23 NZ NZ548254A patent/NZ548254A/en not_active IP Right Cessation
- 2004-12-23 DK DK04803067.0T patent/DK1706489T3/da active
- 2004-12-23 US US11/021,729 patent/US7622453B2/en not_active Expired - Fee Related
- 2004-12-23 AU AU2004303464A patent/AU2004303464B2/en not_active Ceased
- 2004-12-23 KR KR1020067014950A patent/KR20070006709A/ko active IP Right Grant
- 2004-12-23 CA CA002550258A patent/CA2550258A1/en not_active Abandoned
- 2004-12-23 DE DE602004027163T patent/DE602004027163D1/de active Active
-
2006
- 2006-06-15 IL IL176320A patent/IL176320A0/en not_active IP Right Cessation
Non-Patent Citations (1)
| Title |
|---|
| ZANGEMEISTER-WITTKE U., Antisense to apoptosis inhibitors facilitates chemotherapy and TRAIL-induced death signaling, Ann. N. Y. Acad. Sci., 2003, v.1002, p.90-94. ZANGEMEISTER-WITTKE U. et al., A novel bispecific antisense oligonucleotide inhibiting both bcl-2 and bcl-xL expression efficiently induces apoptosis in tumor cells, Clin. Cancer Res., 2000, v.6, n.6, p.2547-2555. MOLOGNI L. et al., In vitro transcriptional and translational block of the bcl-2 gene operated by peptide nucleic acid, Biochem. Biophys. Res. Commun., 1999, v.264, n.2, p.537-543. * |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2649367C2 (ru) * | 2013-01-30 | 2018-04-02 | Ф. Хоффманн-Ля Рош Аг | Конъюгаты углевода и lna-олигонуклеотида |
Also Published As
| Publication number | Publication date |
|---|---|
| CN100569945C (zh) | 2009-12-16 |
| DK1706489T3 (da) | 2010-09-13 |
| RU2006126643A (ru) | 2008-01-27 |
| US20050203042A1 (en) | 2005-09-15 |
| EP1706489B1 (en) | 2010-05-12 |
| JP2007515175A (ja) | 2007-06-14 |
| NZ548254A (en) | 2008-09-26 |
| EP1706489A1 (en) | 2006-10-04 |
| KR20070006709A (ko) | 2007-01-11 |
| ES2344566T3 (es) | 2010-08-31 |
| CN1918292A (zh) | 2007-02-21 |
| IL176320A0 (en) | 2006-10-05 |
| ATE467679T1 (de) | 2010-05-15 |
| BRPI0418104A (pt) | 2007-04-17 |
| DE602004027163D1 (de) | 2010-06-24 |
| US7622453B2 (en) | 2009-11-24 |
| CA2550258A1 (en) | 2005-07-07 |
| WO2005061710A1 (en) | 2005-07-07 |
| JP4642775B2 (ja) | 2011-03-02 |
| AU2004303464B2 (en) | 2009-10-01 |
| AU2004303464A1 (en) | 2005-07-07 |
| EP1706489B9 (en) | 2011-01-05 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2377301C2 (ru) | ОЛИГОМЕРНОЕ СОЕДИНЕНИЕ, ПОНИЖАЮЩЕЕ ЭКСПРЕССИЮ ЧЕЛОВЕЧЕСКОГО ГЕНА Bcl-2, КОНЪЮГАТ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ПРИМЕНЕНИЕ ОЛИГОМЕРНОГО СОЕДИНЕНИЯ ДЛЯ ЛЕЧЕНИЯ РАКА | |
| US8173428B2 (en) | LNA oligonucleotides and the treatment of cancer | |
| US20080188432A1 (en) | Oligomeric compounds for the modulation ras expression | |
| US20090118213A1 (en) | Rna antagonist compounds for the inhibition of apo-b100 expression | |
| WO2007031091A2 (en) | Rna antagonist compounds for the modulation of p21 ras expression | |
| JP2009189372A (ja) | HIF−1α発現を調節するオリゴマー化合物 | |
| CA2644347A1 (en) | Small internally segmented interfering rna | |
| JP2006518999A (ja) | チオレドキシン発現の改変のためのオリゴマー化合物 | |
| MX2008003198A (es) | Compuestos antagonistas de acido ribonucleico (arn) para la inhibicion de expresion apo-b1oo |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20151224 |