RU2334746C2 - Ингибиторы циклин-зависимых киназ и их применение - Google Patents
Ингибиторы циклин-зависимых киназ и их применение Download PDFInfo
- Publication number
- RU2334746C2 RU2334746C2 RU2005102939/04A RU2005102939A RU2334746C2 RU 2334746 C2 RU2334746 C2 RU 2334746C2 RU 2005102939/04 A RU2005102939/04 A RU 2005102939/04A RU 2005102939 A RU2005102939 A RU 2005102939A RU 2334746 C2 RU2334746 C2 RU 2334746C2
- Authority
- RU
- Russia
- Prior art keywords
- trans
- methylpyrrolidin
- hydroxymethyl
- chromen
- dihydroxy
- Prior art date
Links
- 0 Cc(c(*)c(*)c1c2OC(*)=C(*)C1=*)c2P Chemical compound Cc(c(*)c(*)c1c2OC(*)=C(*)C1=*)c2P 0.000 description 5
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/04—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/10—Antimycotics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P33/00—Antiparasitic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/14—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing three or more hetero rings
Landscapes
- Health & Medical Sciences (AREA)
- Organic Chemistry (AREA)
- Chemical & Material Sciences (AREA)
- Veterinary Medicine (AREA)
- Life Sciences & Earth Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Oncology (AREA)
- Communicable Diseases (AREA)
- Virology (AREA)
- Tropical Medicine & Parasitology (AREA)
- Urology & Nephrology (AREA)
- Dermatology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Oxygen Or Sulfur (AREA)
Abstract
Настоящее изобретение касается новых соединений для ингибирования циклин-зависимых киназ, в частности производных хроменона, по формуле Ic
где R1, R2, R3, R4, R5, R6 и А принимают значения, указанные в формуле изобретения. Изобретение также касается способов получения таких соединений, а также применения таких соединений для получения медикаментов, предназначенных для ингибирования циклин-зависимых киназ и ингибирования пролиферации клеток, используемых в лечении и профилактике различных пролиферативных заболеваний.
Изобретение также касается композиций, содержащих такие соединения сами по себе либо в комбинации с другим активным агентом, в смеси или иным образом вместе с инертным носителем, в частности, фармацевтических композиций, содержащих такие соединения сами по себе либо в комбинации с другим активным агентом, вместе с фармацевтически приемлемыми носителями и вспомогательными веществами. 12 н. и 10 з.п. ф-лы, 6 ил., 2 табл.
Description
Claims (22)
1. Соединение общей формулы Ic
где R1 означает арил, незамещенный или замещенный, по меньшей мере, одним заместителем, выбранным из галогена, (С1-С4)-алкила, (С1-С4)-алкокси, нитро, NR9R10, трифторметила, гидроксила, циано, насыщенный, частично ненасыщенный или ароматический гетероцикл, содержащий 1, 2, 3 или 4 идентичных или различных гетероатома, выбранных из азота и серы, причем гетероцикл является незамещенным или замещенным галогеном;
R2 - водород; C1-С6-алкил; арил, незамещенный или замещенный, по меньшей мере, одним заместителем, выбранным из: С1-С4-алкила, С1-С4-алкокси;
R3, R4 и R5 каждый независимо выбран из водорода; OR11;
R6 - С1-С4-алкиленOR11;
R9 и R10 каждый независимо выбран из водорода; С1-С6-алкила;
R11 - водород; С1-С6-алкил; С1-С4-алканоил или С1-С4-алкоксикарбонил;
Z - атом кислорода;
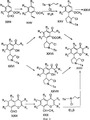
А - насыщенное или ненасыщенное 5-членное кольцо, представленное одной из следующих общих структур (i)-(v):
в которых X1 и Х2 каждый независимо выбран из атома углерода и атома азота при условии, что в структурах (i), (iii) и (iv), по меньшей мере, один из X1 и X2 является атомом азота, который, по меньшей мере, монозамещен R13, где R13 выбран из водорода; С1-С6-алкила; арила, незамещенного или замещенного, по меньшей мере, одним заместителем, выбранным из С1-С4-алкила, С1-С4-алкокси, циано;
R6 - определенный выше заместитель, по меньшей мере, на одном атоме углерода в кольце;
R7 - водород, С1-С4-алкил;
р - целое число 1 или 2, и
его таутомерные формы, стереоизомеры, оптические изомеры, фармацевтически приемлемые соли, фармацевтически приемлемые сольваты.
2. Соединение по п.1 формулы Ic, в которой
R1 - фенил, незамещенный или замещенный 1, 2 или 3 одинаковыми или разными заместителями, выбранными из галогена, С1-С4-алкила, С1-С4-алкокси, нитро, NR9R10, трифторметила, гидроксила, циано или гетероцикла, представляющего собой насыщенное, частично ненасыщенное или ароматическое кольцо, содержащее 5 или 6 атомов в кольце, из которых 1, 2 или 3 представлены одинаковыми или различными гетероатомами, выбранными из азота и серы, причем гетероцикл незамещен или замещен 1, 2 или 3 атомами галогена;
R2 - водород; С1-С6-алкил; фенил, незамещенный или замещенный 1, 2 или 3 одинаковыми или различными заместителями, выбранными из С1-С4-алкила или С1-С4-алкокси;
R3, R4 и R5 каждый независимо выбран из водорода, OR11;
Z - атом кислорода;
А - насыщенное или ненасыщенное 5-членное кольцо, представленное одной из общих структур от (i) до (v), как заявлено в п.1, в которых X1 и Х2 каждый независимо выбран из атома углерода и атома азота при условии, что в структурах (i), (iii) и (iv), по меньшей мере, один из X1 и X2 является азотом, который, по меньшей мере, монозамещен R13, где R13 выбран из водорода, C1-С6-алкила и фенила, который незамещен или замещен, по меньшей мере, одним заместителем, выбранным из С1-С4-алкила, С1-С4-алкокси, a R7 - водород;
R9 и R10 каждый независимо выбран из водорода, С1-С4-алкила;
R11 - водород, С1-С4-алкил, С1-С4-алканоил или С1-С4-алкоксикарбонил.
4. Соединение по п.1 общей формулы Ic, в котором R1 означает фенил, незамещенный или замещенный 1, 2 или 3 одинаковьми или разными заместителями, выбранными из галогена, С1-С4-алкила, С1-С4-алкокси, нитро, NR9R10, трифторметила, гидроксила, циано, карбокси, С1-С4-алкоксикарбонила и С1-С4-алкиленгидроксила; или гетероцикл, представляющий собой насыщенное, частично ненасыщенное или ароматическое кольцо, содержащее 6 атомов в кольце, из которых 1, 2 или 3 представлены идентичными или различными гетероатомами, выбранными из азота и серы, причем этот гетероцикл незамещен или замещен 1, 2 или 3 атомами галогена;
R2 и R4 представлены водородом и
R3 и R5 каждый независимо выбран из гидроксила, С1-С4-алкоксила и С1-С4-алкилкарбонилокси.
5. Соединение по п.1 общей формулы Ic, в котором R1 означает фенил или пиридинил, замещенный 1, 2 или 3 идентичными или различными заместителями, выбранными из галогена и нитрогруппы, R2 и R4 представлены водородом; R3 и R5 представлены гидроксилом, А - насыщенное 5-членное кольцо, представленное одной из общих структур (i)-(v), в которых X1, Х2, R6 и R13 определены выше.
6. Соединение по п.5, в котором X1 - углерод, X2 - азот, R6 - С1-С4-алкиленгидроксил, R13 - С1-С4-алкил.
7. Соединение по п.1 общей формулы Iс, которое представляет собой:
(+/-)-транс-2-(2-хлорфенил)-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметоксихромен-4-он;
(+)-транс-2-(2-хлорфенил)-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметоксихромен-4-он;
(+)-транс-2-(2-хлорфенил)-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(-)-транс-2-(2-хлорфенил)-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметоксихромен-4-он;
(-)-транс-2-(2-хлорфенил)-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(+)-транс-2-(2-бромфенил)-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметоксихромен-4-он;
(+)-транс-2-(2-бромфенил)-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(+)-транс-2-(4-бромфенил)-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметоксихромен-4-он;
(+)-транс-2-(4-бромфенил)-5-гидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-7-метоксихромен-4-он;
(+)-транс-2-(4-бромфенил)-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(+)-транс-2-(3-хлорфенил)-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметоксихромен-4-он;
(+)-транс-2-(3-хлорфенил)-5-гидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-7-метоксихромен-4-он;
(+)-транс-2-(3-хлорфенил)-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(+)-транс-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-2-(2-йодфенил)-5,7-диметоксихромен-4-он;
(+)-транс-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-2-(2-йодфенил)-хромен-4-он;
(+)-транс-2-(2-фторфенил)-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметоксихромен-4-он;
(+)-транс-2-(2-фторфенил)-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(+)-транс-2-(3-фторфенил)-5,7-диметокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(+)-транс-2-(3-фторфенил)-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(+)-транс-2-(2,6-дифторфенил)-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметоксихромен-4-он;
(+)-транс-2-(2,6-дифторфенил)-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(+/-)-транс-4-[8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметокси-4-оксо-4Н-хромен-2-ил]-бензонитрил;
(+/-)-транс-4-[5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-4-оксо-4Н-хромен-2-ил]-бензонитрил;
(+)-транс-4-[8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметокси-4-оксо-4Н-хромен-2-ил]-бензонитрил;
(+)-транс-4-[5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил-4-оксо-4Н-хромен-2-ил]-бензонитрил;
(+/-)-транс-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметокси-2-(4-трифторметилфенил)-хромен-4-он;
(+/-)-транс-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил-)-2-(4-трифторметилфенил)-хромен-4-он;
(+)-транс-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметокси-2-(4-трифторметилфенил)-хромен-4-он;
(+)-транс-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-2-(4-трифторметилфенил)-хромен-4-он;
(-)-транс-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметокси-2-(4-трифторметилфенил)-хромен-4-он;
(-)-транс-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-2-(4-трифторметилфенил)-хромен-4-он;
(+)-транс-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметокси-2-фенилхромен-4-он;
(+)-транс-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-2-фенилхромен-4-он;
(+)-транс-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметокси-2-тиофен-2-илхромен-4-он;
(+)-транс-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-2-тиофен-2-илхромен-4-он;
(+)-транс-4-[5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-4-оксо-4Н-хромен-2-ил]-3-метилбензонитрил;
(+)-транс-4-[8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметокси-4-оксо-4Н-хромен-2-ил]-3-метилбензонитрил;
(+/-)-транс-2-[2-бром-5-метоксифенил)-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметоксихромен-4-он;
(+/-)-транс-2-[2-бром-5-метоксифенил)-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(+)-транс-2-[2-бром-5-метоксифенил)-8-(2-гидроксиметил-1-метилпирролидин-3-ил)]-5,7-диметоксихромен-4-он;
(+)-транс-2-(2-бром-5-метоксифенил)-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(+/-)-транс-2-(2-бром-5-гидроксифенил)-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(+)-транс-2-(2-бром-5-гидроксифенил)-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(+/-)-транс-2-[(3,5-бис-трифторметил)-фенил]-8-[2-гидроксиметил-1-метилпирролидин-3-ил]-5,7-диметоксихромен-4-он;
(+/-)-транс-2-[(3,5-бис-трифторметил)-фенил]-5,7-дигидрокси-8-[2-гидроксиметил-1-метилпирролидин-3-ил]-хромен-4-он;
(+)-транс-2-(2-хлор-5-метилфенил)-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметоксихромен-4-он;
(+)-транс-2-(2-хлор-5-метилфенил)-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(+)-транс-2-[2-бром-5-нитрофенил]-8-[2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметоксихромен-4-он;
(+/-)-транс-2-[2-бром-5-нитрофенил]-8-[2-гидроксиметил-1-метилпирролидин-3-ил]-5,7-дигидроксихромен-4-он;
(+/-)-транс-2-(2-хлорпиридин-3-ил)-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметоксихромен-4-он;
(+/-)-транс-2-(2-хлорпиридин-3-ил)-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(+/-)-транс-2-[2-бром-5-нитрофенил]-8-[2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметоксихромен-4-он;
(+)-транс-2-(2-хлорпиридин-3-ил)-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(+/-)-транс-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметокси-2-(4-нитрофенил)-хромен-4-он;
(+/-)-транс-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-2-(4-нитрофенил)-хромен-4-он;
(+)-транс-2-(4-аминофенил)-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(+/-)-транс-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметокси-2-(2-метоксифенил)-хромен-4-он;
(+/-)-транс-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-2-(2-гидроксифенил)-хромен-4-он;
(+)-транс-3-хлор-4-[8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметокси-4-оксо-4Н-хромен-2-ил]-бензонитрил;
(+)-транс-3-хлор-4-[5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметокси-4-оксо-4Н-хромен-2-ил]-бензонитрил;
(+)-транс-2-(4-бром-2-хлорфенил)-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметоксихромен-4-он;
(+)-транс-2-(4-бром-2-хлорфенил)-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(+/-)-транс-2-(2-хлордиметиламинофенил)-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметоксихромен-4-он;
(+/-)-транс-2-(2-хлорметиламинофенил)-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(+/-)-транс-2-(2-хлор-4-метоксифенил)-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметоксихромен-4-он;
(+/-)-транс-2-(2-хлор-4-гидроксифенил)-5,7-дигидрокси-8-[2-гидроксиметил-1-метилпирролидин-3-ил]-хромен-4-он;
(+/-)-транс-2-(2-хлор-5-фторфенил)-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметоксихромен-4-он;
(+/-)-транс-2-(2-хлор-5-фторфенил)-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(+/-)-транс-2-(2-хлор-5-метоксифенил)-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметоксихромен-4-он;
(+/-)-транс-2-(2-хлор-5-гидроксифенил)-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(+/-)-транс-2-(2-хлор-5-метоксифенил)-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(+/-)-транс-8-(2-азидометил-1-метилпирролидин-3-ил)-2-(2-хлорфенил)-5,7-диметоксихромен-4-он;
(+/-)-транс-8-(2-аминометил-1-метилпирролидин-3-ил)-2-(2-хлорфенил)-5,7-диметоксихромен-4-он;
(+/-)-транс-8-(2-аминометил-1-метилпирролидин-3-ил)-2-(2-хлорфенил)-5,7-дигидроксихромен-4-он;
(+/-)-транс-3-{[2-(2-хлорфенил)-5,7-диметокси-4-оксо-4Н-хромен-8-ил]-1-метилпирролидин-2-ил}-ацетонитрил;
(+/-)-транс-{3-[2-(2-хлорфенил)-5,7-дигидрокси-4-оксо-4Н-хромен-8-ил]-1-метилпирролидин-2-ил}-ацетонитрил;
(+/-)-транс-3-[2-(2-хлорфенил)-5,7-диметокси-4-оксо-4Н-хромен-8-ил]-1-(4-метоксифенил)-пирролидин-2-илметиловый эфир уксусной кислоты;
(+/-)-транс-2-(2-хлорфенил)-8-[2-гидроксиметил-1-(4-метоксифенил)-пирролидин-3-ил]-5,7-диметоксихромен-4-он;
(+/-)-транс-2-(2-хлорфенил)-5,7-дигидрокси-8-[2-гидроксиметил-1-(4-фенил)пирролидин-3-ил]-хромен-4-он;
(+/-)-транс-3-[2-(2-хлорфенил)-5,7-диметокси-4-оксо-4Н-хромен-8-ил]-1-пропилпирролидин-2-илметиловый эфир уксусной кислоты;
(+/-)-транс-2-(2-хлорфенил)-8-(2-гидроксиметил-1-пропилпирролидин-3-ил)-5,7-диметоксихромен-4-он;
(+/-)-транс-2-(2-хлорфенил)-5,7-дигидрокси-8-(2-гидроксиметил-1-пропилпирролидин-3-ил)-хромен-4-он;
(+/-)-транс-2-(2-хлор-4-нитрофенил-5,7-дигидрокси-8-2-гидроксиметил-1-пропилпирролидин-3-ил)-хромен-4-он;
(+/-)-транс-2-(2-бром-4-нитрофенил-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(+/-)-транс-3-хлор-4-[5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-4-оксо-4Н-хромен-2-ил]-бензойная кислота;
(+/-)-транс-3-бром-4-[5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-4-оксо-4Н-хромен-2-ил]-бензойная кислота;
(+/-)-транс-2-(2-хлор-4-фторфенил)-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(+/-)-транс-2-(4-амино-2-хлорфенил)-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(+/-)-транс-2-(2-бром-4-фторфенил)-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(+/-)-транс-2-(4-амино-2-бромфенил)-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(+/-)-транс-4-хлор-3-[5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-4-оксо-4Н-хромен-2-ил]-бензойная кислота;
(+/-)-транс-4-бром-3-[5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-4-оксо-4Н-хромен-2-ил]-бензойная кислота;
(+/-)-транс-4-бром-3-[5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-4-оксо-4Н-хромен-2-ил]-N-гидроксибензамид;
(+/-)-транс-4-хлор-3-[5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-4-оксо-4Н-хромен-2-ил]-N-гидроксибензамид;
(+/-)-транс-3-хлор-4-[5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-4-оксо-4Н-хромен-2-ил]-N-гидроксибензамид;
(+/-)-транс-3-бром-4-[5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-4-оксо-4Н-хромен-2-ил]-N-гидроксибензамид;
(+/-)-транс-2-(2,4-дифторфенил)-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(+)-транс-2-(2-хлор-3-фторфенил)-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметоксихромен-4-он;
(+)-транс-2-(2-хлор-3-фторфенил)-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(+)-транс-2-(2-бром-3-фторфенил)-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметоксихромен-4-он;
(+)-транс-2-(2-бром-3-фторфенил)-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(+)-транс-2-(2-бром-5-фторфенил)-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметоксихромен-4-он;
(+)-транс-2-(2-бром-5-фторфенил)-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(+)-транс-2-(2-хлор-5-йодфенил)-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметоксихромен-4-он;
(+)-транс-2-(2-хлор-5-йодфенил)-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(+)-транс-2-(2-бром-5-хлорфенил)-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметоксихромен-4-он;
(+)-транс-2-(2-бром-5-хлорфенил)-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(+/-)-транс-2-(2-хлорфенил)-5,7-дигидрокси-8-(2-гидроксиметил-1-метилоксипирролидин-3-ил)-хромен-4-он;
(+)-транс-2-(2-бром-4-нитрофенил)-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметоксихромен-4-он;
(+)-транс-2-(2-бром-4-нитрофенил)-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(+)-транс-2-(4-амино-2-бромфенил)-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметоксихромен-4-он;
(+)-транс-2-(4-амино-2-бромфенил)-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(+)-транс-2-(2-бром-4-метоксифенил)-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметоксихромен-4-он;
(+)-транс-2-(2-бром-4-метоксифенил)-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(+)-транс-2-(2-бром-4-гидроксифенил)-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он;
(+)-транс-8-(2-ацетоксиметил-1-метилпирролидин-3-ил)-5-гидрокси-2-(4-нитрофенил)-4-оксо-4Н-хромен-7-иловый эфир уксусной кислоты;
(+)-транс-2-(2,4-дихлор-5-фторфенил)-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-5,7-диметоксихромен-4-он и
(+)-транс-2-(2,4-дихлор-5-фторфенил-5,7-дигидрокси-8-(2-гидроксиметил-1-метилпирролидин-3-ил)-хромен-4-он.
8. Применение соединений по любому из пп.1-7 общей формулы Iс или их фармацевтически приемлемых солей для изготовления медикамента, предназначенного для ингибирования циклин-зависимых киназ.
9. Применение соединений по любому из пп.1-7 общей формулы Iс или их фармацевтически приемлемых солей для изготовления медикамента, предназначенного для лечения или профилактики пролиферативных заболеваний.
10. Применение соединений по любому из пп.1-7 общей формулы Iс или их фармацевтически приемлемых солей для изготовления медикамента, предназначенного для лечения или профилактики рака.
11. Фармацевтическая композиция, применяемая в качестве ингибитора циклин-зависимой киназы, включающая терапевтически эффективное количество, по меньшей мере, одного соединения общей формулы Iс согласно любому из пп.1-7 или его фармацевтически приемлемой соли и фармацевтически приемлемый носитель.
12. Фармацевтическая композиция, применяемая в качестве ингибитора циклин-зависимой киназы, включающая терапевтически эффективное количество, по меньшей мере, одного соединения общей формулы Iс согласно любому из пп.1-7 или его фармацевтически приемлемой соли, а также, по меньшей мере, еще одно фармацевтически активное соединение вместе с фармацевтически приемлемым носителем.
13. Применение соединений общей формулы Ic согласно любому из пп.1-7 или их фармацевтически приемлемых солей для изготовления медикамента, предназначенного для лечения или профилактики заболеваний, связанных с чрезмерной пролиферацией клеток, причем медикамент применяется либо поочередно, либо одновременно с, по меньшей мере, еще одним фармацевтически активным соединением.
14. Способ получения соединения общей формулы Ic согласно любому из пп.1-7 или его фармацевтически приемлемых солей, включающий:
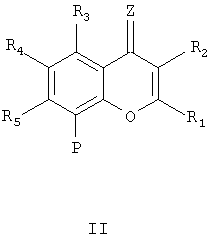
(а) проведение реакции между бензопираноном формулы II
где R1, R2, R3, R4, R5 и Z принимают значения, определенные в любом из пп.1-6, а Р - функциональная группа,
и соединением по формуле III
где А замещено R6 и R7, причем А, R6 и R7 принимают значения, определенные в пп.1-6, за исключением того, что А не является 5-членным кольцом указанной выше общей структуры (ii) или (v), a Q представляет собой функциональную группу, связанную с насыщенным или ненасыщенным атомом углерода в кольце А, причем:
i) если Q образует связь с ненасыщенным атомом углерода, то реакция проводится в присутствии металлического катализатора, органического или неорганического основания и органического или неорганического растворителя, при этом образуется связь С-С между соответствующими атомами углерода, с которыми связаны Р и Q, после чего следует обработка восстановителем для восстановления двойной связи между положениями 1 и 2 или 1 и 5 в 5-членном кольце А с образованием соединения формулы Ic,
ii) если Q образует связь с насыщенным атомом углерода, то реакция проводится в присутствии соответствующего лиганда или катализатора и отщепляемой группы, при этом образуется связь С-С между соответствующими атомами углерода, с которыми связаны Р и Q, с образованием соединения формулы Ic,
и, при необходимости, превращение образовавшегося соединения в фармацевтически приемлемую соль; либо
(b) проведение реакции между бензопираноном формулы II
где R1, R2, R3, R4, R5 и Z принимают значения, определенные в пп.1-6, а Р - функциональная группа,
и соединением формулы IIIA
где Х2 и R6 принимают значения, определенные в пп.1-6,
в присутствии металлического катализатора, органического или неорганического основания и органического или неорганического растворителя с образованием связи N-C между углеродом соединения формулы II, к которому присоединена группа Р, и азотом соединения формулы IIIA и, при необходимости, превращения образовавшегося соединения формулы Ic в фармацевтически приемлемую соль.
15. Способ получения соединения общей формулы Ic согласно любому из пп.1-7 или его фармацевтически приемлемых солей, где Z - атом кислорода, R7 - водород, R1, R2, R3, R4, R5, R6 и А определены выше, включающий
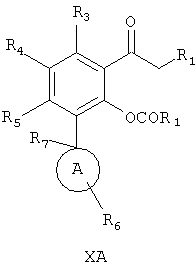
проведение реакции между соединением формулы ХА
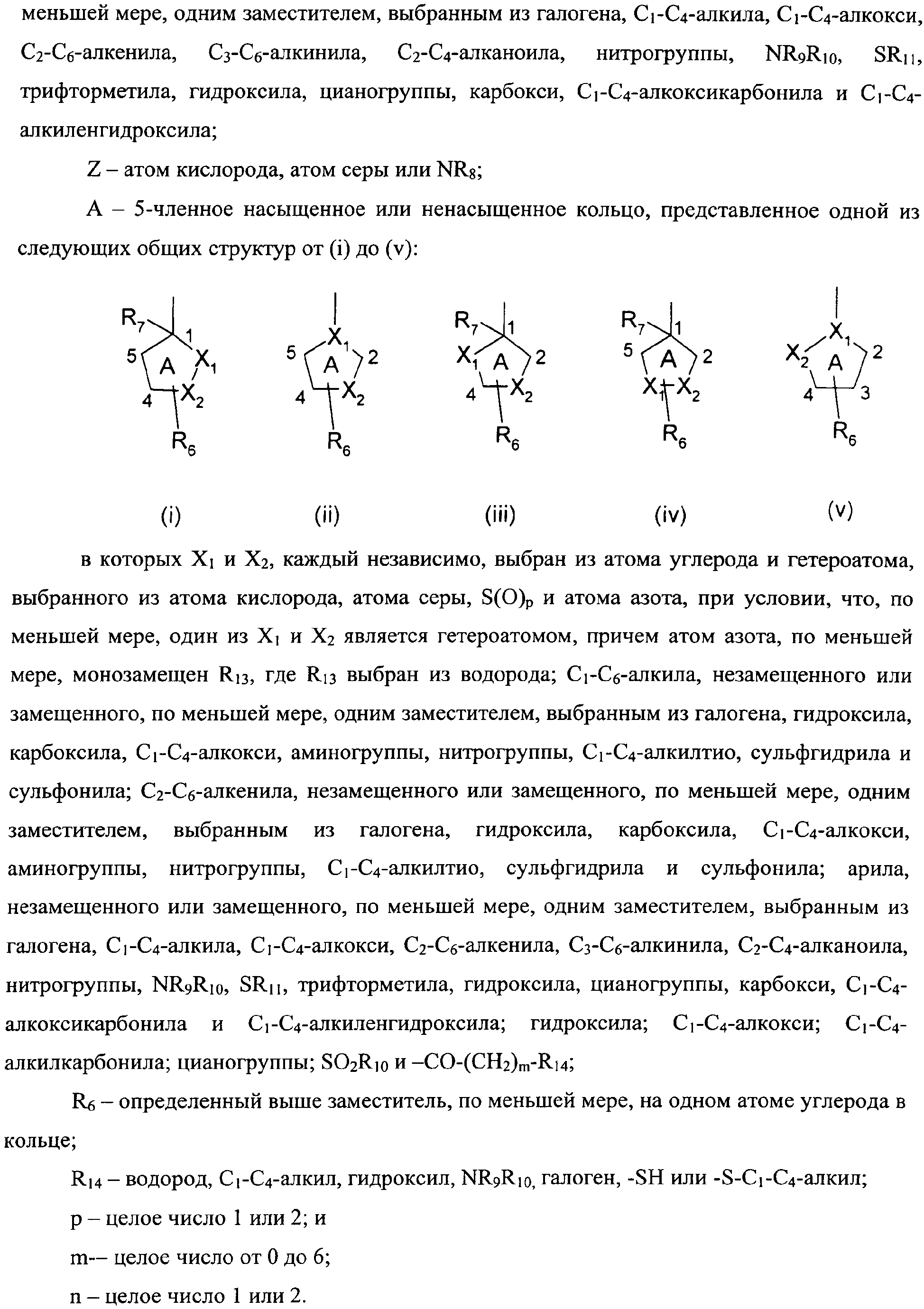
или соединением формулы XIIA
где в обоих случаях R1, R2, R3, R4, R5, R6, R7 и А определены выше,
с органическим или неорганическим основанием с последующим добавлением в реакционную смесь кислоты, способной осуществить циклизацию, после чего добавляют органическое или неорганическое основание и, при необходимости, превращают образовавшееся соединение формулы Ic в фармацевтически приемлемую соль.
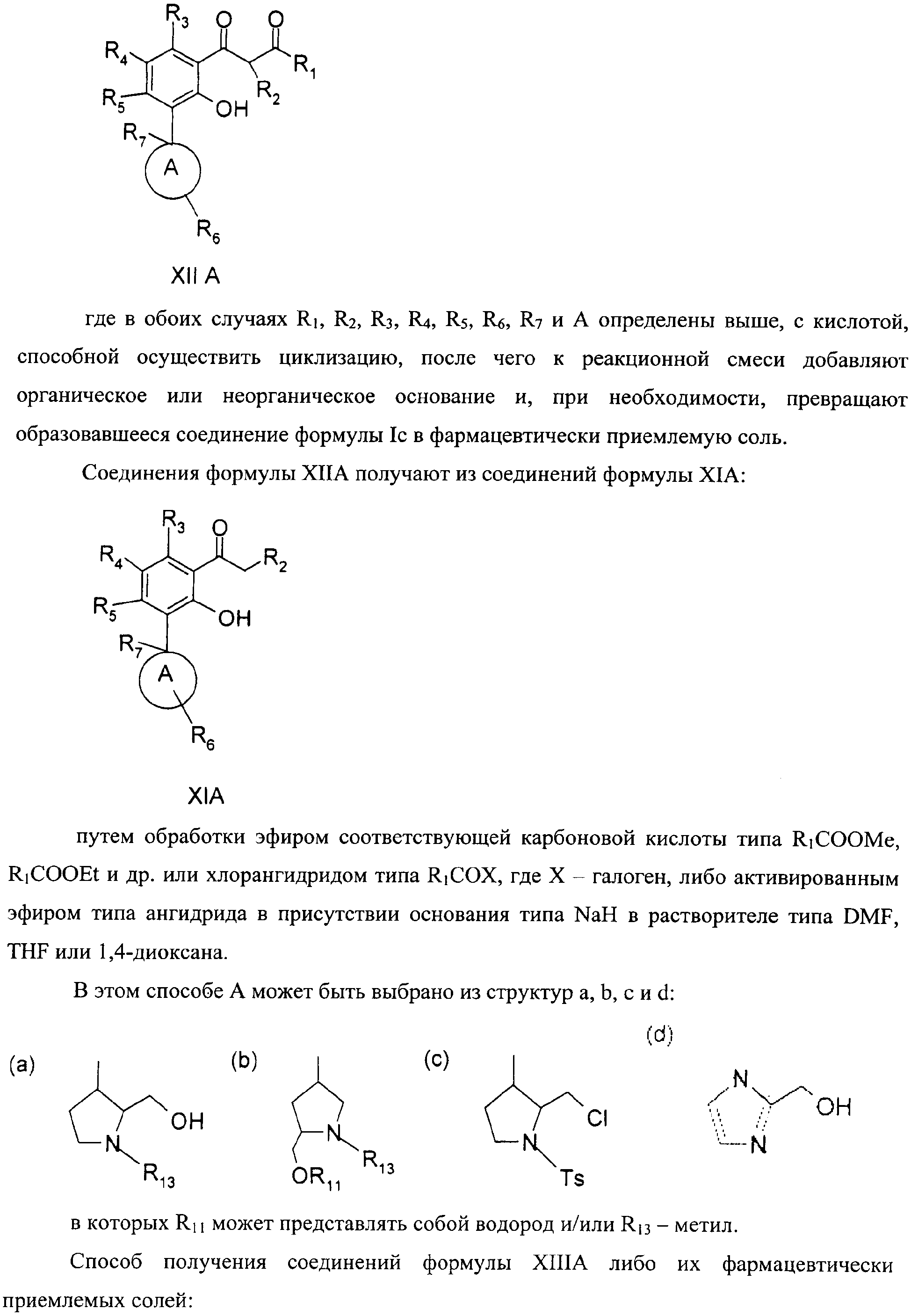
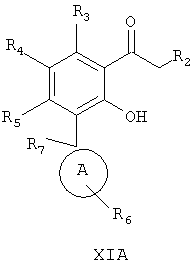
16. Способ по п.15, в котором соединение формулы XIIA получают при реакции соединения формулы XIA
где R1, R2, R3, R4, R5, R6, R7 и А определены выше,
с эфиром карбоновой кислоты, галогенангидридом или активированным эфиром в присутствии органического или неорганического основания в органическом или неорганическом растворителе.
18. Способ по п.19, в котором R11 - водород и/или R13 - метил.
19. Способ получения соединения формулы XIIIA или его фармацевтически приемлемых солей:
где R1, R2, R3, R4, R5, R13 и Z определены в пп.1-6,
включающий проведение реакции между соединением формулы VIIA
где R1, R2, R3, R4, R5, R13 и Z определены в пп.1-6,
с реагентом, способным осуществить замещение группы -ОН на пиперидиновом кольце отщепляемой группой, в присутствии органического или неорганического основания с последующим добавлением подходящего органического основания в присутствии подходящего органического растворителя для осуществления замыкания пиперидинового кольца и, при необходимости, превращения образовавшегося соединения формулы XIIIA в фармацевтически приемлемую соль.
20. Способ получения соединения формулы XXXVII или его фармацевтически приемлемых солей:
где R1, R2, R3, R4, R5 и Z определены в пп.1-6,
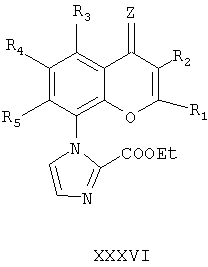
включающий проведение реакции между соединением формулы XXXVI
где R1, R2, R3, R4, R5, R13 и Z определены в пп.1-6,
и восстановителем, способным к восстановлению сложноэфирной группы -C(O)OEt на имидазолильном кольце в группу -СН2OH, и, при необходимости, превращение образовавшегося соединения формулы XXXVII в фармацевтически приемлемую соль.
22. Способ получения соединения формулы XIII
где R1, R2, R3, R4, R5 и R13 определены в пп.1-6,
включающий проведение реакции между рацемическим соединением формулы VIII
где R3, R4, R5 и R13 определены в пп.1-6,
и хиральным вспомогательным реагентом в присутствии растворителя с образованием диастереомерной соли соединения формулы VIII, кристаллизацию требуемой соли диастереомера и последующую обработку основанием для получения требуемого энантиомера соединения формулы VIII, обработку соединения формулы VIII ацилирующим реагентом или активированной формой кислоты в присутствии катализатора типа кислоты Льюиса с получением ацилированного соединения формулы IX
где R2, R3, R4, R5 и R13 определены в пп.1-6,
обработку соединения формулы IX
(a) хлорангидридом типа R1COCl, ангидридом типа (R1CO)2O или эфиром типа R1COOCH3, где R1 определен выше, либо
(b) кислотой типа R1COOH, где R1 определен выше, и оксихлоридом фосфора в присутствии поглотителя кислоты с получением хлорангидрида in situ в нейтральных условиях, либо
(c) R1COOH, где R1 определен выше,
вместе с полифосфорной кислотой,
с образованием соединения формулы X
где R1, R2, R3, R4, R5 и R13 определены в пп.1-6,
обработку соединения формулы Х основанием, после чего обрабатывают сильной кислотой, способной осуществить циклизацию, а затем слабым основанием с образованием требуемого соединения формулы XIII, и необязательно превращают данное соединение в фармацевтически приемлемую соль;
в качестве альтернативы соединение приведенной формулы IX подвергают гидролизу эфирных связей при обработке основанием в водном этаноле или метаноле с образованием соединения формулы XI
где R2, R3, R4, R5 и R13 определены в пп.1-6,
соединение формулы XI обрабатывают эфиром карбоновой кислоты, хлорангидридом или активированным эфиром в присутствии основания в растворителе с образованием соединения формулы XII
где R1, R2, R3, R4, R5 и R13 определены в пп.1-6,
и соединение формулы XII обрабатывают сильной кислотой, способной осуществить циклизацию, а затем слабым основанием с образованием требуемого соединения формулы XIII, и необязательно превращают данное соединение в фармацевтически приемлемую соль.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| IN616/MUM/2002 | 2002-07-08 | ||
| IN616MU2002 | 2002-07-08 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2005102939A RU2005102939A (ru) | 2005-09-10 |
| RU2334746C2 true RU2334746C2 (ru) | 2008-09-27 |
Family
ID=30012269
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2005102939/04A RU2334746C2 (ru) | 2002-07-08 | 2003-07-07 | Ингибиторы циклин-зависимых киназ и их применение |
Country Status (20)
| Country | Link |
|---|---|
| EP (1) | EP1556375B1 (ru) |
| JP (1) | JP4860148B2 (ru) |
| KR (1) | KR100991920B1 (ru) |
| CN (1) | CN1668613B (ru) |
| AR (1) | AR041184A1 (ru) |
| AT (1) | ATE399162T1 (ru) |
| AU (1) | AU2003272070B2 (ru) |
| BR (1) | BR0312633A (ru) |
| CA (1) | CA2492130C (ru) |
| DE (1) | DE60321808D1 (ru) |
| DK (1) | DK1556375T3 (ru) |
| ES (1) | ES2309338T3 (ru) |
| IL (1) | IL166153A (ru) |
| MX (1) | MXPA05000388A (ru) |
| NZ (1) | NZ537518A (ru) |
| PT (1) | PT1556375E (ru) |
| RU (1) | RU2334746C2 (ru) |
| TW (1) | TWI331034B (ru) |
| WO (1) | WO2004004632A2 (ru) |
| ZA (1) | ZA200500138B (ru) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2598028C2 (ru) * | 2011-04-13 | 2016-09-20 | Астразенека Аб | Хроменоновые соединения в качестве ингибиторов рi3-киназы для лечения рака |
Families Citing this family (32)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7915301B2 (en) | 2002-07-08 | 2011-03-29 | Piramal Life Science Limited | Inhibitors of cyclin dependent kinases and their use |
| BRPI0621777A2 (pt) * | 2006-06-21 | 2013-03-12 | Piramal Life Sciences Ltd | derivados de flavona enantiomericamente puros para o tratamento de distérbios proliferativos e processos para sua preparaÇço |
| JP5006396B2 (ja) | 2006-07-07 | 2012-08-22 | ピラマル・ライフ・サイエンシーズ・リミテッド | ピロリジン置換フラボンのエナンチオ選択的合成 |
| BRPI0721626A2 (pt) * | 2007-05-15 | 2013-01-22 | Piramal Life Sciences Ltd | combinaÇço farmacÊutica sinergÍstica para o tratamento de cÂncer |
| CN101333205A (zh) * | 2008-07-10 | 2008-12-31 | 大连理工大学 | 周期素依赖蛋白激酶抑制剂黄芩素哌嗪衍生物及其制法 |
| TWI461194B (zh) | 2009-05-05 | 2014-11-21 | Piramal Entpr Ltd | 吡咯啶取代黃酮作為輻射致敏劑 |
| WO2010129858A1 (en) * | 2009-05-08 | 2010-11-11 | Georgia State University Research Foundation | Compounds and compositions comprising cdk inhibitors and methods for the treatment of cancer |
| US7928067B2 (en) | 2009-05-14 | 2011-04-19 | Ischemix Llc | Compositions and methods for treating ischemia and ischemia-reperfusion injury |
| AU2010346973A1 (en) * | 2010-02-26 | 2012-10-18 | Piramal Enterprises Limited | Pyrrolidine substituted flavones for the treatment of inflammatory disorders |
| CA2817362C (en) | 2010-11-18 | 2018-10-23 | Ischemix Llc | Lipoyl compounds and their use for treating ischemic injury |
| EP2640380A1 (en) * | 2010-11-19 | 2013-09-25 | Piramal Enterprises Limited | Pharmaceutical combination of paclitaxel and a cdk inhibitor |
| WO2012069972A1 (en) | 2010-11-19 | 2012-05-31 | Piramal Life Sciences Limited | A pharmaceutical combination for the treatment of breast cancer |
| WO2012123889A1 (en) | 2011-03-14 | 2012-09-20 | Piramal Healthcare Limited | A synergistic pharmaceutical combination for the treatment of pancreatic cancer |
| TW201300105A (zh) * | 2011-05-31 | 2013-01-01 | Piramal Life Sciences Ltd | 治療頭頸鱗狀細胞癌之相乘藥物組合物 |
| EP2723449A2 (en) | 2011-06-24 | 2014-04-30 | Piramal Enterprises Limited | Compounds for the treatment of cancers associated with human papillomavirus |
| WO2013105056A1 (en) | 2012-01-13 | 2013-07-18 | Piramal Enterprises Limited | Pyrrolidine- substituted flavone derivatives for prevention or treatment of oral mucositis |
| WO2014049515A1 (en) * | 2012-09-25 | 2014-04-03 | Piramal Enterprises Limited | Pyrrolidine substituted flavones for treatment of renal cystic diseases |
| EP3019166B1 (en) | 2013-07-12 | 2019-05-08 | Piramal Enterprises Limited | A pharmaceutical combination for the treatment of melanoma |
| US10555931B2 (en) | 2014-05-28 | 2020-02-11 | Piramal Enterprises Limited | Pharmaceutical combination for the treatment of cancer |
| US10308619B2 (en) * | 2015-06-23 | 2019-06-04 | Covestro Deutschland Ag | Substituted triazines and a method for producing same |
| KR102275758B1 (ko) | 2016-03-28 | 2021-07-12 | 프레시지 바이오싸이언시스, 인크. | 암 치료를 위한 제약학적 조합물 |
| BR112019005526A2 (pt) | 2016-10-20 | 2019-06-18 | Pfizer | agentes antiproliferativos para tratamento de pah |
| US10744115B2 (en) | 2017-04-25 | 2020-08-18 | Ischemix Llc | Compositions and methods for treating traumatic brain injury |
| CN107573270B (zh) * | 2017-09-29 | 2019-11-29 | 河南师范大学 | 一种α-甲酰基吡咯烷类化合物的合成方法 |
| CN112839714A (zh) | 2018-10-19 | 2021-05-25 | 豪夫迈·罗氏有限公司 | 用于治疗和预防乙型肝炎病毒疾病的色烯-4-酮衍生物 |
| CN110028475B (zh) * | 2019-05-13 | 2022-07-01 | 中国药科大学 | 基于苯并吡喃结构的新型cdk9抑制剂、其制备方法及应用 |
| KR20220122637A (ko) | 2019-11-28 | 2022-09-02 | 바이엘 악티엔게젤샤프트 | 면역 활성화를 위한 dgk알파 억제제로서의 치환된 아미노퀴놀론 |
| AR121719A1 (es) | 2020-04-03 | 2022-06-29 | Petra Pharma Corp | Inhibidores alostéricos de cromenona del fosfoinosítido 3-quinasa (pi3k) para el tratamiento de enfermedades |
| IL307950A (en) | 2021-05-03 | 2023-12-01 | Petra Pharma Corp | Allosteric chromanone inhibitors of PHOSPHOINOSITIDE 3-KINASE (PI3K) for the treatment of diseases |
| BR112023022890A2 (pt) | 2021-05-27 | 2024-01-23 | Petra Pharma Corp | Inibidores de cromenona alostéricos de fosfoinositídio 3-cinase (pi3k), composições farmacêuticas que os compreendem e usos dos mesmos |
| CN113549044B (zh) * | 2021-07-23 | 2024-01-23 | 中国药科大学 | 8-氮杂环取代色酮类衍生物及其制备方法与制药用途 |
| TW202329930A (zh) | 2021-09-30 | 2023-08-01 | 美商佩特拉製藥公司 | 用於治療疾病之磷酸肌醇3-激酶(pi3k)之異位色烯酮抑制劑 |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE3836676A1 (de) * | 1988-10-28 | 1990-05-03 | Hoechst Ag | Die verwendung von 4h-1-benzopyran-4-on-derivaten, neue 4h-1-benzopyran-4-on-derivate und diese enthaltende arzneimittel |
| US5733920A (en) * | 1995-10-31 | 1998-03-31 | Mitotix, Inc. | Inhibitors of cyclin dependent kinases |
| US5849733A (en) * | 1996-05-10 | 1998-12-15 | Bristol-Myers Squibb Co. | 2-thio or 2-oxo flavopiridol analogs |
| CN1433410A (zh) * | 2000-05-03 | 2003-07-30 | 株式会社Lg生命科学 | 具有3-羟基色烯-4-酮结构的cdk抑制剂 |
-
2003
- 2003-06-24 TW TW092117185A patent/TWI331034B/zh not_active IP Right Cessation
- 2003-07-04 AR ARP030102432A patent/AR041184A1/es unknown
- 2003-07-07 DE DE60321808T patent/DE60321808D1/de not_active Expired - Lifetime
- 2003-07-07 EP EP03753911A patent/EP1556375B1/en not_active Expired - Lifetime
- 2003-07-07 AT AT03753911T patent/ATE399162T1/de active
- 2003-07-07 ES ES03753911T patent/ES2309338T3/es not_active Expired - Lifetime
- 2003-07-07 KR KR1020057000401A patent/KR100991920B1/ko not_active IP Right Cessation
- 2003-07-07 NZ NZ537518A patent/NZ537518A/en not_active IP Right Cessation
- 2003-07-07 JP JP2004519151A patent/JP4860148B2/ja not_active Expired - Lifetime
- 2003-07-07 BR BR0312633-1A patent/BR0312633A/pt not_active IP Right Cessation
- 2003-07-07 PT PT03753911T patent/PT1556375E/pt unknown
- 2003-07-07 CA CA2492130A patent/CA2492130C/en not_active Expired - Fee Related
- 2003-07-07 WO PCT/IN2003/000234 patent/WO2004004632A2/en active IP Right Grant
- 2003-07-07 DK DK03753911T patent/DK1556375T3/da active
- 2003-07-07 AU AU2003272070A patent/AU2003272070B2/en not_active Ceased
- 2003-07-07 MX MXPA05000388A patent/MXPA05000388A/es active IP Right Grant
- 2003-07-07 CN CN038163241A patent/CN1668613B/zh not_active Expired - Lifetime
- 2003-07-07 RU RU2005102939/04A patent/RU2334746C2/ru not_active IP Right Cessation
-
2005
- 2005-01-05 IL IL166153A patent/IL166153A/en active IP Right Grant
- 2005-01-06 ZA ZA200500138A patent/ZA200500138B/en unknown
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2598028C2 (ru) * | 2011-04-13 | 2016-09-20 | Астразенека Аб | Хроменоновые соединения в качестве ингибиторов рi3-киназы для лечения рака |
Also Published As
| Publication number | Publication date |
|---|---|
| CN1668613B (zh) | 2012-07-04 |
| IL166153A (en) | 2009-11-18 |
| EP1556375A2 (en) | 2005-07-27 |
| JP4860148B2 (ja) | 2012-01-25 |
| KR100991920B1 (ko) | 2010-11-04 |
| AU2003272070B2 (en) | 2009-02-26 |
| IL166153A0 (en) | 2006-01-15 |
| CN1668613A (zh) | 2005-09-14 |
| JP2006502109A (ja) | 2006-01-19 |
| AR041184A1 (es) | 2005-05-04 |
| AU2003272070A1 (en) | 2004-01-23 |
| ATE399162T1 (de) | 2008-07-15 |
| DE60321808D1 (de) | 2008-08-07 |
| TW200406202A (en) | 2004-05-01 |
| WO2004004632A2 (en) | 2004-01-15 |
| DK1556375T3 (da) | 2008-11-03 |
| WO2004004632A8 (en) | 2005-03-24 |
| KR20050017110A (ko) | 2005-02-21 |
| WO2004004632A3 (en) | 2004-09-16 |
| BR0312633A (pt) | 2005-07-19 |
| ZA200500138B (en) | 2006-02-22 |
| PT1556375E (pt) | 2008-10-03 |
| NZ537518A (en) | 2008-02-29 |
| TWI331034B (en) | 2010-10-01 |
| CA2492130A1 (en) | 2004-01-15 |
| MXPA05000388A (es) | 2005-09-30 |
| CA2492130C (en) | 2011-09-06 |
| RU2005102939A (ru) | 2005-09-10 |
| ES2309338T3 (es) | 2008-12-16 |
| EP1556375B1 (en) | 2008-06-25 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2334746C2 (ru) | Ингибиторы циклин-зависимых киназ и их применение | |
| EP3386981B1 (en) | Heterocycles useful as anti-cancer agents | |
| JP2006502109A5 (ru) | ||
| WO2022192794A1 (en) | Kras g12d inhibitors | |
| Peng et al. | Efficient synthesis of 5-fluoroalkylated 1H-1, 2, 3-triazoles and application of the bromodifluoromethylated triazole to the synthesis of novel bicyclic gem-difluorinated 1H-pyrano [3, 4-d][1, 2, 3]-triazol-4-one compounds | |
| JP6785384B2 (ja) | 新規なヘテロ環化合物、その製造方法およびこれを含む薬学的組成物 | |
| RU2008136784A (ru) | Пиразолохинолоновые соединения, фармацевтическая композиция на их основе, способ ингибирования поли(адф-рибоза)полимеразы (parp) и способы лечения воспаления, сепсиса, септического шока и рака | |
| PE20040169A1 (es) | Derivados de quinazolin-4-amina como inhibidores de la transduccion de senal inducida por tirosinquinasas | |
| CA2979537A1 (en) | Piperazine carbamates and methods of making and using same | |
| CA2473572A1 (en) | Quinazoline compounds | |
| JP2019031493A (ja) | ベンゾオキサゼピン化合物の作製方法 | |
| US20110136873A1 (en) | Inhibitors of Cyclin Dependent Kinases and Their Use | |
| CA3162253A1 (en) | Inhibitors of enl/af9 yeats | |
| EP3455226A1 (en) | Spirocycle compounds and methods of making and using same | |
| Khademi et al. | Applications of alkyl orthoesters as valuable substrates in organic transformations, focusing on reaction media | |
| KR940009185A (ko) | 피라졸로[4,3-c]피리딘 및 세로토닌 재흡수 억제제로서의 이의 용도 | |
| TNSN05188A1 (en) | 4-aminopyrimidine-5-one | |
| US7271193B2 (en) | Inhibitors of cyclin-dependent kinases and their use | |
| WO2012061012A2 (en) | 4-amino-2h-pyran-2-one analogs as anticancer agents | |
| US6218381B1 (en) | Fused imidazole derivatives as multidrug resistance modulators | |
| A Soleiman | Some fused/isolated heterocyclic of pyrimidine, β-lactam, thiazolidine and triazine derivatives | |
| AU709683C (en) | Fused imidazole derivatives as multidrug resistance modulators | |
| RU2002129898A (ru) | Производные оксазола и их применение в качестве ингибиторов тирозинкиназы | |
| RU2008152246A (ru) | Энантиомерно чистые производные флавона для лечения пролиферативных нарушений и способы их получения |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PD4A | Correction of name of patent owner | ||
| PC41 | Official registration of the transfer of exclusive right |
Effective date: 20120402 |
|
| PC43 | Official registration of the transfer of the exclusive right without contract for inventions |
Effective date: 20130821 |
|
| PD4A | Correction of name of patent owner | ||
| PD4A | Correction of name of patent owner | ||
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20160708 |