JP5425915B2 - 二環5−(トリフルオロメトキシ)−1h−3−インダゾールカルボン酸アミドの合成におけるインダゾール中間体のジアゾニウムフリーの製造方法 - Google Patents
二環5−(トリフルオロメトキシ)−1h−3−インダゾールカルボン酸アミドの合成におけるインダゾール中間体のジアゾニウムフリーの製造方法 Download PDFInfo
- Publication number
- JP5425915B2 JP5425915B2 JP2011530467A JP2011530467A JP5425915B2 JP 5425915 B2 JP5425915 B2 JP 5425915B2 JP 2011530467 A JP2011530467 A JP 2011530467A JP 2011530467 A JP2011530467 A JP 2011530467A JP 5425915 B2 JP5425915 B2 JP 5425915B2
- Authority
- JP
- Japan
- Prior art keywords
- carbon atoms
- alkyl
- alkoxy
- unsubstituted
- substituted
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 238000003786 synthesis reaction Methods 0.000 title description 3
- 230000015572 biosynthetic process Effects 0.000 title description 2
- BAXOFTOLAUCFNW-UHFFFAOYSA-N 1H-indazole Chemical compound C1=CC=C2C=NNC2=C1 BAXOFTOLAUCFNW-UHFFFAOYSA-N 0.000 title 1
- WGRVNULDGDNTPM-UHFFFAOYSA-N 5-(trifluoromethoxy)-1h-indazole-3-carboxamide Chemical compound C1=C(OC(F)(F)F)C=C2C(C(=O)N)=NNC2=C1 WGRVNULDGDNTPM-UHFFFAOYSA-N 0.000 title 1
- 125000002619 bicyclic group Chemical group 0.000 title 1
- 238000004519 manufacturing process Methods 0.000 title 1
- 125000004432 carbon atom Chemical group C* 0.000 claims description 355
- 125000000217 alkyl group Chemical group 0.000 claims description 165
- 125000003545 alkoxy group Chemical group 0.000 claims description 95
- -1 cyano, hydroxy Chemical group 0.000 claims description 76
- 229910052801 chlorine Inorganic materials 0.000 claims description 69
- 229910052731 fluorine Inorganic materials 0.000 claims description 69
- 150000001875 compounds Chemical class 0.000 claims description 61
- 229910052794 bromium Inorganic materials 0.000 claims description 54
- 229910052736 halogen Inorganic materials 0.000 claims description 54
- 150000002367 halogens Chemical class 0.000 claims description 54
- 229910052740 iodine Inorganic materials 0.000 claims description 54
- 125000004043 oxo group Chemical group O=* 0.000 claims description 51
- 125000004663 dialkyl amino group Chemical group 0.000 claims description 48
- 125000000449 nitro group Chemical class [O-][N+](*)=O 0.000 claims description 45
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 claims description 45
- 125000000446 sulfanediyl group Chemical group *S* 0.000 claims description 38
- 238000000034 method Methods 0.000 claims description 27
- 125000000753 cycloalkyl group Chemical group 0.000 claims description 26
- 125000003118 aryl group Chemical group 0.000 claims description 24
- 150000001350 alkyl halides Chemical class 0.000 claims description 20
- 229920006395 saturated elastomer Polymers 0.000 claims description 19
- 239000003153 chemical reaction reagent Substances 0.000 claims description 18
- 125000006413 ring segment Chemical group 0.000 claims description 18
- 150000002576 ketones Chemical class 0.000 claims description 17
- 125000006552 (C3-C8) cycloalkyl group Chemical group 0.000 claims description 16
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 claims description 13
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 claims description 12
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 claims description 12
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 claims description 12
- XHAJMVPMNOBILF-UHFFFAOYSA-N 5-(trifluoromethoxy)-1h-indole-2,3-dione Chemical compound FC(F)(F)OC1=CC=C2NC(=O)C(=O)C2=C1 XHAJMVPMNOBILF-UHFFFAOYSA-N 0.000 claims description 11
- 239000000203 mixture Substances 0.000 claims description 11
- 125000004433 nitrogen atom Chemical group N* 0.000 claims description 11
- 239000002253 acid Substances 0.000 claims description 10
- 238000005576 amination reaction Methods 0.000 claims description 10
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 claims description 9
- 125000002947 alkylene group Chemical group 0.000 claims description 9
- 125000000623 heterocyclic group Chemical group 0.000 claims description 9
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 9
- 229910052757 nitrogen Inorganic materials 0.000 claims description 9
- 229910052760 oxygen Inorganic materials 0.000 claims description 9
- 125000004430 oxygen atom Chemical group O* 0.000 claims description 9
- 125000004434 sulfur atom Chemical group 0.000 claims description 9
- 125000004423 acyloxy group Chemical group 0.000 claims description 6
- 125000003302 alkenyloxy group Chemical group 0.000 claims description 6
- 125000004453 alkoxycarbonyl group Chemical group 0.000 claims description 6
- 125000004457 alkyl amino carbonyl group Chemical group 0.000 claims description 6
- 125000004644 alkyl sulfinyl group Chemical group 0.000 claims description 6
- 125000004390 alkyl sulfonyl group Chemical group 0.000 claims description 6
- 125000004414 alkyl thio group Chemical group 0.000 claims description 6
- 125000005110 aryl thio group Chemical group 0.000 claims description 6
- 125000004104 aryloxy group Chemical group 0.000 claims description 6
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 claims description 6
- 238000005859 coupling reaction Methods 0.000 claims description 6
- 125000004093 cyano group Chemical group *C#N 0.000 claims description 6
- 125000000000 cycloalkoxy group Chemical group 0.000 claims description 6
- 125000006310 cycloalkyl amino group Chemical group 0.000 claims description 6
- 125000005343 heterocyclic alkyl group Chemical group 0.000 claims description 6
- 125000005113 hydroxyalkoxy group Chemical group 0.000 claims description 6
- 125000002768 hydroxyalkyl group Chemical group 0.000 claims description 6
- 230000008569 process Effects 0.000 claims description 6
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 claims description 6
- 125000003232 p-nitrobenzoyl group Chemical group [N+](=O)([O-])C1=CC=C(C(=O)*)C=C1 0.000 claims description 5
- 238000010992 reflux Methods 0.000 claims description 5
- 239000002904 solvent Substances 0.000 claims description 5
- NWUYHJFMYQTDRP-UHFFFAOYSA-N 1,2-bis(ethenyl)benzene;1-ethenyl-2-ethylbenzene;styrene Chemical compound C=CC1=CC=CC=C1.CCC1=CC=CC=C1C=C.C=CC1=CC=CC=C1C=C NWUYHJFMYQTDRP-UHFFFAOYSA-N 0.000 claims description 4
- FPQQSJJWHUJYPU-UHFFFAOYSA-N 3-(dimethylamino)propyliminomethylidene-ethylazanium;chloride Chemical compound Cl.CCN=C=NCCCN(C)C FPQQSJJWHUJYPU-UHFFFAOYSA-N 0.000 claims description 4
- 239000007821 HATU Substances 0.000 claims description 4
- 239000011260 aqueous acid Substances 0.000 claims description 4
- 239000003729 cation exchange resin Substances 0.000 claims description 4
- 230000008878 coupling Effects 0.000 claims description 4
- 238000010168 coupling process Methods 0.000 claims description 4
- NPZTUJOABDZTLV-UHFFFAOYSA-N hydroxybenzotriazole Substances O=C1C=CC=C2NNN=C12 NPZTUJOABDZTLV-UHFFFAOYSA-N 0.000 claims description 4
- 239000012026 peptide coupling reagents Substances 0.000 claims description 4
- LPNYRYFBWFDTMA-UHFFFAOYSA-N potassium tert-butoxide Chemical compound [K+].CC(C)(C)[O-] LPNYRYFBWFDTMA-UHFFFAOYSA-N 0.000 claims description 4
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 4
- LMDZBCPBFSXMTL-UHFFFAOYSA-N 1-Ethyl-3-(3-dimethylaminopropyl)carbodiimide Substances CCN=C=NCCCN(C)C LMDZBCPBFSXMTL-UHFFFAOYSA-N 0.000 claims description 3
- NGNBDVOYPDDBFK-UHFFFAOYSA-N 2-[2,4-di(pentan-2-yl)phenoxy]acetyl chloride Chemical compound CCCC(C)C1=CC=C(OCC(Cl)=O)C(C(C)CCC)=C1 NGNBDVOYPDDBFK-UHFFFAOYSA-N 0.000 claims description 3
- 125000005079 alkoxycarbonylmethyl group Chemical group 0.000 claims description 3
- 125000004429 atom Chemical group 0.000 claims description 3
- 125000001316 cycloalkyl alkyl group Chemical group 0.000 claims description 3
- 238000010438 heat treatment Methods 0.000 claims description 3
- 239000012442 inert solvent Substances 0.000 claims description 3
- JSJHFVPWEPFNMH-BTQNPOSSSA-N n-[(3s)-1-azabicyclo[2.2.2]octan-3-yl]-5-(trifluoromethoxy)-1h-indazole-3-carboxamide;hydrochloride Chemical compound Cl.C1N(CC2)CCC2[C@@H]1NC(=O)C1=NNC2=CC=C(OC(F)(F)F)C=C21 JSJHFVPWEPFNMH-BTQNPOSSSA-N 0.000 claims description 3
- QDHHCQZDFGDHMP-UHFFFAOYSA-N Chloramine Chemical compound ClN QDHHCQZDFGDHMP-UHFFFAOYSA-N 0.000 claims description 2
- DQPBABKTKYNPMH-UHFFFAOYSA-N amino hydrogen sulfate Chemical compound NOS(O)(=O)=O DQPBABKTKYNPMH-UHFFFAOYSA-N 0.000 claims description 2
- 230000007062 hydrolysis Effects 0.000 claims description 2
- 238000006460 hydrolysis reaction Methods 0.000 claims description 2
- 230000003301 hydrolyzing effect Effects 0.000 claims description 2
- SJGALSBBFTYSBA-UHFFFAOYSA-N oxaziridine Chemical compound C1NO1 SJGALSBBFTYSBA-UHFFFAOYSA-N 0.000 claims description 2
- 229910052799 carbon Inorganic materials 0.000 claims 2
- 125000003236 benzoyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C(*)=O 0.000 claims 1
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 12
- DJKYXGHMEGLNLG-UHFFFAOYSA-N 5-(trifluoromethoxy)-1h-indazole-3-carboxylic acid Chemical compound C1=C(OC(F)(F)F)C=C2C(C(=O)O)=NNC2=C1 DJKYXGHMEGLNLG-UHFFFAOYSA-N 0.000 description 11
- 238000006243 chemical reaction Methods 0.000 description 11
- 239000000243 solution Substances 0.000 description 11
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 10
- ZUOUZKKEUPVFJK-UHFFFAOYSA-N diphenyl Chemical compound C1=CC=CC=C1C1=CC=CC=C1 ZUOUZKKEUPVFJK-UHFFFAOYSA-N 0.000 description 10
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 10
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 9
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 8
- 239000003814 drug Substances 0.000 description 7
- 229940079593 drug Drugs 0.000 description 7
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 6
- 239000004305 biphenyl Substances 0.000 description 5
- 235000010290 biphenyl Nutrition 0.000 description 5
- 125000001624 naphthyl group Chemical group 0.000 description 5
- 150000003839 salts Chemical class 0.000 description 5
- DLFVBJFMPXGRIB-UHFFFAOYSA-N Acetamide Chemical compound CC(N)=O DLFVBJFMPXGRIB-UHFFFAOYSA-N 0.000 description 4
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 4
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 4
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 4
- 235000019439 ethyl acetate Nutrition 0.000 description 4
- 239000012044 organic layer Substances 0.000 description 4
- 229940002612 prodrug Drugs 0.000 description 4
- 239000000651 prodrug Substances 0.000 description 4
- 102000005962 receptors Human genes 0.000 description 4
- 108020003175 receptors Proteins 0.000 description 4
- 239000011347 resin Substances 0.000 description 4
- 229920005989 resin Polymers 0.000 description 4
- 239000000126 substance Substances 0.000 description 4
- 125000000094 2-phenylethyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])C([H])([H])* 0.000 description 3
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 3
- 102000004190 Enzymes Human genes 0.000 description 3
- 108090000790 Enzymes Proteins 0.000 description 3
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 3
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 3
- 235000011114 ammonium hydroxide Nutrition 0.000 description 3
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 3
- 238000007385 chemical modification Methods 0.000 description 3
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 3
- 238000004128 high performance liquid chromatography Methods 0.000 description 3
- 239000004031 partial agonist Substances 0.000 description 3
- 238000002360 preparation method Methods 0.000 description 3
- 239000011541 reaction mixture Substances 0.000 description 3
- 208000024827 Alzheimer disease Diseases 0.000 description 2
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 description 2
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 2
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 2
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 2
- 208000012902 Nervous system disease Diseases 0.000 description 2
- 208000025966 Neurological disease Diseases 0.000 description 2
- 102000019315 Nicotinic acetylcholine receptors Human genes 0.000 description 2
- 108050006807 Nicotinic acetylcholine receptors Proteins 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- 125000003668 acetyloxy group Chemical group [H]C([H])([H])C(=O)O[*] 0.000 description 2
- XXXHSQBVHSJQKS-UHFFFAOYSA-N amino benzoate Chemical class NOC(=O)C1=CC=CC=C1 XXXHSQBVHSJQKS-UHFFFAOYSA-N 0.000 description 2
- 239000000908 ammonium hydroxide Substances 0.000 description 2
- 239000002585 base Substances 0.000 description 2
- 239000012267 brine Substances 0.000 description 2
- 229920001429 chelating resin Polymers 0.000 description 2
- 239000003795 chemical substances by application Substances 0.000 description 2
- 125000004122 cyclic group Chemical group 0.000 description 2
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 2
- 125000004186 cyclopropylmethyl group Chemical group [H]C([H])(*)C1([H])C([H])([H])C1([H])[H] 0.000 description 2
- 125000001664 diethylamino group Chemical group [H]C([H])([H])C([H])([H])N(*)C([H])([H])C([H])([H])[H] 0.000 description 2
- 230000001747 exhibiting effect Effects 0.000 description 2
- 238000001727 in vivo Methods 0.000 description 2
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 2
- 239000010410 layer Substances 0.000 description 2
- 150000007522 mineralic acids Chemical class 0.000 description 2
- 238000005580 one pot reaction Methods 0.000 description 2
- 150000007524 organic acids Chemical class 0.000 description 2
- 239000003960 organic solvent Substances 0.000 description 2
- 230000000144 pharmacologic effect Effects 0.000 description 2
- 239000000047 product Substances 0.000 description 2
- 208000020016 psychiatric disease Diseases 0.000 description 2
- 238000000746 purification Methods 0.000 description 2
- 230000008929 regeneration Effects 0.000 description 2
- 238000011069 regeneration method Methods 0.000 description 2
- 238000007142 ring opening reaction Methods 0.000 description 2
- YGSDEFSMJLZEOE-UHFFFAOYSA-N salicylic acid Chemical compound OC(=O)C1=CC=CC=C1O YGSDEFSMJLZEOE-UHFFFAOYSA-N 0.000 description 2
- 201000000980 schizophrenia Diseases 0.000 description 2
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 2
- WGTYBPLFGIVFAS-UHFFFAOYSA-M tetramethylammonium hydroxide Chemical compound [OH-].C[N+](C)(C)C WGTYBPLFGIVFAS-UHFFFAOYSA-M 0.000 description 2
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 2
- BJEPYKJPYRNKOW-REOHCLBHSA-N (S)-malic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O BJEPYKJPYRNKOW-REOHCLBHSA-N 0.000 description 1
- DHKHKXVYLBGOIT-UHFFFAOYSA-N 1,1-Diethoxyethane Chemical group CCOC(C)OCC DHKHKXVYLBGOIT-UHFFFAOYSA-N 0.000 description 1
- ASOKPJOREAFHNY-UHFFFAOYSA-N 1-Hydroxybenzotriazole Chemical compound C1=CC=C2N(O)N=NC2=C1 ASOKPJOREAFHNY-UHFFFAOYSA-N 0.000 description 1
- REUAXQZIRFXQML-UHFFFAOYSA-N 1-azabicyclo[2.2.2]octan-3-amine Chemical compound C1CC2C(N)CN1CC2 REUAXQZIRFXQML-UHFFFAOYSA-N 0.000 description 1
- STZHBULOYDCZET-UHFFFAOYSA-N 1-azabicyclo[2.2.2]octan-3-amine;hydron;dichloride Chemical compound Cl.Cl.C1CC2C(N)CN1CC2 STZHBULOYDCZET-UHFFFAOYSA-N 0.000 description 1
- FQNVBVOKMHHXCE-UHFFFAOYSA-N 1-methoxyindole-2,3-dione Chemical compound C1=CC=C2N(OC)C(=O)C(=O)C2=C1 FQNVBVOKMHHXCE-UHFFFAOYSA-N 0.000 description 1
- ZNRGQMMCGHDTEI-UHFFFAOYSA-N 1H-indole-3-carboxylic acid (8-methyl-8-azabicyclo[3.2.1]octan-3-yl) ester Chemical compound C1=CC=C2C(C(=O)OC3CC4CCC(C3)N4C)=CNC2=C1 ZNRGQMMCGHDTEI-UHFFFAOYSA-N 0.000 description 1
- BHXVYTQDWMQVBI-UHFFFAOYSA-N 1h-indazole-3-carboxylic acid Chemical compound C1=CC=C2C(C(=O)O)=NNC2=C1 BHXVYTQDWMQVBI-UHFFFAOYSA-N 0.000 description 1
- MEKOFIRRDATTAG-UHFFFAOYSA-N 2,2,5,8-tetramethyl-3,4-dihydrochromen-6-ol Chemical compound C1CC(C)(C)OC2=C1C(C)=C(O)C=C2C MEKOFIRRDATTAG-UHFFFAOYSA-N 0.000 description 1
- BMYNFMYTOJXKLE-UHFFFAOYSA-N 3-azaniumyl-2-hydroxypropanoate Chemical compound NCC(O)C(O)=O BMYNFMYTOJXKLE-UHFFFAOYSA-N 0.000 description 1
- QCQCHGYLTSGIGX-GHXANHINSA-N 4-[[(3ar,5ar,5br,7ar,9s,11ar,11br,13as)-5a,5b,8,8,11a-pentamethyl-3a-[(5-methylpyridine-3-carbonyl)amino]-2-oxo-1-propan-2-yl-4,5,6,7,7a,9,10,11,11b,12,13,13a-dodecahydro-3h-cyclopenta[a]chrysen-9-yl]oxy]-2,2-dimethyl-4-oxobutanoic acid Chemical compound N([C@@]12CC[C@@]3(C)[C@]4(C)CC[C@H]5C(C)(C)[C@@H](OC(=O)CC(C)(C)C(O)=O)CC[C@]5(C)[C@H]4CC[C@@H]3C1=C(C(C2)=O)C(C)C)C(=O)C1=CN=CC(C)=C1 QCQCHGYLTSGIGX-GHXANHINSA-N 0.000 description 1
- QGZKDVFQNNGYKY-UHFFFAOYSA-O Ammonium Chemical compound [NH4+] QGZKDVFQNNGYKY-UHFFFAOYSA-O 0.000 description 1
- OTDUKQFGAUNNCS-UHFFFAOYSA-N CC1N2CCN(C)C1CC2 Chemical compound CC1N2CCN(C)C1CC2 OTDUKQFGAUNNCS-UHFFFAOYSA-N 0.000 description 1
- UWBYHCLTULMDDX-UHFFFAOYSA-N CNC1C(CC2)CCN2C1 Chemical compound CNC1C(CC2)CCN2C1 UWBYHCLTULMDDX-UHFFFAOYSA-N 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 125000004442 acylamino group Chemical group 0.000 description 1
- 239000000556 agonist Substances 0.000 description 1
- 125000003282 alkyl amino group Chemical group 0.000 description 1
- BJEPYKJPYRNKOW-UHFFFAOYSA-N alpha-hydroxysuccinic acid Natural products OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 1
- 230000004075 alteration Effects 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 150000001408 amides Chemical class 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 230000000975 bioactive effect Effects 0.000 description 1
- 230000036983 biotransformation Effects 0.000 description 1
- 210000004556 brain Anatomy 0.000 description 1
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 1
- 150000003857 carboxamides Chemical class 0.000 description 1
- 230000003197 catalytic effect Effects 0.000 description 1
- 210000003169 central nervous system Anatomy 0.000 description 1
- 238000003889 chemical engineering Methods 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- 235000015165 citric acid Nutrition 0.000 description 1
- 239000007822 coupling agent Substances 0.000 description 1
- 125000004851 cyclopentylmethyl group Chemical group C1(CCCC1)C* 0.000 description 1
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 1
- 238000010511 deprotection reaction Methods 0.000 description 1
- 239000012954 diazonium Substances 0.000 description 1
- 238000006193 diazotization reaction Methods 0.000 description 1
- 125000001891 dimethoxy group Chemical group [H]C([H])([H])O* 0.000 description 1
- 239000002552 dosage form Substances 0.000 description 1
- 239000003937 drug carrier Substances 0.000 description 1
- 238000012377 drug delivery Methods 0.000 description 1
- 239000003118 drug derivative Substances 0.000 description 1
- 238000002330 electrospray ionisation mass spectrometry Methods 0.000 description 1
- 230000002255 enzymatic effect Effects 0.000 description 1
- 239000012467 final product Substances 0.000 description 1
- 125000004175 fluorobenzyl group Chemical group 0.000 description 1
- 239000012458 free base Substances 0.000 description 1
- 239000001530 fumaric acid Substances 0.000 description 1
- 235000011087 fumaric acid Nutrition 0.000 description 1
- 125000002541 furyl group Chemical group 0.000 description 1
- XMBWDFGMSWQBCA-UHFFFAOYSA-N hydrogen iodide Chemical compound I XMBWDFGMSWQBCA-UHFFFAOYSA-N 0.000 description 1
- 229940071870 hydroiodic acid Drugs 0.000 description 1
- 125000002883 imidazolyl group Chemical group 0.000 description 1
- 150000007529 inorganic bases Chemical class 0.000 description 1
- 238000005907 ketalization reaction Methods 0.000 description 1
- 239000004310 lactic acid Substances 0.000 description 1
- 235000014655 lactic acid Nutrition 0.000 description 1
- 239000001630 malic acid Substances 0.000 description 1
- 235000011090 malic acid Nutrition 0.000 description 1
- 230000001404 mediated effect Effects 0.000 description 1
- 230000004060 metabolic process Effects 0.000 description 1
- 229940098779 methanesulfonic acid Drugs 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 125000002757 morpholinyl group Chemical group 0.000 description 1
- LNOPIUAQISRISI-UHFFFAOYSA-N n'-hydroxy-2-propan-2-ylsulfonylethanimidamide Chemical compound CC(C)S(=O)(=O)CC(N)=NO LNOPIUAQISRISI-UHFFFAOYSA-N 0.000 description 1
- PSHKMPUSSFXUIA-UHFFFAOYSA-N n,n-dimethylpyridin-2-amine Chemical compound CN(C)C1=CC=CC=N1 PSHKMPUSSFXUIA-UHFFFAOYSA-N 0.000 description 1
- BAJXGRSDFUMTTO-CYBMUJFWSA-N n-[(3s)-1-azabicyclo[2.2.2]octan-3-yl]-5-(trifluoromethoxy)-1h-indazole-3-carboxamide Chemical compound C1N(CC2)CCC2[C@@H]1NC(=O)C1=NNC2=CC=C(OC(F)(F)F)C=C21 BAJXGRSDFUMTTO-CYBMUJFWSA-N 0.000 description 1
- 229910017604 nitric acid Inorganic materials 0.000 description 1
- 231100000252 nontoxic Toxicity 0.000 description 1
- 230000003000 nontoxic effect Effects 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 235000006408 oxalic acid Nutrition 0.000 description 1
- FJKROLUGYXJWQN-UHFFFAOYSA-N papa-hydroxy-benzoic acid Natural products OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 1
- 238000005897 peptide coupling reaction Methods 0.000 description 1
- 239000000546 pharmaceutical excipient Substances 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 230000003389 potentiating effect Effects 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 125000006239 protecting group Chemical group 0.000 description 1
- 125000000719 pyrrolidinyl group Chemical group 0.000 description 1
- 125000001453 quaternary ammonium group Chemical group 0.000 description 1
- 238000001953 recrystallisation Methods 0.000 description 1
- 238000007100 recyclization reaction Methods 0.000 description 1
- 230000001172 regenerating effect Effects 0.000 description 1
- 229960004889 salicylic acid Drugs 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- URGAHOPLAPQHLN-UHFFFAOYSA-N sodium aluminosilicate Chemical class [Na+].[Al+3].[O-][Si]([O-])=O.[O-][Si]([O-])=O URGAHOPLAPQHLN-UHFFFAOYSA-N 0.000 description 1
- 235000017557 sodium bicarbonate Nutrition 0.000 description 1
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- 125000000335 thiazolyl group Chemical group 0.000 description 1
- 125000001544 thienyl group Chemical group 0.000 description 1
- 125000005301 thienylmethyl group Chemical group [H]C1=C([H])C([H])=C(S1)C([H])([H])* 0.000 description 1
- 125000004568 thiomorpholinyl group Chemical group 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 1
- 230000009466 transformation Effects 0.000 description 1
- GKASDNZWUGIAMG-UHFFFAOYSA-N triethyl orthoformate Chemical compound CCOC(OCC)OCC GKASDNZWUGIAMG-UHFFFAOYSA-N 0.000 description 1
- ZNRGQMMCGHDTEI-ITGUQSILSA-N tropisetron Chemical compound C1=CC=C2C(C(=O)O[C@H]3C[C@H]4CC[C@@H](C3)N4C)=CNC2=C1 ZNRGQMMCGHDTEI-ITGUQSILSA-N 0.000 description 1
- 229960003688 tropisetron Drugs 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D453/00—Heterocyclic compounds containing quinuclidine or iso-quinuclidine ring systems, e.g. quinine alkaloids
- C07D453/02—Heterocyclic compounds containing quinuclidine or iso-quinuclidine ring systems, e.g. quinine alkaloids containing not further condensed quinuclidine ring systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/415—1,2-Diazoles
- A61K31/416—1,2-Diazoles condensed with carbocyclic ring systems, e.g. indazole
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D231/00—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings
- C07D231/54—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings condensed with carbocyclic rings or ring systems
- C07D231/56—Benzopyrazoles; Hydrogenated benzopyrazoles
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Neurology (AREA)
- Engineering & Computer Science (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Neurosurgery (AREA)
- Biomedical Technology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Epidemiology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Low-Molecular Organic Synthesis Reactions Using Catalysts (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Indole Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
Description
本発明は、ニコチン性α−7受容体のアゴニスト及び部分アゴニストとして活性がある式(1)の種々の二環アミドの調製の有用な前躯体である5−(トリフルオロメトキシ)−1H−3−インダゾールカルボン酸(3)の新規な調製方法を提供する。式(1)の化合物は、不全又は異常機能ニコチン性アセチルコリン受容体に関連する病状、とりわけ脳の病状の処置、例えば、アルツハイマー病及び統合失調症の処置、ならびに他の精神障害及び神経障害の処置におけるその使用のために研究されている。本発明は、スケールアップしたレベルで化合物(3)を調製するのに有用である。
式(1)の二環インダゾールアミドは、WO 2005/063767、WO 2005/092890、WO 2005/111038、WO 2006/001894及びWO 2006/069097に記載されている。
[式中、
R2は、H、あるいは非置換であるか、又はF、Cl、Br、I、CN、OH、1〜4個の炭素原子を有するアルコキシ(例えばOCH3)、NR4R5、若しくはその組み合わせにより1回以上置換されているC1−4−アルキル(例えばCH3)であり;
R4及びR5は、各々独立してH、あるいは各々が非置換であるか、又はF、Cl、Br、I、CN、OH、1〜4個の炭素原子を有するアルコキシ(例えばOCH3)、モノアルキルアミノ、ジアルキルアミノ(例えばジエチルアミノ)、C3−8−シクロアルキル、若しくはその組み合わせにより1回以上置換されている、Ar、Ar−C1−4−アルキル、Het、C1−4−アルキル(例えばCH3)、C3−8−シクロアルキル(例えばシクロプロピル)、若しくはC4−8−シクロアルキルアルキル(例えばシクロプロピルメチル)であり、そして
mは、1、2又は3である]であるか;
あるいは
R1は、A1[ここで、A1は、
であり;
式中、R6〜R14は、各々独立して
H、
非置換であるか、又はF、Cl、Br、I、CN、1〜4個の炭素原子を有するアルコキシ(例えばOCH3)、Ar(例えばフェニル)、若しくはその組み合わせにより1回以上置換されているC1−4−アルキル(例えばCH3)、
非置換であるか、又はF、Cl、Br、I、CN、1〜4個の炭素原子を有するアルコキシ(例えばOCH3)、Ar(例えばフェニル)、若しくはその組み合わせにより1回以上置換されているC3−6−アルケニル、
非置換であるか、あるいはF、Cl、Br、I、CN、1〜4個の炭素原子を有するアルコキシ(例えばOCH3)、若しくはAr(例えばフェニル)又はその組み合わせにより1回以上置換されているC3−6−アルキニル、
非置換であるか、又はハロゲン、ヒドロキシ、オキソ、シアノ、1〜4個の炭素原子を有するアルキル、1〜4個の炭素原子を有するアルコキシ、若しくはその組み合わせにより1回以上置換されている3〜10個、好ましくは3〜8個の炭素原子を有するシクロアルキル(例えばシクロペンチル)、
非置換であるか、あるいはシクロアルキル部分及び/又はアルキル部分においてハロゲン、オキソ、シアノ、ヒドロキシ、C1−4−アルキル、C1−4−アルコキシ、若しくはその組み合わせにより1回以上置換されている、4〜16個、好ましくは4〜12個の炭素原子を有するシクロアルキルアルキル(例えばシクロペンチルメチル、シクロプロピルメチルなど)、
Ar−アルキル(例えばベンジル)、あるいは
Het−アルキル(例えばチエニルメチル)であり;
ここで、
Arは、
非置換であるか、あるいは
1〜8個の炭素原子を有するアルキル、
1〜8個の炭素原子を有するアルコキシ、
ハロゲン(F、Cl、Br若しくはI、好ましくはF若しくはCl)、
アミノ、
シアノ、
ヒドロキシル、
ニトロ、
1〜8個の炭素原子を有するハロゲン化アルキル、
1〜8個の炭素原子を有するハロゲン化アルコキシ、
1〜8個の炭素原子を有するヒドロキシアルキル、
2〜8個の炭素原子を有するヒドロキシアルコキシ、
3〜8個の炭素原子を有するアルケニルオキシ、
1〜8個の炭素原子を有するモノアルキルアミノ、
ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、
カルボキシ、
アルコキシカルボニル、
アルキルアミノカルボニル、
アシルアミド(例えばアセトアミド)、
アシルオキシ(例えばアセトキシ)、
1〜8個の炭素原子を有するアルキルチオ、
1〜8個の炭素原子を有するアルキルスルフィニル、
1〜8個の炭素原子を有するアルキルスルホニル、
スルホ、
スルホニルアミノ、
Het、
シクロアルキルアミノ(ここで、シクロアルキル基は、3〜7個の炭素原子を有し、かつハロゲン(F、Cl、Br若しくはI、好ましくはF若しくはCl)、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個の炭素原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ又はチオにより場合により置換されている)、
アリールオキシ(ここで、アリール部分は、6〜10個の炭素原子を含み(例えばフェニル、ナフチル、ビフェニル)、かつハロゲン(F、Cl、Br若しくはI、好ましくはF若しくはCl)、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個の炭素原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ又はチオにより場合により置換されている)、
アリールチオ(ここで、アリール部分は、6〜10個の炭素原子を含み(例えばフェニル、ナフチル、ビフェニル)、かつハロゲン(F、Cl、Br若しくはI、好ましくはF若しくはCl)、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個の炭素原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ又はチオにより場合により置換されている)、
シクロアルキルオキシ(ここで、シクロアルキル基は、3〜7個の炭素原子を有し、かつハロゲン(F、Cl、Br若しくはI、好ましくはF若しくはCl)、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個の炭素原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ又はチオにより場合により置換されている)、又は
その組合せにより1回以上置換されている6〜10個の炭素原子を含むアリール基であり;
Ar−アルキルは、
アリール−アルキレン基(例えばベンジル、フェネチル、フェンプロピル)(ここで、アルキレン部分は、1〜4個の炭素原子を含み、かつ非置換であるか、又はハロゲン(F、Cl、Br若しくはI、好ましくはF若しくはCl)、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個の炭素原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ、若しくはチオにより1回以上置換されており、そしてアリール部分は上記で定義されるArである)であり;そして
Hetは、
完全飽和、部分飽和又は完全不飽和であり、少なくとも1個の環原子がN、O又はS原子である5〜10個の環原子を有し、非置換であるか、あるいは
1〜8個の炭素原子を有するアルキル、
1〜8個の炭素原子を有するアルコキシ、
ハロゲン(F、Cl、Br若しくはI、好ましくはF若しくはCl)、
アミノ、
シアノ、
ヒドロキシル、
ニトロ、
1〜8個の炭素原子を有するハロゲン化アルキル、
1〜8個の炭素原子を有するハロゲン化アルコキシ、
1〜8個の炭素原子を有するヒドロキシアルキル、
2〜8個の炭素原子を有するヒドロキシアルコキシ、
3〜8個の炭素原子を有するアルケニルオキシ、
1〜8個の炭素原子を有するモノアルキルアミノ、
ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、
カルボキシ、
アルコキシカルボニル、
アルコキシカルボニルメチル、
アルキルアミノカルボニル、
アシルアミド(例えばアセトアミド)、
アシルオキシ(例えばアセトキシ)、
1〜8個の炭素原子を有するアルキルチオ、
1〜8個の炭素原子を有するアルキルスルフィニル、
1〜8個の炭素原子を有するアルキルスルホニル、
オキソ、
スルホ、
スルホニルアミノ、
シクロアルキルアミノ(ここで、シクロアルキル基は、3〜7個の炭素原子を有し、かつハロゲン(F、Cl、Br若しくはI、好ましくはF若しくはCl)、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個の炭素原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ又はチオにより場合により置換されている)、
アリール(6〜10個の炭素原子を含み(例えばフェニル、ナフチル、ビフェニル)、かつハロゲン(F、Cl、Br若しくはI、好ましくはF若しくはCl)、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個の炭素原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ又はチオにより場合により置換されている)、
アリール−アルキレン基(例えばベンジル、フェネチル、フェンプロピル)(ここで、アリール部分は6〜10個の炭素原子を含み、アルキレン部分は1〜4個の炭素原子を含み、そして非置換であるか、又はハロゲン(F、Cl、Br若しくはI、好ましくはF若しくはCl)、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個の炭素原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ若しくはチオにより1回以上置換されている)、
アリールオキシ(ここで、アリール部分は、6〜10個の炭素原子を含み(例えばフェニル、ナフチル、ビフェニル)、かつハロゲン(F、Cl、Br若しくはI、好ましくはF若しくはCl)、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は1〜8個のC原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ又はチオにより場合により置換されている)、
アリールチオ(ここで、アリール部分は、6〜10個の炭素原子を含み(例えばフェニル、ナフチル、ビフェニル)、かつハロゲン(F、Cl、Br若しくはI、好ましくはF若しくはCl)、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個の炭素原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ又はチオにより場合により置換されている)、
シクロアルキルオキシ(ここで、シクロアルキル基は、3〜7個の炭素原子を有し、かつハロゲン(F、Cl、Br若しくはI、好ましくはF若しくはCl)、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個の炭素原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ又はチオにより場合により置換されている)、
複素環式基(完全飽和、部分飽和又は完全不飽和であり、少なくとも1個の環原子がN、O又はS原子である5〜10個の環原子を有し、非置換であるか、又はハロゲン(F、Cl、Br若しくはI、好ましくはF若しくはCl)、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個の炭素原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ、若しくはチオにより1回以上置換されている)(例えばフリル、チエニル、メチルチエニル、ビチエニル、ベンジルピラゾリル、チアゾリル、イミダゾリル、メチルイミダゾリル、ピロリジニル、モルホリニル、チオモルホリニル)、
複素環式−アルキル基(ここで、複素環部分は完全飽和、部分飽和又は完全不飽和であり、少なくとも1個の環原子がN、O又はS原子である5〜10個の環原子を有し、アルキル部分は1〜4個の炭素原子を含むアルキレン基であり、ここで、該複素環式−アルキル基は非置換であるか、あるいはハロゲン(F、Cl、Br若しくはI、好ましくはF若しくはCl)、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個の炭素原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ、又はチオにより1回以上置換されている)(例えばピペリジニルエチル)、又は
その組み合わせにより1回以上置換されている複素環式基であり;
R15及びR16は、各々独立して
H、
Ar、
Ar−アルキル(例えばベンジル、フルオロベンジル、メトキシベンジル、フェネチル、フェンプロピル)、
Het、
非置換であるか、又はF、Cl、Br、I、CN、OH、1〜4個の炭素原子を有するアルコキシ(例えばOCH3)、モノアルキルアミノ、ジアルキルアミノ(例えばジエチルアミノ)、C3−8−シクロアルキル、若しくはその組み合わせにより1回以上置換されているC1−4−アルキル(例えばCH3)、
非置換であるか、又はハロゲン、ヒドロキシ、オキソ、シアノ、1〜4個の炭素原子を有するアルキル、1〜4個の炭素原子を有するアルコキシ、若しくはその組み合わせにより1回以上置換されている3〜10個、好ましくは3〜8個の炭素原子を有するシクロアルキル(例えばシクロペンチル)、
非置換であるか、又はF、Cl、Br、I、CN、1〜4個の炭素原子を有するアルコキシ(例えばOCH3)、Ar(例えばフェニル)、若しくはその組み合わせにより1回以上置換されているC3−6−アルケニル、あるいは
非置換であるか、あるいはF、Cl、Br、I、CN、1〜4個の炭素原子を有するアルコキシ(例えばOCH3)、若しくはAr(例えばフェニル)又はその組み合わせにより1回以上置換されているC3−6−アルキニルであり;
R17は、H、
非置換であるか、又はF、Cl、Br、I、CN、OH、1〜4個の炭素原子を有するアルコキシ(例えばOCH3)、NR15R16、SH、SR15、SOR16、C3−8−シクロアルキル、SO2R15、SO2NR15R16、Ar、Het、若しくはその組み合わせにより1回以上置換されているC1−6−アルキル(例えばCH3)、
非置換であるか、又はF、Cl、Br、I、CN、OH、1〜4個の炭素原子を有するアルコキシ(例えばOCH3)、NR15R16、SH、SR15、SOR15、C3−8−シクロアルキル、SO2R15、SO2NR15R16、Ar、Het、若しくはその組み合わせにより1回以上置換されているC3−6−アルケニル、
非置換であるか、又はF、Cl、Br、I、CN、OH、1〜4個の炭素原子を有するアルコキシ(例えばOCH3)、NR15R16、SH、SR15、SOR15、C3−8−シクロアルキル、SO2R15、SO2NR15R16、Ar、Het、若しくはその組み合わせにより1回以上置換されているC3−6−アルキニル、
非置換であるか、又はF、Cl、Br、I、CN、OH、1〜4個の炭素原子を有するアルコキシ(例えばOCH3)、NR15R16、SH、SR15、SOR15、非置換C3−8−シクロアルキル、SO2R15、SO2NR15R16、Ar、Het、若しくはその組み合わせにより1回以上置換されているC3−8−シクロアルキル、
非置換であるか、又はF、Cl、Br、I、CN、OH、1〜4個の炭素原子を有するアルコキシ(例えば、OCH3)、NR15R16、SH、SR15、SOR15、非置換C3−8−シクロアルキル、SO2R15、SO2NR15R16、Ar、Het、若しくはその組み合わせにより1回以上置換されているC4−8−シクロアルキルアルキル
であり、
mは、上記のとおりであり;そして
oは、1又は2である]であるか;
あるいは
R1は、
本発明は、式:
で示される化合物(3)の調製方法であって、以下:
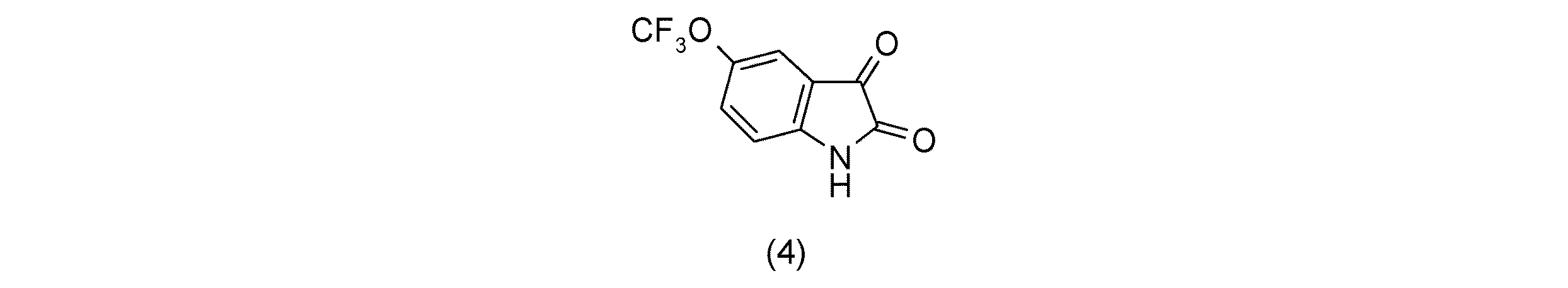
(a)溶媒中、5−トリフルオロメトキシイサチンをケトン保護試薬と反応させてケトンが保護された化合物を得る工程;
(b)不活性溶媒中、工程(a)からのケトンが保護された化合物を求電子アミノ化試薬で処理して求電子的にアミノ化された化合物を得る工程;及び
(c)塩基性条件下、工程(b)からの求電子的にアミノ化された化合物を加水分解して開環中間体を形成し、中間体を酸水溶液で処理して中間体を閉環し、ケトン保護試薬を除去して(3)を得る工程
を含む方法を提供する。
本明細書で使用されるとき、以下の用語は、以下に示す意味を有する。
実施例1
エタノールでの5−トリフルオロメトキシイサチン(4)のケタール化(工程1)
O−ベンゾイルヒドロキシルアミンでの3,3−ジエトキシ−5−トリフルオロメトキシイサチン(7)のアミノ化(工程2)
N−アミノ−3,3−ジエトキシ−5−トリフルオロメトキシイサチン(6)の開環、脱保護及び再環化(工程3)
3−アミノキヌクリジンとカルボン酸をカップリングして対応するカルボキサミドを形成する方法
N,N−ジメチルホルムアミド(65mL)中のカルボン酸(16.1mmol)の溶液に、HBTU(16.1mmol)又はHATU(16.1mmol)、触媒量のジメチルアミノピリジン、N,N−ジイソプロピルエチルアミン(96.6mmol)及び4Å活性化モレキュラーシーブ(2.6g)を加えた。反応混合物を、窒素下、室温で2時間維持し、次に3−アミノキヌクリジン二塩酸塩(16.1mmol)を加えた。18時間後、溶媒を減圧下で除去した。油状残留物を、飽和重炭酸ナトリウム水溶液(25mL)とジクロロメタン(100mL)とに分配した。水層をさらに9/1 ジクロロメタン/メタノール(5×100mL)で抽出し、合わせた有機層を濃縮した。残留物を、クロマトグラフィー[90/10/1 ジクロロメタン/メタノール/水酸化アンモニウム又は1/1〜0/1 酢酸エチル/(70/30/1 酢酸エチル/メタノール/水酸化アンモニウム)]、又は分取HPLCにより精製して、生成物を収率30%〜70%で得た。
N−[(3S)−1−アザビシクロ[2.2.2]オクタ−3−イル]−5−(トリフルオロメトキシ)−1H−インダゾール−3−カルボキサミド塩酸塩
Claims (15)
- 式:
で示される化合物(3)の調製方法であって、以下:
(a)溶媒中、5−トリフルオロメトキシイサチンをケトン保護試薬と反応させてケトンが保護された化合物を得る工程;
(b)不活性溶媒中、工程(a)からのケトンが保護された化合物をクロロアミン、ヒドロキシルアミン−O−スルホン酸、窒素原子において非置換であるオキサジリジン、N−アシルオキサジリジン又は4−ニトロベンゾイルO−ヒドロキシルアミンで処理して求電子的にアミノ化された化合物を得る工程;及び
(c)塩基性条件下、工程(b)からの求電子的にアミノ化された化合物を加水分解して開環中間体を形成し、中間体を酸水溶液で処理して中間体を閉環し、ケトン保護基を脱保護して(3)を得る工程
を含む方法。 - 工程(a)におけるケトン保護試薬が、HC(OEt)3/EtOHである、請求項1に記載の方法。
- 工程(a)におけるケトンが保護された化合物が、3,3−ジエトキシ−5−トリフルオロメトキシイサチンである、請求項1に記載の方法。
- 工程(a)におけるケトンが保護された化合物を、5−トリフルオロメトキシイサチンと、酸カチオン交換樹脂と、HC(OEt)3と、無水エタノールとの混合物を加熱還流することにより調製する、請求項1に記載の方法。
- 工程(b)における求電子アミノ化試薬が、4−ニトロベンゾイルO−ヒドロキシルアミンである、請求項1に記載の方法。
- 工程(b)における求電子的にアミノ化された化合物が、N−アミノ−3,3−ジエトキシ−5−トリフルオロメトキシイサチンである、請求項1に記載の方法。
- 工程(b)における求電子的にアミノ化された化合物を、3,3−ジエトキシ−5−トリフルオロメトキシイサチンとN−メチルピロリドンとを順次混合し、混合物に、<25℃で、テトラヒドロフラン中のカリウムtert−ブトキシド溶液を加え、次に該混合物に、N−メチルピロリドン中の4−ニトロベンゾイルO−ヒドロキシルアミンを加えることにより調製する、請求項1に記載の方法。
- 工程(c)の塩基性条件下での加水分解を、水酸化ナトリウム水溶液を用いて実施する、請求項1に記載の方法。
- 工程(c)の酸水溶液での中間体の処理を、<5℃で酢酸水溶液で実施する、請求項1に記載の方法。
- 式(3)で示される化合物を、ペプチドカップリング試薬の存在下で、式R1−Hのビシクロアミンと反応させて、式(1):
{式中、R1は、
[式中、
R2は、H、あるいは非置換であるか、又はF、Cl、Br、I、CN、OH、1〜4個の炭素原子を有するアルコキシ、NR4R5、若しくはその組み合わせにより1回以上置換されているC1−4−アルキルであり;
R4及びR5は、各々独立してH、あるいは各々が非置換であるか、又はF、Cl、Br、I、CN、OH、1〜4個の炭素原子を有するアルコキシ、モノアルキルアミノ、ジアルキルアミノ、C3−8−シクロアルキル、若しくはその組み合わせにより1回以上置換されている、Ar、Ar−C1−4−アルキル、Het、C1−4−アルキル、C3−8−シクロアルキル若しくはC4−8−シクロアルキルアルキルであり、そして
mは、1、2又は3である]であるか;
あるいは
R1は、A1[ここで、A1は、
であり;
式中、R6〜R14は、各々独立して
H、
非置換であるか、又はF、Cl、Br、I、CN、1〜4個の炭素原子を有するアルコキシ、Ar若しくはその組み合わせにより1回以上置換されているC1−4−アルキル、
非置換であるか、又はF、Cl、Br、I、CN、1〜4個の炭素原子を有するアルコキシ、Ar若しくはその組み合わせにより1回以上置換されているC3−6−アルケニル、
非置換であるか、あるいはF、Cl、Br、I、CN、1〜4個の炭素原子を有するアルコキシ若しくはAr又はその組み合わせにより1回以上置換されているC3−6−アルキニル、
非置換であるか、又はハロゲン、ヒドロキシ、オキソ、シアノ、1〜4個の炭素原子を有するアルキル、1〜4個の炭素原子を有するアルコキシ若しくはその組み合わせにより1回以上置換されている、3〜10個、好ましくは3〜8個の炭素原子を有するシクロアルキル、
非置換であるか、あるいはシクロアルキル部分及び/又はアルキル部分においてハロゲン、オキソ、シアノ、ヒドロキシ、C1−4−アルキル、C1−4−アルコキシ若しくはその組み合わせにより1回以上置換されている、4〜16個、好ましくは4〜12個の炭素原子を有するシクロアルキルアルキル、
Ar−アルキル、あるいは
Het−アルキルであり;
ここで、
Arは、
非置換であるか、あるいは
1〜8個の炭素原子を有するアルキル、
1〜8個の炭素原子を有するアルコキシ、
ハロゲン、
アミノ、
シアノ、
ヒドロキシル、
ニトロ、
1〜8個の炭素原子を有するハロゲン化アルキル、
1〜8個の炭素原子を有するハロゲン化アルコキシ、
1〜8個の炭素原子を有するヒドロキシアルキル、
2〜8個の炭素原子を有するヒドロキシアルコキシ、
3〜8個の炭素原子を有するアルケニルオキシ、
1〜8個の炭素原子を有するモノアルキルアミノ、
ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、
カルボキシ、
アルコキシカルボニル、
アルキルアミノカルボニル、
アシルアミド、
アシルオキシ、
1〜8個の炭素原子を有するアルキルチオ、
1〜8個の炭素原子を有するアルキルスルフィニル、
1〜8個の炭素原子を有するアルキルスルホニル、
スルホ、
スルホニルアミノ、
Het、
シクロアルキルアミノ(ここで、シクロアルキル基は、3〜7個の炭素原子を有し、かつハロゲン、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個の炭素原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ又はチオにより場合により置換されている)、
アリールオキシ(ここで、アリール部分は、6〜10個の炭素原子を含み、かつハロゲン、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個の炭素原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ又はチオにより場合により置換されている)、
アリールチオ(ここで、アリール部分は、6〜10個の炭素原子を含み、かつハロゲン、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個の炭素原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ又はチオにより場合により置換されている)、
シクロアルキルオキシ(ここで、シクロアルキル基は、3〜7個の炭素原子を有し、かつハロゲン、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個の炭素原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ又はチオにより場合により置換されている)、又は
その組合せにより1回以上置換されている6〜10個の炭素原子を含むアリール基であり;
Ar−アルキルは、
アリール−アルキレン基(ここで、アルキレン部分は1〜4個の炭素原子を含み、かつ非置換であるか、又はハロゲン、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個の炭素原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ若しくはチオにより1回以上置換されており、そしてアリール部分は上記のように定義されるArである)であり;
Hetは、
完全飽和、部分飽和又は完全不飽和であり、少なくとも1個の環原子がN、O又はS原子である5〜10個の環原子を有し、非置換であるか、あるいは
1〜8個の炭素原子を有するアルキル、
1〜8個の炭素原子を有するアルコキシ、
ハロゲン、
アミノ、
シアノ、
ヒドロキシル、
ニトロ、
1〜8個の炭素原子を有するハロゲン化アルキル、
1〜8個の炭素原子を有するハロゲン化アルコキシ、
1〜8個の炭素原子を有するヒドロキシアルキル、
2〜8個の炭素原子を有するヒドロキシアルコキシ、
3〜8個の炭素原子を有するアルケニルオキシ、
1〜8個の炭素原子を有するモノアルキルアミノ、
ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、
カルボキシ、
アルコキシカルボニル、
アルコキシカルボニルメチル、
アルキルアミノカルボニル、
アシルアミド、
アシルオキシ、
1〜8個の炭素原子を有するアルキルチオ、
1〜8個の炭素原子を有するアルキルスルフィニル、
1〜8個の炭素原子を有するアルキルスルホニル、
オキソ、
スルホ、
スルホニルアミノ、
シクロアルキルアミノ(ここで、シクロアルキル基は、3〜7個の炭素原子を有し、かつハロゲン、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個の炭素原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ又はチオにより場合により置換されている)、
アリール(6〜10個の炭素原子を含み、かつハロゲン、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個の炭素原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ又はチオにより場合により置換されている)、
アリール−アルキレン基(ここで、アリール部分は6〜10個の炭素原子を含み、アルキレン部分は1〜4個の炭素原子を含み、そして非置換であるか、又はハロゲン、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個の炭素原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ若しくはチオにより1回以上置換されている)、
アリールオキシ(ここで、アリール部分は6〜10個の炭素原子を含み、かつハロゲン、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個のC原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ又はチオにより場合により置換されている)、
アリールチオ(ここで、アリール部分は、6〜10個の炭素原子を含み、かつハロゲン、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個の炭素原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ又はチオにより場合により置換されている)、
シクロアルキルオキシ(ここで、シクロアルキル基は、3〜7個の炭素原子を有し、かつハロゲン、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個の炭素原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ又はチオにより場合により置換されている)、
複素環式基(完全飽和、部分飽和又は完全不飽和であり、少なくとも1個の環原子がN、O又はS原子である5〜10個の環原子を有し、非置換であるか、又はハロゲン、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個の炭素原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ若しくはチオにより1回以上置換されている)、
複素環式−アルキル基(ここで、複素環部分は完全飽和、部分飽和又は完全不飽和であり、少なくとも1個の環原子がN、O又はS原子である5〜10個の環原子を有し、アルキル部分は1〜4個の炭素原子を含むアルキレン基であり、ここで該複素環式−アルキル基は、非置換であるか、あるいはハロゲン、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個の炭素原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ又はチオにより1回以上置換されている)、又は
その組合せにより1回以上置換されている複素環式基であり;
R15及びR16は、各々独立して
H、
Ar、
Ar−アルキル、
Het、
非置換であるか、又はF、Cl、Br、I、CN、OH、1〜4個の炭素原子を有するアルコキシ、モノアルキルアミノ、ジアルキルアミノ、C3−8−シクロアルキル、若しくはその組み合わせにより1回以上置換されているC1−4−アルキル、
非置換であるか、又はハロゲン、ヒドロキシ、オキソ、シアノ、1〜4個の炭素原子を有するアルキル、1〜4個の炭素原子を有するアルコキシ、若しくはその組み合わせにより1回以上置換されている3〜10個、好ましくは3〜8個の炭素原子を有するシクロアルキル、
非置換であるか、又はF、Cl、Br、I、CN、1〜4個の炭素原子を有するアルコキシ、Ar、若しくはその組み合わせにより1回以上置換されているC3−6−アルケニル、あるいは
非置換であるか、あるいはF、Cl、Br、I、CN、1〜4個の炭素原子を有するアルコキシ、若しくはAr、又はその組み合わせにより1回以上置換されているC3−6−アルキニルであり;
R17は、H、
非置換であるか、又はF、Cl、Br、I、CN、OH、1〜4個の炭素原子を有するアルコキシ、NR15R16、SH、SR15、SOR16、C3−8−シクロアルキル、SO2R15、SO2NR15R16、Ar、Het、若しくはその組み合わせにより1回以上置換されているC1−6−アルキル、
非置換であるか、又はF、Cl、Br、I、CN、OH、1〜4個の炭素原子を有するアルコキシ、NR15R16、SH、SR15、SOR15、C3−8−シクロアルキル、SO2R15、SO2NR15R16、Ar、Het、若しくはその組み合わせにより1回以上置換されているC3−6−アルケニル、
非置換であるか、又はF、Cl、Br、I、CN、OH、1〜4個の炭素原子を有するアルコキシ、NR15R16、SH、SR15、SOR15、C3−8−シクロアルキル、SO2R15、SO2NR15R16、Ar、Het、若しくはその組み合わせにより1回以上置換されているC3−6−アルキニル、
非置換であるか、又はF、Cl、Br、I、CN、OH、1〜4個の炭素原子を有するアルコキシ、NR15R16、SH、SR15、SOR15、非置換C3−8−シクロアルキル、SO2R15、SO2NR15R16、Ar、Het、若しくはその組み合わせにより1回以上置換されているC3−8−シクロアルキル、
非置換であるか、又はF、Cl、Br、I、CN、OH、1〜4個の炭素原子を有するアルコキシ、NR15R16、SH、SR15、SOR15、非置換C3−8−シクロアルキル、SO2R15、SO2NR15R16、Ar、Het、若しくはその組み合わせにより1回以上置換されているC4−8−シクロアルキルアルキル
であり、
mは、上記のとおりであり;そして
oは、1又は2である]であるか;
あるいは
R1は、
(式中、mは、上記のとおりである)である}で示される化合物を得る、請求項1〜9のいずれかに記載の方法。 - 式(3)の化合物をその対応する酸塩化物に変換し、それを、ペプチドカップリング試薬の存在下で、式R1−Hのビシクロアミンと反応させて、式(1):
{式中、R1は、
[式中、
R2は、H、あるいは非置換であるか、又はF、Cl、Br、I、CN、OH、1〜4個の炭素原子を有するアルコキシ、NR4R5若しくはその組み合わせにより1回以上置換されているC1−4−アルキルであり;
R4及びR5は、各々独立してH、あるいは各々が非置換であるか、又はF、Cl、Br、I、CN、OH、1〜4個の炭素原子を有するアルコキシ、モノアルキルアミノ、ジアルキルアミノ、C3−8−シクロアルキル、若しくはその組み合わせにより1回以上置換されている、Ar、Ar−C1−4−アルキル、Het、C1−4−アルキル、C3−8−シクロアルキル若しくはC4−8−シクロアルキルアルキルであり、そして
mは、1、2又は3である]であるか;
あるいは
R1は、A1[ここで、A1は、
であり;
式中、R6〜R14は、各々独立して
H、
非置換であるか、又はF、Cl、Br、I、CN、1〜4個の炭素原子を有するアルコキシ、Ar若しくはその組み合わせにより1回以上置換されているC1−4−アルキル、
非置換であるか、又はF、Cl、Br、I、CN、1〜4個の炭素原子を有するアルコキシ、Ar若しくはその組み合わせにより1回以上置換されているC3−6−アルケニル、
非置換であるか、あるいはF、Cl、Br、I、CN、1〜4個の炭素原子を有するアルコキシ若しくはAr又はその組み合わせにより1回以上置換されているC3−6−アルキニル、
非置換であるか、又はハロゲン、ヒドロキシ、オキソ、シアノ、1〜4個の炭素原子を有するアルキル、1〜4個の炭素原子を有するアルコキシ若しくはその組み合わせにより1回以上置換されている、3〜10個、好ましくは3〜8個の炭素原子を有するシクロアルキル、
非置換であるか、あるいはシクロアルキル部分及び/又はアルキル部分においてハロゲン、オキソ、シアノ、ヒドロキシ、C1−4−アルキル、C1−4−アルコキシ若しくはその組み合わせにより1回以上置換されている、4〜16個、好ましくは4〜12個の炭素原子を有するシクロアルキルアルキル、
Ar−アルキル、あるいは
Het−アルキルであり;
ここで、
Arは、
非置換であるか、あるいは
1〜8個の炭素原子を有するアルキル、
1〜8個の炭素原子を有するアルコキシ、
ハロゲン、
アミノ、
シアノ、
ヒドロキシル、
ニトロ、
1〜8個の炭素原子を有するハロゲン化アルキル、
1〜8個の炭素原子を有するハロゲン化アルコキシ、
1〜8個の炭素原子を有するヒドロキシアルキル、
2〜8個の炭素原子を有するヒドロキシアルコキシ、
3〜8個の炭素原子を有するアルケニルオキシ、
1〜8個の炭素原子を有するモノアルキルアミノ、
ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、
カルボキシ、
アルコキシカルボニル、
アルキルアミノカルボニル、
アシルアミド、
アシルオキシ、
1〜8個の炭素原子を有するアルキルチオ、
1〜8個の炭素原子を有するアルキルスルフィニル、
1〜8個の炭素原子を有するアルキルスルホニル、
スルホ、
スルホニルアミノ、
Het、
シクロアルキルアミノ(ここで、シクロアルキル基は、3〜7個の炭素原子を有し、かつハロゲン、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個の炭素原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ又はチオにより場合により置換されている)、
アリールオキシ(ここで、アリール部分は、6〜10個の炭素原子を含み、かつハロゲン、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個の炭素原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ又はチオにより場合により置換されている)、
アリールチオ(ここで、アリール部分は、6〜10個の炭素原子を含み、かつハロゲン、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個の炭素原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ又はチオにより場合により置換されている)、
シクロアルキルオキシ(ここで、シクロアルキル基は、3〜7個の炭素原子を有し、かつハロゲン、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個の炭素原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ又はチオにより場合により置換されている)、又は
その組合せにより1回以上置換されている6〜10個の炭素原子を含むアリール基であり;
Ar−アルキルは、
アリール−アルキレン基(ここで、アルキレン部分は1〜4個の炭素原子を含み、かつ非置換であるか、又はハロゲン、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個の炭素原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ若しくはチオにより1回以上置換されており、そしてアリール部分は上記のように定義されるArである)であり;そして
Hetは、
完全飽和、部分飽和又は完全不飽和であり、少なくとも1個の環原子がN、O又はS原子である5〜10個の環原子を有し、非置換であるか、あるいは
1〜8個の炭素原子を有するアルキル、
1〜8個の炭素原子を有するアルコキシ、
ハロゲン、
アミノ、
シアノ、
ヒドロキシル、
ニトロ、
1〜8個の炭素原子を有するハロゲン化アルキル、
1〜8個の炭素原子を有するハロゲン化アルコキシ、
1〜8個の炭素原子を有するヒドロキシアルキル、
2〜8個の炭素原子を有するヒドロキシアルコキシ、
3〜8個の炭素原子を有するアルケニルオキシ、
1〜8個の炭素原子を有するモノアルキルアミノ、
ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、
カルボキシ、
アルコキシカルボニル、
アルコキシカルボニルメチル、
アルキルアミノカルボニル、
アシルアミド、
アシルオキシ、
1〜8個の炭素原子を有するアルキルチオ、
1〜8個の炭素原子を有するアルキルスルフィニル、
1〜8個の炭素原子を有するアルキルスルホニル、
オキソ、
スルホ、
スルホニルアミノ、
シクロアルキルアミノ(ここで、シクロアルキル基は、3〜7個の炭素原子を有し、かつハロゲン、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個の炭素原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ又はチオにより場合により置換されている)、
アリール(6〜10個の炭素原子を含み、かつハロゲン、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個の炭素原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ又はチオにより場合により置換されている)、
アリール−アルキレン基(ここで、アリール部分は6〜10個の炭素原子を含み、アルキレン部分は1〜4個の炭素原子を含み、そして非置換であるか、又はハロゲン、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個の炭素原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ若しくはチオにより1回以上置換されている)、
アリールオキシ(ここで、アリール部分は6〜10個の炭素原子を含み、かつハロゲン、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個のC原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ又はチオにより場合により置換されている)、
アリールチオ(ここで、アリール部分は、6〜10個の炭素原子を含み、かつハロゲン、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個の炭素原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ又はチオにより場合により置換されている)、
シクロアルキルオキシ(ここで、シクロアルキル基は、3〜7個の炭素原子を有し、かつハロゲン、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個の炭素原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ又はチオにより場合により置換されている)、
複素環式基(完全飽和、部分飽和又は完全不飽和であり、少なくとも1個の環原子がN、O又はS原子である5〜10個の環原子を有し、非置換であるか、又はハロゲン、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個の炭素原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ若しくはチオにより1回以上置換されている)、
複素環式−アルキル基(ここで、複素環部分は完全飽和、部分飽和又は完全不飽和であり、少なくとも1個の環原子がN、O又はS原子である5〜10個の環原子を有し、アルキル部分は1〜4個の炭素原子を含むアルキレン基であり、ここで、該複素環式−アルキル基は、非置換であるか、あるいはハロゲン、1〜8個の炭素原子を有するアルキル、1〜8個の炭素原子を有するハロゲン化アルキル、1〜4個の炭素原子を有するアルコキシ、アミノ、モノアルキルアミノ(ここで、アルキル部分は、1〜8個の炭素原子を有する)、ジアルキルアミノ(ここで、アルキル部分は、各々1〜8個の炭素原子を有する)、COR17、CSR17、シアノ、ヒドロキシル、ニトロ、オキソ又はチオにより1回以上置換されている)、又は
その組合せにより1回以上置換されている複素環式基であり;
R15及びR16は、各々独立して
H、
Ar、
Ar−アルキル、
Het、
非置換であるか、又はF、Cl、Br、I、CN、OH、1〜4個の炭素原子を有するアルコキシ、モノアルキルアミノ、ジアルキルアミノ、C3−8−シクロアルキル、若しくはその組み合わせにより1回以上置換されているC1−4−アルキル、
非置換であるか、又はハロゲン、ヒドロキシ、オキソ、シアノ、1〜4個の炭素原子を有するアルキル、1〜4個の炭素原子を有するアルコキシ、若しくはその組み合わせにより1回以上置換されている3〜10個、好ましくは3〜8個の炭素原子を有するシクロアルキル、
非置換であるか、又はF、Cl、Br、I、CN、1〜4個の炭素原子を有するアルコキシ、Ar、若しくはその組み合わせにより1回以上置換されているC3−6−アルケニル、あるいは
非置換であるか、あるいはF、Cl、Br、I、CN、1〜4個の炭素原子を有するアルコキシ、若しくはAr、又はその組み合わせにより1回以上置換されているC3−6−アルキニルであり;
R17は、H、
非置換であるか、又はF、Cl、Br、I、CN、OH、1〜4個の炭素原子を有するアルコキシ、NR15R16、SH、SR15、SOR16、C3−8−シクロアルキル、SO2R15、SO2NR15R16、Ar、Het、若しくはその組み合わせにより1回以上置換されているC1−6−アルキル、
非置換であるか、又はF、Cl、Br、I、CN、OH、1〜4個の炭素原子を有するアルコキシ、NR15R16、SH、SR15、SOR15、C3−8−シクロアルキル、SO2R15、SO2NR15R16、Ar、Het、若しくはその組み合わせにより1回以上置換されているC3−6−アルケニル、
非置換であるか、又はF、Cl、Br、I、CN、OH、1〜4個の炭素原子を有するアルコキシ、NR15R16、SH、SR15、SOR15、C3−8−シクロアルキル、SO2R15、SO2NR15R16、Ar、Het、若しくはその組み合わせにより1回以上置換されているC3−6−アルキニル、
非置換であるか、又はF、Cl、Br、I、CN、OH、1〜4個の炭素原子を有するアルコキシ、NR15R16、SH、SR15、SOR15、非置換C3−8−シクロアルキル、SO2R15、SO2NR15R16、Ar、Het、若しくはその組み合わせにより1回以上置換されているC3−8−シクロアルキル、
非置換であるか、又はF、Cl、Br、I、CN、OH、1〜4個の炭素原子を有するアルコキシ、NR15R16、SH、SR15、SOR15、非置換C3−8−シクロアルキル、SO2R15、SO2NR15R16、Ar、Het、若しくはその組み合わせにより1回以上置換されているC4−8−シクロアルキルアルキル
であり、
mは、上記のとおりであり;そして
oは、1又は2である]であるか;
あるいは
R1は、
(式中、mは、上記のとおりである)である}で示される化合物を得る、請求項1〜9のいずれかに記載の方法。 - カップリング試薬が、HBTU、HATU、又はHOBt及びEDCIである、請求項10〜11のいずれかに記載の方法。
- カップリング反応を室温で行う、請求項11〜12のいずれかに記載の方法。
- R1が、(3S)−アザビシクロ[2.2.2]オクタ−3−イルである、請求項10〜13のいずれかに記載の方法。
- 式(1)の化合物が、N−[(3S)−1−アザビシクロ[2.2.2]オクタ−3−イル]−5−(トリフルオロメトキシ)−1H−インダゾール−3−カルボキサミド塩酸塩である、請求項10〜14のいずれかに記載の方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US10477708P | 2008-10-13 | 2008-10-13 | |
| US61/104,777 | 2008-10-13 | ||
| PCT/EP2009/062952 WO2010043515A1 (en) | 2008-10-13 | 2009-10-06 | Diazonium-free method to make an indazole intermediate in the synthesis of bicyclic 5-(trifluormethoxy)-1h-3-indazolecarboxylic acid amides |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2012505175A JP2012505175A (ja) | 2012-03-01 |
| JP5425915B2 true JP5425915B2 (ja) | 2014-02-26 |
Family
ID=41508367
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011530467A Expired - Fee Related JP5425915B2 (ja) | 2008-10-13 | 2009-10-06 | 二環5−(トリフルオロメトキシ)−1h−3−インダゾールカルボン酸アミドの合成におけるインダゾール中間体のジアゾニウムフリーの製造方法 |
Country Status (14)
| Country | Link |
|---|---|
| US (2) | US8232412B2 (ja) |
| EP (1) | EP2346833B1 (ja) |
| JP (1) | JP5425915B2 (ja) |
| KR (1) | KR101338726B1 (ja) |
| CN (1) | CN102186826B (ja) |
| BR (1) | BRPI0920187A2 (ja) |
| CA (1) | CA2740311C (ja) |
| DK (1) | DK2346833T3 (ja) |
| ES (1) | ES2407647T3 (ja) |
| IL (1) | IL211931A (ja) |
| MX (1) | MX2011003429A (ja) |
| PL (1) | PL2346833T3 (ja) |
| SI (1) | SI2346833T1 (ja) |
| WO (1) | WO2010043515A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8715807B2 (en) | 2008-07-04 | 2014-05-06 | Saint-Gobain Centre De Recherches Et D'etudes Europeen | Fused grains of oxides comprising Al, Ti and Mg and ceramic products comprising such grains |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JO3250B1 (ar) | 2009-09-22 | 2018-09-16 | Novartis Ag | إستعمال منشطات مستقبل نيكوتينيك أسيتيل كولين ألفا 7 |
| JP2014503568A (ja) | 2011-01-27 | 2014-02-13 | ノバルティス アーゲー | ニコチン酸アセチルコリン受容体α7活性化因子の使用 |
| JP6031458B2 (ja) | 2011-03-18 | 2016-11-24 | ノバルティス アーゲー | パーキンソン病におけるドーパミン誘発ジスキネジアに使用するためのアルファ7ニコチン性アセチルコリン受容体アクティベーターとmGluR5アンタゴニストの組み合わせ剤 |
| MX2014004621A (es) | 2011-10-20 | 2014-08-22 | Novartis Ag | Biomarcadores predictivos de la capacidad de respuesta al receptor de acetil-colina nicotinico alfa-7. |
| CN102837985A (zh) * | 2012-09-21 | 2012-12-26 | 广州广电运通金融电子股份有限公司 | 金融自助设备及其薄片介质传输系统和传输方法 |
| KR102043309B1 (ko) | 2012-12-11 | 2019-11-11 | 노파르티스 아게 | 알파 7 니코틴성 아세틸콜린 수용체 활성화제 치료에 대한 반응성의 예측 바이오마커 |
| ES2883232T3 (es) | 2013-01-15 | 2021-12-07 | Novartis Ag | Uso de agonistas del receptor nicotínico de acetilcolina alfa 7 |
| ES2701083T3 (es) | 2013-01-15 | 2019-02-20 | Novartis Ag | Uso de agonistas del receptor nicotínico alfa 7 para el tratamiento de la narcolepsia |
| BR112015016992A8 (pt) | 2013-01-15 | 2018-01-23 | Novartis Ag | uso de agonistas do receptor alfa 7 nicotínico de acetilcolina |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AU2004309367B2 (en) | 2003-12-22 | 2010-04-01 | Memory Pharmaceuticals Corporation | Indoles, 1H-indazoles, 1,2-benzisoxazoles, and 1,2-benzisothiazoles, and preparation and uses thereof |
| NZ550534A (en) | 2004-03-25 | 2009-07-31 | Memory Pharm Corp | Indazoles, benzothiazoles, benzoisothiazoles, benzisoxazoles, and preparation and uses thereof |
| CA2567977A1 (en) | 2004-04-22 | 2006-01-05 | Memory Pharmaceutical Corporation | Indoles, 1h-indazoles, 1,2-benzisoxazoles, 1,2-benzoisothiazoles, and preparation and uses thereof |
| KR20070015607A (ko) | 2004-05-07 | 2007-02-05 | 메모리 파마슈티칼스 코포레이션 | 1h-인다졸, 벤조티아졸, 1,2-벤조이속사졸,1,2-벤조이소티아졸, 및 크로몬 및 그의 제조법 및 용도 |
| DE102004054666A1 (de) | 2004-11-12 | 2006-05-18 | Bayer Cropscience Gmbh | Substituierte Pyrazol-3-carboxamide, Verfahren zur Herstellung und Verwendung als Herbizide und Pflanzenwachstumsregulatoren |
| US20060142247A1 (en) | 2004-12-17 | 2006-06-29 | Guy Georges | Tricyclic heterocycles |
| MX2007007328A (es) * | 2004-12-22 | 2007-07-25 | Memory Pharm Corp | Ligandos del receptor alfa-7 nicotinico y preparacion y sus usos. |
| KR20080048550A (ko) * | 2005-09-23 | 2008-06-02 | 메모리 파마슈티칼스 코포레이션 | 인다졸, 벤조티아졸, 벤조이소티아졸, 벤즈이속사졸,피라졸로피리딘, 이소티아졸로피리딘, 및 이들의 제법 및용도 |
-
2009
- 2009-10-06 JP JP2011530467A patent/JP5425915B2/ja not_active Expired - Fee Related
- 2009-10-06 EP EP09783778A patent/EP2346833B1/en not_active Not-in-force
- 2009-10-06 KR KR1020117010544A patent/KR101338726B1/ko not_active IP Right Cessation
- 2009-10-06 BR BRPI0920187A patent/BRPI0920187A2/pt not_active IP Right Cessation
- 2009-10-06 SI SI200930588T patent/SI2346833T1/sl unknown
- 2009-10-06 MX MX2011003429A patent/MX2011003429A/es active IP Right Grant
- 2009-10-06 ES ES09783778T patent/ES2407647T3/es active Active
- 2009-10-06 PL PL09783778T patent/PL2346833T3/pl unknown
- 2009-10-06 DK DK09783778.5T patent/DK2346833T3/da active
- 2009-10-06 WO PCT/EP2009/062952 patent/WO2010043515A1/en active Application Filing
- 2009-10-06 CN CN200980140562.3A patent/CN102186826B/zh not_active Expired - Fee Related
- 2009-10-06 CA CA2740311A patent/CA2740311C/en active Active
- 2009-10-09 US US12/576,259 patent/US8232412B2/en not_active Expired - Fee Related
-
2011
- 2011-03-24 IL IL211931A patent/IL211931A/en not_active IP Right Cessation
-
2012
- 2012-06-21 US US13/528,894 patent/US8354536B2/en not_active Expired - Fee Related
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8715807B2 (en) | 2008-07-04 | 2014-05-06 | Saint-Gobain Centre De Recherches Et D'etudes Europeen | Fused grains of oxides comprising Al, Ti and Mg and ceramic products comprising such grains |
Also Published As
| Publication number | Publication date |
|---|---|
| MX2011003429A (es) | 2011-05-02 |
| US20120259120A1 (en) | 2012-10-11 |
| KR101338726B1 (ko) | 2013-12-06 |
| CN102186826A (zh) | 2011-09-14 |
| EP2346833A1 (en) | 2011-07-27 |
| ES2407647T3 (es) | 2013-06-13 |
| BRPI0920187A2 (pt) | 2019-08-27 |
| JP2012505175A (ja) | 2012-03-01 |
| CN102186826B (zh) | 2015-06-17 |
| WO2010043515A1 (en) | 2010-04-22 |
| PL2346833T3 (pl) | 2013-08-30 |
| SI2346833T1 (sl) | 2013-06-28 |
| AU2009304171A1 (en) | 2010-04-22 |
| US20100094011A1 (en) | 2010-04-15 |
| US8232412B2 (en) | 2012-07-31 |
| DK2346833T3 (da) | 2013-04-29 |
| CA2740311C (en) | 2013-09-17 |
| EP2346833B1 (en) | 2013-03-27 |
| IL211931A (en) | 2016-07-31 |
| CA2740311A1 (en) | 2010-04-22 |
| IL211931A0 (en) | 2011-06-30 |
| US8354536B2 (en) | 2013-01-15 |
| KR20110067063A (ko) | 2011-06-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5425915B2 (ja) | 二環5−(トリフルオロメトキシ)−1h−3−インダゾールカルボン酸アミドの合成におけるインダゾール中間体のジアゾニウムフリーの製造方法 | |
| RU2314306C2 (ru) | Производные хинуклидинамида, способ их получения и их применение, фармацевтическая композиция, комбинированный продукт и способ ингибирования мускариновых рецепторов | |
| JP2008525357A (ja) | 抗ムスカリン活性を有するアゾール誘導体 | |
| EP0699199A1 (en) | Heteroatom substituted alkyl benzylaminoquinuclidines as substance p antagonists | |
| ZA200604395B (en) | Novel M3 Muscarinic Acetylcholine receptor antagonists | |
| JPH08333363A (ja) | インドール誘導体 | |
| MXPA02006017A (es) | Antagonistas de neuroquinina selectivos. | |
| JP3939246B2 (ja) | インドロキナゾリノン類 | |
| JP2006513197A (ja) | 5−(4−ブロモフェニル)−1−(2,4−ジクロロフェニル)−4−エチル−n−(ピペリジン−1−イル)−1h−ピラゾール−3−カルボキサミド誘導体、それらの製造法および治療用途 | |
| JP3765543B2 (ja) | Nk−1受容体アンタゴニスト活性を有するピペラジンオキシム誘導体 | |
| JP6317345B2 (ja) | ウレア化合物および酵素阻害剤としてのそれらの使用 | |
| JPH08269058A (ja) | ピペリジン誘導体、その製造方法およびその治療における応用 | |
| US8618116B2 (en) | Deuterium-enriched pyrimidine compounds and derivatives | |
| JPH1087667A (ja) | モルフィナンヒドロキサム酸化合物 | |
| JPH07133273A (ja) | 光学活性イミダゾリジノン誘導体とその製造方法 | |
| JP2010518053A (ja) | アザビシクロアルカン誘導体、これらの調製および治療におけるこれらの使用 | |
| CN101119992A (zh) | 三环δ阿片样物质调节剂 | |
| AU2009304171B2 (en) | Diazonium-free method to make an indazole intermediate in the synthesis of bicyclic 5-(trifluormethoxy)-1H-3-indazolecarboxylic acid amides | |
| TW202227401A (zh) | 用於持續釋放治療劑的前藥及其用途 | |
| JPH1087661A (ja) | サブスタンスpアンタゴニストとしてのテトラゾリル置換キヌクリジン | |
| AU2006334364A1 (en) | Imidazo (1,2-a)pyridin-3-yl-acetic acid hydrazides, processes for their preparation and pharmaceutical uses thereof | |
| WO2006035280A1 (en) | 3,4-dihydroisoquinoline compounds as muscrinic receptor antagonists for the treatment of respiratory, urinary and gastrointestinal diseases | |
| JPH0741481A (ja) | 両性型三環系化合物 | |
| JP2002501919A (ja) | 神経学的障害の治療用の1,4−ジアザシクロヘプタン誘導体 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20130530 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130604 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20130826 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20130902 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20131003 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20131029 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20131127 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5425915 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |