CN1638765A - Hedgehog信号转导途径介质、其相关组合物以及应用 - Google Patents
Hedgehog信号转导途径介质、其相关组合物以及应用 Download PDFInfo
- Publication number
- CN1638765A CN1638765A CNA028186796A CN02818679A CN1638765A CN 1638765 A CN1638765 A CN 1638765A CN A028186796 A CNA028186796 A CN A028186796A CN 02818679 A CN02818679 A CN 02818679A CN 1638765 A CN1638765 A CN 1638765A
- Authority
- CN
- China
- Prior art keywords
- cell
- hedgehog
- aryl
- represent
- heteroaryl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D263/00—Heterocyclic compounds containing 1,3-oxazole or hydrogenated 1,3-oxazole rings
- C07D263/52—Heterocyclic compounds containing 1,3-oxazole or hydrogenated 1,3-oxazole rings condensed with carbocyclic rings or ring systems
- C07D263/54—Benzoxazoles; Hydrogenated benzoxazoles
- C07D263/56—Benzoxazoles; Hydrogenated benzoxazoles with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached in position 2
- C07D263/57—Aryl or substituted aryl radicals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/4164—1,3-Diazoles
- A61K31/4184—1,3-Diazoles condensed with carbocyclic rings, e.g. benzimidazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/42—Oxazoles
- A61K31/423—Oxazoles condensed with carbocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/425—Thiazoles
- A61K31/428—Thiazoles condensed with carbocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P15/00—Drugs for genital or sexual disorders; Contraceptives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/14—Drugs for dermatological disorders for baldness or alopecia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P21/00—Drugs for disorders of the muscular or neuromuscular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D235/00—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, condensed with other rings
- C07D235/02—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, condensed with other rings condensed with carbocyclic rings or ring systems
- C07D235/04—Benzimidazoles; Hydrogenated benzimidazoles
- C07D235/18—Benzimidazoles; Hydrogenated benzimidazoles with aryl radicals directly attached in position 2
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/12—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Public Health (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Epidemiology (AREA)
- Dermatology (AREA)
- Neurology (AREA)
- Physical Education & Sports Medicine (AREA)
- Endocrinology (AREA)
- Pulmonology (AREA)
- Gastroenterology & Hepatology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Biomedical Technology (AREA)
- Neurosurgery (AREA)
- Diabetes (AREA)
- Hematology (AREA)
- Reproductive Health (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Cosmetics (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Steroid Compounds (AREA)
- Liquid Crystal Substances (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Oxygen Or Sulfur (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
本发明提供抑制由于hedgehog功能获得、ptc功能丧失或smoothened功能获得引起的异常生长状态的有效方法和试剂,所述方法包括使所述细胞与足以抑制异常生长状态(如激动正常ptc途径或拮抗smoothened或hedgehog活性)的量的hedgehog拮抗剂(如小分子)接触。
Description
发明背景
图式形成是胚胎细胞借以形成有序空间排列的不同组织的活动。高等生物的生理复杂性来源于胚胎发生期间,通过细胞本身谱系和细胞外部信号的相互作用。诱导型相互作用对于脊椎动物发育中胚胎图式形成是必不可少的,从最早的建立机体计划、到器官系统的图式形成以及组织分化过程中产生不同细胞类型(Davidson,E.,(1990)
Development 108:365-389;Gurdon,J.B.,(1992)
Cell 68:185-199;Jessell,T.M.等,(1992)
Cell 68:257-270)。发育性细胞相互作用的效应各不相同。一般地说,通过诱导与未诱导状态和诱导状态响应细胞不同的细胞(诱导),使所述响应细胞从一个细胞分化途径转到另一个细胞分化途径。有时细胞诱导它们的临近细胞分化成为与它们相似的细胞(自体诱导);在其它情况下,细胞抑制其临近细胞分化成为与其相似的细胞。早期发育中的细胞相互作用可以是顺序的,以便两种细胞类型之间的最初诱导引起多样性的进行性扩增。此外,诱导型相互作用不仅发生在胚胎中,而且发生在成熟细胞中,可以建立和维持形态发生图式以及诱导分化(J.B.Gurdon(1992)
Cell 68:185-199)。
信号分子Hedgehog家族的成员介导无脊椎动物和脊椎动物发育过程中许多重要的短程和长程图式化过程。在苍蝇体内,一个hedgehog基因调节节芽和器官芽的模式化。与此不同,在脊椎动物中,hedgehog基因涉及家族涉及控制左右不对称性、CNS中的极性、体节和肢、器官发生、软骨发生和精子发生。
通过遗传筛选在黑腹果蝇(Drosophila melanogaster)中鉴定出第一个hedgehog基因(Nusslein-Volhard,C.和Wieschaus,E.(1980)
Nature287,795-801)。该筛选鉴定许多影响胚胎发育和幼虫发育的突变。在1992和1993,报道黑腹果蝇(hh)基因的分子本质(C.F.,Lee等(1992)Cell 71,33-50),从此以后,已经从各种脊椎动物物种分离出几种hedgehog同源物。虽然在果蝇属(Drosophila)和其它无脊椎动物中仅发现一种hedgehog基因,但在脊椎动物中存在多种Hedgehog基因。
hedgehog基因的脊椎动物家族包括至少四个成员,如一个果蝇hedgehog基因的共生同源物(paralog)。在PCT公开WO 95/18856和WO 96/17924中描述示例性的hedgehog基因和蛋白。这些成员中的三个在本文中称为Desert hedgehog(Dhh)、Sonic hedgehog(Shh)和Indian hedgehog(Ihh),明显存在于所有脊椎动物中,包括鱼、鸟类和哺乳动物。第四个成员在本文中称为tiggie-winkle hedgehog(Thh),看起来对于鱼是特异性的。Desert hedgehog(Dhh)主要在睾丸中表达,在小鼠胚胎发育和成年啮齿动物和人中都有表达;Indian hedgehog(Ihh)涉及胚胎发生过程中的骨发育以及成体内的骨形成;而如上文所述的Shh主要涉及形态发生活动和神经诱导活动。考虑到hedgehog多肽在脊椎动物器官发育和维持中的关键诱导作用,鉴定hedgehog相互作用蛋白在临床和研究领域都有显著重要性。
各种Hedgehog蛋白包括一个信号肽、一个高度保守的N末端区以及一个更多样化的C末端区。除分泌途径中的信号序列切割(Lee,J.J.等(1992)
Cell 71:33-50;Tabata,T.等(1992)
Genes Dev.2635-2645;Chang,D.E.等(1994)
Development 120:3339-3353)外,Hedgehog前体蛋白被依赖于C末端部分保守序列的内部自我蛋白酶解(Lee等(1994)Science 266:1528-1537;Porter等(1995)
Nature 374:363-366)。所述自我切割导致19kD的N末端肽和26-28kD的C末端肽(Lee等(1992)同上;Tabata等(1992)
同上;Chang等(1994)
同上;Lee等(1994)
同上;Bumcrot,D.A.等(1995)
Mol.Cell.Biol.15:2294-2303;Porter等(1995)同上;Ekker,S.C.等(1995)
Curr.Biol.5:944-955;Lai,C.J.等(1995)Development 121:2349-2360)。所述N末端肽与其合成细胞的细胞表面紧密结合,而所述C末端肽在体内和体外都可自由扩散(Porter等(1995)
Nature 374:363;Lee等(1994)
同上;Bumcrot等(1995)
同上;Mart’,E.等(1995)
Development 121:2537-2547;Roelink,H.等(1995)
Cell 81:445-455)。有趣的是,N末端肽在细胞表面的保留依赖于自我切割,因为在正常内部切割位置精确终止的RNA所编码的一种截短形式HH可以在体外(Porter等(1995)
同上)以及体内(Porter,J.A.等(1996)
Cell 86,21-34)扩散。生物学研究已经显示:所述HH前体蛋白的自我酶解通过一种内部硫酯中间体进行,所述内部硫酯中间体随后在亲核取代中被切割。有可能所述亲核物质是小亲脂分子,与所述N-肽的C末端共价结合(Porter等(1996)
同上),将其粘连到细胞表面。其生物学含意是深远的。粘连的结果是在Hedgehog生产细胞的表面产生N末端Hedgehog肽的高局部浓度。所述N末端肽对于果蝇属和脊椎动物中的短程和长程Hedgehog信号转导活动是必需而充分的(Porter等(1995)
同上;Ekker等(1995)
同上;Lai等(1995)
同上;Roelink,H等(1995)Cell 81:445-455;Porter等(1996)
同上;Fietz,M.J.等(1995)
Curr.Biol.5:643-651;Fan,C.-M.等(1995)
Cell 81:457-465;Mart’,E.等(1995)Nature 375:322-325;Lopez-Martinez等(1995)
Curr.Biol 5:791-795;Ekker,S.C.等(1995)
Development 121:2337-2347;Forbes,A.J.等(1996)Development 122:1125-1135)。
已经提示HH涉及果蝇属发育中不同位点的短程和长程模式化过程。在建立早期胚胎的节极性时,其具有看起来被直接介导的短程效应,而在器官芽的模式化中,其通过诱导第二信号诱导长程效应。
过去几年中,已经克隆脊椎动物中的几种hedgehog基因。在这些基因中,Shh被最大的试验关注,因为它在作为模式化临近组织的信号源的不同组织中心表达。最近的证据提示:Shh涉及这些相互作用。
原肠胚形成开始后不久,在推定中轴中胚层、小鼠(Chang等(1994)同上;Echelard,Y.等(1993)
Cell 75:1417-1430)、大鼠(Roelink,H.等(1994)
Cell 76:761-775)和鸡(Riddle,R.D.等(1993)
Cell 75:1401-1416)的节和斑马鱼鱼鳞(Ekker等(1995)
同上;Krauss,S.等(1993)
Cell 75:1431-1444)内开始Shh表达。在鸡胚中,节内Shh的表达模式发展出左右不对称性,所述左右不对称性看起来引起心脏的左右排列(Levin,M.等(1995)
Cell 82:803-814)。
在CNS中,来自脊索和底板的Shh看起来诱导腹细胞命运。当Shh异位表达时,它导致小鼠(Echelard等(1993)
同上;Goodrich,L.V.等(1996)
Genes Dev.10:301-312)、非洲蟾蜍属(Xenopus)(Roelink,H.等(1994)同上;Ruii Altaba,A.等(1995)
Mol.Cell.Neurosci.6:106-121)和斑马鱼(Ekker等(1995)
同上;Krauss等(1993)
同上;Hammerschmidt,M.等(1996)
Genes Dev.10:647-658)中脑和后脑大区的腹轴化(ventralization)。在脊椎水平中间神经外胚层的外植块中,Shh蛋白以不同浓度阈值诱导底板和运动神经元发育,其中在高浓度阈值诱导底板,在低浓度阈值诱导运动神经元(Roelink等(1995)
同上;Mart’等(1995)
同上;Tanabe,Y.等(1995)
Curr.Biol.5:651-658)。此外,抗体阻断提示:脊索介导的诱导运动神经元命运需要脊索产生的Shh(Mart’等(1995)同上)。因此,在生产Shh的中轴细胞表面高浓度的Shh看起来引起体外观察到的接触介导的底板诱导(Placzek,M.等(1993)Development 117:205-218)以及体内时底板紧接在脊索之上的中轴定位。从脊索和底板释放出的低浓度Shh大概诱导更远腹侧区域的运动神经元,已经显示该过程在体外不依赖于接触(Yamada,T.等(1993)Cell 73:673-686)。在中脑和前脑水平取出的外植体中,Shh也诱导合适的腹侧神经元细胞类型,分别是多巴胺能前体(Heynes,M.等(1995)Neuron 15:35-44;Wang,M.Z.等(1995)
Nature Med.1:1184-1188)和胆碱能前体(Ericson,J.等(1995)
Cell 81:747-756),指示Shh是CNS整个长度上腹轴特化的通用诱导物。这些观察提出关于对Shh的不同响应如何在特定前后位置被调节的问题。
来自中轴的Shh也模式化脊椎动物胚胎的近轴区、躯干的体节(Fan等(1995)
同上)和头端体节的头间充质(Hammerschmidt等(1996)同上)。在鸡和小鼠近轴中轴层外植块中,Shh促进生骨节特异性标记如Pax1和Twist的表达,同时降低皮肤生肌节标记Pax3的表达。此外,过滤屏障实验提示:Shh直接介导生骨节的诱导,而不是通过激活第二信号机制(Fan,C.-M.和Tessier-Lavigne,M.(1994)
Cell 79,1175-1186)。
Shh也诱导生肌节基因表达(Hammerschmidt
等(1996)
同上;Johnson,R.L.等(1994)
Cell 79:1165-1173;Munsterberg,A.E.等(1995)Genes Dev.9:2911-2922;Weinberg,E.S.等(1996)
Development 122:271-280),虽然最近的实验指出同时需要WNT家族的成员,即Drosophila wingless的脊椎动物同源物(Munsterberg等(1995)
同上)。令人疑惑的是,鸡的生肌节诱导需要比诱导生骨节标记更高浓度的Shh(Munsterberg等(1995)
同上),虽然生骨节源自与脊索位置更近的体节细胞。在斑马鱼中获得相似结果,其中高浓度的Hedeghog诱导生肌节标记基因表达,抑制生骨节标记基因表达(Hammerschmidt等(1996)
同上)。然而,与羊膜动物不同,这些观察与鱼胚胎的结构一致,例如,生肌节是体节主要和最轴心的成分。因此,调节Shh信号和获得新信号因子可能在脊椎动物进化过程中已经改变体节结构。
在脊椎动物的肢芽中,一个亚组的后间充质细胞,即“极性活性区”(ZPA),调节前后趾身份(在Honig,L.S.(1981)
Nature 291:72-73中综述)。Shh的异位表达或应用在Shh肽中浸泡的珠模拟前端ZPA移植物的效应,产生趾的映像复制物(Chang等(1994)同上;Lopez-Martinez等(1995)同上;Riddle等(1993)同上)(图2g)。因此,趾的身份看起来主要依赖于Shh浓度,虽然在AP模式化看起来需要的相当长距离内(100-150μm)可能有其它信号传递该信息。与HH和DPP在果蝇属器官芽中的相互作用类似,脊椎动物肢芽中的Shh激活一种dpp同源物Bmp2的表达(Francis,P.H.等(1994)
Developmen 120:209-218)。然而,与果蝇属内的DPP不同,Bmp2当异位应用于鸡肢芽时不能模拟Shh的极化效应(Francis等(1994)
同上)。Shh除涉及前后模式化外,看起来还涉及调节通过诱导后顶外胚层脊中成纤维细胞生长因子FGF4的合成,调节肢的近远端生长晕(Laufer,E.等(1994)
Cell79:993-1003;Niswander,L.等(1994)
Nature 371:609-612)。
Hedgehog蛋白与BMP之间的密切关系可能在许多但不是所有的脊椎动物Hedgehog表达位点保守。例如,在鸡后肠中,已经显示Shh诱导另一种脊椎动物dpp同源物Bmp4的表达(Roberts,D.J.等(1995)
Development 121:3163-3174)。此外,Shh和Bmp2、4或6在胃、泌尿生殖系统、肺、牙胚和毛囊的上皮细胞和间充质细胞的表达中显示惊人相关关系(Bitgood,M.J.和McMahon,A.P.(1995)
Dev. Biol.172:126-138)。另外,两个其它小鼠Hedgehog基因之一Ihh在肠和发育中的软骨内Bmp表达细胞附近表达(Bitgood和McMahon(1995)同上)。
最近的证据提示一个模型,认为Ihh在软骨发生发育的调节中起关键作用(Roberts等(1995)
同上)。在软骨形成过程中,软骨细胞从增殖状态开始,通过一个中间的前肥大状态,到达分化的肥大软骨细胞。Ihh在前肥大软骨细胞中表达,起始阻断软骨细胞分化的信号级联反应。其直接靶是Ihh表达区域周围的软骨膜,所述软骨膜应答,表达Hedgehog信号的保守的转录靶Gli和Patched(Ptc)(见下文)。更有可能这引起二级信号传递,导致关节周围软骨膜内甲状旁腺激素相关蛋白(PTHrP)的合成。PTHrP本身传递信号给前肥大软骨细胞,阻断它们进一步的分化。同时,PTHrP抑制Ihh表达,由此形成调节软骨细胞分化速率的负反馈环。
最初将Patched鉴定为果蝇属中的节极性基因,所述节极性基因是一组发育基因之一,该组发育基因影响沿着胚的前后轴以同源序列发生的各个节内的细胞分化。见Hooper,J.E.等(1989)
Cell 59:751;和Nakano,Y.等(1989)
Nature 341:508。Patched脊椎动物同源物的表达模式提示其涉及神经管、骨骼、肢、颅面结构和皮肤的发育。
遗传研究和功能研究证明:patched是hedgehog信号级联反应的一部分,所述hedgehog信号级联反应是在进化上保守的调节多种下游基因表达的途径。见Perrimon,N.(1995)
Cell80:517;和Perrimon,N.(1996)
Cell 86:513。Patched参与所述靶基因的组成型转录抑制;其效应被诱导转录激活的一种由hedgehog编码的分泌型糖蛋白或其脊椎动物同源物的抑制。在该途径控制下的基因包括Wnt和TGF-β家族的成员。
Patched蛋白具有两个大的细胞外结构域、十二个跨膜区段和几个胞质区段。见Hooper,
同上;Nakano,
同上;Johnson,R.L.等(1996)Science 272:1668;和Hahn,H.等(1996)
Cell 85:841。Patched在hedgehog信号途径中的生物化学作用还不清楚。然而,已经报道与hedgehog蛋白的直接相互作用(Chen,Y.等(1996)
Cell 87:553),并且patched可能与smoothened基因编码的另一种跨膜蛋白一起参与一种hedgehog受体复合物。见Perrimon,
同上;和Chen,
同上。
最近克隆patched的人同源物并将其作图到染色体9q22.3。见Johnson,
同上;和Hahn,
同上。该区涉及基底细胞痣综合征(BCNS),所述基底细胞痣综合征的特征在于发育畸形,包括肋状突起和颅面改变、手和脚畸形以及脊柱裂。
BCNS还容易发展成多种肿瘤类型,最常见的是基底细胞癌(BCC),基底细胞癌出现在身体的许多位置,出现在二十岁之前。然而,大多数BCC病例与该综合征无关,在北欧血统的中年和老年人人暴露于阳光的位点上少量散发性出现。
最近BCNS相关和散发性BCC方面的研究提示:patched两个等位基因的功能丧失导致发生BCC。见Johnson,
同上;Hahn,
同上;和Gailani,M.R.等(1996)
Nature Genetics14:78。在散发性和遗传性BCC中常常出现染色体9q22.3的单个等位基因缺失。谱系分析揭示:在来自BCNS患者的肿瘤中,保留有缺陷的遗传等位基因,而丧失正常的等位基因。
散发性肿瘤也表现丧失patched的两个有功能的等位基因。在用单链构象多态性筛选测定鉴定出patched突变的十二个肿瘤中,九个在第二个等位基因上有染色体缺失,其它三个在两个等位基因上都有失活突变(Gailani,
同上)。在对应种系DNA中没有出现改变。
大多数已经鉴定的突变导致成熟前终止密码子或移码。Lench,N.J.等,Hum.Genet.1997年10月;100(5-6):497-502。然而,有几个突变是引起细胞外或胞质结构域内氨基酸取代的点突变。这些突变位点可能提示与下游信号途径的细胞外蛋白或胞质成员相互作用的功能重要性。
Patched涉及抑制基因表达以及BCC中等位基因缺失的频繁出现支持该基因的肿瘤抑制物功能。Patched在调节已知涉及细胞信号传递和细胞间通信的基因家族中的作用提供肿瘤抑制的可能机制。
发明简述
本发明提供抑制hedgehog信号途径的激活的方法和试剂,其作用是例如抑制表型如ptc功能丧失、hedgehog功能获得或smoothened功能获得引起的不正常生长状态,所述方法包括使所述细胞与足以激活正常ptc活性、拮抗正常hedgehog活性或拮抗smoothened活性如逆转或控制所述异常生长状态的量的试剂如小分子接触。
附图简述
图1-31描述用于合成依照本发明的化合物的反应。
图32a-j图解依照本发明的有代表性的化合物。
图33显示本发明化合物对于人基底细胞癌(BCC)内hedgehog信号传递的效应。
图34图解本发明化合物对于BCC组织中编程性细胞死亡的效应。
图35描述本发明化合物对于S-12和HT-29细胞内hedgehog信号传递的效应。
图36描述本发明化合物对于PC-3和RT-4细胞内hedgehog信号传递的效应。
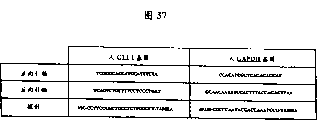
图37提供用于评价细胞内hedgehog活性的探针和引物的序列。
图38和40图解本发明化合物对于pct无效细胞内GLI-1和GAPDH表达的差别效应。
图39和41显示本发明化合物对于HEPM细胞内GLI-1和GAPDH表达的差别效应。
实施本发明的最佳模式
发明详述
I.概述
本发明涉及下面发现:小分子可以抑制(至少部分抑制)hedgehog、patched(ptc)、gli和/或smoothened调节的信号转导途径。虽然不希望被任何具体理论所限制,但激活受体可能是这些试剂起作用的机制。例如,这些试剂抑制patched功能丧失(ptclof)细胞的能力可能是由于所述分子与hedgehog、patched(ptc)或smoothened相互作用,或者至少干扰那些蛋白激活hedgehog、ptc和/或smoothened介导的信号转导途径的能力。
因此,设想这些干扰hedgehog、ptc和/或smoothened信号转导活性各个方面的小分子可能能够抑制正常细胞和/或具有patched功能丧失表型、hedgehog功能获得表型或smoothened功能获得表型的细胞的增殖(或其它生物学结果)。因此,在某些实施方案中,设想这些化合物可用于抑制正常细胞中的hedgehog活性,所述正常细胞如不具有激活hedgehog途径的遗传突变的细胞。在优选实施方案中,主题抑制剂是这样的有机分子:分子量小于2500amu,更优选小于1500amu,甚至更优选小于750amu,并且能够至少部分抑制hedgehog蛋白的生物学活性,最好在靶细胞中特异性发生所述抑制。
因此,本发明的方法包括应用激活ptc对hedgehog信号传递的抑制的小分子,调节多种细胞、组织和器官的修复和/或功能实施,所述激活例如通过抑制smoothened的激活或所述信号途径的下游成分,所述多种细胞、组织和器官包括正常细胞、组织和器官以及那些具有ptc功能丧失表型、hedgehog功能获得表型或smoothened功能获得表型的细胞、组织和器官。例如,本发明主题方法在下面方面有治疗和美容应用:调节神经组织、骨和软骨组织形成和修复、调节精子发生、调节平滑肌、调节肺、肝和从原肠发育而来的其它器官、调节造血功能、调节皮肤和毛发生长等。此外,可以对培养物提供的细胞(体外)或整体动物中的细胞(体内)实施本发明主题方法。见例如PCT公开WO 95/18856和WO 96/17924(其说明书特此通过引用结合到本文中)。
在优选实施方案中,本发明主题方法可用于处理具有ptc功能丧失表型、hedgehog功能获得表型或smoothened功能获得表型的上皮细胞。例如,本发明主题方法可用于治疗或预防基底细胞癌或其它与hedgehog途径有关的疾病。
在某些实施方案中,主题拮抗剂可以通过结合smoothened而抑制hedgehog途径的激活。在某些实施方案中,主题拮抗剂可以通过结合patched而抑制hedgehog途径的激活。
在另一优选实施方案中,本发明主题方法可以用作恶性成神经管细胞瘤和其它原发性CNS恶性神经外胚层肿瘤的治疗方案组成部分。
另一方面,本发明提供药用制剂,所述药用制剂包含作为活性成分的hedgehog拮抗剂、ptc激动剂或smoothened拮抗剂,例如本文所述的上述组分,所述活性成分的配制量足以在体内抑制ptc功能丧失表型、hedgehog功能获得表型或smoothened功能获得表型的增殖或其它生物学结果。
所述使用hedgehog拮抗剂、ptc激动剂或snoothened拮抗剂的主题治疗可以对于人和动物受治疗者都有效。本发明可应用的动物受试验者扩展到或者作为宠物饲养或者为商业目的饲养的家畜和牲畜。例子有狗、猫、牛、马、绵羊、猪和山羊。
II.定义
为方便起见,在此汇集在本说明书、实施例和所附权利要求中使用的某些术语。
基因的“异常修饰或突变”术语指遗传损害例如基因核苷酸的缺失、取代或添加,以及基因的总染色体重排和/或基因的异常甲基化。相似地,基因的错误表达指相对与相似条件下正常细胞内水平的异常基因转录水平,以及从所述基因转录的mRNA的非野生型剪接。
“基底细胞癌”存在多种临床和组织学形式,例如结溃疡性综合征、浅层综合征、色素沉着综合征、硬斑病样综合征、纤维上皮瘤综合征和痣样综合征。基底细胞癌是人类中最常见的皮肤瘤。大多数非黑素瘤皮肤癌的新病例属于该类别。
“烧伤”指由于热和/或化学试剂的作用,个体被去除或损失大表面积皮肤的情况。
术语“癌”指由易于浸润周围组织并产生转移的上皮细胞组成的恶性新的生长。示例性的癌包括:“基底细胞癌”,指一种皮肤的上皮肿瘤,虽然很少转移,但有局部侵袭和破坏的潜力;“鳞状细胞癌”,指从鳞状上皮产生并具有立方形细胞的癌;“癌内瘤”,包括由癌性组织和肉瘤性组织组成的恶性肿瘤;“腺囊型癌”,特征是小上皮细胞巢或索将圆柱状或带状透明基质或粘蛋白基质分开或包围,出现在乳腺和唾液腺以及呼吸道的粘液腺;“表皮样癌”指倾向于以表皮细胞的同样方式分化的癌性细胞;即他们倾向于形成棘细胞并经历角质化;“鼻咽癌”,指鼻后腔上皮层产生的恶性肿瘤;“肾细胞癌”,涉及由不同排列的管状细胞组成的肾实质的癌。其它癌性上皮肿瘤是“乳头瘤”,指从上皮衍生的良性肿瘤,乳头瘤病毒是其病原体;和“表皮样瘤”,指神经沟闭合时通过将外胚层成分卷入而形成的脑肿瘤或脑脊膜肿瘤。
“真皮”指表皮以下的深层皮肤,由密集血管结缔组织床组成,包含感觉神经末端器。毛根、皮脂腺和汗腺是深深包埋在真皮之内的表皮结构。
“牙组织”指口腔内类似于上皮组织的组织,例如齿龈组织。本发明的方法用于治疗牙周疾病。
“浅表性皮肤溃疡”指由表层组织丧失(通常由于炎症)引起的皮肤病变。可以用本发明方法治疗的浅表性皮肤溃疡包括褥疮性溃疡、糖尿病性溃疡、静脉淤滞性溃疡和动脉溃疡。褥疮指由于长时间皮肤受压而引起的慢性溃疡。这种类型的溃疡常常称为褥疮。静脉淤滞性溃疡源自缺陷静脉的血液或其它液体的停滞。动脉溃疡指在血流不畅的动脉周围区域的皮肤坏死。
术语“ED50”指产生50%其最大反应或效应的药物剂量。
就主题治疗方法而言,“有效量”如hedgehog拮抗剂的有效量指制剂内所述拮抗剂的量,当将所述量作为所需剂量方案的组成部分应用时,根据需要治疗的疾病或美容目的的临床接受标准,产生例如细胞增殖速率的改变和/或细胞分化状态的改变和/或细胞存活率的改变。
术语“上皮”、“表皮”指身体内表面和外表面(皮肤、粘膜和浆膜)的覆盖细胞,包括腺体和由此产生的其它结构,如角膜上皮细胞、食管上皮细胞、表皮上皮细胞和毛囊上皮细胞。其它上皮组织例子包括:嗅觉上皮,是鼻腔嗅觉区域的假复层上皮,包括气味感觉的受体;腺上皮,指由分泌细胞组成的上皮;扁平上皮,指由扁平板样细胞组成的上皮。术语上皮也可以指变移上皮,其为特征存在的中空器官内表面,所述层中空器官由于收缩和膨胀而经受巨大机械改变,如代表层形鳞状上皮和柱状上皮之间变移的组织。
术语“上皮化”指通过上皮组织在裸露表面的生长而愈合。
术语“表皮腺体”指与表皮结合细胞聚集物,特化分泌或排泄与它们一般代谢需要无关的物质。例如,“皮脂腺”是真皮内的全质分泌腺,分泌油性物质和皮脂。术语“汗腺”指分泌汗液的腺体,位于真皮或皮下组织,通过导管开口于体表。
术语“表皮”指皮肤的最外面并且无血管的层,起源于胚胎外胚层,厚度从0.07到1.4mm。在手掌和足底表面,表皮从内到外包括五层:基底层,由垂直排列的柱状细胞组成;棘细胞层或棘层,由具有短突起或刺的扁平多角细胞组成;颗粒层,由扁平的颗粒细胞组成;透明层,由几层明亮透明的细胞组成,所述细胞中核模糊或缺失;角质层,由扁平的角质化无核细胞组成。在一般体表的表皮中,通常不存在透明层。
“切割伤”包括皮肤上皮层中的裂伤、擦伤、切伤、刺伤或撕裂伤,并且可能延伸到真皮层甚至皮下脂肪或更深。切割伤可能源于外科手术或意外事故对皮肤的穿透。
细胞的“生长状态”指细胞的增殖速率和/或细胞分化的状态。“生长状态改变”是特征在于不正常增殖速率的生长状态,如相对与正常细胞表现增殖速率增加或降低的细胞。
术语“毛发”指丝状结构,尤其是由角蛋白组成并且从真皮上的乳头状凹陷发育而来的分化表皮结构,仅由哺乳动物产生,并且是哺乳动物的特征。此外,“毛发”可以指所述毛发的聚集物。“毛囊”指围绕毛发的表皮的管状内陷,从毛囊中生长出毛发。“毛囊上皮细胞”指围绕毛囊内真皮乳肉的上皮细胞,如干细胞、外根鞘细胞、基质细胞和内根鞘细胞。所述细胞可以是正常的非恶性细胞或转化的/无限增殖的细胞。
术语“hedgehog拮抗剂”指加强或重现patched的生物活性的试剂,例如以抑制靶基因的转录。优选patched拮抗剂可用于克服ptc功能丧失和/或smoothened功能获得,后者也称为smoothened拮抗剂。本文中使用的术语“hedgehog拮抗剂”不仅指通过直接抑制hedgehog蛋白正常功能而起作用的任何试剂,而且指抑制hedgehog信号途径、因此重现ptc功能的任何试剂。
术语“hedgehog功能获得”指ptc基因、hedgehog基因或smoothened基因的异常修饰或突变或者所述基因表达水平的降低(或损失),从而导致类似于使细胞接触hedgehog蛋白的表型,如hedgehog途径的异常激活。功能获得可以包括ptc基因产物丧失调节Ci基因如Gli1、Gli2和Gli3的表达水平的能力。术语“hedgehong功能获得”在本文中也用于指由于在hedgehog信号转导途径中任一处改变而出现的任何相似细胞表型(如表现过度增殖),包括但不限于hedgehog本身的修饰或突变。例如,由于hedgehog信号途径激活而具有异常高增殖率的肿瘤细胞将具有“hedgehog功能获得”表型,即使所述细胞中hedgehog并未突变。
本文所用的“无限增殖的细胞”指这样的细胞:所述细胞已经通过化学方法和/或重组方法改变,以便所述细胞具有通过在培养物中无限分裂而生长的能力。
“内部上皮组织”指在体内内部、具有与皮肤表皮层相似特征的组织。例子包括肠的层。本发明的方法用于促进某些肠伤口(例如手术导致的伤口)的愈合。
术语“角化病”指特征在于表皮角质层增生的增生性皮肤疾病。角化疾病的例子包括毛囊角化病、掌跖角化病、咽角化病、毛周角化病和光化性角化病。
术语“LD50”指使50%测试受治疗者致死的药物剂量。
术语“指甲”指在手指或脚趾远端背侧面上的角质皮肤板。
术语“patched功能丧失”指ptc基因的异常修饰或突变,或者所述基因表达水平降低,导致类似于使细胞接触hedgehog蛋白的表型,例如hedgehog途径的异常激活。功能丧失可以包括ptc基因产物丧失调节Ci基因如Gli1、Gli2和Gli3的表达水平的能力。术语“ptc功能丧失”在本文中也用于指由于在hedgehog信号转导途径中任一处改变而出现的任何相似细胞表型(如表现过度增殖),包括但不限于ptc本身的修饰或突变。例如,由于hedgehog信号途径激活而具有异常高增殖率的肿瘤细胞将具有“ptc功能丧失”表型,即使所述细胞中ptc并未突变。
主题方法治疗的“患者”或“受治疗者”可以指人类或非人类动物。
术语“前体药物”包括在生理条件下转变成本发明治疗活性试剂的化合物。制造前体药物的一般方法是将在生理条件下被水解的选定部分包括在内,展现所需分子。在另一实施方案,所述前体药物被宿主动物的酶活性转化。
本文所用的“增殖”指经历有丝分裂的细胞。
在本申请全文中,术语“增殖性皮肤病”指特征在于皮肤组织的不需要或异常增殖的任何皮肤疾病/障碍。这些病理状况一般特征在于表皮细胞增殖或不完全细胞分化,包括例如X-连锁鱼鳞病、牛皮癣、特应性皮炎、过敏性接触皮炎、表皮松解性角化过度和脂溢性皮炎。例如,表皮发育不良是表皮发育不完善的一种形式。另一个例子是“表皮松解症”指表皮的松弛状态,或者同时或者在创伤位点形成疱和泡。
本文所用术语“牛皮癣”指改变皮肤调节机制的过度增殖性皮肤病。具体地说,病变形成涉及表皮增殖中的初级和次级改变、皮肤的炎症反应以及调节分子如淋巴因子和炎症因子的表达。牛皮癣皮肤的形态学特征在于表皮细胞更新加快、表皮增厚、不正常的角质化、炎症细胞浸润入真皮层和多形核白细胞浸润入表皮层导致基底细胞循环加快。此外,存在角化过度和角化不全的细胞。
术语“皮肤”指身体的外部保护性覆盖物,由真皮和表皮组成,包括汗腺和皮脂腺以及毛囊结构。在本申请全文中,可以使用形容词“皮肤的”,该形容词的意义根据上下文而定,一般指皮肤特性。
术语“smoothened功能获得”指smo基因的异常修饰或突变或者所述基因表达水平增加,导致类似于使所述细胞接触hedgehog蛋白的表型,如hedgehog途径异常激活。虽然不希望被任何特定理论限制,但注意到ptc不能直接传递信号进细胞,而是与hedgehog信号途径中ptc下游的另一种膜结合蛋白smoothened相互作用(Mango等,(1996)
Nature 384:177-179)。基因smo是果蝇属每个节正常模式化所需的节极性基因(Alcedo等,(1996)
Cell 86:221-232)。已经鉴定smo的人同源物。见例如Stone等(1996)
Nature 384:129-134和GenBank登记号U84401。Smoothened基因编码具有异三聚体G蛋白偶联受体特征(即7个跨膜区)的膜整合蛋白。该蛋白显示与wingless途径成员果蝇属Frizzled(Fz)蛋白同源。最初认为smo编码Hh信号的受体。然而,该理论随后被推翻,因为获得ptc是Hh受体的证据。表达Smo的细胞不能结合Hh,指出smo并不与Hh直接相互作用(Nusse,(1996)Nature 384:119-120)。更合适地说,据认为Sonic hedgehog(SHH)与其受体PTCH的结合防止PTCH对smoothened(SMO,一种七跨膜蛋白)的正常抑制。
最近,已经报道激活smoothened突变出现在散发性基底细胞癌中,Xie等(1998)Nature 391:90-2,以及出现在中枢神经系统的原神经外胚层肿瘤中,Reifenberger等(1998)
Cancer Res 58:1798-803。
术语“治疗指数”指用LD50/ED50定义的药物治疗指数。
本文所用的“转化细胞”指已经自发转化为不受限制生长状态的细胞,即它们获得通过在培养物中无限分裂而生长的能力。关于转化细胞失去生长控制,可以用下面术语表征:瘤、退行性发育和/或增生。
术语“酰氨基”是本领域内公知的术语,指可以用下面通式表示的部分:
其中R9如上文定义,R′11代表氢、烷基、链烯基或-(CH2)m-R8,其中m和R8如上文定义。
本文中术语“脂族基”指直链、支链或环状脂族烃基团,包括饱和和不饱和脂族基,如烷基、链烯基和炔基。
术语“链烯基”和“炔基”指长度和可能取代与上文所述烷基类似的不饱和脂族基,但分别包含至少一个双键或三键。
本文所用术语“烷氧基”指如上文所定义的烷基,其上连接氧基。有代表性的烷氧基包括甲氧基、乙氧基、丙氧基、丁氧基等。“醚”是通过一个氧原子共价连接的两个烃。因此,使烷基成为一种醚的烷基取代基是烷氧基或类似烷氧基,例如可以用-O-烷基、-O-链烯基、-O-炔基、-O-(CH2)m-R8其中之一表示,其中m和R8如上文定义。
术语“烷基”指饱和脂族基,包括直链烷基、支链烷基、环烷基(脂环基)、烷基取代的环烷基和环烷基取代的烷基。在优选实施方案中,直链烷基或支链烷基在其骨架上具有30个或更少碳原子(如直链是C1-C30,支链是C3-C30),更优选20个或更少碳原子。同样,优选的环烷基在它们的环结构上具有从3个到10个碳原子,更优选在环结构上有5、6或7个碳原子。
此外,在本说明书、实施例和权利要求全文中使用的术语“烷基”(或“低级烷基”)包括“未取代的烷基”和“取代的烷基”,后者指取代基取代烃骨架上一个或多个碳原子上的氢的烷基部分。所述取代基可以包括例如卤素、羟基、羰基(例如羧基、烷氧羰基、甲酰基或酰基)、硫代羰基(例如硫代酸酯、硫代乙酸酯、硫代甲酸酯)、烷氧基、磷酰基、磷酸酯、膦酸酯、次膦酸酯、氨基、酰氨基、脒、亚胺、氰基、硝基、叠氮基、硫氢基、烷硫基、硫酸酯、磺酸酯、氨磺酰、亚磺酰氨基、磺酰基、杂环基、芳烷基或芳族或杂芳族部分。本领域内技术人员知道:如果合适,烃链上取代部分本身可以被取代。例如,取代烷基的取代基可以包括取代和未取代形式的氨基、叠氮基、亚氨基、酰氨基、磷酰基(包括膦酸酯和次膦酸酯)、磺酰基(包括硫酸酯、亚磺酰氨基、氨磺酰和磺酸酯)和甲硅烷基以及醚、烷硫基、羰基(包括酮、醛类、羧酸酯和酯)、-CF3、-CN等。取代烷基的例子如下文所述。环烷基可以进一步用烷基、链烯基、烷氧基、烷硫基、氨烷基、羰基取代的烷基、-CF3、CN等取代。
除特别指出碳原子数目外,本文使用的“低级烷基”指如上文定义的烷基,但在其骨架上具有一到十个碳原子,更优选一到六个碳原子。同样,“低级链烯基”和“低级炔基”有相似的链长度。在本申请全文中,优选烷基是低级烷基。在优选实施方案中,本文命名为烷基的取代基是低级烷基。
术语“烷硫基”指如上文定义的烷基,其上连接一个硫基。在优选实施方案中,所述“烷硫基”部分用-S-烷基、-S-链烯基、-S-炔基和-S-(CH2)m-R8之一代表,其中m和R8如上文定义。有代表性的烷硫基包括甲硫基、乙硫基等。
术语“胺”和“氨基”是本领域内公知的术语,指取代和未取代的胺,如可以用下面通式代表的部分:
其中R9、R10和R′10各自独立地代表氢、烷基、链烯基、-(CH2)m-R8,或者R9和R10与它们连接的所述N原子一起构成环状结构内有4到8个原子的杂环;R8代表芳基、环烷基、环烯基、杂环或多环;m是零或1到8范围内的整数。在优选实施方案中,仅R9或R10其中之一可以是羰基,如R9、R10和氮一起不形成二酰亚胺。在某些这样的实施方案中,R9和R10都不通过羰基与N连接,如所述胺不是酰胺或二酰亚胺,并且所述胺最好是碱性的,如其缀合酸的pKa在7以上。在甚至更优选的实施方案中,R9和R10(任选R′10)各自独立地代表氢、烷基、链烯基或-(CH2)m-R8。因此,本文使用的术语“烷基胺”指如上文定义的胺基,其上连接有取代或未取代烷基,即至少R9和R10之一是烷基。
术语“酰氨基”是本领域内公知的术语,指氨基取代的羰基,包括可以用下面通式表示的部分:
其中R9、R10如上文定义。所述酰胺的优选实施方案将不包括不稳定的二酰亚胺。
本文使用的术语“芳烷基”指被芳基(如芳基或杂芳基)取代的烷基。
本文使用的术语“芳基”包括由5-、6-和7-元、可以包括零到四个杂原子的单环芳基,例如苯、吡咯、呋喃、噻吩、咪唑、噁唑、噻唑、三唑、吡唑、吡啶、吡嗪、哒嗪、嘧啶等。这些在环结构上具有杂原子的芳基也可以称为“芳基杂环”或“杂芳基”。所述芳香环可以用上文定义的取代基在一个或多个位置上进行取代,所述取代基例如卤素、叠氮化物、烷基、芳烷基、链烯基、炔基、环烷基、羟基、烷氧基、氨基、硝基、硫氢基、亚氨基、酰氨基、磷酸酯、膦酸酯、次膦酸酯、羰基、羧基、甲硅烷基、醚、烷硫基、磺酰基、亚磺酰氨基、酮、醛、酯、杂环基、芳族部分或杂芳族部分、-CF3、-CN等。术语“芳基”也包括具有两个或多个环的多环系统,其中两个或多个碳为两个临近的环所共用(所述环是“稠合环”),其中至少其中一个环是芳族环,如其它环可以是环烷基、环烯基、环炔基、芳基和/或杂环基。
本文使用的术语“碳环”指所述环中每一个原子都是碳的芳族环和非芳族环。
术语“羰基”是本领域内公知的术语,包括可以用下面通式代表的部分:
其中X是一个键或代表氧或硫,R11代表氢、烷基、链烯基、-(CH2)m-R8或药学上可接受的盐,R′11代表氢、烷基、链烯基或-(CH2)m-R8,其中m和R8如上文定义。当X是氧并且R11或R′11不是氢时,该式代表“酯”。当X是氧,并且R11如上文定义时,所述部分在本文中指羧基,尤其是当R11是氢时,该式代表“羧酸”。当X是氧,并且R′11是氢时,该式代表“甲酸酯”。一般地说,当上式的氧原子被硫取代时,上式代表“硫代羰基”基团。当X是硫并且R11或R′11不是氢时,该式代表“硫代酸酯”。当X是硫并且R11是氢时,该式代表“硫代羧酸”。当X是硫并且R′11是氢时,该式代表“硫羟甲酸酯”。另一方面,当X是一个键并且R11不是氢时,上式代表“酮”基团。当X是一个键并且R11是氢时,上式代表“醛”基团。
本文使用的术语“杂原子”指除碳或氢以外任何元素的原子。优选的杂原子是硼、氮、氧、磷、硫和硒。
术语“杂环基”或“杂环基团”指3-到10-元环结构,更优选3-到7-元环,所述环结构包括一到四个杂原子。杂环也可以是多环。杂环基包括例如噻吩、噻蒽、呋喃、吡喃、异苯并呋喃、苯并吡喃、呫吨、phenoxathiin、吡咯、咪唑、吡唑、异噻唑、异噁唑、吡啶、吡嗪、嘧啶、哒嗪、中氮茚、异吲哚、吲哚、吲唑、嘌呤、喹嗪、异喹啉、喹啉、2,3-二氮杂萘、1,5-二氮杂萘、喹喔啉、喹唑啉、噌啉、蝶啶、咔唑、咔啉、菲啶、吖啶、嘧啶、菲咯啉、吩嗪、吩砒嗪、吩噻嗪、呋咱、吩噁嗪、吡咯烷、噁茂烷、硫茂烷、噁唑、哌啶、哌嗪、吗啉、内酯、内酰胺如β-丙内酰胺和吡咯烷酮、磺内酰胺、磺内酯等。所述杂环可以在一个或多个位置被上文所述取代基的取代,所述取代基例如卤素、烷基、芳烷基、链烯基、炔基、环烷基、羟基、氨基、硝基、硫氢基、亚氨基、酰氨基、磷酸酯、膦酸酯、次膦酸酯、羰基、羧基、甲硅烷基、醚、烷硫基、磺酰基、酮、醛、酯、杂环基、芳族部分或杂芳族部分、-CF3、-CN等。
本文所用术语“硝基”指NO2;术语“卤素”是指-F、-Cl、-Br或-I;术语“硫氢基”指-SH;术语“羟基”指-OH;术语“磺酰基”指-SO2-。
“亚膦酰胺”可以用下面通式代表:
或
其中R9和R10如上文定义,Q2代表O、S或N,R48代表低级烷基或芳基,Q2代表O、S或N。
“亚磷酰胺”可以用下面通式代表:
或
其中R9和R10如上文定义,Q2代表O、S或N。
“磷酰基”一般可以用下面通式代表:
其中Q1代表S或O,R46代表氢、低级烷基或芳基。当用于取代例如烷基时,磷酰基烷基的磷酰基可以用下面通式代表:
其中Q1代表S或O,每个R46独立地代表氢、低级烷基或芳基,Q2代表O、S或N。当Q1是S时,所述磷酰基部分是“硫代磷酸酯”。
术语“多环基”或“多环基团”指其中两个或多个碳为两个临近的环所共用的两个或多个环(如环烷基、环烯基、环炔基、芳基和/或杂环基),如所述环是“稠合环”。通过非临近的原子连接的环称为“桥接”环。所述多环的每一个环可以用上文所述的取代基取代,所述取代基例如卤素、烷基、芳烷基、链烯基、炔基、环烷基、羟基、氨基、硝基、硫氢基、亚氨基、酰氨基、磷酸酯、膦酸酯、次膦酸酯、羰基、羧基、甲硅烷基、醚、烷硫基、磺酰基、酮、醛、酯、杂环基、芳族部分或杂芳族部分、-CF3、-CN等。
本文使用的词组“保护基团”指保护潜在反应性功能基团不发生不希望的化学转化的暂时取代基。所述保护基团的例子分别包括:羧酸的酯、醇的甲硅烷醚、醛和酮的缩醛和缩酮。已经综述保护基团化学的领域(Greene,T.W.;Wuts,P.G.M.Protective Groups inOrganic Synthesis,第二版;Wiley:New York,1991)。
“硒代烷基”指其上连接有取代硒基的烷基。在烷基上可被取代的“硒醚”的例子选自-Se-烷基、-Se-链烯基、-Se-炔基和-Se-(CH2)m-R8,其中m和R8在上文定义。
本文使用的术语“取代(的)”包括有机化合物的所有允许的取代基。在广义方面,允许的取代基包括有机化合物的无环和环状取代基、分支和不分支取代基、碳环型和杂环取代基、芳族和非芳族取代基。示例性的取代基包括例如那些上文描述的取代基。允许的取代基对于合适的有机化合物可以是一个或多个,可以相同或不同。为本发明的目的,杂原子例如氮可以有氢取代基和/或满足所述杂原子化合价的任何允许的本文所述有机化合物取代基。本发明不在任何形式上受限制于所述允许的有机化合物取代基。
应当知道:“取代”或“被取代”包括隐含的限定条件,即所述取代符合所述被取代原子和所述取代基的允许化合价,并且所述取代产生稳定的化合物,如并不通过例如重排、环化、消除等而自发发生转化。
术语“氨磺酰”是本领域内已知的,包括可以用下面通式代表的部分:
其中R9和R10如上文定义。
术语“硫酸酯”是本领域内已知的,包括可以用下面通式代表的部分:
其中R41如上文定义。
术语“亚磺酰氨基”是本领域内已知的,包括可以用下面通式表示的部分:
其中R9和R′11如上文定义。
术语“磺酸酯”是本领域内已知的术语,包括可以用下面通式表示的部分:
其中R41是一个电子对、氢、烷基、环烷基或芳基。
本文使用的术语“亚砜基”或“亚磺酰基”指可以用下面通式代表的部分:
其中R44选自下面基团:氢、烷基、链烯基、炔基、环烷基、杂环基、芳烷基或芳基。
对链烯基和炔基可以进行类似取代,产生例如氨基链烯基、氨基炔基、酰氨基链烯基、酰氨基炔基、亚氨基链烯基、亚氨基炔基、硫代链烯基、硫代炔基、羰基取代的链烯基或炔基。
本文中每种表达的定义,如烷基、m、n等,当在任何结构中出现一次以上时,应当独立于其在同一结构中其它地方的定义。
术语三氟甲磺酰基、甲苯磺酰基、甲磺酰基和九氟丁磺酰基是本领域内公知的术语,分别指三氟甲烷磺酰基、对甲苯磺酰基、甲烷磺酰基和九氟丁烷磺酰基。术语三氟甲磺酸酯、甲苯磺酸酯和九氟丁磺酸酯是本领域内公知的术语,分别指三氟甲烷磺酸酯、对甲苯磺酸酯、甲烷磺酸酯和九氟丁烷磺酸酯功能基团以及包含所述基团的分子。
缩写Me、Et、Ph、Tf、Nf、Ts、Ms分别代表甲基、乙基、苯基、三氟甲烷磺酰基、九氟丁烷磺酰基、对甲苯磺酰基和甲烷磺酰基。本领域内一般有机化学技术人员使用的缩写的更详细列表见Journal of Organic Chemistry每一卷的第一期;该列表通常出现在名为
Standard List of Abbreviations的表内。所述列表中包含的缩写以及本领域内有机化学技术人员使用的所有缩写特此通过引用结合到本文中。
本发明的某些化合物可能以特定几何形式或立体异构形式存在。本发明设想所有这些化合物在本发明的范围内,包括顺反异构体、R-和S-对映异构体、非对映异构体、(D)-异构体、(L)-异构体、它们的外消旋混合物以及其它混合物。在取代基例如烷基中可以存在其它不对称碳原子。所有这些异构体和它们的混合物包括在本发明中。
例如,假如需要本发明化合物的特定对映异构体,可以通过不对称合成制备,或者通过用手性助剂衍生得到,其中分离得到的非对映异构体混合物和切割所述助剂,提供纯化的所需对映异构体。或者,当所述分子包含碱性功能基团(如氨基)或酸性功能基团(如羧基)时,可以用合适旋光型酸或碱形成非对映异构体盐,然后通过分级结晶或本领域内已知的色谱方法拆分如此形成的非对映异构体,随后回收所述纯化的对映异构体。
上文所述本发明设想的等价物包括其其它对应化合物而且有其相同的一般性质(如抑制hedgehog信号传递的能力)的化合物,其中产生了不负面影响所述化合物功效的一个或多个简单取代基变化。一般地说,本发明化合物可以通过例如下文所述的通用反应方案中举例说明的方法制备,或者使用所述方法的修改形式制备,其中使用容易得到的起始材料、试剂和常规合成程序。在这些反应中,还有可能利用已知但本文没有提到的变化方法。
为本发明的目的按照CAS版本,Handbook of Chemistry andPhysics,67版,1986-87内封面的元素周期表鉴定化学元素。为本发明的目的,术语“烃”设想包括具有至少一个氢和一个碳原子的所有允许的化合物。在广义方面,允许的烃包括取代或未取代的无环和环状、分支和非分支、碳环和杂环、芳族和非芳族有机化合物。
III.本发明化合物的例子
如下文更详细所述,设想可以使用例如通过如本文所述的药物筛选测定容易鉴定的各种不同小分子实施本发明主题方法。例如,在本发明主题方法中使用的化合物包括可以用通式(I)代表的化合物:
式I
其中,当化合价和稳定性允许时,
X和Z独立地代表-N(R7)-、-O-、-S-、-(R7)N-N(R7)-、-ON(R7)-或者直接化学键,优选-N(R7)-、-O-、-S-或者直接化学键;
Y代表-C(=O)-、-C(=S)-、-C(=NR7)-、SO2、或SO,优选-C(=O)-、SO2、或-C(=S)-;
A代表O、S或NR7,优选O或NH,最优选NH;
G代表与其所连接的环稠合的环烷基、杂环基、芳基或杂芳基环,优选芳基或杂芳基环。
Ar代表取代或未取代芳基或杂芳基环,例如取代或未取代苯环;
R1代表H或取代或未取代烷基、链烯基、炔基、芳基、杂芳基、杂环基或环烷基,包括多环基;
R2代表其所连接的环上的0-4个取代基,例如卤素、低级烷基、低级链烯基、芳基、杂芳基、羰基(如酯、羧基或甲酰基)、硫代羰基(如硫代酸酯、硫代羧酸酯、硫代甲酸酯)、酮、醛、氨基、酰氨基、酰胺基、脒基、氰基、硝基、叠氮基、磺酰基、亚砜基、硫酸酯、磺酸酯、氨磺酰、亚磺酰氨基、磷酰基、膦酸酯、次膦酸酯、J-R8、J-OH、J-低级烷基、J-低级链烯基、J-R8、J-SH、J-NH2、上述基团的受保护形式,或者任意两个R2,当R2在环结构或多环结构中出现一次以上时,可以一起形成4-到8-元环烷基、芳基或杂芳基;
R7每次出现时独立地代表H、低级烷基(例如取代或未取代的低级烷基)、J-环烷基(例如取代或未取代的)、J-杂环基(例如取代或未取代的)、J-芳基(例如取代或未取代的)、J-杂芳基(例如取代或未取代的);
R8每次出现时独立地代表H、低级烷基(例如取代或未取代的)、环烷基(例如取代或未取代的)、杂环基(例如取代或未取代的)、芳基(例如取代或未取代的)或杂芳基(例如取代或未取代的);和
J每次出现时独立地代表具有0-8个(最好0-4个)单位的链,所述单位选自CK2、NK、O和S,其中K每次出现时独立地代表H或低级烷基。
在某些实施方案中,Z和X至少其中之一不是直接化学键。在某些实施方案中,X-Y-Z包括酰胺、脲或磺酰胺。在某些实施方案中,X选自-N(R8)-、-O-、-S-,优选代表NH。
在某些实施方案中,R1包括芳基或杂芳基环,所述芳基或杂芳基环可选地被1-5个取代基的取代,所述取代基例如硝基、卤素、氰基、低级烷基、酰氨基(如R8-C(=O)NH-)、烷氧基、烷基氨基、与所述芳基或杂芳基环稠合的取代或未取代环烷基、杂环基、芳基或杂芳基。
在某些实施方案中,X和包括A的环以间位(即1,3)关系排列在Ar上。
在某些实施方案中,G代表苯基或哌啶环。
在某些实施方案中,缺失J。
在某些实施方案中,R2代表选自以下的1-4个取代基:卤素、氰基、硝基、烷氧基、氨基、酰氨基(如R8-C(=O)NH-)、与G稠合的取代或未取代的环烷基、杂环基、芳基、或杂芳基以及取代或未取代低级烷基。
在某些实施方案中,主题化合物选自图32中描述的化合物。
在某些实施方案中,本发明使用的化合物可以用通式(II)代表:
式II
其中,当化合价和稳定性允许时,
X和Z独立地代表-N(R7)-、-O-、-S-、-(R7)N-N(R7)-、-ON(R7)-或者直接化学键,优选-N(R7)-、-O-、-S-或者直接化学键;
Y代表-C(=O)-、-C(=S)-、-C(=NR7)-、SO2、或SO,优选-C(=O)-、SO2、或-C(=S)-;
A代表O、S或NR7,优选O或NH,最优选NH;
G代表与其所连接的环稠合的环烷基、杂环基、芳基或杂芳基环,优选芳基或杂芳基环。
R1代表H或取代或未取代烷基、链烯基、炔基、芳基、杂芳基、杂环基或环烷基,包括多环基;
R2代表其所连接的环上的0-4个取代基,例如卤素、低级烷基、低级链烯基、芳基、杂芳基、羰基(如酯、羧基或甲酰基)、硫代羰基(如硫代酸酯、硫代羧酸酯、或硫代甲酸酯)、酮、醛、氨基、酰氨基、酰胺基、脒基、氰基、硝基、叠氮基、磺酰基、亚砜基、硫酸酯、磺酸酯、氨磺酰、亚磺酰氨基、磷酰基、膦酸酯、次膦酸酯、J-R8、J-OH、J-低级烷基、J-低级链烯基、J-R8、J-SH、J-NH2、上述基团的受保护形式,或者任意两个R2,当R2在一个环结构或多环结构中出现一次以上时,可以一起形成4-到8-元环烷基、芳基或杂芳基;
R3代表其所连接的环上的0-4个取代基,例如卤素、羟基、烷氧基、氨基、烷基氨基、氰基、硝基、取代或未取代低级烷基、以及酰基,优选卤素、低级烷氧基或取代或未取代低级烷基。
R7每次出现时独立地代表H、低级烷基(例如取代或未取代的)、J-环烷基(例如取代或未取代的)、J-杂环基(例如取代或未取代的)、J-芳基(例如取代或未取代的)、J-杂芳基(例如取代或未取代的);
R8每次出现时独立地代表H、低级烷基(例如取代或未取代的)、环烷基(例如取代或未取代的)、杂环基(例如取代或未取代的)、芳基(例如取代或未取代的)或杂芳基(例如取代或未取代的);和
J每次出现时独立地代表具有0-8个(最好0-4个)单位的链,所述单位选自CK2、NK、O和S,其中K每次出现时独立地代表H或低级烷基。
在某些实施方案中,Z和X至少其中之一不是直接化学键。在某些实施方案中,X-Y-Z包括酰胺、脲或磺酰胺。在某些实施方案中,X选自-N(R8)-、-O-、-S-,优选代表NH。
在某些实施方案中,R1包括芳基或杂芳基环,所述芳基或杂芳基环可选地被1-5个取代基的取代,所述取代基例如硝基、卤素、氰基、低级烷基、酰氨基(如R8-C(=O)NH-)、烷氧基、烷基氨基、与所述芳基或杂芳基环稠合的取代或未取代环烷基、杂环基、芳基或杂芳基。
在某些实施方案中,G代表苯基或哌啶环。
在某些实施方案中,缺失J。
在某些实施方案中,R2代表选自以下的1-4个取代基:卤素、氰基、硝基、烷氧基、氨基、酰氨基(如R8-C(=O)NH-)、与G稠合的取代或未取代环烷基、杂环基、芳基、或杂芳基,以及取代或未取代低级烷基。
在某些实施方案中,R3包括在X或含A的环的对位的取代基,例如取代或未取代的烷基或卤素。
在某些实施方案中,主题化合物选自图32中描述的化合物。
如下文更详细所述,设想可以使用例如通过如本文所述的药物筛选测定容易鉴定的各种不同小分子实施本发明主题方法。例如,在本发明主题方法中使用的化合物可以用通式(III)代表:
式III
其中,当化合价和稳定性允许时,
X和Z独立地代表-N(R7)-、-O-、-S-、-(R7)N-N(R7)-、-ON(R7)-或者直接化学键,优选-N(R7)-、-O-、-S-或者直接化学键;
Y代表-C(=O)-、-C(=S)-、-C(=NR7)-、SO2、或SO,优选-C(=O)-、SO2、或-C(=S)-;
A代表O、S或NR7,优选O或NH,最优选NH;
G代表与其所连接的环稠合的环烷基、杂环基、芳基或杂芳基环,优选芳基或杂芳基环。
Q不存在,或者代表CK2、NK、O和S,其中K每次出现时独立地代表H或低级烷基;
Ar代表取代或未取代的芳基或杂芳基环,例如取代或未取代的苯环;
R1代表H或取代或未取代烷基、链烯基、炔基、芳基、杂芳基、杂环基或环烷基,包括多环基;
R2代表其所连接的环上的0-4个取代基,例如卤素、低级烷基、低级链烯基、芳基、杂芳基、羰基(如酯、羧基或甲酰基)、硫代羰基(如硫代酸酯、硫代羧酸酯、或硫代甲酸酯)、酮、醛、氨基、酰氨基、酰胺基、脒基、氰基、硝基、叠氮基、磺酰基、亚砜基、硫酸酯、磺酸酯、氨磺酰、亚磺酰氨基、磷酰基、膦酸酯、次膦酸酯、J-R8、J-OH、J-低级烷基、J-低级链烯基、J-R8、J-SH、J-NH2、上述基团的受保护形式,或者任意两个R2,当R2在一个环结构或多环结构中出现一次以上时,可以一起形成4-到8-元环烷基、芳基或杂芳基;
R7每次出现时独立地代表H、低级烷基(例如取代或未取代的)、J-环烷基(例如取代或未取代的)、J-杂环基(例如取代或未取代的)、J-芳基(例如取代或未取代的)、J-杂芳基(例如取代或未取代的);
R8每次出现时独立地代表H、低级烷基(例如取代或未取代的)、环烷基(例如取代或未取代的)、杂环基(例如取代或未取代的)、芳基(例如取代或未取代的)或杂芳基(例如取代或未取代的);和
J每次出现时独立地代表具有0-8个(最好0-4个)单位的链,所述单位选自CK2、NK、O和S。
在某些实施方案中,Z和X至少其中之一不是直接化学键。在某些实施方案中,X-Y-Z包括酰胺、脲或磺酰胺。在某些实施方案中,X选自-N(R8)-、-O-、-S-,优选代表NH。
在某些实施方案中,R1包括芳基或杂芳基环,所述芳基或杂芳基环可选地被1-5个取代基的取代,所述取代基例如硝基、卤素、氰基、低级烷基、酰氨基(如R8-C(=O)NH-)、烷氧基、烷基氨基、与所述芳基或杂芳基环稠合的取代或未取代环烷基、杂环基、芳基或杂芳基。
在某些实施方案中,X和包括A的环以间位(即1,3)关系排列在Ar上。
在某些实施方案中,G代表苯基或哌啶环。
在某些实施方案中,缺失J。
在某些实施方案中,R2代表选自以下的1-4个取代基:卤素、氰基、硝基、烷氧基、氨基、酰氨基(如R8-C(=O)NH-)、与G稠合的取代或未取代的环烷基、杂环基、芳基、或杂芳基以及取代或未取代低级烷基。
在某些实施方案中,主题化合物选自图32中描述的化合物。
在某些实施方案中,本发明使用的化合物可以用通式(IV)代表:
式IV
其中,当化合价和稳定性允许时,
X和Z独立地代表-N(R7)-、-O-、-S-、-(R7)N-N(R7)-、-ON(R7)-或者直接化学键,优选-N(R7)-、-O-、-S-或者直接化学键;
Y代表-C(=O)-、-C(=S)-、-C(=NR7)-、SO2、或SO,优选-C(=O)-、SO2、或-C(=S)-;
A代表O、S或NR7,优选O或NH,最优选NH;
G代表与其所连接的环稠合的环烷基、杂环基、芳基或杂芳基环,优选芳基或杂芳基环。
Q不存在,或者代表CK2、NK、O和S,其中K每次出现时独立地代表H或低级烷基;
R1代表H或取代或未取代烷基、链烯基、炔基、芳基、杂芳基、杂环基或环烷基,包括多环基;
R2代表其所连接的环上的0-4个取代基,例如卤素、低级烷基、低级链烯基、芳基、杂芳基、羰基(如酯、羧基或甲酰基)、硫代羰基(如硫代酸酯、硫代羧酸酯、或硫代甲酸酯)、酮、醛、氨基、酰氨基、酰胺基、脒基、氰基、硝基、叠氮基、磺酰基、亚砜基、硫酸酯、磺酸酯、氨磺酰、亚磺酰氨基、磷酰基、膦酸酯、次膦酸酯、J-R8、J-OH、J-低级烷基、J-低级链烯基、J-R8、J-SH、J-NH2、上述基团的受保护形式,或者任意两个R2,当R2在一个环结构或多环结构中出现一次以上时,可以一起形成4-到8-元环烷基、芳基或杂芳基;
R3代表其所连接的环上的0-4个取代基,例如卤素、羟基、烷氧基、氨基、烷基氨基、氰基、硝基、取代或未取代低级烷基、以及酰基,优选卤素、低级烷氧基或取代或未取代低级烷基。
R7每次出现时独立地代表H、低级烷基(例如取代或未取代的)、J-环烷基(例如取代或未取代的)、J-杂环基(例如取代或未取代的)、J-芳基(例如取代或未取代的)、J-杂芳基(例如取代或未取代的);
R8每次出现时独立地代表H、低级烷基(例如取代或未取代的)、环烷基(例如取代或未取代的)、杂环基(例如取代或未取代的)、芳基(例如取代或未取代的)或杂芳基(例如取代或未取代的);和
J每次出现时独立地代表具有0-8个(最好0-4个)单位的链,所述单位选自CK2、NK、O和S。
在某些实施方案中,Z和X至少其中之一不是直接化学键。在某些实施方案中,X-Y-Z包括酰胺、脲或磺酰胺。在某些实施方案中,X选自-N(R8)-、-O-、-S-,优选代表NH。
在某些实施方案中,R1包括芳基或杂芳基环,所述芳基或杂芳基环可选地被1-5个取代基的取代,所述取代基例如硝基、卤素、氰基、低级烷基、酰氨基(如R8-C(=O)NH-)、烷氧基、烷基氨基、与所述芳基或杂芳基环稠合的取代或未取代环烷基、杂环基、芳基或杂芳基。
在某些实施方案中,G代表苯基或哌啶环。
在某些实施方案中,缺失J。
在某些实施方案中,R2代表选自以下的1-4个取代基:卤素、氰基、硝基、烷氧基、氨基、酰氨基(如R8-C(=O)NH-)、与G稠合的取代或未取代环烷基、杂环基、芳基、或杂芳基,以及取代或未取代低级烷基。
在某些实施方案中,R3包括在X或者包括A的环上处于对位的取代基,例如取代或未取代烷基或卤素。
在某些实施方案中,主题化合物选自图32中描述的化合物。
在某些实施方案中,可以根据主题拮抗剂对hedgehog途径的选择性对它们进行选择。与针对其它途径的比较,所述选择性可以是针对hedgehog途径的,或者是特定hedgehog途径(如ptc-1、ptc-2等)之间的选择性。
在某些优选实施方案中,所述主题抑制剂在1mM或更低的ED50、更优选1μM或更低的ED50、甚至更优选1mM或更低的ED50抑制ptc功能丧失、hedgehog功能获得或smoothened功能获得介导的信号传导。相似地,在某些优选实施方案中,所述主题抑制剂在低于10nM的Ki、优选低于1nM的Ki、甚至更优选低于0.1nM的Ki抑制hedgehog途径的活性。
在特定实施方案中,选择使用小分子,因为其对一种patched异构体与对下一种patched同种型相比更有选择性,如对一种patched途径(ptc-1,ptc-2)与对另一种patched途径相比有10倍、更优选至少100倍甚至1000倍的选择性。
在某些实施方案中,选择作为hedgehog途径拮抗剂的化合物选择性拮抗相对于除PKA外其它蛋白激酶(例如PKC)的hedgehog活性,如所述化合物调节hedgehog途径活性比其调节另一种蛋白激酶活性强至少一个数量级,优选强至少两个数量级,甚至更优选强至少三个数量级。因此,例如,hedgehog途径的优选抑制剂抑制hedgehog活性的Ki比其抑制PKC的Ki低至少一个数量级,优选低至少两个数量级,甚至更优选低至少三个数量级或更低。在某些实施方案中,PKA抑制的Ki小于10nM,优选小于1nM,甚至更优选小于0.1nM。
IV.方法和组合物的应用示例
本发明另一方面涉及调节ptc功能丧失、hedgehog功能获得或smoothened功能获得的细胞的分化状态、存活率和/或增殖的方法,所述方法在情况允许的条件下,使所述细胞接触依照本发明主题方法的hedgdhog拮抗剂。
例如,由于hedge、ptc和smoothened明显广泛参与脊椎动物体内分化组织有序空间排列形成,本发明设想本发明主题方法可用作在体外和体内产生和/或维持不同脊椎动物组织阵列的部分过程。如果合适,所述hedgehog拮抗剂无论对于给定组织的增殖或分化是诱导性或抗诱导性的,可以是上文所述的任何一种制剂。
例如,本方法可应用于其中细胞不论是由于遗传原因或生物化学原因而具有ptc功能丧失、hedgehog功能获得或smoothened功能获得表型的细胞培养技术。已经证明体外神经元培养系统对于研究神经发育以及鉴定神经营养因子如神经生长因子(NGF)、睫营养因子(CNTF)和脑产生的神经营养因子(BDNF)是基本和不可缺少的工具。本发明的一种应用可以是在神经元干细胞的培养物中,例如应用于所述培养物,产生新的神经元和神经胶质。在本发明主题方法的所述实施方案中,可以使培养细胞与本发明的hedgehog拮抗剂接触,以改变所述培养物中神经元干细胞的增殖速率和/或改变分化速率,或者维持某些终末分化的神经元细胞培养物的完整性。在示例性的实施方案中,本发明主题方法可用于培养例如感觉神经元或运动神经元。所述神经元培养物可用作常规测定系统以及用于治疗性治疗的可植入细胞的来源。
根据本发明,通过使大量非致瘤性神经祖细胞接触本发明的hedgehog拮抗剂,可以在体外无限延续所述细胞并且影响它们的增殖和/或分化速率。一般地说,提供包含下面步骤的方法:从动物分离神经祖细胞,使它们在体外或体内无限延续(最好在生长因子存在下),然后通过使所述细胞接触hedgehog拮抗剂,调节这些细胞分化成为特定神经表型,如神经元和神经胶质。
祖细胞据认为处于紧张的抑制影响下,维持所述祖细胞处于抑制状态,直到需要它们的分化。然而,已经提供最近的技术,允许增殖这些细胞,这些细胞与终末分化并因此不分裂的神经元不同,它们能够以无限数量产生,非常适于移植进患有神经退行性疾病的异源或自体宿主。
“祖细胞”指寡能或多能干细胞,所述寡能或多能干细胞能够无限分裂,并且在特定条件下能产生终末分化为例如神经元和神经胶质的子细胞。这些细胞可以用于移植进异源或自体宿主。异源指与所述祖细胞原始来源的动物不同的宿主。自体指与所述细胞原始来源相同宿主。
可以从任何动物的胚神经组织、出生后神经组织、幼年神经组织或成年神经组织获得细胞。任何动物指包含神经组织的任何多细胞动物。更具体地说,指任何鱼、爬行动物、鸟类、两栖动物或哺乳动物。最优选的供体是哺乳动物,尤其是小鼠和人。
在异源供体动物的情况下,可以无痛致死所述动物,使用无菌程序取出脑和特定目的区域。特定目的的脑区域包含从中可以获得祖细胞的任何区域,所述祖细胞用于恢复宿主脑内退行区域的功能。这些区包括中枢神经系统(CNS)的区域和外周神经系统(PNS)的区域,所述中枢神经系统的区域包括大脑皮层、小脑、中脑、脑干、脊髓和室组织,所述外周神经系统的区域包括颈动脉体和肾上腺髓质。更具体地说,这些区域包括基底神经节区,优选包括尾和核的纹状体,或者各种细胞群如苍白球、底丘脑核、在阿尔茨海默病患者体内退化的基底核(nucleus basalis)或者在帕金森病患者体内退化的黑质致密层部(substantia nigra pars compacta)。
人异源神经祖细胞可以来自从选择性堕胎获得的胚胎组织,或者来自出生后、幼年或成年器官供体。自体神经组织可以通过活组织检查获得,或者从接受切除神经组织的神经手术的患者获得,尤其是在癫痫手术期间,更优选在颞叶切除和海马切除术期间。
通过从供体组织的连接细胞外基质解离各个细胞,从所述组织获得细胞。可以使用任何已知程序进行解离,包括用酶如胰蛋白酶、胶原酶等进行处理,或者通过使用物理分离方法,例如用钝器,或者用解剖刀切碎以允许从组织生长出特定细胞类型。可以在组织培养培养基中解离胚胎细胞,用于解离幼年和成年细胞的优选培养基是人造脑脊髓液(aCSF)。常用的aCSF包含124mM NaCl,5mM KCl,1.3mM MgCl2,2mM CaCl2,26mM NaHCO3和10mM D-葡萄糖。低Ca2+aCSF包含同样成分,只是MgCl2浓度为3.2mM,CaCl2浓度为0.1mM。
可以将解离的细胞放置入任何已知能够支持细胞生长的培养基,包括MEM、DMEM、RPMI、F-12等,所述培养基包含细胞代谢所需的补充剂,例如谷氨酰胺和其它氨基酸、维生素、矿物质和有用的蛋白质如转铁蛋白等。培养基也可以包含抗生素,以预防酵母、细菌和真菌的污染,所述抗生素如青霉素、链霉素、艮他霉素等。在一些情况下,所述培养基可以包含来自牛、马、鸡等的血清。一种用于细胞的尤其优选的培养基是DMEM和F-12的混合物。
培养条件应当接近生理条件。所述培养基的pH应当接近生理pH,优选pH6-8之间,更优选接近pH7,甚至更优选约pH7.4。应当在接近生理温度的温度下培养细胞,优选在30℃-40℃之间,更优选在32℃-38℃之间,最优选在35℃-37℃之间。
可以在悬浮液中或固定底物上培养细胞,但祖细胞的增殖优选在悬浮液中完成,通过形成“神经球”产生大量细胞(见,例如,Reynold等(1992)Science 255:1070-1709;和PCT公开WO93/01275、WO94/09119、WO94/10292和WO94/16718)。在繁殖(或分裂)悬浮细胞的情况下,充分振荡瓶子,允许神经球定居在瓶的底部角落。然后将所述球转移到50ml离心管,在低速下离心。吸出培养基,使所述细胞悬浮于少量含生长因子的培养基中,然后通过机械方法解离细胞,重悬浮于分离的培养基等分物。
在培养基的细胞悬浮液中补充允许所述祖细胞增殖的任何生长因子,将所述细胞悬浮液接种到任何能够如上文所述维持细胞的容器中,优选培养瓶或转瓶。细胞通常在37℃培养箱中3-4天之内增殖,在此之后的任何时间,通过解离所述细胞并重悬浮于包含生长因子的新鲜培养基,可以重新起始增殖。
在缺乏支持物的情况下,细胞从瓶的底部长出,继续在悬浮液内增殖,形成未分化细胞的空心球体。在体外约3-10天后,通过温和的离心并重悬浮于包含生长因子的培养基,每2-7天饲喂所述增殖簇(神经球),更优选每2-4天饲喂。
体外6-7天后,用钝器通过物理分离从所述神经球上分离各个细胞,更具体地说用移液管捣碎所述神经球。将来自解离神经球的单个细胞悬浮于包含生长因子的培养基中,通过在hedgehog拮抗剂存在下接种(或重悬浮)所述细胞,可以控制培养物内细胞的分化。
为进一步举例说明主题hedgehog拮抗剂的其它应用,注意到大脑内移植已经成为中枢神经系统疗法的新方法。例如,修复受损脑组织的一种方法涉及将来自胚胎动物或新生动物的细胞移植进成体脑(Dunnett等(1987)J Exp Biol 123:265-289;和Freund等(1985)JNeurosci 5:603-616)。可以将来自各种脑区的胚胎神经元成功地加入成体的脑,所述移植物能够缓解行为缺陷。例如,通过移植胚胎多巴胺能神经元,可以预防由于多巴胺能投射到基底神经节的损伤引起的运动障碍。通过移植胚胎皮质细胞,也可以部分恢复新皮质损伤后损害的复杂认知功能。可以使用本发明主题方法调节培养物内的生长状态,或者当使用胚胎组织尤其是神经元干细胞时,可以使用本发明主题方法调节所述干细胞的分化速率。
本发明内使用的干细胞是众所周知的。例如,已经鉴定几种神经管嵴细胞,其中一些是多功能的,有可能代表未定型的神经管嵴细胞,其它细胞仅产生一种类型细胞(例如感觉神经元),可能代表定型的祖细胞。本发明方法中用于培养所述干细胞的hedgehog拮抗剂的作用可以是调节所述未定型祖细胞的分化,或者调节对于定型祖细胞朝终末分化的神经元细胞变化的命运的进一步限制。例如,本发明可用于体外调节神经管嵴细胞分化为神经胶质细胞、神经膜细胞、嗜铬细胞、胆碱能交感神经元或副交感神经元、以及肽能神经元和5-羟色胺能神经元。所述hedgehog拮抗剂可以单独使用,或者可以与其它神经营养因子组合使用,以更显著地增强神经元祖细胞的具体分化趋势。
除移植在所述主题hedgehog拮抗剂存在下培养的细胞外,本发明的又一方面涉及hedgehog拮抗剂用于调节中枢神经系统和外周神经系统内神经元和其它神经元细胞的生长状态的治疗应用。ptc、hedgehog和smoothened在神经系统发育期间以及大概在成体状态下调节神经元分化的能力指示:在某些情况下,预期所述主题hedgehog拮抗剂能够在下列方面便利控制成体神经元:正常细胞的维持、功能实施和老化;被化学伤害和机械伤害的细胞中的修复和再生过程;治疗某些病理条件下的退化。考虑到这项理解,本发明特地设想应用本发明主题方法于下面原因引起的神经学病理状况的治疗方案(预防和/或减少所述神经学病理状况的严重性):(i)对神经系统的急性、亚急性或慢性损伤,包括创伤、化学损伤、血管损伤和缺血(例如中风引起的局部缺血),以及感染/炎症和肿瘤引起的损伤;(ii)神经系统的老化,包括阿尔茨海默病;(iii)神经系统的慢性神经退行性疾病,包括帕金森病、亨廷顿舞蹈病、肌萎缩性侧索硬化等以及脊髓小脑退化;和(iv)神经系统的慢性免疫疾病或影响神经系统的慢性免疫疾病,包括多发性硬化。
如何合适,本发明主题方法也可以用于产生用于修复中枢和外周神经损害的神经假体。具体地说,当使用假体装置插入粉碎或被切断的轴突时,可以在所述假体装置中加入hedgehog拮抗剂,调节树突生长和再生过程的速率。在美国专利第5,092,871号和第4,955,892号中描述神经制导通道的例子。
在另一实施方案中,本发明主题方法可用于治疗例如在中枢神经系统中出现的肿瘤转化或增生转化。例如,可以利用所述hedgehog拮抗剂导致所述转化细胞进入有丝分裂期后或凋亡。因此,本方法可用作例如恶性神经胶质瘤、脑脊膜瘤、成神经管细胞瘤、神经外胚层肿瘤和室管膜瘤的部分治疗。
在优选实施方案中,本发明主题方法可用作恶性成神经管细胞瘤和其它原发性CNS恶性神经外胚层肿瘤的治疗方案组成部分。
在某些实施方案中,本发明主题方法可用作成神经管细胞瘤的治疗方案组成部分。成神经管细胞瘤是一种原发性脑瘤,是儿童中最常见的脑瘤。成神经管细胞瘤是从后窝产生的原神经外胚层肿瘤。它们在所有儿科脑肿瘤中占约25%(Miller)。在组织学上,它们是通常排列成精确的玫瑰花结的小的圆形细胞肿瘤,但可能表现出一定星形胶质细胞、室管膜细胞或神经元分化(Rorke;Kleihues)。PNET’s可以出现在脑的其它区域,包括松果体(成松果体细胞瘤)和大脑。在脑幕上区出现的那些通常比它们的PF对应物发展更差。
已知成神经管细胞瘤/PNET’s在切除后复发于CNS内的任何地方,并且甚至能够转移到骨。因此,治疗前评价应当包括检查脊髓,以排除“滴落转移(dropped metastasis)”的可能性。在此目的方面,钆增强的MRI已经在很大程度上取代脊髓造影术,并且作为常规程序,在手术后获得CSF细胞学。
在其它实施方案中,本发明主题方法用作室管膜瘤治疗程序的一部分。室管膜瘤引起儿童中约10%的儿科脑瘤。总体而言,它们是从脑室的室管膜层形成的肿瘤,在镜检下形成玫瑰花结、管和血管周的玫瑰花结。在报道患有室管膜瘤的CHOP系列51名儿童中,3/4在组织学上是良性的。约2/3产生于第4室的区域。三分之一存在于脑幕上区。根据SEER数据以及来自CHOP的数据显示,出现的年龄在出生和4岁之间达到峰值。中值年龄是约5岁。因为许多患此疾病的儿童是婴儿,他们常常需要联合治疗。
本发明的再一方面涉及本领域内的如下观察:ptc、hedgehog和/或smoothened除涉及上文所述的神经元分化外,还涉及参与其它脊椎动物器官发生途径的形态发生信号,在其它内胚层模式化以及中胚层和内胚层分化过程中有明显作用。因此,本发明设想包含hedgehog拮抗剂的组合物也可以用于涉及产生和维持非神经元组织的细胞培养物和治疗方法。
在一个实施方案中,本发明利用下面发现:ptc、hedgehog和smoothened明显参与干细胞发育,所述干细胞负责形成消化道、肝、肺和起源于原肠的其它器官的形成。Shh作为从内胚层到中胚层的诱导信号,对于肠形态发生是关键的。因此,例如,可以使用本发明方法的hedgehog拮抗剂调节具有正常肝多种代谢功能的人造肝的发育和维持。在示例性的实施方案中,可以使用本发明主题方法调节消化管干细胞的增殖和分化,形成可用于定居于细胞外基质或可以包囊入生物亲和聚合物的肝细胞培养物,或者形成植入型以及体外型人造肝。
在另一实施方案中,hedgehog拮抗剂的治疗组合物可以与所述人造肝移植以及胚胎肝结构联合使用,调节所述移植肝组织的腹膜内植入、血管化以及体内分化和维持。
在再一实施方案中,在治疗上可以使用本发明主题方法调节物理伤害、化学伤害或病理学伤害后的所述器官。例如,在部分肝切除术后的肝恢复中可以使用包含hedgehog拮抗剂的治疗组合物。
胰腺和小肠从胚胎肠中的产生依赖于所述肠内胚层和中胚层细胞间的细胞间信号传递。具体地说,已经提示肠中胚层到平滑肌的分化依赖于来自临近内胚层细胞的信号。胚胎后肠中内胚层产生的信号的一种候选介质是Sonic hedgehog。见,例如,Apelqvist等(1997)Curr Biol 7:801-4。所述Shh基因在除胰芽内胚层外的整个胚胎肠内胚层中表达,而胰芽内胚层表达高水平发育同源结构域蛋白Ipf1/Pdx1(胰岛素启动子因子1/胰腺和十二指肠同源框1),即早期胰腺发育的基本调节物。Apelqvist等,同上,已经检查Shh在胚胎肠管内的差异表达是否控制周围中胚层分化成为小肠和胰腺的专化中胚层衍生物。为检验这一点,他们使用Ipf1/Pdx1基因的启动子选择性表达发育中的胰上皮内的Shh。在Ipf1/Pdx1转基因小鼠中,所述胰中胚层发育成为肠特征性的平滑肌和Cajal的间质细胞,而不是发育成为胰间充质和脾。另外,暴露于Shh的胰外植块经受肠分化的相似程序。这些结果提供证据证明:内胚层产生的Shh的差异表达控制肠管不同区域临近中胚层的趋势。
因此,在本发明的范围内,设想可以使用所述主题hedgehog拮抗剂在体内和体外控制或调节胰组织的增殖和/或分化。
本发明的抑制剂可以为多种病理性细胞增殖和分化状况提供治疗好处,一般策略是,例如,改正异常胰岛素表达,或者调节分化。然而,更一般地说,本发明涉及诱导和/或维持分化状态、增强存活率和/或影响胰细胞增殖的方法,该方法使所述细胞接触所述主题抑制剂。例如,考虑到ptc、hedgehog和smoothened明显参与胰组织有序空间排列的形成,本发明设想可以使用本发明主题方法作为在体外和体内产生和/或维持所述组织的技术的一部分。例如,调节hedgehog功能可用于细胞培养以及涉及产生和维持β-细胞和可能非胰组织的治疗方法,例如用于控制来自消化道、脾、肺、泌尿生殖器官(如膀胱)和其它起源于原肠的器官的组织的发育和维持。
在示例性的实施方案中,本方法可用于治疗影响胰组织的增生性和瘤性疾病,尤其是那些特征在于胰细胞异常增殖的疾病。例如,胰癌特征在于能够导致胰腺的胰岛素分泌能力改变的胰细胞异常增殖。例如,某些胰增生如胰癌能够由于β-细胞功能紊乱或胰岛细胞量减少而引起低胰岛素血。在疾病发展中可以指示异常ptc、hedgehog和smoothened信号传导的程度,所述主题抑制剂可用于增强抗肿瘤疗法后所述组织的再生。
此外,在不同点操作hedgehog信号传导性质可用作在体内和体外再塑形/修复胰组织的策略的一部分。在一个实施方案中,本发明利用ptc、hedgehog和smoothened明显参与调节胰组织发育的行为。一般地说,在治疗上可以使用本发明主题方法在物理伤害、化学伤害或病理学伤害后调节胰腺。在又一实施方案中,可以应用本发明主题方法于细胞培养技术,具体地说可以应用于增强假体胰组织装置的最初产生。例如,通过改变hedgehog活性操作胰腺组织的增殖和分化可以提供更小心地控制培养组织特性的方法。在示例性的实施方案中,可以使用本发明主题方法增加需要β-胰岛细胞的假体装置的产量,例如可用于在下面专利中描述的包囊装置:例如,Aebischer等美国专利第4,892,538号,Aebischer等美国专利第5,106,627号,Lim美国专利第4,391,909号,和Sefton美国专利第4,353,888号。胰岛的早期祖细胞是多功能的,在它们首次出现后就明显共激活所有胰岛特异性基因。随着发育的进行,胰岛特异性激素例如胰岛素的表达限制于成熟胰岛细胞特征性的表达模式。然而,成熟胰岛细胞的表型在培养物中不稳定,因为可以观察到成熟β-细胞中胚胎性状的重新出现。通过利用所述主题hedgehog拮抗剂,可以调节所述细胞的分化途径或增殖指数。
此外,对胰组织分化状态的操作可以与移植人造胰腺联合应用,以促进移植组织的植入、血管化和体内分化和维持。例如,可以利用操作hedgehog功能以影响组织分化,作为维持移植物生存力的方法。
Bellusci等(1997)
Development 124:53报道:Sonic hedgehog调节体内肺间充质细胞增殖。因此,可以利用本发明方法调节肺组织的再生,如用于治疗肺气肿和呼吸窘迫综合征。
Fujita等(1997)Biochem Biophys Res Commun 238:658报道:Sonichedgehog在人肺鳞状细胞癌和腺癌细胞中表达。在人肺鳞状细胞癌组织中也检测到Sonic hedgehog表达,但在同一患者的正常肺组织中检测不到所述表达。他们还观察到:Sonic hedgehog刺激BrdU掺入癌细胞并刺激它们的细胞生长,而抗Shh-N抑制它们的细胞生长。这些结果提示:ptc、hedgehog和/或smoothened参与所述转化肺组织的细胞生长,因此指示可以使用本发明主题方法作为肺癌和肺腺癌以及涉及肺上皮的其它增殖性疾病治疗的组成部分。
根据例如hedgehog途径涉及这些肿瘤、或者在这些发育中组织中检测到hedgehog或其受体表达的证据,可以通过用本发明主题化合物治疗,影响许多其它肿瘤。所述肿瘤包括但决不限于戈林综合征相关性肿瘤(如基底细胞癌、成神经管细胞瘤、脑膜瘤等)、在pct失效小鼠中观察到的肿瘤(如血管瘤、横纹肌肉瘤等)、源自gli-I扩增的肿瘤(如成胶质细胞瘤、肉瘤等)、与ptc同源物TRC8有关的肿瘤(如肾癌、甲状腺癌等)、与Ext-1有关的肿瘤(如骨癌等)、Shh诱导的肿瘤(如肺癌、软骨肉瘤等)以及其它肿瘤(如乳腺癌、泌尿生殖器癌(如肾、膀胱、输尿管、前列腺等)、肾上腺癌、胃肠癌(如胃、肠等)等)。
在本发明的另一实施方案中,包含hedgehog拮抗剂的组合物可用于体外产生骨组织(例如从成骨干细胞产生骨组织),以及体内治疗骨组织缺陷。本发明尤其设想应用hedgehog拮抗剂调节软骨发生和/或骨发生的速率。“骨组织缺陷”指任何部位的骨和其它骨结缔组织缺陷,所述缺陷需要恢复所述骨或结缔组织,而不论所述缺陷源自何处,如是因为外科手术、切除肿瘤、溃疡、植入、骨折或其它创伤、还是因为退行性病理状况的结果。
例如,可以使用本发明的方法作为恢复软骨功能为结缔组织的治疗方案的组成部分。所述方法用于例如修复源于关节炎的退行性磨损所引起的软骨组织缺陷或病变,以及修复由于对所述组织的创伤引起的其它机械错位,所述创伤例如撕裂的半月板组织的脱臼、半月板切除术、韧带撕裂引起的关节松弛、关节恶性肿瘤、骨折或者遗传疾病。本修复方法也可用于重建软骨基质,例如用于美容手术或重建手术,以及用于牙周手术。本方法还可以应用于例如在手术修复半月板、韧带或软骨后改善前面的修复程序。此外,本发明当在创伤后应用得足够早时,可以预防退行性疾病的起病或加重。
在本发明的一个实施方案中,本发明主题方法包括用在治疗上足够量的hedgehog拮抗剂(尤其是选择性针对Indian hedgehog信号转导的拮抗剂)治疗患病结缔组织,通过控制包埋在所述结缔组织中软骨细胞的分化和/或增殖速率,调节结缔组织中的软骨修复反应。所述结缔组织尤其适用在使用本发明主题方法的重建和/或再生疗法中的治疗,所述结缔组织例如关节软骨、关节间软骨(半月板)、肋软骨(连接真肋和胸骨)、韧带和腱。本文所指的再生治疗包括对已经发展到明显表现组织损害程度的退变状态的治疗,以及退变处于其早期阶段或即将退变的组织的预防性治疗。
在举例说明的实施方案中,可以使用本发明主题方法作为动关节软骨治疗中治疗干预的一部分,所述动关节例如膝、踝、肘、髋、腕、手指或脚趾的指节或者颞下颌关节。所述治疗可以指向关节的半月板、关节的关节软骨或者同时指向二者。为进一步举例说明,可以使用本发明主题方法治疗膝的退行性疾病,例如可能源于创伤(如运动损伤或过度磨损)或骨关节炎的退行性疾病。可以用例如关节内窥镜针将所述主题拮抗剂注射入关节。在一些情况下,所述注射剂可以采取上文所述水凝胶或者其它缓释媒介物的形式,以允许所述试剂与所治疗组织更长久规律性接触。
本发明还设想应用本发明主题方法于软骨移植和假体装置疗法的领域。然而,问题出现了,例如,因为软骨和纤维软骨的特征在不同组织间是不同的:例如在关节软骨、半月板软骨、韧带和肌腱之间不同,在同一韧带或腱的两端不同,以及在所述组织的表层和深层不同。这些组织的区域排列可能反映机械性质的逐渐变化,以及当在那些条件下未分化的植入组织缺乏适当反应的能力时就会治疗失败。例如,当使用半月板软骨修复前十字形韧带时,组织经过组织转化,形成纯粹的纤维组织。可以使用本发明主题方法通过调节软骨形成的速率,帮助适应性控制新环境中的植入细胞并有效模拟所述组织更早期发育阶段的增生性软骨细胞,解决该问题。
本发明主题方法可以按相似方式应用于增强假体软骨装置形成以及应用于它们的移植。对改进治疗的需求已经推动目标在于创造基于胶原-葡糖胺聚糖模板的新型软骨(Stone等(1990)Clin OrthopRelat Red 252:129)、分离的软骨细胞(Grande等(1989)J Orthop Res 7:208;和Takigawa等(1987)Bone Miner 2:449)和连接于天然或合成聚合物的软骨细胞(Walitani等(1989)J Bone Jt Surg 71B:74;Vacanti等(1991)Plast Reconstr Surg 88:753;von Schroeder等(1991)J BiomedMaster Res 25:329;Freed等(1993)J Biomed Master Res 27:11;和Vacanti等美国专利第5,041,138号)的研究。例如,可以在生物可降解、生物匹配性高度多孔支架上的培养物中培养软骨细胞,所述高度多孔支架用聚合物形成,所述聚合物例如聚乙二醇酸、聚乳酸、琼脂糖凝胶或者其它由于水解所述聚合物骨架成为无毒单体而随时间降解的聚合物。设计所述基质,允许在移植前使所述细胞有足够的营养和气体交换。可以体外培养所述细胞直到已经为所需细胞发展出足够细胞数量和密度。所述基质的一个优点是:它们可以在个体基础上浇铸或塑造成所需形状,以便最终产品非常类似于患者本身的耳或鼻(以此为例),或者可以使用允许在移植时例如在关节内进行操作的可变基质。
在本发明主题方法的一个实施方案中,使所述植入物在培养过程的某些阶段与hedgehog拮抗剂接触,以控制所述培养物中软骨细胞分化速率和增生性软骨细胞形成速率。
在另一实施方案中,用hedgehog拮抗剂处理所述植入装置,以积极地重建所述植入基质,使其更适于既定功能。如上文关于组织移植所述,所述人造移植物有同样的缺陷,即并非在与植入所述基质的实际机械环境相似的条件下形成。本发明主题方法调节所述基质中软骨细胞的能力能够允许所述植入物获得与其要取代的组织类似的特性。
在又一实施方案中,使用本发明主题方法增强假体装置的附着。为举例说明,可以在牙周假体的移植中使用本发明主题方法,其中对周围结缔组织的治疗刺激所述假体周围牙周韧带的形成。
在另一实施方案中,可以使用本发明主题方法作为在动物体内所述骨骼组织有缺陷的位点产生骨(骨发生)的治疗方案的组成部分。Indian hedgehog尤其与最终被成骨细胞取代的增生性软骨细胞结合。例如,给予本发明的hedgehog拮抗剂可以作为调节接受者体内骨损失速率的方法的一部分。例如,可以使用包含hedgehog拮抗剂的制剂,例如用于控制为骨化形成“模型”时的软骨内骨化。
在本发明的再一实施方案中,可以使用hedgehog拮抗剂调节精子发生。已经显示所述hedgehog拮抗剂尤其是Dhh参与睾丸生殖细胞的分化和/或增殖以及维持。Sertoli细胞前体内的Dhh表达在Sry(睾丸决定基因)激活后不久起始,并在睾丸内持续直到成年。由于完全缺失成熟精子,男性能生活但没有生育能力。对不同遗传背景下发育中的睾丸的检查提示:Dhh调节精子发生的早期阶段和晚期阶段。Bitgood等(1996)
Curr Biol 6:298。在优选实施方案中,可以使用所述hedgehog拮抗剂作为避孕药。本发明主题方法的hedgehog拮抗剂可以按照相似方式用于调节正常卵巢功能。
本发明主题方法也对于涉及上皮组织的疾病的治疗或预防以及在美容应用中有广泛应用性。一般地说,所述方法特征在于包括下面步骤:给予动物有效改变接受治疗的上皮组织生长状态的量的hedgehog拮抗剂。给药模式和剂量方案将根据需要治疗的上皮组织而变化。例如,当接受治疗的组织是上皮组织例如皮肤组织或粘膜组织时,优选局部制剂。
“促进伤口愈合”的方法导致治疗后的伤口愈合比没有治疗时相似伤口的愈合更快。“促进伤口愈合”也可以指所述方法调节尤其是角化细胞的增殖和/或生长,或者所述伤口愈合形成更少疤痕、更少伤口收缩、更少胶原沉积以及更多表面区域。在某些情况下,“促进伤口愈合”也可以指当伤口愈合的某些方法与本发明的方法一起使用时,提高成功率(如皮肤移植物的接受率)。
尽管重建外科技术有显著进步,但疤痕可能是愈合的皮肤重新获得正常功能和外观的重要障碍。当手或脸的病理性疤痕如疤痕疙瘩或增生性疤痕引起功能性伤残或身体畸形时,这一点尤其重要。在最严重的情况下,所述疤痕可能加重心理忧虑和经济贫困的生活。伤口恢复包括止血、炎症、增殖和重建阶段。增殖阶段涉及成纤维细胞和内皮细胞以及上皮细胞的增多。通过使用本发明主题方法,可以控制伤口周围和临近的上皮细胞的增殖速率,以加速伤口闭合和/或最小化疤痕组织的形成。
本发明治疗法也可有效作为用于治疗例如放射性和/或化疗引起的口腔和口外溃疡的治疗方案的组成部分。所述溃疡一般在化疗或放射性治疗后几天内发展出来。这些溃疡通常开始是小而疼痛的不规则形状损害,常常上面覆盖脆弱的灰色坏死膜,周围是炎症组织。在许多情况下,缺少治疗导致炎症基础上病变周围的组织增殖。例如,溃疡周围的上皮通常表现增殖活性,导致表面上皮连续性的损失。这些损害由于它们大小和上皮完整性的丧失,使机体被可能的继发性感染。对食物和水的日常饮食变成非常痛苦的事情,并且假如所述溃疡在整个消化道内增殖,有明显的腹泻以及它的所有并发因子。根据本发明,包括应用hedgehog拮抗剂的对所述溃疡的治疗能够减少受影响上皮的异常增殖和分化,帮助降低随后炎症事件的严重性。
本发明主题方法和组合物也可用于治疗皮肤病引起的伤口,例如自身免疫病如牛皮癣引起的损害。特应性过敏性皮炎指与变态反应原引起的免疫反应有关的过敏反应引起的皮肤创伤,所述变态反应原例如花粉、食物、毛发皮屑、昆虫毒素和植物毒素。
在其它实施方案中,可以应用hedgehog拮抗剂的抗增殖性制剂抑制晶状体上皮细胞增殖,以预防囊外白内障摘出术的术后并发症。白内障是难以处理的眼科疾病,已经对白内障治疗进行各种研究。但现在,通过外科收获进行对白内障的治疗。白内障外科已经应用很长时间,已经检验了各种手术方法。囊外晶状体摘出术已经成为去除白内障的可选方法。该技术与囊内摘出术的主要医学好处是无晶状体囊状黄斑水肿和视网膜脱离的出现率更低。囊外摘出术也是移植后房型眼内晶状体所需的,而后房型眼内晶状体目前被认为是大多数情况下可选的晶状体。
然而,囊外白内障摘出术的一个缺点是通常称为后发性白内障的晶状体囊后浑浊化的出现率高,后发性白内障可能在手术后三年内在50%的病例中出现。后发性白内障是由囊外晶状体摘出术后残余的中纬线和前房晶状体上皮细胞增殖形成。这些细胞增殖引起Sommerling环,与也在后房沉积和出现的成纤维细胞一起,引起后房的浑浊化,干扰视力。预防后发性白内障对于治疗更可取。为抑制继发性白内障形成,本发明主题方法提供抑制残余的晶状体上皮细胞增殖的方法。例如,移除晶状体后,通过将包含hedgehog拮抗剂制剂的溶液灌输入眼的前房,可以诱导所述细胞保持静止。此外,所述溶液可以保持渗透压平衡,当灌输入眼的前房后提供最小有效剂量,由此以一定特异性抑制囊下上皮生长。
本发明主题方法也可以用于治疗特征在于角膜上皮细胞增殖的角膜病,例如眼上皮疾病如眼表面的上皮向下生长或者鳞状细胞癌。
Levine等(1997)
J Neurosci 17:6277显示:hedgehog蛋白能够调节脊椎动物视网膜中的细胞有丝分裂和光感受器分化,Ihh是来自色素上皮促进视网膜祖细胞增殖和光感受器分化的候选因子。同样,Jensen等(1997)
Development 124:363证明:用Sonic hedgehog蛋白的氨基末端片段处理围生期小鼠视网膜细胞的培养物导致掺入溴脱氧尿苷的细胞占总细胞数的比例增加以及视杆细胞光感受器、无长突细胞和米勒神经胶质细胞增加,这提示Sonic hedgehog促进视网膜前体细胞的增殖。因此,本发明主题方法可以用于治疗视网膜细胞的增殖疾病以及调节光感受器分化。
本发明的再一方面涉及应用本发明主题方法控制毛发生长。毛发基本由一种强硬和不可溶的蛋白即角蛋白组成;其本身的强度依赖于半胱氨酸的二硫键。每根毛发包含圆柱形轴和根,包含在毛囊中,毛囊是皮肤中的长颈瓶状凹陷。毛囊底部包含名为乳头的手指状突出部分,由生长出毛发的结缔组织构成,血管通过乳头为细胞提供营养。轴是从皮肤表面向外延伸的部分,而根被描述为毛发包埋的部分。根的基部延伸到毛球,毛球靠在乳头上。生长出毛发的细胞使毛囊的毛球生长;当细胞在毛囊内增殖时,它们以纤维的形式伸出。毛发“生长”指分裂细胞形成和延伸毛发纤维。
如本领域内众所周知的,普通的毛发循环分为三个阶段:生长初期、生长中期和毛发生长终期。在活跃阶段(生长初期),真皮乳头的上皮干细胞快速分裂。子细胞向上移动,分化形成毛发本身的同心层。过渡阶段(生长中期)特征在于毛囊内干细胞有丝分裂的停止。静止期已知是毛发生长终期,在该期内毛发在头皮内保留几周,然后在它下面发展出新的毛发,从毛囊中移出毛发生长终期的轴。从该模型可以清楚地看到:分化成毛发细胞的分裂干细胞数越大,就出现越多毛发生长。因此,增加或减少毛发生长的方法能够通过分别加强或抑制这些干细胞的增殖来实施。
在某些实施方案中,可以使用本发明主题方法作为减少人类毛发生长的途径,而不采用剪发、削剃或脱发等常规去除方法。例如,本方法可用于治疗特征在于毛发异常快速和密集生长的毛发病如多毛症。在示例性的实施方案中,可以使用hedgehog拮抗剂控制多毛症,即一种特征在于不正常多毛状态的疾病。本发明主题方法也提供延长脱毛时间的方法。
此外,因为hedgehog拮抗剂通常对于上皮细胞是抑制细胞生长的,而没有细胞毒性,所以可以使用所述试剂保护毛囊细胞免受需要使细胞循环进入S期以发挥功效的细胞毒性剂的影响,例如放射性诱导的死亡。使用本发明主题方法的治疗通过使毛囊细胞静止而提供保护,如通过抑制细胞进入S期,并由此防止毛囊细胞经受有丝分裂或程序性细胞死亡。例如,hedgehog拮抗剂可以用于接受化疗或放射疗法的患者,而化疗和放射疗法通常导致脱发。通过抑制所述疗法期间的细胞循环进行,所述主题治疗可以保护毛囊细胞免受在其它情况下源于细胞死亡程序被激活的死亡。完成治疗后,在对毛囊细胞增殖抑制伴随缓解的同时可以去除本发明方法。
本发明主题方法也可用于治疗毛囊炎,例如脱发性毛囊炎、网状萎缩性红斑性毛囊炎或疤痕疙瘩性毛囊炎。例如,在对假毛囊炎的治疗中可以局部应用hedgehog拮抗剂的美容制剂,假毛囊炎是一种常常出现在颈部下颌下区域、与刮面有关的慢性疾病,其损害的特征在于红斑性丘疹和包含包埋的毛发的小疣突。
在本发明的又一方面,可以使用本发明主题方法诱导从上皮衍生的组织的分化和/或抑制所述组织的增殖。这些分子的所述形式可以提供用于治疗涉及上皮组织的增生性和/或瘤性病症的分化疗法基础。例如,可以使用所述制剂治疗其中存在皮肤细胞异常增殖或生长的皮肤疾病。
例如,本发明的药用制剂可用于治疗增生性表皮病症,例如角化病,以及用于治疗瘤性表皮病症,例如那些特征在于高度增殖速率的不同皮肤癌的病症,例如基底细胞癌或鳞状细胞癌。本发明主题方法也可以用于治疗影响皮肤的自身免疫病,尤其是涉及表皮病态增殖和/或角质化的皮肤病,例如牛皮癣或特应性皮炎。
许多普通皮肤病例如牛皮癣、鳞状细胞癌、角化棘皮瘤、光化性角化病的特征在于局部异常增生和生长。例如,在牛皮癣(特征是皮肤上的鳞状红色突起的斑)中,已知角化细胞比正常细胞增殖更快,并且分化较不完全。
在一个实施方案中,本发明的制剂适于治疗与引起皮肤细胞异常增殖的角化疾病有关的皮肤疾病,所述角化疾病的特征在于炎症或非炎症成分。为举例说明,可以使用例如促进静止或分化的hedgehog拮抗剂药用制剂治疗各种形式牛皮癣,因为它们是皮肤性的、粘膜性的或指甲性的。如本文所述,牛皮癣一般特征在于显示显著增殖性激活并沿“再生性”途径分化的表皮角化细胞。使用本发明主题方法的抗增殖性实施方案进行的治疗可以用于逆转病理性表皮激活,提供持续缓解牛皮癣疾病的基础。
各种其它角化病的损害也是用本发明主题方法进行治疗的候选目标。例如光化性角化病是在暴露于太阳和受辐射的皮肤上出现的表面炎性的癌症前期肿瘤。所述损害是红斑性到褐色,有不同程度脱皮。目前的疗法包括切除术和冷冻破坏法。然而,这些治疗是痛苦的,并且常常产生在美容方面无法接受的疤痕。因此,对角化病例如光化性角化病的治疗可以包括应用(最好是局部应用)足以抑制损害内表皮细胞/表皮样细胞过度增殖的量的hedgehog拮抗剂组合物。
痤疮代表另一种可以用本发明主题方法治疗的皮肤病。例如,普通粉刺是最通常出现与青少年和年轻人中的多因素疾病,特征是在脸和上躯干出现炎性和非炎性损害。产生普通粉刺的基本缺陷是过度活跃的皮脂腺导管的过度角化。过度角化阻止皮肤和毛囊微生物的正常流动性,因此刺激细菌疮疱丙酸杆菌(Propinobacterium acnes)和表皮葡萄球菌(Staphylococcus epidermidis)和瓶形酵母(Pitrosporumovale)释放脂肪酶。使用抗增殖性hedgehog拮抗剂(尤其是局部制剂)的治疗可以用于预防所述导管的过渡特征,如导致损害形成的过度角化。所述主题治疗还可以包括例如抗生素、视黄醛衍生物和抗雄激素。
本发明还提供治疗各种形式皮炎的方法。皮炎是描述性术语,指瘙痒、红斑、鳞屑、起疱、渗血、开裂或结痂的难以划分的损害。这些损害由多种病因的任一种产生。皮炎的最常见类型是特应性皮炎、接触性皮炎和尿布皮炎。例如,脂溢性皮炎是在各种区域(尤其是头皮)有红斑、干燥、潮湿或多脂鳞状物以及黄色结痂斑的慢性(通常是瘙痒的)皮炎,有过量干鳞状物的表皮脱落。本发明主题方法也可以用于治疗停滞性皮炎,停滞性皮炎常常是慢性的,一般是湿疹性皮炎。光化性皮炎是由于暴露于光化辐射例如来自太阳、紫外线或X-辐射或γ-辐射的光化辐射而引起的皮炎。根据本发明,可以使用本发明主题方法治疗和/或预防由于表皮细胞不希望的增殖而引起的皮炎的某些症状。用于这些各种形式皮炎的所述疗法还可以包括局部和系统性的皮质甾类、止痒药和抗生素。
例如,设想本发明主题方法可用于抑制血管形成。已知hedgehog刺激血管形成。用hedgehog蛋白浸透并插入小鼠的Matrigel塞表现的新血管形成,而不携带hedgehog的Matrigel塞相对显示较少的血管形成。Hedgehog蛋白也能够增殖正常无血管小鼠角膜的血管形成。ptc-1基因在正常血管组织中表达,包括主动脉的上皮细胞、血管平滑肌细胞、主动脉的外膜成纤维细胞、心房和心室的冠状脉管系统和心肌细胞。这些组织也对hedgehog蛋白敏感。使用外源hedgehog的治疗引起ptc-1表达上调节。此外,hedgehog蛋白在体内刺激血管平滑肌细胞的增殖。Hedgehog蛋白还引起成纤维细胞增加血管形成生长因子如VEGF、bFGF、Ang-1和Ang-2的表达。最近,已知hedgehog蛋白刺激从局部缺血性损伤的恢复和刺激副血管的形成。
考虑到hedgehog促进血管形成,预期hedgehog拮抗剂作为血管形成抑制剂起作用,尤其是其中血管形成需要一定水平hedgehog信号传递的情况下。
血管形成对于许多疾病十分重要。在一系列疾病状态、肿瘤转移和内皮细胞的异常生长中出现持续、不受调节的血管形成。作为血管形成过程的结果创造的脉管系统支持在这些病理条件下观察到的病理损伤。由于不受调节的血管形成而引起的不同病理状况已经分类为依赖于生成血管的疾病或与血管形成有关的疾病。目标在于控制血管形成过程的疗法可能消除或缓解这些疾病。
由血管形成引起、支持或与其有关的疾病包括眼新血管病、与年龄有关的黄斑退化、糖尿病性视网膜病、早产儿视网膜病、角膜抑制排斥、新血管青光眼、晶状体后纤维组织形成、流行性角结膜炎、维生素A缺乏症、接触性晶状体磨损、特应性角膜炎、上缘角膜炎、干燥性翼状胬肉角膜炎(pterygium keratitis sicca)、斯耶格伦综合征、痤疮性酒糟鼻、phylectenulosis、梅毒、分支杆菌感染、脂质变性、化学烧伤、细菌性溃疡、真菌性溃疡、单纯疱疹感染、带状疱疹感染、原生动物感染、卡波西肉瘤、Mooren溃疡、Terrien边缘变性、边缘角质层分离、类风湿性关节炎、系统性狼疮、多动脉炎、创伤、Wegeners结节病、巩膜炎、Stevens Johnson病、periphigoid radialkeratotomy、角膜移植排斥、类风湿性关节炎、骨关节炎慢性炎症(如溃疡性结肠炎或局限性回肠炎疾病)、血管瘤、Osler-Weber-Rendu病以及遗传性出血性毛细管扩张。
此外,血管形成在癌症中起关键作用。肿瘤在没有血液供应提供营养和除去细胞废物的情况下不能扩展。血管形成对其重要的肿瘤包括实体瘤如横纹肌瘤、成视网膜细胞瘤、尤因瘤、成神经细胞瘤和骨肉瘤,还包括良性肿瘤如听神经瘤、神经纤维瘤、沙眼和脓性肉芽肿。已经发现与几种实体瘤有关的血管形成因子。对血管形成的预防能够阻止这些肿瘤的生长以及由于肿瘤存在而对动物造成的伤害。血管形成还与血液性肿瘤例如白血病有关,白血病是骨髓的各种急性或慢性瘤性疾病的任一种,其中出现白血球不受限制的增殖,通常伴随贫血、血液凝集障碍以及淋巴结、肝和脾肿大。相信血管形成在产生白血病样肿瘤的骨髓的异常中起作用。
除肿瘤生长外,血管形成在转移中是重要的。最初,血管形成对于允许癌性细胞进入血流和在整个身体内循环的肿瘤的血管化是重要的。当肿瘤细胞离开原发位点并定居到继发的转移位点后,血管形成必须出现在新肿瘤能够生长和扩展之前。因此,预防血管形成可能导致预防肿瘤转移,并可能抑制原发位点的瘤性生长。
血管形成还涉及正常生理过程如繁殖和伤口愈合。血管形成是排卵和受精后囊胚植入过程中的重要步骤。对血管形成的预防可用于诱导闭经、阻断排卵或预防囊胚植入。
预期本发明将可用于治疗和/或预防呼吸窘迫综合征或其它由于不适当的肺表面张力引起的疾病。呼吸窘迫综合征由肺泡内的表面活性剂不足引起。脊椎动物的肺包含表面活性剂,即一种脂质和蛋白的复杂混合物,引起表面张力在肺扩张期间上升,在肺缩小期间下降。在肺缩小期间,表面活性剂降低,以便没有在其它情况下促进肺泡萎缩的表面力量。在呼气期间没有萎缩的充气肺泡允许血液和肺泡气体之间持续的氧和二氧化碳转运,并且在随后的吸气期间需要更少的力量膨大。在扩张过程中,肺表面活性剂随着肺泡表面积的增加而增加表面张力。扩张的肺泡中上升的表面张力激活这些空间中的过度扩张,倾向于使吸入的气体转移到充气较不充分的肺泡,由此便利均匀的肺换气。
呼吸窘迫综合征在未成熟的婴儿中尤其常见。肺表面活性剂通常在胚胎的最后六周之前以非常低的速率合成。在正常妊娠期之前六周出生的人类婴儿有肺表面活性剂量不足和表面活性剂合成不足的高风险。婴儿出生时越不成熟,表面活性剂缺乏可能越严重。重度表面活性剂缺乏症可能在出生几分钟或数小时内导致呼吸衰竭。所述表面活性剂缺乏症产生肺泡的进行性萎缩(肺不张),因为肺在最大呼吸努力下扩张的能力降低。由此,婴儿血液中氧含量不足。RDS也可能出现在成人中,通常是由于表面活性剂生物合成不足的结果。
成熟前婴儿的肺组织显示高活性的hedgehog信号途径。使用hedgehog拮抗剂抑制该途径增加片层体的形成,并增加涉及表面活性剂生物合成的基因的表达。片层体是与表面活性剂生物合成有关的亚细胞结构。因为这些原因,用hedgehog拮抗剂治疗成熟前婴儿应该刺激表面活性剂生物合成和缓解RDS。在成人RDS与hedgehog途径激活有关的情况下,用hedgehog拮抗剂的治疗应该也是有效的。
还设想hedgehog拮抗剂的应用可以特异性靶向受影响的组织和/或细胞表现高度hedgehog途径激活的疾病。gli基因的表达被hedgehog信号途径激活,其中包括gli-1、gli-2和gli-3。gli-1表达始终与多种组织和疾病中的hedgehog信号传递活性相关,而gli-3的相关性较差。所述gli基因编码转录因子,所述转录因子激活许多引发hedgehog信号传递的完全效应所需的基因的表达。然而,Gli-3转录因子也可以作为hedgehog效应基因的阻抑物起作用,因此gli-3表达引起hedgehog信号转导途径效应降低。Gli-3是作为转录激活物还是作为转录阻抑物起作用取决于翻译后过程,因此预期用于检测Gli-3蛋白活化形式(相对于阻抑形式)的方法也将是hedgehog途径激活的可靠检测方法。预期gli-2基因表达为hedgehog途径激活提供可靠的标记。gli-1基因在多种癌症、增生和不成熟的肺中强表达,作为hedgehog途径相对激活的标记。此外,有高gli基因表达的组织如成熟前的肺被hedgehog抑制剂的强烈影响。因此,设想对gli基因表达的检测可用作有力的预测工具,鉴定尤其可受益于hedgehog拮抗剂治疗的组织和疾病。
在优选实施方案中,通过直接检测转录物或检测蛋白水平或活性来检测gli-1表达水平。可以使用主要依赖于探针与gli-1转录物杂交或与由其合成的eDNA杂交的多种技术中任一种,检测所述转录物。众所周知的技术包括对转录物水平的RNA印迹、逆转录酶PCR和微阵列分析。检测Gli蛋白水平的方法包括蛋白质印迹、免疫沉淀、双向聚丙烯酰胺凝胶电泳(2S SDS-PAGE)(最好与其中已经测定Gli蛋白位置的标准相比较)、以及质谱。质谱可以与一系列纯化步骤偶联,以允许高通量鉴定特定样品中的多种不同蛋白水平。质谱和2D SDS-PAGE也可用于鉴定蛋白的转录后修饰,包括蛋白水解事件、遍在蛋白化、磷酸化、脂质修饰等。也可以通过分析与底物DNA的结合或者靶启动子的体外转录激活,评价Gli活性。凝胶移位测定、DNA足迹测定和DNA-蛋白交联测定都是可用于评价能够与DNA上Gli结合位点相结合的蛋白存在的方法。
在优选实施方案中,测量gli转录物水平,用hedgehog拮抗剂处理显示异常高gli水平的患病或有障碍的组织。在某些病例中,成熟前肺组织、肺癌(如腺癌、支气管肺泡腺癌、小细胞癌)、乳腺癌(如导管下癌、小叶下癌、导管癌)、前列腺癌(如腺癌)和良性前列腺增生都显示强烈升高的gli-1表达水平。因此,gli-1表达水平是确定这些组织中的哪一些应该用hedgehog拮抗剂治疗的有力诊断手段。此外,有切实的相关证据证明:泌尿道上皮的癌症(如膀胱癌、其它泌尿生殖癌)在某些情况下有升高的gli-1水平。例如,已知膀胱癌中常见损失染色体9q22上的杂合性。ptc-1基因位于该位置,ptc-1功能丧失可能是过度增殖的部分原因,正如在许多其它癌症类型中一样。因此,所述癌症也将显示高gli表达,并尤其适用hedgehog拮抗剂的治疗。
ptc-1和ptc-2的表达也被hedgehog信号传递途径的激活,但这些基因作为hedgehog途径激活的标记不如gli基因。在某些组织中虽然hedgehog途径高度活跃的,但仅表达ptc-1或ptc-2的其中之一。例如,在睾丸发育中,Indian hedgehog起重要作用,并且hedgehog途径是活化的,但仅表达ptc-2。因此,这些基因各自无法可靠地作为hedgehog途径激活的标记,虽然设想同时测量所述两个基因以作为可以用hedgehog拮抗剂治疗的组织的有用指标。
可以用本发明主题方法治疗的疾病是对人类以外的动物特异性的疾病,例如家畜的疥癣。
在又一实施方案中,本发明主题方法可以用于治疗人类癌症,尤其是基底细胞癌和上皮组织如皮肤的其它肿瘤。例如,在本发明主题方法中,可以使用hedgehog拮抗剂作为对基底细胞痣综合征(BCNS)和其它人类癌症、腺癌、肉瘤等治疗的组成部分。
在优选实施方案中,本发明主题方法用作治疗(或预防)基底细胞癌的治疗或预防方案的组成部分。hedgehog信号传递途径的去调节可能是ptc突变引起的基底细胞癌的一般特征。根据原位杂交确定,已经描述在家族性和散发性BCC的肿瘤中人ptc mRNA的持续过量表达。预期失活ptc的突变导致突变ptc的过量表达,因为ptc显示负自身调节。先前的研究证明:hedgehog蛋白过量表达也可能导致肿瘤发生。研究已经提示sonic hedgehog(Shh)在小鼠体内肿瘤发生中起作用的事实,在该研究中皮肤内过量表达Shh的转基因小鼠发展出BCNS的特征,包括皮肤发育仅几天后整个皮肤表面多处BCC样表皮增殖。还描述了来自BCC的Shh人基因的突变;提示人体内的Shh或其它Hh基因可以作为人体内的显性癌基因起作用。在来自其它方面正常的个体的BCC中也观察到散发性ptc突变,其中一些是UV-特征突变(signature mutation)。在关于散发性BCC的一个最近研究中,从十五个经测定包含ptc突变的肿瘤中发现五个UV-特征型突变,所述突变是CT或CCTT改变。另一个关于BCC和神经外胚层肿瘤中散发性ptc突变的最近分析揭示在BCC中发现的三个ptc突变的其中之一发生一个CT变化。见,例如,Goodrich等(1997)
Science 277:1109-13;Xie等(1997)
Cancer Res 57:2369-72;Oro等(1997)
Science276:817-21;Xie等(1997)
Genes Chromosomes Cancer 18:305-9;Stone等(1996)
Nature 384:129-34;和Johnson等(1996)
Science 272:1668-71。
本发明主题方法也可以用于治疗患有BCNS的患者,如用于预防BCC或者可能是ptc功能丧失、hedgehog功能获得或smoothened功能获得的结果的疾病其它效应。基底细胞痣综合征是罕见的常染色体显性疾病,其特征是年轻时出现的多处BCC。BCNS患者对这些肿瘤的发展非常敏感;在十多岁时,大量出现,主要在皮肤暴露于阳光的区域。该疾病也导致多种发育异常,包括肋骨、头和脸的改变,有时是多指(趾)、并指(趾)和脊柱裂。他们除BCC外还发展出多种肿瘤类型:卵巢和心的纤维瘤、皮肤和颌的囊肿、以及中枢神经系统中的成神经管细胞瘤和脑脊膜瘤。本发明主题方法可用于预防或治疗BCNS和非BCNS患者中的所述肿瘤类型。对BCNS患者的研究显示:他们在ptc基因中同时有基因组突变和散发性突变,提示这些突变是该疾病的最终病因。
在另一方面,本发明提供包含hedgehog拮抗剂的药用制剂。可以方便地配制用于本发明主题方法的hedgehog拮抗剂,用生物学上可接受的媒介给予,所述生物学上可接受的媒介例如水、缓冲盐溶液、多元醇(例如甘油、丙二醇、液体聚乙二醇等)或它们合适的混合物。依照药物化学家众所周知的程序,可以根据经验确定选定媒介中活性成分的最佳浓度。本文所用术语“生物学上可接受的媒介”包括适于所述药用制剂给药所需途径的任何和所有溶剂、分散媒介等。所述媒介物对于药学活性物质的应用是本领域内已知的。除与hedgehog拮抗剂活性不匹配的任何常规媒介或试剂外,设想其在本发明药学制剂中的应用。在例如书Remington’s PharmaceuticalSciences(Remington’s Pharmaceutical Sciences.Mack PublishingCompany,Easton,Pa.,USA 1985)中描述合适的媒介物和所述媒介物包含其它蛋白的制剂。这些媒介物包括可注射的“沉积制剂(depositformulation)”。
本发明的药用制剂还可以包括兽医组合物,如适于兽医应用的hedgehog拮抗剂的药用制剂,如用于治疗牲畜或家畜如狗。
也可以通过可再装载或生物可降解的装置提供导入方法。近些年来已经为药物的受控传递发展和体内测试各种缓释聚合物装置,其中包括蛋白质生物药剂。可以使用各种生物亲和的聚合物(包括水凝胶),形成用于在特定靶位点持续释放hedgehog拮抗剂的植入物。
本发明的制剂可以口服给予、胃肠外给予、局部给予或直肠给予。以适于各个给药途径的方式给予所述制剂。例如可以采用如下方式给予所述制剂:采用片剂或胶囊剂的形式、通过注射、吸入、眼洗液、软膏剂、栓剂、控释贴剂等,通过注射、灌输或吸入给药;通过洗液或软膏剂局部给药;和通过栓剂直肠给药。优选口服和局部给药。
本文所用词组“胃肠外给药”和“通过胃肠外给予”指除肠给药和局部给药以外的给药模式,通常通过注射,包括但不限于静脉内、肌肉内、动脉内、鞘内、囊内、眶内、心脏内、皮内、腹膜内、经气管、皮下、表皮下、关节内、囊下、蛛网膜下、脊柱内和胸骨内内注射和灌输。
本文所用词组“系统给药”、“系统给予”、“外周给药”和“外周给予”指采用除直接进入中枢神经系统以外的方式给予化合物、药物或其它材料,以便其进入患者系统并因此进入代谢和其它类似过程,例如皮下给药。
可以通过任何合适的给药途径将这些化合物给予人类和其它动物以用于治疗,所述合适的给药途径包括口服给药、经鼻给药(例如通过喷雾剂)、直肠给药、阴道内给药、胃肠外给药、脑池内给药和局部给药(例如通过粉剂、软膏剂或滴剂),其中局部给药包括含服给药和舌下给药。
无论选定的给药途径如何,将本发明的化合物(可以采取合适的含水形式使用)和/或本发明的药用组合物配制成为如下文所述的药学上可接受的剂型,或者用本领域内技术人员已知的其它常规方法配制。
本发明药用组合物中活性成分的实际剂量水平可能是变化的,以获得有效达到针对特定患者、组合物、给药模式的所需治疗反应同时对该患者无毒的所述活性成分的量。
选定剂量水平将依赖于多种因子,包括所使用的本发明特定化合物或其酯、盐或酰胺的活性、给药途径、给药时间、所使用特定化合物的排泄速率、治疗持续时间、与所使用的特定hedgehog拮抗剂联合使用的其它药物、化合物和/或材料、需要治疗的患者的年龄、性别、体重、状况、总体健康以及在先病史、以及在医学领域内众所周知的相似因素。
本领域内有一般技能的医生或兽医能够容易地确定和处方开出所需药用组合物的有效量。例如,医生和兽医在所述药用组合物中使用的本发明化合物的剂量开始可以低于获得所需治疗效应需要的水平,然后逐渐增加剂量,直到达到所需效应。
一般地说,本发明化合物的合适日剂量将是所述化合物有效产生治疗效应的最低剂量。所述有效剂量一般依赖于上文所述的因素。一般地说,本发明化合物用于患者的脑室内剂量和皮下剂量从约0.0001到约100mg/公斤体重/天。
如果需要,所述活性化合物的有效日剂量可以在一天内以合适间隔分两剂、三剂、四剂、五剂、六剂或更多亚剂量给予,可选采用单位剂量的形式给予。
术语“治疗”还包括预防、疗法和治疗。
接受所述治疗的患者是有需要的任何动物,包括灵长类动物,尤其是人,以及其它哺乳类如马、牛、猪和绵羊;以及通常的家禽和宠物。
本发明化合物可以原样给予,或者与药学上可接受的和/或无菌载体混合给予,并且可以与其它抗微生物剂如青霉素、头孢菌素、氨基糖苷类和糖肽类共同给予。联合疗法因此包括顺序、同时和分别给予所述活性化合物,其中在首先给予的试剂的治疗效应没有完全消失前给予后面的试剂。
V.药用组合物
虽然有可能单独给予本发明的化合物,但优选将所述化合物作为药用制剂(组合物)给予。可以用方便应用于人类或兽医医药的任何方式配制用于给药的依照本发明的hedgehog拮抗剂。在某些实施方案中,包括在所述药用制剂中的所述化合物可以是本身有活性的,或者是前体药物,如能够在生理条件下被转化为活性化合物。
因此,本发明的又一方面提供药学上可接受的组合物,所述组合物包含治疗有效量的一种或多种上文所述化合物,与一种或多种药学上可接受的载体(添加剂)和/或稀释剂配制在一起。如下文详细描述,本发明的药用组合物可以专门配制成固体或液体形式以用于给药,所述形式包括适用于下面给药方式的形式:(1)口服给药,例如灌药(水性溶液或非水性溶液或悬浮液)、片剂、大药丸、粉剂、粒剂、应用于舌头的糊剂;(2)胃肠外给药,例如作为无菌溶液或悬浮液例如通过皮下、肌肉内或静脉内注射;(3)局部应用,例如作为应用于皮肤的乳膏剂、软膏剂或喷雾剂;或(4)阴道内或直肠内给药,例如作为阴道栓剂、乳膏剂或泡沫。然而,在某些实施方案中,可以将本发明主题化合物简单地溶解或悬浮于无菌水中。在某些实施方案中,所述药用制剂是无热原的,即不提高患者的体温。
本文所用词组“治疗有效量”指本发明化合物、材料或包含本发明化合物的组合物如下描述的量:该量通过克服动物体内至少一个细胞亚群体中的ptc功能丧失、hedgehog功能获得或smoothened功能获得并由此阻断该途径在受处理细胞中的生物学作用,有效产生一定所需的治疗效果,同时有适用于任何医学治疗的合适的益处/风险比。
本文所用词组“药学上可接受的”指在良好医学判断的范围内,这些化合物、材料、组合物和/或剂型适用于与人类和动物的组织接触,没有过分的毒性、刺激、变态反应或其它问题或并发症,具有合适的益处/风险比。
本文所用词组“药学上可接受的载体”指参与将所述主题拮抗剂从一个器官或身体一部分传送或转运到另一个器官或身体另一部分的药学上可接受的材料、组合物或媒介物,例如液体或固体填充剂、稀释剂、赋形剂、溶剂或包囊材料。每种载体必须在与所述制剂内其它成分匹配的意义上“可接受”,并且不对所述患者有害。可以用作药学上可接受的载体的材料的一些例子包括:(1)糖,如乳糖、葡萄糖和蔗糖;(2)淀粉,如玉米淀粉和马铃薯淀粉;(3)纤维素及其衍生物,例如羧甲基纤维素钠、乙基纤维素和醋酸纤维素;(4)粉末状黄芪胶;(5)麦芽;(6)明胶;(7)滑石粉;(8)赋形剂如可可油和栓剂蜡;(9)油,例如花生油、棉籽油、红花油、芝麻油、橄榄油、玉米油和大豆油;(10)二醇类,如丙二醇;(11)多元醇,如甘油、山梨糖醇、甘露糖醇和聚乙二醇;(12)酯,例如油酸乙酯和十二酸乙酯;(13)琼脂;(14)缓冲剂,例如氢氧化镁和氢氧化铝;(15)藻酸;(16)无热原水;(17)等渗盐水;(18)林格氏液;(19)乙醇;(20)磷酸盐缓冲溶液;和(21)其它在药学制剂中使用的无毒匹配物质。
如上文所述,所述hedgehog拮抗剂的某些实施方案可以包含碱性功能基团,例如氨基或烷氨基,并因此能够与药学上可接受的酸形成药学上可接受的盐。在这一方面,“药学上可接受的盐”指本发明化合物相对无毒的无机和有机酸加成盐。这些盐可以在本发明化合物最后分离和纯化的过程中原位制备,或者通过分别使游离碱形式的纯化的本发明化合物与合适的无机或有机酸反应,然后分离由此形成的盐。有代表性的盐包括氢溴酸盐、氢氯酸盐、硫酸盐、硫酸氢盐、磷酸盐、硝酸盐、乙酸盐、戊酸盐、油酸盐、棕榈酸盐、硬脂酸盐、月桂酸盐、苯甲酸盐、乳酸盐、磷酸盐、甲苯磺酸盐、柠檬酸盐、马来酸盐、延胡索酸盐、琥珀酸盐、酒石酸盐、napthylate、甲磺酸盐、葡庚糖酸盐、乳糖酸盐和月桂基磺酸盐等。(见例如Berge等(1977)“Pharmaceutical Salts”,J.Pharm.Sci.66:1-19)。
本发明主题化合物在药学上可接受的盐包括常规的无毒盐或所述化合物的季铵盐,如从无毒的有机酸或无机酸形成的盐。例如,所述常规的无毒盐包括那些从无机酸如盐酸、氢溴酸、硫酸、氨基磺酸、磷酸、硝酸等形成的盐;从有机酸如乙酸、丙酸、琥珀酸、乙醇酸、硬脂酸、乳酸、苹果酸、酒石酸、柠檬酸、抗坏血酸、棕榈酸、马来酸、羟基马来酸、苯乙酸、谷氨酸、苯甲酸、水杨酸、磺胺酸、2-乙酸基苯甲酸、延胡索酸、甲苯磺酸、甲磺酸、乙二磺酸、草酸、异硫羰酸等。
在其它情况下,本发明的化合物可以包含一种或多种酸性功能基团,并因此能够与药学上可接受的碱形成药学上可接受的盐。在这些情况下,术语“药学上可接受的盐”指本发明化合物相对无毒的无机和有机碱加成盐。这些盐同样能够在所述化合物的最终分离和纯化过程中原位制备,或者通过分别使游离酸形式的所述纯化的化合物与合适的碱例如药学上可接受的金属阳离子的氢氧化物、碳酸盐或碳酸氢盐反应,或与氨水反应,或与药学上可接受的有机伯胺、仲胺或叔胺反应。有代表性的碱金属或碱土金属包括锂盐、钠盐、钾盐、钙盐、镁盐和铝盐等。用于形成碱加成盐的有代表性的有机胺包括乙胺、二乙胺、乙二胺、乙醇胺、二乙醇胺、哌嗪等。(见例如Berge等,同上)。
在所述组合物中也可以存在润湿剂、乳化剂和润滑剂(例如月桂基硫酸钠和硬脂酸镁)以及着色剂、释放剂、包衣剂、甜味剂、矫味剂和香味剂、防腐剂和抗氧化剂。
药学上可接受的抗氧化剂的例子包括:(1)水溶性抗氧化剂,例如抗坏血酸、半胱氨酸盐酸盐、硫酸氢钠、焦亚硫酸钠、亚硫酸钠等;(2)脂溶性抗氧化剂,例如抗坏血酸棕榈酸酯、丁化羟基茴香醚(BHA)、丁基化羟氢甲苯(BHT)、卵磷脂、没食子酸丙酯、α-生育酚等;和(3)金属鳌合剂,例如柠檬酸、乙二胺四乙酸(EDTA)、山梨糖醇、酒石酸、磷酸等。
本发明的制剂包括那些适于口服给药、经鼻给药、局部给药(包括含服给药和舌下给药)、直肠给药、阴道给药和/或胃肠外给药的制剂。所述制剂可以方便地以单位剂型存在,并通过药学领域内众所周知的任何方法制备。所述活性成分的量根据需要治疗的接受体、给药的具体模式而有所不同,可以将所述活性成分与载体材料组合,产生单一剂型。所述活性成分的量一般是需要产生治疗效果的化合物的量,可以将所述活性成分与载体材料组合,产生单一剂型。一般地说,在一百个百分率内,活性成分的量从约1%到约99%,优选从约5%到约70%,最优选从约10%到约30%。
制备这些制剂或组合物的方法包括下面步骤:使本发明的化合物与载体组合,可选地还与一种或多种辅助成分组合。一般地说,如下制备所述制剂:使本发明的化合物均一和紧密地与液体载体结合,或者与精细固体载体结合,或者与二者结合,如果需要,随后使所述产物成型。
本发明适于口服给药的制剂可以采用胶囊剂、扁囊剂、丸剂、片剂、锭剂(使用有味道的主要成分,通常是蔗糖和阿拉伯胶或黄芪胶)、粉剂、粒剂、或作为水性或非水性液体内的溶液或悬浮液、或作为水包油或油包水液体乳剂、或作为酏剂或糖浆剂、或作为锭剂(使用惰性主要成分,如明胶和甘油,或蔗糖和阿拉伯胶)和/或作为口腔洗剂等,每种形式都包含预定量作为活性成分的本发明的化合物。本发明的化合物也可以作为大药丸、干药糖剂或糊剂给予。
在本发明用于口服给药的固体剂型(胶囊剂、片剂、丸剂、糖锭剂、粉剂、粒剂等),所述活性成分与一种或多种药学上可接受的载体(例如柠檬酸钠或磷酸二钙)和/或任何以下成分混合:(1)填充剂或补充剂,例如淀粉、乳糖、蔗糖、葡萄糖、甘露醇和/或硅酸;(2)粘合剂,例如羧甲基纤维素、藻酸盐、明胶、聚乙烯吡咯烷酮、蔗糖和/或阿拉伯胶;(3)保湿剂,例如甘油;(4)崩解剂,例如琼脂-琼脂、碳酸钙、马铃薯淀粉或木薯淀粉、藻酸、某些硅酸盐和碳酸钠;(5)溶液阻滞剂,例如石蜡;(6)吸收加速剂,例如季铵化合物;(7)湿润剂,例如单硬脂酸鲸蜡醇酯和单硬脂酸甘油酯;(8)吸收剂,例如高岭土和膨润土;(9)润滑剂,例如滑石粉、硬脂酸钙、硬脂酸镁、固体聚乙二醇、月桂基硫酸钠和它们的混合物;和(10)着色剂。在胶囊剂、片剂和丸剂的情况下,所述药用组合物还可以包含缓冲剂。也可以使用相似类型的固体组合物,其中软填充和硬填充明胶胶囊中的填充剂,使用赋形剂如乳糖或奶糖以及高分子量聚乙二醇等。
可以通过压制或模制制造片剂,可选地与一种或多种配合剂一起压制或模制。可以使用粘合剂(例如明胶或羟丙基甲基纤维素)、润滑剂、惰性稀释剂、防腐剂、崩解剂(例如羟基乙酸淀粉钠或交联的羧甲基纤维素钠)、表面活性剂或分散剂制备压制的片剂。可以在合适的机器内制造模制的片剂,制造用惰性液体稀释剂湿润的粉末状化合物的混合物。
可以可选地刻痕或用包衣和壳(例如药物配制领域内众所周知的肠溶衣和其它包衣)制备本发明药用组合物的片剂和其它固体剂型,例如糖锭剂、胶囊剂、丸剂和粒剂。也可以配制所述药用组合物,以便提供所述活性成分的缓慢或受控释放,例如使用不同比例的羟甲基纤维素以提供所需的释放形式,也可以使用其它聚合物基质、脂质体和/或微球体。可以如下对所述药用组合物除菌:例如通过保留细菌的滤器过滤,或通过使用前掺入可溶于无菌水或其它无菌可注射介质的固体组合物形式杀菌剂。这些组合物也可以可选地包含遮光剂,并且可以是仅仅或优选在胃肠道的某一部分释放所述活性成分的组合物,可选延迟释放的方式。可以使用的植入组合物的例子包括聚合物和蜡。如果合适,所述活性成分也可以采取含有一种或多种上文所述赋形剂的微囊化形式。
用于口服给予本发明化合物的液体剂型包括药学上可接受的乳剂、微乳、溶液、悬浮液、糖浆剂和酏剂。除所述活性成分外,所述液体剂型可以包含本领域内通常使用的惰性稀释剂(例如水或其它溶剂)、增溶剂和乳化剂(例如乙醇、异丙醇、碳酸乙酯、乙酸乙酯、苯甲醇、苯甲酸苄酯、丙二醇、1,3-丁二醇、油(尤其是棉籽油、花生油、玉米油、胚芽油、橄榄油、蓖麻油和芝麻油)、甘油、四氢呋喃甲醇、聚乙二醇和山梨聚糖的脂肪酸酯以及它们的混合物)。
除惰性稀释剂外,所述口服组合物还可以包括佐剂,例如润湿剂、乳化剂和悬浮剂、甜味剂、矫味剂、着色剂、香味剂和防腐剂。
悬浮液除所述活性成分外,还可包含悬浮剂,例如乙氧基化异硬脂醇、聚氧乙烯山梨糖醇和山梨聚糖酯、微晶纤维素、偏氢氧化铝、膨润土、琼脂-琼脂和黄芪胶以及它们的混合物。
已知固醇例如胆固醇会与环糊精形成复合物。因此,在优选实施方案中,当所述抑制剂是甾体生物碱时,它可以与环糊精一起配制,所述环糊精例如α-、β-和γ-环糊精、二甲基β-环糊精和2-羟丙基-β-环糊精。
用于直肠给药或阴道给药的本发明药用组合物制剂可以是栓剂,通过将本发明的一种或多种化合物与一种或多种合适的非刺激性赋形剂或载体混合制备所述栓剂,所述非刺激性赋形剂或载体包括例如可可油、聚乙二醇、栓剂蜡或水杨酸酯,所述栓剂在室温下是固体,但在体温下是液体,因此在直肠或阴道腔内融化,释放出有活性的hedgehog拮抗剂。
适于阴道给药的本发明制剂还包括阴道栓剂、卫生栓、乳剂、凝胶剂、糊剂、泡沫或喷雾剂制剂,所述制剂包含例如本领域内已知合适的载体。
用于局部给药或经皮给药的本发明化合物的剂型包括粉剂、喷雾剂、软膏剂、糊剂、乳膏剂、洗剂、凝胶剂、溶液、贴剂和吸入剂。所述活性化合物可以在无菌条件下与药学上可接受的载体以及任何可能需要的防腐剂、缓冲剂或推进剂混合。
所述软膏剂、糊剂、乳膏剂和凝胶剂除包含本发明的活性化合物外,还可以包含赋形剂,例如动物脂肪和植物脂肪、油、蜡、石蜡、淀粉、黄芪胶、纤维素衍生物、聚乙二醇、硅酮、膨润土、硅酸、滑石粉和氧化锌以及它们的混合物。
粉剂和喷雾剂除包含本发明的化合物外,还可以包含赋形剂,例如乳糖、滑石粉、硅酸、氢氧化铝、硅酸钙和聚酰胺粉末或这些物质的混合物。喷雾剂还可以包含常用的推进剂,例如氯氟烃和挥发性未取代烃,例如丁烷和丙烷。
经皮贴片有提供本发明化合物受控传递到身体的好处。可以通过将所述hedgehog拮抗剂溶解或分散于合适介质,制造所述剂型。也可以使用吸收增强剂增加hedgehog拮抗剂穿过皮肤的流动。通过提供速率控制膜或使所述化合物分散在聚合物基质或凝胶中,控制所述流动的速率。
本发明的范围内还设想眼科制剂、眼软膏剂、粉剂、溶液等。
本发明适于胃肠外给药的药用组合物包含本发明一种或多种化合物以及一种或多种药学上可接受的无菌等渗水性溶液或非水性溶液、分散剂、悬浮液或乳剂,或者可以在使用前重建成为无菌可注射溶液或分散液的无菌粉末,所述无菌粉末可以包含抗氧化剂、缓冲剂、抑菌药、使所述制剂与预定接受者血液等渗的溶质、或者悬浮剂或增稠剂。
可以在本发明药用组合物中使用的合适的水性和非水性载体的例子包括水、乙醇、多元醇(例如甘油、丙二醇、聚乙二醇等)以及合适的它们的混合物、植物油(例如橄榄油)和可注射有机酯(例如油酸乙酯)。可以如下维持适当的流动性:例如,通过使用包衣材料如卵磷脂,在分散剂的情况下通过维持所需的粒子大小,以及通过使用表面活性剂。
这些组合物也可以包含佐剂,例如防腐剂、润湿剂、乳化剂和分散剂。通过包含各种抗细菌剂和抗真菌剂,可以保证预防微生物的作用,所述抗细菌剂和抗真菌剂例如对羟基苯甲酸酯、氯丁醇、苯酚山梨酸等。也可能需要在所述组合物中包括等渗剂,例如糖、氯化钠等。此外,通过包含延迟吸收的试剂例如单硬脂酸铝和明胶,可以产生所述注射药物形式的延迟吸收。
在一些情况下,为延长所述药物的效应,需要减慢皮下注射或肌肉内注射时所述药物的吸收。这可以通过应用水溶解度差的晶体物质或无定形物质完成。所述药物吸收的速率依赖于其溶解速率,而其溶解速率又依赖于晶体大小和晶型。或者,通过将所述药物溶解或悬浮于油媒介,获得胃肠外给予的药物形式的延迟吸收。
在生物可降解聚合物如聚交酯-聚乙交酯中形成本发明主题化合物的微囊基质,制备注射长效制剂形式。根据药物对聚合物的比例,以及具体使用的聚合物的性质,可以控制药物释放的速率。其它生物可降解聚合物的例子包括聚(原酸酯)和聚(酸酐)。也可以如下制备长效制剂注射形式:用与机体组织亲和的脂质体或微乳俘获所述药物。
当将本发明化合物作为药物给予人和动物时,可以给予它们本身,或者作为包含例如0.1到99.5%(更优选0.5到90%)活性成分以及药学上可接受的载体的药用组合物给予。
优选如下将本发明的活性化合物加入动物饲料中:制备包含有效量所述活性化合物的合适饲料预混合物,然后将所述预混合物加入完整的定量。
或者,可以将包含所述活性成分的中间浓缩物或饲料添加剂混合入所述饲料。参考书中描述了制备和给予所述饲料预混合物和完整定量的方法(例如“Applied Animal Nutrition”,W.H.Freedman andCO.,San Francisco,U.S.A.,1969或”Livestock Feeds and Feeding”Oand B books,Corvallis,Ore.,U.S.A.,1977)。
VI.活性拮抗剂的合成方案和鉴定
可以通过使用Suzuki、Stille等的交叉偶联技术,容易地制备所述主题甾类生物碱及其相关化合物。这些偶联反应在相对温和的条件下进行,容忍大范围的“旁观者”官能度。
a.组合文库
本发明化合物,尤其是具有各种有代表性取代基类型的变体的文库,适用组合化学和其它平行合成方案(见,例如,PCT WO94/08051)。结果是可以在高通量测定中容易地筛选相关化合物的大文库,如上文描述的化合物的多样化文库,以鉴定潜在的hedgehog拮抗剂先导化合物,并研究清楚先导化合物的特异性、毒性和/或细胞毒性动力学概况。例如,可以使用ptc、hedgehog或smoothened生物活性测定筛选本发明主题化合物的文库,寻找那些具有ptc激动剂活性或者hedgehog或smoothened拮抗剂活性的化合物,所述ptc、hedgehog或smoothened生物活性测定例如可以使用具有ptc功能丧失、hedgehog功能获得或smoothened功能获得的细胞发展出来。
仅仅为了举例说明,用于本发明目的的组合文库是同时筛选所需性质的化学相关化合物的混合物。在单一反应中制备许多相关化合物极大地降低和简化了需要进行的筛选过程的数量。可以通过常规方法筛选合适的物理性质。
可以在多个不同水平上创造文库的多样性。例如,在组合反应中使用的底物芳基可以在核心芳基部分多样化,如在环结构上多样化,或者底物芳基可以相对于其它取代基多样化。
本领域内有用于产生小有机分子如所述主题hedgehog拮抗剂的组合文库的各种技术。见,例如,Blondelle等(1995)
Trend Anal.Chem.14:83;Affymax美国专利5,359,115和5,362,899;Ellman美国专利5,288,514;Still等PCT公开WO 94/08051;ArQule美国专利5,736,412和5,712,171;Chen等(1994)
JACS 116:2661;Kerr等(1993)
JACS 115:252;PCT公开WO92/10092、WO93/09668和WO91/07087;和Lerner等PCT公开WO93/20242)。因此,可以根据特定活性或性质合成和筛选数量级为约100到1,000,000或更多所述主题hedgehog拮抗剂diversomers的多种文库。
在示例性的实施方案中,可以利用从Still等PCT公开WO94/08051中所述技术改良的方案合成候选hedgehog拮抗剂diversomer文库,例如通过可水解或可光分解的基团连接到聚合物珠上,所述可水解或可光分解的基团可选地位于所述候选拮抗剂的其中一个位置或合成中间的取代基上。根据Still等的技术,在一组珠上合成所述文库,每个珠包括一组鉴定该珠上特定diversomer的标记。然后将具有hedgehog拮抗剂的ptc功能丧失、hedgehog功能获得或smoothened功能获得的细胞“镀”到所述珠文库上。所述diversomer可以例如通过水解从所述珠上释放出来。
用于本发明的化合物的结构使它们本身容易有效合成。所述结构的性质如式I到II一般描述的性质,允许使用如上文所述的Ar、R1、X、Y和Z部分的某种组合进行所述化合物的组合装配。例如,可以将这些亚单位通过常用的酰化反应或烷基化反应连接到核心环上。所述反应的绝大部分(包括在图11、12、15和16中描述的那些)既非常温和也非常可靠,因此特别适于组合化学。所述组合方法可以使用下文公开的其中一种途径的改变形式。
对上文所述途径和相关途径的各种变化允许合成作为hedgehog功能抑制剂接受测试的化合物的广泛多样化的文库。
制备本发明的示例性化合物
a.举例说明的合成方案
图1-31显示产生用于本发明方法和组合物的hedgehog拮抗剂的示例性合成方案。
在图1-31举例说明的方案中的反应条件如下:
1)R1CH2CN,NaNH2,甲苯
(Arzneim-Forsch,1990,40,11,1242)
2)H2SO4,H2O,回流
(Arzneim-Forsch,1990,40,11,1242)
3)H2SO4,EtOH,回流
(Arzneim-Forsch,1990,40,11,1242)
4)NaOH,EtOH,回流
5)(Boc)2O,2M NaOH,THF
6)LiHDMS,R1X,THF
(Merck Patent Applic#WO 96/06609)
7)Pd-C,H2,MeOH
8)t-BuONO,CuBr,HBr,H2O
(J.Org.Chem.1977,42,2426)
9)ArB(OH)2,Pd(PPh3)4,二氧杂环己烷
(J.Med.Chem.1996,39,217-223)
10)R12(H)C=CR13R14,Pd(OAc)2,Et3N,DMF
(Org.React.1982,27,345)
11)Tf2O,THF
(J.Am.Chem.Soc.1987,109,5478-5486)
12)ArSnBu3,Pd(PPh3)4,二氧杂环己烷
(J.Am.Chem.Soc.1987,109,[5478-5486)
13)KMnO4,Py,H2O
(J.Med.Chem.1996,39,217-223)
14)NaOR1,THF
15)NaSR1,THF
16)HNR1R13,THF
17)HONO,NaBF4
(Adv.Fluorine Chem.1965,4,1-30)
18)Pd(OAc)2,NaH,DPPF,PhCH3,R1OH
(J.Org.Chem.1997,62,5413-5418)
19)i.R1X,Et3N,CH2Cl2,ii.R13X
20)SOCl2,cat DMF
21)CH2N2,Et2O
22)AgO,Na2CO3,Na2S2O3,H2O
(Tetrahedron Lett.1979,2667)
23)AgO2CPh,Et3N,MeOH
(Org.Syn.,1970,50,77;J.Am.Chem.Soc.1987,109,5432)
24)LiOH,THF-MeOH
25)(EtO)2P(O)CH2CO2R,BuLi,THF
26)MeO2CCH(Br)=P(Ph)3,苯
27)KOH或KOtBu
28)碱,X(CH2)NCO2R
29)DPPA,Et3N,甲苯
(Synthesis 1985,220)
30)HONO,H2O
31)SO2,CuCl,HCl,H2O
(Synthesis 1969,1-10,6)
32)Lawesson试剂,甲苯
(Tetrahedron Asym.1996,7,12,3553)
33)R2M,溶剂
34)30%H2O2,冰乙酸
(Helv.Chim.Acta.1968,349,323)
35)三光气,CH2Cl2
(Tetrahedron Lett.,1996,37,8589)
36)i.(EtO)2P(O)CHLiSO2Oi-Pr,THF,ii.NaI
37)Ph3PCH3I,NaCH2S(O)CH3,DMSO
(Synthesis 1987,498)
38)Br2,CHCl3或其它溶剂
(Synthesis 1987,498)
39)BuLi,Bu3SnCl
40)ClSO2OTMS,CCl4
(Chem.Ber.1995,128,575-580)
41)MeOH-HCl,回流
42)LAH,Et2O或LiBH4,EtOH或BH3-THF
(Tetrahedron Lett.,1996,37,8589)
43)MsCl,Et3N,CH2Cl2
(Tetrahedron Lett.,1996,37,8589)
44)Na2SO3,H2O
(Tetrahedron Lett.,1996,37,8589)
45)R2R4NH,Et3N,CH2Cl2
46)R2M,溶剂
47)CH3NH(OCH3),EDC,HOBt,DIEA,CH2Cl2或DMF
(Tetrahedron Lett,1981,22,3815)
48)MeLi,THF
49)mCPBA,CH2Cl2
50)HONO,Cu2O,Cu(NO3)2,H2O
(J.Org.Chem.1977,42,2053)
51)R1M,溶剂
52)HONO,NaS(S)COEt,H2O
(Org.Synth.1947,27,81)
53)HSR2或HSR4,CH2Cl2
54)i-BuOC(O)Cl,Et3N,NH3,THF
55)R2R4NH,CH2Cl2,NaBH(OAc)3
56)R2R4NH,MeOH/CH3CO2H,NaBH3CN
57)R2OH,EDC,HOBt,DIEA,CH2Cl2或DMF
58)R2OH,HBTU,HOBt,DIEA,CH2Cl2或DMF
59)R2R4NH,EDC,HOBt,DIEA,CH2Cl2或DMF
60)R2R4NH,HBTU,HOBt,DIEA,CH2Cl2或DMF
61)POCl3,Py,CH2Cl2
62)R2R4NCO,溶剂
63)R2OC(O)Cl,Et3N,溶剂
64)R2CO2H,EDC或HBTU,HOBt,DIEA,CH2Cl2或DMF
65)R2X,Et3N,溶剂
66)(CH3S)2C=N(CN),DMF,EtOH
(J.Med.Chem.1994,37,57-66)
67)R2SO2Cl,Et3N,CH2Cl2
68)R2-或R3-或R4CHO,MeOH/CH3CO2H,NaBH3CN
(Synthesis 1975,135-146)
69)Boc(Tr)-D或L-CysOH,HBTU,HOBt,DIEA,CH2Cl2或DMF
70)Boc(Tr)-D或L-CysH,NaBH3CN,MeOH/CH3CO2H
(Synthesis 1975,135-146)
71)S-Tr-N-Boc cysteinal,ClCH2CH2Cl或THF,NaBH(OAc)3
(J.Org.Chem.1996,61,3849-3862)
72)TFA,CH2Cl2,Et3SiH或(3∶1∶1)苯硫基甲烷/乙二硫醇/DMS
73)TFA,CH2Cl2
74)DPPA,Et3N,甲苯,HOCH2CH2SiCH3
(Tetrahedron Lett.1984,25,3515)
75)TBAF,THF
76)碱,TrSH或BnSH
77)碱,R2X或R4X
78)R3NH2,MeOH/CH3CO2H,NaBH3CN
79)N2H4,KOH
80)Pd2(dba)3,P(o-tol)3,RNH2,NaOtBu,二氧杂环己烷,R1NH2
(Tetrahedron Lett.1996,37,7181-7184)。
81)氨腈。
82)Fmoc-Cl,碳酸氢钠。
83)BnCOCl,碳酸钠。
84)AllylOCOCl,吡啶。
85)苄基溴,碱。
86)草酰氯,DMSO。
87)RCONH2。
88)羰二咪唑,中性溶剂(如DCM、DMF、THF、甲苯)。
89)硫代羰二咪唑,中性溶剂(如DCM、DMF、THF、甲苯)。
90)溴化氰,中性溶剂(如DCM、DMF、THF、甲苯)。
91)RCOCl,三乙胺
92)RNHNH2,EDC。
93)RO2CCOCl,Et3N,DCM。
94)MsOH,吡啶
(J.Het.Chem.,1980,607.)
95)碱,中性溶剂(如DCM、甲苯、THF)。
96)H2NOR,EDC。
97)RCSNH2。
98)RCOCHBrR,中性溶剂(如DCM、DMF、THF、甲苯),(Org.Proc.Prep.Intl.,1992,24,127)。
99)CH2N2,HCl。(Synthesis,1993,197)。
100)NH2NHR,中性溶剂(如DCM、DMF、THF、甲苯)。
101)RSO2Cl,DMAP。(Tetrahedron Lett.,1993,34,2749)。
102)Et3N,RX。(J.Org.Chem.,1990,55,6037)。
103)NOCl或Cl2(J.Org.Chem,1990,55,3916)。
104)H2NOH,中性溶剂(如DCM、DMF、THF、甲苯)。
105)RCCR,中性溶剂(DCM、THF、甲苯)。
106)RCHCHR,中性溶剂(DCM、THF、甲苯)。
107)H2NOH,HCl。
108)硫代羰二咪唑,SiO2或BF3OEt2。(J.Med.Chem.,1996,39,5228)。
109)硫代羰二咪唑,DBU或DBN。(J.Med.Chem.,1996,39,5228)。
110)HNO2,HCl。
111)ClCH2CO2Et(Org.Reactions,1959,10,143)。
112)吗啉烯胺(Eur.J.Med.Chem.,1982,17,27)。
113)RCOCHR′CN
114)RCOCHR′CO2Et
115)Na2SO3
116)H2NCHRCO2Et
117)EtO2CCHRNCO
118)RCNHNH2。
119)RCOCO2H,(J.Med.Chem.,1995,38,3741)。
120)RCHO,KOAc。
121)2-氟硝基苯。
122)SnCl2,EtOH,DMF。
123)RCHO,NaBH3CN,HOAc。
124)NH3,MeOH。
125)2,4,6-Me3PhSO2NH2。
126)Et2NH,CH2Cl2
127)MeOC(O)Cl,Et3N,CH2Cl2
128)R2NH2,EDC,HOBT,Et3N,CH2Cl2
129)DBU,PhCH3
130)BocNHCH(CH2STr)CH2NH2,EDC,HOBT,Et3N,CH2Cl2
131)R2NHCH2CO2Me,HBTU,HOBT,Et3N,CH2Cl2
132)BocNHCH(CH2STr)CH2OMs,LiHMDS,THF
133)R2NHCH2CO2Me,NaBH(OAc)3,ClCH2CH2Cl或THF
134)R2NHCH2CH(OEt)2,HBTU,HOBT,Et3N,CH2Cl2
135)NaBH(OAc)3,ClCH2CH2Cl或THF,AcOH。
136)哌啶,DMF。
137)Pd(Ph3P)4,Bu3SnH。
138)RCO2H,EDC,HOBT,Et3N,DCM。
139)RNH2,中性溶剂。
140)RCHO,NaBH3CN,HOAc。
141)RNCO,溶剂。
142)RCO2H,EDC或HBTU,HOBt,DIEA,CH2Cl2或DMF。
143)RCOCl,三乙胺
144)RSO2Cl,Et3N,CH2Cl2。
145)SnCl2,EtOH,DMF。
146)RNH2,EDC,HOBt,DIEA,CH2Cl2或DMF。
147)二溴乙烷,Et3N,CH2Cl2
148)草酰氯,中性溶剂。
149)LiOH,THF-MeOH。
150)羰二咪唑,中性溶剂(如DCM、DMF、THF、甲苯)。
151)RNH2,Et3N,CH2Cl2。
152)碱,RX。
153)DBU,PhCH3
154)DPPA,Et3N,甲苯(Synthesis 1985,220)
155)SOCl2,cat DMF。
156)ArH,Lewis Acid(AlCl3、SnCl4、TiCl4),CH2Cl2。
157)H2NCHRCO2Et,中性溶剂。
158)BocHNCHRCO2H,EDC或HBTU,HOBt,DIEA,CH2C12或DMF。
159)TFA、CH2Cl2。
b.筛选测定
有各种测定可用于确定化合物激动ptc功能或拮抗smoothened或hedgehog功能的能力,许多所述测定可以采用高通量的形式进行布置。在许多测试化合物和天然提取物文库的药物筛选程序中,需要高通量测定,以便最大化给定时间内检查的化合物的数目。因此,可以从合成和天然产物文库中取样获得属于hedgehog拮抗剂的其它化合物。
除无细胞测定外,也可以在基于细胞的测定中检测测试化合物。在一个实施方案中,可以使具有ptc功能丧失、hedgehog功能获得或smoothened功能获得表型的细胞与目的测试试剂接触,用所述测定评价例如在测试试剂存在下对细胞增殖的抑制。
已经有多种基因产物涉及patched介导的信号传导,其中包括patched、cubitus interruptus(ci)家族的转录因子、丝氨酸/苏氨酸激酶fused(fu)和costal-2、smoothened和suppressor of fused的基因产物。
hedgehog蛋白对细胞的诱导启动涉及下游效应物激活和抑制的级联反应,在一些情况下,其最终结果是基因转录或翻译的可检测变化。hedgehog介导的信号传递的潜在转录靶是pacthed基因(Hidalgo和Ingham,1990
Development 110,291-301;Marigo等,1996)和果蝇肘脉interruptus基因的脊椎动物同源物,即GLI基因(Hui等(1994)
Dev Biol 162:402-413)。已经显示patched基因表达在响应Shh的肢芽和神经板细胞中被诱导。(Marigo等(1996)
PNAS 93:9346-51;Marigo等(1996)
Development 122:1225-1233)。所述Gli基因编码具有锌指DNA结合结构域的推定的转录因子(Orenic等(1990)
Gene & Dev 4:1053-1067;Kinzler等(1990)
Mol Cell Biol 10:634-642)。已经报道所述Gli基因的转录在肢芽中响应hedgehog而被上调节,而Gli3基因的转录响应hedgehog诱导而被下调节(Marigo等(1996)
Development 122:1225-1233)。通过从引起这些基因响应hedgehog信号传递而上调节或下调节的靶基因(如patched或Gli基因)选择转录调节序列,并有效连接所述启动子到报道基因,技术人员可以发展出基于转录的测定,所述测定对特定测试化合物改变hedgehog介导的信号途径的能力敏感。因此,所述报道基因的表达为发展作为hedgehog拮抗剂起作用的化合物提供有价值的筛选工具。
本发明基于报道基因的测定测量上述事件的末阶段,如转录调节。因此,当实施所述测定的一个实施方案时,将一种报道基因构建物插入所述试剂细胞,以产生依赖于ptc功能丧失、hedgehog功能获得、smoothened功能获得的检测信号,或者产生依赖于SHH本身刺激的检测信号。可以使用本领域内技术人员已知的任何合适方法,测量所述报道基因转录的量。例如,可以使用RNA酶保护或基于RNA的PCR,检测从所述报道基因的mRNA表达,或者通过特征链或内在生物学活性鉴定所述报道基因的蛋白产物。然后将从所述报道基因表达的量与不存在所述测试化合物的同样细胞中表达的量相比较,或者与缺乏靶受体蛋白的在实质上相同的细胞内转录的量相比较。转录量任何在统计学上或者其它方面显著的降低指示所述测试化合物以某种方式激动正常ptc信号(或者拮抗功能获得性hedgehog或smoothened的信号),如所述测试化合物是潜在的hedgehog拮抗剂。
VII.商业方法
本发明一方面涉及药盒,所述药盒包含hedgehog拮抗剂,例如如本文所述,用于治疗或预防患者(优选是人)体内基底细胞癌的hedgehog拮抗剂,以及描述所述制剂用于治疗或预防基底细胞癌的说明书(文字或图画),以及备选性关于可能副效应以及药物-药物或药物-食物相互作用的警示。
本发明另一方面涉及药盒,所述药盒包含hedgehog拮抗剂,例如如本文所述,其中所述hedgehog拮抗剂作为例如本文所述治疗或美容应用(如调节神经组织、骨和软骨形成和修复、调节精子发生、调节平滑肌、调节起源于原肠的肺、肝和其它器官、调节造血功能以及调节皮肤和毛发生长)的一部分给予患者(优选是人),所述药盒还包括描述所述药物或美容应用的说明书(文字和/或图画),以及备选性关于可能副效应和药物-药物或药物-食物相互作用的警示。
本发明还设想进行药物生产销售的方法,所述方法包括:(a)生产包含无菌药用赋形剂和hedgehog拮抗剂的药学制剂;和(b)向保健供应商如医生、医院、诊所等宣传(如提供推广和/或信息介绍(如展示、电话销售和讲座)、提供产品(例如所述制剂的试用样品)和/或文件(包括传单、小册子、网站、海报等))推广使用所述药用制剂治疗或预防基底细胞癌的好处。
本发明又一方面涉及进行药物生产销售的方法,所述方法包括:(a)生产包含无菌药用赋形剂和hedgehog拮抗剂的药用制剂;和(b)向保健供应商如医生、医院、诊所等宣传(如提供推广和/或信息介绍(如展示、电话销售和讲座)、提供产品(例如所述制剂的试用样品)和/或文件(包括传单、小册子、网站、海报等))推广使用所述药用制剂作为治疗应用或美容应用的一部分的好处,所述治疗应用或整型应用如调节神经组织、骨和软骨形成和修复、调节精子发生、调节平滑肌、调节起源于原肠的肺、肝和其它器官、调节造血功能以及调节皮肤和毛发生长。
本发明再一方面提供进行药物生产销售的方法,所述方法包括:(a)利用销售网络销售包含无菌药用赋形剂和hedgehog拮抗剂的药用组合物;和(b)为患者或医生提供使用所述药用组合物治疗或预防基底细胞癌的说明材料。
本发明另一方面涉及进行药物生产销售的方法,所述方法包括:(a)提供销售所述包含无菌药用赋形剂和hedgehog拮抗剂的药用组合物的分销网络;和(b)向患者或医生提供使用所述药用组合物作为治疗应用或美容应用的一部分的说明材料,所述治疗应用或美容应用如上文所述的应用(如调节神经组织、骨和软骨形成和修复、调节精子发生、调节平滑肌、调节起源于原肠的肺、肝和其它器官、调节造血功能以及调节皮肤和毛发生长)。
本发明另一方面提供进行药物生产销售的方法,所述方法包括:(a)确定治疗或预防基底细胞癌的hedgehog的合适药用制剂和剂量;(b)进行所述药用组合物在动物体内治疗或预防病理状况的效价和毒性的治疗剖析;(c)为了销售具有可接受治疗作用的药用组合物而提供分销网络;以及可选地,(d)为了营销所述制剂给保健供应商而提供销售队伍。
本发明另一方面提供进行药物生产销售的方法,所述方法包括:(a)确定治疗或预防疾病或美容缺陷的hedgehog的合适药用制剂和剂量;(b)进行所述药用组合物在动物体内治疗或预防所述状况的效价和毒性情况;(c)为了销售用于治疗或预防所述状况的具有可接受治疗作用的药用组合物而提供分销网络;以及可选地,(d)为了营销所述制剂给保健供应商以治疗或预防所述状况而提供销售队伍。
本发明的再一方面提供进行药物生产销售的方法,所述方法包括:(a)确定治疗或预防基底细胞癌的hedgehog的合适药用制剂和剂量;和(b)许可第三方注册进一步发展和销售所述药用组合物的权利。
本发明的又一方面提供进行药物生产销售的方法,所述方法包括:(a)确定治疗或预防上文所述医学状况或美容状况的hedgehog的合适药用制剂和剂量;和(b)许可第三方注册进一步发展和销售用于治疗或预防所述状况的所述药用组合物的权利。
实施例
目前已经一般性描述本发明,通过参考下面实施例可以更容易地理解本发明,所述实施例仅仅是为举例说明本发明某些方面和实施方案的目的包括进本说明书,而不是限制本发明。
实验
合成示例性抑制剂
途径1
一般方法。除特别指出外,所有反应都使用HPLC级溶剂在烘箱干烤的玻璃器皿中进行。使用5%Et3N(Flash ColumnChromatography)或Jones Chromatography Flash Master 11失活的硅胶40-63u 60A纯化化合物。在Kieselgel 60 F254板(Merck)上进行薄层色谱(TLC)。用氘化溶剂作为内部参比,使用Bruker 300NMR光谱仪测量1H-NMR。在Micromass平台LCZ上获得低分辨率质谱数据。使用Hewlett-Packard 1100测定纯度(LC光谱)。
2-氯-5-硝基-N-(2-硝基-苯基)苯甲酰胺1。室温下,在2-硝基-苯胺(15.00g,109mmol)的CH2Cl2溶液(90ml)中加入吡啶(43ml,2.86vols),然后逐滴加入于0℃下溶解于CH2Cl2(100ml)45分钟的2-氯-4-硝基-苯甲酰氯(27.40g,125mmol)。所述反应混合物在室温下搅拌3小时。一旦完成反应(通过LCMS监测),蒸发所述粗混合物到干燥。获得的棕色粗残余物在乙酸乙酯中制成浆,过滤,产生黄色固体的标题化合物(33g,94%):1H NMR(CDCl3)δ10.91(s,1H),8.85(dd,1H),8.53(app d,1H),8.28-8.21(m,2H),7.70(dd,1H),7.25(dd,1H);MS(ES,正离子模式):363[M++1+41]和322[M++1]。
3-(1H-苯并咪唑-2-基)-4-氯-苯胺2。在酰胺1(15.00g,46.7mmol)的甲苯(125ml)和乙酸(60ml)溶液中加入铁粉(15.42g,280mmol)。所述混合物在125℃下加热约1小时(通过LCMS检测反应完成),获得的粗混合物通过棉花塞过滤(除去铁颗粒)。将所述粗溶液蒸发到干燥,用EtOAc稀释,用饱和NaHCO3洗涤,然后用盐水洗涤,用MgSO4干燥,过滤,然后减压浓缩。得到的棕色固体重新溶于CH2Cl2,加入几滴己烷,形成固体,通过过滤分离所述固体,产生浅褐色固体的2(5.66g,42%):1H NMR(CD3OD)δ7.64(宽s,2H),7.30-7.26(m,3H),7.13(app d,1H),6.84(dd,1H);MS(ES,正离子模式):244[M++1]。
合成脲3。在酰胺2(300mg,1.23mmol)的CH2Cl2溶液(3.0ml)中加入吡啶(0.12ml,1.41mmol)。0℃下逐滴加入异氰酸3,5-二甲氧苯酯(253mg,1.41mmol)的CH2Cl2溶液(4.0ml),在室温下搅拌3小时(通过LCMS监测反应完成情况)。加入1M柠檬酸溶液,猝灭反应,分离有机相,蒸发到干燥。所述粗混合物用EtOAc稀释,用饱和NaHCO3洗涤,然后用盐水洗涤,用MgSO4干燥,过滤,然后减压浓缩。通过快速色谱(EtOAc:己烷,梯度洗脱)纯化所得的粗产物,获得3(40mg,8%):1H NMR(CD3OD)δ8.05(app d,1H),7.82(d,1H),7.81(d,1H)7.80(宽s,1H),7.67(d,1H),7.45(宽m,2H),6.83(s,1H),6.82(s,1H),6.33(宽m,1H),3.91(s,6H);MS(ES,正离子模式):423[M++1];LC(1.22,纯度>97%)。
合成酰胺4。将3,4,5-三甲氧苯甲酰氯(272mg,1.18mmol)的CH2Cl2溶液(4.0ml)在0℃下氮内加入胺2(250mg,1.03mmol)的CH2Cl2溶液(3.0ml)。所述反应混合物在室温下搅拌过夜(通过LCMS监测反应完成情况)。所述粗混合物用含约40%MeOH的EtOAc稀释,用饱和NaHCO3洗涤,然后用盐水洗涤,在MgSO4上干燥,过滤,然后减压浓缩。通过制备型LC纯化得到的粗产物,产生无色固体4(25mg,6%):1H NMR(CD3OD)δ8.31(app d,1H),7.98(dd,1H),7.76-7.74(m,2H),7.67(d,1H),7.46-7.44(m,2H),7.34(宽s,2H);MS(ES,正离子模式):438[M+1];LC(1.15,纯度>95%)。
合成硫脲5。0℃下,在胺2(250mg,1.03mmol)的CH2Cl2溶液(3.0ml)中加入吡啶(0.2ml,2.36mmol),然后逐滴加入苯并二噁烷异硫氰酸(228mg,1.18mmol)的CH2Cl2溶液(4.0ml)。所述混合物在室温下搅拌过夜(通过LCMS监测反应完成情况)。在所述粗反应混合物中加入1M柠檬酸溶液,分离有机相,蒸发到干燥。所述粗固体用EtOAc稀释,顺序用饱和NaHCO3和盐水洗涤,然后在MgSO4上干燥,过滤,减压浓缩。通过快速色谱(含30-50%EtOAc的己烷)纯化得到的粗产物,产生浅黄色固体5(95 mg,21%):1H NMR(CD3OD)δ7.71(appd,1H),7.55(dd,1H),7.50(宽s,2H),7.40(d,1H),7.19-7.13(宽m,2H),6.79(s,1H),6.67(s,2H)4.08(s,4H);MS(ES,正离子模式):438[M++1];LC(0.941,纯度>98%)。
合成磺酰胺6。0℃下,在胺2(250mg,1.03mmol)的CH2Cl2溶液(3.0ml)中加入吡啶(0.20ml,2.36mmol),然后逐滴加入苯磺酰氯(0.15ml,1.18mmol)的CH2Cl2溶液(4.0ml)。所述反应混合物搅拌1小时(通过LCMS监测反应完成情况)。在所述粗反应混合物中加入1M柠檬酸溶液,分离有机相,蒸发到干燥。所述粗固体用EtOAc稀释,顺序用饱和NaHCO3和盐水洗涤,然后在MgSO4上干燥,过滤,减压浓缩。通过快速色谱(1∶39∶60,MeOH∶EtOAc∶己烷)纯化得到的主要包含二烷基化产物的粗混合物,产生无色固体6(20mg,5%):1H NMR(CD3OD)δ8.01-7.99(宽d,2H),7.97(d,1H) 7.95(d,1H),7.84(app d,1H),7.76-7.74(m,4H),7.68(d,1H),7.66(d,1H),7.55(dd,1H);MS(ES,正离子模式)384[M++1];LC(1.190,纯度>99%)。
途径2
2-(2-甲基-5-硝基-苯基)-1H-苯并咪唑7。将苯-1,2-二胺(2.60g,25mmol)和2-甲基-5-硝基苯甲酸(5.0g,27.6mmol)悬浮于聚磷酸(30ml,11vol)中,加热到140℃过夜。一旦反应完成(通过LCMS监测),将绿色粗混合物溶解于水中,用NaOH(pH=14)碱化,萃取进入EtOAc(x2)。用盐水洗涤有机相,在MgSO4上干燥,过滤,减压浓缩,产生橙色/棕色固体7(4.70g,74%):1H MR(C2D6SO)δ13.20(s,1H),8.80(app d,1H),8.84(dd,1H),7.89-7.87(m,2H),7.74(d,1H),7.40-7.45(m2H),2.90(s,3H);MS(ES,正离子模式):254[M++1]。
3-(1H-苯并咪唑-2-基)-4-甲基-苯胺。在硝基苯并咪唑7(4.30g,16.9mmol)的甲苯(30ml)和乙酸(30ml)溶液中加入铁粉(3.0g,50.9mmol),所述反应混合物在125℃下加热约1小时(通过TLC监测反应完成情况)。获得的粗混合物通过棉花塞过滤(除去铁颗粒)。将所述粗溶液蒸发到干燥,用EtOAc稀释,用饱和NaHCO3洗涤(直到pH=7),用EtOAc反萃取水相。混合的有机物用盐水洗涤,用MgSO4干燥,过滤,然后减压浓缩,得到棕色固体8(2.70g,73%):1H NMR(C2D6SO)δ12.55(s,1H),7.73(d,1H),7.57(d,1H),7.16(宽m,2H),7.09(d,1H),7.01(app d,1H),6.70(dd,1H)5.15(宽s,2H),2.39(s,3H);MS(ES,正离子模式):224[M++1]。
合成酰胺9。将苯并咪唑基苯胺8(250mg,1.12mmol)和3-5-二乙氧基苯甲酰氯(246mg,1.23mmol)悬浮于CH2Cl2(10.0ml),室温下搅拌过夜。所述粗混合物用EtOAc稀释,然后用柠檬酸洗涤。水相用NaOH碱化并萃取进EtOAc。合并的有机萃取物用盐水洗涤,在MgSO4上干燥,过滤,然后减压浓缩,产生无色固体9:1H NMR(C2D6SO)δ12.65(s,1H),10.35(s,1H),8.19(s,1H),7.86(d,1H),7.74(d,1H),7.61(d,1H),7.32(d,1H),7.42-7.32(m,2H),7.20(s,2H),6.79(s,1H),3.89(s,6H),2.61(s,3H);MS(ES,正离子模式):388[M++1];LC(1.19,纯度>97%)。
合成酰胺10 。将苯并咪唑苯胺8(250mg,1.12mmol)和苯并二噁烷-4-碳酰氯(220mg,1.23mmol)悬浮于CH2Cl2(10.0ml)中,在室温下搅拌过夜。所述粗混合物用EtOAc稀释,然后用柠檬酸洗涤。水相用NaOH碱化,然后萃取进EtOAc。合并的有机提取物用盐水洗涤,在MgSO4上干燥,过滤,然后减压浓缩,产生无色固体10:1H NMR(C2D6SO)δ12.55(s,1H),10.49(s,1H),9.07(app d,1H),8.70(dd,1H),8.25(dd,1H),8.15(app d,1H),7.72(dd,1H),7.64(d,1H),7.52-7.48(m,1H),7.38(d,1H),7.31(d,1H),7.17-6.95(m,2H),3.28(s,3H);MS(ES,正离子模式):329[M++1];LC(0.858,纯度>97%)。
途径3
2-(2-氯-5-硝基-苯基)-1H-苯并咪唑-5-腈12。将2-氨基-4-氰基-苯胺(0.5g,3.76mmol)和2-氯-4-硝基-苯甲醛(1.39g,7.52mmol)分别溶解于最小量的乙酸,然后在室温下混合。过滤形成的橙色固体,用乙酸和庚烷洗涤,直到滤过物成为无色。显示在该阶段分离的固体是中间体11(600mg,45%):1H NMR(C2D6SO)δ8.99(app d,1H)8.91(s,1H),8.28(dd,1H),7.84(d,1H),7.57(s,1H),7.35(dd,1H),6.75(d,1H),6.36(s,2H);MS(ES,正离子模式):301[M++1]。中间体11的环化:得到的棕色固体悬浮于乙酸中,然后在50℃加热6小时。所述粗混合物用EtOAc稀释,用NaHCO3溶液中和,用盐水洗涤,在MgSO4上干燥,减压浓缩,产生棕色固体12(200mg,99%):1H NMR(C2D6SO)δ12.55(宽s,1H),8.66(app d,1H),8.30(dd,1H),8.20(s,1H),7.90(d,1H),7.76(d,1H),7.50(d,1H);MS(ES,正离子模式):299[M++1]。
生物测定
前导化合物发现/高通量筛选测定
将需要测试的化合物溶解于DMSO中达到10mM的浓度,然后保存于-20℃。为激活所述测定细胞中的Hedgehog途径,使用SonicHedgehog蛋白N末端片段的辛基化(脂修饰)形式(OCT-SHH)。使用细菌产生所述N末端SHH片段。见,例如,Taylor FR等,Biochemistry2001,40,4359-71。
可以在下面“Gli-Luc”测定中测试化合物,该测定使用细胞系10T1/2(s12),其中所述细胞包含利用荧光素酶作为报道基因的Hedgehog响应报道构建物。使用这种方法,能够通过Gli-Luc响应测定Hedgehog途径信号传递活性。
将10t1/2(s12)细胞以20,000细胞/孔接种到96孔板(MTP)内,使用完全培养基[含10%FBS的DMEM]。然后将平板置于培养箱内,在37℃和5%CO2培养过夜(O/N)。24小时后,用荧光素酶测定培养基(含0.5%FBS的DMEM)取代所述培养基。融化化合物,以3∶1000(约300倍)稀释于测定培养基中,获得约0.0003μM到30μM的起始浓度。
然后在第一批孔内加入150μl每种样品(一式三份)。然后将所述MTP样品以3倍稀释到总共七个孔中,最终产生每种化合物一式三份七个稀释度。然后将蛋白配体OCT-SHH稀释于荧光素酶培养基,加入每个孔达到0.3μg/ml的终浓度。然后将平板放回培养箱,继续在37℃和5%CO2培养过夜。约24小时后,从培养箱中取出平板,吸出并弃去培养基。用测定缓冲液[PBS+1mM Mg2+和1mM Ca2+]洗孔一次。然后在每个孔中加入50μl测定缓冲液。根据供应商所述(得自Packard的LucLite试剂盒)制备所述荧光素酶测定试剂,在每孔中加入50μl。在室温下温育板约30分钟,然后再次在室温(RT)下在Topcount(Packard)上读出信号。
使用人细胞系(具体地说是人胚腭间质细胞,如上所述用Gli-Luc构建物修饰)在生长培养基MEM/丙酮酸钠w/10%FBS和测定培养基MEM/丙酮酸钠w/0.5%FBS上进行相似测定。加入OCT-SHH达到1μg/ml的终浓度。
图32描述在上述测定中鉴定的化合物。
下面表1显示具体化合物的活性(除化合物E-V外,活性基于所述基于人的测定的结果):
表1
化合物 IC50(μM) 化合物 IC50(μM)
A <0.05 B <0.05
C <0.5 D <0.5
E <5 F <5
G <5 H <5
I <5 J <5
K <5 L <5
M <5 N <1
O <5 P <5
Q <10 R <10
S >10 T <5
U <5 V <5
W <0.01 X <0.05
Y <0.05 Z <0.05
A’ <0.01 B’ <0.01
C’ <0.05 D’ <0.05
E’ <0.05 F’ <0.05
G’ <0.01 H’ <0.01
I’ <0.05 J’ <0.05
K’ <0.01 L’ <0.05
M’ <0.05 N’ <0.1
O’ <0.1 P’ <0.1
Q’ <0.05 R’ <0.05
S’ <0.05 T’ <0.05
U’ <0.05 V’ <0.05
W’ <0.1 X’ <0.1
Y’ <0.5 Z’ <0.5
A” <0.5 B” <0.5
C” <0.5 D” <0.5
E” <0.5 F” <0.5
G” <0.5 H” <0.5
I” <0.5 J” <0.05
K” <0.05 L” <0.05
M” <0.05 N” <0.05
O” <0.1 P” <0.5
Q” <0.5 R” <0.5
S” <0.1 T” <0.1
U” <0.1 V” <0.5
W” <0.5 X” <0.5
Y” <0.5 Z” <0.5
A_ <0.5 B_ <0.5
C_ <0.5 D_ <0.5
E_ <0.5 F_ <1
G_ <0.1 H_ <0.5
I_ <0.5 J_ <0.5
K_ <0.01 L_ <0.5
M_ <0.5 N_ <0.01
O_ <1 P_ <0.5
Q_ <0.05 R_ <0.5
S_ <0.05 T_ <10
U_ <0.5 V_ <0.05
W_ <0.05 X_ <0.5
Y_ <0.5 Z_ <0.5
A”” <0.5 B”” <0.05
C”” <0.05 D”” <0.05
E”” <0.5 F”” <0.5
G”” <0.05 H”” <0.5
I”” <0.1 J”” <0.05
K”” <5 L”” <0.05
M”” <0.01 N”” <0.1
O”” <0.5 P”” <0.5
Q”” <0.5 R”” <5
S”” <0.5 T”” <0.5
U”” <0.05 V”” <0.05
W”” <0.5 X”” <0.5
Y”” <0.001 Z”” <0.001
A””’ <0.05 B””’ <0.05
C””’ <0.5 D””’ <0.05
E””’ <0.05 F””’ <0.5
化合物对基底细胞癌(BCC)样品的效应
BCC培养物:以器官型培养培养包含一些真皮基质的基底细胞癌刮除标本,即暴露于空气/液体界面。向BCC样品注射媒介物(0.8%无菌NaCl溶液)或化合物,培养物放在塑料格子顶部,并在适于长期培养人类皮肤的培养基中温育达三天(包含或不包含化合物)。培养3天后,根据常规组织学加工所述样品。
当在该系统中培养BCC时,维持BCC的形态学特征,如未分化基底细胞的岛,以及一些情况下外周细胞的栅栏状排列和基质裂。根据暴露于33P标记的RNA探针后的测定,GLI-1基因(hedgehog信号传递的关键指标)在未处理培养物中维持高水平活性。
定量原位杂交:简要地说,将多聚甲醛固定、用石蜡包埋的包含大基底细胞岛的组织的7μm切片清洁、再水合、用蛋白酶K消化、乙酰化、然后与33P标记的RNA探针杂交过夜。高严格性杂交后洗涤后,将载玻片于室温下黑暗中暴露于高灵敏度PhosphorImager屏几个小时。显影后,用Cyclone Scanner(Packard)扫描[[33P]信号。选择各个基底细胞岛,使用OptiQuant软件定量信号,表达为DLU(数字光学单位)/mm2。取对照值的平均值,设为100%;从化合物A处理的样品获得的值表达为对照的%。图33描述结果。
天冬氨酸特异性半胱氨酸蛋白酶3免疫组织化学。编程性细胞死亡或细胞凋亡是去除不希望的细胞的有组织过程,涉及天冬氨酸特异性半胱氨酸蛋白酶激活、DNA片段化、膜形成泡、细胞萎缩和吞噬作用。通过免疫组织化学针对活性天冬氨酸特异性半胱氨酸蛋白酶3分析细胞凋亡,天冬氨酸特异性半胱氨酸蛋白酶3是检测早期细胞凋亡事件的标记。对BCC培养物应用标准组织学分析,按照生产厂商的说明书,对载玻片进行去石蜡处理,用第一抗体预封闭和温育,清洗,然后与酶标记的第二抗体温育。通过酶检测所述抗原-抗体复合物,显现所述特异性信号。在载玻片上滑动加上盖玻片,然后成像。图34描述结果,其中左图是对照组织,右图是A存在图。
主题化合物对于其它肿瘤细胞的效应
结肠癌细胞:将20,000个结肠癌细胞与10,000个10T(S12)细胞(上文所述)混合,将所述混合物加入96孔板的每个孔内。第二天在所述培养物中加入主题化合物或对照媒介物。温育72小时后,裂解细胞,测量荧光酶活性。化合物A能够抑制荧光酶活性,当将这种抑制与该测定中的媒介物相比较时,间接反映hedgohog信号传递途径的活性,图35描述抗体1E6和5E1以及化合物A对于S12细胞中hedgehog诱导的激活的抑制比较,以及这些组合物在结肠癌细胞中对内源性hedgehog活性的抑制比较。
前列腺癌细胞和膀胱癌细胞:图36描述使用激素不应性前列腺癌细胞系PC-3细胞系和尿道膀胱癌细胞系RT-4在同样测定中进行的相关实验。
主题化合物对于其它组织的效应
使用RT-PCR和实时PCR(Taqman),用图37中描述的探针和引物评价所述主题抑制剂对于GLI-1和GAPDH表达的效应。在辛基-SHH和主题化合物存在下培养HEPM细胞24小时。收获总RNA,使用标准RT-PCR评估GLI-1和GAPDH转录物的表达水平。图38描述下面化合物的测试结果:化合物A,0.003-1.0μM;化合物O,0.003-1.0μM;-,阴性对照(仅DMSO);+,阳性对照(辛基-SHH,1mg/ml,无抑制剂)。
在本发明主题化合物存在下培养包含patched纯合破坏性细胞(无ptc细胞)72-96小时。收获总RNA,使用标准RT-PCR评估GLI-1和GAPDH转录物的表达水平。
图39描述下面化合物的测试结果:化合物C,1 & 10μM;化合物O,1 & 10μM;DMSO,阴性对照。
在辛基-SHH和主题化合物存在下培养HEPM细胞24小时。收获总RNA,通过标准RT反应转化为cDNA。然后在实时PCR中使用所述cDNA评估GLI-1和GAPDH转录物的表达水平。图40描述下面化合物的测试结果:化合物A,0.001-0.3μM;化合物O,0.001-0.3μM;DMSO(-),阴性对照;OCT-SHH(+),阳性对照。
在辛基-SHH和化合物A存在下培养CCD-37细胞(肺成纤维细胞)24小时。收获总RNA,通过标准RT反应转化为cDNA。然后在实时PCR中使用所述cDNA评估GLI-1和GAPDH转录物的表达水平。图40描述下面化合物的测试结果:化合物A,0.001-1.0μM;DMSO(-),阴性对照;OCT-SHH(+),阳性对照。
所有上文引用的参考文献特此通过引用结合到本文中。
等同实施方案
本领域内技术人员将认识到或者仅使常规实验就能够确定本文所述的本发明特定实施方案的许多等同实施方案。所述等同实施方案将包括在下面权利要求中。
Claims (36)
1.一种抑制细胞中hedgehog途径激活的方法,该方法包括使所述细胞与足以抑制hedgehog信号传递的量的hedgehog拮抗剂接触,其中所述hedgehog拮抗剂是用下面通式(I)代表的有机分子:
式I
其中,当化合价和稳定性允许时,
X和Z独立地代表-N(R7)-、-O-、-S-、-(R7)N-N(R7)-、-ON(R7)-或者直接化学键;
Y代表-C(=O)-、-C(=S)-、-C(=NR7)-、SO2、或SO;
A代表O、S或NR7;
G代表与其连接环稠合的环烷基、杂环基、芳基或杂芳基环;
Ar代表取代或未取代的芳基或杂芳基环;
R1代表H或取代或未取代的烷基、链烯基、炔基、芳基、杂芳基、杂环基或环烷基,包括多环基;
R2代表其所连接环上的0-4个取代基;
R7每次出现时独立地代表H、低级烷基、J-环烷基、J-杂环基、J-芳基、J-杂芳基;
R8每次出现时独立地代表H、低级烷基、环烷基、杂环基、芳基或杂芳基;和
J每次出现时独立地代表具有0-8个单位的链,所述单位选自CK2、NK、O和S,其中K每次出现时独立地代表H或低级烷基。
2.权利要求1的方法,其中Z和X中至少其中之一不是直接化学键。
3.权利要求1的方法,其中X-Y-Z包括酰胺、脲或磺酰胺。
4.权利要求1的方法,其中X选自-N(R8)-、-O-、-S-,优选代表NH。
5.权利要求1的方法,其中R1包括芳基或杂芳基环,所述芳基或杂芳基环可选地被1-5个取代基取代。
6.权利要求5的方法,其中R1上的取代基选自硝基、卤素、氰基、低级烷基、酰氨基(如R8-C(=O)NH-)、烷氧基、烷基氨基、与所述芳基或杂芳基环稠合的取代或未取代环烷基、杂环基、芳基或杂芳基。
7.权利要求1的方法,其中X和包含A的环在Ar上是间位关系。
8.权利要求1的方法,其中R2代表选自以下的1-4个取代基:卤素、低级烷基、低级链烯基、芳基、杂芳基、羰基、硫代羰基、酮、醛、氨基、酰氨基、酰胺基、脒基、氰基、硝基、叠氮基、磺酰基、亚砜基、硫酸酯、磺酸酯、氨磺酰、亚磺酰氨基、磷酰基、膦酸酯、次膦酸酯、J-R8、J-OH、J-低级烷基、J-低级链烯基、J-R8、J-SH、J-NH2、上述基团的受保护形式,或者任意两个R2,当R2在环结构或多环结构中出现一次以上时,可以一起形成4-到8-元环烷基、芳基或杂芳基。
9.权利要求8的方法,其中R2代表选自以下的1-4个取代基:卤素、氰基、硝基、烷氧基、氨基、酰氨基(如R8-C(=O)NH-)、与G稠合的取代或未取代的环烷基、杂环基、芳基、或杂芳基以及取代或未取代的低级烷基。
10.权利要求1的方法,其中所述细胞具有ptc功能丧失、hedgehog功能获得或smoothened功能获得表型。
11.权利要求1的方法,其中所述hedgehog拮抗剂以1μM或更低的ED50抑制ptc功能丧失、hedgehog功能获得或smoothened功能获得介导的信号传导。
12.权利要求1的方法,其中所述hedgehog拮抗剂以1nM或更低的ED50抑制ptc功能丧失、hedgehog功能获得或smoothened功能获得介导的信号传导。
13.权利要求1的方法,其中所述细胞在体外与所述hedgehog拮抗剂接触。
14.权利要求1的方法,其中所述细胞在体内与所述hedgehog拮抗剂接触。
15.权利要求1的方法,其中所述hedgehog拮抗剂作为治疗应用或美容应用的组成部分给予。
16.权利要求15的方法,其中所述治疗应用或美容应用选自以下应用:调节神经组织、骨和软骨形成和修复、调节精子发生、调节平滑肌、调节起源于原肠的肺、肝和其它器官、调节造血功能以及调节皮肤和毛发生长。
17.一种抑制细胞中hedgehog途径激活的方法,该方法包括使所述细胞与足以抑制hedgehog信号传递的量的hedgehog拮抗剂接触,其中所述hedgehog拮抗剂是用下面通式(II)代表的有机分子:
式II
其中,当化合价和稳定性允许时,
X和Z独立地代表-N(R7)-、-O-、-S-、-(R7)N-N(R7)-、-ON(R7)-或者直接化学键;
Y代表-C(=O)-、-C(=S)-、-C(=NR7)-、SO2、或SO;
A代表O、S或NR7;
G代表与其连接环稠合的环烷基、杂环基、芳基或杂芳基环;
R1代表H或取代或未取代的烷基、链烯基、炔基、芳基、杂芳基、杂环基或环烷基,包括多环基;
R2代表其所连接的环上的0-4个取代基;
R3代表其所连接的环上的0-4个取代基;
R7每次出现时独立地代表H、低级烷基、J-环烷基、J-杂环基、J-芳基、J-杂芳基;
R8每次出现时独立地代表H、低级烷基、环烷基、杂环基、芳基或杂芳基;和
J每次出现时独立地代表具有0-8个单位的链,所述单位选自CK2、NK、O和S,其中K每次出现时独立地代表H或低级烷基。
18.权利要求17的方法,其中Z和X中至少其中之一不是直接化学键。
19.权利要求17的方法,其中X-Y-Z包括酰胺、脲或磺酰胺。
20.权利要求17的方法,其中X选自-N(R8)-、-O-、-S-,优选代表NH。
21.权利要求17的方法,其中R1包括芳基或杂芳基环,所述芳基或杂芳基环可选地被1-5个取代基取代。
22.权利要求21的方法,其中R1上的取代基选自硝基、卤素、氰基、低级烷基、酰氨基(如R8-C(=O)NH-)、烷氧基、烷基氨基、与所述芳基或杂芳基环稠合的取代或未取代环烷基、杂环基、芳基和杂芳基。
23.权利要求17的方法,其中R2代表选自以下的1-4个取代基:卤素、低级烷基、低级链烯基、芳基、杂芳基、羰基、硫代羰基、酮、醛、氨基、酰氨基、酰胺基、脒基、氰基、硝基、叠氮基、磺酰基、亚砜基、硫酸酯、磺酸酯、氨磺酰、亚磺酰氨基、磷酰基、膦酸酯、次膦酸酯、J-R8、J-OH、J-低级烷基、J-低级链烯基、J-R8、J-SH、J-NH2、上述基团的受保护形式,或者任意两个R2,当R2在环结构或多环结构中出现一次以上时,可以一起形成4-到8-元环烷基、芳基或杂芳基。
24.权利要求23的方法,其中R2代表选自以下的1-4个取代基:卤素、氰基、硝基、烷氧基、氨基、酰氨基、与G稠合的取代或未取代的环烷基、杂环基、芳基、或杂芳基以及取代或未取代的低级烷基。
25.权利要求17的方法,其中所述细胞具有ptc功能丧失、hedgehog功能获得或smoothened功能获得表型。
26.权利要求17的方法,其中所述hedgehog拮抗剂以1μM或更低的ED50抑制ptc功能丧失、hedgehog功能获得或smoothened功能获得介导的信号传导。
27.权利要求17的方法,其中所述hedgehog拮抗剂以1nM或更低的ED50抑制ptc功能丧失、hedgehog功能获得或smoothened功能获得介导的信号传导。
28.权利要求17的方法,其中所述细胞在体外与所述hedgehog拮抗剂接触。
29.权利要求17的方法,其中所述细胞在体内与所述hedgehog拮抗剂接触。
30.权利要求17的方法,其中所述hedgehog拮抗剂作为治疗应用或美容应用的组成部分给予。
31.权利要求30的方法,其中所述治疗应用或美容应用选自以下应用:调节神经组织、骨和软骨形成和修复、调节精子发生、调节平滑肌、调节起源于原肠的肺、肝和其它器官、调节造血功能以及调节皮肤和毛发生长。
32.一种药用制剂,所述药用制剂包含无菌药用赋形剂和一种用下面通式(I)代表的化合物:
式I
其中,当化合价和稳定性允许时,
X和Z独立地代表-N(R7)-、-O-、-S-、-(R7)N-N(R7)-、-ON(R7)-或者直接化学键;
Y代表-C(=O)-、-C(=S)-、-C(=NR7)-、SO2、或SO;
A代表O、S或NR7;
G代表与其所连接的环稠合的环烷基、杂环基、芳基或杂芳基环;
Ar代表取代或未取代的芳基或杂芳基环;
R1代表H或取代或未取代的烷基、链烯基、炔基、芳基、杂芳基、杂环基或环烷基,包括多环基;
R2代表其所连接的环上的0-4个取代基;
R7每次出现时独立地代表H、低级烷基、J-环烷基、J-杂环基、J-芳基、J-杂芳基;
R8每次出现时独立地代表H、低级烷基、环烷基、杂环基、芳基或杂芳基;和
J每次出现时独立地代表具有0-8个单位的链,所述单位选自CK2、NK、O和S,其中K每次出现时独立地代表H或低级烷基。
33.一种治疗或预防基底细胞癌的方法,所述方法包括将足以抑制基底细胞癌发展的量的权利要求32的药用制剂给予患者。
34.一种药用制剂,所述药用制剂包含无菌药用赋形剂和一种用下面通式(II)代表的化合物:
式II
其中,当化合价和稳定性允许时,
X和Z独立地代表-N(R7)-、-O-、-S-、-(R7)N-N(R7)-、-ON(R7)-或者直接化学键;
Y代表-C(=O)-、-C(=S)-、-C(=NR7)-、SO2、或SO;
A代表O、S或NR7;
G代表与其所连接的环稠合的环烷基、杂环基、芳基或杂芳基环;
R1代表H或取代或未取代的烷基、链烯基、炔基、芳基、杂芳基、杂环基或环烷基,包括多环基;
R2代表其所连接的环上的0-4个取代基;
R3代表其所连接的环上的0-4个取代基;
R7每次出现时独立地代表H、低级烷基、J-环烷基、J-杂环基、J-芳基、J-杂芳基;
R8每次出现时独立地代表H、低级烷基、环烷基、杂环基、芳基或杂芳基;和
J每次出现时独立地代表具有0-8个单位的链,所述单位选自CK2、NK、O和S,其中K每次出现时独立地代表H或低级烷基。
35.一种治疗或预防基底细胞癌的方法,所述方法包括将足以抑制基底细胞癌发展的量的权利要求34的药用制剂给予患者。
36.权利要求1或17的方法,其中所述细胞具有ptc功能丧失表型、hedgehog功能获得表型或smoothened功能获得表型。
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US30844901P | 2001-07-27 | 2001-07-27 | |
| US60/308,449 | 2001-07-27 | ||
| US33803101P | 2001-11-13 | 2001-11-13 | |
| US60/338,031 | 2001-11-13 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN 200610168841 Division CN101007802A (zh) | 2001-07-27 | 2002-07-29 | Hedgehog信号转导途径介质、其相关组合物以及应用 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN1638765A true CN1638765A (zh) | 2005-07-13 |
Family
ID=26976260
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CNA028186796A Pending CN1638765A (zh) | 2001-07-27 | 2002-07-29 | Hedgehog信号转导途径介质、其相关组合物以及应用 |
Country Status (17)
| Country | Link |
|---|---|
| US (2) | US8354397B2 (zh) |
| EP (1) | EP1482928B1 (zh) |
| JP (1) | JP4658473B2 (zh) |
| KR (1) | KR20040031782A (zh) |
| CN (1) | CN1638765A (zh) |
| AT (1) | ATE443518T1 (zh) |
| AU (1) | AU2002327390B2 (zh) |
| BR (1) | BR0211513A (zh) |
| CA (1) | CA2455100C (zh) |
| DE (1) | DE60233823D1 (zh) |
| EA (1) | EA007339B1 (zh) |
| IL (1) | IL159858A0 (zh) |
| MX (1) | MXPA04000803A (zh) |
| NO (1) | NO20040342L (zh) |
| NZ (1) | NZ530580A (zh) |
| PL (1) | PL366799A1 (zh) |
| WO (1) | WO2003011219A2 (zh) |
Cited By (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN102459233A (zh) * | 2009-06-19 | 2012-05-16 | 伊莱利利公司 | 二取代的酞嗪hedgehog途径拮抗剂 |
| CN102803246A (zh) * | 2009-06-11 | 2012-11-28 | 锡耶纳生物技术股份公司 | Hedgehog途径拮抗剂及其治疗应用 |
| CN101616931B (zh) * | 2006-10-31 | 2013-08-21 | 美国政府卫生与公共服务部 | Smoothened多肽及使用方法 |
| CN103261198A (zh) * | 2010-12-22 | 2013-08-21 | 江苏恒瑞医药股份有限公司 | 2-芳基咪唑并[1, 2-b]哒嗪、2-苯基咪唑并[1, 2-a]吡啶、和2-苯基咪唑并[1, 2-a]吡嗪衍生物 |
| CN104151250A (zh) * | 2014-07-22 | 2014-11-19 | 大连理工大学 | 一类含苯并咪唑基团的二芳基酰胺类化合物及其合成和应用 |
| CN107056723A (zh) * | 2017-04-21 | 2017-08-18 | 云南大学 | 一种具有抑制血管内皮生长因子受体信号传导的化合物 |
| CN115477615A (zh) * | 2022-10-17 | 2022-12-16 | 黄山学院 | N-(3-(苯并咪唑-2-基)苯基)酰胺类化合物及其制备方法和应用 |
Families Citing this family (80)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP4669968B2 (ja) | 1997-02-10 | 2011-04-13 | プレジデント アンド フェローズ オブ ハーバード カレッジ | 造血及び血管生成の調節方法 |
| US6984522B2 (en) | 2000-08-03 | 2006-01-10 | Regents Of The University Of Michigan | Isolation and use of solid tumor stem cells |
| US8044259B2 (en) | 2000-08-03 | 2011-10-25 | The Regents Of The University Of Michigan | Determining the capability of a test compound to affect solid tumor stem cells |
| US7708998B2 (en) | 2000-10-13 | 2010-05-04 | Curis, Inc. | Methods of inhibiting unwanted cell proliferation using hedgehog antagonists |
| CA2425356C (en) | 2000-10-13 | 2015-10-06 | Curis, Inc. | Hedgehog antagonists, methods and uses related thereto |
| TW200304820A (en) * | 2002-03-25 | 2003-10-16 | Avanir Pharmaceuticals | Use of benzimidazole analogs in the treatment of cell proliferation |
| PL211300B1 (pl) | 2002-04-17 | 2012-05-31 | Cytokinetics Inc | Związek i kompozycja zawierająca ten związek |
| CA2483311A1 (en) * | 2002-04-22 | 2003-10-30 | Philip A. Beachy | Modulators of hedgehog signaling pathways, compositions and uses related thereto |
| EP1539727B1 (en) | 2002-07-17 | 2009-02-18 | Cytokinetics, Inc. | Compounds, compositions, and methods for treating cellular proliferative diseases |
| TWI276631B (en) * | 2002-09-12 | 2007-03-21 | Avanir Pharmaceuticals | Phenyl-aza-benzimidazole compounds for modulating IgE and inhibiting cellular proliferation |
| DE602004006852D1 (de) | 2003-04-17 | 2007-07-19 | Janssen Pharmaceutica Nv | 2-phenyl-benzimidazol und 2-phenyl-imidazo-4,5ü-pyridin-derivate als checkpoint-kinase-cds1 (chk2)-hemmer zur behandlung von krebs |
| WO2005030206A1 (en) * | 2003-09-24 | 2005-04-07 | Imclone Systems Incorporated | Aryl-1,3-azole derivatives and methods for inhibiting heparnase activity |
| AU2005231692B2 (en) | 2004-03-26 | 2011-01-27 | Curis, Inc. | RNA interference modulators of Hedgehog signaling and uses thereof |
| ES2362102T3 (es) | 2004-06-30 | 2011-06-28 | Janssen Pharmaceutica Nv | Eteres de bencimidazol e imidazopiridina sustituidos con arilo como agentes anticáncer. |
| KR20200118909A (ko) | 2004-09-02 | 2020-10-16 | 제넨테크, 인크. | 헤지호그 신호전달에 대한 피리딜 억제제 |
| NZ555419A (en) | 2004-11-03 | 2009-07-31 | Curis Inc | Mediators of the hedgehog gene signaling pathways, compositions and uses related thereto |
| WO2006094246A2 (en) * | 2005-03-03 | 2006-09-08 | Sirtris Pharmaceuticals, Inc. | N-arylmethyl benzamide sirtuin modulators |
| AU2006218404A1 (en) * | 2005-03-03 | 2006-09-08 | Sirtris Pharmaceuticals, Inc. | N-phenyl benzamide derivatives as sirtuin modulators |
| WO2006124780A2 (en) * | 2005-05-12 | 2006-11-23 | Kalypsys, Inc. | Ih-benzo [d] imidazole compounds as inhibitors of b-raf kinase |
| US8088928B2 (en) * | 2005-08-04 | 2012-01-03 | Sirtris Pharmaceuticals, Inc. | Sirtuin modulating compounds |
| US7855289B2 (en) | 2005-08-04 | 2010-12-21 | Sirtris Pharmaceuticals, Inc. | Sirtuin modulating compounds |
| JP5203196B2 (ja) | 2005-08-04 | 2013-06-05 | サートリス ファーマシューティカルズ, インコーポレイテッド | サーチュインモジュレーターとしてのオキサゾロピリジン誘導体 |
| US8093401B2 (en) * | 2005-08-04 | 2012-01-10 | Sirtris Pharmaceuticals, Inc. | Sirtuin modulating compounds |
| WO2007053648A2 (en) | 2005-10-31 | 2007-05-10 | The Regents Of The University Of Michigan | Compositions and methods for treating and diagnosing cancer |
| US7625759B2 (en) * | 2005-12-19 | 2009-12-01 | Genentech, Inc. | Method for using BOC/CDO to modulate hedgehog signaling |
| WO2008121102A2 (en) * | 2006-02-21 | 2008-10-09 | The Regents Of The University Of Michigan | Hedgehog signaling pathway antagonist cancer treatment |
| EP2007428A2 (en) | 2006-04-05 | 2008-12-31 | Genentech, Inc. | Method for using boc/cdo to modulate hedgehog signaling |
| US20100029615A1 (en) * | 2006-12-15 | 2010-02-04 | Michael John Munchhof | Benzimidazole derivatives |
| TWI433674B (zh) | 2006-12-28 | 2014-04-11 | Infinity Discovery Inc | 環杷明(cyclopamine)類似物類 |
| WO2008092002A2 (en) | 2007-01-24 | 2008-07-31 | The Regents Of The University Of Michigan | Compositions and methods for treating and diagnosing pancreatic cancer |
| TW200916472A (en) | 2007-06-20 | 2009-04-16 | Sirtris Pharmaceuticals Inc | Sirtuin modulating compounds |
| CL2008001821A1 (es) | 2007-06-20 | 2009-03-13 | Sirtris Pharmaceuticals Inc | Compuestos derivados de imidazo[2,1-b]-tiazol; composicion farmaceutica que comprende a dicho compuesto; y uso del compuesto para el tratamiento de diabetes, sindrome metabolico, resistencia a la insulina, entre otras. |
| CA2690953C (en) | 2007-06-29 | 2012-10-02 | Pfizer Inc. | Benzimidazole derivatives |
| CN101918371A (zh) * | 2007-11-01 | 2010-12-15 | 西特里斯药业公司 | 作为瑟土因调节剂的酰胺衍生物 |
| EA201070579A1 (ru) * | 2007-11-08 | 2010-12-30 | Сертрис Фармасьютикалз, Инк. | Солюбилизированные тиазолопиридины |
| CN101917853B (zh) | 2007-12-27 | 2014-03-19 | 无限药品股份有限公司 | 立体选择性还原的方法 |
| US8193182B2 (en) | 2008-01-04 | 2012-06-05 | Intellikine, Inc. | Substituted isoquinolin-1(2H)-ones, and methods of use thereof |
| FR2930552B1 (fr) | 2008-04-24 | 2012-10-12 | Centre Nat Rech Scient | N-acylthiourees et n-acylurees inhibiteurs de la voie de signalisation des proteines hedgehog |
| WO2010021381A1 (ja) * | 2008-08-22 | 2010-02-25 | 武田薬品工業株式会社 | 縮合複素環誘導体およびその用途 |
| WO2010037715A1 (en) * | 2008-10-01 | 2010-04-08 | Novartis Ag | Smoothened antagonism for the treatment of hedgehog pathway-related disorders |
| SG171835A1 (en) | 2008-12-19 | 2011-07-28 | Sirtris Pharmaceuticals Inc | Thiazolopyridine sirtuin modulating compounds |
| FR2948367A1 (fr) | 2009-07-24 | 2011-01-28 | Centre Nat Rech Scient | Derives d'acyl-guanidines modulateurs de la voie de signalisation des proteines hedgehog |
| WO2011017551A1 (en) | 2009-08-05 | 2011-02-10 | Infinity Pharmaceuticals, Inc. | Enzymatic transamination of cyclopamine analogs |
| PT2470173E (pt) | 2009-08-25 | 2016-06-15 | Abraxis Bioscience Llc | Terapia de combinação com composições nanoparticuladas de taxano e inibidores hedgehog |
| US8604032B2 (en) | 2010-05-21 | 2013-12-10 | Infinity Pharmaceuticals, Inc. | Chemical compounds, compositions and methods for kinase modulation |
| US9394313B2 (en) | 2010-09-14 | 2016-07-19 | Infinity Pharmaceuticals, Inc. | Transfer hydrogenation of cyclopamine analogs |
| CN103298474B (zh) | 2010-11-10 | 2016-06-29 | 无限药品股份有限公司 | 杂环化合物及其用途 |
| US9708299B2 (en) | 2011-01-03 | 2017-07-18 | Genentech, Inc. | Hedgehog antagonists having zinc binding moieties |
| AU2012205669B2 (en) | 2011-01-10 | 2015-08-20 | Infinity Pharmaceuticals Inc. | Processes for preparing isoquinolinones and solid forms of isoquinolinones |
| TWI565709B (zh) | 2011-07-19 | 2017-01-11 | 英菲尼提製藥股份有限公司 | 雜環化合物及其用途 |
| EP2734520B1 (en) | 2011-07-19 | 2016-09-14 | Infinity Pharmaceuticals, Inc. | Heterocyclic compounds and uses thereof |
| AR091790A1 (es) | 2011-08-29 | 2015-03-04 | Infinity Pharmaceuticals Inc | Derivados de isoquinolin-1-ona y sus usos |
| WO2013049332A1 (en) | 2011-09-29 | 2013-04-04 | Infinity Pharmaceuticals, Inc. | Inhibitors of monoacylglycerol lipase and methods of their use |
| US8940742B2 (en) | 2012-04-10 | 2015-01-27 | Infinity Pharmaceuticals, Inc. | Heterocyclic compounds and uses thereof |
| CN103570625A (zh) * | 2012-07-19 | 2014-02-12 | 南京英派药业有限公司 | N-(3-杂芳基芳基)-4-芳基芳基甲酰胺和类似物作为Hedgehog通路抑制剂及其应用 |
| KR102229478B1 (ko) | 2012-11-01 | 2021-03-18 | 인피니티 파마슈티칼스, 인코포레이티드 | Pi3 키나아제 동형단백질 조절인자를 사용하는 암의 치료 |
| WO2014085523A1 (en) | 2012-11-29 | 2014-06-05 | Strasspharma Llc | Methods of modulating follicle stimulating hormone activity |
| WO2014151729A1 (en) | 2013-03-15 | 2014-09-25 | Irm Llc | Compounds and compositions for the treatment of parasitic diseases |
| US9233961B2 (en) | 2013-03-15 | 2016-01-12 | Novartis Ag | Compounds and compositions for the treatment of parasitic diseases |
| US20160024051A1 (en) | 2013-03-15 | 2016-01-28 | Infinity Pharmaceuticals, Inc. | Salts and solid forms of isoquinolinones and composition comprising and methods of using the same |
| US9296754B2 (en) | 2013-03-15 | 2016-03-29 | Novartis Ag | Compounds and compositions for the treatment of parasitic diseases |
| US9192609B2 (en) | 2013-04-17 | 2015-11-24 | Hedgepath Pharmaceuticals, Inc. | Treatment and prognostic monitoring of proliferation disorders using hedgehog pathway inhibitors |
| JP6556702B2 (ja) | 2013-05-30 | 2019-08-07 | インフィニティー ファーマシューティカルズ, インコーポレイテッド | Pi3キナーゼアイソフォームモジュレーターを用いる癌の治療 |
| WO2015036405A1 (en) | 2013-09-10 | 2015-03-19 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Methods for diagnosing and treating basal cell carcinoma |
| AU2014329392B2 (en) | 2013-10-04 | 2018-12-20 | Infinity Pharmaceuticals, Inc. | Heterocyclic compounds and uses thereof |
| WO2015051241A1 (en) | 2013-10-04 | 2015-04-09 | Infinity Pharmaceuticals, Inc. | Heterocyclic compounds and uses thereof |
| US20160244452A1 (en) | 2013-10-21 | 2016-08-25 | Infinity Pharmaceuticals, Inc. | Heterocyclic compounds and uses thereof |
| WO2015073691A1 (en) | 2013-11-14 | 2015-05-21 | The Board Of Trustees Of The Leland Stanford Junior University | Methods for treating cancer by activation of bmp signaling |
| DK3083627T3 (da) | 2013-12-19 | 2019-01-02 | Novartis Ag | [1,2,4]triazol[1,5-a]pyrimidinderivater som protozoiske proteasominhibitorer til behandling af parasitsygdomme, såsom leishmaniasis |
| AU2015231413B2 (en) | 2014-03-19 | 2020-04-23 | Infinity Pharmaceuticals, Inc. | Heterocyclic compounds for use in the treatment of PI3K-gamma mediated disorders |
| US20150320754A1 (en) | 2014-04-16 | 2015-11-12 | Infinity Pharmaceuticals, Inc. | Combination therapies |
| WO2015168079A1 (en) | 2014-04-29 | 2015-11-05 | Infinity Pharmaceuticals, Inc. | Pyrimidine or pyridine derivatives useful as pi3k inhibitors |
| WO2016054491A1 (en) | 2014-10-03 | 2016-04-07 | Infinity Pharmaceuticals, Inc. | Heterocyclic compounds and uses thereof |
| MX2017015681A (es) | 2015-06-04 | 2018-09-11 | Pellepharm Inc | Formulaciones topicas para suministrar compuestos inhibidores de hedgehog y uso de los mismos. |
| US20170231968A1 (en) | 2016-02-11 | 2017-08-17 | PellePharm, Inc. | Method for relief of and treatment of pruritus |
| US10919914B2 (en) | 2016-06-08 | 2021-02-16 | Infinity Pharmaceuticals, Inc. | Heterocyclic compounds and uses thereof |
| MX2018016227A (es) | 2016-06-24 | 2019-07-08 | Infinity Pharmaceuticals Inc | Terapias de combinacion. |
| US10767164B2 (en) | 2017-03-30 | 2020-09-08 | The Research Foundation For The State University Of New York | Microenvironments for self-assembly of islet organoids from stem cells differentiation |
| EP3624798A1 (en) * | 2017-05-18 | 2020-03-25 | Institut National de la Sante et de la Recherche Medicale (INSERM) | Methods and pharmaceutical compositions for the treatment of mast cell diseases |
| CN112511569B (zh) * | 2021-02-07 | 2021-05-11 | 杭州筋斗腾云科技有限公司 | 网络资源访问请求的处理方法、系统及计算机设备 |
Family Cites Families (34)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3164603A (en) * | 1965-01-05 | xnhcox | ||
| DE883284C (de) | 1938-11-27 | 1953-07-16 | Hoechst Ag | Verfahren zur Erzeugung von Azofarbstoffen auf Gebilden aus synthetischen hoehermolekularen Polyamidverbindungen oder auf Faser-gemischen, die Faserstoffe aus den Polyamidverbindungen enthalten |
| US2547307A (en) * | 1948-11-09 | 1951-04-03 | Gen Aniline & Film Corp | Yellow diffusion-fast color formers of the benzimidazole class |
| BE492063A (zh) * | 1948-11-09 | |||
| US2768894A (en) * | 1954-04-30 | 1956-10-30 | Gen Aniline & Film Corp | Photographic element with emulsion layer containing color former and wetting agent |
| DE1079762B (de) * | 1955-09-07 | 1960-04-14 | Bayer Ag | Verfahren zur Herstellung von Kuepenfarbstoffen der Thiazol- und Oxazolreihe |
| US3162642A (en) * | 1960-07-15 | 1964-12-22 | Nat Marking Mach Co | Fluorescent pigments |
| DE1282821B (de) | 1960-07-15 | 1968-11-14 | Natmar Inc | Fluoreszierende Markierungsmittel |
| US5641764A (en) * | 1989-03-31 | 1997-06-24 | Peter Maccallum Institute | Halogenated DNA ligand radiosensitizers for cancer therapy |
| CH685875A5 (fr) | 1991-04-26 | 1995-10-31 | Pierre Baudet | Les N-phényl-benzamides protecteurs contre les effets nocifs de la lumière ultra-violette |
| US5277839A (en) * | 1992-06-03 | 1994-01-11 | Litton Industrial Automation Automated Vehicles | Guidepath material |
| ATE234270T1 (de) | 1992-12-02 | 2003-03-15 | Pfizer | Cathecoldiether als selektive pde iv hemmungsmittel |
| JP3015998B2 (ja) * | 1993-08-31 | 2000-03-06 | キヤノン株式会社 | 液晶性化合物、それを含む液晶組成物、該液晶組成物を用いた液晶素子、液晶装置、並びに表示方法 |
| US5496826A (en) * | 1994-09-02 | 1996-03-05 | Bristol-Myers Squibb Company | Pharmaceutical methods of using heterocyclic derivatives of N-phenylamides |
| US5563143A (en) | 1994-09-21 | 1996-10-08 | Pfizer Inc. | Catechol diether compounds as inhibitors of TNF release |
| US5821258A (en) * | 1994-12-27 | 1998-10-13 | Mitsui Chemicals, Inc. | Phenylbenzimidazole derivatives |
| JP3223090B2 (ja) * | 1994-12-27 | 2001-10-29 | 三井化学株式会社 | フェニルベンズイミダゾール誘導体 |
| GB9503946D0 (en) * | 1995-02-28 | 1995-04-19 | Cancer Res Campaign Tech | Benzazole compounds |
| AU4988997A (en) | 1996-10-23 | 1998-05-15 | Osteoscreen, Inc. | Compositions and methods for treating bone deficit conditions |
| JP2001505585A (ja) | 1996-12-16 | 2001-04-24 | 藤沢薬品工業株式会社 | 新規アミド化合物およびそれらの一酸化窒素シンターゼ阻害剤としての用途 |
| US5994394A (en) * | 1997-03-21 | 1999-11-30 | Industrial Technology Research Institute | Polyheterocyclic compounds |
| US6649631B1 (en) * | 1997-10-23 | 2003-11-18 | The Board Of Regents Of The University Of Texas System | Compositions and methods for treating bone deficit conditions |
| US6046229A (en) * | 1998-01-06 | 2000-04-04 | Industrial Technology Research Institute | Polyaryl antitumor agents |
| US6303645B1 (en) * | 1998-05-22 | 2001-10-16 | Avanir Pharmaceuticals | Benzimidazole derivatives as modulators of IgE |
| US6919366B2 (en) * | 1998-05-22 | 2005-07-19 | Avanir Pharmaceuticals | Benzimidazole derivatives as modulators of IgE |
| CN1721411A (zh) * | 1998-05-22 | 2006-01-18 | 阿文尼尔药品公司 | 作为IgE调节剂的苯并咪唑衍生物 |
| JP2002517396A (ja) | 1998-06-04 | 2002-06-18 | アボット・ラボラトリーズ | 細胞接着阻害抗炎症性化合物 |
| CZ20012006A3 (cs) | 1998-12-18 | 2002-03-13 | Axys Pharmaceuticals, Inc. | Sloučenina a farmaceutický prostředek |
| US6291516B1 (en) * | 1999-01-13 | 2001-09-18 | Curis, Inc. | Regulators of the hedgehog pathway, compositions and uses related thereto |
| ES2234662T3 (es) | 1999-09-16 | 2005-07-01 | Curis, Inc. | Mediadores de rutas de señalizacion hedgehog, composiciones y usos relacionados con los mismos. |
| GB0007934D0 (en) * | 2000-03-31 | 2000-05-17 | Darwin Discovery Ltd | Chemical compounds |
| US6943174B2 (en) * | 2000-06-14 | 2005-09-13 | Warner-Lambert Company | 6,5-Fused bicyclic heterocycles |
| NZ528835A (en) * | 2001-03-12 | 2005-05-27 | Avanir Pharmaceuticals | Benzimidazole compounds for modulating IgE and inhibiting cellular proliferation |
| NZ555419A (en) * | 2004-11-03 | 2009-07-31 | Curis Inc | Mediators of the hedgehog gene signaling pathways, compositions and uses related thereto |
-
2002
- 2002-07-29 EP EP02763383A patent/EP1482928B1/en not_active Expired - Lifetime
- 2002-07-29 EA EA200400080A patent/EA007339B1/ru not_active IP Right Cessation
- 2002-07-29 US US10/484,945 patent/US8354397B2/en not_active Expired - Fee Related
- 2002-07-29 IL IL15985802A patent/IL159858A0/xx unknown
- 2002-07-29 DE DE60233823T patent/DE60233823D1/de not_active Expired - Lifetime
- 2002-07-29 BR BR0211513-1A patent/BR0211513A/pt not_active IP Right Cessation
- 2002-07-29 CA CA2455100A patent/CA2455100C/en not_active Expired - Fee Related
- 2002-07-29 WO PCT/US2002/024073 patent/WO2003011219A2/en active Search and Examination
- 2002-07-29 JP JP2003516451A patent/JP4658473B2/ja not_active Expired - Fee Related
- 2002-07-29 PL PL02366799A patent/PL366799A1/xx not_active Application Discontinuation
- 2002-07-29 KR KR10-2004-7001176A patent/KR20040031782A/ko not_active Application Discontinuation
- 2002-07-29 AT AT02763383T patent/ATE443518T1/de not_active IP Right Cessation
- 2002-07-29 MX MXPA04000803A patent/MXPA04000803A/es not_active Application Discontinuation
- 2002-07-29 AU AU2002327390A patent/AU2002327390B2/en not_active Ceased
- 2002-07-29 NZ NZ530580A patent/NZ530580A/en unknown
- 2002-07-29 CN CNA028186796A patent/CN1638765A/zh active Pending
-
2004
- 2004-01-26 NO NO20040342A patent/NO20040342L/no not_active Application Discontinuation
-
2012
- 2012-12-12 US US13/712,525 patent/US8772275B2/en not_active Expired - Fee Related
Cited By (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN101616931B (zh) * | 2006-10-31 | 2013-08-21 | 美国政府卫生与公共服务部 | Smoothened多肽及使用方法 |
| CN102803246A (zh) * | 2009-06-11 | 2012-11-28 | 锡耶纳生物技术股份公司 | Hedgehog途径拮抗剂及其治疗应用 |
| CN102459233A (zh) * | 2009-06-19 | 2012-05-16 | 伊莱利利公司 | 二取代的酞嗪hedgehog途径拮抗剂 |
| CN102459233B (zh) * | 2009-06-19 | 2014-07-02 | 伊莱利利公司 | 二取代的酞嗪hedgehog途径拮抗剂 |
| CN103261198A (zh) * | 2010-12-22 | 2013-08-21 | 江苏恒瑞医药股份有限公司 | 2-芳基咪唑并[1, 2-b]哒嗪、2-苯基咪唑并[1, 2-a]吡啶、和2-苯基咪唑并[1, 2-a]吡嗪衍生物 |
| CN103261198B (zh) * | 2010-12-22 | 2016-06-08 | 江苏恒瑞医药股份有限公司 | 2-芳基咪唑并[1, 2-b]哒嗪、2-苯基咪唑并[1, 2-a]吡啶、和2-苯基咪唑并[1, 2-a]吡嗪衍生物 |
| CN104151250A (zh) * | 2014-07-22 | 2014-11-19 | 大连理工大学 | 一类含苯并咪唑基团的二芳基酰胺类化合物及其合成和应用 |
| CN104151250B (zh) * | 2014-07-22 | 2016-08-31 | 大连理工大学 | 一类含苯并咪唑基团的二芳基酰胺类化合物及其合成和应用 |
| CN107056723A (zh) * | 2017-04-21 | 2017-08-18 | 云南大学 | 一种具有抑制血管内皮生长因子受体信号传导的化合物 |
| CN115477615A (zh) * | 2022-10-17 | 2022-12-16 | 黄山学院 | N-(3-(苯并咪唑-2-基)苯基)酰胺类化合物及其制备方法和应用 |
| CN115477615B (zh) * | 2022-10-17 | 2024-06-18 | 黄山学院 | N-(3-(苯并咪唑-2-基)苯基)酰胺类化合物及其制备方法和应用 |
Also Published As
| Publication number | Publication date |
|---|---|
| MXPA04000803A (es) | 2004-05-21 |
| KR20040031782A (ko) | 2004-04-13 |
| EP1482928A4 (en) | 2005-10-12 |
| JP4658473B2 (ja) | 2011-03-23 |
| NO20040342L (no) | 2004-03-26 |
| PL366799A1 (en) | 2005-02-07 |
| US20050085519A1 (en) | 2005-04-21 |
| IL159858A0 (en) | 2004-06-20 |
| US8772275B2 (en) | 2014-07-08 |
| EP1482928A2 (en) | 2004-12-08 |
| WO2003011219A2 (en) | 2003-02-13 |
| NZ530580A (en) | 2007-02-23 |
| EA007339B1 (ru) | 2006-08-25 |
| EA200400080A1 (ru) | 2005-02-24 |
| JP2005507860A (ja) | 2005-03-24 |
| CA2455100A1 (en) | 2003-02-13 |
| WO2003011219A3 (en) | 2004-09-23 |
| US8354397B2 (en) | 2013-01-15 |
| DE60233823D1 (de) | 2009-11-05 |
| AU2002327390B2 (en) | 2008-06-26 |
| US20130190350A1 (en) | 2013-07-25 |
| CA2455100C (en) | 2013-05-28 |
| BR0211513A (pt) | 2005-08-30 |
| EP1482928B1 (en) | 2009-09-23 |
| ATE443518T1 (de) | 2009-10-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN1638765A (zh) | Hedgehog信号转导途径介质、其相关组合物以及应用 | |
| JP4898044B2 (ja) | ヘッジホッグシグナル伝達経路のメディエーター、それらと関連する組成物及び利用 | |
| JP4994552B2 (ja) | ヘッジホッグシグナル伝達経路のメディエーター、組成物及びそれらと関連する利用 | |
| CN1578779A (zh) | 细胞增殖的有机小分子调节剂 | |
| US8067608B2 (en) | Hedgehog pathway antagonists | |
| US7652043B2 (en) | WNT pathway antagonists | |
| CN1137125C (zh) | 稠合的1,2,4-噻二嗪衍生物、其制备方法和用途 | |
| US7300929B2 (en) | Mediators of hedgehog signaling pathways, compositions and uses related thereto | |
| CN1215069C (zh) | 调整内皮肽活性的磺酰胺及其衍生物 | |
| CN1149204C (zh) | 1-杂环取代的二芳基胺 | |
| JP2005507860A5 (zh) | ||
| JP2008519044A (ja) | ヘッジホッグ・シグナル伝達経路の伝達物質、調合物、及び、それに関連する使用 | |
| JP2005529876A (ja) | Hedgehogシグナル伝達経路の調節因子、それに関連する組成物および使用 | |
| CN1805743A (zh) | 用作逆转淀粉样变性及其他与之相关疾病的rage拮抗剂 | |
| CN1414965A (zh) | 调整内皮肽活性的磺酰胺及其衍生物 | |
| TW201910338A (zh) | 作為acc抑制劑的化合物及其應用 | |
| CN1956721A (zh) | 用作辣椒素拮抗剂的喹唑啉酮衍生物 | |
| CN1511151A (zh) | 3-喹啉-2(1h)-亚基二氢吲哚-2-酮衍生物 | |
| CN1714076A (zh) | 芳基脲基衍生物及其医药用途 | |
| TW201103914A (en) | Heteroaromatic and aromatic piperazinyl azetidinyl amides as monoacylglycerol lipase inhibitors | |
| WO2005033048A2 (en) | Wnt pathway antagonists | |
| US20020165221A1 (en) | Mediators of hedgehog signaling pathways, compositions and uses related thereto | |
| CN1917897A (zh) | 用于调节cns活性的组合物和方法 | |
| US9688664B2 (en) | Modulators of fatty acid amide hydrolase | |
| CN101007802A (zh) | Hedgehog信号转导途径介质、其相关组合物以及应用 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C02 | Deemed withdrawal of patent application after publication (patent law 2001) | ||
| WD01 | Invention patent application deemed withdrawn after publication |
Open date: 20050713 |