CN1305846C - 脲衍生物 - Google Patents
脲衍生物 Download PDFInfo
- Publication number
- CN1305846C CN1305846C CNB998056928A CN99805692A CN1305846C CN 1305846 C CN1305846 C CN 1305846C CN B998056928 A CNB998056928 A CN B998056928A CN 99805692 A CN99805692 A CN 99805692A CN 1305846 C CN1305846 C CN 1305846C
- Authority
- CN
- China
- Prior art keywords
- compound
- alkyl
- ethyl
- phenyl
- urea groups
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D295/00—Heterocyclic compounds containing polymethylene-imine rings with at least five ring members, 3-azabicyclo [3.2.2] nonane, piperazine, morpholine or thiomorpholine rings, having only hydrogen atoms directly attached to the ring carbon atoms
- C07D295/16—Heterocyclic compounds containing polymethylene-imine rings with at least five ring members, 3-azabicyclo [3.2.2] nonane, piperazine, morpholine or thiomorpholine rings, having only hydrogen atoms directly attached to the ring carbon atoms acylated on ring nitrogen atoms
- C07D295/18—Heterocyclic compounds containing polymethylene-imine rings with at least five ring members, 3-azabicyclo [3.2.2] nonane, piperazine, morpholine or thiomorpholine rings, having only hydrogen atoms directly attached to the ring carbon atoms acylated on ring nitrogen atoms by radicals derived from carboxylic acids, or sulfur or nitrogen analogues thereof
- C07D295/182—Radicals derived from carboxylic acids
- C07D295/185—Radicals derived from carboxylic acids from aliphatic carboxylic acids
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C317/00—Sulfones; Sulfoxides
- C07C317/44—Sulfones; Sulfoxides having sulfone or sulfoxide groups and carboxyl groups bound to the same carbon skeleton
- C07C317/48—Sulfones; Sulfoxides having sulfone or sulfoxide groups and carboxyl groups bound to the same carbon skeleton the carbon skeleton being further substituted by singly-bound nitrogen atoms, not being part of nitro or nitroso groups
- C07C317/50—Sulfones; Sulfoxides having sulfone or sulfoxide groups and carboxyl groups bound to the same carbon skeleton the carbon skeleton being further substituted by singly-bound nitrogen atoms, not being part of nitro or nitroso groups at least one of the nitrogen atoms being part of any of the groups, X being a hetero atom, Y being any atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C323/00—Thiols, sulfides, hydropolysulfides or polysulfides substituted by halogen, oxygen or nitrogen atoms, or by sulfur atoms not being part of thio groups
- C07C323/23—Thiols, sulfides, hydropolysulfides or polysulfides substituted by halogen, oxygen or nitrogen atoms, or by sulfur atoms not being part of thio groups containing thio groups and nitrogen atoms, not being part of nitro or nitroso groups, bound to the same carbon skeleton
- C07C323/39—Thiols, sulfides, hydropolysulfides or polysulfides substituted by halogen, oxygen or nitrogen atoms, or by sulfur atoms not being part of thio groups containing thio groups and nitrogen atoms, not being part of nitro or nitroso groups, bound to the same carbon skeleton at least one of the nitrogen atoms being part of any of the groups, X being a hetero atom, Y being any atom
- C07C323/43—Y being a hetero atom
- C07C323/44—X or Y being nitrogen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C323/00—Thiols, sulfides, hydropolysulfides or polysulfides substituted by halogen, oxygen or nitrogen atoms, or by sulfur atoms not being part of thio groups
- C07C323/50—Thiols, sulfides, hydropolysulfides or polysulfides substituted by halogen, oxygen or nitrogen atoms, or by sulfur atoms not being part of thio groups containing thio groups and carboxyl groups bound to the same carbon skeleton
- C07C323/51—Thiols, sulfides, hydropolysulfides or polysulfides substituted by halogen, oxygen or nitrogen atoms, or by sulfur atoms not being part of thio groups containing thio groups and carboxyl groups bound to the same carbon skeleton having the sulfur atoms of the thio groups bound to acyclic carbon atoms of the carbon skeleton
- C07C323/57—Thiols, sulfides, hydropolysulfides or polysulfides substituted by halogen, oxygen or nitrogen atoms, or by sulfur atoms not being part of thio groups containing thio groups and carboxyl groups bound to the same carbon skeleton having the sulfur atoms of the thio groups bound to acyclic carbon atoms of the carbon skeleton the carbon skeleton being further substituted by nitrogen atoms, not being part of nitro or nitroso groups
- C07C323/58—Thiols, sulfides, hydropolysulfides or polysulfides substituted by halogen, oxygen or nitrogen atoms, or by sulfur atoms not being part of thio groups containing thio groups and carboxyl groups bound to the same carbon skeleton having the sulfur atoms of the thio groups bound to acyclic carbon atoms of the carbon skeleton the carbon skeleton being further substituted by nitrogen atoms, not being part of nitro or nitroso groups with amino groups bound to the carbon skeleton
- C07C323/59—Thiols, sulfides, hydropolysulfides or polysulfides substituted by halogen, oxygen or nitrogen atoms, or by sulfur atoms not being part of thio groups containing thio groups and carboxyl groups bound to the same carbon skeleton having the sulfur atoms of the thio groups bound to acyclic carbon atoms of the carbon skeleton the carbon skeleton being further substituted by nitrogen atoms, not being part of nitro or nitroso groups with amino groups bound to the carbon skeleton with acylated amino groups bound to the carbon skeleton
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C323/00—Thiols, sulfides, hydropolysulfides or polysulfides substituted by halogen, oxygen or nitrogen atoms, or by sulfur atoms not being part of thio groups
- C07C323/50—Thiols, sulfides, hydropolysulfides or polysulfides substituted by halogen, oxygen or nitrogen atoms, or by sulfur atoms not being part of thio groups containing thio groups and carboxyl groups bound to the same carbon skeleton
- C07C323/51—Thiols, sulfides, hydropolysulfides or polysulfides substituted by halogen, oxygen or nitrogen atoms, or by sulfur atoms not being part of thio groups containing thio groups and carboxyl groups bound to the same carbon skeleton having the sulfur atoms of the thio groups bound to acyclic carbon atoms of the carbon skeleton
- C07C323/60—Thiols, sulfides, hydropolysulfides or polysulfides substituted by halogen, oxygen or nitrogen atoms, or by sulfur atoms not being part of thio groups containing thio groups and carboxyl groups bound to the same carbon skeleton having the sulfur atoms of the thio groups bound to acyclic carbon atoms of the carbon skeleton with the carbon atom of at least one of the carboxyl groups bound to nitrogen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C327/00—Thiocarboxylic acids
- C07C327/20—Esters of monothiocarboxylic acids
- C07C327/30—Esters of monothiocarboxylic acids having sulfur atoms of esterified thiocarboxyl groups bound to carbon atoms of hydrocarbon radicals substituted by nitrogen atoms, not being part of nitro or nitroso groups
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C329/00—Thiocarbonic acids; Halides, esters or anhydrides thereof
- C07C329/02—Monothiocarbonic acids; Derivatives thereof
- C07C329/04—Esters of monothiocarbonic acids
- C07C329/06—Esters of monothiocarbonic acids having sulfur atoms of thiocarbonic groups bound to acyclic carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D333/00—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom
- C07D333/02—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom not condensed with other rings
- C07D333/04—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom not condensed with other rings not substituted on the ring sulphur atom
- C07D333/26—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom not condensed with other rings not substituted on the ring sulphur atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D333/30—Hetero atoms other than halogen
- C07D333/32—Oxygen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2601/00—Systems containing only non-condensed rings
- C07C2601/02—Systems containing only non-condensed rings with a three-membered ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2601/00—Systems containing only non-condensed rings
- C07C2601/04—Systems containing only non-condensed rings with a four-membered ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2601/00—Systems containing only non-condensed rings
- C07C2601/06—Systems containing only non-condensed rings with a five-membered ring
- C07C2601/08—Systems containing only non-condensed rings with a five-membered ring the ring being saturated
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2601/00—Systems containing only non-condensed rings
- C07C2601/12—Systems containing only non-condensed rings with a six-membered ring
- C07C2601/14—The ring being saturated
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2601/00—Systems containing only non-condensed rings
- C07C2601/18—Systems containing only non-condensed rings with a ring being at least seven-membered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2603/00—Systems containing at least three condensed rings
- C07C2603/56—Ring systems containing bridged rings
- C07C2603/58—Ring systems containing bridged rings containing three rings
- C07C2603/70—Ring systems containing bridged rings containing three rings containing only six-membered rings
- C07C2603/74—Adamantanes
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
本发明的目的是提供以脲结构作为基本结构、并且在侧链中具有硫原子和酰胺键的化合物,并发现它们的药理学作用,特别是对TNF-α产生的抑制作用。本发明提供了由下列通式[I]代表的化合物,其中R1是H、烷基、芳基、RA-CO-、RC-S-或式[II]基团;R2、R3和R4是H、烷基、烯基、环烷基、环烯基或芳基;R5和R6是H、烷基、烯基、环烷基、环烯基或芳基;R5和R6可以一起形成一个非芳族杂环;R7是H、烷基、环烷基、羟基、巯基、苯基、RB-O-、RC-S-、RD-COS-、RE-OCO-、RF-N(RG)-或-CONHOH;A1和A2是亚烷基。
Description
技术领域
本发明涉及新颖的脲衍生物,它们对TNF-α的产生具有抑制作用,可用作不同疾病的治疗剂,特别是用作自体免疫疾病、例如类风湿性关节炎的治疗剂,本发明还涉及可用作其合成中间体的新化合物。
背景技术
过去人们发现TNF-α(肿瘤坏死因子-α)是一种诱发肿瘤部位出血性坏死的因子,现在人们认识到它是一种通过炎症广泛参与生物防御-免疫机制的细胞素。不过,TNF-α的过长时间和过度产生导致组织病症,是一种引发和加重不同疾病的因素。因此,据报道,在TNF-α过度产生的病患中抑制TNF-α的过度产生是很重要的(Yamazaki《临床免疫学》
27,1270,1995)。上述文献引用了很多疾病作为有TNF-α参与的疾病实例,例如关节风湿病、全身性红斑狼疮(SLE)、恶病质、急性传染病、变态反应、发热、贫血和糖尿病。
据报道,TNF-α在类风湿性关节炎和克罗恩氏病危象中起到重要作用,这些是自体免疫疾病(Andreas Eigler等《今日免疫学》
18,487,1997)。
TNF-α已知参与不同疾病以及自体免疫疾病,例如类风湿性关节炎、克罗恩氏病和全身性红斑狼疮,正如上述文献所报道的。抑制其产生或抑制其作用的化合物预期可用于不同疾病的治疗,并且已经开展了多项研究。上述文献介绍了这些药物研究的概况(Yamazaki《临床免疫学》
27,1270,1995,Andreas Eigler等《今日免疫学》
18,487,1997)。最近,人们发现,一种参与TNF-α分泌的蛋白酶是金属蛋白酶,金属蛋白酶抑制剂对TNF-α产生的抑制作用研究也见诸报道(PCT 508115/1997的公开日文译本)。
如上所述,人们已经研究了对TNF-α产生具有抑制作用的不同药物。不过,把注意力集中在药物的化学结构上就会发现,根本没有具有本发明化合物的化学结构特征的药物是已知的。本发明化合物的化学结构特征是化合物以脲结构作为基本结构,并且在侧链中具有硫原子和酰胺键。这类以脲结构作为基本骨架的药物研究几乎还没有报道。而且,在侧链中具有硫原子的药物实际上迄今还没有报道。
如上所述,由于以脲结构作为基本结构并且在侧链中具有硫原子和酰胺键的化合物实际上还没有报道,这类化合物的合成研究和化合物的药理学作用研究、特别是TNF-α产生的抑制作用研究是非常令人感兴趣的课题。
发明的公开
本发明人把注意力集中在几乎没有研究过的药物的脲结构上,对新颖的脲衍生物的合成进行了研究,其中向其一个侧链引入硫,向其另一个侧链引入酰胺键,成功地制备了很多新颖的化合物。本发明人进一步研究了化合物的药理学作用,发现这些新颖的化合物对TNF-α产生具有优异的抑制作用。在制备上述新颖的脲衍生物的研究过程中,本发明人还成功地制备了可用作该衍生物合成中间体的新化合物。
本发明涉及由下列通式[I]代表的化合物及其盐(就没有附带条件而言,以下称之为“本发明化合物”)、含有其作为活性成分的药物组合物和由通式[III]代表的化合物,该化合物[III]可用作本发明化合物及其盐的合成中间体(就没有附带条件而言,以下称之为“本发明的合成中间体”)。
[其中
R1是氢、低级烷基、芳基、RA-CO-、RC-S-或下式[II]基团
R2、R3和R4相同或不同,是氢、低级烷基、低级烯基、环烷基、环烯基或芳基。当R4是低级烷基时,该低级烷基的末端碳可以与该烷基所键合的碳结合形成一个环烷基环。
R5和R6相同或不同,是氢、低级烷基、低级烯基、环烷基、环烯基或芳基。当R5和R6都是低级烷基时,它们可以彼此结合形成一个环中具有氮和/或氧的非芳族杂环,该杂环可以被低级烷基、低级烯基、环烷基、环烯基、芳基或RA-CO-取代。
R7是氢、低级烷基、环烷基、羟基、巯基、苯基、RB-O-、RC-S-、RD-COS-、RE-OCO-、RF-N(RG)-或-CONHOH。R7可以与毗邻A1的硫结合形成一个环中含有硫的非芳族杂环,该环可以在环中进一步具有羰基。
A1是低级亚烷基。
A2是低级亚烷基。
每个如上定义的低级烷基可以被下列基团取代:羟基、环中具有氮和/或氧的非芳族杂环、环烷基、环烯基、金刚烷基、芳基、邻苯二甲酰亚氨基、可以被低级烷磺酰基或芳磺酰基取代的胍基、RA-CO-、RB-O-、RC-S-、RD-COS-、RE-OCO-、RF-N(RG)-、RH-N(RJ)CO-、RK-CONH-或-CONHOH。
每个如上定义的低级烯基可以被羟基、低级烷基、低级烷氧基、环烷基、环烯基或芳基取代。
每个如上定义的环烷基可以被低级烷基、羟基、氧代或RE-OCO-取代。
每个如上定义的芳基可以被低级烷基、羟基、低级烷氧基、低级烷酰氧基、卤素、硝基、芳基、低级烷磺酰基、芳磺酰基、RE-OCO-、RF-N(RG)-或RK-CONH-取代。
如上定义的环中具有氮和/或氧的非芳族杂环可以被低级烷基、环烷基、芳基或RA-CO-取代,该低级烷基可以被羟基、环烷基、环烯基、芳基、RA-CO-、RB-O-、RE-OCO-或RF-N(RG)-取代。
RA是低级烷基、卤代低级烷基、芳基、低级烷氧基、芳基-低级烷氧基或RF-N(RG)-。RB是低级烷基或芳基。RC是氢、低级烷基或芳基。RD是低级烷基或芳基。RE是氢、低级烷基或芳基。RF和RG相同或不同,是氢、低级烷基、环烷基或芳基。RH和RJ相同或不同,是氢、低级烷基、环烷基或芳基。RK是低级烷基、低级烷氧基或芳基。以下适用相同的定义]
[适用相同的定义,例外的情况是R7与毗邻A1的硫形成环中含有硫的非芳族杂环。以下,合成中间体中所用的R7定义与上述相同。]
以下详细描述如上定义的基团。
低级烷基是具有一至八个碳原子的直链或支链烷基,例如甲基、乙基、丙基、丁基、己基、异丙基、异丁基、异戊基、异己基、叔丁基或3,3-二甲基丁基。
低级烯基是具有二至八个碳原子的直链或支链烯基,例如乙烯基、烯丙基、3-丁烯基、5-己烯基或异丙烯基。
环烷基是具有三至八个碳原子的环烷基,例如环丙基、环丁基、环戊基、环己基或环庚基。
环烯基是具有三至八个碳原子的环烯基,例如环丙烯基、环丁烯基、环戊烯基、环己烯基或环庚烯基。
低级烷氧基是具有一至八个碳原子的直链或支链烷氧基,例如甲氧基、乙氧基、丙氧基、丁氧基、己氧基、异丙氧基或叔丁氧基。
卤素是氟、氯、溴或碘。
低级亚烷基是具有一至八个碳原子的直链或支链亚烷基,例如亚甲基、亚乙基、三亚甲基、四亚甲基、五亚甲基、六亚甲基、甲基亚甲基、亚丙基、乙基亚乙基、二甲基亚乙基、丙基亚乙基、异丙基亚乙基或甲基三亚甲基。
芳基是单环的或稠合多环的芳族烃基,例如苯基或萘基,或者是杂环芳基,例如吡啶基、噻吩基或咪唑基。
环中具有氮和/或氧的非芳族杂环是环中具有一个或两个氮原子的非芳族杂环,例如哌啶、哌嗪、吡咯啉或高哌嗪(homopiperazine),或者是环中具有氮和氧的非芳族杂环,例如吗啉。
环中含有硫的非芳族杂环是环中含有一个或两个硫原子的非芳族杂环,例如二硫戊环,或者是环中进一步具有酮的非芳族杂环,例如硫内酯(硫代内酯)。
本发明中的盐指任意药学上可接受的盐,其实例有无机酸盐,无机酸例如氢氯酸、硝酸或硫酸;有机酸盐,有机酸例如乙酸、富马酸、马来酸、柠檬酸、酒石酸、二酰基酒石酸、苯甲酸或取代的苯甲酸;碱金属或碱土金属盐,例如钠、钾或钙盐,等等。当几何异构体或旋光异构体存在于本发明化合物或本发明中间体中时,这些异构体也包括在本发明的范围之内。本发明化合物或本发明中间体可以是加成盐的形式,例如水合物和有机溶剂化物。
优选的本发明化合物如下。
化合物及其盐,其中通式[I]中的基团是由选自下列1)至8)的任意一个或由1)至8)组成的任意组合所定义的。
1)R1选自氢、低级烷基、苯基、RA-CO-、RC-S-和下式[II]基团
RA选自低级烷基、低级烷氧基、苯基、吡啶基、苯基-低级烷氧基和RF-N(RG)-,RC选自低级烷基和苯基,RF和RG相同或不同,选自氢、低级烷基和苯基,每个低级烷基可以被苯基或低级烷氧羰基取代,每个苯基可以被选自低级烷基、羟基、低级烷氧基、卤素和硝基的基团取代;
2)R2、R3和R4相同或不同,选自氢、低级烷基、低级烯基、环烷基、环烯基、苯基和萘基,该低级烷基可以被选自下列的基团取代:羟基、环烷基、环烯基、金刚烷基、苯基、萘基、吡啶基、噻吩基、咪唑基、可以被低级烷磺酰基或苯磺酰基取代的胍基、RB-O-、RC-S-、RD-COS-、RE-OCO-、RF-N(RG)-和RK-CONH-,该低级烯基可以被低级烷基、苯基或萘基取代,RB选自低级烷基和苯基,RC选自氢、低级烷基和苯基,RD选自低级烷基和苯基,RE选自氢、低级烷基和苯基,RF和RG相同或不同,选自氢、低级烷基、环烷基和苯基,RK选自低级烷基、低级烷氧基和苯基,每个苯基可以被选自低级烷基、羟基、低级烷氧基、低级烷酰氧基、卤素、硝基、氨基、低级烷氨基、低级烷酰氨基、低级烷磺酰基、苯磺酰基、苯基和RE-OCO-的基团取代,每个环烷基可以被低级烷基、羟基、氧代或RE-OCO-取代;
3)R5和R6相同或不同,选自氢、低级烷基、低级烯基、环烷基、环烯基、苯基、萘基和吡啶基,该低级烷基可以被选自羟基、低级烷氧基、环烷基、环烯基、苯基、萘基、吡啶基、噻吩基、咪唑基、邻苯二甲酰亚氨基、哌啶基、哌嗪基、吗啉基、RE-OCO-、RF-N(RG)-、RH-N(RJ)CO-、RK-CONH-和-CONHOH的基团取代,该哌啶基、哌嗪基或吗啉基可以被低级烷基、苯基或萘基取代,RE选自氢、低级烷基和苯基,RF和RG相同或不同,选自氢、低级烷基、环烷基和苯基,RH和RJ相同或不同,选自氢、低级烷基、环烷基和苯基,RK选自低级烷基、低级烷氧基和苯基,每个苯基可以被选自低级烷基、羟基、低级烷氧基、低级烷酰氧基、卤素、硝基、氨基、低级烷氨基、低级烷酰氨基、低级烷磺酰基、苯磺酰基、苯基和RE-OCO-的基团取代,每个环烷基可以被选自低级烷基、羟基、氧代或RE-OCO-的基团取代;
4)R5和R6彼此结合形成一个非芳族杂环,选自吗啉环、哌啶环、哌嗪环、吡咯啉环和高哌嗪环,该非芳族杂环可以被低级烷基、低级烯基、环烷基、环烯基、苯基、萘基或RA-CO-取代,该低级烷基可以被羟基、苯基、萘基、RB-O-、RE-OCO-、RF-N(RG)-或-CONHOH取代,RA是低级烷基、卤代低级烷基、低级烷氧基或苯基,RB是低级烷基或苯基,RE是氢、低级烷基或苯基,RF和RG相同或不同,是氢、低级烷基、环烷基或苯基,每个苯基可以被选自低级烷基、羟基、低级烷氧基、低级烷酰氧基、卤素、硝基、氨基、低级烷氨基、低级烷酰氨基、低级烷磺酰基、苯磺酰基、苯基和RE-OCO-的基团取代,每个环烷基可以被选自低级烷基、羟基、氧代或RE-OCO-的基团取代;
5)R7选自氢、低级烷基、环烷基、羟基、羧基、巯基、苯基、RB-O-、RC-S-、RD-COS-、RF-OCO-、RF-N(RG)-和-CONHOH,该低级烷基可以被选自环烷基、羟基、羧基、巯基、苯基、RB-O-、RC-S-、RD-COS-、RE-OCO-、RF-N(RG)-和-CONHOH的基团取代,RB是低级烷基或苯基,RC是低级烷基或苯基,RD是低级烷基或苯基,RE是低级烷基或苯基,RF和RG相同或不同,是氢、低级烷基、环烷基或苯基,每个苯基可以被选自低级烷基、羟基、低级烷氧基、低级烷酰氧基、卤素、硝基、氨基、低级烷氨基、低级烷酰氨基、低级烷磺酰基、苯磺酰基、苯基和RE-OCO-的基团取代,每个环烷基可以被低级烷基、羟基、氧代或RE-OCO-取代;
6)R7与毗邻A1的硫结合形成一个非芳族杂环,选自硫内酯环和二硫戊环;
7)A1是低级亚烷基;和
8)A2是低级亚烷基。
更优选的本发明化合物实例如下。
化合物及其盐,其中通式[I]中的基团是由选自下列1)至11)的任意一个或由1)至11)组成的任意组合所定义的。
1)R1选自氢、低级烷基、苯基、RA-CO-、RC-S-和下式[II]基团,该低级烷基可以被苯基或低级烷氧羰基取代,
RA选自低级烷基、低级烷氧基、苯基、吡啶基、苯基-低级烷氧基和RF-N(RG)-,RC是苯基,RF是低级烷基,RG是氢;
2)R2选自氢、低级烷基、低级烯基和苯基,该低级烷基可以被选自低级烷氧基、环烷基、环烯基、金刚烷基、苯基、萘基、吡啶基和RB-O-的基团取代,该苯基可以被选自低级烷基、羟基、低级烷氧基、低级烷酰氧基、卤素、硝基和苯基的基团取代,该低级烯基可以被苯基取代,RB是苯基;
3)R3选自氢和低级烷基,该低级烷基可以被苯基取代;
4)R4选自氢、低级烷基和苯基,该低级烷基可以被选自羟基、环烷基、苯基、萘基、吡啶基、噻吩基、咪唑基、甲苯磺酰胍基、RC-S-、RD-COS-、RF-N(RG)-和RK-CONH-的基团取代,每个苯基可以被选自羟基、低级烷氧基、卤素、硝基、低级烷酰氨基、苯磺酰基和苯基的基团取代,RC选自氢、低级烷基和苯基,RD选自低级烷基和苯基,RF和RG是氢,RK是低级烷氧基。当R4是低级烷基时,该低级烷基的末端碳可以与该烷基所键合的碳结合形成一个环烷基环;
5)R5选自氢和低级烷基;
6)R6选自低级烷基和吡啶基,该低级烷基可以被选自吡啶基、咪唑基、邻苯二甲酰亚氨基、哌啶基、哌嗪基、吗啉基、RE-OCO-、RF-N(RG)-、RH-N(RJ)CO-和RK-CONH-的基团取代,RE选自氢和低级烷基,RF和RG相同或不同,选自氢、低级烷基、环烷基和苯基,RH和RJ相同或不同,选自氢和低级烷基,RK是低级烷氧基,该哌嗪基可以被低级烷基取代;
7)R5和R6彼此结合形成一个非芳族杂环,选自吗啉环、哌啶环、哌嗪环、吡咯啉环和高哌嗪环,该哌嗪环或高哌嗪环可以被低级烷基、环烷基、苯基或RA-CO-取代,该低级烷基可以被羟基、苯基或RE-OCO-取代,RA是低级烷基、低级烷氧基或卤代低级烷基,RE是氢或低级烷基;
8)R7选自氢、低级烷基、羟基、巯基、苯基、RB-O-、RC-S-、RD-COS-、RE-OCO-、-CONHOH和RF-N(RG)-,该低级烷基可以被选自羟基、巯基、苯基、RB-O-、RC-S-、RD-COS-、RE-OCO-、-CONHOH和RF-N(RG)-的基团取代,RB是苯基,RC是苯基,RD是低级烷基或苯基,RE是氢或低级烷基,RF和RG是低级烷基;
9)R7与毗邻A1的硫结合形成一个非芳族杂环,选自硫内酯环和二硫戊环;
10)A1是低级亚烷基;和
11)A2是低级亚烷基。
进一步优选的本发明化合物实例如下。
化合物及其盐,其中通式[I]中的基团是由选自下列1)至10)的任意一个或由1)至10)组成的任意组合所定义的。
1)R1选自氢、RA-CO-和下式[II]基团
RA选自低级烷基、苯基和吡啶基;
2)R2是低级烷基或苯基,该低级烷基可以被选自环烷基、环烯基、金刚烷基、苯基和苯氧基的基团取代,该苯基可以被卤素取代;
3)R3是氢;
4)R4是氢或低级烷基,该低级烷基可以被选自苯基、萘基、低级烷硫基和RD-COS-的基团取代,RD是低级烷基,该苯基可以被选自羟基、低级烷氧基、卤素、硝基和苯基的基团取代;
5)R5是氢;
6)R6是低级烷基,该低级烷基可以被选自吡啶基、哌啶基、哌嗪基和RF-N(RG)-的基团取代,RF和RG相同或不同,选自氢、低级烷基和环烷基,该哌嗪基可以被低级烷基取代;
7)R5和R6彼此结合形成一个非芳族杂环,选自哌啶环、吗啉环和哌嗪环,该哌嗪环可以被低级烷基取代;
8)R7是氢;
9)A1是低级亚烷基;和
10)A2是低级亚烷基。
最优选的本发明化合物实例如下。
化合物及其盐,其中通式[I]中的基团是由选自下列1)至10)的任意一个或由1)至10)组成的任意组合所定义的。
1)R1选自乙酰基、苯甲酰基和下式[II]基团
2)R2选自2-环己基乙基、2-环戊基乙基、2-(1-金刚烷基)乙基、2-(环己烯-1-基)乙基、苯乙基和3-(4-氟苯基)丙基;
3)R3是氢;
4)R4选自甲基、乙酰硫基甲基、苄基、2-萘甲基、4-氟苄基、4-氯苄基、4-联苯甲基、4-硝基苄基、3-硝基-4-联苯甲基、4-甲氧基苄基和4-异丙氧基苄基;
5)R5是氢;
6)R6选自2-(二甲氨基)乙基、2-(二乙氨基)乙基、2-(二异丙氨基)乙基、N-甲基-2-(环己氨基)乙基、2-(2-吡啶基)乙基、2-(1-哌啶基)乙基和2-(4-甲基哌嗪基)乙基;
7)R5和R6彼此结合形成一个选自1-哌啶基、4-吗啉基和4-甲基-1-哌嗪基的基团;
8)R7是氢;
9)A1是亚乙基;
10)A2是亚甲基。
最优选的本发明化合物实例是下列化合物及其盐。
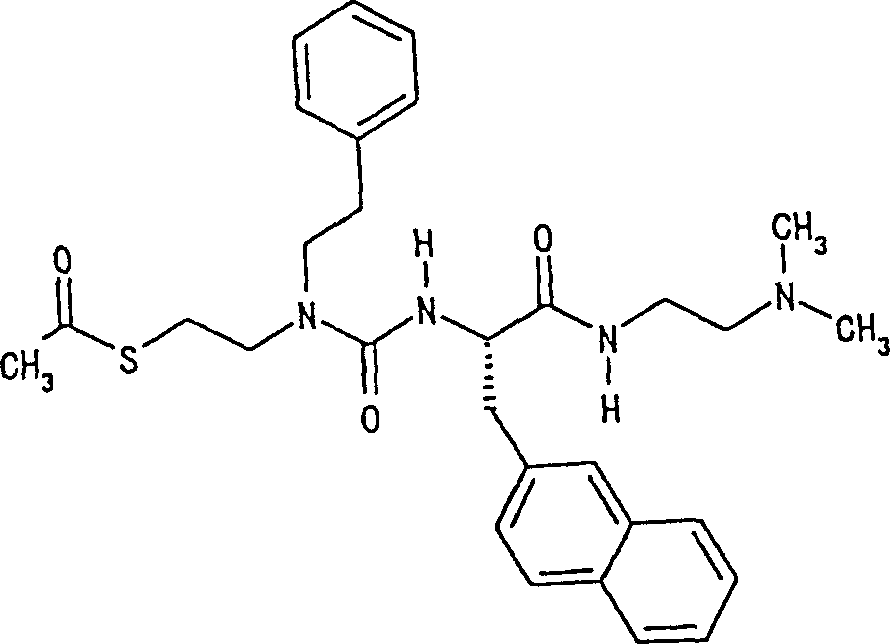
1)(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-[2-(二甲氨基)乙基]-3-(2-萘基)丙酰胺
2)(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-[2-(N-甲基环己氨基)乙基]-3-(4-硝基苯基)丙酰胺
3)(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-[2-(二乙氨基)乙基]-3-(4-硝基苯基)丙酰胺
4)(2S)-2-[3-[2-(苯甲酰硫基)乙基]-3-苯乙基脲基]-N-[2-(二甲氨基)乙基]-3-(4-硝基苯基)丙酰胺
5)(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-(4-联苯基)-N-[2-(二甲氨基)乙基]丙酰胺
6)(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-[2-(二异丙氨基)乙基]-3-(4-硝基苯基)丙酰胺
7)(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-[2-(二甲氨基)乙基]-3-(4-甲氧基苯基)丙酰胺
8)(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-[2-(二甲氨基)乙基]-3-(4-硝基苯基)丙酰胺
9)(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-[2-(二甲氨基)乙基]-3-(2-硝基-4-联苯基)丙酰胺
10)(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-(4-氯苯基)-N-[2-(二甲氨基)乙基]丙酰胺
11)(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-(4-硝基苯基)-N-[2-(2-吡啶基)乙基]丙酰胺
12)(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-[3-(1-咪唑基)丙基]-3-(4-硝基苯基)丙酰胺
13)(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-[2-(二甲氨基)乙基]-3-(4-氟苯基)丙酰胺
14)(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-(4-硝基苯基)-N-[2-(哌啶子基)乙基]丙酰胺
15)(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-[2-(二甲氨基)乙基]-3-(4-异丙氧基苯基)丙酰胺
16)(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-[2-(4-甲基哌嗪-1-基)乙基]-3-(4-硝基苯基)丙酰胺
17)1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环己基乙基)脲基]丙酰基]-4-甲基哌嗪
18)1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环戊基乙基)脲基]丙酰基]-4-甲基哌嗪
19)1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-[2-(环己烯-1-基)乙基]脲基]丙酰基]-4-甲基哌嗪
20)1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-[3-(4-氟苯基)丙基]脲基]丙酰基]-4-甲基哌嗪
21)-[(2R)-3-(乙酰硫基)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]丙酰基]-4-甲基哌嗪
22)4-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-环己基乙基(henethyl)脲基]丙酰基]吗啉
23)1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环己基乙基)脲基]丙酰基]哌啶
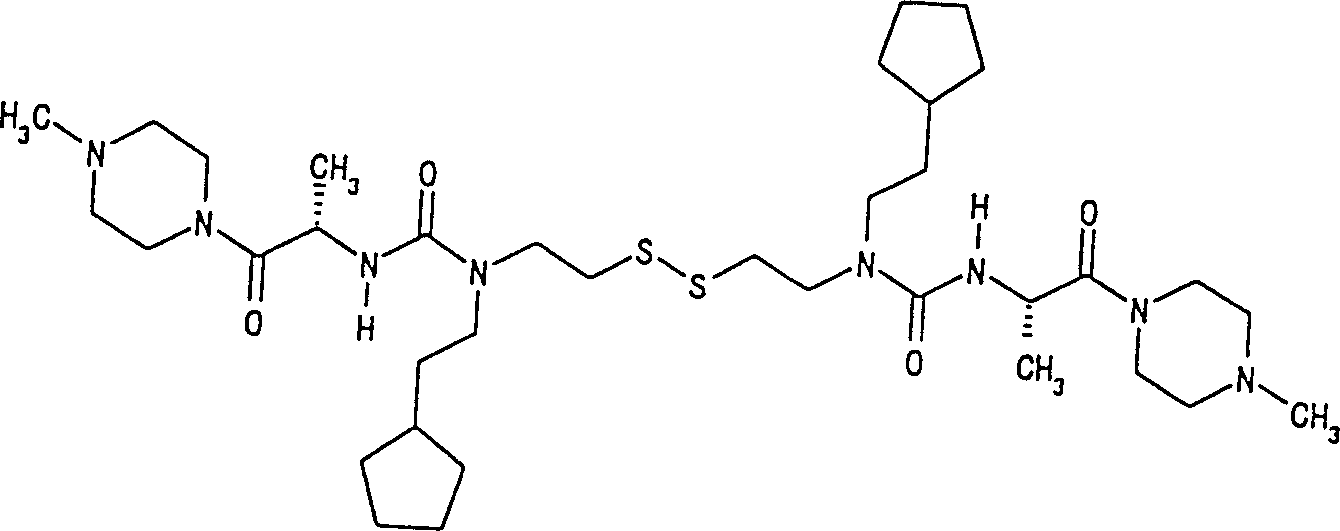
24)1,1’-二甲基-4,4’-[(2S,2’S)-2,2’-[3,3’-二苯乙基-3,3’-(2,2’-二硫基二乙基)二脲基]-3,3’-二苯基二丙酰基]二哌嗪
25)1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-[2-(1-金刚烷基)乙基]脲基]丙酰基]-4-甲基哌嗪
26)4-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-[2-(1-金刚烷基)乙基]脲基]丙酰基]吗啉
27)1,1’-二甲基-4,4’-[(2S,2’S)-2,2’-[3,3’-二苯乙基-3,3’-[2,2’-(二硫基)二乙基]二脲基]二丙酰基]二哌嗪
28)1,1’-[(2S,2’S)-2,2’-[3,3’-双(2-环己基乙基)-3,3’-[2,2’-(二硫基)二乙基]二脲基]二丙酰基]-4,4’-二甲基二哌嗪
29)1,1’-[(2S,2’S)-2,2’-[3,3’-双[2-(1-金刚烷基)乙基]-3,3’-[2,2’-(二硫基)二乙基]二脲基]二丙酰基]-4,4’-二甲基二哌嗪
30)1,1’-[(2S,2’S)-2,2’-[3,3’-双(2-环戊基乙基)-3,3’-[2,2’-(二硫基)二乙基]二脲基]二丙酰基]-4,4’-二甲基二哌嗪
由于本发明的合成中间体是相应于本发明化合物的结构加以选择的,本发明的合成中间体的优选实例也是相应于本发明化合物的优选实例加以选择的。
本发明化合物的典型合成路线流程显示如下。
本发明化合物[I]可以通过不同合成路线合成,例如上述反应路线流程所示。这些合成方法表示为下列每个路线。不过,这些路线举例说明了典型路线,不表示全部的方法。详细合成方法描述在后面的实施例中。
路线A)[IV]→[VII]→[III]→[I]
路线B)[IV]→[X]→[III]→[I]
路线C)[IV]→[VII]→[XI]→[I]
路线D)[IV]→[XI]→[I]
路线E)[IV]→[X]→[I]
这些路线的合成方法详细描述如下。
路线A)
[其中Ra是氢、低级烷基、苯基或苄基。以下适用相同的定义。]
酯衍生物[IV]与氨基醇衍生物[V]在缩合剂(例如1,1’-羰基二咪唑[VI])和碱的存在下反应,转化为脲衍生物[VII],所得脲衍生物与胺衍生物[VIII]反应,得到由式[III]代表的化合物(本发明的合成中间体)。然后,所得化合物[III]与硫醇衍生物[IX]按照Mitsunobu反应缩合,得到本发明化合物[I]。
路线B)
酯衍生物[IV]与胺衍生物[VIII]反应,转化为酰胺衍生物[X],所得酰胺衍生物与氨基醇衍生物[V]在缩合剂(例如1,1’-羰基二咪唑[VI])和碱的存在下反应,得到由式[III]代表的化合物(本发明的合成中间体)。然后,与路线A)相同方式得到本发明化合物[I]。
路线C)
按照路线A)方法得到的脲衍生物[VII]与硫醇衍生物[IX]按照Mitsunobu反应缩合,得到由式[XI]代表的化合物。然后,所得化合物[XI]与胺衍生物[VIII]按照常规方法缩合,得到本发明化合物[I]。
路线D)
酯衍生物[IV]与氨基硫醇衍生物[XII]在缩合剂(例如1,1’-羰基二咪唑[VI])和碱的存在下反应,得到化合物[XI]。然后,所得化合物[XI]与胺衍生物[VIII]按照常规方法缩合,得到本发明化合物[I]。
路线E)
按照路线B)方法得到的酰胺衍生物[X]与氨基硫醇衍生物[XII]在缩合剂(例如1,1’-羰基二咪唑[VI])和碱的存在下反应,得到本发明化合物[I]。
在上述合成方法中,当反应物在其分子中具有羟基、硫醇基或氨基时,这些基团在必要时可以用适当的保护基团加以保护,这些保护基团也可以在反应后按照常规方法除去。当反应物在其分子中具有羧基时,羧基在必要时可以酯化,酯也可以通过水解或酸解转化为羧酸。
在本发明化合物中,当R7与毗邻A1的硫结合形成一个硫内酯环或二硫戊环时,本发明化合物也可以按照下列不同于上述路线的方法合成。
当式[I]中的R7是RE-OCO-、R1是氢时,硫内酯环也可以通过缩合这些基团加以合成。
当式[I]中的R7是巯基、R1是氢时,二硫戊环可以通过结合这些基团加以合成。也就是说,二硫戊环是通过形成分子内二硫化物加以合成的。
上述方法所得化合物可以按照常规方法转化为上述盐。
本发明化合物的化学结构特征是化合物以脲结构作为基本结构,并且在侧链中具有硫原子和酰胺键。这类以脲结构作为基本骨架的药物研究几乎还没有报道。而且,在侧链中具有硫原子的药物实际上迄今还没有报道。限于对TNF-α产生具有抑制作用的药物,已知根本没有化学结构类似于本发明化合物的药物,该药物正是本发明的一个目的。
本发明人恰恰研究了以脲结构作为基本结构的化合物的合成,该化合物迄今几乎没有被研究过,制备了很多新颖的化合物,发现这些新颖的化合物对TNF-α产生具有优异的抑制作用,从而完成了本发明。本发明人还发现另一些新颖的化合物,它们在本发明化合物合成研究过程中可用作本发明化合物的合成中间体。本发明化合物在两种状态下都表现出上述作用,一是侧链中的硫原子与不同基团(式[I]中由R1所代表,除了氢以外)结合,二是该硫原子采取SH的形式(式[I]中的R1是氢)。当R1被用作SH基团的保护基团时,该保护基团有时通过水解等作用除去,所得SH形式表现出上述作用。当本发明化合物在其分子中含有羧酸酯时,本发明化合物即使在酯的状态下也表现出上述作用。酯键有时受到水解等作用,所得羧酸形式表现出上述作用。当本发明化合物含有可转化为游离羟基或氨基的基团时,本发明化合物可以在这些基团用适当的保护基团加以保护的状态下给药。本发明化合物可以在这些保护基团被除去的状态下给药。
为了研究本发明化合物的实用性,检查了本发明化合物对TNF-α产生的抑制作用。具体细节将描述在下列药理学试验中。通过研究体外或体内对由脂多糖(LPS)的刺激作用导致的TNF-α释放的抑制作用,本发明化合物对TNF-α产生表现出优异的抑制作用。
已知TNF-α产生与自体免疫疾病危象密切相关,例如类风湿性关节炎、克罗恩氏病、全身性红斑狼疮、恶病质、急性传染病、变态反应、发热、贫血、糖尿病等。象本发明化合物一样抑制其产生的化合物预期可用于这些不同疾病的治疗。
本发明化合物可以口服或肠胃外给药。剂型的实例有片剂、胶囊、颗粒剂、粉末、注射剂等。本发明化合物可以按照常规方法配制成制剂。例如,片剂、胶囊、颗粒剂和粉末等口服制剂可以如下制备:任选地加入稀释剂,例如乳糖、晶性纤维素、淀粉和植物油;润滑剂,例如硬脂酸镁和滑石;粘合剂,例如羟丙基纤维素和聚乙烯吡咯烷酮;崩解剂,例如羧甲基纤维素钙或低取代的羟丙基甲基纤维素;包衣剂,例如羟丙基甲基纤维素、聚乙二醇(macrogol)或硅氧烷树脂;或成膜剂,例如明胶膜。
本发明化合物的剂量可以根据症状、年龄、剂型等加以适当选择。在口服制剂的情况下,本发明化合物可以每天分一次至多次给药,每日剂量为0.1至5000mg,优选为1至1000mg。
本发明化合物的制备与制剂的实施例和药理学试验结果表示如下。这些实施例不限制发明范围,仅是为使能更清楚地理解发明。
实施发明的最佳方式
化合物的制备
参考例1
L-2-苯基甘氨酸叔丁酯(参考化合物1-1)
1)在压力试管内,在氮气下和干冰-甲醇冷却下,向异丁烯(5ml)中依次加入N-苄氧羰基-L-2-苯基甘氨酸(4.2g)、无水二氯甲烷(10ml)和浓硫酸(0.5ml),将试管密封,混合物然后在室温下搅拌过夜。冷却后的反应混合物加入到含有10%碳酸氢钠水溶液和冰的容器内,搅拌混合物。向混合物中加入乙酸乙酯,全部混合物萃取。有机层依次用水和饱和盐水洗涤,经无水硫酸镁干燥,减压浓缩。所得残余物用硅胶柱色谱法纯化,得到3.5g(75%)N-苄氧羰基-L-2-苯基甘氨酸叔丁酯。
IR(薄膜,cm-1)3352,2978,1722,1498,1455,1369,1331,1228,1151,1050
2)在氮气下,向1)中所得N-苄氧羰基-L-2-苯基甘氨酸叔丁酯(3.4g)的四氢呋喃(18ml)-甲醇(18ml)溶液中加入20%氢氧化钯-碳(200mg)。混合物在氢气气氛下搅拌两天。用硅藻土滤出氢氧化钯-碳,滤液减压浓缩,得到1.3g(63%)标题化合物(参考化合物1-1),为晶体。
(参考化合物1-1)
熔点220.9~223.5℃
IR(KBr,cm-1)3411,2980,2931,1732,1496,1394,1372,1250,1157,750
按照类似于参考例1的方法得到下列化合物。
L-苯丙氨酸叔丁酯(参考化合物1-2)
熔点160~190℃(分解)
[α]D 20+15.6°(c=0.98,甲醇)
IR(KBr,cm-1)2834,1734,1507,1244,1160,703
D-丙氨酸叔丁酯(参考化合物1-3)
IR(薄膜,cm-1)3376,2978,1731,1368,1251
L-2-氨基丁酸叔丁酯(参考化合物1-4)
IR(薄膜,cm-1)3381,2975,2935,2878,1729,1479,1459,1393,1368,1253,1157,849
L-戊氨酸叔丁酯(参考化合物1-5)
IR(薄膜,cm-1)3381,2961,2934,2874,1728,1368,1256,1156,847,756
盐酸DL-3-(叔丁氧基)丙氨酸叔丁酯(参考化合物1-6)
熔点150.7~151.3℃
IR(KBr,cm-1)2979,1747,1497,1248,1156
参考例2
盐酸L-3-(4-硝基苯基)丙氨酸苯基酯(参考化合物2-1)
1)在氮气下,将N-(叔丁氧羰基)-L-3-(4-硝基苯基)丙氨酸(21.6g)、苯酚(7.86g)和二甲氨基吡啶(0.85g)溶于无水二氯甲烷(174ml)。然后在冰冷却下,向该溶液中加入1,3-二环己基碳二亚胺(17.2g),混合物在室温下搅拌一小时。滤出所得沉淀,滤液然后先后用5%碳酸氢钠水溶液、水、5%柠檬酸水溶液、水和饱和盐水洗涤。滤液经无水硫酸镁干燥,减压浓缩,得到21.25g(79%)N-(叔丁氧羰基)-L-3-(4-硝基苯基)丙氨酸苯基酯,为晶体。
熔点115.0~116.0℃
[α]D 20-21.6°(c=1.0,甲醇)
IR(KBr,cm-1)3385,1744,1688,1523,1347,1231,1191,949,745,695
2)向1)中所得N-(叔丁氧羰基)-L-3-(4-硝基苯基)丙氨酸苯基酯(1.93g)的氯仿(10ml)溶液中加入4.6N氯化氢的乙酸乙酯(11ml)溶液,混合物在室温下搅拌一小时。向反应混合物中加入乙醚,滤出所得沉淀,得到1.50g(93%)标题化合物(参考化合物2-1),为晶体。
(参考化合物2-1)
熔点202.5~204.6℃(分解)
[α]D 20+42.7°(c=1.0,甲醇)
IR(KBr,cm-1)2866,1758,1602,1S25,1483,1357,1228,1207,761,698
按照类似于参考例2的方法得到下列化合物。
盐酸L-苯丙氨酸苯基酯(参考化合物2-2)
熔点187~190℃
[α]D 20+37.3°(c=0.98,甲醇)
IR(KBr,cm-1)2864,2646,2610,1764,1616,1591,1455,1226,1208
盐酸L-3-(4-氟苯基)丙氨酸苯基酯(参考化合物2-3)
熔点208.0~209.5℃
[α]D 20+30.2°(c=0.51,甲醇)
IR(KBr,cm-1)2873,1763,1600,1510,1222,1157,823,759,695
盐酸L-3-(4-甲氧基苯基)丙氨酸苯基酯(参考化合物2-4)
熔点178.5~185.0℃(分解)
[α]D 20+27.4°(c=0.51,甲醇)
IR(KBr,cm-1)2865,1766,1513,1225,1209
盐酸L-3-(2-萘基)丙氨酸苯基酯(参考化合物2-5)
熔点190.0~193.2℃
[α]D 20+37.1°(c=0.49,二甲亚砜)
IR(KBr,cm-1)3467,2853,1776,1759,1491,1222,1199
盐酸L-3-(4-联苯基)丙氨酸苯基酯(参考化合物2-6)
熔点215.0~216.5℃
[α]D 20+56.8°(c=0.53,二甲亚砜)
IR(KBr,cm-1)2863,1771,1590,1486,1409,1340,1251,1196
盐酸L-3-(2-噻吩基)丙氨酸苯基酯(参考化合物2-7)
熔点167.0~167.6℃
[α]D 20+12.9°(c=0.99,甲醇)
IR(KBr,cm-1)2843,1764,1731,1588,1524,1495,1456,1240,1201,1164,1139,750,699,691
甲苯磺酸L-酪氨酸苯基酯(参考化合物2-8)
熔点213.0~217.0℃(分解)
[α]D 20+21.4°(c=0.49,甲醇)
IR(KBr,cm-1)3355,2835,1740,1614,1595,1516,1169,1123,1035,1010,818,758,688
盐酸NG-甲苯磺酰基-L-精氨酸苄基酯(参考化合物2-9)
[α]D 20+1.6°(c=1.0,甲醇)
IR(KBr,cm-1)2927,1971,1747,1677,1620,1362,1215,1170,1088,907,816,744
参考例3
甲苯磺酸L-3-(4-硝基苯基)丙氨酸苄基酯(参考化合物3-1)
向装有迪安斯塔克设备的容器内加入L-3-(4-硝基苯基)丙氨酸(2.0g)、苯甲醇(27ml)、苯(29ml)和甲苯磺酸(tosic acid)一水合物(2.0g),混合物在搅拌下回流过夜。在冰冷却下,向反应混合物中加入乙醚,滤出所得沉淀,得到4.12g(定量)标题化合物(参考化合物3-1),为晶体。
(参考化合物3-1)
熔点183.5~186.5℃
[α]D 20-10.1°(c=1.0,甲醇)
IR(KBr,cm-1)3085,2669,1746,1601,1518,1348,1208,1175
按照类似于参考例3的方法得到下列化合物。
甲苯磺酸L-苯丙氨酸苄基酯(参考化合物3-2)
熔点166.6~167.9℃
[α]D 20-6.9°(c=1.0,甲醇)
IR(KBr,cm-1)3032,1741,1525,1498,1206,1129,1037,1013
甲苯磺酸L-3-(4-氯苯基)丙氨酸苄基酯(参考化合物3-3)
熔点171.0~177.5℃
[α]D 20-8.9°(c=1.0,甲醇)
IR(KBr,cm-1)2950,1916,1743,1587
甲苯磺酸L-3-(4-甲氧基苯基)丙氨酸苄基酯(参考化合物3-4)
熔点152.0~162.0℃
[α]D 20-12.8°(c=1.0,甲醇)
IR(KBr,cm-1)3000,1742,1613,1514,1177
甲苯磺酸L-2-苯基甘氨酸苄基酯(参考化合物3-5)
熔点170.0~176.0℃
[α]D 20+44.4°(c=1.0,甲醇)
IR(KBr,cm-1)3039,1748,1598,1497,1222,1173,906,697
甲苯磺酸L-3-(2-萘基)丙氨酸苄基酯(参考化合物3-6)
熔点174.8~184.5℃
[α]D 20-23.0°(c=1.0,甲醇)
IR(KBr,cm-1)3059,1742,1514,1222,1156
甲苯磺酸L-丙氨酸苄基酯(参考化合物3-7)
熔点92.0~100.1℃
[α]D 20-3.4°(c=1.0,甲醇)
IR(KBr,cm-1)3031,1765,1737,1612,1284,1211,1127,1039,1013
甲苯磺酸L-(3-环己基)丙氨酸苄基酯(参考化合物3-8)
熔点157.1~161.7℃
[α]D 20-2.2°(c=1.0,甲醇)
IR(KBr,cm-1)2931,1754,1287,1124
甲苯磺酸S-甲基-L-半胱氨酸苄基酯(参考化合物3-9)
熔点105.0~110.3℃
[α]D 20-8.1°(c=1.0,甲醇)
IR(KBr,cm-1)3093,1748,1523,1218,1178,1125,1038,1013,816,736
甲苯磺酸S-苄基-L-半胱氨酸苄基酯(参考化合物3-10)
熔点141.8~153.3℃
[α]D 20-19.4°(c=1.0,甲醇)
IR(KBr,cm-1)3027,1756,1613,1542,1453,1277,1244,1221,1161,1128,1107,1069,1034,1009,976,817,740
盐酸S-苄基-DL-青霉胺苄基酯(参考化合物3-11)
IR(薄膜,cm-1)3390,2967,1744,1585,1496,1455,1396,1376,1308,1219
盐酸N-甲基-L-丙氨酸苄基酯(参考化合物3-12)
熔点179.0~180.8℃
[α]D 20-12.0°(c=1.0,甲醇)
IR(KBr,cm-1)2992,2734,2643,2470,1732,1497,1482,1239,1207
二甲苯磺酸4-氮杂-DL-亮氨酸乙酯(参考化合物3-13)
熔点104~110℃
IR(KBr,cm-1)3424,2986,1756,1740,1469,1376,1190,1124,1035,1011,815,685
甲苯磺酸D-苯丙氨酸苄基酯(参考化合物3-14),参考化合物3-2的对映体
[α]D 20+6.8°(c=1.0,甲醇)
IR(KBr,cm-1)3033,1741,1609,1206,1129
甲苯磺酸DL-高苯丙氨酸苄基酯(参考化合物3-15)
盐酸2-氨基-2-甲基丙酸甲酯(参考化合物3-16)
熔点186.0~186.5℃(分解)
IR(KBr,cm-1)2960,1748,1596,1522,1468,1438,1388,1366,1318,1282,1239,1195,1087
甲苯磺酸1-氨基-1-环丙烷羧酸苄基酯(参考化合物3-17)熔点90~110℃(分解)
IR(KBr,cm-1)2938,1746,1215,684
甲苯磺酸1-氨基-1-环戊烷羧酸苄基酯(参考化合物3-18)熔点175~189℃(分解)
IR(KBr,cm-1)2960,2718,1741,1525,1213,1124,1013
参考例4
盐酸N-苯乙基-L-苯丙氨酸苄基酯(参考化合物4-1)
向甲苯磺酸L-苯丙氨酸苄基酯(参考化合物3-2,1.0g)的无水二甲基甲酰胺(18ml)溶液中加入苯乙基溴(0.49ml)、无水碳酸钾(1.2g)和碘化钠(2.7g),混合物在加热至60至70℃下搅拌过夜。在冰冷却下,向反应混合物中加入水,全部混合物用乙酸乙酯萃取。有机层先后用水和饱和盐水洗涤,经无水硫酸镁干燥,减压浓缩。残余物用硅胶柱色谱法纯化,将所得油状物溶于乙醚。在冰冷却下,向其中加入4N氯化氢的乙酸乙酯(4ml)溶液,滤出所得沉淀,得到646mg(45%)标题化合物(参考化合物4-1),为晶体。
(参考化合物4-1)
熔点142~159℃
[α]D 20+10.7°(c=1.0,甲醇)
IR(KBr,cm-1)2578,1748,1554,1230,1183
按照类似于参考例4的方法得到下列化合物。
N-异戊基-DL-高苯丙氨酸苄基酯(参考化合物4-2)
IR(薄膜,cm-1)2955,1732,1497,1455,1167,750,698
参考例5
盐酸N-异戊基-3-(苯硫基)-DL-丙氨酸乙酯(参考化合物5-1)
在氮气下和冰冷却下,向1M硼烷-四氢呋喃配盐的四氢呋喃(4.85ml)溶液中滴加N-异戊酰-3-(苯硫基)-DL-丙氨酸乙酯(1.0g)的无水四氢呋喃(3.2ml)溶液,混合物在搅拌下回流一小时。在冰冷却下,向反应混合物中加入3N氯化氢的乙醇(2ml)溶液,混合物进一步回流一小时。反应混合物减压浓缩,向浓缩物中加入5%碳酸氢钠,全部混合物用乙醚萃取。有机层用饱和盐水洗涤,经无水硫酸镁干燥,减压浓缩。残余物用硅胶柱色谱法纯化,将所得油状物溶于乙醚。在冰冷却下,向其中加入4.6N氯化氢的乙酸乙酯溶液,滤出所得沉淀,得到163mg(15%)标题化合物(参考化合物5-1),为晶体。
(参考化合物5-1)
熔点113.0~115.5℃
IR(KBr,cm-1)3459,2963,2660,1747,1737,1560,1472,1330,1254,1213,1033
参考例6
二盐酸N-环己基-N-甲基乙二胺(参考化合物6-1)
1)向N-(叔丁氧羰基)-2-溴乙胺(1.0g)的无水二甲基甲酰胺(15ml)溶液中加入N-甲基环己胺(0.64ml)、无水碳酸钾(0.9g)和碘化钠(2.0g),混合物在室温下搅拌三天。向反应混合物中加入水,全部混合物用乙醚萃取。有机层先后用10%碳酸氢钠水溶液、水和饱和盐水洗涤,经无水硫酸镁干燥,减压浓缩。所得残余物用硅胶柱色谱法纯化,得到0.82g(72%)N-(叔丁氧羰基)-N’-环己基-N’-甲基乙二胺,为油状物。
IR(薄膜,cm-1)3360,2929,1715,1494,1452,1365,1250,1172,1050
2)将1)中所得N-(叔丁氧羰基)-N’-环己基-N’-甲基乙二胺(793mg)溶于4N氯化氢的二_烷(20ml)溶液,溶液在室温下搅拌过夜。反应混合物减压浓缩,向残余物中加入乙酸乙酯。滤出所得沉淀,得到463mg(65%)标题化合物(参考化合物6-1),为晶体。
(参考化合物6-1)
熔点197.0~198.3℃
IR(KBr,cm-1)2859,2603,1601,1521,1472,1454,1339,1016
按照类似于参考例6的方法得到下列化合物。
一盐酸N-甲基-N-苯基乙二胺(参考化合物6-2)
熔点210.0~211.0℃(分解)
IR(KBr,cm-1)3012,2466,1601,1512,1495,1414,1347,1196,1170,1110,1027
盐酸N-(2-氨基乙基)邻苯二甲酰亚胺(参考化合物6-3)
熔点250℃或更高
IR(KBr,cm-1)2909,1708,1507,1428,1396,1361,1324,1072,1045,879,718
二盐酸1-(2-氨基乙基)-4-甲基哌嗪(参考化合物6-4)
熔点250℃或更高
IR(KBr,cm-1)2978,1468,1440,1161,1069,1024,975,958,793,772
二盐酸1-环己基哌嗪(参考化合物6-5)
熔点250℃或更高
IR(KBr,cm-1)3487,2932,2679,2578,1434,1397,1315
1-(羧甲基)哌嗪双(氢三氟乙酸盐)(参考化合物6-6)
熔点173~175℃
IR(KBr,cm-1)2794,1744,1664,1196,1133
盐酸1-(三氟乙酰)哌嗪(参考化合物6-7)
熔点120℃
IR(KBr,cm-1)3524,2937,2753,2480,1716,1699,1457,1216,1189,1182,1169,1151,1130,1022,1013,896,754
参考例7
4-(二甲氨基)丁胺(参考化合物7-1)
1)向N-(苄氧羰基)-4-(甲磺酰氧基)丁胺(2.51g)的无水二甲基甲酰胺(28ml)溶液中加入二甲胺(12.5ml)、无水碳酸钾(1.72g)和碘化钠(3.74g),混合物在室温下搅拌过夜。向反应混合物中加入水,全部混合物用乙醚萃取。有机层先后用水和饱和盐水洗涤,经无水硫酸镁干燥,减压浓缩。所得残余物用硅胶柱色谱法纯化,得到1.59g(76%)N-(苄氧羰基)-4-(二甲氨基)丁胺。
IR(薄膜,cm-1)3331,2942,1715,1536,1455,1260,1037,739,698
2)在氮气下,向1)中所得N-(苄氧羰基)-4-(二甲氨基)丁胺(1.39g)的乙醇(19ml)溶液中加入20%氢氧化钯-碳(200mg)。混合物在氢气下搅拌三天。用硅藻土滤出氢氧化钯-碳,滤液减压浓缩,得到706mg(定量)标题化合物(参考化合物7-1),为非晶性粉末。
(参考化合物7-1)
IR(薄膜,cm-1)3408,2361,1633,1480
参考例8
盐酸(2S)-2-氨基-N1-甲基-4-苯基丁酰胺(参考化合物8-1)
1)在氮气下,将(2S)-2-(叔丁氧基甲酰氨基)-4-苯基丁酸(400mg)、盐酸甲胺(193mg)和1-羟基苯并三唑(193mg)悬浮在无水二氯甲烷(7ml)中。在冰冷却下,向该悬浮液中先后加入N-甲基吗啉(0.52ml)和盐酸1-乙基-3-(3-二甲氨基丙基)碳二亚胺(356mg),混合物在室温下搅拌过夜。反应混合物减压浓缩,向所得油状物中加入水,全部混合物用乙酸乙酯萃取。有机层先后用水和饱和盐水洗涤,经无水硫酸钠干燥,减压浓缩。向所得油状物中加入己烷,滤出所得沉淀,得到370mg(89%)(2S)-2-(叔丁氧基甲酰氨基)-N1-甲基-4-苯基丁酰胺,为晶体。
熔点102.8~104.7℃
[α]D 20-2.8°(c=0.49,氯仿)
IR(KBr,cm-1)3338,2969,1682,1656,1524,1454,1368,1283,1173
2)向1)中所得(2S)-2-(叔丁氧基甲酰氨基)-N1-甲基-4-苯基丁酰胺(332mg)的乙酸乙酯(2ml)-氯仿(1ml)溶液中加入4.6N氯化氢的乙酸乙酯(2ml)溶液,混合物在室温下搅拌一小时。反应混合物减压浓缩,向残余物中加入乙酸乙酯。滤出所得沉淀,得到247mg(95%)标题化合物(参考化合物8-1),为晶体。
(参考化合物8-1)
熔点211.5~214.0℃
[α]D 20+35.5°(c=0.51,甲醇)
IR(KBr,cm-1)3346,2861,2005,1658,1570,1523,1500,1420,749,702
按照类似于实施例8的方法得到下列化合物。
盐酸(2S)-2-氨基-N1-甲基-3-苯基丙酰胺(参考化合物8-2)
熔点197.0~199.6℃
[α]D 20+64.5°(c=1.0,甲醇)
IR(KBr,cm-1)3342,2884,2602,1665,1603,1569,1501,1457,1336,1265,1118
盐酸(2S)-2-氨基-N1,N1-二甲基-3-苯基丙酰胺(参考化合物8-3)
熔点207.5~219.5℃(分解)
[α]D 20+76.3°(c=1.0,甲醇)
IR(KBr,cm-1)3419,3029,1960,1653,1446,1398,1366,1139,1096,1035,767,748,700
二盐酸1-[(2S)-2-氨基-3-苯基丙酰]-4-甲基哌嗪(参考化合物8-4)
[α]D 20+41.5°(c=1.0,甲醇)
IR(薄膜,cm-1)3423,2938,1655,1494,1456,1366,1255,1167
盐酸(2S)-2-氨基-N1-甲基丙酰胺(参考化合物8-5)
熔点200~205℃(分解)
[α]D 20+11.6°(c=1.0,甲醇)
IR(KBr,cm-1)3261,2862,2641,1666,1611,1510,1413,1278,1121,1013,701
二盐酸1-[(2S)-2-氨基丙酰]-4-甲基哌嗪(参考化合物8-6)
[α]D 20+3.9°(c=1.0,甲醇)
盐酸(2S)-2-氨基-N1-丁基-3-(4-联苯基)丙酰胺(参考化合物8-7)
熔点167.5~170.0℃
[α]D 20+52.9°(c=1.0,甲醇)
IR(KBr,cm-1)3331,2955,2643,2587,1659,1601,1568,1486,1259,1166,759,696
二盐酸(2S)-2-氨基-N1-[2-(二甲氨基)乙基]-3-苯基丙酰胺(参考化合物8-8)
[α]D 20+60.1°(c=1.0,甲醇)
IR(薄膜,cm-1)3417,3211,2958,1684,1564,1495,1262,1169,750,703
二盐酸2-(异戊氨基)-N1-[2-(二甲氨基)乙基]乙酰胺(参考化合物8-9)
熔点154.5~157.5℃
IR(KBr,cm-1)3228,2958,1676,1570,1468,1443,1277
盐酸4-[(2S)-2-氨基丙酰]吗啉(参考化合物8-10)
熔点250℃或更高
[α]D 20+5.1°(c=1.0,甲醇)
IR(KBr,cm-1)3007,2787,2719,2626,2580,1645,1517,1480,1380,1271,1246,1114
参考例9
二盐酸(2S)-2-(异戊氨基)-N1-[2-(二甲氨基)乙基]-3-苯基丙酰胺(参考化合物9-1)
向二盐酸(2S)-2-氨基-N1-[2-(二甲氨基)乙基]-3-苯基丙酰胺(参考化合物8-8,2.47g)与异戊醛(0.69g)的乙醇(40ml)溶液中先后加入无水碳酸钾(3.32g)和分子筛3A(5g),混合物在室温下搅拌两小时。进一步向其中加入氰基硼氢化钠(0.55g),混合物在室温下搅拌两小时。向反应混合物中加入水,混合物用硅藻土过滤。滤液减压浓缩,向残余物中加入饱和盐水,全部混合物用乙酸乙酯萃取。有机层先后用10%碳酸氢钠水溶液和饱和盐水洗涤,经无水硫酸钠干燥,减压浓缩。残余物用硅胶柱色谱法纯化,将所得油状物溶于乙醚(5ml)。向其中加入4.6N氯化氢的乙酸乙酯(4ml)溶液,滤出所得沉淀,得到0.40g(13%)标题化合物(参考化合物9-1),为晶体。
(参考化合物9-1)
熔点163.0~166.5℃
[α]D 20+58.9°(c=0.50,甲醇)
IR(KBr,cm-1)3496,3394,3211,2964,2805,2681,1666,1565,1453,1387,1278,750,703
参考例10
2-氨基-N1,N1-二异丙基乙酰胺(参考化合物10-1)
1)在氮气下,将N-(苄氧羰基)甘氨酸(7.0g)、二异丙胺(6.6ml)和1-羟基苯并三唑(4.52g)悬浮在无水二氯甲烷(84ml)中。向该悬浮液中先后加入N-甲基吗啉(5.5ml)和1-乙基-3-(3-二甲氨基丙基)碳二亚胺(9.62g),混合物在室温下搅拌过夜。反应混合物减压浓缩,向所得油状物中加入水,全部混合物用氯仿萃取。有机层先后用10%碳酸氢钠水溶液、水和饱和盐水洗涤,经无水硫酸镁干燥,减压浓缩。所得残余物用硅胶柱色谱法纯化,得到2.74g(28%)2-(苄氧基甲酰氨基)-N1,N1-二异丙基乙酰胺。
IR(薄膜,cm-1)3403,2968,1719,1645,1214,1044,698
2)在氮气下,向1)中所得2-(苄氧基甲酰氨基)-N1,N1-二异丙基乙酰胺(2.61g)的乙醇(22ml)溶液中加入20%氢氧化钯-碳(200mg)。混合物在氢气下搅拌两天。用硅藻土滤出氢氧化钯-碳,滤液减压浓缩,得到0.92g(65%)标题化合物(参考化合物10-1),为晶体。
(参考化合物10-1)
熔点225~230℃(分解)
IR(KBr,cm-1)2971,1652,1456,1326,1213,1135,1038,913,885
按照类似于参考例10的方法得到下列化合物。
2-氨基-N1,N1-二环己基乙酰胺(参考化合物10-2)
IR(薄膜,cm-1)3422,2932,1645,1480,1446
1-甲基-4-[(2S)-2-(苯乙氨基)丙酰]哌嗪(参考化合物10-3)
[α]D 20-9.0°(c=0.98,甲醇)
IR(薄膜,cm-1)2935,2791,1642,1435,1140
参考例11
二盐酸N,N-二异丙基乙二胺(参考化合物11-1)
在氮气下和冰冷却下,将氢化锂铝(408mg)悬浮在无水乙醚(13ml)中,向其中滴加2-氨基-N1,N1-二异丙基乙酰胺(参考化合物10-1,850mg)在无水四氢呋喃(13ml)中的悬浮液。混合物在室温下搅拌一小时。在冰冷却下,向反应混合物中滴加含有水(0.8ml)的四氢呋喃(2ml)溶液。向其中加入4N氢氧化钠水溶液,全部混合物用氯仿萃取。有机层用饱和盐水洗涤,经无水硫酸镁干燥,减压浓缩。将所得油状物溶于氯仿(2ml),向其中加入4.6N氯化氢的乙酸乙酯(3ml)溶液。混合物减压浓缩,向浓缩物中加入异丙醚,滤出所得沉淀,得到734mg(63%)标题化合物(参考化合物11-1),为晶体。
(参考化合物11-1)
熔点145~150℃(分解)
IR(KBr,cm-1)2990,1699,1520,1397
按照类似于参考例11的方法得到下列化合物。
二盐酸N,N-二环己基乙二胺(参考化合物11-2)
熔点72~80℃(分解)
IR(KBr,cm-1)3406,2938,1454,1024,988
参考例12
盐酸(1S)-1-苄基-2-(苄氧基)乙胺(参考化合物12-1)
将(1S)-1-苄基-2-(苄氧基)-N-(叔丁氧羰基)乙胺(205mg)溶于2.3N氯化氢的甲醇(3ml)溶液,溶液搅拌一小时。反应混合物减压浓缩,向浓缩物中加入乙醚,滤出所得沉淀,得到143mg(99%)标题化合物(参考化合物12-1),为晶体。
(参考化合物12-1)
熔点155.3~156.4℃
[α]D 20+34.7°(c=1.0,甲醇)
IR(KBr,cm-1)2863,1598,1509,1496,1453,1362,1171,1117,1086,739,697
按照类似于参考例12的方法得到下列化合物。
盐酸(1R)-1-苄基-2-(苄氧基)乙胺(参考化合物12-2),参考化合物12-1的对映体
熔点153.9~154.6℃
[α]D 20-33.1°(c=1.0,甲醇)
IR(KBr,cm-1)2862,1598,1509,1496,1453,1362,1171,1116,1086,1074,1060
盐酸2-(苄氧基)乙胺(参考化合物12-3)
熔点125~137℃
IR(KBr,cm-1)2907,2034,1606,1508,1496,1457,1360,1126,1049,1027,1006,735,696
盐酸(2S)-2-氨基-4-丁内酯(参考化合物12-4)
盐酸2-(甲硫基)乙胺(参考化合物12-5)
熔点139~145℃
IR(KBr,cm-1)2963,2597,1579,1466,1139,1082
盐酸2-(苯硫基)乙胺(参考化合物12-6)
熔点111.3~114.0℃
IR(KBr,cm-1)2892,2582,1994,1588,1504,1473,1096,897,753,697
盐酸2-(苯二硫基)乙胺(参考化合物12-7)
熔点130.0~132.0℃
IR(KBr,cm-1)2977,1600,1475,733,686
盐酸2-(苄硫基)乙胺(参考化合物12-8)
熔点118~120℃
IR(KBr,cm-1)2670,2575,2440,1960,1586,1490,1452,1096,700
盐酸2-甲基-2-(苄硫基)丙胺(参考化合物12-9)
熔点113~116℃
IR(KBr,cm-1)2934,2612,2031,1601,1522,1494,1461,1435,1398,1376,1149,784,721,698
参考例13
盐酸2-环己基-N-(2-羟乙基)乙胺(参考化合物13-1)
向2-氨基乙醇(1.9ml)与2-环己基乙基溴(4.0g)的乙醇(42ml)溶液中加入无水碳酸钾(3.5g)和碘化钠(9.4g),混合物在搅拌下回流17小时。向反应混合物中加入饱和氯化铵水溶液,混合物用乙醚洗涤。向含水层中加入4N氢氧化钠水溶液,全部混合物用氯仿萃取。有机层用饱和盐水洗涤,经无水硫酸镁干燥,减压浓缩。将所得残余物溶于乙酸乙酯。向溶液中加入4N氯化氢的乙酸乙酯(4ml)溶液,然后在冰冷却下加入乙醚(10ml),滤出所得沉淀,得到2.2g(51%)标题化合物(参考化合物13-1),为晶体。
(参考化合物13-1)
熔点158.5~160.2℃
IR(KBr,cm-1)3316,2922,2856,1560,1467,1454,1407,1351,1084,1058,1049,1001,932
按照类似于参考例13的方法得到下列化合物。
盐酸N-(2-羟乙基)异戊胺(参考化合物13-2)
熔点150~162℃
IR(KBr,cm-1)3376,2961,2471,1595,1472,1369,1075,1004,961,775
N-(2-羟乙基)异丁胺(参考化合物13-3)
IR(薄膜,cm-1)3311,2955,1465,1388,1367,1243,1215,1115,1057,755
盐酸3,3-二甲基-N-(2-羟乙基)丁胺(参考化合物13-4)
熔点115~133℃
IR(KBr,cm-1)3386,2960,1751,1593,1478,1368,1248,1092,1069,997
盐酸N-(2-羟乙基)-4-甲基戊胺(参考化合物13-5)
熔点163.5~166.0℃
IR(KBr,cm-1)3378,2959,2505,2418,1595,1469,1074
盐酸N-(2-羟乙基)-3-丁烯基胺(参考化合物13-6)
N-(3-羟丙基)异戊胺(参考化合物13-7)
IR(薄膜,cm-1)3281,2955,1468,1367,1116,1072
N-(4-羟丁基)异戊胺(参考化合物13-8)
IR(薄膜,cm-1)2955,1470,1367,1115
盐酸N-[(1RS)-2-羟基-1-苯基乙基]异戊胺(参考化合物13-9)
IR(薄膜,cm-1)3350,2958,1587,1458,1076,761,703
盐酸N-[(1R)-1-苄基-2-羟乙基]异戊胺(参考化合物13-10)
熔点171~183℃
[α]D 20+8.3°(c=1.0,甲醇)
IR(KBr,cm-1)3321,2961,2468,1604,1568,1456,1055,987,747,708
盐酸N-(2-羟乙基)苯乙胺(参考化合物13-11)
熔点134.7~138.5℃
IR(KBr,cm-1)3386,2791,2464,1590,1498,1453,1336,1070,1014,743
盐酸N-(2-羟乙基)-4-甲基苯乙胺(参考化合物13-12)
熔点148℃
IR(KBr,cm-1)3283,2956,2784,2461,1516,1451,1082,1063,1008,808
2-(4-联苯基)-N-(2-羟乙基)乙胺(参考化合物13-13)
熔点82~87℃
IR(KBr,cm-1)3029,2925,2887,2825,1488,1126,1098,1071,1048,909,870
盐酸4-氟-N-(2-羟乙基)苯乙胺(参考化合物13-14)
熔点120℃
IR(KBr,cm-1)3313,2957,2793,1600,1577,1515,1448,1232,1063,826
盐酸4-氯-N-(2-羟乙基)苯乙胺(参考化合物13-15)
熔点125.0~126.0℃
IR(KBr,cm-1)3312,2960,2793,2462,1591,1536,1495,1453,1411,1080,1016,918,825,804
N-(2-羟乙基)-4-硝基苯乙胺(参考化合物13-16)
熔点67.2~68.8℃
IR(KBr,cm-1)3271,2828,1596,1510,1461,1441,1347,1063,1035,941,846,724
盐酸N-(2-羟乙基)-4-甲氧基苯乙胺(参考化合物13-17)
熔点135℃
IR(KBr,cm-1)3404,2966,2793,2462,1612,1516,1303,1246,1028,833,815
盐酸N-(2-羟乙基)苄胺(参考化合物13-18)
熔点95℃
IR(KBr,cm-1)3374,2940,2795,1579,1458,1072
盐酸N-(2-羟乙基)-3-苯基丙胺(参考化合物13-19)熔点97~103℃
IR(KBr,cm-1)3382,2957,2789,1454,1069,1023,748,699
盐酸3-(4-氟苯基)-N-(2-羟乙基)丙胺(参考化合物13-20)
熔点78~84℃
IR(KBr,cm-1)3364,3277,2949,2751,1599,1511,1446,1222,1075,821
盐酸3-(4-氯苯基)-N-(2-羟乙基)丙胺(参考化合物13-21)
熔点107℃
IR(KBr,cm-1)3422,2966,2784,1607,1494,1472,1411,1316,1303,1085,1055,930,812
盐酸N-(2-羟乙基)-2-苯氧基乙胺(参考化合物13-22)
熔点131.8~133.9℃
IR(KBr,cm-1)3355,2959,2744,2534,1927,1599,1500,1072,1036
(E)-N-(2-羟乙基)-3-苯基-2-丙烯基胺(参考化合物13-23)
IR(薄膜,cm-1)3298,2838,1495,1448,1357,1120,1049,969,747,693
盐酸N-(3-羟丙基)苯乙胺(参考化合物13-24)
IR(KBr,cm-1)3358,2950,2786,2489,2427,1738,1605,1498,1456,1250,1100,1063,1006,745,697
盐酸N-[(2RS)-2-羟丙基]苯乙胺(参考化合物13-25)
熔点153.5~155.4℃
IR(KBr,cm-1)3420,2972,2798,2523,2450,1590,1497,1456,1404,1282,1147,1076,1052,1020,936,744,697
盐酸N-异戊基丝氨醇(参考化合物13-26)
熔点80~89℃
IR(KBr,cm-1)3340,2969,1566,1466,1098,1072,1007,968,941,777
盐酸N-[2-(环己基)乙基]-2-(甲硫基)乙胺(参考化合物13-27)
熔点210~225℃(分解)
IR(KBr,cm-1)2920,2783,1450
N-异戊基-2-(甲硫基)乙胺(参考化合物13-28)
IR(薄膜,cm-1)3298,2954,1464,1284,1122,957,752
盐酸2-(甲硫基)-N-(苯乙基)乙胺(参考化合物13-29)
熔点222~228℃
IR(KBr,cm-1)2944,2774,2447,1476,1450,1430,1090,991,889,788,743,696
N-异戊基-2-(苯硫基)乙胺(参考化合物13-30)
IR(薄膜,cm-1)3300,2954,1584,1466,1120,740,692
盐酸N-苯乙基-2-(苯二硫基)乙胺(参考化合物13-31)
熔点149~160℃(分解)
IR(KBr,cm-1)2776,1591,1475,739,710
盐酸2-(苄硫基)-N-(苯乙基)乙胺(参考化合物13-32)
熔点150~155℃
IR(KBr,cm-1)2935,2767,2452,1584,1494,1452,1241,1029,984,780,748,698
盐酸2-(苄硫基)-2-甲基-N-(苯乙基)丙胺(参考化合物13-33)
熔点157.4~159.5℃
IR(KBr,cm-1)2956,2708,1590,1571,1496,1470,1460,1420,1372,1291,1146,1064,1030,780,748,711,697
盐酸N-[4-(苄氧基)苯乙基]-2-(苄硫基)乙胺(参考化合物13-34)
熔点177~181℃
IR(KBr,cm-1)3061,3029,2948,2769,1610,1582,1513,1494,1455,1380,1338,1300,1280,1245,1177,1113,1006
盐酸2-环戊基-N-(2-羟乙基)乙胺(参考化合物13-35)
盐酸2-环庚基-N-(2-羟乙基)乙胺(参考化合物13-36)熔点138.5~140.1℃
IR(KBr,cm-1)3305,2924,2853,1565,1465
盐酸2-(1-金刚烷基)-N-(2-羟乙基)乙胺(参考化合物13-37)
熔点195~205℃
IR(KBr,cm-1)3359,2901,2845,1450,1085
盐酸N-(2-羟乙基)-3-甲基-3-丁烯基胺(参考化合物13-38)
熔点141~146℃
IR(KBr,cm-1)3366,2972,2802,1449,1068,893
盐酸2-环己基-N-(3-羟丙基)乙胺(参考化合物13-39)
熔点115℃
IR(KBr,cm-1)3746,3676,3364,2923,2853,2796,2500,2425,1578,1451
2-(1-金刚烷基)-N-(2-羟乙基)乙胺(参考化合物13-40)
熔点63.9~66.5℃
IR(KBr,cm-1)3283,3104,2903,2842,1450,1437,1063,853
2-(1-金刚烷基)-N-[2-(甲硫基)乙基]乙胺(参考化合物13-41)
IR(薄膜,cm-1)2902,2844,1450
2-环戊基-N-[2-(甲硫基)乙基]乙胺(参考化合物13-42)
IR(薄膜,cm-1)3296,2947,2865,1451,1125
参考例14
N-[2-(叔丁基二甲基甲硅烷氧基)乙基]-2-甲氧基乙胺(参考化合物14-1)
向2-甲氧基乙胺(14ml)与2-(叔丁基二甲基甲硅烷氧基)乙基溴(7.00g)的乙醇(65ml)溶液中加入碘化钠(14.48g),混合物在搅拌下回流过夜。反应混合物减压浓缩,向残余物中加入水,全部混合物用氯仿萃取。有机层用饱和盐水洗涤,经无水硫酸钠干燥,减压浓缩。所得残余物用硅胶柱色谱法纯化,得到4.13g(55%)标题化合物(参考化合物14-1)。
(参考化合物14-1)
IR(薄膜,cm-1)2930,2858,1464,1254,1109,952,835,777
按照类似于参考例14的方法得到下列化合物。
N-[2-(叔丁基二甲基甲硅烷氧基)乙基]-2-(4-吡啶基)乙胺(参考化合物14-2)
IR(薄膜,cm-1)3308,2930,2856,1602,1465,1414,1254,1088,938,836,778
2-羟基-N-苯基乙胺(参考化合物14-3)
IR(薄膜,cm-1)3395,3051,3022,1603,1506,1057
二盐酸N-(2-羟乙基)-2-(2-吡啶基)乙胺(参考化合物14-4)
IR(KBr,cm-1)3385,2760,1619,1470,772
盐酸N-[(1RS)-1-(羟甲基)-2-苯氧基乙基]异戊胺(参考化合物14-5)
熔点91~110℃
IR(KBr,cm-1)3213,2962,1601,1567,1499,1471,1450,1252,1078,1045,753
N-[2-(叔丁基二甲基甲硅烷氧基)乙基]-2-(1-环己烯基)乙胺(参考化合物14-6)
IR(薄膜,cm-1)2928,2856,1462,1256,1087,836,811,777
N-[2-(叔丁基二甲基甲硅烷氧基)乙基]-2-环丙基乙胺(参考化合物14-7)
IR(薄膜,cm-1)2928,2857,1463,1256,1098,835,776
N-[2-(叔丁基二甲基甲硅烷氧基)乙基]-2-环丁基乙胺(参考化合物14-8)
IR(薄膜,cm-1)3282,2928,2857,1472,1256,1099,835,777
2-[3,5-二(叔丁基)-4-(甲氧基甲氧基)苯基]-N-(2-羟乙基)乙胺(参考化合物14-9)
参考例15
N-(2-羟乙基)-2-(2-萘基)乙胺(参考化合物15-1)
在氮气下和冰冷却下,将氢化锂铝(0.66g)悬浮在无水乙醚(10ml)中,向该悬浮液中滴加2-羟基-N-(2-萘乙酰)乙胺(2.00g)的无水四氢呋喃(50ml)溶液。混合物在室温下搅拌一小时,然后回流一小时。在冰冷却下,向反应混合物中滴加含水四氢呋喃溶液。进一步向其中加入4N氢氧化钠水溶液,全部混合物用氯仿萃取。有机层用饱和盐水洗涤,经无水硫酸镁干燥,减压浓缩。所得油状物用硅胶柱色谱法纯化,得到0.45g(21%)标题化合物(参考化合物15-1),为晶体。
熔点122~128℃
IR(KBr,cm-1)3132,2902,2834,1442,’1357,1118,1058,930,899,857,823,754
按照类似于参考例15的方法得到下列化合物。
N-[(1RS)-1-(二甲氨基甲基)-2-羟乙基]苯乙胺(参考化合物15-2)
IR(薄膜,cm-1)3300,2941,2820,1635,1603,1496,1455,1264,1128,1043,840,750,700
盐酸N-[(2RS)-3-羟基-2-甲基丙基]苯乙胺(参考化合物15-3)
熔点67~78℃
IR(KBr,cm-1)3381,2964,1560,1457,1241,1105,1041,751,700
盐酸N-[(1RS)-1-(羟甲基)-3-苯丙基]异戊胺(参考化合物15-4)
IR(KBr,cm-1)3312,3030,2961,2844,1559,1457,1336,998,750,699
盐酸N-[(1RS)-1-(羟甲基)-2-(苯硫基)乙基]异戊胺(参考化合物15-5)
熔点104~106℃
IR(KBr,cm-1)3306,2963,2824,1560,1460,1106,1066,999,924,738,689
盐酸(2RS)-2-(苄硫基)-3-甲基-N-(苯乙基)丁胺(参考化合物15-6)
熔点79~88℃
IR(KBr,cm-1)3062,3028,2963,2693,1602,1558,1494,1454,1388,1368,1336,1288
参考例16
2-(苄硫基)-1-(苄硫基甲基)-N-(苯乙基)乙胺(参考化合物16-1)
1)在氮气下和冰-甲醇冷却下,向盐酸2-羟基-1-(羟甲基)-N-(苯乙基)乙胺(2.42g)与二异丙基乙胺(9.1ml)的无水二氯甲烷(30ml)溶液中滴加甲磺酰氯(2.7ml)的无水二氯甲烷(5ml)溶液,混合物搅拌20分钟。向反应混合物中加入水,全部混合物用乙酸乙酯萃取。有机层先后用1N氢氯酸、水和饱和盐水洗涤,经无水硫酸钠干燥,减压浓缩。所得残余物用硅胶柱色谱法纯化,得到2.19g(61%)N-甲磺酰基-2-(甲磺酰氧基)-1-[(甲磺酰氧基)甲基]-N-(苯乙基)乙胺。
IR(薄膜,cm-1)1357,1175,1146,962,830,757
2)在氮气下,向氢化钠的60%矿物油(636mg)分散体在无水甲基甲酰胺(14ml)中的悬浮液中滴加苄基硫醇(1.80g)的无水二甲基甲酰胺(5ml)溶液。然后,向其中滴加1)中所得N-甲磺酰基-2-(甲磺酰氧基)-1-[(甲磺酰氧基)甲基]-N-(苯乙基)乙胺(2.07g)的无水二甲基甲酰胺(5ml)溶液。混合物在室温下搅拌两小时,向反应混合物中加入水,全部混合物用乙醚萃取。有机层先后用1N氢氧化钠水溶液、1N氢氯酸、水和饱和盐水洗涤,经无水硫酸镁干燥,减压浓缩。所得残余物用硅胶柱色谱法纯化,得到1.84g(79%)2-(苄硫基)-1-[(苄硫基)甲基]-N-甲磺酰基-N-(苯乙基)乙胺。
IR(薄膜,cm-1)3026,1497,1453,1330,1144,960,768,701
3)在氮气下,向2)中所得2-(苄硫基)-1-[(苄硫基)甲基]-N-甲磺酰基-N-(苯乙基)乙胺(1.34g)的无水甲苯(5ml)溶液中加入65%双(2-甲氧基乙氧基)氢化锂铝的甲苯溶液(3.3ml),混合物回流过夜。在冰冷却下,向反应混合物中加入2N氢氧化钠水溶液,全部混合物用乙醚萃取。有机层先后用2N氢氧化钠水溶液、水和饱和盐水洗涤,经无水硫酸镁干燥,减压浓缩。所得残余物用硅胶柱色谱法纯化,得到0.80g(71%)标题化合物(参考化合物16-1)。
(参考化合物16-1)
IR(薄膜,cm-1)3026,2913,1602,1494,1452,1238,1114,1071,1028,752,699
参考例17
盐酸N-(2-巯基乙基)苯乙胺(参考化合物17-1)
1)在氮气下,向2-甲基噻唑啉(2.0g)的氯苯(20ml)溶液中加入苯乙基溴(5.4ml),混合物在搅拌下回流六小时。在冰冷却下,向反应混合物中加入水,混合物用氯仿洗涤。
在氮气下和冰冷却下,向含水层中加入氢氧化钠(1.6g)的水(5ml)溶液,混合物搅拌10分钟。向反应混合物中加入6N氢氯酸进行酸化,全部混合物然后用乙醚萃取。有机层用饱和盐水洗涤,经无水硫酸钠干燥,减压浓缩,得到2.45g(55%)N-乙酰-N-(2-巯基乙基)苯乙胺。
IR(薄膜,cm-1)3447,2933,1637,1477,1420,1364,1291,1243,1204,1150
2)在氮气下,向N-乙酰-N-(2-巯基乙基)苯乙胺(500mg)的乙酸(5ml)溶液中加入浓盐酸(5ml),混合物回流24小时。反应混合物减压浓缩,然后向浓缩物中加入10%碳酸钠水溶液。确认液体呈弱碱性,全部混合物用乙酸乙酯萃取。有机层用饱和盐水洗涤,经无水硫酸钠干燥。向有机层中加入4N氯化氢的乙酸乙酯溶液,混合物减压浓缩。向浓缩物中加入乙醚,滤出所得沉淀,得到244mg(50%)标题化合物(参考化合物17-1),为晶体。
(参考化合物17-1)
熔点163~171℃
IR(KBr,cm-1)3028,2944,2770,2433,2361,1589,1454,743,696
按照类似于参考例17的方法得到下列化合物。
盐酸2-环己基-N-(2-巯基乙基)乙胺(参考化合物17-2)
熔点205~230℃
IR(KBr,cm-1)2924,2787,2610,2499,2433,1589,1478,1452盐酸2-(1-金刚烷基)-N-(2-巯基乙基)乙胺(参考化合物17-3)
熔点250℃或更高
IR(KBr,cm-1)2906,2844,2785,1453
参考例18
(3RS)-3-(异戊氨基)-4-(苯硫基)丁酸乙酯(参考化合物18-1)
在氮气下,向(E,Z)-4-(苯硫基)巴豆酸乙酯(908mg)的乙醇(12ml)溶液中加入异戊胺(0.32ml),混合物在搅拌下回流24小时。反应混合物减压浓缩,所得残余物用硅胶柱色谱法纯化,得到360mg(50%)标题化合物(参考化合物18-1)。
(参考化合物18-1)
IR(薄膜,cm-1)2955,1731,1584,1479,1437,1370,1194
按照类似于参考例18的方法得到下列化合物。
(2RS)-2-(异戊氨基)甲基-3-(苯硫基)丙酸叔丁酯(参考化合物18-2)
IR(薄膜,cm-1)3337,2956,1726,1584,1252,1150
(2RS)-2-(异丁氨基)甲基-3-(苯硫基)丙酸叔丁酯(参考化合物18-3)
IR(薄膜,cm-1)3346,2954,1726,1584,1367,1252,1150
参考例19
双[2-[N-(2-环己基乙基)氨基]乙基]二硫化物(参考化合物19-1)
1)向噻唑烷(605mg)的乙腈(15ml)溶液中加入三乙胺(0.81ml)和2-环己基乙基甲磺酸酯(1.0g),混合物在搅拌下回流过夜。反应混合物减压浓缩,向浓缩物中加入水,全部混合物用乙醚萃取。有机层用饱和盐水洗涤,经无水硫酸镁干燥,减压浓缩。所得残余物用硅胶柱色谱法纯化,得到594mg(61%)N-(2-环己基乙基)噻唑烷。
IR(薄膜,cm-1)2920,2849,1308
2)在室温和搅拌下,向N-(2-环己基乙基)噻唑烷(594mg)的甲醇(10ml)溶液中滴加碘(378mg)的甲醇(5ml)溶液。滴加后,混合物在室温下搅拌30分钟。向反应混合物中加入4N氢氧化钠水溶液(10ml),混合物减压浓缩。向浓缩物中加入氯仿,全部混合物萃取。有机层用饱和盐水洗涤,经无水硫酸镁干燥,减压浓缩,得到571mg(51%)标题化合物(参考化合物19-1)。
按照类似于参考例19的方法得到下列化合物。
双[2-[N-[2-(1-金刚烷基)乙基]氨基]乙基]二硫化物(参考化合物19-2)
IR(薄膜,cm-1)2899,2844,1450
双[2-(N-苯乙氨基)乙基]二硫化物(参考化合物19-3)
二氢碘酸双[2-[N-(2-环己基乙基)氨基]乙基]二硫化物(参考化合物19-4)
熔点225.5~229.0℃
IR(KBr,cm-1)3442,2921,2851,2800,1566
实施例1
(2S)-2-[3-(2-环己基乙基)-3-(2-羟乙基)脲基]丙酸叔丁酯(化合物1-1)
在氮气下,向盐酸L-丙氨酸叔丁酯(787mg)、1,1’-羰基二咪唑(983mg)与咪唑(295mg)的混合物中加入四氢呋喃(11ml),混合物在室温下搅拌30分钟。向反应混合物中加入盐酸N-(2-羟乙基)-2-环己基乙胺(参考化合物13-1,900mg),混合物回流一小时。在冰冷却下,向反应混合物中加入5%柠檬酸水溶液,全部混合物用乙酸乙酯萃取。有机层先后用水和饱和盐水洗涤,经无水硫酸镁干燥,减压浓缩。所得油状物用硅胶柱色谱法纯化,得到1.5g(定量)标题化合物(化合物1-1)。
(化合物1-1)
[α]D 20-5.9°(c=1.0,甲醇)
IR(薄膜,cm-1)3359,2977,2924,2851,1729,1629,1531,1450,1409,1368,1221,1157,1054
按照类似于实施例1的方法得到下列化合物。
(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]丙酸叔丁酯(化合物1-2)
[α]D 20-9.6°(c=0.97,甲醇)
IR(薄膜,cm-1)3342,2977,2934,1732,1633,1454,1368,1156
(2R)-2-[3-(2-羟乙基)-3-苯乙基脲基]丙酸叔丁酯(化合物1-3)
[α]D 20+8.8°(c=1.0,甲醇)
IR(薄膜,cm-1)3336,2977,2933,1733,1631,1533,1221,1156
(2S)-2-[3-(4-氟苯乙基)-3-(2-羟乙基)脲基]丙酸叔丁酯(化合物1-4)
IR(薄膜,cm-1)3335,2979,2934,1730,1632,1510,1456,1369,1222,1157
(2S)-2-[3-(4-氯苯乙基)-3-(2-羟乙基)脲基]丙酸叔丁酯(化合物1-5)
[α]D 20-10.4°(c=0.50,甲醇)
IR(薄膜,cm-1)3338,2979,1732,1632,1530,1492,1454,1407,1368,1306,1221,1156,1091,1058,1016,757
(2S)-2-[3-(2-羟乙基)-3-(4-硝基苯乙基)脲基]丙酸叔丁酯(化合物1-6)
[α]D 20-8.0°(c=0.50,甲醇)
IR(薄膜,cm-1)3340,2979,1732,1633,1519,1368,1346,1156,1058,856,750
(2S)-2-[3-(2-羟乙基)-3-(4-甲氧基苯乙基)脲基]丙酸叔丁酯(化合物1-7)
[α]D 20-11.4°(c=1.0,甲醇)
IR(薄膜,cm-1)3343,2978,2935,1732,1633,1513,1454,1368,1247,1156,1037
(2S)-2-[3-(2-羟乙基)-3-(4-甲基苯乙基)脲基]丙酸叔丁酯(化合物1-8)
[α]D 20+4.1°(c=1.0,氯仿)
IR(薄膜,cm-1)3338,2979,2932,1732,1633,1515,1368,1220,1156,1057,755
(2S)-2-[3-(2-羟乙基)-3-(4-苯基苯乙基)脲基]丙酸叔丁酯(化合物1-9)
熔点91.4~94.4℃
[α]D 20-9.8°(c=1.0,甲醇)
IR(KBr,cm-1)3282,3074,2975,2940,1741,1628,1559,1366,1272,1219,1151,762
(2S)-2-[3-(2-羟乙基)-3-[2-(2-吡啶基)乙基]脲基]丙酸叔丁酯(化合物1-10)
[α]D 20-4.9°(c=0.23,甲醇)
IR(薄膜,cm-1)3328,2978,1734,1634,1595,1533,1476,1456,1368,1220,1156
(2S)-2-[3-(2-羟乙基)-3-[2-(2-萘基)乙基]脲基]丙酸叔丁酯(化合物1-11)
[α]D 20-8.8°(c=0.94,甲醇)
IR(薄膜,cm-1)3336,2978,2933,1732,1632,1530,1368,1220,1156,750
(2S)-2-[3-(2-羟乙基)-3-(3-苯丙基)脲基]丙酸叔丁酯(化合物1-12)
[α]D 20-6.7°(c=0.50,甲醇)
IR(KBr,cm-1)3346,2977,2938,1733,1634,1532,1157,1058,751,700
(2S)-2-[3-[3-(4-氟苯基)丙基]-3-(2-羟乙基)脲基]丙酸叔丁酯(化合物1-13)
[α]D 20-5.9°(c=0.50,甲醇)
IR(薄膜,cm-1)3337,2979,2935,1732,1632,1510,1369,1221,1157,1058,848,757
(2S)-2-[3-[3-(4-氯苯基)丙基]-3-(2-羟乙基)脲基]丙酸叔丁酯(化合物1-14)
[α]D 20-6.9°(c=1.0,甲醇)
IR(薄膜,cm-1)3338,2978,2933,1732,1633,1532,1221,1156,1058,848,759
(2S)-2-[3-(2-羟乙基)-3-(3-苯基-2-丙烯基)脲基]丙酸叔丁酯(化合物1-15)
[α]D 20-5.0°(c=0.98,氯仿)
IR(KBr,cm-1)3335,2978,1732,1632,1532,1368,1223,1156,1050,969,747
(2S)-2-[3-(2-羟乙基)-3-(2-苯氧基乙基)脲基]丙酸叔丁酯(化合物1-16)
[α]D 20-8.0°(c=1.0,甲醇)
IR(薄膜,cm-1)3368,2978,2877,1732,1633,1600,1498,1242,1158
(2S)-2-[3-(2-羟乙基)-3-苯基脲基]丙酸叔丁酯(化合物1-17)
熔点94.5~97.4℃
[α]D 20+34.0°(c=1.0,甲醇)
IR(KBr,cm-1)3452,3284,2978,2939,1728,1642,1594,1526,1452,1367,1235
(2S)-2-[3-苄基-3-(2-羟乙基)脲基]丙酸叔丁酯(化合物1-18)
(2S)-2-[3-(3-丁烯基)-3-(2-羟乙基)脲基]丙酸叔丁酯(化合物1-19)
[α]D 20+6.4°(c=0.99,氯仿)
IR(薄膜,cm-1)3305,2978,2934,1728,1628,1537,1479,1456,1368,1224,1155,1059
2-[3-(2-羟乙基)-3-苯乙基脲基]乙酸叔丁酯(化合物1-20)
熔点71.9~73.6℃
IR(KBr,cm-1)3355,2977,2929,1744,1616,1556,1366,1225
2-[3-(2-羟乙基)-3-甲基脲基]乙酸叔丁酯(化合物1-21)
熔点85.5~87.0℃
IR(KBr,cm-1)3357,3254,2950,1749,1630,1555,1390,1365,1224,1153,1056,983,857,775,756,572
(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]丁酸叔丁酯(化合物1-22)
[α]D 20-11.1°(c=1.0,甲醇)
IR(薄膜,cm-1)3326,2973,2934,1732,1632,1530,1455,1368,1157
(2RS)-3-(叔丁氧基)-2-[3-(2-羟乙基)-3-苯乙基脲基]丙酸叔丁酯(化合物1-23)
IR(薄膜,cm-1)3367,2974,1736,1633,1519,1367,1158,1054
(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-2-苯基乙酸叔丁酯(化合物1-24)
熔点87.5~88.8℃
[α]D 20+48.0°(c=1.0,甲醇)
IR(KBr,cm-1)3289,2981,1739,1629,1538,1370,1149
(2S)-2-[3-(2-羟乙基)-3-甲基脲基]-3-苯基丙酸叔丁酯(化合物1-25)
[α]D 20+26.3°(c=0.50,氯仿)
IR(薄膜,cm-1)3358,2977,2932,1730,1633,1530,1455,1393,1368,1220,1155,1050,742,701
(2S)-2-[3-(2-羟乙基)-3-异戊基脲基]-3-苯基丙酸叔丁酯(化合物1-26)
IR(薄膜,cm-1)3354,2956,1732,1632,1524,1455,1409,1368,1221,1156
(2S)-2-[3-(2-环己基乙基)-3-(2-羟乙基)脲基]-3-苯基丙酸叔丁酯
(化合物1-27)
[α]D 20+21.9°(c=0.95,氯仿)
IR(薄膜,cm-1)3340,2977,2924,1730,1631,1520,1368,1221,1156,1051,755,701
3-[3-(2-羟乙基)-3-苯乙基脲基]丙酸叔丁酯(化合物1-28)
IR(薄膜,cm-1)3348,2976,2932,1725,1629,1535,1367,1157,1061,751,701
(2S)-2-[3-[(2RS)-3-羟基-2-甲基丙基]-3-苯乙基脲基]-3-苯基丙酸叔丁酯(化合物1-29)
IR(薄膜,cm-1)3324,2974,1734,1631,1522,1497,1455,1410,1368,1221,1155,1031,987,752,701
(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-苯基丙酸叔丁酯(化合物1-30)
[α]D 20-2.8°(c=0.57,甲醇)
IR(薄膜,cm-1)3365,2977,2932,1728,1632,1523,1368,1155,1049,752,701
(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-4-甲基戊酸乙酯(化合物1-31)
[α]D 20-12.2°(c=1.0,甲醇)
IR(薄膜,cm-1)3339,2957,1737,1631,1531,1199
(2S)-2-[3-(3-羟丙基)-3-苯乙基脲基]-3-苯基丙酸乙酯(化合物1-32)
[α]D 20+16.9°(c=0.96,氯仿)
IR(薄膜,cm-1)3326,2934,1736,1632,1527,1497,1454,1409,1371,1291,1241,1199,1030,751,701
(2S)-2-[3-[(2RS)-2-羟丙基]-3-苯乙基脲基]-3-苯基丙酸乙酯(化合物1-33)
IR(薄膜,cm-1)3338,2977,1736,1633,1525,1497,1454,1408,1372,1199,1079,1057,1030,752,701
(2RS)-2-[3-(2-羟乙基)-3-苯乙基脲基]-4-(甲硫基)丁酸甲酯(化合物1-34)
IR(薄膜,cm-1)3339,2919,1740,1632,1528,1206,1048,750,701
(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(4-硝基苯基)丙酸苯基酯(化合物1-35)
[α]D 20-3.5°(c=0.53,氯仿)
IR(薄膜,cm-1)3308,1761,1634,1520,1492,1346,1192,1165,751,700
(2S)-3-(4-氯苯基)-2-[3-(2-羟乙基)-3-苯乙基脲基]丙酸苄基酯(化合物1-36)
IR(薄膜,cm-1)3367,2935,1739,1631,1528,1493,1454,1176
(2S)-2-[3-(2-羟乙基)-3-异戊基脲基]-3-(4-硝基苯基)丙酸苄基酯(化合物1-37)
[α]D 20-31.2°(c=0.54,氯仿)
IR(薄膜,cm-1)3321,2955,1740,1634,1520,1456,1346,1180
(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(2-硝基-4-联苯基)丙酸苄基酯(化合物1-38)
[α]D 20-14.5°(c=0.61,氯仿)
IR(薄膜,cm-1)3339,1738,1633,1530,1358,756,700
(2S)-3-[4-(苯磺酰)-3-硝基苯基]-2-[3-(2-羟乙基)-3-苯乙基脲基]丙酸苄基酯(化合物1-39)
[α]D 20-9.2°(c=0.53,氯仿)
IR(薄膜,cm-1)3338,3028,1740,1636,1545,1161,752
(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(2-萘基)丙酸苄基酯(化合物1-40)
[α]D 20-18.2°(c=1.0,甲醇)
IR(薄膜,cm-1)3324,1740,1632,1523,1190,1050
(2R)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(甲硫基)丙酸苄基酯(化合物1-41)
[α]D 20-20.7°(c=0.52,甲醇)
IR(薄膜,cm-1)3350,2921,1742,1632,1524,1454,1409,1190,1049,752,700
(2R)-3-(苄硫基)-2-[3-(2-羟乙基)-3-苯乙基脲基]丙酸苄基酯(化合物1-42)
[α]D 20-38.0°(c=0.53,甲醇)
IR(薄膜,cm-1)3354,3027,2926,1741,1632,1523,1454,1410,1309,1186,1048,750,699
(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-苯基丙酸苄基酯(化合物1-43)
[α]D 20-14.4°(c=0.96,氯仿)
IR(薄膜,cm-1)3327,3028,2934,1740,1632,1526,749,699
(2R)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-苯基丙酸苄基酯(化合物1-44),化合物1-43的对映体
[c]D 20+16.1°(c=0.51,甲醇)
IR(薄膜,cm-1)3328,2933,1740,1630,1528,1178,1048,747,699
(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(4-异丙氧基苯基)丙酸苄基酯(化合物1-45)
[α]D 20-18.7°(c=0.50,氯仿)
IR(薄膜,cm-1)3344,2975,1739,1632,1509,1242,1184,1120,955,751,700
(2S)-2-[3-[(1RS)-1-(二甲氨基甲基)-2-羟乙基]-3-苯乙基脲基]-3-苯基丙酸苄基酯(化合物1-46)
[α]D 20-14.1°(c=1.0,甲醇)
IR(薄膜,cm-1)3378,2945,1739,1634,1455,1187
(2S)-2-[3-(2-羟乙基)-3-异戊基脲基]-3-苯基丙酸苄基酯(化合物1-47)
[α]D 20-19.2°(c=1.0,氯仿)
IR(薄膜,cm-1)3341,2955,2870,1740,1631,1527,1189,1051,753,699
(2S)-2-[3-(2-羟乙基)-3-异戊基脲基]-3-(4-甲氧基苯基)丙酸苄基酯(化合物1-48)
[α]D 20-19.5°(c=0.55,氯仿)
IR(薄膜,cm-1)3336,2956,1741,1632,1585,1249,1179,1110,755,699
(2S)-2-[3-(2-羟乙基)-3-异戊基脲基]-2-苯基乙酸苄基酯(化合物1-49)
熔点77.5~79.6℃
[α]D 20+33.7°(c=0.50,氯仿)
IR(KBr,cm-1)3228,2952,1745,1705,1631,1560,1455,1370,1239,1180,1163
(2S)-2-[3-(2-羟乙基)-3-异戊基脲基]-4-甲基戊酸苄基酯(化合物1-50)
[α]D 20-22.9°(c=0.97,氯仿)
IR(薄膜,cm-1)3325,2956,1742,1634,1538,1170,1051,752,697
2-[3-(2-羟乙基)-3-异戊基脲基]乙酸苄基酯(化合物1-51)
IR(薄膜,cm-1)3353,2955,1747,1633,1537,1188,1049,754,698
(2S)-3-环己基-2-[3-(2-羟乙基)-3-异戊基脲基]丙酸苄基酯(化合物1-52)
[α]D 20-21.8°(c=0.52,氯仿)
IR(薄膜,cm-1)3307,2924,1742,1631,1531,1449,1169,1051
(2S)-2-[3-(2-羟乙基)-3-异戊基脲基]-3-(4-咪唑基)丙酸苄基酯(化合物1-53)
[α]D 20-9.5°(c=0.53,氯仿)
IR(KBr,cm-1)3198,2955,1742,1630,1532,1174,1051,754,698
(2S)-2-[3-(2-羟乙基)-3-异戊基脲基]-5-(3-甲苯磺酰胍基)戊酸苄基酯(化合物1-54)
[α]D 20+1.6°(c=0.51,氯仿)
IR(薄膜,cm-1)3336,2954,1738,1626,1548,1261,1170,1132,1082,815,753
(2S)-2-[3-[4-(苄氧基)苯乙基]-3-[2-(苄硫基)乙基]脲基]丙酸苄基酯(化合物1-55)
[α]D 20-8.4°(c=0.98,氯仿)
IR(薄膜,cm-1)3350,3062,3030,2934,1740,1641,1583,1511,1453,1401,1300,1239,1191,1025
(2S)-2-[3-[2-(苄硫基)-2-甲基丙基]-3-苯乙基脲基]丙酸苄基酯(化合物1-56)
[α]D 20-9.8°(c=0.52,甲醇)
IR(薄膜,cm-1)3348,3028,2962,1741,1639,1521,1453,1385,1364,1305,1264,1188,1089,1070,1029,1004,967,912,749,698
(2S)-2-[3-[(2RS)-2-(苄硫基)-3-甲基丁基]-3-苯乙基脲基]丙酸苄基酯(化合物1-57)
IR(薄膜,cm-1)3359,3062,3027,2958,1740,1646,1603,1522,1453,1402,1383,1364,1306,1168
(2RS)-3-(苄硫基)-2-[3-[2-(苄硫基)乙基]-3-苯乙基脲基]-3-甲基丁酸苄基酯(化合物1-58)
IR(薄膜,cm-1)3378,3061,3028,2966,2930,1736,1656,1602,1495,1454,1367,1320,1189
(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-苯基丙酸苯基酯(化合物1-59)
[α]D 20-3.8°(c=0.30,氯仿)
IR(薄膜,cm-1)3334,1760,1633,1527,1493,1454,1408,1367,1192,1047,751,700
(2S)-3-(4-氟苯基)-2-[3-(2-羟乙基)-3-苯乙基脲基]丙酸苯基酯(化合物1-60)
[α]D 20-4.1°(c=0.31,氯仿)
IR(薄膜,cm-1)3305,2932,1762,1632,1510,1223,1192,1163,751,701
(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(4-羟基苯基)丙酸苯基酯(化合物1-61)
[α]D 20-4.6°(c=0.33,氯仿)
IR(薄膜,cm-1)3409,1757,1630,1516,1493,1454,1411,1368,1191,1047,831,751,701
(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(4-甲氧基苯基)丙酸苯基酯(化合物1-62)
熔点91.2~94.0℃
[α]D 20-4.9°(c=1.0,氯仿)
IR(KBr,cm-1)3310,2935,1761,1633,1513,1249,1192,1164,701
(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(2-噻吩基)丙酸苯基酯(化合物1-63)
[α]D 20-9.4°(c=0.66,氯仿)
IR(薄膜,cm-1)3323,1761,1633,1523,1492,1192,1046,750,700
(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(2-萘基)丙酸苯基酯(化合物1-64)
[α]D 20-8.6°(c=0.54,氯仿)
IR(薄膜,cm-1)3312,2931,1760,1634,1524,1493,1192,1164,750
(2S)-3-(4-联苯基)-2-[3-(2-羟乙基)-3-苯乙基脲基]丙酸苯基酯(化合物1-65)
[α]D 20-22.3°(c=0.55,二甲亚砜)
IR(薄膜,cm-1)3305,2930,1763,1633,1520,1487,1192,1164,759,699
(2S)-2-[3-(2-羟乙基)-3-异戊基脲基]-3-(4-硝基苯基)丙酸苯基酯(化合物1-66)
[α]D 20-6.1°(c=0.54,氯仿)
IR(薄膜,cm-1)3306,2956,1761,1633,1520,1492,1346,1192,1165,753
(2S)-3-(4-联苯基)-2-[3-(2-羟乙基)-3-异戊基脲基]丙酸苯基酯(化合物1-67)
[α]D 20-2.3°(c=0.98,氯仿)
IR(薄膜,cm-1)3306,2955,1763,1633,1519,1487,1192,1164,760,698
(2S)-2-[3-苯乙基-3-[2-(苯二硫基)乙基]脲基]-3-苯基丙酸叔丁酯(化合物1-68)
[α]D 20-7.5°(c=0.32,甲醇)
IR(薄膜,cm-1)3369,2977,1729,1649,1512,1155,741,700
(2S)-2-[3-(2-巯基乙基)-3-苯乙基脲基]-4-丁内酯(化合物1-69)
(2S)-2-[3-[2-(甲硫基)乙基]-3-苯乙基脲基]-3-苯基丙酸乙酯(化合物1-70)
[α]D 20-12.3°(c=0.32,甲醇)
IR(薄膜,cm-1)3368,2980,2919,1736,1644,1514,1454,1405,1369,1195,1092,1029,752,701
(2R)-3-(苄硫基)-2-[3-[2-(苄硫基)乙基]-3-苯乙基脲基]丙酸苄基酯(化合物1-71)
[α]D 20-38.1°(c=0.50,甲醇)
IR(薄膜,cm-1)3027,2920,1740,1649,1495,1453,1190,753,700
(2S)-2-[3-[2-(苄硫基)-1-[(苄硫基)甲基]乙基]-3-苯乙基脲基]-3-苯基丙酸苄基酯(化合物1-72)
[α]D 20+2.4°(c=0.51,氯仿)
IR(薄膜,cm-1)3027,1737,1650,1495,1454,1346,1257,1191,753,700
(2S)-6-(苄氧基甲酰氨基)-2-[3-(2-羟乙基)-3-异戊基脲基]己酸苄基酯(化合物1-73)
[α]D 20-14.9°(c=0.47,氯仿)
IR(薄膜,cm-1)3319,2953,1712,1633,1531,1455,1410,1367,1256,1174,1052
(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-[4-(苄氧基)苯基]丙酸苄基酯(化合物1-74)
[α]D 20+3.2°(c=0.51,甲醇)
IR(薄膜,cm-1)3324,1740,1632,1511,1241,1026
2-[3-(2-环己基乙基)-3-(2-羟乙基)脲基]乙酸叔丁酯(化合物1-75)
IR(薄膜,cm-1)3354,2977,2924,2851,1743,1632,1536,1368,1221,1157,754
(2S)-2-[3-(2-环戊基乙基)-3-(2-羟乙基)脲基]丙酸叔丁酯(化合物1-76)
(2S)-2-[3-(2-环庚基乙基)-3-(2-羟乙基)脲基]丙酸叔丁酯(化合物1-77)
[c]D 20-5.2°(c=1.0,甲醇)
IR(薄膜,cm-1)3350,2977,2922,2854,1738,1633,1531,1455
(2S)-2-[3-[2-(1-金刚烷基)乙基]-3-(2-羟乙基)脲基]丙酸叔丁酯(化合物1-78)
[α]D 20-3.5°(c=1.0,甲醇)
IR(薄膜,cm-1)3340,2978,2902,2847,1732,1633,1530,1451,1218,1156
(2S)-2-[3-(2-羟乙基)-3-(3-甲基-3-丁烯基)脲基]丙酸乙酯(化合物1-79)
IR(薄膜,cm-1)3344,2980,2937,1734,1634,1533,1204,1060,889
(2S)-3-(4-联苯基)-2-[3-[(1RS)-1-(乙氧羰基甲基)-2-(苯硫基)乙基]-3-异戊基脲基]丙酸苯基酯(化合物1-80)
IR(薄膜,cm-1)3451,2956,1760,1730,1650,1591,1488,1368,1300,1196,1026
(2S)-2-[3-[2-(甲硫基)乙基]-3-苯乙基脲基]丙酸叔丁酯(化合物1-81)
IR(薄膜,cm-1)3354,3026,2978,2919,1732,1634,1520,1215,1155
2-[3-(2-环己基乙基)-3-(2-羟乙基)脲基]-2-甲基丙酸甲酯(化合物1-82)
IR(薄膜,cm-1)3306,2985,2923,2851,1741,1632,1536,1284,1152,1054,756
1-[3-(2-环己基乙基)-3-(2-羟乙基)脲基]-1-环丙烷羧酸苄基酯(化合物1-83)
熔点101~108℃
IR(薄膜,cm-1)3403,3345,2919,2850,1731,1614,1527,1275,1166,1036,748,705
1-[3-(2-环己基乙基)-3-(2-羟乙基)脲基]-1-环戊烷羧酸苄基酯(化合物1-84)
熔点66.7~68.5℃
IR(KBr,cm-1)3220,2926,1785,1624,1560,1475,1448,1412,1274,1249,1077,732
(2S)-2-[3-(2-环己基乙基)-3-(3-羟丙基)脲基]丙酸叔丁酯(化合物1-85)
[α]D 20-5.7°(c=1.0,甲醇)
IR(薄膜,cm-1)3326,2977,2923,2851,1737,1632,1536,1450,1368,1304,1218,1157
(2R)-2-[3-(2-环己基乙基)-3-(2-羟乙基)脲基]丙酸叔丁酯(化合物1-86)
[α]D 20+6.3°(c=1.0,甲醇)
IR(薄膜,cm-1)3340,2977,2923,1732,1632,1531,1449,1368,1157
2-[3-[2-(1-金刚烷基)乙基]-3-(2-羟乙基)脲基]乙酸叔丁酯(化合物1-87)
熔点120.0~120.5℃
IR(KBr,cm-1)3289,2901,2843,1751,1630,1567,1223,1155
(2S)-2-[3-[2-[3,5-二(叔丁基)-4-(甲氧基甲氧基)苯基]乙基]-3-(2-羟乙基)脲基]丙酸叔丁酯(化合物1-88)
[α]D 20-16.2°(c=1.0,甲醇)
IR(薄膜,cm-1)3347,2958,1731,1630,1530,1452,1260,1164
实施例2
(2S)-2-[3-(2-羟乙基)-1-甲基-3-苯乙基脲基]丙酸苄基酯(化合物2-1)
在氮气下和冰-甲醇冷却下,向三光气(5.5g)的四氯化碳(20ml)溶液中加入N,N-二异丙基乙胺(3.5ml)。向该混合物中滴加从盐酸N-甲基-L-丙氨酸苄基酯(参考化合物3-12,2.10g)得到的游离碱的四氯化碳(5ml)溶液,同时保持温度在-5℃,滴加后混合物搅拌30分钟。向反应混合物中加入从盐酸N-(2-羟乙基)苯乙胺(参考化合物13-11,5.5g)得到的游离碱的四氯化碳(5ml)溶液,混合物在室温下搅拌30分钟,然后回流1.5小时。在冰冷却下,向反应混合物中加入10%碳酸氢钠水溶液,全部混合物用乙醚萃取。有机层先后用10%柠檬酸水溶液、水和饱和盐水洗涤,经无水硫酸镁干燥,减压浓缩。所得油状物用硅胶柱色谱法纯化,得到2.74g(78%)标题化合物(化合物2-1)。
(化合物2-1)
[α]D 20-19.3°(c=1.0,甲醇)
IR(薄膜,cm-1)3410,3062,3027,2941,1740,1620,1454,1164,1089
实施例3
(2S)-2-[3-[2-(叔丁基二甲基甲硅烷氧基)乙基]-3-(2-甲氧基乙基)脲基]丙酸叔丁酯(化合物3-1)
在氮气下,将盐酸L-丙氨酸叔丁酯(1.70g)、1,1’-羰基二咪唑(1.54g)和咪唑(0.47g)悬浮在无水四氢呋喃(11ml)中,悬浮液在室温下搅拌30分钟。向反应混合物中加入N-[2-(叔丁基二甲基甲硅烷氧基)乙基]-2-甲氧基乙胺(参考化合物14-1,1.77g)的无水四氢呋喃(6ml)溶液,混合物回流一小时。放置后,反应混合物减压浓缩。向所得油状物中加入水,全部混合物用乙醚萃取。有机层用饱和盐水洗涤,经无水硫酸镁干燥,减压浓缩。所得油状物用硅胶柱色谱法纯化,得到2.91g(95%)标题化合物(化合物3-1)。
(化合物3-1)
[α]D 20+6.3°(c=1.1,氯仿)
IR(薄膜,cm-1)3348,2931,2858,1737,1650,1530,1462,1368,1225,1159,1117,838,779
按照类似于实施例3的方法得到下列化合物。
(2S)-2-[3-[2-(叔丁基二甲基甲硅烷氧基)乙基]-3-[2-(4-吡啶基)乙基]脲基]丙酸叔丁酯(化合物3-2)
(2S)-2-[3-[2-(叔丁基二甲基甲硅烷氧基)乙基]-3-[2-(1-环己烯基)乙基]脲基]丙酸乙酯(化合物3-3)
IR(薄膜,cm-1)3361,2929,2857,1737,1634,1532,1472,1373,1253,1185,1104,836,778
(2S)-2-[3-[2-(叔丁基二甲基甲硅烷氧基)乙基]-3-(2-环丙基乙基)脲基]丙酸叔丁酯(化合物3-4)
IR(薄膜,cm-1)3358,2930,2857,1736,1644,1525,1472,1368,1256,1221,1158,1104,837
(2S)-2-[3-[2-(叔丁基二甲基甲硅烷氧基)乙基]-3-(2-环丁基乙基)脲基]丙酸叔丁酯(化合物3-5)
[α]D 20-4.3°(c=1.1,甲醇)
IR(薄膜,cm-1)3359,2930,2857,1736,1644,1524,1472,1392,1368,1255,1220,1158,1104,1063,928,837,778
实施例4
(2S)-2-[3-(2-羟乙基)-3-(2-甲氧基乙基)脲基]丙酸叔丁酯(化合物4-1)
在氮气下,将(2S)-2-[3-[2-(叔丁基二甲基甲硅烷氧基)乙基]-3-(2-甲氧基乙基)脲基]丙酸叔丁酯(化合物3-1,2.79g)溶于无水四氢呋喃(11ml)。在室温和搅拌下向溶液中加入四正丁基氟化铵(7.3ml),混合物搅拌一小时。向反应混合物中加入水,全部混合物用乙酸乙酯萃取。有机层用饱和盐水洗涤,经无水硫酸镁干燥,减压浓缩。所得油状物用硅胶柱色谱法纯化,得到2.14g(定量)标题化合物(化合物4-1)。
(化合物4-1)
[α]D 20-2.0°(c=1.0,氯仿)
IR(薄膜,cm-1)3334,2979,2933,1732,1633,1537,1455,1405,1368,1159,1118,1057,756
按照类似于实施例4的方法得到下列化合物。
(2S)-2-[3-(2-羟乙基)-3-[2-(4-吡啶基)乙基]脲基]丙酸叔丁酯(化合物4-2)
IR(薄膜,cm-1)3338,2978,1732,1634,1606,1532,1368,1222,1155,1058,848,810,758
(2S)-2-[3-[2-(1-环己烯基)乙基]-3-(2-羟乙基)脲基]丙酸乙酯(化合物4-3)
[α]D 20-7.5°(c=0.53,甲醇)
IR(薄膜,cm-1)3338,2980,2928,1738,1632,1531,1449,1408,1183,1058
(2S)-2-[3-(2-环丙基乙基)-3-(2-羟乙基)脲基]丙酸叔丁酯(化合物4-4)
[α]D 20-8.2°(c=1.0,甲醇)
IR(薄膜,cm-1)3342,2979,2933,1732,1632,1530,1456,1368,1223,1158,1056,756
(2S)-2-[3-(2-环丁基乙基)-3-(2-羟乙基)脲基]丙酸叔丁酯(化合物4-5)
[α]D 20-7.2°(c=0.54,甲醇)
IR(薄膜,cm-1)3339,2974,1732,1633,1532,1455,1368,1222,1158,1055,756
实施例5
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环己基乙基)脲基]丙酸叔丁酯(化合物5-1)
在氮气下,向(2S)-2-[3-(2-环己基乙基)-3-(2-羟乙基)脲基]丙酸叔丁酯(化合物1-1,1.0g)与三苯膦(1.5g)的混合物中加入无水四氢呋喃(6ml),混合物在盐-冰冷却下搅拌30分钟。向混合物中滴加偶氮二羧酸二异丙酯(1.2ml),同时保持液体温度在5℃,然后历经20分钟向其中滴加硫代乙酸(0.4ml)。混合物搅拌20分钟,向反应混合物中加入10%碳酸氢钠水溶液(30ml),全部混合物用乙醚萃取。有机层先后用10%碳酸氢钠水溶液、水和饱和盐水洗涤,经无水硫酸镁干燥,减压浓缩。所得油状物用硅胶柱色谱法纯化,得到标题化合物(化合物5-1)。
按照类似于实施例5的方法得到下列化合物。
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]丙酸叔丁酯(化合物5-2)
[α]D 20-4.1°(c=0.52,甲醇)
IR(薄膜,cm-1)2928,1735,1680,1650,1368,1216,1154
(2R)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]丙酸叔丁酯(化合物5-3),化合物5-2的对映体
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(4-氟苯乙基)脲基]丙酸叔丁酯(化合物5-4)
[α]D 20+5.2°(c=0.99,氯仿)
IR(薄膜,cm-1)2980,1732,1681,1642,1510,1368,1220,1155,1110
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(4-氯苯乙基)脲基]丙酸叔丁酯(化合物5-5)
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(4-硝基苯乙基)脲基]丙酸叔丁酯(化合物5-6)
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(4-甲氧基苯乙基)脲基]丙酸叔丁酯(化合物5-7)
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(4-甲基苯乙基)脲基]丙酸叔丁酯(化合物5-8)
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(4-苯基苯乙基)脲基]丙酸叔丁酯(化合物5-9)
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-[2-(2-吡啶基)乙基]脲基]丙酸叔丁酯(化合物5-10)
[α]D 20-1.7°(c=0.58,甲醇)
IR(薄膜,cm-1)3390,2978,1732,1683,1651,1531,1437,1367,1216,1154,1119,722,542
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-[2-(2-萘基)乙基]脲基]丙酸叔丁酯(化合物5-11)
IR(薄膜,cm-1)3383,2981,1737,1682,1641,1530,1368,1255,1155
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(3-苯丙基)脲基]丙酸叔丁酯(化合物5-12)
[α]D 20+10.1°(c=0.51,氯仿)
IR(薄膜,cm-1)3385,2979,2935,1735,1683,1644,1529,1255,1217,1155,752,700
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-[3-(4-氟苯基)丙基]脲基]丙酸叔丁酯(化合物5-13)
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-[3-(4-氯苯基)丙基]脲基]丙酸叔丁酯(化合物5-14)
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(3-苯基-2-丙烯基)脲基]丙酸叔丁酯(化合物5-15)
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-苯氧基乙基)脲基]丙酸叔丁酯(化合物5-16)
[α]D 20+2.2°(c=1.0,甲醇)
IR(薄膜,cm-1)3379,2979,2935,1735,1682,1654,1600,1529,1498,1243,1155,1110
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯基脲基]丙酸叔丁酯(化合物5-17)
[α]D 20+19.9°(c=0.98,甲醇)
IR(薄膜,cm-1)3419,2979,2934,1732,1692,1666,1596,1495,1453,1259,1227,1157,1110
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苄基脲基]丙酸叔丁酯(化合物5-18)
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(3-丁烯基)脲基]丙酸叔丁酯(化合物5-19)
2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]乙酸叔丁酯(化合物5-20)
2-[3-[2-(乙酰硫基)乙基]-3-甲基脲基]乙酸叔丁酯(化合物5-21)
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]丁酸叔丁酯(化合物5-22)
[α]D 20-7.1°(c=1.0,甲醇)
IR(薄膜,cm-1)3390,2974,2934,1732,1682,1651,1525,1455,1367,1255,1153
(2RS)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-(叔丁氧基)丙酸叔丁酯(化合物5-23)
IR(薄膜,cm-1)2975,1738,1691,1653,1509,1366,1251,1155,1098
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-2-苯基乙酸叔丁酯(化合物5-24)
IR(薄膜,cm-1)3391,2978,1734,1685,1652,1497,1368,1208,1152,700
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-甲基脲基]-3-苯基丙酸叔丁酯(化合物5-25)
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-异戊基脲基]-3-苯基丙酸叔丁酯(化合物5-26)
IR(薄膜,cm-1)3389,2956,1731,1689,1653,1516,1368,1258,1156,1102
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环己基乙基)脲基]-3-苯基丙酸叔丁酯(化合物5-27)
[α]D 20+16.2°(c=1.0,氯仿)
IR(薄膜,cm-1)3389,2923,1730,1690,1653,1514,1367,1214,1155,701
3-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]丙酸叔丁酯(化合物5-28)
IR(薄膜,cm-1)3392,2978,2932,1726,1691,1634,1531,1367,1256,1157,951,751,701,628
(2S)-2-[3-[(2RS)-3-(乙酰硫基)-2-甲基丙基]-3-苯乙基脲基]-3-苯基丙酸叔丁酯(化合物5-29)
IR(薄膜,cm-1)3436,2975,2930,1728,1693,1650,1510,1454,1368,1256,1155,956,846,751,701,629
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-苯基丙酸叔丁酯(化合物5-30)
[α]D 20-9.5°(c=0.98,甲醇)
IR(薄膜,cm-1)3383,2977,1732,1653,1521,1370,1154,701
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-甲氧基乙基)脲基]丙酸叔丁酯(化合物5-31)
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-[2-(4-吡啶基)乙基]脲基]丙酸叔丁酯(化合物5-32)
IR(薄膜,cm-1)3382,1732,1682,1644,1602,1530,1367,1217,1154
2-[3-[2-(乙酰硫基)乙基]-3-(2-环己基乙基)脲基]乙酸叔丁酯(化合物5-33)
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环戊基乙基)脲基]丙酸叔丁酯(化合物5-34)
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环庚基乙基)脲基]丙酸叔丁酯(化合物5-35)
[α]D 20+1.0°(c=1.0,甲醇)
IR(薄膜,cm-1)3389,2978,2923,2853,1734,1684,1646,1526,1456
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-[2-(1-金刚烷基)乙基]脲基]丙酸叔丁酯(化合物5-36)
熔点111~113℃
[α]D 20+2.2°(c=1.0,甲醇)
IR(KBr,cm-1)3376,2972,2901,2847,1749,1683,1651,1534,1453,1211,1152
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环丙基乙基)脲基]丙酸叔丁酯(化合物5-37)
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环丁基乙基)脲基]丙酸叔丁酯(化合物5-38)
IR(薄膜,cm-1)3390,2978,1738,1682,1644,1530,1454,1368,1258,1156,1108
(2S)-2-[3-[3-(乙酰硫基)丙基]-3-(2-环己基乙基)脲基]丙酸叔丁酯(化合物5-39)
[α]D 20-8.9°(c=1.0,甲醇)
IR(薄膜,cm-1)3390,2980,2924,1737,1682,1644,1530,1450,1368,1216,1156
(2R)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环己基乙基)脲基]丙酸叔丁酯(化合物5-40)
[α]D 20-4.3°(c=1.0,甲醇)
IR(薄膜,cm-1)3362,2978,2924,2852,1732,1694,1633,1520,1450,1407,1368,1258,1215,1156
2-[3-[2-(乙酰硫基)乙基]-3-[2-(1-金刚烷基)乙基]脲基]乙酸叔丁酯(化合物5-41)
IR(薄膜,cm-1)3390,2978,2903,2846,1743,1692,1643,1536,1366,1217,1156,755
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-[2-[3,5-二(叔丁基)-4-(甲氧基甲氧基)苯基]乙基]脲基]丙酸叔丁酯(化合物5-42)
[α]D 20+2.0°(c=1.0,甲醇)
IR(薄膜,cm-1)3390,2963,1737,1683,1645,1526,1481,1453,1430,1392,1367,1260,1164
实施例6
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-甲基丁酸叔丁酯(化合物6-1)
在氮气下,将盐酸L-缬氨酸叔丁酯(1.5g)、1,1’-羰基二咪唑(1.4g)和咪唑(0.49g)悬浮在无水四氢呋喃(72ml)中,悬浮液在室温下搅拌30分钟。向反应混合物中加入盐酸N-(2-巯基乙基)苯乙胺(参考化合物17-1,1.77g),混合物回流一小时。在冰冷却下向反应混合物中加入水,全部混合物用乙醚萃取。有机层先后用水、10%柠檬酸水溶液、水和饱和盐水洗涤,经无水硫酸镁干燥,减压浓缩。在氮气下,将所得油状物溶于氯仿(14ml),在冰冷却下,向该溶液中加入三乙胺(1.5ml)。向其中加入乙酸酐(0.81ml),混合物搅拌30分钟。在冰冷却下,向反应混合物中加入水,全部混合物用乙醚萃取。有机层先后用10%柠檬酸水溶液、水和饱和盐水洗涤,经无水硫酸镁干燥,减压浓缩。所得油状物用硅胶柱色谱法纯化,得到1.95g(65%)标题化合物(化合物6-1)。
(化合物6-1)
[α]D 20-5.1°(c=1.0,甲醇)
IR(薄膜,cm-1)3392,2967,2932,1729,1684,1653,1519,1256,1210,1151
按照类似于实施例6的方法得到下列化合物。
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]戊酸叔丁酯(化合物6-2)
[α]D 20+5.9°(c=1.0,氯仿)
IR(薄膜,cm-1)3385,2962,2873,1732,1681,1644,1530,1454,1367,1214,1153,753,701
实施例7
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环己基乙基)脲基]丙酸(化合物7-1)
向(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环己基乙基)脲基]丙酸叔丁酯(化合物5-1,2.3g)中加入4.0N氯化氢/二_烷溶液(14ml),混合物在室温下搅拌过夜。反应混合物减压浓缩,向所得油状物中加入5%碳酸氢钠水溶液(30ml)和乙酸乙酯(30ml),分离含水层与有机层。向含水层中加入5%柠檬酸水溶液进行酸化,全部混合物用乙酸乙酯萃取。有机层先后用水和饱和盐水洗涤,经无水硫酸镁干燥,减压浓缩。所得油状物用硅胶柱色谱法纯化,得到826mg(42%)标题化合物(化合物7-1),为晶体。
(化合物7-1)
熔点89.5~90.5℃
[α]D 20+7.7°(c=1.0,甲醇)
IR(KBr,cm-1)3382,2926,2853,1715,1674,1600,1549,1485,1454,1421,1381,1355,1328,1298,1223,1168,1136,1106
按照类似于实施例7的方法得到下列化合物。
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]丙酸(化合物7-2)
(2R)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]丙酸(化合物7-3),化合物7-2的对映体
熔点113.0~114.7℃
[α]D 20-2.7°(c=1.0,甲醇)
IR(薄膜,cm-1)3368,2940,1716,1675,1598,1548,1298
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(4-氟苯乙基)脲基]丙酸(化合物7-4)
[α]D 20-28.6°(c=1.0,氯仿)
IR(薄膜,cm-1)2938,1729,1679,1605,1535,1510,1220,1157
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(4-氯苯乙基)脲基]丙酸(化合物7-5)
[α]D 20+1.8°(c=1.0,甲醇)
IR(薄膜,cm-1)3376,2938,1732,1681,1614,1537,1492,1205,1143
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(4-硝基苯乙基)脲基]丙酸(化合物7-6)
[α]D 20-19.4°(c=0.54,氯仿)
IR(薄膜,cm-1)3372,2938,1735,1680,1603,1519,1345,1206,751
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(4-甲氧基苯乙基)脲基]丙酸(化合物7-7)
[α]D 20-37.9°(c=1.0,氯仿)
IR(薄膜,cm-1)3380,2937,1732,1682,1613,1513,1455,1247,1178,1035,756
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(4-甲基苯乙基)脲基]丙酸(化合物7-8)
[α]D 20-44.1°(c=0.58,氯仿)
IR(薄膜,cm-1)3377,2937,1731,1682,1614,1537,1215,1143,810,757,631
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(4-苯基苯乙基)脲基]丙酸(化合物7-9)
IR(薄膜,cm-1)3377,3025,1732,1681,1614,1537,1486,1216,1142,761
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-[2-(2-吡啶基)乙基]脲基]丙酸(化合物7-10)
IR(薄膜,cm-1)3392,1682,1594,1531,1409
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-[2-(2-萘基)乙基]脲基]丙酸(化合物7-11)
[α]D 20-38.5°(c=0.22,氯仿)
IR(薄膜,cm-1)3375,2921,1734,1679,1609,1533,1205,1141,752
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(3-苯丙基)脲基]丙酸(化合物7-12)
[α]D 20+4.9°(c=0.50,甲醇)
IR(薄膜,cm-1)3378,2938,1732,1682,1614,1536,1207,1140,753,700,631
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-[3-(4-氟苯基)丙基]脲基]丙酸(化合物7-13)
[α]D 20-31.6°(c=1.0,氯仿)
IR(薄膜,cm-1)3377,2938,1736,1680,1604,1535,1510,1219,952,832,760,630
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-[3-(4-氯苯基)丙基]脲基]丙酸(化合物7-14)
[α]D 20-33.1°(c=1.0,氯仿)
IR(薄膜,cm-1)3377,2938,1736,1680,1612,1536,1203,951,833,759,630
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(3-苯基-2-丙烯基)脲基]丙酸(化合物7-15)
[α]D 20-35.3°(c=1.0,氯仿)
IR(薄膜,cm-1)3375,2985,1730,1680,1611,1534,1210,751,629
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-苯氧基乙基)脲基]丙酸(化合物7-16)
[α]D 20+5.1°(c=0.99,甲醇)
IR(薄膜,cm-1)3374,2938,1737,1680,1600,1535,1496,1239
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯基脲基]丙酸(化合物7-17)
[α]D 20+26.0°(c=0.98,甲醇)
IR(薄膜,cm-1)3408,2985,1736,1692,1625,1594,1453
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苄基脲基]丙酸(化合物7-18)
[α]D 20+6.5°(c=0.5,甲醇)
IR(薄膜,cm-1)3375,2985,1730,1679,1612,1534,1496,1452,1410,1357,1211,1140,755,630
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(3-丁烯基)脲基]丙酸(化合物7-19)
IR(薄膜,cm-1)3378,2980,2938,1732,1682,1614,1535,1456,1411,1356,1297,1210,1137
2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]乙酸(化合物7-20)
熔点132.5~134.5℃(分解)
IR(KBr,cm-1)2937,1740,1680,1606,1555,1204
2-[3-[2-(乙酰硫基)乙基]-3-甲基脲基]乙酸(化合物7-21)
熔点94.8~101.0℃
IR(KBr,cm-1)3385,2926,1756,1684,1603,1560,1398,1220,1142,1099,912,766,694,628
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]丁酸(化合物7-22)
熔点101.0~104.2℃
[α]D 20-2.5°(c=1.0,甲醇)
IR(KBr,cm-1)3385,2942,1716,1676,1609,1546,1411,1301,1254,1217,700
(2RS)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-羟基丙酸(化合物7-23)
熔点113.0~119.0℃
IR(KBr,cm-1)3156,2942,1741,1682,1630,1546,1212,1018
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-2-苯基乙酸(化合物7-24)
[α]D 20+51.2°(c=1.0,甲醇)
IR(薄膜,cm-1)3378,3027,1732,1686,1613,1519,1454,1356,1216,1139,754
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-甲基脲基]-3-苯基丙酸(化合物7-25)
[α]D 20-19.6°(c=0.47,甲醇)
IR(薄膜,cm-1)3369,2928,1730,1691,1612,1530,1397,1355,1301,1209,1136,1048,952,756,701,627
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-异戊基脲基]-3-苯基丙酸(化合物7-26)
[α]D 20-18.9°(c=0.97,甲醇)
IR(薄膜,cm-1)3376,2955,1734,1690,1612,1527,1420,1356,1211,1135
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环己基乙基)脲基]-3-苯基丙酸(化合物7-27)
[α]D 20-33.9°(c=1.0,氯仿)
IR(薄膜,cm-1)3376,2923,2851,1732,1691,1613,1527,1202,1134,950,755,701,627
3-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]丙酸(化合物7-28)
熔点110.4~113.6℃
IR(KBr,cm-1)3364,2948,1708,1679,1599,1556,1228,952,744,702
(2S)-2-[3-[(2RS)-3-(乙酰硫基)-2-甲基丙基]-3-苯乙基脲基]-3-苯基丙酸(化合物7-29)
IR(薄膜,cm-1)3433,2928,1732,1692,1606,1523,1454,1418,1356,1202,1135,955,752,701,628
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-苯基丙酸(化合物7-30)
[α]D 20-17.4°(c=0.51,甲醇)
IR(薄膜,cm-1)3369,3027,2927,1734,1678,1612,1529,1201,751,701
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-甲氧基乙基)脲基]丙酸(化合物7-31)
[α]D 20-60.3°(c=1.0,氯仿)
IR(薄膜,cm-1)3370,2936,1732,1682,1633,1538,1455,1409,1357,1205,1115,1066,1008,952,758
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-[2-(4-吡啶基)乙基]脲基]丙酸(化合物7-32)
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-甲基丁酸(化合物7-33)
[α]D 20+9.1°(c=1.0,氯仿)
IR(薄膜,cm-1)3854,3386,2964,1730,1684,1615,1526,1454,1416,1203
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]戊酸(化合物7-34)
[α]D 20-22.0°(c=1.0,氯仿)
IR(薄膜,cm-1)3375,2960,2873,1728,1680,1616,1534,1454,1203,1143,952,701
(2S)-2-[3-苯乙基-3-[2-(苯二硫基)乙基]脲基]-3-苯基丙酸(化合物7-35)
[α]D 20-6.0°(c=1.0,甲醇)
IR(薄膜,cm-1)3434,2925,1728,1603,1524,1199,740,700
2-[3-[2-(乙酰硫基)乙基]-3-(2-环己基乙基)脲基]乙酸(化合物7-36)
IR(薄膜,cm-1)3386,2923,2851,1732,1692,1614,1538,1417,757
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环戊基乙基)脲基]丙酸(化合物7-37)
IR(薄膜,cm-1)3378,2947,2867,1732,1682,1614,1532,1454,1413,1374,1356,1298,1216,1138,1110,757
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环庚基乙基)脲基]丙酸(化合物7-38)
[α]D 20+4.6°(c=1.0,甲醇)
IR(薄膜,cm-1)3379,2922,2853,1729,1685,1602,1534,1457,1413
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-[2-(1-金刚烷基)乙基]脲基]丙酸(化合物7-39)
[α]D 20+4.6°(c=1.0,甲醇)
IR(薄膜,cm-1)3380,2902,2846,1734,1684,1527,1452,1418,1207
(2S)-2-[3-[2-(甲硫基)乙基]-3-苯乙基脲基]丙酸(化合物7-40)
IR(薄膜,cm-1)3368,2919,1727,1603,1529,1203
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环丙基乙基)脲基]丙酸(化合物7-41)
[α]D 20+7.0°(c=0.52,甲醇)
IR(薄膜,cm-1)3379,2998,1732,1682,1614,1536,1454,1413,1212,1135,757
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环丁基乙基)脲基]丙酸(化合物7-42)
[α]D 20+5.3°(c=0.49,甲醇)
IR(薄膜,cm-1)3379,2936,1729,1690,1612,1533,1454,1412,1204,1134
(2S)-2-[3-[3-(乙酰硫基)丙基]-3-(2-环己基乙基)脲基]丙酸(化合物7-43)
[α]D 20-35.8°(c=1.0,氯仿)
IR(薄膜,cm-1)3418,2923,2852,1731,1693,1614,1524,1454,1415,1207
(2R)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环己基乙基)脲基]丙酸(化合物7-44)
[α]D 20-5.2°(c=1.0,甲醇)
IR(薄膜,cm-1)3380,2923,2851,1732,1682,1614,1531,1450,1206
2-[3-[2-(乙酰硫基)乙基]-3-[2-(1-金刚烷基)乙基]脲基]乙酸(化合物7-45)
IR(薄膜,cm-1)3390,2902,2846,1732,1689,1640,1538,1211,756
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-[2-[3,5-二(叔丁基)-4-羟基苯基]乙基]脲基]丙酸(化合物7-46)
[α]D 20-11.9°(c=0.52,甲醇)
IR(KBr,cm-1)3639,3582,3391,2958,1743,1684,1609,1540,1435,1236,1197
实施例8
(2S)-4-羟基-2-[3-(2-巯基乙基)-3-苯乙基脲基]丁酸(化合物8-1)
在氮气下,将(2S)-2-[3-(2-巯基乙基)-3-苯乙基脲基]-4-丁内酯(化合物1-69,2.9g)溶于甲醇(19ml)。在冰冷却下,向其中加入2N氢氧化锂水溶液(5.6ml),混合物在冰冷却下搅拌50分钟,进一步在室温下搅拌35分钟。反应混合物减压浓缩,向浓缩物中加入10%柠檬酸水溶液,全部混合物用乙酸乙酯萃取。有机层先后用水和饱和盐水洗涤,经无水硫酸镁干燥,减压浓缩,得到1.5g(48%)标题化合物(化合物8-1)。
按照类似于实施例8的方法得到下列化合物。
(2S)-2-[3-[2-(甲硫基)乙基]-3-苯乙基脲基]-3-苯基丙酸(化合物8-2)
[α]D 20-2.8°(c=0.49,甲醇)
IR(薄膜,cm-1)3435,3027,2918,1728,1604,1522,1454,1201,752,701
(2R)-3-(苄硫基)-2-[3-[2-(苄硫基)乙基]-3-苯乙基脲基]丙酸(化合物8-3)
[α]D 20-32.4°(c=0.48,甲醇)
IR(薄膜,cm-1)3426,3026,2920,1729,1602,1520,1453,1422,1364,1303,1201,1071,1028,753,701
实施例9
(2S)-2-[3-[2-巯基-1-(巯基甲基)乙基]-3-苯乙基脲基]-3-苯基丙酸(化合物9-1)
在氮气下和干冰-甲醇冷却下,向液氨(80ml)中滴加(2S)-2-[3-[2-(苄硫基)-1-[(苄硫基)甲基]乙基]-3-苯乙基脲基]-3-苯基丙酸苄基酯(化合物1-72,996mg)的无水四氢呋喃(20ml)溶液。然后,向其中分批加入金属钠(300mg),直到颜色不消失为止,混合物搅拌一小时。向反应混合物中分批加入氯化铵进行脱色,然后在室温下向混合物中通入氮气,使氨蒸发。向所得残余物中加入1N氢氯酸进行酸化,全部混合物用乙酸乙酯萃取。有机层先后用水和饱和盐水洗涤,经无水硫酸镁干燥,减压浓缩,得到标题化合物(化合物9-1)。
实施例10
(2S)-2-[3-(1,2-二硫戊环-4-基)-3-苯乙基脲基]-3-苯基丙酸(化合物10-1)
将(2S)-2-[3-[2-巯基-1-(巯基甲基)乙基]-3-苯乙基脲基]-3-苯基丙酸(化合物9-1,780mg)溶于甲醇(2ml)。向该溶液中加入1N氨水(10ml)和1%氯化铁水溶液(0.5ml),混合物在室温下搅拌两小时,同时通入空气。反应混合物减压浓缩,在冰冷却下向浓缩物中加入2N氢氯酸进行酸化,全部混合物用乙酸乙酯萃取。有机层先后用水和饱和盐水洗涤,经无水硫酸钠干燥,减压浓缩。所得油状物用硅胶柱色谱法纯化,得到514mg(66%)标题化合物(化合物10-1),为油状物。
(化合物10-1)
[α]D 20-8.4°(c=0.50,甲醇)
IR(薄膜,cm-1)3437,3339,3026,2934,1732,1603,1520,1454,1417,1345,1215,753,701
实施例11
(2S)-2-[3-(2-巯基乙基)-3-苯乙基脲基]-3-苯基丙酸(化合物11-1)
在氮气下,将(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-苯基丙酸(化合物7-30,646mg)溶于28%氨水(15ml),溶液在室温下搅拌一小时。向反应混合物中加入水和乙酸乙酯,分离含水层与有机层。在冰冷却下,向含水层中加入6N氢氯酸进行酸化,全部混合物用乙酸乙酯萃取。有机层先后用水和饱和盐水洗涤,经无水硫酸钠干燥,减压浓缩。所得油状物用硅胶柱色谱法纯化,得到415mg(81%)标题化合物(化合物11-1)。
(化合物11-1)
[α]D 20-8.6°(c=0.15,甲醇)
IR(薄膜,cm-1)3368,3027,2933,1727,1604,1526,1203,752,701
按照类似于实施例11的方法得到下列化合物。
(2S,2’S)-2,2’-[3,3’-二苯乙基-3,3’-(2,2’-二硫基二乙基)二脲基]-3,3’-二苯基二(丙酸)(化合物11-2)
[α]D 20-10.0°(c=0.43,甲醇)
IR(薄膜,cm-1)3372,3026,2926,1726,1604,1524,1202,752,701
实施例12
(2S)-2-[3-[2-(苄氧羰基硫基)乙基]-3-苯乙基脲基]-3-苯基丙酸(化合物12-1)
在氮气下,将(2S)-2-[3-(2-巯基乙基)-3-苯乙基脲基]-3-苯基丙酸(化合物11-1,108mg)溶于无水二氯甲烷(1.5ml),溶液搅拌。在冰冷却下,向该溶液中先后加入N,N-二异丙基乙胺(0.07ml)和苄氧羰基氯(0.05ml),混合物在室温下搅拌过夜。反应混合物减压浓缩,向残余物中加入水,全部混合物用乙酸乙酯萃取。有机层先后用10%柠檬酸水溶液、水和饱和盐水洗涤,经无水硫酸钠干燥,减压浓缩。所得油状物用硅胶柱色谱法纯化,得到102mg(69%)标题化合物(化合物12-1)。
(化合物12-1)
[α]D 20-14.9°(c=0.34,甲醇)
IR(薄膜,cm-1)3381,3028,1698,1614,1530,1144,751,699
按照类似于实施例12的方法得到下列化合物。
(2S)-2-[3-[2-(叔丁氧羰基硫基)乙基]-3-苯乙基脲基]-3-苯基丙酸(化合物12-2)
实施例13
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环己基乙基)脲基]丙酰]-4-甲基哌嗪(化合物13-1)
在氮气下,将(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环己基乙基)脲基]丙酸(化合物7-1,826mg)、N-甲基哌嗪(0-27ml)和1-羟基苯并三唑(357mg)溶于无水二氯甲烷(5ml)。在冰冷却下,向该溶液中先后加入N-甲基吗啉(0.29ml)和盐酸1-乙基-3-(3-二甲氨基丙基)碳二亚胺(506mg),混合物在室温下搅拌过夜。反应混合物减压浓缩,向所得油状物中加入5%碳酸氢钠水溶液(30ml),全部混合物用乙酸乙酯萃取。有机层先后用水和饱和盐水洗涤,经无水硫酸镁干燥,减压浓缩。所得油状物用硅胶柱色谱法纯化,得到801mg(78%)标题化合物(化合物13-1)。
(化合物13-1)
[α]D 20+25.2°(c=0.99,氯仿)
IR(薄膜,cm-1)3378,2923,2850,1691,1633,1519,1448,1292,1215,1140,754
按照类似于实施例13的方法得到下列化合物。
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]丙酰]-4-甲基哌嗪(化合物13-2)
[α]D 20+11.9°(c=0.50,甲醇)
IR(薄膜,cm-1)3377,2976,2938,2794,1688,1636,1530,1448,
1356,1292,1249,1216,1172,1141,1032,1002,952,752,702,628
1-[(2R)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]丙酰]-4-甲基哌嗪(化合物13-3),化合物13-2的对映体
[α]D 20-11.4°(c=1.0,甲醇)
IR(薄膜,cm-1)3376,2938,1688,1634,1529,1449,1292,1215,1141
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(4-氟苯乙基)脲基]丙酰]-4-甲基哌嗪(化合物13-4)
[α]D 20+10.4°(c=1.0,甲醇)
IR(薄膜,cm-1)2939,1687,1632,1510,1448,1292,1220,1142,1002,754
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(4-氯苯乙基)脲基]丙酰]-4-甲基哌嗪(化合物13-5)
[α]D 20+10.7°(c=0.53,甲醇)
IR(薄膜,cm-1)3369,2938,2794,1688,1635,1532,1492,1448,1292,1216,1141,1002,754
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(4-硝基苯乙基)脲基]丙酰]-4-甲基哌嗪(化合物13-6)
[α]D 20+13.2°(c=0.55,甲醇)
IR(薄膜,cm-1)3370,2938,2795,1688,1633,1519,1345,1291,1216,1141,750
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(4-甲氧基苯乙基)脲基]丙酰]-4-甲基哌嗪(化合物13-7)
[α]D 20+8.8°(c=0.99,甲醇)
IR(薄膜,cm-1)3378,2937,2794,1688,1632,1513,1463,1292,1247,1215,1141,1002
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(4-甲基苯乙基)脲基]丙酰]-4-甲基哌嗪(化合物13-8)
[α]D 20+24.3°(c=1.0,氯仿)
IR(薄膜,cm-1)3370,2937,1689,1632,1514,1447,1291,1214,1141,1102,627
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(4-苯基苯乙基)脲基]丙酰]-4-甲基哌嗪(化合物13-9)
[α]D 20+10.0°(c=0.55,甲醇)
IR(薄膜,cm-1)3378,2937,2794,1687,1633,1518,1447,1141,1002,756
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-[2-(2-吡啶基)乙基]脲基]丙酰]-4-甲基哌嗪(化合物13-10)
[α]D 20+11.0°(c=0.52,甲醇)
IR(薄膜,cm-1)3377,2936,2794,1689,1637,1441,1292,1141,1001
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-[2-(2-萘基)乙基]脲基]丙酰]-4-甲基哌嗪(化合物13-11)
[α]D 20+8.7°(c=0.96,甲醇)
IR(薄膜,cm-1)3376,1687,1633,1508,1446,1141,751
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(3-苯丙基)脲基]丙酰]-4-甲基哌嗪(化合物13-12)
[α]D 20+15.5°(c=0.50,甲醇)
IR(薄膜,cm-1)3368,2937,2793,1689,1632,1530,1450,1291,1141,751
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-[3-(4-氟苯基)丙基]脲基]丙酰]-4-甲基哌嗪(化合物13-13)
[α]D 20+27.3°(c=1.0,氯仿)
IR(薄膜,cm-1)3369,2938,1689,1636,1510,1448,1292,1219,1141,755
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-[3-(4-氯苯基)丙基]脲基]丙酰]-4-甲基哌嗪(化合物13-14)
[α]D 20+26.2°(c=0.95,氯仿)
IR(薄膜,cm-1)3369,2937,1689,1633,1530,1492,1292,1214,1141,754,628
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(3-苯基-2-丙烯基)脲基]丙酰]-4-甲基哌嗪(化合物13-15)
[α]D 20+30.0°(c=1.0,氯仿)
IR(薄膜,cm-1)3374,2937,2794,1689,1632,1529,1448,1292,1141,752
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-苯氧基乙基)脲基]丙酰]-4-甲基哌嗪(化合物13-16)
[α]D 20+14.6°(c=1.0,甲醇)
IR(薄膜,cm-1)3369,2794,1688,1638,1497,1462,1242
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯基脲基]丙酰]-4-甲基哌嗪(化合物13-17)
[α]D 20+35.1°(c=1.0,甲醇)
IR(薄膜,cm-1)3400,2976,2938,1693,1640,1596,1494,1447
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苄基脲基]丙酰]-4-甲基哌嗪(化合物13-18)
[α]D 20+12.1°(c=0.5,甲醇)
IR(薄膜,cm-1)3376,2937,1687,1530,1451,1291,1217,1141,1002,753
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(3-丁烯基)脲基]丙酰]-4-甲基哌嗪(化合物13-19)
[α]D 20+15.2°(c=1.0,甲醇)
IR(薄膜,cm-1)3350,2976,2937,2793,1690,1637,1530,1447,1292,1218,1140
1-[2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]乙酰]-4-甲基哌嗪(化合物13-20)
IR(薄膜,cm-1)2937,1688,1640,1507,1442,1291,1141
1-[2-[3-[2-(乙酰硫基)乙基]-3-甲基脲基]乙酰]-4-甲基哌嗪(化合物13-21)
熔点74.6~77.0℃
IR(KBr,cm-1)3361,2937,2794,1688,1653,1633,1547,1459,1348,1289,1228,1145,1054,1042,998,956,629,574
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]丁酰]-4-甲基哌嗪(化合物13-22)
[α]D 20+10.1°(c=1.0,甲醇)
IR(薄膜,cm-1)3368,2967,2936,1689,1633,1528,1453,1293,1141
1-[(2RS)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-羟基丙酰]-4-甲基哌嗪(化合物13-23)
IR(薄膜,cm-1)3376,2939,1689,1628,1520,1454,1292,1142,1001
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-2-苯基乙酰]-4-甲基哌嗪(化合物13-24)
[α]D 20+36.4°(c=1.0,甲醇)
IR(薄膜,cm-1)3390,2939,1689,1636,1497,1445,1293,1142,1001,753,701
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-甲基脲基]-3-苯基丙酰]-4-甲基哌嗪(化合物13-25)
[α]D 20+29.7°(c=0.50,氯仿)
IR(薄膜,cm-1)3329,2938,2797,1691,1632,1531,1454,1386,1355,1292,1250,1217,1141,1033,1002,752,701,626
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-异戊基脲基]-3-苯基丙酰]-4-甲基哌嗪(化合物13-26)
[α]D 20+27.5°(c=1.0,甲醇)
IR(薄膜,cm-1)3345,2951,1690,1630,1528,1449,1357,1292,1217,1140
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环己基乙基)脲基]-3-苯基丙酰]-4-甲基哌嗪(化合物13-27)
[α]D 20+30.3°(c=1.0,氯仿)
IR(薄膜,cm-1)3350,2922,1691,1632,1526,1448,1292,1249,1215,753,700,627
1-[3-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]丙酰]-4-甲基哌嗪(化合物13-28)
熔点81.3~84.8℃
IR(KBr,cm-1)3312,2936,2789,1694,1626,1532,1477,1292,1140,1003,700,629
1-[(2S)-2-[3-[(2RS)-3-乙酰硫基-2-甲基丙基]-3-苯乙基脲基]-3-苯基丙酰]-4-甲基哌嗪(化合物13-29)
IR(薄膜,cm-1)3360,2934,2794,1691,1631,1497,1454,1291,1141,1002,751,700,628
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-苯基丙酰]-4-乙基哌嗪(化合物13-30)
[α]D 20+21.1°(c=1.0,甲醇)
IR(薄膜,cm-1)3368,2970,2930,1689,1632,1526,1454,1353,1285,1138
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-苯基丙酰]-4-(2-羟乙基)哌嗪(化合物13-31)
[α]D 20+18.4°(c=1.0,甲醇)
IR(薄膜,cm-1)3374,2936,1688,1627,1526,1454,1354,1217,1138
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-苯基丙酰]-4-(羧甲基)哌嗪(化合物13-32)
熔点230℃(分解)
IR(KBr,cm-1)3373,1636,1522,1123
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-苯基丙酰]-4-甲基高哌嗪(化合物13-33)
[α]D 20+17.7°(c=1.0,甲醇)
IR(薄膜,cm-1)3363,2940,1688,1628,1527,1496,1454,1357,1288,1202,1134
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-(4-吡啶基)丙酰胺(化合物13-34)
[α]D 20-27.2°(c=1.0,氯仿)
IR(薄膜,cm-1)3266,3184,3026,1686,1628,1595,1530,1415,1290,1194,1140,754
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-(3-吡啶基)丙酰胺(化合物13-35)
[α]D 20-34.0°(c=1.0,氯仿)
IR(薄膜,cm-1)3263,3026,1682,1621,1538,1483,1424,1286,1200,1137,752
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-甲氧基乙基)脲基]丙酰]-4-甲基哌嗪(化合物13-36)
[α]D 20+30.0°(c=0.33,氯仿)
IR(薄膜,cm-1)3368,2978,2936,1690,1636,1530,1463,1141,1114,1002,628
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-[2-(4-吡啶基)乙基]脲基]丙酰]-4-甲基哌嗪(化合物13-37)
[α]D 20+8.1°(c=1.0,甲醇)
IR(薄膜,cm-1)2981,1687,1636,1603,1448,1142,754
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-甲基丁酰]-4-甲基哌嗪(化合物13-38)
[α]D 20+31.4°(c=1.1,氯仿)
IR(薄膜,cm-1)3387,2937,2794,1689,1633,1519
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]戊酰]-4-甲基哌嗪(化合物13-39)
[α]D 20+22.4°(c=1.0,氯仿)
IR(薄膜,cm-1)3370,2938,1688,1632,1531,1454,1291,1217,1141,753
1-[(2S)-2-[3-[2-(苄氧羰基硫基)乙基]-3-苯乙基脲基]-3-苯基丙酰]-4-甲基哌嗪(化合物13-40)
[α]D 20+8.7°(c=0.51,甲醇)
IR(薄膜,cm-1)3382,2937,1705,1633,1454,1142,751,700
1-[(2S)-2-[3-[2-(叔丁氧羰基硫基)乙基]-3-苯乙基脲基]-3-苯基丙酰]-4-甲基哌嗪(化合物13-41)
IR(薄膜,cm-1)3367,2979,1698,1632,1528,1453,1204,1130,752,701
1-[(2S)-2-[3-苯乙基-3-[2-(苯二硫基)乙基]脲基]-3-苯基丙酰]-4-甲基哌嗪(化合物13-42)
[α]D 20+16.4°(c=0.96,甲醇)
IR(薄膜,cm-1)3340,2936,1627,1530,1454,746,700
1-[(2S)4-羟基-2-[3-(2-巯基乙基)-3-苯乙基脲基]丁酰]-4-甲基哌嗪(化合物13-43)
1-甲基-4-[(2S)-2-[3-[2-(甲硫基)乙基]-3-苯乙基脲基]-3-苯基丙酰]哌嗪(化合物13-44)
[α]D 20+15.1°(c=0.52,甲醇)
IR(薄膜,cm-1)3346,2918,1628,1497,1452,1291,1214,1144,1002,750,700
1-[(2R)-3-(苄硫基)-2-[3-[2-(苄硫基)乙基]-3-苯乙基脲基]丙酰]-4-甲基哌嗪(化合物13-45)
[α]D 20-19.9°(c=0.48,甲醇)
IR(薄膜,cm-1)3349,3026,2937,2794,1632,1495,1452,1365,1293,1206,1143,1072,1029,1001,753,701
1-[(2S)-2-[3-(1,2-二硫戊环-4-基)-3-苯乙基脲基]-3-苯基丙酰]-4-甲基哌嗪(化合物13-46)
[α]D 20+16.2°(c=0.50,氯仿)
IR(薄膜,cm-1)3344,2938,2796,1628,1497,1454,1291,1248,1217,1143,1001,752,701
1,1’-二甲基-4,4’-[(2S,2’S)-2,2’-[3,3’-二苯乙基-3,3’-(2,2’-二硫基二乙基)二脲基]-3,3’-二苯基二丙酰]二哌嗪(化合物13-47)
[α]D 20+3.0°(c=0.86,甲醇)
IR(薄膜,cm-1)3341,3026,1628,1514,1452,750,700
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-苯基丙酰]-4-(三氟乙酰)哌嗪(化合物13-48)
[α]D 20+33.1°(c=0.52,甲醇)
IR(薄膜,cm-1)3370,3026,2928,1694,1644,1524,1454,1366,1284,1243,1200,1142,1010,952,753,701
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环己基乙基)脲基]丙酰]哌啶(化合物13-49)
[α]D 20+29.3°(c=0.47,氯仿)
IR(薄膜,cm-1)3379,2923,2852,1691,1632,1530,1447,1214,1135,752
4-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环己基乙基)脲基]丙酰]吗啉(化合物13-50)
[α]D 20+26.1°(c=0.49,氯仿)
IR(薄膜,cm-1)3370,2922,2851,1690,1635,1526,1447,1270,1116,1030,755
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环己基乙基)脲基]-N-[2-(二甲氨基)乙基]-N-甲基丙酰胺(化合物13-51)
[α]D 20+6.2°(c=1.0,甲醇)
IR(薄膜,cm-1)3341,2923,2851,1692,1634,1490,1448,1418,1355,1295,1223,1184,1135,1043
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环己基乙基)脲基]-N-[2-(二甲氨基)乙基]丙酰胺(化合物13-52)
[α]D 20+12.7°(c=0.99,甲醇)
IR(薄膜,cm-1)3296,3089,2923,2851,2818,2768,1691,1662,1626,1535,1448,1409,1355,1225,1135
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环己基乙基)脲基]-N,N-二甲基丙酰胺(化合物13-53)
[α]D 20+10.1°(c=1.0,甲醇)
IR(薄膜,cm-1)3350,2924,2851,1691,1642,1503,1448,1419,1356,1297,1227,1184,1135
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环己基乙基)脲基]丙酰]-4-甲基高哌嗪(化合物13-54)
[α]D 20+21.9°(c=1.1,氯仿)
IR(薄膜,cm-1)3350,2922,2849,1691,1633,1527,1449,1203,1134,951,755
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环己基乙基)脲基]丙酰]-3-吡咯啉(化合物13-55)
[α]D 20+19.7°(c=1.0,氯仿)
IR(薄膜,cm-1)3338,2980,2922,2851,1690,1644,1621,1530,1460,1357,1294,1221,1136,950,754
1-[2-[3-[2-(乙酰硫基)乙基]-3-(2-环己基乙基)脲基]乙酰]-4-甲基哌嗪(化合物13-56)
IR(薄膜,cm-1)3400,2922,2850,1691,1641,1508,1444,1292,1142
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环戊基乙基)脲基]丙酰]-4-甲基哌嗪(化合物13-57)
[α]D 20+13.5°(c=1.0,甲醇)
IR(薄膜,cm-1)3377,2942,2865,2794,1690,1632,1510,1448,1292,1216,1141
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环庚基乙基)脲基]丙酰]-4-甲基哌嗪(化合物13-58)
[α]D 20+12.2°(c=0.97,甲醇)
IR(薄膜,cm-1)3378,2923,2852,1692,1632,1446,1292
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-[2-(1-金刚烷基)乙基]脲基]丙酰]-4-甲基哌嗪(化合物13-59)
[α]D 20+14.0°(c=1.0,甲醇)
IR(薄膜,cm-1)3380,2902,2845,1690,1636,1507,1448,1292
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环丙基乙基)脲基]丙酰]-4-甲基哌嗪(化合物13-60)
[α]D 20+9.4°(c=1.5,甲醇)
IR(薄膜,cm-1)3369,2997,2938,1691,1632,1510,1447,1141,1002,753
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环丁基乙基)脲基]丙酰]-4-甲基哌嗪(化合物13-61)
[α]D 20+13.9°(c=0.53,甲醇)
IR(薄膜,cm-1)3368,2938,1691,1632,1530,1447,1140,754
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环己基乙基)脲基]丙酰]-4-环己基哌嗪(化合物13-62)
[α]D 20+13.6°(c=1.0,甲醇)
IR(薄膜,cm-1)3382,2925,2852,1693,1632,1510,1448,1298,1276,1238,1216,1138
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环己基乙基)脲基]-N-(2-吡啶甲基)丙酰胺(化合物13-63)
[α]D 20+16.0°(c=1.0,甲醇)
IR(薄膜,cm-1)3293,2923,1682,1632,1594,1531,1449,754
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环己基乙基)脲基]-N-(4-吡啶甲基)丙酰胺(化合物13-64)
[α]D 20+17.1°(c=1.0,甲醇)
IR(薄膜,cm-1)3286,2923,2851,1682,1632,1531,1449,1416
2-[3-[2-(乙酰硫基)乙基]-3-(2-环己基乙基)脲基]-N-(2-羟乙基)乙酰胺(化合物13-65)
IR(薄膜,cm-1)3334,2923,2851,1633,1538,755
1-[(2S)-2-[3-[3-(乙酰硫基)丙基]-3-(2-环己基乙基)脲基]丙酰]-4-甲基哌嗪(化合物13-66)
[α]D 20+5.9°(c=1.0,甲醇)
IR(薄膜,cm-1)3354,2922,2850,2793,1693,1632,1507,1448,1292,1214,1140
1-[(2R)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环己基乙基)脲基]丙酰]-4-甲基哌嗪(化合物13-67)
[α]D 20-11.9°(c=1.0,甲醇)
IR(薄膜,cm-1)3380,2923,2851,1692,1633,1447,1292,1140
1-[2-[3-[2-(乙酰硫基)乙基]-3-[2-(1-金刚烷基)乙基]脲基]乙酰]-4-甲基哌嗪(化合物13-68)
IR(薄膜,cm-1)3400,2902,2846,2795,1692,1640,1510,1443,754
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-[2-[3,5--二(叔丁基)-4-羟基苯基]乙基]脲基]丙酰]-4-甲基哌嗪(化合物13-69)
实施例14
1-[(2S)-2-[3-[4-(乙酰氧基)苯乙基]-3-[2-(乙酰硫基)乙基]脲基]丙酰]-4-甲基哌嗪(化合物14-1)
在氮气下和干冰-甲醇冷却下,向液氨(40ml)中滴加(2S)-2-[3-[4-(苄氧基)苯乙基]-3-[2-(苄硫基)乙基]脲基]丙酸苄基酯(化合物1-55,843mg)的无水四氢呋喃(10ml)溶液。然后,向其中分批加入金属钠(300mg),直到颜色不消失为止,混合物搅拌一小时。向反应混合物中分批加入氯化铵进行脱色,然后在室温下向混合物中通入氮气,使氨蒸发。向所得残余物中加入1N氢氯酸(50ml),全部混合物用乙酸乙酯萃取。有机层用饱和盐水洗涤,经无水硫酸镁干燥,减压浓缩。
在氮气下,将所得油状物溶于无水二氯甲烷(7.2ml),向该溶液中加入N-甲基哌嗪(0.32ml)和1-羟基苯并三唑(192mg)。在冰冷却下,向该混合物中加入盐酸1-乙基-3-(3-二甲氨基丙基)碳二亚胺(360mg),混合物在室温下避光搅拌过夜。反应混合物减压浓缩,向所得油状物中加入10%碳酸氢钠水溶液(50ml),全部混合物用乙酸乙酯萃取。有机层用饱和盐水洗涤,经无水硫酸镁干燥,减压浓缩。
在氮气下,将所得油状物溶于丙酮(10ml)-水(10ml),向该溶液中加入三正丁基膦(0.25ml),混合物搅拌15分钟。在冰冷却下,向该混合物中先后加入三乙胺(0.61ml)和乙酸酐(0.41ml),混合物在室温下搅拌30分钟。向反应混合物中加入乙酸乙酯。有机层先后用10%碳酸氢钠水溶液和饱和盐水洗涤,经无水硫酸钠干燥,减压浓缩。所得油状物用硅胶柱色谱法纯化,得到324mg(47%)标题化合物(化合物14-1)。
(化合物14-1)
[α]D 20+21.8°(c=0.98,氯仿)
IR(薄膜,cm-1)3375,2937,2794,1762,1688,1636,1508,1447,1368,1292,1195,1141
按照类似于实施例14的方法得到下列化合物。
1-[(2S)-2-[3-[2-(乙酰硫基)-2-甲基丙基]-3-苯乙基脲基]丙酰]-4-甲基哌嗪(化合物14-2)
[α]D 20+11.5°(c=0.53,甲醇)
IR(薄膜,cm-1)3420,2970,2937,2793,1680,1636,1498,1448,1364,1292,1202,1142,1112,1002,751,702
1-[(2S)-2-[3-[(2RS)-2-(乙酰硫基)-3-甲基丁基]-3-苯乙基脲基]丙酰]-4-甲基哌嗪(化合物14-3)
IR(薄膜,cm-1)3382,2960,2794,1687,1633,1505,1462,1366,1292,1230,1173,1142
1-[(2RS)-3-(乙酰硫基)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-甲基丁酰]-4-甲基哌嗪(化合物14-4)
实施例15
(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-4-甲基戊酸(化合物15-1)
将(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-4-甲基戊酸乙酯(化合物1-31,1.00g)溶于四氢呋喃(3.5ml)-乙醇(2.8ml)的混合溶剂。在冰冷却下,向其中加入2N氢氧化锂水溶液(1.7ml),混合物在冰冷却下搅拌25分钟,进一步在室温下搅拌一小时。向反应混合物中加入5%柠檬酸水溶液,全部混合物用乙酸乙酯萃取。有机层先后用水和饱和盐水洗涤,经无水硫酸镁干燥,减压浓缩,得到1.02g(定量)标题化合物(化合物15-1)。
(化合物15-1)
[α]D 20-4.7°(c=0.95,甲醇)
IR(薄膜,cm-1)3340,2957,1724,1620,1536,1217
按照类似于实施例15的方法得到下列化合物。
(2S)-2-[3-(3-羟丙基)-3-苯乙基脲基]-3-苯基丙酸(化合物15-2)
[α]D 20-12.4°(c=0.50,甲醇)
IR(薄膜,cm-1)3340,3027,2933,1728,1622,1526,1496,1454,1418,1357,1216,1079,1054,1031,946,753,701
(2S)-2-[3-[(2RS)-2-羟丙基]-3-苯乙基脲基]-3-苯基丙酸(化合物15-3)
IR(薄膜,cm-1)3362,3027,2970,1728,1622,1526,1497,1455,1416,1375,1217,1079,1057,753,701
(2RS)-2-[3-(2-羟乙基)-3-苯乙基脲基]-4-(甲硫基)丁酸(化合物15-4)
IR(薄膜,cm-1)3374,2918,1732,1614,1532,1219,1047,752,701
(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(4-硝基苯基)丙酸(化合物15-5)
[α]D 20-34.4°(c=0.52,氯仿)
IR(薄膜,cm-1)3384,2934,1725,1605,1519,1454,1346,1047
(2S)-3-(4-氯苯基)-2-[3-(2-羟乙基)-3-苯乙基脲基]丙酸(化合物15-6)
[α]D 20-46.4°(c=0.50,氯仿)
IR(薄膜,cm-1)3353,2933,1721,1622,1529,1493,1362,1217
(2S)-2-[3-(2-羟乙基)-3-异戊基脲基]-3-(4-硝基苯基)丙酸(化合物15-7)
[α]D 20-28.6°(c=0.96,氯仿)
IR(薄膜,cm-1)3352,2955,1725,1606,1520,1468,1346,1219,1049
(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(2-硝基-4-联苯基)丙酸(化合物15-8)
[α]D 20-30.6°(c=0.51,氯仿)
IR(薄膜,cm-1)3371,2933,1726,1620,1529,1358,1218,756,701
(2S)-3-[4-(苯磺酰)-3-硝基苯基]-2-[3-(2-羟乙基)-3-苯乙基脲基]丙酸(化合物15-9)
[α]D 20-24.7°(c=0.48,氯仿)
IR(薄膜,cm-1)3390,2932,1728,1604,1544,1159,752
(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(2-萘基)丙酸(化合物15-10)
[α]D 20+3.1°(c=1.1,甲醇)
IR(薄膜,cm-1)3366,3025,2932,1727,1620,1530,1217,1047
(2R)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(甲硫基)丙酸(化合物15-11)
[α]D 20+6.2°(c=0.5,甲醇)
IR(薄膜,cm-1)3369,2921,1729,1616,1526,1454,1420,1367,1213,1047,751,701
(2R)-3-(苄硫基)-2-[3-(2-羟乙基)-3-苯乙基脲基]丙酸(化合物15-12)
[α]D 20-31.8°(c=0.50,甲醇)
IR(薄膜,cm-1)3382,2926,1730,1615,1524,1454,1418,1366,1305,1210,1047,752,701
(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-[4-(苄氧基)苯基]丙酸(化合物15-13)
[α]D 20+1.2°(c=0.95,甲醇)
IR(KBr,cm-1)3364,2932,1728,1613,1511,1241,1043
(2S)-2-[3-[2-(1-环己烯基)乙基]-3-(2-羟乙基)脲基]丙酸(化合物15-14)
IR(薄膜,cm-1)3374,2929,1732,1614,1537,1216,757
(2S)-2-[3-(2-羟乙基)-3-(3-甲基-3-丁烯基)脲基]丙酸(化合物15-15)
[α]D 20-66.8°(c=0.52,氯仿)
IR(薄膜,cm-1)3370,2937,1728,1614,1536,1218,1046,893,758
2-[3-(2-环己基乙基)-3-(2-羟乙基)脲基]-2-甲基丙酸(化合物15-16)
IR(薄膜,cm-1)3308,2923,2851,1716,1623,1530,1411,1363,1276,1168,1051,757
1-[3-(2-环己基乙基)-3-(2-羟乙基)脲基]-1-环丙烷羧酸(化合物15-17)
IR(薄膜,cm-1)3360,2923,2851,1714,1632,1529,1448,1416,1273,1194,1050,756
1-[3-(2-环己基乙基)-3-(2-羟乙基)脲基]-1-环戊烷羧酸(化合物15-18)
熔点126.0~127.5℃(分解)
IR(KBr,cm-1)3300,2923,1670,1629,1533,1302
实施例16
(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-苯基丙酸(化合物16-1)
在氮气下,向(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-4-苯基丙酸苄基酯(化合物1-43,1.92g)的四氢呋喃(14ml)溶液中加入20%氢氧化钯-碳(200mg)。混合物在氢气下搅拌2.5天。用硅藻土滤出氢氧化钯-碳,滤液减压浓缩,得到1.50g(98%)标题化合物(化合物16-1)。
(化合物16-1)
[α]D 20-4.6°(c=0.49,甲醇)
IR(薄膜,cm-1)3357,2934,1726,1623,1528,1216,1047,752,701
按照类似于实施例16的方法得到下列化合物。
(2R)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-苯基丙酸(化合物16-2),化合物16-1的对映体
[α]D 20+5.1°(c=0.52,甲醇)
IR(薄膜,cm-1)3339,3027,2931,1726,1619,1530,1216,1047,753,701
(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(4-异丙氧基苯基)丙酸(化合物16-3)
[α]D 20-53.0°(c=0.36,氯仿)
IR(薄膜,cm-1)3369,2977,1732,1614,1510,1243,1184,1121,1048,955,755,701
(2S)-2-[3-[(1RS)-1-(二甲氨基甲基)-2-羟乙基]-3-苯乙基脲基]-3-苯基丙酸(化合物16-4)
[α]D 20-9.8°(c=0.5,甲醇)
IR(薄膜,cm-1)3344,2951,1722,1632,1514,1402,1217,753
(2S)-2-[3-(2-羟乙基)-3-异戊基脲基]-3-苯基丙酸(化合物16-5)
[α]D 20-43.5°(c=0.98,甲醇)
IR(薄膜,cm-1)3339,2955,1727,1611,1529,1217,1049,757,701
(2S)-2-[3-(2-羟乙基)-3-异戊基脲基]-3-(4-甲氧基苯基)丙酸(化合物16-6)
[α]D 20-40.8°(c=0.53,氯仿)
IR(薄膜,cm-1)3367,2956,1732,1614,1513,1249,1179,1037,758
(2S)-2-[3-(2-羟乙基)-3-异戊基脲基]-2-苯基乙酸(化合物16-7)
[α]D 20+57.3°(c=0.45,氯仿)
IR(薄膜,cm-1)3307,2956,1727,1615,1520,1217,1187,1049,758,698
(2S)-2-[3-(2-羟乙基)-3-异戊基脲基]-4-甲基戊酸(化合物16-8)
[α]D 20-60.1°(c=0.98,氯仿)
IR(薄膜,cm-1)3342,2955,1720,1612,1529,1219,1048,756
2-[3-(2-羟乙基)-3-异戊基脲基]乙酸(化合物16-9)
IR(薄膜,cm-1)3357,2957,1730,1613,1538,1415,1219,1048,759
(2S)-3-环己基-2-[3-(2-羟乙基)-3-异戊基脲基]丙酸(化合物16-10)
熔点68.5~71.5℃
[α]D 20-62.7°(c=0.96,氯仿)
IR(KBr,cm-1)2926,2611,1750,1725,1620,1538,1450,1367,1223,1054
盐酸(2S)-2-[3-(2-羟乙基)-3-异戊基脲基]-3-(4-咪唑基)丙酸(化合物16-11)
[α]D 20-21.1°(c=0.53,甲醇)
IR(KBr,cm-1)3311,3133,2961,1739,1621,1531,1238,1046,832,760
(2S)-2-[3-(2-羟乙基)-3-异戊基脲基]-5-(3-甲苯磺酰胍基)戊酸(化合物16-12)
[α]D 20-13.9°(c=0.52,氯仿)
IR(薄膜,cm-1)3340,2956,1723,1625,1548,1412,1255,1132,1082,815,756
(2S)-2-[3-(2-羟乙基)-1-甲基-3-苯乙基脲基]丙酸(化合物16-13)
[α]D 20-25.8°(c=1.0,甲醇)
IR(薄膜,cm-1)3368,3001,1738,1615,1496
实施例17
(2S)-6-(叔丁氧基甲酰氨基)-2-[3-(2-羟乙基)-3-异戊基脲基]己酸(化合物17-1)
在氮气下,向(2S)-6-(苄氧基甲酰氨基)-2-[3-(2-羟乙基)-3-异戊基脲基]己酸苄基酯(化合物1-73,2.85g)的四氢呋喃(60ml)溶液中加入1N氢氯酸(12ml)和20%氢氧化钯-碳(285mg)。混合物在氢气下搅拌两小时。用硅藻土滤出氢氧化钯-碳。
在冰冷却下,向所得滤液中加入4N氢氧化钠水溶液(3ml)。然后,向该混合物中先后滴加三乙胺(1.09g)和二碳酸二叔丁酯(2.36g)的四氢呋喃(10ml)溶液,混合物进一步在室温下搅拌四小时。反应混合物减压浓缩,向残余物中加入10%柠檬酸水溶液,全部混合物用乙酸乙酯萃取。有机层先后用10%柠檬酸水溶液、水和饱和盐水洗涤,经无水硫酸钠干燥,减压浓缩。所得油状物用硅胶柱色谱法纯化,得到1.92g(88%)标题化合物(化合物17-1)。
(化合物17-1)
[α]D 20-37.1°(c=0.53,氯仿)
IR(薄膜,cm-1)3330,2956,1712,1694,1631,1530,1367,1251,1172,1051,757
实施例18
1-[(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-4-甲基戊酰]-4-甲基哌嗪(化合物18-1)
在氮气下,将(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-4-甲基戊酸(化合物15-1,700mg)、N-甲基哌嗪(0.25ml)和1-羟基苯并三唑(440mg)溶于无水二氯甲烷(10ml)。然后在冰冷却下,向该溶液中先后加入N-甲基吗啉(0.29ml)和盐酸1-乙基-3-(3-二甲氨基丙基)碳二亚胺(504mg)。混合物在冰冷却下搅拌30分钟,然后在室温下搅拌两小时。反应混合物减压浓缩,向所得油状物中加入5%碳酸氢钠水溶液,全部混合物用乙酸乙酯萃取。有机层先后用水和饱和盐水洗涤,经无水硫酸镁干燥,减压浓缩。所得油状物用硅胶柱色谱法纯化,得到808mg(92%)标题化合物(化合物18-1)。
(化合物18-1)
[α]D 20+1.6°(c=0.99,甲醇)
IR(薄膜,cm-1)3346,2950,1631,1449,1291,1223,1171,1143
按照类似于实施例18的方法得到下列化合物。
1-[(2S)-2-[3-(3-羟丙基)-3-苯乙基脲基]-3-苯基丙酰]-4-甲基哌嗪(化合物18-2)
[α]D 20+16.6°(c=0.50,甲醇)
IR(薄膜,cm-1)3358,2937,1624,1528,1496,1453,1290,1249,1144,1001,750,701
1-[(2S)-2-[3-[(2RS)-2-羟丙基]-3-苯乙基脲基]-3-苯基丙酰]-4-甲基哌嗪(化合物18-3)
IR(薄膜,cm-1)3362,2937,1625,1522,1454,1291,1234,1144,1001,751,701
1-[(2RS)-2-[3-(2-羟乙基)-3-苯乙基脲基]-4-(甲硫基)丁酰]-4-甲基哌嗪(化合物18-4)
熔点115.7~117.2℃
IR(KBr,cm-1)3421,3289,2932,2794,1621,1532,1449,1255,1218,1053,1002,754,704
1-(叔丁氧羰基)-4-[(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(4-硝基苯基)丙酰]哌嗪(化合物18-5)
[α]D 20+11.4°(c=1.0,氯仿)
IR(薄膜,cm-1)3400,293I,1691,1630,1521,1456,1420,1346,1236,1167
1-[(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(4-硝基苯基)丙酰]-4-甲基哌嗪(化合物18-6)
[α]D 20+2.6°(c=0.53,氯仿)
IR(薄膜,cm-1)3376,2941,1627,1519,1451,1346,1291,1224,1144,1049,1000,751,700
1-环己基-4-[(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(4-硝基苯基)丙酰]哌嗪(化合物18-7)
[α]D 20+6.1°(c=1.0,氯仿)
IR(薄膜,cm-1)3341,2930,2855,1627,1520,1451,1346,1225
1-[(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(4-硝基苯基)丙酰]-4-苯基哌嗪(化合物18-8)
IR(薄膜,cm-1)3412,2928,1627,1602,1519,1346,1228,755,698
1-苄基-4-[(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(4-硝基苯基)丙酰]哌嗪(化合物18-9)
[α]D 20+7.7°(c=1.0,氯仿)
IR(薄膜,cm-1)3371,2936,1626,1519,1453,1346,1221,750,700
(2S)-N-[2-(二异丙氨基)乙基]-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(4-硝基苯基)丙酰胺(化合物18-10)
[α]D 20-12.9°(c=1.0,氯仿)
IR(薄膜,cm-1)3389,2968,1630,1520,1346,751,700
(2S)-N-[2-(二环己基氨基)乙基]-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(4-硝基苯基)丙酰胺(化合物18-11)
[α]D 20-10.3°(c=0.50,氯仿)
IR(薄膜,cm-1)3301,2929,1634,1520,1346,755
(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-N-[2-(4-甲基哌嗪-1-基)乙基]-3-(4-硝基苯基)丙酰胺(化合物18-12)
熔点89.0~91.5℃
[α]D 20-20.0°(c=0.50,氯仿)
IR(KBr,cm-1)3289,2939,2804,1668,1617,1518,1455,1347,1284,1235,1165,1012,700
(2S)-N-[2-(叔丁氧基甲酰氨基)乙基]-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(4-硝基苯基)丙酰胺(化合物18-13)
[α]D 20-25.9°(c=1.0,氯仿)
IR(薄膜,cm-1)3304,2976,2933,1693,1625,1519,1346,1168,753
1-[(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(4-硝基苯基)丙酰]哌啶(化合物18-14)
[α]D 20+11.1°(c=0.53,氯仿)
IR(薄膜,cm-1)3348,2939,1622,1519,1346,1221,1050,1016,855,750,700
4-[(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(4-硝基苯基)丙酰]吗啉(化合物18-15)
[α]D 20+9.4°(c=1.0,氯仿)
IR(薄膜,cm-1)3415,2927,2860,1626,1519,1346,751
(2S)-N-(叔丁氧羰基甲基)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(4-硝基苯基)丙酰胺(化合物18-16)
[α]D 20-17.7°(c=0.54,甲醇)
IR(薄膜,cm-1)3292,2979,2933,1740,1663,1624,1521,1346,1225,1156,752
(2S)-3-(4-氯苯基)-N-[2-(二甲氨基)乙基]-2-[3-(2-羟乙基)-3-苯乙基脲基]丙酰胺(化合物18-17)
[α]D 20-20.7°(c=0.51,氯仿)
IR(薄膜,cm-1)3291,2944,1714,1626,1534,1493,1365,1232,1092
(2S)-2-[3-(2-羟乙基)-3-异戊基脲基]-N-甲基-3-(4-硝基苯基)丙酰胺(化合物18-18)
[α]D 20-18.4°(c=0.50,氯仿)
IR(KBr,cm-1)3304,2957,1670,1616,1519,1408,1348,1047
(2S)-N-[2-(二甲氨基)乙基]-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(2-硝基-4-联苯基)丙酰胺(化合物18-19)
[α]D 20-21.9°(c=0.50,氯仿)
IR(薄膜,cm-1)3305,2945,1626,1529,755,701
(2S)-3-[4-(苯磺酰)-3-硝基苯基]-N-[2-(二甲氨基)乙基]-2-[3-(2-羟乙基)-3-苯乙基脲基]丙酰胺(化合物18-20)
[α]D 20-21.0°(c=0.50,氯仿)
IR(薄膜,cm-1)3297,2943,1625,1544,752
1-[(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(2-萘基)丙酰]-4-甲基哌嗪(化合物18-21)
[α]D 20+2.0°(c=1.0,甲醇)
IR(薄膜,cm-1)3348,2937,1626,1524,1447,1225
1-[(2R)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(甲硫基)丙酰]-4-甲基哌嗪(化合物18-22)
[α]D 20-4.1°(c=0.51,甲醇)
IR(薄膜,cm-1)3352,2921,1628,1521,1455,1365,1293,1224,1170,1143,1047,1000,752,701
1-[(2R)-3-(苄硫基)-2-[3-(2-羟乙基)-3-苯乙基脲基]丙酰]-4-甲基哌嗪(化合物18-23)
熔点88.2~90.7℃
[α]D 20+25.2°(c=0.50,甲醇)
IR(KBr,cm-1)3423,3309,2941,2788,1620,1549,1451,1293,1229,1141,1060,1002,786,754,710
1-[(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-苯基丙酰]-4-甲基哌嗪
(化合物18-24)
[α]D 20+14.7°(c=0.46,甲醇)
IR(薄膜,cm-1)3354,2938,1626,1526,1452,751,701
1-[(2R)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-苯基丙酰]-4-甲基哌嗪(化合物18-25),化合物18-24的对映体
[α]D 20-14.6°(c=0.53,甲醇)
IR(薄膜,cm-1)3348,2935,1626,1526,1450,750,701
(2S)-N-[2-(二甲氨基)乙基]-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(4-异丙氧基苯基)丙酰胺(化合物18-26)
熔点87.5~100.0℃
[α]D 20-14.9°(c=0.32,氯仿)
IR(KBr,cm-1)3276,2975,1669,1614,1550,1510,1238,1183,1119,1053,956,748,701
1-[(2S)-2-[3-[(1RS)-1-(二甲氨基甲基)-2-羟乙基]-3-苯乙基脲基]-3-苯基丙酰]-4-甲基哌嗪(化合物18-27)
[α]D 20+14.3°(c=0.30,甲醇)
IR(薄膜,cm-1)3420,2941,1626,1496,1291,1145,752
(2S)-N-[2-(二甲氨基)乙基]-2-[3-(2-羟乙基)-3-异戊基脲基]-3-苯基丙酰胺(化合物18-28)
[α]D 20-21.3°(c=1.0,氯仿)
IR(薄膜,cm-1)3305,2954,1630,1530,1234,1051,754,701
(2S)-2-[3-(2-羟乙基)-3-异戊基脲基]-N-[(1S)-1-(甲基氨基甲酰基)乙基]-3-苯基丙酰胺(化合物18-29)
熔点106.5~111.0℃
[α]D 20-13.2°(c=1.0,氯仿)
IR(KBr,cm-1)3276,2950,1647,1554,1456,1410,1050,701
(2S)-2-[3-(2-羟乙基)-3-异戊基脲基]-3-(4-甲氧基苯基)-N-甲基丙酰胺(化合物18-30)
熔点96.5~99.0℃
[α]D 20+5.2°(c=0.50,氯仿)
IR(KBr,cm-1)3270,2955,1668,1620,1550,1513,1410,1246,1177,1042,824
(2S)-2-[3-(2-羟乙基)-3-异戊基脲基]-N-甲基-2-苯基乙酰胺(化合物18-31)
熔点164.5~165.5℃
[α]D 20+1.7°(c=0.50,甲醇)
IR(KBr,cm-1)3410,3274,2961,1659,1618,1539,1375,1361,1232,1160,1087,727,700
1-[(2S)-2-[3-(2-羟乙基)-3-异戊基脲基]-4-甲基戊酰]-4-甲基哌嗪(化合物18-32)
[α]D 20+2.2°(c=1.0,甲醇)
IR(薄膜,cm-1)3344,2954,2868,1633,1463,1172,1144
(2S)-N,4-二甲基-2-[3-(2-羟乙基)-3-异戊基脲基]戊酰胺(化合物18-33)
[α]D 20-23.4°(c=0.48,氯仿)
IR(薄膜,cm-1)3294,2956,2871,1626,1535,1469,1410,1236,1051,756
2-[3-(2-羟乙基)-3-异戊基脲基]-N-甲基乙酰胺(化合物18-34)熔点124.5~126.0℃
IR(KBr,cm-1)3420,3352,3272,2955,1668,1616,1533,1413,1237,1078,751
(2S)-3-环己基-2-[3-(2-羟乙基)-3-异戊基脲基]-N-甲基丙酰胺(化合物18-35)
[α]D 20-21.9°(c=0.51,氯仿)
IR(薄膜,cm-1)3297,2924,1630,1535,1468,1448,1411,1235,1051
(2S)-2-[3-(2-羟乙基)-3-异戊基脲基]-3-(4-咪唑基)-N-甲基丙酰胺(化合物18-36)
熔点94.0~97.0℃
[α]D 20+14.3°(c=0.33,二甲亚砜)
IR(KBr,cm-1)3270,2956,1663,1412,1241,1070,977,770
(2S)-2-[3-(2-羟乙基)-3-异戊基脲基]-N-甲基-5-(3-甲苯磺酰胍基)戊酰胺(化合物18-37)
[α]D 20+11.6°(c=0.50,氯仿)
IR(薄膜,cm-1)3335,2955,1627,1550,1410,1258,1132,1082,814,755
1-[(2S)-2-[3-(2-羟乙基)-1-甲基-3-苯乙基脲基]丙酰]-4-甲基哌嗪(化合物18-38)
[α]D 20-11.4°(c=0.97,氯仿)
IR(薄膜,cm-1)3417,2938,1634,1455,1291,1252,1077,1034
(2S)-6-(叔丁氧基甲酰氨基)-2-[3-(2-羟乙基)-3-异戊基脲基]-N-甲基己酰胺(化合物18-39)
[α]D 20-6.2°(c=0.51,氯仿)
IR(薄膜,cm-1)3308,2956,1693,1632,1530,1366,1251,1172,1052,756
1-[(2S)-3-[4-(苄氧基)苯基]-2-[3-(2-羟乙基)-3-苯乙基脲基]丙酰]-4-甲基哌嗪(化合物18-40)
[α]D 20+2.2°(c=0.50,甲醇)
IR(薄膜,cm-1)3354,2938,1623,1510,1454,1240,1038
(2S)-N-[2-(叔丁氧羰基)乙基]-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(4-硝基苯基)丙酰胺(化合物18-41)
熔点109.0~111.5℃
[α]D 20-27.2°(c=0.49,氯仿)
IR(KBr,cm-1)3271,3078,2937,1729,1653,1617,1521,1347,1155,844,749,702
1-[(2S)-2-[3-[2-(1-环己烯基)乙基]-3-(2-羟乙基)脲基]丙酰]-4-甲基哌嗪(化合物18-42)
[α]D 20+8.3°(c=0.99,甲醇)
IR(薄膜,cm-1)3361,2930,1632,1520,1447,1292,1225,754
1-[(2S)-2-[3-(2-羟乙基)-3-(3-甲基-3-丁烯基)脲基]丙酰]-4-甲基哌嗪(化合物18-43)
[α]D 20+10.3°(c=0.47,甲醇)
IR(薄膜,cm-1)3355,2937,1632,1526,1448,1292,1225,1144,1034,1002,890,757
1-[2-[3-(2-环己基乙基)-3-(2-羟乙基)脲基]-2-甲基丙酰]-4-甲基哌嗪(化合物18-44)
熔点50~60℃
IR(KBr,cm-1)3294,2924,1645,1627,1546,1421,1356,1284,1170,1140,1048,1001,749
1-[1-[3-(2-环己基乙基)-3-(2-羟乙基)脲基]-1-环丙烷羰基]-4-甲基哌嗪(化合物18-45)
IR(薄膜,cm-1)3338,2921,2850,2796,1633,1520,1446,1288,1213,1143,1050,1002,753
1-[1-[3-(2-环己基乙基)-3-(2-羟乙基)脲基]-1-环戊烷羰基]-4-甲基哌嗪(化合物18-46)
熔点128.5~131.4℃
IR(KBr,cm-1)3306,2927,1652,1542,1444,1418,1284,995,779
实施例19
(2S)-N-[2-(二甲氨基)乙基]-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(4-硝基苯基)丙酰胺(化合物19-1)
在冰冷却下,向(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(4-硝基苯基)丙酸苯基酯(化合物1-35,392mg)的四氢呋喃(5ml)溶液中加入2-(二甲氨基)乙胺(362mg)的四氢呋喃(3ml)溶液,混合物在室温下搅拌1.5小时。反应混合物减压浓缩,向浓缩物中加入水,全部混合物用乙酸乙酯萃取。有机层先后用水和饱和盐水洗涤,经无水硫酸钠干燥,减压浓缩。所得油状物用硅胶柱色谱法纯化,得到314mg(81%)标题化合物(化合物19-1)。
(化合物19-1)
[α]D 20-39.3°(c=0.27,氯仿)
IR(薄膜,cm-1)3293,2943,1625,1519,1346,1231,1044,856,751,701
按照类似于实施例19的方法得到下列化合物。
(2S)-N-[3-(二甲氨基)丙基]-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(4-硝基苯基)丙酰胺(化合物19-2)
[α]D 20-35.2°(c=0.50,氯仿)
IR(薄膜,cm-1)3270,3100,2943,1664,1615,1519,1350,749
(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-N-[2-(4-吗啉基)乙基]-3-(4-硝基苯基)丙酰胺(化合物19-3)
[α]D 20-17.2°(c=1.0,氯仿)
IR(薄膜,cm-1)3295,2941,1627,1519,1346,1116,752
(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(4-硝基苯基)-N-[2-(邻苯二甲酰亚氨基)乙基]丙酰胺(化合物19-4)
[α]D 20-33.6°(c=0.49,氯仿)
IR(薄膜,cm-1)3289,1712,1622,1519,1395,1346,1229,1037,752,720
(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-N-[2-[(N-甲基)环己基氨基]乙基]-3-(4-硝基苯基)丙酰胺(化合物19-5)
[α]D 20-16.5°(c=0.53,氯仿)
IR(薄膜,cm-1)3296,2930,1624,1520,1453,1409,1345,1230,1048
(2S)-N-[2-(二乙氨基)乙基]-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(4-硝基苯基)丙酰胺(化合物19-6)
熔点890~92.5℃
[α]D 20-17.6°(c=0.49,氯仿)
IR(KBr,cm-1)3274,2971,1663,1617,1517,1440,1347
(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-N-[2-[(N-甲基)苯基氨基]乙基]-3-(4-硝基苯基)丙酰胺(化合物19-7)
[α]D 20-26.3°(c=0.51,氯仿)
IR(薄膜,cm-1)3290,2935,1660,1624,1601,1519,1346,1216
(2S)-N-[4-(二甲氨基)丁基]-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(4-硝基苯基)丙酰胺(化合物19-8)
[α]D 20-81.5°(c=0.51,氯仿)
IR(薄膜,cm-1)3291,2940,1625,1519,1346,750
(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(4-硝基苯基)-N-[2-(2-吡啶基)乙基]丙酰胺(化合物19-9)
熔点112.0~118.0℃
[α]D 20-26.0°(c=0.51,氯仿)
IR(KBr,cm-1)3277,3090,2937,1666,1612,1516,1436,1347,1279,1224,1049,748,703
(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-N-[3-(1-咪唑基)丙基]-3-(4-硝基苯基)丙酰胺(化合物19-10)
[α]D 20-46.3°(c=1.0,氯仿)
IR(薄膜,cm-1)3416,2938,1628,1518,1346,750
(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(4-硝基苯基)-N-[2-(1-哌啶基)乙基]丙酰胺(化合物19-11)
[α]D 20-15.9°(c=0.49,氯仿)
IR(薄膜,cm-1)3404,2937,1633,1519,1345,749,700
(2S)-N-[2-(二甲氨基)乙基]-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-苯基丙酰胺(化合物19-12)
熔点97.5~101.2℃
[α]D 20-13.2°(c=0.51,氯仿)
IR(KBr,cm-1)3271,3087,2942,1667,1617,1546,1498,1455,1280,1230,1048,748,699
(2S)-N-[2-(二甲氨基)乙基]-3-(4-氟苯基)-2-[3-(2-羟乙基)-3-苯乙基脲基]丙酰胺(化合物19-13)
熔点108.5~111.0℃
[α]D 20-15.7°(c=0.53,氯仿)
IR(KBr,cm-1)3268,3088,2945,1666,1614,1549,1456,1417,1373,1280,1227,1049,828,748,699
(2S)-N-[2-(二甲氨基)乙基]-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(4-羟基苯基)丙酰胺(化合物19-14)
[α]D 20-4.7°(c=0.50,氯仿)
IR(薄膜,cm-1)3293,2947,1629,1515,1454,1367,1238,1047,752,701
(2S)-N-[2-(二甲氨基)乙基]-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(4-甲氧基苯基)丙酰胺(化合物19-15)
[α]D 20-10.8°(c=0.50,氯仿)
IR(薄膜,cm-1)3287,2939,1622,1513,1247,1037,751
(2S)-N-[2-(二甲氨基)乙基]-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(2-噻吩基)丙酰胺(化合物19-16)
[α]D 20-17.4°(c=0.51,氯仿)
IR(薄膜,cm-1)3295,2944,1629,1531,1454,1408,1231,1043,751,700
(2S)-N-[2-(二甲氨基)乙基]-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(2-萘基)丙酰胺(化合物19-17)
[α]D 20-8.1°(c=0.97,氯仿)
IR(薄膜,cm-1)3296,2945,1629,1532,1233,1045,751
(2S)-3-(4-联苯基)-N-[2-(二甲氨基)乙基]-2-[3-(2-羟乙基)-3-苯乙基脲基]丙酰胺(化合物19-18)
[α]D 20-14.4°(c=1.0,氯仿)
IR(薄膜,cm-1)3290,2943,1626,1534,1230,1094,757,699
(2S)-N-[2-(二甲氨基)乙基]-2-[3-(2-羟乙基)-3-异戊基脲基]-3-(4-硝基苯基)丙酰胺(化合物19-19)
[α]D 20-31.4°(c=0.29,氯仿)
IR(薄膜,cm-1)3290,2954,1660,1624,1521,1467,1346,1233,1052,856,755
(2S)-3-(4-联苯基)-N-丁基-2-[3-(2-羟乙基)-3-异戊基脲基]丙酰胺(化合物19-20)
实施例20
(2S)-2-[3-(2-羟乙基)-3-异戊基脲基]-N-甲基-3-苯基丙酰胺(化合物20-1)
在氮气下,将盐酸N-甲基-L-苯基丙氨酸酰胺(参考化合物8-2,429mg)、1,1’-羰基二咪唑(422mg)和咪唑(136mg)悬浮在无水四氢呋喃(7ml)中,该悬浮液在室温下搅拌20分钟。向反应混合物中加入N-(2-羟乙基)异戊胺(参考化合物13-2,525mg)的无水四氢呋喃(3ml)溶液,混合物回流0.5小时。反应混合物减压浓缩,向浓缩物中加入10%柠檬酸水溶液,全部混合物用乙酸乙酯萃取。有机层先后用10%柠檬酸水溶液、水和饱和盐水洗涤,经无水硫酸镁干燥,减压浓缩。所得油状物用硅胶柱色谱法纯化,得到626mg(93%)标题化合物(化合物20-1)。
(化合物20-1)
[α]D 20+9.4°(c=0.24,甲醇)
IR(薄膜,cm-1)3295,2955,1625,1537,1234,1051
按照类似于实施例20的方法得到下列化合物。
(2S)-2-[3-(2-羟乙基)-3-异丁基脲基]-N-甲基-3-苯基丙酰胺(化合物20-2)
[α]D 20+8.3°(c=0.54,甲醇)
IR(薄膜,cm-1)3296,2958,1626,1531,1339,1269,1042
(2S)-2-[3-(2-羟乙基)-3-(4-甲基戊基)脲基]-N-甲基-3-苯基丙酰胺(化合物20-3)
[α]D 20-3.5°(c=0.56,氯仿)
IR(薄膜,cm-1)3340,2954,1630,1531,1468,1411,1367,1231,1164,1051
(2S)-2-[3-(3,3-二甲基丁基)-3-(2-羟乙基)脲基]-N-甲基-3-苯基丙酰胺(化合物20-4)
IR(薄膜,cm-1)3294,2954,2360,1625,1534,1411,1365,1246,1051,754,699
(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-N-甲基-3-苯基丙酰胺(化合物20-5)
[α]D 20-3.0°(c=0.49,氯仿)
IR(薄膜,cm-1)3294,2929,1626,1537,1497,1410,1232,750,700
(2S)-2-[3-[2-羟基-1-(羟甲基)乙基]-3-异戊基脲基]-N-甲基-3-苯基丙酰胺(化合物20-6)
[α]D 20+4.6°(c=0.36,氯仿)
IR(薄膜,cm-1)3305,2955,1626,1519,1455,1411,1367,1239,1048,754,700
(2S)-2-[3-[(1RS)-2-羟基-1-(苯硫基甲基)乙基]-3-异戊基脲基]-N-甲基-3-苯基丙酰胺(化合物20-7)
IR(薄膜,cm-1)3297,2955,1626,1519,1237,1088,1026,748,699
(2S)-N,N-二甲基-2-[3-(2-羟乙基)-3-异戊基脲基]-3-苯基丙酰胺(化合物20-8)
[α]D 20+45.1°(c=0.99,氯仿)
IR(薄膜,cm-1)3349,2955,1632,1530,1422,1235,1054,754,701
(2S)-N,N-二甲基-2-[3-(3-羟丙基)-3-异戊基脲基]-3-苯基丙酰胺(化合物20-9)
[α]D 20+43.2°(c=1.0,氯仿)
IR(薄膜,cm-1)3418,2955,1634,1538,1240,1058,946,752,702
(2S)-N,N-二甲基-2-[3-(4-羟丁基)-3-异戊基脲基]-3-苯基丙酰胺(化合物20-10)
IR(薄膜,cm-1)3418,2927,1628,1522,754,701
(2S)-N,N-二甲基-2-[3-[(1RS)-2-羟基-1-苯基乙基]-3-异戊基脲基]-3-苯基丙酰胺(化合物20-11)
IR(薄膜,cm-1)3406,2955,1626,1495,753,701
(2S)-N,N-二甲基-2-[3-[(1RS)-1-(羟甲基)-3-苯丙基]-3-异戊基脲基]-3-苯基丙酰胺(化合物20-12)
(2S)-N,N-二甲基-2-[3-[(1RS)-2-羟基-1-(苯氧基甲基)乙基]-3-异戊基脲基]-3-苯基丙酰胺(化合物20-13)
IR(薄膜,cm-1)3413,2955,1628,1497,1243,754
(2S)-2-[3-(2-羟乙基)-3-异戊基脲基]-N-甲基-4-苯基丁酰胺(化合物20-14)
[α]D 20-17.3°(c=0.51,氯仿)
IR(薄膜,cm-1)3292,2955,1624,1537,1410,1234,1052,754,700
(2S)-2-[3-[(1R)-1-苄基-2-羟乙基]-3-异戊基脲基]-3-(4-联苯基)-N-丁基丙酰胺(化合物20-15)
[α]D 20+22.6°(c=0.70,二甲亚砜)
IR(薄膜,cm-1)3421,2957,2060,1626,1558,1520,1291,760,698
4.[(2S)-2-[3-[2-(1-金刚烷基)乙基]-3-(2-羟乙基)脲基]丙酰]吗啉(化合物20-16)
[α]D 20+6.1°(c=0.97,甲醇)
IR(薄膜,cm-1)3372,2902,2846,1628,1520,1448,1361,1346,1300,1270,1224,1117,1030,754
4-[(2S)-2-[3-(2-环己基乙基)-3-(2-羟乙基)脲基]丙酰]吗啉(化合物20-17)
[α]D 20+6.5°(c=1.0,甲醇)
IR(薄膜,cm-1)3360,2922,2851,1632,1520,1446,1372,1301,1270,1226,1116,1030,754
1-[(2S)-2-[3-[2-(1-金刚烷基)乙基]-3-(2-羟乙基)脲基]丙酰]-4-甲基哌嗪(化合物20-18)
IR(薄膜,cm-1)3356,2902,2846,2796,1628,1522,1448,1374,1292,1221,1144,1051,1002,754
实施例21
(2S)-2-[3-[2-(苄氧基)乙基]-1-异戊基脲基]-N-[2-(二甲氨基)乙基]-3-苯基丙酰胺(化合物21-1)
在氮气下,将盐酸2-(苄氧基)乙胺(参考化合物12-3,203mg)、1,1’-羰基二咪唑(233mg)和咪唑(74mg)悬浮在无水四氢呋喃(9ml)中,该悬浮液在室温下搅拌15分钟。向反应混合物中加入二盐酸N1-[2-(二甲氨基)乙基]-N2-异戊基-L-苯基丙氨酸酰胺(参考化合物9-1,341mg),混合物回流过夜。反应混合物减压浓缩,向浓缩物中加入10%碳酸氢钠水溶液,全部混合物用乙酸乙酯萃取。有机层先后用10%碳酸氢钠水溶液和饱和盐水洗涤,经无水硫酸钠干燥,减压浓缩。所得油状物用硅胶柱色谱法纯化,得到386mg(89%)标题化合物(化合物21-1)。
(化合物21-1)
[α]D 20-43.5°(c=0.51,氯仿)
IR(薄膜,cm-1)3294,2952,1634,1524,1455,1366,1289,1099,748,699
按照类似于实施例21的方法得到下列化合物。
2-[3-[(1R)-1-苄基-2-(苄氧基)乙基]-1-异戊基脲基]-N-[2-(二甲氨基)乙基]乙酰胺(化合物21-2)
[α]D 20+21.1°(c=0.49,氯仿)
IR(薄膜,cm-1)3384,2956,1634,1527,751
2-[3-[(1S)-1-苄基-2-(苄氧基)乙基]-1-异戊基脲基]-N-[2-(二甲氨基)乙基]乙酰胺(化合物21-3),化合物21-2的对映体
[α]D 20-21.8°(c=0.48,氯仿)
IR(薄膜,cm-1)3295,2953,1633,1533,746,699
实施例22
(2S)-N-[2-(二甲氨基)乙基]-2-[3-(2-羟乙基)-1-异戊基脲基]-3-苯基丙酰胺(化合物22-1)
在氮气下,向(2S)-2-[3-[2-(苄氧基)乙基]-1-异戊基脲基]-N-[2-(二甲氨基)乙基]-3-苯基丙酰胺(化合物21-1,300mg)的甲醇(10ml)溶液中加入20%氢氧化钯-碳(30mg)。混合物在氢气下搅拌4.5小时。用硅藻土滤出氢氧化钯-碳,滤液减压浓缩。将浓缩物溶于乙酸乙酯。溶液先后用10%碳酸氢钠水溶液、水和饱和盐水洗涤,经无水硫酸钠干燥,减压浓缩。所得油状物用硅胶柱色谱法纯化,得到167mg(68%)标题化合物(化合物22-1)。
(化合物22-1)
[α]D 20-44.8°(c=0.47,氯仿)
IR(薄膜,cm-1)3320,2953,1657,1629,1531,1457,1291,1076,751,700
按照类似于实施例22的方法得到下列化合物。
2-[3-[(1R)-1-苄基-2-羟乙基]-1-异戊基脲基]-N-[2-(二甲氨基)乙基]乙酰胺(化合物22-2)
[α]D 20+17.8°(c=0.31,甲醇)
IR(薄膜,cm-1)3386,2958,1656,1546,1466,1273,1032,750,701
2-[3-[(1S)-1-苄基-2-羟乙基]-1-异戊基脲基]-N-[2-(二甲氨基)乙基]乙酰胺(化合物22-3),化合物22-2的对映体
[α]D 20-40.6°(c=0.22,二甲亚砜)
IR(KBr,cm-1)3413,2957,1636,1542,1248,1088,701
实施例23
1-[(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(4-羟基苯基)丙酰]-4-甲基哌嗪(化合物23-1)
在氮气下,向1-[(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-[4-(苄氧基)苯基]丙酰]-4-甲基哌嗪(化合物18-40,1.09g)的四氢呋喃(2ml)-甲醇(2ml)溶液中加入20%氢氧化钯-碳(200mg)。混合物在氢气下搅拌三天。用硅藻土滤出氢氧化钯-碳,滤液减压浓缩,得到685mg(75%)标题化合物(化合物23-1),为非晶性粉末。
(化合物23-1)
[α]D 20+20.0°(c=0.54,甲醇)
IR(薄膜,cm-1)3364,1626,1515,1452,1229,1029
实施例24
(2S)-3-(4-氨基苯基)-N-[2-(二甲氨基)乙基]-2-[3-(2-羟乙基)-3-苯乙基脲基]丙酰胺(化合物24-1)
在氮气下,向(2S)-N-[2-(二甲氨基)乙基]-2-[3-(2-羟乙基)-3-苯乙基脲基]-3-(4-硝基苯基)丙酰胺(化合物19-1,921mg)的乙醇(30ml)溶液中加入5%钯-碳(92mg)。混合物在氢气下搅拌三小时。用硅藻土滤出钯-碳,滤液减压浓缩。所得油状物用硅胶柱色谱法纯化,得到418mg(49%)标题化合物(化合物24-1),为非晶性粉末。
(化合物24-1)
[α]D 20-23.8°(c=0.48,氯仿)
IR(薄膜,cm-1)3346,2945,1627,1517,1408,1367,1274,1181,1043,753,702
实施例25
(2S)-2-[3-(2-乙酰氧基乙基)-3-苯乙基脲基]-3-[4-(乙酰氨基)苯基]-N-[2-(二甲氨基)乙基]丙酰胺(化合物25-1)
在氮气下,将(2S)-3-(4-氨基苯基)-N-[2-(二甲氨基)乙基]-2-[3-(2-羟乙基)-3-苯乙基脲基]丙酰胺(化合物24-1,265mg)溶于无水二氯甲烷(5ml),搅拌溶液。向溶液中加入三乙胺(152mg),然后在冰冷却下滴加乙酸酐(123mg)的无水二氯甲烷(1ml)溶液,混合物搅拌30分钟,进一步在室温下搅拌1.5小时。反应混合物减压浓缩,向残余物中加入10%碳酸氢钠水溶液,全部混合物用乙酸乙酯萃取。有机层先后用水和饱和盐水洗涤,经无水硫酸钠干燥,减压浓缩。所得油状物用硅胶柱色谱法纯化,得到200mg(63%)标题化合物(化合物25-1),为晶体。
(化合物25-1)
熔点87.0~100℃
[α]D 20-2.7°(c=0.50,氯仿)
IR(KBr,cm-1)3292,2943,1742,1665,1625,1539,1455,1412,1370,1319,1232,1040,748,702
实施例26
(2S)-3-[4-(乙酰氨基)苯基]-N-[2-(二甲氨基)乙基]-2-[3-(2-羟乙基)-3-苯乙基脲基]丙酰胺(化合物26-1)
将(2S)-2-[3-(2-乙酰氧基乙基)-3-苯乙基脲基]-3-[4-(乙酰氨基)苯基]-N-[2-(二甲氨基)乙基]丙酰胺(化合物25-1,158mg)溶于四氢呋喃(3ml)。在冰冷却下,向其中加入1N氢氧化锂水溶液(1.7ml),混合物搅拌40分钟。反应混合物用氯仿萃取。有机层用饱和盐水洗涤,经无水硫酸钠干燥,减压浓缩,得到140mg(97%)标题化合物(化合物26-1),为晶体。
(化合物26-1)
熔点132.0~137.0℃
[α]D 20-4.2°(c=0.51,氯仿)
IR(KBr,cm-1)3288,3095,2939,1667,1613,1541,1411,1372,1320,1242,1052,754,700
实施例27
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-4-甲基戊酰]-4-甲基哌嗪(化合物27-1)
在氮气下,将1-[(2S)-2-[3-(2-羟乙基)-3-苯乙基脲基]-4-甲基戊酰]-4-甲基哌嗪(化合物18-1,500mg)和三苯膦(654mg)溶于无水四氢呋喃(3ml),该溶液在盐-冰冷却下搅拌30分钟。向该溶液中先后滴加偶氮二羧酸二乙酯(435mg)的无水四氢呋喃(1ml)溶液和硫代乙酸(0.2ml)的无水四氢呋喃(2ml)溶液,同时保持液体温度在5℃。混合物搅拌一小时,向反应混合物中加入10%碳酸氢钠水溶液,全部混合物用乙醚萃取。有机层用10%碳酸氢钠水溶液、水和饱和盐水洗涤,经无水硫酸镁干燥,减压浓缩。所得油状物用硅胶柱色谱法纯化,得到472mg(82%)标题化合物(化合物27-1)。
(化合物27-1)
[α]D 20+1.2°(c=1.0,甲醇)
IR(薄膜,cm-1)2953,1689,1633,1447,1290,1217,1172,1141
按照类似于实施例27的方法得到下列化合物。
1-[(2S)-2-[3-[3-(乙酰硫基)丙基]-3-苯乙基脲基]-3-苯基丙酰]-4-甲基哌嗪(化合物27-2)
[α]D 20+10.4°(c=1.0,甲醇)
IR(薄膜,cm-1)3351,2939,1690,1628,1496,1454,1291,1249,1217,1142,1002,753,701
1-[(2S)-2-[3-[(2RS)-2-(乙酰硫基)丙基]-3-苯乙基脲基]-3-苯基丙酰]-4-甲基哌嗪(化合物27-3)
IR(薄膜,cm-1)3370,2937,1684,1633,1497,1454,1355,1291,1248,1218,1143,1116,1002,751,701
1-[(2RS)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-4-(甲硫基)丁酰]-4-甲基哌嗪(化合物27-4)
IR(薄膜,cm-1)3367,2936,2792,1688,1634,1522,1445,1294,1213,1002,750,701
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-(4-硝基苯基)丙酰]-4-(叔丁氧羰基)哌嗪(化合物27-5)
[α]D 20+6.9°(c=0.50,氯仿)
IR(薄膜,cm-1)3368,2977,2929,1694,1640,1520,1417,1365,1346,1286,1235,1167
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-(4-硝基苯基)丙酰]-4-甲基哌嗪(化合物27-6)
[α]D 20-2.0°(c=0.49,氯仿)
IR(薄膜,cm-1)3368,2939,1687,1633,1519,1447,1346,1291,1217,1142,752,700
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-(4-硝基苯基)丙酰]-4-环己基哌嗪(化合物27-7)
[α]D 20-28.8°(c=0.53,二甲亚砜)
IR(薄膜,cm-1)3366,2929,1690,1633,1519,1452,1345,1281,1217,1138
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-(4-硝基苯基)丙酰]-4-苯基哌嗪(化合物27-8)
IR(薄膜,cm-1)3429,1536,1519,1345,1228,757,698
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-(4-硝基苯基)丙酰]-4-苄基哌嗪(化合物27-9)
[α]D 20-6.7°(c=1.0,氯仿)
IR(薄膜,cm-1)3426,1634,1519,1345,747
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-[2-(二异丙氨基)乙基]-3-(4-硝基苯基)丙酰胺(化合物27-10)
[α]D 20-38.1°(c=0.99,氯仿)
IR(薄膜,cm-1)3442,2968,1628,1521,1345
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-[2-(二环己基氨基)乙基]-3-(4-硝基苯基)丙酰胺(化合物27-11)
[α]D 20-27.0°(c=0.52,氯仿)
IR(薄膜,cm-1)3428,2929,1628,1520,1345
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-[2-(4-甲基哌嗪-1-基)乙基]-3-(4-硝基苯基)丙酰胺(化合物27-12)
熔点103.0~105.5℃(分解)
[α]D 20-19.4°(c=0.50,氯仿)
IR(KBr,cm-1)3289,2936,2794,1694,1664,1619,1519,1347,1284,1166,747,699
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-[2-(叔丁氧基甲酰氨基)乙基]-3-(4-硝基苯基)丙酰胺(化合物27-13)
熔点66.4~73.7℃
[α]D 20-11.3°(c=0.52,甲醇)
IR(KBr,cm-1)3305,2977,2932,1711,1697,1658,1622,1520,1346,750
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-(4-硝基苯基)丙酰]哌啶(化合物27-14)
[α]D 20+3.5°(c=0.51,氯仿)
IR(薄膜,cm-1)3369,2939,1688,1633,1519,1445,1345,1215,1136,749,700
4-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-(4-硝基苯基)丙酰]吗啉(化合物27-15)
[α]D 20-2.6°(c=0.50,氯仿)
IR(薄膜,cm-1)3422,1634,1519,1346,1114,749,700
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-(叔丁氧羰基)甲基-3-(4-硝基苯基)丙酰胺(化合物27-16)
熔点125.5~130.0℃
[α]D 20-39.2°(c=0.53,氯仿)
IR(KBr,cm-1)3299,2981,1741,1674,1620,1522,1348,1222,1155
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-(4-氯苯基)-N-[2-(二甲氨基)乙基]丙酰胺(化合物27-17)
熔点111.0~115.0℃
[α]D 20-12.0°(c=0.31,氯仿)
IR(KBr,cm-1)3290,2939,1663,1618,1545,1493,1454,1355,1229
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-异戊基脲基]-N-甲基-3-(4-硝基苯基)丙酰胺(化合物27-18)
熔点109.0~116.0℃
[α]D 20-35.0°(c=0.50,氯仿)
IR(KBr,cm-1)3303,2957,1694,1668,1617,1516,1469,1346,1237,1134,1109
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-[2-(二甲氨基)乙基]-3-(2-硝基-4-联苯基)丙酰胺(化合物27-19)
熔点90℃
[α]D 20-24.1°(c=0.52,氯仿)
IR(KBr,cm-1)3286,2940,1692,1664,1621,1530,1355,700
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-[4-(苯磺酰)-3-硝基苯基]-N-[2-(二甲氨基)乙基]丙酰胺(化合物27-20)
[α]D 20-22.3°(c=0.55,氯仿)
IR(薄膜,cm-1)3305,2943,1668,1628,1544,1160,753
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-(2-萘基)丙酰]-4-甲基哌嗪(化合物27-21)
[α]D 20+14.5°(c=1.1,甲醇)
IR(薄膜,cm-1)2937,1688,1632,1527,1447,1216,1142
1-[(2R)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-(甲硫基)丙酰]-4-甲基哌嗪(化合物27-22)
[α]D 20-6.0°(c=0.5,甲醇)
IR(薄膜,cm-1)3368,2937,2794,1689,1636,1525,1446,1356,1292,1253,1212,1142,1001,751,701
1-[(2R)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-(苄硫基)丙酰]-4-甲基哌嗪(化合物27-23)
[α]D 20-23.4°(c=0.50,甲醇)
IR(薄膜,cm-1)3367,2938,2794,1689,1633,1494,1453,1356,1293,1213,1141,1002,753,701
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-苯基丙酰]-4-甲基哌嗪(化合物27-24)
[α]D 20+19.6°(c=0.52,甲醇)
IR(薄膜,cm-1)3359,2937,1689,1631,1526,1453,1215,1142,751,700
1-甲基-4-[(2S)-2-[3-苯乙基-3-[2-(新戊酰硫基)乙基]脲基]-3-苯基丙酰]哌嗪(化合物27-25)
[α]D 20+19.3°(c=0.98,甲醇)
IR(薄膜,cm-1)3349,2968,2936,1675,1632,1525,1455,950,750,700
1-甲基-4-[(2S)-2-[3-[2-(烟酰硫基)乙基]-3-苯乙基脲基]-3-苯基丙酰]哌嗪(化合物27-26)
[α]D 20+17.3°(c=0.57,甲醇)
IR(薄膜,cm-1)3370,2938,1632,1528,1453,1218,916,751,701
1-[(2R)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-苯基丙酰]-4-甲基哌嗪(化合物27-27),化合物27-24的对映体
[α]D 20-18.1°(c=0.52,甲醇)
IR(薄膜,cm-1)3364,2937,2794,1687,1636,1522,1496,1453,1291,1142,750,700
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-[2-(二甲氨基)乙基]-3-(4-异丙氧基苯基)丙酰胺(化合物27-28)
熔点110.0~112.5℃
[α]D 20-4.3°(c=0.30,氯仿)
IR(KBr,cm-1)3283,2974,1695,1664,1618,1550,1510,1240,1132,954,750,702
1-[(2S)-2-[3-[(1RS)-2-(乙酰硫基)-1-(二甲氨基甲基)乙基]-3-苯乙基脲基]-3-苯基丙酰]-4-甲基哌嗪(化合物27-29)
[α]D 20+11.8°(c=0.56,甲醇)
IR(薄膜,cm-1)2939,2793,1690,1633,1455,1292,1142,752
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-异戊基脲基]-N-[2-(二甲氨基)乙基]-3-苯基丙酰胺(化合物27-30)
[α]D 20+5.5°(c=0.50,氯仿)
IR(薄膜,cm-1)3285,2954,1694,1659,1620,1544,1228,1135
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-异戊基脲基]-N-[(1S)-1-(甲基氨基甲酰基)乙基]-3-苯基丙酰胺(化合物27-31)
[α]D 20-7.6°(c=1.0,氯仿)
IR(薄膜,cm-1)3293,3064,1629,1534,1227,1135,754,700
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-异戊基脲基]-3-(4-甲氧基苯基)-N-甲基丙酰胺(化合物27-32)
熔点113.0~118.0℃
[α]D 20-9.1°(c=0.52,氯仿)
IR(KBr,cm-1)3309,2959,1695,1667,1616,1545,1514,1247,1136,1036,948,832
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-异戊基脲基]-N-甲基-2-苯基乙酰胺(化合物27-33)
[α]D 20+1.3°(c=0.79,氯仿)
IR(薄膜,cm-1)3304,2956,2360,1688,1629,1513,1411,1355,1214,1135,950,755,698
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-异戊基脲基]-4-甲基戊酰]-4-甲基哌嗪(化合物27-34)
[α]D 20+8.0°(c=0.51,甲醇)
IR(薄膜,cm-1)2954,2868,1691,1632,1462,1291,1140
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-异戊基脲基]-N,4-二甲基戊酰胺(化合物27-35)
[α]D 20-24.4°(c=0.97,氯仿)
IR(薄膜,cm-1)3295,2956,1661,1623,1537,1235,1136,757
2-[3-[2-(乙酰硫基)乙基]-3-异戊基脲基]-N-甲基乙酰胺(化合物27-36)
IR(薄膜,cm-1)3399,2956,1633,1535,1412,1299,1236,1136,951,756
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-异戊基脲基]-3-环己基-N-甲基丙酰胺(化合物27-37)
[α]D 20-23.1°(c=0.54,氯仿)
IR(薄膜,cm-1)3295,2923,1693,1660,1623,1537,1489,1448,1355,1235,1136
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-异戊基脲基]-3-(4-咪唑基)-N-甲基丙酰胺(化合物27-38)
[α]D 20-16.1°(c=0.12,氯仿)
IR(薄膜,cm-1)3292,2956,2361,1633,1532,1411,1236,1135,950,756
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-异戊基脲基]-N-甲基-5-(3-甲苯磺酰胍基)戊酰胺(化合物27-39)
[α]D 20-7.2°(c=0.51,氯仿)
IR(薄膜,cm-1)3338,2955,1630,1549,1410,1259,1132,1083,755
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-1-甲基-3-苯乙基脲基]丙酰]-4-甲基哌嗪(化合物27-40)
[α]D 20-14.6°(c=1.0,氯仿)
IR(薄膜,cm-1)2937,2792,1692,1644,1548,1141,1076
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-[2-(二甲氨基)乙基]-3-(4-硝基苯基)丙酰胺(化合物27-41)
熔点71~86℃
[α]D 20-30.7°(c=0.49,氯仿)
IR(KBr,cm-1)3292,3085,1693,1664,1621,1519,1347,1287,1227,1135,951,860,748,700
(2S)-2-[3-[2-(苯甲酰硫基)乙基]-3-苯乙基脲基]-N-[2-(二甲氨基)乙基]-3-(4-硝基苯基)丙酰胺(化合物27-42)
[α]D 20-56.5°(c=0.47,氯仿)
IR(薄膜,cm-1)3408,1632,1519,1345,1208,913,750,690
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-[3-(二甲氨基)丙基]-3-(4-硝基苯基)丙酰胺(化合物27-43)
IR(薄膜,cm-1)3282,2942,1691,1663,1618,1520,1346,750
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-[2-(4-吗啉基)乙基]-3-(4-硝基苯基)丙酰胺(化合物27-44)
[α]D 20-31.4°(c=0.50,氯仿)
IR(薄膜,cm-1)3368,2941,1667,1631,1519,1454,1346,1116,701
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-(4-硝基苯基)-N-[2-(邻苯二甲酰亚氨基)乙基]丙酰胺(化合物27-45)
熔点110℃
[α]D 20-41.6°(c=0.53,氯仿)
IR(KBr,cm-1)3284,1716,1668,1618,1519,1395,1345,1280,1227,1137,1108,720,703
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-[2-[(N-甲基)环己基氨基]乙基]-3-(4-硝基苯基)丙酰胺(化合物27-46)
熔点90℃
[α]D 20-29.7°(c=0.47,氯仿)
IR(KBr,cm-1)3295,2930,1693,1661,1622,1520,1452,1346,1281,1136
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-[2-(二乙氨基)乙基]-3-(4-硝基苯基)丙酰胺(化合物27-47)
熔点65℃
[α]D 20-34.7°(c=0.49,氯仿)
IR(KBr,cm-1)3293,2970,1692,1620,1612,1520,1452,1346,1228,1135
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-[2-[(N-甲基)苯氨基]乙基]-3-(4-硝基苯基)丙酰胺(化合物27-48)
熔点129.0~131.0℃
[α]D 20-44.1°(c=0.51,氯仿)
IR(KBr,cm-1)3284,2928,1693,1665,1618,1518,1450,1347,1280,1135
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-[4-(二甲氨基)丁基]-3-(4-硝基苯基)丙酰胺(化合物27-49)
[α]D 20-26.2°(c=0.53,氯仿)
IR(薄膜,cm-1)3283,2940,1694,1661,1619,1519,1347,748
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-(4-硝基苯基)-N-[2-(2-吡啶基)乙基]丙酰胺(化合物27-50)
熔点106.0~112.5℃
[α]D 20-39.5°(c=0.50,氯仿)
IR(KBr,cm-1)3282,3084,2929,1692,1667,1618,1519,1436,1346,1228,1135,1108,749,701
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-[3-(1-咪唑基)丙基]-3-(4-硝基苯基)丙酰胺(化合物27-51)
[α]D 20-33.9°(c=0.49,氯仿)
IR(薄膜,cm-1)3294,2938,1672,1630,1519,1346,1227,753
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-(4-硝基苯基)-N-[2-(1-哌啶基)乙基]丙酰胺(化合物27-52)
熔点104.0~106.0℃
[α]D 20-20.5°(c=0.53,氯仿)
IR(KBr,cm-1)3291,2934,1694,1664,1620,1520,1347,1132,747,700
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-[2-(二甲氨基)乙基]-3-苯基丙酰胺(化合物27-53)
熔点111.5~114.5℃
[α]D 20-3.7°(c=0.51,氯仿)
IR(KBr,cm-1)3290,2939,1693,1662,1620,1542,1497,1454,1229,1135,749,700
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-[2-(二甲氨基)乙基]-3-(4-氟苯基)丙酰胺(化合物27-54)
熔点90℃
[α]D 20-6.1°(c=0.48,氯仿)
IR(KBr,cm-1)3286,2943,1695,1662,1621,1542,1511,1454,1354,1224,1135,949,749,700
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-[2-(二甲氨基)乙基]-3-(4-羟基苯基)丙酰胺(化合物27-55)
[α]D 20-20.8°(c=0.37,二甲亚砜)
IR(薄膜,cm-1)3290,2946,1629,1516,1454,1357,1229,1137,1029,952,831,753,701
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-[2-(二甲氨基)乙基]-3-(4-甲氧基苯基)丙酰胺(化合物27-56)
熔点95.5~106.0℃(分解)
[α]D 20-5.3°(c=1.0,氯仿)
IR(KBr,cm-1)3288,2941,1695,1664,1619,1547,1250
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-[2-(二甲氨基)乙基]-3-(2-噻吩基)丙酰胺(化合物27-57)
熔点89.0~92.0℃(分解)
[α]D 20-8.4°(c=0.99,氯仿)
IR(KBr,cm-1)3280,2941,1691,1664,1620,1549,1498,1292,1229,1136,700
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-[2-(二甲氨基)乙基]-3-(2-萘基)丙酰胺(化合物27-58)
[α]D 20-7.2°(c=0.50,氯仿)
IR(薄膜,cm-1)3291,2942,1690,1660,1622,1538,751
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-(4-联苯基)-N-[2-(二甲氨基)乙基]丙酰胺(化合物27-59)
[α]D 20-10.5°(c=1.0,氯仿)
IR(薄膜,cm-1)3294,2942,1663,1626,1535,1488,759,700
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-异戊基脲基]-N-[2-(二甲氨基)乙基]-3-(4-硝基苯基)丙酰胺(化合物27-60)
熔点112.5~114.5℃(分解)
[α]D 20-20.1°(c=0.51,氯仿)
IR(KBr,cm-1)3290,2954,1696,1663,1618,1520,1349,1237,1137,954,860
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-异戊基脲基]-3-(4-联苯基)-N-丁基丙酰胺(化合物27-61)
熔点101.5~103.7℃
[α]D 20-22.9°(c=0.51,二甲亚砜)
IR(KBr,cm-1)3279,3096,2958,1696,1664,1617,1546,1227,1135,759,698
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-异戊基脲基]-N-甲基-3-苯基丙酰胺(化合物27-62)
熔点116.5~120.5℃
[α]D 20-16.5°(c=0.97,氯仿)
IR(KBr,cm-1)3299,3087,2955,1695,1671,1620,1544,1412,1230,1135,700
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-异丁基脲基]-N-甲基-3-苯基丙酰胺(化合物27-63)
[α]D 20-6.7°(c=0.02,甲醇)
IR(KBr,cm-1)3299,2960,1693,1664,1621,1543,1135,950
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(4-甲基戊基)脲基]-N-甲基-3-苯基丙酰胺(化合物27-64)
[α]D 20-20.9°(c=0.09,氯仿)
IR(KBr,cm-1)3298,2954,1691,1661,1622,1537,1494,1410,1367,1136
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(3,3-二甲基丁基)脲基]-N-甲基-3-苯基丙酰胺(化合物27-65)
[α]D 20-13.1°(c=0.33,氯仿)
IR(薄膜,cm-1)3294,2956,1693,1666,1620,1537,1411,1228,1136,756
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-甲基-3-苯基丙酰胺(化合物27-66)
[α]D 20-21.7°(c=0.68,氯仿)
IR(薄膜,cm-1)3295,2934,1689,1661,1622,1536,1410,1228,1136,753,700
(2S)-2-[3-[2-(乙酰硫基)-1-(乙酰硫基甲基)乙基]-3-异戊基脲基]-N-甲基-3-苯基丙酰胺(化合物27-67)
[α]D 20-8.8°(c=0.93,氯仿)
IR(薄膜,cm-1)3307,2956,1694,1630,1516,1355,1134,957,756
(2S)-2-[3-[2-(乙酰硫基)-1-(苯硫基甲基)乙基]-3-异戊基脲基]-N-甲基-3-苯基丙酰胺(化合物27-68)
IR(薄膜,cm-1)2955,1690,1624,1513,1439,1354,1231,1132,956,743,696
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-异戊基脲基]-N,N-二甲基-3-苯基丙酰胺(化合物27-69)
[α]D 20+47.6°(c=0.50,氯仿)
IR(薄膜,cm-1)3340,2955,1692,1633,1531,1421,1136,952,754,701
(2S)-2-[3-[3-(乙酰硫基)丙基]-3-异戊基脲基]-N,N-二甲基-3-苯基丙酰胺(化合物27-70)
[α]D 20+34.3°(c=1.0,氯仿)
IR(薄膜,cm-1)3343,2955,1694,1634,1531,1494,1267,1134,954,753,701
(2S)-2-[3-[4-(乙酰硫基)丁基]-3-异戊基脲基]-N,N-二甲基-3-苯基丙酰胺(化合物27-71)
IR(薄膜,cm-1)2962,1732,1694,1634,1505,1255,755
(2S)-2-[3-[(1RS)-2-(乙酰硫基)-1-苯基乙基]-3-异戊基脲基]-N,N-二甲基-3-苯基丙酰胺(化合物27-72)
IR(薄膜,cm-1)2927,1694,1634,1495,756,701
(2S)-2-[3-[(1RS)-1-(乙酰硫基甲基)-3-苯丙基]-3-异戊基脲基]-N,N-二甲基-3-苯基丙酰胺(化合物27-73)
IR(薄膜,cm-1)3423,2927,1691,1634,1496,1260,1133,754,700
(2S)-2-[3-[(1RS)-2-(乙酰硫基)-1-(苯氧基甲基)乙基]-3-异戊基脲基]-N,N-二甲基-3-苯基丙酰胺(化合物27-74)
IR(薄膜,cm-1)2955,1693,1634,1495,1242,755
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-异戊基脲基]-N-甲基-4-苯基丁酰胺(化合物27-75)
[α]D 20-9.9°(c=0.50,氯仿)
IR(薄膜,cm-1)3291,2955,1694,1660,1621,1538,1410,1225,1134,749,699
(2S)-2-[3-[(1R)-2-(乙酰硫基)-1-苄基乙基]-3-异戊基脲基]-3-(4-联苯基)-N-丁基丙酰胺(化合物27-76)
[α]D 20-16.7°(c=1.1,二甲亚砜)
IR(薄膜,cm-1)3422,3306,2957,1689,1661,1624,1512,1225,1133,759,699
(2S)-2-[3-[2-(乙酰硫基)乙基]-1-异戊基脲基]-N-[2-(二甲氨基)乙基]-3-苯基丙酰胺(化合物27-77)
[α]D 20-43.7°(c=0.30,氯仿)
IR(KBr,cm-1)3350,2954,1690,1661,1632,1528,1466,1365,1243,1133,753,700
2-[3-[(1R)-2-(乙酰硫基)-1-苄基乙基]-1-异戊基脲基]-N-[2-(二甲氨基)乙基]乙酰胺(化合物27-78)
2-[3-[(1S)-2-(乙酰硫基)-1-苄基乙基]-1-异戊基脲基]-N-[2-(二甲氨基)乙基]乙酰胺(化合物27-79),化合物27-78的对映体
[α]D 20-3.2°(c=0.47,氯仿)
IR(薄膜,cm-1)3312,2954,1634,1532,1244,752
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-异戊基脲基]-6-(叔丁氧基甲酰氨基)-N-甲基己酰胺(化合物27-80)
[α]D 20-14.6°(c=0.37,氯仿)
IR(薄膜,cm-1)3305,2955,1693,1624,1534,1365,1248,1172,1136,756
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-(4-羟基苯基)丙酰]-4-甲基哌嗪(化合物27-81)
[α]D 20+20.4°(c=0.50,甲醇)
IR(薄膜,cm-1)3232,3009,2940,2800,1684,1626,1515,1450,1248
(2S)-3-[4-乙酰氨基)苯基]-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-[2-(二甲氨基)乙基]丙酰胺(化合物27-82)
熔点95℃(分解)
[α]D 20-5.3°(c=0.48,氯仿)
IR(KBr,cm-1)3279,2941,1668,1614,1540,1411,1369,1318,1138,750,702
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-[2-(叔丁氧羰基)乙基]-3-(4-硝基苯基)丙酰胺(化合物27-83)
熔点142.0~143.5℃
[α]D 20-35.0°(c=0.52,氯仿)
IR(KBr,cm-1)3298,1729,1695,1676,1661,1617,1550,1517,1348,1158,747,735,697
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-[2-(1-环己烯基)乙基]脲基]丙酰]-4-甲基哌嗪(化合物27-84)
[α]D 20+10.3°(c=1.1,甲醇)
IR(薄膜,cm-1)3370,2929,2793,1690,1632,1529,1447,1292,1214,1140,1002
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(3-甲基-3-丁烯基)脲基]丙酰]-4-甲基哌嗪(化合物27-85)
[α]D 20+32.2°(c=0.50,氯仿)
IR(薄膜,cm-1)3368,2937,1689,1634,1531,1447,1291,1214,1141,1002
1-[2-[3-[2-(乙酰硫基)乙基]-3-(2-环己基乙基)脲基]-2-甲基丙酰]-4-甲基哌嗪(化合物27-86)
IR(薄膜,cm-1)3369,2923,1644,1524,1426,1291,1224,1169,1139,1004,753
1-[1-[3-[2-(乙酰硫基)乙基]-3-(2-环己基乙基)脲基]-1-环丙烷羰基]-4-甲基哌嗪(化合物27-87)
IR(薄膜,cm-1)3338,2981,2923,2851,1650,1524,1446,1288,1214,1142,1109,754
1-[1-[3-[2-(乙酰硫基)乙基]-3-(2-环己基乙基)脲基]-1-环戊烷羰基]-4-甲基哌嗪(化合物27-88)
IR(薄膜,cm-1)3377,2922,2850,2794,1648,1522,1448,1291,1143,1110,753
4-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-[2-(1-金刚烷基)乙基]脲基]丙酰]吗啉(化合物27-89)
[α]D 20+12.9°(c=1.0,甲醇)
IR(薄膜,cm-1)3380,2902,2847,2677,1692,1633,1514,1446,1357,1296,1271,1238,1214,1116,1030,754
4-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环己基乙基)脲基]丙酰]吗啉(化合物27-90)
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-[2-(1-金刚烷基)乙基]脲基]丙酰]-4-甲基哌嗪(化合物27-91)
实施例28
(2S)-N,N-二甲基-2-[3-异戊基-3-[2-(甲硫基)乙基]脲基]-3-苯基丙酰胺(化合物28-1)
在氮气下,将盐酸N1,N1-二甲基-L-苯基丙氨酸酰胺(参考化合物8-3,206mg)、1,1’-羰基二咪唑(190mg)和咪唑(61mg)悬浮在无水四氢呋喃(3.5ml)中,悬浮液在室温下搅拌20分钟。向反应混合物中加入N-[2-(甲硫基)乙基]异戊胺(参考化合物13-28,161mg)的无水四氢呋喃(1.5ml)溶液,混合物回流一小时。反应混合物减压浓缩,向浓缩物中加入10%柠檬酸水溶液,全部混合物用乙醚萃取。有机层先后用水和饱和盐水洗涤,经无水硫酸镁干燥,减压浓缩。所得油状物用硅胶柱色谱法纯化,得到306mg(89%)标题化合物(化合物28-1)。
(化合物28-1)
[α]D 20+39.1°(c=0.96,氯仿)
IR(薄膜,cm-1)3338,2955,1632,1496,1420,1295,1236,753,701
按照类似于实施例28的方法得到下列化合物。
(2S)-3-(4-联苯基)-N-丁基-2-[3-异戊基-3-[2-(甲硫基)乙基]脲基]丙酰胺(化合物28-2)
熔点134.0~136.2℃
[α]D 20-17.5°(c=0.52,二甲亚砜)
IR(KBr,cm-1)3284,3090,2957,1667,1617,1546,1236,759,697
1-[(2S)-2-[3-(2-环己基)乙基-3-[2-(甲硫基)乙基]脲基]丙酰]-4-甲基哌嗪(化合物28-3)
IR(薄膜,cm-1)3352,2921,2850,2794,1633,1506,1447,1292,1213,1142,1002,754
1-[(2S)-2-[3-(2-甲硫基)乙基]-3-苯乙基脲基]丙酰]-4-甲基哌嗪(化合物28-4)
IR(薄膜,cm-1)3418,2976,2937,2794,1632,1510,1292,1215
(2S)-3-(4-联苯基)-N-丁基-2-[3-异戊基-3-[2-(苯硫基)乙基]脲基]丙酰胺(化合物28-5)
熔点111.0~111.7℃
[α]D 20-15.2°(c=0.48,二甲亚砜)
IR(KBr,cm-1)3284,3078,2956,1666,1617,1550,1234,737,690
(2S)-3-(4-联苯基)-N-丁基-2-[3-[(1RS)-1-(乙氧羰基)-2-(苯硫基)乙基]-3-异戊基脲基]丙酰胺(化合物28-6)
IR(薄膜,cm-1)3310,2957,1736,1626,1520,1411,1368,1301,1231,1093
(2S)-2-[3-[(2RS)-2-(叔丁氧羰基)-3-(苯硫基)丙基]-3-异戊基脲基]-N-甲基-3-苯基丙酰胺(化合物28-7)
[α]D 20-28.2°(c=0.40,氯仿)
IR(薄膜,cm-1)3299,2956,1712,1664,1624,1536,1150
(2S)-2-[3-[(2RS)-2-(叔丁氧羰基)-3-(苯硫基)丙基]-3-异丁基脲基]-N-甲基-3-苯基丙酰胺(化合物28-8)
[α]D 20-29.6°(c=0.48,氯仿)
IR(薄膜,cm-1)3301,2959,1712,1622,1536,1258,1150
1-[(2S)-2-[3-[2-(1-金刚烷基)乙基]-3-[2-(甲硫基)乙基]脲基]丙酰]-4-甲基哌嗪(化合物28-9)
[α]D 20+10.0°(c=1.0,甲醇)
IR(薄膜,cm-1)3419,2903,2846,1632,1508,1448
1-[(2S)-2-[3-(2-环戊基乙基)-3-[2-(甲硫基)乙基]脲基]丙酰]-4-甲基哌嗪(化合物28-10)
[α]D 20+8.3°(c=1.0,甲醇)
IR(薄膜,cm-1)3349,2942,1632,1504,1446
1,1’-[(2S,2’S)-2,2’-[3,3’-双(2-环己基乙基)-3,3’-[2,2’-(二硫基)二乙基]二脲基]二丙酰]-4,4’-二甲基二哌嗪(化合物28-11)
IR(薄膜,cm-1)3350,2922,1632,1510,1447
1,1’-[(2S,2’S)-2,2’-[3,3’-双[2-(1-金刚烷基)乙基]-3,3’-[2,2’-(二硫基)二乙基]二脲基]二丙酰]-4,4’-二甲基二哌嗪(化合物28-12)
1,1’-(二甲基)-4,4’-[(2S,2’S)-2,2’-[3,3’-二苯乙基-3,3’-[2,2’-(二硫基)二乙基]二脲基]二丙酰]二哌嗪(化合物28-13)
IR(薄膜,cm-1)3352,1632,1454,1292
1,1’-(二甲基)-4,4’-[(2S,2’S)-2,2’-[3,3’-[2,2’-(二硫基)二乙基]二脲基]二丙酰]二哌嗪(化合物28-14)
[α]D 20-8.1°(c=1.0,甲醇)
IR(薄膜,cm-1)3341,2976,2938,2796,1632,1555,1446,1367,1293,1237,1173,1144,1074,1034,1002
实施例29
1-甲基-4-[(2S)-2-[3-(3RS)-2-氧代四氢噻吩-3-基]-1-苯乙基脲基]丙酰]哌嗪(化合物29-1)
在氮气下,将盐酸DL-高半胱氨酸硫内酯(280mg)、1,1’-羰基二咪唑(324mg)和咪唑(124mg)悬浮在无水四氢呋喃(5ml)中,悬浮液在室温下搅拌15分钟。向反应混合物中加入1-甲基-4-[(2S)-2-(苯乙氨基)丙酰]哌嗪(参考化合物10-3,500mg)的无水四氢呋喃(5ml)溶液,混合物回流20分钟。向反应混合物中加入10%碳酸氢钠水溶液,全部混合物用乙酸乙酯萃取。有机层先后用水和饱和盐水洗涤,经无水硫酸镁干燥,减压浓缩。所得油状物用硅胶柱色谱法纯化,得到592mg(78%)标题化合物(化合物29-1)。
(化合物29-1)
IR(薄膜,cm-1)2940,1704,1632,1524,1454,1291,1253
实施例30
1-[(2S)-2-[3-(2-巯基乙基)-3-苯乙基脲基]丙酰]-4-甲基哌嗪(化合物30-1)
在氮气下,将1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]丙酰]-4-甲基哌嗪(化合物13-2,36.6g)溶于甲醇(87ml),溶液用冰冷却。向其中滴加1N氢氧化钠水溶液(87ml),混合物在冰冷却下搅拌10分钟。在冰冷却下,向反应混合物中加入10%柠檬酸水溶液,调pH至7。混合物减压浓缩,向浓缩物中加入10%碳酸氢钠水溶液(300ml),全部混合物用乙酸乙酯萃取。有机层先后用水和饱和盐水洗涤,经无水硫酸钠干燥,减压浓缩。所得油状物用硅胶柱色谱法纯化,得到标题化合物(化合物30-1)。
(化合物30-1)
按照类似于实施例30的方法得到下列化合物。
1-[(2S)-2-[3-(2-巯基乙基)-3-苯乙基脲基]丁酰]-4-甲基哌嗪(化合物30-2)
[α]D 20+9.8°(c=0.44,甲醇)
IR(薄膜,cm-1)3345,2936,2793,1630,1529,1451,1293
1-[(2S)-2-[3-(2-巯基乙基)-3-苯乙基脲基]-3-苯基丙酰]-4-甲基哌嗪(化合物30-3)
[α]D 20+12.5°(c=0.52,甲醇)
IR(薄膜,cm-1)3343,2937,2795,1628,1528,1452,1291,1215,1144,1002,751,700
(2S)-6-(叔丁氧基甲酰氨基)-2-[3-异戊基-3-(2-巯基乙基)脲基]-N-甲基己酰胺(化合物30-4)
熔点119.0~124.0℃
[α]D 20-14.5°(c=0.50,氯仿)
IR(薄膜,cm-1)3322,2934,2545,1711,1653,1619,1530,1410,1366,1246,1166
1-[(2S)-2-[3-(2-巯基乙基)-3-苯乙基脲基]-3-苯基丙酰]哌嗪(化合物30-5)
1-[(2S)-2-[3-(2-环己基乙基)-3-(2-巯基乙基)脲基]丙酰]-4-甲基哌嗪(化合物30-6)
熔点85.5~88.0℃
IR(KBr,cm-1)2925,2848,2791,2544,1647,1621,1534,1451,1290,1219,1142
1-[(2S)-2-[3-(2-环戊基乙基)-3-(2-巯基乙基)脲基]丙酰]-4-甲基哌嗪(化合物30-7)
1-[(2S)-2-[3-[2-(1-金刚烷基)乙基]-3-(2-巯基乙基)脲基]丙酰]-4-甲基哌嗪(化合物30-8)
实施例31
1-[(2R)-3-巯基-2-[3-(2-巯基乙基)-3-苯乙基脲基]丙酰]-4-甲基哌嗪(化合物31-1)
在氮气下和干冰-甲醇冷却下,向液氨(60ml)中滴加1-[(2R)-3-(苄硫基)-2-[3-[2-(苄硫基)乙基]-3-苯乙基脲基]丙酰]-4-甲基哌嗪(化合物13-45,1.05g)的无水四氢呋喃(10ml)溶液,向其中分批加入金属钠(271mg),直到颜色不消失为止,混合物搅拌一小时。向反应混合物中加入晶体氯化铵进行脱色,然后在室温下向混合物中通入氮气,使氨蒸发。向所得残余物中加入10%碳酸氢钠水溶液,全部混合物用乙酸乙酯萃取。有机层先后用水和饱和盐水洗涤,经无水硫酸钠干燥,减压浓缩,得到标题化合物(化合物31-1)。
实施例32
1-[(2S)-2-[3-[2-(苯甲酰硫基)乙基]-3-苯乙基脲基]丙酰]-4-甲基哌嗪(化合物32-1)
在氮气下,将1-[(2S)-2-[3-(2-巯基乙基)-3-苯乙基脲基]丙酰]-4-甲基哌嗪(化合物30-1,32.9g)溶于氯仿(87ml),搅拌溶液。向该溶液中加入三乙胺(13.3ml),然后在冰冷却下滴加苯甲酰氯(10.1ml),混合物搅拌25分钟。反应混合物减压浓缩,向残余物中加入10%碳酸氢钠水溶液,全部混合物用乙酸乙酯萃取。有机层先后用10%碳酸氢钠水溶液、水和饱和盐水洗涤,经无水硫酸钠干燥,减压浓缩。所得油状物用硅胶柱色谱法纯化,得到标题化合物(化合物32-1)。
(化合物32-1)
IR(薄膜,cm-1)3374,2937,2794,1637,1529,1448,1366,1292,1209,1175,1144,1030,1001
按照类似于实施例32的方法得到下列化合物。
1-[(2S)-2-[3-[2-(异丙基氨基甲酰基硫基)乙基]-3-苯乙基脲基]丙酰]-4-甲基哌嗪(化合物32-2)
[α]D 20+18.7°(c=1.0,氯仿)
IR(薄膜,cm-1)3264,2974,2938,2797,1632,1536,1454,1362,1291,1218,1172,1144
1-[(2R)-3-(乙酰硫基)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]丙酰]-4-甲基哌嗪(化合物32-3)
[α]D 20-24.3°(c=0.53,甲醇)
IR(薄膜,cm-1)3363,2937,2794,1689,1638,1528,1450,1355,1293,1255,1212,1138,1001,954,752,702
实施例33
(2S,2’S)-N,N’-双[2-(叔丁氧基甲酰氨基)乙基]-3,3’-双(4-硝基苯基)-2,2’-[3,3’-二苯乙基-3,3’-[2,2’-(二硫基)二乙基]二脲基]双(丙酰胺)
(化合物33-1)
将(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-[2-(叔丁氧基甲酰氨基)乙基]-3-(4-硝基苯基)丙酰胺(化合物27-13,800mg)溶于四氢呋喃(5ml),向该溶液中加入1N氨水(7ml),混合物在室温下搅拌3.5天。向反应混合物中加入水,全部混合物用乙酸乙酯萃取。有机层用饱和盐水洗涤,经无水硫酸钠干燥,减压浓缩。所得油状物用硅胶柱色谱法纯化,得到738mg(99%)标题化合物(化合物33-1)。
(化合物33-1)
[α]D 20-15.3°(c=0.57,甲醇)
IR(薄膜,cm-1)3293,2977,2933,1708,1660,1619,1520,1346,1168,755
按照类似于实施例33的方法得到下列化合物。
(2S,2’S)-N,N’-双[2-(二甲氨基)乙基]-3,3’-双(4-硝基苯基)-2,2’-[3,3’-二苯乙基-3,3’-[2,2’-(二硫基)二乙基]二脲基]双(丙酰胺)(化合物33-2)
[α]D 20-21.0°(c=0.48,氯仿)
IR(薄膜,cm-1)3291,2940,1658,1620,1520,1346,751
(2S,2’S)-2,2’-[3,3’-二异丁基-3,3’-[2,2’-(二硫基)二乙基]二脲基]-N,N’-二甲基-3,3’-二苯基双(丙酰胺)(化合物33-3)
IR(KBr,cm-1)3298,3090,2960,1664,1621,1538,1386,1366
(2S,2’S)-2,2’-[3,3’-二异戊基-3,3’-[2,2’-(二硫基)二乙基]二脲基]-N,N’-二甲基-3,3’-二苯基双(丙酰胺)(化合物33-4)
IR(KBr,cm-1)3300,3091,2955,1667,1621,1538,1367,1300
(2S,2’S)-N,N’-双[(1S)-1-(甲基氨基甲酰基)乙基]-2,2’-[3,3’-二异戊基-3,3’-[2,2’-(二硫基)二乙基]二脲基]-3,3’-二苯基双(丙酰胺)(化合物33-5)
[α]D 20-20.2°(c=0.19,氯仿)
IR(KBr,cm-1)3305,2956,1668,1626,1541,1228,732,699
1,1’-二甲基-4,4’-[(2S,2’S)-2,2’-[3,3’-二苯乙基-3,3’-[(2RS,2’RS)-2,2’-(二硫基)二丙基]二脲基]-3,3’-二苯基二丙酰]二哌嗪(化合物33-6)
IR(薄膜,cm-1)3357,2938,1628,1514,1454,1364,1291,1218,1172,1143,1002,752,700
1,1’-[(2S,2’S)-2,2’-[3,3’-双(2-环戊基乙基)-3,3’-[2,2’-(二硫基)二乙基]二脲基]二丙酰]-4,4’-二甲基二哌嗪(化合物33-7)
1,1’-[(2S,2’S)-2,2’-[3,3’-双[2-(1-金刚烷基)乙基]-3,3’-[2,2’-(二硫基)二乙基]二脲基]二丙酰]-4,4’-二甲基二哌嗪(化合物33-8)
实施例34
盐酸(2S)-6-氨基-2-[3-异戊基-3-(2-巯基乙基)脲基]-N-甲基己酰胺(化合物34-1)
在氮气下,向(2S)-6-(叔丁氧基甲酰氨基)-2-[3-异戊基-3-(2-巯基乙基)脲基]-N-甲基己酰胺(化合物30-4,346mg)的氯仿(4ml)溶液中加入4.6N氯化氢的乙酸乙酯(2ml)溶液。混合物搅拌一小时,然后减压浓缩,得到292mg(99%)标题化合物(化合物34-1)。
(化合物34-1)
[α]D 20+10.4°(c=0.48,二甲亚砜)
IR(薄膜,cm-1)3303,2955,1694,1622,1532,1366,1247,1171,757
按照类似于实施例34的方法得到下列化合物。
二盐酸(2S,2’S)-N,N’-双(2-氨基乙基)-3,3’-双(4-硝基苯基)-2,2’-[3,3’-二苯乙基-3,3’-[2,2’-(二硫基)二乙基]二脲基]双(丙酰胺)(化合物34-2)
[α]D 20-15.3°(c=0.99,甲醇)
IR(薄膜,cm-1)2929,1624,1518,1345,748,700
实施例35
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-苯基丙酰]-4-甲基哌嗪富马酸氢盐(化合物35-1)
将1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-苯基丙酰]-4-甲基哌嗪(化合物27-24,16.39g)溶于乙醚(150ml),在冰冷却下,向其中加入富马酸(3.83g)的甲醇(100ml)溶液。反应混合物减压浓缩,将所得油状物溶于二乙基酮(40ml),溶液在冰箱中放置过夜,得到9.04g(45%)标题化合物(化合物35-1),为晶体。
(化合物35-1)
熔点117.5~120.3℃
[α]D 20+25.3°(c=0.99,甲醇)
IR(KBr,cm-1)3400,3025,2936,2464,1718,1693,1636,1530,1498,1452,1360,1284,1172,979,790,754,703
按照类似于实施例35的方法得到下列化合物。
1-[(2RS)-3-(乙酰硫基)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-3-甲基丁酰]-4-甲基哌嗪乙酸氢盐(化合物35-2)
IR(薄膜,cm-1)3391,2936,2794,1686,1636,1509,1453,1364,1294,1249,1202,1143,1110
1-[(2S)-2-[3-(2-巯基乙基)-3-苯乙基脲基]-3-苯基丙酰]-4-甲基哌嗪富马酸氢盐(化合物35-3)
[α]D 20+14.9°(c=1.0,甲醇)
IR(薄膜,cm-1)3343,3006,2527,1710,1632,1529,1452,1366,1246,979,752,702
1-[(2S)-2-[3-[2-(苯甲酰硫基)乙基]-3-苯乙基脲基]丙酰]-4-甲基哌嗪L-酒石酸氢盐(化合物35-4)
熔点126.5~131.5℃
[α]D 20+29.9°(c=1.0,甲醇)
IR(KBr,cm-1)3270,3026,1736,1662,1614,1518,1458,1301,1250,1210,1130,1080,1020,976,916,688
1-[(2S)-2-[3-(2-巯基乙基)-3-苯乙基脲基]-3-苯基丙酰]哌嗪富马酸氢盐(化合物35-5)
[α]D 20+16.1°(c=0.53,甲醇)
IR(KBr,cm-1)3348,3027,1717,1636,1522,1455,1369,1247,1083,1029,979,750,701
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环己基乙基)脲基]丙酰]-4-甲基哌嗪L-酒石酸氢盐(化合物35-6)
熔点106~111℃
[α]D 20+27.4°(c=1.0,甲醇)
IR(KBr,cm-1)3308,2924,2851,1693,1632,1514,1452,1300,1250,1215,1130,1083,1018
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环己基乙基)脲基]丙酰]-4-甲基哌嗪柠檬酸氢盐(化合物35-7)
熔点75℃(分解)
[α]D 20+18.3°(c=1.0,甲醇)
IR(KBr,cm-1)3392,2925,2852,1733,1691,1628,1531,1456,1219,1135
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环己基乙基)脲基]丙酰]-4-甲基哌嗪富马酸氢盐(化合物35-8)
熔点69~80℃
[α]D 20+20.6°(c=1.0,甲醇)
IR(KBr,cm-1)3385,2925,2852,2471,1710,1690,1652,1526,1448,1247,1137,1057
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环戊基乙基)脲基]丙酰]-4-甲基哌嗪L-酒石酸氢盐(化合物35-9)
熔点100℃
[α]D 20+27.8°(c=1.0,甲醇)
IR(KBr,cm-1)3325,2948,1633,1526,1454,1217,1133
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环戊基乙基)脲基]丙酰]-4-甲基哌嗪二乙酰-L-酒石酸氢盐(化合物35-10)
熔点56~58℃
[α]D 20+11.4°(c=1.0,甲醇)
IR(KBr,cm-1)3392,1740,1636,1540,1457,1374,1222
双[1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环戊基乙基)脲基]丙酰]-4-甲基哌嗪]二苯甲酰-L-酒石酸氢盐(化合物35-11)
熔点112.0~115.3℃
[α]D 20-17.5°(c=1.0,甲醇)
IR(KBr,cm-1)3412,2949,1717,1694,1636,1522,1452,1374,1268,1116
双[1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环戊基乙基)脲基]丙酰]-4-甲基哌嗪]二对甲苯磺酰-L-酒石酸氢盐(化合物35-12)
熔点131~136℃(分解)
[α]D 20-29.1°(c=1.0,甲醇)
IR(KBr,cm-1)3419,2949,2868,1710,1643,1503,1275,1128
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环戊基乙基)脲基]丙酰]-4-甲基哌嗪柠檬酸氢盐(化合物35-13)
熔点75~83℃
[α]D 20+18.4°(c=1.0,甲醇)
IR(KBr,cm-1)3391,2952,1693
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环戊基乙基)脲基]丙酰]-4-甲基哌嗪4-硝基苯甲酸氢盐(化合物35-14)
熔点76.5~78.5℃
IR(KBr,cm-1)3390,2947,2360,1691,1631,1516,1350,718
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-(2-环庚基乙基)脲基]丙酰]-4-甲基哌嗪L-酒石酸氢盐(化合物35-15)
熔点85~100℃
[α]D 20+24.5°(c=1.0,甲醇)
IR(KBr,cm-1)3322,2922,2853,2699,1693,1632,1528,1460,1303,1264,1216,1135,1068,976
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-[2-[3,5-二(叔丁基)-4-羟基苯基]乙基]脲基]丙酰]-4-甲基哌嗪L-酒石酸氢盐(化合物35-16)
熔点85℃(分解)
[α]D 20+5.3°(c=1.0,甲醇)
IR(KBr,cm-1)3391,2968,1736,1690,1632,1530,1435,1365,1234,1122
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-[2-(1-金刚烷基)乙基]脲基]丙酰]-4-甲基哌嗪L-酒石酸氢盐(化合物35-17)
熔点125.5~130.0℃
[α]D 20+24.2°(c=1.0,甲醇)
IR(KBr,cm-1)3325,2903,2846,1691,1635,1518,1452,1299,1248,1216,1132,1086,976
双[1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-[2-(1-金刚烷基)乙基]脲基]丙酰]-4-甲基哌嗪]二苯甲酰-L-酒石酸氢盐(化合物35-18)
熔点137.5~138.3℃分解)
[α]D 20-16.8°(c=1.0,甲醇)
IR(KBr,cm-1)3420,2902,2846,2324,1717,1690,1644,1507,1452,1360,1315,1267,1211,1128
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-[2-(1-金刚烷基)乙基]脲基]丙酰]-4-甲基哌嗪二对甲苯磺酰-L-酒石酸氢盐(化合物35-19)
熔点136.0~140.0℃
[α]D 20-46.9°(c=1.0,甲醇)
IR(KBr,cm-1)3400,2903,2846,1717,1688,1636,1532,1451,1408,1381,1347,1265,1211,1177,1127,1113,1022
双[1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-[2-(1-金刚烷基)乙基]脲基]丙酰]-4-甲基哌嗪]二对甲苯磺酰-L-酒石酸氢盐(化合物35-20)
熔点135.0~138.5℃
[α]D 20-23.9°(c=1.0,甲醇)
IR(KBr,cm-1)3412,2902,2846,2416,2298,1717,1636,1508,1451,1346,1276,1212,1178,1112,1035,980
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-[2-(1-金刚烷基)乙基]脲基]丙酰]-4-甲基哌嗪柠檬酸氢盐(化合物35-21)
熔点80℃(分解)
[α]D 20+15.1°(c=1.0,甲醇)
IR(KBr,cm-1)3392,2903,2846,1728,1636,1534,1451,1218,1136,1055
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-[2-(1-金刚烷基)乙基]脲基]丙酰]-4-甲基哌嗪富马酸氢盐(化合物35-22)
熔点90℃(分解)
[α]D 20+17.5°(c=1.0,甲醇)
IR(KBr,cm-1)3401,2902,2846,2658,1690,1636,1526,1452,1357,1297,1245,1146,1055,979
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-[2-(1-金刚烷基)乙基]脲基]丙酰]-4-甲基哌嗪4-硝基苯甲酸氢盐(化合物35-23)
熔点111.0~114.0℃
[α]D 20+16.0°(c=1.0,甲醇)
IR(KBr,cm-1)3391,2900,2845,1691,1633,1516,1477,1403,1352,1319,1288,1245,1217,1137,1104,1039,1010
1-[(2S)-2-[3-(2-环己基乙基)-3-(2-巯基乙基)脲基]丙酰]-4-甲基哌嗪L-酒石酸氢盐(化合物35-24)
熔点70~90℃
[α]D 20+22.8°(c=1.0,甲醇)
IR(KBr,cm-1)3326,2923,2851,1732,1627,1531,1449,1247,1217,1133,1077
1-[(2S)-2-[3-(2-环戊基乙基)-3-(2-巯基乙基)脲基]丙酰]-4-甲基哌嗪L-酒石酸氢盐(化合物35-25)
熔点60~80℃
[α]D 20+23.1°(c=1.0,甲醇)
IR(KBr,cm-1)3322,1627,1529,1453,1304,1216,1135
1-[(2S)-2-[3-[2-(1-金刚烷基)乙基]-3-(2-巯基乙基)脲基]丙酰]-4-甲基哌嗪L-酒石酸氢盐(化合物35-26)
熔点84~130℃
[α]D 20+20.4°(c=1.0,甲醇)
IR(KBr,cm-1)3325,2902,2846,2547,1728,1631,1519,1451,1299,1248,1216,1130,1079
1,1’-[(2S,2’S)-2,2’-[3,3’-双(2-环戊基乙基)-3,3’-[2,2’-(二硫基)二乙基]二脲基]二丙酰]-4,4’-二甲基二哌嗪双(L-酒石酸)氢盐(化合物35-27)
熔点55~70℃
[α]D 20+11.2°(c=0.55,甲醇)
IR(KBr,cm-1)3416,2949,1738,1633,1532,1455,1247,1130
1,1’-[(2S,2’S)-2,2’-[3,3’-双[2-(1-金刚烷基)乙基]-3,3’-[2,2’-(二硫基)二乙基]二脲基]二丙酰]-4,4’-二甲基二哌嗪双(L-酒石酸)氢盐(化合物35-28)
熔点73~90℃
[α]D 20+11.4°(c=0.54,甲醇)
IR(KBr,cm-1)3406,2902,2846,1738,1632,1524,1451,1246,1134,1078,978
1-[(2S)-2-[3-[2-(1-金刚烷基)乙基]-3-[2-(甲硫基)乙基]脲基]丙酰]-4-甲基哌嗪L-酒石酸氢盐(化合物35-29)
熔点95~105℃
[α]D 20+18.7°(c=1.0,甲醇)
IR(KBr,cm-1)3306,2903,2846,1736,1624,1522,1452,1247,1129,1083
1-[(2S)-2-[3-(2-环己基乙基)-3-[2-[2-(甲氧羰基)乙基]硫基乙基]脲基]丙酰]-4-甲基哌嗪L-酒石酸氢盐(化合物35-30)
[α]D 20+16.3°(c=0.51,甲醇)
IR(KBr,cm-1)3418,2923,2851,1738,1632,1526,1450,1361,1247,1130,1078,977
1-[(2S)-2-[3-(2-环戊基乙基)-3-[2-[2-(甲氧羰基)乙基]硫基乙基]脲基]丙酰]-4-甲基哌嗪L-酒石酸氢盐(化合物35-31)
熔点47~60℃
[α]D 20+17.6°(c=1.0,甲醇)
IR(KBr,cm-1)3321,2950,1738,1634,1520,1436,1304,1249,1134,1068
1-[(2S)-2-[3-[2-(1-金刚烷基)乙基]-3-[2-[2-(甲氧羰基)乙基]硫基乙基]脲基]丙酰]-4-甲基哌嗪L-酒石酸氢盐(化合物35-32)
熔点73~100℃
[α]D 20+16.5°(c=0.51,甲醇)
IR(KBr,cm-1)3415,2903,2846,1736,1631,1527,1452,1364,1216,1134,1078,1021,977
实施例36
(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-(2-羧乙基)-3-(4-硝基苯基)丙酰胺(化合物36-1)
将(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-N-[2-(叔丁氧羰基)乙基]-3-(4-硝基苯基)丙酰胺(化合物27-83,235mg)溶于4N氯化氢的二_烷(2ml)溶液,溶液搅拌过夜。反应混合物减压浓缩,得到146mg(69%)标题化合物(化合物36-1),为晶体。
(化合物36-1)
熔点113.5~117.5℃
[α]D 20-20.1°(c=0.51,甲醇)
IR(KBr,cm-1)3346,2929,1699,1664,1603,1510,1345,1201,950,891,839,750,726,698
按照类似于实施例36的方法得到下列化合物。
(2S)-2-[3-[(2RS)-2-羧基-3-(苯硫基)丙基]-3-异戊基脲基]-N-甲基-3-苯基丙酰胺(化合物36-2)
[α]D 20-11.7°(c=0.35,氯仿)
IR(KBr,cm-1)3305,2957,1707,1621,1534,1228,1165
(2S)-2-[3-[(2RS)-2-羧基-3-(苯硫基)丙基]-3-异丁基脲基]-N-甲基-3-苯基丙酰胺(化合物36-3)
[α]D 20-15.0°(c=0.34,氯仿)
IR(KBr,cm-1)3306,2958,1707,1624,1531,1265,1165
实施例37
1-[(2S)-2-[3-[2-[2-(甲氧羰基)乙基]硫基乙基]-3-苯乙基脲基]-3-苯基丙酰]-4-甲基哌嗪(化合物37-1)
在氮气下,将1-[(2S)-2-[3-[2-(乙酰硫基)乙基]-3-苯乙基脲基]-丙酰]-4-甲基哌嗪(化合物27-24,353mg)和丙烯酸甲酯(0.26ml)溶于四氢呋喃(3ml),溶液用冰冷却。向该溶液中滴加浓氨水(1ml),混合物在冰冷却下搅拌30分钟,进一步在室温下搅拌3.5小时。反应混合物减压浓缩,向浓缩物中加入水,全部混合物用乙醚萃取。有机层先后用水和饱和盐水洗涤,经无水硫酸镁干燥,减压浓缩。所得油状物用硅胶柱色谱法纯化,得到368mg(96%)标题化合物(化合物37-1)。
(化合物37-1)
[α]D 20+9.2°(c=0.98,甲醇)
IR(薄膜,cm-1)3347,2937,1737,1630,1497,1448,1360,1291,1214,1144,1001,750,701
按照类似于实施例37的方法得到下列化合物。
1-[(2S)-2-[3-(2-环己基乙基)-3-[2-[2-(甲氧羰基)乙基]硫基乙基]脲基]丙酰]-4-甲基哌嗪(化合物37-2)
1-[(2S)-2-[3-(2-环戊基乙基)-3-[2-[2-(甲氧羰基)乙基]硫基乙基]脲基]丙酰]-4-甲基哌嗪(化合物37-3)
1-[(2S)-2-[3-[2-(1-金刚烷基)乙基]-3-[2-[2-(甲氧羰基)乙基]硫基乙基]脲基]丙酰]-4-甲基哌嗪(化合物37-4)
实施例38
(2S)-3-(4-联苯基)-N-丁基-2-[3-[(1RS)-1-(乙氧羰基甲基)-2-(苯硫基)乙基]-3-异戊基脲基]丙酰胺(化合物38-1)
向(2S)-3-(4-联苯基)-2-[3-[(1RS)-1-(乙氧羰基甲基)-2-(苯硫基)乙基]-3-异戊基脲基]丙酸苯基酯(化合物1-80,464mg)的四氢呋喃(7ml)溶液中加入正丁胺(0.35ml),混合物在室温下搅拌1.5小时。反应混合物减压浓缩,向浓缩物中加入水,全部混合物用乙酸乙酯萃取。有机层先后用水和饱和盐水洗涤,经无水硫酸钠干燥,减压浓缩。所得油状物用硅胶柱色谱法纯化,得到402mg(90%)标题化合物(化合物38-1)。
(化合物38-1)
IR(薄膜,cm-1)3306,2957,1733,1664,1622,1520,1369,1299,1207,1027
实施例39
(2S)-3-(4-联苯基)-N-丁基-2-[3-[(1RS)-1-(羧甲基)-2-(苯硫基)乙基]-3-异戊基脲基]丙酰胺(化合物39-1)
将(2S)-3-(4-联苯基)-N-丁基-2-[3-[(1RS)-1-(乙氧羰基甲基)-2-(苯硫基)乙基]-3-异戊基脲基]丙酰胺(化合物38-1,402mg)溶于乙醇(2ml),向其中加入1N氢氧化锂水溶液(0.96ml),混合物在室温下搅拌45分钟。向反应混合物中加入10%柠檬酸水溶液,全部混合物用乙醚萃取。有机层先后用水和饱和盐水洗涤,经无水硫酸镁干燥,减压浓缩。所得油状物用硅胶柱色谱法纯化,得到386mg(定量)标题化合物(化合物39-1),为非晶性粉末。
(化合物39-1)
IR(KBr,cm-1)3306,2957,2871,1705,1623,1520,1439,1366,1295,1225
实施例40
(2S)-2-[3-[(2RS)-2-(羟基氨基甲酰基)-3-(苯硫基)丙基]-3-异戊基脲基]-N-甲基-3-苯基丙酰胺(化合物40-1)
在氮气下,将(2S)-2-[3-[(2RS)-2-羧基-3-(苯硫基)丙基]-3-异戊基脲基]-N-甲基-3-苯基丙酰胺(化合物36-2,100mg)、1-羟基苯并三唑(68mg)和盐酸1-乙基-3-(3-二甲氨基丙基)碳二亚胺(96mg)溶于无水二氯甲烷(4ml)。然后在冰冷却下,向该溶液中加入N-甲基吗啉(0.05ml),混合物搅拌30分钟。下一步向该混合物中加入含有羟基氯化铵(52mg)和N-甲基吗啉(0.08ml)的二甲基甲酰胺(1ml)溶液,混合物在冰冷却下搅拌10分钟,然后在室温下搅拌过夜。向反应混合物中加入5%柠檬酸水溶液,全部混合物用乙酸乙酯萃取。有机层先后用5%碳酸氢钠水溶液和饱和盐水洗涤,经无水硫酸镁干燥,减压浓缩。所得油状物用硅胶柱色谱法纯化,得到57mg(54%)标题化合物(化合物40-1),为非晶性粉末。
(化合物40-1)
[α]D 20+5.0°(c=0.34,氯仿)
IR(KBr,cm-1)3291,2955,1625,1529,1234,1165
按照类似于实施例40的方法得到下列化合物。
(2S)-2-[3-[(2RS)-2-(羟基氨基甲酰基)-3-(苯硫基)丙基]-3-异丁基脲基]-N-甲基-3-苯基丙酰胺(化合物40-2)
IR(KBr,cm-1)3285,2978,1629,1530,1253,1164
(2S)-3-(4-联苯基)-N-丁基-2-[3-[(1RS)-1-[(羟基氨基甲酰基)甲基]-2-(苯硫基)乙基]-3-异戊基脲基]丙酰胺(化合物40-3)
IR(薄膜,cm-1)3272,2957,2870,1625,1518,1220,1157,1075
实施例41
1-[(2S)-2-[3-[2-(乙酰硫基)乙基]脲基]丙酰]-4-甲基哌嗪(化合物41-1)
将1,1’-二甲基-4,4’-[(2S,2’S)-2,2’-[3,3’-[2,2’-(二硫基)二乙基]二脲基]二丙酰]二哌嗪(化合物28-14,487mg)溶于丙酮(10ml)-水(2.5ml),向该溶液中加入三正丁基膦(0.27ml),混合物在室温下搅拌40分钟。向该混合物中先后加入三乙胺(0.31ml)和乙酸酐(0.21ml),混合物在室温下搅拌20分钟。反应混合物减压浓缩,向残余物中加入氯仿。有机层先后用10%碳酸氢钠水溶液和饱和盐水洗涤,经无水硫酸钠干燥,减压浓缩。所得油状物用硅胶柱色谱法纯化,得到448mg(79%)标题化合物(化合物41-1)。
(化合物41-1)
[α]D 20+3.6°(c=0.97,甲醇)
IR(薄膜,cm-1)3358,2976,2938,2794,1692,1632,1556,1446,1355,1293,1248,1172,1141,1034,1002
制剂
利用本发明化合物的口服制剂和注射剂的一般制剂实施例表示如下。
1)片剂
制剂1,以100mg计
本发明化合物 1mg
乳糖 66.4mg
玉米淀粉 20mg
羧甲基纤维素钙 6mg
羟丙基纤维素 4mg
硬脂酸镁 0.6mg
将按照上述配方的片剂用2mg/片的包衣剂(这是一种常规的包衣剂,例如羟丙基甲基纤维素、聚乙二醇或硅氧烷树脂)包衣,得到所需包衣片。(相同操作也适用于下述片剂。)
制剂2,以100mg计
本发明化合物 5mg
乳糖 62.4mg
玉米淀粉 20mg
羧甲基纤维素钙 6mg
羟丙基纤维素 4mg
硬脂酸镁 0.6mg
包衣剂 2mg
制剂3,以100mg计
本发明化合物 20mg
乳糖 51mg
玉米淀粉 15mg
羧甲基纤维素钙 5mg
羟丙基纤维素 5mg
硬脂酸镁 1mg
滑石 1mg
包衣剂 2mg
制剂4,以100mg计
本发明化合物 40mg
乳糖 34mg
玉米淀粉 10mg
羧甲基纤维素钙 5mg
羟丙基纤维素 5mg
硬脂酸镁 2mg
滑石 2mg
包衣剂 2mg
制剂5,以220mg计
本发明化合物 100mg
乳糖 67mg
玉米淀粉 20mg
羧甲基纤维素钙 10mg
羟丙基纤维素 10mg
硬脂酸镁 4mg
滑石 4mg
包衣剂 5mg
2)胶襄剂
制剂1,以150mg计
本发明化合物 5mg
乳糖 145mg
改变本发明化合物与乳糖的混合比例,也制备了本发明化合物含量为10mg/粒、30mg/粒、50mg/粒和100mg/粒的胶囊剂。
3)颗粒剂
制剂1,以100mg计
本发明化合物 30mg
甘露糖醇 46.5mg
聚乙烯吡咯烷酮K-30 7mg
Eudragit RL 15mg
甘油三乙酸酯 1.5mg
制剂2,以130mg计
本发明化合物 50mg
乳糖 55mg
白马铃薯淀粉 20mg
羟丙基纤维素 4mg
滑石 痕量
4)注射剂
制剂1,以10ml计
本发明化合物 10-100mg
氯化钠 90mg
氢氧化钠 适量
无菌纯净水 适量
药理学试验
按照McGeehan等人的方法(《自然》370,558-561(1994)),通过体外或体内试验研究了对由脂多糖(LPS)刺激作用诱发的TNF-α产生的抑制作用。
1)体外试验
通过测量LPS刺激TNF-α从人单核细胞系THP-1的产生,进行分析。
培养基使用RPMI1640培养基,其中含有胎牛血清(10%)、L-谷氨酰胺(2mM)、2-巯基乙醇(50μM)、青霉素(50单位/ml)和链霉素(50μg/ml)。
关于细胞,将在上述培养基中培养过的人单核细胞系THP-1细胞在100xg下离心五分钟,除去上清液,然后再次悬浮在培养基中。关于LPS,将来自S.Typhimurium的LPS溶于纯净水,然后用培养基稀释。将供试化合物溶于二甲基亚砜(DMSO),然后用培养基稀释。
将如上准备好的细胞(106/ml)、LPS(2μg/ml)和供试化合物(10-5M)混合,该混合物在37℃下培养两小时,然后在1000xg下离心五分钟。用人TNF-α特异性ELISA试剂盒测量培养后的上清液中的TNF-α水平。在没有LPS存在的培养后的上清液(对照)中,没有观察到TNF-α的产生。
按照下列等式测定供试化合物对TNF-α产生的抑制率。
抑制率(%)=[(A-B)/A]×100
A:在没有供试化合物存在的培养基上清液中的TNF-α水平
B:在有供试化合物存在的培养基上清液中的TNF-α水平
(结果)
表1表示在10-5M浓度下的TNF-α抑制率(%),作为试验结果的实例。
表1
| 供试化合物 | 抑制率(%) |
| 化合物27-10 | 100 |
| 化合物27-17 | 93.5 |
| 化合物27-19 | 93.5 |
| 化合物27-41 | 93.8 |
| 化合物27-42 | 100 |
| 化合物27-46 | 100 |
| 化合物27-47 | 100 |
| 化合物27-56 | 96.9 |
| 化合物27-58 | 100 |
| 化合物27-59 | 100 |
如表1所示,本发明化合物在低浓度下对TNF-α产生具有抑制作用。
2)体内试验
使用体重约200g、约八周龄的雌性大鼠(每组五只)作为试验动物。关于所用的LPS,将来自沙门氏菌属的LPS溶于生理盐水(1mg/ml)。将供试化合物溶解或均匀地悬浮在1%甲基纤维素水溶液中。
将上述LPS溶液(0.5ml/kg)皮下对大鼠给药。LPS给药后,立即将供试化合物预备液(5ml/kg,含50mg/kg供试化合物)口服给药。LPS给药后两小时,从腹主动脉采血,在4℃和3000rpm下离心十分钟。用大鼠TNF-α特异性ELISA试剂盒测量所得血浆中的TNF-α水平。非LPS给药组(对照)血浆中没有观察到TNF-α。
按照下列等式测定供试化合物对TNF-α产生的抑制率。
抑制率(%)=[(A-B)/A]×100
A:在非供试化合物给药组血浆中的TNF-α水平
B:在供试化合物给药组血浆中的TNF-α水平
(结果)
表2表示口服给药50mg/kg后的TNF-α产生抑制率(%)。
表2
| 供试化合物 | 抑制率(%) |
| 化合物13-1 | 84.6 |
| 化合物13-3 | 66.8 |
| 化合物13-12 | 62.3 |
| 化合物13-16 | 54.1 |
| 化合物13-17 | 50.3 |
| 化合物13-20 | 66.6 |
| 化合物13-49 | 90.0 |
| 化合物13-50 | 93.5 |
| 化合物13-57 | 90.1 |
| 化合物27-4 | 60.9 |
| 化合物27-84 | 56.7 |
从上述结果明显看出,本发明化合物对TNF-α产生表现出优异的抑制作用,作为用于有TNF-α参与的疾病的治疗剂具有不同的医学用途,例如自体免疫疾病,如类风湿性关节炎、克罗恩氏病和全身性红斑狼疮,恶病质、急性传染病、变态反应、发热、贫血、糖尿病等。
工业实用性
本发明提供了新颖的脲衍生物,它们对TNF-α的产生具有抑制作用,可用作不同疾病的治疗剂,特别是用作自体免疫疾病、例如类风湿性关节炎的治疗剂,本发明还提供了可用作其合成中间体的新化合物。
Claims (9)
1、由下列通式[I]代表的化合物或其盐
其中
R1选自氢、C1-C8烷基、苯基、RA-CO-、RC-S-和下式[II]基团,该C1-C8烷基可以被苯基或(C1-C8烷氧基)羰基取代,
RA选自C1-C8烷基、C1-C8烷氧基、苯基、吡啶基、苯基-C1-C8烷氧基和RF-N(RG)-,RC是苯基,RF是C1-C8烷基,RG是氢;
R2选自氢、C1-C8烷基、C2-C8烯基和苯基,该C1-C8烷基可以被选自C1-C8烷氧基、环烷基、环烯基、金刚烷基、苯基、萘基、吡啶基和RB-O-的基团取代,该苯基可以被选自C1-C8烷基、羟基、C1-C8烷氧基、卤素、硝基和苯基的基团取代,该C2-C8烯基可以被苯基取代,RB是苯基;
R3选自氢和C1-C8烷基,该C1-C8烷基可以被苯基取代;
R4选自氢、C1-C8烷基和苯基,该C1-C8烷基可以被选自羟基、环烷基、苯基、萘基、吡啶基、噻吩基、咪唑基、甲苯磺酰胍基、RC-S-、RD-COS-、RF-N(RG)-和RK-CONH-的基团取代,每个苯基可以被选自羟基、C1-C8烷氧基、卤素、硝基、苯磺酰基和苯基的基团取代,RC选自氢、C1-C8烷基和苯基,RD选自C1-C8烷基和苯基,RF和RG是氢,RK是C1-C8烷氧基,当R4是C1-C8烷基时,该C1-C8烷基的末端碳可以与该烷基所键合的碳结合形成一个环烷基环;
R5选自氢和C1-C8烷基;
R6选自C1-C8烷基和吡啶基,该C1-C8烷基可以被选自吡啶基、咪唑基、邻苯二甲酰亚氨基、哌啶基、哌嗪基、吗啉基、RE-OCO-、RF-N(RG)-、RH-N(RJ)CO-和RK-CONH-的基团取代,RE选自氢和C1-C8烷基,RF和RG相同或不同,选自氢、C1-C8烷基、环烷基和苯基,RH和RJ相同或不同,选自氢和C1-C8烷基,RK是C1-C8烷氧基,该哌嗪基可以被C1-C8烷基取代;或者
R5和R6可以与它们相连的氮一起形成一个非芳族杂环,选自吗啉环、哌啶环、哌嗪环、吡咯啉环和高哌嗪环,该哌嗪环或高哌嗪环可以被C1-C8烷基、环烷基、苯基或RA-CO-取代,该C1-C8烷基可以被羟基、苯基或RE-OCO-取代,RA是C1-C8烷基、C1-C8烷氧基或卤代C1-C8烷基,RE是氢或C1-C8烷基;
R7选自氢、C1-C8烷基、羟基、巯基、苯基、RB-O-、RC-S-、RD-COS-、RE-OCO-、-CONHOH和RF-N(RG)-,该C1-C8烷基可以被选自羟基、巯基、苯基、RB-O-、RC-S-、RD-COS-、RE-OCO-、-CONHOH和RF-N(RG)-的基团取代,RB是苯基,RC是苯基,RD是C1-C8烷基或苯基,RE是氢或C1-C8烷基,RF和RG是C1-C8烷基;或者
R7可以与R1、A1以及毗邻A1的硫一起形成一个非芳族杂环,选自2-氧代四氢噻吩和二硫戊环;
A1是C1-C8亚烷基;和
A2是C1-C8亚烷基。
2、如权利要求1所要求保护的化合物或其盐,其中通式[I]中的基团是由选自下列1)至10)的任意一个或由1)至10)组成的任意组合所定义的,
1)R1选自氢、RA-CO-和下式[II]基团
RA选自C1-C8烷基、苯基和吡啶基;
2)R2是C1-C8烷基或苯基,该C1-C8烷基可以被选自环烷基、环烯基、金刚烷基、苯基和苯氧基的基团取代,该苯基可以被卤素取代;
3)R3是氢;
4)R4是氢或C1-C8烷基,该C1-C8烷基可以被选自苯基、萘基、C1-C8烷硫基和RD-COS-的基团取代,RD是C1-C8烷基,该苯基可以被选自羟基、C1-C8烷氧基、卤素、硝基和苯基的基团取代;
5)R5是氢;
6)R6是C1-C8烷基,该C1-C8烷基可以被选自吡啶基、哌啶基、哌嗪基和RF-N(RG)-的基团取代,RF和RG相同或不同,选自氢、C1-C8烷基和环烷基,该哌嗪基可以被C1-C8烷基取代;
7)R5和R6与它们相连的氮一起形成一个非芳族杂环,选自哌啶环、吗啉环和哌嗪环,该哌嗪环可以被C1-C8烷基取代;
8)R7是氢;
9)A1是C1-C8亚烷基;和
10)A2是C1-C8亚烷基。
3、如权利要求1所要求保护的化合物或其盐,其中通式[I]中的基团是由选自下列1)至10)的任意一个或由1)至10)组成的任意组合所定义的,
1)R1选自乙酰基、苯甲酰基和下式[II]基团
2)R2选自2-环己基乙基、2-环戊基乙基、2-(1-金刚烷基)乙基、2-(环己烯-1-基)乙基、苯乙基和3-(4-氟苯基)丙基;
3)R3是氢;
4)R4选自甲基、乙酰硫基甲基、苄基、2-萘甲基、4-氟苄基、4-氯苄基、4-联苯甲基、4-硝基苄基、3-硝基-4-联苯甲基、4-甲氧基苄基和4-异丙氧基苄基;
5)R5是氢;
6)R6选自2-(二甲氨基)乙基、2-(二乙氨基)乙基、2-(二异丙氨基)乙基、N-甲基-2-(环己氨基)乙基、2-(2-吡啶基)乙基、2-(1-哌啶基)乙基和2-(4-甲基哌嗪基)乙基;
7)R5和R6与它们相连的氮一起形成一个选自1-哌啶基、4-吗啉基和4-甲基-1-哌嗪基的基团;
8)R7是氢;
9)A1是亚乙基;和
10)A2是亚甲基。
4、如权利要求1所要求保护的化合物或其盐,其中R5和R6与它们相连的氮一起形成一个非芳族杂环,选自吗啉环、哌啶环、哌嗪环、吡咯啉环和高哌嗪环,该哌嗪环或高哌嗪环可以被C1-C8烷基、环烷基、苯基或RA-CO-取代,该C1-C8烷基可以被羟基、苯基或RE-OCO-取代,RA是C1-C8烷基、C1-C8烷氧基或卤代C1-C8烷基,RE是氢或C1-C8烷基。
5、如权利要求1所要求保护的化合物或其盐,其中R6选自C1-C8烷基和吡啶基,该C1-C8烷基可以被选自吡啶基、咪唑基、邻苯二甲酰亚氨基、哌啶基、哌嗪基、吗啉基、RE-OCO-、RF-N(RG)-、RH-N(RJ)CO-和RK-CONH-的基团取代,RE选自氢和C1-C8烷基,RF和RG相同或不同,选自氢、C1-C8烷基、环烷基和苯基,RH和RJ相同或不同,选自氢和C1-C8烷基,RK是C1-C8烷氧基,该哌嗪基可以被C1-C8烷基取代。
6、药物组合物,含有如权利要求1所要求保护的化合物或其盐作为活性成分。
7、TNF-α产生抑制剂,含有如权利要求1所要求保护的化合物或其盐作为活性成分。
8、自体免疫疾病治疗剂,含有如权利要求1所要求保护的化合物或其盐作为活性成分。
9、由下列通式[III]代表的化合物或其盐
R2选自氢、C1-C8烷基、C2-C8烯基和苯基,该C1-C8烷基可以被选自C1-C8烷氧基、环烷基、环烯基、金刚烷基、苯基、萘基、吡啶基和RB-O-的基团取代,该苯基可以被选自C1-C8烷基、羟基、C1-C8烷氧基、卤素、硝基和苯基的基团取代,该C2-C8烯基可以被苯基取代,RB是苯基;
R3选自氢和C1-C8烷基,该C1-C8烷基可以被苯基取代;
R4选自氢、C1-C8烷基和苯基,该C1-C8烷基可以被选自羟基、环烷基、苯基、萘基、吡啶基、噻吩基、咪唑基、甲苯磺酰胍基、RC-S-、RD-COS-、RF-N(RG)-和RK-CONH-的基团取代,每个苯基可以被选自羟基、C1-C8烷氧基、卤素、硝基、苯磺酰基和苯基的基团取代,RC选自氢、C1-C8烷基和苯基,RD选自C1-C8烷基和苯基,RF和RG是氢,RK是C1-C8烷氧基,当R4是C1-C8烷基时,该C1-C8烷基的末端碳可以与该烷基所键合的碳结合形成一个环烷基环;
R5选自氢和C1-C8烷基;
R6选自C1-C8烷基和吡啶基,该C1-C8烷基可以被选自吡啶基、咪唑基、邻苯二甲酰亚氨基、哌啶基、哌嗪基、吗啉基、RE-OCO-、RF-N(RG)-、RH-N(RJ)CO-和RK-CONH-的基团取代,RE选自氢和C1-C8烷基,RF和RG相同或不同,选自氢、C1-C8烷基、环烷基和苯基,RH和RJ相同或不同,选自氢和C1-C8烷基,RK是C1-C8烷氧基,该哌嗪基可以被C1-C8烷基取代;或者
R5和R6可以与它们相连的氮一起形成一个非芳族杂环,选自吗啉环、哌啶环、哌嗪环、吡咯啉环和高哌嗪环,该哌嗪环或高哌嗪环可以被C1-C8烷基、环烷基、苯基或RA-CO-取代,该C1-C8烷基可以被羟基、苯基或RE-OCO-取代,RA是C1-C8烷基、C1-C8烷氧基或卤代C1-C8烷基,RE是氢或C1-C8烷基;
R7选自氢、C1-C8烷基、羟基、巯基、苯基、RB-O-、RC-S-、RD-COS-、RE-OCO-、-CONHOH和RF-N(RG)-,该C1-C8烷基可以被选自羟基、巯基、苯基、RB-O-、RC-S-、RD-COS-、RE-OCO-、-CONHOH和RF-N(RG)-的基团取代,RB是苯基,RC是苯基,RD是C1-C8烷基或苯基,RE是氢或C1-C8烷基,RF和RG是C1-C8烷基;
A1是C1-C8亚烷基;和
A2是C1-C8亚烷基。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP7915498 | 1998-03-26 | ||
| JP79154/98 | 1998-03-26 | ||
| JP79154/1998 | 1998-03-26 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN1299344A CN1299344A (zh) | 2001-06-13 |
| CN1305846C true CN1305846C (zh) | 2007-03-21 |
Family
ID=13682055
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CNB998056928A Expired - Fee Related CN1305846C (zh) | 1998-03-26 | 1999-03-25 | 脲衍生物 |
Country Status (6)
| Country | Link |
|---|---|
| US (2) | US6492370B1 (zh) |
| EP (1) | EP1072591A4 (zh) |
| KR (1) | KR100589474B1 (zh) |
| CN (1) | CN1305846C (zh) |
| CA (1) | CA2325741C (zh) |
| WO (1) | WO1999050238A1 (zh) |
Families Citing this family (41)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AU6001299A (en) * | 1998-10-02 | 2000-04-26 | Sankyo Company Limited | Dithiol derivatives |
| AU3673300A (en) * | 1999-04-07 | 2000-11-14 | Santen Pharmaceutical Co. Ltd. | N-substituted-n'-substituted urea derivative and use thereof as tnf-alpha production inhibitor |
| CN1188394C (zh) | 1999-04-07 | 2005-02-09 | 参天制药株式会社 | N-取代-n′-取代脲衍生物及含有它的药物组合物 |
| EP1216988A4 (en) * | 1999-09-28 | 2005-04-20 | Nihon Nohyaku Co Ltd | THIOALKYLAMINE DERIVATIVES AND METHOD FOR THE PRODUCTION THEREOF |
| AU6067401A (en) * | 2000-05-31 | 2001-12-11 | Santen Pharmaceutical Co Ltd | Tnf-alpha production inhibitors |
| EP1296949A2 (en) | 2000-06-21 | 2003-04-02 | Bristol-Myers Squibb Pharma Company | Piperidine amides as modulators of chemokine receptor activity |
| DE10101324C1 (de) * | 2001-01-13 | 2001-12-13 | Ibfb Gmbh Privates Inst Fuer B | 1-Dimercaptoalkylchinazolin-2,4-(1H,3H)-dione als Matrix-Metalloproteinase(MMP)-Inhibitoren |
| WO2002056886A1 (fr) * | 2001-01-19 | 2002-07-25 | Santen Pharmaceutical Co., Ltd. | Inhibiteurs de l'angiogenese contenant un derive d'uree comme ingredient actif |
| FR2820136A1 (fr) * | 2001-01-26 | 2002-08-02 | Aventis Pharma Sa | Nouveaux derives de l'uree, leur procede de preparation, leur application a titre de medicaments, compositions pharmaceutiques et nouvelle utilisation |
| ES2907826T3 (es) | 2001-06-26 | 2022-04-26 | Amgen Inc | Anticuerpos para OPGL |
| WO2003024401A2 (en) * | 2001-09-18 | 2003-03-27 | Bristol-Myers Squibb Company | Piperizinones as modulators of chemokine receptor activity |
| JP2005538066A (ja) | 2002-07-09 | 2005-12-15 | ベーリンガー インゲルハイム ファルマ ゲゼルシャフト ミット ベシュレンクテル ハフツング ウント コンパニー コマンディトゲゼルシャフト | 新規な抗コリン作用薬及びp38キナーゼ阻害剤を用いた新規な医薬組成物 |
| WO2004024283A2 (en) * | 2002-09-13 | 2004-03-25 | Valentis, Inc. | Apparatus and method for preparative scale purification of nucleic acids |
| MXPA05007019A (es) | 2002-12-30 | 2005-08-18 | Amgen Inc | Terapia de combinacion con factores co-estimuladores. |
| US7517887B2 (en) * | 2003-04-09 | 2009-04-14 | General Atomics | Reversible inhibitors of S-adenosyl-L-homocysteine hydrolase and uses thereof |
| US7196093B2 (en) * | 2003-04-09 | 2007-03-27 | General Atomics | Reversible inhibitors of SAH hydrolase and uses thereof |
| US7868011B2 (en) * | 2003-04-09 | 2011-01-11 | General Atomics | Use of reversible inhibitors of S-adenosyl-L-homocysteine hydrolase for treating lupus |
| DK2332921T3 (en) * | 2003-06-17 | 2016-05-09 | Arena Pharm Inc | 8-Chloro-1-methyl-2,3,4,5-tetrahydro-1H-3benzazepine hydrochloride |
| JP2007513928A (ja) * | 2003-12-12 | 2007-05-31 | オサケユイチア ユバンティア ファーマ リミティド | ソマトスタチン受容体サブタイプ1(sstr1)活性化合物及び治療におけるその使用 |
| US20060035893A1 (en) | 2004-08-07 | 2006-02-16 | Boehringer Ingelheim International Gmbh | Pharmaceutical compositions for treatment of respiratory and gastrointestinal disorders |
| PE20060777A1 (es) | 2004-12-24 | 2006-10-06 | Boehringer Ingelheim Int | Derivados de indolinona para el tratamiento o la prevencion de enfermedades fibroticas |
| KR100724406B1 (ko) * | 2005-01-08 | 2007-06-04 | 엘지전자 주식회사 | 이동 통신 단말기의 ptt 서비스 제공 방법 및 이를 위한 이동 통신 단말기 및 이동 통신 시스템 |
| JP5199997B2 (ja) | 2006-04-03 | 2013-05-15 | アリーナ ファーマシューティカルズ, インコーポレイテッド | 8−クロロ−1−メチル−2,3,4,5−テトラヒドロ−1h−3−ベンズアゼピンおよびこれに関連する中間体を調製するためのプロセス |
| EP1992344A1 (en) | 2007-05-18 | 2008-11-19 | Institut Curie | P38 alpha as a therapeutic target in pathologies linked to FGFR3 mutation |
| PL212489B1 (pl) | 2008-01-22 | 2012-10-31 | Univ Jagiellonski | Pochodne fenoksyalkiloaminoalkanoli i ich zastosowania |
| WO2009111004A1 (en) | 2008-03-04 | 2009-09-11 | Arena Pharmaceuticals, Inc. | Processes for the preparation of intermediates related to the 5-ht2c agonist (r)-8-chloro-1-methyl-2,3,4,5-tetrahydro-1h-3-benzazepine |
| FR2937973B1 (fr) * | 2008-11-04 | 2010-11-05 | Galderma Res & Dev | Modulateurs des recepteurs de la melanocortine, leur procede de preparation et leur utilisation en medecine humaine ainsi qu'en cosmetique |
| FR2937868B1 (fr) * | 2008-11-04 | 2010-11-05 | Galderma Res & Dev | Composes antagonistes des recepteurs de la melanocortine, leur procede de preparation et leur utilisation en medecine humaine ainsi qu'en cosmetique |
| US8765817B1 (en) | 2008-12-03 | 2014-07-01 | Arrowhead Center, Inc. | Selective inhibitors of EG5 motors and methods of use |
| US8349899B1 (en) | 2008-12-03 | 2013-01-08 | Arrowhead Center, Inc. | Selective inhibitors of EG5 motors and methods of use |
| HRP20090186A2 (hr) | 2009-03-31 | 2010-10-31 | Institut Ruđer Bošković | Adamantanski bisureidni derivati, metoda priprave i primjena u detekciji aniona |
| US8952197B2 (en) | 2009-06-18 | 2015-02-10 | Arena Pharmaceuticals, Inc. | Processes for the preparation of 5-HT2C receptor agonists |
| US20110004011A1 (en) | 2009-07-01 | 2011-01-06 | Declan Costello | Novel process |
| WO2011153206A1 (en) | 2010-06-02 | 2011-12-08 | Arena Pharmaceuticals, Inc. | Processes for the preparation of 5-ht2c receptor agonists |
| CN103189360A (zh) | 2010-09-01 | 2013-07-03 | 艾尼纳制药公司 | 5-ht2c激动剂的非吸湿性盐 |
| SG10201506874UA (en) | 2010-09-01 | 2015-10-29 | Arena Pharm Inc | Modified-release dosage forms of 5-ht2c agonists useful for weight management |
| AU2011296015B2 (en) | 2010-09-01 | 2015-11-12 | Arena Pharmaceuticals, Inc. | Administration of lorcaserin to individuals with renal impairment |
| CN103189359A (zh) | 2010-09-01 | 2013-07-03 | 艾尼纳制药公司 | 5-ht2c激动剂的光学活性酸盐 |
| AU2011328904A1 (en) | 2010-11-16 | 2013-06-06 | Texas Heart Institute | Agonists that enhance binding of integrin-expressing cells to integrin receptors |
| CA2886875A1 (en) | 2012-10-09 | 2014-04-17 | Arena Pharmaceuticals, Inc. | Method of weight management |
| CN110294696B (zh) * | 2018-03-24 | 2021-07-02 | 复旦大学 | 巯乙基脲/硫脲类二聚体衍生物及其制备方法和药用用途 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1100413A (zh) * | 1993-05-12 | 1995-03-22 | 美国氰胺公司 | 诱导产生细胞素的尿烷类和尿素化合物 |
| WO1995019957A1 (en) * | 1994-01-21 | 1995-07-27 | British Biotech Pharmaceuticals Limited | Hydroxamic acid derivatives as metalloproteinase inhibitors |
| JPH09118658A (ja) * | 1995-08-22 | 1997-05-06 | Japan Tobacco Inc | アミド化合物及びその用途 |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2921091A (en) * | 1958-12-29 | 1960-01-12 | U S Vitamin And Pharmaceutical | N1-carbamidomethyl-n2-(beta-hydroxyethyl) urea |
| EP0396065A1 (en) * | 1989-05-02 | 1990-11-07 | Japan Tobacco Inc. | Novel amino acid derivatives possessing renin-inhibitory activities |
| US5430022A (en) * | 1990-05-14 | 1995-07-04 | Fujisawa Pharmaceutical Co., Ltd. | Peptide compound and its preparation |
| US5173506A (en) * | 1990-08-16 | 1992-12-22 | Schering Corporation | N-(mercaptoalkyl)ureas and carbamates |
| JPH06502859A (ja) * | 1990-11-19 | 1994-03-31 | モンサント カンパニー | レトロウイルスプロテアーゼ阻害剤 |
-
1999
- 1999-03-25 CN CNB998056928A patent/CN1305846C/zh not_active Expired - Fee Related
- 1999-03-25 EP EP99910724A patent/EP1072591A4/en not_active Withdrawn
- 1999-03-25 US US09/623,779 patent/US6492370B1/en not_active Expired - Fee Related
- 1999-03-25 CA CA002325741A patent/CA2325741C/en not_active Expired - Fee Related
- 1999-03-25 WO PCT/JP1999/001554 patent/WO1999050238A1/ja not_active Application Discontinuation
- 1999-03-25 KR KR1020007010678A patent/KR100589474B1/ko not_active IP Right Cessation
-
2002
- 2002-05-15 US US10/147,131 patent/US6730784B2/en not_active Expired - Fee Related
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1100413A (zh) * | 1993-05-12 | 1995-03-22 | 美国氰胺公司 | 诱导产生细胞素的尿烷类和尿素化合物 |
| WO1995019957A1 (en) * | 1994-01-21 | 1995-07-27 | British Biotech Pharmaceuticals Limited | Hydroxamic acid derivatives as metalloproteinase inhibitors |
| JPH09118658A (ja) * | 1995-08-22 | 1997-05-06 | Japan Tobacco Inc | アミド化合物及びその用途 |
Also Published As
| Publication number | Publication date |
|---|---|
| WO1999050238A1 (fr) | 1999-10-07 |
| EP1072591A1 (en) | 2001-01-31 |
| US6730784B2 (en) | 2004-05-04 |
| CN1299344A (zh) | 2001-06-13 |
| KR20010042191A (ko) | 2001-05-25 |
| US20020198376A1 (en) | 2002-12-26 |
| CA2325741C (en) | 2007-05-08 |
| CA2325741A1 (en) | 1999-10-07 |
| EP1072591A4 (en) | 2005-01-05 |
| KR100589474B1 (ko) | 2006-06-14 |
| US6492370B1 (en) | 2002-12-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN1305846C (zh) | 脲衍生物 | |
| CN1087736C (zh) | 新型的脒基萘基衍生物或其盐 | |
| CN1166633C (zh) | 新的α-氨基酸磺酰基化合物、其制备方法和含有它们的药物组合物 | |
| CN1149204C (zh) | 1-杂环取代的二芳基胺 | |
| CN1285572C (zh) | 大麻素受体配位体 | |
| CN1341590A (zh) | 蛋白酶抑制剂 | |
| CN1324012C (zh) | TNF-α生成抑制剂 | |
| CN1553897A (zh) | 多拉司他汀10衍生物 | |
| CN1348442A (zh) | 新的磺胺化合物及其应用 | |
| CN1230884A (zh) | 硫羟砜金属蛋白酶抑制剂 | |
| CN1993333A (zh) | 三唑衍生物 | |
| CN1238688A (zh) | 硫羟磺酰胺金属蛋白酶抑制剂 | |
| CN1910158A (zh) | 含有氮杂环的β淀粉样蛋白生成的杂环磺酰胺抑制剂 | |
| CN1471511A (zh) | 用作半光氨酸蛋白酶可逆抑制剂的螺杂环腈 | |
| CN1268116A (zh) | 3-脒基苯胺衍生物,活化血凝固因子x抑制剂和制备这些物质的中间体 | |
| CN101068783A (zh) | 用于制备半胱氨酸蛋白酶抑制剂的方法和中间体 | |
| CN1842515A (zh) | 组织蛋白酶抑制剂 | |
| CN1520408A (zh) | 哌嗪化合物 | |
| CN1764655A (zh) | 芳族砜异羟肟酸酯及其作为蛋白酶抑制剂的用途 | |
| CN1360577A (zh) | 作为基质金属蛋白酶抑制剂的异羟肟酸衍生物 | |
| CN1116847A (zh) | 用作血小板激活因子拮抗物的N-(3-哌啶基碳酰)-β-氨基丙酸衍生物 | |
| CN1665778A (zh) | 羟基四氢-萘基脲衍生物 | |
| CN1558761A (zh) | 取代的苯并咪唑化合物和它们在治疗癌症中的用途 | |
| CN1458922A (zh) | 尿素衍生物及以其作为有效成分的粘连分子阻断剂 | |
| CN1774245A (zh) | 用于视网膜神经疾病的含有烷基醚衍生物或其盐的预防剂/治疗剂 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C14 | Grant of patent or utility model | ||
| GR01 | Patent grant | ||
| C17 | Cessation of patent right | ||
| CF01 | Termination of patent right due to non-payment of annual fee |
Granted publication date: 20070321 |