질산바나딜
Vanadyl nitrate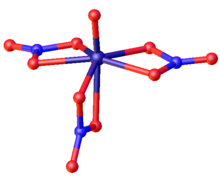 | |
| 이름 | |
|---|---|
| 기타 이름 트리니트라톡소바나듐 | |
| 식별자 | |
3D 모델(JSmol) | |
| 켐스파이더 | |
PubChem CID | |
| |
| |
| 특성. | |
| VO(NO3)3 | |
| 몰 질량 | 252.953 g/g |
| 외모 | 노란 액체 |
| 녹는점 | 2 °C (36 °F, 275 [1]K) |
| 비등점 | 0.7mm Hg에서 86~91°C(187~196°F, 359~364K) |
| 물. | |
| 위험 요소 | |
| 산업안전보건(OHS/OSH): | |
주요 위험 요소 | 산화제 |
| 관련 화합물 | |
관련 화합물 | 질산티타늄, 과염소산바나딜 |
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |
바나듐 옥시트리니트레이트 또는 바나듐 옥시질산염이라고도 불리는 질산 바나듐은 질산염 배위자와 산소를 포함한 +5 산화 상태의 바나듐 무기 화합물이다.공식은 VO(NO)3입니다3.옅은 노란색의 점성이 있는 [2]액체입니다.
생산.
오산화바나듐을 액상 오산화이질소에 이틀 정도 담가 상온에서 제조합니다.이 방법의 수율은 약 85%[3]입니다.
- VO25 + 3 NO25 → 2 VO(NO3)3
정화는 진공 [3]증류를 통해 이루어질 수 있다.
모노니트라톡소바나듐(VONO)23은 이 합성물의 중간체이다.벽돌로 된 [4][5]붉은 고체입니다.
질산바나딜은 삼염화바나딜3 VOCl 및 [6]오산화이질소에서도 제조할 수 있다.
구조.
VO(NO3)3는 이상적인s C(거울) 대칭을 가진 왜곡된 오각쌍체 형상을 가지고 있다.바나듐 산소 결합(157.2pm)은 바나딜(V)의 전형적인 형태입니다.오각형 평면의 2개의 질산염 그룹은 2등분이다(V-O 거리는 199~206pm).세 번째 질산염은 오각형 평면(197 pm)에 걸쳐 옥소로 전환되는 위치(223 pm)[7][8]에 도달합니다.
특성.
질산바나딜은 디클로로메탄, 니트로메탄, 사염화탄소 및 포화 [1]탄화수소에 용해된다. 1-헥센 또는 기타 불포화 탄화수소는 질산바나딜과 [3][9]접촉하면 발화한다.물과 접촉하면 돌이킬 수 없는 가수분해로 질산을 [3]방출한다.물과의 [10]반응으로 질산이 형성된다.
액체의 자외선 스펙트럼은 흡수 대역을 208nm에서, 어깨는 242nm에서 피킹합니다.55°C에서 질산바나딜 가스는 가시광선 [10]스펙트럼에서도 486, 582, 658 nm의 흡수 밴드를 가진다.적외선 영역에서 액체 질산 바나딜은 1880,[10] 1633, 1612, 1560, 1306, 1205, 1016, 996, 965, 895, 783, 632, 457, 357, 301, 283, 193, 133, 59cm에서−1 흡수된다.질산바나딜가스는 775,[2] 783, 786, 962.5, 994.4, 997.5, 1000.5, 1006.2, 1012, 1016.3, 1020, 1198, 1211, 1216.3, 1564, 1629, 1632, 1635, 1648cm의 흡수대역을−1 가진다.이러한 대역의 대부분은 질소-산소 결합으로 늘어나지만, 1016.3cm는−1 이중 바나듐-산소 결합으로 인해 발생한다.786은 N-O에서의 위상차이로 인해, 775는 미러 [2]평면에서의 O-N=O의 변형으로 인해 발생합니다.
반응
방향족 화합물용 질화제입니다.상온에서 반응이 진행됩니다.디클로로메탄은 종종 불활성 [1]용매로 사용됩니다.니트로톨루엔, 벤조산메틸 및 벤조산은 [1]며칠에 걸친 장기노출에 의해 질화된다.벤조니트릴은 [1]반응하지 않는다.[11]
질산바나딜은 [3]삼불화붕소와 함께 고체 옅은 노란색 부가체를 형성한다.아세토니트릴에 [1]의한 부가물도 형성된다.
레퍼런스
- ^ a b c d e f Dove, Michael F. A.; Berthold Manz; John Montgomery; Gerald Pattenden; Simon A. Wood (1998). "Vanadium(V) oxytrinitrate, VO(NO3)3. A powerful reagent for the nitration of aromatic compounds at room temperature under non-acidic conditions". Journal of the Chemical Society, Perkin Transactions 1 (10): 1589–1590. doi:10.1039/A801771I. ISSN 0300-922X.
- ^ a b c Brandán, Silvia A.; C. Socolsky; Aida Ben Altabef (2009). "DFT Calculations of the Molecular Force Field of Vanadyl Nitrate, VO(NO3)3". Zeitschrift für anorganische und allgemeine Chemie. 635 (3): 582–592. doi:10.1002/zaac.200801244. ISSN 0044-2313.
- ^ a b c d e Harris, Arlo D.; John C. Trebellas (26 April 1962). "AD296097 Experimental Studies of the Reactions of N2O5 with Metal Acid Anhydrides and BF3". Arlington Hall Station: Armed Services Technical Information Agency. Archived from the original on September 24, 2015. Retrieved 30 September 2014.
- ^ Cotton, F. Albert; Wilkinson, Geoffrey (1966). Advanced Inorganic Chemistry A Comprehensive Text (5 ed.). John Wiley. p. 814.
- ^ Pantonin, John A.; Albert K. Fischer; Edward A. Heintz (1960). "The preparation of mononitratodioxovanadium(V), VO2NO3". Journal of Inorganic and Nuclear Chemistry. 14 (1–2): 145–147. doi:10.1016/0022-1902(60)80220-5. ISSN 0022-1902.
- ^ Schmeisser, Martin (1955). "Die Chemie der anorganischen Acylnitrate (ein Problem des Nitrylchlorids) und Acylperchlorate (ein Problem des Dichlorhexoxyds)". Angewandte Chemie (in German). 67 (17–18): 493–501. doi:10.1002/ange.19550671708. ISSN 0044-8249.
- ^ 스마트, 브루스 A.;헤더는 E. 로버트슨;DavidW.H. 랭킨, 에릭은 G.호프, 콜린 J. 말 스덴(1999년).바나듐의 바나 딜 질산염, VO(NO3)3에서``은 무엇인가 조정 숫자일까?관한 연구는 분자 구조의 가스 단계에서의 전자 회절과 어릴 때 첫머리에 calculations".대한 화학 회지, 돌턴 거래 신고에 관한 법률(3):473–478. doi:10.1039/A806710D.ISSN 0300-9246.(무료로 다운로드)
- ^ Davidson, G. (2000-01-01). Spectroscopic Properties of Inorganic and Organometallic Compounds. Royal Society of Chemistry. pp. 516–517. ISBN 9780854044269. Retrieved 30 September 2014.
- ^ Fedoroff, Basil T; Sheffield, Oliver E. Encyclopedia of Explosives and Related Items Vol 10 of 10- U to Z. Vol. 10. p. V4.
- ^ a b c Brandán, S.A.; A. Ben Altabef, E.L. Varetti; Varetti, E. L. (1995). "Vibrational and electronic spectra of vanadyl nitrate, VO(NO3)3". Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy. 51 (4): 669–675. Bibcode:1995AcSpA..51..669B. doi:10.1016/0584-8539(94)00154-4. ISSN 1386-1425.
- ^ Aitken, R. Alan; Alajarin, Mateo; Allen, D. W.; Mikael Begtrup; Daniel Bellus; J. Berna-Canovas; H. Boeckemeier; Stefan Bräse; I.R. Butler; Jose Chiara; Henri-J. Cristau; I. Gorrell; D. Keck; Terence Kee; Carmen Lopez-Leonardo; T. Muller; Patrick J. Murphy; Patrick O'Leary; Beate Priewisch; L.K. Rasmussen; Karola Rück-Braun; Bjoern Schlummer; Andreas Schmidt; Paul James Stevenson; J.C. Tebby; David Virieux (2014-05-14). Science of Synthesis: Houben-Weyl Methods of Molecular Transformations Vol. 31b: Arene-X (X=N, P). Georg Thieme Verlag. p. 1215. ISBN 9783131720719. Retrieved 29 September 2014.
기타 판독치
- Gmelin, 시스템 No 48, Teil A & Teil B (Liferung 1 & 2) (1967);Teil A(Liferung 1) 및 Teil A(Liferung 2)(1968) erganzungwerk(Band 2)(1971)
- M. Schmeisser, "화학적 추상", (1955), 49, 10873
- L. Bretherick, Ed, "화학 실험실의 위험", 영국 왕립화학회, 영국 런던(1979), 1160페이지
| HNO3 | 그 | ||||||||||||||||
| LiNO3 | Be(NO3)2 | B(NO 3)− 4 | 로노2 | 아니요− 3 NH4NO3 | 훈오2 | FNO3 | 네 | ||||||||||
| NaNO3 | Mg(NO3)2 | 알(NO3)3 | 시 | P | S | 클로노2 | 아르 | ||||||||||
| 키보드3 | Ca(NO3)2 | Sc(NO3)3 | Ti(NO3)4 | VO(NO3)3 | Cr(NO3)3 | Mn(NO3)2 | Fe(NO3)2 Fe(NO3)3 | Co(NO3)2 Co(NO3)3 | Ni(NO3)2 | CuNO3 Cu(NO3)2 | Zn(NO3)2 | Ga(NO3)3 | ge | ~하듯이 | 세 | BrNO3 | Kr |
| RbNO3 | Sr(NO3)2 | Y(NO3)3 | Zr(NO3)4 | Nb | 모 | Tc | Ru(NO3)3 | Rh(NO3)3 | PD(NO3)2 PD(NO3)4 | 아그노3 Ag(NO3)2 | CD(NO3)2 | 입력3(NO)3 | Sn(NO3)4 | Sb(NO3)3 | 테 | 이노3 | Xe(NO3)2 |
| CsNO3 | Ba(NO3)2 | Hf(NO3)4 | 타 | W | 레 | OS | Ir | Pt(NO3)2 Pt(NO3)4 | AU(NO3)3 | Hg2(NO3)2 Hg(NO3)2 | TLNO3 TL(NO3)3 | Pb(NO3)2 | Bi(NO3)3 BiO(NO3) | Po(NO3)4 | 앳 | Rn | |
| 프루노3 | Ra(NO3)2 | Rf | 데이터베이스 | Sg | Bh | Hs | 산 | Ds | Rg | Cn | Nh | 플 | 맥 | Lv | Ts | 오그 | |
| ↓ | |||||||||||||||||
| La(NO3)3 | Ce(NO3)3 Ce(NO3)4 | Pr(NO3)3 | Nd(NO3)3 | PM(NO3)3 | SM(NO3)3 | Eu(NO3)3 | Gd(NO3)3 | Tb(NO3)3 | Dy(NO3)3 | 호(NO3)3 | Er(NO3)3 | Tm(NO3)3 | Yb(NO3)3 | 루(NO3)3 | |||
| AC(NO3)3 | Th(NO3)4 | PaO2(NO3)3 | UO2(NO3)2 | Np(NO3)4 | Pu(NO3)4 | AM(NO3)3 | Cm(NO3)3 | Bk(NO3)3 | Cf | Es | Fm | Md | 아니요. | Lr | |||


