파인레논
Finerenone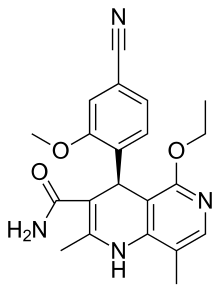 | |
| 임상자료 | |
|---|---|
| 상명 | 케렌디아 |
| 기타 이름 | 베이 94-8862 |
| 라이센스 데이터 | |
| 경로: 행정 | 입으로 |
| 마약류 | 칼륨-스파잉 이뇨제 |
| ATC 코드 | |
| 법적현황 | |
| 법적현황 | |
| 식별자 | |
| |
| CAS 번호 | |
| 펍켐 CID | |
| 드러그뱅크 | |
| 켐스파이더 | |
| 유니 | |
| 케그 | |
| 켐벨 | |
| CompTox 대시보드 (EPA) | |
| ECHA InfoCard | 100.247.614 |
| 화학 및 물리적 데이터 | |
| 공식 | C21H22N4O3 |
| 어금질량 | 378.432 g·1998−1 |
| 3D 모델(JSmol) | |
| |
| |
케렌디아라는 상표명으로 판매되는 파인레논은 제2형 당뇨병과 관련된 만성 신장질환을 앓고 있는 성인의 신장기능 저하, 신부전, 심혈관질환, 비치과성 심장마비, 심부전 입원 등의 위험을 줄이기 위해 사용하는 약이다.[2] 파인레논은 비스테로이드성 미네랄코르티코이드 수용체 길항제(MRA)이다.[1]
흔한 부작용으로는 고칼륨혈증(칼륨이 높은 수준), 저혈압(저혈압), 저나트륨혈증(저나트륨 수치) 등이 있다.[2]
파인레논은 2021년 7월 미국에서 의료용 허가를 받았다.[2][3]
의학적 용법
파인레논은 제2형 당뇨병과 관련된 만성 신장질환을 가진 성인의 신장기능 저하, 신부전, 심혈관 사망, 비치과성 심장마비, 심부전 입원 등의 위험을 줄이는 것으로 나타났다.[2]
약리학
파인레논은 현재 이용 가능한 에플레논, 스피로놀락톤 등 알도스테론 길항작용제보다 다른 스테로이드 호르몬 수용체에 대한 상대적 친화력이 떨어지기 때문에 자네코마스티아, 발기불능, 성욕저하 등의 부작용이 적어야 한다.[4][5]
파인레논은 미네랄로코르티코이드 수용체를 차단해 칼륨-스페어링 이뇨제가 된다.
이 표는 세 개의 안티미노코르티코이드의 억제(차단) 농도(IC50, 단위:nM)를 비교한다. 미네랄코르티코이드 수용체 억제는 약물의 바람직한 작용을 담당하는 반면, 다른 수용체들의 억제는 부작용을 초래할 수 있다. 값이 낮다는 것은 더 강한 억제를 의미한다.[6][full citation needed]
| 스피로놀락톤 | 에플레논 | 파인레논 | |
|---|---|---|---|
| 미네랄코르티코이드수용체 | 24 | 990 | 18 |
| 글루코르티코이드수용체 | 2400 | 22,000 | >10,000 |
| 안드로겐 수용체 | 77 | 21,200 | >10,000 |
| 프로게스테론수용체 | 740 | 31,200 | >10,000 |
위에 열거된 약들은 에스트로겐 수용체에 대한 친화력이 미미하다.[citation needed]
파인레논은 우발적으로 작용하는 스피로놀락톤, 에플레논과 같은 다른 전통적인 MR 억제제와 달리 S810L 돌연변이를 내포하고 있는 미네랄로코르티코르티코이드 수용체에 대한 대항제 역할을 한다.[7]
역사
신장 및 심장 결과 개선을 위한 파인레논의 효능은 제2형 당뇨병과 관련된 만성 신장 질환을 가진 성인을 대상으로 무작위화, 다중점, 이중맹, 위약 조절 연구를 통해 평가되었다.[2] 본 연구에서는 5,674명의 참가자를 무작위로 배정하여 파인레논이나 위약을 받았다.[2]
이 연구는 질병이 복합적(또는 복합적) 말단까지 진행된 참여자 수에 대해 두 그룹을 비교했는데, 여기에는 신장 기능 저하, 신장 기능 저하로 진행 또는 신장 사망이 최소 40% 이상 포함된다.[2] 결과, 파인레논을 받은 2,833명의 참가자 중 504명이 종합 엔드포인트에서 적어도 하나의 이벤트를 가졌는데, 이는 플라시보를 받은 2,841명의 참가자 중 600명이었던 것과 비교된다.[2]
미국 식품의약국(FDA)은 파인레논 우선 검토와 패스트트랙 지정 신청을 허가했다.[2] FDA는 바이엘 헬스케어에 케렌디아의 승인을 허가했다.[2]
사회와 문화
법적현황
2021년 12월 16일, 유럽 의약품청(EMA)의 인간 사용을 위한 의약품 위원회(CHMP)는 성인의 제2형 당뇨병과 관련된 만성 신장 질환의 치료를 목적으로 하는 약품 케렌디아에 대한 시판 허가를 권고하는 긍정적인 의견을 채택했다.[8] 이 약품의 지원자는 Bayer AG이다.[8]
리서치
2단계 ACTS-DN 연구에서는 당뇨병성 신장질환 환자의 크레아티닌 비율에 따라 미세레논이 소변 알부민을 용량 의존적으로 감소시켰다.[9] 이러한 발견에 기초하여, 파인레논은 만성 신장 질환과 제2형 당뇨병을 앓고 있는 환자의 CKD 진행 및 이상 심혈관 질환의 위험을 감소시키는지를 평가하기 위해 고안된 대규모 3상 피델리오와 FIGARO 결과 연구에서 연구되고 있다. 이번 임상시험에는 2020년, 2021년 FIGARO IN PILDIO의 1차 완료를 목표로 1만3000명 이상의 환자가 등록됐다.[10][full citation needed][11][full citation needed]
참조
- ^ a b "Kerendia- finerenone tablet, film coated". DailyMed. Retrieved 20 August 2021.
- ^ a b c d e f g h i j k "FDA Approves Drug for Chronic Kidney Disease". U.S. Food and Drug Administration (FDA). 9 July 2021. Retrieved 9 July 2021.
 이 글은 공개 도메인에 있는 이 출처의 텍스트를 통합한다..
이 글은 공개 도메인에 있는 이 출처의 텍스트를 통합한다.. - ^ "Bayer's Kerendia (finerenone) Receives U.S. FDA Approval for Treatment of Patients with Chronic Kidney Disease Associated with Type 2 Diabetes" (Press release). Bayer. 9 July 2021. Retrieved 9 July 2021 – via Business Wire.
- ^ Ruilope LM, Tamargo J (April 2017). "Renin-angiotensin system blockade: Finerenone". Nephrologie & Therapeutique. 13 Suppl 1: S47–S53. doi:10.1016/j.nephro.2017.02.003. PMID 28577743.
- ^ Pitt B, Anker SD, Böhm M, Gheorghiade M, Køber L, Krum H, et al. (February 2015). "Rationale and design of MinerAlocorticoid Receptor antagonist Tolerability Study-Heart Failure (ARTS-HF): a randomized study of finerenone vs. eplerenone in patients who have worsening chronic heart failure with diabetes and/or chronic kidney disease" (PDF). European Journal of Heart Failure. 17 (2): 224–32. doi:10.1002/ejhf.218. hdl:2027.42/110733. PMID 25678098. S2CID 205781715.
- ^ Schubert-Zsilavecz M, Wurglics M (Fall 2015). "Finerenone". Neue Arzneimittel.
- ^ Amazit L, Le Billan F, Kolkhof P, Lamribet K, Viengchareun S, Fay MR, et al. (September 2015). "Finerenone Impedes Aldosterone-dependent Nuclear Import of the Mineralocorticoid Receptor and Prevents Genomic Recruitment of Steroid Receptor Coactivator-1". The Journal of Biological Chemistry. 290 (36): 21876–89. doi:10.1074/jbc.M115.657957. PMC 4571943. PMID 26203193.
- ^ a b "Kerendia: Pending EC decision". European Medicines Agency. 16 December 2021. Retrieved 18 December 2021. 본문은 유럽 의약청의 저작권을 가지고 있는 이 출처에서 복사되었다. 출처가 인정되면 재생산은 허가된다.
- ^ Bakris GL, Agarwal R, Chan JC, Cooper ME, Gansevoort RT, Haller H, et al. (September 2015). "Effect of Finerenone on Albuminuria in Patients With Diabetic Nephropathy: A Randomized Clinical Trial". JAMA. 314 (9): 884–94. doi:10.1001/jama.2015.10081. PMID 26325557.
- ^ 임상시험 번호 NCT02540993은 ClinicalTrials.gov에서 "유형 2형 당뇨병 멜리투스 및 당뇨병 신장질환(FDILO-DKD)을 가진 피험자의 파인레논의 효능과 안전성"이다.
- ^ 임상시험 번호 NCT02545049 ClinicalTrials.gov에서 "타입 2형 당뇨병 멜리투스와 당뇨병 신장질환의 임상진단(FIGARO-DKD)"에 대한 임상시험 번호 NCT02545049
추가 읽기
- Bakris GL, Agarwal R, Anker SD, Pitt B, Ruilope LM, Rossing P, et al. (December 2020). "Effect of Finerenone on Chronic Kidney Disease Outcomes in Type 2 Diabetes". N Engl J Med. 383 (23): 2219–2229. doi:10.1056/NEJMoa2025845. PMID 33264825.
외부 링크
- "Finerenone". Drug Information Portal. U.S. National Library of Medicine.


