베르가프텐
Bergapten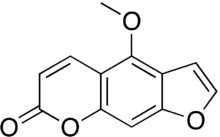 | |
 | |
 | |
| 이름 | |
|---|---|
| 우선 IUPAC 이름 4-메톡시-7H-퓨로[3,2-g][1]벤조피란-7-원 | |
기타 이름
| |
| 식별자 | |
3D 모델(JSmol) | |
| 체비 | |
| 첸블 | |
| 켐스파이더 | |
| ECHA 정보 카드 | 100.006.913 |
| EC 번호 |
|
| 케그 | |
PubChem CID | |
| 유니 | |
| UN 번호 | 1759 |
CompTox 대시보드 (EPA ) | |
| |
| |
| 특성. | |
| C12H8O4 | |
| 몰 질량 | 216.192g/표준 |
| 약리학 | |
| D05BA03 (WHO) | |
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |
베르가프텐(5-메톡시스포라렌)은 많은 식물종, 특히 당근과, 감귤과에서 생산되는 자연발생 유기화합물이다.예를 들어, 베르가프텐은 백합과의 [1][2]헤라클룸속 24종에서 추출되었다.루타과에는 다양한 감귤류 종들이 상당한 양의 베르가프텐을 [3]포함하고 있는데, 특히 베르가못 오렌지, 미크란타, 그리고 특정한 종류의 라임과 쓴 오렌지가 있다.
베르가프텐은 플라노코우마린으로 알려진 화합물 종류에 속합니다.1834년 칼브루너는 베르가못 에센셜 [4]오일에서 5-메톡시프소랄렌을 분리하여 "베르가프텐"이라는 통칭으로 불렀다.그것은 분리되고 확인된 최초의 푸라노쿠마린이었다.
독성
베르가프텐은 선형 푸라노쿠마린으로 알려진 자연적으로 발생하는 유기 화합물의 모체인 솔라렌의 유도체이다.베르가프텐을 포함한 일부 선형 플라노쿠마린은 국소적으로 피부에 바르면 강한 광감작제 역할을 합니다.
베르갑텐은 잠재적으로 심각한 피부 염증인 식물성 피부염과 [5]관련된 식물에서 종종 발견됩니다.베르가프텐(및 다른 선형 플루노코마린)을 포함한 식물 부분과 접촉한 후 자외선에 노출되면 식물성 피부염이 발생할 수 있습니다.특히 베르가프텐은 감귤류 유도 식물성 피부염을 [3]일으키는 1차 광독성 화합물인 것으로 보인다.
베르가프텐 및 기타 선형 플루노코우마린은 RNA 합성을 위한 템플릿 활성 손실을 유도한다.또한 5-메톡시스포랄렌은 돌연변이 유발 효과와 염색체 이상을 유도하는 매우 강력한 약제로서의 능력으로 알려져 있다.충분히 높은 농도로 완전한 유사분열 억제가 [4]관찰되었다.
베르가펜이 동물에게 암을 촉진한다는 증거는 충분하지만 사람에게 발암성이 있다는 증거는 부족하다.국제 암 연구 기구에 따르면 베르가프텐은 아마도 [6]사람에게 발암을 일으킬 수 있다.
의료용도
베르가프텐은 피부가 더 많은 빛을 흡수하도록 하는 역할을 하며 백반증이나 건선과 같은 색소성 질환은 종종 태양 노출이나 태양 방사선과 함께 후라노코마린과 관련된 치료법을 가지고 있다.햇볕에 잘 타는 사람들에게, 후라노코마린은 또한 태양 [4]복사에 대한 피부의 내성을 증가시킬 수 있다.베르가프텐은 백반증 환자의 색소 침착을 완화하기 위해 대상자의 민감도, 용량, 습도 등 다양한 요인에 따라 피부 반응을 일정하게 유도하는 것으로 나타났지만 효과는 일관되지 [7]않을 수 있다.
건선과 함께, 베르가펜은 그 효과와 광독성 및 약물에 민감하지 않은 반응의 결여로 경구 광화학 치료제로 평가되어 왔다.건선 [8]병변 클리어에 있어 8-메톡시소라렌보다 효과적이거나 충분히 높은 용량으로 광감작약으로 작용한다.적혈구, 가려움증, [9]메스꺼움 등의 치료 중 부작용의 상대적 결여로 인해 8-메톡시스포랄렌의 귀중한 대안으로 나타났다.
Bergapten은 또한 햇빛과 관련된 피부암을 예방하는 잠재적인 방법으로도 알려져 있다.한 연구는 베르가프텐으로 얻은 태닝이 인간 [10]피실험자의 DNA 손상을 줄인다는 것을 발견했다.Bergapten은 유방암 세포에서 자가마법 과정을 유도하는 것과 같은 항종양 효과가 있는 것으로 나타났다.한 연구는 이러한 유방암 [11]세포에서 PTEN 유전자 발현을 상향 조절함으로써 이것이 가능했다고 시사했다.
베르가프텐은 다른 플루노코우마린과 함께 시토크롬 P450 [12]억제에도 관여하고 있다.
합성
베르가프텐은 일반적인 무화과와 같은 식물에서 나오는 천연 화합물이지만 합성될 수도 있다.선형 플라노쿠마린의 대부분의 합성에는 중심 방향족 단위에서 시작하여 두 개의 복소환 고리를 추가하는 것이 포함됩니다.위치 화학적 문제를 피하고 적당한 산출량을 얻기 위해서는 대체 합성 경로가 바람직하다.여기서 설명하는 합성에는 위치 화학적 무결성과 [13]수렴을 보장하기 위해 요오드가 제거 가능한 기로 포함됩니다.그림과 같이 프롤로글루시놀(복합 1)이 시작 물질이었다.모노메틸화는 ZnCl의2 존재 하에서 에틸프로피올레이트와의 반응을 거쳐 68%의 수율로 7-히드록시-5-메톡시쿠마린(제품 3)을 산출하였다.그런 다음 7-히드록시-5-메톡시쿠마린의 8-위치를 요오드로 보호하여 각진 플루아노쿠마린의 형성을 방지하였다.그림의 제품 4는 해당 요오드 보호의 결과입니다.제품 5는 제품 4의 알릴화 결과입니다.O-알릴 유도체를 디올 중간체(제품 6, 도시하지 않음)를 통해 알데히드 제품 7에 산화 분해하기 위해 테트라옥시드 및 메트라페리오드산나트륨을 사용하였다.다음으로 브롬화테트라-n-부틸암모늄 중 BF-EtO를32 이용한 알데히드 생성물 7의 환화를 실시하여 프랑환을 구성한다.마지막 단계는 Pd(OAc)2를 통해 요오드 보호기를 제거하여 최종적으로 수율이 90%인 베르가프텐(제품9)을 생산하는 것이었다.합성 베르가펜은 천연물과 분광학적으로 동일한 성질을 가진 무색 화합물로 분리되었다.
베르가프텐의 알려진 용도는 프락시놀 [14]합성에 있다.이 합성의 핵심 반응은 비스나긴과 베르가프텐의 프랑 고리를 크롬산으로 [14]산화시키는 것이다.
레퍼런스
- ^ Nielsen, B. E. (1970). Coumarins of Umbelliferous plants. Copenhagen: Royal Danish School of Pharmacy. 미첼과 룩(1979년)이 인용했다.
- ^ Mitchell, John; Rook, Arthur (1979). Botanical Dermatology: Plants and Plant Products Injurious to the Skin. Vancouver: Greengrass. pp. 692–699.
- ^ a b Dugrand-Judek, Audray; Olry, Alexandre; Hehn, Alain; Costantino, Gilles; Ollitrault, Patrick; Froelicher, Yann; Bourgaud, Frédéric (November 2015). "The Distribution of Coumarins and Furanocoumarins in Citrus Species Closely Matches Citrus Phylogeny and Reflects the Organization of Biosynthetic Pathways". PLOS ONE. 10 (11): e0142757. Bibcode:2015PLoSO..1042757D. doi:10.1371/journal.pone.0142757. PMC 4641707. PMID 26558757.
- ^ a b c Scott, B. R.; Pathak, M. A.; Mohn, G. R. (1976). "Molecular and genetic basis of furocoumarin reactions". Mutat Res. 39 (1): 29–74. doi:10.1016/0165-1110(76)90012-9. PMID 13299.
- ^ McGovern, Thomas W.; Barkley, Theodore M. (2000). "Botanical Dermatology". The Electronic Textbook of Dermatology. Internet Dermatology Society. Section Phytophotodermatitis. Retrieved November 29, 2018.
- ^ "Monographs on the Evaluation of the Carcinogenic Risk of Chemicals to Humans". Geneva: World Health Organization, International Agency for Research on Cancer, 1972-PRESENT. 1987. p. S7 66. Retrieved 4 January 2019.
- ^ "Side effects of earl grey tea".
- ^ Honigsmann (Oct 1979). "5-Methoxypsoralen (Bergapten) in photochemotherapy of psoriasis". British Journal of Dermatology. 101 (4): 369–378. doi:10.1111/j.1365-2133.1979.tb00014.x. PMID 508604. S2CID 46371217.
- ^ Tanew, Adrian (February 1988). "5-Methoxypsoralen (Bergapten) for photochemotherapy: Bioavailability, phototoxicity, and clinical efficacy in psoriasis of a new drug preparation". Journal of the American Academy of Dermatology. 18 (2 Pt 1): 333–338. doi:10.1016/S0190-9622(88)70048-1. PMID 3279089.
- ^ Tisserand, Robert (2014). Essential Oil Safety. Churchill Livingstone.
- ^ De Amicis, Francesca (2015). "Bergapten drives autophagy through the up-regulation of PTEN expression in breast cancer cells". Molecular Cancer. 14: 130. doi:10.1186/s12943-015-0403-4. PMC 4498523. PMID 26148846.
- ^ Aldred, Elaine (2009). Haschek and Rousseaux's Handbook of Toxicologic Pathology (Third ed.). Churchill livingstone.
- ^ Oda, Kazuaki (June 2005). "An Efficient Synthesis of Bergapten". Heterocycles. 65 (8): 1985–1988. doi:10.3987/com-05-10451 – via ResearchGate.
- ^ a b Schönberg, Alexander; Badran, Nasry; Starkowsky, Nicolas A. (1955). "Furo-chromones and -Coumarins. XII. Synthesis of Fraxinol from Bergapten and of Baicalein from Visnagin". Journal of the American Chemical Society. 77 (20): 5390–5392. doi:10.1021/ja01625a055. ISSN 0002-7863.



