Singlett oksygen er en aktivert form av oksygen og en kjemisk reaktiv forbindelse som oksiderer organiske stoffer i organismer og forårsaker skader og celledød. Utslett og vabler på hud forårsaket av planten kjempebjørnekjeks skyldes fotodynamiske effekter fra singlett oksygen. Singlett oksygen brukes også i kreftbehandling for å drepe kreftceller.
singlett oksygen
Danning og funksjon
Singlett oksygen dannes i kombinasjon med lys og fotosensitiserende stoffer. Lysenergi blir overført til vanlig oksygen i grunntilstanden triplett oksygen. Triplett og singlett oksygen henspiller på retningen av elektronspinn for elektronene rundt oksygenmolekylet (O2).
Forskjell i plassering av elektroner i elektronskall gjør at triplett oksygen (3O2) og singlett oksygen (1O2) har forskjellige kjemiske egenskaper. Singlett oksygen er en reaktiv oksygenforbindelse som oksiderer organiske stoffer i organismene mer effektivt enn triplett oksygen, og forårsaker skader og celledød.
Virkninger
Flere av innholdsstoffene i planter virker fototoksisk og blir brukt som beskyttelse mot dyr som spiser av plantene eller mot sykdomsfremkallende organismer. Fotosensitiserende stoffer fra planter kan ved direkte hudkontakt sammen med sollys gi utslett og vabler (fytofotodermatitt) som skyldes fotodynamiske effekter fra singlett oksygen. Et eksempel på dette er kjempebjørnekjeks. Det samme gjelder mat fra planter som inneholder lysabsorberende stoffer som kan akkumulere i huden og gi singlett oksygen. Hos beitende husdyr kan singlett oksygen bidra til å lage sår på huden i sola om våren og gi huldrabrent eller sauesykdommen alveld. Et annet eksempel er bokhveteutslett.
Singlett oksygen en del av virkningsmekanismen i fotodynamisk terapi brukt i kreftbehandling hvor porfyriner overfører lysenergi til oksygen, og hvor singlett oksygen kan drepe kreftcellene.
Triplett og singlett oksygen

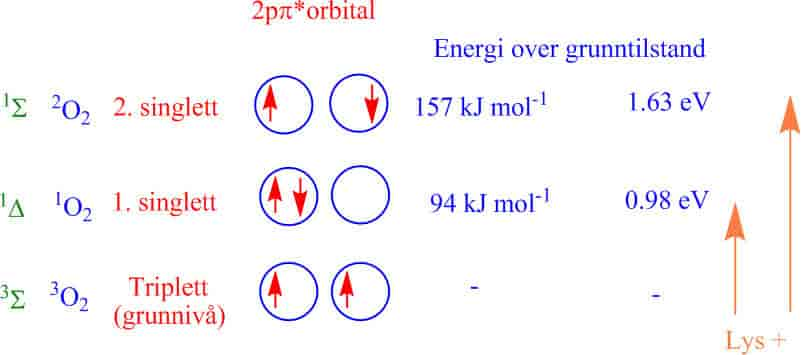
Hvordan elektroner er organisert i orbitaler i et atom eller et molekyl er med å bestemmer de kjemiske egenskapene. Et orbital angir sannsynligheten for å finne et elektron på et sted til en gitt tid. Oksygen i atmosfæren er i grunntilstanden et triplett oksygen med to uparete elektroner med parallelle spinn i det ytterste antibindende orbital. Dette gir en kinetisk barriære som hindrer vanlig triplett oksygen i å reagere lett.
Spinkvantetallet S, et av de fire kvantetallene, har to mulige verdier, spinn pluss halv (+ ½ ) og minus halv (– ½ ). De 16 elektronene rundt de to oksygenatomene (O) fordeles i dioksygen (O2) etter Hunds regler og Paulis eksklusjonsprinsipp. Det er plass til to elektroner i hver orbital, og disse må ha motsatt spinn når de befinner seg i samme orbital. En av Hunds regler er at multiplisitet M er gitt ved:
M= 2|S| + 1
hvor S er den totale sum spinn for alle elektronene i molekylet
Spinn + ½ og – ½ gir magnetfelt 0
Spinn + ½ og +1/2 gir magnetfelt 1
Dette gir innsatt i formelen for multiplisitet
Triplett oksygen M = 2·1 + 1 = 3
Singlett oksygen M = 1 ·0 + 1 = 1
For en gitt plassering av elektroner har den med høyest multiplisitet lavest energi og er mest stabil. Stadier med triplett og singlett gjelder også andre molekyler slik som klorofyll og andre fotosensitiserende stoffer.
Fotosensitiserende stoffer og singlett oksygen
Porfyriner, bilirubiner, rhodopsiner, melaniner, pteriner, flaviner (vitamin B6) og kinoner (vitamin K) er eksempler på stoffer i vanlig stoffskifte som kan virke som fotosensitiserende. Skjermplanter og sitrusfrukter kan inneholde lineære furanokoumariner (psoralener) som virker fototoksisk, for eksempel bergapten.
I et fotosensitiserende stoff, her kalt FST, absorberer et elektron lysenergi og gir et eksitert singlett.
FST + lysenergi → 1FST* (eksitert singlett)
Det eksiterte elektronet kan enten falle meget raskt tilbake til grunntilstanden, men det er også en sannsynlighet for at det kan skje en reversering av spinretningen på det eksiterte elektronet slik at det fotosensistiverende stoffet danner en triplett
1FST*(S1) → 3FST* (eksitert triplett)
Det fotosensistiserende stoffet i eksitert triplett har lavere energi enn singlett, men har lang nok levetid til at lysenergien blir overført til triplett oksygen og man får dannet singlett oksygen (1O2).
3FST* + 3O2 → FST + 1O2
Det er også mulig at det eksiterte triplettstadiet kan avgi et elektron til oksygen hvor man får dannet superoksidanionradiakalet av oksygen ((O2•- ). Det er en nær sammenheng mellom reaktive oksygenforbindelser og reaktive nitrogenforbindelser, hvor både hydrogenperoksid (H2O2), radikalet og signalmolekylet nitrogenmonoksid (NO•), og hydroksylradiakalet i fentonreaksjoner (OH•) kan samvirke når immunceller deltar i angrep mot bakterier og virus.


Kommentarer
Kommentarer til artikkelen blir synlig for alle. Ikke skriv inn sensitive opplysninger, for eksempel helseopplysninger. Fagansvarlig eller redaktør svarer når de kan. Det kan ta tid før du får svar.
Du må være logget inn for å kommentere.