JP6790490B2 - 情報処理装置、情報処理方法及び情報処理システム - Google Patents
情報処理装置、情報処理方法及び情報処理システム Download PDFInfo
- Publication number
- JP6790490B2 JP6790490B2 JP2016123226A JP2016123226A JP6790490B2 JP 6790490 B2 JP6790490 B2 JP 6790490B2 JP 2016123226 A JP2016123226 A JP 2016123226A JP 2016123226 A JP2016123226 A JP 2016123226A JP 6790490 B2 JP6790490 B2 JP 6790490B2
- Authority
- JP
- Japan
- Prior art keywords
- pulse waveform
- information
- information processing
- unit
- pulse
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 230000010365 information processing Effects 0.000 title claims description 145
- 238000003672 processing method Methods 0.000 title claims description 23
- 238000004458 analytical method Methods 0.000 claims description 71
- 230000001678 irradiating effect Effects 0.000 claims description 8
- 230000002238 attenuated effect Effects 0.000 claims description 4
- 238000005259 measurement Methods 0.000 description 91
- 210000004027 cell Anatomy 0.000 description 49
- 239000000427 antigen Substances 0.000 description 33
- 102000036639 antigens Human genes 0.000 description 33
- 108091007433 antigens Proteins 0.000 description 33
- 239000000523 sample Substances 0.000 description 31
- 238000000034 method Methods 0.000 description 25
- 238000004891 communication Methods 0.000 description 24
- 238000009826 distribution Methods 0.000 description 23
- 238000010586 diagram Methods 0.000 description 20
- 230000004071 biological effect Effects 0.000 description 17
- 238000004422 calculation algorithm Methods 0.000 description 14
- 230000003287 optical effect Effects 0.000 description 14
- 239000007850 fluorescent dye Substances 0.000 description 13
- 238000012545 processing Methods 0.000 description 13
- 239000002245 particle Substances 0.000 description 11
- 230000008569 process Effects 0.000 description 11
- 230000006870 function Effects 0.000 description 9
- 238000007796 conventional method Methods 0.000 description 7
- 230000004807 localization Effects 0.000 description 7
- 230000000694 effects Effects 0.000 description 6
- 238000011156 evaluation Methods 0.000 description 6
- GNBHRKFJIUUOQI-UHFFFAOYSA-N fluorescein Chemical compound O1C(=O)C2=CC=CC=C2C21C1=CC=C(O)C=C1OC1=CC(O)=CC=C21 GNBHRKFJIUUOQI-UHFFFAOYSA-N 0.000 description 6
- 238000002372 labelling Methods 0.000 description 6
- 230000008859 change Effects 0.000 description 5
- 239000003153 chemical reaction reagent Substances 0.000 description 5
- 238000004364 calculation method Methods 0.000 description 4
- 238000006243 chemical reaction Methods 0.000 description 4
- 238000000546 chi-square test Methods 0.000 description 4
- BZTDTCNHAFUJOG-UHFFFAOYSA-N 6-carboxyfluorescein Chemical compound C12=CC=C(O)C=C2OC2=CC(O)=CC=C2C11OC(=O)C2=CC=C(C(=O)O)C=C21 BZTDTCNHAFUJOG-UHFFFAOYSA-N 0.000 description 3
- -1 BCECF Chemical compound 0.000 description 3
- 239000012472 biological sample Substances 0.000 description 3
- 238000004590 computer program Methods 0.000 description 3
- 239000000203 mixture Substances 0.000 description 3
- 239000004065 semiconductor Substances 0.000 description 3
- 238000001228 spectrum Methods 0.000 description 3
- YBJHBAHKTGYVGT-ZKWXMUAHSA-N (+)-Biotin Chemical group N1C(=O)N[C@@H]2[C@H](CCCCC(=O)O)SC[C@@H]21 YBJHBAHKTGYVGT-ZKWXMUAHSA-N 0.000 description 2
- OZLGRUXZXMRXGP-UHFFFAOYSA-N Fluo-3 Chemical compound CC1=CC=C(N(CC(O)=O)CC(O)=O)C(OCCOC=2C(=CC=C(C=2)C2=C3C=C(Cl)C(=O)C=C3OC3=CC(O)=C(Cl)C=C32)N(CC(O)=O)CC(O)=O)=C1 OZLGRUXZXMRXGP-UHFFFAOYSA-N 0.000 description 2
- 229930187135 Olivomycin Natural products 0.000 description 2
- 108010004729 Phycoerythrin Proteins 0.000 description 2
- 238000000862 absorption spectrum Methods 0.000 description 2
- DPKHZNPWBDQZCN-UHFFFAOYSA-N acridine orange free base Chemical compound C1=CC(N(C)C)=CC2=NC3=CC(N(C)C)=CC=C3C=C21 DPKHZNPWBDQZCN-UHFFFAOYSA-N 0.000 description 2
- DZBUGLKDJFMEHC-UHFFFAOYSA-N benzoquinolinylidene Natural products C1=CC=CC2=CC3=CC=CC=C3N=C21 DZBUGLKDJFMEHC-UHFFFAOYSA-N 0.000 description 2
- 229960002685 biotin Drugs 0.000 description 2
- 239000011616 biotin Substances 0.000 description 2
- 210000003855 cell nucleus Anatomy 0.000 description 2
- 230000001186 cumulative effect Effects 0.000 description 2
- 238000001514 detection method Methods 0.000 description 2
- 238000000295 emission spectrum Methods 0.000 description 2
- 239000000284 extract Substances 0.000 description 2
- 238000002189 fluorescence spectrum Methods 0.000 description 2
- 239000002502 liposome Substances 0.000 description 2
- 244000005700 microbiome Species 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- CZDBNBLGZNWKMC-MWQNXGTOSA-N olivomycin Chemical compound O([C@@H]1C[C@@H](O[C@H](C)[C@@H]1O)OC=1C=C2C=C3C[C@H]([C@@H](C(=O)C3=C(O)C2=C(O)C=1)O[C@H]1O[C@@H](C)[C@H](O)[C@@H](OC2O[C@@H](C)[C@H](O)[C@@H](O)C2)C1)[C@H](OC)C(=O)[C@@H](O)[C@@H](C)O)[C@H]1C[C@H](O)[C@H](OC)[C@H](C)O1 CZDBNBLGZNWKMC-MWQNXGTOSA-N 0.000 description 2
- 229950005848 olivomycin Drugs 0.000 description 2
- 210000003463 organelle Anatomy 0.000 description 2
- 230000001151 other effect Effects 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- 238000012706 support-vector machine Methods 0.000 description 2
- PRDFBSVERLRRMY-UHFFFAOYSA-N 2'-(4-ethoxyphenyl)-5-(4-methylpiperazin-1-yl)-2,5'-bibenzimidazole Chemical compound C1=CC(OCC)=CC=C1C1=NC2=CC=C(C=3NC4=CC(=CC=C4N=3)N3CCN(C)CC3)C=C2N1 PRDFBSVERLRRMY-UHFFFAOYSA-N 0.000 description 1
- FWBHETKCLVMNFS-UHFFFAOYSA-N 4',6-Diamino-2-phenylindol Chemical compound C1=CC(C(=N)N)=CC=C1C1=CC2=CC=C(C(N)=N)C=C2N1 FWBHETKCLVMNFS-UHFFFAOYSA-N 0.000 description 1
- 108090001008 Avidin Proteins 0.000 description 1
- 241000894006 Bacteria Species 0.000 description 1
- 241000196324 Embryophyta Species 0.000 description 1
- 241000588724 Escherichia coli Species 0.000 description 1
- 244000187656 Eucalyptus cornuta Species 0.000 description 1
- 241000233866 Fungi Species 0.000 description 1
- 238000003657 Likelihood-ratio test Methods 0.000 description 1
- 108091005461 Nucleic proteins Proteins 0.000 description 1
- 238000001358 Pearson's chi-squared test Methods 0.000 description 1
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 1
- 240000004808 Saccharomyces cerevisiae Species 0.000 description 1
- 241000723873 Tobacco mosaic virus Species 0.000 description 1
- 241000700605 Viruses Species 0.000 description 1
- CAWBRCOBJNWRLK-UHFFFAOYSA-N acetyloxymethyl 2-[4-[bis[2-(acetyloxymethoxy)-2-oxoethyl]amino]-3-[2-[2-[bis[2-(acetyloxymethoxy)-2-oxoethyl]amino]-5-methylphenoxy]ethoxy]phenyl]-1h-indole-6-carboxylate Chemical compound CC(=O)OCOC(=O)CN(CC(=O)OCOC(C)=O)C1=CC=C(C)C=C1OCCOC1=CC(C=2NC3=CC(=CC=C3C=2)C(=O)OCOC(C)=O)=CC=C1N(CC(=O)OCOC(C)=O)CC(=O)OCOC(C)=O CAWBRCOBJNWRLK-UHFFFAOYSA-N 0.000 description 1
- NTECHUXHORNEGZ-UHFFFAOYSA-N acetyloxymethyl 3',6'-bis(acetyloxymethoxy)-2',7'-bis[3-(acetyloxymethoxy)-3-oxopropyl]-3-oxospiro[2-benzofuran-1,9'-xanthene]-5-carboxylate Chemical compound O1C(=O)C2=CC(C(=O)OCOC(C)=O)=CC=C2C21C1=CC(CCC(=O)OCOC(C)=O)=C(OCOC(C)=O)C=C1OC1=C2C=C(CCC(=O)OCOC(=O)C)C(OCOC(C)=O)=C1 NTECHUXHORNEGZ-UHFFFAOYSA-N 0.000 description 1
- 210000004102 animal cell Anatomy 0.000 description 1
- 238000013528 artificial neural network Methods 0.000 description 1
- 235000020958 biotin Nutrition 0.000 description 1
- 210000000601 blood cell Anatomy 0.000 description 1
- ZYVSOIYQKUDENJ-WKSBCEQHSA-N chromomycin A3 Chemical compound O([C@@H]1C[C@@H](O[C@H](C)[C@@H]1OC(C)=O)OC=1C=C2C=C3C[C@H]([C@@H](C(=O)C3=C(O)C2=C(O)C=1C)O[C@@H]1O[C@H](C)[C@@H](O)[C@H](O[C@@H]2O[C@H](C)[C@@H](O)[C@H](O[C@@H]3O[C@@H](C)[C@H](OC(C)=O)[C@@](C)(O)C3)C2)C1)[C@H](OC)C(=O)[C@@H](O)[C@@H](C)O)[C@@H]1C[C@@H](O)[C@@H](OC)[C@@H](C)O1 ZYVSOIYQKUDENJ-WKSBCEQHSA-N 0.000 description 1
- 210000000349 chromosome Anatomy 0.000 description 1
- 238000010835 comparative analysis Methods 0.000 description 1
- 230000000295 complement effect Effects 0.000 description 1
- 238000013500 data storage Methods 0.000 description 1
- 238000013135 deep learning Methods 0.000 description 1
- CFCUWKMKBJTWLW-UHFFFAOYSA-N deoliosyl-3C-alpha-L-digitoxosyl-MTM Natural products CC=1C(O)=C2C(O)=C3C(=O)C(OC4OC(C)C(O)C(OC5OC(C)C(O)C(OC6OC(C)C(O)C(C)(O)C6)C5)C4)C(C(OC)C(=O)C(O)C(C)O)CC3=CC2=CC=1OC(OC(C)C1O)CC1OC1CC(O)C(O)C(C)O1 CFCUWKMKBJTWLW-UHFFFAOYSA-N 0.000 description 1
- 238000004043 dyeing Methods 0.000 description 1
- 230000005684 electric field Effects 0.000 description 1
- ZMMJGEGLRURXTF-UHFFFAOYSA-N ethidium bromide Chemical compound [Br-].C12=CC(N)=CC=C2C2=CC=C(N)C=C2[N+](CC)=C1C1=CC=CC=C1 ZMMJGEGLRURXTF-UHFFFAOYSA-N 0.000 description 1
- 229960005542 ethidium bromide Drugs 0.000 description 1
- 230000001747 exhibiting effect Effects 0.000 description 1
- 238000013213 extrapolation Methods 0.000 description 1
- 238000000684 flow cytometry Methods 0.000 description 1
- MHMNJMPURVTYEJ-UHFFFAOYSA-N fluorescein-5-isothiocyanate Chemical compound O1C(=O)C2=CC(N=C=S)=CC=C2C21C1=CC=C(O)C=C1OC1=CC(O)=CC=C21 MHMNJMPURVTYEJ-UHFFFAOYSA-N 0.000 description 1
- VPSRLGDRGCKUTK-UHFFFAOYSA-N fura-2-acetoxymethyl ester Chemical compound CC(=O)OCOC(=O)CN(CC(=O)OCOC(C)=O)C1=CC=C(C)C=C1OCCOC(C(=C1)N(CC(=O)OCOC(C)=O)CC(=O)OCOC(C)=O)=CC2=C1OC(C=1OC(=CN=1)C(=O)OCOC(C)=O)=C2 VPSRLGDRGCKUTK-UHFFFAOYSA-N 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- PNDZEEPOYCVIIY-UHFFFAOYSA-N indo-1 Chemical compound CC1=CC=C(N(CC(O)=O)CC(O)=O)C(OCCOC=2C(=CC=C(C=2)C=2N=C3[CH]C(=CC=C3C=2)C(O)=O)N(CC(O)=O)CC(O)=O)=C1 PNDZEEPOYCVIIY-UHFFFAOYSA-N 0.000 description 1
- 150000002540 isothiocyanates Chemical class 0.000 description 1
- 239000004973 liquid crystal related substance Substances 0.000 description 1
- 238000010801 machine learning Methods 0.000 description 1
- 229910044991 metal oxide Inorganic materials 0.000 description 1
- 150000004706 metal oxides Chemical class 0.000 description 1
- CFCUWKMKBJTWLW-BKHRDMLASA-N mithramycin Chemical compound O([C@@H]1C[C@@H](O[C@H](C)[C@H]1O)OC=1C=C2C=C3C[C@H]([C@@H](C(=O)C3=C(O)C2=C(O)C=1C)O[C@@H]1O[C@H](C)[C@@H](O)[C@H](O[C@@H]2O[C@H](C)[C@H](O)[C@H](O[C@@H]3O[C@H](C)[C@@H](O)[C@@](C)(O)C3)C2)C1)[C@H](OC)C(=O)[C@@H](O)[C@@H](C)O)[C@H]1C[C@@H](O)[C@H](O)[C@@H](C)O1 CFCUWKMKBJTWLW-BKHRDMLASA-N 0.000 description 1
- 210000003470 mitochondria Anatomy 0.000 description 1
- 102000039446 nucleic acids Human genes 0.000 description 1
- 108020004707 nucleic acids Proteins 0.000 description 1
- 150000007523 nucleic acids Chemical class 0.000 description 1
- 230000002093 peripheral effect Effects 0.000 description 1
- 229910052698 phosphorus Inorganic materials 0.000 description 1
- 239000011574 phosphorus Substances 0.000 description 1
- INAAIJLSXJJHOZ-UHFFFAOYSA-N pibenzimol Chemical compound C1CN(C)CCN1C1=CC=C(N=C(N2)C=3C=C4NC(=NC4=CC=3)C=3C=CC(O)=CC=3)C2=C1 INAAIJLSXJJHOZ-UHFFFAOYSA-N 0.000 description 1
- 229960003171 plicamycin Drugs 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- XJMOSONTPMZWPB-UHFFFAOYSA-M propidium iodide Chemical compound [I-].[I-].C12=CC(N)=CC=C2C2=CC=C(N)C=C2[N+](CCC[N+](C)(CC)CC)=C1C1=CC=CC=C1 XJMOSONTPMZWPB-UHFFFAOYSA-M 0.000 description 1
- 102000004169 proteins and genes Human genes 0.000 description 1
- 238000000611 regression analysis Methods 0.000 description 1
- 230000002787 reinforcement Effects 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- MUSLHCJRTRQOSP-UHFFFAOYSA-N rhodamine 101 Chemical compound [O-]C(=O)C1=CC=CC=C1C(C1=CC=2CCCN3CCCC(C=23)=C1O1)=C2C1=C(CCC1)C3=[N+]1CCCC3=C2 MUSLHCJRTRQOSP-UHFFFAOYSA-N 0.000 description 1
- TUFFYSFVSYUHPA-UHFFFAOYSA-M rhodamine 123 Chemical compound [Cl-].COC(=O)C1=CC=CC=C1C1=C(C=CC(N)=C2)C2=[O+]C2=C1C=CC(N)=C2 TUFFYSFVSYUHPA-UHFFFAOYSA-M 0.000 description 1
- 238000005070 sampling Methods 0.000 description 1
- 238000010187 selection method Methods 0.000 description 1
- 230000005236 sound signal Effects 0.000 description 1
- 238000010186 staining Methods 0.000 description 1
- MPLHNVLQVRSVEE-UHFFFAOYSA-N texas red Chemical compound [O-]S(=O)(=O)C1=CC(S(Cl)(=O)=O)=CC=C1C(C1=CC=2CCCN3CCCC(C=23)=C1O1)=C2C1=C(CCC1)C3=[N+]1CCCC3=C2 MPLHNVLQVRSVEE-UHFFFAOYSA-N 0.000 description 1
- ACOJCCLIDPZYJC-UHFFFAOYSA-M thiazole orange Chemical compound CC1=CC=C(S([O-])(=O)=O)C=C1.C1=CC=C2C(C=C3N(C4=CC=CC=C4S3)C)=CC=[N+](C)C2=C1 ACOJCCLIDPZYJC-UHFFFAOYSA-M 0.000 description 1
- 230000032258 transport Effects 0.000 description 1
- 238000012795 verification Methods 0.000 description 1
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume or surface-area of porous materials
- G01N15/10—Investigating individual particles
- G01N15/14—Optical investigation techniques, e.g. flow cytometry
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume or surface-area of porous materials
- G01N15/10—Investigating individual particles
- G01N15/14—Optical investigation techniques, e.g. flow cytometry
- G01N15/1429—Signal processing
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume or surface-area of porous materials
- G01N15/10—Investigating individual particles
- G01N15/14—Optical investigation techniques, e.g. flow cytometry
- G01N15/1456—Optical investigation techniques, e.g. flow cytometry without spatial resolution of the texture or inner structure of the particle, e.g. processing of pulse signals
- G01N15/1459—Optical investigation techniques, e.g. flow cytometry without spatial resolution of the texture or inner structure of the particle, e.g. processing of pulse signals the analysis being performed on a sample stream
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N21/6428—Measuring fluorescence of fluorescent products of reactions or of fluorochrome labelled reactive substances, e.g. measuring quenching effects, using measuring "optrodes"
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume or surface-area of porous materials
- G01N15/01—Investigating characteristics of particles; Investigating permeability, pore-volume or surface-area of porous materials specially adapted for biological cells, e.g. blood cells
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume or surface-area of porous materials
- G01N15/10—Investigating individual particles
- G01N2015/1006—Investigating individual particles for cytology
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Physics & Mathematics (AREA)
- Immunology (AREA)
- General Physics & Mathematics (AREA)
- Life Sciences & Earth Sciences (AREA)
- Analytical Chemistry (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- Pathology (AREA)
- Dispersion Chemistry (AREA)
- Signal Processing (AREA)
- Engineering & Computer Science (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Optics & Photonics (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Investigating, Analyzing Materials By Fluorescence Or Luminescence (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Investigating Or Analysing Materials By Optical Means (AREA)
- Apparatus Associated With Microorganisms And Enzymes (AREA)
Description
前記ピーク位置に関連する情報に基づいて前記生物由来対象の推定される特性候補を決定する、特性候補決定部と、
を備える情報処理装置が提供される。
前記ピーク位置に関連する情報に基づいて前記生物由来対象の推定される特性候補を決定することと、
を含む、情報処理方法が提供される。
前記パルス波形のデータに基づき前記パルス波形のピーク位置に関連する情報を特定するパルス波形解析部および前記ピーク位置に関連する情報に基づいて前記生物由来対象の推定される特性候補を決定する特性候補決定部を備える情報処理装置と、
を備える、情報処理システムが提供される。
なお、上記の効果は必ずしも限定的なものではなく、上記の効果とともに、または上記の効果に代えて、本明細書に示されたいずれかの効果、または本明細書から把握され得る他の効果が奏されてもよい。
1.第1の実施の形態(セルアナライザ)
1.1.情報処理システムの概要
1.2.測定サンプル
1.3.測定ユニットの構成
1.4.情報処理装置の構成
1.5.情報処理方法の流れ
2.第2の実施の形態(セルソータ)
2.1.情報処理システムの構成
2.2.情報処理方法の流れ
3.情報処理装置のハードウェア構成
以下では、図1〜図18を参照しながら、本開示の第1の実施形態について詳細に説明する。
まず、図1を参照しながら、本実施形態に係る情報処理システムについて説明する。図1は、第1の実施形態に係る情報処理システムを示した説明図である。図2および図3は、図1に示す情報処理システムが備える測定ユニットを説明する概要図である。
測定サンプルである生物由来対象は、蛍光スペクトルの測定に先立って、1以上の蛍光色素により標識(染色)されることができる。生物由来対象の蛍光色素標識は、公知の任意の手法によって行うことができる。例えば測定対象を細胞とする場合には、細胞表面分子に対する蛍光標識抗体と細胞とを混合し、細胞表面分子に抗体を結合させる。蛍光標識抗体は、抗体に直接蛍光色素を結合させたものであってもよく、ビオチン標識した抗体にアビジンを結合した蛍光色素をアビジン・ビオチン反応によって結合させたものであってもよい。また、抗体は、モノクローナル抗体又はポリクローナル抗体であってもよい。
測定ユニット20の一例であるフローサイトメーターは、本実施形態においては、各生物由来試料Sを分析することのできるセルアナライザである。図2に示したように、サンプルSの染色に利用された蛍光色素を励起可能な波長を有するレーザ光を、レーザ光源21からフローセル231を流れる染色された生物由来試料Sに対して射出する。また、フローサイトメーターに設けられた光検出器25は、レーザ光の照射された生物由来試料Sから放射される蛍光を、光電子増倍管251等の光検出器により検出する。なお、図2の例では1台のレーザ光源21しか描画されていないが、複数のレーザ光源が設けられていてもよい。
続いて、図4を参照しながら、本実施形態に係る情報処理装置10について、詳細に説明する。図4は、本実施形態に係る情報処理装置10の構成を示すブロック図である。
例えば、パルス波形解析部104は、第1のパルス波形の検出に用いられた波長帯とは異なる波長帯で検出された第2のパルス波形中のピークに関する情報に基づき、第1のパルス波形中のピークを特定することができる。そして、パルス波形解析部104は、第1のパルス波形において特定されたピークについて解析を行い、当該ピークのピーク位置に関連する情報を含む、第1のパルス波形の形状情報を得ることができる。第2のパルス波形中のピークに関する情報としては、例えば、ピークの位置、高さ、面積、幅等が挙げられる。
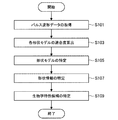
続いて、図18を参照しながら、本実施形態に係る情報処理方法の流れについて、その一例を簡単に説明する。図18は、第1の実施形態に係る情報処理方法の流れの一例を示したフローチャートである。
以上、図18を参照しながら、本実施形態に係る情報処理の流れの一例を簡単に説明した。
以下では、図19〜図21を参照しながら、本開示の第2の実施形態について詳細に説明する。
まず、図19を参照しながら、本実施形態に係る情報処理システムについて説明する。図19は、第2の実施形態に係る情報処理システムを示したブロック図である。図19に示すように、本実施形態に係る情報処理システム1Aは、主に測定ユニット20Aが分取部29を備えている点で、すなわち測定ユニット20が分取可能なセルソータである点で、第1の実施形態に係る情報処理システム1と相違する。以下、本実施形態の第1の実施形態との相違点を主として説明し、同様の事項については説明を省略する。
測定部28は、第1の実施形態における測定ユニット20に相当する。そして、測定部28は、測定サンプルSについての測定を行うとともに、測定後の測定サンプルSを分取部29に輸送する。
なお分取部29への指示は、決定された生物由来対象の生物学特性候補に基づいて行われてもよいし、形状情報の解析結果に基づいて行われてもよい。
続いて、図20、図21を参照しながら、本実施形態に係る情報処理方法の流れについて、その例を簡単に説明する。図20、図21は、第2の実施形態に係る情報処理方法の流れの一例を示したフローチャートである。なお、本実施形態に係る情報処理システム1Aは、分取部29を備えているため、本実施形態に係る情報処理方法は、分取方法の一部を構成する。
以上、図20および図21に基づいて、本開示の第2の実施形態に係る情報処理方法の流れについて説明した。
次に、図22を参照しながら、本開示の第1の実施形態に係る情報処理装置10のハードウェア構成について、詳細に説明する。図22は、本開示の第1の実施形態に係る情報処理装置10のハードウェア構成を説明するためのブロック図である。なお、本開示の第2の実施形態に係る情報処理装置10Aの構成は、情報処理装置10の構成と同様とすることができるため、以下、情報処理装置10について代表的に説明する。
(1) 移動する生物由来対象に対して光線を照射することにより検出されるパルス波形のデータに基づき前記パルス波形のピーク位置に関連する情報を特定する、パルス波形解析部と、
前記ピーク位置に関連する情報に基づいて前記生物由来対象の推定される特性候補を決定する、特性候補決定部と、
を備える情報処理装置。
(2) 前記ピーク位置に関連する情報は、前記パルス波形におけるピークの数を含む、(1)に記載の情報処理装置。
(3) 前記パルス波形が複数のピークを有する場合、前記ピーク位置に関連する情報は、複数の前記ピーク間の強度の比較を含む、(1)または(2)に記載の情報処理装置。
(4) 前記パルス波形が複数のピークを有する場合、前記ピーク位置に関連する情報は、複数の前記ピーク位置の比較を含む、(1)〜(3)のいずれか一項に記載の情報処理装置。
(5) 前記パルス波形解析部は、互いに異なる波長帯の複数の前記パルス波形について解析し、それぞれについての前記ピーク位置に関連する情報を特定する、(1)〜(4)のいずれか一項に記載の情報処理装置。
(6) 前記ピーク位置に関連する情報は、前記互いに異なる波長帯の複数の前記パルス波形の位置の比較を含む、(5)に記載の情報処理装置。
(7) 前記パルス波形解析部は、複数の所定の形状モデルから、前記パルス波形と関連する前記形状モデルを選択し、選択された前記形状モデルと前記パルス波形とを比較することにより、解析を行う、(1)〜(6)のいずれか一項に記載の情報処理装置。
(8) 前記パルス波形解析部は、第1のパルス波形の検出に用いられた波長帯とは異なる波長帯で検出された第2のパルス波形中のピークに基づき、第1のパルス波形中のピークを特定する、(1)〜(7)のいずれか一項に記載の情報処理装置。
(9) 前記パルス波形解析部は、前記パルス波形中の少なくとも1以上のピークを減衰させたベースラインを得、当該パルス波形と当該ベースラインとの比較に基づき当該パルス波形中の前記少なくとも1以上のピークを特定する、(1)〜(7)のいずれか一項に記載の情報処理装置。
(10) さらに、前記ピーク位置に関連する情報と前記特性候補とを関連付ける関連情報を記憶する記憶部を備える、(1)〜(9)のいずれか一項に記載の情報処理装置。
(11) さらに、前記特性候補と前記ピーク位置に関連する情報との関連を学習する、学習部を備える、(1)〜(10)のいずれか一項に記載の情報処理装置。
(12) 前記生物由来対象は、異方性を有する形状をなす、(1)〜(11)のいずれか一項に記載の情報処理装置。
(13) 推定された前記特性候補は、前記生物由来対象の分取のための情報として用いられる、(1)〜(12)のいずれか一項に記載の情報処理装置。
(14) 移動する生物由来対象に対して光線を照射することにより検出されるパルス波形のデータに基づき前記パルス波形のピーク位置に関連する情報を特定することと、
前記ピーク位置に関連する情報に基づいて前記生物由来対象の推定される特性候補を決定することと、
を含む、情報処理方法。
(15) 移動する生物由来対象に対して光線を照射し、パルス波形を検出するフローサイトメーターと、
前記パルス波形のデータに基づき前記パルス波形のピーク位置に関連する情報を特定するパルス波形解析部および前記ピーク位置に関連する情報に基づいて前記生物由来対象の推定される特性候補を決定する特性候補決定部を備える情報処理装置と、
を備える、情報処理システム。
(16) 前記フローサイトメーターは、前記生物由来対象を分取可能な分取部を備え、
前記分取部は、前記ピーク位置に関連する情報に応じて前記生物由来対象を分取するように構成されている、(15)に記載の情報処理システム。
10、10A 情報処理装置
20、20A 測定ユニット
21 レーザ光源
23 フロー系
231 フローセル
25 光検出器
251 光電子増倍管
253 ディテクタ
27 光学系
271 波長選択フィルタ
28 測定部
29 分取部
102 データ取得部
104 パルス波形解析部
106、106A 特性候補決定部
108 記憶部
110 学習部
112、112A 出力部
114 表示制御部
116 入力部
300、300A 細胞
301A、301B、302、303 抗原
304 蛍光色素
310 細胞核
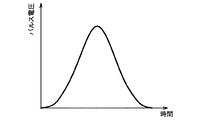
400、401、402 パルス波形
403 ベースライン
404 スパイクデータ
405 スパイク
410 ピーク
901 CPU
902 ROM
903 RAM
907 ホストバス
909 ブリッジ
911 外部バス
913 インターフェース
915 入力装置
917 出力装置
919 ストレージ装置
921 ドライブ
923 接続ポート
925 通信装置
927 リムーバブル記録媒体
929 外部接続機器
931 通信網
Claims (16)
- 移動する生物由来対象に対して光線を照射することにより検出されるパルス波形のデータに基づき、前記パルス波形の1パルスに含まれる時間軸上の位置が異なる複数のピークの情報を特定する、パルス波形解析部と、
前記特定された複数のピークのそれぞれの情報毎に前記生物由来対象の推定される特性候補を決定する、特性候補決定部と、
前記決定された特性候補を出力する出力部と、
を備える情報処理装置。 - 前記ピークの情報は、前記複数のピークの数を含む、請求項1に記載の情報処理装置。
- 前記ピークの情報は、前記複数のピーク間の強度を比較した情報を含む、請求項1に記載の情報処理装置。
- 前記ピークの情報は、前記複数のピークの時間軸上の位置を比較した情報を含む、請求項1に記載の情報処理装置。
- 前記パルス波形解析部は、互いに異なる波長帯の複数の前記パルス波形について解析し、複数の前記パルス波形に含まれる時間軸上の位置が異なる複数のピークの情報を特定する、請求項1に記載の情報処理装置。
- 前記ピークの情報は、前記互いに異なる波長帯の複数の前記パルス波形の時間軸上の位置を比較した情報を含む、請求項5に記載の情報処理装置。
- 前記パルス波形解析部は、複数の所定の形状モデルから、前記パルス波形と関連する前記形状モデルを選択し、選択された前記形状モデルと前記パルス波形とを比較することにより、解析を行う、請求項1に記載の情報処理装置。
- 前記パルス波形解析部は、第1のパルス波形の検出に用いられた波長帯とは異なる波長帯で検出された第2のパルス波形中のピークの情報に基づき、第1のパルス波形中のピークを特定する、請求項1に記載の情報処理装置。
- 前記パルス波形解析部は、前記パルス波形中の少なくとも1以上のピークを減衰させたベースラインを得、当該パルス波形と当該ベースラインとの比較に基づき当該パルス波形中の前記複数のピークを特定する、請求項1に記載の情報処理装置。
- さらに、前記ピークの情報と前記特性候補とを関連付ける関連データを記憶する記憶部を備える、請求項1に記載の情報処理装置。
- さらに、前記特性候補と前記ピークの情報との関連を学習する、学習部を備える、請求項1に記載の情報処理装置。
- 前記生物由来対象は、異方性を有する形状をなす、請求項1に記載の情報処理装置。
- 前記出力された前記特性候補は、前記生物由来対象の分取のための情報として用いられる、請求項1に記載の情報処理装置。
- 移動する生物由来対象に対して光線を照射することにより検出されるパルス波形のデータに基づき前記パルス波形の1パルスに含まれる時間軸上の位置が異なる複数のピークの情報を特定することと、
前記特定された複数のピークのそれぞれの情報毎に前記生物由来対象の推定される特性候補を決定することと、
前記決定された特性候補を出力することと、
を含む、情報処理方法。 - 移動する生物由来対象に対して光線を照射し、パルス波形を検出するフローサイトメーターと、
前記パルス波形のデータに基づき前記パルス波形の1パルスに含まれる時間軸上の位置が異なる複数のピークの情報を特定するパルス波形解析部、前記特定された複数のピークのそれぞれの情報毎に前記生物由来対象の推定される特性候補を決定する特性候補決定部および前記決定された特性候補を出力する出力部を備える情報処理装置と、
を備える、情報処理システム。 - 前記フローサイトメーターは、前記生物由来対象を分取可能な分取部を備え、
前記分取部は、前記複数のピークのそれぞれの情報に応じて前記生物由来対象を分取するように構成されている、請求項15に記載の情報処理システム。
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| PCT/JP2016/003449 WO2017046988A1 (en) | 2015-09-18 | 2016-07-25 | Information processing apparatus, information processing method, and information processing system |
| EP16750498.4A EP3300517B1 (en) | 2015-09-18 | 2016-07-25 | Information processing system comprising a flow cytometer, flow cytometer information processing method, and computer-readable storage medium for performing a flow cytometer information processing method |
| CN201680052528.0A CN108012553B (zh) | 2015-09-18 | 2016-07-25 | 信息处理设备、信息处理方法和信息处理系统 |
| US15/759,173 US11022537B2 (en) | 2015-09-18 | 2016-07-25 | Information processing apparatus, information processing method, and information processing system |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2015185107 | 2015-09-18 | ||
| JP2015185107 | 2015-09-18 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2017058361A JP2017058361A (ja) | 2017-03-23 |
| JP6790490B2 true JP6790490B2 (ja) | 2020-11-25 |
Family
ID=58391508
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016123226A Active JP6790490B2 (ja) | 2015-09-18 | 2016-06-22 | 情報処理装置、情報処理方法及び情報処理システム |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US11022537B2 (ja) |
| EP (1) | EP3300517B1 (ja) |
| JP (1) | JP6790490B2 (ja) |
| CN (1) | CN108012553B (ja) |
Families Citing this family (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3617691A4 (en) * | 2017-04-24 | 2020-05-13 | Sony Corporation | INFORMATION PROCESSING DEVICE, PARTICLE FRACTIONATION SYSTEM, PROGRAM AND PARTICLE FRACTIONATION METHOD |
| JP6928948B2 (ja) * | 2017-08-09 | 2021-09-01 | 学校法人日本大学 | 口臭判定装置及びプログラム |
| JP6872034B2 (ja) * | 2017-11-09 | 2021-05-19 | 富士通株式会社 | 波形解析装置 |
| EP4306931A3 (en) * | 2018-06-13 | 2024-02-07 | ThinkCyte K.K. | Methods and systems for cytometry |
| CN112368562A (zh) * | 2018-07-11 | 2021-02-12 | 香港大学 | 用于液滴的连续和定量收集的自动微流控系统 |
| JP7201297B2 (ja) * | 2018-09-26 | 2023-01-10 | シスメックス株式会社 | フローサイトメーター、データ送信方法及び情報処理システム |
| JP7280683B2 (ja) * | 2018-10-25 | 2023-05-24 | 株式会社日立ハイテク | 試料判別システム及びそれを用いた試料自動処理装置、並びに試料判別方法 |
| JP2020139824A (ja) | 2019-02-27 | 2020-09-03 | ソニー株式会社 | 微小粒子解析装置、解析装置、解析プログラム、および微小粒子解析システム |
| CN109827944A (zh) * | 2019-02-27 | 2019-05-31 | 山东省食品药品检验研究院 | 一种阿德福韦酯片的鉴别方法 |
| JP7367343B2 (ja) | 2019-05-28 | 2023-10-24 | ソニーグループ株式会社 | 分取システム、及び分取方法 |
| US11841373B2 (en) * | 2019-06-28 | 2023-12-12 | Canon Kabushiki Kaisha | Information processing apparatus, method for controlling information processing apparatus, and program |
| JP2021143988A (ja) * | 2020-03-13 | 2021-09-24 | ソニーグループ株式会社 | 粒子解析システムおよび粒子解析方法 |
| KR20230142732A (ko) * | 2021-02-08 | 2023-10-11 | 씨-스퀘어 바이오사이언스 게엠베하 | 미생물의 함량을 조정하기 위한 디바이스 및 방법 |
| CN113419020A (zh) * | 2021-06-30 | 2021-09-21 | 成都师范学院 | 糖化血红蛋白重叠峰识别方法、装置、系统、设备及介质 |
| CN117233053A (zh) * | 2023-11-13 | 2023-12-15 | 北京普能世纪科技有限公司 | 实现电解液监测的方法、系统、计算机存储介质及终端 |
Family Cites Families (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5452237A (en) * | 1994-02-28 | 1995-09-19 | Abbott Laboratories | Coincidence error correction system for particle counters |
| US6060322A (en) * | 1998-10-20 | 2000-05-09 | Coulter International Corp. | Method for identification of reticulated cells |
| CN1204267C (zh) * | 2000-05-05 | 2005-06-01 | 朱学军 | 一种检测细胞内核酸的方法和装置 |
| DK2305832T3 (da) | 2003-03-28 | 2022-05-23 | Inguran Llc | Fremgangsmåde til tilvejebringelse af kønssorteret dyresæd |
| WO2006103920A1 (ja) * | 2005-03-29 | 2006-10-05 | Sysmex Corporation | 癌・異型細胞および凝集粒子を弁別する方法および細胞分析装置 |
| CN1970788A (zh) * | 2005-11-23 | 2007-05-30 | 郑芳 | 流式细胞仪-细胞内分子探针技术 |
| US7457709B2 (en) * | 2005-12-20 | 2008-11-25 | Beckman Coulter, Inc. | Systems and methods for particle counting |
| US8209128B1 (en) * | 2007-02-21 | 2012-06-26 | Paul L. Gourley | Nanolaser spectroscopy and micro-optical resonators for detecting, analyzing, and manipulating bioparticles |
| CN101846626B (zh) * | 2010-05-24 | 2012-07-11 | 天津商业大学 | 一种利用流式细胞仪检测腹腔吞噬细胞活性的方法 |
| JP5856962B2 (ja) * | 2010-09-10 | 2016-02-10 | オリンパス株式会社 | 単一発光粒子の光強度を用いた光分析方法 |
| JP2013015357A (ja) * | 2011-07-01 | 2013-01-24 | Shimadzu Corp | フローサイトメータ |
| JP5712396B2 (ja) * | 2012-03-30 | 2015-05-07 | 公益財団法人神奈川科学技術アカデミー | イメージングセルソーター |
| ES2880609T3 (es) | 2013-03-14 | 2021-11-25 | Abbott Lab | Métodos para detectar eventos de muestras coincidentes |
| US10451482B2 (en) | 2014-02-14 | 2019-10-22 | Palo Alto Research Center Incorporated | Determination of color characteristics of objects using spatially modulated light |
-
2016
- 2016-06-22 JP JP2016123226A patent/JP6790490B2/ja active Active
- 2016-07-25 EP EP16750498.4A patent/EP3300517B1/en active Active
- 2016-07-25 US US15/759,173 patent/US11022537B2/en active Active
- 2016-07-25 CN CN201680052528.0A patent/CN108012553B/zh active Active
Also Published As
| Publication number | Publication date |
|---|---|
| EP3300517B1 (en) | 2020-11-25 |
| JP2017058361A (ja) | 2017-03-23 |
| CN108012553A (zh) | 2018-05-08 |
| CN108012553B (zh) | 2021-05-04 |
| US11022537B2 (en) | 2021-06-01 |
| EP3300517A1 (en) | 2018-04-04 |
| US20180259440A1 (en) | 2018-09-13 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6790490B2 (ja) | 情報処理装置、情報処理方法及び情報処理システム | |
| WO2017046988A1 (en) | Information processing apparatus, information processing method, and information processing system | |
| JP5870851B2 (ja) | 情報処理装置、情報処理方法、及びプログラム | |
| JP5834584B2 (ja) | 情報処理装置、情報処理方法、プログラム及び蛍光スペクトルの強度補正方法 | |
| Nolan et al. | Detection of platelet vesicles by flow cytometry | |
| US10061973B2 (en) | Method and apparatus for automated platelet identification within a whole blood sample from microscopy images | |
| Bagwell et al. | Automated data cleanup for mass cytometry | |
| JP7176697B2 (ja) | 細胞評価システム及び方法、細胞評価プログラム | |
| JP5425814B2 (ja) | サポートベクタマシンを用いてフローサイトメトリーデータを分析するための方法及びシステム | |
| US8128890B2 (en) | Methods and algorithms for cell enumeration in a low-cost cytometer | |
| EP2204643B1 (en) | Cell analysis apparatus and cell analysis method | |
| JP4921356B2 (ja) | 癌・異型細胞および凝集粒子を弁別する方法および細胞分析装置 | |
| EP2414536B1 (en) | Fluorescence cued raman identification of viable organisms | |
| WO2017191699A1 (ja) | 情報処理装置、情報処理方法、プログラム及び情報処理システム | |
| WO2005008254A1 (ja) | 臨床検査分析装置、臨床検査分析方法およびその方法をコンピュータに実行させるプログラム | |
| WO2011106402A1 (en) | Method and system for detecting fluorochromes in a flow cytometer | |
| JP4749637B2 (ja) | 画像解析方法、装置、及び記録媒体 | |
| JP2023179666A (ja) | 分取システム、及び分取方法 | |
| EP4257974A1 (en) | Sample analysis method, sample analyzer, and computer-readable storage medium | |
| JPWO2019031048A1 (ja) | 情報処理装置、情報処理方法及びプログラム | |
| Lerner et al. | GELFISH–Graphical environment for labelling fluorescence in‐situ hybridization images | |
| JP2023550130A (ja) | 機械学習分析のためのサイトメトリックデータの最適なスケーリング方法及びそのシステム | |
| Beal | Flow Cytometry Quantification of Transient Transfections in Mammalian Cells | |
| JP2007101412A (ja) | フローサイトメトリーを用いた物質の測定方法及びフローサイトメトリーにおける測定用微粒子 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20190208 |
|
| RD03 | Notification of appointment of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7423 Effective date: 20190214 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20190222 |
|
| RD02 | Notification of acceptance of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7422 Effective date: 20190515 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20190522 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20190610 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20200728 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200918 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20201006 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20201019 |
|
| R151 | Written notification of patent or utility model registration |
Ref document number: 6790490 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R151 |