JP5543963B2 - エウスタキオ管機能障害を有する哺乳動物の治療方法 - Google Patents
エウスタキオ管機能障害を有する哺乳動物の治療方法 Download PDFInfo
- Publication number
- JP5543963B2 JP5543963B2 JP2011510783A JP2011510783A JP5543963B2 JP 5543963 B2 JP5543963 B2 JP 5543963B2 JP 2011510783 A JP2011510783 A JP 2011510783A JP 2011510783 A JP2011510783 A JP 2011510783A JP 5543963 B2 JP5543963 B2 JP 5543963B2
- Authority
- JP
- Japan
- Prior art keywords
- eustachian tube
- betahistine
- otitis media
- topical composition
- composition according
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 206010015543 Eustachian tube dysfunction Diseases 0.000 title claims description 31
- 238000000034 method Methods 0.000 title description 11
- 241000124008 Mammalia Species 0.000 title description 3
- UUQMNUMQCIQDMZ-UHFFFAOYSA-N betahistine Chemical compound CNCCC1=CC=CC=N1 UUQMNUMQCIQDMZ-UHFFFAOYSA-N 0.000 claims description 69
- 229960004536 betahistine Drugs 0.000 claims description 59
- 210000002388 eustachian tube Anatomy 0.000 claims description 50
- 239000000203 mixture Substances 0.000 claims description 39
- 206010033078 Otitis media Diseases 0.000 claims description 32
- 230000000699 topical effect Effects 0.000 claims description 31
- 210000001989 nasopharynx Anatomy 0.000 claims description 14
- 208000022760 infectious otitis media Diseases 0.000 claims description 13
- 239000003814 drug Substances 0.000 claims description 9
- 239000012458 free base Substances 0.000 claims description 6
- 150000003839 salts Chemical class 0.000 claims description 6
- 239000000850 decongestant Substances 0.000 claims description 5
- 230000001225 therapeutic effect Effects 0.000 claims description 5
- 239000003085 diluting agent Substances 0.000 claims description 2
- 239000003172 expectorant agent Substances 0.000 claims description 2
- 229940066491 mucolytics Drugs 0.000 claims description 2
- 239000007922 nasal spray Substances 0.000 claims description 2
- 229940097496 nasal spray Drugs 0.000 claims description 2
- 239000000546 pharmaceutical excipient Substances 0.000 claims description 2
- 239000013543 active substance Substances 0.000 claims 2
- 239000003937 drug carrier Substances 0.000 claims 1
- 239000007923 nasal drop Substances 0.000 claims 1
- 210000000959 ear middle Anatomy 0.000 description 22
- 230000000694 effects Effects 0.000 description 17
- NTYJJOPFIAHURM-UHFFFAOYSA-N Histamine Chemical compound NCCC1=CN=CN1 NTYJJOPFIAHURM-UHFFFAOYSA-N 0.000 description 14
- 241001465754 Metazoa Species 0.000 description 14
- 230000006870 function Effects 0.000 description 14
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 9
- -1 dihydrochloride) Chemical compound 0.000 description 9
- 208000024891 symptom Diseases 0.000 description 9
- 230000037396 body weight Effects 0.000 description 8
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 7
- 239000012530 fluid Substances 0.000 description 7
- 229960001340 histamine Drugs 0.000 description 7
- 238000005259 measurement Methods 0.000 description 7
- 239000000843 powder Substances 0.000 description 7
- 238000012360 testing method Methods 0.000 description 7
- 206010011878 Deafness Diseases 0.000 description 6
- 208000027530 Meniere disease Diseases 0.000 description 6
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 6
- 238000002474 experimental method Methods 0.000 description 6
- 238000009472 formulation Methods 0.000 description 6
- 230000010370 hearing loss Effects 0.000 description 6
- 231100000888 hearing loss Toxicity 0.000 description 6
- 208000016354 hearing loss disease Diseases 0.000 description 6
- XVDFMHARQUBJRE-UHFFFAOYSA-N hydron;n-methyl-2-pyridin-2-ylethanamine;dichloride Chemical compound Cl.Cl.CNCCC1=CC=CC=N1 XVDFMHARQUBJRE-UHFFFAOYSA-N 0.000 description 6
- 241000700159 Rattus Species 0.000 description 5
- 230000009471 action Effects 0.000 description 5
- 239000006196 drop Substances 0.000 description 5
- 229940002612 prodrug Drugs 0.000 description 5
- 239000000651 prodrug Substances 0.000 description 5
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 4
- 239000002585 base Substances 0.000 description 4
- 230000008859 change Effects 0.000 description 4
- 238000006243 chemical reaction Methods 0.000 description 4
- 150000001875 compounds Chemical class 0.000 description 4
- 229940124581 decongestants Drugs 0.000 description 4
- 208000002173 dizziness Diseases 0.000 description 4
- 239000011780 sodium chloride Substances 0.000 description 4
- 239000000243 solution Substances 0.000 description 4
- 239000012453 solvate Substances 0.000 description 4
- 239000007921 spray Substances 0.000 description 4
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 4
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- 206010015544 Eustachian tube obstruction Diseases 0.000 description 3
- 206010020751 Hypersensitivity Diseases 0.000 description 3
- 206010028813 Nausea Diseases 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- 206010047700 Vomiting Diseases 0.000 description 3
- 239000004480 active ingredient Substances 0.000 description 3
- 229940125715 antihistaminic agent Drugs 0.000 description 3
- 239000000739 antihistaminic agent Substances 0.000 description 3
- 239000003795 chemical substances by application Substances 0.000 description 3
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 3
- 239000006071 cream Substances 0.000 description 3
- 230000007423 decrease Effects 0.000 description 3
- 201000010099 disease Diseases 0.000 description 3
- 208000035475 disorder Diseases 0.000 description 3
- 239000002552 dosage form Substances 0.000 description 3
- 210000003027 ear inner Anatomy 0.000 description 3
- 239000000796 flavoring agent Substances 0.000 description 3
- 239000000499 gel Substances 0.000 description 3
- 210000003801 laryngeal nerve Anatomy 0.000 description 3
- 238000004519 manufacturing process Methods 0.000 description 3
- 230000008693 nausea Effects 0.000 description 3
- 239000002674 ointment Substances 0.000 description 3
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 3
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 3
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 3
- 230000011514 reflex Effects 0.000 description 3
- 239000002904 solvent Substances 0.000 description 3
- 239000002562 thickening agent Substances 0.000 description 3
- 238000011200 topical administration Methods 0.000 description 3
- 210000003454 tympanic membrane Anatomy 0.000 description 3
- 230000008673 vomiting Effects 0.000 description 3
- OMDMTHRBGUBUCO-IUCAKERBSA-N (1s,5s)-5-(2-hydroxypropan-2-yl)-2-methylcyclohex-2-en-1-ol Chemical compound CC1=CC[C@H](C(C)(C)O)C[C@@H]1O OMDMTHRBGUBUCO-IUCAKERBSA-N 0.000 description 2
- GVJHHUAWPYXKBD-UHFFFAOYSA-N (±)-α-Tocopherol Chemical compound OC1=C(C)C(C)=C2OC(CCCC(C)CCCC(C)CCCC(C)C)(C)CCC2=C1C GVJHHUAWPYXKBD-UHFFFAOYSA-N 0.000 description 2
- VBICKXHEKHSIBG-UHFFFAOYSA-N 1-monostearoylglycerol Chemical compound CCCCCCCCCCCCCCCCCC(=O)OCC(O)CO VBICKXHEKHSIBG-UHFFFAOYSA-N 0.000 description 2
- IZHVBANLECCAGF-UHFFFAOYSA-N 2-hydroxy-3-(octadecanoyloxy)propyl octadecanoate Chemical compound CCCCCCCCCCCCCCCCCC(=O)OCC(O)COC(=O)CCCCCCCCCCCCCCCCC IZHVBANLECCAGF-UHFFFAOYSA-N 0.000 description 2
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 2
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 2
- 206010014020 Ear pain Diseases 0.000 description 2
- JVTAAEKCZFNVCJ-UHFFFAOYSA-M Lactate Chemical compound CC(O)C([O-])=O JVTAAEKCZFNVCJ-UHFFFAOYSA-M 0.000 description 2
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 2
- 238000009825 accumulation Methods 0.000 description 2
- 239000000443 aerosol Substances 0.000 description 2
- 208000026935 allergic disease Diseases 0.000 description 2
- 230000007815 allergy Effects 0.000 description 2
- 235000010323 ascorbic acid Nutrition 0.000 description 2
- 239000011668 ascorbic acid Substances 0.000 description 2
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 2
- 230000009286 beneficial effect Effects 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- 239000000872 buffer Substances 0.000 description 2
- 239000000969 carrier Substances 0.000 description 2
- 239000011248 coating agent Substances 0.000 description 2
- 230000009189 diving Effects 0.000 description 2
- 229940079593 drug Drugs 0.000 description 2
- 230000004064 dysfunction Effects 0.000 description 2
- 210000000416 exudates and transudate Anatomy 0.000 description 2
- 235000013355 food flavoring agent Nutrition 0.000 description 2
- 235000003599 food sweetener Nutrition 0.000 description 2
- 208000015181 infectious disease Diseases 0.000 description 2
- 230000005764 inhibitory process Effects 0.000 description 2
- 238000003780 insertion Methods 0.000 description 2
- 230000037431 insertion Effects 0.000 description 2
- 239000008101 lactose Substances 0.000 description 2
- 230000008140 language development Effects 0.000 description 2
- 239000006210 lotion Substances 0.000 description 2
- 239000000314 lubricant Substances 0.000 description 2
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 2
- 230000014759 maintenance of location Effects 0.000 description 2
- 239000000463 material Substances 0.000 description 2
- 230000007246 mechanism Effects 0.000 description 2
- LXCFILQKKLGQFO-UHFFFAOYSA-N methylparaben Chemical compound COC(=O)C1=CC=C(O)C=C1 LXCFILQKKLGQFO-UHFFFAOYSA-N 0.000 description 2
- 239000001788 mono and diglycerides of fatty acids Substances 0.000 description 2
- 210000003928 nasal cavity Anatomy 0.000 description 2
- 210000002850 nasal mucosa Anatomy 0.000 description 2
- 210000001331 nose Anatomy 0.000 description 2
- 208000005923 otitis media with effusion Diseases 0.000 description 2
- 239000001301 oxygen Substances 0.000 description 2
- 229910052760 oxygen Inorganic materials 0.000 description 2
- WYWIFABBXFUGLM-UHFFFAOYSA-N oxymetazoline Chemical compound CC1=CC(C(C)(C)C)=C(O)C(C)=C1CC1=NCCN1 WYWIFABBXFUGLM-UHFFFAOYSA-N 0.000 description 2
- 239000002245 particle Substances 0.000 description 2
- 239000003755 preservative agent Substances 0.000 description 2
- 230000008569 process Effects 0.000 description 2
- QELSKZZBTMNZEB-UHFFFAOYSA-N propylparaben Chemical compound CCCOC(=O)C1=CC=C(O)C=C1 QELSKZZBTMNZEB-UHFFFAOYSA-N 0.000 description 2
- 230000004044 response Effects 0.000 description 2
- 208000024036 serous otitis media Diseases 0.000 description 2
- 150000003431 steroids Chemical class 0.000 description 2
- 239000004094 surface-active agent Substances 0.000 description 2
- 239000000725 suspension Substances 0.000 description 2
- 239000003765 sweetening agent Substances 0.000 description 2
- 230000009885 systemic effect Effects 0.000 description 2
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 2
- 239000001993 wax Substances 0.000 description 2
- GVJHHUAWPYXKBD-IEOSBIPESA-N α-tocopherol Chemical compound OC1=C(C)C(C)=C2O[C@@](CCC[C@H](C)CCC[C@H](C)CCCC(C)C)(C)CCC2=C1C GVJHHUAWPYXKBD-IEOSBIPESA-N 0.000 description 2
- DDMOUSALMHHKOS-UHFFFAOYSA-N 1,2-dichloro-1,1,2,2-tetrafluoroethane Chemical compound FC(F)(Cl)C(F)(F)Cl DDMOUSALMHHKOS-UHFFFAOYSA-N 0.000 description 1
- IIZPXYDJLKNOIY-JXPKJXOSSA-N 1-palmitoyl-2-arachidonoyl-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCC\C=C/C\C=C/C\C=C/C\C=C/CCCCC IIZPXYDJLKNOIY-JXPKJXOSSA-N 0.000 description 1
- SMZOUWXMTYCWNB-UHFFFAOYSA-N 2-(2-methoxy-5-methylphenyl)ethanamine Chemical compound COC1=CC=C(C)C=C1CCN SMZOUWXMTYCWNB-UHFFFAOYSA-N 0.000 description 1
- NIXOWILDQLNWCW-UHFFFAOYSA-N 2-Propenoic acid Natural products OC(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 1
- LBLYYCQCTBFVLH-UHFFFAOYSA-M 2-methylbenzenesulfonate Chemical compound CC1=CC=CC=C1S([O-])(=O)=O LBLYYCQCTBFVLH-UHFFFAOYSA-M 0.000 description 1
- LEACJMVNYZDSKR-UHFFFAOYSA-N 2-octyldodecan-1-ol Chemical compound CCCCCCCCCCC(CO)CCCCCCCC LEACJMVNYZDSKR-UHFFFAOYSA-N 0.000 description 1
- 229920001817 Agar Polymers 0.000 description 1
- 206010001497 Agitation Diseases 0.000 description 1
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 1
- 108010011485 Aspartame Proteins 0.000 description 1
- 208000035143 Bacterial infection Diseases 0.000 description 1
- 241000167854 Bourreria succulenta Species 0.000 description 1
- 239000004322 Butylated hydroxytoluene Substances 0.000 description 1
- NLZUEZXRPGMBCV-UHFFFAOYSA-N Butylhydroxytoluene Chemical compound CC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 NLZUEZXRPGMBCV-UHFFFAOYSA-N 0.000 description 1
- KRKNYBCHXYNGOX-UHFFFAOYSA-K Citrate Chemical compound [O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O KRKNYBCHXYNGOX-UHFFFAOYSA-K 0.000 description 1
- 206010009269 Cleft palate Diseases 0.000 description 1
- 229920002261 Corn starch Polymers 0.000 description 1
- 229920000858 Cyclodextrin Polymers 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- 239000004338 Dichlorodifluoromethane Substances 0.000 description 1
- 208000010201 Exanthema Diseases 0.000 description 1
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 108010068370 Glutens Proteins 0.000 description 1
- 206010019233 Headaches Diseases 0.000 description 1
- 102000004384 Histamine H3 receptors Human genes 0.000 description 1
- 108090000981 Histamine H3 receptors Proteins 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-N Hydrogen bromide Chemical compound Br CPELXLSAUQHCOX-UHFFFAOYSA-N 0.000 description 1
- 206010061218 Inflammation Diseases 0.000 description 1
- PWKSKIMOESPYIA-BYPYZUCNSA-N L-N-acetyl-Cysteine Chemical compound CC(=O)N[C@@H](CS)C(O)=O PWKSKIMOESPYIA-BYPYZUCNSA-N 0.000 description 1
- OFOBLEOULBTSOW-UHFFFAOYSA-L Malonate Chemical compound [O-]C(=O)CC([O-])=O OFOBLEOULBTSOW-UHFFFAOYSA-L 0.000 description 1
- XOGTZOOQQBDUSI-UHFFFAOYSA-M Mesna Chemical compound [Na+].[O-]S(=O)(=O)CCS XOGTZOOQQBDUSI-UHFFFAOYSA-M 0.000 description 1
- CERQOIWHTDAKMF-UHFFFAOYSA-N Methacrylic acid Chemical compound CC(=C)C(O)=O CERQOIWHTDAKMF-UHFFFAOYSA-N 0.000 description 1
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 1
- 229920000881 Modified starch Polymers 0.000 description 1
- HSHXDCVZWHOWCS-UHFFFAOYSA-N N'-hexadecylthiophene-2-carbohydrazide Chemical compound CCCCCCCCCCCCCCCCNNC(=O)c1cccs1 HSHXDCVZWHOWCS-UHFFFAOYSA-N 0.000 description 1
- 150000001204 N-oxides Chemical class 0.000 description 1
- 208000000592 Nasal Polyps Diseases 0.000 description 1
- 206010028980 Neoplasm Diseases 0.000 description 1
- 208000008589 Obesity Diseases 0.000 description 1
- 206010030111 Oedema mucosal Diseases 0.000 description 1
- 208000002193 Pain Diseases 0.000 description 1
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 1
- 229920001214 Polysorbate 60 Polymers 0.000 description 1
- 241001282135 Poromitra oscitans Species 0.000 description 1
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 1
- 208000003251 Pruritus Diseases 0.000 description 1
- 206010037660 Pyrexia Diseases 0.000 description 1
- 206010057190 Respiratory tract infections Diseases 0.000 description 1
- 240000007651 Rubus glaucus Species 0.000 description 1
- 235000011034 Rubus glaucus Nutrition 0.000 description 1
- 235000009122 Rubus idaeus Nutrition 0.000 description 1
- GBFLZEXEOZUWRN-VKHMYHEASA-N S-carboxymethyl-L-cysteine Chemical compound OC(=O)[C@@H](N)CSCC(O)=O GBFLZEXEOZUWRN-VKHMYHEASA-N 0.000 description 1
- 101100149312 Saccharomyces cerevisiae (strain ATCC 204508 / S288c) SER1 gene Proteins 0.000 description 1
- 229920001800 Shellac Polymers 0.000 description 1
- DWAQJAXMDSEUJJ-UHFFFAOYSA-M Sodium bisulfite Chemical compound [Na+].OS([O-])=O DWAQJAXMDSEUJJ-UHFFFAOYSA-M 0.000 description 1
- BCKXLBQYZLBQEK-KVVVOXFISA-M Sodium oleate Chemical compound [Na+].CCCCCCCC\C=C/CCCCCCCC([O-])=O BCKXLBQYZLBQEK-KVVVOXFISA-M 0.000 description 1
- HVUMOYIDDBPOLL-XWVZOOPGSA-N Sorbitan monostearate Chemical compound CCCCCCCCCCCCCCCCCC(=O)OC[C@@H](O)[C@H]1OC[C@H](O)[C@H]1O HVUMOYIDDBPOLL-XWVZOOPGSA-N 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- 235000021355 Stearic acid Nutrition 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- 208000009205 Tinnitus Diseases 0.000 description 1
- YTGJWQPHMWSCST-UHFFFAOYSA-N Tiopronin Chemical compound CC(S)C(=O)NCC(O)=O YTGJWQPHMWSCST-UHFFFAOYSA-N 0.000 description 1
- 206010046306 Upper respiratory tract infection Diseases 0.000 description 1
- 208000024780 Urticaria Diseases 0.000 description 1
- 208000036142 Viral infection Diseases 0.000 description 1
- 229930003427 Vitamin E Natural products 0.000 description 1
- 206010048232 Yawning Diseases 0.000 description 1
- 229920002494 Zein Polymers 0.000 description 1
- 206010000059 abdominal discomfort Diseases 0.000 description 1
- 239000002250 absorbent Substances 0.000 description 1
- 229960004308 acetylcysteine Drugs 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 230000001154 acute effect Effects 0.000 description 1
- 239000008272 agar Substances 0.000 description 1
- 229940023476 agar Drugs 0.000 description 1
- 235000010419 agar Nutrition 0.000 description 1
- 239000000556 agonist Substances 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- 239000000783 alginic acid Substances 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- 229960001126 alginic acid Drugs 0.000 description 1
- 150000004781 alginic acids Chemical class 0.000 description 1
- 239000013566 allergen Substances 0.000 description 1
- 229940087168 alpha tocopherol Drugs 0.000 description 1
- 150000001408 amides Chemical class 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 229940121375 antifungal agent Drugs 0.000 description 1
- 239000003429 antifungal agent Substances 0.000 description 1
- 229940072107 ascorbate Drugs 0.000 description 1
- 229960005070 ascorbic acid Drugs 0.000 description 1
- IAOZJIPTCAWIRG-QWRGUYRKSA-N aspartame Chemical compound OC(=O)C[C@H](N)C(=O)N[C@H](C(=O)OC)CC1=CC=CC=C1 IAOZJIPTCAWIRG-QWRGUYRKSA-N 0.000 description 1
- 239000000605 aspartame Substances 0.000 description 1
- 235000010357 aspartame Nutrition 0.000 description 1
- 229960003438 aspartame Drugs 0.000 description 1
- 239000012298 atmosphere Substances 0.000 description 1
- 238000000889 atomisation Methods 0.000 description 1
- 208000022362 bacterial infectious disease Diseases 0.000 description 1
- 230000003542 behavioural effect Effects 0.000 description 1
- 239000000440 bentonite Substances 0.000 description 1
- 229910000278 bentonite Inorganic materials 0.000 description 1
- 229940092782 bentonite Drugs 0.000 description 1
- 235000012216 bentonite Nutrition 0.000 description 1
- SVPXDRXYRYOSEX-UHFFFAOYSA-N bentoquatam Chemical compound O.O=[Si]=O.O=[Al]O[Al]=O SVPXDRXYRYOSEX-UHFFFAOYSA-N 0.000 description 1
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 230000000975 bioactive effect Effects 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 210000000988 bone and bone Anatomy 0.000 description 1
- 229960003870 bromhexine Drugs 0.000 description 1
- OJGDCBLYJGHCIH-UHFFFAOYSA-N bromhexine Chemical compound C1CCCCC1N(C)CC1=CC(Br)=CC(Br)=C1N OJGDCBLYJGHCIH-UHFFFAOYSA-N 0.000 description 1
- 239000006172 buffering agent Substances 0.000 description 1
- 235000010354 butylated hydroxytoluene Nutrition 0.000 description 1
- 229960004399 carbocisteine Drugs 0.000 description 1
- 239000001569 carbon dioxide Substances 0.000 description 1
- 229910002092 carbon dioxide Inorganic materials 0.000 description 1
- 229960004424 carbon dioxide Drugs 0.000 description 1
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 1
- 210000000845 cartilage Anatomy 0.000 description 1
- 229940081733 cetearyl alcohol Drugs 0.000 description 1
- 235000019693 cherries Nutrition 0.000 description 1
- 230000001055 chewing effect Effects 0.000 description 1
- KYKAJFCTULSVSH-UHFFFAOYSA-N chloro(fluoro)methane Chemical compound F[C]Cl KYKAJFCTULSVSH-UHFFFAOYSA-N 0.000 description 1
- 230000001684 chronic effect Effects 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 238000011109 contamination Methods 0.000 description 1
- 229920001577 copolymer Polymers 0.000 description 1
- 239000008120 corn starch Substances 0.000 description 1
- KWGRBVOPPLSCSI-UHFFFAOYSA-N d-ephedrine Natural products CNC(C)C(O)C1=CC=CC=C1 KWGRBVOPPLSCSI-UHFFFAOYSA-N 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 230000001934 delay Effects 0.000 description 1
- 230000006866 deterioration Effects 0.000 description 1
- PXBRQCKWGAHEHS-UHFFFAOYSA-N dichlorodifluoromethane Chemical compound FC(F)(Cl)Cl PXBRQCKWGAHEHS-UHFFFAOYSA-N 0.000 description 1
- 235000019404 dichlorodifluoromethane Nutrition 0.000 description 1
- 229940042935 dichlorodifluoromethane Drugs 0.000 description 1
- 229940087091 dichlorotetrafluoroethane Drugs 0.000 description 1
- 239000007884 disintegrant Substances 0.000 description 1
- 239000002270 dispersing agent Substances 0.000 description 1
- 239000002612 dispersion medium Substances 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- DLNKOYKMWOXYQA-UHFFFAOYSA-N dl-pseudophenylpropanolamine Natural products CC(N)C(O)C1=CC=CC=C1 DLNKOYKMWOXYQA-UHFFFAOYSA-N 0.000 description 1
- 229960001700 domiodol Drugs 0.000 description 1
- NEIPZWZQHXCYDV-UHFFFAOYSA-N domiodol Chemical compound OCC1COC(CI)O1 NEIPZWZQHXCYDV-UHFFFAOYSA-N 0.000 description 1
- 108010067396 dornase alfa Proteins 0.000 description 1
- 231100000673 dose–response relationship Toxicity 0.000 description 1
- 210000000613 ear canal Anatomy 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 239000008387 emulsifying waxe Substances 0.000 description 1
- 229960002561 eprazinone Drugs 0.000 description 1
- BSHWLCACYCVCJE-UHFFFAOYSA-N eprazinone Chemical compound C=1C=CC=CC=1C(OCC)CN(CC1)CCN1CC(C)C(=O)C1=CC=CC=C1 BSHWLCACYCVCJE-UHFFFAOYSA-N 0.000 description 1
- 229960003262 erdosteine Drugs 0.000 description 1
- QGFORSXNKQLDNO-UHFFFAOYSA-N erdosteine Chemical compound OC(=O)CSCC(=O)NC1CCSC1=O QGFORSXNKQLDNO-UHFFFAOYSA-N 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- 201000005884 exanthem Diseases 0.000 description 1
- 230000029142 excretion Effects 0.000 description 1
- 150000002191 fatty alcohols Chemical class 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- 235000019634 flavors Nutrition 0.000 description 1
- WIGCFUFOHFEKBI-UHFFFAOYSA-N gamma-tocopherol Natural products CC(C)CCCC(C)CCCC(C)CCCC1CCC2C(C)C(O)C(C)C(C)C2O1 WIGCFUFOHFEKBI-UHFFFAOYSA-N 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 239000007903 gelatin capsule Substances 0.000 description 1
- 239000003349 gelling agent Substances 0.000 description 1
- 230000000762 glandular Effects 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 229960001031 glucose Drugs 0.000 description 1
- 235000001727 glucose Nutrition 0.000 description 1
- 235000021312 gluten Nutrition 0.000 description 1
- 229940074045 glyceryl distearate Drugs 0.000 description 1
- 229940075507 glyceryl monostearate Drugs 0.000 description 1
- 210000003128 head Anatomy 0.000 description 1
- 231100000869 headache Toxicity 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 230000005802 health problem Effects 0.000 description 1
- 239000003395 histamine H3 receptor antagonist Substances 0.000 description 1
- 239000001866 hydroxypropyl methyl cellulose Substances 0.000 description 1
- 235000010979 hydroxypropyl methyl cellulose Nutrition 0.000 description 1
- 229920003088 hydroxypropyl methyl cellulose Polymers 0.000 description 1
- 238000001727 in vivo Methods 0.000 description 1
- 230000006698 induction Effects 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- 206010022000 influenza Diseases 0.000 description 1
- 239000007928 intraperitoneal injection Substances 0.000 description 1
- 239000007951 isotonicity adjuster Substances 0.000 description 1
- 229960001375 lactose Drugs 0.000 description 1
- 239000000787 lecithin Substances 0.000 description 1
- 235000010445 lecithin Nutrition 0.000 description 1
- 229940067606 lecithin Drugs 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 1
- 230000010534 mechanism of action Effects 0.000 description 1
- 239000001525 mentha piperita l. herb oil Substances 0.000 description 1
- 229960004635 mesna Drugs 0.000 description 1
- 229920000609 methyl cellulose Polymers 0.000 description 1
- 239000004292 methyl p-hydroxybenzoate Substances 0.000 description 1
- 235000010270 methyl p-hydroxybenzoate Nutrition 0.000 description 1
- OSWPMRLSEDHDFF-UHFFFAOYSA-N methyl salicylate Chemical compound COC(=O)C1=CC=CC=C1O OSWPMRLSEDHDFF-UHFFFAOYSA-N 0.000 description 1
- 239000001923 methylcellulose Substances 0.000 description 1
- 235000010981 methylcellulose Nutrition 0.000 description 1
- 229960002216 methylparaben Drugs 0.000 description 1
- 239000002480 mineral oil Substances 0.000 description 1
- 235000010446 mineral oil Nutrition 0.000 description 1
- 150000007522 mineralic acids Chemical class 0.000 description 1
- 235000019426 modified starch Nutrition 0.000 description 1
- 210000004877 mucosa Anatomy 0.000 description 1
- 210000004400 mucous membrane Anatomy 0.000 description 1
- 210000003097 mucus Anatomy 0.000 description 1
- 210000001640 nerve ending Anatomy 0.000 description 1
- 230000001537 neural effect Effects 0.000 description 1
- 230000003957 neurotransmitter release Effects 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- 125000004433 nitrogen atom Chemical group N* 0.000 description 1
- 230000003040 nociceptive effect Effects 0.000 description 1
- 235000020824 obesity Nutrition 0.000 description 1
- GLDOVTGHNKAZLK-UHFFFAOYSA-N octadecan-1-ol Chemical compound CCCCCCCCCCCCCCCCCCO GLDOVTGHNKAZLK-UHFFFAOYSA-N 0.000 description 1
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 1
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 1
- 210000000056 organ Anatomy 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 229960001528 oxymetazoline Drugs 0.000 description 1
- 230000001734 parasympathetic effect Effects 0.000 description 1
- 239000006072 paste Substances 0.000 description 1
- 230000001575 pathological effect Effects 0.000 description 1
- 235000019477 peppermint oil Nutrition 0.000 description 1
- 230000002093 peripheral effect Effects 0.000 description 1
- 230000002085 persistent effect Effects 0.000 description 1
- WVDDGKGOMKODPV-ZQBYOMGUSA-N phenyl(114C)methanol Chemical compound O[14CH2]C1=CC=CC=C1 WVDDGKGOMKODPV-ZQBYOMGUSA-N 0.000 description 1
- 229960001802 phenylephrine Drugs 0.000 description 1
- SONNWYBIRXJNDC-VIFPVBQESA-N phenylephrine Chemical compound CNC[C@H](O)C1=CC=CC(O)=C1 SONNWYBIRXJNDC-VIFPVBQESA-N 0.000 description 1
- DLNKOYKMWOXYQA-APPZFPTMSA-N phenylpropanolamine Chemical compound C[C@@H](N)[C@H](O)C1=CC=CC=C1 DLNKOYKMWOXYQA-APPZFPTMSA-N 0.000 description 1
- 229960000395 phenylpropanolamine Drugs 0.000 description 1
- 239000002504 physiological saline solution Substances 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 239000001818 polyoxyethylene sorbitan monostearate Substances 0.000 description 1
- 235000010989 polyoxyethylene sorbitan monostearate Nutrition 0.000 description 1
- 229920001451 polypropylene glycol Polymers 0.000 description 1
- 229940113124 polysorbate 60 Drugs 0.000 description 1
- 239000003380 propellant Substances 0.000 description 1
- 230000000069 prophylactic effect Effects 0.000 description 1
- 235000010232 propyl p-hydroxybenzoate Nutrition 0.000 description 1
- 239000004405 propyl p-hydroxybenzoate Substances 0.000 description 1
- 229960003415 propylparaben Drugs 0.000 description 1
- KWGRBVOPPLSCSI-WCBMZHEXSA-N pseudoephedrine Chemical compound CN[C@@H](C)[C@@H](O)C1=CC=CC=C1 KWGRBVOPPLSCSI-WCBMZHEXSA-N 0.000 description 1
- 229960003908 pseudoephedrine Drugs 0.000 description 1
- 206010037844 rash Diseases 0.000 description 1
- 238000011552 rat model Methods 0.000 description 1
- 102000005962 receptors Human genes 0.000 description 1
- 108020003175 receptors Proteins 0.000 description 1
- 210000002345 respiratory system Anatomy 0.000 description 1
- 208000020029 respiratory tract infectious disease Diseases 0.000 description 1
- CVHZOJJKTDOEJC-UHFFFAOYSA-N saccharin Chemical compound C1=CC=C2C(=O)NS(=O)(=O)C2=C1 CVHZOJJKTDOEJC-UHFFFAOYSA-N 0.000 description 1
- 235000019204 saccharin Nutrition 0.000 description 1
- 229940081974 saccharin Drugs 0.000 description 1
- 239000000901 saccharin and its Na,K and Ca salt Substances 0.000 description 1
- HFHDHCJBZVLPGP-UHFFFAOYSA-N schardinger α-dextrin Chemical compound O1C(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(O)C2O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC2C(O)C(O)C1OC2CO HFHDHCJBZVLPGP-UHFFFAOYSA-N 0.000 description 1
- 230000028327 secretion Effects 0.000 description 1
- 239000004208 shellac Substances 0.000 description 1
- ZLGIYFNHBLSMPS-ATJNOEHPSA-N shellac Chemical compound OCCCCCC(O)C(O)CCCCCCCC(O)=O.C1C23[C@H](C(O)=O)CCC2[C@](C)(CO)[C@@H]1C(C(O)=O)=C[C@@H]3O ZLGIYFNHBLSMPS-ATJNOEHPSA-N 0.000 description 1
- 229940113147 shellac Drugs 0.000 description 1
- 235000013874 shellac Nutrition 0.000 description 1
- 231100000046 skin rash Toxicity 0.000 description 1
- 229960000230 sobrerol Drugs 0.000 description 1
- WXMKPNITSTVMEF-UHFFFAOYSA-M sodium benzoate Chemical compound [Na+].[O-]C(=O)C1=CC=CC=C1 WXMKPNITSTVMEF-UHFFFAOYSA-M 0.000 description 1
- 239000004299 sodium benzoate Substances 0.000 description 1
- 235000010234 sodium benzoate Nutrition 0.000 description 1
- 229940001607 sodium bisulfite Drugs 0.000 description 1
- 235000010267 sodium hydrogen sulphite Nutrition 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 238000007614 solvation Methods 0.000 description 1
- 239000001587 sorbitan monostearate Substances 0.000 description 1
- 235000011076 sorbitan monostearate Nutrition 0.000 description 1
- 229940035048 sorbitan monostearate Drugs 0.000 description 1
- 238000013223 sprague-dawley female rat Methods 0.000 description 1
- 238000013222 sprague-dawley male rat Methods 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 239000008117 stearic acid Substances 0.000 description 1
- 229960000353 stepronin Drugs 0.000 description 1
- JNYSEDHQJCOWQU-UHFFFAOYSA-N stepronin Chemical compound OC(=O)CNC(=O)C(C)SC(=O)C1=CC=CS1 JNYSEDHQJCOWQU-UHFFFAOYSA-N 0.000 description 1
- 230000004936 stimulating effect Effects 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-L succinate(2-) Chemical compound [O-]C(=O)CCC([O-])=O KDYFGRWQOYBRFD-UHFFFAOYSA-L 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 229960004793 sucrose Drugs 0.000 description 1
- 230000001629 suppression Effects 0.000 description 1
- 238000011477 surgical intervention Methods 0.000 description 1
- 239000000375 suspending agent Substances 0.000 description 1
- 238000013268 sustained release Methods 0.000 description 1
- 239000012730 sustained-release form Substances 0.000 description 1
- 230000009747 swallowing Effects 0.000 description 1
- 230000002889 sympathetic effect Effects 0.000 description 1
- 239000000454 talc Substances 0.000 description 1
- 229910052623 talc Inorganic materials 0.000 description 1
- 230000008685 targeting Effects 0.000 description 1
- 229940095064 tartrate Drugs 0.000 description 1
- 231100001274 therapeutic index Toxicity 0.000 description 1
- 230000008719 thickening Effects 0.000 description 1
- 231100000886 tinnitus Toxicity 0.000 description 1
- 229960004402 tiopronin Drugs 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- 229960000984 tocofersolan Drugs 0.000 description 1
- OMDMTHRBGUBUCO-UHFFFAOYSA-N trans-sobrerol Natural products CC1=CCC(C(C)(C)O)CC1O OMDMTHRBGUBUCO-UHFFFAOYSA-N 0.000 description 1
- 230000009466 transformation Effects 0.000 description 1
- 230000001052 transient effect Effects 0.000 description 1
- CYRMSUTZVYGINF-UHFFFAOYSA-N trichlorofluoromethane Chemical compound FC(Cl)(Cl)Cl CYRMSUTZVYGINF-UHFFFAOYSA-N 0.000 description 1
- 229940029284 trichlorofluoromethane Drugs 0.000 description 1
- 238000011870 unpaired t-test Methods 0.000 description 1
- 210000005166 vasculature Anatomy 0.000 description 1
- 230000009385 viral infection Effects 0.000 description 1
- 229940046009 vitamin E Drugs 0.000 description 1
- 235000019165 vitamin E Nutrition 0.000 description 1
- 239000011709 vitamin E Substances 0.000 description 1
- 238000005303 weighing Methods 0.000 description 1
- 239000009637 wintergreen oil Substances 0.000 description 1
- 239000000230 xanthan gum Substances 0.000 description 1
- 235000010493 xanthan gum Nutrition 0.000 description 1
- 229920001285 xanthan gum Polymers 0.000 description 1
- 229940082509 xanthan gum Drugs 0.000 description 1
- 239000005019 zein Substances 0.000 description 1
- 229940093612 zein Drugs 0.000 description 1
- 239000002076 α-tocopherol Substances 0.000 description 1
- 235000004835 α-tocopherol Nutrition 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4402—Non condensed pyridines; Hydrogenated derivatives thereof only substituted in position 2, e.g. pheniramine, bisacodyl
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0043—Nose
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/08—Drugs for disorders of the alimentary tract or the digestive system for nausea, cinetosis or vertigo; Antiemetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/02—Drugs for disorders of the nervous system for peripheral neuropathies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/16—Otologicals
Landscapes
- Health & Medical Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Medicinal Chemistry (AREA)
- Epidemiology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Otolaryngology (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Neurology (AREA)
- Hospice & Palliative Care (AREA)
- Biomedical Technology (AREA)
- Neurosurgery (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicinal Preparation (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Description
ある局面において、本発明は患者に有効量のベタヒスチンを局所適用する工程を含むエウスタキオ管機能障害(例えば中耳炎)の治療方法を提供する。
ベタヒスチンはメニエール病の治療に全身的に用いられてきた。ベタヒスチンは、商標SERC(登録商標)(Solvay Pharma Inc)で8mg、16mg、および24mg錠として利用可能である。メニエール病は、例えば一過性のめまい、耳鳴り(tinnitus)、耳内の充満感または圧迫感、難聴、悪心、および嘔吐のような症状を特徴とする平衡障害である。メニエール病の治療におけるベタヒスチンの正確な作用機序(すなわち主な局所作用)はわかっていない。ヒスタミン様薬剤として報告されている複数の効果が想定されている。しかしながら、血管系に対するその作用は内耳への有益な酸素供給をもたらすだろう。末梢器官の興奮過剰の抑制および中枢神経メカニズムの抑制も考えられる治療効果と推定される。
方 法
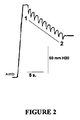
動物実験は、体重250〜450gの雄および雌のSprague Dawleyラットを用いて行った。実験の各セクションで5匹以下のラットを用いた。実験の設定を図1に示す。この図では、麻酔したラット(A)の鼓室胞に小さなチューブを接着する。該チューブをシリンジポンプ(B)、圧変換器(C)、およびデータレコーダー(D)、および圧力計(E)に接続する。シリンジポンプを用いて中耳内の圧を増加させる。上喉頭神経を電気刺激して燕下反射を強制することによりエウスタキオ管を瞬間的に開かせる。麻酔ラットのエウスタキオ管機能の圧記録の例を図2に示す。これから、鼓室胞内圧が周囲圧(Amb)から約130mm水に増加したことがわかる。ポイント1からポイント2まで上喉頭神経を刺激して10回燕下反射を生じさせ、そのそれぞれでエウスタキオ管を瞬間的に開かせ、中耳内の圧を部分的に均等にする。全体の圧低下がエウスタキオ管による均圧効果の測定値である。
結 果
Claims (14)
- ベタヒスチンを含む鼻咽頭に適用するための局所用組成物であって、エウスタキオ管機能障害を治療するための局所用組成物。
- 点鼻剤または定量鼻スプレーの形の請求項1記載の局所用組成物。
- ベタヒスチンが塩の形である請求項1または2記載の局所用組成物。
- ベタヒスチンが二塩酸塩の形である請求項3記載の局所用組成物。
- さらに少なくとも1の医薬的に許容される担体、希釈剤、または賦形剤を含む請求項1〜4のいずれかに記載の局所用組成物。
- ベタヒスチン(遊離塩基で計算)/担体濃度が0.1mg/mL〜50mg/mLである請求項5記載の局所用組成物。
- 該濃度が10mg/mL以下である請求項6記載の局所用組成物。
- さらに医薬活性物質を含む請求項1〜7のいずれかに記載の局所用組成物。
- さらなる医薬活性物質が粘膜溶解薬または充血除去剤である請求項8記載の局所用組成物。
- エウスタキオ管機能障害が中耳炎である請求項1〜9のいずれかに記載の局所用組成物。
- エウスタキオ管機能障害が滲出性中耳炎である請求項1〜9のいずれかに記載の局所用組成物。
- エウスタキオ管機能障害が急性中耳炎(AOM)または航空性中耳炎(AM)である請求項1〜9のいずれかに記載の局所用組成物。
- エウスタキオ管機能障害の治療を要する対象のエウスタキオ管に局所適用するためのベタヒスチンを含むエウスタキオ管機能障害治療用医薬を製造するためのベタヒスチンの使用。
- エウスタキオ管機能障害が中耳炎、滲出性中耳炎、急性中耳炎、または航空性中耳炎である請求項13に記載の使用。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| AU2008902659 | 2008-05-27 | ||
| AU2008902659A AU2008902659A0 (en) | 2008-05-27 | Method of Treatment | |
| PCT/AU2009/000664 WO2009143572A1 (en) | 2008-05-27 | 2009-05-27 | Methods of treating mammals with eustachian tube dysfunctions |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2011520992A JP2011520992A (ja) | 2011-07-21 |
| JP2011520992A5 JP2011520992A5 (ja) | 2012-05-17 |
| JP5543963B2 true JP5543963B2 (ja) | 2014-07-09 |
Family
ID=41376479
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011510783A Expired - Fee Related JP5543963B2 (ja) | 2008-05-27 | 2009-05-27 | エウスタキオ管機能障害を有する哺乳動物の治療方法 |
Country Status (15)
| Country | Link |
|---|---|
| US (1) | US8642631B2 (ja) |
| EP (1) | EP2293794B1 (ja) |
| JP (1) | JP5543963B2 (ja) |
| KR (1) | KR101621726B1 (ja) |
| CN (1) | CN102046170B (ja) |
| AU (1) | AU2009253739B2 (ja) |
| BR (1) | BRPI0912126A2 (ja) |
| CA (1) | CA2765190C (ja) |
| DK (1) | DK2293794T3 (ja) |
| EA (1) | EA022565B1 (ja) |
| ES (1) | ES2419204T3 (ja) |
| HK (1) | HK1155387A1 (ja) |
| NZ (1) | NZ589742A (ja) |
| PT (1) | PT2293794E (ja) |
| WO (1) | WO2009143572A1 (ja) |
Families Citing this family (47)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE10105592A1 (de) | 2001-02-06 | 2002-08-08 | Achim Goepferich | Platzhalter zur Arzneistofffreigabe in der Stirnhöhle |
| US8317816B2 (en) | 2002-09-30 | 2012-11-27 | Acclarent, Inc. | Balloon catheters and methods for treating paranasal sinuses |
| US8435285B2 (en) * | 2003-11-25 | 2013-05-07 | Boston Scientific Scimed, Inc. | Composite stent with inner and outer stent elements and method of using the same |
| US9351750B2 (en) | 2004-04-21 | 2016-05-31 | Acclarent, Inc. | Devices and methods for treating maxillary sinus disease |
| US9554691B2 (en) | 2004-04-21 | 2017-01-31 | Acclarent, Inc. | Endoscopic methods and devices for transnasal procedures |
| US7803150B2 (en) | 2004-04-21 | 2010-09-28 | Acclarent, Inc. | Devices, systems and methods useable for treating sinusitis |
| US8764729B2 (en) | 2004-04-21 | 2014-07-01 | Acclarent, Inc. | Frontal sinus spacer |
| US20060063973A1 (en) | 2004-04-21 | 2006-03-23 | Acclarent, Inc. | Methods and apparatus for treating disorders of the ear, nose and throat |
| US20070208252A1 (en) * | 2004-04-21 | 2007-09-06 | Acclarent, Inc. | Systems and methods for performing image guided procedures within the ear, nose, throat and paranasal sinuses |
| US20060004323A1 (en) | 2004-04-21 | 2006-01-05 | Exploramed Nc1, Inc. | Apparatus and methods for dilating and modifying ostia of paranasal sinuses and other intranasal or paranasal structures |
| US10188413B1 (en) | 2004-04-21 | 2019-01-29 | Acclarent, Inc. | Deflectable guide catheters and related methods |
| US7462175B2 (en) | 2004-04-21 | 2008-12-09 | Acclarent, Inc. | Devices, systems and methods for treating disorders of the ear, nose and throat |
| US8702626B1 (en) | 2004-04-21 | 2014-04-22 | Acclarent, Inc. | Guidewires for performing image guided procedures |
| US8894614B2 (en) | 2004-04-21 | 2014-11-25 | Acclarent, Inc. | Devices, systems and methods useable for treating frontal sinusitis |
| US9101384B2 (en) | 2004-04-21 | 2015-08-11 | Acclarent, Inc. | Devices, systems and methods for diagnosing and treating sinusitis and other disorders of the ears, Nose and/or throat |
| US7559925B2 (en) | 2006-09-15 | 2009-07-14 | Acclarent Inc. | Methods and devices for facilitating visualization in a surgical environment |
| US9089258B2 (en) | 2004-04-21 | 2015-07-28 | Acclarent, Inc. | Endoscopic methods and devices for transnasal procedures |
| US9399121B2 (en) | 2004-04-21 | 2016-07-26 | Acclarent, Inc. | Systems and methods for transnasal dilation of passageways in the ear, nose or throat |
| US7419497B2 (en) | 2004-04-21 | 2008-09-02 | Acclarent, Inc. | Methods for treating ethmoid disease |
| US8932276B1 (en) | 2004-04-21 | 2015-01-13 | Acclarent, Inc. | Shapeable guide catheters and related methods |
| US20070167682A1 (en) | 2004-04-21 | 2007-07-19 | Acclarent, Inc. | Endoscopic methods and devices for transnasal procedures |
| US7654997B2 (en) | 2004-04-21 | 2010-02-02 | Acclarent, Inc. | Devices, systems and methods for diagnosing and treating sinusitus and other disorders of the ears, nose and/or throat |
| US20190314620A1 (en) | 2004-04-21 | 2019-10-17 | Acclarent, Inc. | Apparatus and methods for dilating and modifying ostia of paranasal sinuses and other intranasal or paranasal structures |
| US8747389B2 (en) | 2004-04-21 | 2014-06-10 | Acclarent, Inc. | Systems for treating disorders of the ear, nose and throat |
| US8951225B2 (en) | 2005-06-10 | 2015-02-10 | Acclarent, Inc. | Catheters with non-removable guide members useable for treatment of sinusitis |
| US7816975B2 (en) * | 2005-09-20 | 2010-10-19 | Hewlett-Packard Development Company, L.P. | Circuit and method for bias voltage generation |
| US8114113B2 (en) | 2005-09-23 | 2012-02-14 | Acclarent, Inc. | Multi-conduit balloon catheter |
| US9820688B2 (en) | 2006-09-15 | 2017-11-21 | Acclarent, Inc. | Sinus illumination lightwire device |
| US8439687B1 (en) | 2006-12-29 | 2013-05-14 | Acclarent, Inc. | Apparatus and method for simulated insertion and positioning of guidewares and other interventional devices |
| WO2008124787A2 (en) | 2007-04-09 | 2008-10-16 | Acclarent, Inc. | Ethmoidotomy system and implantable spacer devices having therapeutic substance delivery capability for treatment of paranasal sinusitis |
| US8118757B2 (en) | 2007-04-30 | 2012-02-21 | Acclarent, Inc. | Methods and devices for ostium measurement |
| US8485199B2 (en) | 2007-05-08 | 2013-07-16 | Acclarent, Inc. | Methods and devices for protecting nasal turbinate during surgery |
| US10206821B2 (en) | 2007-12-20 | 2019-02-19 | Acclarent, Inc. | Eustachian tube dilation balloon with ventilation path |
| US8182432B2 (en) | 2008-03-10 | 2012-05-22 | Acclarent, Inc. | Corewire design and construction for medical devices |
| WO2010014799A1 (en) | 2008-07-30 | 2010-02-04 | Acclarent, Inc. | Paranasal ostium finder devices and methods |
| AU2009293312B2 (en) | 2008-09-18 | 2015-07-09 | Acclarent, Inc. | Methods and apparatus for treating disorders of the ear nose and throat |
| US20100241155A1 (en) | 2009-03-20 | 2010-09-23 | Acclarent, Inc. | Guide system with suction |
| US7978742B1 (en) | 2010-03-24 | 2011-07-12 | Corning Incorporated | Methods for operating diode lasers |
| US8435290B2 (en) * | 2009-03-31 | 2013-05-07 | Acclarent, Inc. | System and method for treatment of non-ventilating middle ear by providing a gas pathway through the nasopharynx |
| US9155492B2 (en) | 2010-09-24 | 2015-10-13 | Acclarent, Inc. | Sinus illumination lightwire device |
| US9629684B2 (en) | 2013-03-15 | 2017-04-25 | Acclarent, Inc. | Apparatus and method for treatment of ethmoid sinusitis |
| US9433437B2 (en) | 2013-03-15 | 2016-09-06 | Acclarent, Inc. | Apparatus and method for treatment of ethmoid sinusitis |
| US11410751B2 (en) | 2016-05-27 | 2022-08-09 | Life Technologies Corporation | Methods and systems for graphical user interfaces for biological data |
| DK3474850T3 (da) * | 2017-02-02 | 2020-08-03 | Otolanum Ag | Intranasal sammensætning omfattende betahistin |
| WO2018170532A1 (en) * | 2017-03-22 | 2018-09-27 | Franz, Lilian Ann | Treatment method |
| AU2019208152B2 (en) * | 2017-03-22 | 2021-07-01 | Burkhard Karl-Heinz Gunther Franz | Treatment method |
| SI3600276T1 (sl) | 2017-03-28 | 2023-08-31 | IntraBio Ltd, Summit House | Betahistin ali njegova farmacevtsko sprejemljiva sol in inhibitor monoaminoksidaze, za uporabo pri zdravljenju ali preprečevanju enega ali več simptomov vrtoglavice pri subjektu |
Family Cites Families (49)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3149034A (en) | 1961-07-17 | 1964-09-15 | Umimed Inc | Method of relieving pain with (pyridyllower alkyl)-amines |
| US3632765A (en) | 1969-07-18 | 1972-01-04 | Unimed Inc | Treatment of shock |
| GB1241906A (en) | 1969-11-01 | 1971-08-04 | Unimed Inc | Salts of beta-(pyridyl alkyl) amines with 21-hydroxy steroid polybasic acid esters |
| JPS5938202B2 (ja) | 1976-03-05 | 1984-09-14 | エーザイ株式会社 | 難聴治療剤 |
| GB1577871A (en) | 1976-05-28 | 1980-10-29 | Unimed Inc | Prevention of myocardial infarction |
| FR2397840B1 (ja) | 1977-07-22 | 1981-03-20 | Cherqui Jean | |
| FR2432313A1 (fr) | 1978-08-01 | 1980-02-29 | Foulhoux Pierre | Nouvelle forme galenique de la betahistine et son procede d'obtention |
| JPS55154915A (en) * | 1979-05-21 | 1980-12-02 | Jiyan Sadeia Shieruki | Medicine mold |
| DE3634016A1 (de) | 1986-04-17 | 1987-10-29 | Lohmann Gmbh & Co Kg | Flaechenfoermiges therapeutisches system, verfahren zu seiner herstellung und seine verwendung |
| IT1229237B (it) | 1989-05-08 | 1991-07-26 | Prodotti Formenti | Sali di (2-(piridil)etil) metilammina |
| GB9104854D0 (en) | 1991-03-07 | 1991-04-17 | Reckitt & Colmann Prod Ltd | Sustained release compositions |
| JPH06219947A (ja) | 1993-01-26 | 1994-08-09 | Kinki Univ | 経皮投与製剤 |
| GB2280604B (en) | 1993-07-02 | 1997-04-30 | Resource Medical Limited | Processing of active agents |
| IT1309591B1 (it) | 1999-03-05 | 2002-01-24 | Formenti Farmaceutici Spa | Composizioni a rilascio controllato di betaistina. |
| JP2001064205A (ja) | 1999-06-25 | 2001-03-13 | Dai Ichi Seiyaku Co Ltd | 製剤組成物 |
| US6156294A (en) * | 1999-11-28 | 2000-12-05 | Scientific Development And Research, Inc. | Composition and method for treatment of otitis media |
| US20020106408A1 (en) | 2000-12-01 | 2002-08-08 | Johnatan Bacon | Prolamin-based sustained-release compositions and delayed-onset compositions |
| WO2002064088A2 (en) | 2001-02-14 | 2002-08-22 | Niazi Sarfaraz K | Pharmaceutical composition for the treatment of alopecia |
| WO2002094240A1 (en) | 2001-05-24 | 2002-11-28 | Alexza Molecular Delivery Corporation | Delivery of physiologically active compounds through an inhalation route |
| US20030051728A1 (en) | 2001-06-05 | 2003-03-20 | Lloyd Peter M. | Method and device for delivering a physiologically active compound |
| WO2003026631A1 (en) | 2001-05-24 | 2003-04-03 | Alexza Molecular Delivery Corporation | Delivery of drug esters through an inhalation route |
| EP1392262A1 (en) | 2001-05-24 | 2004-03-03 | Alexza Molecular Delivery Corporation | Delivery of drug esters through an inhalation route |
| US7090830B2 (en) | 2001-05-24 | 2006-08-15 | Alexza Pharmaceuticals, Inc. | Drug condensation aerosols and kits |
| WO2004089313A2 (en) | 2003-04-01 | 2004-10-21 | Transform Pharmaceuticals, Inc. | Novel olanzapine forms and related methods of treatment |
| WO2003077902A1 (en) | 2002-02-19 | 2003-09-25 | Xenoport, Inc. | Methods for synthesis of prodrugs from 1-acyl-alkyl derivatives and compositions thereof |
| AU2003243354A1 (en) | 2002-05-31 | 2003-12-19 | Transform Pharmaceuticals, Inc. | Novel conazole crystalline forms and related processes, pharmaceutical compositions and methods |
| GB0213869D0 (en) | 2002-06-17 | 2002-07-31 | Arakis Ltd | The treatment of pain |
| AU2003281158A1 (en) | 2002-07-12 | 2004-02-02 | Arakis Ltd. | The treatment of emesis |
| CA2503155A1 (en) | 2002-10-25 | 2004-05-06 | Labopharm Inc. | Sustained-release tramadol formulations with 24-hour efficacy |
| US8487002B2 (en) | 2002-10-25 | 2013-07-16 | Paladin Labs Inc. | Controlled-release compositions |
| MXPA05004410A (es) | 2002-10-25 | 2005-11-23 | Labopharm Inc | Composiciones de liberacion controlada. |
| US7220431B2 (en) | 2002-11-27 | 2007-05-22 | Regents Of The University Of Minnesota | Methods and compositions for applying pharmacologic agents to the ear |
| PT1493435E (pt) | 2003-07-04 | 2008-08-14 | Formenti Farmaceutici Spa | Composições de libertação controlada de beta-histina |
| WO2005011665A1 (en) | 2003-07-22 | 2005-02-10 | Arakis Ltd. | The use of proglumide for the treatment of emesis |
| KR20060134041A (ko) | 2004-04-22 | 2006-12-27 | 모르 리서치 애플리케이션즈 리미티드 | 음식물 섭취 관리 방법 |
| CN1568986A (zh) | 2004-05-13 | 2005-01-26 | 南昌弘益科技有限公司 | 盐酸倍他司汀滴丸及其制备方法 |
| GB0506800D0 (en) | 2005-04-04 | 2005-05-11 | Merck Sharp & Dohme | New uses |
| CA2605341A1 (en) | 2005-05-09 | 2006-11-16 | Drugtech Corporation | Modified-release pharmaceutical compositions |
| US20070009564A1 (en) | 2005-06-22 | 2007-01-11 | Mcclain James B | Drug/polymer composite materials and methods of making the same |
| EP1909973B1 (en) | 2005-07-15 | 2018-08-22 | Micell Technologies, Inc. | Polymer coatings containing drug powder of controlled morphology |
| CN1732934B (zh) | 2005-08-10 | 2011-10-05 | 陈学峰 | 注射用盐酸倍他司汀冻干粉针剂及其制备方法 |
| US8158152B2 (en) | 2005-11-18 | 2012-04-17 | Scidose Llc | Lyophilization process and products obtained thereby |
| WO2007076140A2 (en) | 2005-12-23 | 2007-07-05 | University Of Cincinnati | Treatment methods employing histamine h3 receptor antagonists, including betahistine |
| US7951845B2 (en) | 2006-01-19 | 2011-05-31 | The Regents Of The University Of Michigan | Composition and method of treating hearing loss |
| US20070231390A1 (en) | 2006-03-29 | 2007-10-04 | Andrx Labs, Llc | Formulations including hygroscopic compounds |
| RU2308941C1 (ru) | 2006-05-10 | 2007-10-27 | Открытое акционерное общество "Московское производственное химико-фармацевтическое объединение им. Н.А. Семашко" | Твердая лекарственная форма, обладающая гистаминоподобным действием, и способ ее получения |
| US20080066739A1 (en) | 2006-09-20 | 2008-03-20 | Lemahieu Edward | Methods and systems of delivering medication via inhalation |
| CN101668544B (zh) * | 2006-12-26 | 2013-04-24 | 株式会社新日本科学 | 经鼻投用制剂 |
| US8101782B2 (en) | 2007-02-02 | 2012-01-24 | Colucid Pharmaceuticals, Inc. | Compounds that inhibit cholinesterase |
-
2009
- 2009-05-27 JP JP2011510783A patent/JP5543963B2/ja not_active Expired - Fee Related
- 2009-05-27 US US12/994,709 patent/US8642631B2/en not_active Expired - Fee Related
- 2009-05-27 EA EA201071361A patent/EA022565B1/ru not_active IP Right Cessation
- 2009-05-27 WO PCT/AU2009/000664 patent/WO2009143572A1/en active Application Filing
- 2009-05-27 BR BRPI0912126A patent/BRPI0912126A2/pt not_active Application Discontinuation
- 2009-05-27 DK DK09753336.8T patent/DK2293794T3/da active
- 2009-05-27 ES ES09753336T patent/ES2419204T3/es active Active
- 2009-05-27 NZ NZ589742A patent/NZ589742A/en not_active IP Right Cessation
- 2009-05-27 CA CA2765190A patent/CA2765190C/en not_active Expired - Fee Related
- 2009-05-27 PT PT97533368T patent/PT2293794E/pt unknown
- 2009-05-27 AU AU2009253739A patent/AU2009253739B2/en not_active Ceased
- 2009-05-27 CN CN2009801195324A patent/CN102046170B/zh not_active Expired - Fee Related
- 2009-05-27 KR KR1020107029075A patent/KR101621726B1/ko active IP Right Grant
- 2009-05-27 EP EP09753336.8A patent/EP2293794B1/en not_active Not-in-force
-
2011
- 2011-09-14 HK HK11109700.9A patent/HK1155387A1/xx not_active IP Right Cessation
Also Published As
| Publication number | Publication date |
|---|---|
| KR20110022624A (ko) | 2011-03-07 |
| CN102046170A (zh) | 2011-05-04 |
| CA2765190C (en) | 2016-07-19 |
| EP2293794A4 (en) | 2011-06-22 |
| DK2293794T3 (da) | 2013-08-19 |
| CN102046170B (zh) | 2012-11-28 |
| WO2009143572A1 (en) | 2009-12-03 |
| EP2293794B1 (en) | 2013-05-22 |
| EA201071361A1 (ru) | 2011-06-30 |
| ES2419204T3 (es) | 2013-08-19 |
| KR101621726B1 (ko) | 2016-05-17 |
| AU2009253739B2 (en) | 2014-02-06 |
| EP2293794A1 (en) | 2011-03-16 |
| HK1155387A1 (en) | 2012-05-18 |
| AU2009253739A1 (en) | 2009-12-03 |
| EA022565B1 (ru) | 2016-01-29 |
| NZ589742A (en) | 2012-06-29 |
| PT2293794E (pt) | 2013-07-10 |
| BRPI0912126A2 (pt) | 2015-11-03 |
| US20110166190A1 (en) | 2011-07-07 |
| CA2765190A1 (en) | 2009-12-03 |
| US8642631B2 (en) | 2014-02-04 |
| JP2011520992A (ja) | 2011-07-21 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5543963B2 (ja) | エウスタキオ管機能障害を有する哺乳動物の治療方法 | |
| JP5683719B2 (ja) | ベポタスチン組成物 | |
| EP1265615B1 (de) | Neue kombination nichtsedierender antihistaminika mit substanzen, die die leukotrienwirkung beeinflussen, zur behandlung der rhinitis/konjunktivitis | |
| US20180325921A1 (en) | Compositions for the treatment of inflammation of the gastrointestinal tract | |
| JP2020502206A (ja) | Task−1およびtask−3チャネル阻害剤を含む医薬剤形、ならびに呼吸障害療法におけるその使用 | |
| ES2389539T3 (es) | Métodos y composiciones para el tratamiento del asma | |
| AU2005210086A1 (en) | Treatment of rhinitis with anticholinergics alone in combination with antihistamines phosphodiesterase 4 inhibitors, or corticosteroids | |
| JP2020502215A (ja) | Task−1およびtask−3チャネル阻害剤を含む医薬剤形、ならびに呼吸障害療法におけるその使用 | |
| RU2409356C2 (ru) | Применение амброксола для лечения риновирусных инфекций | |
| EP1503763B1 (en) | Therapeutic 1,2,3,6-tetrahydropyrimidine-2-one compositions and methods therewith | |
| US11235013B2 (en) | Cannabinoid, menthol and caffeine dissolvable film compositions, devices and methods | |
| RU2685277C1 (ru) | Применение бисамидного производного малоновой кислоты для лечения аллергических и других заболеваний человека и животных | |
| KR101920050B1 (ko) | 〔((1r,2s,5r)―2―이소프로필―5―메틸―시클로헥산카르보닐)―아미노〕―아세트산 이소프로필 에스테르와 관련 화합물 및 요법에서 그의 용도 | |
| KR20190039735A (ko) | 주사비의 치료 또는 예방을 위한 조성물 및 이의 용도 | |
| UA150749U (uk) | Спосіб одержання фармацевтичної композиції для інтраназального введення | |
| MXPA06008935A (en) | Treatment of rhinitis with anticholinergics alone in combination with antihistamines phosphodiesterase 4 inhibitors, or corticosteroids | |
| KR20180123738A (ko) | 〔((1r,2s,5r)―2―이소프로필―5―메틸―시클로헥산카르보닐)―아미노〕―아세트산 이소프로필 에스테르와 관련 화합물 및 요법에서 그의 용도 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120319 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20120319 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130730 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20131126 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20140225 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20140415 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20140509 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5543963 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| S111 | Request for change of ownership or part of ownership |
Free format text: JAPANESE INTERMEDIATE CODE: R313113 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |