누시네르센
Nusinersen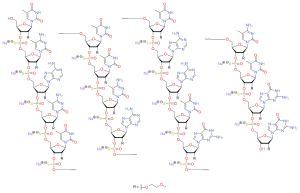 | |
| 임상자료 | |
|---|---|
| 상명 | 스피프라자 |
| 기타 이름 | 아이오니스-SMNRx, IS-SMNRx |
| AHFS/Drugs.com | 모노그래프 |
| 메드라인플러스 | a617010 |
| 라이센스 데이터 | |
| 임신 , 카테고리 |
|
| 경로: 행정 | 자궁내부 |
| ATC 코드 | |
| 법적현황 | |
| 법적현황 | |
| 약동학 데이터 | |
| 생체이용가능성 | 100%(하수체) |
| 단백질 결합 | <25%(CSF), >94%(플라즈마)[2] |
| 신진대사 | Exonuclease(3'-' 및 5')-수력해석법 |
| 제거 반감기 | 135-177일(CSF), 63-87일(플라즈마) |
| 식별자 | |
| |
| CAS 번호 | |
| 펍켐 CID | |
| 드러그뱅크 | |
| 켐스파이더 | |
| 유니 | |
| 케그 | |
| 화학 및 물리적 데이터 | |
| 공식 | C234H323N61나17O128P17S17[1] |
| 어금질량 | 7500.86 g·migration−1 |
| |
스피프라자([3]Spinraza)로 시판되는 누시네르센은 희귀 신경근육질환인 척수근위축증(SMA) 치료에 사용되는 약물이다.[1][4][1]2016년 12월 이 질환을 치료하는 데 최초로 승인된 약이 됐다.
누시네르센은 치료하는 상태가 매우 드물기 때문에 미국과 유럽연합(EU)에서 이른바 '모르핀 약물' 지정을 받고 있다.[5]
의학적 용법
이 약은 SMN1 유전자의 돌연변이와 관련된 척추 근육 위축을 치료하는데 사용된다.체내주사를 이용하여 중추신경계(CNS)에 직접 투여한다.[1]
임상 실험에서 그 약은 질병 진행을 중단시켰다.제1형 척수성 근위축증에 걸린 유아의 약 60%에서 운동기능을 향상시킨다.[1]
부작용
누시네르센으로 치료받은 사람들은 상하의 호흡기 감염과 충혈, 귀 감염, 변비, 폐 흡인, 차오름, 척추측만증의 위험이 증가했다.유아와 아동의 성장이 저해될 위험이 있다.나이든 임상 실험 대상자의 경우 가장 흔한 부작용은 두통, 요통, 그리고 경막후 두통 등 척추 주사로 인한 다른 부작용이었다.[1]
임상시험 환자에서는 관찰되지 않았지만 신장 손상 위험뿐만 아니라 혈소판 감소는 항산화제의 이론적 위험성이므로 치료 중 혈소판과 신장 기능을 모니터링해야 한다.[1]
2018년, 뉴시너센으로 치료된 어린이와 성인의 수두통 의사소통 사례가 여러 건 발생했는데, 이것이 마약과 관련이 있는지는 여전히 불분명하다.[6]
약리학
척추 근육 위축은 생존 운동 뉴런(SMN) 단백질을 암호화하는 SMN1 유전자의 기능상실 돌연변이에 의해 발생한다.사람들은 SMN2 유전자에서 생성된 적은 양의 SMN 단백질 때문에 살아남는다.누시네르센은 SMN2 유전자의 대체적 스플라이싱을 변조하여 기능적으로 SMN1 유전자로 전환하여 CNS에서 SMN 단백질의 수준을 높인다.[7]
그 약은 CNS와 말초조직에 분배된다.[1]
반감기는 뇌척수액(CSF) 135~177일, 혈장 63~87일로 추정된다.이 약물은 엑소누클리스(3㎛- 및 5㎛)를 통해 대사되며 CYP450 효소와 상호작용하지 않는다.[1]1차 제거 경로는 누시네르센과 그 대사물에 대한 소변 배설을 통해 발생할 수 있다.[1]
화학.
누시네르센은 리보푸라노실 링의 2'히드록시 그룹이 2'O-2-메톡시틸 그룹으로 대체되고 인산염 연결은 인광로티오테이트 연결로 대체되는 항이센스 올리고뉴클레오티드다.[1][7][8]
역사
누시네르센은 콜드 스프링 하버 연구소의 아드리안 크라이너와 이오니스 제약회사(옛 이시스 제약회사)의 합작으로 개발되었다.[9][10][11][12]뉴시네르센의 목표 발견에 대한 초기 작업은 라빈드라 싱 박사와 큐어 SMA가 후원하는 매사추세츠 의과대학의 동료들이 했다.[13][14]
2012년부터 이오니아는 바이오젠과 개발 계약을 맺고 2015년에는 바이오젠이 7500만 달러의 라이선스 수수료와 최대 1억5000만 달러의 마일스톤 결제, 그 이후 계층화된 로열티로 이 약품에 대한 독점 라이선스를 취득했으며, 바이오젠은 라이선스 취득에 따른 개발 비용도 지불했다.[15]바이오젠 면허에는 이오니스가 콜드 스프링 하버 연구소와 매사추세츠 대학교에서 취득한 지적 재산에 대한 면허가 포함되었다.[16]
2016년 11월에는 3단계 임상시험의 강도와 미충족 필요성에 대한 FDA의 우선 검토 과정에 따라 신약 출원이 받아들여졌고, 당시 유럽 의약청(EMA)에서도 심사를 위해 받아들여졌다.[17][18]2016년 12월 FDA로부터, 2017년 5월 EMA로부터 SMA 치료제 1호로 승인을 받았으며,[19][20] 이어 캐나다(2017년 7월),[21] 일본(2017년 7월),[22] 브라질(2017년 8월),[23] 스위스(2017년 9월),[24] 중국(2019년 2월)에서 뉴시너센이 SMA 치료제 허가를 받았다.[25]
사회와 문화
경제학
미국의 누시네르센 정가는 주사당 미화 12만5천 달러로, 치료비는 첫 해에 미화 75만 달러, 그 후로는 연간 37만5천 달러다.[26]뉴욕타임스에 따르면, 이곳은 "세계에서 가장 비싼 약 중 하나"[18]라고 한다.
덴마크 당국은 2017년 10월 누시넨을 SMA 1형(젊은 아기)의 작은 서브셋에만 사용할 것을 권고했고, SMA가 혜택에 비해 '합리할 수 없이 높은 가격'을 인용하면서 다른 모든 사람에게 표준 치료제로 제공하기를 거부했다.[27]
노르웨이 당국은 2017년 10월 의약품 가격이 "윤리적으로 높다"[28]는 이유로 자금 지원을 거부했다.2018년 2월 만 18세 미만에게 지원금이 승인됐다.[28]
8월 2018년이면 국립 보건원과 관리 우수에(NICE)영국과 웨일즈의 국민 의료 보험의 치료법의 비용 효율성 무게가 나가SMA.[29]어린이 SMA과 유형 1은 영국에 Biogen-funded 확장된 액세스 프로그램은 치료를 받은 사람들에게 nusinersen을 제공하는 것에 반대하며 80 두는데 후에 추천했다.그2018년 11월에 새로운 사람들에게 공개되지 [30]않은 계획그러나 2019년 5월 NICE는 입장을 번복하고 5년간 광범위한 SMA에 걸쳐 뉴시넨 사용을 권고하기로 방침을 밝혔다.[31][32]
아일랜드 보건국 집행부는 2019년 2월 뉴시너센이 너무 비싸서 자금을 조달할 수 없다고 결정했는데, 이 비용은 아일랜드에 거주하고 있는 25명의 SMA 아동에 대해 "5년 동안 추정 예산 영향이 2,000만 유로를 초과하는" 첫 해에 환자 1명당 약 60만 유로가 될 것이고, 그 이후로는 연간 약 38만 유로가 될 것이라고 말했다.제조사와 환자단체 모두 이 수치를 놓고 논쟁을 벌이며 아일랜드에 대한 실제 가격 책정이 아일랜드가 2018년 6월부터 가입해 온 베넬룩사 이니셔티브의 협상 가격과 일치한다고 지적했다.[33]
2019년 5월 현재 40여 개국의 공중보건의료에서 뉴시네르센을 이용할 수 있었다.[34]
2021년 12월 중국의 보험 확대 적용 대상에 뉴시네르센이 포함되면서 가격은 바이알당 69만7000원에서 바이알당 33만3000원(약 5100달러) 수준으로 낮아졌다.[35][36][37]
참조
- ^ a b c d e f g h i j k l "Spinraza- nusinersen injection, solution". DailyMed. 30 June 2020. Retrieved 3 November 2020.
- ^ Paton, D.M. (2017). "Nusinersen: antisense oligonucleotide to increase SMN protein production in spinal muscular atrophy". Drugs of Today. Clarivate Analytics (US). 53 (6): 327–337. doi:10.1358/dot.2017.53.6.2652413. ISSN 1699-3993. PMID 28799578.
- ^ a b "International Nonproprietary Names for Pharmaceutical Substances (INN). Recommended International Nonproprietary Names: List 74" (PDF). World Health Organization. pp. 413–414. Retrieved 13 March 2017.
- ^ Ottesen EW (January 2017). "ISS-N1 makes the First FDA-approved Drug for Spinal Muscular Atrophy". Translational Neuroscience. 8 (1): 1–6. doi:10.1515/tnsci-2017-0001. PMC 5382937. PMID 28400976.
- ^ "Nusinersen". UK Specialist Pharmacy Service. Retrieved 31 December 2016.
- ^ "New warning of nusinersen-related communicating hydrocephalus". Reactions Weekly. 1714 (1): 3. 2018-08-01. doi:10.1007/s40278-018-50183-2. ISSN 1179-2051. S2CID 195086499.
- ^ a b Zanetta C, Nizzardo M, Simone C, Monguzzi E, Bresolin N, Comi GP, Corti S (January 2014). "Molecular therapeutic strategies for spinal muscular atrophies: current and future clinical trials". Clinical Therapeutics. 36 (1): 128–40. doi:10.1016/j.clinthera.2013.11.006. PMID 24360800.
- ^ Pao PW, Wee KB, Yee WC, Pramono ZA, Dwipramono ZA (April 2014). "Dual masking of specific negative splicing regulatory elements resulted in maximal exon 7 inclusion of SMN2 gene". Molecular Therapy. 22 (4): 854–61. doi:10.1038/mt.2013.276. PMC 3982506. PMID 24317636. 누시네르센(UCACUUUCAUGCUG)의 순서는 표 I에 N1-화(Hua)로 수록되어 있다.
- ^ Garber K (October 2016). "Big win possible for Ionis/Biogen antisense drug in muscular atrophy". Nature Biotechnology. 34 (10): 1002–1003. doi:10.1038/nbt1016-1002. PMID 27727217. S2CID 37479367.
- ^ Wadman M (23 December 2016). "Updated: FDA approves drug that rescues babies with fatal neurodegenerative disease". Science. doi:10.1126/science.aal0476.
- ^ Offord C (December 1, 2016). "Oligonucleotide Therapeutics Near Approval". The Scientist.
- ^ Tarr P (24 December 2016). "CSHL FDA approval of life-saving SMA drug is hailed by its researcher-inventor at CSHL". Cold Spring Harbor Laboratory. Archived from the original on 1 January 2017. Retrieved 1 January 2017.
- ^ "Therapeutic Approaches". www.curesma.org. Cure SMA. Archived from the original on 1 January 2017. Retrieved 1 January 2017.
- ^ Singh NN, Howell MD, Androphy EJ, Singh RN (2019). "How the discovery of ISS-N1 led to the first medical therapy for spinal muscular atrophy". Gene Therapy. 24 (9): 520–526. doi:10.1038/gt.2017.34. PMC 5623086. PMID 28485722.
- ^ "Biogen Shells Out $75M to Develop Ionis' Nusinersen after Positive Phase III Results", Genetic Engineering News, August 1, 2016
- ^ "Press release: Biogen and Ionis Pharmaceuticals Report Nusinersen Meets Primary Endpoint at Interim Analysis of Phase 3 ENDEAR Study in Infantile-Onset Spinal Muscular Atrophy Biogen Media". Biogen. August 1, 2016. Archived from the original on August 10, 2017. Retrieved January 1, 2017.
- ^ "Regulatory Applications for SMA Therapy Nusinersen Accepted in US, EU". BioNews Services, LLC. Retrieved 2016-11-15.
- ^ a b Thomas K (December 30, 2016). "Costly Drug for Fatal Muscular Disease Wins F.D.A. Approval". New York Times.
- ^ Grant C (2016-12-27). "Surprise Drug Approval Is Holiday Gift for Biogen". Wall Street Journal. ISSN 0099-9660. Retrieved 2016-12-27.
- ^ "Spinraza (nusinersen)". European Medicines Agency. Retrieved 2017-10-27.
- ^ "Biogen's SPINRAZA™ (nusinersen) Receives Notice of Compliance from Health Canada for the Treatment of 5q Spinal Muscular Atrophy (SMA)". Cision. 2017-07-04.
- ^ "Biogen to launch Spinraza in Japan soon". 2017-07-10.
- ^ "Remédio inédito para atrofia muscular espinhal é liberado" (in Brazilian Portuguese). 2017-08-25.
- ^ "Spinraza – Zulassung nun auch in der Schweiz" (in Swiss High German). SMA Schweiz. 2017-09-30.
- ^ "Biogen Further Expands Presence in China with Approval of SPINRAZA® (nusinersen), the First and Only Treatment for Spinal Muscular Atrophy Biogen". investors.biogen.com. Retrieved 2022-01-10.
- ^ "Spinraza Prices, Coupons & Patient Assistance Programs". Drugs.com. Retrieved 2021-09-10.
- ^ Medicinrådet siger nej to lægemiddel to børn meddes muskelsvind: 'Urimeligt' dyrt Retried 2017년 10월 13일 검색됨.
- ^ a b Dette er uforstelig og utrolig uretferdig.이것은 이해할 수 없고 믿을 수 없을 정도로 불공평하다(구글 번역)
- ^ "Biogen's pricey muscle drug Spinraza too costly for Britain". Reuters. 2018-08-13. Retrieved 2019-05-28.
- ^ "Biogen statement on Expanded Access Programme". Muscular Dystrophy UK. 2 December 2018. Retrieved 27 February 2019.
- ^ "NICE recommends first ever treatment for children with rare muscle-wasting condition". National Institute of Health and Care Excellence. 15 May 2019. Retrieved 2019-05-28.
- ^ 척추 근위축증을 치료하기 위한 누시너센. NICE Technology 평가 지침[TA588] 2019
- ^ "Drugmaker urges HSE to revisit pricing of muscle-wasting disease treatment". Irish Times. 25 February 2019. Retrieved 27 February 2019.
- ^ "Spinraza access by country". TreatSMA. Retrieved 2019-05-28.
- ^ "Biogen's Spinraza, Fosun Kite's Yescarta and a controversial Alzheimer's drug: All you need to know about China's new state coverage". FiercePharma. Retrieved 2022-01-27.
- ^ "China's 2021 NDRL listing sees price cuts of up to 95%". www.thepharmaletter.com. Retrieved 2022-01-27.
- ^ 陈子琰. "China increases accessibility to rare disease treatment". www.chinadaily.com.cn. Retrieved 2022-01-27.
추가 읽기
- Finkel RS, Chiriboga CA, Vajsar J, Day JW, Montes J, De Vivo DC, et al. (December 2016). "Treatment of infantile-onset spinal muscular atrophy with nusinersen: a phase 2, open-label, dose-escalation study". Lancet. 388 (10063): 3017–3026. doi:10.1016/S0140-6736(16)31408-8. PMID 27939059. S2CID 40696239.
외부 링크
- "Cut and Paste: Treating Spinal Muscular Atrophy with Nusinersen". Youreka Science. Retrieved 2019-05-28.
- "Spinraza access by country". TreatSMA. Retrieved 2019-05-28.


