플루오렌
Fluorene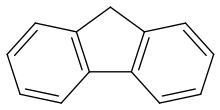 | |
 | |
 | |
| 이름 | |
|---|---|
| 우선 IUPAC 이름 9H-플루오렌[2] | |
| 시스템 IUPAC 이름 트리시클로[7.4.0.02,7]트리데카-2,4,6,9,11,13-헥사엔 | |
| 식별자 | |
3D 모델(JSmol) | |
| 체비 | |
| 첸블 | |
| 켐스파이더 | |
| ECHA 정보 카드 | 100.001.541 |
| EC 번호 |
|
| 케그 | |
PubChem CID | |
| RTECS 번호 |
|
| 유니 | |
CompTox 대시보드 (EPA ) | |
| |
| |
| 특성. | |
| C13H10 | |
| 몰 질량 | 166.223 g/120−1 |
| 밀도 | 1.202 g/mL |
| 녹는점 | 116 ~ 117 °C (241 ~243 °F, 389 ~390 K) |
| 비등점 | 295°C(563°F, 568K) |
| 1.992mg/L | |
| 용해성 | 유기 용제 |
| 로그 P | 4.18 |
| 산도(pKa) | 22.6 |
자화율(δ) | - 110.5 · 10−6 cm3 / 가로 |
| 위험 요소 | |
| NFPA 704(파이어 다이아몬드) | |
| 플래시 포인트 | 152 °C (306 °F, 425 K) |
| 치사량 또는 농도(LD, LC): | |
LD50(중간선량) | 16000 mg/kg (구강, 쥐) |
| 안전 데이터 시트(SDS) | 시그마알드리히 |
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |
플루오렌 /flflərinn/ 또는 9H-플루오렌은 (CH64)2CH의2 유기화합물이다.그것은 나프탈렌과 유사한 특징적이고 향기로운 냄새를 나타내는 하얀 결정을 형성합니다.그것은 보라색 형광을 가지고 있어서 이름이 붙여졌다.상업적인 목적으로 [3]콜타르에서 얻는다.그것은 물에 녹지 않고 많은 유기 용제에 녹는다.때때로 다환 방향족 탄화수소로 분류되기도 하지만, 5원 고리는 방향족 특성이 없습니다.플루오렌은 약산성이다.
합성, 구조 및 반응성
콜타르로부터 플루오렌을 얻을 수 있지만, 디페닐메탄의 [3]탈수소화에 의해서도 제조할 수 있다.또는 아연 또는[4] 하이포인산-아이오딘과 [5]플루오레논을 환원하여 제조할 수 있다.두 개의 벤젠 고리 각각이 중심 탄소 [7]9와 동일 평면이지만, 플루오렌 분자는 거의 [6]평면입니다.
플루오렌은 PS, PE 및 [8]PVC와 같은 플라스틱의 불완전 연소 후에 발견될 수 있습니다.
산도
플루오렌 고리의 C9-H 부위는 약산성이다(pKa = DMSO의 22.6).[9] 탈토닝은 안정적인 플루오렌질 음이온인 명목상139− CH를 제공하며, 방향족이며 강렬한 주황색을 띤다.음이온은 친핵성이야전자 친필은 9개의 위치에 더하여 반응합니다.플루오렌의 정화는 플루오렌의 산성도와 탄화수소 용매에서의 나트륨 유도체의 낮은 용해도를 이용한다.
두 양성자는 모두 C9에서 제거될 수 있습니다.예를 들어 플루오렌을 끓는 다이옥산에서 [10]칼륨 금속으로 처리함으로써 9,9-플루오릴디포탈륨을 얻을 수 있다.
배위자 특성
플루오렌 및 그 유도체를 탈양성자화하여 시클로펜타디에니드와 유사한 리간드를 얻을 수 있다.
사용하다
플루오렌은 다른 플루오렌 화합물의 전구체이다; 모종은 거의 응용되지 않는다.플루오렌-9-카르본산은 의약품의 전구체이다.플루오렌의 산화는 상업적으로 유용한 유도체를 얻기 위해 질화된 플루오렌을 생성한다. 9-플루오렌메틸클로로포름산염(Fmoc)은 펩타이드 [3]합성의 아민에 9-플루오렌메틸카르바민산염(Fmoc) 보호기를 도입하기 위해 사용된다.
폴리플루오렌 폴리머(여기서는 한 단위의 탄소 7이 다음 단위의 탄소 2에 연결되어 있고, 두 개의 수소를 치환한다)는 전기 전도성 및 일렉트로루미네센스이며, 유기 발광 다이오드에서 광단자로서 많이 연구되어 왔다.
플루오렌 물감
플루오렌 염료가 잘 발달되어 있다.대부분은 활성 메틸렌기와 카르보닐기를 축합하여 제조되며 2-아미노플루오렌, 3,6-비스(디메틸아미노)플루오렌 및 2,7-디요오드플루오렌은 [12]염료의 전구체이다.
「 」를 참조해 주세요.
레퍼런스
- ^ Merck Index, 제11판, 4081호
- ^ International Union of Pure and Applied Chemistry (2014). Nomenclature of Organic Chemistry: IUPAC Recommendations and Preferred Names 2013. The Royal Society of Chemistry. p. 207. doi:10.1039/9781849733069. ISBN 978-0-85404-182-4.
- ^ a b c Griesbaum, Karl; Behr, Arno; Biedenkapp, Dieter; Voges, Heinz-Werner; Garbe, Dorothea; Paetz, Christian; Collin, Gerd; Mayer, Dieter; Höke (2000). "Hydrocarbons". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a13_227.
- ^ Fittig, Rud. (1873), "Uber einen neuen Kohlenwasserstoff aus dem Dipenylenketon" 베르.츠치, 화학.제6권 187.doi: 10.1002/cber.18730060169
- ^ Hicks, Latorya D.; Han, Ja Kyung; Fry, Albert J. (2000). "Hypophosphorous acid–iodine: a novel reducing system". Tetrahedron Letters. Elsevier BV. 41 (41): 7817–7820. doi:10.1016/s0040-4039(00)01359-9. ISSN 0040-4039.
- ^ D. M. Burns, John Iball(1954), 플루오렌 자연 분자 구조 173, 페이지 635. doi:10.1038/173635a0
- ^ Gerkin, R. E.; Lundstedt, A. P.; Reppart, W. J. (1984). "Structure of fluorene, C13H10, at 159 K". Acta Crystallographica Section C Crystal Structure Communications. 40 (11): 1892–1894. doi:10.1107/S0108270184009963.
- ^ Wang, Zhenlei; Richter, Henning; Howard, Jack B.; Jordan, Jude; Carlson, Joel; Levendis, Yiannis A. (2004-06-01). "Laboratory Investigation of the Products of the Incomplete Combustion of Waste Plastics and Techniques for Their Minimization". Industrial & Engineering Chemistry Research. 43 (12): 2873–2886. doi:10.1021/ie030477u. ISSN 0888-5885.
- ^ F. G. Bordwell (1988). "Equilibrium acidities in dimethyl sulfoxide solution". Acc. Chem. Res. 21 (12): 456–463. doi:10.1021/ar00156a004.
- ^ 를 클릭합니다G. W. Scherf; R. K. Brown (1960). "Potassium Derivatives of Fluorene as Intermediates in the Preparation of C9-substituted Fluorenes. I. The Preparation of 9-fluorenyl Potassium and the Infrared Spectra of Fluorene and Some C9-substituted Fluorenes". Canadian Journal of Chemistry. 38: 697. doi:10.1139/v60-100..
- ^ Ewen, J. A.; Jones, R. L.; Razavi, A.; Ferrara, J. D. (1988). "Syndiospecific Propylene Polymerizations with Group IVB Metallocenes". Journal of the American Chemical Society. 110 (18): 6255–6256. doi:10.1021/ja00226a056. PMID 22148816.
- ^ Kurdyukova, I. V.; Ishchenko, A. A. (2012). "Organic dyes based on fluorene and its derivatives". Russian Chemical Reviews. 81 (3): 258–290. Bibcode:2012RuCRv..81..258K. doi:10.1070/RC2012v081n03ABEH004211.
{{cite journal}}: CS1 maint: 작성자 파라미터 사용(링크)
외부 링크
- 미국 국립표준기술연구소 데이터베이스의 Fluorene.




