Nomenclatura de sustancias orgánicas
| ||||
Nomenclatura de Sustancias Orgánicas. El presente artículo tiene como objetivo brindar una visión global de las principales reglas que rigen la nomenclatura de compuestos orgánicos de acuerdo con la Unión Internacional de Química Pura y Aplicada (IUPAC). No se pretende tratar en forma exhaustiva todas las reglas o los posibles casos que se pueden presentar, sino más bien presentar los casos y grupos estructurales funcionales sin profundizar en estructuras muy complicadas.
Sumario
Historia
La ubicación de la Química en las ciencias naturales hace que sea considerada como una de las ciencias básicas. La química es de gran importancia en muchos campos del conocimiento, como las ciencias de materiales, la Biología, la farmacia, la medicina, la Geología, la ingeniería y la Astronomía, entre otros.
Los procesos naturales estudiados por la química involucran partículas fundamentales (electrones, protones y neutrones), partículas compuestas (núcleos atómicos, átomos y moléculas) o estructuras microscópicas como cristales y superficies.
Desde el punto de vista microscópico, las partículas involucradas en una Reacción química pueden considerarse como un sistema cerrado que intercambia energía con su entorno. En Procesos exotérmicos, el sistema libera energía a su entorno, mientras que un Proceso endotérmico solamente puede ocurrir cuando el entorno aporta energía al sistema que reacciona.
En la gran mayoría de las reacciones químicas hay flujo de energía entre el sistema y su campo de influencia, por lo cual podemos extender la definición de reacción química e involucrar la energía cinética (calor) como un reactivo o producto.
Las primeras experiencias del hombre como químico se dieron con la utilización del fuego en la transformación de la materia, la obtención de hierro a partir del mineral y de vidrio a partir de arena son claros ejemplos. Poco a poco el hombre se dio cuenta de que otras sustancias también tienen este poder de transformación.
Se dedicó un gran empeño en buscar una sustancia que transformara un metal en oro, lo que llevó a la creación de la alquimia. La acumulación de experiencias alquímicas jugó un papel vital en el futuro establecimiento de la química.
La química es una ciencia empírica, ya que estudia fenómenos por medio de la experimentación a través del método científico, es decir, por medio de la observación y la cuantificación.
En su sentido más amplio, la química estudia las diversas sustancias que existen en nuestro planeta así como las reacciones que las transforman en otras sustancias. Por otra parte, la química estudia la estructura de las sustancias a su nivel molecular o de agregados atómicos. Y por último, pero no menos importante, sus propiedades, de las cuales se derivan las diferentes aplicaciones de las sustancias y las reacciones químicas.
Subdisciplinas de la química
La Química cubre un campo de estudios bastante amplio, por lo que en la práctica se estudia de cada tema de manera particular. Las seis principales y más estudiadas ramas de la química son:
Química inorgánica
- Síntesis y estudio de las propiedades eléctricas, magnéticas y ópticas de los elementos químicos del sistema periódico y los compuestos formados por átomos que no sean de carbono (aunque con algunas excepciones). Trata especialmente los nuevos compuestos con metales de transición, los ácidos y las bases, entre otros compuestos.
- Química orgánica: Síntesis y estudio de los compuestos que se basan en cadenas de carbono, que en su gran mayoría contienen carbono formando enlaces covalentes entre carbonos.
- Bioquímica: estudia las reacciones químicas en los seres vivos, estudia el organismo y los seres vivos.
- Química física: estudia los fundamentos y bases físicas de los sistemas y procesos químicos. En particular, son de interés para el químico físico los aspectos energéticos y dinámicos de tales sistemas y procesos.
Entre sus áreas de estudio más importantes se incluyen la termodinámica química, la cinética química, la electroquímica, la mecánica estadística y la espectroscopia. Usualmente se la asocia también con la química cuántica y la química teórica.
- Química industrial: Estudia los métodos de producción de reactivos químicos en cantidades elevadas, de la manera económicamente más beneficiosa. En la actualidad también intenta aunar sus intereses iníciales, con un bajo daño al medio ambiente.
- Química analítica: Estudia los métodos de detección (identificación) y cuantificación (determinación) de una sustancia en una muestra. Se subdivide en Cuantitativa y Cualitativa.
Aunque hay una gran variedad de ramas de la química, una de las más importante y estudiada es: Química orgánica, rama de la química en la que se estudian los compuestos del carbono y sus reacciones. Existe una amplia gama de sustancias (medicamentos, vitaminas, plásticos, fibras sintéticas y naturales, hidratos de carbono, proteínas y grasas) formadas por moléculas orgánicas.
Los químicos orgánicos determinan la estructura de las moléculas orgánicas, estudian sus reacciones y desarrollan procedimientos para sintetizar compuestos orgánicos.
Esta rama de la química ha afectado profundamente a la vida en el Siglo XX: ha perfeccionado los materiales naturales y ha sintetizado sustancias naturales y artificiales que, a su vez, han mejorado la salud, han aumentado el bienestar y han favorecido la utilidad de casi todos los productos utilizados en la actualidad.
Los compuestos orgánicos son todas las especies químicas que en su composición contienen el elemento carbono y, usualmente, elementos tales como el Oxígeno (O), Hidrógeno (H), Fósforo (F), Cloro (CL), Yodo (I) y Nitrógeno (N), con la excepción del Anhídrido carbónico, los carbonatos y los cianuros.
Estos compuestos constituyen la mayor cantidad de sustancias que se encuentran sobre la tierra. Contienen desde un átomo de carbono como el gas metano CH4 que utilizamos como combustible, hasta moléculas muy grandes o macromoléculas con cientos de miles de átomos de carbono como el almidón, las proteínas y los ácidos nucléicos.
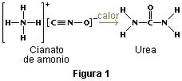
La aparición de la química orgánica se asocia a menudo al descubrimiento en 1828 por parte del químico alemán Friedrich Wöhler, de que la sustancia inorgánica cianato de amonio podía convertirse en Urea, una sustancia orgánica que se encuentra en la orina de muchos animales.
Antes de este descubrimiento, los químicos creían que para sintetizar sustancias orgánicas, era necesaria la intervención de lo que llamaban 'la fuerza vital' es decir, los organismos vivos.
El experimento de Wöhler rompió la barrera entre sustancias orgánicas e inorgánicas. Los químicos modernos consideran compuestos orgánicos a aquellos que contienen carbono y otros elementos (que pueden ser uno o más), siendo los más comunes: hidrógeno, oxígeno, nitrógeno, Azufre y los Halógenos. En la actualidad, a la química orgánica se la llama también química del carbono. Fig.1
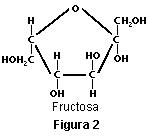
Ni siquiera un análisis que proporcione los porcentajes de carbono, hidrógeno y oxígeno, puede distinguir el C6H12O6 de la fructosa del C5H10O5 de la ribosa, otro azúcar con la misma proporción entre sus elementos (1:2:1).
Las fuerzas que mantienen unidos a los átomos en una molécula son los enlaces químicos, y pueden ser de tres tipos: Iónico, Covalente y Metálico.
La capacidad del carbono para formar enlaces covalentes con otros átomos de carbono en largas cadenas y ciclos, distingue al carbono de los demás elementos. No se conocen otros elementos que formen cadenas con más de ocho átomos.
Esta propiedad del carbono, y el hecho de que pueda formar hasta cuatro enlaces con otros átomos, explica el gran número de compuestos conocidos. Al menos un 80% de los 5 millones de compuestos químicos registrados a principios de la década de 1980 contenían carbono.
Clasificación y nomenclatura
Las consecuencias de las propiedades únicas del carbono se ponen de manifiesto en el tipo más sencillo de compuestos orgánicos, los Hidrocarburos alifáticos o de cadena abierta. Alcanos.
Nomenclatura alifática simple
Los Compuestos alifáticos son el grupo más simple de los compuestos orgánicos. Sólo contienen hidrógeno y carbono, y generalmente forman cadenas abiertas. Los nombres de los compuestos describen su identidad.
El prefijo indica cuántos carbonos hay en la cadena, y el sufijo a cuál de los tres grupos funcionales pertenece una cadena. Por ejemplo, los compuestos con el prefijo pent- tienen siempre cinco carbonos, pero el penteno es un alqueno con un doble enlace, mientras que el pentano es un alcano con enlaces simples. El compuesto más sencillo de la serie de los alcanos es el Metano, CH4. Los siguientes miembros de la serie son: Etano (C2H6), Propano (C3H8) y Butano (C4H10); la fórmula general de cualquier miembro de esta familia es CnH2n+2.
Para los compuestos que contienen más de cuatro átomos de carbono, se usan los prefijos numéricos griegos y el sufijo -ano: Hexano, Heptano, Octano, y así sucesivamente.
Sin embargo, los nombres butano, pentano, etc..., no especifican la estructura molecular. Por ejemplo, pueden escribirse dos fórmulas estructurales distintas para la fórmula molecular C4H10.
Los compuestos con la misma fórmula molecular pero distinta fórmula estructural se llaman Isómeros. En el caso del butano, los nombres usuales para los isómeros son el butano normal y el metilpropano (antiguamente isobutano). La urea y el cianato de amonio también son isómeros estructurales de fórmula molecular CH4N2O. Fig. 3
La fórmula C8H18 tiene 18 isómeros y la C20H42 tiene 366.319 isómeros teóricos. Por este motivo, cuando se descubren nuevos compuestos, los nombres poco sistemáticos o triviales usados comúnmente deben ceder su puesto a nombres sistemáticos que puedan utilizarse en todos los idiomas. La Unión Internacional de Química Pura y Aplicada (IUPAC) acordó en 1890 un sistema de nomenclatura, y lo ha revisado posteriormente en numerosas ocasiones para incorporar nuevos descubrimientos.
En el sistema de nomenclatura de la IUPAC, se numera la cadena más larga de átomos de carbono de forma que los números de las cadenas laterales proporcionen la suma menor. Las tres cadenas laterales del primer compuesto de la figura 4 están en los átomos de carbono 2, 2 y 4; si la cadena se numera en sentido opuesto, las cadenas laterales estarían en los átomos de carbono 2, 4 y 4. Por tanto, el nombre correcto es 2,2,4-trimetilpentano. Fig.4
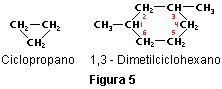
Entre los Hidrocarburos existen también estructuras cíclicas o ciclos, por ejemplo la de la familia de los ciclanos o cicloalcanos; el ciclo menor contiene tres átomos de carbono. La fórmula general de los cicloalcanos es CnH2n, y los nombres de la IUPAC son consistentes con los de los alcanos. Fig.5
Alquenos y alquinos
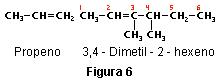
Los alquenos son isómeros de los cicloalcanos y se representan por la fórmula general CnH2n. Esta familia de hidrocarburos se caracteriza por contener uno o más dobles enlaces entre los átomos de carbono. Por ejemplo, el propeno y el ciclopropano son isómeros, igual que el 1,3-dimetilciclohexano y el 3,4-dimetil-2-hexeno. (La posición del doble enlace se indica con '2-hexeno'). Los dobles enlaces también pueden presentarse en los compuestos cíclicos, por ejemplo en el α-pineno, un componente de la trementina, y en la vitamina A. Fig.6
Se suelen utilizar notaciones simbólicas para escribir las fórmulas estructurales de los compuestos orgánicos cíclicos. Los vértices de los ángulos de esas fórmulas representan átomos de carbono.
Se sobreentiende que cada átomo de carbono está unido a 2, 1 o 0 átomos de hidrógeno, dependiendo de si tiene 2, 3 o 4 enlaces, respectivamente, con otros átomos (normalmente de carbono). Como ejemplo, ver en la figura 7 la fórmula estructural completa del a-pineno. Fig.7
Los alquinos o acetilenos, la tercera familia más importante de los hidrocarburos alifáticos, tienen la fórmula general CnH2n-2, y contienen aún menos átomos de hidrógeno que los alcanos o los alquenos. El acetileno, HC¿CH, que es el ejemplo más común, se denomina etino en el sistema de la IUPAC.
En un alcano, los átomos de hidrógeno pueden ser sustituidos por otros átomos (de cloro, oxígeno o nitrógeno, por ejemplo), siempre que se respete el número correcto de enlaces químicos (el cloro forma un enlace sencillo con los otros átomos, el oxígeno forma dos enlaces y el nitrógeno forma tres). El átomo de cloro en el cloruro de etilo, el grupo OH en el alcohol etílico y el grupo NH2 en la etilamina se llaman grupos funcionales. Estos grupos funcionales determinan la mayoría de las propiedades químicas de los compuestos. En la tabla adjunta se muestran otros grupos funcionales con sus fórmulas generales, prefijos o sufijos que se añaden a los nombres, y un ejemplo de cada clase.
Isómeros ópticos y geométricos. La Estructura tetraédrica de los enlaces del carbono dicta algunas propiedades de los compuestos orgánicos que sólo pueden explicarse por medio de las relaciones espaciales. Cuando cuatro grupos distintos de átomos están unidos a un átomo de carbono central, pueden construirse dos moléculas diferentes en el espacio. Por ejemplo, el ácido láctico (ver figura 9) existe en dos formas; este fenómeno es conocido como isomería óptica.
Los isómeros ópticos se relacionan del mismo modo que un objeto y su imagen en el espejo: el CH3 de uno refleja la posición del CH3 del otro, el OH refleja al OH, ... al igual que un espejo colocado ante un guante de la mano derecha refleja la imagen de un guante de la mano izquierda.
Los isómeros ópticos tienen exactamente las mismas propiedades químicas y físicas, excepto una: la dirección en que cada isómero gira el plano de la luz polarizada (véase Óptica).
El Ácido dextroláctico, o Ácido D-láctico, gira el plano de la luz polarizada a la derecha, y el Ácido levoláctico, o Ácido L-láctico, a la izquierda. El ácido láctico racémico (una mezcla 1:1 de ácido D-láctico y ácido L-láctico) presenta una rotación cero porque los giros hacia derecha e izquierda se cancelan mutuamente.
Los dobles enlaces en los compuestos del carbono dan lugar a la isomería geométrica (que no tiene relación con la isomería óptica) si cada carbono del doble enlace está unido a grupos distintos.
Por ejemplo, una molécula de 2-hepteno puede estar distribuida en dos formas distintas en el espacio porque la rotación alrededor del doble enlace está restringida. Cuando los grupos iguales (átomos de hidrógeno en este caso) están en partes opuestas de los átomos de carbono unidos por el doble enlace, el isómero se llama trans y cuando los grupos iguales están en la misma parte, el isómero se llama cis.
Saturación
Los compuestos que contienen dobles o triples enlaces se llaman compuestos insaturados. Estos compuestos pueden experimentar reacciones de adición con varios reactivos que hacen que los dobles o triples enlaces sean sustituidos por enlaces simples. Las reacciones de adición convierten los compuestos insaturados en saturados. Aunque estos últimos son por lo general más estables que los insaturados, dos dobles enlaces en la misma molécula pueden producir menos inestabilidad si están separados por un enlace simple; a estos dobles enlaces se les llama conjugados.
El Isopreno, que es la base que forma el caucho (o hule) natural, tiene esta estructura conjugada, igual que la vitamina A y el retinal, compuestos importantes en el proceso de la visión. La conjugación completa en un ciclo de seis átomos de carbono tiene un efecto más profundo; su influencia estabilizadora es tan fuerte que el compuesto deja de actuar como insaturado. Es el caso del benceno, C6H6, y la familia de compuestos cíclicos denominados hidrocarburos aromáticos.
De hecho, las propiedades de los compuestos aromáticos son tan distintas, que el símbolo más apropiado para el benceno es el hexágono de la derecha de la figura 13, y no los otros dos. El círculo dentro del hexágono sugiere que los seis electrones representados como tres dobles enlaces conjugados pertenecen a todo el hexágono, y no a los carbonos individuales en los ángulos del hexágono. En la figura 14 se muestran también otros compuestos aromáticos.
Las Moléculas cíclicas pueden contener átomos de elementos distintos al carbono; se llaman hetero átomos y los más comunes son el azufre, el nitrógeno y el oxígeno, aunque se conocen otros como el boro, el fósforo y el selenio.
Fuentes de compuestos orgánicos.El alquitrán de hulla era antiguamente la única fuente de compuestos aromáticos y de algunos heterocíclicos. El petróleo era la fuente de compuestos alifáticos, contenidos en ciertas sustancias como la gasolina, el queroseno y el aceite lubricante.
El Gas natural suministraba metano y etino. Estas tres categorías de sustancias naturales siguen siendo las principales fuentes de compuestos orgánicos en la mayoría de los países. Sin embargo, cuando no se dispone de petróleo, una industria química puede funcionar a base de etino, que a su vez puede ser sintetizado a partir de la caliza y el carbón.
Durante la II Guerra Mundial, Alemania tuvo que adoptar esa solución cuando le fueron cortadas las fuentes de petróleo y gas natural. El azúcar de mesa procedente de la caña o la remolacha es el producto químico puro más abundante extraído de una fuente vegetal. Otras sustancias importantes derivadas de los vegetales son los hidratos de carbono (como la celulosa), los alcaloides, la cafeína y los aminoácidos. Los animales se alimentan de vegetales y de otros animales para sintetizar aminoácidos, proteínas, grasas e hidratos de carbono.
Propiedades físicas de los compuestos orgánicos
En general, los compuestos orgánicos covalentes se distinguen de las sales inorgánicas en que tienen puntos de fusión y ebullición más bajos. Por ejemplo, el compuesto iónico cloruro de sodio (NaCl) tiene un punto de fusión de unos 800 °C, pero el tetra cloruro de carbono (CCl4), molécula estrictamente covalente, tiene un punto de fusión de 76,7 °C.
Entre esas temperaturas se puede fijar arbitrariamente una línea de unos 300 °C para distinguir la mayoría de los compuestos covalentes de los iónicos. Gran parte de los compuestos orgánicos tienen los puntos de fusión y ebullición por debajo de los 300 °C, aunque existen excepciones. Por lo general, los compuestos orgánicos se disuelven en disolventes no polares (líquidos sin carga eléctrica localizada) como el octano o el tetra cloruro de carbono, o en disolventes de baja polaridad como los alcoholes, el ácido etanoico (ácido acético) y la propanona (acetona).
Los compuestos orgánicos suelen ser insolubles en agua, un disolvente fuertemente polar.Los hidrocarburos tienen densidades relativas bajas, con frecuencia alrededor del 0,8, pero los grupos funcionales pueden aumentar la densidad de los compuestos orgánicos. Sólo unos pocos compuestos orgánicos tienen densidades mayores de 1,2, y son generalmente aquellos que contienen varios átomos de halógenos.
Los grupos funcionales capaces de formar enlaces de hidrógeno aumentan generalmente la viscosidad (resistencia a fluir). Por ejemplo, las viscosidades del etanol, 1,2-etanodiol (etilenglicol) y glicerina aumentan en ese orden. Estos compuestos contienen uno, dos y tres grupos OH respectivamente, que forman enlaces de hidrógeno fuertes.
Fuentes
Referencias Bibliográficas
- René Planche Jardines. MsC. en Química Inorgánica. Profesor Auxiliar. Departamento de Química, Universidad de Guantánamo.
- Andrés Caballero y Froilan Ramos.2DO AÑO CICLO DIVERSIFICADO CIENCIAS Y CICLO PROFESIONAL. Editorial: Distribuidora Escolar S.A.
- Margarita Cuesta Piz. Química Orgánica. Registrado con el ISBN 978-959-13-2096-4 en la Cámara Cubana del Libro. Publicado por Editorial Pueblo y Educación en el año 2014 en la ciudad de Playa, en Cuba.
- Rolando Miguel Bermejo Correa. OM Química FOC I. Publicado por Editorial Pueblo y Educación en el año 2012 en la ciudad de Playa, en Cuba.
- Rolando Miguel Bermejo Correa. OM Química FOC II. Publicado por Editorial Pueblo y Educación en el año 2014 en la ciudad de Playa, en Cuba.
- Pérez Álvarez, F. e Y. J. Hedesa Pérez “El experimento en el proceso de enseñanza aprendizaje de la Química”. Didácticas de las Ciencias Nuevas perspectivas. Tercera parte ISBN 978-959-18-0542-3, 2010 P. 100
- Delgado Yanes, N. y Y. Reyes Cárdenas. El uso del software educativo en los laboratorios escolares de Química. Memorias del VIII Congreso Internacional Didácticas de las Ciencia y XIII Taller Internacional de la Enseñanza de la Física. Palacio de Convenciones. La Habana, Cuba. ISBN: 978-959-18-0973-5, 2014
- Colectivo de autores. Libro: Química orgánica. Castellón de la Plana, España: Editorial Universidad Jaume I. 2005
- Rojas Arce, C. y otros. “Metodología de la enseñanza de la Química” Editorial Pueblo y Educación, ISBN 978-959-13-0656-2, segunda edición, pág. 295. 2010.