Cefuroxime
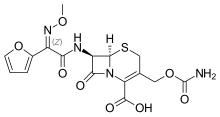 | |
 | |
| Dữ liệu lâm sàng | |
|---|---|
| Tên thương mại | Zinacef, Ceftin, others |
| AHFS/Drugs.com | Chuyên khảo |
| MedlinePlus | a601206 |
| Danh mục cho thai kỳ |
|
| Dược đồ sử dụng | Intramuscular, intravenous, by mouth |
| Nhóm thuốc | Second-generation cephalosporin |
| Mã ATC | |
| Tình trạng pháp lý | |
| Tình trạng pháp lý |
|
| Dữ liệu dược động học | |
| Sinh khả dụng | 37% on an empty stomach, up to 52% if taken after food |
| Chu kỳ bán rã sinh học | 80 minutes |
| Bài tiết | Urine 66–100% unchanged |
| Các định danh | |
Tên IUPAC
| |
| Số đăng ký CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| Định danh thành phần duy nhất | |
| KEGG | |
| ChEMBL | |
| ECHA InfoCard | 100.054.127 |
| Dữ liệu hóa lý | |
| Công thức hóa học | C16H16N4O8S |
| Khối lượng phân tử | 424,38 g·mol−1 |
| Mẫu 3D (Jmol) | |
SMILES
| |
Định danh hóa học quốc tế
| |
| (kiểm chứng) | |
Cefuroxime là một thuốc kháng sinh cephalosporin thế hệ thứ hai. Thuốc do Glaxo, hiện tại là GlaxoSmithKline phát hiện và đưa ra thị trường đầu tiên vào năm 1978 dưới tên thương mại Zinacef. Thuốc nhận được sự chấp thuận của FDA vào tháng 10 năm 1983.[1] GlaxoSmithKline bán loại kháng sinh này ở Anh, Úc, Thổ Nhĩ Kỳ, Israel, Bangladesh, Thái Lan và Ba Lan dưới tên Zinnat.
Tác dụng
[sửa | sửa mã nguồn]Cũng như các cephalosporin khác, cefuroxime nhạy cảm với beta-lactamase, mặc dù yếu hơn. Do đó, thuốc có tác dụng chống lại Haemophilus influenzae, Neisseria gonorrhoeae, và bệnh Lyme. Không giống như hầu hết các cephalosporin thế hệ thứ hai khác, cefuroxime có thể đi qua hàng rào máu não.
Một nghiên cứu hệ thống cho thấy bằng chứng cao rằng nhỏ mắt với cefuroxime sau khi phẫu thuật đục thủy tinh thể sẽ làm giảm tình trạng viêm nội nhãn (endophthalmitis) sau phẫu thuật.[2]
Tác dụng phụ
[sửa | sửa mã nguồn]Cefuroxime nói chung thường hấp thu tốt và ít tác dụng phụ. Nếu uống sau ăn, kháng sinh này được hấp thụ tốt hơn và giảm khả năng gây ra tác dụng phụ như tiêu chảy, buồn nôn, nôn mửa, nhức đầu/đau nửa đầu, chóng mặt và đau bụng so với hầu hết thuốc kháng sinh nhóm này.[cần dẫn nguồn]
Mặc dù có khoảng 10% nguy cơ dị ứng chéo giữa cephalosporin và penicillin, những đánh giá gần đây đã cho thấy không có hiện tượng tăng nguy cơ phản ứng dị ứng chéo của cefuroxime và một số thuốc thế hệ thứ hai hay các nhóm cephalosporin thế hệ sau.[3] GSK had continued marketing a pediatric oral suspension as Ceftin; however, this presentation was discontinued as of ngày 24 tháng 6 năm 2017.[4]
Tên thương mại
[sửa | sửa mã nguồn]Ở US, thuốc có tên Zinacef phân phối bởi Covis Pharmaceuticals.[3]
Ở Bangladesh, thuốc có tên Kilbac phân phối bởi Incepta và Xorimax phân phối bởi Sandoz. Ở Ấn Độ, thuốc có tên Ceftum dưới dạng vỉ và Supacef dưới dạng tiêm phân phối bởi GSK.[5] Ở Ba Lan, thuốc có tên Zamur phân phối bởi Mepha, chi nhánh của Tập đoàn Dược phẩm Teva.[6]
Tham khảo
[sửa | sửa mã nguồn]- ^ “Cefuroxime medical facts from”. Drugs.com.
- ^ Gower EW, Lindsley K, Tulenko SE, Nanji AA, Leyngold I, McDonnell PJ (2017). “Perioperative antibiotics for prevention of acute endophthalmitis after cataract surgery”. Cochrane Database Syst Rev. 2: CD006364. doi:10.1002/14651858.CD006364.pub3. PMC 5375161. PMID 28192644.
- ^ a b “Bản sao đã lưu trữ” (PDF). Bản gốc (PDF) lưu trữ ngày 8 tháng 8 năm 2014. Truy cập ngày 25 tháng 8 năm 2018.
- ^ https://www.accessdata.fda.gov/scripts/drugshortages/dsp_ActiveIngredientDetails.cfm?AI=Cefuroxime+Axetil+%28Ceftin%29+Oral+Suspension&st=d&tab=tabs-2
- ^ “GlaxoSmithKline Pharmaceuticals Limited – Prescription Medicines – Anti-Infective”. Gsk-india.com. ngày 26 tháng 3 năm 2013. Bản gốc lưu trữ ngày 22 tháng 3 năm 2016. Truy cập ngày 25 tháng 8 năm 2018.
- ^ “Charakterystyka produktu lecznicznego” (PDF). Urząd Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych. ngày 12 tháng 11 năm 2015.
