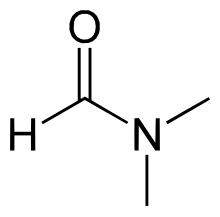
Dimetilformamid
| |
| Adlandırmalar | |
|---|---|
N,N-Dimethylformamide | |
N,N-Dimethylmethanamide | |
Diğer adlar DMF, Dimethylformamide | |
| Tanımlayıcılar | |
3D model (JSmol)
|
|
| Kısaltmalar | DMF |
| ECHA InfoCard | 100.000.617 |
| MeSH | Dimethylformamide |
PubChem CID
|
|
| UN numarası | 2265 |
CompTox Bilgi Panosu (EPA)
|
|
| |
| Özellikler | |
| Kimyasal formül | C3H7NO |
| Molekül kütlesi | 73,09 g mol−1 |
| Görünüm | renksiz sıvı |
| Yoğunluk | 0,948 |
| Erime noktası | -60,5°C |
| Kaynama noktası | 152°C |
| Çözünürlük (su içinde) | suyla karışır |
| log P | -0,829 |
| Buhar basıncı | 516 Pa |
| Tehlikeler | |
| NFPA 704 (yangın karosu) |
|
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa).
| |
| Bilgi kutusu kaynakları | |
Dimetilformamid ya da kısaca DMF, (CH
3)
2NC(O)H formüllü bir organik bileşik. Su ve birçok organik madde ile karışabilen renksiz bir sıvıdır. DMF bir organik çözücüdür. Saf DMF kokusuzdur ancak ticarî tip DMF dimetilamine bozunmadan dolayı kötü bir kokuya sahip olabilir. Bozunma kalıntıları argon gibi inert gazlarla temizlenebilir. Adından da anlaşılacağı üzere dimetilformamid formik asitin amididir. DMF yüksek kaynama noktasına sahip polar aprotik bir çözücüdür.
Üretimi
[değiştir | kaynağı değiştir]DMF ilk olarak 1893'te Fransız kimyager Albert Verley tarafından dimetilamin hidroklorür ve potasyum format karışımının damıtılması ile elde edilmiştir. DMF dimetilamin ve metil formatın birleşimi ya da karbonmonoksit ve dimetilaminin tepkimesi ile hazırlanır.
Kullanım alanları
[değiştir | kaynağı değiştir]DMF'in ana kullanım alanı düşük buharlaşma hızına sahip olarak solventtir. DMF akrilik lifler ve plastiklerin üretiminde kullanılır.

