WO1994001401A1 - Herbizide und insektizide 3-benzoyl-pyrrolidin-2,4-dion-derivate - Google Patents
Herbizide und insektizide 3-benzoyl-pyrrolidin-2,4-dion-derivate Download PDFInfo
- Publication number
- WO1994001401A1 WO1994001401A1 PCT/EP1993/001690 EP9301690W WO9401401A1 WO 1994001401 A1 WO1994001401 A1 WO 1994001401A1 EP 9301690 W EP9301690 W EP 9301690W WO 9401401 A1 WO9401401 A1 WO 9401401A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- alkyl
- alkoxy
- halogen
- substituted
- optionally
- Prior art date
Links
- 0 *C(C1)=CC=C(C(N)=O)C(*)=*1[Zn] Chemical compound *C(C1)=CC=C(C(N)=O)C(*)=*1[Zn] 0.000 description 2
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/34—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with one nitrogen atom as the only ring hetero atom
- A01N43/36—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with one nitrogen atom as the only ring hetero atom five-membered rings
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/34—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with one nitrogen atom as the only ring hetero atom
- A01N43/36—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with one nitrogen atom as the only ring hetero atom five-membered rings
- A01N43/38—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with one nitrogen atom as the only ring hetero atom five-membered rings condensed with carbocyclic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D207/00—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D207/02—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D207/30—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having two double bonds between ring members or between ring members and non-ring members
- C07D207/34—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having two double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D207/36—Oxygen or sulfur atoms
- C07D207/38—2-Pyrrolones
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/02—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom condensed with one carbocyclic ring
- C07D209/54—Spiro-condensed
Definitions
- the invention relates to new substituted 3-benzoyl-pyrrolidine-2,4-dione derivatives, several processes for their preparation, new intermediates for their preparation and their use as herbicides, insecticides and acaricides.
- WO 8804-652 describes 3-benzoyl-furan-2-one derivatives with herbicidal properties, including the compound 3- (2,4-dichlorobenzoyl) -4-hydroxy-6-methyl-N-methyl-pyridone- 2nd
- B for hydrogen, optionally substituted by halogen, alkyl, cycloalkyl, alkoxyalkyl, alkylthioalkyl or optionally by alkyl,
- a and B together with the atoms to which they are attached form a saturated or unsaturated cycle which may be substituted by halogen or optionally halogenated alkyl or alkoxy and which may be interrupted by oxygen and / or sulfur, or in which
- R 3 represents alkyl with amino acid esters of the general formula (III)
- A, B and C have the meanings given above and R 4 represents alkyl, optionally condensed in the presence of a solvent and in the presence of a base, or that B) compounds of the formula (Ia)
- A, B, C, X, Y, Z and n have the meanings given above, optionally rearranged in the presence of a diluent, optionally in the presence of a base and optionally in the presence of a suitable catalyst,
- L represents halogen, -OSO 2 -alkyl, -OSO 2 O-alkyl or -OSO 2 -aryl,
- M represents halogen, -OE 3 , CN, O-SO 2 alkyl, O-SO 2 aryl and imidazolyl, if appropriate in the presence of a diluent and if appropriate in the presence of a base, or that Compounds of the general formula (Id)
- Me stands for mono- or divalent metal ions
- s and t stand for the numbers 1 and 2 and R 4 , R 5 and R 6 independently of one another represent hydrogen and alkyl, optionally in the presence of a diluent.
- X represents hydrogen, C 1 -C 6 alkyl, halogen, C 1 -C 6 alkoxy, C 1 -C 6 haloalkyl, C 1 -C 6 haloalkoxy, nitro, C 1 - C 6 alkoxycarbonyl, C 1 -C 6 -Carboxy, Cyano or
- S (O) m -R 1 stands for Y, hydrogen, C 1 -C 6 alkyl, halogen, C 1 -C 6 alkoxy, C 1 -C 4 haloalkyl, C 1 -C 6 haloalkoxy, nitro, C 1 -C 6 alkoxycarbonyl, C 1 -C 6 carboxy, cyano or S (O) mR 1 , Z represents C 1 -C 6 alkyl, halogen, C 1 -C 6 alkoxy, C 1 -C 6 - haloalkyl, C 1 -C 6 haloalkoxy, C 1 -C 6 alkoxy C 2 -C 6 alkyl, C 1 -C 6 haloalkoxy-C 2 -C 6 alkyl, C 1 - C 6 alkoxy-C 2 -C 6 haloalkyl, C 1 -C 6 alkoxycarbonyl or C 1 -C 6 haloalkoxycarbonyl,
- A represents hydrogen or optionally substituted by halogen, straight-chain or branched C 1 -C 12 alkyl, C 3 -C 8 alkenyl, C 3 -C 8 alkynyl, C 1 -C 10 alkoxy-C 2 -C 8 alkyl , C 1 -C 8 polyalkoxy-C 2 -C 8 alkyl, C 1 -C 10 alkylthio-C 2 -C 8 alkyl, cycloalkyl with 3-8 ring atoms, which can be interrupted by oxygen and / or sulfur or phenyl or arylC 1 -C 6 alkyl optionally substituted by halogen, C 1 -C 6 alkyl, C 1 -C 6 haloalkyl, C 1 -C 6 alkoxy, nitro,
- B for hydrogen, straight-chain or branched and optionally substituted by halogen C 1 -C 62 -alkyl, C 1 -C 8 alkoxy-C 1 -C 8 alkyl, C 1 -C 8 alkyl-C 1 -C 8 - thioalkyl, cycloalkyl with 3-8 ring atoms, which can be interrupted by oxygen and / or sulfur, or optionally by halogen, C 1 -C 6 alkyl, C 1 -C 6 haloalkyl, C 1 -C 6 alkoxy, nitro substituted phenyl or aryl-C 1 -C 6 -alkyl,
- C represents hydrogen or C 1 -C 12 alkyl optionally substituted by halogen, or in which A and B together with the atoms to which they are attached form a 5 to 8-membered saturated or unsaturated cycle which is interrupted by oxygen and / or sulfur and by optionally halogenated C 1 -C 6 -alkyl, C 1 -C 6 -alkoxy or halogen may be substituted, or wherein
- Halogen or optionally halogenated C 1 -C 6 alkyl, C 1 -C 6 alkoxy may be substituted
- E 2 C 1 -C 12 alkyl, C 2 -C 6 haloalkyl, C 3 -C 8 alkenyl, C 3 -C 8 alkynyl, C 3 -C 8 haloalkenyl, C 3 - C 8 - Halogenalkynyl, C 1 -C 6 alkoxy-C 2 -C 6 alkyl, C 1 -C 6 - haloalkoxy-C 2 -C 6 alkyl, aryl-C 1 -C 6 alkyl,
- E 4 a metal ion or a metal equivalent, R 1 is optionally substituted by halogen
- X represents hydrogen, C 1 -C 4 alkyl, halogen, C 1 -C 4 alkoxy, C 1 -C 4 haloalkyl, C 1 -C 4 haloalkoxy,
- Y for hydrogen, C 1 -C 6 alkyl, halogen, C 1 -C 4 alkoxy, C 1 -C 3 haloalkyl, C 1 -C 4 haloalkoxy, nitro, C 1 -C 4 alkoxycarbonyl, carboxy, Cyano or S (O) m -R 1 ,
- n stands for a number from 0-3, m represents a number from 0-2,
- Sulfur atoms can be interrupted or optionally substituted by halogen, C 1 -C 4 alkyl, C 1 -C 4 haloalkyl, C 1 -C 4 alkoxy or nitro
- B for hydrogen, straight-chain or branched and optionally substituted by halogen C 1 -C 10 alkyl, C 1 -C 6 alkoxy-C 1 -C 6 alkyl, C 1 -C 6 alkylthio-C 1 - C 6 - alkyl, cycloalkyl with 3-7 ring atoms which can be interrupted by 1-2 oxygen and / or sulfur atoms or optionally by halogen, C 1 -C 4 alkyl, C 1 -C 4 haloalkyl, C 1 -C 4 alkoxy or Nitro substituted phenyl or aryl-C 1 -C 4 alkyl,
- C represents hydrogen or C 1 -C 8 -alkyl optionally substituted by halogen, or in which
- R 1 represents optionally halogen-substituted C 1 - C 6 alkyl or optionally substituted by fluorine, chlorine, bromine, nitro, cyano, C 1 -C 3 alkoxy, C 1 -C 3 haloalkoxy, C 1 -C 3 - Alkylthio, C 1 -C 3 haloalkylthio, C 1 - C 3 alkyl, C 1 -C 3 haloalkyl substituted phenyl, and
- R 2 represents optionally halogen-substituted C 1 - C 6 alkyl, C 1 -C 6 alkoxy, C 1 -C 6 alkylthio, C 2 -C 6 alkenyl, C 1 -C 6 -alkoxy-C 2 - C 6 alkyl or for phenyl optionally substituted by halogen, C 1 -C 5 haloalkyl, C 1 -C 6 alkyl or C 1 -Cg alkoxy, for optionally substituted by halogen, C 1 -Cg alkyl, C 1 - C 5 haloalkyl or C 1 -C 5 alkoxy substituted arylC 1 - C 4 alkyl.
- A represents hydrogen, optionally halogen-substituted straight-chain or branched C 1 -C 8 - alkyl, C 3 -C 4 alkenyl, C 3 -C 4 alkynyl, C 1 -C 6 alkoxy C 2 -C 4 alkyl , C 1 -C 4 polyalkoxy-C 2 -C 4 alkyl, C 1 -C 6 alkylthio-C 2 -C 4 alkyl, cycloalkyl with 3-6 ring atoms, which is replaced by 1-2 oxygen and / or Sulfur atoms can be interrupted or optionally substituted by fluorine, chlorine, bromine, methyl, ethyl, propyl, iso-propyl, methoxy, ethoxy, trifluoromethyl, nitro or aryl-C 1 - C 3 alkyl,
- B for hydrogen, straight-chain or branched and optionally substituted by halogen C 1 -C 8 alkyl, C 1 -C 4 alkoxy-C 1 -C 4 alkyl, C 1 -C 4 alkylthio-C 1 - C 4 - alkyl, cycloalkyl with 3-6 ring atoms, which can be interrupted by 1-2 oxygen and / or sulfur atoms or optionally by halogen, C 1 -C 4 alkyl, C 1 -C 4 haloalkyl, C 1 -C 4 alkoxy or nitro substituted phenyl or aryl-C 1 -C 3 alkyl,
- C represents hydrogen, C 1 -C 6 alkyl or C 1 -C 6 haloalkyl, or wherein
- a and B together with the atoms to which they are attached form a 5 to 6-membered saturated or unsaturated cycle which is substituted by C 1 -C 3 alkyl, C 1 -C 3 alkoxy, fluorine or chlorine and which may be interrupted by oxygen and / or sulfur, or wherein
- E 2 C 1 -C 6 alkyl, C 2 -C 3 haloalkyl, C 3 -C 4 alkenyl, C 3 -C 4 alkynyl, C 3 -C 4 haloal kenyl, C 3 -C 4 haloalkynyl, C 1 -C 3 alkoxy-C 2 -C 3 ⁇ alkyl, C 1 -C 3 haloalkoxy-C 2 - C 3 alkyl, aryl-C 1 -C 3 - alkyl stands,
- E 4 Li ⁇ , Na ⁇ , K ⁇ , NH 4 ⁇ , C 1 -C 4 alkyl optionally substituted by fluorine or optionally fluorine, chlorine, bromine, nitro, cyano, C 1 -C 2 - Alkoxy, C 1 -C 2 fluoroalkoxy, C 1 -C 2 chloroalkoxy, C 1 -C 2 alkylthio, C 1 -C 2 fluoroalkylthio, C 1 -C 2 chloroalkylthio, C 1 -C 3 alkyl, C 1 -C 2 fluoroalkyl, C 1 -C 2 difluoroalkyl, C 1 -C 2 trifluoroalkyl, C 1 -C 2 chloroalkyl, C 1 -C 2 dichloroalkyl, C 1 -C 2 trichloroalkyl substituted phenyl , R 2 for optionally by fluorine, chlorine, bromine, nitro,
- C 1 -C 4 alkyl substituted C 1 -C 4 alkyl, C 1 -C 4 alkoxy, C1 -C 4 alkylthio, C 1 -C 4 alkoxy- (C 2 -C 4 ) alkyl or for optionally by fluorine, chlorine, bromine, Trif luormethyl, C j -C 4 ⁇ alkyl or C 1 -C 4 alkoxy substituted phenyl, for aryl optionally substituted by fluorine, chlorine, bromine, C 1 -C 4 alkyl, trif luormethyl or C 1 -C 4 alkoxy -C 1 -C 2 alkyl.
- A, B, C and R 4 have the meanings given above, are known in some cases or can be prepared by known processes, as described in the literature, if, for example, ⁇ -halocarboxylic acids or esters are reacted with amines (Advanced Organic Chemistry, J. March, S, 377 (Mc Graw-Hill Inc. 1977).
- the compounds of the formula (IV) required as starting materials in process (B) above are known in some cases or can be prepared by known processes, as described in the literature, if, for example, ⁇ -halocarboxylic acids or esters are reacted with amines (Advanced Organic Chemistry, J. March, S, 377 (Mc Graw-Hill Inc. 1977).
- A, B, C, X, Y, Z and n have the meanings given above, are new and are also part of the claim.
- M represents halogen or cyano in the presence of a diluent and optionally in the presence of a base.
- Process (A) is characterized in that
- Tetralin, mesitylene, triisopropylbenzene also ethers, such as dibutyl ether, tetrahydrofuran, dioxane, glycol dimethyl ether and diglycol dimethyl ether, and also polar solvents, such as dimethyl sulfoxide, sulfolane, dimethylformamide and N-methyl-pyrrolidone.
- ethers such as dibutyl ether, tetrahydrofuran, dioxane, glycol dimethyl ether and diglycol dimethyl ether
- polar solvents such as dimethyl sulfoxide, sulfolane, dimethylformamide and N-methyl-pyrrolidone.
- Deprotonating agents which can be used when carrying out process (a) according to the invention are all customary
- Proton acceptors are used.
- Alkali metal and alkaline earth metal oxides, hydroxides and carbonates, such as sodium hydroxide, potassium hydroxide, magnesium oxide, calcium oxide, sodium carbonate, are preferably usable.
- Potassium carbonate and calcium carboate which can also be used in the presence of phase transfer catalysts such as e.g. Triethylbenzylammoniumchlorid, Tetrabutylammoniumbromid, Adogen 464 and TDA 1 can be used.
- phase transfer catalysts such as e.g. Triethylbenzylammoniumchlorid, Tetrabutylammoniumbromid, Adogen 464 and TDA 1
- Alkali metal and alkaline earth metal amides and hydrides such as sodium amide, sodium hydride and calcium hydride, and also alkali metal alcoholates, such as sodium methylate, sodium methylate and potassium tert-butoxide, can also be used.
- Adogen 464 methyltrialkyl (C 8 -C 10 ) ammonium chloride
- TDA 1 tris (methoxyethoxyethyl) amine
- Process (A) according to the invention is generally carried out under normal pressure.
- reaction components of the formulas (II) and (III) and the deprotonating bases are generally employed in approximately equimolar amounts. However, it is also possible to use one or the other component in a larger excess (up to 3 moles).
- Process (B) is characterized in that enol esters of the formula (IV) in which A, B, C, X, Y, Z and n have the meanings given above in the presence of a solvent, optionally in the presence of a base and be rearranged in the presence of a suitable catalyst »
- the catalyst e.g.
- Cyanide-releasing reagent are compounds that release hydrogen cyanide and / or cyanide anions during the reaction.
- cyanide-releasing reagents are alkali cyanides such as sodium and potassium cyanide; Cyanohydrins of methyl-alkyl-ketones with 1 to 4 carbon atoms in the alkyl radical, such as acetone- or methyl isobutylketone-cyanohydrin, cyanohydrins of benzaldehyde or C 2 -C 6 -alkyl-substituted aldehydes, such as acetaldehyde, propional dehyde, zinc cyanide, tri (lower alkyl ) Silyl cyanide such as trimethylsilyl cyanide and hydrogen cyanide. Hydrogen cyanide is preferred because it reacts very quickly and is inexpensive. Furthermore, it can be used in liquid or gaseous
- Acetone cyanohydrin is preferred among the cyanohydrins.
- the reagent supplying cyanide 1 is used in a concentration of 1 to 50 mol-Ji in relation to the enol ester. 1-10 mol% are preferred.
- an excess of mild base is used in relation to the enol ester.
- Mild base refers to bases whose basicity lies between strong bases such as alkali hydroxide solutions (which would result in hydrolysis of the enol ester in the present case) and weak bases such as alkali bicarbonates (which would not result in a reaction in the present case) »Organic bases belong to the mild bases such as tertiary amines and inorganic bases such as alkali metal carbonates and alkali metal phosphates.
- Organic bases are preferably trialkylamines such as triethylamine or trialkanolamines such as triethanolamine and pyridine.
- Preferred inorganic bases are potassium carbonate and trisodium phosphate.
- the base is in a concentration between 1 and 4
- cyanide-releasing reagent is an alkali metal cyanide, for example potassium cyanide
- a phase transfer catalyst can be added. Crown ethers are preferably used. Only diluents that may be used are solvents that do not react with the acid chloride or the acylated product. 1,2-dichloroethane is preferably used. Other possible diluents depending on the reactants or products are toluene, acetonitrile, methylene chloride, ethylene acetate, dimethylformamide and methyl isobutyl ketone.
- the production process (B) is carried out at a temperature of 80 ° C., depending on the reagent supplying cyanide and the reactants.
- reaction temperature should be at its maximum at 40 ° C.
- potassium or lithium cyanide is used as the cyanide source, but is used in a stoichiometric amount without the use of an additional base. Only a catalytic amount of phase transfer catalyst is added, usually a crown ether or an acyclic analog.
- the preferred crown ether is
- This second process variant is preferred for the preparation of compounds of the formula (I), in particular if the reaction has to be carried out under mild reaction conditions and by-products are to be avoided, as are known, for example, in the reaction with ortho-cyanophenyl-substituted benzoylated cyclohexanediones.
- This second process variant of the production process (B) is carried out at room temperature.
- the diluents used correspond to those used in the first process variant of process (B), acetonitrile being preferred.
- Both process variants of the production process (B) are carried out with the enol ester of the formula (IV) as the starting substance.
- the enol ester can also be prepared in situ, for example by reacting the acylation reagent with a diketone, enol ester being the enol ester of a carboxylic acid. If the enol ester is presented as the starting substance in both process variants, it can be prepared beforehand using processes known from the literature, e.g. by acylation of a ß-dicarbonyl compound with acid halides.
- the synthesis of the acylated pyrrolidine-2,4-diones by the preparation process (B), starting with the acylating reagent and pyrrolidinedione (e.g. acid halide such as benzoyl chloride and pyrrolidinedione) can be carried out with or without isolation of the intermediate enol ester.
- the acylating reagent and pyrrolidinedione e.g. acid halide such as benzoyl chloride and pyrrolidinedione
- the acid halide or other acylating reagent and the pyrrolidinedione are allowed to react in the presence of a mild base such as triethylamine.
- a mild base such as triethylamine.
- the resulting enol ester can by known Methods from organic chemistry are isolated.
- This procedure is recommended if another solvent is used in the second reaction step to rearrange the enol ester into an acylated diketone.
- the dried enol ester is dissolved in a suitable solvent such as acetonitrile or 1,2-dichloroethane, and the cyanide-providing reagent of choice and a weak base or a crown ether are added.
- a suitable solvent such as acetonitrile or 1,2-dichloroethane
- the one-pot variant is available, the enol ester remaining in the reaction medium and the cyanide-providing reagent and optionally a base being added directly in the second stage in the same solvent.
- the acylated pyrrolidinedione is obtained in a one-step fraction by in situ synthesis and rearrangement of the enol ester, by combining the acid halide or other acylating reagents with pyrrolidinediones in the presence of suitable amounts of cyanide-providing reagent and mild base or
- the product may be contaminated by small amounts of carboxylic acid derived from the carboxylic acid chloride. These impurities are removed by adding aqueous sodium hydroxide solution or other suitable bases to the acidic product in order to separate the acid as a salt.
- the acylated pyrrolidinedione is obtained directly in pure form.
- Process (C) is characterized in that compounds of the formula (Ia) are reacted with alkylating reagents of the formula (V), if appropriate in the presence of a diluent and if appropriate in the presence of an acid binder.
- the compounds of the formula (I) are compounds according to the invention and can be obtained by the process described above.
- Formula (V) provides a general definition of the alkylating agents which are furthermore required as starting materials for the preparation of the compounds (Ib) according to the invention.
- E preferably represents the meanings given in the preferred ranges, very particularly preferably methyl, ethyl, propyl or isopropyl, Allyl, propynyl and benzyl substituted by fluorine, chlorine, methyl, methoxy or trifluoromethyl.
- L preferably represents chlorine, bromine or lad, C 1 -C 6 -alkylsulfonyloxy, C 1 -C 4 -alkoxysulfonyloxy or p-toluenesulfonyloxy, such as, for example, methanesulfonyloxy, methoxysulfonyloxy or ethoxysulfonyloxy.
- the alkylation reagents of the formula (V) are known compounds of organic chemistry.
- Inert organic solvents are suitable as diluents for carrying out the process (C) according to the invention for the preparation of the compounds (Ib) according to the invention.
- Aliphatic, alicyclic or aromatic, optionally halogenated hydrocarbons such as, for example, gasoline, benzene, toluene, xylene, pentane, hexane, heptane, cyclohexane, petroleum ether, ligroin, methylene chloride, are preferably used.
- Suitable acid binders are all commonly used inorganic and organic bases.
- Alkali metal hydrides, hydroxides, amides, carbonates or bicarbonates such as sodium hydride, sodium amide, sodium hydroxide, sodium carbonate or sodium bicarbonate, or tertiary amines, such as triethylamine, are preferably used , N, N-dimethylaniline, pyridine, 4- (N, N-dimethylamino) pyridine, diazoabicyclooctane (DABCO), diazabicyclonones (DBN) or diazabicycloundecene (DBU).
- DABCO diazoabicyclooctane
- DBN diazabicyclonones
- DBU diazabicycloundecene
- Process (D) according to the invention is characterized in that compounds of the formula (Ia) are reacted with acylating reagents of the formula (VI).
- inert solvents can be used as diluents in process (D) according to the invention.
- Hydrocarbons such as gasoline, benzene, toluene, xylene and tetralin are also preferably usable
- Halogenated hydrocarbons such as methylene chloride, chloroform, carbon tetrachloride, chlorobenzene and o-dichlorobenzene, also ketones, such as acetone and methyl isopropyl ketone, furthermore ethers, such as diethyl ether, tetrahydrofuran and dioxane, and also carboxylic acid esters, such as ethyl acetate or solvents, such as dimethyl sulfoxide and sulfolane. If the hydrolysis stability of the acylation reagent permits, the reaction can also be carried out in the presence of water.
- Suitable acid binders for the reaction according to process (D) according to the invention are all customary acid acceptors.
- Tertiary amines such as triethylamine, pyridine, diazabicyclooctane (DABCO), diazabicycloundecene (DBU), diazabicyclonones (DBN), Hunig base and N, N-dimethylaniline, furthermore alkaline earth metal oxides, such as magnesium and calcium oxide, and also alkali metal oxides, are preferably usable. and alkaline earth metal carbonates such as sodium carbonate, potassium carbonate and calcium carbonate.
- reaction temperatures can also be within a larger range Range can be varied. In general, temperatures between -20 ° C and + 150 ° C, preferably between 0 ° C and 100 ° C.
- the starting materials of the formula (Ia) and the acylating reagent of the formula (VI) are generally used in approximately equivalent amounts. However, it is also possible to use the acylating reagent in a larger excess (up to 5 mol). The processing takes place according to usual methods.
- Process (E) according to the invention is characterized in that compounds of the formula (Ia) with
- Diluents which can be used in process (E) according to the invention are preferably ethers such as tetrahydrofuran, dioxane, diethyl ether, nitriles or acetonitrile or alcohols such as methanol, ethanol, isopropanol, but also water.
- Process (E) according to the invention is generally carried out under normal pressure.
- the reaction temperatures are generally between -20 ° C and 100 ° C, preferably between 0 ° C and 50 ° C.
- the starting materials of the formula (Ia) or (VII) or (VIII) are generally used in approximately equimolar amounts. However, it is also possible to use one or the other component in a larger excess (up to 2 mol).
- the general procedure is to concentrate the reaction mixture by removing the diluent in vacuo. The processing is again carried out using customary methods.
- the active substances are suitable for controlling animal pests, preferably arthropods and nematodes, in particular insects and arachnids, which occur in agriculture, in forests, in the protection of stored goods and materials and in the hygiene sector. They are effective against normally sensitive and resistant species as well as against all or individual stages of development.
- animal pests preferably arthropods and nematodes, in particular insects and arachnids, which occur in agriculture, in forests, in the protection of stored goods and materials and in the hygiene sector. They are effective against normally sensitive and resistant species as well as against all or individual stages of development.
- the pests mentioned above include:
- Isopoda e.g. Oniscus asellus, Armadillidium vulgare, Porcellio scaber.
- Thysanura e.g. Lepisma saccharina.
- Collembola e.g. Onychiurus armatus.
- Orthoptera e.g. Blatta orientalis, Periplaneta americana, Leucophaea maderae, Blattella germanica, Acheta domesticus, Gryllotalpa spp., Locusta migratoria migratorioides, Melanoplus dif ferentialis, Schistocerca gregaria.
- Thysanoptera e.g. Hercinothrips femoralis, Thrips tabaci.
- Homoptera e.g. Aleurodes brassicae, Bemisia tabaci, Trialeurodes vaporariorum, Aphis gossypii, Brevicoryne brassicae, Cryptomyzus ribis, Aphis fabae, Doralis pomi, Eriosoma lanigerum, Hyalopterus arundinis, Macrosiphum avenae, Myzus spp., Phorodoniphasis, spp.
- Homoptera e.g. Aleurodes brassicae, Bemisia tabaci, Trialeurodes vaporariorum, Aphis gossypii, Brevicoryne brassicae, Cryptomyzus ribis, Aphis fabae, Doralis pomi, Eriosoma lanigerum, Hyalopterus arundinis, Macrosiphum avenae, Myzus spp., Phorodoniphasis,
- Nephotettix cincticeps Lecanium corni, Saissetia oleae, Laodelphax striatellus, Nilaparvata lugens, Aonidiella aurantii, Aspidiotus hederae, Pseudococcus spp. Psylla spp.
- Otiorrhynchus sulcatus Otiorrhynchus sulcatus, Cosmopolites sordidus, Ceuthorrhynchus assimilis, Hypera postica, Dermestes spp., Trogoderma spp., Anthrenus spp., Attagenus spp., Lyctus spp., Meligethes aeneus, Ptinus spp. Tenebrio molitor, Agriotes spp., Cono derus spp., Melolontha melolontha, Amphimallon solsti tialis, Costelytra zealandica.
- Hymenoptera e.g. Diprion spp., Hoplocampa spp., Lasius spp., Monomorium pharaonis, Vespa spp.
- Chrysomyia spp. Cuterebra spp., Gastrophilus spp., Hyppobosca spp., Stomoxys spp., Oestrus spp., Hypoderma spp., Tabanus spp., Tannia spp., Bibio hortulanus, Oscinella frit, Phorbia spp., Pegomyia hyoscyami, Cerati tis capitata, Dacus oleae, Tipula paludosa.
- Acarina e.g. Acarus siro, Argas spp., Ornithodoros spp., Dermanyssus gallinae, Eriophyes ribis, Phyllocoptruta oleivora, Boophilus spp., Rhipicephalus spp., Amblyomma spp «, Hyalomma spp., Ixodes spp., Psoroptes spp.,. Chori ., Tarsonemus spp., Bryobia praetiosa, Panonychus spp., Tetranychus spp ..
- the active compounds according to the invention are notable for high insecticidal activity.
- the active compounds according to the invention also show acaricidal activity.
- the active compounds according to the invention can furthermore be used as defoliants, desiccants, haulm killers and in particular as weed killers. Weeds in the broadest sense are all plants that grow in places where they are undesirable. Whether the substances according to the invention act as total or selective herbicides depends essentially on the amount used.
- the active compounds according to the invention can e.g. can be used in the following plants:
- Beta Daucus, Phaseolus, Pisum, Solanum, Linum, Ipomoea, Vicia, Nicotiana, Lycopersicon, Arachis, Brassica, Lactuca, Cucumis, Cucurbita.
- the compounds are suitable for total weed control, e.g. on industrial and track systems and on paths and squares with and without tree cover.
- the compounds for weed control in permanent crops e.g. Forest, ornamental wood, fruit, wine, citrus, nut, banana, coffee, tea, rubber, oil palm, cocoa, berry fruit and hop plants, on ornamental and sports turf and pasture land and for selective weed control in annual crops.
- the compounds of the invention are suitable for the selective control of monocotyledonous and dicotyledon weeds in monocotyledon crops in the pre- and post-emergence process.
- the active compounds can be converted into the customary formulations, such as solutions, emulsions, wettable powders, suspensions, powders, dusts, pastes, soluble powders, granules, suspension emulsion concentrates, active substance-impregnated natural and synthetic substances and very fine encapsulations in polymeric substances .
- These formulations are prepared in a known manner, for example by mixing the active ingredients with
- Extenders that is to say liquid solvents and / or solid carriers, optionally using surface-active agents, that is to say emulsifiers and / or dispersants and / or foam-generating agents.
- organic solvents can also be used as auxiliary solvents.
- auxiliary solvents e.g. organic solvents
- aromatics such as xylene, toluene, or alkylnaphthalenes
- chlorinated aromatics and chlorinated aliphatic hydrocarbons such as chlorobenzenes, chlorethylenes or methylene chloride
- aliphatic hydrocarbons such as cyclohexane or paraffins, e.g.
- Petroleum fractions mineral and vegetable oils, alcohols such as butanol or glycol as well as their ethers and esters, ketones such as acetone, methyl ethyl ketone, methyl isobutyl ketone or cyclohexanone, strongly polar solvents such as dimethylformamide and dimethyl sulfoxide, and water.
- ammonium salts and natural rock powders such as kaolins, clays, talc, chalk, quartz, attapulgite, montmorillonite or diatomaceous earth and synthetic rock powders, such as highly disperse silica, aluminum oxide and silicates, as solid carriers for granules are possible: e.g.
- suitable emulsifiers and / or foam-generating agents are: for example nonionic and anionic emulsifiers, such as polyoxyethylene fatty acid esters, polyoxyethylene fatty alcohol ethers, for example alkylaryl polyglycol ethers, alkyl sulfonates, alkyl sulfates, aryl sulfonates and protein hydrolyzates; Possible dispersants are: eg lignin sulfite liquor and methyl cellulose.
- Adhesives such as carboxymethyl cellulose, natural and synthetic polymers in the form of powders, granules or latices, such as gum arabic, polyvinyl alcohol, polyvinyl acetate, and natural phospholipids such as cephalins and lecithins and synthetic phospholipids can be used in the formulations.
- Other additives can be mineral and vegetable oils.
- Dyes such as inorganic pigments, e.g.
- Iron oxide, titanium oxide, ferrocyan blue and organic dyes such as alizarin, azo and metal lphthalocyanine dyes and trace nutrients such as salts of iron, manganese, boron, copper, cobalt, molybdenum and zinc can be used.
- the formulations generally contain between 0.1 and 95 parts by weight. Active ingredient, preferably between 0.5 and 90%.
- the active compounds according to the invention can also be used for combating weeds, in a mixture with known herbicides, finished formulations or tank mixes being possible.
- a mixture with other known active compounds such as fungicides, insecticides, acaricides, nematicides, bird repellants, plant nutrients and agents which improve soil structure, is also possible.
- the active compounds can be used as such, in the form of their formulations or in the use forms prepared therefrom by further dilution, such as ready-to-use solutions, suspensions, emulsions, powders, pastes and granules. They are used in the usual way, e.g. by pouring, spraying, spraying, sprinkling.
- the active compounds according to the invention can be applied both before and after emergence of the plants. They can also be worked into the soil before sowing.
- the amount of active ingredient used can vary over a wide range. It essentially depends on the type of effect desired. In general, the application rates are between 0.01 and 10 kg of active ingredient per hectare of soil, preferably between 0.05 and 5 kg per ha.
- Emulsifier 1 part by weight of alkylaryl polyglycol ether
- active compound 1 part by weight of active compound is mixed with the stated amount of solvent, the stated amount of emulsifier is added and the concentrate is diluted with water to the desired concentration.
- Seeds of the test plants are sown in normal soil and watered with the active ingredient preparation after 24 hours.
- the amount of water per unit area is expediently kept constant.
- the concentration of active substance in the preparation is irrelevant, the only decisive factor is the amount of active substance applied per unit area.
- the degree of damage to the plants is rated 54 damage in comparison to the development of the untreated control. It means:
- Emulsifier 1 part by weight of alkylaryl polyglycol ether
- active compound 1 part by weight of active compound is mixed with the stated amount of solvent, the stated amount of emulsifier is added and the concentrate is diluted with water to the desired concentration.
- Test plants which have a height of 5-15 cm are sprayed with the active substance preparation in such a way that the desired amounts of active substance are applied per unit area. After three weeks, the degree of damage to the plants is rated 54 damage in comparison to the development of the untreated control. It means:
- the compound according to preparation example 2 shows a clear superiority in effectiveness as well as in crop selectivity compared to the prior art
- Emulsifier 1 part by weight of alkylaryl polyglycol ether
- Cabbage leaves (Brassica oleracea) are treated by immersing them in the preparation of active ingredient at the desired concentration and populated with caterpillars of the cockroach (Plutella maculipennis) while the leaves are still moist.
- the kill is determined in%. 100 * /. Means that all caterpillars have been killed; 0% means that no caterpillars have been killed.
- Emulsifier 1 part by weight of alkyl aryl polyglycol ether
- active compound 1 part by weight of active compound is mixed with the stated amount of solvent and the stated amount of emulsifier, and the concentrate is diluted with water to the desired concentration.
- Cabbage leaves (Brassica oleracea) are treated by being dipped into the preparation of the active compound of the desired concentration and populated with horseradish leaf beetle larvae (Phaedon c ⁇ chleariae) while the leaves are still moist.
- the kill is determined in * /%. 100% means that all beetle larvae have been killed; 0% means that no beetle larvae have been killed.
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Agronomy & Crop Science (AREA)
- Pest Control & Pesticides (AREA)
- Plant Pathology (AREA)
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Dentistry (AREA)
- General Health & Medical Sciences (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Environmental Sciences (AREA)
- Plural Heterocyclic Compounds (AREA)
- Pyrrole Compounds (AREA)
Abstract
Die Erfindung betrifft neue substituierte 3-Benzoyl-pyrrolidin-2,4-dion-Derivate der allgemeinen Formel (I) in welcher A, B, C, E, X, Y, Z und n die in der Beschreibung angegebenen Bedeutungen haben, mehrere Verfahren zu ihrer Herstellung, neue Zwischenprodukte zu ihrer Herstellung und ihre Verwendung als Herbizide, Insektizide und Akarizide.
Description
HERBIZIDE UND INSEKTIZIDE 3-BENZOYL-PYRROLIDIN-2.4-DION-DERIVATE
Die Erfindung betrifft neue substituierte 3-Benzoyl-pyrrolidin-2,4-dion-Derivate, mehrere Verfahren zu ihrer Herstellung, neue Zwischenprodukte zu ihrer Herstellung und ihre Verwendung als Herbizide, Insektizide und Akarizide.
Von 3-Acyl-pyrrolidin-2,4-dionen sind pharmazeutische Eigenschaften vorbeschrieben (S. Suzuki et. al. Chem. Pharm. Bull. 15 1120 (1967), S Toda et al. J.
Antibiotics 33, 173 (1980), Reichart Jr. K.L. et al. J. Am. Chem. Soc. 100, 4225 (1978).
In WO 8804-652 werden 3-Benzoyl-furan-2-on-Derivate mit herbiziden Eigenschaften beschrieben, unter anderem die Verbindung 3-(2,4-Dichlorbenzoyl)-4-hydroxy-6-methyl-N-methyl-pyridon-2.
Es wurden nun neue substituierte 3-Benzoyl-pyrrolidin-2,4-dion-Derivate gefunden, die durch die Formel (I) dargestellt sind
,
in welcher für Wasserstoff, Alkyl, Halogen, Alkoxy, Halogenalkyl, Halogenalkoxy, Nitro, Alkoxycarbonyl, Carboxy, Cyano oder -S(O)m-R1 steht, für Wasserstoff, Alkyl, Halogen, Alkoxy, Halogenalkyl, Halogenalkoxy, Nitro, Alkoxycarbonyl, Carboxy, Cyano oder -S(O)m-R1 steht, für Alkyl, Halogen, Alkoxy, Halogenalkyl, gegebenenfalls durch Halogen substituiertes Alkoxy, Alkoxyalkyl oder Alkoxycarbonyl steht, für eine Zahl von 0-3 steht, m für eine Zahl von 0-2 steht, für Wasserstoff, gegebenenfalls durch Halogen substituiertes Alkyl, Alkoxyalkyl, Polyalkoxyalkyl, Alkylthioalkyl, Alkenyl, Alkinyl, gegebenenfalls durch Heteroatome unterbrochenes Cycloalkyl oder gegebenenfalls durch Halogen-, Alkyl-, Halogen-
alkyl-, Alkoxy-, Nitro substituiertes Phenyl oder Arylalkyl steht,
B für Wasserstoff, gegebenenfalls durch Halogen substituiertes Alkyl, Cycloalkyl, Alkoxyalkyl, Alkylthioalkyl oder gegebenenfalls durch Alkyl,
Alkoxy, Halogen, Nitro, Halogenalkyl, substituiertes Phenyl oder Aralkyl steht,
C für Wasserstoff, oder gegebenenfalls durch
Halogen substituiertes Alkyl steht, oder worin
A und B gemeinsam mit den Atomen, an die sie gebunden sind, einen gegebenenfalls durch Halogen oder gegebenenfalls halogeniertes Alkyl oder Alkoxy substituierten gesättigten oder ungesättigten Cyclus bilden, der durch Sauerstoff und/oder Schwefel unterbrochen sein kann, oder worin
B und C gemeinsam mit dem Kohlenstoffatom, an das sie gebunden sind, einen gesättigten oder ungesättigten Cyclus bilden, der durch Halogen, oder gegebenenfalls durch halogeniertes Alkyl oder Alkoxy substituiert sein kann und durch Sauerstoff und/oder Schwefel unterbrochen sein kann,
E für Wasserstoff (= E1 ) , oder für gegebenenenfalls durch Halogen substituiertes Alkyl, Alkenyl, Alkinyl, Alkoxyalkyl, Aralkyl ( = E2) , für eine Gruppe CO-R2 ( = E3 ) oder für ein Metallion oder Metal lequivalent ( = E4) steht, R1 für gegebenenfalls durch Halogen substituiertes Alkyl oder für einen gegebenenfalls substituierten Phenylrest steht und R2 für gegebenenfalls durch Halogen substituiertes Alkyl, Alkenyl, Alkoxy, Alkoxyalkyl, Alkylthio oder gegebenenfalls substituiertes Phenyl oder Aralkyl steht. Weiterhin wurde gefunden, daß man 3-Benzoyl-pyrrolidin-2,4-dion-Derivate der Formel (I) bzw. deren Enole der Formel (Ia)
A) Benzoylessigester der Formel (II)
X, Y, Z und n die oben angegebenen Bedeutungen haben und R3 für Alkyl steht mit Aminosäureestern der allgemeinen Formel (III)
A, B und C die oben angegebenen Bedeutungen haben und R4 für Alkyl steht,
gegebenenfalls in Gegenwart eines Lösungsmittels und in Gegenwart einer Base kondensiert, oder daß man B) Verbindungen der Formel (Ia)
A, B, C, X, Y, Z, und n die oben angegebenen
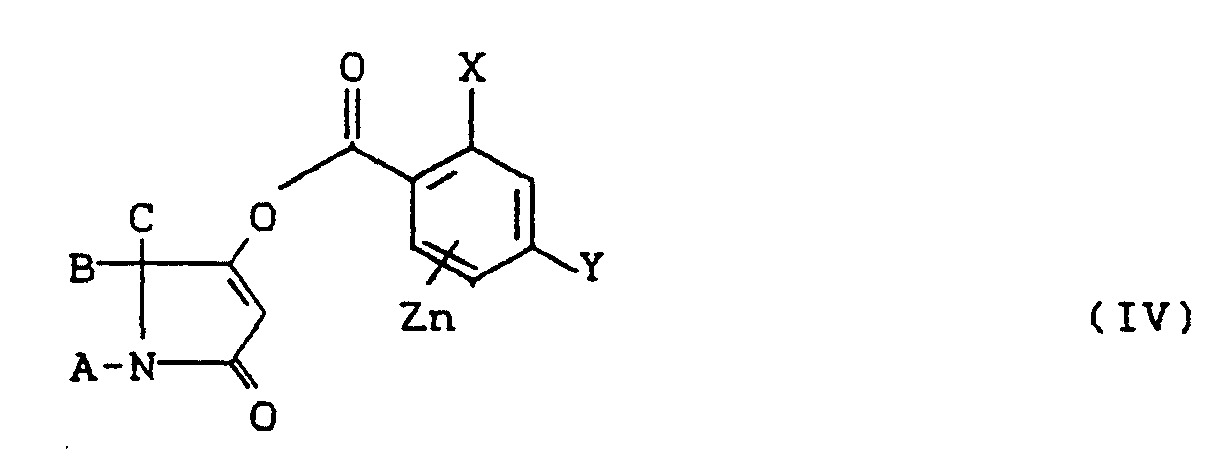
Bedeutungen haben, erhält, wenn man 4-Benzoyloxy-pyrrolin-2-one der Formel (IV)
in welcher
A, B, C, X, Y, Z und n die oben angegebenen Bedeutungen haben, gegebenenfalls in Gegenwart eines Verdünnungsmittels, gegebenenfalls in Gegenwart einer Base und gegebenenfalls in Gegenwart eines geeigneten Katalysators umlagert,
oder daß man C) Verbindungen der Formel (Ib)
A, B, C, E2, X, Y, Z und n die oben angegebenen
Bedeutungen haben, erhält, wenn man Verbindungen der Formel (Ia)
A, B, C, X, Y, Z und n die oben angegebenen
Bedeutungen haben, mit Alkyl ierungsmitteln der allgemeinen Formel (V) E2-L (V) in welcher
E2 die oben angegebene Bedeutung hat und
L für Halogen, -OSO2-Alkyl, -OSO2O-Alkyl oder -OSO2-Aryl steht,
gegebenenfalls in Gegenwart eines Verdünnungsmittels und gegebenenfalls in Gegenwart einer Base umsetzt, oder daß man D) Verbindungen der Formel (Ic)
A, B, C, E3 , X, Y, Z und n die oben angegebenen
Bedeutungen haben, erhält, wenn man Verbindungen der Formel (Ia)
A, B, C, X, Y, Z und n die oben angegebenen Bedeutungen haben mit Acylierungsreagenzien der Formel (VI)
E3 -M (VI) in welcher E3 die oben angegebene Bedeutung hat und
M für Halogen, -OE3 , CN, O-SO2-Alkyl, O- SO2-Aryl und Imidazolyl steht, gegebenenfalls in Gegenwart eines Verdünnungsmittels und gegebenenfalls in Gegenwart eieer Base umsetzt, oder daß man
Verbindungen der allgemeinen Formel (Id)
X, Y, Z, A, B, C, E4 und n die oben angegebenen Bedeutungen haben, erhält, wenn man Verbindungen der Formel (Ia)
X, Y, Z, A, B, C und n die oben angegebenen
Bedeutungen haben, mit Metallhydroxiden oder Aminen der allgemeinen Formel (VII) und (VIII)
Me für ein- oder zweiwertige Metallionen, s und t für die Zahlen 1 und 2 stehen und R4, R5 und R6 unabhängig voneinander für Wasserstoff und Alkyl stehen, gegebenenfalls in Gegenwart eines Verdünnungsmittels, umsetzt.
Überraschenderweise wurde gefunden, daß die neuen 3-Benzoyl-pyrrolidin-2,4-dion-Derivate der Formel I sich durch sehr gute herbizide Wirkungen auszeichnen.
Bevorzugt sind substituierte 3-Benzoyl-pyrrolidin-2,4-dion-Derivate der Formel (I), in welcher
X für Wasserstoff, C1-C6-Alkyl, Halogen, C1-C6-Alkoxy, C1-C6-Halogenalkyl, C1-C6-Halogenalkoxy, Nitro, C1- C6-Alkoxycarbonyl, C1-C6-Carboxy, Cyano oder
S(O)m-R1 steht, Y für Wasserstoff, C1-C6-Alkyl, Halogen, C1-C6- Alkoxy, C1-C4-Halogenalkyl, C1-C6-Halogenalkoxy, Nitro, C1-C6-Alkoxycarbonyl, C1-C6-Carboxy, Cyano oder S(O)m-R1 steht, Z für C1-C6-Alkyl, Halogen, C1-C6-Alkoxy, C1-C6- Halogenalkyl, C1-C6-Halogenalkoxy, C1-C6-Alkoxy
C2-C6 - alkyl , C 1 -C6 -Halogenalkoxy-C2-C6 -alkyl , C 1 - C6 -Alkoxy-C2-C6 -hal ogenalkyl , C1-C6-Al koxycarbonyl oder C1-C6-Hal ogenalkoxycarbonyl steht , n für eine Zahl von 0-3 steht, m für eine Zahl von 0-2 steht,
A für Wasserstoff oder gegebenenfalls durch Halogen substituiertes geradkettiges oder verzweigtes C1- C12-Alkyl, C3-C8-Alkenyl, C3-C8-Alkinyl, C1-C10- Alkoxy-C2-C8-alkyl, C1-C8-Polyalkoxy-C2-C8-alkyl, C1-C10-Alkylthio-C2-C8-alkyl, Cycloalkyl mit 3-8 Ringatomen, das durch Sauerstoff und/oder Schwefel unterbrochen sein kann oder gegebenenfalls durch Halogen, C1-C6-Alkyl-, C1-C6-Haloalkyl-, C1-C6- Alkoxy-, Nitro substituiertes Phenyl oder Aryl- C1-C6-alkyl steht,
B für Wasserstoff, geradkettiges oder verzweigtes und gegebenenfalls durch Halogen substituiertes C1-C62~ Alkyl, C1-C8-Alkoxy-C1-C8-alkyl, C1-C8-Alkyl-C1-C8- thioalkyl, Cycloalkyl mit 3-8 Ringatomen, das durch Sauerstoff und/oder Schwefel unterbrochen sein kann, oder gegebenenfalls durch Halogen, C1-C6- Alkyl, C1-C6-Halogenalkyl, C1-C6-Alkoxy, Nitro substituiertes Phenyl oder Aryl-C1-C6-alkyl steht ,
C für Wasserstoff oder gegebenenfalls durch Halogen substituiertes C1-C12-Alkyl steht, oder worin
A und B gemeinsam mit den Atomen, an die sie gebunden sind, einen 5 bis 8-gliedrigen gesättigten oder ungesättigten Cyclus bilden, der durch Sauerstoff und/oder Schwefel unterbrochen und durch gegebenenfalls halogeniertes C1-C6-Alkyl, C1-C6-Alkoxy oder Halogen substituiert sein kann, oder worin
B und C gemeinsam mit dem Kohlenstoffatom, an das sie
gebunden sind einen 3 bis 8-gliedrigen gesättigten oder ungesättigten Cyclus bilden, der durch Sauerstoff und/oder Schwefel unterbrochen und durch
Halogen oder gegebenenfalls halogeniertes C1-C6- Alkyl, C1-C6-Alkoxy substituiert sein kann,
E für E1 = Wasserstoff,
für E2 = C1-C12-Alkyl, C2-C6-Halogenalkyl, C3-C8- Alkenyl, C3-C8-Alkinyl, C3-C8-Halogenalkenyl, C3- C8-Hal ogenalkinyl, C1-C6-Alkoxy-C2-C6-alkyl, C1-C6- Halogenalkoxy-C2-C6-alkyl, Aryl-C1-C6-alkyl,
für E3 = eine Gruppe CO-R2 oder
für E4 = ein Metallion oder ein Metallequivalent steht, R1 für gegebenenfalls durch Halogen substituiertes
C1-C8-Alkyl, oder für gegebenenfalls durch Halogen,
Nitro, Cyano, C1-C4-Alkoxy, C1-C6-Halogenalkoxy, C1- C4-Alkylthio, C1-C4-Halogenalkylthio, C1-C4-Alkyl, C1-C6-Halogenalkyl substituiertes Phenyl steht und
R2 für gegebenenfalls durch Halogen substituiertes
C1-C8-Alkyl, C1-C8-Alkoxy, C1-C8-Alkylthio, C2-C8- Alkenyl, C1-C8-Alkoxy-C2-C8-alkyl oder für gegebenenfalls durch Halogen, C1-C8-Halogenalkyl, C1-C8- Alkyl oder C1-C8-Alkoxy substituiertes Phenyl, für gegebenenfalls durch Halogen, C1-C8-Alkyl, C1-C8- Halogenalkyl oder C1-C8-Alkoxy substituiertes Aryl- C1-C6-alkyl steht.
Besonders bevorzugt sind Verbindungen der Formel (I) in welcher
X für Wasserstoff, C1-C4-Alkyl, Halogen, C1-C4-Alkoxy, C1-C4-Halogenalkyl, C1-C4-Halogenalkoxy,
Nitro, Cyano, C1-C4-Alkoxycarbonyl, Carboxy oder S(O)m-R1 steht,
Y für Wasserstoff, C1-C6-Alkyl, Halogen, C1-C4- Alkoxy, C1-C3-Halogenalkyl, C1-C4-Halogenalkoxy, Nitro, C1-C4-Alkoxycarbonyl, Carboxy, Cyano oder S(O)m-R1 steht,
Z für C1-C4-Alkyl, Halogen, C1-C4-Alkoxy, C1-C4- Halogenalkyl, C1-C4-Halogenalkoxy, C1-C4-Alkoxy-C2- C4-alkyl, C1-C4-Halogenalkoxy-C2-C4-alkyl, C1-C4-Alkoxy-C2-C4-halogenalkyl, C1-C4-Alkoxycarbonyl oder C1-C4-Halogenalkoxycarbonyl steht, n für eine Zahl von 0-3 steht,
m für eine Zahl von 0-2 steht,
A für Wasserstoff oder gegebenenfalls durch Halogen substituiertes geradkettiges oder verzweigtes C1- C10-Alkyl, C3-C6-Alkenyl, C3-C6-Alkinyl, C1-C8- Alkoxy-C2-C6-alkyl, C1-C6-Polyalkoxy-C2-C6-alkyl, C1-C8-Alkylthio-C2-C6-alkyl, Cycloalkyl mit 3-7 Ringatomen, das durch 1-2 Sauerstoff- und/oder
Schwefelatome unterbrochen sein kann oder gegebenenfalls durch Halogen, C1-C4-Alkyl-, C1-C4-Haloalkyl-, C1-C4-Alkoxy oder Nitro substituiertes
Phenyl oder Aryl-C1-C4-alkyl steht,
B für Wasserstoff, geradkettiges oder verzweigtes und gegebenenfalls durch Halogen substituiertes C1-C10- Alkyl, C1-C6-Alkoxy-C1-C6-alkyl, C1-C6-Alkylthio-C1- C6-alkyl, Cycloalkyl mit 3-7 Ringatomen das durch 1-2 Sauerstoff und/oder Schwefelatome unterbrochen sein kann oder gegebenenfalls durch Halogen, C1-C4- Alkyl, C1-C4-Halogenalkyl, C1-C4-Alkoxy oder Nitro substituiertes Phenyl oder Aryl-C1-C4-alkyl steht,
C für Wasserstoff oder gegebenenfalls durch Halogen substituiertes C1-C8-Alkyl steht, oder worin
A und B gemeinsam mit den Atomen, an die sie gebunden sind, einen 5 bis 7-gliedrigen gesättigten oder un
gesättigten Cyclus bilden, der durch C1-C4-Alkyl,
C1- 4-Alkoxy, Fluor oder Chlor substituiert und der durch Sauerstoff und/oder Schwefel unterbrochen sein kann, oder worin
B und C gemeinsam mit dem Kohlenstoffatom, an das sie
gebunden sind, einen 3 bis 7-gliedrigen gesättigten oder ungesättigten Cyclus bilden, der durch Sauer- stoff und/oder Schwefel unterbrochen und durch
Fluor, Chlor, C1-C4-Alkyl, C1-C4-Alkoxy, C1-C4- Halogenalkyl, C1-C4-Halogenalkoxy substituiert sein kann, E für E1 = Wasserstoff
für E2 = C1-C8-Alkyl, C2-C4-Halogenalkyl, C3-C6- Alkenyl, C3-C6-Alkinyl, C3-C6-Halogenalkenyl, C3-C6-Halogenalkinyl, C1-C4-Alkoxy-C2-C4-alkyl, C1-C4-Halogenalkoxy-C2- C4-alkyl, Aryl-C1-C4-alkyl, für E3 = eine Gruppe CO-R2 oder
für E4 = ein Metallion oder ein Metallequivalent
steht,
R1 für gegebenenfalls durch Halogen substituiertes C1- C6-Alkyl oder für gegebenenfalls durch Fluor, Chlor, Brom, Nitro, Cyano, C1-C3-Alkoxy, C1-C3-Halogenalkoxy, C1-C3-Alkylthio, C 1-C3-Halogenalkylthio, C1-
C3-Alkyl, C1-C3-Halogenalkyl substituiertes Phenyl, steht und
R2 für gegebenenfalls durch Halogen substituiertes C1- C6-Alkyl, C1-C6-Alkoxy, C1-C6-Alkylthio, C2-C6-Alkenyl, C1-C6-Alkoxy-C2-C6-alkyl oder für gegebenenfalls durch Halogen, C1-C5-Halogenalkyl, C1-C6-Alkyl oder C1-Cg-Alkoxy substituiertes Phenyl, für gegebenenfalls durch Halogen, C1-Cg-Alkyl, C1-C5-Halogenalkyl oder C1-C5-Alkoxy substituiertes Aryl-C1- C4-alkyl steht.
Ganz besonders bevorzugt sind Verbindungen der Formel (I) in welcher
X für Wasserstoff, Methyl, Ethyl, Propyl, i-Propyl,
Fluor, Chlor, Brom, Methoxy, Ethoxy, Trifluormethyl, Difluormethyl, Trifluormethoxy, Nitro, Methoxycarbonyl, Ethoxycarbonyl, Cyano oder S(O)mR1 steht,
Y für. Wasserstoff, Methyl, Ethyl, Propyl, i-Propyl, Butyl, i-Butyl, tert.-Butyl, Fluor, Chlor, Brom, Methoxy, Ethoxy, Trifluormethyl, Trifluormethoxy, Difluormethyl, Nitro, Methoxycarbonyl, Ethoxycarbonyl, Cyano oder S(O)mR1 steht,
Z für Methyl, Ethyl, i-Propyl, Butyl, i-Butyl, tert.- Butyl, Fluor, Chlor, Brom, Methoxy, Ethoxy, Trifluormethyl, Difluormethyl, Trifluormethoxy,
Methoxyethyl, Ethoxyethyl, Propoxyethyl, Isoproxyethyl, Methoxycarbonyl, Ethoxycarbonyl steht, n für eine Zahl von 0-3 steht, m für eine Zahl von 0-2 steht,
A für Wasserstoff, gegebenenfalls durch Halogen substituiertes geradkettiges oder verzweigtes C1-C8- Alkyl, C3-C4-Alkenyl, C3-C4-Alkinyl, C1-C6-Alkoxy- C2-C4-alkyl, C1-C4-Polyalkoxy-C2-C4-alkyl, C1-C6- Alkylthio-C2-C4-alkyl, Cycloalkyl mit 3-6 Ringatomen, das durch 1-2 Sauerstoff- und/oder Schwe- felatome unterbrochen sein kann oder gegebenenfalls durch Fluor-, Chlor-, Brom-, Methyl-, Ethyl-, Propyl-, iso-Propyl-, Methoxy-, Ethoxy-, Trif luormethyl-, Nitro substituiertes Phenyl oder Aryl-C1- C3-alkyl steht,
B für Wasserstoff, geradkettiges oder verzweigtes und gegebenenfalls durch Halogen substituiertes C1-C8- Alkyl, C1-C4-Alkoxy-C1-C4-alkyl, C1-C4-Alkylthio-C1- C4-alkyl, Cycloalkyl mit 3-6 Ringatomen, das durch 1-2 Sauerstoff und/oder Schwefelatome unterbrochen sein kann oder gegebenenfalls durch Halogen,
C1-C4-Alkyl, C1-C4-Halogenalkyl, C1-C4-Alkoxy oder Nitro substituiertes Phenyl oder Aryl-C1-C3-alkyl steht,
C für Wasserstoff, C1-C6-Alkyl oder C1-C6-Halogenalkyl steht, oder worin
A und B gemeinsam mit den Atomen, an die sie gebunden sind, einen 5 bis 6-gliedrigen gesättigten oder ungesättigten Cyclus bilden, der durch C1-C3-Alkyl, C1-C3-Alkoxy, Fluor oder Chlor substituiert und der durch Sauerstoff und/oder Schwefel unterbrochen sein kann, oder worin
B und C gemeinsam mit dem Kohlenstoff, an das sie gebunden sind, einen 3 bis 6-gliedrigen gesättigten oder ungesättigten Cyclus bilden, der durch Sauerstoff und/oder Schwefel unterbrochen und durch Fluor, Chlor, C1-C4-Alkyl, C1-C4-Alkoxy, Trifluormethyl oder Trif luormethoxy substituiert sein kann, E für E1 = Wasserstoff steht,
für E2 = C1-C6-Alkyl, C2-C3-Halogenalkyl, C3-C4- Alkenyl, C3-C4-Alkinyl, C3-C4-Halogenal
kenyl, C3-C4-Halogenalkinyl, C1-C3-Alkoxy-C2-C3~alkyl, C1-C3-Halogenalkoxy-C2- C3-alkyl, Aryl-C1-C3-alkyl steht,
für E3 = eine Gruppe CO-R2 oder
für E4 = Li⊕, Na⊕, K⊕, NH4 ⊕ steht, für gegebenenfalls durch Fluor substituiertes C1-C4- Alkyl oder für gegebenenfalls durch Fluor, Chlor, Brom, Nitro, Cyano, C1-C2-Alkoxy, C1-C2-Fluoralkoxy, C1-C2-Chloralkoxy, C1-C2-Alkylthio, C1-C2-Fluoralkylthio, C1-C2-Chloralkylthio, C1-C3-Alkyl, C1-C2- Fluoralkyl, C1-C2-Difluoralkyl, C1-C2-Trifluoralkyl, C1-C2-Chloralkyl, C1-C2-Dichloralkyl, C1-C2-Trichloralkyl substituiertes Phenyl steht, R2 für gegebenenfalls durch Fluor, Chlor, Brom
substituiertes C1-C4-Alkyl, C1-C4-Alkoxy, C1-C4- Alkylthio, C1-C4-Alkoxy- (C2-C4)alkyl oder für gegebenenfalls durch Fluor, Chlor, Brom, Trif luormethyl, Cj-C4~Alkyl oder C1-C4-Alkoxy substituiertes Phenyl, für gegebenenfalls durch Fluor, Chlor, Brom, C1-C4-Alkyl, Trif luormethyl oder C1-C4-Alkoxy substituiertes Aryl-C1-C2-alkyl steht.
Im einzelnen seien außer den bei den Herstellungsbeispielen genannten Verbindungen die folgenden substituierten 3-Benzoyl-pyrrolidin-2 ,4-dion-Derivate der allgemeinen Formel I genannt:
Verwendet man gemäß Verfahren (A) 2,4-Dichlor-benzoyl- essigsäure-methylester und N-Isopropyl-glycin-ethylester als Ausgangsstof fe und Natriumethylat als Base, so kann der Verlauf des erfindungsgemäßen Verfahrens durch folgendes Reaktionsschema wiedergegeben werden:
Verwendet man gemäß Verfahren (B) 4-(2-Nitrobenzoyloxy)- 5,5-dimethyl-pyrrolin-2-on, Triethylamin als Base und Acetoncyanhydrin als Katalysator (EP 186 117), so kann das erfindungsgemäße Verfahren durch folgendes Reaktionsschema beschrieben werden:
Verwendet man gemäß Verfahren (C) 3-(4-Chlorbenzoyl)-1- cyclopentanyl-pyrrolidin-2,4-dion und Toluolsulfonsäuremethylester, so kann der Verlauf des erfindungsgemäßen Verfahrens durch folgendes ReaktionsSchema wiedergegeben werden.
Verwendet man gemäß Verfahren (D) 1,5-Dimethyl-3-(2,4- dichlorbenzoyl)-pyrrolidin-2,4-dion und Pivaloylchlorid, so kann der Verlauf des erfindungsgemäßen Verfahrens durch folgendes Reaktionsschema wiedergegeben werden:
Verwendet man gemäß Verfahren (E) 3-(2,4-Dichlorbenzoyl)-pyrrolidin-2,4-dion und Natriumhydroxid, so kann der Verlauf des erfindungsgemäßen Verfahrens durch folgendes Reakt ionsschema wiedergegeben werden:
haben, sind teilweise bekannt oder lassen sich nach bekannten Methoden in einfacher Weise herstellen. So erhält man z.B. Benzoylessigester der Formel (II), wenn man
Acetophenone der Formel (IX)
X, Y, Z und n die oben angegebenen Bedeutungen haben, mit Alkylcarbonaten der Formel (X)
R3-O-CO-O-R3 (X) in welcher R3 die oben angegebenen Bedeutungen hat, in Gegenwart von Basen kondensiert (Brändström, A., Acta chem. scand. 4, 1315 (1950).
Die bei dem obigen Verfahren (A) als Ausgangsstoffe weiterhin benotigten Verbindungen der Formel (III)
A, B, C und R4 die oben angegebenen Bedeutungen haben, sind teilweise bekannt oder lassen sich nach bekannten Verfahren, wie sie in der Literatur beschrieben werden, herstellen, wenn man z.B. α-Halogencarbonsäuren bzw. -ester mit Aminen umsetzt (Advanced Organic Chemistry, J. March, S, 377 (Mc Graw-Hill Inc. 1977).
Die bei dem obigen Verfahren (B) als Ausgangsstoffe benötigten Verbindungen der Formel (IV)
A, B, C, X, Y, Z und n die oben angegebenen Bedeutungen haben, sind neu und sind ebenfalls Teil des Anspruchs.
Die Verbindungen (IV) erhält man, wenn man Verbindungen der Formel (XI)
in welcher
A, B und C die oben angegebenen Bedeutungen haben, mit Benzoylverbindungen der Formel (XII)
in welcher
X, Y, Z und n die oben angegebenen Bedeutungen
haben, und M für Halogen oder Cyano steht in Gegenwart eines Verdünnungsmittels und gegebenenfalls in Gegenwart eine Base umsetzt.
Die Verbindungen (XI) sind teilweise bekannt oder lassen sich nach literaturbekannten Verfahren herstellen, z.B. Matsuo, Tanaka; Chem. Pharm. Bull. 32, 3724 (1984); Noland, Sundberg, J. Org. Chem. 28, 3150, (1963).
Verbindungen der Formel (XII) sind teilweise käuflich, oder sind nach allgemein bekannten Literaturverfahren einfach herzustellen.
Das Verfahren (A) ist dadurch gekennzeichnet, daß man
Verbindungen der Formel (II), in welcher X, Y, Z, n und R3 die oben angegebenen Bedeutungen haben, mit Aminosäureester der Formel (III), in welcher A, B, C und R4 die oben angegebenen Bedeutungen haben, in Substanz oder in Gegenwart eines Lösungsmittels umsetzt und die dabei erhaltenen Verbindungen mit einer Base kondensiert.
Als Verdünnungsmittel können bei dem erfindungsgemäßen Verfahren (A) alle üblichen inerten organischen Solventien eingesetzt werden. Vorzugsweise verwendbar sind Kohlenwasserstoffe, wie Toluol, Xylol, Dekalin,
Tetralin, Mesitylen, Triisopropylbenzol, ferner Ether, wie Dibutylether, Tetrahydrofuran, Dioxan, Glykoldimethylether und Diglykoldimethylether, außerdem polare Lö-sungsmittel, wie Dimethylsulfoxid, Sulfolan, Di-methylformamid und N-Methyl-pyrrolidon. Als Deprotonierungsmittel können bei der Durchführung des erfindungsgemäßen Verfahrens (a) alle üblichen
Protonenakzeptoren eingesetzt werden. Vorzugsweise verwendbar sind Alkalimetall- und Erdalkalimetall-oxide, -hydroxide und -carbonate, wie Natriumhydroxid, Kalium-hydroxid, Magnesiumoxid, Calciumoxid, Natriumcarbonat,
Kaliumcarbonat und Calciumcarboat, die auch in Gegenwart von Phasentransferkatalysatoren wie z.B. Triethylbenzylammoniumchlorid, Tetrabutylammoniumbromid, Adogen 464 und TDA 1 eingesetzt werden können. Ferner sind Alkalimetall- und Erdalkalimetallamide und -hydride, wie Natriumamid, Natriumhydrid und Calciumhydrid, und außerdem auch Alkaliraetall-alkoholate, wie Natrium-methylat, Natriummethylat und Kalium-tert.-butylat einsetzbar.
Adogen 464 = Methyltrialkyl (C8-C10)ammoniumchlorid TDA 1 = Tris-(methoxyethoxyethyl)-amin
Die Reaktionstemperaturen können bei der Durchführung des erfindungsgemäßen Verfahrens (A) innerhalb eines größeren Bereiches variiert werden. Im allgemeinen arbeitet man bei Temperaturen zwischen 0° C und 250° C, vorzugsweise zwischen 50° C und 200° C.
Das erfindungsgemäße Verfahren (A) wird im allgemeinen unter Normaldruck durchgeführt.
Bei der Durchführung des erfindungsgemäßen Verfahrens (A) setzt man die Reaktionskomponenten der Formeln (II) und (III) und die deprotonierenden Basen im allgemeinen in etwa äquimolaren Mengen ein. Es ist jedoch auch möglich, die eine oder andere Komponente in einem größeren Überschuß (bis zu 3 Mol) zu verwenden.
Das Verfahren (B) ist dadurch gekennzeichnet, daß Enol- ester der Formel (IV), in welcher A, B, C, X, Y, Z und n die oben angegebenen Bedeutungen haben in Gegenwart eines Lösungsmittels, gegebenenfalls in Gegenwart einer Base und in Gegenwart eines geeigneten Katalysators umgelagert werden»
Als Katalysator sind vorzugsweise verwendbar, z.B.
Lewissäuren wie ZnCl2, AlCl3, BF3-Etherat, Ti4+-Salze etc., sowie Acylierungskatalysatoren wie z.B. 4-N,N-Di-methylaminopyridin oder 4-Pyrrolidino-pyridin, wie auch Verbindungen die prinzipiell Cyanid abspalten können.
Cyanid-abspaltende Reagenzin sind Verbindungen, die während der Reaktion Cyanwasserstoff und/oder Cyanid-Anionen abspalten.
Zwei Verfahrensvarianten sind dabei möglich. Bei der einen wird das Verfahren in Gegenwart katalytischer Mengen des Cyanid- oder Cyanwasserstof f-abspaltenden Reagens zusammen mit einem molaren Überschuß einer milden Base durchgeführt. Bevorzugte Cyanid-abspaltende Reagenzien sind Alkali-cyanide wie Natrium- und Kaliumcyanid; Cyanhydrine von methyl-alkyl-Ketonen mit 1 bis 4 Kohlenstoffatomen im Alkylrest wie Aceton- oder Methyl isobutylketon-cyan- hydrinj Cyanhydrine des Benzaldehyd oder C2-Cg-Alkyl substituierter Aldehyde wie Acetaldehyd, Propional- dehyd, Zinkcyanid, tri(nieder-Alkyl)Silylcyanid wie Trimethylsilylcyanid und Cyanwasserstoff. Zu bevorzugen ist Cyanwasserstoff, da es sehr schnell reagiert und kostengünstig ist. Desweiteren kann es in flüssiger Form oder gasförmig eingesetzt werden. Wird es als Gas eingesetzt, kann es aus einer Vorratsflasche oder durch Reaktion einer Säure mit einen Metallcyanid gewonnen werden.
Unter den Cyanhydrinen wird Aceton-cyanhydrin bevorzugt.
Bei der Durchführung des erfindungsgemäßen Verfahrens (B) wird das Cyanid- 1 iefernde Reagens in einer Konzentration von 1 bis 50 Mol-Ji in Bezug auf der Enolester eingesetzt. Bevorzugt werden 1-10 Mol-%.
Bei der Durchführung des erfindungsgemäßen Verfahrens (B) wird ein Überschuß an milder Base in Bezug auf den Enolester eingesetzt. Mit milder Base bezeichnet man Basen deren Basizität zwischen starken Basen wie Alkalihydroxidlösungen (die im vorliegenden Fall Hydrolyse des Enolesters zur Folge hätten) und schwacher Base wie Alkalibicarbonate (die im vorliegenden Fall keine Reaktion zur Folge hätten) liegen» Zu den milden Basen gehören organische Basen wie tertiäre Amine und anorganische Basen wie Alkalimetallcarbonate und Alkalimetallphos- phate. Bevorzugt organische Basen sind Trialkylamine wie Triethylamin oder Trialkanolamine wie Triethanolamin und Pyridin.
Bevorzugte anorganische Basen sind Kaliumcarbonat und Trinatriumphosphat.
Die Base wird in einer Konzentration zwischen 1 und 4
Mol pro Mol Enolester eingesetzt, bevorzugt in einer
Konzentration von 2 Mol.
Ist das Cyanid-abspaltende Reagens ein Alkalicyanid, z.B. Kaliumcyanid, kann ein Phasen-transfer-Katalysator zugesetzt werden. Bevorzugt werden Kronenether eingesetzt. Als gegebenenfalls eingesetzte Verdünnungsmittel kommen nur Lösungsmittel in Frage, die mit dem Säurechlorid oder dem acylierten Produkt keine Reaktion eingehen. Bevorzugt wird 1,2-Dichlorethan eingesetzt. Weitere mögliche Verdünnungsmittel je nach Reaktanden oder Produkte sind Toluol, Acetonitril, Methylenchlorid, Ethylenacetat, Dimethylformamid und Methylisobutylketon.
Das Herstellungsverfahren (B) wird in Abhängigkeit vom Cyanid- 1 iefernden Reagens und der Reaktanten bei einer Temperatur von 80° C durchgeführt. In einigen Fällen, wenn zum Beispiel viel Nebenprodukte entstehen, was bei Einsatz von Ortho-Cyanobenzoylhalogenid und Alkalimetallcyanid oder Aceton-cyanhydrin auftreten kann, sollte die Reaktionstemperatur bei 40° C ihr Maximum haben.
In der zweiten Verfahrensvariante des Herstellungsverfahrens (B) dient Kalium oder Lithiumcyanid als Cyanid-Quelle, die ohne Einsatz einer zusätzlichen Base jedoch in stöchiometrischer Menge eingesetzt wird. Hinzugefügt wird nur noch eine katalytische Menge an Phasentransferkatalysator, in der Regel ein Kronenether oder ein acyclisches Analogen. Bevorzugter Kronenether ist
18 Krone 6. Andere hexadentale Reagenzien wie Cyclohexyl-18-Krone-6, Dibenzo-18-Krone-6, und acyclische Verbindungen wie Pentaethylenglycoldimethylether können ebenfalls verwendet werden. Für Lithiumcyanid empfiehlt sich 15-Krone-5 als Phasentrans ferkatalysator.
Diese zweite Verfahrensvariante ist zu bevorzugen für die Herstellung von Verbindungen der Formel (I), insbesondere wenn unter milden Reaktionsbedingungen verfahren werden muß und Nebenprodukte zu vermeiden sind, wie sie z.B. bei der Reaktion mit ortho-cyanophenyl-substituierten benzoylierten Cyclohexandionen bekannt sind. Diese
zweite Verfahrensvariante des Herstellungsverfahrens (B) wird bei Raumtemperatur durchgeführt. Die verwendeten Verdünnungsmittel entsprechen denen, wie sie in der ersten Verfahrensvariante des Verfahrens (B) verwendet werden, wobei Acetonitril bevorzugt wird.
Beide Verfahrensvarianten des Herstellungsverfahrens (B) werden mit dem Enol-Ester der Formel (IV) als Ausgangssubstanz durchgeführt. Der Enolester kann aber auch in situ hergestellt werden, zum Beispiel durch Reaktion des Acylierungsreagens mit einem Diketon, wobei mit Enolester der Enolester einer Carbonsäure gemeint ist. Wird der Enolester als Ausgangssubstanz in beiden Verfahrensvarianten vorgelegt, so kann er zuvor nach literaturbekannten Verfahren hergestellt werden z.B. durch Acylierung einer ß-Dicarbonylverbindung mit Säurehalogeniden.
Die Synthese der acylierten Pyrrolidin-2,4-dione nach dem Herstellungsverfahren (B), beginnend mit dem Acylierungsreagens und Pyrrolidindion (z.B. Säurehalogenid wie Benzoylchlorid und Pyrrolidindion) kann mit oder ohne Isolierung des intermediär gebildeten Enolesters erfolgen.
Im ersten Fall läßt man das Säurehalogenid oder ein anderes acylierendes Reagens und das Pyrrolidindion in Gegenwart einer milden Base wie Triethylamin reagieren. Der daraus anfallende Enolester kann durch bekannte
Methoden aus der organischen Chemie isoliert werden.
Diese Verfahrensweise empfiehlt sich dann, wenn im zweiten Reaktionsschritt ein anderes Lösungsmittel eingesetzt wird, um den Enolester in ein acyliertes Diketon umzulagern. Der getrocknete Enolester wird dazu in einem geeigneten Lösungsmittel wie Acetonitril- oder 1,2-Dichlorethan gelöst und mit dem Cyanid-liefernden Reagens der Wahl und einer schwachen Base oder einem Kronenether versetzt. Die Reaktionstemperatur richtet sich dabei nach der Verfahrensvariante.
Als Alternative steht die Eintopfvariante zur Verfügung, wobei der Enolester im Reaktionsmedium verbleibt und direkt in der zweiten Stufe in demselben Lösungsmittel mit dem Cyanid-liefernden Reagens und gegebenenfalls einer Base versetzt wird.
In einer weiteren Verfahrensvariante erhält man das acylierte Pyrrolidindion in einer Einstufenraktion durch in situ Synthese und Umlagerung des Enolesters, indem man das Säurehalogenid oder andere acylierende Reagenzien mit Pyrrolidindionen in Gegenwart geeigneter Mengen Cyanid-liefernden Reagens und milder Base oder
Kronenether umsetzt, je nachdem, welches
Herstellungsverfahren herangezogen wird.
Man erhält bei beiden Verfahrensvarianten, d.h. mit oder ohne Isolierung der Enolester, vergleichbare Ausbeuten.
Das acylierte Pyrrolidindion erhält man durch dieses
Herstellungsverfahren (B) in Form seines Salzes, woraus es durch Ansäuern und Extraktion mit einem geeigneten Lösungsmittel freigesetzt werden kann. In einigen Fällen kann das Produkt durch geringe Mengen Carbonsäure, entstanden aus dem Carbonsäurechlorid, verunreinigt sein. Diese Verunreingungen entfernt man durch Versetzen des sauren Produkts mit wäßriger Natriumhydroxyd-Lösung oder anderer geeigneter Basen, um die Säure als Salz abzutrennen. In der zweiten Verfahrensvariante des Herstellungsverfahrens erhält man das acylierte Pyrrolidindion direkt in reiner Form.
Das Verfahren (C) ist dadurch gekennzeichnet, daß man Verbindungen der Formel (Ia) mit Alkylierungsreagenzien der Formel (V) gegebenenfalls in Gegenwart eines Verdünnungsmittels und gegebenenfalls in Gegenwart eines Säurebindemittels umsetzt. Die Verbindungen der Formel (I) sind erfindungsgemäße Verbindungen und nach dem oben beschriebenen Verfahren erhältlich.
Die weiterhin als Ausgangsstoffe zur Herstellung der erfindungsgemäßen Verbindungen (Ib) als Ausgangsstoffe benötigten Alkylierungsmittel sind durch die Formel (V) allgemein definiert.
In der Formel (V) steht E vorzugsweise für die in den Vorzugsbereichen angegebenen Bedeutungen, ganz besonders bevorzugt für Methyl, Ethyl, Propyl oder iso-Propyl,
Allyl, Propinyl und durch Fluor, Chlor, Methyl, Methoxy oder Trif luormethyl substituiertes Benzyl. In der Formel (V) steht L bevorzugt für Chlor, Brom oder lad, C1-C6- Alkylsulfonyloxy, C 1-C4-Alkoxysulfonyloxy oder p-Toluolsulfonyloxy, wie beispielsweise Methansulfonyloxy, Methoxysulfonyloxy oder Ethoxysulfonyloxy.
Die Alkylierungsreagenzien der Formel (V) sind bekannte Verbindungen der organischen Chemie. Zur Durchführung des erfindungsgemäßen Verfahrens (C) zur Herstellung der erfindungsgemäßen Verbindungen (Ib) kommen als Verdünnungsmittel inerte organische Lösungsmittel in Frage. Vorzugsweise verwendet man aliphatische, alicyclische oder aromatische, gegebenenfalls halogenierte Kohlenwasserstoffe, wie beispielsweise Benzin, Benzol, Toluol, Xylol, Pentan, Hexan, Heptan Cyclohexan, Petrolether, Ligroin, Methylenchlorid,
Chloroform, Tetrachlorkohlenstoff, Chlorbenzol oder Dichlorbenzol, Ether, wie Diethylether, Diisopropylether, Dioxan, Tetrahydrofuran oder Ethylenglykoldiethylether oder -dimethylether, Ketone wie Aceton, Butanon, Methyl isopropylketon oder Methylisobutylketon, Ester, wie Essigsäureethylester, Säuren, wie Essigsäure, Nitrile, wie Acetonitril oder Propionitril, Amide, wie Dimethylformamid, Dimethylacetamid, N-Methyl-pyrrolidon oder Hexamethylphosphorsäuretriamid. Verwendet man als Reaktionspartner Verbindungenn der Formel (V) in flüssi
ger Form, so ist es auch möglich, diese in entsprechendem Überschuß gleichzeitig als Verdünnungsmittel einzusetzen.
Als Säurebindemittel kommen alle üblicherweise verwendbaren anorganischen und organischen Basen in Frage, Vorzugsweise verwendet man Alkalimetallhydride, -hydroxide, -amide, -carbonate oder -hydrogencarbonate, wie beispielsweise Natriumhydrid, Natriumamid, Natriumhydroxid, Natriumcarbonat oder Natriumhydrogencarbonat, oder auch tertiäre Amine, wie beispielsweise Triethylamin, N,N-Di-methylanilin, Pyridin, 4-(N,N-Dimethylamino)-pyridin, Diazoabicyclooctan (DABCO), Diazabicyclononen (DBN) oder Diazabicycloundecen (DBU), Die Reaktionstemperaturen können bei der Durchführung in einem größeren Bereich variiert werden. Im allgemeinen arbeitet man zwischen -20° C und +150°C, vorzugsweise zwischen 0° C und +100° C, z.ur Durchführung des erfindungsgemäßen Verfahrens (C) zur Herstellung der erfindungsgemäßen Verbindungen (Ib) setzt man pro Mol an Verbindungen der Formel (Ia) im allgemeinen jeweils 1 bis 20 Mol, vorzugsweise jeweils 1 bis 15 Mol, Alkyl ierungsmittel der Formel (V) und gegebenenfalls 1 bis 3 Mol, vorzugsweise 1 bis 2 Mol
Säurebindemittel ein. Die Reaktionsdurchführung, Aufarbeitung und Isolierung der Reaktionsprodukte der Formel (Ib) erfolgt nach den in der organischen Chemie üblichen
Methoden.
Das erfindungsgemäße Verfahren (D) ist dadurch gekennzeichnet, daß man Verbindungen der Formel (Ia) mit Acylierungsreagenzien der Formel (VI) umsetzt.
Als Verdünnungsmitel können bei dem erfindungsgemäßen Verfahren (D) alle inerten Solventien eingesetzt werden. Vorzugsweise verwendbar sind Kohlenwasserstoffe, wie Benzin, Benzol, Toluol, Xylol und Tetralin, ferner
Halogenkohlenwasserstoffe, wie Methylenchlorid, Chloroform, Tetrachlorkohlenstoff, Chlorbenzol und o-Dichlorbenzol, außerdem Ketone, wie Aceton und Methylisopropylketon, weiterhin Ether, wie Diethylether, Tetrahydrofuran und Dioxan, darüber hinaus Carbonsäureester wie Essigsäureethylester oder Solventien, wie Dimethylsulfoxid und Sulfolan. Wenn die Hydrolysestabilität des Acylierungsreagens es zuläßt, kann die Umsetzung auch in Gegenwart von Wasser durchgeführt werden.
Als Säurebindemittel kommen bei der Umsetzung nach dem erfindungsgemäßen Verfahren (D) alle üblichen Säureakzeptoren in Betracht. Vorzugsweise verwendbar sind tertiäre Amine , wie Triethylamin, Pyridin, Diazabicyclooctan (DABCO), Diazabicycloundecen (DBU), Diazabicyclononen (DBN), Hünig-Base und N,N-Dimethyl-anilin, ferner Erdalkalimetalloxide, wie Magnesium- und Calciumoxid, außerdem Alkali- und Erdalkali-metall-carbonate, wie Natriumcarbonat, Kaliumcarbonat und Calciumcarbonat.
Die Reaktionstemperaturen können auch bei dem erfindungsgemäßen Verfahren (D) innerhalb eines größeren
Bereiches variiert werden. Im allgemeinen arbeitet man bei Temperaturen zwischen -20° C und +150° C, vorzugsweise zwischen 0° C und 100° C.
Bei der Durchführung des erfindungsgemäßen Verfahrens (D) werden die Ausgangsstoffe der Formel (Ia) und das Acyl ierungsreagens der Formel (VI) im allgemeinen in angenähert äquivalenten Mengen verwendet. Es ist jedoch auch möglich, das Acyl ierungsreagens in einem größeren Überschuß (bis zu 5 Mol) einzusetzen. Die Aufarbeitung erfolgt nach üblichen Methoden.
Das erfindungsgemäße Verfahren (E) ist dadurch gekennzeichnet, daß man Verbindungen der Formel (Ia) mit
Metallhydroxiden (VII) oder Aminen (VIII) umsetzt.
Als Verdünnungsmittel können bei dem erfindungsgemäßen Verfahren (E) vorzugsweise Ether wie Tetrahydrofuran, Dioxan, Diethylether, Nitrile oder Acetonitril oder aber Alkohole wie Methanol, Ethanol, Isopropanol, aber auch Wasser eingesetzt werden. Das erfindungsgemäße Verfahren (E) wird im allgemeinen unter Normaldruck durchgeführt. Die Reaktionstemperaturen liegen im allgemeinen zwischen -20° C und 100° C, vorzugsweise zwischen 0° C und 50° C.
Bei der Durchführung des erfindungsgemäßen Verfahrens (E) werden die Ausgangsstoffe der Formel (Ia) bzw. (VII) oder (VIII) im allgemeinen in angenähert äquimolaren Mengen verwendet. Es ist jedoch auch möglich, die eine oder andere Komponente in einem größeren Überschuß (bis zu 2 Mol) einzusetzen. Im allgemeinen geht man so vor, daß man das Reakt ionsgemisch durch Entfernen des Verdünnungsmittels im Vakuum einengt.
Die Aufarbeitung erfolgt wiederum nach üblichen Methoden.
Die Wirkstoffe eignen sich zur Bekämpfung von tierischen Schädlingen, vorzugsweise Arthropoden und Nematoden, insbesondere Insekten und Spinnentieren, die in der Landwirtschaft, in Forsten, im Vorrats- und Materialschutz sowie auf dem Hygienesektor vorkommen. Sie sind gegen normal sensible und resistente Arten sowie gegen alle oder einzelne Entwicklungsstadien wirksam. Zu den oben erwähnten Schädlingen gehören:
Aus der Ordnung der Isopoda z.B. Oniscus asellus, Armadillidium vulgäre, Porcellio scaber.
Aus der Ordnung der Diplopoda z.B. Blaniulus guttula- tus.
Aus der Ordnung der Chilopoda z.B. Geophilus carpophagus, Scutigera spec.
Aus der Ordnung der Symphyla z.B. Scutigerella Immaculata.
Aus der Ordnung der Thysanura z.B. Lepisma saccharina. Aus der Ordnung der Collembola z.B. Onychiurus armatus. Aus der Ordnung der Orthoptera z.B. Blatta orientalis, Periplaneta americana, Leucophaea maderae, Blattella germanica, Acheta domesticus, Gryllotalpa spp., Locusta migratoria migratorioides, Melanoplus dif ferentialis, Schistocerca gregaria.
Aus der Ordnung der Dermaptera z.B. Forficula auricularia.
Aus der Ordnung der Isoptera z.B. Reticul itermes spp,. Aus der Ordnung der Anoplura z.B. Phylloxera vastatrix, Pemphigus spp., Pediculus humanus corporis, Haematopinus spp», Linognathus spp. Aus der Ordnung der Mallophaga z.B. Trichodectes spp,,
Damalinea spp.
Aus der Ordnung der Thysanoptera z.B. Hercinothrips femoralis, Thrips tabaci.
Aus der Ordnung der Heteroptera z.B. Eurygaster spp., Dysdercus intermedius, Piesma quadrata, Cimex lectularius, Rhodnius prolixus, Triatoma spp.
Aus der Ordnung der Homoptera z.B. Aleurodes brassicae, Bemisia tabaci, Trialeurodes vaporariorum, Aphis gossypii, Brevicoryne brassicae, Cryptomyzus ribis, Aphis fabae, Doralis pomi , Eriosoma lanigerum, Hyalopterus arundinis, Macrosiphum avenae, Myzus spp., Phorodon humuli, Rhopalosiphum padi, Empoasca spp., Euscelis bilobatus, Nephotettix cincticeps, Lecanium corni, Saissetia oleae, Laodelphax striatellus, Nilaparvata lugens, Aonidiella aurantii, Aspidiotus hederae, Pseudococcus spp. Psylla spp.
Aus der Ordnung der Lepidoptera z.B. Pectinophora gossypiella, Bupalus piniarius, Cheimatobia brumata, Litho- colletis blancardella, Hyponomeuta padella, Plutella maculipennis, Malacosoma neustria, Euproctis chrysorrhoea, Lymantria spp. Bucculatrix thurberiella, Phyllocnistis citrella, Agrotis spp., Euxoa spp., Feltia spp., Earias insulana, Heliothis spp,, Spodoptera exigua, Mamestra brassicae, Panolis flammea, Prodenia litura,
Spodoptera spp., Trichoplusia ni, Carpocapsa pomonella, Pieris spp., Chilo spp., Pyrausta nubilalis, Ephestia kuehniella, Galleria mellonella, Tineola bisselliella, Tinea pellionella, Hofmannophi la pseudospretel la, Cacoecia podana, Capua reticulana, Choristoneura fumi- ferana, Clysia ambiguella, Homona magnanima, Tortrix vir idana.
Aus der Ordnung der Coleoptera z.B. Anobium punctatum, Rhizopertha dominica, Acanthoscelides obtectus, Acanthoscelides obtectus, Hylotrupes bajulus, Agelastica alni, Leptinotarsa decemlineata, Phaedon cochleariae, Diabrotica spp., Psylliodes chrysocsphala, Epilachna varive stis, Atomaria spp», Oryzaephilus surinamensis, Antho nomus spp., Sitophilus spp., Otiorrhynchus sulcatus, Cosmopolites sordidus, Ceuthorrhynchus assimilis, Hypera postica, Dermestes spp», Trogoderma spp., Anthrenus spp., Attagenus spp», Lyctus spp., Meligethes aeneus, Ptinus spp., Niptus hololeucus, Gibbium psylloides, Tribolium spp., Tenebrio molitor, Agriotes spp., Cono derus spp., Melolontha melolontha, Amphimallon solsti tialis, Costelytra zealandica.
Aus der Ordnung der Hymenoptera z.B. Diprion spp., Hoplocampa spp., Lasius spp., Monomorium pharaonis, Vespa spp.
Aus der Ordnung der Diptera z.B. Aedes spp., Anopheles spp., Culex spp«, Drosophila melanogaster, Musca spp.,
Fannia spp., Calliphora erythrocephala, Lucilia spp.,
Chrysomyia spp., Cuterebra spp., Gastrophilus spp., Hyppobosca spp., Stomoxys spp., Oestrus spp., Hypoderma
spp., Tabanus spp., Tannia spp., Bibio hortulanus, Oscinella frit, Phorbia spp., Pegomyia hyoscyami, Cerati tis capitata, Dacus oleae, Tipula paludosa.
Aus der Ordnung der Siphonaptera z.B. Xenopsylla cheopis, Ceratophyllus spp..
Aus der Ordnung der Arachnida z.B. Scorpio maurus,
Latrodectus mactans.
Aus der Ordnung der Acarina z.B. Acarus siro, Argas spp., Ornithodoros spp., Dermanyssus gallinae, Eriophyes ribis, Phyllocoptruta oleivora, Boophilus spp., Rhipicephalus spp., Amblyomma spp«, Hyalomma spp., Ixodes spp., Psoroptes spp., Chorioptes spp., Sarcoptes spp., Tarso- nemus spp., Bryobia praetiosa, Panonychus spp., Tetranychus spp..
Die erfindungsgemäßen Wirkstoffe zeichnen sich durch eine hohe insektizide Wirksamkeit aus.
Sie lassen sich mit besonders gutem Erfolg zur Bekämpfung von pf lanzenschädigenden Insekten, wie beispielsweise gegen die Larven des Meerrettichblattkäfers
(Phaedon cochleariae) oder gegen die Larven der Kohlschabe (Plutella maculipennis) einsetzen.
Darüber hinaus zeigen die erfindungsgemäßen Wirkstoffe auch akarizide Wirksamkeit.
Die erfindungsgemäßen Wirkstoffe können weiterhin als Defoliants, Desiccants, Krautabtötungsmittel und insbesondere als Unkrautvernichtungsmittel verwendet werden. Unter Unkraut im weitesten Sinne sind alle Pflanzen zu verstehen, die an Orten aufwachsen, wo sie unerwünscht sind. Ob die erfindungsgemäßen Stoffe als totale oder selektive Herbizide wirken, hängt im wesentlichen von der angewendeten Menge ab.
Die erfindungsgemäßen Wirkstoffe können z.B. bei den folgenden Pflanzen verwendet werden:
Dikotyle Unkräuter der Gattungen: Sinapis, Lepidium, Galium, Stellaria, Matricaria, Anthemis, Galinsoga, Chenopodium, Urtica, Senecio, Amaranthus, Portulaca, Xanthi- um, Convo lvulus , Ipomoea , Po lygonum, Sesbania , Ambros ia , C irsium, Carduus, Sonchus, Solanum, Rorippa, Rotala, Lindernia, Lamium, Veronica, Abutilon, Emex, Datura, Viola, Galeopsis, Papaver, Centaurea, Trifolium, Ranunculus, Taraxacum. Dikotyle Kulturen der Gattungen: Gossypium, Glycine,
Beta, Daucus, Phaseolus, Pisum, Solanum, Linum, Ipomoea, Vicia, Nicotiana, Lycopersicon, Arachis, Brassica, Lactuca, Cucumis, Cucurbita.
Monokotyle Unkräuter der Gattungen: Echinochloa, Setaria, Panicum, Digitaria, Phleum, Poa, Festuca, Eleusine, Brachiaria, Lolium, Bromus, Avena, Cyperus, Sorghum, Agropyron, Cynodon, Monochoria, Fimbristylis, Sagitta
ria, Eleocharis, Scirpus, Paspalum, Ischaemum, Sphenoclea, Dactyloctenium, Agrostis, Alopecurus, Apera.
Monokotyle Kulturen der Gattungen: Oryza, Zea, Triticum, Hordeum, Avena, Seeale, Sorghum, Panicum, Saccharum, Ananas, Asparagus, Allium,
Die Verwendung der erfindungsgemäßen Wirkstoffe ist jedoch keineswegs auf diese Gattungen beschränkt, sondern erstreckt sich in gleicher Weise auch auf andere Pflanzen.
Die Verbindungen eignen sich in Abhängigkeit von der Konzentration zur Totalunkrautbekämpfung z.B. auf Industrie- und Gleisanlagen und auf Wegen und Plätzen mit und ohne Baumbewuchs. Ebenso können die Verbindungen zur Unkrautbekämpfung in Dauerkulturen, z.B. Forst, Zierge- hδlz-, Obst-, Wein-, Citrus-, Nuß-, Bananen-, Kaffee-, Tee-, Gummi-, Ölpalm-, Kakao-, Beerenfrucht- und Hopfenanlagen, auf Zier- und Sportrasen und Weideflächen und zur selektiven Unkrautbekämpfung in einjährigen Kulturen eingesetzt werden.
Die erfindungsgemäßen Verbindungen eignen sich zur selektiven Bekämpfung von mono- und dikotylen Unkräutern in monokotylen Kulturen im Vor- und Nachauf laufverfahren.
Die Wirkstoffe können in die üblichen Formulierungen überführt werden, wie Lösungen, Emulsionen, Spritzpulver, Suspensionen, Pulver, Stäubemittel, Pasten, lösliehe Pulver, Granulate, Suspensions-Emuls ions-Konzentrate, Wirkstoff-imprägnierte Natur- und synthetische Stoffe sowie Feinstverkapselungen in polymeren Stoffen.
Diese Formulierungen werden in bekannter Weise hergestellt, z.B. durch Vermischen der Wirkstoffe mit
Streckmitteln, also flüssigen Lösungsmitteln und/oder festen Trägerstoffen, gegebenenfalls unter Verwendung von oberflächenaktiven Mitteln, also Emulgiermitteln und/oder Dispergiermitteln und/oder schaumerzeugenden Mitteln.
Im Falle der Benutzung von Wasser als Streckmittel können z.B. auch organische Lösungsmittel als Hilfslösungsmittel verwendet werden. Als flüssige Lösungsmittel kommen im wesentlichen in Frage: Aromaten, wie Xylol, Toluol, oder Alkylnaphthaline, chlorierte Aromaten und chlorierte aliphatische Kohlenwasserstoffe, wie Chlorbenzole, Chlorethylene oder Methylenchlorid, aliphatische Kohlenwasserstoffe, wie Cyclohexan oder Paraffine, z.B. Erdöl fraktionen, mineralische und pflanzliche Öle, Alkohole, wie Butanol oder Glykol sowie deren Ether und Ester, Ketone wie Aceton, Methylethylketon, Methylisobutylketon oder Cyclohexanon, stark polare Lösungsmittel, wie Dimethylformamid und Dimethylsulfoxid, sowie Wasser.
Als feste Trägerstoffe kommen in Frage:
z.B. Ammoniumsalze und natürliche Gesteinsmehle, wie Kaoline, Tonerden, Talkum, Kreide, Quarz, Attapulgit, Montmorillonit oder Diatomeenerde und synthetische Gesteinsmehle, wie hochdisperse Kieselsäure, Aluminiumoxid und Silikate, als feste Trägerstoffe für Granulate kommen in Frage: z.B. gebrochene und fraktionierte natürliche Gesteine wie Calcit, Marmor, Bims, Sepiolith, Dolomit sowie synthetische Granulate aus anorganischen und organischen Mehlen sowie Granulate aus organischem Mate
rial wie Sägemehl, Kokosnußschalen, Maiskolben und Tabakstengeln; als Emulgier- und/oder schaumerzeugende Mittel kommen in Frage: z.B. nichtionogene und anionische Emulgatoren, wie Polyoxyethylen-Fettsäure-Ester, Polyoxyethylen-Fettalkohol-Ether, z.B. Alkylaryl-polyglykolether, Alkylsulfonate, Alkylsulfate, Arylsulfonate sowie Einweißhydrolysate; als Dispergiermittel kommen in Frage: z.B. Lignin-Sulf itablaugen und Methylcellulose.
Es können in den Formulierungen Haftmittel wie Carboxymethylcellulose, natürliche und synthetische pulvrige, körnige oder latexformige Polymere verwendet werden, wie Gummiarabicum, Polyvinylalkohol, Polyvinylacetat, sowie natürliche Phospholipide, wie Kephaline und Lecithine und synthetische Phospholipide. Weitere Additive können mineralische und vegetabile Öle sein.
Es können Farbstoffe wie anorganische Pigmente, z.B.
Eisenoxid, Titanoxid, Ferrocyanblau und organische Farbstoffe, wie Alizarin-, Azo- und Metal lphthalocyaninfarbstoffe und Spurennährstoffe wie Salze von Eisen, Mangan, Bor, Kupfer, Kobalt, Molybdän und Zink verwendet werden.
Die Formulierungen enthalten im allgemeinen zwischen 0,1 und 95 Gew.-5. Wirkstoff, vorzugsweise zwischen 0,5 und 90 %.
Die erfindungsgemäßen Wirkstoffe können als solche oder in ihren Formulierungen auch in Mischung mit bekannten Herbiziden zur Unkrautbekämpfung Verwendung finden, wobei Fertigformulierungen oder Tankmischungen möglich sind.
Auch eine Mischung mit anderen bekannten Wirkstoffen, wie Fungiziden, Insektiziden, Akariziden, Nematiziden, Schutzstoffen gegen Vogelfraß, Pflanzennährstoffen und Bodenstrukturverbesserungsmitteln ist möglich.
Die Wirkstoffe können als solche, in Form ihrer Formulierungen oder den daraus durch weiteres Verdünnen bereiteten Anwendungsformen, wie gebrauchsfertige Lösungen, Suspensionen, Emulsionen, Pulver, Pasten und Granulate angewandt werden. Die Anwendung geschieht in üblicher Weise, z.B. durch Gießen, Spritzen, Sprühen, Streuen.
Die erfindungsgemäßen Wirkstoffe können sowohl vor als auch nach dem Auflaufen der Pflanzen appliziert werden. Sie können auch vor der Saat in den Boden eingearbeitet werden.
Die angewandte Wirkstoffmenge kann in einem größeren Bereich schwanken. Sie hängt im wesentlichen von der Art des gewünschten Effektes ab. Im allgemeinen liegen die Aufwandmengen zwischen 0,01 und 10 kg Wirkstoff pro Hektar Bodenfläche, vorzugsweise zwischen 0,05 und 5 kg pro ha.
Die Herstellung und Verwendung der erfindungsgemäßen Wirkstoffe geht aus den nachfolgenden Beispielen hervor.
Herstellungsbeispiele
Beispiel 1
12,36 g (50 mmol) Methoxycarbonyl-2,4-dichloracetophenon und 9,6 g (50 mmol) N-Methylamino-phenylessig- säureethylester werden in 50 ml absolutem Xylol 12 Stunden bei 120-125° C gerührt. Das Reaktionsgemisch wird dann in eine Lösung von 3,75 g Natriumethylat (55 mmol) in 40 ml absolutem Ethanol eingetropft und 4 Stunden bei 70° C gerührt.
Danach nimmt man die Lösung in einen Gemisch aus
Methylenchlorid und 1 normaler Salzsäure auf, extrahiert, trennt die wäßrige Phase ab und wiederholt den
Vorgang mit Natriumhydrogencarbonat-Lösung. Nach Trennen der beiden Phasen voneinander säuert man die wäßrige Phase an, wobei ein klebriger Niederschlag ausfällt, der mit Methylenchlorid aufgenommen wird. Das Lösungsmittel wird im Vakuum entfernt und man erhält 9,98 g (55 % der Theorie). 3-(2,4-Dichlorbenzoyl)-1-methy1-5-phenylpyrrolidin-2,4-dion mit Schmelzpunkt 137-138° C.
Beispiel 2 nach Verfahren B
2,4 g (8 mmol) 4-(2,4-Dichlor-benzoyloxy)-5,5-dimethyl- 1H-pyrrolin-2-on werden in 40 ml absolutem Acetonitril vorgelegt und mit 2,24 ml (16 mmol) Triethylamin und 0,18 ml (2 mmol) Hydroxyisobuttersäurenitril bei Raumtemperatur zur Reaktion gebracht. Nach Beendigung der Reaktion, was durch Dünnschichtchromatographie festgestellt wird, rührt man das Reaktionsgemisch in 100 ml
1 normaler HCl ein, filtriert den dabei anfallenden
Niederschlag ab, trocknet und erhält 1,9 g (79 % der
Theorie) 3-(2,4-Dichlorbenzoyl)-5,5-dimethyl-1H-pyrrolidin-2,4-dion vom Schmelzpunkt 144-146°C.
In analoger Weise zu Beispiel 1 und unter Berücksichtigung der Angaben in der Beschreibung zu den erfindungsgemäßen Verfahren, werden die nachfolgend in
Tabelle 2 aufgeführten Endprodukte der Formel (I)
erhalten.
Tabelle 2
Präparat- A B C X Y Zn Fp.[°C]
Nummer
3 H CH3 CH3 NO2 H H 182
4 CH3 CH3 H CI CI H 99-100
5 CH3 C6H5-CH2- H CI CI H Öl
6 i-C3H7 H H CI CI H 99-100
7 cyclo-C5H9 H H CI CI H 96-97
8 cyclo-C5H9 CH3 H CI CI H 98-99
9 C6H7 CH3 H CI CI H 158-159
10 C6H5-CH2- H H CI CI H 82-84
11 -(CH2)4 - H CI CI H 107-108
12 H CH3 CH3 CI SO2CH3 O-(CH2)2-OCH3 Harz
13 CH3 H H CI CI H 125 (Zers.)
14 CH3 C2H5 H CI CI H Öl
Tabelle 2
Präparat- A B C X Y Zn Fp.[°C]
Nummer
15 H -(CH2)5- CI CI H 211
16 H CH3 cyclo-C3H7 CI CI H 158
17 H CH3 H CI CI H 150
18 H CH3 CH3 CI NO2 H 173
19 H CH3 i-C4H9 CI CI H 117
20 H CH3 CH3 F CF3 H >200
21 H CH3 CH3 CI OCF3 H 116
22 H CH3 i-C3H7 CI CI H 153
23 H CH3 CH3 F F H 136
24 H CH3 CH3 CI F H 132
25 H CH3 CH3 CH3 Br H
26 H CH3 CH3 CI Br H 148
27 H CH3 CH3 F CI H >230
Vorprodukte für Verfahren B
Zu 1,9 g (15 mmol) 2,2-Dimethyl-1H-pyrrolidin-3,5-dion, gelöst in 50 ml absolutem Methylenchlorid, gibt man bei 0-10°C, 2,1 ml Triethylamin und 3,14 g (15 mmol) 2,4-Di- chlor-benzoylchlorid, die ihrerseits in 5 ml absolutem Methylenchlorid gelöst sind. Dann läßt man bei Raumtem-
peratur nachreagieren und kontrolliert den Reaktionsablauf durch Dünnschichtchromatographie.
Nach Beendigung der Reaktion entfernt man das Lösungsmittel im Vakuum, wäscht mit 200 ml 0,1 normaler Natriumhydroxid-Lösung nach, trocknet die oganische Phase mit Magnesiumsulfat und engt wiederum im Vakuum ein. Der Rückstand wird aus Essigester/n-Hexan umkristallisiert. Man erhält 3,2 g (71 54 der Theorie) 4-(2,4-Dichlorbenzoyloxy)-5,5-dimethylpyrrolin-1H-2-on der Formel (IV-1) mit Schmelzpunkt 167° C.
Tabelle 3
Präparat- A B C X Y Zn Fp.
Nummer [°C]
IV-2 H CH3 CH3 NO2 H H 144
IV-3 H CH3 CH3 CI NO2 H 226
IV-4 H CH3 CH3 F CF3 H 178
IV-5 H CH3 CH3 CI SO2CH3 O(CH2)2OCH3 181
IV-6 H -(CH2)5- CI CI H 238
IV-7 H -(CH2)5- CI SO2CH3 O(CH2)2OCH3 193
IV-8 H CH3 cyclo- CI CI H 175
C3H7
IV-9 H CH3 H CI CI H 137
IV-10 H CH3 CH3 CI OCF3 H 136
IV-11 H CH3 i-C4H9 CI CI H 128
IV-12 H CH3 i-C3H7 CI CI H 204
IV-13 H CH3 CH3 CI F H 177
IV-14 H CH3 CH3 F F H 184
Tabelle 3
Präparat- A B C X Y Zn Fp.
Nummer [°C]
IV-15 H CH3 CH3 CI Br H 186
IV-16 H CH3 CH3 CH3 Br H 176
IV-17 H CH3 CH3 F CI H >220
IV-18 H CH3 CH3 CI SO2CH3 H 171
Anwendungsbeispiele
In den folgenden Anwendungsbeispielen wurde die nachstehend aufgeführte Verbindung als Vergleichssubstanz eingesetzt:
3-(2,4-Dichlorbenzoyl)-2,5-dihydro-4-hydroxy-5-methyl- furan-2-on
Be i sp i e l A
Pre-emergence-Test
Lösungsmittel: 5 Gewichtsteile Aceton
Emulgator: 1 Gewichtsteil Alkylarylpolyglykolether
Zur Herstellung einer zweckmäßigen Wirkstoff Zubereitung vermischt man 1 Gewichtsteil Wirkstoff mit der angegebenen Menge Lösungsmittel, gibt die angegebene Menge Emulgator zu und verdünnt das Konzentrat mit Wasser auf die gewünschte Konzentration.
Samen der Testpflanzen werden in normalen Boden ausgesät und nach 24 Stunden mit der WirkstoffZubereitung begossen. Dabei hält man die Wassermenge pro Flächeneinheit zweckmäßigerweise konstant. Die Wirkstoffkonzentration in der Zubereitung spielt keine Rolle, entscheidend ist nur die Aufwandmenge des Wirkstoffs pro Flächeneinheit. Nach drei Wochen wird der Schädigungsgrad der Pflanzen bonitiert in 54 Schädigung im Vergleich zur Entwicklung der unbehandelten Kontrolle. Es bedeuten:
0 % = keine Wirkung (wie unbehandelte Kontrolle) 100 % = totale Vernichtung
Eine deutliche Überlegenheit in der Wirksamkeit ebenso wie in der Nutzpflanzenselektivität gegenüber dem Stand der Technik zeigen in diesem Test z.B. die Verbindungen gemäß folgender Herstellungsbeispiele: 2 und 6.
Be i sp i e l B
Post-emergence-Test
Lösungsmittel: 5 Gewichtsteile Aceton
Emulgator: 1 Gewichtsteil Alkylarylpolyglykolether
Zur Herstellung einer zweckmäßigen WirkstoffZubereitung vermischt man 1 Gewichtsteil Wirkstoff mit der angegebenen Menge Lösungsmittel, gibt die angegebene Menge Emulgator zu und verdünnt das Konzentrat mit Wasser auf die gewünschte Konzentration.
Mit der Wirkstoffzubereitung spritzt man Testpflanzen, welche eine Höhe von 5 - 15 cm haben, so, daß die jeweils gewünschten Wirkstoffmengen pro Flächeneinheit ausgebracht werden. Nach drei Wochen wird der Schädigungsgrad der Pflanzen bonitiert in 54 Schädigung im Vergleich zur Entwicklung der unbehandelten Kontrolle. Es bedeuten:
0 % = keine Wirkung (wie unbehandelte Kontrolle) 100 % = totale Vernichtung
Eine deutliche Überlegenheit in der Wirksamkeit ebenso wie in der Nutzpflanzenselektivität gegenüber dem Stand der Technik zeigen in diesem Test z.B. die Verbindung gemäß Herstel lungsbeispiel 2,
Be i sp i e l C
Plutella-Test
Lösungsmittel: 7 Gewichtsteile Dimethyl formamid
Emulgator: 1 Gewichtsteil Alkylarylpolyglykαlether
Zur Herstellung einer zweckmäßigen WirkstoffZubereitung vermischt man 1 Gewichtsteil Wirkstoff mit der angegebenen Menge Losungsmittel und der angegebenen Menge Emulgator und verdünnt das Konzentrat mit Wasser auf die gewünschte Konzentration«
Kohlblätter (Brassica oleracea) werden durch Tauchen in die WirkstoffZubereitung der gewünschten Konzentration behandelt und mit Raupen der Kαhlschabe (Plutella maculipennis ) besetzt, solange die Blätter noch feucht sind.
Nach der gewünschten Zeit wird die Abtötung in % bestimmt. Dabei bedeutet 100 */., daß alle Raupen abgetötet wurden; 0 % bedeutet, daß keine Raupen abgetötet wurden.
Bei diesem Test zeigt z.B. die Verbindung 4 der Her- stellungsbeispiele überlegene Wirksamkeit gegenüber dem Stand der Technik.
Be i sp i e l D
Phaedon-Larven-Test
Lösungsmittel: 7 Gewichtsteile Dimethylformamid
Emulgator: 1 Gewichtsteil Alkylarylpαlyglykαlether
Zur Herstellung einer zweckmäßigen WirkstoffZubereitung vermischt man 1 Gewichtsteil Wirkstoff mit der angegebenen Menge Lösungsmittel und der angegebenen Menge Emul- gator und verdünnt das Konzentrat mit Wasser auf die gewünschte Konzentration.
Kohlblätter (Brassica oleracea) werden durch Tauchen in die WirkstoffZubereitung der gewünschten Konzentration behandelt und mit Meerrettichblattkäfer-Larven (Phaedon cαchleariae) besetzt, solange die Blätter noch feucht sind.
Nach der gewünschten Zeit wird die Abtδtung in */% be- stimmt. Dabei bedeutet 100 %, daß alle Käferlarven abgetötet wurden; 0 % bedeutet, daß keine Käfer-Larven abgetötet wurden.
Claims
1. Substituierte 3-Benzoyl-pyrrolidin-2,4-dion- Derivate der allgemeinen Formel (I)
,
in welcher X für Wasserstoff, Alkyl, Halogen, Alkoxy, Halogenalkyl, Halogenalkoxy, Nitro, Alkoxycarbonyl, Carboxy, Cyano oder -S(O)m-R1 steht, Y für Wasserstoff, Alkyl, Halogen, Alkoxy, Halogenalkyl, Halogenalkoxy, Nitro, Alkoxycarbonyl, Carboxy, Cyano oder -S(O)m-R1 steht, Z für Alkyl, Halogen, Alkoxy, Halogenalkyl, gegebenenfalls durch Halogen substituiertes Alkoxy, Alkoxyalkyl oder Alkoxycarbonyl steht, n für eine Zahl von 0-3 steht, m für eine Zahl von 0-2 steht, A für Wasserstoff, gegebenenfalls durch Halogen subtuiertes Alkyl, Alkoxyalkyl, Polyalkoxyalkyl, Alkylthioalkyl, Alkenyl, Alkinyl, gegebenenfalls durch Heteroatome unterbrochenes Cycloalkyl oder gegebenenfalls durch Halogen-, Alkyl-, Halogenalkyl-, Alkoxy-, Nitro substituiertes Phenyl oder Arylalkyl steht,
B für Wasserstoff, gegebenenfalls durch Halogen substituiertes Alkyl, Cycloalkyl, Alkoxyalkyl, Alkylthioalkyl oder gegebenenfalls durch Alkyl, Alkoxy, Halogen, Nitro, Halogenalkyl, substituiertes Phenyl oder Aralkyl steht,
C für Wasserstoff, oder gegebenenfalls durch
Halogen substituiertes Alkyl steht, oder worin
A und B gemeinsam mit den Atomen, an die sie gebunden sind, einen gegebenenfalls durch Halogen oder gegebenenfalls halogeniertes Alkyl oder Alkoxy substituierten gesättigten oder ungesättigten Cyclus bilden, der durch Sauerstoff und/oder Schwefel unterbrochen sein kann, oder worin
B und C gemeinsam mit dem Kohlenstoffatom, an das sie gebunden sind, einen gesättigten oder ungesättigten Cyclus bilden, der durch Halogen oder gegebenenfalls durch halogeniertes Alkyl oder Alkoxy substituiert sein kann und durch
Sauerstoff und/oder Schwefel unterbrochen sein kann.
E für Wasserstoff (= E1 ), oder für gegebenenenfalls durch Halogen substituiertes Alkyl, Alkenyl, Alkinyl, Alkoxyalkyl, Aralkyl ( - E2),
für eine Gruppe CO-R2 ( = Ε3) oder für ein
Metallion oder Metallequivalent ( = E4) steht, R1 für gegebenenfalls durch Halogen substituiertes Alkyl oder für einen gegebenenfalls substituierten Phenylrest steht und
R2 für gegebenenfalls durch Halogen substituiertes Alkyl, Alkenyl, Alkoxy, Alkoxyalkyl,
Alkylthio oder gegebenenfalls substituiertes
Phenyl oder Aralkyl steht.
2. Substituierte 3-Benzoyl-pyrrolidin-2,4-dion-Derivate der Formel (I) gemäß Anspruch 1, dadurch gekennzeichnet, daß
X für Wasserstoff, C1-C6-Alkyl, Halogen, C1-C6-Alkoxy, C1-C6-Halogenalkyl, C1-C6-Halogenalkoxy, Nitro, C1- C6-Alkoxycarbonyl, C1-C6-Carboxy, Cyano oder
S(O)m-R1 steht, für Wasserstoff, C1-C6-Alkyl, Halogen, C1-C6- Alkoxy, C1-C4-Halogenalkyl, C1-C6-Halogenalkoxy, Nitro, C1-C6-Alkoxycarbonyl, C1-C6-Carboxy, Cyano oder S(O)m-R1 steht,
Z für C1-C6-Alkyl, Halogen, C1-C6-Alkoxy, C1-C6- Halogenalkyl, C1-C6-Halogenalkoxy, C1-C6-Alkoxy- C2-C6-alkyl, C1-C6-Halogenalkσxy-C2-C6-alkyl, C1- C6-Alkoxy-C2-C6-halogenalkyl, C1-C6-Alkoxycarbonyl oder C1-C6-Halogenalkoxycarbonyl steht, n für eine Zahl von 0-3 steht, m für eine Zahl von 0-2 steht, A für Wasserstoff oder gegebenenfalls durch Halogen substituiertes geradkettiges oder verzweigtes C1- C12-Alkyl, C3-C8-Alkenyl, C3-C8-Alkinyl, C1 -C1 0- Alkoxy-C2-C8-alkyl, C1-C8-Polyalkoxy-C2-C8-alkyl, C1-C10-Alkylthio-C2-C8-alkyl, Cycloalkyl mit 3-8 Ringatomen, das durch Sauerstoff und/oder Schwefel unterbrochen sein kann oder gegebenenfalls durch
Halogen, C1-C6-Alkyl-, C1-C6-Haloalkyl-, C1-C6- Alkoxy-, Nitro substituiertes Phenyl oder Aryl-C1- C6-alkyl steht,
B für Wasserstoff, geradkettiges oder verzweigtes und gegebenenfalls durch Halogen substituiertes C1-C12- Alkyl, C1-C8-Alkoxy-C1-C8-alkyl , C1-C8-Alkylthio- C1-C8-alkyl, Cycloalkyl mit 3-8 Ringatomen, das durch Sauerstoff und/oder Schwefel unterbrochen sein kann oder gegebenenfalls durch Halogen, C1-C6-Alkyl, C1-C6-Halogenalkyl, C1-C6-Alkoxy, Nitro substituiertes Phenyl oder Aryl-C1-C6-alkyl steht, für Wasserstoff oder gegebenenfalls durch Halogen substituiertes C1-C12-Alky! steht, oder worin
A und B gemeinsam mit den Atomen, an die sie gebunden sind, einen 5 bis 8-gliedrigen gesättigten oder ungesättigten Cyclus bilden, der durch Sauerstoff und/oder Schwefel unterbrochen und durch gegebenenfalls halogeniertes C1-C6-Alky!, C1-C6- Alkoxy oder Halogen substituiert sein kann, oder worin
B und C gemeinsam mit dem Kohlenstoffatom, an das sie gebunden sind einen 3 bis 8-gliedrigen gesättigten oder ungesättigten Cyclus bilden, der durch Sauerstoff und/oder Schwefel unterbrochen und durch Halogen oder gegebenenfalls halogeniertes C1-C6- Alkyl, C1-C6-Alkoxy substituiert sein kann,
E für E1 = Wasserstoff,
für E2 = C1-C12-Alkyl, C2-C6-Halogenalkyl, C3-C8- Alkenyl, C3-C8-Alkinyl, C3-C8-Halogenalkenyl, C3- C8-Halogenalkinyl, C1-C6-Alkoxy-C2-C6-alkyl, C1-C6- Halogenalkoxy-C2-C6-alkyl, C1-C6-Alkoxy-, Aryl-C1- C6-alkyl, für E3 = eine Gruppe CO-R2 oder
für E4 = ein Metallion oder ein Metal lequivalent steht, R1 für gegebenenfalls durch Halogen substituiertes
C1-C8-Alkyl, oder für gegebenenfalls durch Halogen, Nitro, Cyano, C1-C4-Alkoxy, C1-C4-Halogenalkoxy, C1- C4-Alkylthio, C1-C4-Halogenalkylthio, C1-C4-Alkyl, C1-C4-Halogenalkyl substituiertes Phenyl steht und R2 für gegebenenfalls durch Halogen substituiertes
C1-C8-Alkyl, C1-C8-Alkoxy, C1-C8-Alkylthio, C2-C8- Alkenyl, C1-C8-Alkoxy-C2-C8-alkyl oder für gegebenenfalls durch Halogen, C1-C8-Halogenalkyl, C1-C8- Alkyl oder C1-C8-Alkoxy substituiertes Phenyl, für gegebenenfalls durch Halogen, C1-C8-Alkyl, C1-C8- Halogenalkyl oder C1-C8-Alkoxy substituiertes Aryl- C1-C6-alkyl steht.
3. Substituierte 3-Benzoyl-pyrrolidin-2,4-dion-Derivate der Formel (I) gemäß Anspruch 1, dadurch gekennzeichnert, daß
X für Wasserstoff, C1-C4~Alkyl, Halogen, C1-C4-Alkoxy, C1-C4-Halogenalkyl, C1-C4-Halogenalkoxy, Nitro, C1-C4-Alkoxycarbonyl, Carboxy, Cyano oder S(O)m-R1 steht,
Y für Wasserstoff, C1-C6-Alkyl, Halogen, C1-C4- Alkoxy, C1-C3-Halogenalkyl, C1-C4-Halogenalkoxy, Nitro, C1-C4-Alkoxycarbonyl, Carboxy, Cyano oder S(O)m-R1 steht, für C1-C4-Alkyl, Halogen, C1-C4-Alkoxy, C1-C4- Halogenalkyl, C1-C4-Halogenalkoxy, C1-C4-Alkoxy-C2- C4-alkyl, C1-C4-Halogenalkoxy-C2-C4-alkyl, C1-C4-Alkoxy-C2-C4-halogenalkyl, C1-C4-Alkoxycarbonyl oder C1-C4-Halogenalkoxycarbonyl steht, n für eine Zahl von 0-3 steht, m für eine Zahl von 0-2 steht,
A für Wasserstoff oder gegebenenfalls durch Halogen substituiertes geradkettiges oder verzweigtes C1- C10-Alkyl, C3-C6-Alkenyl, C3-C6-Alkinyl, C1-C8- Alkoxy-C2-C6-alkyl, C1-C6-Polyalkoxy-C2-C6-alkyl, C1-C8-Alkylthio-C2-C6-alkyl, Cycloalkyl mit 3-7 Ringatomen, das durch 1-2 Sauerstoff- und/oder Schwefelatome unterbrochen sein kann oder gegebenenfalls durch Halogen, C1-C4-Alkyl-, C1-C4-Haloalkyl-, C1-C4-Alkoxy oder Nitro substituiertes Phenyl oder Aryl-C1-C4-alkyl steht,
B für Wasserstoff, geradkettiges oder verzweigtes und gegebenenfalls durch Halogen substituiertes C1-C10- Alkyl, C1-C6-Alkoxy-C1-C6-alkyl, C1-C6-Alkylthio- C1-C6-alkyl, Cycloalkyl mit 3-7 Ringatσmen das durch 1-2 Sauerstoff und/oder Schwefelatome unterbrochen sein kann, oder gegebenenfalls durch Halo gen, C1-C4-Alkyl, C1-C4-Halogenalkyl, C1-C4-Alkoxy oder Nitro substituiertes Phenyl oder Aryl-C1-C4- alkyl steht, für Wasserstoff oder gegebenenfalls durch Halogen substituiertes C1-C8-Alky! steht, oder worin
A und B gemeinsam mit den Atomen, an die sie gebunden sind, einen 5 bis 7-gliedrigen gesättigten oder ungesättigten Cyclus bilden, der durch C1-C4-Alkyl, C1-C4-Alkoxy, Fluor oder Chlor substituiert und der durch Sauerstoff und/oder Schwefel unterbrochen sein kann, oder worin
B und C gemeinsam mit dem Kohlenstoffatom, an das sie gebunden sind, einen 3 bis 7-gliedrigen gesättigten oder ungesättigten Cyclus bilden, der durch Sauerstoff und/oder Schwefel unterbrochen und durch Fluor, Chlor, C1-C4-Alkyl, C1-C4-Alkoxy, C1-C4- Halogenalkyl, C1-C4-Halogenalkoxy substituiert sein kann,
E für E1 = Wasserstoff
für E2 = C1-C8-Alkyl, C2-C4-Halogenalkyl, C3-C6- Alkenyl, C3-C6-Alkinyl, C3-C6-Halogenalkenyl, C3-C6-Halogenalkinyl, C1-C4-Alkoxy-C2-C4-alkyl, C1-C4-Halogenalkoxy-C2- C4-alkyl, Aryl-C1-C4-alkyl, für E3 = eine Gruppe CO-R2 oder
für E4 = ein Metallion oder ein Metal lequivalent
steht,
R1 für gegebenenfalls durch Halogen substituiertes C 1- C6-Alkyl oder für gegebenenfalls durch Fluor, Chlor, Brom, Nitro, Cyano, C1-C3-Alkoxy, C1-C3-Halogenalkoxy, C1-C3-Alkylthio, C1-C3-Halogenalkylthio, C1 - C3-Alkyl, C1-C3-Halogenalkyl substituiertes Phenyl, steht und
R2 für gegebenenfalls durch Halogen substituiertes C1- C6-Alkyl, C1-C6-Alkoxy, C1-C6-Alkylthio, C2~C6-A1- kenyl, C1-C6-Alkoxy-C2-C1-alkyl oder für gegebenenfalls durch Halogen, C1-C5-Halogenalkyl, C1-C5-Alkyl oder C1-C5-Alkoxy substituiertes Phenyl, für gegebenenfalls durch Halogen, C1-C5-Alkyl, C1-C5-Halogenalkyl oder C1-C5-Alkoxy substituiertes Aryl-C1- C4-alkyl steht. 4. Substituierte 3-Benzoyl-pyrrolidin-2,
4-dion- Derivate der allgemeinen Formel (I) gemäß Anspruch 1, dadurch gekennzeichnet, daß
X für Wasserstoff, Methyl, Ethyl, Propyl, i-Propyl,
Fluor, Chlor, Brom, Methoxy, Ethoxy, Trifluormethyl, Difluormethyl, Trifluormethoxy, Nitro, Methoxycarbonyl Ethoxycarbonyl, Cyano oder S(O)mRl steht, Y für Wasserstoff, Methyl, Ethyl, Propyl, i-Propyl, Butyl, i-Butyl, tert.-Butyl, Fluor, Chlor, Brom, Methoxy, Ethoxy, Trifluormethyl, Trifluormethoxy, Difluormethyl, Nitro, Methoxycarbonyl, Ethoxycarbonyl, Cyano oder S(O)mR1 steht,
Z für Methyl, Ethyl, i-Propyl, Butyl, i-Butyl, tert.
Butyl, Fluor, Chlor, Brom, Methoxy, Ethoxy, Tri- fluormethyl, Difluormethyl, Trifluormethoxy,
Methoxyethyl, Ethoxyethyl, Propoxyethyl, iso-Propoxyethyl, Methoxycarbonyl, Ethoxycarbonyl, Trifluormethoxycarbonyl, Trichlormethoxycarbonyl, Difluormethoxycarbonyl steht, n für eine Zahl von 0-3 steht, m für eine Zahl von 0-2 steht, A für Wasserstoff, gegebenenfalls durch Halogen substituiertes geradkettiges oder verzweigtes C1-C8- Alkyl, C3-C4-Alkenyl, C3-C4-Alkinyl, C1-C6-Alkoxy- C2-C4-alkyl, C1-C4-Polyalkoxy-C2-C4-alkyl, C1-C6- Alkylthio-C2-C4-alkyl, Cycloalkyl mit 3-6 Ringatomen, das durch 1-2 Sauerstoff- und/oder Schwefelatome unterbrochen sein kann oder gegebenenfalls durch Fluor-, Chlor-, Brom-, Methyl-, Ethyl-,
Propyl-, iso-Propyl-, Methoxy-, Ethoxy-, Trifluor- methyl-, Nitro substituiertes Phenyl oder Aryl-C1- C3-alkyl steht,
B für Wasserstoff, geradkettiges oder verzweigtes und gegebenenfalls durch Halogen substituiertes C1-C8- Alkyl, C1-C4-AlkoxyC1-C4-alkyl, C1-C4-Alkylthio-C1- C3-alkyl, Cycloalkyl mit 3-6 Ringatomen, das durch 1-2 Sauerstoff und/oder Schwefelatome unterbrochen sein kann oder gegebenenfalls durch Halogen, C1-C4- Alkyl, C1-C4-Halogenalkyl, C1-C4-Alkoxy oder Nitro substituiertes Phenyl oder Aryl-C1-C3-alkyl steht,
C für Wasserstoff, Cj-C1-Alkyl oder C1-C6-Halogenalkyl steht, oder worin
A und B gemeinsam mit den Atomen, an die sie gebunden sind, einen 5 bis 6-gliedrigen gesättigten oder ungesättigten Cyclus bilden, der durch C1-C3-Alkyl, C1-C3-Alkoxy, Fluor oder Chlor substituiert und der durch Sauerstoff und/oder Schwefel unterbrochen sein kann, oder worin
B und C gemeinsam mit dem Kohlenstoff, an das sie gebunden sind, einen 3 bis 6-gliedrigen gesättigten oder ungesättigten Cyclus bilden, der durch Sauer stoff und/oder Schwefel unterbrochen und durch
Fluor, Chlor, C1-C4-Alkyl, C1-C4-Alkoxy, Trifluormethyl, Trifluormethoxy substituiert sein kann,
E für E1 = Wasserstoff steht,
für E2 = C1-C6-Alkyl, C2-C3-Halogenalkyl, C3-C4- Alkenyl, C3-C4-Alkinyl, C3-C4-Halogenalkenyl, C3-C4-Halogenalkinyl, C1-C3-Alkoxy-C2-C3-alkyl, C1-C3-Halogenalkoxy-C2- C3-alkyl, Aryl-C1-C3-alkyl steht,
für E3 = eine Gruppe CO-R2 oder
für E4 = Li⊕, Na⊕, K , NH4 ⊕ steht,
R1 für gegebenenfalls durch Fluor substituiertes C1- C4-Alkyl oder für gegebenenfalls durch Fluor,
Chlor, Brom, Nitro, Cyano, C1-C2-Alkoxy, C1-C2- Fluoralkoxy, C1-C2-Chloralkoxy, C1-C2-Alkylthio, C1-C2-Fluoralkylthio, C1-C2-Chloralkylthio, C1-C3- Alkyl, C1-C2-Fluoralkyl, C1-C2-Difluoralkyl, C1-C3- Trifluoralkyl, C1-C2-Chloralkyl, C1-C2-Dichloralkyl, C1-C2-Trichloralkyl substituiertes Phenyl steht und
R2 für gegebenenfalls durch Fluor, Chlor, Brom
substituiertes C1-C4-Alkyl, C1-C4-Alkoxy, C1-C4- Alkylthio, C1-C4-Alkoxy-(C2-C4)alkyl oder für gegebenenfalls durch Fluor, Chlor, Brom, Trifluormethyl, C1-C4-Alkyl oder C1-C4-Alkoxy substituiertes Phenyl, für gegebenenfalls durch Fluor, Chlor, Brom, C1-C4-Alkyl, Trifluormethyl oder C1-C4-Alkoxy substituiertes Aryl-C1-C2-alkyl steht.
5. Verfahren zur Herstellung substituierter 3-Benzoylpyrrolidin-2,4-dion-Derivate der allgemeinen Formel (I)
,
in welcher X für Wasserstoff, Alkyl, Halogen, Alkoxy, Halogenalkyl, Halogenalkoxy, Nitro, Alkoxycarbonyl, Carboxy, Cyano oder -S(O)m-R1 steht, Y für Wasserstoff, Alkyl, Halogen, Alkoxy, Halogenalkyl, Halogenalkoxy, Nitro, Alkoxycarbonyl, Carboxy, Cyano oder -S(O)m-R1 steht, Z für Alkyl, Halogen, Alkoxy, Halogenalkyl, gegebenenfalls durch Halogen substituiertes Alkoxy, Alkoxyalkyl oder Alkoxycarbonyl steht, n für eine Zahl von 0-3 steht, m für eine Zahl von 0-2 steht, A für Wasserstoff, gegebenenfalls durch Halogen substituiertes Alkyl, Alkoxyalkyl, Polyalkoxyalkyl, Alkylthioalkyl, Alkenyl, Alkinyl, gegebenenfalls durch Heteroatome unterbrochenes Cycloalkyl oder gegebenenfalls durch Halogen-, Alkyl-, Halogenalkyl-, Alkoxy-, Nitro substituiertes Phenyl oder Arylalkyl steht,
B für Wasserstoff, gegebenenfalls durch Halogen substituiertes Alkyl, Cycloalkyl, Alkoxyalkyl, Alkylthioalkyl oder gegebenenfalls durch Alkyl,
Alkoxy, Halogen, Nitro, Halogenalkyl, substituiertes Phenyl oder Aralkyl steht, C für Wasserstoff, oder gegebenenfalls durch
Halogen substituiertes Alkyl steht, oder worin
A und B gemeinsam mit den Atomen, an die sie gebunden sind, einen gegebenenfalls durch Halogen oder gegebenenfalls halogeniertes Alkyl oder Alkoxy substituierten gesättigten oder ungesättigten Cyclus bilden, der durch Sauerstoff und/oder Schwefel unterbrochen sein kann, oder worin
B und C gemeinsam mit dem Kohlenstoffatom, an das sie gebunden sind, einen gesättigten oder ungesättigten Cyclus bilden, der durch Halogen, gegebenenfalls durch halogeniertes Alkyl oder Alkoxy substituiert sein kann und durch Sauerstoff oder Schwefel unterbrochen sein kann,
E für Wasserstoff (= E1 ), oder für gegebenenen- falls durch Halogen substituiertes Alkyl, Alkenyl, Alkinyl, Alkoxyalkyl, Aralkyl ( = E2), für eine Gruppe CO-R2 ( = E3) oder für ein Metallion oder Metallequivalent ( = E4) steht, R1 für gegebenenfalls durch Halogen substituiertes Alkyl oder für einen gegebenenfalls substituierten Phenylrest steht und
R2 für gegebenenfalls durch Halogen substituiertes Alkyl, Alkenyl, Alkoxy, Alkoxyalkyl, Alkylthio oder gegebenenfalls substituiertes Phenyl oder Aralkyl steht, dadurch gekennzeichnet, daß man 3-Benzoyl-pyrrolidin-2,4-dion-Derivate der Formel (I) bzw. deren Enole der Formel (Ia)
A) Benzoylessigester der Formel (II)
X, Y, Z und n die oben angegebenen Bedeutungen haben und
R3 für Alkyl steht mit Aminosäureestern der allgemeinen Formel (III)
A, B und C die oben angegebenen Bedeutungen haben und
R4 für Alkyl steht, gegebenenfalls in Gegenwart eines Lösungsmittels und in Gegenwart einer Base kondensiert, oder daß man Verbindungen der Formel (Ia)
A, B, C, X, Y, Z, und n die oben angegebenen
Bedeutungen haben, erhält, wenn man 4-Benzoyloxy-pyrrolin-2-one der Formel (IV)
A, B, C, X, Y, Z und n die oben angegebenen Bedeutungen haben, gegebenenfalls in Gegenwart eines Verdünnungsmittels, gegebenenfalls in Gegenwart einer Base und gegebenenfalls in Gegenwart eines geeigneten Katalysators umlagert, oder daß man
Verbindungen der Formel (Ib)
A, B, C, E2, X, Y, Z und n die oben angegebenen
Bedeutungen haben, erhält, wenn man Verbindungen der Formel (Ia)
A, B, C, X, Y, Z und n die oben angegebenen
Bedeutungen haben, mit Alkylierungsmitteln der allgemeinen Formel (V) E2-L (V) in welcher E2 die oben angegebene Bedeutung hat und
L für Halogen, -OSO2-Alkyl, -OSO2O-Alkyl oder -OSO2-Aryl steht,
gegebenenfalls in Gegenwart eines Verdünnungsmittels und gegebenenfalls in Gegenwart einer Base umsetzt, oder daß man Verbindungen der Formel (Ic)
A, B, C, E3 , X, Y, Z und n die oben angegebenen
Bedeutungen haben, erhält, wenn man Verbindungen der Formel (Ia)
in welcher
A, B, C, X, Y, Z und n die oben angegebenen Bedeutungen haben, mit Acylierungsreagenzien der Formel (VI)
E3-M (VI) in welcher
E3 die oben angegebene Bedeutung hat und M für Halogen, -OE3 , CN, O-SO2-Alkyl, O- SO2-Aryl und Imidazolyl steht, gegebenenfalls in Gegenwart eines Verdünnungsmittels und gegebenenfalls in Gegenwart einer Base umsetzt, oder daß man erbindungen der allgemeinen Formel (Id)
X, Y, Z, A, B, C, E4 und n die oben angegebenen Bedeutungen haben, erhält, wenn man Verbindungen der Formel (Ia)
X, Y, Z, A, B, C und n die oben angegebenen
Bedeutungen haben, mit Metallhydroxiden oder Aminen der allgemeinen Formel (VII) und (VIII)
MesOHt (VII)
Me für ein- oder zweiwertige Metallionen, s und t für die Zahlen 1 und 2 stehen
R4, R5 und R6 unabhängig voneinander für
Wasserstoff und Alkyl stehen, gegebenenfalls in Gegenwart eines Verdunnungsmittels, umsetzt.
6. Verfahren zur Bekämpfung von unerwünschten Pflanzzen, dadurch gekennzeichet, daß man 3-Benzoylpyrrolidin-2,4-dion-Derivate der Formel (I) gemäß den Ansprüchen 1 bis 5 auf unerwünschte Pflanzen und/oder ihren Lebensraum einwirken läßt.
7. Verwendung von 3-Benzoyl-pyrrolidin-2,4-dion-Deri- vate der Formel (I) gemäß den Ansprüchen 1 bis 5 zur Bekämpfung von unerwünschten Pflanzen»
8. Verfahren zur Herstellung von herbiziden, insektiziden Mitteln, dadurch gekennzeichnet, daß man 3-Benzoyl-pyrrolidin-2,4-dion-Derivate der Formel (i) gemäß den Ansprüchen 1 bis 5 mit Streckmitteln und/oder oberflächenaktiven Substanzen vermischt.
9. 4-Benzoyloxy-pyrrol in-2-one der allgemeinen Formel (IV)
Halogenalkyl, Halogenalkoxy, Nitro, Alkoxycarbonyl, Carboxy, Cyano oder -S(O)m-R1 steht, Y für Wasserstoff, Alkyl, Halogen, Alkoxy,
Halogenalkyl, Halogenalkoxy, Nitro, Alkoxycarbonyl, Carboxy, Cyano oder -S(O)m-R1 steht, Z für Alkyl, Halogen, Alkoxy, Halogenalkyl, gegebenenfalls durch Halogen substituiertes Alkoxy, Alkoxyalkyl oder Alkoxycarbonyl steht, n für eine Zahl von 0-3 steht, m für eine Zahl von 0-2 steht,
A für Wasserstoff, gegebenenfalls durch Halogen substituiertes Alkyl, Alkoxyalkyl, Polyalkoxyalkyl, Alkylthioalkyl, Alkenyl, Alkinyl, gegebenenfalls durch Heteroatome unterbrochenes Cycloalkyl oder gegebenenfalls durch Halogen-, Alkyl-, Halogenalkyl-, Alkoxy-, Nitro substituiertes Phenyl oder Arylalkyl steht, B für Wasserstoff, gegebenenfalls durch Halogen substituiertes Alkyl, Cycloalkyl, Alkoxyalkyl, Alkylthioalkyl oder gegebenenfalls durch
Alkyl, Alkoxy, Halogen, Nitro, Halogenalkyl, substituiertes Phenyl oder Aralkyl steht,
C für Wasserstoff, oder gegebenenfalls durch
Halogen substituiertes Alkyl steht, oder worin
A und B gemeinsam mit den Atomen, an die sie gebunden sind, einen gesättigten oder ungesättigten Cyclus bilden, der gegebenenfalls durch Halogen oder gegebenenfalls durch halogeniertes Alkyl oder Alkoxy substituiert sein kann und durch Sauerstoff und/oder Schwefel unterbrochen sein kann, oder worin B und C gemeinsam mit dem Kohlenstoffatom, an das sie gebunden sind, einen gesättigten oder ungesättigten Cyclus bilden, der durch Halogen oder gegebenenfalls durch halogeniertes Alkyl oder Alkoxy substituiert sein kann und durch Sauerstoff und/oder
Schwefel unterbrochen sein kann und R1 für gegebenenfalls durch Halogen substituiertes Alkyl oder für einen gegebenenfalls substituierten Phenylrest steht.
10. Verfahren zur Bekämpfung von Insekten, dadurch gekennzeichnet, daß man 3-Benzoyl-pyrrolidin-2,4- dion-Derivate der allgemeinen Formel (I) gemäß den Ansprüchen 1 bis 5 auf Insekten und/oder ihren Lebensraum einwirken läßt.
11. Verwendung von 3-Benzoyl-pyrrolidin-2,4-dion-Derivaten der allgemeinen Formel (I) gemäß den Ansprüchen 1 bis 5 zur Bekämpfung von Insekten.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| AU45623/93A AU4562393A (en) | 1992-07-13 | 1993-06-30 | Herbicidal and insecticidal 3-benzoyl-pyrrolidin-2,4-dione derivates |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DEP4223015.2 | 1992-07-13 | ||
| DE19924223015 DE4223015A1 (de) | 1992-07-13 | 1992-07-13 | Substituierte 3-Benzoyl-pyrrolidin-2,4-dion-Derivate |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO1994001401A1 true WO1994001401A1 (de) | 1994-01-20 |
Family
ID=6463097
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/EP1993/001690 WO1994001401A1 (de) | 1992-07-13 | 1993-06-30 | Herbizide und insektizide 3-benzoyl-pyrrolidin-2,4-dion-derivate |
Country Status (3)
| Country | Link |
|---|---|
| AU (1) | AU4562393A (de) |
| DE (1) | DE4223015A1 (de) |
| WO (1) | WO1994001401A1 (de) |
Cited By (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0668267A1 (de) * | 1994-02-09 | 1995-08-23 | Bayer Ag | Substituierte 1H-3-Aryl-pyrrolidin-2,4-dion-Derivate |
| WO2007033544A1 (fr) | 2005-09-26 | 2007-03-29 | Sheng Qiang | Technique de modification de la molécule d'un bio-produit et application pour la lutte contre les mauvaises herbes |
| CN102050776A (zh) * | 2010-12-07 | 2011-05-11 | 南京农业大学 | 5-取代甲基吡咯烷-2,4-二酮类化合物及其用途 |
| WO2012101047A1 (de) | 2011-01-25 | 2012-08-02 | Bayer Cropscience Ag | Verfahren zur herstellung von 1-h-pyrrolidin-2,4-dion-derivaten |
| CN107922333A (zh) * | 2015-06-22 | 2018-04-17 | 拜耳作物科学股份公司 | 新的炔基取代的3‑苯基吡咯烷‑2,4‑二酮及其作为除草剂的用途 |
| CN113402436A (zh) * | 2021-06-09 | 2021-09-17 | 安徽农业大学 | 特胺酸衍生物及其制备方法与应用 |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE10215723A1 (de) * | 2002-04-10 | 2003-10-30 | Bayer Cropscience Gmbh | 3-Keto oder 3-Oximether substituierte Benzoylcyclohexandione |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1988004652A1 (en) * | 1986-12-17 | 1988-06-30 | Nippon Soda Co., Ltd. | Heterocyclic compounds having triketo skeleton |
| EP0377893A2 (de) * | 1989-01-07 | 1990-07-18 | Bayer Ag | 3-Aryl-pyrrolidin-2,4-dion-Derivate |
-
1992
- 1992-07-13 DE DE19924223015 patent/DE4223015A1/de not_active Withdrawn
-
1993
- 1993-06-30 AU AU45623/93A patent/AU4562393A/en not_active Abandoned
- 1993-06-30 WO PCT/EP1993/001690 patent/WO1994001401A1/de active Application Filing
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1988004652A1 (en) * | 1986-12-17 | 1988-06-30 | Nippon Soda Co., Ltd. | Heterocyclic compounds having triketo skeleton |
| EP0377893A2 (de) * | 1989-01-07 | 1990-07-18 | Bayer Ag | 3-Aryl-pyrrolidin-2,4-dion-Derivate |
Non-Patent Citations (3)
| Title |
|---|
| IL FARMACO Bd. 47, Nr. 10, 1092, PAVIA IT Seiten 1323 - 1333 M.E. TRANQUILLINI 'Synthesis of 3-Aroyltetramic acids' * |
| JOURNAL OF INORGANIC BIOCHEMISTRY Bd. 39, Nr. 4, 1990, NEW YORK US Seiten 307 - 316 O. MARKOPOULOU ET AL. 'Synthesis of 3-Butanoyl- and 3-Benzoyl-4-hydroxy-3-pyrrolin-2-ones and their Complexes with Metal Ions' * |
| TETRAHEDRON LETTERS Bd. 24, Nr. 43, 1983, OXFORD GB Seiten 4751 - 4754 R.C.F. JONES ET AL. 'Direct Metallation of Tetramic acids: A New Synthesis of 3-Acyl Tetramic Acids' * |
Cited By (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5622917A (en) * | 1994-02-09 | 1997-04-22 | Bayer Aktiengesellschaft | Substituted 1H--3-aryl-pyrrolidine-2,4-dione derivatives |
| US5847211A (en) * | 1994-02-09 | 1998-12-08 | Bayer Aktiengesellschaft | Substituted 1H-3-Aryl-pyrrolidine-2,4-dione derivatives |
| EP0668267A1 (de) * | 1994-02-09 | 1995-08-23 | Bayer Ag | Substituierte 1H-3-Aryl-pyrrolidin-2,4-dion-Derivate |
| CN103922990A (zh) * | 2005-09-26 | 2014-07-16 | 南京农业大学 | 一种生物源化合物的分子修饰和用于除草的方法 |
| WO2007033544A1 (fr) | 2005-09-26 | 2007-03-29 | Sheng Qiang | Technique de modification de la molécule d'un bio-produit et application pour la lutte contre les mauvaises herbes |
| JP2009509944A (ja) * | 2005-09-26 | 2009-03-12 | 南京▲農業▼大学 | 生物源化合物の分子修飾及び除草への応用方法 |
| CN102050776A (zh) * | 2010-12-07 | 2011-05-11 | 南京农业大学 | 5-取代甲基吡咯烷-2,4-二酮类化合物及其用途 |
| WO2012101047A1 (de) | 2011-01-25 | 2012-08-02 | Bayer Cropscience Ag | Verfahren zur herstellung von 1-h-pyrrolidin-2,4-dion-derivaten |
| EP3372580A1 (de) | 2011-01-25 | 2018-09-12 | Bayer CropScience Aktiengesellschaft | Verfahren zur herstellung von 1-h-pyrrolidin-2,4-dion-derivaten |
| CN107922333A (zh) * | 2015-06-22 | 2018-04-17 | 拜耳作物科学股份公司 | 新的炔基取代的3‑苯基吡咯烷‑2,4‑二酮及其作为除草剂的用途 |
| CN107922333B (zh) * | 2015-06-22 | 2021-03-30 | 拜耳作物科学股份公司 | 新的炔基取代的3-苯基吡咯烷-2,4-二酮及其作为除草剂的用途 |
| CN113402436A (zh) * | 2021-06-09 | 2021-09-17 | 安徽农业大学 | 特胺酸衍生物及其制备方法与应用 |
| CN113402436B (zh) * | 2021-06-09 | 2024-07-12 | 安徽农业大学 | 特胺酸衍生物及其制备方法与应用 |
Also Published As
| Publication number | Publication date |
|---|---|
| DE4223015A1 (de) | 1994-01-20 |
| AU4562393A (en) | 1994-01-31 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP0528156B1 (de) | 3-Aryl-4-hydroxy-delta3-dihydrofuranon- und 3-Aryl-4-hydroxy-delta3-dihydrothiophenon-Derivate | |
| EP0613885B1 (de) | Substituierte 1-H-3-Phenyl-5-cycloalkylpyrrolidin-2,4-dione, ihre Herstellung und ihre Verwendung als Schädlingsbekämpfungsmittel und Herbizide | |
| EP0521334B1 (de) | Substituierte 1-H-3-Aryl-pyrrolidin-2,4-dion-Derivate, deren Herstellung und deren Verwendung als Insektizide, Akarizide und Herbizide | |
| EP0613884B1 (de) | Dialkyl-1-H-3-(2,4-dimethylphenyl)-pyrrolidin-2,4-dione, ihre Herstellung und ihre Verwendung als Schädlingsbekämpfungsmittel und Herbizide | |
| EP0508126B1 (de) | 3-Hydroxy-4-aryl-5-oxo-pyrazolin Derivate | |
| EP0415211B1 (de) | 3-Aryl-pyrrolidin-2,4-dion-derivate | |
| EP0377893B1 (de) | 3-Aryl-pyrrolidin-2,4-dion-Derivate | |
| EP0442073A2 (de) | Polycyclische 3-Aryl-pyrrolidin-2,4,-dion-Derivate | |
| EP0596298A2 (de) | 5-Spiro-substituierte 1-H-3-Aryl-pyrrolidin-2,4-dion-Derivate als Herbizide, Insektizide und Akarizide | |
| EP0706527A1 (de) | Substituierte spiroheterocyclische 1h-3-aryl-pyrrolidin-2,4-dion-derivate, verfahren zu deren herstellung und deren verwendung als schädlingsbekämpfungsmittel | |
| EP0300218A1 (de) | Verwendung von substituierten 1,4-naphthochinonen zur Bekämpfung von Spinnentieren und Pilzen | |
| EP0076957B1 (de) | Substituierte Hydroxymalonsäurediamide, Verfahren zu ihrer Herstellung sowie ihre Verwendung als Schädlingsbekämpfungsmittel | |
| WO1994001401A1 (de) | Herbizide und insektizide 3-benzoyl-pyrrolidin-2,4-dion-derivate | |
| EP0421102A2 (de) | Substituierte Acrylsäureester | |
| EP0373425A2 (de) | Substituierte Pyridazinone, Verfahren zu ihrer Herstellung und ihre Verwendung als Schädlingsbekämpfungsmittel | |
| EP0591806A1 (de) | Substituierte 2-Arylpyrrole | |
| EP0276406A1 (de) | Substituierte 4-Amino-pyrimidine | |
| DE3110725A1 (de) | 3-alken-1-yl-2,2-dimethyl- cyclopropancarbonsaeure-(4-fluor-3-phenoxy-benzyl)-ester, verfahren zu ihrer herstellung und ihre verwendung in schaedlingsbekaempfungsmitteln | |
| EP0501129B1 (de) | Substituierte bicyclische 3-Aryl-pyrrolidin-2,4-dion-Derivate | |
| DE3605002A1 (de) | Phosphorsaeureester | |
| DE4326909A1 (de) | Substituierte 1-H-3-Aryl-pyrrolidin-2,4-dion-Derivate | |
| EP0361185B1 (de) | Substituierte 2-(Halogenmethylthio)-pyrimidin-Derivate | |
| DE4303658A1 (de) | Substituierte Tetrahydropyridazincarboxamide | |
| EP0192150A2 (de) | 1-Acyl-1-phenyl-harnstoffe | |
| EP0642303B1 (de) | Substituierte 2-arylpyrrole |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| AK | Designated states |
Kind code of ref document: A1 Designated state(s): AU BR BY CA CZ HU JP KR KZ NZ RU SK UA US |
|
| AL | Designated countries for regional patents |
Kind code of ref document: A1 Designated state(s): AT BE CH DE DK ES FR GB GR IE IT LU MC NL PT SE |
|
| DFPE | Request for preliminary examination filed prior to expiration of 19th month from priority date (pct application filed before 20040101) | ||
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application | ||
| 122 | Ep: pct application non-entry in european phase | ||
| NENP | Non-entry into the national phase |
Ref country code: CA |