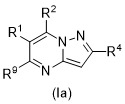
TW202233620A - Cftr調節劑化合物、組合物及其用途 - Google Patents
Cftr調節劑化合物、組合物及其用途 Download PDFInfo
- Publication number
- TW202233620A TW202233620A TW110139341A TW110139341A TW202233620A TW 202233620 A TW202233620 A TW 202233620A TW 110139341 A TW110139341 A TW 110139341A TW 110139341 A TW110139341 A TW 110139341A TW 202233620 A TW202233620 A TW 202233620A
- Authority
- TW
- Taiwan
- Prior art keywords
- optionally substituted
- compound
- alkyl
- pyrazolo
- heterocycle
- Prior art date
Links
- 150000001875 compounds Chemical class 0.000 title claims abstract description 488
- 239000000203 mixture Substances 0.000 title claims abstract description 139
- 238000000034 method Methods 0.000 claims abstract description 132
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims abstract description 32
- 208000027866 inflammatory disease Diseases 0.000 claims abstract description 28
- 230000002401 inhibitory effect Effects 0.000 claims abstract description 21
- 208000035475 disorder Diseases 0.000 claims abstract description 18
- -1 NH 2 Inorganic materials 0.000 claims description 405
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 claims description 180
- 125000001072 heteroaryl group Chemical group 0.000 claims description 172
- 125000003107 substituted aryl group Chemical group 0.000 claims description 168
- 125000000623 heterocyclic group Chemical group 0.000 claims description 147
- 229910052736 halogen Inorganic materials 0.000 claims description 123
- 150000002367 halogens Chemical class 0.000 claims description 115
- 125000005346 substituted cycloalkyl group Chemical group 0.000 claims description 113
- 108010079245 Cystic Fibrosis Transmembrane Conductance Regulator Proteins 0.000 claims description 112
- 102000012605 Cystic Fibrosis Transmembrane Conductance Regulator Human genes 0.000 claims description 111
- 125000002950 monocyclic group Chemical group 0.000 claims description 101
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 claims description 98
- 125000000008 (C1-C10) alkyl group Chemical group 0.000 claims description 95
- 125000003118 aryl group Chemical group 0.000 claims description 80
- 125000000217 alkyl group Chemical group 0.000 claims description 71
- 150000003839 salts Chemical class 0.000 claims description 71
- 125000000592 heterocycloalkyl group Chemical group 0.000 claims description 65
- MSYGAHOHLUJIKV-UHFFFAOYSA-N 3,5-dimethyl-1-(3-nitrophenyl)-1h-pyrazole-4-carboxylic acid ethyl ester Chemical compound CC1=C(C(=O)OCC)C(C)=NN1C1=CC=CC([N+]([O-])=O)=C1 MSYGAHOHLUJIKV-UHFFFAOYSA-N 0.000 claims description 62
- 102000011017 Type 4 Cyclic Nucleotide Phosphodiesterases Human genes 0.000 claims description 62
- 108010037584 Type 4 Cyclic Nucleotide Phosphodiesterases Proteins 0.000 claims description 62
- 125000003545 alkoxy group Chemical group 0.000 claims description 60
- 125000002618 bicyclic heterocycle group Chemical group 0.000 claims description 54
- 125000002619 bicyclic group Chemical group 0.000 claims description 53
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 claims description 52
- 229940002612 prodrug Drugs 0.000 claims description 52
- 239000000651 prodrug Substances 0.000 claims description 52
- 125000003710 aryl alkyl group Chemical group 0.000 claims description 51
- 125000001424 substituent group Chemical group 0.000 claims description 50
- 125000004432 carbon atom Chemical group C* 0.000 claims description 49
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 47
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 47
- 239000012453 solvate Substances 0.000 claims description 47
- 208000003556 Dry Eye Syndromes Diseases 0.000 claims description 45
- 125000000027 (C1-C10) alkoxy group Chemical group 0.000 claims description 44
- 206010013774 Dry eye Diseases 0.000 claims description 44
- 229910052760 oxygen Inorganic materials 0.000 claims description 44
- 239000008194 pharmaceutical composition Substances 0.000 claims description 42
- 229910004013 NO 2 Inorganic materials 0.000 claims description 40
- YNAVUWVOSKDBBP-UHFFFAOYSA-N Morpholine Chemical compound C1COCCN1 YNAVUWVOSKDBBP-UHFFFAOYSA-N 0.000 claims description 38
- 229910052717 sulfur Inorganic materials 0.000 claims description 38
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 claims description 35
- 125000004433 nitrogen atom Chemical group N* 0.000 claims description 31
- 125000004122 cyclic group Chemical group 0.000 claims description 28
- 229910052757 nitrogen Inorganic materials 0.000 claims description 28
- GLUUGHFHXGJENI-UHFFFAOYSA-N diethylenediamine Natural products C1CNCCN1 GLUUGHFHXGJENI-UHFFFAOYSA-N 0.000 claims description 26
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 claims description 26
- 125000006725 C1-C10 alkenyl group Chemical group 0.000 claims description 25
- RWRDLPDLKQPQOW-UHFFFAOYSA-N Pyrrolidine Chemical class C1CCNC1 RWRDLPDLKQPQOW-UHFFFAOYSA-N 0.000 claims description 24
- 125000000753 cycloalkyl group Chemical group 0.000 claims description 24
- 230000000694 effects Effects 0.000 claims description 24
- 229910052739 hydrogen Inorganic materials 0.000 claims description 21
- 125000004191 (C1-C6) alkoxy group Chemical group 0.000 claims description 20
- 150000001335 aliphatic alkanes Chemical class 0.000 claims description 17
- 125000003277 amino group Chemical group 0.000 claims description 14
- 201000010099 disease Diseases 0.000 claims description 14
- 239000000546 pharmaceutical excipient Substances 0.000 claims description 14
- 230000007812 deficiency Effects 0.000 claims description 12
- 150000004885 piperazines Chemical class 0.000 claims description 12
- 150000001412 amines Chemical class 0.000 claims description 11
- 208000006545 Chronic Obstructive Pulmonary Disease Diseases 0.000 claims description 10
- 206010010774 Constipation Diseases 0.000 claims description 10
- 125000005842 heteroatom Chemical group 0.000 claims description 10
- 208000024891 symptom Diseases 0.000 claims description 10
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 claims description 9
- 208000006673 asthma Diseases 0.000 claims description 9
- 238000001727 in vivo Methods 0.000 claims description 9
- VNWKTOKETHGBQD-UHFFFAOYSA-N methane Chemical compound C VNWKTOKETHGBQD-UHFFFAOYSA-N 0.000 claims description 9
- 208000011580 syndromic disease Diseases 0.000 claims description 9
- JCXJVPUVTGWSNB-UHFFFAOYSA-N Nitrogen dioxide Chemical compound O=[N]=O JCXJVPUVTGWSNB-UHFFFAOYSA-N 0.000 claims description 8
- HONIICLYMWZJFZ-UHFFFAOYSA-N azetidine Chemical class C1CNC1 HONIICLYMWZJFZ-UHFFFAOYSA-N 0.000 claims description 8
- 230000002757 inflammatory effect Effects 0.000 claims description 8
- 239000000779 smoke Substances 0.000 claims description 8
- 125000000876 trifluoromethoxy group Chemical group FC(F)(F)O* 0.000 claims description 8
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 claims description 8
- 208000023275 Autoimmune disease Diseases 0.000 claims description 7
- 208000015943 Coeliac disease Diseases 0.000 claims description 7
- 150000001413 amino acids Chemical class 0.000 claims description 7
- MDFFNEOEWAXZRQ-UHFFFAOYSA-N aminyl Chemical compound [NH2] MDFFNEOEWAXZRQ-UHFFFAOYSA-N 0.000 claims description 7
- 229910052731 fluorine Inorganic materials 0.000 claims description 7
- 208000009299 Benign Mucous Membrane Pemphigoid Diseases 0.000 claims description 6
- 206010010071 Coma Diseases 0.000 claims description 6
- 206010010741 Conjunctivitis Diseases 0.000 claims description 6
- 206010010804 Contact lens intolerance Diseases 0.000 claims description 6
- 208000028006 Corneal injury Diseases 0.000 claims description 6
- 201000004624 Dermatitis Diseases 0.000 claims description 6
- ROSDSFDQCJNGOL-UHFFFAOYSA-N Dimethylamine Chemical compound CNC ROSDSFDQCJNGOL-UHFFFAOYSA-N 0.000 claims description 6
- 208000029462 Immunodeficiency disease Diseases 0.000 claims description 6
- 208000022559 Inflammatory bowel disease Diseases 0.000 claims description 6
- 208000009319 Keratoconjunctivitis Sicca Diseases 0.000 claims description 6
- 208000002720 Malnutrition Diseases 0.000 claims description 6
- 208000023715 Ocular surface disease Diseases 0.000 claims description 6
- 206010042033 Stevens-Johnson syndrome Diseases 0.000 claims description 6
- 231100000168 Stevens-Johnson syndrome Toxicity 0.000 claims description 6
- 206010006451 bronchitis Diseases 0.000 claims description 6
- 208000030212 nutrition disease Diseases 0.000 claims description 6
- 208000015200 ocular cicatricial pemphigoid Diseases 0.000 claims description 6
- 230000035807 sensation Effects 0.000 claims description 6
- 201000009267 bronchiectasis Diseases 0.000 claims description 5
- 230000002829 reductive effect Effects 0.000 claims description 5
- 208000023504 respiratory system disease Diseases 0.000 claims description 5
- 210000001519 tissue Anatomy 0.000 claims description 5
- 206010008635 Cholestasis Diseases 0.000 claims description 4
- 206010009137 Chronic sinusitis Diseases 0.000 claims description 4
- 206010067125 Liver injury Diseases 0.000 claims description 4
- 201000004681 Psoriasis Diseases 0.000 claims description 4
- 201000002661 Spondylitis Diseases 0.000 claims description 4
- 239000000853 adhesive Substances 0.000 claims description 4
- 230000001070 adhesive effect Effects 0.000 claims description 4
- 125000005119 alkyl cycloalkyl group Chemical group 0.000 claims description 4
- 239000007864 aqueous solution Substances 0.000 claims description 4
- 125000002837 carbocyclic group Chemical group 0.000 claims description 4
- 229910052801 chlorine Inorganic materials 0.000 claims description 4
- 208000037976 chronic inflammation Diseases 0.000 claims description 4
- 208000037893 chronic inflammatory disorder Diseases 0.000 claims description 4
- 208000027157 chronic rhinosinusitis Diseases 0.000 claims description 4
- 208000035623 congenital anemia Diseases 0.000 claims description 4
- 239000003517 fume Substances 0.000 claims description 4
- 231100000234 hepatic damage Toxicity 0.000 claims description 4
- 238000000338 in vitro Methods 0.000 claims description 4
- 230000008818 liver damage Effects 0.000 claims description 4
- VSEAAEQOQBMPQF-UHFFFAOYSA-N morpholin-3-one Chemical compound O=C1COCCN1 VSEAAEQOQBMPQF-UHFFFAOYSA-N 0.000 claims description 4
- 230000001185 psoriatic effect Effects 0.000 claims description 4
- 206010039073 rheumatoid arthritis Diseases 0.000 claims description 4
- 125000003762 3,4-dimethoxyphenyl group Chemical group [H]C1=C([H])C(OC([H])([H])[H])=C(OC([H])([H])[H])C([H])=C1* 0.000 claims description 3
- 125000001255 4-fluorophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C([H])=C1F 0.000 claims description 3
- 206010053990 Dacryostenosis acquired Diseases 0.000 claims description 3
- 206010012438 Dermatitis atopic Diseases 0.000 claims description 3
- 206010029240 Neuritis Diseases 0.000 claims description 3
- 206010034960 Photophobia Diseases 0.000 claims description 3
- 208000021386 Sjogren Syndrome Diseases 0.000 claims description 3
- 230000001154 acute effect Effects 0.000 claims description 3
- 201000008937 atopic dermatitis Diseases 0.000 claims description 3
- 125000002527 bicyclic carbocyclic group Chemical group 0.000 claims description 3
- 230000006378 damage Effects 0.000 claims description 3
- 210000000744 eyelid Anatomy 0.000 claims description 3
- 210000004907 gland Anatomy 0.000 claims description 3
- 208000015181 infectious disease Diseases 0.000 claims description 3
- 210000004561 lacrimal apparatus Anatomy 0.000 claims description 3
- 208000000617 lacrimal duct obstruction Diseases 0.000 claims description 3
- 230000000144 pharmacologic effect Effects 0.000 claims description 3
- 238000011084 recovery Methods 0.000 claims description 3
- 208000001730 Familial dysautonomia Diseases 0.000 claims description 2
- 201000001638 Riley-Day syndrome Diseases 0.000 claims description 2
- 238000001035 drying Methods 0.000 claims description 2
- 208000002551 irritable bowel syndrome Diseases 0.000 claims description 2
- 239000002245 particle Substances 0.000 claims description 2
- 125000002911 monocyclic heterocycle group Chemical group 0.000 claims 2
- 206010052140 Eye pruritus Diseases 0.000 claims 1
- 239000000443 aerosol Substances 0.000 claims 1
- 208000028774 intestinal disease Diseases 0.000 claims 1
- 239000002243 precursor Substances 0.000 abstract description 3
- 208000030533 eye disease Diseases 0.000 abstract description 2
- 101100296720 Dictyostelium discoideum Pde4 gene Proteins 0.000 abstract 3
- 101100082610 Plasmodium falciparum (isolate 3D7) PDEdelta gene Proteins 0.000 abstract 3
- 238000005481 NMR spectroscopy Methods 0.000 description 368
- IAZDPXIOMUYVGZ-WFGJKAKNSA-N Dimethyl sulfoxide Chemical compound [2H]C([2H])([2H])S(=O)C([2H])([2H])[2H] IAZDPXIOMUYVGZ-WFGJKAKNSA-N 0.000 description 98
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 63
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 58
- 239000007787 solid Substances 0.000 description 58
- 239000011541 reaction mixture Substances 0.000 description 57
- 230000015572 biosynthetic process Effects 0.000 description 55
- 238000003786 synthesis reaction Methods 0.000 description 55
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 51
- 238000005160 1H NMR spectroscopy Methods 0.000 description 50
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 48
- 238000003820 Medium-pressure liquid chromatography Methods 0.000 description 35
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 33
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 30
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 29
- 235000017557 sodium bicarbonate Nutrition 0.000 description 29
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 29
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 28
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 27
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 26
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 26
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 26
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 25
- BCJQJAVVUTUJPF-UHFFFAOYSA-N pyrazolo[1,5-a]pyrimidine-2-carboxamide Chemical compound N1=CC=CN2N=C(C(=O)N)C=C21 BCJQJAVVUTUJPF-UHFFFAOYSA-N 0.000 description 25
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 21
- 239000000243 solution Substances 0.000 description 20
- 238000003756 stirring Methods 0.000 description 20
- 239000002253 acid Substances 0.000 description 18
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 17
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 16
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 16
- 230000005764 inhibitory process Effects 0.000 description 16
- XHJFJCDSODRMRL-UHFFFAOYSA-N 7-(3,4-dimethoxyphenyl)pyrazolo[1,5-a]pyrimidine-2-carboxylic acid Chemical compound C1=C(OC)C(OC)=CC=C1C1=CC=NC2=CC(C(O)=O)=NN12 XHJFJCDSODRMRL-UHFFFAOYSA-N 0.000 description 15
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 15
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 15
- 150000004677 hydrates Chemical class 0.000 description 15
- 239000000523 sample Substances 0.000 description 15
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 15
- OHCQJHSOBUTRHG-KGGHGJDLSA-N FORSKOLIN Chemical compound O=C([C@@]12O)C[C@](C)(C=C)O[C@]1(C)[C@@H](OC(=O)C)[C@@H](O)[C@@H]1[C@]2(C)[C@@H](O)CCC1(C)C OHCQJHSOBUTRHG-KGGHGJDLSA-N 0.000 description 14
- 125000004429 atom Chemical group 0.000 description 14
- 239000003814 drug Substances 0.000 description 14
- 125000004435 hydrogen atom Chemical class [H]* 0.000 description 14
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 14
- 235000019341 magnesium sulphate Nutrition 0.000 description 14
- 239000012044 organic layer Substances 0.000 description 14
- 208000022873 Ocular disease Diseases 0.000 description 13
- 239000002585 base Substances 0.000 description 13
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 13
- 210000004027 cell Anatomy 0.000 description 13
- CKJNUZNMWOVDFN-UHFFFAOYSA-N methanone Chemical compound O=[CH-] CKJNUZNMWOVDFN-UHFFFAOYSA-N 0.000 description 13
- 238000010992 reflux Methods 0.000 description 13
- 238000012360 testing method Methods 0.000 description 13
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 12
- 239000002953 phosphate buffered saline Substances 0.000 description 12
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonia chloride Chemical compound [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 11
- 125000003342 alkenyl group Chemical group 0.000 description 11
- 235000019270 ammonium chloride Nutrition 0.000 description 11
- 238000001816 cooling Methods 0.000 description 11
- 230000001225 therapeutic effect Effects 0.000 description 11
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 10
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 9
- 229910052799 carbon Inorganic materials 0.000 description 9
- 229940079593 drug Drugs 0.000 description 9
- 230000006870 function Effects 0.000 description 9
- 238000007429 general method Methods 0.000 description 9
- 239000000463 material Substances 0.000 description 9
- 238000011282 treatment Methods 0.000 description 9
- 239000003981 vehicle Substances 0.000 description 9
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 8
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical group [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 8
- 241000699670 Mus sp. Species 0.000 description 8
- 229940123932 Phosphodiesterase 4 inhibitor Drugs 0.000 description 8
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 8
- 125000002947 alkylene group Chemical group 0.000 description 8
- 229910052805 deuterium Inorganic materials 0.000 description 8
- 150000002576 ketones Chemical class 0.000 description 8
- 239000002587 phosphodiesterase IV inhibitor Substances 0.000 description 8
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 8
- 239000000126 substance Substances 0.000 description 8
- 229930000680 A04AD01 - Scopolamine Natural products 0.000 description 7
- SUZLHDUTVMZSEV-UHFFFAOYSA-N Deoxycoleonol Natural products C12C(=O)CC(C)(C=C)OC2(C)C(OC(=O)C)C(O)C2C1(C)C(O)CCC2(C)C SUZLHDUTVMZSEV-UHFFFAOYSA-N 0.000 description 7
- YZCKVEUIGOORGS-OUBTZVSYSA-N Deuterium Chemical compound [2H] YZCKVEUIGOORGS-OUBTZVSYSA-N 0.000 description 7
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 7
- STECJAGHUSJQJN-GAUPFVANSA-N Hyoscine Natural products C1([C@H](CO)C(=O)OC2C[C@@H]3N([C@H](C2)[C@@H]2[C@H]3O2)C)=CC=CC=C1 STECJAGHUSJQJN-GAUPFVANSA-N 0.000 description 7
- STECJAGHUSJQJN-UHFFFAOYSA-N N-Methyl-scopolamin Natural products C1C(C2C3O2)N(C)C3CC1OC(=O)C(CO)C1=CC=CC=C1 STECJAGHUSJQJN-UHFFFAOYSA-N 0.000 description 7
- 239000003153 chemical reaction reagent Substances 0.000 description 7
- OHCQJHSOBUTRHG-UHFFFAOYSA-N colforsin Natural products OC12C(=O)CC(C)(C=C)OC1(C)C(OC(=O)C)C(O)C1C2(C)C(O)CCC1(C)C OHCQJHSOBUTRHG-UHFFFAOYSA-N 0.000 description 7
- 238000001704 evaporation Methods 0.000 description 7
- 239000001257 hydrogen Substances 0.000 description 7
- 239000000543 intermediate Substances 0.000 description 7
- 125000004194 piperazin-1-yl group Chemical group [H]N1C([H])([H])C([H])([H])N(*)C([H])([H])C1([H])[H] 0.000 description 7
- FUXJMHXHGDAHPD-UHFFFAOYSA-N pyrimidine-2-carboxamide Chemical compound NC(=O)C1=NC=CC=N1 FUXJMHXHGDAHPD-UHFFFAOYSA-N 0.000 description 7
- 229920006395 saturated elastomer Polymers 0.000 description 7
- STECJAGHUSJQJN-FWXGHANASA-N scopolamine Chemical compound C1([C@@H](CO)C(=O)O[C@H]2C[C@@H]3N([C@H](C2)[C@@H]2[C@H]3O2)C)=CC=CC=C1 STECJAGHUSJQJN-FWXGHANASA-N 0.000 description 7
- 229960002646 scopolamine Drugs 0.000 description 7
- 238000006467 substitution reaction Methods 0.000 description 7
- 108091005957 yellow fluorescent proteins Proteins 0.000 description 7
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 6
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 6
- 125000000304 alkynyl group Chemical group 0.000 description 6
- 229940024606 amino acid Drugs 0.000 description 6
- 235000001014 amino acid Nutrition 0.000 description 6
- 230000003110 anti-inflammatory effect Effects 0.000 description 6
- 238000003556 assay Methods 0.000 description 6
- 239000013078 crystal Substances 0.000 description 6
- 238000011038 discontinuous diafiltration by volume reduction Methods 0.000 description 6
- 230000008020 evaporation Effects 0.000 description 6
- 238000002474 experimental method Methods 0.000 description 6
- 238000001914 filtration Methods 0.000 description 6
- ZHNUHDYFZUAESO-UHFFFAOYSA-N formamide Substances NC=O ZHNUHDYFZUAESO-UHFFFAOYSA-N 0.000 description 6
- QPJVMBTYPHYUOC-UHFFFAOYSA-N methyl benzoate Chemical compound COC(=O)C1=CC=CC=C1 QPJVMBTYPHYUOC-UHFFFAOYSA-N 0.000 description 6
- BUXUEPKVOZSCGP-UHFFFAOYSA-N 5-(3-bromophenyl)-n-(pyridin-4-ylmethyl)pyrazolo[1,5-a]pyrimidin-7-amine Chemical compound BrC1=CC=CC(C2=NC3=CC=NN3C(NCC=3C=CN=CC=3)=C2)=C1 BUXUEPKVOZSCGP-UHFFFAOYSA-N 0.000 description 5
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 5
- 238000004458 analytical method Methods 0.000 description 5
- 238000012512 characterization method Methods 0.000 description 5
- 239000003085 diluting agent Substances 0.000 description 5
- 150000002148 esters Chemical class 0.000 description 5
- OAKJQQAXSVQMHS-UHFFFAOYSA-N hydrazine group Chemical group NN OAKJQQAXSVQMHS-UHFFFAOYSA-N 0.000 description 5
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 description 5
- 150000007522 mineralic acids Chemical class 0.000 description 5
- REPVNSJSTLRQEQ-UHFFFAOYSA-N n,n-dimethylacetamide;n,n-dimethylformamide Chemical compound CN(C)C=O.CN(C)C(C)=O REPVNSJSTLRQEQ-UHFFFAOYSA-N 0.000 description 5
- 150000007524 organic acids Chemical class 0.000 description 5
- 239000001301 oxygen Substances 0.000 description 5
- 238000002360 preparation method Methods 0.000 description 5
- 239000011780 sodium chloride Substances 0.000 description 5
- SZUVGFMDDVSKSI-WIFOCOSTSA-N (1s,2s,3s,5r)-1-(carboxymethyl)-3,5-bis[(4-phenoxyphenyl)methyl-propylcarbamoyl]cyclopentane-1,2-dicarboxylic acid Chemical compound O=C([C@@H]1[C@@H]([C@](CC(O)=O)([C@H](C(=O)N(CCC)CC=2C=CC(OC=3C=CC=CC=3)=CC=2)C1)C(O)=O)C(O)=O)N(CCC)CC(C=C1)=CC=C1OC1=CC=CC=C1 SZUVGFMDDVSKSI-WIFOCOSTSA-N 0.000 description 4
- 125000006274 (C1-C3)alkoxy group Chemical group 0.000 description 4
- RAXXELZNTBOGNW-UHFFFAOYSA-N 1H-imidazole Chemical compound C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 4
- VHYFNPMBLIVWCW-UHFFFAOYSA-N 4-Dimethylaminopyridine Chemical compound CN(C)C1=CC=NC=C1 VHYFNPMBLIVWCW-UHFFFAOYSA-N 0.000 description 4
- RLTQOBXSWLHJGS-UHFFFAOYSA-N COC(C=CC(C(C=NC1=C2)=CN1N=C2C(O)=O)=C1)=C1OC Chemical compound COC(C=CC(C(C=NC1=C2)=CN1N=C2C(O)=O)=C1)=C1OC RLTQOBXSWLHJGS-UHFFFAOYSA-N 0.000 description 4
- 206010010744 Conjunctivitis allergic Diseases 0.000 description 4
- IVOMOUWHDPKRLL-KQYNXXCUSA-N Cyclic adenosine monophosphate Chemical compound C([C@H]1O2)OP(O)(=O)O[C@H]1[C@@H](O)[C@@H]2N1C(N=CN=C2N)=C2N=C1 IVOMOUWHDPKRLL-KQYNXXCUSA-N 0.000 description 4
- RGSFGYAAUTVSQA-UHFFFAOYSA-N Cyclopentane Chemical compound C1CCCC1 RGSFGYAAUTVSQA-UHFFFAOYSA-N 0.000 description 4
- 108010061711 Gliadin Proteins 0.000 description 4
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 4
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Chemical compound NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 description 4
- 230000004913 activation Effects 0.000 description 4
- 239000012190 activator Substances 0.000 description 4
- 125000002252 acyl group Chemical group 0.000 description 4
- 239000002671 adjuvant Substances 0.000 description 4
- 208000002205 allergic conjunctivitis Diseases 0.000 description 4
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 4
- 208000024998 atopic conjunctivitis Diseases 0.000 description 4
- 230000008901 benefit Effects 0.000 description 4
- 239000011203 carbon fibre reinforced carbon Substances 0.000 description 4
- 239000000969 carrier Substances 0.000 description 4
- 238000006243 chemical reaction Methods 0.000 description 4
- 239000003795 chemical substances by application Substances 0.000 description 4
- 239000000460 chlorine Substances 0.000 description 4
- 229940126543 compound 14 Drugs 0.000 description 4
- NZNMSOFKMUBTKW-UHFFFAOYSA-N cyclohexanecarboxylic acid Chemical compound OC(=O)C1CCCCC1 NZNMSOFKMUBTKW-UHFFFAOYSA-N 0.000 description 4
- HGCIXCUEYOPUTN-UHFFFAOYSA-N cyclohexene Chemical compound C1CCC=CC1 HGCIXCUEYOPUTN-UHFFFAOYSA-N 0.000 description 4
- 125000001153 fluoro group Chemical group F* 0.000 description 4
- 125000002541 furyl group Chemical group 0.000 description 4
- 150000002430 hydrocarbons Chemical group 0.000 description 4
- 125000006574 non-aromatic ring group Chemical group 0.000 description 4
- 230000003287 optical effect Effects 0.000 description 4
- 235000005985 organic acids Nutrition 0.000 description 4
- 125000004076 pyridyl group Chemical group 0.000 description 4
- 150000003254 radicals Chemical class 0.000 description 4
- 235000019615 sensations Nutrition 0.000 description 4
- 230000000707 stereoselective effect Effects 0.000 description 4
- 125000000475 sulfinyl group Chemical group [*:2]S([*:1])=O 0.000 description 4
- FYSNRJHAOHDILO-UHFFFAOYSA-N thionyl chloride Chemical compound ClS(Cl)=O FYSNRJHAOHDILO-UHFFFAOYSA-N 0.000 description 4
- DTQVDTLACAAQTR-UHFFFAOYSA-N trifluoroacetic acid Substances OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 4
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 4
- IUSARDYWEPUTPN-OZBXUNDUSA-N (2r)-n-[(2s,3r)-4-[[(4s)-6-(2,2-dimethylpropyl)spiro[3,4-dihydropyrano[2,3-b]pyridine-2,1'-cyclobutane]-4-yl]amino]-3-hydroxy-1-[3-(1,3-thiazol-2-yl)phenyl]butan-2-yl]-2-methoxypropanamide Chemical compound C([C@H](NC(=O)[C@@H](C)OC)[C@H](O)CN[C@@H]1C2=CC(CC(C)(C)C)=CN=C2OC2(CCC2)C1)C(C=1)=CC=CC=1C1=NC=CS1 IUSARDYWEPUTPN-OZBXUNDUSA-N 0.000 description 3
- STBLNCCBQMHSRC-BATDWUPUSA-N (2s)-n-[(3s,4s)-5-acetyl-7-cyano-4-methyl-1-[(2-methylnaphthalen-1-yl)methyl]-2-oxo-3,4-dihydro-1,5-benzodiazepin-3-yl]-2-(methylamino)propanamide Chemical compound O=C1[C@@H](NC(=O)[C@H](C)NC)[C@H](C)N(C(C)=O)C2=CC(C#N)=CC=C2N1CC1=C(C)C=CC2=CC=CC=C12 STBLNCCBQMHSRC-BATDWUPUSA-N 0.000 description 3
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 3
- LMDZBCPBFSXMTL-UHFFFAOYSA-N 1-Ethyl-3-(3-dimethylaminopropyl)carbodiimide Substances CCN=C=NCCCN(C)C LMDZBCPBFSXMTL-UHFFFAOYSA-N 0.000 description 3
- PVOAHINGSUIXLS-UHFFFAOYSA-N 1-Methylpiperazine Chemical compound CN1CCNCC1 PVOAHINGSUIXLS-UHFFFAOYSA-N 0.000 description 3
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 3
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 3
- UHNRLQRZRNKOKU-UHFFFAOYSA-N CCN(CC1=NC2=C(N1)C1=CC=C(C=C1N=C2N)C1=NNC=C1)C(C)=O Chemical compound CCN(CC1=NC2=C(N1)C1=CC=C(C=C1N=C2N)C1=NNC=C1)C(C)=O UHNRLQRZRNKOKU-UHFFFAOYSA-N 0.000 description 3
- KXDNPBNAMCPMPI-UHFFFAOYSA-N COC(C1=NN2C(C(C=C3OC)=CC=C3OC)=CC=NC2=C1)=O Chemical compound COC(C1=NN2C(C(C=C3OC)=CC=C3OC)=CC=NC2=C1)=O KXDNPBNAMCPMPI-UHFFFAOYSA-N 0.000 description 3
- ZLNBYXOQUCNKRF-UHFFFAOYSA-N COC(C=C(C=C1)C2=CC=NC3=CC(C(O)=O)=NN23)=C1F Chemical compound COC(C=C(C=C1)C2=CC=NC3=CC(C(O)=O)=NN23)=C1F ZLNBYXOQUCNKRF-UHFFFAOYSA-N 0.000 description 3
- FTJXJJFFZFQODT-UHFFFAOYSA-N COC(C=C1)=CC(F)=C1C1=CC=NC2=CC(C(O)=O)=NN12 Chemical compound COC(C=C1)=CC(F)=C1C1=CC=NC2=CC(C(O)=O)=NN12 FTJXJJFFZFQODT-UHFFFAOYSA-N 0.000 description 3
- XGKZHCDTQNWECA-UHFFFAOYSA-N COC(C=CC(C1=CC=NC2=CC(C(Cl)=O)=NN12)=C1)=C1OC Chemical compound COC(C=CC(C1=CC=NC2=CC(C(Cl)=O)=NN12)=C1)=C1OC XGKZHCDTQNWECA-UHFFFAOYSA-N 0.000 description 3
- URNBRMKZODIDAQ-UHFFFAOYSA-N COC(C=CC(C1=CC=NC2=CC(N)=NN12)=C1)=C1OC Chemical compound COC(C=CC(C1=CC=NC2=CC(N)=NN12)=C1)=C1OC URNBRMKZODIDAQ-UHFFFAOYSA-N 0.000 description 3
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 3
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 3
- BELBBZDIHDAJOR-UHFFFAOYSA-N Phenolsulfonephthalein Chemical compound C1=CC(O)=CC=C1C1(C=2C=CC(O)=CC=2)C2=CC=CC=C2S(=O)(=O)O1 BELBBZDIHDAJOR-UHFFFAOYSA-N 0.000 description 3
- YZCKVEUIGOORGS-NJFSPNSNSA-N Tritium Chemical compound [3H] YZCKVEUIGOORGS-NJFSPNSNSA-N 0.000 description 3
- SORGEQQSQGNZFI-UHFFFAOYSA-N [azido(phenoxy)phosphoryl]oxybenzene Chemical compound C=1C=CC=CC=1OP(=O)(N=[N+]=[N-])OC1=CC=CC=C1 SORGEQQSQGNZFI-UHFFFAOYSA-N 0.000 description 3
- 150000007513 acids Chemical class 0.000 description 3
- 239000000654 additive Substances 0.000 description 3
- 125000002029 aromatic hydrocarbon group Chemical group 0.000 description 3
- 229940125878 compound 36 Drugs 0.000 description 3
- 229940125807 compound 37 Drugs 0.000 description 3
- 125000004093 cyano group Chemical group *C#N 0.000 description 3
- 238000007876 drug discovery Methods 0.000 description 3
- 230000004064 dysfunction Effects 0.000 description 3
- 239000003995 emulsifying agent Substances 0.000 description 3
- 230000002255 enzymatic effect Effects 0.000 description 3
- 238000006911 enzymatic reaction Methods 0.000 description 3
- 125000001188 haloalkyl group Chemical group 0.000 description 3
- 238000004128 high performance liquid chromatography Methods 0.000 description 3
- 238000005259 measurement Methods 0.000 description 3
- LZXXNPOYQCLXRS-UHFFFAOYSA-N methyl 4-aminobenzoate Chemical compound COC(=O)C1=CC=C(N)C=C1 LZXXNPOYQCLXRS-UHFFFAOYSA-N 0.000 description 3
- 229940095102 methyl benzoate Drugs 0.000 description 3
- 231100000252 nontoxic Toxicity 0.000 description 3
- 230000003000 nontoxic effect Effects 0.000 description 3
- 239000003921 oil Substances 0.000 description 3
- 210000000056 organ Anatomy 0.000 description 3
- 150000002894 organic compounds Chemical class 0.000 description 3
- 229960003531 phenolsulfonphthalein Drugs 0.000 description 3
- 229910052698 phosphorus Inorganic materials 0.000 description 3
- 239000000843 powder Substances 0.000 description 3
- 230000000770 proinflammatory effect Effects 0.000 description 3
- 238000000746 purification Methods 0.000 description 3
- LDIJKUBTLZTFRG-UHFFFAOYSA-N pyrazolo[1,5-a]pyrimidine Chemical compound N1=CC=CN2N=CC=C21 LDIJKUBTLZTFRG-UHFFFAOYSA-N 0.000 description 3
- 125000000246 pyrimidin-2-yl group Chemical group [H]C1=NC(*)=NC([H])=C1[H] 0.000 description 3
- FOVRZAGACROHCK-UHFFFAOYSA-N pyrimidine-2-carbonyl chloride Chemical compound ClC(=O)C1=NC=CC=N1 FOVRZAGACROHCK-UHFFFAOYSA-N 0.000 description 3
- 229930195734 saturated hydrocarbon Natural products 0.000 description 3
- DCKVNWZUADLDEH-UHFFFAOYSA-N sec-butyl acetate Chemical compound CCC(C)OC(C)=O DCKVNWZUADLDEH-UHFFFAOYSA-N 0.000 description 3
- 239000011734 sodium Substances 0.000 description 3
- 229910000029 sodium carbonate Inorganic materials 0.000 description 3
- 229910000104 sodium hydride Inorganic materials 0.000 description 3
- FVAUCKIRQBBSSJ-UHFFFAOYSA-M sodium iodide Chemical compound [Na+].[I-] FVAUCKIRQBBSSJ-UHFFFAOYSA-M 0.000 description 3
- 239000002904 solvent Substances 0.000 description 3
- 239000007858 starting material Substances 0.000 description 3
- 238000007920 subcutaneous administration Methods 0.000 description 3
- 239000004094 surface-active agent Substances 0.000 description 3
- 239000000725 suspension Substances 0.000 description 3
- 238000001308 synthesis method Methods 0.000 description 3
- 238000002560 therapeutic procedure Methods 0.000 description 3
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 3
- 230000009466 transformation Effects 0.000 description 3
- 229910052722 tritium Inorganic materials 0.000 description 3
- QFLWZFQWSBQYPS-AWRAUJHKSA-N (3S)-3-[[(2S)-2-[[(2S)-2-[5-[(3aS,6aR)-2-oxo-1,3,3a,4,6,6a-hexahydrothieno[3,4-d]imidazol-4-yl]pentanoylamino]-3-methylbutanoyl]amino]-3-(4-hydroxyphenyl)propanoyl]amino]-4-[1-bis(4-chlorophenoxy)phosphorylbutylamino]-4-oxobutanoic acid Chemical compound CCCC(NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](Cc1ccc(O)cc1)NC(=O)[C@@H](NC(=O)CCCCC1SC[C@@H]2NC(=O)N[C@H]12)C(C)C)P(=O)(Oc1ccc(Cl)cc1)Oc1ccc(Cl)cc1 QFLWZFQWSBQYPS-AWRAUJHKSA-N 0.000 description 2
- MRBFGEHILMYPTF-UHFFFAOYSA-N 1-(2-Pyrimidyl)piperazine Chemical compound C1CNCCN1C1=NC=CC=N1 MRBFGEHILMYPTF-UHFFFAOYSA-N 0.000 description 2
- YBYIRNPNPLQARY-UHFFFAOYSA-N 1H-indene Natural products C1=CC=C2CC=CC2=C1 YBYIRNPNPLQARY-UHFFFAOYSA-N 0.000 description 2
- HBEDSQVIWPRPAY-UHFFFAOYSA-N 2,3-dihydrobenzofuran Chemical compound C1=CC=C2OCCC2=C1 HBEDSQVIWPRPAY-UHFFFAOYSA-N 0.000 description 2
- HUTKDPINCSJXAA-CMDGGOBGSA-N 3-(dimethylamino)-1-phenylprop-2-en-1-one Chemical compound CN(C)\C=C\C(=O)C1=CC=CC=C1 HUTKDPINCSJXAA-CMDGGOBGSA-N 0.000 description 2
- QCQCHGYLTSGIGX-GHXANHINSA-N 4-[[(3ar,5ar,5br,7ar,9s,11ar,11br,13as)-5a,5b,8,8,11a-pentamethyl-3a-[(5-methylpyridine-3-carbonyl)amino]-2-oxo-1-propan-2-yl-4,5,6,7,7a,9,10,11,11b,12,13,13a-dodecahydro-3h-cyclopenta[a]chrysen-9-yl]oxy]-2,2-dimethyl-4-oxobutanoic acid Chemical compound N([C@@]12CC[C@@]3(C)[C@]4(C)CC[C@H]5C(C)(C)[C@@H](OC(=O)CC(C)(C)C(O)=O)CC[C@]5(C)[C@H]4CC[C@@H]3C1=C(C(C2)=O)C(C)C)C(=O)C1=CN=CC(C)=C1 QCQCHGYLTSGIGX-GHXANHINSA-N 0.000 description 2
- XSVKDCVIWOKXSX-UHFFFAOYSA-N 4-[tert-butyl(dimethyl)silyl]oxyaniline Chemical compound CC(C)(C)[Si](C)(C)OC1=CC=C(N)C=C1 XSVKDCVIWOKXSX-UHFFFAOYSA-N 0.000 description 2
- PLIKAWJENQZMHA-UHFFFAOYSA-N 4-aminophenol Chemical compound NC1=CC=C(O)C=C1 PLIKAWJENQZMHA-UHFFFAOYSA-N 0.000 description 2
- 229960000549 4-dimethylaminophenol Drugs 0.000 description 2
- IMPPGHMHELILKG-UHFFFAOYSA-N 4-ethoxyaniline Chemical compound CCOC1=CC=C(N)C=C1 IMPPGHMHELILKG-UHFFFAOYSA-N 0.000 description 2
- NSPMIYGKQJPBQR-UHFFFAOYSA-N 4H-1,2,4-triazole Chemical compound C=1N=CNN=1 NSPMIYGKQJPBQR-UHFFFAOYSA-N 0.000 description 2
- YXCMYAXABXJNTQ-UHFFFAOYSA-N 7-(3,4-difluorophenyl)pyrazolo[1,5-a]pyrimidine-2-carboxylic acid Chemical compound OC(=O)c1cc2nccc(-c3ccc(F)c(F)c3)n2n1 YXCMYAXABXJNTQ-UHFFFAOYSA-N 0.000 description 2
- PCRKTPKIWRHNRX-UHFFFAOYSA-N 7-phenylpyrazolo[1,5-a]pyrimidine-2-carboxylic acid Chemical compound N12N=C(C(=O)O)C=C2N=CC=C1C1=CC=CC=C1 PCRKTPKIWRHNRX-UHFFFAOYSA-N 0.000 description 2
- KWOLFJPFCHCOCG-UHFFFAOYSA-N Acetophenone Chemical compound CC(=O)C1=CC=CC=C1 KWOLFJPFCHCOCG-UHFFFAOYSA-N 0.000 description 2
- 206010057380 Allergic keratitis Diseases 0.000 description 2
- ZNSMNVMLTJELDZ-UHFFFAOYSA-N Bis(2-chloroethyl)ether Chemical compound ClCCOCCCl ZNSMNVMLTJELDZ-UHFFFAOYSA-N 0.000 description 2
- OJRUSAPKCPIVBY-KQYNXXCUSA-N C1=NC2=C(N=C(N=C2N1[C@H]3[C@@H]([C@@H]([C@H](O3)COP(=O)(CP(=O)(O)O)O)O)O)I)N Chemical compound C1=NC2=C(N=C(N=C2N1[C@H]3[C@@H]([C@@H]([C@H](O3)COP(=O)(CP(=O)(O)O)O)O)O)I)N OJRUSAPKCPIVBY-KQYNXXCUSA-N 0.000 description 2
- 101150029409 CFTR gene Proteins 0.000 description 2
- GEWOYSRXTCFVGW-UHFFFAOYSA-N COC(C(C1)(C2)CC12NC(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O)=O Chemical compound COC(C(C1)(C2)CC12NC(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O)=O GEWOYSRXTCFVGW-UHFFFAOYSA-N 0.000 description 2
- USLRATOPKVKTRX-UHFFFAOYSA-N COC(C(CC1)(CC2)CCC12N1CCOCC1)=O Chemical compound COC(C(CC1)(CC2)CCC12N1CCOCC1)=O USLRATOPKVKTRX-UHFFFAOYSA-N 0.000 description 2
- IQDFCDTYTUHMAV-UHFFFAOYSA-N COC(C1=NN2C(C(C=C3)=CC(F)=C3F)=CC=NC2=C1)=O Chemical compound COC(C1=NN2C(C(C=C3)=CC(F)=C3F)=CC=NC2=C1)=O IQDFCDTYTUHMAV-UHFFFAOYSA-N 0.000 description 2
- YYKPAERHCOUIMY-UHFFFAOYSA-N COC(C1=NN2C(C(C=C3)=CC(OC)=C3F)=CC=NC2=C1)=O Chemical compound COC(C1=NN2C(C(C=C3)=CC(OC)=C3F)=CC=NC2=C1)=O YYKPAERHCOUIMY-UHFFFAOYSA-N 0.000 description 2
- WDDZPMOIWRRWAE-UHFFFAOYSA-N COC(C1=NN2C(C3=CC=CC=C3)=CC=NC2=C1)=O Chemical compound COC(C1=NN2C(C3=CC=CC=C3)=CC=NC2=C1)=O WDDZPMOIWRRWAE-UHFFFAOYSA-N 0.000 description 2
- GGZXWKHTLJJWDV-UHFFFAOYSA-N COC(C=CC(C1=CC=NC2=CC(C(N3CCN(CC4=CC=CC=C4)CC3)=O)=NN12)=C1)=C1OC Chemical compound COC(C=CC(C1=CC=NC2=CC(C(N3CCN(CC4=CC=CC=C4)CC3)=O)=NN12)=C1)=C1OC GGZXWKHTLJJWDV-UHFFFAOYSA-N 0.000 description 2
- RIZDIXKWOXXKIS-UHFFFAOYSA-N COC(C=CC(C1=CC=NC2=CC(C(NC(C3)(C4)CC34C(O)=O)=O)=NN12)=C1)=C1OC Chemical compound COC(C=CC(C1=CC=NC2=CC(C(NC(C3)(C4)CC34C(O)=O)=O)=NN12)=C1)=C1OC RIZDIXKWOXXKIS-UHFFFAOYSA-N 0.000 description 2
- FOGKCXRMQKIHNF-UHFFFAOYSA-N COC(C=CC(C1=CC=NC2=CC(C(NC(C=C3)=CC=C3C(O)=O)=O)=NN12)=C1)=C1OC Chemical compound COC(C=CC(C1=CC=NC2=CC(C(NC(C=C3)=CC=C3C(O)=O)=O)=NN12)=C1)=C1OC FOGKCXRMQKIHNF-UHFFFAOYSA-N 0.000 description 2
- PCBGCCSACCKGFL-UHFFFAOYSA-N COC(C=CC(C1=CC=NC2=CC(NC(C(CC3)(CC4)CCC34N3CCOCC3)=O)=NN12)=C1)=C1OC Chemical compound COC(C=CC(C1=CC=NC2=CC(NC(C(CC3)(CC4)CCC34N3CCOCC3)=O)=NN12)=C1)=C1OC PCBGCCSACCKGFL-UHFFFAOYSA-N 0.000 description 2
- RWKUXWXZBMMNQG-UHFFFAOYSA-N COC(C=CC(C1=CC=NC2=CC(NC(NC(C=C3)=CC=C3C(O)=O)=O)=NN12)=C1)=C1OC Chemical compound COC(C=CC(C1=CC=NC2=CC(NC(NC(C=C3)=CC=C3C(O)=O)=O)=NN12)=C1)=C1OC RWKUXWXZBMMNQG-UHFFFAOYSA-N 0.000 description 2
- 239000004215 Carbon black (E152) Substances 0.000 description 2
- 102000011045 Chloride Channels Human genes 0.000 description 2
- 108010062745 Chloride Channels Proteins 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 2
- 241000699802 Cricetulus griseus Species 0.000 description 2
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 2
- IGXWBGJHJZYPQS-SSDOTTSWSA-N D-Luciferin Chemical compound OC(=O)[C@H]1CSC(C=2SC3=CC=C(O)C=C3N=2)=N1 IGXWBGJHJZYPQS-SSDOTTSWSA-N 0.000 description 2
- 206010012735 Diarrhoea Diseases 0.000 description 2
- 102000004190 Enzymes Human genes 0.000 description 2
- 108090000790 Enzymes Proteins 0.000 description 2
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 2
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 2
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 description 2
- 108010068370 Glutens Proteins 0.000 description 2
- 241000282412 Homo Species 0.000 description 2
- 208000019693 Lung disease Diseases 0.000 description 2
- 241000124008 Mammalia Species 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- FXHOOIRPVKKKFG-UHFFFAOYSA-N N,N-Dimethylacetamide Chemical compound CN(C)C(C)=O FXHOOIRPVKKKFG-UHFFFAOYSA-N 0.000 description 2
- 208000012902 Nervous system disease Diseases 0.000 description 2
- ABOICKCOWJPBJR-UHFFFAOYSA-N O=C(C(CC1)(CC2)CCC12N1CCOCC1)Cl Chemical compound O=C(C(CC1)(CC2)CCC12N1CCOCC1)Cl ABOICKCOWJPBJR-UHFFFAOYSA-N 0.000 description 2
- WHOKVQGXRGNOMR-UHFFFAOYSA-N OC(C(CC1)(CC2)CCC12N1CCOCC1)=O Chemical compound OC(C(CC1)(CC2)CCC12N1CCOCC1)=O WHOKVQGXRGNOMR-UHFFFAOYSA-N 0.000 description 2
- 229930182555 Penicillin Natural products 0.000 description 2
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 2
- QOSMNYMQXIVWKY-UHFFFAOYSA-N Propyl levulinate Chemical compound CCCOC(=O)CCC(C)=O QOSMNYMQXIVWKY-UHFFFAOYSA-N 0.000 description 2
- 208000003251 Pruritus Diseases 0.000 description 2
- 241000700159 Rattus Species 0.000 description 2
- 229910006124 SOCl2 Inorganic materials 0.000 description 2
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 2
- DKGAVHZHDRPRBM-UHFFFAOYSA-N Tert-Butanol Chemical compound CC(C)(C)O DKGAVHZHDRPRBM-UHFFFAOYSA-N 0.000 description 2
- IQZLUWLMQNGTIW-UHFFFAOYSA-N acetoveratrone Chemical compound COC1=CC=C(C(C)=O)C=C1OC IQZLUWLMQNGTIW-UHFFFAOYSA-N 0.000 description 2
- 230000002378 acidificating effect Effects 0.000 description 2
- 230000009471 action Effects 0.000 description 2
- 230000003213 activating effect Effects 0.000 description 2
- 239000013543 active substance Substances 0.000 description 2
- 125000005073 adamantyl group Chemical group C12(CC3CC(CC(C1)C3)C2)* 0.000 description 2
- 230000002411 adverse Effects 0.000 description 2
- 229960003767 alanine Drugs 0.000 description 2
- 125000001931 aliphatic group Chemical group 0.000 description 2
- 150000001450 anions Chemical class 0.000 description 2
- 239000002260 anti-inflammatory agent Substances 0.000 description 2
- 229940121363 anti-inflammatory agent Drugs 0.000 description 2
- 229960005261 aspartic acid Drugs 0.000 description 2
- 229910052789 astatine Inorganic materials 0.000 description 2
- OTKPPUXRIADSGD-PPRNARJGSA-N avoparcina Chemical compound O([C@@H]1C2=CC=C(C(=C2)Cl)OC=2C=C3C=C(C=2O[C@H]2C([C@@H](O)[C@H](O)[C@@H](CO)O2)O[C@@H]2O[C@@H](C)[C@H](O)[C@H](N)C2)OC2=CC=C(C=C2)[C@@H](O)[C@H](C(N[C@H](C(=O)N[C@H]3C(=O)N[C@H]2C(=O)N[C@@H]1C(N[C@@H](C1=CC(O)=CC(O)=C1C=1C(O)=CC=C2C=1)C(O)=O)=O)C=1C=CC(O)=CC=1)=O)NC(=O)[C@H](NC)C=1C=CC(O[C@H]2[C@@H]([C@H](O)[C@@H](O)[C@H](C)O2)O)=CC=1)[C@H]1C[C@@H](N)[C@@H](O)[C@H](C)O1 OTKPPUXRIADSGD-PPRNARJGSA-N 0.000 description 2
- 150000007514 bases Chemical class 0.000 description 2
- 125000004196 benzothienyl group Chemical group S1C(=CC2=C1C=CC=C2)* 0.000 description 2
- WGQKYBSKWIADBV-UHFFFAOYSA-N benzylamine Chemical compound NCC1=CC=CC=C1 WGQKYBSKWIADBV-UHFFFAOYSA-N 0.000 description 2
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 2
- 210000001124 body fluid Anatomy 0.000 description 2
- 239000010839 body fluid Substances 0.000 description 2
- 230000037396 body weight Effects 0.000 description 2
- 229910052796 boron Inorganic materials 0.000 description 2
- 239000000872 buffer Substances 0.000 description 2
- 239000002775 capsule Substances 0.000 description 2
- 239000004202 carbamide Substances 0.000 description 2
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 2
- 230000003197 catalytic effect Effects 0.000 description 2
- 150000001768 cations Chemical class 0.000 description 2
- 238000004113 cell culture Methods 0.000 description 2
- 238000000576 coating method Methods 0.000 description 2
- 229940125758 compound 15 Drugs 0.000 description 2
- 125000001316 cycloalkyl alkyl group Chemical group 0.000 description 2
- PAFZNILMFXTMIY-UHFFFAOYSA-N cyclohexylamine Chemical compound NC1CCCCC1 PAFZNILMFXTMIY-UHFFFAOYSA-N 0.000 description 2
- NNBZCPXTIHJBJL-UHFFFAOYSA-N decalin Chemical compound C1CCCC2CCCCC21 NNBZCPXTIHJBJL-UHFFFAOYSA-N 0.000 description 2
- 238000001514 detection method Methods 0.000 description 2
- 235000005911 diet Nutrition 0.000 description 2
- 235000014113 dietary fatty acids Nutrition 0.000 description 2
- BDUPRNVPXOHWIL-UHFFFAOYSA-N dimethyl sulfite Chemical compound COS(=O)OC BDUPRNVPXOHWIL-UHFFFAOYSA-N 0.000 description 2
- 239000003937 drug carrier Substances 0.000 description 2
- 239000000839 emulsion Substances 0.000 description 2
- 239000000194 fatty acid Substances 0.000 description 2
- 229930195729 fatty acid Natural products 0.000 description 2
- 239000004220 glutamic acid Substances 0.000 description 2
- 235000013922 glutamic acid Nutrition 0.000 description 2
- 235000021312 gluten Nutrition 0.000 description 2
- 150000004820 halides Chemical class 0.000 description 2
- 125000000262 haloalkenyl group Chemical group 0.000 description 2
- 125000000232 haloalkynyl group Chemical group 0.000 description 2
- DMEGYFMYUHOHGS-UHFFFAOYSA-N heptamethylene Natural products C1CCCCCC1 DMEGYFMYUHOHGS-UHFFFAOYSA-N 0.000 description 2
- 125000004446 heteroarylalkyl group Chemical group 0.000 description 2
- 125000005885 heterocycloalkylalkyl group Chemical group 0.000 description 2
- 229930195733 hydrocarbon Natural products 0.000 description 2
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 2
- 125000001841 imino group Chemical group [H]N=* 0.000 description 2
- PQNFLJBBNBOBRQ-UHFFFAOYSA-N indane Chemical compound C1=CC=C2CCCC2=C1 PQNFLJBBNBOBRQ-UHFFFAOYSA-N 0.000 description 2
- 125000003454 indenyl group Chemical group C1(C=CC2=CC=CC=C12)* 0.000 description 2
- 125000001041 indolyl group Chemical group 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- 230000003834 intracellular effect Effects 0.000 description 2
- 238000007918 intramuscular administration Methods 0.000 description 2
- 238000001990 intravenous administration Methods 0.000 description 2
- 230000007803 itching Effects 0.000 description 2
- 206010023332 keratitis Diseases 0.000 description 2
- 238000004895 liquid chromatography mass spectrometry Methods 0.000 description 2
- 239000007937 lozenge Substances 0.000 description 2
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 238000004949 mass spectrometry Methods 0.000 description 2
- 239000002609 medium Substances 0.000 description 2
- 239000012528 membrane Substances 0.000 description 2
- HDIKFAFEMDBXOS-UHFFFAOYSA-N methyl 4-aminobicyclo[2.2.2]octane-1-carboxylate Chemical compound C1CC2(N)CCC1(C(=O)OC)CC2 HDIKFAFEMDBXOS-UHFFFAOYSA-N 0.000 description 2
- QWQDSBMSESLQEC-UHFFFAOYSA-N methyl 6-bromopyrazolo[1,5-a]pyrimidine-2-carboxylate Chemical compound N1=CC(Br)=CN2N=C(C(=O)OC)C=C21 QWQDSBMSESLQEC-UHFFFAOYSA-N 0.000 description 2
- 239000004530 micro-emulsion Substances 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 2
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 2
- 125000001624 naphthyl group Chemical group 0.000 description 2
- 208000019180 nutritional disease Diseases 0.000 description 2
- 239000002997 ophthalmic solution Substances 0.000 description 2
- 229940054534 ophthalmic solution Drugs 0.000 description 2
- 210000001672 ovary Anatomy 0.000 description 2
- 150000002923 oximes Chemical class 0.000 description 2
- 210000000496 pancreas Anatomy 0.000 description 2
- 238000007911 parenteral administration Methods 0.000 description 2
- 229940049954 penicillin Drugs 0.000 description 2
- 239000006187 pill Substances 0.000 description 2
- 125000003367 polycyclic group Chemical group 0.000 description 2
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 2
- 108090000765 processed proteins & peptides Proteins 0.000 description 2
- 125000000168 pyrrolyl group Chemical group 0.000 description 2
- 230000009467 reduction Effects 0.000 description 2
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 2
- 201000009881 secretory diarrhea Diseases 0.000 description 2
- 229910052710 silicon Inorganic materials 0.000 description 2
- 241000894007 species Species 0.000 description 2
- 238000010561 standard procedure Methods 0.000 description 2
- UCSJYZPVAKXKNQ-HZYVHMACSA-N streptomycin Chemical compound CN[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O[C@H]1O[C@@H]1[C@](C=O)(O)[C@H](C)O[C@H]1O[C@@H]1[C@@H](NC(N)=N)[C@H](O)[C@@H](NC(N)=N)[C@H](O)[C@H]1O UCSJYZPVAKXKNQ-HZYVHMACSA-N 0.000 description 2
- 125000000547 substituted alkyl group Chemical group 0.000 description 2
- 238000010189 synthetic method Methods 0.000 description 2
- 239000006188 syrup Substances 0.000 description 2
- 235000020357 syrup Nutrition 0.000 description 2
- LFKDJXLFVYVEFG-UHFFFAOYSA-N tert-butyl carbamate Chemical compound CC(C)(C)OC(N)=O LFKDJXLFVYVEFG-UHFFFAOYSA-N 0.000 description 2
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 2
- CXWXQJXEFPUFDZ-UHFFFAOYSA-N tetralin Chemical compound C1=CC=C2CCCCC2=C1 CXWXQJXEFPUFDZ-UHFFFAOYSA-N 0.000 description 2
- 125000000335 thiazolyl group Chemical group 0.000 description 2
- 125000001544 thienyl group Chemical group 0.000 description 2
- 238000004809 thin layer chromatography Methods 0.000 description 2
- 125000004149 thio group Chemical group *S* 0.000 description 2
- RIOQSEWOXXDEQQ-UHFFFAOYSA-N triphenylphosphine Chemical compound C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 RIOQSEWOXXDEQQ-UHFFFAOYSA-N 0.000 description 2
- CANZBRDGRHNSGZ-NSHDSACASA-N (2s)-3-methyl-2-(phenylmethoxycarbonylamino)butanoic acid Chemical compound CC(C)[C@@H](C(O)=O)NC(=O)OCC1=CC=CC=C1 CANZBRDGRHNSGZ-NSHDSACASA-N 0.000 description 1
- RCVDPBFUMYUKPB-UHFFFAOYSA-N (3,4-dimethoxyphenyl)boronic acid Chemical compound COC1=CC=C(B(O)O)C=C1OC RCVDPBFUMYUKPB-UHFFFAOYSA-N 0.000 description 1
- QEDUHUVHFNYHFX-UHFFFAOYSA-N (3-methylpiperazin-1-yl)methanone Chemical compound CC1CN([C]=O)CCN1 QEDUHUVHFNYHFX-UHFFFAOYSA-N 0.000 description 1
- NHAYDXCUCXRAMF-UHFFFAOYSA-N (4-methoxycarbonylcyclohexyl)azanium;chloride Chemical compound Cl.COC(=O)C1CCC(N)CC1 NHAYDXCUCXRAMF-UHFFFAOYSA-N 0.000 description 1
- 125000006832 (C1-C10) alkylene group Chemical group 0.000 description 1
- 125000003837 (C1-C20) alkyl group Chemical group 0.000 description 1
- 125000006273 (C1-C3) alkyl group Chemical group 0.000 description 1
- 125000006527 (C1-C5) alkyl group Chemical group 0.000 description 1
- 125000006833 (C1-C5) alkylene group Chemical group 0.000 description 1
- 125000003161 (C1-C6) alkylene group Chemical group 0.000 description 1
- 125000004209 (C1-C8) alkyl group Chemical group 0.000 description 1
- 125000006651 (C3-C20) cycloalkyl group Chemical group 0.000 description 1
- 125000006555 (C3-C5) cycloalkyl group Chemical group 0.000 description 1
- 125000005913 (C3-C6) cycloalkyl group Chemical group 0.000 description 1
- 125000006552 (C3-C8) cycloalkyl group Chemical group 0.000 description 1
- 125000006570 (C5-C6) heteroaryl group Chemical group 0.000 description 1
- WNTKCCNQWUMQSR-VOTSOKGWSA-N (E)-3-(dimethylamino)-1-(2-fluoro-4-methoxyphenyl)prop-2-en-1-one Chemical compound COC1=CC=C(C(=O)\C=C\N(C)C)C(F)=C1 WNTKCCNQWUMQSR-VOTSOKGWSA-N 0.000 description 1
- UVNPEUJXKZFWSJ-LMTQTHQJSA-N (R)-N-[(4S)-8-[6-amino-5-[(3,3-difluoro-2-oxo-1H-pyrrolo[2,3-b]pyridin-4-yl)sulfanyl]pyrazin-2-yl]-2-oxa-8-azaspiro[4.5]decan-4-yl]-2-methylpropane-2-sulfinamide Chemical compound CC(C)(C)[S@@](=O)N[C@@H]1COCC11CCN(CC1)c1cnc(Sc2ccnc3NC(=O)C(F)(F)c23)c(N)n1 UVNPEUJXKZFWSJ-LMTQTHQJSA-N 0.000 description 1
- LMRJHGLZTUEMNZ-AATRIKPKSA-N (e)-1-(3,4-difluorophenyl)-3-(dimethylamino)prop-2-en-1-one Chemical compound CN(C)\C=C\C(=O)C1=CC=C(F)C(F)=C1 LMRJHGLZTUEMNZ-AATRIKPKSA-N 0.000 description 1
- SUPCYQIUOSDKPA-BQYQJAHWSA-N (e)-1-(3,4-dimethoxyphenyl)-3-(dimethylamino)prop-2-en-1-one Chemical compound COC1=CC=C(C(=O)\C=C\N(C)C)C=C1OC SUPCYQIUOSDKPA-BQYQJAHWSA-N 0.000 description 1
- PIRRWUMTIBFCCW-UHFFFAOYSA-N 1-(2-fluoro-4-methoxyphenyl)ethanone Chemical compound COC1=CC=C(C(C)=O)C(F)=C1 PIRRWUMTIBFCCW-UHFFFAOYSA-N 0.000 description 1
- VWJSSJFLXRMYNV-UHFFFAOYSA-N 1-(3,4-difluorophenyl)ethanone Chemical compound CC(=O)C1=CC=C(F)C(F)=C1 VWJSSJFLXRMYNV-UHFFFAOYSA-N 0.000 description 1
- AUERUDPETOKUPT-UHFFFAOYSA-N 1-(3-chloropropyl)-4-methylpiperazine Chemical compound CN1CCN(CCCCl)CC1 AUERUDPETOKUPT-UHFFFAOYSA-N 0.000 description 1
- PFEGFUCYOHBDJF-UHFFFAOYSA-N 1-(4-fluoro-3-methoxyphenyl)ethanone Chemical compound COC1=CC(C(C)=O)=CC=C1F PFEGFUCYOHBDJF-UHFFFAOYSA-N 0.000 description 1
- DCLMJYZEOSDVCL-UHFFFAOYSA-N 1-(chloromethyl)-4-ethoxybenzene Chemical compound CCOC1=CC=C(CCl)C=C1 DCLMJYZEOSDVCL-UHFFFAOYSA-N 0.000 description 1
- WHKWMTXTYKVFLK-UHFFFAOYSA-N 1-propan-2-ylpiperazine Chemical compound CC(C)N1CCNCC1 WHKWMTXTYKVFLK-UHFFFAOYSA-N 0.000 description 1
- QWENRTYMTSOGBR-UHFFFAOYSA-N 1H-1,2,3-Triazole Chemical compound C=1C=NNN=1 QWENRTYMTSOGBR-UHFFFAOYSA-N 0.000 description 1
- QKNYBSVHEMOAJP-UHFFFAOYSA-N 2-amino-2-(hydroxymethyl)propane-1,3-diol;hydron;chloride Chemical compound Cl.OCC(N)(CO)CO QKNYBSVHEMOAJP-UHFFFAOYSA-N 0.000 description 1
- 125000002941 2-furyl group Chemical group O1C([*])=C([H])C([H])=C1[H] 0.000 description 1
- 125000001494 2-propynyl group Chemical group [H]C#CC([H])([H])* 0.000 description 1
- 125000000175 2-thienyl group Chemical group S1C([*])=C([H])C([H])=C1[H] 0.000 description 1
- VHMICKWLTGFITH-UHFFFAOYSA-N 2H-isoindole Chemical compound C1=CC=CC2=CNC=C21 VHMICKWLTGFITH-UHFFFAOYSA-N 0.000 description 1
- WPWNEKFMGCWNPR-UHFFFAOYSA-N 3,4-dihydro-2h-thiochromene Chemical compound C1=CC=C2CCCSC2=C1 WPWNEKFMGCWNPR-UHFFFAOYSA-N 0.000 description 1
- FPQQSJJWHUJYPU-UHFFFAOYSA-N 3-(dimethylamino)propyliminomethylidene-ethylazanium;chloride Chemical compound Cl.CCN=C=NCCCN(C)C FPQQSJJWHUJYPU-UHFFFAOYSA-N 0.000 description 1
- ICASMSGEUGPHGI-UHFFFAOYSA-N 3-amino-1h-pyrazole-5-carboxylic acid Chemical compound NC=1C=C(C(O)=O)NN=1 ICASMSGEUGPHGI-UHFFFAOYSA-N 0.000 description 1
- 125000005917 3-methylpentyl group Chemical group 0.000 description 1
- UJJLDDNKCAHWIT-UHFFFAOYSA-N 4-pyrimidin-2-ylpiperazine-1-carbaldehyde Chemical compound C1CN(C=O)CCN1C1=NC=CC=N1 UJJLDDNKCAHWIT-UHFFFAOYSA-N 0.000 description 1
- QDMPMBFLXOWHRY-UHFFFAOYSA-N 5-(4-methylpiperazin-1-yl)pyridin-2-amine Chemical compound C1CN(C)CCN1C1=CC=C(N)N=C1 QDMPMBFLXOWHRY-UHFFFAOYSA-N 0.000 description 1
- JPBRHMIVZVUWCZ-UHFFFAOYSA-N 5-pyrrolidin-1-ylpyridin-2-amine Chemical compound C1=NC(N)=CC=C1N1CCCC1 JPBRHMIVZVUWCZ-UHFFFAOYSA-N 0.000 description 1
- FWLUWMPAKXGNKH-UHFFFAOYSA-N 7-(3,4-dimethoxyphenyl)-n-(2-ethoxyphenyl)pyrazolo[1,5-a]pyrimidine-2-carboxamide Chemical compound CCOC1=CC=CC=C1NC(=O)C1=NN2C(C=3C=C(OC)C(OC)=CC=3)=CC=NC2=C1 FWLUWMPAKXGNKH-UHFFFAOYSA-N 0.000 description 1
- SUOWEWGYOSSWKU-UHFFFAOYSA-N 7-(3,4-dimethoxyphenyl)-n-(3,5-dimethylphenyl)pyrazolo[1,5-a]pyrimidine-2-carboxamide Chemical compound C1=C(OC)C(OC)=CC=C1C1=CC=NC2=CC(C(=O)NC=3C=C(C)C=C(C)C=3)=NN12 SUOWEWGYOSSWKU-UHFFFAOYSA-N 0.000 description 1
- UYJBNLRABLFIRG-UHFFFAOYSA-N 7-(3,4-dimethoxyphenyl)-n-(3-ethylphenyl)pyrazolo[1,5-a]pyrimidine-2-carboxamide Chemical compound CCC1=CC=CC(NC(=O)C2=NN3C(C=4C=C(OC)C(OC)=CC=4)=CC=NC3=C2)=C1 UYJBNLRABLFIRG-UHFFFAOYSA-N 0.000 description 1
- BBTZOOKFDQBYSH-UHFFFAOYSA-N 7-(3,4-dimethoxyphenyl)-n-(4-ethoxyphenyl)pyrazolo[1,5-a]pyrimidine-2-carboxamide Chemical compound C1=CC(OCC)=CC=C1NC(=O)C1=NN2C(C=3C=C(OC)C(OC)=CC=3)=CC=NC2=C1 BBTZOOKFDQBYSH-UHFFFAOYSA-N 0.000 description 1
- KRPXAJUUDCDVSQ-UHFFFAOYSA-N 7-(3,4-dimethoxyphenyl)-n-(4-ethylphenyl)pyrazolo[1,5-a]pyrimidine-2-carboxamide Chemical compound C1=CC(CC)=CC=C1NC(=O)C1=NN2C(C=3C=C(OC)C(OC)=CC=3)=CC=NC2=C1 KRPXAJUUDCDVSQ-UHFFFAOYSA-N 0.000 description 1
- AKBXBSKRZDRPIY-UHFFFAOYSA-N 7-(3,4-dimethoxyphenyl)-n-(4-methylphenyl)pyrazolo[1,5-a]pyrimidine-2-carboxamide Chemical compound C1=C(OC)C(OC)=CC=C1C1=CC=NC2=CC(C(=O)NC=3C=CC(C)=CC=3)=NN12 AKBXBSKRZDRPIY-UHFFFAOYSA-N 0.000 description 1
- OAJSNNHETXPTFH-UHFFFAOYSA-N 7-(3,4-dimethoxyphenyl)-n-(4-propan-2-ylphenyl)pyrazolo[1,5-a]pyrimidine-2-carboxamide Chemical compound C1=C(OC)C(OC)=CC=C1C1=CC=NC2=CC(C(=O)NC=3C=CC(=CC=3)C(C)C)=NN12 OAJSNNHETXPTFH-UHFFFAOYSA-N 0.000 description 1
- OFLMNCVUXVELKH-UHFFFAOYSA-N 7-(4-fluorophenyl)-n-(2-methoxyphenyl)pyrazolo[1,5-a]pyrimidine-2-carboxamide Chemical compound COC1=CC=CC=C1NC(=O)C1=NN2C(C=3C=CC(F)=CC=3)=CC=NC2=C1 OFLMNCVUXVELKH-UHFFFAOYSA-N 0.000 description 1
- ANEONEBHEZRYDD-UHFFFAOYSA-N 7-(4-fluorophenyl)-n-(2-methylphenyl)pyrazolo[1,5-a]pyrimidine-2-carboxamide Chemical compound CC1=CC=CC=C1NC(=O)C1=NN2C(C=3C=CC(F)=CC=3)=CC=NC2=C1 ANEONEBHEZRYDD-UHFFFAOYSA-N 0.000 description 1
- BZZANVFZCNVVIB-UHFFFAOYSA-N 7-(4-fluorophenyl)-n-(3-methoxyphenyl)pyrazolo[1,5-a]pyrimidine-2-carboxamide Chemical compound COC1=CC=CC(NC(=O)C2=NN3C(C=4C=CC(F)=CC=4)=CC=NC3=C2)=C1 BZZANVFZCNVVIB-UHFFFAOYSA-N 0.000 description 1
- GPKPSRSHLBWZBK-UHFFFAOYSA-N 7-(4-fluorophenyl)-n-(3-methylphenyl)pyrazolo[1,5-a]pyrimidine-2-carboxamide Chemical compound CC1=CC=CC(NC(=O)C2=NN3C(C=4C=CC(F)=CC=4)=CC=NC3=C2)=C1 GPKPSRSHLBWZBK-UHFFFAOYSA-N 0.000 description 1
- CIEMKBMBKIPXSH-UHFFFAOYSA-N 7-(4-methylphenyl)-n-(2,4,6-trimethylphenyl)pyrazolo[1,5-a]pyrimidine-2-carboxamide Chemical compound C1=CC(C)=CC=C1C1=CC=NC2=CC(C(=O)NC=3C(=CC(C)=CC=3C)C)=NN12 CIEMKBMBKIPXSH-UHFFFAOYSA-N 0.000 description 1
- JRLTTZUODKEYDH-UHFFFAOYSA-N 8-methylquinoline Chemical group C1=CN=C2C(C)=CC=CC2=C1 JRLTTZUODKEYDH-UHFFFAOYSA-N 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 1
- APKFDSVGJQXUKY-KKGHZKTASA-N Amphotericin-B Natural products O[C@H]1[C@@H](N)[C@H](O)[C@@H](C)O[C@H]1O[C@H]1C=CC=CC=CC=CC=CC=CC=C[C@H](C)[C@@H](O)[C@@H](C)[C@H](C)OC(=O)C[C@H](O)C[C@H](O)CC[C@@H](O)[C@H](O)C[C@H](O)C[C@](O)(C[C@H](O)[C@H]2C(O)=O)O[C@H]2C1 APKFDSVGJQXUKY-KKGHZKTASA-N 0.000 description 1
- 206010003645 Atopy Diseases 0.000 description 1
- 239000005711 Benzoic acid Substances 0.000 description 1
- 241000283690 Bos taurus Species 0.000 description 1
- 206010006458 Bronchitis chronic Diseases 0.000 description 1
- BGGALFIXXQOTPY-NRFANRHFSA-N C1(=C(C2=C(C=C1)N(C(C#N)=C2)C[C@@H](N1CCN(CC1)S(=O)(=O)C)C)C)CN1CCC(CC1)NC1=NC(=NC2=C1C=C(S2)CC(F)(F)F)NC Chemical compound C1(=C(C2=C(C=C1)N(C(C#N)=C2)C[C@@H](N1CCN(CC1)S(=O)(=O)C)C)C)CN1CCC(CC1)NC1=NC(=NC2=C1C=C(S2)CC(F)(F)F)NC BGGALFIXXQOTPY-NRFANRHFSA-N 0.000 description 1
- 125000004399 C1-C4 alkenyl group Chemical group 0.000 description 1
- 125000006374 C2-C10 alkenyl group Chemical group 0.000 description 1
- 238000011740 C57BL/6 mouse Methods 0.000 description 1
- 125000000041 C6-C10 aryl group Chemical group 0.000 description 1
- 125000005915 C6-C14 aryl group Chemical group 0.000 description 1
- LYLRDHCFGWPWQU-UHFFFAOYSA-N CC(C)(C)OC(N(CC1)CCC1NC(C1=NN2C(C(C=C3OC)=CC=C3OC)=CC=NC2=C1)=O)=O Chemical compound CC(C)(C)OC(N(CC1)CCC1NC(C1=NN2C(C(C=C3OC)=CC=C3OC)=CC=NC2=C1)=O)=O LYLRDHCFGWPWQU-UHFFFAOYSA-N 0.000 description 1
- SSUSWJVBQSZBDO-UHFFFAOYSA-N CC(C)(C)OC(N(CC1)CCN1C(C1=NN2C(C(C=C3OC)=CC=C3OC)=CC=NC2=C1)=O)=O Chemical compound CC(C)(C)OC(N(CC1)CCN1C(C1=NN2C(C(C=C3OC)=CC=C3OC)=CC=NC2=C1)=O)=O SSUSWJVBQSZBDO-UHFFFAOYSA-N 0.000 description 1
- JBUQETCUEFIUEH-UHFFFAOYSA-N CC(C)(C)OC(NC(C1)CN1C(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O)=O Chemical compound CC(C)(C)OC(NC(C1)CN1C(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O)=O JBUQETCUEFIUEH-UHFFFAOYSA-N 0.000 description 1
- DELICMPOPRTRBV-UHFFFAOYSA-N CC(C)(C)OC(NC(CC1)CCN1C(C1=NN2C(C(C=C3OC)=CC=C3OC)=CC=NC2=C1)=O)=O Chemical compound CC(C)(C)OC(NC(CC1)CCN1C(C1=NN2C(C(C=C3OC)=CC=C3OC)=CC=NC2=C1)=O)=O DELICMPOPRTRBV-UHFFFAOYSA-N 0.000 description 1
- KKIGPRQDYHUBNZ-MRXNPFEDSA-N CC(C)(C)OC(N[C@H](CC1)CN1C(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O)=O Chemical compound CC(C)(C)OC(N[C@H](CC1)CN1C(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O)=O KKIGPRQDYHUBNZ-MRXNPFEDSA-N 0.000 description 1
- JKSAWVWIOQPDDF-UHFFFAOYSA-N CC(C)(C)[Si](C)(C)OC(C=C1)=CC=C1NC(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O Chemical compound CC(C)(C)[Si](C)(C)OC(C=C1)=CC=C1NC(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O JKSAWVWIOQPDDF-UHFFFAOYSA-N 0.000 description 1
- PCYDHXFTWMZNOU-UHFFFAOYSA-N CC(C)(C1)NCCN1C(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O Chemical compound CC(C)(C1)NCCN1C(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O PCYDHXFTWMZNOU-UHFFFAOYSA-N 0.000 description 1
- ILARLEHBLFUZDA-UHFFFAOYSA-N CC(C)N(CC1)CCN1C(C(C=C1)=CC=C1NC(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O)=O Chemical compound CC(C)N(CC1)CCN1C(C(C=C1)=CC=C1NC(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O)=O ILARLEHBLFUZDA-UHFFFAOYSA-N 0.000 description 1
- NBNYINGKBBWILI-UHFFFAOYSA-N CC(C)N(CC1)CCN1C(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O Chemical compound CC(C)N(CC1)CCN1C(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O NBNYINGKBBWILI-UHFFFAOYSA-N 0.000 description 1
- SCNGGZFMLIDFBC-UHFFFAOYSA-N CC(NC(C=C1)=CC=C1NC(C1=NN2C(C3=CC=CC=C3)=CC=NC2=C1)=O)=O Chemical compound CC(NC(C=C1)=CC=C1NC(C1=NN2C(C3=CC=CC=C3)=CC=NC2=C1)=O)=O SCNGGZFMLIDFBC-UHFFFAOYSA-N 0.000 description 1
- MNCPQSAKAJTBTE-UHFFFAOYSA-N CCOC(C1(CC1)NC(C1=NN2C(C(C=C3OC)=CC=C3OC)=CC=NC2=C1)=O)=O Chemical compound CCOC(C1(CC1)NC(C1=NN2C(C(C=C3OC)=CC=C3OC)=CC=NC2=C1)=O)=O MNCPQSAKAJTBTE-UHFFFAOYSA-N 0.000 description 1
- LOVAJNWDCXMPCF-UHFFFAOYSA-N CCOC(C=C1)=CC=C1NC(NC1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O Chemical compound CCOC(C=C1)=CC=C1NC(NC1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O LOVAJNWDCXMPCF-UHFFFAOYSA-N 0.000 description 1
- YQQNTTWKMIBPEV-UHFFFAOYSA-N CCOC(COC(C=C1)=CC=C1NC(C1=NN2C(C(C=C3OC)=CC=C3OC)=CC=NC2=C1)=O)=O Chemical compound CCOC(COC(C=C1)=CC=C1NC(C1=NN2C(C(C=C3OC)=CC=C3OC)=CC=NC2=C1)=O)=O YQQNTTWKMIBPEV-UHFFFAOYSA-N 0.000 description 1
- LOVOEEJCFJLYGN-VOTSOKGWSA-N CN(C)/C=C/C(C(C=C1)=CC(OC)=C1F)=O Chemical compound CN(C)/C=C/C(C(C=C1)=CC(OC)=C1F)=O LOVOEEJCFJLYGN-VOTSOKGWSA-N 0.000 description 1
- DNHPHOUVZWEYEV-UHFFFAOYSA-N CN(CC1)CCN1C(C(C=C1)=CC(F)=C1NC(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O)=O Chemical compound CN(CC1)CCN1C(C(C=C1)=CC(F)=C1NC(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O)=O DNHPHOUVZWEYEV-UHFFFAOYSA-N 0.000 description 1
- CAMTYXBHCCSCFE-UHFFFAOYSA-N CN(CC1)CCN1C(C(CC1)(CC2)CCC12NC(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O)=O Chemical compound CN(CC1)CCN1C(C(CC1)(CC2)CCC12NC(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O)=O CAMTYXBHCCSCFE-UHFFFAOYSA-N 0.000 description 1
- OXSIHKLUARHEGD-UHFFFAOYSA-N CN(CC1)CCN1C(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O Chemical compound CN(CC1)CCN1C(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O OXSIHKLUARHEGD-UHFFFAOYSA-N 0.000 description 1
- GVVCTYNWAMLSSG-UHFFFAOYSA-N CN(CC1)CCN1C(C=C1)=CN=C1NC(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O Chemical compound CN(CC1)CCN1C(C=C1)=CN=C1NC(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O GVVCTYNWAMLSSG-UHFFFAOYSA-N 0.000 description 1
- QZCPXJNHNVHSNF-UHFFFAOYSA-N COC(C(C=C1)=CC(Cl)=C1NC(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O)=O Chemical compound COC(C(C=C1)=CC(Cl)=C1NC(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O)=O QZCPXJNHNVHSNF-UHFFFAOYSA-N 0.000 description 1
- VCBVQEYVZLCGJF-UHFFFAOYSA-N COC(C(C=C1)=CC(F)=C1NC(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O)=O Chemical compound COC(C(C=C1)=CC(F)=C1NC(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O)=O VCBVQEYVZLCGJF-UHFFFAOYSA-N 0.000 description 1
- IPNGAWAXRSPHQT-UHFFFAOYSA-N COC(C(C=C1)=CC(O)=C1NC(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O)=O Chemical compound COC(C(C=C1)=CC(O)=C1NC(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O)=O IPNGAWAXRSPHQT-UHFFFAOYSA-N 0.000 description 1
- ZLNBWTQCAXUQJD-UHFFFAOYSA-N COC(C(C=C1)=CC(OC)=C1NC(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O)=O Chemical compound COC(C(C=C1)=CC(OC)=C1NC(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O)=O ZLNBWTQCAXUQJD-UHFFFAOYSA-N 0.000 description 1
- DQLLBRMROWFMSY-UHFFFAOYSA-N COC(C(C=C1)=CC=C1NC(C1=NN2C(C(C=C3)=CC=C3OC)=CC=NC2=C1)=O)=O Chemical compound COC(C(C=C1)=CC=C1NC(C1=NN2C(C(C=C3)=CC=C3OC)=CC=NC2=C1)=O)=O DQLLBRMROWFMSY-UHFFFAOYSA-N 0.000 description 1
- BUYRNPMCROETBA-UHFFFAOYSA-N COC(C(C=C1)=CC=C1NC(C1=NN2C(C(C=C3Cl)=CC=C3Cl)=CC=NC2=C1)=O)=O Chemical compound COC(C(C=C1)=CC=C1NC(C1=NN2C(C(C=C3Cl)=CC=C3Cl)=CC=NC2=C1)=O)=O BUYRNPMCROETBA-UHFFFAOYSA-N 0.000 description 1
- LXGLCMHESCQZMA-UHFFFAOYSA-N COC(C(C=C1)=CC=C1NC(C1=NN2C(C(C=C3Cl)=CC=C3OC)=CC=NC2=C1)=O)=O Chemical compound COC(C(C=C1)=CC=C1NC(C1=NN2C(C(C=C3Cl)=CC=C3OC)=CC=NC2=C1)=O)=O LXGLCMHESCQZMA-UHFFFAOYSA-N 0.000 description 1
- OEQWSCVJXMVXFL-UHFFFAOYSA-N COC(C(C=C1)=CC=C1NC(NC1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O)=O Chemical compound COC(C(C=C1)=CC=C1NC(NC1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O)=O OEQWSCVJXMVXFL-UHFFFAOYSA-N 0.000 description 1
- UXGIQNYMIMQYSM-UHFFFAOYSA-N COC(C(C=CC(NC(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O)=C1)=C1Cl)=O Chemical compound COC(C(C=CC(NC(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O)=C1)=C1Cl)=O UXGIQNYMIMQYSM-UHFFFAOYSA-N 0.000 description 1
- NEOVNZCTKOYCPL-UHFFFAOYSA-N COC(C(C=CC(NC(C1=NN2C(C(C=C3OC)=CC=C3OC)=CC=NC2=C1)=O)=C1)=C1O)=O Chemical compound COC(C(C=CC(NC(C1=NN2C(C(C=C3OC)=CC=C3OC)=CC=NC2=C1)=O)=C1)=C1O)=O NEOVNZCTKOYCPL-UHFFFAOYSA-N 0.000 description 1
- MNNSBOSDPDDTOD-UHFFFAOYSA-N COC(C(C=CC=C1)=C1NC(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O)=O Chemical compound COC(C(C=CC=C1)=C1NC(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O)=O MNNSBOSDPDDTOD-UHFFFAOYSA-N 0.000 description 1
- CUSVRXPOCPDRGR-UHFFFAOYSA-N COC(C(CC1)(CC2)CCC12NC(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O)=O Chemical compound COC(C(CC1)(CC2)CCC12NC(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O)=O CUSVRXPOCPDRGR-UHFFFAOYSA-N 0.000 description 1
- BAYMHSRLYALBOD-UHFFFAOYSA-N COC(C(OC)=C1)=CC=C1C1=CC=NC2=CC(C(NC(C=C3)=CC=C3C(N3CCOCC3)=O)=O)=NN12 Chemical compound COC(C(OC)=C1)=CC=C1C1=CC=NC2=CC(C(NC(C=C3)=CC=C3C(N3CCOCC3)=O)=O)=NN12 BAYMHSRLYALBOD-UHFFFAOYSA-N 0.000 description 1
- OQQMKYVBOMTNAH-UHFFFAOYSA-N COC(C(OC)=C1)=CC=C1C1=CC=NC2=CC(C(NC(C=C3)=NC=C3C(OCC3=CC=CC=C3)=O)=O)=NN12 Chemical compound COC(C(OC)=C1)=CC=C1C1=CC=NC2=CC(C(NC(C=C3)=NC=C3C(OCC3=CC=CC=C3)=O)=O)=NN12 OQQMKYVBOMTNAH-UHFFFAOYSA-N 0.000 description 1
- KUQUDJJVPLTAIG-UHFFFAOYSA-N COC(C(OC)=C1)=CC=C1C1=CC=NC2=CC(C(NC3=CC=CC=C3)=O)=NN12 Chemical compound COC(C(OC)=C1)=CC=C1C1=CC=NC2=CC(C(NC3=CC=CC=C3)=O)=NN12 KUQUDJJVPLTAIG-UHFFFAOYSA-N 0.000 description 1
- SPSWEHPPQXFOIC-UHFFFAOYSA-N COC(C(OC)=C1)=CC=C1C1=CC=NC2=CC(C(NC3CCNCC3)=O)=NN12 Chemical compound COC(C(OC)=C1)=CC=C1C1=CC=NC2=CC(C(NC3CCNCC3)=O)=NN12 SPSWEHPPQXFOIC-UHFFFAOYSA-N 0.000 description 1
- KOQUVXYNNPZMFC-UHFFFAOYSA-N COC(C1=CC=C(CNC(C2=NN3C(C(C=C4)=CC(OC)=C4OC)=CC=NC3=C2)=O)C=C1)=O Chemical compound COC(C1=CC=C(CNC(C2=NN3C(C(C=C4)=CC(OC)=C4OC)=CC=NC3=C2)=O)C=C1)=O KOQUVXYNNPZMFC-UHFFFAOYSA-N 0.000 description 1
- NJZQHYAMMLPOBD-UHFFFAOYSA-N COC(C1=NN2C(C(C=CC(OC)=C3)=C3F)=CC=NC2=C1)=O Chemical compound COC(C1=NN2C(C(C=CC(OC)=C3)=C3F)=CC=NC2=C1)=O NJZQHYAMMLPOBD-UHFFFAOYSA-N 0.000 description 1
- RJKWYHWRJDFHCD-UHFFFAOYSA-N COC(C=CC(C1=CC=NC2=CC(C(N(CC3)CCN3C(C3CC3)=O)=O)=NN12)=C1)=C1OC Chemical compound COC(C=CC(C1=CC=NC2=CC(C(N(CC3)CCN3C(C3CC3)=O)=O)=NN12)=C1)=C1OC RJKWYHWRJDFHCD-UHFFFAOYSA-N 0.000 description 1
- ZHNDPTNLCMKPSV-UHFFFAOYSA-N COC(C=CC(C1=CC=NC2=CC(C(N(CC3)CCN3C3=CC=CC=C3)=O)=NN12)=C1)=C1OC Chemical compound COC(C=CC(C1=CC=NC2=CC(C(N(CC3)CCN3C3=CC=CC=C3)=O)=NN12)=C1)=C1OC ZHNDPTNLCMKPSV-UHFFFAOYSA-N 0.000 description 1
- ZBCCLSVGXMXQMM-UHFFFAOYSA-N COC(C=CC(C1=CC=NC2=CC(C(N(CC3)CCN3C3=NC=CC=N3)=O)=NN12)=C1)=C1OC Chemical compound COC(C=CC(C1=CC=NC2=CC(C(N(CC3)CCN3C3=NC=CC=N3)=O)=NN12)=C1)=C1OC ZBCCLSVGXMXQMM-UHFFFAOYSA-N 0.000 description 1
- KSUVSKFKVGQFLA-UHFFFAOYSA-N COC(C=CC(C1=CC=NC2=CC(C(N(CC3)CCN3C3CC3)=O)=NN12)=C1)=C1OC Chemical compound COC(C=CC(C1=CC=NC2=CC(C(N(CC3)CCN3C3CC3)=O)=NN12)=C1)=C1OC KSUVSKFKVGQFLA-UHFFFAOYSA-N 0.000 description 1
- XOSZMLXGNQWHSS-UHFFFAOYSA-N COC(C=CC(C1=CC=NC2=CC(C(N3CCNCC3)=O)=NN12)=C1)=C1OC Chemical compound COC(C=CC(C1=CC=NC2=CC(C(N3CCNCC3)=O)=NN12)=C1)=C1OC XOSZMLXGNQWHSS-UHFFFAOYSA-N 0.000 description 1
- ZLQWHCFHFWYZIN-UHFFFAOYSA-N COC(C=CC(C1=CC=NC2=CC(C(NC(C=C3)=CC=C3N3CCOCC3)=O)=NN12)=C1)=C1OC Chemical compound COC(C=CC(C1=CC=NC2=CC(C(NC(C=C3)=CC=C3N3CCOCC3)=O)=NN12)=C1)=C1OC ZLQWHCFHFWYZIN-UHFFFAOYSA-N 0.000 description 1
- HAOGJKOMJPWJDF-UHFFFAOYSA-N COC(C=CC(C1=CC=NC2=CC(C(NC(C=C3)=CC=C3O)=O)=NN12)=C1)=C1OC Chemical compound COC(C=CC(C1=CC=NC2=CC(C(NC(C=C3)=CC=C3O)=O)=NN12)=C1)=C1OC HAOGJKOMJPWJDF-UHFFFAOYSA-N 0.000 description 1
- AJRYTPNAVBLXIW-UHFFFAOYSA-N COC(C=CC(C1=CC=NC2=CC(C(NC(C=C3)=CC=C3OCCN3CCOCC3)=O)=NN12)=C1)=C1OC Chemical compound COC(C=CC(C1=CC=NC2=CC(C(NC(C=C3)=CC=C3OCCN3CCOCC3)=O)=NN12)=C1)=C1OC AJRYTPNAVBLXIW-UHFFFAOYSA-N 0.000 description 1
- HQLDEPZGTCTJBP-UHFFFAOYSA-N COC(C=CC(C1=CC=NC2=CC(C(NC(C=C3)=NC=C3N3CCCC3)=O)=NN12)=C1)=C1OC Chemical compound COC(C=CC(C1=CC=NC2=CC(C(NC(C=C3)=NC=C3N3CCCC3)=O)=NN12)=C1)=C1OC HQLDEPZGTCTJBP-UHFFFAOYSA-N 0.000 description 1
- DDMKLRKPUUHDSP-UHFFFAOYSA-N COC(C=CC(C1=CC=NC2=CC(C(NC(C=CC(C(O)=O)=C3)=C3F)=O)=NN12)=C1)=C1OC Chemical compound COC(C=CC(C1=CC=NC2=CC(C(NC(C=CC(C(O)=O)=C3)=C3F)=O)=NN12)=C1)=C1OC DDMKLRKPUUHDSP-UHFFFAOYSA-N 0.000 description 1
- SEWCFMDWKLNXFW-UHFFFAOYSA-N COC(C=CC(C1=CC=NC2=CC(C(NC(CC3)(CC4)CCC34C(O)=O)=O)=NN12)=C1)=C1OC Chemical compound COC(C=CC(C1=CC=NC2=CC(C(NC(CC3)(CC4)CCC34C(O)=O)=O)=NN12)=C1)=C1OC SEWCFMDWKLNXFW-UHFFFAOYSA-N 0.000 description 1
- ZBJRHRHSLCTPSO-UHFFFAOYSA-N COC(C=CC(C1=CC=NC2=CC(C(NC3(CC3)C(O)=O)=O)=NN12)=C1)=C1OC Chemical compound COC(C=CC(C1=CC=NC2=CC(C(NC3(CC3)C(O)=O)=O)=NN12)=C1)=C1OC ZBJRHRHSLCTPSO-UHFFFAOYSA-N 0.000 description 1
- SOWYMYUCPHXSPF-UHFFFAOYSA-N COC(C=CC(C1=CC=NC2=CC(C(NC3CCCCC3)=O)=NN12)=C1)=C1OC Chemical compound COC(C=CC(C1=CC=NC2=CC(C(NC3CCCCC3)=O)=NN12)=C1)=C1OC SOWYMYUCPHXSPF-UHFFFAOYSA-N 0.000 description 1
- TWLDBZDMRYTNDK-UHFFFAOYSA-N COC(C=CC(C1=CC=NC2=CC(C(NCC(C=C3)=CC=C3N3CCOCC3)=O)=NN12)=C1)=C1OC Chemical compound COC(C=CC(C1=CC=NC2=CC(C(NCC(C=C3)=CC=C3N3CCOCC3)=O)=NN12)=C1)=C1OC TWLDBZDMRYTNDK-UHFFFAOYSA-N 0.000 description 1
- JLMAJNOAQPTKMO-ZDUSSCGKSA-N C[C@@H](C1)NCCN1C(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O Chemical compound C[C@@H](C1)NCCN1C(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O JLMAJNOAQPTKMO-ZDUSSCGKSA-N 0.000 description 1
- JLMAJNOAQPTKMO-CYBMUJFWSA-N C[C@H](C1)NCCN1C(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O Chemical compound C[C@H](C1)NCCN1C(C1=NN2C(C(C=C3)=CC(OC)=C3OC)=CC=NC2=C1)=O JLMAJNOAQPTKMO-CYBMUJFWSA-N 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- KXDHJXZQYSOELW-UHFFFAOYSA-M Carbamate Chemical compound NC([O-])=O KXDHJXZQYSOELW-UHFFFAOYSA-M 0.000 description 1
- OKTJSMMVPCPJKN-NJFSPNSNSA-N Carbon-14 Chemical compound [14C] OKTJSMMVPCPJKN-NJFSPNSNSA-N 0.000 description 1
- 244000201986 Cassia tora Species 0.000 description 1
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 1
- 206010008631 Cholera Diseases 0.000 description 1
- 208000029767 Congenital, Hereditary, and Neonatal Diseases and Abnormalities Diseases 0.000 description 1
- 229920002261 Corn starch Polymers 0.000 description 1
- XFXPMWWXUTWYJX-UHFFFAOYSA-N Cyanide Chemical compound N#[C-] XFXPMWWXUTWYJX-UHFFFAOYSA-N 0.000 description 1
- 201000003883 Cystic fibrosis Diseases 0.000 description 1
- CYCGRDQQIOGCKX-UHFFFAOYSA-N Dehydro-luciferin Natural products OC(=O)C1=CSC(C=2SC3=CC(O)=CC=C3N=2)=N1 CYCGRDQQIOGCKX-UHFFFAOYSA-N 0.000 description 1
- OKKJLVBELUTLKV-MZCSYVLQSA-N Deuterated methanol Chemical compound [2H]OC([2H])([2H])[2H] OKKJLVBELUTLKV-MZCSYVLQSA-N 0.000 description 1
- ZAFNJMIOTHYJRJ-UHFFFAOYSA-N Diisopropyl ether Chemical compound CC(C)OC(C)C ZAFNJMIOTHYJRJ-UHFFFAOYSA-N 0.000 description 1
- YTPLMLYBLZKORZ-UHFFFAOYSA-N Divinylene sulfide Natural products C=1C=CSC=1 YTPLMLYBLZKORZ-UHFFFAOYSA-N 0.000 description 1
- YCAGGFXSFQFVQL-UHFFFAOYSA-N Endothion Chemical compound COC1=COC(CSP(=O)(OC)OC)=CC1=O YCAGGFXSFQFVQL-UHFFFAOYSA-N 0.000 description 1
- 241000283086 Equidae Species 0.000 description 1
- 241000282326 Felis catus Species 0.000 description 1
- BJGNCJDXODQBOB-UHFFFAOYSA-N Fivefly Luciferin Natural products OC(=O)C1CSC(C=2SC3=CC(O)=CC=C3N=2)=N1 BJGNCJDXODQBOB-UHFFFAOYSA-N 0.000 description 1
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 1
- 230000005526 G1 to G0 transition Effects 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Natural products NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 1
- 239000004471 Glycine Substances 0.000 description 1
- 239000007821 HATU Substances 0.000 description 1
- 229910004373 HOAc Inorganic materials 0.000 description 1
- 241000238631 Hexapoda Species 0.000 description 1
- 239000004233 Indanthrene blue RS Substances 0.000 description 1
- SIKJAQJRHWYJAI-UHFFFAOYSA-N Indole Chemical compound C1=CC=C2NC=CC2=C1 SIKJAQJRHWYJAI-UHFFFAOYSA-N 0.000 description 1
- 206010061218 Inflammation Diseases 0.000 description 1
- 108090000862 Ion Channels Proteins 0.000 description 1
- 102000004310 Ion Channels Human genes 0.000 description 1
- 239000004395 L-leucine Substances 0.000 description 1
- STECJAGHUSJQJN-USLFZFAMSA-N LSM-4015 Chemical compound C1([C@@H](CO)C(=O)OC2C[C@@H]3N([C@H](C2)[C@@H]2[C@H]3O2)C)=CC=CC=C1 STECJAGHUSJQJN-USLFZFAMSA-N 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- DDWFXDSYGUXRAY-UHFFFAOYSA-N Luciferin Natural products CCc1c(C)c(CC2NC(=O)C(=C2C=C)C)[nH]c1Cc3[nH]c4C(=C5/NC(CC(=O)O)C(C)C5CC(=O)O)CC(=O)c4c3C DDWFXDSYGUXRAY-UHFFFAOYSA-N 0.000 description 1
- 108010052285 Membrane Proteins Proteins 0.000 description 1
- 102000018697 Membrane Proteins Human genes 0.000 description 1
- LFZAGIJXANFPFN-UHFFFAOYSA-N N-[3-[4-(3-methyl-5-propan-2-yl-1,2,4-triazol-4-yl)piperidin-1-yl]-1-thiophen-2-ylpropyl]acetamide Chemical compound C(C)(C)C1=NN=C(N1C1CCN(CC1)CCC(C=1SC=CC=1)NC(C)=O)C LFZAGIJXANFPFN-UHFFFAOYSA-N 0.000 description 1
- 150000001204 N-oxides Chemical class 0.000 description 1
- 208000036110 Neuroinflammatory disease Diseases 0.000 description 1
- 208000025966 Neurological disease Diseases 0.000 description 1
- 101100030361 Neurospora crassa (strain ATCC 24698 / 74-OR23-1A / CBS 708.71 / DSM 1257 / FGSC 987) pph-3 gene Proteins 0.000 description 1
- 206010052143 Ocular discomfort Diseases 0.000 description 1
- 208000030053 Opioid-Induced Constipation Diseases 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 208000016222 Pancreatic disease Diseases 0.000 description 1
- 208000037273 Pathologic Processes Diseases 0.000 description 1
- 229910002666 PdCl2 Inorganic materials 0.000 description 1
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 1
- 201000001263 Psoriatic Arthritis Diseases 0.000 description 1
- 208000036824 Psoriatic arthropathy Diseases 0.000 description 1
- WTKZEGDFNFYCGP-UHFFFAOYSA-N Pyrazole Chemical class C=1C=NNC=1 WTKZEGDFNFYCGP-UHFFFAOYSA-N 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- KEAYESYHFKHZAL-UHFFFAOYSA-N Sodium Chemical compound [Na] KEAYESYHFKHZAL-UHFFFAOYSA-N 0.000 description 1
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 1
- 101000585507 Solanum tuberosum Cytochrome b-c1 complex subunit 7 Proteins 0.000 description 1
- 235000021355 Stearic acid Nutrition 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- 230000029662 T-helper 1 type immune response Effects 0.000 description 1
- 210000001744 T-lymphocyte Anatomy 0.000 description 1
- 206010047571 Visual impairment Diseases 0.000 description 1
- 208000016807 X-linked intellectual disability-macrocephaly-macroorchidism syndrome Diseases 0.000 description 1
- SJZAPSHKTOTRBQ-UHFFFAOYSA-N [dimethylamino(triazolo[4,5-b]pyridin-1-yl)methylidene]-dimethylazanium Chemical group C1=CC=C2[N+](=C(N(C)C)N(C)C)N=NC2=N1 SJZAPSHKTOTRBQ-UHFFFAOYSA-N 0.000 description 1
- CSCPPACGZOOCGX-WFGJKAKNSA-N acetone d6 Chemical compound [2H]C([2H])([2H])C(=O)C([2H])([2H])[2H] CSCPPACGZOOCGX-WFGJKAKNSA-N 0.000 description 1
- 239000004480 active ingredient Substances 0.000 description 1
- 125000002015 acyclic group Chemical group 0.000 description 1
- 230000003044 adaptive effect Effects 0.000 description 1
- 239000003463 adsorbent Substances 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 150000001340 alkali metals Chemical class 0.000 description 1
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 1
- 150000001336 alkenes Chemical class 0.000 description 1
- 125000005741 alkyl alkenyl group Chemical group 0.000 description 1
- 125000001118 alkylidene group Chemical group 0.000 description 1
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 1
- 230000001668 ameliorated effect Effects 0.000 description 1
- 125000003368 amide group Chemical group 0.000 description 1
- APKFDSVGJQXUKY-INPOYWNPSA-N amphotericin B Chemical compound O[C@H]1[C@@H](N)[C@H](O)[C@@H](C)O[C@H]1O[C@H]1/C=C/C=C/C=C/C=C/C=C/C=C/C=C/[C@H](C)[C@@H](O)[C@@H](C)[C@H](C)OC(=O)C[C@H](O)C[C@H](O)CC[C@@H](O)[C@H](O)C[C@H](O)C[C@](O)(C[C@H](O)[C@H]2C(O)=O)O[C@H]2C1 APKFDSVGJQXUKY-INPOYWNPSA-N 0.000 description 1
- 229960003942 amphotericin b Drugs 0.000 description 1
- 125000002178 anthracenyl group Chemical group C1(=CC=CC2=CC3=CC=CC=C3C=C12)* 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 230000000181 anti-adherent effect Effects 0.000 description 1
- 239000003911 antiadherent Substances 0.000 description 1
- 229940088710 antibiotic agent Drugs 0.000 description 1
- 230000000890 antigenic effect Effects 0.000 description 1
- 239000004599 antimicrobial Substances 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 125000003785 benzimidazolyl group Chemical group N1=C(NC2=C1C=CC=C2)* 0.000 description 1
- 125000004603 benzisoxazolyl group Chemical group O1N=C(C2=C1C=CC=C2)* 0.000 description 1
- 125000000499 benzofuranyl group Chemical group O1C(=CC2=C1C=CC=C2)* 0.000 description 1
- 235000010233 benzoic acid Nutrition 0.000 description 1
- 125000005874 benzothiadiazolyl group Chemical group 0.000 description 1
- 125000001164 benzothiazolyl group Chemical group S1C(=NC2=C1C=CC=C2)* 0.000 description 1
- 125000003354 benzotriazolyl group Chemical group N1N=NC2=C1C=CC=C2* 0.000 description 1
- 125000004541 benzoxazolyl group Chemical group O1C(=NC2=C1C=CC=C2)* 0.000 description 1
- KCXMKQUNVWSEMD-UHFFFAOYSA-N benzyl chloride Chemical compound ClCC1=CC=CC=C1 KCXMKQUNVWSEMD-UHFFFAOYSA-N 0.000 description 1
- 229940073608 benzyl chloride Drugs 0.000 description 1
- 125000000440 benzylamino group Chemical group [H]N(*)C([H])([H])C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- MKCBRYIXFFGIKN-UHFFFAOYSA-N bicyclo[1.1.1]pentane Chemical compound C1C2CC1C2 MKCBRYIXFFGIKN-UHFFFAOYSA-N 0.000 description 1
- PUNFICOCZAPAJV-UHFFFAOYSA-N bicyclo[2.2.2]octane-4-carboxylic acid Chemical compound C1CC2CCC1(C(=O)O)CC2 PUNFICOCZAPAJV-UHFFFAOYSA-N 0.000 description 1
- JAPMJSVZDUYFKL-UHFFFAOYSA-N bicyclo[3.1.0]hexane Chemical compound C1CCC2CC21 JAPMJSVZDUYFKL-UHFFFAOYSA-N 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 230000000903 blocking effect Effects 0.000 description 1
- 125000004106 butoxy group Chemical group [*]OC([H])([H])C([H])([H])C(C([H])([H])[H])([H])[H] 0.000 description 1
- FJDQFPXHSGXQBY-UHFFFAOYSA-L caesium carbonate Chemical compound [Cs+].[Cs+].[O-]C([O-])=O FJDQFPXHSGXQBY-UHFFFAOYSA-L 0.000 description 1
- 229910000024 caesium carbonate Inorganic materials 0.000 description 1
- 239000001506 calcium phosphate Substances 0.000 description 1
- 229910000389 calcium phosphate Inorganic materials 0.000 description 1
- 235000011010 calcium phosphates Nutrition 0.000 description 1
- 239000000378 calcium silicate Substances 0.000 description 1
- 229910052918 calcium silicate Inorganic materials 0.000 description 1
- CJZGTCYPCWQAJB-UHFFFAOYSA-L calcium stearate Chemical compound [Ca+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O CJZGTCYPCWQAJB-UHFFFAOYSA-L 0.000 description 1
- 239000008116 calcium stearate Substances 0.000 description 1
- 235000013539 calcium stearate Nutrition 0.000 description 1
- OYACROKNLOSFPA-UHFFFAOYSA-N calcium;dioxido(oxo)silane Chemical compound [Ca+2].[O-][Si]([O-])=O OYACROKNLOSFPA-UHFFFAOYSA-N 0.000 description 1
- 125000001951 carbamoylamino group Chemical group C(N)(=O)N* 0.000 description 1
- 150000001721 carbon Chemical group 0.000 description 1
- 238000001460 carbon-13 nuclear magnetic resonance spectrum Methods 0.000 description 1
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 1
- 210000000170 cell membrane Anatomy 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 238000000633 chiral stationary phase gas chromatography Methods 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- 208000007451 chronic bronchitis Diseases 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 229940125773 compound 10 Drugs 0.000 description 1
- 229940125782 compound 2 Drugs 0.000 description 1
- 238000007906 compression Methods 0.000 description 1
- 230000006835 compression Effects 0.000 description 1
- 239000000356 contaminant Substances 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 239000008120 corn starch Substances 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 230000008025 crystallization Effects 0.000 description 1
- 150000001924 cycloalkanes Chemical class 0.000 description 1
- 125000000596 cyclohexenyl group Chemical group C1(=CCCCC1)* 0.000 description 1
- 125000000640 cyclooctyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 125000003493 decenyl group Chemical group [H]C([*])=C([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 210000004443 dendritic cell Anatomy 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 150000001975 deuterium Chemical group 0.000 description 1
- 239000008121 dextrose Substances 0.000 description 1
- MQYQOVYIJOLTNX-UHFFFAOYSA-N dichloromethane;n,n-dimethylformamide Chemical group ClCCl.CN(C)C=O MQYQOVYIJOLTNX-UHFFFAOYSA-N 0.000 description 1
- 230000037213 diet Effects 0.000 description 1
- 230000000378 dietary effect Effects 0.000 description 1
- 239000012470 diluted sample Substances 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- LDCRTTXIJACKKU-ONEGZZNKSA-N dimethyl fumarate Chemical compound COC(=O)\C=C\C(=O)OC LDCRTTXIJACKKU-ONEGZZNKSA-N 0.000 description 1
- 239000007884 disintegrant Substances 0.000 description 1
- BNIILDVGGAEEIG-UHFFFAOYSA-L disodium hydrogen phosphate Chemical compound [Na+].[Na+].OP([O-])([O-])=O BNIILDVGGAEEIG-UHFFFAOYSA-L 0.000 description 1
- 229910000397 disodium phosphate Inorganic materials 0.000 description 1
- 235000019800 disodium phosphate Nutrition 0.000 description 1
- 239000002270 dispersing agent Substances 0.000 description 1
- 238000010494 dissociation reaction Methods 0.000 description 1
- 230000005593 dissociations Effects 0.000 description 1
- 238000009509 drug development Methods 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- 230000008482 dysregulation Effects 0.000 description 1
- 230000008030 elimination Effects 0.000 description 1
- 238000003379 elimination reaction Methods 0.000 description 1
- 238000010828 elution Methods 0.000 description 1
- 239000003623 enhancer Substances 0.000 description 1
- LJQKCYFTNDAAPC-UHFFFAOYSA-N ethanol;ethyl acetate Chemical compound CCO.CCOC(C)=O LJQKCYFTNDAAPC-UHFFFAOYSA-N 0.000 description 1
- 150000002170 ethers Chemical class 0.000 description 1
- 235000019439 ethyl acetate Nutrition 0.000 description 1
- 125000004494 ethyl ester group Chemical group 0.000 description 1
- 125000000219 ethylidene group Chemical group [H]C(=[*])C([H])([H])[H] 0.000 description 1
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 1
- 150000004665 fatty acids Chemical class 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- 239000000796 flavoring agent Substances 0.000 description 1
- 235000019634 flavors Nutrition 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- 239000007850 fluorescent dye Substances 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 235000003599 food sweetener Nutrition 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 239000003205 fragrance Substances 0.000 description 1
- 239000000417 fungicide Substances 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 235000001727 glucose Nutrition 0.000 description 1
- 125000005456 glyceride group Chemical group 0.000 description 1
- 150000002334 glycols Chemical class 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 210000003958 hematopoietic stem cell Anatomy 0.000 description 1
- 125000004404 heteroalkyl group Chemical group 0.000 description 1
- 125000004836 hexamethylene group Chemical group [H]C([H])([*:2])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[*:1] 0.000 description 1
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 238000000589 high-performance liquid chromatography-mass spectrometry Methods 0.000 description 1
- 230000036571 hydration Effects 0.000 description 1
- 238000006703 hydration reaction Methods 0.000 description 1
- BNRNAKTVFSZAFA-UHFFFAOYSA-N hydrindane Chemical compound C1CCCC2CCCC21 BNRNAKTVFSZAFA-UHFFFAOYSA-N 0.000 description 1
- XMBWDFGMSWQBCA-UHFFFAOYSA-N hydrogen iodide Chemical compound I XMBWDFGMSWQBCA-UHFFFAOYSA-N 0.000 description 1
- 230000007062 hydrolysis Effects 0.000 description 1
- 238000006460 hydrolysis reaction Methods 0.000 description 1
- 125000002632 imidazolidinyl group Chemical group 0.000 description 1
- 125000002883 imidazolyl group Chemical group 0.000 description 1
- 210000002865 immune cell Anatomy 0.000 description 1
- 230000036039 immunity Effects 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 125000003387 indolinyl group Chemical group N1(CCC2=CC=CC=C12)* 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- 230000004941 influx Effects 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 239000003112 inhibitor Substances 0.000 description 1
- 239000000976 ink Substances 0.000 description 1
- 150000007529 inorganic bases Chemical class 0.000 description 1
- 210000002490 intestinal epithelial cell Anatomy 0.000 description 1
- 210000002011 intestinal secretion Anatomy 0.000 description 1
- 238000010255 intramuscular injection Methods 0.000 description 1
- 239000007927 intramuscular injection Substances 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000001972 isopentyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000002183 isoquinolinyl group Chemical group C1(=NC=CC2=CC=CC=C12)* 0.000 description 1
- 125000000842 isoxazolyl group Chemical group 0.000 description 1
- ZLVXBBHTMQJRSX-VMGNSXQWSA-N jdtic Chemical compound C1([C@]2(C)CCN(C[C@@H]2C)C[C@H](C(C)C)NC(=O)[C@@H]2NCC3=CC(O)=CC=C3C2)=CC=CC(O)=C1 ZLVXBBHTMQJRSX-VMGNSXQWSA-N 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 229960003136 leucine Drugs 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 238000004811 liquid chromatography Methods 0.000 description 1
- 238000001294 liquid chromatography-tandem mass spectrometry Methods 0.000 description 1
- 239000012280 lithium aluminium hydride Substances 0.000 description 1
- 210000004185 liver Anatomy 0.000 description 1
- 208000019423 liver disease Diseases 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 210000004072 lung Anatomy 0.000 description 1
- 210000002540 macrophage Anatomy 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 230000001404 mediated effect Effects 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- 102000006240 membrane receptors Human genes 0.000 description 1
- 108020004084 membrane receptors Proteins 0.000 description 1
- 230000002503 metabolic effect Effects 0.000 description 1
- 229960004452 methionine Drugs 0.000 description 1
- WUKSVVOCYHTIMV-UHFFFAOYSA-N methyl 3-amino-1h-pyrazole-5-carboxylate Chemical compound COC(=O)C=1C=C(N)NN=1 WUKSVVOCYHTIMV-UHFFFAOYSA-N 0.000 description 1
- LCACMDQIVIBGNJ-UHFFFAOYSA-N methyl 3-aminobicyclo[1.1.1]pentane-1-carboxylate;hydrochloride Chemical compound Cl.C1C2(N)CC1(C(=O)OC)C2 LCACMDQIVIBGNJ-UHFFFAOYSA-N 0.000 description 1
- NKOHBUUCRADLQD-UHFFFAOYSA-N methyl 4-[[7-(3,4-dimethoxyphenyl)pyrazolo[1,5-a]pyrimidine-2-carbonyl]amino]benzoate Chemical compound C1=CC(C(=O)OC)=CC=C1NC(=O)C1=NN2C(C=3C=C(OC)C(OC)=CC=3)=CC=NC2=C1 NKOHBUUCRADLQD-UHFFFAOYSA-N 0.000 description 1
- DSHBGNPOIBSIOQ-UHFFFAOYSA-N methyl 4-amino-2-chlorobenzoate Chemical compound COC(=O)C1=CC=C(N)C=C1Cl DSHBGNPOIBSIOQ-UHFFFAOYSA-N 0.000 description 1
- DOMJYWCXCVFKCA-UHFFFAOYSA-N methyl 4-amino-3-fluorobenzoate Chemical compound COC(=O)C1=CC=C(N)C(F)=C1 DOMJYWCXCVFKCA-UHFFFAOYSA-N 0.000 description 1
- 150000004702 methyl esters Chemical class 0.000 description 1
- 125000000325 methylidene group Chemical group [H]C([H])=* 0.000 description 1
- 230000005012 migration Effects 0.000 description 1
- 238000013508 migration Methods 0.000 description 1
- 210000001616 monocyte Anatomy 0.000 description 1
- 125000006682 monohaloalkyl group Chemical group 0.000 description 1
- 235000019799 monosodium phosphate Nutrition 0.000 description 1
- 125000002757 morpholinyl group Chemical group 0.000 description 1
- 238000010172 mouse model Methods 0.000 description 1
- 230000000420 mucociliary effect Effects 0.000 description 1
- 210000003097 mucus Anatomy 0.000 description 1
- 230000035772 mutation Effects 0.000 description 1
- NLQJCGDLLVTQNL-UHFFFAOYSA-N n-(2,4-difluorophenyl)-7-(3,4-dimethoxyphenyl)pyrazolo[1,5-a]pyrimidine-2-carboxamide Chemical compound C1=C(OC)C(OC)=CC=C1C1=CC=NC2=CC(C(=O)NC=3C(=CC(F)=CC=3)F)=NN12 NLQJCGDLLVTQNL-UHFFFAOYSA-N 0.000 description 1
- LZQZVQXHGIZFBY-UHFFFAOYSA-N n-(2,4-difluorophenyl)-7-(4-fluorophenyl)pyrazolo[1,5-a]pyrimidine-2-carboxamide Chemical compound C1=CC(F)=CC=C1C1=CC=NC2=CC(C(=O)NC=3C(=CC(F)=CC=3)F)=NN12 LZQZVQXHGIZFBY-UHFFFAOYSA-N 0.000 description 1
- URDQEOGSWAPEJR-UHFFFAOYSA-N n-(2,5-difluorophenyl)-7-(4-fluorophenyl)pyrazolo[1,5-a]pyrimidine-2-carboxamide Chemical compound C1=CC(F)=CC=C1C1=CC=NC2=CC(C(=O)NC=3C(=CC=C(F)C=3)F)=NN12 URDQEOGSWAPEJR-UHFFFAOYSA-N 0.000 description 1
- LZOAHXBKJSWMKW-UHFFFAOYSA-N n-(2-ethoxyphenyl)-7-(4-fluorophenyl)pyrazolo[1,5-a]pyrimidine-2-carboxamide Chemical compound CCOC1=CC=CC=C1NC(=O)C1=NN2C(C=3C=CC(F)=CC=3)=CC=NC2=C1 LZOAHXBKJSWMKW-UHFFFAOYSA-N 0.000 description 1
- XVNADOMXCGYCTN-UHFFFAOYSA-N n-(2-fluorophenyl)-7-(4-fluorophenyl)pyrazolo[1,5-a]pyrimidine-2-carboxamide Chemical compound C1=CC(F)=CC=C1C1=CC=NC2=CC(C(=O)NC=3C(=CC=CC=3)F)=NN12 XVNADOMXCGYCTN-UHFFFAOYSA-N 0.000 description 1
- IQRDSJYMGRQOPQ-UHFFFAOYSA-N n-(3,4-dimethoxyphenyl)-7-(4-fluorophenyl)pyrazolo[1,5-a]pyrimidine-2-carboxamide Chemical compound C1=C(OC)C(OC)=CC=C1NC(=O)C1=NN2C(C=3C=CC(F)=CC=3)=CC=NC2=C1 IQRDSJYMGRQOPQ-UHFFFAOYSA-N 0.000 description 1
- VIYZNRMZYMOADR-UHFFFAOYSA-N n-(4-acetamidophenyl)-7-(4-fluorophenyl)pyrazolo[1,5-a]pyrimidine-2-carboxamide Chemical compound C1=CC(NC(=O)C)=CC=C1NC(=O)C1=NN2C(C=3C=CC(F)=CC=3)=CC=NC2=C1 VIYZNRMZYMOADR-UHFFFAOYSA-N 0.000 description 1
- XYGKWWWLULFUAH-UHFFFAOYSA-N n-(4-acetylphenyl)-7-(4-fluorophenyl)pyrazolo[1,5-a]pyrimidine-2-carboxamide Chemical compound C1=CC(C(=O)C)=CC=C1NC(=O)C1=NN2C(C=3C=CC(F)=CC=3)=CC=NC2=C1 XYGKWWWLULFUAH-UHFFFAOYSA-N 0.000 description 1
- GKYFSVYVUJVKFU-UHFFFAOYSA-N n-(4-ethoxyphenyl)-7-(4-fluorophenyl)pyrazolo[1,5-a]pyrimidine-2-carboxamide Chemical compound C1=CC(OCC)=CC=C1NC(=O)C1=NN2C(C=3C=CC(F)=CC=3)=CC=NC2=C1 GKYFSVYVUJVKFU-UHFFFAOYSA-N 0.000 description 1
- MHKPRPNYHHOKFA-UHFFFAOYSA-N n-(4-fluoro-2-methylphenyl)-7-(4-fluorophenyl)pyrazolo[1,5-a]pyrimidine-2-carboxamide Chemical compound CC1=CC(F)=CC=C1NC(=O)C1=NN2C(C=3C=CC(F)=CC=3)=CC=NC2=C1 MHKPRPNYHHOKFA-UHFFFAOYSA-N 0.000 description 1
- SXHGJDSINSZYRN-UHFFFAOYSA-N n-(4-methoxy-2-methylphenyl)-7-(4-methylphenyl)pyrazolo[1,5-a]pyrimidine-2-carboxamide Chemical compound CC1=CC(OC)=CC=C1NC(=O)C1=NN2C(C=3C=CC(C)=CC=3)=CC=NC2=C1 SXHGJDSINSZYRN-UHFFFAOYSA-N 0.000 description 1
- WQHNEODNNQVKLA-UHFFFAOYSA-N n-(5-fluoro-2-methylphenyl)-7-(4-fluorophenyl)pyrazolo[1,5-a]pyrimidine-2-carboxamide Chemical compound CC1=CC=C(F)C=C1NC(=O)C1=NN2C(C=3C=CC(F)=CC=3)=CC=NC2=C1 WQHNEODNNQVKLA-UHFFFAOYSA-N 0.000 description 1
- SYSQUGFVNFXIIT-UHFFFAOYSA-N n-[4-(1,3-benzoxazol-2-yl)phenyl]-4-nitrobenzenesulfonamide Chemical class C1=CC([N+](=O)[O-])=CC=C1S(=O)(=O)NC1=CC=C(C=2OC3=CC=CC=C3N=2)C=C1 SYSQUGFVNFXIIT-UHFFFAOYSA-N 0.000 description 1
- BZQLHWRZVKYXKJ-UHFFFAOYSA-N n-[4-(dimethylamino)phenyl]-7-(4-fluorophenyl)pyrazolo[1,5-a]pyrimidine-2-carboxamide Chemical compound C1=CC(N(C)C)=CC=C1NC(=O)C1=NN2C(C=3C=CC(F)=CC=3)=CC=NC2=C1 BZQLHWRZVKYXKJ-UHFFFAOYSA-N 0.000 description 1
- 125000004370 n-butenyl group Chemical group [H]\C([H])=C(/[H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000001280 n-hexyl group Chemical group C(CCCCC)* 0.000 description 1
- 125000000740 n-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 239000002105 nanoparticle Substances 0.000 description 1
- 125000001971 neopentyl group Chemical group [H]C([*])([H])C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 230000003959 neuroinflammation Effects 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 1
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 1
- 238000010606 normalization Methods 0.000 description 1
- 239000002773 nucleotide Substances 0.000 description 1
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 1
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 1
- 125000004365 octenyl group Chemical group C(=CCCCCCC)* 0.000 description 1
- 235000019198 oils Nutrition 0.000 description 1
- 229940126701 oral medication Drugs 0.000 description 1
- 150000007530 organic bases Chemical class 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- 125000002524 organometallic group Chemical group 0.000 description 1
- 125000002971 oxazolyl group Chemical group 0.000 description 1
- 125000003544 oxime group Chemical group 0.000 description 1
- 125000004430 oxygen atom Chemical group O* 0.000 description 1
- BHAAPTBBJKJZER-UHFFFAOYSA-N p-anisidine Chemical compound COC1=CC=C(N)C=C1 BHAAPTBBJKJZER-UHFFFAOYSA-N 0.000 description 1
- PIBWKRNGBLPSSY-UHFFFAOYSA-L palladium(II) chloride Chemical compound Cl[Pd]Cl PIBWKRNGBLPSSY-UHFFFAOYSA-L 0.000 description 1
- 208000024691 pancreas disease Diseases 0.000 description 1
- 230000001575 pathological effect Effects 0.000 description 1
- 230000009054 pathological process Effects 0.000 description 1
- 230000007170 pathology Effects 0.000 description 1
- 230000008823 permeabilization Effects 0.000 description 1
- 239000008196 pharmacological composition Substances 0.000 description 1
- NCAIGTHBQTXTLR-UHFFFAOYSA-N phentermine hydrochloride Chemical compound [Cl-].CC(C)([NH3+])CC1=CC=CC=C1 NCAIGTHBQTXTLR-UHFFFAOYSA-N 0.000 description 1
- 229960005190 phenylalanine Drugs 0.000 description 1
- 125000002467 phosphate group Chemical group [H]OP(=O)(O[H])O[*] 0.000 description 1
- 239000011574 phosphorus Substances 0.000 description 1
- 208000024335 physical disease Diseases 0.000 description 1
- 125000004193 piperazinyl group Chemical group 0.000 description 1
- 125000003386 piperidinyl group Chemical group 0.000 description 1
- 208000030761 polycystic kidney disease Diseases 0.000 description 1
- 229940068918 polyethylene glycol 400 Drugs 0.000 description 1
- 125000006684 polyhaloalkyl group Polymers 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 229910000027 potassium carbonate Inorganic materials 0.000 description 1
- 238000011533 pre-incubation Methods 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 102000004196 processed proteins & peptides Human genes 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 229960002429 proline Drugs 0.000 description 1
- 125000004368 propenyl group Chemical group C(=CC)* 0.000 description 1
- 238000011321 prophylaxis Methods 0.000 description 1
- 125000006412 propinylene group Chemical group [H]C#CC([H])([H])* 0.000 description 1
- OSFBJERFMQCEQY-UHFFFAOYSA-N propylidene Chemical group [CH]CC OSFBJERFMQCEQY-UHFFFAOYSA-N 0.000 description 1
- 238000000159 protein binding assay Methods 0.000 description 1
- 238000000425 proton nuclear magnetic resonance spectrum Methods 0.000 description 1
- 230000005588 protonation Effects 0.000 description 1
- 230000002685 pulmonary effect Effects 0.000 description 1
- 208000005069 pulmonary fibrosis Diseases 0.000 description 1
- 125000000561 purinyl group Chemical group N1=C(N=C2N=CNC2=C1)* 0.000 description 1
- 125000003373 pyrazinyl group Chemical group 0.000 description 1
- 125000003226 pyrazolyl group Chemical group 0.000 description 1
- 125000002098 pyridazinyl group Chemical group 0.000 description 1
- 125000000714 pyrimidinyl group Chemical group 0.000 description 1
- 125000000719 pyrrolidinyl group Chemical group 0.000 description 1
- 125000002943 quinolinyl group Chemical group N1=C(C=CC2=CC=CC=C12)* 0.000 description 1
- 230000002285 radioactive effect Effects 0.000 description 1
- 239000000376 reactant Substances 0.000 description 1
- 230000035484 reaction time Effects 0.000 description 1
- 230000008707 rearrangement Effects 0.000 description 1
- 230000007115 recruitment Effects 0.000 description 1
- 238000001953 recrystallisation Methods 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 230000003938 response to stress Effects 0.000 description 1
- 230000002441 reversible effect Effects 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 238000007363 ring formation reaction Methods 0.000 description 1
- 125000006413 ring segment Chemical group 0.000 description 1
- 238000005070 sampling Methods 0.000 description 1
- 229960004499 scopolamine hydrobromide Drugs 0.000 description 1
- WTGQALLALWYDJH-MOUKNHLCSA-N scopolamine hydrobromide (anhydrous) Chemical compound Br.C1([C@@H](CO)C(=O)O[C@H]2C[C@@H]3N([C@H](C2)[C@@H]2[C@H]3O2)C)=CC=CC=C1 WTGQALLALWYDJH-MOUKNHLCSA-N 0.000 description 1
- 230000000580 secretagogue effect Effects 0.000 description 1
- 230000003248 secreting effect Effects 0.000 description 1
- 230000028327 secretion Effects 0.000 description 1
- 229960001153 serine Drugs 0.000 description 1
- 239000000741 silica gel Substances 0.000 description 1
- 229910002027 silica gel Inorganic materials 0.000 description 1
- AJPJDKMHJJGVTQ-UHFFFAOYSA-M sodium dihydrogen phosphate Chemical compound [Na+].OP(O)([O-])=O AJPJDKMHJJGVTQ-UHFFFAOYSA-M 0.000 description 1
- 239000012312 sodium hydride Substances 0.000 description 1
- 235000009518 sodium iodide Nutrition 0.000 description 1
- 229910000162 sodium phosphate Inorganic materials 0.000 description 1
- 229910052938 sodium sulfate Inorganic materials 0.000 description 1
- 235000011152 sodium sulphate Nutrition 0.000 description 1
- 239000008117 stearic acid Substances 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 229960005322 streptomycin Drugs 0.000 description 1
- 238000010254 subcutaneous injection Methods 0.000 description 1
- 239000007929 subcutaneous injection Substances 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 125000000472 sulfonyl group Chemical group *S(*)(=O)=O 0.000 description 1
- 239000011593 sulfur Substances 0.000 description 1
- 125000004434 sulfur atom Chemical group 0.000 description 1
- 239000004173 sunset yellow FCF Substances 0.000 description 1
- 239000003765 sweetening agent Substances 0.000 description 1
- 239000000454 talc Substances 0.000 description 1
- 229910052623 talc Inorganic materials 0.000 description 1
- 235000012222 talc Nutrition 0.000 description 1
- 125000004213 tert-butoxy group Chemical group [H]C([H])([H])C(O*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- DATRVIMZZZVHMP-QMMMGPOBSA-N tert-butyl (2s)-2-methylpiperazine-1-carboxylate Chemical compound C[C@H]1CNCCN1C(=O)OC(C)(C)C DATRVIMZZZVHMP-QMMMGPOBSA-N 0.000 description 1
- BCNZYOJHNLTNEZ-UHFFFAOYSA-N tert-butyldimethylsilyl chloride Chemical compound CC(C)(C)[Si](C)(C)Cl BCNZYOJHNLTNEZ-UHFFFAOYSA-N 0.000 description 1
- FPGGTKZVZWFYPV-UHFFFAOYSA-M tetrabutylammonium fluoride Chemical compound [F-].CCCC[N+](CCCC)(CCCC)CCCC FPGGTKZVZWFYPV-UHFFFAOYSA-M 0.000 description 1
- 125000003831 tetrazolyl group Chemical group 0.000 description 1
- 229940124597 therapeutic agent Drugs 0.000 description 1
- 125000001113 thiadiazolyl group Chemical group 0.000 description 1
- 125000004568 thiomorpholinyl group Chemical group 0.000 description 1
- 229930192474 thiophene Natural products 0.000 description 1
- 150000003577 thiophenes Chemical class 0.000 description 1
- 210000001685 thyroid gland Anatomy 0.000 description 1
- 238000003354 tissue distribution assay Methods 0.000 description 1
- 238000011200 topical administration Methods 0.000 description 1
- 230000000699 topical effect Effects 0.000 description 1
- 238000000844 transformation Methods 0.000 description 1
- 230000032258 transport Effects 0.000 description 1
- 125000001425 triazolyl group Chemical group 0.000 description 1
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 1
- 230000006433 tumor necrosis factor production Effects 0.000 description 1
- 229960004295 valine Drugs 0.000 description 1
- PXXNTAGJWPJAGM-UHFFFAOYSA-N vertaline Natural products C1C2C=3C=C(OC)C(OC)=CC=3OC(C=C3)=CC=C3CCC(=O)OC1CC1N2CCCC1 PXXNTAGJWPJAGM-UHFFFAOYSA-N 0.000 description 1
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 1
- 229920002554 vinyl polymer Polymers 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/04—Ortho-condensed systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/519—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim ortho- or peri-condensed with heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
- A61K31/5375—1,4-Oxazines, e.g. morpholine
- A61K31/5377—1,4-Oxazines, e.g. morpholine not condensed and containing further heterocyclic rings, e.g. timolol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/06—Antipsoriatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D519/00—Heterocyclic compounds containing more than one system of two or more relevant hetero rings condensed among themselves or condensed with a common carbocyclic ring system not provided for in groups C07D453/00 or C07D455/00
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Medicinal Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Dermatology (AREA)
- Rheumatology (AREA)
- Pain & Pain Management (AREA)
- Ophthalmology & Optometry (AREA)
- Epidemiology (AREA)
- Pulmonology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Nitrogen And Oxygen Or Sulfur-Condensed Heterocyclic Ring Systems (AREA)
- Medicinal Preparation (AREA)
Abstract
本發明提供CFTR調節劑化合物及包括該等化合物之組合物。本發明亦提供抑制PDE4之化合物及包括該等化合物之組合物。本發明亦提供使用該等化合物及組合物調節CFTR之方法、治療眼部疾病或疾患之方法及治療CFTR相關適應症之方法。本發明亦提供使用該等化合物及組合物抑制PDE4、治療發炎性疾病或疾患及治療其他PDE4相關適應症之方法。本發明亦提供該等化合物及組合物之製備方法,及該等化合物之合成前體。
Description
本發明係關於CFTR調節劑化合物及包括該等化合物之組合物。本發明亦係關於抑制PDE4之化合物及包括該等化合物之組合物。本發明亦係關於該等化合物及組合物之醫學用途及製備方法,及該等化合物之合成前體。
囊腫纖維化跨膜傳導調節蛋白(CFTR)係一種由CFTR基因編碼之膜蛋白且編碼引導氯離子跨細胞膜之ABC轉運蛋白類離子通道蛋白。CFTR基因之某些突變可對氯離子通道功能產生不利影響,導致許多器官(諸如肺及胰臟)中上皮流體轉運之失調,導致囊腫纖維化。此外,野生型CFTR蛋白可由直接活化機制調節,但其不適當之活化可導致分泌性腹瀉(諸如霍亂)。
野生型CFTR之活化劑受關注以在臨床適應症中用於便祕及乾眼症之促分泌療法及用於肝、胰臟及呼吸道疾患。CFTR抑制劑受關注以治療某些分泌性腹瀉及多囊腎病。
磷酸二酯酶4 (PDE4)係負責水解環磷酸腺苷(cAMP)之關鍵酶,該環磷酸腺苷係控制多種促發炎及抗發炎介體之細胞內信使。增加之細胞內cAMP量可由PDE4之抑制產生,且藉由阻斷免疫細胞之募集及促發炎介體之釋放而具有顯著抗發炎效應。造血細胞(諸如樹突細胞、T細胞、巨噬細胞及單核細胞)受PDE4控制。
本發明提供CFTR調節劑化合物及包括該等化合物之組合物。本發明亦提供使用該等化合物及組合物調節CFTR之方法、用於治療眼部疾病或疾患之方法及用於治療CFTR相關適應症之方法。本發明亦提供抑制PDE4之化合物及包括該等化合物之組合物。在一些實施例中,本發明之PDE4抑制劑化合物係可活化目標CFTR之抗發炎化合物。本發明亦提供使用該等化合物及組合物抑制PDE4、治療發炎性疾病或疾患及治療PDE4相關適應症之方法。本發明亦提供該等化合物及組合物之製備方法,及該等化合物之合成前體。
在第一態樣中,本發明提供一種式(Ia)化合物:
,
或其醫藥上可接受之鹽、溶劑化物、水合物、前藥或立體異構體,其中:
R
1係選自H、鹵素、視需要經取代之芳基、視需要經取代之(C
1-C
10)烷基及視需要經取代之(C
1-C
10)烷氧基;
R
2係選自H、視需要經取代之(C
1-C
10)烷基、視需要經取代之環烷基、視需要經取代之芳基、視需要經取代之雜芳基及視需要經取代之雜環,及芳基、雜芳基及雜環上之任選取代基係獨立地選自:H、OH、NH
2、NO
2、OCF
3、CF
3、-鹵素、視需要經取代之胺基、視需要經取代之(C
1-C
5)烷基及視需要經取代之(C
1-C
5)烷氧基;
R
4係選自
、
及
;
R
5及R
6係獨立地選自H、視需要經取代之(C
1-C
10)烷基、視需要經取代之(C
1-C
10)烯基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之單環或雙環碳環及視需要經取代之單環或雙環雜環;
或R
5及R
6連同其等結合之氮原子一起環狀連接以形成視需要經取代之單環或雙環雜環;
R
7係選自NR
5R
6、視需要經取代之(C
1-C
10)烷基、視需要經取代之(C
1-C
10)烷氧基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基及視需要經取代之雜環烷基;
R
8係選自H及視需要經取代之(C
1-C
10)烷基;及
R
9係選自H及鹵素。
在第二態樣中,本發明提供一種醫藥組合物,該醫藥組合物包含化合物(例如,如本文描述,式(Ia)至(Ie)化合物)或其醫藥上可接受之鹽、溶劑化物、水合物、前藥或立體異構體及醫藥上可接受之賦形劑。在一些實施例中,該醫藥組合物係眼科組合物。
在第三態樣中,本發明提供一種調節囊腫纖維化跨膜傳導調節蛋白(CFTR)之方法,其包括使包括目標CFTR之樣本或生物系統與有效量調節CFTR之化合物(例如,如本文描述,式(Ia)至(Ie)化合物),或其醫藥上可接受之鹽、溶劑化物、水合物、前藥或立體異構體接觸,以調節CFTR。
在第四態樣中,本發明提供一種活化囊腫纖維化跨膜傳導調節蛋白(CFTR)之方法,對受試者投與治療有效量調節CFTR之化合物(例如,如本文描述,式(Ia)至(Ie)化合物),或如本文描述之眼科組合物(例如,如本文描述,包括式(Ia)至(Ie)化合物之組合物)。
在第五態樣中,本發明提供一種抑制PDE4之方法,其包括使包括目標PDE4之樣本或生物系統與有效量之抑制PDE4之化合物(例如,如本文描述,式(Ia)至(Ie)化合物),或其醫藥上可接受之鹽、溶劑化物、水合物、前藥或立體異構體接觸,以抑制PDE4。
在第六態樣中,本發明提供一種治療乾眼症或CFTR相關適應症之方法,其包括對受試者之眼睛投與治療有效量之如本文描述之化合物及/或眼科組合物(例如,如本文描述,包括式(Ia)至(Ie)化合物之組合物)。在一些實施例中,治療乾眼症之方法進一步包括鑑定罹患乾眼症之受試者,或鑑定與該乾眼症相關聯之潛在疾病或病症。在一些實施例中,該受試者可為患有乾眼症或症狀,或CFTR相關適應症之人類受試者。
在第七態樣中,本發明提供一種治療發炎性疾病或PDE4相關適應症之方法,其包括對受試者投與治療有效量之抑制PDE4之化合物(例如,如本文描述,式(Ia)至(Ie)化合物),或其醫藥上可接受之鹽、溶劑化物、水合物、前藥或立體異構體,或包括其之醫藥組合物。在一些實施例中,該受試者可為患有發炎性疾病或PDE4相關適應症之人類受試者。
相關申請案之交叉參考
本申請案主張2020年10月23日申請之美國臨時申請案第63/104,979號之權益,該案係以全文引用之方式併入本文中。
5.1. CFTR調節劑及/或PDE4抑制劑化合物
如上文總結,本發明提供用於調節CFTR之化合物及組合物。本發明亦提供用於抑制PDE4之化合物及組合物。在一些實施例中,本發明之化合物具有調節CFTR及/或抑制PDE4之活性。在一些實施例中,本發明之PDE4抑制劑化合物係可活化目標CFTR之抗發炎化合物。
在本發明之化合物中,含有吡唑并[1,5-a]嘧啶核心之化合物可於該核心結構之2位置經視需要經取代之芳基、視需要經取代之雜芳基及視需要經取代之雜環取代基取代、於該核心結構之5位置經鹵素取代、於該核心結構之6位置經鹵素、視需要經取代之芳基、視需要經取代之(C
1-C
10)烷基及視需要經取代之(C
1-C
10)烷氧基取代基取代,及於該核心結構之7位置經視需要經取代之芳基、視需要經取代之雜芳基及視需要經取代之雜環取代。在如本文描述之各種實施例中,該核心結構之一或多個位置之視需要經取代之取代基可視需要經進一步取代。具有如本文描述之此經取代之吡唑并[1,5-a]嘧啶核心結構之化合物可具有所需之調節CFTR及抑制PDE4之活性且發現可用於各種應用中。
因此,在第一態樣中,本發明提供一種式(Ia)化合物:
,
或其醫藥上可接受之鹽、溶劑化物、水合物、前藥或立體異構體,其中:
R
1係選自H、鹵素、視需要經取代之芳基、視需要經取代之(C
1-C
10)烷基及視需要經取代之(C
1-C
10)烷氧基;
R
2係選自視需要經取代之H、視需要經取代之(C
1-C
10)烷基、視需要經取代之環烷基、視需要經取代之芳基、視需要經取代之雜芳基及視需要經取代之雜環,及芳基、雜芳基及雜環上之任選取代基係獨立地選自:H、OH、NH
2、NO
2、OCF
3、CF
3、-鹵素、視需要經取代之胺基、視需要經取代之(C
1-C
5)烷基及視需要經取代之(C
1-C
5)烷氧基;
R
4係選自
、
及
;
R
5及R
6係獨立地選自H、視需要經取代之(C
1-C
10)烷基、視需要經取代之(C
1-C
10)烯基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之單環或雙環碳環及視需要經取代之單環或雙環雜環;或R
5及R
6連同其等結合之氮原子一起環狀連接以形成視需要經取代之單環或雙環雜環;
R
7係選自NR
5R
6、視需要經取代之(C
1-C
10)烷基、視需要經取代之(C
1-C
10)烷氧基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基及視需要經取代之雜環烷基;
R
8係選自H及視需要經取代之(C
1-C
10)烷基;及
R
9係選自H及鹵素。
在式(Ia)之一些實施例中,R
2係經取代之芳基。在某些情況下,R
2係單取代之芳基。在某些情況下,R
2係二取代之芳基。在某些情況下,R
2係三取代之芳基。在某些情況下,該二取代之芳基或該三取代之芳基中之取代基彼此相鄰。在某些情況下,該二取代之芳基係2,3-二取代之芳基。在某些情況下,該二取代之芳基係3,4-二取代之芳基。在某些情況下,該二取代之芳基係4,5-二取代之芳基。在某些情況下,該二取代之芳基係5,6-二取代之芳基。在某些情況下,該二取代之芳基係2,4-二取代之芳基。在某些情況下,該二取代之芳基係2,5-二取代之芳基。在某些情況下,該二取代之芳基係2,6-二取代之芳基。在某些情況下,該二取代之芳基係3,5-二取代之芳基。在某些情況下,該二取代之芳基係3,6-二取代之芳基。在某些情況下,該二取代之芳基係4,6-二取代之芳基。在某些情況下,該三取代之芳基係2,3,4-三取代之芳基。在某些情況下,該三取代之芳基係3,4,5-三取代之芳基。在某些情況下,該三取代之芳基係4,5,6-三取代之芳基。在某些情況下,該三取代之芳基係2,3,5-三取代之芳基。在某些情況下,該三取代之芳基係2,3,6-三取代之芳基。在某些情況下,該三取代之芳基係2,4,5-三取代之芳基。在某些情況下,該三取代之芳基係2,4,6-三取代之芳基。在某些情況下,該三取代之芳基係2,5,6-三取代之芳基。在某些情況下,該三取代之芳基係3,4,6-三取代之芳基。在某些情況下,該三取代之芳基係3,5,6-三取代之芳基。
在式(Ia)之一些實施例中,R
2係視需要經取代之雜芳基。在另一實施例中,R
2係選自視需要經取代之呋喃基(例如,2-呋喃基)及視需要經取代之噻吩(例如,2-噻吩基)。在另一實施例中,R
2係視需要經取代之苯并稠合雜環。
在式(Ia)之一些實施例中,R
2係視需要經取代之苯基或視需要經取代之雜芳基。在某些情況下,R
2係具有1至3個取代基之經取代之苯基或具有1至3個取代基之經取代之雜芳基。在某些情況下,R
2係3-取代之苯基。在某些情況下,R
2係4-取代之苯基。在某些情況下,R
2係二取代之苯基。在某些情況下,該二取代之苯基上之取代基彼此相鄰。在某些情況下,該二取代之苯基係2,3-二取代之苯基。在某些情況下,該二取代之苯基係3,4-二取代之苯基。在某些情況下,該二取代之苯基係4,5-二取代之苯基。在某些情況下,該二取代之苯基係5,6-二取代之苯基。在某些情況下,該二取代之苯基係2,4-二取代之苯基。在某些情況下,該二取代之苯基係2,5-二取代之苯基。在某些情況下,該二取代之苯基係2,6-二取代之苯基。在某些情況下,該二取代之苯基係3,5-二取代之苯基。在某些情況下,該二取代之苯基係3,6-二取代之苯基。在某些情況下,該二取代之苯基係4,6-二取代之苯基。在某些情況下,R
2係三取代之苯基。在某些情況下,該三取代之苯基係2,3,4-三取代之苯基。在某些情況下,該三取代之苯基係3,4,5-三取代之苯基。在某些情況下,該三取代之苯基係4,5,6-三取代之苯基。在某些情況下,該三取代之苯基係2,3,5-三取代之苯基。在某些情況下,該三取代之苯基係2,3,6-三取代之苯基。在某些情況下,該三取代之苯基係2,4,5-三取代之苯基。在某些情況下,該三取代之苯基係2,4,6-三取代之苯基。在某些情況下,該三取代之苯基係2,5,6-三取代之苯基。在某些情況下,該三取代之苯基係3,4,6-三取代之苯基。在某些情況下,該三取代之苯基係3,5,6-三取代之苯基。
在式(Ia)之一些實施例中,其中R
2係視需要經取代之苯基或視需要經取代之雜芳基,該化合物係式(Ib)化合物:
其中:
X
1係CR
10’或N;
R
1b係選自H、鹵素、視需要經取代之芳基、視需要經取代之(C
1-C
10)烷基及視需要經取代之(C
1-C
10)烷氧基;
R
4b係選自
、
及
;
R
5及R
6係獨立地選自H、視需要經取代之(C
1-C
10)烷基、視需要經取代之(C
1-C
10)烯基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之單環或雙環碳環及視需要經取代之單環或雙環雜環;或R
5及R
6連同其等結合之氮原子一起環狀連接以形成視需要經取代之單環或雙環雜環;
R
7係選自NR
5R
6、視需要經取代之(C
1-C
10)烷基、視需要經取代之(C
1-C
10)烷氧基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基及視需要經取代之雜環烷基;
R
8係選自H及視需要經取代之(C
1-C
10)烷基;
R
9b係選自H及鹵素;
各R
10及R
10’係獨立地選自H、OH、NH
2、NO
2、鹵素、視需要經取代之(C1-C6)烷基、視需要經取代之(C
1-C
6)烷氧基及經取代之胺基;及
n係0至4。
在式(Ib)化合物之一些實施例中,各R
10及R
10 ’係獨立地選自H、OH、CH
3、CF
3、OCF
3、OCH
3、NO
2、F、Cl及二甲胺。
在式(Ia)之一些實施例中,R
2係:
其中:
各R
100a至R
100c係獨立地選自H、OH、NH
2、NO
2、鹵素、視需要經取代之(C
1-C
6)烷基、視需要經取代之(C
1-C
6)烷氧基及經取代之胺基;及R
100a、R
100b及R
100c中之至少一者不為H。在某些實施例中,R
100a至R
100c係獨立地選自H、NO
2、鹵素、視需要經取代之(C
1-C
3)烷基及視需要經取代之(C
1-C
3)烷氧基。在某些實施例中,R
100a至R
100c中之各者係不同基團。在某些實施例中,R
100a至R
100c中之各者係不同且獨立地選自H、鹵素、NO
2、甲氧基及甲基。在某些實施例中,R
100a至R
100c中之各者係相同,且不為H。在某些情況下,R
100a至R
100c中之各者係(C
1-C
3)烷氧基。在某些情況下,R
100a至R
100c中之各者係甲氧基。在某些情況下,R
100a至R
100c中之兩者係(C
1-C
3)烷氧基,且R
100a至R
100c中之另一者係H。在某些情況下,R
100a至R
100c中之兩者係甲氧基,且R
100a至R
100c中之另一者係H。在某些情況下,R
100a及R
100b中之各者係(C
1-C
3)烷氧基,且R
100c係H。在某些情況下,R
100a及R
100b中之各者係甲氧基,且R
100c係H。
在式(Ib)之一些實施例中,化合物係式(Ic)化合物:
其中:
X
2係CR
10c’或N;
R
21係選自H及視需要經取代之(C
1-C
10)烷基;視需要經取代之醯基;視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之單環或雙環碳環及視需要經取代之單環或雙環雜環;
R
1c係選自H、鹵素、視需要經取代之芳基、視需要經取代之(C
1-C
10)烷基及視需要經取代之(C
1-C
10)烷氧基;
R
4c係選自
、
及
;
R
5及R
6係獨立地選自H、視需要經取代之(C
1-C
10)烷基、視需要經取代之(C
1-C
10)烯基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之單環或雙環碳環及視需要經取代之單環或雙環雜環;或R
5及R
6連同其等結合之氮原子一起環狀連接以形成視需要經取代之單環或雙環雜環;
R
7係選自NR
5R
6、視需要經取代之(C
1-C
10)烷基、視需要經取代之(C
1-C
10)烷氧基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基及視需要經取代之雜環烷基;
R
8係選自H及視需要經取代之(C
1-C
10)烷基;
R
9c係選自H及鹵素;
各R
10c及R
10c'係獨立地選自H、OH、NH
2、NO
2、鹵素、視需要經取代之(C
1-C
6)烷基、視需要經取代之(C
1-C
6)烷氧基及經取代之胺基;及
n係0至3。
在式(Ic)之一些實施例中,R
21係H或視需要經取代之(C
1-C
6)烷基。在式(Ic)之一些實施例中,R
21係(C
1-C
6)烷基。在式(Ic)之一些實施例中,R
21係甲基。
在式(Ic)之一些實施例中,-O-R
21係於對位連接至苯基環。在式(Ic)之一些實施例中,-O-R
21係於間位連接至苯基環。
在式(Ic)之某些實施例中,化合物係式(Id)化合物:
,
其中:
X
3係CR
10d ’或N;
各R
21d係獨立地選自H及視需要經取代之(C
1-C
10)烷基;視需要經取代之醯基;視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之單環或雙環碳環及視需要經取代之單環或雙環雜環;
R
1d係選自H、鹵素、視需要經取代之芳基、視需要經取代之(C
1-C
10)烷基及視需要經取代之(C
1-C
10)烷氧基;
R
4d係選自
、
及
;
R
5及R
6係獨立地選自H、視需要經取代之(C
1-C
10)烷基、視需要經取代之(C
1-C
10)烯基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之單環或雙環碳環及視需要經取代之單環或雙環雜環;
或R
5及R
6連同其等結合之氮原子一起環狀連接以形成視需要經取代之單環或雙環雜環;
R
7係選自NR
5R
6、視需要經取代之(C
1-C
10)烷基、視需要經取代之(C
1-C
10)烷氧基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基及視需要經取代之雜環烷基;
R
8係選自H及視需要經取代之(C
1-C
10)烷基;
R
9d係選自H及鹵素;
各R
10d及R
10d'係獨立地選自H、OH、NH
2、NO
2、鹵素、視需要經取代之(C
1-C
6)烷基、視需要經取代之(C
1-C
6)烷氧基及經取代之胺基;及
n係0至2。
在式(Id)之一些實施例中,各R
21d獨立地係H或視需要經取代之(C
1-C
6)烷基。在式(Id)之一些實施例中,各R
21d獨立地係(C
1-C
6)烷基。在式(Id)之一些實施例中,各R
21d係甲基。
在式(Id)之某些實施例中,X
3係CR
10d ’。在式(Id)之某些實施例中,X
3係CH。在式(Id)之某些實施例中,X
3係CR
10d ’,其中R
10d ’係-視需要經取代之(C
1-C
6)烷氧基。在式(Id)之某些實施例中,X
3係CR
10d ’,其中R
10d ’係-OCH
3。在式(Id)之某些實施例中,R
10d ’係-OCH
3及n係0。
在式(Id)之某些實施例中,X
3係N。
在式(Id)之某些實施例中,X
3係CR
10d ’。在式(Id)之某些實施例中,X
3係CR
10d ’,n係0。在式(Id)之某些實施例中,X
3係CR
10d ’,及n係1。在式(Id)之某些實施例中,當n係1或2時,各R
10d係獨立地選自鹵素及視需要經取代之(C
1-C
6)烷基。
在式(Id)之某些實施例中,各R
21d係視需要經取代之(C
1-C
6)烷基,X
3係CR
10d ’,n係0或1及R
10d及R
10d ’獨立地係視需要經取代之(C
1-C
6)烷基或鹵素。
在式(Id)之某些實施例中,各R
21d係甲基,X
3係CR
10d ’,其中R
10d ’係-OCH
3,及n係0。
在式(Id)之某些實施例中,各R
21d係視需要經取代之(C
1-C
6)烷基,X
3係CH,n係1及R
10d係視需要經取代之(C
1-C
6)烷基或鹵素。在式(Id)之某些實施例中,各R
21d係甲基,X
3係CH,及n係1,其中該R
10d係位於鄰位之甲基。
在式(Id)之一些實施例中,各R
21d係甲基,及n係0。
在式(Ia)至(Id)之一些實施例中,R
4至R
4d中之任一者係
。
在式(Ia)至(Id)之一些實施例中,R
5及R
6連同其等結合之氮原子一起環狀連接以提供視需要經取代之單環或雙環(C
4-C
10)雜環。
在式(Ia)至(Id)之一些實施例中,R
4至R
4d中之任一者係
其中:
環A係視需要經取代之單環或雙環(C
4-C
10)雜環;
Z
1係CR
14或N,其中R
14係選自H、OH、NH
2、CN、CF
3、OCF
3、CH
2NH
2、鹵素、視需要經取代之(C
1-C
5)烷基、視需要經取代之(C
1-C
5)烷氧基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之碳環及視需要經取代之雜環;及
R
16係選自H、鹵素、-OR
22a、-C(O)R
22b、-CO
2R
22c及-C(O)NR
50R
60、-NR
50R
60、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之碳環、視需要經取代之雜環、視需要經取代之(C
1-C
5)烷基及視需要經取代之(C
1-C
5)烷氧基;
R
22a、R
22b及R
22c係獨立地選自H、視需要經取代之(C
1-C
10)烷基、視需要經取代之環烷基、視需要經取代之芳基、視需要經取代之雜芳基及視需要經取代之雜環;及
R
50及R
60係獨立地選自H、視需要經取代之(C
1-C
10)烷基、視需要經取代之(C
1-C
10)烯基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之單環或雙環碳環及視需要經取代之單環或雙環雜環;
或R
50及R
60連同其等結合之氮原子一起環狀連接以形成視需要經取代之雜環或視需要經取代之雜芳基。
在式(Ia)至(Id)之一些實施例中,當R
4至R
4d中之任一者係
及A環係哌啶時,則R
16包含至少一個係選自視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之碳環、視需要經取代之雜環之環形基團。在某些情況下,該A環係哌啶及R
16包含視需要經取代之芳基。在某些情況下,該視需要經取代之芳基係視需要經取代之苯基。在某些情況下,該A環係哌啶及R
16包含視需要經取代之雜芳基。在某些情況下,該A環係哌啶及R
16包含視需要經取代之碳環。在某些情況下,該A環係哌啶及R
16包含視需要經取代之雜環。
在式(Ia)至(Id)之一些實施例中,當R
4至R
4d中之任一者係
時,A環係視需要經取代之哌嗪、吡咯啶或氮雜環丁烷。在某些情況下,該A環係:
其中:
R
23至R
26各係獨立地選自H、鹵素、OH、NO
2、OCF
3、CF
3、視需要經取代之胺基、視需要經取代之(C
1-C
6)烷基、視需要經取代之(C
1-C
6)烷氧基、視需要經取代之環烷基、視需要經取代之芳基、視需要經取代之雜芳基及視需要經取代之雜環;或
R
23至R
24及R
25至R
26中之一或兩者連同其等結合之碳原子一起環狀連接以形成視需要經取代之碳環或視需要經取代之雜環;及
R
40a及R
40b各係獨立地選自H、鹵素、OH、NO
2、OCF
3、CF
3、視需要經取代之胺基、視需要經取代之(C
1-C
6)烷基、視需要經取代之(C
1-C
6)烷氧基、視需要經取代之環烷基、視需要經取代之芳基、視需要經取代之雜芳基及視需要經取代之雜環。
在一些實施例中,R
23係選自視需要經取代之(C
1-C
6)烷基及視需要經取代之環烷基;及R
24至R
26、R
40a及R
40b各為H。在某些情況下,R
23係選自甲基、乙基、丙基、異丙基、丁基及第三丁基。在某些情況下,R
23係甲基。在某些情況下,R
23係乙基。在某些情況下,R
23係丙基。在某些情況下,R
23係異丙基。在一些實施例中,R
23係(C
1-C
6)環烷基。在某些情況下,R
23係環丙基。在某些情況下,R
23係環丁基。在某些情況下,R
23係環戊基。在某些情況下,R
23係環己基。
在A環之某些實施例中,R
23、R
25及R
40b中之兩者係獨立地選自視需要經取代之(C
1-C
6)烷基及視需要經取代之環烷基;及R
23、R
25及R
40b中之另一者係H及R
24、R
26及R
40a各為H。在A環之某些情況下,R
23、R
25及R
40b中之兩者係視需要經取代之(C
1-C
6)烷基。在A環之某些情況下,R
23、R
25及R
40b中之兩者各係獨立地選自甲基、乙基、丙基、異丙基、丁基及第三丁基。在A環之某些情況下,R
23、R
25及R
40b中之兩者係甲基。在A環之某些情況下,R
23、R
25及R
40b中之兩者係乙基。在某些情況下,R
23、R
25及R
40b中之兩者係丙基。在A環之某些情況下,R
23、R
25及R
40b中之兩者係異丙基。在A環之一些實施例中,R
23、R
25及R
40b中之兩者係(C
1-C
6)環烷基。在A環之某些情況下,R
23、R
25及R
40b中之兩者係環丙基。在某些情況下,R
23、R
25及R
40b中之兩者係環丁基。在A環之某些情況下,R
23、R
25及R
40b中之兩者係環戊基。在A環之某些情況下,R
23、R
25及R
40b中之兩者係環己基。
在A環之某些實施例中,R
23及R
25各係獨立地選自視需要經取代之(C
1-C
6)烷基及視需要經取代之環烷基;及R
24、R
26及R
40a至R
40b各為H。在A環之某些情況下,R
23及R
25均為視需要經取代之(C
1-C
6)烷基。在A環之某些情況下,R
23及R
25各係獨立地選自甲基、乙基、丙基、異丙基、丁基及第三丁基。在A環之某些情況下,R
23及R
25均為甲基。在A環之某些情況下,R
23及R
25均為乙基。在A環之某些情況下,R
23及R
25均為丙基。在A環之某些情況下,R
23及R
25均為異丙基。在A環之一些實施例中,R
23及R
25均為(C
1-C
6)環烷基。在A環之某些情況下,R
23及R
25均為環丙基。在某些情況下,R
23及R
25均為環丁基。在A環之某些情況下,R
23及R
25均為環戊基。在A環之某些情況下,R
23及R
25均為環己基。
在A環之某些實施例中,R
23及R
40b各係獨立地選自視需要經取代之(C
1-C
6)烷基及視需要經取代之環烷基;及R
24至R
26及R
40a各為H。在某些情況下,R
23及R
40b均為視需要經取代之(C
1-C
6)烷基。在某些情況下,R
23及R
40b各係獨立地選自甲基、乙基、丙基、異丙基、丁基及第三丁基。在某些情況下,R
23及R
40b均為甲基。在某些情況下,R
23及R
40b均為乙基。在某些情況下,R
23及R
40b均為丙基。在某些情況下,R
23及R
40b均為異丙基。在一些實施例中,R
23及R
40b均為(C
1-C
6)環烷基。在某些情況下,R
23及R
40b均為環丙基。在某些情況下,R
23及R
40b均為環丁基。在某些情況下,R
23及R
40b均為環戊基。在某些情況下,R
23及R
40b均為環己基。
在A環之某些實施例中,R
23及R
24各係獨立地選自視需要經取代之(C
1-C
6)烷基及視需要經取代之環烷基;及R
25至R
26、R
40a及R
40b各為H。在某些情況下,R
23及R
24均為視需要經取代之(C
1-C
6)烷基。在某些情況下,R
23及R
24各係獨立地選自甲基、乙基、丙基、異丙基、丁基及第三丁基。在某些情況下,R
23及R
24均為甲基。在某些情況下,R
23及R
24均為乙基。在某些情況下,R
23及R
24均為丙基。在某些情況下,R
23及R
25均為異丙基。在一些實施例中,R
23及R
24均為(C
1-C
6)環烷基。在某些情況下,R
23及R
24均為環丙基。在某些情況下,R
23及R
24均為環丁基。在某些情況下,R
23及R
24均為環戊基。在某些情況下,R
23及R
24均為環己基。
在A環之某些實施例中,R
23及R
24連同其等結合之碳原子一起環狀連接以形成碳環;及R
25至R
26、R
40a及R
40b各為H。在一些實施例中,R
23及R
24連同其等結合之碳原子一起環狀連接以形成(C
1-C
6)環烷基。在某些情況下,R
23及R
24連同其等結合之碳原子一起環狀連接以形成環丙基。在某些情況下,R
23及R
24連同其等結合之碳原子一起環狀連接以形成環丁基。在某些情況下,R
23及R
24連同其等結合之碳原子一起環狀連接以形成環戊基。在某些情況下,R
23及R
24連同其等結合之碳原子一起環狀連接以形成環己基。
在式(Ia)至(Id)之一些實施例中,當R
4至R
4d中之任一者係:
時,A環係選自:
、
、
、
、
、
、
、
、
、
、
及
。
在一些實施例中,R
16係選自H、鹵素、-OR
22a、-C(O)R
22b、-CO
2R
22c及-C(O)NR
50R
60、-NR
50R
60、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之碳環、視需要經取代之雜環、視需要經取代之(C
1-C
5)烷基及視需要經取代之(C
1-C
5)烷氧基,其中R
22a、R
22b、R
22c、R
50及R
60係如上文定義。
在式(Ia)至(Id)之一些實施例中,R
4至R
4d中之任一者係
,其中R
16係:
-(R
110)
nR
210其中:
各R
110係獨立地選自視需要經取代之(C
1-C
6)烷基、
、-C(O)(R
110a)n
1、-C(O)O(R
110b)n
2、-S(O)(R
110c)n
3、-SO
2(R
110d)n
4及-C(O)NR
27(R
110e)n
5;其中R
110a至R
110e各獨立地係視需要經取代之(C
1-C
6)烷基、
;R
27至R
28各係獨立地選自H及視需要經取代之(C
1-C
6)烷基;及n至n
5各獨立地係0至3;及
R
210係選自視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之碳環及視需要經取代之雜環。
在一些實施例中,R
110係選自-C(O)-、-C(O)O-、-C(O)NH-、-S(O)-及-SO
2-;及R
210係選自視需要經取代之芳基及視需要經取代之雜芳基。在某些實施例中,R
110係-C(O)-及R
210係視需要經取代之芳基。在某些實施例中,R
110係-C(O)O-及R
210係視需要經取代之芳基。在某些實施例中,R
110係-C(O)NH-及R
210係視需要經取代之芳基。在某些實施例中,R
110係-S(O)-及R
210係視需要經取代之芳基。在某些實施例中,R
110係-SO
2-及R
210係視需要經取代之芳基。在某些實施例中,R
110係-C(O)-及R
210係視需要經取代之雜芳基。在某些實施例中,R
110係-C(O)O-及R
210係視需要經取代之雜芳基。在某些實施例中,R
110係-C(O)NH-及R
210係視需要經取代之雜芳基。在某些實施例中,R
110係-S(O)-及R
210係視需要經取代之雜芳基。在某些情況下,R
110係-SO
2-及R
210係視需要經取代之雜芳基。
在一些實施例中,R
210係選自:
、
、
、
及
,其中:
X
4至X
7、X
9及X
11各係獨立地選自CH、CR
31、S、O及N;
X
8、X
10、X
12及X
13各係獨立地選自S、O及NR
29;
R
29係選自H及視需要經取代之(C
1-C
6)烷基;
R
30至R
32各係獨立地選自H、鹵素、OH、NO
2、OCF
3、CF
3、視需要經取代之胺基、視需要經取代之(C
1-C
6)烷基、視需要經取代之(C
1-C
6)烷氧基、視需要經取代之環烷基、視需要經取代之芳基、視需要經取代之雜芳基及視需要經取代之雜環;及
m
1至m
2各獨立地係0至5。
在一些實施例中,R
210係
,其中X
9係選自CH、CR
31、S、O及N;及X
8係選自S、O及NR
29。在某些情況下,R
29係甲基。在R
210的一些實施例中,X
9係CH、CR
31、S、O及N;及X
8係選自S、O及NR
29。在某些情況下,X
9係CH,及X
8係S。在某些情況下,R
30係H。在某些情況下,R
30係甲基。在一些實施例中,X
9係CH,X
8係S及R
30係H。在某些情況下,X
9係CH,X
8係NR
29及R
30係H。在某些情況下,X
9係CH,及X
8係NH。在某些情況下,X
9係CH,X
8係O及R
30係(C
1-C
6)烷基。在某些情況下,X
9係CH,X
8係O及R
30係甲基。
在一些實施例中,R
210係
,其中X
9係N,及X
8係選自S、O及NR
29。在某些情況下,X
8係NR
29。在某些情況下,R
29係H。在某些情況下,R
29係甲基。在某些情況下,X
8係O。在某些情況下,X
8係S。
在一些實施例中,R
210係
,其中X
10係選自S、O及NR
29。在某些情況下,X
10係O。在某些情況下,X
10係S。在某些情況下,X
10係NR
29,其中R
29係(C
1-C
6)烷基。在某些情況下,R
29係H。在某些情況下,R
29係甲基。
在一些實施例中,R
210係
,其中X
11係選自CH、CR
31、S、O及N,及X
12係選自S、O及NR
29。在某些情況下,X
11係N。在某些情況下,X
12係O或S。在某些情況下,X
11係N,及X
12係O。在某些情況下,X
11係N,及X
12係S。
在一些實施例中,R
210係
,其中X
13係選自S、O及NR
29。在某些情況下,X
13係NR
29。在某些情況下,R
29係H。在某些情況下,R
29係甲基。在某些情況下,X
13係S。在某些情況下,X
13係O。
在式(Ia)至(Id)之一些實施例中,R
4至R
4d中之任一者係選自:
,
其中:
各R
33係獨立地選自視需要經取代之(C
1-C
6)烷基及視需要經取代之環烷基。在某些情況下,各R
33係獨立地選自甲基、乙基、丙基、異丙基、丁基及第三丁基。在某些情況下,各R
33係甲基。在某些情況下,各R
33係乙基。在某些情況下,各R
33係丙基。在某些情況下,各R
33係異丙基。在一些實施例中,各R
33係獨立地選自(C
1-C
6)環烷基。在某些情況下,各R
33係環丙基。在某些情況下,各R
33係環丁基。在某些情況下,各R
33係環戊基。在某些情況下,各R
33係環己基。
在式(Ia)至(Id)之一些實施例中,R
4至R
4d中之任一者係
,R
5係H或Me及R
6係選自:
、
及
;其中:
Y
1、Y
2及Y
3係獨立地選自CR
14及N;
Z係選自O、S、CHR
11及nR
12;
n係0至4;
R
11係選自H、NH
2、CN、CH
2NH
2、NO
2、鹵素、OR
2a、C(O)R
2b、CO
2R
2c、C(O)NR
5R
6、視需要經取代之胺基、視需要經取代之(C
1-C
5)烷基及視需要經取代之(C
1-C
5)烷氧基,及視需要經取代之雜環;
R
12係選自H、NH
2、鹵素、C(O)R
2d、CO
2R
2e、C(O)NR
5R
6及視需要經取代之(C
1-C
5)烷基;
係選自視需要經取代之(C
1-C
6)烷基-環烷基、視需要經取代之雜環烷基、視需要經取代之單環或雙環(C
4-C
10)碳環,及視需要經取代之單環或雙環(C
4-C
10)雜環;
R
13係選自H、NH
2、CN、CH
2NH
2、NO
2、鹵素、OR
2f、C(O)R
2g、CO
2R
2h、C(O)NR
5R
6、NR
5R
6、視需要經取代之(C
1-C
5)烷基及視需要經取代之(C
1-C
5)烷氧基,及視需要經取代之雜環;
R
14係選自H、OH、NH
2、CN、CF
3、OCF
3、CH
2NH
2、鹵素、視需要經取代之(C
1-C
5)烷基、視需要經取代之(C
1-C
5)烷氧基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之碳環及視需要經取代之雜環;
R
15係選自H、鹵素、NHC(O)R
2i、OR
2j、C(O)R
2k、OC(O)R
2l、CO
2R
2m、C(O)NR
5R
6、NR
5R
6、視需要經取代之(C
1-C
5)烷基、視需要經取代之(C
1-C
5)烷氧基、視需要經取代之環烷基及視需要經取代之雜環;
R
20係選自H、鹵素、視需要經取代之(C
1-C
5)烷基、視需要經取代之(C
1-C
5)烷氧基、視需要經取代之碳環及視需要經取代之雜環;及
R
2a至R
2m係獨立地選自H、視需要經取代之(C
1-C
10)烷基、視需要經取代之環烷基、視需要經取代之芳基、視需要經取代之雜芳基及視需要經取代之雜環,及烷基、環烷基、芳基、雜芳基及雜環上之任選取代基係獨立地選自:H、OH、NH
2、NO
2、OCF
3、CF
3、-鹵素、雜環、雜芳基、視需要經取代之胺基、視需要經取代之(C
1-C
5)烷基及視需要經取代之(C
1-C
5)烷氧基。
在一些實施例中,R
6係選自:
,
其中:
環B及環C各係獨立地選自視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之碳環及視需要經取代之雜環;
各R
111係獨立地選自視需要經取代之(C
1-C
6)烷基、
、-C(O)(R
111a)p
1、-C(O)O(R
111b)p
2、-S(O)(R
111c)p
3、-SO
2(R
111d)p
4及-C(O)NR
27(R
111e)p
5;其中R
111a至R
111e各獨立地係視需要經取代之(C
1-C
6)烷基、
;
R
27至R
28各係獨立地選自H及視需要經取代之(C
1-C
6)烷基;及
p至p
5各獨立地係0至3。
在R
6之一些實施例中,R
111係選自-C(O)-、-C(O)O-、-C(O)NH-、-S(O)-及-SO
2-;及B環及C環係獨立地選自視需要經取代之芳基、視需要經取代之碳環、視需要經取代之雜芳基及視需要經取代之雜環。在某些實施例中,R
111係-C(O)-且該B環及該C環中之一或兩者係視需要經取代之芳基。R
111係-C(O)O-且該B環及該C環中之一或兩者係視需要經取代之芳基。R
111係-C(O)NH-且該B環及該C環中之一或兩者係視需要經取代之芳基。R
111係-S(O)-且該B環及該C環中之一或兩者係視需要經取代之芳基。在某些實施例中,R
111係-SO
2-且該B環及該C環中之一或兩者係視需要經取代之芳基。在某些實施例中,R
111係-C(O)-且該B環及該C環中之一或兩者係視需要經取代之碳環。R
111係-C(O)O-且該B環及該C環中之一或兩者係視需要經取代之碳環。R
111係-C(O)NH-且該B環及該C環中之一或兩者係視需要經取代之碳環。R
111係-S(O)-且該B環及該C環中之一或兩者係視需要經取代之碳環。在某些實施例中,R
111係-SO
2-且該B環及該C環中之一或兩者係視需要經取代之碳環。在某些實施例中,R
111係-C(O)-且該B環及該C環中之一或兩者係視需要經取代之雜芳基。R
111係-C(O)O-且該B環及該C環中之一或兩者係視需要經取代之雜芳基。R
111係-C(O)NH-且該B環及該C環中之一或兩者係視需要經取代之雜芳基。R
111係-S(O)-且該B環及該C環中之一或兩者係視需要經取代之雜芳基。在某些情況下,R
111係-SO
2-且該B環及該C環中之一或兩者係視需要經取代之雜芳基。在某些實施例中,R
111係-C(O)-且該B環及該C環中之一或兩者係視需要經取代之雜環。R
111係-C(O)O-且該B環及該C環中之一或兩者係視需要經取代之雜環。R
111係-C(O)NH-且該B環及該C環中之一或兩者係視需要經取代之雜環。R
111係-S(O)-且該B環及該C環中之一或兩者係視需要經取代之雜環。在某些情況下,R
111係-SO
2-且該B環及該C環中之一或兩者係視需要經取代之雜環。
在某些實施例中,B環及C環中之一或兩者係視需要經取代之哌嗪。在某些情況下,該B環係視需要經取代之哌嗪及該C環係選自視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之碳環及視需要經取代之雜環。在某些情況下,該C環係視需要經取代之哌嗪及該B環係選自視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之碳環及視需要經取代之雜環。在某些情況下,該B及該C環均為哌嗪。
在一些實施例中,R
6係
且係選自:
及
。在某些實施例中,R
13係-C(O)OR
41a、-NHC(O)R
41b、-C(O)NHR
41c、C(O)R
41d、C(O)NH
2、雜環,其中R
41a至R
41d係獨立地選自H、視需要經取代之(C
1-C
6)烷基、視需要經取代之雜環(例如,嗎啉、哌啶、嗎啉-3-酮),及視需要經取代之(C
1-C
6)烷基-雜環。
在一些實施例中,R
6係
。在另一實施例中,Y
2及Y
3各為CR
14。在另一實施例中,各R
14係獨立地選自H、OH、NH
2、CN、CF
3、OCF
3、CH
2NH
2、鹵素、-C(O)R
42f、-OC(O)R
42g、視需要經取代之(C
1-C
5)烷基及視需要經取代之(C
1-C
5)烷氧基,其中R
42f至R
42g係獨立地選自-OH、視需要經取代之胺基、視需要經取代之(C
1-C
6)烷基、視需要經取代之環烷基、視需要經取代之(C
1-C
10)烷氧基、視需要經取代之雜環(例如,哌嗪、吡咯啶、氮雜環丁烷、哌啶或嗎啉)、視需要經取代之-O-(C
1-C
6)烷基-雜環,及胺基酸。在另一實施例中,R
15係選自H、鹵素、OC(O)R
42a、-C(O)R
42b、-C(O)NHR
42c、R
42d或-OR
42e,其中R
42a至R
42e係獨立地選自-OH、視需要經取代之胺基、視需要經取代之(C
1-C
6)烷基、視需要經取代之環烷基、視需要經取代之(C
1-C
10)烷氧基、視需要經取代之雜環(例如,哌嗪、吡咯啶、氮雜環丁烷、哌啶或嗎啉)、視需要經取代之-O-(C
1-C
6)烷基-雜環,及胺基酸。在R
6之一些實施例中,其中n係1或更大,一個R
14基團係-C(O)R
42f,其中R
42f係選自視需要經取代之雜環(例如,哌嗪、吡咯啶、氮雜環丁烷、哌啶或嗎啉),及視需要經取代之(C
1-C
10)烷氧基(例如,-OCH
3)。在R
6之一些實施例中,R
15係-C(O)R
42b,其中R
42b係選自視需要經取代之雜環(例如,哌嗪、吡咯啶、氮雜環丁烷、哌啶或嗎啉),及視需要經取代之(C
1-C
10)烷氧基(例如,-OCH
3)。
在一些實施例中,R
6係
及n係0至3。在一些實施例中,R
15係H、C(O)OR
51或C(O)R
51,其中R
51係H或視需要經取代之(C
1-C
6)烷基,或視需要經取代之雜環(例如,嗎啉或哌嗪)。在另一實施例中,R
6係選自:
在一些實施例中,R
7係選自視需要經取代之N-苯胺基、視需要經取代之苯基及視需要經取代之雙環碳環。
在一些實施例中,化合物係式(Ie)化合物:
其中:
R
5e及R
6e係獨立地選自H、視需要經取代之(C
1-C
10)烷基、視需要經取代之(C
1-C
10)烯基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之單環或雙環碳環及視需要經取代之單環或雙環雜環;
或R
5e及R
6e連同其等結合之氮原子一起環狀連接以形成視需要經取代之單環或雙環雜環。
在式(Ie)之一些實施例中,R
5e係H或Me及R
6e係選自:
、
及
;其中:
Y
1、Y
2及Y
3係獨立地選自CR
14及N;
Z係選自O、S、CHR
11及NR
12;
n係0至4;
R
11係選自H、NH
2、CN、CH
2NH
2、NO
2、鹵素、OR
2a、C(O)R
2b、CO
2R
2c、C(O)NR
5R
6、視需要經取代之胺基、視需要經取代之(C
1-C
5)烷基及視需要經取代之(C
1-C
5)烷氧基,及視需要經取代之雜環;
R
12係選自H、NH
2、鹵素、C(O)R
2d、CO
2R
2e、C(O)NR
5R
6,及視需要經取代之(C
1-C
5)烷基;
係選自視需要經取代之(C
1-C
6)烷基-環烷基、視需要經取代之雜環烷基、視需要經取代之單環或雙環(C
4-C
10)碳環,及視需要經取代之單環或雙環(C
4-C
10)雜環;
R
13係選自H、NH
2、CN、CH
2NH
2、NO
2、鹵素、OR
2f、C(O)R
2g、CO
2R
2h、C(O)NR
5R
6、NR
5R
6、視需要經取代之(C
1-C
5)烷基及視需要經取代之(C
1-C
5)烷氧基,及視需要經取代之雜環;
R
14係選自H、OH、NH
2、CN、CF
3、OCF
3、CH
2NH
2、鹵素、視需要經取代之(C
1-C
5)烷基、視需要經取代之(C
1-C
5)烷氧基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之碳環及視需要經取代之雜環;
R
15係選自H、鹵素、NHC(O)R
2i、OR
2j、C(O)R
2k、OC(O)R
2l、CO
2R
2m、C(O)NR
5R
6、NR
5R
6、視需要經取代之(C
1-C
5)烷基、視需要經取代之(C
1-C
5)烷氧基、視需要經取代之環烷基及視需要經取代之雜環;及
R
20係選自H、鹵素、視需要經取代之(C
1-C
5)烷基、視需要經取代之(C
1-C
5)烷氧基、視需要經取代之碳環及視需要經取代之雜環;及
R
2a-R
2m係獨立地選自H、視需要經取代之(C
1-C
10)烷基、視需要經取代之環烷基、視需要經取代之芳基、視需要經取代之雜芳基及視需要經取代之雜環,及烷基、環烷基、芳基、雜芳基及雜環上之任選取代基係獨立地選自:H、OH、NH
2、NO
2、OCF
3、CF
3、鹵素、雜環、雜芳基、視需要經取代之胺基、視需要經取代之(C
1-C
5)烷基及視需要經取代之(C
1-C
5)烷氧基。
在一些實施例中,R
6e係選自:
其中:
環B及環C各係獨立地選自視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之碳環及視需要經取代之雜環;
各R
111係獨立地選自視需要經取代之(C
1-C
6)烷基、
、-C(O)(R
111a)p
1、-C(O)O(R
111b)p
2、-S(O)(R
111c)p
3、-SO
2(R
111d)p
4及-C(O)NR
27(R
111e)p
5;其中R
111a至R
111e各獨立地係視需要經取代之(C
1-C
6)烷基、
;
R
27至R
28各係獨立地選自H及視需要經取代之(C
1-C
6)烷基;及
p至p
5各獨立地係0至3。
在R
6e之一些實施例中,R
111係選自-C(O)-、-C(O)O-、-C(O)NH-、-S(O)-及-SO
2-;且B環及C環係獨立地選自視需要經取代之芳基、視需要經取代之碳環、視需要經取代之雜芳基及視需要經取代之雜環。在某些實施例中,R
111係-C(O)-且該B環及該C環中之一或兩者係視需要經取代之芳基。在某些實施例中,R
111係-C(O)O-且該B環及該C環中之一或兩者係視需要經取代之芳基。在某些實施例中,R
111係-C(O)NH-且該B環及該C環中之一或兩者係視需要經取代之芳基。在某些實施例中,R
111係-S(O)-且該B環及該C環中之一或兩者係視需要經取代之芳基。在某些實施例中,R
111係-SO
2-且該B環及該C環中之一或兩者係視需要經取代之芳基。在某些實施例中,R
111係-C(O)-且該B環及該C環中之一或兩者係視需要經取代之碳環。在某些實施例中,R
111係-C(O)O-且該B環及該C環中之一或兩者係視需要經取代之碳環。R
111係-C(O)NH-且該B環及該C環中之一或兩者係視需要經取代之碳環。在某些實施例中,R
111係-S(O)-且該B環及該C環中之一或兩者係視需要經取代之碳環。在某些實施例中,R
111係-SO
2-且該B環及該C環中之一或兩者係視需要經取代之碳環。在某些實施例中,R
111係-C(O)-且該B環及該C環中之一或兩者係視需要經取代之雜芳基。在某些實施例中,R
111係-C(O)O-且該B環及該C環中之一或兩者係視需要經取代之雜芳基。在某些實施例中,R
111係-C(O)NH-且該B環及該C環中之一或兩者係視需要經取代之雜芳基。在某些實施例中,R
111係-S(O)-且該B環及該C環中之一或兩者係視需要經取代之雜芳基。在某些情況下,R
111係-SO
2-且該B環及該C環中之一或兩者係視需要經取代之雜芳基。在某些實施例中,R
111係-C(O)-且該B環及該C環中之一或兩者係視需要經取代之雜環。在某些實施例中,R
111係-C(O)O-且該B環及該C環中之一或兩者係視需要經取代之雜環。在某些實施例中,R
111係-C(O)NH-且該B環及該C環中之一或兩者係視需要經取代之雜環。在某些實施例中,R
111係-S(O)-且該B環及該C環中之一或兩者係視需要經取代之雜環。在某些情況下,R
111係-SO
2-且該B環及該C環中之一或兩者係視需要經取代之雜環。
在某些實施例中, B環及C環中之一或兩者係視需要經取代之哌嗪。在某些情況下,該B環係視需要經取代之哌嗪及該C環係選自視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之碳環及視需要經取代之雜環。在某些情況下,該C環係視需要經取代之哌嗪及該B環係選自視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之碳環及視需要經取代之雜環。在某些情況下,該B及該C環均為哌嗪。
在一些實施例中,R
6e係
且係選自:
及
。在另一實施例中,R
13係-C(O)OR
41a、-NHC(O)R
41b、-C(O)NHR
41c或C(O)R
41d,其中R
41a、R
41b、R
41c及R
41d係獨立地選自H、視需要經取代之(C
1-C
6)烷基、視需要經取代之雜環(例如,嗎啉、哌啶、嗎啉-3-酮),及視需要經取代之(C
1-C
6)烷基-雜環。
在一些實施例中,R
6e係
。在另一實施例中,Y
2及Y
3各為CR
14。在另一實施例中,各R
14係獨立地選自H、OH、NH
2、CN、CF
3、OCF
3、CH
2NH
2、鹵素、-C(O)R
42f、-OC(O)R
42g、視需要經取代之(C
1-C
5)烷基及視需要經取代之(C
1-C
5)烷氧基,其中R
42f至R
42g係獨立地選自-OH、視需要經取代之胺基、視需要經取代之(C
1-C
6)烷基、視需要經取代之環烷基、視需要經取代之(C
1-C
10)烷氧基、視需要經取代之雜環(例如,哌啶或嗎啉)、視需要經取代之-O-(C
1-C
6)烷基-雜環,及胺基酸。在另一實施例中,R
15係選自H、鹵素、OC(O)R
42a、-C(O)R
42b、-C(O)NHR
42c、R
42d或-OR
42e,其中R
42a至R
42e係獨立地選自-OH、視需要經取代之胺基、視需要經取代之(C
1-C
6)烷基、視需要經取代之環烷基、視需要經取代之(C
1-C
10)烷氧基、視需要經取代之雜環(例如,哌啶或嗎啉)、視需要經取代之-O-(C
1-C
6)烷基-雜環,及胺基酸。在R
6e之一些實施例中,其中n係1或更大,一個R
14基團係-C(O)R
42f,其中R
42f係選自視需要經取代之雜環(例如,哌啶或嗎啉),及視需要經取代之(C
1-C
10)烷氧基(例如,-OCH
3)。在R
6e之一些實施例中,R
15係-C(O)R
42b,其中R
42b係選自視需要經取代之雜環(例如,哌啶或嗎啉),及視需要經取代之(C
1-C
10)烷氧基(例如,-OCH
3)。
在一些實施例中,R
6e係
及n係0至3。在一些實施例中,R
15係H、-C(O)OR
51或-C(O)R
51,其中R
51係H、視需要經取代之(C
1-C
6)烷基,或視需要經取代之雜環(例如,嗎啉或哌嗪)。在另一實施例中,R
6e係選自:
在式(Ie)之一些實施例中,R
5e及R
6e連同其等結合之氮原子一起環狀連接以形成視需要經取代之單環或雙環(C
4-C
10)雜環。
在式(Ie)之一些實施例中,R
5e及R
6e連同其等結合之氮原子一起環狀連接以形成:
其中:
環A係視需要經取代之單環或雙環(C
4-C
10)雜環;
Z
1係CR
14或N,其中R
14係選自H、OH、NH
2、CN、CF
3、OCF
3、CH
2NH
2、鹵素、視需要經取代之(C
1-C
5)烷基、視需要經取代之(C
1-C
5)烷氧基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之碳環及視需要經取代之雜環;及
R
16係選自H、鹵素、-OR
22a、-C(O)R
22b、-CO
2R
22c及-C(O)NR
50R
60、-NR
50R
60、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之碳環、視需要經取代之雜環、視需要經取代之(C
1-C
5)烷基及視需要經取代之(C
1-C
5)烷氧基;
R
22a、R
22b及R
22c係獨立地選自H、視需要經取代之(C
1-C
10)烷基、視需要經取代之環烷基、視需要經取代之芳基、視需要經取代之雜芳基及視需要經取代之雜環;及
R
50及R
60係獨立地選自H、視需要經取代之(C
1-C
10)烷基、視需要經取代之(C
1-C
10)烯基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之單環或雙環碳環及視需要經取代之單環或雙環雜環;
或R
50及R
60連同其等結合之氮原子一起環狀連接以形成視需要經取代之雜環或視需要經取代之雜芳基。
在式(Ie)之一些實施例中,當R
5e及R
6e一起形成:
及A環係哌啶時,則R
16包含至少一個係選自視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之碳環、視需要經取代之雜環之環形基團。在某些情況下,該A環係哌啶及R
16包含視需要經取代之芳基。在某些情況下,該視需要經取代之芳基係視需要經取代之苯基。在某些情況下,該A環係哌啶及R
16包含視需要經取代之雜芳基。在某些情況下,該A環係哌啶及R
16包含視需要經取代之碳環。在某些情況下,該A環係哌啶及R
16包含視需要經取代之雜環。
在式(Ie)之一些實施例中,當R
5e及R
6e一起形成:
時,A環係視需要經取代之哌嗪、吡咯啶或氮雜環丁烷。在某些情況下,該A環係:
其中:
R
23至R
26各係獨立地選自H、鹵素、OH、NO
2、OCF
3、CF
3、視需要經取代之胺基、視需要經取代之(C
1-C
6)烷基、視需要經取代之(C
1-C
6)烷氧基、視需要經取代之環烷基、視需要經取代之芳基、視需要經取代之雜芳基及視需要經取代之雜環;或
R
23至R
24及R
25至R
26中之一或兩者連同其等結合之碳原子一起環狀連接以形成視需要經取代之碳環或視需要經取代之雜環;及
R
40a及R
40b各係獨立地選自H、鹵素、OH、NO
2、OCF
3、CF
3、視需要經取代之胺基、視需要經取代之(C
1-C
6)烷基、視需要經取代之(C
1-C
6)烷氧基、視需要經取代之環烷基、視需要經取代之芳基、視需要經取代之雜芳基及視需要經取代之雜環。
在A環之一些實施例中,R
23係選自視需要經取代之(C
1-C
6)烷基、視需要經取代之環烷基;及R
24至R
26、R
40a及R
40b各為H。在某些情況下,R
23係選自甲基、乙基、丙基、異丙基、丁基及第三丁基。在某些情況下,R
23係甲基。在某些情況下,R
23係乙基。在某些情況下,R
23係丙基。在某些情況下,R
23係異丙基。在一些實施例中,R
23係(C
1-C
6)環烷基。在某些情況下,R
23係環丙基。在某些情況下,R
23係環丁基。在某些情況下,R
23係環戊基。在某些情況下,R
23係環己基。
在A環之某些實施例中,R
23、R
25及R
40b中之兩者係獨立地選自視需要經取代之(C
1-C
6)烷基及視需要經取代之環烷基;及R
23、R
25及R
40b中之另一者係H,且R
24、R
26及R
40a各為H。在A環之某些情況下,R
23、R
25及R
40b中之兩者係視需要經取代之(C
1-C
6)烷基。在A環之某些情況下,R
23、R
25及R
40b中之兩者各係獨立地選自甲基、乙基、丙基、異丙基、丁基及第三丁基。在A環之某些情況下,R
23、R
25及R
40b中之兩者係甲基。在A環之某些情況下,R
23、R
25及R
40b中之兩者係乙基。在某些情況下,R
23、R
25及R
40b中之兩者係丙基。在A環之某些情況下,R
23、R
25及R
40b中之兩者係異丙基。在A環之一些實施例中,R
23、R
25及R
40b中之兩者係(C
1-C
6)環烷基。在A環之某些情況下,R
23、R
25及R
40b中之兩者係環丙基。在某些情況下,R
23、R
25及R
40b中之兩者係環丁基。在A環之某些情況下,R
23、R
25及R
40b中之兩者係環戊基。在A環之某些情況下,R
23、R
25及R
40b中之兩者係環己基。
在A環之某些實施例中,R
23及R
25各係獨立地選自視需要經取代之(C
1-C
6)烷基及視需要經取代之環烷基;且R
24、R
26及R
40a至R
40b各為H。在A環之某些情況下,R
23及R
25均為視需要經取代之(C
1-C
6)烷基。在A環之某些情況下,R
23及R
25各係獨立地選自甲基、乙基、丙基、異丙基、丁基及第三丁基。在A環之某些情況下,R
23及R
25均為甲基。在A環之某些情況下,R
23及R
25均為乙基。在A環之某些情況下,R
23及R
25均為丙基。在A環之某些情況下,R
23及R
25均為異丙基。在A環之一些實施例中,R
23及R
25均為(C
1-C
6)環烷基。在A環之某些情況下,R
23及R
25均為環丙基。在某些情況下,R
23及R
25均為環丁基。在A環之某些情況下,R
23及R
25均為環戊基。在A環之某些情況下,R
23及R
25均為環己基。
在A環之某些實施例中,R
23及R
40b各係獨立地選自視需要經取代之(C
1-C
6)烷基及視需要經取代之環烷基;且R
24至R
26及R
40a各為H。在某些情況下,R
23及R
40b均為視需要經取代之(C
1-C
6)烷基。在某些情況下,R
23及R
40b各係獨立地選自甲基、乙基、丙基、異丙基、丁基及第三丁基。在某些情況下,R
23及R
40b均為甲基。在某些情況下,R
23及R
40b均為乙基。在某些情況下,R
23及R
40b均為丙基。在某些情況下,R
23及R
40b均為異丙基。在一些實施例中,R
23及R
40b均為(C
1-C
6)環烷基。在某些情況下,R
23及R
40b均為環丙基。在某些情況下,R
23及R
40b均為環丁基。在某些情況下,R
23及R
40b均為環戊基。在某些情況下,R
23及R
40b均為環己基。
在A環之某些實施例中,R
23及R
24各係獨立地選自視需要經取代之(C
1-C
6)烷基及視需要經取代之環烷基;且R
25至R
26、R
40a及R
40b各為H。在某些情況下,R
23及R
24均為視需要經取代之(C
1-C
6)烷基。在某些情況下,R
23及R
24各係獨立地選自甲基、乙基、丙基、異丙基、丁基及第三丁基。在某些情況下,R
23及R
24均為甲基。在某些情況下,R
23及R
24均為乙基。在某些情況下,R
23及R
24均為丙基。在某些情況下,R
23及R
25均為異丙基。在一些實施例中,R
23及R
24均為(C
1-C
6)環烷基。在某些情況下,R
23及R
24均為環丙基。在某些情況下,R
23及R
24均為環丁基。在某些情況下,R
23及R
24均為環戊基。在某些情況下,R
23及R
24均為環己基。
在A環之某些實施例中,R
23及R
24連同其等連結之碳原子一起環狀連接形成碳環;且R
25至R
26、R
40a及R
40b各為H。在一些實施例中,R
23及R
24連同其等連結之碳原子一起環狀連接形成(C
1-C
6)環烷基。在某些情況下,R
23及R
24連同其等連結之碳原子一起環狀連接形成環丙基。在某些情況下,R
23及R
24連同其等連結之碳原子一起環狀連接形成環丁基。在某些情況下,R
23及R
24連同其等連結之碳原子一起環狀連接形成環戊基。在某些情況下,R
23及R
24連同其等連結之碳原子一起環狀連接形成環己基。
在式(Ie)之一些實施例中,當R
5e及R
6e一起形成:
時,A環係選自:
、
、
、
、
、
、
、
、
、
、
及
。在一些實施例中,R
16係選自H、鹵素、-OR
22a、-C(O)R
22b、-CO
2R
22c及-C(O)NR
50R
60、-NR
50R
60、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之碳環、視需要經取代之雜環、視需要經取代之(C
1-C
5)烷基及視需要經取代之(C
1-C
5)烷氧基,其中R
22a、R
22b、R
22c、R
50及R
60係如上文定義。
在式(Ie)之一些實施例中,R
5e及R
6e一起形成:
,其中R
16係:
-(R
110)
nR
210其中:
各R
110係獨立地選自視需要經取代之(C
1-C
6)烷基、
、-C(O)(R
110a)n
1、-C(O)O(R
110b)n
2、-S(O)(R
110c)n
3、-SO
2(R
110d)n
4及-C(O)NR
27(R
110e)n
5;其中R
110a至R
110e各獨立地係視需要經取代之(C
1-C
6)烷基、
;R
27至R
28各係獨立地選自H及視需要經取代之(C
1-C
6)烷基;及n至n
5各獨立地係0至3;及
R
210係選自視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之碳環及視需要經取代之雜環。
在一些實施例中,R
110係選自-C(O)-、-C(O)O-、-C(O)NH-、-S(O)-及-SO
2-;及R
210係選自視需要經取代之芳基及視需要經取代之雜芳基。在某些實施例中,R
110係-C(O)-及R
210係視需要經取代之芳基。在某些實施例中,R
110係-C(O)O-及R
210係視需要經取代之芳基。在某些實施例中,R
110係-C(O)NH-及R
210係視需要經取代之芳基。在某些實施例中,R
110係-S(O)-及R
210係視需要經取代之芳基。在某些實施例中,R
110係-SO
2-及R
210係視需要經取代之芳基。在某些實施例中,R
110係-C(O)-及R
210係視需要經取代之芳基。在某些實施例中,R
110係-C(O)O-及R
210係視需要經取代之雜芳基。在某些實施例中,R
110係-C(O)NH-及R
210係視需要經取代之雜芳基。在某些實施例中,R
110係-S(O)-及R
210係視需要經取代之雜芳基。在某些情況下,R
110係-SO
2-及R
210係視需要經取代之雜芳基。
在一些實施例中,R
210係選自:
、
、
、
及
,其中:
其中:
X
4至X
7、X
9及X
11各係獨立地選自CH、CR
31、S、O及N;
X
8、X
10、X
12及X
13各係獨立地選自S、O及NR
29;
R
29係選自H及視需要經取代之(C
1-C
6)烷基;
R
30至R
32各係獨立地選自H、鹵素、OH、NO
2、OCF
3、CF
3、視需要經取代之胺基、視需要經取代之(C
1-C
6)烷基、視需要經取代之(C
1-C
6)烷氧基、視需要經取代之環烷基、視需要經取代之芳基、視需要經取代之雜芳基及視需要經取代之雜環;及
m
1至m
2各獨立地係0至5。
在一些實施例中,R
210係
,其中X
9係選自CH、CR
31、S、O及N;及X
8係選自S、O及NR
29。在某些情況下,R
29係甲基。在R
210之一些實施例中,X
9係CH、CR
31、S、O及N;及X
8係選自S、O及NR
29。在某些情況下,X
9係CH,及X
8係S。在某些情況下,R
30係H。在某些情況下,R
30係甲基。在一些實施例中,X
9係CH,X
8係S及R
30係H。在某些情況下,X
9係CH,X
8係NR
29及R
30係H。在某些情況下,X
9係CH,及X
8係NH。在某些情況下,X
9係CH,X
8係O及R
30係(C
1-C
6)烷基。在某些情況下,X
9係CH,X
8係O及R
30係甲基。
在一些實施例中,R
210係
,其中X
9係N,及X
8係選自S、O及NR
29。在某些情況下,X
8係NR
29。在某些情況下,R
29係H。在某些情況下,R
29係甲基。在某些情況下,X
8係O。在某些情況下,X
8係S。
在一些實施例中,R
210係
,其中X
10係選自S、O及NR
29。在某些情況下,X
10係O。在某些情況下,X
10係S。在某些情況下,X
10係NR
29,其中R
29係(C
1-C
6)烷基。在某些情況下,R
29係H。在某些情況下,R
29係甲基。
在一些實施例中,R
210係
,其中X
11係選自CH、CR
31、S、O及N,及X
12係選自S、O及NR
29。在某些情況下,X
11係N。在某些情況下,X
12係O或S。在某些情況下,X
11係N,及X
12係O。在某些情況下,X
11係N,及X
12係S。
在一些實施例中,R
210係
,其中X
13係選自S、O及NR
29。在某些情況下,X
13係NR
29。在某些情況下,R
29係H。在某些情況下,R
29係甲基。在某些情況下,X
13係S。在某些情況下,X
13係O。
在式(Ie)之一些實施例中,
係選自:
其中:
各R
33係獨立地選自視需要經取代之(C
1-C
6)烷基及視需要經取代之環烷基。在某些情況下,各R
33係獨立地選自甲基、乙基、丙基、異丙基、丁基及第三丁基。在某些情況下,各R
33係甲基。在某些情況下,各R
33係乙基。在某些情況下,各R
33係丙基。在某些情況下,各R
33係異丙基。在一些實施例中,各R
33係獨立地選自(C
1-C
6)環烷基。在某些情況下,各R
33係環丙基。在某些情況下,各R
33係環丁基。在某些情況下,各R
33係環戊基。在某些情況下,各R
33係環己基。
在式(Ia)至(Ie)之一些實施例中,化合物係表1化合物,或其醫藥上可接受之鹽、溶劑化物、水合物、前藥或立體異構體。
| 表1:例示性化合物 | ||
| 化合物 | 結構 | 名稱 |
| 1 | 7-(3,4-二甲氧基苯基)-N-苯基吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 2 | N-環己基-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 4 | 7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羧酸甲酯 | |
| 6 | 7-(3,4-二甲氧基苯基)-N-(4-甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 7 | 2-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸甲酯 | |
| 8 | 3-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸甲酯 | |
| 9 | (1S,4S)-4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)環己烷-1-羧酸甲酯 | |
| 10 | (1r,4r)-4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)環己烷-1-羧酸甲酯 | |
| 12 | 4-((7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)甲基)苯甲酸甲酯 | |
| 13 | N-(4-乙氧基苯基)-7-(4-甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 14 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸 | |
| 15 | 7-(3,4-二甲氧基苯基)-N-(4-羥基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 16 | 3-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸 | |
| 17 | 7-(3,4-二甲氧基苯基)-N-(吡啶-2-基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 18 | 7-(3,4-二甲氧基苯基)-N-(吡啶-3-基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 19 | (1S,4S)-4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)環己烷-1-羧酸 | |
| 20 | (7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羰基)甘胺酸乙酯 | |
| 21 | (1R,4R)-4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)環己烷-1-羧酸 | |
| 22 | (7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羰基)甘胺酸 | |
| 23 | 4-(7-(4-甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸甲酯 | |
| 24 | N-(4-乙氧基苯基)-7-(3-甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 25 | 4-(7-(3-甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸甲酯 | |
| 26 | 1-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)環丙烷-1-羧酸乙酯 | |
| 27 | 7-(3,4-二甲氧基苯基)-N-(4-(二甲基胺基)環己基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 28 | (4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲醯基)甘胺酸乙酯 | |
| 29 | 1-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)環丙烷-1-羧酸 | |
| 30 | (4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲醯基)甘胺酸 | |
| 31 | 6-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)菸鹼酸甲酯 | |
| 32 | 4-(7-(3,4,5-三甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸甲酯 | |
| 33 | 4-(7-(3-氟-4-甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸甲酯 | |
| 34 | 2-(4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯氧基)乙酸乙酯 | |
| 35 | 2-(4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯氧基)乙酸 | |
| 36 | 3-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)雙環[1.1.1]戊烷-1-羧酸甲酯 | |
| 37 | 3-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)雙環[1.1.1]戊烷-1-羧酸 | |
| 38 | 7-(3,4-二羥基苯基)-N-(4-羥基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 39 | 4-(7-(3-氯-4-甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸甲酯 | |
| 40 | 4-(7-(3,4-二氯苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸甲酯 | |
| 41 | 7-(3,4-二甲氧基苯基)-N-(4-(嗎啉-4-羰基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 42 | (4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲醯基)-L-丙胺酸甲酯 | |
| 43 | (4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲醯基)-L-絲胺酸甲酯 | |
| 44 | (4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲醯基)-L-丙胺酸 | |
| 45 | (4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲醯基)-L-絲胺酸 | |
| 46 | (4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲醯基)-L-苯基丙胺酸甲酯 | |
| 47 | (4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲醯基)-L-脯胺酸甲酯 | |
| 48 | N-(4-胺甲醯基苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 49 | (4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲醯基)-L-苯基丙胺酸 | |
| 50 | (4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲醯基)-L-脯胺酸 | |
| 51 | 4-(4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲醯基)哌嗪-1-羧酸第三丁酯 | |
| 52 | 7-(3,4-二甲氧基苯基)-N-(4-(哌嗪-1-羰基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 53 | 7-(3,4-二甲氧基苯基)-N-(4-((2-羥基乙基)胺甲醯基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 54 | N-(3-胺甲醯基苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 55 | 7-(3,4-二甲氧基苯基)-N-(3-(嗎啉-4-羰基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 56 | 4-(3-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲醯基)哌嗪-1-羧酸第三丁酯 | |
| 57 | (4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲醯基)-L-白胺酸甲酯 | |
| 58 | (4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲醯基)-L-纈胺酸甲酯 | |
| 59 | (4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲醯基)-L-甲硫胺酸甲酯 | |
| 60 | (4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲醯基)-L-天冬胺酸二甲酯 | |
| 61 | (7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(嗎啉基)甲酮 | |
| 62 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羰基)哌嗪-1-羧酸第三丁酯 | |
| 63 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)哌啶-1-羧酸第三丁酯 | |
| 64 | (4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲醯基)-D-丙胺酸甲酯 | |
| 65 | 1-(4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲醯基)氮雜環丁烷-3-羧酸甲酯 | |
| 66 | (7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(哌嗪-1-基)甲酮 | |
| 67 | 7-(3,4-二甲氧基苯基)-N-(哌啶-4-基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 68 | 7-(3,4-二甲氧基苯基)-N-(4-甲基哌嗪-1-基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 69 | 7-(3,4-二甲氧基苯基)-N-((1R,4R)-4-羥基環己基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 70 | 4-(7-(2,3-二氫苯并[b][1,4]二噁英-6-基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸甲酯 | |
| 71 | N-((1S,4S)-4-胺甲醯基環己基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 72 | 7-(3,4-二甲氧基苯基)-N-((1S,4S)-4-(嗎啉-4-羰基)環己基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 73 | 4-((1S,4S)-4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)環己烷-1-羰基)哌嗪-1-羧酸第三丁酯 | |
| 74 | N-((1R,4R)-4-胺甲醯基環己基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 75 | 7-(3,4-二甲氧基苯基)-N-((1R,4R)-4-(嗎啉-4-羰基)環己基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 76 | 4-((1R,4R)-4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)環己烷-1-羰基)哌嗪-1-羧酸第三丁酯 | |
| 77 | (2-(4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲醯胺基)乙基)胺甲酸第三丁酯 | |
| 78 | 6-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)菸鹼酸 | |
| 79 | N-(4-((2-胺基乙基)胺甲醯基)苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 80 | 7-(3,4-二甲氧基苯基)-N-(3-(哌嗪-1-羰基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 81 | 7-(3,4-二甲氧基苯基)-N-((1S,4S)-4-(哌嗪-1-羰基)環己基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 82 | 7-(3,4-二甲氧基苯基)-N-((1R,4R)-4-(哌嗪-1-羰基)環己基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 83 | 2-(4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羰基)哌嗪-1-基)-2-側氧基乙酸乙酯 | |
| 84 | 乙酸2-(4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)哌啶-1-基)-2-側氧基乙酯 | |
| 85 | (4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲醯基)-L-白胺酸 | |
| 86 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羰基)哌嗪-1-羧酸乙酯 | |
| 87 | (4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲醯基)-L-甲硫胺酸 | |
| 88 | (4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲醯基)-L-天冬胺酸 | |
| 89 | (4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲醯基)-D-丙胺酸 | |
| 90 | 1-(4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羰基)哌嗪-1-基)-2-羥基乙-1-酮 | |
| 91 | 7-(3,4-二甲氧基苯基)-N-(1-(2-羥基乙醯基)哌啶-4-基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 92 | 4-(3-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)雙環[1.1.1]戊烷-1-羰基)哌嗪-1-羧酸第三丁酯 | |
| 93 | 4-(3-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)脲基)苯甲酸甲酯 | |
| 94 | 4-((7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)甲基)苯甲酸 | |
| 95 | N-(3-胺甲醯基雙環[1.1.1]戊-1-基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 96 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸3-嗎啉基丙酯 | |
| 97 | 7-(3,4-二甲氧基苯基)-N-(4-(4-甲基哌嗪-1-羰基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 98 | 7-(3,4-二甲氧基苯基)-N-(3-(哌嗪-1-羰基)雙環[1.1.1]戊-1-基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 99 | 7-(3,4-二甲氧基苯基)-N-嗎啉基吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 100 | (1-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羰基)哌啶-4-基)胺甲酸第三丁酯 | |
| 101 | (7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(4-甲基哌嗪-1-基)甲酮 | |
| 102 | 7-(3,4-二甲氧基苯基)-N-((1S,4S)-4-羥基環己基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 103 | (R)-N-(1-(2,3-二羥基丙基)哌啶-4-基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 104 | 3-氯-4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸甲酯 | |
| 105 | 2-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)-3-苯基丙烯酸甲酯 | |
| 106 | 3-氯-4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸 | |
| 107 | 4-(3-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)脲基)苯甲酸 | |
| 108 | 2-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)-3-苯基丙烯酸 | |
| 109 | 1-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)-3-(4-乙氧基苯基)脲 | |
| 110 | (4-(環丙烷羰基)哌嗪-1-基)(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)甲酮 | |
| 111 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羰基)哌嗪-1-羧酸乙酯 | |
| 112 | (S)-4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羰基)-2-甲基哌嗪-1-羧酸第三丁酯 | |
| 113 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羰基)-2,2-二甲基哌嗪-1-羧酸第三丁酯 | |
| 114 | 6-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)菸鹼酸苯甲酯 | |
| 115 | (R)-(1-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羰基)吡咯啶-3-基)胺甲酸第三丁酯 | |
| 116 | (1-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羰基)氮雜環丁烷-3-基)胺甲酸第三丁酯 | |
| 117 | 1-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羰基)吡咯啶-3-酮 | |
| 118 | 7-(3,4-二甲氧基苯基)-N-(4-((2-(二甲基胺基)乙基)胺甲醯基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 119 | 7-(3,4-二甲氧基苯基)-N-(4-((2-(哌啶-1-基)乙基)胺甲醯基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 120 | N-(4-((2-(二異丙基胺基)乙基)胺甲醯基)苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 121 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸3-嗎啉基丙酯 | |
| 122 | 7-(3,4-二甲氧基苯基)-N-(5-甲基吡啶-2-基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 123 | 7-(3,4-二甲氧基苯基)-N-(3-(4-甲基哌嗪-1-羰基)雙環[1.1.1]戊-1-基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 124 | 7-(3,4-二甲氧基苯基)-N-(5-(4-甲基哌嗪-1-羰基)吡啶-2-基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 125 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)-3-甲基苯甲酸甲酯 | |
| 126 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)-3-甲基苯甲酸 | |
| 127 | 7-(3,4-二甲氧基苯基)-N-(2-甲基-4-(嗎啉-4-羰基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 128 | 7-(3,4-二甲氧基苯基)-N-(2-甲基-4-(4-甲基哌嗪-1-羰基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 129 | 1-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)-3-(4-(嗎啉-4-羰基)苯基)脲 | |
| 130 | 1-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羰基)吲哚啉-5-羧酸甲酯 | |
| 131 | 2-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羰基)-1,2,3,4-四氫異喹啉-7-羧酸甲酯 | |
| 132 | 1-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羰基)吲哚啉-6-羧酸甲酯 | |
| 133 | 1-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羰基)-1,2,3,4-四氫喹啉-6-羧酸甲酯 | |
| 134 | 7-(3,4-二甲氧基苯基)-N-(3-(4-甲基哌嗪-1-基)-3-側氧基-1-苯基丙-1-烯-2-基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 135 | 7-(3,4-二甲氧基苯基)-N-(5-(嗎啉-4-羰基)吡啶-2-基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 136 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)-3-氟苯甲酸甲酯 | |
| 137 | N-(2-氯-4-(4-甲基哌嗪-1-羰基)苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 138 | N-(3-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)雙環[1.1.1]戊-1-基)嗎啉-4-甲醯胺 | |
| 139 | 7-(3,4-二甲氧基苯基)-N-(4-((2-嗎啉基乙基)胺甲醯基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 140 | 2-氯-4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸甲酯 | |
| 141 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)-2-氟苯甲酸甲酯 | |
| 142 | 6-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)菸鹼酸3-嗎啉基丙酯 | |
| 143 | (R)-(3-胺基吡咯啶-1-基)(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)甲酮 | |
| 144 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)雙環[2.2.2]辛烷-1-羧酸甲酯 | |
| 145 | (S)-(1-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羰基)吡咯啶-3-基)胺甲酸第三丁酯 | |
| 146 | (S)-7-(3,4-二甲氧基苯基)-N-(4-((3-甲基-1-(4-甲基哌嗪-1-基)-1-側氧基丁-2-基)胺甲醯基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 147 | (S)-7-(3,4-二甲氧基苯基)-N-(4-((3-甲基-1-嗎啉基-1-側氧基丁-2-基)胺甲醯基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 148 | (S)-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(3-羥基吡咯啶-1-基)甲酮 | |
| 149 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)雙環[2.2.2]辛烷-1-羧酸 | |
| 150 | (R)-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(3-羥基吡咯啶-1-基)甲酮 | |
| 151 | 7-(3,4-二甲氧基苯基)-N-(4-(4-甲基哌嗪-1-羰基)雙環[2.2.2]辛-1-基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 152 | (7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(4-苯基哌嗪-1-基)甲酮 | |
| 153 | (7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(4-(吡啶-2-基)哌嗪-1-基)甲酮 | |
| 154 | (4-苯甲基哌嗪-1-基)(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)甲酮 | |
| 155 | 2-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羰基)-1,2,3,4-四氫異喹啉-7-羧酸 | |
| 156 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)-3-氟苯甲酸 | |
| 157 | 7-(3,4-二甲氧基苯基)-N-(2-氟-4-(嗎啉-4-羰基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 158 | 7-(3,4-二甲氧基苯基)-N-(2-氟-4-(4-甲基哌嗪-1-羰基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 159 | 7-(3,4-二甲氧基苯基)-N-(4-(4-異丙基哌嗪-1-羰基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 160 | N-(3-氯-4-(嗎啉-4-羰基)苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 161 | N-(3-氯-4-(4-甲基哌嗪-1-羰基)苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 162 | 2-氯-4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸3-嗎啉基丙酯 | |
| 163 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)-2-氟苯甲酸3-嗎啉基丙酯 | |
| 164 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸2-嗎啉基乙酯 | |
| 165 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸3-(4-甲基哌嗪-1-基)丙酯 | |
| 166 | 7-(3,4-二甲氧基苯基)-N-(4-(6-甲基-2,6-二氮雜螺[3.3]庚烷-2-羰基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 167 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)-2-羥基苯甲酸甲酯 | |
| 168 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)-2-羥基苯甲酸 | |
| 169 | 7-(3,4-二甲氧基苯基)-N-(3-羥基-4-(嗎啉-4-羰基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 170 | 7-(3,4-二甲氧基苯基)-N-(3-羥基-4-(4-甲基哌嗪-1-羰基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 171 | ((苯甲氧基)羰基)-L-纈胺酸4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯酯 | |
| 172 | L-纈胺酸4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯酯 | |
| 173 | 7-(3,4-二甲氧基苯基)-N-(4-((3-嗎啉基丙基)胺甲醯基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 174 | 7-(3,4-二甲氧基苯基)-N-(3-氟-4-(嗎啉-4-羰基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 175 | 7-(3,4-二甲氧基苯基)-N-(3-氟-4-(4-甲基哌嗪-1-羰基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 176 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)-3-羥基苯甲酸甲酯 | |
| 177 | 7-(3,4-二甲氧基苯基)-N-(4-((3-(4-甲基哌嗪-1-基)丙基)胺甲醯基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 178 | 7-(3,4-二甲氧基苯基)-N-(4-((2-(4-甲基哌嗪-1-基)乙基)胺甲醯基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 179 | (7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(4-異丙基哌嗪-1-基)甲酮 | |
| 180 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羰基)哌嗪-2-酮 | |
| 181 | (S)-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(3-甲基哌嗪-1-基)甲酮 | |
| 182 | (7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(3,3-二甲基哌嗪-1-基)甲酮 | |
| 183 | 4-(7-(3,4-二甲氧基苯基)-N-甲基吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸甲酯 | |
| 184 | (4-環丙基哌嗪-1-基)(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)甲酮 | |
| 185 | (7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(4-(嘧啶-2-基)哌嗪-1-基)甲酮 | |
| 186 | 7-(3,4-二甲氧基苯基)-N-(4-(嗎啉-4-羰基)雙環[2.2.2]辛-1-基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 187 | (R)-N-(1-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羰基)吡咯啶-3-基)-4-甲基哌嗪-1-甲醯胺 | |
| 188 | (R)-N-(1-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羰基)吡咯啶-3-基)-1-甲基哌啶-4-甲醯胺 | |
| 189 | 6-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)菸鹼酸3-(4-甲基哌嗪-1-基)丙酯 | |
| 190 | 5-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)吡啶甲酸甲酯 | |
| 191 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)-2-甲基苯甲酸甲酯 | |
| 192 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)-2-甲氧基苯甲酸甲酯 | |
| 193 | 7-(3,4-二甲氧基苯基)-N-(4-(4-甲基哌嗪-1-基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 194 | 7-(3,4-二甲氧基苯基)-N-(4-嗎啉基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 195 | (S)-7-(3,4-二甲氧基苯基)-N-(4-(3,4-二甲基哌嗪-1-羰基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 196 | (1s,4s)-4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)環己烷-1-羧酸3-嗎啉基丙酯 | |
| 197 | (1r,4r)-4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)環己烷-1-羧酸3-嗎啉基丙酯 | |
| 198 | 7-(3,4-二甲氧基苯基)-N-(4-(2-嗎啉基乙氧基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 199 | 3-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)雙環[1.1.1]戊烷-1-羧酸3-嗎啉基丙酯 | |
| 200 | (第三丁氧基羰基)-L-纈胺酸4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯酯 | |
| 201 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)-3-甲氧基苯甲酸甲酯 | |
| 202 | 7-(3,4-二甲氧基苯基)-N-((1r,4r)-4-((2-嗎啉基乙基)胺甲醯基)環己基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 203 | 7-(3,4-二甲氧基苯基)-N-((1r,4r)-4-((3-嗎啉基丙基)胺甲醯基)環己基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 204 | 7-(3,4-二甲氧基苯基)-N-(5-(4-甲基哌嗪-1-基)吡啶-2-基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 205 | 7-(3,4-二甲氧基苯基)-N-(5-嗎啉基吡啶-2-基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 206 | (S)-(4-苯甲基-3-甲基哌嗪-1-基)(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)甲酮 | |
| 207 | (4-苯甲基-3,3-二甲基哌嗪-1-基)(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)甲酮 | |
| 208 | (S)-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(3,4-二甲基哌嗪-1-基)甲酮 | |
| 209 | (4-苯甲醯基哌嗪-1-基)(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)甲酮 | |
| 210 | (S)-(4-苯甲醯基-3-甲基哌嗪-1-基)(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)甲酮 | |
| 211 | (4-苯甲醯基-3,3-二甲基哌嗪-1-基)(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)甲酮 | |
| 212 | (4-(2,6-二氟苯甲基)哌嗪-1-基)(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)甲酮 | |
| 213 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)-2-甲基苯甲酸 | |
| 214 | 7-(3,4-二甲氧基苯基)-N-(3-甲基-4-(嗎啉-4-羰基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 215 | 7-(3,4-二甲氧基苯基)-N-(3-甲基-4-(4-甲基哌嗪-1-羰基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 216 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)-2-甲氧基苯甲酸 | |
| 217 | 7-(3,4-二甲氧基苯基)-N-(3-甲氧基-4-(嗎啉-4-羰基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 218 | 7-(3,4-二甲氧基苯基)-N-(3-甲氧基-4-(4-甲基哌嗪-1-羰基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 219 | 7-(3,4-二甲氧基苯基)-N-(4-((2-(二甲基胺基)乙基)(甲基)胺甲醯基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 220 | 7-(3,4-二甲氧基苯基)-N-(4-((3-(二甲基胺基)丙基)胺甲醯基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 221 | N-(4-((2-(二乙基胺基)乙基)胺甲醯基)苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 222 | N-(4-((3-(二乙基胺基)丙基)胺甲醯基)苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 223 | 7-(3,4-二甲氧基苯基)-N-(4-((2-(吡咯啶-1-基)乙基)胺甲醯基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 224 | 7-(3,4-二甲氧基苯基)-N-(4-((3-(吡咯啶-1-基)丙基)胺甲醯基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 225 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸2-(吡咯啶-1-基)乙酯 | |
| 226 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸3-(吡咯啶-1-基)丙酯 | |
| 227 | (第三丁氧基羰基)甘胺酸4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯酯 | |
| 228 | (第三丁氧基羰基)-L-丙胺酸4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯酯 | |
| 229 | N-(4-丁氧基苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 230 | 7-(3,4-二甲氧基苯基)-N-(4-丙氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 231 | 1-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羰基)吲哚啉-5-羧酸 | |
| 232 | 1-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羰基)吲哚啉-6-羧酸 | |
| 233 | 1-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羰基)-1,2,3,4-四氫喹啉-6-羧酸 | |
| 234 | 4-(7-(3,4-二甲氧基苯基)-N-甲基吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸 | |
| 235 | (7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(6-(4-甲基哌嗪-1-羰基)-3,4-二氫喹啉-1(2H)-基)甲酮 | |
| 236 | (7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(6-(嗎啉-4-羰基)-3,4-二氫喹啉-1(2H)-基)甲酮 | |
| 237 | (7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(7-(4-甲基哌嗪-1-羰基)-3,4-二氫異喹啉-2(1H)-基)甲酮 | |
| 238 | (7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(7-(嗎啉-4-羰基)-3,4-二氫異喹啉-2(1H)-基)甲酮 | |
| 239 | 7-(3,4-二甲氧基苯基)-N-((1S,4S)-4-(4-甲基哌嗪-1-羰基)環己基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 240 | 7-(3,4-二甲氧基苯基)-N-((1S,4S)-4-(4-甲基哌嗪-1-羰基)環己基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 241 | 7-(3,4-二甲氧基苯基)-N-((1r,4r)-4-(4-甲基哌嗪-1-羰基)環己基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 242 | 6-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)菸鹼酸2-嗎啉基乙酯 | |
| 243 | 7-(3,4-二甲氧基苯基)-N-(4-((4-甲基哌嗪-1-基)甲基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 244 | 7-(3,4-二甲氧基苯基)-N-(4-(嗎啉基甲基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 245 | 7-(3,4-二甲氧基苯基)-N-(4-(4-甲基哌嗪-1-基)苯甲基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 246 | 7-(3,4-二甲氧基苯基)-N-(4-嗎啉基苯甲基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 247 | (1S,4S)-4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)環己烷-1-羧酸吡啶-2-基甲酯 | |
| 248 | 7-(3,4-二甲氧基苯基)-N-甲基-N-(4-(4-甲基哌嗪-1-羰基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 249 | 7-(3,4-二甲氧基苯基)-N-甲基-N-(4-(嗎啉-4-羰基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 250 | (7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(5-(4-甲基哌嗪-1-羰基)吲哚啉-1-基)甲酮 | |
| 251 | (7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(5-(嗎啉-4-羰基)吲哚啉-1-基)甲酮 | |
| 252 | (7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(6-(4-甲基哌嗪-1-羰基)吲哚啉-1-基)甲酮 | |
| 253 | (7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(6-(嗎啉-4-羰基)吲哚啉-1-基)甲酮 | |
| 254 | 6-(3,4-二甲氧基苯基)-N-(4-乙氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 255 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)雙環[2.2.2]辛烷-1-羧酸3-嗎啉基丙酯 | |
| 256 | (4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯基)胺甲酸第三丁酯 | |
| 257 | N-(4-胺基苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 258 | 7-(3,4-二甲氧基苯基)-N-(4-(2-(二甲基胺基)乙醯胺基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 259 | (S)-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(3-甲基-4-(全氟苯甲醯基)哌嗪-1-基)甲酮 | |
| 260 | (S)-(4-(2-氯苯甲醯基)-3-甲基哌嗪-1-基)(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)甲酮 | |
| 261 | (S)-(4-(3-氯苯甲醯基)-3-甲基哌嗪-1-基)(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)甲酮 | |
| 262 | (S)-(4-(4-氯苯甲醯基)-3-甲基哌嗪-1-基)(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)甲酮 | |
| 263 | (S)-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(4-(3-氟苯甲醯基)-3-甲基哌嗪-1-基)甲酮 | |
| 264 | 7-(3,4-二甲氧基苯基)-N-(6-(嗎啉-4-羰基)吡啶-3-基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 265 | 7-(3,4-二甲氧基苯基)-N-(6-(4-甲基哌嗪-1-羰基)吡啶-3-基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 266 | 7-(3,4-二甲氧基苯基)-N-(4-(4-異丙基哌嗪-1-基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 268 | N-(4-溴苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 269 | 7-(3,4-二甲氧基苯基)-N-(4-(哌啶-1-基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 270 | 7-(3,4-二甲氧基苯基)-N-(4-(4-乙基哌嗪-1-基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 271 | 4-(4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯基)哌嗪-1-羧酸第三丁酯 | |
| 272 | 4-(6-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)吡啶-3-基)哌嗪-1-羧酸第三丁酯 | |
| 273 | N-(4-(3,6-二氫吡啶-1(2H)-基)苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 274 | N-(4-(1,4-二氧雜-8-氮雜螺[4.5]癸-8-基)苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 275 | 4-(2-((4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲醯基)氧基)乙基)哌嗪-1-羧酸第三丁酯 | |
| 276 | 7-(3,4-二甲氧基苯基)-N-(4-(二甲基胺基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 277 | 7-(3,4-二甲氧基苯基)-N-(4-(吡咯啶-1-基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 278 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)-2-氟苯甲酸 | |
| 279 | 2-氯-4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸 | |
| 280 | (2-((4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯基)胺基)-2-側氧基乙基)胺甲酸第三丁酯 | |
| 281 | (S)-(1-((4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯基)胺基)-1-側氧基丙-2-基)胺甲酸第三丁酯 | |
| 282 | (S)-(1-((4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯基)胺基)-3-甲基-1-側氧基丁-2-基)胺甲酸第三丁酯 | |
| 283 | N-(4-(2-胺基乙醯胺基)苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 284 | (S)-N-(4-(2-胺基丙醯胺基)苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 285 | 7-(3,4-二甲氧基苯基)-N-(4-(4-側氧基哌啶-1-基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 286 | 7-(3,4-二甲氧基苯基)-N-(5-(哌嗪-1-基)吡啶-2-基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 287 | N-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)-4-乙氧基苯甲醯胺 | |
| 288 | N-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)-4-嗎啉基雙環[2.2.2]辛烷-1-甲醯胺 | |
| 289 | 7-(3,4-二甲氧基苯基)-N-(5-(吡咯啶-1-基)吡啶-2-基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 290 | 7-(3,4-二甲氧基苯基)-N-(4-異丙氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 291 | N-(3,5-雙(三氟甲基)苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 292 | 7-(3,4-二甲氧基苯基)-N-(4-(羥基甲基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 293 | 7-(3,4-二氟苯基)-N-(4-乙氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 294 | 7-(4-甲氧基-3-硝基苯基)-N-(5-嗎啉基吡啶-2-基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 295 | N-(4-乙氧基苯基)-7-(4-甲氧基-3-硝基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 296 | N-(4-乙氧基苯基)-7-(2-氟-4-甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 297 | 7-(2-氟-4-甲氧基苯基)-N-(5-嗎啉基吡啶-2-基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 298 | 7-(3-氯-4-(三氟甲氧基)苯基)-N-(4-乙氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 299 | 7-(3-氯-4-(三氟甲氧基)苯基)-N-(5-嗎啉基吡啶-2-基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 301 | N-(4-乙氧基苯基)-7-(間甲苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 302 | N-(4-乙氧基苯基)-7-(4-氟-3-甲基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 303 | N-(4-乙氧基苯基)-7-(噻吩-2-基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 304 | 7-(4-氯-2-氟苯基)-N-(4-乙氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 306 | N-(5-嗎啉基吡啶-2-基)-7-(間甲苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 307 | N-(4-乙氧基苯基)-7-(4-氟-3-甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 308 | N-(4-乙氧基苯基)-7-(3-氟-4-甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 309 | 7-(3,4-二甲氧基苯基)-N-(1-甲基-1H-吲哚-5-基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 311 | 7-(3,4-二甲氧基苯基)-N-(2-氟-4-嗎啉基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 312 | 7-(3,4-二甲氧基苯基)-N-(5-(二甲基胺基)吡啶-2-基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 313 | 7-(2,3-二氫苯并呋喃-5-基)-N-(4-乙氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 314 | 7-(3,4-二甲氧基苯基)-N-(5-乙氧基吡啶-2-基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 315 | 7-(3,5-二甲氧基苯基)-N-(4-乙氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 316 | 7-(3-氯-4-氟苯基)-N-(4-乙氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 317 | (S)-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(4-(2-甲氧基苯甲醯基)-3-甲基哌嗪-1-基)甲酮 | |
| 318 | (S)-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(4-(3-甲氧基苯甲醯基)-3-甲基哌嗪-1-基)甲酮 | |
| 319 | (S)-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(4-(4-甲氧基苯甲醯基)-3-甲基哌嗪-1-基)甲酮 | |
| 320 | 7-(3,4-二甲氧基苯基)-N-(4-嗎啉基雙環[2.2.2]辛-1-基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 321 | (R)-4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羰基)-2-甲基哌嗪-1-羧酸第三丁酯 | |
| 322 | (R)-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(3-甲基哌嗪-1-基)甲酮 | |
| 323 | N-(4-乙氧基苯基)-7-(6-甲氧基吡啶-3-基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 324 | 7-(4-(二甲基胺基)苯基)-N-(4-乙氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 325 | 7-(3,4-二甲氧基苯基)-N-(2-氟-4-甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 326 | N-(2,3-二氟-4-甲氧基苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 327 | 7-(3,4-二甲氧基苯基)-N-(5-羥基吡啶-2-基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 328 | (1R,4R)-4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)環己烷-1-羧酸(2-甲氧基乙氧基)甲酯 | |
| 329 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸(2-甲氧基乙氧基)甲酯 | |
| 330 | (1R,4R)-4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)環己烷-1-羧酸乙酯 | |
| 331 | (1R,4R)-4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)環己烷-1-羧酸丙酯 | |
| 332 | (1r,4r)-4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)環己烷-1-羧酸丁酯 | |
| 333 | (1r,4r)-4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)環己烷-1-羧酸癸酯 | |
| 335 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸丙酯 | |
| 336 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸丁酯 | |
| 337 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸癸酯 | |
| 338 | 7-(3,4-二甲氧基苯基)-N-(4-(4-(吡啶-2-基)哌嗪-1-羰基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 339 | 7-(4,5-二甲氧基-2-甲基苯基)-N-(4-乙氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 340 | 7-(3,4-二甲氧基苯基)-N-((1R,4R)-4-((1-(四氫-2H-哌喃-4-基)哌啶-4-基)胺甲醯基)環己基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 341 | 7-(3,4-二甲氧基苯基)-N-((1R,4R)-4-(4-嗎啉基哌啶-1-羰基)環己基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 342 | 7-(3,4-二甲氧基苯基)-N-((1R,4R)-4-(4-(吡啶-2-基)哌嗪-1-羰基)環己基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 343 | N-((1R,4R)-4-([1,4'-聯哌啶]-1'-羰基)環己基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 344 | (R)-(4-苯甲醯基-3-甲基哌嗪-1-基)(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)甲酮 | |
| 345 | 7-(3,4-二甲氧基苯基)-N-((1R,4R)-4-嗎啉基環己基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 346 | 7-(3,4-二甲氧基苯基)-N-(4-((2-甲氧基乙氧基)甲氧基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 347 | (7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(3,5-二甲基哌嗪-1-基)甲酮 | |
| 348 | (4-苯甲醯基-3,5-二甲基哌嗪-1-基)(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)甲酮 | |
| 349 | 7-(3,4-二甲氧基苯基)-N-(2-氟-4-(4-嗎啉基哌啶-1-羰基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 | |
| 350 | (S)-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(4-(4-氟苯甲醯基)-3-甲基哌嗪-1-基)甲酮 | |
| 351 | (S)-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(3-甲基-4-(4-甲基苯甲醯基)哌嗪-1-基)甲酮 | |
| 352 | (S)-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(3-甲基-4-(噻吩-2-羰基)哌嗪-1-基)甲酮 | |
| 353 | (S)-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(4-(呋喃-2-羰基)-3-甲基哌嗪-1-基)甲酮 | |
| 354 | (S)-4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羰基)-2-甲基-N-苯基哌嗪-1-甲醯胺 | |
| 355 | (S)-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(3-甲基-4-(苯基磺醯基)哌嗪-1-基)甲酮 | |
| 356 | (S)-(4-(2,5-二氟苯甲醯基)-3-甲基哌嗪-1-基)(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)甲酮 | |
| 357 | (S)-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(4-異菸鹼醯基-3-甲基哌嗪-1-基)甲酮 | |
| 358 | (7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)((3R,5S)-3,5-二甲基哌嗪-1-基)甲酮 | |
| 359 | (7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)((3S,5S)-3,5-二甲基哌嗪-1-基)甲酮 | |
| 360 | (7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)((2R,5S)-2,5-二甲基哌嗪-1-基)甲酮 | |
| 361 | (7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(4,7-二氮雜螺[2.5]辛-7-基)甲酮 | |
| 362 | (7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)((2S,5S)-2,5-二甲基哌嗪-1-基)甲酮 | |
| 363 | ((3R,5S)-4-苯甲醯基-3,5-二甲基哌嗪-1-基)(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)甲酮 | |
| 364 | ((3S,5S)-4-苯甲醯基-3,5-二甲基哌嗪-1-基)(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)甲酮 | |
| 365 | ((2R,5S)-4-苯甲醯基-2,5-二甲基哌嗪-1-基)(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)甲酮 | |
| 366 | ((2S,5S)-4-苯甲醯基-2,5-二甲基哌嗪-1-基)(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)甲酮 | |
| 367 | (4-苯甲醯基-4,7-二氮雜螺[2.5]辛-7-基)(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)甲酮 | |
| 368 | (S)-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(4-(2-氟苯甲醯基)-3-甲基哌嗪-1-基)甲酮 | |
| 369 | (S)-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(3-甲基-4-(3-甲基苯甲醯基)哌嗪-1-基)甲酮 | |
| 370 | (S)-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(4-(呋喃-3-羰基)-3-甲基哌嗪-1-基)甲酮 | |
| 371 | (S)-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(3-乙基哌嗪-1-基)甲酮 | |
| 372 | (S)-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(3-異丙基哌嗪-1-基)甲酮 | |
| 373 | (S)-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(3-丙基哌嗪-1-基)甲酮 | |
| 374 | (S)-(3-環丙基哌嗪-1-基)(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)甲酮 | |
| 375 | (S)-(4-苯甲醯基-3-乙基哌嗪-1-基)(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)甲酮 | |
| 376 | (S)-(4-苯甲醯基-3-異丙基哌嗪-1-基)(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)甲酮 | |
| 377 | (S)-(4-苯甲醯基-3-丙基哌嗪-1-基)(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)甲酮 | |
| 378 | (S)-(4-苯甲醯基-3-環丙基哌嗪-1-基)(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)甲酮 | |
| 379 | (S)-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(3-甲基-4-(噻吩-3-羰基)哌嗪-1-基)甲酮 | |
| 380 | (S)-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(3-甲基-4-吡啶甲醯基哌嗪-1-基)甲酮 | |
| 381 | (S)-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(3-甲基-4-(2-甲基苯甲醯基)哌嗪-1-基)甲酮 | |
| 382 | (S)-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(3-甲基-4-菸鹼醯基哌嗪-1-基)甲酮 | |
| 383 | (S)-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(3-甲基-4-(嘧啶-2-羰基)哌嗪-1-基)甲酮 | |
| 384 | (R)-N-(1-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羰基)吡咯啶-3-基)苯甲醯胺 | |
| 385 | (S)-(4-(1H-咪唑-2-羰基)-3-甲基哌嗪-1-基)(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)甲酮 | |
| 386 | (S)-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(3-甲基-4-(1-甲基-1H-咪唑-2-羰基)哌嗪-1-基)甲酮 | |
| 387 | (S)-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(3-甲基-4-(1H-吡咯-2-羰基)哌嗪-1-基)甲酮 | |
| 388 | (S)-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(3-甲基-4-(1-甲基-1H-吡咯-2-羰基)哌嗪-1-基)甲酮 | |
| 389 | (S)-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(4-(異噁唑-3-羰基)-3-甲基哌嗪-1-基)甲酮 | |
| 390 | (S)-(4-(1H-吲哚-2-羰基)-3-甲基哌嗪-1-基)(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)甲酮 | |
| 391 | (S)-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(4-(異噁唑-5-羰基)-3-甲基哌嗪-1-基)甲酮 | |
| 392 | (S)-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(3-甲基-4-(噁唑-2-羰基)哌嗪-1-基)甲酮 | |
| 393 | (S)-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(3-甲基-4-(5-甲基呋喃-2-羰基)哌嗪-1-基)甲酮 | |
| 394 | (S)-(4-(苯并呋喃-2-羰基)-3-甲基哌嗪-1-基)(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)甲酮 | |
| 395 | (S)-苯并[b]噻吩-2-基(4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羰基)-2-甲基哌嗪-1-基)甲酮 |
在式(Ia)之一些實施例中,化合物係表2化合物,或其醫藥上可接受之鹽、溶劑化物、水合物、前藥或立體異構體。
在式(Ia)之一些實施例中,化合物不為表2化合物,或其醫藥上可接受之鹽、溶劑化物、水合物、前藥或立體異構體。
在式(Ia)之一些實施例中,當R
1及R
9係H,R
4係
、R
5係H及R
6係經取代之芳基時;則R
2不為4-氟-苯基。在式(Ia)之一些實施例中,當R
1及R
9係H,R
4係
,R
5係H及R
6係經取代之芳基時;則R
2不為對甲苯。在式(Ia)之一些實施例中,當R
1及R
9係H,R
4係
,R
5係H及R
6係經取代之芳基時;則R
2不為3,5-二氯-苯基。在式(Ia)之一些實施例中,當R
1及R
9係H,R
4係
,R
5係H及R
6係視需要經取代之芳基時;則R
2不為苯基。
在式(Ia)之一些實施例中,當R
1及R
9係H及R
4係下列中之任一者:
時,則R
2不為3,4-二甲氧基-苯基。
| 表2:例示性化合物 | |
| 化合物 | 名稱 |
| 3 | 7-(3,4-二甲氧基苯基)-N-(4-乙氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 5 | 7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羧酸 |
| 11 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸甲酯 |
| 267 | 7-(3,4-二甲氧基苯基)-N-(4-氟苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 300 | N-(4-乙氧基苯基)-7-苯基吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 305 | 4-(7-苯基吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸甲酯 |
| 310 | N-(苯并[d][1,3]二噁唑-5-基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 334 | 4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸乙酯 |
| 396 | 7-(3,4-二甲氧基苯基)-N-(對甲苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 397 | N-(4-氯苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 398 | 7-(3,4-二甲氧基苯基)-N-(4-乙基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 399 | 7-(3,4-二甲氧基苯基)-N-(4-(三氟甲氧基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 400 | 7-(3,4-二甲氧基苯基)-N-(4-異丙基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 401 | N-(2-氯-4-甲基苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 402 | N-(3-氯-4-甲基苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 403 | N-(3-氯-4-甲氧基苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 404 | 7-(3,4-二甲氧基苯基)-N-(3-氟-4-甲基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 405 | 7-(3,4-二甲氧基苯基)-N-(3,4-二甲基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 406 | N-(3-氯-4-氟苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 407 | N-(4-乙醯胺基苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 408 | N-(4-氯-2-甲基苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 409 | N-(2,4-二氟苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 410 | N-(4-溴-2-甲基苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 411 | N-(2,4-二甲氧基苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 412 | N-(5-氯-2,4-二甲氧基苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 413 | N-(4-氯-2-甲氧基-5-甲基苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 414 | 7-(3,4-二甲氧基苯基)-N-(2-甲氧基-5-甲基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 415 | 7-(3,4-二甲氧基苯基)-N-(2,5-二甲基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 416 | N-(2,5-二乙氧基苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 417 | N-(5-氯-2-甲基苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 418 | N-(2,5-二甲氧基苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 419 | 7-(3,4-二甲氧基苯基)-N-(5-氟-2-甲基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 420 | 7-(3,4-二甲氧基苯基)-N-(2-乙氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 421 | 7-(3,4-二甲氧基苯基)-N-(鄰甲苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 422 | 7-(3,4-二甲氧基苯基)-N-(2-乙基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 423 | 7-(3,4-二甲氧基苯基)-N-(2-氟苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 424 | 7-(3,4-二甲氧基苯基)-N-(2,3-二甲基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 425 | N-(3-氯-2-甲基苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 426 | N-(3-氯苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 427 | N-(4-(4-氯-1H-吡唑-1-基)苯基)-7-(3,5-二氯苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 428 | 7-(3,4-二甲氧基苯基)-N-(3-氟苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 429 | 7-(3,4-二甲氧基苯基)-N-(3-乙基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 430 | 7-(3,4-二甲氧基苯基)-N-(3-(甲基硫基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 431 | N-(3-乙醯基苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 432 | 3-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸乙酯 |
| 433 | 7-(3,4-二甲氧基苯基)-N-(3,5-二甲基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 434 | 7-(3,4-二甲氧基苯基)-N-(3,5-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 435 | N-(2,5-二甲氧基苯基)-7-苯基吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 436 | N-(2,4-二甲氧基苯基)-7-苯基吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 437 | N-(4-甲氧基-2-甲基苯基)-7-苯基吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 438 | N-(4-氟-2-甲基苯基)-7-苯基吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 439 | N-(2,4-二氟苯基)-7-苯基吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 440 | N-(3-甲氧基苯基)-7-苯基吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 441 | N-(2-甲氧基苯基)-7-苯基吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 442 | N-(2-乙氧基苯基)-7-苯基吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 443 | N-(4-甲氧基苯基)-7-苯基吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 445 | N-(4-氟苯基)-7-苯基吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 446 | N-(2-氟苯基)-7-苯基吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 447 | N-(3-氟苯基)-7-苯基吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 448 | N-(3-氟-4-甲基苯基)-7-苯基吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 449 | N-(3,4-二氟苯基)-7-苯基吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 450 | N-(2-乙氧基苯基)-7-苯基吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 451 | N-(3-氯-4-甲氧基苯基)-7-苯基吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 452 | N-(3-氯-4-氟苯基)-7-苯基吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 453 | N-(5-氯-2-甲氧基苯基)-7-苯基吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 454 | N-(2-甲氧基-5-甲基苯基)-7-苯基吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 455 | N-(5-氟-2-甲基苯基)-7-苯基吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 456 | N-(2-氟-5-甲基苯基)-7-苯基吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 457 | N-(2,5-二氟苯基)-7-苯基吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 458 | N-(4-乙醯胺基苯基)-7-苯基吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 459 | 7-苯基-N-(4-(三氟甲氧基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 460 | 吲哚啉-1-基(7-苯基吡唑并[1,5-a]嘧啶-2-基)甲酮 |
| 461 | 7-(4-氟苯基)-N-(3-甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 462 | 7-(4-氟苯基)-N-(2-甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 463 | N-(2-乙氧基苯基)-7-(4-氟苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 464 | N-(3,4-二甲氧基苯基)-7-(4-氟苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 465 | 7-(4-氟苯基)-N-(4-甲氧基-2-甲基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 466 | N-(2,5-二氟苯基)-7-(4-氟苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 467 | N-(4-乙醯基苯基)-7-(4-氟苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 468 | N-(2,4-二氟苯基)-7-(4-氟苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 469 | N-(5-氟-2-甲基苯基)-7-(4-氟苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 470 | N-(4-氟-2-甲基苯基)-7-(4-氟苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 471 | N-(4-乙氧基苯基)-7-(4-氟苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 472 | N-(4-(二甲基胺基)苯基)-7-(4-氟苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 473 | N-(4-乙醯胺基苯基)-7-(4-氟苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 474 | N-(4-胺甲醯基苯基)-7-(4-氟苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 475 | N-(2-氟苯基)-7-(4-氟苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 476 | 7-(4-氟苯基)-N-(鄰甲苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 474 | 7-(4-氟苯基)-N-(間甲苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 478 | 7-(4-氟苯基)-N-苯基吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 479 | N-(3-乙醯基苯基)-7-(4-氟苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 480 | N-(4-氟-3-硝基苯基)-7-(4-氟苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 481 | (7-(4-氟苯基)吡唑并[1,5-a]嘧啶-2-基)(吲哚啉-1-基)甲酮 |
| 482 | N-均三甲苯基-7-(對甲苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 483 | N-(4-甲氧基-2-甲基苯基)-7-(對甲苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 484 | N-(2-氯-6-甲基苯基)-7-(對甲苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
| 485 | N-(4-(4-氯-1H-吡唑-1-基)苯基)-7-(3,5-二氯苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺 |
應瞭解本文描述之化合物之鹽、溶劑化物、水合物、前藥及/或立體異構體之所有變化意欲包含於本發明內。
5.1.1. 同位素標記類似物
本發明亦包含同位素標記化合物,除一或多個原子經具有與自然界中通常發現之原子質量或質量數不同之原子質量或質量數之原子置換外,該等化合物與彼等如本文描述之化合物相同(「類同位素分子」)。本發明之化合物亦可於一或多個原子處含有非自然比例之原子同位素構成此等化合物。可併入本文描述之化合物內之同位素之實例包括氫、碳、氮、氧、磷、氟及氯之同位素,諸如分別
2H (「D」)、
3H、
13C、
14C、
15N、
18O、
17O、
31P、
32P、
35S、
18F及
36Cl。例如,本文描述之化合物可具有一或多個經氘置換之H原子。
一般而言,對某種元素(諸如氫或H)之參考或描述意欲包括該元素之所有同位素。例如,若R基團係經定義以包括氫或H,則其亦包括氘及氚。因此,包含放射性同位素(諸如氚、
14C、
32P及
35S)之化合物係於現有技術之範疇內。基於本文之揭示內容,熟習此項技術者將顯而易見用於將此等標記插入現有技術之化合物內之程序。
除非另有規定,否則本文描述之化合物旨在包括不同之處僅在於存在一或多個同位素富集原子之化合物。例如,除氘或氚置換氫,或
13C或
14C富集碳置換碳外,具有本發明結構之化合物係於本發明之範圍內。
在一些實施例中,某些同位素標記化合物(諸如彼等經
3H及
14C標記者)可適用於化合物及/或受質組織分佈分析中。氚化(
3H)及碳14 (
14C)同位素可因其等易於製備及可偵測性而特別佳。此外,經較重同位素(諸如氘)之取代可提供某些由較大之代謝穩定性產生之治療優勢,諸如活體內半衰期增加或劑量要求減少,且因此在某些情況下可較佳。同位素標記化合物一般可藉由遵循與彼等本文(例如,實例部分中)揭示者類似之程序,藉由用同位素標記試劑取代非同位素標記試劑製備。
在一些實施例中,如本文描述,本發明中揭示之化合物係化合物,或其醫藥上可接受之鹽、溶劑化物、水合物、前藥或立體異構體中之任一者之氘化類似物。式(Ia)至(Ie)化合物之氘化類似物係其中一或多個氫原子經氘取代之化合物。在一些實施例中,該氘化類似物係式(Ia)化合物,其包括氘化R
x基團,例如,R
1至R
9基團。在式(Ia)化合物之氘化類似物之一些實施例中,其中任選取代基係包括至少一個氘原子之視需要經取代之雜環烷基(例如
、
、
及
)。
經氘取代之化合物係使用諸如描述於以下中之各種方法合成:Dean, Dennis C.編;Recent Advances in the Synthesis and Applications of Radiolabeled Compounds for Drug Discovery and Development. [於以下中:Curr., Pharm. Des., 2000; 6(10)] 2000,第110頁;George W.;Varma, Rajender S. The Synthesis of Radiolabeled Compounds via Organometallic Intermediates, Tetrahedron, 1989, 45(21), 6601-21;及Evans, E. Anthony. Synthesis of radiolabeled compounds, J. Radioanal. Chem., 1981, 64(1-2), 9-32。
氘化起始材料容易獲得且經受本文描述之合成方法以提供含氘化合物之合成。大量含氘試劑及建構組元可自化學品供應商(諸如Aldrich Chemical Co)購買獲得。
5.1.2. 氟化類似物
在一些實施例中,如本文描述,本發明中揭示之化合物係化合物,或其醫藥上可接受之鹽、溶劑化物、水合物、前藥或立體異構體中之任一者之氟化類似物。式(Ia)至(Ie)化合物之氟化類似物係其中一或多個氫原子或取代基經氟原子取代之化合物。在一些實施例中,該氟化類似物係式(Ia)至(Ie)化合物,其包括氟化R
1、R
2、R
3、R
4、R
5、R
6、R
7、R
8、R
9、R
10、R
11、R
12、R
13、R
14、R
15、R
16、R
17、R
18、R
19、R
20、R
31、R
32基團,或其他取代基R基團。在式(Ia)至(Ie)化合物之氟化類似物之一些實施例中,脂族或芳族C-H鍵之氫原子係經氟原子置換。在式(Ia)至(Ie)化合物之氟化類似物之一些實施例中,視需要經取代之芳基或視需要經取代之雜芳基中之至少一個氫係經氟原子置換。在式(Ia)至(Ie)化合物之氟化類似物之一些實施例中,羥基取代基(-OH)或胺基取代基(-NH
2)係經氟原子置換。
5.1.3. 異構體
如本文描述,術語「化合物」意欲包括本文繪示結構之所有立體異構體、幾何異構體、互變異構體及同位素。
本文描述之化合物可具有不對稱中心、幾何中心(例如,雙鍵),或兩者。除非明確指示特定立體化學或異構形式,否則預期結構之所有對掌性、非對映異構、外消旋形式及所有幾何異構形式。在一些實施例中,本文描述之化合物具有一或多個對掌性中心。應瞭解若未明確指示絕對立體化學,則各對掌性中心可獨立地係R構型或S構型或其混合物。因此,如自本描述顯而易見,本文描述之化合物包括於任何及所有不對稱原子處富集或拆分之光學異構體。可分離或合成R對映體及S對映體之外消旋混合物,及包含R及S對映體之對映體富集之立體異構混合物,及個別光學異構體以便於大體上不含其等對映異構或非對映異構夥伴,且此等立體異構體均於現有技術之範疇內。
含有經不對稱取代之原子之本發明之化合物可以光學活性或外消旋形式分離。此項技術中熟知製備光學活性形式之方式,諸如藉由拆分外消旋形式、藉由自光學活性起始材料合成或通過使用對掌性助劑。
由取代基圍繞碳-碳雙鍵排佈或取代基圍繞環烷基或雜環排佈產生之幾何異構體亦可存在於本發明之化合物中。烯烴、C=N雙鍵或其他類型之雙鍵之幾何異構體可存在於本文描述之化合物中,且所有此等穩定異構體均包括於本發明中。具體言之,本發明之化合物之順式及反式幾何異構體亦可存在且可呈異構體之混合物或呈分離之異構形式分離。
本發明之化合物亦包括互變異構形式。互變異構形式由單鍵與相鄰雙鍵交換及質子之伴隨遷移產生。互變異構形式包括質子互變異構體,其等係具有相同實驗式及總電荷之異構質子化狀態。實例質子互變異構體,包括酮-烯醇對、醯胺-醯亞胺酸對、內醯胺-內醯亞胺對、醯胺-醯亞胺酸對、烯胺-亞胺對,及其中一個質子可佔據雜環系統之兩個或更多個位置之環形形式,諸如,1H-及3H-咪唑、1H-、2H-及4H-1,2,4-三唑、1H-及2H-異吲哚,及1H-及2H-吡唑。互變異構形式可處於平衡或藉由適當取代在空間上鎖定為一種形式。
5.1.4. 鹽及其他形式
在一些實施例中,本文描述之化合物係以鹽形式存在。在一些實施例中,該等化合物係以醫藥上可接受之鹽之形式提供。
包括於本發明組合物中之本質上呈鹼性之化合物可與各種無機及有機酸形成多種鹽。可用以製備此等鹼性化合物之醫藥上可接受之酸加成鹽的酸係彼等形成無毒酸加成鹽(即,含有醫藥上可接受之陰離子之鹽)者,包括(但不限於)氯化物。
含有胺官能基或含氮雜芳基之化合物本質上可呈鹼性且可與多種無機及有機酸反應以形成相應之鹽。該等化合物可以自無機酸或有機酸衍生之醫藥上可接受之鹽的形式使用。在一些實施例中,該醫藥上可接受之鹽可為自鹽酸衍生之鹽(即,如本文描述之化合物之鹽酸鹽),或類似物。
本發明之化合物之醫藥上可接受之鹽可藉由將該化合物溶解於與水混溶之有機溶劑(諸如丙酮、甲醇、乙醇或乙腈等)中,並添加過量之有機酸或無機酸水溶液,且沈澱或結晶產生。然後,可能藉由自此混合物蒸發該溶劑或過量酸及然後將其乾燥或藉由過濾經萃取之鹽產生鹽來獲得另外鹽。
鹽之其他實例包括本發明之化合物之陰離子與合適陽離子之化合。針對治療用途,本發明之化合物之鹽可為醫藥上可接受的。然而,非醫藥上可接受之酸及鹼之鹽亦發現可用於(例如)製備或純化醫藥上可接受之化合物。
包括於本發明組合物中之本質上呈酸性之化合物可與多種醫藥上可接受之陽離子形成鹼鹽。此等鹽之實例包括鹼金屬或鹼土金屬鹽。
包括鹼性或酸性部分之化合物亦可與多種胺基酸形成醫藥上可接受之鹽。本發明之化合物可含有酸性及鹼性基團兩者;例如,一個胺基及一個羧基。在此情況下,該化合物可以酸加成鹽、兩性離子或鹼鹽的形式存在。
本文描述之化合物可以多種形式存在,包括彼等化合物、醫藥上可接受之鹽之結晶、粉末及非晶型形式,例如,該等化合物之多晶型、假多晶型、溶劑化物、水合物、非溶劑化多晶型(包括水合物)、構象多晶型及非晶型形式,及其混合物。
本文描述之化合物可以溶劑化物,尤其水合物的形式存在,且除非另有規定,否則所有此等溶劑化物及水合物均為預期的。水合物可在製造化合物或包含該等化合物之組合物期間形成,或水合物可由於該等化合物之吸濕性而經時形成。現有技術之化合物亦可以有機溶劑化物的形式存在,包括DMF、醚及醇溶劑化物等。任何特定溶劑化物之識別及製備係於合成有機或醫藥化學之一般技工之技能內。
在一些實施例中,本文描述之化合物係以溶劑化物形式存在。在一些實施例中,當該溶劑化物之溶劑組分係水時,本文描述之化合物係以水合物形式存在。
5.1.5. 前藥
本發明之態樣包括本文描述之化合物中之任一者之前藥形式。標的化合物之任何便利之前藥形式可例如根據由Rautio等人,(「Prodrugs: design and clinical applications」, Nature Reviews Drug Discovery 7, 255-270 (2008年2月))描述之方案及方法加以製備。
術語「前藥」係指藉由一些生理或化學方法轉化為活體內生物活性藥物之藥劑。在一些實施例中,當在生理pH下經受生物系統時,前藥轉化為所需之藥物形式。在一些實施例中,當經受生物系統時,前藥酶促轉化為所需之藥物形式。
本文描述之化合物中之任一者之前藥形式可由於所得化合物於體內之半衰期延長,或所需活性劑量減少之結果而適用於(例如)提供特定之治療益處。
前藥因為其等比母藥更容易投與而亦可用於某些情況。前藥可藉由經口投與而為例如生物可利用,而母藥則不可。相比於該母藥,該前藥亦可具有於藥理組合物中經改善之溶解度。
本發明之化合物之前藥形式或衍生物一般於該化合物之合適不穩定位點包括前部分(promoiety)取代基。該前部分係指當前藥活體內轉化為藥物時,可由酶促或化學反應去除之基團。
在一些實施例中,前部分係經由對化合物或藥物之羥基或羧基之酯鍵聯結合之基團(例如,視需要經取代之C1-6烷醯基或視需要經取代之C1-6烷基)。
5.2. 化合物合成
本發明之化合物可根據此項技術中已知的標準方法合成[參見例如Morrison及Boyd於「Organic Chemistry」,第6版,Prentice Hall (1992)中]。本發明之一些化合物及/或中間體可購買獲得、為參考文獻中已知或可由熟習此項技術者使用標準程序容易獲得。本發明之一些化合物可使用本文描述之方案、實例或中間體合成。在未充分描述化合物、中間體或其變體之合成之情況下,熟習此項技術者可認知可自本文描述之反應修飾反應時間、試劑之當量數及/或溫度以製備本文呈現之化合物或其中間體或變體,且不同之處理及/或純化技術可為製備此等化合物、中間體或變體必需或所欲之。
合成化合物之正確結構可藉由熟習此項技術者已知的方法,例如藉由核磁共振(NMR)光譜術及/或質譜法驗證。
在各種實施例中,如本文描述之化合物係由下文實例2之表3A至3B之化合物中之一者的結構表示。本發明意欲包含表1至2中任一者之化合物,或其鹽、單一立體異構體、立體異構體混合物及/或同位素標記形式。
5.3. 醫藥組合物
本發明之化合物可包括於醫藥組合物中,該醫藥組合物包括一或多種化合物及至少一種賦形劑(例如,醫藥上可接受之賦形劑)。此等組合物可包括式(Ia)至(Ie)之CFTR調節劑及/或PDE4抑制劑化合物,或其醫藥上可接受之鹽、溶劑化物、水合物、前藥或立體異構體,例如,如本文描述。
本文描述之化合物發現可用於醫藥組合物中,以在需調節CFTR或抑制PDE4之多種治療應用中對有需要受試者投與。
因此,本發明之另一態樣提供包含至少一種本文描述之化合物、其醫藥上可接受之鹽、或其前藥、溶劑化物、水合物或立體異構體,及至少一種醫藥上可接受之賦形劑之醫藥組合物。
片語「醫藥上可接受之賦形劑」係指除本文描述之本發明之化合物外且具有在病患中大體上無毒且非發炎性之性質之任何成分(例如,可懸浮或溶解活性化合物之媒劑)。賦形劑可包括(例如):抗黏附劑、抗氧化劑、黏合劑、塗料、壓縮助劑、崩解劑、染料(顏色)、軟化劑、乳化劑、填充劑(稀釋劑)、成膜劑或包衣劑、香料、香精、助流劑(流動增強劑)、潤滑劑、防腐劑、印刷油墨、吸附劑、配藥或分散劑、甜味劑及水合水。在一些實施例中,該醫藥組合物包含治療有效量之如本文描述之化合物、其醫藥上可接受之鹽、或其前藥、溶劑化物、水合物或立體異構體。
5.3.1.1. 眼科組合物
在一些實施例中,醫藥組合物係經調配用於眼科投與。在一些實施例中,該等醫藥組合物係經調配用於局部投與(例如,對人類受試者之眼睛投與)之眼科組合物。在眼科組合物之一些實施例中,該組合物係水溶液。
因此,本發明提供一種眼科組合物,其包括治療有效量之本文描述之化合物或如本文描述之其醫藥上可接受之鹽、溶劑化物、水合物、前藥或立體異構體,及生理上可相容之眼科媒劑。
5.3.1.2. 其他組合物
本發明之醫藥組合物可根據任何便利之方法調配,且亦可製備成用於經口投與的多種形式,諸如錠劑、藥丸、粉末、奈米顆粒、膠囊、糖漿、懸浮液、乳液及微乳液,或製備成用於非經口投與之形式,諸如用於肌內、靜脈內或皮下投與之製劑。
在一特定實例中,醫藥組合物可含有醫藥上容許之載劑、賦形劑或添加劑。該醫藥組合物可作為藥物以習知方法產生,及可作為各種經口藥物(諸如錠劑、藥丸、粉末、膠囊、糖漿、乳液、微乳液等)產生,或可作為非經口藥物(諸如肌內注射劑、血管注射劑或皮下注射劑)產生。
若醫藥組合物係以經口藥物之形式存在,則所用添加劑或載劑之實例可包括纖維素、矽鈣、玉米澱粉、乳糖、蔗糖、葡萄糖、磷酸鈣、硬脂酸、硬脂酸鎂、硬脂酸鈣、明膠、滑石、表面活性劑、懸浮液、乳化劑、稀釋劑等。若本發明之醫藥組合物係以注射劑之形式產生,則該等添加劑或載劑可包括水、鹽水、葡萄糖水溶液、類似糖溶性溶液、醇、二醇、醚(例如,聚乙二醇400)、油、脂肪酸、脂肪酸酯、甘油酯、表面活性劑、懸浮液、乳化劑等。
在一些實施例中,醫藥組合物係經調配用於對有需要受試者非經腸投與。在一些非經腸實施例中,該等醫藥組合物係經調配用於對有需要受試者靜脈內投與。在一些非經腸實施例中,該等醫藥組合物係經調配用於對有需要受試者皮下投與。
5.4. 調節CFTR之方法
本發明之態樣包括用如本文描述之化合物調節CFTR之方法。此等方法可包括藉由使生物系統與CFTR調節劑化合物(例如,具有根據彼等表1中之任一者之結構之CFTR調節劑化合物或其醫藥上可接受之鹽、溶劑化物、水合物、前藥或立體異構體)接觸來調節此等系統中CFTR之方法。生物系統可包括(但不限於)細胞、組織、器官、體液、有機體、非哺乳動物受試者及哺乳動物受試者(例如,人類)。使生物系統與CFTR調節劑化合物接觸之方法可藉由對受試者投與該等化合物進行。
術語「調節劑」係指增加目標含量或目標功能之化合物或組合物,目標可為(但不限於) CFTR。在一些實施例中,該調節劑化合物可促效或活化目標,諸如CFTR,並增加該目標之含量或該目標之功能。在此方面,調節CFTR之方法包括活化CFTR或CFTR功能之方法。
在一些實施例中,本文描述之CFTR調節劑化合物係可活化CFTR蛋白並增加該等CFTR蛋白之功能程度之CFTR活化劑化合物。在另一實施例中,本文描述之CFTR活化劑化合物可調節或活化由CFTR活化產生之下游功能。
在一些實施例中,調節CFTR之方法包括使包含CFTR之生物系統或樣本與有效量的如本文描述調節CFTR之化合物或其醫藥上可接受之鹽、溶劑化物、水合物、前藥或立體異構體中之任一者,或如本文描述包括其之醫藥組合物接觸,以調節CFTR。在某些實施例中,該生物系統或樣本係活體外。在另一實施例中,該生物系統或樣本係活體內。
CFTR調節劑可調節樣本中CFTR之酶促活性。例如,可使用如實例4中描述的基於黃色螢光蛋白(YFP之結合分析以量測CFTR功能。使用此分析,該CFTR功能係自應對細胞外添加碘離子及接著毛喉素的細胞螢光時間過程加以評定,此細胞外添加導致YFP螢光由於CFTR介導之碘化物進入而降低。CFTR活性亦可藉由實例5中描述之分析評估。根據此方法之CFTR調節劑可顯示調節CFTR功能(例如如藉由實例5之短路電流量測分析評估)小於2000 nM (諸如200 nM或更小)之EC
50值。生物系統可包括受試者(例如,人類受試者)。
在一些實施例中,本發明提供調節受試者中CFTR活性之方法。在某些情況下,受試者中調節之CFTR活性之百分比可為至少10%、至少20%、至少30%、至少40%、至少50%、至少60%、至少70%、至少80%、至少85%、至少90%、至少95%、至少96%、至少97%、至少98%、至少99%、至少99.5%或至少99.9%。在一些實施例中,相較於該受試者之樣本中量測之CFTR活性之基線水準,該CFTR活性增加(例如)至少10%或更大。
在一些實施例中,本發明之化合物可用於分析中以評估CFTR調節活性。一些分析可包括診斷分析。在某些情況下,化合物可包括於藥物發現之方法中。在一些實施例中,本發明之方法包括使用本發明調節CFTR之化合物以評估其他化合物之CFTR調節。此等方法可包括使調節CFTR之化合物與一或多種可偵測標記(例如,螢光染料)結合並在其他化合物之存在下量測CFTR解離(經由可偵測標記偵測)。該等可偵測標記可包括螢光化合物。
5.5. 抑制PDE4之方法
本發明之態樣包括藉由與顯示抑制PDE4活性之化合物(例如,具有根據彼等表1至2中之任一者之結構之PDE4抑制劑化合物,或其醫藥上可接受之鹽、溶劑化物、水合物、前藥或立體異構體)接觸來抑制生物系統或樣本中PDE4活性之方法。使生物系統與CFTR調節劑化合物接觸之方法可藉由對受試者投與該等化合物進行。
生物系統可包括(但不限於)細胞、組織、器官、體液、有機體、非哺乳動物受試者及哺乳動物受試者(例如,人類)。在某些實施例中,該生物系統或樣本係活體外。在另一實施例中,該生物系統或樣本係活體內。在某些情況下,該樣本係細胞樣本。
在一些實施例中,本發明提供抑制受試者中PDE4活性之方法。在某些情況下,受試者中抑制之PDE4活性之百分比可為至少10%、至少20%、至少30%、至少40%、至少50%、至少60%、至少70%、至少80%、至少85%、至少90%、至少95%、至少96%、至少97%、至少98%、至少99%、至少99.5%,或至少99.9%。在某些情況下,PDE4活性之此抑制及/或最大抑制程度可在投與後約1小時至約投與後3小時、投與後約2小時至投與後約4小時、投與後約3小時至投與後約10小時、投與後約5小時至投與後約20小時、或投與後約12小時至約投與後24小時達成。PDE4活性之抑制可繼續至少1天、至少2天、至少3天、至少4天、至少5天、至少6天、至少7天、至少2週、至少3週、至少4週、至少8週、至少3個月、至少6個月或至少1年之整個週期。在某些情況下,此抑制程度可通過每日投與達成。此每日投與可包括投與至少2天、至少3天、至少4天、至少5天、至少6天、至少7天、至少2週、至少3週、至少4週、至少2個月、至少4個月、至少6個月、至少1年或至少5 年。在某些情況下,受試者可在此受試者之一生中投與本發明之化合物或組合物。
5.6. 治療適應症
本發明之方法包括使用本文揭示之化合物及/或組合物治療適應症之方法。術語「治療適應症」係指可藉由一些形式之治療或其他治療干預(例如,通過CFTR調節劑或PDE4抑制劑投與)減輕、穩定、改善、 治癒或另外解決之任何症狀、病症、疾患或疾病。
5.6.1. CFTR相關適應症
與CFTR活性及/或功能障礙相關聯之治療適應症在本文中稱為「CFTR相關適應症」。在一些實施例中,本發明之方法可包括藉由投與本文揭示之化合物及/或組合物(例如,CFTR調節劑化合物)治療CFTR相關適應症。
術語「治療(treat)」、「治療(treatment)」及類似物係指病理過程之緩解或減輕。在本發明之內文中,就其關於下文中本文列舉之其他病症中之任一者之內文而言,術語「治療(treat)」、「治療(treatment)」及類似物意謂緩解或減輕至少一種與此病症相關聯之症狀,或減緩或逆轉此病症之進展或預期進展。
5.6.1.1. 眼部疾病或疾患
在另一態樣中,本發明提供一種治療眼部疾病或疾患之方法,其包括對受試者之眼睛投與治療有效量之如本文描述之眼科組合物。在一些實施例中,該受試者係人類。在該方法之一些實施例中,該眼部疾病或疾患係乾眼症。
乾眼症係導致眼睛不適、視覺障礙及眼表病理學之異質性淚膜障礙。CFTR係眼表主要之促分泌氯通道。眼表CFTR活性之活化劑可導致局部遞送後淚液分泌增加且適用於治療乾眼症。
在一些實施例中,該方法進一步包括鑑定罹患乾眼症之受試者。在一些實施例中,該方法進一步包括鑑定與該乾眼症相關聯之潛在疾病或病症。
在一些實施例中,乾眼症係由以下組成之群之一或多種疾病或病症引起:過敏性結膜炎、乾燥性角膜結膜炎、年齡相關性乾眼症、史蒂文斯-強生症候群(Stevens-Johnson syndrome)、休格倫氏症候群(Sjogren's syndrome)、眼瘢痕性類天皰瘡、角膜損傷、感染、雷德二氏症候群(Riley-Day syndrome)、先天性無淚症、營養失調或缺乏、藥理副作用、隱形眼鏡不耐症、眼部壓力導致腺體及組織破壞、自體免疫疾病、免疫缺陷病症、無法眨眼之昏迷患者、或環境曝露於煙霧、煙、過度乾燥之空氣、空中懸浮微粒、淚腺缺乏症、淚腺導管阻塞、瞼板油缺乏症、眼瞼開口病症及眼表疾病(OSD)。
在一些實施例中,乾眼症係係由乾燥性角膜結膜炎、年齡相關性乾眼症、史蒂文斯-強生症候群、休格倫氏症候群、眼瘢痕性類天皰瘡、角膜損傷、雷德二氏症候群或先天性無淚症引起。
在一些實施例中,根據本發明之方法治療之眼部疾病或疾患係休格倫氏症候群。
在一些實施例中,乾眼症係由營養失調或缺乏、隱形眼鏡不耐症、自體免疫疾病、免疫缺陷病症、無法眨眼之昏迷患者、或環境曝露於煙霧、煙、過度乾燥之空氣或空中懸浮微粒引起。
在一些實施例中,根據本發明之方法治療之眼部疾病或疾患係結膜炎。在一些實施例中,該結膜炎係過敏性結膜炎或角膜結膜炎。
在一些實施例中,眼部疾病或疾患係角膜炎。
在一些實施例中,在投與本文揭示之化合物或組合物後,受試者中乾眼症之一或多種症狀減少或減輕。
在一些實施例中,乾眼症之一或多種症狀係選自乾燥、灼燒、眼癢、畏光、異物感及砂礫感。
在一些實施例中,該方法進一步包括評估投與後眼中天然淚膜之恢復。
在一些實施例中,對眼睛每天或視需要局部投與眼科組合物。在某些實施例中,該眼科組合物係溶液。
可使用乾眼症之眼淚體積減少小鼠模型以評估本發明之化合物調節莨菪鹼誘導之受試者中眼淚體積之能力。在一些實施例中,如由實例6闡述,投與本發明之化合物可引起眼淚體積之顯著變化。
5.6.1.2. 其他疾病或疾患
其他可作為治療目標之CFTR相關適應症包括(但不限於)慢性阻塞性肺病(COPD)、哮喘、支氣管炎、支氣管擴張、乳糜瀉、便祕、膽汁淤積性肝病、慢性鼻竇炎及肝損害。
CFTR功能障礙或CFTR機能減退可於慢性阻塞性肺病(COPD)中獲得且可有助於共用臨床特徵之其他疾病(諸如哮喘、支氣管炎及支氣管擴張)。慢性阻塞性肺病(COPD)及慢性支氣管炎之疾病之特徵在於黏液充血及氣道發炎。在一些實施例中,本發明之化合物可用作通過CFTR活化同時恢復或增強黏膜纖毛清除率之抗發炎劑。
在一些實施例中,CFTR相關適應症係COPD。
在一些實施例中,CFTR相關適應症係支氣管炎。
在一些實施例中,CFTR相關適應症係支氣管擴張。
在一些實施例中,CFTR相關適應症係哮喘。
在一些實施例中,CFTR相關適應症係便祕。便祕係成人及兒童常見之臨床症狀,其對生活品質產生不利影響。在一些實施例中,該便祕係阿片類藥物誘導之便祕、慢性特發性便祕或以便祕為主之腸易激症候群。在一些實施例中,本發明之調節CFTR之化合物可刺激腸液分泌並使排便正常化以治療該便祕。
在一些實施例中,CFTR相關適應症係乳糜瀉。在乳糜瀉中,對膳食麩質/麥膠蛋白、抗原性麥膠蛋白肽之不耐症觸發HLADQ2/DQ8限制之適應性Th1免疫反應。CFTR用作麩質/麥膠蛋白衍生肽(P31-43)之膜受體,麩質/麥膠蛋白衍生肽(P31-43)抑制腸上皮細胞中之CFTR,引起有助於乳糜瀉之免疫病理學之局部應激反應。在一些實施例中,用本發明之活化CFTR之化合物刺激CFTR功能可減弱麥膠蛋白之自噬抑制及促發炎效應,並提供乳糜瀉之治療。
在一些實施例中,CFTR相關適應症係膽汁淤積性肝病。
在一些實施例中,CFTR相關適應症係慢性鼻竇炎。
在一些實施例中,CFTR相關適應症係肝損害。
5.6.2. PDE4相關適應症
本發明之態樣包括使用本文揭示之化合物及/或組合物治療受關注治療適應症之方法。與PDE4活性及/或功能障礙相關聯之治療適應症在本文中稱為「PDE4相關適應症」。在一些實施例中,本發明之方法可包括藉由投與本文揭示之化合物及/或組合物(例如,PDE4抑制劑化合物)治療PDE4相關適應症。
PDE4抑制劑係一類經充分表徵的具有多種抗發炎活性之藥劑。可使用宿主細胞中人類磷酸二酯酶4 (PDE4)抑制分析以評估本發明之化合物抑制目標PDE4之能力。在一些實施例中,如由實例7闡述,投與本發明之化合物可引起PDE4活性之顯著變化。
在一些實施例中,本發明之抑制PDE4之化合物具有廣泛之抗發炎效應,諸如抑制TNF-α之產生及數種其他介體。PDE4係用於治療多種肺部、皮膚病及嚴重之神經系統疾病之治療目標。
在方法之一些實施例中,PDE4相關適應症係發炎性疾病或疾患。在一些實施例中,發炎性疾病或疾患係慢性發炎性疾病或疾患。在一些實施例中,發炎性疾病或疾患係急性發炎性疾病或疾患。在該方法之一些實施例中,該PDE4相關適應症係自體免疫疾病。
在該方法之一些實施例中,PDE4相關適應症係發炎性肺部疾病。在一些實施例中,該發炎性肺部疾病係慢性阻塞性肺病(COPD)、哮喘、肺纖維化或發炎性呼吸道疾病。
在方法之一些實施例中,PDE4相關適應症係發炎性皮膚疾病。在一些實施例中,該發炎性皮膚疾病係牛皮癬或牛皮癬性病症,諸如牛皮癬性關節炎。在一些實施例中,該發炎性皮膚疾病係異位性皮膚炎。
在方法之一些實施例中,PDE4相關適應症係發炎性腸病(IBD)。
在方法之一些實施例中,PDE4相關適應症係類風溼性關節炎。
在方法之一些實施例中,PDE4相關適應症係關節黏連性脊椎炎。
在方法之一些實施例中,PDE4相關適應症係神經系統疾病,諸如神經發炎。
在該方法之一些實施例中,PDE4相關適應症係結膜炎。在一些實施例中,該結膜炎係過敏性結膜炎或角膜結膜炎。
在一些實施例中,PDE4相關適應症係角膜炎。
因此,可為根據本發明之方法之治療目標之受關注之PDE4相關適應症包括(但不限於) COPD、哮喘、發炎性呼吸道疾病、牛皮癬、牛皮癬性病症、異位性皮膚炎、發炎性腸病(IBD)、類風溼性關節炎、關節黏連性脊椎炎、神經發炎及過敏性結膜炎。
5.6.3.投與方法
在一些實施例中,該方法包括經口投與標的化合物或組合物。投與劑量可根據目的以在所述個體或病患中有效預防或治療之量經口或非經口投與。當經口投與時,可投與該化合物使得每1 kg體重投與0.01至1000 mg,更具體言之0.1至300 mg活性劑,及當非經口投與時,可投與該化合物使得每1 kg體重投與0.01至100 mg,更具體言之0.1至50 mg活性劑。該劑量可一次或經多次投與進行投與。用於特定個體或病患之投與劑量應基於多種相關因素(諸如體重、年齡、性別、健康、飲食、投與時間間個、投與方法及疾病之嚴重程度)決定,且可由專家適當增加或減少。上文規定之投與劑量無意以任何方式限制本發明之範疇。在相關領域中具有一般技術之醫生或獸醫可容易決定並規定醫藥組合物之有效所需劑量。例如,醫生或獸醫可以小於達成目標治療效應所需含量之含量開始,逐漸增加醫藥組合物中本發明之化合物之劑量,直至達成預期效應。
本發明之化合物及組合物可單獨、與根據本發明之另一實例之化合物組合投與,或與至少一種其他治療劑,例如與其他醫藥活性成分(諸如眼部疾病治療劑、抗生素、抗發炎劑及抗微生物劑)同時、分別或循序伴隨投與。
5.7. 定義
除非另有定義,否則本文使用之所有技術及科學術語均具有與如由本發明所屬領域中之一般技術者通常瞭解之含義相同之含義。
應瞭解本文提供之定義無意互相排斥。因此,一些化學部分可落於多於一個術語之定義內。
術語「C
x-C
y」當結合化學部分(諸如烷基、烯基或炔基)一起使用時意欲包括鏈中含有x至y個碳之基團。例如,術語「C
1-C
6烷基」係指經取代或未經取代之飽和烴基,包括含有1至6個碳之直鏈烷基及分支鏈烷基。在一些實施例中,術語「(C
x-C
y)伸烷基」係指伸烷基鏈中具有x至y個碳之經取代或未經取代之伸烷基鏈。例如「(C
x-C
y)伸烷基可選自亞甲基、伸乙基、伸丙基、伸丁基、伸戊基及伸己基,其等中之任一者係視需要經取代。
術語「烷基」係指未分支或分支飽和烴鏈。在一些實施例中,如本文使用之烷基具有1至20個碳原子((C
1-C
20)烷基)、1至10個碳原子((C
1-C
10)烷基)、1至8個碳原子((C
1-C
8)烷基)、1至6個碳原子((C
1-C
6)烷基)、1至5個碳原子((C
1-C
5)烷基)或1至3個碳原子((C
1-C
5)烷基)。實例包括(但不限於)甲基、乙基、正丙基、異丙基、正丁基、第二丁基、第三丁基、正戊基、2-戊基、異戊基、新戊基、正己基、2-己基、3-己基及3-甲基戊基。當命名具有規定數量碳之烷基殘基時,具有該數量碳之所有幾何異構體均可包含。例如,「丁基」可包括正丁基、第二丁基、異丁基及第三丁基,及「丙基」可包括正丙基及異丙基。除非說明書中另有明確說明,否則烷基鏈係視需要經一或多個取代基(諸如彼等本文描述之取代基)取代。
術語「烷氧基」係指結合至氧原子之未分支或分支烷基(烷基-O-)。在一些實施例中,如本文使用之烷氧基具有1至20個碳原子((C
1-C
20)烷氧基)、1至10個碳原子((C
1-C
10)烷氧基)、1至8個碳原子((C
1-C
8)烷氧基)、1至6個碳原子((C
1-C
6)烷氧基)、1至5個碳原子((C
1-C
5)烷氧基)或1至3個碳原子((C
1-C
3)烷氧基)。實例包括(但不限於)甲氧基、乙氧基、正丙氧基及丁氧基。當命名具有規定數量碳之烷氧基殘基時,具有該數量碳之所有幾何異構體均可包含,諸如異丙氧基、異丁氧基及第三丁氧基。除非說明書中另有明確說明,否則烷氧基鏈係視需要經一或多個取代基(諸如彼等本文描述之取代基)取代。
術語「伸烷基」係指將分子之剩餘部分連接至自由基之僅由碳及氫構成之直鏈二價烴鏈,其不含不飽和度,且較佳具有1至20個碳原子((C
1-C
20)伸烷基)、1至10個碳原子((C
1-C
10)伸烷基)、1至6個碳原子((C
1-C
6)伸烷基)或1至5個碳原子((C
1-C
5)伸烷基)。實例包括(但不限於)亞甲基、伸乙基、伸丙基、伸丁基,及類似物。伸烷基鏈通過單鍵結合至分子之剩餘部分及通過單鍵結合至自由基。伸烷基鏈對分子之剩餘部分及自由基之結合點係分別通過末端碳。除非說明書中另有明確說明,否則伸烷基鏈係視需要經一或多個取代基(諸如彼等本文描述之取代基)取代。實例包括亞甲基(-CH
2-)、伸乙基(-CH
2CH
2-)、伸丙基(-CH
2CH
2CH
2-)、2-甲基伸丙基(-CH
2-CH(CH
3)-CH
2-)、伸己基(-(CH
2)
6-)及類似物。
術語「烯基」係指含有至少一個碳-碳雙鍵之脂族烴基,包括直鏈、分支鏈及環形烯基。在一些實施例中,該烯基具有2至10個碳原子((C
2-C
10)烯基)。在另一實施例中,該烯基之鏈中具有2至4個碳原子((C
2-C
4)烯基)。例示性烯基包括(但不限於)乙烯基、丙烯基、正丁烯基、異丁烯基、3-甲基丁-2-烯基、正戊烯基、庚烯基、辛烯基、環己基-丁烯基及癸烯基。烷基烯基係鍵合至如本文定義之烯基之如本文定義之烷基。該烯基可未經取代或通過可用碳原子經上文針對烷基定義之一或多個基團取代。
術語「炔基」係指具有2至6個碳原子及較佳2至3個碳原子且具有至少1及較佳1至2個乙炔(C≡C-)不飽和位點之直鏈或分支鏈單價烴基。此等炔基之實例包括(但不限於)乙炔基(C≡CH)及炔丙基(CH
2C≡CH)。
術語「芳基」係指具有至少一個烴芳環之單環或多環基團,其中至少一個烴芳環之所有環原子均為碳。芳基可包括具有單個芳環之基團(例如,苯基)及具有多個稠合芳環之基團(例如,萘基、蒽基)。芳基可進一步包括一或多個芳族烴環與一或多個非芳族烴環稠合之基團(例如,茀基;2,3-二氫-1H-茚;1,2,3,4-四氫萘)。在某些實施例中,芳基包括芳族烴環與非芳環稠合之基團,其中該非芳環包含至少一個獨立地選自由N、O及S組成之群之環雜原子。例如,在一些實施例中,芳基包括苯基環與非芳環稠合之基團,其中該非芳環包含至少一個獨立地選自由N、O及S組成之群之環雜原子 (例如,色原烷;硫色原烷;2,3-二氫苯并呋喃;吲哚啉)。在一些實施例中,如本文使用之芳基具有6至14個碳原子((C
6-C
14)芳基)或6至10個碳原子((C
6-C
10)芳基)。在芳基包括稠環之情況下,該芳基可通過化合價允許之稠環之任何原子連接至一或多個本文描述之式之取代基或部分。
術語「環烷基」係指單環或多環飽和烴。在一些實施例中,環烷基具有3至20個碳原子((C
3-C
20)環烷基)、3至8個碳原子((C
3-C
8)環烷基)、3至6個碳原子((C
3-C
6)環烷基)或3至5個碳原子((C
3-C
5)環烷基)。在一些實施例中,環烷基具有3至8個碳原子,其具有單個或多個環(包括稠環、橋環及螺環系統)。合適環烷基之實例包括(但不限於)金剛烷基、環丙基、環丁基、環戊基、環辛基、八氫戊烯基、八氫-1H-茚、十氫萘、立方烷、雙環[3.1.0]己烷及雙環[1.1.1]戊烷,及類似物。
術語「碳環」係指一種飽和、不飽和或芳環系統,其中該環系統之各原子均為碳。碳環包括3至10員單環、6至12員雙環及6至12員橋環。雙環碳環之各環可係選自飽和、不飽和及芳環。在一例示性實施例中,芳環(例如,苯基)可與飽和或不飽和環(例如,環己烷、環戊烷或環己烯)稠合。只要化合價允許,雙環碳環即包括飽和、不飽和及芳族雙環之任何組合。雙環碳環包括環尺寸之任何組合,諸如4-5稠環系統、5-5稠環系統、5-6稠環系統、6-6稠環系統、5-7稠環系統、6-7稠環系統、5-8稠環系統及6-8稠環系統。例示性碳環包括環戊基、環己基、環己烯基、金剛烷基、苯基、二氫茚基及萘基。
術語「鹵烷基」係指可進一步經取代或未經取代之單鹵烷基或多鹵烷基。
術語「雜環」係指包含一或多個雜原子之飽和、不飽和或芳環。例示性雜原子包括N、O、Si、P、B及S原子。雜環包括3至10員單環、6至12員雙環及6至12員橋環。只要化合價允許,雙環雜環即包括飽和、不飽和及芳族雙環之任何組合。在一例示性實施例中,芳環(例如,吡啶基)可與飽和或不飽和環(例如,環己烷、環戊烷、嗎啉、哌啶或環己烯)稠合。雙環雜環包括環尺寸之任何組合,諸如4-5稠環系統、5-5稠環系統、5-6稠環系統、6-6稠環系統、5-7稠環系統、6-7稠環系統、5-8稠環系統及6-8稠環系統。
術語「雜芳基」係指環內具有4至10個碳原子及1至4個雜原子(例如,氧、氮及/或硫)之芳基。此等雜芳基可具有單個環(即,吡啶基或呋喃基)或多個稠環(即,吲哚啉基或苯并噻吩基),其中該等稠環可為或可不為芳族及/或含有雜原子,限制條件為結合點係通過芳族雜芳基之原子。在一項實施例中,該雜芳基之氮及/或硫環原子視需要經氧化以提供N氧化物(N→O)、亞磺醯基或磺醯基部分。單環雜芳基之實例包括吡唑基、吡咯基、噻唑基、噁唑基、噻吩基、呋喃基、咪唑基、異噁唑基、三唑基、噻二唑基、四唑基、噁二唑基、吡啶基、噠嗪基、嘧啶基、吡嗪基、噻唑基,及類似基團,但不限於前述基團。雙環雜芳基之實例包括吲哚基、苯并噻吩基、苯并呋喃基、苯并咪唑基、苯并噁唑基、苯并異噁唑基、苯并噻唑基、苯并噻二唑基、苯并三唑基、喹啉基、異喹啉基、嘌呤基、呋喃吡啶基、側氧基克羅烯基(oxocromen)、二側氧基異吲哚啉基、吡唑并吡啶基、吡唑并[1,5-a]吡啶基,及類似基團,但不限於前述基團。較佳之雜芳基包括5或6員雜芳基(諸如吡啶基、吡咯基、吲哚基、噻吩基及呋喃基)。
術語「雜烷基」係指其中碳原子中之一或多者及任何結合之氫原子獨立地係經相同或不同之雜原子基團置換之烷基取代基。例如,1、2或3個碳原子可獨立地經相同或不同之雜原子取代基置換。
術語「雜環烷基」係指含有一或多個雜原子(例如,B、N、O、S、P(=O)、Si或P)之經取代或未經取代之單環烷基。實例包括哌啶基、哌嗪基、嗎啉基、吡咯啶基、硫嗎啉基、咪唑啶基、四氫糠基,及類似基團,但不限於前述基團。
術語「經取代」係指化合物之一或多個碳或可取代雜原子(例如,NH或NH
2)上之氫經取代基置換之部分。將瞭解「取代」或「經……取代」包括此取代係根據經取代之原子及取代基允許之化合價,且該取代導致穩定化合物之隱含條件。例如,穩定化合物包括(但不限於)不自發經受轉化(諸如藉由重排、環化、消除等)之化合物。在某些實施例中,經取代係指相同碳原子上之兩個氫原子經取代基置換,諸如單個碳上之兩個氫原子經側氧基、亞胺基或硫基取代之部分。經審慎考慮術語「經取代」包括有機化合物之所有可允許取代基。在一廣泛態樣中,該等可允許取代基包括有機化合物之非環及環、分支及未分支、碳環及雜環、芳族及非芳族取代基。針對適當之有機化合物,該等可允許取代基可為一或多個且相同或不同。
熟習此項技術者將瞭解視需要,取代基可本身經取代。除非明確規定為「未經取代」,否則應瞭解對本文化學部分之參考包括經取代之變體。例如,除非另有規定,否則對「雜芳基」基團或部分之參考暗示包括經取代及未經取代之變體兩者。
當提及化合物特徵時,片語「視需要經取代」可與片語「未經取代或經取代」互換使用及係指當非氫取代基可存在或可不存在於給定原子或基團上時,且因此,該描述包括其中存在非氫取代基之結構及其中不存在非氫取代基之結構。例如,「視需要經取代之烷基」包含如本文定義之「烷基」及「經取代之烷基」。熟習此項技術者將瞭解,關於含有一或多個取代基之任何基團,此等基團無意引入空間上不切實際、合成上不可行及/或固有不穩定之任何取代或取代模式。
在一些實施例中,取代基可包括本文描述之任何取代基,例如:鹵素、羥基、側氧基(=O)、硫基(=S)、氰基(-CN)、硝基(-NO
2)、亞胺基(=N-H)、肟基(=N-OH)、肼基(=N-NH
2)、-R
b-OR
a、-R
b-OC(O)-R
a、-R
b-OC(O)-OR
a、-R
b-OC(O)-N(R
a)
2、-R
b-N(R
a)
2、-R
b-C(O)R
a、-R
b-C(O)OR
a、-R
b-C(O)N(R
a)
2、-R
b-O-R
c-C(O)N(R
a)
2、-R
b-N(R
a)C(O)OR
a、-R
b-N(R
a)C(O)R
a、-R
bN (R
a)S(O)
tR
a(其中t係1或2)、-R
b-S(O)
tR
a(其中t係1或2)、-R
b-S(O)
tOR
a(其中t係1或2),及-R
b-S(O)
tN(R
a)
2(其中t係1或2)。在另一例示性實施例中,取代基包括烷基、烯基、炔基、芳基、芳烷基、芳烯基、芳炔基、環烷基、環烷基烷基、雜環烷基、雜環烷基烷基、雜芳基及雜芳基烷基,其等中之任一者可視需要經烷基、烯基、炔基、鹵素、鹵烷基、鹵烯基、鹵炔基、側氧基、硫基、氰基、硝基、亞胺基、肟基、肼基、-R
bOR
a、-R
b-OC(O)-R
a、-R
b-OC(O)-OR
a、-R
b-OC(O)-N(R
a)
2、-R
b-N(R
a)
2、-R
b-C(O)R
a、-R
b-C(O)OR
a、-R
b-C(O)N(R
a)
2、-R
b-O-R
c-C(O)N(R
a)
2、-R
b-N(R
a)C(O)OR
a、-R
b-N(R
a)C(O)R
a、-R
b-N (R
a)S(O)
tR
a(其中t係1或2)、-R
b-S(O)
tR
a(其中t係1或2)、-R
b-S(O)
tOR
a(其中t係1或2)及-R
b-S(O)
tN(R
a)
2(其中t係1或2)取代;且其中各R
a、R
b及R
c係獨立地選自氫、烷基、環烷基、環烷基烷基、芳基、芳烷基、雜環烷基、雜環烷基烷基、雜芳基及雜芳基烷基;且其中化合價允許,各R
a、R
b及R
c可視需要經烷基、烯基、炔基、鹵素、鹵烷基、鹵烯基、鹵炔基、側氧基、硫基、氰基、硝基、亞胺基、肟基、肼基、-R
bOR
a、-R
b-OC(O)-R
a、-R
b-OC(O)-OR
a、-R
b-OC(O)-N(R
a)
2、-R
b-N(R
a)
2、-R
b-C(O)R
a、-R
b-C(O)OR
a、-R
b-C(O)N(R
a)
2、-R
b-O-R
c-C(O)N(R
a)
2、-R
b-N(R
a)C(O)OR
a、-R
b-N(R
a)C(O)R
a、-R
b-N (R
a)S(O)
tR
a(其中t係1或2)、-R
b-S(O)
tR
a(其中t係1或2)、-R
b-S(O)
tOR
a(其中t係1或2)及-R
b-S(O)
tN(R
a)
2(其中t係1或2)取代。
術語「異構體」係指包含相同數量及類型之原子、基團或組分,但具有不同之結構排佈及該等原子之連接性之兩種或更多種化合物。
術語「互變異構體」係指容易自一種異構形式轉化為另一種且平衡存在之兩種或更多種結構異構體中之一者。
「立體異構體」係指由相同鍵鍵合之相同原子但具有不同三維結構(其等不可互換)構成之化合物。本發明審慎考慮各種立體異構體及其混合且包括「對映體」,其係指其等分子係彼此不可重疊之鏡像的兩種立體異構體。
本發明之化合物之個別對映體及非對映體可自含有不對稱或立體中心之市售起始材料合成製備,或藉由製備外消旋混合物,接著一般技術者熟知的拆分方法製備。此等拆分方法係由以下例示:(1)將對映體之混合物結合至對掌性助劑,藉由重結晶或層析術自非對映體之所得混合物分離,並自該助劑釋放光學純產物,(2)採用光學活性光學拆分劑形成鹽,(3)於對掌性液相層析管柱上直接分離光學對映體之混合物,或(4)使用立體選擇性化學或酶促試劑進行動力學拆分。外消旋混合物亦可藉由熟知方法諸如對掌性相氣相層析術或於對掌性溶劑中使該化合物結晶而拆分成其等各別對映體。此項技術中熟知立體選擇性合成,其中單一反應物在產生新立體中心期間或在預先存在者之轉化期間形成立體異構體之不等混合物之化學或酶促反應。立體選擇性合成包含對映及非對映選擇性轉化兩者。參見例如Carreira及Kvaerno,Classics in Stereoselective Synthesis, Wiley-VCH: Weinheim, 2009。
符號=表示一個鍵,其可為如本文描述之單鍵、雙鍵或三鍵。碳-碳雙鍵周圍之取代基指定為「Z」或「E」構型,其中術語「Z」及「E」係根據IUPAC標準使用。除非另有規定,否則繪示雙鍵之結構包含「E」及「Z」異構體兩者。
碳-碳雙鍵周圍之取代基或者可稱為「順式」或「反式」,其中「順式」表示取代基位於雙鍵同側及「反式」表示取代基位於該雙鍵對側。取代基於碳環周圍之排佈亦可稱為「順式」或「反式」。術語「順式」表示取代基位於環平面同側及術語「反式」表示取代基位於環平面對側。取代基配置於環平面同側及對側兩者之化合物之混合物稱為「順式/反式」。
在描述元素之內文中,除非本文另有指示或與內文明顯矛盾,否則單數冠詞(諸如「一」、「一個」及「該」)及相似參考物應解釋為涵蓋單數及複數兩者。除非本文另有指示,否則本文中對值範圍之引用僅旨在用作個別提及落於該範圍內(包括該範圍之上限及下限)之各單獨值之速記方法,且將各單獨值併入本說明書內,該併入之程度就如同將其個別地併入本文中一樣。除非本文另有指示或另外與內文明確矛盾,否則本文描述之所有方法可以任何合適之順序進行。除非另有說明,否則任何及所有實例,或本文提供之例示性語言(即,「諸如」)的使用均僅旨在更好地闡述本實施例且無意限制隨附申請專利範圍之範疇。
在一些實施例中,除非另有明確說明,否則在定量值前使用術語「約」之情況下,本發明亦包括該特定定量值本身。如本文使用,除非另有指示或推斷,否則術語「約」係指自標稱值±10%之變化。除非內文另有說明或瞭解,否則在關於組合物中組分或材料之量提供百分比時,應瞭解該百分比係基於重量之百分比。
除非內文另有說明或瞭解,否則在提供分子量(例如,聚合物的分子量)且其非絕對值之情況下,則應瞭解該分子量係平均分子量。
應瞭解步驟順序或進行某些行動之順序係不重要的,只要本發明保持可操作即可。此外,兩個或更多個步驟或行動可同時進行。
不在兩個字母或符號之間的破折號(「-」)符號係指取代基之鍵合或結合點。例如,-NH
2係通過氮原子結合。
術語「醫藥上可接受之鹽」係指可接受對受試者投與之鹽。應瞭解針對給定劑量方案,具有相對離子之此等鹽將具有可接受之哺乳動物安全性。此等鹽亦可衍生自醫藥上可接受之無機或有機鹼及醫藥上可接受之無機或有機酸,且可包含有機及無機相對離子。本文描述之化合物之中性形式可藉由使該化合物與鹼或酸接觸並分離所得鹽而轉化為相應之鹽形式。
術語「醫藥上可接受之賦形劑」、「醫藥上可接受之稀釋劑」、「醫藥上可接受之載劑」及「醫藥上可接受之佐劑」可互換使用且係指適用於製備一般安全、無毒且既非生物學亦非其他非所需之醫藥組合物之賦形劑、稀釋劑、載劑或佐劑,且包括針對獸醫用途及人類醫藥用途可接受之賦形劑、稀釋劑、載劑及佐劑。片語「醫藥上可接受之賦形劑」包括一種及超過一種此賦形劑、稀釋劑、載劑及/或佐劑兩者。
術語「醫藥組合物」意欲包含適用於對受試者(諸如哺乳動物,尤其人類)投與之組合物。一般而言,「醫藥組合物」係無菌,且較佳不含可於受試者內引起非所需反應之污染物(即,該醫藥組合物中之該(等)化合物為醫藥級)。醫藥組合物可經設計用於經由許多不同之投與途徑(包括經口、經頰、經直腸、非經腸、腹膜內、皮內、氣管內、肌內、皮下,及類似物)對有需要受試者或病患投與。
術語「個體」及「受試者」可互換使用且係指需治療疾病之受試者。更具體言之,本文提及者係人類或非人類靈長類動物、小鼠、狗、貓、馬、奶牛、兔、大鼠或其他哺乳動物。
5.8 例示性實施例
如本文描述,文本係指本發明化合物、組合物及方法之各種實施例。本文描述之各種實施例意欲提供各種說明性實例且不應解釋為替代物種之描述。相反,應注意本文提供之各種實施例之描述可具有重疊範疇。本文討論之實施例係僅說明性的且無意限制現有技術之範疇。
儘管具有隨附申請專利範圍,但本發明之態樣由下列條項闡述。
條項1. 一種式(Ia)化合物:
,
或其醫藥上可接受之鹽、溶劑化物、水合物、前藥或立體異構體,其中:
R
1係選自H、鹵素、視需要經取代之芳基、視需要經取代之(C
1-C
10)烷基及視需要經取代之(C
1-C
10)烷氧基;
R
2係選自H、視需要經取代之(C
1-C
10)烷基、視需要經取代之環烷基、視需要經取代之芳基、視需要經取代之雜芳基及視需要經取代之雜環,及芳基、雜芳基及雜環上之任選取代基係獨立地選自:H、OH、NH
2、NO
2、OCF
3、CF
3、鹵素、視需要經取代之胺基、視需要經取代之(C
1-C
5)烷基及視需要經取代之(C
1-C
5)烷氧基;
R
4係選自
、
及
;
R
5及R
6係獨立地選自H、視需要經取代之(C
1-C
10)烷基、視需要經取代之(C
1-C
10)烯基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之單環或雙環碳環及視需要經取代之單環或雙環雜環;
或R
5及R
6連同其等結合之氮原子一起環狀連接以形成視需要經取代之單環或雙環雜環;
R
7係選自NR
5R
6、視需要經取代之(C
1-C
10)烷基、視需要經取代之(C
1-C
10)烷氧基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基及視需要經取代之雜環烷基;
R
8係選自H及視需要經取代之(C
1-C
10)烷基;及
R
9係選自H及鹵素。
條項2. 如條項1之化合物,其中該R
2係具有1至3個取代基之經取代之芳基或具有1至3個取代基之經取代之雜芳基。
條項3. 如條項1之化合物,其中該R2係視需要經取代之苯基或視需要經取代之雜芳基。
條項4. 如條項3之化合物,其中該化合物係式(Ib)化合物:
,
其中:
X
1係CR
10’或N;
R
1b係選自H、鹵素、視需要經取代之芳基、視需要經取代之(C
1-C
10)烷基及視需要經取代之(C
1-C
10)烷氧基;
R
4b係選自
、
及
;
R
5及R
6係獨立地選自H、視需要經取代之(C
1-C
10)烷基、視需要經取代之(C
1-C
10)烯基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之單環或雙環碳環及視需要經取代之單環或雙環雜環;
或R
5及R
6連同其等結合之氮原子一起環狀連接以形成視需要經取代之單環或雙環雜環;
R
7係選自NR
5R
6、視需要經取代之(C
1-C
10)烷基、視需要經取代之(C
1-C
10)烷氧基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基及視需要經取代之雜環烷基;
R
8係選自H及視需要經取代之(C
1-C
10)烷基;
R
9b係選自H及鹵素;
各R
10及R
10’係獨立地選自H、OH、NH
2、NO
2、鹵素、視需要經取代之(C
1-C
6)烷基、視需要經取代之(C
1-C
6)烷氧基,及經取代之胺基;及
n係0至4。
條項5. 如條項4之化合物,其中各R
10及R
10 ’係獨立地選自H、OH、CH
3、CF
3、OCF
3、OCH
3、NO
2、F及Cl,及二甲胺。
條項7. 如條項5或6之化合物,其中該化合物係式(Ic)化合物:
,
其中:
X
2係CR
10c’或N;
R
21係選自H及視需要經取代之(C
1-C
10)烷基;視需要經取代之醯基;視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之單環或雙環碳環及視需要經取代之單環或雙環雜環;
R
1c係選自H、鹵素、視需要經取代之芳基、視需要經取代之(C
1-C
10)烷基及視需要經取代之(C
1-C
10)烷氧基;
R
4c係選自
、
及
;
R
5及R
6係獨立地選自H、視需要經取代之(C
1-C
10)烷基、視需要經取代之(C
1-C
10)烯基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之單環或雙環碳環及視需要經取代之單環或雙環雜環;或R
5及R
6連同其等結合之氮原子一起環狀連接以形成視需要經取代之單環或雙環雜環;
R
7係選自NR
5R
6、視需要經取代之(C
1-C
10)烷基、視需要經取代之(C
1-C
10)烷氧基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基及視需要經取代之雜環烷基;
R
8係選自H及視需要經取代之(C
1-C
10)烷基;
R
9c係選自H及鹵素;
各R
10c及R
10c’係獨立地選自H、OH、NH
2、NO
2、鹵素、視需要經取代之(C
1-C
6)烷基、視需要經取代之(C
1-C
6)烷氧基,及經取代之胺基;及
n係0至3。
條項8. 如條項7之化合物,其中該化合物係式(Id)化合物:
,
其中:
X
3係CR
10d’或N;
各R
21d係獨立地選自H及視需要經取代之(C
1-C
10)烷基;視需要經取代之醯基;視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之單環或雙環碳環及視需要經取代之單環或雙環雜環;
R
1d係選自H、鹵素、視需要經取代之芳基、視需要經取代之(C
1-C
10)烷基及視需要經取代之(C
1-C
10)烷氧基;
R
4d係選自
、
及
;
R
5及R
6係獨立地選自H、視需要經取代之(C
1-C
10)烷基、視需要經取代之(C
1-C
10)烯基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之單環或雙環碳環及視需要經取代之單環或雙環雜環;
或R
5及R
6連同其等結合之氮原子一起環狀連接以形成視需要經取代之單環或雙環雜環;
R
7係選自NR
5R
6、視需要經取代之(C
1-C
10)烷基、視需要經取代之(C
1-C
10)烷氧基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基及視需要經取代之雜環烷基;
R
8係選自H及視需要經取代之(C
1-C
10)烷基;
R
9d係選自H及鹵素;
各R
10d及R
10d’係獨立地選自H、OH、NH
2、NO
2、鹵素、視需要經取代之(C
1-C
6)烷基、視需要經取代之(C
1-C
6)烷氧基,及經取代之胺基;及
n係0至2。
條項9. 如條項7或8之化合物,其中R21或R21d係甲基。
條項11. 如條項10之化合物,其中R5及R6連同其等結合之氮原子一起環狀連接以提供視需要經取代之單環或雙環(C4-C10)雜環。
條項12. 如條項10或11之化合物,其中R
4係
,
其中:
環A係視需要經取代之單環或雙環(C
4-C
10)雜環;
Z
1係CR
14或N,其中R
14係選自H、OH、NH
2、CN、CF
3、OCF
3、CH
2NH
2、鹵素、視需要經取代之(C
1-C
5)烷基、視需要經取代之(C
1-C
5)烷氧基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之碳環及視需要經取代之雜環;及
R
16係選自H、鹵素、-OR
22a、-C(O)R
22b、-CO
2R
22c及-C(O)NR
50R
60、-NR
50R
60、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之碳環、視需要經取代之雜環、視需要經取代之(C
1-C
5)烷基及視需要經取代之(C
1-C
5)烷氧基;
R
22a、R
22b及R
22c係獨立地選自H、視需要經取代之(C
1-C
10)烷基、視需要經取代之環烷基、視需要經取代之芳基、視需要經取代之雜芳基及視需要經取代之雜環;及
R
50及R
60係獨立地選自H、視需要經取代之(C
1-C
10)烷基、視需要經取代之(C
1-C
10)烯基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之單環或雙環碳環及視需要經取代之單環或雙環雜環;
或R
50及R
60連同其等結合之氮原子一起環狀連接以形成視需要經取代之雜環或視需要經取代之雜芳基。
條項13. 如條項12之化合物,其中當該A環係哌啶時,則R16包含至少一個選自視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之碳環、視需要經取代之雜環之環形基團。
條項14. 如條項12之化合物,其中該A環係視需要經取代之哌嗪、吡咯啶或氮雜環丁烷。
條項15. 如條項14之化合物,其中該A環係:
,
其中:
R
23至R
26各係獨立地選自H、鹵素、OH、NO
2、OCF
3、CF
3、視需要經取代之胺基、視需要經取代之(C
1-C
6)烷基、視需要經取代之(C
1-C
6)烷氧基、視需要經取代之環烷基、視需要經取代之芳基、視需要經取代之雜芳基及視需要經取代之雜環;或
R
23至R
24及R
25至R
26中之一或兩者連同其等結合之碳原子一起環狀連接以形成視需要經取代之碳環或視需要經取代之雜環;及
R
40a及R
40b各係獨立地選自H、鹵素、OH、NO
2、OCF
3、CF
3、視需要經取代之胺基、視需要經取代之(C
1-C
6)烷基、視需要經取代之(C
1-C
6)烷氧基、視需要經取代之環烷基、視需要經取代之芳基、視需要經取代之雜芳基及視需要經取代之雜環。
條項16. 如條項15之化合物,其中:
R
23係選自視需要經取代之(C
1-C
6)烷基、視需要經取代之環烷基;及
R
24至R
26、R
40a及R
40b各為H。
條項17. 如條項15之化合物,其中:
R
23、R
25及R
40b中之兩者係獨立地選自視需要經取代之(C
1-C
6)烷基、視需要經取代之環烷基;
R
23、R
25及R
40b中之另一者係H;及
R
24、R
26及R
40a各為H。
條項18. 如條項15之化合物,其中:
R
23及R
24連同其等結合之碳原子一起環狀連接以形成碳環或R
23及R
24各係獨立地選自視需要經取代之(C
1-C
6)烷基及視需要經取代之環烷基;及
R
25至R
26、R
40a及R
40b各為H。
條項20. 如條項12至19中任一項之化合物,其中R
16係:
-(R
110)
nR
210,
其中:
各R
110係獨立地選自視需要經取代之(C
1-C
6)烷基、
、-C(O)(R
110a)n
1、-C(O)O(R
110b)n
2、-S(O)(R
110c)n
3、-SO
2(R
110d)n
4及-C(O)NR
27(R
110e)n
5;其中R
110a至R
110e各獨立地係視需要經取代之(C
1-C
6)烷基、
;R
27至R
28各係獨立地選自H及視需要經取代之(C
1-C
6)烷基;及n至n
5各獨立地係0至3;及
R
210係選自視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之碳環及視需要經取代之雜環。
條項21. 如條項20之化合物,其中:
R
110係選自-C(O)-、-C(O)O-、-C(O)NH-、-S(O)-及-SO
2-;及
R
210係選自視需要經取代之芳基及視需要經取代之雜芳基。
條項22. 如條項20或21之化合物,其中R
210係選自:
、
、
、
及
,
其中:
X
4至X
7、X
9及X
11各係獨立地選自CH、CR
31、S、O及N;
X
8、X
10、X
12及X
13各係獨立地選自S、O及NR
29;
R
29係選自H及視需要經取代之(C
1-C
6)烷基;
R
30至R
32各係獨立地選自H、鹵素、OH、NO
2、OCF
3、CF
3、視需要經取代之胺基、視需要經取代之(C
1-C
6)烷基、視需要經取代之(C
1-C
6)烷氧基、視需要經取代之環烷基、視需要經取代之芳基、視需要經取代之雜芳基及視需要經取代之雜環;及
m
1至m
2各獨立地係0至5。
條項25. 如條項10之化合物,其中R
5係H或Me及R
6係選自:
、
及
;
其中:
Y
1、Y
2及Y
3係獨立地選自CR
14及N;
Z係選自O、S、CHR
11及NR
12;
n係0至4;
R
11係選自H、NH
2、CN、CH
2NH
2、NO
2、鹵素、OR
2a、C(O)R
2b、CO
2R
2c、C(O)NR
5R
6、視需要經取代之胺基、視需要經取代之(C
1-C
5)烷基及視需要經取代之(C
1-C
5)烷氧基,及視需要經取代之雜環;
R
12係選自H、NH
2、鹵素、C(O)R
2d、CO
2R
2e、C(O)NR
5R
6,及視需要經取代之(C
1-C
5)烷基;
係選自視需要經取代之(C
1-C
6)烷基-環烷基、視需要經取代之雜環烷基、視需要經取代之單環或雙環(C
4-C
10)碳環,及視需要經取代之單環或雙環(C
4-C
10)雜環;
R
13係選自H、NH
2、CN、CH
2NH
2、NO
2、鹵素、OR
2f、C(O)R
2g、CO
2R
2h、C(O)NR
5R
6、NR
5R
6、NHC(O)R
2、視需要經取代之(C
1-C
5)烷基及視需要經取代之(C
1-C
5)烷氧基,及視需要經取代之雜環;
R
14係選自H、OH、NH
2、CN、CF
3、OCF
3、CH
2NH
2、鹵素、CO
2R
2、C(O)NR
5R
6、視需要經取代之(C
1-C
5)烷基、視需要經取代之(C
1-C
5)烷氧基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之碳環及視需要經取代之雜環;
R
15係選自H、鹵素、NHC(O)R
2i、OR
2j、C(O)R
2k、OC(O)R
2l、CO
2R
2m、C(O)NR
5R
6、NR
5R
6、視需要經取代之(C
1-C
5)烷基、視需要經取代之(C
1-C
5)烷氧基、視需要經取代之環烷基及視需要經取代之雜環;
R
20係選自H、鹵素、視需要經取代之(C
1-C
5)烷基、視需要經取代之(C
1-C
5)烷氧基、視需要經取代之碳環及視需要經取代之雜環;及
R
2a至R
2m係獨立地選自H、視需要經取代之(C
1-C
10)烷基、視需要經取代之環烷基、視需要經取代之芳基、視需要經取代之雜芳基及視需要經取代之雜環,及烷基、環烷基、芳基、雜芳基及雜環上之任選取代基係獨立地選自:H、OH、NH
2、NO
2、OCF
3、CF
3、鹵素、雜環、雜芳基、視需要經取代之胺基、視需要經取代之(C
1-C
5)烷基及視需要經取代之(C
1-C
5)烷氧基。
條項26. 如條項25之化合物,其中R
6係選自:
,
其中:
環B及環C各係獨立地選自視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之碳環及視需要經取代之雜環;
各R
111係獨立地選自視需要經取代之(C
1-C
6)烷基、
、-C(O)(R
111a)p
1、-C(O)O(R
111b)p
2、-S(O)(R
111c)p
3、-SO
2(R
111d)p
4及-C(O)NR
27(R
111e)p
5;其中R
111a至R
111e各獨立地係視需要經取代之(C
1-C
6)烷基、
;
R
27至R
28各係獨立地選自H及視需要經取代之(C
1-C
6)烷基;及
p至p
5各獨立地係0至3。
條項27. 如條項26之化合物,其中該B環及該C環中之一或兩者係視需要經取代之哌嗪。
條項30. 如條項29之化合物,其中R
13係-C(O)OR
41a、-NHC(O)R
41b、-C(O)NHR
41c、C(O)R
41d、C(O)NH
2、雜環(例如,嗎啉),其中R
41a至R
41d係獨立地選自H、視需要經取代之(C
1-C
6)烷基、視需要經取代之雜環(例如,嗎啉、哌啶、嗎啉-3-酮),及視需要經取代之(C
1-C
6)烷基-雜環。
條項33. 如條項32之化合物,其中Y2及Y3各為CR14。
條項34. 如條項32或33之化合物,其中:
各R
14係獨立地選自H、OH、NH
2、CN、CF
3、OCF
3、CH
2NH
2、鹵素、-C(O)R
42f、-OC(O)R
42g、視需要經取代之(C
1-C
5)烷基及視需要經取代之(C
1-C
5)烷氧基;及
R
15係選自H、鹵素、-OC(O)R
42a、-C(O)R
42b、-C(O)NHR
42c、R
42d或-OR
42e,其中R
42a至R
42g係獨立地選自-OH、視需要經取代之胺基、視需要經取代之(C
1-C
6)烷基、視需要經取代之環烷基、視需要經取代之(C
1-C
10)烷氧基、視需要經取代之雜環、視需要經取代之-O-(C
1-C
6)烷基-雜環,及胺基酸。
條項41. 如條項1至40中任一項之化合物,其中該化合物係式(Ie)化合物:
,
其中:
R
5e及R
6e係獨立地選自H、視需要經取代之(C
1-C
10)烷基、視需要經取代之(C
1-C
10)烯基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之單環或雙環碳環及視需要經取代之單環或雙環雜環;
或R
5e及R
6e連同其等結合之氮原子一起環狀連接以形成視需要經取代之單環或雙環雜環。
條項43. 如條項42之化合物,其中R
7係選自視需要經取代之N-苯胺基、視需要經取代之苯基及視需要經取代之雙環碳環。
條項45. 如條項1至44中任一項之化合物,其中該化合物係表1化合物。
條項46. 如條項1至44中任一項之化合物,其中該化合物不為表2化合物。
條項47. 如條項1至46中任一項之化合物,其中:
當R
1及R
9係H,R
4係
,R
5係H及R
6係視需要經取代之芳基時;則R
2不為4-氟-苯基、對甲苯、3,5-二氯-苯基或苯基;或
當R
1及R
9係H,及R
4係下列中之任一者:
時,則R
2不為3,4-二甲氧基-苯基。
條項48. 一種醫藥組合物,其包含:
治療有效量之根據條項1之式(Ia)化合物,或其醫藥上可接受之鹽、溶劑化物、水合物、前藥或立體異構體;及
醫藥上可接受之賦形劑。
條項49. 如條項48之醫藥組合物,其中式(Ia)化合物係根據條項2至47中任一項之化合物或其醫藥上可接受之鹽、溶劑化物、水合物、前藥或立體異構體。
條項50. 如條項48至49中任一項之醫藥組合物,其中該組合物係眼科組合物,且包含生理上可相容之眼科媒劑。
條項51. 如條項48至50中任一項之醫藥組合物,其中該組合物係水溶液。
條項52. 一種用於調節囊腫纖維化跨膜傳導調節蛋白(CFTR)之化合物,其中該化合物係根據條項1至47中之任一項。
條項53. 一種用於調節CFTR之醫藥組合物,其中該醫藥組合物係根據條項48至51中之任一項。
條項54. 一種用於抑制磷酸二酯酶4 (PDE4)之化合物,其中該化合物係根據條項1至47中之任一項。
條項55. 一種用於抑制PDE4之醫藥組合物,其中該醫藥組合物係根據條項48至51中之任一項。
條項56. 一種調節CFTR之方法,該方法包括使樣本或生物系統與有效量之化合物接觸以調節該CFTR,其中該化合物係根據條項1之式(Ia)化合物,或其醫藥上可接受之鹽、溶劑化物、水合物、前藥或立體異構體。
條項57. 一種抑制PDE4之方法,該方法包括使樣本或生物系統與有效量之抑制PDE之化合物接觸以抑制PDE4,其中該化合物係根據條項1之式(Ia)化合物,或其醫藥上可接受之鹽、溶劑化物、水合物、前藥或立體異構體。
條項58. 如條項56或57之方法,其中該樣本係活體外。
條項59. 如條項56或57之方法,其中該生物系統係活體內。
條項60. 一種治療乾眼症之方法,該方法包括對受試者之眼睛投與治療有效量之根據條項1至47中任一項之化合物或治療有效量之根據條項50之眼科組合物。
條項61. 如條項60之方法,其進一步包括鑑定罹患乾眼症之受試者。
條項62. 如條項60之方法,其進一步包括鑑定與該乾眼症相關聯之潛在疾病或病症。
條項63. 如條項60之方法,其中該乾眼症係由以下組成之群之一或多種疾病或病症引起:乾燥性角膜結膜炎、年齡相關性乾眼症、史蒂文斯-強生症候群、休格倫氏症候群、眼瘢痕性類天皰瘡、角膜損傷、感染、雷德二氏症候群、先天性無淚症、營養失調或缺乏、藥理副作用、隱形眼鏡不耐症、眼部壓力導致腺體及組織破壞、自體免疫疾病、免疫缺陷病症、無法眨眼之昏迷患者、或環境曝露於煙霧、煙、過度乾燥之空氣、空中懸浮微粒、淚腺缺乏症、淚腺導管阻塞、瞼板油缺乏症、眼瞼開口病症及眼表疾病(OSD)。
條項64. 如條項60之方法,其中該乾眼症係由乾燥性角膜結膜炎、年齡相關性乾眼症、史蒂文斯-強生症候群、休格倫氏症候群、眼瘢痕性類天皰瘡、角膜損傷、雷德二氏症候群或先天性無淚症引起。
條項65. 如條項60之方法,其中該乾眼症係由營養失調或缺乏、隱形眼鏡不耐症、自體免疫疾病、免疫缺陷病症、無法眨眼之昏迷患者、或環境曝露於煙霧、煙、過度乾燥之空氣或空中懸浮微粒引起。
條項66. 如條項60至65中任一項之方法,其中在投與後在受試者中減少或減輕一或多種乾眼症症狀。
條項67. 如條項66之方法,其中該一或多種乾眼症症狀係選自乾燥、灼燒、眼癢、畏光、異物感及砂礫感。
條項68. 如條項60至67中任一項之方法,其進一步包括評估投與後眼中天然淚膜之恢復。
條項69. 如條項60至68中任一項之方法,其中對眼睛局部投與該化合物或該眼科組合物。
條項70. 一種治療發炎性疾病之方法,其包括對受試者投與治療有效量之化合物,其中該化合物係根據條項1之式(Ia)化合物,或其醫藥上可接受之鹽、溶劑化物、水合物、前藥或立體異構體。
條項71. 如條項70之方法,其中該受試者患有發炎性疾病。
條項72. 如條項70或71之方法,其中該發炎性疾病係慢性發炎性疾病。
條項73. 如條項70或71之方法,其中該發炎性疾病係急性發炎性疾病。
條項74. 如條項70至73中任一項之方法,其中該發炎性疾病係選自慢性阻塞性肺病(COPD)、哮喘、發炎性呼吸道疾病、牛皮癬、牛皮癬性病症、異位性皮膚炎、發炎性腸病(IBD)、類風溼性關節炎、關節黏連性脊椎炎、神經發炎及結膜炎。
條項75. 如條項70至73中任一項之方法,其中該發炎性疾病係發炎性皮膚疾病。
條項76. 一種治療 CFTR相關適應症之方法,其包括對有需要受試者投與治療有效量之化合物,其中該化合物係根據條項1之式(Ia)化合物,或其醫藥上可接受之鹽、溶劑化物、水合物、前藥或立體異構體。
條項77. 如條項76之方法,其中該CFTR相關適應症係選自慢性阻塞性肺病(COPD)、哮喘、支氣管炎、支氣管擴張、乳糜瀉、便祕、膽汁淤積性肝病、慢性鼻竇炎及肝損害。
條項78. 如條項56至77中任一項之方法,其中該式(Ia)化合物或其醫藥上可接受之鹽、溶劑化物、水合物、前藥或立體異構體係根據條項1至47中之任一項。
條項79. 如條項78之方法,其中該式(Ia)化合物係表1或表2化合物,或其醫藥上可接受之鹽、溶劑化物、水合物、前藥或立體異構體。
條項80. 如條項78之方法,其中該式(Ia)化合物係表1化合物,或其醫藥上可接受之鹽、溶劑化物、水合物、前藥或立體異構體。
如本文描述,本內文係指本發明化合物、組合物及方法之各種實施例。本文描述之各種實施例意欲提供各種說明性實例且不應解釋為替代物種之描述。相反,應注意本文提供之各種實施例之描述可具有重疊之範疇。本文討論之實施例係僅說明性的且無意限制現有技術之範疇。
6. 實例
提供下列實例以闡述本發明且不應以任何方式解釋為限制現有技術之範疇。功能上等同之任何方法係於現有技術之範疇內。除彼等本文描述者外,現有技術之各種修飾對於熟習此項技術者而言將自前述描述及隨附圖式變得顯而易見。此等修飾落於隨附申請專利範圍之範疇內。
除非另有規定,否則所有溫度均以攝氏度計。已努力確保所用數值(例如,數量、溫度等)之精確性,但應容許一些實驗誤差及偏差。
所有實驗均符合在有意識之動物中進行研究之道德準則且完全符合以色列中央動物護理委員會之要求。
在下文實例中,若縮寫未經定義,則該縮寫具有其普遍接受之含義。
aq. = 水性
LC-MS = 液相層析術-質譜法
MS = 質譜法
THF = 四氫呋喃
NaHCO
3= 碳酸氫鈉
Cs
2CO
3= 碳酸銫
NaH = 氫化鈉
o/n = 整夜
HATU = 1-[雙(二甲基胺基)亞甲基]-1H-1,2,3-三唑并[4,5-b]吡啶鎓3-氧化六氟磷酸鹽
r.t. = 室溫
LAH = 氫化鋁鋰
DCM = 二氯甲烷
DMF = 二甲基甲醯胺
DMSO = 二甲基亞碸
DIEA = 二異丙基乙胺
equiv. = 當量
EtOAc或EA = 乙酸乙酯
EtOH = 乙醇
EDCI = 1-乙基-3-(3-二甲基胺基丙基)碳二亞胺
g = 公克
h = 小時
HCl = 鹽酸
HPLC = 高效液相層析術
HOAc = 乙酸
HBTU = O-苯并三唑-N,N,N`,N`-四甲基脲鎓-六氟磷酸鹽
M = 莫耳
MeOH = 甲醇
mg = 毫克
mL = 毫升
mmol = 毫莫耳
mp = 熔點
m/z = 質荷比
NaCl = 氯化鈉
Na
2CO
3= 碳酸鈉
NMR = 核磁共振
NaOH = 氫氧化鈉
Na
2SO
4= 硫酸鈉
ppm = 百萬分率
TFA = 三氟乙酸
TLC = 薄層層析術
SCOP = 莨菪鹼
TsOH = 對甲苯磺酸
UV = 紫外線
重量% = 重量百分比
μM = 微莫耳
一般合成方法
最終化合物係藉由HPLC/MS分析確認且以重量計測定為>90%純。
1H及
13C NMR光譜係以CDCl
3(殘留內標CHCl
3= δ 7.26)、DMSO-d
6(殘留內標CD
3SOCD
2H = δ 2.50)、甲醇-d
4(殘留內標CD
2HOD = δ 3.20)或丙酮-d
6(殘留內標CD
3COCD
2H = δ 2.05)記錄。報告之化學位移(δ)係以百萬分率(ppm)給定及偶合常數(J)係以赫茲(Hz)給定。自旋多重性報告為s =單峰,bs =寬單峰,bm =寬多重峰,d =雙峰,t =三重峰,q =四重峰,p =五重峰,dd =雙峰之雙峰,ddd =雙峰之雙峰之雙峰,dt =三重峰之雙峰,td =雙峰之三重峰,tt =三重峰之三重峰及m =多重峰。
以梯度溶析進行HPLC-MS分析。以矽膠管柱於正相及反相兩者中進行中壓液相層析術(MPLC)。
實例1:常見中間體之合成
方法A:7-取代之吡唑并[1,5-a]嘧啶-2-羧酸(式II-a)之合成
7-苯基吡唑并[1,5-a]嘧啶-2-羧酸之合成
步驟1
將苯乙酮(0.29 mL,2.5 mmol)及DMF-DMA (1.33 mL,10 mmol)組合於DMF (2.5 mL)中並加熱至回流,歷時17小時。藉由DCM及NH
4Cl水溶液萃取該反應混合物。有機層係經無水MgSO
4乾燥並濃縮。藉由EA及NH
4Cl水溶液萃取該混合物以產生呈黃色固體之(E)-3-(二甲基胺基)-1-苯基丙-2-烯-1-酮(193 mg,43%)。
1H NMR (400 MHz, DMSO-d
6) δ 7.94 - 7.85 (m, 2H), 7.72 (d, J = 12.3 Hz, 1H), 7.55 - 7.38 (m, 3H), 5.83 (d, J = 12.3 Hz, 1H), 3.15 (s, 3H), 2.91 (s, 3H)。
步驟2
將(E)-3-(二甲基胺基)-1-苯基丙-2-烯-1-酮(190 mg,1.08 mmol)及5-胺基-1H-吡唑-3-羧酸甲酯(152 mg,1.08 mmol)溶解於乙酸(5.4 mL)中並加熱至回流,歷時2.5小時。藉由DCM及NaHCO
3水溶液萃取該反應混合物。有機層係經無水MgSO
4乾燥並濃縮。藉由MPLC純化該反應混合物。藉由使用DCM及己烷固化粗混合物以產生呈白色固體之7-苯基吡唑并[1,5-a]嘧啶-2-羧酸甲酯(87.8 mg,32%)。
1H NMR (400 MHz, DMSO-d
6) δ 8.75 (d, J = 4.3 Hz, 1H), 8.14 - 8.04 (m, 2H), 7.71 - 7.61 (m, 3H), 7.41 (d, J = 4.3 Hz, 1H), 7.31 (s, 1H), 3.90 (s, 3H)。
步驟3
將7-苯基吡唑并[1,5-a]嘧啶-2-羧酸甲酯(87 mg,0.34 mmol)溶解於H
2O/THF/MeOH (1.4/2.2/1.1 mL)中,接著添加於H
2O中之氫氧化鈉(1 N,0.68 mL)並在60℃下攪拌2小時。在0℃下冷卻後,藉由添加1 N HCl酸化該混合物。然後藉由使用H
2O濾除沈澱晶體以產生呈黃色固體之7-苯基吡唑并[1,5-a]嘧啶-2-羧酸(65.5 mg,80%)。
1H NMR (400 MHz, DMSO-d
6) δ 13.3 (bs, 1H), 8.72 (d, J = 4.3 Hz, 1H), 8.16 - 8.05 (m, 2H), 7.73 - 7.60 (m, 3H), 7.39 (d, J = 4.3 Hz, 1H), 7.23 (s, 1H)。
7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羧酸之合成
步驟1
將3’,4’-二甲氧基苯乙酮(1 g,5.55 mmol)及DMF-DMA (2.95 mL,22.2 mmol)組合於DMF (5.55 mL)中並加熱至回流,歷時18小時。藉由DCM及NH
4Cl水溶液萃取該混合物。藉由使用乙醚固化該反應混合物以產生呈橙色固體之(E)-1-(3,4-二甲氧基苯基)-3-(二甲基胺基)丙-2-烯-1-酮(797 mg,61%)。
1H NMR (400 MHz, DMSO-d
6) δ 7.66 (d, J = 12.4 Hz, 1H), 7.54 (dd, J = 8.4, 2.0 Hz, 1H), 7.45-7.44 (m, 1H), 6.98 (d, J = 8.4 Hz, 1H), 5.82 (d, J = 12.4 Hz, 1H), 3.82 - 3.80 (m, 6H), 3.13 (s, 3H), 2.91 (s, 3H)。
步驟2
將(E)-1-(3,4-二甲氧基苯基)-3-(二甲基胺基)丙-2-烯-1-酮(790 mg,3.35 mmol)及5-胺基-1H-吡唑-3-羧酸甲酯(473 mg,3.35 mmol)溶解於乙酸(15 mL)中並加熱至回流,歷時2小時。在蒸發乙酸後,藉由使用乙醚固化該混合物以產生呈白色固體之7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羧酸甲酯(919 mg,88%)。
1H NMR (400 MHz, DMSO-d
6): δ 8.69 (d, J = 4.4 Hz, 1H), 7.87 (dd, J = 8.6 Hz, 2.4 Hz, 1H), 7.78 (d, J = 2.4 Hz, 1H), 7.46 (d, J = 4.4 Hz, 1H), 7.25 (s, 1H), 7.21 (d, J = 8.8 Hz, 1H), 3.91 (s, 3H), 3.89 (s, 3H), 3.87 (s, 3H)。
步驟 3
將7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羧酸甲酯(915 mg,2.92 mmol)溶解於H
2O/THF/MeOH (12/20/10 mL)中,接著添加於H
2O中之氫氧化鈉(1 N,5.84 mL)並在60℃下攪拌2小時。在0℃下冷卻後,藉由添加1 N HCl酸化該混合物。然後藉由使用H
2O濾除沈澱晶體以產生呈淺黃色固體之7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羧酸(980 mg,>99%)。
1H NMR (400 MHz, DMSO-d
6): δ 13.35 (s, 1H), 8.68 (d, J = 4.4 Hz, 1H), 7.90 (dd, J = 8.4 Hz, 2.0 Hz, 1H), 7.80 (d, J = 2.0 Hz, 1H), 7.44 (d, J = 4.4 Hz, 1H), 7.22 - 7.20 (m, 2H), 3.89 (s, 3H), 3.87 (s, 3H)。
7-(4- 氟 -3- 甲氧基苯基 ) 吡唑并 [1,5-a] 嘧啶 -2- 羧酸之合成 步驟 1
將1-(4-氟-3-甲氧基苯基)乙-1-酮(500 mg,2.97 mmol)及DMF-DMA (1.58 mL,11.9 mmol)組合於DMF (2.97 mL)中並加熱至回流,歷時21小時。藉由DCM及NH
4Cl水溶液萃取該混合物。藉由使用DCM及己烷固化該反應混合物以產生呈橙色固體之(E)-3-(二甲基胺基)-1-(4-氟-3-甲氧基苯基)丙-2-烯-1-酮(516 mg,77%)。
1H NMR (400 MHz, DMSO-d
6) δ 7.71 (d, J = 12.2 Hz, 1H), 7.60 (dd, J = 8.7, 2.0 Hz, 1H), 7.56 - 7.49 (m, 1H), 7.29 - 7.20 (m, 1H), 5.82 (d, J = 12.2 Hz, 1H), 3.89 (s, 3H), 3.15 (s, 3H), 2.92 (s, 3H)。
步驟 2
將(E)-3-(二甲基胺基)-1-(4-氟-3-甲氧基苯基)丙-2-烯-1-酮(515 mg,2.3 mmol)及5-胺基-1H-吡唑-3-羧酸甲酯(325 mg,2.3 mmol)溶解於乙酸(12 mL)中並加熱至回流,歷時2小時。藉由DCM及NaHCO
3水溶液萃取該反應混合物。有機層係經無水MgSO
4乾燥並濃縮。藉由使用DCM及己烷固化粗混合物以產生呈白色固體之7-(4-氟-3-甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羧酸甲酯(1950 mg,>99%)。
1H NMR (400 MHz, DMSO-d
6) δ 8.75 (d, J = 4.4 Hz, 1H), 7.92 (dd, J = 8.4, 2.1 Hz, 1H), 7.80 - 7.74 (m, 1H), 7.55 - 7.45 (m, 2H), 7.31 (s, 1H), 3.94 (s, 3H), 3.91 (s, 3H)。
步驟 3
將7-(4-氟-3-甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羧酸甲酯(693 mg,2.3 mmol)溶解於H
2O/THF/MeOH (9/15/8 mL)中,接著添加於H
2O中之氫氧化鈉(1 N,4.6 mL)並在60℃下攪拌4小時。在0℃下冷卻後,藉由添加1 N HCl酸化該混合物。然後藉由使用H
2O濾除沈澱晶體以產生呈黃色固體之7-(4-氟-3-甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羧酸(521 mg,79%)。
1H NMR (400 MHz, DMSO-d
6) δ 13.40 (s, 1H), 8.73 (d, J = 4.4 Hz, 1H), 7.93 (dd, J = 8.4, 2.1 Hz, 1H), 7.83 - 7.76 (m, 1H), 7.56 - 7.42 (m, 2H), 7.23 (s, 1H), 3.94 (s, 3H)。
7-(3,4- 二氟苯基 ) 吡唑并 [1,5-a] 嘧啶 -2- 羧酸之合成 步驟 1
將1-(3,4-二氟苯基)乙-1-酮(1000 mg,6.41 mmol)及DMF-DMA (3.40 mL,25.62 mmol)組合於DMF (3 mL)中並加熱至回流,歷時22小時。藉由DCM及水溶液NH
4Cl萃取該混合物。有機層係經無水MgSO
4乾燥並濃縮以產生呈橙色固體之(E)-1-(3,4-二氟苯基)-3-(二甲基胺基)丙-2-烯-1-酮(1275.4 mg,>99%)。
1H NMR (400 MHz, DMSO-d
6) δ 7.96 - 7.88 (m, 1H), 7.82 - 7.77 (m, 1H), 7.74 (d, J = 12.2 Hz, 1H), 7.53 - 7.45 (m, 1H), 5.85 (d, J = 12.2 Hz, 1H), 3.15 (s, 3H), 2.93 (s, 3H)。
步驟2
將(E)-1-(3,4-二氟苯基)-3-(二甲基胺基)丙-2-烯-1-酮(1275 mg,6.04 mmol)及5-胺基-1H-吡唑-3-羧酸甲酯(852 mg,6.04 mmol)溶解於乙酸(30 mL)中並加熱至回流,歷時1小時。藉由DCM及NaHCO
3水溶液萃取該反應混合物。有機層係經無水MgSO
4乾燥並濃縮。藉由使用DCM及己烷固化粗混合物以產生呈黃色固體之7-(3,4-二氟苯基)吡唑并[1,5-a]嘧啶-2-羧酸甲酯(1188 mg,68%)。
1H NMR (400 MHz, DMSO-d
6) δ 8.76 (d, J = 4.4 Hz, 1H), 8.32 - 8.23 (m, 1H), 8.05 - 7.97 (m, 1H), 7.80 - 7.70 (m, 1H), 7.48 (d, J = 4.4 Hz, 1H), 7.33 (s, 1H), 3.90 (s, 3H)。
步驟 3
將7-(3,4-二氟苯基)吡唑并[1,5-a]嘧啶-2-羧酸甲酯(1188 mg,4.11 mmol)溶解於H
2O/THF/MeOH (16/20/10 mL)中,接著添加於H
2O中之氫氧化鈉(1 N,8.22 mL)並在60℃下攪拌2小時。在0℃下冷卻後,藉由添加1 N HCl酸化該混合物。然後藉由使用H
2O濾除沈澱晶體以產生呈淺橙色固體之7-(3,4-二氟苯基)吡唑并[1,5-a]嘧啶-2-羧酸(280 mg,25%)。
1H NMR (400 MHz, DMSO-d
6) δ 13.45 (s, 1H), 8.74 (d, J = 4.4 Hz, 1H), 8.36 - 8.27 (m, 1H), 8.09 - 8.01 (m, 1H), 7.79 - 7.70 (m, 1H), 7.46 (d, J = 4.4 Hz, 1H), 7.25 (s, 1H)。
7-(2- 氟 -4- 甲氧基苯基 ) 吡唑并 [1,5-a] 嘧啶 -2- 羧酸之合成 步驟 1
將1-(2-氟-4-甲氧基苯基)乙-1-酮(1000 mg,5.95 mmol)及DMF-DMA (3.2 mL,23.8 mmol)組合於DMF (6 mL)中並加熱至回流,歷時18小時。藉由DCM及NH
4Cl水溶液萃取該混合物。在蒸發DCM後,藉由EA及NH
4Cl水溶液萃取該混合物。藉由使用乙醚固化該反應混合物以產生呈橙色固體之(E)-3-(二甲基胺基)-1-(2-氟-4-甲氧基苯基)丙-2-烯-1-酮(1057 mg,80%)。
1H NMR (400 MHz, DMSO-d
6) δ 7.69 - 7.57 (m, 2H), 6.87 - 6.77 (m, 2H), 6.99 (d, J = 12.2 Hz, 1H), 3.80 (s, 3H), 3.12 (s, 3H), 2.84 (s, 3H)。
步驟 2
將(E)-3-(二甲基胺基)-1-(2-氟-4-甲氧基苯基)丙-2-烯-1-酮(1057 mg,4.74 mmol)及5-胺基-1H-吡唑-3-羧酸甲酯(668 mg,4.74 mmol)溶解於乙酸(24 mL)中並加熱至回流,歷時8小時。在蒸發乙酸後,藉由EA及NaOH水溶液萃取該混合物以產生呈淺橙色固體之7-(2-氟-4-甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羧酸甲酯(972 mg,68%)。
1H NMR (400 MHz, DMSO-d
6) δ 8.73 (d, J = 4.3 Hz, 1H), 7.77 (t, J = 8.5 Hz, 1H), 7.32 (dd, J = 4.3, 0.7 Hz, 1H), 7.30 (s, 1H), 7.14 (dd, J = 12.4, 2.4 Hz, 1H), 7.04 (dd, J = 8.7, 2.5 Hz, 1H), 3.89 (s, 3H), 3.87 (s, 3H)。
步驟 3
將7-(2-氟-4-甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羧酸甲酯(970 mg,3.22 mmol)溶解於H
2O/THF/MeOH (12/20/10 mL)中,接著添加於H
2O中之氫氧化鈉(1 N,6.44 mL)並在60℃下攪拌4小時。在0℃下冷卻後,藉由添加1 N HCl酸化該混合物。然後藉由使用H
2O濾除沈澱晶體以產生呈白色固體之7-(2-氟-4-甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羧酸(790 mg,85%)。
1H NMR (400 MHz, DMSO-d
6) δ 13.38 (s, 1H), 8.70 (d, J = 4.3 Hz, 1H), 7.78 (t, J = 8.5 Hz, 1H), 7.29 (dd, J = 4.2, 0.7 Hz, 1H), 7.22 (s, 1H), 7.13 (dd, J = 12.4, 2.4 Hz, 1H), 7.03 (dd, J = 8.7, 2.5 Hz, 1H), 3.89 (s, 3H)。
方法B:6-取代之吡唑并[1,5-a]嘧啶-2-羧酸(式II-b)之合成
6-(3,4- 二甲氧基苯基 ) 吡唑并 [1,5-a] 嘧啶 -2- 羧酸之合成 步驟 1
將2-溴丙二醛(200 mg,1.32 mmol)及5-胺基-1H-吡唑-3-羧酸甲酯(187 mg,1.32 mmol)溶解於乙酸(13 mL)中並加熱至回流,歷時22小時。在蒸發乙酸後,藉由DCM及HCl水溶液萃取該混合物。藉由MPLC純化該反應混合物以產生呈白色固體之產物6-溴吡唑并[1,5-a]嘧啶-2-羧酸甲酯(138 mg,41%)。
1H NMR (400 MHz, DMSO-d
6) δ 9.72 (dd, J = 2.2, 0.9 Hz, 1H), 8.77 (d, J = 2.2 Hz, 1H), 7.28 (d, J = 0.8 Hz, 1H), 3.91 (s, 3H)。
步驟 2 及 3
在真空中吹掃6-溴吡唑并[1,5-a]嘧啶-2-羧酸甲酯(130 mg,0.508 mmol)及PdCl
2(PPh
3)
2(4 mg,0.01 mmol)。40 min後,將試劑溶解於二噁烷(5 mL)中。向溶液添加於水中之碳酸鈉(2 M,2.29 mL)並加熱至90℃。0.5小時後,添加3,4-二甲氧基苯基硼酸於二噁烷(2 mL)中之溶液並攪拌1小時。有機層係經無水MgSO
4乾燥並濃縮。將該反應混合物溶解於H
2O/THF/MeOH (2/4/2 mL)中,接著添加於H
2O中之氫氧化鈉(1 N,1.1 mL)並在60℃下攪拌4小時。在0℃下冷卻後,藉由添加1 N HCl酸化該混合物。然後藉由使用H
2O濾除沈澱晶體以產生呈白色固體之6-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羧酸(90 mg,59%)。
1H NMR (400 MHz, DMSO-d6) δ 13.23 (s, 1H), 9.54 (s, 1H), 9.08 (d, J = 2.2 Hz, 1H), 7.48 - 7.45 (m, 1H), 7.43 (d, J = 8.3 Hz, 1H), 7.16 (s, 1H), 7.11 (d, J = 8.4 Hz, 1H), 3.89 (s, 3H), 3.83 (s, 3H)。
方法C:7-取代之吡唑并[1,5-a]嘧啶-2-羰基氯(式II-c)之合成
7-(3,4- 二甲氧基苯基 ) 吡唑并 [1,5-a] 嘧啶 -2- 羰基氯之合成
向7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羧酸(70 mg,0.23 mmol)於氯仿(2.3 mL)中之溶液添加DMF (催化量)及SOCl
2(0.084 mL,1.15 mmol)並在60℃下攪拌2小時。濃縮該混合物且無需進一步純化即可用於下一步驟中。
1H NMR (400 MHz, DMSO-d
6) δ 8.68 (d, J = 4.4 Hz, 1H), 7.90 (d, J = 8.5 Hz, 1H), 7.81 - 7.76 (m, 1H), 7.45 (d, J = 4.4 Hz, 1H), 7.24 - 7.16 (m, 2H), 3.89 (s, 3H), 3.86 (s, 3H)。
方法D:7-取代之吡唑并[1,5-a]嘧啶-2-胺(式II-d)之合成
7-(3,4- 二甲氧基苯基 ) 吡唑并 [1,5-a] 嘧啶 -2- 胺之合成 步驟 1
將7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羧酸(1 g,3.34 mmol)、DPPA (0.79 mL,3.68 mmol)、TEA (5.17 mL,3.68 mmol)組合於t-BuOH (0.2 M,15 mL)中並加熱至回流,歷時18.5小時。在蒸發後,藉由DCM及NaHCO
3水溶液萃取該反應混合物。藉由MPLC純化該混合物。藉由使用DCM及己烷固化粗混合物以產生呈白色固體之產物(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)胺甲酸第三丁酯(260 mg,21%)。
1H NMR (400 MHz, DMSO-d
6) δ 10.25 (s, 1H), 8.45 (d, J = 4.6 Hz, 1H), 7.97 (d, J = 2.1 Hz, 1H), 7.74 (dd, J = 8.5, 2.2 Hz, 1H), 7.18 - 7.13 (m, 2H), 6.71 (s, 1H), 3.88 (s, 3H), 3.86 (s, 3H), 1.49 (s, 9H)。
步驟 2
將(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)胺甲酸第三丁酯(250 mg,0.675 mmol)溶解於甲醇(6 mL)中,然後在室溫下添加於二噁烷中之鹽酸鹽(4 N,3 mL)。16.5小時後,藉由添加1 N NaOH鹼化該混合物並藉由DCM萃取。藉由MPLC純化該混合物。藉由使用DCM及己烷固化粗混合物以產生呈黃色固體之產物7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-胺(157 mg,86%)。1H NMR (400 MHz, DMSO-d6) δ 8.23 (d, J = 4.6 Hz, 1H), 7.81 - 7.75 (m, 2H), 7.13 (d, J = 8.5 Hz, 1H), 6.87 (d, J = 4.6 Hz, 1H), 5.76 (s, 1H), 5.70 (s, 2H), 3.85 (s, 3H), 3.84 (s, 3H)。
實例2:式(Ia)至(Ic)化合物之合成
一般方法A
化合物 2 之合成
將7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羧酸(50 mg,0.17 mmol)、環己基胺(0.022 mL,0.18 mmol)、HBTU (70 mg,0.18 mmol)、二異丙基乙胺(0.057 mL,0.33 mmol)組合於DCM中。在室溫下攪拌1小時後,由DCM及NaHCO
3水溶液萃取該反應混合物。藉由MPLC純化該反應混合物。使用DCM及己烷固化粗混合物以產生呈白色固體之化合物2,N-環己基-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺(34.8 mg,55%產率)。
化合物 10 之合成
將7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羧酸(100 mg,0.33 mmol)、反式4-胺基環己烷羧酸甲酯鹽酸鹽(71.3 mg,0.37 mmol)、HBTU (140 mg,0.37 mmol)、二異丙基乙胺(0.17 mL,1 mmol)組合於DCM中。在室溫下攪拌1小時後,藉由DCM及NaHCO
3水溶液萃取該反應混合物。藉由MPLC純化該反應混合物。使用DCM及己烷固化粗混合物以產生呈淺黃色固體之化合物10,(1r,4r)-4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)環己烷-1-羧酸甲酯(135 mg,92%產率)。
化合物 144 之合成
將7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羧酸(1688 mg,5.639 mmol)、4-胺基雙環[2,2,2]辛烷-1-羧酸甲基酯(1033.1 mg,5.639 mmol)、HBTU (2352 mg,6.203 mmol)、二異丙基乙胺(1.943 mL,11.278 mmol)組合於DCM中。在室溫下攪拌2小時後,藉由DCM及NaHCO
3水溶液萃取該反應混合物。藉由MPLC純化該反應混合物。使用DCM及己烷固化粗混合物以產生呈黃色固體之化合物144,4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)雙環[2.2.2]辛烷-1-羧酸甲酯(3167.6 mg,>99%產率)。
化合物 149 之合成
將化合物144 (3167.6 mg,6.819 mmol)溶解於H
2O/THF/MeOH (27/22/11 mL)中,接著添加於H
2O中之氫氧化鈉(1 N,13.638 mL)並在60℃下攪拌2小時。在0℃下冷卻後,藉由添加1 N HCl酸化該混合物。然後藉由使用H
2O過濾該固體以產生呈淺黃色固體之化合物149,4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)雙環[2.2.2]辛烷-1-羧酸(1989 mg,65%)。
化合物 151 之合成
將化合物149 (1000 mg,2.220 mmol)、1-甲基哌嗪(0.271 mL,2.442 mmol)、HBTU (926 mg,2.442 mmol)、二異丙基乙胺(0.765 mL,4.440 mmol)組合於DCM中。在室溫下攪拌4小時後,該反應混合物藉由DCM及NaHCO
3水溶液萃取並藉由MPLC純化。使用DCM及乙醚固化粗混合物以產生呈白色固體之化合物151,7-(3,4-二甲氧基苯基)-N-(4-(4-甲基哌嗪-1-羰基)雙環[2.2.2]辛-1-基)吡唑并[1,5-a]嘧啶-2-甲醯胺(961.6 mg,81%產率)。
一般方法B
化合物 36 之合成
向3-胺基雙環[1.1.1]戊烷-1-羧酸甲酯鹽酸鹽(47.5 mg,0.267 mmol)及吡啶(0.136 mL,1.67 mmol)於氯仿中之溶液滴加溶解於氯仿中之7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羰基氯(106 mg,0.334 mmol)並在0℃下攪拌1小時。藉由DCM及水溶液NH
4Cl萃取該反應混合物。藉由MPLC純化該反應混合物。藉由使用DCM及己烷固化粗混合物以產生呈白色固體之化合物36,3-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)雙環[1.1.1]戊烷-1-羧酸甲酯(40.7 mg,29%)。
化合物 37 之合成
將化合物36 (60 mg,0.142 mmol)溶解於H
2O/THF/MeOH (0.6/1/0.5 mL)中,接著添加於H
2O中之氫氧化鈉(1 N,0.284 mL)並在30℃攪拌2小時。在0℃冷卻後,藉由添加1 N HCl酸化該混合物。藉由DCM及H
2O萃取該混合物。藉由使用DCM及己烷固化粗混合物,產生呈黃色固體之化合物37,3-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)雙環[1.1.1]戊烷-1-羧酸(36.8 mg,63%)。
化合物 96 之合成
將化合物37 (874 mg,2.140 mmol)、嗎啉(0.205 mL,2.354 mmol)、HBTU (893 mg,2.354 mmol)、二異丙基乙胺(0.746 mL,4.280 mmol)組合於DCM中。在室溫攪拌4小時後,該反應混合物藉由DCM及NaHCO
3水溶液萃取並藉由MPLC純化。使用DCM及正庚烷固化粗混合物,產生呈白色固體之化合物96,7-(3,4-二甲氧基苯基)-N-(3-(嗎啉-4-羰基)雙環[1.1.1]戊-1-基)吡唑并[1,5-a]嘧啶-2-甲醯胺(728.9 mg,71%產率)。
化合物 140 之合成
向4-胺基-2-氯苯甲酸甲酯(278 mg,1.5 mmol)及吡啶(0.25 mL,3 mmol)於氯仿中之溶液滴加溶解於氯仿中之7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羰基氯(318 mg,1 mmol)並在0℃攪拌17小時。藉由DCM及NH
4Cl水溶液萃取該反應混合物。有機層係經無水MgSO
4乾燥並濃縮。藉由MPLC純化該反應混合物。藉由使用DCM及己烷固化粗混合物,產生呈白色固體之化合物140,2-氯-4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸甲酯(353 mg,76%)。
化合物 136 之合成
向4-胺基-3-氟苯甲酸甲酯(339 mg,2.01 mmol)及吡啶(0.33 mL,4.01 mmol)於氯仿中之溶液滴加溶解於氯仿中之7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羰基氯(637 mg,2.01 mmol)並在0℃下攪拌2小時。藉由DCM及水溶液NH
4Cl萃取該反應混合物。藉由MPLC純化該混合物以產生呈白色固體之化合物136,4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)-3-氟苯甲酸甲酯(684 mg,76%)。
化合物 156 之合成
將化合物136 (550 mg,1.22 mmol)溶解於H
2O/THF/MeOH (5/8/4 mL)中,接著添加於H
2O中之氫氧化鈉(1 N,2.44 mL)並在60℃下攪拌30小時。在0℃下冷卻後,藉由添加1 N HCl酸化該混合物。然後藉由使用H
2O過濾該固體。藉由MPLC純化粗混合物以產生呈白色固體之化合物156,4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)-3-氟苯甲酸(175 mg,20%)。
化合物 158 之合成
將化合物156 (80 mg,0.183 mmol)、1-甲基哌嗪(0.022 mL,0.202 mmol)、HBTU (77 mg,0.202 mmol)、二異丙基乙胺(0.063 mL,0.366 mmol)組合於DCM中。在室溫下攪拌1小時後,該反應混合物由DCM及NaHCO
3水溶液萃取並藉由MPLC純化。使用DCM及己烷固化粗混合物以產生化合物呈白色固體之158,7-(3,4-二甲氧基苯基)-N-(2-氟-4-(4-甲基哌嗪-1-羰基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺(43.8 mg,46%產率)。
化合物 289 之合成
向5-(吡咯啶-1-基)吡啶-2-胺(108 mg,0.66 mmol)及吡啶(0.183 mL,0.99 mmol)於氯仿中之溶液滴加溶解於氯仿中之7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羰基氯(210 mg,0.66 mmol)並在0℃下攪拌17.5小時。該反應混合物由DCM及NaHCO
3水溶液萃取並藉由MPLC純化。使用DCM及己烷固化粗混合物以產生呈棕色固體之化合物289,7-(3,4-二甲氧基苯基)-N-(5-(吡咯啶-1-基)吡啶-2-基)吡唑并[1,5-a]嘧啶-2-甲醯胺(43.5 mg,14%)。
一般方法C
化合物 6 之合成
將7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羧酸(50 mg,0.167 mmol)、對甲氧苯胺(22.7 mg,0.184 mmol)、HBTU (70 mg,0.184 mmol)、二異丙基乙胺(0.057 mL,0.334 mmol)組合於DCM中。在室溫下攪拌1小時後,藉由DCM及NaHCO
3水溶液萃取該反應混合物。藉由MPLC純化該反應混合物。使用DCM及己烷固化粗混合物以產生呈白色固體之化合物6,7-(3,4-二甲氧基苯基)-N-(4-甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺(56.3 mg,83%產率)。
化合物 15 之合成 步驟 1
將4-胺基苯酚(3 g,27.49 mmol)、咪唑(2.246 g,32.988 mmol)、DMAP (34 mg,0.275 mmol)及TBDMSCl (4.972 g,32.988 mmol)組合於DCM中。在室溫下攪拌21小時後,藉由使用H
2O過濾該反應混合物,及然後藉由DCM及H
2O萃取。藉由MPLC純化粗混合物以產生呈液體之產物4-((第三丁基二甲基矽基)氧基)苯胺(2709.5 mg,44%產率)。
步驟 2
將7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羧酸(3.629 g,12.127 mmol)、4-((第三丁基二甲基矽基)氧基)苯胺(2.709 g,12.127 mmol)、HBTU (5.059 g,13.340 mmol)、二異丙基乙胺(4.214 mL,24.454 mmol)組合於DCM中。在室溫下攪拌5小時後,藉由DCM及NaHCO
3水溶液萃取該反應混合物。藉由MPLC純化該混合物以產生呈白色固體之N-(4-((第三丁基二甲基矽基)氧基)苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺(5409.7 mg,88%產率)。
步驟 3
在0℃下將N-(4-((第三丁基二甲基矽基)氧基)苯基)-7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺(5.409 g,10.718 mmol)溶解於THF (50 mL)中,及然後添加於THF中之TBAF (1 M,10.718 mL)。15 min後,該反應混合物藉由使用H
2O (50 mL)淬滅並藉由EA萃取。藉由MPLC純化該混合物。使用DCM及乙醚固化粗混合物以產生呈白色固體之化合物15,7-(3,4-二甲氧基苯基)-N-(4-羥基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺(2805.6 mg,67%產率)。
化合物 11 之合成
將7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羧酸(100 mg,0.334 mmol)、4-胺基苯甲酸甲酯(55.64 mg,0.368 mmol)、HBTU (140 mg,0.368 mmol)、二異丙基乙胺(0.114 mL,0.668 mmol)組合於DCM中。在室溫下攪拌1小時後,藉由DCM及NaHCO
3水溶液萃取該反應混合物。藉由MPLC純化該反應混合物。使用DCM及己烷固化粗混合物以產生呈淺黃色固體之化合物11,4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸甲酯(75 mg,52%產率)。
化合物 14 之合成
將化合物11 (550 mg,1.22 mmol)溶解於H2O/THF/MeOH (5/8/4 mL)中,接著添加於H
2O中之氫氧化鈉(1 N,2.44 mL)並在60℃下攪拌30小時。在0℃下冷卻後,藉由添加1 N HCl酸化該混合物。然後藉由使用H
2O過濾該固體。藉由MPLC純化該反應混合物以產生呈黃色固體之化合物14,4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸(464 mg,91%)。
化合物 97 之合成
將化合物14 (80 mg,0.183 mmol)、1-甲基哌嗪(0.022 mL,0.202 mmol)、HBTU (77 mg,0.202 mmol)、二異丙基乙胺(0.063 mL,0.366 mmol)組合於DCM中。在室溫下攪拌24小時後,該反應混合物藉由DCM及NaHCO
3水溶液萃取並藉由MPLC純化。使用DCM及己烷固化粗混合物以產生呈白色固體之化合物97,7-(3,4-二甲氧基苯基)-N-(4-(4-甲基哌嗪-1-羰基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺(43.8 mg,46%產率)。
化合物 159 之合成
將化合物14 (1700 mg,4.063 mmol)、1-異丙基哌嗪(0.637 mL,4.469 mmol)、HBTU (1695 mg,4.469 mmol)、二異丙基乙胺(1.4 mL,8.126 mmol)組合於DCM中。在室溫下攪拌26小時後,該反應混合物藉由DCM及NaHCO
3水溶液萃取並藉由MPLC純化。使用DCM及乙醚固化粗混合物以產生呈白色固體之化合物159,7-(3,4-二甲氧基苯基)-N-(4-(4-異丙基哌嗪-1-羰基)苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺(1641.6 mg,76%產率)。
化合物 165 之合成
將化合物14 (180 mg,0.43 mmol)、1-(3-氯丙基)-4-甲基哌嗪(0.15 mL,0.86 mmol)及碳酸鉀(178 mg,1.29 mmol)組合於DMF中並加熱至60℃,歷時26小時。該反應混合物藉由DCM及NH
4Cl水溶液萃取並藉由MPLC純化。使用DCM及己烷固化粗混合物以產生呈白色固體之化合物165,4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸3-(4-甲基哌嗪-1-基)丙酯(15.31 mg,6%產率)。
化合物 204 之合成
將7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羧酸(114 mg,0.38 mmol)、5-(4-甲基哌嗪-1-基)吡啶-2-胺(80 mg,0.42 mmol)、HBTU (159 mg,0.42 mmol)、二異丙基乙胺(0.196 mL,1.14 mmol)組合於DCM中。在室溫下攪拌22小時後,藉由DCM及NaHCO
3水溶液萃取該反應混合物。藉由MPLC純化該反應混合物。使用DCM及己烷固化粗混合物以產生呈黃色固體之化合物204,7-(3,4-二甲氧基苯基)-N-(5-(4-甲基哌嗪-1-基)吡啶-2-基)吡唑并[1,5-a]嘧啶-2-甲醯胺(120 mg,67%產率)。
一般方法D
化合物 112 之合成
向((S)-1-N-Boc-2-甲基哌嗪) (1205 mg,6.014 mmol)及吡啶(2.724 mL,33.410mmol)於氯仿(66.82 mL)中之溶液滴加溶解於氯仿(134 mL)中之7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羰基氯(2123 mg,6.682 mmol)並在0℃下攪拌4.5小時。藉由EA及NaHCO
3水溶液萃取該反應混合物。有機層係經無水MgSO
4乾燥並濃縮。使用DCM、己烷及乙醚固化粗混合物以產生呈米色固體之化合物112,(S)-4-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羰基)-2-甲基哌嗪-1-羧酸第三丁酯(2335.6 mg,73%)。
化合物 181 之合成
在室溫下將化合物112 (2335 mg,4.849 mmol)、TFA (3.614 mL,48.489 mmol)組合於DCM (48.489 mL)中,歷時20小時。在蒸發後,由DCM及NaHCO
3水溶液萃取該反應混合物。有機層係經無水MgSO
4乾燥並在真空中濃縮以產生呈黃色固體之化合物181,(S)-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(3-甲基哌嗪-1-基)甲酮(1784 mg,97%)。
化合物 210 之合成
在室溫下將化合物181 (1784 mg,4.688 mmol)、苯甲醯氯(986 mg,7.016 mmol)、TEA (2366 mg,23.385 mmol)、DMAP (6 mg,0.01當量)組合於DCM中,歷時14小時。藉由DCM及NaHCO
3水溶液萃取該反應混合物。有機層係經無水MgSO
4乾燥並濃縮。藉由MPLC純化該反應混合物。使用DCM及異丙醚固化粗混合物以產生呈黃色固體之化合物210,(S)-(4-苯甲醯基-3-甲基哌嗪-1-基)(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)甲酮(1689 mg,74%產率)。
化合物 185 之合成
向2-(哌嗪-1-基)嘧啶(36 mg,0.22 mmol)及吡啶(0.036 mL,0.44 mmol)於氯仿(2 mL)中之溶液滴加溶解於氯仿(2 mL)中之7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羰基氯(70 mg,0.22 mmol)並在0℃下攪拌2小時。藉由EA及NaHCO
3水溶液萃取該反應混合物。有機層係經無水MgSO
4乾燥並濃縮。使用DCM、己烷及乙醚固化粗混合物以產生呈白色固體之化合物185,(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)(4-(嘧啶-2-基)哌嗪-1-基)甲酮(50 mg,51%)。
一般方法E
化合物 109 之合成
將7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羧酸(80 mg,0.267 mmol)、對乙氧苯胺(0.023 mL,0.178 mmol)、DPPA (0.046 mL,0.214 mmol)、TEA (0.075 mL,0.534 mmol)組合於甲苯(1 mL)中。在微波中在100℃下將該混合物攪拌25 min。藉由DCM及NaHCO
3水溶液萃取該反應混合物。藉由MPLC純化該反應混合物。使用DCM及己烷固化粗混合物以產生呈淺灰色固體之化合物109,1-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)-3-(4-乙氧基苯基)脲(25 mg,22%產率)。
化合物 93 之合成
將7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羧酸(80 mg,0.267 mmol)、4-胺基苯甲酸甲酯(30.3 mg,0.200 mmol)、DPPA (0.047 mL,0.216 mmol)、TEA (0.083 mL,0.594 mmol)組合於甲苯(1 mL)中。在微波中在100℃下將該混合物攪拌15 min。藉由DCM及NaHCO
3水溶液萃取該反應混合物。藉由MPLC純化該反應混合物。使用DCM、甲醇及己烷固化粗混合物以產生呈淺黃色固體之化合物93,4-(3-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)脲基)苯甲酸甲酯(55.5 mg,42%產率)。
化合物 107 之合成
將化合物93 (55 mg,0.123 mmol)溶解於H
2O/THF/MeOH (0.5/0.8/0.4 mL)中,接著添加於H
2O中之氫氧化鈉(1 N,0.246 mL)並在60℃下攪拌7小時。在0℃下冷卻後,藉由添加1 N HCl酸化該混合物。然後藉由使用H
2O過濾該固體以產生呈橙色固體之化合物107,4-(3-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)脲基)苯甲酸(31.4 mg,59%產率)。
化合物 129 之合成
將化合物107 (24 mg,0.0554 mmol)、嗎啉(0.005 mL,0.0609 mmol)、HBTU (23 mg,0.0609 mmol)、二異丙基乙胺(0.019 mL,0.1108 mmol)組合於DCM中。在室溫下攪拌22小時後,藉由DCM及NaHCO
3水溶液萃取該反應混合物。藉由MPLC純化該反應混合物。使用DCM及己烷固化粗混合物以產生呈淺黃色固體之化合物129,1-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)-3-(4-(嗎啉-4-羰基)苯基)脲(16 mg,57%產率)。
一般方法F
化合物 287 之合成
向7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-胺(31 mg,0.12 mmol)及吡啶(0.019 mL,0.23 mmol)於氯仿(1 mL)中之溶液滴加溶解於氯仿(1 mL)中之4-乙氧基苯甲醯氯(21 mg,0.12 mmol)並在0℃下攪拌2小時。藉由EA及NaHCO
3水溶液萃取該反應混合物。有機層係經無水MgSO
4乾燥並濃縮。藉由MPLC純化該反應混合物以產生呈白色固體之化合物287,N-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)-4-乙氧基苯甲醯胺(20 mg,42%)。
化合物 288 之合成 步驟 1
將4-胺基雙環[2.2.2]辛烷-1-羧酸甲酯(109 mg,0.59 mmol)、2-氯乙醚(0.077 mL,0.65 mmol)、碳酸鈉(189 mg,1.78 mmol)及碘化鈉(178 mg,1.19 mmol)組合於N,N-二甲基乙醯胺(DMAc) (2 mL)中並在110℃下攪拌。每30分鐘添加2-氯乙醚(0.070 mL)兩次。16小時後,藉由DCM及H
2O萃取該混合物。有機層係經無水MgSO
4乾燥並濃縮以產生呈白色固體之4-嗎啉基雙環[2.2.2]辛烷-1-羧酸甲酯(115.5 mg,77%)。
步驟 2
將4-嗎啉基雙環[2.2.2]辛烷-1-羧酸甲酯(143 mg,0.56 mmol)溶解於MeOH (5 mL)中,接著添加於H
2O中之氫氧化鈉(1 N,1.130 mL)並加熱至回流,歷時2小時。濃縮該混合物以產生呈淺紅色固體之4-嗎啉基雙環[2.2.2]辛烷-1-羧酸(51 mg,38%)。
步驟 3
向4-嗎啉基雙環[2.2.2]辛烷-1-羧酸(32 mg,0.13 mmol)於氯仿(2 mL)中之溶液添加DMF (催化量)及SOCl
2(0.048 mL,0.67 mmol)並在60℃下攪拌2小時。濃縮該混合物以產生4-嗎啉基雙環[2.2.2]辛烷-1-羰基氯(34 mg,99%)。
步驟 4
向2-(哌嗪-1-基)嘧啶(36 mg,0.13 mmol)及吡啶(0.054 mL,0.67 mmol)於氯仿(2 mL)中之溶液滴加溶解於氯仿(2 mL)中之4-嗎啉基雙環[2.2.2]辛烷-1-羰基氯(34 mg,0.13 mmol)並在0℃下攪拌2小時。藉由EA及NaHCO
3水溶液萃取該反應混合物。有機層係經無水MgSO
4乾燥並濃縮。藉由MPLC純化粗混合物以產生呈淺黃色固體之化合物288,N-(7-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-基)-4-嗎啉基雙環[2.2.2]辛烷-1-甲醯胺(24.1 mg,37%)。
一般方法G
化合物 239 之合成
將6-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羧酸(50 mg,0.0554 mmol)、4-胺基苯甲酸甲酯(28 mg,0.184 mmol)、HBTU (70 mg,0.184 mmol)、二異丙基乙胺(0.058 mL,0.334 mmol)組合於DCM中。在室溫下攪拌22小時後,藉由EA及NaHCO
3水溶液萃取該反應混合物。藉由MPLC純化該反應混合物。使用DCM及己烷固化粗混合物以產生呈白色固體之化合物239,4-(6-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺基)苯甲酸甲酯(12 mg,17%產率)。
化合物 254 之合成
將6-(3,4-二甲氧基苯基)吡唑并[1,5-a]嘧啶-2-羧酸(34.4 mg,0.115 mmol)、對乙氧苯胺(0.016 mL,0.126 mmol)、HBTU (48 mg,0.126 mmol)、二異丙基乙胺(0.040 mL,0.230 mmol)組合於DCM中。在室溫下攪拌22小時後,由EA及NaHCO
3水溶液萃取該反應混合物。藉由MPLC純化該反應混合物。使用DCM及己烷固化粗混合物以產生呈白色固體之化合物254,6-(3,4-二甲氧基苯基)-N-(4-乙氧基苯基)吡唑并[1,5-a]嘧啶-2-甲醯胺(10 mg,21%產率)。
本發明之化合物之化學結構、所選表徵及合成方法以表格形式列於下表3A及3B中。
實例3:化合物之磷酸鹽緩衝液(PBS)溶解度
材料
| 表3A:化合物結構、表徵數據及合成方法 | ||||
| 化合物 | 結構 | 表徵數據 | 一般方法(實例2) | |
| 1 | 1H NMR (400 MHz, DMSO-d 6) δ 10.24 (s, 1H), 8.69 (d, J = 4.5 Hz, 1H), 8.02 (dd, J = 8.5, 2.0 Hz, 1H), 7.96 (d, J = 2.0 Hz, 1H), 7.81 (d, J = 7.8 Hz, 2H), 7.49 (d, J = 4.5 Hz, 1H), 7.38 (t, J = 7.9 Hz, 2H), 7.30 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 7.14 (t, J = 7.4 Hz, 1H), 3.93 - 3.87 (m, 6H). | C | ||
| 2 | 1H NMR (400 MHz, DMSO-d 6) δ 8.64 (d, J = 4.5 Hz, 1H), 8.05 (d, J = 8.3 Hz, 1H), 7.97 (d, J = 2.1 Hz, 1H), 7.89 (dd, J = 8.5, 2.1 Hz, 1H), 7.42 (d, J = 4.5 Hz, 1H), 7.20 (d, J = 8.6 Hz, 1H), 7.13 (s, 1H), 3.90 - 3.88 (m, 6H), 3.85 - 3.76 (m, 1H), 1.90 - 1.68 (m, 4H), 1.66 - 1.55 (m, 1H), 1.45 - 1.24 (m, 4H), 1.21 - 1.07 (m, 1H). | A | ||
| 4 | 1H NMR (400 MHz, DMSO-d 6) δ 8.69 (d, J = 4.4 Hz, 1H), 7.87 (dd = 8.6, 2.4 Hz, 1H), 7.78 (d, J = 2.4 Hz, 1H), 7.46 (d, J = 4.4 Hz, 1H), 7.25 (s, 1H), 7.21 (d, J = 8.8 Hz, 1H), 3.91 (s, 3H), 3.89 (s, 3H), 3.87 (s, 3H). | A (實例1) | ||
| 6 | 1H NMR (400 MHz, DMSO-d 6) δ 10.13 (s, 1H), 8.69 (d, J = 4.5 Hz, 1H), 8.02 (dd, J = 8.5, 2.1 Hz, 1H), 7.95 (d, J = 2.1 Hz, 1H), 7.72 (d, J = 9.0 Hz, 2H), 7.48 (d, J = 4.5 Hz, 1H), 7.27 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 6.96 (d, J = 9.1 Hz, 2H), 3.92 - 3.89 (m, 6H), 3.76 (s, 3H). | C | ||
| 7 | 1H NMR (400 MHz, DMSO-d 6) δ 12.52 (s, 1H), 8.87 (d, J = 8.5 Hz, 1H), 8.72 (d, J = 4.5 Hz, 1H), 8.25 (dd, J = 8.5, 2.0 Hz, 1H), 8.09 (d, J = 7.8 Hz, 1H), 7.81 (d, J = 1.9 Hz, 1H), 7.73 (t, J = 7.8 Hz, 1H), 7.55 (d, J = 4.5 Hz, 1H), 7.31 (s, 1H), 7.29 - 7.21 (m, 2H), 3.95 (s, 3H), 3.92 - 3.89 (m, 6H). | C | ||
| 8 | 1H NMR (400 MHz, DMSO-d 6) δ 10.52 (s, 1H), 8.70 (d, J = 4.5 Hz, 1H), 8.52 (s, 1H), 8.13 - 8.06 (m, 1H), 8.03 (dd, J = 8.5, 2.1 Hz, 1H), 7.95 (d, J = 2.0 Hz, 1H), 7.74 (d, J = 7.7 Hz, 1H), 7.54 (t, J = 7.9 Hz, 1H), 7.50 (d, J = 4.5 Hz, 1H), 7.33 (s, 1H), 7.23 (d, J = 8.6 Hz, 1H), 3.93 - 3.87 (m, 9H). | C | ||
| 9 | 1H NMR (400 MHz, DMSO-d 6) δ 8.64 (d, J = 4.5 Hz, 1H), 8.07 (d, J = 7.9 Hz, 1H), 7.98 (d, J = 2.1 Hz, 1H), 7.90 (dd, J = 8.5, 2.1 Hz, 1H), 7.43 (d, J = 4.5 Hz, 1H), 7.20 (d, J = 8.6 Hz, 1H), 7.14 (s, 1H), 3.99 - 3.86 (m, 7H), 3.64 (s, 3H), 2.65 - 2.57 (m, 1H), 2.01 - 1.88 (m, 2H), 1.74 - 1.56 (m, 6H). | A | ||
| 10 | 1H NMR (400 MHz, DMSO-d 6) δ 8.64 (d, J = 4.5 Hz, 1H), 8.10 (d, J = 8.3 Hz, 1H), 7.96 (d, J = 2.1 Hz, 1H), 7.90 (dd, J = 8.5, 2.1 Hz, 1H), 7.42 (d, J = 4.5 Hz, 1H), 7.20 (d, J = 8.6 Hz, 1H), 7.13 (s, 1H), 3.91 - 3.88 (m, 6H), 3.86 - 3.74 (m, 1H), 3.61 (s, 3H), 2.35 - 2.24 (m, 1H), 2.01 - 1.83 (m, 4H), 1.52 - 1.35 (m, 4H). | A | ||
| 12 | 1H NMR (400 MHz, DMSO-d 6) δ 9.09 (t, J = 6.3 Hz, 1H), 8.66 (dd, J = 4.5, 0.7 Hz, 1H), 7.97 - 7.90 (m, 3H), 7.86 (d, J = 1.4 Hz, 1H), 7.48 (d, J = 8.1 Hz, 2H), 7.44 - 7.41 (m, 1H), 7.21 - 7.15 (m, 2H), 4.60 (d, J = 6.2 Hz, 2H), 3.90 - 3.83 (m, 9H). | A | ||
| 13 | 1H NMR (400 MHz, DMSO-d 6) δ 10.09 (s, 1H), 8.68 (d, J = 4.5 Hz, 1H), 8.35 (d, J = 9.0 Hz, 2H), 7.69 (d, J = 9.0 Hz, 2H), 7.41 (d, J = 4.5 Hz, 1H), 7.26 (s, 1H), 7.20 (d, J = 9.0 Hz, 2H), 6.94 (d, J = 9.1 Hz, 2H), 4.03 (q, J = 7.0 Hz, 2H), 3.90 (s, 3H), 1.34 (t, J = 7.0 Hz, 3H). | C | ||
| 14 | 1H NMR (400 MHz, DMSO-d 6) δ 12.72 (s, 1H), 10.53 (s, 1H), 8.71 (d, J = 4.1 Hz, 1H), 8.09 - 7.84 (m, 6H), 7.50 (d, J = 4.3 Hz, 1H), 7.34 (s, 1H), 7.23 (d, J = 8.4 Hz, 1H), 4.00 - 3.82 (m, 6H). | C | ||
| 15 | 1H NMR (400 MHz, DMSO-d 6) δ 10.00 (s, 1H), 9.32 (s, 1H), 8.68 (d, J = 3.4 Hz, 1H), 8.03 (d, J = 8.6 Hz, 1H), 7.93 (s, 1H), 7.57 (d, J = 7.9 Hz, 2H), 7.47 (d, J = 4.3 Hz, 1H), 7.28 - 7.15 (m, 2H), 6.77 (d, J = 7.7 Hz, 2H), 3.94 - 3.88 (m, 6H). | C | ||
| 16 | 1H NMR (400 MHz, DMSO-d 6) δ 10.47 (s, 1H), 8.70 (d, J = 4.5 Hz, 1H), 8.47 - 8.44 (m, 1H), 8.10 - 8.00 (m, 2H), 7.95 (d, J = 2.1 Hz, 1H), 7.71 (d, J = 7.9 Hz, 1H), 7.56 - 7.47 (m, 2H), 7.33 (s, 1H), 7.23 (d, J = 8.6 Hz, 1H), 3.92 - 3.89 (m, 6H). | C | ||
| 17 | 1H NMR (400 MHz, DMSO-d 6) δ 10.02 (s, 1H), 8.76 - 8.67 (m, 1H), 8.45 - 8.37 (m, 1H), 8.25 (d, J = 8.3 Hz, 1H), 7.99 - 7.87 (m, 3H), 7.53 - 7.48 (m, 1H), 7.39 (d, J = 3.5 Hz, 1H), 7.30 - 7.17 (m, 2H), 3.96 - 3.89 (m, 6H). | C | ||
| 18 | 1H NMR (400 MHz, DMSO-d 6) δ 10.51 (s, 1H), 8.98 (d, J = 2.1 Hz, 1H), 8.70 (d, J = 4.5 Hz, 1H), 8.40 - 8.33 (m, 1H), 8.29 - 8.20 (m, 1H), 8.09 - 7.90 (m, 2H), 7.58 - 7.39 (m, 2H), 7.33 (s, 1H), 7.22 (d, J = 8.5 Hz, 1H), 4.01 - 3.88 (m, 6H). | C | ||
| 19 | 1H NMR (400 MHz, DMSO-d 6) δ 8.64 (d, J = 4.5 Hz, 1H), 8.08 (d, J = 7.7 Hz, 1H), 7.98 (d, J = 2.0 Hz, 1H), 7.94 - 7.88 (m, 1H), 7.43 (d, J = 4.5 Hz, 1H), 7.21 (s, 1H), 7.14 (s, 1H), 3.94 - 3.86 (m, J = 8.0 Hz, 7H), 2.48 - 2.43 (m, 1H), 1.99 - 1.90 (m, 2H), 1.72 - 1.57 (m, 6H)。 | A | ||
| 20 | 1H NMR (400 MHz, DMSO-d 6) δ 8.75 (t, J = 6.0 Hz, 1H), 8.67 (d, J = 4.5 Hz, 1H), 7.93 (dd, J = 8.5, 2.1 Hz, 1H), 7.82 (d, J = 2.1 Hz, 1H), 7.43 (d, J = 4.5 Hz, 1H), 7.20 (d, J = 8.6 Hz, 1H), 7.16 (s, 1H), 4.13 (q, J = 7.1 Hz, 2H), 4.06 (d, J = 6.1 Hz, 2H), 3.91 - 3.87 (m, 6H), 1.21 (t, J = 7.1 Hz, 3H). | A | ||
| 21 | 1H NMR (400 MHz, DMSO-d 6) δ 12.06 (s, 1H), 8.64 (d, J = 4.5 Hz, 1H), 8.10 (d, J = 8.3 Hz, 1H), 7.96 (d, J = 2.1 Hz, 1H), 7.90 (dd, J = 8.5, 2.1 Hz, 1H), 7.43 (d, J = 4.5 Hz, 1H), 7.20 (d, J = 8.6 Hz, 1H), 7.13 (s, 1H), 3.92 - 3.87 (m, 6H), 3.82 - 3.73 (m, 1H), 2.22 - 2.12 (m, 1H), 2.02 - 1.85 (m, 4H), 1.52 - 1.35 (m, 4H). | A | ||
| 22 | 1H NMR (400 MHz, DMSO-d 6) δ 8.67 (d, J = 4.5 Hz, 1H), 8.60 (t, J = 5.4 Hz, 1H), 7.92 (dd, J = 8.5, 2.1 Hz, 1H), 7.85 (d, J = 2.0 Hz, 1H), 7.43 (d, J = 4.5 Hz, 1H), 7.20 (d, J = 8.6 Hz, 1H), 7.15 (d, J = 0.6 Hz, 1H), 3.98 (d, J = 6.0 Hz, 2H), 3.92 - 3.86 (m, 6H). | A | ||
| 23 | 1H NMR (400 MHz, DMSO-d 6) δ 10.56 (s, 1H), 8.70 (d, J = 4.5 Hz, 1H), 8.35 (d, J = 8.8 Hz, 2H), 8.00 (s, 4H), 7.43 (d, J = 4.4 Hz, 1H), 7.34 (s, 1H), 7.20 (d, J = 8.8 Hz, 2H), 3.91 (s, 3H), 3.85 (s, 3H). | C | ||
| 24 | 1H NMR (400 MHz, DMSO-d 6) δ 10.14 (s, 1H), 8.72 (d, J = 4.2 Hz, 1H), 7.86 - 7.79 (m, 2H), 7.68 (d, J = 8.7 Hz, 2H), 7.56 (t, J = 7.9 Hz, 1H), 7.45 (d, J = 4.3 Hz, 1H), 7.31 (s, 1H), 7.24 (d, J = 7.7 Hz, 1H), 6.93 (d, J = 8.8 Hz, 2H), 4.02 (q, J = 13.9, 6.9 Hz, 2H), 3.88 (s, 3H), 1.33 (t, J = 6.9 Hz, 3H). | C | ||
| 25 | 1H NMR (400 MHz, DMSO-d 6) δ 10.60 (s, 1H), 8.74 (d, J = 4.4 Hz, 1H), 7.98 (s, 4H), 7.86 - 7.79 (m, 2H), 7.57 (t, J = 8.0 Hz, 1H), 7.47 (d, J = 4.4 Hz, 1H), 7.38 (s, 1H), 7.24 (dd, J = 8.3, 2.5 Hz, 1H), 3.88 (s, 3H), 3.85 (s, 3H). | C | ||
| 26 | 1H NMR (400 MHz, DMSO-d 6) δ 9.08 (s, 1H), 8.66 (d, J = 4.5 Hz, 1H), 7.99 (dd, J = 8.5, 2.0 Hz, 1H), 7.85 (d, J = 2.0 Hz, 1H), 7.44 (d, J = 4.4 Hz, 1H), 7.23 - 7.12 (m, 2H), 4.10 - 4.03 (m, 2H), 3.93 - 3.87 (m, 6H), 1.51 - 1.46 (m, 2H), 1.25 - 1.20 (m, 2H), 1.13 (t, J = 7.1 Hz, 3H). | A | ||
| 27 | 1H NMR (400 MHz, DMSO-d 6) δ 8.64 (d, J = 4.5 Hz, 1H), 8.00 - 7.92 (m, 3H), 7.42 (d, J = 4.5 Hz, 1H), 7.22 - 7.14 (m, 2H), 4.04 - 3.94 (m, 1H), 3.93 - 3.85 (m, 6H), 2.30 - 2.08 (m, 7H), 1.86 - 1.68 (m, 4H), 1.65 - 1.48 (m, 4H). | A | ||
| 28 | 1H NMR (400 MHz, DMSO-d 6) δ 10.50 (s, 1H), 8.89 (t, J = 5.8 Hz, 1H), 8.71 (d, J = 4.5 Hz, 1H), 8.03 (dd, J = 8.5, 2.1 Hz, 1H), 7.97 - 7.88 (m, 5H), 7.50 (d, J = 4.5 Hz, 1H), 7.33 (s, 1H), 7.23 (d, J = 8.6 Hz, 1H), 4.13 (q, J = 7.1 Hz, 2H), 4.00 (d, J = 5.8 Hz, 2H), 3.95 - 3.87 (m, 6H), 1.22 (t, J = 7.1 Hz, 3H). | C | ||
| 29 | 1H NMR (400 MHz, DMSO-d 6) δ 8.97 (s, 1H), 8.65 (d, J = 4.5 Hz, 1H), 7.99 (dd, J = 8.5, 2.2 Hz, 1H), 7.85 (d, J = 2.1 Hz, 1H), 7.44 (d, J = 4.5 Hz, 1H), 7.19 (d, J = 8.6 Hz, 1H), 7.14 (s, 1H), 3.91 - 3.87 (m, 6H), 1.47 - 1.39 (m, 2H), 1.22 - 1.15 (m, 2H). | A | ||
| 30 | 1H NMR (400 MHz, DMSO-d 6) δ 12.59 (s, 1H), 10.50 (s, 1H), 8.79 (t, J = 5.9 Hz, 1H), 8.71 (d, J = 4.5 Hz, 1H), 8.03 (dd, J = 8.5, 2.1 Hz, 1H), 7.98 - 7.87 (m, 5H), 7.50 (d, J = 4.5 Hz, 1H), 7.34 (s, 1H), 7.23 (d, J = 8.6 Hz, 1H), 3.96 - 3.87 (m, 8H). | C | ||
| 31 | 1H NMR (400 MHz, CDCl 3) δ 9.73 (s, 1H), 8.97 (d, J = 2.1 Hz, 1H), 8.63 (d, J = 4.3 Hz, 1H), 8.52 (d, J = 8.7 Hz, 1H), 8.39 (dd, J = 8.7, 2.2 Hz, 1H), 7.80 (d, J = 2.1 Hz, 1H), 7.71 (dd, J = 8.4, 2.1 Hz, 1H), 7.45 (s, 1H), 7.21 - 7.07 (m, 2H), 4.13 - 4.03 (m, 6H), 3.97 (s, 3H). | B | ||
| 32 | 1H NMR (400 MHz, DMSO-d 6) δ 10.64 (s, 1H), 8.74 (d, J = 4.4 Hz, 1H), 8.04 - 7.92 (m, 4H), 7.67 (s, 2H), 7.57 (d, J = 4.4 Hz, 1H), 7.37 (s, 1H), 3.96 - 3.88 (m, 6H), 3.85 (s, 3H), 3.80 (s, 3H). | C | ||
| 33 | 1H NMR (400 MHz, DMSO-d 6) δ 10.64 (s, 1H), 8.72 (d, J = 4.5 Hz, 1H), 8.33 (dd, J = 12.8, 2.2 Hz, 1H), 8.24 (d, J = 8.7 Hz, 1H), 8.00 (s, 4H), 7.51 (d, J = 4.5 Hz, 1H), 7.44 (t, J = 8.9 Hz, 1H), 7.37 (s, 1H), 3.99 (s, 3H), 3.85 (s, 3H). | C | ||
| 34 | 1H NMR (400 MHz, DMSO-d 6) δ 10.18 (s, 1H), 8.68 (d, J = 4.5 Hz, 1H), 8.02 (dd, J = 8.5, 2.1 Hz, 1H), 7.94 (d, J = 2.1 Hz, 1H), 7.71 (d, J = 9.1 Hz, 2H), 7.48 (d, J = 4.5 Hz, 1H), 7.27 (s, 1H), 7.21 (d, J = 8.6 Hz, 1H), 6.95 (d, J = 9.1 Hz, 2H), 4.77 (s, 2H), 4.18 (q, J = 7.1 Hz, 2H), 3.96 - 3.87 (m, 6H), 1.22 (t, J = 7.1 Hz, 3H). | C | ||
| 35 | 1H NMR (400 MHz, DMSO-d 6) δ 13.07 (s, 1H), 10.16 (s, 1H), 8.68 (d, J = 4.5 Hz, 1H), 8.02 (dd, J = 8.5, 1.9 Hz, 1H), 7.94 (d, J = 1.9 Hz, 1H), 7.70 (d, J = 9.0 Hz, 2H), 7.48 (d, J = 4.5 Hz, 1H), 7.27 (s, 1H), 7.21 (d, J = 8.6 Hz, 1H), 6.93 (d, J = 9.0 Hz, 2H), 4.66 (s, 2H), 3.93 - 3.87 (m, 6H). | C | ||
| 36 | 1H NMR (400 MHz, DMSO-d 6) δ 9.08 (s, 1H), 8.64 (d, J = 4.5 Hz, 1H), 7.97 (dd, J = 8.5, 2.1 Hz, 1H), 7.80 (d, J = 2.0 Hz, 1H), 7.42 (d, J = 4.5 Hz, 1H), 7.19 (d, J = 8.6 Hz, 1H), 7.12 (s, 1H), 3.91 - 3.86 (m, 6H), 3.63 (s, 3H), 2.36 (s, 6H). | B | ||
| 37 | 1H NMR (400 MHz, DMSO-d 6) δ 12.49 (s, 1H), 9.03 (s, 1H), 8.64 (d, J = 4.5 Hz, 1H), 7.97 (dd, J = 8.5, 2.1 Hz, 1H), 7.80 (d, J = 2.1 Hz, 1H), 7.42 (d, J = 4.5 Hz, 1H), 7.19 (d, J = 8.6 Hz, 1H), 7.12 (s, 1H), 3.93 - 3.87 (m, 6H), 2.32 (s, 6H). | B | ||
| 38 | 1H NMR (400 MHz, DMSO-d 6) δ 9.89 (s, 1H), 9.74 - 9.06 (m, 3H), 8.61 (d, J = 4.5 Hz, 1H), 7.82 (d, J = 2.2 Hz, 1H), 7.69 (dd, J = 8.4, 2.3 Hz, 1H), 7.56 (d, J = 8.9 Hz, 2H), 7.29 (d, J = 4.5 Hz, 1H), 7.21 (s, 1H), 6.96 (d, J = 8.4 Hz, 1H), 6.77 (d, J = 8.9 Hz, 2H). | C | ||
| 39 | 1H NMR (400 MHz, DMSO-d 6) δ 10.60 (s, 1H), 8.71 (d, J = 4.4 Hz, 1H), 8.50 - 8.33 (m, 2H), 8.09 - 7.90 (m, 4H), 7.50 (d, J = 4.4 Hz, 1H), 7.42 (d, J = 8.5 Hz, 1H), 7.37 (s, 1H), 4.01 (s, 3H), 3.85 (s, 3H). | C | ||
| 40 | 1H NMR (400 MHz, DMSO-d 6) δ 10.58 (s, 1H), 8.77 (d, J = 4.4 Hz, 1H), 8.52 (d, J = 2.1 Hz, 1H), 8.31 (dd, J = 8.5, 2.1 Hz, 1H), 7.99 (s, 4H), 7.93 (d, J = 8.5 Hz, 1H), 7.55 (d, J = 4.4 Hz, 1H), 7.41 (s, 1H), 3.85 (s, 3H). | C | ||
| 41 | 1H NMR (400 MHz, DMSO-d6) δ 10.43 (s, 1H), 8.70 (d, J = 4.5 Hz, 1H), 8.01 (dd, J = 8.5, 2.1 Hz, 1H), 7.96 (d, J = 2.0 Hz, 1H), 7.90 (d, J = 8.5 Hz, 2H), 7.49 (d, J = 4.5 Hz, 1H), 7.45 (d, J = 8.5 Hz, 2H), 7.32 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 3.93 - 3.87 (m, 6H), 3.67 - 3.39 (m, 8H). | C | ||
| 42 | 1H NMR (400 MHz, DMSO-d 6) δ 10.49 (s, 1H), 8.77 - 8.64 (m, 2H), 8.03 (dd, J = 8.5, 2.1 Hz, 1H), 7.99 - 7.84 (m, 5H), 7.50 (d, J = 4.5 Hz, 1H), 7.34 (s, 1H), 7.23 (d, J = 8.6 Hz, 1H), 4.57 - 4.41 (m, 1H), 3.95 - 3.83 (m, 6H), 3.66 (s, 3H), 1.42 (d, J = 7.3 Hz, 3H). | C | ||
| 43 | 1H NMR (400 MHz, DMSO-d 6) δ 10.49 (s, 1H), 8.71 (d, J = 4.4 Hz, 1H), 8.51 (d, J = 7.3 Hz, 1H), 8.09 - 7.99 (m, 1H), 7.99 - 7.88 (m, 5H), 7.51 (d, J = 4.5 Hz, 1H), 7.34 (s, 1H), 7.23 (d, J = 8.6 Hz, 1H), 5.07 (t, J = 6.1 Hz, 1H), 4.64 - 4.40 (m, 1H), 3.98 - 3.87 (m, 6H), 3.81 (t, J = 5.7 Hz, 2H), 3.67 (s, 3H). | C | ||
| 44 | 1H NMR (400 MHz, DMSO-d 6) δ 12.53 (s, 1H), 10.47 (s, 1H), 8.71 (d, J = 4.4 Hz, 1H), 8.58 (d, J = 7.2 Hz, 1H), 8.09 - 8.00 (m, 1H), 8.00 - 7.84 (m, 5H), 7.50 (d, J = 4.4 Hz, 1H), 7.33 (s, 1H), 7.23 (d, J = 8.6 Hz, 1H), 4.54 - 4.29 (m, 1H), 4.00 - 3.71 (m, 6H), 1.41 (d, J = 7.3 Hz, 3H). | C | ||
| 45 | 1H NMR (400 MHz, DMSO-d 6) δ 12.64 (s, 1H), 10.47 (s, 1H), 8.70 (d, J = 4.5 Hz, 1H), 8.32 (d, J = 7.7 Hz, 1H), 8.02 (dd, J = 8.5, 2.1 Hz, 1H), 7.99 - 7.85 (m, 5H), 7.49 (d, J = 4.5 Hz, 1H), 7.33 (s, 1H), 7.23 (d, J = 8.6 Hz, 1H), 4.98 (s, 1H), 4.56 - 4.36 (m, 1H), 3.98 - 3.85 (m, 6H), 3.85 - 3.67 (m, 2H). | C | ||
| 46 | 1H NMR (400 MHz, DMSO-d 6) δ 10.48 (s, 1H), 8.79 (d, J = 7.6 Hz, 1H), 8.71 (d, J = 4.2 Hz, 1H), 8.08 - 7.77 (m, 6H), 7.50 (d, J = 4.3 Hz, 1H), 7.40 - 7.14 (m, 7H), 4.73 - 4.57 (m, 1H), 4.02 - 3.80 (m, 6H), 3.65 (s, 3H), 3.24 - 3.03 (m, 2H). | C | ||
| 47 | 1H NMR (400 MHz, DMSO-d 6) δ 10.53 - 10.31 (m, 1H), 8.71 (d, J = 4.3 Hz, 1H), 8.03 (d, J = 8.3 Hz, 1H), 7.99 - 7.81 (m, 3H), 7.68 - 7.36 (m, 3H), 7.33 (s, 1H), 7.23 (d, J = 8.4 Hz, 1H), 4.57 - 4.42 (m, 1H), 3.99 - 3.81 (m, 6H), 3.74 - 3.41 (m, 5H), 2.37 - 2.21 (m, 1H), 2.03 - 1.73 (m, 3H). | C | ||
| 48 | 1H NMR (400 MHz, DMSO-d 6) δ 10.46 (s, 1H), 8.70 (d, J = 4.5 Hz, 1H), 8.02 (dd, J = 8.5, 2.1 Hz, 1H), 7.96 (d, J = 2.1 Hz, 1H), 7.94 - 7.87 (m, 5H), 7.50 (d, J = 4.5 Hz, 1H), 7.34 - 7.27 (m, 2H), 7.22 (d, J = 8.6 Hz, 1H), 3.94 - 3.87 (m, 6H). | C | ||
| 49 | 1H NMR (400 MHz, DMSO-d 6) δ 12.77 (s, 1H), 10.46 (s, 1H), 8.70 (d, J = 4.4 Hz, 1H), 8.62 (d, J = 8.0 Hz, 1H), 8.12 - 7.72 (m, 6H), 7.50 (d, J = 4.4 Hz, 1H), 7.39 - 7.07 (m, 7H), 4.62 (s, 1H), 4.06 - 3.66 (m, 6H), 3.24 - 3.04 (m, 2H). | C | ||
| 50 | 1H NMR (400 MHz, DMSO-d 6) δ 12.53 (s, 1H), 10.56 - 10.40 (m, 1H), 8.70 (d, J = 4.4 Hz, 1H), 8.03 (d, J = 8.4 Hz, 1H), 7.97 - 7.78 (m, 3H), 7.65 - 7.37 (m, 3H), 7.33 (s, 1H), 7.23 (d, J = 8.5 Hz, 1H), 4.48 - 4.35 (m, 1H), 4.05 - 3.76 (m, 6H), 3.68 - 3.45 (m, 2H), 2.38 - 2.10 (m, 1H), 2.05 - 1.66 (m, 3H). | C | ||
| 51 | 1H NMR (400 MHz, DMSO-d 6) δ 10.45 (s, 1H), 8.70 (d, J = 4.5 Hz, 1H), 8.02 (dd, J = 8.5, 2.1 Hz, 1H), 7.96 (d, J = 2.1 Hz, 1H), 7.90 (d, J = 8.6 Hz, 2H), 7.50 (d, J = 4.5 Hz, 1H), 7.45 (d, J = 8.6 Hz, 2H), 7.32 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 3.92 - 3.88 (m, 6H), 3.61 - 3.35 (m, 8H), 1.41 (s, 9H). | C | ||
| 52 | 1H NMR (400 MHz, DMSO-d 6) δ 10.49 (s, 1H), 9.46 (s, 2H), 8.70 (d, J = 4.5 Hz, 1H), 8.01 (dd, J = 8.5, 2.1 Hz, 1H), 7.96 (d, J = 2.1 Hz, 1H), 7.93 (d, J = 8.7 Hz, 2H), 7.53 - 7.48 (m, 3H), 7.35 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 3.92 - 3.86 (m, 6H), 3.81 - 3.64 (m, 4H), 3.21 - 3.09 (m, 4H). | C | ||
| 53 | 1H NMR (400 MHz, CDCl 3) δ 9.00 (s, 1H), 8.63 (d, J = 4.4 Hz, 1H), 7.89 - 7.75 (m, 5H), 7.75 - 7.67 (m, 2H), 7.41 (s, 1H), 7.14 (d, J = 8.4 Hz, 1H), 7.08 (d, J = 4.4 Hz, 1H), 6.70 (s, 1H), 4.11 - 4.00 (m, 6H), 3.92 - 3.85 (m, 2H), 3.71 - 3.65 (m, 2H). | C | ||
| 54 | 1H NMR (400 MHz, DMSO-d 6) δ 10.28 (s, 1H), 8.61 (d, J = 4.4 Hz, 1H), 8.18 (s, 1H), 8.00 - 7.92 (m, 1H), 7.91 - 7.80 (m, 3H), 7.54 (d, J = 7.7 Hz, 1H), 7.42 - 7.34 (m, 2H), 7.29 (s, 1H), 7.23 (s, 1H), 7.13 (d, J = 8.5 Hz, 1H), 3.83 - 3.78 (m, 6H). | C | ||
| 55 | 1H NMR (400 MHz, DMSO-d 6) δ 10.42 (s, 1H), 8.70 (d, J = 4.5 Hz, 1H), 8.03 (dd, J = 8.5, 2.1 Hz, 1H), 7.95 (d, J = 2.1 Hz, 1H), 7.93 - 7.86 (m, 2H), 7.52 - 7.43 (m, 2H), 7.32 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 7.19 - 7.16 (m, 1H), 3.94 - 3.87 (m, 6H), 3.74 - 3.35 (m, 8H). | C | ||
| 56 | 1H NMR (400 MHz, CDCl 3) δ 8.94 (s, 1H), 8.63 (s, 1H), 7.85 (s, 1H), 7.73 (dd, J = 8.4, 2.1 Hz, 2H), 7.62 (d, J = 2.0 Hz, 1H), 7.49 - 7.41 (m, 2H), 7.21 (d, J = 7.6 Hz, 1H), 7.14 (d, J = 8.5 Hz, 1H), 7.06 (d, J = 4.0 Hz, 1H), 4.06 (s, 3H), 4.01 (s, 3H), 3.87 - 3.39 (m, 8H), 1.49 (s, 9H). | C | ||
| 57 | 1H NMR (400 MHz, DMSO-d 6) δ 10.48 (s, 1H), 8.71 (d, J = 4.5 Hz, 1H), 8.65 (d, J = 7.7 Hz, 1H), 8.02 (dd, J = 8.5, 2.1 Hz, 1H), 7.99 - 7.84 (m, 5H), 7.50 (d, J = 4.5 Hz, 1H), 7.34 (s, 1H), 7.23 (d, J = 8.6 Hz, 1H), 4.59 - 4.40 (m, 1H), 3.97 - 3.77 (m, 6H), 3.66 (s, 3H), 1.86 - 1.66 (m, 2H), 1.63 - 1.54 (m, 1H), 0.94 (d, J = 6.5 Hz, 3H), 0.90 (d, J = 6.4 Hz, 3H). | C | ||
| 58 | 1H NMR (400 MHz, DMSO-d 6) δ 10.48 (s, 1H), 8.71 (d, J = 4.5 Hz, 1H), 8.52 (d, J = 7.8 Hz, 1H), 8.02 (dd, J = 8.5, 2.1 Hz, 1H), 8.00 - 7.84 (m, 5H), 7.50 (d, J = 4.5 Hz, 1H), 7.33 (s, 1H), 7.23 (d, J = 8.6 Hz, 1H), 4.30 (t, J = 7.6 Hz, 1H), 3.97 - 3.82 (m, 6H), 3.67 (s, 3H), 2.27 - 2.10 (m, 1H), 1.00 (d, J = 6.7 Hz, 3H), 0.95 (d, J = 6.8 Hz, 3H). | C | ||
| 59 | 1H NMR (400 MHz, DMSO-d 6) δ 10.48 (s, 1H), 8.78 - 8.62 (m, 2H), 8.10 - 7.81 (m, 6H), 7.50 (d, J = 4.5 Hz, 1H), 7.34 (s, 1H), 7.23 (d, J = 8.5 Hz, 1H), 4.59 (dd, J = 14.3, 7.2 Hz, 1H), 3.97 - 3.83 (m, 6H), 3.67 (s, 3H), 2.70 - 2.53 (m, 2H), 2.12 - 2.03 (m, 5H). | C | ||
| 60 | 1H NMR (400 MHz, DMSO-d 6) δ 10.49 (s, 1H), 8.85 (d, J = 7.9 Hz, 1H), 8.71 (d, J = 4.5 Hz, 1H), 8.07 - 7.99 (m, 1H), 7.99 - 7.91 (m, 3H), 7.91 - 7.83 (m, 2H), 7.50 (d, J = 4.5 Hz, 1H), 7.33 (s, 1H), 7.23 (d, J = 8.4 Hz, 1H), 4.91 - 4.77 (m, 1H), 3.96 - 3.86 (m, 6H), 3.66 (s, 3H), 3.63 (s, 3H), 3.03 - 2.91 (m, 1H), 2.91 - 2.76 (m, 1H). | C | ||
| 61 | 1H NMR (400 MHz, DMSO-d 6) δ 8.66 (d, J = 4.5 Hz, 1H), 7.82 (dd, J = 8.5, 2.1 Hz, 1H), 7.77 (d, J = 2.1 Hz, 1H), 7.39 (d, J = 4.5 Hz, 1H), 7.21 (d, J = 8.6 Hz, 1H), 7.04 (s, 1H), 3.94 - 3.78 (m, 8H), 3.73 - 3.64 (m, 4H), 3.63 - 3.51 (m, 2H). | D | ||
| 62 | 1H NMR (400 MHz, DMSO-d 6) δ 8.66 (d, J = 4.4 Hz, 1H), 7.83 (dd, J = 8.5, 2.0 Hz, 1H), 7.77 (d, J = 2.0 Hz, 1H), 7.39 (d, J = 4.5 Hz, 1H), 7.21 (d, J = 8.6 Hz, 1H), 7.04 (s, 1H), 3.93 - 3.78 (m, 8H), 3.73 - 3.61 (m, 2H), 3.50 - 3.41 (m, 2H), 3.39 - 3.34 (m, 2H), 1.42 (s, 9H). | D | ||
| 63 | 1H NMR (400 MHz, DMSO-d 6) δ 8.65 (d, J = 4.5 Hz, 1H), 8.23 (d, J = 8.3 Hz, 1H), 7.96 (d, J = 2.1 Hz, 1H), 7.91 (dd, J = 8.5, 2.2 Hz, 1H), 7.43 (d, J = 4.5 Hz, 1H), 7.20 (d, J = 8.6 Hz, 1H), 7.14 (s, 1H), 4.09 - 3.83 (m, 9H), 2.99 - 2.74 (m, 2H), 1.85 - 1.72 (m, 2H), 1.61 - 1.32 (m, 11H). | A | ||
| 64 | 1H NMR (400 MHz, DMSO-d 6) δ 10.49 (s, 1H), 8.84 - 8.56 (m, 2H), 8.19 - 7.73 (m, 6H), 7.68 - 7.43 (m, 1H), 7.34 (s, 1H), 7.23 (d, J = 7.4 Hz, 1H), 4.61 - 4.35 (m, 1H), 4.13 - 3.78 (m, 6H), 3.66 (s, 3H), 1.42 (d, J = 6.6 Hz, 3H). | C | ||
| 65 | 1H NMR (400 MHz, DMSO-d 6) δ 10.49 (s, 1H), 8.71 (d, J = 4.5 Hz, 1H), 8.10 - 8.00 (m, 1H), 8.00 - 7.83 (m, 3H), 7.68 (d, J = 8.6 Hz, 2H), 7.50 (d, J = 4.5 Hz, 1H), 7.33 (s, 1H), 7.23 (d, J = 8.5 Hz, 1H), 4.63 - 4.48 (m, 1H), 4.48 - 4.35 (m, 1H), 4.35 - 4.19 (m, 1H), 4.18 - 4.00 (m, 1H), 3.97 - 3.82 (m, 6H), 3.69 (s, 3H), 3.66 - 3.52 (m, 1H). | C | ||
| 66 | 1H NMR (400 MHz, DMSO-d 6) δ 9.25 (s, 2H), 8.68 (d, J = 4.4 Hz, 1H), 7.81 (d, J = 8.5 Hz, 1H), 7.76 (s, 1H), 7.41 (d, J = 4.4 Hz, 1H), 7.20 (d, J = 8.6 Hz, 1H), 7.10 (s, 1H), 4.23 - 4.03 (m, 2H), 3.98 - 3.76 (m, 8H), 3.36 - 3.09 (m, 4H). | D | ||
| 67 | 1H NMR (400 MHz, DMSO-d 6) δ 8.98 - 8.83 (m, 1H), 8.81 - 8.68 (m, 1H), 8.66 (d, J = 4.5 Hz, 1H), 8.53 (d, J = 7.8 Hz, 1H), 7.99 (d, J = 2.1 Hz, 1H), 7.91 (dd, J = 8.5, 2.1 Hz, 1H), 7.44 (d, J = 4.5 Hz, 1H), 7.20 (d, J = 8.6 Hz, 1H), 7.18 (s, 1H), 4.18 - 4.04 (m, 1H), 3.93 - 3.86 (m, 6H), 3.31 (d, J = 12.2 Hz, 2H), 3.09 - 2.95 (m, 2H), 2.04 - 1.92 (m, 2H), 1.91 - 1.76 (m, 2H). | A | ||
| 68 | 1H NMR (400 MHz, DMSO-d 6) δ 9.36 (s, 1H), 8.65 (d, J = 4.5 Hz, 1H), 7.97 (d, J = 2.1 Hz, 1H), 7.93 (dd, J = 8.5, 2.2 Hz, 1H), 7.44 (d, J = 4.5 Hz, 1H), 7.20 (d, J = 8.6 Hz, 1H), 7.12 (s, 1H), 3.95 - 3.69 (m, 6H), 3.00 - 2.74 (m, 4H), 2.49 - 2.34 (m, 4H), 2.19 (s, 3H). | A | ||
| 69 | 1H NMR (400 MHz, DMSO-d 6) δ 8.64 (d, J = 4.4 Hz, 1H), 8.03 (d, J = 8.2 Hz, 1H), 7.96 (d, J = 1.8 Hz, 1H), 7.90 (dd, J = 8.4, 2.0 Hz, 1H), 7.42 (d, J = 4.5 Hz, 1H), 7.20 (d, J = 8.6 Hz, 1H), 7.12 (s, 1H), 4.57 (d, J = 4.4 Hz, 1H), 3.96 - 3.84 (m, 6H), 3.83 - 3.67 (m, 1H), 3.50 - 3.36 (m, 1H), 1.92 - 1.76 (m, 4H), 1.51 - 1.37 (m, 2H), 1.34 - 1.18 (m, 2H). | A | ||
| 70 | 1H NMR (400 MHz, DMSO-d 6) δ 10.59 (s, 1H), 8.68 (d, J = 4.5 Hz, 1H), 8.03 - 7.92 (m, 4H), 7.91 - 7.82 (m, 2H), 7.41 (d, J = 4.5 Hz, 1H), 7.34 (s, 1H), 7.12 (d, J = 8.5 Hz, 1H), 4.46 - 4.14 (m, 4H), 3.86 (s, 3H). | C | ||
| 71 | 1H NMR (400 MHz, DMSO-d 6) δ 8.65 (d, J = 4.5 Hz, 1H), 7.98 (d, J = 2.1 Hz, 1H), 7.95 - 7.88 (m, 2H), 7.43 (d, J = 4.5 Hz, 1H), 7.25 - 7.19 (m, 2H), 7.15 (s, 1H), 6.75 (s, 1H), 4.06 - 3.95 (m, 1H), 3.94 - 3.85 (m, 6H), 2.31 - 2.21 (m, 1H), 1.87 - 1.70 (m, 4H), 1.70 - 1.48 (m, 4H). | A | ||
| 72 | 1H NMR (400 MHz, DMSO-d 6) δ 8.65 (d, J = 4.5 Hz, 1H), 7.97 (d, J = 2.1 Hz, 1H), 7.95 - 7.87 (m, 2H), 7.44 (d, J = 4.5 Hz, 1H), 7.24 (d, J = 8.6 Hz, 1H), 7.16 (s, 1H), 4.11 - 4.03 (m, 1H), 3.92 - 3.86 (m, 6H), 3.62 - 3.40 (m, 8H), 2.78 - 2.69 (m, 1H), 1.94 - 1.81 (m, 2H), 1.76 - 1.63 (m, 4H), 1.61 - 1.51 (m, 2H). | A | ||
| 73 | 1H NMR (400 MHz, DMSO-d 6) δ 8.65 (d, J = 4.5 Hz, 1H), 7.97 (d, J = 2.1 Hz, 1H), 7.95 - 7.85 (m, 2H), 7.44 (d, J = 4.5 Hz, 1H), 7.24 (d, J = 8.6 Hz, 1H), 7.16 (s, 1H), 4.11 - 4.03 (m, 1H), 3.93 - 3.86 (m, 6H), 3.52 - 3.39 (m, 4H), 3.32 - 3.25 (m, 4H), 2.78 - 2.71 (m, 1H), 1.92 - 1.83 (m, 2H), 1.74 - 1.62 (m, 4H), 1.62 - 1.51 (m, 2H), 1.42 (s, 9H). | A | ||
| 74 | 1H NMR (400 MHz, DMSO-d 6) δ 8.64 (d, J = 4.5 Hz, 1H), 8.12 (d, J = 8.3 Hz, 1H), 7.99 (d, J = 2.1 Hz, 1H), 7.89 (dd, J = 8.5, 2.1 Hz, 1H), 7.43 (d, J = 4.5 Hz, 1H), 7.26 - 7.17 (m, 2H), 7.13 (s, 1H), 6.71 (s, 1H), 3.94 - 3.86 (m, 6H), 3.83 - 3.70 (m, 1H), 2.11 - 2.00 (m, 1H), 1.95 - 1.75 (m, 4H), 1.51 - 1.33 (m, 4H). | A | ||
| 75 | 1H NMR (400 MHz, DMSO-d 6) δ 8.65 (d, J = 4.5 Hz, 1H), 8.10 (d, J = 8.2 Hz, 1H), 7.98 (d, J = 2.1 Hz, 1H), 7.89 (dd, J = 8.5, 2.2 Hz, 1H), 7.43 (d, J = 4.5 Hz, 1H), 7.20 (d, J = 8.6 Hz, 1H), 7.13 (s, 1H), 3.92 - 3.87 (m, 6H), 3.87 - 3.72 (m, 1H), 3.66 - 3.37 (m, 8H), 2.59 - 2.52 (m, 1H), 1.99 - 1.66 (m, 4H), 1.55 - 1.39 (m, 4H). | A | ||
| 76 | 1H NMR (400 MHz, DMSO-d 6) δ 8.65 (d, J = 4.5 Hz, 1H), 8.10 (d, J = 8.2 Hz, 1H), 7.98 (d, J = 2.1 Hz, 1H), 7.89 (dd, J = 8.5, 2.1 Hz, 1H), 7.43 (d, J = 4.5 Hz, 1H), 7.20 (d, J = 8.6 Hz, 1H), 7.13 (s, 1H), 3.93 - 3.87 (m, 6H), 3.86 - 3.70 (m, 1H), 3.55 - 3.39 (m, 4H), 3.33 - 3.24 (m, 4H), 2.60 - 2.54 (m, 1H), 1.99 - 1.65 (m, 4H), 1.56 - 1.45 (m, 4H), 1.42 (s, 9H). | A | ||
| 77 | 1H NMR (400 MHz, DMSO-d 6) δ 10.45 (s, 1H), 8.70 (d, J = 4.5 Hz, 1H), 8.40 (t, J = 5.5 Hz, 1H), 8.02 (dd, J = 8.5, 2.1 Hz, 1H), 7.96 (d, J = 2.1 Hz, 1H), 7.94 - 7.82 (m, 4H), 7.50 (d, J = 4.5 Hz, 1H), 7.33 (s, 1H), 7.23 (d, J = 8.6 Hz, 1H), 6.92 (t, J = 5.5 Hz, 1H), 3.93 - 3.86 (m, 6H), 3.31 - 3.25 (m, 2H), 3.15 - 3.07 (m, 2H), 1.39 (s, 9H). | C | ||
| 78 | 1H NMR (400 MHz, DMSO-d 6) δ 10.19 (s, 1H), 8.81 (s, 1H), 8.72 (d, J = 4.5 Hz, 1H), 8.31 - 8.18 (m, 2H), 7.97 (dd, J = 8.5, 2.1 Hz, 1H), 7.92 (d, J = 2.1 Hz, 1H), 7.50 (d, J = 4.5 Hz, 1H), 7.41 (s, 1H), 7.25 (d, J = 8.6 Hz, 1H), 3.95 - 3.89 (m, 6H). | B | ||
| 79 | 1H NMR (400 MHz, DMSO-d 6) δ 10.50 (s, 1H), 8.73 - 8.64 (m, 2H), 8.13 - 7.85 (m, 9H), 7.51 (d, J = 4.5 Hz, 1H), 7.34 (s, 1H), 7.23 (d, J = 8.6 Hz, 1H), 3.93 - 3.87 (m, 6H), 3.56 - 3.49 (m, 2H), 3.04 - 2.96 (m, 2H). | C | ||
| 80 | 1H NMR (400 MHz, DMSO-d 6) δ 10.40 (s, 1H), 8.70 (d, J = 4.5 Hz, 1H), 8.03 (dd, J = 8.5, 2.1 Hz, 1H), 7.95 (d, J = 2.1 Hz, 1H), 7.92 - 7.84 (m, 2H), 7.51 - 7.42 (m, 2H), 7.32 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 7.16 - 7.09 (m, 1H), 3.93 - 3.88 (m, 6H), 3.42 - 3.17 (m, 4H), 2.81 - 2.59 (m, 4H). | C | ||
| 81 | 1H NMR (400 MHz, DMSO-d 6) δ 8.65 (d, J = 4.5 Hz, 1H), 8.07 (d, J = 8.1 Hz, 1H), 7.97 (d, J = 2.1 Hz, 1H), 7.89 (dd, J = 8.5, 2.1 Hz, 1H), 7.43 (d, J = 4.5 Hz, 1H), 7.20 (d, J = 8.6 Hz, 1H), 7.13 (s, 1H), 3.92 - 3.84 (m, 6H), 3.84 - 3.71 (m, 1H), 3.43 - 3.36 (m, 4H), 2.74 - 2.58 (m, 4H), 2.57 - 2.53 (m, 1H), 1.96 - 1.85 (m, 2H), 1.76 - 1.66 (m, 2H), 1.54 - 1.39 (m, 4H). | A | ||
| 82 | 1H NMR (400 MHz, DMSO-d 6) δ 8.65 (d, J = 4.5 Hz, 1H), 7.97 (d, J = 2.1 Hz, 1H), 7.92 (dd, J = 8.5, 2.1 Hz, 1H), 7.88 (d, J = 7.4 Hz, 1H), 7.45 (d, J = 4.5 Hz, 1H), 7.25 (d, J = 8.6 Hz, 1H), 7.16 (s, 1H), 4.11 - 4.03 (m, 1H), 3.92 - 3.86 (m, 6H), 3.43 - 3.36 (m, 4H), 2.74 - 2.58 (m, 5H), 1.91 - 1.82 (m, 2H), 1.73 - 1.62 (m, 4H), 1.59 - 1.48 (m, 2H). | A | ||
| 83 | 1H NMR (400 MHz, DMSO-d 6) δ 8.67 (d, J = 4.5 Hz, 1H), 7.84 (t, J = 9.2 Hz, 1H), 7.76 (d, J = 2.0 Hz, 1H), 7.46 - 7.34 (m, 1H), 7.21 (d, J = 8.1 Hz, 1H), 7.06 (s, 1H), 4.88 - 4.71 (m, 2H), 3.89 - 3.83 (m, 8H), 3.77 - 3.61 (m, 2H), 3.60 - 3.45 (m, 4H), 2.09 (s, 3H). | D | ||
| 84 | 1H NMR (400 MHz, DMSO-d 6) δ 8.65 (d, J = 4.5 Hz, 1H), 8.29 (d, J = 8.2 Hz, 1H), 7.96 (d, J = 2.1 Hz, 1H), 7.92 (dd, J = 8.5, 2.2 Hz, 1H), 7.44 (d, J = 4.5 Hz, 1H), 7.20 (d, J = 8.6 Hz, 1H), 7.15 (s, 1H), 4.90 - 4.68 (m, 2H), 4.36 - 4.22 (m, 1H), 4.18 - 4.05 (m, 1H), 3.92 - 3.84 (m, 6H), 3.81 - 3.66 (m, 1H), 3.17 - 3.07 (m, 1H), 2.82 - 2.69 (m, 1H), 2.09 (s, 3H), 1.92 - 1.77 (m, 2H), 1.67 - 1.40 (m, 2H). | A | ||
| 85 | 1H NMR (400 MHz, DMSO-d 6) δ 12.56 (s, 1H), 10.48 (s, 1H), 8.71 (d, J = 4.5 Hz, 1H), 8.52 (d, J = 7.9 Hz, 1H), 8.02 (dd, J = 8.5, 2.1 Hz, 1H), 7.97 (d, J = 2.1 Hz, 1H), 7.93 (s, 4H), 7.50 (d, J = 4.5 Hz, 1H), 7.34 (s, 1H), 7.23 (d, J = 8.6 Hz, 1H), 4.54 - 4.32 (m, 1H), 3.99 - 3.72 (m, 6H), 1.88 - 1.65 (m, 2H), 1.65 - 1.51 (m, 1H), 0.94 (d, J = 6.4 Hz, 3H), 0.89 (d, J = 6.4 Hz, 3H). | C | ||
| 86 | 1H NMR (400 MHz, DMSO-d 6) δ 12.63 (s, 1H), 10.48 (s, 1H), 8.71 (d, J = 4.5 Hz, 1H), 8.32 (d, J = 8.0 Hz, 1H), 8.02 (dd, J = 8.5, 2.1 Hz, 1H), 7.97 (d, J = 2.1 Hz, 1H), 7.95 - 7.84 (m, 4H), 7.50 (d, J = 4.5 Hz, 1H), 7.34 (s, 1H), 7.23 (d, J = 8.6 Hz, 1H), 4.39 - 4.10 (m, 1H), 4.00 - 3.75 (m, 6H), 2.31 - 1.97 (m, 1H), 1.04 - 0.92 (m, 6H). | C | ||
| 87 | 1H NMR (400 MHz, DMSO-d 6) δ 12.67 (s, 1H), 10.49 (s, 1H), 8.71 (d, J = 4.5 Hz, 1H), 8.58 (d, J = 7.7 Hz, 1H), 8.02 (dd, J = 8.5, 2.1 Hz, 1H), 7.99 - 7.95 (m, 1H), 7.95 - 7.89 (m, 4H), 7.51 (d, J = 4.5 Hz, 1H), 7.34 (s, 1H), 7.23 (d, J = 8.6 Hz, 1H), 4.53 (dd, J = 14.4, 7.7 Hz, 1H), 3.96 - 3.85 (m, 6H), 2.67 - 2.53 (m, 2H), 2.12 - 2.03 (m, 5H). | C | ||
| 88 | 1H NMR (400 MHz, DMSO-d 6) δ 12.69 (s, 2H), 10.49 (s, 1H), 8.71 (d, J = 4.5 Hz, 1H), 8.66 (d, J = 7.4 Hz, 1H), 8.03 (dd, J = 8.5, 2.1 Hz, 1H), 7.98 - 7.85 (m, 5H), 7.50 (d, J = 4.5 Hz, 1H), 7.33 (s, 1H), 7.29 - 7.14 (m, 1H), 4.81 - 4.53 (m, 1H), 4.01 - 3.70 (m, 6H), 2.93 - 2.79 (m, 1H), 2.78 - 2.57 (m, 1H). | C | ||
| 89 | 1H NMR (400 MHz, DMSO-d 6) δ 12.54 (s, 1H), 10.48 (s, 1H), 8.71 (d, J = 4.5 Hz, 1H), 8.59 (d, J = 7.2 Hz, 1H), 8.03 (dd, J = 8.5, 2.1 Hz, 1H), 7.97 (d, J = 2.1 Hz, 1H), 7.95 - 7.86 (m, 4H), 7.51 (d, J = 4.5 Hz, 1H), 7.34 (s, 1H), 7.23 (d, J = 8.7 Hz, 1H), 4.50 - 4.35 (m, 1H), 3.96 - 3.86 (m, 6H), 1.41 (d, J = 7.3 Hz, 3H). | C | ||
| 90 | 1H NMR (400 MHz, DMSO-d 6) δ 8.67 (d, J = 4.5 Hz, 1H), 7.83 (d, J = 7.8 Hz, 1H), 7.77 (d, J = 2.1 Hz, 1H), 7.40 (d, J = 4.4 Hz, 1H), 7.21 (d, J = 8.5 Hz, 1H), 7.06 (s, 1H), 4.68 (t, J = 5.4 Hz, 1H), 4.21 - 4.05 (m, 2H), 3.95 - 3.78 (m, 8H), 3.75 - 3.65 (m, 2H), 3.64 - 3.56 (m, 1H), 3.56 - 3.45 (m, 2H), 3.45 - 3.37 (m, 1H). | D | ||
| 91 | 1H NMR (400 MHz, DMSO-d 6) δ 8.65 (d, J = 4.5 Hz, 1H), 8.26 (d, J = 8.1 Hz, 1H), 7.95 (d, J = 2.0 Hz, 1H), 7.92 (dd, J = 8.5, 2.1 Hz, 1H), 7.44 (d, J = 4.5 Hz, 1H), 7.20 (d, J = 8.5 Hz, 1H), 7.14 (s, 1H), 4.53 (t, J = 5.4 Hz, 1H), 4.41 - 4.26 (m, 1H), 4.20 - 4.00 (m, 3H), 3.96 - 3.82 (m, 6H), 3.77 - 3.63 (m, 1H), 3.14 - 3.00 (m, 1H), 2.77 (t, J = 12.4 Hz, 1H), 1.84 (d, J = 11.8 Hz, 2H), 1.64 - 1.41 (m, 2H). | A | ||
| 92 | 1H NMR (400 MHz, DMSO-d 6) δ 9.04 (s, 1H), 8.65 (d, J = 4.5 Hz, 1H), 7.97 (dd, J = 8.5, 2.1 Hz, 1H), 7.83 (d, J = 2.1 Hz, 1H), 7.43 (d, J = 4.5 Hz, 1H), 7.20 (d, J = 8.7 Hz, 1H), 7.13 (s, 1H), 3.92 - 3.84 (m, 6H), 3.60 - 3.52 (m, 2H), 3.46 - 3.40 (m, 2H), 3.40 - 3.34 (m, 2H), 3.32 - 3.25 (m, 2H), 2.41 (s, 6H), 1.42 (s, 9H). | B | ||
| 93 | 1H NMR (400 MHz, DMSO-d 6) δ 9.81 (s, 1H), 9.36 (s, 1H), 8.50 (d, J = 4.5 Hz, 1H), 7.92 (d, J = 8.8 Hz, 2H), 7.83 (dd, J = 8.5, 2.1 Hz, 1H), 7.78 (d, J = 2.0 Hz, 1H), 7.61 (d, J = 8.8 Hz, 2H), 7.24 - 7.13 (m, 2H), 6.80 (s, 1H), 3.92 - 3.85 (m, 6H), 3.83 (s, 3H). | E | ||
| 94 | 1H NMR (400 MHz, DMSO-d 6) δ 12.87 (s, 1H), 9.08 (t, J = 6.3 Hz, 1H), 8.66 (d, J = 4.5 Hz, 1H), 7.95 (dd, J = 8.5, 2.1 Hz, 1H), 7.91 (d, J = 8.2 Hz, 2H), 7.86 (d, J = 2.1 Hz, 1H), 7.49 - 7.39 (m, 3H), 7.23 - 7.14 (m, 2H), 4.59 (d, J = 6.2 Hz, 2H), 3.90 - 3.84 (m, 6H). | A | ||
| 95 | 1H NMR (400 MHz, DMSO-d 6) δ 8.97 (s, 1H), 8.65 (d, J = 4.5 Hz, 1H), 7.98 (dd, J = 8.5, 2.2 Hz, 1H), 7.82 (d, J = 2.1 Hz, 1H), 7.43 (d, J = 4.5 Hz, 1H), 7.32 (s, 1H), 7.20 (d, J = 8.6 Hz, 1H), 7.12 (s, 1H), 6.98 (s, 1H), 3.92 - 3.86 (m, 6H), 2.26 (s, 6H). | B | ||
| 96 | 1H NMR (400 MHz, DMSO-d 6) δ 9.03 (s, 1H), 8.65 (d, J = 4.5 Hz, 1H), 7.96 (dd, J = 8.5, 2.1 Hz, 1H), 7.82 (d, J = 2.1 Hz, 1H), 7.42 (d, J = 4.5 Hz, 1H), 7.19 (d, J = 8.6 Hz, 1H), 7.12 (s, 1H), 3.92 - 3.87 (m, 6H), 3.61 - 3.53 (m, 6H), 3.48 - 3.42 (m, 2H), 2.41 (s, 6H). | B | ||
| 97 | 1H NMR (400 MHz, DMSO-d 6) δ 10.44 (s, 1H), 8.70 (d, J = 4.5 Hz, 1H), 8.02 (dd, J = 8.5, 2.1 Hz, 1H), 7.96 (d, J = 2.1 Hz, 1H), 7.90 (d, J = 8.6 Hz, 2H), 7.50 (d, J = 4.5 Hz, 1H), 7.43 (d, J = 8.6 Hz, 2H), 7.32 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 3.94 - 3.85 (m, 6H), 3.68 - 3.37 (m, 4H), 2.44 - 2.27 (m, 4H), 2.22 (s, 3H). | C | ||
| 98 | 1H NMR (400 MHz, DMSO-d 6) δ 9.03 (s, 1H), 8.65 (d, J = 4.5 Hz, 1H), 7.97 (dd, J = 8.5, 2.2 Hz, 1H), 7.82 (d, J = 2.1 Hz, 1H), 7.43 (d, J = 4.5 Hz, 1H), 7.20 (d, J = 8.6 Hz, 1H), 7.12 (s, 1H), 3.92 - 3.85 (m, 6H), 3.51 - 3.35 (m, 4H), 2.70 - 2.59 (m, 4H), 2.39 (s, 6H). | B | ||
| 99 | 1H NMR (400 MHz, DMSO-d 6) δ 9.50 (s, 1H), 8.65 (d, J = 4.5 Hz, 1H), 8.01 - 7.86 (m, 2H), 7.44 (d, J = 4.5 Hz, 1H), 7.20 (d, J = 8.5 Hz, 1H), 7.13 (s, 1H), 3.95 - 3.80 (m, 6H), 3.74 - 3.60 (m, 4H), 3.00 - 2.82 (m, 4H). | A | ||
| 100 | 1H NMR (400 MHz, DMSO-d 6) δ 8.65 (d, J = 4.5 Hz, 1H), 7.82 (dd, J = 8.5, 2.1 Hz, 1H), 7.76 (d, J = 2.1 Hz, 1H), 7.37 (d, J = 4.5 Hz, 1H), 7.19 (d, J = 8.5 Hz, 1H), 6.99 (s, 1H), 6.92 (d, J = 7.6 Hz, 1H), 4.44 - 4.24 (m, 2H), 3.88 (s, 3H), 3.85 (s, 3H), 3.65 - 3.48 (m, 1H), 3.30 - 3.20 (m, 1H), 3.04 - 2.92 (m, 1H), 2.91 - 2.83 (m, 2H), 1.88 - 1.69 (m, 2H), 1.39 (s, 9H). | D | ||
| 101 | 1H NMR (400 MHz, DMSO-d 6) δ 8.65 (d, J = 4.5 Hz, 1H), 7.85 - 7.74 (m, 2H), 7.38 (d, J = 4.4 Hz, 1H), 7.20 (d, J = 8.2 Hz, 1H), 7.01 (s, 1H), 3.88 (s, 3H), 3.86 (s, 3H), 3.83 - 3.77 (m, 2H), 3.72 - 3.61 (m, 2H), 2.43 - 2.35 (m, 2H), 2.35 - 2.28 (m, 2H), 2.21 (s, 3H). | D | ||
| 102 | 1H NMR (400 MHz, DMSO-d 6) δ 8.64 (d, J = 4.5 Hz, 1H), 8.03 - 7.95 (m, 2H), 7.92 (dd, J = 8.5, 2.1 Hz, 1H), 7.43 (d, J = 4.5 Hz, 1H), 7.21 (d, J = 8.6 Hz, 1H), 7.15 (s, 1H), 4.41 (d, J = 2.9 Hz, 1H), 3.93 - 3.79 (m, 7H), 3.79 - 3.71 (m, 1H), 1.88 - 1.72 (m, 2H), 1.72 - 1.46 (m, 6H). | A | ||
| 103 | 1H NMR (400 MHz, DMSO-d 6) δ 8.65 (d, J = 4.5 Hz, 1H), 8.15 (d, J = 8.2 Hz, 1H), 7.98 (d, J = 2.1 Hz, 1H), 7.91 (dd, J = 8.5, 2.2 Hz, 1H), 7.43 (d, J = 4.5 Hz, 1H), 7.20 (d, J = 8.6 Hz, 1H), 7.13 (s, 1H), 4.72 (s, 2H), 3.92 - 3.86 (m, 6H), 3.86 - 3.71 (m, 1H), 3.64 - 3.51 (m, 1H), 2.98 - 2.78 (m, 2H), 2.42 - 2.32 (m, 1H), 2.30 - 2.20 (m, 1H), 2.15 - 2.01 (m, 2H), 1.84 - 1.70 (m, 2H), 1.70 - 1.56 (m, 2H). | A | ||
| 104 | 1H NMR (400 MHz, CDCl 3) δ 9.92 (s, 1H), 8.81 (d, J = 8.7 Hz, 1H), 8.64 (d, J = 4.4 Hz, 1H), 8.13 (d, J = 1.9 Hz, 1H), 8.04 (dd, J = 8.6, 1.9 Hz, 1H), 7.78 (dd, J = 8.4, 2.1 Hz, 1H), 7.73 (d, J = 2.1 Hz, 1H), 7.45 (s, 1H), 7.12 - 7.07 (m, 2H), 4.04 (s, 3H), 4.01 (s, 3H), 3.95 (s, 3H). | B | ||
| 105 | 1H NMR (400 MHz, DMSO-d 6) δ 10.05 (s, 1H), 8.70 (d, J = 4.5 Hz, 1H), 7.97 (dd, J = 8.5, 2.1 Hz, 1H), 7.91 (d, J = 2.0 Hz, 1H), 7.78 - 7.70 (m, 2H), 7.50 (s, 1H), 7.47 (d, J = 4.5 Hz, 1H), 7.40 - 7.36 (m, 3H), 7.25 (s, 1H), 7.17 (d, J = 8.6 Hz, 1H), 3.88 (s, 3H), 3.83 (s, 3H), 3.75 (s, 3H). | A | ||
| 106 | 1H NMR (400 MHz, DMSO-d 6) δ 9.97 (s, 1H), 8.74 (d, J = 4.5 Hz, 1H), 8.38 (d, J = 8.4 Hz, 1H), 8.02 (d, J = 1.7 Hz, 1H), 7.97 - 7.91 (m, 2H), 7.85 (d, J = 2.1 Hz, 1H), 7.51 (d, J = 4.5 Hz, 1H), 7.35 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 3.94 - 3.86 (m, 6H). | B | ||
| 107 | 1H NMR (400 MHz, DMSO-d 6) δ 9.83 (s, 1H), 9.49 (s, 1H), 8.49 (d, J = 4.6 Hz, 1H), 7.89 (d, J = 8.7 Hz, 2H), 7.85 - 7.78 (m, 2H), 7.59 (d, J = 8.7 Hz, 2H), 7.22 - 7.16 (m, 2H), 6.80 (s, 1H), 3.91 - 3.85 (m, 6H). | E | ||
| 108 | 1H NMR (400 MHz, DMSO-d 6) δ 12.88 (s, 1H), 9.88 (s, 1H), 8.69 (d, J = 4.5 Hz, 1H), 7.97 (dd, J = 8.5, 2.1 Hz, 1H), 7.92 (d, J = 2.0 Hz, 1H), 7.74 - 7.67 (m, 2H), 7.50 (s, 1H), 7.47 (d, J = 4.5 Hz, 1H), 7.38 - 7.33 (m, 3H), 7.24 (s, 1H), 7.18 (d, J = 8.6 Hz, 1H), 3.88 (s, 3H), 3.84 (s, 3H). | A | ||
| 109 | 1H NMR (400 MHz, DMSO-d 6) δ 9.55 (s, 1H), 8.83 (s, 1H), 8.47 (d, J = 4.6 Hz, 1H), 7.83 (dd, J = 8.5, 2.1 Hz, 1H), 7.76 (d, J = 2.1 Hz, 1H), 7.38 - 7.32 (m, 2H), 7.21 - 7.13 (m, 2H), 6.91 - 6.84 (m, 2H), 6.73 (s, 1H), 3.99 (q, J = 7.0 Hz, 2H), 3.89 (s, 3H), 3.86 (s, 3H), 1.32 (t, J = 7.0 Hz, 3H). | E | ||
| 110 | 1H NMR (400 MHz, DMSO-d 6) δ 8.67 (d, J = 4.5 Hz, 1H), 7.92 - 7.80 (m, 1H), 7.77 (s, 1H), 7.43 - 7.35 (m, 1H), 7.21 (d, J = 8.4 Hz, 1H), 7.06 (s, 1H), 3.98 - 3.44 (m, 14H), 2.12 - 1.89 (m, 1H), 0.85 - 0.59 (m, 4H). | D | ||
| 111 | 1H NMR (400 MHz, DMSO-d 6) δ 8.67 (d, J = 4.5 Hz, 1H), 7.83 (dd, J = 8.5, 2.1 Hz, 1H), 7.76 (d, J = 2.1 Hz, 1H), 7.40 (d, J = 4.5 Hz, 1H), 7.21 (d, J = 8.6 Hz, 1H), 7.04 (s, 1H), 4.07 (q, J = 7.1 Hz, 2H), 3.93 - 3.78 (m, 8H), 3.74 - 3.61 (m, 2H), 3.53 - 3.46 (m, 2H), 3.44 - 3.37 (m, 2H), 1.20 (t, J = 6.8 Hz, 3H). | D | ||
| 112 | 1H NMR (400 MHz, DMSO-d 6) δ 8.66 (d, J = 4.4 Hz, 1H), 7.87 - 7.64 (m, 2H), 7.39 (dd, J = 7.8, 4.5 Hz, 1H), 7.20 (dd, J = 8.4, 4.8 Hz, 1H), 7.05 (d, J = 21.4 Hz, 1H), 4.51 - 4.02 (m, 3H), 3.93 - 3.63 (m, 7H), 3.26 - 2.86 (m, 3H), 1.41 (d, J = 2.2 Hz, 9H), 1.05 (dd, J = 33.4, 6.7 Hz, 3H). | D | ||
| 113 | 1H NMR (400 MHz, DMSO-d 6) δ 8.66 (d, J = 4.4 Hz, 1H), 7.95 - 7.66 (m, 2H), 7.38 (dd, J = 10.5, 4.4 Hz, 1H), 7.19 (dd, J = 11.7, 8.5 Hz, 1H), 7.07 (d, J = 28.1 Hz, 1H), 4.04 - 3.91 (m, 2H), 3.91 - 3.80 (m, 6H), 3.78 - 3.52 (m, 4H), 1.51 - 1.35 (m, 12H), 1.26 (s, 3H). | D | ||
| 114 | 1H NMR (400 MHz, CDCl 3) δ 9.69 (s, 1H), 8.98 (d, J = 1.5 Hz, 1H), 8.61 (d, J = 4.4 Hz, 1H), 8.49 (d, J = 8.7 Hz, 1H), 8.39 (dd, J = 8.7, 2.1 Hz, 1H), 7.78 (d, J = 2.0 Hz, 1H), 7.68 (dd, J = 8.4, 2.1 Hz, 1H), 7.56 - 7.33 (m, 6H), 7.10 (dd, J = 9.8, 6.4 Hz, 2H), 5.39 (s, 2H), 4.16 - 3.96 (m, 6H). | B | ||
| 115 | 1H NMR (400 MHz, DMSO-d 6) δ 8.65 (dd, J = 4.4, 1.2 Hz, 1H), 7.86 - 7.76 (m, 2H), 7.38 (dd, J = 4.4, 1.2 Hz, 1H), 7.29 - 7.15 (m, 2H), 7.09 (d, J = 3.8 Hz, 1H), 4.13 - 3.95 (m, 2H), 3.90 - 3.82 (m, 6H), 3.77 - 3.37 (m, 3H), 2.16 - 1.97 (m, 1H), 1.89 - 1.74 (m, 1H), 1.46 - 1.28 (m, 9H). | D | ||
| 116 | 1H NMR (400 MHz, DMSO-d 6) δ 8.66 (d, J = 4.4 Hz, 1H), 7.82 (dd, J = 8.3, 1.7 Hz, 1H), 7.74 (d, J = 1.4 Hz, 1H), 7.65 (d, J = 6.5 Hz, 1H), 7.40 (d, J = 4.4 Hz, 1H), 7.20 (d, J = 8.6 Hz, 1H), 7.10 (s, 1H), 4.89 - 4.68 (m, 1H), 4.46 - 4.26 (m, 3H), 3.95 - 3.82 (m, 7H), 1.39 (s, 9H). | D | ||
| 117 | 1H NMR (400 MHz, DMSO-d 6) δ 8.72 - 8.62 (m, 1H), 7.87 - 7.68 (m, 2H), 7.44 - 7.36 (m, 1H), 7.24 - 7.13 (m, 2H), 4.46 (s, 1H), 4.40 (t, J = 7.8 Hz, 1H), 4.01 - 3.95 (m, 2H), 3.92 - 3.80 (m, 6H), 2.68 (t, J = 7.8 Hz, 1H), 2.61 (t, J = 8.0 Hz, 1H). | D | ||
| 118 | 1H NMR (400 MHz, DMSO-d 6) δ 10.48 (s, 1H), 8.70 (d, J = 4.5 Hz, 1H), 8.58 - 8.46 (m, 1H), 8.01 (dd, J = 8.5, 2.1 Hz, 1H), 7.98 - 7.84 (m, 5H), 7.50 (d, J = 4.5 Hz, 1H), 7.32 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 3.92 - 3.86 (m, 6H), 3.58 - 3.48 (m, 2H), 3.07 - 2.94 (m, 2H), 2.65 (s, 6H). | C | ||
| 119 | 1H NMR (400 MHz, DMSO-d 6) δ 10.51 (s, 1H), 9.35 (s, 1H), 8.71 (d, J = 4.5 Hz, 1H), 8.02 (dd, J = 8.5, 2.1 Hz, 1H), 7.98 - 7.84 (m, 5H), 7.51 (d, J = 4.5 Hz, 1H), 7.34 (s, 1H), 7.23 (d, J = 8.6 Hz, 1H), 3.96 - 3.86 (m, 6H), 3.73 - 3.41 (m, 4H), 3.01 - 2.78 (m, 2H), 1.84 - 1.32 (m, 8H). | C | ||
| 120 | 1H NMR (400 MHz, DMSO-d 6) δ 10.46 (s, 1H), 8.71 (d, J = 4.4 Hz, 1H), 8.34 (s, 1H), 8.03 (d, J = 6.7 Hz, 1H), 8.00 - 7.74 (m, 5H), 7.50 (d, J = 4.4 Hz, 1H), 7.33 (s, 1H), 7.23 (d, J = 8.5 Hz, 1H), 4.05 - 3.72 (m, 6H), 3.29 - 3.10 (m, 2H), 3.10 - 2.85 (m, 2H), 1.25 - 0.74 (m, 12H). | C | ||
| 121 | 1H NMR (400 MHz, DMSO-d 6) δ 10.61 (s, 1H), 8.71 (d, J = 4.5 Hz, 1H), 8.07 - 7.88 (m, 6H), 7.51 (d, J = 4.5 Hz, 1H), 7.35 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 4.31 (t, J = 6.4 Hz, 2H), 3.98 - 3.78 (m, 6H), 3.65 - 3.48 (m, 4H), 2.46 - 2.27 (m, 6H), 2.00 - 1.75 (m, 2H). | C | ||
| 122 | 1H NMR (400 MHz, DMSO-d 6) δ 9.98 (s, 1H), 8.71 (d, J = 4.5 Hz, 1H), 8.25 - 8.21 (m, 1H), 8.15 (d, J = 8.5 Hz, 1H), 7.95 (dd, J = 8.5, 2.1 Hz, 1H), 7.91 (d, J = 2.1 Hz, 1H), 7.72 (dd, J = 8.5, 2.2 Hz, 1H), 7.49 (d, J = 4.5 Hz, 1H), 7.38 (s, 1H), 7.24 (d, J = 8.6 Hz, 1H), 3.93 - 3.89 (m, 6H), 2.30 (s, 3H). | C | ||
| 123 | 1H NMR (400 MHz, DMSO-d 6) δ 9.05 (s, 1H), 8.65 (d, J = 4.5 Hz, 1H), 7.97 (dd, J = 8.5, 2.1 Hz, 1H), 7.82 (d, J = 2.1 Hz, 1H), 7.43 (d, J = 4.5 Hz, 1H), 7.20 (d, J = 8.6 Hz, 1H), 7.13 (s, 1H), 3.92 - 3.86 (m, 6H), 3.72 - 3.40 (m, 4H), 2.75 - 2.54 (m, 4H), 2.45 - 2.33 (m, 9H). | B | ||
| 124 | 1H NMR (400 MHz, DMSO-d 6) δ 10.20 (s, 1H), 8.63 (d, J = 4.5 Hz, 1H), 8.38 - 8.34 (m, 1H), 8.22 (d, J = 8.5 Hz, 1H), 7.91 - 7.85 (m, 2H), 7.83 (d, J = 2.1 Hz, 1H), 7.42 (d, J = 4.5 Hz, 1H), 7.34 (s, 1H), 7.15 (d, J = 8.6 Hz, 1H), 3.87 - 3.80 (m, 6H), 3.61 - 3.28 (m, 4H), 2.35 - 2.18 (m, 4H), 2.12 (s, 3H). | B | ||
| 125 | 1H NMR (400 MHz, DMSO-d 6) δ 9.85 (s, 1H), 8.71 (d, J = 4.5 Hz, 1H), 8.05 - 7.99 (m, 2H), 7.92 - 7.82 (m, 3H), 7.50 (d, J = 4.5 Hz, 1H), 7.31 (s, 1H), 7.20 (d, J = 8.6 Hz, 1H), 3.92 - 3.82 (m, 9H), 2.38 (s, 3H). | B | ||
| 126 | 1H NMR (400 MHz, DMSO-d 6) δ 12.86 (s, 1H), 9.84 (s, 1H), 8.71 (d, J = 4.5 Hz, 1H), 8.03 (dd, J = 8.5, 2.0 Hz, 1H), 7.97 (d, J = 8.4 Hz, 1H), 7.91 - 7.81 (m, 3H), 7.50 (d, J = 4.5 Hz, 1H), 7.31 (s, 1H), 7.20 (d, J = 8.6 Hz, 1H), 3.93 - 3.86 (m, 6H), 2.37 (s, 3H). | B | ||
| 127 | 1H NMR (400 MHz, DMSO-d 6) δ 9.84 (s, 1H), 8.71 (d, J = 4.5 Hz, 1H), 8.03 (dd, J = 8.5, 1.9 Hz, 1H), 7.86 (d, J = 2.1 Hz, 1H), 7.79 (d, J = 8.1 Hz, 1H), 7.50 (d, J = 4.5 Hz, 1H), 7.37 (s, 1H), 7.34 - 7.28 (m, 2H), 7.20 (d, J = 8.6 Hz, 1H), 3.92 - 3.86 (m, 6H), 3.71 - 3.37 (m, 8H), 2.33 (s, 3H). | B | ||
| 128 | 1H NMR (400 MHz, DMSO-d 6) δ 9.83 (s, 1H), 8.71 (d, J = 4.5 Hz, 1H), 8.03 (dd, J = 8.5, 1.9 Hz, 1H), 7.86 (d, J = 2.1 Hz, 1H), 7.78 (d, J = 8.1 Hz, 1H), 7.50 (d, J = 4.5 Hz, 1H), 7.36 - 7.25 (m, 3H), 7.20 (d, J = 8.6 Hz, 1H), 3.93 - 3.86 (m, 6H), 3.71 - 3.38 (m, 4H), 2.43 - 2.28 (m, 7H), 2.22 (s, 3H). | B | ||
| 129 | 1H NMR (400 MHz, DMSO-d 6) δ 9.76 (s, 1H), 9.24 (s, 1H), 8.40 (d, J = 4.6 Hz, 1H), 7.80 - 7.68 (m, 2H), 7.45 (d, J = 8.5 Hz, 2H), 7.29 (d, J = 8.5 Hz, 2H), 7.15 - 7.07 (m, 2H), 6.69 (s, 1H), 3.85 - 3.74 (m, 6H), 3.58 - 3.35 (m, 8H). | E | ||
| 130 | 1H NMR (400 MHz, CDCl 3) δ 8.60 (d, J = 4.4 Hz, 1H), 8.50 - 8.33 (m, 1H), 8.03 - 7.93 (m, 1H), 7.91 (d, J = 1.2 Hz, 1H), 7.77 - 7.59 (m, 2H), 7.37 (s, 1H), 7.12 - 6.92 (m, 2H), 4.75 - 4.52 (m, 2H), 4.11 - 3.80 (m, 9H), 3.22 (t, J = 8.5 Hz, 2H). | D | ||
| 131 | 1H NMR (400 MHz, DMSO-d 6) δ 8.72 - 8.61 (m, 1H), 7.95 - 7.65 (m, 4H), 7.48 - 7.30 (m, 2H), 7.19 (dd, J = 23.1, 8.6 Hz, 1H), 7.07 (d, J = 17.2 Hz, 1H), 5.17 (s, 1H), 4.92 (s, 1H), 4.05 (t, J = 5.8 Hz, 1H), 3.93 (t, J = 6.0 Hz, 1H), 3.90 - 3.71 (m, 9H), 3.05 - 2.88 (m, 2H). | D | ||
| 132 | 1H NMR (400 MHz, DMSO-d 6) δ 8.86 (s, 1H), 8.71 (d, J = 4.4 Hz, 1H), 7.94 - 7.79 (m, 2H), 7.74 (d, J = 7.1 Hz, 1H), 7.52 - 7.40 (m, 2H), 7.28 (s, 1H), 7.22 (d, J = 8.7 Hz, 1H), 4.73 - 4.56 (m, 2H), 3.95 - 3.76 (m, 9H), 3.32 - 3.23 (m, 2H). | D | ||
| 133 | 1H NMR (400 MHz, DMSO-d 6) δ 8.65 (d, J = 4.5 Hz, 1H), 7.88 (d, J = 1.9 Hz, 1H), 7.58 (dd, J = 9.2, 1.9 Hz, 2H), 7.52 - 7.43 (m, 1H), 7.40 (d, J = 4.5 Hz, 1H), 7.25 (d, J = 8.1 Hz, 1H), 7.05 (s, 1H), 6.97 (d, J = 8.6 Hz, 1H), 4.00 - 3.90 (m, 2H), 3.89 - 3.71 (m, 9H), 2.90 (t, J = 6.6 Hz, 2H), 2.04 - 1.92 (m, 2H). | D | ||
| 134 | 1H NMR (400 MHz, DMSO-d 6) δ 10.04 (s, 1H), 8.70 (d, J = 4.5 Hz, 1H), 8.01 (dd, J = 8.5, 2.1 Hz, 1H), 7.74 (d, J = 2.1 Hz, 1H), 7.64 - 7.59 (m, 2H), 7.48 (d, J = 4.5 Hz, 1H), 7.38 - 7.31 (m, 3H), 7.30 (s, 1H), 7.10 (d, J = 8.6 Hz, 1H), 6.33 (s, 1H), 3.88 (s, 3H), 3.76 (s, 3H), 3.70 - 3.48 (m, 4H), 2.42 - 2.32 (m, 4H), 2.22 (s, 3H). | A | ||
| 135 | 1H NMR (400 MHz, DMSO-d 6) δ 10.29 (s, 1H), 8.72 (d, J = 4.5 Hz, 1H), 8.50 - 8.46 (m, 1H), 8.31 (d, J = 8.5 Hz, 1H), 8.02 - 7.94 (m, 2H), 7.92 (d, J = 2.1 Hz, 1H), 7.51 (d, J = 4.5 Hz, 1H), 7.43 (s, 1H), 7.24 (d, J = 8.6 Hz, 1H), 3.95 - 3.88 (m, 6H), 3.74 - 3.38 (m, 8H). | B | ||
| 136 | 1H NMR (400 MHz, DMSO-d 6) δ 10.00 (s, 1H), 8.72 (d, J = 4.5 Hz, 1H), 8.28 (t, J = 8.1 Hz, 1H), 7.95 (d, J = 2.1 Hz, 1H), 7.92 - 7.80 (m, 3H), 7.50 (d, J = 4.5 Hz, 1H), 7.34 (s, 1H), 7.21 (d, J = 8.6 Hz, 1H), 3.93 - 3.85 (m, 9H). | B | ||
| 137 | 1H NMR (400 MHz, DMSO-d 6) δ 9.96 (s, 1H), 8.73 (d, J = 4.5 Hz, 1H), 8.34 (d, J = 8.4 Hz, 1H), 7.92 (dd, J = 8.5, 2.1 Hz, 1H), 7.87 (d, J = 2.1 Hz, 1H), 7.66 (d, J = 1.9 Hz, 1H), 7.53 - 7.46 (m, 2H), 7.35 (s, 1H), 7.21 (d, J = 8.6 Hz, 1H), 3.94 - 3.82 (m, 6H), 3.77 - 3.40 (m, 4H), 2.86 - 2.55 (m, 4H), 2.40 (s, 3H). | B | ||
| 138 | 1H NMR (400 MHz, DMSO-d 6) δ 8.94 (s, 1H), 8.65 (d, J = 4.5 Hz, 1H), 7.99 (dd, J = 8.5, 2.1 Hz, 1H), 7.82 (d, J = 2.1 Hz, 1H), 7.43 (d, J = 4.5 Hz, 1H), 7.22 - 7.15 (m, 2H), 7.12 (s, 1H), 3.93 - 3.84 (m, 6H), 3.57 - 3.48 (m, 4H), 3.27 - 3.21 (m, 4H), 2.28 (s, 6H). | B | ||
| 139 | 1H NMR (400 MHz, DMSO-d 6) δ 10.48 (s, 1H), 8.71 (d, J = 4.5 Hz, 1H), 8.37 (t, J = 5.7 Hz, 1H), 8.03 (dd, J = 8.5, 2.1 Hz, 1H), 7.96 (d, J = 2.1 Hz, 1H), 7.94 - 7.89 (m, 2H), 7.89 - 7.82 (m, 2H), 7.51 (d, J = 4.5 Hz, 1H), 7.33 (s, 1H), 7.23 (d, J = 8.7 Hz, 1H), 3.93 - 3.87 (m, 6H), 3.61 - 3.55 (m, 4H), 3.44 - 3.35 (m, 2H), 2.50 - 2.38 (m, 6H). | C | ||
| 140 | 1H NMR (400 MHz, DMSO-d 6) δ 10.72 (s, 1H), 8.71 (d, J = 4.5 Hz, 1H), 8.17 (s, 1H), 8.03 (dd, J = 8.5, 2.2 Hz, 1H), 7.96 - 7.85 (m, 3H), 7.52 (d, J = 4.5 Hz, 1H), 7.35 (s, 1H), 7.23 (d, J = 8.6 Hz, 1H), 3.95 - 3.88 (m, 6H), 3.86 (s, 3H). | B | ||
| 141 | 1H NMR (400 MHz, DMSO-d 6) δ 10.79 (s, 1H), 8.71 (d, J = 4.5 Hz, 1H), 8.02 (dd, J = 8.5, 2.1 Hz, 1H), 7.96 - 7.84 (m, 3H), 7.77 (dd, J = 8.7, 1.9 Hz, 1H), 7.52 (d, J = 4.5 Hz, 1H), 7.35 (s, 1H), 7.23 (d, J = 8.6 Hz, 1H), 3.94 - 3.86 (m, 6H), 3.85 (s, 3H). | B | ||
| 142 | 1H NMR (400 MHz, DMSO-d 6) δ 10.49 (s, 1H), 8.95 - 8.84 (m, 1H), 8.73 (d, J = 4.4 Hz, 1H), 8.46 - 8.29 (m, 2H), 8.00 - 7.83 (m, 2H), 7.52 (d, J = 4.5 Hz, 1H), 7.45 (s, 1H), 7.24 (d, J = 8.5 Hz, 1H), 4.35 (t, J = 6.5 Hz, 2H), 3.98 - 3.77 (m, 6H), 3.56 (t, J = 4.5 Hz, 4H), 2.43 (t, J = 7.1 Hz, 2H), 2.40 - 2.30 (m, 4H), 1.94 - 1.85 (m, 2H). | B | ||
| 143 | 1H NMR (400 MHz, DMSO-d 6) δ 8.68 (dd, J = 4.4, 2.5 Hz, 1H), 8.38 (s, 3H), 7.97 - 7.69 (m, 2H), 7.42 (dd, J = 13.9, 4.4 Hz, 1H), 7.25 (dd, J = 34.4, 8.8 Hz, 1H), 7.14 (s, 1H), 4.21 - 4.12 (m, 3H), 3.90 - 3.84 (m, 6H), 3.82 - 3.63 (m, 2H), 2.33 - 2.17 (m, 1H), 2.15 - 1.99 (m, 1H). | D | ||
| 144 | 1H NMR (400 MHz, DMSO-d 6) δ 8.64 (d, J = 4.5 Hz, 1H), 8.00 (d, J = 2.1 Hz, 1H), 7.85 (dd, J = 8.5, 2.1 Hz, 1H), 7.46 - 7.40 (m, 2H), 7.19 (d, J = 8.6 Hz, 1H), 7.09 (s, 1H), 3.90 - 3.87 (m, 6H), 3.58 (s, 3H), 2.05 - 1.92 (m, 6H), 1.89 - 1.77 (m, 6H). | A | ||
| 145 | 1H NMR (400 MHz, DMSO-d 6) δ 8.69 - 8.64 (m, 1H), 7.87 - 7.76 (m, 2H), 7.41 - 7.37 (m, 1H), 7.29 - 7.17 (m, 2H), 7.09 (d, J = 3.8 Hz, 1H), 4.16 - 4.03 (m, 2H), 3.90 - 3.82 (m, 6H), 3.81 - 3.50 (m, 3H), 2.13 - 2.00 (m, 1H), 1.92 - 1.78 (m, 1H), 1.45 - 1.35 (m, 9H). | D | ||
| 146 | 1H NMR (400 MHz, DMSO-d 6) δ 10.48 (s, 1H), 8.70 (d, J = 4.5 Hz, 1H), 8.43 (d, J = 8.6 Hz, 1H), 8.05 - 7.99 (m, 1H), 7.99 - 7.87 (m, 5H), 7.50 (d, J = 4.5 Hz, 1H), 7.33 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 4.71 (t, J = 8.6 Hz, 1H), 3.94 - 3.87 (m, 6H), 3.70 - 3.59 (m, 2H), 3.55 - 3.47 (m, 2H), 2.35 - 2.23 (m, 4H), 2.22 - 2.14 (m, 4H), 0.96 - 0.88 (m, 6H). | C | ||
| 147 | 1H NMR (400 MHz, DMSO-d 6) δ 10.48 (s, 1H), 8.70 (d, J = 4.5 Hz, 1H), 8.48 (d, J = 8.4 Hz, 1H), 8.02 (dd, J = 8.5, 2.1 Hz, 1H), 7.99 - 7.87 (m, 5H), 7.50 (d, J = 4.5 Hz, 1H), 7.33 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 4.69 (t, J = 8.6 Hz, 1H), 3.93 - 3.88 (m, 6H), 3.73 - 3.64 (m, 2H), 3.62 - 3.47 (m, 6H), 2.26 - 2.10 (m, 1H), 1.00 - 0.89 (m, 6H). | C | ||
| 148 | 1H NMR (400 MHz, DMSO-d 6) δ 8.65 (s, 1H), 7.82 (s, 2H), 7.38 (s, 1H), 7.19 (s, 1H), 7.09 (s, 1H), 5.12 - 4.87 (m, 1H), 4.49 - 4.18 (m, 1H), 4.16 - 3.97 (m, 1H), 3.96 - 3.72 (m, 7H), 3.70 - 3.44 (m, 2H), 2.03 - 1.74 (m, 2H). | D | ||
| 149 | 1H NMR (400 MHz, DMSO-d 6) δ 12.12 (s, 1H), 8.64 (d, J = 4.4 Hz, 1H), 8.10 - 7.93 (m, 1H), 7.90 - 7.78 (m, 1H), 7.52 - 7.34 (m, 2H), 7.20 (d, J = 8.6 Hz, 1H), 7.09 (s, 1H), 4.04 - 3.73 (m, 6H), 2.06 - 1.89 (m, 6H), 1.88 - 1.70 (m, 6H). | A | ||
| 150 | 1H NMR (400 MHz, DMSO-d 6) δ 8.66 (d, J = 4.4 Hz, 1H), 7.93 - 7.74 (m, 2H), 7.39 (d, J = 4.3 Hz, 1H), 7.20 (d, J = 8.3 Hz, 1H), 7.10 (d, J = 3.0 Hz, 1H), 5.14 - 4.94 (m, 1H), 4.41 - 4.27 (m, 1H), 4.10 - 3.82 (m, 8H), 3.70 - 3.45 (m, 2H), 2.13 - 1.65 (m, 2H). | D | ||
| 151 | 1H NMR (400 MHz, DMSO-d 6) δ 8.64 (d, J = 4.5 Hz, 1H), 8.02 (d, J = 2.1 Hz, 1H), 7.84 (dd, J = 8.5, 2.1 Hz, 1H), 7.46 - 7.41 (m, 2H), 7.20 (d, J = 8.6 Hz, 1H), 7.10 (s, 1H), 3.92 - 3.86 (m, 6H), 3.63 - 3.48 (m, 4H), 2.30 - 2.20 (m, 4H), 2.17 (s, 3H), 2.03 - 1.94 (m, 6H), 1.94 - 1.84 (m, 6H). | A | ||
| 152 | 1H NMR (400 MHz, DMSO-d 6) δ 8.67 (d, J = 4.4 Hz, 1H), 7.85 (dd, J = 8.5, 2.1 Hz, 1H), 7.80 (d, J = 2.1 Hz, 1H), 7.41 (d, J = 4.5 Hz, 1H), 7.31 - 7.15 (m, 3H), 7.07 (s, 1H), 6.97 (d, J = 7.9 Hz, 2H), 6.82 (t, J = 7.3 Hz, 1H), 4.05 - 3.92 (m, 2H), 3.91 - 3.78 (m, 8H), 3.28 - 3.21 (m, 2H), 3.21 - 3.11 (m, 2H). | D | ||
| 153 | 1H NMR (400 MHz, DMSO-d 6) δ 8.67 (d, J = 4.5 Hz, 1H), 8.16 - 8.09 (m, 1H), 7.85 (dd, J = 8.5, 2.1 Hz, 1H), 7.79 (d, J = 2.1 Hz, 1H), 7.65 - 7.50 (m, 1H), 7.41 (d, J = 4.5 Hz, 1H), 7.22 (d, J = 8.6 Hz, 1H), 7.07 (s, 1H), 6.87 (d, J = 8.5 Hz, 1H), 6.75 - 6.62 (m, 1H), 4.00 - 3.91 (m, 2H), 3.88 (s, 3H), 3.86 (s, 3H), 3.83 - 3.75 (m, 2H), 3.70 - 3.59 (m, 2H), 3.59 - 3.47 (m, 2H). | D | ||
| 154 | 1H NMR (400 MHz, DMSO-d 6) δ 8.65 (d, J = 4.5 Hz, 1H), 7.85 - 7.72 (m, 2H), 7.42 - 7.30 (m, 5H), 7.30 - 7.24 (m, 1H), 7.19 (d, J = 8.6 Hz, 1H), 7.01 (s, 1H), 3.88 (s, 3H), 3.86 - 3.75 (m, 5H), 3.74 - 3.64 (m, 2H), 3.52 (s, 2H), 2.47 - 2.42 (m, 2H), 2.42 - 2.36 (m, 2H). | D | ||
| 155 | 1H NMR (400 MHz, DMSO-d 6) δ 12.92 (s, 1H), 8.74 - 8.55 (m, 1H), 7.93 - 7.73 (m, 4H), 7.40 (t, J = 3.8 Hz, 1H), 7.33 (dd, J = 7.8, 4.5 Hz, 1H), 7.27 - 7.14 (m, 1H), 7.07 (d, J = 12.2 Hz, 1H), 5.21 (s, 1H), 4.90 (s, 1H), 4.04 (t, J = 5.8 Hz, 1H), 3.93 (t, J = 5.8 Hz, 1H), 3.85 (m, 6H), 3.02 - 2.92 (m, 2H). | D | ||
| 156 | 1H NMR (400 MHz, DMSO-d 6) δ 9.97 (s, 1H), 8.72 (d, J = 4.5 Hz, 1H), 8.20 (t, J = 8.1 Hz, 1H), 7.95 (d, J = 2.0 Hz, 1H), 7.90 (dd, J = 8.4, 2.0 Hz, 1H), 7.86 - 7.82 (m, 1H), 7.78 (dd, J = 11.3, 1.6 Hz, 1H), 7.50 (d, J = 4.5 Hz, 1H), 7.34 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 3.93 - 3.88 (m, 6H). | B | ||
| 157 | 1H NMR (400 MHz, DMSO-d 6) δ 9.97 (s, 1H), 8.72 (d, J = 4.5 Hz, 1H), 8.08 (t, J = 8.0 Hz, 1H), 7.96 (d, J = 2.1 Hz, 1H), 7.91 (dd, J = 8.5, 2.0 Hz, 1H), 7.50 (d, J = 4.5 Hz, 1H), 7.45 (dd, J = 10.9, 1.7 Hz, 1H), 7.36 - 7.31 (m, 2H), 7.21 (d, J = 8.6 Hz, 1H), 3.94 - 3.87 (m, 6H), 3.72 - 3.38 (m, 8H). | B | ||
| 158 | 1H NMR (400 MHz, DMSO-d 6) δ 9.96 (s, 1H), 8.72 (d, J = 4.5 Hz, 1H), 8.07 (t, J = 8.0 Hz, 1H), 7.96 (d, J = 2.1 Hz, 1H), 7.91 (dd, J = 8.5, 2.0 Hz, 1H), 7.50 (d, J = 4.5 Hz, 1H), 7.42 (dd, J = 10.8, 1.7 Hz, 1H), 7.35 - 7.27 (m, 2H), 7.21 (d, J = 8.6 Hz, 1H), 3.92 - 3.87 (m, 6H), 3.72 - 3.39 (m, 4H), 2.44 - 2.27 (m, 4H), 2.22 (s, 3H). | B | ||
| 159 | 1H NMR (400 MHz, DMSO-d 6) δ 10.45 (s, 1H), 8.71 (d, J = 4.5 Hz, 1H), 8.02 (dd, J = 8.5, 2.1 Hz, 1H), 7.97 (d, J = 2.1 Hz, 1H), 7.90 (d, J = 8.5 Hz, 2H), 7.51 (d, J = 4.5 Hz, 1H), 7.43 (d, J = 8.3 Hz, 2H), 7.33 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 3.94 - 3.88 (m, 6H), 3.71 - 3.39 (m, 4H), 2.75 - 2.65 (m, 1H), 2.50 - 2.38 (m, 4H), 1.07 - 0.91 (m, 6H). | C | ||
| 160 | 1H NMR (400 MHz, DMSO-d 6) δ 10.59 (s, 1H), 8.71 (d, J = 4.5 Hz, 1H), 8.10 (s, 1H), 8.02 (d, J = 8.5 Hz, 1H), 7.94 (s, 1H), 7.86 (d, J = 8.3 Hz, 1H), 7.51 (d, J = 4.5 Hz, 1H), 7.41 (d, J = 8.4 Hz, 1H), 7.33 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 3.99 - 3.84 (m, 6H), 3.75 - 3.61 (m, 4H), 3.60 - 3.50 (m, 2H), 3.24 - 3.13 (m, 2H). | B | ||
| 161 | 1H NMR (400 MHz, DMSO-d 6) δ 10.59 (s, 1H), 8.71 (d, J = 4.4 Hz, 1H), 8.10 (s, 1H), 8.02 (d, J = 8.4 Hz, 1H), 7.94 (s, 1H), 7.86 (d, J = 7.9 Hz, 1H), 7.51 (d, J = 4.5 Hz, 1H), 7.38 (d, J = 8.4 Hz, 1H), 7.33 (s, 1H), 7.23 (d, J = 8.6 Hz, 1H), 3.95 - 3.84 (m, 6H), 3.76 - 3.51 (m, 2H), 3.23 - 3.08 (m, 2H), 2.47 - 2.38 (m, 2H), 2.38 - 2.29 (m, 2H), 2.29 - 2.14 (m, 3H). | B | ||
| 162 | 1H NMR (400 MHz, DMSO-d 6) δ 10.72 (s, 1H), 8.70 (d, J = 4.5 Hz, 1H), 8.15 (s, 1H), 8.01 (dd, J = 8.5, 2.1 Hz, 1H), 7.95 - 7.83 (m, 3H), 7.50 (d, J = 4.5 Hz, 1H), 7.34 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 4.30 (t, J = 6.4 Hz, 2H), 3.98 - 3.78 (m, 6H), 3.56 (t, J = 4.5 Hz, 4H), 2.42 (t, J = 7.0 Hz, 2H), 2.40 - 2.28 (m, 4H), 1.91 - 1.78 (m, 2H). | B | ||
| 163 | 1H NMR (400 MHz, DMSO-d 6) δ 10.79 (s, 1H), 8.72 (d, J = 4.4 Hz, 1H), 8.01 (d, J = 8.5 Hz, 1H), 7.98 - 7.85 (m, 3H), 7.77 (d, J = 8.6 Hz, 1H), 7.52 (d, J = 4.4 Hz, 1H), 7.36 (s, 1H), 7.23 (d, J = 8.6 Hz, 1H), 4.31 (t, J = 6.4 Hz, 2H), 3.96 - 3.81 (m, 6H), 3.63 - 3.47 (m, 4H), 2.45 - 2.26 (m, 6H), 1.97 - 1.75 (m, 2H). | B | ||
| 164 | 1H NMR (400 MHz, DMSO-d 6) δ 10.61 (s, 1H), 8.71 (d, J = 4.5 Hz, 1H), 8.08 - 7.90 (m, 6H), 7.51 (d, J = 4.4 Hz, 1H), 7.35 (s, 1H), 7.22 (d, J = 8.5 Hz, 1H), 4.38 (t, J = 5.6 Hz, 2H), 3.99 - 3.83 (m, 6H), 3.65 - 3.49 (m, 4H), 2.70 (t, J = 5.8 Hz, 2H), 2.49 - 2.36 (m, 4H). | C | ||
| 165 | 1H NMR (400 MHz, DMSO-d 6) δ 10.60 (s, 1H), 8.71 (d, J = 4.3 Hz, 1H), 8.11 - 7.83 (m, 6H), 7.51 (d, J = 4.4 Hz, 1H), 7.34 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 4.29 (t, J = 6.3 Hz, 2H), 3.97 - 3.87 (m, 6H), 2.50 - 2.21 (m, 10H), 2.16 (s, 3H), 1.94 - 1.74 (m, 2H). | C | ||
| 166 | 1H NMR (400 MHz, DMSO-d 6) δ 10.49 (s, 1H), 8.71 (d, J = 4.5 Hz, 1H), 8.02 (dd, J = 8.5, 2.1 Hz, 1H), 7.96 (d, J = 2.1 Hz, 1H), 7.91 (d, J = 8.7 Hz, 2H), 7.66 (d, J = 8.7 Hz, 2H), 7.51 (d, J = 4.5 Hz, 1H), 7.33 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 4.41 (s, 2H), 4.12 (d, J = 19.2 Hz, 2H), 3.95 - 3.86 (m, 6H), 3.26 (s, 4H), 2.17 (s, 3H). | C | ||
| 167 | 1H NMR (400 MHz, DMSO-d 6) δ 10.73 - 10.48 (m, 2H), 8.71 (d, J = 4.5 Hz, 1H), 8.02 (dd, J = 8.5, 2.1 Hz, 1H), 7.96 (d, J = 2.1 Hz, 1H), 7.80 (d, J = 8.8 Hz, 1H), 7.63 (d, J = 2.0 Hz, 1H), 7.51 (d, J = 4.5 Hz, 1H), 7.41 (dd, J = 8.8, 2.0 Hz, 1H), 7.34 (s, 1H), 7.23 (d, J = 8.6 Hz, 1H), 3.93 - 3.87 (m, 9H). | B | ||
| 168 | 1H NMR (400 MHz, DMSO-d 6) δ 13.79 (s, 1H), 11.47 (s, 1H), 10.50 (s, 1H), 8.71 (d, J = 4.5 Hz, 1H), 8.02 (dd, J = 8.5, 2.1 Hz, 1H), 7.96 (d, J = 2.1 Hz, 1H), 7.79 (d, J = 8.7 Hz, 1H), 7.58 (d, J = 2.0 Hz, 1H), 7.51 (d, J = 4.5 Hz, 1H), 7.43 - 7.31 (m, 2H), 7.23 (d, J = 8.6 Hz, 1H), 3.93 - 3.87 (m, 6H). | B | ||
| 169 | 1H NMR (400 MHz, DMSO-d 6) δ 10.28 (s, 1H), 10.03 (s, 1H), 8.70 (d, J = 4.5 Hz, 1H), 8.04 - 7.96 (m, 2H), 7.58 (d, J = 1.7 Hz, 1H), 7.50 (d, J = 4.5 Hz, 1H), 7.31 (s, 1H), 7.25 - 7.19 (m, 2H), 7.14 (d, J = 8.3 Hz, 1H), 3.93 - 3.88 (m, 6H), 3.68 - 3.36 (m, 8H). | B | ||
| 170 | 1H NMR (400 MHz, DMSO-d 6) δ 10.27 (s, 1H), 9.97 (s, 1H), 8.70 (d, J = 4.5 Hz, 1H), 8.03 - 7.95 (m, 2H), 7.57 (d, J = 1.8 Hz, 1H), 7.50 (d, J = 4.5 Hz, 1H), 7.31 (s, 1H), 7.22 (d, J = 8.5 Hz, 2H), 7.11 (d, J = 8.3 Hz, 1H), 3.94 - 3.87 (m, 6H), 3.65 - 3.35 (m, 4H), 2.38 - 2.24 (m, 4H), 2.19 (s, 3H). | B | ||
| 171 | 1H NMR (400 MHz, DMSO-d 6) δ 10.38 (s, 1H), 8.70 (d, J = 4.5 Hz, 1H), 8.02 (dd, J = 8.5, 2.0 Hz, 1H), 7.98 - 7.92 (m, 2H), 7.86 (d, J = 8.9 Hz, 2H), 7.50 (d, J = 4.5 Hz, 1H), 7.42 - 7.30 (m, 6H), 7.22 (d, J = 8.6 Hz, 1H), 7.09 (d, J = 8.9 Hz, 2H), 5.12 - 5.07 (m, 2H), 4.20 - 4.14 (m, 1H), 3.94 - 3.87 (m, 6H), 2.30 - 2.14 (m, 1H), 1.03 (d, J = 6.7 Hz, 6H). | C | ||
| 172 | 1H NMR (400 MHz, DMSO-d 6) δ 10.37 (s, 1H), 8.70 (d, J = 4.5 Hz, 1H), 8.02 (dd, J = 8.5, 2.0 Hz, 1H), 7.96 (s, 1H), 7.86 (d, J = 8.9 Hz, 2H), 7.50 (d, J = 4.5 Hz, 1H), 7.31 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 7.13 (d, J = 8.9 Hz, 2H), 3.93 - 3.88 (m, 6H), 3.73 - 3.71 (m, 1H), 2.09 - 1.98 (m, 1H), 1.94 - 1.78 (m, 2H), 1.01 (d, J = 6.8 Hz, 3H), 0.96 (d, J = 6.8 Hz, 3H). | C | ||
| 173 | 1H NMR (400 MHz, DMSO-d 6) δ 10.47 (s, 1H), 8.71 (d, J = 4.4 Hz, 1H), 8.50 - 8.36 (m, 1H), 8.02 (d, J = 8.5 Hz, 1H), 7.99 - 7.77 (m, 5H), 7.51 (d, J = 4.4 Hz, 1H), 7.33 (s, 1H), 7.23 (d, J = 8.6 Hz, 1H), 4.02 - 3.77 (m, 6H), 3.64 - 3.47 (m, 4H), 3.31 - 3.22 (m, 2H), 2.44 - 2.18 (m, 6H), 1.76 - 1.58 (m, 2H). | C | ||
| 174 | 1H NMR (400 MHz, DMSO-d 6) δ 10.65 (s, 1H), 8.71 (d, J = 4.3 Hz, 1H), 8.01 (d, J = 8.4 Hz, 1H), 7.96 (s, 1H), 7.89 (d, J = 12.3 Hz, 1H), 7.72 (d, J = 7.9 Hz, 1H), 7.51 (d, J = 4.2 Hz, 1H), 7.44 (t, J = 8.0 Hz, 1H), 7.34 (s, 1H), 7.23 (d, J = 8.7 Hz, 1H), 3.95 - 3.80 (m, 6H), 3.73 - 3.58 (m, 4H), 3.60 - 3.46 (m, 2H), 3.32 - 3.20 (m, 2H). | B | ||
| 175 | 1H NMR (400 MHz, DMSO-d 6) δ 10.64 (s, 1H), 8.71 (d, J = 4.5 Hz, 1H), 8.01 (d, J = 8.6 Hz, 1H), 7.95 (s, 1H), 7.89 (d, J = 12.4 Hz, 1H), 7.71 (d, J = 8.4 Hz, 1H), 7.51 (d, J = 4.5 Hz, 1H), 7.41 (t, J = 8.2 Hz, 1H), 7.34 (s, 1H), 7.23 (d, J = 8.6 Hz, 1H), 3.96 - 3.86 (m, 6H), 3.74 - 3.55 (m, 2H), 3.31 - 3.22 (m, 2H), 2.47 - 2.39 (m, 2H), 2.39 - 2.30 (m, 2H), 2.26 (s, 3H). | B | ||
| 176 | 1H NMR (400 MHz, DMSO-d 6) δ 11.00 (s, 1H), 9.82 (s, 1H), 8.72 (d, J = 4.3 Hz, 1H), 8.48 (d, J = 8.3 Hz, 1H), 8.00 (s, 1H), 7.73 (d, J = 8.4 Hz, 1H), 7.57 - 7.38 (m, 3H), 7.31 (s, 1H), 7.21 (d, J = 8.4 Hz, 1H), 3.95 - 3.85 (m, 6H), 3.82 (s, 3H). | B | ||
| 177 | 1H NMR (400 MHz, DMSO-d 6) δ 10.47 (s, 1H), 8.70 (d, J = 4.4 Hz, 1H), 8.57 - 8.36 (m, 1H), 8.02 (d, J = 8.3 Hz, 1H), 7.98 - 7.75 (m, 5H), 7.50 (d, J = 4.4 Hz, 1H), 7.33 (s, 1H), 7.22 (d, J = 8.7 Hz, 1H), 3.98 - 3.79 (m, 6H), 3.31 - 3.20 (m, 2H), 2.50 - 2.27 (m, 10H), 2.24 (s, 3H), 1.75 - 1.58 (m, 2H). | C | ||
| 178 | 1H NMR (400 MHz, DMSO-d 6) δ 10.47 (s, 1H), 8.70 (d, J = 4.0 Hz, 1H), 8.40 - 8.32 (m, 1H), 8.10 - 7.70 (m, 6H), 7.51 (d, J = 3.5 Hz, 1H), 7.33 (s, 1H), 7.22 (d, J = 8.5 Hz, 1H), 4.0 - 3.8 (m, 6H), 3.42 - 3.36 (m, 2H), 2.48 - 2.00 (m, 13H). | C | ||
| 179 | 1H NMR (400 MHz, DMSO-d 6) δ 8.65 (d, J = 4.5 Hz, 1H), 7.86 - 7.72 (m, 2H), 7.38 (d, J = 4.5 Hz, 1H), 7.20 (d, J = 8.4 Hz, 1H), 7.00 (s, 1H), 3.88 (s, 3H), 3.85 (s, 3H), 3.81 - 3.71 (m, 2H), 3.71 - 3.59 (m, 2H), 2.77 - 2.60 (m, 1H), 2.46 - 2.39 (m, 2H), 0.97 (d, J = 6.5 Hz, 6H). | D | ||
| 180 | 1H NMR (400 MHz, DMSO-d 6) δ 8.67 (d, J = 4.4 Hz, 1H), 8.21 - 8.07 (m, 1H), 7.88 - 7.69 (m, 2H), 7.45 - 7.32 (m, 1H), 7.26 - 7.13 (m, 1H), 7.09 (d, J = 8.9 Hz, 1H), 4.55 (s, 1H), 4.17 (s, 1H), 4.10 - 3.97 (m, 1H), 3.92 - 3.72 (m, 7H), 3.32 - 3.21 (m, 2H). | D | ||
| 181 | 1H NMR (400 MHz, DMSO-d 6) δ 8.65 (d, J = 4.4 Hz, 1H), 7.87 - 7.69 (m, 2H), 7.44 - 7.32 (m, 1H), 7.18 (t, J = 8.3 Hz, 1H), 6.99 (s, 1H), 4.43 - 4.18 (m, 2H), 3.87 (s, 3H), 3.85 (s, 3H), 3.15 - 2.90 (m, 1H), 2.87 - 2.56 (m, 4H), 2.47 - 2.36 (m, 1H), 1.05 - 0.80 (m, 3H). | D | ||
| 182 | 1H NMR (400 MHz, DMSO-d 6) δ 8.64 (dd, J = 4.4, 2.0 Hz, 1H), 7.85 - 7.70 (m, 2H), 7.37 (dd, J = 11.6, 4.5 Hz, 1H), 7.18 (t, J = 8.4 Hz, 1H), 6.98 (d, J = 20.0 Hz, 1H), 3.90 - 3.83 (m, 6H), 3.68 - 3.59 (m, 1H), 3.59 - 3.52 (m, 1H), 3.51 (s, 1H), 3.40 (s, 1H), 2.85 - 2.70 (m, 2H), 2.27 - 1.95 (m, 1H), 1.06 (s, 3H), 0.93 (s, 3H). | D | ||
| 183 | 1H NMR (400 MHz, DMSO-d 6) δ 8.58 (d, J = 4.5 Hz, 1H), 7.98 - 7.84 (m, 2H), 7.47 - 7.35 (m, 3H), 7.32 (d, J = 4.5 Hz, 1H), 7.06 (d, J = 8.4 Hz, 1H), 6.96 (s, 1H), 6.86 (d, J = 8.6 Hz, 1H), 3.88 (s, 3H), 3.85 - 3.77 (m, 6H), 3.48 (s, 3H). | B | ||
| 184 | 1H NMR (400 MHz, DMSO-d 6) δ 8.65 (d, J = 4.5 Hz, 1H), 7.84 - 7.74 (m, 2H), 7.38 (d, J = 4.5 Hz, 1H), 7.20 (d, J = 8.4 Hz, 1H), 7.01 (s, 1H), 3.88 (s, 3H), 3.85 (s, 3H), 3.78 - 3.70 (m, 2H), 3.69 - 3.58 (m, 2H), 2.65 - 2.57 (m, 2H), 2.55 - 2.52 (m, 2H), 1.71 - 1.57 (m, 1H), 0.48 - 0.40 (m, 2H), 0.37 - 0.28 (m, 2H). | D | ||
| 185 | 1H NMR (400 MHz, DMSO-d 6) δ 8.67 (d, J = 4.4 Hz, 1H), 8.40 (d, J = 4.7 Hz, 2H), 7.88 - 7.81 (m, 1H), 7.79 (s, 1H), 7.40 (d, J = 4.5 Hz, 1H), 7.21 (d, J = 8.5 Hz, 1H), 7.07 (s, 1H), 6.68 (t, J = 4.7 Hz, 1H), 3.97 - 3.90 (m, 2H), 3.89 - 3.81 (m, 8H), 3.81 - 3.69 (m, 4H). | D | ||
| 186 | 1H NMR (400 MHz, DMSO-d 6) δ 8.64 (d, J = 4.4 Hz, 1H), 8.02 (s, 1H), 7.84 (d, J = 8.5 Hz, 1H), 7.53 - 7.39 (m, 2H), 7.20 (d, J = 8.6 Hz, 1H), 7.10 (s, 1H), 3.96 - 3.86 (m, 6H), 3.62 - 3.51 (m, 8H), 2.05 - 1.87 (m, 12H). | A | ||
| 187 | 1H NMR (400 MHz, DMSO-d 6) δ 8.66 (d, J = 3.2 Hz, 1H), 7.90 - 7.75 (m, 2H), 7.39 (d, J = 4.3 Hz, 1H), 7.20 (t, J = 8.3 Hz, 1H), 7.10 (d, J = 3.1 Hz, 1H), 6.73 - 6.53 (m, 1H), 4.33 - 4.11 (m, 2H), 4.09 - 3.99 (m, 1H), 3.94 - 3.80 (m, 6H), 3.80 - 3.64 (m, 2H), 3.61 - 3.39 (m, 4H), 2.48 - 2.33 (m, 4H), 2.31 - 2.20 (m, 3H), 2.13 - 2.01 (m, 1H), 1.96 - 1.83 (m, 1H). | D | ||
| 188 | 1H NMR (400 MHz, DMSO-d 6) δ 8.66 (d, J = 3.0 Hz, 1H), 8.20 - 8.00 (m, 1H), 7.89 - 7.67 (m, 2H), 7.47 - 7.36 (m, 1H), 7.28 - 7.15 (m, 1H), 7.10 (d, J = 5.9 Hz, 1H), 4.36 - 4.22 (m, 1H), 4.21 - 3.98 (m, 2H), 3.84 (s, 6H), 3.80 - 3.54 (m, 2H), 2.80 - 2.67 (m, 2H), 2.11 (d, J = 3.4 Hz, 3H), 2.08 - 1.90 (m, 2H), 1.91 - 1.69 (m, 3H), 1.66 - 1.43 (m, 4H). | D | ||
| 189 | 1H NMR (400 MHz, DMSO-d 6) δ 10.48 (s, 1H), 8.92 (s, 1H), 8.72 (d, J = 4.4 Hz, 1H), 8.49 - 8.27 (m, 2H), 8.03 - 7.82 (m, 2H), 7.51 (d, J = 4.4 Hz, 1H), 7.44 (s, 1H), 7.24 (d, J = 8.6 Hz, 1H), 4.33 (t, J = 6.5 Hz, 2H), 3.99 - 3.81 (m, 6H), 2.49 - 2.18 (m, 10H), 2.13 (s, 3H), 1.95 - 1.81 (m, 2H). | B | ||
| 190 | 1H NMR (400 MHz, DMSO-d 6) δ 10.85 (s, 1H), 9.12 (s, 1H), 8.71 (d, J = 4.4 Hz, 1H), 8.48 (d, J = 8.4 Hz, 1H), 8.12 (d, J = 8.6 Hz, 1H), 8.00 (d, J = 8.4 Hz, 1H), 7.95 (s, 1H), 7.51 (d, J = 4.4 Hz, 1H), 7.37 (s, 1H), 7.23 (d, J = 8.6 Hz, 1H), 3.98 - 3.83 (m, 9H). | B | ||
| 191 | 1H NMR (400 MHz, DMSO-d 6) δ 10.46 (s, 1H), 8.71 (d, J = 4.4 Hz, 1H), 8.03 (d, J = 8.0 Hz, 1H), 7.95 (s, 1H), 7.90 (d, J = 8.5 Hz, 1H), 7.85 - 7.74 (m, 2H), 7.50 (d, J = 4.4 Hz, 1H), 7.33 (s, 1H), 7.23 (d, J = 8.6 Hz, 1H), 3.97 - 3.86 (m, 6H), 3.82 (s, 3H), 2.55 (s, 3H). | B | ||
| 192 | 1H NMR (400 MHz, DMSO-d 6) δ 10.53 (s, 1H), 8.71 (d, J = 4.4 Hz, 1H), 8.10 - 7.86 (m, 2H), 7.83 - 7.64 (m, 2H), 7.64 - 7.40 (m, 2H), 7.33 (s, 1H), 7.22 (d, J = 8.8 Hz, 1H), 3.97 - 3.87 (m, 6H), 3.83 (s, 3H), 3.77 (s, 3H). | B | ||
| 193 | 1H NMR (400 MHz, DMSO-d 6) δ 10.05 (s, 1H), 8.68 (d, J = 4.4 Hz, 1H), 8.02 (d, J = 6.8 Hz, 1H), 7.95 (s, 1H), 7.65 (d, J = 8.8 Hz, 2H), 7.47 (d, J = 4.4 Hz, 1H), 7.26 (s, 1H), 7.21 (d, J = 8.6 Hz, 1H), 6.95 (d, J = 8.8 Hz, 2H), 3.98 - 3.76 (m, 6H), 3.22 - 3.01 (m, 4H), 2.58 - 2.52 (m, 4H), 2.28 (s, 3H). | C | ||
| 194 | 1H NMR (400 MHz, DMSO-d 6) δ 10.06 (s, 1H), 8.68 (d, J = 4.5 Hz, 1H), 8.02 (dd, J = 8.5, 2.0 Hz, 1H), 7.94 (d, J = 2.0 Hz, 1H), 7.66 (d, J = 9.0 Hz, 2H), 7.47 (d, J = 4.5 Hz, 1H), 7.26 (s, 1H), 7.21 (d, J = 8.6 Hz, 1H), 6.96 (d, J = 9.0 Hz, 2H), 3.97 - 3.82 (m, 6H), 3.82 - 3.70 (m, 4H), 3.13 - 2.97 (m, 4H). | C | ||
| 195 | 1H NMR (400 MHz, DMSO-d 6) δ 10.46 (s, 1H), 8.71 (d, J = 4.5 Hz, 1H), 8.02 (dd, J = 8.5, 2.1 Hz, 1H), 7.96 (d, J = 2.1 Hz, 1H), 7.90 (d, J = 8.6 Hz, 2H), 7.50 (d, J = 4.5 Hz, 1H), 7.43 (d, J = 8.5 Hz, 2H), 7.33 (s, 1H), 7.22 (d, J = 8.7 Hz, 1H), 4.35 - 4.07 (m, 1H), 3.96 - 3.87 (m, 6H), 3.69 - 3.42 (m, 1H), 3.08 - 2.58 (m, 3H), 2.34 - 1.91 (m, 5H), 1.14 - 0.86 (m, 3H). | C | ||
| 196 | 1H NMR (400 MHz, DMSO-d 6) δ 8.64 (d, J = 4.5 Hz, 1H), 8.08 (d, J = 7.8 Hz, 1H), 8.00 (d, J = 2.1 Hz, 1H), 7.89 (dd, J = 8.5, 2.2 Hz, 1H), 7.43 (d, J = 4.5 Hz, 1H), 7.20 (d, J = 8.6 Hz, 1H), 7.14 (s, 1H), 4.09 (t, J = 6.5 Hz, 2H), 3.96 - 3.85 (m, 7H), 3.59 - 3.51 (m, 4H), 2.62 - 2.55 (m, 1H), 2.40 - 2.25 (m, 6H), 2.01 - 1.88 (m, 2H), 1.80 - 1.57 (m, 8H). | A | ||
| 197 | 1H NMR (400 MHz, DMSO-d 6) δ 8.64 (d, J = 4.5 Hz, 1H), 8.12 (d, J = 8.2 Hz, 1H), 7.97 (d, J = 2.1 Hz, 1H), 7.90 (dd, J = 8.5, 2.1 Hz, 1H), 7.43 (d, J = 4.5 Hz, 1H), 7.20 (d, J = 8.6 Hz, 1H), 7.13 (s, 1H), 4.06 (t, J = 6.2 Hz, 2H), 3.94 - 3.83 (m, 6H), 3.85 - 3.72 (m, 1H), 3.62 - 3.51 (m, 4H), 2.41 - 2.22 (m, 7H), 2.01 - 1.85 (m, 4H), 1.80 - 1.67 (m, 2H), 1.54 - 1.38 (m, 4H). | A | ||
| 198 | 1H NMR (400 MHz, DMSO-d 6) δ 10.13 (s, 1H), 8.68 (d, J = 4.5 Hz, 1H), 8.02 (dd, J = 8.5, 2.1 Hz, 1H), 7.94 (d, J = 2.1 Hz, 1H), 7.70 (d, J = 9.0 Hz, 2H), 7.48 (d, J = 4.5 Hz, 1H), 7.27 (s, 1H), 7.21 (d, J = 8.6 Hz, 1H), 6.96 (d, J = 9.1 Hz, 2H), 4.08 (t, J = 5.8 Hz, 2H), 3.94 - 3.86 (m, 6H), 3.63 - 3.54 (m, 4H), 2.69 (t, J = 5.8 Hz, 2H), 2.49 - 2.44 (m, 4H). | C | ||
| 199 | 1H NMR (400 MHz, DMSO-d 6) δ 9.08 (s, 1H), 8.65 (d, J = 4.5 Hz, 1H), 7.97 (dd, J = 8.5, 2.1 Hz, 1H), 7.80 (d, J = 2.1 Hz, 1H), 7.42 (d, J = 4.5 Hz, 1H), 7.19 (d, J = 8.6 Hz, 1H), 7.12 (s, 1H), 4.08 (t, J = 6.6 Hz, 2H), 3.90 - 3.85 (m, 6H), 3.61 - 3.51 (m, 4H), 2.40 - 2.26 (m, J = 8.1 Hz, 12H), 1.80 - 1.70 (m, 2H). | B | ||
| 200 | 1H NMR (400 MHz, DMSO-d 6) δ 10.36 (s, 1H), 8.69 (d, J = 4.5 Hz, 1H), 8.02 (dd, J = 8.5, 2.1 Hz, 1H), 7.95 (d, J = 2.1 Hz, 1H), 7.85 (d, J = 8.9 Hz, 2H), 7.49 (d, J = 4.5 Hz, 1H), 7.45 (d, J = 7.6 Hz, 1H), 7.30 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 7.09 (d, J = 8.9 Hz, 2H), 4.10 - 4.01 (m, 1H), 3.94 - 3.85 (m, 6H), 2.23 - 2.14 (m, 1H), 1.42 (s, 9H), 1.01 (d, J = 6.8 Hz, 6H). | C | ||
| 201 | 1H NMR (400 MHz, DMSO-d 6) δ 9.88 (s, 1H), 8.73 (d, J = 4.4 Hz, 1H), 8.54 (d, J = 8.4 Hz, 1H), 7.91 (d, J = 2.1 Hz, 1H), 7.81 (dd, J = 8.4, 2.1 Hz, 1H), 7.69 (dd, J = 8.4, 1.7 Hz, 1H), 7.59 (d, J = 1.7 Hz, 1H), 7.49 (d, J = 4.4 Hz, 1H), 7.31 (s, 1H), 7.26 (d, J = 8.6 Hz, 1H), 3.99 - 3.84 (m, 12H). | B | ||
| 202 | 1H NMR (400 MHz, DMSO-d 6) δ 8.65 (d, J = 4.5 Hz, 1H), 8.13 (d, J = 8.3 Hz, 1H), 7.99 (d, J = 2.1 Hz, 1H), 7.89 (dd, J = 8.5, 2.2 Hz, 1H), 7.70 (t, J = 5.7 Hz, 1H), 7.43 (d, J = 4.5 Hz, 1H), 7.21 (d, J = 8.6 Hz, 1H), 7.13 (s, 1H), 3.92 - 3.86 (m, 6H), 3.83 - 3.72 (m, 1H), 3.59 - 3.52 (m, 4H), 3.20 - 3.12 (m, 2H), 2.40 - 2.28 (m, 6H), 2.12 - 2.02 (m, 1H), 1.92 - 1.84 (m, 2H), 1.82 - 1.73 (m, 2H), 1.53 - 1.37 (m, 4H). | A | ||
| 203 | 1H NMR (400 MHz, DMSO-d 6) δ 8.65 (d, J = 4.5 Hz, 1H), 8.14 (d, J = 8.3 Hz, 1H), 7.99 (d, J = 2.1 Hz, 1H), 7.89 (dd, J = 8.5, 2.1 Hz, 1H), 7.85 - 7.77 (m, 1H), 7.43 (d, J = 4.5 Hz, 1H), 7.20 (d, J = 8.6 Hz, 1H), 7.13 (s, 1H), 3.91 - 3.87 (m, 6H), 3.83 - 3.71 (m, 1H), 3.69 - 3.51 (m, 4H), 3.11 - 3.02 (m, 2H), 2.50 - 2.29 (m, 6H), 2.11 - 2.01 (m, 1H), 1.93 - 1.85 (m, 2H), 1.82 - 1.72 (m, 2H), 1.65 - 1.53 (m, 2H), 1.53 - 1.36 (m, 4H). | A | ||
| 204 | 1H NMR (400 MHz, DMSO-d 6) δ 9.87 (s, 1H), 8.70 (d, J = 4.4 Hz, 1H), 8.12 - 8.00 (m, 2H), 7.95 (d, J = 8.4 Hz, 1H), 7.92 - 7.85 (m, 1H), 7.56 - 7.42 (m, 2H), 7.34 (s, 1H), 7.24 (d, J = 8.6 Hz, 1H), 3.95 - 3.85 (m, 6H), 3.21 - 3.12 (m, 4H), 2.48 - 2.44 (m, 4H), 2.23 (s, 3H). | C | ||
| 205 | 1H NMR (400 MHz, DMSO-d 6) δ 9.90 (s, 1H), 8.70 (d, J = 4.4 Hz, 1H), 8.15 - 8.03 (m, 2H), 7.95 (d, J = 8.5 Hz, 1H), 7.93 - 7.82 (m, 1H), 7.63 - 7.43 (m, 2H), 7.35 (s, 1H), 7.24 (d, J = 8.6 Hz, 1H), 3.99 - 3.82 (m, 6H), 3.80 - 3.67 (m, 4H), 3.20 - 3.07 (m, 4H). | B | ||
| 206 | 1H NMR (400 MHz, DMSO-d 6) δ 8.70 - 8.60 (m, 1H), 7.83 - 7.76 (m, 1H), 7.75 (d, J = 2.1 Hz, 1H), 7.40 - 7.28 (m, 5H), 7.28 - 7.22 (m, 1H), 7.17 (t, J = 8.2 Hz, 1H), 7.00 (d, J = 2.8 Hz, 1H), 4.21 - 3.74 (m, 9H), 3.51 - 3.42 (m, 1H), 3.32 - 3.22 (m, 2H), 3.15 - 3.03 (m, 1H), 2.75 - 2.57 (m, 1H), 2.20 - 2.09 (m, 1H), 1.19 - 0.97 (m, 3H). | D | ||
| 207 | 1H NMR (400 MHz, DMSO-d 6) δ 8.68 - 8.59 (m, 1H), 7.84 - 7.69 (m, 2H), 7.40 - 7.27 (m, 5H), 7.27 - 7.11 (m, 2H), 7.01 (d, J = 7.3 Hz, 1H), 3.93 - 3.76 (m, 6H), 3.76 - 3.55 (m, 3H), 3.54 - 3.41 (m, 3H), 2.44 - 2.35 (m, 2H), 1.15 (s, 3H), 1.01 (s, 3H). | D | ||
| 208 | 1H NMR (400 MHz, DMSO-d 6) δ 8.65 (d, J = 4.4 Hz, 1H), 7.82 - 7.76 (m, 2H), 7.38 - 7.36 (m, 1H), 7.21 - 7.16 (m, 1H), 7.01 (s, 1H), 4.33 - 4.25 (m, 2H), 3.88 (s, 3H), 3.86 (s,3H) 3.09 - 2.95 (m, 1H), 2.84 - 2.66 (m, 2H), 2.20 (s, 3H), 2.15 - 2.01 (m, 2H), 1.07 - 0.90 (m, 3H). | D | ||
| 209 | 1H NMR (400 MHz, DMSO-d 6) δ 8.66 (d, J = 4.1 Hz, 1H), 8.01 - 7.66 (m, 2H), 7.54 - 7.31 (m, 6H), 7.28 - 7.09 (m, 1H), 7.05 (s, 1H), 4.03 - 3.56 (m, 12H), 3.56 - 3.40 (m, 2H). | D | ||
| 210 | 1H NMR (400 MHz, CDCl 3) δ 8.59 - 8.54 (m, 1H), 7.75 - 7.55 (m, 2H), 7.49 - 7.34 (m, 5H), 7.17 (d, J = 7.4 Hz, 1H), 7.07 - 6.96 (m, 2H), 4.98 - 4.47 (m, 3H), 4.05 - 3.79 (m, 7H), 3.54 - 2.83 (m, 3H), 1.38 - 1.14 (m, 3H). | D | ||
| 211 | 1H NMR (400 MHz, DMSO-d 6) δ 8.70 - 8.60 (m, 1H), 7.88 - 7.67 (m, 2H), 7.51 - 7.31 (m, 6H), 7.24 - 7.00 (m, 2H), 4.14 - 3.77 (m, 8H), 3.71 - 3.48 (m, 4H), 1.64 - 1.35 (m, 6H). | D | ||
| 212 | 1H NMR (400 MHz, DMSO-d 6) δ 8.65 (d, J = 4.5 Hz, 1H), 7.82 (dd, J = 8.5, 2.1 Hz, 1H), 7.76 (d, J = 2.1 Hz, 1H), 7.49 - 7.39 (m, 1H), 7.38 (d, J = 4.5 Hz, 1H), 7.18 (d, J = 8.6 Hz, 1H), 7.15 - 7.05 (m, 2H), 7.00 (s, 1H), 3.89 (s, 3H), 3.84 (s, 3H), 3.82 - 3.74 (m, 2H), 3.71 - 3.57 (m, 4H), 2.50 - 2.45 (m, 2H), 2.46 - 2.38 (m, 2H). | D | ||
| 213 | 1H NMR (400 MHz, DMSO-d 6) δ 12.89 - 12.43 (m, 1H), 10.42 (s, 1H), 8.70 (d, J = 4.5 Hz, 1H), 8.02 (d, J = 8.5 Hz, 1H), 7.94 (s, 1H), 7.89 (d, J = 8.6 Hz, 1H), 7.82 - 7.73 (m, 2H), 7.53 - 7.46 (m, 1H), 7.33 (s, 1H), 7.22 (d, J = 8.1 Hz, 1H), 3.96 - 3.85 (m, 6H), 2.55 (s, 3H). | B | ||
| 214 | 1H NMR (400 MHz, DMSO-d 6) δ 10.30 (s, 1H), 8.69 (d, J = 4.4 Hz, 1H), 8.08 - 7.99 (m, 1H), 7.99 - 7.87 (m, 1H), 7.81 - 7.64 (m, 2H), 7.49 (d, J = 4.5 Hz, 1H), 7.30 (s, 1H), 7.21 (t, J = 8.5 Hz, 2H), 3.98 - 3.81 (m, 6H), 3.65 (s, 4H), 3.56 - 3.43 (m, 2H), 3.23 - 3.08 (m, 2H), 2.24 (s, 3H). | B | ||
| 215 | 1H NMR (400 MHz, DMSO-d 6) δ 10.29 (s, 1H), 8.69 (d, J = 4.4 Hz, 1H), 8.02 (d, J = 8.6 Hz, 1H), 7.94 (s, 1H), 7.77 - 7.63 (m, 2H), 7.49 (d, J = 4.4 Hz, 1H), 7.30 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 7.16 (d, J = 8.3 Hz, 1H), 3.99 - 3.82 (m, 6H), 3.74 - 3.53 (m, 2H), 3.20 - 3.08 (m, 2H), 2.41 - 2.29 (m, 2H), 2.26 - 2.13 (m, 8H). | B | ||
| 216 | 1H NMR (400 MHz, DMSO-d 6) δ 10.49 (s, 1H), 8.70 (d, J = 3.7 Hz, 1H), 8.08 - 7.90 (m, 2H), 7.86 - 7.62 (m, 2H), 7.60 - 7.45 (m, 2H), 7.33 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 3.96 - 3.87 (m, 6H), 3.83 (s, 3H). | B | ||
| 217 | 1H NMR (400 MHz, DMSO-d 6) δ 10.39 (s, 1H), 8.70 (d, J = 4.5 Hz, 1H), 8.15 - 7.88 (m, 2H), 7.67 (s, 1H), 7.59 - 7.41 (m, 2H), 7.32 (s, 1H), 7.28 - 7.10 (m, 2H), 4.01 - 3.85 (m, 6H), 3.82 (s, 3H), 3.69 - 3.58 (m, 4H), 3.57 - 3.50 (m, 2H), 3.25 - 3.05 (m, 2H). | B | ||
| 218 | 1H NMR (400 MHz, DMSO-d 6) δ 10.38 (s, 1H), 8.70 (d, J = 4.4 Hz, 1H), 8.07 - 7.87 (m, 2H), 7.66 (s, 1H), 7.50 (d, J = 4.6 Hz, 2H), 7.31 (s, 1H), 7.22 (d, J = 9.2 Hz, 1H), 7.18 (d, J = 8.3 Hz, 1H), 3.93 - 3.88 (m, 6H), 3.80 (s, 3H), 3.73 - 3.45 (m, 2H), 3.25 - 3.03 (m, 2H), 2.37 - 2.14 (m, 7H). | B | ||
| 219 | 1H NMR (400 MHz, DMSO-d 6) δ 10.42 (s, 1H), 8.70 (d, J = 4.5 Hz, 1H), 8.02 (d, J = 8.5 Hz, 1H), 7.95 (s, 1H), 7.88 (d, J = 8.4 Hz, 2H), 7.50 (d, J = 4.5 Hz, 1H), 7.42 (d, J = 8.3 Hz, 2H), 7.32 (s, 1H), 7.22 (d, J = 8.5 Hz, 1H), 3.99 - 3.79 (m, 6H), 3.64 - 3.45 (m, 2H), 2.96 (s, 3H), 2.49 - 2.35 (m, 2H), 2.28 (s, 3H), 2.01 (s, 3H). | C | ||
| 220 | 1H NMR (400 MHz, DMSO-d 6) δ 10.48 (s, 1H), 8.71 (d, J = 4.1 Hz, 1H), 8.63 - 8.44 (m, 1H), 8.02 (d, J = 8.4 Hz, 1H), 7.99 - 7.79 (m, 5H), 7.51 (d, J = 4.3 Hz, 1H), 7.34 (s, 1H), 7.23 (d, J = 8.7 Hz, 1H), 4.00 - 3.79 (m, 6H), 2.87 - 2.66 (m, 2H), 2.59 - 2.52 (m, 8H), 1.91 - 1.67 (m, 2H). | C | ||
| 221 | 1H NMR (400 MHz, DMSO-d 6) δ 10.51 (s, 1H), 9.77 (s, 1H), 8.78 (s, 1H), 8.71 (d, J = 3.5 Hz, 1H), 8.02 (d, J = 8.4 Hz, 1H), 7.98 - 7.79 (m, 4H), 7.51 (d, J = 3.5 Hz, 1H), 7.34 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 3.97 - 3.83 (m, 6H), 3.73 - 3.51 (m, 2H), 3.32 - 3.00 (m, 6H), 1.38 - 0.97 (m, 6H). | C | ||
| 222 | 1H NMR (400 MHz, DMSO-d 6) δ 10.49 (s, 1H), 8.70 (d, J = 4.4 Hz, 1H), 8.66 - 8.52 (m, 1H), 8.07 - 7.99 (m, 1H), 7.99 - 7.82 (m, 5H), 7.51 (d, J = 4.4 Hz, 1H), 7.34 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 3.99 - 3.77 (m, 6H), 3.16 - 2.79 (m, 6H), 1.95 - 1.71 (m, 2H), 1.25 - 1.08 (m, 6H). | C | ||
| 223 | 1H NMR (400 MHz, DMSO-d 6) δ 10.49 (s, 1H), 8.70 (d, J = 4.3 Hz, 1H), 8.67 - 8.54 (m, 1H), 8.02 (d, J = 8.2 Hz, 1H), 7.98 - 7.79 (m, 5H), 7.50 (d, J = 4.2 Hz, 1H), 7.33 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 3.98 - 3.80 (m, 6H), 3.63 - 3.47 (m, 2H), 3.16 - 2.91 (m, 6H), 1.95 - 1.74 (m, 4H). | C | ||
| 224 | 1H NMR (400 MHz, DMSO-d 6) δ 10.49 (s, 1H), 8.70 (d, J = 4.4 Hz, 1H), 8.68 - 8.47 (m, 1H), 8.07 - 8.00 (m, 1H), 8.00 - 7.79 (m, 5H), 7.50 (d, J = 4.5 Hz, 1H), 7.34 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 4.05 - 3.74 (m, 6H), 3.45 - 3.38 (m, 2H), 3.30 - 2.89 (m, 6H), 2.06 - 1.74 (m, 6H). | C | ||
| 225 | 1H NMR (400 MHz, DMSO-d 6) δ 10.59 (s, 1H), 8.70 (d, J = 4.4 Hz, 1H), 8.17 - 7.82 (m, 6H), 7.50 (d, J = 4.5 Hz, 1H), 7.34 (s, 1H), 7.22 (d, J = 8.5 Hz, 1H), 4.36 (t, J = 5.6 Hz, 2H), 4.01 - 3.79 (m, 6H), 2.90 - 2.70 (m, 2H), 2.62 - 2.52 (m, 4H), 1.79 - 1.56 (m, 4H). | C | ||
| 226 | 1H NMR (400 MHz, DMSO-d 6) δ 10.62 (s, 1H), 8.71 (s, 1H), 8.13 - 7.87 (m, 6H), 7.62 - 7.44 (m, 1H), 7.35 (s, 1H), 7.22 (d, J = 8.4 Hz, 1H), 4.38 - 4.23 (m, 2H), 4.01 - 3.74 (m, 6H), 3.20 - 2.70 (m, 6H), 2.13 - 1.96 (m, 2H), 1.92 - 1.67 (m, 4H). | C | ||
| 227 | 1H NMR (400 MHz, DMSO-d 6) δ 10.36 (s, 1H), 8.70 (d, J = 4.5 Hz, 1H), 8.02 (dd, J = 8.5, 2.1 Hz, 1H), 7.95 (d, J = 2.1 Hz, 1H), 7.85 (d, J = 9.0 Hz, 2H), 7.49 (d, J = 4.5 Hz, 1H), 7.42 (t, J = 6.1 Hz, 1H), 7.31 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 7.14 (d, J = 8.9 Hz, 2H), 3.97 (d, J = 6.1 Hz, 2H), 3.94 - 3.87 (m, 6H), 1.42 (s, 9H). | C | ||
| 228 | 1H NMR (400 MHz, DMSO-d 6) δ 10.36 (s, 1H), 8.70 (d, J = 4.3 Hz, 1H), 8.03 (d, J = 8.1 Hz, 1H), 7.95 (s, 1H), 7.85 (d, J = 8.3 Hz, 2H), 7.52 (dd, J = 17.9, 5.6 Hz, 2H), 7.31 (s, 1H), 7.22 (d, J = 8.4 Hz, 1H), 7.11 (d, J = 8.8 Hz, 2H), 4.28 - 4.19 (m, 1H), 3.95 - 3.85 (m, 6H), 1.51 - 1.30 (m, 12H). | C | ||
| 229 | 1H NMR (400 MHz, DMSO-d 6) δ 10.13 (s, 1H), 8.69 (d, J = 4.5 Hz, 1H), 8.03 (dd, J = 8.5, 2.2 Hz, 1H), 7.94 (d, J = 2.1 Hz, 1H), 7.70 (d, J = 9.1 Hz, 2H), 7.48 (d, J = 4.5 Hz, 1H), 7.27 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 6.95 (d, J = 9.1 Hz, 2H), 3.97 (t, J = 6.5 Hz, 2H), 3.92 - 3.88 (m, 6H), 1.75 - 1.65 (m, 2H), 1.49 - 1.40 (m, 2H), 0.95 (t, J = 7.4 Hz, 3H). | C | ||
| 230 | 1H NMR (400 MHz, DMSO-d 6) δ 10.13 (s, 1H), 8.68 (d, J = 4.5 Hz, 1H), 8.03 (d, J = 8.6 Hz, 1H), 7.98 - 7.92 (m, 1H), 7.70 (d, J = 9.0 Hz, 2H), 7.48 (d, J = 4.5 Hz, 1H), 7.27 (s, 1H), 7.21 (d, J = 8.6 Hz, 1H), 6.94 (d, J = 9.0 Hz, 2H), 3.97 - 3.86 (m, 8H), 1.77 - 1.68 (m, 2H), 0.99 (t, J = 7.4 Hz, 3H). | C | ||
| 231 | 1H NMR (400 MHz, DMSO-d 6) δ 12.79 (s, 1H), 8.76 - 8.62 (m, 1H), 8.39 - 8.17 (m, 1H), 7.96 - 7.71 (m, 4H), 7.45 (d, J = 4.5 Hz, 1H), 7.33 - 7.12 (m, 2H), 4.81 - 4.44 (m, 2H), 3.93 - 3.78 (m, 6H), 3.24 (t, J = 8.4 Hz, 2H). | D | ||
| 232 | 1H NMR (400 MHz, DMSO-d 6) δ 12.95 (s, 1H), 8.83 (s, 1H), 8.73 - 8.65 (m, 1H), 7.96 - 7.76 (m, 2H), 7.71 (d, J = 8.2 Hz, 1H), 7.47 - 7.38 (m, 2H), 7.31 - 7.14 (m, 2H), 4.66 (t, J = 8.3 Hz, 2H), 3.90 - 3.84 (m, 6H), 3.26 (t, J = 8.4 Hz, 2H). | D | ||
| 233 | 1H NMR (400 MHz, DMSO-d 6) δ 8.65 (dd, J = 14.3, 4.5 Hz, 1H), 7.86 (m, 2H), 7.61 - 7.51 (m, 1H), 7.50 - 7.35 (m, 2H), 7.26 - 6.90 (m, 3H), 4.00 - 3.90 (m, 2H), 3.84 (m, 8H), 2.88 (t, J = 6.6 Hz, 1H), 2.04 - 1.88 (m, 1H). | D | ||
| 234 | 1H NMR (400 MHz, DMSO-d 6) δ 13.06 (s, 1H), 8.58 (d, J = 4.5 Hz, 1H), 7.99 - 7.85 (m, 2H), 7.44 (d, J = 1.9 Hz, 1H), 7.41 - 7.31 (m, 3H), 7.03 (d, J = 7.7 Hz, 1H), 6.97 (s, 1H), 6.88 (d, J = 8.6 Hz, 1H), 3.88 (s, 3H), 3.83 (s, 3H), 3.48 (s, 3H). | B | ||
| 235 | 1H NMR (400 MHz, DMSO-d 6) δ 8.64 (d, J = 4.5 Hz, 1H), 7.70 - 7.63 (m, 1H), 7.61 - 7.51 (m, 1H), 7.41 (d, J = 4.5 Hz, 1H), 7.30 (s, 1H), 7.23 - 7.08 (m, 2H), 7.08 - 6.97 (m, 2H), 3.94 (t, J = 5.9 Hz, 2H), 3.87 (s, 3H), 3.80 (s, 3H), 3.69 - 3.36 (m, 4H), 2.86 (t, J = 6.5 Hz, 2H), 2.40 - 2.06 (m, 7H), 2.02 - 1.90 (m, 2H). | D | ||
| 236 | 1H NMR (400 MHz, DMSO-d 6) δ 8.64 (d, J = 4.5 Hz, 1H), 7.66 (d, J = 1.9 Hz, 1H), 7.57 (d, J = 8.2 Hz, 1H), 7.41 (d, J = 4.5 Hz, 1H), 7.33 (d, J = 1.6 Hz, 1H), 7.26 - 6.99 (m, 4H), 4.01 - 3.91 (m, 2H), 3.91 - 3.83 (m, 3H), 3.80 (s, 3H), 3.71 - 3.38 (m, 8H), 2.86 (t, J = 6.6 Hz, 2H), 2.04 - 1.88 (m, 2H). | D | ||
| 237 | 1H NMR (400 MHz, DMSO-d 6) δ 8.68 (dd, J = 4.4, 2.0 Hz, 1H), 7.88 (dd, J = 8.5, 2.1 Hz, 1H), 7.79 (dd, J = 15.8, 2.0 Hz, 1H), 7.41 (d, J = 4.4 Hz, 1H), 7.34 - 7.12 (m, 4H), 7.07 (d, J = 11.9 Hz, 1H), 5.14 (s, 1H), 4.87 (s, 1H), 4.04 (t, J = 5.7 Hz, 1H), 3.96 - 3.78 (m, 7H), 3.69 - 3.51 (m, 2H), 3.49 - 3.36 (m, 2H), 3.01 - 2.87 (m, 2H), 2.43 - 2.10 (m, 7H). | D | ||
| 238 | 1H NMR (400 MHz, DMSO-d 6) δ 8.68 (d, J = 4.4 Hz, 1H), 7.88 (dd, J = 8.5, 2.1 Hz, 1H), 7.79 (dd, J = 15.4, 2.0 Hz, 1H), 7.41 (d, J = 4.4 Hz, 1H), 7.38 - 7.13 (m, 4H), 7.07 (d, J = 10.7 Hz, 1H), 5.14 (s, 1H), 4.88 (s, 1H), 4.04 (t, J = 5.8 Hz, 1H), 3.98 - 3.72 (m, 7H), 3.72 - 3.35 (m, 8H), 3.02 - 2.85 (m, 2H). | D | ||
| 239 | 1H NMR (400 MHz, DMSO-d 6) δ 10.79 (s, 1H), 9.47 (dd, J = 2.2, 0.8 Hz, 1H), 9.11 (d, J = 2.2 Hz, 1H), 8.08 - 8.02 (m, 2H), 8.02 - 7.97 (m, 2H), 7.50 - 7.41 (m, 2H), 7.33 (d, J = 0.7 Hz, 1H), 7.13 (d, J = 8.4 Hz, 1H), 3.90 (s, 3H), 3.88 - 3.83 (m, 6H). | G | ||
| 240 | 1H NMR (400 MHz, DMSO-d 6) δ 8.65 (d, J = 4.5 Hz, 1H), 7.97 (d, J = 2.1 Hz, 1H), 7.92 (dd, J = 8.5, 2.2 Hz, 1H), 7.87 (d, J = 7.4 Hz, 1H), 7.44 (d, J = 4.5 Hz, 1H), 7.24 (d, J = 8.6 Hz, 1H), 7.16 (s, 1H), 4.10 - 4.02 (m, 1H), 3.90 (s, 3H), 3.88 (s, 3H), 3.52 - 3.42 (m, 4H), 2.79 - 2.71 (m, 1H), 2.35 - 2.21 (m, 4H), 2.19 (s, 3H), 1.92 - 1.81 (m, 2H), 1.73 - 1.63 (m, 4H), 1.61 - 1.50 (m, 2H). | A | ||
| 241 | 1H NMR (400 MHz, DMSO-d 6) δ 8.65 (d, J = 4.5 Hz, 1H), 8.06 (d, J = 8.1 Hz, 1H), 7.97 (d, J = 2.1 Hz, 1H), 7.89 (dd, J = 8.5, 2.1 Hz, 1H), 7.43 (d, J = 4.5 Hz, 1H), 7.20 (d, J = 8.6 Hz, 1H), 7.13 (s, 1H), 3.92 - 3.86 (m, 6H), 3.84 - 3.72 (m, 1H), 3.52 - 3.42 (m, 4H), 2.62 - 2.53 (m, 1H), 2.34 - 2.21 (m, 4H), 2.19 (s, 3H), 1.95 - 1.86 (m, 2H), 1.77 - 1.65 (m, 2H), 1.54 - 1.42 (m, 4H). | A | ||
| 242 | 1H NMR (400 MHz, DMSO-d 6) δ 10.47 (s, 1H), 8.93-8.90 (m, 1H), 8.73 (d, J = 4.5 Hz, 1H), 8.41-8.38 (m, 2H), 7.97-7.93 (m, 2H), 7.51 (d, J = 4.5 Hz, 1H), 7.45 (s, 1H), 7.24 (d, J = 8.5 Hz, 1H), 4.42 (t, J = 5.7 Hz, 2H), 3.94-3.88 (m, 6H), 3.57 (t, J = 4.6 Hz, 4H), 2.71 (t, J = 5.7 Hz, 2H), 2.49-2.45 (m, 4H). | B | ||
| 243 | 1H NMR (400 MHz, DMSO-d 6) δ 10.21 (s, 1H), 8.69 (d, J = 4.4 Hz, 1H), 8.01 (d, J = 8.4 Hz, 1H), 7.95 (s, 1H), 7.75 (d, J = 8.2 Hz, 2H), 7.48 (d, J = 4.4 Hz, 1H), 7.37 - 7.25 (m, 3H), 7.21 (d, J = 8.5 Hz, 1H), 4.00 - 3.79 (m, 6H), 3.43 (s, 2H), 2.49 - 2.21 (m, 8H), 2.18 (s, 3H). | B | ||
| 244 | 1H NMR (400 MHz, DMSO-d 6) δ 10.22 (s, 1H), 8.69 (d, J = 4.4 Hz, 1H), 8.01 (d, J = 8.7 Hz, 1H), 7.95 (s, 1H), 7.76 (d, J = 8.2 Hz, 2H), 7.48 (d, J = 4.2 Hz, 1H), 7.39 - 7.24 (m, 3H), 7.21 (d, J = 8.6 Hz, 1H), 4.02 - 3.78 (m, 6H), 3.66 - 3.51 (m, 4H), 3.50 - 3.42 (m, 2H), 2.43 - 2.20 (m, 4H). | B | ||
| 245 | 1H NMR (400 MHz, DMSO-d 6) δ 8.89 - 8.76 (m, 1H), 8.64 (d, J = 4.3 Hz, 1H), 7.92 (d, J = 8.1 Hz, 1H), 7.85 (s, 1H), 7.41 (d, J = 4.2 Hz, 1H), 7.27 - 7.07 (m, 4H), 6.88 (d, J = 8.2 Hz, 2H), 4.40 (d, J = 5.7 Hz, 2H), 3.91 - 3.80 (m, 6H), 3.15 - 2.98 (m, 4H), 2.45 - 2.37 (m, 4H), 2.20 (s, 3H). | B | ||
| 246 | 1H NMR (400 MHz, DMSO-d 6) δ 8.92 - 8.77 (m, 1H), 8.64 (d, J = 4.3 Hz, 1H), 7.92 (d, J = 7.6 Hz, 1H), 7.85 (s, 1H), 7.41 (d, J = 4.4 Hz, 1H), 7.33 - 7.06 (m, 4H), 6.89 (d, J = 8.4 Hz, 2H), 4.41 (d, J = 5.9 Hz, 2H), 3.89 - 3.82 (m, 6H), 3.80 - 3.67 (m, 4H), 3.17 - 2.98 (m, 4H). | B | ||
| 247 | 1H NMR (400 MHz, DMSO-d 6) δ 8.64 (d, J = 4.5 Hz, 1H), 8.57 - 8.52 (m, 1H), 8.05 (d, J = 7.8 Hz, 1H), 7.98 (d, J = 2.1 Hz, 1H), 7.89 (dd, J = 8.5, 2.2 Hz, 1H), 7.86 - 7.79 (m, 1H), 7.45 - 7.39 (m, 2H), 7.35 - 7.29 (m, 1H), 7.19 (d, J = 8.6 Hz, 1H), 7.14 (s, 1H), 5.20 (s, 2H), 3.99 - 3.91 (m, 1H), 3.88 (s, 3H), 3.86 (s, 3H), 2.76 - 2.69 (m, 1H), 2.06 - 1.96 (m, 2H), 1.77 - 1.60 (m, 6H). | A | ||
| 248 | 1H NMR (400 MHz, DMSO-d 6) δ 8.58 (d, J = 4.5 Hz, 1H), 7.50 (s, 1H), 7.43 - 7.23 (m, 6H), 7.12 (d, J = 8.7 Hz, 1H), 6.91 (s, 1H), 3.89 (s, 3H), 3.84 (s, 3H), 3.68 - 3.42 (m, 5H), 3.25 - 3.07 (m, 2H), 2.42 - 1.97 (m, 7H). | B | ||
| 249 | 1H NMR (400 MHz, DMSO-d 6) δ 8.58 (d, J = 4.4 Hz, 1H), 7.50 - 7.27 (m, 7H), 7.12 (d, J = 8.8 Hz, 1H), 6.91 (s, 1H), 3.90 (s, 3H), 3.84 (s, 3H), 3.75 - 3.34 (m, 9H), 3.30 - 3.00 (m, 2H). | B | ||
| 250 | 1H NMR (400 MHz, DMSO-d 6) δ 8.70 (d, J = 4.5 Hz, 1H), 8.33 - 8.15 (m, 1H), 7.93 - 7.74 (m, 2H), 7.44 (d, J = 4.5 Hz, 1H), 7.38 - 7.32 (m, 1H), 7.32 - 7.14 (m, 3H), 4.73 - 4.55 (m, 2H), 3.95 - 3.77 (m, 6H), 3.62 - 3.36 (m, 4H), 3.23 (t, J = 8.6 Hz, 2H), 2.43 - 2.24 (m, 4H), 2.21 (s, 3H). | D | ||
| 251 | 1H NMR (400 MHz, DMSO-d 6) δ 8.70 (d, J = 4.4 Hz, 1H), 8.33 - 8.19 (m, 1H), 7.96 - 7.70 (m, 2H), 7.44 (d, J = 4.4 Hz, 1H), 7.40 - 7.14 (m, 4H), 4.73 - 4.55 (m, 2H), 4.02 - 3.72 (m, 6H), 3.70 - 3.40 (m, 8H), 3.23 (t, J = 8.6 Hz, 2H). | D | ||
| 252 | 1H NMR (400 MHz, DMSO-d 6) δ 8.70 (d, J = 4.4 Hz, 1H), 8.26 (s, 1H), 7.92 - 7.73 (m, 2H), 7.44 (d, J = 4.4 Hz, 1H), 7.38 (d, J = 7.5 Hz, 1H), 7.31 - 7.18 (m, 2H), 7.11 (d, J = 8.0 Hz, 1H), 4.73 - 4.53 (m, 2H), 4.01 - 3.74 (m, 6H), 3.72 - 3.35 (m, 4H), 3.26 - 3.18 (m, 2H), 2.44 - 2.26 (m, 4H), 2.22 (s, 3H). | D | ||
| 253 | 1H NMR (400 MHz, DMSO-d 6) δ 8.70 (d, J = 4.5 Hz, 1H), 8.28 (s, 1H), 7.94 - 7.74 (m, 2H), 7.44 (d, J = 4.4 Hz, 1H), 7.38 (d, J = 7.6 Hz, 1H), 7.31 - 7.17 (m, 2H), 7.14 (d, J = 7.8 Hz, 1H), 4.74 - 4.50 (m, 2H), 3.96 - 3.76 (m, 6H), 3.77 - 3.39 (m, 8H), 3.26 - 3.18 (m, 2H). | D | ||
| 254 | 1H NMR (400 MHz, DMSO-d 6) δ 10.26 (s, 1H), 9.45 - 9.42 (m, 1H), 9.08 (d, J = 2.3 Hz, 1H), 7.75 (d, J = 9.0 Hz, 2H), 7.46 (d, J = 2.1 Hz, 1H), 7.43 (dd, J = 8.3, 2.2 Hz, 1H), 7.25 (s, 1H), 7.13 (d, J = 8.4 Hz, 1H), 6.94 (d, J = 9.1 Hz, 2H), 4.03 (q, J = 7.0 Hz, 2H), 3.90 (s, 3H), 3.84 (s, 3H), 1.34 (t, J = 7.0 Hz, 3H). | G | ||
| 255 | 1H NMR (400 MHz, DMSO-d 6) δ 8.64 (d, J = 4.5 Hz, 1H), 8.01 (d, J = 2.1 Hz, 1H), 7.85 (dd, J = 8.5, 2.2 Hz, 1H), 7.46 - 7.40 (m, 2H), 7.20 (d, J = 8.6 Hz, 1H), 7.10 (s, 1H), 4.04 (t, J = 6.4 Hz, 2H), 3.91 - 3.86 (m, 6H), 3.59 - 3.54 (m, 4H), 2.38 - 2.30 (m, 6H), 2.04 - 1.96 (m, 6H), 1.90 - 1.80 (m, 6H), 1.76 - 1.69 (m, 2H). | A | ||
| 256 | 1H NMR (400 MHz, DMSO-d 6) δ 10.11 (s, 1H), 9.31 (s, 1H), 8.68 (d, J = 4.5 Hz, 1H), 8.02 (dd, J = 8.5, 2.0 Hz, 1H), 7.94 (d, J = 2.0 Hz, 1H), 7.68 (d, J = 9.0 Hz, 2H), 7.49 - 7.41 (m, 3H), 7.27 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 3.94 - 3.87 (m, 6H), 1.49 (s, 9H). | C | ||
| 257 | 1H NMR (400 MHz, DMSO-d 6) δ 9.81 (s, 1H), 8.67 (d, J = 4.5 Hz, 1H), 8.03 (dd, J = 8.5, 2.1 Hz, 1H), 7.92 (d, J = 2.1 Hz, 1H), 7.46 (d, J = 4.5 Hz, 1H), 7.41 (d, J = 8.7 Hz, 2H), 7.24 - 7.19 (m, 2H), 6.57 (d, J = 8.7 Hz, 2H), 4.97 (s, 2H), 3.93 - 3.87 (m, 6H). | C | ||
| 258 | 1H NMR (400 MHz, DMSO-d 6) δ 10.18 (s, 1H), 9.75 (s, 1H), 8.69 (d, J = 4.5 Hz, 1H), 8.02 (dd, J = 8.5, 2.1 Hz, 1H), 7.95 (d, J = 2.1 Hz, 1H), 7.74 (d, J = 9.0 Hz, 2H), 7.65 (d, J = 9.0 Hz, 2H), 7.48 (d, J = 4.5 Hz, 1H), 7.28 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 3.93 - 3.88 (m, 6H), 3.13 (s, 2H), 2.33 (s, 6H). | C | ||
| 259 | 1H NMR (400 MHz, DMSO-d 6) δ 8.74 - 8.58 (m, 1H), 7.93 - 7.63 (m, 2H), 7.48 - 7.31 (m, 1H), 7.28 - 7.00 (m, 2H), 4.94 - 4.15 (m, 3H), 3.95 - 3.70 (m, 6H), 3.65 - 3.36 (m, 2H), 3.29 - 3.14 (m, 1H), 3.08 - 2.89 (m, 1H), 1.33 - 0.97 (m, 3H). | D | ||
| 260 | 1H NMR (400 MHz, DMSO-d 6) δ 8.73 - 8.57 (m, 1H), 7.92 - 7.65 (m, 2H), 7.62 - 7.29 (m, 5H), 7.27 - 6.97 (m, 2H), 5.00 - 4.16 (m, 3H), 3.99 - 3.67 (m, 6H), 3.61 - 3.36 (m, 1H), 3.28 - 2.91 (m, 3H), 1.37 - 0.89 (m, 3H). | D | ||
| 261 | 1H NMR (400 MHz, DMSO-d 6) δ 8.67 (d, J = 4.3 Hz, 1H), 7.91 - 7.64 (m, 2H), 7.60 - 7.43 (m, 3H), 7.43 - 7.28 (m, 2H), 7.27 - 7.13 (m, 1H), 7.06 (d, J = 22.4 Hz, 1H), 4.67 - 4.15 (m, 3H), 3.97 - 3.69 (m, 6H), 3.59 - 3.36 (m, 1H), 3.30 - 2.90 (m, 3H), 1.37 - 0.99 (m, 3H). | D | ||
| 262 | 1H NMR (400 MHz, DMSO-d 6) δ 8.66 (s, 1H), 7.88 - 7.67 (m, 2H), 7.59 - 7.29 (m, 5H), 7.25 - 7.13 (m, 1H), 7.06 (d, J = 23.0 Hz, 1H), 4.66 - 4.15 (m, 3H), 3.95 - 3.67 (m, 6H), 3.58 - 3.40 (m, 1H), 3.28 - 2.89 (m, 3H), 1.28 - 1.00 (m, 3H). | D | ||
| 263 | 1H NMR (400 MHz, DMSO-d 6) δ 8.66 (d, J = 4.2 Hz, 1H), 7.74 (d, J = 24.2 Hz, 2H), 7.51 (dd, J = 13.6, 7.9 Hz, 1H), 7.45 - 7.11 (m, 5H), 7.05 (d, J = 22.9 Hz, 1H), 4.43 (m, 3H), 3.84 (m, 6H), 3.60 - 2.91 (m, 4H), 1.15 (m, 3H). | D | ||
| 264 | 1H NMR (400 MHz, DMSO-d 6) δ 10.70 (s, 1H), 9.01 (s, 1H), 8.85 - 8.61 (m, 1H), 8.37 (d, J = 8.1 Hz, 1H), 8.00 (d, J = 8.7 Hz, 1H), 7.94 (s, 1H), 7.69 (d, J = 8.7 Hz, 1H), 7.58 - 7.42 (m, 1H), 7.35 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 4.00 - 3.79 (m, 6H), 3.74 - 3.62 (m, 4H), 3.62 - 3.51 (m, 4H). | C | ||
| 265 | 1H NMR (400 MHz, DMSO-d 6) δ 10.69 (s, 1H), 9.00 (s, 1H), 8.71 (d, J = 3.7 Hz, 1H), 8.36 (d, J = 8.3 Hz, 1H), 8.00 (d, J = 8.4 Hz, 1H), 7.94 (s, 1H), 7.64 (d, J = 8.9 Hz, 1H), 7.50 (d, J = 4.4 Hz, 1H), 7.34 (s, 1H), 7.22 (d, J = 8.3 Hz, 1H), 4.00 - 3.72 (m, 6H), 3.73 - 3.56 (m, 2H), 3.55 - 3.42 (m, 2H), 2.43 - 2.34 (m, 2H), 2.34 - 2.24 (m, 2H), 2.20 (s, 3H). | C | ||
| 266 | 1H NMR (400 MHz, DMSO-d 6) δ 10.01 (s, 1H), 8.67 (d, J = 4.4 Hz, 1H), 8.01 (d, J = 8.5 Hz, 1H), 7.95 (s, 1H), 7.64 (d, J = 8.8 Hz, 2H), 7.46 (d, J = 4.4 Hz, 1H), 7.25 (s, 1H), 7.21 (d, J = 8.6 Hz, 1H), 6.94 (d, J = 8.8 Hz, 2H), 4.06 - 3.72 (m, 6H), 3.22 - 2.99 (m, 4H), 2.84 - 2.54 (m, 5H), 1.18 - 0.86 (m, 6H). | B | ||
| 268 | 1H NMR (400 MHz, DMSO-d 6) δ 10.40 (s, 1H), 8.70 (d, J = 4.5 Hz, 1H), 8.02 (dd, J = 8.5, 2.1 Hz, 1H), 7.95 (d, J = 2.1 Hz, 1H), 7.82 (d, J = 8.9 Hz, 2H), 7.57 (d, J = 8.9 Hz, 2H), 7.49 (d, J = 4.5 Hz, 1H), 7.30 (s, 1H), 7.21 (d, J = 8.6 Hz, 1H), 3.98 - 3.70 (m, 6H). | B | ||
| 269 | 1H NMR (400 MHz, DMSO-d 6) δ 10.02 (s, 1H), 8.68 (d, J = 4.5 Hz, 1H), 8.08 - 7.99 (m, 1H), 7.94 (s, 1H), 7.62 (d, J = 8.8 Hz, 2H), 7.47 (d, J = 4.4 Hz, 1H), 7.25 (s, 1H), 7.21 (d, J = 8.6 Hz, 1H), 6.94 (d, J = 9.0 Hz, 2H), 4.00 - 3.79 (m, 6H), 3.19 - 3.01 (m, 4H), 1.73 - 1.57 (m, 4H), 1.57 - 1.44 (m, 2H). | B | ||
| 270 | 1H NMR (400 MHz, DMSO-d 6) δ 10.05 (s, 1H), 8.68 (d, J = 4.4 Hz, 1H), 8.01 (d, J = 7.2 Hz, 1H), 7.95 (s, 1H), 7.65 (d, J = 8.8 Hz, 2H), 7.47 (d, J = 4.2 Hz, 1H), 7.26 (s, 1H), 7.21 (d, J = 8.3 Hz, 1H), 6.95 (d, J = 8.8 Hz, 2H), 4.01 - 3.76 (m, 6H), 3.25 - 3.03 (m, 4H), 2.49 - 2.32 (m, 4H), 1.18 - 0.93 (m, 3H). | B | ||
| 271 | 1H NMR (400 MHz, DMSO-d 6) δ 10.07 (s, 1H), 8.68 (d, J = 4.4 Hz, 1H), 8.09 - 7.98 (m, 1H), 7.98 - 7.88 (m, 1H), 7.66 (d, J = 8.9 Hz, 2H), 7.47 (d, J = 4.4 Hz, 1H), 7.26 (s, 1H), 7.21 (d, J = 8.6 Hz, 1H), 6.98 (d, J = 9.0 Hz, 2H), 4.00 - 3.82 (m, 6H), 3.55 - 3.43 (m, 4H), 3.15 - 2.96 (m, 4H), 1.42 (s, 9H). | B | ||
| 272 | 1H NMR (400 MHz, DMSO-d 6) δ 9.92 (s, 1H), 8.70 (d, J = 4.2 Hz, 1H), 8.23 - 8.04 (m, 2H), 7.95 (d, J = 8.0 Hz, 1H), 7.91 (s, 1H), 7.61 - 7.51 (m, 1H), 7.48 (d, J = 4.4 Hz, 1H), 7.35 (s, 1H), 7.23 (d, J = 8.4 Hz, 1H), 3.91 (s, 6H), 3.54 - 3.43 (m, 4H), 3.19 - 3.03 (m, 4H), 1.43 (s, 9H). | B | ||
| 273 | 1H NMR (400 MHz, DMSO-d 6) δ 10.04 (s, 1H), 8.68 (d, J = 4.3 Hz, 1H), 8.03 (d, J = 7.4 Hz, 1H), 7.95 (s, 1H), 7.65 (d, J = 8.6 Hz, 2H), 7.48 (d, J = 3.9 Hz, 1H), 7.26 (s, 1H), 7.22 (d, J = 8.4 Hz, 1H), 6.96 (d, J = 8.8 Hz, 2H), 5.96 - 5.69 (m, 2H), 4.01 - 3.79 (m, 6H), 3.74 - 3.55 (m, 2H), 3.33 - 3.29 (m, 2H), 2.31 - 2.14 (m, 2H). | B | ||
| 274 | 1H NMR (400 MHz, DMSO-d 6) δ 10.05 (s, 1H), 8.68 (d, J = 4.4 Hz, 1H), 8.11 - 8.00 (m, 1H), 7.99 - 7.91 (m, 1H), 7.64 (d, J = 8.9 Hz, 2H), 7.48 (d, J = 4.4 Hz, 1H), 7.26 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 6.98 (d, J = 9.0 Hz, 2H), 4.07 - 3.73 (m, 10H), 3.31 - 3.16 (m, 4H), 1.86 - 1.65 (m, 4H). | B | ||
| 275 | 1H NMR (400 MHz, DMSO-d 6) δ 10.61 (s, 1H), 8.71 (d, J = 4.5 Hz, 1H), 8.15 - 7.81 (m, 6H), 7.51 (d, J = 4.5 Hz, 1H), 7.35 (s, 1H), 7.23 (d, J = 8.6 Hz, 1H), 4.49 - 4.25 (m, 2H), 4.01 - 3.76 (m, 6H), 3.33 - 3.26 (m, 4H), 2.72 (t, J = 5.5 Hz, 2H), 2.49 - 2.39 (m, 4H), 1.40 (s, 9H). | C | ||
| 276 | 1H NMR (400 MHz, DMSO-d 6) δ 9.98 (s, 1H), 8.68 (d, J = 4.3 Hz, 1H), 8.03 (d, J = 8.5 Hz, 1H), 7.95 (s, 1H), 7.61 (d, J = 8.4 Hz, 2H), 7.47 (d, J = 4.0 Hz, 1H), 7.25 (s, 1H), 7.22 (d, J = 8.7 Hz, 1H), 6.75 (d, J = 8.3 Hz, 2H), 3.99 - 3.81 (m, 6H), 2.89 (s, 6H). | C | ||
| 277 | 1H NMR (400 MHz, DMSO-d 6) δ 9.94 (s, 1H), 8.68 (d, J = 4.4 Hz, 1H), 8.03 (d, J = 6.6 Hz, 1H), 7.94 (s, 1H), 7.58 (d, J = 8.8 Hz, 2H), 7.47 (d, J = 4.5 Hz, 1H), 7.33 - 7.10 (m, 2H), 6.55 (d, J = 8.9 Hz, 2H), 3.97 - 3.75 (m, 6H), 3.29 - 3.13 (m, 4H), 2.06 - 1.87 (m, 4H). | B | ||
| 278 | 1H NMR (400 MHz, DMSO-d 6) δ 10.54 (s, 1H), 8.70 (d, J = 4.3 Hz, 1H), 8.07 - 7.98 (m, 1H), 7.98 - 7.90 (m, 1H), 7.86 - 7.69 (m, 2H), 7.60 (d, J = 8.4 Hz, 1H), 7.49 (d, J = 4.4 Hz, 1H), 7.32 (s, 1H), 7.22 (d, J = 8.5 Hz, 1H), 3.99 - 3.78 (m, 6H). | B | ||
| 279 | 1H NMR (400 MHz, DMSO-d 6) δ 10.58 (s, 1H), 8.71 (d, J = 4.4 Hz, 1H), 8.07 (s, 1H), 8.03 (d, J = 8.7 Hz, 1H), 7.94 (s, 1H), 7.89 - 7.70 (m, 2H), 7.50 (d, J = 4.4 Hz, 1H), 7.34 (s, 1H), 7.23 (d, J = 8.6 Hz, 1H), 3.98 - 3.81 (m, 6H). | B | ||
| 280 | 1H NMR (400 MHz, DMSO-d 6) δ 10.21 (s, 1H), 9.95 (s, 1H), 8.69 (d, J = 4.5 Hz, 1H), 8.03 (dd, J = 8.5, 2.1 Hz, 1H), 7.94 (d, J = 2.1 Hz, 1H), 7.74 (d, J = 8.9 Hz, 2H), 7.59 (d, J = 9.0 Hz, 2H), 7.49 (d, J = 4.5 Hz, 1H), 7.29 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 7.07 (t, J = 6.2 Hz, 1H), 3.93 - 3.87 (m, 6H), 3.72 (d, J = 6.1 Hz, 2H), 1.41 (s, 9H). | C | ||
| 281 | 1H NMR (400 MHz, DMSO-d 6) δ 10.20 (s, 1H), 9.94 (s, 1H), 8.69 (d, J = 4.5 Hz, 1H), 8.03 (dd, J = 8.5, 2.0 Hz, 1H), 7.94 (d, J = 2.0 Hz, 1H), 7.74 (d, J = 8.9 Hz, 2H), 7.60 (d, J = 8.9 Hz, 2H), 7.49 (d, J = 4.5 Hz, 1H), 7.29 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 7.07 (d, J = 7.5 Hz, 1H), 4.16 - 4.07 (m, 1H), 3.93 - 3.88 (m, 6H), 1.40 (s, 9H), 1.27 (d, J = 7.0 Hz, 3H). | C | ||
| 282 | 1H NMR (400 MHz, DMSO-d 6) δ 10.18 (s, 1H), 9.97 (s, 1H), 8.69 (d, J = 4.5 Hz, 1H), 8.02 (dd, J = 8.5, 2.1 Hz, 1H), 7.95 (d, J = 2.1 Hz, 1H), 7.74 (d, J = 9.0 Hz, 2H), 7.60 (d, J = 9.0 Hz, 2H), 7.48 (d, J = 4.5 Hz, 1H), 7.29 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 6.85 (d, J = 8.7 Hz, 1H), 3.98 - 3.85 (m, 7H), 2.05 - 1.94 (m, 1H), 1.40 (s, 9H), 0.91 (d, J = 6.6 Hz, 6H). | C | ||
| 283 | 1H NMR (400 MHz, DMSO-d 6) δ 10.17 (s, 1H), 8.69 (d, J = 4.5 Hz, 1H), 8.03 (dd, J = 8.5, 2.1 Hz, 1H), 7.94 (d, J = 2.1 Hz, 1H), 7.74 (d, J = 9.0 Hz, 2H), 7.64 (d, J = 9.0 Hz, 2H), 7.48 (d, J = 4.4 Hz, 1H), 7.28 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 3.92 - 3.89 (m, 6H), 3.29 -3.27 (m, 2H). | C | ||
| 284 | 1H NMR (400 MHz, DMSO-d 6) δ 10.16 (s, 1H), 8.68 (d, J = 4.5 Hz, 1H), 8.02 (dd, J = 8.5, 2.1 Hz, 1H), 7.93 (d, J = 2.1 Hz, 1H), 7.73 (d, J = 9.0 Hz, 2H), 7.64 (d, J = 9.0 Hz, 2H), 7.47 (d, J = 4.5 Hz, 1H), 7.27 (s, 1H), 7.21 (d, J = 8.6 Hz, 1H), 3.92 - 3.88 (m, 6H), 3.42 (q, J = 6.9 Hz, 1H), 1.22 (d, J = 6.9 Hz, 3H). | C | ||
| 285 | 1H NMR (400 MHz, DMSO-d 6) δ 10.04 (s, 1H), 8.68 (d, J = 4.9 Hz, 1H), 8.02 (dd, J = 8.5, 2.1 Hz, 1H), 7.96-7.95 (m, 1H), 7.68 (d, J = 9.0 Hz, 2H), 7.47 (d, J = 4.9 Hz, 1H), 7.26 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 7.06 (d, J = 9.1 Hz, 2H), 3.92 - 3.88 (m, 6H), 3.59 (t, J = 6.0 Hz, 4H), 2.44 (t, J = 6.0 Hz, 4H). | B | ||
| 286 | 1H NMR (400 MHz, DMSO-d 6) δ 9.90 (s, 1H), 8.71 (d, J = 4.5 Hz, 1H), 8.15-8.12 (m, 2H), 7.96-7.93 (m, 2H), 7.57 (dd, J = 9.0, 3.0 Hz, 1H), 7.48 (d, J = 4.5 Hz, 1H), 7.36 (s, 1H), 7.24 (d, J = 8.2 Hz, 1H), 3.94 - 3.89 (m, 6H), 3.38-3.36 (m, 4H), 3.24-3.22 (m, 4H). | B | ||
| 287 | 1H NMR (400 MHz, DMSO-d 6) δ 11.14 (s, 1H), 8.51 (d, J = 4.5 Hz, 1H), 8.05 (d, J = 8.9 Hz, 2H), 7.84 - 7.78 (m, 2H), 7.20 - 7.15 (m, 2H), 7.13 (s, 1H), 7.03 (d, J = 9.0 Hz, 2H), 4.12 (q, J= 7.0 Hz, 2H), 3.90 - 3.84 (m, 6H), 1.35 (t, J = 7.0 Hz, 3H). | F | ||
| 288 | 1H NMR (400 MHz, DMSO-d 6) δ 10.27 (s, 1H), 8.47 (d, J = 4.5 Hz, 1H), 7.80 (dd, J = 8.5, 2.1 Hz, 1H), 7.67 (d, J = 2.0 Hz, 1H), 7.17 -7.13 (m, 2H), 6.96 (s, 1H), 3.88 - 3.84 (m, 6H), 3.55 - 3.49 (m, 4H), 2.47 - 2.41 (m, 4H), 1.90 - 1.82 (m, 6H), 1.56 - 1.47 (m, 6H). | F | ||
| 289 | 1H NMR (400 MHz, DMSO-d 6) δ 9.76 (s, 1H), 8.70 (d, J = 4.5 Hz, 1H), 8.05 (d, J = 8.9 Hz, 1H), 7.96 (dd, J = 8.5 Hz, 2.1 Hz, 1H), 7.90 (d, J = 4.9 Hz, 1H), 7.72 (d, J = 2.9 Hz, 1H), 7.48 (d, J = 4.5 Hz, 1H), 7.33 (s, 1H), 7.24 (d, J = 8.6 Hz, 1H), 7.08 (dd, J = 9.0, 3.0 Hz, 1H), 3.94-3.89 (m, 6H), 3.31-3.25 (m, 4H), 1.99-1.96 (m, 4H). | B | ||
| 290 | 1H NMR (400 MHz, DMSO-d 6) δ 10.10 (s, 1H), 8.68 (d, J = 4.5 Hz, 1H), 8.02 (dd, J = 8.5, 2.1 Hz, 1H), 7.93 (d, J = 2.1 Hz, 1H), 7.68 (d, J = 9.0 Hz, 2H), 7.47 (d, J = 4.5 Hz, 1H), 7.26 (s, 1H), 7.21 (d, J = 8.6 Hz, 1H), 6.92 (d, J = 9.0 Hz, 2H), 4.63 - 4.53 (m, 1H), 3.92 - 3.86 (m, 6H), 1.28 - 1.24 (m, 6H). | C | ||
| 291 | 1H NMR (400 MHz, DMSO-d 6) δ 10.95 (s, 1H), 8.71 (d, J = 4.5 Hz, 1H), 8.60 (s, 2H), 8.01 (dd, J = 8.5, 2.2 Hz, 1H), 7.91 (d, J = 2.1 Hz, 1H), 7.85 (s, 1H), 7.51 (d, J = 4.5 Hz, 1H), 7.35 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 3.92 - 3.88 (m, 6H). | B | ||
| 292 | 1H NMR (400 MHz, DMSO-d 6) δ 10.23 (s, 1H), 8.69 (d, J = 4.5 Hz, 1H), 8.02 (dd, J = 8.5, 2.1 Hz, 1H), 7.95 (d, J = 2.1 Hz, 1H), 7。76 (d, J = 8.5 Hz, 2H), 7.49 (d, J = 4.5 Hz, 1H), 7.34 - 7.28 (m, 3H), 7.21 (d, J = 8.6 Hz, 1H), 5.17 (t, J = 5.7 Hz, 1H), 4.47 (d, J = 5.7 Hz, 2H), 3.92 - 3.86 (m, 6H). | C | ||
| 293 | 1H NMR (400 MHz, DMSO-d 6) δ 10.17 (s, 1H), 8.74 (d, J = 4.4 Hz, 1H), 8.52 - 8.45 (m, 1H), 8.22 - 8.15 (m, 1H), 7.77 - 7.65 (m, 3H), 7.49 (d, J = 4.4 Hz, 1H), 7.32 (s, 1H), 6.97 - 6.91 (m, 2H), 4.01 (q, J = 7.0 Hz, 2H), 1.33 (t, J = 7.0 Hz, 3H). | B | ||
| 294 | 1H NMR (400 MHz, DMSO-d 6) δ 10.10 (s, 1H), 8.86 (d, J = 2.3 Hz, 1H), 8.74 (d, J = 4.4 Hz, 1H), 8.61 (dd, J = 8.9, 2.3 Hz, 1H), 8.12 - 8.06 (m, 2H), 7.63 (d, J = 9.0 Hz, 1H), 7.54 - 7.48 (m, 2H), 7.39 (s, 1H), 4.10 (s, 3H), 3.80 - 3.70 (m, 4H), 3.20 - 3.10 (m, 4H). | B | ||
| 295 | 1H NMR (400 MHz, DMSO-d 6) δ 10.12 (s, 1H), 8.94 (d, J = 2.3 Hz, 1H), 8.73 (d, J = 4.4 Hz, 1H), 8.65 (dd, J = 8.9, 2.3 Hz, 1H), 7.71 - 7.66 (m, 2H), 7.61 (d, J = 9.0 Hz, 1H), 7.55 (d, J = 4.4 Hz, 1H), 7.31 (s, 1H), 6.98 - 6.91 (m, 2H), 4.10 - 3.98 (m, 5H), 1.33 (t, J = 7.0 Hz, 3H). | C | ||
| 296 | 1H NMR (400 MHz, DMSO-d 6) δ 10.04 (s, 1H), 8.70 (d, J = 4.3 Hz, 1H), 7.94 (t, J = 8.6 Hz, 1H), 7.68 - 7.62 (m, 2H), 7.33 - 7.29 (m, 2H), 7.13 (dd, J = 12.5, 2.4 Hz, 1H), 7.03 (dd, J = 8.7, 2.5 Hz), 6.93 - 6.87 (m, 2H), 4.01 (q, J = 7.0 Hz, 2H), 3.90 (s, 3H), 1.32 (t, J = 7.0 Hz, 2H). | C | ||
| 297 | 1H NMR (400 MHz, DMSO-d 6) δ 9.77 (s, 1H), 8.72 (d, J = 4.3 Hz, 1H), 8.10 - 8.04 (m, 2H), 7.93 (t, J = 8.6 Hz, 1H), 7.50 (dd, J = 9.1, 3.1 Hz, 1H), 7.40 (s, 1H), 7.33 (dd, J = 4.3, 0.8 Hz, 1H), 7.17 (dd, J = 12.5, 2.4 Hz, 1H), 7.06 (dd, J = 8.7, 2.5 Hz, 1H), 3.91 (s, 3H), 3.78 -3.71 (m, 4H), 3.17 - 3.11 (m, 4H). | B | ||
| 298 | 1H NMR (400 MHz, DMSO-d 6) δ 10.16 (s, 1H), 8.76 (d, J = 4.4 Hz, 1H), 8.57 (d, J = 2.2 Hz, 1H), 8.41 (dd, J = 8.7, 2.2 Hz, 1H), 7.87 - 7.81 (m, 1H), 7.71 - 7.64 (m, 2H), 7.54 (d, J = 4.4 Hz, 1H), 7.34 (s, 1H), 6.96 - 6.90 (m, 2H), 4.01 (q, J = 7.0 Hz, 2H), 1.32 (t, J = 7.0 Hz, 3H). | C | ||
| 299 | 1H NMR (400 MHz, DMSO-d 6) δ 10.12 (s, 1H), 8.77 (d, J = 4.4 Hz, 1H), 8.56 (d, J = 2.2 Hz, 1H), 8.37 (dd, J = 8.7。2,2 Hz, 1H), 8.12 - 8.05 (m, 2H), 7.90 - 7.84 (m, 1H), 7.56 - 7.48 (m, 2H), 7.43 (s, 1H), 3.80 - 3.70 (m, 4H), 3.18 - 3.12 (m, 4H). | B | ||
| 301 | 1H NMR (400 MHz, DMSO-d 6) δ 10.11 (s, 1H), 8.71 (d, J = 4.4 Hz, 1H), 8.09-8.04 (m, 2H), 7.69 (d, J = 9.0 Hz, 2H), 7.56-7.47 (m, 2H), 7.40 (d, J = 4.4 Hz, 1H), 7.30 (s, 1H), 6.94 (d, J = 9.0 Hz, 2H), 4.02 (q, J = 7.0 Hz, 2H), 2.46 (s, 1H), 1.33 (t, J = 7.0 Hz, 3H). | B | ||
| 302 | 1H NMR (400 MHz, DMSO-d 6) δ 10.12 (s, 1H), 8.72 (d, J = 4.4 Hz, 1H), 8.24-8.20 (m, 2H), 7.70-7.68 (m, 2H), 7.44-7.40 (m, 2H), 7.30 (s, 1H), 6.95-6.93 (m, 2H), 4.02 (q, J = 7.0 Hz, 2H), 2.40-2.38 (m, 3H), 1.33 (t, J = 7.0 Hz, 3H). | C | ||
| 303 | 1H NMR (400 MHz, DMSO-d 6) δ 10.14 (s, 1H), 8.75 (dd, J = 3.9, 1.1 Hz, 1H), 8.70 (d, J = 4.7 Hz, 1H), 8.16 (dd, J = 5.0, 1.1 Hz, 1H), 7.84 (d, J = 4.7 Hz, 1H), 7.74-7.72 (m, 2H), 7.45-7.43 (m, 1H), 7.32 (s, 1H), 6.98-6.96 (m, 2H), 4.04 (q, J = 7.0 Hz, 2H), 1.34 (t, J = 7.0 Hz, 3H). | C | ||
| 304 | 1H NMR (400 MHz, DMSO-d 6) δ 10.07 (s, 1H), 8.76 (d, J = 4.2 Hz, 1H), 8.01 (t, J = 8.0 Hz, 1H), 7.79 (dd, J = 10.1, 1.9 Hz, 1H), 7.65 (d, J = 9.0 Hz, 2H), 7.59 (dd, J = 8.4, 1.9 Hz, 1H), 7.39 (d, J = 4.2 Hz, 1H), 7.36 (s, 1H), 6.92 (d, J = 9.0 Hz, 2H), 4.01 (q, J = 7.0 Hz, 2H), 1.32 (t, J = 7.0 Hz, 3H). | C | ||
| 306 | 1H NMR (400 MHz, DMSO-d 6) δ 9.94 (s, 1H), 8.73 (d, J = 4.4 Hz, 1H), 8.11-8.05 (m, 3H), 7.97 (s, 1H), 7.58-7.48 (m, 3H), 7.40-7.39 (m, 2H), 3.76 (t, J = 4.8 Hz, 4H), 3.15 (t, J = 4.8 Hz, 4H), 2.46 (s, 3H). | B | ||
| 307 | 1H NMR (400 MHz, DMSO-d 6) δ 10.13 (s, 1H), 8.73 (d, J = 4.4 Hz, 1H), 8.09 (dd, J = 8.4, 2.1 Hz, 1H), 7.94-7.90 (m, 1H), 7.70-7.68 (m, 2H), 7.52-7.47 (m, 2H), 7.31 (s, 1H), 6.95-6.93 (m, 2H), 4.02 (q, J = 7.0 Hz, 2H), 3.99 (s, 3H), 1.33 (t, J = 7.0 Hz, 3H). | C | ||
| 308 | 1H NMR (400 MHz, DMSO-d 6) δ 10.16 (s, 1H), 8.69 (d, J = 4.5 Hz, 1H), 8.32 (dd, J = 12.9, 2.2 Hz, 1H), 8.25-8.23 (m, 1H), 7.70-7.68 (m, 2H), 7.47 (d, J = 4.5 Hz, 1H), 7.42 (t, J = 8.9 Hz, 1H), 7.28 (s, 1H), 6.95-6.93 (m, 2H), 4.02 (q, J = 7.0 Hz, 2H), 3.98 (s, 3H), 1.33 (t, J = 7.0 Hz, 3H). | C | ||
| 309 | 1H NMR (400 MHz, DMSO-d 6) δ 10.10 (s, 1H), 8.69 (d, J = 4.5 Hz, 1H), 8.07-8.04 (m, 2H), 7.96 (d, J = 2.1 Hz, 1H), 7.49-7.48 (m, 2H), 7.44-7.42 (m, 1H), 7.34 (d, J = 3.2 Hz, 1H), 7.29 (s, 1H), 7.23 (d, J = 8.6 Hz, 1H), 6.43 (dd, J = 3.0, 0.7 Hz, 1H), 3.92 (s, 3H), 3.90 (s, 3H), 3.80 (s, 3H). | C | ||
| 311 | 1H NMR (400 MHz, DMSO-d 6) δ 9.72 (s, 1H), 8.69 (d, J = 4.5 Hz, 1H), 7.97-7.93 (m, 2H), 7.64 (t, J = 9.0 Hz, 1H), 7.48 (d, J = 4.5 Hz, 1H), 7.26 (s, 1H), 7.20 (d, J = 8.5 Hz, 1H), 6.92 (dd, J = 14.1, 2.6 Hz, 1H), 6.81 (dd, J = 8.9, 2.4 Hz, 1H), 3.90 (s, 3H), 3.89 (s, 3H), 3.74 (t, J = 4.8 Hz, 4H), 3.15 (t, J = 4.8 Hz, 4H). | B | ||
| 312 | 1H NMR (400 MHz, DMSO-d 6) δ 9.78 (s, 1H), 8.69 (d, J = 4.5 Hz, 1H), 8.06 (d, J = 9.0 Hz, 1H), 7.95 (dd, J = 8.5, 2.1 Hz, 1H), 7.91-7.89 (m, 2H), 7.47 (d, J = 4.5 Hz, 1H), 7.33 (s, 1H), 7.29 (dd, J = 9.1, 3.1 Hz, 1H), 7.24 (d, J = 8.6 Hz, 1H), 3.92-3.90 (m, 6H), 2.92 (s, 6H). | B | ||
| 313 | 1H NMR (400 MHz, DMSO-d 6) δ 10.10 (s, 1H), 8.65 (d, J = 4.8 Hz, 1H), 8.27 (s, 1H), 8.11 (dd, J = 8.5, 2.0 Hz, 1H), 7.71-7.69 (m, 2H), 7.35 (d, J = 4.8 Hz, 1H), 7.25 (s, 1H), 7.01 (d, J = 8.5 Hz, 1H), 6.95-6.92 (m, 2H), 4.68 (t, J = 8.8 Hz, 2H), 4.02 (q, J = 7.0 Hz, 2H), 3.39-3.34 (m, 2H), 1.33 (t, J = 7.0 Hz, 3H). | C | ||
| 314 | 1H NMR (400 MHz, DMSO-d 6) δ 9.98 (s, 1H), 8.70 (d, J = 4.5 Hz, 1H), 8.16 (d, J = 9.1 Hz, 1H), 8.09 (d, J = 2.9 Hz, 1H), 7.96 (dd, J = 8.5, 2.1 Hz, 1H), 7.89 (d, J = 2.1 Hz, 1H), 7.53 (dd, J = 9.0, 3.1 Hz, 1H), 7.48 (d, J = 4.5 Hz, 1H), 7.36 (s, 1H), 7.23 (d, J = 8.6 Hz, 1H), 4.11 (q, J = 7.0 Hz, 2H), 3.93 - 3.87 (m, 6H), 1.35 (t, J = 7.0 Hz, 3H). | B | ||
| 315 | 1H NMR (400 MHz, DMSO-d 6) δ 10.13 (s, 1H), 8.71 (d, J = 4.4 Hz, 1H), 7.67 (d, J = 9.1 Hz, 2H), 7.45 (d, J = 4.4 Hz, 1H), 7.38 (d, J = 2.3 Hz, 2H), 7.30 (s, 1H), 6.95 - 6.90 (m, 2H), 6.78 (t, J = 2.3 Hz, 1H), 4.01 (q, J = 7.0 Hz, 2H), 3.90 - 3.82 (m, 6H), 1.32 (t, J = 7.0 Hz, 3H). | C | ||
| 316 | 1H NMR (400 MHz, DMSO-d 6) δ 10.15 (s, 1H), 8.74 (d, J = 4.4 Hz, 1H), 8.51 (dd, J = 7.2, 2.3 Hz, 1H), 8.39 - 8.31 (m, 1H), 7.74 - 7.64 (m, 3H), 7.49 (d, J = 4.4 Hz, 1H), 7.32 (s, 1H), 6.98 - 6.89 (m, 2H), 4.01 (q, J = 7.0 Hz, 2H), 1.33 (t, J = 7.0 Hz, 3H). | C | ||
| 317 | 1H NMR (400 MHz, CDCl 3) δ 8.61 - 8.52 (m, 1H), 7.80 - 7.53 (m, 2H), 7.44 - 7.28 (m, 1H), 7.25 - 6.83 (m, 6H), 5.23 - 4.36 (m, 3H), 4.05 - 3.74 (m, 10H), 3.70 - 2.77 (m, 3H), 1.39 - 1.07 (m, 3H). | D | ||
| 318 | 1H NMR (400 MHz, CDCl 3) δ 8.61 - 8.53 (m, 1H), 7.76 - 7.54 (m, 2H), 7.38 - 7.30 (m, 1H), 7.17 (d, J = 7.3 Hz, 1H), 7.08 - 6.89 (m, 5H), 4.95 - 4.47 (m, 3H), 4.04 - 3.78 (m, 10H), 3.63 - 2.69 (m, 3H), 1.41 - 1.19 (m, 3H). | D | ||
| 319 | 1H NMR (400 MHz, CDCl 3) δ 8.61 - 8.54 (m, 1H), 7.75 - 7.54 (m, 2H), 7.41 - 7.32 (m, 2H), 7.17 (d, J = 7.3 Hz, 1H), 7.07 - 6.90 (m, 4H) , 4.86 - 4.42 (m, 3H), 4.03 - 3.79 (m, 10H), 3.46 - 2.86 (m, 3H), 1.38 - 1.19 (m, 3H). | D | ||
| 320 | 1H NMR (400 MHz, CDCl 3) δ 8.54 (d, J = 4.4 Hz, 1H), 7.75 (d, J = 2.1 Hz, 1H), 7.60 (dd, J = 8.4, 2.1 Hz, 1H), 7.25 (s, 1H), 7.06 (d, J = 8.5 Hz, 1H), 6.99 (d, J = 4.4 Hz, 1H), 6.82 (s, 1H), 4.01 (s, 3H), 3.97 (s, 3H), 3.75 - 3.68 (m, 4H), 2.60 - 2.51 (m, 4H), 2.12 - 2.06 (m, 6H), 1.78 - 1.69 (m, 6H)。 | A | ||
| 321 | 1H NMR (400 MHz, CDCl 3) δ 8.59 - 8.53 (m, 1H), 7.74 - 7.58 (m, 2H), 7.15 (d, J = 7.5 Hz, 1H), 7.07 - 6.95 (m, 2H), 4.70 - 4.18 (m, 3H), 4.03 - 3.80 (m, 7H), 3.43 - 2.87 (m, 3H), 1.51 - 1.41 (m, 9H), 1.24 - 1.08 (m, 3H). | D | ||
| 322 | 1H NMR (400 MHz, CDCl 3) δ 8.60 - 8.52 (m, 1H), 7.76 - 7.65 (m, 2H), 7.12 - 7.07 (m, 1H), 7.06 - 6.95 (m, 2H), 4.71 - 4.43 (m, 2H), 4.01 - 3.87 (m, 6H), 3.26 - 3.07 (m, 1H), 3.01 - 2.45 (m, 4H), 1.18 - 0.95 (m, 3H)。 | D | ||
| 323 | 1H NMR (400 MHz, DMSO-d 6) δ 10.16 (s, 1H), 9.18 (d, J = 2.3 Hz, 1H), 8.74 - 8.63 (m, 2H), 7.71 - 7.64 (m, 2H), 7.50 (d, J = 4.4 Hz, 1H), 7.28 (s, 1H), 7.09 (d, J = 8.8 Hz, 1H), 6.97 - 6.90 (m, 2H), 4.06 - 3.98 (m, 5H), 1.33 (t, J = 7.0 Hz, 3H). | C | ||
| 324 | 1H NMR (400 MHz, DMSO-d 6) δ 10.10 (s, 1H), 8.59 (d, J = 4.6 Hz, 1H), 8.37 (d, J = 9.1 Hz, 2H), 7.74 - 7.67 (m, 2H), 7.37 (d, J = 4.6 Hz, 1H), 7.19 (s, 1H), 6.98 - 6.86 (m, 4H), 4.02 (q, J = 7.0 Hz, 2H), 3.07 (s, 6H), 1.33 (t, J = 7.0 Hz, 3H). | C | ||
| 325 | 1H NMR (400 MHz, DMSO-d 6) δ 9.83 (s, 1H), 8.69 (d, J = 4.5 Hz, 1H), 8.10 - 7.87 (m, 2H), 7.67 (t, J = 9.0 Hz, 1H), 7.48 (d, J = 4.5 Hz, 1H), 7.27 (s, 1H), 7.20 (d, J = 8.6 Hz, 1H), 6.98 (dd, J = 12.4, 2.7 Hz, 1H), 6.90 - 6.80 (m, 1H), 3.95 - 3.86 (m, 6H), 3.79 (s, 3H). | C | ||
| 326 | 1H NMR (400 MHz, DMSO-d 6) δ 10.05 (s, 1H), 8.70 (d, J = 4.4 Hz, 1H), 7.98 (d, J = 8.4 Hz, 1H), 7.90 (s, 1H), 7.58 - 7.38 (m, 2H), 7.28 (s, 1H), 7.20 (d, J = 8.6 Hz, 1H), 7.07 (t, J = 8.4 Hz, 1H), 3.94 - 3.85 (m, 9H). | C | ||
| 327 | 1H NMR (400 MHz, DMSO-d 6) δ 9.94 - 9.67 (m, 2H), 8.70 (d, J = 4.5 Hz, 1H), 8.07 (d, J = 8.9 Hz, 1H), 7.99 - 7.85 (m, 3H), 7.48 (d, J = 4.5 Hz, 1H), 7.38 - 7.27 (m, 2H), 7.23 (d, J = 8.6 Hz, 1H), 3.91 (s, 6H). | B | ||
| 328 | 1H NMR (400 MHz, DMSO-d 6) δ 8.64 (d, J = 4.0 Hz, 1H), 8.13 (d, J = 8.0 Hz, 1H), 7.96 (s, 1H), 7.90 (d, J = 8.1 Hz, 1H), 7.43 (d, J = 4.0 Hz, 1H), 7.20 (d, J = 8.4 Hz, 1H), 7.13 (s, 1H), 5.25 (s, 2H), 3.89 (s, 6H), 3.85 - 3.75 (m, 1H), 3.75 - 3.65 (m, 2H), 3.53 - 3.43 (m, 2H), 3.25 (s, 3H), 2.39 - 2.20 (m, 1H), 2.07 - 1.82 (m, 4H), 1.58 - 1.37 (m, 4H). | A | ||
| 329 | 1H NMR (400 MHz, DMSO-d 6) δ 10.63 (s, 1H), 8.71 (d, J = 4.5 Hz, 1H), 8.10 - 7.98 (m, 5H), 7.96 (d, J = 2.1 Hz, 1H), 7.51 (d, J = 4.5 Hz, 1H), 7.35 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 5.50 (s, 2H), 3.97 - 3.86 (m, 6H), 3.86 - 3.78 (m, 2H), 3.55 - 3.45 (m, 2H), 3.24 (s, 3H). | C | ||
| 330 | 1H NMR (400 MHz, DMSO-d 6) δ 8.64 (d, J = 4.5 Hz, 1H), 8.12 (d, J = 8.2 Hz, 1H), 7.96 (d, J = 2.0 Hz, 1H), 7.90 (dd, J = 8.5, 2.0 Hz, 1H), 7.42 (d, J = 4.5 Hz, 1H), 7.20 (d, J = 8.6 Hz, 1H), 7.13 (s, 1H), 4.06 (q, J = 7.1 Hz, 2H), 3.95 - 3.85 (m, 6H), 3.84 - 3.73 (m, 1H), 2.31 - 2.18 (m, 1H), 2.02 - 1.81 (m, 4H), 1.53 - 1.36 (m, 4H), 1.19 (t, J = 7.1 Hz, 3H). | A | ||
| 331 | 1H NMR (400 MHz, DMSO-d 6) δ 8.64 (d, J = 4.5 Hz, 1H), 8.13 (d, J = 8.2 Hz, 1H), 7.96 (d, J = 2.0 Hz, 1H), 7.89 (dd, J = 8.5, 2.1 Hz, 1H), 7.43 (d, J = 4.5 Hz, 1H), 7.20 (d, J = 8.6 Hz, 1H), 7.13 (s, 1H), 3.98 (t, J = 6.6 Hz, 2H), 3.94 - 3.86 (m, 6H), 3.85 - 3.70 (m, 1H), 2.35 - 2.20 (m, 1H), 2.06 - 1.81 (m, 4H), 1.68 - 1.52 (m, 2H), 1.52 - 1.35 (m, 4H), 0.89 (t, J = 7.4 Hz, 3H). | A | ||
| 332 | 1H NMR (400 MHz, DMSO-d 6) δ 8.64 (d, J = 4.5 Hz, 1H), 8.11 (d, J = 8.3 Hz, 1H), 7.96 (d, J = 2.0 Hz, 1H), 7.89 (dd, J = 8.5, 2.0 Hz, 1H), 7.42 (d, J = 4.5 Hz, 1H), 7.20 (d, J = 8.6 Hz, 1H), 7.13 (s, 1H), 4.02 (t, J = 6.5 Hz, 2H), 3.95 - 3.84 (m, 6H), 3.83 - 3.72 (m, 1H), 2.33 - 2.19 (m, 1H), 2.05 - 1.80 (m, 4H), 1.63 - 1.51 (m, 2H), 1.51 - 1.38 (m, 4H), 1.38 - 1.27 (m, 2H), 0.90 (t, J = 7.4 Hz, 3H). | A | ||
| 333 | 1H NMR (400 MHz, DMSO-d 6) δ 8.64 (d, J = 4.5 Hz, 1H), 8.12 (d, J = 8.2 Hz, 1H), 7.96 (d, J = 2.0 Hz, 1H), 7.89 (dd, J = 8.5, 2.1 Hz, 1H), 7.43 (d, J = 4.5 Hz, 1H), 7.20 (d, J = 8.6 Hz, 1H), 7.13 (s, 1H), 4.01 (t, J = 6.5 Hz, 2H), 3.94 - 3.85 (m, 6H), 3.83 - 3.72 (m, 1H), 2.33 - 2.20 (m, 1H), 2.03 - 1.81 (m, 4H), 1.62 - 1.51 (m, 2H), 1.51 - 1.36 (m, 4H), 1.33 - 1.18 (m, 14H), 0.86 (t, J = 6.8 Hz, 3H). | A | ||
| 335 | 1H NMR (400 MHz, DMSO-d 6) δ 10.59 (s, 1H), 8.70 (d, J = 4.5 Hz, 1H), 8.07 - 7.91 (m, 6H), 7.50 (d, J = 4.5 Hz, 1H), 7.34 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 4.22 (t, J = 6.6 Hz, 2H), 3.94 - 3.85 (m, 6H), 1.79 - 1.67 (m, 2H), 0.98 (t, J = 7.4 Hz, 3H). | C | ||
| 336 | 1H NMR (400 MHz, DMSO-d 6) δ 10.61 (s, 1H), 8.71 (d, J = 4.8 Hz, 1H), 8.08 - 7.91 (m, 6H), 7.51 (d, J = 4.5 Hz, 1H), 7.34 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 4.27 (t, J = 6.5 Hz, 2H), 3.98 - 3.85 (m, 6H), 1.78 - 1.63 (m, 2H), 1.51 - 1.37 (m, 2H), 0.95 (t, J = 7.4 Hz, 3H). | C | ||
| 337 | 1H NMR (400 MHz, DMSO-d 6) δ 10.61 (s, 1H), 8.71 (d, J = 4.5 Hz, 1H), 8.09 - 7.91 (m, 6H), 7.51 (d, J = 4.5 Hz, 1H), 7.35 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 4.26 (t, J = 6.5 Hz, 2H), 3.97 - 3.80 (m, 6H), 1.77 - 1.65 (m, 2H), 1.49 - 1.13 (m, 14H), 0.94 - 0.79 (m, 3H). | C | ||
| 338 | 1H NMR (400 MHz, DMSO-d 6) δ 10.47 (s, 1H), 8.70 (d, J = 4.5 Hz, 1H), 8.13 (dd, J = 4.8, 1.4 Hz, 1H), 8.02 (dd, J = 8.5, 2.1 Hz, 1H), 7.99 - 7.88 (m, 3H), 7.61 - 7.53 (m, 1H), 7.53 - 7.45 (m, 3H), 7.33 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 6.86 (d, J = 8.6 Hz, 1H), 6.71 - 6.65 (m, 1H), 3.96 - 3.85 (m, 6H), 3.81 - 3.43 (m, 8H). | C | ||
| 339 | 1H NMR (400 MHz, DMSO-d 6) δ 10.01 (s, 1H), 8.70 (d, J = 4.2 Hz, 1H), 7.68 - 7.58 (m, 2H), 7.32 (s, 1H), 7.20 - 7.12 (m, 2H), 7.04 (s, 1H), 6.94 - 6.86 (m, 2H), 4.00 (q, J = 7.0 Hz, 2H), 3.86 (s, 3H), 3.76 (s, 3H), 2.08 (s, 3H), 1.32 (t, J = 7.0 Hz, 3H). | C | ||
| 340 | 1H NMR (400 MHz, DMSO-d 6) δ 8.64 (d, J = 4.5 Hz, 1H), 8.15 (d, J = 8.3 Hz, 1H), 7.99 (d, J = 1.7 Hz, 1H), 7.88 (dd, J = 8.5, 1.6 Hz, 1H), 7.75 - 7.62 (m, 1H), 7.43 (d, J = 4.5 Hz, 1H), 7.20 (d, J = 8.4 Hz, 1H), 7.13 (d, J = 0.5 Hz, 1H), 3.96 - 3.83 (m, 8H), 3.82 - 3.71 (m, 1H), 3.59 - 3.48 (m, 1H), 3.31 - 3.20 (m, 3H), 3.03 - 2.81 (m, 2H), 2.43 - 2.17 (m, 2H), 2.13 - 1.98 (m, 1H), 1.95 - 1.83 (m, 2H), 1.81 - 1.62 (m, 6H), 1.57 - 1.28 (m, 8H). | A | ||
| 341 | 1H NMR (400 MHz, DMSO-d 6) δ 8.64 (d, J = 4.5 Hz, 1H), 8.09 (d, J = 8.1 Hz, 1H), 7.96 (d, J = 2.0 Hz, 1H), 7.89 (dd, J = 8.5, 2.1 Hz, 1H), 7.43 (d, J = 4.5 Hz, 1H), 7.20 (d, J = 8.6 Hz, 1H), 7.13 (s, 1H), 4.44 - 4.32 (m, 1H), 3.98 - 3.91 (m, 1H), 3.91 - 3.84 (m, 6H), 3.83 - 3.71 (m, 1H), 3.56 (t, J = 4.2 Hz, 4H), 3.06 - 2.95 (m, 1H), 2.48 - 2.41 (m, 4H), 2.41 - 2.30 (m, 1H), 1.95 - 1.66 (m, 6H), 1.54 - 1.39 (m, 4H), 1.36 - 1.07 (m, 4H). | A | ||
| 342 | 1H NMR (400 MHz, DMSO-d 6) δ 8.65 (d, J = 4.5 Hz, 1H), 8.19 - 8.08 (m, 2H), 7.97 (d, J = 2.1 Hz, 1H), 7.90 (dd, J = 8.5, 2.1 Hz, 1H), 7.61 - 7.51 (m, 1H), 7.43 (d, J = 4.5 Hz, 1H), 7.20 (d, J = 8.6 Hz, 1H), 7.14 (s, 1H), 6.85 (d, J = 8.6 Hz, 1H), 6.71 - 6.63 (m, 1H), 3.96 - 3.84 (m, 6H), 3.85 - 3.73 (m, 1H), 3.66 - 3.41 (m, 8H), 2.66 - 2.55 (m, 1H), 1.98 - 1.84 (m, 2H), 1.83 - 1.69 (m, 2H), 1.59 - 1.38 (m, 4H). | A | ||
| 343 | 1H NMR (400 MHz, MeOD-d 4) δ 8.61 (d, J = 4.5 Hz, 1H), 7.88 (d, J = 2.1 Hz, 1H), 7.80 (dd, J = 8.5, 2.1 Hz, 1H), 7.28 (d, J = 4.5 Hz, 1H), 7.24 - 7.15 (m, 2H), 4.70 - 4.60 (m, 1H), 4.22 - 4.09 (m, 1H), 4.00 - 3.95 (m, 6H), 3.18 - 3.06 (m, 1H), 2.82 - 2.52 (m, 7H), 2.16 - 1.93 (m, 4H), 1.91 - 1.79 (m, 2H), 1.75 - 1.60 (m, 6H), 1.59 - 1.35 (m, 7H). | A | ||
| 344 | 1H NMR (400 MHz, CDCl 3) δ 8.57 (s, 1H), 7.75 - 7.54 (m, 2H), 7.49 - 7.33 (m, 5H), 7.17 (d, J = 7.4 Hz, 1H), 7.07 - 6.94 (m, 2H), 5.04 - 4.44 (m, 3H), 4.07 - 3.85 (m, 7H), 3.51 - 2.85 (m, 3H), 1.37 - 1.22 (m, 3H). | D | ||
| 345 | 1H NMR (400 MHz, MeOD-d 4) δ 8.59 (d, J = 4.5 Hz, 1H), 7.85 (d, J = 2.1 Hz, 1H), 7.80 (dd, J = 8.5, 2.1 Hz, 1H), 7.27 (d, J = 4.5 Hz, 1H), 7.21 - 7.14 (m, 2H), 3.98 - 3.85 (m, 7H), 3.78 - 3.67 (m, 4H), 2.77 - 2.63 (m, 4H), 2.51 - 2.36 (m, 1H), 2.18 - 2.01 (m, 4H), 1.55 - 1.38 (m, 4H)。 | A | ||
| 346 | 1H NMR (400 MHz, DMSO-d 6) δ 10.13 (s, 1H), 8.64 (d, J = 4.5 Hz, 1H), 7.97 (dd, J = 8.5, 2.1 Hz, 1H), 7.89 (d, J = 2.1 Hz, 1H), 7.70 - 7.63 (m, 2H), 7.43 (d, J = 4.5 Hz, 1H), 7.23 (s, 1H), 7.16 (d, J = 8.6 Hz, 1H), 7.03 - 6.96 (m, 2H), 5.19 (s, 2H), 3.90 - 3.81 (m, 6H), 3.73 - 3.63 (m, 2H), 3.45 - 3.39 (m, 2H), 3.18 (s, 3H). | C | ||
| 347 | 1H NMR (400 MHz, CDCl 3) δ 8.56 (d, J = 4.4 Hz, 1H), 7.72 (dd, J = 8.4, 2.1 Hz, 1H), 7.68 (d, J = 2.1 Hz, 1H), 7.09 (s, 1H), 7.03 (d, J = 8.5 Hz, 1H), 6.99 (d, J = 4.4 Hz, 1H), 4.74 - 4.65 (m, 1H), 4.54 - 4.46 (m, 1H), 4.00 - 3.94 (m, 6H), 3.00 - 2.85 (m, 2H), 2.77 - 2.67 (m, 1H), 2.46 - 2.37 (m, 1H), 1.15 (d, J = 6.3 Hz, 3H), 0.98 (d, J = 6.3 Hz, 3H). | D | ||
| 348 | 1H NMR (400 MHz, CDCl 3) δ 8.57 (d, J = 4.4 Hz, 1H), 7.66 (dd, J = 8.4, 1.6 Hz, 1H), 7.56 (d, J = 2.1 Hz, 1H), 7.45 - 7.39 (m, 3H), 7.38 - 7.32 (m, 2H), 7.21 (s, 1H), 7.06 - 6.94 (m, 2H), 4.86 - 4.22 (4H), 4.02 - 3.90 (m, 6H) 3.45 -3.30 (m, 1H), 3.09 - 2.96 (m, 1H), 1.44 - 1.33 (m, 3H), 1.32 - 1.24 (m, 3H). | D | ||
| 349 | 1H NMR (400 MHz, CDCl 3) δ 9.31 (d, J = 3.1 Hz, 1H), 8.65 - 8.60 (m, 2H), 7.85 (d, J = 2.1 Hz, 1H), 7.63 (dd, J = 8.4, 2.1 Hz, 1H), 7.43 (s, 1H), 7.28 - 7.22 (m, 2H), 7.10 (dd, J = 6.4, 2.1 Hz, 2H), 4.80 - 4.50 (m, 1H), 4.06 - 3.96 (m, 6H), 3.95 - 3.79 (m, 1H), 3.78 - 3.66 (m, 4H), 3.16 - 2.70 (m, 2H), 2.64 - 2.52 (m, 4H), 2.51 - 2.38 (m, 1H), 2.06 - 1.74 (m, 2H), 1.56 - 1.35 (m, 2H). | B | ||
| 350 | ¹H NMR (400 MHz, DMSO-d6) δ 8.67 (dd, J = 4.3, 1.8 Hz, 1H), 7.83 - 7.70 (m, 2H), 7.53 - 7.46 (m, 2H), 7.38 (dd, J = 9.1, 4.3 Hz, 1H), 7.34 - 7.26 (m, 2H), 7.21 - 7.14 (m, 1H), 7.05 (d, J = 23.7 Hz, 1H), 4.77 - 4.24 (m, 3H), 3.87 (s, 3H), 3.82 (s, 3H), 3.56 - 3.47 (m, 1H), 3.27 - 2.95 (m, 3H), 1.23 - 1.06 (m, 3H). | D | ||
| 351 | ¹H NMR (400 MHz, DMSO-d6) δ 8.66 (dd, J = 4.2, 2.3 Hz, 1H), 7.86 - 7.69 (m, 2H), 7.38 (dd, J = 9.6, 4.3 Hz, 1H), 7.34 - 7.24 (m, 4H), 7.22 - 7.13 (m, 1H), 7.06 (d, J = 24.2 Hz, 1H), 4.62 - 4.25 (m, 3H), 3.94 - 3.72 (m, 6H), 3.51 - 3.47 (m, 1H), 3.29 - 2.93 (m, 3H), 2.35 (s, 3H), 1.27 - 1.01 (m, 3H). | D | ||
| 352 | ¹H NMR (400 MHz, DMSO-d6) δ 8.70 - 8.63 (m, 1H), 7.85 - 7.72 (m, 3H), 7.46 - 7.35 (m, 2H), 7.23 - 7.12 (m, 2H), 7.07 (d, J = 23.6 Hz, 1H), 4.75 - 4.03 (m, 5H), 3.94 - 3.80 (m, 6H), 3.53 (dd, J = 13.5, 3.4 Hz, 1H), 3.20 - 3.00 (m, 1H), 1.31 - 1.12 (m, 3H). | D | ||
| 353 | ¹H NMR (400 MHz, DMSO-d6) δ 8.67 (dd, J = 4.3, 1.6 Hz, 1H), 7.89 - 7.70 (m, 3H), 7.39 (dd, J = 8.8, 4.4 Hz, 1H), 7.20 (dd, J = 8.4, 3.9 Hz, 1H), 7.11 - 7.01 (m, 2H), 6.67 - 6.61 (m, 1H), 4.78 - 4.10 (m, 5H), 3.90 - 3.81 (m, 6H), 3.57 - 3.48 (m, 1H), 3.20 - 2.99 (m, 1H), 1.30 - 1.12 (m, 3H). | D | ||
| 354 | ¹H NMR (400 MHz, DMSO-d6) δ 8.71 - 8.63 (m, 1H), 8.55 (d, J = 3.8 Hz, 1H), 7.89 - 7.70 (m, 2H), 7.52 - 7.35 (m, 3H), 7.30 - 7.16 (m, 3H), 7.14 - 7.02 (m, 1H), 6.94 (t, J = 7.3 Hz, 1H), 4.59 - 4.27 (m, 3H), 4.06 - 3.97 (m, 1H), 3.95 - 3.82 (m, 6H), 3.52 - 3.40 (m, 1H), 3.32 - 2.93 (m, 2H), 1.20 - 1.02 (m, 3H). | D | ||
| 355 | ¹H NMR (400 MHz, DMSO-d6) δ 8.65 (t, J = 4.3 Hz, 1H), 7.89 - 7.73 (m, 4H), 7.73 - 7.58 (m, 3H), 7.38 (dd, J = 10.9, 4.4 Hz, 1H), 7.19 (dd, J = 12.3, 8.6 Hz, 1H), 7.01 (d, J = 26.4 Hz, 1H), 4.46 - 3.97 (m, 3H), 3.95 - 3.77 (m, 6H), 3.77 - 3.58 (m, 1H), 3.31 - 3.07 (m, 2H), 2.99 - 2.77 (m, 1H), 0.99 - 0.82 (m, 3H). | D | ||
| 356 | ¹H NMR (400 MHz, DMSO-d6) δ 8.73 - 8.62 (m, 1H), 7.90 - 7.66 (m, 2H), 7.49 - 7.28 (m, 4H), 7.26 - 7.00 (m, 2H), 4.94 - 4.19 (m, 3H), 3.97 - 3.71 (m, 6H), 3.71 - 3.48 (m, 1H), 3.30 - 2.90 (m, 3H), 1.32 - 1.02 (m, 3H). | D | ||
| 357 | ¹H NMR (400 MHz, DMSO-d6) δ 8.76 - 8.59 (m, 3H), 7.90 - 7.64 (m, 2H), 7.50 - 7.30 (m, 3H), 7.26 - 6.98 (m, 2H), 4.93 - 4.15 (m, 4H), 3.95 - 3.68 (m, 6H), 3.65 - 3.46 (m, 1H), 3.19 - 2.91 (m, 2H), 1.33 - 1.00 (m, 3H). | D | ||
| 358 | ¹H NMR (400 MHz, DMSO-d6) δ 8.65 (d, J = 4.4 Hz, 1H), 7.84 - 7.74 (m, 2H), 7.37 (d, J = 4.5 Hz, 1H), 7.17 (d, J = 8.5 Hz, 1H), 7.01 (s, 1H), 4.54 - 4.31 (m, 2H), 3.91 - 3.82 (m, 6H), 2.89 - 2.61 (m, 3H), 2.36 (t, J = 12.2 Hz, 1H), 1.06 (d, J = 6.1 Hz, 3H), 0.91 (d, J = 6.0 Hz, 3H). | D | ||
| 359 | ¹H NMR (400 MHz, DMSO-d6) δ 8.65 (d, J = 4.5 Hz, 1H), 7.84 - 7.73 (m, 2H), 7.37 (d, J = 4.5 Hz, 1H), 7.18 (d, J = 8.5 Hz, 1H), 7.00 (s, 1H), 3.97 - 3.65 (m, 8H), 3.53 - 3.42 (m, 2H), 3.22 - 3.05 (m, 2H), 1.06 (d, J = 6.5 Hz, 3H), 0.94 (d, J = 6.5 Hz, 3H). | D | ||
| 360 | ¹H NMR (400 MHz, DMSO-d6) δ 8.65 (d, J = 4.4 Hz, 1H), 7.91 - 7.70 (m, 2H), 7.37 (d, J = 4.5 Hz, 1H), 7.19 (d, J = 8.5 Hz, 1H), 6.99 (s, 1H), 4.73 - 3.97 (m, 2H), 3.94 - 3.75 (m, 6H), 3.29 - 3.01 (m, 4H), 1.30 (d, J = 6.9 Hz, 3H), 1.09 (d, J = 6.4 Hz, 3H). | D | ||
| 361 | ¹H NMR (400 MHz, DMSO-d6) δ 8.64 (dd, J = 6.3, 4.5 Hz, 1H), 7.85 - 7.64 (m, 2H), 7.36 (dd, J = 18.4, 4.4 Hz, 1H), 7.19 (dd, J = 12.2, 8.6 Hz, 1H), 6.99 (d, J = 18.0 Hz, 1H), 3.92 - 3.82 (m, 6H), 3.80 - 3.50 (m, 4H), 2.84 - 2.73 (m, 2H), 0.56 - 0.45 (m, 2H), 0.42 - 0.34 (m, 2H). | D | ||
| 362 | ¹H NMR (400 MHz, DMSO-d6) δ 8.65 (d, J = 4.4 Hz, 1H), 7.90 - 7.70 (m, 2H), 7.37 (t, J = 4.6 Hz, 1H), 7.18 (dd, J = 8.4, 5.9 Hz, 1H), 6.99 (s, 1H), 4.72 - 4.14 (m, 2H), 3.92 - 3.82 (m, 6H), 2.93 - 2.53 (m, 4H), 1.37 - 1.20 (m, 3H), 1.13 - 0.88 (m, 3H). | D | ||
| 363 | ¹H NMR (400 MHz, DMSO-d6) δ 8.67 (d, J = 4.4 Hz, 1H), 7.83 - 7.74 (m, 1H), 7.71 (s, 1H), 7.52 - 7.42 (m, 3H), 7.42 - 7.32 (m, 3H), 7.17 (d, J = 8.6 Hz, 1H), 7.08 (s, 1H), 4.59 - 4.21 (m, 3H), 3.87 (s, 3H), 3.80 (s, 3H), 3.52 - 3.40 (m, 2H), 3.18 - 3.07 (m, 1H), 1.34 - 1.04 (m, 6H). | D | ||
| 364 | ¹H NMR (400 MHz, DMSO-d6) δ 8.74 - 8.57 (m, 1H), 7.97 - 7.70 (m, 2H), 7.57 - 7.27 (m, 6H), 7.20 (d, J = 7.3 Hz, 1H), 7.15 - 7.02 (m, 1H), 4.48 - 3.98 (m, 4H), 3.96 - 3.63 (m, 8H), 1.35 - 1.00 (m, 6H). | D | ||
| 365 | ¹H NMR (400 MHz, DMSO-d6) δ 8.71 - 8.60 (m, 1H), 7.87 (dd, J = 34.8, 7.5 Hz, 1H), 7.78 - 7.65 (m, 1H), 7.54 - 7.28 (m, 6H), 7.26 - 7.10 (m, 1H), 7.04 (dd, J = 24.4, 8.8 Hz, 1H), 5.00 - 4.49 (m, 1H), 4.38 - 4.08 (m, 2H), 4.00 - 3.68 (m, 6H), 3.63 - 3.43 (m, 1H), 3.32 - 3.11 (m, 2H), 1.35 - 1.06 (m, 6H). | D | ||
| 366 | ¹H NMR (400 MHz, DMSO-d6) δ 8.67 (d, J = 4.4 Hz, 1H), 7.88 - 7.57 (m, 2H), 7.53 - 7.19 (m, 6H), 7.19 - 7.00 (m, 2H), 4.83 - 4.57 (m, 1H), 4.55 - 4.06 (m, 3H), 3.94 - 3.74 (m, 6H), 3.31 - 2.84 (m, 2H), 1.23 - 0.93 (m, 6H). | D | ||
| 367 | ¹H NMR (400 MHz, DMSO-d6) δ 8.69 - 8.62 (m, 1H), 7.95 - 7.64 (m, 2H), 7.53 - 7.29 (m, 6H), 7.23 - 7.11 (m, 1H), 7.09 - 7.00 (m, 1H), 4.07 - 3.53 (m, 12H), 1.02 - 0.42 (m, 4H). | D | ||
| 368 | ¹H NMR (400 MHz, DMSO-d6) δ 8.72 - 8.60 (m, 1H), 7.89 - 7.66 (m, 2H), 7.59 - 7.16 (m, 6H), 7.15 - 6.99 (m, 1H), 4.95 - 4.54 (m, 1H), 4.53 - 4.23 (m, 2H), 3.96 - 3.69 (m, 6H), 3.65 - 3.48 (m, 1H), 3.30 - 2.87 (m, 3H), 1.31 - 0.98 (m, 3H). | D | ||
| 369 | ¹H NMR (400 MHz, DMSO-d6) δ 8.65 (d, J = 3.3 Hz, 1H), 7.90 - 7.67 (m, 2H), 7.46 - 7.00 (m, 7H), 4.72 - 4.21 (m, 3H), 3.94 - 3.69 (m, 6H), 3.56 - 3.42 (m, 1H), 3.32 - 2.91 (m, 3H), 2.33 (s, 3H), 1.33 - 0.98 (m, 3H). | D | ||
| 370 | ¹H NMR (400 MHz, DMSO-d6) δ 8.67 (dd, J = 4.3, 1.9 Hz, 1H), 8.05 (d, J = 2.9 Hz, 1H), 7.87 - 7.69 (m, 3H), 7.39 (dd, J = 9.4, 4.4 Hz, 1H), 7.19 (dd, J = 8.6, 3.7 Hz, 1H), 7.07 (d, J = 22.3 Hz, 1H), 6.69 (s, 1H), 4.62 - 3.96 (m, 3H), 3.94 - 3.80 (m, 6H), 3.48 (dd, J = 13.3, 3.1 Hz, 1H), 3.32 - 2.93 (m, 3H), 1.28 - 1.08 (m, 3H). | D | ||
| 371 | ¹H NMR (400 MHz, DMSO-d6) δ 8.65 (d, J = 4.4 Hz, 1H), 7.86 - 7.72 (m, 2H), 7.39 (d, J = 4.4 Hz, 1H), 7.19 (dd, J = 11.5, 8.5 Hz, 1H), 7.01 (d, J = 2.1 Hz, 1H), 4.47 - 4.22 (m, 2H), 3.93 - 3.81 (m, 6H), 3.21 - 2.96 (m, 2H), 2.94 - 2.58 (m, 3H), 1.46 - 1.18 (m, 2H), 0.97 - 0.66 (m, 3H). | D | ||
| 372 | ¹H NMR (400 MHz, DMSO-d6) δ 8.68 - 8.62 (m, 1H), 7.86 - 7.71 (m, 2H), 7.38 (d, J = 4.5 Hz, 1H), 7.19 (t, J = 8.9 Hz, 1H), 7.00 (d, J = 4.5 Hz, 1H), 4.49 - 4.18 (m, 2H), 3.92 - 3.82 (m, 6H), 3.16 - 2.97 (m, 1H), 2.91 - 2.54 (m, 3H), 2.37 - 2.24 (m, 1H), 1.68 - 1.35 (m, 1H), 0.95 (d, J = 6.6 Hz, 3H), 0.78 - 0.56 (m, 3H). | D | ||
| 373 | ¹H NMR (400 MHz, DMSO-d6) δ 8.65 (dd, J = 4.4, 1.6 Hz, 1H), 7.85 - 7.71 (m, 2H), 7.37 (t, J = 4.6 Hz, 1H), 7.18 (dd, J = 11.9, 8.6 Hz, 1H), 7.00 (d, J = 3.1 Hz, 1H), 4.43 - 4.19 (m, 2H), 3.91 - 3.81 (m, 6H), 3.16 - 2.57 (m, 5H), 1.45 - 1.29 (m, 2H), 1.24 - 0.99 (m, 2H), 0.95 - 0.66 (m, 3H). | D | ||
| 374 | ¹H NMR (400 MHz, DMSO-d6) d 8.65 (t, J = 4.3 Hz, 1H), 7.85 - 7.71 (m, 2H), 7.38 (dd, J = 4.4, 1.4 Hz, 1H), 7.19 (d, J = 8.6 Hz, 1H), 7.00 (d, J = 9.0 Hz, 1H), 4.49 - 4.23 (m, 2H), 3.90 - 3.81 (m, 6H), 3.21 - 2.53 (m, 5H), 1.96 - 1.85 (m, 1H), 0.84 - -0.31 (m, 4H). | D | ||
| 375 | ¹H NMR (400 MHz, DMSO-d6) δ 8.65 (d, J = 3.1 Hz, 1H), 7.91 - 7.64 (m, 2H), 7.45 - 7.30 (m, 6H), 7.29 - 6.98 (m, 2H), 4.80 - 4.21 (m, 3H), 3.99 - 3.63 (m, 6H), 3.61 - 3.42 (m, 1H), 3.31 - 2.85 (m, 3H), 1.80 - 1.39 (m, 2H), 0.83 - 0.33 (m, 3H). | D | ||
| 376 | ¹H NMR (400 MHz, DMSO-d6) δ 8.65 (dd, J = 12.3, 3.9 Hz, 1H), 7.88 - 7.66 (m, 2H), 7.53 - 7.33 (m, 6H), 7.28 - 7.03 (m, 2H), 4.82 - 4.15 (m, 3H), 3.95 - 3.71 (m, 6H), 3.67 - 3.42 (m, 1H), 3.29 - 2.84 (m, 3H), 2.11 - 1.90 (m, 1H), 1.16 - 0.45 (m, 6H). | D | ||
| 377 | ¹H NMR (400 MHz, DMSO-d6) δ 8.66 (d, J = 3.4 Hz, 1H), 7.91 - 7.61 (m, 2H), 7.53 - 7.29 (m, 6H), 7.26 - 7.11 (m, 1H), 7.11 - 7.00 (m, 1H), 4.88 - 4.16 (m, 3H), 3.97 - 3.66 (m, 6H), 3.59 - 3.40 (m, 1H), 3.29 - 2.83 (m, 3H), 1.80 - 0.38 (m, 7H). | D | ||
| 378 | ¹H NMR (400 MHz, DMSO-d6) δ 8.66 (d, J = 4.4 Hz, 1H), 7.88 - 7.68 (m, 2H), 7.51 - 7.33 (m, 6H), 7.23 - 7.13 (m, 1H), 7.06 (d, J = 19.0 Hz, 1H), 4.74 - 4.37 (m, 3H), 3.93 - 3.71 (m, 6H), 3.62 - 3.38 (m, 2H), 3.25 - 3.11 (m, 1H), 3.10 - 2.97 (m, 1H), 1.39 - 1.21 (m, 1H), 0.59 - 0.02 (m, 4H). | D | ||
| 379 | ¹H NMR (400 MHz, DMSO-d6) δ 8.66 (dd, J = 4.3, 2.3 Hz, 1H), 7.86 - 7.70 (m, 3H), 7.67 - 7.61 (m, 1H), 7.38 (dd, J = 9.5, 4.4 Hz, 1H), 7.26 - 7.14 (m, 2H), 7.07 (d, J = 23.3 Hz, 1H), 4.62 - 4.27 (m, 3H), 3.92 - 3.76 (m, 6H), 3.54 - 3.44 (m, 1H), 3.32 - 3.08 (m, 2H), 3.06 - 2.93 (m, 1H), 1.25 - 1.06 (m, 3H). | D | ||
| 380 | ¹H NMR (400 MHz, DMSO-d6) δ 8.72 - 8.54 (m, 2H), 8.01 - 7.90 (m, 1H), 7.88 - 7.66 (m, 2H), 7.59 (d, J = 7.6 Hz, 1H), 7.54 - 7.44 (m, 1H), 7.44 - 7.32 (m, 1H), 7.27 - 7.00 (m, 2H), 4.94 - 4.55 (m, 1H), 4.51 - 4.26 (m, 2H), 4.15 - 3.37 (m, 8H), 3.31 - 2.92 (m, 2H), 1.32 - 1.06 (m, 3H). | D | ||
| 381 | ¹H NMR (400 MHz, DMSO-d6) δ 8.66 (dd, J = 11.8, 3.9 Hz, 1H), 7.90 - 7.76 (m, 1H), 7.76 - 7.63 (m, 1H), 7.44 - 7.14 (m, 5H), 7.09 (d, J = 7.4 Hz, 1H), 7.03 (d, J = 8.8 Hz, 1H), 4.98 - 4.19 (m, 3H), 3.93 - 3.67 (m, 6H), 3.66 - 3.44 (m, 1H), 3.28 - 2.81 (m, 3H), 2.32 - 2.09 (m, 3H), 1.31 - 0.95 (m, 3H). | D | ||
| 382 | ¹H NMR (400 MHz, DMSO-d6) δ 8.74 - 8.59 (m, 3H), 7.93 - 7.65 (m, 3H), 7.56 - 7.44 (m, 1H), 7.43 - 7.32 (m, 1H), 7.27 - 7.12 (m, 1H), 7.06 (d, J = 23.5 Hz, 1H), 4.95 - 4.16 (m, 3H), 3.99 - 3.66 (m, 6H), 3.60 - 3.40 (m, 1H), 3.31 - 2.93 (m, 3H), 1.34 - 1.02 (m, 3H). | D | ||
| 383 | ¹H NMR (400 MHz, DMSO-d6) δ 8.96 - 8.86 (m, 2H), 8.71 - 8.61 (m, 1H), 7.89 - 7.66 (m, 2H), 7.66 - 7.56 (m, 1H), 7.44 - 7.32 (m, 1H), 7.27 - 7.00 (m, 2H), 4.92 - 4.56 (m, 1H), 4.50 - 4.23 (m, 2H), 3.95 - 3.72 (m, 6H), 3.71 - 3.55 (m, 1H), 3.28 - 2.93 (m, 3H), 1.32 - 1.06 (m, 3H). | D | ||
| 384 | ¹H NMR (400 MHz, DMSO-d6) δ 8.71 - 8.61 (m, 2H), 7.90 - 7.74 (m, 4H), 7.57 - 7.50 (m, 1H), 7.50 - 7.36 (m, 3H), 7.23 - 7.09 (m, 2H), 4.64 - 4.48 (m, 1H), 4.35 - 4.26 (m, 1H), 4.19 - 4.04 (m, 1H), 3.99 - 3.82 (m, 4H), 3.82 - 3.73 (m, 3H), 3.71 - 3.58 (m, 1H), 2.30 - 1.96 (m, 2H). | D | ||
| 385 | ¹H NMR (400 MHz, DMSO-d6) δ 12.95 (s, 1H), 8.67 (d, J = 4.1 Hz, 1H), 7.88 - 7.70 (m, 2H), 7.43 - 7.34 (m, 1H), 7.27 (s, 1H), 7.24 - 7.16 (m, 1H), 7.14 - 7.02 (m, 2H), 6.23 - 5.63 (m, 1H), 4.94 - 4.51 (m, 2H), 4.51 - 4.23 (m, 2H), 3.92 - 3.80 (m, 6H), 3.66 - 3.48 (m, 1H), 3.25 - 3.07 (m, 1H), 1.36 - 1.07 (m, 3H). | D | ||
| 386 | ¹H NMR (400 MHz, DMSO-d6) δ 8.66 (d, J = 4.0 Hz, 1H), 7.91 - 7.69 (m, 2H), 7.46 - 7.27 (m, 2H), 7.26 - 7.13 (m, 1H), 7.12 - 6.94 (m, 2H), 5.08 - 4.27 (m, 4H), 3.94 - 3.73 (m, 9H), 3.21 - 3.04 (m, 3H), 1.34 - 1.10 (m, 3H). | D | ||
| 387 | ¹H NMR (400 MHz, DMSO-d6) δ 11.49 (s, 1H), 8.67 (dd, J = 4.3, 2.0 Hz, 1H), 7.89 - 7.69 (m, 2H), 7.39 (dd, J = 9.0, 4.4 Hz, 1H), 7.20 (dd, J = 8.6, 3.3 Hz, 1H), 7.07 (d, J = 24.1 Hz, 1H), 6.91 (s, 1H), 6.56 - 6.45 (m, 1H), 6.14 (s, 1H), 4.91 - 4.18 (m, 5H), 3.98 - 3.78 (m, 6H), 3.58 - 3.47 (m, 1H), 3.19 - 2.99 (m, 1H), 1.34 - 1.10 (m, 3H). | D | ||
| 388 | ¹H NMR (400 MHz, DMSO-d6) δ 8.67 (dd, J = 4.4, 2.3 Hz, 1H), 7.87 - 7.69 (m, 2H), 7.38 (dd, J = 9.4, 4.5 Hz, 1H), 7.19 (dd, J = 8.5, 3.9 Hz, 1H), 7.06 (d, J = 22.5 Hz, 1H), 6.94 - 6.88 (m, 1H), 6.36 - 6.30 (m, 1H), 6.07 - 6.01 (m, 1H), 4.78 - 4.04 (m, 5H), 3.91 - 3.81 (m, 6H), 3.66 (d, J = 1.9 Hz, 3H), 3.52 - 3.42 (m, 1H), 3.17 - 2.94 (m, 1H), 1.27 - 1.09 (m, 3H). | D | ||
| 389 | ¹H NMR (400 MHz, DMSO-d6) δ 9.17 - 9.07 (m, 1H), 8.73 - 8.63 (m, 1H), 7.88 - 7.67 (m, 2H), 7.44 - 7.33 (m, 1H), 7.26 - 7.01 (m, 2H), 6.91 - 6.83 (m, 1H), 4.92 - 4.07 (m, 5H), 3.92 - 3.76 (m, 6H), 3.64 - 3.43 (m, 1H), 3.27 - 2.93 (m, 1H), 1.28 - 1.12 (m, 3H). | D | ||
| 390 | ¹H NMR (400 MHz, DMSO-d6) δ 11.65 - 11.59 (m, 1H), 8.67 (dd, J = 4.4, 2.5 Hz, 1H), 7.87 - 7.71 (m, 2H), 7.61 (d, J = 8.0 Hz, 1H), 7.47 - 7.37 (m, 2H), 7.24 - 7.16 (m, 2H), 7.14 - 7.02 (m, 2H), 6.82 (d, J = 8.0 Hz, 1H), 4.94 - 4.25 (m, 5H), 3.92 - 3.81 (m, 6H), 3.57 (dd, J = 13.6, 3.6 Hz, 1H), 3.24 - 3.05 (m, 1H), 1.35 - 1.16 (m, 3H). | D | ||
| 391 | ¹H NMR (400 MHz, DMSO-d6) δ 8.76 (s, 1H), 8.67 (d, J = 4.3 Hz, 1H), 7.89 - 7.67 (m, 2H), 7.39 (dd, J = 9.4, 4.4 Hz, 1H), 7.26 - 7.13 (m, 1H), 7.08 (d, J = 24.6 Hz, 1H), 6.96 (s, 1H), 4.91 - 3.97 (m, 4H), 3.93 - 3.74 (m, 6H), 3.64 - 3.45 (m, 1H), 3.25 - 2.93 (m, 2H), 1.36 - 1.09 (m, 3H). | D | ||
| 392 | ¹H NMR (400 MHz, DMSO-d6) δ 8.67 (dd, J = 4.3, 1.8 Hz, 1H), 8.61 (s, 1H), 8.56 - 8.51 (m, 1H), 7.85 - 7.71 (m, 2H), 7.38 (dd, J = 9.4, 4.5 Hz, 1H), 7.23 - 7.16 (m, 1H), 7.07 (d, J = 24.2 Hz, 1H), 4.96 - 4.23 (m, 5H), 3.91 - 3.80 (m, 6H), 3.60 - 3.44 (m, 1H), 3.22 - 2.91 (m, 1H), 1.28 - 1.09 (m, 3H). | D | ||
| 393 | ¹H NMR (400 MHz, DMSO-d6) δ 8.67 (dd, J = 4.4, 1.6 Hz, 1H), 7.86 - 7.71 (m, 2H), 7.39 (dd, J = 8.6, 4.5 Hz, 1H), 7.20 (dd, J = 8.5, 3.6 Hz, 1H), 7.07 (d, J = 22.7 Hz, 1H), 6.90 (t, J = 3.9 Hz, 1H), 6.26 (d, J = 3.3 Hz, 1H), 4.80 - 4.10 (m, 5H), 3.91 - 3.81 (m, 6H), 3.52 (dd, J = 14.3, 3.9 Hz, 1H), 3.20 - 2.98 (m, 1H), 2.32 (s, 3H), 1.30 - 1.11 (m, 3H). | D | ||
| 394 | ¹H NMR (400 MHz, DMSO-d6) δ 8.67 (dd, J = 4.3, 1.7 Hz, 1H), 7.86 - 7.71 (m, 3H), 7.70 - 7.63 (m, 1H), 7.50 - 7.31 (m, 4H), 7.19 (dd, J = 8.3, 3.4 Hz, 1H), 7.09 (d, J = 23.8 Hz, 1H), 4.84 - 4.13 (m, 5H), 3.91 - 3.78 (m, 6H), 3.63 - 3.52 (m, 1H), 3.24 - 3.02 (m, 1H), 1.36 - 1.14 (m, 3H). | D | ||
| 395 | ¹H NMR (400 MHz, DMSO-d6) δ 8.67 (dd, J = 4.3, 2.8 Hz, 1H), 8.07 - 8.00 (m, 1H), 7.97 - 7.90 (m, 1H), 7.86 - 7.70 (m, 3H), 7.51 - 7.42 (m, 2H), 7.39 (dd, J = 10.0, 4.5 Hz, 1H), 7.19 (dd, J = 8.4, 5.1 Hz, 1H), 7.08 (d, J = 23.0 Hz, 1H), 4.79 - 4.09 (m, 5H), 3.88 - 3.79 (m, 6H), 3.58 (dd, J = 13.3, 3.0 Hz, 1H), 3.24 - 3.03 (m, 1H), 1.33 - 1.14 (m, 3H). | D |
| 表3B:化合物結構、表徵數據及合成方法 | |||
| 化合物 | 結構 | 表徵數據 | 一般方法(實例2) |
| 3 | 1H NMR (400 MHz, CDCl 3) δ 8.76 (s, 1H), 8.58 (d, J = 4.3 Hz, 1H), 7.70 - 7.65 (m, 2H), 7.62 - 7.57 (m, 2H), 7.40 (s, 1H), 7.10 (d, J = 8.2 Hz, 1H), 7.02 (d, J = 4.4 Hz, 1H), 6.93 - 6.88 (m, 2H), 4.09 - 3.95 (m, 8H), 1.42 (t, J = 7.0 Hz, 3H). | C | |
| 5 | 1H NMR (400 MHz, DMSO-d 6) δ 13.35 (s, 1H), 8.67 (d, J = 4.4 Hz, 1H), 7.90 (dd, J = 8.5, 2.1 Hz, 1H), 7.79 (d, J = 2.1 Hz, 1H), 7.44 (d, J = 4.4 Hz, 1H), 7.25 - 7.15 (m, 2H), 3.89 (s, 3H), 3.86 (s, 3H). | A (實例1) | |
| 11 | 1H NMR (400 MHz, DMSO-d 6) δ 10.59 (s, 1H), 8.71 (d, J = 4.5 Hz, 1H), 8.05 - 7.94 (m, 6H), 7.51 (d, J = 4.5 Hz, 1H), 7.34 (s, 1H), 7.23 (d, J = 8.6 Hz, 1H), 3.93 - 3.89 (m, 6H), 3.85 (s, 3H). | C | |
| 267 | 1H NMR (400 MHz, DMSO-d 6) δ 10.35 (s, 1H), 8.69 (d, J = 4.5 Hz, 1H), 8.02 (dd, J = 8.5, 1.9 Hz, 1H), 7.94 (d, J = 1.9 Hz, 1H), 7.84 (dd, J = 9.0, 5.0 Hz, 2H), 7.49 (d, J = 4.5 Hz, 1H), 7.29 (s, 1H), 7.26 - 7.12 (m, 3H), 3.96 - 3.81 (m, 6H). | B | |
| 300 | 1H NMR (400 MHz, DMSO-d 6) δ 10.11 (s, 1H), 8.73 (d, J = 4.4 Hz, 1H), 8.28-8.26 (m, 2H), 7.69-7.65 (m, 5H), 7.43 (d, J = 4.4 Hz, 1H), 7.31 (s, 1H), 6.95-6.92 (m, 2H), 4.02 (q, J = 7.0 Hz, 2H), 1.33 (t, J = 7.0 Hz, 3H). | C | |
| 305 | 1H NMR (400 MHz, DMSO-d 6) δ 10.57 (s, 1H), 8.75 (d, J = 4.4 Hz, 1H), 8.29-8.26 (m, 2H), 8.00-7.98 (m, 4H), 7.68-7.66 (m, 3H), 7.45 (d, J = 4.4 Hz, 1H), 7.38 (s, 1H), 3.85 (s, 3H). | C | |
| 310 | 1H NMR (400 MHz, DMSO-d 6) δ 10.19 (s, 1H), 8.69 (d, J = 4.5 Hz, 1H), 8.02 (dd, J = 8.5, 2.1 Hz, 1H), 7.94 (d, J = 2.1 Hz, 1H), 7.49-7.48 (m, 2H), 7.27-7.21 (m, 3H), 6.93 (d, J = 8.4 Hz, 1H), 6.03 (s, 2H), 3.92-3.89 (m, 6H). | C | |
| 334 | 1H NMR (400 MHz, DMSO-d 6) δ 10.59 (s, 1H), 8.70 (d, J = 4.5 Hz, 1H), 8.09 - 7.90 (m, 6H), 7.50 (d, J = 4.5 Hz, 1H), 7.34 (s, 1H), 7.22 (d, J = 8.6 Hz, 1H), 4.31 (q, J = 7.1 Hz, 2H), 3.98 - 3.86 (m, 6H), 1.33 (t, J = 7.1 Hz, 3H). | C |
根據下列組合物製備PBS溶液(pH 7.5)並儲存在4℃下。
| 試劑 | 含量 |
| 81% 0.0667M Na 2HPO 4 | 162 mL |
| 19% 0.0667 M NaH 2PO 4 | 38 mL |
| NaCl | 0.8 g |
以0.5 mg/mL將測試化合物溶解於PBS (pH 7.5)中並渦漩90 min。使該PBS溶液循序濾過0.45,1.2,5.0 μM注射器過濾器。
分析
使用LC-MS/MS以適當稀釋之樣本測定測試化合物之濃度。
資料
各種化合物於PBS中之溶解度匯總於下表4中。溶解度範圍(ng/mL):(A)係指≥ 10,000 ng/mL;(B)係指100 < B < 10,000 ng/mL;及(C)係指≤ 100 ng/mL。
實例4:基於細胞之YFP分析
材料及儀器
| 表4:化合物之PBS溶解度 | |||||
| 化合物編號 | 溶解度範圍 | 化合物編號 | 溶解度範圍 | 化合物編號 | 溶解度範圍 |
| 1 | C | 2 | C | 3 | C |
| 6 | C | 7 | C | 8 | C |
| 9 | B | 10 | B | 11 | C |
| 12 | C | 14 | B | 15 | C |
| 16 | A | 17 | C | 18 | C |
| 19 | A | 21 | A | 28 | C |
| 31 | C | 32 | C | 33 | C |
| 34 | C | 36 | B | 39 | C |
| 41 | C | 42 | C | 43 | C |
| 46 | C | 47 | C | 48 | C |
| 51 | C | 55 | C | 56 | C |
| 57 | C | 58 | C | 62 | B |
| 63 | B | 65 | C | 69 | A |
| 72 | A | 73 | B | 75 | A |
| 76 | B | 85 | A | 86 | A |
| 92 | C | 96 | B | 97 | B |
| 100 | B | 105 | C | 106 | C |
| 109 | C | 114 | C | 121 | C |
| 125 | C | 126 | B | 127 | C |
| 130 | C | 131 | C | 132 | C |
| 133 | C | 135 | C | 136 | C |
| 139 | C | 140 | C | 141 | C |
| 142 | C | 144 | C | 145 | B |
| 146 | C | 147 | C | 149 | A |
| 151 | A | 156 | B | 157 | C |
| 158 | C | 159 | B | 160 | C |
| 161 | B | 163 | C | 164 | C |
| 165 | C | 166 | C | 167 | C |
| 168 | C | 169 | C | 170 | B |
| 178 | A | 186 | A | 204 | C |
| 210 | B | 212 | B | 256 | C |
| 257 | C | 259 | B | 271 | C |
| 272 | C | 273 | C | 274 | C |
| 276 | C | 277 | C | 280 | C |
| 281 | C | 282 | C | 283 | C |
| 284 | B |
毛喉素(Tocris cat. # 1099)、二甲基亞碸(Sigma cat. # D4540)、FLUO星歐米茄酶標儀(BMG Labtech, Ortenberg, Germany)、MARS資料分析軟體(BMG Labtech)、GraphPad Prism 5 (GraphPad Software, Inc.)
細胞培養條件
表現人類野生型CFTR及鹵化物感測器YFP-H148Q/I152L之中國倉鼠卵巢(CHO-K1)細胞係經構築並於用10% FBS、2 mM麩醯胺酸、100個單位/ml青黴素及100 µg/ml鏈黴素補充之杜爾貝科改良之伊格爾培養基(DMEM)中生長。
實驗程序
以2×10
4個細胞/孔將表現人類野生型CFTR及鹵化物感測器YFP-H148Q/I152L之中國倉鼠卵巢(CHO-K1)細胞接種於96孔微量滴定盤中並在37℃下培養48小時。然後,各孔用PBS清洗3次並於各孔中添加100 µL PBS。將毛喉素、測試化合物(100X)添加於各孔中並在37℃下培養10分鐘。受I
-離子流入通過CFTR通道影響之YFP螢光信號係於37℃,FLUO星歐米茄酶標儀中根據下列步驟量測:
i)潛在2秒;
ii)將140 mM I
-溶液100 µL添加至各孔;
iii) 6秒後開始量測YFP螢光信號;及
iv)在每0.4秒週期內進行14秒信號偵測。
使用每秒毛喉素20 µM之螢光信號作為各濃度中螢光信號數據標準化之100%活性。一式三份進行實驗且數據取平均值。用MARS資料分析軟體(BMG Labtech)及GraphPad Prism 5計算EC
50值。
資料
化合物之EC
50濃度範圍匯總於下表5中。EC
50(nM)濃度範圍:(A)係指EC
50< 200 nM;(B)係指200 ≤ EC
50<2000 nM;及(C)係指EC
50≥ 2000 nM。
實例5:短路電流量測
材料及儀器
| 表5:基於細胞之YFP分析(EC 50) | |||||
| 化合物編號 | 濃度範圍 | 化合物編號 | 濃度範圍 | 化合物編號 | 濃度範圍 |
| 1 | A | 2 | A | 3 | A |
| 4 | B | 5 | C | 6 | A |
| 7 | B | 8 | A | 9 | A |
| 10 | A | 11 | A | 12 | B |
| 13 | B | 14 | B | 15 | A |
| 16 | C | 17 | A | 18 | B |
| 19 | C | 20 | B | 21 | C |
| 22 | C | 23 | C | 24 | C |
| 25 | C | 26 | B | 27 | C |
| 28 | A | 29 | C | 30 | C |
| 31 | A | 32 | A | 33 | B |
| 34 | A | 35 | C | 36 | B |
| 37 | C | 38 | B | 39 | B |
| 40 | C | 41 | A | 42 | A |
| 43 | A | 44 | B | 45 | C |
| 46 | A | 47 | A | 48 | A |
| 49 | B | 50 | C | 51 | A |
| 53 | B | 54 | B | 55 | A |
| 56 | A | 57 | A | 58 | A |
| 59 | A | 60 | A | 61 | C |
| 62 | B | 63 | B | 64 | A |
| 65 | A | 68 | C | 69 | B |
| 70 | C | 71 | C | 72 | B |
| 73 | B | 74 | C | 75 | C |
| 76 | B | 77 | A | 78 | B |
| 80 | C | 81 | C | 82 | C |
| 83 | C | 84 | C | 85 | B |
| 86 | B | 87 | C | 88 | C |
| 89 | C | 90 | C | 91 | C |
| 92 | A | 93 | B | 94 | C |
| 95 | C | 96 | B | 97 | B |
| 98 | C | 99 | C | 100 | B |
| 101 | C | 102 | C | 103 | C |
| 104 | C | 105 | A | 106 | A |
| 107 | C | 108 | C | 109 | B |
| 110 | B | 111 | B | 112 | A |
| 113 | A | 114 | A | 115 | B |
| 116 | B | 117 | C | 118 | C |
| 119 | B | 120 | A | 121 | A |
| 122 | A | 123 | C | 124 | A |
| 125 | A | 126 | B | 127 | B |
| 128 | A | 129 | B | 130 | A |
| 131 | A | 132 | A | 133 | A |
| 134 | A | 135 | A | 136 | A |
| 137 | B | 138 | C | 139 | A |
| 140 | A | 141 | A | 142 | A |
| 144 | A | 145 | B | 146 | A |
| 147 | A | 148 | C | 149 | B |
| 150 | C | 151 | A | 152 | B |
| 153 | B | 154 | B | 155 | C |
| 156 | A | 157 | A | 158 | A |
| 159 | B | 160 | B | 161 | B |
| 162 | C | 163 | B | 164 | A |
| 165 | B | 166 | B | 167 | A |
| 168 | B | 169 | A | 170 | A |
| 171 | A | 172 | A | 173 | A |
| 174 | A | 175 | A | 176 | C |
| 177 | C | 178 | B | 179 | C |
| 180 | C | 181 | C | 182 | C |
| 183 | B | 184 | B | 185 | B |
| 186 | A | 187 | C | 188 | C |
| 189 | A | 190 | B | 191 | A |
| 192 | A | 193 | A | 194 | A |
| 195 | B | 196 | B | 197 | B |
| 198 | A | 199 | B | 200 | A |
| 201 | C | 202 | C | 203 | C |
| 204 | A | 205 | A | 206 | B |
| 207 | B | 208 | C | 209 | A |
| 210 | A | 211 | B | 212 | A |
| 213 | C | 214 | C | 215 | C |
| 216 | C | 217 | C | 218 | C |
| 219 | C | 220 | C | 221 | C |
| 222 | C | 223 | C | 224 | C |
| 225 | C | 226 | C | 227 | A |
| 228 | A | 229 | A | 230 | A |
| 231 | C | 232 | C | 233 | C |
| 234 | C | 235 | C | 236 | C |
| 237 | C | 238 | C | 239 | C |
| 240 | C | 241 | C | 242 | A |
| 243 | B | 244 | A | 245 | C |
| 246 | B | 247 | B | 248 | C |
| 249 | C | 250 | B | 251 | B |
| 252 | C | 253 | B | 254 | C |
| 255 | A | 256 | A | 257 | A |
| 258 | A | 259 | B | 260 | B |
| 261 | B | 262 | B | 263 | B |
| 264 | C | 265 | C | 266 | A |
| 267 | A | 268 | A | 269 | A |
| 270 | A | 271 | A | 272 | A |
| 273 | A | 274 | A | 275 | A |
| 276 | A | 277 | A | 278 | C |
| 279 | C | 280 | A | 281 | A |
| 282 | A | 283 | B | 284 | A |
| 285 | A | 286 | A | 287 | B |
| 288 | C | 289 | A | 290 | B |
| 291 | C | 292 | A | 293 | C |
| 294 | C | 295 | C | 296 | C |
| 297 | C | 298 | C | 299 | C |
| 300 | C | 301 | C | 302 | C |
| 303 | C | 304 | C | 305 | C |
| 306 | C | 307 | B | 308 | B |
| 309 | A | 310 | A | 311 | A |
| 312 | A | 313 | C | 314 | A |
| 315 | C | 316 | C | 317 | B |
| 318 | B | 319 | B | 320 | B |
| 321 | B | 322 | C | 323 | C |
| 324 | C | 325 | A | 326 | B |
| 327 | A | 328 | B | 329 | A |
| 330 | B | 331 | B | 332 | B |
| 333 | C | 334 | A | 335 | A |
| 336 | B | 337 | C | 338 | A |
| 339 | C | 340 | C | 341 | C |
| 342 | B | 343 | C | 344 | B |
| 345 | C | 346 | A | 347 | C |
| 348 | B | 349 | A | 350 | A |
| 351 | A | 352 | A | 353 | A |
| 354 | A | 355 | A | 356 | A |
| 357 | B | 358 | B | 359 | B |
| 360 | B | 361 | B | 362 | B |
| 363 | A | 364 | A | 365 | A |
| 366 | A | 367 | A | 368 | A |
| 369 | A | 370 | A | 371 | B |
| 372 | B | 373 | B | 374 | B |
| 375 | A | 376 | A | 377 | A |
| 378 | A | 379 | A | 380 | A |
| 381 | A | 382 | A | 383 | B |
| 384 | A |
毛喉素(Tocris cat. # 1099)、CFTR
inh-172 (Tocris cat. # 3430)、雙性殺黴素B (Tocris cat. # 6930)、二甲基亞碸(Sigma cat. # D4540)、EVC4000多通道V/I鉗夾(World Precision Instruments, Sarasota, FL)、PowerLab 4/35 (AD Instruments, Castle Hill, Australia)、Labchart Pro 7、GraphPad Prism 5 (GraphPad Software, Inc.)。
細胞培養
表現人類野生型CFTR之費舍爾大鼠甲狀腺(FRT)細胞由Alan Verkman博士(加州大學舊金山分校)提供並於用10% FBS、2 mM麩醯胺酸、100個單位/ml青黴素及100 µg/ml鏈黴素補充之DMEM/F12培養基(1:1)中生長。
實驗程序
將含有表現CFTR之FRT細胞之膜嵌套插入物安裝於尤斯室(Ussing chamber) (Physiologic Instruments, San Diego, CA)中。頂端浴充滿半Cl
-溶液及基底外側浴充滿HCO
3緩衝液以產生跨上皮Cl-梯度(頂端,64 mM;基底外側,129 mM),且該基底外側膜用250 µg/mL雙性殺黴素B透化。將細胞浸泡20 min穩定期並在37℃下用95% O
2/5% CO
2充氣。將毛喉素、測試化合物及CFTR
inh-172添加至該頂端及基底外側浴溶液。用EVC4000多通道V/I鉗夾(World Precision Instruments, Sarasota, FL)量測頂端膜電流及短路電流並使用PowerLab 4/35 (AD Instruments, Castle Hill, Australia)記錄。收集資料並用ADInstruments採集軟體Labchart Pro 7軟體分析。採樣率係4 Hz。使用毛喉素20 µM之信號作為數據標準化中之100%活性並用GraphPad Prism 5計算EC
50。
資料
EC
50濃度範圍匯總於下表6中。EC
50(nM)濃度範圍:(A)係指EC
50< 200 nM;(B)係指200 ≤ EC
50<2000 nM;及(C)係指EC
50≥ 2000 nM。
實例6:莨菪鹼誘導之眼淚體積減少模型中之CFTR調節劑
| 表6:短路電流量測(EC 50) | |||||
| 化合物編號 | 濃度範圍 | 化合物編號 | 濃度範圍 | 化合物編號 | 濃度範圍 |
| 2 | B | 3 | A | 6 | A |
| 7 | C | 8 | B | 9 | C |
| 10 | B | 11 | A | 12 | C |
| 14 | C | 15 | A | 17 | A |
| 28 | A | 31 | A | 33 | C |
| 36 | C | 41 | B | 69 | C |
| 72 | C | 78 | B | 86 | C |
| 96 | C | 97 | B | 100 | B |
| 105 | B | 106 | C | 111 | C |
| 126 | C | 127 | B | 129 | C |
| 130 | B | 131 | A | 132 | B |
| 133 | A | 135 | A | 136 | A |
| 137 | B | 140 | A | 141 | A |
| 142 | A | 144 | A | 146 | A |
| 147 | A | 149 | C | 151 | B |
| 158 | A | 159 | B | 186 | B |
| 197 | B | 198 | A | 200 | A |
| 205 | A | 210 | B | 212 | C |
| 256 | A | 257 | B | 259 | B |
| 271 | A | 274 | A | 277 | A |
| 280 | A | 285 | A | 289 | A |
此實例證實在如由莨菪鹼誘導之眼淚體積減少模型中,投藥CFTR調節劑化合物之小鼠中眼淚體積之變化。
材料
使用七週齡C57BL/6雌性小鼠。
莨菪鹼氫溴酸鹽購買自Sigma Aldrich (Cat No. S0929),溶解於鹽水中,並在使用前殺菌。
Zone-Quick酚紅線(phenol red thread)獲自Menicon。
製備磷酸鹽緩衝液(PBS,pH 7.5,17% 0.0667 M NaH
2PO
4/83% 0.066 M Na
2HPO
4)。
將用於此實驗中之測試化合物溶解於含有1%表面活性劑之PBS中。
一天3次皮下注射莨菪鹼(0.2 ml 2.5 mg/mL溶液)以在小鼠中誘導眼淚體積減小。同時,將測試化合物或媒劑之眼科溶液一天3次局部投與至雙眼上。在投藥前(基礎水準)及最後一次投與莨菪鹼及眼科溶液後1小時由酚紅線量測眼淚體積。藉由量測由眼淚變紅之酚紅線之長度獲得結果。研究時間表表示為圖1。
結果
第2天,注射莨菪鹼之小鼠中之眼淚量減少至基礎水準之約50%。此眼淚減少顯示相較於經媒劑治療之小鼠,投與一些測試化合物之小鼠中之減輕趨勢。
結果作為測試化合物治療組之眼淚體積與媒劑治療組之眼淚體積之比率匯總於表7中。若評估該測試化合物兩次,則使用平均值。
實例7:人類磷酸二酯酶4 (PDE4)抑制
實驗程序
| 表7:眼淚體積減少模型結果 | |||||
| 化合物編號 | 眼淚體積之比率 (測試化合物與媒劑) | 化合物編號 | 眼淚體積之比率 (測試化合物與媒劑) | 化合物編號 | 眼淚體積之比率 (測試化合物與媒劑) |
| 2 | 1.40 | 3 | 1.20 | 6 | 1.58 |
| 9 | 1.16 | 10 | 1.89 | 15 | 1.29 |
| 36 | 1.23 | 69 | 0.76 | 72 | 1.06 |
| 96 | 1.35 | 97 | 0.95 | 126 | 0.97 |
| 140 | 1.48 | 141 | 1.34 | 144 | 1.18 |
| 147 | 1.03 | 149 | 1.26 | 151 | 1.40 |
| 158 | 1.40 | 159 | 2.11 | 186 | 1.05 |
| 197 | 1.18 | 205 | 1.12 | 210 | 1.43 |
| 212 | 1.43 | 257 | 1.16 | 259 | 0.94 |
| 271 | 1.17 | 272 | 1.14 | 273 | 0.80 |
| 274 | 1.07 | 276 | 1.21 | 280 | 1.32 |
中國人類重組PDE4A1A、PDE4B1、PDE4C1及PDE4D2分別表現於各宿主細胞(昆蟲Sf9細胞,BPS Bioscience)中。10 μM測試化合物或媒劑與20 ng/ml PDE4A1A或4 ng/ml PDE4B1或8 ng/ml PDE4C1或5 ng/ml PDE4D2酶於Tris-HCl緩衝液pH 7.2中之預培養在25℃下進行15分鐘。添加另一30分鐘培養期之100 nM螢光素(FAM)標記之cAMP以開始酶促反應並在其終止後添加IMAP結合溶液。具體言之,IMAP與環核苷酸通過PDE活性產生之單磷酸核苷酸上之磷酸基複合。藉由讀取470 nm/525 nm下的螢光分光光度計信號測定形成之複合物之量。
資料
PDE4抑制效應匯總於下表8中。PDE4抑制(10 uM下之%)範圍:(A)係指≥ 80%抑制;(B)係指50% ≤抑制<80%;及(C)係指<50%抑制。
7. 等同物及藉由參考併入
| 表8:人類磷酸二酯酶4 (hPDE4)抑制 | ||||
| 化合物編號 | 10 uM下之抑制範圍% | |||
| PDE4A1A | PDE4B1 | PDE4C1 | PDE4D2 | |
| 7 | C | C | C | C |
| 10 | A | A | A | A |
| 11 | A | A | A | A |
| 12 | A | B | B | B |
| 15 | A | A | A | A |
| 33 | B | B | C | B |
| 41 | A | A | A | A |
| 96 | A | A | B | A |
| 97 | A | A | A | A |
| 105 | A | A | A | A |
| 129 | A | A | A | A |
| 135 | A | A | A | A |
| 136 | A | A | A | A |
| 144 | A | A | A | A |
| 147 | A | A | A | A |
| 151 | A | A | A | A |
| 192 | A | A | A | A |
| 194 | A | A | A | A |
| 198 | A | A | A | A |
| 205 | A | A | A | A |
| 210 | A | A | A | A |
| 239 | C | C | C | C |
| 257 | A | A | A | A |
| 287 | B | B | C | B |
| 323 | C | B | C | C |
| 352 | A | A | A | A |
| 355 | A | A | A | A |
| 380 | A | A | B | A |
| 384 | A | A | B | A |
儘管已參考較佳實施例及各種替代實施例特定顯示並描述本發明,但熟習相關領域者將瞭解可於其中在形式及細節上作出各種變化而不背離本發明之精神及範疇。
本說明中正文中引用之所有參考文獻、已授權專利及專利申請案出於所有目的均以全文引用之方式併入本文中。
結合以下實施方式及隨附圖式將更好地瞭解本發明之此等及其他特徵、態樣及優點,其中:
圖1顯示小鼠淚液體積減少活體內研究之研究時間表。
Claims (80)
- 一種式(Ia)化合物, , 或其醫藥上可接受之鹽、溶劑化物、水合物、前藥或立體異構體,其中: R 1係選自H、鹵素、視需要經取代之芳基、視需要經取代之(C 1-C 10)烷基及視需要經取代之(C 1-C 10)烷氧基; R 2係選自H、視需要經取代之(C 1-C 10)烷基、視需要經取代之環烷基、視需要經取代之芳基、視需要經取代之雜芳基及視需要經取代之雜環,及芳基、雜芳基及雜環上之視需要取代基係獨立地選自:H、OH、NH 2、NO 2、OCF 3、CF 3、鹵素、視需要經取代之胺基、視需要經取代之(C 1-C 5)烷基及視需要經取代之(C 1-C 5)烷氧基; R 4係選自 、 及 ; R 5及R 6係獨立地選自H、視需要經取代之(C 1-C 10)烷基、視需要經取代之(C 1-C 10)烯基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之單環或雙環碳環及視需要經取代之單環或雙環雜環; 或R 5及R 6連同其等連結之氮原子一起環狀連接形成視需要經取代之單環或雙環雜環; R 7係選自NR 5R 6、視需要經取代之(C 1-C 10)烷基、視需要經取代之(C 1-C 10)烷氧基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基及視需要經取代之雜環烷基; R 8係選自H及視需要經取代之(C 1-C 10)烷基;及 R 9係選自H及鹵素。
- 如請求項1之化合物,其中該R 2係具有1至3個取代基之經取代之芳基或具有1至3個取代基之經取代之雜芳基。
- 如請求項1之化合物,其中該R 2係視需要經取代之苯基或視需要經取代之雜芳基。
- 如請求項3之化合物,其中該化合物係式(Ib)化合物: , 其中: X 1係CR 10’或N; R 1b係選自H、鹵素、視需要經取代之芳基、視需要經取代之(C 1-C 10)烷基及視需要經取代之(C 1-C 10)烷氧基; R 4b係選自 、 及 ; R 5及R 6係獨立地選自H、視需要經取代之(C 1-C 10)烷基、視需要經取代之(C 1-C 10)烯基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之單環或雙環碳環及視需要經取代之單環或雙環雜環; 或R 5及R 6連同其等連結之氮原子一起環狀連接形成視需要經取代之單環或雙環雜環; R 7係選自NR 5R 6、視需要經取代之(C 1-C 10)烷基、視需要經取代之(C 1-C 10)烷氧基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基及視需要經取代之雜環烷基; R 8係選自H及視需要經取代之(C 1-C 10)烷基; R 9b係選自H及鹵素; 各R 10及R 10’係獨立地選自H、OH、NH 2、NO 2、鹵素、視需要經取代之(C 1-C 6)烷基、視需要經取代之(C 1-C 6)烷氧基及經取代之胺基;及 n係0至4。
- 如請求項4之化合物,其中各R 10及R 10’係獨立地選自H、OH、CH 3、CF 3、OCF 3、OCH 3、NO 2、F及Cl,及二甲胺。
- 如請求項5或6之化合物,其中該化合物係式(Ic)化合物: , 其中: X 2係CR 10c’或N; R 21係選自H及視需要經取代之(C 1-C 10)烷基;視需要經取代之醯基;視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之單環或雙環碳環及視需要經取代之單環或雙環雜環; R 1c係選自H、鹵素、視需要經取代之芳基、視需要經取代之(C 1-C 10)烷基及視需要經取代之(C 1-C 10)烷氧基; R 4c係選自 、 及 ; R 5及R 6係獨立地選自H、視需要經取代之(C 1-C 10)烷基、視需要經取代之(C 1-C 10)烯基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之單環或雙環碳環及視需要經取代之單環或雙環雜環;或R 5及R 6連同其等連結之氮原子一起環狀連接形成視需要經取代之單環或雙環雜環; R 7係選自NR 5R 6、視需要經取代之(C 1-C 10)烷基、視需要經取代之(C 1-C 10)烷氧基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基及視需要經取代之雜環烷基; R 8係選自H及視需要經取代之(C 1-C 10)烷基; R 9c係選自H及鹵素; 各R 10c及R 10c’係獨立地選自H、OH、NH 2、NO 2、鹵素、視需要經取代之(C 1-C 6)烷基、視需要經取代之(C 1-C 6)烷氧基及經取代之胺基;及 n係0至3。
- 如請求項7之化合物,其中該化合物係式(Id)化合物: , 其中: X 3係CR 10d’或N; 各R 21d係獨立地選自H及視需要經取代之(C 1-C 10)烷基;視需要經取代之醯基;視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之單環或雙環碳環及視需要經取代之單環或雙環雜環; R 1d係選自H、鹵素、視需要經取代之芳基、視需要經取代之(C 1-C 10)烷基及視需要經取代之(C 1-C 10)烷氧基; R 4d係選自 、 及 ; R 5及R 6係獨立地選自H、視需要經取代之(C 1-C 10)烷基、視需要經取代之(C 1-C 10)烯基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之單環或雙環碳環及視需要經取代之單環或雙環雜環; 或R 5及R 6連同其等連結之氮原子一起環狀連接形成視需要經取代之單環或雙環雜環; R 7係選自NR 5R 6、視需要經取代之(C 1-C 10)烷基、視需要經取代之(C 1-C 10)烷氧基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基及視需要經取代之雜環烷基; R 8係選自H及視需要經取代之(C 1-C 10)烷基; R 9d係選自H及鹵素; 各R 10d及R 10d’係獨立地選自H、OH、NH 2、NO 2、鹵素、視需要經取代之(C 1-C 6)烷基、視需要經取代之(C 1-C 6)烷氧基及經取代之胺基;及 n係0至2。
- 如請求項7或8之化合物,其中R 21或R 21d係甲基。
- 如請求項10之化合物,其中R 5及R 6連同其等連結之氮原子一起環狀連接提供視需要經取代之單環或雙環(C 4-C 10)雜環。
- 如請求項10或11之化合物,其中R 4係 , 其中: 環A係視需要經取代之單環或雙環(C 4-C 10)雜環; Z 1係CR 14或N,其中R 14係選自H、OH、NH 2、CN、CF 3、OCF 3、CH 2NH 2、鹵素、視需要經取代之(C 1-C 5)烷基、視需要經取代之(C 1-C 5)烷氧基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之碳環及視需要經取代之雜環;及 R 16係選自H、鹵素、-OR 22a、-C(O)R 22b、-CO 2R 22c及-C(O)N R 50R 60、-NR 50R 60、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之碳環、視需要經取代之雜環、視需要經取代之(C 1-C 5)烷基及視需要經取代之(C 1-C 5)烷氧基; R 22a、R 22b及R 22c係獨立地選自H、視需要經取代之(C 1-C 10)烷基、視需要經取代之環烷基、視需要經取代之芳基、視需要經取代之雜芳基及視需要經取代之雜環;及 R 50及R 60係獨立地選自H、視需要經取代之(C 1-C 10)烷基、視需要經取代之(C 1-C 10)烯基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之單環或雙環碳環及視需要經取代之單環或雙環雜環; 或R 50及R 60連同其等連結之氮原子一起環狀連接形成視需要經取代之雜環或視需要經取代之雜芳基。
- 如請求項12之化合物,其中當該A環係哌啶時,則R 16包含至少一個選自以下之環形基團:視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之碳環、視需要經取代之雜環。
- 如請求項12之化合物,其中該A環係視需要經取代之哌嗪、吡咯啶或氮雜環丁烷。
- 如請求項14之化合物,其中該A環係: , 其中: R 23至R 26各係獨立地選自H、鹵素、OH、NO 2、OCF 3、CF 3、視需要經取代之胺基、視需要經取代之(C 1-C 6)烷基、視需要經取代之(C 1-C 6)烷氧基、視需要經取代之環烷基、視需要經取代之芳基、視需要經取代之雜芳基及視需要經取代之雜環;或 R 23-R 24及R 25-R 26中之一或兩者連同其等連結之碳原子一起環狀連接形成視需要經取代之碳環或視需要經取代之雜環;及 R 40a及R 40b各係獨立地選自H、鹵素、OH、NO 2、OCF 3、CF 3、視需要經取代之胺基、視需要經取代之(C 1-C 6)烷基、視需要經取代之(C 1-C 6)烷氧基、視需要經取代之環烷基、視需要經取代之芳基、視需要經取代之雜芳基及視需要經取代之雜環。
- 如請求項15之化合物,其中: R 23係選自視需要經取代之(C 1-C 6)烷基、視需要經取代之環烷基;及 R 24至R 26、R 40a及R 40b各為H。
- 如請求項15之化合物,其中: R 23、R 25及R 40b中之兩者係獨立地選自視需要經取代之(C 1-C 6)烷基、視需要經取代之環烷基; R 23、R 25及R 40b中之另一者係H;及 R 24、R 26及R 40a各為H。
- 如請求項15之化合物,其中: R 23及R 24連同其等連結之碳原子一起環狀連接形成碳環,或R 23及R 24各係獨立地選自視需要經取代之(C 1-C 6)烷基及視需要經取代之環烷基;及 R 25至R 26、R 40a及R 40b各為H。
- 如請求項12至19中任一項之化合物,其中R 16係: -(R 110) nR 210, 其中: 各R 110係獨立地選自視需要經取代之(C 1-C 6)烷基、 、-C(O)(R 110a)n 1、-C(O)O(R 110b)n 2、-S(O)(R 110c)n 3、-SO 2(R 110d)n 4及-C(O)NR 27(R 110e)n 5;其中R 110a至R 110e各獨立地係視需要經取代之(C 1-C 6)烷基、 ;R 27至R 28各係獨立地選自H及視需要經取代之(C 1-C 6)烷基;及n至n 5各獨立地係0至3;及 R 210係選自視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之碳環及視需要經取代之雜環。
- 如請求項20之化合物,其中: R 110係選自-C(O)-、-C(O)O-、-C(O)NH-、-S(O)-及-SO 2-;及 R 210係選自視需要經取代之芳基及視需要經取代之雜芳基。
- 如請求項10之化合物,其中R 5係H或Me,及R 6係選自: 、 及 ; 其中: Y 1、Y 2及Y 3係獨立地選自CR 14及N; Z係選自O、S、CHR 11及NR 12; n係0至4; R 11係選自H、NH 2、CN、CH 2NH 2、NO 2、鹵素、OR 2a、C(O)R 2b、CO 2R 2c、C(O)NR 5R 6、視需要經取代之胺基、視需要經取代之(C 1-C 5)烷基及視需要經取代之(C 1-C 5)烷氧基,及視需要經取代之雜環; R 12係選自H、NH 2、鹵素、C(O)R 2d、CO 2R 2e、C(O)NR 5R 6及視需要經取代之(C 1-C 5)烷基; 係選自視需要經取代之(C 1-C 6)烷基-環烷基、視需要經取代之雜環烷基、視需要經取代之單環或雙環(C 4-C 10)碳環及視需要經取代之單環或雙環(C 4-C 10)雜環; R 13係選自H、NH 2、CN、CH 2NH 2、NO 2、鹵素、OR 2f、C(O)R 2g、CO 2R 2h、C(O)NR 5R 6、NR 5R 6、NHC(O)R 2、視需要經取代之(C 1-C 5)烷基及視需要經取代之(C 1-C 5)烷氧基,及視需要經取代之雜環; R 14係選自H、OH、NH 2、CN、CF 3、OCF 3、CH 2NH 2、鹵素、CO 2R 2、C(O)NR 5R 6、視需要經取代之(C 1-C 5)烷基、視需要經取代之(C 1-C 5)烷氧基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之碳環及視需要經取代之雜環; R 15係選自H、鹵素、NHC(O)R 2i、OR 2j、C(O)R 2k、OC(O)R 2l、CO 2R 2m、C(O)NR 5R 6、NR 5R 6、視需要經取代之(C 1-C 5)烷基、視需要經取代之(C 1-C 5)烷氧基、視需要經取代之環烷基及視需要經取代之雜環; R 20係選自H、鹵素、視需要經取代之(C 1-C 5)烷基、視需要經取代之(C 1-C 5)烷氧基、視需要經取代之碳環及視需要經取代之雜環;及 R 2a至R 2m係獨立地選自H、視需要經取代之(C 1-C 10)烷基、視需要經取代之環烷基、視需要經取代之芳基、視需要經取代之雜芳基及視需要經取代之雜環,及烷基、環烷基、芳基、雜芳基及雜環上之視需要取代基係獨立地選自:H、OH、NH 2、NO 2、OCF 3、CF 3、鹵素、雜環、雜芳基、視需要經取代之胺基、視需要經取代之(C 1-C 5)烷基及視需要經取代之(C 1-C 5)烷氧基。
- 如請求項25之化合物,其中R 6係選自: , 其中: 環B及環C各係獨立地選自視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之碳環及視需要經取代之雜環; 各R 111係獨立地選自視需要經取代之(C 1-C 6)烷基、 、-C(O)(R 111a)p 1、-C(O)O(R 111b)p 2、-S(O)(R 111c)p 3、-SO 2(R 111d)p 4及-C(O)NR 27(R 111e)p 5;其中R 111a至R 111e各獨立地係視需要經取代之(C 1-C 6)烷基、 ; R 27至R 28各係獨立地選自H及視需要經取代之(C 1-C 6)烷基;及 p至p 5各獨立地係0至3。
- 如請求項26之化合物,其中該B環及該C環中之一或兩者係視需要經取代之哌嗪。
- 如請求項29之化合物,其中R 13係-C(O)OR 41a、-NHC(O)R 41b、-C(O)NHR 41c、C(O)R 41d、C(O)NH 2、雜環(例如,嗎啉、哌啶、嗎啉-3-酮),其中R 41a至R 41d係獨立地選自H、視需要經取代之(C 1-C 6)烷基、視需要經取代之雜環(例如,嗎啉、哌啶、嗎啉-3-酮),及視需要經取代之(C 1-C 6)烷基-雜環。
- 如請求項32之化合物,其中Y 2及Y 3各為CR 14。
- 如請求項32或33之化合物,其中: 各R 14係獨立地選自H、OH、NH 2、CN、CF 3、OCF 3、CH 2NH 2、鹵素、-C(O)R 42f、-OC(O)R 42g、視需要經取代之(C 1-C 5)烷基及視需要經取代之(C 1-C 5)烷氧基;及 R 15係選自H、鹵素、-OC(O)R 42a、-C(O)R 42b、-C(O)NHR 42c、R 42d或-OR 42e,其中R 42a至R 42g係獨立地選自-OH、視需要經取代之胺基、視需要經取代之(C 1-C 6)烷基、視需要經取代之環烷基、視需要經取代之(C 1-C 10)烷氧基、視需要經取代之雜環、視需要經取代之-O-(C 1-C 6)烷基-雜環,及胺基酸。
- 如請求項42之化合物,其中R 7係選自視需要經取代之N-苯胺基、視需要經取代之苯基及視需要經取代之雙環碳環。
- 如請求項1至44中任一項之化合物,其中該化合物係表1之化合物。
- 如請求項1至44中任一項之化合物,其中該化合物不為表2之化合物。
- 一種醫藥組合物,其包含: 治療有效量之式(Ia)化合物: , 或其醫藥上可接受之鹽、溶劑化物、水合物、前藥或立體異構體,其中: R 1係選自H、鹵素、視需要經取代之芳基、視需要經取代之(C 1-C 10)烷基及視需要經取代之(C 1-C 10)烷氧基; R 2係選自H、視需要經取代之(C 1-C 10)烷基、視需要經取代之環烷基、視需要經取代之芳基、視需要經取代之雜芳基及視需要經取代之雜環,及芳基、雜芳基及雜環上之視需要取代基係獨立地選自:H、OH、NH 2、NO 2、OCF 3、CF 3、-鹵素、視需要經取代之胺基、視需要經取代之(C 1-C 5)烷基及視需要經取代之(C 1-C 5)烷氧基; R 4係選自 、 及 ; R 5及R 6係獨立地選自H、視需要經取代之(C 1-C 10)烷基、視需要經取代之(C 1-C 10)烯基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之單環或雙環碳環及視需要經取代之單環或雙環雜環;或R 5及R 6連同其等連結之氮原子一起環狀連接形成視需要經取代之單環或雙環雜環; R 7係選自NR 5R 6、視需要經取代之(C 1-C 10)烷基、視需要經取代之(C 1-C 10)烷氧基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基及視需要經取代之雜環烷基; R 8係選自H及視需要經取代之(C 1-C 10)烷基;及 R 9係選自H及鹵素;及 醫藥上可接受之賦形劑。
- 如請求項48之醫藥組合物,其中該式(Ia)化合物係如請求項2至47中任一項之化合物或其醫藥上可接受之鹽、溶劑化物、水合物、前藥或立體異構體。
- 如請求項48至49中任一項之醫藥組合物,其中該組合物係眼科組合物,且包含生理上可相容之眼科媒劑。
- 如請求項48至50中任一項之醫藥組合物,其中該組合物係水溶液。
- 一種用於調節囊腫纖維化跨膜傳導調節蛋白(CFTR)之化合物,其中該化合物係如請求項1至47中之任一項。
- 一種用於調節CFTR之醫藥組合物,其中該醫藥組合物係如請求項48至51中之任一項。
- 一種用於抑制磷酸二酯酶4 (PDE4)之化合物,其中該化合物係如請求項1至47中之任一項。
- 一種用於抑制PDE4之醫藥組合物,其中該醫藥組合物係如請求項48至51中之任一項。
- 一種調節CFTR之方法,該方法包括使樣本或生物系統與有效量之化合物接觸以調節該CFTR,其中該化合物係式(Ia)化合物: , 或其醫藥上可接受之鹽、溶劑化物、水合物、前藥或立體異構體,其中: R 1係選自H、鹵素、視需要經取代之芳基、視需要經取代之(C 1-C 10)烷基及視需要經取代之(C 1-C 10)烷氧基; R 2係選自H、視需要經取代之(C 1-C 10)烷基、視需要經取代之環烷基、視需要經取代之芳基、視需要經取代之雜芳基及視需要經取代之雜環,及芳基、雜芳基及雜環上之視需要取代基係獨立地選自:H、OH、NH 2、NO 2、OCF 3、CF 3、-鹵素、視需要經取代之胺基、視需要經取代之(C 1-C 5)烷基及視需要經取代之(C 1-C 5)烷氧基; R 4係選自 、 及 ; R 5及R 6係獨立地選自H、視需要經取代之(C 1-C 10)烷基、視需要經取代之(C 1-C 10)烯基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之單環或雙環碳環及視需要經取代之單環或雙環雜環;或R 5及R 6連同其等連結之氮原子一起環狀連接形成視需要經取代之單環或雙環雜環; R 7係選自NR 5R 6、視需要經取代之(C 1-C 10)烷基、視需要經取代之(C 1-C 10)烷氧基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基及視需要經取代之雜環烷基; R 8係選自H及視需要經取代之(C 1-C 10)烷基;及 R 9係選自H及鹵素。
- 一種抑制PDE4之方法,該方法包括使樣本或生物系統與有效量之抑制PDE之化合物接觸以抑制PDE4,其中該化合物係式(Ia)化合物: , 或其醫藥上可接受之鹽、溶劑化物、水合物、前藥或立體異構體,其中: R 1係選自H、鹵素、視需要經取代之芳基、視需要經取代之(C 1-C 10)烷基及視需要經取代之(C 1-C 10)烷氧基; R 2係選自H、視需要經取代之(C 1-C 10)烷基、視需要經取代之環烷基、視需要經取代之芳基、視需要經取代之雜芳基及視需要經取代之雜環,及芳基、雜芳基及雜環上之視需要取代基係獨立地選自:H、OH、NH 2、NO 2、OCF 3、CF 3、-鹵素、視需要經取代之胺基、視需要經取代之(C 1-C 5)烷基及視需要經取代之(C 1-C 5)烷氧基; R 4係選自 、 及 ; R 5及R 6係獨立地選自H、視需要經取代之(C 1-C 10)烷基、視需要經取代之(C 1-C 10)烯基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之單環或雙環碳環及視需要經取代之單環或雙環雜環;或R 5及R 6連同其等連結之氮原子一起環狀連接形成視需要經取代之單環或雙環雜環; R 7係選自NR 5R 6、視需要經取代之(C 1-C 10)烷基、視需要經取代之(C 1-C 10)烷氧基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基及視需要經取代之雜環烷基; R 8係選自H及視需要經取代之(C 1-C 10)烷基;及 R 9係選自H及鹵素。
- 如請求項56或57之方法,其中該樣本係在活體外。
- 如請求項56或57之方法,其中該生物系統係在活體內。
- 一種治療乾眼症之方法,該方法包括對個體之眼睛投與治療有效量之如請求項1至47中任一項之化合物或治療有效量之如請求項50之眼科組合物。
- 如請求項60之方法,其進一步包括鑑定罹患乾眼症之個體。
- 如請求項60之方法,其進一步包括鑑定與該乾眼症相關聯之潛在(underlying)疾病或病症。
- 如請求項60之方法,其中該乾眼症係由一或多種以下組成之群之疾病或病症引起:乾燥性角膜結膜炎、年齡相關性乾眼症、史蒂文斯-強生症候群(Stevens-Johnson syndrome)、休格倫氏症候群(Sjogren's syndrome)、眼瘢痕性類天皰瘡、角膜損傷、感染、雷德二氏症候群(Riley-Day syndrome)、先天性無淚症(alacrima)、營養失調或缺乏、藥理副作用、隱形眼鏡不耐症、眼部壓力導致腺體及組織破壞、自體免疫疾病、免疫缺陷病症、無法眨眼之昏迷患者,或環境曝露於煙霧、煙、過度乾燥之空氣、空中懸浮微粒,淚腺缺乏症、淚腺導管阻塞、瞼板油(Meibomian)缺乏症、眼瞼開口(eyelid aperture)病症,及眼表疾病(OSD)。
- 如請求項60之方法,其中該乾眼症係由乾燥性角膜結膜炎、年齡相關性乾眼症、史蒂文斯-強生症候群、休格倫氏症候群、眼瘢痕性類天皰瘡、角膜損傷、雷德二氏症候群或先天性無淚症引起。
- 如請求項60之方法,其中該乾眼症係由營養失調或缺乏、隱形眼鏡不耐症、自體免疫疾病、免疫缺陷病症、無法眨眼之昏迷患者,或環境曝露於煙霧、煙、過度乾燥之空氣或空中懸浮微粒引起。
- 如請求項60至65中任一項之方法,其中在投與後於該個體中一或多種乾眼症症狀減少或減輕。
- 如請求項66之方法,其中該一或多種乾眼症症狀係選自乾燥、灼燒、眼癢、畏光、異物感及砂礫感。
- 如請求項60至67中任一項之方法,其進一步包括評估投與後眼中天然淚膜之恢復。
- 如請求項60至68中任一項之方法,其中對眼睛局部投與該化合物或該眼科組合物。
- 一種治療發炎性疾病之方法,其包括對個體投與治療有效量之化合物,其中該化合物係式(Ia)化合物: , 或其醫藥上可接受之鹽、溶劑化物、水合物、前藥或立體異構體,其中: R 1係選自H、鹵素、視需要經取代之芳基、視需要經取代之(C 1-C 10)烷基及視需要經取代之(C 1-C 10)烷氧基; R 2係選自H、視需要經取代之(C 1-C 10)烷基、視需要經取代之環烷基、視需要經取代之芳基、視需要經取代之雜芳基及視需要經取代之雜環,及芳基、雜芳基及雜環上之視需要取代基係獨立地選自:H、OH、NH 2、NO 2、OCF 3、CF 3、-鹵素、視需要經取代之胺基、視需要經取代之(C 1-C 5)烷基及視需要經取代之(C 1-C 5)烷氧基; R 4係選自 、 及 ; R 5及R 6係獨立地選自H、視需要經取代之(C 1-C 10)烷基、視需要經取代之(C 1-C 10)烯基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之單環或雙環碳環及視需要經取代之單環或雙環雜環;或R 5及R 6連同其等連結之氮原子一起環狀連接形成視需要經取代之單環或雙環雜環; R 7係選自NR 5R 6、視需要經取代之(C 1-C 10)烷基、視需要經取代之(C 1-C 10)烷氧基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基及視需要經取代之雜環烷基; R 8係選自H及視需要經取代之(C 1-C 10)烷基;及 R 9係選自H及鹵素。
- 如請求項70之方法,其中該個體患有發炎性疾病。
- 如請求項70或71之方法,其中該發炎性疾病係慢性發炎性疾病。
- 如請求項70或71之方法,其中該發炎性疾病係急性發炎性疾病。
- 如請求項70至73中任一項之方法,其中該發炎性疾病係選自慢性阻塞性肺病(COPD)、哮喘、發炎性呼吸道疾病、牛皮癬、牛皮癬性病症、異位性皮膚炎、發炎性腸病(IBD)、類風溼性關節炎、關節黏連性脊椎炎、神經發炎及結膜炎。
- 如請求項70至73中任一項之方法,其中該發炎性疾病係發炎性皮膚疾病。
- 一種治療CFTR相關適應症之方法,其包括對有需要個體投與治療有效量之化合物,其中該化合物為式(Ia)化合物: , 或其醫藥上可接受之鹽、溶劑化物、水合物、前藥或立體異構體,其中: R 1係選自H、鹵素、視需要經取代之芳基、視需要經取代之(C 1-C 10)烷基及視需要經取代之(C 1-C 10)烷氧基; R 2係選自H、視需要經取代之(C 1-C 10)烷基、視需要經取代之環烷基、視需要經取代之芳基、視需要經取代之雜芳基及視需要經取代之雜環,及芳基、雜芳基及雜環上之視需要取代基係獨立地選自:H、OH、NH 2、NO 2、OCF 3、CF 3、-鹵素、視需要經取代之胺基、視需要經取代之(C 1-C 5)烷基及視需要經取代之(C 1-C 5)烷氧基; R 4係選自 、 及 ; R 5及R 6係獨立地選自H、視需要經取代之(C 1-C 10)烷基、視需要經取代之(C 1-C 10)烯基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基、視需要經取代之雜環烷基、視需要經取代之單環或雙環碳環及視需要經取代之單環或雙環雜環;或R 5及R 6連同其等連結之氮原子一起環狀連接形成視需要經取代之單環或雙環雜環; R 7係選自NR 5R 6、視需要經取代之(C 1-C 10)烷基、視需要經取代之(C 1-C 10)烷氧基、視需要經取代之芳基、視需要經取代之雜芳基、視需要經取代之芳基烷基、視需要經取代之環烷基及視需要經取代之雜環烷基; R 8係選自H及視需要經取代之(C 1-C 10)烷基;及 R 9係選自H及鹵素。
- 如請求項76之方法,其中該CFTR相關適應症係選自慢性阻塞性肺病(COPD)、哮喘、支氣管炎、支氣管擴張、乳糜瀉、便祕、膽汁淤積性肝病、慢性鼻竇炎及肝損害。
- 如請求項56至77中任一項之方法,其中該式(Ia)化合物或其醫藥上可接受之鹽、溶劑化物、水合物、前藥或立體異構體係如請求項1至47中之任一項。
- 如請求項78之方法,其中該式(Ia)化合物係表1或表2之化合物,或其醫藥上可接受之鹽、溶劑化物、水合物、前藥或立體異構體。
- 如請求項78之方法,其中該式(Ia)化合物係表1之化合物,或其醫藥上可接受之鹽、溶劑化物、水合物、前藥或立體異構體。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US202063104979P | 2020-10-23 | 2020-10-23 | |
| US63/104,979 | 2020-10-23 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| TW202233620A true TW202233620A (zh) | 2022-09-01 |
Family
ID=81290147
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| TW110139341A TW202233620A (zh) | 2020-10-23 | 2021-10-22 | Cftr調節劑化合物、組合物及其用途 |
Country Status (15)
| Country | Link |
|---|---|
| US (2) | US11827640B2 (zh) |
| EP (1) | EP4232451A4 (zh) |
| JP (1) | JP2023547389A (zh) |
| KR (1) | KR20230096026A (zh) |
| CN (1) | CN116348468A (zh) |
| AR (1) | AR123884A1 (zh) |
| AU (1) | AU2021363703A1 (zh) |
| CA (1) | CA3196061A1 (zh) |
| CL (1) | CL2023001139A1 (zh) |
| CO (1) | CO2023006647A2 (zh) |
| IL (1) | IL302247A (zh) |
| MX (1) | MX2023004712A (zh) |
| TW (1) | TW202233620A (zh) |
| UY (1) | UY39482A (zh) |
| WO (1) | WO2022084741A1 (zh) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN114380835B (zh) * | 2022-01-06 | 2022-12-27 | 南京桦冠生物技术有限公司 | 一种7-(3,4-二甲氧苯基)-2-吡唑[1,5-a]嘧啶羧酸的制备方法 |
| WO2024096629A1 (ko) * | 2022-11-02 | 2024-05-10 | 일동제약 주식회사 | Cftr 조절제 화합물을 포함하는 점안용 조성물 |
Family Cites Families (35)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4178449A (en) | 1978-04-17 | 1979-12-11 | American Cyanamid Company | Pyrazolo[1,5-a]pyrimidines and imidazo-[1,5-a]pyrimidines |
| US4281000A (en) | 1979-07-09 | 1981-07-28 | American Cyanamid Company | Substituted pyrazolo (1,5-a)pyrimidines and their use as anxiolytic agents |
| CA2107479C (en) | 1991-04-22 | 1997-12-16 | Makoto Inoue | Pyrazolo[1,5-a]pyrimidine derivatives and anti-inflammatory agent containing the same |
| CA2465326C (en) * | 2001-11-01 | 2011-03-29 | Icagen, Inc. | Pyrazolopyrimidines for decreasing ion flow through a voltage-dependent sodium channel |
| DE60319820T2 (de) * | 2002-06-04 | 2009-03-26 | Schering Corp. | Pyrazoloä1,5-aüpyrimidin-verbindungen als antivirale agentien |
| JP2004170323A (ja) | 2002-11-22 | 2004-06-17 | Sumitomo Pharmaceut Co Ltd | 皮膚疾患治療剤のスクリーニング方法 |
| EP1608369B1 (en) | 2003-03-28 | 2013-06-26 | Novartis Vaccines and Diagnostics, Inc. | Use of organic compounds for immunopotentiation |
| WO2004089416A2 (en) * | 2003-04-11 | 2004-10-21 | Novo Nordisk A/S | Combination of an 11beta-hydroxysteroid dehydrogenase type 1 inhibitor and an antihypertensive agent |
| WO2004089471A2 (en) | 2003-04-11 | 2004-10-21 | Novo Nordisk A/S | NEW PYRAZOLO[1,5-a] PYRIMIDINES DERIVATIVES AND PHARMACEUTICAL USE THEREOF |
| US20070270408A1 (en) | 2003-04-11 | 2007-11-22 | Novo Nordisk A/S | Pharmaceutical use of substituted pyrazolo[1,5-a]pyrimidines |
| US20070129383A1 (en) * | 2003-10-17 | 2007-06-07 | Hiroshi Kuramochi | Substituted 2-amino-[1,2,4]triazolo[1,5-a]pyrimidine derivative and use thereof |
| DE602004025747D1 (de) | 2004-01-14 | 2010-04-08 | Mallinckrodt Inc | Zweiphasiges verfahren zur synthese ausgewählter pyrazolopyrimidine |
| US20080051409A1 (en) | 2004-08-02 | 2008-02-28 | Peter Gmeiner | Indolizine Carboxamides and Aza and Diaza Derivatives Thereof |
| EP1849465A4 (en) | 2005-02-18 | 2008-12-24 | Takeda Pharmaceutical | AGENT FOR CONTROLLING THE FUNCTION OF THE GPR34 RECEPTOR |
| CA2623982C (en) | 2005-10-21 | 2012-01-10 | Mitsubishi Tanabe Pharma Corporation | Pyrazolo[1,5-a]pyrimidine compounds as cannabinoid receptor antagonists |
| AR061793A1 (es) | 2006-07-05 | 2008-09-24 | Mitsubishi Tanabe Pharma Corp | Compuesto de pirazolo[1,5-a] pirimidina y composicion farmaceutica |
| WO2008045664A2 (en) | 2006-10-06 | 2008-04-17 | Kalypsys, Inc. | Heterocyclic pde4 inhibitors as antiinflammatory agents |
| WO2008056176A1 (en) * | 2006-11-10 | 2008-05-15 | Scottish Biomedical Limited | Pyrazolopyrimidines as phosphodiesterase inhibitors |
| JP2011503103A (ja) * | 2007-11-07 | 2011-01-27 | フォールドアールエックス ファーマシューティカルズ インコーポレーティッド | タンパク質輸送の調節方法 |
| WO2010063487A1 (en) * | 2008-12-05 | 2010-06-10 | Merz Pharma Gmbh & Co. Kgaa | Pyrazolopyrimidines, a process for their preparation and their use as medicine |
| JP5578490B2 (ja) | 2008-12-26 | 2014-08-27 | 味の素株式会社 | ピラゾロピリミジン化合物 |
| WO2010086040A1 (en) | 2009-01-29 | 2010-08-05 | Biomarin Iga, Ltd. | Pyrazolo-pyrimidines for treatment of duchenne muscular dystrophy |
| WO2011050245A1 (en) | 2009-10-23 | 2011-04-28 | Yangbo Feng | Bicyclic heteroaryls as kinase inhibitors |
| WO2012000970A1 (en) | 2010-07-01 | 2012-01-05 | Cellzome Limited | Triazolopyridines as tyk2 inhibitors |
| US8883789B2 (en) * | 2011-12-14 | 2014-11-11 | Boehringer Ingelheim International Gmbh | Piperazine derivatives and their use as positive allosteric modulators of mGluR5 receptors |
| WO2013144172A1 (en) * | 2012-03-29 | 2013-10-03 | Boehringer Ingelheim International Gmbh | Novel pyrazolopyrimidines |
| US9718816B2 (en) | 2013-03-15 | 2017-08-01 | Epizyme, Inc. | 1-phenoxy-3-(alkylamino)-propan-2-ol derivatives as CARM1 inhibitors and uses thereof |
| CN103923105B (zh) | 2014-04-17 | 2016-08-24 | 北京大学 | 2-中氮茚甲酰胺类化合物及其制备和用途 |
| WO2016012896A1 (en) * | 2014-07-24 | 2016-01-28 | Pfizer Inc. | Pyrazolopyrimidine compounds |
| JP2018076234A (ja) | 2015-03-16 | 2018-05-17 | 大正製薬株式会社 | ピラゾロ[1,5−a]ピリミジン化合物 |
| US20190031630A1 (en) | 2015-12-24 | 2019-01-31 | The Regents Of The University Of California | Cftr regulators and methods of use thereof |
| CN107286156A (zh) | 2016-04-05 | 2017-10-24 | 江苏新元素医药科技有限公司 | 新型urat1抑制剂及其在医药上的应用 |
| WO2018078005A1 (en) * | 2016-10-29 | 2018-05-03 | Bayer Pharma Aktiengesellschaft | Amido-substituted azaspiro derivatives as tankyrase inhibitors |
| JP2020514323A (ja) | 2017-02-06 | 2020-05-21 | ケース ウエスタン リザーブ ユニバーシティ | 短鎖デヒドロゲナーゼ活性を調節する組成物と方法 |
| WO2018226150A1 (en) | 2017-06-05 | 2018-12-13 | Medivir Aktiebolag | Pyrazolopyrimidine as malt-1 inhibitors |
-
2021
- 2021-10-22 AR ARP210102922A patent/AR123884A1/es unknown
- 2021-10-22 CN CN202180072298.5A patent/CN116348468A/zh active Pending
- 2021-10-22 EP EP21882228.6A patent/EP4232451A4/en active Pending
- 2021-10-22 CA CA3196061A patent/CA3196061A1/en active Pending
- 2021-10-22 US US17/508,198 patent/US11827640B2/en active Active
- 2021-10-22 KR KR1020237017551A patent/KR20230096026A/ko active Search and Examination
- 2021-10-22 JP JP2023524685A patent/JP2023547389A/ja active Pending
- 2021-10-22 IL IL302247A patent/IL302247A/en unknown
- 2021-10-22 WO PCT/IB2021/000710 patent/WO2022084741A1/en active Application Filing
- 2021-10-22 TW TW110139341A patent/TW202233620A/zh unknown
- 2021-10-22 AU AU2021363703A patent/AU2021363703A1/en active Pending
- 2021-10-22 MX MX2023004712A patent/MX2023004712A/es unknown
- 2021-10-22 UY UY0001039482A patent/UY39482A/es unknown
-
2023
- 2023-04-20 CL CL2023001139A patent/CL2023001139A1/es unknown
- 2023-05-19 CO CONC2023/0006647A patent/CO2023006647A2/es unknown
- 2023-10-17 US US18/488,925 patent/US20240199623A1/en active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| IL302247A (en) | 2023-06-01 |
| CA3196061A1 (en) | 2022-04-28 |
| US20240199623A1 (en) | 2024-06-20 |
| KR20230096026A (ko) | 2023-06-29 |
| AR123884A1 (es) | 2023-01-18 |
| MX2023004712A (es) | 2023-05-09 |
| CO2023006647A2 (es) | 2023-05-29 |
| EP4232451A1 (en) | 2023-08-30 |
| US11827640B2 (en) | 2023-11-28 |
| AU2021363703A1 (en) | 2023-06-22 |
| US20230080486A1 (en) | 2023-03-16 |
| JP2023547389A (ja) | 2023-11-10 |
| UY39482A (es) | 2022-05-31 |
| EP4232451A4 (en) | 2024-11-06 |
| CN116348468A (zh) | 2023-06-27 |
| CL2023001139A1 (es) | 2023-11-17 |
| WO2022084741A1 (en) | 2022-04-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US10538498B2 (en) | 1,3,4-oxadiazole sulfonamide derivative compounds as histone deacetylase 6 inhibitor, and the pharmaceutical composition comprising the same | |
| EP1536797B1 (en) | 1-amido-4-phenyl-4-benzyloxymethyl-piperidine derivatives and related comounds as neurokinin-1 (nk-1) antagonsists for the treatment of emesis, depression, anxiety and cough | |
| DE60223715T2 (de) | Glyt1 transporter inhibitoren und deren anwendung in der behandlung von neurologischen und neuropsychiatischen krankheiten | |
| TWI557127B (zh) | 布魯頓氏酪胺酸激酶抑制劑 | |
| US20170355712A1 (en) | Amine-substituted aryl or heteroaryl compounds | |
| JP4732354B2 (ja) | グリシン輸送阻害薬としての二環式[3.1.0]誘導体 | |
| US20240199623A1 (en) | SUBSTITUTED PYRAZOLO[1,5-a]PYRIMIDINES AS CFTR MODULATORS | |
| TW201331177A (zh) | 治療活性組合物及其使用方法 | |
| BR112021015853A2 (pt) | Compostos de tieno[3,2-b]piridin-7-amina para o tratamento de disautonomia familiar | |
| KR20150042269A (ko) | N형 칼슘 채널 차단제로서의 치환된 피라졸 | |
| TW202229256A (zh) | 雜芳基甲醯胺化合物 | |
| JP2011525924A (ja) | プロリルヒドロキシラーゼ阻害剤 | |
| KR20150042271A (ko) | N형 칼슘 채널 차단제로서의 치환된 피롤로피라졸 | |
| TW202128661A (zh) | 對核受體具有活性之化合物 | |
| WO2021052501A1 (zh) | 杂环酰胺类化合物、其可药用的盐及其制备方法和用途 | |
| KR20220098160A (ko) | 아드레날린수용체 adrac2의 억제제 | |
| CN111718332B (zh) | 2-取代吡唑氨基-4-取代氨基-5-嘧啶甲酰胺类化合物、组合物及其应用 | |
| JP2023516102A (ja) | ヒストン脱アセチル化酵素6阻害剤としての1,3,4-オキサジアゾール誘導体化合物、およびそれを含む医薬組成物 | |
| KR20170067728A (ko) | 아미노설포닐계 화합물, 이의 제조 방법 및 용도 | |
| JP2023503091A (ja) | Trpv4受容体リガンド | |
| WO2023067388A1 (en) | Uses of cftr modulator and/or pde4 inhibitor compounds | |
| WO2023187677A1 (en) | N-(pyrrolidin-3-yl or piperidin-4-yl)acetamide derivatives | |
| JP2023527792A (ja) | Tlr2調節剤化合物、医薬組成物、及びそれらの使用 | |
| IL296602A (en) | n-(Heterocyclyl and heterocyclylalkyl)-3-benzylpyridine-2-amine derivatives as sstr4 agonists | |
| KR20200022710A (ko) | T-형 칼슘 채널에 활성을 가지는 피롤리딘 또는 피페리딘 화합물 |