KR20210112425A - Organic electroluminescence device and organometallic compound for organic electroluminescence device - Google Patents
Organic electroluminescence device and organometallic compound for organic electroluminescence device Download PDFInfo
- Publication number
- KR20210112425A KR20210112425A KR1020200026896A KR20200026896A KR20210112425A KR 20210112425 A KR20210112425 A KR 20210112425A KR 1020200026896 A KR1020200026896 A KR 1020200026896A KR 20200026896 A KR20200026896 A KR 20200026896A KR 20210112425 A KR20210112425 A KR 20210112425A
- Authority
- KR
- South Korea
- Prior art keywords
- formula
- group
- substituted
- unsubstituted
- carbon atoms
- Prior art date
Links
- 150000002902 organometallic compounds Chemical class 0.000 title claims abstract description 84
- 238000005401 electroluminescence Methods 0.000 title abstract description 4
- 239000000126 substance Substances 0.000 claims abstract description 13
- 150000001875 compounds Chemical class 0.000 claims description 120
- 125000004431 deuterium atom Chemical group 0.000 claims description 59
- 125000004432 carbon atom Chemical group C* 0.000 claims description 55
- 229910052805 deuterium Inorganic materials 0.000 claims description 54
- 238000000034 method Methods 0.000 claims description 42
- 125000000217 alkyl group Chemical group 0.000 claims description 30
- 125000003118 aryl group Chemical group 0.000 claims description 28
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 25
- 239000002019 doping agent Substances 0.000 claims description 23
- 125000005843 halogen group Chemical group 0.000 claims description 14
- 125000000623 heterocyclic group Chemical group 0.000 claims description 13
- 125000003277 amino group Chemical group 0.000 claims description 8
- 125000001820 oxy group Chemical group [*:1]O[*:2] 0.000 claims description 7
- 125000003808 silyl group Chemical group [H][Si]([H])([H])[*] 0.000 claims description 7
- 125000003342 alkenyl group Chemical group 0.000 claims description 6
- 229910052802 copper Inorganic materials 0.000 claims description 6
- 125000004093 cyano group Chemical group *C#N 0.000 claims description 6
- 229910052760 oxygen Inorganic materials 0.000 claims description 6
- 229910052763 palladium Inorganic materials 0.000 claims description 6
- 229910052697 platinum Inorganic materials 0.000 claims description 6
- 229910052717 sulfur Inorganic materials 0.000 claims description 6
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 claims description 5
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 4
- 229910052723 transition metal Inorganic materials 0.000 claims description 4
- 150000003624 transition metals Chemical class 0.000 claims description 4
- 125000006743 (C1-C60) alkyl group Chemical group 0.000 claims description 2
- 125000006744 (C2-C60) alkenyl group Chemical group 0.000 claims description 2
- 125000006745 (C2-C60) alkynyl group Chemical group 0.000 claims description 2
- 125000001183 hydrocarbyl group Chemical group 0.000 claims 2
- 239000010410 layer Substances 0.000 description 128
- -1 phthalocyanine compound Chemical class 0.000 description 78
- 230000015572 biosynthetic process Effects 0.000 description 73
- 238000003786 synthesis reaction Methods 0.000 description 73
- 239000000463 material Substances 0.000 description 44
- 230000005525 hole transport Effects 0.000 description 36
- 238000002347 injection Methods 0.000 description 30
- 239000007924 injection Substances 0.000 description 30
- 230000000052 comparative effect Effects 0.000 description 26
- 229910052751 metal Inorganic materials 0.000 description 20
- 239000002184 metal Substances 0.000 description 20
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 18
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 16
- 229910052757 nitrogen Inorganic materials 0.000 description 16
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 15
- 238000006243 chemical reaction Methods 0.000 description 15
- 230000000903 blocking effect Effects 0.000 description 14
- 239000000203 mixture Substances 0.000 description 13
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 12
- 239000002356 single layer Substances 0.000 description 12
- 239000002904 solvent Substances 0.000 description 12
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 9
- 238000004440 column chromatography Methods 0.000 description 9
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Substances [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 9
- 229910052938 sodium sulfate Inorganic materials 0.000 description 9
- 235000011152 sodium sulphate Nutrition 0.000 description 9
- 239000000243 solution Substances 0.000 description 9
- 125000001424 substituent group Chemical group 0.000 description 9
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Chemical compound O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 9
- 229940127204 compound 29 Drugs 0.000 description 8
- 239000011780 sodium chloride Substances 0.000 description 8
- AWXGSYPUMWKTBR-UHFFFAOYSA-N 4-carbazol-9-yl-n,n-bis(4-carbazol-9-ylphenyl)aniline Chemical compound C12=CC=CC=C2C2=CC=CC=C2N1C1=CC=C(N(C=2C=CC(=CC=2)N2C3=CC=CC=C3C3=CC=CC=C32)C=2C=CC(=CC=2)N2C3=CC=CC=C3C3=CC=CC=C32)C=C1 AWXGSYPUMWKTBR-UHFFFAOYSA-N 0.000 description 7
- LJOOWESTVASNOG-UFJKPHDISA-N [(1s,3r,4ar,7s,8s,8as)-3-hydroxy-8-[2-[(4r)-4-hydroxy-6-oxooxan-2-yl]ethyl]-7-methyl-1,2,3,4,4a,7,8,8a-octahydronaphthalen-1-yl] (2s)-2-methylbutanoate Chemical compound C([C@H]1[C@@H](C)C=C[C@H]2C[C@@H](O)C[C@@H]([C@H]12)OC(=O)[C@@H](C)CC)CC1C[C@@H](O)CC(=O)O1 LJOOWESTVASNOG-UFJKPHDISA-N 0.000 description 7
- 239000000872 buffer Substances 0.000 description 7
- 239000012153 distilled water Substances 0.000 description 7
- 125000001072 heteroaryl group Chemical group 0.000 description 7
- 150000002430 hydrocarbons Chemical group 0.000 description 7
- 239000012044 organic layer Substances 0.000 description 7
- KDLHZDBZIXYQEI-UHFFFAOYSA-N palladium Substances [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 7
- 239000011541 reaction mixture Substances 0.000 description 7
- 229920006395 saturated elastomer Polymers 0.000 description 7
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 6
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 6
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 6
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 6
- 229910052782 aluminium Inorganic materials 0.000 description 6
- 125000004429 atom Chemical group 0.000 description 6
- 229910052799 carbon Inorganic materials 0.000 description 6
- 239000003446 ligand Substances 0.000 description 6
- PQXKHYXIUOZZFA-UHFFFAOYSA-M lithium fluoride Inorganic materials [Li+].[F-] PQXKHYXIUOZZFA-UHFFFAOYSA-M 0.000 description 6
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 6
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 6
- SIOXPEMLGUPBBT-UHFFFAOYSA-N picolinic acid Chemical compound OC(=O)C1=CC=CC=N1 SIOXPEMLGUPBBT-UHFFFAOYSA-N 0.000 description 6
- 229920000767 polyaniline Polymers 0.000 description 6
- 125000000304 alkynyl group Chemical group 0.000 description 5
- 239000010949 copper Substances 0.000 description 5
- 229910044991 metal oxide Inorganic materials 0.000 description 5
- 150000004706 metal oxides Chemical class 0.000 description 5
- 125000004433 nitrogen atom Chemical group N* 0.000 description 5
- 238000012546 transfer Methods 0.000 description 5
- GEYOCULIXLDCMW-UHFFFAOYSA-N 1,2-phenylenediamine Chemical compound NC1=CC=CC=C1N GEYOCULIXLDCMW-UHFFFAOYSA-N 0.000 description 4
- ABDDQTDRAHXHOC-QMMMGPOBSA-N 1-[(7s)-5,7-dihydro-4h-thieno[2,3-c]pyran-7-yl]-n-methylmethanamine Chemical compound CNC[C@@H]1OCCC2=C1SC=C2 ABDDQTDRAHXHOC-QMMMGPOBSA-N 0.000 description 4
- VFUDMQLBKNMONU-UHFFFAOYSA-N 9-[4-(4-carbazol-9-ylphenyl)phenyl]carbazole Chemical compound C12=CC=CC=C2C2=CC=CC=C2N1C1=CC=C(C=2C=CC(=CC=2)N2C3=CC=CC=C3C3=CC=CC=C32)C=C1 VFUDMQLBKNMONU-UHFFFAOYSA-N 0.000 description 4
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 4
- 101000837344 Homo sapiens T-cell leukemia translocation-altered gene protein Proteins 0.000 description 4
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 4
- 102100028692 T-cell leukemia translocation-altered gene protein Human genes 0.000 description 4
- 239000007983 Tris buffer Substances 0.000 description 4
- XLOMVQKBTHCTTD-UHFFFAOYSA-N Zinc monoxide Chemical compound [Zn]=O XLOMVQKBTHCTTD-UHFFFAOYSA-N 0.000 description 4
- 125000003545 alkoxy group Chemical group 0.000 description 4
- 238000011161 development Methods 0.000 description 4
- 125000000524 functional group Chemical group 0.000 description 4
- 125000005842 heteroatom Chemical group 0.000 description 4
- AMGQUBHHOARCQH-UHFFFAOYSA-N indium;oxotin Chemical compound [In].[Sn]=O AMGQUBHHOARCQH-UHFFFAOYSA-N 0.000 description 4
- 229910052749 magnesium Inorganic materials 0.000 description 4
- LMDPJJFWLNRVEH-UHFFFAOYSA-N norharmine Chemical compound N1=CC=C2C3=CC=C(OC)C=C3NC2=C1 LMDPJJFWLNRVEH-UHFFFAOYSA-N 0.000 description 4
- 229910052709 silver Inorganic materials 0.000 description 4
- 239000007787 solid Substances 0.000 description 4
- 238000003756 stirring Methods 0.000 description 4
- 239000000758 substrate Substances 0.000 description 4
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 4
- 238000001931 thermography Methods 0.000 description 4
- YVTHLONGBIQYBO-UHFFFAOYSA-N zinc indium(3+) oxygen(2-) Chemical compound [O--].[Zn++].[In+3] YVTHLONGBIQYBO-UHFFFAOYSA-N 0.000 description 4
- MPDDTAJMJCESGV-CTUHWIOQSA-M (3r,5r)-7-[2-(4-fluorophenyl)-5-[methyl-[(1r)-1-phenylethyl]carbamoyl]-4-propan-2-ylpyrazol-3-yl]-3,5-dihydroxyheptanoate Chemical compound C1([C@@H](C)N(C)C(=O)C2=NN(C(CC[C@@H](O)C[C@@H](O)CC([O-])=O)=C2C(C)C)C=2C=CC(F)=CC=2)=CC=CC=C1 MPDDTAJMJCESGV-CTUHWIOQSA-M 0.000 description 3
- ATTVYRDSOVWELU-UHFFFAOYSA-N 1-diphenylphosphoryl-2-(2-diphenylphosphorylphenoxy)benzene Chemical compound C=1C=CC=CC=1P(C=1C(=CC=CC=1)OC=1C(=CC=CC=1)P(=O)(C=1C=CC=CC=1)C=1C=CC=CC=1)(=O)C1=CC=CC=C1 ATTVYRDSOVWELU-UHFFFAOYSA-N 0.000 description 3
- HYZJCKYKOHLVJF-UHFFFAOYSA-N 1H-benzimidazole Chemical group C1=CC=C2NC=NC2=C1 HYZJCKYKOHLVJF-UHFFFAOYSA-N 0.000 description 3
- GEQBRULPNIVQPP-UHFFFAOYSA-N 2-[3,5-bis(1-phenylbenzimidazol-2-yl)phenyl]-1-phenylbenzimidazole Chemical compound C1=CC=CC=C1N1C2=CC=CC=C2N=C1C1=CC(C=2N(C3=CC=CC=C3N=2)C=2C=CC=CC=2)=CC(C=2N(C3=CC=CC=C3N=2)C=2C=CC=CC=2)=C1 GEQBRULPNIVQPP-UHFFFAOYSA-N 0.000 description 3
- JYFKMOCKASWCPZ-UHFFFAOYSA-N 7-bromo-5h-pyrido[4,3-b]indole Chemical compound C1=NC=C2C3=CC=C(Br)C=C3NC2=C1 JYFKMOCKASWCPZ-UHFFFAOYSA-N 0.000 description 3
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical group C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 3
- LNUFLCYMSVYYNW-ZPJMAFJPSA-N [(2r,3r,4s,5r,6r)-2-[(2r,3r,4s,5r,6r)-6-[(2r,3r,4s,5r,6r)-6-[(2r,3r,4s,5r,6r)-6-[[(3s,5s,8r,9s,10s,13r,14s,17r)-10,13-dimethyl-17-[(2r)-6-methylheptan-2-yl]-2,3,4,5,6,7,8,9,11,12,14,15,16,17-tetradecahydro-1h-cyclopenta[a]phenanthren-3-yl]oxy]-4,5-disulfo Chemical compound O([C@@H]1[C@@H](COS(O)(=O)=O)O[C@@H]([C@@H]([C@H]1OS(O)(=O)=O)OS(O)(=O)=O)O[C@@H]1[C@@H](COS(O)(=O)=O)O[C@@H]([C@@H]([C@H]1OS(O)(=O)=O)OS(O)(=O)=O)O[C@@H]1[C@@H](COS(O)(=O)=O)O[C@H]([C@@H]([C@H]1OS(O)(=O)=O)OS(O)(=O)=O)O[C@@H]1C[C@@H]2CC[C@H]3[C@@H]4CC[C@@H]([C@]4(CC[C@@H]3[C@@]2(C)CC1)C)[C@H](C)CCCC(C)C)[C@H]1O[C@H](COS(O)(=O)=O)[C@@H](OS(O)(=O)=O)[C@H](OS(O)(=O)=O)[C@H]1OS(O)(=O)=O LNUFLCYMSVYYNW-ZPJMAFJPSA-N 0.000 description 3
- 125000006267 biphenyl group Chemical group 0.000 description 3
- 125000004122 cyclic group Chemical group 0.000 description 3
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 3
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 3
- 238000004519 manufacturing process Methods 0.000 description 3
- IBHBKWKFFTZAHE-UHFFFAOYSA-N n-[4-[4-(n-naphthalen-1-ylanilino)phenyl]phenyl]-n-phenylnaphthalen-1-amine Chemical compound C1=CC=CC=C1N(C=1C2=CC=CC=C2C=CC=1)C1=CC=C(C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C3=CC=CC=C3C=CC=2)C=C1 IBHBKWKFFTZAHE-UHFFFAOYSA-N 0.000 description 3
- 229940081066 picolinic acid Drugs 0.000 description 3
- 125000003367 polycyclic group Chemical group 0.000 description 3
- 238000001771 vacuum deposition Methods 0.000 description 3
- YJTKZCDBKVTVBY-UHFFFAOYSA-N 1,3-Diphenylbenzene Chemical group C1=CC=CC=C1C1=CC=CC(C=2C=CC=CC=2)=C1 YJTKZCDBKVTVBY-UHFFFAOYSA-N 0.000 description 2
- IYZMXHQDXZKNCY-UHFFFAOYSA-N 1-n,1-n-diphenyl-4-n,4-n-bis[4-(n-phenylanilino)phenyl]benzene-1,4-diamine Chemical compound C1=CC=CC=C1N(C=1C=CC(=CC=1)N(C=1C=CC(=CC=1)N(C=1C=CC=CC=1)C=1C=CC=CC=1)C=1C=CC(=CC=1)N(C=1C=CC=CC=1)C=1C=CC=CC=1)C1=CC=CC=C1 IYZMXHQDXZKNCY-UHFFFAOYSA-N 0.000 description 2
- AIAJGVRFXREWPK-UHFFFAOYSA-N 2,8-bis(diphenylphosphoryl)dibenzofuran Chemical compound C=1C=CC=CC=1P(C=1C=C2C3=CC(=CC=C3OC2=CC=1)P(=O)(C=1C=CC=CC=1)C=1C=CC=CC=1)(=O)C1=CC=CC=C1 AIAJGVRFXREWPK-UHFFFAOYSA-N 0.000 description 2
- STTGYIUESPWXOW-UHFFFAOYSA-N 2,9-dimethyl-4,7-diphenyl-1,10-phenanthroline Chemical compound C=12C=CC3=C(C=4C=CC=CC=4)C=C(C)N=C3C2=NC(C)=CC=1C1=CC=CC=C1 STTGYIUESPWXOW-UHFFFAOYSA-N 0.000 description 2
- JOACEYFXFYWUIK-UHFFFAOYSA-N 2-bromo-4-tert-butylpyridine Chemical compound CC(C)(C)C1=CC=NC(Br)=C1 JOACEYFXFYWUIK-UHFFFAOYSA-N 0.000 description 2
- HNWFFTUWRIGBNM-UHFFFAOYSA-N 2-methyl-9,10-dinaphthalen-2-ylanthracene Chemical compound C1=CC=CC2=CC(C3=C4C=CC=CC4=C(C=4C=C5C=CC=CC5=CC=4)C4=CC=C(C=C43)C)=CC=C21 HNWFFTUWRIGBNM-UHFFFAOYSA-N 0.000 description 2
- OBAJPWYDYFEBTF-UHFFFAOYSA-N 2-tert-butyl-9,10-dinaphthalen-2-ylanthracene Chemical compound C1=CC=CC2=CC(C3=C4C=CC=CC4=C(C=4C=C5C=CC=CC5=CC=4)C4=CC=C(C=C43)C(C)(C)C)=CC=C21 OBAJPWYDYFEBTF-UHFFFAOYSA-N 0.000 description 2
- ZVFQEOPUXVPSLB-UHFFFAOYSA-N 3-(4-tert-butylphenyl)-4-phenyl-5-(4-phenylphenyl)-1,2,4-triazole Chemical compound C1=CC(C(C)(C)C)=CC=C1C(N1C=2C=CC=CC=2)=NN=C1C1=CC=C(C=2C=CC=CC=2)C=C1 ZVFQEOPUXVPSLB-UHFFFAOYSA-N 0.000 description 2
- DHDHJYNTEFLIHY-UHFFFAOYSA-N 4,7-diphenyl-1,10-phenanthroline Chemical compound C1=CC=CC=C1C1=CC=NC2=C1C=CC1=C(C=3C=CC=CC=3)C=CN=C21 DHDHJYNTEFLIHY-UHFFFAOYSA-N 0.000 description 2
- ZOKIJILZFXPFTO-UHFFFAOYSA-N 4-methyl-n-[4-[1-[4-(4-methyl-n-(4-methylphenyl)anilino)phenyl]cyclohexyl]phenyl]-n-(4-methylphenyl)aniline Chemical compound C1=CC(C)=CC=C1N(C=1C=CC(=CC=1)C1(CCCCC1)C=1C=CC(=CC=1)N(C=1C=CC(C)=CC=1)C=1C=CC(C)=CC=1)C1=CC=C(C)C=C1 ZOKIJILZFXPFTO-UHFFFAOYSA-N 0.000 description 2
- DIVZFUBWFAOMCW-UHFFFAOYSA-N 4-n-(3-methylphenyl)-1-n,1-n-bis[4-(n-(3-methylphenyl)anilino)phenyl]-4-n-phenylbenzene-1,4-diamine Chemical compound CC1=CC=CC(N(C=2C=CC=CC=2)C=2C=CC(=CC=2)N(C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C=C(C)C=CC=2)C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C=C(C)C=CC=2)=C1 DIVZFUBWFAOMCW-UHFFFAOYSA-N 0.000 description 2
- AOQKGYRILLEVJV-UHFFFAOYSA-N 4-naphthalen-1-yl-3,5-diphenyl-1,2,4-triazole Chemical compound C1=CC=CC=C1C(N1C=2C3=CC=CC=C3C=CC=2)=NN=C1C1=CC=CC=C1 AOQKGYRILLEVJV-UHFFFAOYSA-N 0.000 description 2
- QIIQCUUHBSIRSM-UHFFFAOYSA-N 7-bromo-9h-pyrido[3,4-b]indole Chemical compound N1=CC=C2C3=CC=C(Br)C=C3NC2=C1 QIIQCUUHBSIRSM-UHFFFAOYSA-N 0.000 description 2
- VIZUPBYFLORCRA-UHFFFAOYSA-N 9,10-dinaphthalen-2-ylanthracene Chemical compound C12=CC=CC=C2C(C2=CC3=CC=CC=C3C=C2)=C(C=CC=C2)C2=C1C1=CC=C(C=CC=C2)C2=C1 VIZUPBYFLORCRA-UHFFFAOYSA-N 0.000 description 2
- UJOBWOGCFQCDNV-UHFFFAOYSA-N 9H-carbazole Chemical compound C1=CC=C2C3=CC=CC=C3NC2=C1 UJOBWOGCFQCDNV-UHFFFAOYSA-N 0.000 description 2
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonia chloride Chemical compound [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 2
- MZRVEZGGRBJDDB-UHFFFAOYSA-N N-Butyllithium Chemical compound [Li]CCCC MZRVEZGGRBJDDB-UHFFFAOYSA-N 0.000 description 2
- 229910052779 Neodymium Inorganic materials 0.000 description 2
- 229920001609 Poly(3,4-ethylenedioxythiophene) Polymers 0.000 description 2
- LSZMVESSGLHDJE-FIBGUPNXSA-N [2H]C([2H])([2H])C1=CC=NC(Br)=C1 Chemical compound [2H]C([2H])([2H])C1=CC=NC(Br)=C1 LSZMVESSGLHDJE-FIBGUPNXSA-N 0.000 description 2
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 2
- 125000002490 anilino group Chemical group [H]N(*)C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 2
- MWPLVEDNUUSJAV-UHFFFAOYSA-N anthracene Chemical compound C1=CC=CC2=CC3=CC=CC=C3C=C21 MWPLVEDNUUSJAV-UHFFFAOYSA-N 0.000 description 2
- 125000006615 aromatic heterocyclic group Chemical group 0.000 description 2
- 150000004945 aromatic hydrocarbons Chemical group 0.000 description 2
- HUMNYLRZRPPJDN-UHFFFAOYSA-N benzaldehyde Chemical compound O=CC1=CC=CC=C1 HUMNYLRZRPPJDN-UHFFFAOYSA-N 0.000 description 2
- UFVXQDWNSAGPHN-UHFFFAOYSA-K bis[(2-methylquinolin-8-yl)oxy]-(4-phenylphenoxy)alumane Chemical compound [Al+3].C1=CC=C([O-])C2=NC(C)=CC=C21.C1=CC=C([O-])C2=NC(C)=CC=C21.C1=CC([O-])=CC=C1C1=CC=CC=C1 UFVXQDWNSAGPHN-UHFFFAOYSA-K 0.000 description 2
- 229910052796 boron Inorganic materials 0.000 description 2
- 229910052791 calcium Inorganic materials 0.000 description 2
- 238000005266 casting Methods 0.000 description 2
- 229910052804 chromium Inorganic materials 0.000 description 2
- ZUOUZKKEUPVFJK-UHFFFAOYSA-N diphenyl Chemical group C1=CC=CC=C1C1=CC=CC=C1 ZUOUZKKEUPVFJK-UHFFFAOYSA-N 0.000 description 2
- DKHNGUNXLDCATP-UHFFFAOYSA-N dipyrazino[2,3-f:2',3'-h]quinoxaline-2,3,6,7,10,11-hexacarbonitrile Chemical compound C12=NC(C#N)=C(C#N)N=C2C2=NC(C#N)=C(C#N)N=C2C2=C1N=C(C#N)C(C#N)=N2 DKHNGUNXLDCATP-UHFFFAOYSA-N 0.000 description 2
- 238000011156 evaluation Methods 0.000 description 2
- 230000001747 exhibiting effect Effects 0.000 description 2
- NIHNNTQXNPWCJQ-UHFFFAOYSA-N fluorene Chemical compound C1=CC=C2CC3=CC=CC=C3C2=C1 NIHNNTQXNPWCJQ-UHFFFAOYSA-N 0.000 description 2
- 125000001153 fluoro group Chemical group F* 0.000 description 2
- 239000011521 glass Substances 0.000 description 2
- 229910052737 gold Inorganic materials 0.000 description 2
- 239000010931 gold Substances 0.000 description 2
- 229910052738 indium Inorganic materials 0.000 description 2
- APFVFJFRJDLVQX-UHFFFAOYSA-N indium atom Chemical compound [In] APFVFJFRJDLVQX-UHFFFAOYSA-N 0.000 description 2
- 238000007641 inkjet printing Methods 0.000 description 2
- 229910052741 iridium Inorganic materials 0.000 description 2
- 238000007648 laser printing Methods 0.000 description 2
- 239000002346 layers by function Substances 0.000 description 2
- 229910052744 lithium Inorganic materials 0.000 description 2
- IMKMFBIYHXBKRX-UHFFFAOYSA-M lithium;quinoline-2-carboxylate Chemical compound [Li+].C1=CC=CC2=NC(C(=O)[O-])=CC=C21 IMKMFBIYHXBKRX-UHFFFAOYSA-M 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 229910052750 molybdenum Inorganic materials 0.000 description 2
- 125000002950 monocyclic group Chemical group 0.000 description 2
- 229910052759 nickel Inorganic materials 0.000 description 2
- PXHVJJICTQNCMI-UHFFFAOYSA-N nickel Substances [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 2
- 125000002524 organometallic group Chemical group 0.000 description 2
- ATGAWOHQWWULNK-UHFFFAOYSA-I pentapotassium;[oxido(phosphonatooxy)phosphoryl] phosphate Chemical compound [K+].[K+].[K+].[K+].[K+].[O-]P([O-])(=O)OP([O-])(=O)OP([O-])([O-])=O ATGAWOHQWWULNK-UHFFFAOYSA-I 0.000 description 2
- 229910052698 phosphorus Inorganic materials 0.000 description 2
- 229920003227 poly(N-vinyl carbazole) Polymers 0.000 description 2
- 150000004059 quinone derivatives Chemical class 0.000 description 2
- 238000001953 recrystallisation Methods 0.000 description 2
- FGDZQCVHDSGLHJ-UHFFFAOYSA-M rubidium chloride Chemical compound [Cl-].[Rb+] FGDZQCVHDSGLHJ-UHFFFAOYSA-M 0.000 description 2
- 229910052710 silicon Inorganic materials 0.000 description 2
- 235000017557 sodium bicarbonate Nutrition 0.000 description 2
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 2
- MFRIHAYPQRLWNB-UHFFFAOYSA-N sodium tert-butoxide Chemical compound [Na+].CC(C)(C)[O-] MFRIHAYPQRLWNB-UHFFFAOYSA-N 0.000 description 2
- 238000004528 spin coating Methods 0.000 description 2
- PCCVSPMFGIFTHU-UHFFFAOYSA-N tetracyanoquinodimethane Chemical compound N#CC(C#N)=C1C=CC(=C(C#N)C#N)C=C1 PCCVSPMFGIFTHU-UHFFFAOYSA-N 0.000 description 2
- 229910052719 titanium Inorganic materials 0.000 description 2
- ODHXBMXNKOYIBV-UHFFFAOYSA-N triphenylamine Chemical compound C1=CC=CC=C1N(C=1C=CC=CC=1)C1=CC=CC=C1 ODHXBMXNKOYIBV-UHFFFAOYSA-N 0.000 description 2
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 2
- TYHJXGDMRRJCRY-UHFFFAOYSA-N zinc indium(3+) oxygen(2-) tin(4+) Chemical compound [O-2].[Zn+2].[Sn+4].[In+3] TYHJXGDMRRJCRY-UHFFFAOYSA-N 0.000 description 2
- BNEMLSQAJOPTGK-UHFFFAOYSA-N zinc;dioxido(oxo)tin Chemical compound [Zn+2].[O-][Sn]([O-])=O BNEMLSQAJOPTGK-UHFFFAOYSA-N 0.000 description 2
- TXBFHHYSJNVGBX-UHFFFAOYSA-N (4-diphenylphosphorylphenyl)-triphenylsilane Chemical compound C=1C=CC=CC=1P(C=1C=CC(=CC=1)[Si](C=1C=CC=CC=1)(C=1C=CC=CC=1)C=1C=CC=CC=1)(=O)C1=CC=CC=C1 TXBFHHYSJNVGBX-UHFFFAOYSA-N 0.000 description 1
- MIOPJNTWMNEORI-GMSGAONNSA-N (S)-camphorsulfonic acid Chemical compound C1C[C@@]2(CS(O)(=O)=O)C(=O)C[C@@H]1C2(C)C MIOPJNTWMNEORI-GMSGAONNSA-N 0.000 description 1
- POILWHVDKZOXJZ-ARJAWSKDSA-M (z)-4-oxopent-2-en-2-olate Chemical compound C\C([O-])=C\C(C)=O POILWHVDKZOXJZ-ARJAWSKDSA-M 0.000 description 1
- UGUHFDPGDQDVGX-UHFFFAOYSA-N 1,2,3-thiadiazole Chemical group C1=CSN=N1 UGUHFDPGDQDVGX-UHFFFAOYSA-N 0.000 description 1
- JYEUMXHLPRZUAT-UHFFFAOYSA-N 1,2,3-triazine Chemical group C1=CN=NN=C1 JYEUMXHLPRZUAT-UHFFFAOYSA-N 0.000 description 1
- BCMCBBGGLRIHSE-UHFFFAOYSA-N 1,3-benzoxazole Chemical group C1=CC=C2OC=NC2=C1 BCMCBBGGLRIHSE-UHFFFAOYSA-N 0.000 description 1
- SSPNOMJZVHXOII-UHFFFAOYSA-N 1,3-dibromo-5-tert-butylbenzene Chemical compound CC(C)(C)C1=CC(Br)=CC(Br)=C1 SSPNOMJZVHXOII-UHFFFAOYSA-N 0.000 description 1
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 1
- IANQTJSKSUMEQM-UHFFFAOYSA-N 1-benzofuran Chemical group C1=CC=C2OC=CC2=C1 IANQTJSKSUMEQM-UHFFFAOYSA-N 0.000 description 1
- FCEHBMOGCRZNNI-UHFFFAOYSA-N 1-benzothiophene Chemical group C1=CC=C2SC=CC2=C1 FCEHBMOGCRZNNI-UHFFFAOYSA-N 0.000 description 1
- 125000004973 1-butenyl group Chemical group C(=CCC)* 0.000 description 1
- SPDPTFAJSFKAMT-UHFFFAOYSA-N 1-n-[4-[4-(n-[4-(3-methyl-n-(3-methylphenyl)anilino)phenyl]anilino)phenyl]phenyl]-4-n,4-n-bis(3-methylphenyl)-1-n-phenylbenzene-1,4-diamine Chemical compound CC1=CC=CC(N(C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C=CC(=CC=2)C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C=CC(=CC=2)N(C=2C=C(C)C=CC=2)C=2C=C(C)C=CC=2)C=2C=C(C)C=CC=2)=C1 SPDPTFAJSFKAMT-UHFFFAOYSA-N 0.000 description 1
- 125000001637 1-naphthyl group Chemical group [H]C1=C([H])C([H])=C2C(*)=C([H])C([H])=C([H])C2=C1[H] 0.000 description 1
- 125000006023 1-pentenyl group Chemical group 0.000 description 1
- MYKQKWIPLZEVOW-UHFFFAOYSA-N 11h-benzo[a]carbazole Chemical group C1=CC2=CC=CC=C2C2=C1C1=CC=CC=C1N2 MYKQKWIPLZEVOW-UHFFFAOYSA-N 0.000 description 1
- VSIKJPJINIDELZ-UHFFFAOYSA-N 2,2,4,4,6,6,8,8-octakis-phenyl-1,3,5,7,2,4,6,8-tetraoxatetrasilocane Chemical compound O1[Si](C=2C=CC=CC=2)(C=2C=CC=CC=2)O[Si](C=2C=CC=CC=2)(C=2C=CC=CC=2)O[Si](C=2C=CC=CC=2)(C=2C=CC=CC=2)O[Si]1(C=1C=CC=CC=1)C1=CC=CC=C1 VSIKJPJINIDELZ-UHFFFAOYSA-N 0.000 description 1
- VCYDUTCMKSROID-UHFFFAOYSA-N 2,2,4,4,6,6-hexakis-phenyl-1,3,5,2,4,6-trioxatrisilinane Chemical compound O1[Si](C=2C=CC=CC=2)(C=2C=CC=CC=2)O[Si](C=2C=CC=CC=2)(C=2C=CC=CC=2)O[Si]1(C=1C=CC=CC=1)C1=CC=CC=C1 VCYDUTCMKSROID-UHFFFAOYSA-N 0.000 description 1
- FUGJJMVGGAWCAU-UHFFFAOYSA-N 2,2,4,4,6,6-hexakis-phenyl-1,3,5-triaza-2$l^{5},4$l^{5},6$l^{5}-triphosphacyclohexa-1,3,5-triene Chemical compound C1=CC=CC=C1P1(C=2C=CC=CC=2)=NP(C=2C=CC=CC=2)(C=2C=CC=CC=2)=NP(C=2C=CC=CC=2)(C=2C=CC=CC=2)=N1 FUGJJMVGGAWCAU-UHFFFAOYSA-N 0.000 description 1
- IXHWGNYCZPISET-UHFFFAOYSA-N 2-[4-(dicyanomethylidene)-2,3,5,6-tetrafluorocyclohexa-2,5-dien-1-ylidene]propanedinitrile Chemical compound FC1=C(F)C(=C(C#N)C#N)C(F)=C(F)C1=C(C#N)C#N IXHWGNYCZPISET-UHFFFAOYSA-N 0.000 description 1
- 125000006176 2-ethylbutyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(C([H])([H])*)C([H])([H])C([H])([H])[H] 0.000 description 1
- CINYXYWQPZSTOT-UHFFFAOYSA-N 3-[3-[3,5-bis(3-pyridin-3-ylphenyl)phenyl]phenyl]pyridine Chemical compound C1=CN=CC(C=2C=C(C=CC=2)C=2C=C(C=C(C=2)C=2C=C(C=CC=2)C=2C=NC=CC=2)C=2C=C(C=CC=2)C=2C=NC=CC=2)=C1 CINYXYWQPZSTOT-UHFFFAOYSA-N 0.000 description 1
- WCXKTQVEKDHQIY-UHFFFAOYSA-N 3-[3-[3-(3,5-dipyridin-3-ylphenyl)phenyl]-5-pyridin-3-ylphenyl]pyridine Chemical compound C1=CN=CC(C=2C=C(C=C(C=2)C=2C=NC=CC=2)C=2C=C(C=CC=2)C=2C=C(C=C(C=2)C=2C=NC=CC=2)C=2C=NC=CC=2)=C1 WCXKTQVEKDHQIY-UHFFFAOYSA-N 0.000 description 1
- BMYNFMYTOJXKLE-UHFFFAOYSA-N 3-azaniumyl-2-hydroxypropanoate Chemical compound NCC(O)C(O)=O BMYNFMYTOJXKLE-UHFFFAOYSA-N 0.000 description 1
- UFHDRXLWKJJPIY-UHFFFAOYSA-N 3-bromo-5H-pyrido[4,3-b]indole Chemical compound BrC1=CC=2NC=3C=CC=CC=3C=2C=N1 UFHDRXLWKJJPIY-UHFFFAOYSA-N 0.000 description 1
- SUISZCALMBHJQX-UHFFFAOYSA-N 3-bromobenzaldehyde Chemical compound BrC1=CC=CC(C=O)=C1 SUISZCALMBHJQX-UHFFFAOYSA-N 0.000 description 1
- 125000005917 3-methylpentyl group Chemical group 0.000 description 1
- CATUKADCLPCACU-UHFFFAOYSA-N 4-(4-aminophenyl)-3-(4-phenylphenyl)aniline Chemical compound C1=CC(N)=CC=C1C1=CC=C(N)C=C1C1=CC=C(C=2C=CC=CC=2)C=C1 CATUKADCLPCACU-UHFFFAOYSA-N 0.000 description 1
- CCAKQVWVCHJVDB-UHFFFAOYSA-N 4-[1-(4-diphenylphosphorylphenyl)cyclohexyl]-N,N-diphenylaniline Chemical compound O=P(C1=CC=CC=C1)(C1=CC=CC=C1)C1=CC=C(C=C1)C1(CCCCC1)C1=CC=C(C=C1)N(C1=CC=CC=C1)C1=CC=CC=C1 CCAKQVWVCHJVDB-UHFFFAOYSA-N 0.000 description 1
- 125000004920 4-methyl-2-pentyl group Chemical group CC(CC(C)*)C 0.000 description 1
- QYNTUCBQEHUHCS-UHFFFAOYSA-N 4-n-(3-methylphenyl)-1-n-[4-[4-(n-[4-(n-(3-methylphenyl)anilino)phenyl]anilino)phenyl]phenyl]-1-n,4-n-diphenylbenzene-1,4-diamine Chemical compound CC1=CC=CC(N(C=2C=CC=CC=2)C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C=CC(=CC=2)C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C=C(C)C=CC=2)=C1 QYNTUCBQEHUHCS-UHFFFAOYSA-N 0.000 description 1
- HNVCRBYESIZILY-UHFFFAOYSA-N 7-bromo-5H-pyrido[3,2-b]indole Chemical compound BrC=1C=CC=2C3=C(NC=2C=1)C=CC=N3 HNVCRBYESIZILY-UHFFFAOYSA-N 0.000 description 1
- GXNDURPJXSLEMM-UHFFFAOYSA-N 7-methoxy-1,3-dimethyl-9H-pyrido[3,4-b]indole Chemical compound N1=C(C)C=C2C3=CC=C(OC)C=C3NC2=C1C GXNDURPJXSLEMM-UHFFFAOYSA-N 0.000 description 1
- VARBZMZHZMZRFP-UHFFFAOYSA-N 7-methoxy-5H-pyrido[3,4-b]indole Chemical compound COC1=CCC2=C3C(=NC2=C1)C=NC=C3 VARBZMZHZMZRFP-UHFFFAOYSA-N 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical group [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- MZYDBGLUVPLRKR-UHFFFAOYSA-N 9-(3-carbazol-9-ylphenyl)carbazole Chemical compound C12=CC=CC=C2C2=CC=CC=C2N1C1=CC(N2C3=CC=CC=C3C3=CC=CC=C32)=CC=C1 MZYDBGLUVPLRKR-UHFFFAOYSA-N 0.000 description 1
- LTUJKAYZIMMJEP-UHFFFAOYSA-N 9-[4-(4-carbazol-9-yl-2-methylphenyl)-3-methylphenyl]carbazole Chemical compound C12=CC=CC=C2C2=CC=CC=C2N1C1=CC=C(C=2C(=CC(=CC=2)N2C3=CC=CC=C3C3=CC=CC=C32)C)C(C)=C1 LTUJKAYZIMMJEP-UHFFFAOYSA-N 0.000 description 1
- QXDWMAODKPOTKK-UHFFFAOYSA-N 9-methylanthracen-1-amine Chemical group C1=CC(N)=C2C(C)=C(C=CC=C3)C3=CC2=C1 QXDWMAODKPOTKK-UHFFFAOYSA-N 0.000 description 1
- MAIALRIWXGBQRP-UHFFFAOYSA-N 9-naphthalen-1-yl-10-naphthalen-2-ylanthracene Chemical compound C12=CC=CC=C2C(C2=CC3=CC=CC=C3C=C2)=C(C=CC=C2)C2=C1C1=CC=CC2=CC=CC=C12 MAIALRIWXGBQRP-UHFFFAOYSA-N 0.000 description 1
- VIJYEGDOKCKUOL-UHFFFAOYSA-N 9-phenylcarbazole Chemical compound C1=CC=CC=C1N1C2=CC=CC=C2C2=CC=CC=C21 VIJYEGDOKCKUOL-UHFFFAOYSA-N 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- ROFVEXUMMXZLPA-UHFFFAOYSA-N Bipyridyl Chemical group N1=CC=CC=C1C1=CC=CC=N1 ROFVEXUMMXZLPA-UHFFFAOYSA-N 0.000 description 1
- BTBUEUYNUDRHOZ-UHFFFAOYSA-N Borate Chemical compound [O-]B([O-])[O-] BTBUEUYNUDRHOZ-UHFFFAOYSA-N 0.000 description 1
- ZOXJGFHDIHLPTG-UHFFFAOYSA-N Boron Chemical group [B] ZOXJGFHDIHLPTG-UHFFFAOYSA-N 0.000 description 1
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical group [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 1
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- 238000004057 DFT-B3LYP calculation Methods 0.000 description 1
- 238000003775 Density Functional Theory Methods 0.000 description 1
- YLQBMQCUIZJEEH-UHFFFAOYSA-N Furan Chemical group C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 1
- 229910018068 Li 2 O Inorganic materials 0.000 description 1
- NSGDYZCDUPSTQT-UHFFFAOYSA-N N-[5-bromo-1-[(4-fluorophenyl)methyl]-4-methyl-2-oxopyridin-3-yl]cycloheptanecarboxamide Chemical compound Cc1c(Br)cn(Cc2ccc(F)cc2)c(=O)c1NC(=O)C1CCCCCC1 NSGDYZCDUPSTQT-UHFFFAOYSA-N 0.000 description 1
- CBENFWSGALASAD-UHFFFAOYSA-N Ozone Chemical compound [O-][O+]=O CBENFWSGALASAD-UHFFFAOYSA-N 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- VMHLLURERBWHNL-UHFFFAOYSA-M Sodium acetate Chemical compound [Na+].CC([O-])=O VMHLLURERBWHNL-UHFFFAOYSA-M 0.000 description 1
- FZWLAAWBMGSTSO-UHFFFAOYSA-N Thiazole Chemical group C1=CSC=N1 FZWLAAWBMGSTSO-UHFFFAOYSA-N 0.000 description 1
- YTPLMLYBLZKORZ-UHFFFAOYSA-N Thiophene Chemical group C=1C=CSC=1 YTPLMLYBLZKORZ-UHFFFAOYSA-N 0.000 description 1
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 1
- 229910052769 Ytterbium Inorganic materials 0.000 description 1
- WDJHALXBUFZDSR-UHFFFAOYSA-M acetoacetate Chemical compound CC(=O)CC([O-])=O WDJHALXBUFZDSR-UHFFFAOYSA-M 0.000 description 1
- 125000005073 adamantyl group Chemical group C12(CC3CC(CC(C1)C3)C2)* 0.000 description 1
- 125000001931 aliphatic group Chemical group 0.000 description 1
- 150000001338 aliphatic hydrocarbons Chemical group 0.000 description 1
- 125000003282 alkyl amino group Chemical group 0.000 description 1
- 125000005103 alkyl silyl group Chemical group 0.000 description 1
- 235000019270 ammonium chloride Nutrition 0.000 description 1
- 125000002178 anthracenyl group Chemical group C1(=CC=CC2=CC3=CC=CC=C3C=C12)* 0.000 description 1
- 125000005264 aryl amine group Chemical group 0.000 description 1
- 125000005104 aryl silyl group Chemical group 0.000 description 1
- 125000004104 aryloxy group Chemical group 0.000 description 1
- LPTWEDZIPSKWDG-UHFFFAOYSA-N benzenesulfonic acid;dodecane Chemical compound OS(=O)(=O)C1=CC=CC=C1.CCCCCCCCCCCC LPTWEDZIPSKWDG-UHFFFAOYSA-N 0.000 description 1
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 1
- IOJUPLGTWVMSFF-UHFFFAOYSA-N benzothiazole Chemical group C1=CC=C2SC=NC2=C1 IOJUPLGTWVMSFF-UHFFFAOYSA-N 0.000 description 1
- 239000004305 biphenyl Substances 0.000 description 1
- 235000010290 biphenyl Nutrition 0.000 description 1
- JDOBIJWMPMUWNO-UHFFFAOYSA-N bis(4-carbazol-9-ylphenyl)-diphenylsilane Chemical compound C1=CC=CC=C1[Si](C=1C=CC(=CC=1)N1C2=CC=CC=C2C2=CC=CC=C21)(C=1C=CC(=CC=1)N1C2=CC=CC=C2C2=CC=CC=C21)C1=CC=CC=C1 JDOBIJWMPMUWNO-UHFFFAOYSA-N 0.000 description 1
- XZCJVWCMJYNSQO-UHFFFAOYSA-N butyl pbd Chemical compound C1=CC(C(C)(C)C)=CC=C1C1=NN=C(C=2C=CC(=CC=2)C=2C=CC=CC=2)O1 XZCJVWCMJYNSQO-UHFFFAOYSA-N 0.000 description 1
- YVVVSJAMVJMZRF-UHFFFAOYSA-N c1cncc(c1)-c1cccc(c1)-c1cccc(c1)-c1nc(nc(n1)-c1cccc(c1)-c1cccc(c1)-c1cccnc1)-c1cccc(c1)-c1cccc(c1)-c1cccnc1 Chemical compound c1cncc(c1)-c1cccc(c1)-c1cccc(c1)-c1nc(nc(n1)-c1cccc(c1)-c1cccc(c1)-c1cccnc1)-c1cccc(c1)-c1cccc(c1)-c1cccnc1 YVVVSJAMVJMZRF-UHFFFAOYSA-N 0.000 description 1
- XJHCXCQVJFPJIK-UHFFFAOYSA-M caesium fluoride Inorganic materials [F-].[Cs+] XJHCXCQVJFPJIK-UHFFFAOYSA-M 0.000 description 1
- MIOPJNTWMNEORI-UHFFFAOYSA-N camphorsulfonic acid Chemical compound C1CC2(CS(O)(=O)=O)C(=O)CC1C2(C)C MIOPJNTWMNEORI-UHFFFAOYSA-N 0.000 description 1
- 125000004556 carbazol-9-yl group Chemical group C1=CC=CC=2C3=CC=CC=C3N(C12)* 0.000 description 1
- 125000000609 carbazolyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3NC12)* 0.000 description 1
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- 229910052801 chlorine Inorganic materials 0.000 description 1
- 125000001309 chloro group Chemical group Cl* 0.000 description 1
- 125000002676 chrysenyl group Chemical group C1(=CC=CC=2C3=CC=C4C=CC=CC4=C3C=CC12)* 0.000 description 1
- XCJYREBRNVKWGJ-UHFFFAOYSA-N copper(II) phthalocyanine Chemical compound [Cu+2].C12=CC=CC=C2C(N=C2[N-]C(C3=CC=CC=C32)=N2)=NC1=NC([C]1C=CC=CC1=1)=NC=1N=C1[C]3C=CC=CC3=C2[N-]1 XCJYREBRNVKWGJ-UHFFFAOYSA-N 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000000640 cyclooctyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 230000003111 delayed effect Effects 0.000 description 1
- TXCDCPKCNAJMEE-UHFFFAOYSA-N dibenzofuran Chemical group C1=CC=C2C3=CC=CC=C3OC2=C1 TXCDCPKCNAJMEE-UHFFFAOYSA-N 0.000 description 1
- IYYZUPMFVPLQIF-ALWQSETLSA-N dibenzothiophene Chemical group C1=CC=CC=2[34S]C3=C(C=21)C=CC=C3 IYYZUPMFVPLQIF-ALWQSETLSA-N 0.000 description 1
- VVAOPCKKNIUEEU-PHFPKPIQSA-L dichloro(cycloocta-1,5-diene)platinum(ii) Chemical compound Cl[Pt]Cl.C\1C\C=C/CC\C=C/1 VVAOPCKKNIUEEU-PHFPKPIQSA-L 0.000 description 1
- 125000002147 dimethylamino group Chemical group [H]C([H])([H])N(*)C([H])([H])[H] 0.000 description 1
- DMBHHRLKUKUOEG-UHFFFAOYSA-N diphenylamine Chemical group C=1C=CC=CC=1NC1=CC=CC=C1 DMBHHRLKUKUOEG-UHFFFAOYSA-N 0.000 description 1
- 229940060296 dodecylbenzenesulfonic acid Drugs 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 1
- 230000005284 excitation Effects 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- 125000003983 fluorenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3CC12)* 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- RBTKNAXYKSUFRK-UHFFFAOYSA-N heliogen blue Chemical compound [Cu].[N-]1C2=C(C=CC=C3)C3=C1N=C([N-]1)C3=CC=CC=C3C1=NC([N-]1)=C(C=CC=C3)C3=C1N=C([N-]1)C3=CC=CC=C3C1=N2 RBTKNAXYKSUFRK-UHFFFAOYSA-N 0.000 description 1
- 125000005241 heteroarylamino group Chemical group 0.000 description 1
- 125000002883 imidazolyl group Chemical group 0.000 description 1
- 125000001041 indolyl group Chemical group 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000002183 isoquinolinyl group Chemical group C1(=NC=CC2=CC=CC=C12)* 0.000 description 1
- 125000000842 isoxazolyl group Chemical group 0.000 description 1
- 229910052747 lanthanoid Inorganic materials 0.000 description 1
- 150000002602 lanthanoids Chemical class 0.000 description 1
- 239000004973 liquid crystal related substance Substances 0.000 description 1
- 125000000040 m-tolyl group Chemical group [H]C1=C([H])C(*)=C([H])C(=C1[H])C([H])([H])[H] 0.000 description 1
- 150000002736 metal compounds Chemical class 0.000 description 1
- 229910001092 metal group alloy Inorganic materials 0.000 description 1
- 229910001507 metal halide Inorganic materials 0.000 description 1
- 150000005309 metal halides Chemical class 0.000 description 1
- PKAUVIXBZJUYRV-UHFFFAOYSA-N methane;hydroiodide Chemical compound C.I PKAUVIXBZJUYRV-UHFFFAOYSA-N 0.000 description 1
- 125000000250 methylamino group Chemical group [H]N(*)C([H])([H])[H] 0.000 description 1
- 239000011259 mixed solution Substances 0.000 description 1
- 229910000476 molybdenum oxide Inorganic materials 0.000 description 1
- 125000002911 monocyclic heterocycle group Chemical group 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000003136 n-heptyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000001280 n-hexyl group Chemical group C(CCCCC)* 0.000 description 1
- 125000000740 n-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000001624 naphthyl group Chemical group 0.000 description 1
- 125000005184 naphthylamino group Chemical group C1(=CC=CC2=CC=CC=C12)N* 0.000 description 1
- 125000001971 neopentyl group Chemical group [H]C([*])([H])C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- QGLKJKCYBOYXKC-UHFFFAOYSA-N nonaoxidotritungsten Chemical compound O=[W]1(=O)O[W](=O)(=O)O[W](=O)(=O)O1 QGLKJKCYBOYXKC-UHFFFAOYSA-N 0.000 description 1
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 1
- 150000002894 organic compounds Chemical class 0.000 description 1
- 125000000962 organic group Chemical group 0.000 description 1
- 229910052762 osmium Inorganic materials 0.000 description 1
- SYQBFIAQOQZEGI-UHFFFAOYSA-N osmium atom Chemical compound [Os] SYQBFIAQOQZEGI-UHFFFAOYSA-N 0.000 description 1
- WCPAKWJPBJAGKN-UHFFFAOYSA-N oxadiazole Chemical group C1=CON=N1 WCPAKWJPBJAGKN-UHFFFAOYSA-N 0.000 description 1
- 125000002971 oxazolyl group Chemical group 0.000 description 1
- MPQXHAGKBWFSNV-UHFFFAOYSA-N oxidophosphanium Chemical group [PH3]=O MPQXHAGKBWFSNV-UHFFFAOYSA-N 0.000 description 1
- PQQKPALAQIIWST-UHFFFAOYSA-N oxomolybdenum Chemical compound [Mo]=O PQQKPALAQIIWST-UHFFFAOYSA-N 0.000 description 1
- 125000004430 oxygen atom Chemical group O* 0.000 description 1
- NFHFRUOZVGFOOS-UHFFFAOYSA-N palladium;triphenylphosphane Chemical compound [Pd].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 NFHFRUOZVGFOOS-UHFFFAOYSA-N 0.000 description 1
- QNGNSVIICDLXHT-UHFFFAOYSA-N para-ethylbenzaldehyde Natural products CCC1=CC=C(C=O)C=C1 QNGNSVIICDLXHT-UHFFFAOYSA-N 0.000 description 1
- 125000000538 pentafluorophenyl group Chemical group FC1=C(F)C(F)=C(*)C(F)=C1F 0.000 description 1
- 125000005561 phenanthryl group Chemical group 0.000 description 1
- 125000001484 phenothiazinyl group Chemical group C1(=CC=CC=2SC3=CC=CC=C3NC12)* 0.000 description 1
- 125000001644 phenoxazinyl group Chemical group C1(=CC=CC=2OC3=CC=CC=C3NC12)* 0.000 description 1
- XYFCBTPGUUZFHI-UHFFFAOYSA-N phosphine group Chemical group P XYFCBTPGUUZFHI-UHFFFAOYSA-N 0.000 description 1
- LFSXCDWNBUNEEM-UHFFFAOYSA-N phthalazine Chemical group C1=NN=CC2=CC=CC=C21 LFSXCDWNBUNEEM-UHFFFAOYSA-N 0.000 description 1
- 229920001643 poly(ether ketone) Polymers 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- 125000002568 propynyl group Chemical group [*]C#CC([H])([H])[H] 0.000 description 1
- FQOBINBWTPHVEO-UHFFFAOYSA-N pyrazino[2,3-b]pyrazine Chemical group N1=CC=NC2=NC=CN=C21 FQOBINBWTPHVEO-UHFFFAOYSA-N 0.000 description 1
- 125000003373 pyrazinyl group Chemical group 0.000 description 1
- 125000001725 pyrenyl group Chemical group 0.000 description 1
- PBMFSQRYOILNGV-UHFFFAOYSA-N pyridazine Chemical group C1=CC=NN=C1 PBMFSQRYOILNGV-UHFFFAOYSA-N 0.000 description 1
- GRJJQCWNZGRKAU-UHFFFAOYSA-N pyridin-1-ium;fluoride Chemical compound F.C1=CC=NC=C1 GRJJQCWNZGRKAU-UHFFFAOYSA-N 0.000 description 1
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 1
- YEYHFKBVNARCNE-UHFFFAOYSA-N pyrido[2,3-b]pyrazine Chemical group N1=CC=NC2=CC=CN=C21 YEYHFKBVNARCNE-UHFFFAOYSA-N 0.000 description 1
- BWESROVQGZSBRX-UHFFFAOYSA-N pyrido[3,2-d]pyrimidine Chemical group C1=NC=NC2=CC=CN=C21 BWESROVQGZSBRX-UHFFFAOYSA-N 0.000 description 1
- 125000000714 pyrimidinyl group Chemical group 0.000 description 1
- 125000000168 pyrrolyl group Chemical group 0.000 description 1
- 125000002294 quinazolinyl group Chemical group N1=C(N=CC2=CC=CC=C12)* 0.000 description 1
- 125000002943 quinolinyl group Chemical group N1=C(C=CC2=CC=CC=C12)* 0.000 description 1
- 125000001567 quinoxalinyl group Chemical group N1=C(C=NC2=CC=CC=C12)* 0.000 description 1
- 239000002994 raw material Substances 0.000 description 1
- 238000005215 recombination Methods 0.000 description 1
- 230000006798 recombination Effects 0.000 description 1
- WFUBYPSJBBQSOU-UHFFFAOYSA-M rubidium iodide Inorganic materials [Rb+].[I-] WFUBYPSJBBQSOU-UHFFFAOYSA-M 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 238000004088 simulation Methods 0.000 description 1
- 239000001632 sodium acetate Substances 0.000 description 1
- 235000017281 sodium acetate Nutrition 0.000 description 1
- VNFWTIYUKDMAOP-UHFFFAOYSA-N sphos Chemical compound COC1=CC=CC(OC)=C1C1=CC=CC=C1P(C1CCCCC1)C1CCCCC1 VNFWTIYUKDMAOP-UHFFFAOYSA-N 0.000 description 1
- 125000003011 styrenyl group Chemical group [H]\C(*)=C(/[H])C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- 125000005504 styryl group Chemical group 0.000 description 1
- WSANLGASBHUYGD-UHFFFAOYSA-N sulfidophosphanium Chemical group S=[PH3] WSANLGASBHUYGD-UHFFFAOYSA-N 0.000 description 1
- 125000000475 sulfinyl group Chemical group [*:2]S([*:1])=O 0.000 description 1
- 125000000472 sulfonyl group Chemical group *S(*)(=O)=O 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- 125000001973 tert-pentyl group Chemical group [H]C([H])([H])C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- VJYJJHQEVLEOFL-UHFFFAOYSA-N thieno[3,2-b]thiophene Chemical group S1C=CC2=C1C=CS2 VJYJJHQEVLEOFL-UHFFFAOYSA-N 0.000 description 1
- 125000004149 thio group Chemical group *S* 0.000 description 1
- TVIVIEFSHFOWTE-UHFFFAOYSA-K tri(quinolin-8-yloxy)alumane Chemical compound [Al+3].C1=CN=C2C([O-])=CC=CC2=C1.C1=CN=C2C([O-])=CC=CC2=C1.C1=CN=C2C([O-])=CC=CC2=C1 TVIVIEFSHFOWTE-UHFFFAOYSA-K 0.000 description 1
- 150000003852 triazoles Chemical group 0.000 description 1
- GKASDNZWUGIAMG-UHFFFAOYSA-N triethyl orthoformate Chemical compound CCOC(OCC)OCC GKASDNZWUGIAMG-UHFFFAOYSA-N 0.000 description 1
- 125000000026 trimethylsilyl group Chemical group [H]C([H])([H])[Si]([*])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- DETFWTCLAIIJRZ-UHFFFAOYSA-N triphenyl-(4-triphenylsilylphenyl)silane Chemical compound C1=CC=CC=C1[Si](C=1C=CC(=CC=1)[Si](C=1C=CC=CC=1)(C=1C=CC=CC=1)C=1C=CC=CC=1)(C=1C=CC=CC=1)C1=CC=CC=C1 DETFWTCLAIIJRZ-UHFFFAOYSA-N 0.000 description 1
- 150000001651 triphenylamine derivatives Chemical class 0.000 description 1
- 125000006617 triphenylamine group Chemical group 0.000 description 1
- 125000003960 triphenylenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3C3=CC=CC=C3C12)* 0.000 description 1
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 1
- 229910001930 tungsten oxide Inorganic materials 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
Images
Classifications
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/30—Coordination compounds
- H10K85/341—Transition metal complexes, e.g. Ru(II)polypyridine complexes
- H10K85/346—Transition metal complexes, e.g. Ru(II)polypyridine complexes comprising platinum
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/06—Luminescent, e.g. electroluminescent, chemiluminescent materials containing organic luminescent materials
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/30—Coordination compounds
- H10K85/331—Metal complexes comprising an iron-series metal, e.g. Fe, Co, Ni
-
- H01L51/0083—
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F15/00—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic Table
- C07F15/0006—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic Table compounds of the platinum group
- C07F15/0086—Platinum compounds
-
- H01L51/0071—
-
- H01L51/5024—
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
- H10K50/12—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers comprising dopants
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1029—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1044—Heterocyclic compounds characterised by ligands containing two nitrogen atoms as heteroatoms
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/18—Metal complexes
- C09K2211/185—Metal complexes of the platinum group, i.e. Os, Ir, Pt, Ru, Rh or Pd
-
- H01L2251/30—
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2101/00—Properties of the organic materials covered by group H10K85/00
- H10K2101/10—Triplet emission
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2102/00—Constructional details relating to the organic devices covered by this subclass
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Inorganic Chemistry (AREA)
- Crystallography & Structural Chemistry (AREA)
- Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Optics & Photonics (AREA)
- Electroluminescent Light Sources (AREA)
Abstract
Description
본 발명은 유기 전계 발광 소자 및 이에 사용되는 유기 금속 화합물에 관한 것이다.The present invention relates to an organic electroluminescent device and an organometallic compound used therefor.
최근, 영상 표시 장치로서, 유기 전계 발광 표시 장치(Organic Electroluminescence Display)의 개발이 왕성하게 이루어져 왔다. 유기 전계 발광 표시 장치는 액정 표시 장치 등과는 다르고, 제1 전극 및 제2 전극으로부터 주입된 정공 및 전자를 발광층에 있어서 재결합시킴으로써, 발광층에 있어서 유기 화합물을 포함하는 발광 재료를 발광시켜서 표시를 실현하는 소위 자발광형의 표시 장치이다.Recently, as an image display device, an organic electroluminescence display has been actively developed. An organic electroluminescent display device is different from a liquid crystal display device, and by recombination of holes and electrons injected from the first and second electrodes in the light emitting layer, the light emitting material containing the organic compound is emitted in the light emitting layer to realize display. It is a so-called self-luminous type display device.
유기 전계 발광 소자를 표시 장치에 응용함에 있어서는, 유기 전계 발광 소자의 저 구동 전압화, 고 발광 효율화 및 장수명화가 요구되고 있으며, 이를 안정적으로 구현할 수 있는 유기 전계 발광 소자용 재료 개발이 지속적으로 요구되고 있다.In applying the organic electroluminescent device to a display device, low driving voltage, high luminous efficiency, and long life of the organic electroluminescent device are required, and the development of a material for an organic electroluminescent device that can stably implement this is continuously required. have.
한편, 발광층 재료의 개발에 있어서 도펀트 재료로 사용되는 유기 금속 화합물에 대한 개발이 지속되고 있으나, 청색 발광 영역에서 높은 효율을 나타내는 도펀트 재료에 대한 개발이 여전히 요구되고 있다.On the other hand, although development of an organometallic compound used as a dopant material in the development of a light emitting layer material continues, development of a dopant material exhibiting high efficiency in a blue light emitting region is still required.
본 발명의 목적은 우수한 발광 효율 및 장수명 특성을 갖는 유기 금속 화합물을 제공하는 것이다.An object of the present invention is to provide an organometallic compound having excellent luminous efficiency and long life characteristics.
또한, 본 발명의 목적은 유기 금속 화합물을 발광층에 포함하여 고효율 및 장수명의 특성을 갖는 유기 전계 발광 소자를 제공하는 것이다.Another object of the present invention is to provide an organic electroluminescent device having high efficiency and long lifespan by including an organometallic compound in a light emitting layer.
일 실시예는 제1 전극; 상기 제1 전극 상에 배치된 제2 전극; 및 상기 제1 전극과 상기 제2 전극 사이에 배치된 발광층; 을 포함하고, 상기 발광층은 하기 화학식 1로 표시되는 유기 금속 화합물을 포함하는 유기 전계 발광 소자를 제공한다.One embodiment is a first electrode; a second electrode disposed on the first electrode; and a light emitting layer disposed between the first electrode and the second electrode. Including, wherein the light emitting layer provides an organic electroluminescent device comprising an organometallic compound represented by the following formula (1).
[화학식 1][Formula 1]
상기 화학식 1에서, M은 전이 금속이고, X1 내지 X6 중 선택되는 하나 또는 둘이 N이고, 나머지는 CR4이고, X1이 N인 경우, X2 내지 X6 중 어느 하나는 N이고, R4는 수소 원자, 중수소 원자, 또는 치환 또는 비치환된 탄소 수 1 이상 10 이하의 알킬기이고, A1 내지 A3은 각각 독립적으로 치환 또는 비치환된 고리형성 탄소수 5 이상 60 이하의 탄화수소 고리, 또는 치환 또는 비치환된 고리형성 탄소수 1 이상 60 이하의 헤테로 고리이고, b1 내지 b3은 각각 독립적으로 1 이상 4 이하의 정수이고, R1 내지 R3은 각각 독립적으로 수소 원자, 중수소 원자, 할로겐 원자, 히드록시기, 시아노기, 니트로기, 치환 또는 비치환된 실릴기, 치환 또는 비치환된 아민기, 치환 또는 비치환된 옥시기, 치환 또는 비치환된 탄소수 1 이상 60 이하의 알킬기, 치환 또는 비치환된 탄소수 2 이상 60 이하의 알케닐기, 치환 또는 비치환된 탄소수 2 이상 60 이하의 알키닐기, 치환 또는 비치환된 고리형성 탄소수 6 이상 60 이하의 아릴기, 또는 치환 또는 비치환된 고리형성 탄소수 1 이상 10 이하의 헤테로 고리기이고, R1 내지 R3 중 적어도 하나는 중수소 원자 또는 CD3이거나, 또는 R1 내지 R3 중 적어도 하나는 중수소 원자 또는 CD3으로 치환된 것이고, L은 직접 결합, O, S, ―CR11R12―, ―CR13=CR14―, ―C≡C―, ―C(=O)―, ―C(=S)―, ―BR15―, ―NR16―, ―PR17R18―, 또는 ―GeR19R20― 이고, R11 내지 R20은 각각 독립적으로 수소 원자, 중수소 원자, 할로겐 원자, 치환 또는 비치환된 탄소수 1 이상 30 이하의 알킬기, 또는 치환 또는 비치환된 고리 형성 탄소수 6 이상 30 이하의 아릴기이다.In Formula 1, M is a transition metal, one or two selected from X 1 to X 6 is N, the rest is CR 4 , and when X 1 is N, any one of X 2 to X 6 is N, R 4 is a hydrogen atom, a deuterium atom, or a substituted or unsubstituted alkyl group having 1 to 10 carbon atoms, A 1 to A 3 are each independently a substituted or unsubstituted hydrocarbon ring having 5 to 60 carbon atoms, or a substituted or unsubstituted heterocyclic ring having 1 or more and 60 or less ring carbon atoms, b1 to b3 are each independently an integer of 1 or more and 4 or less, and R 1 to R 3 are each independently a hydrogen atom, a deuterium atom, or a halogen atom. , hydroxyl group, cyano group, nitro group, substituted or unsubstituted silyl group, substituted or unsubstituted amine group, substituted or unsubstituted oxy group, substituted or unsubstituted alkyl group having 1 to 60 carbon atoms, substituted or unsubstituted an alkenyl group having 2 to 60 carbon atoms, a substituted or unsubstituted alkynyl group having 2 to 60 carbon atoms, a substituted or unsubstituted aryl group having 6 to 60 carbon atoms, or a substituted or unsubstituted
상기 M은 Pt, Pd, Cu, 또는 Os일 수 있다.M may be Pt, Pd, Cu, or Os.
상기 발광층은 인광 발광할 수 있다.The light emitting layer may emit phosphorescence.
상기 발광층은 호스트 및 도펀트를 포함하고, 상기 도펀트는 상기 화학식 1로 표시되는 유기 금속 화합물을 포함할 수 있다.The emission layer may include a host and a dopant, and the dopant may include an organometallic compound represented by Formula 1 above.
상기 화학식 1은 하기 화학식 2-1 또는 화학식 2-2로 표시될 수 있다.Formula 1 may be represented by Formula 2-1 or Formula 2-2 below.
[화학식 2-1][Formula 2-1]
[화학식 2-2][Formula 2-2]
상기 화학식 2-1 및 화학식 2-2에서, A1 내지 A3, X1 내지 X6, R1 내지 R3, 및 b1 내지 b3은 상기 화학식 1에서 정의한 바와 동일하다.In Formulas 2-1 and 2-2, A 1 to A 3 , X 1 to X 6 , R 1 to R 3 , and b 1 to b 3 are the same as defined in Formula 1 above.
상기 화학식 1은 하기 화학식 3으로 표시될 수 있다.Formula 1 may be represented by Formula 3 below.
[화학식 3][Formula 3]
상기 화학식 3에서 R50은 수소 원자, 중수소 원자, 할로겐 원자, 치환 또는 비치환된 탄소수 1 이상 30 이하의 알킬기, 또는 치환 또는 비치환된 탄소수 6 이상 30 이하의 아릴기이고, M, L, X1 내지 X6, R1 내지 R3, 및 b1 내지 b3은 상기 화학식 1에서 정의한 바와 동일하다.In Formula 3, R 50 is a hydrogen atom, a deuterium atom, a halogen atom, a substituted or unsubstituted alkyl group having 1 to 30 carbon atoms, or a substituted or unsubstituted aryl group having 6 to 30 carbon atoms, and M, L, X 1 to X 6 , R 1 to R 3 , and b 1 to b 3 are the same as defined in Formula 1 above.
상기 화학식 3은 하기 화학식 3-1로 표시될 수 있다.Formula 3 may be represented by Formula 3-1 below.
[화학식 3-1][Formula 3-1]
상기 화학식 3-1에서, X2 내지 X6 중 어느 하나는 N이고, 나머지는 CR4이고, M, L, R1 내지 R4, R50 및 b1 내지 b3은 상기 화학식 3에서 정의한 바와 동일하다.In Formula 3-1, any one of X 2 to X 6 is N, the rest is CR 4 , M, L, R 1 to R 4 , R 50 and b 1 to b 3 are as defined in Formula 3 same.
상기 화학식 3은 하기 화학식 3-1로 표시될 수 있다.Formula 3 may be represented by Formula 3-1 below.
[화학식 3-1][Formula 3-1]
상기 화학식 3-1에서, X2 내지 X6 중 어느 하나는 N이고, 나머지는 CR4이고, M, L, R1 내지 R4, R50 및 b1 내지 b3은 상기 화학식 3에서 정의한 바와 동일하다.In Formula 3-1, any one of X 2 to X 6 is N, the rest is CR 4 , M, L, R 1 to R 4 , R 50 and b 1 to b 3 are as defined in Formula 3 same.
상기 화학식 3은 하기 화학식 3-2 또는 화학식 3-3으로 표시될 수 있다.Formula 3 may be represented by Formula 3-2 or Formula 3-3.
[화학식 3-2][Formula 3-2]
[화학식 3-3][Formula 3-3]
상기 화학식 3-2에서, X2 내지 X4 중 어느 하나는 N이고, 나머지는 CR4이고, R5는 수소 원자, 중수소 원자, 또는 치환 또는 비치환된 탄소 수 1 이상 10 이하의 알킬기이고, 상기 화학식 3-3에서, X5 및 X6 중 어느 하나는 N이고, 나머지는 CR6이고, b4는 1 이상 4 이하의 정수이고, R6은 수소 원자, 중수소 원자, 또는 치환 또는 비치환된 탄소 수 1 이상 10 이하의 알킬기이고, M, L, R1 내지 R4, b1 내지 b3, 및 R50은 상기 화학식 3에서 정의한 바와 동일하다.In Formula 3-2, any one of X 2 to X 4 is N, the rest is CR 4 , R 5 is a hydrogen atom, a deuterium atom, or a substituted or unsubstituted alkyl group having 1 or more and 10 or less carbon atoms, In Formula 3-3, any one of X 5 and X 6 is N, the rest is CR 6 , b4 is an integer of 1 or more and 4 or less, and R 6 is a hydrogen atom, a deuterium atom, or a substituted or unsubstituted It is an alkyl group having 1 or more and 10 or less carbon atoms, and M, L, R 1 to R 4 , b 1 to b 3 , and R 50 are the same as defined in Formula 3 above.
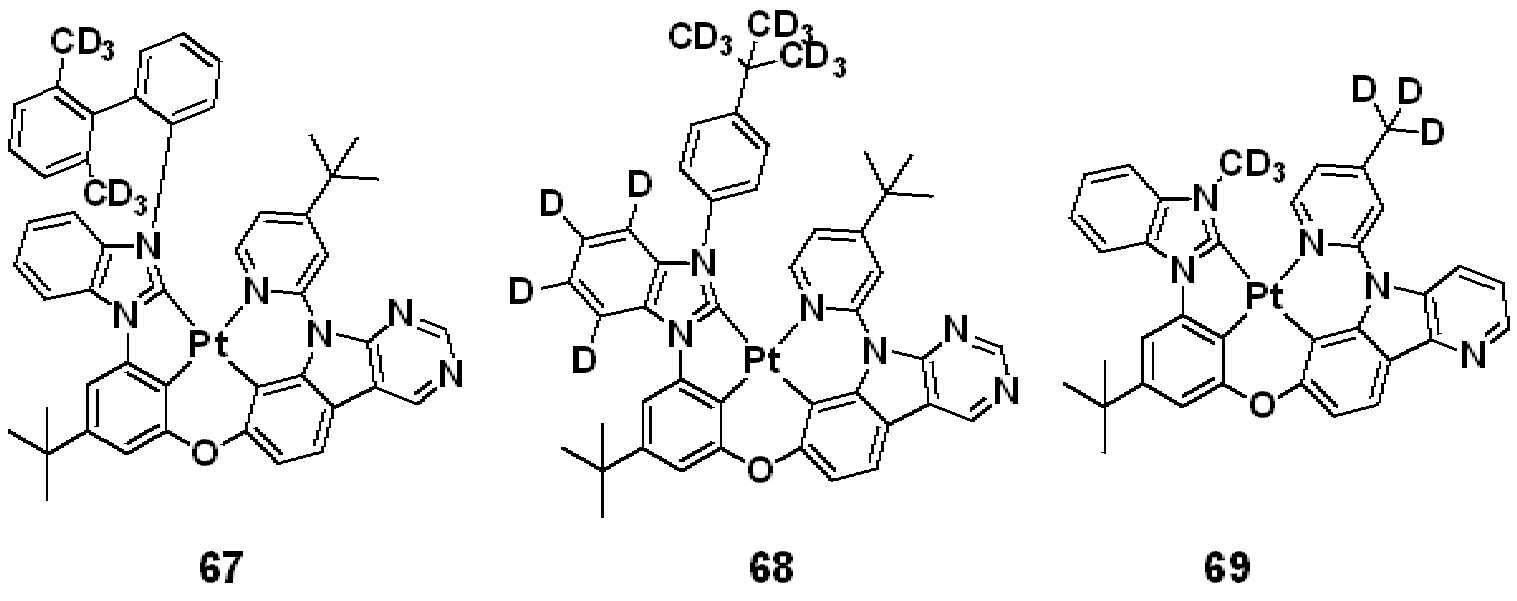
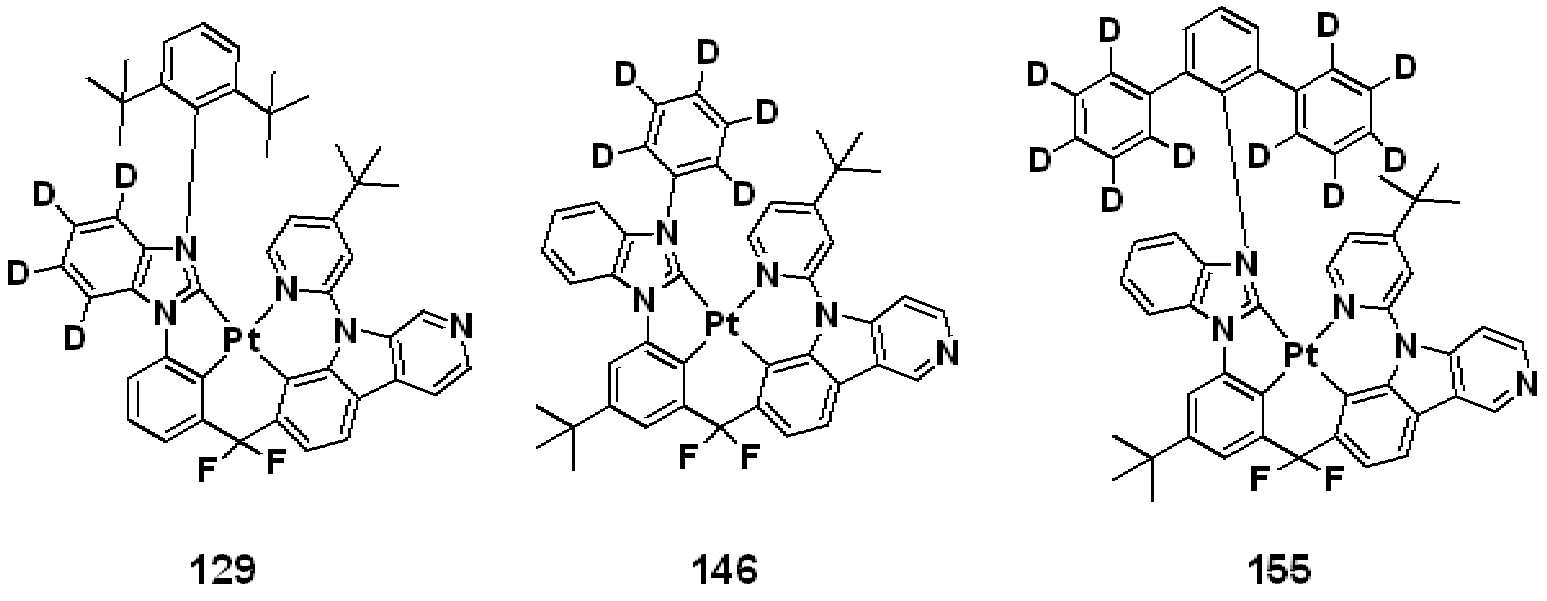
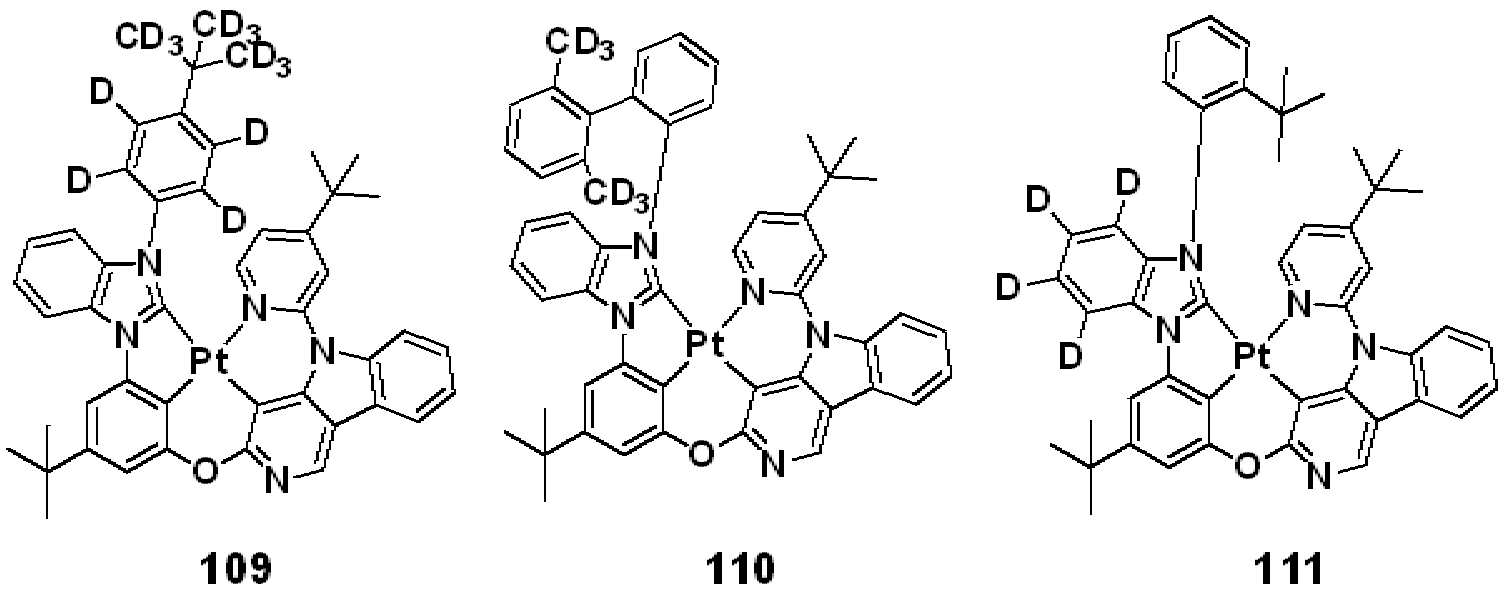
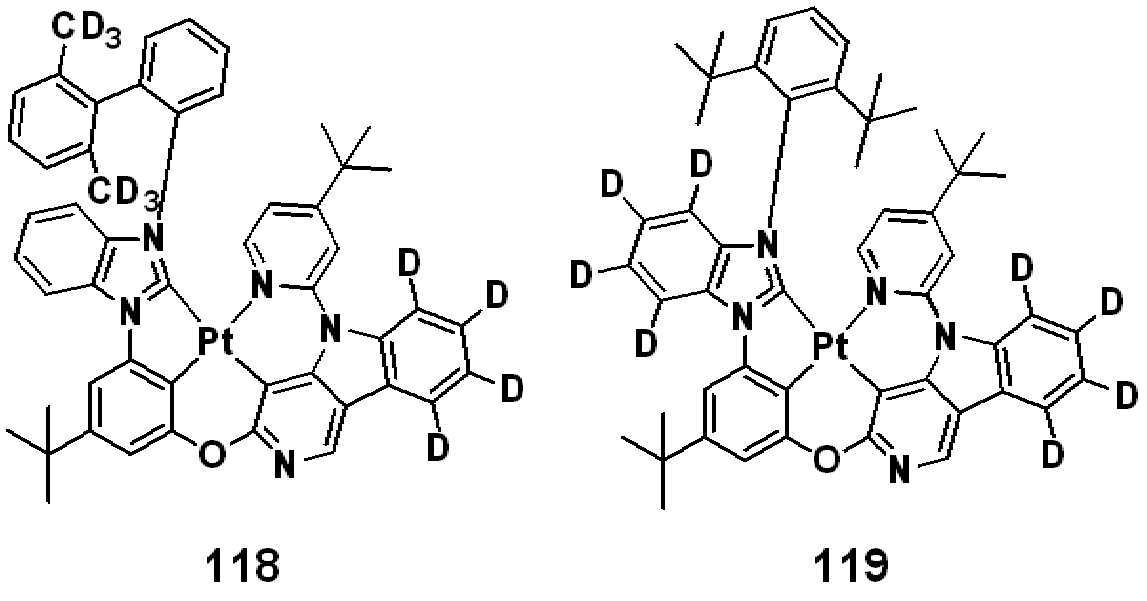
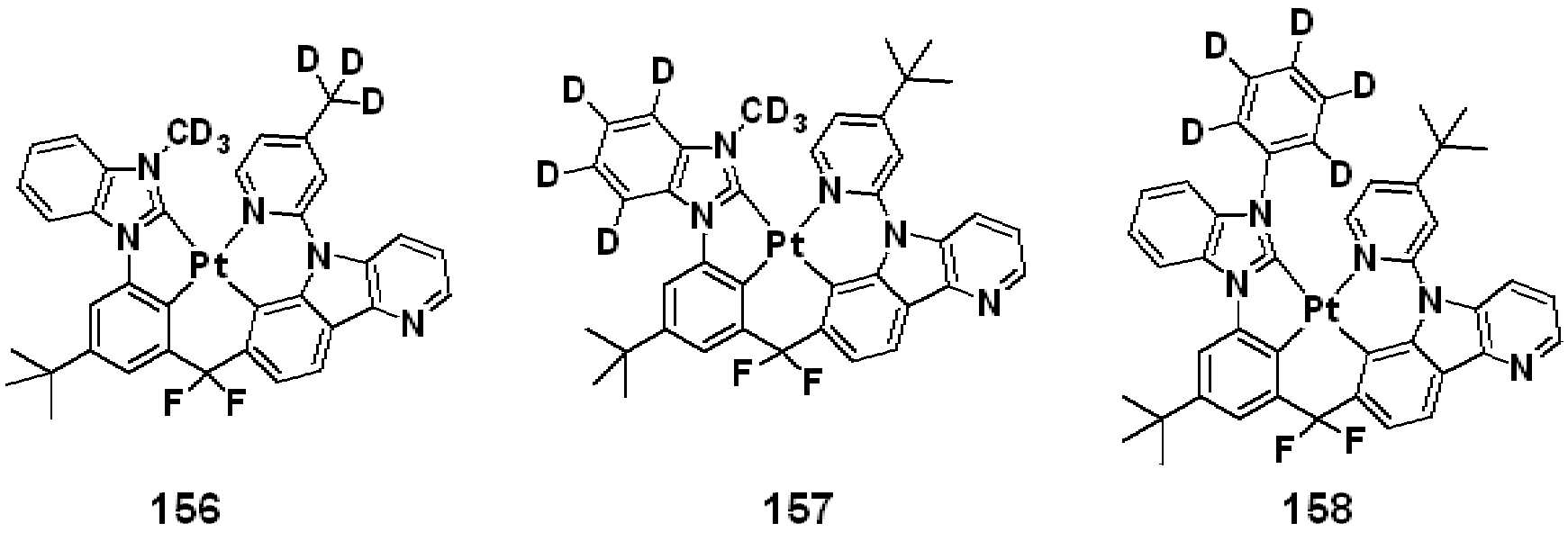
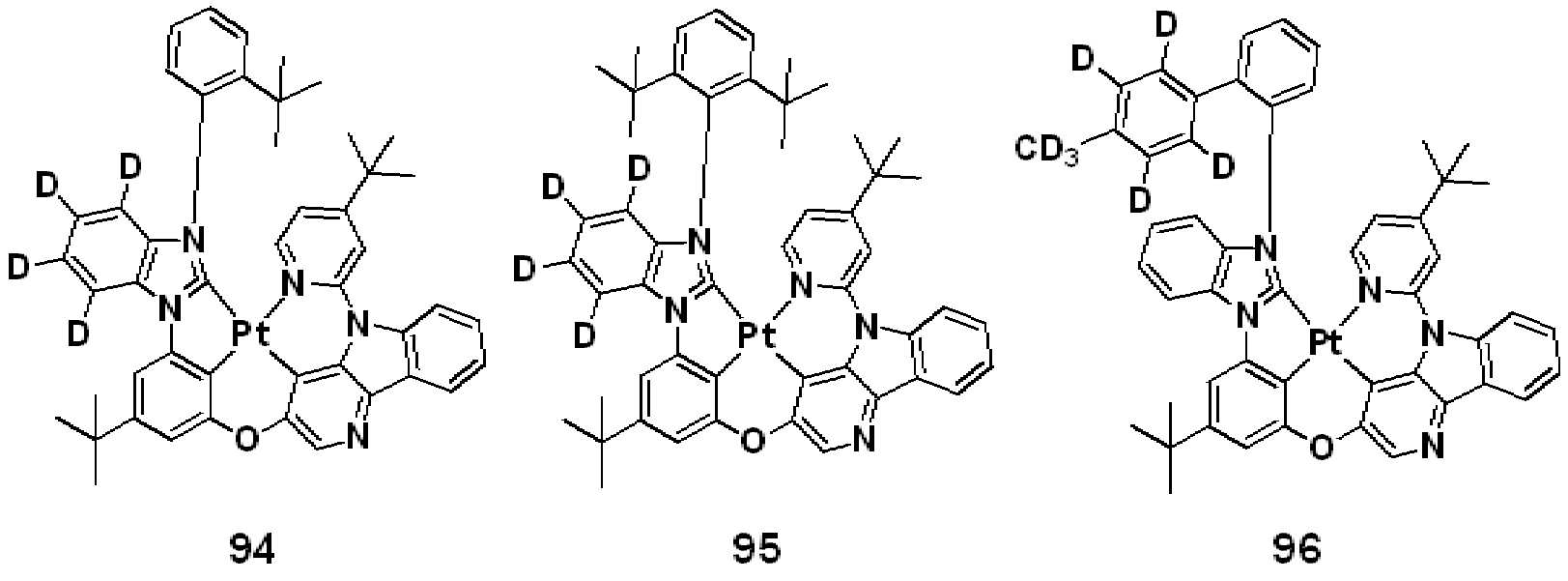
상기 R50은 하기 화합물군 R의 화합물들 중 어느 하나로 표시될 수 있다.R 50 may be represented by any one of the compounds of the following compound group R.
[화합물군 R][Compound group R]
. .
상기 R50이 화합물 R-7 또는 R-8인 경우, R1은 적어도 하나의 중수소 원자를 포함할 수 있다.When R 50 is the compound R-7 or R-8, R 1 may include at least one deuterium atom.
일 실시예는 상기 화학식 1로 표시되는 유기 금속 화합물을 제공한다.One embodiment provides an organometallic compound represented by Formula 1 above.
일 실시예의 유기 금속 화합물은 카볼린기 및 중수소 원자를 포함하여 유기 전계 발광 소자의 고효율 및 장수명 특성에 기여할 수 있다.The organometallic compound of an embodiment may include a carboline group and a deuterium atom to contribute to high efficiency and long lifespan characteristics of the organic electroluminescent device.
일 실시예의 유기 전계 발광 소자는 카볼린기 및 중수소 원자를 포함하는 유기 금속 화합물을 포함하여 고효율 및 장수명의 소자 특성을 나타낼 수 있다.The organic electroluminescent device of an exemplary embodiment may include an organometallic compound including a carboline group and a deuterium atom to exhibit high efficiency and long lifespan device characteristics.
도 1은 본 발명의 일 실시예에 따른 유기 전계 발광 소자를 개략적으로 나타낸 단면도이다.
도 2는 본 발명의 일 실시예에 따른 유기 전계 발광 소자를 개략적으로 나타낸 단면도이다.
도 3은 본 발명의 일 실시예에 따른 유기 전계 발광 소자를 개략적으로 나타낸 단면도이다.
도 4는 본 발명의 일 실시예에 따른 유기 전계 발광 소자를 개략적으로 나타낸 단면도이다.1 is a cross-sectional view schematically showing an organic electroluminescent device according to an embodiment of the present invention.
2 is a cross-sectional view schematically showing an organic electroluminescent device according to an embodiment of the present invention.
3 is a cross-sectional view schematically illustrating an organic electroluminescent device according to an embodiment of the present invention.
4 is a cross-sectional view schematically illustrating an organic electroluminescent device according to an embodiment of the present invention.
본 발명은 다양한 변경을 가할 수 있고 여러 가지 형태를 가질 수 있는 바, 특정 실시예들을 도면에 예시하고 본문에 상세하게 설명하고자 한다. 그러나, 이는 본 발명을 특정한 개시 형태에 대해 한정하려는 것이 아니며, 본 발명의 사상 및 기술 범위에 포함되는 모든 변경, 균등물 내지 대체물을 포함하는 것으로 이해되어야 한다.Since the present invention can have various changes and can have various forms, specific embodiments are illustrated in the drawings and described in detail in the text. However, this is not intended to limit the present invention to the specific disclosed form, it should be understood to include all modifications, equivalents and substitutes included in the spirit and scope of the present invention.
본 명세서에서, 어떤 구성요소(또는 영역, 층, 부분 등)가 다른 구성요소 "상에 있다", "연결 된다", 또는 "결합된다"고 언급되는 경우에 그것은 다른 구성요소 상에 직접 배치/연결/결합될 수 있거나 또는 그들 사이에 제3의 구성요소가 배치될 수도 있다는 것을 의미한다. In this specification, when a component (or region, layer, part, etc.) is referred to as being “on,” “connected to,” or “coupled to” another component, it is directly disposed/on the other component. It means that it can be connected/coupled or a third component can be placed between them.
동일한 도면부호는 동일한 구성요소를 지칭한다. 또한, 도면들에 있어서, 구성요소들의 두께, 비율, 및 치수는 기술적 내용의 효과적인 설명을 위해 과장된 것이다.Like reference numerals refer to like elements. In addition, in the drawings, thicknesses, ratios, and dimensions of components are exaggerated for effective description of technical content.
"및/또는"은 연관된 구성들이 정의할 수 있는 하나 이상의 조합을 모두 포함한다. “and/or” includes any combination of one or more that the associated configurations may define.
제1, 제2 등의 용어는 다양한 구성요소들을 설명하는데 사용될 수 있지만, 상기 구성요소들은 상기 용어들에 의해 한정되어서는 안 된다. 상기 용어들은 하나의 구성요소를 다른 구성요소로부터 구별하는 목적으로만 사용된다. 예를 들어, 본 발명의 권리 범위를 벗어나지 않으면서 제1 구성요소는 제2 구성요소로 명명될 수 있고, 유사하게 제2 구성요소도 제1 구성요소로 명명될 수 있다. 단수의 표현은 문맥상 명백하게 다르게 뜻하지 않는 한, 복수의 표현을 포함한다.Terms such as first, second, etc. may be used to describe various elements, but the elements should not be limited by the terms. The above terms are used only for the purpose of distinguishing one component from another. For example, without departing from the scope of the present invention, a first component may be referred to as a second component, and similarly, a second component may also be referred to as a first component. The singular expression includes the plural expression unless the context clearly dictates otherwise.
또한, "아래에", "하측에", "위에", "상측에" 등의 용어는 도면에 도시된 구성들의 연관관계를 설명하기 위해 사용된다. 상기 용어들은 상대적인 개념으로, 도면에 표시된 방향을 기준으로 설명된다.In addition, terms such as "below", "below", "above", "upper" and the like are used to describe the relationship between the components shown in the drawings. The above terms are relative concepts, and are described based on directions indicated in the drawings.
다르게 정의되지 않는 한, 본 명세서에서 사용된 모든 용어 (기술 용어 및 과학 용어 포함)는 본 발명이 속하는 기술 분야의 당업자에 의해 일반적으로 이해되는 것과 동일한 의미를 갖는다. 또한, 일반적으로 사용되는 사전에서 정의된 용어와 같은 용어는 관련 기술의 맥락에서 의미와 일치하는 의미를 갖는 것으로 해석되어야 하고, 이상적인 또는 지나치게 형식적인 의미로 해석되지 않는 한, 명시적으로 여기에서 정의된다.Unless defined otherwise, all terms (including technical and scientific terms) used herein have the same meaning as commonly understood by one of ordinary skill in the art to which this invention belongs. Also, terms such as terms defined in commonly used dictionaries should be construed as having a meaning consistent with their meaning in the context of the relevant art, and unless they are interpreted in an ideal or overly formal sense, they are explicitly defined herein do.
"포함하다" 또는 "가지다" 등의 용어는 명세서 상에 기재된 특징, 숫자, 단계, 동작, 구성요소, 부품 또는 이들을 조합한 것이 존재함을 지정하려는 것이지, 하나 또는 그 이상의 다른 특징들이나 숫자, 단계, 동작, 구성요소, 부분품 또는 이들을 조합한 것들의 존재 또는 부가 가능성을 미리 배제하지 않는 것으로 이해되어야 한다. Terms such as “comprise” or “have” are intended to designate that a feature, number, step, action, component, part, or combination thereof described in the specification is present, and includes one or more other features, numbers, or steps. , it should be understood that it does not preclude the possibility of the existence or addition of , operation, components, parts, or combinations thereof.
이하, 도면들을 참조하여 본 발명의 일 실시예에 따른 유기 전계 발광 소자 및 이에 포함된 일 실시예의 유기 금속 화합물에 대하여 설명한다.Hereinafter, an organic electroluminescent device according to an embodiment of the present invention and an organometallic compound included therein according to an embodiment will be described with reference to the drawings.
도 1 내지 도 4는 본 발명의 일 실시예에 따른 유기 전계 발광 소자를 개략적으로 나타낸 단면도이다. 도 1 내지 도 4를 참조하면, 일 실시예의 유기 전계 발광 소자(10)에서 제1 전극(EL1)과 제2 전극(EL2)은 서로 마주하고 배치되며, 제1 전극(EL1)과 제2 전극(EL2) 사이에는 발광층(EML)이 배치될 수 있다.1 to 4 are cross-sectional views schematically illustrating an organic electroluminescent device according to an embodiment of the present invention. 1 to 4 , in the
또한, 일 실시예의 유기 전계 발광 소자(10)는 제1 전극(EL1)과 제2 전극(EL2) 사이에 발광층(EML) 이외에 복수의 기능층들을 더 포함한다. 복수의 기능층들은 정공 수송 영역(HTR) 및 전자 수송 영역(ETR)을 포함할 수 있다. 즉, 일 실시예에 따른 유기 전계 발광 소자(10)는 순차적으로 적층된 제1 전극(EL1), 정공 수송 영역(HTR), 발광층(EML), 전자 수송 영역(ETR), 및 제2 전극(EL2)을 포함할 수 있다. 또한 일 실시예의 유기 전계 발광 소자(10)는 제2 전극(EL2) 상에 배치된 캡핑층(CPL)을 포함할 수 있다.In addition, the
일 실시예의 유기 전계 발광 소자(10)는 제1 전극(EL1)과 제2 전극(EL2) 사이에 배치된 발광층(EML)에 후술하는 일 실시예의 유기 금속 화합물을 포함할 수 있다. The
한편, 도 2는 도 1과 비교하여, 정공 수송 영역(HTR)이 정공 주입층(HIL) 및 정공 수송층(HTL)을 포함하고, 전자 수송 영역(ETR)이 전자 주입층(EIL) 및 전자 수송층(ETL)을 포함하는 일 실시예의 유기 전계 발광 소자(10)의 단면도를 나타낸 것이다. 또한, 도 3은 도 1과 비교하여 정공 수송 영역(HTR)이 정공 주입층(HIL), 정공 수송층(HTL), 및 전자 저지층(EBL)을 포함하고, 전자 수송 영역(ETR)이 전자 주입층(EIL), 전자 수송층(ETL), 및 정공 저지층(HBL)을 포함하는 일 실시예의 유기 전계 발광 소자(10)의 단면도를 나타낸 것이다. 도 4는 도 2와 비교하여 제2 전극(EL2) 상에 배치된 캡핑층(CPL)을 포함하는 일 실시예의 유기 전계 발광 소자(10)의 단면도를 나타낸 것이다.Meanwhile, in FIG. 2 , compared with FIG. 1 , the hole transport region HTR includes the hole injection layer HIL and the hole transport layer HTL, and the electron transport region ETR includes the electron injection layer EIL and the electron transport layer. A cross-sectional view of the
제1 전극(EL1)은 도전성을 갖는다. 제1 전극(EL1)은 금속 합금 또는 도전성 화합물로 형성될 수 있다. 제1 전극(EL1)은 애노드(anode)일 수 있다. 또한, 제1 전극(EL1)은 화소 전극일 수 있다. 제1 전극(EL1)은 투과형 전극, 반투과형 전극 또는 반사형 전극일 수 있다. 제1 전극(EL1)이 투과형 전극인 경우, 제1 전극(EL1)은 투명 금속 산화물, 예를 들어, ITO(indium tin oxide), IZO(indium zinc oxide), ZnO(zinc oxide), ITZO(indium tin zinc oxide) 등을 포함할 수 있다. 제1 전극(EL1)이 반투과형 전극 또는 반사형 전극인 경우, 제1 전극(EL1)은 Ag, Mg, Cu, Al, Pt, Pd, Au, Ni, Nd, Ir, Cr, Li, Ca, LiF/Ca, LiF/Al, Mo, Ti 또는 이들의 화합물이나 혼합물(예를 들어, Ag와 Mg의 혼합물)을 포함할 수 있다. 또는 상기 물질로 형성된 반사막이나 반투과막 및 ITO(indium tin oxide), IZO(indium zinc oxide), ZnO(zinc oxide), ITZO(indium tin zinc oxide) 등으로 형성된 투명 도전막을 포함하는 복수의 층 구조일 수 있다. 예를 들어, 제1 전극(EL1)은 ITO/Ag/ITO의 3층 구조를 가질 수 있으나, 이에 한정되는 것은 아니다. 제1 전극(EL1)의 두께는 약 1000Å 내지 약 10000Å, 예를 들어, 약 1000Å 내지 약 3000Å일 수 있다.The first electrode EL1 has conductivity. The first electrode EL1 may be formed of a metal alloy or a conductive compound. The first electrode EL1 may be an anode. Also, the first electrode EL1 may be a pixel electrode. The first electrode EL1 may be a transmissive electrode, a transflective electrode, or a reflective electrode. When the first electrode EL1 is a transmissive electrode, the first electrode EL1 is a transparent metal oxide, for example, indium tin oxide (ITO), indium zinc oxide (IZO), zinc oxide (ZnO), or indium (ITZO). tin zinc oxide) and the like. When the first electrode EL1 is a transflective electrode or a reflective electrode, the first electrode EL1 may include Ag, Mg, Cu, Al, Pt, Pd, Au, Ni, Nd, Ir, Cr, Li, Ca, LiF/Ca, LiF/Al, Mo, Ti, or a compound or mixture thereof (eg, a mixture of Ag and Mg). Or a plurality of layer structures including a reflective or semi-transmissive film formed of the above material and a transparent conductive film formed of indium tin oxide (ITO), indium zinc oxide (IZO), zinc oxide (ZnO), indium tin zinc oxide (ITZO), etc. can be For example, the first electrode EL1 may have a three-layer structure of ITO/Ag/ITO, but is not limited thereto. The thickness of the first electrode EL1 may be about 1000 Å to about 10000 Å, for example, about 1000 Å to about 3000 Å.
정공 수송 영역(HTR)은 제1 전극(EL1) 상에 제공된다. 정공 수송 영역(HTR)은 정공 주입층(HIL), 정공 수송층(HTL), 정공 버퍼층(미도시), 및 전자 저지층(EBL) 중 적어도 하나를 포함할 수 있다. 정공 수송 영역(HTR)의 두께는 예를 들어, 약 50Å 내지 약 15000Å인 것일 수 있다.The hole transport region HTR is provided on the first electrode EL1 . The hole transport region HTR may include at least one of a hole injection layer HIL, a hole transport layer HTL, a hole buffer layer (not shown), and an electron blocking layer EBL. The thickness of the hole transport region HTR may be, for example, about 50 Å to about 15000 Å.
정공 수송 영역(HTR)은 단일 물질로 이루어진 단일층, 복수의 서로 다른 물질로 이루어진 단일층 또는 복수의 서로 다른 물질로 이루어진 복수의 층을 갖는 다층 구조를 가질 수 있다.The hole transport region HTR may have a single layer made of a single material, a single layer made of a plurality of different materials, or a multilayer structure having a plurality of layers made of a plurality of different materials.
예를 들어, 정공 수송 영역(HTR)은 정공 주입층(HIL) 또는 정공 수송층(HTL)의 단일층의 구조를 가질 수도 있고, 정공 주입 물질 및 정공 수송 물질로 이루어진 단일층 구조를 가질 수도 있다. 또한, 정공 수송 영역(HTR)은, 복수의 서로 다른 물질로 이루어진 단일층의 구조를 갖거나, 제1 전극(EL1)로부터 차례로 적층된 정공 주입층(HIL)/정공 수송층(HTL), 정공 주입층(HIL)/정공 수송층(HTL)/정공 버퍼층(미도시), 정공 주입층(HIL)/정공 버퍼층(미도시), 정공 수송층(HTL)/정공 버퍼층 또는 정공 주입층(HIL)/정공 수송층(HTL)/전자 저지층(EBL)의 구조를 가질 수 있으나, 실시예가 이에 한정되는 것은 아니다.For example, the hole transport region HTR may have a single-layer structure of the hole injection layer HIL or the hole transport layer HTL, or may have a single-layer structure including a hole injection material and a hole transport material. In addition, the hole transport region HTR has a single layer structure made of a plurality of different materials, or a hole injection layer HIL/hole transport layer HTL, hole injection that are sequentially stacked from the first electrode EL1 . Layer (HIL) / hole transport layer (HTL) / hole buffer layer (not shown), hole injection layer (HIL) / hole buffer layer (not shown), hole transport layer (HTL) / hole buffer layer or hole injection layer (HIL) / hole transport layer (HTL)/electron blocking layer (EBL) may have a structure, but the embodiment is not limited thereto.
정공 수송 영역(HTR)은, 진공 증착법, 스핀 코팅법, 캐스트법, LB법(Langmuir-Blodgett), 잉크젯 프린팅법, 레이저 프린팅법, 레이저 열전사법(Laser Induced Thermal Imaging, LITI) 등과 같은 다양한 방법을 이용하여 형성될 수 있다.The hole transport region (HTR) is a vacuum deposition method, a spin coating method, a casting method, a LB method (Langmuir-Blodgett), an inkjet printing method, a laser printing method, a laser thermal imaging method (Laser Induced Thermal Imaging, LITI), such as various methods It can be formed using
정공 주입층(HIL)은 예를 들어, 구리프탈로시아닌(copper phthalocyanine) 등의 프탈로시아닌(phthalocyanine) 화합물; DNTPD(N,N'-diphenyl-N,N'-bis-[4-(phenyl-m-tolyl-amino)-phenyl]-biphenyl-4,4'-diamine), m-MTDATA(4,4',4"-[tris(3-methylphenyl)phenylamino] triphenylamine), TDATA(4,4'4"-Tris(N,N-diphenylamino)triphenylamine), 2-TNATA(4,4',4"-tris{N-(2-naphthyl)-N-phenylamino}-triphenylamine), PEDOT/PSS(Poly(3,4-ethylenedioxythiophene)/Poly(4-styrenesulfonate)), PANI/DBSA(Polyaniline/Dodecylbenzenesulfonic acid), PANI/CSA(Polyaniline/Camphor sulfonicacid), PANI/PSS(Polyaniline/Poly(4-styrenesulfonate)), NPB(N,N'-di(naphthalene-l-yl)-N,N'-diphenyl-benzidine), 트리페닐아민을 포함하는 폴리에테르케톤(TPAPEK), 4-Isopropyl-4'-methyldiphenyliodonium [Tetrakis(pentafluorophenyl)borate], HAT-CN(dipyrazino[2,3-f: 2',3'-h] quinoxaline-2,3,6,7,10,11-hexacarbonitrile) 등을 포함할 수도 있다.The hole injection layer HIL may include, for example, a phthalocyanine compound such as copper phthalocyanine; DNTPD(N,N'-diphenyl-N,N'-bis-[4-(phenyl-m-tolyl-amino)-phenyl]-biphenyl-4,4'-diamine), m-MTDATA(4,4' ,4"-[tris(3-methylphenyl)phenylamino] triphenylamine), TDATA(4,4'4"-Tris(N,N-diphenylamino)triphenylamine), 2-TNATA(4,4',4"-tris{ N-(2-naphthyl)-N-phenylamino}-triphenylamine), PEDOT/PSS(Poly(3,4-ethylenedioxythiophene)/Poly(4-styrenesulfonate)), PANI/DBSA(Polyaniline/Dodecylbenzenesulfonic acid), PANI/CSA (Polyaniline/Camphor sulfonicacid), PANI/PSS (Polyaniline/Poly(4-styrenesulfonate)), NPB(N,N'-di(naphthalene-l-yl)-N,N'-diphenyl-benzidine), triphenylamine Polyether ketone containing (TPAPEK), 4-Isopropyl-4'-methyldiphenyliodonium [Tetrakis (pentafluorophenyl) borate], HAT-CN (dipyrazino [2,3-f: 2',3'-h] quinoxaline-2, 3,6,7,10,11-hexacarbonitrile) and the like.
정공 수송층(HTL)은 예를 들어, N-페닐카바졸, 폴리비닐카바졸 등의 카바졸계 유도체, 플루오렌(fluorene)계 유도체, TPD(N,N'-bis(3-methylphenyl)-N,N'-diphenyl-[1,1-biphenyl]-4,4'-diamine), TCTA(4,4',4"-tris(N-carbazolyl)triphenylamine) 등과 같은 트리페닐아민계 유도체, NPB(N,N'-di(naphthalene-l-yl)-N,N'-diphenyl-benzidine), TAPC(4,4′-Cyclohexylidene bis[N,N-bis(4-methylphenyl)benzenamine]), HMTPD(4,4'-Bis[N,N'-(3-tolyl)amino]-3,3'-dimethylbiphenyl), mCP(1,3-Bis(N-carbazolyl)benzene) 등을 더 포함할 수도 있다.The hole transport layer (HTL) is, for example, a carbazole-based derivative such as N-phenylcarbazole and polyvinylcarbazole, a fluorene-based derivative, TPD (N,N'-bis(3-methylphenyl)-N, Triphenylamine derivatives such as N'-diphenyl-[1,1-biphenyl]-4,4'-diamine), TCTA(4,4',4"-tris(N-carbazolyl)triphenylamine), NPB(N ,N'-di(naphthalene-l-yl)-N,N'-diphenyl-benzidine), TAPC(4,4′-Cyclohexylidene bis[N,N-bis(4-methylphenyl)benzenamine]), HMTPD(4 ,4'-Bis[N,N'-(3-tolyl)amino]-3,3'-dimethylbiphenyl), mCP(1,3-Bis(N-carbazolyl)benzene), etc. may be further included.
정공 수송 영역(HTR)의 두께는 약 50Å 내지 약 10000Å, 예를 들어, 약 100Å 내지 약 5000Å일 수 있다. 정공 주입층(HIL)의 두께는, 예를 들어, 약 30Å 내지 약 1000Å이고, 정공 수송층(HTL)의 두께는 약 30Å 내지 약 1000Å 일 수 있다. 예를 들어, 전자 저지층(EBL)의 두께는 약 10Å 내지 약 1000Å일 수 있다. 정공 수송 영역(HTR), 정공 주입층(HIL), 정공 수송층(HTL) 및 전자 저지층(EBL)의 두께가 전술한 바와 같은 범위를 만족할 경우, 실질적인 구동 전압 상승 없이 만족스러운 정도의 정공 수송 특성을 얻을 수 있다.The hole transport region HTR may have a thickness of about 50 Å to about 10000 Å, for example, about 100 Å to about 5000 Å. The thickness of the hole injection layer HIL may be, for example, about 30 Å to about 1000 Å, and the thickness of the hole transport layer HTL may be about 30 Å to about 1000 Å. For example, the thickness of the electron blocking layer (EBL) may be about 10 Å to about 1000 Å. When the thicknesses of the hole transport region (HTR), the hole injection layer (HIL), the hole transport layer (HTL), and the electron blocking layer (EBL) satisfy the above-described ranges, satisfactory hole transport characteristics without a substantial increase in driving voltage can get
정공 수송 영역(HTR)은 앞서 언급한 물질 외에, 도전성 향상을 위하여 전하 생성 물질을 더 포함할 수 있다. 전하 생성 물질은 정공 수송 영역(HTR) 내에 균일하게 또는 불균일하게 분산되어 있을 수 있다. 전하 생성 물질은 예를 들어, p-도펀트(dopant)일 수 있다. p-도펀트는 퀴논(quinone) 유도체, 금속 산화물 및 시아노(cyano)기 함유 화합물 중 하나일 수 있으나, 이에 한정되는 것은 아니다. 예를 들어, p-도펀트의 비제한적인 예로는, TCNQ(Tetracyanoquinodimethane) 및 F4-TCNQ(2,3,5,6-tetrafluoro-7,7',8,8'-tetracyanoquinodimethane) 등과 같은 퀴논 유도체, 텅스텐 산화물 및 몰리브덴 산화물 등과 같은 금속 산화물 등을 들 수 있으나, 이에 한정되는 것은 아니다.The hole transport region HTR may further include a charge generating material to improve conductivity, in addition to the aforementioned materials. The charge generating material may be uniformly or non-uniformly dispersed in the hole transport region HTR. The charge generating material may be, for example, a p-dopant. The p-dopant may be one of a quinone derivative, a metal oxide, and a cyano group-containing compound, but is not limited thereto. For example, non-limiting examples of p-dopants include quinone derivatives such as TCNQ (Tetracyanoquinodimethane) and F4-TCNQ (2,3,5,6-tetrafluoro-7,7',8,8'-tetracyanoquinodimethane); and metal oxides such as tungsten oxide and molybdenum oxide, but is not limited thereto.
전술한 바와 같이, 정공 수송 영역(HTR)은 정공 주입층(HIL) 및 정공 수송층(HTL) 외에, 정공 버퍼층(미도시) 및 전자 저지층(EBL) 중 적어도 하나를 더 포함할 수 있다. 정공 버퍼층(미도시)은 발광층(EML)에서 방출되는 광의 파장에 따른 공진 거리를 보상하여 광 방출 효율을 증가시킬 수 있다. 정공 버퍼층(미도시)에 포함되는 물질로는 정공 수송 영역(HTR)에 포함될 수 있는 물질을 사용할 수 있다. 전자 저지층(EBL)은 전자 수송 영역(ETR)으로부터 정공 수송 영역(HTR)으로의 전자 주입을 방지하는 역할을 하는 층이다.As described above, the hole transport region HTR may further include at least one of a hole buffer layer (not shown) and an electron blocking layer EBL, in addition to the hole injection layer HIL and the hole transport layer HTL. The hole buffer layer (not shown) may increase light emission efficiency by compensating for a resonance distance according to a wavelength of light emitted from the emission layer EML. As a material included in the hole buffer layer (not shown), a material capable of being included in the hole transport region HTR may be used. The electron blocking layer EBL is a layer serving to prevent electron injection from the electron transport region ETR to the hole transport region HTR.
발광층(EML)은 정공 수송 영역(HTR) 상에 제공된다. 발광층(EML)은 예를 들어 약 100Å 내지 약 1000Å 또는, 약 100Å 내지 약 300Å의 두께를 갖는 것일 수 있다. 발광층(EML)은 단일 물질로 이루어진 단일층, 복수의 서로 다른 물질로 이루어진 단일층 또는 복수의 서로 다른 물질로 이루어진 복수의 층을 갖는 다층 구조를 가질 수 있다.The emission layer EML is provided on the hole transport region HTR. The emission layer EML may have a thickness of, for example, about 100 Å to about 1000 Å, or about 100 Å to about 300 Å. The emission layer EML may have a single layer made of a single material, a single layer made of a plurality of different materials, or a multilayer structure having a plurality of layers made of a plurality of different materials.
일 실시예의 유기 전계 발광 소자(10)에서 발광층(EML)은 후술하는 일 실시예의 유기 금속 화합물을 포함하는 것일 수 있다. In the
본 명세서에서, “치환 또는 비치환된” 은 중수소 원자, 할로겐 원자, 시아노기, 니트로기, 아미노기, 실릴기, 옥시기, 티오기, 설피닐기, 설포닐기, 카보닐기, 붕소기, 포스핀기, 포스핀 옥사이드기, 포스핀 설파이드기, 알킬기, 알케닐기, 알키닐기, 알콕시기, 탄화수소 고리기, 아릴기 및 헤테로 고리기로 이루어진 군에서 선택되는 1개 이상의 치환기로 치환 또는 비치환된 것을 의미할 수 있다. 또한, 상기 예시된 치환기 각각은 치환 또는 비치환된 것일 수 있다. 예를 들어, 비페닐기는 아릴기로 해석될 수도 있고, 페닐기로 치환된 페닐기로 해석될 수도 있다.In the present specification, "substituted or unsubstituted" is a deuterium atom, a halogen atom, a cyano group, a nitro group, an amino group, a silyl group, an oxy group, a thio group, a sulfinyl group, a sulfonyl group, a carbonyl group, a boron group, a phosphine group, A phosphine oxide group, a phosphine sulfide group, an alkyl group, an alkenyl group, an alkynyl group, an alkoxy group, a hydrocarbon ring group, an aryl group and one or more substituents selected from the group consisting of a heterocyclic group may mean unsubstituted or substituted. have. In addition, each of the substituents exemplified above may be substituted or unsubstituted. For example, a biphenyl group may be interpreted as an aryl group or a phenyl group substituted with a phenyl group.
본 명세서에서, 할로겐 원자의 예로는 불소 원자, 염소 원자, 브롬 원자 또는 요오드 원자가 있다.In the present specification, examples of the halogen atom include a fluorine atom, a chlorine atom, a bromine atom or an iodine atom.
본 명세서에서, 알킬기는 직쇄, 분지쇄 또는 고리형일 수 있다. 알킬기의 탄소수는 1 이상 50 이하, 1 이상 30 이하, 1 이상 20 이하, 1 이상 10 이하 또는 1 이상 6 이하이다. 알킬기의 예로는 메틸기, 에틸기, n-프로필기, 이소프로필기, n-부틸기, s-부틸기, t-부틸기, i-부틸기, 2- 에틸부틸기, 3, 3-디메틸부틸기, n-펜틸기, i-펜틸기, 네오펜틸기, t-펜틸기, 시클로펜틸기, 1-메틸펜틸기, 3-메틸펜틸기, 2-에틸펜틸기, 4-메틸-2-펜틸기, n-헥실기, 1-메틸헥실기, 2-에틸헥실기, 2-부틸헥실기, 시클로헥실기, 4-메틸시클로헥실기, 4-t-부틸시클로헥실기, n-헵틸기, 1-메틸헵틸기, 2,2-디메틸헵틸기, 2-에틸헵틸기, 2-부틸헵틸기, n-옥틸기, t-옥틸기, 2-에틸옥틸기, 2-부틸옥틸기, 2-헥실옥틸기, 3,7-디메틸옥틸기, 시클로옥틸기, n-노닐기, n-데실기, 아다만틸기, 2-에틸데실기, 2-부틸데실기, 2-헥실데실기, 2-옥틸데실기, n-운데실기, n-도데실기, 2-에틸도데실기, 2-부틸도데실기, 2-헥실도데실기, 2-옥틸도데실기, n-트리데실기, n-테트라데실기, n-펜타데실기, n-헥사데실기, 2-에틸헥사데실기, 2-부틸헥사데실기, 2-헥실헥사데실기, 2-옥틸헥사데실기, n-헵타데실기, n-옥타데실기, n-노나데실기, n-이코실기, 2-에틸이코실기, 2-부틸이코실기, 2-헥실이코실기, 2-옥틸이코실기, n-헨이코실기, n-도코실기, n-트리코실기, n-테트라코실기, n-펜타코실기, n-헥사코실기, n-헵타코실기, n-옥타코실기, n-노나코실기, 및 n-트리아콘틸기 등을 들 수 있지만, 이들에 한정되지 않는다.In the present specification, the alkyl group may be linear, branched or cyclic. Carbon number of an alkyl group is 1 or more and 50 or less, 1 or more and 30 or less, 1 or more and 20 or less, 1 or more and 10 or less, or 1 or more and 6 or less. Examples of the alkyl group include methyl group, ethyl group, n-propyl group, isopropyl group, n-butyl group, s-butyl group, t-butyl group, i-butyl group, 2-ethylbutyl group, 3, 3-dimethylbutyl group , n-pentyl group, i-pentyl group, neopentyl group, t-pentyl group, cyclopentyl group, 1-methylpentyl group, 3-methylpentyl group, 2-ethylpentyl group, 4-methyl-2-pentyl group , n-hexyl group, 1-methylhexyl group, 2-ethylhexyl group, 2-butylhexyl group, cyclohexyl group, 4-methylcyclohexyl group, 4-t-butylcyclohexyl group, n-heptyl group, 1 -Methylheptyl group, 2,2-dimethylheptyl group, 2-ethylheptyl group, 2-butylheptyl group, n-octyl group, t-octyl group, 2-ethyloctyl group, 2-butyloctyl group, 2-hexyl group Siloctyl group, 3,7-dimethyloctyl group, cyclooctyl group, n-nonyl group, n-decyl group, adamantyl group, 2-ethyldecyl group, 2-butyldecyl group, 2-hexyldecyl group, 2-ox Tyldecyl group, n-undecyl group, n-dodecyl group, 2-ethyldodecyl group, 2-butyldodecyl group, 2-hexyldodecyl group, 2-octyldodecyl group, n-tridecyl group, n-tetradecyl group, n -pentadecyl group, n-hexadecyl group, 2-ethylhexadecyl group, 2-butylhexadecyl group, 2-hexylhexadecyl group, 2-octylhexadecyl group, n-heptadecyl group, n-octadecyl group , n-nonadecyl group, n-icosyl group, 2-ethyl icosyl group, 2-butyl icosyl group, 2-hexyl icosyl group, 2-octyl icosyl group, n-henicosyl group, n-docosyl group, n-tricho Sil group, n-tetracosyl group, n-pentacosyl group, n-hexacosyl group, n-heptacosyl group, n-octacosyl group, n-nonacosyl group, and n-triacontyl group, etc. are mentioned, It is not limited to these.
본 명세서에서 알케닐기는, 탄소수 2이상의 알킬기의 중간 또는 말단에 하나 이상의 탄소 이중 결합을 포함한 탄화수소 그룹을 의미한다. 알케닐기는 직쇄 또는 분지쇄일 수 있다. 탄소수는 특별히 한정되지 않으나, 2 이상 30 이하, 2 이상 20 이하 또는 2 이상 10 이하이다. 알케닐기의 예로는 비닐기, 1-부테닐기, 1-펜테닐기, 1,3-부타디에닐 아릴기, 스티레닐기, 스티릴비닐기 등이 있으나, 이들에 한정되지 않는다.In the present specification, the alkenyl group refers to a hydrocarbon group including one or more carbon double bonds in the middle or terminal of an alkyl group having 2 or more carbon atoms. The alkenyl group may be straight-chain or branched. Although carbon number is not specifically limited, 2 or more and 30 or less, 2 or more and 20 or less, or 2 or more and 10 or less. Examples of the alkenyl group include, but are not limited to, a vinyl group, a 1-butenyl group, a 1-pentenyl group, a 1,3-butadienyl aryl group, a styrenyl group, and a styryl vinyl group.
본 명세서에서 알키닐기는, 탄소수 2이상의 알킬기의 중간 또는 말단에 하나 이상의 탄소 삼중 결합을 포함한 탄화수소 그룹을 의미한다. 알키닐기는 직쇄, 분지쇄, 또는 고리형일 수 있다. 탄소수는 특별히 한정되지 않으나, 2 이상 30 이하, 2 이상 20 이하 또는 2 이상 10 이하이다. 알키닐기의 구체적인 예에는, 에티닐기, 프로피닐기, 등이 포함될 수 있으나, 이들에 한정되지 않는다.In the present specification, the alkynyl group refers to a hydrocarbon group including one or more carbon triple bonds in the middle or terminal of an alkyl group having 2 or more carbon atoms. The alkynyl group may be straight chain, branched chain, or cyclic. Although carbon number is not specifically limited, 2 or more and 30 or less, 2 or more and 20 or less, or 2 or more and 10 or less. Specific examples of the alkynyl group include, but are not limited to, an ethynyl group, a propynyl group, and the like.
본 명세서에서, 탄화수소 고리기는 지방족 탄화수소 고리로부터 유도된 임의의 작용기 또는 치환기, 또는 방향족 탄화수소 고리로부터 유도된 임의의 작용기 또는 치환기일 수 있다. 탄화수소 고리기의 고리 형성 탄소수 5 이상 60 이하, 5 이상 30 이하, 또는 5 이상 20 이하일 수 있다.In the present specification, the hydrocarbon ring group may be any functional group or substituent derived from an aliphatic hydrocarbon ring, or any functional group or substituent derived from an aromatic hydrocarbon ring. The number of ring carbon atoms of the hydrocarbon ring group may be 5 or more and 60 or less, 5 or more and 30 or less, or 5 or more and 20 or less.
본 명세서에서, 아릴기는 방향족 탄화수소 고리로부터 유도된 임의의 작용기 또는 치환기를 의미한다. 아릴기는 단환식 아릴기 또는 다환식 아릴기일 수 있다. 아릴기의 고리 형성 탄소수는 6 이상 30 이하, 6 이상 20 이하, 또는 6 이상 15 이하일 수 있다. 아릴기의 예로는 페닐기, 나프틸기, 플루오레닐기, 안트라세닐기, 페난트릴기, 비페닐기, 터페닐기, 쿼터페닐기, 퀸크페닐기, 섹시페닐기, 트리페닐에닐기, 피레닐기, 벤조 플루오란테닐기, 크리세닐기 등을 예시할 수 있지만, 이들에 한정되지 않는다.As used herein, the aryl group means any functional group or substituent derived from an aromatic hydrocarbon ring. The aryl group may be a monocyclic aryl group or a polycyclic aryl group. The number of ring carbon atoms of the aryl group may be 6 or more and 30 or less, 6 or more and 20 or less, or 6 or more and 15 or less. Examples of the aryl group include a phenyl group, a naphthyl group, a fluorenyl group, an anthracenyl group, a phenanthryl group, a biphenyl group, a terphenyl group, a quarterphenyl group, a quinkphenyl group, a sexyphenyl group, a triphenylenyl group, a pyrenyl group, a benzofluoranthenyl group , a chrysenyl group, and the like can be exemplified, but the present invention is not limited thereto.
본 명세서에서, 헤테로 고리기는 헤테로 원자로 B, O, N, P, Si 및 S 중 1개 이상을 포함하는 고리로부터 유도된 임의의 작용기 또는 치환기를 의미한다. 헤테로 고리기는 지방족 헤테로 고리기 및 방향족 헤테로 고리기를 포함한다. 방향족 헤테로 고리기는 헤테로아릴기일 수 있다. 지방족 헤테로 고리 및 방향족 헤테로 고리는 단환 또는 다환일 수 있다.As used herein, the heterocyclic group refers to any functional group or substituent derived from a ring including at least one of B, O, N, P, Si and S as a hetero atom. The heterocyclic group includes an aliphatic heterocyclic group and an aromatic heterocyclic group. The aromatic heterocyclic group may be a heteroaryl group. The aliphatic heterocycle and the aromatic heterocycle may be monocyclic or polycyclic.
본 명세서에서, 헤테로아릴기는 헤테로 원자로 B, O, N, P, Si 및 S 중 1개 이상을 포함하는 것일 수 있다. 헤테로아릴기가 헤테로 원자를 2개 이상 포함할 경우, 2개 이상의 헤테로 원자는 서로 동일할 수도 있고, 상이할 수도 있다. 헤테로아릴기는 단환식 헤테로 고리기 또는 다환식 헤테로 고리기일 수 있다. 헤테로아릴기의 고리 형성 탄소수는 2 이상 30 이하, 2 이상 20 이하, 또는 2 이상 10 이하일 수 있다. 헤테로아릴기의 예로는 티오펜기, 퓨란기, 피롤기, 이미다졸기, 트리아졸기, 피리딘기, 비피리딘기, 피리미딘기, 트리아진기, 아크리딜기, 피리다진기, 피라지닐기, 퀴놀린기, 퀴나졸린기, 퀴녹살린기, 페녹사진기, 프탈라진기, 피리도 피리미딘기, 피리도 피라진기, 피라지노 피라진기, 이소퀴놀린기, 인돌기, 카바졸기, N-아릴카바졸기, N-헤테로아릴카바졸기, N-알킬카바졸기, 벤조옥사졸기, 벤조이미다졸기, 벤조티아졸기, 벤조카바졸기, 벤조티오펜기, 디벤조티오펜기, 티에노티오펜기, 벤조퓨란기, 페난트롤린기, 티아졸기, 이소옥사졸기, 옥사졸기, 옥사디아졸기, 티아디아졸기, 페노티아진기, 디벤조실롤기 및 디벤조퓨란기 등이 있으나, 이들에 한정되지 않는다.In the present specification, the heteroaryl group may include one or more of B, O, N, P, Si and S as a hetero atom. When the heteroaryl group includes two or more hetero atoms, the two or more hetero atoms may be the same as or different from each other. The heteroaryl group may be a monocyclic heterocyclic group or a polycyclic heterocyclic group. The number of ring carbon atoms of the heteroaryl group may be 2 or more and 30 or less, 2 or more and 20 or less, or 2 or more and 10 or less. Examples of the heteroaryl group include a thiophene group, a furan group, a pyrrole group, an imidazole group, a triazole group, a pyridine group, a bipyridine group, a pyrimidine group, a triazine group, an acridyl group, a pyridazine group, a pyrazinyl group, a quinoline group, quinazoline group, quinoxaline group, phenoxazine group, phthalazine group, pyridopyrimidine group, pyridopyrazine group, pyrazinopyrazine group, isoquinoline group, indole group, carbazole group, N-arylcarbazole group, N -Heteroarylcarbazole group, N-alkylcarbazole group, benzooxazole group, benzoimidazole group, benzothiazole group, benzocarbazole group, benzothiophene group, dibenzothiophene group, thienothiophene group, benzofuran group, phenane Trollin group, thiazole group, isoxazole group, oxazole group, oxadiazole group, thiadiazole group, phenothiazine group, dibenzosilol group and dibenzofuran group, but are not limited thereto.
본 명세서에서, 실릴기는 알킬 실릴기 및 아릴 실릴기를 포함한다. 실릴기의 예로는 트리메틸실릴기, 트리에틸실릴기, t-부틸디메틸실릴기, 비닐디메틸실릴기, 프로필디메틸실릴기, 트리페닐실릴기, 디페닐실릴기, 페닐실릴기 등이 있으나, 이들에 한정되지 않는다.In the present specification, the silyl group includes an alkyl silyl group and an aryl silyl group. Examples of the silyl group include a trimethylsilyl group, a triethylsilyl group, a t-butyldimethylsilyl group, a vinyldimethylsilyl group, a propyldimethylsilyl group, a triphenylsilyl group, a diphenylsilyl group, a phenylsilyl group, and the like. not limited
본 명세서에서, 옥시기는 알콕시기 및 아릴 옥시기를 포함할 수 있다. 알콕시기는 직쇄, 분지쇄 또는 고리쇄일 수 있다. 알콕시기의 탄소수는 특별히 한정되지 않으나, 예를 들어 1 이상 20 이하 또는 1 이상 10 이하인 것일 수 있다. 옥시기의 예로는 메톡시, 에톡시, n-프로폭시, 이소프로폭시, 부톡시, 펜틸옥시, 헥실옥시, 옥틸옥시, 노닐옥시, 데실옥시, 벤질옥시 등이 있으나, 이들에 한정되는 것은 아니다.In the present specification, the oxy group may include an alkoxy group and an aryl oxy group. The alkoxy group may be straight-chain, branched-chain or cyclic. The number of carbon atoms of the alkoxy group is not particularly limited, but may be, for example, 1 or more and 20 or less or 1 or more and 10 or less. Examples of the oxy group include, but are not limited to, methoxy, ethoxy, n-propoxy, isopropoxy, butoxy, pentyloxy, hexyloxy, octyloxy, nonyloxy, decyloxy, benzyloxy, etc. it is not
본 명세서에서, 아민기의 탄소수는 특별히 한정되지 않으나, 1 이상 30 이하일 수 있다. 아민기는 알킬 아민기, 아릴 아민기, 또는 헤테로아릴 아민기를 포함할 수 있다. 아민노기의 예로는 메틸아민기, 디메틸아민기, 페닐아민기, 디페닐아민기, 나프틸아민기, 9-메틸-안트라세닐아민기, 트리페닐아민기 등이 있으나, 이들에 한정되지 않는다.In the present specification, the number of carbon atoms of the amine group is not particularly limited, but may be 1 or more and 30 or less. The amine group may include an alkyl amine group, an aryl amine group, or a heteroaryl amine group. Examples of the amino group include, but are not limited to, a methylamine group, a dimethylamine group, a phenylamine group, a diphenylamine group, a naphthylamine group, a 9-methyl-anthracenylamine group, and a triphenylamine group.
한편, 본 명세서에서 "" 는 연결되는 위치를 의미한다.On the other hand, in this specification " " means the location to be connected.
일 실시예에 따른 유기 금속 화합물은 하기 화학식 1로 표시될 수 있다.The organometallic compound according to an embodiment may be represented by Formula 1 below.
[화학식 1][Formula 1]
화학식 1에서, M은 중심 금속 원자로, M은 전이 금속이다.In Formula 1, M is a central metal atom, and M is a transition metal.
화학식 1에서, X1 내지 X6 중 선택되는 하나 또는 둘이 N(Nitrogen)이고, 나머지는 CR4이다. X1 내지 X6 중 하나를 선택하는 경우, X2 내지 X6 중 하나가 선택될 수 있다. 또한, X1 내지 X6 중 둘을 선택하는 경우에는 X1이 선택되고 X2 내지 X6 중 하나가 선택되거나, X2 내지 X6 중 둘이 선택될 수 있다. 화학식 1에서, X1 내지 X6 중 선택되는 하나 또는 둘이 N(Nitrogen)이고, 나머지는 CR4인 방향족 축합환은 카볼린(carboline)기일 수 있다.In Formula 1, one or two selected from X 1 to X 6 is N(Nitrogen), and the remainder is CR 4 . When one of X 1 to X 6 is selected, one of X 2 to X 6 may be selected. In the case of selecting the two of X 1 to X 6 is or X 1 is selected and X 2 to X 6 is selected from one, two may be selected from X 2 to X 6. In Formula 1, one or two selected from X 1 to X 6 may be N (Nitrogen), and the remaining aromatic condensed ring having CR 4 may be a carboline group.
X1이 N인 경우, X2 내지 X6 중 적어도 하나는 N이다. 즉, X1이 N이고, X2 내지 X6이 모두 CR4인 경우는 제외한다. R4는 수소 원자, 중수소 원자, 또는 치환 또는 비치환된 탄소 수 1 이상 10 이하의 알킬기이다. 예를 들어, X1이 N인 경우, X3이 N이고, X2, X4, X5 및 X6은 CH일 수 있다. When X 1 is N, at least one of X 2 to X 6 is N. That is, the case where X 1 is N and X 2 to X 6 is all CR 4 is excluded. R 4 is a hydrogen atom, a deuterium atom, or a substituted or unsubstituted alkyl group having 1 to 10 carbon atoms. For example, when X 1 is N, X 3 may be N, and X 2 , X 4 , X 5 and X 6 may be CH.
A1 내지 A3은 각각 독립적으로 치환 또는 비치환된 고리형성 탄소수 5 이상 60 이하의 탄화수소 고리, 또는 치환 또는 비치환된 고리형성 탄소수 1 이상 60 이하의 헤테로 고리일 수 있다. 예를 들어, A1 및 A2는 각각 독립적으로 고리형성 탄소수 5 이상 10 이하의 헤테로 아릴기이고, A3은 탄소수 5 이상 10 이하의 아릴기일 수 있다.A 1 to A 3 may each independently represent a substituted or unsubstituted hydrocarbon ring having 5 to 60 carbon atoms, or a substituted or unsubstituted heterocyclic ring having 1 to 60 carbon atoms. For example, A 1 and A 2 may each independently be a heteroaryl group having 5 or more and 10 or less ring carbon atoms, and A 3 may be an aryl group having 5 or more and 10 or less carbon atoms.
b1 내지 b3은 각각 독립적으로 1 이상 4 이하의 정수이다. b1 내지 b3이 2 이상의 정수인 경우, 복수의 R1 내지 R3은 각각 독립적으로 모두 동일하거나 적어도 하나가 상이한 것일 수 있다. 예를 들어, b1이 2 이상의 정수인 경우, 복수의 R1은 모두 동일하거나, 적어도 하나의 R1은 나머지 R1과 상이할 수 있다.b1 to b3 are each independently an integer of 1 or more and 4 or less. When b1 to b3 are an integer of 2 or more, a plurality of R 1 to R 3 may be each independently all the same or at least one different. For example, when b1 is an integer of 2 or more, a plurality of R 1 may be all the same, or at least one R 1 may be different from the remaining R 1 .
R1 내지 R3은 각각 독립적으로 수소 원자, 중수소 원자, 할로겐 원자, 히드록시기, 시아노기, 니트로기, 치환 또는 비치환된 실릴기, 치환 또는 비치환된 아민기, 치환 또는 비치환된 옥시기, 치환 또는 비치환된 탄소수 1 이상 60 이하의 알킬기, 치환 또는 비치환된 탄소수 2 이상 60 이하의 알케닐기, 치환 또는 비치환된 탄소수 2 이상 60 이하의 알키닐기, 치환 또는 비치환된 고리형성 탄소수 6 이상 60 이하의 아릴기, 또는 치환 또는 비치환된 고리형성 탄소수 1 이상 10 이하의 헤테로 고리기일 수 있다. R 1 to R 3 are each independently a hydrogen atom, a deuterium atom, a halogen atom, a hydroxyl group, a cyano group, a nitro group, a substituted or unsubstituted silyl group, a substituted or unsubstituted amine group, a substituted or unsubstituted oxy group, A substituted or unsubstituted C1-C60 alkyl group, a substituted or unsubstituted C2-C60 alkenyl group, a substituted or unsubstituted C2-C60 alkynyl group, a substituted or unsubstituted C6-C6 It may be an aryl group of 60 or more, or a substituted or unsubstituted heterocyclic group having 1 or more and 10 or less ring carbon atoms.
R1 내지 R3 중 적어도 하나는 중수소 원자 또는 CD3이거나, 또는 R1 내지 R3 중 적어도 하나는 중수소 원자 또는 CD3으로 치환된 것일 수 있다. "D"는 중수소 원자일 수 있다. 예를 들어, b1이 2 이상의 정수인 경우, 복수의 R1은 중수소 원자일 수 있다. 이와 달리, R1은 중수소 원자로 치환된 아릴기일 수 있다. At least one of R 1 to R 3 may be a deuterium atom or CD 3 , or at least one of R 1 to R 3 may be substituted with a deuterium atom or CD 3 . "D" may be a deuterium atom. For example, when b1 is an integer of 2 or more, a plurality of R 1 may be deuterium atoms. Alternatively, R 1 may be an aryl group substituted with a deuterium atom.
예를 들어, R2는 t-부틸기 또는 3개의 중수소 원자로 치환된 메틸기일 수 있다. R3은 수소 원자, 또는 t-부틸기일 수 있다. 또한, R3은 알킬기로 치환된 페닐기를 포함하는 것으로, 알킬기는 메틸기, 이소프로필기, 및 중수소 원자로 치환된 메틸기 중 어느 하나일 수 있다. 하지만, 이는 예시적인 것이며, 실시예가 이에 한정되지 않는다.For example, R 2 may be a t-butyl group or a methyl group substituted with 3 deuterium atoms. R 3 may be a hydrogen atom or a t-butyl group. In addition, R 3 includes a phenyl group substituted with an alkyl group, and the alkyl group may be any one of a methyl group, an isopropyl group, and a methyl group substituted with a deuterium atom. However, this is exemplary, and the embodiment is not limited thereto.
L은 직접 결합(direct linkage), O, S, ―CR11R12―, ―CR13=CR14―, ―C≡C―, ―C(=O)―, ―C(=S)―, ―BR15―, ―NR16―, ―PR17R18―, 또는 ―GeR19R20― 일 수 있다. 예를 들어, L은 산소 원자일 수 있다.L is a direct linkage, O, S, —CR 11 R 12 —, —CR 13 =CR 14 —, —C≡C—, —C(=O)—, —C(=S)—, —BR 15 —, —NR 16 —, —PR 17 R 18 —, or —GeR 19 R 20 —. For example, L may be an oxygen atom.
R11 내지 R20은 각각 독립적으로 수소 원자, 중수소 원자, 할로겐 원자, 치환 또는 비치환된 탄소수 1 이상 30 이하의 알킬기, 또는 치환 또는 비치환된 고리 형성 탄소수 6 이상 30 이하의 아릴기일 수 있다.R 11 to R 20 may each independently be a hydrogen atom, a deuterium atom, a halogen atom, a substituted or unsubstituted alkyl group having 1 to 30 carbon atoms, or a substituted or unsubstituted aryl group having 6 to 30 ring carbon atoms.
화학식 1로 표시되는 일 실시예의 유기 금속 화합물은 X1 내지 X6 중 선택되는 하나 또는 둘이 질소 원자이고, 이에 따라 개선된 MLCT(Metal to Ligand Charge Transfer) 비율을 나타낼 수 있다. 일 실시예의 유기 금속 화합물은 높은 MLCT 비율을 나타냄으로써, 발광층 재료로 사용될 경우 유기 전계 발광 소자의 효율 향상에 기여할 수 있다. 한편 본 명세서에서 설명된 MLCT 비율은 3MLCT(triplet Metal to Ligand Charge Transfer) 비율을 지칭하는 것으로, 금속 원자에서 리간드로 100% 전하 이동되는 경우를 기준으로 할 때의 상대적인 비율을 나타낸 것이다. One or two selected from the group consisting of X 1 to X 6 of the organometallic compound represented by Chemical Formula 1 is a nitrogen atom, and thus may exhibit an improved MLCT (Metal to Ligand Charge Transfer) ratio. The organometallic compound of an embodiment exhibits a high MLCT ratio, and when used as a light emitting layer material, may contribute to improving the efficiency of an organic electroluminescent device. Meanwhile, the MLCT ratio described herein refers to a triplet metal to ligand charge transfer (MLCT) ratio of 3 , and represents a relative ratio based on 100% charge transfer from a metal atom to a ligand.
또한, 일 실시예의 유기 금속 화합물은 중수소 원자를 치환기로 포함함으로써, 발광층 재료로 사용될 경우 수명 및 효율이 향상된 소자 특성을 나타낼 수 있다.In addition, since the organometallic compound according to an exemplary embodiment includes a deuterium atom as a substituent, when used as a material for the light emitting layer, device characteristics with improved lifespan and efficiency may be exhibited.
화학식 1에서, M은 4배위 리간드와 결합하는 금속 원자일 수 있다. M은 Pt(백금), Pd(팔라듐), Cu(구리), 또는 Os(오스뮴) 등의 금속 원자일 수 있으며, 구체적으로 M은 Pt일 수 있다.In Formula 1, M may be a metal atom bonded to a tetracoordinate ligand. M may be a metal atom such as Pt (platinum), Pd (palladium), Cu (copper), or Os (osmium), specifically, M may be Pt.
한편, 화학식 1은 하기 화학식 2-1 또는 화학식 2-2로 표시될 수 있다. 화학식 2-1은 화학식 1에서 금속 원자 M이 Pt이고, L이 O인 유기 금속 화합물에 해당한다. 화학식 2-2는 화학식 1에서 금속 원자 M이 Pt이고, L이 ―CR11R12― 에서 R11R12가 모두 플루오린(fluorine)원자인 유기 금속 화합물에 해당한다.Meanwhile, Chemical Formula 1 may be represented by the following Chemical Formula 2-1 or Chemical Formula 2-2. Formula 2-1 corresponds to an organometallic compound in which metal atom M is Pt and L is O in Formula 1; Formula 2-2 corresponds to an organometallic compound in which metal atom M in Formula 1 is Pt, and L is —CR 11 R 12 — to R 11 R 12 are all fluorine atoms.
[화학식 2-1][Formula 2-1]
[화학식 2-2][Formula 2-2]
화학식 2-1 및 화학식 2-2에서, X1 내지 X6, R1 내지 R3, 및 b1 내지 b3에 대해서는 화학식 1에서 설명한 내용과 동일한 내용이 적용될 수 있다. 또한, 화학식 1은 하기 화학식 3으로 표시될 수 있다. 화학식 3은 화학식 1에서 A1 내지 A3이 방향족 고리인 경우를 나타낸 것이다. A1은 이미다졸(imidazole), A2는 피리딘(pyridine), A3은 아릴기인 경우를 나타낸 것이다.In Formulas 2-1 and 2-2, the same contents as those described in Formula 1 may be applied to X 1 to X 6 , R 1 to R 3 , and b 1 to b 3 . In addition, Chemical Formula 1 may be represented by Chemical Formula 3 below. Formula 3 shows a case in which A 1 to A 3 in Formula 1 is an aromatic ring. A 1 is imidazole, A 2 is pyridine, and A 3 is an aryl group.
[화학식 3][Formula 3]
화학식 3에서 R50은 수소 원자, 중수소 원자, 할로겐 원자, 치환 또는 비치환된 탄소수 1 이상 30 이하의 알킬기, 또는 치환 또는 비치환된 탄소수 6 이상 30 이하의 아릴기일 수 있다.In Formula 3, R 50 may be a hydrogen atom, a deuterium atom, a halogen atom, a substituted or unsubstituted alkyl group having 1 to 30 carbon atoms, or a substituted or unsubstituted aryl group having 6 to 30 carbon atoms.
예를 들어, R50은 중수소 원자 및 방향족 고리기 중 어느 하나를 포함하는 것일 수 있다. R50은 중수소 원자로 치환된 메틸기, 중수소 원자로 치환된 아릴기일 수 있다. R50은 1개 내지 2개의 이소프로필기로 치환된 페닐기 또는 1개 내지 2개의 페닐기로 치환된 페닐기일 수 있다. 1개 내지 2개의 페닐기는 중수소 원자를 치환기로 포함하고, 페닐기의 모든 수소가 중수소 원자로 치환된 것일 수 있다. 하지만, 이는 예시적인 것이며, 실시예가 이에 한정되는 것은 아니다.For example, R 50 may include any one of a deuterium atom and an aromatic ring group. R 50 may be a methyl group substituted with a deuterium atom or an aryl group substituted with a deuterium atom. R 50 may be a phenyl group substituted with 1 to 2 isopropyl groups or a phenyl group substituted with 1 to 2 phenyl groups. One or two phenyl groups may include a deuterium atom as a substituent, and all hydrogens of the phenyl group may be substituted with deuterium atoms. However, this is an example, and the embodiment is not limited thereto.
화학식 3에서 M, L, X1 내지 X6, R1 내지 R3, 및 b1 내지 b3에 대해서는 화학식 1에서 설명한 내용과 동일한 내용이 적용될 수 있다.In Formula 3, the same contents as those described in Formula 1 may be applied to M, L, X 1 to X 6 , R 1 to R 3 , and b 1 to b 3 .
화학식 3은 하기 화학식 3-1로 표시되는 것일 수 있다. 화학식 3에서 X1 내지 X6 중 선택되는 둘이 N인 경우를 나타낸 것이다. Chemical formula 3 may be represented by the following Chemical Formula 3-1. In Formula 3, X 1 to X 6 represents a case where two selected from N are N.
[화학식 3-1] [Formula 3-1]
화학식 3-1에서 X1은 N이고, X2 내지 X6 중 어느 하나가 N이고, 나머지는 CR4일 수 있다. 예를 들어, X1 및 X3이 N이고, X2, X4, X5 및 X6이 CH일 수 있다.In Formula 3-1, X 1 may be N, any one of X 2 to X 6 may be N, and the rest may be CR 4 . For example, X 1 and X 3 may be N, and X 2 , X 4 , X 5 and X 6 may be CH.
화학식 3-1에서 M, L, R1 내지 R4, R50 및 b1 내지 b3에 대해서는 화학식 3에서 설명한 내용과 동일한 내용이 적용될 수 있다.In Formula 3-1, the same contents as those described in Formula 3 may be applied to M, L, R 1 to R 4 , R 50 and b 1 to b 3 .
또한, 화학식 3은 하기 화학식 3-2 또는 화학식 3-3으로 표시되는 것일 수 있다. 화학식 3-1과 달리 X1 내지 X6 중 선택되는 하나가 N인 경우를 나타낸 것으로, 화학식 3-2 및 화학식 3-3은 X1이 CR5이고, X2 내지 X6 중 어느 하나가 N이고 나머지는 CR4인 경우를 나타낸 것이다.In addition, Chemical Formula 3 may be represented by the following Chemical Formula 3-2 or Chemical Formula 3-3. Unlike Formula 3-1 , it represents a case in which one selected from X 1 to X 6 is N, and in Formulas 3-2 and 3-3, X 1 is CR 5 , and any one of X 2 to X 6 is N and the rest is CR 4 .
[화학식 3-2][Formula 3-2]
[화학식 3-3][Formula 3-3]
화학식 3-2에서, X2 내지 X4 중 어느 하나는 N이고, 나머지는 CR4일 수 있다. 예를 들어, X2는 N, X3 및 X4는 CR4일 수 있다. R5는 수소 원자, 중수소 원자, 또는 치환 또는 비치환된 탄소 수 1 이상 10 이하의 알킬기일 수 있다. 예를 들어, R4 및 R5는 메틸기로 동일한 것일 수 있다. In Formula 3-2, any one of X 2 to X 4 may be N, and the rest may be CR 4 . For example, X 2 may be N, X 3 and X 4 may be CR 4 . R 5 may be a hydrogen atom, a deuterium atom, or a substituted or unsubstituted alkyl group having 1 to 10 carbon atoms. For example, R 4 and R 5 may be the same as a methyl group.
화학식 3-3에서, X5 및 X6 중 어느 하나는 N이고, 나머지는 CR6일 수 있다. R6은 수소 원자, 중수소 원자, 또는 치환 또는 비치환된 탄소 수 1 이상 10 이하의 알킬기일 수 있다. b4는 1 이상 4 이하의 정수일 수 있다. 예를 들어, X5는 N, X6은 CH이고, R4는 중수소 원자일 수 있다. In Formula 3-3, any one of X 5 and X 6 may be N, and the rest may be CR 6 . R 6 may be a hydrogen atom, a deuterium atom, or a substituted or unsubstituted alkyl group having 1 to 10 carbon atoms. b4 may be an integer of 1 or more and 4 or less. For example, X 5 may be N, X 6 may be CH, and R 4 may be a deuterium atom.
화학식 3-2 및 화학식 3-3에서 M, L, R1 내지 R4, b1 내지 b3, 및 R50에 대해서는 화학식 3에서 설명한 내용과 동일한 내용이 적용될 수 있다.In Formulas 3-2 and 3-3, the same contents as those described in Formula 3 may be applied to M, L, R 1 to R 4 , b 1 to b 3 , and R 50 .
한편, R50은 화합물군 R의 화합물들 중 어느 하나로 표시되는 것일 수 있다.Meanwhile, R 50 may be represented by any one of the compounds of the compound group R.
[화합물군 R][Compound group R]
화합물군 R에서 R50이 중수소 원자를 포함하지 않는 화합물인 경우, R1은 중수소 원자를 치환기로 포함할 수 있다. R50이 R-7 또는 R-8인 경우에 R1은 중수소 원자일 수 있다. 예를 들어, R50이 R-7이고 b1이 4인 경우, 복수의 R1은 모두 중수소 원자일 수 있다.In the compound group R, when R 50 is a compound that does not include a deuterium atom, R 1 may include a deuterium atom as a substituent. When R 50 is R-7 or R-8, R 1 may be a deuterium atom. For example, when R 50 is R-7 and b1 is 4, a plurality of R 1 may all be deuterium atoms.
일 실시예의 유기 금속 화합물은 청색 광을 발광하는 발광 도펀트일 수 있다. 또한, 일 실시예의 유기 금속 화합물은 인광 도펀트일 수 있다.The organometallic compound of an embodiment may be a light emitting dopant emitting blue light. In addition, the organometallic compound according to an embodiment may be a phosphorescent dopant.
일 실시예의 유기 금속 화합물은 하기 화합물군 1에 표시된 화합물들 중 어느 하나로 표시될 수 있다. 발광층(EML)은 하기 화합물군 1에 표시된 화합물들 중 적어도 하나를 포함할 수 있다.The organometallic compound of an embodiment may be represented by any one of the compounds shown in Compound Group 1 below. The emission layer EML may include at least one of the compounds shown in Compound Group 1 below.
[화합물군 1][Compound group 1]
. .
화합물군 1에서 제시된 구체예 화합물들에서, "D"는 중수소 원자에 해당한다.In the embodiment compounds set forth in compound group 1, "D" corresponds to a deuterium atom.
일 실시예의 유기 전계 발광 소자(10)에서 발광층(EML)은 카볼린기 및 중수소 원자를 포함하는 일 실시예의 유기 금속 화합물을 포함하여 개선된 발광 효율 특성을 나타낼 수 있다. 일 실시예의 유기 금속 화합물은 카볼린기 및 중수소 원자를 포함하여 향상된 3MLCT 비율을 나타낼 수 있다.In the
한편, 도 1 내지 도 4에 도시된 일 실시예의 유기 전계 발광 소자(10)에서 발광층(EML)은 호스트 및 도펀트를 포함할 수 있고, 발광층(EML)은 화학식 1로 표시되는 유기 금속 화합물을 도펀트 재료로 포함할 수 있다. On the other hand, in the
일 실시예에서 발광층(EML)은 인광 발광하는 것일 수 있다. 예를 들어, 화학식 1로 표시되는 일 실시예에 따른 유기 금속 화합물은 인광 도펀트일 수 있다.In an embodiment, the emission layer EML may emit phosphorescence. For example, the organometallic compound according to the exemplary embodiment represented by Formula 1 may be a phosphorescent dopant.
한편, 발광층(EML)은 상술한 일 실시예의 유기 금속 화합물 이외에 호스트 물질을 더 포함할 수 있다. 일 실시예의 유기 전계 발광 소자(10)에서 발광층(EML)은 호스트 물질로 당 기술분야에 알려진 일반적인 재료를 포함할 수 있다. 예를 들어, DPEPO(Bis[2-(diphenylphosphino)phenyl] ether oxide), CBP(4,4'-Bis(carbazol-9-yl)biphenyl), mCP(1,3-Bis(carbazol-9-yl)benzene), PPF (2,8-Bis(diphenylphosphoryl)dibenzo[b,d]furan), TCTA(4,4',4''-Tris(carbazol-9-yl)-triphenylamine) 및 TPBi(1,3,5-tris(1-phenyl-1H-benzo[d]imidazole-2-yl)benzene) 중 적어도 하나를 포함하는 것일 수 있다. 다만, 이에 의하여 한정되는 것은 아니며, 예를 들어, Alq3(tris(8-hydroxyquinolino)aluminum), CBP(4,4'-bis(N-carbazolyl)-1,1'-biphenyl), PVK(poly(n-vinylcabazole), ADN(9,10-di(naphthalene-2-yl)anthracene), TCTA(4,4',4''-Tris(carbazol-9-yl)-triphenylamine), TPBi(1,3,5-tris(N-phenylbenzimidazole-2-yl)benzene), TBADN(3-tert-butyl-9,10-di(naphth-2-yl)anthracene), DSA(distyrylarylene), CDBP(4,4′-bis(9-carbazolyl)-2,2′-dimethyl-biphenyl), MADN(2-Methyl-9,10-bis(naphthalen-2-yl)anthracene), DPEPO(bis[2-(diphenylphosphino)phenyl]ether oxide), CP1(Hexaphenyl cyclotriphosphazene), UGH2 (1,4-Bis(triphenylsilyl)benzene), DPSiO3 (Hexaphenylcyclotrisiloxane), DPSiO4 (Octaphenylcyclotetra siloxane), PPF(2,8-Bis(diphenylphosphoryl)dibenzofuran), BCPDS(bis(4-(9H-carbazol-9-yl)phenyl)diphenylsilane), POPCPA((4-(1-(4-(diphenylamino)phenyl)cyclohexyl)phenyl)diphenylphosphine oxide) 등을 호스트 재료로 사용할 수 있다.Meanwhile, the emission layer EML may further include a host material in addition to the organometallic compound of the above-described exemplary embodiment. In the
또한, 일 실시예의 유기 전계 발광 소자(10)의 발광층(EML)은 상술한 유기 금속 화합물 이외에 공지의 도펀트 재료를 더 포함할 수 있다. 예를 들어, 발광층(EML)은 공지의 형광 도펀트 재료, 공지의 지연형광 도펀트 재료, 또는 공지의 인광 도펀트 재료를 더 포함할 수 있다.In addition, the light emitting layer (EML) of the
한편, 도면에 도시되지는 않았으나 일 실시예의 유기 전계 발광 소자(10)는 복수의 발광층들을 포함하는 것일 수 있다. 복수의 발광층들은 순차적으로 적층되어 제공되는 것일 수 있으며, 예를 들어 복수의 발광층들을 포함하는 유기 전계 발광 소자(10)는 백색광을 방출하는 것일 수 있다. 복수의 발광층들을 포함하는 유기 전계 발광 소자는 탠덤(Tandem) 구조의 유기 전계 발광 소자일 수 있다. 유기 전계 발광 소자(10)가 복수의 발광층들을 포함하는 경우 적어도 하나의 발광층(EML)은 상술한 바와 같이 일 실시예의 유기 금속 화합물을 포함할 수 있다.Meanwhile, although not shown in the drawings, the
도 1 내지 도 4에 도시된 일 실시예의 유기 전계 발광 소자(10)에서, 전자 수송 영역(ETR)은 발광층(EML) 상에 제공된다. 전자 수송 영역(ETR)은, 정공 저지층(HBL), 전자 수송층(ETL) 및 전자 주입층(EIL) 중 적어도 하나를 포함할 수 있으나, 실시예가 이에 한정되는 것은 아니다.In the
전자 수송 영역(ETR)은 단일 물질로 이루어진 단일층, 복수의 서로 다른 물질로 이루어진 단일층 또는 복수의 서로 다른 물질로 이루어진 복수의 층을 갖는 다층 구조를 가질 수 있다. The electron transport region ETR may have a single layer made of a single material, a single layer made of a plurality of different materials, or a multilayer structure having a plurality of layers made of a plurality of different materials.
예를 들어, 전자 수송 영역(ETR)은 전자 주입층(EIL) 또는 전자 수송층(ETL)의 단일층의 구조를 가질 수도 있고, 전자 주입 물질과 전자 수송 물질로 이루어진 단일층 구조를 가질 수도 있다. 또한, 전자 수송 영역(ETR)은, 복수의 서로 다른 물질로 이루어진 단일층의 구조를 갖거나, 발광층(EML)으로부터 차례로 적층된 전자 수송층(ETL)/전자 주입층(EIL), 정공 저지층(HBL)/전자 수송층(ETL)/전자 주입층(EIL) 구조를 가질 수 있으나, 이에 한정되는 것은 아니다. 전자 수송 영역(ETR)의 두께는 예를 들어, 약 1000Å 내지 약 1500Å인 것일 수 있다.For example, the electron transport region ETR may have a single layer structure of the electron injection layer EIL or the electron transport layer ETL, or may have a single layer structure including an electron injection material and an electron transport material. In addition, the electron transport region ETR has a single layer structure made of a plurality of different materials, or an electron transport layer (ETL)/electron injection layer (EIL), a hole blocking layer ( HBL)/electron transport layer (ETL)/electron injection layer (EIL) structure, but is not limited thereto. The thickness of the electron transport region ETR may be, for example, about 1000 Å to about 1500 Å.
전자 수송 영역(ETR)은, 진공 증착법, 스핀 코팅법, 캐스트법, LB법(Langmuir-Blodgett), 잉크젯 프린팅법, 레이저 프린팅법, 레이저 열전사법(Laser Induced Thermal Imaging, LITI) 등과 같은 다양한 방법을 이용하여 형성될 수 있다.Electron transport region (ETR), vacuum deposition method, spin coating method, casting method, LB method (Langmuir-Blodgett), inkjet printing method, laser printing method, laser thermal imaging (Laser Induced Thermal Imaging, LITI) various methods such as It can be formed using
전자 수송 영역(ETR)이 전자 수송층(ETL)을 포함할 경우, 전자 수송 영역(ETR)은 안트라센계 화합물을 포함하는 것일 수 있다. 다만, 이에 한정되는 것은 아니며, 전자 수송 영역은 예를 들어, Alq3(Tris(8-hydroxyquinolinato)aluminum), 1,3,5-tri[(3-pyridyl)-phen-3-yl]benzene, 2,4,6-tris(3'-(pyridin-3-yl)biphenyl-3-yl)-1,3,5-triazine, 2-(4-(N-phenylbenzoimidazol-1-yl)phenyl)-9,10-dinaphthylanthracene, TPBi(1,3,5-Tri(1-phenyl-1H-benzo[d]imidazol-2-yl)benzene), BCP(2,9-Dimethyl-4,7-diphenyl-1,10-phenanthroline), Bphen(4,7-Diphenyl-1,10-phenanthroline), TAZ(3-(4-Biphenylyl)-4-phenyl-5-tert-butylphenyl-1,2,4-triazole), NTAZ(4-(Naphthalen-1-yl)-3,5-diphenyl-4H-1,2,4-triazole), tBu-PBD(2-(4-Biphenylyl)-5-(4-tert-butylphenyl)-1,3,4-oxadiazole), BAlq(Bis(2-methyl-8-quinolinolato-N1,O8)-(1,1'-Biphenyl-4-olato)aluminum), Bebq2(berylliumbis(benzoquinolin-10-olate), ADN(9,10-di(naphthalene-2-yl)anthracene), BmPyPhB(1,3-Bis[3,5-di(pyridin-3-yl)phenyl]benzene) 및 이들의 혼합물을 포함하는 것일 수 있다. 전자 수송층(ETL)들의 두께는 약 100Å 내지 약 1000Å, 예를 들어 약 150Å 내지 약 500Å일 수 있다. 전자 수송층(ETL)들의 두께가 전술한 바와 같은 범위를 만족할 경우, 실질적인 구동 전압 상승 없이 만족스러운 정도의 전자 수송 특성을 얻을 수 있다.When the electron transport region ETR includes the electron transport layer ETL, the electron transport region ETR may include an anthracene-based compound. However, the present invention is not limited thereto, and the electron transport region is, for example, Alq 3 (Tris(8-hydroxyquinolinato)aluminum), 1,3,5-tri[(3-pyridyl)-phen-3-yl]benzene, 2,4,6-tris(3'-(pyridin-3-yl)biphenyl-3-yl)-1,3,5-triazine, 2-(4-(N-phenylbenzoimidazol-1-yl)phenyl)- 9,10-dinaphthylanthracene, TPBi(1,3,5-Tri(1-phenyl-1H-benzo[d]imidazol-2-yl)benzene), BCP(2,9-Dimethyl-4,7-diphenyl-1 ,10-phenanthroline), Bphen(4,7-Diphenyl-1,10-phenanthroline), TAZ(3-(4-Biphenylyl)-4-phenyl-5-tert-butylphenyl-1,2,4-triazole), NTAZ(4-(Naphthalen-1-yl)-3,5-diphenyl-4H-1,2,4-triazole), tBu-PBD(2-(4-Biphenylyl)-5-(4-tert-butylphenyl) -1,3,4-oxadiazole), BAlq(Bis(2-methyl-8-quinolinolato-N1,O8)-(1,1'-Biphenyl-4-olato)aluminum), Bebq 2 (berylliumbis(benzoquinolin-10) -olate), ADN(9,10-di(naphthalene-2-yl)anthracene), BmPyPhB(1,3-Bis[3,5-di(pyridin-3-yl)phenyl]benzene) and mixtures thereof The thickness of the electron transport layers (ETL) may be from about 100 Å to about 1000 Å, for example, from about 150 Å to about 500 Å. A satisfactory degree of electron transport characteristics can be obtained without increasing the driving voltage.
전자 수송 영역(ETR)이 전자 주입층(EIL)을 포함할 경우, 전자 수송 영역(ETR)은 LiF, NaCl, CsF, RbCl, RbI와 같은 할로겐화 금속, Yb와 같은 란타넘족 금속, Li2O, BaO 와 같은 금속 산화물, 또는 Liq(Lithium quinolate) 등이 사용될 수 있으나 이에 한정되는 것은 아니다. 전자 주입층(EIL)은 또한 전자 수송 물질과 절연성의 유기 금속염(organo metal salt)이 혼합된 물질로 이루어질 수 있다. 유기 금속염은 에너지 밴드 갭(energy band gap)이 대략 4eV 이상의 물질이 될 수 있다. 구체적으로 예를 들어, 유기 금속염은 금속 아세테이트(metal acetate), 금속 벤조에이트(metal benzoate), 금속 아세토아세테이트(metal acetoacetate), 금속 아세틸아세토네이트(metal acetylacetonate) 또는 금속 스테아레이트(stearate)를 포함할 수 있다. 전자 주입층(EIL)들의 두께는 약 1Å 내지 약 100Å, 약 3Å 내지 약 90Å일 수 있다. 전자 주입층(EIL)들의 두께가 전술한 바와 같은 범위를 만족할 경우, 실질적인 구동 전압 상승 없이 만족스러운 정도의 전자 주입 특성을 얻을 수 있다.When the electron transport region ETR includes the electron injection layer EIL, the electron transport region ETR includes a metal halide such as LiF, NaCl, CsF, RbCl, and RbI, a lanthanide metal such as Yb, Li 2 O, A metal oxide such as BaO or lithium quinolate (Liq) may be used, but is not limited thereto. The electron injection layer EIL may also be formed of a material in which an electron transport material and an insulating organo metal salt are mixed. The organometallic salt may be a material having an energy band gap of about 4 eV or more. Specifically, for example, the organometallic salt may include metal acetate, metal benzoate, metal acetoacetate, metal acetylacetonate, or metal stearate. can The electron injection layers EIL may have a thickness of about 1 Å to about 100 Å, and about 3 Å to about 90 Å. When the thickness of the electron injection layers EIL satisfies the above range, a satisfactory level of electron injection characteristics may be obtained without a substantial increase in driving voltage.
전자 수송 영역(ETR)은 앞서 언급한 바와 같이, 정공 저지층(HBL)을 포함할 수 있다. 정공 저지층(HBL)은 예를 들어, BCP(2,9-dimethyl-4,7-diphenyl-1,10-phenanthroline) 및 Bphen(4,7-diphenyl-1,10-phenanthroline) 중 적어도 하나를 포함할 수 있으나, 이에 한정되는 것은 아니다.As described above, the electron transport region ETR may include the hole blocking layer HBL. The hole blocking layer (HBL) may include, for example, at least one of 2,9-dimethyl-4,7-diphenyl-1,10-phenanthroline (BCP) and 4,7-diphenyl-1,10-phenanthroline (Bphen). may be included, but is not limited thereto.
제2 전극(EL2)은 전자 수송 영역(ETR) 상에 제공된다. 제2 전극(EL2)은 공통 전극 또는 캐소드(cathode)일 수 있다. 제2 전극(EL2)은 투과형 전극, 반투과형 전극 또는 반사형 전극일 수 있다. 제2 전극(EL2)이 투과형 전극인 경우, 제2 전극(EL2)은 투명 금속 산화물, 예를 들어, ITO(indium tin oxide), IZO(indium zinc oxide), ZnO(zinc oxide), ITZO(indium tin zinc oxide) 등으로 이루어질 수 있다.The second electrode EL2 is provided on the electron transport region ETR. The second electrode EL2 may be a common electrode or a cathode. The second electrode EL2 may be a transmissive electrode, a transflective electrode, or a reflective electrode. When the second electrode EL2 is a transmissive electrode, the second electrode EL2 is a transparent metal oxide, for example, indium tin oxide (ITO), indium zinc oxide (IZO), zinc oxide (ZnO), or indium (ITZO). tin zinc oxide) and the like.
제2 전극(EL2)이 반투과형 전극 또는 반사형 전극인 경우, 제2 전극(EL2)은 Ag, Mg, Cu, Al, Pt, Pd, Au, Ni, Nd, Ir, Cr, Li, Ca, LiF/Ca, LiF/Al, Mo, Ti 또는 이들을 포함하는 화합물이나 혼합물(예를 들어, Ag와 Mg의 혼합물)을 포함할 수 있다. 또는 상기 물질로 형성된 반사막이나 반투과막 및 ITO(indium tin oxide), IZO(indium zinc oxide), ZnO(zinc oxide), ITZO(indium tin zinc oxide) 등으로 형성된 투명 도전막을 포함하는 복수의 층 구조일 수 있다.When the second electrode EL2 is a transflective electrode or a reflective electrode, the second electrode EL2 may include Ag, Mg, Cu, Al, Pt, Pd, Au, Ni, Nd, Ir, Cr, Li, Ca, LiF/Ca, LiF/Al, Mo, Ti, or a compound or mixture containing them (eg, a mixture of Ag and Mg). Or a plurality of layer structures including a reflective or semi-transmissive film formed of the above material and a transparent conductive film formed of indium tin oxide (ITO), indium zinc oxide (IZO), zinc oxide (ZnO), indium tin zinc oxide (ITZO), etc. can be
도시하지는 않았으나, 제2 전극(EL2)은 보조 전극과 연결될 수 있다. 제2 전극(EL2)이 보조 전극과 연결되면, 제2 전극(EL2)의 저항을 감소 시킬 수 있다.Although not shown, the second electrode EL2 may be connected to the auxiliary electrode. When the second electrode EL2 is connected to the auxiliary electrode, the resistance of the second electrode EL2 may be reduced.
한편, 일 실시예의 유기 전계 발광 소자(10)의 제2 전극(EL2) 상에는 캡핑층(CPL)이 더 배치될 수 있다. 캡핑층(CPL)은 예를 들어, α-NPD, NPB, TPD, m-MTDATA, Alq3, CuPc, TPD15(N4,N4,N4',N4'-tetra (biphenyl-4-yl) biphenyl-4,4'-diamine), TCTA(4,4',4"- Tris (carbazol-9-yl) triphenylamine), N, N'-bis (naphthalen-1-yl) 등을 포함하는 것일 수 있다.Meanwhile, a capping layer CPL may be further disposed on the second electrode EL2 of the
본 발명의 일 실시예에 따른 유기 전계 발광 소자(10)는 상술한 바와 같이 카볼린기 및 중수소 원자를 포함하는 유기 금속 화합물을 발광층(EML)에 포함하여 우수한 발광 효율 특성을 나타낼 수 있다. As described above, the
이하에서는, 실시예 및 비교예를 참조하면서, 본 발명의 일 실시 형태에 따른 유기 금속 화합물 및 일 실시예의 유기 전계 발광 소자에 대해서 구체적으로 설명한다. 또한, 이하에 나타내는 실시예는 본 발명의 이해를 돕기 위한 일 예시이며, 본 발명의 범위가 이에 한정되는 것은 아니다.Hereinafter, an organic metal compound according to an embodiment of the present invention and an organic electroluminescent device according to an embodiment will be described in detail with reference to Examples and Comparative Examples. In addition, the examples shown below are examples for helping understanding of the present invention, and the scope of the present invention is not limited thereto.
[실시예][Example]
1. 유기 금속 화합물의 합성1. Synthesis of organometallic compounds
본 발명의 일 실시예에 따른 유기 금속 화합물은 예를 들어, 하기와 같이 합성할 수 있다. 다만, 본 발명의 일 실시예에 따른 유기 금속 화합물의 합성 방법이 이에 한정되는 것은 아니다.The organometallic compound according to an embodiment of the present invention may be synthesized as follows, for example. However, the method for synthesizing the organometallic compound according to an embodiment of the present invention is not limited thereto.
(1) 유기 금속 화합물 18의 합성(1) Synthesis of organometallic compound 18
일 실시예에 따른 유기 금속 화합물 18은 예를 들어 하기 반응식 1의 단계에 의해 합성될 수 있다.The organometallic compound 18 according to an embodiment may be synthesized, for example, by the step of Scheme 1 below.
[반응식 1][Scheme 1]
(중간체 A-1의 합성)(Synthesis of Intermediate A-1)
7-메톡시-9H-피리도[3,4-b]인돌 9.91g (50mmol)과 2-브로모-4-(메틸-d3)피리딘 13.1g (75mmol), 삼인삼칼륨 23g (100mmol), CuI 1.83g (10mmol), 피콜린산 1.17g (10mmol)을 반응용기에 넣고 디메틸술폭시드 150mL 에 현탁시켰다. 반응 혼합물을 가온하여 160℃에서 24시간 교반하였다. 반응 종결 후 상온으로 식히고 300mL 증류수를 가하고 에틸아세테이트로 추출하였다. 추출된 유기층을 포화염화나트륨 수용액으로 세척하고 소듐설페이트로 건조하였다. 용매를 제거한 잔여물을 컬럼 크로마토그래피를 이용하여 분리하여 13.1g (45mmol) 목적 화합물을 수득하였다.7-methoxy-9H-pyrido[3,4-b]indole 9.91g (50mmol) and 2-bromo-4-(methyl-d3)pyridine 13.1g (75mmol), potassium triphosphate 23g (100mmol), CuI 1.83 g (10 mmol) and picolinic acid 1.17 g (10 mmol) were placed in a reaction vessel and suspended in 150 mL of dimethyl sulfoxide. The reaction mixture was warmed and stirred at 160° C. for 24 hours. After completion of the reaction, it was cooled to room temperature, 300 mL distilled water was added, and the mixture was extracted with ethyl acetate. The extracted organic layer was washed with a saturated aqueous sodium chloride solution and dried over sodium sulfate. The residue after removing the solvent was separated using column chromatography to obtain 13.1 g (45 mmol) of the target compound.
(중간체 A-2의 합성)(Synthesis of Intermediate A-2)
중간체 [A-1] 13.1g (45mmol)을 과량의 브롬산 용액에 현탁시켰다. 반응 혼합물을 가온하여 110℃에서 24시간 교반하였다. 반응 종결 후 상온으로 식히고 적정량의 탄산수소나트륨을 가하여 중화시켰다. 300mL 증류수를 가하고 에틸아세테이트로 추출하였다. 추출된 유기층을 포화염나트륨 수용액으로 세척하고 소듐설페이트로 건조하였다. 용매를 제거한 잔여물을 컬럼 크로마토그래피를 이용하여 분리하여 9.56g (35mmol) 목적 화합물을 수득하였다.13.1 g (45 mmol) of intermediate [A-1] was suspended in an excess of hydrobromic acid solution. The reaction mixture was warmed and stirred at 110° C. for 24 hours. After completion of the reaction, the mixture was cooled to room temperature and neutralized by adding an appropriate amount of sodium hydrogen carbonate. 300 mL of distilled water was added, followed by extraction with ethyl acetate. The extracted organic layer was washed with a saturated aqueous sodium chloride solution and dried over sodium sulfate. The residue after removing the solvent was separated using column chromatography to obtain 9.56 g (35 mmol) of the target compound.
(중간체 A-3의 합성)(Synthesis of Intermediate A-3)
1-(3-브로모-5-t-뷰틸)페닐)1H-벤조[d]이미다졸 14.2g (43mmol), 중간체 [A-2] 9.1g (35mmol), 삼인삼칼륨 16.2g (70mmol), CuI 1.3g (7.0mmol), 피콜린산 0.8g (7.0mmol)을 반응용기에 넣고 디메틸술폭시드 100mL에 현탁시켰다. 반응 혼합물을 가온하여 160℃에서 24시간 교반하였다. 반응 종결 후 상온으로 식히고 300mL 증류수를 가하고 에틸아세테이트로 추출하였다. 추출된 유기층을 포화염화나트륨 수용액으로 세척하고 소듐설페이트로 건조하였다. 용매를 제거한 잔여물을 컬럼 크로마토그래피를 이용하여 분리하여 13.4g (26mmol) 목적 화합물을 수득하였다.1-(3-bromo-5-t-butyl)phenyl)1H-benzo[d]imidazole 14.2g (43mmol), intermediate [A-2] 9.1g (35mmol), triphosphate potassium 16.2g (70mmol) , CuI 1.3g (7.0mmol), and picolinic acid 0.8g (7.0mmol) were placed in a reaction vessel and suspended in 100 mL of dimethyl sulfoxide. The reaction mixture was warmed and stirred at 160° C. for 24 hours. After completion of the reaction, it was cooled to room temperature, 300 mL distilled water was added, and the mixture was extracted with ethyl acetate. The extracted organic layer was washed with a saturated aqueous sodium chloride solution and dried over sodium sulfate. The residue after removing the solvent was separated using column chromatography to obtain 13.4 g (26 mmol) of the target compound.
(중간체 A-4의 합성)(Synthesis of Intermediate A-4)
중간체 [A-3] 13.4g (26mmol)을 과량의 요오드화메탄에 현탁시켰다. 반응 혼합물을 가온하여 110℃에서 24시간 교반하였다. 반응 종결 후 상온으로 식히고 생성된 고체를 필터하여 에테르로 세척하였다. 세척된 고체를 재결정 이용하여 분리하여 14.8g (22mmol) 목적 화합물을 수득하였다.13.4 g (26 mmol) of intermediate [A-3] was suspended in an excess of methane iodide. The reaction mixture was warmed and stirred at 110° C. for 24 hours. After completion of the reaction, the mixture was cooled to room temperature, and the resulting solid was filtered and washed with ether. The washed solid was isolated by recrystallization to obtain 14.8 g (22 mmol) of the target compound.
(중간체 A-5의 합성)(Synthesis of Intermediate A-5)
중간체 [A-4] 14.8g (22mmol)과 헥사플루오로인산암모늄 14.6g (88mmol)을 반응용기에 넣고 메틸알코올 240mL와 물 60mL의 혼합용액에 현탁시켰다. 반응 혼합물을 상온에서 24시간 교반하였다. 반응 종결 후 생성된 고체를 필터하여 에테르로 세척하였다. 세척된 고체를 건조하여 12.4g (18 mmol) 목적 화합물을 수득하였다.Intermediate [A-4] 14.8 g (22 mmol) and 14.6 g (88 mmol) of ammonium hexafluorophosphate were placed in a reaction vessel, and suspended in a mixed solution of 240 mL of methyl alcohol and 60 mL of water. The reaction mixture was stirred at room temperature for 24 hours. After completion of the reaction, the resulting solid was filtered and washed with ether. The washed solid was dried to give 12.4 g (18 mmol) of the desired compound.
(화합물 18의 합성)(Synthesis of compound 18)
중간체 [A-5] 6.2g (9mmol)과 Dichloro(1,5-cyclooctadiene)platinum 3.7g (9.9mmol), 초산나트륨 4.4g (54mmol)을 디옥산 140ml에 현탁시켰다. 반응 혼합물을 가온하여 110 ℃에서 72시간 교반하였다. 반응 종결 후 상온으로 식히고 100ml의 증류수를 가하고 에틸아세테이트로 추출하였다. 추출된 유기층을 포화염화나트륨 수용액으로 세척하고 소듐설페이트로 건조하였다. 용매를 제거한 잔여물을 컬럼 크로마토그래피를 이용하여 분리하여 1.77g (2.4 mmol) 목적 화합물을 수득하였다.Intermediate [A-5] 6.2g (9mmol), Dichloro(1,5-cyclooctadiene)platinum 3.7g (9.9mmol), and sodium acetate 4.4g (54mmol) were suspended in 140ml dioxane. The reaction mixture was warmed and stirred at 110 °C for 72 hours. After completion of the reaction, it was cooled to room temperature, 100 ml of distilled water was added, and the mixture was extracted with ethyl acetate. The extracted organic layer was washed with a saturated aqueous sodium chloride solution and dried over sodium sulfate. The solvent was removed and the residue was separated using column chromatography to obtain 1.77 g (2.4 mmol) of the target compound.
(2) 유기 금속 화합물 29의 합성(2) Synthesis of organometallic compound 29
일 실시예에 따른 화합물 29는 예를 들어 하기 반응식 2의 단계에 의해 합성될 수 있다.Compound 29 according to an embodiment may be synthesized, for example, by the steps of Scheme 2 below.
[반응식 2][Scheme 2]
(중간체 A-6의 합성)(Synthesis of Intermediate A-6)
2-브로모-4-(메틸-d3)피리딘 대신 2-브로모-4-(t-뷰틸)피리딘을 사용하는 것을 제외하고는 상기 합성예 18의 중간체 A-2와 동일한 방법을 이용하여 목적 화합물을 수득하였다. Using the same method as Intermediate A-2 of Synthesis Example 18, except for using 2-bromo-4-(t-butyl)pyridine instead of 2-bromo-4-(methyl-d3)pyridine, The compound was obtained.
(중간체 A-7의 합성) (Synthesis of Intermediate A-7)
중간체 [A-2] 대신, 중간체 [A-6]을 사용하고, 1-(3-브로모-5-t-뷰틸)페닐) 1H-벤조[d]이미다졸 대신 1,3-디브로모-5-(t-뷰틸)벤젠을 사용하는 것을 제외하고는 상기 합성예 18의 중간체 A-3와 동일한 방법을 이용하여 목적 화합물을 수득하였다. Use intermediate [A-6] instead of intermediate [A-2] and 1,3-dibromo instead of 1-(3-bromo-5-t-butyl)phenyl) 1H-benzo[d]imidazole The target compound was obtained in the same manner as in Intermediate A-3 of Synthesis Example 18, except that -5-(t-butyl)benzene was used.
(중간체 A-8의 합성)(Synthesis of Intermediate A-8)
중간체 [A-7] 5.28g (10mmol)과 N-{[1,1`:3,1"-터페닐]-2`-닐-d13}벤젠-1,2-디아민 3.84 g (11mmol), SPhos (0.75mmol), Pd2(dba)3 (0.5mmol), 소듐 t-부톡시드 (20mmol)을 톨루엔 용매 100ml로 현탁하고 100 ℃로 승온하여 5시간동안 교반하였다. 반응 종결 후 감압하여 용매를 제거하고, 염화메틸렌과 증류수로 추출하였다. 추출된 유기층을 포화염화나트륨 수용액으로 세척하고 소듐설페이트로 건조하였다. 용매를 제거한 잔여물을 컬럼 크로마토그래피를 이용하여 분리하여 6.06g (7.6 mmol) 목적 화합물을 수득하였다.Intermediate [A-7] 5.28g (10mmol) and N-{[1,1`:3,1"-terphenyl]-2`-yl-d13}benzene-1,2-diamine 3.84 g (11mmol), SPhos (0.75 mmol), Pd 2 (dba) 3 (0.5 mmol), and sodium t-butoxide (20 mmol) were suspended in 100 ml of a toluene solvent, heated to 100 ° C., and stirred for 5 hours. After completion of the reaction, the solvent was reduced under reduced pressure. Removed, extracted with methylene chloride and distilled water.The extracted organic layer was washed with saturated aqueous sodium chloride solution and dried over sodium sulfate.The residue after removing the solvent was separated by column chromatography to obtain 6.06g (7.6 mmol) of the target compound. obtained.
(중간체 A-9의 합성)(Synthesis of Intermediate A-9)
중간체 [A-8] 6.06g (7.6 mmol) 1 mmol을 트리에틸오쏘포메이트 380 mmol 에 녹인 후, HCl 9.12mmol을 적가한다. 100 ℃로 승온하여 20시간동안 교반하였다. 반응 종결 후 감압하여 용매를 제거하고, 염화메틸렌과 증류수로 추출하였다. 추출된 유기층을 포화염화나트륨 수용액으로 세척하고 소듐설페이트로 건조하였다. 용매를 제거한 잔여물을 컬럼 크로마토그래피를 이용하여 분리하여 4.98g (5.9 mmol) 목적 화합물을 수득하였다.After dissolving 6.06 g (7.6 mmol) of Intermediate [A-8] 1 mmol in 380 mmol of triethyl orthoformate, 9.12 mmol of HCl is added dropwise. The temperature was raised to 100 °C and stirred for 20 hours. After completion of the reaction, the solvent was removed under reduced pressure, and the mixture was extracted with methylene chloride and distilled water. The extracted organic layer was washed with a saturated aqueous sodium chloride solution and dried over sodium sulfate. The residue after removing the solvent was separated using column chromatography to obtain 4.98 g (5.9 mmol) of the target compound.
(중간체 A-10의 합성)(Synthesis of Intermediate A-10)
중간체 [A-4] 대신 중간체 [A-9]를 사용하는 것을 제외하고는 상기 합성예 18의 중간체 [A-5]와 동일한 방법을 이용하여 목적 화합물을 수득하였다. The target compound was obtained in the same manner as in Intermediate [A-5] of Synthesis Example 18, except that Intermediate [A-9] was used instead of Intermediate [A-4].
(화합물 29의 합성)(Synthesis of compound 29)
중간체 [A-5] 대신 중간체 [A-10]를 사용하는 것을 제외하고는 상기 합성예 18과 동일한 방법을 이용하여 목적 화합물을 수득하였다. The target compound was obtained in the same manner as in Synthesis Example 18, except that Intermediate [A-10] was used instead of Intermediate [A-5].
(3) 유기 금속 화합물 50의 합성(3) Synthesis of organometallic compound 50
일 실시예에 따른 유기 금속 화합물 50은 예를 들어 하기 반응식 3의 단계에 의해 합성될 수 있다.The organometallic compound 50 according to an embodiment may be synthesized, for example, by the steps of Scheme 3 below.
[반응식 3][Scheme 3]
(중간체 A-11의 합성)(Synthesis of Intermediate A-11)
7-메톡시-9H-피리도[3,4-b]인돌 대신 7-메톡시-1,3-디메틸-9H-피리도[3,4-b]인돌 을 사용하는 것을 제외하고는 상기 합성예 29의 중간체 [A-6]과 동일한 방법을 이용하여 목적 화합물을 수득하였다. The above synthesis except that 7-methoxy-1,3-dimethyl-9H-pyrido[3,4-b]indole is used instead of 7-methoxy-9H-pyrido[3,4-b]indole. The target compound was obtained in the same manner as in Intermediate [A-6] of Example 29.
(중간체 A-12의 합성) (Synthesis of Intermediate A-12)
중간체 [A-6] 대신 중간체 [A-11]을 사용하고, 1,3-디브로모-5-(t-뷰틸)벤젠 대신 중간체 [B-1]을 사용하는 것을 제외하고는 상기 합성예 29의 중간체 [A-7]과 동일한 방법을 이용하여 목적 화합물을 수득하였다. The above synthesis example except that the intermediate [A-11] is used instead of the intermediate [A-6] and the intermediate [B-1] is used instead of the 1,3-dibromo-5-(t-butyl)benzene The target compound was obtained by using the same method as Intermediate [A-7] of 29.
(중간체 A-13의 합성)(Synthesis of Intermediate A-13)
중간체 [A-7] 대신 중간체 [A-12]을 사용하고, N-{[1,1`:3,1''-터페닐]-2`-닐-d13}벤젠-1,2-디아민 대신 중간체 [B-2]을 사용하는 것을 제외하고는 상기 합성예 29의 중간체 A-8과 동일한 방법을 이용하여 목적 화합물을 수득하였다. Use intermediate [A-12] instead of intermediate [A-7], N-{[1,1`:3,1''-terphenyl]-2`-yl-d13}benzene-1,2-diamine Instead, the target compound was obtained in the same manner as in Intermediate A-8 of Synthesis Example 29, except that Intermediate [B-2] was used.
(중간체 A-14의 합성)(Synthesis of Intermediate A-14)
중간체 [A-8] 대신 중간체 [A-13]을 사용하는 것을 제외하고는 상기 합성예 29의 중간체 [A-9]와 동일한 방법을 이용하여 목적 화합물을 수득하였다. The target compound was obtained in the same manner as in Intermediate [A-9] of Synthesis Example 29, except that Intermediate [A-13] was used instead of Intermediate [A-8].
(중간체 A-15의 합성)(Synthesis of Intermediate A-15)
중간체 [A-9] 대신 중간체 [A-14]를 사용하는 것을 제외하고는 상기 합성예 29의 중간체 [A-10]와 동일한 방법을 이용하여 목적 화합물을 수득하였다. The target compound was obtained in the same manner as in Intermediate [A-10] of Synthesis Example 29, except that Intermediate [A-14] was used instead of Intermediate [A-9].
(화합물 50의 합성)(Synthesis of compound 50)
중간체 [A-10] 대신 중간체 [A-15]를 사용하는 것을 제외하고는 상기 합성예 29와 동일한 방법을 이용하여 목적 화합물인 유기 금속 화합물 50을 수득하였다. An organometallic compound 50 as a target compound was obtained in the same manner as in Synthesis Example 29, except that Intermediate [A-15] was used instead of Intermediate [A-10].
(4) 유기 금속 화합물 79의 합성(4) Synthesis of organometallic compound 79
7-메톡시-9H-피리도[3,4-b]인돌 대신 7-메톡시-5H-피리도[3,4-b]인돌을 사용하고, N-{[1,1`:3,1''-터페닐]-2`-닐-d13}벤젠-1,2-디아민 대신 N1-{4`-(메틸-d3)-[1,1`[디페닐]-2-닐-2`,3`,5`,6`-d4)벤젠-1,2-디아민을 사용한 것을 제외하고는 상기 화합물 29의 합성과 동일한 방법을 이용하여 목적 화합물인 유기 금속 화합물 79를 수득하였다. Using 7-methoxy-5H-pyrido[3,4-b]indole instead of 7-methoxy-9H-pyrido[3,4-b]indole, N-{[1,1`:3, 1''-terphenyl]-2`-nyl-d 13 } benzene-1,2-diamine instead of N 1 -{4`-(methyl-d 3 )-[1,1`[diphenyl]-2- nyl-2`,3`,5`,6`-d 4 ) The target compound, organometallic compound 79, was obtained in the same manner as in the synthesis of compound 29, except that benzene-1,2-diamine was used. did.
(5) 유기 금속 화합물 119의 합성(5) Synthesis of organometallic compound 119
7-메톡시-9H-피리도[3,4-b]인돌 대신 3-메톡시-5H-피리도[4,3-b]인돌-6,7,8,9-d4 를 사용하고, N-{[1,1`:3,1''-터페닐]-2`-닐-d13}벤젠-1,2-디아민 대신 N1-(2,6-디-t-뷰틸페닐)벤젠-d3-1,2-디아민을 사용한 것을 제외하고는 상기 화합물 29의 합성과 동일한 방법을 이용하여 목적 화합물인 유기 금속 화합물 119를 수득하였다. Using 3-methoxy-5H-pyrido [4,3-b] indole-6,7,8,9-d 4 instead of 7-methoxy-9H-pyrido [3,4-b] indole, N-{[1,1`:3,1''-terphenyl]-2`-yl-d 13 } benzene-1,2-diamine instead of N 1 -(2,6-di-t-butylphenyl) A target compound, organometallic compound 119, was obtained in the same manner as in the synthesis of compound 29, except that benzene-d 3 -1,2-diamine was used.
(6) 유기 금속 화합물 129의 합성(6) Synthesis of organometallic compound 129
일 실시예에 따른 유기 금속 화합물 129는 예를 들어 하기 반응식 4의 단계에 의해 합성될 수 있다.The organometallic compound 129 according to an embodiment may be synthesized, for example, by the steps of Scheme 4 below.
[반응식 4][Scheme 4]
(중간체 C-1의 합성)(Synthesis of Intermediate C-1)
7-브로모-9H-피리도[3,4-b]인돌 12.35g (50mmol)과 2-브로모-4-(t-뷰틸)피리딘을 16.06g (75mmol), 삼인삼칼륨 23g (100 mmol), CuI 1.83g (10mmol), 피콜린산 1.17g (10mmol)을 반응 용기에 넣고 디메틸술폭시드 150mL 에 현탁시켰다. 반응 혼합물을 가온하여 160℃에서 24시간 교반하였다. 반응 종결 후 상온으로 식히고 300mL 증류수를 가하고 에틸아세테이트로 추출하였다. 추출된 유기층을 포화염화나트륨 수용액으로 세척하고 소듐설페이트로 건조하였다. 용매를 제거한 잔여물을 컬럼 크로마토그래피를 이용하여 분리하여 14.45g (38 mmol) 목적 화합물을 수득하였다.7-bromo-9H-pyrido[3,4-b]indole 12.35g (50mmol) and 2-bromo-4-(t-butyl)pyridine 16.06g (75mmol), trigins potassium 23g (100mmol) ), CuI 1.83 g (10 mmol), and picolinic acid 1.17 g (10 mmol) were placed in a reaction vessel and suspended in 150 mL of dimethyl sulfoxide. The reaction mixture was warmed and stirred at 160° C. for 24 hours. After completion of the reaction, it was cooled to room temperature, 300 mL distilled water was added, and the mixture was extracted with ethyl acetate. The extracted organic layer was washed with a saturated aqueous sodium chloride solution and dried over sodium sulfate. The residue after removing the solvent was separated using column chromatography to obtain 14.45 g (38 mmol) of the target compound.
(중간체 C-2의 합성)(Synthesis of Intermediate C-2)
중간체 [C-1] 14.45 g (38 mmol)을 THF 500 mL에 녹인 후, -78℃에서 노르말 부틸리튬 41.8 mmol (2.5M in Hexane)을 천천히 첨가하였다. 한 시간 후 0℃에서 3-브로모벤즈알데히드 10.5 g (57 mmol)을 첨가하였다. 2시간 동안 교반한 후 암모늄 클로라이드를 첨가하고 디에틸에테르 (30 mL)로 3회 세척하였다. 세척된 디에틸에테르층을 소듐설페이트로 건조하였다. 용매를 제거한 잔여물을 컬럼 크로마토그래피를 이용하여 분리하여 10.7 g (22 mmol) 목적 화합물을 수득하였다.After dissolving 14.45 g (38 mmol) of the intermediate [C-1] in 500 mL of THF, 41.8 mmol (2.5M in Hexane) of n-butyllithium was slowly added at -78°C. After one hour at 0° C., 10.5 g (57 mmol) of 3-bromobenzaldehyde was added. After stirring for 2 hours, ammonium chloride was added and the mixture was washed 3 times with diethyl ether (30 mL). The washed diethyl ether layer was dried over sodium sulfate. The solvent was removed and the residue was separated using column chromatography to obtain 10.7 g (22 mmol) of the target compound.
(중간체 C-3의 합성)(Synthesis of Intermediate C-3)
중간체 [C-2] 10.7 g (22 mmol) 을 디메클로라이드에 녹인 후, DDQ 14.9 g (66 mmol) 을 첨가한 후, 실온에서 12시간 동안 교반한다. 반응 종결 후 컬럼 크로마토그래피를 이용하여 분리하여 8.72 g (18 mmol) 목적 화합물을 수득하였다.After 10.7 g (22 mmol) of the intermediate [C-2] was dissolved in dimechloride, 14.9 g (66 mmol) of DDQ was added, followed by stirring at room temperature for 12 hours. After completion of the reaction, it was separated using column chromatography to obtain 8.72 g (18 mmol) of the target compound.
(중간체 C-4의 합성)(Synthesis of Intermediate C-4)
중간체 [C-3] 8.72 g (18 mmol) 을 질소 조건하에서 디메클로라이드에 녹인 후, HF-피리딘 18 mL를 첨가한 후, 50℃ 에서 24시간 동안 교반한다. 반응 종결 후 용매를 제거한 잔여물에 디에틸에테르를 첨가한 후, 중탄산나트륨 용액으로 세척하였다. 세척된 디에틸에테르층을 소듐설페이트로 건조하였다. 용매를 제거한 잔여물을 헥산 하에서 교반한 후, 재결정을 통해 8.6 g (17 mmol) 목적 화합물을 수득하였다.After dissolving 8.72 g (18 mmol) of the intermediate [C-3] in dimechloride under nitrogen condition, 18 mL of HF-pyridine was added thereto, followed by stirring at 50° C. for 24 hours. After completion of the reaction, diethyl ether was added to the residue from which the solvent was removed, followed by washing with sodium bicarbonate solution. The washed diethyl ether layer was dried over sodium sulfate. After removing the solvent and stirring the residue under hexane, 8.6 g (17 mmol) of the target compound was obtained through recrystallization.
(중간체 C-5의 합성)(Synthesis of Intermediate C-5)
중간체 [A-7] 대신 중간체 [C-4]을 사용하고, N-{[1,1`:3,1”-터페닐]-2`-닐-d13}벤젠-1,2-디아민 대신 N1-(2,6-디-t-뷰틸페닐)벤젠-디4-1,2-디아민 을 사용하는 것을 제외하고는 상기 합성예 29의 중간체 A-8과 동일한 방법을 이용하여 목적화합물을 수득하였다.Use intermediate [C-4] instead of intermediate [A-7] and replace N-{[1,1`:3,1”-terphenyl]-2`-yl-d13}benzene-1,2-diamine N 1 -(2,6-di-t-butylphenyl)benzene-di4-1,2-diamine was prepared using the same method as Intermediate A-8 of Synthesis Example 29, except that the target compound was prepared obtained.
(중간체 C-6의 합성)(Synthesis of Intermediate C-6)
중간체 [A-8] 대신 중간체 [C-5]을 사용하는 것을 제외하고는 상기 합성예 29의 중간체 [A-9]와 동일한 방법을 이용하여 목적화합물을 수득하였다. A target compound was obtained in the same manner as in Intermediate [A-9] of Synthesis Example 29, except that Intermediate [C-5] was used instead of Intermediate [A-8].
(중간체 C-7의 합성)(Synthesis of Intermediate C-7)
중간체 [A-9] 대신 중간체 [C-6]를 사용하는 것을 제외하고는 상기 합성예 29의 중간체 [A-10]와 동일한 방법을 이용하여 목적화합물을 수득하였다. A target compound was obtained in the same manner as in Intermediate [A-10] of Synthesis Example 29, except that Intermediate [C-6] was used instead of Intermediate [A-9].
(화합물 129의 합성)(Synthesis of compound 129)
중간체 [A-10] 대신 중간체 [C-7]를 사용하는 것을 제외하고는 상기 합성예 29와 동일한 방법을 이용하여 목적화합물인 유기 금속 화합물 129를 수득하였다.An organometallic compound 129 as a target compound was obtained in the same manner as in Synthesis Example 29, except that Intermediate [C-7] was used instead of Intermediate [A-10].
(7) 유기 금속 화합물 146의 합성(7) Synthesis of organometallic compound 146
일 실시예에 따른 유기 금속 화합물 146은 예를 들어 하기 반응식 5의 단계에 의해 합성될 수 있다.The organometallic compound 146 according to an embodiment may be synthesized, for example, by the steps of Scheme 5 below.
[반응식 5][Scheme 5]
(중간체 C-8의 합성)(Synthesis of Intermediate C-8)
7-브로모-9H-피리도[3,4-b]인돌 대신 7-브로모-5H-피리도[4,3-b]인돌, 3-브로모벤즈알데히드 대신 3-브로모-5-(t-뷰틸)벤즈알데히드 를 사용하는 것을 제외하고는 상기 합성예 129의 중간체 [C-1]과 동일한 방법을 이용하여 목적화합물을 수득하였다. 7-bromo-5H-pyrido [4,3-b] indole instead of 7-bromo-9H-pyrido [3,4-b] indole, 3-bromo-5- ( The target compound was obtained in the same manner as in Intermediate [C-1] of Synthesis Example 129, except that t-butyl)benzaldehyde was used.
(중간체 C-9의 합성)(Synthesis of Intermediate C-9)
중간체 [C-1] 대신 중간체 [C-8]을 사용하는 것을 제외하고는 상기 합성예 129의 중간체 [C-2]과 동일한 방법을 이용하여 목적화합물을 수득하였다. A target compound was obtained in the same manner as in Intermediate [C-2] of Synthesis Example 129, except that Intermediate [C-8] was used instead of Intermediate [C-1].
(중간체 C-10의 합성)(Synthesis of Intermediate C-10)
중간체 [C-2] 대신 중간체 [C-9]을 사용하는 것을 제외하고는 상기 합성예 129의 중간체 [C-3]과 동일한 방법을 이용하여 목적화합물을 수득하였다. A target compound was obtained in the same manner as in Intermediate [C-3] of Synthesis Example 129, except that Intermediate [C-9] was used instead of Intermediate [C-2].
(중간체 C-11의 합성)(Synthesis of Intermediate C-11)
중간체 [C-3] 대신 중간체 [C-10]을 사용하는 것을 제외하고는 상기 합성예 129의 중간체 [C-4]과 동일한 방법을 이용하여 목적화합물을 수득하였다. A target compound was obtained in the same manner as in Intermediate [C-4] of Synthesis Example 129, except that Intermediate [C-10] was used instead of Intermediate [C-3].
(중간체 C-12의 합성)(Synthesis of Intermediate C-12)
중간체 [A-7] 대신 중간체 [C-11]을 사용하고, N-{[1,1`:3,1”-터페닐]-2`-닐-d13}벤젠-1,2-디아민 대신 N1-(페닐-디5)벤젠-1,2-디아민 을 사용하는 것을 제외하고는 상기 합성예 29의 중간체 [A-8]과 동일한 방법을 이용하여 목적화합물을 수득하였다.Use intermediate [C-11] instead of intermediate [A-7] and replace N-{[1,1`:3,1”-terphenyl]-2`-yl-d13}benzene-1,2-diamine A target compound was obtained in the same manner as in Intermediate [A-8] of Synthesis Example 29, except that N 1 -(phenyl-di5)benzene-1,2-diamine was used.
(중간체 C-13의 합성)(Synthesis of Intermediate C-13)
중간체 [A-8] 대신 중간체 [C-12]을 사용하는 것을 제외하고는 상기 합성예 29의 중간체 [A-9]와 동일한 방법을 이용하여 목적화합물을 수득하였다. A target compound was obtained in the same manner as in Intermediate [A-9] of Synthesis Example 29, except that Intermediate [C-12] was used instead of Intermediate [A-8].
(중간체 C-14의 합성)(Synthesis of Intermediate C-14)
중간체 [A-9] 대신 중간체 [C-13]를 사용하는 것을 제외하고는 상기 합성예 29의 중간체 [A-10]와 동일한 방법을 이용하여 목적화합물을 수득하였다. A target compound was obtained in the same manner as in Intermediate [A-10] of Synthesis Example 29, except that Intermediate [C-13] was used instead of Intermediate [A-9].
(화합물 146의 합성)(Synthesis of compound 146)
중간체 [A-10] 대신 중간체 [C-14]를 사용하는 것을 제외하고는 상기 합성예 29와 동일한 방법을 이용하여 목적화합물인 유기 금속 화합물 146을 수득하였다.An organometallic compound 146, a target compound, was obtained in the same manner as in Synthesis Example 29, except that Intermediate [C-14] was used instead of Intermediate [A-10].
(8) 유기 금속 화합물 155의 합성(8) Synthesis of organometallic compound 155
N1-(페닐-디5)벤젠-1,2-디아민 대신 N1-([1,1':3',1''-터페닐]-2'-닐-2,2'',3,3'',4,4'',5,5'',6,6''-d10)벤젠-1,2-디아민 을 사용하는 것을 제외하고는 상기 합성예 146와 동일한 방법을 이용하여 목적화합물인 유기 금속 화합물 155를 수득하였다.N 1 - (phenyl-di-5), benzene-1,2-diamine instead of N 1 - ([1,1 ': 3', 1 '' - terphenyl] -2' carbonyl-2,2 '', 3 , 3'', 4,4'', 5,5'', 6,6''-d10) Using the same method as in Synthesis Example 146, except for using benzene-1,2-diamine The compound organometallic compound 155 was obtained.
(9) 유기 금속 화합물 167의 합성(9) Synthesis of organometallic compound 167
7-브로모-5H-피리도[4,3-b]인돌 대신 7-브로모-5H-피리도[3,2-b]인돌 을 사용하는 것을 제외하고는 상기 합성예 155와 동일한 방법을 이용하여 목적화합물인 유기 금속 화합물 167을 수득하였다.The same method as in Synthesis Example 155 was followed except that 7-bromo-5H-pyrido [3,2-b] indole was used instead of 7-bromo-5H-pyrido [4,3-b] indole. The target compound, organometallic compound 167, was obtained.
(10) 유기 금속 화합물 191의 합성(10) Synthesis of organometallic compound 191
7-브로모-5H-피리도[4,3-b]인돌 대신 3-브로모-5H-피리도[4,3-b]인돌 을 사용하는 것을 제외하고는 상기 합성예 155와 동일한 방법을 이용하여 목적화합물인 유기 금속 화합물 191을 수득하였다.The same method as in Synthesis Example 155 was followed except that 3-bromo-5H-pyrido[4,3-b]indole was used instead of 7-bromo-5H-pyrido[4,3-b]indole. The target compound, organometallic compound 191, was obtained.
상기 합성예에서 합성된 화합물들의 1H NMR 및 MS/FAB을 하기 표 1에 나타내었다. 표 1에 나타낸 화합물 이외의 다른 화합물들도 위의 합성 경로 및 원료 물질을 참조하여 기술 분야에 숙련된 이들이 그 합성 방법을 용이하게 인식할 수 있다. 1 H NMR and MS/FAB of the compounds synthesized in the above synthesis example are shown in Table 1 below. Compounds other than those shown in Table 1 can also be easily recognized by those skilled in the art by referring to the above synthetic routes and raw materials.
2. 유기 금속 화합물의 특성 평가2. Characterization of organometallic compounds
실시예 화합물 18, 29, 50, 79, 119, 129, 146, 155, 167, 191, 및 비교예 화합물 C1 내지 C3의 유기 금속 화합물의 발광 특성을 평가하여 하기 표 2에 나타내었다.Example compounds 18, 29, 50, 79, 119, 129, 146, 155, 167, 191, and Comparative Example compounds C1 to C3 to evaluate the emission characteristics of the organometallic compounds of the compounds are shown in Table 2 below.
실시예 화합물들과 비교예 화합물들은 아래와 같다.Example compounds and comparative example compounds are as follows.
[실시예 화합물][Example compound]
[비교예 화합물][Comparative Example Compound]
표 2는 각각의 화합물에 대한 최저 삼중항 여기 에너지 준위(T1 level), 3MLCT(Metal to Ligand Charge Transfer) 및 3MC (3 Metal Centered state) 에너지를 B3LYP DFT 계산 방법에 따라 양자 시뮬레이션하여 그 결과를 나타낸 것이다.Table 2 shows the quantum simulation results of the lowest triplet excitation energy level (T1 level), 3 MLCT (Metal to Ligand Charge Transfer) and 3 MC (3 Metal Centered state) energy for each compound according to the B3LYP DFT calculation method. is shown.
표 2의 결과를 참조하면, 실시예 화합물인 유기 금속 화합물 18, 29, 50, 79, 119, 129, 146, 155, 167, 및 191은 비교예 화합물 C1 내지 C3과 비교하여 증가된 3MLCT(Metal to Ligand Charge Transfer) 값을 나타내고, 실시예의 유기 금속 화합물들은 비교예 화합물 C1 내지 C3과 비교하여 유사한 수준 또는 증가된 3MC (3 Metal Centered state) 값을 나타내는 것을 알 수 있다. 이에 따라, 실시예의 유기 금속 화합물들을 발광 소자에 적용하였을 때 비교예 화합물들을 적용한 경우에 비하여 개선된 소자 수명과 발광 효율 특성을 나타낼 것을 기대할 수 있다.Referring to the results of Table 2, the example compounds, organometallic compounds 18, 29, 50, 79, 119, 129, 146, 155, 167, and 191 were 3 MLCT ( Metal to Ligand Charge Transfer) values, and it can be seen that the organometallic compounds of Examples exhibit a similar level or an increased 3 MC (3 Metal Centered state) value compared to Comparative Examples C1 to C3. Accordingly, when the organometallic compounds of the example are applied to the light emitting device, it can be expected that the device lifespan and the light emitting efficiency characteristics are improved compared to the case where the compounds of the comparative example are applied.
또한, 실시예 화합물인 유기 금속 화합물 18, 29, 50, 79, 119, 129, 146, 155, 167 및 191은 비교예 화합물 C1 내지 C3과 비교하여 단파장을 갖는 것을 알 수 있다. 비교예 화합물 C1은 카볼린기의 X1만 질소 원자인 것으로, 즉 카볼린기의 α(alpha) 위치에만 질소 원자가 포함되어 실시예의 화합물들보다 긴 파장 값을 나타내는 것으로 판단된다. 비교예 화합물 C3은 카볼린기를 포함하지 않아, 실시예 화합물들 및 비교예 화합물 C1에 비해 긴 파장 값을 나타내는 것으로 판단된다.In addition, it can be seen that the organometallic compounds 18, 29, 50, 79, 119, 129, 146, 155, 167 and 191, which are the example compounds, have shorter wavelengths than those of the comparative example compounds C1 to C3. In Comparative Example Compound C1, only X 1 of the carboline group is a nitrogen atom, that is, it is determined that a nitrogen atom is included only in the α (alpha) position of the carboline group to exhibit a longer wavelength value than the compounds of Examples. Comparative Example Compound C3 does not include a carboline group, and thus it is determined that it exhibits a longer wavelength value than the Example compounds and Comparative Example Compound C1.
한편, 비교예 화합물 C1과 비교하여, 실시예 화합물 29 및 화합물 119는 중수소 원자 치환기를 복수로 포함하여 높은 3MC (3 Metal Centered state) 값을 나타내는 것으로 판단된다.On the other hand, as compared to Comparative Example Compound C1, Example Compound 29 and Compound 119 include a plurality of deuterium atom substituents, it is determined to exhibit a high 3 MC (3 Metal Centered state) value.
3. 유기 전계 발광 소자의 제작 및 평가3. Fabrication and evaluation of organic electroluminescent devices
(유기 전계 발광 소자의 제작)(Production of organic electroluminescent device)
일 실시예의 유기 금속 화합물을 발광층에 포함하는 일 실시예의 유기 전계 발광 소자를 아래의 방법으로 제조하였다. 상술한 화합물 18, 29, 50, 79, 119, 129, 146, 155, 167 및 191을 발광층의 도펀트 재료로 사용하여 실시예 1 내지 실시예 10의 유기 전계 발광 소자를 제작하였다. 비교예 1 및 비교예 2는 상술한 비교예 화합물 C1 및 C3을 발광층 도펀트 재료로 사용하여 유기 전계 발광 소자를 제작하였다.The organic electroluminescent device of one embodiment including the organometallic compound of one embodiment in the light emitting layer was prepared by the following method. The organic electroluminescent devices of Examples 1 to 10 were prepared by using the compounds 18, 29, 50, 79, 119, 129, 146, 155, 167 and 191 as described above as dopant materials for the emission layer. In Comparative Examples 1 and 2, organic electroluminescent devices were manufactured by using the above-described Comparative Examples Compounds C1 and C3 as dopant materials for the emission layer.
기판 및 애노드로서 코닝(corning)사의 15Ω/cm2 (1200Å) ITO가 형성된 유리 기판을 50mm x 50mm x 0.7mm 크기로 잘라서 이소프로필 알코올과 순수를 이용하여 각 5분 동안 초음파 세정한 후, 30분 동안 자외선을 조사하고 오존에 노출시켜 세정하고 진공증착장치에 상기 유리 기판을 설치하였다. As a substrate and an anode, Corning's 15Ω/cm 2 (1200Å) ITO-formed glass substrate was cut into 50mm x 50mm x 0.7mm and ultrasonically cleaned using isopropyl alcohol and pure water for 5 minutes each, 30 minutes During the period, ultraviolet rays were irradiated and cleaned by exposure to ozone, and the glass substrate was installed in a vacuum deposition apparatus.
상기 유기 기판에 형성된 ITO 애노드 상부에 2-TNATA를 진공 증착하여 600Å 두께의 정공 주입층을 형성하고, 상기 정공 주입층 상부에 NPB를 진공 증착하여 300Å 두께의 정공 수송층을 형성하였다.2-TNATA was vacuum deposited on the ITO anode formed on the organic substrate to form a hole injection layer having a thickness of 600 Å, and NPB was vacuum deposited on the hole injection layer to form a hole transport layer having a thickness of 300 Å.
상기 정공 수송층 상부에 코-호스트인 BCPDS 및 POPCPA (BCPDS와 POPCPA의 중량비는 1:1)와 도펀트인 실시예 화합물들 또는 비교예 화합물들을 코-호스트와 도펀트의 중량비가 90 : 10이 되도록 공증착하여 300Å 두께의 발광층을 형성하였다. On the hole transport layer, co-host BCPDS and POPCPA (weight ratio of BCPDS and POPCPA) and dopant Example compounds or comparative example compounds were co-deposited so that the weight ratio of co-host and dopant was 90: 10 to form a light emitting layer with a thickness of 300 Å.
상기 발광층 상부에 TSPO1을 증착하여 50Å 두께의 정공 저지층을 형성하고, 상기 정공 저지층 상부에 Alq3를 증착하여 300Å 두께의 전자 수송층을 형성한 다음, 상기 전자 수송층 상부에 LiF를 증착하여 10Å 두께의 전자 주입층을 형성한 후, 상기 전자 주입층 상부에 Al를 진공 증착하여 3000Å 두께의 캐소드를 형성하여, 유기 전계 발광 소자를 제작하였다. TSPO1 was deposited on the light emitting layer to form a hole blocking layer with a thickness of 50 Å, Alq 3 was deposited on the hole blocking layer to form an electron transport layer with a thickness of 300 Å, and then LiF was deposited on the electron transport layer to a thickness of 10 Å After forming the electron injection layer of, Al was vacuum-deposited on the electron injection layer to form a cathode with a thickness of 3000 Å, thereby manufacturing an organic electroluminescent device.
(mA/cm2)current density
(mA/cm 2 )
(cd/m2)luminance
(cd/m 2 )
(cd/A)Luminous Efficiency
(cd/A)
표 3에서는 실시예 1 내지 실시예 10, 비교예 1 및 비교예 2에 대한 유기 전계 발광 소자의 평가 결과를 나타내었다. 표 3에서는 제작된 유기 전계 발광 소자에서의 구동전압, 휘도, 발광 효율, 발광 파장 및 수명을 비교하여 나타내었다. 발광 효율은 전류 밀도 50mA/cm2에 대한 전류 효율 값을 나타낸 것이다. Table 3 shows the evaluation results of the organic electroluminescent devices for Examples 1 to 10, Comparative Example 1 and Comparative Example 2. Table 3 compares the driving voltage, luminance, luminous efficiency, emission wavelength, and lifetime of the manufactured organic electroluminescent device. The luminous efficiency represents a current efficiency value for a current density of 50 mA/cm 2 .
표 3의 결과를 참조하면, 실시예 1 내지 실시예 10의 유기 전계 발광 소자는 비교예 1 및 비교예 2의 유기 전계 발광 소자와 비교하여 우수한 휘도 및 발광 효율을 나타내는 것을 알 수 있다. 또한, 실시예 1 내지 실시예 10의 유기 전계 발광 소자는 비교예 1 및 비교예 2의 유기 전계 발광 소자에 비하여 구동 전압이 낮아지고, 수명이 증가한 것을 확인할 수 있다. Referring to the results in Table 3, it can be seen that the organic electroluminescent devices of Examples 1 to 10 exhibit excellent luminance and luminous efficiency as compared to the organic electroluminescent devices of Comparative Examples 1 and 2. In addition, it can be seen that the organic electroluminescent devices of Examples 1 to 10 have a lower driving voltage and an increased lifespan compared to the organic electroluminescent devices of Comparative Examples 1 and 2 .
비교예 화합물 C1은 카볼린기의 X1만 질소 원자인 것으로, 즉 카볼린기의 α(alpha) 위치에만 질소 원자가 포함되어 실시예의 화합물들보다 낮은 발광 효율을 나타내는 것으로 판단된다.In Comparative Example Compound C1, only X 1 of the carboline group is a nitrogen atom, that is, it is determined that a nitrogen atom is included only in the α (alpha) position of the carboline group, thereby exhibiting lower luminous efficiency than the compounds of Examples.
일 실시예의 유기 금속 화합물은 카볼린기 및 중수소 원자를 포함하여 향상된 MLCT 비율을 나타내고, 이에 따라 개선된 발광 효율을 나타낼 수 있다. 또한, 일 실시예의 유기 전계 발광 소자는 발광층에 카볼린기 및 중수소 원자를 포함하는 유기 금속 화합물을 포함하여 우수한 발광 효율 및 개선된 수명 특성을 나타낼 수 있다.The organometallic compound of an exemplary embodiment may include a carboline group and a deuterium atom to exhibit an improved MLCT ratio, and thus may exhibit improved luminous efficiency. In addition, the organic electroluminescent device of an embodiment may include an organometallic compound including a carboline group and a deuterium atom in the light emitting layer to exhibit excellent luminous efficiency and improved lifespan characteristics.
이상에서는 본 발명의 바람직한 실시예를 참조하여 설명하였지만, 해당 기술 분야의 숙련된 당업자 또는 해당 기술 분야에 통상의 지식을 갖는 자라면, 후술될 특허청구범위에 기재된 본 발명의 사상 및 기술 영역으로부터 벗어나지 않는 범위 내에서 본 발명을 다양하게 수정 및 변경시킬 수 있음을 이해할 수 있을 것이다.Although the above has been described with reference to the preferred embodiment of the present invention, those skilled in the art or those having ordinary knowledge in the technical field will not depart from the spirit and technical scope of the present invention described in the claims to be described later. It will be understood that various modifications and variations of the present invention can be made without departing from the scope of the present invention.
따라서, 본 발명의 기술적 범위는 명세서의 상세한 설명에 기재된 내용으로 한정되는 것이 아니라 특허청구범위에 의해 정하여져야만 할 것이다.Accordingly, the technical scope of the present invention should not be limited to the contents described in the detailed description of the specification, but should be defined by the claims.
10 : 유기 전계 발광 소자 EL1 : 제1 전극
EL2 : 제2 전극 HTR : 정공 수송 영역
EML : 발광층 ETR : 전자 수송 영역10: organic electroluminescent element EL1: first electrode
EL2: second electrode HTR: hole transport region
EML: light emitting layer ETR: electron transport region
Claims (20)
상기 제1 전극 상에 배치된 제2 전극; 및
상기 제1 전극과 상기 제2 전극 사이에 배치된 발광층; 을 포함하고,
상기 발광층은 하기 화학식 1로 표시되는 유기 금속 화합물을 포함하는 유기 전계 발광 소자:
[화학식 1]
상기 화학식 1에서,
M은 전이 금속이고,
X1 내지 X6 중 선택되는 하나 또는 둘이 N이고, 나머지는 CR4이고,
X1이 N인 경우, X2 내지 X6 중 어느 하나는 N이고,
R4는 수소 원자, 중수소 원자, 또는 치환 또는 비치환된 탄소 수 1 이상 10 이하의 알킬기이고,
A1 내지 A3은 각각 독립적으로 치환 또는 비치환된 고리형성 탄소수 5 이상 60 이하의 탄화수소 고리, 또는 치환 또는 비치환된 고리형성 탄소수 1 이상 60 이하의 헤테로 고리이고,
b1 내지 b3은 각각 독립적으로 1 이상 4 이하의 정수이고,
R1 내지 R3은 각각 독립적으로 수소 원자, 중수소 원자, 할로겐 원자, 히드록시기, 시아노기, 니트로기, 치환 또는 비치환된 실릴기, 치환 또는 비치환된 아민기, 치환 또는 비치환된 옥시기, 치환 또는 비치환된 탄소수 1 이상 60 이하의 알킬기, 치환 또는 비치환된 탄소수 2 이상 60 이하의 알케닐기, 치환 또는 비치환된 탄소수 2 이상 60 이하의 알키닐기, 치환 또는 비치환된 고리형성 탄소수 6 이상 60 이하의 아릴기, 또는 치환 또는 비치환된 고리형성 탄소수 1 이상 10 이하의 헤테로 고리기이고,
R1 내지 R3 중 적어도 하나는 중수소 원자 또는 CD3이거나, 또는 R1 내지 R3 중 적어도 하나는 중수소 원자 또는 CD3으로 치환된 것이고,
L은 직접 결합, O, S, ―CR11R12―, ―CR13=CR14―, ―C≡C―, ―C(=O)―, ―C(=S)―, ―BR15―, ―NR16―, ―PR17R18―, 또는 ―GeR19R20― 이고,
R11 내지 R20은 각각 독립적으로 수소 원자, 중수소 원자, 할로겐 원자, 치환 또는 비치환된 탄소수 1 이상 30 이하의 알킬기, 또는 치환 또는 비치환된 고리 형성 탄소수 6 이상 30 이하의 아릴기이다.a first electrode;
a second electrode disposed on the first electrode; and
a light emitting layer disposed between the first electrode and the second electrode; including,
The light emitting layer is an organic electroluminescent device comprising an organometallic compound represented by the following Chemical Formula 1:
[Formula 1]
In Formula 1,
M is a transition metal,
One or two selected from X 1 to X 6 is N, the rest is CR 4 ,
When X 1 is N, any one of X 2 to X 6 is N,
R 4 is a hydrogen atom, a deuterium atom, or a substituted or unsubstituted alkyl group having 1 to 10 carbon atoms,
A 1 to A 3 are each independently a substituted or unsubstituted hydrocarbon ring having 5 to 60 carbon atoms, or a substituted or unsubstituted heterocyclic ring having 1 to 60 carbon atoms,
b1 to b3 are each independently an integer of 1 or more and 4 or less,
R 1 to R 3 are each independently a hydrogen atom, a deuterium atom, a halogen atom, a hydroxyl group, a cyano group, a nitro group, a substituted or unsubstituted silyl group, a substituted or unsubstituted amine group, a substituted or unsubstituted oxy group, A substituted or unsubstituted C1-C60 alkyl group, a substituted or unsubstituted C2-C60 alkenyl group, a substituted or unsubstituted C2-C60 alkynyl group, a substituted or unsubstituted C6-C6 An aryl group of 60 or less, or a substituted or unsubstituted heterocyclic group having 1 or more and 10 or less ring carbon atoms,
At least one of R 1 to R 3 is a deuterium atom or CD 3 , or at least one of R 1 to R 3 is substituted with a deuterium atom or CD 3 ,
L is a direct bond, O, S, —CR 11 R 12 —, —CR 13 =CR 14 —, —C≡C—, —C(=O)—, —C(=S)—, —BR 15 — , —NR 16 —, —PR 17 R 18 —, or —GeR 19 R 20 —,
R 11 to R 20 are each independently a hydrogen atom, a deuterium atom, a halogen atom, a substituted or unsubstituted alkyl group having 1 to 30 carbon atoms, or a substituted or unsubstituted aryl group having 6 to 30 ring carbon atoms.
상기 M은 Pt, Pd, Cu, 또는 Os인 유기 전계 발광 소자.The method of claim 1,
Wherein M is Pt, Pd, Cu, or Os organic electroluminescent device.
상기 발광층은 인광 발광하는 것인 유기 전계 발광 소자.The method of claim 1,
The light emitting layer is an organic electroluminescent device that emits phosphorescence.
상기 발광층은 호스트 및 도펀트를 포함하고,
상기 도펀트는 상기 화학식 1로 표시되는 유기 금속 화합물을 포함하는 유기 전계 발광 소자.The method of claim 1,
The light emitting layer includes a host and a dopant,
The dopant is an organic electroluminescent device comprising an organometallic compound represented by Formula 1.
상기 화학식 1은 하기 화학식 2-1 또는 화학식 2-2로 표시되는 유기 전계 발광 소자:
[화학식 2-1]
[화학식 2-2]
상기 화학식 2-1 및 화학식 2-2에서,
A1 내지 A3, X1 내지 X6, R1 내지 R3, 및 b1 내지 b3은 상기 화학식 1에서 정의한 바와 동일하다.The method of claim 1,
Formula 1 is an organic electroluminescent device represented by Formula 2-1 or Formula 2-2:
[Formula 2-1]
[Formula 2-2]
In Formulas 2-1 and 2-2,
A 1 to A 3 , X 1 to X 6 , R 1 to R 3 , and b 1 to b 3 are the same as defined in Formula 1 above.
상기 화학식 1은 하기 화학식 3으로 표시되는 유기 전계 발광 소자:
[화학식 3]
상기 화학식 3에서,
R50은 수소 원자, 중수소 원자, 할로겐 원자, 치환 또는 비치환된 탄소수 1 이상 30 이하의 알킬기, 또는 치환 또는 비치환된 탄소수 6 이상 30 이하의 아릴기이고,
M, L, X1 내지 X6, R1 내지 R3, 및 b1 내지 b3은 상기 화학식 1에서 정의한 바와 동일하다.The method of claim 1,
Formula 1 is an organic electroluminescent device represented by Formula 3 below:
[Formula 3]
In Formula 3,
R 50 is a hydrogen atom, a deuterium atom, a halogen atom, a substituted or unsubstituted alkyl group having 1 to 30 carbon atoms, or a substituted or unsubstituted aryl group having 6 to 30 carbon atoms,
M, L, X 1 to X 6 , R 1 to R 3 , and b 1 to b 3 are the same as defined in Formula 1 above.
상기 화학식 3은 하기 화학식 3-1로 표시되는 유기 전계 발광 소자:
[화학식 3-1]
상기 화학식 3-1에서,
X2 내지 X6 중 어느 하나는 N이고, 나머지는 CR4이고,
M, L, R1 내지 R4, R50 및 b1 내지 b3은 상기 화학식 3에서 정의한 바와 동일하다.7. The method of claim 6,
Formula 3 is an organic electroluminescent device represented by the following Formula 3-1:
[Formula 3-1]
In Formula 3-1,
Any one of X 2 to X 6 is N, the rest is CR 4 ,
M, L, R 1 to R 4 , R 50 and b 1 to b 3 are the same as defined in Formula 3 above.
상기 화학식 3은 하기 화학식 3-2 또는 화학식 3-3으로 표시되는 유기 전계 발광 소자:
[화학식 3-2]
[화학식 3-3]
상기 화학식 3-2에서,
X2 내지 X4 중 어느 하나는 N이고, 나머지는 CR4이고,
R5는 수소 원자, 중수소 원자, 또는 치환 또는 비치환된 탄소 수 1 이상 10 이하의 알킬기이고,
상기 화학식 3-3에서,
X5 및 X6 중 어느 하나는 N이고, 나머지는 CR6이고,
b4는 1 이상 4 이하의 정수이고,
R6은 수소 원자, 중수소 원자, 또는 치환 또는 비치환된 탄소 수 1 이상 10 이하의 알킬기이고,
M, L, R1 내지 R4, b1 내지 b3, 및 R50은 상기 화학식 3에서 정의한 바와 동일하다.7. The method of claim 6,
Formula 3 is an organic electroluminescent device represented by Formula 3-2 or Formula 3-3:
[Formula 3-2]
[Formula 3-3]
In Formula 3-2,
Any one of X 2 to X 4 is N, the rest is CR 4 ,
R 5 is a hydrogen atom, a deuterium atom, or a substituted or unsubstituted alkyl group having 1 to 10 carbon atoms,
In Formula 3-3,
Any one of X 5 and X 6 is N, the other is CR 6 ,
b4 is an integer of 1 or more and 4 or less,
R 6 is a hydrogen atom, a deuterium atom, or a substituted or unsubstituted alkyl group having 1 to 10 carbon atoms,
M, L, R 1 to R 4 , b 1 to b 3 , and R 50 are the same as defined in Formula 3 above.
상기 R50은 하기 화합물군 R의 화합물들 중 어느 하나로 표시되는 유기 전계 발광 소자:
[화합물군 R]
.7. The method of claim 6
Wherein R 50 is an organic electroluminescent device represented by any one of the compounds of the following compound group R:
[Compound group R]
.
상기 R50이 화합물 R-7 또는 R-8인 경우, R1은 적어도 하나의 중수소 원자를 포함하는 유기 전계 발광 소자.10. The method of claim 9,
When R 50 is a compound R-7 or R-8, R 1 is an organic electroluminescent device comprising at least one deuterium atom.
상기 발광층은 하기 화합물군 1에 표시된 화합물들 중 적어도 하나를 포함하는 유기 전계 발광 소자:
[화합물군 1]
.The method of claim 1,
The light emitting layer is an organic electroluminescent device comprising at least one of the compounds shown in the following compound group 1:
[Compound group 1]
.
[화학식 1]
상기 화학식 1에서,
M은 전이 금속이고,
X1 내지 X6 중 선택되는 하나 또는 둘이 N이고, 나머지는 CR4이고,
X1이 N인 경우, X2 내지 X6 중 어느 하나는 N이고,
R4는 수소 원자, 중수소 원자, 또는 치환 또는 비치환된 탄소 수 1 이상 10 이하의 알킬기이고,
A1 내지 A3은 각각 독립적으로 치환 또는 비치환된 고리형성 탄소수 5 이상 60 이하의 탄화수소 고리, 또는 치환 또는 비치환된 고리형성 탄소수 1 이상 60 이하의 헤테로 고리이고,
b1 내지 b3은 각각 독립적으로 1 이상 4 이하의 정수이고,
R1 내지 R3 중 적어도 하나는 중수소 원자를 포함하고, 나머지는 각각 독립적으로 수소 원자, 중수소 원자, 할로겐 원자, 히드록시기, 시아노기, 니트로기, 치환 또는 비치환된 실릴기, 치환 또는 비치환된 아민기, 치환 또는 비치환된 옥시기, 치환 또는 비치환된 탄소수 1 이상 60 이하의 알킬기, 치환 또는 비치환된 탄소수 2 이상 60 이하의 알케닐기, 치환 또는 비치환된 탄소수 2 이상 60 이하의 알키닐기, 치환 또는 비치환된 고리형성 탄소수 6 이상 60 이하의 아릴기, 또는 치환 또는 비치환된 고리형성 탄소수 1 이상 10 이하의 헤테로 고리기이고,
L은 직접 결합, O, S, ―CR11R12―, ―CR13=CR14―, ―C≡C―, ―C(=O)―, ―C(=S)―, ―BR15―, ―NR16―, ―PR17R18―, 또는 ―GeR19R20― 이고,
R11 내지 R20은 각각 독립적으로 수소 원자, 중수소 원자, 할로겐 원자, 치환 또는 비치환된 탄소수 1 이상 30 이하의 알킬기, 또는 치환 또는 비치환된 고리 형성 탄소수 6 이상 30 이하의 아릴기이다.An organometallic compound represented by the following formula (1):
[Formula 1]
In Formula 1,
M is a transition metal,
One or two selected from X 1 to X 6 is N, the rest is CR 4 ,
When X 1 is N, any one of X 2 to X 6 is N,
R 4 is a hydrogen atom, a deuterium atom, or a substituted or unsubstituted alkyl group having 1 to 10 carbon atoms,
A 1 to A 3 are each independently a substituted or unsubstituted hydrocarbon ring having 5 to 60 carbon atoms, or a substituted or unsubstituted heterocyclic ring having 1 to 60 carbon atoms,
b1 to b3 are each independently an integer of 1 or more and 4 or less,
At least one of R 1 to R 3 includes a deuterium atom, and the rest are each independently a hydrogen atom, a deuterium atom, a halogen atom, a hydroxy group, a cyano group, a nitro group, a substituted or unsubstituted silyl group, a substituted or unsubstituted An amine group, a substituted or unsubstituted oxy group, a substituted or unsubstituted alkyl group having 1 to 60 carbon atoms, a substituted or unsubstituted alkenyl group having 2 to 60 carbon atoms, or a substituted or unsubstituted alkyl group having 2 to 60 carbon atoms a nyl group, a substituted or unsubstituted aryl group having 6 to 60 ring carbon atoms, or a substituted or unsubstituted heterocyclic group having 1 to 10 ring carbon atoms,
L is a direct bond, O, S, —CR 11 R 12 —, —CR 13 =CR 14 —, —C≡C—, —C(=O)—, —C(=S)—, —BR 15 — , —NR 16 —, —PR 17 R 18 —, or —GeR 19 R 20 —,
R 11 to R 20 are each independently a hydrogen atom, a deuterium atom, a halogen atom, a substituted or unsubstituted alkyl group having 1 to 30 carbon atoms, or a substituted or unsubstituted aryl group having 6 to 30 ring carbon atoms.
상기 M은 Pt, Pd, Cu, 또는 Os인 유기 금속 화합물.13. The method of claim 12,
Wherein M is Pt, Pd, Cu, or Os organometallic compound.
상기 화학식 1은 하기 화학식 2-1 또는 화학식 2-2로 표시되는 유기 전계 발광 소자:
[화학식 2-1]
[화학식 2-2]
상기 화학식 2-1 및 화학식 2-2에서,
A1 내지 A3, X1 내지 X6, R1 내지 R3, 및 b1 내지 b3은 상기 화학식 1에서 정의한 바와 동일하다.13. The method of claim 12,
Formula 1 is an organic electroluminescent device represented by Formula 2-1 or Formula 2-2:
[Formula 2-1]
[Formula 2-2]
In Formulas 2-1 and 2-2,
A 1 to A 3 , X 1 to X 6 , R 1 to R 3 , and b 1 to b 3 are the same as defined in Formula 1 above.
상기 화학식 1은 하기 화학식 3으로 표시되는 유기 금속 화합물:
[화학식 3]
상기 화학식 3에서
R50은 수소 원자, 중수소 원자, 할로겐 원자, 치환 또는 비치환된 탄소수 1 이상 30 이하의 알킬기, 또는 치환 또는 비치환된 탄소수 6 이상 30 이하의 아릴기이고,
M, L, X1 내지 X6, R1 내지 R3, 및 b1 내지 b3은 상기 화학식 1에서 정의한 바와 동일하다.13. The method of claim 12,
Formula 1 is an organometallic compound represented by Formula 3 below:
[Formula 3]
In the above formula (3)
R 50 is a hydrogen atom, a deuterium atom, a halogen atom, a substituted or unsubstituted alkyl group having 1 to 30 carbon atoms, or a substituted or unsubstituted aryl group having 6 to 30 carbon atoms,
M, L, X 1 to X 6 , R 1 to R 3 , and b 1 to b 3 are the same as defined in Formula 1 above.
상기 화학식 3은 하기 화학식 3-1로 표시되는 유기 금속 화합물:
[화학식 3-1]
상기 화학식 3-1에서
X2 내지 X6 중 어느 하나는 N이고, 나머지는 CR4이고,
M, L, R1 내지 R4, R50 및 b1 내지 b3은 상기 화학식 3에서 정의한 바와 동일하다.16. The method of claim 15,
Formula 3 is an organometallic compound represented by the following Formula 3-1:
[Formula 3-1]
In the above formula 3-1
Any one of X 2 to X 6 is N, the rest is CR 4 ,
M, L, R 1 to R 4 , R 50 and b 1 to b 3 are the same as defined in Formula 3 above.
상기 화학식 3은 하기 화학식 3-2 또는 화학식 3-3으로 표시되는 유기 금속 화합물:
[화학식 3-2]
[화학식 3-3]
상기 화학식 3-2에서,
X2 내지 X4 중 어느 하나는 N이고, 나머지는 CR4이고,
상기 화학식 3-3에서,
X5 및 X6 중 어느 하나는 N이고, 나머지는 CR5이고,
b4는 1 이상 4 이하의 정수이고,
R5는 수소 원자, 중수소 원자, 또는 치환 또는 비치환된 탄소 수 1 이상 10 이하의 알킬기이고,
M, L, R1 내지 R4, b1 내지 b3, 및 R50은 상기 화학식 3에서 정의한 바와 동일하다.16. The method of claim 15,
Formula 3 is an organometallic compound represented by Formula 3-2 or Formula 3-3:
[Formula 3-2]
[Formula 3-3]
In Formula 3-2,
Any one of X 2 to X 4 is N, the rest is CR 4 ,
In Formula 3-3,
any one of X 5 and X 6 is N, the other is CR 5 ,
b4 is an integer of 1 or more and 4 or less,
R 5 is a hydrogen atom, a deuterium atom, or a substituted or unsubstituted alkyl group having 1 to 10 carbon atoms,
M, L, R 1 to R 4 , b 1 to b 3 , and R 50 are the same as defined in Formula 3 above.
상기 R50은 하기 화합물군 R의 화합물들 중 어느 하나로 표시되는 유기 금속 화합물:
[화합물군 R]
.16. The method of claim 15,
Wherein R 50 is an organometallic compound represented by any one of the compounds of the following compound group R:
[Compound group R]
.
상기 R50이 화합물 R-7 또는 R-8인 경우, R1은 적어도 하나의 중수소 원자를 포함하는 유기 금속 화합물.19. The method of claim 18,
When R 50 is compound R-7 or R-8, R 1 is an organometallic compound containing at least one deuterium atom.
상기 화학식 1은 하기 화합물군 1의 화합물들 중 어느 하나로 표시되는 유기 금속 화합물:
[화합물군 1]
.
13. The method of claim 12,
Formula 1 is an organometallic compound represented by any one of the compounds of the following compound group 1:
[Compound group 1]
.
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020200026896A KR20210112425A (en) | 2020-03-04 | 2020-03-04 | Organic electroluminescence device and organometallic compound for organic electroluminescence device |
| US17/074,493 US11849630B2 (en) | 2020-03-04 | 2020-10-19 | Organic electroluminescence device and organometallic compound for organic electroluminescence device |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020200026896A KR20210112425A (en) | 2020-03-04 | 2020-03-04 | Organic electroluminescence device and organometallic compound for organic electroluminescence device |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20210112425A true KR20210112425A (en) | 2021-09-15 |
Family
ID=77665022
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020200026896A KR20210112425A (en) | 2020-03-04 | 2020-03-04 | Organic electroluminescence device and organometallic compound for organic electroluminescence device |
Country Status (2)
| Country | Link |
|---|---|
| US (1) | US11849630B2 (en) |
| KR (1) | KR20210112425A (en) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2024080842A1 (en) * | 2022-10-13 | 2024-04-18 | 에스케이 주식회사 | Organometallic compound and organic electroluminescent device comprising same |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20210142032A (en) * | 2020-05-14 | 2021-11-24 | 삼성디스플레이 주식회사 | Organometallic compound and organic light emitting device comprising the same |
Family Cites Families (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9318725B2 (en) | 2012-02-27 | 2016-04-19 | Jian Li | Microcavity OLED device with narrow band phosphorescent emitters |
| JP6804823B2 (en) | 2013-10-14 | 2020-12-23 | アリゾナ・ボード・オブ・リージェンツ・オン・ビハーフ・オブ・アリゾナ・ステイト・ユニバーシティーArizona Board of Regents on behalf of Arizona State University | Platinum complex and device |
| US10008679B2 (en) | 2014-04-14 | 2018-06-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9923155B2 (en) | 2014-07-24 | 2018-03-20 | Arizona Board Of Regents On Behalf Of Arizona State University | Tetradentate platinum (II) complexes cyclometalated with functionalized phenyl carbene ligands and their analogues |
| US10153443B2 (en) * | 2016-07-19 | 2018-12-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11152579B2 (en) | 2016-12-28 | 2021-10-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11101435B2 (en) * | 2017-05-19 | 2021-08-24 | Arizona Board Of Regents On Behalf Of Arizona State University | Tetradentate platinum and palladium complexes based on biscarbazole and analogues |
| KR20180137311A (en) | 2017-06-16 | 2018-12-27 | 삼성전자주식회사 | Organometallic compound, organic light emitting device including the same and a composition for diagnosing including the same |
| KR20190014187A (en) * | 2017-07-27 | 2019-02-12 | 삼성디스플레이 주식회사 | Organometallic compound and organic light-emitting device including the same |
| US11424420B2 (en) * | 2017-09-07 | 2022-08-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11081659B2 (en) * | 2018-01-10 | 2021-08-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| KR20190121418A (en) * | 2018-04-17 | 2019-10-28 | 삼성디스플레이 주식회사 | Organic electroluminescence device and nitrogen-containing compound for organic electroluminescence device |
-
2020
- 2020-03-04 KR KR1020200026896A patent/KR20210112425A/en not_active Application Discontinuation
- 2020-10-19 US US17/074,493 patent/US11849630B2/en active Active
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2024080842A1 (en) * | 2022-10-13 | 2024-04-18 | 에스케이 주식회사 | Organometallic compound and organic electroluminescent device comprising same |
Also Published As
| Publication number | Publication date |
|---|---|
| US20210288270A1 (en) | 2021-09-16 |
| US11849630B2 (en) | 2023-12-19 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR20200071192A (en) | Organic electroluminescence device and polycyclic compound for organic electroluminescence device | |
| KR102599981B1 (en) | Organic electroluminescence device and polycyclic compound for organic electroluminescence device | |
| KR102400585B1 (en) | Compound including nitrogen and organic electroluminescence device including the same | |
| KR20210083464A (en) | Organic electroluminescence device and polycyclic compound for organic electroluminescence device | |
| KR20210006554A (en) | Organic electroluminescence device and fused polycyclic compound for organic electroluminescence device | |
| KR20200107028A (en) | Organic electroluminescence device and polycyclic compound for organic electroluminescence device | |
| KR20210038761A (en) | Organic electroluminescence device | |
| KR20210038785A (en) | Organic electroluminescence device and compound for organic electroluminescence device | |
| KR20210070453A (en) | Organic electroluminescence device and condensed polycyclic compound for organic electroluminescence device | |
| KR102399932B1 (en) | Compound for thermally activated delayed fluorescence and organic electroluminescence device including the same | |
| KR20200074352A (en) | Organic electroluminescence device and spiro compound for organic electroluminescence device | |
| KR20210154288A (en) | Organic electroluminescence device and fused polycyclic compound for organic electroluminescence device | |
| KR20210059126A (en) | Organic electroluminescence device and organometallic compound for organic electroluminescence device | |
| KR102613305B1 (en) | Organic electroluminescence device and condensed cyclic compound for organic electroluminescence device | |
| US11849630B2 (en) | Organic electroluminescence device and organometallic compound for organic electroluminescence device | |
| KR102405140B1 (en) | Heterocyclic compound and organic electroluminescence device including the same | |
| KR20220086223A (en) | Organic light-emitting compound and organic electroluminescent device using the same | |
| KR20220008985A (en) | Organic electroluminescent element and polycyclic compound for organic electroluminescent element | |
| KR102405134B1 (en) | Nitrogen contaiing compound and organic electroluminescence device including the same | |
| KR20200078755A (en) | Organic electroluminescence device and polycyclic compound for organic electroluminescence device | |
| KR20200068791A (en) | Organic electroluminescence device and polycyclic compound for organic electroluminescence device | |
| KR102668795B1 (en) | Organic electroluminescence device and polycyclic compound for organic electroluminescence device | |
| KR20210055589A (en) | Organic electroluminescence device and polycyclic compound for organic electroluminescence device | |
| KR20220014443A (en) | Organic electroluminescence device and polycyclic compound for organic electroluminescence device | |
| KR20210099678A (en) | Organic electroluminescence device and polycyclic compound for organic electroluminescence device |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| E902 | Notification of reason for refusal |