KR102106756B1 - Composition for preventing or treating skin damages caused by ultraviolet rays - Google Patents
Composition for preventing or treating skin damages caused by ultraviolet rays Download PDFInfo
- Publication number
- KR102106756B1 KR102106756B1 KR1020130112649A KR20130112649A KR102106756B1 KR 102106756 B1 KR102106756 B1 KR 102106756B1 KR 1020130112649 A KR1020130112649 A KR 1020130112649A KR 20130112649 A KR20130112649 A KR 20130112649A KR 102106756 B1 KR102106756 B1 KR 102106756B1
- Authority
- KR
- South Korea
- Prior art keywords
- leu
- arg
- ala
- val
- pro
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/96—Cosmetics or similar toiletry preparations characterised by the composition containing materials, or derivatives thereof of undetermined constitution
- A61K8/98—Cosmetics or similar toiletry preparations characterised by the composition containing materials, or derivatives thereof of undetermined constitution of animal origin
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L33/00—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof
- A23L33/10—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof using additives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q17/00—Barrier preparations; Preparations brought into direct contact with the skin for affording protection against external influences, e.g. sunlight, X-rays or other harmful rays, corrosive materials, bacteria or insect stings
- A61Q17/04—Topical preparations for affording protection against sunlight or other radiation; Topical sun tanning preparations
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q19/00—Preparations for care of the skin
- A61Q19/004—Aftersun preparations
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Engineering & Computer Science (AREA)
- Dermatology (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Zoology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Birds (AREA)
- Mycology (AREA)
- Nutrition Science (AREA)
- Food Science & Technology (AREA)
- Polymers & Plastics (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Gastroenterology & Hepatology (AREA)
- Immunology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Cosmetics (AREA)
Abstract
본 명세서에는 유효성분으로서 펩티드 또는 그 단편을 포함하는 자외선에 의한 피부 손상 예방 또는 치료용 조성물이 개시된다. 특히 본 발명에 따른 펩티드가 포함된 조성물은 UVA 및 UVB 모두에 의한 피부 손상에 치료 또는 예방 효과가 우수한 장점이 있다.Disclosed herein is a composition for preventing or treating skin damage caused by ultraviolet rays comprising a peptide or a fragment thereof as an active ingredient. In particular, the composition containing the peptide according to the present invention has an advantage of excellent treatment or prevention effect on skin damage caused by both UVA and UVB.
Description
본 명세서에는 인간 단백질 유래의 펩티드를 유효성분으로 포함한 자외선에 의한 피부 손상 예방 또는 치료용 조성물에 관한 것이다. The present specification relates to a composition for preventing or treating skin damage caused by ultraviolet rays containing a peptide derived from human protein as an active ingredient.
텔로미어(telomere)는 염색체의 말단에 반복적으로 존재하는 유전 물질로서, 해당 염색체의 손상이나 다른 염색체와의 결합을 방지한다고 알려져 있다. 세포가 분열할 때마다 텔로미어의 길이는 조금씩 짧아지는데, 일정한 횟수 이상의 세포 분열이 있게 되면 텔로미어는 매우 짧아지고, 그 세포는 분열을 멈추고 죽게 된다. 반면 텔로미어를 길게 하면 세포의 수명이 연장된다고 알려져 있으며, 그 예로 암세포에서는 텔로머라제(telomerase)라는 효소가 분비되어 텔로미어가 짧아지는 것을 막기 때문에, 암세포가 죽지 않고 계속 증식할 수 있다고 알려져 있다.Telomere is a genetic material that is repeatedly present at the ends of chromosomes and is known to prevent damage to the chromosome or binding to other chromosomes. Each time a cell divides, the length of the telomeres decreases slightly, but if there is a cell division over a certain number of times, the telomeres become very short, and the cells stop dividing and die. On the other hand, it is known that prolonging telomeres prolongs the lifespan of cells, and for example, cancer cells secrete an enzyme called telomerase to prevent telomeres from shortening, so that cancer cells can continue to proliferate without dying.
본 발명의 일측면은 피부에 유용한 펩티드를 제공하고자 한다.One aspect of the present invention is to provide a peptide useful for the skin.
본 발명의 일측면은 인간 단백질 유래의 펩티드를 유효성분으로 포함하는 조성물을 제공하고자 한다.One aspect of the present invention is to provide a composition comprising a peptide derived from human protein as an active ingredient.
본 발명의 일측면은 피부 손상을 예방 또는 치료하는 효능을 갖는 펩티드를 제공하고자 한다.One aspect of the present invention is to provide a peptide having the efficacy of preventing or treating skin damage.
본 발명의 일측면은 자외선에 의한 피부 손상의 예방 또는 치료에 유용한 펩티드를 제공하고자 한다.One aspect of the present invention is to provide a peptide useful for the prevention or treatment of skin damage caused by ultraviolet rays.
본 발명의 일측면은 자외선에 의한 피부 손상의 예방 또는 치료 효능을 갖는 조성물을 제공하고자 한다.One aspect of the present invention is to provide a composition having the effect of preventing or treating skin damage caused by ultraviolet rays.
본 발명의 일측면은 자외선에 의한 피부 손상의 예방 또는 치료 효능을 갖는 화장료 조성물을 제공하고자 한다.One aspect of the present invention is to provide a cosmetic composition having the effect of preventing or treating skin damage caused by ultraviolet rays.
본 발명의 일측면은 자외선에 의한 피부 손상의 예방 또는 치료 효능을 갖는 건강식품 조성물을 제공하고자 한다.One aspect of the present invention is to provide a health food composition having the efficacy of preventing or treating skin damage caused by ultraviolet rays.
본 발명의 일측면은 자외선에 의한 피부 손상의 예방 또는 치료 효능을 갖는 약학 조성물을 제공하고자 한다.One aspect of the present invention is to provide a pharmaceutical composition having the efficacy of preventing or treating skin damage caused by ultraviolet rays.
본 발명의 일측면은 서열번호 1을 포함하는 펩티드, 상기 펩티드 서열과 80% 이상의 서열 상동성을 갖는 펩티드, 또는 그것의 단편을 유효성분으로 포함하는, 자외선에 의한 세포 독성 완화 기능을 보유한 자외선에 의한 피부 손상 예방 또는 치료용 조성물을 제공한다.One aspect of the present invention comprises a peptide comprising SEQ ID NO: 1, a peptide having a sequence homology of 80% or more with the peptide sequence, or a fragment thereof as an active ingredient, in ultraviolet light having a function of alleviating cytotoxicity by ultraviolet light It provides a composition for preventing or treating skin damage caused by.
본 발명의 다른 일측면은 UVA 및 UVB 모두에 의한 피부 손상 예방 또는 치료에 우수한 효과가 있는 조성물은 제공한다. Another aspect of the present invention provides a composition having an excellent effect on preventing or treating skin damage caused by both UVA and UVB.
본 발명의 다른 일측면은 상기 자외선에 의한 피부 손상 예방 또는 치료용 조성물을 포함하는 화장료, 약학 또는 건강식품 조성물을 제공한다.Another aspect of the present invention provides a cosmetic, pharmaceutical or health food composition comprising a composition for preventing or treating skin damage caused by ultraviolet rays.
본 발명에 따른 조성물은 서열번호 1을 포함하는 펩티드, 상기 펩티드 서열과 80% 이상의 서열 상동성을 갖는 펩티드, 또는 그것의 단편을 유효성분으로 포함함으로써 우수한 자외선에 의한 세포 독성 완화 효과를 나타낸다. 따라서, 피부의 자외선에 의한 세포 독성 완화를 통하여 자외선에 의한 피부 손상 예방 또는 치료할 수 있다. 특히 본 발명에 따른 펩티드가 포함된 조성물은 UVA 및 UVB 모두에 의한 피부 손상에 치료 또는 예방 효과가 우수한 장점이 있다. The composition according to the present invention shows an effect of alleviating cytotoxicity caused by excellent ultraviolet rays by including a peptide comprising SEQ ID NO: 1, a peptide having 80% or more sequence homology with the peptide sequence, or a fragment thereof as an active ingredient. Therefore, it is possible to prevent or treat skin damage caused by ultraviolet rays by alleviating cytotoxicity caused by ultraviolet rays of the skin. In particular, the composition containing the peptide according to the present invention has an advantage of excellent treatment or prevention effect on skin damage caused by both UVA and UVB.
도 1은 본 발명의 일측면에 따른 서열번호 1의 펩티드의 농도변화에 대한 자외선 조사에 의한 세포독성 완화효과에 따른 세포 생존율(Cell viability, %)을 측정한 결과를 도시한 그래프이다.
도 2는 자외선 B 조사 후 서열번호 1의 펩티드(Pep1)을 농도별로 첨가하였을 경우에 IL-1α, IL-6, TNF-α를 억제한 결과를 나타낸 그래프이다.1 is a graph showing the results of measuring the cell viability (Cell viability,%) according to the cytotoxic alleviation effect by ultraviolet irradiation for the concentration change of the peptide of SEQ ID NO: 1 according to an aspect of the present invention.
2 is a graph showing the results of inhibiting IL-1α, IL-6, and TNF-α when peptide (Pep1) of SEQ ID NO: 1 is added by concentration after irradiation with ultraviolet B.
서열번호 1 에 기재된 펩티드는 아래 표 1과 같다. 서열번호 2는 인간의 텔로머라제 전장 단백질의 서열이다. 서열번호 1은 텔로머라제로부터 유래된 펩티드로서 16개 아미노산으로 구성된 펩티드이다. 아래 표 1의 "이름"은 펩티드를 구별하기 위해 명명한 것이다. 본 발명의 다른 일측면에서, 서열 번호 1의 펩티드는 텔로머라제에 포함된 펩티드 중 해당 위치의 펩티드를 선별해 합성한 "합성 펩티드"를 포함한다.
The peptide described in SEQ ID NO: 1 is shown in Table 1 below. SEQ ID NO: 2 is the sequence of a human telomerase full-length protein. SEQ ID NO: 1 is a peptide derived from telomerase and is a peptide composed of 16 amino acids. The “name” in Table 1 below is used to distinguish peptides. In another aspect of the present invention, the peptide of SEQ ID NO: 1 includes a "synthetic peptide" synthesized by selecting a peptide at a corresponding position among peptides included in telomerase.
본 발명의 일측면은 서열번호 1의 단편들인 펩티드 또는 상기 펩티드 서열과 80% 이상의 서열 상동성을 갖는 펩티드를 코딩하는 폴리뉴클레오티드를 제공한다. 상기 폴리뉴클레오티드를 이용하여 서열번호 1의 단편들인 펩티드 또는 상기 펩티드 서열과 80% 이상의 서열 상동성을 갖는 펩티드를 대량 생산할 수 있다. 예컨대, 서열번호 1의 단편들인 펩티드 중 하나 이상의 펩티드를 코딩하는 폴리뉴클레오티드를 포함하는 벡터를 숙주 세포에 넣어 배양함으로써, 서열번호 1의 단편들인 펩티드 중 하나 이상의 펩티드를 대량 생산할 수 있다.
One aspect of the present invention provides a polynucleotide encoding a peptide that is a fragment of SEQ ID NO: 1 or a peptide having at least 80% sequence homology to the peptide sequence. The polynucleotide can be used to mass-produce peptides that are fragments of SEQ ID NO: 1 or peptides having 80% or more sequence homology with the peptide sequences. For example, by culturing a vector containing a polynucleotide encoding one or more of the peptides of the fragments of SEQ ID NO: 1 into a host cell, the peptides of one or more of the peptides of the fragments of SEQ ID NO: 1 can be mass produced.
본 명세서에 개시된 펩티드는 서열번호 1의 단편들인 펩티드와, 80% 이상, 85% 이상, 90% 이상, 95% 이상 또는 96% 이상의 서열 상동성을 갖는 펩티드를 포함할 수 있다. 또한, 본 명세서에 개시된 펩티드는 서열번호 1의 단편들인 펩티드와, 1개 이상의 아미노산, 2개 이상의 아미노산, 3개 이상의 아미노산, 4개 이상의 아미노산, 5개 이상의 아미노산, 6개 이상의 아미노산 또는 7개 이상의 아미노산이 변화된 펩티드를 포함할 수 있다. The peptides disclosed herein may include peptides that are fragments of SEQ ID NO: 1, and peptides having sequence homology of 80% or more, 85% or more, 90% or more, 95% or more, or 96% or more. In addition, the peptides disclosed herein are peptides that are fragments of SEQ ID NO: 1, 1 or more amino acids, 2 or more amino acids, 3 or more amino acids, 4 or more amino acids, 5 or more amino acids, 6 or more amino acids, or 7 or more amino acids It may include peptides with amino acid changes.
본 발명의 일측면에서, 아미노산 변화는 펩티드의 물리화학적 특성이 변경되도록 하는 성질에 속한다. 예를 들어, 펩티드의 열안정성을 향상시키고, 기질 특이성을 변경시키고, 최적의 pH를 변화시키는 등의 아미노산 변화가 수행될 수 있다.In one aspect of the invention, amino acid changes belong to properties that allow the physicochemical properties of the peptide to be altered. For example, amino acid changes can be performed, such as improving the thermal stability of the peptide, changing the substrate specificity, and changing the optimum pH.
본 명세서에서 “아미노산”이라 함은 자연적으로 펩티드로 통합되는 22개의 표준 아미노산들 뿐만 아니라 D-아이소머 및 변형된 아미노산들을 포함한다. 이에 따라, 본 발명의 일측면에서 펩티드는 D-아미노산을 포함하는 펩티드일 수 있다. 한편, 본 발명의 다른 측면에서 펩티드는 번역 후 변형(post-translational modification)된 비표준 아미노산 등을 포함할 수 있다. 번역 후 변형의 예는 인산화(phosphorylation), 당화(glycosylation), 아실화(acylation) (예컨대, 아세틸화(acetylation), 미리스토일화(myristoylation) 및 팔미토일화(palmitoylation)를 포함), 알킬화(alkylation), 카르복실화(carboxylation), 히드록실화(hydroxylation), 당화반응(glycation), 비오티닐화(biotinylation), 유비퀴티닐화(ubiquitinylation), 화학적 성질의 변화(예컨대, 베타-제거 탈이미드화, 탈아미드화) 및 구조적 변화(예컨대, 이황화물 브릿지의 형성) 를 포함한다. 또한, 펩티드 컨쥬게이트를 형성하기 위한 가교제(crosslinker)들과의 결합과정에서 일어나는 화학 반응들에 의해 생기는 아미노산의 변화, 예컨대 아미노기, 카르복시기 또는 사이드 체인에서의 변화와 같은 아미노산의 변화를 포함한다. As used herein, “amino acid” includes 22 standard amino acids that are naturally incorporated into peptides, as well as D-isomers and modified amino acids. Accordingly, in one aspect of the present invention, the peptide may be a peptide containing D-amino acid. Meanwhile, in another aspect of the present invention, the peptide may include a non-standard amino acid that has been post-translational modification. Examples of post-translational modifications include phosphorylation, glycosylation, acylation (e.g., acetylation, myristoylation and palmitoylation), alkylation ), Carboxylation, hydroxylation, glycation, biotinylation, ubiquitinylation, changes in chemical properties (e.g. beta-eliminated deimide , Deamidation) and structural changes (eg, formation of disulfide bridges). It also includes changes in amino acids, such as changes in amino groups, carboxyl groups or side chains, caused by chemical reactions that occur in the course of binding with crosslinkers to form peptide conjugates.
본 명세서에 개시된 펩티드는 자연 그대로의 공급원으로부터 동정 및 분리된 야생형 펩티드일 수 있다. 한편, 본 명세서에 개시된 펩티드는 서열번호 1의 단편들인 펩티드와 비교하여 하나 이상의 아미노산이 치환, 결실 및/또는 삽입된 아미노산 서열을 포함하는, 인공 변이체일 수 있다. 인공 변이체에서 뿐만 아니라 야생형 폴리펩티드에서의 아미노산 변화는 단백질의 폴딩(folding) 및/또는 활성에 유의한 영향을 미치지 않는 보존성 아미노산 치환을 포함한다. 보존성 치환의 예들은 염기성 아미노산(아르기닌, 리신 및 히스티딘), 산성 아미노산(글루탐산 및 아스파르트산), 극성 아미노산(글루타민 및 아스파라긴), 소수성 아미노산(루신, 이소로이신, 발린 및 메티오닌), 방향족 아미노산(페닐알라닌, 트립토판 및 티로신), 및 작은 아미노산(글리신, 알라닌, 세린 및 트레오닌)의 군의 범위 내에 있다. 일반적으로 특이적 활성을 변경시키지 않는 아미노산 치환이 본 분야에 공지되어 있다. 가장 흔하게 발생하는 교환은 Ala/Ser, Val/Ile, Asp/Glu, Thr/Ser, Ala/Gly, Ala/Thr, Ser/Asn, Ala/Val, Ser/Gly, Tyr/Phe, Ala/Pro, Lys/Arg, Asp/Asn, Leu/Ile, Leu/Val, Ala/Glu, 및 Asp/Gly, 그리고 이들과 반대인 것들이다.
The peptides disclosed herein can be wild-type peptides that have been identified and isolated from intact sources. Meanwhile, the peptide disclosed herein may be an artificial variant comprising an amino acid sequence in which one or more amino acids have been substituted, deleted, and / or inserted compared to a peptide that is a fragment of SEQ ID NO: 1. Amino acid changes in wild-type polypeptides as well as in artificial variants include conservative amino acid substitutions that do not significantly affect the folding and / or activity of the protein. Examples of conservative substitutions are basic amino acids (arginine, lysine and histidine), acidic amino acids (glutamic acid and aspartic acid), polar amino acids (glutamine and asparagine), hydrophobic amino acids (leucine, isoleucine, valine and methionine), aromatic amino acids (phenylalanine, Tryptophan and tyrosine), and small amino acids (glycine, alanine, serine and threonine). In general, amino acid substitutions that do not alter specific activity are known in the art. The most common exchanges are Ala / Ser, Val / Ile, Asp / Glu, Thr / Ser, Ala / Gly, Ala / Thr, Ser / Asn, Ala / Val, Ser / Gly, Tyr / Phe, Ala / Pro, Lys / Arg, Asp / Asn, Leu / Ile, Leu / Val, Ala / Glu, and Asp / Gly, and vice versa.
또한, 본 발명의 다른 일측면은 상기와 같은 인간 단백질 유래의 펩티드 또는 상기 펩티드 서열과 80% 이상의 서열 상동성을 갖는 펩티드 또는 그 단편을 유효성분으로 포함하는 조성물을 제공한다. In addition, another aspect of the present invention provides a composition comprising a peptide or a fragment thereof having 80% or more sequence homology with a peptide or a peptide derived from the human protein as described above as an active ingredient.
피부 세포는 외부로부터 가해지는 자외선, 환경오염물질, 급격한 기온의 변화 등과 같은 세포손상 자극들에 의해 세포내의 다양한 생화학적 변화가 유도되어 세포 손상 반응을 나타낸다. 피부 세포의 세포막이 활성산소나 다른 라디칼에 의해 지속적으로 손상을 입게 되면 단백질이나 지질단백질(lipoprotein)의 가교(cross- linkage)가 증가하거나 분해가 되어, 과산화 지질의 양도 증가하게 된다. 따라서, 세포막의 투과성이 변화하여 세포 내의 이온 균형이 깨지게 되고, 이런 변화는 세포 내의 대사 찌꺼기의 배출을 막고, 이 대사 찌꺼기를 제독하는 세포의 기능을 또한 감소시키게 된다. 그리고, 세포 내의 칼륨 농도의 증가로 콜로이드 밀도가 증가하면, mRNA나 단백질의 합성이 방해를 받게 되어 세포 손상을 치유할 수 있는 능력은 더욱 떨어지게 된다.Skin cells exhibit a cell damage response by inducing various biochemical changes in the cells by stimulation of cell damage such as ultraviolet rays, environmental pollutants, and rapid temperature changes applied from the outside. When the cell membrane of skin cells is continuously damaged by free radicals or other radicals, cross-linkage of proteins or lipoproteins increases or decomposes, thereby increasing the amount of lipid peroxide. Therefore, the permeability of the cell membrane is changed and the ion balance in the cell is broken, and this change prevents the discharge of metabolic debris in the cell and also decreases the function of the cell to detoxify the metabolic debris. And, if the colloid density increases due to the increase in the concentration of potassium in the cell, the synthesis of mRNA or protein is hindered, and the ability to repair cell damage is further reduced.
이처럼 세포 수준의 변화가 지속되면, 피부 조직의 구조(tissue structure)가 규칙성을 잃게 됨과 동시에 개별 세포들은 상대적으로 커지면서, 전체 세포 수는 감소하게 된다. 또한, 진피(dermis)에 국소적인 상흔이 나타나고, 콜라겐 섬유(collagen fiber)나 탄력섬유(elastic fiber)의 감소로 진피 두께가 줄어든다. 콜라겐 섬유끼리의 가교도 증가하며 탄력섬유의 미세한 구조도 손상되어 전체적으로 피부의 탄력 저하가 나타난다. 즉, 외부 자극원에 의한 피부 세포의 산화적 손상은 궁극적으로 피부의 노화를 촉진시키게 된다.If the cell-level change continues as described above, the tissue structure of the skin tissue loses its regularity, and at the same time, the individual cells are relatively large, and the total cell number is decreased. In addition, local scars appear on the dermis, and the thickness of the dermis is reduced due to the reduction of collagen fibers or elastic fibers. The crosslinking between collagen fibers also increases, and the fine structure of the elastic fibers is also damaged, resulting in a decrease in elasticity of the skin as a whole. That is, oxidative damage of skin cells caused by an external stimulus ultimately promotes aging of the skin.
이러한 산화적 세포 손상을 일으키는 물질들로는, 산화적 스트레스에 의해 발생하는 과산화수소(H2O2), 초과산화물 음이온(superoxide anion), 수산화라디칼 (hydroxy radical) 등이 있으며, 이러한 유해 활성 산소종들의 세포내독성을 제거하기 위해 우리 신체는 글루타치온(glutathione), 초과산화물 불균등화 효소(superoxide dismutase;SOD)와 같은 내인성 항산화 시스템을 갖추고 있다. 그러나, 세포내 대사활동이 지나치게 증가하거나, 신체가 감염, 과도한 운동, 방사선 또는 화합물과 같은 외인성 스트레스에 노출되면 이러한 내인성 항산화 능력을 초과하게 되는 경우가 있으며, 이때 자유라디칼에 의한 세포 손상이 나타나게 된다. Substances causing such oxidative cell damage include hydrogen peroxide (H 2 O 2 ), superoxide anion, and hydroxyl radical generated by oxidative stress. To eliminate endotoxins, our bodies are equipped with endogenous antioxidant systems such as glutathione and superoxide dismutase (SOD). However, when the metabolic activity in the cell is excessively increased, or when the body is exposed to an exogenous stress such as infection, excessive exercise, radiation, or a compound, the endogenous antioxidant capacity may be exceeded. At this time, cell damage caused by free radicals may occur. .
이에 본 발명의 일측면은 인간 단백질 유래의 펩티드로서, 서열번호 1의 단편들인 펩티드 또는 상기 펩티드 서열과 80% 이상의 서열 상동성을 갖는 펩티드 또는 그 단편을 유효성분으로 포함하는 조성물을 제공함으로써, 피부 세포 자체의 내인성 항산화력, 즉 세포의 생리적인 환원력을 증가시켜 자외선과 같은 자극으로부터 세포 손상을 억제할 수 있다. 따라서, 이를 피부에 도포 또는 투여할 경우 펩티드가 세포내 독성을 완화시킴으로써 자외선과 같은 자극으로부터 피부를 보호하고 피부의 손상을 예방 또는 치료할 수 있다.
Accordingly, one aspect of the present invention is a peptide derived from a human protein, by providing a composition comprising a peptide that is a fragment of SEQ ID NO: 1 or a peptide having 80% or more sequence homology with the peptide sequence or a fragment thereof as an active ingredient, skin By increasing the endogenous antioxidant power of the cell itself, that is, the physiological reducing power of the cell, it is possible to suppress cell damage from stimulation such as ultraviolet light. Therefore, when applied or administered to the skin, the peptide can protect the skin from irritation such as ultraviolet rays by preventing intracellular toxicity and prevent or treat skin damage.
본 발명의 일측면에 따른 조성물은 서열번호 1의 단편들인 펩티드 또는 상기 펩티드 서열과 80% 이상의 서열 상동성을 갖는 펩티드를 0.1 ㎍/㎎ 내지 1 ㎎/㎎, 구체적으로 1 ㎍/㎎ 내지 0.5 ㎎/㎎, 더 구체적으로 10 ㎍/㎎ 내지 0.1 ㎎/㎎ 함량으로 포함할 수 있다. 상기 범위로 포함하는 경우 본 발명의 의도한 효과를 나타내기에 적절할 뿐만 아니라, 조성물의 안정성 및 안전성을 모두 만족할 수 있으며, 비용 대비 효과의 측면에서도 상기 범위로 포함하는 것이 적절할 수 있다.The composition according to one aspect of the present invention is a peptide of the fragments of SEQ ID NO: 1 or a peptide having a sequence homology of 80% or more with the peptide sequence is 0.1 μg / mg to 1 mg / mg, specifically 1 μg / mg to 0.5 mg / Mg, more specifically, 10 μg / mg to 0.1 mg / mg. When included in the above range, it is not only suitable to exhibit the intended effect of the present invention, but also satisfies both the stability and safety of the composition, and it may be appropriate to include the above range in terms of cost effectiveness.
본 발명의 일측면에 따른 조성물은 인간, 개, 닭, 돼지, 소, 양, 기니아피그 또는 원숭이를 포함하는 모든 동물에 적용될 수 있다.The composition according to one aspect of the present invention can be applied to all animals including humans, dogs, chickens, pigs, cows, sheep, guinea pigs or monkeys.
본 발명의 일측면에 따른 약학 조성물은 경구, 직장, 경피, 정맥 내, 근육 내, 복강 내, 골수 내, 경막 내 또는 피하 등으로 투여될 수 있다.The pharmaceutical composition according to one aspect of the present invention may be administered orally, rectal, transdermal, intravenous, intramuscular, intraperitoneal, intramedullary, intrathecal or subcutaneous.
경구 투여를 위한 제형은 정제, 환제, 연질 또는 경질 캅셀제, 과립제, 산제, 액제 또는 유탁제일 수 있으나, 이에 제한되는 것은 아니다. 비경구 투여를 위한 제형은 주사제, 점적제, 로션, 연고, 겔, 크림, 현탁제, 유제, 좌제, 패취 또는 분무제일 수 있으나, 이에 제한되는 것은 아니다.Formulations for oral administration may be tablets, pills, soft or hard capsules, granules, powders, liquids or emulsions, but are not limited thereto. Formulations for parenteral administration may be, but are not limited to, injections, drops, lotions, ointments, gels, creams, suspensions, emulsions, suppositories, patches or sprays.
본 발명의 일측면에 따른 약학 조성물은 필요에 따라 희석제, 부형제, 활택제, 결합제, 붕해제, 완충제, 분산제, 계면 활성제, 착색제, 향료 또는 감미제 등의 첨가제를 포함할 수 있다. 본 발명의 일측면에 따른 약학 조성물은 당업계의 통상적인 방법에 의해 제조될 수 있다.The pharmaceutical composition according to one aspect of the present invention may include additives such as diluents, excipients, lubricants, binders, disintegrants, buffers, dispersants, surfactants, colorants, flavors or sweeteners, if necessary. Pharmaceutical compositions according to one aspect of the present invention can be prepared by conventional methods in the art.
본 발명의 일측면에 따른 약학 조성물의 유효성분은 투여 받을 대상의 연령, 성별, 체중, 병리 상태 및 그 심각도, 투여 경로 또는 처방자의 판단에 따라 달라질 것이다. 이러한 인자에 기초한 적용량 결정은 당업자의 수준 내에 있으며, 이의 1일 투여 용량은 예를 들어 0.1 ㎍/kg/일 내지 1 g/kg/일, 구체적으로는 1 ㎍/kg/일 내지 10 mg/kg/일, 더 구체적으로는 10 ㎍/kg/일 내지 1 mg/kg/일, 보다 더 구체적으로는 50 ㎍/kg/일 내지 100 ㎍/kg/일이 될 수 있으나, 이에 제한되는 것은 아니다. 본 발명의 일측면에 따른 약학 조성물은 1일 1회 내지 3회 투여될 수 있으나, 이에 제한되는 것은 아니다.The active ingredient of the pharmaceutical composition according to one aspect of the present invention will vary depending on the age, gender, weight, pathology and severity of the subject to be administered, the route of administration or the judgment of the prescriber. Determination of the application amount based on these factors is within the level of those skilled in the art, the daily dosage of which is, for example, 0.1 μg / kg / day to 1 g / kg / day, specifically 1 μg / kg / day to 10 mg / kg / Day, more specifically 10 μg / kg / day to 1 mg / kg / day, and more specifically 50 μg / kg / day to 100 μg / kg / day, but is not limited thereto. The pharmaceutical composition according to one aspect of the present invention may be administered once to three times a day, but is not limited thereto.
본 발명의 일측면에 따른 약학 조성물에 의하면, 자외선이 피부에 조사됨에 따른 다양한 증상 또는 질병을 예방 또는 개선할 수 있다. 예를 들면, 자외선에 의해 유발된 피부 자극으로 인한 일광화상, 홍반, 부종, 색소침착, 피부 염증, 피부 각화뿐만 아니라, 광알레르기, 광독성과 같은 광감작현상, 만성반응으로서 광노화 또는 흑색종과 같은 피부암 등의 발생을 예방 또는 개선할 수 있다.
According to the pharmaceutical composition according to an aspect of the present invention, it is possible to prevent or improve various symptoms or diseases as ultraviolet rays are irradiated to the skin. For example, sunburn caused by UV-induced skin irritation, erythema, edema, pigmentation, skin irritation, skin exfoliation, as well as photosensitization phenomena such as photoallergy, phototoxicity, photoaging or melanoma as a chronic reaction. It can prevent or improve the occurrence of skin cancer.
본 발명의 일측면에 따른 화장품 조성물은 국소 적용에 적합한 모든 제형으로 제공될 수 있다. 예를 들면, 용액, 수상에 유상을 분산시켜 얻은 에멀젼, 유상에 수상을 분산시켜 얻은 에멀젼, 현탁액, 고체, 겔, 분말, 페이스트, 포말(foam) 또는 에어로졸의 제형으로 제공될 수 있다. 이러한 제형은 당해 분야의 통상적인 방법에 따라 제조될 수 있다.The cosmetic composition according to one aspect of the present invention may be provided in any formulation suitable for topical application. For example, it may be provided in the form of a solution, an emulsion obtained by dispersing an oil phase in an aqueous phase, an emulsion obtained by dispersing an oil phase in an oil phase, suspension, solid, gel, powder, paste, foam or aerosol. Such formulations can be prepared according to conventional methods in the art.
또한, 본 발명의 일측면에 따른 화장품 조성물은 주사액 제형으로 제공될 수 있다. 이 주사액 제형의 화장품 조성물은 1개의 니들을 갖는 주사기, 복수개의 니들을 갖는 주사기, 패치, 마이크로 니들 또는 마이크로젯 방식으로 고속 분사하거나 알루미늄 호일(foil)에 레이저 빔을 가함으로써 유발되는 충격파를 통해 주사액을 분사하는 기구를 예로 들 수 있는 다양한 전달기구를 통하여 피부에 주입될 수 있다. 상기 레이저를 이용하는 방식에 의하면 주사바늘을 사용하지 않으므로, 주사시의 통증 및 주사 바늘 사용으로 인한 상처 등을 방지할 수 있다. 이와 같이 주사액 제형에 의하면 화장품 조성물에 포함된 활성성분을 피부와 같은 표적 부위에 직접적으로 전달할 수 있어 효과를 극대화시킬 수 있다. 또한, 레이저를 이용하는 방식에 의하면 주사바늘을 사용하지 않으므로, 주사시의 통증 및 주사 바늘 사용으로 인한 상처 등을 방지할 수 있다.
In addition, the cosmetic composition according to an aspect of the present invention may be provided as an injection liquid formulation. The cosmetic composition of this injection solution formulation is a syringe with a single needle, a syringe with a plurality of needles, a patch, a micro needle or a microjet method, or a high-speed injection or injection solution through a shock wave caused by applying a laser beam to an aluminum foil. It can be injected into the skin through a variety of delivery mechanisms, such as a mechanism for spraying. According to the method using the laser, since an injection needle is not used, it is possible to prevent pain at the time of injection and wound due to the use of an injection needle. As described above, according to the injection solution formulation, the active ingredient included in the cosmetic composition can be directly delivered to the target site such as the skin, thereby maximizing the effect. In addition, according to the method using a laser, since an injection needle is not used, pain during injection and a wound due to the use of an injection needle can be prevented.
본 발명의 일측면에 따른 화장품 조성물은 주 효과를 손상시키지 않는 범위 내에서, 바람직하게는 주 효과에 상승 효과를 줄 수 있는 다른 성분들을 포함할 수 있다. 또한 본 발명의 일측면에 따른 화장품 조성물은 보습제, 에몰리언트제, 계면 활성제, 자외선 흡수제, 방부제, 살균제, 산화 방지제, pH 조정제, 유기 또는 무기 안료, 향료, 냉감제 또는 제한(制汗)제를 더 포함할 수 있다. 상기 성분의 배합량은 본 발명의 목적 및 효과를 손상시키지 않는 범위 내에서 당업자가 용이하게 선정 가능하며, 그 배합량은 화장품 조성물 전체 중량을 기준으로 0.01 내지 5 중량%, 구체적으로 0.01 내지 3 중량%일 수 있다.
The cosmetic composition according to an aspect of the present invention may include other ingredients that can give a synergistic effect to the main effect, within a range that does not impair the main effect. In addition, the cosmetic composition according to an aspect of the present invention is a moisturizer, emollient, surfactant, ultraviolet absorber, preservative, disinfectant, antioxidant, pH adjusting agent, organic or inorganic pigment, fragrance, cooling agent, or limiting agent It can contain. The blending amount of the components can be easily selected by those skilled in the art within a range that does not impair the object and effect of the present invention, the blending amount is 0.01 to 5% by weight based on the total weight of the cosmetic composition, specifically 0.01 to 3% by weight You can.
본 발명의 일측면에 따른 식품 조성물의 제형은 특별히 한정되지 않으나, 예를 들어, 정제, 과립제, 분말제, 액제, 고형 제제 등으로 제형화될 수 있다. 각 제형은 유효성분 이외에 해당 분야에서 통상적으로 사용되는 성분들을 제형 또는 사용 목적에 따라 당업자가 어려움 없이 적의 선정하여 배합할 수 있으며, 다른 원료와 동시에 적용할 경우 상승 효과가 일어날 수 있다.The formulation of the food composition according to one aspect of the present invention is not particularly limited, but may be formulated into, for example, tablets, granules, powders, liquids, solid preparations, and the like. Each formulation can be formulated by appropriately selecting the ingredients commonly used in the field other than the active ingredient according to the formulation or purpose of use without difficulty, and synergistic effects may occur when applied simultaneously with other raw materials.
상기 유효성분의 투여량 결정은 당업자의 수준 내에 있으며, 이의 1일 투여 용량은 예를 들어 구체적으로는 1 ㎍/kg/일 내지 10 mg/kg/일, 더 구체적으로는 10 ㎍/kg/일 내지 1 mg/kg/일, 보다 더 구체적으로는 50 ㎍/kg/일 내지 100 ㎍/kg/일이 될 수 있으나, 이에 제한되지 않으며, 투여하고자 하는 대상의 연령, 건강 상태, 합병증 등 다양한 요인에 따라 달라질 수 있다.
Determination of the dosage of the active ingredient is within the level of those skilled in the art, the daily dosage of which is, for example, specifically 1 μg / kg / day to 10 mg / kg / day, more specifically 10 μg / kg / day To 1 mg / kg / day, more specifically, 50 µg / kg / day to 100 µg / kg / day, but is not limited thereto, and various factors such as age, health condition, and complications of the subject to be administered May vary.
자외선은 체내에서 비타민D를 합성하고, 살균작용을 하는 등 이로운 역할을 하는 동시에 피부노화, 피부암, 건조, 피부염, 잔주름, 기미, 주근깨 등을 생기게도 한다. 자외선(Ultraviolet; UV)은 파장길이에 따라 A, B, C의 세 가지로 나뉘는데, 이 중 UVC는 오존층에서 차단되고, UVA와 UVB가 피부에 영향을 미친다. UVA는 자외선의 90% 이상을 차지하며 피부노화의 주원인으로 꼽힌다. 일출부터 일몰 때까지 하루 종일, 사계절 내내 존재한다. 구름 낀 흐린 날, 비 오는 날에도 피할 수 없으며 유리도 투과한다. UVB는 여름에 증가하며, UVA보다 파장이 짧아 피부 깊숙이 침투하지는 못하지만 과다하게 쪼이면 일광화상을 일으키거나 홍반, 물집, 화상, 염증을 일으키며 피부노화의 원인이 된다.
Ultraviolet rays synthesize beneficial vitamin D in the body and act as a bactericidal agent, while also producing skin aging, skin cancer, dryness, dermatitis, fine lines, blemishes, and freckles. Ultraviolet (UV) is divided into three types, A, B, and C, depending on the wavelength, of which UVC is blocked in the ozone layer, and UVA and UVB affect the skin. UVA accounts for more than 90% of ultraviolet rays and is considered a major cause of skin aging. It exists throughout the four seasons, from sunrise to sunset. Even on cloudy and cloudy days, it cannot be avoided, and the glass also penetrates. UVB increases in the summer and has a shorter wavelength than UVA, so it does not penetrate deep into the skin, but excessive exposure can cause sunburn, erythema, blisters, burns, and inflammation, which can cause skin aging.
이하, 본 발명에 따른 펩티드 PEP 1이 UVA 및 UVB에 미치는 영향을 실시예 및 실험예로 확인함으로써 본 발명의 구성 및 효과를 보다 구체적으로 설명하도록 한다. 그러나 아래 실시예 및 실험예는 본 발명에 대한 이해를 돕기 위해 예시의 목적으로만 제공된 것일 뿐 본 발명의 범주 및 범위가 그에 의해 제한되는 것은 아니다.
Hereinafter, the composition and effects of the present invention will be described in more detail by confirming the effect of the
실시예Example
1: 펩티드의 합성 1: Synthesis of peptides
본 명세서에 개시된 펩티드들은 종래에 알려진 고상 펩티드 합성법에 따라 제조하였다. 구체적으로, 펩티드들은 ASP48S(Peptron, Inc., 대한민국 대전)를 이용하여 Fmoc 고상 합성법(solid phase peptide synthesis, SPPS)을 통해 C-말단부터 아미노산 하나씩 커플링함으로써 합성하였다. 다음과 같이, 펩티드들의 C-말단의 첫번째 아미노산이 수지에 부착된 것을 사용하였다. 예컨대 다음과 같다:The peptides disclosed herein were prepared according to a conventionally known solid-phase peptide synthesis method. Specifically, peptides were synthesized by coupling amino acids one by one from the C-terminal through Fmoc solid phase peptide synthesis (SPPS) using ASP48S (Peptron, Inc., Daejeon, Korea). As follows, the first amino acid at the C-terminal of the peptides was used. For example:
NH2-Lys(Boc)-2-chloro-Trityl ResinNH 2 -Lys (Boc) -2-chloro-Trityl Resin
NH2-Ala-2-chloro-Trityl ResinNH 2 -Ala-2-chloro-Trityl Resin
NH2-Arg(Pbf)-2-chloro-Trityl Resin
NH 2 -Arg (Pbf) -2-chloro-Trityl Resin
펩타이드 합성에 사용한 모든 아미노산 원료는 N-term이 Fmoc으로 보호(protection)되고, 잔기는 모두 산에서 제거되는 Trt, Boc, t-Bu (t-butylester), Pbf (2,2,4,6,7-pentamethyl dihydro-benzofuran-5-sulfonyl) 등으로 보호된 것을 사용하였다. 예컨대 다음과 같다: All amino acid raw materials used for peptide synthesis are Trt, Boc, t-Bu (t-butylester), Pbf (2,2,4,6, where N-term is protected by Fmoc and all residues are removed from the acid. 7-pentamethyl dihydro-benzofuran-5-sulfonyl). For example:
Fmoc-Ala-OH, Fmoc-Arg(Pbf)-OH, Fmoc-Glu(OtBu)-OH, Fmoc-Pro-OH, Fmoc-Leu-OH, Fmoc-Ile-OH, Fmoc-Phe-OH, Fmoc-Ser(tBu)-OH, Fmoc-Thr(tBu)-OH, Fmoc-Lys(Boc)-OH, Fmoc-Gln(Trt)-OH, Fmoc-Trp(Boc)-OH, Fmoc-Met-OH, Fmoc-Asn(Trt)-OH, Fmoc-Tyr(tBu)-OH, Fmoc-Ahx-OH, Trt-Mercaptoacetic acid.Fmoc-Ala-OH, Fmoc-Arg (Pbf) -OH, Fmoc-Glu (OtBu) -OH, Fmoc-Pro-OH, Fmoc-Leu-OH, Fmoc-Ile-OH, Fmoc-Phe-OH, Fmoc- Ser (tBu) -OH, Fmoc-Thr (tBu) -OH, Fmoc-Lys (Boc) -OH, Fmoc-Gln (Trt) -OH, Fmoc-Trp (Boc) -OH, Fmoc-Met-OH, Fmoc -Asn (Trt) -OH, Fmoc-Tyr (tBu) -OH, Fmoc-Ahx-OH, Trt-Mercaptoacetic acid.
커플링 시약(Coupling reagent)으로는 HBTU[2-(1H-Benzotriazole-1-yl)-1,1,3,3-tetamethylaminium hexafluorophosphate] / HOBt [N-Hydroxxybenzotriazole] /NMM [4-Methylmorpholine] 를 사용하였다. Fmoc 제거는 20%의 DMF 중 피페리딘(piperidine in DMF)을 이용하였다. 합성된 펩타이드를 Resin에서 분리 및 잔기의 보호기 제거에는 절단 칵테일(Cleavage Cocktail) [TFA (trifluoroacetic acid) /TIS (triisopropylsilane) / EDT (ethanedithiol) / H2O=92.5/2.5/2.5/2.5] 를 사용하였다.HBTU [2- (1H-Benzotriazole-1-yl) -1,1,3,3-tetamethylaminium hexafluorophosphate] / HOBt [N-Hydroxxybenzotriazole] / NMM [4-Methylmorpholine] is used as the coupling reagent. Did. Fmoc removal was performed using piperidine in DMF in 20% of DMF. Cleavage Cocktail [TFA (trifluoroacetic acid) / TIS (triisopropylsilane) / EDT (ethanedithiol) / H 2 O = 92.5 / 2.5 / 2.5 / 2.5] is used for separating the synthesized peptide from Resin and removing the protecting group of the residue. Did.
아미노산 보호기가 결합된 출발 아미노산이 고상 지지체에 결합되어 있는 상태를 이용하여 여기에 해당 아미노산들을 각각 반응시키고 용매로 세척한 후 탈보호하는 과정을 반복함으로써 각 펩티드를 합성하였다. 합성된 펩티드를 수지로부터 끊어낸 후 HPLC로 정제하고, 합성 여부를 MS로 확인하고 동결 건조하였다.
Each peptide was synthesized by reacting the corresponding amino acids therein, washing with a solvent, and repeating the deprotection process using the state in which the amino acid protecting group-bound starting amino acid is bound to the solid support. The synthesized peptide was removed from the resin and then purified by HPLC. Synthesis was confirmed by MS and lyophilized.
서열번호 1의 Pep 1을 예로 들어 구체적인 과정을 설명하면 다음과 같다.
The specific process will be described using
1) 커플링 1) Coupling
NH2-Lys(Boc)-2-chloro-Trityl Resin 에 보호된 아미노산(8당량)와 커플링 시약 HBTU(8당량)/HOBt(8당량)/NMM(16당량) 을 DMF에 녹여서 첨가한 후, 상온에서 2시간 동안 반응하고 DMF, MeOH, DMF순으로 세척하였다.NH 2 -Lys (Boc) -2-chloro-Trityl Resin protected amino acid (8 eq) and coupling reagent HBTU (8 eq) / HOBt (8 eq) / NMM (16 eq) dissolved in DMF and added , Reacted at room temperature for 2 hours, washed with DMF, MeOH, and DMF.
2) Fmoc 탈보호 2) Fmoc deprotection
20%의 DMF 중의 피페리딘(piperidine in DMF) 을 가하고 상온에서 5분 간 2회 반응하고 DMF, MeOH, DMF순으로 세척하였다.Piperidine in DMF was added in 20% of DMF, reacted twice at room temperature for 5 minutes, and washed in the order of DMF, MeOH, and DMF.
3) 1과 2의 반응을 반복적으로 하여 펩타이드 기본 골격 NH2-E(OtBu)-A-R(Pbf)-P-A-L-L-T(tBu)-S(tBu)-R(Pbf)L-R(Pbf)-F-I-P-K(Boc)-2-chloro-Trityl Resin)을 만들었다. 3) The reaction of 1 and 2 is repeated to the peptide base skeleton NH 2 -E (OtBu) -AR (Pbf) -PALLT (tBu) -S (tBu) -R (Pbf) LR (Pbf) -FIPK (Boc) -2-chloro-Trityl Resin).
4) 절단(Cleavagge): 합성이 완료된 펩타이드 Resin에 절단 칵테일(Cleavage Cocktail) 을 가하여 펩타이드를 Resin에서 분리하였다.4) Cleavagge: Cleavage Cocktail was added to the synthesized peptide Resin to separate the peptide from Resin.
5) 얻어진 mixture에 Cooling diethyl ether를 가한 후, 원심 분리하여 얻어진 펩타이드를 침전시킨다.5) After adding cooling diethyl ether to the obtained mixture, the obtained peptide is precipitated by centrifugation.
6) Prep-HPLC로 정제 후, LC/MS로 분자량을 확인하고 동결하여 powder로 제조하였다.
6) After purification by Prep-HPLC, molecular weight was confirmed by LC / MS and frozen to prepare powder.
실시예Example
2: 서열번호 1의 펩티드( 2: Peptide of SEQ ID NO: 1
Pep1Pep1
)의 자외선에 의한 세포 독성 완화 효과 실험) To test the effect of alleviating cytotoxicity by ultraviolet rays
1)세포배양1) Cell culture
인간 진피 섬유아세포(human dermal fibroblast)를 Gibco로부터 구입하였다. 구입한 인간 진피 섬유아세포를 Medium 106 배지에서 LSGS(Low Serum Growth Supplement)를 첨가하여 37℃, 5% CO2 조건하에서 배양하고 트립신처리법(Trypsinization)으로 계대 배양하여 3~5세대 세포를 얻었다.
Human dermal fibroblasts were purchased from Gibco. The purchased human dermal fibroblasts were cultured under Medium 5 medium by adding Low Serum Growth Supplement (LSGS) at 37 ° C. under 5% CO 2 conditions and subcultured by trypsinization to obtain 3-5th generation cells.
2)UVA 조사에 의한 세포독성 완화 효과2) Effect of alleviating cytotoxicity by UVA irradiation
상기와 같이 배양한 인간 진피 섬유아세포를 96-well plate에 1 ⅹ 104/well을 넣고 16~18시간 동안 배양하였다. UVA 조사 전에 배양배지를 제거한 후 인산염완충용액(PBS)로 세척한 후에 4.5 J/㎠ UVA를 조사하였다. UVA 조사 후에 serum을 첨가하지 않은 Medium 106 배지에 본 발명의 일측면에 따른 서열번호 1의 펩티드(Pep1)를 농도별(10, 100, 500 ㎍/㎖)로 처리하여 24시간 배양하였다.Human dermal fibroblasts cultured as above were put in 1 ⅹ 10 4 / well in a 96-well plate and cultured for 16-18 hours. After the culture medium was removed before UVA irradiation, 4.5 J / cm 2 UVA was irradiated after washing with a phosphate buffer solution (PBS). After UVA irradiation, the peptide (Pep1) of SEQ ID NO: 1 according to one aspect of the present invention was treated with medium (10, 100, 500 µg / ml) according to one aspect of the present invention without serum, and cultured for 24 hours.
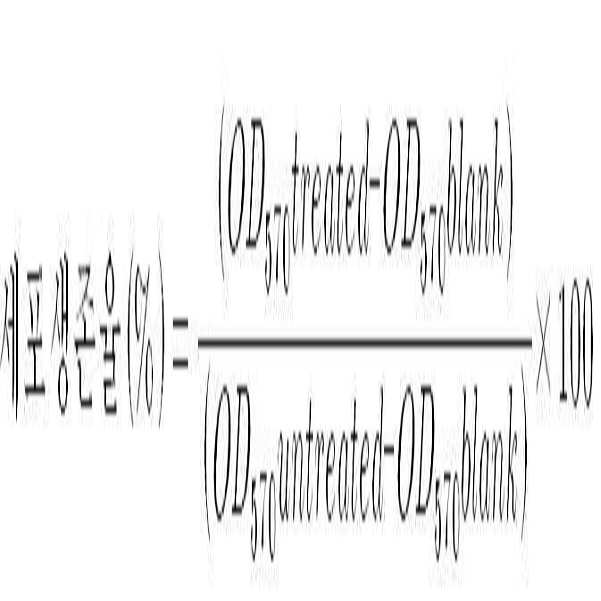
24시간이 경과한 후에 MTT 용액(3-(4,5-Dimethylthiazol-2-yl)-2,5-diphenyltetrazoliumbromide; 5 ㎎/㎖)를 10 ㎕ 첨가하고 2시간 동안 37℃, 5% CO2 조건하에서 배양하였다. 배지를 제거하고 DMSO(dimethylsulfoxide)를 100 ㎕를 넣고 상온에서 10분간 흔들어준 다음, 570 nm에서 마이크로 플레이트 판독기를 사용하여 흡광도를 측정하였다. 측정된 흡광도를 통하여 세포의 생존율을 계산한 결과를 도 1에 나타내었다. 이때 세포의 생존율은 하기 수학식 1에 의하여 계산하였다.After 24 hours, 10 μl of the MTT solution (3- (4,5-Dimethylthiazol-2-yl) -2,5-diphenyltetrazoliumbromide; 5 mg / ml) was added and 37 ° C and 5% CO 2 conditions for 2 hours Cultured under. The medium was removed, 100 μl of DMSO (dimethylsulfoxide) was added, shaken at room temperature for 10 minutes, and absorbance was measured using a microplate reader at 570 nm. The results of calculating the survival rate of cells through the measured absorbance are shown in FIG. 1. At this time, the survival rate of the cells was calculated by
Blank: 세포 배양 배지만을 발색반응한 웰의 570nm 흡광도Blank: Absorbance at 570 nm of wells that developed only the cell culture medium
treated: 시료(Pep1)를 처리한 웰을 발색 반응한 웰의 570nm 흡광도treated : 570nm absorbance of the wells that developed and reacted the wells treated with the sample (Pep1)
untreated: 시료(Pep1)를 처리하지 않은 웰을 발색 반응한 웰의 570nm 흡광도
untreated: 570nm absorbance of the wells that developed and reacted wells not treated with the sample (Pep1)
도 1에 나타난 바와 같이, 자외선 조사 후 세포의 생존율은 자외선을 조사하지 않고, 본 발명의 일측면에 따른 서열번호 1의 펩티드(Pep1)도 첨가하지 않았을 때를 100%로 할 때, 자외선 조사시에는 80%로 감소한 것으로 나타났다. 또한, 자외선 조사 후 서열번호 1의 펩티드를 10, 100, 500 ㎍/㎖의 농도로 첨가한 경우 세포의 생존율이 농도가 증가함에 따라 증가하는 것으로 나타났으며, 특히 펩티드를 100 ㎍/㎖의 농도로 첨가한 경우 세포의 생존율이 거의 100%로 나타났고, 펩티드를 500 ㎍/㎖의 농도로 첨가한 경우에는 세포의 생존율이 자외선을 조사하지 않은 경우보다 더 높게 나타났다. 이는 본 발명의 일측면에 따른 펩티드가 자외선 조사에 의해 발생하는 세포 독성을 완화시킴으로써 세포의 생존율도 그에 따라 증가한 것임을 의미한다. 따라서, 이를 통하여 본 발명의 일측면에 따른 펩티드에 의하면 자외선에 의한 피부의 손상을 예방하거나 이를 치료할 수 있음을 알 수 있다.
As shown in Figure 1, when the survival rate of the cells after irradiation with ultraviolet light is not irradiated with ultraviolet light, and when the peptide of SEQ ID NO: 1 according to an aspect of the present invention is not added to 100%, when irradiated with ultraviolet light There was a decrease of 80%. In addition, when the peptide of SEQ ID NO: 1 was added at a concentration of 10, 100, 500 µg / ml after UV irradiation, it was found that the survival rate of the cells increased as the concentration increased, and in particular, the concentration of the peptide was 100 µg / ml. When added as, the survival rate of the cells was almost 100%, and when the peptide was added at a concentration of 500 µg / ml, the survival rate of the cells was higher than that without irradiation with ultraviolet rays. This means that the survival rate of cells is increased accordingly by alleviating the cytotoxicity caused by ultraviolet irradiation of the peptide according to one aspect of the present invention. Therefore, it can be seen through this that the peptide according to one aspect of the present invention can prevent or treat skin damage caused by ultraviolet rays.
실시예Example
3: 서열번호 1의 펩티드( 3: Peptide of SEQ ID NO: 1
Pep1Pep1
)의 자외선 조사에 의한 염증성 사이토카인 발현 억제 효과 실험) Inhibitory effect of inflammatory cytokine expression by ultraviolet irradiation
1)세포배양1) Cell culture
정상 인간 상피 각질형성세포(normal human epidermal keratinocyte)를 Gibco로부터 구입하였다. 구입한 정상 인간 상피 각질형성세포를 Keratinocyte-SFM 배지에 BPE(Bovine Pituitary Extract)와 EGF (Epidermal Growth Factor, Human Recombinant)를 첨가하여 37℃, 5% CO2 조건하에서 배양하고 트립신처리법(Trypsinization)으로 계대 배양하여 3~5세대 세포를 얻었다.
Normal human epidermal keratinocytes were purchased from Gibco. The purchased normal human epithelial keratinocytes were added to Keratinocyte-SFM medium by adding Bovine Pituitary Extract (BPE) and EGF (Epidermal Growth Factor, Human Recombinant), and cultured under 37 ° C and 5% CO 2 conditions, followed by trypsinization. Passage cultures yielded 3 to 5 generation cells.
2)UVB 조사에 의한 염증성 사이토카인 억제 효과2) Inhibitory effect of inflammatory cytokines by UVB irradiation
상기와 같이 배양한 인간 상피 각질형성세포를 12-well plate에 2 ⅹ 105/well을 넣고 16~18시간 동안 배양하였다. UVB 조사 전에 배양배지를 제거한 후 인산염완충용액(PBS)로 세척한 후에 25 mJ/㎠ UVB를 조사하였다. UVB 조사 후에 BPE(Bovine Pituitary Extract)와 EGF (Epidermal Growth Factor, Human Recombinant)를 첨가하지 않은 Keratinocyte-SFM 배지에 본 발명의 일측면에 따른 서열번호 1의 펩티드(Pep1)를 농도별(1, 10, 100, 500, 1000 ㎍/㎖)로 처리하여 24시간 배양하였다.The human epithelial keratinocytes cultured as above were put in a 2 ⅹ 10 5 / well in a 12-well plate and cultured for 16-18 hours. After removing the culture medium before UVB irradiation, 25 mJ / cm 2 UVB was irradiated after washing with a phosphate buffer solution (PBS). After UVB irradiation, BPE (Bovine Pituitary Extract) and EGF (Epidermal Growth Factor, Human Recombinant) are not added to the Keratinocyte-SFM medium according to one aspect of the present invention. , 100, 500, 1000 μg / ml) and cultured for 24 hours.
24시간이 경과한 후에 배양 상층액을 수거하여 IL-1α, IL-6 및 TNF-α를 정량화하여 염증성 사이토카인 발현억제효과를 판단하였다. 염증성 사이토카인의 양은 ELISA를 이용하여 정량화하였으며, 염증성 사이토카인의 생성율은 수학식 2에 의해 계산하였다.
After 24 hours, the culture supernatant was collected to quantify IL-1α, IL-6, and TNF-α to determine the inhibitory effect of inflammatory cytokine expression. The amount of inflammatory cytokines was quantified using ELISA, and the production rate of inflammatory cytokines was calculated by Equation 2.
B0: 자외선을 조사하지 않고 시료(Pep1)를 처리하지 않은 웰의 염증성 사이토카인 생성량B0: Inflammatory cytokine production in wells that did not irradiate with ultraviolet light and did not process the sample (Pep1)
Bt: 자외선을 조사하고 시료(Pep1)를 처리하지 않은 웰의 염증성 사이토카인 생성량Bt: Inflammatory cytokine production in wells that were not irradiated with ultraviolet light and treated with the sample (Pep1)
St: 자외선을 조사하고 시료(Pep1)을 처리한 웰의 염증성 사이토카인 생성량
St: Inflammatory cytokine production in wells treated with UV and sample (Pep1)
도 2에 나타난 바와 같이, 자외선 B 조사 후 서열번호 1의 펩티드(Pep1)을 농도별로 첨가하였을 경우에 IL-1α는 38.1%, 32.9%, 27.2%. 12.1%, 30.7% 억제하였고, IL-6는 55.6%, 51.6%, 34.4%, 33.5%, 36.8%를 억제하였으며, 또한 TNF-α는 20.7%, 20.3%, 16.1%, 20.4%, 32.4%를 억제하였다. 이러한 결과들은 낮은 펩티드(Pep1) 처리 농도에서도 자외선에 의한 염증 발생을 효과적으로 방어함을 알 수 있다.As shown in FIG. 2, IL-1α was 38.1%, 32.9%, and 27.2% when peptide (Pep1) of SEQ ID NO: 1 was added by concentration after irradiation with ultraviolet B. 12.1%, 30.7%, IL-6 inhibited 55.6%, 51.6%, 34.4%, 33.5%, 36.8%, and TNF-α was 20.7%, 20.3%, 16.1%, 20.4%, 32.4%. Suppressed. It can be seen that these results effectively prevent the occurrence of inflammation caused by ultraviolet rays even at a low concentration of peptide (Pep1) treatment.
따라서, 이를 통하여 본 발명의 일측면에 따른 펩티드에 의하면 자외선에 의한 염증 반응을 억제하여 피부의 손상을 예방하거나 이를 치료할 수 있음을 알 수 있다.Accordingly, it can be seen that according to the peptide according to one aspect of the present invention, it is possible to prevent or treat skin damage by suppressing an inflammatory reaction caused by ultraviolet rays.
<110> KAEL-GemVax Co.,Ltd. KIM, SANGJAE <120> Composition for preventing or treating skin damages caused by ultraviolet rays <130> 13P540IND <150> KR 10-2012-0145501 <151> 2012-12-13 <160> 2 <170> KopatentIn 2.0 <210> 1 <211> 16 <212> PRT <213> Homo sapiens <400> 1 Glu Ala Arg Pro Ala Leu Leu Thr Ser Arg Leu Arg Phe Ile Pro Lys 1 5 10 15 <210> 2 <211> 1132 <212> PRT <213> Homo sapiens <400> 2 Met Pro Arg Ala Pro Arg Cys Arg Ala Val Arg Ser Leu Leu Arg Ser 1 5 10 15 His Tyr Arg Glu Val Leu Pro Leu Ala Thr Phe Val Arg Arg Leu Gly 20 25 30 Pro Gln Gly Trp Arg Leu Val Gln Arg Gly Asp Pro Ala Ala Phe Arg 35 40 45 Ala Leu Val Ala Gln Cys Leu Val Cys Val Pro Trp Asp Ala Arg Pro 50 55 60 Pro Pro Ala Ala Pro Ser Phe Arg Gln Val Ser Cys Leu Lys Glu Leu 65 70 75 80 Val Ala Arg Val Leu Gln Arg Leu Cys Glu Arg Gly Ala Lys Asn Val 85 90 95 Leu Ala Phe Gly Phe Ala Leu Leu Asp Gly Ala Arg Gly Gly Pro Pro 100 105 110 Glu Ala Phe Thr Thr Ser Val Arg Ser Tyr Leu Pro Asn Thr Val Thr 115 120 125 Asp Ala Leu Arg Gly Ser Gly Ala Trp Gly Leu Leu Leu Arg Arg Val 130 135 140 Gly Asp Asp Val Leu Val His Leu Leu Ala Arg Cys Ala Leu Phe Val 145 150 155 160 Leu Val Ala Pro Ser Cys Ala Tyr Gln Val Cys Gly Pro Pro Leu Tyr 165 170 175 Gln Leu Gly Ala Ala Thr Gln Ala Arg Pro Pro Pro His Ala Ser Gly 180 185 190 Pro Arg Arg Arg Leu Gly Cys Glu Arg Ala Trp Asn His Ser Val Arg 195 200 205 Glu Ala Gly Val Pro Leu Gly Leu Pro Ala Pro Gly Ala Arg Arg Arg 210 215 220 Gly Gly Ser Ala Ser Arg Ser Leu Pro Leu Pro Lys Arg Pro Arg Arg 225 230 235 240 Gly Ala Ala Pro Glu Pro Glu Arg Thr Pro Val Gly Gln Gly Ser Trp 245 250 255 Ala His Pro Gly Arg Thr Arg Gly Pro Ser Asp Arg Gly Phe Cys Val 260 265 270 Val Ser Pro Ala Arg Pro Ala Glu Glu Ala Thr Ser Leu Glu Gly Ala 275 280 285 Leu Ser Gly Thr Arg His Ser His Pro Ser Val Gly Arg Gln His His 290 295 300 Ala Gly Pro Pro Ser Thr Ser Arg Pro Pro Arg Pro Trp Asp Thr Pro 305 310 315 320 Cys Pro Pro Val Tyr Ala Glu Thr Lys His Phe Leu Tyr Ser Ser Gly 325 330 335 Asp Lys Glu Gln Leu Arg Pro Ser Phe Leu Leu Ser Ser Leu Arg Pro 340 345 350 Ser Leu Thr Gly Ala Arg Arg Leu Val Glu Thr Ile Phe Leu Gly Ser 355 360 365 Arg Pro Trp Met Pro Gly Thr Pro Arg Arg Leu Pro Arg Leu Pro Gln 370 375 380 Arg Tyr Trp Gln Met Arg Pro Leu Phe Leu Glu Leu Leu Gly Asn His 385 390 395 400 Ala Gln Cys Pro Tyr Gly Val Leu Leu Lys Thr His Cys Pro Leu Arg 405 410 415 Ala Ala Val Thr Pro Ala Ala Gly Val Cys Ala Arg Glu Lys Pro Gln 420 425 430 Gly Ser Val Ala Ala Pro Glu Glu Glu Asp Thr Asp Pro Arg Arg Leu 435 440 445 Val Gln Leu Leu Arg Gln His Ser Ser Pro Trp Gln Val Tyr Gly Phe 450 455 460 Val Arg Ala Cys Leu Arg Arg Leu Val Pro Pro Gly Leu Trp Gly Ser 465 470 475 480 Arg His Asn Glu Arg Arg Phe Leu Arg Asn Thr Lys Lys Phe Ile Ser 485 490 495 Leu Gly Lys His Ala Lys Leu Ser Leu Gln Glu Leu Thr Trp Lys Met 500 505 510 Ser Val Arg Asp Cys Ala Trp Leu Arg Arg Ser Pro Gly Val Gly Cys 515 520 525 Val Pro Ala Ala Glu His Arg Leu Arg Glu Glu Ile Leu Ala Lys Phe 530 535 540 Leu His Trp Leu Met Ser Val Tyr Val Val Glu Leu Leu Arg Ser Phe 545 550 555 560 Phe Tyr Val Thr Glu Thr Thr Phe Gln Lys Asn Arg Leu Phe Phe Tyr 565 570 575 Arg Lys Ser Val Trp Ser Lys Leu Gln Ser Ile Gly Ile Arg Gln His 580 585 590 Leu Lys Arg Val Gln Leu Arg Glu Leu Ser Glu Ala Glu Val Arg Gln 595 600 605 His Arg Glu Ala Arg Pro Ala Leu Leu Thr Ser Arg Leu Arg Phe Ile 610 615 620 Pro Lys Pro Asp Gly Leu Arg Pro Ile Val Asn Met Asp Tyr Val Val 625 630 635 640 Gly Ala Arg Thr Phe Arg Arg Glu Lys Arg Ala Glu Arg Leu Thr Ser 645 650 655 Arg Val Lys Ala Leu Phe Ser Val Leu Asn Tyr Glu Arg Ala Arg Arg 660 665 670 Pro Gly Leu Leu Gly Ala Ser Val Leu Gly Leu Asp Asp Ile His Arg 675 680 685 Ala Trp Arg Thr Phe Val Leu Arg Val Arg Ala Gln Asp Pro Pro Pro 690 695 700 Glu Leu Tyr Phe Val Lys Val Asp Val Thr Gly Ala Tyr Asp Thr Ile 705 710 715 720 Pro Gln Asp Arg Leu Thr Glu Val Ile Ala Ser Ile Ile Lys Pro Gln 725 730 735 Asn Thr Tyr Cys Val Arg Arg Tyr Ala Val Val Gln Lys Ala Ala His 740 745 750 Gly His Val Arg Lys Ala Phe Lys Ser His Val Ser Thr Leu Thr Asp 755 760 765 Leu Gln Pro Tyr Met Arg Gln Phe Val Ala His Leu Gln Glu Thr Ser 770 775 780 Pro Leu Arg Asp Ala Val Val Ile Glu Gln Ser Ser Ser Leu Asn Glu 785 790 795 800 Ala Ser Ser Gly Leu Phe Asp Val Phe Leu Arg Phe Met Cys His His 805 810 815 Ala Val Arg Ile Arg Gly Lys Ser Tyr Val Gln Cys Gln Gly Ile Pro 820 825 830 Gln Gly Ser Ile Leu Ser Thr Leu Leu Cys Ser Leu Cys Tyr Gly Asp 835 840 845 Met Glu Asn Lys Leu Phe Ala Gly Ile Arg Arg Asp Gly Leu Leu Leu 850 855 860 Arg Leu Val Asp Asp Phe Leu Leu Val Thr Pro His Leu Thr His Ala 865 870 875 880 Lys Thr Phe Leu Arg Thr Leu Val Arg Gly Val Pro Glu Tyr Gly Cys 885 890 895 Val Val Asn Leu Arg Lys Thr Val Val Asn Phe Pro Val Glu Asp Glu 900 905 910 Ala Leu Gly Gly Thr Ala Phe Val Gln Met Pro Ala His Gly Leu Phe 915 920 925 Pro Trp Cys Gly Leu Leu Leu Asp Thr Arg Thr Leu Glu Val Gln Ser 930 935 940 Asp Tyr Ser Ser Tyr Ala Arg Thr Ser Ile Arg Ala Ser Leu Thr Phe 945 950 955 960 Asn Arg Gly Phe Lys Ala Gly Arg Asn Met Arg Arg Lys Leu Phe Gly 965 970 975 Val Leu Arg Leu Lys Cys His Ser Leu Phe Leu Asp Leu Gln Val Asn 980 985 990 Ser Leu Gln Thr Val Cys Thr Asn Ile Tyr Lys Ile Leu Leu Leu Gln 995 1000 1005 Ala Tyr Arg Phe His Ala Cys Val Leu Gln Leu Pro Phe His Gln Gln 1010 1015 1020 Val Trp Lys Asn Pro Thr Phe Phe Leu Arg Val Ile Ser Asp Thr Ala 1025 1030 1035 1040 Ser Leu Cys Tyr Ser Ile Leu Lys Ala Lys Asn Ala Gly Met Ser Leu 1045 1050 1055 Gly Ala Lys Gly Ala Ala Gly Pro Leu Pro Ser Glu Ala Val Gln Trp 1060 1065 1070 Leu Cys His Gln Ala Phe Leu Leu Lys Leu Thr Arg His Arg Val Thr 1075 1080 1085 Tyr Val Pro Leu Leu Gly Ser Leu Arg Thr Ala Gln Thr Gln Leu Ser 1090 1095 1100 Arg Lys Leu Pro Gly Thr Thr Leu Thr Ala Leu Glu Ala Ala Ala Asn 1105 1110 1115 1120 Pro Ala Leu Pro Ser Asp Phe Lys Thr Ile Leu Asp 1125 1130 <110> KAEL-GemVax Co., Ltd. KIM, SANGJAE <120> Composition for preventing or treating skin damages caused by ultraviolet rays <130> 13P540IND <150> KR 10-2012-0145501 <151> 2012-12-13 <160> 2 <170> KopatentIn 2.0 <210> 1 <211> 16 <212> PRT <213> Homo sapiens <400> 1 Glu Ala Arg Pro Ala Leu Leu Thr Ser Arg Leu Arg Phe Ile Pro Lys 1 5 10 15 <210> 2 <211> 1132 <212> PRT <213> Homo sapiens <400> 2 Met Pro Arg Ala Pro Arg Cys Arg Ala Val Arg Ser Leu Leu Arg Ser 1 5 10 15 His Tyr Arg Glu Val Leu Pro Leu Ala Thr Phe Val Arg Arg Leu Gly 20 25 30 Pro Gln Gly Trp Arg Leu Val Gln Arg Gly Asp Pro Ala Ala Phe Arg 35 40 45 Ala Leu Val Ala Gln Cys Leu Val Cys Val Pro Trp Asp Ala Arg Pro 50 55 60 Pro Pro Ala Ala Pro Ser Phe Arg Gln Val Ser Cys Leu Lys Glu Leu 65 70 75 80 Val Ala Arg Val Leu Gln Arg Leu Cys Glu Arg Gly Ala Lys Asn Val 85 90 95 Leu Ala Phe Gly Phe Ala Leu Leu Asp Gly Ala Arg Gly Gly Pro Pro 100 105 110 Glu Ala Phe Thr Thr Ser Val Arg Ser Tyr Leu Pro Asn Thr Val Thr 115 120 125 Asp Ala Leu Arg Gly Ser Gly Ala Trp Gly Leu Leu Leu Arg Arg Val 130 135 140 Gly Asp Asp Val Leu Val His Leu Leu Ala Arg Cys Ala Leu Phe Val 145 150 155 160 Leu Val Ala Pro Ser Cys Ala Tyr Gln Val Cys Gly Pro Pro Leu Tyr 165 170 175 Gln Leu Gly Ala Ala Thr Gln Ala Arg Pro Pro Pro His Ala Ser Gly 180 185 190 Pro Arg Arg Arg Leu Gly Cys Glu Arg Ala Trp Asn His Ser Val Arg 195 200 205 Glu Ala Gly Val Pro Leu Gly Leu Pro Ala Pro Gly Ala Arg Arg Arg 210 215 220 Gly Gly Ser Ala Ser Arg Ser Leu Pro Leu Pro Lys Arg Pro Arg Arg 225 230 235 240 Gly Ala Ala Pro Glu Pro Glu Arg Thr Pro Val Gly Gln Gly Ser Trp 245 250 255 Ala His Pro Gly Arg Thr Arg Gly Pro Ser Asp Arg Gly Phe Cys Val 260 265 270 Val Ser Pro Ala Arg Pro Ala Glu Glu Ala Thr Ser Leu Glu Gly Ala 275 280 285 Leu Ser Gly Thr Arg His Ser His Pro Ser Val Gly Arg Gln His His 290 295 300 Ala Gly Pro Pro Ser Thr Ser Arg Pro Pro Arg Pro Trp Asp Thr Pro 305 310 315 320 Cys Pro Pro Val Tyr Ala Glu Thr Lys His Phe Leu Tyr Ser Ser Gly 325 330 335 Asp Lys Glu Gln Leu Arg Pro Ser Phe Leu Leu Ser Ser Leu Arg Pro 340 345 350 Ser Leu Thr Gly Ala Arg Arg Leu Val Glu Thr Ile Phe Leu Gly Ser 355 360 365 Arg Pro Trp Met Pro Gly Thr Pro Arg Arg Leu Pro Arg Leu Pro Gln 370 375 380 Arg Tyr Trp Gln Met Arg Pro Leu Phe Leu Glu Leu Leu Gly Asn His 385 390 395 400 Ala Gln Cys Pro Tyr Gly Val Leu Leu Lys Thr His Cys Pro Leu Arg 405 410 415 Ala Ala Val Thr Pro Ala Ala Gly Val Cys Ala Arg Glu Lys Pro Gln 420 425 430 Gly Ser Val Ala Ala Pro Glu Glu Glu Asp Thr Asp Pro Arg Arg Leu 435 440 445 Val Gln Leu Leu Arg Gln His Ser Ser Pro Trp Gln Val Tyr Gly Phe 450 455 460 Val Arg Ala Cys Leu Arg Arg Leu Val Pro Pro Gly Leu Trp Gly Ser 465 470 475 480 Arg His Asn Glu Arg Arg Phe Leu Arg Asn Thr Lys Lys Phe Ile Ser 485 490 495 Leu Gly Lys His Ala Lys Leu Ser Leu Gln Glu Leu Thr Trp Lys Met 500 505 510 Ser Val Arg Asp Cys Ala Trp Leu Arg Arg Ser Pro Gly Val Gly Cys 515 520 525 Val Pro Ala Ala Glu His Arg Leu Arg Glu Glu Ile Leu Ala Lys Phe 530 535 540 Leu His Trp Leu Met Ser Val Tyr Val Val Glu Leu Leu Arg Ser Phe 545 550 555 560 Phe Tyr Val Thr Glu Thr Thr Phe Gln Lys Asn Arg Leu Phe Phe Tyr 565 570 575 Arg Lys Ser Val Trp Ser Lys Leu Gln Ser Ile Gly Ile Arg Gln His 580 585 590 Leu Lys Arg Val Gln Leu Arg Glu Leu Ser Glu Ala Glu Val Arg Gln 595 600 605 His Arg Glu Ala Arg Pro Ala Leu Leu Thr Ser Arg Leu Arg Phe Ile 610 615 620 Pro Lys Pro Asp Gly Leu Arg Pro Ile Val Asn Met Asp Tyr Val Val 625 630 635 640 Gly Ala Arg Thr Phe Arg Arg Glu Lys Arg Ala Glu Arg Leu Thr Ser 645 650 655 Arg Val Lys Ala Leu Phe Ser Val Leu Asn Tyr Glu Arg Ala Arg Arg 660 665 670 Pro Gly Leu Leu Gly Ala Ser Val Leu Gly Leu Asp Asp Ile His Arg 675 680 685 Ala Trp Arg Thr Phe Val Leu Arg Val Arg Ala Gln Asp Pro Pro Pro 690 695 700 Glu Leu Tyr Phe Val Lys Val Asp Val Thr Gly Ala Tyr Asp Thr Ile 705 710 715 720 Pro Gln Asp Arg Leu Thr Glu Val Ile Ala Ser Ile Ile Lys Pro Gln 725 730 735 Asn Thr Tyr Cys Val Arg Arg Tyr Ala Val Val Gln Lys Ala Ala His 740 745 750 Gly His Val Arg Lys Ala Phe Lys Ser His Val Ser Thr Leu Thr Asp 755 760 765 Leu Gln Pro Tyr Met Arg Gln Phe Val Ala His Leu Gln Glu Thr Ser 770 775 780 Pro Leu Arg Asp Ala Val Val Ile Glu Gln Ser Ser Ser Leu Asn Glu 785 790 795 800 Ala Ser Ser Gly Leu Phe Asp Val Phe Leu Arg Phe Met Cys His His 805 810 815 Ala Val Arg Ile Arg Gly Lys Ser Tyr Val Gln Cys Gln Gly Ile Pro 820 825 830 Gln Gly Ser Ile Leu Ser Thr Leu Leu Cys Ser Leu Cys Tyr Gly Asp 835 840 845 Met Glu Asn Lys Leu Phe Ala Gly Ile Arg Arg Asp Gly Leu Leu Leu 850 855 860 Arg Leu Val Asp Asp Phe Leu Leu Val Thr Pro His Leu Thr His Ala 865 870 875 880 Lys Thr Phe Leu Arg Thr Leu Val Arg Gly Val Pro Glu Tyr Gly Cys 885 890 895 Val Val Asn Leu Arg Lys Thr Val Val Asn Phe Pro Val Glu Asp Glu 900 905 910 Ala Leu Gly Gly Thr Ala Phe Val Gln Met Pro Ala His Gly Leu Phe 915 920 925 Pro Trp Cys Gly Leu Leu Leu Asp Thr Arg Thr Leu Glu Val Gln Ser 930 935 940 Asp Tyr Ser Ser Tyr Ala Arg Thr Ser Ile Arg Ala Ser Leu Thr Phe 945 950 955 960 Asn Arg Gly Phe Lys Ala Gly Arg Asn Met Arg Arg Lys Leu Phe Gly 965 970 975 Val Leu Arg Leu Lys Cys His Ser Leu Phe Leu Asp Leu Gln Val Asn 980 985 990 Ser Leu Gln Thr Val Cys Thr Asn Ile Tyr Lys Ile Leu Leu Leu Gln 995 1000 1005 Ala Tyr Arg Phe His Ala Cys Val Leu Gln Leu Pro Phe His Gln Gln 1010 1015 1020 Val Trp Lys Asn Pro Thr Phe Phe Leu Arg Val Ile Ser Asp Thr Ala 1025 1030 1035 1040 Ser Leu Cys Tyr Ser Ile Leu Lys Ala Lys Asn Ala Gly Met Ser Leu 1045 1050 1055 Gly Ala Lys Gly Ala Ala Gly Pro Leu Pro Ser Glu Ala Val Gln Trp 1060 1065 1070 Leu Cys His Gln Ala Phe Leu Leu Lys Leu Thr Arg His Arg Val Thr 1075 1080 1085 Tyr Val Pro Leu Leu Gly Ser Leu Arg Thr Ala Gln Thr Gln Leu Ser 1090 1095 1100 Arg Lys Leu Pro Gly Thr Thr Leu Thr Ala Leu Glu Ala Ala Ala Asn 1105 1110 1115 1120 Pro Ala Leu Pro Ser Asp Phe Lys Thr Ile Leu Asp 1125 1130
Claims (8)
서열번호 1로 이루어지는 펩티드를 포함하는 자외선에 의한 피부 손상 예방 또는 치료용 약학 조성물로서,
상기 자외선에 의한 피부 손상은 일광화상, 홍반, 부종, 색소침착, 피부 염증, 피부 각화, 광알레르기, 광독성, 광감작현상, 및 광노화로 이루어진 군에서 선택된 어느 하나인 것인 약학 조성물.As an active ingredient,
As a pharmaceutical composition for preventing or treating skin damage caused by ultraviolet rays comprising a peptide consisting of SEQ ID NO: 1,
The skin damage caused by the ultraviolet rays is any one selected from the group consisting of sunburn, erythema, edema, pigmentation, skin inflammation, skin keratinization, photoallergy, phototoxicity, photosensitization, and photoaging.
상기 유효성분은 자외선에 의한 세포 독성 완화 기능을 수행하는, 자외선에 의한 피부 손상 예방 또는 치료용 약학 조성물.According to claim 1,
The active ingredient is a pharmaceutical composition for preventing or treating skin damage caused by ultraviolet rays, which performs a function of alleviating cytotoxicity by ultraviolet rays.
상기 자외선은 UVA인 자외선에 의한 피부 손상 예방 또는 치료용 약학 조성물.According to claim 2,
The ultraviolet rays are UVA, a pharmaceutical composition for preventing or treating skin damage caused by ultraviolet rays.
상기 자외선은 UVB인 자외선에 의한 피부 손상 예방 또는 치료용 약학 조성물.According to claim 2,
The ultraviolet light is UVB, a pharmaceutical composition for preventing or treating skin damage caused by ultraviolet light.
서열번호 1로 이루어지는 펩티드를 포함하는 자외선에 의한 피부 손상 예방 또는 개선용 화장료 조성물로서,
상기 자외선에 의한 피부 손상은 일광화상, 홍반, 부종, 색소침착, 피부 염증, 피부 각화, 광알레르기, 광독성, 광감작현상, 및 광노화로 이루어진 군에서 선택된 어느 하나인 것인 화장료 조성물.As an active ingredient,
As a cosmetic composition for preventing or improving skin damage caused by ultraviolet rays comprising a peptide consisting of SEQ ID NO: 1,
The skin damage caused by ultraviolet rays is any one selected from the group consisting of sunburn, erythema, edema, pigmentation, skin inflammation, skin keratinization, photoallergy, phototoxicity, photosensitization, and photoaging.
서열번호 1로 이루어지는 펩티드를 포함하는 자외선에 의한 피부 손상 예방 또는 개선용 건강식품 조성물로서,
상기 자외선에 의한 피부 손상은 일광화상, 홍반, 부종, 색소침착, 피부 염증, 피부 각화, 광알레르기, 광독성, 광감작현상, 및 광노화로 이루어진 군에서 선택된 어느 하나인 것인 건강식품 조성물.
As an active ingredient,
As a health food composition for preventing or improving skin damage caused by ultraviolet rays comprising a peptide consisting of SEQ ID NO: 1,
The skin damage caused by ultraviolet rays is any one selected from the group consisting of sunburn, erythema, edema, pigmentation, skin inflammation, skin keratinization, photoallergy, phototoxicity, photosensitization, and photoaging.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020120145501 | 2012-12-13 | ||
| KR20120145501 | 2012-12-13 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20140077100A KR20140077100A (en) | 2014-06-23 |
| KR102106756B1 true KR102106756B1 (en) | 2020-05-06 |
Family
ID=51129174
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020130112649A KR102106756B1 (en) | 2012-12-13 | 2013-09-23 | Composition for preventing or treating skin damages caused by ultraviolet rays |
Country Status (1)
| Country | Link |
|---|---|
| KR (1) | KR102106756B1 (en) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20160010212A (en) * | 2014-07-18 | 2016-01-27 | 주식회사 젬백스앤카엘 | Anti-aging and wound-healing peptide and composition comprising the same |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20000048820A (en) | 1996-10-01 | 2000-07-25 | 게론 코포레이션 | Telomerase reverse transcriptase |
| US7030211B1 (en) | 1998-07-08 | 2006-04-18 | Gemvax As | Antigenic peptides derived from telomerase |
-
2013
- 2013-09-23 KR KR1020130112649A patent/KR102106756B1/en active IP Right Grant
Also Published As
| Publication number | Publication date |
|---|---|
| KR20140077100A (en) | 2014-06-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR102436084B1 (en) | Novel peptides and compositions comprising them | |
| KR102077983B1 (en) | Composition for improving skin wrinkles and skin whitening | |
| KR20210022405A (en) | Peptide having activities of skin condition improvement and uses thereof | |
| CN107667112B (en) | Novel peptides and compositions containing same | |
| KR102093093B1 (en) | Composition for improving skin anti-aging | |
| KR101342488B1 (en) | Tetrapeptide Having Anti-Aging And Anti-Inflammatory Activities And Cosmetic Composition Containing The Same | |
| KR20130028403A (en) | Peptides inhibiting the activity of matrix metalloproteases and use thereof | |
| EP1868631B1 (en) | Use of compounds inducing the synthesis of sirt proteins in or for the preparation of a cosmetic or pharmaceutical composition | |
| CN118055939A (en) | Peptides with anti-aging activity and uses thereof | |
| US8962565B2 (en) | Peptides involved in the SCF c-Kit signaling pathway and compositions comprising same | |
| KR102106756B1 (en) | Composition for preventing or treating skin damages caused by ultraviolet rays | |
| US20130336904A1 (en) | Novel anti-ageing peptides modulating survivin and compositions including same | |
| CN118043341A (en) | Peptides with anti-aging activity and uses thereof | |
| US8809279B2 (en) | Peptides that are modulators of the protein TRF2 and compositions containing same | |
| CN118201945A (en) | Peptides with anti-aging activity and uses thereof | |
| US8304392B2 (en) | Pharmaceutical and/or cosmetic composition containing an active principle activator of cytochrome C | |
| KR102077984B1 (en) | Composition for preventing and improving skin wrinkles | |
| US9029329B2 (en) | Caspase-14 activator peptides and compositions comprising said peptides | |
| JP2009184986A (en) | New peptide | |
| KR102726837B1 (en) | Peptide Having Anti-Aging Activity and Uses Thereof | |
| KR102166543B1 (en) | Composition and Method for Inhibiting Keloid | |
| KR102667428B1 (en) | Peptide having antioxidative effect and composition comprising same | |
| KR102232319B1 (en) | Composition for preventing or treating cerebrovascular diseases comprising a telomerase peptide as an active ingredient | |
| KR101945946B1 (en) | Gentisic acid derivative, method for production thereof and external skin composition containing the same | |
| KR101942844B1 (en) | Gallic acid derivative, method for production thereof and external skin composition containing the same |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| N231 | Notification of change of applicant | ||
| E902 | Notification of reason for refusal | ||
| E701 | Decision to grant or registration of patent right | ||
| GRNT | Written decision to grant |