CN109423486B - 新型udp-糖基转移酶及其应用 - Google Patents
新型udp-糖基转移酶及其应用 Download PDFInfo
- Publication number
- CN109423486B CN109423486B CN201810995580.0A CN201810995580A CN109423486B CN 109423486 B CN109423486 B CN 109423486B CN 201810995580 A CN201810995580 A CN 201810995580A CN 109423486 B CN109423486 B CN 109423486B
- Authority
- CN
- China
- Prior art keywords
- leu
- polypeptide
- glu
- ser
- gly
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/10—Transferases (2.)
- C12N9/1048—Glycosyltransferases (2.4)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P19/00—Preparation of compounds containing saccharide radicals
- C12P19/02—Monosaccharides
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P19/00—Preparation of compounds containing saccharide radicals
- C12P19/12—Disaccharides
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P19/00—Preparation of compounds containing saccharide radicals
- C12P19/18—Preparation of compounds containing saccharide radicals produced by the action of a glycosyl transferase, e.g. alpha-, beta- or gamma-cyclodextrins
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Health & Medical Sciences (AREA)
- Genetics & Genomics (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Health & Medical Sciences (AREA)
- Biochemistry (AREA)
- General Engineering & Computer Science (AREA)
- Microbiology (AREA)
- Biotechnology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Molecular Biology (AREA)
- Biomedical Technology (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
Abstract
本发明涉及新型UDP‑糖基转移酶及其应用,所述的糖基转移酶能够特异和高效地催化四环二萜类化合物的特定位点加上糖基,从而产生一类糖基化的四环二萜化合物。
Description
技术领域
本发明属于植物学及化工领域,更具体地,本发明涉及新型UDP-糖基转移酶及其应用。
背景技术
糖基化修饰是天然产物中广泛存在的一类后修饰反应,往往发生在生物合成途径的终端,因此对天然产物的理化性质和生理活性有着重要影响。许多植物来源的活性次级代谢产物以糖苷的形式存在于自然界中。植物次级代谢产物的糖基化修饰反应主要由尿苷二磷酸(UDP)-糖基转移酶催化发生。UDP-糖基转移酶(UGT)将糖基从活化的糖基供体分子转移到糖基受体分子上。
甜菊糖苷(Steviol glycosides)是一类贝壳杉烯型四环二萜类糖苷化合物,原产自菊科植物甜叶菊(Stevia rebaudiana),具有甜度高、热量低、无毒性、耐高温、耐酸碱和水溶性好等优点,因此成为天然甜味剂的佼佼者,广泛应用于食品、饮料、调味剂加工等生产工业中,可以避免蔗糖等传统糖料长期或过量食用引发的肥胖病、高血压、糖尿病和龋齿等危害健康的疾病。欧盟于2011年批准甜菊糖可作为食品添加剂使用。
甜菊糖苷迄今为止仅在四个植物物种中被报道过,分别是菊科甜菊属的甜叶菊S.rebaudiana和Stevia phlebophylla A.Gray、蔷薇科悬钩子属甜叶悬钩子Rubussuavissimus S.Lee以及伞形科当归属明日叶Angelica keiskei(Miq.)Koidz.。甜叶悬钩子又名甜茶、甜叶覆盆子等,产自我国广西壮族自治区的山区,是一种珍稀的天然植物。在中国西南少数民族民间有着悠久的应用历史,有清热解毒、生津、润肺、止咳、利咽的功效。目前已经从甜叶悬钩子中分离得到多种甜菊糖苷类化合物,主要包括甜叶悬钩子苷(rubusoside,占叶干重5%以上)和suaviosdie A~L,然而,本领域尚没有从该物种中获得有价值的糖基转移酶,也不了解该物种中各个甜菊糖苷类化合物的精确的合成机制。
随着近十年合成生物学技术的进步,利用微生物异源合成的方法生产某些化合物成为可能,它具有成本低,占地面积少,产品质量易控等优点。因此,本领域有必要发现和鉴定新的糖基转移酶,以更为精确、专一地进行糖基转移,高效生产工业上或食品行业中有用的化合物。
发明内容
本发明的目的在于提供新型UDP-糖基转移酶及其应用。
在本发明的第一方面,提供分离的多肽,所述多肽选自:
(a)具有SEQ ID NO:1,SEQ ID NO:2,SEQ ID NO:3,SEQ ID NO:4或SEQ ID NO:5所示氨基酸序列的多肽;
(b)在SEQ ID NO:1所示氨基酸序列的多肽的空间结构中,第21位和第121位氨基酸不变,但位于第21位和第121位氨基酸位置附近或底物受体结合口袋内发生氨基酸残基变异的多肽;
(c)在SEQ ID NO:1所示氨基酸序列基础上,在第16、82、83、86、90、119、124、126、140、141、142、143、145、149、153、198、199、200、210、212、302、379、397或398位发生氨基酸变异的多肽;较佳地,发生P82S,T83I,I86R,I90L,F119I,A126V,A140M,L141M,S149G,L153F,Y212F或I302T变异的多肽;
(d)(a)或(b)或(c)的保守性变异多肽。
在一个优选例中,所述的保守性变异多肽选自:
(1)由(a)或(b)或(c)所述的任一多肽经过一个或多个(如1-20个,较佳地1-10个;更佳地1-5个;更佳地1-3个)氨基酸残基的取代、缺失或添加而形成的,且具有多肽(a)功能的多肽;
(2)氨基酸序列与(a)或(b)或(c)的多肽的氨基酸序列有80%以上(较佳地85%以上;更佳地90%以上;更佳地95%以上;更佳地99%以上)相同性,且具有多肽(a)功能的多肽;或
(3)在(a)或(b)或(c)所述多肽的N或C末端添加标签序列,或在其N末端添加信号肽序列后形成的多肽;
较佳地,SEQ ID NO:1的保守性变异多肽中,第21位是组氨酸,第121位是天门冬氨酸。
在另一优选例中,SEQ ID NO:1所示氨基酸序列的多肽的保守性变异多肽包括(但不限于):(b)或(c)中,所述突变不发生在第21位组氨酸附近的丙氨酸的位置。
在另一优选例中,(b)或(c)中,所述的多肽是在第16、82、83、86、90、119、124、126、140、141、142、143、145、149、153、198、199、200、210、212、302、379、397或398位发生氨基酸变异的多肽;较佳地,所述的多肽是发生P82S,T83I,I86R,I90L,F119I,A126V,A140M,L141M,S149G,L153F,Y212F或I302T变异的多肽。
在另一优选例中,SEQ ID NO:1所示氨基酸序列的多肽的保守性变异多肽不包括:在第16、198、199、397或398位发生氨基酸变异的多肽;较佳地不存在A16F、S198L、F199D、F397S或A398W的变异。
在本发明的另一方面,提供分离的多核苷酸,它编码前面任一所述的多肽。
在本发明的另一方面,提供一种载体,它含有所述的多核苷酸。
在本发明的另一方面,提供一种遗传工程化的宿主细胞,它含有所述的载体,或其基因组中整合有所述的多核苷酸。
在本发明的另一方面,提供一种前面任一所述的多肽的制备方法,该方法包含:培养所述的宿主细胞;收集含有所述的多肽的培养物。
在另一优选例中,所述的方法还包括:从培养物中分离出权利要求1~4任一所述的多肽。
在本发明的另一方面,提供多肽的用途,其中所述的多肽是具有SEQ ID NO:2,SEQID NO:3,SEQ ID NO:4或SEQ ID NO:5所示氨基酸序列的多肽或它们的保守性变异多肽;用于在具有母核(I)结构的化合物上转移上一个糖基(Glc),形成如式(II)结构的化合物:
其中,R独立地选自:H,OH,O-β-D-葡萄糖基,O-β-D-葡萄糖基-(2→1)-β-D-葡萄糖基。
在一个优选例中,,所述的具有母核(I)结构的化合物包括:甜菊醇,对映-贝壳杉烯酸,甜菊醇单糖苷,甜菊醇双糖苷;或所述的式(II)结构的化合物包括:甜菊醇-19-O-葡萄糖酯,对映-贝壳杉烯酸-19-O-葡萄糖酯,甜叶悬钩子苷,甜菊苷。
在另一优选例中,其中所述的多肽是具有SEQ ID NO:1所示氨基酸序列的多肽或其保守性变异多肽;用于在具有母核(III)结构的化合物上转移上一个糖基(Glc),形成如式(IV)结构的化合物:
其中,R’独立地选自:H,O-β-D-葡萄糖基。
在另一优选例中,所述的具有母核(III)结构的化合物包括:甜菊醇-19-O-葡萄糖酯,甜菊醇;或所述的式(IV)结构的化合物包括:甜叶悬钩子苷,甜菊醇单糖苷。
在另一优选例中,所述的糖基的供体是含有糖基的化合物;较佳地,所述的供体包括(但不限于):UDP-葡萄糖,UDP-鼠李糖,UDP-木糖;或者概括为UDP-糖。
在本发明的另一方面,提供一种用于糖基转移的组合物,它含有所述的多肽或含有所述的宿主细胞、其培养物或裂解产物。
在本发明的另一方面,提供一种在具有母核(I)结构的化合物上转移上一个糖基的方法,所述方法包括:以多肽,表达该多肽的宿主细胞、其培养物或裂解产物,或含有该多肽的组合物将糖基转移到具有母核(I)结构的化合物;
其中,R独立地选自:H,OH,O-β-D-葡萄糖基,O-β-D-葡萄糖基-(2→1)-β-D-葡萄糖基;
其中,该多肽具有SEQ ID NO:2,SEQ ID NO:3,SEQ ID NO:4或SEQ ID NO:5所示氨基酸序列的多肽或它们的保守性变异多肽。
在本发明的另一方面,提供一种在具有母核(III)结构的化合物上转移上一个糖基的方法,所述方法包括:以多肽,表达该多肽的宿主细胞、其培养物或裂解产物,或含有该多肽的组合物将糖基转移到具有母核(III)结构的化合物;
其中,R’独立地选自:H,O-β-D-葡萄糖基;
其中,该多肽具有SEQ ID NO:1所示氨基酸序列的多肽或它们的保守性变异多肽。
在一个优选例中,所述的糖基的供体是含有糖基的化合物;较佳地,所述的供体包括(但不限于):UDP-葡萄糖,UDP-鼠李糖,UDP-木糖;或者概括为UDP-糖。
本发明的其它方面由于本文的公开内容,对本领域的技术人员而言是显而易见的。
附图说明
图1A、以甜菊醇(Steviol)为底物,RsS19GT1、RsS19GT2、RsS19GT3和RsS19GT4体外酶催化反应转化产物的HPLC分析。
图1B、以甜菊醇(Steviol)为底物,RsS19GT1体外酶催化反应转化产物的LC-MS图谱。
图1C、以甜菊醇(Steviol)为底物,RsS19GT2体外酶催化反应转化产物的LC-MS图谱。
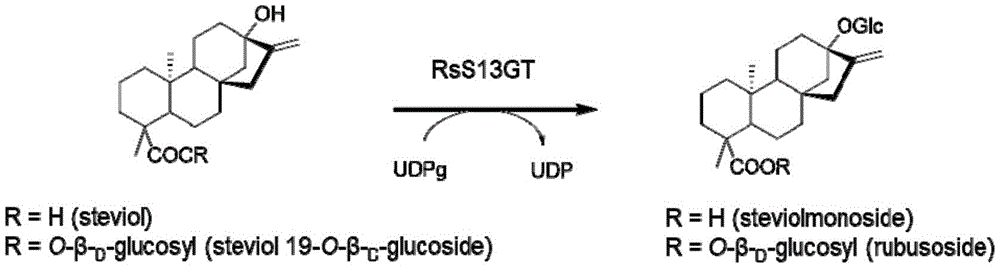
图2A、以甜菊醇-19-O-葡萄糖酯(steviol 19-O-β-D-glucoside)为底物,RsS13GT体外酶催化反应转化产物的HPLC分析。
图2B、以甜菊醇-19-O-葡萄糖酯(steviol 19-O-β-D-glucoside)为底物,RsS13GT体外酶催化反应转化产物的LC-MS图谱。
图3A、RsS19GT1、RsS19GT2、RsS19GT3和RsS19GT4体外酶催化反应转化对映-贝壳杉烯酸(ent-kaur-16-en-19-oic acid)的HPLC分析。
图3B、以对映-贝壳杉烯酸(ent-kaur-16-en-19-oic acid)为底物,RsS19GT1体外酶催化反应转化的LC-MS图谱。
图3C、以对映-贝壳杉烯酸(ent-kaur-16-en-19-oic acid)为底物,RsS19GT2体外酶催化反应转化的LC-MS图谱。
图4A、RsS19GT1、RsS19GT2、RsS19GT3和RsS19GT4体外酶催化反应转化甜菊醇单糖苷(steviolmonoside)的HPLC分析。
图4B、以甜菊醇单糖苷(steviolmonoside)为底物,RsS19GT1体外酶催化反应转化的LC-MS图谱。
图4C、以甜菊醇单糖苷(steviolmonoside)为底物,RsS19GT2体外酶催化反应转化的LC-MS图谱。
图5A、RsS19GT1、RsS19GT2、RsS19GT3和RsS19GT4体外酶催化反应转化甜菊醇双糖苷(steviolbioside)的HPLC分析。
图5B、以甜菊醇双糖苷(steviolbioside)为底物,RsS19GT1体外酶催化反应转化的LC-MS图谱。
图5C、以甜菊醇双糖苷(steviolbioside)为底物,RsS19GT2体外酶催化反应转化的LC-MS图谱。
图6A、以甜菊醇(steviol)为底物,RsS13GT体外酶催化反应转化steviol的HPLC分析。
图6B、以甜菊醇(steviol)为底物,RsS13GT体外酶催化反应转化steviol的LC-MS图谱。
图7、RsS13GT各突变体的相对活性(以RsS13GT野生型为100%)。
图8、RsS13GT各突变体的相对活性(以RsS13GT野生型为100%),测定6次,取平均值。
具体实施方式
本发明人经过大规模的筛选和深入的研究,从甜叶悬钩子这一物种中筛选出一系列新型的参与萜类糖基化的尿苷二磷酸(UDP)-糖基转移酶。所述的糖基转移酶能够特异和高效地催化四环二萜类化合物的C-4羧基或C-13羟基的糖基化,从而产生一类糖基化的四环二萜化合物。
活性多肽、其编码基因、载体及宿主
如本文所用,“分离的多肽”是指所述多肽基本上不含天然与其相关的其它蛋白、脂类、糖类或其它物质。本领域的技术人员能用标准的蛋白质纯化技术纯化所述多肽。基本上纯的多肽在非还原聚丙烯酰胺凝胶上能产生单一的主带。所述多肽的纯度还可以用氨基酸序列进行进一步分析。
本发明揭示了一组新的、参与萜类糖基化的尿苷二磷酸(UDP)-糖基转移酶。优选地,它们是RsS13GT,RsS19GT1,RsS19GT2,RsS19GT3,RsS19GT4和;它们分别具有SEQ ID NO:1,SEQ ID NO:2,SEQ ID NO:3,SEQ ID NO:4或SEQ ID NO:5所示氨基酸序列的多肽。本发明也包括它们的保守性变异多肽。
在本发明中,所述的“保守性变异多肽”是指基本上保持所述多肽相同的生物学功能或活性的多肽。
所述的“保守性变异多肽”可以是(i)有一个或多个保守或非保守性氨基酸残基(优选保守性氨基酸残基)被取代的多肽,而这样的取代的氨基酸残基可以是也可以不是由遗传密码编码的,或(ii)在一个或多个氨基酸残基中具有取代基团的多肽,或(iii)成熟多肽与另一个化合物(比如延长多肽半衰期的化合物,例如聚乙二醇)融合所形成的多肽,或(iv)附加的氨基酸序列融合到此多肽序列而形成的多肽(如前导序列或分泌序列或用来纯化此多肽的序列或蛋白原序列,或与抗原IgG片段的形成的融合蛋白)。根据本文的教导,这些片段、衍生物和类似物属于本领域熟练技术人员公知的范围。
所述的“保守性变异多肽”可以包括(但并不限于):一个或多个(通常为1-50个,较佳地1-30个,更佳地1-20个,最佳地1-10个)氨基酸的缺失、插入和/或取代,以及在C末端和/或N末端添加或缺失一个或数个(如50个以内,较20个或10个以内,更佳地为5个以内)氨基酸。例如,在本领域中,用性能相近或相似的氨基酸进行取代时,通常不会改变蛋白质的功能。又比如,在C末端和/或N末端添加一个或数个氨基酸通常也不会改变蛋白质的功能。本发明还提供所述多肽的类似物。这些类似物与天然多肽的差别可以是氨基酸序列上的差异,也可以是不影响序列的修饰形式上的差异,或者兼而有之。这些多肽包括天然或诱导的遗传变异体。诱导变异体可以通过各种技术得到,如通过辐射或暴露于诱变剂而产生随机诱变,还可通过定点诱变法或其他已知分子生物学的技术。类似物还包括具有不同于天然L-氨基酸的残基(如D-氨基酸)的类似物,以及具有非天然存在的或合成的氨基酸(如β、γ-氨基酸)的类似物。应理解,本发明的多肽并不限于上述例举的代表性的多肽。
修饰(通常不改变一级结构)形式包括:体内或体外的多肽的化学衍生形式如乙酰化或羧基化。修饰还包括糖基化,如那些在多肽的合成和加工中或进一步加工步骤中进行糖基化修饰而产生的多肽。这种修饰可以通过将多肽暴露于进行糖基化的酶(如哺乳动物的糖基化酶或去糖基化酶)而完成。修饰形式还包括具有磷酸化氨基酸残基(如磷酸酪氨酸,磷酸丝氨酸,磷酸苏氨酸)的序列。还包括被修饰从而提高了其抗蛋白水解性能或优化了溶解性能的多肽。
本发明的多肽的氨基端或羧基端还可含有一个或多个多肽片段,作为蛋白标签。任何合适的标签都可以用于本发明。例如,所述的标签可以是FLAG、HA、HA1、c-Myc、Poly-His、Poly-Arg、Strep-TagII、AU1、EE、T7、4A6、ε、B、gE、以及Ty1。这些标签可用于对蛋白进行纯化。
为了使翻译的蛋白分泌表达(如分泌到细胞外),还可在本发明的多肽的氨基端添加上信号肽序列。信号肽在多肽从细胞内分泌出来的过程中可被切去。
在天然的序列的基础上,进行适当的变异,将获得活性更高的蛋白。作为本发明的优选方式,将SEQ ID NO:1所示氨基酸序列的多肽(RsS13GT)进行定点突变,将这些单突变体克隆并异源表达在大肠杆菌中,发现异源表达的重组突变体蛋白能够更高效地催化四环二萜类化合物甜菊醇-19-O-葡萄糖酯(steviol19-O-β-D-glucoside)的C-13羟基的糖基化,从而更高效地产生甜叶悬钩子苷(rubusoside)。因此,在本发明所揭示的天然的序列的基础上,进行适当的变异后获得的多肽也被包含在本发明的保护范围内。
本发明还揭示了一系列保留生物活性的多肽变体,包括:在SEQ ID NO:1所示氨基酸序列基础上,在第16、82、83、86、90、119、124、126、140、141、142、143、145、149、153、198、199、200、210、212、302、379、397或398位发生氨基酸变异的多肽;较佳地,为在第82、83、86、90、119、126、140、141、149、153、212或302位发生氨基酸变异的多肽。更具体地,包括:在SEQID NO:1所示氨基酸序列基础上,发生A16F,P82S,T83I,I86R,I90L,F119I,M124L,A126V,A140M,L141M,I142Y,Y143W,I145L,S149G,L153F,S198L,F199D,C200W,F210L,Y212F,I302T,N379G,F397S或A398W变异的多肽;较佳地,为发生P82S,T83I,I86R,I90L,F119I,A126V,A140M,L141M,S149G,L153F,Y212F或I302T的多肽。
本发明的活性多肽可以是重组多肽、天然多肽、合成多肽。本发明的多肽可以是天然纯化的产物,或是化学合成的产物,或使用重组技术从原核或真核宿主(例如,细菌、酵母、高等植物)中产生。根据重组生产方案所用的宿主,本发明的多肽可以是糖基化的,或可以是非糖基化的。本发明的多肽还可包括或不包括起始的甲硫氨酸残基。
本发明的多核苷酸可以是DNA形式或RNA形式。DNA形式包括cDNA、基因组DNA或人工合成的DNA。DNA可以是单链的或是双链的。DNA可以是编码链或非编码链。术语“编码多肽的多核苷酸”可以是包括编码此多肽的多核苷酸,也可以是还包括附加编码和/或非编码序列的多核苷酸。
本发明还涉及上述多核苷酸的变异体,其编码与本发明有相同的氨基酸序列的多肽或多肽的片段、类似物和衍生物。此多核苷酸的变异体可以是天然发生的等位变异体或非天然发生的变异体。这些核苷酸变异体包括取代变异体、缺失变异体和插入变异体。如本领域所知的,等位变异体是一个多核苷酸的替换形式,它可能是一个或多个核苷酸的取代、缺失或插入,但不会从实质上改变其编码的多肽的功能。
本发明还涉及与上述的序列杂交且两个序列之间具有至少50%,较佳地至少70%,更佳地至少80%相同性的多核苷酸。本发明特别涉及在严格条件(或严紧条件)下与本发明所述多核苷酸可杂交的多核苷酸。在本发明中,“严格条件”是指:(1)在较低离子强度和较高温度下的杂交和洗脱,如0.2×SSC,0.1%SDS,60℃;或(2)杂交时加有变性剂,如50%(v/v)甲酰胺,0.1%小牛血清/0.1%Ficoll,42℃等;或(3)仅在两条序列之间的相同性至少在90%以上,更好是95%以上时才发生杂交。
本发明还涉及与上述的序列杂交的核酸片段。如本文所用,“核酸片段”的长度至少含15个核苷酸,较好是至少30个核苷酸,更好是至少50个核苷酸,最好是至少100个核苷酸以上。
本发明中的多肽和多核苷酸优选以分离的形式提供,更佳地被纯化至均质。
本发明的核苷酸全长序列或其片段通常可以用PCR扩增法、重组法或人工合成的方法获得。一旦获得了有关的序列,就可以用重组法来大批量地获得有关序列。这通常是将其克隆入载体,再转入细胞,然后通过常规方法从增殖后的宿主细胞中分离得到有关序列。此外,还可用人工合成的方法来合成有关序列,尤其是片段长度较短时。还可通过化学合成将突变引入本发明蛋白序列中。
应用PCR技术扩增DNA/RNA的方法被优选用于获得本发明的基因。特别是很难从文库中得到全长的cDNA时,可优选使用RACE法(RACE-cDNA末端快速扩增法),用于PCR的引物可根据本文所公开的本发明的序列信息适当地选择,并可用常规方法合成。可用常规方法如通过凝胶电泳分离和纯化扩增的DNA/RNA片段。
本发明也涉及包含本发明的多核苷酸的载体,以及用本发明的载体或多肽编码序列经基因工程产生的宿主细胞,以及经重组技术产生本发明所述多肽的方法。
通过常规的重组DNA技术,可利用本发明的多聚核苷酸序列可用来表达或生产重组的RsS19GT1,RsS19GT2,RsS19GT3,RsS19GT4和RsS13GT多肽。一般来说有以下步骤:
(1).用本发明的编码RsS19GT1,RsS19GT2,RsS19GT3,RsS19GT4和RsS13GT多肽(含其保守性变异多肽)的多核苷酸,或用含有该多核苷酸的重组表达载体转化或转导合适的宿主细胞;
(2).在合适的培养基中培养的宿主细胞;
(3).从培养基或细胞中分离、纯化蛋白质。
本发明中,编码RsS19GT1,RsS19GT2,RsS19GT3,RsS19GT4或RsS13GT的多核苷酸序列可插入到重组表达载体中。术语“重组表达载体”指本领域熟知的细菌质粒、噬菌体、酵母质粒、植物细胞病毒、哺乳动物细胞病毒如腺病毒、逆转录病毒或其他载体。只要能在宿主体内复制和稳定,任何质粒和载体都可以用。表达载体的一个重要特征是通常含有复制起点、启动子、标记基因和翻译控制元件。
本领域的技术人员熟知的方法能用于构建含RsS19GT1,RsS19GT2,RsS19GT3,RsS19GT4和RsS13GT的编码DNA序列和合适的转录/翻译控制信号的表达载体。这些方法包括体外重组DNA技术、DNA合成技术、体内重组技术等。所述的DNA序列可有效连接到表达载体中的适当启动子上,以指导mRNA合成。此外,表达载体优选地包含一个或多个选择性标记基因,以提供用于选择转化的宿主细胞的表型性状。
包含上述的适当DNA序列以及适当启动子或者控制序列的载体,可以用于转化适当的宿主细胞,以使其能够表达蛋白质。宿主细胞可以是原核细胞,如细菌细胞;或是低等真核细胞,如酵母细胞;或是高等真核细胞,如哺乳动物细胞。代表性例子有:大肠杆菌,链霉菌属,枯草杆菌;鼠伤寒沙门氏菌的细菌细胞;真菌细胞如酵母,植物细胞,灵芝细胞;果蝇S2或Sf9的昆虫细胞;CHO、COS、293细胞、或Bowes黑素瘤细胞的动物细胞等。
本发明的方法中,所述的重组多肽可在细胞内、或在细胞膜上表达、或分泌到细胞外。如果需要,可利用其物理的、化学的和其它特性通过各种分离方法分离和纯化重组的蛋白。这些方法是本领域技术人员所熟知的。这些方法的例子包括但并不限于:常规的复性处理、用蛋白沉淀剂处理(盐析方法)、离心、渗透破菌、超处理、超离心、分子筛层析(凝胶过滤)、吸附层析、离子交换层析、高效液相层析(HPLC)和其它各种液相层析技术及这些方法的结合。
作为本发明的优选方式,所述的宿主细胞是原核细胞;较佳地,所述原核宿主细胞包括(但不限于):大肠杆菌。在本发明的较佳实施例中,将糖基转移酶基因RsS19GT1、RsS19GT2、RsS19GT3、RsS19GT4和RsS13GT克隆并异源表达在大肠杆菌中,发现异源表达的重组蛋白能够特异和/或高效地催化四环二萜类化合物贝壳杉烯酸、甜菊醇及其衍生物的C-4羧基或C-13羟基的糖基化,从而产生甜叶悬钩子苷(rubusoside)等糖基化的四环二萜化合物。
在本发明的较佳实施例中,将携带甜叶悬钩子新型糖基转移酶RsS19GT1和RsS13GT的质粒与携带构建甜菊醇(steviol)骨架所需关键功能基因的质粒,共转于大肠杆菌中,获得大肠杆菌工程菌。将构建的大肠杆菌工程菌,在TB培养基中低温培养发酵,获得发酵液。发酵液离心,获得上清液和菌体。菌体用水混悬,经破碎后用正丁醇萃取;上清液用正丁醇萃取,合并正丁醇萃取液。将正丁醇萃取液蒸发后用甲醇复溶,进行HPLC分析,获得所需的产物。
应用
本发明的RsS19GT1,RsS19GT2,RsS19GT3,RsS19GT4或RsS13GT多肽或它们的保守性变异多肽,可应用于特异和高效地催化四环二萜类化合物的C-4羧基或C-13羟基的糖基化,从而产生一类糖基化的四环二萜化合物。
作为本发明的一种优选方式,发挥催化活性的多肽为RsS19GT1,RsS19GT2,RsS19GT3或RsS19GT4,并且能够催化下述反应:
此处,所述的四环二萜类化合物例如但不限于甜菊醇,对映-贝壳杉烯酸,甜菊醇单糖苷,甜菊醇双糖苷及其衍生物;其加上一个糖基后的产物分别为甜菊醇-19-O-葡萄糖酯,对映-贝壳杉烯酸-19-葡萄糖酯,甜叶悬钩子苷,甜菊苷。
作为本发明的一种优选方式,发挥催化活性的多肽为RsS13GT,并且能够催化下述反应:
此处,所述的四环二萜类化合物例如但不限于甜菊醇-19-O-葡萄糖酯,甜菊醇;其加上一个糖基后的产物分别为所述的式(IV)结构的化合物包括:甜叶悬钩子苷,甜菊醇单糖苷。
在应用时,特别是工业化生产中,本发明的RsS19GT1,RsS19GT2,RsS19GT3,RsS19GT4和RsS13GT多肽或它们的保守性变异多肽还可被固定于其它的固相载体上,获得固定化的酶,应用于与底物进行体外反应。所述的固相载体例如是一些无机物制成的微球,管状体等。固定化酶的制备方法有物理法和化学法两大类。物理方法包括物理吸附法、包埋法等。化学法包括结合法、交联法。结合法又分为离子结合法和共价结合法。上述的固定化酶的方法均可被应用于本发明中。
下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。下列实施例中未注明具体条件的实验方法,通常按照常规条件如J.萨姆布鲁克等编著,分子克隆实验指南,第三版,科学出版社,2002中所述的条件,或按照制造厂商所建议的条件。
材料
甜叶悬钩子(Rubus suavissimus S.Lee)植物叶片取自中国科学院华南植物园。
寡核苷酸引物购自生工科技(Sangon Biotech)有限公司。
序列分析委托上海美吉生物医药有限公司。
AxyPrep总RNA小量制备试剂盒,多聚酶链式反应(PCR)胶回收试剂盒,质粒抽提试剂盒均为美国Axygen产品。
PrimeScript RT reagent Kit with gDNA Eraser(Perfect Real Time)聚合酶试剂盒,聚合酶链式反应(PCR)高保真酶PrimeSTAR Max DNA Polymerase为日本宝生物公司(TAKARA)产品。
限制性内切酶均为NEB产品。
大肠杆菌DH10B、Rosetta(DE3)菌株和pET21a、pET28a载体用于基因克隆及蛋白表达。
标准品化合物甜菊醇(steviol)、甜菊醇双糖苷(steviolbioside)购自上海源叶生物科技有限公司、甜叶悬钩子苷(rubusoside)购自南京广润生物制品有限公司。
UDP葡萄糖购自北京中泰生物有限公司。
其他试剂为国产分析纯或色谱纯试剂,购自国药集团化学试剂有限公司。色谱分离使用反相硅胶(ODS-A-HG,12nm,S-50μm,YMC Co.,Ltd.,Tokyo,Japan)。
PCR使用Arktik Thermal Cycler(Thermo Fisher Scientific);恒温培养使用ZXGP-A2050恒温培养箱(智城)和ZWY-211G恒温培养振荡器(智城);离心使用5418R高速冷冻式离心机和5418小型离心机(Eppendorf)。真空浓缩使用Concentrator plus浓缩仪(Eppendorf);OD600使用UV-1200紫外可见分光光度计检测(上海美谱达仪器有限公司)。旋转蒸发系统由IKA RV 10 digital旋转蒸发仪(IKA)和MZ 2C NT化学隔膜泵、CVC3000真空控制器(vacuubrand)组成。高效液相色谱使用Dionex UltiMate 3000液相色谱系统(Thermo Fisher Scientific)。核磁共振波谱由Bruker DRX 500测定得到;高分辨质谱由Thermo Fisher Scientific静电场轨道阱组合质谱Q Exactive测得。
实施例1、新型尿苷二磷酸(UDP)-糖基转移酶
1、甜叶悬钩子叶片cDNA的制备
取甜叶悬钩子成熟叶片,清水清洗干净表面污渍,用吸水纸轻轻擦拭干叶片表面水渍,称重备用。使用锡箔纸包裹,液氮速冻,-80℃超低温保存备用。参考Axygen的AxyPrep总RNA小量制备试剂盒说明书制备叶片总RNA。参考TaKaRa的PrimeScript RT reagent Kitwith gDNA Eraser(Perfect Real Time)反转录试剂盒说明书,反转录RNA制备cDNA。
2、RsS19GT1、RsS19GT2、RsS19GT3、RsS19GT4和RsS13GT基因克隆和表达质粒构建
设计表1所示的引物并在上下游引入合适的酶切位点。PCR扩增体系50μL:PrimeSTAR Max Premix,25μL;Primer 1/Primer 2终浓度0.2~0.3μM;cDNA<200ng;剩余体积用灭菌蒸馏水补足。
PCR反应条件:98℃预变性2min,然后98℃变性10s,55℃退火15s,72℃延伸20s,28个循环,72℃延伸10min,琼脂糖电泳检测,扩增得到约1.5kb的片段,纯化后用引入的酶切位点消化。
消化后片段连入相同酶消化过的pET21a和pET28a载体,连接产物转化大肠杆菌DH10B感受态细胞,提取质粒经构建时引入酶切位点双酶切验证和基因测序,筛选得到重组质粒。
表1、引物
3、RsS19GT1、RsS19GT2、RsS19GT3、RsS19GT4和RsS13GT的表达
将重组质粒转化到大肠杆菌Rosetta(DE3)的感受态细胞中,LB固体培养基(氯霉素34μg/mL,氨苄青霉素100μg/mL)37℃培养过夜。挑取单个克隆到2mL LB液体培养基(氯霉素34μg/mL,氨苄青霉素100μg/mL),转接过夜培养的菌液到新的LB液体抗性培养基中37℃,250r/min培养至OD600=0.3~0.5,水浴降温至16℃左右,然后加入诱导剂IPTG至终浓度0.1mM,转至16℃低温诱导培养,在摇床转速180r/min条件下继续培养20h。携带未连入外来基因的pET21a和pET28a空质粒的Rosetta(DE3)重组菌株作为空白对照,培养操作同上。表达结束后,使用SDS-PAGE检验表达情况。菌液离心(12000r/min,1min),弃去上清,用等体积无菌水重悬,置冰上超声破碎至澄清,超声过后粗酶液冷冻离心(10000r/min,10min,4℃),分别取上清和沉淀,SDS-PAGE验证蛋白表达情况。
实施例2、RsS19GT1、RsS19GT2、RsS19GT3、RsS19GT4和RsS13GT的体外功能鉴定
转接保存的单克隆甘油菌到2mL LB液体培养基(氯霉素34μg/mL,氨苄青霉素100μg/mL)中,37℃、250rpm过夜培养,按1%(v/v)转接过夜培养的菌液到新的50mL LB液体培养基中,37℃、250rpm培养至OD600=0.3~0.5,加入IPTG至终浓度0.1mM,16℃,180rpm诱导培养20h。携带pET21a和pET28a空质粒的Rosetta(DE3)重组菌株作为空白对照,操作同上。离心收菌,使用5mL破菌缓冲液Buffer A(20mM Tris-HCl,pH 8.0;100mM NaCl)重悬,加入DNase至终浓度为5μg/mL,Mg2+终浓度为2mM,蛋白酶抑制剂PMSF终浓度为1mM,冰上孵育30min后超声破碎;离心(10000rpm,30min,4℃),通过0.2μm滤膜过滤,获得上清粗酶液。
体外酶催化测定体系为500μL,反应体系包括:0.25mM的糖基受体(甜菊醇,甜菊醇单糖苷,甜菊醇双糖苷,对映-贝壳杉烯酸,甜菊醇-19-O-葡萄糖酯),1.5mM的UDP葡萄糖,10mM MgCl2,200μL上清粗酶液,用Buffer A补足体积到500μL。37℃反应2h。待反应结束后,加等体积乙酸乙酯(以甜菊醇和贝壳杉烯酸为底物时)或正丁醇(其他底物时)终止反应,用等体积的乙酸乙酯或正丁醇萃取3次,将3次萃取的有机相混合,在真空浓缩仪中离心蒸干,然后使用500μL甲醇或甲醇-水(50/50,v/v)复溶,使用HPLC进行产物分析。HPLC检测条件:色谱柱:反相C18 column[TSKge1 ODS-1V ],检测波长为205nm;流动相:乙腈-水混合物梯度洗脱,在0到25min内比例由30:70升到80:20,流速1mL/min。
RsS19GT1、RsS19GT2、RsS19GT3和RsS19GT4参与反应获得的产物的HPLC检测结果如图1A。根据图1A,RsS19GT1、RsS19GT2、RsS19GT3和RsS19GT4可以将底物甜菊醇(Steviol)转化为其糖基化产物。该糖基化产物经负离子模式高分辨质谱检测确认分子式为C26H40O8,核磁共振氢谱和碳谱显示贝壳杉烯型四环二萜母核特征信号和糖基特征信号,在二维核磁异核多重键相关谱(HMBC)中证实该化合物葡萄糖1’位端基氢与甜菊醇母核19位羧基具有远程相关峰。
以甜菊醇(Steviol)为底物,RsS19GT1将之转化为甜菊醇-19-O-葡萄糖酯(steviol 19-O-β-D-glucoside)的LC-MS图谱如图1B。
以甜菊醇(Steviol)为底物,RsS19GT2将之转化为甜菊醇-19-O-葡萄糖酯(steviol 19-O-β-D-glucoside)的LC-MS图谱如图1C。
因此,可以确定所获得的糖基化产物为甜菊醇-19-O-葡萄糖酯(steviol-19-O-β-D-glucoside),发生的反应的反应式如下:
RsS13GT参与反应获得的产物的HPLC检测结果如图2A,LC-MS图谱如图2B。根据图2,RsS13GT可以将底物甜菊醇-19-O-葡萄糖酯(steviol19-O-β-D-glucoside)转化为其糖基化产物。该产物经负离子模式高分辨质谱检测确认分子式为C32H50O13,与甜叶悬钩子苷(rubusoside)的分子式一致,其HPLC保留时间亦与甜叶悬钩子苷标准品一致,因此鉴定该产物为甜叶悬钩子苷。
实施例3、RsS19GT1、RsS19GT2、RsS19GT3、RsS19GT4和RsS13GT的底物专一性研究
1、RsS19GT1、RsS19GT2、RsS19GT3、RsS19GT4
RsS19GT1、RsS19GT2、RsS19GT3和RsS19GT4不仅可以识别甜菊醇(Steviol),同时对于甜菊醇的结构类似物对映-贝壳杉烯酸(ent-kaur-16-en-19-oic acid),甜菊醇单糖苷(steviolmonoside),甜菊醇双糖苷(steviolbioside)具有19位的糖基化催化活性,分别生成对映-贝壳杉烯酸-19-葡萄糖酯(β-D-glucosyl-ent-kaur-16-en-19-oate),甜叶悬钩子苷(rubusoside)和甜菊苷(stevioside)。HPLC分析图如图3A、4A、5A。
以对映-贝壳杉烯酸(ent-kaur-16-en-19-oic acid)为底物,RsS19GT1将之转化为对映-贝壳杉烯酸-19-葡萄糖酯(β-D-glucosyl-ent-kaur-16-en-19-oate)的LC-MS图谱如图3B。以RsS19GT2进行相应转化的LC-MS图谱如图3C。
以甜菊醇单糖苷(steviolmonoside)为底物,RsS19GT1将之转化为甜叶悬钩子苷(rubusoside)的LC-MS图谱如图4B。以RsS19GT2进行相应转化的LC-MS图谱如图4C。
以甜菊醇双糖苷(steviolbioside)为底物,RsS19GT1将之转化为甜菊苷(stevioside)的LC-MS图谱如图5B。以RsS19GT2进行相应转化的LC-MS图谱如图5C。
RsS19GT1、RsS19GT2、RsS19GT3和RsS19GT4识别的底物母核及其产物结构通式如下:
2、RsS13GT
RsS13GT不仅可以识别甜菊醇-19-O-葡萄糖酯(steviol 19-O-β-D-glucoside),同时对于甜菊醇亦具有13位的糖基化催化活性,生成甜菊醇单糖苷(steviolmonoside)。HPLC分析图如图6A,LC-MS图谱如图6B。
RsS13GT识别的底物及其酶反应催化产物的反应通式如下:
实施例4、尿苷二磷酸(UDP)-糖基转移酶RsS13GT的改造
1、突变位点的选择
尿苷二磷酸(UDP)-糖基转移酶的21位组氨酸(以RsS13GT为例)及121位天门冬氨酸(以RsS13GT为例)为其催化中心,此催化中心周围的氨基酸残基可能影响底物与酶的结合。本发明人选择H21及D121周围距离范围内的残基进行突变。本发明人预测到可能与底物结构的受体口袋,选择可能与底物发生相互作用的残基进行突变。
2、RsS13GT基因突变体的表达载体的构建
设计表2所示的引物以用于引入定点突变。
表2、用于RsS13GT基因突变体构建的引物
PCR扩增体系50μL:PrimeSTAR Max Premix,25μL;Primer 1/Primer 2终浓度0.2μM;RsS13GT野生型表达载体质粒10ng;剩余体积用灭菌蒸馏水补足。
PCR反应条件:98℃预变性2min,然后98℃变性10s,55℃退火5s,72℃延伸3min,30个循环,琼脂糖电泳检测,扩增得到约6kb的片段。
PCR反应产物经DpnI处理后,转化大肠杆菌DMT感受态细胞,提取质粒经基因测序,筛选得到定点突变体。
3、RsS13GT突变体的表达
将重组突变体质粒转化到大肠杆菌JM109(DE3)的感受态细胞中,LB固体培养基(卡纳霉素50μg/mL,萘啶酸20μg/mL)37℃培养过夜。挑取单个克隆到2mL LB液体培养基(卡纳霉素50μg/mL,萘啶酸20μg/mL),转接过夜培养的菌液到新的LB液体抗性培养基中37℃,250r/min培养至OD600=0.3~0.5,水浴降温至16℃左右,然后加入诱导剂IPTG至终浓度0.1mM,转至16℃低温诱导培养,在摇床转速200r/min条件下继续培养20h。携带野生型RsS13GT基因表达载体的JM109(DE3)重组菌株作为对照,培养操作同上。表达结束后,使用SDS-PAGE检验表达情况。菌液离心(6000r/min,5min),弃去上清,用1/10体积Buffer A(20mM Tris-HCl,pH 8.0;100mM NaCl)重悬,加入DNase至终浓度为5μg/mL,Mg2+终浓度为2mM,蛋白酶抑制剂PMSF终浓度为1mM,冰上孵育30min后超声破碎;离心(10000rpm,30min,4℃),分别取上清和沉淀,SDS-PAGE验证蛋白表达情况。上清液通过0.2μm滤膜过滤,获得上清粗酶液。
实施例5、RsS13GT突变体的体外功能鉴定1
体外酶催化测定体系为500μL,反应体系包括:0.25mM的甜菊醇-19-O-葡萄糖酯(steviol 19-O-β-D-glucoside),1.5mM的UDP葡萄糖,10mM MgCl2,100μL突变体上清粗酶液,用Buffer A补足体积到500μL。37℃反应2h。待反应结束后,加等体积正丁醇终止反应,用等体积的正丁醇萃取3次,将3次萃取的有机相混合,在真空浓缩仪中离心蒸干,然后使用500μL甲醇或甲醇-水(50/50,v/v)复溶,使用HPLC进行产物分析。HPLC检测条件:色谱柱:反相检测波长为205nm;流动相:乙腈-水混合物梯度洗脱,在0到20min内比例由20:80升到60:40,流速1mL/min。
经HPLC检测,突变体RsS13GT F119I,RsS13GT L141M,RsS13GT Y143W,RsS13GTI145L,RsS13GT N379G和RsS13GT FA398SW均可以将底物甜菊醇-19-O-葡萄糖酯(steviol19-O-β-D-glucoside)转化为其13位糖基化产物甜叶悬钩子苷(rubusoside),其HPLC保留时间亦与甜叶悬钩子苷标准品一致。与野生型RsS13GT相比,这些突变体的相对活性显示如图7。突变体RsS13GT F119I(相对活性167%),RsS13GT M124L(相对活性213%),RsS13GTL141M(相对活性155%)和RsS13GT I142Y(相对活性112%)较野生型RsS13GT的活性相对提高。
实施例6、RsS13GT突变体的体外功能鉴定2
对RsS13GT突变体A16F,P82S,T83I,I86R,I90L,F119I,M124L,A126V,A140M,L141M,I142Y,Y143W,I145L,S149G,L153F,S198L,F199D,C200W,F210L,Y212F,I302T,N379G,F397S,A398W。
体外酶催化测定体系、HPLC检测体系及方法基本同实施例6,不同点在于进行6次HPLC实验测定,取数据平均值。
结果显示,突变体RsS13GT P82S,RsS13GT T83I,RsS13GT I86R,RsS13GT I90L,RsS13GT F119I,RsS13GT M124L,RsS13GT A126V,RsS13GT A140M,RsS13GT L141M,RsS13GTI142Y,RsS13GT Y143W,RsS13GT I145L,RsS13GT S149G,RsS13GT L153F,RsS13GT S198L,RsS13GT C200W,RsS13GT F210L,RsS13GT Y212F,RsS13GT I302T,RsS13GT N379G,RsS13GTF397S和RsS13GT A398W均可以将底物甜菊醇-19-O-葡萄糖酯(steviol 19-O-β-D-glucoside)转化为其13位糖基化产物甜叶悬钩子苷(rubusoside),其HPLC保留时间亦与甜叶悬钩子苷标准品一致。与野生型RsS13GT相比,这些突变体的相对活性显示如图8。突变体RsS13GT P82S(相对活性240%),RsS13GT T83I(相对活性231%),RsS13GT I86R(相对活性197%),RsS13GT I90L(相对活性113%),RsS13GT F119I(相对活性192%),RsS13GT A126V(相对活性247%),RsS13GT A140M(相对活性250%),RsS13GT L141M(相对活性224%),RsS13GT S149G(相对活性175%),RsS13GT L153F(相对活性230%),RsS13GT Y212F(相对活性382%)和RsS13GT I302T(相对活性134%)较野生型RsS13GT的活性相对提高。
该结果表明,D121的空间结构的附近距离范围内的氨基酸残基(第120-140位)突变后活性有较大提高,第80-90位,第149、153、212和302位突变后可能影响与底物的相互作用,使得活性较大提高。另外,对于第21位组氨酸附近的丙氨酸(A)的改造可能使得活性有大幅下降(突变体A16F,A398W)。
在本发明提及的所有文献都在本申请中引用作为参考,就如同每一篇文献被单独引用作为参考那样。此外应理解,在阅读了本发明的上述讲授内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本申请所附权利要求书所限定的范围。
序列表
<110> 中国科学院上海生命科学研究院
<120> 新型UDP-糖基转移酶及其应用
<130> 176554Z1
<160> 63
<170> SIPOSequenceListing 1.0
<210> 1
<211> 481
<212> PRT
<213> 甜叶悬钩子(Rubus suavissimus S. Lee)
<400> 1
Met Ala Ser Gly Tyr Asn His Lys Pro His Ala Val Cys Ile Pro Ala
1 5 10 15
Pro Ala Gln Ser His Ile Lys Ala Met Leu Lys Leu Ala Lys Ile Leu
20 25 30
His His Arg Gly Phe His Ile Thr Phe Val Asn Thr Glu Phe Asn His
35 40 45
Lys Arg Phe Leu Glu Ser Arg Gly Pro Asn Ser Leu Asp Gly Leu Pro
50 55 60
Asp Phe His Phe Glu Ala Ile Pro Asp Gly Phe Pro Glu Ser Gly Glu
65 70 75 80
Asp Pro Thr Gln Asp Ile Thr Val Leu Ile Glu Ser Val Arg Ile His
85 90 95
Leu Leu Ala Pro Phe Arg Asp Leu Leu Ile Lys Leu Asn Ser Thr Ser
100 105 110
Ser Pro Val Thr Cys Ile Phe Ser Asp Gly Phe Met Ser Ala Phe Thr
115 120 125
Thr Arg Ala Ala Glu Glu Leu Gly Ile Pro Ile Ala Leu Ile Tyr Thr
130 135 140
Ile Ser Ala Cys Ser Phe Met Gly Leu Arg Lys Phe Arg Thr Leu Leu
145 150 155 160
Glu Lys Gly Leu Ala Pro Leu Lys Asp Glu Ser Cys Met Thr Asn Gly
165 170 175
Phe Leu Asp Lys Val Ile Glu Trp Ile Pro Arg Lys Lys Asp Ile Arg
180 185 190
Leu Trp Asp Leu Pro Ser Phe Cys Arg Thr Thr Asn Pro Asp Asp Ile
195 200 205
Met Phe His Tyr Thr Met Glu Ala Ala Glu Glu Ala Asn Lys Ala Ser
210 215 220
Ala Val Val Leu Leu Thr Tyr Asp Ala Leu Glu Lys Asp Val Leu Glu
225 230 235 240
Val Leu Ser Ser Ser Ile Ser Pro Pro Val Tyr Thr Ile Gly Pro Leu
245 250 255
Gln Leu Leu Leu Asp Gln Ile Ala Glu Asp Pro Leu Lys Pro Met Gly
260 265 270
Tyr Ser Leu Trp Lys Glu Glu Thr Asp Cys Leu Gln Trp Leu Gln Ser
275 280 285
Lys Ala Pro Asn Ser Ile Val Tyr Val Asn Phe Gly Ser Ile Ala Val
290 295 300
Leu Thr Pro Glu Gln Leu Val Glu Phe Gly Trp Gly Leu Ala Asn Thr
305 310 315 320
Lys Leu Pro Phe Phe Trp Val Ile Arg Pro Asp Leu Val Val Gly Asn
325 330 335
Ser Ala Ile Leu Pro Pro Glu Phe Glu Thr Glu Thr Lys Asp Arg Gly
340 345 350
Leu Ile Ala Ser Trp Cys Pro Gln Glu Gln Val Leu Asn His Pro Ser
355 360 365
Val Gly Gly Phe Leu Thr His Ser Gly Trp Asn Ser Ile Ile Glu Ser
370 375 380
Val Thr Ala Gly Val Pro Met Leu Cys Trp Pro Phe Phe Ala Asp Gln
385 390 395 400
Gln Thr Asn Ser Tyr Tyr Thr Cys Asn Glu Trp Gly Ile Gly Met Glu
405 410 415
Ile Asn Ser Asn Val Lys Arg Asp Asn Val Glu Lys Leu Val Arg Glu
420 425 430
Leu Met Asp Gly Glu Lys Gly Lys Lys Met Lys Asn Lys Val Leu Glu
435 440 445
Trp Lys Arg Leu Ala Glu Glu Ala Thr Ala Pro His Gly Ser Ser Ser
450 455 460
Thr Asn Leu Asp Asn Leu Val Asn Gln Val Leu Leu Arg Lys Arg Thr
465 470 475 480
Tyr
<210> 2
<211> 471
<212> PRT
<213> 甜叶悬钩子(Rubus suavissimus S. Lee)
<400> 2
Met Thr Gln His Arg Phe Leu Leu Val Thr Tyr Pro Ala Gln Gly His
1 5 10 15
Ile Asn Pro Ser Leu Gln Phe Ala Lys Arg Leu Ile Ser Thr Thr Gly
20 25 30
Ala Asp Val Thr Phe Val Thr Ala Leu Ser Ala His His Arg Ile Asn
35 40 45
Asn Gly Ser Ser Thr Pro Arg Gly Leu Thr Phe Ala Pro Phe Ser Asp
50 55 60
Gly Tyr Asp Asp Gly Tyr Lys Pro Glu Asp Asp Ile Asp His Tyr Met
65 70 75 80
Ser Glu Leu Arg Arg Arg Gly Ser Lys Ala Ile Ala Asp Ile Val Val
85 90 95
Ser Ser Ala Asn Gln Gly His Pro Tyr Thr Cys Ile Val Tyr Thr Met
100 105 110
Leu Leu Pro Trp Val Glu Glu Val Ala Arg Glu Leu His Leu Pro Thr
115 120 125
Ala Phe Val Trp Ile Gln Pro Ala Thr Val Phe Ala Ile Tyr Tyr Tyr
130 135 140
Tyr Phe Asn Gly Tyr Lys Asp Leu Ile Arg Asn Asn Ala Asn Asn Ser
145 150 155 160
Asp Pro Ser Tyr Ala Val Glu Leu Pro Gly Leu Pro Leu Ala Met Lys
165 170 175
Ser Arg Asp Leu Pro Ser Phe Met Val Asp Ser Asn Pro Tyr Asn Phe
180 185 190
Ala Leu Pro Leu Ile Glu Glu His Phe Lys Leu Leu Gly Lys Glu Arg
195 200 205
Lys Pro Thr Ile Met Val Asn Thr Phe Asp Ala Leu Glu Pro Glu Ala
210 215 220
Leu Lys Ala Ile Asp Lys Tyr Asn Leu Ile Gly Ile Gly Pro Leu Met
225 230 235 240
Pro Ser Ala Phe Leu Asp Gly Lys Asp Pro Ser Asp Lys Ser Phe Gly
245 250 255
Gly Asp Leu Phe Gln Lys Ser Lys Asp Ser Ser Tyr Ile Glu Trp Leu
260 265 270
Asn Ser Lys Pro Lys Glu Ser Ile Val Tyr Val Ser Phe Gly Ser Met
275 280 285
Ser Val Leu Ser Lys Ile Gln Met Glu Glu Ile Ala Lys Gly Leu Leu
290 295 300
Asp Ser Gly Arg Pro Phe Leu Trp Val Ile Arg Glu Asn Arg Lys Asn
305 310 315 320
Ala Glu Asp Lys Glu Glu Lys Leu Ser Cys Arg Glu Glu Leu Glu Glu
325 330 335
Leu Gly Met Ile Val Pro Trp Cys Ser Gln Val Glu Val Leu Ser Asn
340 345 350
Pro Ser Leu Gly Cys Phe Val Thr His Cys Gly Trp Asn Ser Ser Leu
355 360 365
Glu Ser Leu Val Ser Gly Ile Pro Val Val Ala Phe Pro Gln Trp Thr
370 375 380
Asp Gln Gly Thr Asn Ala Lys Leu Ile Glu Asp Thr Trp Lys Thr Gly
385 390 395 400
Met Arg Val Ala Pro Asn Glu Glu Gly Val Val Val Gly Glu Glu Leu
405 410 415
Lys Arg Cys Leu Asp Ile Val Met Gly Ser Glu Glu Met Arg Arg Asn
420 425 430
Ala Lys Lys Trp Lys Asp Leu Ala Arg Glu Ala Val Ser Glu Gly Gly
435 440 445
Ser Ser Asp Lys Asn Leu Lys Ala Phe Leu Asp Glu Ile Gly Asp Gly
450 455 460
Cys Thr Phe Gly Ser Leu Glu
465 470
<210> 3
<211> 484
<212> PRT
<213> 甜叶悬钩子(Rubus suavissimus S. Lee)
<400> 3
Met Glu Thr Lys Ser His Gln Lys Leu His Ile Phe Phe Leu Pro Phe
1 5 10 15
Met Gly Arg Gly His Thr Leu Pro Leu Ile Asp Ile Ala Lys Leu Phe
20 25 30
Ala Ser Arg Gly Val Lys Ser Thr Met Ile Thr Thr Pro Ala Asn Ala
35 40 45
Pro Leu Phe Ser Lys Ala Ile Gln Thr Ser Lys Ser Ser Gly Leu Glu
50 55 60
Ile Glu Leu Leu Leu Ile Lys Phe Pro Ser Thr Glu Val Gly Leu Pro
65 70 75 80
Glu Gly Ile Glu Ser Thr Asn Trp Ala Glu Thr Lys Glu Met Arg Glu
85 90 95
Lys Phe Tyr Lys Ala Leu Thr Leu Leu Glu Pro Gln Val Glu Gln Leu
100 105 110
Leu Asp Gln His Arg Pro His Cys Leu Val Ala Ser Thr Leu Phe His
115 120 125
Trp Thr Thr Asp Val Ala Ala Lys Phe Gly Ile Pro Arg Leu Met Phe
130 135 140
His Gly Pro Gly Tyr Phe Pro Leu Cys Ala Ala Met Ser Val Arg Gln
145 150 155 160
Tyr Gln Pro His Met Lys Val Ser Ser Asp Ser Glu Ser Phe Val Ile
165 170 175
Pro Asn Leu Pro His Glu Ile Lys Thr Thr Arg Asn Glu Leu Pro Ser
180 185 190
Phe Val Thr Gln Asn Gly Glu Thr Glu Leu Thr Lys Leu Leu Lys Ala
195 200 205
Cys Arg Glu Thr Glu Glu Arg Ser Tyr Gly Thr Ile Ile Asn Ser Phe
210 215 220
Tyr Glu Leu Glu Pro Asp Tyr Ala Asp His Tyr Arg Lys Val Phe Gly
225 230 235 240
Arg Lys Ser Trp His Ile Gly Pro Val Ser Leu Cys Asn Met Ala Glu
245 250 255
Lys Glu Lys Leu Glu Arg Gly Arg Glu Gly Ser Val Val Asp Glu Val
260 265 270
His Asp Cys Leu Asn Trp Leu Asn Ser Lys Lys Pro Asn Ser Val Val
275 280 285
Tyr Ile Cys Phe Gly Ser Ile Asn Ser Phe Ser Asp Cys Glu Leu Leu
290 295 300
Glu Ile Ala Leu Gly Leu Glu Ala Ser Arg Gln Gln Phe Ile Trp Val
305 310 315 320
Val Lys Arg Glu Lys Asn Asp Asn Asp Glu Trp Leu Pro Glu Gly Phe
325 330 335
Glu Gln Arg Met Glu Gly Arg Gly Leu Ile Ile Arg Gly Trp Ala Pro
340 345 350
Gln Leu Leu Ile Leu Gln His Glu Ala Thr Gly Ala Phe Leu Thr His
355 360 365
Cys Gly Trp Asn Ser Ile Leu Glu Gly Val Ser Ala Gly Val Pro Met
370 375 380
Ile Thr Trp Pro Val Phe Ala Asp Gln Phe Asn Asn Glu Lys Leu Val
385 390 395 400
Thr Gln Ile Leu Gly Ile Gly Val Ala Val Gly Ala Gln Lys Ser Glu
405 410 415
Asp Gly Ser Met Lys Ser Glu Ala Arg Val Lys Arg Glu Ala Ile Glu
420 425 430
Lys Ala Val Thr Glu Ile Met Val Gly Asp Glu Gln Glu Glu Met Arg
435 440 445
Arg Lys Val Phe Ala Leu Ala Glu Met Ala Arg Arg Ala Val Glu Glu
450 455 460
Gly Gly Ser Ser Phe Thr Asn Leu Thr Ala Leu Met Glu Glu Leu Arg
465 470 475 480
Ser Phe Val Ser
<210> 4
<211> 456
<212> PRT
<213> 甜叶悬钩子(Rubus suavissimus S. Lee)
<400> 4
Met Glu Ser Lys Ile His His Phe Leu Ile Ile Ser Cys Ala Gly Gln
1 5 10 15
Gly His Leu Asn Pro Ser Leu Gln Leu Ala Lys Arg Leu Ile Asp Leu
20 25 30
Gly Gly Ser His Val Thr Phe Val Thr Asn Ala His Gly Leu Thr Gln
35 40 45
Ile Lys Ser Leu Pro Ser Leu Glu Gly Leu Ser Phe Ala Ser Phe Cys
50 55 60
Asp Gly Phe Asp Gly Gly Val Lys Pro Asp Asp Pro Asn His Ile Met
65 70 75 80
Ser Glu Leu Lys Arg Ala Gly Ser Gln Ser Leu Ala Ala Leu Ile Glu
85 90 95
Lys Ile Ser Lys Ser Asp Glu His Gly Pro Ile Thr Phe Leu Ile Tyr
100 105 110
Thr Ile Leu Leu Pro Trp Ala Ala Glu Val Ala Ser Asp Phe Gly Ile
115 120 125
Ala Ser Ala Phe Leu Cys Ile Gln Ser Thr Thr Ser Phe Ala Leu Cys
130 135 140
Tyr His Tyr Phe Lys Asp Cys Tyr Lys Asp Gln Ser Thr Leu Pro Phe
145 150 155 160
Pro Ser Cys Ile Thr Ile Asp Gly Met Pro Pro Phe Ala Pro Glu Ala
165 170 175
Leu Pro Ser Tyr Leu Leu Pro Thr Ser Pro His Val Ser Ile Leu Pro
180 185 190
Thr Phe Gln Glu His Tyr Gln Ile Leu Glu Arg Asp Pro Asn Ser Cys
195 200 205
Val Leu Leu Asn Thr Phe Asp Gly Leu Glu Glu Ala Ala Ile Arg Asp
210 215 220
Met Arg Gly His Met Asn Leu Ile Thr Val Gly Pro Leu Phe Arg Ser
225 230 235 240
Asn Asp Ala Glu Val Arg Cys Asp Leu Phe Asp Arg Ser Gly Asp Asp
245 250 255
Tyr Leu Gln Trp Leu Asp Ser Lys Ala Asp Ser Ser Val Val Tyr Val
260 265 270
Ser Phe Gly Ser Met Val Val Leu Lys Ser Gly Gln Ile Glu Glu Ile
275 280 285
Leu His Gly Leu Val Asp Ser Gly Leu Pro Val Leu Trp Val Ile Arg
290 295 300
Lys Ser Gly Asn Glu Gly Asp Glu Glu Thr Leu Gln Asn Leu Ile Asn
305 310 315 320
Ser Thr Leu Lys Lys Glu Gln Gly Leu Ile Val Pro Trp Cys Ser Gln
325 330 335
Val Glu Val Leu Ser His Lys Ser Ile Gly Cys Phe Val Thr His Cys
340 345 350
Gly Trp Asn Ser Thr Ile Glu Ser Leu Ala Ala Gly Val Pro Ile Val
355 360 365
Gly Cys Pro His Phe Ser Asp Gln Asn Thr Asn Ala Lys Leu Val Glu
370 375 380
Glu Leu Trp Gly Thr Gly Val Arg Ala Arg Val Asn Ala Glu Gly Leu
385 390 395 400
Phe Glu His Asp Glu Ile Lys Arg Cys Leu Glu Met Val Ile Gly Asp
405 410 415
Gly Gln Thr Gly Glu Glu Ile Arg Arg Asn Ala Gln Lys Trp Lys Gly
420 425 430
Leu Ala Met Glu Ala Val Lys Glu Gly Gly Ala Ser Asn Asp Asn Leu
435 440 445
Met Asn Phe Val Ile Arg Leu Ser
450 455
<210> 5
<211> 489
<212> PRT
<213> 甜叶悬钩子(Rubus suavissimus S. Lee)
<400> 5
Met Ala Ser Gln Glu Cys Gln Leu His Phe Val Leu Phe Pro Phe Met
1 5 10 15
Ala Gln Gly His Met Ile Pro Met Ile Asp Ile Ala Arg Leu Leu Ala
20 25 30
Glu Arg Gly Leu Ile Ile Thr Ile Val Thr Thr Pro His Asn Ala Ser
35 40 45
Arg Phe Asp Lys Val Leu Ala Arg Ala Arg Glu Ser Gly Leu Gln Ile
50 55 60
Arg Leu Ile Gln Leu Lys Phe Pro Cys Glu Glu Ala Gly Leu Pro Arg
65 70 75 80
Gly Cys Glu Asn Val Asp Met Met Pro Ser Thr Asn Leu Ala Ser Ser
85 90 95
Phe Phe Asn Gly Thr Lys Gly Leu Gln Glu Pro Val Glu Lys Leu Phe
100 105 110
Glu Glu Leu Thr Pro Lys Pro Ser Cys Ile Ile Ser Asp Met Cys Leu
115 120 125
Pro Trp Thr Ile Asn Ile Ser His Met Phe Lys Ile Pro Arg Ile Ser
130 135 140
Phe Ser Gly Thr Cys Cys Phe Leu Leu Val Cys Phe Gly Asn Ala Cys
145 150 155 160
Ile Ser Lys Val Val Pro Asp Ile Thr Ser Glu Thr Glu Tyr Phe Val
165 170 175
Leu Pro Asp Leu Pro Asp Arg Ile Glu Val Thr Lys Ala Gln Leu Pro
180 185 190
Ala Ala Ile Ala Pro Asn Met Thr Asp Phe Thr Glu Thr Leu Arg Ala
195 200 205
Ala Glu Leu Ala Ser Tyr Gly Val Ile Met Asn Ser Phe Glu Glu Leu
210 215 220
Glu Pro Ala Tyr Val Glu Glu Tyr Lys Lys Val Lys Lys Asp Lys Leu
225 230 235 240
Trp Cys Ile Gly Pro Ala Ser Leu Cys Asn Lys Asp Glu Leu Asp Lys
245 250 255
Ala Gln Arg Gly Asn Lys Ala Ser Val Asp Glu His His Cys Leu Lys
260 265 270
Trp Leu Asp Ser Trp Glu Pro Ser Ser Val Leu Tyr Ala Cys Phe Gly
275 280 285
Ser Leu Cys Asn Leu Ile Pro Ala Gln Leu Ile Glu Leu Gly Leu Gly
290 295 300
Leu Glu Ala Ser Asn Lys Pro Phe Ile Trp Val Val Arg Gly Ser Ser
305 310 315 320
Gln Leu Glu Glu Leu Asp Lys Trp Ile Ala Glu Asn Arg Phe Glu Glu
325 330 335
Arg Thr Lys Gly Arg Ser Leu Leu Ile Arg Gly Trp Ala Pro Gln Thr
340 345 350
Leu Ile Leu Ser His Pro Ala Val Gly Gly Phe Leu Thr His Cys Gly
355 360 365
Trp Asn Ser Thr Leu Glu Gly Ile Cys Ala Gly Val Pro Leu Ile Thr
370 375 380
Trp Pro Leu Phe Gly Asp Gln Phe Leu Asn Glu Lys Leu Val Glu Gln
385 390 395 400
Ile Leu Lys Ile Ala Val Arg Val Gly Val Glu Tyr Pro Met Lys Trp
405 410 415
Gly Glu Glu Glu Asn Ile Gly Val Leu Val Lys Lys Glu Asn Val Met
420 425 430
Glu Ala Ile Asp Lys Leu Met Asp Gly Glu Glu Ser Leu Ala Arg Arg
435 440 445
Asp Arg Ala Arg Glu Leu Ala Lys Met Ala Lys Arg Ala Val Glu Glu
450 455 460
Gly Gly Ser Ser His Leu Asn Ile Glu Leu Leu Ile Lys Asp Ile Met
465 470 475 480
Gln Gln Gly Asn Cys Thr Lys Thr Asn
485
<210> 6
<211> 29
<212> DNA
<213> 引物(Primer)
<400> 6
ggaattccat atgatgacgc agcaccgct 29
<210> 7
<211> 32
<212> DNA
<213> 引物(Primer)
<400> 7
ataagaatgc ggccgctcat tctaggctac ca 32
<210> 8
<211> 38
<212> DNA
<213> 引物(Primer)
<400> 8
ggaattccat atggaaacta aatcccatca gaagcttc 38
<210> 9
<211> 45
<212> DNA
<213> 引物(Primer)
<400> 9
ataagaatgc ggccgcttaa gacacaaaag acctcagctc ttcca 45
<210> 10
<211> 27
<212> DNA
<213> 引物(Primer)
<400> 10
ctagctagca tggagagtaa gattcat 27
<210> 11
<211> 32
<212> DNA
<213> 引物(Primer)
<400> 11
ataagaatgc ggccgctcag ctcaaccttc tg 32
<210> 12
<211> 33
<212> DNA
<213> 引物(Primer)
<400> 12
cgggatccat ggcttctcaa gaatgccagc ttc 33
<210> 13
<211> 46
<212> DNA
<213> 引物(Primer)
<400> 13
ataagaatgc ggccgcttag tttgtctttg tgcaatttcc ttgttg 46
<210> 14
<211> 38
<212> DNA
<213> 引物(Primer)
<400> 14
ctagctagca tggcttctgg ttataatcat aagcctca 38
<210> 15
<211> 43
<212> DNA
<213> 引物(Primer)
<400> 15
ataagaatgc ggccgcctag tacgtgcgct tccttaatag gac 43
<210> 16
<211> 41
<212> DNA
<213> 引物(Primer)
<400> 16
gctgtttgta ttccatttcc tgctcaaagc cacattaagg c 41
<210> 17
<211> 33
<212> DNA
<213> 引物(Primer)
<400> 17
aaatggaata caaacagcat gaggcttatg att 33
<210> 18
<211> 36
<212> DNA
<213> 引物(Primer)
<400> 18
gaatcaggtg aagattcaac gcaagatatc actgtg 36
<210> 19
<211> 31
<212> DNA
<213> 引物(Primer)
<400> 19
aatcttcacc tgattctgga aatccatcag g 31
<210> 20
<211> 45
<212> DNA
<213> 引物(Primer)
<400> 20
caggtgaaga tccaattcaa gatatcactg tgcttattga atccg 45
<210> 21
<211> 32
<212> DNA
<213> 引物(Primer)
<400> 21
aattggatct tcacctgatt ctggaaatcc at 32
<210> 22
<211> 39
<212> DNA
<213> 引物(Primer)
<400> 22
gatccaacgc aagatcgcac tgtgcttatt gaatccgtc 39
<210> 23
<211> 31
<212> DNA
<213> 引物(Primer)
<400> 23
cgatcttgcg ttggatcttc acctgattct g 31
<210> 24
<211> 44
<212> DNA
<213> 引物(Primer)
<400> 24
gatatcactg tgcttctgga atccgtcaga atccatcttt tggc 44
<210> 25
<211> 30
<212> DNA
<213> 引物(Primer)
<400> 25
cagaagcaca gtgatatctt gcgttggatc 30
<210> 26
<211> 31
<212> DNA
<213> 引物(Primer)
<400> 26
ccagtgactt gcattatttc agatggtttc a 31
<210> 27
<211> 32
<212> DNA
<213> 引物(Primer)
<400> 27
taatgcaagt cactggagaa ctagtactgt tg 32
<210> 28
<211> 33
<212> DNA
<213> 引物(Primer)
<400> 28
ttttcagatg gtttcctttc cgcttttacc acc 33
<210> 29
<211> 33
<212> DNA
<213> 引物(Primer)
<400> 29
aaggaaacca tctgaaaaaa tgcaagtcac tgg 33
<210> 30
<211> 33
<212> DNA
<213> 引物(Primer)
<400> 30
ttcagatggt ttcatgtccg tttttaccac cag 33
<210> 31
<211> 33
<212> DNA
<213> 引物(Primer)
<400> 31
acggacatga aaccatctga aaaaatgcaa gtc 33
<210> 32
<211> 45
<212> DNA
<213> 引物(Primer)
<400> 32
cttggaattc ctattatgtt gatctacact atttctgctt gcagc 45
<210> 33
<211> 28
<212> DNA
<213> 引物(Primer)
<400> 33
cataatagga attccaagtt cctcggca 28
<210> 34
<211> 36
<212> DNA
<213> 引物(Primer)
<400> 34
ggaattccta ttgcaatgat ctacactatt tctgct 36
<210> 35
<211> 30
<212> DNA
<213> 引物(Primer)
<400> 35
cattgcaata ggaattccaa gttcctcggc 30
<210> 36
<211> 39
<212> DNA
<213> 引物(Primer)
<400> 36
attcctattg cattgtatta cactatttct gcttgcagc 39
<210> 37
<211> 30
<212> DNA
<213> 引物(Primer)
<400> 37
atacaatgca ataggaattc caagttcctc 30
<210> 38
<211> 37
<212> DNA
<213> 引物(Primer)
<400> 38
cctattgcat tgatctggac tatttctgct tgcagct 37
<210> 39
<211> 31
<212> DNA
<213> 引物(Primer)
<400> 39
ccagatcaat gcaataggaa ttccaagttc c 31
<210> 40
<211> 33
<212> DNA
<213> 引物(Primer)
<400> 40
ctattgcatt gatctacact ctttctgctt gca 33
<210> 41
<211> 33
<212> DNA
<213> 引物(Primer)
<400> 41
gagtgtagat caatgcaata ggaattccaa gtt 33
<210> 42
<211> 29
<212> DNA
<213> 引物(Primer)
<400> 42
actatttctg cttgcggctt catgggatt 29
<210> 43
<211> 33
<212> DNA
<213> 引物(Primer)
<400> 43
cgcaagcaga aatagtgtag atcaatgcaa tag 33
<210> 44
<211> 30
<212> DNA
<213> 引物(Primer)
<400> 44
tgcagcttca tgggatttag gaaattccgc 30
<210> 45
<211> 29
<212> DNA
<213> 引物(Primer)
<400> 45
aaatcccatg aagctgcaag cagaaatag 29
<210> 46
<211> 51
<212> DNA
<213> 引物(Primer)
<400> 46
ttatgggatc taccactgtt ttgccgaact acaaatcctg atgacatcat g 51
<210> 47
<211> 38
<212> DNA
<213> 引物(Primer)
<400> 47
cagtggtaga tcccataatc ggatatcttt ctttctcg 38
<210> 48
<211> 35
<212> DNA
<213> 引物(Primer)
<400> 48
tgggatctac caagcgattg ccgaactaca aatcc 35
<210> 49
<211> 38
<212> DNA
<213> 引物(Primer)
<400> 49
atcgcttggt agatcccata atcggatatc tttctttc 38
<210> 50
<211> 34
<212> DNA
<213> 引物(Primer)
<400> 50
gatctaccaa gcttttggcg aactacaaat cctg 34
<210> 51
<211> 33
<212> DNA
<213> 引物(Primer)
<400> 51
ccaaaagctt ggtagatccc ataatcggat atc 33
<210> 52
<211> 35
<212> DNA
<213> 引物(Primer)
<400> 52
cctgatgaca tcatgctgca ctacaccatg gaagc 35
<210> 53
<211> 32
<212> DNA
<213> 引物(Primer)
<400> 53
cagcatgatg tcatcaggat ttgtagttcg gc 32
<210> 54
<211> 37
<212> DNA
<213> 引物(Primer)
<400> 54
gacatcatgt tccactttac catggaagct gctgaag 37
<210> 55
<211> 35
<212> DNA
<213> 引物(Primer)
<400> 55
aaagtggaac atgatgtcat caggatttgt agttc 35
<210> 56
<211> 29
<212> DNA
<213> 引物(Primer)
<400> 56
gtcaattttg gcagcaccgc ggttttgac 29
<210> 57
<211> 36
<212> DNA
<213> 引物(Primer)
<400> 57
ggtgctgcca aaattgacat aaacaattga gtttgg 36
<210> 58
<211> 33
<212> DNA
<213> 引物(Primer)
<400> 58
tctcacacac agtggttggg gttcaatcat tga 33
<210> 59
<211> 33
<212> DNA
<213> 引物(Primer)
<400> 59
ccccaaccac tgtgtgtgag aaatcctcca act 33
<210> 60
<211> 37
<212> DNA
<213> 引物(Primer)
<400> 60
gctgtgttgg ccattcagcg cagaccagca aacaaac 37
<210> 61
<211> 27
<212> DNA
<213> 引物(Primer)
<400> 61
gctgaatggc caacacagca tcggcac 27
<210> 62
<211> 42
<212> DNA
<213> 引物(Primer)
<400> 62
tgttggccat tcttttggga ccagcaaaca aacagttact ac 42
<210> 63
<211> 30
<212> DNA
<213> 引物(Primer)
<400> 63
ccaaaagaat ggccaacaca gcatcggcac 30
Claims (18)
1.分离的多肽,其特征在于,所述多肽选自:
(a) SEQ ID NO: 1所示氨基酸序列的多肽;或
(b) 在SEQ ID NO: 1所示氨基酸序列基础上,将第119或141位进行单突变,所述单突变为F119I或L141M。
2.如权利要求1所述的多肽,其特征在于,所述的多肽是将第119位进行突变,所述突变为F119I。
3.如权利要求1所述的多肽,其特征在于,所述的多肽是将第141位进行突变,所述突变为L141M。
4.分离的多核苷酸,其特征在于,它编码权利要求1所述的多肽。
5.一种载体,其特征在于,它含有权利要求4所述的多核苷酸。
6.一种遗传工程化的宿主菌,其特征在于,它含有权利要求5所述的载体,或其基因组中整合有权利要求4所述的多核苷酸。
7.一种权利要求1所述的多肽的制备方法,其特征在于,该方法包含:培养权利要求6所述的宿主菌;收集含有权利要求1所述的多肽的培养物。
9.如权利要求8所述的用途,其特征在于,所述的具有母核(III)结构的化合物为:甜菊醇-19-O-葡萄糖酯或甜菊醇。
10.如权利要求8所述的用途,其特征在于,所述的式(IV)结构的化合物为:甜叶悬钩子苷或甜菊醇单糖苷。
11.如权利要求8~10任一所述的用途,其特征在于,所述的糖基的供体是含有糖基的化合物。
12.如权利要求11所述的用途,其特征在于,所述的糖基的供体为UDP-糖。
13.如权利要求12所述的用途,其特征在于,所述的UDP-糖为:UDP-葡萄糖,UDP-鼠李糖或UDP-木糖。
14.一种用于糖基转移的组合物,其特征在于,它含有权利要求1所述的多肽或含有权利要求6所述的宿主菌。
16.如权利要求15所述的方法,其特征在于,所述的糖基的供体是含有糖基的化合物。
17.如权利要求16所述的方法,其特征在于,所述的糖基的供体为UDP-糖。
18.如权利要求17所述的方法,其特征在于,所述的UDP-糖为UDP-葡萄糖,UDP-鼠李糖或UDP-木糖。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201710758391 | 2017-08-29 | ||
| CN2017107583917 | 2017-08-29 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN109423486A CN109423486A (zh) | 2019-03-05 |
| CN109423486B true CN109423486B (zh) | 2022-02-25 |
Family
ID=65514743
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201810995580.0A Active CN109423486B (zh) | 2017-08-29 | 2018-08-29 | 新型udp-糖基转移酶及其应用 |
Country Status (1)
| Country | Link |
|---|---|
| CN (1) | CN109423486B (zh) |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN110592040A (zh) * | 2019-09-18 | 2019-12-20 | 江苏施宇甜生物科技有限公司 | 一种用于生产upd糖基转移酶的重组枯草芽孢杆菌的工艺 |
| CN110592043B (zh) * | 2019-11-01 | 2022-10-18 | 广西师范大学 | 一种udp-葡萄糖基转移酶突变体及其应用 |
| CN113136373B (zh) * | 2020-01-20 | 2023-12-08 | 中国科学院分子植物科学卓越创新中心 | 碳苷糖基转移酶及其应用 |
| CN113265433B (zh) * | 2020-02-17 | 2023-12-26 | 中国科学院分子植物科学卓越创新中心 | 双功能碳苷糖基转移酶及其应用 |
| CN117343919B (zh) * | 2023-10-07 | 2024-04-19 | 广州佰数生物科技有限公司 | 一种类黄酮双羟基位点糖基转移酶及其应用 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN104093837A (zh) * | 2012-02-06 | 2014-10-08 | 三得利控股株式会社 | 来自啤酒花的单萜糖基转移酶及其利用方法 |
| CN105492453A (zh) * | 2013-05-28 | 2016-04-13 | 可口可乐公司 | 高纯度的甜菊醇糖苷 |
| CN106103729A (zh) * | 2013-11-01 | 2016-11-09 | 科纳根公司 | 甜菊醇糖苷的重组制备 |
| CN112080480A (zh) * | 2019-06-14 | 2020-12-15 | 中国科学院分子植物科学卓越创新中心 | 糖基转移酶突变体及其应用 |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9522929B2 (en) * | 2014-05-05 | 2016-12-20 | Conagen Inc. | Non-caloric sweetener |
-
2018
- 2018-08-29 CN CN201810995580.0A patent/CN109423486B/zh active Active
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN104093837A (zh) * | 2012-02-06 | 2014-10-08 | 三得利控股株式会社 | 来自啤酒花的单萜糖基转移酶及其利用方法 |
| CN105492453A (zh) * | 2013-05-28 | 2016-04-13 | 可口可乐公司 | 高纯度的甜菊醇糖苷 |
| CN106103729A (zh) * | 2013-11-01 | 2016-11-09 | 科纳根公司 | 甜菊醇糖苷的重组制备 |
| CN112080480A (zh) * | 2019-06-14 | 2020-12-15 | 中国科学院分子植物科学卓越创新中心 | 糖基转移酶突变体及其应用 |
Non-Patent Citations (5)
| Title |
|---|
| "PREDICTED: Prunus mume 7-deoxyloganetin glucosyltransferase-like (LOC103328851), transcript variant X1, mRNA";NCBI;《GenBank DataBase》;20160511;Accession No. XM_008231253.2 * |
| Diterpenoid UDP-Glycosyltransferases from Chinese Sweet Tea and Ashitaba Complete the Biosynthesis of Rubusoside;Yuwei Sun等;《Molecular Plant》;20180605;第11卷(第10期);图1和补充图9 * |
| NCBI."PREDICTED: Prunus mume 7-deoxyloganetin glucosyltransferase-like (LOC103328851), transcript variant X1, mRNA".《GenBank DataBase》.2016, * |
| UGT85A57[Rubus chingii var.suavissimus];Sun Y等;《GenBank DataBase》;20180620;Accession No.AWU66064.1 * |
| 穿心莲糖基转移酶的基因克隆及功能研究;李媛;《中国博士学位论文全文数据库(电子期刊)》;20200515;第17页 * |
Also Published As
| Publication number | Publication date |
|---|---|
| CN109423486A (zh) | 2019-03-05 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN109423486B (zh) | 新型udp-糖基转移酶及其应用 | |
| CN112080480B (zh) | 糖基转移酶突变体及其应用 | |
| EP2902410B1 (en) | Method for producing stevioside compounds by microorganism | |
| CN106103729A (zh) | 甜菊醇糖苷的重组制备 | |
| KR101455624B1 (ko) | 기능성 희귀당 사이코스의 생산능을 지닌 신규 클로스트리디움 볼티에 유래의 사이코스-3-에피머화 효소 및 이를 이용한 사이코스 생산방법 | |
| CN113136373B (zh) | 碳苷糖基转移酶及其应用 | |
| WO2021164673A1 (zh) | 双功能碳苷糖基转移酶及其应用 | |
| JP7000327B2 (ja) | 小分子グリコシル化のための方法 | |
| KR20210132405A (ko) | 알룰로스 에피머화 효소 변이체, 이의 제조방법 및 이를 이용한 알룰로스의 제조방법 | |
| CN115094074B (zh) | 双功能udp-糖基转移酶及其应用 | |
| CN112831481A (zh) | 糖基转移酶以及催化糖链延伸的方法 | |
| CN114045273B (zh) | 糖基转移酶OsUGT91C1突变体及其应用 | |
| US20240263152A1 (en) | Glycosyltransferase and application thereof | |
| CN114032222B (zh) | 糖链延伸糖基转移酶突变体及其编码基因以及基因工程菌和它们的应用 | |
| US20220275351A1 (en) | Preparation of Glycosyltransferase UGT76G1 Mutant and Use Thereof | |
| CN106434586B (zh) | 海藻糖合成酶突变体及其基因 | |
| KR20240032944A (ko) | 람노스가 고도로 특이적인 글리코실트랜스퍼라제 및 이의 응용 | |
| CN114277024B (zh) | 一种新型三萜合酶及其应用 | |
| CN116656641A (zh) | 咖啡酸o-甲基转移酶突变体及其应用 | |
| CN109868265B (zh) | 新型糖基转移酶及其应用 | |
| KR102131638B1 (ko) | 과당으로부터 타가토스로의 전환 활성이 향상된 헥수론산 c4-에피머화 효소 변이체 | |
| CN111424065A (zh) | 使用糖基转移酶对甜菊糖苷类化合物进行糖基化方法 | |
| KR101781259B1 (ko) | 진세노사이드 글리코시다제를 이용한 지페노사이드 lxxv 생산 방법 | |
| CN113881649B (zh) | 糖基转移酶OsUGT91C1突变体及其用途 | |
| KR20230120591A (ko) | 레바우디오사이드 생산 내열성 또는 고효율의 ugt 효소 제조방법 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| TA01 | Transfer of patent application right | ||
| TA01 | Transfer of patent application right |
Effective date of registration: 20200609 Address after: 200032 building 4, No. 300 Fenglin Road, Xuhui District, Shanghai Applicant after: Center for excellence and innovation in molecular plant science, Chinese Academy of Sciences Address before: 200031 Yueyang Road, Shanghai, No. 319, No. Applicant before: SHANGHAI INSTITUTES FOR BIOLOGICAL SCIENCES, CHINESE ACADEMY OF SCIENCES |
|
| GR01 | Patent grant | ||
| GR01 | Patent grant |