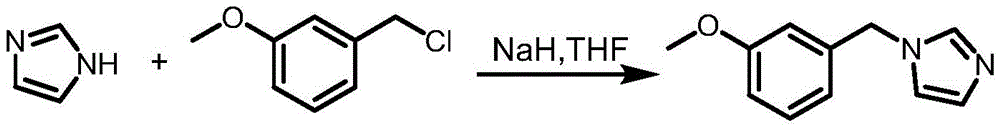CN109174181B - 一种负载双功能离子液体介孔聚合物的制备及其应用 - Google Patents
一种负载双功能离子液体介孔聚合物的制备及其应用 Download PDFInfo
- Publication number
- CN109174181B CN109174181B CN201810907784.4A CN201810907784A CN109174181B CN 109174181 B CN109174181 B CN 109174181B CN 201810907784 A CN201810907784 A CN 201810907784A CN 109174181 B CN109174181 B CN 109174181B
- Authority
- CN
- China
- Prior art keywords
- imidazole
- reaction
- preparation
- mesoporous polymer
- ionic liquid
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 229920000642 polymer Polymers 0.000 title claims abstract description 39
- 238000002360 preparation method Methods 0.000 title claims abstract description 34
- 239000002608 ionic liquid Substances 0.000 title claims abstract description 28
- 230000001588 bifunctional effect Effects 0.000 title claims abstract description 20
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 claims abstract description 115
- 239000003054 catalyst Substances 0.000 claims abstract description 26
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 claims abstract description 21
- -1 amine compounds Chemical class 0.000 claims abstract description 12
- ZHNUHDYFZUAESO-UHFFFAOYSA-N Formamide Chemical compound NC=O ZHNUHDYFZUAESO-UHFFFAOYSA-N 0.000 claims abstract description 10
- PAAZPARNPHGIKF-UHFFFAOYSA-N 1,2-dibromoethane Chemical compound BrCCBr PAAZPARNPHGIKF-UHFFFAOYSA-N 0.000 claims abstract description 8
- VMHLLURERBWHNL-UHFFFAOYSA-M Sodium acetate Chemical compound [Na+].CC([O-])=O VMHLLURERBWHNL-UHFFFAOYSA-M 0.000 claims abstract description 8
- 238000007210 heterogeneous catalysis Methods 0.000 claims abstract description 8
- 239000001632 sodium acetate Substances 0.000 claims abstract description 8
- 235000017281 sodium acetate Nutrition 0.000 claims abstract description 8
- 238000005342 ion exchange Methods 0.000 claims abstract description 4
- 238000006243 chemical reaction Methods 0.000 claims description 64
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Chemical compound O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 32
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 claims description 30
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 claims description 27
- 239000008367 deionised water Substances 0.000 claims description 26
- 229910021641 deionized water Inorganic materials 0.000 claims description 26
- 238000002156 mixing Methods 0.000 claims description 23
- 239000000047 product Substances 0.000 claims description 23
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 claims description 20
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 claims description 20
- 239000000203 mixture Substances 0.000 claims description 20
- 238000005406 washing Methods 0.000 claims description 20
- 239000000706 filtrate Substances 0.000 claims description 16
- 238000003756 stirring Methods 0.000 claims description 16
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 claims description 15
- 229910002092 carbon dioxide Inorganic materials 0.000 claims description 15
- 239000000243 solution Substances 0.000 claims description 15
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 claims description 14
- 238000001035 drying Methods 0.000 claims description 14
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 claims description 12
- PARWUHTVGZSQPD-UHFFFAOYSA-N phenylsilane Chemical compound [SiH3]C1=CC=CC=C1 PARWUHTVGZSQPD-UHFFFAOYSA-N 0.000 claims description 12
- 239000000543 intermediate Substances 0.000 claims description 11
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 11
- 238000010992 reflux Methods 0.000 claims description 11
- 239000001569 carbon dioxide Substances 0.000 claims description 10
- 238000001914 filtration Methods 0.000 claims description 10
- 239000002243 precursor Substances 0.000 claims description 10
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 claims description 10
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 claims description 9
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 claims description 8
- 238000004440 column chromatography Methods 0.000 claims description 8
- 238000002390 rotary evaporation Methods 0.000 claims description 8
- 125000006497 3-methoxybenzyl group Chemical group [H]C1=C([H])C(=C([H])C(OC([H])([H])[H])=C1[H])C([H])([H])* 0.000 claims description 7
- BMYNFMYTOJXKLE-UHFFFAOYSA-N 3-azaniumyl-2-hydroxypropanoate Chemical compound NCC(O)C(O)=O BMYNFMYTOJXKLE-UHFFFAOYSA-N 0.000 claims description 6
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 claims description 6
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 claims description 5
- 125000004218 chloromethyl group Chemical group [H]C([H])(Cl)* 0.000 claims description 5
- UZKWTJUDCOPSNM-UHFFFAOYSA-N methoxybenzene Substances CCCCOC=C UZKWTJUDCOPSNM-UHFFFAOYSA-N 0.000 claims description 5
- 239000011259 mixed solution Substances 0.000 claims description 5
- 238000003786 synthesis reaction Methods 0.000 claims description 5
- 229910052757 nitrogen Inorganic materials 0.000 claims description 4
- KEAYESYHFKHZAL-UHFFFAOYSA-N Sodium Chemical compound [Na] KEAYESYHFKHZAL-UHFFFAOYSA-N 0.000 claims description 3
- 238000001354 calcination Methods 0.000 claims description 3
- 238000010520 demethylation reaction Methods 0.000 claims description 3
- 239000008098 formaldehyde solution Substances 0.000 claims description 3
- 239000011521 glass Substances 0.000 claims description 3
- 239000002994 raw material Substances 0.000 claims description 3
- 229920006395 saturated elastomer Polymers 0.000 claims description 3
- 239000011734 sodium Substances 0.000 claims description 3
- 239000012312 sodium hydride Substances 0.000 claims description 3
- 229910000104 sodium hydride Inorganic materials 0.000 claims description 3
- 239000004721 Polyphenylene oxide Substances 0.000 claims description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical class [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 claims description 2
- 239000012295 chemical reaction liquid Substances 0.000 claims description 2
- 238000001816 cooling Methods 0.000 claims description 2
- 229920000570 polyether Polymers 0.000 claims description 2
- OWYXVLZOHHQSAF-UHFFFAOYSA-N 4-[(chloroamino)methyl]aniline Chemical compound NC1=CC=C(CNCl)C=C1 OWYXVLZOHHQSAF-UHFFFAOYSA-N 0.000 claims 1
- FGHDDLYDTJEWEQ-UHFFFAOYSA-N 4-[(fluoroamino)methyl]aniline Chemical compound NC1=CC=C(CNF)C=C1 FGHDDLYDTJEWEQ-UHFFFAOYSA-N 0.000 claims 1
- AFBPFSWMIHJQDM-UHFFFAOYSA-N N-methylaniline Chemical compound CNC1=CC=CC=C1 AFBPFSWMIHJQDM-UHFFFAOYSA-N 0.000 claims 1
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 claims 1
- 239000013335 mesoporous material Substances 0.000 abstract description 6
- 230000003197 catalytic effect Effects 0.000 abstract description 5
- 239000000126 substance Substances 0.000 abstract description 5
- 239000011148 porous material Substances 0.000 abstract description 4
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 15
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 10
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 6
- 239000000463 material Substances 0.000 description 5
- 239000012044 organic layer Substances 0.000 description 5
- 239000003208 petroleum Substances 0.000 description 5
- 238000010791 quenching Methods 0.000 description 5
- 230000000171 quenching effect Effects 0.000 description 5
- 238000000967 suction filtration Methods 0.000 description 5
- 238000000034 method Methods 0.000 description 4
- 229920000620 organic polymer Polymers 0.000 description 4
- 238000006170 formylation reaction Methods 0.000 description 3
- UGFAIRIUMAVXCW-UHFFFAOYSA-N Carbon monoxide Chemical compound [O+]#[C-] UGFAIRIUMAVXCW-UHFFFAOYSA-N 0.000 description 2
- ATHHXGZTWNVVOU-UHFFFAOYSA-N N-methylformamide Chemical compound CNC=O ATHHXGZTWNVVOU-UHFFFAOYSA-N 0.000 description 2
- 238000002441 X-ray diffraction Methods 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 229910002091 carbon monoxide Inorganic materials 0.000 description 2
- 230000022244 formylation Effects 0.000 description 2
- 239000002861 polymer material Substances 0.000 description 2
- 230000001105 regulatory effect Effects 0.000 description 2
- 238000000926 separation method Methods 0.000 description 2
- 238000001291 vacuum drying Methods 0.000 description 2
- IDWXQRMUCRXFAK-UHFFFAOYSA-N (2-phenyldiazenylhydrazinyl)benzene Chemical compound C=1C=CC=CC=1N=NNNC1=CC=CC=C1 IDWXQRMUCRXFAK-UHFFFAOYSA-N 0.000 description 1
- HEONFBNOPUNGFB-UHFFFAOYSA-N CON=NCC(C=C1)=CC=C1N Chemical compound CON=NCC(C=C1)=CC=C1N HEONFBNOPUNGFB-UHFFFAOYSA-N 0.000 description 1
- 238000002159 adsorption--desorption isotherm Methods 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 230000005540 biological transmission Effects 0.000 description 1
- 238000006555 catalytic reaction Methods 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 230000001351 cycling effect Effects 0.000 description 1
- 230000007547 defect Effects 0.000 description 1
- 238000003795 desorption Methods 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- 239000003814 drug Substances 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- 239000011261 inert gas Substances 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 238000001000 micrograph Methods 0.000 description 1
- 239000000178 monomer Substances 0.000 description 1
- 238000005580 one pot reaction Methods 0.000 description 1
- 239000012074 organic phase Substances 0.000 description 1
- 238000006116 polymerization reaction Methods 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 238000004064 recycling Methods 0.000 description 1
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical class O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- 238000004627 transmission electron microscopy Methods 0.000 description 1
- 238000010792 warming Methods 0.000 description 1
Images
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J31/00—Catalysts comprising hydrides, coordination complexes or organic compounds
- B01J31/02—Catalysts comprising hydrides, coordination complexes or organic compounds containing organic compounds or metal hydrides
- B01J31/06—Catalysts comprising hydrides, coordination complexes or organic compounds containing organic compounds or metal hydrides containing polymers
- B01J31/08—Ion-exchange resins
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J35/00—Catalysts, in general, characterised by their form or physical properties
- B01J35/60—Catalysts, in general, characterised by their form or physical properties characterised by their surface properties or porosity
- B01J35/61—Surface area
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C231/00—Preparation of carboxylic acid amides
- C07C231/10—Preparation of carboxylic acid amides from compounds not provided for in groups C07C231/02 - C07C231/08
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Catalysts (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
本发明公开了一种负载双功能化离子液体介孔聚合物的制备及其应用,其特点是以咪唑功能化有序介孔聚合物为载体,且以共价键的形式连接1,2‑二溴乙烷和三乙胺,并用醋酸钠与双功能化离子液体进行离子交换,制得负载双功能化离子液体介孔聚合物作为催化剂在CO2与胺基化合物的多相催化合成甲酰胺的反应。本发明与现有技术相比具有介孔材料的高比表面积、孔道均一、热稳定性和化学稳定好等特点,可以在温和的条件下催化CO2与胺基化合物反应,催化活性高,易分离回收分离,可循环使用,是一种新型环境友好型催化剂,在多相催化领域有着巨大的发展潜力。
Description
技术领域
本发明涉及多孔有机聚合物催化剂技术领域,尤其是一种可循环使用于催化CO2甲酰胺化反应的负载双功能化离子液体介孔聚合物的制备及其应用。
背景技术
二氧化碳导致全球变暖,同时也是廉价的、丰富的C1资源,因此将过多的CO2转化为有价值的化学产品,有非常好的工业发展前景。甲酰胺是重要的医药中间体,通常是用一氧化碳胺的甲酰化产生,利用CO2代替有毒的一氧化碳对于N-H键的甲酰化是一条绿色且安全的合成路线。
目前,关于二氧化碳那和胺基化合物的反应在各种催化体系中有广泛的报道,并且取得了巨大的进展。然而,这些报道的合成路线存在的问题是:需要金属催化剂,惰性气体气氛,复杂反应体系,高温和压力,以及催化剂分离困难等。因此,探索简单、可回收、绿色的催化体系,仍然是非常可取的。离子液体功能化的有序介孔聚合物材料是一类非常好的结合了介孔材料的高比表面积、高热稳定性、孔径均一和离子液体多功能催化等优点。因此,制备离子液体负载型有序介孔材料,不仅可以有效的催化有机合成反应,且容易回收利用符合绿色化学理念。
现有技术的多孔有机聚合物合成工艺复杂,原料成本高,难以被广泛应用,因此发展一种制备简单,催化活性高且循环稳定性好的多孔有机聚合物对CO2化学转化研究具有重要的意义。
发明内容
本发明的目的是针对现有技术的不足而提供的一种负载双功能离子液体介孔聚合物的制备及其应用,采用以咪唑功能化有序介孔聚合物为载体,以共价键的形式陆续连接1,2-二溴乙烷和三乙胺,并用醋酸钠与双功能化离子液体材料进行离子交换,得到的双功能化离子液体介孔聚合物,该介孔聚合物作为催化剂应用在二氧化碳甲酰化反应中,具有优良的反应活性和再循环能力,可以在温和的反应条件下得到非常高的产率,合成操作简单,重复性好,可通过调控单体的摩尔比改变自身的比表面积、孔容等,产物选择性好,底物普适性强,反应条件温和,催化剂易分离回收,是一种可循环使用的高效催化剂,在多相催化领域有着巨大的发展潜力。
实现本发明目的的具体技术方案是:一种负载双功能化离子液体介孔聚合物的制备,其特点是以咪唑功能化有序介孔聚合物为载体,且以共价键的形式连接1,2-二溴乙烷和三乙胺,并用醋酸钠与双功能化离子液体进行离子交换,得负载双功能化离子液体的介孔聚合物,其制备具体步骤如下:
(一)、咪唑功能化有序介孔聚合物的制备
a、1-(3-甲氧苄基)-1-氢-咪唑中间体的制备
将四氢呋喃与氢化钠按1~6:1摩尔比混合后滴加到咪唑和四氢呋喃混合液中,搅拌40~60min后加入1-(氯甲基)-3-苯甲醚,在70℃温度下回流24h,进行如下反应结构式的合成反应:
反应结束后用去离子水洗涤和二氯甲烷萃取,萃取液依次用去离子和饱和盐水洗涤后经干燥和柱层析分离,得产物为1-(3-甲氧苄基)-1-氢-咪唑中间体,所述咪唑和四氢呋喃混合液为咪唑与四氢呋喃按1:8~15摩尔比混合;所述1-(氯甲基)-3-苯甲醚与咪唑的摩尔比为按1~5:1。
b、3-((1-氢-咪唑-1-)甲基)苯酚的制备
将上述制备的中间体与氢溴酸按1:6~10摩尔比混合,在120℃温度下回流24h,进行如下反应结构式的脱甲基化反应:
反应结束后用Na2CO3中和氢溴酸,当pH值为7时加入饱和NaHCO3溶液,将反应液的pH值调至7.5,然后经水洗、过滤后得产物为3-((1-氢-咪唑-1-)甲基)苯酚。
c、咪唑功能化前驱体的制备
将上述制备的3-((1-氢-咪唑-1-)甲基)苯酚与浓度为38wt%的甲醛溶液和浓度为10wt%的氢氧化钠溶液混合,常温下搅拌10~20min后加入苯酚,在70~75℃温度下搅拌1~2h,反应结束后冷却至常温,反应液用盐酸将pH值调至7后经旋转蒸发,得产物为咪唑功能化前驱体,所述3-((1-氢-咪唑-1-)甲基)苯酚与苯酚、甲醛和氢氧化钠的摩尔比为1:8~10:14~18:2~4。
d、咪唑功能化有序介孔聚合物的制备
将上述制备的咪唑功能化前驱体与聚醚(F127)和乙醇按1:1:18~25混合,搅拌20~50min后将其平铺在玻璃板上,室温下挥发8~12h后置于100~120℃烘箱中干燥18~24h,然后将固化的薄膜在350℃氮气管式炉中煅烧3h,得产物为咪唑功能化有序介孔聚合物。
(二)、咪唑功能化有序介孔聚合物的离子化
a、3-IMP-MPs-Et-Br的制备
将上述制备的咪唑功能化有序介孔聚合物与1,2-二溴乙烷和乙腈按4~6:1:35~45质量比混合,在70~83℃温度下搅拌回流12~24小时,反应液经过滤后,滤出物依次用丙酮和去离子水交替洗涤三次,然后在60~80℃温度下真空干燥12~24小时,得产物为3-IMP-MPs-Et-Br。
b、3-IMP-MPs-Et-(NEt4)Br的制备
将上述制备的3-IMP-MPs-Et-Br与三乙胺和去离子水按5:2~8:35~45质量比混合,在60~80℃温度下搅拌回流12~24小时,反应液经过滤后,滤出物依次用丙酮和去离子水交替洗涤三次,然后在60~80℃温度下真空干燥12~24小时,得产物为3-IMP-MPs-Et-(NEt4)Br。
c、3-IMP-MPs-Et-(NEt4)AcO的制备
将上述制备的3-IMP-MPs-Et-(NEt4)Br与醋酸钠和去离子水按5:2~8:35~45质量比混合,常温下搅拌12~24小时,反应液经过滤后,滤出物用去离子水洗涤后在60~80℃温度下真空干燥12~24小时,得产物为负载双功能化离子液体的介孔聚合物(3-IMP-MPs-Et-(NEt4)AcO)。
一种所述负载双功能化离子液体介孔聚合物的应用,其特点是将负载含双功能化离子液体介孔聚合物作为催化剂应用在CO2与胺基化合物的多相催化合成甲酰胺的反应,其多相催化合成的反应温度为30~40℃,反应时间为18~24小时,所述多相催化合成甲酰胺的反应,其催化剂与胺基化合物、苯硅烷和乙腈的摩尔比为0.03~0.06:1:2~4:35~45;所述二氧化碳的压力为0.5~2MPa;所述胺基化合物为氮甲基苯胺、甲基氮甲基苯胺、甲氧基氮甲基苯胺、对氯氮甲基苯胺或对氟氮甲基苯胺,其结构通式如下:
本发明与现有技术相比具有介孔材料的高比表面积、孔道均一、热稳定性和化学稳定好等特点,可以在温和的条件下催化CO2与胺基化合物反应,催化活性高,易分离回收分离,可循环使用,是一种新型环境友好型催化剂,在多相催化领域有着巨大的发展潜力。
附图说明
图1为实施例1制备的负载双功能化离子液体介孔聚合物X射线衍射图;
图2为实施例1制备的负载双功能化离子液体介孔聚合物N2吸附-脱附等温线;
图3为实施例1制备的负载双功能化离子液体介孔聚合物透射电镜图。
具体实施方式
通过以下具体实施例对本发明作进一步的详细说明。
实施例1
(一)、咪唑功能化有序介孔材料的制备
a、1-(3-甲氧苄基)-1-氢-咪唑中间体的制备
将5mL质量浓度为99.9%的四氢呋喃与4.3g(0.18mol)氢化钠混合后,逐滴加入到40mL质量浓度为99.9%的四氢呋喃与6.8g(0.1mol)咪唑的混合液中,搅拌混合40min后加入15.7g(0.1mol)质量浓度为99.9%1-(氯甲基)-3-苯甲醚,在70℃温度下回流24h,其反应结构式如下:
反应产物经去离子水洗涤三次后用二氯甲烷萃取,萃取后用去离子水洗涤有机相两次和饱和盐水洗涤一次,然后用无水硫酸钠干燥,旋干二氯甲烷后经柱层析分离,得15.3g产物为1-(3-甲氧苄基)-1-氢-咪唑中间体,其产率为81%。
b、3-((1-氢-咪唑-1-)甲基)苯酚(3-IMP)的制备
取10g上述制备的1-(3-甲氧苄基)-1-氢-咪唑中间体加入到50mL质量浓度为33%氢溴酸中,在120℃温度下回流24h进行如下反应结构式的脱甲基化反应:
反应结束后用Na2CO3中和氢溴酸,当pH值快到7时加入饱和NaHCO3溶液,将反应液的pH值调至7.5,然后经过滤、水洗后再过滤,得9.2g产物为3-((1-氢-咪唑-1-)甲基)苯酚,其产率为100%。
c、咪唑功能化前驱体的制备
取0.19g上述制备的3-((1-氢-咪唑-1-)甲基)苯酚与2.9g质量浓度为38wt%的甲醛溶液和1.15g质量浓度为10wt%的氢氧化钠溶液混合,常温下搅拌10min后加入1.15g质量浓度为99.9%苯酚,然后在75℃温度下搅拌2h,一锅法合成功能化前驱体,将反应液冷却至常温后用2mol/L HCl溶液调至pH为7,旋转蒸发2h除掉体系中的水后得2g咪唑功能化前驱体。
d、咪唑功能化有序介孔聚合物的制备
将2g F127溶解在50mL质量浓度为99%的乙醇溶液中,然后加入1.6g上述制备的咪唑功能化前驱体,搅拌混合45min后将其平铺在玻璃板上,室温下挥发8h后置于120℃烘箱中干燥24h,将固化的薄膜在350℃温度下的氮气管式炉中煅烧3h,去除模板剂F127后得1.5g咪唑功能化有序介孔聚合物(3-IMP-MPs)。
(二)、咪唑功能化有序介孔聚合物的离子化
a、3-IMP-MPs-Et-Br的制备
将上述制备的3-IMP-MPs与1,2-二溴乙烷离子化得到3-IMP-MPs-Et-Br,其具体操作过程为:将5g 3-IMP-MPs与50ml质量浓度为99.9%的乙腈和1g质量浓度为99.9%的1,2-二溴乙烷加入圆底烧瓶中,在83℃温度下搅拌回流24小时,反应后过滤并用丙酮和去离子水交替洗涤三次,然后放置在80℃真空干燥箱中干燥24小时,得1.51g产物为3-IMP-MPs-Et-Br。
b、3-IMP-MPs-Et-(NEt4)Br的制备
将5g 3-IMP-MPs-Et-Br与2g质量浓度为99.9%的三乙胺水溶液和50ml的去离子水加入圆底烧瓶中,在60℃温度下搅拌回流24小时,反应后过滤用丙酮和去离子水交替洗涤三次,然后在80℃真空干燥箱中干燥24小时,得到1.51g产物为3-IMP-MPs-Et-(NEt4)Br。
c、3-IMP-MPs-Et-(NEt4)AcO的制备
将5g 3-IMP-MPs-Et-(NEt4)Br与50ml的去离子水和2g醋酸钠固体分别加入圆底烧瓶中,常温下搅拌24小时,反应后过滤用去离子水洗涤三次,以充分去除掉附着在材料上的醋酸钠,在80℃真空干燥箱中干燥24小时,得到1.51g产物为负载双功能化离子液体的介孔聚合(3-IMP-MPs-Et-(NEt4)AcO)。
参阅附图1,上述3-IMP-MPs-Et-(NEt4)AcO产物经X射线衍射表征,所得材料为有序二维六方结构。
参阅附图2,上述3-IMP-MPs-Et-(NEt4)AcO产物经氮气等温吸脱附表征,所得材料的比表面积为398m2/g,孔体积为0.43cm3/g。
参阅附图3,上述3-IMP-MPs-Et-(NEt4)AcO产物经透射电子显微镜表征,所得材料为有序介孔材料。
实施例2
称取100mg(4mol%)上述实施例1制备的3-IMP-MPs-Et-(NEt4)AcO为催化剂与107mg(1mmol)氮甲基苯胺、210mg(2mmol)苯硅烷和2ml乙腈放入高压反应釜中,并充入压力为1MPa的二氧化碳,加热至30℃,反应18小时,其反应结构式为:
在反应过程中CO2压力一直保持不变,反应结束后将反应釜冷却至室温,加20ml的去离子水洗涤并淬灭苯硅烷,抽滤分离出的催化剂可循环使用。在滤液中加入60ml的二氯甲烷进行萃取三次取有机层,合并有机层后加入无水硫酸钠干燥半小时,旋蒸得到的油状混合物经柱层析分离(石油醚:乙酸乙酯=4:1),得128mg氮甲基甲酰胺,其产率为95%。
实施例3
称取100mg(4mol%)上述实施例1制备的3-IMP-MPs-Et-(NEt4)AcO为催化剂与121mg(1mmol)对甲基氮甲基苯胺、210mg(2mmol)苯硅烷和2ml乙腈放入15ml的高压反应釜中,并充入压力为1MPa的二氧化碳,加热至30℃,反应18小时,其反应结构式为:
在反应过程中CO2压力一直保持不变,反应结束后将反应釜冷却至室温,加20ml的去离子水洗涤并淬灭苯硅烷,抽滤分离出的催化剂可循环使用。在滤液中加入60ml的二氯甲烷进行萃取三次取有机层,合并有机层后加入无水硫酸钠干燥半小时,旋蒸得到的油状混合物经柱层析分离(石油醚:乙酸乙酯=4:1),得138.6mg对甲基氮甲基甲酰胺,其产率为93%。
实施例4
称取100mg(4mol%)上述实施例1制备的3-IMP-MPs-Et-(NEt4)AcO为催化剂与137mg(1mmol)对甲氧基氮甲基苯胺、210mg(2mmol)苯硅烷和2ml乙腈放入高压反应釜中,并充入压力为1MPa的二氧化碳,加热至30℃,反应18小时,其反应结构式为:
在反应过程中CO2压力一直保持不变,反应结束后将反应釜冷却至室温,加20ml的去离子水洗涤并淬灭苯硅烷,抽滤分离出的催化剂可循环使用。在滤液中加入60ml的二氯甲烷进行萃取三次取有机层,合并有机层后加入无水硫酸钠干燥半小时,旋蒸得到的油状混合物经柱层析分离(石油醚:乙酸乙酯=4:1),得158.4mg产物为对甲氧基氮甲基甲酰胺,其产率为96%。
实施例5
称取100mg(4mol%)上述实施例1制备的3-IMP-MPs-Et-(NEt4)AcO为催化剂与141mg(1mmol)对氯氮甲基苯胺、210mg(2mmol)苯硅烷和2ml乙腈放入高压反应釜中,并充入压力为1MPa的二氧化碳,加热至30℃,反应18小时,其反应结构式为:
在反应过程中CO2压力一直保持不变,反应结束后将反应釜冷却至室温,加20ml的去离子水洗涤并淬灭苯硅烷,抽滤分离出的催化剂可循环使用。在滤液中加入60ml的二氯甲烷进行萃取三次取有机层,合并有机层后加入无水硫酸钠干燥半小时,旋蒸得到的油状混合物经柱层析分离(石油醚:乙酸乙酯=4:1),得152.1mg产物为对氯氮甲基甲酰胺,其产率为90%。
实施例6
称取100mg(4mol%)上述实施例1制备的3-IMP-MPs-Et-(NEt4)AcO为催化剂与125mg(1mmol)对氟氮甲基苯胺、210mg(2mmol)苯硅烷和2ml乙腈放入高压反应釜中,并充入压力为1MPa的二氧化碳,加热至30℃,反应18小时,其反应结构式为:
在反应过程中CO2压力一直保持不变,反应结束后将反应釜冷却至室温,加20ml的去离子水洗涤并淬灭苯硅烷,抽滤分离出的催化剂可循环使用。在滤液中加入60ml的二氯甲烷进行萃取三次取有机层,合并有机层后加入无水硫酸钠干燥半小时,旋蒸得到的油状混合物经柱层析分离(石油醚:乙酸乙酯=4:1),得134.6mg产物为对氟氮甲基甲酰胺,其产率为88%。
以上各实施例只是对本发明做进一步说明,并非用以限制本发明专利,凡为本发明等效实施,均应包含于本发明专利的权利要求范围之内。
Claims (2)
1.一种负载双功能化离子液体介孔聚合物的制备,其特征在于以咪唑功能化有序介孔聚合物为载体,且以共价键的形式连接1,2-二溴乙烷和三乙胺,并用醋酸钠与双功能化离子液体进行离子交换,得负载双功能化离子液体的介孔聚合物,其制备具体步骤如下:
(一)、咪唑功能化有序介孔聚合物的制备
a、1-(3-甲氧苄基)-1-氢-咪唑中间体的制备
将四氢呋喃与氢化钠按1~6:1摩尔比混合后滴加到咪唑和四氢呋喃混合液中,搅拌40~60min后加入1-(氯甲基)-3-苯甲醚,在70℃温度下回流24h,进行如下反应结构式的合成反应:
反应结束后用去离子水洗涤和二氯甲烷萃取,萃取液依次用去离子和饱和盐水洗涤后经干燥和柱层析分离,得产物为1-(3-甲氧苄基)-1-氢-咪唑中间体,所述咪唑和四氢呋喃混合液为咪唑与四氢呋喃按1:8~15摩尔比混合;所述1-(氯甲基)-3-苯甲醚与咪唑的摩尔比为1~5:1;
b、3-((1-氢-咪唑-1-)甲基)苯酚的制备
将上述制备的中间体与氢溴酸按1:6~10摩尔比混合,在120℃温度下回流24h,进行如下反应结构式的脱甲基化反应:
反应结束后用Na2CO3中和氢溴酸,当pH值为7时加入饱和NaHCO3溶液,将反应液的pH值调至7.5,然后经水洗、过滤后得产物为3-((1-氢-咪唑-1-)甲基)苯酚;
c、咪唑功能化前驱体的制备
将上述制备的3-((1-氢-咪唑-1-)甲基)苯酚与浓度为38wt%的甲醛溶液和浓度为10wt%的氢氧化钠溶液混合,常温下搅拌10~20min后加入苯酚,在70~75℃温度下搅拌1~2h,反应结束后冷却至常温,反应液用盐酸将pH值调至7后经旋转蒸发,得产物为咪唑功能化前驱体,所述3-((1-氢-咪唑-1-)甲基)苯酚与苯酚、甲醛和氢氧化钠的摩尔比为1:8~10:14~18:2~4;
d、咪唑功能化有序介孔聚合物的制备
将上述制备的咪唑功能化前驱体与聚醚和乙醇按1:1:18~25混合,搅拌20~50min后将其平铺在玻璃板上,室温下挥发8~12h后置于100~120℃烘箱中干燥18~24h,然后将固化的薄膜在350℃氮气管式炉中煅烧3h,得产物为咪唑功能化有序介孔聚合物;
(二)、咪唑功能化有序介孔聚合物的离子化
a、3-IMP-MPs-Et-Br的制备
将上述制备的咪唑功能化有序介孔聚合物与1,2-二溴乙烷和乙腈按4~6:1:35~45质量比混合,在70~83℃温度下搅拌回流12~24小时,反应液经过滤后,滤出物依次用丙酮和去离子水交替洗涤三次,然后在60~80℃温度下真空干燥12~24小时,得产物为3-IMP-MPs-Et-Br;
b、3-IMP-MPs-Et-(NEt4)Br的制备
将上述制备的3-IMP-MPs-Et-Br与三乙胺和去离子水按5:2~8:35~45质量比混合,在60~80℃温度下搅拌回流12~24小时,反应液经过滤后,滤出物依次用丙酮和去离子水交替洗涤三次,然后在60~80℃温度下真空干燥12~24小时,得产物为3-IMP-MPs-Et-(NEt4)Br;
c、3-IMP-MPs-Et-(NEt4)AcO的制备
将上述制备的3-IMP-MPs-Et-(NEt4)Br与醋酸钠和去离子水按5:2~8:35~45质量比混合,常温下搅拌12~24小时,反应液经过滤后,滤出物用去离子水洗涤后在60~80℃温度下真空干燥12~24小时,得产物为负载双功能化离子液体的介孔聚合物3-IMP-MPs-Et-(NEt4)AcO。
2.一种权利要求1所述负载双功能离子液体介孔聚合物的制备方法制备的负载双功能离子液体介孔聚合物的应用,其特征在于将负载含双功能化离子液体介孔聚合物作为催化剂应用在CO2与胺基化合物的多相催化合成甲酰胺的反应,其多相催化合成的反应温度为30~40℃,反应时间为18~24小时,所述多相催化合成甲酰胺的反应,其催化剂与胺基化合物、苯硅烷和乙腈的摩尔比为0.03~0.06:1:2~4:35~45;所述胺基化合物为氮甲基苯胺、甲基氮甲基苯胺、甲氧基氮甲基苯胺、对氯氮甲基苯胺或对氟氮甲基苯胺;所述二氧化碳的压力为0.5~2MPa。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201810907784.4A CN109174181B (zh) | 2018-08-10 | 2018-08-10 | 一种负载双功能离子液体介孔聚合物的制备及其应用 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201810907784.4A CN109174181B (zh) | 2018-08-10 | 2018-08-10 | 一种负载双功能离子液体介孔聚合物的制备及其应用 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN109174181A CN109174181A (zh) | 2019-01-11 |
| CN109174181B true CN109174181B (zh) | 2021-05-25 |
Family
ID=64920955
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201810907784.4A Active CN109174181B (zh) | 2018-08-10 | 2018-08-10 | 一种负载双功能离子液体介孔聚合物的制备及其应用 |
Country Status (1)
| Country | Link |
|---|---|
| CN (1) | CN109174181B (zh) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN111229320B (zh) * | 2020-01-16 | 2022-07-19 | 辽宁大学 | 一种接枝离子液体的金属有机框架复合材料及其制备方法和应用 |
| CN117624052B (zh) * | 2024-01-26 | 2024-04-12 | 四川益能康生环保科技有限公司 | 一种用于捕集二氧化碳的离子液体及其制备方法 |
Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1092771A (zh) * | 1992-12-10 | 1994-09-28 | 美国辉瑞有限公司 | 氨基亚甲基取代的非芳香杂环化合物 |
| CN101790413A (zh) * | 2007-10-19 | 2010-07-28 | 川崎重工业株式会社 | 含聚醚砜的分离膜、其制造方法及制膜原液 |
| CN103041866A (zh) * | 2013-01-18 | 2013-04-17 | 绍兴文理学院 | 二氧化钛-介孔聚合物纳米多孔复合可见光催化材料的制备方法 |
| JP2014005418A (ja) * | 2012-06-27 | 2014-01-16 | Central Glass Co Ltd | フッ素化不飽和炭化水素を含む熱伝達媒体 |
| CN104448381A (zh) * | 2014-11-07 | 2015-03-25 | 华东师范大学 | 咪唑功能化有序介孔酚醛树脂材料的制备及其应用 |
| CN106977676A (zh) * | 2017-03-14 | 2017-07-25 | 华东师范大学 | 一种含氮功能化介孔聚合物的合成及其应用 |
| CN108456276A (zh) * | 2018-05-17 | 2018-08-28 | 华东师范大学 | 一种咪唑盐多孔有机聚合物的制备及其应用 |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2015117147A1 (en) * | 2014-02-03 | 2015-08-06 | Quadriga Biosciences, Inc. | Beta-substituted beta-amino acids and analogs as chemotherapeutic agents |
-
2018
- 2018-08-10 CN CN201810907784.4A patent/CN109174181B/zh active Active
Patent Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1092771A (zh) * | 1992-12-10 | 1994-09-28 | 美国辉瑞有限公司 | 氨基亚甲基取代的非芳香杂环化合物 |
| CN101790413A (zh) * | 2007-10-19 | 2010-07-28 | 川崎重工业株式会社 | 含聚醚砜的分离膜、其制造方法及制膜原液 |
| JP2014005418A (ja) * | 2012-06-27 | 2014-01-16 | Central Glass Co Ltd | フッ素化不飽和炭化水素を含む熱伝達媒体 |
| CN103041866A (zh) * | 2013-01-18 | 2013-04-17 | 绍兴文理学院 | 二氧化钛-介孔聚合物纳米多孔复合可见光催化材料的制备方法 |
| CN104448381A (zh) * | 2014-11-07 | 2015-03-25 | 华东师范大学 | 咪唑功能化有序介孔酚醛树脂材料的制备及其应用 |
| CN106977676A (zh) * | 2017-03-14 | 2017-07-25 | 华东师范大学 | 一种含氮功能化介孔聚合物的合成及其应用 |
| CN108456276A (zh) * | 2018-05-17 | 2018-08-28 | 华东师范大学 | 一种咪唑盐多孔有机聚合物的制备及其应用 |
Non-Patent Citations (2)
| Title |
|---|
| Highly recyclable polymer supported ionic liquids as efficient heterogeneous catalysts for batch and flow conversion of CO2 to cyclic carbonates;Tao Wang et al;《RSC Advances》;20170112;第7卷;全文 * |
| 咪唑功能化介孔聚合物的合成及其在二氧化碳转化中的应用;卢小伟;《中国优秀硕士学位论文全文数据库 工程科技I辑》;20171115(第11期);全文 * |
Also Published As
| Publication number | Publication date |
|---|---|
| CN109174181A (zh) | 2019-01-11 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Chen et al. | Function-oriented ionic polymers having high-density active sites for sustainable carbon dioxide conversion | |
| CN109939731B (zh) | 一种用于常压co2环加成反应的介孔聚离子液体催化剂、制备方法及应用 | |
| CN112159517B (zh) | 朝格尔碱基共轭微孔聚合物光催化剂及其制备方法和应用 | |
| CN109174181B (zh) | 一种负载双功能离子液体介孔聚合物的制备及其应用 | |
| CN101456855A (zh) | 1,3-丙磺酸内酯的制备方法 | |
| CN111138591A (zh) | 一种氮杂环卡宾/co2加合物功能化有机多孔聚合物、制备方法及应用 | |
| CN108671959B (zh) | 双功能有机多孔材料及其制备方法 | |
| CN111889141A (zh) | 一种催化二氧化碳与环氧化物环加成反应的离子液体功能化联吡啶类多孔聚合物催化剂 | |
| CN112206808B (zh) | 一种用于合成异丁酸异丁酯的催化剂及其制备方法和应用 | |
| CN112169836A (zh) | 一种多孔离子聚合物多相催化剂及其催化合成n-甲酰胺的方法 | |
| CN113912843B (zh) | 含苯并咪唑离子液体的多孔金属卟啉聚合物及其制备方法与应用 | |
| CN114621453B (zh) | 一种双功能吡啶羧酸卟啉配体的锆的金属有机框架材料的制备及应用 | |
| CN110152739B (zh) | 原位负载钯纳米颗粒的多孔有机复合物、合成方法及应用 | |
| CN117843978A (zh) | 一种二维超分子卤键有机骨架XOFs、其制备方法及应用 | |
| CN113045533B (zh) | 一种环状碳酸酯的合成方法 | |
| CN113072511B (zh) | 一种含氟三嗪基有机多孔材料的制备方法 | |
| CN109651398B (zh) | 一种合成劳拉替尼的溴代物中间体及催化合成劳拉替尼的方法 | |
| CN116970166B (zh) | 一种离子型共价三嗪骨架聚合物、制备方法及其应用 | |
| CN112778153A (zh) | 酰胺基桥连六羧酸配体和金属有机框架材料及其制备方法和应用 | |
| CN116178650A (zh) | 一种碳碳双键桥联的金属-salen基二维共轭有机框架材料及其制备方法 | |
| CN112892605A (zh) | 用于氮甲酰化反应的具有碱性多相催化剂及制备和应用 | |
| CN115232094B (zh) | 一种香豆素化合物Murraol的合成方法 | |
| CN114316261B (zh) | 一种三嗪框架多相催化剂及其制备方法与应用 | |
| CN111545247B (zh) | 一种sba-15负载的多相手性膦金催化剂及其制备方法和应用 | |
| CN112892603B (zh) | 一种用于氮甲酰化反应的固体多相催化剂及其制备和应用 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| GR01 | Patent grant | ||
| GR01 | Patent grant |