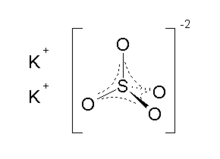
Kalium sulfat
 Arcanite
| |
| |
| Nama | |
|---|---|
| Nama lain
Potassium sulphate
| |
| Penanda | |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| Nomor EC | |
| KEGG | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| K2SO4 | |
| Massa molar | 174.259 g/mol |
| Penampilan | White solid |
| Bau | odorless |
| Densitas | 2.66 g/cm3[1] |
| Titik lebur | 1.069[2] °C (1.956 °F; 1.342 K) |
| Titik didih | 1.689 °C (3.072 °F; 1.962 K) |
| 111 g/L (20 °C) 120 g/L (25 °C) 240 g/L (100 °C) | |
| Kelarutan | slightly soluble in glycerol insoluble in acetone, alcohol, CS2 |
| −67.0·10−6 cm3/mol | |
| Indeks bias (nD) | 1.495 |
| Struktur | |
| orthorhombic | |
| Bahaya | |
| Bahaya utama | Irritant |
| Lembar data keselamatan | External MSDS |
| Frasa-R | R22 |
| Frasa-S | S36 |
| Titik nyala | Non-flammable |
| Dosis atau konsentrasi letal (LD, LC): | |
LD50 (dosis median)
|
6600 mg/kg (oral, rat)[3] |
| Senyawa terkait | |
Anion lain
|
Potassium selenate Potassium tellurate |
Kation lainnya
|
Lithium sulfate Sodium sulfate Rubidium sulfate Caesium sulfate |
Senyawa terkait
|
Potassium hydrogen sulfate Potassium sulfite Potassium bisulfite Potassium persulfate |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Kalium sulfat (K2SO4) (juga dikenal sebagai garam abu sulfur) merupakan garam yang terdiri dari kristal putih yang dapat larut dalam air. Tak mudah terbakar.
Bahan kimia ini biasanya digunakan dalam pupuk, menyediakan potasium dan sulfur.
Kalium sulfat juga merupakan biproduk pada produksi asam sendawa.
Kalium sulfat, K2SO4, ialah garam yang awalnya dikenal pada abad ke-14, dan dipelajari oleh Glauber, Boyle dan Tachenius, disebut pada abad ke-17 sebagai arcanuni atau sal duplicatum, dianggap sebagai kombinasi garam asam dengan garam alkalin.
Dihasilkan sebagai biproduk dalam banyak reaksi kimia, dan kemudian digunakan untuk disuling dari kainit, salah satu mineral Stassfurt, tetapi proses itu telah ditinggalkan karena garam dapat dibuat cukup murah dari klorida dengan membusukkannya dengan asam belerang dan calcining residunya. Untuk memurnikan produk mentahnya maka dilarutkan dalam air panas dan larutan yang disaring dan bisa didinginkan, saat bagian terbesar garam yang dilarutkan itu menghablur dengan promptitule yang khas.
Kristal yang amat bagus memiliki bentuk piramida sisi 6 ganda, tetapi sesungguhnya termasuk sistem rhombik. Kristal-kristal itu transparan, amat keras dan sama sekali permanen di udara. Memiliki ras pahit, asin. Garamnya dapat larut dalam air, tetapi tak dapat larut dalam garam abu tajam dari sp. gr. 1,35, dan dalam alkohol sebenarnya. Melebur pada suhu 1078 °C. Garanm mentah itu biasa digunakan dalam pengolahan kaca.
Sulfat asam atau bisulfat, KHSO4, siap diproduksi dengan memfusikan 13 bagian garam mormal berbubuk dengan 8 bagian asam belerang. Membentuk piramida rhombik, yang melebur pada 197. Melebur pada 3 bagian air 0 °C. Kelarutannya menunjukkan reaksi banyak seolah 2 kongenernya, K2SO4 and H2SO4, hadir berdampingan satu sama lain yang tak tergabung. Kelebihan alkohol, nyatanya, endapan sulfat normal (dengan sedikit bisulfat) dan asam bebas tetap dalam larutan.
Kemiripannya ialah garam kering yang bergabung pada tekanan merah pudar; berlaku pada silikat, titanat, dsb., seolah merupakan asam belerang yang ditingkatkan melebihi titik didih alaminya. Itulah sebabnya penerapannya yang sering dalam analisis ialah sebagai alat penghancur. Untuk garam dari asam belerang lainnya, lihat sulfur.
Rujukan
[sunting | sunting sumber]- ^ Patnaik, Pradyot (2002). Handbook of Inorganic Chemicals. McGraw-Hill. ISBN 978-0-07-049439-8.
- ^ Windholtz, M; Budavari, S, ed. (1983). The Merck Index. Rahway, New Jersey: Merck & Co.
- ^ Chambers, Michael. "Potassium sulfate RN: 7778-80-5". ChemIDplus. United States National Library of Medicine.
