Peroxyde de méthyléthylcétone
| Peroxyde de méthyléthylcétone | |
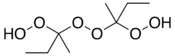 Structure du peroxyde de méthyléthylcétone |
|
| Identification | |
|---|---|
| Nom UICPA | 2-hydroperoxy-2-(2-hydroperoxybutan-2-ylperoxy)butane |
| Synonymes |
peroxyde d'éthylméthylcétone, |
| No CAS | |
| No ECHA | 100.014.238 |
| No CE | 215-661-2 |
| PubChem | 3672772 |
| SMILES | |
| InChI | |
| Apparence | liquide incolore à l'odeur légèrement âcre |
| Propriétés chimiques | |
| Formule | C8H18O6 [Isomères] |
| Masse molaire[1] | 210,224 9 ± 0,009 5 g/mol C 45,71 %, H 8,63 %, O 45,66 %, |
| Propriétés physiques | |
| T° ébullition | décomposition au-delà de 80 °C[2] |
| Solubilité | pratiquement insoluble dans l'eau |
| Masse volumique | 1,1 g·cm-3[2] |
| Point d’éclair | 75 °C[2] |
| Précautions | |
| SGH[2] | |
| H242, H302 et H314 |
|
| Transport[2] | |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Le peroxyde de méthyléthylcétone, ou peroxyde d'éthylméthylcétone, est un peroxyde organique de formule brute C8H18O6, en équilibre avec le peroxyde d'hydrogène H2O2 et un dimère C8H16O4 présentant un hétérocycle central à deux atomes de carbone et quatre d'oxygène ; c'est cependant la forme non cyclique de la molécule qui semble prépondérante[3], et c'est cette représentation linéaire qui généralement reprise dans le commerce.
Il s'agit d'un liquide huileux incolore ayant une odeur légèrement âcre, pratiquement insoluble dans l'eau, inflammable car comburant autant que combustible et par conséquent explosif, semblable en cela au peroxyde d'acétone. Il est généralement commercialisé dans un solvant stabilisant destiné à en réduire la sensibilité au choc, tel que phtalate de diméthyle, le peroxyde de benzoyle ou encore le diisobutyrate de 2,2,4-triméthyl-1,3-pentanediol, à une concentration pondérale inférieure à 40 %.
Le peroxyde de méthyléthylcétone est utilisé dans l'industrie et par certains modélistes pour catalyser la réticulation des colles polyester utilisés dans les plastiques à renfort de verre et dans certains moulages.
C'est un composé corrosif, très irritant pour la peau et susceptible de conduire à la cécité.
Sécurité
[modifier | modifier le code]Le peroxyde de méthyléthylcétone (PMEC) présente un potentiel de décomposition spontanée et explosive lorsqu'il est soumis à des stress thermiques ou mécaniques.
Certains facteurs, tels que les chocs, les impacts, les frottements et la présence d'impuretés comme des métaux lourds ou des accélérateurs, peuvent agir en tant que catalyseurs, accélérant ainsi le processus de décomposition. En conséquence, le PMEC est classé dans le cadre réglementaire des substances explosives.
Il est important de noter que le PMEC est sensible à la température et peut subir une décomposition exothermique. En l'absence de mécanismes de refroidissement efficaces, la température peut augmenter, accélérant ainsi la réaction de décomposition.
À des températures élevées, le PMEC peut subir une décomposition spontanée, entraînant des risques d'incendie. De plus, si cette décomposition se produit dans un espace confiné, le gaz résultant peut augmenter la pression, entraînant potentiellement des explosions dans des réacteurs, des cuves ou d'autres conteneurs.
En outre, les produits de décomposition volatils du PMEC peuvent contribuer à la formation d'explosions en phase vapeur. Afin d'assurer un stockage sûr, il est essentiel de limiter la température maximale de stockage à moins de 30 °C.[4]
Notes et références
[modifier | modifier le code]- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Entrée « 2-Butanone peroxide » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 10 mars 2013 (JavaScript nécessaire)
- (en) Nicholas A. Milas et Aleksandar Golubović, « Studies in Organic Peroxides. XXV. Preparation, Separation and Identification of Peroxides Derived from Methyl Ethyl Ketone and Hydrogen Peroxide », Journal of the American Chemical Society, vol. 81, no 21, , p. 5824-5826 (lire en ligne) DOI 10.1021/ja01530a068
- « Peroxyde De Méthyléthylcétone (PMEC): Production Et Utilisations », (consulté le )




