GS-441524
| GS-441524 | |
| |
| Identification | |
|---|---|
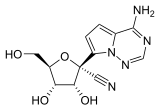
| Nom UICPA | (2R,3R,4S,5R)-2-(4-aminopyrrolo[2,1-f][1,2,4]triazin-7-yl)-3,4-dihydroxy-5-(hydroxymethyl)oxolane-2-carbonitrile |
| No CAS | |
| PubChem | |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C12H13N5O4 |
| Masse molaire[1] | 291,262 7 ± 0,012 7 g/mol C 49,48 %, H 4,5 %, N 24,04 %, O 21,97 %, |
| Considérations thérapeutiques | |
| Classe thérapeutique | Antiviral |
| Voie d’administration | sous-cutanée, per os |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Le GS-441524 est un analogue de nucléoside antiviral développé par Gilead Sciences. Il constitue le principal métabolite plasmatique de sa prodrogue nommée Remdesivir. Il a une demi-vie d’environ 24h chez le patient humain. Le Remdesivir et le GS-441524 ont tous les deux été démontrés comme efficace de manière in vitro contre le coronavirus félin, responsable de la péritonite infectieuse féline (PIF). La PIF est une maladie systémique létale affectant notamment les chats domestiques. Le Remdesivir n’a jamais été testé chez les chats, mais le GS-441524 a été démontré comme efficace chez environ 80% des chats atteints par la PIF et est maintenant largement utilisé malgré l’absence d’autorisation de mise sur le marché (AMM). Cette absence d'AMM est due au refus du laboratoire Gilead de mettre celui-ci à disposition pour un usage vétérinaire, malgré des résultats concluants [2],[3],[4],[5]. Le GC-376 semble, lui, n'être efficace face à la PIF qu'en l'absence d'implication neurologique ou oculaire, mais peut être utilisé en cas de résistance viral au GS-441524[6],[7],[5]. Des effets bénéfiques sur la PIF sont attendus du Monupiravir mais peu de résultats sont encore disponibles à ce jour.
Utilisation et Recherche
[modifier | modifier le code]Puisque la PIF est normalement fatale et qu’il n’existe pas de traitement autorisé disponible, le GS-441524 a couramment été retrouvé sur le marché noir et est utilisé par les propriétaires de chats dans un but curatif. Son efficacité a été démontrée à de multiples reprises via des essais de terrain[2],[3],[8] et des essais cliniques, de même que dans les formes sévères de la PIF affichant une implication systémique, oculaire et neurologique.
Le GS-441524 est soit similaire soit plus efficace que le Remdesivir contre le SARS-CoV-2 en culture cellulaire. Certains chercheurs argumentent que le GS-441524 serait meilleur que le Remdesivir pour le traitement de la Covid-19. Les avantages spécifiques incluent sa plus grande facilité de synthèse, ses plus faibles toxicité rénales et hépatiques, ainsi que son potentiel d’administration per os (qui est écarté pour le Remdesivir en raison d’un effet de premier passage hépatique et de sa faible stabilité hépatique). L’efficacité directe contre le SARS-CoV-2 a été démontrée dans un modèle murin de la Covid-19[9]. Une version modifiée par deutérium a été produite et a montré une efficacité pré-clinique à la fois en culture cellulaire et dans des modèles murins[10].
Le GS-441524 est vendu en tant que composé chimique en très grande pureté (>99% en résonance magnétique nucléaire et en chromatographie en phase liquide à haute performance) par plusieurs fournisseurs tels que MedKoo, Selleckchem, MedChemExpress et TargetMol.
Le GS-441524 a été directement administré chez un sujet humain sain[11]. La plus haute concentration plasmatique atteinte était alors de 12uM ce qui est plus de dix fois la concentration requise pour une activité contre le SARS-CoV-2 en culture cellulaire.
Pharmacologie
[modifier | modifier le code]Pharmacodynamie
[modifier | modifier le code]Le GS-441524 est un nucléoside phosphorylé par les nucléosides kinases (probablement l’adenosine kinase, qui est l’enzyme phosphorylant la ribavarine de structure similaire), puis est rephosphorylé par la nucléoside-diphosphate kinase en forme nucléotide triphosphate active. Le triphosphate du GS-441524 est le GS-443902. Ce dernier est également un agent antiviral généré par le Remdesivir, mais est généré par un mécanisme biochimique différent.
Pharmacocinétique
[modifier | modifier le code]Le GS-441524 est un analogue de nucléoside 1’-cyano-substitué. C’est le métabolite prédominant du Remdesivir circulant dans le sérum du fait d’une hydrolyse rapide (demi-vie de moins d’une heure) suivie d’une déphosphorylation[12],[13],[14].
La biodisponibilité orale a été montrée comme excellente chez le chien, bonne chez la souris, mais modeste chez le singe macaque. La prédiction d’une biodisponibilité orale humaine à partir de ces données tend à suggérer que celle-ci peut se situer entre celle du chien et celle du singe macaque. Puisque le GS-441524 a un peu moins que la moitié du poids moléculaire du Remdesivir, il délivrera autant de métabolite actif au sang que la même dose de Remdesivir, même si la biodisponibilité orale humaine est de 50%, comparable en cela à la ribavarine. Des données plus récentes montrent que le GS-441524 est toléré à 1 000 mg/Kg avec une concentration plasmatique maximale (Cmax) de presque 100µM, soit environ 100 fois plus que les concentrations requises pour une activité contre le virus en culture cellulaire[15].
La demi-vie d’élimination du GS-441524 est d’environ 2 heures chez le singe macaque, ce qui est bien moins que les 24 heures rapportées chez l’humain. La plus longue demi-vie suggère qu’une administration unique quotidienne est possible per os chez l’humain.
Mécanisme d'action
[modifier | modifier le code]La triple phosphorylation intracellulaire du GS-441524 mène à l’analogue de nucléoside triphosphate actif 1’-cyano-substitué. Ce dernier empêche directement la réplication de l’ARN viral en entrant en compétition avec les nucléotides triphosphates endogènes pour l’incorporation au sein des transcripts d’ARN naissants, ce qui déclenche une terminaison délayée de la chaîne par l’ARN-polymérase ARN-dépendante[4].
Tolérance
[modifier | modifier le code]Des expériences in vitro dans les cellules rénales félines de Crandell-Rees (CRF-CR) ont montré que le GS-441524 n’était pas toxique à des concentrations de 100µM, soit 100 fois la dose effective pour inhiber la réplication du virus de la PIF en culture cellulaire de CRF-CR et de macrophages[4],[16]. Des essais cliniques indiquent que le médicament est bien toléré, avec comme premier effet secondaire une irritation dermale au site d’injection due aux excipients[4],[16] de la forme galénique (acide chlorydrique utilisé pour la dilution, menant à une solution stable de pH inférieur ou égal à 3).
Certains chercheurs suggèrent son utilité dans le traitement du Covid-19 et ont montré ses avantages sur le Remdesivir tels que le manque de toxicité hépatique ciblée, la demi-vie ainsi que l’exposition plus longue au principe actif, ainsi qu’une synthèse bien plus simple et bien moins coûteuse[17],[18],[19].
Traitement par GS-441524
[modifier | modifier le code]Chez le félin
[modifier | modifier le code]Idéalement, le protocole thérapeutique doit toujours être précédé d'un diagnostic relativement certain (chat de moins de 5 ans présentant la sémiologie de la PIF, à jour de ses vaccinations, avec éventuellement une virologie positive au coronavirus félin). Il est important de s'assurer chez le chat âgé de la bonne suivie des vaccinations, notamment contre la leucose féline (de sémiologie parfois similaire), la prévalence de la PIF décroissant de manière exponentielle avec l'âge et étant quasiment nulle à 10 ans, avant de réapparaître chez quelques rares chats d'environ 11 à 12 ans[20]. Le traitement par GS-441524 ne fonctionnera pas sur une étiologie de type leucose, puisque le virus responsable de cette dernière est un rétrovirus fonctionnant donc par transcriptase inverse.
Le protocole thérapeutique courant associé au traitement de la PIF par le GS-441524 consiste en une seule et unique injection sous-cutanée quotidienne administrée à heure fixe, pendant 84 jours, soit 12 semaines de traitement. La posologie va généralement de 4mg/Kg à 12mg/Kg de poids de corps (cette posologie est celle pour la solution injectable). La posologie de départ est de 4-6mg/Kg pendant 12 semaines pour les PIF sans implication oculaire ou neurologique, la borne inférieure étant utilisée principalement chez les sujets jeunes à PIF effusive, les formes non effusives et les sujets âgés requièrant plutôt le dosage supérieur. Les formes à sémiologie oculaire ou neurologique nécessiteraient un départ à 10mg/Kg de principe actif en solution. La posologie est adaptée de manière à prendre en compte les gains de poids (venant soit de l'effusion soit de la nutrition). L'augmentation d'une posologie se fait par palliers de 2 ou 5mg/Kg pour un minimum de 4 semaines, en étendant la durée du protocole si cela est nécessaire[6]. Une dose est considérée comme très haute au-delà de 15mg/Kg. Cette posologie est adaptée selon la présence de signes nerveux (ataxie, hernie au travers du foramen magnum objectivée en IRM, hydrocéphalie, syringomyélie, épilepsie, nystagmus, méningite, etc.) ou oculaires (uvéite, œil nuageux, etc.)[6], selon l'âge du patient, ou encore selon la présence d'un volume d'ascite important mettant le pronostic vital en danger. Lorsque le traitement est administré per os, celui-ci peut être fourni toutes les 12 heures ou toutes les 24 heures[21], sa biodisponibilité étant alors moindre avec, au-delà de 15mg/Kg per os, un effet de saturation au sein des entérocytes justifiant l'administration toutes les 12 heures, voire toutes les 8 heures. Selon Niels Pedersen, la forme orale du GS-441524 semble efficace contre les formes de PIF qui requièrent moins de 10mg/Kg de solution injectable.
Dans sa thèse, la Dr en médecine vétérinaire Juliette Sotin [22], observe une corrélation entre l'administration de traitements palliatifs tels que les anti-inflammatoires de type corticoïdes et la présence d’une évolution clinique défavorable, ou, au mieux, d’une stagnation de la PIF. Elle évoque également que la totalité des propriétaires français de son étude utilisent le traitement antiviral fourni par le laboratoire SAK de Chine, tel que préconisé par un groupe de propriétaires présents sur le réseau social Facebook. Elle note toutefois que les propriétaires rapportent des effets secondaires tels que nausées, problèmes rénaux ou encore hépatiques qui ne sont pas notés dans l'étude americaine de Sarah Jones [23] sur des chats utilisant d'autres marques de GS-441524. Toutefois, il faut noter la limite de ces études préliminaires se basant avant tout sur la réponse des propriétaires à un questionnaire et non sur un examen clinique rigoureux des chats composant l'étude. À l'heure actuelle il existe d'autres marques que SAK sur le marché mondial, dont Mutian, Shire, Capella, Hero, Oscar ou encore Pine. Or, tel que très justement décrit dans l'étude de Sarah Jones et al. (2021) " En raison de la pléthore de différentes marques non autorisées de médicaments antiviraux de type GS-441524, avec de nombreux propriétaires qui ont utilisé plusieurs marques au cours du traitement, notre étude n'a pas été habilitée à découvrir si une marque était plus efficace qu'une autre. "
Il peut arriver qu’il y ait nécessité d’une modification de la dose de principe actif administré en cours de traitement, ou qu’il y ait nécessité de prolonger le traitement au-delà des 84 jours initialement prévu. Le Dr Juliette Sotin rapporte également que les traitements associés au GS-441524 sont souvent des anti-inflammatoires, des antibiotiques, des protecteurs hépatiques, des anti-vomitifs, ou encore une supplémentation (B12, probiotiques). Le protecteur hépatique Denamarin est démontré chez l’espèce canine comme protégeant contre le stress-oxydatif au sein des cellules hépatiques[24]. L’évolution clinique se fait majoritairement dans la semaine suivant le démarrage du traitement (reprise d’appétit, disparition de la fièvre, diminution de la distension abdominale, de la dyspnée, de la sémiologie neurologique et oculaire). La rechute en cours de traitement concernerait 13% des chats avec souvent une augmentation conséquente de la posologie. 98,5% des chats concernés par son étude se sont avérés toujours en vie en fin de traitement (ce résultat encourageant pouvant être à relativiser du fait d'un possible biais d'échantillonnage). Enfin, il faut noter que l’étude du Dr Sotin met en avant l'efficacité du principe actif sur la symptomatologie du névraxe et des yeux, contrairement à ce que l’article de Niels Pedersen et al.[25] suggérait concernant une biodisponibilité trop limitée.
En effet, du fait d'un manque de groupe carboxyle, la nature lipophile et/ou amphiphile du GS-441524 est questionnable. Il est admis que la barrière hémato-encéphalique exclue en moyenne 80% des médicaments, contre 70% pour la barrière hémato-oculaire. Ainsi, si la concentration plasmatique atteint 10uM, celle encéphalique est estimée à 2 uM et celle de l'humeur aqueuse à 3 uM [6]. Des niveaux plus hauts pourraient potentiellement être atteints dans les tissus inflammés, mais moins haut en l'absence d'inflammation.
Améliorations cliniques attendues
[modifier | modifier le code]Les signes cliniques censés s'améliorer incluent la température corporelle (idéalement de 38,5 °C chez le chat adulte) le niveau d'activité, l'appétit, la qualité de la fourrure, les valeurs de comptage en numération de la formule sanguine, et les valeurs de biochimies sérique. Le niveau d'activité doit revenir à la normale entre la huitième et la dizième semaine de traitement. La biochimie sérique et l'hématologie doivent être préférentiellement examinées de manière mensuelle. En hématologie, il est important de prendre en compte l'hématocrite, le nombre total de globules blancs (relatif et absolu) dont les neutrophiles et lymphocytes. Les valeurs sériques à prendre en compte sont les niveaux totaux en globuline et albumine (dont le rapport Alb/Glob) et les taux en bilirubine (élevée chez les chats avec effusion). Le choix d'étendre ou d'arrêter le protocole de traitement doit préférentiellement n'être fait que sur la base d'une présence concomitante de tests encourageants et de signes de santé externe. Il est admis qu'un rapport Alb/Glob > 0,6 exclue la présence d'une PIF lors d'un diagnostic, mais ce critère ne constitue pas forcément un signe suffisant pour arrêter le traitement chez un chat précédemment atteint.
En cas de sémiologie effusive (PIF dite humide), il semble important dans un premier temps de monitorer la dyspnée et le rythme respiratoire du chat. Une fréquence respiratoire normale chez un chat est comprise entre 20 et 40 inspirations par minute (chronométrage sur 15 secondes multiplié par 4) ; toutefois il est à noter qu'un rythme normal peut être concomitant à une respiration laborieuse. Cette sémiologie est à lier au volume d'effusion thoracique. Par chance, ces effusions thoraciques sont les plus faciles à inhiber par traitement antiviral, elles doivent être diminuées dans les premières 72 heures et plus ou moins grossièrement disparues en fin de première semaine. Ces effusions sont quasiment toujours retirées par centèse pour soulager la dyspnée et sont les plus lentes à réapparaître sous traitement. Concernant l'ascite, définie par une effusion abdominale de liquide, celles-ci est la plus difficile à faire disparaître et elle revient couramment après ponction. Elles doivent normalement être diminuées en 2 semaines de traitement et grossièrement disparues en un mois. Toutefois une faible persistance de l'effusion peut s'observer aux ultrasons. Il est important de noter qu'un drainage important des effusions abdominales peut causer un déséquilibre électrolytique chez les chats fortement atteints ainsi qu'une dépletion en protéines. Ce faisant, les effusions abdominales ne sont généralement pas retirées à moins d'une nette interférence avec les processus ventilatoires, du fait qu'elles reviennent rapidement[26].
C'est lorsque le GS-441524 est utilisé de manière chronique et avec des doses sous-optimales, ou lorsque des jours d'administration manquent qu'apparaît généralement une résistance à l'agent antiviral. Cette résistance est généralement partielle et peut être surpassée avec une augmentation conséquente de la dose de traitement[27].
Persistance sémiologique
[modifier | modifier le code]Selon Niels Pedersen, les principales raisons d'une persistance effusive sont : une posologie trop faible (e.g., par utilisation d'une forme per os), le développement d'une résistance à l'antiviral, une infection de bas grade ou une fibrose des veinules avec pression capillaire augmentée, ou une polypathologie (e.g., atteinte rénale ou entérique). Les effusions persistantes dues à une fibrose veinulaire chez les chats pourtant soignés de l'infection se résout généralement en plusieurs semaines ou mois[26].
Il peut exister des rechutes à la suite du protocole de traitement. Ces rechutes ont couramment un prodrome neurologique ou oculaire et les signes correspondants doivent être monitorés. Il est habituellement conseillé d'instaurer douze semaines d'observation à la suite de l'arrêt du GS-441524. Ces rechutes sont souvent traitées pour un minimum de 8 nouvelles semaines avec une dose de démarrage au moins plus haute de 5mg/Kg que la dernière posologie utilisée. Il est alors exclu d'utiliser toute forme d'administration orale. Il est admis que le but du traitement est l'instauration d'une immunité face à la PIF et de stopper la réplication au sein des macrophages et microgliocytes stoppant dès lors la production de cytokines immunosuppressives et de molécules pro-inflammatoires, oxydantes et sclérosantes causant la sémiologie de la PIF [28],[6].
Effets secondaires
[modifier | modifier le code]Les effets secondaires du GS-441524 chez le chat sont minimes. Ceux-ci comprennent de faibles dommages rénaux sans handicap de la fonction rénale et des vascularites systémiques chez quelques rares chats. Ces effets secondaires répondraient correctement à une administration de stéroïdes à faible dose et à court terme.
L'effet secondaire majeur du traitement par GS-441524 est dû aux excipients de sa forme galénique injectable qui comprennent l'acide chlorydrique. Ce dernier stabilise la dilution du traitement via un pH total compris entre 1 et 3 au maximum. Cet effet secondaire se caractérise par une corrosion au site d'injection ainsi qu'une douleur conséquente. Les plaies de l'injection sont nettoyées de la fourrure environnante (à raser) et rincées 4 fois par jour avec des boules de cotton stérile diluée dans une solution de peroxyde d'hydrogène prévue à cet effet. La gabapentine, antiépileptique et antalgique, est couramment utilisée pour calmer la douleur due au traitement ainsi qu'à l'injection[6].
Notes et références
[modifier | modifier le code]- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- James Westgate, « Vet science ‘being ignored’ in quest for COVID-19 drug », sur Vet Times, 2020-05-07bst05:54:00+00:00 (consulté le )
- (en) Sarah Zhang, « A Much-Hyped COVID-19 Drug Is Almost Identical to a Black-Market Cat Cure », sur The Atlantic, (consulté le )
- B.G. Murphy, M. Perron, E. Murakami et K. Bauer, « The nucleoside analog GS-441524 strongly inhibits feline infectious peritonitis (FIP) virus in tissue culture and experimental cat infection studies », Veterinary Microbiology, vol. 219, , p. 226–233 (ISSN 0378-1135, PMID 29778200, PMCID 7117434, DOI 10.1016/j.vetmic.2018.04.026, lire en ligne, consulté le )
- Niels C Pedersen, Michel Perron, Michael Bannasch et Elizabeth Montgomery, « Efficacy and safety of the nucleoside analog GS-441524 for treatment of cats with naturally occurring feline infectious peritonitis », Journal of Feline Medicine and Surgery, vol. 21, no 4, , p. 271–281 (ISSN 1098-612X, PMID 30755068, PMCID 6435921, DOI 10.1177/1098612X19825701, lire en ligne, consulté le )
- Niels Pedersen, « Neurological & Ocular FIP », sur Sockfip, (consulté le )
- (en) Peter J. Dickinson, Michael Bannasch, Sara M. Thomasy et Vishal D. Murthy, « Antiviral treatment using the adenosine nucleoside analogue GS ‐441524 in cats with clinically diagnosed neurological feline infectious peritonitis », Journal of Veterinary Internal Medicine, vol. 34, no 4, , p. 1587–1593 (ISSN 0891-6640 et 1939-1676, PMID 32441826, PMCID PMC7379040, DOI 10.1111/jvim.15780, lire en ligne, consulté le )
- (en) « FIP drugs continue to show promise, while being sold on black market », sur American Veterinary Medical Association (consulté le )
- Yingjun Li, Liu Cao, Ge Li et Feng Cong, « Remdesivir Metabolite GS-441524 Effectively Inhibits SARS-CoV-2 Infection in Mouse Models », Journal of Medicinal Chemistry, , acs.jmedchem.0c01929 (ISSN 0022-2623, PMID 33523654, PMCID 7875336, DOI 10.1021/acs.jmedchem.0c01929, lire en ligne, consulté le )
- (en) Wanchao Yin, Xiaodong Luan, Zhihai Li et Yuanchao Xie, « Structural basis for repurpose and design of nucleoside drugs for treating COVID-19 », bioRxiv, , p. 2020.11.01.363812 (DOI 10.1101/2020.11.01.363812, lire en ligne, consulté le )
- (en) « Essai clinique numéro NCT04859244 pour "First-in-Human Study of Orally Administered GS-441524 for COVID-19" », sur ClinicalTrials.gov
- Travis K. Warren, Robert Jordan, Michael K. Lo et Adrian S. Ray, « Therapeutic efficacy of the small molecule GS-5734 against Ebola virus in rhesus monkeys », Nature, vol. 531, no 7594, , p. 381–385 (ISSN 0028-0836, PMID 26934220, PMCID 5551389, DOI 10.1038/nature17180, lire en ligne, consulté le )
- Timothy P. Sheahan, Amy C. Sims, Rachel L. Graham et Vineet D. Menachery, « Broad-spectrum antiviral GS-5734 inhibits both epidemic and zoonotic coronaviruses », Science translational medicine, vol. 9, no 396, , eaal3653 (ISSN 1946-6234, PMID 28659436, PMCID 5567817, DOI 10.1126/scitranslmed.aal3653, lire en ligne, consulté le )
- Brandi N. Williamson, Friederike Feldmann, Benjamin Schwarz et Kimberly Meade-White, « Clinical benefit of remdesivir in rhesus macaques infected with SARS-CoV-2 », bioRxiv, , p. 2020.04.15.043166 (PMID 32511319, PMCID 7239049, DOI 10.1101/2020.04.15.043166, lire en ligne, consulté le )
- « COVID-19 », sur opendata.ncats.nih.gov (consulté le )
- (en) Aaron M. Izes, Jane Yu, Jacqueline M. Norris et Merran Govendir, « Current status on treatment options for feline infectious peritonitis and SARS-CoV-2 positive cats », Veterinary Quarterly, vol. 40, no 1, , p. 322–330 (ISSN 0165-2176 et 1875-5941, PMID 33138721, PMCID PMC7671703, DOI 10.1080/01652176.2020.1845917, lire en ligne, consulté le )
- (en) Victoria C. Yan et Florian L. Muller, « Advantages of the Parent Nucleoside GS-441524 over Remdesivir for Covid-19 Treatment », ACS Medicinal Chemistry Letters, vol. 11, no 7, , p. 1361–1366 (ISSN 1948-5875 et 1948-5875, PMID 32665809, PMCID PMC7315846, DOI 10.1021/acsmedchemlett.0c00316, lire en ligne, consulté le )
- (en-US) « Gilead should ditch remdesivir and focus on its simpler and safer ancestor », sur STAT, (consulté le )
- (en-US) « Feline coronavirus treatment could stop spread of COVID-19 in humans, doctor says », sur FOX 13 News, (consulté le )
- (en) Niels Pedersen, « FIP in Aged Cats », sur Sock FIP, (consulté le )
- (en) Niels Pedersen, « FIP treatment with oral formulations of GS-441524 » [PDF], sur Sockfip, (consulté le )
- Juliette Sotin, Traitement de la péritonite infectieuse féline par les molécules antivirales GC376 et GS-441524 : état des lieux sur leur utilisation en dehors du cadre légal en France, Faculté de Médecine de Nantes, Oniris - École Nationale Vétérinaire, Agroalimentaire et de l’Alimentation, Nantes Atlantique, , 98 p. (lire en ligne)
- Sarah Jones, Wendy Novicoff, Julie Nadeau et Samantha Evans, « Unlicensed GS-441524-Like Antiviral Therapy Can Be Effective for at-Home Treatment of Feline Infectious Peritonitis », Animals: an open access journal from MDPI, vol. 11, no 8, , p. 2257 (ISSN 2076-2615, PMID 34438720, PMCID 8388366, DOI 10.3390/ani11082257, lire en ligne, consulté le )
- (en) A. Y. Au, J. M. Hasenwinkel et C. G. Frondoza, « Hepatoprotective effects of S-adenosylmethionine and silybin on canine hepatocytes in vitro: Hepatoprotective effects of S-adenosylmethionine and silybin », Journal of Animal Physiology and Animal Nutrition, vol. 97, no 2, , p. 331–341 (DOI 10.1111/j.1439-0396.2012.01275.x, lire en ligne, consulté le )
- (en) Niels C Pedersen, Michel Perron, Michael Bannasch et Elizabeth Montgomery, « Efficacy and safety of the nucleoside analog GS-441524 for treatment of cats with naturally occurring feline infectious peritonitis », Journal of Feline Medicine and Surgery, vol. 21, no 4, , p. 271–281 (ISSN 1098-612X et 1532-2750, PMID 30755068, PMCID PMC6435921, DOI 10.1177/1098612X19825701, lire en ligne, consulté le )
- (en) Niels Pedersen, « Origin of abdominal or thoracic effusions in cats with wet FIP and reasons for their persistence during treatment », sur Sockfip, (consulté le )
- (en) Niels Pedersen, « The Neurological Form of FIP and GS-441524 Treatment », sur Sockfip, (consulté le )
- (en) Niels Pedersen, « Miscellaneous Questions Frequently Arising During Antiviral Drug Treatment for FIP and Aftercare », sur Sockfip, (consulté le )
