Palonosétron
| Palonosétron | ||
| ||
 | ||
| Identification | ||
|---|---|---|
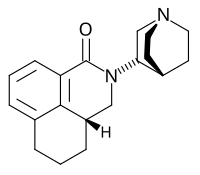
| Nom UICPA | (3aR)-2-[(3S)-1-azabicyclo[2.2.2]oct-3-yl]-2,3,3a, 4,5,6-hexahydro-1H-benz[de]isoquinolin-1-one |
|
| No CAS | ||
| Code ATC | A04 | |
| DrugBank | APRD00351 | |
| PubChem | 6337614 | |
| ChEBI | 651486 (HCl) | |
| SMILES | ||
| InChI | ||
| Propriétés chimiques | ||
| Formule | C19H24N2O [Isomères] |
|
| Masse molaire[1] | 296,406 7 ± 0,017 6 g/mol C 76,99 %, H 8,16 %, N 9,45 %, O 5,4 %, |
|
| Unités du SI et CNTP, sauf indication contraire. | ||
| modifier |
||
Le palonosétron (DCI, nom commercial : Aloxi) est un antagoniste 5-HT3 utilisé dans la prévention et le traitement de chimiothérapie induisant nausées et vomissements. Il est le plus efficace des antagonistes 5-HT3 concernant le retardement des nausées et des vomissements, ceux-ci apparaissent au-delà des 24 heures qui suivent la première dose d'un traitement de chimiothérapie, et est le seul médicament de sa catégorie à avoir été approuvé par Food and Drug Administration[2]. En 2008, il est le plus récent antagoniste 5-HT3 à utilisation clinique.
Le palonosétron est administré soit par voie intraveineuse, une seule dose, 30 minutes avant la chimiothérapie, soit comme une seule gélule par voie orale une heure avant la chimiothérapie[3]. La voie orale a été approuvée le pour la prévention de graves problèmes de chimiothérapie induisant nausées et vomissements[3].
Pharmacocinétique
[modifier | modifier le code]Il a une demi-vie plus longue et une affinité plus importante avec le récepteur 5-HT3 que les antagonistes 5-HT3 plus anciens[4]. Cette propriété d'antagonisme est de type allostérique[5].
Efficacité
[modifier | modifier le code]Il s'avère être supérieur au dolasétron[6] ou à l'ondansétron[7] dans la prévention des nausées ou vomissements tardifs après une chimiothérapie anticancéreuse. En association avec un corticoïde, il s'avère également meilleur que le granisétron[8]. Le traitement corticoïde peut d'ailleurs être écourté sans perte d'efficacité[9].
Notes et références
[modifier | modifier le code]- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) De Leon A, « Palonosetron (Aloxi): a second-generation 5-HT(3) receptor antagonist for chemotherapy-induced nausea and vomiting », Proceedings (Baylor University. Medical Center), vol. 19, no 4, , p. 413–6 (PMID 17106506)
- (en) Waknine, Yael, « FDA Approvals: Nplate, Aloxi, Vidaza », Medscape, (consulté le )ly available with registration.
- Rojas C, Stathis M, Thomas AG et al. Palonosetron exhibits unique molecular interactions with the 5-HT3 receptor, Anesth Analg, 2008;107:469-478
- Eisenberg P, Figueroa-Vadillo J, Zamora R et al. Improved prevention of moderately emetogenic chemotherapy-induced nausea and vomiting with palonosetron, a pharmacologically novel 5-HT3 receptor antagonist: results of a phase III, single-dose trial versus dolasetron, Cancer, 2003;98:2473-2482
- Gralla R, Lichinitser M, Van Der Vegt S et al. Palonosetron improves prevention of chemotherapy-induced nausea and vomiting following moderately emetogenic chemotherapy: results of a double-blind randomized phase III trial comparing single doses of palonosetron with ondansetron, Ann Oncol, 2003;14:1570-1577
- Saito M, Aogi K, Sekine I et al. Palonosetron plus dexamethasone versus granisetron plus dexamethasone for prevention of nausea and vomiting during chemotherapy: a double-blind, double-dummy, randomised, comparative phase III trial, Lancet Oncol, 2009;10:115-124
- Aapro M, Fabi A, Nolè F et al. Double-blind, randomised, controlled study of the efficacy and tolerability of palonosetron plus dexamethasone for 1 day with or without dexamethasone on days 2 and 3 in the prevention of nausea and vomiting induced by moderately emetogenic chemotherapy, Ann Oncol, 2010;21:1083-1088
