Trioza-fosfat izomeraza
| Triozofosfatna izomeraza | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 Side view of triose P isomerase monomer, active site at top center} | |||||||||
| Identifikatori | |||||||||
| EC broj | 5.3.1.1 | ||||||||
| CAS broj | 9023-78-3 | ||||||||
| Baze podataka | |||||||||
| IntEnz | IntEnz pregled | ||||||||
| BRENDA | BRENDA unos | ||||||||
| ExPASy | NiceZyme pregled | ||||||||
| KEGG | KEGG unos | ||||||||
| MetaCyc | metabolički put | ||||||||
| PRIAM | profil | ||||||||
| PDB strukture | RCSB PDB PDBj PDBe PDBsum | ||||||||
| Ontologija gena | AmiGO / QuickGO | ||||||||
| |||||||||
Trioza-fosfat izomeraza (TPI ili TIM) je enzim (5.3.1.1) koji katalizira reverzibilnu međukonverziju trioza fosfat izomera dihidroksiaceton fosfata i D-gliceraldehid 3-fosfata.[1][2][3][4]
TPI ima važnu ulogu u glikolizi pa je od suštinskog značaja za efikasnu proizvodnju energije. Pronađena je u gotovo svakom organizmu u kojem su se tražili enzimi, uključujući i životinje kao što su sisari i insekati, kao i u gljivama, biljkama i bakterijama. Međutim, neke bakterije koje ne prerađuju glikolizu, poput onih iz roda Ureaplasma, nemaju TPI.
Kod ljudi, nedostaci u TPI su povezani sa progresivnim, teškim neurološki poremećajem koji se zove nedostatak trioza fosfat izomeraze. Taj nedostatak se ispoljava u hroničnim hwmolitskim anamijama. Iako postoje različite mutacije koje uzrokuju ovu bolest, većina uključuje mutaciju glutaminske kiseline na poziciji 104 u aspartamskoj kiselini.
Triozo fosfat izomeraza je vrlo učinkovit enzim, obavljajući reakcije milijardama puta brže nego što bi prirodno javljale u otopini. Reakcija je toliko efikasna da se može reći da je katalitski savršena: ograničena je samo onda kada rata podloge može difuzndirati u i iz aktivnog mjesta enzima.
Mehanizam
[uredi | uredi izvor]Mehanizam djelovanja ovog enzima uključuje formiranje međuprodukta "enediol". Relativna slobodna energija svakog stanja podloge i i njihova tranzicija utvrđeni su eksperimentalno, a prikazuje se na slici.
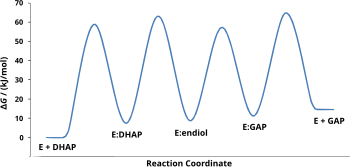
Struktura TPI olakšava konverziju između dihidroksiaceton fosfata (DHAP) i gliceraldehid 3-fosfata (GAP). Glutamatnom TPI, u podlozi se deprotonizira 165 nukleofilnih ostataka, a 95 histidinskih ostatak elektrofilnih ostataka donira proton da se formira endiolni međuprodukt.[5] [6][7][8][9]
Kada se deprotonizirani enediolati onda razlože i, apstrahujući proton iz protoniziranog glutamata 165, nastaje GAP proizvod. Kataliza u obrnutoj reakciji se nastavlja analogno, formiranjem istog endiola ali sa enediolatnim oduzimannjem iz kisika u C2.
Difuzija TPI je ograničena. Što se tiče termodinamike, formiranje DHAP je češće u omjeru 20:1 nego proizvodnja GAP. Međutim, u glikolizi, korištenje GAP u narednim koracima metabolizma pokreće reakcija prema njegovoj proizvodnji.TPI inhibiraju sulfatni, fosfatni i arsenatni ioni, koji se vezuju za aktivna mjesta.
Ostali inhibitori uključuju 2-fosfoglikolat, tranzicijski analog iD-glicerol-1-fosfat, analog supstrata.

Struktura
[uredi | uredi izvor]Trioza fosfat izomeraza je dimer identičnih podjedinica, od kojih je svaka sastavljena od oko 250 aminokiselinskih ostataka. Trodimenzionalna struktura podjedinice sadrži osam i alfa; -heliksa na vanjskoj strani i osam paralelnih unutrašnjih beta; -lanaca. Kao ilustracija, vrpce okosnice svake od podjedinica su obojene plavom u crvenom bojom N-terminusa i C-terminusa. Ovaj strukturni motiv se zove αβ-barel ili TIM-barel, a daleko je najčešći u naborima proteina. Aktivno mjesto ovog enzima je u središtu. A glutaminska kiselina ostataka i histidin su uključeni u katalitičkog mehanizam. Slijed oko aktivne ostataka stranice se štedi u svim poznatim trioza fosfat izomeraze.
Struktura trioza fosfat izomeraze doprinosi njenoj funkciji. Osim precizno postavljenog glutamatnog i histidinskog ostatka za formiranje endiolaj, lanac TPI od deset ili jedanaest aminokiselina djeluje kao petlja za stabilizaciju međuprodukta. Petlja, formirana od 166-176 ostataka, zatvara i formira vodikova veza na fosfatnoj grupi podloge. Ova akcija stabilizira endiolne međuprodukte i druga tranzicijska stanje zokom reakcije.
Pored toga što je reakcija kinetički izvodiva, TPI petlja veže reaktivne endiolne intermedijere za sprečavanje razgradnje u metilglioksal i anorganski fosfat. Veza vodika između enzima i fosfatne grupe podloge čini stereoelektronski nepovoljna razlaganja. Metilglioksal je otrov i, ako je formiran, uklanja se iz glioksalaznog sistema. Gubitak veza visoke energije fosfata i podloge za ostatak glikolize čini formiranje metiloksalat neefikasnim.
Studije pokazuju da se blizu aktivnog mjesta nalazi lizin (na poziciji 12), što je je također od ključnog značaja za funkciju enzima. Lizin, protonovan u fiziološkoj pH sredini, može pomoći neutralizaciju negativnog duga fosfatne grupe. Kada ovaj lizin mutirao na neutralnj aminokiselini, TPI gubi sve funkcije, ali mutant sa različitim pozitivnim nabojem aminokiselina zadržava neke funkcije.
Također pogledajte
[uredi | uredi izvor]Reference
[uredi | uredi izvor]- ^ Voet D., Voet J. (1995): Biochemistry, 2nd Ed. Wiley, https://www.wiley.com/college/math/chem/cg/sales/voet.html.
- ^ Bugg T. (1997): An introduction to enzyme and coenzyme chemistry. Blackwell Science, Oxford, ISBN 0-86542-793-3.
- ^ Lindhorst T. (2007): Essentials of carbohydrate chemistry and biochemistry. Wiley-VCH, 3527315284}}
- ^ Robyt F. (1997): Essentials of carbohydrate chemistry. Springer, ISBN 0387949518.
- ^ Kornberg A. (1989): For the love of enzymes – The Odyssay of a biochemist. Harvard University Press, Cambridge (Mass.), London,ISBN 0-674-30775-5, ISBN 0-674-30776-3.
- ^ Laidler K. J. (1978): Physical chemistry with biological applications. Benjamin/Cummings, Menlo Park, ISBN 0-8053-5680-0.
- ^ Bajrović K, Jevrić-Čaušević A., Hadžiselimović R., Ed. (2005): Uvod u genetičko inženjerstvo i biotehnologiju. Institut za genetičko inženjerstvo i biotehnologiju (INGEB), Sarajevo, ISBN 9958-9344-1-8.
- ^ Hunter G. K. (2000): Vital Forces. The discovery of the molecular basis of life. Academic Press, London 2000, ISBN 0-12-361811-8.
- ^ Nelson D. L., Cox M. M. (2013): Lehninger principles of biochemistry. W. H. Freeman and Co., ISBN 978-1-4641-0962-1.
