塩基性基を含有する化合物およびその用途
技術分野
本発明は、 医薬として有用な塩基性基を含有する化合物およびその用途に 関する。 明
さらに詳しく言えば、 本発明は、 (1田) 一般式'(1—0 )
A1— ΒΊ
D— G— E— L— J° (I-0)
/
A2— B2
(式中、 すべての記号は、 後記と同じ意味を表わす。 )
で示される化合物、 その塩、 その N—ォキシド体もしくはその溶媒和物、 ま たはそれらのプロドラッグ、 (2 ) その用途、 および (3 ) その製造方法に 関する。
背景技術
ケモカインは、 内因性の白血球に対して走化性と活性化作用を有し、 へパ リン結合性の強い塩基性蛋白質として知られている。 現在では、 ケモカイン は炎症、 免疫反応時の特異的白血球の浸潤を制御するのみならず、 発生、 生 理的条件下でのリンパ球のホーミング、 血球前駆細胞や体細胞の移動にも関 わると考えられている。
血球細胞は種々のサイトカインによつてその分化、 増殖およぴ細胞死が制 御されている。 生体内において炎症は局所的にみられ、 リンパ球の分化、 成 熟等はある特定の部位で行なわれている。 すなわち、 必要とされる種々の細 胞がある特定の部位に移動、 集積して、 一連の炎症や免疫反応が起こる。 従 つて、 細胞の分化、 増殖や死に加えて、 細胞の移動も免疫系にとって必要不
可欠な現象である。
生体内での血球細胞の移動は、まず発生過程において、 A GM (Aorta Gonad Mesonephros;大動脈 ·性腺 ·中腎) 領域に始まる造血が胎児肝を経て、 骨 髄での永久造血へと移行することから始まる。 さらに、 胎児肝、 骨髄から胸 腺へと、 T細胞、 胸腺樹状細胞の前駆細胞が移動し、 胸腺環境下で細胞分化 する。 クローン選択を受けた T細胞は二次リンパ組織へ移動し、 末梢におけ る免疫反応に関与する。 抗原を捕らえて、 活性化、 分ィ匕した皮膚のランゲル ハンス細胞は、 局所リンパ節の τ細胞領域に移動し、 榭状突起細胞としてナ ィープ T細胞を活性ィヒする。 メモリー T細胞はリンパ管、 血管を経て、 再び リンパ節にホーミングする。 また、 B細胞、腸管上皮内 T細胞、 Ί δ Τ細胞、 ΝΚΤ細胞、 樹状細胞は、 骨髄より胸腺を経ずに移動、 分化し、 免疫反応に 関与する。
ケモカインは、このような種々の細胞の移動に深く関与している。例えば、 S D F - 1 (Stromal cell derived factor- 1;ストロ一マ細胞由来因子一 1 ) およびその受容体である C X C R 4は種々の免疫 ·炎症反応にも作用してい る。 例えば、 関節リウマチのヒト患者由来の滑膜における C D 4 + T細胞の 蓄積と活性化に関与していることが報告されている (J. Immunol., 165, 6590-6598 (2000)) 。 さらに、' C I Aモデルマウスにおいても C X C R 4阻 害薬は関節への白血球の集積を抑制し、関節炎スコアを劇的に減少させた(J. Immunol., 167, 4648-4692 (2001» 。 マウス O VA誘発気道過敏性モデルに おいて、 抗 C X C R 4抗体は肺間質に集積する好酸球数を減らし、 気道過敏 性を抑制した (J. Immunol., 165, 499-508 (2000)) 。
S D F— 1とその受容体である C X C R 4は造血幹細胞の骨髄での維持に 重要な働きをしていることも報告されている (J. Exp. Med., 185, 111 - 120 (1997)、 Blood, 97, 3354-3360 (2001)) 。 従って、 S D F— 1および C X C R 4の制御は末梢血への造血幹細胞動員を調節することが期待され、 末梢血幹
細胞移植、 さらには再生移植治療に有用である。
SDF—1ぉょぴCXCR4は乳癌、 前立腺癌、 卵巣癌等の種々の癌細胞 浸潤に関与しており (Nature, 410, 50-56 (2001)、 Cancer Res., 62, 1832-1837 (2002)、 Cancer Res., 62, 5930—5938 (2002)) 、 S C I Dマウスへ のヒト乳癌細胞株の移入モデルにおいて抗 C XCR4抗体が乳癌細胞の肺へ の転移を抑制した(Nature, 410, 50- 56 (2001))。 またヒト卵巣上皮性腫瘍に おいて S D F— 1が高発現することにより、 形質性細胞様樹状細胞の蓄積を 促進して腫瘍免疫に関与する骨髄樹状細胞の働きを阻害し、 腫瘍免疫を抑制 している (Nat. Med., 12, 1339 (2001)) 。 さらに非ホジキンリンパ腫細胞の 増殖、 移動に関与し、 ヒト非ホジキンリンパ腫細胞の NOD/SC I Dマウ スへの移入モデルにおいて、 抗 C X C R 4抗体が腫瘍細胞の増殖を抑制し、 マウスの死亡率を改善した (Cancer Res., 62,3106-3112(2002)) 。
SDF— 1および CXCR4は記憶と学習に必須の海馬歯状回顆粒細胞の 形成に重要な役割を果たしており、 成人の可塑性と海馬の病態に関連した疾 患、 例えばアルツハイマー病や脳卒中、 癲癇等の進展に関与している
(Development, 129, 4249-4260 (2002)、 Trends in Neuroscience, 25, 548-549 (2002)) 。
SDF— 1および CXCR4は糖尿病の進展に関与する自己反応性 B細胞 の機能に必須であり、 NODマウスに対して、 抗 SDF— 1抗体が血糖値を 減少させ、 末梢組織中の成熟 I g M+ B細胞数を減少させた (Imimmology, 107, 222-232 (2002))。またヒト動脈硬化プラークで S D F— 1が高発現し、 血小板を活性ィ匕させた (Cixc. Kes., 86, 131-138 (2000)) 。
SDF- 1および C X C R 4は, 造血幹細胞や造血前駆細胞の骨髄中への 滞留に関与しており, CXCR4アンタゴニストである AMD 3100が G 一 C S Fとの併用により, 末梢血中に造血幹細胞や造血前駆細胞数を増加さ せた (Journal Experimental Medicine, 2001,1307-1318 (2005)。
また SDF— 1ZCXCR4ノックァゥトマウスの結果から、 SDF— 1 はリンパ球以外に中枢神経組織、 心臓、 胃腸管の血管の機能に必須であるこ とが示されている (Nature, 382, 635-639 (1996)、 Nature, 393, 591-594 (1998)、 Nature, 393, 595-599 (1998)) 。 このことから、 これらの組織の疾 患に関与していると考えられる。
このように、 ケモカイン受容体は種々の特異的な細胞において、 ある特定 した時期に発現し、 そのエフェクター細胞がケモカインの産生される個所に 集積するというメカニズムを通じて、 炎症、 免疫反応の制御に大きく関与し ている。
ヒト免疫不全ウィルス (以下、 H IVと略する。 ) 感染によって引き起こ される後天性免疫不全症侯群 (エイズ (AIDS) と呼ばれている。 ) は、 近年最もその治療法を切望されている疾患の一つである。 主要な標的細胞で ある CD 4陽性細胞に H I Vの感染が一度成立すると、 H I Vは患者の体内 で増殖をくり返し、 やがては免疫機能を司る T細胞を壊滅的に破壌する。 こ の過程で徐々に免疫機能が低下し、 発熱、 下痢、 リンパ節の腫脹等の様々な 免疫不全状態を示すようになり、 カリ -肺炎等の種々の日和見感染症を併発 し易くなる。 このような状態がエイズの発症であり、 力ポジ肉腫等の悪性腫 瘍を誘発し、 重篤化することはよく知られている。
現在エイズに対する各種の予防および/または治療方法としては、 例えば、 (1) 逆転写酵素阻害薬やプロテアーゼ阻害薬の投与による HI Vの増殖抑 制、 (2) 免疫賦活作用のある薬物の投与による曰和見感染症の予防、 緩和 等が試みられている。
HIVは、 免疫系の中枢を司るヘルパー T細胞に主に感染する。 その際、 T細胞の膜上に発現している膜蛋白 CD4を利用することは、 1985年より知 られている (Cell, 52, 631 (1985))。 CD 4分子は 433個のアミノ酸残基か らなり、 成熟へノレパー T細胞以外にマクロファージ、 一部の B細胞、 血管內
皮細胞、 皮膚組織のランゲノレハンス細胞、 リンパ組織にある樹状細胞、 中枢 神経系のグリア細胞等で宪現が見られる。 しかし、 CD 4分子のみでは HI Vの感染が成立しないことが明らかになるにつれて、 H I Vが細胞に感染す る際に関わる CD 4分子以外の因子が存在する可能性が示唆されるようにな つた。
1996年に CD 4分子以外の H I V感染にかかわる因子としてフージン (Fusin) という細胞膜蛋白が同定された (Science, 272, 872 (1996)) 。 この フージン分子は、 SDF— 1の受容体、 すなわち' CXCR 4であることが証 明された。 さらに、 イン ' ビトロ (in vitro) で S D F— 1が、 T細胞指向性 (Χ4) HI Vの感染を特異的に抑制することも証明された (Nature, 382, 829 (1996)、 Nature, 382, 833 (1996)) 。 すなわち、 S D F— 1が H I Vより 先に CXCR 4に結合することによって、 H I Vが細胞に感染するための足 掛かりを奪い、 HI Vの感染が阻害されたと考えられる。
また同じ頃、別のケモカイン受容体であり、 RANTES、 MI P— 1 α、 MI Ρ— 1 ]3の受容体である CCR 5も、 マクロファージ指向性 (R5) H I Vが感染する際に利用されることが発見された (Science, 272, 1955 (1996)) 。
従って、 HI Vと CXCR4や CCR5を奪い合うことのできるもの、 あ るいは H I Vウィルスに結合し、 該ウィルスが CXCR4や CCR 5に結合 できない状態にさせるものは、 HI V感染阻害薬となり得る可能性がある。 また当初、 HI V感染阻害薬として発見された低分子化合物が、 実は CXC R 4の拮抗薬であることが示された例もある (Nature Medicine, 4, 72 (1998)) 。
以上のことから、 CXCR 4拮抗作用を有する化合物は、 例えば、 炎症- 免疫性疾患、 アレルギー性疾患、 感染症、 特に HI V感染およびそれに随伴 する疾患、 精神,神経性疾患、 脳疾患、 心 ·血管性疾患、 代謝性疾患、 癌疾
患の予防および/または治療に有効である。 また、 細胞医療ならびに再生医 療にも有用である。
現在まで、 CXCR 4拮抗作用を有する化合物がいくつ力報告されている。 例えば、 一般式 (X) (
χ)
(式中、 Axは、
R1X R2X R1X
Aix_Gix_j_ または A1X— 一 —
A2X
を表わし、 A1Xおよび A2Xはそれぞれ独立して、 水素原子、 置換していても よい単環もしくは多環式の複素芳香族環または置換していてもよい単環もし くは多環式の芳香族環を表わし、 G1Xは、 単結合または一 CR2XR3X—を表 わし、 R1X、 R2X、 R3Xは置換されていてもよい炭素数 1〜6アルキル基等 を表わし、 Wxは置換していてもよい炭素数 1〜 7アルキレン基、 置換してい てもよい単環もしくは多環式の複素芳香族環または置換していてもよレヽ単環 もしくは多環式の芳香族環等を表わし、 xxは、一 Z 1X— CO— Z —等を表 わし、 z lx、 z2xはそれぞれ独立して、 単結合、 NR13X等を表わし、 yxは 一 CO—等を表わし、 D1Xおよび D2Xはそれぞれ独立して、 水素原子または 一 G2X— R4Xを表わし、 G2Xは置換していてもよい炭素数 1〜15アルキレ ン基等を表わし、 R4Xは水素原子、 置換していてもよい単環もしくは多環式 の複素芳香族環または置換していてもよい単環もしくは多環式の芳香族環等 を表わし、 2 は0〜4を表ゎし、 11 1 は0〜3を表ゎし、 BXは、 一 NR6XR7X等を表わす。 なお、 各基の定義は必要な部分のみを抜粋した。 ) で示される化合物またはその薬学的に許容される塩が C X C R 4拮抗作用を
有することが開示されている (WO03/029218号パンフレット参照) 。
(式中、 n1Y、 n2Y、 η3Υは 0〜3を表わし、 R1Y、 R2Y、 R3Y、 R4Y、 R5Y、 R6Yはそれぞれ独立して、 水素原子、 置換していてもよい炭素数 1〜 15アルキノレ基等を表わし、 A1Yおよび A2Yはそれぞれ独立して、 置換して いてもよい単環もしくは多環式の複素芳香族環等を表わし、 WYは置換してい てもよい炭素数 1〜15アルキレン基等を表わし、 Χγは 0、 CH2、 NR11 γ等を表わし、 DYは— QY— Υγ— Βγ等を表わし、 QYは Χγが NR11Yの場合 には単結合または一 CO—等を表わし、 Υγは一 (CR18YR19Y) m3Y—等を 表わし、 R18Y、 R19Yはそれぞれ独立して、 水素原子、 置換していてもよい 炭素数 1〜15アルキル基等を表わし、 m3Yは 0〜6を表わし、 Βγは一 N R25YR26Y等を表わし、 R25Y、 R26Yは、 Χγが CH2でない場合には水素 原子、 置換していてもよい炭素数 1〜15アルキル基等を表わす。 なお、 各 基の定義は必要な部分のみを抜粋した。 )
で示される化合物またはその薬学的に許容される塩、 もしくはそのプロドラ ッグが C X C R 4拮抗作用を有することが開示されている (WO2004/024697 号パンフレツト参照) 。 発明の開示
炎症 ·免疫性疾患 (例えば、 関節リウマチ、 関節炎、 網膜症、 肺線維症、 移植臓器拒絶反応等) 、 アレルギー性疾患、 感染症 (例えば、 ヒト免疫不全 ウィルス感染、 後天性免疫不全症候群等) 、 癌疾患 (例えば、 癌、 癌転移等) 等の予防および Zまたは治療剤、 または再生医療用剤は医薬品として有用で
あり、 副作用の少ない、 安全な CXCR 4拮抗薬の開発が切望されている。 本発明者らは、 鋭意検討した結果、 驚くべきことに、 後述の一般式 (I一 0) で示される化合物が強い CXCR4拮抗活 14を有することを見出し、 本 発明を完成した。
すなわち、 本発明は、
(式中、 A1および A2はそれぞれ独立して、塩基性基を含有する基を表わし; B 1および B 2はそれぞれ独立して、 結合手または主鎖の原子数 1〜 4のスぺ 一サーを表わし; Eは、主鎖の原子数 1〜 10のスぺーサーを表わし; Lは、 結合手または主鎖の原子数 1〜4のスぺ一サーを表わし; J。は、 (1) 塩基 性基を含有する基によって置換され、 さらに置換基を有していてもよい脂肪 族炭化水素基、 (2) 塩基性基を含有する基によって置換され、 さらに置換 基を有していてもよい環状基、 (3>塩基性基を含有する基によって置換さ れていてもよく、さらに置換基を有していてもよいスピロ環状基、または(4) 塩基性基を含有する基によって置換されていてもよく、 さらに置換基を有し ていてもよい架橋した環状基を表わし;
は一重結合または二重結合を表わし;
― がー重結合を表わす場合、 Dは、窒素原子または置換基を有していても よい炭素原子を表わし、 Gは、 置換基を有していてもよい炭素原子、 カルボ -ル基、 酸素原子、 置換基を有していてもよい窒素原子または酸化されてい てもよい硫黄原子を表わし;
=^ が二重結合を表わす場合、 Dは炭素原子を表わし、 Gは置換基を有して いてもよい炭素原子または窒素原子を表わす。
ただし、 J。が前記 (1) または (2) を表わし、 かつ Dが窒素原子を表わす
場合、 Gがカルボ二ノレ基、 酸素原子、 置換基を有していてもよい窒素原子ま たは酸化されていてもよい硫黄原子を表わすか、 B^S— 0—、 一S—、 一 C O—、 一 SO—、 一 so2—、 および置換基を有していてもよい二価の窒素原 子から選択される少なくとも一つを含有する主鎖の原子数 1〜 4のスぺーサ 一を表わすものとする。 ) で示される化合物、 その塩、 その N—ォキシド体 もしくはその溶媒和物、 またはそれらのプロドラッグ;
[2] 一般式 (I)
A1— B1
D— G一 E— L ~ J (I)
A2-B2
(式中、 Jは、 [1] 記載の J°の (1) または (2) と同じ意味を表わし、 その他の記号は [1] と同じ意味を表わす。
ただし、 Dが窒素原子を表わす場合、 Gがカルボ二ノレ基、 酸素原子、 置換基 を有していてもよい窒素原子または酸化されていてもよい硫黄原子を表わす 力 B1が一 O—、 一 S—、 一 CO—、 一 SO—、 一SO2—、 および置換基 を有していてもよい二価の窒素原子から選択される少なくとも一つを含有す る主鎖の原子数 1〜4のスぺ一サーを表わすものとする。 ) で示される [1] 記載の化合物;
[3] J。が [1] 記載の (3) または (4) である [1] 記載の化合物;
[4] J °が塩基性基を含有する基によって置換されていてもよく、 さらに 置換基を有していてもよい、 少なくとも一つの窒素原子を含有し、 さらに酸 素原子おょぴ Zまたは酸化されていてもよい硫黄原子を含有していてもよい スピロ複素環または架橋した複素環である [3] 記載の化合物;
[5] J °が塩基性基を含有する基によって置換され、 さらに置換基を有し ていてもよいスピロ炭素環または架橋した炭素環である [3〕記載の化合物;
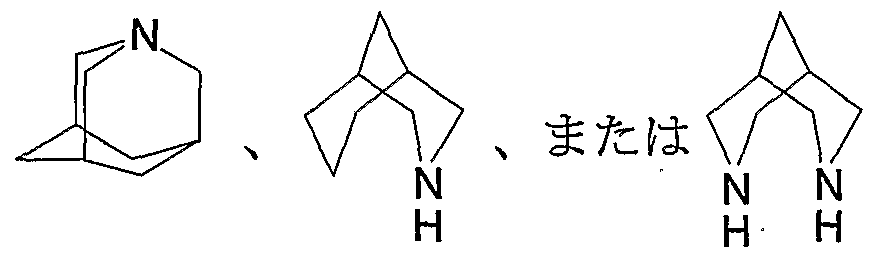
[6] 少なくとも一つの窒素原子を含有し、' さらに酸素原子および/また は酸化されていてもよい硫黄原子を含有していてもよいスピロ複素環または
架橋した複素環が
である [4] 記載の化合物;
[7] スピロ複素環を構成する環が、 少なくとも一つの窒素原子、 および 炭素原子からなる単環、 および Zまたは少なくとも一つの窒素原子、 酸素原 子一つ、 および炭素原子からなる単環からなる 7〜15員の二環式のスピロ 複素環である [4] 記載の化合物;
である [7] 記載の化合物;
である [5] 記載の化合物;
[10] A 1および A 2がそれぞれ独立して、 置換基を有していてもよい含 窒素複素環である [1] 記載の化合物;
[1 1] 含窒素複素環がィミダゾール環またはべンゾィミダゾール環であ る [10] 記載の化合物;
[12] B1および B2で表わされる主鎖の原子数 1〜4のスぺーサ一が、 それぞれ独立して一 CO—、 一 S02—または一 CH2—である [1] 記載の 化合物;
[13] Dが窒素原子である [1] 記載の化合物;
[14] Gがー CO—、 一S02—または一 CH2—である [1] 記載の f匕 合物;
[15] Eが置換基を有していてもよい二価の 3〜 8員の単環式環状基で ある [1] 記載の化合物;
[16] 3〜8員の単環式環状基が、 ベンゼン環である [15] 記載の化 合物;
[17] Lがー CH2—、 一 CONH—または一 CH2— NH— (ただし、 各基の右側に J °が結合するものとする。 ) である [1〕 記載の化合物;
[18] 塩基性基が、 モノーまたはジー置換アミノ基である [2] 記載の化 合物;
[1 9] ジー置換アミノ基の置換基が、 C 1〜8アルキル基および Zまた は環状基である [18] 記載の化合物;
[20] ジー置換アミノ基が、 ジプロピルアミノ基、 または N—シクロへ キシ Λ^— N—プロピルァミノ基である [19] 記載の化合物;
[21] 脂肪族炭化水素基がプチル基、 または環状基がシクロへキシル基 である [2] 記載の化合物;
[22] 一般式 (I一 3)
(式中、 環 A1Aおよぴ環 A2Aはそれぞれ独立して置換基を有していてもよい 含窒素複素環基を表わし; B 1A、 B 2 Aおよび G Aはそれぞれ独立して一 C O—、 一 S02—または一 CH2—を表わし;環 EAは置換基を有していてもよい二価 の 3〜 8員の単環式環状基または置換基を有していてもよい二価の 9または 10員の多環式環状基を表わし、 Lは [1] と同じ意味を表わし、 Jは [2] と同じ意味を表わす。 ただし、 B1Aおよび GAのいずれかは一 CO—または一 S02—を表わす。 ) で示される [2] 記載の化合物;
[23] Lが結合手、 —CH2—、 — CONH—、 — CH2— NH—、 一 O 一 CH2—、 一S— CH2—または一 CH2— CH2— (ただし、 各基の右側に Jが結合するものとする。 ) である [22] 記載の化合物;
[24] 一般式 (I一 4)
(式中、 環 A1Bおよび環 A2Bは、 それぞれ独立して置換基を有していてもよ いイミダゾールまたはべンゾイミダゾールを表わし、 環 EAは [22] と同じ 意味を表わし、 その他の記号は [1] と同じ意味を表わす。 ) である [1] 記載の化合物;
(基中、
(a) LAが、 一 (置換基を有していてもよい炭素数 1〜 3の脂肪族炭化水 素基) 一 (置換基を有していてもよい窒素原子) 一である場合は、 環 J ま、 (i) C3〜l 0の単環または二環式炭素環、 または (ii) 炭素原子、 酸素原 子およひ:/または酸化されていてもよい硫黄原子からなる 3〜10員の単環 または二環式複素環を表わし、
(b) LAが、 置換基を有していてもよい二価の炭素数 1〜4の脂肪族炭化 水素基である場合は、 環 J1は、 少なくとも一つの窒素原子を含有し、 さらに 酸素原子および Zまたは酸化されていてもよい硫黄原子を含有していてもよ い 3〜10員の単環または二環式複素環を表わし、
環 J2は (i) 塩基性基を含有する基によって置換された、 C 3〜10の単 環または二環式炭素環、 (ii) 塩基性基を含有する基によって置換された、 炭 素原子、 酸素原子および/または酸化されていてもよい硫黄原子からなる 3 〜10員の単環または二環式複素環、 または(iii)塩基性基を含有する基によ つて置換されてもよい、 少なくとも一つの窒素原子を含有し、 さらに酸素原 子または酸化されていてもよい硫黄原子を含有していてもよい 3〜10員の 単環または二環式複素環を表わし、
環 J 1および環 J 2は置換可能な位置に 1〜 8個の置換基を有していてもよ く、 置換基が 2つ以上ある場合、 複数の置換基は同じでも異なっていてもよ い。
ただし、 LA中の (置換基を有していてもよい窒素原子) は環 J1に結合する ものとする。 ) である [24] 記載の化合物;
[26]
原子に結合していてもよく、 一 NH—の窒素原子は置換基を有していてもよ い。 ) である [25] 記載の化合物;
(基中、 LAは [25] と同じ意味を表わす。 ただし、 LAは一 NH—の窒素 原子に結合していてもよく、 一 NH—の窒素原子は置換基を有していてもよ い。 ) である [25] 記載の化合物;
[28] —般式 (I一 4一 1 a)
または一般
(式中、 L A1は置換基を有していてもよい二価の炭素数 1 ~ 4の脂肪族炭化 水素基を表わし、 R1は水素原子、または置換基を表わし、その他の記号は [2 4] と同じ意味を表わす。 ) である [24] 記載の化合物;
[29] 一般式 (I一 4一 2)
(式中、 全ての記号は [24] 、 および [28] と同じ意味を表わす。 ) で
ある [24] 記載の化合物;
[30] 一般式 (Iー4一 3 a)
または一般式 (I一 4— 3 b)
(式中、 全ての記号は [24] 、 および [28] と同じ意味を表わす。 ) で ある [24] 記載の化合物;
[31] 一般式 (I一 4一 4)
(式中、 全ての記号は [24] 、 および [28] と同じ意味を表わす。 ) で ある [24] 記載の化合物;
[32] 一般式 (I一 4一 5)
(式中、 全ての記号は [24] 、 および [28] と同じ意味を表わす。 ) で ある [24] 記載の化合物;
[33] R1で示される置換基が脂肪族炭化水素基、 環状基、 環状基で置換 された脂肪族炭化水素基である [28] 乃至 [32] のいずれかに記載の化合 物;
[34]
(基中、 環 J 3は (i) 塩基性基を含有する基によって置換された、 架橋した 多環式炭素環、 (ϋ) 塩基性基を含有する基によって置換された、 炭素原子、 酸素原子およぴ κまたは酸化されていてもょ 、硫黄原子からなる架橋した多 環式複素環、 または (iii) 塩基性基を含有する基によって置換されてもよい、 少なくとも一つの窒素原子を含有し、 さらに酸素原子および/または酸化さ れていてもよい硫黄原子を含有していてもよい架橋した多環式複素環を表わ し、
環 J 3は置換可能な位置に 1〜 8個の置換基を有していてもよく、 置換基が 2つ以上ある場合、 複数の置換基は同じでも異なっていてもよく、 LAは [2 5] と同じ意味を表わす。 ) である [24] 記載の化合物;
[35〕 架橋した多環式炭素環が
、ま である [34] 記載の化合物;
[36] 少なくとも一つの窒素原子を含有し、 さらに酸素原子およひ ま たは酸化されていてもよい硫黄原子を含有していてもよい架橋した多環式複
[37]
(基中、 環 J4は (i) 塩基性基を含有する基によって置換された、 C 3〜l 5の単環または縮合した炭素環、 (ii) 塩基性基を含有する基によって置換さ れた、 炭素原子、 酸素原子および Zまたは酸化されていてもよい硫黄原子か らなる 3〜15員の単環または縮合した複素環、または(iii)塩基性基を含有 する基によって置換されてもよい、 少なくとも一つの窒素原子を含有し、 さ らに酸素原子および Zまたは酸化されていてもよい硫黄原子を含有していて もよい 3~15員の単環または縮合した複素環を表わし、
環 J 4は置換可能な位置に 1 ~ 8個の置換基を有していてもよく、 置換基が 2つ以上ある場合、 複数の置換基は同じでも異なっていてもよく、 LAは [2 5] と同じ意味を表わす。 ) である [24] 記載の化合物;
[38] C 3〜l 5の単環または縮合した炭素環が
である [37] 記載の化合物;
[39] C 3〜 15の単環または縮合した炭素環がシク口へキシル基であ る [38] 記載の化合物;
[40] 一般式 (I一 4一 6)
(式中、 L
A2は置換基を有していてもよい炭素数 1〜 3の脂肪族炭化水素基 を表わし、 R
2、 R
3および R
4は、 それぞれ独立して水素原子または置換基を 表わし、 R
2と R
3は結合する窒素原子と一緒になつて置換基を有していても よい環を形成してもよく、 その他の記号は [24] と同じ意味を表わす。 ) である [24] 記載の化合物;
[41] R 2および R 3がそれぞれ独立して、水素原子、脂肪族炭化水素基、 C3〜l 5の単環または縮合した炭素環、 または C3〜l 5の単環または縮 合した炭素環によって置換された脂肪族炭化水素基であるか、 または R 2およ ぴ R 3が結合する窒素原子と一緒になつて単環または縮合した複素環を形成 し、ただし、結合する窒素原子以外の複素環の構成原子が炭素原子である [4 0] 記載の化合物;
[42] R4が、 水素原子、 脂肪族炭化水素基、 または水酸基によって置換 された脂肪族炭化水素基である [40] 記載の化合物;
[43] 少なくとも一つの窒素原子を含有し、 さらに酸素原子および Zま たは酸化されていてもよい硫黄原子を含有していてもよい 3〜15員の単環 または縮合した複素環が
(式中、 環 A
1A、 環 A
2Aおよび環 E
Aは [22] と同じ意味を表わし、 L
Aは [25] と同じ意味を表わし、 J
0は [1] 記載の J
0の (3) または (4) と同じ意味を表わす。 ) である [1] 記載の化合物;
[45]
(基中、 LA1および R1は [28] と同じ意味を表わす。 ) である [44] 記 載の化合物;
[46] R1で示される置換基が脂肪族炭化水素基、 環状基、 または環状基 で置換された脂肪族炭化水素基である [45] 記載の化合物;
[47] 4- ( { [4- (ジプロピルァミノ) プチル] アミノ} メチル) 一 N, N—ビス (1 H—イミダゾ一/レー 2—イノレメチル) ベンズアミ ド、 4 一 ( { [3— (ジブチノレアミノ) プロピル] ァミノ) メチノレ) 一 N, N—ビ ス ( 1 H—イミダゾールー 2—イノレメチル) ベンズアミ ド、 4一 ( { [5— (ジプロピルァミノ) ペンチル] アミノ} メチル) 一 N, N—ビス (1H— イミダゾールー 2—ィルメチル) ベンズアミ ド、 4一 ( {4— [ (ジプロピ ルァミノ) メチル] 一 1ーピペリジニル } メチル) 一 N, N—ビス (1H— イミダゾールー 2—ィルメチル) ベンズアミ ド、 4一 ( { [4一 (ジプロピ ノレァミノ) シクロへキシル] ァミノ) メチノレ) 一 N, N—ビス (1H—イミ ダゾーノレ一 2—ィルメチル) ベンズアミ ド、 4ー ( { [3— (ジプロピルァ ミノ) プロピノレ] ァミノ) メチル) 一 N, N—ビス (1 H—ィミダゾーノレ一 2—イノレメチノレ) べンズアミ ド、 4一 [ (2—ペンジノレー 2. 9—ジァザス
ピロ [5· 5〕 ゥンデ力一 9一ィル) メチル] 一 Ν, Ν—ビス (1H—イミ ダゾーノレ一 2一イノレメチノレ) ベンズアミ ド、 4- [ (2—シク口へキシルー 2, 9—ジァザスピロ [5. 5] ゥンデカー 9一ィル) メチル] 一 Ν, Ν— ビス ( 1 Η—イミダゾールー 2—ィルメチル) ベンズアミ ド、 2— [4一 (ジ プロピルァミノ) ブチル] — Ν, Ν—ビス ( 1 Η—ィミダゾ一/レー 2ーィル メチル) 一 1, 2, 3, 4—テトラヒドロー 6—イソキノリンカノレポキサミ ド、 Ν— [4一 ( { [4— (ジプロピルアミノ) プチル] アミノ} メチル) ベンジル] — N— (1H—イミダゾールー 2—ィルメチル) 一 1 Η— ^ ミダ ゾールー 2—力ルポキサミド、 4一 ( { [4一 (ジプロピルァミノ) プチル] アミノ} メチル) 一 N, N—ビス (1H—イミダゾールー 2— ^ ルメチル) ベンゼンスルホンアミ ド、 4一 [ ( {トランス一 4一 [シクロへキシル (プ 口ピル) ァミノ] シクロへキシル } ァミノ) メチル] 一 N, N—ビス (1 H 一イミダゾールー 2—ィルメチル) ベンズァミド、 4一 [ (2—シクロへキ シルー 2, 8—ジァザスピロ [4. 5] デカー 8—^ fル) メチル] — N, N 一ビス (1 H—イミダゾールー 2—ィルメチル) ベンズアミ ド、 または 4一 [ (8—シクロへキシルー 2, 8—ジァザスピロ [4. 5] デカー 2—ィノレ) メチル] — N, N—ビス (1H—イミダゾールー 2—ィルメチル) ベンズァ ミドである [1] 記載の化合物;
[48] 4- [ (2—シクロへキシルー 2, 8—ジァザスピロ [4. 5] デカー 8—ィル) メチル] -N, N—ビス (1H—イミダゾールー 2—ィル メチル) ベンズァミ ド、 4一 [ ( 8—シク口へキシル一 2, 8ージァザスピ 口 [4. 5] デカ一 2—ィル) メチル] 一 N, N—ビス (1H—イミダゾー ルー 2一^ ルメチル) ベンズアミ ド、 4— [ (2—シクロへキシルー 2, 8 ージァザスピロ [4. 5] デカー 8—ィル) メチル] 一 N, N—ビス (1H ーィミダゾーノレ一 2一ィルメチル) ベンズアミド、 4一 [ (8—シク口へキ シル一 2, 8ージァザスピロ [4. 5] デカ一 2—ィル) メチル] 一 N, N
—ビス (1H—イミダゾールー 2—^ Tルメチル) ベンズアミド、 N, N—ビ ス (1H—^ f ミダゾ一ノレ一 2—イノレメチノレ) 一4— { [8 - (2—チェ二ノレ メチル) 一2, 8ージァザスピロ [4. 5] デカー 2—ィル] メチル } ベン ズアミド、 N— (1 H—ベンゾイミダゾール一 2—ィルメチル) 一 4一 [ (8 ーシクロへキシルー 2, 8—ジァザスピロ [4. 5] デカー 2—ィル) メチ ル]— N— ( 1 H—ィミダゾ一/レー 2—イノレメチル)ベンズァミ ド、 4一 [ ( 8 ーシク口へプチ/レー 2, 8—ジァザスピロ [4. 5] デカー 2—ィル) メチ ル] 一 N, N—ビス (1H— ^ ミダゾ一ルー 2—ィルメチル) ベンズアミド、 N, N—ビス (1 H—イミダゾールー 2—ィルメチル) 一 4一 ( {8— [ (3 ーメチルー 2—チェニル) メチル] —2, 8ージァザスピロ [4. 5] デカ — 2—ィル } メチル) ベンズアミド、 または 4— { [8— (1一ェチルプロ ピル) 一 2, 8—ジァザスピロ [4. 5] デカー 2—ィル] メチル } -N, N—ビス ( 1 H—イミダゾール一 2—ィルメチル) ベンズアミ ドである [1] 記載の化合物;
[49] 4- [ ( {トランスー4一 [シクロへキシル (プロピル) ァミノ] シクロへキシル } ァミノ) メチル] 一 N, N—ビス (1H—イミダゾールー 2—イノレメチノレ) ベンズアミ ド、 4一 [ ( {トランス一 4— [ベンジノレ (プ 口ピル) ァミノ] シクロへキシル } ァミノ) メチル] 一 N, N—ビス (1H 一^ ミダゾ一ノレ一 2—ィルメチル) ベンズアミド、 4一 ( { [4— (1ーァ ゼパエル) シクロへキシル] ァミノ) メチル) 一 N, N—ビス (1H—イミ ダゾールー 2—ィルメチル) ベンズアミ ド、 N— (1H—べンゾイミダゾー ルー 2—ィルメチル) —4— [ ( {トランス一 4一 [シクロへキシノレ (プロ ピル) ァミノ] シクロへキシル } ァミノ) メチル] — N— (1H—イミダゾ 一ルー 2—ィルメチル) ベンズアミド、 4— [ ( {トランス一 4— [ (1一 ェチルプロピル) (プロピル) ァミノ] シクロへキシル } ァミノ) メチル] — N, N—ビス (1H—イミダゾールー 2—ィルメチル) ベンズアミド、 4
一 { [ {トランス一 4一 [シクロへキシノレ (プロピノレ) ァミノ] シクロへキ シル } (メチル) ァミノ] メチル } 一 N, N—ビス (1H—イミダゾールー 2—ィルメチル) ベンズアミ ド、 4一 { [ {トランス一 4一 [シクロへキシ ル (プロピル) ァミノ] シクロへキシル } (2—ヒ ドロキシェチル) ァミノ] メチル } 一 N, N—ビス (1H—イミダゾールー 2—^ ルメチル) ベンズァ ミ ド、 または 4一 [ ( {トランス一 4一 [ (1一ェチルプロピル) (2—ヒ ドロキシェチノレ) ァミノ] シクロへキシル } ァミノ) メチノレ] -N, N—ビ ス ( 1 H—イミダゾールー 2—ィルメチル) ベンズアミドである [1] 記載 の化合物;
[50] [1] 記載の一般式 (1— 0) で示される化合物、 その塩、 その N—ォキシド体もしくはその溶媒和物、 またはそれらのプロドラッグを含有 してなる医薬組成物;
[51] CXCR4拮抗剤である [50] 記載の医薬組成物;
[52] CXCR4介在性疾患の予防および/または治療剤、 または再生 医療用剤である [51] 記載の医薬組成物;
[53] CXCR4介在性疾患が、 ヒ ト免疫不全ウィルス感染、 後天性免 疫不全症候群、 癌、 癌転移、 関節リウマチ、 関節炎、 網膜症、 肺線維症また は移植臓器拒絶反応であるか、または再生医療用剤が移植医療用剤である [5 2] 記載の医薬組成物;
[54] CXCR 4介在性疾患が、 ヒ ト免疫不全ウィルス感染である [5 2] 記載の医薬組成物;
[55] [1] 記載の一般式 (1 -0) で示される化合物、 その塩、 その N—ォキシド体もしくはその溶媒和物、 またはそれらのプロドラッグと、 逆 転写酵素阻害薬、 プロテアーゼ阻害薬、 CCR2拮抗薬、 CCR3拮抗薬、 CCR4拮抗薬、 CCR5拮抗薬、 CXCR4拮抗薬、 H IVインテグラー ゼ阻害薬、 フュージョン阻害薬、 CD 4拮抗薬、 H I Vの表面抗原に対する
抗体、 短鎖干渉 RNA、 および H I Vのワクチンから選択される 1種または 2種以上を組み合わせてなる医薬;
[56] [1] 記載の一般式 (1—0) で示される化合物、 その塩、 その N—ォキシド体もしくはその溶媒和物、 またはそれらのプロドラッグの有効 量を哺乳動物に投与することを特徴とする哺乳動物における C X C R 4を拮 抗する方法;
[57] [1] 記載の一般式 (1—0) で示される化合物、 その塩、 その N—ォキシド体もしくはその溶媒和物またはそれらのプロドラッグの有効量 を哺乳動物に投与することを特徴とする、 哺乳動物における C X C R 4介在 性疾患の予防および/または治療方法;
[58] CXCR 4拮抗剤を製造するための [1] 記載の一般式 (1—0) で示される化合物、 その塩、 その N—ォキシド体もしくはその溶媒和物また はそれらのプロドラッグの使用;
[59] CXCR4介在性疾患の予防および/または治療剤を製造するた めの [1] 記載の一般式 (1—0) で示される化合物、 その塩、 その N—ォ キシド体もしくはその溶媒和物またはそれらのプロドラッグの使用;
[60] 一般式 (I)
(式中、 A 1および A2はそれぞれ独立して、塩基性基を含有する基を表わし; B1および B 2はそれぞれ独立して、 結合手または主鎖の原子数 1~4のスぺ 一サーを表わし; Eは、主鎖の原子数 1〜10のスぺーサーを表わし; Lは、 結合手または主鎖の原子数 1〜 2のスぺーサーを表わし; Jは、 塩基性基を 含有する基によって置換され、 さらに置換基によって置換されていてもよい 脂肪族炭化水素基、 または塩基性基を含有する基によって置換され、 さらに
置換基によって置換されていてもよい環状基を表わし;
― は一重結合または二重結合を表わし;
=^ がー重結合を表わす場合、 Dは窒素原子または置換基を有していてもよ い炭素原子を表わし、 Gは置換基を有していてもよい炭素原子、 カルボニゾレ 基、 酸素原子または酸化されていてもよい硫黄原子を表わし;
― が二重結合を表わす場合、 Dは炭素原子を表わし、 Gは置換基を有して いてもょ 、炭素原子または窒素原子を表わす。
ただし、 '
Dが窒素原子を表わす場合、 Gがカルボュル基、 酸素原子または酸化されて いてもよい硫黄原子を表わす力、、 B ^S—〇一、一 S—、一 C O—、一S O—、 一 s o 2—、 置換基を有していてもよい二価の窒素原子、 および置換基を有し ていてもよい二価の 3〜8員の単環式環状基から選択される少なくとも一つ を含有する主鎖の原子数 1〜4のスぺ一サーを表わすものとする。 ) で示される化合物、 その塩、 その N—ォキシド体もしくはその溶媒和物、 ま たはそれらのプロドラッグ;、 または
[ 6 1 ] 一般式 (1—0 ) で示される化合物、 その塩、 その N—ォキシド 体もしくはその溶媒和物、 またはそれらのプロドラッグの製造方法に関する。 本明細書中、 「環状基」 としては、 例えば炭素環または複素環等が挙げら れる。 この 「炭素環」 としては、 例えば C 3〜1 5の単環または多環式炭素 環等が挙げられる。 ここで 「C 3〜1 5の単環または多環式炭素環」 には、 C 3〜l 5の単環または多環式不飽和炭素環、 その一部または全部が飽和さ れている炭素環、 スピロ結合した多環式炭素環および架橋した多環式炭素環 が含まれる。 この 「C 3〜1 5の単環または多環式不飽和炭素環、 その一部 または全部が飽和されている炭素環」 としては、 例えば、 シクロプロパン、 シクロブタン、 シク口ペンタン、 シク口へキサン、 シクロヘプタン、 シクロ オタタン、 シクロノナン、 シク口デカン、 シク口ゥンデカン、 シク口ドデカ
ン、 シクロトリデカン、 シクロテトラデカン、 シク口ペンタデカン、 シクロ ペンテン、 シクロへキセン、 シクロヘプテン、 シクロオタテン、 シクロペン タジェン、 シクロへキサジェン、シクロへブタジエン、 シクロォクタジェン、 ベンゼン、 ペンタレン、 パーヒドロペンタレン、 ァズレン、 パーヒドロアズ レン、 ィンデン、 パーヒドロインデン、 インダン、 ナフタレン、 ジヒドロナ フタレン、 テトラヒ ドロナフタレン、 パーヒドロナフタレン、 ヘプタレン、 パーヒドロヘプタレン、 ビフエ二レン、 a sーィンダセン、 sーィンダセン、 ァセナフチレン、 ァセナフテン、 フノレオレン、 フ夂ナレン、 フエナントレン、 アントラセン、 1, 2, 3, 5, 6, 7—へキサヒドロー s—インダセン環 等が挙げられ、 「スピロ結合した多環式炭素環」 としては、 例えば、 スピロ [4. 4] ノナン、 スピロ [4. 5] デカン、 スピロ [5. 5] ゥンデカン、 スピロ [3. 4] オクタン、 スピロ [3. 5] ノナン環等が挙げられ、 「架 橋した多環式炭素環」 としては、 例えば、 ビシクロ [2. 2. 1]ヘプタン、 ビシクロ [2. 2. 1] ヘプター 2—ェン、 ビシクロ [3. 1. 1] ヘプタ ン、 ビシクロ [3. 1. 1] ヘプター 2—ェン、 ビシクロ [3. 2. 1] ォ クタン、 ビシクロ [2. 2. 2] オクタン、 ビシクロ [2. 2. 2] ォクタ 一 2—ェン、 ァダマンタン、 ノ ァダマンタン、 ビシクロ [2. 1, 1] へ キサン、 ビシクロ [3. 3. 1] ノナン、 ビシクロ [3. 2. 1] オクタン、 ビシクロ [3. 3. 2] デカン環等が挙げられる。 これらのうち、 「C 3〜 1 5の単環または多環式芳香族炭素環」 としては、 例えば、 ベンゼン、 ァズ レン、 ナフタレン、 フエナントレン、 アントラセン環等が挙げられる。
この複素環としては、 例えば 「ヘテロ原子として 1〜4個の窒素原子、 1 〜2個の酸素原子おょぴ Zまたは 1〜2個の硫黄原子を含む 3〜1 5員の単 環または多環式複素環」 等が挙げられる。 ここで 「ヘテロ原子として 1〜4 個の窒素原子、 1〜 2個の酸素原子および/または 1〜 2個の硫黄原子を含 む 3~1 5員の単環または多環式複素環」 には、 ヘテロ原子として 1〜4個
の窒素原子、 1〜 2個の酸素原子おょぴ Zまたは 1〜 2個の硫黄原子を含む 3〜1 5員の単環または多環式不飽和複素環、 その一部または全部が飽和さ れている複素環、 スピロ結合した多環式複素環および架橋した多環式複素環 が含まれる。 この 「ヘテロ原子として 1〜 4個の窒素原子、 1 ~ 2個の酸素 原子および/または 1〜 2個の硫黄原子を含む 3〜1 5員の単環または多環 式不飽和複素環、 その一部または全部が飽和されている複素環」 としては、 ί列えば、 ピロ一ノレ、 イミダゾーノレ、 トリァゾーノレ、 テトラゾーノレ、 ピラゾー ノレ、 ピリジン、 ピラジン、 ピリミジン、 ピリダジン、 ァゼピン、 ジァゼピン、 フラン、 ピラン、 才キセピン、 チォフェン、 チォピラン、 チェピン、 ォキサ ゾール、 イソォキサゾール、 チアゾール、 イソチアゾール、 フラザン、 ォキ サジァゾール、 才キサジン、 才キサジァジン、 ォキサゼピン、 ォキサジァゼ ピン、 チアジアゾーノレ、 チアジン、 チアジアジン、 チアゼピン、 チアジアゼ ピン、 ィンドーノレ、 イソインドーノレ、 インドリジン、 ベンゾフラン、 ィソべ ンゾフラン、ベンゾチォフェン、イソベンゾチォフェン、 ジチアナフタレン、 インダゾール、 キノリン、 イソキノリン、 キノリジン、 プリン、 フタラジン、 プテリジン、 ナフチリジン、 キノキサリン、 キナゾリン、 シンノリン、 ベン ゾ才キサゾ一/レ、 ベンゾチアゾーノレ、 ベンゾィミダゾ一ノレ、 クロメン、 ベン ゾォキセピン、 ベンゾォキサゼピン、 ベンゾォキサジァゼピン、 ベンゾチェ ピン、 ベンゾチアゼピン、 ベンゾチアジアゼピン、 ベンゾァゼピン、 ベンゾ ジァゼピン、ベンゾフラザン、ベンゾチアジアゾール、ベンゾトリァゾール、 カルパゾール、 —力ルポリン、 アタリジン、 フエナジン、 ジベンゾフラン、 キサンテン、 ジベンゾチォフェン、 フエノチアジン、 フエノキサジン、 フエ ノキサチイン、 チアンスレン、 フエナントリジン、 フエナント口リン、 ペリ ミジン、 アジリジン、 ァゼチジン、 ピロリン、 ピロリジン、 ィミダゾリン、 イミダゾリジン、 トリァゾリン、 トリァゾリジン、 テトラゾリン、 テトラゾ リジン、 ビラゾリン、 ビラゾリジン、 ジヒ ドロピリジン、 テトラヒドロピリ
ジン、 ピぺリジン、 ジヒドロビラジン、 テトラヒドロビラ.ジン、 ピぺラジン、 ジヒドロピリミジン、 テトラヒドロピリミジン、 パーヒドロピリミジン、 ジ ヒドロピリダジン、 テトラヒドロピリダジン、 パーヒドロピリダジン、 ジヒ ドロアゼピン、 テトラヒドロアゼピン、 パーヒドロアゼピン、 ジヒドロジァ ゼピン、 テトラヒドロジァゼピン、 パーヒドロジァゼピン、 ォキシラン、 ォ キセタン、 ジヒドロフラン、 テトラヒドロフラン、 ジヒドロピラン、 テトラ ヒドロピラン、 ジヒドロォキセピン、 テトラヒドロォキセピン、 パーヒドロ ォキセピン、 チイラン、 チェタン、 ジヒドロチォフェン、 テトラヒドロチォ フェン、 ジヒドロチォピラン、テトラヒドロチォピラン、 ジヒドロチェピン、 テトラヒドロチェピン、 パーヒドロチェピン、 ジヒドロォキサゾ一ノレ、 テト ラヒドロォキサゾール (ォキサゾリジン) 、 ジヒドロイソォキサゾーノレ、 テ トラヒドロイソォキサゾール (ィソォキサゾリジン) 、 ジヒドロチアゾール、 テトラヒドロチアゾール (チアゾリジン) 、 ジヒドロイソチアゾール、 テト ラヒドロイソチアゾール (イソチアゾリジン) 、 ジヒドロブラザン、 テトラ ヒドロブラザン、 ジヒドロォキサジァゾール、 テトラヒドロォキサジァゾ一 ノレ (ォキサジァゾリジン) 、 ジヒ ドロォキサジン、 テトラヒドロォキサジン、 ジヒドロォキサジァジン、 テトラヒドロォキサジァジン、 ジヒドロォキサゼ ピン、 テトラヒドロォキサゼピン、 パーヒドロォキサゼピン、 ジヒドロォキ サジァゼピン、 テトラヒドロォキサジァゼピン、 パーヒドロォキサジァゼピ ン、 ジヒドロチアジアゾール、 テトラヒドロチアジアゾール (チアジアゾリ ジン) 、 ジヒドロチアジ 、 テトラヒドロチアジン、 ジヒドロチアジアジン、 テトラヒドロチアジアジン、ジヒドロチアゼピン、テトラヒドロチアゼピン、 パーヒドロチアゼピン、 ジヒ ドロチアジアゼピン、 テトラヒドロチアジアゼ ピン、 パーヒドロチアジァゼピン、 モノレホリン、 チォモノレホリン、 ォキサチ アン、 インドリン、 イソインドリン、 ジヒドロべンゾフラン、 パーヒドロべ ンゾフラン、 ジヒドロイソべンゾフラン、 パーヒドロイソべンゾフラン、 ジ
ヒ ドロベンゾチォフェン、 パーヒ ドロベンゾチォフェン、 ジヒ ドロイソベン ゾチォフェン、 ノ ーヒドロイソベンゾチォフェン、 ジヒドロインダゾーノレ、 パーヒドロインダゾール、 ジヒドロキノリン、 テトラヒドロキノリン、 パー ヒドロキノリン、 ジヒドロイソキノリン、 テトラヒドロイソキノリン、 パー ヒドロイソキノリン、 ジヒドロフタラジン、 テトラヒドロフタラジン、 パー ヒドロフタラジン、 ジヒドロナフチリジン、 テトラヒドロナフチリジン、 パ ーヒドロナフチリジン、ジヒドロキノキサリン、テトラヒドロキノキサリン、 パ一ヒドロキノキサリン、 ジヒドロキナゾリン、 テトラヒドロキナゾリン、 パーヒドロキナゾリン、 ジヒドロシンノリン、 テトラヒドロシンノリン、 パ ーヒドロシンノリン、 ベンゾォキサチアン、 ジヒドロべンゾォキサジン、 ジ ヒドロべンゾチアジン、 ピラジノモノレホリン、ジヒドロベンゾォキサゾーノレ、 ノヽ。ーヒ ドロベンゾォキサゾーノレ、 ジヒドロべンゾチアゾーノレ、 パーヒ ドロべ ンゾチアゾーノレ、 ジヒドロべンゾイミダゾール、 パーヒドロべンゾイミダゾ ール、 ジヒドロベンゾァゼピン、 テトラヒドロベンゾァゼピン、 ジヒドロべ ンゾジァゼピン、 テトラヒドロべンゾジァゼピン、 ベンゾジォキセパン、 ジ ヒ ドロべンゾォキサゼピン、 テトラヒドロべンゾォキサゼピン、 ジヒドロ力 ルバゾーノレ、 テトラヒドロカルバゾール、 パーヒドロカルパゾール、 ジヒド ロアクリジン、 テトラヒドロアクリジン、 パーヒドロアクリジン、 ジヒドロ ジベンゾフラン、 ジヒドロジベンゾチォフェン、 テトラヒドロジベンゾフラ ン、 テトラヒドロジベンゾチォフェン、 ノ ーヒドロジべンゾフラン、 ノヽ。ーヒ ドロジベンゾチォフェン、 ジォキソラン、 ジォキサン、 ジチオラン、 ジチア ン、 ジ才キサインダン、 ベンゾジ才キサン、 クロマン、 ベンゾジチ才ラン、 ベンゾジチアン、 6, 7—ジヒドロー 5H—シクロペンタ [b] ピラジン、 5 H—シクロペンタ [b] ピラジン、 イミダゾ [2, 1一 b] [1, 3] チ ァゾール、 ピリ ド [2, 3-b] ピラジン、 ピリ ド [3, 4-b] ピラジン、 [1, 3] チアゾロ [4, 5-b] ピラジン、 チエノ [2, 3-b] ピラジ
ン、 3, 4—ジヒドロー 2H—ビラジノ [2, 3-b] [1, 4] ォキサジ ン、 6, 7—ジヒドロー 5 H—シクロペンタ [b] ピラジン、 イミダゾ [1, 2 - a] ピラジン、 6, 7—ジヒドロ一 5H—シクロペンタ [b] ピリジン、 フロ [3, 2-b] ピリジン、 ピリ ド [2, 3-d] ピリミジン、 2, 3- ジヒドロ一 1H—ピロ口 [2, 3-b] ピリジン、 5, 6, 7, 8—テトラ ヒドロ一 1, 6一ナフチリジン、 6, 7, 8, 9ーテトラヒドロー 5H—ピ リ ド [2, 3— d] ァゼピン、 3, 4—ジヒドロー 2H—ピラノ [3, 2— c] ピリジン、 2, 3—ジヒドロフロ [3, 2— c] ピリジン、 へキサヒド ロー 1H—ピロリジン、 ォクタヒドロシクロペンタ [c] ピロ一ノレ、 ォクタ ヒドロシクロペンタ [b] ピロ一ノレ、 ォクタヒドロピロ口 [3, 2-b] ピ ローノレ、 ォクタヒドロピロ口 [3, 4— c] ピロ一ノレ、 へキサヒドロー 2H ーフロ [3, 2-b] ピロール、 へキサヒドロー 2H—チエノ [3, 2-b] ピロ一ノレ、 デカヒドロキノリン、 デカヒドロー 2, 6—ナフチリジン、 オタ タヒドロー 2 H—キノリジン、 ォクタヒドロー 1H—ピリ ド [1, 2— c] ピリミジン、 ォクタヒドロー 2H— 1, 4一べンゾォキサジン、 デカヒドロ 一 1, 5—ナフチリジン、 ォクタヒドロ一 1H—ピロ口 [3, 4-b] ピリ ジン、 ォクタヒドロー 1H—ピロ口 [3, 4-c] ピリジン環等が挙げられ、 「スピロ結合した多環式複素環」 としては、 例えば、 ァザスピロ [4. 4] ノナン、 ォキサザスピロ [4. 4] ノナン、 ジォキサスピロ [4. 4] ノナ ン、 ァザスピロ [4. 5] デカン、 チアスピロ [4. 5] デカン、 ジチアス ピロ [4. 5] デカン、 ジォキサスピロ [4. 5] デカン、 ォキサザスピロ [4. 5] デカン、 ァザスピロ [5. 5] ゥンデカン、 ォキサスピロ [5. 5] ゥンデカン、 ジォキサスピロ [5. 5] ゥンデカン、 2, 7—ジァザス ピロ [3. 5] ノナン、 2, 8—ジァザスピロ [4. 5] デカン、 2, 7— ジァザスピロ [4. 5] デカン、 2, 9ージァザスピロ [5. 5] ゥンデ力 ン、 2, 8—ジァザスピロ [5. 5] ゥンデカン、 3, 9ージァザスピロ [5.
5] ゥンデカン、 2, 7—ジァザスピロ [4. 4] ノナン、 1, 2—ジヒド ロスピロ [インドーノレ一 3, 4,ーピペリジン] 、 2, 3—ジヒドロー 1H— スピロ [イソキノリンー4, 4'—ピぺリジン] 、 1,, 4,一ジヒドロー 2Ή— スピロ [ピペリジン一 4, 3,一キノリン] 、 2,, 3,一ジヒドロー 1Ή—スピ 口 [ピペリジン一 4, 4,一キノリン] 、 8—ァザスピロ [4. 5] デカン、 7—ァザスピロ [4. 5] デカン、 3一ァザスピロ [5. 5] ゥンデカン、 2—ァザスピロ [5. 5] ゥンデカン、 1—ォキサ一 4, 8—ジァザスピロ [5. 5] ゥンデカン、 1一ォキサ一4, 9ージァザスピロ [5. 5] ゥン デカン、 3, 4ージヒドロスピロ [クロメン一 2, 4'—ピペリジン] 、 2— ァザスピロ [4. 4] ノナン、 7—ァザスピロ [3. 5] ノナン、 2, 3— ジヒドロスピロ [インデン一 1, 4,ーピペリジン] 、 3, 4—ジヒドロ一 2 H—スピロ [ナフタレン一 1, 4,ーピペリジン] 、 3, 4ージヒドロー 1H ースピロ [ナフタレン一 2, 4,ーピペリジン] 、 2—ァザスピロ [4.5] デ カン、 2—ァザスピロ [3. 5] ノナン、 1,, 2'—ジヒ ドロスピロ [シク口 へキサン一 1, 3'—インドール] 、 2,, 3,ージヒドロー 1Ήースピロ [シク 口へキサン一 1, 4,一イソキノリン]、 1,, 4,ージヒドロー 2Ή—スピロ [シ クロへキサン一 1, 3,一キノリン] 、 6—ジァザスピロ [3. 4] オタ タン、 1, 5—ジァザスピロ [3. 4]オクタン、 1, 7—ジァザスピロ [3. 5] ノナン、 1, 6—ジァザスピロ [3. 5] ノナン、 1, 5—ジァザスピ 口 [3. 5] ノナン、 1, 7—ジァザスピロ [4. 4] ノナン、 1, 6—ジ ァザスピロ [4. 4] ノナン、 1, 8—ジァザスピロ [4. 5] デカン、 1, 7—ジァザスピロ [4. 5] デカン、 2, 6ージァザスピロ [3. 4] オタ タン、 1, 6—ジァザスピロ [4. 5] デカン、 2, 6—ジァザスピロ [3. 5] ノナン、 1, 9ージァザスピロ [5. 5] ゥンデカン、 1, 8—ジァザ スピロ [5. 5] ゥンデカン、 6—ァザスピロ [3. 5] ノナン、 6—ァザ スピロ [3. 4] オクタン、 2—ァザスピロ [3. 4] オクタン、 1, 7—
ジァザスピロ [5. 5] ゥンデカン、 1, 4, 9一トリァザスピロ [5. 5] ゥンデカン、 1, 3, 8—トリァザスピロ [4. 5] デカン、 1—チア一 4, 9ージァザスピロ [5. 5] ゥンデカン、 1一チア一 4, 8—ジァザスピロ [5. 5] ゥンデカン環等が挙げられ、 「架橋した多環式複素環 j としては、 例えば、 ァザビシクロ [2. 2. 1] ヘプタン、 ォキサビシクロ [2. 2. 1] ヘプタン、 ァザビシクロ [3. 1. 1] ヘプタン、 ァザビシクロ [3. 2. 1] オクタン、 ォキサビシクロ [3. 2. 1] オクタン、 ァザビシクロ [2. 2. 2] オクタン、 ジァザビシクロ [2. 2. 2] オクタン、 1ーァ ザトリシクロ [3. 3. 1. 13' 7] デカン、 3—ァザビシクロ [3. 3. 1] ノナン、 3, 7—ジァザビシクロ [3. 3. 1] ノナン環等が挙げられる。 これらのうち、 「ヘテロ原子として 1〜 4個の窒素原子、 1~ 2個の酸素原 子および/または 1〜 2個の硫黄原子を含む 3〜 15員の単環または多環式 芳香族複素環」 としては、 例えば、 ピロール、 イミダゾール、 トリァゾール、 テトラゾール、 ピラゾール、 ピリジン、 ピラジン、 ピリミジン、 ピリダジン、 フラン、 チォフェン、 ォキサゾール、 ィソォキサゾーノレ、 チアゾーノレ、 イソ チアゾール、 フラザン、 ォキサジァゾール、 チアジアゾ一/レ、 インドール、 イソインド^ゾレ、 ベンゾフラン、 イソべンゾフラン、 ベンゾチォフェン、 ィ ソベンゾチォフェン、 インダゾール、 キノリン、 イソキノリン、 プリン、 フ タラジン、 プテリジン、 ナフチリジン、 キノキサリン、 キナゾリン、 シンノ リン、 ベンゾ才キサゾーノレ、 ベンゾチアゾー/レ、 ベンゾイミダゾーノレ、 ベン ゾフラザン、 ベンゾチアジアゾーノレ、 ベンゾトリァゾ一/レ、 カノレバゾーノレ、 ]3—カノレポリン、 アタリジン、 フエナジン、 ジベンゾフラン、 ジベンゾチォ フェン、 フエナントリジン、 フエナント口リン、 ペリミジン環等が挙げられ る。
本明細書中、 「脂肪族炭化水素基」 としては、 例えば 「直鎖状または分枝 状の脂肪族炭化水素基」 等が挙げられる。 「直鎖状または分枝状の脂肪族炭
化水素基」 としては、 例えば 「炭素数 1〜8の脂肪族炭化水素基」 等が挙げ られ、 「炭素数 1〜 8の脂肪族炭化水素基」 としては、 例えば C 1〜 8アル キノレ基、 C 2〜8アルケ-ル基、 C 2〜 8アルキ-ル基等が挙げられる。
C 1〜8アルキル基としては、 例えば、 メチル、 ェチル、 プロピル、 イソ プロピノレ、 プチノレ、 sec—プチノレ、 tert—プチノレ、 ペンチノレ、 へキシノレ、 ヘプ チル、 オタチル基およびこれらの異性体基等が挙げられる。
C 2〜8アルケニル基としては、例えば、 ビュル、 プロぺュル、 ブテュル、 ペンテニノレ、 へキセニゾレ、 ヘプテニノレ、 ォクテエル、 プタジェェノレ、 ペンタ ジェニノレ、 へキサジェ -ル、 ヘプタジェュノレ、 ォクタジェ-ノレ、 へキサトリ ェニル、 ヘプタトリエニル、 オタタトリエエル基およびこれらの異性体基等 が挙げられる。
C 2〜 8アルキニル基としては、 例えば、 ェチ ル、 プロピエル、 プチ二 ノレ、 ペンチ二ノレ、 へキシュノレ、 へプチ二ノレ、 ォクチ二ノレ、 ブタジィニル、 ぺ ンタジィニノレ、 へキサジィ-ノレ、 ヘプタジィ二ノレ、 ォクタジイエノレ、 へキサ トリイニル、 ヘプタトリイ -ル、 オタタトリイエル基およびこれらの異性体 基等が挙げられる。
本明細書中、 A 1および A 2によって表わされる 「塩基性基を含有する基」 としては、 塩基性基を含むものであれば特に限定されない。 例えば、 (1 ) 塩基性基、 (2 ) 塩基性基によって置換され、 さらに置換基を有していても よい脂肪族炭化水素基、 (3 ) 塩基性基によって置換され、 さらに置換基を 有していてもよい環状基等が挙げられる。
「塩基性基によって置換され、 さらに置換基を有していてもよい脂肪族炭 化水素基」 における 「脂肪族炭化水素基」 は、 前記した脂肪族炭化水素基と 同じ意味を表わす。
「塩基性基によって置換され、 さらに置換基を有していてもよい環状基」 における 「環状基」 は、 前記した環状基と同じ意味を表わす。
「塩基性基によって置換され、 さらに置換基を有していてもよい脂肪族炭 化水素基」 または 「塩基性基によって置換され、 さらに置換基を有していて もよい環状基」 における 「置換基」 としては、 置換基であれば特に限定され ない。 例えば、 以下の Tとして定義される置換基等が挙げられる。
Tは、
(1)脂肪族炭化水素基、
(2) C 1〜8アルキリデン基 (例えばメチリデン、ェチリデン、プロピリデン、 ブチリデン、 ペンチリデン、 へキシリデン、 ヘプチリデン、 オタチリデン基 およびこれらの異 1"生体等) 、
(3)環状基、
(4)環状基で置換された脂肪族炭化水素基 (例えば、 シクロプロピルメチル、 シクロペンチノレメチル、 シクロへキシノレメチノレ、 フエニルスメチル、 ナフチ ノレメチノレ、 ピリジニノレメチノレ、 シク口プロピノレエチノレ、 シク口ペンチ/レエチ ノレ、 シクロへキシノレエチル、 フエニノレスェチノレ、 ナフチノレエチノレ、 ピリジニ ルェチル、 シク口プロピルプロピル、 シクロペンチルプロピル、 シク口へキ シルプロピル、 フエニルメチル、 フエニルプロピル、 ナフチルプロピル、 ピ リジ -ルプロピル等) 、
(5)水酸基、
(6)— O—旨肪族炭化水素基 (例えば、 メトキシ、 エトキシ、 プロボキシ、 ィ ソプロボキシ、 ブトキシ、 イソブトキシ、 tert—ブトキシ、 ペントキシ、 へキ シルォキシ、 ヘプチルォキシ、 ォクチルォキシ、 プロぺニルォキシ、 プテニ ゾレオキシ、 ペンテ-/レオキシ、 へキセニノレオキシ、 プロピニノレオキシ、 プチ ニルォキシ、 ペンチニルォキシ、 へキシュノレォキシ等) 、
(7)— O—環状基 (例えば、 シクロプロピルォキシ、 シクロペンチルォキシ、 シク口へキシルォキシ、フエノキシ、ナフチルォキシ、ピリジ-ルォキシ等)、
(8)— O—脂肪族炭化水素基一環状基 (例えば、 シクロペンチルメトキシ、 シ
ク口へキシルメ トキシ、 フエ-ノレメ トキシ等) 、
(9)メルカプト基、
(10)— S一脂肪族炭化水素基 (例えば、 メチルチオ、 ェチルチオ、 プロピルチ ォ、 イソプロピルチオ、 プチルチオ、 ィソブチルチオ、 tert—プチルチオ、 ぺ ンチルチオ、 へキシルチオ、へプチルチオ、 ォクチルチオ、 プロぺニルチオ、 ブテ-ノレチォ、 ペンテ-ノレチォ、 へキセニノレチォ、 プロピニノレチォ、 ブチニ ルチオ、 ペンチニノレチォ、 へキシニノレチォ等) 、
(11)—S—環状基 (例えば、 シクロプロピルチオ、 シクロペンチルチオ、 シク 口へキシルチオ、 フエ二ルチオ、 ナフチルチオ、 ピリジニルチオ等) 、 (12)— S—脂肪族炭化水素基一環状基 (例えば、 シクロペンチルメチルチオ、 シクロへキシルメチルチオ、 フエ二ルメチルチオ等) 、
(13)— S (O) 一脂肪族炭化水素基 (例えば、 メチルスルフィニル、 ェチルス ノレフィュノレ、 プロピノレスノレフィ二ノレ、 イソプロピノレスノレフィニル、 プチノレス ルフィエル、 ィソブチルスルフィニル、 tert—プチルスルフィニル、 ペンチル スルフィエル、 へキシルスルフィエル、 へプチルスルフィエル、 ォクチルス ノレフイエノレ、 プロぺニノレス/レフィニ レ、 プテ-ノレスノレフィニノレ、 ペンテ二ノレ ス /レフィュノレ、 へキセニノレスルフィ二ノレ、 プロピニノレスノレフィュル、 プチ二 ノレスノレフィニノレ、 ペンチュノレスルフィ二ノレ、 へキシュノレスノレフィニノレ等) 、
(14) - S (O) 一環状基 (例えば、 シクロプロピルスルブイニル、 シクロペン チノレススレフィ-ノレ、 シクロへキシゾレスノレフィニノレ、 フエニノレスノレフィ二/レ、 ナフチルスルフィエル、 ピリジニルスルフィエル等) 、
(15)— S (O) 一脂肪族炭化水素基一環状基 (例えば、 シクロペンチルメチル スノレフィュノレ、 シクロへキシノレメチノレスノレフィ -ノレ、 フエ- 7レメチノレスノレフ ィニル等) 、
(16)— S 02—脂肪族炭化水素基 (例えば、 メチルスルホニル、 ェチルスルホ ニル、 プロピノレスノレホニノレ、 イソプロピゾレスゾレホニ/レ、 プチ/レスゾレホニ 7レ、
イソプチ7レスノレホニノレ、 tert—ブチノレスノレホニノレ、 ペンチノレスノレホニノレ、 へキ シノレスルホュノレ、 ヘプチノレスノレホニノレ、 オタチノレスノレホニノレ、 プロぺニルス ノレホニノレ、 ブテニノレスノレホニノレ、 ペンテニノレスノレホニノレ、 へキセニノレスノレホ 二 7レ、プロピニノレスノレホニノレ、プチ二/レスノレホニノレ、ペンチニノレスノレホニノレ、 へキシュルスルホニル等) 、
(17)— S O 2—環状基 (例えば、 シクロプロピルスルホニル、 シクロペンチル スノレホニノレ、 シク口へキシノレスノレホニノレ、 フエニノレスノレホェノレ、 ナフチノレス ノレホニノレ、 ピリジニノレス/レホニル等) 、
(18)— S 02—脂肪族炭化水素基一環状基 (例えば、 シクロペンチルメチルス ノレホニノレ、シク口へキシルメチルスルホュル、フエニルメチルスルホュル等)、
(19)一 O— C O—脂肪族炭化水素基 (例えば、 メタノィルォキシ、 エタノィル 才キシ、 プロパノィルォキシ、ィソプロパノィルォキシ、 ブタノィルォキシ、 ィソブタノイノレオキシ、 tert-プタノィノレォキシ、 ペンタノィルォキシ、 へキ サノィルォキシ、 ヘプタノィルォキシ、 オタタノィルォキシ、 プロぺノィル 才キシ、 ブテノィルォキシ、 ペンテノィルォキシ、 へキセノィルォキシ、 プ 口ピノィルォキシ、 ブチノィルォキシ、 ペンチノィ /レオキシ、 へキシノィノレ ォキシ等) 、
(20)—〇一C O—環状基 (例えば、 シクロプロピル力ルポ-ルォキシ、 シクロ ペンチノレカノレポニノレオキシ、 シクロへキシノレカスレボニノレオキシ、 フエ二ノレ力 ノレボ-/レオキシ、 ナフチ /レカルポニノレオキシ、 ピリジニノレ力/レポエノレオキシ 等) 、
(21)—〇一 C O—脂肪族炭化水素基一環状基(例えば、 シクロペンチルメタノ ィズレオキシ、 シク口へキシルメタノィルォキシ、 フエニルメタノィル才キシ 等) 、
(22)— C O—脂肪族炭化水素基 (例えば、 メタノィル、 エタノィル、 プロパノ ィル、 ィソプロパノィル、 プ'タノイノレ、 ィソプタノィル、 tert—プタノィル、
ペンタノイスレ、へキサノィノレ、 ヘプタノィノレ、 ォクタノィノレ、 プロぺノィノレ、 ブテノィノレ、 ペンテノィル、 へキセノィノレ、 プロピノィル、 ブチノィル、 ベ ンチノィル、 へキシノィル等) 、
(23)— C O—環状基(例えば、 シクロプロピル力ルポニル、 シクロペンチルカ ルポ-ノレ、 シクロへキシノレカノレポ二ノレ、 フエ-ノレカノレポ二 7レ、 ナフチノレカノレ ポニル、 ピリジニルカルボ-ル等) 、
(24)— C O一脂肪族炭化水素基一環状基(例えば、シク口ペンチルメタノィル、 シクロへキシルメタノィル、 フエニルメタノィル等) 、
(25)ォキソ基、
(26)チォキソ基、
(27)スルフィノ基、
(28)スルホ基、
(29)アミノ基、
(30)モノーまたはジー置換アミノ基(ここでの 「モノーまたはジー置換アミノ 基」 における 「置換基」 としては、例えば、(1)脂肪族炭化水素基、(2)環状基、
(3)環状基によって置換された脂肪族炭化水素基等が挙げられる。 例えば、 メ チルァミノ、 ェチルァミノ、 プロピルァミノ、 イソプロピルァミノ、 プチル ァミノ、 イソプチノレァミノ、 tert—プチノレアミノ、 ペンチノレアミノ、 へキシル ァミノ、 ヘプチルァミノ、 ォクチルァミノ、 ジメチルァミノ、 ジェチルアミ ノ、 ジプロピルァミノ、 ジプチルァミノ、 ジペンチルァミノ、 ジへキシルァ ミノ、 ジヘプチルァミノ、 ジォクチルァミノ、 N—メチルー N—ェチルアミ ノ、 シクロプロピルァミノ、 シク口ペンチルァミノ、 シク口へキシルァミノ、 フエュズレアミノ、 ジフエニノレアミノ、 ジペンジノレアミノ、 N—フエ二ルー N ーメチノレアミノ、 N—フエ二ノレ一 N—ェチノレアミノ、 N—ベンジノレ一 N—メ チノレアミノ、 N—べンジノレ一 N—ェチ 7レアミノ、 N—シクロへキシノレ一 N— プロピルアミノ等) 、
(31)スルファモイル基、
(32)モノ一またはジ一置換スルファモイル基(ここでの 「モノーまたはジ一置 痪スルファモイル基」 における 「置換基」 としては、 例えば、 (1)脂肪族炭化 水素基、 (2)環状基、 (3)環状基によって置換された脂肪族炭化水素基等が挙げ られる。 例えば N—メチルスルファモイル、 N—ェチノレス /レファモイノレ、 N 一プロピルスルファモイル、 N—ィソプロピ/レスノレファモイノレ、 N—プチノレ スルファモイル、 N—イソプチルスルファモイル、 N— (tert—ブチル) スル ファモイノレ、 N—ペンチノレスノレファモイノレ、 N—'へキシルスノレファモイノレ、 N—へプチルスルファモイル、 N—ォクチルスルファモイル、 N , N—ジメ チルスルファモイル、 N, N—ジェチルスルファモイル、 N, N—ジプロピ ルスルファモイル、 N, N—ジプチルスルファモイル、 N, N—ジペンチル スノレファモイズレ、 N, N—ジへキシノレス /レファモイノレ、 N—メチノレー N—ェ チルスノレファモイル、 N—シク口プロピノレス/レファモイノレ、 N—シク口ペン チノレスノレファモイノレ、 N—シク口へキシノレスルファモイル、 N—フエニルス ノレファモイノレ、 N, N—ジフエニノレスノレファモイノレ、 N, N—ジべンジノレス ノレファモイノレ、 N—フエニノレー N—メチノレスゾレファモイノレ、 N—フエ-ノレ一 N—ェチルスルファモイル、 N—ベンジル一 N—メチルスルファモイル、 N 一べンジノレ一 N—ェチノレスノレファモイノレ、 N—シク口へキシスレー N—プロピ ノレアミノ等) 、
(33)カルポキシ基、
(34)— C O O—脂肪族炭化水素基 (例えば、 メ トキシカルボ二/レ、 エトキシカ ノレポュノレ、 プロポキシ力/レポュ /レ、 イソプロポキシカノレポ二/レ、 プトキシカ ルポュル、 イソプトキシカルボ二ノレ、 tert—ブトキシカルポニル、 ペントキシ カルボニル、 へキシルォキシ力ルポニル、 ヘプチルォキシカルボニル、 オタ チルォキシカルボニル、 プロぺニルォキシ力ルポニル、 ブテニノレオキシカノレ ボニノレ、 ペンテニノレオキシカノレポ二ノレ、 へキセニルォキシカノレボニノレ、 プロ
ピ二/レオキシカノレポ二ノレ、 プチ二ノレ才キシカノレボニノレ、 ペンチエノレオキシカ ルポニル、 へキシュノレォキシカルボュル等) 、
(35)—C O O—環状基 (例えば、 シクロプロピルォキシカルボニル、 シクロぺ ンチルォキシカルボニル、 シクロへキシルォキシカルボ-ル、 フエノキシ力 /レポ二/レ、 ナフチルォキシ力/レポ二/レ、 ピリジュノレォキシカノレポ-ノレ等) 、
(36)— C O O—脂肪族炭化水素基一環状基(例えば、 シクロペンチルメ トキシ カノレポ二ノレ、 シクロへキシノレメ トキシカノレポュノレ、 フエニノレメ トキシ力/レポ ニル等) 、
(37)力ルバモイル基、
(38)モノーまたはジー置換力ルバモイル基 (ここでの 「モノーまたはジー置換 カノレバモイ/レ基」 における 「置換基」 としては、 例えば、 (1)脂肪族炭化水素 基、 (2)環状基、 (3)環状基によって置換された脂肪族炭化水素基等が挙げられ る。 例えば、 N—メチルカルバモイル、 N—ェチルカルバモイル、 N—プロ ピノレカノレバモイル、 N—イソプロピノレカノレバモイノレ、 N—ブチルカノレバモイ ル、 N—イソブチルカルバモイル、 N— (tert—プチル) 力ルバモイノレ、 N— ペンチノレカノレノ モイノレ、 N—へキシノレカノレバモイノレ、 N—へプチノレカノレバモ ィル、 N—ォクチルカルバモイル、 N—シクロプロピル力ルバモイル、 N— シクロペンチノレカノレバモイノレ、 N—シクロへキシノレ力 ^ /レバモイノレ、 N—フエ 二ルカルバモイル、 N, N—ジメチルカルバモイル、 N, N—ジェチルカル パモイル、 N, N—ジプロピル力ルバモイル、 N, N—ジプチルカルバモイ ル、 N, N—ジペンチルカルバモイル、 N, N—ジへキシルカルバモイル、 N—メチルー N—ェチルカルバモイル、 N, N—ジフエ二ルカルバモイル、 N, N—ジベンジルカノレパモイル、 N—フエニノレー N—メチルカルパモイル、 N—フエ -ノレー N—ェチルカルバモイル、 N—ベンジル一 N—メチルカルバ モイル、 N—べンジルー N—ェチルカルバモイル等) 、
(39)— NH— C O—脂肪族炭化水素基 (例えば、 メタノィルァミノ、 エタノィ
ルァミノ、 プロパノィルァミノ、 イソプロパノィルァミノ、.プタノィルアミ ノ、 イソプタノイノレアミノ、 tert—ブタノイノレアミノ、 ペンタノィルァミノ、 へキサノィルァミノ、 ヘプタノイノレアミノ、 ォクタノィルァミノ、 プロぺノ イノレアミノ、 ブテノイノレアミノ、ペンテノイノレアミノ、 へキセノイノレアミノ、 プロピノィルァミノ、 ブチノィルァミノ、 ペンチノィルァミノ、 へキシノィ ルァミノ等) 、
(40)— NH— C O—環状基 (例えば、 シクロプロピルカルボニルァミノ、 シク 口ペンチルカノレポニノレアミノ、 シクロへキシルカルポニルァミノ、 フエニル カルボエルァミノ、 ナフチルカルポニルァミノ、 ピリジニルカルポニルァミ ノ等) 、
(41)— NH— C O—脂肪族炭化水素基一環状基 (例えば、 シクロペンチルメタ ノィルァミノ、 シク口へキシルメタノィルァミノ、 フエニルメタノィルアミ ノ等) 、
(42)— NH— S 02—脂肪族炭化水素基 (例えば、 メチルスルホニルァミノ、 ェチルスルホニルァミノ、 プロピルスルホュルァミノ、 ィソプロピルスルホ ニルァミノ、 ブチルスルホエルァミノ、 イソプチルス/レホニ/レアミノ、 tert 一プチルスルホニルァミノ、 ペンチルスルホュノレアミノ、 へキシルスルホニ /レアミノ、 へプチルスルホエルァミノ、 ォクチルスルホニルァミノ、 プロぺ ニルスノレホエノレアミノ、 プテ ルスルホニルァミノ、 ペンテュルスルホニル ァミノ、 へキセニルスルホュルァミノ、 プロピニルスルホエルァミノ、 プチ ニルスルホエノレアミノ、 ペンチニルスルホエルァミノ、 へキシュルスルホ- ル等) 、
(43)— NH— S O 2—環状基 (例えば、 シクロプロピルスルホニルァミノ、 シ ク口ペンチルスルホニルァミノ、 シク口へキシルスルホニルァミノ、 フエェ ルスルホニノレアミノ、ナフチルスルホエルァミノ、 ピリジニルスルホ-ル等)、
(44)— NH— S 02—脂肪族炭化水素基一環状基 (例えば、 シクロペンチルメ
チグレス/レホニ /レアミノ、 シク口へキシノレメチノレスノレホニノレアミノ、 フエ二ノレ メチノレスノレホェノレ等) 、
(45)シァノ基、
(46)ヒドラジノ基、
(47)ニトロ基、
(48)ュト口ソ基、
(49)ィミノ基、
(50)モノ一置換イミノ基 (ここでのモノー置換イミノ基における 「置換基」 と しては、 例えば、 (1)脂肪族炭化水素基、 (2)環状基、 (3)環状基によって置換さ れた脂肪族炭化水素基、 (4)水酸基、 (5)— O—脂肪族炭化水素基、 (6)— O—環 状基、 (7)— O—脂肪族炭化水素基—環状基等が挙げられる。 例えば、 メチル ィミノ、 ェチルイミノ、 プロピルイミノ、 イソプロピルイミノ、 プチルイミ ノ、 ィソプチノレイミノ、 (tert—ブチル) ィミノ、 ペンチ ィミノ、 へキシル ィミノ、 へプチルイミノ、 ォクチルイミノ、 シクロプロピルイミノ、 シクロ ペンチルイミノ、 シク口へキシルイミノ、 フエ二ルイミノ、ベンジルイミノ、 ヒ ドロキシィミノ、 エトキシィミノ、 プロボキシィミノ、 イソプポキシイミ ノ、 ブトキシィミノ、 シクロペントキシィミノ、 シクロへキシルォキシィミ ノ、 フエノキシィミノ、 ベンジノレオキシィミノ等) 、
(51)ハロゲン原子(例えば、フッ素原子、塩素原子、臭素原子、 ョゥ素原子)、 (52) 1〜 3個のハロゲン原子によって置換したメチル基(例えば、 フルォロメ チノレ、 ジフルォロメチル、. トリフルォロメチル、 トリクロロメチ/レ等) 、 (53) 1 ~ 3個のハロゲン原子によって置換したメトキシ基(例えば、 フルォロ メ トキシ、 ジフノレオ口メ トキシ、 トリフノレオ口メ トキシ、 トリクロロメ トキ シ等) 等が挙げられる。 これら任意の置換基は置換可能な任意の位置に、 置 換可能な任意の数だけ置換していてもよい。 好ましくは、 1〜8個、 より好 ましくは 1〜5個置換していてもよい。 Τ中の 「脂肪族炭化水素基」 および
「環状基」 は、 それぞれ前記と同じ意味を表わす。
「塩基性基を含有する基」 における 「塩基性基」 としては、 塩基性窒素原 子を含むものであれば特に限定されない。 例えば、 (a ) アミノ基、 (b ) アミジノ基、 (c ) グァ -ジノ基、 (d ) ヒドラジノ基、 (e ) モノーまた はジー置換アミノ基、 (f )モノー、ジ一またはトリー置換アミジノ基、 (g ) モノー、 ジ一、 トリーまたはテトラー置換グァニジノ基、 (h ) モノー、 ジ 一またはトリー置換ヒドラジノ基、 (i ) 置換基を有していてもよい含窒素 複素環基等が挙げられる。 ここでの 「モノ一まだはジ一置換アミノ基」 にお ける 「置換基」 としては、 例えば、 (1)脂肪族炭化水素基 (前記と同じ意味を 表わす) 、 (2)環状基 (前記と同じ意味を表わす) 、 (3)環状基によって置換さ れた脂肪族炭化水素基 (脂肪族炭化水素および環状基は前記と同じ意味を表 わす) 、 (4)置換基で置換された環状基 (置換基は前記した Tと前記と同じ意 味を表わし、 環状基は前記と同じ意味を表わす) 、 (5)置換基で置換された脂 肪族炭化水素基 (置換基は前記した Tと同じ意味を表わし、 脂肪族炭化水素 は前記と同じ意味を表わす) (6)置換基で置換された環状基によって置換され た脂肪族炭化水素基 (置換基は前記した Tと同じ意味を表わし、 脂肪族炭化 水素および環状基は前記と同じ意味を表わす) 、 (7)前記した置換基の T等が 挙げられ、 これら任意の置換基は置換可能な任意の位置に、 置換可能な任意 の数だけ置換していてもよい。 好ましくは、 1〜8個、 より好ましくは 1〜 5個置換していてもよい。 例えば、 メチルァミノ、 ェチルァミノ、 プロピル ァミノ、 イソプロピルァミノ、 ブチルァミノ、 イソブチルアミノ、 tert—プチ ルァミノ、 ペンチノレアミノ、 へキシ /レアミノ、 ヘプチルァミノ、 ォクチルァ ミノ、 ジメチルァミノ、 ジェチノレアミノ、 ジプロピルァミノ、 ジブチルァミ ノ、 ジペンチルァミノ、 ジへキシルァミノ、 ジヘプチルァミノ、 ジォクチル ァミノ、 N—メチルー N—ェチルァミノ、 シクロプロピルァミノ、 シクロべ ンチノレァミノ、 シクロへキシ ァミノ、 フエニノレアミノ、ジフエニノレアミノ、
ジべンジ /レアミノ、 N—フエュメレー N—メチノレアミノ、 N—フエエノレー N— ェチノレアミノ、 N—ベンジスレー N—メチノレアミノ、 N—ペンジノレー N—ェチ ノレアミノ、 N—ペンジノレー N—シクロへキシノレアミノ、 N—シクロへキシノレ 一 N—プロピルァミノ、 N—シクロへキシノレ一 N— ( 3—ヒドロキシプロピ ル) ァミノ、 N— (4—ヒドロキシシクロへキシル) 一 N—プロピルァミノ、 N— (4ーヒドロキシシクロへキシル) 一 N— ( 3—ヒドロキシプロピノレ) ァミノ、 N— ( 4—ヒドロキシシクロへキシ /レ) メチルー N—プロピノレアミ ノ、 N—シクロへキシゾレー N—ァセチノレアミノ、 N— ( 3—メ トキシプロピ ル) 一 N—プロピルァミノ、 N— ( 2—カルボシキエチル) 一 N—プロピル ァミノ、 N— ( 2—ェチルプロピル) 一 N—プロピルァミノ、 N—シクロへ キシル一 N— (メチルスルホニル) ァミノ、 N— (テトラヒドロピラン一 4 一ィル) 一N—プロピルアミノ、 N— (インダン一 2—ィル) 一 N—プロピ ルァミノ等が挙げられる。
「モノー、 ジーまたはトリ一置換アミジノ基」 における 「置換基」 として は例えば、 (1)脂肪族炭化水素基 (前記と同じ意味を表わす) 、 (2)環状基 (前 記と同じ意味を表わす)、(3)環状基によって置換された脂肪族炭化水素基(脂 肪族炭化水素および環状基は前記と同じ意味を表わす)等が挙げられる。 「モ ノー、 ジーまたはトリー置換アミジノ基」 としては、 例えば、 メチルアミジ ノ、 ェチノレアミジノ、 プロピルアミジノ、 イソプロピルアミジノ、 ブチルァ ミジノ、 ィソプチルァミジノ、 tert—ブチノレアミジノ、 ペンチルァミジノ、 へ キシルアミジノ、 ヘプチルアミジノ、 ォクチルアミジノ、 N, N—ジメチル アミジノ、 N, N,一ジメチ 7レアミジノ、 N, N, N,一トリメチルアミジノ、 N, N—ジェチルアミジノ、 N, N,ージェチルアミジノ、 N, N, N,一トリ ェチルアミジノ、 N, N—ジプロピルアミジノ、 N, N,ージプロピルアミジ ノ、 N, N, N,一トリプロピルアミジノ、 N, N—ジプチルアミジノ、 N, N'—ジプチルアミジノ、 N, N , N,一トリブチルアミジノ、 N, N—ジペン
チルアミジノ、 N, N,ージペンチノレアミジノ、 N, N, N,一トリペンチルァ ミジノ、 N, N—ジへキシノレアミジノ、 N, N,一ジへキシルアミジノ、 N, N, N,一トリへキシルアミジノ、 N, N—ジヘプチルアミジノ、 N, N'—ジ ヘプチルアミジノ、 N , N , N,一トリへプチルアミジノ、 N, N—ジォクチ ルアミジノ、 N, N,一ジォクチルアミジノ、 N, N, N,一トリオクチルアミ ジノ、 N—メチルー N—ェチルアミジノ、 N—メチルー Ν'—ェチルアミジノ、 シクロプロピルァミジノ、 シク口ペンチルァミジノ、 シク口へキシルァミジ ノ、 フエエノレアミジノ、 Ν, Ν—ジフエ二ノレアミジノ、 Ν , Ν,ージフエ二ノレ アミジノ、 Ν , Ν , Ν,一トリフエエルアミジノ、 Ν, Ν—ジベンジルアミジ ノ、 Ν , Ν,ージベンジルアミジノ、 Ν, Ν, Ν,一トリベンジルアミジノ、 Ν 一フエュルー Ν'—メチルアミジノ、 Ν—フエ二ルー Ν,一ェチルアミジノ、 Ν 一ベンジル一 Ν—メチルァミジノ、 Ν—べンジルー Ν—ェチルァミジノ等が 挙げられる。
「モノ一、 ジー、 トリーまたはテトラー置換グァニジノ基」 における 「置 換基」 としては例えば、 (1)脂肪族炭化水素基 (前記と同じ意味を表わす) 、 (2)環状基 (前記と同じ意味を表わす) 、 (3)環状基によって置換された脂肪族 炭化水素基 (脂肪族炭化水素および環状基は前記と同じ意味を表わす) 等が 挙げられる。 「モノー、 ジ一、 トリーまたはテトラ一置換グァェジノ基」 と しては、 例えば、 メチルダァ-ジノ、 ェチルダァニジノ、 プロピルグァニジ ノ、イソプロピルグァニジノ、プチルグァニジノ、ィソブチルダァ -ジノ、 tert 一プチルグァ二ジノ、 ペンチルグァ二ジノ、 へキシルグァ-ジノ、 ヘプチル グァニジノ、 ォクチルグァュジノ、 N, N—ジメチルダァェジノ、 N, Ν'- ジメチノレグァ-ジノ、 Ν, Ν, Ν,一トリメチノレグァニジノ、 Ν, Ν, Ν,, Ν" —テトラメチノレグァ二ジノ、 Ν, Ν—ジェチルダァニジノ、 Ν, Ν,一ジェチ ルグァ二ジノ、 N, N, N'—トリエチルダァ-ジノ、 Ν, Ν , Ν', Ν"—テト ラエチルダァニジノ、 Ν, Ν—ジプロピルグァニジノ、 Ν, Ν,ージプロピル
グァニジノ、 N, N, N,一トリプロピノレグァ-ジノ、 N, . N, N', N"—テト ラプロピ グァニジノ、 Ν, Ν—ジプチノレグァュジノ、 Ν, Ν,ージプチ グ ァニジノ、 Ν, Ν, Ν,ートリブチルダァニジノ、 Ν, Ν , Ν', Ν"—テトラプ チルダァェジノ、 Ν, Ν—ジペンチルグァ-ジノ、 Ν, Ν,ージペンチルグァ 二ジノ、 Ν, Ν, Ν,一トリペンチルグァ二ジノ、 Ν, Ν, Ν,, Ν"—テトラべ ンチルダァュジノ、 Ν, Ν—ジへキシ^/グァュジノ、 Ν, Ν,ージへキシ グ ァニジノ、 Ν, Ν, Ν,一トリへキシノレグァェジノ、 Ν, Ν, Ν,, Ν"—テトラ へキシルグァ-ジノ、 Ν, Ν—ジヘプチルダァ-'ジノ、 N, N'—ジヘプチル グァニジノ、 Ν, Ν, Ν,一トリへプチルグァ二ジノ、 Ν, Ν, Ν', Ν"—テト ラヘプチルダァニジノ、 Ν , Ν—ジォクチルグァ二ジノ、 Ν, Ν,一ジォクチ ルグァュジノ、 Ν, Ν, Ν,一トリオクチルグァ-ジノ、 Ν, Ν, Ν,, Ν,,一テ トラオクチ^/グァニジノ、 Ν—メチ^^レー Ν—ェチ グァニジノ、 Ν—メチル 一 Ν,ーェチルダァニジノ、 シクロプロピルグァニジノ、 シク口ペンチルグァ 二ジノ、 シクロへキシルグァニジノ、 フエ二 グァニジノ、 Ν, Ν—ジフエ ニルダァ-ジノ、 Ν , N'—ジフエ -ルグァ二ジノ、 Ν, Ν, Ν,一トリフエ二 ルグァュジノ、 Ν, Ν, Ν', Ν"—テトラフエ二ノレグァ-ジノ、 Ν, Ν—ジべ ンジルグァ-ジノ、 Ν, Ν,ージベンジルグァェジノ、 Ν, Ν, Ν,一トリベン ジルグァ-ジノ、 Ν, Ν, Ν', Ν,,一テトラべンジルグァュジノ、 Ν—フエ二 ノレ一 Ν,一メチノレグァェジノ、 Ν—フエ二ルー N'—ェチノレグァニジノ、 Ν—ベ ンジル一Ν—メチルダァェジノ、 Ν—ベンジル一 Ν—ェチルダァュジノ等が 挙げられる。
「モノー、 ジーまたはトリ一置換ヒドラジノ基」 における 「置換基」 とし ては例えば、(1)脂肪族炭化水素基(前記と同じ意味を表わす)、(2)環状基(前 記と同じ意味を表わす)、(3)環状基によって置換された脂肪族炭化水素基(月旨 肪族炭化水素および環状基は前記と同じ意味を表わす)等が挙げられる。 「モ ノー、 ジ一またはトリ一置換ヒドラジノ基」 としては、 例えば、 メチルヒド
ラジノ、ェチルヒドラジノ、 プロピルヒドラジノ、イソプロピノレヒドラジノ、 プチルヒドラジノ、 イソプチルヒドラジノ、 tert—プチルヒドラジノ、 ペンチ ルヒドラジノ、 へキシルヒドラジノ、 ヘプチルヒドラジノ、 ォクチルヒドラ ジノ、 N, N—ジメチルヒドラジノ、 N, N,一ジメチルヒドラジノ、 N, N, N,一トリメチルヒドラジノ、 N, N—ジェチルヒドラジノ、 Ν, Ν'—ジェチ ルヒドラジノ、 Ν, Ν, Ν,一トリェチルヒドラジノ、 Ν, Ν—ジプロピルヒ ドラジノ、 Ν, Ν,ージプロピノレヒドラジノ、 Ν, Ν, Ν,一トリプロピノレヒド ラジノ、 Ν, Ν—ジブチノレヒドラジノ、 Ν, Ν,一ジブチルヒドラジノ、 Ν , Ν, Ν,一トリブチルヒドラジノ、 Ν, Ν—ジペンチルヒドラジノ、 N, N'— ジペンチルヒドラジノ、 Ν, Ν , Ν,一トリペンチルヒドラジノ、 Ν, Ν—ジ へキシルヒドラジノ、 Ν, Ν,ージへキシルヒドラジノ、 Ν, Ν, Ν'—トリへ キシルヒドラジノ、 Ν, Ν—ジヘプチルヒドラジノ、 Ν, Ν,ージヘプチルヒ ドラジノ、 Ν, Ν, Ν,一トリへプチノレヒドラジノ、 Ν, Ν—ジォクチルヒド ラジノ、 Ν, Ν,一ジォクチルヒドラジノ、 Ν, Ν, Ν,一トリオクチルヒドラ ジノ、 Ν—メチルー Ν—ェチルヒドラジノ、 Ν—メチルー Ν,一ェチルヒドラ ジノ、 シクロプロピルヒドラジノ、 シクロペンチルヒ ドラジノ、 シクロへキ シノレヒドラジノ、 フエ-/レヒドラジノ、 Ν, Ν—ジフエェレヒドラジノ、 Ν, Ν,ージフエュルヒドラジノ、 Ν, Ν, Ν,一トリフエ-ルヒドラジノ、 Ν, Ν ージベンジルヒドラジノ、 Ν, Ν,ージベンジルヒドラジノ、 Ν, Ν , N'—ト リベンジルヒドラジノ、 Ν—フエ二ルー Ν,一メチルヒドラジノ、 Ν—フエ二 ルー Ν,ーェチルヒドラジノ、 Ν—ベンジル一 Ν—メチルヒドラジノ、 Ν—べ ンジルー Ν—ェチルヒドラジノ等が挙げられる。
「置換基を有していてもよい含窒素複素環」 における 「含窒素複素環」 と しては、 例えば、 ピロール、 イミダゾール、 トリァゾール、 ピラゾール、 ピ リジン、 ピラジン、 ピリミジン、 ピリダジン、 ァゼピン、 ジァゼピン、 ォキ サゾーノレ、 チアゾーノレ、 イソォキサゾーノレ、 イソチアゾーノレ、 インドー/レ、
イソインドール、 キノリン、 イソキノリン、 ベンゾォキサゾーノレ、 ベンゾチ ァゾー Λ^、 ベンゾイミダゾー^;レ、 アジリジン、 ァゼチジン、 ピロリジン、 ピ ペリジン、 ピぺラジン、 モノレホリン、 チォモノレホリン、 パーヒドロアゼピン、 パーヒドロジァゼピン、 インドリン、 イソインドリン、 キナゾリン、 テトラ ヒドロキノリン、 パーヒドロキノリン、 テトラヒドロイソキノリン、 パーヒ ドロイソキノリン、 テトラヒドロナフチリジン、 キノキサリン、 テトラヒド 口キノキサリン、 ジヒドロべンゾィミダゾーノレ、 パーヒドロべンゾィミダゾ ール、 カルバゾール、 テトラヒドロカルパゾール、 ァザビシク口 [ 3. 2. 1] オクタン、 キヌタリジン、 2, 8—ジァザスピロ [4. 5] デカン、 1, 4, 9一トリァザスピロ [5. 5] ゥンデカン、 3, 9—ジァザスピロ [5. 5] ゥンデカン、 2, 9ージァザスピロ [5. 5] ゥンデカン、 1, 6—ジ ァザスピロ [3. 4] オクタン、 1, 5—ジァザスピロ [3. 4] オクタン、 1, 7—ジァザスピロ [3. 5] ノナン、 1, 6—ジァザスピロ [3. 5] ノナン、 1, 5—ジァザスピロ [3. 5] ノナン、 1, 7—ジァザスピロ [4. 4] ノナン、 1, 6—ジァザスピロ [4. 4] ノナン、 1, 8—ジァザスピ 口 [4. 5] デカン、 1, 7—ジァザスピロ [4. 5] デカン、 2, 6—ジ ァザスピロ [3. 4] オクタン、 1, 6—ジァザスピロ [4. 5] デカン、 2, 6—ジァザスピロ [3. 5] ノナン、 1, 9ージァザスピロ [5. 5] ゥンデカン、 1, 8—ジァザスピロ [5. 5] ゥンデカン、 6—ァザスピロ [3. 5] ノナン、 6—ァザスピロ [3. 4]オクタン、 2—ァザスピロ [3. 4] オクタン、 1, 7—ジァザスピロ [5. 5] ゥンデカン、 1, 4, 9― トリァザスピロ [5. 5] ゥンデカン、 1, 3, 8—トリァザスピロ [4. 5] デカン、 1一チア一 4, 9ージァザスピロ [5. 5] ゥンデカン、 1一 チア一 4, 8—ジァザスピロ [5. 5] ゥンデカン環等が挙げられる。
「置換基を有していてもよい含窒素複素環」 における 「置換基」 としては、 前記した Τと同じ意味を表わし、 これら任意の置換基は置換可能な任意の位
置に、置換可能な任意の数だけ置換していてもよい。好ましくは、 1〜8個、 より好ましくは 1〜 5個置換していてもよい。
本明細書中、 環 A 1 Aおよび環 A2 Aによって表わされる 「置換基を有してい てもよい含窒素複素環基」 は A 1および A2中における 「置換基を有していて もよい含窒素複素環」 と同じ意味を表わす。
本明細書中、 環 A 1 Bおよび環 A 2 Bによって表わされる 「置換基を有してい てもよいイミダゾールまたはべンゾィミダゾール」 の 「置換基」 としては、 例えば、 A 1および A2中における Tとして例示したもの等が挙げられ、 これ らの任意の置換基は置換可能な位置に 1〜 5個、 好ましくは 1〜 2個置換し ていてもよい。
本明細書中、 B 1および B 2によって表わされる 「主鎖の原子数 1〜4のス ぺーサ一」 、 および Lによって表わされる 「主鎖の原子数 1〜4のスぺーサ 一」 とは、 主鎖の原子が 1〜 4個連なっている間隔を意味する。 ここで、 「主 鎖の原子数」 は、 主鎖の原子が最小となるように数えるものとする。 例えば 1, 2—シクロペンチレンの原子数を 2偭、 1, 3—シクロペンチレンの原 子数を 3個として数える。 「主鎖の原子数 1 ~ 4のスぺーサ一」 としては、 例えば一 O—、 一 S—、 一C O—、 一 S O—、 一 s o 2—、 置換基を有してい てもよい二価の窒素原子、 置換基を有していてもよい二価の炭素数 1〜 4の 月旨肪族炭化水素基、 置換基を有していてもよい二価の 3〜 8員の単環式環状 基から任意に選択される 1〜4個からなる、 主鎖の原子が 1〜 4個連なって いる二価基等が挙げられる。
「置換基を有していてもよい二価の窒素原子」 としては、 一 NH—の他、 「一 NH―」 基中の水素原子が任意に、 (1)脂肪族炭化水素、 (2)環状基、 (3) 環状基によって置換された脂肪族炭化水素基、 (4)水酸基、 (5)— O—脂肪族炭 化水素基、 (6)— O—環状基、 (7)— O—脂肪族炭化水素基一環状基、 (8)— S O 2一脂肪族炭化水素基、(9)一 S O 2一環状基、(10)— S O 2—脂肪族炭化水素基
一環状基、 (11)一 CO—脂肪族炭化水素、 (12)— CO—環状基、 (13)— CO— 月旨肪族炭化水素基一環状基、 (14)カルポキシ基、 (15)— CO O—脂肪族炭化水 素、 (16)— CO O—環状基、 (17)— COO—脂肪族炭化水素基一環状基等に置 換したものを表わす。 ここでの (1)〜(17)の置換基は、 前記と同じ意味を表わ す。
「置換基を有していてもよい二価の炭素数 1〜4の脂肪族炭化水素基 j に おける Γ二価の炭素数 1〜4の脂肪族炭化水素基」 としては、 例えば Cl〜 4アルキレン基(例えば一 CH2—、 一 (CH2) 2—、 一 (CH2) 3—、 一 (C H2) 4一等) 、 〇2〜4ァルケ-レン基 (例えば一 CH-CH—、 一 CH2— CH=CH—、 一 CH-CH— CH2—、 一 (CH2) 2— CH=CH—、 一 C H=CH— (CH2) 2—、 — CH2— CH = CH— CH2—等) 、 じ2〜4ァ ルキエレン基 (例えば一 C三 C―、 一 CH2— C≡C—、 一 C≡C— CH2—、 一 (CH2) 2— Cミ C一、 一 C≡C一 (CH2) 2一、 —CH2一 C≡C一 CH2一 等) 等が挙げられる。 また、 「置換基を有していてもよい二価の炭素数 1〜 4の脂肪族炭化水素基」 における 「置換基」 としては、 例えば、 A1および A 2中における Tとして例示したもの等が挙げられ、 これらの任意の置換基は置 換可能な位置に 1〜 5個、 好ましくは 1〜2個置換していてもよい。
「置換基を有していてもよい二価の 3~ 8員の単環式環状基」における 「二 価の 3〜 8員の単環式環状基」 としては、 例えば 「 C 3〜 8の単環式環状基」 力 ら任意の 2個の水素原子を除いてできる二価基等が挙げられる。 ここでの 「C 3〜8の単環式環状基」 としては、例えば「C 3〜8の単環式炭素環」 、 「3〜8員の単環式複素環」 等が挙げられる。 「C3〜8の単環式炭素環」 には、 C 3〜 8の単環式不飽和炭素環、 その一部または全部が飽和されてい る炭素環が含まれる。 この 「C3〜8の単環式不飽和炭素環、 その一部また は全部が飽和されている炭素環」 としては、 例えば、 シクロプロパン、 シク ロブタン、 シクロペンタン、 シクロへキサン、 シクロヘプタン、 シクロオタ
タン、 シクロペンテン、 シクロへキセン、 シクロヘプテン、 シクロオタテン、 シクロペンタジェン、 シクロへキサジェン、 シクロへブタジエン、 シクロォ クタジェン、 ベンゼン環等が挙げられる。 これらのうち、 「C 3〜8の単環 式芳香族炭秦環」 としては、 例えばベンゼン環等が挙げられる。
「 3〜8員の単環式複素環」 としては、 例えば 「ヘテロ原子として、 1〜
4個の窒素原子、 1〜 2個の酸素原子および Zまたは 1〜 2個の硫黄原子を 含む 3〜 8員の単環式複素環」等が挙げられる。 ここで「ヘテロ原子として、 1〜 4個の窒素原子、 1〜 2個の酸素原子および Zまたは 1〜 2個の硫黄原 子を含む 3〜 8員の単環式複素環」 には、 ヘテロ原子として、 1〜4個の窒 素原子、 1〜 2個の酸素原子および/または 1〜 2個の硫黄原子を含む 3〜 8員の単環式不飽和複素環、 その一部または全部が飽和されている複素環が 含まれる。 この 「ヘテロ原子として、 1〜4個の窒素原子、 1〜 2個の酸素 原子および Zまたは 1〜 2個の硫黄原子を含む 3〜 8員の単環式不飽和複素 環、 その一部または全部が飽和されている複素環」 としては、 例えば、 ピロ ール、 イミダゾール、 トリァゾール、 テトラゾール、 ピラゾール、 ピリジン、 ピラジン、 ピリミジン、 ピリダジン、 ァゼピン、 ジァゼピン、 フラン、 ピラ ン、 ォキセピン、 チォフェン、 チォピラン、 チェピン、 ォキサゾー Λ\ イソ ォキサゾーノレ、 チアゾーノレ、 イソチアゾ一/レ、 フラザン、 ォキサジァゾ一ノレ、 ォキサジン、 ォキサジァジン、 ォキサゼピン、 ォキサジァゼピン、 チアジア ゾール、 チアジン、 チアジアジン、 チアゼピン、 チアジアゼピン、 アジリジ ン、 ァゼチジン、 ピロリン、 ピロリジン、 ィミダゾリン、 イミダゾリジン、 トリァゾリン、 トリァゾリジン、 テトラゾリン、 テトラゾリジン、 ビラゾリ ン、 ビラゾリジン、 ジヒドロピリジン、 テトラヒドロピリジン、 ピぺリジン、 ジヒドロビラジン、 テトラヒドロビラジン、 ピペラジン、 ジヒドロピリミジ ン、テトラヒドロピリミジン、パ—ヒドロピリミジン、 ジヒドロピリダジン、 テトラヒドロピリダジン、 パ一ヒドロピリダジン、 ジヒドロアゼピン、 テト
ラヒドロアゼピン、 パーヒドロアゼピン、 ジヒドロジァゼピン、 テトラヒ ド 口ジァゼピン、 パーヒドロジァゼピン、 ォキシラン、 ォキセタン、 ジヒドロ フラン、 テトラヒドロフラン、 ジヒドロピラン、 テトラヒドロピラン、 ジヒ ドロォキセピン、 テトラヒドロォキセピン、 パーヒドロォキセピン、 チイラ ン、 チェタン、 ジヒドロチォフェン、 テトラヒドロチォフェン、 ジヒドロチ ォピラン、 テトラヒドロチォピラン、 ジヒドロチェピン、 テトラヒドロチェ ピン、 パーヒドロチェピン、 ジヒドロォキサゾ一ル、 テトラヒドロォキサゾ ール (ォキサゾリジン) 、 ジヒドロイソォキサゾ'ール、 テトラヒドロイソォ キサゾール (イソォキサゾリジン) 、 ジヒドロチアゾール、 テトラヒドロチ ァゾーノレ (チアゾリジン) 、 ジヒドロイソチアゾール、 テトラヒドロイソチ ァゾ^ ~ル(イソチアゾリジン) 、 ジヒドロフラザン、 テトラヒドロフラザン、 ジヒドロォキサジァゾ一ノレ、 テトラヒドロォキサジァゾール (ォキサジァゾ リジン) 、 ジヒドロォキサジン、 テトラヒドロォキサジン、 ジヒドロォキサ ジァジン、 テトラヒドロォキサジァジン、 ジヒドロォキサゼピン、 テトラヒ ドロォキサゼピン、 パーヒドロォキサゼピン、 ジヒドロォキサジァゼピン、 テトラヒドロォキサジァゼピン、 パーヒドロォキサジァゼピン、 ジヒドロチ アジアゾーノレ、 テトラヒ ドロチアジアゾール (チアジアゾリジン) 、 ジヒ ド 口チアジン、 テトラヒドロチアジン、 ジヒドロチアジアジン、 テトラヒ ドロ チアジアジン、 ジヒドロチアゼピン、 テトラヒドロチアゼピン、 パーヒドロ チアゼピン、 ジヒドロチアジアゼピン、 テトラヒドロチアジアゼピン、 パー ヒドロチアジアゼピン、 モ /レホリン、 チオモルホリン、 ォキサチアン、 ジォ キソラン、 ジォキサン、 ジチオラン、 ジチアン環等が挙げられる。 これらの うち、 「ヘテロ原子として 1〜 4個の窒素原子、 1〜 2個の酸素原子おょぴ ノまたは 1〜2個の硫黄原子を含む 3〜8員の単環式芳香族複素環」 として は、 例えば、 ピロール、 イミダゾール、 トリァゾール、 テトラゾール、 ビラ ゾ^ "ル、 ピリジン、 ピラジン、 ピリミジン、 ピリダジン、 フラン、 チォフエ
ン、 ォキサゾール、 イソォキサゾーノレ、 チアゾール、 イソチアゾーノレ、 ブラ ザン、 ォキサジァゾ一ノレ、 チアジアゾーノレ環等が挙げられる。 「置換基を有 していてもよい二価の 3〜 8員の単環式環状基」 における 「置換基」 として は、 例えば、 A 1および A2中の Tとして例示したもの等が挙げられ、 これら 任意の置換基は置換可能な位置に 1 ~ 8個、 好ましくは 1〜 5個置換してい てもよい。
本明細書中、 Eによって表わされる 「主鎖の原子数 1〜1 0のスぺーサ一」 とは、 主鎖の原子が 1〜1 0個連なっている間隔を意味する。 ここで、 「主 鎖の原子数」 は、主鎖の原子が最小となるように数えるものとする。例えば、 は、主鎖の原子数を 4個、 f ]j は、主鎖の原子数
を 6個と数えるものとする。 「主鎖の原子数 1〜1 0のスぺーサ一」 として は、 例えば一 O—、 一 S―、 一 c〇一、 一 s o—、 一 s o 2—、 置換基を有し ていてもよい二価の窒素原子、 置換基を有していてもよい二価の炭素数 1〜 1 0の脂肪族炭化水素基、 置換基を有していてもよい二価の 3〜1 5員の環 状基から任意に選択される 1〜1 0個からなる、 主鎖の原子が 1〜1 0個連 なっている二価基等が挙げられる。 「置換基を有していてもよい二価の窒素 原子」 は、 前記したものと同じ意味を表わす。 「置換基を有していてもよい 二価の炭素数 1〜 1 0の脂肪族炭化水素基」 における 「二価の炭素数 1〜1 0の脂肪族炭化水素基」 としては、 例えば、 C l〜1 0アルキレン基 (メチ レン、 エチレン、 トリメチレン、 テトラメチレン、 ペンタメチレン、 へキサ メチレン、 ヘプタメチレン、 ォクタメチレン、 ノナメチレン、 デカメチレン 基おょぴそれらの異性体) 、 C 2〜1 0アルケュレン基 (ェテエレン、 プロ ぺニレン、 ブテニレン、 ペンテ二レン、 へキセ レン、 ヘプテニレン、 才ク テニレン、 ノネ二レン、 デセ-レン基およびそれらの異性体) 、 C 2〜1 0 ァ /レキ-レン基 (ェチ-レン、 プロピエレン、 プチ二レン、 ペンチ二レン、 へキシュレン、 へプチ二レン、 ォクチュレン、 ノニュレン、 デシ二レン基お
よびそれらの異性体) 等が挙げられる。 また、 「置換基を有していてもよい 二価の炭素数 1 ~ 1 0の脂肪族炭化水素基」 における 「置換基」 としては、 例えば、 A 1および A2中における Tとして例示したもの等が挙げられ、 これ らの任意の置換基は置換可能な位置に 1〜 5個、 好ましくは 1〜 2個置換し ていてもよい。 「置換基を有していてもよい二価の 3〜1 5員の環状基」 に おける 「二価の 3〜1 5員の環状基」 とは、 例えば 「3〜 1 5員の環状基」 カ ら任意の 2個の水素原子を除いてできる二価基等が挙げられる。ここで「3 〜 1 5員の環状基」 としては、 例えば、 前記で定義した C 3 ~ 1 5の単環ま たは多環式炭素環、 またはへテロ原子として 1〜 4個の窒素原子、 1〜2個 の酸素原子および/または 1〜 2個の硫黄原子を含む 3〜1 5員の単環また は多環式複素環等が挙げられる。 「置換基を有していてもよい二価の 3〜 1 5員の環状基」 における 「置換基」 としては、 例えば、 A 1および A 2中にお ける Tとして例示したもの等が挙げられ、 これらの任意の置換基は置換可能 な位置に 1〜 5個、 好ましくは 1〜 2個置換していてもよい。
本明細書中、 環 EAによって表わされる 「置換基を有していてもよい二価の 3〜 8員の単環式環状基または置換基を有していてもよい二価の 9または 1 0員の多環式環状基」 の 「置換基を有していてもよい二価の 3 ~ 8員の単環 式環状基」 とは、 B 1および B 2中における 「置換基を有していてもよい二価 の 3〜8員の単環式環状基」 と同じ意味を表わす。 環 EAによって表わされる 「置換基を有していてもよい二価の 3〜 8員の単環式環状基または置換基を 有していてもよい二価の 9または 1 0員の多環式環状基」 の 「置換基を有し ていてもよい二価の 9または 1 0員の多環式環状基」 としては、 E中の 「置 換基を有していてもよい二価の 3〜1 5員の環状基」 のうち、 9または 1 0 員のものが選択される。
本明細書中、 LAおよび LA 1によって表わされる 「一 (置換基を有していて もよい炭素数 1〜3の脂肪族炭化水素基) 一 (置換基を有していてもよい窒
素原子) 一」 における 「一 (置換基を有していてもよい窒素原子) 一」 とは、 前記「置換基を有していてもよい二価の窒素原子」 と同じ意味を表わす。 「置 換基を有していてもよい炭素数 1〜 3の脂肪族炭化水素基」 における 「炭素 数 1〜 3の脂肪族炭化水素」 としては、 例えば C 1〜 3アルキレン基 (例え ば、 メチレン、 エチレン、 トリメチレン等) 、 C 2〜 3ァノレケニレン基 (例 えば、 エテュレン、 プロぺ-レン等) 、 C 2〜3のアルキニレン基(例えば、 ェチ-レン、 プロピニレン等) 等が挙げられる。 また、 「置換基を有してい てもよい炭素数 1〜 3の脂肪族炭化水素基」 における 「置換基」 としては、 例えば、 A 1および A 2中の Tとして例示したもの等が挙げられ、 これらの任 意の置換基は置換可能な位置に 1〜 3個置換していてもよい。
本明細書中、 LAおよび L A 2によって表わされる 「置換基を有していてもよ い二価の炭素数 1〜4の脂肪族炭化水素基」 は前記と同じ意味を表わす。 本明細書中、 J °によって表わされる 「塩基性基を含有する基によって置換 され、 さらに置換基を有していてもよい脂肪族炭化水素基」 としては、 (1)塩 基性基によって置換され、 さらに置換基を有していてもよい脂肪族炭化水素 基、 (2)塩基性基によって置換された環状基によって置換され、 さらに置換基 を有していてもよい脂肪族炭化水素基、 (3)塩基性基によって置換された脂肪 族炭化水素基によって置換され、 さらに置換基を有していてもよい脂肪族炭 化水素基が挙げられる。 また、 J °によって表わされる 「塩基性基を含有する 基によって置換され、 さらに置換基を有していてもよい環状基」 としては、(1) 塩基性基によって置換され、 さらに置換基を有していてもよい環状基、 (2)塩 基性基によつて置換された環状基によつて置換され、 さらに置換基を有して いてもよい環状基、 (3)塩基性基によつて置換された脂肪族炭化水素基によつ て置換され、 さらに置換基を有していてもよい環状基が挙げられる。 J。で表 わされる 「塩基性基を含有する基によって置換されていてもよく、 さらに置 換基を有していてもよいスピロ環状基」 としては、 (1)塩基性基によって置換
されていてもよく、 さらに置換基を有していてもよいスピロ環状基、 (2)塩基 性基によつて置換された環状基によって置換されていてもよく、 さらに置換 基を有していてもよぃスピロ環状基、 (3)塩基性基によつて置換された脂肪族 炭化水素基によつて置換されていてもよく、 さらに置換基を有じていてもよ ぃスピロ環状基が挙げられる。 また、 J。で表わされる 「塩基性基を含有する 基によって置換されていてもよく、 さらに置換基を有していてもよい架橋し た環状基」 としては、 (1)塩基性基によって置換されていてもよく、 さらに置 換基を有していてもよい架橋した環状基、 (2)塩基性基によつて置換された環 状基によって置換されていてもよく、 さらに置換基を有していてもよい架橋 した環状基、 (3)塩基性基によって置換された脂肪族炭化水素基によって置換 さ ていてもよく、 さらに置換基を有していてもよい架橋した環状基が挙げ られる。 ここで 「塩基性基を含有する基によって置換されていてもよく、 さ らに置換基を有していてもよいスピロ環状基」 における 「スピロ環状基」 と は前記 「環状基」 における 「炭素環」 の 「スピロ結合した多環式炭素環」 ま たは前記 「環状基」 における 「複素環」 の 「スピロ結合した多環式複素環」 と同じ意味を表わす。 「塩基性基を含有する基によって置換されていてもよ く、 さらに置換基を有していてもよい架橋した環状基」 の 「架橋した環状基」 としては、 前記 「環状基」 における 「炭素環」 の 「架橋した多環式炭素環」 または 「複素環」 の 「架橋した多環式複素環」 と同じ意味を表わす。 ここで の 「脂肪族炭化水素基」 および「環状基」 は前記と同じ意味を表わす。 また、 ここでの 「塩基性基」 としては、 A 1および A 2中の 「塩基性基」 と同じ意味 を表わす。 ここでの 「置換基」 としては、 特に限定されない。 例えば、 お ょぴ A 2中の Tとして例示したもの等が挙げられ、 これらの任意の置換基は置 換可能な位置に 1〜 5個置換していてもよい。
本明細書中、 J。で表わされる 「塩基性基を含有する基によって置換されて いてもよく、 さらに置換基を有していてもよい、 少なくとも一つの窒素原子
を含有し、 さらに酸素原子および Zまたは酸化されていてもよい硫黄原子を 含有していてもよいスピロ複素環または架橋した複素環」 における 「少なく とも一つの窒素原子を含有し、 さらに酸素原子および zまたは酸化されてい てもよい硫黄原子を含有していてもよいスピロ複素環または架橋した複素 環」 には、 少なくとも一つの窒素原子を含有し、 さらに酸素原子および/ま たは酸化されていてもよい硫黄原子を含有していてもよいスピロ複素環、 お よび少なくとも一つの窒素原子を含有し、 さらに酸素原子および zまたは酸 化されていてもよい硫黄原子を含有していてもよい架橋した複素環が含まれ る。 「少なくとも一つの窒素原子を含有し、 さらに酸素原子おょぴ zまたは 硫黄原子を含有していてもよいスピロ複素環」 としては、 例えば、 ァザスピ 口 [4. 4] ノナン、 ォキサザスピロ [4. 4] ノナン、 ァザスピロ [4. 5] デカン、 才キサザスピロ [4. 5] デカン、 ァザスピロ [5. 5] ゥン デカン、 2, 7—ジァザスピロ [3. 5]ノナン、 2, 8—ジァザスピロ [4. 5] デカン、 2, 7—ジァザスピロ [4. 5] デカン 2, 9ージァザスピロ [5. 5] ゥンデカン、 2, 8—ジァザスピロ [5. 5] ゥンデカン、 3, 9ージァザスピロ [5. 5] ゥンデカン、 2, 7—ジァザスピロ [4. 4] ノナン、 1, 2—ジヒドロスピロ [インドールー 3, 4,一ピぺリジン] 、 2, 3—ジヒドロー 1 H—スピロ [イソキノリン一4, 4,ーピペリジン] 、 1,, 4,一ジヒドロー 2,H—スピロ [ピペリジン一 4, 3,一キノリン] 、 2,, 3, ージヒドロ一 1,H—スピロ [ピペリジン一 4, 4'—キノリン] 、 8—ァザス ピロ [4. 5] デカン、 8—ァザスピロ [4. 5] デカン、 7—ァザスピロ [4. 5] デカン、 3—ァザスピロ [5. 5] ゥンデカン、 2—ァザスピロ [5. 5] ゥンデカン、 1一ォキサ一 4, 8—ジァザスピロ [5. 5] ゥン デカン、 1—ォキサ一 4, 9ージァザスピロ [5. 5] ゥンデカン、 3, 4 —ジヒドロスピロ [クロメンー 2, 4,ーピペリジン]、 2—ァザスピロ [4. 4] ノナン、 7—ァザスピロ [3. 5] ノナン、 2, 3—ジヒドロスピロ [ィ
ンデン一 1, 4,ーピペリジン] 、 3, 4ージヒドロー 2H—スピロ [ナフタ レン一 1, 4,ーピペリジン] 、 3, 4ージヒドロー 1 H—スピロ [ナフタレ ンー 2, 4,一ピぺリジン〕 、 2—ァザスピロ [4. 5] デカン、 2—ァザス ピロ [3. 5] ノナン、 1', 2'—ジヒドロスピロ [シクロへキサン一 1, 3, 一^ ンドーノレ] 、 2,, 3,ージヒ ドロ一 1Ήースピロ [シクロへキサン一 1, 4'一イソキノリン] 、 , 4,一ジヒドロー 2Ή—スピロ [シクロへキサン一 1, 3'—キノリン] 、 1, 6—ジァザスピロ [3. 4] オクタン、 1, 5— ジァザスピロ [3. 4]オクタン、 1, 7—ジァザスピロ [3. 5] ノナン、 1, 6—ジァザスピロ [3. 5] ノナン、 1, 5—ジァザスピロ [3. 5] ノナン、 1, 7—ジァザスピロ [4. 4]ノナン、 1, 6—ジァザスピロ [4. 4] ノナン、 1, 8—ジァザスピロ [4. 5] デカン、 1, 7—ジァザスピ 口 [4. 5] デカン、 2, 6—ジァザスピロ [3. 4] オクタン、 1, 6一 ジァザスピロ [4. 5] デカン、 2, 6—ジァザスピロ [3. 5] ノナン、 1, 9ージァザスピロ [5. 5] ゥンデカン、 1, 8—ジァザスピロ [5. 5] ゥンデカン、 6—ァザスピロ 〔3, 5] ノナン、 6—ァザスピロ [3. 4] オクタン、 2—ァザスピロ [3. 4] オクタン、 1, 7—ジァザスピロ [5. 5] ゥンデカン、 1, 4, 9一トリァザスピロ [5. 5] ゥンデカン、 1, 3, 8—トリァザスピロ [4. 5] デカン、 1_チア一 4, 9一ジァザ スピロ [5. 5] ゥンデカン、 1一チア一 4, 8—ジァザスピロ [5. 5] ゥンデカン等が挙げられる。 「少なくとも一つの窒素原子を含有し、 さらに 酸素原子およぴ /または硫黄原子を含有していてもょレ、架橋した複素環」 と しては、 例えば、 ァザビシクロ [2. 2. 1] ヘプタン、 ァザビシクロ [3. 1. 1]ヘプタン、 ァザビシクロ [3. 2. 1]オクタン、 ァザビシクロ [2. 2. 2] オクタン、 ジァザビシクロ [2. 2. 2] オクタン、 1ーァザトリ シクロ [3. 3. 1. I3' 7] デカン、 3—ァザビシクロ [3. 3. 1] ノナ ン、 3, 7—ジァザビシクロ [3. 3. 1] ノナン等が挙げられる。
本明細書中、 J。で表わされる 「スピロ複素環を構成する ¾が、 少なくとも 一つの窒素原子、 および炭素原子からなる単環、 および Zまたは少なくとも 一つの窒素原子、 酸素原子一つ、 および炭素原子からなる単環で構成される
7〜1 5員の二環式のスピロ複秦環」 には (1 ) スピロ複素環を構成する環 1 二つの (a)少なくとも一つの窒素原子、 および炭素原子からなる 4〜 8員 の単環から構成される 7 ~ 1 5員の二環式のスピロ複素環、 (2 ) スピロ複 素環を構成する環が、 (a)少なくとも一つの窒素原子、 および炭素原子からな る 4〜 8員の単環、 および (b)少なくとも一つの窒素原子、 酸素原子一つ、 お よび炭素原子からなる 4〜8員の単環から構成される 7〜1 5員の二環式の スピロ複素環、 および (3 ) スピロ複素環を構成する環が、 二つの (b)少なく とも一つの窒素原子、 酸素原子一つ、 および炭素原子からなる単環から構成 される 7〜1 5員の二環式のスピロ複素環が含まれる。
「 (1 ) スピロ複素環を構成する環が、 二つの (a)少なくとも一つの窒素原 子、 および炭素原子からなる :〜 8員の単環から構成される 7〜1 5員の二 環式のスピロ複素環」 とは、 「(a)少なくとも一つの窒素原子、 および炭素原 子からなる :〜 8員の単環」 から任意に選ばれる二つの環が一つの炭素原子 を共有していることを表わす。 共有する炭素原子は単環を構成する炭素原子 であれば、 いずれの炭素原子でもよい。
「 (2 ) スピロ複素環を構成する環が、 (a)少なくとも一つの窒素原子、 お よび炭素原子からなる 4〜8員の単環、および (b)少なくとも一つの窒素原子、 酸素原子一つ、 および炭素原子からなる 4〜8員の単環から構成される 7〜 1 5員の二環式のスピロ複素環」 とは、 「(a)少なくとも一つの窒素原子、 お よび炭素原子からなる 4〜 8員の単環」から任意に選ばれる一つの環と、 「(b) 少なくとも一つの窒素原子、 酸素原子一つ、 および炭素原子からなる 4〜8 員の単環」 力 ら任意に選ばれる一つの環が、 一つの炭素原子を共有している ことを表わす。 共有する炭素原子は単環を構成する炭素原子であれば、 いず
れの炭素原子でもよい。
「 (3) スピロ複素環を構成する環が、 二つの (b)少なくとも一つの窒素原 子、 酸素原子一つ、 および炭素原子からなる単環から構成される 7〜15員 の二環式のスピロ複素環」 とは、 「(b)少なくとも一つの窒素原子、 酸素原子 一つ、 および炭素原子からなる単環」 力 ^任意に選ばれる二つの環が一つの 炭素原子を共有していることを表わす。 共有する炭素原子は単環を構成する 炭素原子であれば、 いずれの炭素原子でもよい。
「少なくとも一つの窒素原子、 および炭素原子からなる :〜 8員の単環」 としては、 例えば、 ァゼチジン、 ピロリジン、 ピぺリジン、 ピぺラジン、 ァ ゼパン、 1, 4一ジァゼパン、 ァゾカン、 1, 4一ジァゾカン、 1, 5—ジ ァゾカン、 モルホリン等が挙げられる。
「少なくとも一つの窒素原子、 酸素原子一つ、 および炭素原子からなる 4 〜8員の単環」 としては、 例えば、 1, 4—ォキサゼパン、 1, 4一ォキサ ゾカン、 1, 5—ォキサゾカン等が挙げられる。
「 (1) スピロ複素環を構成する環が、 二つの (a)少なくとも一つの窒素原 子、 および炭素原子からなる 4〜 8員の単環から構成される 7〜15員の二 環式のスピロ複素環」 としては、 例えば、 2, 7—ジァザスピロ [3. 5] ノナン、 2, 8—ジァザスピロ [4. 5]デカン、 2, 7—ジァザスピロ [4. 5] デカン、 2, 9ージァザスピロ [5. 5] ゥンデカン、 2, 8—ジァザ スピロ [5. 5] ゥンデカン、 2, 6—ジァザスピロ [3. 5] ノナン、 3, 9ージァザスピロ [5. 5] ゥンデカン、 2, 7—ジァザスピロ [4. 4] ノナン、 1, 3, 8—トリァザスピロ [4. 5] デカン、 1, 4, 9一トリ ァザスピロ [5. 5] ゥンデカン等が挙げられる。
「 (2) スピロ複素環を構成する環が、 (a)少なくとも一つの窒素原子、 お ょぴ炭素原子からなる 4〜 8員の単環、および (b)少なくとも一つの窒素原子、 酸素原子一つ、 および炭素原子からなる :〜 8員の単環から構成される 7~
1 5員の二環式のスピロ複素環」 としては、 例えば、 1一ォキサ一 4, 9一 ジァザスピロ [ 5 . 5 ] ゥンデカン、 1一ォキサ一4, 8—ジァザスピロ [ 5 . 5 ] ゥンデカン等が挙げられる。
「 (3 ) スピロ複素環を構成する環が、 二つの (b)少なくとも一つの窒素原 子、 酸素原子一つ、 および炭素原子からなる単環から構成される 7〜1 5員 の二環式のスピロ複素環」 としては、 例えば、 2, 9ージォキサ一 5, 1 2 ージァザスピロ [ 6 . 6 ] トリデカン等が挙げられる。
本明細書中、 J。で表わされる 「塩基性基を含有する基によって置換され、 さらに置換基を有していてもよいスピロ炭素環または架橋した炭素環」 にお ける 「スピロ炭素環または架橋した炭素環」 としては前記「環状基」 中の 「ス ピロ結合した多環式炭素環」 、 または 「架橋した多環式炭素環」 が挙げられ る。
また、 J °基中の 「置換基」 とは、 特に限定されない。 例えば、 A 1および A 2中の Tとして例示したもの等が挙げられ、 これらの任意の置換基は置換可 能な位置に 1〜 5個置換していてもよい。 さらに、 J °基中の 「脂肪族炭化水 素基」 、 「環状基」 および 「塩基性基」 は、 前記 「脂肪族炭化水素基」 、 前 記 「環状基」 および前記 「塩基性基」 とそれぞれ同じ意味を表わす。
本明細書中、 環 J 1および環 J 2はスピ口環を形成する環を表わす。
本明細書中、環 J 1および環 J l aで表わされる 「C 3〜1 0の単環または二 環式炭素環」 には C 3〜 1 0の単環または二環式不飽和炭素環、 C 3〜 1 0 の一部または全部が飽和されている単環または二環式炭素環が含まれる。 例 えば、 ベンゼン、 ァズレン、 ナフタレン、 シクロプロパン、 シクロブタン、 シクロペンタン、 シクロへキサン、 シクロヘプタン、 シクロオクタン、 シク ロノナン、 シクロデカン、 シクロへキセン、 シクロヘプテン、 シクロォクテ ン、 シクロペンタジェン、 シクロへキサジェン、 シクロへブタジエン、 シク 口才クタジェン、ペンタレン、パーヒドロペンタレン、パーヒドロアズレン、
インデン、 パ^ "ヒドロインデン、 インダン、 ジヒドロナフタレン、 テトラヒ ドロナフタレン、 パーヒドロナフタレン、 ヘプタレン、 パーヒドロヘプタレ ン等が挙げられる。
本明細書中、環 J 1および環 J l aで表わされる 「炭素原子、 酸素原子おょぴ Zまたは酸化されていてもよい硫黄原子からなる 3 〜 1 0員の単環または二 環式複素環」 には炭素原子、 酸素原子および/または酸化されていてもよい 硫黄原子からなる 3 〜 1 0員の単環または二環式不飽和複素環、 および炭素 原子、 酸素原子および Zまたは酸化されていても'よい硫黄原子からなる、 一 部または全部が飽和されている 3 〜 1 0員の単環または二環式複素環が含ま れる。 例えば、 フラン、 ピラン、 ォキセピン、 チォフェン、 チォピラン、 チ ェピン、 ベンゾフラン、 イソべンゾフラン、 ベンゾチォフェン、 イソべンゾ チォフェン、 ジチアナフタレン、 クロメン、 ベンゾォキセピン、 ベンゾチェ ピン、 ォキシラン、 ォキセタン、 ジヒドロフラン、 テトラヒドロフラン、 ジ ヒドロピラン、 テトラヒドロピラン、 ジヒドロォキセピン、 テトラヒドロォ キセピン、 パーヒドロォキセピン、 チイラン、 チェタン、 ジヒドロチォフエ ン、 テトラヒドロチォフェン、 ジヒドロチォピラン、 テトラヒドロチォビラ ン、 ジヒ ドロチェピン、 テトラヒドロチェピン、 パーヒドロチェピン、 ォキ サチアン、 ジヒドロべンゾフラン、 パーヒドロベンゾフラン、 ジヒドロイソ ベンゾフラン、 パーヒドロイソべンゾフラン、 ジヒドロベンゾチォフェン、 ノ ーヒドロベンゾチォフェン、 ジヒドロイソベンゾチォフェン、 ノヽ0 ヒドロ イソベンゾチォフェン、 ベンゾォキサチアン、 ベンゾジォキセパン、 ジォキ ソラン、 ジォキサン、 ジチオラン、 ジチアン、 ジォキサインダン、 ベンゾジ ォキサン、 クロマン、 ベンゾジチオラン、 ベンゾジチアン等が挙げられる。 本明細書中、環 J 1および環 J l bで表わされる 「少なくとも一つの窒素原子 を含有し、 さらに酸素原子または酸化されていてもよい硫黄原子を含有して いてもよい 3 〜 1 0員の単環または二環式複素環」 には少なくとも一つの窒
素原子を含有し、 さらに酸素原子または酸化されていてもよい硫黄原子を含 有していてもよい 3〜1 0員の単環または二環式不飽和複素環、 および少な くとも一つの窒素原子を含有し、 さらに酸素原子または酸化されていてもよ い硫黄原子を含有していてもよい、 一部または全部が飽和されている 3〜1 0員の単環または二環式複素環が含まれる。 例えば、 アジリジン、 ァゼチジ ン、 ピロリン、 ピロリジン、 ィミダゾリン、 イミダゾリジン、 トリァゾリン、 トリァゾリジン、 テトラゾリン、 テトラゾリジン、 ピラゾリン、 ビラゾリジ ン、 ジヒドロピリジン、 テトラヒドロピリジン、 'ピペリジン、 ジヒドロビラ ジン、 テトラヒドロビラジン、 ピぺラジン、 ジヒドロピリミジン、 テトラヒ ドロピリミジン、 パーヒドロピリミジン、 ジヒドロピリダジン、 テトラヒド 口ピリダジン、 パーヒドロピリダジン、 ジヒドロアゼピン、 テトラヒドロア ゼピン、 パーヒドロアゼピン、 ジヒドロジァゼピン、 テトラヒドロジァゼピ ン、 パーヒ ドロジァゼピン、 ジヒドロォキサゾー Λ^、 テトラヒドロォキサゾ ール (ォキサゾリジン) 、 ジヒドロイソォキサゾール、 テトラヒ ドロイソ才 キサゾール (イソォキサゾリジン) 、 ジヒドロチアゾール、 テトラヒドロチ ァゾール (チアゾリジン) 、 ジヒ ドロイソチアゾール、 テトラヒドロイソチ ァゾーグレ(イソチアゾリジン) 、 ジヒドロフラザン、 テトラヒ ドロプラザン、 ジヒドロォキサジァゾール、 テトラヒドロォキサジァゾール (ォキサジァゾ リジン) 、 ジヒドロォキサジン、 テトラヒドロォキサジン、 ジヒドロォキサ ジァジン、 テトラヒドロォキサジァジン、 ジヒドロォキサゼピン、 テトラヒ ドロォキサゼピン、 パーヒドロォキサゼピン、 ジヒドロォキサジァゼピン、 テトラヒドロォキサジァゼピン、 パーヒドロォキサジァゼピン、 ジヒドロチ アジアゾーノレ、 テトラヒドロチアジアゾール (チアジアゾリジン) 、 ジヒド 口チアジン、 テトラヒドロチアジン、 ジヒドロチアジアジン、 テトラヒドロ チアジアジン、 ジヒドロチアゼピン、 テトラヒドロチアゼピン、 パーヒドロ チアゼピン、 ジヒドロチアジナゼピン、 テトラヒ ドロチアジアゼピン、 パー
ヒドロチアジアゼピン、 モノレホリン、 チォモ ホリン、 インドリン、 イソィ ンドリン、 ジヒドロインダゾーノレ、 ハ。ーヒドロインダゾーノレ、 ジヒドロキノ リン、テトラヒドロキノリン、パーヒドロキノリン、 ジヒドロイソキノリン、 テトラヒドロイソキノリン、パーヒドロイソキノリン、ジヒドロフタラジン、 テトラヒ ドロフタラジン、 パーヒドロフタラジン、 ジヒドロナフチリジン、 テトラヒ ドロナフチリジン、 パーヒドロナフチリジン、 ジヒドロキノキサリ ン、 テトラヒドロキノキサリン、 パーヒドロキノキサリン、 ジヒドロキナゾ リン、 テトラヒドロキナゾリン、 パーヒドロキナ'ゾリン、 ジヒドロシンノリ ン、 テトラヒドロシンノリン、 パーヒドロシンノリン、 ジヒドロベンゾォキ サジン、 ジヒドロべンゾチアジン、 ビラジノモノレホリン、 ジヒドロべンゾォ キサゾ一/レ、 ノ、。ーヒ ドロべンゾォキサゾ一ノレ、 ジヒドロべンゾチアゾーノレ、 /■?ーヒドロべンゾチアゾーノレ、 ジヒドロべンゾイミダゾーノレ、 ノ ーヒドロべ ンゾィミダゾ一ノレ、ジヒドロベンゾァゼピン、テトラヒドロベンゾァゼピン、 ジヒドロべンゾジァゼピン、 テトラヒドロべンゾジァゼピン、 ベンゾジォキ セパン、 ジヒドロべンゾォキサゼピン、 テトラヒドロべンゾォキサゼピン、 ピロール、 イミダゾール、 トリァゾール、 テトラゾール、 ピラゾーノレ、 ピリ ジン、 ピラジン、 ピリミジン、 ピリダジン、 ァゼピン、 ジァゼピン、 ォキサ ゾール、 イソォキサゾーノレ、 チアゾーノレ、 イソチアゾール、 フラザン、 ォキ サジァゾー^ ォキサジン、 ォキサジァジン、 ォキサゼピン、 ォキサジァゼ ピン、 チアジアゾール、 チアジン、 チアジアジン、 チアゼピン、 チアジアゼ ピン、 インドール、 イソインドール、 インドリジン、 ィンダゾール、 キノリ ン、 イソキノリン、 キノリジン、 プリン、 フタラジン、 プテリジン、 ナフチ リジン、 キノキサリン、 キナゾリン、 シンノリン、 ベンゾォキサゾール、 ベ ンゾチアゾーノレ、 ベンゾイミダゾール、 ベンゾ才キサゼピン、 ベンゾ才キサ ジァゼピン、 ベンゾチェピン、 ベンゾチアゼピン、 ベンゾチアジアゼピン、 ベンゾァゼピン、 ベンゾジァゼピン、 ベンゾフラザン、 ベンゾチアジアゾー
ル、 ベンゾトリアゾール等が挙げられる。
環 J 2で表わされる 「塩基性基を含有する基によって置換された、 C 3〜l 0の単環または二環式炭素環」 、 「塩基性基を含有する基によって置換され た、 炭素原子、 酸素原子および/または酸化されていてもよい硫黄原子から なる 3〜1 0員の単環または二環式複素環」 、 または 「塩基性基を含有する 基によって置換されてもよい、 少なくとも一つの窒素原子を含有し、 さらに 酸素原子または酸化されていてもよい硫黄原子を含有していてもよい 3〜 1 0員の単環または二環式複素環」 における 「C 3 ~ 1 0の単環または二環式 炭素環」 、 「炭素原子、 酸素原子および/または酸化されていてもよい硫黄 原子からなる 3〜1 0員の単環または二環式複素環」 、 または 「少なくとも 一つの窒素原子を含有し、 さらに酸素原子または酸化されていてもよい硫黄 原子を含有していてもよい 3〜1 0員の単環または二環式複素環」 はそれぞ れ前記と同じ意味を表わす。 環 J 2 aで表わされる 「塩基性基を含有する基に よって置換された、 C 3〜l 0の単環または二環式炭素環」 または 「塩基性 基を含有する基によって置換された、 炭素原子、 酸素原子および Zまたは酸 化されていてもよい硫黄原子からなる 3〜1 0員の単環または二環式複素 環」 における 「C 3〜1 0の単環または二環式炭素環」 または 「炭素原子、 酸素原子おょぴ Zまたは酸化されていてもよい硫黄原子からなる 3〜1 0員 の単環または二環式複素環」 はそれぞれ前記と同じ意味を表わす。 環 J で 表わされる 「塩基性基を含有する基によって置換されてもよレ、、 少なくとも 一つの窒素原子を含有し、 さらに酸素原子または酸化されていてもよい硫黄 原子を含有していてもよい 3〜1 0員の単環または二環式複素環」 における 「少なくとも一つの窒素原子を含有し、 さらに酸素原子または酸ィヒされてい てもよい硫黄原子を含有していてもよい 3〜1 0員の単環または二環式複素 環」 は前記と同じ意味を表わす。 ここでの 「塩基性基を含有する基」 は前記 「塩基性基を含有する基によって置換されていてもよく、 さらに置換基を有
していてもよいスピロ環状基」 における 「塩基性基を含有する基」 と同じ意 味を表わす。
本明細書中、 環 J 3で表わされる 「塩基性基を含有する基によって置換され た、 架橋した多環式炭素環」 における 「架橋した多環式炭素環」 とは 「環状 基」 中の 「架橋した多環式炭素環」 と同じ意味を表わす。
本明細書中、 環 J 3で表わされる 「塩基性基を含有する基によって置換され た、 炭素原子、 酸素原子および Zまたは酸化されていてもよい硫黄原子から なる架橋した多環式複素環」 の 「炭素原子、 酸素原子おょぴ Zまたは酸化さ れていてもよい硫黄原子からなる架橋した多環式複素環」 としては、例えば、 ォキサビシクロ [2. 2. 1] ヘプタン、 ォキサビシクロ [3. 2. 1] ォ クタン等が挙げられる。
本明細書中、 環 J 3で表わされる 「塩基性基を含有する基によって置換され ていてもよい、 少なくとも一つの窒素原子を含有し、 さらに酸素原子および /または酸化されていてもよい硫黄原子を含有していてもよい架橋した多環 式複素環」 の 「少なくとも一つの窒素原子を含有し、 さらに酸素原子および
Zまたは酸化されていてもょレ、硫黄原子を含有していてもよ 1、架橋した多環 式複素環」 としては、 例えば、 ァザビシクロ [2. 2. 1] ヘプタン、 ォキ サビシクロ [2. 2. 1] ヘプタン、 ァザビシクロ [3. 1. 1]ヘプタン、 ァザビシクロ [3. 2. 1] オクタン、 ォキサビシクロ [3. 2. 1] オタ タン、 ァザビシクロ [2. 2. 2] オクタン、 ジァザビシクロ [2. 2. 2] オクタン、 1一ァザトリシクロ [3. 3. 1. I3' 7] デカン、 3—ァザビシ クロ [3. 3. 1] ノナン、 3, 7—ジァザビシクロ [3. 3. 1] ノナン 等が挙げられる。
環 J 3における 「塩基性基を含有する基」 は前記 「塩基性基を含有する基に よって置換されていてもよく、 さらに置換基を有していてもよい架橋した環 状基」 における 「塩基性基を含有する基」 と同じ意味を表わす。
本明細書中、 環 J 4で表わされる 「塩基性基を含有する基によって置換され た、 C 3〜1 5の単環または縮合した炭素環」 における 「C 3〜1 5の単環 または縮合した炭素環」 とは 「環状基」 中の 「C 3〜1 5の単環または多環 式不飽和炭素環、 その一部または全部が飽和されている炭素環」 と同じ意味 を表わす。
本明細書中、 環 J 4で表わされる 「塩基性基を含有する基によって置換され た、 炭素原子、 酸素原子および/または酸化されていてもよい硫黄原子から なる 3〜1 5員の単環または縮合した複素環」 め 「3〜1 5員の単環または 縮合した複素環」 には、 炭素原子、 酸素原子およびノまたは酸化されていて もよい硫黄原子からなる 3〜1 5員の単環または縮合した不飽和複素環、 炭 素原子、 酸素原子および Zまたは酸化されていてもょレ、硫黄原子からなる一 部または全部飽和されている 3〜1 5員の単環または縮合した複素環が含ま れる。 例えば、 フラン、 ピラン、 ォキセピン、 チォフェン、 チォピラン、 チ ェピン、 ベンゾフラン、 イソべンゾフラン、 ベンゾチ才フェン、 イソべンゾ チォフェン、 ジチアナフタレン、 クロメン、 ベンゾォキセピン、 ベンゾチェ ピン、 ジベンゾフラン、 キサンテン、 ジベンゾチォフェン、 フエノキサチイ ン、 チアンスレン、 ォキシラン、 ォキセタン、 ジヒドロフラン、 テトラヒド 口フラン、 ジヒドロピラン、 テトラヒドロピラン、 ジヒドロォキセピン、 テ トラヒ ドロォキセピン、 パーヒドロォキセピン、 チイラン、 チェタン、 ジヒ ドロチォフェン、 テトラヒドロチォフェン、 ジヒドロチォピラン、 テトラヒ ドロチォピラン、 ジヒドロチェピン、 テトラヒドロチェピン、 パ一ヒドロチ ェピン、 ォキサチアン、 ジヒドロべンゾフラン、 パーヒドロべンゾフラン、 ジヒドロイソべンゾフラン、 ノ、。ーヒドロイソべンゾフラン、 ジヒドロべンゾ チォフェン、パーヒドロベンゾチォフェン、ジヒドロイソベンゾチォフェン、 パーヒドロイソベンゾチォフェン、 ベンゾォキサチアン、 ベンゾジォキセパ ン、 ジヒドロジべンゾフラン、 ジヒドロジベンゾチォフェン、 テトラヒドロ
ジベンゾフラン、 テトラヒドロジベンゾチ才フェン、 パーヒドロジべンゾフ ラン、 パーヒドロジベンゾチォフェン、 ジォキソラン、 ジォキサン、 ジチォ ラン、 ジチアン、 ジォキサインダン、 ベンゾジォキサン、 クロマン、 ベンゾ ジチオラン、 ベンゾジチアン等が挙げられる。
本明細書中、 環 J 4で表わされる 「塩基性基を含有する基によって置換され ていてもよい、 少なくとも一つの窒素原子を含有し、 さらに酸素原子および または酸化されていてもよい硫黄原子を含有していてもよい 3〜1 5員の 単環または縮合した複素環」 の 「少なくともーづの窒素原子を含有し、 さら に酸素原子および Zまたは酸化されていてもよい硫黄原子を含有していても よい 3〜1 5員の単環または縮合した複素環」 には、 少なくとも一つの窒素 原子を含有し、 さらに酸素原子および Zまたは酸化されていてもよい硫黄原 子を含有していてもよい単環または縮合した 3〜1 5員の不飽和複素環、 少 なくとも一つの窒素原子を含有し、 さらに酸素原子および/または酸化され ていてもよい硫黄原子を含有していてもよい、 一部または全部飽和されてい る 3〜1 5員の単環または縮合した複素環が含まれる。 例えば、 ピロール、 ィミダゾール、 トリァゾール、 テトラゾール、 ピラゾール、 ピリジン、 ビラ ジン、 ピリミジン、 ピリダジン、 ァゼピン、 ジァゼピン、 ォキサゾール、 ィ ソォキサゾール、 チアゾール、 イソチアゾール、 フラザン、 ォキサジァゾ一 ; ォキサジン、 ォキサジァジン、 ォキサゼピン、 ォキサジァゼピン、 チア ジァゾール、 チアジン、 チアジアジン、 チアゼピン、 チアジアゼピン、 イン ドール、 イソインドール、 インドリジン、 ィンダゾール、 キノリン、 イソキ ノリン、 キノリジン、 プリン、 フタラジン、 プテリジン、 ナフチリジン、 キ ノキサリン、 キナゾリン、 シンノリン、 ベンゾォキサゾーノレ、 ベンゾチアゾ ール、ベンゾィミダゾール、 ベンゾォキサゼピン、ベンゾォキサジァゼピン、 ベンゾチアゼピン、 ベンゾチアジアゼピン、 ベンゾァゼピン、 ベンゾジァゼ ピン、 ベンゾフラザン、 ベンゾチアジアゾール、 ベンゾトリァゾール、 カル
パゾール、 β—力ルポリン、 アタリジン、 フエナジン、 フエノチアジン、 フ エノキサジン、 フヱナントリジン、 フエナント口リン、 ペリミジン、 アジリ ジン、 ァゼチジン、 ピロリン、 ピロリジン、 ィミダゾリン、 イミダゾリジン、 トリァゾリン、 トリァゾリジン、 テトラゾリン、 テトラゾリジン、 ビラゾリ ン、 ビラゾリジン、 ジヒドロピリジン、 テトラヒドロピリジン、 ピぺリジン、 ジヒドロビラジン、 テトラヒドロビラジン、 ピぺラジン、 ジヒドロピリミジ ン、テトラヒドロピリミジン、パーヒドロピリミジン、 ジヒドロピリダジン、 テトラヒドロピリダジン、 パーヒドロピリダジン、 ジヒドロアゼピン、 テト ラヒドロアゼピン、 パーヒドロアゼピン、 ジヒドロジァゼピン、 テトラヒド 口ジァゼピン、 パーヒドロジァゼピン、 ジヒドロォキサゾール、 テトラヒド ロォキサゾーノレ (ォキサゾリジン) 、 ジヒドロイソォキサゾーノレ、 テトラヒ ドロイソォキサゾール (イソォキサゾリジン) 、 ジヒドロチアゾール、 テト ラヒドロチアゾール (チアゾリジン) 、 ジヒドロイソチアゾール、 テトラヒ ドロイソチアゾーノレ (イソチアゾリジン) 、 ジヒドロフラザン、 テトラヒド ロフラザン、 ジヒドロォキサジァゾール、テトラヒドロォキサジァゾール(ォ キサジァゾリジン) 、 ジヒドロォキサジン、 テトラヒドロォキサジン、 ジヒ ドロォキサジァジン、テトラヒドロォキサジァジン、ジヒドロォキサゼピン、 テトラヒドロォキサゼピン、 パーヒドロォキサゼピン、 ジヒドロォキサジァ ゼピン、 テトラヒドロォキサジァゼピン、 パーヒドロォキサジァゼピン、 ジ ヒドロチアジァゾール、テトラヒドロチアジアゾール(チアジアゾリジン) 、 ジヒドロチアジン、 テトラヒドロチアジン、 ジヒドロチアジアジン、 テトラ ヒドロチアジアジン、 ジヒドロチアゼピン、 テトラヒドロチアゼピン、 パー ヒドロチアゼピン、ジヒドロチアジアゼピン、テトラヒドロチアジアゼピン、 パーヒドロチアジアゼピン、 モノレホリン、 チォモ ホリン、 インドリン、 ィ ソインドリン、 ジヒドロインダゾーノレ、 パーヒドロインダゾーノレ、 ジヒドロ キノリン、 テトラヒドロキノリン、 パーヒドロキノリン、 ジヒドロイソキノ
リン、 テトラヒドロイソキノリン、 パーヒドロイソキノリン、 ジヒドロフタ ラジン、 テトラヒドロフタラジン、 パーヒドロフタラジン、 ジヒドロナフチ リジン、 テトラヒドロナフチリジン、 パーヒドロナフチリジン、 ジヒドロキ ノキサリン、 テトラヒドロキノキサリン、 パーヒドロキノキサリン、 ジヒド 口キナゾリン、 テトラヒドロキナゾリン、 パーヒドロキナゾリン、 ジヒドロ シンノリン、 テトラヒドロシンノリン、 パーヒドロシンノリン、 ジヒドロべ ンゾォキサジン、 ジヒドロべンゾチアジン、 ビラジノモ /レホリン、 ジヒドロ ベンゾォキサゾーノレ、 ノ ーヒドロベンゾォキサゾーノレ、 ジヒドロべンゾチア ゾーノレ、 ノ、°ーヒドロべンゾチアゾーノレ、 ジヒドロべンゾイミダゾーノレ、 ノヽ0— ヒドロべンゾイミダゾーノレ、 ジヒドロベンゾァゼピン、 テトラヒドロべンゾ ァゼピン、 ジヒドロべンゾジァゼピン、 テトラヒドロべンゾジァゼピン、 ジ ヒドロべンゾォキサゼピン、 テトラヒドロべンゾォキサゼピン、 ジヒドロ力 ノレノ ゾ一ノレ、 テ トラヒ ドロカノレバゾーノレ、 ノヽ。ーヒ ドロ力ノレパゾーノレ、 ジヒ ド ロアタリジン、 テトラヒドロアクリジン、 パーヒドロアクリジン、 へキサヒ ドロ一 1H—ピロリジン、 ォクタヒドロシクロペンタ [c] ピロ一ノレ、 オタ タヒドロシクロペンタ [b] ピロ一ノレ、 ォクタヒドロピロ口 [3, 2-b] ピロ一/レ、 ォクタヒ ドロピロ口 [3, 4— c] ピロ一ノレ、 へキサヒドロ一 2 H—フロ [3, 2-b] ピロ一ノレ、 へキサヒドロー 2H—チエノ [3, 2— b] ピロ一ノレ、 デカヒドロキノリン、 デカヒドロー 2, 6—ナフチリジン、 ォクタヒドロ一 2H—キノリジン、 ォクタヒドロー 1H—ピリ ド [1, 2— c] ピリミジン、 ォクタヒドロー 2H—1, 4—べンゾォキサジン、 デカヒ ドロー 1, 5—ナフチリジン、 ォクタヒドロー 1H—ピロ口 [3, 4— b] ピリジン、 ォクタヒドロ一 1H—ピロ口 [3, 4- c] ピリジン等が挙げら れる。
環 J 4における 「塩基性基を含有する基」 は、 前記 「塩基性基を含有する基 によって置換され、 さらに置換基を有していてもよい環状基」 における 「塩
基性基を含有する基」 と同じ意味を表わす。
(基中、 L
A 1は、 一 (置換基を有していてもよい炭素数 1〜3の脂肪族炭化 水素基) 一 (置換基を有していてもよい窒素原子) 一を表わし、 環 J
l aおよ ぴ環 J
2 aは、それぞれ独立して ( i ) C 3〜l 0の単環または二環式炭素環、 または (ii) 炭素原子、 酸素原子および Zまたは酸化されていてもよい硫黄原 子からなる 3〜 1 0員の単環または二環式複素環を表わし、 Rは塩基性基を 含有する基を表わし、 環 J
l aおよび環 J
2 aは置換可能な位置に置換可能な数 の置換基を有していてもよく、 置換基が 2つ以上ある場合、 複数の置換基は 同じでも異なっていてもよい。 ただし、 L
A中の (置換基を有していてもよい 窒素原子) は環 J
1に結合するものとする。 ) 、
(基中、 L
A 2は、 置換基を有していてもよい二価の炭素数 1〜4の脂肪族炭 化水素基を表わし、 環 J
1 bは、 少なくとも一つの窒素原子を含有し、 さらに 酸素原子および/または酸化されていてもよい硫黄原子を含有していてもよ い 3〜1 0員の単環または二環式複素環を表わし、 環 J
l bは置換可能な位置 に置換可能な数の置換基を有していてもよく、 置換基が 2つ以上ある場合、 複数の置換基は同じでも異なっていてもよく、 その他の記号は前記と同じ意 味を表わす。 ) 、
(基中、 環 J
2 bは、 塩基性基を含有する基によって置換されてもよく、 少な くとも一つの窒素原子を含有し、 さらに酸素原子または酸化されていてもよ い硫黄原子を含有していてもよい 3〜1 0員の単環または二環式複素環を表 わし、環 J
2 bは置換可能な位置に置換可能な数の置換基を有していてもよく、 置換基が 2つ以上ある場合、 複数の置換基は同じでも異なっていてもよく、 その他の記号は前記と同じ意味を表わす。 ) 、 または
(基中、 全ての記号は前記と同じ意味を表わす。 ) である。
としては、 例えば、
としては、 例えば、
(ただし、 LA 2は一 NH—の窒素原子の置換基であってもよく、 一 NH—の 窒素原子は置換基を有していてもよい。 ) 等が挙げられる。
本明細書中、 の 「塩基性基を含有する基」 は前記 「塩基性基を含有する 基によって置換されていてもよく、 さらに置換基を有していてもよいスピロ 環状基」 における 「塩基性基を含有する基」 と同じ意味を表わす。
本明細書中、 環 J 1、 環】2、 環 ^、 環^! 環^ 環】1 15、 環 J 2 aおよ び環 J 2 bの 「置換可能な位置に置換可能な数の置換基」 の 「置換基」 として
は、 特に限定されない。 例えば、 A 1および A 2中の Tとして例示したもの等 が挙げられ、 これら任意の置換基は置換可能な位置に 1〜 8個、 好ましくは 1〜 5個置換していてもよい。
本明細書中、 Dおよび Gによって表わされる 「置換基を有していてもよい 炭素原子」 における 「置換基」 としては、 特に限定されない。 例えば、 A 1お よび A2中の Tとして例示したもの等が挙げられ、 これらの任意の置換基は置 換可能な位置に 1〜 2個置換していてもよい。
本明細書中、 Gによって表わされる 「置換基を'有していてもよい二価の窒 素原子」 は前記 「置換基を有していてもよい二価の窒素原子」 と同じ意味を 表わす。
本明細書中、 「酸化されていてもよい硫黄原子」 とは、 一S—、 一 s o—、 一 s o 2—を意味する。
本明細書中、 R 1および R 4で示される 「置換基」 は、 特に限定されない。 例えば、 (1)置換基を有していてもよい脂肪族炭化水素基、 (2)置換基を有して いてもよい環状基、 (3)置換基を有していてもよい環状基で置換した脂肪族炭 化水素基、 (4)前記した置換基の T等が挙げられる。 ここでの 「置換基を有し ていてもよい脂肪族炭化水素基」 、 「置換基を有していてもよい環状基」 お よび 「置換基を有していてもよい環状基で置換した脂肪族炭化水素基」 にお ける 「脂肪族炭化水素基」 、 「環状基」 は前記と同じ意味を表わし、 「置換 基」 は A 1および A2中の Tとして例示したもの等が挙げられる。
本明細書中、 R 2および R 3で示される 「置換基」 は、 A 1および A 2によつ て表わされる 「塩基性基を含有する基」 の 「塩基性基」 のうち、 (e ) モノ —またはジー置換アミノ基における 「置換基」 と同じ意味を表わす。
R 2および R 3が結合する窒素原子と一緒になつて形成する環は、環 J 1で表 わされる 「少なくとも一つの窒素原子を含有し、 さらに酸素原子および /"ま たは酸化されていてもよい硫黄原子を含有していてもよい 3〜1 0員の単環
または縮合した複素環」 と同じ意味を表わす。
「 R 2および R 3が結合する窒素原子と一緒になつて単環または縮合した複 素環を形成し、 ただし、 結合する窒素原子以外の複素環の構成原子は炭素原 子である」 とは、 例えば、 ピロール、 インドール、 イソインドール、 ベンゾ ァゼピン、 カルバゾール、 アタリジン、 アジリジン、 ァゼチジン、 ピロリン、 ピロリジン、 ジヒドロピリジン、 テトラヒドロピリジン、 ピぺリジン、 ジヒ ドロアゼピン、 テトラヒドロアゼピン、 パーヒドロアゼピン、 インドリン、 イソインドリン、 ジヒドロキノリン、 テトラヒドロキノリン、 パ^ "ヒドロキ ノリン、 ジヒドロイソキノリン、 テトラヒドロイソキノリン、 パ^ "ヒドロイ ソキノリン、 ジヒドロベンゾァゼピン、 テトラヒドロベンゾァゼピン、 ジヒ ドロカノレバゾーノレ、 テトラヒ ドロ力/レバゾ一/レ、 パーヒ ドロカノレノ ゾーノレ、 ジヒドロアクリジン、 テトラヒドロアクリジン等が挙げられる。
本発明においては、 特に指示しない限り異性体はこれをすベて包含する。 例えば、 アルキル基、 ァルケ-ル基、 アルキュル基、 アルキレン基、 ァルケ 二レン基、 アルキニレン基、 アルキリデン基等には直鎖のものおよぴ分枝鎖 のものが含まれる。 さらに、 二重結合、環、縮合環における異性体 (E、 Z、 シス、 トランス体) 、 不斉炭素の存在等による異性体 (R、 S体、 α、 配 置、ェナンチォマー、 ジァステレオマー) 、旋光性を有する光学活性体 (D、 L、 d、 1体) 、 クロマトグラフ分離による極性体 (高極性体、 低極性体) 、 平衡化合物、 回転異性体、 これらの任意の割合の混合物、 ラセミ混合物は、 すべて本発明に含まれる。
本発明においては、 特に断わらない限り、 当業者にとって明らかなように 記号 ..、、、、、、、^ は紙面の向こう側(すなわち α配置) に結合していることを表わ し、記号 は紙面の手前側 (すなわち J3配置) に結合していることを表 わし、 記号 は、 α配置と ]3配置の混合物であることを表わす。
[塩]
一般式 (1—0 ) で示される化合物の塩には、 非毒性塩や薬理学的に許容 される塩等すべてが含まれる。 薬理学的に許容される塩は毒性の少ない、 水 溶性のものが好ましい。 一般式 (1—0 ) で示される化合物の適当な塩とし て、 例えば、 アルカリ金属 (カリウム、 ナトリウム、 リチウム等) の塩、 ァ ルカリ土類金属 (カルシウム、 マグネシウム等) の塩、 アンモ-ゥム塩 (テ トラメチルアンモニゥム塩、 テトラプチルアンモ ウム塩等) 、 有機アミン (トリェチルァミン、 メチルァミン、 ジメチルァミン、 シク口ペンチルァミ ン、 ベンジノレアミン、 フエネチノレアミン、 ピペリ'ジン、 モノエタノ ノレアミ ン、 ジエタノールァミン、 トリス (ヒドロキシメチ /レ) メチノレァミン、 リジ ン、 アルギニン、 N—メチルー D—グルカミン等) の塩、 酸付加物塩 [無機 酸塩 (塩酸塩、 臭化水素酸塩、 ョゥ化水素酸塩、 硫酸塩、 リン酸塩、 硝酸塩 等) 、 有機酸塩 (酢酸塩、 トリフノレオ口酢酸塩、 乳酸塩、 酒石酸塩、 シユウ 酸塩、 フマル酸塩、 マレイン酸塩、 安息香酸塩、 クェン酸塩、 メタンスルホ ン酸塩、 エタンスルホン酸塩、 ベンゼンスルホン酸塩、 トルエンスルホン酸 塩、 イセチオン酸塩、 グルクロン酸塩、 ダルコン酸塩等) 等] が挙げられる。 さらに塩には、四級アンモ-ゥム塩も含まれる。四級アンモニゥム塩とは、 一般式 (I一 0 ) で示される化合物の窒素原子が、 R。基 (R °基は、 C l〜 8アルキル基、 フエニル基によって置換された C 1〜8アルキル基を表わ す。 ) によって四級化されたものを表わす。
また、 塩には N—ォキシドも含まれる。 本樂明化合物は任意の方法で N— ォキシドにすることができる。 N—ォキシドとは、 一般式 (1—0 ) で示さ れる化合物の窒素原子が、 酸化されたものを表わす。
一般式 (1—0 ) で示される化合物の適当な溶媒和物としては、 例えば、 水、 アルコ ^ル系溶媒 (例えば、 メタノール、 エタノール等) 等の溶媒和物 が挙げられる。 溶媒和物は非毒性かつ水溶性であることが好ましい。 また、 本発明化合物の溶媒和物には、上記本発明化合物のアル力リ (土類)金属塩、
アンモェゥム塩、 有機アミン塩、 酸付加物塩の溶媒和物も含まれる。
本発明化合物は、 公知の方法で上記の塩、 上記の溶媒和物に変換すること ができる。
[プロドラッグ]
一般式 (1—0 ) で示される化合物のプロドラッグは、 生体内において酵 素や胃酸等による反応により一般式 ( 1 - 0 ) で示される化合物に変換され る化合物をいう。 一般式 (I一 0 ) で示される化合物のプロドラッグとして は、 例えば一般式 (I一 0 ) で示される化合物がアミノ基を有する場合、 そ のァミノ基がァシル化、 アルキル化、 リン酸化された化合物 (例えば、 一般 式(Iー0 )で示される化合物のァミノ基がエイコサノイノレイ匕、ァラエル化、 ペンチルァミノカルボニル化、 ( 5—メチルー 2—ォキソ一 1 , 3—ジォキ ソレン一 4 Tル) メ トキシカルボニル化、 テトラヒドロフラニル化、 ピロ リジルメチル化、 ビバロイルォキシメチル化、 ァセトキシメチル化、 tert—ブ チノレ化された化合物等) ;一般式 (I一 0 ) で示される化合物が水酸基を有 する場合、 その水酸基がァシル化、 アルキル化、 リン酸化、 ホウ酸化された 化合物 (例えば、一般式(I一 0 ) で示される化合物の水酸基がァセチル化、 パルミ トイル化、 プロパノィル化、 ピバロ,ィル化、 サクシュル化、 フマリル 化、 ァラュル化、 ジメチルアミノメチルカルポ-ル化された化合物等) ;一 般式 (1—0 ) で示される化合物が力ルポキシ基を有する場合、 そのカルボ キシ基がエステル化、 アミド化された化合物 (例えば、 一般式 (1—0 ) で 示される化合物のカルボキシ基がェチルエステル化、 フェニルエステル化、 力ルポキシメチルエステル化、 ジメチルァミノメチルエステル化、 ビバロイ /レオキシメチノレエステノレ化、 ェトキシカノレポニノレオキシェチノレエステノレ化、 フタリジルエステル化、 (5—メチルー 2—ォキソ一 1, 3—ジォキソレン 一 4—イスレ) メチノレエステル化、 シクロへキシノレォキシ力/レポュルェチルェ ステル化、 メチルアミド化された化合物等) 等が挙げられる。 これらの化合
物は、 それら自体公知の方法によって製造することができる。 また、 一般式
( 1 - 0 ) で示される化合物のプロドラッグは水和物および非水和物のいず れであってもよい。 また、 一般式 (I一 0 ) で示される化合物のプロドラッ グは、 廣川書店 1990年刊 「医薬品の開発」 第 7巻 「分子設計」 163〜: 198頁に 記載されているような、 生理的条件で、 一般式 (I一 0 ) で示される化合物 に変化するものであってもよい。 さらに、 一般式 (1—0 ) で示される化合 物は同位元素 (例えば3 H、 1 4 C、 3 5 S、 1 2 5 I等) 等で標識されていてもよ い。
本発明の一般式 (I一 0 ) で示される化合物、 その塩、 その溶媒和物、 ま たはそれらのプロドラッグ (以下、 本発明化合物と略記することがある。 ) は、 溶解性および経口吸収性に優れ、 かつ長時間薬理活性が持続し、 しかも 薬物代謝酵素の阻害が弱く、 毒性も低い化合物である。 これらの性質は医薬 品として開発するにあたって要求される最も重要な物理的、 化学的、 薬学的 性質であり、 本発明化合物はこれらの条件を満たし、 大変優れた医薬品とな る可能性を有している [ザ 'メルク 'マニュアル ·ォプ ·ダイァグノゥシス · アンド'セラピー (第 1 7版) 、 メルク & C o . 出版 (The Merck Manual of Diagnosis and Therapy (17th Ed.), Merck & Co.) 参照] 。
本発明化合物が、 医薬品として有用であることは、 後述する各種実験系、 生 物学的実施例に記載の方法およびそれらを適宜改良して実施できる方法によ り評価することができる。 また、 本発明化合物が動態学的に、 例えば、 血中 半減期の長さ、 消化管内安定性、 経口吸収性、 パイォアベイラビリティ等の 点において優れているということは、 公知の方法、 例えば、 「薬物バイオア ベイラビリティ (評価と改善の科学) 」 、 現代医療社、 1998年 7月 6日発行 に記載の方法等によっても容易に評価することができる。
本発明の一般式 (1—0 ) において、 A 1 A B B 2、 D、 G、 E、 L、 J。が表わすそれぞれの定¾はいずれも好ましい。 以下に好ましい基を列
記するが、 ここで用いられる記号は全て前記と同じ意味を表わす。
A 1および A 2として、 好ましくは、 例えば、 塩基性基等であり、 より好ま しくは、 例えば、 置換基を有していてもよい含窒素複素環基等である。 ここ での 「含窒素複素環基」 として好ましくは、 例えば、 ピロ一ノレ、 イミダゾー ル、 トリァゾール、 ピラゾーノレ、 ピリジン、 ピラジン、 ピリミジン、 ベンゾ ィミダゾール、 ァザべンゾィミダゾーノレ、テトラヒ ドロキノリン環等であり、 より好ましくは、 例えば、 ィミダゾーノレ、 ベンゾィミダゾール環等であり、 特に好ましくは、 例えば、 イミダゾールー 2—ィル、 ベンゾイミダゾールー 2—ィル等である。 ここでの 「置換基」 としては、 例えば、 無置換または脂 肪族炭化水素基等が好ましく、 より好ましくは、 例えば、 無置換または C 1 〜 8アルキル基等であり、 特に好ましくは、 例えば、 無置換またはメチル基 等であり、 最も好ましくは、 無置換である。 A 1および A 2は、 同じでも異な つていてもよい。
B 1および B 2として、 好ましくは、 主鎖の原子数 1のスぺーサ一であり、 より好ましくは、 一 C O—、 一 S 0 2—、 置換基を有していてもよいメチレン 基(一 C H 2—) である。 ここでの「置換基」 としては、好ましくは、例えば、 無置換またはメチル基等であり、 より好ましくは、 無置換である。 B 1および B 2は、 同じでも異なっていてもよい。
Dとして好ましくは、 例えば、 窒素原子または置換基を有していてもよい 炭素原子等であり、 より好ましくは、 窒素原子である。
Gとして好ましくは、 例えば、 置換基を有していてもよい炭素原子、 カル ボ-ル基、 酸化されていてもよい硫黄原子等である。 ここでの 「置換基」 と しては、 好ましくは、 例えば、 無置換またはメチル基等であり、 より好まし くは、 無置換である。 Gとしてより好ましくは、 カルボュル基 (一C O—) 、 スルホ -ル基 (一 S 0 2—) 、 置換基を有していてもよいメチレン基である。 ここで、 「置換基を有していてもよいメチレン基」 における 「置換基」 とし
ては、 特に限定されず、 例えば、 A 1および A 2中の 「置換基」 として例示し たもの等が挙げられ、 これらの任意の置換基は置換可能な位置に 1〜 2個置 換していてもよい。 ただし、 「置換基を有していてもよいメチレン基」 は力 ルボエル基 (—C O—) を表わさない。
Eとして好ましくは、 例えば、 置換基を有していてもよい二価の炭素数 1 〜 4の脂肪族炭化水素基、 置換基を有していてもよい二価の 3〜 8員の単環 式環状基または置換基を有していてもよい二価の 9または 1 0員の多環式環 状基等であり、 より好ましくは、 置換基を有していてもよい二価の 3 ~ 8員 の単環式環状基または置換基を有していてもよい二価の 9または 1 0員の多 環式環状基である。 「置換基を有していてもよい二価の 3〜 8員の単環式環 状基」 は、 前記 B 1において定義したものと同じ意味を表わす。 ここでの 「3 〜 8員の単環式環状基 J として好ましくは、 C 5〜7の単環式炭素環 (前記 した C 3〜 8の単環式炭素環から炭素数が 5〜7のものが選択される。 ) 、 5〜 7員の単環式複素環 (前記した 3〜 8員の単環式複素環から環の員数が 5〜7のものが選択される。 ) であり、 より好ましくは、 例えば、 シクロべ ンタン、 シクロへキサン、 シクロへキセン、 シクロへキサジェン、ベンゼン、 ピリジン、 ピラジン、 ピリミジン、 ピリダジン、 ピぺリジン、 ピぺラジン環 等であり、 特に好ましくは、 ベンゼン環である。
「置換基を有していてもよい二価の 9または 1 0員の多環式環状基」 にお ける 「二価の 9または 1 0員の多環式環状基」 としては、 例えば 「9または 1 0員の多環式環状基」 から任意の 2個の水素原子を除いてできる二価基等 が挙げられる。 ここでの 「9または 1 0員の多環式環状基」 としては、 例え ば 「9または 1◦員の多環式炭素環」 、 「9または 1 0員の多環式複素環」 等が挙げられる。 「9または 1 0員の多環式炭素環」 には、 9または 1 0員 の多環式不飽和炭素環、 その一部または全部が飽和されている炭素環が含ま れる。 この 「9または 1 0員の多環式不飽和炭素環、 その一部または全部が
飽和されている炭素環としては、 例えば、 ァズレン、 ナフタレン、 パーヒ ド ロアズレン、 インデン、 パーヒドロインデン、 インダン、 ジヒドロナフタレ ン、 テトラヒドロナフタレン、 パーヒドロナフタレン環等が挙げられる。
「9または 1 0員の多環式複素環」 としては、例えば「ヘテロ原子として、 1〜 4個の窒素原子、 1〜 2個の酸素原子および/または 1〜 2個の硫黄原 子を含む 9または 1 0員の多環式複素環」 等が挙げられる。 ここで 「ヘテロ 原子として、 1〜 4個の窒素原子、 1〜 2個の酸素原子および Zまたは 1 〜 2個の硫黄原子を含む 9または 1 0員の多環式複素環」 には、 ヘテロ原子と して、 1〜 4個の窒素原子、 1〜 2個の酸素原子および Zまたは 1〜 2個の 硫黄原子を含む 9または 1 0員の多環式不飽和複素環、 その一部または全部 が飽和されている複秦環が含まれる。 この 「ヘテロ原子として、 1〜 4個の 窒素原子、 1〜 2個の酸素原子および /または 1〜 2個の硫黄原子を含む 9 または 1 0員の多環式不飽和複素環、 その一部または全部が飽和されている 複素環」 としては、 例えば、 インドール、 イソインドール、 インドリジン、 ベンゾフラン、 イソべンゾフラン、 ベンゾチォフェン、 イソベンゾチォフエ ン、 ジチアナフタレン、 ィンダゾール、 キノリン、 ィソキノリン、 キノリジ ン、 プリン、 フタラジン、 プテリジン、 ナフチリジン、 キノキサリン、 キナ ゾリン、 シンノリン、 ベンゾォキサゾ一/レ、 ベンゾチアゾー/レ、 ベンゾイミ ダゾーノレ、 クロメン、 ベンゾフラザン、 ベンゾチアジアゾーノレ、 ベンゾトリ ァゾーノレ、 インドリン、 イソインドリン、 ジヒドロべンゾフラン、 パ^ "ヒド 口べンゾフラン、ジヒドロイソベンゾフラン、 / ーヒドロイソベンゾフラン、 ジヒドロベンゾチォフェン、 ノ、。ーヒドロベンゾチォフェン、 ジヒドロイソべ ンゾチ才フェン、ノ、。ーヒドロイソベンゾチォフェン、ジヒドロインダゾーノレ、 パーヒ ドロインダゾーノレ、 ジヒドロキノリン、 テトラヒ ドロキノリン、 パー ヒドロキノリン、 ジヒドロイソキノリン、 テトラヒドロイソキノリン、 パー ヒドロイソキノリン、 ジヒドロフタラジン、 テトラヒドロフタラジン、 パー
ヒドロフタラジン、 ジヒドロナフチリジン、 テトラヒドロナフチリジン、 ノ、。 ーヒドロナフチリジン、ジヒドロキノキサリン、テトラヒドロキノキサリン、 パーヒドロキノキサリン、 ジヒドロキナゾリン、 テトラヒドロキナゾリン、 パーヒドロキナゾリン、 ジヒドロシンノリン、 テトラヒドロシンノリン、 パ ーヒドロシンノリン、 ベンゾォキサチアン、 ジヒドロべンゾォキサジン、 ジ ヒドロべンゾチアジン、 ピラジノモ /レホリン、ジヒドロベンゾォキサゾーノレ、 ハ°ーヒドロべンゾォキサゾ一ノレ、 ジヒドロべンゾチアゾーノレ、 ハ。ーヒドロべ ンゾチアゾーノレ、 ジヒドロべンゾィミダゾ一ノレ、 'パーヒドロべンゾィミダゾ ール環等が挙げられる。
ここでの 「9または 10員の多環式環状基」 として好ましくは、 9または 10員の多環式複素環基であり、 より好ましくは、 例えば、 テトラヒドロイ ソキノリン環が挙げられる。
「置換基を有していてもよい二価の 3〜8員の単環式環状基」 または 「置 換基を有していてもよい二価の 9または 10員の多環式環状基」 の 「置換基」 としては、 好ましくは、 例えば、 無置換、 ハロゲン原子またはメチル基等で あり、 より好ましくは、 無置換である。
Lとして好ましくは、例えば、主鎖の原子数 1〜 2のスぺーサ一等である。 ここでの 「主鎖の原子数 1~2のスぺーサ一」 として好ましくは一 O—、 一 S—、 一CO—、 一 so2—、 置換基を有していてもよい二価の窒素原子、 置 換基を有していてもよい二価の炭素数 1の脂肪族炭化水素基から任意に選択 される 1〜 2個からなる、 主鎖の原子が 1〜 2個連なっている二価基等であ り、 より好ましくは、 例えば一 CH2—、 一 0— CH2—、 一S— CH2—、 一 NH— CH2—、 一 CH2— CH2—、 一 CH=CH—、 一 C≡C―、 一 CH2 一 O—、一 CH2— S—、一 CH2— NH—、一 CONH—、一S02— NH—、 — NHCO—、 一 NHS02—等であり、 特に好ましくは、 例えば、 一 CH2 一、 一 CONH—、 一 CH2— NH—、 一 O— CH2—、 一 S— CH2—、 一 C
H2 - C H2 - (右側に J。が結合する) 等である。 また、 結合手も好ましい。 J 0として好ましくは、 塩基性基によって置換され、 さらに置換基を有して いてもよい脂肪族炭化水素基、 塩基性基によつて置換された脂肪族炭化水素 基によって置換され、 さらに置換基を有していてもよい環状基、 または塩基 性基によって置換された環状基によって置換され、 さらに置換基を有してい てもよい脂肪族炭化水素基である。 ここでの「塩基性基」 として好ましくは、 例えば、 モノーまたはジー置換アミノ基、 置換基を有していてもよい含窒素 複素環基等である。 ここでの 「モノーまたはジー置換アミノ基」 として好ま しくは、 ジ一置換アミノ基であり、 より好ましくは、 例えば、 ジメチルアミ ノ、 ジェチルァミノ、 ジプロピルァミノ、 ジブチルァミノ、 N—シクロへキ シル一 N—プロピルアミノ等であり、 特に好ましくは、 ジプロピルァミノ、 N—シクロへキシルー N—プロピルァミノである。 ここでの 「置換基を有し ていてもよい含窒素複素環基」 として好ましくは、 無置換、 または C l〜 8 アルキル基またはォキソ基で置換された含窒素複素環であり、 好ましい 「含 窒素複素環」 としては、 例えば、 ピロリジン、 ピぺリジン、 モルホリン、 チ オモルホリン、 パーヒドロジァゼピン、 テトラヒドロイソキノリン、 2, 8 ージァザスピロ [ 4 . 5 ] デカン、 1, 4 , 9一トリァザスピロ [ 5 . 5 ] ゥンデカン、 3, 9ージァザスピロ [ 5 . 5 ] ゥンデカン、 2, 9—ジァザ スピロ [ 5 . 5 ] ゥンデカン環等である。
ここでの 「塩基性基によって置換され、 さらに置換基を有していてもよい 脂肪族炭化水素基」 または 「塩基性基によって置換された環状基によって置 換され、 さらに置換基を有していてもよい脂肪族炭化水素基」 における 「月旨 肪族炭化水素基」 として好ましくは、 例えば、 C 1〜 8アルキル基、 C 2〜 8アルケニノレ基等であり、 より好ましくは、 例えば、 メチル、 ェチル、 プロ ピル、 プチル、 ペンチル、 へキシル等である。 ここでの 「塩基性基によって 置換された脂肪族炭化水素基によって置換され、 さらに置換基を有していて
もよい環状基」 における 「環状基」 として好ましくは、 例えば、 C 5~7の 単環式炭素環 (前記した C 3〜l 5の単環または多環式炭素環から炭素数が 5〜7のものが選択される。 ) 、 5〜7員の単環式複素環 (前記した 3〜1 5員の単環または多環式複素環から環の員数が 5〜 7のものが選択される。 ) 等であり、 より好ましくは、 例えば、 シクロペンタン、 シクロへキサン、 シ クロへキセン、 ァダマンチノレ、 シクロへキサジェン、 ベンゼン、 ピリジン、 ピラジン、 テトラヒドロピラン、 ピリミジン、 ピリダジン、 ピぺリジン、 ピ ペラジン環等である。 ここでの 「置換基」 としては、 好ましくは、 例えば、 無置換、 ハロゲン原子、 メチル基、 水酸基、 アミノ基またはォキソ基等であ り、 より好ましくは、 無置換である。
さらに J。として好ましくは、 「塩基性基を含有する基によって置換され、 さらに置換基を有していてもよい環状基」 、 「塩基性基を含有する基によつ て置換されていてもよく、 さらに置換基を有していてもよいスピロ環状基 J、 または 「塩基性基を含有する基によって置換されていてもよく、 さらに置換 基を有していてもよい架橋した環状基」 である。 ここでの 「環状基」 または 「スピロ環状基 J 、 または 「架橋した環状基」 として好ましくは、 (1) ス ピロ環状基、 (2) 架橋した多環式炭素環、 (3) 炭素原子、 酸素原子およ び Zまたは酸化されていてもよい硫黄原子からなる架橋した多環式複素環、
(4) 少なくとも一つの窒素原子を含有し、 さらに酸素原子および /または 酸化されていてもよい硫黄原子を含有していてもよい架橋した多環式複素環、
(5) C 3〜l 5の単環または縮合した炭素環、 (6) 炭素原子、 酸素原子 および Zまたは酸化されていてもよい硫黄原子からなる 3〜15員の単環ま たは縮合した複素環、 (7) 少なくとも一つの窒素原子を含有し、 さらに炭 素原子、 酸素原子および Zまたは酸化されていてもよい硫黄原子からなる 3 〜15員の単環または縮合した複素環等である。
「スピロ環状基」 として好ましくは、 2, 7—ジァザスピロ [3. 5] ノ
ナン、 2, 8—ジァザスピロ [4. 5] デカン、 2, 7—ジァザスピロ [4. 5] デカン、 2, 9—ジァザスピロ [5. 5] ゥンデカン、 2, 8—ジァザ スピロ [5. 5] ゥンデカン、 3, 9—ジァザスピロ [5. 5] ゥンデカン、 2, 7—ジァザスピロ [4. 4] ノナン、 1, 2—ジヒドロスピロ [インド 一ルー 3, 4,ーピペリジン] 、 2, 3—ジヒドロ一 1 H—スピロ [イソキノ リン一 4, 4,一ピぺリジン] 、 1,, 4,一ジヒドロ一 2Ή—スピロ [ピペリジ ンー 4, 3,一キノリン] 、 2,, 3,一ジヒドロー 1Ήースピロ [ピペリジン一 4, 4,一キノリン]、 8—ァザスピロ [4. 5]デカン、 8—ァザスピロ [4. 5] デカン、 7—ァザスピロ [4. 5] デカン、 3—ァザスピロ [5. 5] ゥンデカン、 2—ァザスピロ [5. 5] ゥンデカン、 1一ォキサ一 4, 8— ジァザスピロ [5. 5]ゥンデカン、 1一ォキサ一 4, 9ージァザスピロ [5. 5]ゥンデカン、 3, 4—ジヒドロスピロ [クロメンー 2, 4,ーピペリジン]、
2—ァザスピロ [4. 4] ノナン、 7—ァザスピロ [3. 5] ノナン、 2,
3—ジヒドロスピロ [インデンー 1, 4,一ピぺリジン] 、 3, 4ージヒドロ 一 2H—スピロ [ナフタレン一 1, 4'ーピペリジン] 、 3, 4—ジヒドロー
1H—スピロ [ナフタレン一 2, 4,ーピペリジン] 、 2—ァザスピロ [4.5] デカン、 2—ァザスピロ [3. 5] ノナン、 1,, 2'—ジヒドロスピロ [シク 口へキサン一 1, 3,一インドーノレ] 、 2,, 3,ージヒドロー 1Ήースピロ [シ クロへキサン一 1, 4,一イソキノリン] 、 1,, 4'ージヒドロー 2Ή—スピロ [シクロへキサン一 1, 3,一キノリン] 、 1, 6—ジァザスピロ [3. 4] オクタン、 1, 5—ジァザスピロ [3. 4] オクタン、 1, 7—ジァザスピ 口 [3. 5] ノナン、 1, 6—ジァザスピロ [3. 5] ノナン、 1, 5—ジ ァザスピロ [3. 5] ノナン、 1, 7—ジァザスピロ [4. 4] ノナン、 1, 6—ジァザスピロ [4, 4] ノナン、 1, 8—ジァザスピロ [4. 5] デカ ン、 1, 7—ジァザスピロ [4. 5] デカン、 2, 6—ジァザスピロ [3. 4] オクタン、 1, 6—ジァザスピロ [4. 5] デカン、 2, 6—ジァザス
2005/016066
ピロ [3. 5] ノナン、 1, 9ージァザスピロ [5. 5] ゥンデカン、 1, 8—ジァザスピロ [5. 5] ゥンデカン、 6—ァザスピロ [3. 5] ノナン、 6—ァザスピロ [3. 4] オクタン、 2—ァザスピロ [3. 4] オクタン、 1, 7—ジァザスピロ [5. 5] ゥンデカン、 1, 4, 9一トリァザスピロ [5. 5] ゥンデカン、 1, 3, 8—トリァザスピロ [4.5] デカン、 1— チア一 4, 9ージァザスピロ [5. 5] ゥンデカン、 1—チア一 4, 8—ジ ァザスピロ [5. 5] ゥンデカン、 スピロ [4. 4] ノナン、 スピロ [4. 5] デカン、 スピロ [5. 5] ゥンデカン、 スピロ [3. 4] オクタン、 ス ピロ [3. 5] ノナン等である。 「スピロ環状基」 としてより好ましくは、 2, 7—ジァザスピロ [3. 5] ノナン、 2, 8—ジァザスピロ [4. 5] デカン、 2, 7—ジァザスピロ [4. 5]デカン、 2, 9—ジァザスピロ [5. 5] ゥンデカン、 2, 8—ジァザスピロ [5. 5] ゥンデカン、 3, 9—ジ ァザスピロ [5. 5] ゥンデカン、 2, 7—ジァザスピロ [4. 4] ノナン、 1, 2—ジヒドロスピロ [インドールー 3, 4,一ピぺリジン] 、 2, 3—ジ ヒドロー 1H—スピロ [イソキノリン一 4, 4,ーピペリジン] 、 1,, 4,ージ ヒドロー 2Ή—スピロ [ピペリジン一 4, 3,一キノリン] 、 2,, 3,一ジヒド ロー 1Ήースピロ [ピペリジン一 4, 4,一キノリン]、 8—ァザスピロ [4. 5] デカン、 1—ォキサ一 4, 8—ジァザスピロ [5. 5] ゥンデカン、 1 —ォキサー 4, 9ージァザスピロ [5. 5] ゥンデカン、 3, 4—ジヒドロ スピロ [クロメンー 2, 4,ーピペリジン] 、 1, 6—ジァザスピロ [3. 4] オクタン、 1, 5—ジァザスピロ [3. 4] オクタン、 1, 7—ジァザスピ 口 [3. 5] ノナン、 1, 6—ジァザスピロ [3. 5] ノナン、 1, 5—ジ ァザスピロ [3. 5] ノナン、 1, 7—ジァザスピロ [4. 4] ノナン、 1, 6—ジァザスピロ [4. 4] ノナン、 1, 8—ジァザスピロ [4. 5] デカ ン、 1, 7—ジァザスピロ [4. 5] デカン、 2, 6—ジァザスピロ [3, 4] オクタン、 1, 6—ジァザスピロ [4. 5] デカン、 2, 6—ジァザス
P T/JP2005/016066
ピロ [3. 5] ノナン、 1, 9ージァザスピロ [5. 5] ゥンデカン、 1, 8—ジァザスピロ [5. 5] ゥンデカン、 1, 7—ジァザスピロ [5. 5] ゥンデカン、 1, 4, 9一トリァザスピロ [5. 5] ゥンデカン、 1, 3, 8—トリァザスピロ [4. 5]デカン、 1一チア一 4, 9ージァザスピロ [5. 5] ゥンデカン、 1一チア一 4, 8—ジァザスピロ [5. 5] ゥンデカン等 である。 「スピロ環状基」として特に好ましくは、 2, 7—ジァザスピロ [4. 5] デカン、 2, 8—ジァザスピロ [4. 5] デカン、 2, 8—ジァザスピ 口 [5. 5] ゥンデカン、 2, 9—ジァザスピロ ' [5. 5] ゥンデカン、 2, 7—ジァザスピロ [3. 5]ノナン、 1—ォキサ一 4, 9—ジァザスピロ [5. 5] ゥンデカンである。
「架橋した多環式炭素環」 として好ましくはビシクロ [2. 1. 1] へキ サン、 ビシクロ [2. 2. 1]ヘプタン、 ビシクロ [2. 2. 2] オクタン、 ビシクロ [3. 2. 1] オクタン、 ァダマンタン、 ビシクロ [3. 3. 1] ノナン、 ビシクロ [3. 2. 1] オクタン、 ビシクロ [3. 3. 2] デカン 等である。
「少なくとも一つの窒素原子を含有し、 さらに酸素原子および/または酸 化されていてもよい硫黄原子を含有していてもよい架橋した多環式複素環 J として好ましくは、 1一ァザトリシクロ [3. 3. 1. 13' 7] デカン、 3— ァザビシクロ [3. 3. 1] ノナン、 3, 7—ジァザビシクロ [3. 3. 1] ノナン等である。
「スピロ複素環を構成する環が、 少なくとも一つの窒素原子、 および炭素 原子からなる単環、 および/ /または少なくとも一つの窒素原子、 酸素原子一 つ、 および炭素原子からなる単環で構成される 7~1 5員の二環式のスピロ 複素環」 として、 好ましくは、 スピロ複素環を構成する環が、 少なくとも一 つの窒素原子、 および炭素原子からなる単環、 および/または少なくとも一 つの窒素原子、 酸素原子一つ、 および炭素原子からなる単環で構成される 9
〜11員の二環式のスピロ複素環等である。
「スピロ複素環を構成する環が、 少なくとも一つの窒素原子、 および炭素 原子からなる単環、 および Zまたは少なくとも一つの窒素原子、 酸素原子一 つ、 および炭素原子からなる単環で構成される 9~11員の二環式のスピロ 複素環」 として好ましくは、 2, 7—ジァザスピロ [4. 5] デカン、 2, 8—ジァザスピロ [4. 5] デカン、 2, 8—ジァザスピロ [5. 5] ゥン デカン、 2, 9ージァザスピロ [5. 5] ゥンデカン、 2, 7—ジァザスピ 口 [3. 5] ノナン、 1一ォキサ一 4, 9—ジ Tザスピロ [5. 5] ゥンデ カン等である。
「C3〜15の単環または縮合した炭素環」 として、 好ましくはシクロプ ロノ ン、 シクロブタン、 シク口ペンタン、 シクロへキサン、 シクロヘプタン、 シクロオクタン、 シクロペンテン、 シクロへキセン、 シクロヘプテン、 シク ロォクテン、 シクロペンタジェン、 シクロへキサジェン、 シクロヘプタジェ ン、 シクロォクタジェン、 ベンゼン、 ペンタレン、 パ一ヒドロペンタレン、 ァズレン、 パーヒドロアズレン、 インデン、 パーヒドロインデン、 インダン、 ナフタレン、 ジヒドロナフタレン、 テトラヒドロナフタレン、 ノ、。一ヒドロナ フタレン、 1, 2, 3, 5, 6, 7—へキサヒドロ一 s—インダセン等であ る。 より好ましくは、 シクロペンタン、 シクロへキサン、 シクロオクタンで ある。 最も好ましくはシクロへキサンである。
「炭素原子、 酸素原子および/または酸化されていてもよい硫黄原子から なる 3〜 15員の単環または縮合した複素環」 として好ましくは炭素原子、 酸素原子および Zまたは酸化されていてもょ 、硫黄原子からなる一部または 全部飽和されている 3〜15員の単環または縮合した複素環等である。
「少なくとも一つの窒素原子を含有し、 さらに炭素原子、 酸素原子および /または酸化されていてもよい硫黄原子からなる 3〜15員の単環または縮 合した複素環」 として好ましくは少なくとも一つの窒素原子を含有し、 さら
に炭素原子、 酸素原子および Zまたは酸化されていてもよい硫黄原子からな る、 一部または全部飽和されている 3〜1 5員の単環または縮合した複素環 等である。
環 1、 環 J 2、 環 J 3、 および環 J 4の 「置换基によって置換されていても よ V、」 の 「置換基」 として好ましくは、 脂肪族炭化水素基、 環状基、 環状基 によって置換された脂肪族炭化水素基等であり、 より好ましくは、 炭素数 1 〜 8の脂肪族炭化水素基、 C 3〜 1 0の単環または二環式炭素環である。 環 J 2、環 J 3、および環 J 4の「塩基性基を含有する基によって置換され」、 または 「塩基性基によって置換されていてもよい」 の 「塩基性基を含有する 置換基』 として好ましくは、 例えば、 モノーまたはジー置換アミノ基、 置換 基を有していてもよい含窒素複素環基等である。 ここでの 「モノーまたはジ —置換アミノ基」 として好ましくは、 ジー置換アミノ基等であり、 より好ま しくは、 例えば、 ジメチルァミノ、 ジェチルァミノ、 ジプロピルァミノ、 ジ プチルァミノ、 N—シク口へキシルー N—プロピルアミノ等であり、 特に好 ましくは、 ジプロピルァミノ、 N—シクロへキシルー N—プロピルァミノで ある。
Rとして好ましくは、 例えば、 モノーまたはジー置換アミノ基、 置換基を 有していてもよい含窒素複素環基等である。 ここでの 「モノ一またはジ一置 換ァミノ基」 として好ましくは、 ジー置換アミノ基等であり、 より好ましく は、 例えば、 ジメチルァミノ、 ジェチルァミノ、 ジプロピルァミノ、 ジブチ ルァミノ、 N—シクロへキシルー N—プロピルアミノ等であり、 特に好まし くは、ジプロピルァミノ、 N—シクロへキシルー N—プロピルァミノである。 本発明においては、先に列挙した好ましい基の組み合わせを含む一般式( I —0 ) の化合物が好ましい。
一般式 (I一 0 ) で示される化合物のうち、 好ましい化合物としては、 一 般式 (I一 1 )
(式中、 すべての記号は、 前記と同じ意味を表わす。 ) 、
一般式 (1—2)
(式中、 すべての記号は、 前記と同じ意味を表わす。 ) 、
一般式 (I一 3)
(式中、 環 A
1Aおよび環 A
2Aはそれぞれ独立して置換基を有していてもよい 含窒素複素環基を表わし; B
1 A、 B
2 Aおよび G
Aはそれぞれ独立して一 C O—、 — S0
2—または一 CH
2—を表わし;環 E
Aは置換基を有していてもよい二価 の 3〜 8員の単環式環状基または置換基を有していてもよい二価の 9または 10員の多環式環状基を表わし、 その他の記号は前記と同じ意味を表わす。 ただし、 B
1Aおよび G
Aのいずれかは一 CO—または一 S0
2—を表わす。 )、 一般式 ( I一 5— 1 )
(式中、 すべての記号は前記と同じ意味を表わす。 ) 、
一般 — 5— 2 )
(式中、 すべての記号は前記と同じ意味を表わす。 ) 、
一般式 ( I一 5— 3 )
(式中、 すべての記号は前記と同じ意味を表わす。 )
一般式 (I—5— 4 )
(式中、 全ての記号は前記と同じ意味を表わす。 )
一般式 ( I一 6 )
(式中、 全ての記号は 記と同じ意味を表わす。 ) 、 一般式 (I一 7 )
(式中、 全ての記号は前記と同じ意味を表わす。 ) 、 一般式 ( I一 8— 1 )
(式中、 全ての記号は前記と同じ意味を表わす。 ) 、 一般式 (I一 8— 2 )
(式中、 全ての記号は前記と同じ意味を表わす。 ) 一般式 (1—8— 3 )
(式中、 全ての記号は前記と同じ意味を表わす。 ) 、
一般式 (I一 8— 4 )
(式中、 全ての記号は前記と同じ意味を表わす。 ) 、
一般式 ( I一 8— 5 )
(式中、 全ての記号は前記と同じ意味を表わす。 ) 、
一般式 ( I一 8— 6 )
(式中、 全ての記号は前記と同じ意味を表わす。 ) 、
一般式 (I一 8— 7 )
(式中、 全ての記号は前記と同じ意味を表わす。 ) 、 一般式 (I一 9一 2)
(式中、 全ての記号は前記と同じ意味を表わす。 ) 、 一般式 (1—9— 3)
(式中、 全ての記号は前記と同じ意味を表わす。 ) 、 一般式 (1— 9— 4)
(式中、 全ての記号は前記と同じ意味を表わす。 ) 、
(式中、 全ての記号は前記と同じ意味を表わす。 )
で示される化合物、 その塩、 その N—ォキシド体もしくはその溶媒和物また はそれらのプロドラッグ等が挙げられる。
一般式 (1 -0) で示される化合物のうち、 さらに好ましい化合物として は、 一般式 ( I一 4一 1 a )
(式中、 全ての記号は前記と同じ意味を表わす。 ) 、
一般式 (I— 4一 l b)
(式中、 全ての記号は前記と同じ意味を表わす。 ) 、 一般式 (I一 4一 2)
(式中、 全ての記号は前記と同じ意味を表わす。 ) 、 一般式 ( I— 4一 3 a )
(式中、 全ての記号は前記と同じ意味を表わす。 ) 、 一般式 (I一 4一 3 b)
(式中、 全ての記号は前記と同じ意味を表わす。 ) 、 一般式 (I一 4一 4)
05 016066
(式中、 全ての記号は前記と同じ意味を表わす。 ) 、
一般式 ( I— 4一 6 )
(式中、 全ての記号は前記と同じ意味を表わす。 ) 、
一般式 ( I一 8— 1 )
(式中、 全ての記号は前記と同じ意味を表わす。 ) 、 または
(式中、 全ての記号は前記と同じ意味を表わす。 ) 、 で示される化合物、 そ の塩、 その N—ォキシド体もしくはその溶媒和物またはそれらのプロドラッ グ等が挙げられる。
環 J 2bの置換基としては R1が好ましい。 .
R1として好ましくは、 水素原子、 脂肪族炭化水素基、 環状基、 環状基によ つて置換された脂肪族炭化水素基等である。 R 1で表わされる脂肪族炭化水素 基して好ましくは、 C 1~8アルキル基等である。 R1で表わされる環状基し て好ましくは、 C 3〜 15の単環または多環式不飽和炭素環、 その一部また は全部が飽和されている炭素環等である。 より好ましくは、 C3〜8の単環 飽和炭素環等であり、 特に好ましくは、 シクロプロパン、 シクロブタン、 シ クロペンタン、 シクロへキサン、 シクロヘプタンである。 環状基によって置 換された脂肪族炭化水素基等の 「環状基」 として好ましくは、 チォフェンで ある。
R2または R3として好ましくは、 水素原子、 脂肪族炭化水素基、 環状基、 または環状基によって置換された脂肪族炭化水素基が挙げられる。 R 2または R 3で表わされる脂肪族炭化水素基として好ましくは、 C 1〜8アルキル基等 である。 R2または R3で表わされる環状基、 または環状基によって置換され た脂肪族炭化水素基の 「環状基」 として好ましくは、 C 3〜15の単環また は多環式不飽和炭素環、 その一部または全部が飽和されている炭素環等であ る。 R2または R3で表わされる環状基、 または環状基によって置換された脂 肪族炭化水素基の 「環状基」 としてより好ましくは、 C3~8の単環飽和炭 素環等であり、 特に好ましくはシクロプロパン、 シクロブタン、 シクロペン タン、 シクロへキサン、 シクロヘプタンである。
R 2および R 3が結合する窒素原子と一緒になつて形成する置換基を有して いてもよい複素環の 「複素環」 として好ましくは、 少なくとも一つの窒素原 子を含有し、 さらに酸素原子おょぴ/または酸化されていてもよい硫黄原子 を含有していてもよい 3〜1 5員の単環または縮合した複素環である。 より 好ましくは、 少なくとも一つの窒素原子を含有し、 さらに酸素原子および Z または酸化されていてもよい硫黄原子を含有していてもよい 3〜1 5員の単 環または縮合した複素環のうち、 一つの窒素原子と炭素原子からなるものが 選択される。 特に好ましくは、 ピロリジン、 ピぺ'リジン、 パーヒドロアゼピ ン、 テトラヒドロイソキノリン、 テトラヒドロキノリン、 パーヒドロイソキ ノリン等である。
R 4として好ましくは、 水素原子、 脂肪族炭化水素基、 置換基で置換された 脂肪族炭化水素基等である。 R 4で表わされる置換基で置換された脂肪族炭化 水素基の置換基として好ましくは、 水酸基である。 脂肪族炭化水素基、 置換 基で置換された脂肪族炭化水素基の 「脂肪族炭化水素基」 として好ましくは C 3〜 8の脂肪族炭化水素基等である。
本 明の具体的な化合物としては、 例えば、 以下の (1 ) 〜 (6 4 ) で示 された化合物、 実施例に記載した化合物、 その塩、 その N—ォキシド体もし くはその溶媒和物またはそれらのプロドラッグ等が挙げられる。
( 1 ) N- [ 4 - ( { [ 4 - (ジイソプロピルァミノ) プチル] アミノ} メ チル) ベンジル] 一 N— (1 H—イミダゾールー 2—ィルメチル) 一 1 H— イミダゾール一 2—カルボキシアミド; (2 ) 4— ( { [ 4一 (ジイソプロ ピルァミノ) ブチル] ァミノ) メチル) 一 N, N—ビス (1 H—イミダゾー ルー 2—ィルメチル) ベンゼンスルホンアミ ド; (3 ) N— [ 4一 ( { [ 4 一 (ジイソプロピルァミノ) ブチル] アミノ} メチル) ベンジル] -N- ( 1 H—ィミダゾーノレ一 2一ィルメチル) 一 1 H—ィミダゾーノレ一 2ースノレホン アミド; (4 ) N 1 - [ 4一 (ジイソプロピルァミノ) プチル] 一 N4, N4—
ビス ( 1 H—ィミダゾールー 2—イノレメチル) テレフタノレアミ ド; (5) N5 - [4- (ジイソプロピルァミノ) プチノレ] 一 N2, N2—ビス (1H—イミ ダゾーノレ一 2—ィルメチル) ピリジン一 2, 5—ジカルポキシァミド; ( 6 ) N2— [4一 (ジイソプロピルァミノ).プチル] — N5, N5—ビス (1H—ィ ミダゾール一 2—^ fルメチル) ピリジン一 2, 5ージカルポキシァミ ド; ( 7 ) N2— [4— (ジイソプロピルァミノ) ブチル] 一 N5, N5—ビス (1H—ィ ミダゾ一ルー 2—ィルメチル) ピラジン一 2, 5—ジカルボキシアミド; (8) N5- [4一 (ジイソプロピノレアミノ) プチル] -N2, N2—ビス (1H—ィ ミダゾール一 2—ィルメチル) ピリミジン一 2 , 5ージカルポキシァミ ド; (9) N2— [4一 (ジイソプロピルァミノ) プチル] 一 N5, N5—ビス (1 H—ィミダゾールー 2—ィルメチル) ピリミジン一 2 , 5ージカルポキシァ ミ ド; (10) N2— [4— (ジイソプロピルァミノ) プチノレ] 一 N5, N5— ビス (1H—イミダゾール一 2—ィルメチル) 一 1H—ピロ一ルー 2, 5— ジカルポキシァミド; (11) N2— [4— (ジィソプロピルァミノ) プチル] 一 N5, N5—ビス (1 H—イミダゾールー 2—ィルメチル) 一 1H—イミダ ゾールー 2, 5—ジカルボキシアミ ド; (12) N5— [4— (ジイソプロピ ルァミノ) プチル] 一 N2, N2—ビス (1H—イミダゾールー 2—ィルメチ ル) 一 1 H f ミダゾーノレ一 2, 5ージカノレポキシァミ ド; (13) N5— [4 一 (ジイソプロピルァミノ) プチル] — N2, N2—ビス (1H—イミダゾー ノレ一 2—ィルメチル) 一1, 3—ォキサゾールー 2, 5—ジカルボキシアミ ド; (14) N2— [4— (ジイソプロピルァミノ) ブチル] — N5, N5—ビ ス (1H—イミダゾールー 2—^ fルメチル) 一1, 3—ォキサゾールー 2, 5—ジカルボキシアミ ド; (15) N2— [4— (ジイソプロピルァミノ) ブ チル] —N5, N5—ビス (1H—イミダゾールー 2—ィルメチル) 一1, 3 一チアゾールー 2, 5—ジカルポキシアミド; (16) N5— [4一 (ジイソ プロピルァミノ) ブチル] 一 N2, N2—ビス (1H—イミダゾールー 2—ィ
ルメチル) _ 1, 3—チアゾールー 2 , 5—ジカノレポキシァミ ド; (17) N2— [4— (ジイソプロピルァミノ) プチル] — N5, N5—ビス (1H—ィ ミダゾ一ノレ一 2—ィルメチル) チォフェン一 2, 5—ジカルポキシアミ ド ;
(18) N2— [4— (ジィソプロピノレアミノ) プチル] 一 N5, N5—ビス (1 H—イミダゾール一 2—ィルメチル) フラン一 2, 5ージカルボキシァミ ド;
(19) N2- [4一 (ジイソプロピルァミノ) プチル] — N5, N5—ビス (1 H—ィミダゾ一ルー 2—ィルメチル) 一 1, 3 , 4一ォキサジァゾ一ルー 2 , 5—ジカルボキシアミド; (20) N3— [4— ' (ジイソプロピルァミノ) ブ チル] — N5, N5—ビス (1H—イミダゾールー 2—ィルメチル) 一 1, 2, 4一ォキサジァゾ一ルー 3, 5—ジカルポキシアミド; (21) N3— [4— (ジイソプロピルァミノ) プチル] 一 N5, N5—ビス (1H—イミダゾール 一 2—イノレメチル) 一 1, 2, 4—チアジアゾールー 3, 5—ジカノレポキシ アミド; (22) N5- [4一 (ジイソプロピルァミノ) ブチル] —N3, N3 一ビス (1H—イミダゾールー 2—ィルメチル) 一 1, 2, 4ーォキサジァ ゾール一3, 5—ジカルポキシアミド; (23) N5— [4一 (ジイソプロピ ルァミノ ) プチル] 一 N 3 , N 3—ビス ( 1 H—イミダゾールー 2—イノレメチ ル) 一1, 2, 4ーチアジアゾーノレ一 3, 5—ジカノレポキシアミ ド; (24) N2- [4- (ジイソプロピルァミノ) プチル] -N5, N5—ビス (1H—ィ ミダゾーノレ一 2—ィルメチノレ) 一 1 , 3, 4ーチアジアゾールー 2, 5—ジ カルボキシアミ ド; (25) 4- ( { [4一 (ジイソプロピルァミノ) プチ ル] ァミノ) スルホニル) 一 N, N—ビス (1H—イミダゾールー 2—ィル メチル) ベンズァミド; (26) 4一 { [5- (ジィソプロピルァミノ) ぺ ンチル] スルファニル } — N, N—ビス (1H—イミダゾールー 2—ィルメ チル) ベンズアミド; (27) 4— { [5— (ジイソプロピルァミノ) ペン チル] ォキシ } 一 N, N—ビス (1 H—イミダゾールー 2—ィルメチル) ベ ンズアミド; (28) 4— { [5— (ジイソプロピルァミノ) ペンチル] ァ
ミノ) 一 N, N—ビス (1H—イミダゾーノレ一 2—イノレメチノレ) ベンズアミ ド; (29) 4— [ (1 E) —6— (ジイソプロピルァミノ) へキサー 1一 ェニノレ] -N, N—ビス (1H—イミダゾール一 2—^ fルメチル) ベンズァ ミ ド; (30) 4— { [5- (ジイソプロピルァミノ) ペンタノィル] アミ ノ} 一 N, N—ビス ( 1 H—イミダゾールー 2—ィルメチル) ベンズアミ ド;
(31) 4— ( { [4- (ジイソプロピルァミノ) プチル] スルホュル } ァ ミノ) 一 N, N—ビス (1 H—イミダゾーノレ一 2 fノレメチノレ) ベンズアミ ド; (32) 4— ( { [4一 (ジイソプロピルアミノ) ブチル] スルファニ ル} メチル) — N, N—ビス (1 H—ィミダゾ一ルー 2一^ fルメチル) ベン ズアミ ド; (33) 4— { [4一 (ジイソプロピルァミノ) ブトキシ] メチ ノレ } 一 N, N—ビス (1H—イミダゾ一/レー 2—^ /レメチノレ) ベンズアミ ド;
(34) 4— { [5— (ジイソプロピルァミノ) ペンチル] スルホ二ル} 一 N, N—ビス (1H—イミダゾール一 2—ィルメチル) ベンズアミ ド; (3
5) 4— ( { [4— (ジイソプロピルァミノ) プチル] スルホ二ル} メチル) 一 N, N—ビス (1H—イミダゾールー 2—ィルメチル) ベンズアミ ド; (3
6) 4— [6— (ジィソプロピノレアミノ) 一 2—ォキソへキシル] 一 N, N ―ビス ( 1 H—ィミダゾール一 2—ィルメチル) ベンズァミ ド; (37) 4 一 [6 - (ジイソプロピノレアミノ) へキサー 1ーィニル] 一 N, N—ビス (1 H—イミダゾーノレ一 2—イノレメチノレ) ベンズアミ ド; (38) N— [4— (ジ イソプロピルァミノ) プチル] 一 4— [3— (1H—イミダゾール一 2—ィ ル) 一2— (1 H—イミダゾールー 2—ィルメチル) プロパノィル] ベンズ アミ ド; (39) N— [4— (ジイソプロピルァミノ) プチル] —4一 [3 一 (1H—イミダゾール一 2 fル) 一 2— (1H—イミダゾールー 2—ィ ルメチル) プロピル] ベンズアミ ド; (40) N— [4一 (ジイソプロピル ァミノ) プチル] 一 4— { [2— (1H—イミダゾールー 2—ィル) 一 1一 ( 1 H—イミダゾールー 2—ィルメチル) ェチル] スルホ二ル} ベンズァミ
ド; (41) N— [4一 (ジイソプロピルァミノ) プチル] — 4一 [2- (1 H—イミダゾール一 2—ィノレ) 一1— (1H—イミダゾールー 2—ィルメチ ノレ) エトキシ] ベンズアミ ド; (42) N- [4一 (ジイソプロピルァミノ) プチル] -4- { [2— (1H—イミダゾールー 2 fル) 一 1— (1H— イミダゾールー 2—ィルメチル) ェチル] スルフ了二ル} ベンズァミ ド; (4 3) N- [4- (ジイソプロピルァミノ) プチル〕 一 4一 { [2— (1H— イ ミダゾ一/レー 2—ィノレ) 一1— (1 H—イ ミダゾーノレ一 2—イノレメチノレ) ェチル] ァミノ) ベンズアミ ド; (44) N- 〔4一 (ジイソプロピルアミ ノ) プチル] -4- [3— (1H—イミダゾールー 2—ィル) 一 2— (1H ーィミダゾールー 2一ィルメチル) プロパー 1—ェニル] ベンズァミ ド; (4 5.) N1— [4- (ジイソプロピルァミノ) プチル] — N4, N4—ビス (1H 一イミダゾールー 2—ィルメチル) シクロへキサン一 1, 4ージカルポキシ アミ ド; (46) N1- [4- (ジイソプロピルァミノ) ブチル] — N3, N3 一ビス (1 H f ミダゾール一 2—ィルメチル) ィソフタルアミ ド; (47) N— [4— ( { [4一 (ジイソプロピルァミノ) ブチル] アミノ} メチル) ベンジル] — N— (1 H—イミダゾールー 2—ィルメチル) 一 1H—イミダ ゾール一2—カルボキシアミ ド; (48) N1, N1—ビス (1H—ベンゾィ ミダゾ一ルー 2—ィルメチル) 一 N4— [4- (ジイソプロピルァミノ) ブチ ノレ] テレフタルアミ ド; (49) N1— [4— (ジイソプロピルァミノ) プチ ノレ] —N4— (1H—イミダゾール一 2—ィルメチル) ^N4— [ (1ーメチ ル一1H—イミダゾールー 2—ィル) メチル] テレフタルアミ ド; (50) N1- [4一 (ジイソプロピルァミノ) プチル] — N4, N4—ビス [ (1ーメ チル一 1 H (ミダゾールー 2—ィノレ) メチノレ] テレフタノレアミ ド; (51) N1— [4- (ジイソプロピルァミノ) プチル] 一 N4— (1H—イミダゾー ルー 2—ィルメチル) 一 N4— (ピリジン一 2—ィルメチル) テレフタルアミ ド; (δ Ζί Ν1— [4— (ジイソプロピルァミノ) プチル] — Ν4, Ν4—ビ
ス (ピリジン一 2—^ fルメチル) テレフタノレアミ ド; (53) N1— [4一 (ジ イソプロピルァミノ) ブチル] — N4— (1H—イミダゾールー 2—ィルメチ ル) 一 N4— (5, 6, 7, 8—テトラヒ ドロキノリン一 8—ィル) テレフタ ルァミ ド; (54) N1— (1 H—べンゾィミダゾールー 2—^ fルメチル) 一 N4— [4— (ジイソプロピルァミノ) ブチル] 一 N1— (5, 6, 7, 8— テトラヒ ドロキノリン一 8—^ I レ) テレフタルアミ ド; (55) N1— {3— [ (ジイソプロピルァミノ) メチノレ] フエ二ル} 一 N4, N4—ビス (1H— ィミダゾールー 2—イノレメチル) テレフタルァミ ド; ( 56 ) N 1— [ 3— (ジ イソプロピルァミノ) ベンジル] 一 N4, N4—ビス (1H— ^ f ミダゾ一ルー 2—ィルメチル) テレフタルアミ ド; (57) N1- { 3 - [ (ジイソプロピ ルァミノ) メチル] シクロへキシル } -N4, N4—ビス (1H—イミダゾー ルー 2—^ルメチル) テレフタルアミ ド; (58) N1- { [3— (ジイソプ 口ピルアミノ) シクロへキシル] メチル } — N4, N4—ビス (1H—イミダ ゾール一2—ィルメチル) テレフタルアミ ド; (59) N1— [4一 (ジメチ ルァミノ) プチル] 一 N4, N4—ビス (1 H—イミダゾールー 2—ィルメチ ル) テレフタルアミ ド; (60) N1- [4一 (ジェチルァミノ) プチル] 一 N4, N4—ビス (1H—イミダゾールー 2—ィルメチル) テレフタルアミ ド; (61) N1, N1—ビス (1 H—イミダゾーノレ一 2—イノレメチノレ) 一N4—(4 一ピロリジン一 1ーィルプチル) テレフタルアミ ド; (62) N1, N1—ビ ス (1 H—イミダゾール一 2—ィルメチル) 一 N4— (4—ピぺリジン一 1一 ィルプチル) テレフタルアミ ド; (63) 4— { [ [4一 (ジイソプロピル ァミノ) プチル] (メチル) ァミノ] メチル } — N, N—ビス (1H—イミ ダゾ一/レー 2—イノレメチノレ) ベンズアミ ド; (64) N- [4一 ( { [4一 (ジイソプロピノレアミノ) プチノレ] アミノ} カルボニル) ベンジル] 一 N— (1H—イミダゾール一 2—ィルメチル) ピリジン一 2—カルボキシアミ ド、 その塩、 その N—ォキシド体もしくはその溶媒和物またはそれらのプロドラ
ッグ等が挙げられる。
さらに好ましい化合物としては、 実施例に記載された化合物、 その塩、 そ の N—ォキシド体もしくはその溶媒和物またはそれらのプロドラッグ等が挙 げられる。
特に好ましい化合物としては、 例えば、 (1) 4一 [ ( {トランス一 4一 [シク口へキシル (プロピル) ァミノ] シクロへキシル } ァミノ) メチル]
— N, N—ビス (1H—イミダゾールー 2—ィルメチル)ベンズアミ ド; (2) 4一 [ (2—シクロへキシルー 2, 8—ジァザズピロ [4. 5] デカー 8— ィル) メチル] 一 N, N—ビス (1H—イミダゾールー 2—ィルメチル) ベ ンズアミド; (3) 4— [ (8—シクロへキシルー 2, 8—ジァザスピロ [4. 5] デカー 2—ィル) メチル] — N, N—ビス (1H—イミダゾールー 2— ィルメチル) ベンズアミ ド; (4) 4一 [ (2—シクロへキシル一 2, 8— ジァザスピロ [4. 5] デカ一 8—ィル) メチル] 一 N, N—ビス (1H— イミダゾールー 2—ィルメチノレ) ベンズアミド; (5) 4— [ (8—シクロ へキシルー 2, 8—ジァザスピロ [4. 5]デカー 2—ィル) メチル] 一 N, N—ビス (1 H—イミダゾールー 2—ィルメチル) ベンズアミド; (6) 4 一 [ (7—シクロへキシルー 2, 7—ジァザスピロ [4. 5] デカー 2—ィ ル) メチル〕 一 N, N—ビス (1H—イミダゾールー 2—ィルメチル) ベン ズアミ ド; (7) 4- [ (7—シクロへキシルー 2, 7—ジァザスピロ [4. 4] ノナ一 2—ィル) メチル] 一 N, N—ビス (1H—イミダゾールー 2— ィルメチル) ベンズアミ ド; (8) 4— [ (9ーシクロへキシルー 3, 9- ジァザスピロ [5. 5] ゥンデカー 3—^ル) メチノレ] 一 N, N—ビス (1 H—イミダゾーノレ一 2—イノレメチノレ) ベンズアミ ド; (9) 4一 { [8— (シ ク口へキシノレメチル) 一 2, 8ージァザスピロ [4. 5] デカ一 2—ィル] メチル } — N, N—ビス (1 H—イミダゾールー 2—ィルメチル) ベンズァ ミド; (10) 4— { [8— (シクロプロピルメチル) 一 2, 8—ジァザス
ピロ [4. 5] デカー 2—ィル] メチノレ } 一 N, N—ビス (1H—イミダゾ 一ノレ一 2—イノレメチノレ) ベンズアミ ド; (11) 4— { [8— (シクロペン チルメチル) —2, 8—ジァザスピロ [4. 5] デカ一 2—ィル] メチル } 一 N, N—ビス (1H—イミダゾールー 2—ィルメチル) ベンズアミ ド; (1 2) N, N—ビス (1H—イミダゾールー 2—ィルメチル) 一 4一 { [8— (2—チェュルメチル) 一2, 8—ジァザスピロ [4. 5] デカー 2—ィル] メチル } ベンズァミド; (13) N, N—ビス (1H—イミダゾールー 2— イノレメチル) -4- { [8 - (3—チェ二ルメ ル) -2, 8—ジァザスピ 口 [4. 5] デカー 2—ィル] メチル } ベンズアミド; (14) 4— { [8 一 (3—フルォロベンジル) —2, 8—ジァザスピロ [4. 5] デカ一 2— ィル] メチル } -N, N—ビス (1 H—イミダゾーノレ一 2—イノレメチノレ) ベ ンズアミ ド; (15) 4— { [8 - (4一フルォロベンジル) —2, 8—ジ ァザスピロ [4. 5] デカー 2—ィル] メチル } -N, N—ビス (1H—ィ ミダゾ一ルー 2—^ Tルメチル) ベンズアミド; (16) N— (1H—べンゾ イミダゾールー 2—ィルメチル) 一 4一 [ (8—シクロへキシノレ一 2, 8 - ジァザスピロ [4. 5] デカー 2—ィル) メチル] 一 N— (1H—イミダゾ 一ルー 2—ィルメチル) ベンズアミ ド; (17) N— (1H—べンゾイミダ ゾ一/レー 2—イノレメチノレ) 一 N— {4- [ (8—シクロへキシノレ一 2, 8— ジァザスピロ [4. 5] デカ一 2—ィル) メチル] ベンズ y 1 } — 1H—ィ ミダゾ一ルー 2—力ルポキサミド; (18) 4- [ (8—シクロペンチルー 2, 8—ジァザスピロ [4. 5] デカー 2—ィル) メチル] 一 N, N—ビス (1 H—イミダゾールー 2—ィルメチル) ベンズアミ ド; (19) N, N— ビス (1H— ^ f ミダゾール一 2—ィルメチル) -4- { [8— (2—ナフチ ルメチル) 一 2, 8-ジァザスピロ [4. 5] デカー 2—ィル] メチル } ベ ンズアミド; (20) 4— [ (8—シクロへプチルー 2, 8—ジァザスピロ [4. 5] デカー 2—ィル) メチル] 一 N, N—ビス (1H—イミダゾール
一 2—^ fルメチル) ベンズアミド; (21) 4— { [8— (2, 3—ジヒド ロー 1H—^ ンデン一 2—ィル) -2, 8—ジァザスピロ [4. 5] デカー 2一ィル] メチル } 一 N, N—ビス (1H—イミダゾール一 2—ィルメチル) ベンズアミド; (22) 4— [ (8—シクロブチノレー 2, 8—ジァザスピロ [4. 5] デカー 2—ィル) メチル] 一 N, N—ビス (1 H—イミダゾーズレ 一 2—ィルメチル) ベンズアミド; (23) N, N—ビス (1H—イミダゾ 一グレー 2—/ I レメチノレ) 一 4一 [ (8—イソプチノレ一 2, 8—ジァザスピロ [4. 5] デカー 2—ィル) メチノレ] ベンズアミ'ド; (24) 4— [ (2- シクロへキシルー 2, 8—ジァザスピロ [4. 5] デカー 8—ィル) メチル] — N, N—ビス (1 H—イミダゾールー 2—ィルメチル) 一 2—メチルベン ズァミ ド; (25) N, N—ビス (1H—イミダゾールー 2—ィルメチル) 一 4一 { [8— (3—メチルー 2—プテン一 1ーィノレ) 一 2, 8—ジァザス ピロ [4. 5] デカー 2—ィル] メチル } ベンズァミ ド; (26) 4— { [8 一 (2—ェチルプチル) —2, 8—ジァザスピロ [4. 5] デカ— 2—ィル] メチル } 一 N, N—ビス (1 H (ミダゾールー 2—ィルメチル) ベンズァ ミド; (27) N, N—ビス (1 H—イミダゾールー 2—ィルメチル) 一 4 一 ( { 8— [ ( 3—メチル一 2—チェエル) メチル] 一 2, 8—ジァザスピ 口 [4. 5] デカー 2—ィル } メチル) ベンズアミ ド; (28) 4— { [8 一 (1一ェチルプロピル) 一2, 8—ジァザスピロ [4. 5] デカー 2—ィ ル] メチル } 一 N, N—ビス (1H—イミダゾールー 2—ィルメチル) ベン ズアミ ド; (29) N, N—ビス (1H— ^ f ミダゾ一ルー 2—ィルメチル) 一 4一 ( {8- [ (5—メチルー 2—チェエル) メチル] —2, 8—ジァザ スピロ [4. 5]デカ一 2—ィル } メチノレ) ベンズアミ ド; (30) 4— ( {8 一 [ (5—クロロー 2—チェニル) メチノレ] —2, 8—ジァザスピロ [4. 5] デカー 2—ィル } メチル) 一 N, N—ビス (1H—イミダゾールー 2— ィルメチル) ベンズアミド; (31) 4- [ (8—シクロへキシル一 2, 8
ージァザスピロ [4. 5] デカ一 2—ィル) メチル] 一 N, N—ビス (1H 一^ f ミダゾールー 2—イノレメチル) 一 2—メ トキシベンズァミド; (32) 1一 {4一 [ (8—シクロへキシル一2, 8—ジァザスピロ [4. 5] デカ —2—ィ レ) メチノレ] フエ-ル} — N, N—ビス (1 H—イ ミダゾーノレ一 2 一ィルメチル) メタンァミン; (33) 3—クロロー 4一 [ (8—シク口へ キシル一2, 8—ジァザスピロ [4. 5] デカー 2—ィル) メチル] 一 N, N—ビス ( 1 H (ミダゾールー 2—イノレメチノレ) ベンズァミ ド; (34) 4— [ (8—シクロォクチルー 2, 8—ジァザス'ピロ [4. 5] デカ一 2— ィノレ) メチノレ] -N, N—ビス (1H—イ ミダゾーノレ一 2—イノレメチノレ) ベ ンズアミド; (35) 1— {4— [ (8—シクロへキシルー 2, 8—ジァザ スピロ [4. 5] デカー 2—ィル) カルボエル] フエ二ル} 一 N, N—ビス ( 1 H—イミダゾールー 2—ィルメチル) メタンァミン; (36) 4— [ (7 ーシクロへプチルー 2, 7—ジァザスピロ [3. 5] ノナー 2—ィル) メチ ノレ] 一 N, N—ビス (1 H—イミダゾールー 2—ィルメチル) ベンズアミ ド; (37) (2E) -3- {4- [ ( 8—シクロへキシルー 2, 8—ジァザス ピロ [4. 5] デカー 2—ィル) メチル] フエ二ル} 一 N, N—ビス (1H 一イミダゾールー 2—ィルメチル) アクリルアミ ド; (38) 3 - {4- [ (8 ーシクロへキシル一2, 8—ジァザスピロ [4. 5] デカー 2—ィル) メチ ル] フエ-ル} 一 N, N—ビス (1H— ^ f ミダゾ一ルー 2—ィルメチル) プ 口パンアミド; (39) 4— { [8— (シクロブチルメチル) 一2, 8—ジ ァザスピロ [4. 5] デカ一 2—ィル] メチル } 一 N, N—ビス (1H—ィ ミダゾールー 2—ィルメチル) ベンズァミ ド; (40) 4— [ ( {トランス 一 4— [ベンジル (プロピル) ァミノ] シクロへキシル } ァミノ) メチル] 一 N, N—ビス (1H—イミダゾール一 2—イノレメチノレ) ベンズアミド; (4 1) 4— [ ( {トランス一 4一 [シクロへキシル (ェチル) ァミノ] シクロ へキシル } ァミノ) メチル] — N, N—ビス ( 1 H—ィミダゾールー 2—ィ
ルメチル) ベンズアミ ド; (42) 4— ( { [4一 (3, 4—ジヒ ドロー 2 (1H) 一イソキノリニル) シクロへキシル] ァミノ) メチル) 一N, N— ビス (1 H—イミダゾールー 2—ィルメチル) ベンズアミ ド; (43) N, N—ビス (1 H—イミダゾールー 2—ィルメチル) 一 4一 ( { [4一 (1一 ピぺリジュル) シク口へキシル] アミノ } メチル) ベンズァミ ド; (44) 4一 ( { [4一 (1—ァゼパ二ル) シクロへキシル] アミノ} メチノレ) 一 N, N—ビス ( 1 H—イミダゾールー 2—ィルメチル) ベンズァミ ド; (45) 4一 ( { [トランス一 4一 (シク口へキシ ァミノ) シク口へキシル] アミ ノ} メチル) 一 Ν, Ν—ビス (1 Η—イミダゾーノレ一 2—イノレメチノレ) ベン ズアミ ド; (46) Ν— (1H—べンゾイミダゾールー 2—ィルメチル) ― 4一 [ ( {トランス一 4一 [シク口へキシル (プロピル) ァミノ] シクロへ キシル } ァミノ) メチル] 一 Ν— ( 1 Η—イミダゾーノレ一 2—イノレメチノレ) ベンズアミ ド; (47) 4- [ ( {トランス一 4一 [ ( 1一ェチルプロピル) (プロピル) ァミノ] シクロへキシル } ァミノ) メチル] -Ν, Ν—ビス (1 Η—イミダゾールー 2—ィルメチル) ベンズアミ ド; (48) 4一 { [ {ト ランス一 4— [シクロへキシル (プロピル) ァミノ] シクロへキシノレ } (メ チル) ァミノ] メチゾレ} — Ν, Ν—ビス (1H—^ f ミダゾ一ノレ一 2—イノレメ チル) ベンズアミ ド; (49) 4一 { [ {トランス一 4一 [シクロへキシル (プロピル) ァミノ] シクロへキシル } (ェチル) ァミノ] メチル } 一 N, N—ビス ( 1 H—イミダゾールー 2—ィルメチル) ベンズァミ ド; (50) 4— { [ {トランス一 4— [シクロへキシル (プロピル) ァミノ] シクロへ キシル } (プロピル) ァミノ] メチル } -N, N—ビス (1H—イミダゾー ルー 2—ィルメチル) ベンズァミ ド; ( 51 ) 4— { [ {トランス一 4— [シ クロへキシル (プロピル) ァミノ] シクロへキシル } (2—ヒ ドロキシェチ ル) ァミノ] メチル } — N, N—ビス (1H—イミダゾールー 2—ィルメチ ル) ベンズアミ ド; (52) 4- [ ( {トランス一 4一 [ (1一ェチルプロ
ピル) ( 2—ヒ ドロキシェチノレ) ァミノ] シクロへキシル } アミノ) メチル] 一 N, N—ビス ( 1 H—イ ミダゾーノレ一 2—ィルメチル) ベンズアミ ド ; (5 3) 4一 ( { [トランス一 4一 (ジプロピルァミノ) シクロへキシル] アミ ノ} メチル) -N, N—ビス (1 H—イミダゾールー 2—ィルメチル) 一2 —メ トキシベンズアミ ド; (54) 3—クロ口一 4一 ( { [トランス一 4一 (ジプロピルァミノ) シク口へキシル] アミノ } メチル) 一 N, N—ビス ( 1 H—ィミダゾーグレー 2ーィ /レメチル) ベンズァミ ド; (55) 4— ( { [4 一 (1—ァゾカニル) シクロへキシル] アミノ} チル) 一 N, N—ビス (1 H—イミダゾールー 2—ィルメチル) ベンズアミ ド; (56) 4- ( { [4 一 (1—ァゾカニル) シクロへキシル] ァミノ) メチル) 一 N, N—ビス (1 H—イミダゾールー 2一ィルメチル) ベンズァミ ド; (57) 4— ( { [ (1 一シク口へプチルー 4ーピペリジニル) メチル] ァミノ) メチル) 一 N, N 一ビス (1H—イミダゾールー 2—ィルメチル) ベンズアミ ド; (58) 4 一 ( { [4一 (ジプロピノレアミノ) プチル] ァミノ) メチル) — N, N—ビ ス ( 1 H—イミダゾーノレ一 2一イノレメチル)ベンズァミ ド; (59) 4—({ [3 一 (ジブチルァミノ) プロピル] アミノ} メチル) -N, N—ビス (1H— ィミダゾールー 2—ィルメチル) ベンズァミ ド; ( 60 ) 4— ( { [ 5— (ジ プロピノレアミノ) ペンチル] ァミノ) メチル) 一N, N—ビス (1H—イミ ダゾーノレ一 2—イノレメチノレ) ベンズアミ ド; (61) 4— ( {4- [ (ジプ 口ピルァミノ) メチル] —1—ピペリジニル } メチル) 一 N, N—ビス (1 H—イミダゾールー 2—ィルメチル) ベンズアミ ド; (62) 4— ( { [4 一 (ジプロピルァミノ) シクロへキシル] アミノ} メチノレ) 一 N, N—ビス ( 1 H—イミダゾーレー 2一イノレメチル) ベンズァミ ド; (63) 4— ( { [3 一 (ジプロピルァミノ) プロピル] ァミノ) メチル) 一 N, N—ビス (1H 一イミダゾールー 2—ィルメチル) ベンズアミ ド; (64) 4- [ (2—べ ンジル一2, 9—ジァザスピロ [5. 5] ゥンデ力一 9一ィル) メチル] 一
N, N—ビス (1H—イミダゾールー 2—ィルメチル) ベンズアミド; (6 5) 4— [ (2—シクロへキシルー 2, 9—ジァザスピロ [5. 5] ゥンデ カー 9一ィル) メチル] 一 N, N—ビス (1H—イミダゾールー 2—^ fルメ チル) ベンズァミド; (66) 2— [4一 (ジプロピルァミノ) ブチル] 一 N, N—ビス (1H—イミダゾールー 2—ィルメチル) 一 1, 2, 3, 4一 テトラヒドロ一 6—イソキノリンカノレポキサミ ド; (67) N— [4一 ( { [4 一 (ジプロピルァミノ) プチノレ] ァミノ) メチル) ベンジル] 一 N— (1H ーィミダゾーノレ一 2一^ルメチル) 一 1 H—ィミダゾ一ルー 2—カルポキサ ミ ド; (68) 4— ( { [4一 (ジプロピルアミノ) プチル] アミノ} メチ ル) 一 N, N—ビス ( 1 H—イミダゾールー 2—ィルメチル) ベンゼンスル ホンアミ ド、 その塩、 その N—ォキシド体もしくはその溶媒和物またはそれ らのプロドラッグ等が挙げられる。
最も好ましい化合物としては、 例えば、 4一 ( { [4一 (ジプロピルアミ ノ ) プチル] アミノ } メチル) 一 N, N—ビス ( 1 H—イミダゾールー 2一 ィルメチル) ベンズアミド (化合物 10) 、 4— ( { [3— (ジブチルアミ ノ) プロピル] アミノ} メチル) 一 N, N—ビス (1H—イミダゾールー 2 一ィルメチル) ベンズァミ ド (化合物 11) 、 4一 ( { [5— (ジプロピノレ ァミノ) ペンチル] ァミノ) メチル) 一 N, N—ビス (1H—イミダゾール 一 2—ィルメチル) ベンズアミド (化合物 11一 2) 、 4ー ( {4一 [ (ジ プロピルァミノ) メチル] 一 1ーピぺリジ-ル } メチル) _N, N—ビス ( 1 H—イミダゾールー 2—ィルメチノレ) ベンズアミド (化合物 11一 3) 、 4 一 ( { [4- (ジプロピルァミノ) シクロへキシル] ァミノ) メチノレ) 一 N, N—ビス (1H— ^ f ミダゾール一 2—ィルメチル) ベンズアミ ド (化合物 1 1-4) 、 4一 ( { [3— (ジプロピルアミノ) プロピル] アミノ} メチル) 一 N, N—ビス (1H—イミダゾールー 2—ィルメチル) ベンズアミ ド (化 合物 11— 10) 、 4一 [ (2—ベンジル一 2, 9—ジァザスピロ [5. 5]
ゥンデ力一 9一ィル) メチル] 一 N, N—ビス (1 H—イミダゾールー 2— イノレメチノレ) ベンズアミド (化合物 11— 17) 、 4一 [ (2—シクロへキ シル一2, 9—ジァザスピロ [5. 5] ゥンデカー 9一ィル) メチル] — N, N—ビス (1H—イミダゾールー 2—ィルメチル) ベンズアミド (化合物 1 1— 18) 、 2 - [4- (ジプロピルァミノ) プチル] 一 N, N—ビス (1 H—イミダゾーノレ一 2—イノレメチノレ) 一 1, 2, 3, 4—テトラヒ ドロ一 6 一イソキノリンカルポキサミド (化合物 15) 、 N- [4— ( { [4一 (ジ プロピルァミノ) プチル] アミノ} メチル) ベンジル] 一 N— (1H—イミ ダゾールー 2—ィルメチル)一 1 H—ィミダゾールー 2—力ルポキサミ ド(化 合物 19) 、 4一 ( { [4一 (ジプロピノレアミノ) プチル] アミノ} メチル) 一 N, N—ビス (1H—イミダゾールー 2—^ルメチル) ベンゼンスルホン アミ ド (化合物 38 ) 、 4一 [ ( {トランス一 4一 [シクロへキシノレ (プロ ピル) ァミノ] シクロへキシル } ァミノ) メチル] 一 N, N—ビス (1H— ィミダゾールー 2—ィルメチル)ベンズァミド (化合物 43— 4)、 4 - [ (2 ーシクロへキシルー 2, 8—ジァザスピロ [4. 5] デカ一 8—ィル) メチ ル] 一 N, N—ビス (1H—イミダゾールー 2—ィ /レメチル) ベンズアミ ド (化合物 49—1) 、 4— [ (8—シクロへキシルー 2, 8—ジァザスピロ [4. 5] デカー 2—ィル) メチル] 一 N, N—ビス (1H—イミダゾール 一 2—ィルメチル) ベンズアミド (化合物 49一 2) 、 4一 [ (2—シクロ へキシルー 2, 8—ジァザスピロ [4. 5]デカー 8—ィル) メチル] —N, N—ビス (1H—イミダゾールー 2—ィルメチル) ベンズアミド (化合物 5 0-92) 、 4一 [ (8—シクロへキシノレ一 2, 8—ジァザスピロ [4. 5] デカー 2—ィノレ) メチル] 一 N, N—ビス (1H—イミダゾールー 2—ィル メチノレ) ベンズアミド (化合物 50— 95) 、 N, N—ビス (1H—イミダ ゾールー 2一^ ルメチル) 一 4一 { [8 - (2一チェニルメチル) 一 2, 8 ージァザスピロ [ 4. 5 ] デカー 2—ィル] メチル } ベンズァミド (化合物
50-29) 、 N— ( 1 H—ベンゾイミダゾールー 2一ィルメチル) 一 4— [ (8—シクロへキシルー 2, 8—ジァザスピロ [4. 5] デカー 2—ィル) メチル] -N- (1H—イミダゾールー 2—ィルメチル) ベンズアミ ド (ィヒ 合物 50— 38) 、 4一 [ (8—シクロへプチルー 2, 8—ジァザスピロ [4. 5] デカ一 2—ィル) メチノレ] — N, N—ビス (1H—イミダゾールー 2— ィルメチノレ) ベンズアミ ド (化合物 50— 49) 、 N, N—ビス (1H—ィ ミダゾ一ノレ一 2—イスレメチノレ) 一 4— ( { 8 - [ (3—メチノレ一 2—チェ二 ル) メチル] —2, 8—ジァザスピロ [4. 5] デカー 2—^ 1^レ} メチル) ベンズアミ ド (化合物 50— 78) 、 4一 { [8— (1一ェチルプロピル) -2, 8—ジァザスピロ [4. 5] デカー 2—ィル] メチル } — N, N—ビ ス (1 H—ィミダゾールー 2一^ Tルメチル) ベンズァミ ド (化合物 50-8 1) 、 4— [ ( {トランス一 4一 [ベンジル (プロピル) ァミノ] シクロへ キシル } ァミノ) メチル] — N, N—ビス (1H—イミダゾール一 2—ィル メチル) ベンズアミ ド (化合物 50— 1) 、 4ー ( { [4— (1—ァゼパ- ル) シクロへキシル] アミノ} メチル) 一 N, N—ビス (1H—イミダゾー ルー 2—ィルメチル)ベンズァミド(化合物 50— 19、化合物 50— 20)、 N— (1 H—ベンゾイミダゾールー 2—ィルメチル) 一 4一 [ ( {トランス —4— [シクロへキシル (プロピル) ァミノ] シクロへキシル } ァミノ) メ チル] -N- ( 1 H—イミダゾールー 2—ィルメチル) ベンズァミ ド (化合 物 50— 39) 、 4- [ ( {トランス一 4— [ (1一ェチルプロピル) (プ 口ピル) ァミノ] シクロへキシル } ァミノ) メチル] 一 N, N—ビス (1H 一イミダゾールー 2—ィルメチル) ベンズアミ ド (化合物 50— 41) 、 4 一 { [ {トランス一 4一 [シクロへキシ /レ (プロピ 7レ) ァミノ] シクロへキ シル } (メチ /レ) ァミノ] メチル } 一 N, N—ビス (1H— ^ f ミダゾール一 2—イノレメチノレ) ベンズアミド (化合物 50— 67) 、 4一 { [ {トランス 一 4— [シクロへキシル (プロピル) ァミノ] シクロへキシル } (2—ヒ ド
口キシェチル) ァミノ] メチノレ) 一 N, N—ビス (1 H—イミダゾールー 2 一ィルメチル) ベンズァミ ド (化合物 5 0— 1 0 3 ) 、 4一 [ ( {トランス 一 4— [ ( 1一ェチルプロピル) ( 2—ヒドロキシェチル) ァミノ] シクロ へキシル } ァミノ) メチル] 一 N, N—ビス (1 H—イミダゾールー 2—ィ ルメチル) ベンズアミド (化合物 5 0 - 1 0 5 ) 、 その塩、 その N—ォキシ ド体もしくはその溶媒和物またはそれらのプロドラッグ等が挙げられる。
[本発明化合物の製造方法]
一般式 (1—0 ) で示される本発明化合物は、 ^知の方法、 例えば、 以下 に示す方法、 実施例に記載した方法あるいは、 コンプレヘンシブ 'オーガ二 ック ' トフンスフォーメーションス (Comprehensive Organic
Transformations: A Guide to Functional Group Pre arationss 第 2 fe)
(Richard C丄 arock著、 John Wiley & Sons Inc、 1999) に記載された方法等 を適宜改良し、組み合わせて用いることにより製造することができる。なお、 以下の各製造方法において、 原料化合物は塩として用いてもよい。 このよう な塩としては、 前記した一般式 (1—0 ) の塩として記載したものが用いら れる。
般式 (1—0 ) で示される本発明化合物のうち、 がー重結合を表 わし、 Dが窒素原子を表わし、 かつ Gがカルボュル基を表わす化合物、 すな わち一般式 ( I一 A)
(式中、 すべての記号は前記と同じ意味を表わす。 )
(式中、 すべての記号は前記と同じ意味を表わす。 )
(式中、 Wは水酸基または塩素原子を表わし、 他の記号は前記と同じ意味を 表わす。 )
で示される化合物をアミド化反応に付し、 さらに所望により、 保護基の脱保 護反応およぴ Zまたは樹脂からの切断反応に付すことにより製造することが できる。
このアミド化反応は公知であり、 例えば、
( 1 ) 酸ハライドを用いる方法、
( 2 ) 混合酸無水物を用いる方法、
( 3 ) 縮合剤を用いる方法等が挙げられる。
これらの方法を具体的に説明すると、
( 1 ) 酸ハライドを用いる方法は、 例えば、 カルボン酸を有機溶媒 (クロ 口ホルム、 ジクロロメタン、 ジェチルエーテル、 テトラヒドロフラン等) 中 または無溶媒で、 酸ノヽライド化剤 (ォキザリルクロライド、 チォユルクロラ ィド等) と一 2 0 °C〜還流温度で反応させ、 得られた酸ハライドを塩基 (ピ リジン、 トリェチルァミン、 N, N—ジメチルァ-リン、 4—ジメチルアミ ノビリジン、 ジイソプロピルェチルァミン等) の存在下、 ァミンと有機溶媒 (クロロホノレム、 ジクロロメタン、 ジェチ /レエーテノレ、 テトラヒドロフラン 等) 中、 0〜4 0 °Cの温度で反応させることにより行なわれる。 また、 得ら れた酸ハライドを有機溶媒 (ジォキサン、 テトラヒドロフラン等) 中、 アル カリ水溶液 (重曹水または水酸化ナトリウム溶液等) を用いて、 ァミンと 0
〜4 0 °Cで反応させることにより行なうこともできる。
( 2 ) 混合酸無水物を用いる方法は、 例えば、 カルボン酸を有機溶媒 (ク ロロホ /レム、 ジクロロメタン、 ジェチノレエーテノレ、 テトラヒドロフラン等) 中または無溶媒で、 塩基 (ピリジン、 トリェチルァミン、 N, N—ジメチル ァニリン、 4—ジメチルァミノピリジン、 ジイソプロピルェチルァミン等) の存在下、 酸ハライド (ピバロイルク口ライド、 トシルク口ライド、 メシル クロライド等) 、 または酸誘導体 (クロ口ギ酸ェチル、 クロ口ギ酸ィソプチ ル等) と、 0〜4 0 °Cで反応させ、 得られた混合酸無水物を有機溶媒 (クロ ロホノレム、 ジクロロメタン、 ジェチルエーテル、 テトラヒドロフラン等) 中、 ァミンと 0〜4 0 °Cで反応させることにより行なわれる。
( 3 ) 縮合剤を用いる方法は、 例えば、 カルボン酸とアミンを、 有機溶媒 (クロ口ホノレム、 ジクロロメタン、 ジメチ/レホ/レムァミ ド、 ジェチノレエーテ ル、 テトラヒドロフラン等) 中、 または無溶媒で、 塩基 (ピリジン、 トリエ チノレアミン、 ジイソプロピルェチルァミン、 N, N—ジメチルァ二リン、 N 一メチルモルホリン、 4ージメチルァミノピリジン等) の存在下または非存 在下、 縮合剤 (1 , 3—ジシクロへキシルカルポジイミド (D C C) 、 1一 ェチルー 3— [ 3—(ジメチルァミノ)プロピル]カルポジィミ ド(E D C) 、 1, 1,一カノレポ-ノレジィミダゾーノレ (C D I ) 、 O— ( 7ーァザべンゾトリ ァゾールー 1一ィル) N, N, N,, N,一テトラメチノレゥロニゥムへキサフノレ ォロホスフェート (HATU) 、 2—クロロー 1—メチルピリジユウムヨウ 素、 1一プロピルホスホン酸環状無水物 (1- propanephosphonic acid cyclic anhydride, P P A) 等) を用い、 1ーヒドロキシベンズトリアゾール (HO B t ) または 1ーヒドロキシー 7—ァザべンゾトリアゾール (HOA t ) を 用いるカ用いないで、 0〜4 0 °Cで反応させることにより行なわれる。
これら (1 ) 、 (2 ) および (3 ) の反応は、 いずれも不活性ガス (アル ゴン、 窒素等) 雰囲気下、 無水条件で行なうことが望ましい。
保護基の脱保護反応は、 公知の方法、 例えば、 プロテクティブ'グループ ス ' ン 'オーカニック ·シンセシス (Protective Groups in Organic Synthesis) (T.W.Greene著、 John Wiley & Sons Incヽ 1 9 9 9 ) に記載さ れた方法を用いて行なうことができる。 また、 保護基としては、 上記した文 献に記載されたもの、 またはそれ以外にも容易にかつ選択的に脱離できる基 であれば特に限定されない。
また、 分子内に樹脂と結合している部分が存在し、 その樹脂がポリスチレ ン樹脂の場合、 以下の方法によって樹脂から本発明化合物を切断することが できる。 この樹脂からの切断反応は公知であり、 例えば、 有機溶媒 (ジクロ ロメタン、 1, 2—ジクロロェタン、 トルエン等) 中、 酸 (酢酸、 トリフル ォロ酢酸、 塩酸等) を用いて、 0〜1 0 o °cで反応させることにより行なわ れる。
さらに必要であれば、 この反応に引き続いて公知の方法によって、 目的の 塩に変換する操作を行なってもよい。
一般式 (1—0 ) で示される本発明化合物のうち、 が一重結合を表 わし、 Dが窒素原子を表わし、 かつ Gがー S 02—基を表わす化合物、 すなわ ち一般式 (I一 B ) (| B)
(式中、 すべての記号は前記と同じ意味を表わす。 )
で示される化合物は、 一般式 (2) で示される化合物と一般式 (4 )
-
(式中、 Xはハロゲン原子を表わし、 その他の記号は前記と同じ意味を表わ す。 )
で示される化合物をスルホンアミド化反応に付し、 さらに所望により、 保護 基の脱保護反応および/または樹脂からの切断反応に付すことにより製造す ることができる。
スルホンァミド化反応は公知であり、 以下の方法で行うことができる。 例 えば、 スルホン酸を有機溶媒 (クロ口ホルム、 ジクロロメタン、 ジクロロェ タン、 ジェチノレエーテノレ、 テトラヒドロフラン、 メチノレ t一プチノレ エー テル等) 中または無溶媒で、 酸ハライド (ォキザリルクロライド、 チォニル クロライド、 五塩化リン、 三塩化リンまたはォキシ塩化リン、 またはこれら の混合物等) と、 ジメチルホルムアミドの存在下もしくは非存在下で、 一 2 o°c〜還流温度で反応させるか、またはチオールを酸水溶液(例えば、塩酸、 硫酸、 硝酸、 酢酸等) 中、 塩素ガスと o °c〜還流温度で反応させてスルホ二 ルハライドを合成することができる。 前記で合成したスルホニルハラィドを 塩基 (ジイソプロピルェチルァミン、 ピリジン、 トリェチルァミン、 N, N ージメチルァユリン、 4—ジメチルァミノピリジン等) の存在下、 有機溶媒 (クロロホノレム、 ジクロロメタン、 ジクロロエタン、 ジェチノレエーテノレ、 テ トラヒドロフラン等) 中、 ァミンと 0〜4 0 °Cで反応させることにより行な われる。 また、 保護基の脱保護反応または樹脂からの切断反応は前記と同じ 方法によって行うことができる。
一般式 (1—0 ) で示される本宪明化合物のうち、 Lがアミド結合を表わ す化合物、 すなわち一般式 (I一 C一 1 )
(式中、 RC 1は水素原子または L中に定義された 「置換基を有していてもよ い二価の窒素原子」 における置換基を表わし、 他の記号は前記と同じ意味を 表わす。 )
または一般式 (I一 C一 2 )
(式中、 すべての記号は前記と同じ意味を表わす。 )
(式中、 すべての記号は前記と同じ意味を表わす。 )
(式中、 すべての記号は前記と同じ意味を表わす。 )
で示される化合物をアミド化反応に付し、 さらに所望により、 保護基の脱保 護反応および/または樹脂からの切断反応に付す力 \ 一般式 (7 )
H
(式中、 すべての記号は前記と同じ意味を表わす。 )
で示される化合物と一般式 (8 )
(式中、 すべての記号は前記と同じ意味を表わす。 )
で示される化合物をアミド化反応に付し、 さらに所望により、 保護基の脱保 護反応および/または樹脂からの切断反応に付すことにより製造することが できる。
アミド化反応、 保護基の脱保護反応または樹脂からの切断反応は前記と同 じ方法によって行うことができる。
一般式 (1—0 ) で示される本発明化合物のうち、 Lがスルホンアミド結 合を表わす化合物、 すなわち一般式 ( I一 D— 1 )
(式中、 すべての記号は前記と同じ意味を表わす。 )
(式中、 すべての記号は前記と同じ意味を表わす。 )
で示される化合物は、 一般式 (5 ) で示される化合物と一般式 (9 )
(式中、 すべての記号は前記と同じ意味を表わす。 )
で示される化合物をスルホンアミド化反応に付し、 さらに所望により、 保護 基の脱保護反応および/または樹脂からの切断反応に付すか、 一般式 (7 ) で示される化合物と一般式 (1 0 )
(式中、 すべての記号は前記と同じ意味を表わす。 )
で示される化合物をスルホンアミド化反応に付し、 さらに所望により、 保護 基の脱保護反応および/または樹脂からの切断反応に付すことにより製造す
ることができる。
スルホンアミド化反応、 保護基の脱保護反応または樹脂からの切断反応は 前記と同じ方法によって行うことができる。
一般式 (1—0) で示される本発明化合物のうち、 Lが置換基を有してい てもよい一 CH (— R
E1) —NH—または一 NH—CH (-R
E1) 一 (基中、 R
E1は、 水素原子または L中に定義された [置換基を有していてもよい二価 の炭素数 1〜4の脂肪族炭化水素基] における置換基を表わす。 ) を表わす 化合物、 すなわち一般式 ( I一 E— 1 ) '
(式中、 すべての記号は前記と同じ意味を表わす。 )
または- -般式 (I E— 2)
(式中、 すべての記号は前記と同じ意味を表わす。
(式中、 すべての記号は前記と同じ意味を表わす。
(式中、 すべての記号は前記と同.じ意味を表わす。 )
で示される化合物を還元的ァミノ化反応に付し、 さらに所望により、.保護基 の脱保護反応および Zまたは樹脂からの切断反応に付す力 一般式 (1 3 )
H2N-J° (13)
(式中、 すべての記号は前記と同じ意味を表わす。 )
で示される化合物と一般式 (1 4 )
(14)
A2— B2
(式中、 すべての記号は前記と同じ意味を表わす。 )
で示される化合物を還元的ァミノ化反応に付し、 さらに所望により、 保護基 の脱保護反応および/または樹脂からの切断反応に付すことにより製造する ことができる。
この還元的ァミノ化反応は公知であり、 例えば、 有機溶媒 (ジクロ口エタ ン、 ジクロロメタン、 ジメチルホルムアミド、 酢酸およびこれらの混合物等) 中、 還元剤 (水素化トリァセトキシホウ素ナトリウム、 シァノ水素化ホウ素 ナトリウム、 水素化ホウ素ナトリウム等) の存在下、 0〜4 0 °Cの温度で行 なわれる。 保護基の脱保護反応または樹脂からの切断反応は前記と同じ方法 によって行うことができる。
一般式 (1—0 ) で示される本発明化合物のうち、 J °基中の塩基性基がモ ノー置換アミノ基である化合物、 すなわち、 一般式 (I一 F )
A1— B1
D— G— E— L ~~ JF-N— RF1 (l-F)
2 / H
A2— B2
(式中、 J Fは、 置換基を有していてもよい二価の脂肪族炭化水素基、 置換基 を有していてもよい二価の環状基、 置換基を有していてもよい二価の環状基 によつて置換された脂肪族炭化水素基、 置換基を有していてもよレ、二価の脂
肪族炭化水素基によって置換された環状基、 置換基を有していてもよ 、二価 のスピロ環状基、 または置換基を有していてもよい二価の架橋した環状基を 表わし、 R F 1は、 J。中に定義された 「モノー置換アミノ基」 における置換基 を表わし、 他の記号は前記と同じ意味を表わす。 )
で示される化合物は、 前記方法で製造した化合物、 すなわち一般式 (I一 F - 1 )
(式中、 すべての記号は前記と同じ意味を表わす。 )
で示される化合物と一般式 (1 5 )
RF1— CHO (15)
(式中、 すべての記号は前記と同じ意味を表わす。 )
で示される化合物を還元的ァミノ化反応に付し、 さらに所望により、 保護基 の脱保護反応および κまたは樹脂からの切断反応に付すことにより製造する ことができる。
還元的ァミノ化反応、 保護基の脱保護反応または樹脂からの切断反応は前 記と同じ方法によって行うことができる。
一般式 (1—0 ) で示される本発明化合物のうち、 J °基中の塩基性基がジ 一置換アミノ基である化合物、 すなわち、 一般式 (I一 G) (l-G)
(式中、 R F 2は、 J °中に定義された 「ジー置換アミノ基」 における置換基を 表わし、 他の記号は前記と同じ意味を表わす。 )
で示される化合物は、 前記した方法によって製造した化合物、 すなわち、 一
般式 (I一 F) で示される化合物と一般式 (16)
RF2— CH0 (16)
(式中、 すべての記号は前記と同じ意味を表わす。 )
で示される化合物を還元的ァミノ化反応に付し、 さらに所望により、 保護基 の脱保護反応および Zまたは樹脂からの切断反応に付すことにより製造する ことができる。
還元的ァミノ化反応、 保護基の脱保護反応または樹脂からの切断反応は前 記と同じ方法によって行うことができる。
なお、 一般式 (I一 G) のうち、 RF1と RF 2が同じ置換基を表わす化合物 は、 一般式 (I一 F— 1) で示される化合物と 2当量以上の一般式 (15) または一般式 (16) で示される化合物を還元的ァミノ化反応に付し、 さら に所望により、 保護基の脱保護反応および Zまたは樹脂からの切断反応に付 すことにより製造することができる。
還元的ァミノ化反応、 保護基の脱保護反応または樹脂からの切断反応は前 記と同じ方法によって行うことができる。
一般式 (1—0) で示される本発明化合物のうち、 A1および A2がイミダ ゾール一2—ィル基である化合物、 すなわち、 一般式 (I— H)
H
(式中、 すべての記号は前記と同じ意味を表わす。 )
で示される化合物は、 一般式 (17)
(17)
(式中、 すべての記号は俞記と同じ意味を表わす。 )
で示される化合物と [ 2 , 2—ビス (メチルォキシ) ェチル] ァミンまたは [ 2, 2—ビス (ェチルォキシ) ェチル] アミンを用いて環化反応に付し、 さらに所望により、 保護基の脱保護反応および/または樹脂からの切断反応 に付すことにより製造することができる。
この環化反応は公知であり、例えば、シンセシス(Synthesis) , 2001, (10) , 1546— 1550に記載された方法を改良し、 行うことができる。 例えば、 二トリ ル化合物を有機溶媒 (メタノール、 エタノール等) 中、 塩基 (ナトリウムメ トキシド、 ナトリウムエトキシド等) の存在下、 0〜4 0 °Cで反応し、 さら にこの溶液を、 ァセタールと脱水剤 (酢酸等) の存在下、 4 0〜1 5 0 °Cで 反応させることにより行なわれる。 また、 保護基の脱保護反応または樹脂か らの切断反応は前記と同じ方法によって行うことができる。
一般式 (1—0 ) で示される本発明化合物のうち、 -"^ が二重結合を表 わし、 Dが炭素原子を表わし、 かつ Gが窒素原子である化合物、 すなわち、 一般式 (I— J )
A1— B1
一 E— L ~ J° (I-J)
A2— B2
(式中、 すべての記号は前記と同じ意味を表わす。 )
で示される化合物は、 一般式 (1 8 ) ( )
(式中、 すべての記号は前記と同じ意味を表わす。 )
で示される化合物と一般式 (1 9 )
H2 — E—し ~ J0 (19)
(式中、 すべての記号は前記と同じ意味を表わす。 )
で示される化合物をィミノ化反応に付し、 さらに所望により、 保護基の脱保 護反応および Zまたは樹脂からの切断反応に付すことにより製造することが できる。
このィミノ化反応は公知であり、 例えば、 有機溶媒 (メタノール、 エタノ 一ノレ、 ジクロロメタン、 クロ口ホスレム、 ジクロロエタン、 ベンゼン、 トノレエ ン等) 中、 脱水剤 (無水硫酸マグネシウム、 モレキュラーシープ (商品名) 等) の存在下または非存在下、 酸(塩酸、酢酸等) の存在下または非存在下、
2 0 °C〜還流温度で行なわれる。
一般式 (I一 0 ) で示される本発明化合物のうち、 Dが窒素原子であり、 B 1中、 Dと隣接する二価基が一 C O—である化合物、 すなわち、 一般式 (I - K)
(式中、 B 1 Kは結合手または主鎖の原子数 1〜 3のスぺ一サーを表わし、 そ の他の記号は前記と同じ意味を表わす。 ) で示される化合物は、 一般式 (2 0 ) A2— B2— NH— G— E一 L ~ J0 (20)
(式中、 すべての記号は前記と同じ意味を表わす。 ) で示される化合物と、 一般式 (2 1 )
(式中、 すべての記号は前記と同じ意味を表わす。 ) で示される化合物をァ ミド化反応に付し、 さらに所望により、 保護基の脱保護反応および/または 樹脂からの切断反応に付すことにより製造することができる。
アミド化反応、 保護基の脱保護反応または樹脂からの切断反応は前記と同 じ方法によって行うことができる。
一般式 (I一 0 ) で示される本発明化合物のうち、 Dが窒素原子であり、 B 1中、 Dと隣接する二価基が一 S 02—である化合物、すなわち、一般式(I 一 L)
(式中、 B
1 Lは結合手または主鎖の原子数 1〜 3のスぺーサーを表わし、 そ の他の記号は前記と同じ意味を表わす。 ) で示される化合物は、 一般式 (2 0 ) で示される化合物と、 一般式 (2 2 )
(式中、 すべての記号は前記と同じ意味を表わす。 ) で示される化合物をス ルホンアミド化反応に付し、 さらに所望により、 保護基の脱保護反応おょぴ zまたは樹脂からの切断反応に付すことにより製造することができる。
スルホンアミド化反応、 保護基の脱保護反応または樹脂からの切断反応は 前記と同じ方法によって行うことができる。
一般式 (I一 0 ) で示される化合物のうち、 =^ がー重結合を表わし、 D が窒素原子を表わし、 Gが 1個の置換基を有していてもよい炭素原子を表わ し、 かつ B
1および B
2中の Dと隣接する二価基が一 C H
2—である化合物、す なわち、 一般式 ( I一 M)
(式中、 B K 2は結合手または主鎖の原子数 1〜 3のスぺーサーを表わし、 RM 1は水素原子または Gに定義された 「置換基を有していてもよい炭素原子」 に おける置換基を表わし、 その他の記号は前記と同じ意味を表わす。 ) で示さ れる化合物は、 一般式 (2 3 )
(式中、 全ての記号は前記と同じ意味を表わす。 ) で示される化合物と、 般式 (2 4 )
(式中、 全ての記号は前記と同じ意味を表わす。 )
で示される化合物を還元的ァミノ化反応に付し、 さらに所望により、 保護基 の脱保護反応、 および Zまたは樹脂からの切断反応に付すことにより製造す ることができる。
還元的ァミノ化反応、 保護基の脱保護反応または樹脂からの切断方法は前 記と同じ反応によって行なうことができる。
また、 一般式 (I—M) で示される化合物は、 般式
R M1
H2N— C—— E— L ~ J1 (25)
H
(式中、 全ての記号は前記と同じ意味を表わす。 ) で示される化合物と一般 式 (2 6 )
05 016066
A1― B1K-CHO (26)
(式中、 全ての記号は前記と同じ意味を表わす。 )
で示される化合物を還元的ァミノ化反応に付し、 さらに、 得られた化合物と 一般式 (2 7 )
A2― B2K-CHO (27)
(式中、 全ての記号は前記と同じ意味を表わす。 )
で示される化合物を還元的ァミノ化反応に付し、 さらに所望により、 保護基 の脱保護反応、 および/または樹脂からの切断反応に付すことにより製造す ることができる。
還元的ァミノ化反応、 保護基の脱保護反応、 または樹脂からの切断反応は 前記と同じ方法によつて行なうことができる。
なお、 一般式 (I一 M) 中、 A 1— B 1 K—C H 2基と A2— B 2 K— C H2基が 同じ置換基を表わす化合物は、 一般式 (2 5 ) で示される化合物と 2当量以 上の一般式 (2 6 ) または一般式 (2 7 ) で示される化合物を還元的ァミノ 化反応に付し、 さらに所望により、 保護基の脱保護反応、 および/または樹 脂からの切断反応に付すことにより製造することができる。
還元的ァミノ化反応、 保護基の脱保護反応または樹脂からの切断反応は前 記と同じ方法によつて行なうことができる。
その他の出発原料または試薬として用いる一般式 (2 ) 〜 (2 7 ) で示さ れる化合物は、 それ自体公知であるか、 あるいは公知の方法、 例えば、 コン プレヘンシブ ·オーガ二ック · トランスフォーメーションズ(Comprehensive Organic Transformations: A Guide to Functional Group
第 2 版) (Richard CLarock著、 John Wiley & Sons Inc、 1999) に記載された方 法等を組み合わせて用いることで容易に製造することができる。
本明細書中の各反応において、 加熱を伴なう反応は、 当業者にとって明ら かなように、 水浴、 油浴、 砂浴またはマイクロウエーブを用いて行なうこと
ができる。
本明細書中の各反応において、 適宜、 高分子ポリマー (例えば、 ポリスチ レン、 ポリアクリルアミド、 ポリプロピレン、 ポリエチレングリコール等) に担持させた固相担持試薬を用いてもよい。
本明細書中の各反応において、 反応生成物は通常の精製手段、 例えば、 常 圧下または減圧下における蒸留、 シリカゲルまたはケィ酸マグネシウムを用 いた高速液体クロマトグラフィ^"、 薄層クロマトグラフィー、 イオン交換樹 脂、 スカベンジャー樹脂あるいはカラムクロマトグラフィーまたは洗净、 再 結晶等の方法により精製することができる。 精製は各反応ごとに行なっても よいし、 いくつかの反応終了後に行なってもよい。
本明細書中のポリスチレン樹脂を用いた反応においては、 反応生成物は通 常の精製手段、 例えば、 溶媒 (N, N—ジメチルホルムアミド、 ジクロロメ タン、 メタノール、 テトラヒ ドロフラン、 トルエン、酢酸/トルエン等) で、 複数回洗浄することにより精製することができる。
[毒性]
本発明化合物の毒性は非常に低いものであり、 医薬として使用するために 十分安全であると判断できる。
[医薬品への適用]
ヒトを含めた動物、 特にヒトにおいて、 本発明化合物は、 C X C R 4拮抗 作用を有するので、例えば、炎症'免疫性疾患、 アレルギー性疾患、感染症、 特に H I V感染およびそれに随伴する疾患、精神 ·神経性疾患、脳疾患、 心 · 血管性疾患、 代謝性疾患、 癌疾患の予防および Zまたは治療に有効である。 また、 遺伝子治療のための幹細胞のィン 'ビトロ (in vitro) またはィン ·ビ ボ (in vivo) 増幅ならぴに末梢血幹細胞動員、 組織修復等を目的とした再生 医療用剤としても有用である。 再生医療の中でも、 骨髄移植、 末梢血幹細胞 移植、 組織修復を含めた各臓器移植等に用いられる移植医療用剤として有用
である。 さらに、 例えば網膜症 (糖尿病性網膜症、 加齢性黄斑変性症、 緑內 障等) や、 癌増殖等の血管新生が原因となる疾患の予防および Zまたは治療 に有効な血管新生抑制剤としても有用である。
炎症 '免疫性疾患としては、 例えば、 関節リウマチ、 関節炎、 網膜症、 痛 風、 移植臓器拒絶、 移植片対宿主病 (G VHD) 、 腎炎、 乾癬、 鼻炎、 結膜 炎、 多発性硬化症、 潰瘍性大腸炎、 クローン病、 細菌感染に伴うショック、 肺線維症、 全身性応答症候群 (S I R S ) 、 急性肺障害、 糖尿病等が挙げら れる。
アレルギー性疾患としては、 例えば、 喘息、 アトピー性皮膚炎、 鼻炎、 結 膜炎等が挙げられる。
感染症、 特に H I V感染おょぴそれに随伴する疾患としては、 例えば、 後 天性免疫不症候群 (A I D S ) 、 力ンジダ症、 力リ二肺炎、 サイトメガロウ イノレス網膜炎、 力ポジ肉腫、 悪性リンパ腫、 エイズ脳症、 細菌性敗血症等が 挙げられる。
精神 '神経性疾患、 脳疾患としては、 例えば、 アルツハイマー病を含む痴 呆症、 パーキンソン病、脳卒中、 脳梗塞、脳出血、 てんかん、 統合性失調症、 末梢神経障害等が挙げられる。
心 -血管性疾患としては、 例えば、 動脈硬化、 虚血再灌流傷害、 高血圧、 心筋梗塞、 狭心症、 心不全等が挙げられる。
代謝性疾患としては、 例えば、 糖尿病、 骨粗鬆症、 前立腺肥大、 頻尿等が 挙げられる。
癌疾患としては、 例えば、 乳癌、 悪性リンパ腫等の悪性腫瘍、 癌転移、 放 射線療法 Z化学療法後の骨髄抑制または血小板減少症等が挙げられる。
本発明化合物は、
1 ) その化合物の予防および Zまたは治療効果の補完および/または増強、 2 ) その化合物の動態 ·吸収改善、 投与量の低減、
および/または
3) その化合物の副作用の軽減のために他の薬剤と組み合わせて、 併用剤と して投与してもよい。
また、 併用する他の薬剤の (1) 予防および Zまたは治療効果の補完およ び/または増強、 (2)動態'吸収改善、投与量の低減、および/ /または(3) 副作用の低減のために本発明化合物を組み合わせて、 併用剤として投与して もよい。
本発明化合物と他の薬剤の併用剤は、 1つの鍵剤中に两成分を配合した配 合剤の形態で投与してもよく、 また別々の製剤にして投与する形態をとって もよい。 別々の製剤にして投与する場合には、 同時投与および時間差による 投与が含まれる。 また、 時間差による投与は、 本努明化合物を先に投与し、 他の薬剤を後に投与してもよいし、 他の薬剤を先に投与し、 本発明化合物を 後に投与してもかまわない。 それぞれの投与方法は同じでも異なっていても よい。
上記併用剤により、 予防および Zまたは治療効果を奏する疾患は特に限定 されず、 本発明化合物の予防およぴ Zまたは治療効果を補完およぴ Zまたは 増強する疾患であればよい。
本発明化合物と他の薬剤の質量比は特に限定されない。
他の薬剤は、 任意の 2種以上を組み合わせて投与してもよい。
また、 本発明化合物の予防および/または治療効果を補完および Zまたは 増強する他の薬剤には、 上記したメカニズムに基づいて、 現在までに見出さ れているものだけでなく今後見出されるものも含まれる。
本発明化合物と組み合わせて用いられる他の H I V感染および後天性免疫 不全症候群の予防および Zまたは治療剤の例としては、 逆転写酵素阻害薬、 プロテアーゼ阻害薬、 ケモカイン (例えば、 CCR2、 CCR3、 CCR4、 CCR5、 CXCR4等) 拮抗薬、 CD 4拮抗薬、 HI V (例えば、 HI V
- Is H I V— 2等) の表面抗原に対する抗体、 H I V (例えば、 H I V— 1、 H IV— 2等) のワクチン等が挙げられる。
逆転写酵素阻害薬としては、 例えば (1) 核酸系逆転写酵素阻害薬のジド ブジン (商品名: レトロビ/レ) 、 ジダノシン (商品名: ヴアイデッタス) 、 ザルシタビン (商品名:ハイビッド) 、 スタブジン (商品名:ゼリット) 、 ラミブジン (商品名:ェピビノレ) 、 アバカビノレ (商品名:ザィアジェン) 、 ディアノシン (商品名: ビディックス) 、 ァデフオビ ^ /レ、 ジピボキシル、 ェ ントリシタビン(商品名:ネビラシル)、テノフォビル(商品名:ビリヤド)、 コンビビル、 トリジビル、 トルバタ、 イビジェム等、 (2) 非核酸系逆転写 酵素阻害薬のネビラピン (商品名:ビラミューン) 、デラビルジン (商品名 : レスクリプター) 、 エフアビレンツ (商品名:サスティバ、 ストックリン) 、 カブラヴイリン (AG 1549) 等が挙げられる。
プロテアーゼ阻害薬としては、 例えばィンジナビル (商品名:クリキシバ ン) 、 リ トナビル (商品名: ノービア) 、 ネルフィナビル (商品名: ビラセ プト) 、 サキナビル (商品名:インビラーゼ、 フォートベース) 、 アンプリ ナビル (商品名:エジネラーゼ) 、 口ピナビル (商品名:カレトラ) 、 ァタ ザナビル ( (商品名: レャタズ) 、 フォスアンプレナビノレ (商品名: レキシ バ) 、 ティプラナビ 等が挙げられる。
ケモカイン拮抗薬としては、 例えば、 ケモカインレセプターの内因性のリ ガンド、 またはその誘導体おょぴ非ペプチド性低分子化合物、 またはケモカ インレセプターに対する抗体等が含まれる。
ケモカインレセプターの内因性のリガンドとしては、 例えば MI P— 1ひ、
MI P— 1 /3、 RANTE Ss SDF— 1 、 S D F— 1 、 MC P— 1、
MCP— 2、 MCP— 4、ェォタキシン(Eotaxin)、 MDC等が挙げられる。 内因性リガンドの誘導体としては、 例えば AOP— RANTES、 Me t 一 SDF—1 CK、 Me t— SDF— 1 等が挙げられる。
ケモカインレセプターの抗体としては、 P r o— 1 4 0等が挙げられる。 C C R 2拮抗薬としては、 例えば WO99/07351号、 WO99/40913号、 WO00/46195号、 WO00/46196号、 WO00/46197号、 WO00/46198号、 WO00/46199号、 WO00/69432号、 WO00/69815号または Bioorg. Med. Chem. Lett., 10, 1803 (2000) に記載された化合物等が挙げられる。
C C R 3拮抗薬としては、 例えば DE19837386号、 W099/55324号、 WO99/55330号、 WO00/04003号、 WO00/27800号、 WO00/27835号、 WO00/27843号、 WO00/29377号、 WO00/31032¾\ WO00/31033号、 WO00/34278号、 WO00/35449号、 WO00/35451号、 WO00/35452号、 WO00/35453号、 WO00/35454号、 WO00/35876号、 WO00/35877号、 WO00/41685号、 WO00/51607号、 WO00/51608号、 WO00/51609号、 WO00/51610号、 WO00/53172号、 WO00/53600号、 WO00/58305号、 WO00/59497号、 WO00/59498号、 WO00/59502号、 WO00/59503号、 WO00/62814号、 WO00/73327号または WO01/09088号に記載された化合物等 が挙げられる。
C C R 4拮抗薬としては、例えば WO02/030357号、 WO02/030358号に記載 された化合物等が挙げられる。
C C R 5拮抗薬としては、 W099/17773号、 WO99/32100号、 WO00/06085 号、 WO00/06146号、 WO00/10965号、 WO00/06153号、 WO00/21916号、 WO00/37455号、 EP1013276号、 WO00/38680号、 WO00/39125号、
WO00/40239号、 WO00/42045号、 WO00/53175号、 WO00/42852号、 WO00/66551号、 WO00/66558号、 WO00/66559号、 WO00/66141号、 WO00/68203号、 JP2000- 309598号、 WO00/51607号、 WO00/51608号、 WO00/51609号、 WO00/51610号、 WO00/56729号、 WO00/59497号、 WO00/59498号、 WO00/59502号、 WO00/59503号、 WO00/76933号、
WO98/25605号、 WO99/04794号、 W099/38514号、 Bioorg. Med. Chem. Lett.,
10, 1803 (2000) に記載された化合物、 TAK— 779、 S CH- 35112 5 (S CH-C) 、 S CH-417690 (SCH— D) 、 UK— 4278 57、 GW 8731 OA (ONO— 4128) 、 TAK— 220、 TA K一 652等が挙げられる。 , CXCR4拮抗薬としては、 例えば AMD— 3100、 AMD— 070、 T一 22、 KRH— 1120、 KRH- 1636, KRH— 2731、 C S — 3955、 WO00/66112号、 WO2004/024697号または WO2004/052862号 に記載された化合物等が挙げられる。
フュージョン阻害薬としては、 例えば T— 20 (pentafuside) 、 T一 12 49等が挙げられる。
H I Vインテグラーゼ阻害薬としては、 ェキセチン (Equisetin) 、 テマク ラジン (Ibmacrazine) 、 PL— 2500、 V— 165、 NSC— 61892 9、 L一 870810、 L— 708906アナログ、 S— 1360、 183 8等が挙げられる。
短鎖干渉 RN Aとしては、 HIV—1、 H IV— 1構成蛋白質、 ゲノム H I V RNA等を標的とした短鎖干渉 RNAが挙げられる。
代表的な逆転写酵素阻害薬およびプロテアーゼ阻害薬の通常の臨床投与量 は、 例えば、 以下に示すとおりであるが、 本発明はこれらに限定されるもの ではない。
ジドプジン: 100m g力プセル、 1回 200m g、 1日 3回; 300m g錠剤、 1 回 300m g、 1日 2回;
ジダノシン: 25〜200m g錠剤、 1回 125〜200m g、 1日 2回;
ザルシタビン: 0.375m g〜0.75m g錠剤、 1回 0.75m g、 1日 3回; スタプジン: 15〜40m g力プセノレ、 1回 30〜40m g、 1日 2回;
ラミプジン: 150m g錠剤、 1回 150m g、 1日 2回;
アバ力ビル: 300m g錠剤、 1回 300m g、 1日 2回;
ネビラピン: 200m g錠剤、 1回 200m g、 14曰間 1日 1回、その後 1日 2回; デラビルジン: 100m g錠剤、 1回 400m g、 1日 3回;
エフアビレンツ: 50〜200m gカプセル、 1回 600m g、 1日 1回; ィンジナビル: 200〜400m g力プセル、 1回 800m g、 1日 3回; リ トナビル: 100m gカプセル、 1回 600m g、 1日 2回;
ネルフィナビル: 250m g錠剤、 1回 750m g、 1日 3回;
サキナビル: 200m gカプセル、 1回 1,200m g、 1 0 3回;
アンプレナビル: 50〜: L50m g錠剤、 1回 l,200m g、 1日 2回。
本発明化合物の喘息に対する予防および/または治療効果の補完および Z または增強のための他の薬剤としては、 例えば、 抗ヒスタミン薬、 抗アレル ギー薬 (化学伝達物質遊離抑制薬、 ヒスタミン拮抗薬、 トロンボキサン合成 酵素阻害薬、 トロンポキサン拮抗薬、 T h 2サイト力イン阻害薬) 、 ステロ ィド薬、 気管支拡張薬 (キサンチン誘導体、 交感神経刺激薬、 副交感神経遮 断薬) 、 ワクチン療法薬、 金製剤、 漢方薬、 塩基性非ステロイド抗炎症薬、 5—リポキシゲナーゼ阻害薬、 5—リポキシゲナーゼ活†生化タンパク質拮抗 薬、 ロイコトリェン合成阻害薬、 プロスタグランジン類、 カンナビノイド一 2受容体刺激薬、 鎮咳薬、 去痰薬等が挙げられる。
抗ヒスタミン薬としては、 例えば、 ジフェンヒドラミン、 塩酸ジフエ二ル ピラリン、 テオクル酸ジフエ二ルビラリン、 フマル酸クレマスチン、 ジメン ヒドリ^ "一ト、 d 1—マレイン酸クロルフエ二ラミン、 d—マレイン酸クロ ルフエ二ラミン、 塩酸トリプロリジン、 塩酸プロメタジン、 酒石酸ァリメマ ジン、 塩酸イソチペンジル、 塩酸ホモクロルシクリジン、 ヒドロキシジン、 塩酸シプロへプタジン、 塩酸レポ力バスチン、 ァステミゾール、 べポタスチ ン、 デス口ラタジン、 T AK—4 2 7、 Z C R— 2 0 6 0、 N I P— 5 3 0、 モメタゾンフ口エート、 ミゾラスチン、 B P— 2 9 4、 アンドラスト、 ォー ラノフィン、 アタリバスチン等が挙げられる。
化学伝達物質遊離抑制薬としては、 例えば、 クロモグリク酸ナトリゥム、 トラユラスト、 アンレキサノクス、 レビリナスト、 イブジラスト、 ぺミロラ ストカリウム、 ダザノラスト、 ネドクロミノレ、 クロモグリカート、 イスラパ ファント等が挙げられる。
ヒスタミン拮抗薬としては、 例えば、 フマル酸ケトチフェン、 塩酸ァゼラ スチン、 才キサトミ ド、 メキタジン、 テルフエナジン、 フマル酸ェメダスチ ン、 塩酸ェピナスチン、 ェバスチン、 塩酸セチリジン、 塩酸ォロパタジン、 口ラタジン、 フエキソフエナジン等が挙げられる。
トロンポキサン合成酵素阻害薬としては、 例えば、 塩酸ォザダレル、 イミ トロダストナトリウム等が挙げられる。
トロンポキサン拮抗薬としては、例えば、セラトロダスト、 ラマトロバン、 ドミ トロバンカルシウム水和物、 K T - 2 - 9 6 2等が挙げられる。
T h 2サイト力イン阻害薬としては、 例えば、 トシノレ酸スプラタスト等が 挙げられる。
ステロイド薬としては、 例えば、 外用薬としては、 プロピオン酸クロベタ ゾール、酢酸ジフロラゾン、 フルオシノニド、 フランカルボン酸モメタゾン、 ジプロピオン酸ベタメタゾン、 酪酸プロピオン酸ベタメタゾン、 吉草酸ベタ メタゾン、 ジフルプレドナート、 プデソュド、 吉草酸ジフルコルトロン、 ァ ムシノ-ド、ハルシノニド、デキサメタゾン、 プロピオン酸デキサメタゾン、 吉草酸デキサメタゾン、 酢酸デキサメタゾン、 酢酸ヒドロコルチゾン、 酪酸 ヒドロコノレチゾン、 酪酸プロピオン酸ヒドロコルチゾン、 プロピオン酸デプ 口ドン、 吉草酸酢酸プレドニゾロン、 フルオシノ口ンァセトュド、 プロピオ ン酸べク口メタゾン、 トリアムシノロンァセト二ド、 ピバル酸フルメタゾン、 プロピオン酸ァノレクロメタゾン、 酪酸クロベタゾン、 プレドニゾロン、 プロ ピオン酸ぺクロメタゾン、 フルドロキシコルチド等が挙げられ、 内服薬、 注 射剤としては、 酢酸コルチゾン、 ヒドロコルチゾン、 リン酸ヒドロコルチゾ
ンナトリウム、 コハク酸ヒドロコルチゾンナトリウム、 酢酸フルド口コルチ ゾン、 プレド-ゾロン、 酢酸プレドニゾロン、 コハク酸プレドニゾロンナト リウム、 ブチル酢酸プレドニゾロン、 リン酸プレドニゾロンナトリウム、 酢 酸ハロプレドン、 メチルプレドニゾロン、 酢酸メチルプレドエゾロン、 コハ ク酸メチ プレドニゾロンナトリウム、 トリアムシノロン、 酢酸トリアムシ ノロン、 トリアムシノロンァセトニド、 デキサメタゾン、 酢酸デキサメタゾ ン、 リン酸デキサメタゾンナトリウム、 パルミチン酸デキサメタゾン、 酢酸 パラメタゾン、 ベタメタゾン等が挙げられ、 吸入^としてほ、 プロピオン酸 ベクロメタゾン、 プロピオン酸フルチ力ゾン、 ブデソニド、 フルニソリ ド、 トリアムシノロン、 S T— 1 2 6 Ρ、 シクレソニド、 デキサメタゾンパロミ チォネート、 モメタゾンフランカ/レポネート、 プラステロンスノレホネート、 デフラザコート、 メチルプレドニゾロンスレプタネート、 メチノレプレド-ゾ ロンナトリゥムスクシネート等が挙げられる。
キサンチン誘導体としては、 例えば、 アミノフィリン、 テオフィリン、 ド キソフィリン、 シパムフィリン、 ジプロフィリン、 プロキシブイリン、 コリ ンテオフィリン等が挙げられる。
交感神経刺激薬としては、 例えば、 ェピネフリン、 塩酸エフェドリン、 d 1—塩酸メチルエフェドリン、 塩酸メ トキシフエナミン、 硫酸イソプロテレ ノーノレ、 塩酸イソプロテレノール、 硫酸オルシプレナリン、 塩酸クロルプレ ナリン、 塩酸トリメトキノール、 硫酸サルプタモール、 硫酸テルブタリン、 硫酸へキソプレナリン、 塩酸ッロブテロール、 塩酸プロ力テロール、 臭化水 素酸フエノテロール、 フマル酸フオルモテロール、 塩酸クレンプテロール、 塩酸マプテロ一ノレ、キシナホ酸サノレメテローノレ、 R , R—フオノレモテロ一ノレ、 ッロプテロール、 塩酸ピルブテロール、 塩酸リ トドリン、 バンプテロール、 塩酸ドぺキサミン、 酒石酸メルァドリン、 A R— C 6 8 3 9 7、 レポサルプ タモ一ル、 KU R— 1 2 4 6、 KU L - 7 2 1 1 , A R - C 8 9 8 5 5 , S
一 1319等が挙げられる。
副交感神経遮断薬としては、 例えば、 臭化ィプラト口ピウム、 臭化フルト 口ピウム、 臭化ォキシトロピウム、 臭化シメトロピウム、 テミベリン、 臭化 チォトロピウム、 レバトロペート (UK— 1 12166) 等が挙げられる。 ワクチン療法薬としては、 例えば、 パスパート、 ァストレメジン、 ブロン カスマ 'ベルナ、 C S— 560等が挙げられる。
金製剤としては、 例えば、 金チオリンゴ酸ナトリウム等が挙げられる。 塩基性非ステロイド抗炎症薬としては、 例えば、 塩酸チケラミド、 塩酸チ ノリジン、 ェピリゾーノレ、 ェモルファゾン等が挙げられる。
5—リポキシゲナーゼ阻害薬としては、 例えば、 ザィリュートン、 ドセべ ノン、 ピリポスト、 SCH— 40120、 WY- 50295、 E— 6700、 ML— 3000、 TMK— 688、 ZD— 2138、 メシル酸ダルブフエロ ン、 R— 681 51、 E— 6080、 DuP— 654、 SC— 45662、 CV— 6504、 NE— 11740、 CM 1 -977, NC- 2000 E 一 3040、 PD— 136095、 CM I— 392、 TZ I— 41078、 Or f - 20485、 I DB - 18024、 BF— 389、 A - 78773、 TA— 270、 FLM—501 1、 CGS— 23885、 A— 79175、 ETH-615等が挙げられる。
5—リポキシゲナーゼ活性化タンパク質拮抗薬としては、 例えば、 MK— 591、 MK— 886等が挙げられる。
ロイコトリェン合成阻害薬としては、 例えば、 オーラノフィン、 マレイン 酸プログルメタシン、 L— 674636、 A— 81834、 UPA— 780、 A— 931 78、 MK-886、 REV— 5901 A、 SCH— 40120、 MK- 59 1、 B a y— x— 1005、 B a y— y— 1015、 DT I— 0 026、 アムレキサノックス、 E— 6700等が挙げられる。
プロスタグランジン類 (以下、 PGと略記する。 ) としては、 例えば、 P
TJP2005/016066
G受容体作動薬、 PG受容体拮抗薬等が挙げられる。
PG受容体としては、 例えば、 PGE受容体 (EP 1、 EP 2、 EP 3、 EP4) 、 PGD受容体 (DP、 CRTH2) 、 PGF受容体 (FP) 、 P G I受容体 (I P) 、 TX受容体 (TP) 等が挙げられる。
鎮咳薬としては、 例えば、 リン酸コディン、 リン酸ジヒドロコディン、 ォ キシメテバノール、 臭化水素酸デキストロメ トルファン、 クェン酸ペントキ シベリン、 リン酸ジメモルフアン、 クェン酸ォキセラジン、 クロペラスチン、 リン酸ベンプロペリン、 塩酸クロフエダノール、 : ^酸ホミノベン、 ノスカピ ン、 ヒベンズ酸チぺミジン、 塩酸ェプラジノン、 シャゼンソゥエキス等が挙 げられる。
去痰薬としては、例えば、アンモユアウイキヨゥ精、炭酸水素ナトリウム、 ヨウ化カリウム、 塩酸ブロムへキシン、 桜皮エキス、 カルボシスティン、 フ ドスティン、 塩酸アンプロキソール、 塩酸アンブロキゾール徐放剤、 メチル システィン塩酸塩、 ァセチルシスティン、 塩酸 L—ェチルシスティン、 チロ キサポール等が挙げられる。
本発明化合物のアトピー性皮膚炎 (蓴麻疹等) に対する予防および/また ' は治療効果の補完および Zまたは増強のための他の薬剤としては、 例えば、 ステロイド薬、 非ステロイド系抗炎症薬 (NSAI D) 、 免疫抑制薬、 プロ スタグランジン類、 抗アレルギー薬、 メディエーター遊離抑制薬、 抗ヒスタ ミン薬、 フオルスコリン製剤、 ホスホジエステラーゼ阻害薬、 カンナビノィ ドー 2受容体刺激薬等が挙げられる。
本発明化合物のァレルギ一性疾患 (ァレルギ一性気管支肺ァスペルギルス 症、 アレルギー性好酸球性胃腸症等) に対する予防および Zまたは治療効果 の補完および Zまたは増強のための他の薬剤としては、 例えば、 抗喘息薬、 吸入ステロイド、 吸入 β 2刺激薬、 メチルキサンチン系喘息薬、 抗アレルギ 一薬、 抗炎症薬、 抗コリン薬、 トロンポキサン拮抗薬、 ロイコトリェン拮抗
薬、 L T D 4拮抗薬、 P A F拮抗薬、 ホスホジエステラーゼ阻害薬、 2作 動薬、 ステロイド薬、 メディエーター遊離抑制薬、 好酸球化学遊走抑制薬、 マクロライド系抗生物質、 免疫抑制薬、 減感作療法 (アレルゲン) 注射剤等 が挙げられる。
抗喘息薬としては、 例えば、 テオフィリン、 プロ力テロール、 ケトチフエ ン、 ァゼラスチン等が挙げられる。
吸入ステロイドとしては、 例えば、 ベクロメタゾン、 フルチ力ゾン、 ブデ ソナイド等が挙げられる。
吸入 i3 2刺激薬としては、 例えば、 フエノテロール、 サブタモール、 フォ ルモテロール、 サルメテロール等が挙げられる。
メチルキサンチン系喘息薬としては、 例えば、 テオフィリン等が挙げられ る。
抗アレルギー薬としては、 例えば、 ケトチフェン、 テルフエナジン、 ァゼ ラスチン、 ェピナスチン、 スプラタスト、 クロモグリク酸ナトリウム等が挙 げられる。
抗炎症薬としては、例えば、ジクロフェナクナトリウム、イブプロフェン、 ィンドメタシン等が挙げられる。
抗コリン薬としては、 例えば、 臭化ィプラト口ピウム、 臭化フルト口ピウ ム、 臭化ォキシトロピウム、 臭化チオト口ピウム等が挙げられる。
トロンボキサン拮抗薬としては、 例えば、 ォザダレル、 セラトロダスト等 が挙げられる。
ロイコトリェン拮抗薬としては、 例えば、 プランルカスト、 モンテルカス ト、 ザフリルカスト、 ザイリユートン等が挙げられる。
マクロライド系抗生物質としては、 例えば、 エリスロマイシン、 ロキシス口 マイシン等が挙げられる。
免疫抑制薬としては、 例えば、 シクロスポリン、 タクロリムス、 F T Y 7
2 0等が挙げられる。
本発明化合物の肝炎に対する予防および/または治療効果の補完およぴ/ または増強のための他の薬剤としては、 例えば、 肝水解物製剤、 ポリェンホ スファチジルコリン、グリチルリチン製剤、プロトボルフィリンナトリウム、 ウルソデォキシコール酸、 ステロイド薬、 抗コリン薬、 制酸薬、 プロパゲル マ-ゥム、 脂質過酸化酵素阻害薬、 ミ トコンドリアルベンゾジァゼピン受容 体拮抗薬等が挙げられる。
本発明化合物の関節炎おょぴ関節リゥマチに対十る予防および Zまたは治 療効果の補完および/または増強のための他の薬剤としては、 例えば、 メタ 口プロティナーゼ阻害薬、 免疫抑制薬、 非ステロイド系抗炎症薬 (N S A I D) 、 ステロイド薬、 プロスタグランジン類、 ホスホジエステラーゼ阻害薬、 カンナピノイド一 2受容体刺激薬、 疾患修飾性抗リウマチ薬 (遅効性抗リウ マチ薬) 、 消炎酵素薬、 軟骨保護薬、 T細胞阻害薬、 T N F a阻害薬、 プロ スタグランジン合成酵素阻害薬、 I L— 6阻害薬、 インターフェロン y作動 薬、 I L一 1阻害薬等が挙げられる。
本発明化合物の乾癬に対する予防および/または治療効果の補完および Z または増強のための他の薬剤としては例えば、 ステロイド薬、 ビタミン D誘 導体等が挙げられる。
本発明化合物の鼻炎に対する予防および/または治療効果の補完およびノ または増強のための他の薬剤としては、 例えば、 抗ヒスタミン薬、 メデイエ 一ター遊離抑制薬、 トロンボキサン合成酵素阻害薬、 トロンポキサン A 2受容 体拮抗薬、 ロイコトリェン受容体拮抗薬、 ステロイド薬、 αアドレナリン受 容体刺激薬、 キサンチン誘導体、 抗コリン薬、 プロスタグランジン類、 一酸 化窒素合成酵素阻害薬、 3 2アドレナリン受容体刺激薬、 ホスホジエステラー ゼ阻害薬、 カンナビノイド一 2受容体刺激薬等が挙げられる。
本発明化合物の結膜炎に対する予防および /"または治療効果の補完およぴ
/または増強のための他の薬剤としては、 例えば、 ロイコトリェン受容体拮 抗薬、 抗ヒスタミン薬、 メディエーター遊離抑制薬、 非ステロイ ド系抗炎症 薬、 プロスタグランジン類、 ステロイ ド薬、 一酸化窒素合成酵素阻害薬、 力 ンナビノィドー 2受容体刺激薬等が挙げられる。
本発明化合物の多発性硬化症に対する予防および/または治療効果の補完 および/ /または増強のための他の薬剤としては、 例えば、 免疫抑制薬、 カン ナビノィドー 2受容体刺激薬等が挙げられる。
本発明化合物の潰瘍性大腸炎に対する予防および Zまたほ治療効果の補完 および Zまたは増強のための他の薬剤としては、 例えば、 メサラジン、 サラ ゾスルファピリジン、 消化管潰瘍用薬、 抗コリン薬、 ステロイ ド薬、 5—リ ポキシゲナーゼ阻害薬、 抗酸化薬、 L T B 4拮抗薬、 局所麻酔薬、 免疫抑制 薬、 防御因子増強薬、 MMP阻害薬、 ミトコンドリアルベンゾジァゼピン受 容体拮抗薬等が挙げられる。
本発明化合物の糖尿病合併症治療に対する予防および Zまたは治療効果の 補完および Zまたは増強のための他の薬剤としては、 例えば、 スルホュル尿 素系血糖低下薬、 ビグアナイド系薬、 一ダルコシダーゼ阻害薬、 速効型ィ ンスリン分泌促進薬、 インスリン薬、 P P AR作動薬、 P P ARァゴュスト 作用を有しないィンスリン感受性増強薬、 ]3 3アドレナリン受容体作動薬、 アルドース還元酵素阻害薬、 ジぺプチジルぺプチダーゼ I V阻害薬等が挙げ られる。
スルホエル尿素系血糖低下薬としては、 例えば、 ァセトへキサミド、 ダリ ベンクラミド、 グリクラジド、 グリクロビラミド、 ク口/レブロノヽ。ミド、 トラ ザミド、 トルプタミド、 グリメピリド等が挙げられる。
ビグアナィド系薬としては、 例えば、 塩酸プフォルミン、 塩酸メトフオル ミン等が挙げられる。
α—ダルコシダーゼ阻害薬としては、 例えば、 ァカルボース、 ボグリポー
ス等が挙げられる。
途効型インスリン分泌促進薬としては、 例えば、 ナテグリニド、 レパダリ ニド等が挙げられる。
P P AR作動薬としては、 例えば、 ピオグリタゾン、 トログリタゾン、 口 シグリタゾン、 J TT— 50 1等が挙げられる。
P PARァゴニス ト作用を有しないインスリン感受性增強薬としては、 例 えば、 ONO— 58 1 6、 YM— 440等が挙げられる。
β 3ァドレナリン受容体作動薬としては、 例えば、 A J 96 77, L 75 0 3 5 5、 CP 3 3 1 648等が挙げられる。
アルドース還元酵素阻害薬としては、 例えば、 ェパルレスタツト、 フイダ レスタツト、 ゼナレスタツト等が挙げられる。
本発明化合物の癌 (悪性腫瘍) や癌転移の予防および/または治療効果の 補完おょぴ zまたは増強のための他の薬剤としては、 例えば、 抗癌剤 (例え ば、 MM P阻害薬、 アルキル化薬 (例えば、 シクロフォスフアミド、 メルブ ァラン、 チォテパ、 マイ トマイシン C、 ブスルファン、 塩酸プロカルバジン 等) 、 代謝拮抗薬 (例えば、 メトトレキサート、 メルカプトプリン、 ァザチ ォプリン、 フ /レオロウラシ^/、 テガフーノレ、 シタラビン、 ァザセリン等) 、 抗生物質 (例えば、 マイ トマイシン C、 ブレオマイシン、 ぺプロマイシン、 塩酸ドキソルビシン、 アクラルビシン、 ダウノルビシン、 ァクチノマイシン D等) 、 有糸分裂阻害薬、 白金錯体 (例えば、 シスブラチン) 、 植物由来抗 悪性腫瘍薬 (例えば、 硫酸ビンクリスチン、 硫酸ビンブラスチン等) 、 抗腫 瘍性ホルモン (例えば、 メチルテストステロン、 プロピオンサンテス トステ ロン、 ェナント酸テストステロン、 メピチ才スタン、 ホスフェストローノレ、 酢酸クロルマジノン等) 、 免疫賦活薬 (例えば、 ピシパユール、 クレスチン 等) 、 インターフェロン (例えば、 I FNひ、 I FNa— 2 a、 I FN CE— 2 b、 I FN/3、 I FNy— l a等) 等が挙げられる。 T細胞活性化を行う
生物製剤 (例えば、 抗 C T L A— 4抗体、 抗 P D— 1抗体等)、 血管新生阻害 薬(例えば、べバシツマブ(bevacizumab) 、ぺガプタニブ (pegaptanib) 、 S U— 6 6 6 8、 ノ タラ-ブ (vatalanib) 、 ラニビツマプ(raoibizumab) 、 ソラフェュプ(sorafenib)、 S U— 1 1 2 4 8、ネオバスタツト (Neovastat) 等) 等が挙げられる。
本発明化合物の骨髄移植、 末梢血幹細胞移植、 組織修復を含めた治療の捕 完および Zまたは増強のための他の薬剤としては, たとえが G— C S Fや A MD 3 1 0 0等が挙げられる。
本発明化合物の免疫疾患 (例えば、 自己免疫疾患、 移植臓器拒絶反応等) の予防およぴ Zまたは治療効果の補完およひゾまたは増強のための他の薬剤 としては、 例えば、 免疫抑制薬 (例えば、 シクロスポリン、 タクロリムス、
F T Y 7 2 0等) 等が挙げられる。
本発明化合物のァノレツハイマー型老年痴呆症等の痴呆症に対する予防およ び Zまたは治療効果の補完および Zまたは増強のための他の薬剤としては、 例えば、 アセチルコリンエステラーゼ阻害薬、 ニコチン受容体調節薬、 脳循 環代謝改善薬、 モノアミンォキシダーゼ阻害薬、 ビタミン E、 アルドース還 元酵素阻害薬等が挙げられる。
本発明化合物のてんかんに対する予防および/または治療効果の補完およ び/または増強のための他の薬剤としては、 例えば、 フエ-トイン、 トリメ タジオン、 エトスクシミド、 カルバマゼピン、 フエノバルビタール、 プリミ ドン、 ァセタゾラミ ド、 スノレチアム、 バルプロ酸ナトリウム、 クロナゼパム、 ジァゼパム、 ニトラゼパム等が挙げられる。
本発明化合物の動脈硬化に対する予防および Zまたは治療効果の補完およ ぴ /または増強のための他の薬剤としては、 例えば、 HMG— C o A還元酵 素阻害薬、 フイブラート系薬、 プロブコール製剤、 陰イオン交換樹脂、 E P A製剤、 ニコチン酸製剤、 MT P阻害薬、 その他の抗高コレステロール薬、
6
EDG-2拮抗薬等が挙げられる。
本発明化合物を再生医療に用いる際のその効果の補完および/または増強 を目的とした他の薬剤としては、 サイト力イン類や各種増殖因子、 例えば各 種 CSF (例えば、 G— CSF、 GM— CSF等) 、 各種インターロイキン (例えば、 I L—3、 6、 7、 1 1、 12等) 、 EPO、 TPO、 SCF、 FLT3リガンド、 MI P— 1ひ等が挙げられる。
本発明化合物の網膜症に対する予防およぴ Zまたは治療効果の補完およぴ /または増強のための他の薬剤としては、例えば、血管新生阻害薬(例えば、 べバシツマプ (bevacizumab) 、 ぺガプタュブ (pegaptanib) 、 SU- 66 68、 ノ タラ-ブ (vatalanib) 、 ラニビツマブ (ranibizumab) 、 ソラフエ ニブ (sorafenib) 、 S U— 1 1248、 ネオバスタツト (neovastat) 等) 等 が挙げられる。
本発明化合物は、 安全で低毒性であるので、 例えばヒトゃヒト以外の哺乳 動物 (例えば、 ラット、 マウス、 ゥサギ、 ヒッジ、 プタ、 ゥシ、 ネコ、 ィヌ、 サル等) に対して投与することができる。
本発明化合物または本発明化合物と他の薬剤の併用剤を含有してなる医薬 組成物を上記の目的で用いるには、 通常、 全身的または局所的に、 経口また は非経口の形で投与される。
投与量は、 年齢、 体重、 症状、 治療効果、 投与方法、 処理時間等により異 なるが、 通常、 成人一人当たり、 一回につき、 O.lmgから 100 Omgの範 囲で一日一回から数回経口投与されるか、 または成人一人当たり、 一回につ き、 O.Olmgから 10 Omgの範囲で一日一回から数回非経口投与される力 または一日 1時間から 24時間の範囲で静脈内に持続投与される。
もちろん前記したように、 投与量は種々の条件により変動するので、 上記 投与量より少ない量で十分な場合もあるし、 また範囲を越えて投与の必要な 場合もある。
本発明化合物または本発明化合物と他の薬剤の併用剤を含有してなる医薬 組成物を投与する際には、 経口投与のための内服用固形剤、 内服用液剤、 お よび非経口投与のための注射剤、 外用剤、 坐剤、 点眼剤、 点鼻剤、 吸入剤等 として用いられる。
経口投与のための内服用固形剤には、 錠剤、 丸剤、 カプセル剤、 散剤、 顆 粒剤等が含まれる。 カプセル剤には、 ハードカプセルおよびソフトカプセル が含まれる。
このような内服用固形剤においては、 ひとつまたはそれ以上の活'生物質は そのままか、 または賦形剤 (ラクトース、 マンニトール、 グルコース、 微結 晶セルロース、 デンプン等) 、 .結合剤 (ヒドロキシプロピルセルロース、 ポ リビエルピロリ ドン、 メタケイ酸アルミン酸マグネシウム等) 、 崩壊剤 (繊 維素グリコール酸カルシウム等) 、 滑沢剤 (ステアリン酸マグネシウム等) 、 安定剤、 溶解補助剤 (グルタミン酸、 ァスパラギン酸等) 等と混合され、 常 法に従って製剤化して用いられる。 また、必要によりコーティング剤(白糖、 ゼラチン、 ヒ ドロキシプロピルセルロース、 ヒ ドロキシプロピノレメチノレセノレ ロースフタレート等) で被覆していてもよいし、 また 2以上の層で被覆して いてもよい。 さらにゼラチンのような吸収されうる物質のカプセルも包含さ れる。
経口投与のための内服用液剤は、薬剤的に許容される水剤、懸濁剤、乳剤、 シロップ剤、 エリキシル剤等を含む。 このような液剤においては、 ひとつま たはそれ以上の活性物質が、 一般的に用いられる希釈剤 (精製水、 エタノー ルまたはそれらの混液等) に溶解、 懸濁または乳化される。 さらにこの液剤 は、 湿潤剤、 懸濁化剤、 乳化剤、 甘味剤、 風味剤、 芳香剤、 保存剤、 緩衝剤 等を含有していてもよい。
非経口投与のための外用剤の剤形には、 例えば、 軟膏剤、 ゲル剤、 タリー ム剤、 ?显布剤、 貼付剤、 リニメント剤、 噴霧剤、 吸入剤、 スプレー剤、 エア
ゾル剤、 点眼剤、 およぴ点鼻剤等が含まれる。 これらはひとつまたはそれ以 上の活性物質を含み、 公知の方法または通常使用されている処方により調製 される。
軟膏剤は公知または通常使用されている処方により製造される。 例えば、 ひとつまたはそれ以上の活性物質を基剤に研和、 または溶融させて調製され る。軟膏基剤は公知あるいは通常使用されているものから選ばれる。例えば、 高級脂肪酸または高級脂肪酸エステル (アジピン酸、 ミリスチン酸、 ノ ルミ チン酸、 ステアリン酸、 ォレイン酸、 アジピン酸エステル、 ミリスチン酸ェ ステノレ、 ノ レミチン酸エステル、 ステアリン酸エステル、 ォレイン酸エステ ル等) 、 ロウ類 (ミツロウ、 鯨ロウ、 セレシン等) 、 界面活性剤 (ポリオキ シエチレンアルキルエーテルリン酸エステル等) 、 高級アルコール (セタノ ール、 ステアリルアルコール、 セトステアリルアルコール等) 、 シリコン油
(ジメチルポリシロキサン等) 、炭化水素類(親水ワセリン、 白色ワセリン、 精製ラノリン、 流動パラフィン等) 、 グリコール類 (エチレングリコール、 ジエチレングリコーゾレ、 プロピレンダリコーノレ、 ポリエチレングリコーノレ、 マクロゴール等)、植物油(ヒマシ油、ォリーブ油、ごま油、テレビン油等)、 動物油 (ミンク油、 卵黄油、 スクヮラン、 スクワレン等) 、 水、 吸収促進剤、 かぶれ防止剤から選ばれるもの単独または 2種以上を混合して用いられる。 さらに、 保湿剤、 保存剤、 安定化剤、 抗酸化剤、 着香剤等を含んでいてもよ い。
ゲル剤は公知または通常使用されている処方により製造される。 例えば、 ひとつまたはそれ以上の活性物質を基剤に溶融させて調製される。 ゲル基剤 は公知あるいは通常使用されているものから選ばれる。 例えば、 低級アルコ ール (エタノール、 イソプロピルアルコール等) 、 ゲル化剤 (カルボキシメ チノレセノレロース、 ヒ ドロキシェチノレセノレロース、 ヒ ドロキシプロピノレセノレ口 ース、 ェチルセルロース等) 、 中和剤 (トリエタノールァミン、 ジイソプロ
パノールァミン等) 、 界面活性剤 (モノステアリン酸ポリェチレングリコー ル等) 、 ガム類、 水、 吸収促進剤、 かぶれ防止剤から選ばれるもの単独また は 2種以上を混合して用いられる。 さらに、 保存剤、 抗酸化剤、 着香剤等を 含んでいてもよい。
クリーム剤は公知または通常使用されている処方により製造される。 例え ば、 ひとつまたはそれ以上の活性物質を基剤に溶融または乳化させて調製さ れる。 クリーム基剤は公知あるいは通常使用されているものから選ばれる。 例えば、 高級脂肪酸エステル、 低級アルコール、 炭化水素類、 多価アルコー ル (プロピレングリコール、 1 , 3—ブチレングリコール等) 、 高級アルコ ール (2 —へキシルデカノール、 セタノール等) 、 乳化剤 (ポリオキシェチ レンアルキルエーテル類、 脂肪酸エステル類等) 、 水、 吸収促進剤、 かぶれ 防止剤から選ばれるもの単独または 2種以上を混合して用いられる。 さらに、 保存剤、 抗酸化剤、 着香剤等を含んでいてもよい。
湿布剤は公知または通常使用されている処方により製造される。 例えば、 ひとつまたはそれ以上の活性物質を基剤に溶融させ、 練合物とし支持体上に 展延塗布して製造される。 湿布基剤は公知あるいは通常使用されているもの から選ばれる。 例えば、 増粘剤 (ポリアクリル酸、 ポリビュルピロリドン、 アラビアゴム、 デンプン、ゼラチン、 メチルセルロース等) 、湿潤剤 (尿素、 グリセリン、 プロピレングリコール等) 、 充填剤 (カオリン、 酸化亜鉛、 タ ルク、 カルシウム、 マグネシウム等) 、 水、 溶解補助剤、 粘着付与剤、 かぶ れ防止剤から選ばれるもの単独または 2種以上を混合して用いられる。 さら に、 保存剤、 抗酸化剤、 着香剤等を含んでいてもよい。
貼付剤は公知または通常使用されている処方により製造される。 例えば、 ひとつまたはそれ以上の活性物質を基剤に溶融させ、 支持体上に展延塗布し て製造される。 貼付剤用基剤は公知あるいは通常使用されているものから選 ばれる。 例えば、 高分子基剤、 油脂、 高級脂肪酸、 粘着付与剤、 かぶれ防止
剤から選ばれるもの単独または 2種以上を混合して用いられる。 さらに、 保 存剤、 抗酸化剤、 着香剤等を含んでいてもよい。
リニメント剤は公知または通常使用されている処方により製造される。 例 えば、 ひとつまたはそれ以上の活性物を水、 アルコール (エタノ^"ル、 ポリ エチレングリコール等) 、 高級脂肪酸、 グリセリン、 セッケン、 乳化剤、 懸 濁化剤等から選ばれるもの単独または 2種以上に溶解、 懸濁または乳化させ て調製される。 さらに、 保存剤、 抗酸化剤、 着香剤等を含んでいてもよい。 噴霧剤、 吸入剤、 およびスプレー剤は、 一般的に用いられる希釈剤以外に 亜硫酸水素ナトリウムのような安定剤と等張性を与えるような緩衝剤、 例え ば塩化ナトリウム、 クェン酸ナトリウムあるいはクェン酸のような等張剤を 含有していてもよい。 スプレー剤の製造方法は、 例えば米国特許第 2,868,691 号および同第 3,095,355号に詳しく記載されている。
非経口投与のための注射剤としては、 すべての注射剤を含み、 点滴剤をも 包含する。 例えば、 筋肉への注射剤、 皮下への注射剤、 皮内への注射剤、 動 脈内への注射剤、静脈内への注射剤、腹腔内への注射剤、脊髄腔への注射剤、 静脈内への点滴剤等を含む。
非経口投与のための注射剤としては、 溶液、 懸濁液、 乳濁液およぴ用時溶 剤に溶解または懸濁して用いる固形の注射剤を包含する。 注射剤は、 ひとつ またはそれ以上の活性物質を溶剤に溶解、 懸濁または乳化させて用いられる。 溶剤として、 例えば注射用蒸留水、 生理食塩水、 植物油、 プロピレングリコ ール、 ポリエチレングリコール、 エタノールのようなアルコール類等および それらの組み合わせが用いられる。 さらにこの注射剤は、 安定剤、 溶解捕助 剤 (グルタミン酸、 ァスパラギン酸、 ポリソルベート 8 0 (登録商標) 等) 、 懸濁化剤、 乳化剤、 無痛化剤、 緩衝剤、 保存剤等を含んでいてもよい。 これ らは最終工程において滅菌するか無菌操作法によって調製される。 また無菌 の固形剤、 例えば凍結乾燥品を製造し、 その使用前に無菌化または無菌の注
射用蒸留水または他の溶剤に溶解して使用することもできる。
非経口投与のための点眼剤には、 点眼液、 懸濁型点眼液、 ? L濁型点眼液、 用時溶解型点眼液およぴ眼軟膏が含まれる。
これらの点眼剤は公知の方法に準じて調製される。 例えば、 ひとつまたは それ以上の活性物質を溶剤に溶解、 懸濁または乳化させて用いられる。 点眼 剤の溶剤としては、 例えば、 滅菌精製水、 生理食塩水、 その他の水性溶剤ま たは注射用非水性用剤 (例えば、 植物油等) 等おょぴそれらの組み合わせが 用いられる。 点眼剤は、 等張化剤 (塩化ナトリウム、 濃グリセリン等) 、 緩 衝化剤 (リン酸ナトリウム、 酢酸ナトリウム等) 、 界面活性化剤 (ポリソル ペート 8 0 (商品名) 、 ステアリン酸ポリオキシ 0、 ポリオキシェチレ ン硬化ヒマシ油等) 、 安定化剤 (タエン酸ナトリウム、 ェデト酸ナトリウム 等) 、 防腐剤 (塩化ベンザルコユウム、 パラベン等) 等を必要に応じて適宜 選択して含んでいてもよい。 これらは最終工程において滅菌する力 無菌操 作法によって調製される。 また無菌の固形剤、 例えば凍結乾燥品を製造し、 その使用前に無菌化または無菌の滅菌精製水または他の溶剤に溶解して使用 することもできる。
非経口投与のための吸入剤としては、 エアロゾノレ剤、 吸入用粉末剤または 吸入用液剤が含まれ、 当該吸入用液剤は用時に水または他の適当な媒体に溶 解または懸濁させて使用する形態であってもよい。
これらの吸入剤は公知の方法に準じて製造される。
例えば、 吸入用液剤の場合には、 防腐剤 (塩化ベンザルコニゥム、 パラべ ン等) 、 着色剤、 緩衝化剤 (リン酸ナトリウム、 酢酸ナトリウム等) 、 等張 化剤 (塩化ナトリウム、 濃グリセリン等) 、 增粘剤 (カリポキシビュルポリ マー等) 、 吸収促進剤等を必要に応じて適宜選択して調製される。
吸入用粉末剤の場合には、 滑沢剤 (ステアリン酸およびその塩等) 、 結合 剤 (デンプン、 デキストリン等) 、 賦形剤 (乳糖、 セルロース等) 、 着色剤、
防腐剤 (塩化ベンザ/レコニゥム、 パラベン等) 、 吸収促進剤等を必要に応じ て適宜選択して調製される。
吸入用液剤を投与する際には通常噴霧器 (アトマイザ一、ネブライザ一) が使用され、 吸入用粉末剤を投与する際には通常粉末薬剤用吸入投与器が使 用される。
非経口投与のためその他の組成物としては、 ひとつまたはそれ以上の活性 物質を含み、 常法により処方される直腸内投与のための坐剤、 および膣内投 与のためのペッサリー等が含まれる。
本発明化合物の命名について以下に示す。
本明細書中に用いた化合物名は、 一般的に I UP ACの規則に準じて命名 を行なうコンピュータプログラム、 ACD/Nameバッチ (登録商標、 Advanced Chemistry Development Inc.社製) を用いるか、 または IUPAC命名法に 準じて命名したものである。 例えば、 A1および A2がイミダゾールー 2—ィ ル基、 B1および B 2がメチレン基、 Dが窒素原子、 Gがカルボ-ル基、 Eが 1, 4一フエエレン基、 Lがー CH2— NH—、 Jがー (CH2) 4— N (CH 2CH2CH3) 2を表わす化合物、 すなわち、
で示される化合物は、 4一 ( { [4— (ジプロピルァミノ) プチル] アミノ} メチル) 一 N, N—ビス (1H—イミダゾールー 2—ィルメチル) ベンゾァ ミドと命名される。
[発明の効果]
本発明化合物は、 CXCR4拮抗作用を有することから、 CXCR4が関 与する疾患、 すなわち CXCR4介在性疾患の予防および Zまたは治療剤と
して有用である 発明を実施するための最良の形態
以下、 実施例によって本発明を詳述するが、 本発明はこれらに限定される ものではない。
固体生成物は偏光顕微鏡を用いて結晶性を確認した。
クロマトグラフィーによる分離の箇所、 TLCに示されているカツコ内の 溶媒は、 使用した溶出溶媒または展開溶媒を示し、 割合は体積比を表わす。
NMRは、 30 OMHzの1 HNMRの測定値であり、 NMRの箇所に示さ れているカツコ内の溶媒は、 測定に使用した溶媒を示している。
MSは、 特に記載していなければ E S I (エレクトロンスプレ■ fオン) 法を用い、 陽イオン (pos.) のみの検出を行なった。
なお、 HPLC条件は、 以下の通りである。
使用機器: Waters LC/MS,
カラム: Xterra (登録商標) MS C18 5 /z m, 3x50 mm ID. 、 流速: 1. 5 mL/ m i nN
溶媒: A液: 0.1%トリフルォロ酢酸水溶液、
B液: 0.1%トリフルォロ酢酸一ァセトュトリノレ溶液。
測定開始後 1分間は A液と B液の混合比を 95 : 5に固定した。 その後 3 分間で A液と B液の混合比を 5 : 95に直線的に変えた。 その後 0.5分間 A液 と B液の混合比を 5: 95に固定した。その後 0.01分間で A液と B液の混合比 を 95 : 5に直線的に変えた。
実施例 1 : N— (4ーメ トキシベンジル) — N, N—ビス [ (1一 { [2— (トリメチルシリル) エトキシ] メチル } —1H—イミダゾールー 2—ィル) メチル] ァミン (化合物 1 )
1 - ( { [2- (トリメチルシリル) ェチルォキシ] メチル } 一 1H—ィ
P2005/016066
ミダゾール -2—カルボアルデヒド (CAS登録番号: 101226-42-0、 1.5 g) と { [4— (メチルォキシ) フエ-ル] メチル } ァミン (0.39m L) の 1 %酢 酸ジクロロメタン (l OmL) 溶液に三ァセトキシ水素化ホウ素ナトリウム (1.91 g) を加えた。反応混合物を室温で 16時間撹拌した。反応混合物に 1 N水酸化ナトリウム水溶液を加え、 ジクロロメタンで抽出した。 抽出物を飽 和食塩水で洗浄し、 無水硫酸ナトリウムで乾燥し、 濃縮した。 得られた残渣 をシリカゲルカラムクロマトグラフィー (酢酸ェチル:メタノール: トリエ チノレアミン = 1 : 0 : 0→10 : 1 : 0→10 : 1 : 0. i) によって精製 し、 以下の物性値を有する標題ィ匕合物 (1.71 g) を得た。
TLC:Rf 0.51 (クロ口ホルム:メタノール: 28%アンモエア水 =80:10:1) ;
NMR (CDCla): δ 7.20 (d, 2H), 6.97 (m, 4H), 6.83 (d, 2H), 5.11 (s, 4H), 3.82 (s, 4H), 3.78 (s, 3H), 3.60 (s, 2H), 3.24 (m, 4H), 0.77 (m, 4H), -0.05 (s, 18H)。 実施例 2 : N, N—ビス [ (1— { [2— (トリメチレシリ /レ) エトキシ] メチル } 一 1H—イミダゾールー 2一^ Tル) メチル] ァミン (化合物 2) 化合物 1 (665m g) のエタノール (5mL) 溶液に、 アルゴン雰囲気下、 20%水酸化パラジウム一炭素 (500m g) を加えた。 反応混合物を水素ガス 雰囲気下、 65°Cで 3時間撹拌した。 反応混合物を、 セライト (商品名) を 通してろ過し、 濃縮した。 得られた残渣をシリカゲルカラムクロマトグラフ ィー (ジクロロメタン:メタノール: 28%アンモニア水 = 10 : 1 : 0→80 : 10 : 1) によって精製し、 以下の物性値を有する標題化合物 (467m g) を 得た。
TLC: Rf 0.32 (クロ口ホルム:メタノール: 28%ァンモユア水 = 80:10:1); NMR (CDCla): δ 6.97 (m, 4H), 5.35 (s, 4H), 3.47 (m, 4H), 3.18 (m, 4H), 0.88 (m, 4H), -0.03 (s, 18H)。
実施例 3 :メチノレ 4- [ ( {4- [ (tert—ブトキシカノレポ二ノレ) ァミノ] ブチル } ァミノ) メチル] ベンゾエート (化合物 3)
1一 ( { [ 2— (トリメチルシリル) ェチルォキシ] メチル } 一 1 H—ィ ミダゾーノレ一 2—カルポアノレデヒドの代わりに、 メチル 4ーホルミノレベン ゾエートを、 { [4- (メチルォキシ) フエュル] メチル } ァミンの代わり に、 1, 1ージメチルェチル (4一アミノブチル) カーバメートを用いて、 実施例 1と同様の操作をし、 以下の物性値を有する標題化合物を得た。
TLC: Rf0.45 (クロ口ホルム:メタノール = 10: 1);
NMR (CDCla): δ 7.99 (d, 2H), 7.39 (d, 2H), 4.77 (m, IH), 3.91 (s, 3H), 3.84 (s, 2H), 3.13 (m, 2H), 2.64 (m, 2H), 1.54 (m, 4H); 1.44 (s, 9H)。
実施例 4 :メチル 4一 [ ( [ (ベンジルォキシ) カルボニル] {4- [ (tert 一ブトキシカルボニル) ァミノ] プチル} ァミノ) メチル]ベンゾエート (化 合物 4)
化合物 3 (810m g) と炭酸ナトリウム (383m g) の水 (5mL) とテト ラヒドロフラン (2mL) 溶液に、 0°Cでべンジル クロ口ホルメート (413 μ 1 ) を加えた。 反応混合物を 0°Cで 1時間撹拌した。 反応混合物を酢酸ェ チルで希釈した。 有機層を水、 飽和食塩水で洗浄し、 無水硫酸ナトリウムで 乾燥し、濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィー (へ キサン:酢酸ェチル =4 : 1→3 : 1) によって精製し、 以下の物性値を有 する標題化合物 (1.16 g) を得た。
TLC: Rf 0.27 (へキサン:酢酸ェチル = 3:1);
NMR (CDCla): δ 7.97 (m, 2H), 7.27 (m, 7H), 5.17 (m, 2H), 4.53 (s, 2H),
4.41 (m, 1H), 3.91 (s, 3H), 3.26 (m, 2H), 3.09 (m, 2H), 1.47 (m, 4H), 1.43 (s, 9H)。
実施例 5 : 4— [ ( [ (ベンジルォキシ) カノレポ二ノレ] {4一 [ (tert—ブト キシカルボニル) ァミノ] ブチル } ァミノ) メチル] 安息香酸 (化合物 5) 化合物 4 (1.13 g) のメタノール (4mL)溶液に 2 N水酸化ナトリウム水 溶液 (4mL) を加えた。 反応混合物を室温で 3時間撹拌した。 反応混合物
を濃縮した。 得られた残渣に 2 N塩酸を加え、 酢酸ェチルで抽出した。 抽出 物を飽和食塩水で洗浄し、 無水硫酸ナトリウムで乾燥し、 濃縮し、 以下の物 性値を有する標題化合物を得た。
TLC:Rf0.51(クロ口ホルム:メタノール:酢酸 =90:10:5);
NMR (CDCls): 58.03 (m, 2H), 7.26 (m, 7H), 5.17 (m, 2H), 4.55 (s, 2H),
4.39 (m, 1H), 3.26 (m, 2H), 3.05 (m, 2H), 1.49 (m, 4H), 1.44 (s, 9H)。
実施例 6 :フエニノレメチノレ ( {4— [ (ビス { [1一 ( { [2— (トリメ チルシリル) ェチル] ォキシ } メチル) 一 1 H—イミダゾールー 2—ィル] メチル } ァミノ) 力ルポ-ル] フエュル } メチル) [4- ( { [ (1, 1一 ジメチルェチル) ォキシ] カルボ二ル} ァミノ) ブチル] カーバメート (化 合物 6)
化合物 5 (137m g) のジクロロメタン (3mL) 溶液に、 化合物 2 (131 mg) 、 1—ヒドロキシベンゾトリアゾール (69m g) 、 1—ェチルー 3— [3- (ジメチルァミノ) プロピル] カルポジイミ ド塩酸塩 (86m g ) 、 ジ イソプロピゾレエチルァミン (105 μ 1) を加えた。 反応混合物を室温で 5時間 撹拌した。 反応混合物に水を加え、 ジクロロメタンで抽出した。 抽出物を飽 和食塩水で洗浄し、 無水硫酸ナトリウムで乾燥し、 濃縮した。 得られた残渣 をシリカゲルカラムクロマトグラフィー (へキサン:酢酸ェチル = 100 : 0→0 : 100→ジクロロメタン:メタノーノレ- 10 : 1) によって精製し、 以下の物性値を有する標題化合物 (225m g) を得た。
TLC: Rf0.38 (クロ口ホルム:メタノール:酢酸 = 90:10:5);
NMR (GDGls): 57.33 (m, 9B), 7.16 (m, 4H), 5.55 (s, 2H), 5.15 (s, 4H), 4.89
05016066
(m, 2H), 4.47 (s, 2H), 4.41 (m, 1H), 3.60 (m, 4H), 3.22 (m, 6H), 1.58 (m, 4H), 1.44 (s, 9H),- 0.92 (m, 4H),0.05 (s, 18H)。
実施例 7 :ベンジル 4一アミノブチル [4一 ( {ビス [ (1一 { [2— (ト リメチルシリル) エトキシ] メチル } — 1 H—イミダゾールー 2—ィル) メ チル] アミノ} 力ルポュル) ベンジル] カーバメート (化合物 7)
化合物 6 (225m g ) に 25%トリフルォロ酢酸のジクロロメタン溶液 (6 mL) を加えた。 反応混合物を室温で 1時間撹拌した。 反応混合物を濃縮し た。 残渣に 1 N水酸化ナトリゥムを加え、 ジクロロメタンで抽出した。 抽出 物を飽和食塩水で洗浄し、 無水硫酸ナトリウムで乾燥し、 濃縮した。 得られ た残渣をシリカゲルカラムクロマトグラフィー (ジクロロメタン:メタノー ル: 28%アンモニア水 = 80 : 10 : 1) によって精製し、 以下の物性値を 有する標題化合物 (92m g) を得た。
TLC:Rf 0.31 (クロ口ホルム:メタノール: 28%アンモニア水 =80:10:1); NMR (CDCls): 57.32 (m, 9H), 7.14 (m, 4H), 5.51 (s, 2H), 5.16 (s, 4H), 4.88 (m, 2H), 4.47 (s, 2H), 3.53 (m, 4H), 3.25 (m, 6H), 1.58 (m, 4H), 0.92 (m, 4H), -0.04 (s, 18H)。
実施例 8 :ベンジノレ 4一 ( {ビス [ (1— { [2— (トリメチルシリル) エトキシ] メチル } 一 1H—イミダゾール一 2—ィル) メチル] アミノ} 力 ルポュル) ベンジル [4一 (ジプロピルァミノ) プチル] カーバメート (化 合物 8 )
1— ( { [2— (トリメチルシリル) ェチルォキシ] メチル } —1H—ィ ミダゾ一ルー 2—力ルポアルデヒドの代わりに、 1—プロパ^ "一ルを、 { [4 一 (メチ /レオキシ) フエ-ル] メチノレ } ァミンの代わりに、 化合物 7を用い て、 実施例 1と同様の操作をし、 以下の物性値を有する標題化合物を得た。 TLC:Rf 0.63 (クロ口ホルム:メタノール: 28%アンモニア水 =80:10:1) ;
NMR (CDC13): δ 7.63 (d, J=8.1 Hz, 2H), 7.29 (m, 7H), 7.02 (m, 4H), 5.51
(m, 2H), 5.17 (s, 4H), 4.84 (m, 2H), 4.66 (s, 2H), 4.47 (s, 2H), 3.53 (m, 2H), 3.35 (m, 2H), 3.24 (m, 2H), 2.58 (m, 6H), 1.55 (m, 8H), 0.92 (m, 6H), 0.76 (m, 4H),-0.03 (s, 18H)。
実施例 9 : 4一 ( { [4— (ジプロピルァミノ) ブチル] アミノ } メチル) 一 N, N—ビス [ (1一 { [2— (トリメチルシリル) エトキシ] メチル } 一 1H—イミダゾールー 2—ィル) メチノレ] ベンズアミ ド (化合物 9) 化合物 1の代わりに、 化合物 8を、 20%水酸化パラジウム一炭素の代わ りに、 10%パラジウム一炭素を用 て実施例 2と同様の操作をし、 以下の 物性値を有する標題化合物を得た。
TLC: Rf 0.45 (クロロホルム:メタノール: 28%アンモニア水二 80:10:1)。
実施例 10 : 4— ( { [4一 (ジプロピルァミノ) プチル] アミノ } メチル) 一 N, N—ビス (1H—イミダゾールー 2—ィルメチル) ベンズアミ ド (化 合物 10)
化合物 9のメタノール (2mL) 溶液に濃塩酸 (2mL) を加えた。 反応 混合物を 80でで 5時間撹拌した。 反応混合物に 5 N水酸化ナトリゥム水溶 液を加え、 ジクロロメタンで抽出した。 抽出物を飽和食塩水で洗浄し、 無水 硫酸ナトリウムで乾燥し、 濃縮した。 得られた残渣をシリカゲルカラムクロ マトグラフィー (ジクロロメタン:メタノール: 28%アンモニア水 = 80 : 1 0 : 1→80 : 20 : 4) によって精製し、 以下の物性値を有する標題化合 物 (21m g) を得た。
TLC: Rf 0.67 (クロ口ホルム:メタノール: 28%アンモニア水 = 80:20:4); MR (DMSO-de): 50.80 (t, J=7.20 Hz, 6H), 1.18-1.49 (m, 8H), 2.18-2.36
(m, 6H), 2.39-2.47 (m, 2H), 3.68 (s, 2H), 4.47-4.68 (m, 4H), 6.78-7.18 (m, 4H), 7.32 (d, J=7.80 Hz, 2H), 7.42 ( J=7.80 Hz, 2H), 11.85-12.96 (m, 2H)。 実施例 1 1 : 4一 ( { [ 3 - (ジブチノレアミノ) プロピル] アミノ} メチル) 一 N, N—ビス (1 H—イミダゾールー 2—ィルメチル) ベンズアミ ド (化 合物 1 1 )
1— ( { [ 2— (トリメチルシリル) ェチルォキシ] メチル } — 1 H—ィ ミダゾール一 2一カルポアノレデヒドの代わりにメチル 4一ホルミルべンゾ エートを、 { [ 4一 (メチルォキシ) フエ-ノレ] メチル } ァミンの代わりに N, N—ジブチルー 1 , 3—プロパンジァミンを用いて、 実施例 1と同様の 操作をして、 メチル 4— ( { [ 3— (ジブチルァミノ) プロピル] アミ ノ} メチル) ベンゾエート (化合物 1 1— a ) を得た。 実施例 4の工程にお いて、 化合物 3の代わりに化合物 1 1— aを用いて、 実施例 4→実施例 5→ 実施例 6→実施例 9→実施例 1 0と同様の操作をし、 以下の物性値を有する 標題化合物を得た。
性状:油状物
TLC: Ef 0.51 (ジクロロメタン:メタノール: 28%アンモニア水 = 80:20:3) ;
NMR (CDCls): δ 0.89 (t, J=7.2 Hz, 6H), 1.16-1.46 (m, 8H), 1.55-1.72 (m,
2H), 2.31-2.50 (m, 6H), 2.64 (t, J=6.9 Hz, 2H), 3.78 (s, 2H), 4.51-4.77 (m, 4H), 6.89-7.11 (m, 4H), 7.35 (d, J=8.1 Hz, 2H), 7.55 (d, J=8.1 Hz, 2H)。 実施例 1 1 ( 1 ) 〜実施例 1 1 ( 2 1 )
N, N—ジプチルー 1 , 3—プロパンジァミンの代わりに相当するァミン 化合物を用いて、実施例 1 1と同様の操作をし、以下の本発明化合物を得た。
実施例 11 (1) : 4一 ( { [4- (ジプロピルアミノ) 一 4一ォキソプチ ル] アミノ} メチル) 一 N, N〜ビス (1 H—イミダゾールー 2—ィルメチ ル) ベンズァミ ド (化合物 11— 1)
性状:アモルファス
TLC: Rf 0.58 (ジクロロメタン:メタノール: 28%アンモニア水 = 80:20:3); NME (CDCls): 50.77-0.98 (m, 6H), 1.40-1.64 (m, 4H), 1.72-1.91 (m, 2H), 2.36 (t, J=7.2 Hz, 2H), 2.68 (t, J=7.2 Hz, 2H), 3.08—3.32 (m, 4H), 3.81 (s, 2H), 4.45-4.80 (m, 4H), 6.92-7.10 (m, 4H), 7.33 (d, J=8.1 Hz, 2H), 7.48 (d, J=8.1Hz, 2H)。
実施例 11 (2) : 4一 ( { [5— (ジプロピルアミノ) ペンチル] ァミノ) メチル) 一 N, N—ビス (1H— ^ ミダゾ一ルー 2—ィルメチル) ベンズァ ミド (化合物 11— 2)
性状:ァモノレファス
TLC: Rf 0.52 (ジクロロメタン:メタノール: 28%アンモユア水 = 80:20:3); NME (CDCla): δ 0.86 (t, J=7.5 Hz, 6H), 1.16-1.64 (m, 10H), 2.26-2.48 (m, 6H), 2.60 (t, J=7.2 Hz, 2H), 3.78 (s, 2H), 4.48-4.78 (m, 4H), 6.85-7.10 (m, 4H), 7.33 (d, J=8.1 Hz, 2H), 7.52 (d, J=8.1 Hz, 2H)。
実施例 11 (3) : 4— ( {4一 [ (ジプロピルアミノ) メチル] 一 1—ピ ペリジ-ル } メチル) 一 N, N—ビス (1H—イミダゾールー 2—ィルメチ ル) ベンズァミ ド (化合物 11-3)
性状:ァモルファス
TLC: Ef 0.40 (メタノール: 28%アンモニア水 = 99:1);
NMR (CDCla): δ 0.85 (t, J=7.5 Hz, 6H), 1.04—1.26 m, 2H), 1.29—1.50 (m, 5H), 1.62-1.80 (m, 2H), 1.83-2.02 (m, 2H), 2.18 (d, J=6.9 Hz, 2H),
2.23-2.37 m, 4H), 2.72-2.90 (m, 2H), 3.48 (s, 2H), 4.55-4.78 (m, 4H), 6.87-7.12 (m, 4B), 7.35 (d, J=8.1 Hz, 2H), 7.57 (d, J=8.1 Hz, 2H)。
実施例 1 1 (4) : 4- ( { [4- (ジプロピルァミノ) シクロへキシル] ァミノ) メチル) 一 Ν, Ν—ビス ( 1 Η—イミダゾールー 2—^ ルメチル) ベンズアミド (化合物 1 1—4)
性状:アモルファス
TLC: Rf0.22 (メタノール: 28%アンモニア水 = 99: 1);
NMR (CDCls): 50.77-0.92 (m, 6H), 0.99-2.06 (m, 12H), 2.28-2.56 (m, 6H), 3.69-3.89 (m, 2H), 4.52-4.78 (m, 4H), 6.91-7.15 (m, 4H), 7.29-7.45 (m, 2H), 7.48-7.64 (m, 2H)。
実施例 1 1 (5) : N, N—ビス (1H—イミダゾール一 2—ィルメチル) -4- [ (2—プロピル一 2, 9—ジァザスピロ [5. 5] ゥンデカー 9一 ィル) メチル] ベンズァミ ド (化合物 1 1— 5)
性状:アモルファス
TLC: Rf 0.32 (メタノール: 28%アンモニア水 = 99:1);
NMR (CDC13): δ 0.87 (t, J=7.5 Hz, 3H), 1.20-1.34 (m, 2H), 1.36-1.64 (m, 8H), 2.01-2.45 (m, 10H), 3.41-3.54 (m, 2H), 4.56-4.77 (m, 4H), 6.89-7.13 (m, 4H), 7.35 (d, J=8.1 Hz, 2H), 7.54 (d, J=8.1 Hz, 2H)。
実施例 1 1 (6) : N, N—ビス (1H—イミダゾールー 2—ィルメチル) 一 4一 [ (2—プロピル一 2, 8—ジァザスピロ [4. 5] デカ一 8—ィル) メチル] ベンズァミド (化合物 1 1— 6)
性状:アモルファス
TLC :Rf 0.13 (メタノール: 28%アンモエア水 =99:1);
NMR (CDCls): δ 0.89 (t, J=7.5 Hz, 3H), 1.40-1.69 (m, 8H), 2.23-2.44 (m, 8H), 2.57 (t, J=6.9 Hz, 2H), 3.46 (s, 2H), 4.55-4.77 (m, 4H), 6.86—7.14 (m, 4H), 7.35 (d, J=8.1 Hz, 2H), 7.56 (d, J=8.1 Hz, 2H)。
'実施例 1 1 (7) : N, N—ビス (1H—イミダゾールー 2—ィルメチル) -4- [ (4 _プロピル一 1, 4—ジァゼパン一 1一ィル) メチル] ベンズ
アミ ド (化合物 1 1-7)
性状:アモルファス
TLC :Kf 0.22 (メタノール: 28%アンモニア水 =99:1);
NMR (CDCls): δ 0.87 (t, J=7.5 Hz, 2H), 1.32-1.60 (m, 3H), 1.68—1.85 (m, 2H), 2.34-2.50 (m, 2H), 2.56-2.80 (m, 8H), 3.62 (s, 2H), 4.52-4.80 (m, 4H), 6.85-7.13 (m, 4H), 7.37 (d, J=8.1 Hz, 2H), 7.54 (d, J=8.1 Hz, 2H)。
実施例 1 1 (8) : 4- { [ (3 S) 一 1—プチルー 3—イソプチルー 2, 5—ジォキソー1, 4, 9_トリァザスピロ [5: 5] ゥシデ力一 9一ィル] メチル } -N, N—ビス (1 H—イミダゾールー 2—ィルメチル) ベンズァ ミド (化合物 1 1一 8)
性状:アモルファス
TLC: Rf 0.69 (メタノ一ノレ: 28%アンモニア水 = 99:1);
NMR (COCW: 50.83-1.06 (m, 9H), 1.21-2.23 (m, 11H), 2.47-2.96 (m, 4H), 3.25-3.50 (m, 2H), 3.56 (s, 2H), 3.86-4.02 (m, IH), 4.54-4.78 (m, 4H), 6.09-6.29 (m, IH), 6.90-7.12 (m, 4H), 7.37 (d, J=8.1 Hz, 2H), 7.58 (d, J=8.1
実施例 1 1 ( 9 ) : N, N—ビス ( 1 H—イミダゾールー 2—ィルメチル) -4- (1ーピペリジエルメチル) ベンズアミ ド (化合物 1 1一 9) 性状:ァモレファス
TLC: Rf 0.51 (メタノール: 28%アンモエア水 = 99:1);
NMR (CDC13): 51.33-1.48 (m, 2H), 1.48 - 1.63 (m, 4H), 2.24-2.45 (m, 4H), 3.46 (s, 2H), 4.54-4.76 (m, 4H), 6.95-7.11 (m, 4H), 7.36 (d, J=8.1 Hz, 2H), 7.58(d, J=8.1Hz, 2H)。
実施例 1 1 (10) : 4— ( { [3— (ジブ口ピルァミノ) プロピル] ァミ ノ} メチル) 一 N, N—ビス (1H—イミダゾールー 2—ィルメチル) ベン ズアミド (化合物 1 1— 10)
'I生状:ァモノレファス
TLC: Kf0.28 (メタノール: 28%アンモエア水 = 99:1);
NMR (GDCls): 60.84 (t, J=7.5 Hz, 6H), 1.31-1.52 (m, 4H), 1.53-1.74 (m, 2H), 2.26-2.39 (m, 4H), 2.45 (t, J=6.86 Hz, 2H), 2.64 (t, J=6.9 Hz, 2H), 3.77 (s, 2H), 4.50-4.79 (m, 4H), 6.84-7.13 (m, 4H), 7.32 (d, J=8.1 Hz, 2H), 7.51 (d, J=8.1Hz,2H)。
実施例 11 (11) : 4— ( { [2— (ジプロピルアミノ) ェチル] アミノ} メチル) 一N, N—ビス (1H—イミダゾールー 2—ィルメチル) ベンズァ ミド (化合物 11-1 1)
性状:アモルファス
TLC: Rf0.42 (メタノール: 28%アンモエア水 = 99:1);
NMK (CDC13): 50.84 (t, J=7.5 Hz, 6H), 1.30-1.53 (m, 4H), 2.25-2.41 (m, 4H), 2.48-2.58 (m, 2H), 2.59-2.70 (m, 2H), 3.80 (s, 2H), 4.50-4.79 (m, 4H), 6.86-7.14 (m, 4H), 7.34 (d, J=8.1 Hz, 2H), 7.56 (d, J=8.1 Hz, 2H)。
実施例 11 (12) : 4- { [7- (ジブ口ピルァミノ) _3, 4—ジヒ ド 口一 2 (1H) —イソキノリニル] メチル } 一 N, N—ビス (1H—イミダ ゾールー 2—ィルメチル) ベンズァミド (化合物 11— 12)
性状 : アモルファス
TLC: RfO.54 (メタノール: 28%アンモニア水 = 99:1);
NMR (CDCls): 50.89 (t, 3=1.5 Hz, 6H), 1.42-1.68 (m, 4H), 2.61-2.87 (m, 4H), 3.06-3.25 (m, 4H), 3.54 (s, 2H), 3.67 (s, 2H), 4.56-4.77 (m, 4H), 6.23 (d, J=2.7 Hz, IH), 6.48 (dd, J=8.7, 2.4 Hz, IH), 6.93 (d, J=8.7 Hz, IH), 6.96-7.13 (m, 4H), 7.45 (d, J=8.1 Hz, 2H), 7.59 (d, J=8.1 Hz, 2H)。
実施例 1 1 (13) : N, N—ビス (IH—イミダゾールー 2—ィルメチル) 一 4— [ (9一プロピル一 3, 9ージァザスピロ [5. 5] ゥンデ力一3— ィル) メチル] ベンズアミ ド (化合物 11— 13)
性状:アモルファス
TLC: RfO.61 (ジクロロメタン:メタノール: 28%アンモユア水 = 80:20:3); NMK, (CDCls): δ 0.88 (t, J=7.5 Hz, 3H), 1.33-1.66 (m, 10H), 2.16-2.49 (m, 10H), 3.50 (s, 2H), 4.54-4.79 (m, 4H), 6.91-7.12 (m, 4H), 7.35 (d, J=8.1 Hz, 2H), 7.55 (d, J=8.1 Hz, 2H)。
実施例 1 1 (14) : N, N—ビス (1 H—イミダゾールー 2—ィルメチル) — 4一 [ (9一プロピル一 2, 9ージァザスピロ [5. 5] ゥンデカー 2— ィル) メチル] ベンズァミド (化合物 1 1 - 14)
性状:アモルファス
TLC: RfO.64 (ジクロロメタン:メタノール: 28%アンモユア水 = 80:20:3); NME, (CDCls): 50.85 (t, J=7.5 Hz, 3H), 1.21-1.68 (m, 10H), 1.99-2.49 (m, 10H), 3.42 (s, 2H), 4.51-4.80 (m, 4H), 6.87-7.15 (m, 4H), 7.35 (d, J=8.1 Hz, 2H), 7.55(d, J=8.1Hz, 2H)。
実施例 1 1 (1 5) : N, N—ビス (1 H—イミダゾール一 2—ィルメチル) -4- ( { [ (1—プロピル一 4ーピペリジニル) メチル] アミノ} メチル) ベンズァミド (化合物 1 1 - 1 5)
性状:アモルファス
TLC: R£0.15 (ジクロロメタン:メタノール: 28%アンモ-ァ水 = 80:20:3); NMR (CDC13): δ 0.88 (t, J=7.32 Hz, 3H), 1.14 - 1.35 (m, 2H), 1.37-1.60 (m, 3H), 1.63-1.79 (m, 2H), 1.81-1.98 (m, 2H), 2.19-2.34 (m, 2H), 2.48 (d, J=6.77 Hz, 2H), 2.84-3.02 (m, 2H), 3.79 (s, 2H), 4.51-4.76 (m, 4H),
6.91-7.16 (m, 4H), 7.37 (d, J=8.1 Hz, 2H), 7.63 (d, J=8.1 Hz, 2H)。
実施例 1 1 (1 6) : 4— ( { [4— (ジプロピルァミノ) フエ-ル] アミ ノ} メチル) -N, N—ビス (1 H—イミダゾーノレ一 2—イノレメチノレ) ベン ズァミド (化合物 1 1 - 1 6)
性状:暗緑色 アモルファス
TLC: Rf 0.64 (ジクロロメタン:メタノール: 28%アンモユア水 = 80:20:3); NMR (CDCla): 50.70-1.06 (m, 6H), 1.31-1.74 (m, 4H), 2.68—3.50 (m, 4H), 4.01-4.57 (m, 2H), 4.57-4.84 (m, 4H), 6.22-6.89 (m, 4H), 6.90-7.14 (m, 4H) 7.41 (d, J=8.1 Hz, 2H), 7.60 (d, J=8.1 Hz, 2H)。
実施例 1 1 (1 7) : 4— [ (2—ベンジル一 2, 9—ジァザスピロ [5. 5] ゥンデカー 9一^ fル) メチル] 一 N, N—ビス (1H—イミダゾールー 2—イノレメチル) ベンズァミド (化合物 1 1 - 1 7)
性状:アモルファス '
TLC: Rf0.67 (ジクロロメタン:メタノール: 28%アンモニア水 = 80:20:1); NMR (CDCla): δ 1.21-1.38 (m, 2H), 1.40 - 1.66 (m, 6H), 1.99-2.44 (m, 8H), 3.34-3.47 (m, 4H), 4.53-4.81 (m, 4H), 6.92-7.12 (m, 4H), 7.19-7.30 (m, 5H) 7.32 (d, J=8.1 Hz, 2H), 7.52 (d, J=8.1 Hz, 2H)。
実施例 1 1 (1 8) : 4— [ (2—シクロへキシル一 2, 9—ジァザスピロ
[5. 5] ゥンデ力一 9一ィル) メチル] — N, N—ビス (1H—イミダゾ 一ルー 2 fルメチル) ベンズァミ ド (化合物 1 1 - 1 8)
性状:アモルファス
TLC :Rf 0.40 (ジクロロメタン:メタノール: 28%アンモニア水 =80:20:1); NMR (CDC13): 61.08-1.84 (m, 18H), 2.13-2.54 (m, 9H), 3.48 (s, 2H), 4.57-4.77 (m, 4H), 6.93-7.13 (m, 4H), 7.36 (d, J=8.1 Hz, 2H), 7.53 (d, J=8.1 Hz, 2H)。
実施例 1 1 (1 9) : 4- { [ (3 S) 一 1一プチルー 3—イソブチルー 5 一ォキソ一 1, 4, 9一トリァザスピロ [5. 5] ゥンデカー 9—ィル] メ チル } — N, N—ビス (1H—イミダゾールー 2—ィルメチル) ベンズアミ ド (化合物 1 1- 1 9)
性状:アモルファス
TLC: Rf 0.60 (ジクロロメタン:メタノール: 28%アンモニア水 = 80:20:1);
NMR (CDCla): 80.81-1.03 (m, 9H), 1.13—1.53 (m, 6H), 1.56-1.73 (m, IH), 1.75-3.06 (m, 12H), 3.56 (s, 2H), 3.59-3.73 m, IH), 4.51-4.84 (m, 4H), 5.66 (s, IH), 6.91-7.10 (m, 4H), 7.36 (d, J=8.1 Hz, 2H), 7.49 (d, J=8.1 Hz, 2H)0
実施例 1 1 (20) : 4- { [ (3 S) 一 1一プチル一 3—イソブチル— 2 一ォキソ一4一プロピル一 1 , 4, 9一トリァザスピロ [5. 5] ゥンデ力 一 9一ィル] メチル } -N, N—ビス (1 H—イミダゾール一 2—ィルメチ ル) ベンズァミ ド (化合物 1 1 - 20)
性状: アモルファス
TLC: Rf 0.69 (ジクロロメタン:メタノール: 28%アンモニア水 = 80:20:1); NMR (CDCla): δ 0.75-1.02 (m, 12H), 1.19-2.22 (m, 17H), 2.45-2.67 (m, IH), 2.67-2.84 (m, 2H), 2.86-2.98 (m, IH), 2.98-3.16 (m, IH), 3.16-3.27 (m: 1H), 3.28-3.43 (m, IH), 3.50 (s, 2H), 4.54-4.81 (m, 4H), 6.93-7.12 (m, 4H), 7.37 (d, J=8.1 Hz, 2H), 7.58 (d, J=8.1 Hz, 2H)。
実施例 1 1 (2 1) : 4- { [ (3 S) - 1—プチルー 3—ィソプチル一 4 —プロピル一 1, 4, 9 _トリァザスピロ [5. 5] ゥンデカー 9—ィル] メチル } 一 N, N—ビス (1 H—イミダゾールー 2—ィルメチル) ベンズァ ミド (化合物 1 1— 2 1)
性状: アモルファス
TLC :Rf 0.67 (ジクロロメタン:メタノール: 28%アンモエア水 =80:20:1) ; NME, (CDCls): 80.78-1.00 (m, 12H), 1.10—1.69 (m, 11H), 1.78-2.35 (m, 9H), 2.49-2.82 (m, 5H), 2.93 - 3.09 (m, 1H), 3.37-3.58 (m, 2H), 4.51-4.82 (m: 4H), 6.91-7.14 (m, 4H), 7.36 (d, J=8.1 Hz, 2H), 7.55 (d, J=8.1 Hz, 2H)。
実施例 1 2 :ベンジル 6— ( {ビス [ (1一 { [2- (トリメチノレシリノレ) エトキシ] メチル } 一 1 H—イミダゾール一 2—ィル) メチル] ァミノ) 力 ルポュル) ー3, 4—ジヒドロ一 2 (1 H) —イソキノリンカルポキシレー
ト (化合物 12)
化合物 2、 および化合物 5の代わりに 2— [ (ベンジルォキシ) カルボ- ル] 一 1, 2, 3, 4ーテトラヒドロ一 6—イソキノリンカルボン酸を用い て、実施例 6と同様の操作をして、以下の物性値を有する標題化合物を得た。 TLC: R£0.34 (クロ口ホルム:メタノール = 10:1);
NMR (CDCla): 67.37 (m, 6H), 7.00 (m, 6H), 5.55 (m, 2H), 5.21 (m, 2H), 5.17 (s, 2H), 4.87 (m, 4H), 4.62 (s, 2H), 3.69 (t, J=5.7 Hz, 2H), 3.53 (m, 4H), 3.33 (m, 2H), 0.88 (m, 2H), 0.74 (m, 2H), -0.05 (s, 18H)。
実施例 13 : N, N—ビス [ (1一 { [2— (トリメチルシリル) エトキシ] メチル } 一 1 H—イミダゾール一 2—ィル) メチノレ] —1, 2, 3, 4—テ トラヒドロー 6—イソキノリンカルポキサミド (化合物 13)
化合物 1の代わりに化合物 12を、 20 %水酸化パラジウム一炭素の代わ りに 10%パラジウム一炭素を用いて実施例 2と同様の操作をし、 以下の物 性値を有する標題化合物を得た。
TLC:Rf 0.50 (クロ口ホルム:メタノール: 28%アンモニア水 =80:10:1) ;
NMK (CDC13): 57.43 (d, J=6.0 Hz, 1H), 7.36 (s, 1H), 6.99 (m, 5H), 5.50 (m, 2H), 5.15 (m, 2H), 4.84 (m, 2H), 4.69 (m, 2H), 4.04 (s, 2H), 3.53 (m, 2H), 3.52 (m, 2H), 3.15 (t, J=5.7 Hz, 2H), 2.81 (m, 2H), 0.77 (m, 2H), -0.05 (s, 18H)0
実施例 14 : 2- [4一 (ジプロピルアミノ) ブチル] — N, N—ビス [ (1 - { [2- (トリメチルシリル) エトキシ] メチノレ } - 1 H一^ f ミダゾ一ノレ —2—ィル) メチル] —1, 2, 3, 4ーテトラヒドロ一 6—イソキノリン カルボキサミド (化合物 14)
1― ( { [2- (トリメチルシリル) ェチルォキシ] メチル } 一 1 H—ィ ミダゾールー 2—力ノレボアノレデヒドの代わりに、 4一 (ジプロピルァミノ) プタナールを、 { [4一 (メチルォキシ) フエニル] メチル } ァミンの代わ
りに、 化合物 1 3を用いて、 実施例 1と同様の操作をし、 以下の物性値を有 する標題化合物を得た。
TLC : Rf 0.39 (クロ口ホルム:メタノール: 28%アンモニア水 = 80:10:1); NMR (CDCls) : 8 7.38 (m, 2H), 6.99 (m, 5H), 5.50 (s, 2H), 5.15 (sm, 2H), 4.84 (s, 2H), 4.68 (s, 2H), 3.58 (m, 4H), 3.33 (m, 2H), 2.84 (t, J=5.7 Hz, 2H), 2.70 (t, J=5.7 Hz, 2H), 2.51 (m, 4H), 1.60 (m, 12H), 0.90 (m, 10H), -0.05 (s, 18H)。
実施例 1 5 : 2— [ 4一 (ジプロピルァミノ) プチル] 一 N, N—ビス (1 H—ィミダゾーノレ一 2一イノレメチノレ) — 1, 2, 3, 4ーテトラヒドロー 6 一イソキノリンカルボキサミド (化合物 1 5 )
化合物 9の代わりに化合物 1 4を用いて、 実施例 1 0と同様の操作をして、 以下の物性値を有する標題化合物を得た。
性状: アモルファス
TLC : Ilf 0.67 (クロ口ホルム:メタノール: 28%アンモニア水 = 80:20:4) ; NMR (DMSO-de) : δ 0.81 (t, J=7.20 Hz, 6H), 1.27-1.43 (m, 6H), 1.43-1.59 (m, 2H), 2.22-2.31 (m, 4H), 2.34 (t, J=6.9 Hz, 2H), 2.41 (t, J=7.20 Hz, 2H), 2.59 (t, J=6.3 Hz, 2H), 2.72 (t, J=6.30 Hz, 2H), 3.50 (s, 2H), 4.43-4.57 (m, 2H), 4.57-4.71 (m, 2H), 6.75-6.98 (m, 2H), 6.99-7.16 (m, 4H), 7.20 (dd, J=7.8, 1.5 Hz, 1H), 12.03-12.57 (m, 2H)。
実施例 1 5 ( 1 ) 〜実施例 1 5 ( 3 )
実施例 1 2の工程において、 化合物 2またはその代わりにビス [ ( 1ーメ チルー 1 H—イミダゾール一 2—ィル) メチル] ァミンまたはビス (2—ピ
リジニノレメチル) アミンを用いて、 2— [ (ベンジルォキシ) カルボ-ノレ] —1 , 2 , 3, 4ーテトラヒドロー 6—イソキノリンカルボン酸またはその 代わりに 2— [ (ベンジルォキシ) カルボ-ル] —1, 2, 3, 4ーテトラ ヒドロ一 7—イソキノリンカノレボン酸を用いて、 実施例 1 2→実施例 1 3→ 実施例 1 4、 および所望により実施例 1 5と同様の操作をして、 以下の本発 明化合物を得た。
実施例 1 5 ( 1 ) : 2— [ 4— (ジプロピルァミノ) プチル] —N, N—ビ ス (1 H—イミダゾーノレ一 2—ィルメチノレ) 一 1, 2, 3 , 4—テトラヒド ロー 7—イソキノリンカルポキサミド (化合物 1 5— 1 )
性状:ァモルファス
TLC: Rf 0.30 (クロ口ホルム:メタノール: 28%ァンモユア水 二 80:10:1); NMR (DMSO-de): 80.81 (t, J=7.2 Hz, 6H), 1.27-1.45 (m, 6H), 1.45-1.58 (m, 2H), 2.22-2.31 (m, 4H), 2.32-2.37 (m, 2H), 2.37-2.45 (m, 2H), 2.60 (t, J=5.4 Hz, 2H), 2.78 (t, J=5.4 Hz, 2H), 3.43 (s, 2H), 4.45-4.70 (m, 4H), 6.72-6.99 (m, 2H), 6.99—7.15 (m, 3H), 7.16-7.31 (m, 2H), 11.94-12.28 (m, 1H), 12.28-12.63 (m, 1H)。
実施例 1 5 ( 2 ) : 2— [ 4— (ジプロピルァミノ) プチル] -N, N—ビ ス [ ( 1ーメチノレ一 1 H—イミダゾールー 2 fル) メチル] —1 , 2 , 3 , 4—テトラヒドロー 6—イソキノリンカルボキサミド (化合物 1 5 - 2 ) 性状: 油状物
TLC : Rf 0.33 (クロ口ホルム:メタノール: 28%アンモニア水 = 80:10:1); NMR (DMSO-de): 60.81 (t, J=7.5 Hz, 6H), 1.25-1.43 (m, 6H), 1.44 - 1.59 (m, 2H), 2.22-2.31 (m, 4H), 2.34 (t, J=6.0 Hz, 2H), 2.38-2.46 (m, 2H), 2.59 (t, J=5.7 Hz, 2H), 2.67-2.82 (m, 2H), 3.14-3.43 (m, 3H), 3.50 (s, 2H), 3.53-3.75 (m, 3H), 4.30-4.51 (m, 2H), 4.52-4.75 (m, 2H), 6.74-6.91 m, 2H) 6.97-7.13 (m, 3H), 7.15-7.23 (m, IH), 7.28 (d, J=8.1 Hz, 1H)。
実施例 15 (3) : 2— [4— (ジプロピルァミノ) プチル] 一 N, N—ビ ス ( 2—ピリジニルメチル) —1, 2, 3, 4—テトラヒドロー 6—イソキ ノリンカルボキサミド (化合物 15-3)
性状:油状物
TLC :Ef 0.48 (クロ口ホルム:メタノール: 28%アンモ-ァ水 =80:10:1) ; NMR (DMSO-de): 60.70-0.91 (m, 6H), 1.21-1.42 (m, 6H), 1.43-1.59 (m, 2H), 2.17-2.45 (m, 8H), 2.55-2.66 (m, 2H), 2.68-2.80 (m, 2H), 3.43-3.59 (m 2H), 4.60 (s, 2H), 4.67 (s, 2H), 6.99-7.09 (m, IH), 7.16-7.25 (m, 3H), 7.25-7.32 (m, 2H), 7.36 (d, J=8.4 Hz, IH), 7.65-7.93 (m, 2H), 8.42-8.72 (m, 2H)。
実施例 16 : 1— [4一 (ジエトキシメチル) フエュル] 一 N— [ (1 - { [2 — (トリメチノレシリル) エトキシ] メチノレ} 一 1 H—イミダゾールー 2—ィ ル) メチル] メタンァミン (化合物 16 )
1一 ( { [2- (トリメチノレシリノレ) ェチルォキシ] メチル } ― 1 H—ィ ミダゾールー 2—力ルポアルデヒドの代わりに 4一 (ジェトキシメチル) ベ ンズアルデヒドを、 { [4— (メチルォキシ) フエ二ノレ] メチル } アミンの 代わりに 1— (1一 { [2- (トリメチルシリル) エトキシ] メチル } 一 1 H—イミダゾール一 2—ィル) メタンアミンを用いて、 実施例 1と同様の操 作をし、 以下の物性値を有する標題化合物を得た。
TLC:Ef 0.63 (クロ口ホルム:メタノール: 28%アンモユア水 =80:10:1) ;
NME, (CDC13): 57.43 (d, J=7.8 Hz, 2H), 7.33 (J=7.8 Hz, 2H), 6.97 (m, 2H), 5.49 (s, 1H), 5.32 (s, 2H), 3.94 (s, 2H), 3.84 (s, 2H), 3.52 (m, 6H), 1.24 (m, 6H), 0.88 (m, 2H), -0.03 (s, 9H)。
実施例 17: N— [4一 (ジエトキシメチル)ベンジル] 一 N— [ (1— { [2 一 (トリメチルシリル) エトキシ] メチル } 一 1H—イミダゾールー 2—ィ ル) メチル] 一 1 H—イミダゾールー 2—カルボキサミ ド (化合物 17 )
化合物 16 (1.93 g)、 1H—イミダゾールー 2—力ルボン酸(773 mg) およびジイソプロピノレエチ ァミン (2.97 g) のジクロロメタン (15 mL) 溶液に O— (7—ァザべンゾトリァゾールー 1一ィル) N, N, N,, N,ーテ トラメチルゥロニゥムへキサフルォロホスフェート (HATU) (2.62 g) を氷冷下加えた。 反応混合物を室温で 4時間撹拌した。 反応混合物に IN水 酸化ナトリウム水溶液 (30 mL) を加えた。 水層をジクロロメタン (50 m L) で 2回抽出した。 有機層を合わせて飽和食塩水で洗浄し、 無水硫酸マグ ネシゥムで乾燥し、 濃縮した。 残渣をシリカゲルクロマトグラフィー (酢酸 ェチル:メタノール = 1 : 0→10: 1) によって精製し、 以下の物性値を有 する標題化合物 (977 mg) を得た。
TLC: Rf 0.44 (クロロホルム:メタノール: 28%アンモニア水 =80:10:1); NMR (CDCls): 57.41 (m, 4H), 7.15 (s, 2H), 7.04 (s, 1H), 6.96 (m, 1H), 5.82 (s, 1H), 5.77 (s, 1H), 5.46 (s, 1H), 5.37 (s, 1H), 5.23 (s, 1H), 4.83 (s, 1H), 4.76 (s, 1H), 3.51 (m, 6H), 1.25 (m, 6H), 0.82 (t, J=8.1 Hz, 2H), -0.06 (s, 9H)0
実施例 18 : N— (4一ホルミルベンジル) 一 N— (1H—イミダゾール一 2一ィルメチル) 一 1 H—イミダゾール一 2—カルボキサミ ド (化合物 18 ) 化合物 1 7 (970 mg) に 50 %トリフルォロ酢酸一ジクロロメタン溶液 (10 mL) を氷冷下加えた。 反応混合物を室温で 3時間撹拌した。 反応混合 物を濃縮した。 残渣に 2 N水酸化ナトリウム水溶液 (20 mL) を加えた。 水 層をジクロロメタン (50 mL) で 2回抽出した。 有機層を合わせて飽和食塩 水で洗浄し、 無水硫酸マグネシウムで乾燥し、 濃縮し、 以下の物性値を有す る標題化合物を得た。 得られた化合物は精製することなく次の反応に用いた。 TLC:Rf 0.50 (クロ口ホルム:メタノール: 28%アンモエア水 =80:10:1); NMR (CDCls): 89.98 (s, 1H), 7.81 (d, J=8.1 Hz, 2H), 7.49 (d, J=8.1 Hz, 2H), 7.23 (s, 2H), 7.08 (s, 2H), 5.04 (s, 2H), 4.87 (s, 2H)。
実施例 19 : N— [4一 ( { [4一 (ジプロピルァミノ) プチル] アミノ } メチル) ベンジル] 一 N— (1H—イミダゾールー 2—ィルメチル) 一 1H ーィミダゾールー 2—力ルポキサミド (化合物 19)
1— ( { [2— (トリメチルシリル) ェチルォキシ] メチル } —1H—ィ ミダゾールー 2一力ノレボアルデヒドの代わりに化合物 18を、 { [4一 (メ チルォキシ) フエ-ノレ] メチル } ァミンの代わりに N, N—ジプロピル一 1, 4—プタンジァミンを用いて、 実施例 1と同様の操作をし、 以下の物性値を 有する標題化合物を得た。
性状:半固体
TLC :Rf 0.64 (クロ口ホルム:メタノール: 28%アンモユア水 =80:20:4);
NMK (DMSO-de): 60.80 (t, J=7.5 Hz, 6H), 1.22—1.51 (m, 8H), 2.16-2.35 (m, 6H), 2.44 (t, J=6.3 Hz, 2H), 3.63 (s, 2H), 4.48 (s, IH), 4.54 (s, 1H), 5.25 (s, 1H), 5.53 (s, IH), 6.72-6.92 (m, IH), 6.92-7.10 (m, IH), 7.11-7.22 (m, 3H), 7.22-7.36 (m, 3H), 11.70-12.25 (m, 2H)。
実施例 19 (1) 〜実施例 19 (19)
実施例 16の工程において、 1— (1— { [2— (トリメチルシリル) ェ トキシ] メチ /レ} — 1 H—イミダゾールー 2—ィノレ) メタンァミンまたはそ の代わりに相当するァミン化合物を、 実施例 17の工程において、 1H—ィ ミダゾールー 2—力ルボン酸またはその代わりに相当するカルボン酸を、 実 施例 19の工程において、 N, N—ジプロピル一 1, 4一ブタンジァミンま たはその代わりに相当するァミンを用いて、 実施例 16→実施例 17→実施
例 1 8→実施例 1 9と同様の操作をして、 以下の本発明化合物を得た。
実施例 1 9 ( 1 ) : N— [ 4— ( { [ 4— .(ジプロピルァミノ) ブチル] ァ ミノ } メチル) ベンジル] — N— [ ( 5—メチル一 2—ピリジエル) メチル] 一 1 H—イミダゾールー 2—カルボキサミド (化合物 1 9— 1 )
性状:油状物
TLC: Rf 0.27 (クロ口ホルム:メタノール: 28%アンモニア水 = 80:10:1); NME (DMSO-de): δ 0.80 (t, J=7.5 Hz, 6H), 1.25-1.46 (m, 8H), 2.18-2.34 (m, 9H), 2.37-2.47 (m, 2H), 3.62 (s, 2H), 4.53 (s, IH), 4.57 (s, 1H), 5.48 (s, 1H), 5.52 (s, IH), 6.86-7.41 (m, 7H), 7.47-7.61 (m, IH), 8.24-8.40 (m, IH), 12.50-13.44 (m, 1H)。
実施例 1 9 ( 2 ) : N— [ 4一 ( { [ 4— (ジブ口ピルァミノ) プチル] ァ ミノ } メチル) ベンジル] — N— (1 H—イミダゾールー 2—ィルメチノレ) 一 4—メチルー 1 H—イミダゾールー 2—カルボキサミド (化合物 1 9 - 2 ) TLC: Rf 0.47 (ジクロロメタン:メタノール: 28%ァンモユア水 - 90:10:2); NMR (CDCls): δ 0.86 (m, 6H), 1.38—1.60 (m, 8H), 2.15-2.50 (m, 9H), 2.58-2.68 (m, 2H), 3.78 (m, 2H), 4.45-4 98(m, 4H), 6.92-7.42 (m, 7H)。
実施例 1 9 ( 3 ) : N— [ 4— ( { [ 4— (ジプロピルァミノ) ブチル] ァ ミノ } メチル) ベンジル] 一 N— (1 H—イミダゾールー 2—ィルメチル) 一 2—ピリジンカノレポキサミド (化合物 1 9— 3 )
性状: 油状物
TLC : Rf 0.20 (クロ口ホルム:メタノール: 28%アンモニア水 = 80:10:1); NMR (DMSO-de): 8 0.75-0.90 (m, 6H), 1.26-1.47 (m, 8H), 2.16-2.37 (m, 6H), 2.38-2.47 (m, 2H), 3.63 (s, IH), 3.66 (s, IH), 4.47 (s, 1H), 4.52 (s, IH), 4.57 (s, IH), 4.59 (s, IH), 6.77-6.91 (m, IH), 7.05 (s, 1H), 7.15 (d, J=7.8 Hz, IH), 7.19-7.35 (m, 3H), 7.42-7.55 (m, IH), 7.59-7.76 (m, IH), 7.84-8.02 (m: IH), 8.50-8.72 (m, IH), 11.71-12.10 (m, 1H)。
実施例 19 (4) : N— [4— ( { [4一 (ジプロピルァミノ) プチノレ] ァ ミノ } メチル) ベンジル] — N— (2—ピリジ -ルメチル) 一1H— ^ f ミダ ゾール—2—力ルポキサミド (化合物 19-4)
性状: 油状物
TLC :Rf 0.31 (クロ口ホルム:メタノール: 28%アンモニア水 =80:10:1) ;
NMR (DMSO-de): δ 0.80 (t, J=7.5 Hz, 6H), 1.24-1.48 (m, 8H), 2.17-2.36 (m, 6H), 2.37-2.46 (m, 2H), 3.63 (s, 2H), 4.51-4.68 (m, 2H), 5.47-5.64 (m, 2H), 6.91-7.14 (m, IH), 7.24 (t, 7H), 7.73 (t, J=7.5 Hz, IH), 8.38-8.63 (m, 実施例 19 (5) : N— [4— ( { [4— (ジプロピルァミノ) プチル] 了 ミノ } メチル) ベンジル] — N— (2—ピリジエルメチル) 一 2—ピリジン カルボキサミ ド (化合物 19-5)
性状:油状物
TLC :Rf 0.29 (クロ口ホルム:メタノール: 28%アンモエア水 =80:10:1); NMR (DMSO-de): δ 0.70-0.89 (m, 6H), 1.24-1.48 (m, 8H), 2.16-2.36 (m, 6H), 2.36-2.47 (m, 2H), 3.57-3.72 (m, 2H), 4.51-4.73 (m, 4H), 7.11-7.18 (m: 1H), 7.19-7.38 (m, 5H), 7.39-7.51 (m, IH), 7.56-7.67 (m, IH), 7.67-7.97 (m 2H), 8.41-8.68 (m, 2H)。
実施例 19 (6) : N— [4- ( { [4一 (ジプロピルアミノ) プチル] ァ ミノ) メチル) ベンジル] 一 N— (1 H—ィミダゾール一 2一ィルメチル) 一 1 H—ピロ一ルー 2—力ルポキサミド (化合物 19-6)
性状:油状物
TLC :Rf 0.27 (クロ口ホルム:メタノール: 28%アンモニア水 =80:10:1); NMR (DMSO-de): 80.81 (t, J=7.50 Hz, 6H), 1.18-1.51 (m, 8H), 2.15—2.40 (m, 8H), 3.72 (s, 2H), 4.31-4.48 (m, 2H), 4.51-4.72 (m, 2H), 5.97-6.14 (m, IH), 6.73-7.47 (m, 9H), 11.58-12.28 (m, 1H)。
実施例 19 (7) : N— [4— ( { [4— (ジプロピルアミノ) プチノレ] ァ ミノ } メチノレ) ベンジル] -N- (5, 6, 7, 8—テトラヒ ドロ一 8—キ ノリ -ル) 一 1 H—イミダゾールー 2—カルボキサミド (化合物 19一 7 ) 性状: 油状物
TLC :Rf 0.43 (クロ口ホルム:メタノール: 28%アンモニア水 =80:10:1) ; NMR (DMSO-de): δ 0.80 (t, J=7.2 Hz, 6H), 1.22-1.51 (m, 8H), 1.61—2.08 (m, 2H), 2.17-2.35 (m, 8H), 2.36-2.47 (m, 2H), 2.58-2.96 (m, 2H),
3.51-3.71 (m, 3H), 4.73-5.11 (m, 1H), 5.34-5.67 (m, 1H), 6.92-7.36 (m, 7H) 7.39-7.59 (m, 1H), 8.19-8.43 (m, 1H), 12.43-13.40 (m, 1H)。
実施例 19 (8) : N— [4— ( { [4- (ジプロピルァミノ) プチル] 了 ミノ } メチノレ) ベンジル] —N— (1H—イミダゾールー 2—ィルメチル) 一 1 H—ピラゾールー 4一力ノレボキサミ ド (化合物 19-8)
性状:油状物
TLC: Rf0.15 (酢酸ェチル:メタノール: 28%アンモニア水 = 80:20:3); NMR (DMSO-de): 87.40-6.70 (m, 8H), 4.60-4.38 (m, 4H), 3.76 (m, 2H), 2.57 (m, 2H), 2.40-2.22 (m, 6H), 1.60-1.28 m, 8H), 0.82 (t, J=7.2 Hz, 6H)。 実施例 19 (9) : N— [4一 ( { [4一 (ジプロピルァミノ) ブチル] ァ ミノ } メチノレ) ベンジル] 一 N— (1H—イミダゾールー 2—ィルメチル) 一 1 H—イミダゾ一/レー 4一力ルポキサミド (化合物 19— 9)
性状:油状物
TLC: Rf 0.12 (酢酸ェチル:メタノール: 28%アンモユア水 = 80:20:3); NMR (DMSO-de): 87.88-7.65 (m, 2H), 7.35-7.18 (m, 4H), 7.18-6.75 (m, 2H), 5.42-4.85 (m, 2H), 4.60-4.35 (m, 2H), 3.63 (m, 2H), 2.55 - 2.38 (m, 2H), 2.38-2.00 (m, 6H), 1.48-1.24 (m, 8H), 0.80 (t, J=7.2 Hz, 6H)。
実施例 19 (10) : N- ( 1 H—イミダゾール一 2—ィルメチル) 一 N—
[4— ( { [4- (1ーピペリジニル) プチル] アミノ} メチル) ベンジル]
一 1 H—イミダゾールー 2—カルボキサミド (化合物 1 9- 1 0)
性状:ァモ ファス
TLC :Kf 0.55 (クロ口ホルム:メタノール: 28%アンモニア水 =80:20:4); NMR (DMSO-de): δ 1.21-1.56 (m, 10H), 2.07-2.20 (m, 2H), 2.19—2.35 (m, 4H), 2.36-2.47 (m, 2H), 3.63 (s, 2H), 4.48 (s, IH), 4.54 (s, IH), 5.25 (s, 1H), 5.53 (s, IH), 6.72-7.10 (m, 3H), 7.10-7.36 (m, 5H), 11.68-12.15 (m, 2H)。 実施例 1 9 (1 1) : N— (IH ミダゾ一ルー 2—ィルメチル) 一 N— [4- ( { [4- (4一モルホリニル) ブチル] アミノ} メチル) ベンジル] 一 1 H—イミダゾールー 2—カルボキサミド (化合物 1 9— 1 1)
性状:アモルファス
TLC :Rf 0.58 (クロ口ホルム:メタノール: 28%アンモニア水 =80:10:1); NMR (DMSO-de): δ 1.34-1.48 (m, 4H), 2.14-2.25 (m, 2H), 2.24-2.36 (m, 4H), 2.38-2.48 (m, 2H), 3.46-3.58 (m, 4H), 3.65 (s, 2H), 4.48 (s, IH), 4.55 (s 1H), 5.26 (s, 1H), 5.53 (s, IH), 6.70-6.92 (m, IH), 6.93-7.12 (m, IH), 7.13-7.24 (m, 3H), 7.24-7.45 (m, 3H), 11.65-12.34 (m, 2H)。
実施例 1 9 (1 2) : N— (1 H—べンゾィミダゾールー 2—/ fルメチル) 一 N— [4一 ( { [4一 (ジプロピルアミノ) プチル] アミノ} メチル) ベ ンジル] 一 1 H—ィミダゾーノレ一 2—カノレポキサミド (化合物 1 9- 1 2) 性状:アモルファス
TLC: Rf 0.26 (クロ口ホルム:メタノール: 28%ァンモ -ァ水 = 80:10:1); NMR (DMSO-de): δ 0.80 (t, J=7.5 Hz, 6H), 1.24-1.50 (m, 8H), 2.19-2,38 (m, 8H), 3.67 (s, 2H), 4.68 (s, 2H), 5.61 (s, IH), 5.65 (s, IH), 6.99-7.19 (m, 3H), 7.19-7.37 (m, 5H), 7.37-7.50 (m, IH), 7.50—7.65 (m, 1H), 12.10 - 12.70 (m, 2H)。
実施例 1 9 (1 3) : N— [4— ( { [4— (3, 4—ジヒドロー 2 ( 1 H) 一イソキノリニル) プチル] アミノ} メチル) ベンジル] — N— (1 [—ィ
ミダゾールー 2—^ Tルメチル) 一 1 H—ィミダゾ ルー 2—力ルポキサミ ド (化合物 19-1 3)
性状:アモルファス
TLC :Rf 0.36 (クロ口ホルム:メタノール: 28%アンモニア水 =80:10:1); NME (DMSO-de): 81.34-1.66 (m, 4H), 2.39 (t, J=6.9 Hz, 2H), 2.44-2.56 (m, 2H), 2.59 (t, J=6.0 Hz, 2H), 2.76 (t, J=6.0 Hz, 2H), 3.48 (s, 2H), 3.64 (s, 2H), 4.48 (s, 1H), 4.54 (s, 1H), 5.25 (s, 1H), 5.53 (s, 1H), 6.73-6.91 (m, 1H), 6.92-7.13 (m, 5H), 7.12-7.43 (m, 6H), 11.70-12.33 (m, 2H)。
実施例 19 (14) : N— [4— ( { [4— (ジプロピルァミノ) プチル] アミノ} メチル) ベンジル] —2— (1 H一^ f ミダゾ一ノレ一 4一イスレ) 一 N 一 (1H—イミダゾールー 2—ィルメチル) ァセトアミ ド (化合物 19一 1 4)
性状:油状物
TLC: Rf 0.36 (酢酸ェチル:メタノール: 28%アンモニア水 = 20:2:1);
NMR CDMSO-de): 50.81 (t, J =7.5 Hz, 6H), 1.20 - 1.50 (m, 8H), 2.20-2.40 (m, 8H), 3.60-3.95 (m, 4H), 4.38-4.68 (m, 4H), 6.78-7.35 (m, 7H), 7.60 (m, 1H)。
実施例 1 9 (15) : N- [4- ( { [4- (ジプロピルァミノ) プチル] アミノ} メチノレ) ベンジル] 一 N— (1H—イミダゾールー 2—^ ルメチル) 一 1 H—ピラゾールー 3—カルボキサミド (化合物 19— 15)
性状: 油状物
TLC: Rf 0.35 (ジクロロメタン:メタノール: 28%アンモニア水 = 90:10:3); NMR (CDCls): 60.86 (t, J=7.5 Hz, 6H), 1.39—1.60 (m, 8H), 2.30-2.52 (m, 6H), 2.58-2.72 (m, 2H), 3.72-3.84 (m, 2H), 4.56-5.05 (m, 4H), 6.70-6.94 (m 1H), 6.95-7.05 (m, 2H), 7.18-7.40 (m, 4H), 7.55-7.68 (m, 1H)。
実施例 19 (16) : N— [4一 ( { [4一 (ジプロピルァミノ) プチル]
アミノ} メチル) ベンジル] — N— (1H—イミダゾール一 2—ィルメチル) 一 4ーメチルー 1 H—ィミダゾ ルー 2—力ルポキサミド (化合物 19一 1 6)
性状:油状物
TLC: Rf 0.47 (ジクロロメタン:メタノール: 28%アンモニア水 = 90:10:2); NMR (CDCls): δ d 0.86 (m, 6H), 1.38-1.60 (m, 8H), 2.15-2.50 (m, 9H), 2.58-2.68 (m, 2H), 3.78 (m, 2H), 4.45-498(m, 4H), 6.92 - 7.42 (m, 7H), 8.40-8.50(m, 1H)。
実施例 19 (17) : N- [4- ( { [4- (ジプロピルァミノ) プチル] アミノ} メチル) ベンジル] — N— (1H—イミダゾールー 2—ィルメチル) — 5—メチルー 2—ピリジンカルボキサミ ド (化合物 19-17)
性状:油状物
TLC: Rf 0.16 (酢酸ェチル:メタノール: 28%アンモユア水 = 90:10:2); NMR (CDCls): δ d 0.87 (t, J=7.5 Hz, 6H), 1.38 - 1.60 (m, 8H), 2.30-2.55 (m, 6H), 2.43 (s, 3H), 2.64 (t, J=6.0 Hz, 2H), 3.78 (s, 2H), 4.40-4.78 (m, 4H), 7.00-7.18 (m, 2H), 7.29 (d, J=8.1 Hz, 2H), 7.39 (d, J=8.1 Hz, 2H), 7.59-7.82 (m, 2H), 8.40-8.50 (m,lH)。
実施例 19 (18) : N— [4— ( { [4— (ジプロピルァミノ) プチル] アミノ } メチル) ベンジル] 一 N— ( 1 H—イミダゾール一 2—ィルメチル) — 1H— 1, 2, 4—トリァゾール一 5—カルボキサミ ド (化合物 19一 1 8)
性状:アモルファス
TLC: Rf 0.33 (ジクロロメタン:メタノール: 28%アンモニア水 = 80:20:3); NME (CDCls): δ d 0.78-0.95 (m, 6H), 1.35-1.78 (m, 8H), 2.40-2.68 (m, 6H) 2.70-2.85 (m, 2H), 3.80-4.00 (m, 2H), 4.52-5.12 (m, 4H), 6.95-7.12 (m, 2H) 7.08-7.40 (m, 4H), 8.10-8.21 (m, 1H)。
実施例 1 9 (1 9) : N— (4— { [ {4— [ (ジプロピルァミノ) メチル] ベンジル } (メチル) ァミノ] メチル } ベンジル) -N- (1H—イミダゾ 一ノレ一 2—ィルメチル) 一 1 H—イミダゾールー 2—カルボキサミ ド 性状:アモルファス
TLC: Rf 0.44 (ジクロロメタン:メタノール: 28%アンモニア水 = 90:10:1); NMR (CDCla): 50.84 (t, J=7.2 Hz, 6H), 1.41-1.53 (m, 4H), 2.16 (s, 3H), 2.33-2.38 (m, 4H), 3.48 (s, 2H), 3.49 (s, 2H), 3.53 (s, 2H), 4.77 (s, 2H), 4.97 (s, 2H), 6.94-7.38 (m, 12H)。
実施例 20 :メチル 2— [4— (ジプロピルァミノ) プチル] 一 1, 2, 3, 4—テトラヒドロー 6—イソキノリンカルボキシラート (化合物 20) 1一 ( { [2— (トリメチノレシリノレ) ェチルォキシ] メチル } 一 1H—ィ ミダゾールー 2一カルボアルデヒドの代わりに 4— (ジプロピルァミノ) ブ タナーノレを、 { [4- (メチノレオキシ) フエエル] メチル } ァミンの代わり にメチル 1, 2, 3, 4ーテトラヒドロ一 6—ィソキノリンカルボキシラ ート 塩酸塩を用いて、 実施例 1と同様の操作をし、 以下の物性値を有する 標題化合物を得た。
TLC :Rf 0.30 (クロ口ホルム:メタノール: 28%アンモニア水 =80:10:1); NMR (CDCls): 67.77 (m, 2H), 7.08 (d, J=7.8 Hz, 1H), 3.890 (s, 3H), 3.66 (s 2H), 2.94 (t, J=6.3 Hz, 2H), 2.74(t, J=6.0 Hz, 2H), 2.47 (m, 2H), 2.42 (m, 2H), 2.36 (m, 4H), 1.28 (m, 6H), 0.86 (m, 8H)。
実施例 21 : {2— [4一 (ジプロピルァミノ) プチル] — 1, 2, 3, 4 ーテトラヒドロー 6—イソキノリニル} メタノール (化合物 2 1)
化合物 20 (3.02 g) のテトラヒドロフラン (25 mL) 溶液に、 水素化 リチウムアルミニウム (330 mg) を一 78°Cで加えた。 反応混合物を一 7 8 °Cで 30分撹拌した。反応混合物に硫酸ナトリウム 10水和物 (2.8 g ) と ジェチルエーテル (100 mL) を加え、 反応混合物を室温まで上昇させた。
反応混合物をセライト (商品名) でろ過し、 濃縮した。 残渣をシリカゲル力 ラムクロマトグラフィー (酢酸ェチル:メタノール: トリェチルァミン= 1 0 : 1 : 0→10 : 1 : 0. 5) によって精製し、 以下の物性を有する標題 化合物 (2.28 g) を得た。
TLC :Rf 0.57 (クロ口ホルム:メタノール: 28%アンモユア水 =80:10:1) ; NMR (CDCls): 67.10 (m, 2H), 7.00 (d, J=8.4 Hz, 1H), 4.62 (s, 2H), 3.61 (s, 2H), 2.89 (t, J=5.7 Hz, 2H), 2.72 (t, J=5.7 Hz, 2H), 2.51 (m, 2H), 2.45 (m, 2H), 2.37 (m, 4H), 1.46 (m, 8H), 0.83 (m, 6H)。
実施例 22 : 2- [4- (ジプロピルァミノ) プチル] 一 1, 2, 3, 4一 テトラヒドロー 6—^ f ソキノリンカルボアルデヒド (化合物 22 )
化合物 2 1 (2.28 g) およびトリェチルァミン (4.99 mL) のジメチルス ルホキシド (30 mL) 溶液に、 三酸化硫黄一ピリジン錯体 (2.28 g) をゆ つくり加えた。 反応混合物を室温で 1時間撹拌した。 反応液に水 (100 mL) を加えた。 水層をジクロロメタン (50 mL) で 2回抽出した。 有機層を合わ せて飽和食塩水で洗浄し、 無水硫酸マグネシウムで乾燥し、 濃縮した。 残渣 をシリカゲルク口マトグラフィー (酢酸ェチノレ:メタノール: トリェチルァ ミン = 10 : 1 : 0→ 1 0 : 1 : 0. 5) によって精製し、 以下の物性値を 有する標題化合物 (2.26 g) を得た。
TLC :Rf 0.40 (クロロホルム:メタノール: 28%アンモニア水 =80:10:1); NMR (CDCls): δ 9.94 (s, 1H), 7.62 (m, 2H), 7.18 (d, 8.4 Hz, 1H), 3.69 (s, 2H), 2.98 (t, J=5.7 Hz, 2H), 2.75 (t, J=6.3 Hz, 2H), 2.54 (m, 2H), 2.42 (m, 2H), 2.34 (m, 4H), 1.46 (m, 8H), 0.87 (m, 6H)。
実施例 23 : N— ( {2— [4— (ジプロピルァミノ) プチル] 一 1, 2, 3, 4—テトラヒドロー 6 f ソキノリ-ル} メチル) -N- [ (1ーメチ ルー 1 H—^ (ミダゾールー 2—ィル) メチル] — 1 H—イミダゾールー 2― カルボキサミド (化合物 23)
ミダゾールー 2一カルボアルデヒドの代わりに化合物 22を、 { [4一 (メ チルォキシ) フエニル] メチル } ァミンの代わりに [ (1ーメチルー111ー イミダゾーノレ一 2—ィル) メチル] 了ミンを用いて、 実施例 1と同様の操作 をして、 ( {2- [4- (ジプロピノレアミノ) プチル] 一 1, 2, 3, 4一 テトラヒドロ一 6—イソキノリニル} メチル) [ (1ーメチルー 1H—イミ ダゾールー 2—ィル) メチル] ァミン (化合物 23— a ) を得た。 得られた 化合物 23— aを化合物 16の代わりに用いて、 実施例 17と同様の操作を して、 以下の物性値を有する標題化合物を得た。
性状:油状物
TLC :Ef 0.28 (クロ口ホルム:メタノール: 28%アンモニア水 =80:10:1); NMR (DMSO-de): 50.81 (t, J=7.50 Hz, 6H), 1.26-1.44 (m, 6H), 1.44-1.59 (m, 2H), 2.21-2.32 (m, 4H), 2.32-2.37 (m, 2H), 2.37-2.46 (m, 2H),
2.55-2.66 (m, 2H), 2.67-2.83 (m, 2H), 3.43-3.53 (m, 3H), 3.57 (s, IH), 3.62 (s, IH), 4.34-4.51 (m, 2H), 4.51—4.66 (m, IH), 5.46 - 5.62 (m, 1H), 6.75-6.80 (m, IH), 6.80-6.84 (m, IH), 6.87—7.01 (m, 2H), 7.01-7.15 (m, 2H), 7.28 (s, 1H), 13.04 (s, 1H)。
実施例 23 (1) 〜実施例 23 (2)
化合物 16の代わりに化合物 23— aを用いて、 1 H—ィミダゾーノレ一 2 一力ルボン酸の代わりに 2—ピリジンカルボン酸または 3—ピリジン力ルポ ン酸を用いて、 実施例 17と同様の操作をして、 以下の物性値を有する標題 化合物を得た。
実施例 23 (1) : N— ( {2— [4— (ジプロピルアミノ) プチル] 一 1, 2, 3, 4ーテトラヒドロ一 6—イソキノリ-ノレ) メチル) -N- [ (1一 メチル一 1 H—イミダゾールー 2—ィル) メチル] 一 2—ピリジンカルボキ サミド (化合物 2 3- 1)
性状:油状物
TLC :Rf 0.60 (クロロホルム:メタノール: 28%アンモニア水 =80:20:4); NMR (DMSO-de): δ 0.82 (t, J=7.2 Hz, 6H), 1.22-1.44 (m, 6H), 1.44-1.61 (m, 2H), 2.19-2.45 (m, 8H), 2.54 - 2.66 (m, 2H), 2:67—2.82 (m, 2H),
3.40-3.56 (m, 2H), 3.64 (s, 2H), 4.50 (s, 2H), 4.54-4.71 (m, 3H), 6.70-7.07 (m, 4H), 7.12 (s, 1H), 7.39-7.52 (m, IH), 7.58 (t, J=7.5 Hz, IH), 7.89 (td, J=7.5, 1.8 Hz, IH), 8.56 (t, J=4.8 Hz, 1H)。
実施例 23 (2) : N— ( {2— [4— (ジプロピルァミノ) プチル] 一 1, 2, 3, 4—テトラヒドロー 6—イソキノリエル) メチル) 一 N— [ (1一 メチル一 1 H—イミダゾールー 2—ィル) メチル] ニコチンアミド (化合物 23-2)
性状:油状物
TLC: Rf0.60 (クロ口ホルム:メタノール: 28%アンモニア水 = 80:20:4); NMR (DMSO-de): 60.82 (t, J=7.2 Hz, 6H), 1.25-1.45 (m, 6H), 1.45 - 1.61 (m, 2H), 2.18-2.46 (m, 8H), 2.54-2.66 (m, 2H), 2.67-2.86 (m, 2H), 3.48 (s, 2H), 3.64 (s, 2H), 4.27-4.38 (m, 1H), 4.39-4.45 (m, 1H), 4.45-4.51 (m, IH), 4.51-4.59 (m, 1H), 4.59-4.72 (m, 1H), 6.69-7.22 (m, 5H), 7.42 (dd, J=7.8, 4.8 Hz, 1H), 7.71-8.06 (m, IH), 8.52-8.82 (m, 2H)。
実施例 24 :メチル 4— [ (5—ヒドロキシペンチル) ォキシ] ベンゾェ ート (化合物 24)
P—ヒドロキシ安息香酸メチル(3.38 g )、 1, 5—ペンタンジオール (2.30 g)およびトリフエ-ルホスフィン(5.96 g)のテトラヒドロフラン(100 m
L) 溶液に、 氷冷下ジェチルァゾジカルポキシラート (2. 2 Nトルエン溶 液、 10 mL) をゆつくり加えた。 反応混合物を氷冷下 1 6時間撹拌した。 反 応混合物を濃縮し、 残渣を n—へキサン一酢酸ェチノレ溶液 (n—へキサン:酢 酸ェチル = 1 : 1) で洗浄した。 反応混合物を濃縮後、 シリカゲルクロマト グラフィー (n—へキサン:酢酸ェチル = 64 : 3 6→4 5 : 5 5) によって 精製し、 以下の物性値を有する標題化合物 (3.58 g) を得た。
TLC: Rf0.36 (n一へキサン:酢酸ェチル = 1:1);
NME (CDCls): δ 1.47-1.73 (m, 4H), 1.76-1.92 (m, 2H), 3.69 (t, J=6.3 Hz, 2H), 3.88 (s, 3H), 4.02 (t, J=6.3 Hz, 2H), 6.90 (d, J=9.0 Hz, 2H), 7.97 (d, J=9.0 Hz, 2H)。
実施例 25 :メチル 4一 ( {5- [ (メチルスルホニル) 才キシ] ペンチ ル} 才キシ) ベンゾエート (化合物 25 )
化合物 24 (3.58 g) およぴトリエチルァミン (2.76 mL) の酢酸ェチル (50 mL) 溶液に、 メタンスルホユルクロリド (0.78 mL) を氷冷下ゆつ くり加えた。 反応混合物を氷冷下 2時間撹拌した。 反応混合物を齚酸ェチル (100 mL) で希釈した。 希釈液を水および飽和食塩水で順次洗浄し、 無水 硫酸マグネシウムで乾燥し、 濃縮した。 残渣をシリカゲルクロマトグラフィ 一(酢酸ェチル:メタノール = 1 : 0→10 : 1) によって精製し、 以下の物 性値を有する標題化合物 (3.70 g) を得た。
TLC: Rf 0.39 (n—へキサン:酢酸ェチル = 1:1);
N纖 (CDCla): 81.56-1.69 (m, 2H), 1.76-1.93 (m, 4H), 3.01 (s, 3H), 3.89 (s, 3H), 4.03 (t, J=6.3 Hz, 2H), 4.27 (t, J=6.3 Hz, 2H), 6.90 (d, J=9.0 Hz, 2H), 7.98 (d, J=9.0 Hz, 2H)。
実施例 26 :メチノレ 4- { [5— (ジプロピルァミノ) ペンチル] ォキシ } ベンゾエート (化合物 26 )
化合物 25 (3.70 g) およびジプロピルアミン (3.00 mL) のイソプロピ
ルアルコール (40 mL) 溶液を 60°Cで 16時間撹拌した。 反応混合物を室 温まで冷却後、 飽和重曹水 (40 mL) を加えた。 水層を酢酸ェチル (50 m L) で 2回抽出した。 有機層を合わせて飽和食塩水で洗浄し、 無水硫酸マグ ネシゥムで乾燥し、 濃縮した。 残渣をシリカゲルクロマトグラフィー (酢酸 ェチル:メタノール = 10 : 90→0 : 100) によって精製し、 以下の物性 値を有する標題化合物 (1.94 g) を得た。
TLC: Rf 0.30 (酢酸ェチル:メタノール = 10:90);
NMR (CDC13): δ 0.87 (t, J=7.5 Hz, 6H), 1.33—1.59 (m, 8H), 1.73-1.91 (m, 2H), 2.29-2.39 (m, 4H), 2.39-2.48 (m, 2H), 3.88 (s, 3H), 4.01 (t, J=6.6 Hz, 2H), 6.89 (d, J=9.0 Hz, 2H), 7.97 (d, J=9.0 Hz, 2H)。
実施例 27 : 4- { [5— (ジプロピルァミノ) ペンチル] 才キシ } 一 N, N—ビス (1H—イミダゾ^"ル一2—ィルメチル) ベンズアミ ド (化合物 2 7)
実施例 5の工程において、 化合物 4の代わりに化合物 26を用いて、 実施 例 5→実施例 6—実施例 10と同様の操作をして、 以下の物性値を有する標 題化合物を得た。
性状:アモルファス
TLC: Rf 0.66 (ジクロロメタン:メタノール: 28%アンモニア水 = 16:4:1); NMR (CDCls): δ 0.86 (t, J=7.5 Hz, 6H), 1.31-1.57 (m, 8H), 1.69-1.87 (m, 2H), 2.28-2.49 (m, 6H), 3.96 (t, J=6.6 Hz, 2H), 4.65 (s, 4H), 6.89 (d, J=8.7 Hz, 2H), 6.93-7.12 (m, 4H), 7.66 (d, J=8.7 Hz, 2H)。
実施例 28 : (5E) -6- [4- (メ トキシカルボニル) フエニル] 一 5
一へキセン酸 (化合物 28)
5- (トリフエ二ノレホスホニゥム) ペンタン酸臭化物 (26.8 g) のトルェ ン (200 mL) 溶液に t—ブトキシカリウム (13.5 g) を加えた。 反応混合 物を 80°Cで 1時間撹拌した。 反応混合物を 0°Cに冷却後、 反応混合物に 4 一ホルミル安息香酸メチル(3.41 g )を加えた。反応混合物を 0 °Cで 2時間、 室温で 30分撹拌した。 反応混合物に水 (150 mL) を加えた。 水層に 5N 塩酸 (15 mL) を加え、 酸性とした後、 水層を酢酸ェチル (100 mL) で 2 回抽出した。 有機層を合わせて飽和食塩水で洗浄し、 無水硫酸マグネシウム で乾燥し、 濃縮した。 残渣をシリ力ゲルク口マトグラフィー ( n—へキサン: 酢酸ェチル = 3 : 1→2 : 1) によって精製し、 以下の物性値を有する標題 化合物 (3.10 g) を得た。
TLC: Rf0.50 (n—へキサン:酢酸ェチル = 1:9);
NME (CDCla): 51.71-1.94 (m, 2H), 2.23-2.50 (m, 4H), 3.84-3.96 (m, 3H), 5.66-6.39 (m, IH), 6.40-6.56 (m, IH), 7.28-7.44 (m, 2H), 7.90-8.06 (m, 2H)。 実施例 29 :メチル 4— [ (1 E) 一 6—ヒドロキシ一 1一へキセン一 1 一ィル] ベンゾエート (化合物 29)
化合物 28 (3.10 g) のテトラヒドロフラン (40 mL) 溶液に、 氷冷下 ボランーテトラヒドロフラン錯体 (0.98N/THF, 13 mL) をゆつくり加え た。 反応混合物を 0°Cで 20分撹拌した。 反応混合物に水 (10 mL) をゆつ くり加え、 さらに炭酸カリウム (3 g) を加えた。 この溶液を水 (100 mL) で希釈し、 水層を酢酸ェチル (100 mL) で 2回抽出した。 有機層を合わせ て飽和食塩水で洗浄し、 無水硫酸マグネシウムで乾燥し、 濃縮した。 残渣を シリカゲノレクロマトグラフィー(n—へキサン:酢酸ェチル = 7: 3→3: 7) によって精製し、 以下の物性値を有する標題化合物 (2.50 g) を得た。
TLC: Rf 0.45 (n—へキサン:酢酸ェチル = 1:1);
NMR (CDCla): δ 1.47-1.74 (m, 4H), 2.21-2.72 (m, 2H), 3.55-3.76 (m, 2H),
3.82-3.97 (m, 3H), 5.68-6.54 (m, 2H), 7.28-7.44 m, 2H), 7.88-8.06 (m, 2H)0 実施例 3 0 : メチル 4一 { 6 - [ (メチルスルホニル) ォキシ] へキシル } ベンゾエート (化合物 3 0 )
化合物 2 9 (2.50 g ) のメタノール (30 m L) 溶液にアルゴン雰囲気下 1 0 %パラジウム一炭素(250 m g ) を加えた。反応混合物を水素雰囲気下、 室温で 3時間撹拌した。 反応混合物をセライト (商品名) で濾過し、 ろ液を 濃縮した。残渣をシリカゲルクロマトグラフィー(n—へキサン:酢酸ェチル = 7 : 3→3 : 7 ) によって精製し、 メチル 4— ( 6—ヒドロキシへキシル) ベンゾエート (2.22 g ) を得た。 化合物 2 4の代わりにメチル 4一 (6— ヒドロキシへキシル) ベンゾエートを用いて実施例 2 5と同様の操作をし、 以下の物性値を有する標題化合物を得た。
TLC : Rf 0.56 (n—へキサン:酢酸ェチル = 1:1) ;
NMR (CDC13) : δΙ.29-1.52 (m, 4H), 1.58-1.83 (m, 4H), 2.59-2.73 (m, 2H), 2.99 (s, 3H), 3.90 (s, 3H), 4.21 (t, J=6.6 Hz, 2H), 7.24 (d, J=8.4 Hz, 2H), 7.95 (d, J=8.4 Hz, 2H)。
実施例 3 1 : 4— [ 6 - (ジプロピルァミノ) へキシル] -N, N—ビス (1 H—ィミダゾーノレ一 2—イスレメチル) ベンズァミ ド (化合物 3 1 )
化合物 2 5の代わりに化合物 3 0を用いて、 実施例 2 6と同様の操作をし、 メチル 4— [ 6— (ジプロピルァミノ) へキシル] ベンゾエートを得た。 実施例 5の工程において、 化合物 4の代わりにメチル 4一 [ 6— (ジプロ ピ /レアミノ) へキシル] ベンゾエートを用いて、 実施例 5→実施例 6→実施 例 1 0と同様の操作をして、 以下の物性値を有する標題化合物を得た。
性状:油状物
TLC: Rf 0.37 (ジクロロメタン:メタノール: 28%アンモニア水 = 90:10:1); NMR (CDCls): δ 0.87 (t, J=7.5 Hz, 6H), 1.14-1.71 (m, 12H), 2.30-2.49 (m, 6H), 2.60 (t, J=7.5 Hz, 2H), 4.68 (m, 4H), 6.90-7.09 (m, 4H), 7.19 (d, J=8.1 Hz, 2H), 7.51 (d, J=8.1 Hz, 2H)。
実施例 3 2 : メチル 4— [ ( 5—ブロモペンチノレ) チォ] ベンゾエート (化 合物 3 2 )
4一メルカプト安息香酸メチル (3.39 g ) および 1, 5—ジプロモペンタ ン(9.31 g )のジメチルホルムアミ ド(100 m L)溶液に、炭酸力リウム(3.07 g ) を加えた。反応混合物を室温で 3時間撹拌した。反応混合物に水(300 m L) を加え、 水層を n —へキサン一酢酸ェチル溶液 (n —へキサン:酢酸ェチ ル = 1 : 1 ) (150 m L) で 2回抽出した。 有機層を合わせて飽和食塩水で 洗浄し、 無水硫酸マグネシウムで乾燥し、 濃縮した。 残渣をシリカゲルクロ マトグラフィー (11一へキサン:酢酸ェチル - 1 : 0→8 : 2 ) によって精製 し、 以下の物性値を有する標題化合物 (4.69 g) を得た。
TLC: Iぱ 0.68 (n—へキサン:酢酸ェチル: 4:1);
NMR (CDCla): δ 1.54-1.80 (m, 4H), 1.80-1.98 (m, 2H), 3.00 (t, J=6.9 Hz, 2H), 3.41 (t, J=6.6 Hz, 2H), 3.90 (s, 3H), 7.28 (d, J=8.7 Hz, 2H), 7.92 (d, J=8.7 Hz, 2H)。
実施例 3 3 : 4 - { [ 5 - (ジプロピルァミノ) ペンチル] スルファニル } 一 N, N—ビス ( 1 H—イミダゾール一 2—ィルメチル) ベンズアミ ド (化 合物 3 3 )
化合物 2 5の代わりに化合物 3 2を用いて、 実施例 2 6と同様の操作をし、 メチル 4一 { [ 5— (ジプロピルァミノ) ペンチル] チォ } ベンゾエート を得た。 実施例 5の工程において、 化合物 4の代わりにメチル 4一 { [ 5 一 (ジプロピルァミノ) ペンチル] チォ } ベンゾエートを用いて、 実施例 5 →実施例 6→実施例 1 0と同様の操作をして、 以下の物性値を有する標題化 合物を得た。
性状:ァモルファス
TLC: Rf 0.24 (ジクロロメタン:メタノール: 28%アンモニア水 = 80:20:1); NMR (DMSO-de): δ 0.81 (t, J=7.5 Hz, 6H), 1.25-1.46 (m, 8H), 1.49-1.67 (m, 2H), 2.19-2.45 (m, 6H), 2.97 (t, J=7.2 Hz, 2H), 4.56 (s, 4H), 6.79-7.13 (m, 4H), 7.27 (d, J=8.4 Hz, 2H), 7.44 (d, J=8.4 Hz, 2H), 10.97-13.23 (m, 2H)。
実施例 3 4 :メチル 4— { [ ( 4ーヒドロキシプチル) ァミノ] カルポュ ル} ベンゾエート (化合物 3 4 )
化合物 1 6の代わりに 4ーァミノ一 1ーブタノールを用いて、 1 H—イミ ダゾールー 2—力ルボン酸の代わりに 4一 (メ トキシカルボエル) 安息香酸 を用いて、 実施例 1 7と同様の操作をして、 以下の物性値を有する標題化合 物を得た。
TLC: Rf 0.31 (酢酸ェチル)。
実施例 3 5 : N 1 - [ 4 - (ジプロピルァミノ) プチル] 一 N 4 , N4—ビス (1 H—イミダゾールー 2—ィルメチル) テレフタルアミ ド (化合物 3 5 )
実施例 2 5の工程において、 化合物 2 4の代わりに化合物 3 4を用いて
実施例 2 5→実施例 2 6と同様の操作をし、 メチル 4— ( { [ 4一 (ジブ 口ピノレアミノ) プチノレ] アミノ} カノレポ二ノレ) ベンゾエートを得た。 実施例 5の工程において、 化合物 4の代わりにメチル 4一 ( { [ 4一 (ジプロピ ルァミノ) プチル] アミノ} カルボニル) ベンゾエートを用いて、 実施例 5 —実施例 6—実施例 1 0と同様の操作をして、 以下の物性値を有する標題化 合物を得た。
性状:アモルファス
TLC: Rf 0.58 (ジクロロメタン:メタノール: 28%アンモニア水 = 16:4:1); NMR (CDC13): δ 0.86 (t, J=7.5 Hz, 6H), 1.34-1.54 (m, 4H), 1.54-1.74 (m, 4H), 2.33-2.48 (m, 4H), 2.51 (t, J=6.6 Hz, 2H), 3.31-3.56 (m, 2H), 4.55 (s, 2H), 4.66 (s, 2H), 6.85-7.03 (m, 2H), 7.08 (s, 2H), 7.18-7.37 (m, 1H), 7.43-7.79 (m, 4H)。
実施例 3 5 ( 1 ) : 4一 ( { [ 4 - (ジプロピルアミノ) プチル] アミノ} メチル) 一 N— (1 H—イミダゾールー 2—ィルメチル) 一 N— ( 3—ピリ ジエルメチル) ベンズァミド (化合物 3 5— 1 )
実施例 6の工程において化合物 2の代わりに 1— ( 1 H—イミダゾールー 2—ィル) 一 N— (ピリジン一 3—^ Tルメチル) メタンアミンを用いて、 実 施例 3 5と同様の操作をして、 以下の物性値を有する標題化合物を得た。 性状:油状物
TLC: Rf 0.83 (クロ口ホルム:メタノール: 28%アンモニア水 = 40:10:2);
NMR (CDCla): δ 0.85 (t, J=7.2 Hz, 6 H), 1.22-1.70 (m, 8 H), 2.24-2.48 (m, 6 H), 2.54-2.66 (m, 2 H), 3.49 (s, 2 H), 3.79 (s, 2 H), 4.63 (s, 2 H), 6.82—7.11 (m, 2 H), 7.19-7.44 (m, 5 H), 7.45-7.64 (m, 1 H), 8.46 (s, 1 H), 8.55 (d, J=1.5 Hz, 1 H)。
実施例 3 6 : 1 H—ィミダゾールー 2—スルホユルクロリ ド 塩酸塩 (化合 物 3 6 )
2—メルカプトイミダゾール (3.0 g) の IN塩酸 (30 mL) 溶液に氷冷 下塩素ガスを 1時間吹き込んだ。 反応混合物を 2時間氷冷下撹拌した。 反応 混合物をろ過し、 ろ取した固体を氷水で洗浄し、 乾燥して、 以下の物性値を 有する標題化合物 (1.76 g) を得た。
NMR (DMSO-de): 514.82 (m, 2H), 7.58 (s, 2H)。
実施例 37 : N— ( { 2— [4— (ジプロピルァミノ ) プチル] 一 1 , 2, 3, 4—テトラヒドロー 6—^ f ソキノリエル) メチル) 一 N— [ (1ーメチ ノレ一 1 H— ^ f ミダゾールー 2一ィル) メチル] —1 H—ィミダゾールー 2一 スルホンアミド (化合物 37)
化合物 23- a (100 mg) およびピリジン (59 mL) のジクロロメタン (3 mL) 溶液に化合物 36 (74 mg) を加えた。 反応混合物を室温で 30 分撹拌した。反応混合物に 1 N水酸化ナトリゥム水溶液(15 mL)を加えた。 水層をジクロロメタン (30 mL) で 2回抽出した。 有機層を合わせて飽和食 塩水で洗浄し、 無水硫酸マグネシウムで乾燥し、 濃縮した。 残渣をシリカゲ ルクロマトグラフィー (酢酸ェチル:メタノール: トリェチルァミン = 10 :
1 : 0→10 : 1 : 0. 5) によって精製し、 以下の物性値を有する標題化 合物 (119 mg) を得た。
性状:半固体
TLC:Rf 0.71 (クロ口ホルム:メタノール: 28%アンモニア水 =80:20:4) ;
NMR (DMSO-de): 50.82 (t, J=7.5 Hz, 6H), 1.27-1.44 (m, 6H), 1.45-1.57 (m, 2H), 2.22-2.32 (m, 4H), 2.32-2.45 (m, 4H), 2.53-2.62 (m, 2H),
2.62-2.70 (m, 2H), 3.41-3.49 (m, 5H), 4.26 (s, 2H), 4.41 (s, 2H), 6.59 (s, 1H),
6.79 (s, IH), 6.80-6.86 (m, IH), 6.87-6.94 m, 1H), 7.00 (s, 1H), 7.25 (s, 2H)。 実施例 3 7 ( 1 ) : N— [ 4一 ( { [ 4一 (ジプロピルァミノ) プチル] ァ ミノ } メチル) ベンジル] — N— (1 H—イミダゾールー 2—ィルメチル) 一 1 H—ィミダゾールー 2—スルホンァミ ド (化合物 3 7— 1 )
メチル 1, 2, 3, 4ーテトラヒ ドロー 6—イソキノリンカルボキシラ ート塩酸塩の代わりに 4— (アミノメチル) 安息香酸を用いて実施例 2 0→ 実施例 2 1→実施例 2 2→実施例 2 3と同様の操作をした。得られた N,一(4 一 { [ (シク口ペンター 1 , 3—ジェン一 1一^ fルメチル) ァミノ] メチル } ベンジル) 一 N , N—ジプロピルプロパン一 1, 3ージァミンを化合物 2 3 一 aの代わりに用いて実施例 3 5と同様の操作をし、 以下の物性値を有する 標題化合物を得た。
性状:アモルファス
TLC: Rf 0.26 (酢酸ェチル:メタノール: 28%アンモニア水 = 90:10:2);
NMR (CDCls): δ d 0.88 (t, J=7.2 Hz, 6H), 1.38-1.68 (m, 8H), 2.30-2.60 (m, 6H), 2.74 (m, 2H), 3.70 (m, 2H), 3.77 (s, 2H), 4.56(m, 2H), 6.98-7.30 (m, 8H)。
実施例 3 8 : 4— ( { [ 4一 (ジプロピノレアミノ) プチル] アミノ } メチル) 一 N, N—ビス (1 H—イミダゾールー 2—イノレメチル) ベンゼンスルホン アミド (化合物 3 8 )
化合物 2 3— aの代わりに化合物 2を用いて、 化合物 3 6の代わりに 4一 ホルミルベンゼンスルホユルクロリ ドを用いて、 実施例 3 7と同様の操作を して、 4ーホ /レミノレ一 N, N—ビス [ ( 1— { [ 2— (トリメチ 7レシリ/レ)
エトキシ] メチノレ } 一 1 H—イミダゾーノレ一 2—ィノレ) メチル〕 ベンズアミ ド (化合物 3 8— a ) を得た。 実施例 1の工程において、 1一 ( { [ 2— (ト リメチルシリル) ェチルォキシ] メチル } 一 1 H—イミダゾールー 2—カル ボアルデヒドの代わりに化合物 3 8— aを、 { [ 4一 (メチルォキシ) フエ ニル] メチル } ァミンの代わりに N, N—ジプロピル一 1 , 4一ブタンジァ ミンを用いて、 実施例 1→実施例 1 0と同様の操作をし、 以下の物性値を有 する標題化合物を得た。
性状:アモルファス '
TLC: Rf 0.66 (クロロホルム:メタノール: 28%アンモ-ァ水 = 80:20:4); NME, (DMSO-de): 5 0.81 (t, J=7.5 Hz, 6H), 1.24-1.48 (m, 8H), 2.18-2.37 (m, 6H), 2.42 (t, J=6.3 Hz, 2H), 3.70 (s, 2H), 4.49 (s, 4H), 6.68-6.91 (m, 2H) 6.91-7.16 (m, 2H), 7.40 (d, J=8.1 Hz, 2H), 7.54 (d, J=8.1 Hz, 2H),
12.19-12.64 (m, 2H)。
実施例 3 9 : N— [ 4 - ( { [ 4一 (ジメチルァミノ) プチル] アミノ } 力 ルポ-ル) ベンジル] 一 N— ( 1 H—イミダゾールー 2—ィルメチル) 一 1 H—イミダゾールー 2—カルボキサミ ド (化合物 3 9 )
4一 (ジェトキシメチル) ベンズアルデヒドの代わりにメチル 4一ホル ミルベンゾエートを用いて、 実施例 1 6→実施例 1 7と同様の操作をして、 メチル 4— ( { ( 1 H—イミダゾールー 2—ィルカルポニル) [ ( 1一 { [ 2 — (トリメチルシリル) エトキシ] メチル } 一 1 H -イミダゾールー 2—ィ ル) メチル] アミノ } メチル) ベンゾエート (化合物 3 9— a ) を得た。 実 施例 5の工程において、 化合物 4の代わりに化合物 3 9— aを用いて、 実施
例 6の工程において、 化合物 2の代わりに N, N—ジメチルー 1 , 4ープタ ンァミンを用いて、 実施例 5→実施例 6→実施例 1 0と同様の操作をして、 以下の物性値を有する標題化合物を得た。
性状:アモルファス .
TLC : Ef 0.24 (クロ口ホルム:メタノール: 28%アンモ ア水 = 80:20:4) ; N籠 (DMSO-de): δ 1.32-1.64 (m, 4H), 2.09 (s, 6H), 2.13-2.27 (m, 2H), 3.14-3.29 (m, 2H), 3.65 (s, IH), 3.71 (s, IH), 4.52 (s, 0.5H), 4.62 (s, 0.5H), 5.31 (s, 0.5H), 5.60 (s, 0.5H), 6.71-6.89 (m, 1H), 6.94- 7.11 (m, IH),
7.24-7.35 (m, IH), 7.41 (d, J=8.1 Hz, IH), 7.77 (d, J=8.1 Hz, 2H), 7.92-8.08 (m, 2H), 8.35-8.50 (m, IH), 8.62-8.78 (m, IH), 10.06 (s, 1H)。
実施例 3 9 ( 1 ) : N— [ 4— ( { [4— (ジプロピルァミノ) プチル] ァ ミノ } カノレポ二ノレ) ベンジノレ] 一 N— ( 1 H一^ {ミダゾーノレ一 2—イノレメチ ル) 一 1 H—イミダゾーノレ一 2—カルポキサミド (化合物 3 9— 1 )
N, N—ジメチル一 1 , 4—ブタンァミンの代わりに N, N—ジプロピル - 1 , 4—プタンァミンを用いて、 実施例 3 9と同様の操作に付し、 以下の 物性値を有する標題化合物を得た。
性状:アモルファス
TLC : Rf 0.32 (クロ口ホルム:メタノール: 28%アンモニア水 = 80:20:4); NMR (DMSO-de): 8 0.80 (t, J=7.5 Hz, 6H), 1.20-1.44 (m, 6H), 1.44-1.65 (m, 2H), 2.14-2.42 (m, 6H), 3.14-3.28 (m, 2H), 4.51 (s, IH), 4.62 (s, IH), 5.30 (s, 1H), 5.60 (s, IH), 6.82 (s, IH), 6.96-7.19 (m, 2H), 7.22-7.44 (m, 3H) 7.77 (d, J=8.4 Hz, 2H), 8.27-8.55 (m, IH), 11.77-12.18 (m, IH),
12.90-13.27 (m, 1H)。
実施例 4 0 : 4ーホノレミノレー N, N—ビス [ ( 1— { [ 2— (トリメチルシ リル) エトキシ] メチル } 一 1 H—イミダゾールー 2—ィル) メチル] ベン ズアミド (化合物 4 0 )
化合物 1 6の代わりに化合物 2を用い、 1 H— ^ f ミダゾールー 2—力ルポ ン酸の代わりに 4一ホルミル安息香酸を用いて実施例 1 7と同様の操作をし、 以下の物性値を示す標題化合物を得た。
TLC : Rf 0.47 (クロ口ホルム:メタノール = 10:1) ;
NMR (CDC13): 5 10.01 (s, 1H), 7.85 (m, 2H), 7.77 (m, 2H), 7.04 (m, 4H), 5.51 (s, 2H), 5.15 (s, 2H), 4.93 (s, 2H), 4.67 (s, 2H), 3.59 (t, J=8.1 Hz, 2H), 3.30 (t, J=8.1 Hz, 2H), 0.94 (t, J=8.1 Hz, 2H), 0.70 (t, J=8.1 Hz, 2H), 0.00 (s, 9H), -0.09 (s, 9H)。
実施例 4 1 : 4一ホルミル一 N, N—ビス (1 H—イミダゾールー 2—ィル メチル) ベンズアミ ド (実施例 4 1 )
化合物 4 0 (1.7 g ) に 5 0 %トリフルォロ酢酸ージクロロメタン溶液(10 m L ) を加えた。 反応混合物を室温で 3時間撹拌した。 反応混合物を濃縮し た。 残渣に 5 N水酸化ナトリウム水溶液 (15 m L) を加えた。 水層を 5 0 m Lのジクロロメタンで 3回抽出した。 有機層を合わせて飽和食塩水で洗浄し、 無水硫酸マグネシウムで乾燥した。 溶媒を濃縮し、 以下の物性値を有する標 題化合物 (化合物 (922 m g ) を得た。
TLC - Rf O.60 (クロ口ホルム:メタノール: 28%アンモエア水 = 80:10:1) ; NMR (CDCls): 5 10.03 (s, 1H), 7.92 (d, J=8.1 Hz, 2H), 7.74 (d, J=8.1 Hz, 2H), 7.12-6.94 (m, 4H), 4.73 (s, 2H), 4.58 (s, 2H)。
実施例 4 2 : シス一 N, N—ジプロビルシクロへキサン一 1, 4ージァミン (化合物 4 2 )
実施例 8の工程で化合物 7の代わりに tert—プチル 4一アミノシクロへ キシルカルバメ一トを用いて実施例 8と同様に操作し、 得られた化合物に 1 0 %塩化水素一メタノール溶液 (10 m L) を加えた。 反応混合物を室温で 2 時間撹拌した。 溶媒を濃縮し、 残渣をメタノール (30 m L ) に溶解した。 こ の溶液にカーボネート樹脂 (商品名: MP- Carbonate, Argonaut社製,製品番
号: 800267, 3 g )を加え、室温で 2時間撹拌した。反応混合物をろ過した後、 ろ液を濃縮した。 残渣を精製することなく以下の物性値を有する標題化合物 (467 mg) を得た。
TLC: Rf 0.26 (ジクロロメタン:メタノール: 28%ァンモ -ァ水 - 80:20:3); NMR (CDCls): 83.35-3.29 (m, 1 H), 2.85-2.73 (m, 1 H), 2.72-2.64 (m, 4 H); 1.95-1.56 (m, 12 H), 0.92 (t, J=7.2 Hz, 6 H)。
実施例 43 : 4— ( { [シス一 4一 (ジプロピノレアミノ) シクロへキシル] ァミノ) メチル) 一 N, N—ビス ( 1 H—イミダゾールー 2—ィルメチル) ベンズアミ ド (化合物 43)
化合物 41 (116 mg) と化合物 42 (203 mg) の 1%酢酸ージクロ口 メタン溶液 (5 mL) に無水硫酸ナトリウム (220 mg) を加えた。 混合物 を室温で 30分撹拌した。 反応混合物に三ァセトキシ水素化ホウ素ナトリウ ム (225 mg) を加えた。 混合物を室温で 6時間撹拌した。 反応混合物に飽 和炭酸水素ナトリゥム水溶:液 (10 mL) を加えた。 水層をジクロロメタン: メタノール =3 : 1混合物 (50 mL) で 2回抽出した。 有機層を合わせて飽 和食塩水で洗浄し、 無水硫酸マグネシウムで乾燥した。 溶媒を濃縮し、 シリ 力ゲルク口マトグラフィ一で精製して以下の物性値を有する標題化合物(149 mg) を得た。
性状:アモルファス
96ΐ
。(Η Ζ 'ΖΗ S'L=r 'Ρ) Τ9Ί '(Η Ζ '^Η 8·ム =f 'Ρ) 9S L '(Η f '∞) 2Γム- ΐ6·9 '(Η f ) 6L'f-Z9'f '(Η Ζ 's) 6f 8 '(Η Ζ '∞)ム OS'S '(Η S '∞) f Z-^ Z ' B. Ζ
'TO) S0'S-t8*X '(Η 8 'ra 9ム Ί- 6ΖΊ '(Η 9 <ΖΗ Z'L= 980 g: (εΐθαθ) m
- (T:02:08 =氺 0 /08 & — / べ ^^ xi ^^) 6V0M: 0ΊΛ
丄 士 :
[ -^ η^ - τ - < 4/ ^) -^] } - : (z) ε um^
°(H Z 'ZH T"8=f 'Ρ) 6Sム '( 、H Z ' T'8=f 'P) SS'ム '(H f LVL-699 '(H t 'ra) Lff-Z 'f '(H Z 's) fV£ '(R '
s) 96 Z '(H 9 VZ-6TZ '(H
<ZH 0^ S=f ZL'l '(H Z ) Wl- Z'l '(H 8 '
ZH S"2,=f ')ム 8'09: (
8Τθαθ) ¾ΗΝ • (1:02:08 =氺 - ¾
: ΟΊΧ ST
^ /¾ : ^¾
(ι-ε ^ ^ >- [ ^≠
-ζ) ] — ー
^ '- ζー ^ ^; ^一 Η τ) 一Ν ' : (τ) s 牽 邋 § 袅 '呦 土 « n
(I D m ,- (T) z mw s
°(H Z 'ZH I'8=f 'Ρ) SSム '(H Z '^H I"8=f ' ) 8 ム '(H f <TO) fVL-W9 '(H 'ra) X8- -8S '(H 's) 9 ε '(Η I ) '(H S '∞) LS'S-^S'^ '(Η Z 'TO) 98 Τ-0ΛΊ '(H 01 ) 69Ί-0ε ΐ '(H 9 ' Ζ'1=ΐ 9809: (εΐθαθ) ΗΜΝ
9909l0/S00Zdf/X3d 900Z OAV
実施例 43 (3) : 4一 ( { [トランス一 4— (ジプロピルァミノ) シクロ へキシル〕 アミノ} メチル) 一 N, N—ビス (1H—イミダゾールー 2—ィ ルメチル) ベンズァミド (化合物 43-3)
性状: アモルファス
TLC: Rf 0.57 (ジクロロメタン:メタノール: 28%ァンモニァ水 = 80:20:3); NMR (CDC13): δ 0.85 (t, J=7.2 Hz, 6 H), 0.98-1.33 (m, 4 H), 1.33-1.51 (m, 4 H), 1.71-1.86 (m, 2 H), 1.91—2.07 (m, 2 H), 2.28 - 2.56 (m, 6 H), 3.81 (s, 2 H), 4.53-4.77 (m, 4 H), 6.91-7.13 (m, 4 H), 7.34 (d, J=8.1 Hz, 2 H), 7.54 (d, J=8.1Hz, 2H)0
実施例 43 (4) : 4— [ ( {トランス一 4一 [シクロへキシル (プロピル) ァミノ] シクロへキシル } ァミノ) メチノレ] — N, N—ビス (1H—イミダ ゾールー 2—イノレメチル) ベンズァミド (化合物 43— 4)
TLC: Rf 0.60 (ジクロロメタン:メタノール: 28%アンモユア水 = 80:20:3); NMR (CDCls): 50.81 (t, J=7.2 Hz, 3 H), 0.96-1.46 (m, 11 H), 1.51 - 1.65 (m, 1 H), 1.65 - 1.82 (m, 6 H), 1.88—2.04 (m, 2 H), 2.28—2.68 (m, 5 H), 3.81 (s, 2 H), 4.51-4.80 (m, 4 H), 6.89-7.16 (m, 4 H), 7.34 (d, J=8.1 Hz, 2 H), 7.55 (d, J=8.1Hz, 2H)0
実施例 43 (5) : 4一 [ (7—シクロへキシノレ一 2, 7—ジァザスピロ [3. 5] ノン一 2—ィル) メチル] 一 N, N—ビス (1H—イミダゾーノレ一 2— ィルメチル) ベンズァミド (化合物 43- 5)
性状:アモルファス
TLC: Rf 0.37 (ジクロロメタン:メタノール: 28%アンモニア水 = 80:20:3);
NMR (CDCls): 80.98-1.33 (m, 5 H), 1.52-1.96 (m, 9 H), 2.20-2.62 (m, 5 H)
2.99 (s, 4 H), 3.63 (s, 2 H), 4.52-4.81 (m, 4 H), 6.92-7.14 (m, 4 H), 7.29 (d,
J=8.1 Hz, 2 H), 7.48 (d, J=8.1 Hz, 2 H)。
実施例 43 (6) : 4— ( { [3— (ジプロピルァミノ) シク口へキシル] ァミノ) メチル) 一 N, N—ビス (1H—イミダゾールー 2—ィルメチル) ベンズァミ ド (化合物 43-6)
性状:アモルファス
TLC :Rf 0.32 (クロ口ホルム:メタノール: 28%アンモエア水 =80:10:1); NMR CDMSO-De): δ d 0.78 (t, J=7.5 Hz, 6 H), 1.28 (m, 7 H), 1.61 (m, 4 H), 1.94 (m, 1 H), 2.28 (m, 4 H), 2.86 (m, 2 H), 3.65 (m, 2 H), 4.58 (m, 4 H), 6.88 (m, 2 H), 7.08 (m, 2 H), 7.33 (d, J=8.1 Hz, 2 H), 7.43 (d, J=8.10 Hz, 2 H), 12.14 (m, 1 H), 12.36 (m, 1 H)。
実施例 43 (7) : 4 - ( { [3- (ジプロピルアミノ) シクロへキシル] ァミノ) メチル) 一 N, N—ビス (1 H—イミダゾール一 2—ィルメチル) ベンズァミド (化合物 43-7)
66ΐ ^ /·3Γ :
(ο τ— ε
( /^^ ^一 s—^— ^ ^一 Ητ) ^r -N 'Ν— {Λ^^ { ^
— s] } ) - ■ (0 τ) ε Ϊ^Μ^ °(HS 'TO) WL-Z 'L '(HS 'TO) ZVL-Z 'L '(Hf 2ΓΔ-86·9 {(H '∞) 08' -SS-f '(IK <s) '(H ^Ζ-
'(Hi '∞) os's '(HI '∞) oz z '(mi '∞) 0Τ 2-0ΓΤ p 9 : (ετοαο)丽 N oz
- (ΐ :01:06 = 氺 士 0 /08S:4Z— べ ^≠ ^^) SS0J¾[: 0ΊΧ
厶 : ¾c¾
(6 -ε ^ ψλ ) ^ xベ (4/ ^ / 一 s— /— 一HI) ー N 'N: (6) ε SI
。(ΙΚ 'ΖΗ
8·ム =f 'Ρ) 'L \ΉΖ 'ΖΗ 8·ム =f 'Ρ) Of'L '(Ht 0£'L-ZZ L '(Rf '^) ^0^-969
ΧΉ.Ζ 's) 89 \ΉΖ 's) Ψ9 \RZ 's) SS 8 '(H <s) TS 8 '(H ' ) 2 Z-2 Z
's) 9Tz m 'TO) ss x-i i '(H9 'ZH s' =f ss o 9: (8ιοαο) HHN
- (T:0T:06 = 氺 0 /08 & —/ べ ^^ /^^) gSOJH: ΟΊΧ 0T 士 : ¾ί¾
. (8-ε ^ λ A ^ ^ -
Z— —、 ^ ^ ^一 H T ) 一 N 'Ν- {Λί =^ ( -^^) {
^ベ Λ(^≠ ( ^ ^) ] -ε} ] } : (8) ε ^ m
°(H 1 ) xg-gi '(H Z '∞) ZVL '(H Z 88 , '(H f ム 6·9 '(H S f '∞) 9S '(Η T 'πι) Sム ·ε '(Η τ 'TO) 998 '(Η I '∞) 68^ '(Η 9 '∞) Ζ2 Ζ '(Η Ζ '∞) ^6 Τ '(Η 8 'τπ) 991 '(Η 9 '∞) '(Η 9 ' ) 080 Ρ 9: (9α - OSHCI) HHN
• (1:01:08= ^ .-^K %^Ζ· ί— ^ ^:^ ^ τχ ^) 9^0 JH: ΟΊΧ
9909l0/£00idf/X3d 而 9002: OM
TLC: Rf 0.70 (クロ口ホルム:メタノール: 28%アンモニア水 = 40:10:2); NMR (CDCls): 50.80 (t, J=7.2 Hz, 3 H), 0.87 (t, J=7.2 Hz, 3 H), 1.00-1.56 (m, 8 H), 1.55-1.87 (m, 4H), 1.98—2.56 (m, 6 H), 3.65 (d, J=13.5 Hz, 1 H), 3.88 (d, J=13.5 Hz, 1 H), 4.48-4.80 (m, 4 H), 6.85-7.12 m, 4 H), 7.33 (d, J=8.1 Hz, 2 H), 7.57 (d, J=8.1 Hz, 2 H)。
実施例 43 (11) : 4— ( { [5— (ジプロピルァミノ) ォクタヒドロ一 2—ペンタレニル] アミノ} メチル) 一 N, N—ビス (1H—イミダゾール 一 2—イノレメチノレ) ベンズアミ ド (化合物 43- 11)
性状:アモルファス
TLC:Rf 0.35 (クロ口ホルム:メタノール: 28%アンモユア水 =40:10:2) ; NMR (CDC13): 80.87 (t, J=7.2 Hz, 6 H), 1.07-1.63 (m, 8 H), 1.96-2.41 (m, 6 H), 2.44-2.63 (m, 4 H), 2.87-3.19 (m, 2 H), 3.79 (s, 2 H), 4.49-4.79 (m, 4 H), 6.86-7.15 (m, 4 H), 7.36 (d, J=8.1 Hz, 2 H), 7.58 (d, J=8.1 Hz, 2 H)。 実施例 44 : tert—ブチル 4— (2- {ビス [ (1— { [2— (トリメチノレ シリル) エトキシ] メチル } 一 1H—イミダゾールー 2—ィル) メチル] ァ ミノ } 一 2—ォキソェチル) 一 1ーピペリジンカルボキシラート (化合物 4 4)
アルゴン雰囲気下室温において、 [1一 (tert—ブトキシカルボ-ル) 一 4 ーピペリジニノレ] 酢酸 (500 mg) と化合物 2 (899 mg) を無水ジメチル ホルムアミド (12 mL) に溶かし、 ここに 1ーェチルー 3— [3— (ジメチ ルァミノ) プロピル] カルポジイミ ド (590 mg) 、 1ーヒドロキシベンズ トリァゾール (417 mg) 、 4ージメチルァミノピリジン (377 m g ) を加 えて室温で 16時間撹拌した。 巿水を加えて撹拌後、 酢酸ェチルで 3回抽出 した。 有機層を集めて飽和食塩水で洗浄した。 無水硫酸ナトリウムで乾燥後 溶媒留去した。 シリカゲルカラムクロマトグラフィーで精製して以下の物性 値を有する標題化合物 (216 mg) を得た。
TLC : Rf 0.85 (クロ口ホルム:メタノール: 28%アンモニア水 = 90:10:1); NMR (CDCls): 5 7.00-6.91 (m, 4H), 5.36 (s, 2H), 5.33 (s, 2H), 4.77 (s, 2H), 4.68 (s, 2H), 4.08 (m, 2H), 3.50 (m, 2H), 2.75 (m, 2H), 2,46 (d, J=6.6 Hz, 2H), 2.12 (m, 1H), 1.76 (m, 2H), 1.65 (s, 9H), 1.14 (m, 2H), 0.90 (m, 2H), 0.00 (m,恵)。
実施例 4 5 : N, N—ビス ( 1 H—イミダゾールー 2一ィルメチル) 一 2— ( 4—ピペリジニル) ァセトアミ ド 三塩酸塩 (化合物 4 5 )
実施例 4 4で製造した化合物 (216 m g ) に 4 N塩化水素 Zジォキサン (8 m L ) をカロえ、 室温で 3時間、 7 0でで 3時間撹拌した。 これを溶媒留去し て残渣を精製することなく標題化合物を得た。
TLC : Rf 0.11 (クロ口ホルム:メタノール: 28%アンモユア水 = 40:10:2); 実施例 4 6 : 2— { 1 - [ 4一 (ジプロピルァミノ) ブチル] 一 4—ピペリ ジニル } -N, N—ビス ( 1 H—ィミダゾ一ルー 2—ィルメチル) ァセトァ ミド (化合物 4 6 )
化合物 4 5と 4一 (ジプロピルァミノ) プタナール (55.6 m g ) を加え、 1 0 %酢酸一無水ジメチルホルムアミ ド溶液 (3 m L) をアルゴン雰囲気下 5分間撹拌した。 反応液に三ァセトキシ水素化ホウ素ナトリウム (103 m g ) を加えて室温で 1 5時間撹拌した。反応液に 2 N水酸化ナトリゥム水溶液(10 m L) を加え、 水層を酢酸ェチルで 3回抽出した。 有機層を集めて飽和食塩 水で洗浄した後、 無水硫酸ナトリウムで乾燥、 溶媒留去した。 残渣をシリカ ゲル力ラムクロマトグラフィ一で精製して以下の物性値を示す標題化合物
(86.4 m g ) を得た。
性状:油状物
TLC : Ef 0.78 (クロ口ホルム:メタノール: 28%アンモニア水 = 40:10:2); NMR (CDCls) : 5 0.86 (t, J=7.2 Hz, 6 H), 1.10—1.29 (m, 2 H), 1.34-1.52 (m; 8 H), 1.53-1.77 (m, 3 H), 1.77-1.95 (m, 2 H), 2.19-2.51 (m, 10 H),
2.70-2.94 (m, 2 H), 4.66 (s, 2 H), 4.75 (s, 2 H), 6.90-7.06 (m, 4 H)。
実施例 4 6 ( 1 ) 〜実施例 4 6 ( 2 )
[ 1一 (tert—ブトキシカルボニル) 一 4—ピ リジニル] 齚酸の代わりに 相当するカルボン酸を用いて実施例 4 4→実施例 4 5→実施例 4 6と同様の 操作をし、 必要に応じて塩に置換することによって以下の本発明化合物を得
7 。■
実施例 4 6 ( 1 ) : 1一 [ 4一 (ジプロピルァミノ) プチル] 一 N, N—ビ ス ( 1 H—イミダゾールー 2—ィルメチル) 一 4—ピペリジンカルボキサミ ド 四塩酸塩 (化合物 4 6— 1 )
性状:アモルファス
TLC: R£ 0.68 (クロ口ホルム:メタノール: 28%アンモニア水 = 40:10:2);
NMR (METHANOL- D4) : δ 1.02 (t, J=7.5 Hz, 6 H), 1.54-1.90 (m, 7 H),
1.94-2.21 (m, 5 H), 2.88-3.25 (m, 12 H), 3.50-3.74 (m, 1 H), 4.81-5.01 (m,
2 H), 5.42 (s, 2 H), 7.50 (s, 2 H), 7.61 (s, 2 H)。
実施例 4 6 ( 2 ) : 3 - { 1 - [ 4 - (ジプロピルァミノ) プチル] 一 4一 ピペリジニル } 一 N, N—ビス (1 H—イミダゾールー 2—ィルメチル) プ 口パンアミド (化合物 4 6— 2 )
性状:油状物
TLC: Rf 0.78 (クロ口ホルム:メタノール: 28%アンモニア水 = 40:10:2); NMR (CDCls): δ 0.86 (t, J=7.5 Hz, 6 H), 1.09-1.28 (m, 2 H), 1.32-1.62 (m, 11 H), 1.73-1.84 (m, 2 H), 2.17-2.48 (m, 12 H), 2.80-2.89 (m, 2 H), 4.65 (s,
2 H), 4.74 (s, 2 H), 6.92-7.03 (m, 4 H)。
実施例 47 :ェチル 4一 ( {ビス [ (1— { [2- (トリメチルシリル) ェ 1、キシ] メチル } — 1 H—イミダゾールー 2—ィル) メチル] アミノ } 力 ルポュルァミノ) ベンゾエート (化合物 47 )
プチル 4一イソシアナートベンゾアート (250.4 mg) と化合物 2 (500 mg) のジクロロメタン (3 mL) 溶液を、 室温で 1時間撹拌した。 反応液 を減圧下濃縮し、 残渣をシリカゲル力ラムクロマトグラフィ一で精製して以 下の物性値を有する標題化合物 (731.9 mg) を獰た。
TLC: Rf0.24 (n一へキサン:メタノール =3:1);
NMR (CDCls): δ 7.98 ( d , J=9.0 Hz, 2 H), 7.58 ( d, J=9.0 Hz, 2 H), 7.04 (s, 1 H), 7.00 (s, 1 H), 5.43 (s, 4 H), 4.74 (s, 4 H), 4.30 (t, J=6.6 Hz, 2 H), 3.50 (m, 4 H), 1.75 (m, 2 H), 1.49 (m, 2 H), 0.98 (t, J=7.5 Hz, 3 H), 0.88 (m, 4 H), -0.55 (s, 18 H)。
実施例 48 : 4一 ( { [ビス (1H—イミダゾールー 2一^ fルメチル) アミ ノ] カルボ二ル} ァミノ) 一N— [4一 (ジプロピルァミノ) プチル] ベン ズアミド (化合物 48)
化合物 47 (195 mg) のメタノール (2 mL) 溶液に濃塩酸を 2mL加 えた。 反応液を 60°Cで 6時間撹拌した。 室温まで冷却した後、 反応液を減 圧下濃縮した。 このようにして得られた化合物と N, N—ジプロピル一 1, 4—プタンジァミンを用いて実施例 17と同様の操作を行ない、 以下の物性 値を有する標題化合物 (76.6 mg) を得た。
性状:アモルファス
TLC :Rf 0.67 (クロ口ホルム:メタノール: 28%アンモニア水 =80:20:4); NMR (DMSO-De): δ d 0.81 (t, J=7.5 Hz, 6 H), 1.22-1.60 (m, 8 H),
2.13-2.43 (m, 6 H), 3.22 (q, J=6.6 Hz, 2 H), 4.59 (s, 4 H), 6.73-6.98 (m, 2 H), 6.98-7.24 (m, 2 H), 7.50 (d, J=9.0 Hz, 2 H), 7.74 (d, J=9.0 Hz, 2 H),
8.25 (t, J=5.7 Hz, 1 H), 9.57(s, 1 H), 11.99- 12.39(m, 2 H)。
実施例 49 : 4一 [ (2—シクロへキシルー 2, 7—ジァザスピロ [3. 5] ノナ一 7—ィル) メチル] 一 N, N—ビス (1H—イミダゾール一 2—ィル メチノレ) ベンズアミド (化合物 49)
化合物 41と 2—シク口へキシルー 2, 7ージァザスピロ [3. 5] ノナ ンを用いて実施例 43と同様の操作をして、 以下の物性値を示す標題化合物 を得た。
MS : 502 (M+H)+; HPL C保持時間: 2.74分。
実施例 49 (1) 〜実施例 49 (20)
2—シクロへキシルー 2, 7—ジァザスピロ [3. 5] ノナンの代わりに 相当するァミン化合物を用いて実施例 49と同様の操作を行ない、 以下の物 性値を示す標題化合物を得た。
実施例 49 (1) : 4一 [ (2—シクロへキシルー 2, 8—ジァザスピロ [4. 5] デカー 8—^ fル) メチル] 一 N, N—ビス (1H—イミダゾーノレ一 2— ィルメチル) ベンズァミド (化合物 49-1)
MS : 516 (M+H)+; HPL C保持時間: 2.40分。
実施例 49 (2) : 4— [ (8—シクロへキシルー 2, 8—ジァザスピロ [4.
5] デカ一 2—ィノレ) メチル] — N, N—ビス (1H—イミダゾールー 2— ィルメチル) ベンズァミ ド (化合物 49-2)
MS : 516 (M+H)+; HPL C保持時間: 2.41分。
実施例 49 (3) : 4一 [ (9—シクロへキシル一2, 9ージァザスピロ [5. 5] ゥンデカー 2—ィノレ) メチル] -N, N—ビス (1 H—イミダゾールー 2一イノレメチル) ベンズァミド (化合物 49— 3)
MS : 530 (M+H)+; HPL C保持時間: 2.46分。
実施例 49 (4) : 4一 [ (7—シクロへキシルー 2, 7—ジァザスピロ [4. 5] デカー 2—ィル) メチル] 一 N, N—ビス (1H-イミダゾーノレ一 2— ィ /レメチノレ) ベンズアミド (化合物 49-4)
MS : 516 (M+H)+; HPL C保持時間: 2.43分。
実施例 49 (5) : 4一 [ (8—シクロへキシル一2, 8—ジァザスピロ [5. 5] ゥンデカー 2—ィル) メチル] —N, N—ビス (1H—イミダゾールー 2—ィルメチル) ベンズアミ ド (化合物 49-5)
MS : 530 (M+H)+; HPL C保持時間: 2.46分。
実施例 49 (6) : 4- [ (1,ーシクロへキシルスピロ [インドールー 3, 4'—ピぺリジン] —1 (2H) —ィル) メチル] 一 N, N—ビス (1H—ィ ミダゾール一 2—ィルメチル) ベンズァミ ド (化合物 49— 6)
MS : 564 (M+H)+; HPL C保持時間: 2.80分。
実施例 49 (7) : 4— [ (1,ーシクロへキシルー 5—メチルスピロ [イン ドール一 3, 4,ーピペリジン] 一 1 (2H) —ィル) メチル] 一 N, N—ビ ス ( 1 H— ^ f ミダゾーノレ一 2一ィルメチル) ベンズァミド (化合物 49— 7)
MS : 578 (M+H)+; HPL C保持時間: 2.88分。 i
実施例 49 (8) : 4- [ (1,—シクロへキシルー 一フルォロスピロ [ィ ンドール一 3, 4,ーピペリジン] 一 1 (2H) —イノ!^) メチル] 一 N, N— ビス (1H—イミダゾールー 2—ィルメチル) ベン:^アミド (化合物 49一 8) ,.
MS : 582 (M+H)+; HPL C保持時間: 2.84分。
実施例 49 (9) : 4一 [ (5—クロ口一 1'ーシクロへキシルスピロ [イン ドール一 3, 4,ーピペリジン] ー1 (2H) —ィル) メチル] 一 N, N—ビ ス ( 1 H—イミダゾールー 2 fルメチル) ベンズァミ ド (化合物 49-9) MS : 598 (M+H)+; HP L C保持時間: 2.93分。
実施例 49 (10) : 4— [ (1—シクロへキシルー 1, 2—ジヒドロー 1, H—スピロ [インドール一 3, 4,ーピペリジン] 一 1,一ィル) メチル] — N, N—ビス ( 1 H— ^ f ミダゾールー 2—ィルメチル) ベンズァミ ド (化合物 4 9-10)
MS : 564 (M+H)+; HPL C保持時間: 2.95分。
実施例 49 (11) : 4— { [3— (ジプロピルァミノ) 一2, 3—ジヒ ド 口一 1Ήースピロ [インデン一 1, 4,ーピペリジン] 一 1,一ィル] メチノレ } 一 N, N—ビス ( 1 H—イミダゾールー 2—ィルメチル) ベンズァミ ド (化 合物 49-11)
MS : 580 (M+H)+; HP L C保持時間: 2.59分。
実施例 49 (12) : 4一 [ (1ーシクロへキシル一5—メチルー 1, 2— ジヒ ドロ一 1Ήースピロ [インドー/レー 3, 4,ーピペリジン] — 1,ーィノレ) メチノレ] -N, N—ビス (1H—イミダゾールー 2—ィルメチル) ベンズァ ミド (化合物 49-12)
MS : 576 (M+H)+; HPL C保持時間: 2.76分。
実施例 49 (13) : 4— [ (4ーシクロへキシルー 1—ォキサ一 4, 9—
ジァザスピロ [5. 5] ゥンデカー 9一ィル) メチ /レ] 一 N, N—ビス (1 H—ィミダゾールー 2—ィルメチル) ベンズァミド (化合物 49— 13)
M S,: 532, (M+H)+; HP L C保持時間: 2.39分。
実施例 49 (14) : 4— [ (9ーシクロへキシルー 1一ォキサ一4, 9一 ジァザスピロ [5. 5] ゥンデカー 4ーィノレ) メチノレ] 一 N, N—ビス (1 H—ィミダゾーノレ一 2—イノレメチル) ベンズァミド (化合物 49— 14) MS : 532 (M+H)+; HPL C保持時間: 2.47分。
実施例 49 (15) : 4— [ (4ーシクロへキシルー 1一ォキサ一 4, 8— ジァザスピロ [5. 5] ゥンデカー 8—ィル) メチノレ] 一 N, N—ビス (1 H—ィミダゾールー 2一ィルメチル) ベンズァミ ド (化合物 49— 15)
MS : 532 (M+H)+; HPL C保持時間: 2.41分。
実施例 49 (16) : 4— [ (8—シクロへキシルー 1一ォキサ一4, 8— ジァザスピ [5. 5] ゥンデカー 4一ィル) メチル] 一 N, N—ビス (1 H—イミダゾールー 2—ィルメチル) ベンズァミ ド (化合物 49— 16) MS : 532 (M+H)+; HPL C保持時間: 2.41分。
実施例 49 (17) : 4— [ (2—ジクロへキシルー 2, 3—ジヒドロー 1 H, 1Ή—スピロ [イソキノリンー4, 4,ーピペリジン] 一 1,一ィル) メチ ル] — N, N—ビス (1 H—イミダゾールー 2—ィルメチル) ベンズアミ ド (化合物 49一 17)
MS : 578 (M+H)+; HPL C保持時間: 2.60分。
実施例 49 (18) : 4— [ (1'—シクロへキシルー 1 H—スピロ [イソキ ノリンー 4, 4'ーピペリジン] —2 (3H) 一ィル) メチル] 一 N, N—ビ
ス ( 1 H—ィミダゾ一/レー 2一イノレメチル) ベンズァミド (化合物 49一 18)
MS : 578 (M+H)+; HP L C保持時間: 2.54分。
実施例 49 (19) :ェチル 8— (4一 { [ビス (1H-イミダゾーノレ一 2—ィルメチル) ァミノ] 力ルポ二ル} ベンジル) 一 2—シクロへキシルー 2, 8—ジァザスピロ [4.5] デカン一 3—カルボキシラート (化合物 49 - 19)
MS : 588 (M+H)+; HP L C保持時間: 2.57分。
実施例 49 (20) : 4- { [4- (ジプロピルァミノ) 一3, 4一ジヒ ド ロー 1Ήースピロ [クロメン一 2, 4'—ピペリジン] ー1, ル] メチル } 一 N, N—ビス (1 H—イミダゾールー 2—ィルメチル) ベンズアミ. ド (化 合物 49— 20)
MS : 596 (M+H)+; HP L C保持時間: 2.61分。
実施例 50 (1) 〜実施例 50 (147)
化合物 41の代わりに相当するアルデヒド、 化合物 42の代わりに相当す るアミンを用いて実施例 43と同様の操作をし、 以下の物性値を有する標題 化合物を得た。
実施例 50 (1) : 4一 [ ( {トランス一 4一 [ベンジル (プロピル) アミ ノ] シクロへキシル } ァミノ) メチル] 一 N, N—ビス (1H—イミダゾー ル一2—ィルメチル) ベンズアミ ド
TLC: Rf 0.48 (酢酸ェチル:メタノール: 28%アンモニア水 = 90:10:2); NME (CDCls): δ d 0.81 (t, J=7.2 Hz, 3H), 1.02-1.42 (m, 6H), 1.78-1.90 (m, 2H), 1.95-2.06 (m, 2H), 2.40 (t, J=7.2 Hz, 2H), 2.40-2.60 (m, 2H), 3.59 (s, 2H), 3.81 (s, 2H), 4.50-4.75 (m, 4H), 6.96-7.10 (m, 4H), 7.15—7.40 (m, 7H), 7.50-7.60 (m, 2H)。
実施例 50 (2) : 4一 [ ( {トランス一 4— [シク口へキシノレ (ェチル) ァミノ] シクロへキシル } ァミノ) メチノレ] — N', N—ビス (1H—イミダ ゾールー 2—ィルメチル) ベンズァミ ド (化合物 50— 2)
性状:アモルファス
TLC: Rf 0.21 (酢酸ェチル:メタノール: 28%アンモニア水 = 90:10:2); NME (CDCls): δ d 0.98-2.05 (m, 21H), 2.40 (m, 1H), 2.50-2.75 (m, 4H), 3.81 (s, 2H), 4.58-4.75 (m, 4H), 6.98-7.10 (m, 4H), 7.35 (d, J=8.1 Hz, 2H), 7.59(d, J=8.1Hz, 2H)0
実施例 50 (3) : 4— [ (7—シクロへキシル一 2, 7—ジァザスピロ [4. 4] ノナ一 2—ィル) メチノレ] 一 N, N—ビス (1 H—イミダゾールー 2— ィルメチル) ベンズァミ ド (化合物 50-3)
性状:アモルファス
TLC: Rf 0.65 (クロロホルム:メタノール: 28%アンモニア水 = 40:10:2); NMR (CDCls): δ 1.00-1.45 (m, 6 H), 1.53-2.10 (m, 8 H), 2.19-2.41 (m, 2 H): 2.47-3.00 (m, 7 H), 3.53-3.68 (m, 2 H), 4.48-4.88 (m, 4 H), 6.95-7.09 (m, 4 H), 7.33 (d, J=8.1 Hz, 2 H), 7.53 (d, J=8.1 Hz, 2 H)。
実施例 50 (4) : 4一 [ (2—シクロへキシル一 2, 7—ジァザスピロ [4.
5] デカー 7—ィル) メチル] 一 N, N—ビス (1 H—イミダゾールー 2— ィルメチル) ベンズァミド (化合物 50— 4)
性状:アモルファス
TLG:Rf0.72 (クロ口ホルム:メタノール: 28%アンモニア水 =40:10:2);
NMR (CDCls): δ 0.94-1.30 (m, 4 H), 1.30-2.57 (m, 19 H), 2.56-2.91 (m, 2
H), 3.24-3.51 (m, 2 H), 4.40-4.92 (m, 4 H), 7.01 (s, 4 H), 7.33 (d, J=8.1 Hz,
2H), 7.50(d, J=8.1Hz,2H)。
実施例 50 (5) : 4— ( { [4— (3, 4ージヒドロイソキノリン一 2 (1
H) ーィノレ) シクロへキシノレ] アミノ} メチノレ) 一 N, N—ビス (1H—ィ ミダゾールー 2—イノレメチル) ベンズァミド (低極性体) (化合物 50-5) 性状:アモルファス
TLC: Rf 0.55 (酢酸ェチル:メタノール: 28%アンモニア水 = 90:10:2);
NMR (CDCls): δ d 1.44-1.92 (m, 8H), 2.48 (m, 1H), 2.75-2.95 (m, 5H), 3.78 (s, 2H), 3.79 (s, 2H), 4.55-4.72 (m, 4H), 6.98-7.18 (m, 8H), 7.40 (d, J=7.8 Hz, 2H), 7.63 (d, J=7.8 Hz, 2H)。
実施例 50 (6) : 4— ( { [4一 (3, 4—ジヒドロー 2 ( 1 H) 一イソ キノリエル) シクロへキシル] ァミノ) メチル) 一 N, N—ビス (1H—ィ ミダゾーノレ一 2—イノレメチル) ベンズァミ ド (高極†生体) (化合物 50-6)
性状:アモルファス
TLC: Rf 0.41 (酢酸ェチル:メタノール: 28%アンモニア水 = 90:10:2);
NMR (CDGls): δ d 1.15-2.60 (m, 10H), 2.80-2.98 (m, 4H), 3.79 (s, 2H), 3.86 (s, 2H), 4.55-4.75 (m, 4H), 6.98-7.15 (m, 8H), 7.39 (d, J=8.4Hz, 2H), 7.63 (d, J=8.4Hz, 2H)。
実施例 50 (7) : N, N—ビス (1H—イミダゾールー 2—ィルメチル) -4- [ ( {4- [ (4 a S, 8 a R) ーォクタヒドロイソキノリン一 2 (1 H) —ィル] シクロへキシル } ァミノ) メチノレ] ベンズアミ ド (低極性体)
(化合物 50— 7)
性状: ァモノレファス
TLC: Rf 0.50 (酢酸ェチル:メタノール: 28%アンモニア水 = 90:10:2);
NMR (CDCls): 5 d 0.80-2.82 (m, 24H), 2.94 (m, IH), 3.12 (m, 1H), 3.75 (s, 2H), 4.52-4.72 (m, 4H), 6.98-7.18 (m, 4H), 7.39 (d, J=8.4Hz, 2H), 7.63 (d, J=8.4 Hz, 2H)。
実施例 50 (8) : 4- [ ( {4- [ (4 a S, 8 a R) —ォクタヒドロ一 2 (1 H) 一イソキノリエル] シクロへキシル } ァミノ) メチル] 一 N, N 一ビス (1 H—ィミダゾールー 2—ィルメチル) ベンズァミド (高極性体)
(τ ι-ο 9呦 、 χ {Λί^
(4/ i^^y-z—へ (一 、 ^ ) ^一 Hi) r ~N 'N : (τ T) o s闘
°(H T 'TO)
99 Zl- Z ZT '(Η T '∞) Z Zl-96'U '(H Z '¾ί V9=D 'V) ZVL '(Η Z '^Η '8=f 'Ρ) £S'L '(H Z 'TO) 91 L-00L '(Η Z '∞) 00·ム- 9 9 '(H f '^) '(Η Z s) L92 '(H 'ra) Ι9·ε-8^ε '(Η X '∞) Ψ9 Ζ-Ψ Ζ '(H f '∞) VZ-Z^Z '(Η I '^) ST'S- '(H f <ra) SA t-891 '(H f '∞) LVT-9Z X P 9: (9a-OS d)丽 N ^ /¾ : ¾ί¾ (0 τ -09 ψ ) ^ Xペ {Λ(4=
{Λ^≠ΛΟ ζ -Λ(-^ .^ y-ui) ー Ν 'Ν : (ο τ ) ο 9 Μ
°(HS 'ΖΗ Τ"8=Γ 'Ρ) 69 L '(Ηム OfL-^VL l(m 'πι) 2Γム- 86·9 '(Η '^) f -Z^ '(Ή.Ζ 's) 088 '(ΉΖ (s) ZL'£ '(RU '∞) 292-260 Ρ 9: (8ΐθαθ) ΗΗΝ
- {z = 氺 % ^ ' ^エ蠲 f o :ΟΊΛ
(6-09呦 、 Xぺ ( ^ i^^ - Z - — C 、、 一 Ηΐ) ー N !N- [4/ ^" ム {Λ^ ^η [/^ {Λί ^τχ ) Λ(^ ^ 一,— ベ 4} ) ] — ·· (6) O S闘
°( <ΖΗ VS=
'Ρ) 91 '(RZ ( f'8=f 'Ρ) 9£ L '(Jif '^) 8Γム- 86·9 '(ΉΡ '∞) L' -Z 'f RZ <s) Ι8Έ '(HI <ra) 86'g '(HX '^) 062 '(H 2 092-080 P 9: (εΐθαθ) HHN '· (2:01:06 =氺 二士 0 — ^ ^ェ鏹1) L '0 :0Ίί
4 :
(8-0 g
9909T0/S00Zdf/X3d
性状: アモルファス
TLC: Rf0.50 (クロ口ホルム:メタノール: 28%アンモニア水 = 80:20:4); NME CDMSO-De): δ 0.86-1.26 (m, 4Η), 1.66-1.82 (m, 2 H), 1.84-1.99 (m, 2 H), 2.04-2.18 (m, 1 H), 2.19-2.33 (m, 1 H), 2.34-2.45 (m, 4 H), 3.44-3.58 (m, 4 H), 3.70 (s, 2 H), 4.42-4.69 (m, 4 H), 6.76-6.98 (m, 2 H), 6.98-7.17 (m 2 H), 7.31 (d, J=8.4 Hz, 2 H), 7.41 (d, J=8.4 Hz, 2 H), 11.99-12.25 (m, 1 H), 12.26-12.50 (m, 1 H)。
実施例 50 (12) : N, N—ビス (1H—イミダゾールー 2—^ fルメチル) —4— { [ (4—ピペリジン一 1ーィルシク口へキシル) ァミノ] メチル } ベンズァミド (低極性体) (化合物 50-12)
性状: ァモルファス
TLC: Rf0.21 (齚酸ェチル:メタノール: 28%アンモニア水 - 80:20:4); NMR (CDCls): 5 d 1.10—2.10 (m, 14H), 2.88—3.10 (m, 6H), 3.73 (s, 2H), 4.55-4.78 (m, 4B), 6.98-7.10 (m, 4H), 7.35 (d, J=8.1 Hz, 2H), 7.55 (d, J=8.1 Hz, 2H)。
実施例 50 (13) : N, N—ビス (1H—イミダゾールー 2—^ルメチル) 一 4— ( { [4- (1—ピペリジニル) シク口へキシル] アミノ } メチル) ベンズァミド (高極性体) (化合物 50-13)
性状:アモルファス
TLC: Rf 0.15 (酢酸ェチル:メタノール: 28%アンモニア水 = 80:20:4);
NMR (CDCla): δ d 1.10-1.30 (m, 2H), 1.38-1.65 (m, 4H), 1.78-1.95 (m, 4H) 2.00-2.20 (m, 4H), 2.43 (m, 1H), 2.70-3.00 m, 5H), 3.82 (s, 2H), 4.55-4.78 (m, 4H), 6.98-7.10 (m, 4H), 7.33 (d, J=8.1 Hz, 2H), 7.53 (d, J=8.1 Hz, 2H)。 実施例 50 (14) : N, N—ビス (1 H—ィミダゾールー 2—ィルメチル) — 4— ( { [4一 (4ーメチルビペラジン一 1一^ fル) シクロへキシル] ァ ミノ } メチル) ベンズァミド (低極性体) (化合物 50—14)
性状:アモルファス
TLC: Rf 0.22 (酢酸ェチル:メタノール: 28%アンモ ア水 = 80:20:4);
NMR (CDCla): 8 d 1.45 - 1.90 (m, 8H), 2.28—2.90 (m, 10H), 2.37 (s, 3H), 3.79 (s, 2H), 4.55-4.78 (m, 4H), 6.98-7.12 (m, 4H), 7.39 (d, J=7.8 Hz, 2H), 7.53 (d, J=7.8 Hz, 2H)。
実施例 50 (15) : N, N—ビス (1 H—イミダゾールー 2—ィルメチル) 一 4— ( { [4- (4ーメチルー 1ーピぺラジュル) シクロへキシル] アミ ノ } メチル) ベンズァミド (高極性体) (化合物 50-15)
性状:アモルファス
TLC: Rf 0.19 (酢酸ェチル:メタノ—ル :28%アンモニア水 - 80:20:4);
NMR (CDCls): 6 d 1.20-1.48 (m, 4H), 1.99 (m, 2H), 2.15 (m,2H), 2.34 (s, 3H), 2.38 (m, lH),2.45-2.80 (m, 9H), 3.88 (s, 2H), 4.50-4.78 (m, 4H), 7.03 (s, 4H), 7.40 (s, 4H)。
実施例 50 (16)
4- ( { [4一 (4, 4ージフルォロピペリジン一 1一^ ル) シクロへキシ ル] アミノ} メチル) 一 N, N—ビス (1H—イミダゾールー 2—ィルメチ ル) ベンズァミ ド (低極性体) (化合物 50-16)
性状:アモルファス
TLC: Rf 0.69 (酢酸ェチル:メタノール: 28%アンモニア水 = 80:20:4);
NMR (CDC13): δ d 1.45-2.10 (m, 12H), 2.40 (m, 1H), 2.60-2.74 (m, 4H),
2.92 (m, IH), 3.84 (s, 2H), 4.55-4.78 (m, 4H), 7.05 (s, 4H), 7.38-7.50 (m, 4H)0
実施例 50 (17) : 4- ( { [4- (4, 4ージフルオロー 1ーピペリジ ニル) シク口へキシル] アミノ } メチル) 一N, N-ビス ( 1 H—ィミダゾ 一ルー 2—イノレメチル) ベンズァミ ド (高極性体) (化合物 50-17) 性状:アモルファス
TLC: Rf0.55 (酢酸ェチル:メタノ一ノレ: 28%アンモニア水 = 80:20:4); NMR (CDCls): δ d 1.23-1.42 (m, 4H), 1.82-2.20 (m,8H), 2.42 (m, IH), 2.60 (m, 1H), 2.60-2.70 (m, 4H), 3.87 (s, 2H), 4.52-4.76 (m, 4H), 7.04 (s, 4H), 7.35-7.48 (m, 4H)。
実施例 50 (18) : 4一 { [ (4ーァゼパン一 1一ィルシクロへキシル) ァミノ] メチル } 一 N, N—ビス (1 H—イミダゾールー 2—ィルメチル) ベンズァミド (低極性体) (化合物 50— 18)
性状:アモルファス
TLC: Rf 0.52 (酢酸ェチル:メタノール: 28%アンモニア水 = 80:20:4); NME, (CDCls): 5 d 1.40-1.95 (m, 16H), 2.75-3.10 (m,6H), 3.73 (s, 2H), 4.55-4.78 (m, 4H), 7.00-7.10 (m, 4H), 7.35 (d, J=8.4 Hz, 2H), 7.55 (d, J=8.4 Hz, 2H)0
実施例 50 (19) : 4— ( { [4一 (1—ァゼパエル) シクロへキシル] アミノ} メチル) 一 N, N—ビス (1H—イミダゾールー 2—ィルメチル) ベンズァミ ド (高極性体) (化合物 50—19)
性状:ァモノレファス
TLC: Rf 0.29 (酢酸ェチル:メタノール: 28%アンモ ァ水 = 80:20:4); NMR (CDC13): 8 d 1.10-1.25 (m, 2H), 1.32-1.52 (m, 2H), 1.60 - 2.20 (m, 12H), 2.41 (m, 1H), 2.70-3.22 m, 5H), 3.81 (s, 2H), 4.55-4.78 (m, 4H), 6.98-7.10 (m, 4H), 7.33 (d, J=8.4 Hz, 2H), 7.56 (d, J=8.4 Hz, 2H)。
実施例 5 0 ( 2 0 ) : 4— ( { [ 4— (ジベンジルァミノ) シクロへキシル] アミノ} メチノレ) 一 N, N—ビス ( 1 H—イミダゾールー 2—ィルメチル) ベンズァミド (低極性体) (化合物 5 0— 2 0 )
性状:アモルファス
TLC:: Rf 0.52 (酢酸ェチル:メタノール: 28%アンモニア水 = 90:10:2);
NMR (GDCls): 6 d 1.30-2.00 (m, 8H), 2.52 (m, 1H), 2.90 (m, 1H), 3.55 - 3.70 (m, 4H), 3.81 (s, 2H), 4.55-4.78 (m, 4H), 7.01 (s, 4H), 7.15-7.42 (m, 14H)。 実施例 5 0 ( 2 1 ) : 4一 ( { [ 4一 (ジベンジスレアミノ) シクロへキシル] アミノ} メチル) 一 N, N—ビス (1 H—イミダゾールー 2—ィルメチル) ベンズァミド (高極性体) (化合物 5 0— 2 1 )
性状:ァモ /レファス
TLC: Rf 0.40 (酢酸ェチル:メタノール: 28%アンモニア水 = 90:10:2);
NMR (CDCls): δ d 1.00-1.20 (m, 2H), 1.30-1.50 (m, 2H), 1.82-1.98 (m, 2H) 1.98-2.10 (m, 2H), 2.40-2.60 (tn, 2H), 3.60 (s, 4H), 3.81 (s, 2H), 4.50-4.76 (m, 4H), 6.90-7.08 (m, 4H), 7.18-7.40 (m, 12H), 7.47 (d, J=8.1 Hz, 2H)。
LIZ
(^ 2-09呦导 ^ ^ 、 ベ y Λ(^≠ Ζ -Λί— Ζ
^ } ^一 Η τ) «-Ν 'Ν- {Λ^ -^- ^ ^ [9 *g] a ^ ^— 6 '8- ^Jp^ci^^-6) ] - - { Ζ) 09
。(ΙΠ 's) Z9L '(ΗΤ '∞) f9'L '(ΉΖ '^) 'L-92'L '(Hf ^q)
0'L
((ΐίΖ 's-tq) L' ΈΖ 's-^q) XS'
((BZ 's) 6L' '(HZ ' ) 99 ー I9'S '(Η9 'ra) VZ-2 Z '(Η8 6^'T-68! '(Η9 '
ΖΗ Sム =f '%) S809: (
8Τθαθ) ΗΗΝ ST - (ΐ:0ΐ:09 = 氺 ご¾ %8 一
ヽ 80JH
m -
(82-09 <#^» 、 ム w {Λ(^≠^ - Z一へ (一、 ί、 ^; Η Τ) ー Ν 'Ν- ( ^ {/ [4/ (/ ^。 an ) ー ] } ) -£ ■ (ε Ζ) 09 p翁 0Τ
。(HS ' rS=P'V)£9'L
'(ΉΖ <ZH l'8=f 'Ρ) 2£'L '(Rf '∞) 0T A-S69 '(Rf 08 ^-9 '(HZ 's) I8"8
'QIZ ) ^8^-29^ '(HT '∞) WZ '(H8T <ra) ZYZ-Z^\ P 9: (8ΐθαθ) HHN - (S:0T:06 =氺 ご士 0 /08S:4/— ^^ x ^^) IVOm :01
:
( — o s ψλ A ん ベ ( ^ ^^y -- Z 一^— ^ HT) ー N
9909T0/S00Zdf/X3d 1^H0/900Z OAV
性状:アモルファス
TLC: Rf0.37 (メタノール: 28%アンモ-ァ水 = 98:2);
NMR (CDCls): 60.97-1.34 (m, 5 H), 1.37—1.69 (m, 9 H), 1.71-1.98 (m, 4 H) 2.24-2.42 (m, 5 H), 2.45-2.64 (m, 4 H), 3.48 (s, 2 H), 4.53-4.85 (m, 4 H), 6.86-7.13 (m, 4 H), 7.33 (d, J=8.1 Hz, 2 H), 7.48 (d, J=8.1 Hz, 2 H)。
実施例 50 (25) : 4一 { [8— (シクロへキシルメチル) -2, 8—ジ ァザスピロ [4. 5] デカー 2—^ ル] メチル } 一 N, N—ビス (1H-ィ ミダゾ一ルー 2一ィルメチル) ベンズァミド (化合物 50-25)
性状:アモルファス
TLC: Rf 0.73 (酢酸ェチル:メタノール: 28%アンモニア水 = 50:10:1);
NMR (CDGla): 50.78-0.92 (m, 2H), 1.10 - 1.30 (m, 3H), 1.40-1.79 (m, 12H) 2.07 (d, J=7.2 Hz, 2H), 2.22-2.36 (m, 6H), 2.54 (t, J=6.9 Hz, 2H), 3.58 (s, 2H), 4.59-4.68 (m, 4H), 6.95-7.10 (m, 4H), 7.38 (d, J=8.4 Hz, 2H), 7.64 (d, J=8.4Hz, 2H)。
実施例 50 (26) : 4— [ (8—べンジル一2, 8—ジァザスピロ [4. 5] デカー 2—ィル) メチノレ] 一 N, N—ビス (1H—イミダゾール一2— ィルメチル) ベンズァミ ド (化合物 50-26)
性状:アモルファス
TLC: Rf 0.73 (酢酸ェチル:メタノール: 28%アンモニア水二 50:10:1) ; NMR (CDCls): δ 1.53-1.64 (m, 6H), 2.27-2.41 (m, 6H), 2.55 (t, J=6.9 Hz, 2H), 3.46 (s, 2H), 3.58 (s, 2H), 4.60-4.68 (m, 4H), 6.96-7.08 (m, 4H), 7.20-7.32 m, 5H), 7.37 (d, J=8.4Hz, 2H), 7.64 (d, J=8.4 Hz, 2H)。
実施例 5 0 ( 2 7 ) : 4— { [ 8— (シクロプロピルメチル) 一 2, 8—ジ ァザスピロ [4. 5 ] デカー 2—ィル] メチル } -N, N—ビス (1 H—ィ ミダゾーノレ一 2—ィルメチル) ベンズァミ ド (化合物 5 0— 2 7 )
性状:アモルファス
TLC: Rf 0.42 (酢酸ェチル:メタノール: 28%アンモニア水 = 50:10:1); NMR (CDCls): 8 0.06-0.14 (m, 2H), 0.46-0.54 (m, 2H), 0.87 (m, 1H), 1.56-1.67 (m, 6H), 2.23 (d, J=6.6 Hz, 2H), 2.34 (s, 2H), 2.34-2.54 (m, 4H), 2.56 (t, J=6.9 Hz, 2H), 3.58 (s, 2H), 4.58-4.65 (m, 4H)S 6.94-7.10 (m, 4H), 7.38 (d, J=8.4 Hz, 2H), 7.66 (d, J=8.4 Hz, 2H)。
実施例 5 0 ( 2 8 ) : 4— { [ 8— (シクロペンチルメチル) 一 2, 8—ジ ァザスピロ [4. 5 ] デカー 2— fル] メチル } -N, N—ビス (1 H—ィ ミダゾーノレ一 2—ィルメチル) ベンズァミ ド (化合物 5 0— 2 8 )
( o ε - o s 、 xペ { ( =^
[9 · ] a ^ ー 8 'Z - ( ^^ -or^-S) 一 8] } — ー {Λί-^≠Λ ^一 S— /—/、^ ^— H "C) ー Ν 'Ν: (O S) 0 Q Wi^
。(HS <ZH 8=f 'Ρ) 89· ΧΉ.Ζ 'ΖΗ fS=£ 'Ρ) 8 ム Rl 'ΖΗ 9'Ψ= 'Ρ) OZ-L m '∞) Orム- 86·9 '(ΗΤ 'ΖΗ 08 ' = 'ΡΡ) 869 '(ΗΤ 'ΖΗ 08=Γ 'Ρ) 88'9 '(Η '∞) S9 -8S '(RZ <s) Ld £ '(Ή.Ζ 's) 82*8 \ΐΙΖ 'ΖΗ 69=f '%) Z '(Η9 LVZ-Z^Z '(Η9 S9 I-8S I 9: (εΐθαθ) ΗΗΝ '· (T:0I:0S =氺 - 0 /。8 & ^ / ^ 邈 41) 090JH :0 L
3r : ¾
(62 -09呦导 ¾ 、 Xベ {Λί^≠ i^ -z - f^
[S -^] α ^一 8 ( ^ - ^ー —8] }
( /^ 一 一 、、 y-hl l) M-N 'Ν: (6 Ζ) 0 闘牽
^'8=f 'Ρ) '(H^ '∞) 0Γム 6·9 '(Ή. '^) S9 - 8S' '(Ή.Ζ 's) 8 Έ '(H^ 'ΖΗ 69=f SS^ '(Η9 ) 0 - 8S'S '(RZ ' Z'L=£ 'Ρ) Z Z '(HZ '^) 0X 2-861 Ή.Ζ sra) 08Ί-89Ί '(H6 '^) S9T-ffT '( 'TO) -60Ί 9: (8ΐθαθ) Ή Κ ' (T:0T:0S = 氺 -士 %8 & 一 ^ 4 翘 6S 0J?I -O L
Z9r : ^¾
9909T0/S00Zdf/X3d
性状:アモルファス
TLC: Rf 0.60 (酢酸ェチル:メタノール: 28%アンモニア水 = 50:10:1); NMR (CDCls): 61.53-1.65 (m, 6H), 2.28-2.42 (m, 6H), 2.55 (t, J=6.9 Hz, 2H), 3.49 (s, 2H), 3.58 (s, 2H), 4.58-4.65 (m, 4H), 6.96-7.14 (m, 6H), 7.25 (m, IH), 7.38 (d, J=8.4Hz, 2H), 7.68 (d, J=8.4Hz, 2H)。
実施例 50 (31) : 4一 ( { [4- (3, 4—ジヒドロキノリン一 1 (2 H) —ィノレ) シクロへキシル] ァミノ) メチノレ) 一 N, N—ビス (1H—ィ ミダゾーブレー 2—イノレメチル) ベンズァミ ド (低極性体) (化合物 50— 3 1)
性状:アモルファス
TLC: Rf 0.46 (酢酸ェチル:メタノール: 28%アンモニア水 = 90:10:2);
NMR (CDCla): 8 d 1.50-1.75 (m, 4H), 1.82-2.10 (m, 6H), 2.71 (t, J=6.3 Hz, 2H), 3.00 (m, IH), 3.24 (t, J=5.4 Hz, 2H), 3.60 (m, IH), 3.83 (s, 2H), 4.58-4.80 (m, 4H), 6.53 (dd, J=7.8, 7.8 Hz, IH), 6.62 (d, J=7.8 Hz, IH), 6.93 (d, J=7.5 Hz, 1H), 6.99-7.12 (m, 5H), 7.45 (d, J=8.1 Hz, 2H), 7.54 (d, J=8.1Hz, 2H)0
実施例 50 (32) : 4- ( { [4- (3, 4ージヒドロ一 1 (2H) —キ ノリュル) シクロへキシル] ァミノ) メチノレ) 一 N, N—ビス (1H-イミ ダゾールー 2一ィルメチル) ベンズァミ ド (高極性体) (化合物 50— 32) 性状:アモルファス
TLC: Rf 0.30 (酢酸ェチル:メタノール: 28%アンモニア水 = 90:10:2);
NMR (CDCla): 5 d 1.22-2.20 (m, 10H), 2.55 (m, 1H), 2.71 (t, J=6.0 Hz, 2H)
3.15 (t, J=5.7 Hz, 2H), 3.63 (m, 1H), 3.87 (s, 2H), 4.55-4.78 (m, 4H), 6.54 (dd, J=7.5, 7.5 Hz, IH), 6.62 (d, J=7.5 Hz, IH), 6.93 (d, J=7.5 Hz, IH), 7.00—7.12 (m, 5H), 7.36-7.45 (m, 2H), 7.50-7.62 (m, 2H)。
実施例 50 (3 3) : 4— ( {8— [4一 (ジェチルァミノ) ベンジル] 一 2, 8—ジァザスピロ [4. 5] デカ一 2—ィル } メチノレ) -N, N—ビス ( 1 H—ィミダゾールー 2—ィルメチル) ベンズァミド (化合物 50-3 3) 性状:アモルファス
TLC:Hf 0.44 (酢酸ェチル:メタノール: 28%アンモニア水 =50:10:1); NME, (CDC13): δ 1.14 (t, J=7.2 Hz, 6H), 1.51—1.64 (m, 6H), 2.25-2.42 (m, 6H), 2.53 (t, J=6.9 Hz, 2H), 3.28-3.38 (m, 6H), 3.56 (s, 2H), 4.60-4.67 (m, 4H), 6.61 (d, J=8.7 Hz, 2H), 6.94-7.08 (m, 4H), 7.12(d, J=8.7 Hz, 2H), 7.36 (d, J=8.4 Hz, 2H), 7.59 (d, J=8.4 Hz, 2H)。
実施例 50 (34) : 4— { [8— (2—フルォロベンジル) 一 2, 8—ジ ァザスピロ [4. 5] デカ一 2—ィル] メチル } 一 N, N—ビス (1H—ィ ミダゾールー 2—ィルメチル) ベンズァミ ド (化合物 50— 34)
性状:アモルファス
TLC: Rf 0.44 (酢酸ェチル:メタノール: 28%アンモニア水 = 50:10:1);
NMR (CDCls): 61.56-1.64 (m, 6H), 2.32-2.44 (m, 6H), 2.54 (t, J=6.9 Hz, 2H), 3.54 (s, 2H), 3.58 (s, 2H), 4.60-4.68 (m, 4H), 6.97-7.13 (m, 6H), 7.25 (m, 1H), 7.38-7.42 (m, 3H), 7.61 (d, J=8.4 Hz, 2H)。
実施例 50 (3 5) : 4- { [8- (3—フルォロベンジル) 一 2, 8—ジ ァザスピロ [4. 5] デカー 2—ィル] メチル } 一 Ν, Ν—ビス (1H—ィ ミダゾールー 2一^ ルメチノレ) ベンズァミド (化合物 50— 3 5)
性状:アモルファス
TLC: Rf0.44 (酢酸ェチノレ:メタノ一ノレ: 28%アンモニア水 = 50:10:1); NMR (CDCls): 51.50-1.66 (m, 6H), 2.24-2.41 (m, 6H), 2.56 (t, J=6.9 Hz, 2H), 3.43 (s, 2H), 3.59 (s, 2H), 4.60-4.68 (m, 4H), 6.90 (m, 1H), 6.95-7.09 (m, 6H), 7.23 (m, 1H), 7.36 (d, J=8.4 Hz, 2H), 7.60 (d, J=8.4 Hz, 2H)。 実施例 50 (36) : 4— { [8— (4—フルォロベンジル) 一 2, 8—ジ ァザスピロ [4. 5] デカー 2—ィル] メチル } 一 N, N—ビス (1H—ィ ミダゾールー 2一ィルメチル) ベンズァミド (化合物 50- 36)
性状:ァモルファス
TLC: Rf0.44 (酢酸ェチル:メタノール: 28%アンモニア水 = 50:10:1); NMR (CDCls): 61.52-1.62 (m, 6H), 2.24-2.41 (m, 6H), 2.55 (t, J=6.9 Hz, 2H), 3.41 (s, 2H), 3.58 (s, 2H), 4.60—4.68 (m, 4H), 6.93-7.09 (m, 6H), 7.20-7.28 (m, 2H), 7.35 (d, J=8.4 Hz, 2H), 7.60 (d, J=8.4 Hz, 2H)。
実施例 50 (37) : 4- [ ( {トランス一 4一 [ァセチル (シクロへキシ ル) ァミノ] シクロへキシル } ァミノ) メチル] 一 N, N—ビス (1H—ィ ミダゾールー 2—ィルメチル) ベンズァミ ド (化合物 50— 37) 性状:アモルファス
TLC: Rf 0.50 (酢酸ェチル:メタノール: 28%アンモ-ァ水 = 80:20:2);
NMR (CDCls): 5 d 1.05-2.62 (m, 19H), 2.06 (s, 3H), 3.00 (brs, 1H), 3.39 (m: 1H), 3.82 (s, 2H), 4.50-4.80 (m, 4H), 6.95-7.12 (m, 4H), 7.30-7.40 (m, 2H), 7.45-7.60 (m, 2H) '
実施例 5 0 ( 3 8 ) : N- ( 1 H—べンゾィミダゾールー 2—イノレメチル) 一 4— [ ( 8—シクロへキシルー 2, 8—ジァザスピロ [ 4. 5 ] デカー 2 —ィノレ) メチル] 一 N— ( 1 H—イミダゾールー 2—ィルメチル) ベンズァ ミド (化合物 5 0 - 3 8 )
性状: アモルファス
TLC: Rf 0.34 (メタノール: 28%アンモ-ァ水 = 98:2);
NMR (CDCls): δ 1.12-1.26 (m, 5 H), 1.53-1.65 (m, 7 H), 1.74-1.89 (m, 4 H); 2.23-2.33 (m, 3 H), 2.44-2.57 (m, 6 H), 3.55 (s, 2 H), 4.67-4.81 (m, 2 H), 4.83-4.91 (m, 2 H), 6.99—7.08 (m, 2 H), 7.23-7.37 (m, 4 H), 7.49-7.64 (m, 4 H)。
実施例 5 0 ( 3 9 ) : N— ( 1 H—べンゾィミダゾールー 2—ィルメチル) —4一 [ ( {トランス一 4一 [シクロへキシル (プロピル) ァミノ] シクロ へキシル } ァミノ) メチノレ] 一 N— ( 1 H—イミダゾールー 2一^ fノレメチノレ) ベンズァミド (化合物 5 0— 3 9 )
性状:アモルファス
TLC: Rf 0.38 (メタノール: 28%ァンモユア水 = 98:2);
NMR (CDCls): 5 0.76-0.88 (m, 3 H), 1.09-1.15 (m, 2 H), 1.17-1.27 (m, 5 H) 1.29-1.41 (m, 4 H), 1.56-1.63 (m, 1 H), 1.67-1.80 (m, 6 H), 1.90-2.03 (m, 2 H), 2.34-2.47 (m, 3 H), 2.50-2.63 (m, 2 H), 3.79 (s, 2 H), 4.62—4.69 (m, 1 H); 4.72-4.79 (m, 1 H), 4.84 (s, 2 H), 6.97-7.11 (m, 2 H), 7.22-7.35 (m, 4 H), 7.49-7.65 (m, 4 H)。
実施例 5 0 ( 4 0 ) : N, N—ビス (1 H—イミダゾール一 2—ィルメチル) 一 4一 [ ( {トランスー4一 [ ( 3—メ トキシプロピル) (プロピル) アミ ノ] シクロへキシル } ァミノ) メチノレ] ベンズアミ ド (化合物 5 0— 4 0 ) 性状:油状物
TLC: Rf 0.49 (酢酸ェチル:メタノール: 28%アンモニア水 = 40:10:1);
NMR (CDCls): 80.84 (t, J=7.5 Hz, 3H), 1.08-2.02 (m, 12H), 2.33-2.50 (m, 6H), 3.31 (s, 3H), 3.39 (t, J=6.0 Hz, 2H), 3.82 (s, 2H), 4.56 (br-s, 2H), 4,60 (br-s, 2H), 7.01 (br-s, 2H), 7.08 (br~s, 2H), 7.37 (d, J=7.5 Hz, 2H), 7.29 (d, J=7.5 Hz, 2H)。
実施例 5 0 ( 4 1 ) : 4— [ ( {トランス一 4一 [ ( 1一ェチルプロピル)
(プロピル) ァミノ] シクロへキシル } ァミノ) メチノレ] —N, N—ビス (1 H—イミダゾーノレ一 2—ィルメチル) ベンズァミド (化合物 5 0— 4 1 )
性状:油状物
TLC: Rf 0.69 (酢酸ェチル:メタノール: 28%アンモニア水 = 40:10:1); NMR (CDCls): 50.82 (t, J=7.5 Hz, 3H), 0.86 (t, J=7.5 Hz, 6H), 1.10-2.02 (m, 14H), 2.17-2.49 (m, 5H), 3.82 (s, 2H), 4.59 (br-s, 2H), 4,63 (br-s, 2H), 7.02 (br-s, 2H), 7.08 (br-s, 2H), 7.37 (d, J=8.1 Hz, 2H), 7.66 (d, J=8.1 Hz, 2H)。
実施例 5 0 ( 4 2 ) : 4— { [ [ 4— (ジプロピノレアミノ) プチル] (メチ ル) ァミノ] メチル } 一 N, N—ビス (1 H— ^ ミダゾ一ルー 2—ィルメチ ル) ベンズアミド (化合物 5 0 - 4 2 )
性状:油状物
TLC: Rf 0.58 (酢酸ェチル:メタノール: 28%アンモニア水 = 40:10:1); NMR (CDCla): 50.86 (t, J=7.5 Hz, 6H), 1.41-1.50 (m, 8H), 2.16 (s, 3H), 2.33-2.44 (m, 8H), 3.47 (s, 2H), 4.61 (br-s, 2H), 4,65 (br-s, 2H), 7.02 (br-s, 2H), 7.07 (br-s, 2H), 7.37 (d, J=8.1 Hz, 2H), 7.64 (d, J=8.1 Hz, 2H;)。
実施例 5 0 ( 4 3 ) : 4— [ ( 8—シクロペンチルー 2, 8—ジァザスピロ
[ 4. 5〕 デカー 2—ィノレ) メチル] 一 N, N—ビス (1 H—イミダゾール
LZZ
- (T:OX:OS =氺 -士 %8 & 一/
9fOJH: 1∑
^ : ^ ¾ οζ (s 一ο 9 Λ ム W { ^^ [Q
' ] 口 ^ ^一 8 ' Ζ - {Λ ^,^ Ζ - 8] } 一 ー
( ^^y~Z一へ【一 、 一 H T ) «-N 'N ·· (9 ) 09聽牽
°(H Z ' T'8=f 'Ρ) 99'L '(Η Ζ '^Η T*8=f 'Ρ) 98'Λ '(Η f 8X"i<-I6"9 '(Η <ra) LL'f-£9'f '(Η Z 80 -S68 '(H Z 's) S'S '(Η '∞) 8 '8-SS"8 SI (H 6 ^ Z-^ZZ '(H 1 '∞) 18· ム 9Ί '(Η 8 '∞)ム 9Ί一 Ί 9: (810Q0) HHN
■ (Z:86 =氺 -士 %8 & 一 / SS 0JU :ΟΊ
^ ι/士 : mi
-O S ^ψλϊ) Α Xペ {Λ(^ ^ Λ( y-Z - (. [g · ] α ^
'S - (^ -- -^^0 -Η Ζ - ΧΛ ^16 - 8] } 一 ー {Λ^^ΛΟ ^一 Ζ -Λ^ .^ ^ y-ui) r^-N 'N : ( 09
°(H τ ( i"8=f ' ) ^S'L H Ί> ' x-8=f 'ρ) s '(H
'∞) Srム- 88·9 '(H ) T8'f-^S" '(Η τ 's) Ζ,9Έ '(H Z ' S6'9=f WZ '(H
L 'ra) QYZ-Q Z '(H Z ) Wl- L'l '(H Zl '∞) L'l- Z l 9: (εΐθαθ) HHN
■ (2:86 =氺 - r %8S:4/ , ^) 680 :OTL
/ : ^ lC¾
(ε ^-o 9 、 、 ( ^Λ ^一 ζ
9909T0/S00Zdf/X3d
NMR (CDCls): δ 1.54-1.65 (m, 6H), 2.32-2.48 (m, 6H), 2.55 (t, J=6.9 Hz, 2H), 3.58 (s, 2H), 3.61 (s, 2H), 4.60-4.72 (m, 4H), 6.94-7.09 (m, 4H), 7.14 (dd, J=4.8, 7.5 Hz, 1H), 7.35 (d, J=8.4Hz, 2H), 7.40 (d, J=7.5 Hz, IH), 7.53 (d, J=8.4Hz, 2H), 7.63 (dt, J=1.8, 7.5 Hz, IH), 8.53 (d, J=4.8 Hz, 1H)。
実施例 50 (46) : N, N—ビス (IH—イミダゾールー 2—^ fルメチル) —4— { [8— (ピリジン一 3—ィルメチル) 一 2, 8—ジァザスピロ [4. 5] デカー 2—^ fル] メチル } ベンズァミ ド (化合物 50-46)
性状:アモルファス
TLC: Rf 0.46 (酢酸ェチル:メタノール: 28%アンモニア水 = 50:10:1);
NMR (CDCls): δ 1.50-1.64 (m, 6H), 2.24-2.41 (m, 6H), 2.56 (t, J=6.9 Hz, 2H), 3.46 (s, 2H), 3.58 (s, 2H), 4.61-4.72 (m, 4H), 6.98-7.10 (m, 4H), 7.23 (dd, J=4.8, 7.5 Hz, IH), 7.36 (d, J=8.4 Hz, 2H), 7.54 (d, J=8.4 Hz, 2H), 7.65 (dt, J=7.5, 1.8 Hz, IH), 8.49 (dd, J=1.8, 4.8 Hz, IH), 8.51 (d, J=1.8 Hz, IH), 実施例 50 (47) : N, N—ビス (IH—イミダゾールー 2—^ fルメチル) -4- { [8- (ピリジン一 4一ィルメチル) 一 2, 8—ジァザスピロ [4. 5] デカー 2—ィル] メチル } ベンズアミ ド (化合物 50-47)
性状:アモルファス
TLC: Rf0.46 (酢酸ェチル:メタノール: 28%アンモニア水 - 50:10:1);
N魔 (CDC13): δ 1.55—1.68 (m, 6H), 2.24-2.42 (m, 6B), 2.56 (t, J=6.9 Hz, 2H), 3.44 (s, 2H), 3.58 (s, 2H), 4.60-4.72 (m, 4H), 6.97-7.08 (m, 4H), 7.23 (d, J=6.0 Hz, 2H), 7.34 (d, J=8.4Hz, 2H), 7.52 (d, J=8.4 Hz, 2H), 8.50 (d, J=6.0 Hz, 2H)。
実施例 50 (48) : N, N—ビス (1 H—^ f ミダゾーノレ一 2一イノレメチル) —4一 { [8 - (2—ナフチルメチル) 一2, 8—ジァザスピロ [4. 5] デカ一 2—ィル] メチル } ベンズァミ ド (化合物 50-48)
性状:アモルファス
TLC: Rf 0.52 (齚酸ェチル:メタノール :28%アンモニア水 = 50:10:1); NMR (CDCls): 51.56-1.65 (m, 6H), 2.32-2.48 (m, 6H), 2.58 (t, J=6.9 Hz, 2H), 3.57 (s, 2H), 3.62 (s, 2H), 4.60-4.70 (m, 4H), 6.97-7.08 (m, 4H), 7.35 (d, J=8.4 Hz, 2H), 7.40-7.50 (m, 3H), 7.54 (d, J=8.4 Hz, 2H), 7.71 (s, 1H), 7.74-7.82 (m, 3H)0
実施例 50 (49) : 4— [ (8—シクロへプチルー 2, 8—ジァザスピロ [4. 5] デカー 2—ィル) メチル] -N, N—ビス ( 1 H—イミダゾーノレ 一 2—イノレメチル) ベンズァミド (化合物 50-49)
性状:アモルファス
TLC: RfO.32 (メタノール: 28%ァンモユア水 = 98:2);
NMR (CDCls): 51.27-1.86 (m, 18 H), 2.23-2.63 (m, 9 H), 3.57 (s, 2 H), 4.51-4.75 (m, 4 H), 6.90-7.11 (m, 4 H), 7.36 (d, J=8.1 Hz, 2 H), 7.59 (d, J=8.1Hz, 2HX
実施例 50 (50) : 4— [ ( {トランスー4一 [シクロへキシル (メチノレ) ァミノ] シクロへキシル } ァミノ) メチル] — N, N—ビス (1H—イミダ ゾールー 2—ィルメチル) ベンズァミ ド (化合物 50— 50)
性状:アモルファス
TLC: Rf 0.43 (酢酸ェチル:メタノール: 28%アンモニア水 = 80:20:2); NME (CDC ): δ d 1.00-2.06 (m, 18H), 2.30 (s, 3H), 2.42 (m, 1H),
2.55-2.75 (m, 2H), 3.81 (s, 2H), 4.52-4.75 m, 4H), 6.95-7.10 (m, 4H), 7.35 (d, J=8.4 Hz, 2H), 7.61 (d, J=8.4 Hz, 2H)。
実施例 50 (51) : 4— [ ( {トランス一 4一 [ベンジル (メチル) ァミ ノ] シクロへキシル } ァミノ) メチノレ] — N, N—ビス (1H—イミダゾー ルー 2—イノレメチル) ベンズァミ ド (化合物 50-51)
性状:アモルファス
TLC: Rf 0.24 (酢酸ェチル:メタノール: 28%アンモニア水 = 90:10:2); NMR (CDCls): 6 d 1.15-1.50 (m, 4H), 1.90—2.18 (m, 4H), 2.21 (s, 3H), 2.45-2.62 (m, 2H), 3.60 (s, 2H), 3.85 (s, 2H), 4.50—4.78 (m, 4H), 6.98—7.12 (m, 5H), 7.20-7.40 (m, 4H), 7.38 (d, J=8.4Hz, 2H), 7.55 (d, J=8.4 Hz, 2H)。 実施例 50 (52) : 4— [ ( {トランスー4ー [シクロへキシル (メチノレ スノレホェノレ) ァミノ] シクロへキシル } ァミノ) メチノレ] -N, N—ビス (1 H—イミダゾーノレ— 2一ィルメチル) ベンズァミ ド (化合物 50— 52) 性状: アモルファス
TLC: Rf 0.22 (酢酸ェチル:メタノール: 28%アンモニア水 = 90:10:2); NMR (CDCls): δ d 1.00-2.12 (m, 18H), 2.49 (m,lH), 2.86 (s, 3H), 3.10-3.42 (m, 2H), 3.83 (s, 2H), 4.58-4.75 (m, 4H), 6.98-7.10 (m, 4H), 7.37 (d, J=8.1 Hz, 2H), 7.65 (d, J=8.1 Hz, 2H)。
実施例 50 (53) : N, N—ビス (1H—イミダゾールー 2—イノレメチノレ) 一 4— { [7— (2—フエニノレエチノレ) 一2, 7—ジァザスピロ [4. 5] デカ一 2—^ Tル] メチル } ベンズァミ ド (化合物 50— 53)
性状:アモルファス
TLC: Rf 0.51 (メタノール: 28%ァンモ -ァ水 = 98:2);
NMR (CDCls): δ 1.28-1.81 (m, 6 H), 2.24 (d, J=9.3 Hz, 2 H), 2.28-2.68 (m, 8 H), 2.70-2.85 (m, 2 H), 3.59 (s, 2 H), 4.53-4.75 (m, 4H), 6.90-7.11 (m, 4 H), 7.13-7.31 (m, 5 H), 7.38 (d, J=8.1 Hz, 2 H), 7.61 (d, J=8.1 Hz, 2 H)。 実施例 50 (54) : N, N—ビス (1H—イミダゾールー 2—ィルメチル) 一 4一 { [7— (2—ピペリジン一 1一イノレエチノレ) -2, 7ージァザスピ 口 [4. 5] デカ一 2一ィル] メチル } ベンズァミ ド (化合物 50-54) 性状: アモルファス
TLC:Rf 0.24 (メタノール: 28%アンモニア水 =98:2);
NMR (CDCls): δ 1.15-1.77 (m, 12 H), 2.06-2.76 (m, 16 H), 3.58 (q, J=13.2 Hz, 2 H), 4.47-4.82 (m, 4 H), 6.87-7.14 (m, 4 H), 7.36 (d, J=8.1 Hz, 2 H), 7.58(d, J=8.1Hz,2H)。
実施例 50 (55) : 4- { [8- (2, 3—ジヒ ドロー 1H—インデンー 2—ィル) 一 2, 8—ジァザスピロ [4. 5] デカー 2—ィル] メチル } 一 N, N—ビス (1H—イミダゾールー 2—ィルメチル) ベンズアミド (化合 物 50— 55)
性状: アモルファス
TLC:Ef 0.37 (メタノール: 28%アンモニア水 =98:2);
NMR (CDCls): 81.58-1.71 (m, 6 H), 2.35-2.39 (m, 3 H), 2.42-2.51 (m, 3 H) 2.53-2.59 (m, 2 H), 2.84-2.98 (m, 2 H), 3.01-3.17 (m, 3 H), 3.59 (s, 2 H), 4.61-4.74 (m, 4 H), 6.94-7.07 (m, 4 H), 7.09-7.19 (m, H), 7.30-7.41 (m, 2 H), 7.51-7.62 (m, 2 H)。
実施例 50 (56) : 4— [ (8—シクロプチルー 2, 8—ジァザスピロ [4.
Z2Z
'· (2:86 =氺 -arベ %sz:^- r ^^) os oja ·ΌΊΛ
^ :
(89-09 λ ) 、 xペ (Ί -^≠ ( y-z— — /、
^^ 一 HT) 一N 'Ν- {Λ( =≠ ίΛί y-z-c^ [s · ] a。 oz ^ — 8 'Z- ( / べ ^ 一 -8] } · (8 S) 091 Μ^
°(Η Ζ '∞) 89· — SS 'ム '(Η Ζ
TO) ZVL-02'L '(Η f Οΐ Δ-269 '(Η '∞) ZL' -^ '(Η Ζ 's) L9 £ '(Η Ζ '∞)
90"ε-ε6'2 '(Η 9 ) 8S^-2fg '(Η 9 '∞) L^Z-ZZZ '(Η Ζ 961-281 '(Η
Ζ '∞) δ8Ί-Τ^·Τ '(Η ΟΤ '∞) 291-021 '(Η 8 '^) 960-S809: (εΤθαθ) ΗΗΝ SX
- (2:86 = ^ -^ 1.Ύ^Ζ·Λ(— / ^ 1^0 J¾ :0ΊΧ
乙^! 士 : ^¾
^ — 8 'z- - ίί^ 0^ -τ) 一 8] } - - Λ(^ ^^ - ζ ^ y-u Τ ) «-Ν 'Ν : (Ζ 9) O S H:牽 οτ
°(Η
Ζ 'TO) WL-^'L '(Η Ζ 'TO) QVL-l^L '(Η <ra) 0X L-S69 '(Η f Zff-e^f
'(H Z 's) 82Έ '(H I '∞) 69Ή9Έ '(H Z '∞) 6S - SS'S '(H S '∞) 2 Ζ-6ΓΖ
(H 8 '∞) S0 S-S61 '(H Z 861-281 '(H 8 ) TZ, I-9S T 9: (εΐθαθ) ΉΜΚ
- 86 =氺 -·3Γ / / ? s oja :0ΊΧ s
^ ^ : ¾ί¾
(99-09 ψλ\ Α X { ί^
- ζ -Λ(—^^ y-ατ) 'Ν~ Λ^^ (Λ ^一 n [9
9909T0/S00Zdf/X3d 1^H0/900Z OAV
NMR (CDCla): δ 1.32-1.43 (m, 2 H), 1.55-1.70 (m, 10 H), 1.74-1.87 (m, 4 H), 1.98-2.11 (m, 6 H), 2.27-2.43 (m, 5 H), 2.51 - 2.65 (m, 2 H), 3.60 (s, 2 H) 4.59-4.73 (m, 4 H), 6.94-7.08 (m, 4 H), 7.30-7.41 (m, 2 H), 7.55-7.66 (m, 2 H)。
実施例 50 (5 9) : N, N—ビス (1H—イミダゾーノレ一 2 fルメチル) 一 4— [ (8—イソプチルー 2, 8—ジァザスピロ [4. 5] デカー 2—ィ ル) メチル] ベンズァミ ド (化合物 50- 59)
性状:アモルファス
TLC: Rf0.48 (メタノール: 28%アンモユア水 = 98:2);
NMR (GDCls): 50.80-0.94 (m, 6 H), 1.51-1.65 (m, 6 H), 1.68-1.83 (m, 1 H)
I.97-2.11 (m, 2 H), 2.22-2.37 (m, 6 H), 2.47-2.61 (m, 2 H), 3.58 (s, 2 H), 4.57-4.72 (m, 4 H), 6.95-7.10 (m, 4 H), 7.30-7.45 (m, 2 H), 7.51-7.66 (m, 2 H)。
実施例 50 (60) : 4— (2, 8—ジァザスピロ [4. 5] デカー 8—ィ ルメチル) 一 N, N—ビス ( 1 H—イミダゾーノレ一 2—^ fルメチル) 一 2— メチルベンズァミド (化合物 50— 60)
性状:アモルファス
TLC:Rf 0.38 (クロ口ホルム:メタノール: 28%アンモニア水 =80:20:4); N脆 (DMSO-De): δ 1.36-1.51 (m, 6 H), 2.11 (s, 3 H), 2.21-2.34 (m, 4 H), 2.51-2.56 (m, 2 H), 2.77 (t, J=7.2 Hz, 2 H), 3.16 (s, 2 H), 4.40 (s, 2 H), 4.68 (s, 2 H), 6.79-7.02 (m, 4 H), 7.02-7.08 (m, 1 H), 7.08—7.19 (m, 2 H),
II.47- 13.11(m, 2H)。
実施例 50 (6 1) : 4- [ (2—シクロへキシルー 2, 8.—ジァザスピロ [4. 5] デカー 8—ィノレ) メチノレ] -N, N—ビス (1H—イミダゾーノレ 一 2—イノレメチル) 一 2—メチルベンズァミド (化合物 50-6 1)
性状:アモルファス
TLC: Rf 0.30 (クロ口ホルム:メタノール: 28%アンモニア水 = 80:10:1); NMR (DMSO-De): 81.04-1.28 (m, 6 H), 1.36-1.56 (m, 8 H), 1.58 - 1.71 (m, 2 H), 1.71-1.85 (m, 2 H), 1.88—1.97 m, 1 H), 2.11 (s, 3 H), 2.17-2.31 (m, 4 H), 2.31-2.39 (m, 2 H), 3.34 (s, 2 H), 4.39 (s, 2 H), 4.67 (s, 2 H), 6.64-7.00 (m, 4H), 7.00-7.07 (m, 1H), 7.07-7.18 (m, 2H), 12.05-12.42 (m, 2 H)。
実施例 50 (6 2) : 4一 { [ (3—ァゼパン一 1ーィルー 2, 2—ジメチ ノレプロピル) ァミノ] メチル } 一 N, N—ビス (1H—イミダゾールー 2— ィルメチル) ベンズァミド (化合物 50-6 2)
性状: アモルファス
TLC: Rf 0.52 (酢酸ェチル:メタノール: 28%アンモニア水 = 50:10:1);
NMR (CDC13): 50.86 (s, 6H), 1.48-1.62 (m, 8H), 2.36 (s, 2H), 2.44 (s, 2H), 2.67-2.70 (m, 4H), 3.79 (s, 2H), 4.61 (br-s, 2H), 4,66 (br-s, 2H), 7.00 (br-s, 2H), 7.07 (br-s, 2H), 7.38 (d, J=8.1 Hz, 2H), 7.62 (d, J=8.1 Hz, 2H)。
実施例 50 (6 3) : N, N—ビス (1H—イミダゾールー 2 fルメチル) —4— [ ( {トランス一 4一 [メチル (プロピル) ァミノ] シクロへキシル } ァミノ) メチル] ベンズァミ ド (化合物 50-6 3)
十生状:ァモ/レファス
TLC:Rf0.44(ジクロロメタン:メタノール: 28%アンモニア水 =50:10:1);
NMR (CDCls): δ 0.87 (t, J=7.2 Hz, 3H), 1.07-1.33 (m, 4H), 1.41-1.53 (m, 2H), 1.82-1.86 (m, 2H), 1.99-2.02 (m, 2H), 2.25 (s, 3H), 2.36-2.41 (m, 4H), 3.81 (s, 2H), 4.59 (br-s, 2H), 4,65 (br-s, 2H), 6.99 (br-s, 2H), 7.06 (br-s, 2H), 7.35 (d, J=8.4 Hz, 2H), 7.61 (d, J=8.4 Hz, 2H)。
実施例 5 0 ( 6 4 ) : N, N—ビス ( 1 H—イミダゾ一/レー 2一^ ルメチル) 一 4— [ ( {トランス一 4一 [プロピル (テトラヒ ドロー 2 H—ピラン一 4 -ィル) ァミノ] シクロへキシル } ァミノ) メチル] ベンズアミ ド (化合物 5 0 - 6 4 )
性状:アモルファス
TLC: Rf 0.46 (酢酸ェチル:メタノール: 28%アンモニア水 = 50:10:1);
NMR (CDCls): δ 0.81 (t, J=7.2 Hz, 3H), 1.06-1.18 (m, 2H), 1.25-1.42 (m, 4H), 1.58-1.73 (m, 6H), 1.95-1.99 (m, 2H), 2.35-2.44 (m, 3H), 2.58 (m, 1H), 2.73 (m, 1H), 3.35 (dt, J=11.0, 3.0 Hz, 2H), 3.81 (s, 2H), 3.96 - 3.99 (m, 2H), 4.59 (br-s, 2H), 4.64 (br-s, 2H), 6.99 (br-s, 2H), 7.06 (br-s, 2H), 7.35 (d, J=8.1 Hz, 2H), 7.62 (d, J=8.1 Hz, 2H)。
実施例 5 0 ( 6 5 ) : 4— ( { [トランス一 4一 (ベンジ /レアミノ) シクロ へキシノレ] アミノ} メチノレ) 一 N, N—ビス (1 H—イミダゾ^ ·ルー 2—ィ ルメチル) ベンズァミド (化合物 5 0— 6 5 )
性状:アモルファス
TLC: Rf 0.54 (酢酸ェチル:メタノール: 28%アンモニア水 = 50:10:1);
NMR (CDCls): 8 1.13-1.20 (m, 4H), 1.97-2.02 (m, 4H), 2.40-2.60 (m, 2H), 3.81 (s, 2H), 3.82 (s, 2H),4.57 (br-s, 2H), 4.62 (br-s, 2H), 7.00 (br-s, 2H), 7.06 (br-s, 2H), 7.24-7.32 (m, 5H), 7.36 (d, J=8.1 Hz, 2H), 7.62 (d, J=8.1 Hz, 2H)0
実施例 5 0 ( 6 6 ) : N, N—ビス ( 1 H—イミダゾールー 2—ィルメチル) - 4 - ( { [トランス一 4一 (プロピルァミノ) シクロへキシル] アミノ}
メチル) ベンズァミ ド (化合物 5 0 - 6 6 )
性状:油状物
TLC: Rf 0.27 (ジクロロメタン:メタノール: 28%アンモニア水 = 50:10:1); NMR (CDCls): δ 0.91 (t, J=7.2 Hz, 3H), 1.04—1.23 (m, 4H), 1.45-1.96 (m, 6H), 2.40 - 2.50 (m, 2H), 2.58 (t, J=7.2 Hz, 2H), 3.82 (s, 2H), 4.55 (br-s, 2H), 4.59 (br-s, 2H), 7.01 (br-s, 2H), 7.08 (br-s, 2H), 7.37 (d, J=8.1 Hz, 2H), 7.72 (d, J=8.1 Hz, 2H)。
実施例 5 0 ( 6 7 ) : 4— { [ {トランス一 4一' [シクロへキシル (プロピ ル) ァミノ] シクロへキシル } (メチル) ァミノ] メチル } — N, N—ビス ( 1 H—イミダゾールー 2—ィルメチル) ベンズァミ ド (化合物 5 0 - 6 7 )
性状:油状物
TLC: Rf 0.65 (酢酸ェチル:メタノール: 28%アンモニア水 = 50:10:1);
NMR (CDCls): δ 0.81 (t, J=7.2 Hz, 3H), 1.07—2.51 (m, 25H), 2.26 (s, 3H), 3.55 (s, 2H), 4.63 (br-s, 2H), 4.65 (br-s, 2H), 6.98 (br- s, 2H), 7.06 (br-s, 2H), 7.36 (d, J=8.1 Hz, 2H), 7.61 (d, J=8.1 Hz, 2H)。
実施例 5 0 ( 6 8 ) : 4— [ (ベンジル {トランス一 4— [シクロへキシル (プロピル) ァミノ] シクロへキシル } ァミノ) メチル] — N, N—ビス (1 H—イミダゾールー 2—ィルメチル) ベンズァミ ド (化合物 5 0 - 6 8 ) 性状:油状物
TLC: Rf O.83 (酢酸ェチル:メタノール: 28%アンモニア水 = 50:10:1);
NMR (CDCls): δ 0.81 (t, J=7.2 Hz, 3H), 1.22-2.60 On, 25H), 3.60 (s, 2H), 3.61 (s, 2H), 4.59 (br-s, 4H), 7.01 (br-s, 2H), 7.09 (br-s, 2H), 7.18-7.35 (m, 5H), 7.42 (d, J=8.1 Hz, 2H), 7.67 (d, J=8.1 Hz, 2H)。
実施例 50 (69) : 4— ( { [トランス一 4一 (ジプロピルァミノ) シク 口へキシノレ] アミノ} メチル) 一 N, N—ビス (1H—イミダゾールー 2— ィルメチル) 一 2—メチルベンズァミ ド (化合物 50-69)
性状:ァモノレファス
TLC: Rf 0.60 (クロ口ホルム:メタノール: 28%ァン ュア水 = 80:20:4); NMR (DMSO-De): δ 0.79 (t, J=7.50 Hz, 6 H), 0.90-1.06 (m, 2 H),
1.07-1.23 (m, 2 H), 1.23-1.39 (m, 4 H), 1.56-1.72 (m, 2 H), 1.83-1.98 (m, 2 H), 2.11 (s, 3 H), 2.17-2.42 (m, 6 H), 3.63 (s, 2 H), 4.39 (s, 2 H), 4.67 (s, 2 H), 6.72-7.05 (m, 4H), 7.05-7.20 (m, 3H), 11.97-12.55 (m, 2 H)。
実施例 50 (70) : 4— [ (2— tert—プチルー 2, 8—ジァザスピロ [4. 5] デカー 8—ィル) メチル] 一 N, N—ビス (1 H—イミダゾールー 2— ィルメチル) ベンズァミ ド (化合物 50-70)
性状:アモルファス
TLC: 0.52 (酢酸ェチ /レ:メタノール: 28%アンモニア水 = 50:10:1);
NMR (CDC13): δ 1.07 (s, 9H), 1.52-1.66 (m, 6H), 2.24-2.44 (m, 4H), 2.54 (s
2H), 2.71 (t, J=6.6 Hz, 2H), 3.48 (s, 2H), 4.58-4.66 (m, 4H), 6.98-7.10 (m, 4H), 7.37 (d, J=8.4 Hz, 2H), 7.65 (d, J=8.4 Hz, 2H)。
実施例 50 (71) : 4一 ( { [4一 (tert—プチルァミノ) シクロへキシル] アミノ} メチル) 一 N, N—ビス (1H— ^ ミダゾ一ルー 2—ィルメチル) ベンズァミ ド (化合物 50-71)
性状:ァモノレファス
TLC:Rf 0.26 (酢酸ェチル:メタノール: 28%アンモニア水 =90:10:2);
NMR (CDC1
3): S d 1.12 (s, 9H), 1.48-1.75 (tn, 8H), 2.62-2.78 (m, 2H), 3.76
(s, 2H), 4.50-4.75 (m, 4H), 6.95-7.12 (m, 4H), 7.36 (d, J=8.4Hz, 2H), 7.60
実施例 50 (72) : 4— ( { [4- (tert—ブチルァミノ) シクロへキシル] アミノ} メチル) 一 N, N—ビス (1H—イミダゾールー 2—ィルメチル) ベンズァミド (化合物 50-72)
性状:ァモルファス
TLC: Rf 0.19 (酢酸ェチル:メタノール: 28%アンモニア水 = 90:10:2); NMR (CDC13): δ d 1.12 (s, 9H), 1.10-1.30 (m, 4甘), 1.75-2.00 (m, 4H), 2.42 (m, 1H), 2.54 (m, 1H), 3.81 (s, 2H), 4.50-4.72 (m, 4H), 6.90-7.12 (m, 4H), 7.35 (d, J=8.4 Hz, 2H), 7.63 (d, J=8.4 Hz, 2H)。
実施例 50 (73) : 4一 [ ( {トランス一 4一 [ (シク口へキシルメチル) ァミノ] シクロへキシル } ァミノ) メチル] 一 N, N—ビス (1H—イミダ ゾ一ルー 2一イノレメチル) ベンズァミド (化合物 50-73)
性状:アモルファス
TLC: Rf 0.67 (酢酸ェチル:メタノール: 28%アンモニア水 = 80:20:2);
NMR (CDCls): 5 d 0.80-2.04 (m, 19H), 2.38-2.54 (m, 4H), 3.81 (s, 2H), 4.50-4.68 (m, 4H), 6.92-7.12 (m, 4H), 7.35 (d, J=8.4 Hz, 2H), 7.64 (d, J=8A Hz, 2H)。
実施例 50 (74) : 4— { [ (4ーァニリノシクロへキシル) ァミノ] メ チル } 一 N, N—ビス (1 H—イミダゾール一 2—ィルメチル) ベンズアミ ド (低極性体) (化合物 50-74)
性状:ァモルファス
TLC: Rf 0.47 (酢酸ェチル:メタノール: 28%アンモニア水 = 90:10:2);
NMR (CDCls): 5 d 1.50-1.85 (m, 8H), 2.70 (αι, 1Η), 3.49 (m, 1H), 3.82 (s, 2H), 4.50-4.68 (m, 4H), 6.59 (d, J=7.5 Hz, 2H), 6.66 (dd, J=7.5, 7.5 Hz, 1H) 6.98-7.10 (m, 4B), 7.15 (dd, J=8.7, 7.5 Hz, 2H), 7.39 (d, J=8.4 Hz, 2H),
7.68(d, J=8.4Hz, 2H)0
実施例 50 (75) : 4- { [ (4—ァエリノシクロへキシル) ァミノ] メ チル } — N, N—ビス (1H—イミダゾールー 2—ィルメチル) ベンズアミ ド (高極性体) (化合物 50-75)
性状:アモルファス
TLC: RfO.45 (酢酸ェチル:メタノール: 28%アンモニア水 = 90:10:2);
NMR (CDCls): 5 d 1.04-1.38 (m, 4H), 1.98-2.08 (m, 2H), 2.12-2.22 (m, 2H) 2.52 (m, IH), 3.24 (m, IH), 3.85 (s, 2H), 4.46-4.70 (m, 4H), 6.58 (d, J=7.5 Hz, 2H), 6.66 (dd, J=7.5, 7.5 Hz, IH), 6.98-7.10 (m, 4H), 7.15 (dd, J=8.4, 7.5 Hz, 2H), 7.39 (d, J=8.1 Hz, 2H), 7.70 (d, J=8.1 Hz, 2H)。
実施例 50 (76) : 4— { [8— (2—シクロへキシルェチル) 一 2, 8 ージァザスピロ [4. 5] デカー 2—ィル] メチノレ) 一 N, N—ビス (1H ーィミダゾールー 2一ィルメチル) ベンズァミ ド (化合物 50-76) 性状:アモルファス
TLC: Rf 0.28 (メタノール: 28%アンモ-ァ水 = 98:2);
NMR (CDC13): 80.83-0.97 (m, 2 H), 1.13-1.27 (m, 4 H), 1.36-1.45 (m, 2 H); 1.58-1.72 (m, 10 H), 2.32-2.48 (m, 9 H), 2.52-2.61 (m, 2 H), 3.59 (s, 2 H),
4.58- 4.70 (m, 4 H), 6.98-7.12 (m, 4 H), 7.32-7.43 (m, 2 H), 7.62-7.74 (m, 2 H)。
実施例 50 (77) : 4— { [8— ( 3—シクロへキシルプロピル) 一 2, 8—ジァザスピロ [4. 5] デカー 2—ィル] メチル } 一 N, N—ビス (1 H—ィミダゾールー 2—イノレメチル) ベンズァミ ド (化合物 50-77) 性状:アモルファス
TLC: Rf 0.28 (メタノール: 28%ァンモ -ァ水 = 98:2);
NMR (CDCls): δ 0.78-0.92 (tn, 2 H), 1.10-1.26 (m, 6 H), 1.53-1.57 (m, 2 H),
1.59- 1.71 (m, 11 H), 2.31—2.41 (m, 6 H), 2.44-2.52 (m, 2 H), 2.55-2.60 (m,
2 H), 3.59 (s, 2 H), 4.56-4.68 (m, 4 H), 6.98-7.12 (m, 4 H), 7.33-7.42 (m, 2 H), 7.63-7.73 (m, 2 H)。
実施例 50 (78) : N, N—ビス (1H—イミダゾールー 2 _ィルメチル) -4- ( {8- [ (3—メチル一 2—チェ-ル) メチル] —2, 8—ジァザ スピロ [4. 5] デカー 2—ィル } メチル) ベンズアミ ド (化合物 50— 7 8)
性状:アモルファス
TLC: Rf0.40 (メタノール: 28%ァンモユア水 = 98:2);
NMR (CDCls): 51.52 - 1.65 (m, 6 H), 2.15-2.21 (m, 3 H), 2.30-2.45 (m, 6 H); 2.49-2.59 (m, 2 H), 3.52-3.63 (m, 4 H), 4.57-4.69 (m, 4H), 6.73—6.80 (m, 1 H), 6.97-7.12 (m, 5 H), 7.32-7.43 (m, 2 H), 7.60-7.69 (m, 2 H)。
実施例 50 (79) : 4- { [8— (1—ベンゾチェン一 2—ィルメチル) 一 2, 8—ジァザスピロ [4. 5] デカー 2—ィル] メチル } 一 N, N—ビ ス ( 1 H—ィミダゾール一 2—^ Tルメチル) ベンズァミド (化合物 50— 7 9)
性状:アモルファス
TLC: Rf 0.40 (メタノール: 28%ァンモエア水 = 98:2);
NMR (CDC13): 81.54-1.67 (m, 6 H), 2.34-2.49 (m, 6 H), 2.51—2.60 (m, 2 H); 3.59 (s, 2 H), 3.74 (s, 2 H), 4.57 - 4.69 (m, 4 H), 6.97-7.12 (m, 5 H),
7.22-7.34 (m, 2 H), 7.35-7.41 (m, 2 H), 7.61-7.69 (m, 3 H), 7.72-7.80 (m, 1 H)。
実施例 50 (80) : 4— { [8— (4ーヒドロキシシクロへキシル) 一2,
8—ジァザスピロ [4. 5] デカー 2—ィル] メチル } — N, N—ビス (1 H—イミダゾールー 2—ィルメチル) ベンズァミド (化合物 50-80) 性状:アモルファス
TLC: Rf 0.23 (メタノール: 28%ァンモユア水 = 98:2);
NMR (CDC13): δ 1.22-1.38 (m, 2 H), 1.51-2.05 (m, 12 H), 2.26—2.58 (m, 9 H), 3.53-4.02 (m, 3 H), 4.56-4.66 (m, 4 H), 6.95-7.10 (m, 4 H), 7.33-7.44 (m, 2 H), 7.64-7.74 (m, 2 H)。
実施例 50 (81) : 4— { [8— (1一ェチル ロピル) 一 2, 8—ジァ ザスピロ [4. 5] デカ一 2—ィル] メチル } 一 N, N—ビス (1H—イミ ダゾールー 2一ィルメチル) ベンズァミ ド (化合物 50— 81)
性状:ァモノレファス
TLC: Rf 0.40 (メタノール: 28%ァンモエア水 = 98:2);
NMR (CDCls): δ 0.82-0.94 (m, 6 H), 1.21-1.37 (m, 3 H), 1.49-1.64 (m, 8 H) 2.17-2.28 (m, 1 H), 2.36 (s, 2 H), 2.45-2.53 (m, 3 H), 2.55-2.61 (m, 2 H), 3.54-3.65 (m, 2 H), 4.58-4.73 (m, 4 H), 6.95—7.09 (m, 4H), 7.32-7.41 (m, 2 H), 7.58-7.68 (m, 2 H)。
実施例 50 (82) : 4— [ (8—ェチル一2, 8—ジァザスピロ [4. 5] デカ一 2—^ fル) メチル] -N, N—ビス (1 H—イミダゾールー 2—ィル メチル) ベンズァミド (化合物 50-82)
性状:アモルファス
TLC: Rf 0.16 (メタノール: 28%アンモユア水 = 98:2);
NMR (CDCls): δ 1.02—1.12 (m, 3 H), 1.54-1.66 (m, 6 H), 2.27-2.42 (m, 8 H);
2.46-2.60 (m, 2 H), 3.58 (s, 2 H), 4.57—4.70 (tn, 4 H), 6.95-7.10 (m, 4 H), 7.32-7.41 (m, 2 H), 7.54-7.65 (m, 2 H)。
実施例 50 (83) : 4- { [8- (1—ァザビシクロ [2. 2. 2] オタ ター 3—ィル) 一 2, 8—ジァザスピロ [4. 5] デカー 2—ィル] メチル } 一 N, N—ビス (1 H—イミダゾールー 2—ィルメチル) ベンズアミ ド (化 合物 50— 83)
性状:ァモノレファス
TLC: Rf0.25 (メタノール: 28%アンモニア水二 9:1);
NMR (CDCls): δ 1.23—2.11 (m, 11 H), 2.12-2.41 (m, 6 H), 2.55 (t, J=6.9 Hz, 2 H), 2.63-3.15 (m, 7 H), 3.58 (s, 2 H), 4.54-4.72 (m, 4 H), 6.92-7.15 (m, 4 H), 7.37 (d, J=8.1 Hz, 2 B), 7.64 (d, J=8.1 Hz, 2 H)。
実施例 50 (84) : 4— { [2— (シクロペンチルメチル) 一2, 8—ジ ァザスピロ [4. 5] デカー 8—ィル] メチル } 一 N, N—ビス (1H—ィ ミダゾールー 2—ィルメチル) ベンズァミド (化合物 50-84)
性状:アモルファス
TLC: Rf 0.47 (メタノール: 28%アンモニア水二 98:2);
NMR (CDCls): 61.06-1.30 (m, 2 H), 1.41-1.67 (m, 10 H), 1.66-1.85 (m, 2 H), 1.88-2.08 (m, 1 H), 2.25-2.44 (m, 8 H), 2.55 (t, J=6.6 Hz, 2 H), 3.47 (s, 2 H), 4.52-4.73 (m, 4 H), 6.89-7.17 (m, 4 H), 7.38 (d, J=8.1 Hz, 2 H), 7.66 (d, J=8.1Hz,2H)。
実施例 50 (85) : N, N—ビス (1 H—ィミダゾールー 2—^ Tルメチル) -4- { [2— (2—チェニノレメチノレ) -2, 8ージァザスピロ [4. 5] デカ― 8一ィル] メチル } ベンズァミ ド (化合物 50-85)
性状:アモ^/レファス
TLC: Rf 0.58 (メタノール: 28%ァンモユア水 = 98:2);
NMR (CDC13): δ 1.49-1.70 (m, 6 H), 2.20-2.38 (m, 4 H), 2.41 (s, 2 H), 2.62
(t, J=6.9 Hz, 2 H), 3.46 (s, 2 H), 3.78 (s, 2 H), 4.51-4.73 (m, 4H), 6.89 (dd, J=3.6, 1.2 Hz, 1 H), 6.93 (dd, J=4.8, 3.6 Hz, 1 H), 6.96-7.13 (m, 4H), 7.20 (dd, J=4.8, 1.2 Hz, 1H), 7.37 (d, J=8.1 Hz, 2H), 7.65 (d, J=8.1 Hz, 2 H)。 実施例 50 (86) : 4— { [2— (4一フルォロベンジル) 一 2, 8—ジ ァザスピロ [4. 5] デカー 8—ィル] メチノレ) 一 N, N—ビス (1H—ィ ミダゾールー 2—イノレメチル) ベンズァミ ド (化合物 50-86)
性状:アモルファス
TLC: Rf0.53 (メタノール: 28%ァンモユア水 = 98:2);
NMR (CDCla): δ 1.47-1.68 (m, 6 H), 2.23-2.42 (m, 6 H), 2.54 (t, J=6.9 Hz, 2 H), 3.46 (s, 2 H), 3.53 (s, 2 H), 4.52-4.72 m, 4 H), 6.86-7.15 (m, 6 H), 7.19-7.32 (m, 2 H), 7.37 (d, J=8.1 Hz, 2 H), 7.65 (d, J=8.1 Hz, 2 H)。
実施例 50 (87) : 4— ( {2— [4一 (ジェチルァミノ) ベンジル] 一 2, 8—ジァザスピロ [4. 5] デカー 8—ィル } メチル) 一 N, N—ビス ( 1 H—イミダゾールー 2一ィルメチル) ベンズァミド (化合物 50-87) 性状:アモルファス
TLC: Rf 0.44 (メタノール: 28%アンモニア水二 98:2);
NMR (CDCls): δ 1.15 (t, J=7.2 Hz, 6 H), 1.45-1.68 (m, 6 H), 2.24-2.43 (m, 6 H), 2.55 (t, J=6.6 Hz, 2 H), 3.33 (q, J=7.2 Hz, 4 H), 3.45 (s, 2 H), 3.47 (s, 2 H), 4.51-4.73 (m, 4 H), 6.62 (d, J=9.0 Hz, 2 H), 6.92-7.09 (m, 4 H), 7.13 (d, J=9.0 Hz, 2H), 7.36 (d, J=8.1 Hz, 2H), 7.62 (d, J=8.1 Hz, 2 H)。
実施例 50 (88) : 4- { [4- (シクロペンチルメチル) 一 1一ォキサ 一 4, 9ージァザスピロ [5. 5] ゥンデ力一 9ーィノレ] メチル } -N, N 一ビス (1H—イミダゾールー 2—ィルメチル) ベンズアミド (化合物 50 -88)
性状:アモルファス
TLC:Rf0.71(メタノール: 28%アンモユア水 =98:2);
NMR (CDCls): δ 1.08-1.30 (m, 2 H), 1.40-1.79 (m, 8 H), 1.84-2.25 (m, 7 H):
2.27- 2.56 (m, 6 H), 3.52 (s, 2 H), 3.62-3.75 m, 2 H), 4.50-4.75 (m, 4 H), 6.89-7.18 (m, 4 H), 7.39 (d, J=8.1 Hz, 2 H), 7.66 (d, J=8.l Hz, 2 H)。
実施例 5 0 ( 8 9 ) : N, N—ビス (1 H—イミダゾールー 2—^ ルメチル) 一 4一 { [ 4一 (2—チェニノレメチノレ) 一1一ォキサ一 4, 9—ジァザスピ 口 [ 5 . 5 ] ゥンデカー 9一^ fル] メチル } ベンズァミ ド (化合物 5 0— 8 9 )
性状:アモルファス '
TLC: Rf 0.73 (メタノール: 28%アンモユア水 = 98:2);
NMR (CDC13): δ 1.43-1.65 (m, 2 H), 1.82-2.03 (m, 2 H), 2.24 (s, 2 H),
2.28- 2.57 (m, 6 H), 3.49 (s, 2 H), 3.63 (s, 2 H), 3.67-3.80 (m, 2 H),
4.50-4.74 (m, 4 H), 6.88 (dd, J=3.6, 1.2 Hz, 1 H), 6.92 (dd, J=5.1, 3.6 Hz, 1 H), 6.95-7.12 (m, 4H), 7.21 (dd, J=5.1, 1.2 Hz, 1H), 7.37 (d, J=8.1 Hz, 2H), 7.63 (d, J=8.1 Hz,2 H)。
実施例 5 0 ( 9 0 ) : 4— { [ { 1^ランスー4ー [シクロへキシル (プロピ ル) ァミノ] シクロへキシル } (ェチル) ァミノ] メチル } 一 N, N—ビス ( 1 H—イミダゾールー 2一^ fルメチル) ベンズァミド (化合物 5 0 - 9 0 )
性状:アモルファス
TLC: Rf 0.69 (酢酸ェチル:メタノール: 28%アンモニア水 = 50:10:1);
NMR (CDCls): 5 0.81 (t, J=7.2 Hz, 3H), 0.93 (t, J=7.2 Hz, 3H), 1.18-1.81
(m, 20H), 2.39-2.53 (m, 7H), 3.59 (s, 2H), 4.64 (br-s, 4H), 6.99 (br-s, 2H), 7.07 (br-s, 2H), 7.40 (d, J=8.1 Hz, 2H), 7.62 (d, J=8.1 Hz, 2H)。
実施例 50 (91) : 4— { [ {トランス一 4一 [シクロへキシル (プロピ ル) ァミノ] シク口へキシル } (プロピル) ァミノ] メチル } — N, N—ビ ス (1 H一^ f ミダゾールー 2—ィルメチル) ベンズァミ ド (化合物 50-9 1)
性状:油状物
TLC: Rf 0.73 (酢酸ェチル:メタノール: 28%アンモニア水 = 50:10:1); NMR (CDC13): δ 0.78—0.85 (m, 6H), 1.06 - 1.92 (m, 22H), 2.36-2.59 (m, 7H) 3.60 (s, 2H), 4.62 (br-s, 4H), 7.01 (br-s, 2H), 7.09 (br-s, 2H), 7.41 (d, J=8.1 Hz, 2H), 7.68 (d, J=8.1 Hz, 2H)。
実施例 50 (92) : 4— [ (2—シクロへキシルー 2, 8—ジァザスピロ [4, 5] デカー 8—ィル) メチル] 一 N, N—ビス (1H—イミダゾーノレ — 2—イノレメチル) ベンズァミド (化合物 50-92)
性状:アモルファス
TLC:Rf 0.15 (メタノール: 28%アンモユア水 =99:1);
9fZ
(96-09 r ^ ん , ( ^ i^^y- z― ^— ^^ -Hl) 'N- [ ^ {^y-z- ^^ [9 ' ] a。a ^ ー 8
(Ζ~Λί ^ ] - ^ : (96) 09
οζ
'Ρ) S9'ム '(Η Ζ 'ΖΗ 8*L=f 'Ρ) 68 , '(Η f '^) fVL-f6'9 '(Η f '∞) L -6Vf
'(Η Ζ '∞) S S - S '(Η Ζ 's) Ζ9'£ '(Η £Ζ '∞) 9: (εΐθαθ)丽 Ν
- (1:66 =氺 0 /。8 /— / Zf'QM :0ΊΛ
士 : ^¾ ST
( 6— 0 s嗨 ¾ 、 ^ ^ { (4= ^Λ^ y-z一へ (一ί、 ^ y-u
I) ー N 'Ν- Λ(·ί=^ ( / 一 6— ^ [S "9] α^^^
- 6 ',一 4^ 一τ一 4/4·^^ 一 ] ー ·· ( 6) 0 g
°(H Z ' T'8=f 'Ρ) WL '(Η Z 'ΖΗ Γ8=Γ 'Ρ) WL '(H f 'ra) ZVL-S^9 '(H f '(Η Z '∞) 192-Z22 '(H 6 '∞) ε9^-Χ0Έ OT
(H ) 98 Τ-99Ί '(H L '∞) S9 T-f8 I '(H L 'm) T8 I-L609: (εΐθαθ)丽 N
- (2:86 =氺 -士 %8Z:^— ヽ 890 m :0ΊΛ
^ /士 :
(86-09 ) 、 {Λί-ί= ί y-Ζ-Λί— ^ ^一 Ητ) «-Ν 'N—
{Λ( [Q "9] s
'Ζ-Λί ^ ^^-^) ] : (86) 09 M
°(H Z 'ZH I'8=f 'P) I9 A '(H Z ' I'8=f 'Ρ) 98 Z, '(H IVL-ZQ'd
'(H ) S OS '(H Z 's) LY '(Η Z ' 9'9=f U'Z '(H Z 's) 922 '(H f ) fZ-XZ-Z '(H Zl '∞) S0 S-9f T '(H 9 '∞) 9: (sT0Q0) HHN
9909T0/S00Zdf/X3d 1^H0/900Z OAV
性状:アモルファス
TLC: Rf 0.33 (酢酸ェチル:メタノール: 28%アンモニア水 = 50:10:1);
NMR (CDC13): 81.00-2.56 (m, 25H), 3.56 (s, 2H), 4.64 (s, 2H), 4.68 (s, 2H) 6.96 (s, 2H), 7.03 (s, 2H), 7.34 (d, J=8.1 Hz, 2H), 7.53 (d, J=8.1 Hz, 2H)。 実施例 50 (96) : 4一 [ (7—シクロへキシルー 2, 7—ジァザスピロ [4. 5] デカー 2—ィル) メチル] — N, N—ビス (1H—イミダゾール 一 2一イノレメチル) ベンズァミド (化合物 50- 96)
性状:ァモノレファス
TLC:Rf 0.46 (酢酸ェチル:メタノール: 28%アンモニア水 =50:10:1);
NMR (CDC13): 51.00-2.65 (m, 25H), 3.56 (d, J=13.8 Hz, 1H), 3.59 (d, J=13.8 Hz, 1H), 4.62-4.66 (m, 4H), 6.99 (s, 2H), 7.06 (s, 2H), 7.38 (d, J=8.1 Hz, 2H), 7.62 (d, J=8.1 Hz, 2H)。
実施例 50 (9 7) : 4— [ (9—シクロへキシルー 2, 9—ジァザスピロ [5. 5] ゥンデカー 2—ィル) メチル] — N, N—ビス (1H—イミダゾ ール— 2—^ fルメチル) ベンズァミド (化合物 50— 97)
性状:ァモルファス
TLC: Rf 0.44 (酢酸ェチル:メタノール: 28%アンモ-ァ水 = 50:10:1);
NMR (CDCls): 81.00-2.55 (m, 27H), 3.43 (s, 2H), 4.60—4.65 (m, 4H), 7.00 (s, 2H), 7.07 (s, 2H), 7.37 (d, J=8.1 Hz, 2H), 7.40 (d, J=8.1 Hz, 2H)。
実施例 50 (98) : 4— [ (2—シクロへキシルー 2, 7—ジァザスピロ [3. 5] ノナ一 7—ィル) メチル] 一 N, N—ビス (1H—イミダゾール - 2—ィルメチル) ベンズァミド (化合物 50-98)
性状:アモルファス '
TLC: Rf 0.42 (メタノール: 28%ァンモユア水 = 98:2);
NMR (GDC13): 80.89-1.31 (m, 5 H), 1.51-1.65 m, 1 H), 1.65-1.82 (m, 8 H); 1.95-2.11 (m, 1 H), 2.16-2.41 (m, 4 H), 3.06 (s, 4 H), 3.43 (s, 2 H),
4.54-4.81 (m, 4 H), 6.89-7.11 (m, 4 H), 7.32 (d, J=8.1 Hz, 2 H), 7.48 (d, J=8.1Hz,2H;)。
実施例 50 (99) : 4— [ (9—シクロへキシルー 1—ォキサ一 4, 9一 ジァザスピロ [5. 5] ゥンデカー 4—ィル) メチル] 一 N, N—ビス (1 H—ィミダゾール一 2—イノレメチル) ベンズァミ ド (化合物 50-99) 性状:アモルファス
TLC: Rf 0.51 (メタノール: 28%アンモニア水 = 98:2);
NMR (CDCk): δ 0.96-1.36 (m, 5 H), 1.44-1.69 (m, 3 H), 1.70-2.09 (m, 6 H): 2.18 (s, 2 H), 2.24-2.46 (m, 3 H), 2.48-2.70 m, 4 H), 3.34-3.47 (m, 2 H), 3.62-3.78 (m, 2 H), 4.53-4.83 (m, 4 H), 6.90—7.12 (m, 4 H), 7.33 (d, J=8.1 Hz, 2 H), 7.47 (d, J=8.1 Hz, 2 H)。
実施例 50 (100) : 4一 [ (4ーシクロへキシル一 1一ォキサ一 4, 8 ージァザスピロ [5. 5] ゥンデカー 8— fル) メチル] 一 N, N—ビス (1 H—イミダゾールー 2—イノレメチル) ベンズァミ ド (化合物 50- 100) 性状:アモルファス
{Λί^ ^ ί ^ (^ c^Jp Χ^ -Ζ) {Λ( ^ [ , {ΛΙ ) 、 ] 一 一 べ 4 } ] } 一, : ( 8 0 T ) 09 ^ :^
°(HS ¾f8=f 'Ρ) WL \EZ ' f8=f
'V)Zf'L '(Ηΐ 80·ム \RZ 's- Jq) 0'L '(RZ 's- Jq) Τ0·ム '(H.Z 899-99'9 '(Ηΐ '∞) Lf9 \ 's-iq) L9'f '(RZ 's, 09 f '(HZ 's) 92 f '(HS 's) 9 S Έί
<ra) S£-Z-££-Z '(H '∞) IS*T-68 T '(H9 'ZH Z L=2 ( ) 8809: (8TOQO) ΉΗΝ
'· (T:0T:0S = 氺 - べ %8&4— / : ェ邈 ) S9 JH :OTL OS : /士 :
0 I -0 S λ Α l^ ,、 ( ≠
^y- z - — / ^ ^ y-u τ ) ー N 'Ν- Λ^ ( ^
\Λ(^≠ { ^ Ά^ ^) ] 一 ε} ) ] — : (S O T) o g um^
°(H Z ' I"8=f 'P) 29 L '(H I <ZH ^'8=f 'Ρ) LVL '(H Z ' T8=f ST £P) ZVL '(H X 'TO) fZ L-£T'L '(H S '^) srム- 86·9 '(Η ΐ '^Η L8'L=f 'Ρ) S69 '(Η
'ιπ) L2'f-Wf '(Η Ζ 's) 99·ε '(Η Ζ 098 '(Η Ζ '^) ^'Ζ-ΙΘ'Ζ '(Η Ζ 's) Ζ9 Ζ (Ή.9 L£ Z- 6 l '(Η L '^) £6'l- f'l '(Η 9 '^) 28 Ϊ-6809: (8Τθαθ) ΗΗΝ
• (2:86 =氺 0 / Z90m :0TL
厶 : ' 0T
(τ οτ
-09 Λ χ ^>- ( ^ ^ / - ζ - (-^ :^ -H τ )
~[ ci^^-H X d ] - ' (T 0 T) 09
'Ρ) 2VL '(Η Ζ 'ΖΗ Ι-8=Γ 'Ρ) f L '(Η '^) ム- 68·9 '(Η f '∞) 8 -8
'(Η Ζ '∞) 8 S- 62·ε '(Η Τ 'ΖΗ 8'ST=f 'Ρ) S'S '(Η Τ 'ΖΗ 8'8ΐ=Γ 'Ρ) 8f8 (Η 6 ΤΖ '(Η 6 061-Ζ,ε Τ '(Η 9 '^) εε Τ-86Ό 9: (εΐθαθ) WR
- (2:86 =氺 Μ^ΖΛ- ί^ / ja :0ΊΛ
9909T0/S00Zdf/X3d
一 N, N—ビス (1 H—イミダゾールー 2—ィルメチル) ベンズァ
合物 5 0 - 1 0 3 )
性状: アモルファス
TLC: Rf 0.47 (ジクロロメタン:メタノール: 28%アンモニア水 = 50:10:1); NMR (CDC13): 60.81 (t, J=7.5 Hz, 3H), 1.18-2.00 (m, 20H), 2.38—2.58 (m, 5H), 2.65 (t, J=5.3 Hz, 2H), 3.41 (t, J=5.4 Hz, 2H), 3.63 (s, 2H), 4.57 (br-s, 2H), 4.69 (br-s, 2H), 7.02 (br-s, 2H), 7.05 (br-s, 2H), 7.34 (d, J=8.1 Hz, 2H) 7.61 (d, J=8.1 Hz,2H)。
実施例 5 0 ( 1 0 4 ) : 4— [ ( {トランス一 4一 [ ( 2—ヒドロキシェチ ル) (プロピル) ァミノ] シクロへキシル } ァミノ) メチル] — N, N—ビ ス (1 H—イミダゾールー 2—ィルメチル) ベンズアミ ド (化合物 5 0— 1 0 4 )
性状:油状物
TLC: Rf 0.41 (ジクロロメタン:メタノール: 28%アンモニア水 = 50:10:1); NMR (CDC13): δ 0.86 (t, J=7.5 Hz, 3H), 1.06 - 2.04 (m, 10H), 2.35-2.52 (m, 4H), 2.59 (t, J=5.4 Hz, 2H), 3.48 (t, J=5.4 Hz, 2H), 3.82 (s, 2H), 4.58 (br-s, 2H), 4.61 (br-s, 2H), 7.02 (br-s, 2H), 7.09 (br-s, 2H), 7.37 (d, J=8.1 Hz, 2H) 7.71 (d, J=8.1 Hz, 2H)。
実施例 5 0 ( 1 0 5 ) : 4一 [ ( {トランス一 4一 [ ( 1一ェチルプロピル) ( 2—ヒ ドロキシェチル) ァミノ] シクロへキシル } ァミノ) メチル] -N,
N—ビス (I H—^ iミダソール一 2一ィルメチル) ベンズアミ ド (化合物 5 0 - 1 0 5 )
性状:アモルファス
TLC: Rf 0.50 (ジクロロメタン:メタノール: 28%アンモニア水 = 50:10:1); NMR (CDCls) : 8 0.89 (t, J=7.2 Hz, 6H), 1.11-1.42 (m, 8H), 1.71-1.75 (m, 2H), 1.98-2.01 (m, 2H), 2.26 (m, IH), 2.41 (m, 1H), 2.54 (m, IH), 2.68 (t, J=5.1 Hz, 2H), 3.45 (t, J=5.1 Hz, 2H), 3.81 (s, 2H), 4.60 (br-s, 2H), 4.66 (br-s, 2H), 6.99 (br-s, 2H), 7.04 (br-s, 2H), 7.34 (d, J=7.8 Hz, 2H), 7.52 (d, J=7.8 Hz, 2H)。
実施例 5 0 ( 1 0 6 ) : 4— ( { [トランスー4一 (ジブ口ピルァミノ) シ ク口へキシル] アミノ } メチル) 一N, N—ビス ( 1 H—ィミダゾールー 2 一ィルメチル) 一 2—メ トキシベンズァミド (化合物 5 0— 1 0 6 )
性状:アモルファス
TLC: Rf 0.67 (クロ口ホルム:メタノール: 28%アンモニア水 = 80:20:4);
NMR (DMSO-De): δ 0.79 (t, J=7.2 Hz, 6 H), 0.90-1.07 (m, 2 H), 1.07-1.23 (m, 2 H), 1.24-1.40 (m, 4 H), 1.57-1.71 (m, 2 H), 1.85-1.98 (m, 2 H), 2.17-2.43 (m, 6 H), 3.64 (s, 3 H), 3.67 (s, 2 H), 4.43 (s, 2 H), 4.54-4.95 (m, 2 H), 6.61-7.27 (m, 7 H), 11.95 - 12.74 (m, 2 H)。
実施例 5 0 ( 1 0 7 ) : 4一 [ ( {トランス一 4— [ 2, 3—ジヒ ドロ一 1 H—インデン一 2—ィル (プロピル) ァミノ] シクロへキシル } ァミノ) メ チル] 一 N, N—ビス (1 H—イミダゾール一 2—ィルメチル) ベンズアミ ド (化合物 5 0 - 1 0 7 )
性状: アモルファス
TLC: Ef 0.64 (酢酸ェチル:メタノール: 28%アンモエア水 = 80:20:3);
NMR (CDC13): δ d 0.85 (t, J=7.2 Hz, 3H), 1.15—1.60 (m, 6H), 1.82-1.95 (m, 2H), 2.02-2.12 (m, 2H), 2.40-2.58 (m, 3H), 2.70 (m, 1H), 2.90 - 3.02 (m, 4H), 3.77 (m, 1H), 3.84 (s, 2H), 4.52-4.75 (m, 4H), 6.98-7.10 (m, 4H), 7.10-7.20 (m, 4H), 7.38 (d, J=8.4 Hz, 2H), 7.60 (d, J=8.4 Hz, 2H)。
実施例 5 0 ( 1 0 8 ) : N, N—ビス ( 1 H—イミダゾールー 2—ィルメチ ル) 一 4一 [ ( {トランス一 4一 [ ( 2—ナフチルメチル) (プロピル) ァ ミノ] シク口へキシル } ァミノ) メチル] ベンズァミ ド (化合物 5 0— 1 0 8 )
性状: アモルファス
TLC: Rf 0.68 (酢酸ェチル:メタノール: 28%アンモエア水 = 80:20:3);
NMR (CDCls): δ d 0.81 (t, J=7.2 Hz, 3H), 1.10-1.50 (m, 6H), 1.82—1.98 (m, 2H), 2.00-2.12 (m, 2H), 2.42-2.50 (m, 2H), 2.50-2.70 (m, 2H), 3.75 (s, 2H), 3.84 (s, 2H), 4.45-4.70 (m, 4H), 6.98-7.10 (m, 4H), 7.35-7.85 (m, 11H)。 実施例 5 0 ( 1 0 9 ) : 4— [ ( 8—シクロへキシル一2, 8—ジァザスピ 口 [ 4 . 5 ] デカー 2—ィル) メチル] — N, N—ビス (1 H— ^ ミダゾ一 ルー 2—ィルメチル) 一 2—メ トキシベンズァミ ド (化合物 5 0 - 1 0 9 )
性状:アモルファス
TLC: Kf0.63 (クロ口ホルム:メタノール: 28%アンモニア水 = 80:20:4); NME (DMSO-De): δ 0.91-1.30 (m, 5 H), 1.36-1,60 (m, 7 H), 1.61-1.80 (m, 4 H), 2.09-2.23 (m, 1 H), 2.26 (s, 2 H), 2.33 - 2.47 (m, 6 H), 3.49 (s, 2 H), 3.63 (s, 3 H), 4.31-4.54 (m, 2 H), 4.58-4.87 (m, 2 H), 6.59—7.25 (m, 7 H), 12.04 - 12.76 (m, 2 H)。
実施例 50 (110) : 4- [ ( {4- [ (ジプロピルァミノ) メチル] ベ ンジル } ァミノ) メチル] — N, N—ビス ( 1 H— ^ f ミダゾーノレ一 2—ィノレ メチル) ベンズァミ ド (化合物 50-110)
性状:アモルファス
TLC: R£0.59 (酢酸ェチル:メタノール: 28%アンモニア水 = 50:10:1);
NME, (CDCls): δ 0.85 (t, J=7.5 Hz, 6H), 1.41-1.54 (m, 4H), 2.34-2.39 (m, 4H), 3.54 (s, 2H), 3.77 (s, 2H), 3.82 (s, 2H), 4.61 (br-s, 2H), 4,66 (br-s, 2H): 6.97 (br-s, 2H), 7.04 (br-s, 2H), 7.23-7.30 (m, 4H), 7.38 (d, J=7.8 Hz, 2H), 7.58-7.61 (m, 2H)。
実施例 50 (111) : 4— [ ( {3— [ (ジプロピルァミノ) メチル] ベ ンジル } ァミノ) メチル] 一 N, N—ビス (1 H—イミダゾール一 2—ィル メチノレ) ベンズアミド (化合物 50-111)
性状:アモルファス
TLC: Rf0.59 (酢酸ェチル:メタノール: 28%アンモニア水 = 50:10:1);
NMR (CDC13): 50.85 (t, J=7.5 Hz, 6H), 1.42-1.54 (m, 4H), 2.35- 2.40(m, 4H), 3.55 (s, 2H), 3.78 (s, 2H), 3.82 (s, 2H), 4.58 (br-s, 2H), 4,62 (br-s, 2H),
7.01 (br-s, 2H), 7.08 (br-s, 2H), 7.17-7.29 (m, 4H), 7.41 (d, J =8.1 Hz, 2H), 7.7l(d, J=8.1Hz, 2H)。
実施例 50 (112) : 3- [ {4- [ (4- { [ビス (1H—イミダゾー ル一2—ィルメチル) ァミノ] カルボ二ル} ベンジル) ァミノ] シクロへキ シル } (プロピル) ァミノ] プロパン酸 (高極性体) (化合物 50— 112) 性状:アモルファス
TLC: Rf0.24 (ジクロロメタン:メタノール: 28%ァンモニァ水 = 80:20:2); NMR (DMSO-De): δ d 0.81 (t, J=7.5 Hz, 3H), 0:95—1.12 (m, 2H), 1.15—1.32 (m, 2H), 1.32-1.48 (m, 2H), 1.60-1.72 (m, 2H), 1.85-1.98 (m, 2H), 2.16 (t, J=7.2 Hz, 2H), 2.25 (m, 1H), 2.43 (t, J = 7.2 Hz, 2H), 2.56 (m, 1H), 2.69 (t, J=6.6 Hz, 2H), 3.70 (s, 2H), 4.45-4.68 (m, 4H), 6.90-7.08 (m, 4H), 7.32 (d, J=8.4 Hz, 2H), 7.42 (d, J=8.4Hz, 2H)。
実施例 50 (113) : N, N—ビス (1H— ^ f ミダゾ一ルー 2—ィルメチ ノレ) 一 4一 { [8— (3—メチルー 2—プテン一 1一ィル) 一 2, 8—ジァ ザスピロ [4. 5] デカー 2—ィル] メチル } ベンズアミ ド (化合物 50— 113)
性状:アモルファス
TLC: R 0.44 (メタノール: 28%ァンモユア水 = 98:2);
NMR (CDCls): δ 1.49-1.66 (m, 9 H), 1.72 (s, 3 H), 2.21-2.46 (m, 6 H), 2.55 (t, J=6.9 Hz, 2 H), 2.92 (d, J=6.9 Hz, 2 H), 3.57 (s, 2 H), 4.52-4.73 (m, 4 H) 5.15-5.33 (m, 1 H), 6.86-7.14 (m, 4 H), 7.36 (d, J=8.1 Hz, 2 H), 7.61 (d,
9Z
(H Z 'πι) 69 Ζ-6Ψ Ζ '(Η 6 ' 'Z-l£'Z '(Η 9 '^) Ψ9'Τ-Ζ Ί 9: (δΐθαθ) ΗΗΝ 厶 士 :翻
(911- ST
8 'Ζ - [ Ζ -Λ (-^ ^ - 9 ) ] -8} ) 一 一 {Λ(
y- \) ^ -N 'Ν : (9 τ τ) ο s ¾¾
°(Η ^ <ΖΗ Γ8=Γ 'Ρ) 69"Λ '(Η
Ζ 'ZH VS= 'Ρ) 9£ L '(Η f 9Γム- '(Η f '∞) LLy-09' '(Η Ζ 's) L9'2 OT '(Η Ζ ( 99= ') Ψ9 Ζ '(Η 9 682-912 '(Η Ζ ' 9"9=Γ 'Ρ) 80 S '(Η 9 <ra) 89 Τ-8Π '(Η S ) 9^ I-QX I '(Η 9 '^Η Ζ'ί=ΐ '%) 8809: (8ΐθαθ) ¾ΗΝ
- (2:86 =氺 ご べ %8 / ^γ^) 82 ί3:ΟΊ
4A3r :
( τ τ一 ο 9 λ\) χベ {Λ( =≠^ - ζ—へ (一/、
-Hl) ー Ν 'Ν- {Λ(~^^ [9 ' ] ^\^ ^ ^一 8 'z- { (4^^Λ(^-Ζ) -8] } - · ( τ τ) ο g mm
9909T0/S00Zdf/X3d
3.52-3.63 (m, 4 H), 4.58-4.71 (m, 4 H), 6.52-6.59 (m, 1 H), 6.62-6.68 (m, 1 H), 6.95-7.09 (m, 4 H), 7.31-7.40 (m, 2 H), 7.56-7.65 (m, 2 H)。
実施例 50 (116) : 4一 ( {8— [ (5—クロロー 2—チエ-ノレ) メチ ル] —2, 8—ジァザスピロ [4. 5] デカー 2—ィル } メチル) 一 N, N 一ビス ( 1 H—イミダゾールー 2—イノレメチル) ベンズァミ ド (化合物 50 -116)
性状:アモルファス
TLC: Rf 0.40 (メタノール: 28%アンモニア水 = 98:2);
NMR (CDCls): δ 1.52-1.65 (m, 6 H), 2.29-2.43 (m, 6 H), 2.47-2.60 (m, 2 H): 3.51-3.61 (m, 4 H), 4.58-4.71 (m, 4 H), 6.60-6.66 (m, 1 H), 6.67-6.74 (m, 1 H), 6.95-7.09 (m, 4 H), 7.31-7.41 (m, 2 H), 7.55-7.65 (m, 2 H)。
実施例 50 (117) : N, N—ビス (1 H—イミダゾーノレ一 2—イノレメチ ル) -4- { [8— (1, 3—チアゾールー 2—ィルメチル) 一 2, 8—ジ ァザスピロ [4. 5] デカー 2—ィル] メチル } ベンズアミ ド (化合物 50 -117)
性状:アモルファス
TLC: Rf 0.41 (メタノール: 28%ァンモユア水 = 98:2);
NMR (CDC13): 81.54-1.67 (m, 6 H), 2.34 (s, 2 H), 2.43-2.58 (m, 6 H), 3.58 (s, 2 H), 3.79 (s, 2 H), 4.58-4.70 (m, 4 H), 6.94-7.08 (m, 4 H), 7.22-7.28 (m, 1 H), 7.30-7.40 (m, 2 H), 7.56-7.65 (m, 2 H), 7.65-7.71 (m, 1 H)。
実施例 50 (118) : N, N—ビス (1H— ^ f ミダゾ一ルー 2—ィルメチ ル) 一 4一 { [8— (1, 3—ォキサゾール— 2—ィルメチル) 一 2, 8—
ジァザスピロ [4. 5] デカ一 2—ィノレ] メチノレ } ベンズアミ ド (化合物 5
0-118)
性状:アモルファス
TLC:Ef 0.41 (メタノール: 28%アンモニア水 =98:2);
NME, (CDC13): δ 1.54-1.67 (m, 6 H), 2.32 (s, 2 H), 2.37-2.49 (m, 4 H), 2.49-2.57 (m, 2 H), 3.57 (s, 2 H), 3.65 (s, 2 H), 4.57-4.69 (m, 4 H),
6.95-7.09 (m, 5 H), 7.31-7.39 (m, 2 H), 7.57-7.66 (m, 3 H)。
実施例 50 (119) : 3—クロ口一 4一 ( { [トランス一 4一 (ジプロピ ノレァミノ) シクロへキシル] アミノ} メチノレ) 一 N, N—ビス (1H—イミ ダゾール一 2—ィルメチル) ベンズァミド (化合物 50-119)
性状:油状物
TLC: Rf 0.49 (クロ口ホルム:メタノール: 28%アンモニア水 = 40:10:2); NMR (METHANOL- D
4): 50.77-0.93 (m, 6 H), 1.04-1.54 (m, 8 H), 1.68-1.92 (m, 2 H), 1.96-2.14 (m, 2 H), 2.26 - 2.59 (m, 6 H), 3.83-3.93 (m, 2 H), 4.31-4.87 (m, 4 H), 7.01 (s, 4 H), 7.33-7.51 (m, 2 H), 7.55 (s, 1 H)。 実施例 50 (120) : 3—クロロー 4一 [ (8—シクロへキシル一2, 8 ージァザスピロ [4. 5] デカー 2—ィル) メチル] — N, N—ビス (1H ーィミダゾールー 2—ィルメチル) ベンズァミド (化合物 50— 120)
性状:ァモノレファス
TLC:Rf0.49 (クロロホルム:メタノール: 28%アンモニア水 =40:10:2); NMR (METHANOL - D4): δ 1.01-1.35 (m, 6 H), 1.46-1.70 (m, 6 H), 1.72-1.83 (m, 2 H), 1.85-1.99 (m, 2 H), 2.15-2.36 (m, 1 H), 2.40-2.76 (m, 8 H), 3.60-3.93 (m, 2 H), 4.33-4.85 (m, 4 H), 6.80 - 7.22 (m, 4 H), 7.34-7.46 (m, 1 H), 7.47-7.65 (m, 2 H)。
実施例 50 (121) : 4— [ (8—シクロォクチルー 2 , 8ージァザスピ 口 [4. 5] デカー 2—ィル) メチノレ] — N, N—ビス (1H—イミダゾー ルー 2—イノレメチノレ) ベンズァミド (化合物 50-121)
性状:ァモルファス
TLC: Rf 0.22 (メタノール: 28%アンモニア水 - 98:2);
NMR (CDCla): 61.40-1.75 (m, 18 H), 2.31-2.60 (m, 11 H), 3.59 (s, 2 H),
4.55-4.69 (m, 4 H), 6.94-7.10 (m, 4 H), 7.31-7.41 (m, 2 H), 7.59-7.68 (m, 2
H)。
実施例 50 (122) : N, N—ビス (1 H f ミダゾールー 2一ィルメチ ル) -4- [ (8—メチル一2, 8—ジァザスピロ [4. 5] デカー 2—ィ ル) メチル] ベンズァミド (化合物 50-122)
G9Z
^ ^ : 9Ζ (Q Z X - O Q呦^ ¾ ^ ぺ。、,ci (
( ^ ^a^) — 一 44] } — ε : (s ζ τ) o Μ^
°(Η 19 L-6 L '(Η f 60· - 00·ム '(H f 'ΪΠ) S8 ^-6S^ '(H Z 's) ΐ8·ε '(H Z 's) 9S S '(H < a) 988-ST 8 Z (H Z '∞) 6 S '(H Z 'ra) 2 '(H 9 '^ 86 X-6L T 9: (eTOaO) HHN
- 86 = ^ -^ %SZ: — " SS OJH :0Ί
/; /士 : ^¾
O s τ— 0 s λΥ) i^ - 8 - ^ [9 a。3 ^ — 8 'Ζ - ( ^^ / [ ( /^ ST 一 s— /— /ゝ、 ^一 Ητ) } 一,) 一 s] : ( ζ τ) 0 g mm^
°(H Z 'τπ) Ld'L-9 'L '(Η Z ' -OS'ム '(Η t 'TO) L0 L-Z6'9 XB.f '∞) Wt— 09· '(H 9 '∞) W£-9Z £ '(Η Z '∞) 89^-8 2
'(H Z '∞) WZ~l^Z '(H 8 's) 90 Z '(H 9 '^) 91Ί- 0919: ( οαθ) ΉΜΝ
• (Z-.86 =氺 - ¾ %sz: 4/— r ^^) WQ .ΟΊ OX ム 4 ·3Γ : ¾†v¾
(ε ζ τ -o 9 ψλ\) ペ ( ^
一 s— /— 、、 一 Ητ)
[g
- - (ε s τ) o Q醒牽
°(H Z ' 99·ム- ss^ e '(H Z ) ZVL-0£-L '(H <ra) 0Γム- S69 '(H <ni) '(H Z 's) 098
(H Z <ra) WZ- YZ '(H 6 'we) WZ-QTZ '(H 9 '∞) 99 T-8S T 9: (εΙθαθ) ¾HN
- (Z:S6 = -^ X%SZ: Λ (-^ , : Ί1
9909l0/S00Zdf/X3d 1^H0/900 OAV
NMR (CDGla): δ 0.85 (t, J=7.2 Hz, 6H), 1.00-1.48 (m, 8H), 1.74-1.84 (m, 2H), 1.90-2.00 (m, 2H), 2.30-2.50 (m, 6H), 2.72 (t, J=6.0 Hz, 2H), 2.92 (t, J=6.0 Hz, 2H), 4.64 (s, 2H), 4.69 (s, 2H), 6.96 (s, 4H)。
実施例 50 (126) : 3— (8—シクロへキシルー 2, 8—ジァザスピロ [4. 5] デカー 2—ィル) 一 N, N—ビス (1H—イミダゾールー 2—ィ ルメチル) プロパンアミド (化合物 50- 126)
性状:アモルファス
TLC:Rf 0.61 (ジクロロメタン:メタノール:アンモユア水 =40:10:1); NME, (CDCls): 51.00-1.34 (m, 6H), 1.59-1.73 (m, 6H), 1.78-1.85 (m, 2H), 1.88-1.97 (m, 2H), 2.48 (m, IH), 2.56 (s, 2H), 2.58-2.70 (m, 4H), 2.77 (t, J=6.9 Hz, 2H), 2.81 (t, J=6.6 Hz, 2H), 2.91 (t, J=6.9 Hz, 2H), 4.67 (s, 2H), 4.71 (s, 2H), 6.99 (s, 4H)。
実施例 50 (127) : 4- (8—シクロへキシルー 2, 8—ジァザスピロ
[4. 5] デカー 2—ィル) 一 N, N—ビス (1H—イミダゾール一 2—ィ ルメチル) ブタンァミ ド (化合物 50- 127)
性状:アモルファス
TLC:Rf 0.57 (ジクロロメタン:メタノール:アンモニア水 =40:10:1);
NME (CDCls): δ 1.03-1.44 (m, 8H), 1.63-1.73 (m, 2H), 1.79 - 2.10 (m, 10H)
2.64 (t, J=6.9 Hz, 2H), 2.70 (s, 2H), 2.78—2.94 (m, 5H), 3.02 (t, J=6.9 Hz, 2H), 4.72 (s, 2H), 4.76 (s, 2H), 6.99 (s, 2H), 7.00 (s, 2H)。
実施例 50 (128) : 5- (8—シクロへキシルー 2, 8—ジァザスピロ [4. 5] デカー 2—ィノレ) 一 N, N—ビス (1 H—イミダゾール一 2—ィ ルメチル) ペンタンァミド (化合物 50— 128)
性状:アモルファス
TLC:Rf 0.60 (ジクロロメタン:メタノール:アンモニア水 =40:10:1) ;
NMR (CDC13): δ 1.06—1.50 (m, 8H), 1.58-1.76 (m, 4H), 1.84-1.96 (m, 4H),
2.00-2.20 (m, 4H), 2.47 (t, J=6.6 Hz, 2H), 2.80-3.18 (m, IIH), 4.80 (s, 2H), 4.82 (s, 2H), 7.00 (s, 2H), 7.02 (s, 2H)。
実施例 50 (129) : 4— [ ( {4— [ (4, 4ージフルォロシクロへキ シル) ァミノ] シクロへキシル } ァミノ) メチル] 一 N, N—ビス (1H— イミダゾールー 2一ィルメチル) ベンズァミド (低極性体) (化合物 50— 129)
性状:アモルファス
TLC:Rf 0.38 (酢酸ェチル:メタノール: 28%アンモニア水 = 80:20:3); NMR (CDCla): δ d 1.40-2.20 (m, 16H), 2.65-2.80 (m, 3H), 3.79 (s, 2H), 4.52-4.72 (m, 4H), 6.95-7.12 (m, 4H), 7.37 (d, J=8.1 Hz, 2H), 7.62 (d, J=8.1 Hz, 2H)0
実施例 50 (130) : 4一 [ ( {4— [ (4, 4ージフルォロシクロへキ シル) ァミノ] シク口へキシル } ァミノ) メチル] 一 N, N—ビス (1 H- ィミダゾールー 2—ィルメチル) ベンズァミド (高極性体) (化合物 50- .130)
性状:アモルファス
TLC: Rf0.28 (酢酸ェチル:メタノール: 28%アンモニア水 = 80:20:3); NMR (CDCls): 6 d 1.00-2.20 (m, 16H), 2.40-3.00 (m, 3H), 3.84 (s, 2H), 4.50-4.70 (m, 4H), 6.95-7.12 (m, 4H), 7.38 (d, J=8.1 Hz, 2H), 7.67 (d, J=8.1 Hz, 2H)。
実施例 50 (131) : (2E) —3— {4一 〔 (8—シクロへキシル一 2, 8—ジァザスピロ [4. 5] デカー 2—^ fル) メチノレ] フエ-ル} 一 N, N 一ビス (1H—イミダゾールー 2—ィルメチル) アクリルアミド (化合物 5 0-131)
性状:アモルファス
TLC: Rf0.60 (齚酸ェチル:メタノール:アンモユア水 = 50:10:1);
NMR (GDCls): 51.05-2.33 (m, 16H), 2.44-2.57 (m, 9H), 3.56 (s, 2H), 4.80 (br-s, 2H), 4.90 (br-s, 2H), 6.99 (br-s, 2H), 7.01 (br-s, 2H), 7.08 (d, J=15.3 Hz, 1H), 7.29 (d, J=6.9 Hz, 2H), 7.45 (d, J=6.9 Hz, 2H), 7.61 (d, J=15.3 Hz, 1H)。
実施例 50 (132) : (2 E) — 3— [4— ( ί [トランス一 4一 (ジブ 口ピルァミノ) シクロへキシノレ] ァミノ) メチノレ) フエニル] —Ν, Ν—ビ ス (1H—イミダゾールー 2—ィルメチル) アクリルアミド (化合物 50— 132)
性状:アモルファス
TLC: Rf 0.59 (酢酸ェチル:メタノール:アンモユア水 = 50:10:1);
NMR (CDCls): δ 0.85 (t, J=7.5 Hz, 6H), 1.06-1.50 (m, 8H), 1.80-1.83 (m, 2H), 1.98-2.02 (m, 2H), 2.37-2.51 (m, 6H), 3.79 (s, 2H) , 4.79 (br-s, 2H), 4.89 (br-s, 2H), 7.00 (br-s, 4H), 7.07 (d, J=15.3 Hz, 1H), 7.27 (d, J=8.4Hz, 2H), 7.45 (d, J=8.4Hz, 2H), 7.59 (d, J=15.3 Hz, 1H)。
実施例 50 (133) : 3— {4— [ (8—シクロへキシル一2, 8—ジァ ザスピロ [4. 5]デカー 2—ィル) メチル] フエ二/レ} 一 N, N—ビス (1 H—イミダゾール— 2—ィルメチル) プロパンアミ ド (化合物 50-133)
性状:アモルファス
TLC: Rf 0.55 (酢酸ェチル:メタノール:アンモニア水 = 50:10:1);
NMR (CDCls): δ 1.05-1.27 (m, 6H), 1.57-1.63 (m, 8H), 1.70-1.80 (m, 2H), 1.85-1.90 (m, 2H), 2.28 (m, 1H), 2.45-2.57 (m, 6H), 2.76-2.88 (m, 4H), 3.49 (s, 2H), 4.48 (br-s, 2H), 4.56 (br-s, 2H), 6.97 (br-s, 2H), 6.98 (br-s, 2H), 7.01 (d, J=8.1 Hz, 2H), 7.12 (d, J=8.1 Hz, 2H)。
実施例 5 0 ( 1 3 4 ) : 3— [4— ( { [トランス一 4一 (ジプロピルァミ ノ) シクロへキシル] アミノ} メチノレ) フエ二ノレ] 一 N, N—ビス (1 H— イミダゾーノレ一 2—ィルメチル) プロパンアミ ド (化合物 5 0— 1 3 4 ) 性状:アモルファス
TLC: Rf 0.56 (酢酸ェチル:メタノール:アンモニア水 = 50:10:1);
NMR (CDCla): 50.86 (t, J=7.5 Hz, 6H), 1.10-2.03 (m, 12H), 2.39-2.51 (m,
6H), 2.76-2.85 (m, 4H), 3.74 (s, 2H), 4.46 (br-s, 2H), 4.52 (br-s, 2H), 6.97 (br-s, 2H), 6.98 (br-s, 2H), 7.02 (d, J=8.1 Hz, 2H), 7.12 (d, J=8.1 Hz, 2H)。 実施例 5 0 ( 1 3 5 ) : 2 - { 4 - [ ( 8—シクロへキシル一 2 , 8—ジァ ザスピロ [ 4 . 5 ] デカ一 2—ィル) メチル] フエ二ル} — N, N—ビス (1 H—イミダゾールー 2—ィルメチル) ァセトアミ ド (化合物 5 0— 1 3 5 ) 性状:アモルファス
TLC: Rf 0.59 (酢酸ェチル:メタノ一ノレ:アンモニア水 = 50:10:1);
NME (CDCla): δ 1.10-1.30 (m, 6H), 1.59-2.02 m, 14B), 2.44 - 2.63 (m, 5H), 3.54 (s, 2H), 3.79 (s, 2H), 4.64 (br-s, 2H), 4.73 (br-s, 2H), 6.98 (br-s, 2H), 6.99 (br-s, 2H), 7.13 (d, J=8.1 Hz, 2H), 7.23 (d, J=8.1 Hz, 2H)。
実施例 50 (136) : 2— [4— ( { [トランス一 4— (ジプロピルァミ ノ) シクロへキシノレ] ァミノ) メチノレ) フエエル] 一 N, N—ビス (1H— ィミダゾール一 2—ィルメチル) ァセトアミド (化合物 50— 136) 性状:ァモルファス
TLC: f0.57(酢酸ェチル:メタノール:アンモユア水 =50:10:1);
NMR (CDC13): δ 0.86 (t, J=7.5 Hz, 6H), 1.09-1.49 (m, 8H), 1.81-1.85 (m, 2H), 2.00-2.04 (m, 2H), 2.40-2.52 (m, 6H), 3.76 (s, 2H), 3.78 (s, 2H), 4.61 (br-s, 2H), 4.72 (br-s, 2H), 6.97 (br-s, 2H), 7.00 (br-s, 2H), 7.11 (d, J=8.1 Hz, 2H), 7.21 (d, J=8.1 Hz, 2H)。
実施例 50 (137) : 4- { [8- (シクロブチルメチル) 一 2, 8—ジ ァザスピロ [4. 5] デカー 2—ィル] メチル } — N, N—ビス (1H—ィ ミダゾールー 2一ィルメチル) ベンズァミド (化合物 50— 137)
性状:アモルファス
TLC: Rf 0.34 (メタノール: 28%アンモニア水 = 98:2);
NMR (CDC13): δ 1.57-1.90 (m, 10 H), 1.96-2.11 (m, 3 H), 2.31-2.46 (m, 7 H), 2.50-2.62 (m, 3 H), 3.58 (s, 2 H), 457-4.71 (m, 4 H), 6.93-7.08 (m, 4 H) 7.29-7.39 (m, 2 H), 7.54-7.64 (m, 2 H)。
実施例 50 (138) : 4- [ ( {4- [ (4, 4ージフルォロシクロへキ シル) (プロピル) ァミノ] シクロへキシル } ァミノ) メチル] — N, N- ビス ( 1 H—イミダゾーノレ一 2—イノレメチノレ) ベンズァミ ド (低極性体) (化 合物 50- 138)
性状:ァモノレファス
TLC: Rf0.73 (酢酸ェチル:メタノール: 28%アンモニア水 = 80:20:3); NME (CDCls): 60.82 (t, J, 7.5 Hz, 3H), 1.30-1.84 (m, 16H), 2.00-2.20 (m, 2H), 2.43 (t, J, 7.5 Hz, 2H), 2.54 (m, 1H), 2.72 (m, 1H), 2.76 (m, 1H), 3.77 (s, 2H), 4.60-4.80 (m, 4H), 6.95-7.12 m, 4H), 7.37 (d, J= 8.4 Hz, 2H), 7.51 (d, J=8.4 Hz, 2H)。
実施例 50 (139) : 4一 [ ( {4一 [ (4, 4ージフルォロシク口へキ シル) (プロピル) ァミノ] シクロへキシル } ァミノ) メチノレ] 一 N, N— ビス ( 1 H—イミダゾールー 2—ィルメチル) ベシズァミド(高極性体) (化 合物 50— 139)
性状:アモルファス
TLC: Rf 0.60 (酢酸ェチル:メタノール: 28%アンモニア水 = 80:20:3);
MR (CDCls): 5 d 0.82 (t, J = 7.5 Hz, 3H), 1.02—1.90 (m, 14H), 1.92-2.20 (m, 4H), 2.38 (m, 1H), 2.40 (t, J, 7.5 Hz, 2H), 2.52 (m, 1H), 2.64 (m, 1H), 3.81 (s, 2H), 4.60-4.80 (m, 4H), 6.98-7.12 (m, 4H), 7.34 (d, J=8.1 Hz, 2H), 7.52 (d, J=8.1Hz,2H)。
実施例 50 (140) : 4- ( { [4- (1—ァゾカ二ル) シクロへキシル] ァミノ) メチル) 一 N, N—ビス (1H—イミダゾールー 2—ィルメチル) ベンズァミド (低極性体) (化合物 50— 140)
性状:アモルファス
TLC: Rf0.53 (酢酸ェチル:メタノール: 28%アンモニア水 = 90:10:2);
NMR (CDCls): δ d 1.40-1.82 (m, 18H), 2.41 (m, IH), 2.55-2.70 (m, 4H), 2.73 (m, IH), 3.78 (s, 2H), 4.60-4.80 (m, 4H), 6.98-7.12 (m, 4H), 7.37 (d, J=8.1 Hz, 2H), 7.53 (d, J, 8.1 Hz, 2H)。
実施例 50 (141) : 4一 ( { [4一 (1一ァゾカニル) シクロへキシル] アミノ} メチル) 一 N, N—ビス (1 H—イミダゾールー 2—ィルメチル) ベンズァミ ド (高極性体) (化合物 50-141)
性状:アモルファス
TLC: Rf 0.37 (酢酸ェチル:メタノール: 28%ァンモユア水 二 90:10:2); NMR (CDCls): δ d 1.04-1.38 (m, 4H), 1.45-1.68 (m, 10H), 1.75-1.88 (m, 2H), 1.92-2.08 (m, 2H), 2.32-2.48 (m, 2H), 2.50-2.68 (m, 4H), 3.81 (s, 2H), 4.58-4.78 (m, 4H), 6.92-7.12 (m, 4H), 7.33 (d, J=8.1 Hz, 2H), 7.53 (d, J = 8.1Hz, 2H)。
実施例 50 (142) : 4— ( { [ (2E) —4— (ジェチルァミノ) 一 2 ーブテン一 1一ィル] アミノ} メチノレ) 一 N, N—ビス (1H—イミダゾー ルー 2—ィルメチル) ベンズァミ ド (化合物 50— 142)
性状:油状物
TLC: M 0.26 (メタノール: 28%アンモユア水 = 98:2);
NMR (CDC13): 51.02 (t, J=6.9 Hz, 3 H), 1.10 (t, J = 7.2 Hz, 3 H), 2.48 (q, J = 6.9 Hz, 2 H), 2.64 (q, J = 7.2 Hz, 2 H), 3.03 (d, J = 4.8 Hz, 2 H), 3.22 (d, J = 4.8 Hz, 2 H), 3.55 (s, 2 H), 4.64 (m, 4 H), 5.64 (m, 2 H), 7.01 (m, 4 H),
7.37 (d, J = 8.1 Hz, 2 H), 7.59 (d, J = 8.1 Hz, 2 H)。
実施例 50 (143) : N, N—ビス (1H—イミダゾールー 2—ィルメチ ノレ) 一 4一 { [8- (2, 2, 6, 6—テトラメチルー 4ーピペリジニル) -2, 8—ジァザスピロ [4. 5] デカー 2—ィル] メチル } ベンズアミド
(化合物 50-143)
性状:アモルファス
TLC: Rf0.25 (メタノール: 28%アンモニア水 = 98:2);
NMR (CDCls): δ 1.05 (t, J = 12.3 Hz, 2 H), 1.12 (s, 6 H), 1.18 (s, 6 H),
1.51-1.66 (m, 6 H), 1.74 (dd, J = 12.3, 3.0 Hz, 2 H), 2.33 (s, 2 H), 2.37-2.63
(m, 6 H), 2.68-2.87 (m, 1 H), 3.58 (s, 2 H), 4.51-4.76 (m, 4 H), 6.86-7.16 (m
4 H), 7.38 (d, J = 8.1 Hz, 2 H), 7.64 (d, J = 8.1 Hz, 2 H)。
実施例 50 (144) : 4— [ (7—シクロへプチルー 2, 7—ジァザスピ 口 [3. 5] ノナ一 2—ィル) メチル] 一 N, N—ビス (1H—イミダゾ一 ルー 2—ィルメチル) ベンズァミ ド (化合物 50-144)
性状:アモルファス
TLC: Rf0.34 (メタノール: 28%ァンモ -ァ水二 98:2);
NMR (CDCls): 61.24-1.86 (m, 16 H), 2.30-2.45 (m, 4H), 2.44-2.59 (m, 1 H), 2.99 (s, 4 H), 3.63 (s, 2 H), 4.49-4.73 (m, 4 H), 6.88 - 7.15 (m, 4 H), 7.32 (d, J = 8.1 Hz, 2 H), 7.62 (d, J = 8.1 Hz, 2 H)0
実施例 50 (145) : 4一 [ (5—シクロへプチルー 2, 5—ジァザビシ クロ [2. 2. 1] ヘプター 2—ィル) メチル] — N, N—ビス (1H—ィ ミダゾールー 2—ィルメチル) ベンズァミ ド (化合物 50-145)
性状:アモルファス
TLC: Rf 0.38 (メタノール: 28%アンモエア水 = 98:2);
NMR (CDCls): 8 1.19-1.88 ( , 14 H), 2.42-2.62 (m, 3 H), 2.82 (d, J = 9.6 Hz, 1 H), 2.96 (dd, J = 9.6, '2.7 Hz, 1 H), 3.21 (s, 1 H), 3.56 (s, 1 H), 3.66 (d, J = 13.9 Hz, 1 H), 3.76 (d, J = 13.90 Hz, 1 H), 4.51-4.77 (m, 4 H), 6.89-7.16 (m, 4 H), 7.41 (d, J = 8.1 Hz, 2 H), 7.64 (d, J = 8. l Hz, 2 H)。
実施例 5 0 ( 1 4 6 ) : 4— ( { [ ( 1—シクロへプチルー 4ーピベリジ- ル) メチノレ] アミノ} メチル) 一 N, N—ビス ( 1 H—ィミダゾールー 2 - ィルメチル) ベンズァミ ド (化合物 5 0 - 1 4 6 )
性状:アモルファス
TLC: Rf 0.30 (メタノ一ノレ: 28%ァンモユア水 = 98:2);
NMR (CDCls): 5 1.08-1.90 (m, 17 H), 2.12-2.31 (m, 2 H), 2.47 (d, J = 6.9
Hz, 2 H), 2.50-2.61 (m, 1 H), 2.69 - 2.87 (m, 2 H), 3.77 (s, 2 H), 4.46-4.76 (m 4 H), 6.86-7.14 (m, 4 H), 7.30-7.43 (m, 2 H), 7.54-7.70 (m, 2 H)0
実施例 5 0 ( 1 4 7 ) : 3— [ { 4一 [ ( 4— { [ビス (1 H—イミダゾー ルー 2—ィルメチル) ァミノ] カノレポ-ル} ベンジル) ァミノ] シクロへキ シル } (プロピル) ァミノ] プロパン酸 (低極性体) (化合物 5 0— 1 4 7 ) 性状:アモルファス
TLC: Rf 0.47 (ジクロロメタン:メタノール: 28%アンモユア水 = 80:20:2) ; NMR (DMSO-De): δ d 0.84 (t, J=7.5 Hz, 3H), 1.22-1.82 (m, 10H), 2.21 (t, J=6.6 Hz, 2H), 2.53 (m, 2H), 2.60-2.75 (m, 2H), 2.78 (t, J, 6.6 Hz, 2H), 3.66 (s, 2H), 4.50-4.68 (m, 4H), 6.90-7.08 (m, 4H), 7.35 (d, J = 8.1 Hz, 2H),
7.43(d, J=8.1Hz, 2H)。
実施例 51 (1) 〜実施例 51 (2)
実施例 16の工程において、 1一 (1— { [2- (トリメチルシリノレ) ェ トキシ] メチル } 一 1 H—イミダゾールー 2—ィル) メタンァミンまたはそ の代わりに相当するァミン化合物を、 実施例 17の工程において、 1H—ィ ミダゾ一/レー 2一力ルボン酸またはその代わりに相当するカルボン酸を、 実 施例 19の工程において、 N, N—ジプロピノレー 1, 4ープタンジァミンま たはその代わりに相当するァミンを用いて、 実施例 16→実施例 17→実施 例 18→実施例 19と同様の操作をして、 以下の物性値を有する標題化合物 を得た。
実施例 51 (1) : N- ( 1 H—ベンゾィミダゾールー 2—ィルメチル) 一 N— {4- [ (8—シクロへキシノレ一 2, 8—ジァザスピロ [4. 5] デカ 一 2—ィル) メチル] ベンジル } 一 1 H—イミダゾールー 2一力ルポキサミ ド (化合物 51-1)
性状:アモルファス
TLC: Rf 0.32 (メタノール: 28%アンモニア水 = 98:2);
NMR (DMSO-de): δ 1.06-1.19 (m, 5 H), 1.40-1.56 (m, 7 H), 1.61-1.74 (m, 4 H), 2.12-2.20 (m, 1 H), 2.22-2.28 (m, 2 H), 2.32-2.47 (m, 6 H), 3.48 (s, 2 H), 4.61-4.74 (m, 2 H), 5.57-5.69 (m, 2 H), 7.11-7.26 (m, 8 H), 7.43-7.55 (m, 2 H)o
実施例 51 (2) : N— ( 1 H—ベンゾィミダゾール一 2一ィルメチル) 一
N— {4— [ ( {トランス一 4一 [シクロへキシル (プロピル) ァミノ] シ クロへキシノレ } ァミノ) メチル〕 ベンジル } — 1 H—イミダゾールー 2—力 ルポキサミド (化合物 51— 2)
性状:アモルファス
TLC: Rf 0.28 (メタノール: 28%アンモニア水 = 98:2);
NMR (DMSO-de): δ 0.73-0.83 (m, 3 H), 0.97-1.10 (m, 4H), 1.13-1.29 (m,
7 H), 1.53-1.69 (m, 7 H), 1.85-1.98 (m, 2 H), 2.21-2.31 (m, 1 H), 2.35-2.45
(m, 4H), 3.67 (s, 2 H), 4.62-4.73 (m, 2 H), 5.56—5.69 (m, 2 H), 7.09-7.17 (m 3 H), 7.20-7.31 (m, 5 H), 7.41-7.57 (m, 2 H)。
実施例 52 (1) 〜実施例 52 (4)
[ 1一 (tert-プトキシカルボ-ル) 一 4一ピぺリジ -ル] 酢酸の代わりに 相当するカルボン酸を用いて実施例 44→実施例 45→実施例 46と同様の 操作をし、 以下の物性値を有する標題化合物を得た。
実施例 52 (1) : 3— { 1— [3- (ジブ口ピルァミノ) プロピル] ピぺ リジン一 4一^ fM 一 N, N—ビス ( 1 H—イミダゾールー 2—ィルメチル) プロパンアミ ド (化合物 52— 1)
性状:アモルファス
TLC: Ef 0.84 (クロ口ホルム:メタノール: 28%ァンモニァ水 = 40:10:2); NMR (METHANOL- D4): δ 0.89 (t, J=7.2 Hz, 6 H), 1.09-1.36 (m, 3 H),
1.36-1.55 (m, 6 H), 1.57-1.71 (m, 4 H), 1.83-1.98 (m, 2 H), 2.25-2.34 (m, 2 H), 2.35-2.51 (m, 8 H), 2.84-2.97 (m, 2 H), 4.66 (s, 2 H), 4.70 (s, 2 H), 6.96 (s, 2 H), 7.02 (s, 2 H)。
実施例 52 (2) : 1一 [6- (ジプロピルァミノ) へキシル] 一 N, N— ビス (1H— ^ f ミダゾ一ノレ一 2—^ fルメチル) ピぺリジン一 4一力ルポキサ ミド (化合物 52-2)
性状:油状物
TLC:Rf 0.73 (クロ口ホルム:メタノール: 28%ァンモユア水 = 40:10:2); NMR (METHANOL— D4>: δ 0.88 (t, J=7.5 Hz, 6 H), 1.16-1.36 (m, 6 H), 1.39-1.59 (m, 8 H), 1.60-1.84 (m, 2 H), 1.86-2.06 (m, 2 H), 2.22 - 2.33 (m, 2 H), 2.36-2.55 (m, 6 H), 2.57-2.77 (m, 1 H), 2.82—3.00 (m, 2 H), 4.66 (s, 2 H) 4.75 (s, 2 H), 6.97 (s, 2 H), 7.03 (s, 2 H)。
実施例 52 (3) : 4— { [トランス一 4— (ジプロピルァミノ) シクロへ キシル] ァミノ) 一 N, N—ビス (1H—イミダゾールー 2—ィルメチル) ブタンアミ ド (化合物 52- 3)
性状:アモルファス
TLC: RfO.39 (ジクロロメタン:メタノール: 28%アンモニア水 =40:10:1);
NMR (CDGla): δ 0.88 (t, J=7.2 Hz, 6H), 1.32-1.68 (m, 8H), 1.90-2.04 (m,
2H), 2.13-2.24 (m, 2H), 2.47-2.79 (m, 9H), 2.86 - 3.03 (m, 3H), 4.69 (s, 2H),
4.72 (s, 2H), 6.94 (s, 2H), 6.97 (s, 2H)。
実施例 5 2 (4) : 5— { [トランス一 4一 (ジプロピルァミノ) シクロへ キシル] アミノ} 一 N, N—ビス (1 H—イミダゾールー 2—ィルメチル) ペンタンアミ ド (化合物 5 2-4)
性状:アモルファス
TLC: RfO.39 (ジクロロメタン:メタノール: 28%アンモニア水 = 40:10:1); NMR (CDCla): 80.88 (t, J=7.2 Hz, 6H), 1.29—1.81 (m, 10H), 1.90—2.00 (m, 2H), 2.12-2.22 (m, 2H), 2.41-2.53 (m, 6H), 2.60-2.72 (m, 3H), 2.78-2.93 (m, 3H), 4.71 (s, 4H), 6.96 (s, 2H), 6.98 (s, 2H)。
実施例 5 3 : 1— {4一 [ (8—シク口へキシル一 2, 8ージァザスピロ [4. 5] デカー 2—ィル) メチノレ] フエ二ル} — N, N—ビス (1H—イミダゾ 一ルー 2—ィルメチル) メタンァミン (化合物 5 3 )
実施例 1 6の工程において、' 1一 (1 - { [2- (トリメチノレシリノレ) ェ
16066
トキシ] メチル } 一 1H—イミダゾールー 2—ィル) メタンァミンまたはそ の代わりに相当するァミン化合物を用いて、 実施例 16→実施例 18→実施 例 19と同様の操作をし、 以下の物性値を有する標題化合物を得た。
性状:アモルファス
TLC: Rf 0.22 (クロ口ホルム:メタノール: 28%アンモニア水 - 80:10:1);
NMR (DMSO-De): δ 0.92-1.28 (m, 5 H), 1.35-1.60 (m, 7 H), 1.61-1.77 (m, 4 H), 2.10-2.23 (m, 1 H), 2.25 (s, 2 H), 2.32-2.48 (m, 6 H), 3.44-3.51 (m, 4 H), 3.55 (s, 4 H), 6.72-7.16 (m, 4 H), 7.21 (d, J=7.80 Hz, 2 H), 7.32 (d, J=7.80 Hz, 2 H), 11.61-12.37 (m, 2 H)。
実施例 54 (1) 〜実施例 54 (2)
実施例 3において、 4一ホルミル安息香酸と t—ブトキシカルボ二ルー 1 , 4—プチレンジァミンの代わりに対応するァミンを用い、 実施例 6において ジィミダゾールァミンの変わりに対応するアミンを用いて、 実施例 3→実施 例 5→実施例 6→実施例 10の順に反応を行い、 標題化合物を得た。
実施例 54 (1) : 1— [4一 (2, 8—ジァザスピロ [4. 5] デカー 2 ーィルカルポニル) フエュノレ] — N, N—ビス (1H—イミダゾーノレ一 2— ィルメチル) メタンァミン (化合物 54— 1 )
性状:アモルファス
TLC:Rf 0.60 (クロ口ホルム:メタノール: 28%アンモニア水 =80:20:4); N諷 (DMSO-De): 51.21-1.36 (m, 2 H), 1.37-1.54 (m, 2 H), 1.61-1.81 (m, 2 H), 2.55-2.76 (m, 3 H), 3.10-3.27 (m, 3 H), 3.38-3.51 (m, 2 H), 3.51-3.56 (m, 2 H), 3.56-3.66 (m, 4 H), 6.71-6.97 (m, 2 H), 6.99—7.24 (m, 2 H), 7.34-7.54 (m, 4 H), 11.85-12.20 (m, 2 H)。
実施例 54 (2) : 1- {4- [ (8—シクロへキシルー 2, 8—ジァザス ピロ [4. 5] デカ一 2—ィル) カルボニル] フエ二ル} 一 N, N—ビス (1 H一^ f ミダゾールー 2—イノレメチル) メタンァミン (化合物 54-2)
性状:アモルファス
TLC: Rf 0.64 (クロ口ホルム:メタノール: 28%アンモニア水 = 80:20:4); NMR (DMSO-De): 6 1.15 (m, 5 H), 1.40 (m, 2 H), 1.56 (m, 3 H), 1.71 (m, 6 H), 2.27 (m, 2 H), 2.43 (m, 2 H), 3.23 (m, 3 H), 3.45 (m, 2 H), 3.54 (m, 2 H), 3.58 (m, 4 H), 6.97 (m, 4 H), 7.43 (m, 4 H), 12.00 (m, 2 H)。
[生物学的実施例]
本発明化合物の有効性、 例えば本発明化合物が C X C R 4拮抗作用を有す ることは、 以下の実験によって証明された。
本発明の測定方法は、 以下のように、 本発明化合物を評価するために、 測 定精度の向上および/または測定感度の改良を加えたものである。 以下に詳 細な実験方法を示した。
先述したように、 H I Vが C D 4陽性細胞上の受容体である C X C R 4に 結合することを阻害する化合物のスクリーニングをするためには、 H I Vゥ ィルスを用いたアツセィ系で行うことがより直接的な手法である。 しかし、 H I Vウィルスを大量スクリーニングに使用することは、 その取り扱いの難 しさから実用的ではない。 一方、 T細胞指向性 (X 4 ) ^1 1 ¥—1と3 0 一 1が共に C X C R 4に結合すること力 ら、 H I V側と S D F— 1側双方の C X C R 4結合部位、 並びに C X C R 4側の S D F— 1および H I V結合部 位には、 何らかの共通する特徴があるものと予測し得る。 従って、 既存の抗 A I D S薬 (逆転写酵素阻害薬やプロテアーゼ阻害薬) と異なる作用機序で ある H I Vウィルスの細胞への吸着を阻害する化合物を発見するため、 H I Vの代わりに C X C R 4の内因性リガンドである S D F— 1を用いたアツセ
16066
ィ系が利用可能である。
具体的には、 SDF— 1と CXCR 4の結合を阻害する化合物をスクリー ユングする系として、 例えば、 ョードラべノレした SDF— 1と CXCR4を 発現していることが知られているヒト T細胞株との結合を測定する系が実施 可能である。 マクロファージ (R 5) H I Vと、 RANTES、 MI P— 1 α、 MI Ρ— 1 J3が共に CCR 5に結合することから、 同様な考え方が可能 である。
[実験方法] '
実験例 1 : ヒ ト30 ー1の〇 EM細胞への結合に対する阻害実験
結合緩衝液中 (H E P E S, B S A含有) でヒト T細胞株 C EM細胞に被 験化合物と125 I— SDF— 1 (NEN) を添加し 4 °Cで 60分間インキュべ ートした。 反応させた C E M細胞を GF/B membrane filter plate (Packard) で急速ろ過して吸着させ、 PB Sで 3回洗浄した後、 乾燥させ Mcroscint+20 (Packard)を加えた。 CEM細胞に結合した放射能量を Top Count (Packard) を用いて測定し、試験化合物の阻害率(%) を以下の計算式により算出した。
阻害率 ={ (Et— Ea)/(Et— Ec) } X100
Et:被験化合物を添加しな力 た時の放射能量、,
Ec:被験化合物として125I— SDF— 1の 1000倍量の非放射性 SDF— 1
(Pepro Tech)を添加した時の放射能量、
Ea:被験化合物を添加した時の放射能量。
実施例に示したすベての本発明化合物は、 1 0 μ Μの濃度で 50 %以上の 阻害率を示した。 例えば、 化合物 1 0の I C 5。値は 27 ηΜであった。
実験例 2 :本発明化合物の血圧および心拍数に対する影響の測定
ラットをウレタンにより麻酔した (1.2 g k g皮下投与) 。 頸部正中切 開後、 血圧測定用のカテーテルを右総頸動脈に揷入した。 その後、 鼠径部を 切開後、 薬液投与用のカテーテルを大腿静脈に挿入し固定した。 血圧測定用
のカテーテルを圧トランデューサ一に連結し、 ひずみ圧用アンプ (AP— 6 41G (日本光電) ) を介して熱書ペンレコーダーに血圧波形を記録した。 この際、 心拍数は、 上記ひずみ圧用アンプから得られた血圧波形をトリガー とする瞬時心拍計 (AT— 601G (日本光電) ) を介した値を熱書ペンレ コーダ一に記録した。 被験化合物は 10%可溶化溶媒生理食塩液 (ポリオキ シエチレンヒ ドロキシステアレート :プロピレンダリコール:生理食塩液 = 7 : 3 : 190体積比) に溶解し、 0.1および 0.3、 1、 3、 1 Omg/m Lの濃度になるように調製した。 これを lmL/'k gで、 尾静脈より約 10 秒間かけて静脈内投与した。 1個体に対して、 投与用量を段階的にあげてい く累積投与を行った。
化合物 19の投与において、 3 m g /k g以下の濃度では血圧低下作用が 見られず、 1◦ m g k g投与時の心拍数増加率は 2 %であり、 低用量では 心拍数に影響を与えなかった。
[製剤実施例]
製剤例 1 :
4— ( { [4一 (ジプロピノレアミノ) プチル] ァミノ) メチル) 一 N, N 一ビス ( 1 H—ィミダゾール一 2—ィルメチル) ベンゾァミ ド ( 200 g ) 、 カルボキシメチルセルロースカルシウム (崩壊剤、 20.0 g) 、 ステアリン 酸マグネシウム (潤滑剤、 l O.O g) 、 微結晶セルロース (870 g) を常 法により混合した後打錠して、 一錠中に 2 Omgの活性成分を含有する錠剤 10000錠を得た。
製剤例 2 :
4— ( { [4一 (ジプロピルァミノ) プチノレ] アミノ} メチル) 一 N, N 一ビス ( 1 H—イミダゾール一 2—ィルメチル) ベンゾァミ ド ( 100 g ) 、 マンュトール (2 k g) 、 蒸留水 (50 L) を常法により混合した後、 除塵 フィルターでろ過し、 5 mLずつアンプルに充填し、 オートクレーブで加熱
滅菌して、 1ァンプル中 1 0 m gの活性成分を含有するァンプル 10000本を得
産業上の利用可能性
本発明化合物は、 C X C R 4拮抗作用を有することから、 C X C R 4介在 性疾患に対する予防および Zまたは治療剤として有用である。 そのため、 本 発明化合物は、 医薬品として利用可能である。 例えば、 炎症 ·免疫性疾患 (例 えば、 関節リウマチ、 関節炎、 網膜症、 肺線維症、 移植臓器拒絶反応等) 、 アレルギー性疾患、 感染症 (例えば、 ヒト免疫不全ウィルス感染、 後天性免 疫不全症候群等) 、 精神 ·神経性疾患、 脳疾患、 心 ·血管性疾患、 代謝性疾 患、 癌疾患 (例えば、 癌、 癌転移等) 等の予防および Zまたは治療剤、 また は再生医療用剤等として有用である。