KR20080050430A - 베타-세크레타제 (bace) 억제제로서아미노-5-[4-(디플루오로메톡시)페닐]-5-페닐이미다졸론화합물 - Google Patents
베타-세크레타제 (bace) 억제제로서아미노-5-[4-(디플루오로메톡시)페닐]-5-페닐이미다졸론화합물 Download PDFInfo
- Publication number
- KR20080050430A KR20080050430A KR1020087007179A KR20087007179A KR20080050430A KR 20080050430 A KR20080050430 A KR 20080050430A KR 1020087007179 A KR1020087007179 A KR 1020087007179A KR 20087007179 A KR20087007179 A KR 20087007179A KR 20080050430 A KR20080050430 A KR 20080050430A
- Authority
- KR
- South Korea
- Prior art keywords
- phenyl
- difluoromethoxy
- methyl
- amino
- dihydro
- Prior art date
Links
- 0 CN(C1=O)C(N)=NC1(c(cc1)ccc1OC(F)F)c1cccc(*)c1 Chemical compound CN(C1=O)C(N)=NC1(c(cc1)ccc1OC(F)F)c1cccc(*)c1 0.000 description 4
- DBBZSMZFFFJZRP-UHFFFAOYSA-N C#Cc(cc1)ccc1OC(F)F Chemical compound C#Cc(cc1)ccc1OC(F)F DBBZSMZFFFJZRP-UHFFFAOYSA-N 0.000 description 2
- KQJQPCJDKBKSLV-UHFFFAOYSA-N C=Cc1cc(Br)ccc1 Chemical compound C=Cc1cc(Br)ccc1 KQJQPCJDKBKSLV-UHFFFAOYSA-N 0.000 description 1
- HVHZEKKZMFRULH-UHFFFAOYSA-N CC(C)(C)c1nc(C(C)(C)C)cc(C)c1 Chemical compound CC(C)(C)c1nc(C(C)(C)C)cc(C)c1 HVHZEKKZMFRULH-UHFFFAOYSA-N 0.000 description 1
- RQZWLTPIMXZNCX-UHFFFAOYSA-N CCS(Nc1cc(C#Cc(cc2)ccc2OC(F)F)ccc1)(=O)=O Chemical compound CCS(Nc1cc(C#Cc(cc2)ccc2OC(F)F)ccc1)(=O)=O RQZWLTPIMXZNCX-UHFFFAOYSA-N 0.000 description 1
- WGYLRQAVKIEEMY-UHFFFAOYSA-N CCS(Nc1cc(C2(c(cc3)ccc3OC(F)F)N=C(N)N(C)C2=O)ccc1)(=O)=O Chemical compound CCS(Nc1cc(C2(c(cc3)ccc3OC(F)F)N=C(N)N(C)C2=O)ccc1)(=O)=O WGYLRQAVKIEEMY-UHFFFAOYSA-N 0.000 description 1
- LAYJGGMFDRDOEY-UHFFFAOYSA-N CN(C(C(c(cc1)ccc1OC(F)F)c1cc(OC(F)F)ccc1)=O)C(N)=N Chemical compound CN(C(C(c(cc1)ccc1OC(F)F)c1cc(OC(F)F)ccc1)=O)C(N)=N LAYJGGMFDRDOEY-UHFFFAOYSA-N 0.000 description 1
- LBGKTMHMJXSPFM-UHFFFAOYSA-N CN(C1=O)C(N)=NC1(c(cc1)ccc1OC(F)F)c(cc1OCCC=C(F)F)ccc1F Chemical compound CN(C1=O)C(N)=NC1(c(cc1)ccc1OC(F)F)c(cc1OCCC=C(F)F)ccc1F LBGKTMHMJXSPFM-UHFFFAOYSA-N 0.000 description 1
- KMESKSVXSOFRDY-UHFFFAOYSA-N CN(C1=O)C(N)=NC1(c(cc1)ccc1OC(F)F)c1cccc(C#CCCO)c1 Chemical compound CN(C1=O)C(N)=NC1(c(cc1)ccc1OC(F)F)c1cccc(C#CCCO)c1 KMESKSVXSOFRDY-UHFFFAOYSA-N 0.000 description 1
- HVLWHRXIHDMKOQ-UHFFFAOYSA-N CN(C1=O)C(N)=NC1(c(cc1)ccc1OC(F)F)c1cccc(C(C2)CC2=O)c1 Chemical compound CN(C1=O)C(N)=NC1(c(cc1)ccc1OC(F)F)c1cccc(C(C2)CC2=O)c1 HVLWHRXIHDMKOQ-UHFFFAOYSA-N 0.000 description 1
- GUZQFYDEDMEBAJ-SFHVURJKSA-N CN(C1=O)C(N)=N[C@@]1(c(cc1)ccc1OC(F)F)c1cc(OC(F)F)ccc1 Chemical compound CN(C1=O)C(N)=N[C@@]1(c(cc1)ccc1OC(F)F)c1cc(OC(F)F)ccc1 GUZQFYDEDMEBAJ-SFHVURJKSA-N 0.000 description 1
- WSIDFIREQDHYPW-UHFFFAOYSA-N FC(F)=CCCBr Chemical compound FC(F)=CCCBr WSIDFIREQDHYPW-UHFFFAOYSA-N 0.000 description 1
- JNMURBKTGFUAFL-UHFFFAOYSA-N FC(F)=CCCOc(cc(cc1)Br)c1F Chemical compound FC(F)=CCCOc(cc(cc1)Br)c1F JNMURBKTGFUAFL-UHFFFAOYSA-N 0.000 description 1
- RLKCJCIUTBLVRJ-UHFFFAOYSA-N O=C(C1)CC1c1cccc(Br)c1 Chemical compound O=C(C1)CC1c1cccc(Br)c1 RLKCJCIUTBLVRJ-UHFFFAOYSA-N 0.000 description 1
- YPTHSYKJDRMAJY-UHFFFAOYSA-N Oc(cc(cc1)Br)c1F Chemical compound Oc(cc(cc1)Br)c1F YPTHSYKJDRMAJY-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D233/00—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, not condensed with other rings
- C07D233/54—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, not condensed with other rings having two double bonds between ring members or between ring members and non-ring members
- C07D233/66—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, not condensed with other rings having two double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D233/88—Nitrogen atoms, e.g. allantoin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/4164—1,3-Diazoles
- A61K31/4168—1,3-Diazoles having a nitrogen attached in position 2, e.g. clonidine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings
- C07D409/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Veterinary Medicine (AREA)
- Engineering & Computer Science (AREA)
- Medicinal Chemistry (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Biomedical Technology (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Hospice & Palliative Care (AREA)
- Psychiatry (AREA)
- Epidemiology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
Abstract
Description
본 발명은 2-아미노-5-[4-(디플루오로메톡시)페닐]-5-페닐-3,5-디히드로이미다졸-4-온 화합물, 및 β-세크레타제 (BACE)를 억제하고 β-아밀로이드 침착 및 신경섬유 농축을 치료하는 데 사용하기 위한 방법에 관한 것이다.
β-아밀로이드 침착 및 신경섬유 농축은 알쯔하이머병 (AD)과 관련된 두 가지 주요 병리학적 특징이다. 임상적으로, AD는 기억, 인지, 추리, 판단 및 인식의 상실을 특징으로 한다. 상기 질환이 진행됨에 따라 다중 인지 기능의 전반적인 손상이 일어날 때까지 운동, 감각 및 언어 능력 또한 영향을 받는다. 이러한 인지 상실은 점진적으로 일어나며, 전형적으로 4 내지 12년 내에 심각한 손상 및 최종적으로 사망에 이르게 한다.
아밀로이드 생성 플라크 및 혈관성 아밀로이드 맥관병증은 또한 21번 삼염색체증 (다운 증후군), 네덜란드형의 아밀로이드증성 유전성 뇌출혈 (HCHWA-D) 및 다른 신경퇴행성 장애를 가진 환자의 뇌에서 특징적이다. 신경섬유 농축은 또한 치매-유도 장애를 포함한 다른 신경퇴행성 장애에서 일어난다 (문헌 [Varghese, J., et al, Journal of Medicinal Chemistry, 2003, 46, 4625-4630]).
β-아밀로이드 침착물은 주로 Aβ 펩티드의 응집물이고, 이는 아밀로이드 전구체 단백질 (APP)의 단백질 가수분해의 산물이다. 더욱 구체적으로, Aβ 펩티드는 β-아밀로이드 생성 경로의 일부로서, 하나 이상의 γ-세크레타제에 의한 C-말단에서 APP의 절단, 및 β-세크레타제 효소 (BACE, 아스파르틸 프로테아제로도 알려짐)에 의한 N-말단에서 APP의 절단으로 인해 생성된다.
BACE 활성은 APP로부터 Aβ의 생성과 직접적으로 상호 관련되고 (문헌 [Sinha, et al., Nature, 1999, 402, 537-540]), 여러 연구에서는 BACE의 억제가 Aβ 펩티드의 생성을 억제한다는 것을 더욱더 지적하였다 (문헌 [Roberds, S. L., et al, Human Molecular Genetics, 2001, 10, 1317-1324]).
따라서, 본 발명의 목적은, β-세크레타제 억제제이고, 환자에서 β-아밀로이드 침착 또는 β-아밀로이드 수준 상승을 특징으로 하는 질환 또는 장애의 치료, 예방 또는 경감에서 치료제로서 유용한 화합물을 제공하는 것이다.
본 발명의 또다른 목적은, 환자에서 상승된 β-아밀로이드 침착 또는 β-아밀로이드 수준을 특징으로 하는 질환 또는 장애의 치료, 예방 또는 경감에 유용한 치료 방법 및 제약 조성물을 제공하는 것이다.
본 발명의 특징은, 제공되는 화합물이 또한 β-세크레타제 효소를 더 연구하고 설명하는 데 유용할 수 있다는 점이다.
본 발명의 이들 및 다른 목적 및 특징은 후술할 발명의 상세한 설명에 의해 더욱 명백해질 것이다.
<발명의 개요>
본 발명의 하기 화학식 I의 화합물, 또는 그의 호변이성질체, 그의 입체이성질체 또는 그의 제약상 허용가능한 염을 제공한다.
식 중,
R1 및 R2는 각각 독립적으로 H, 또는 각각 임의로 치환된 알킬, 시클로알킬, 시클로헤테로알킬, 아릴 또는 헤테로아릴 기이거나, 또는 R1 및 R2는 이들이 부착된 원자와 함께 O, N 또는 S로부터 선택된 추가의 헤테로원자를 임의로 함유하는 임의로 치환된 5- 내지 7-원 고리를 형성할 수 있고;
R3은 H, 또는 각각 임의로 치환된 알킬, 시클로알킬, 시클로헤테로알킬, 아릴 또는 헤테로아릴 기이고;
R4, R5 및 R6은 각각 독립적으로 H, 할로겐, NO2, CN, COR7, NR10CO2R11, NR15COR16, OR14, NR12R13, SOnR17, 또는 각각 임의로 치환된 알킬, 할로알킬, 알케닐, 할로알케닐, 알키닐, 시클로알킬 또는 시클로헤테로알킬 기이거나, 또는 인접 탄소 원자에 부착된 경우 R4 및 R5는 이들이 부착된 원자와 함께 O, N 또는 S로부터 선택된 1 또는 2개의 헤테로원자를 임의로 함유하는 임의로 치환된 5- 내지 7-원 고리를 형성할 수 있고;
n은 0, 1 또는 2이고;
R7 및 R17은 각각 독립적으로 H, NR8R9, 또는 각각 임의로 치환된 알킬, 할로알킬, 알콕시알킬, 알케닐, 알키닐, 시클로알킬 또는 아릴 기이고;
R8 및 R9는 각각 독립적으로 H, 또는 각각 임의로 치환된 알킬, 알케닐, 알키닐 또는 시클로알킬 기이거나, 또는 R8 및 R9는 이들이 부착된 원자와 함께 O, N 또는 S로부터 선택된 추가의 헤테로원자를 임의로 함유하는 임의로 치환된 5- 내지 7-원 고리를 형성할 수 있고;
R11, R14 및 R16은 각각 독립적으로 H, 또는 각각 임의로 치환된 알킬, 할로알킬, 알콕시알킬, 알케닐, 알키닐, 시클로알킬 또는 아릴 기이고;
R10 및 R15는 각각 독립적으로 H 또는 임의로 치환된 알킬 기이며;
R12 및 R13은 각각 독립적으로 H, 또는 각각 임의로 치환된 알킬 또는 시클로알킬 기이거나, 또는 R12 및 R13은 이들이 부착된 원자와 함께 O, N 또는 S로부터 선택된 추가의 헤테로원자를 임의로 함유하는 임의로 치환된 5- 내지 7-원 고리를 형성할 수 있다.
본 발명은 또한 β-아밀로이드 침착 및 신경섬유 농축의 치료를 위한 이러한 화합물의 용도에 관한 것이다. 화학식 I의 화합물은 알쯔하이머병, 인지 장애, 다운 증후군, HCHWA-D, 인지 저하, 노인성 치매, 대뇌 아밀로이드 맥관병증, 퇴행성 치매 또는 다른 신경퇴행성 장애의 치료에 특히 유용하다.
알쯔하이머병 (AD)은 임상적으로 기억, 인지, 추리, 판단 및 감정적 안정의 진행성 상실을 나타내며 점진적으로 심각한 정신적 악화 및 사망을 유도하는, 뇌의 주요한 퇴행성 질환이다. AD의 정확한 원인은 알려져 있지 않지만, 아밀로이드 베타 펩티드 (A-베타)가 상기 질환의 병인에 중추적인 역할을 한다는 증거가 늘어나고 있다 (문헌 [D. B. Schenk; R. E. Rydel et al, Journal of Medicinal Chemistry, 1995, 21, 4141] 및 [D. J. Selkoe, Physiology Review, 2001, 81, 741]). AD 환자는 특징적인 신경병리학적 마커, 예컨대 신경염증성 플라크 (및 β-아밀로이드 맥관병증, 뇌혈관에서의 침착) 뿐만 아니라, 부검시 뇌에서 검출된 신경섬유 농축을 나타낸다. A-베타는 AD 뇌에서 신경염증성 플라크의 주성분이다. 또한, β-아밀로이드 침착 및 혈관성 β-아밀로이드 맥관병증은 또한 다운 증후군, 네덜란드형의 아밀로이드증성 유전성 뇌출혈, 및 다른 신경퇴행성 및 치매-유도 장애를 가진 개체에서 특징적이다. 아밀로이드 전구체 단백질 (APP)의 과발현, APP에서 A-베타로의 변경된 절단, 또는 환자 뇌로부터 A-베타 제거율의 감소는 뇌에서 A-베타의 가용성 또는 섬유성 형태의 수준을 증가시킬 수 있다. 메마프신-2 또는 Asp-2로도 지칭되는 β-부위 APP 절단 효소, BACE1이 1999년에 확인되었다 (문헌 [R. Vassar, B. D. Bennett, et al, Nature, 1999, 402, 537]). BACE1은 β-세크레타제의 모든 공지된 기능적 특성 및 특징을 갖는 막-결합 아스파르트산 프로테아제이다. BACE1 또는 β-세크레타제의 저분자량, 비-펩티드, 비-기질-관련 억제제가 β-세크레타제 효소 연구에 대한 보조제로서 및 잠재적인 치료제로서 절실히 요구된다.
놀랍게도, 본 발명에 이르러 화학식 I의 아미노-5-[4-(디플루오로메톡시)페닐]-5-페닐이미다졸론 화합물이 β-세크레타제의 억제제 및 BACE1의 선택적 억제제임이 입증되었다. 유리하게는, 상기 페닐이미다졸론 화합물은 환자에서 상승된 β-아밀로이드 침착 또는 β-아밀로이드 수준을 특징으로 하는 질환 또는 장애의 치료, 예방 또는 경감을 위한 효과적인 치료제로서 사용될 수 있다. 따라서, 본 발명은 하기 화학식 I의 아미노-5-[4-(디플루오로메톡시)페닐]-5-페닐이미다졸론 화합물, 또는 그의 호변이성질체, 그의 입체이성질체 또는 그의 제약상 허용가능한 염을 제공한다.
<화학식 I>
식 중,
R1 및 R2는 각각 독립적으로 H, 또는 각각 임의로 치환된 알킬, 시클로알킬, 시클로헤테로알킬, 아릴 또는 헤테로아릴 기이거나, 또는 R1 및 R2는 이들이 부착된 원자와 함께 O, N 또는 S로부터 선택된 추가의 헤테로원자를 임의로 함유하는 임의로 치환된 5- 내지 7-원 고리를 형성할 수 있고;
R3은 H, 또는 각각 임의로 치환된 알킬, 시클로알킬, 시클로헤테로알킬, 아릴 또는 헤테로아릴 기이고;
R4, R5 및 R6은 각각 독립적으로 H, 할로겐, NO2, CN, COR7, NR10CO2R11, NR15COR16, OR14, NR12R13, SOnR17, 또는 각각 임의로 치환된 알킬, 할로알킬, 알케닐, 할로알케닐, 알키닐, 시클로알킬 또는 시클로헤테로알킬 기이거나, 또는 인접 탄소 원자에 부착된 경우 R4 및 R5는 이들이 부착된 원자와 함께 O, N 또는 S로부터 선택된 1 또는 2개의 헤테로원자를 임의로 함유하는 임의로 치환된 5- 내지 7-원 고리를 형성할 수 있고;
n은 0, 1 또는 2이고;
R7 및 R17은 각각 독립적으로 H, NR8R9, 또는 각각 임의로 치환된 알킬, 할로알킬, 알콕시알킬, 알케닐, 알키닐, 시클로알킬 또는 아릴 기이고;
R8 및 R9는 각각 독립적으로 H, 또는 각각 임의로 치환된 알킬, 알케닐, 알키닐 또는 시클로알킬 기이거나, 또는 R8 및 R9는 이들이 부착된 원자와 함께 O, N 또는 S로부터 선택된 추가의 헤테로원자를 임의로 함유하는 임의로 치환된 5- 내지 7-원 고리를 형성할 수 있고;
R11, R14 및 R16은 각각 독립적으로 H, 또는 각각 임의로 치환된 알킬, 할로알킬, 알콕시알킬, 알케닐, 알키닐, 시클로알킬 또는 아릴 기이고;
R10 및 R15는 각각 독립적으로 H 또는 임의로 치환된 알킬 기이며;
R12 및 R13은 각각 독립적으로 H, 또는 각각 임의로 치환된 알킬 또는 시클로알킬 기이거나, 또는 R12 및 R13은 이들이 부착된 원자와 함께 O, N 또는 S로부터 선택된 추가의 헤테로원자를 임의로 함유하는 임의로 치환된 5- 내지 7-원 고리를 형성할 수 있다.
청구항은 모든 가능한 입체이성질체 및 전구약물을 포함하는 것으로 이해된다. 또한, 달리 언급하지 않는 한, 각각의 알킬, 알콕시, 알케닐, 알키닐, 시클로알킬, 시클로헤테로알킬, 아릴 또는 헤테로아릴 기는 임의로 치환되는 것으로 고려된다.
임의로 치환된 잔기는 1개 이상의 치환기로 치환될 수 있다. 임의로 존재하는 치환기는 제약학적 화합물의 개발, 또는 그들의 구조/활성, 지속성, 흡수성, 안정성 또는 다른 유익한 특성에 영향을 주기 위한 상기 화합물의 변형에 통상적으로 사용되는 1개 이상의 치환기일 수 있다. 이러한 치환기의 구체적인 예로는 할로겐원자, 니트로, 시아노, 티오시아네이토, 시아네이토, 히드록실, 알킬, 할로알킬, 알콕시, 할로알콕시, 아릴옥시, 아미노, 알킬아미노, 디알킬아미노, 포르밀, 카르보닐, 알콕시카르보닐, 카르복실, 알카노일, 알킬티오, 알킬술피닐, 알킬술포닐, 카르바모일, 알킬아미도, 페닐, 페녹시, 벤질, 벤질옥시, 시클로알킬 또는 시클로헤테로알킬 기, 바람직하게는 할로겐원자 또는 저급 알킬 또는 저급 알콕시 기를 들 수 있고, 여기서 '저급'은 1 내지 4개의 탄소 원자이다. 한 실시양태에서, 치환기는 할로, 시아노, 히드록시, 알킬, 알케닐, 알키닐, 알콕시 또는 시클로알킬로부터 선택될 수 있다. 달리 언급하지 않는 한, 전형적으로 0 내지 4개의 치환기가 존재할 수 있다. 상기 임의의 치환기가 알킬 치환기를 나타내거나 함유하는 경우, 이는 선형 또는 분지형일 수 있고, 12개 이하의 탄소 원자, 바람직하게는 6개 이하의 탄소 원자, 보다 바람직하게는 4개 이하의 탄소 원자를 함유할 수 있다.
본원에서 사용된 용어 "알킬"은 1 내지 12개의 탄소 원자, 바람직하게는 1 내지 6개의 탄소 원자, 보다 바람직하게는 1 내지 4개의 탄소 원자의 '저급' 알킬의 직쇄 및 분지쇄 (달리 정의하지 않는 한) 1가 포화 탄화수소 잔기 모두를 포함한다. 포화 탄화수소 알킬 잔기의 예로는 화학기, 예컨대 메틸, 에틸, n-프로필, 이소프로필, n-부틸, tert-부틸, 이소부틸, sec-부틸; 고급 동족체, 예컨대 n-펜틸, n-헥실 등을 들 수 있지만, 이에 제한되지는 않는다. 알킬기는 임의로 치환될 수 있다. 적합한 알킬 치환기로는 CN, OH, 할로겐, 알케닐, 알키닐, 시클로알킬, 페닐, 카르바모일, 카르보닐, 알콕시 또는 아릴옥시를 들 수 있지만, 이에 제한되지는 않는다.
본원에서 사용된 용어 "할로알킬"은 동일하거나 상이할 수 있는 1 내지 2n+1개의 할로겐원자를 갖는 CnH2n +1기를 나타낸다. 할로알킬기의 예로는 CF3, CH2Cl, C2H3BrCl, C3H5F2 등을 들 수 있다. 유사하게, 용어 할로알콕시는 동일하거나 상이할 수 있는 1 내지 2n+1개의 할로겐원자를 갖는 OCnH2n +1기를 나타낸다.
본원에서 사용된 용어 "알콕시알킬"은 하나 이상의 C1-C4알콕시기로 치환된 상기에서 정의된 바와 같은 알킬기를 지칭한다.
본원에서 사용된 용어 "알케닐"은 하나 이상의 이중 결합을 함유하고, 2 내지 12개의 탄소 원자, 바람직하게는 2 내지 6개의 탄소 원자, 보다 바람직하게는 2 내지 4개의 탄소 원자를 갖는 직쇄 또는 분지쇄 탄화수소 잔기를 지칭한다. 이러한 탄화수소 알케닐 잔기는 단일 또는 다중불포화일 수 있고, E 또는 Z 배위로 존재할 수 있다. 본 발명의 화합물은 모든 가능한 E 및 Z 배위를 포함한다. 단일 또는 다중불포화 탄화수소 알케닐 잔기의 예로는 화학기, 예컨대 비닐, 2-프로페닐, 이소프로페닐, 크로틸, 2-이소펜테닐, 부타디에닐, 2-(부타디에닐), 2,4-펜타디에닐, 3-(1,4-펜타디에닐), 및 고급 동족체, 이성질체 등을 들 수 있지만, 이에 제한되지는 않는다.
본원에서 사용된 용어 "할로알케닐"은 동일하거나 상이할 수 있는 하나 이상의 할로겐원자로 치환된 상기에서 정의된 바와 같은 알케닐기를 나타낸다.
본원에서 사용된 용어 "알키닐"은 하나 이상의 삼중 탄소-탄소 결합을 갖는 알킬기를 지칭한다. 알키닐기는 바람직하게는 2 내지 6개의 탄소 원자를 함유한다. 알키닐기의 예로는 에티닐, 프로피닐, 부티닐, 펜티닐 등을 들 수 있지만, 이에 제한되지는 않는다. 일부 실시양태에서, 알키닐기는 상술한 바와 같은 4개 이하의 치환기로 치환될 수 있다.
본원에서 사용된 용어 "시클로알킬"은 3 내지 10개의 탄소 원자의 모노시클릭, 비시클릭, 트리시클릭, 융합된, 가교된 또는 스피로 치환된 카르보시클릭 잔기를 지칭한다. 시클로알킬 잔기의 임의의 적합한 고리 위치가, 정의된 화학 구조에 공유결합으로 연결될 수 있다. 시클로알킬 잔기의 예로는 화학기, 예컨대 시클로프로필, 시클로부틸, 시클로펜틸, 시클로헥실, 시크로헵틸, 노르보르닐, 아다만틸, 스피로[4.5]데카닐, 및 동족체, 이성질체 등을 들 수 있지만, 이에 제한되지는 않는다.
본원에서 사용된 용어 "시클로헤테로알킬"은 N, O 또는 S로부터 선택된, 동일하거나 상이할 수 있는 1, 2 또는 3개의 헤테로원자를 함유하고, 임의로 하나의 이중 결합을 함유하는 5- 내지 7-원 시클로알킬 고리 시스템을 나타낸다. 상기에서 나타낸 용어에 포함되는 시클로헤테로알킬 고리계의 예로는 하기 고리가 있으며, 여기서, X1은 NR', O 또는 S이고, R'은 H 또는 상기에 정의된 바와 같은 임의의 치환기이다.
본원에서 사용된 용어 "아릴"은 단일 고리 (모노시클릭) 또는 함께 융합되거나 공유결합으로 연결된 다중 고리 (비시클릭, 3개 이하의 고리)일 수 있는, 20개 이하의 탄소 원자, 예를 들어 6 내지 20개의 탄소 원자의 방향족 카르보시클릭 잔기를 나타낸다. 아릴 잔기의 예로는 화학기, 예컨대 페닐, 1-나프틸, 2-나프틸, 디히드로나프틸, 테트라히드로나프틸, 비페닐, 안트릴, 페난트릴, 플루오레닐, 인다닐, 비페닐레닐, 아세나프테닐, 아세나프틸레닐 등을 들 수 있지만, 이에 제한되지는 않는다. 일부 실시양태에서, "아릴"기는 1 내지 5개의 치환기로 치환될 수 있다.
본원에서 사용된 용어 "헤테로아릴"은 단일 고리 (모노시클릭) 또는 함께 융합되거나 공유결합으로 연결된 다중 고리 (비시클릭, 3개 이하의 고리)일 수 있는, 예를 들어 5 내지 20개의 고리 원자를 갖는 방향족 헤테로시클릭 고리 시스템을 나타낸다. 바람직하게는, 헤테로아릴은 5- 내지 6-원 고리이다. 상기 고리는 질소, 산소 또는 황으로부터 선택되는 1 내지 4개의 헤테로원자를 함유할 수 있고, 여기서 질소 또는 황 원자는 임의로 산화되거나, 또는 질소 원자는 임의로 4차화(quaternized)된다. 헤테로아릴 잔기의 예로는 헤테로사이클, 예컨대 푸란, 티오펜, 피롤, 피라졸, 이미다졸, 옥사졸, 이속사졸, 티아졸, 이소티아졸, 1H-테트라졸, 1,3,4-옥사디아졸, 1H-1,2,4-트리아졸, 1,3,4-트리아졸, 피리딘, 피리미딘, 피라진, 피리다진, 벤족사졸, 벤즈이속사졸, 벤조티아졸, 벤조푸란, 벤조티오펜, 티안트렌, 벤즈이미다졸, 인돌, 인다졸, 퀴놀린, 이소퀴놀린, 퀴나졸린, 퀴녹살린, 퓨린, 프테리딘, 9H-카르바졸, α-카르볼린 등을 들 수 있지만, 이에 제한되지는 않는다.
본원에서 사용된 용어 "할로겐"은 불소, 염소, 브롬 또는 요오드를 나타낸다.
본 발명의 화합물은 당업계에 공지된 절차를 이용하여 염, 특히 제약상 허용가능한 염으로 전환될 수 있다. 적합한 염기와의 염은, 예를 들어 금속염, 예컨대 알칼리 금속 또는 알칼리 토금속 염, 예를 들어 나트륨, 칼륨 또는 마그네슘 염, 또는 암모니아 또는 유기 아민과의 염, 예컨대 모르폴린, 티오모르폴린, 피페리딘, 피롤리딘, 모노-, 디- 또는 트리-저급 알킬아민, 예를 들어 에틸-tert-부틸-, 디에틸-, 디이소프로필-, 트리에틸-, 트리부틸- 또는 디메틸프로필아민, 또는 모노-, 디- 또는 트리히드록시 저급 알킬아민, 예를 들어 모노-, 디- 또는 트리에탄올아민이 있다. 내부 염이 또한 형성될 수 있다. 제약 용도로는 적합하지 않지만, 예를 들어 유리 화합물 또는 그의 제약상 허용가능한 염의 단리 또는 정제에 사용될 수 있는 염이 또한 포함된다. 본원에서 사용된 용어 "제약상 허용가능한 염"은 유기 및 무기산, 예컨대 아세트산, 프로피온산, 락트산, 시트르산, 타르타르산, 숙신산, 푸마르산, 말레산, 말론산, 만델산, 말산, 프탈산, 염산, 브롬화수소산, 인산, 질산, 황산, 메탄술폰산, 나프탈렌술폰산, 벤젠술폰산, 톨루엔술폰산, 캄포르술폰산, 및 본 발명의 화합물이 염기성 잔기를 함유하는 경우 유사하게 공지된 허용가능한 산으로부터 유도된 염을 지칭한다. 본 발명의 화합물이 카르복실레이트 또는 페놀 잔기, 또는 염기 부가염을 형성할 수 있는 유사한 잔기를 함유한 경우, 염은 또한 유기 및 무기 염기로부터 형성될 수 있고, 알칼리 금속염, 예를 들어 나트륨, 리튬 또는 칼륨 염이 바람직하다.
본 발명의 화합물은 하나 이상의 호변이성질체로서 존재할 수 있다. 당업자는 화학식 I의 화합물이 하기와 같이 나타낸 호변이성질체로서 존재할 수 있다는 것을 알 것이다.
호변이성질체는 대개 서로 평형을 이루어 존재한다. 이들 호변이성질체는 환경적 및 물리학적 조건하에 상호 전환되기 때문에, 이들은 동일한 유효한 생물학적 효과를 제공한다. 본 발명은 이러한 호변이성질체의 혼합물뿐 아니라 개별 호변이성질체, 예를 들어 화학식 I, It, Ita 및 Itb 등의 화합물을 포함한다.
본 발명의 화합물은 비대칭 탄소 원자를 함유할 수 있고, 본 발명의 화합물의 일부는 또는 1개 이상의 비대칭 중심을 함유할 수 있고, 따라서 광학 이성질체 및 부분입체이성질체가 형성될 수 있다. 화학식 I의 입체화학을 나타내지 않고 도시하였지만, 본 발명은 이러한 광학 이성질체 및 부분입체이성질체뿐 아니라, 라세미화된 및 분할된 거울상이성질체적으로 순수한 R 및 S 입체이성질체, 및 R 및 S 입체이성질체 및 그의 제약상 허용가능한 염의 다른 혼합물을 포함한다. 입체이성질체가 바람직한 경우, 일부 실시양태에서는 상응하는 거울상이성질체가 실질적으로 없이 제공될 수 있다. 따라서, 상응하는 거울상이성질체가 실질적으로 없는 거울상이성질체는 분리 기술을 통해 단리 또는 분리되거나, 상응하는 거울상이성질체가 없도록 제조된 화합물을 지칭한다. 본원에서 사용된 "실질적으로 없는"은 화합 물이 하나의 입체이성질체로 대부분, 바람직하게는 약 50% 미만, 더욱 바람직하게는 약 75% 미만, 더욱더 바람직하게는 약 90% 미만으로 이루어지는 것을 의미한다.
화학식 I의 바람직한 화합물은 R1 및 R2가 H인 화합물이다.
바람직한 화합물의 또다른 군은 R3이 C1-C4알킬인 화학식 I의 화합물이다.
R4, R5 및 R6이 각각 독립적으로 H, 할로겐, COR7, OR14, 또는 각각 임의로 치환된 알킬, 할로알킬, 알콕시, 할로알콕시, 알키닐 또는 시클로알킬 기인 화학식 I의 화합물이 또한 바람직하다.
본 발명의 보다 바람직한 화합물은 R1 및 R2가 H이고, R3이 메틸인 화학식 I의 화합물이다.
본 발명의 보다 바람직한 화합물의 또다른 군은 R4가 H, COR7, OR14, 또는 각각 임의로 치환된 알킬, 할로알킬, 알콕시, 할로알콕시, 알키닐 또는 시클로알킬 기이며; R5 및 R6이 각각 독립적으로 H 또는 할로겐인 화학식 I의 화합물이다. 한 실시양태에서, R4는 알케닐, 알키닐, 할로, 히드록시, 알콕시 또는 시클로알킬로부터 선택되는 하나 이상의 기로 임의로 치환된다. 또다른 실시양태에서, R4는 페닐 고리의 3-위치에 존재한다.
본 발명의 보다 바람직한 화합물의 추가 군은 R1 및 R2가 H이고; R3이 메틸이 고; R4가 H, COR7, OR14, 또는 각각 임의로 치환된 알킬, 할로알킬, 알콕시, 할로알콕시, 알키닐 또는 시클로알킬 기이고; R5 및 R6이 각각 독립적으로 H 또는 할로겐이며; R4가 페닐 고리의 3-위치에 존재하는 화학식 I의 화합물이다.
본 발명의 바람직한 화합물로는
(5S)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-페닐-3,5-디히드로-4H-이미다졸-4-온;
(5R)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-페닐-3,5-디히드로-4H-이미다졸-4-온;
(5R)-2-아미노-5-(3-브로모페닐)-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
(5S)-2-아미노-5-(3-브로모페닐)-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
(5R)-2-아미노-5-(3-브로모-4-플루오로페닐)-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
(5S)-2-아미노-5-(3-브로모-4-플루오로페닐)-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
(5R)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-(3-프로필페닐)-3,5-디히드로-4H-이미다졸-4-온;
(5S)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-(3-프로필페닐)-3,5- 디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(3-플루오로프로필)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(3,3-디플루오로프로필)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(4-플루오로부틸)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[3-(4,4-디플루오로부틸)페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(2-플루오로에틸)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[3-(2,2-디플루오로에틸)페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-[3-(2,2,2-트리플루오로에틸)페닐]-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-[3-(3,3,3-트리플루오로프로필)페닐]-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-[3-(4,4,4-트리플루오로부틸)페닐]-3,5-디히드로-4H-이미다졸-4-온;
(5R)-2-아미노-5-(3-부틸페닐)-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디 히드로-4H-이미다졸-4-온;
(5S)-2-아미노-5-(3-부틸페닐)-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-(3-펜틸페닐)-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-[3-(2-메틸부틸)페닐]-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-(3-부트-3-엔-1-일페닐)-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[3-(시클로프로필메틸)페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
3-(3-{2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}페닐)프로판니트릴;
(5R)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-(3-펜트-4-엔-1-일페닐)-3,5-디히드로-4H-이미다졸-4-온;
(5S)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-(3-펜트-4-엔-1-일페닐)-3,5-디히드로-4H-이미다졸-4-온;
N-(3-{(4R)-2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}페닐)-2-메톡시아세트아미드;
N-(3-{(4S)-2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히 드로-1H-이미다졸-4-일}페닐)-2-메톡시아세트아미드;
(5S)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-페닐-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(4-히드록시부트-1-인-1-일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(4-히드록시부틸)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(5-플루오로펜틸)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(4-플루오로부틸)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(6-플루오로헥실)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(4-메톡시부틸)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[(1Z)-3-메톡시프로프-1-엔-1-일]페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(3-메톡시프로필)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[3-(4,4-디플루오로부틸)페닐]-5-[4-(디플루오로메톡시)페닐]-3- 메틸-3,5-디히드로-4H-이미다졸-4-온;
3-{2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}-N-프로필벤즈아미드;
(1E)-3-클로로프로프-1-에닐 2,5-디클로로페닐 술폰;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[(2-플루오로에톡시)메틸]페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-{3-[(3,3,3-트리플루오로프로폭시)메틸]페닐}-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(메톡시메틸)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[3-(부톡시메틸)페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-{3-[(시클로프로필메톡시)메틸]페닐}-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(에톡시메틸)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-[3-(프로폭시메틸)페닐]-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-(3-{[2-플루오로-1-(플루오로메틸)에톡시]메틸}페닐)-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-{3-[(2,2,2-트리플루오로에톡시)메틸]페닐}-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-{3-[(2,2,3,3-테트라플루오로프로폭시)메틸]페닐}-3,5-디히드로-4H-이미다졸-4-온;
4-[4-(디플루오로메톡시)페닐]-4-[3-(3-메톡시프로프-1-인-1-일)페닐]-1-메틸-4,5-디히드로-1H-이미다졸-2-아민;
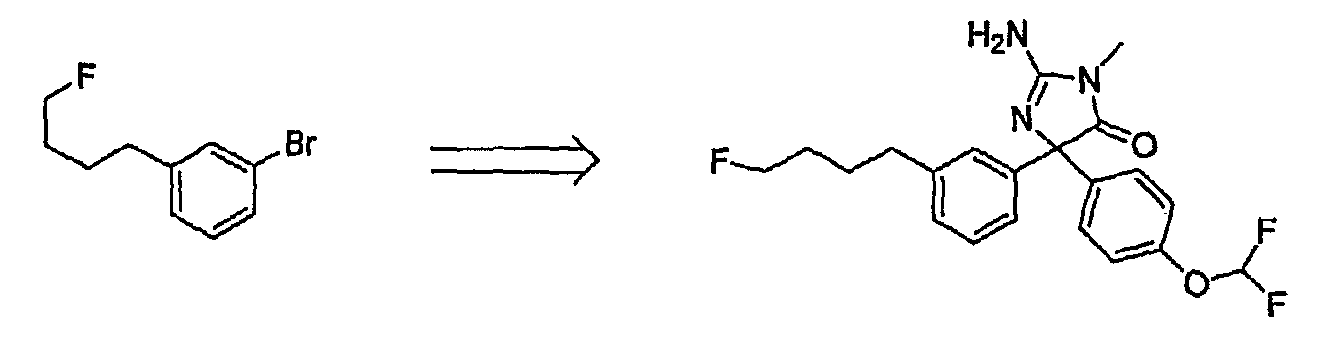
2-아미노-5-[3-(1,4-디플루오로부틸)페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(3-플루오로부트-3-엔-1-일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[3-(4,4-디플루오로부트-3-엔-1-일)페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-[3-(4,4,4-트리플루오로부틸)페닐]-3,5-디히드로-4H-이미다졸-4-온;
5-(3-{2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}페닐)펜탄니트릴;
4-(3-{2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}페닐)부탄니트릴;
2-아미노-5-{3-[(1E)-4,4-디플루오로부트-1-엔-1-일]페닐}-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(3-히드록시헥스-4-인-1-일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[(1E)-6-메톡시헥스-1-엔-1-일]페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[(1E)-5-메톡시펜트-1-엔-1-일]페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[2-(메톡시메틸)시클로프로필]페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[(1E)-5-히드록시펜트-1-엔-1-일}페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[(1E)-3-메톡시프로프-1-엔-1-일]페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[(1E)-4-메톡시부트-1-엔-1-일]페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[(1E)-4-히드록시부트-1-엔-1-일]페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[2-(2-메톡시에틸)시클로프로필]페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[(1E)-4-플루오로부트-1-엔-1-일]페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[(1E)-5-플루오로펜트-1-엔-1-일]페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
5-(3-아세틸페닐)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{4-플루오로-3-[(1E)-4-플루오로부트-1-엔-1-일]페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(3-플루오로프로프-1-인-1-일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-(3-히드록시페닐)-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(3-플루오로프로폭시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[3-(시클로프로필메톡시)페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-[3-(4,4,4-트리플루오로부톡시)페닐]-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[3-(2,2-디플루오로에톡시)페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(4-플루오로부톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-[3-(3-페녹시프로폭시)페닐]-3,5-디히드로-4H-이미다졸-4-온;
4-(3-{2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}페녹시)부탄니트릴;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[4-플루오로-3-(3-플루오로프로폭시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[3-(부트-2-인-1-일옥시)-4-플루오로페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[4-플루오로-3-(4-플루오로부톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[3-(2,2-디플루오로에톡시)-4-플루오로페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
(5R)-2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[4-플루오로-3-(3-플루오로프로폭시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
(5S)-2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[4-플루오로-3-(3-플루오로프로폭시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-{3-[(4,4-디플루오로부트-3-엔-1-일)옥시]페닐}-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
(5S)-2-아미노-5-[3-(2,2-디플루오로에톡시)-4-플루오로페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
(5R)-2-아미노-5-[3-(2,2-디플루오로메톡시)-4-플루오로페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(2-플루오로에틸)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(5-플루오로펜타노일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(4-플루오로부타노일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[3-(부트-3-엔-1-일옥시)페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[3-(부트-3-엔-1-일옥시)-4-플루오로페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
(5R)-2-아미노-5-[3-(부트-3-엔-1-일옥시)페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
(5S)-2-아미노-5-[3-(부트-3-엔-1-일옥시)페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-{3-[(4,4-디플루오로부트-3-엔-1-일)옥시]-4-플루오로페닐}-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-(4-플루오로-3-펜트-4-엔-1-일페닐)-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-(3-부트-3-엔-1-일-4-플루오로페닐)-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
3-{2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}벤즈알데히드;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(1-히드록시부트-2-인-1-일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(1,4-디히드록시부트-2-인-1-일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
(5R)-2-아미노-5-[3-(디플루오로메톡시)페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(2,2-디메틸-3-옥소시클로부틸)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-[3-(3-옥소시클로부틸)페닐]-3,5-디히드로-4H-이미다졸-4-온;
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(3-히드록시시클로부틸)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
메틸 [3-(3-{2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}페닐)시클로부틸]아세테이트;
메틸 [3-(3-{2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}페닐)시클로부틸리덴]아세테이트; 또는
이들의 호변이성질체, 이들의 입체이성질체 또는 이들의 제약상 허용가능한 염을 들 수 있다.
보다 바람직한 본 발명의 화합물로는
(5S)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-페닐-3,5-디히드로-4H-이미다졸-4-온;
(5R)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-(3-펜트-4-엔-1-일페닐)-3,5-디히드로-4H-이미다졸-4-온;
(5R)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-(3-프로프-1-인-1-일페닐)-3,5-디히드로-4H-이미다졸-4-온;
(5R)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-(3-펜트-1-인-1-일페닐)-3,5-디히드로-4H-이미다졸-4-온;
(5R)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-[3-(3-메틸부트-1-인-1-일)페닐]-3,5-디히드로-4H-이미다졸-4-온;
(5R)-2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(3-메톡시프로프-1-인-1-일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
(5R)-2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(4-메톡시부트-1-인-1-일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
(5R)-2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(5-플루오로펜트-1-인-1-일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
(5R)-2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[(3S)-3-히드록시부트-1- 인-1-일]페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
(5R)-2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[4-플루오로-3-(3-메톡시프로프-1-인-1-일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
(5R)-2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[4-플루오로-3-(4-메톡시부트-1-인-1-일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
(5R)-2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[4-플루오로-3-(3-플루오로프로폭시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
(5R)-2-아미노-5-[3-(2,2-디플루오로에톡시)-4-플루오로페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;
(5R)-2-아미노-5-{3-[(4,4-디플루오로부르-3-엔-1-일)옥시]페닐}-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온; 또는
이들의 호변이성질체, 이들의 입체이성질체 또는 이들의 제약상 허용가능한 염을 들 수 있다.
통상적인 합성 방법, 및 필요한 경우 표준 분리 또는 단리 기술을 이용하여 화학식 I의 화합물을 제조할 수 있다. 예를 들어, 화학식 I의 화합물은, 화학식 II의 디케톤을 염기, 예컨대 금속 카르보네이트의 존재하에 화학식 III의 아미노구아니딘 유도체와 반응시켜 목적하는 화학식 I의 화합물을 수득함으로써 제조할 수 있다. 상기 반응을 하기 반응식 I으로 도시한다.
화학식 II의 디케톤 화합물은, 화학식 IV의 알킨을 산화제, 예컨대 Pd(II)Cl/DMSO, N-브로모숙신이미드/DMSO, 오존, 루테늄 (IV) 옥시드 수화물과의 과요오드산나트륨, 삼산화황, KMnO4, I2/DMSO 또는 이들의 조합, 바람직하게는 KMnO4 및 I2/DMSO와 반응시켜 제조할 수 있다. 상기 반응을 하기 반응식 II으로 도시한다.
화학식 IV의 알킨 화합물은, 화학식 V의 에티닐벤젠 화합물을 Pd 촉매, 예컨대 디클로로비스(트리페닐포스핀)팔라듐(II) 및 CuI의 존재하에 4-(디플루오로메톡시)-1-요오도벤젠과 반응시켜 목적하는 화학식 IV의 페닐에티닐벤젠 화합물을 수득함으로써 제조할 수 있다. 상기 반응을 하기 반응식 III으로 도시한다.
유리하게는, 화학식 I의 화합물은 알쯔하이머병, 21번 삼염색체증 (다운 증후군), 네덜란드형의 아밀로이드증성 유전성 뇌출혈 (HCHWA-D) 및 다른 신경퇴행성 장애와 같은 질환과 관련된 β-아밀로이드 침착 또는 신경섬유 농축의 치료를 위한 BACE 억제제로서 작용한다. 따라서, 본 발명의 화합물은 BACE를 조정하는 방법, 및 알쯔하이머병, 21번 삼염색체증 (다운 증후군), 네덜란드형의 아밀로이드증성 유전성 뇌출혈 (HCHWA-D) 또는 다른 신경퇴행성 장애와 같은 질환 및 장애와 관련된 β-아밀로이드 침착 및 신경섬유 농축을 치료, 예방 또는 경감시키는 방법을 제공한다. 이러한 방법은 유효량의 화학식 I의 화합물을, 과도한 BACE 활성과 관련된 질환 또는 손상을 앓고 있거나 여기에 민감한 환자에게 제공하는 것을 포함한다. 또한 본 발명에 따라, 유효량의 본 발명의 화합물을 인간 또는 다른 포유동물에게 투여하는 것을 포함하는, 인간 또는 다른 포유동물에서 알쯔하이머병 및 관련 노인성 치매를 치료하는 방법이 제공된다.
본 발명은 또한, 치료가 필요한 환자에게 치료 유효량의 하나 이상의 화학식 I의 화합물을 제공하는 것을 포함하는, 상기 환자에서 과도한 BACE 활성과 관련되거나 또는 이와 연관된 장애를 치료하는 방법을 제공한다. 대표적인 장애로는 알쯔하이머병, 인지 장애, 다운 증후군, HCHWA-D, 인지 저하, 노인성 치매, 대뇌 아 밀로이드 맥관병증, 퇴행성 치매 또는 다른 신경퇴행성 장애를 들 수 있다. 이들 특정한 질환은 β-아밀로이드 침착 또는 신경섬유 농축의 생성을 특징으로 한다.
본 발명은 또한 유효량의 하나 이상의 화학식 I의 화합물을 환자에게 투여하거나 그의 수용체와 접촉시키는 것을 포함하는, BACE 활성을 억제하는 방법을 제공한다.
본 발명은 또한 유효량의 하나 이상의 화학식 I의 화합물을 포유동물에게 제공하는 것을 포함하는, 상기 포유 동물에서 β-아밀로이드 침착 또는 신경섬유 농축을 경감시키는 방법을 제공한다.
본 발명은 또한 유효량의 하나 이상의 화학식 I의 화합물을 포유동물에게 제공하는 것을 포함하는, 상기 포유 동물에서 알쯔하이머병, 인지 장애, 다운 증후군, HCHWA-D, 인지 저하, 노인성 치매, 대뇌 아밀로이드 맥관병증, 퇴행성 치매 또는 다른 신경퇴행성 장애를 경감시키는 방법을 제공한다.
추가 방법은 알쯔하이머병, 인지 장애, 다운 증후군, HCHWA-D, 인지 저하, 노인성 치매, 대뇌 아밀로이드 맥관병증, 퇴행성 치매 또는 다른 신경퇴행성 장애를 앓고 있거나 앓을 위험이 있을 것으로 예상되는 포유동물에서 상기 질환을 예방한다. 이들 방법은 유효량의 하나 이상의 화학식 I의 화합물을 상기 포유동물에게 제공하는 것을 포함한다.
본 발명에 포함된 화합물 또는 물질을 제공하는 데 있어서 본원에 따라 사용된 용어 "제공하는"은 이러한 화합물 또는 물질을 직접 투여하거나, 또는 체내에서 유효량의 상기 화합물 또는 물질을 형성할 전구약물, 유도체 또는 유사체를 투여하 는 것을 의미한다. 본 발명은 또한 본원에 개시된 질환 상태를 치료하기 위해 치료에 유용한 본 발명의 화합물을 제공하는 것을 포함한다.
본원에 사용된 용어 "환자"는 포유동물, 바람직하게는 인간을 지칭한다.
본원에 사용된 용어 "투여하다", "투여하는" 또는 "투여"는 화합물 또는 조성물을 환자에게 직접 투여하거나, 또는 환자의 체내에서 유효량의 활성 화합물 또는 물질을 형성할 상기 화합물의 전구약물, 유도체 또는 유사체를 환자에게 투여하는 것을 지칭한다.
본원에 사용된 용어 "유효량", "치료 유효량" 및 "효과적인 투여량"은 환자에게 투여되었을 때 환자가 앓고 있는 상태를 적어도 부분적으로 경감시키는 데 (바람직한 실시양태에서는 치료하는 데) 효과적인 화합물의 양을 나타낸다.
본 발명의 활성 화합물의 효과적인 투여량은 사용된 특정 화합물, 투여 방식, 상태, 치료할 상태 및 그의 중증도, 및 치료할 개체과 관련된 다양한 물리적 요인들에 따라 달라질 수 있는 것으로 이해된다. 알쯔하이머병 및 다른 관련 노인성 치매를 치료하는 데 있어서, 치료가 필요한 개체에게 본 발명의 화합물을 체중 1 kg 당 약 0.1 mg 내지 약 1 mg의 일일 투여량으로 투여하는 경우, 바람직하게는 하루에 2 내지 6회 나누어서 투여하거나 또는 지속 방출형으로 투여하는 경우, 일반적으로 만족스러운 결과를 얻을 수 있다. 가장 대형의 포유동물의 경우, 총 일일 투여량은 약 3.5 mg 내지 약 140 mg, 바람직하게는 약 3.5 내지 약 5 mg이다. 70 kg 성인의 경우, 총 일일 투여량은 일반적으로 약 7 mg 내지 약 70 mg일 것이고, 최적의 치료 결과를 제공하기 위해 조절될 수 있다. 상기 요법은 최적의 치료 반응을 제공하기 위해 조절될 수 있다.
한 측면에서, 본 발명은 하나 이상의 화학식 I의 화합물 및 하나 이상의 제약상 허용가능한 담체를 포함하는 조성물에 관한 것이다.
본 발명은 또한 상술한 화학식 I의 화합물 및 제약상 허용가능한 담체를 포함하는 제약 조성물을 포함한다.
본원에 사용된 용어 "담체"는 담체, 부형제 및 희석제를 포함한다. 담체의 예는 당업계에 널리 공지되어 있으며, 허용되는 제약학적 절차에 따라, 예를 들어 그의 전문이 인용을 통해 본원에 포함된 문헌 [Remington's Pharmaceutical Sciences, 17th edition, ed. Alfonoso R. Gennaro, Mack Publishing Company, Easton, PA (1985)]에 기재된 바와 같이 제조된다. 제약상 허용가능한 담체는 제제 중의 다른 성분들과 상용성이고, 생물학적으로 허용되는 것이다.
본 발명의 화합물은 경구 또는 비경구로, 순수하게 또는 통상적인 제약학적 담체와 조합하여 투여될 수 있다. 사용될 수 있는 고체 담체로는 향미제, 윤활제, 가용화제, 현탁화제, 충전제, 활주제, 압축 보조제, 결합제, 정제-붕해제 또는 캡슐화 물질로서 작용할 수 있는 1종 이상의 물질이 있다. 이들은 통상적인 방식으로, 예를 들어 공지된 항고혈압제, 이뇨제 및 β-차단제에 사용되는 것과 유사한 방식으로 제제화된다. 본 발명의 활성 화합물을 함유하는 경구용 제제는 통상적으로 사용되는 임의의 경구 형태, 예컨대 정제, 캡슐, 협측 형태, 트로키제, 로젠지제 및 경구용 액체, 현탁액 또는 용액을 포함할 수 있다. 분말에서, 담체는 미분된 고체일 수 있고, 이는 미분된 활성 화합물과의 혼합물이다. 정제에서, 활성 성 분은 필요한 압축 특성을 갖는 담체와 적합한 비율로 혼합되어, 목적하는 형태 및 크기로 압축된다. 분말제 및 정제는 바람직하게는 활성 성분을 99%까지 함유한다.
캡슐은 활성 화합물과 불활성 충전제 및/또는 희석제, 예컨대 제약상 허용되는 전분 (예를 들어, 옥수수, 감자 또는 타피오카 전분), 당, 인공 감미료, 분말상 셀룰로스, 예컨대 결정형 및 미세결정형 셀룰로스, 밀가루, 젤라틴, 검 등의 혼합물을 함유할 수 있다.
유용한 정제 제제는 통상적인 압축, 습식 과립화 또는 건식 과립화 방법에 의해 제조될 수 있고, 제약상 허용되는 희석제, 결합제, 윤활제, 붕해제, 표면 개질제 (예컨대, 계면활성제), 현탁화제 또는 가용화제, 비제한적인 예로서 스테아르산마그네슘, 스테아르산, 나트륨 라우릴 술페이트, 활석, 당, 락토스, 덱스트린, 전분, 젤라틴, 셀룰로스, 메틸 셀룰로스, 미세결정형 셀룰로스, 나트륨 카르복시메틸 셀룰로스, 카르복시메틸셀룰로스 칼슘, 폴리비닐피롤리돈, 알긴산, 아카시아 검, 크산탄검, 시트르산나트륨, 복합 실리케이트, 탄산칼슘, 글리신, 수크로스, 소르비톨, 인산이칼슘, 황산칼슘, 락토스, 카올린, 만니톨, 염화나트륨, 저융점 왁스 및 이온 교환 수지를 이용할 수 있다. 바람직한 표면 개질제로는 비이온성 및 음이온성 표면 개질제가 있다. 표면 개질제의 대표적인 예로는 폴록사머 188, 벤즈알코늄 클로라이드, 스테아르산칼슘, 세토스테아릴 알콜, 세토마크로골 유화 왁스, 소르비탄 에스테르, 콜로이드성 이산화규소, 포스페이트, 나트륨 도데실술페이트, 마그네슘 알루미늄 실리케이트 및 트리에탄올아민이 있으나, 이로 한정되는 것은 아니다. 본원에서 경구용 제제는 활성 화합물의 흡수성을 변경하기 위해 표준 지연 또는 시간 방출을 이용할 수 있다. 경구용 제제는 또한 적절한 가용화제 또는 유화제를 필요에 따라 함유하는 물 또는 과일 쥬스 중의 활성 성분의 투여로 이루어질 수 있다.
액체 담체는 용액, 현탁액, 에멀젼, 시럽 및 엘릭시르를 제조하는데 이용될 수 있다. 본 발명의 활성 성분은 제약상 허용되는 액체 담체, 예컨대 물, 유기 용매, 이들의 혼합물, 또는 제약상 허용되는 오일 또는 지방에 용해되거나 현탁될 수 있다. 액체 담체는 적합한 제약학적 첨가제, 예컨대 가용화제, 유화제, 완충제, 보존제, 감미제, 향미제, 현탁화제, 증점제, 착색제, 점도 조절제, 안정화제 또는 삼투-조절제를 함유할 수 있다. 경구 및 비경구 투여를 위한 액체 담체의 적합한 예로는 물 (특히, 상기와 같은 첨가제, 예를 들어 셀룰로스 유도체를 함유하는 물, 바람직하게는 나트륨 카르복시메틸 셀룰로스 용액), 알콜 (예컨대, 1가 알콜 및 다가 알콜, 예를 들어 글리콜) 및 이들의 유도체, 및 오일 (예를 들어, 분별화된 코코넛 오일 및 아라키스 오일)이 있다. 비경구 투여를 위해, 담체는 또한 유성 에스테르, 예컨대 에틸 올레에이트 및 이소프로필 미리스테이트일 수 있다. 멸균 액체 담체는 비경구 투여를 위한 멸균 액체 형태 조성물로 사용된다. 가압된 조성물을 위한 액체 담체는 할로겐화 탄화수소 또는 다른 제약상 허용되는 추진제일 수 있다.
멸균 용액 또는 현탁액인 액체 제약 조성물은 예를 들어 근육내, 복막내 또는 피하 주사에 의해 이용될 수 있다. 멸균 용액은 또한 정맥내로 투여될 수 있 다. 경구 투여를 위한 조성물은 액체 또는 고체 형태일 수 있다.
바람직하게는, 제약 조성물은 단위 투여 형태, 예를 들어 정제, 캡슐, 분말, 용액, 현탁액, 에멀젼, 과립 또는 좌약일 수 있다. 이러한 형태에서, 조성물은 활성 성분의 적절한 양을 함유하는 단위 투여량으로 나누어지고, 단위 투여 형태는 포장된 조성물, 예를 들어 패킷화된 분말, 바이알, 앰플, 예비 충전된 시린지 또는 액체 함유 사쉐(sachet)일 수 있다. 단위 투여 형태는 예를 들어 캡슐 또는 정제 자체이거나, 포장된 형태의 적절한 개수의 임의의 조성물일 수 있다. 이러한 단위 투여 형태는 약 1 mg/kg 내지 약 250 mg/kg을 함유할 수 있고, 단일 투여량으로 또는 2회 이상의 나누어진 투여량으로 제공될 수 있다. 이러한 투여량은 수용자의 혈류, 예컨대 경구, 이식편을 통해, 비경구 (예컨대, 정맥내, 복막내 및 피하 주사), 직장, 질 및 경피로 활성 화합물을 향하게 하는데 유용한 임의의 방식으로 투여될 수 있다. 이러한 투여는 로션, 크림, 발포체, 패치, 현탁액, 용액 및 좌약 (직장 및 질)으로서 본 발명의 화합물 또는 그의 제약상 허용가능한 염을 이용하여 수행될 수 있다.
특정 질환 상태 또는 장애의 치료 또는 억제를 위해 투여할 경우, 사용되는 특정 화합물, 투여 방식, 증상 및 그의 중증도뿐 아니라, 치료할 개체와 관련된 다양한 물리학적 인자에 따라 효과적인 투여량이 달라질 수 있음을 이해한다. 치료 용도에서, 본 발명의 화합물은 질환을 이미 앓고 있는 환자에게 상기 질환의 징후 및 그의 합병증을 치료하거나 적어도 부분적으로 경감시키는데 충분한 양으로 제공된다. 이를 달성하는데 적합한 양은 "치료적 유효량"으로 정의된다. 특정한 경우 의 치료에 사용되는 투여량은 의사에 의해 주관적으로 결정되어야 한다. 관련된 변수로는 특정 증상, 및 환자의 크기, 연령 및 반응 패턴이 있다.
일부 경우에, 화합물을 에어로졸 형태로 기도에 직접 투여하는 것이 바람직할 수 있다. 비강내 또는 기관지내 흡입에 의한 투여를 위해, 본 발명의 화합물을 수성 또는 부분 수성 용액으로 제제화할 수 있다.
본 발명의 화합물은 비경구 또는 복막내로 투여될 수 있다. 유리 염기 또는 제약상 허용가능한 염으로서 이들 활성 화합물의 용액 또는 현탁액은 계면활성제, 예컨대 히드록실-프로필셀룰로스와 적합하게 혼합된 물 중에서 제조될 수 있다. 분산액은 또한 오일 중 글리세롤, 액체 폴리에틸렌 글리콜 및 이들의 혼합물로 제조될 수 있다. 저장 및 사용의 일반적인 조건하에, 이들 제제는 미생물의 성장을 억제하는 보존제를 함유한다.
주사용으로 적합한 제약학적 형태는 멸균 수성 용액 또는 분산액, 및 멸균 주사용 용액 또는 분산액의 즉석 제조를 위한 멸균 분말을 포함한다. 모든 경우에, 상기 형태는 멸균이어야 하고, 주사기에 용이하게 존재하는 정도로 유동성이어야 한다. 이는 제조 및 저장 조건하에 안정해야 하고, 박테리아 및 진균과 같은 미생물의 오염 작용으로부터 보호되어야 한다. 담체는 예를 들어, 물, 에탄올, 폴리올 (예를 들어, 글리세롤, 프로필렌 글리콜 및 액체 폴리에틸렌 글리콜), 이들의 적합한 혼합물, 및 식물성유를 함유하는 용매 및 분산 매질일 수 있다.
본 발명의 화합물은 경피 패치의 사용을 통해 경피적으로 투여될 수 있다. 본 발명의 목적상, 경피 투여는 신체 표면, 및 신체 통로의 내부층, 예컨대 상피 및 점막 조직을 가로질러 투여하는 것을 모두 포함하는 것으로 이해한다. 이러한 투여는 로션, 크림, 발포체, 패치, 현탁액, 용액 및 좌약 (직장 및 질)으로서 본 발명의 화합물 또는 그의 제약상 허용가능한 염을 이용하여 수행될 수 있다.
경피 투여는 활성 화합물, 및 상기 활성 화합물에 불활성이고 피부에 무독성이며 피부를 통해 혈류로 전신 흡수를 위한 전달을 가능하게 하는 담체를 함유하는 경피 패치를 사용하여 달성될 수 있다. 담체는 크림 및 연고, 페이스트, 겔 및 폐쇄형 기구와 같은 수많은 형태를 가질 수 있다. 크림 및 연고는 수중유 또는 유중수 유형의 점성 액체 또는 반고체 에멀젼일 수 있다. 활성 성분을 함유하는 석유 또는 친수성 석유에 분산된 흡수성 분말로 이루어진 페이스트 또한 적합할 수 있다. 다양한 폐쇄형 기구, 예컨대 담체의 존재 또는 부재하에 활성 성분을 함유하는 저장소를 둘러싸는 반투과성 막, 또는 활성 섬유를 함유하는 매트릭스를 사용하여 본 발명의 화합물을 혈류로 방출할 수 있다. 다른 폐쇄형 기구는 문헌을 통해 알려져 있다.
본 발명의 화합물은 통상적인 좌약의 형태로 직장 또는 질로 투여될 수 있다. 좌약 제제는 통상적인 물질, 예컨대 좌약의 융점을 변경시키기 위해 왁스가 첨가되거나 첨가되지 않은 코코아 버터, 및 글리세린으로 제조될 수 있다. 수용성 좌약 베이스, 예컨대 다양한 분자량의 폴리에틸렌 글리콜 또한 사용할 수 있다.
특정 실시양태에서, 본 발명은 전구약물에 관한 것이다. 다양한 형태의 전구약물이 당업계에 공지되어 있으며, 예를 들어 그의 전문이 인용을 통해 포함된 문헌 [Bundgaard, (ed.), Design of Prodrugs, Elsevier (1985)], [Widder, et al. (ed.), Methods in Enzymology, vol. 4, Academic Press (1985)], [Krogsgaard-Larsen, et al. (ed.), "Design and Application of Prodrugs", Textbook of Drug Design and Development, Chapter 5, 113-191 (1991)], [Bundgaard, et al., Journal of Drug Deliver reviews, 8:1-38 (1992), Bundgaard, J. of Pharmaceutical Sciences, 77:285 et seq. (1988)] 및 [Higuchi and Stella (eds.) Prodrugs as Novel Drug Delivery Systems, American Chemical Society (1975)]에 논의되어 있다.
이들 화합물의 투여량, 투여 요법 및 방식은 치료할 질병 및 개체에 따라 달라질 것이며, 의사의 판단하에 있음을 이해한다. 본원의 1종 이상의 화합물을 낮은 투여량으로 투여하기 시작하여, 목적하는 효과가 달성될 때까지 투여량을 증가시키는 것이 바람직하다.
본 발명의 이해를 돕고, 본 발명을 더욱 명확하게 설명하기 위해, 구체적인 실시예가 이후 기재된다. 하기 실시예는 단지 예시를 위한 것이며, 본 발명의 범위 및 원리를 어떠한 방식으로도 제한하는 것이 아님을 이해해야 한다.
달리 언급하지 않는 한, 모든 부는 중량부이다. 용어 TEA, DMSO 및 DMF는 각각 트리에틸 아민, 디메틸 술폭시드 및 N,N-디메틸포름아미드를 나타낸다. 용어 EtOAc 및 THF는 각각 에틸 아세테이트 및 테트라히드로푸란을 나타낸다. 용어 NMR은 양성자 핵 자기 공명을 나타내고, 용어 MS는 질량 분광측정 (여기서, (+)는 일반적으로 M+1 (또는 M+H)의 흡수를 제공하는 양의 방식을 나타내고, M은 분자량을 나타냄)을 나타낸다. 모든 화합물은 적어도 MS 및 NMR에 의해 분석된다.
양성자 핵 자기 공명 스펙트럼은 300 MHz에서 브루커 아반스(Bruker AVANCE) 300 분광계 또는 400 MHz에서 배리안(VARIAN) 400 분광계 상에서 얻어졌다. 스펙트럼은 ppm (δ)으로 제공되고, 커플링 상수 J 값은 헤르츠(Hertz)로 기록된다. 테트라메틸실란을 초기 참조 표준물로서 사용하였다. 질량 스펙트럼은 퍼킨 엘머 사이엑스(Perkin Elmer Sciex) 100 상에서 얻어졌다.
(5S)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-페닐-3,5-디히드로-4H-이미다졸-4-온 [A] 및 (5R)-2-아미노-5-[4-(디플루오로메톡시)-페닐]-3-메틸-5-페닐-3,5-디히드로-4H-이미다졸-4-온 [B]의 제조
단계 a) 1-(디플루오로메톡시)-4-(페닐에티닐)벤젠
에티닐벤젠 (1.9 g, 18.5 mmol), 1-(디플루오로메톡시)-4-요오도벤젠 (5 g, 18.5 mmol), N,N-디메틸포름아미드 (35 mL) 및 트리에틸아민 (12.8 mL, 92.6 mmol)의 혼합물에 무수 아르곤을 5분 동안 투입하였다. 이어서, 요오드화구리 (1.85 mmol, 351 mg) 및 디클로로비스(트리페닐포스핀)팔라듐(II) (1.11, 0.71 g)을 상기 혼합물에 첨가하고, 새로운 혼합물을 60 ℃에서 3시간 동안 교반하였다. 상기 혼합물을 실온으로 냉각하고, 물에 붓고, 에틸 에테르로 추출하였다. 유기 추출물을 MgSO4로 건조하였다. 증발시키고, 용리 용매로서 헥산/EtOAc (100/1)를 사용하여 실리카 겔 (ISCO) 상에서 정제하여 1-(디플루오로메톡시)-4-(페닐에티닐)벤젠을 투명 오일로서 수득하였다 (3.45 g, 수율 76%).
단계 b) 1-[4-(디플루오로메톡시)페닐]-2-페닐에탄-1,2-디온
1-(디플루오로메톡시)-4-(페닐에티닐)벤젠 (2.85 g, 11.68 mmol) 및 디메틸술폭시드 (40 mL)의 혼합물에 무수 아르곤 기체를 5분 동안 투입하였다. 이어서, 비스(아세토니트릴)디클로로팔라듐(II) (1.16, 0.3 g)을 상기 혼합물에 첨가하고, 새로운 혼합물을 145 ℃에서 20시간 동안 교반하였다. 상기 혼합물을 실온으로 냉각하고, 물에 붓고, EtOAc로 추출하였다. 유기 추출물을 MgSO4로 건조하였다. 증발시키고, 용리 용매로서 헥산/EtOAc (30/1)를 사용하여 실리카 겔 (ISCO) 상에서 정제하여 1-[4-(디플루오로메톡시)페닐]-2-페닐에탄-1,2-디온을 투명 오일로서 수득하였다 (2.92 g, 수율 91%).
단계 c) 2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-페닐-3,5-디히드 로-4H-이미다졸-4-온
1-[4-(디플루오로메톡시)페닐]-2-페닐에탄-1,2-디온 (3.7 g, 13.4 mmol), 디옥산 (180 mL) 및 EtOH (240 mL)의 혼합물에 1-메틸구아니딘 히드로클로라이드 (6.6 g, 60.3 mmol), 및 H2O (20 mL) 중 Na2CO3 (6.4 g, 60.3 mmol)의 용액을 첨가하였다. 상기 새로운 혼합물을 95 ℃에서 3시간 동안 교반하였다. 이어서, 휘발 물질을 진공하에 제거하고, 잔류물을 물에 분산시키고, EtOAc로 추출하였다. 유기 추출물을 MgSO4로 건조하였다. 증발시키고, 용리 용매로서 MeOH/EtOAc (1/20)를 사용하여 실리카 겔 (ISCO) 상에서 정제하여 2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-페닐-3,5-디히드로-4H-이미다졸-4-온을 백색 고체로서 수득하였다 (3.65 g, 수율 94%).
단계 d) (5S)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-페닐-3,5-디히드로-4H-이미다졸-4-온 [A] 및 (5R)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-페닐-3,5-디히드로-4H-이미다졸-4-온 [B]
2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-페닐-3,5-디히드로-4H-이미다졸-4-온의 라세믹 혼합물을 키랄 크로마토그래피 기술 (키랄셀(Chiralcel) OJ, 0.46 x 10 cm, 이동상으로서 85% 헥산 중 15% 에탄올 및 디에틸아민 사용)로 분리하여 2종의 거울상이성질체를 백색 고체로서 제조하였다: [A] (5S)-2-아미노-5- [4-(디플루오로메톡시)페닐]-3-메틸-5-페닐-3,5-디히드로-4H-이미다졸-4-온,
[B] (5R)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-페닐-3,5-디히드로-4H-이미다졸-4-온,
실시예 2
(5R)-2-아미노-5-(3-브로모페닐)-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
본질적으로 상기 실시예 1, 단계 a 내지 d에 기재된 동일한 절차를 이용하고, 단계 a에서 1-브로모-3-에티닐벤젠을 사용하여 2-아미노-5-(3-브로모페닐)-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 라세믹 혼합물을 수득하고, 키랄 크로마토그래피 기술 (키랄셀 OJ, 2 x 25 cm, 이동상으로서 95% 헥산 중 5% 에탄올 및 디에틸아민 사용)로 분리하여 표제의 거울상이성질체를 수득하였다.
실시예 3
(5R)-2-아미노-5-(3-브로모-4-플루오로페닐)-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
본질적으로 상기 실시예 1, 단계 a 내지 d에 기재된 동일한 절차를 이용하고, 3-브로모-4-플루오로-1-에티닐벤젠을 사용하여 2-아미노-5-(3-브로모-4-플루오로페닐)-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 라세믹 혼합물을 수득하고, 키랄 크로마토그래피 기술 (키랄셀 OJ, 0.46 x 10 cm, 이동상으로서 85% 헥산 중 15% 에탄올 및 디에틸아민 사용)로 분리하여 표제의 거울상이성질체를 수득하였다.
실시예 4
(5R)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-(3-프로필페닐)-3,5-디히드로-4H-이미다졸-4-온 [A] 및 (5S)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-(3-프로필페닐)-3,5-디히드로-4H-이미다졸-4-온 [B]의 제조
단계 a) 2-(3-에티닐페닐)-1,3-디옥솔란
에티닐(트리메틸)실란 (36 g, 367 mmol), 2-(3-브로모페닐)-1,3-디옥솔란 (78 g, 342 mmol), N,N-디메틸포름아미드 (400 mL) 및 트리에틸아민 (1.1 81 mL, mmol)의 혼합물을 무수 아르곤으로 5분 동안 버블링하고, 요오드화구리 (0.94 g, 4.96 mmol) 및 디클로로비스(트리페닐포스핀) 팔라듐(II) (7.7 g, 11.01 mmol)으로 처리하고, 60 ℃에서 3시간 동안 교반하고, 실온으로 냉각하고, 물에 붓고, 에틸 에테르로 추출하였다. 유기 추출물을 합하고, MgSO4로 건조하고, 진공에서 농축하여 {[3-(1,3-디옥솔란-2-일)페닐]에티닐}-(트리메틸)실란을 황색 오일로서 수득하였다 (63 g, 256 mmol). 상기 황색 오일을 MeOH (600 mL) 및 CH2Cl2 (600 mL)에 용해하고, 탄산세슘 (91.8 g, 281.6 mmol)으로 처리하고, 실온에서 10시간 동안 교반하고, 물에 붓고, 에틸 에테르로 추출하였다. 상기 에테르 추출물을 합하고, MgSO4로 건조하고, 진공에서 농축하고, 증류하여 2-(3-에티닐페닐)-1,3-디옥솔란을 황색 오일로서 수득하였다 (42 g, 수율 71%).
단계 b) 2-(3-{[4-(디플루오로메톡시)페닐]에티닐}페닐)-1,3-디옥솔란
본질적으로 상기 실시예 1, 단계 a에 기재된 동일한 절차를 이용하고, 2-(3-에티닐페닐)-1,3-디옥솔란 및 1-(디플루오로메톡시)-4-요오도벤젠을 사용하여 커플링된 생성물을 수득하였다. 상기 생성물을, 용리 용매로서 헥산/EtOAc 5/1을 사용하여 실리카 겔 (ISCO) 상에서 정제하여 2-(3-{[4-(디플루오로메톡시)페닐]에티닐}페닐)-1,3-디옥솔란을 황색 오일로서 수득하였다 (7.9 g, 수율 85%).
단계 c) 3-{[4-(디플루오로메톡시)페닐]에티닐}벤즈알데히드
2-(3-{[4-(디플루오로메톡시)페닐]에티닐}페닐)-1,3-디옥솔란 (1.0 g, 3.1 mmol) 및 THF (5 mL)의 혼합물에 HCl (2 N, 1 mL)을 첨가하였다. 상기 혼합물을 실온에서 2시간 동안 교반하고, 물에 붓고, EtOAc/에틸 에테르 1/1로 추출하였다. 유기 추출물을 MgSO4로 건조하였다. 증발시키고, 용리 용매로서 헥산/EtOAc (3/1)를 사용하여 실리카 겔 (ISCO) 상에서 정제하여 3-{[4-(디플루오로메톡시)페닐]에티닐}벤즈알데히드를 황색 오일로서 수득하였다 (3.65 g, 수율 95%).
단계 d) N'-[(1E)-(3-{[4-(디플루오로메톡시)페닐]에티닐}페닐)메틸렌]-4-메틸벤젠술포노히드라지드
3-{[4-(디플루오로메톡시)페닐]에티닐}벤즈알데히드 (3.69 g, 13.57 mmol), 4-메틸벤젠술포노히드라지드 (2.9 g, 15.6 mmol) 및 EtOH (11 mL)의 혼합물을 30분 동안 환류하고, 실온으로 냉각하고, 물에 붓고, 에틸 에테르로 추출하였다. 유기 추출물을 합하고, MgSO4로 건조하고, 진공에서 농축하였다. 얻어진 잔류물을, 용리 용매로서 헥산/EtOAc (2/1)를 사용하여 실리카 겔 (바이오타지(Biotage)) 상에서 정제하여 N'-[(1E)-(3-{[4-(디플루오로메톡시)페닐]에티닐}페닐)메틸렌]-4-메틸벤젠술포노히드라지드를 황갈색 고체로서 수득하였다 (5.4 g, 수율 90%).
단계 e) 1-{[4-(디플루오로메톡시)페닐]에티닐}-3-프로필벤젠
THF 중 N'-[(1E)-(3-{[4-(디플루오로메톡시)페닐]에티닐}페닐)메틸렌]-4-메틸벤젠술포노히드라지드 (0.67 mg, 1.52 mmol)의 혼합물을 트리에틸 보란 (THF 중 1.0 M, 1.52 mL, 1.52 mmol)으로 처리하고, 2분 동안 교반하고, NaOH (2.5 N, 0.61 mL, 1.52 mmol)로 처리하고, 2시간 동안 환류하고, 실온으로 냉각하고, 물에 붓고, EtOAc로 추출하였다. 유기 추출물을 합하고, MgSO4로 건조하고, 진공에서 농축하였다. 얻어진 잔류물을, 용리 용매로서 헥산/EtOAc (50/1)를 사용하여 실리카 겔 (ISCO) 상에서 정제하여 1-{[4-(디플루오로메톡시)페닐]에티닐}-3-프로필벤젠을 투명 오일로서 수득하였다 (386 mg, 수율 89%).
단계 f) 1-[4-(디플루오로메톡시)페닐]-2-(3-프로필페닐)에탄-1,2-디온
본질적으로 상기 실시예 1, 단계 b에 기재된 동일한 절차를 이용하고, 1-{[4-(디플루오로메톡시)페닐]에티닐}-3-프로필벤젠을 사용하여 디온 생성물을 수득하였다. 상기 생성물을, 용리 용매로서 헥산/EtOAc 30/1을 사용하여 실리카 겔 (ISCO) 상에서 정제하여 1-[4-(디플루오로메톡시)페닐]-2-(3-프로필페닐)-에탄-1,2-디온을 황색 오일로서 수득하였다 (수율 82%).
단계 g) 2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-(3-프로필페닐)-3,5-디히드로-4H-이미다졸-4-온
본질적으로 상기 실시예 1, 단계 c에 기재된 동일한 절차를 이용하고, 1-[4-(디플루오로메톡시)페닐]-2-(3-프로필페닐)에탄-1,2-디온을 사용하여 히단토인 생성물을 수득하였다. 상기 생성물을, 용리 용매로서 헥산/MeOH 20/1을 사용하여 실리카 겔 (ISCO) 상에서 정제하여 2-아미노-5-[4-(디플루오로메톡시)-페닐]-3-메틸-5-(3-프로필페닐)-3,5-디히드로-4H-이미다졸-4-온을 백색 고체로서 수득하였다 (수율 91%).
단계 h) (5R)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-(3-프로필페닐)-3,5-디히드로-4H-이미다졸-4-온 [A] 및 (5S)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-(3-프로필페닐)-3,5-디히드로-4H-이미다졸-4-온 [B]
2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-(3-프로필페닐)-3,5-디히드로-4H-이미다졸-4-온의 라세미 혼합물을 키랄 크로마토그래피 기술 (키랄셀 OJ, 0.46 x 10 cm, 이동상으로서 CO2 (100 bar) 중 20% 에탄올 및 디에틸아민 사용)로 분리하여 2종의 거울상이성질체를 제조하였다: [A] (5R)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-(3-프로필페닐)-3,5-디히드로-4H-이미다졸-4-온,
[B] (5S)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-(3-프로필페닐)-3,5-디히드로-4H-이미다졸-4-온,
실시예 5
(5R)-2-아미노-5-(3-부틸페닐)-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온 [A] 및 (5S)-2-아미노-5-(3-부틸페닐)-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온 [B]의 제조
단계 a) 3-브로모-N-메톡시-N-메틸벤즈아미드
N-메톡시메탄아민 히드로클로라이드 (22.1 g, 228.5 mmol), 디이소프로필 에틸 아민 (63.5 mL, 365.6 mmol) 및 CH2Cl2의 혼합물을 CH2Cl2 중 3-브로모벤조일 클로라이드 (15 g, 68.5 mmol)로 적가 처리하고, 실온에서 30분 동안 교반하고, 진공하에 농축하였다. 얻어진 잔류물을 물에 분산시키고, 에틸 에테르로 추출하였다. 유기 추출물을 합하고, MgSO4로 건조하고, 진공에서 농축하였다. 얻어진 잔류물을, 용리 용매로서 헥산/EtOAc (2/1)를 사용하여 실리카 겔 (바이오타지) 상에서 정제하여 3-브로모-N-메톡시-N-메틸벤즈아미드를 황갈색 고체 (15.1 g, 수율 90%)로서 수득하였다.
단계 b) 1-(3-브로모페닐)부탄-1-온
THF 중 3-브로모-N-메톡시-N-메틸벤즈아미드 (3 g, 12.3 mmol)의 냉각 (0 ℃) 용액을 프로필마그네슘 브로마이드 (6.15 mL, 12.3 mmol)로 처리하고, 실온에서 1시간 동안 교반하고, 수성 NH4Cl로 켄칭하고, HCl (2 N)로 산성화하고, 에틸 에테르로 추출하였다. 유기 추출물을 합하고, MgSO4로 건조하고, 진공하에 농축하였다. 얻어진 잔류물을, 용리 용매로서 헥산/EtOAc (20/1)를 사용하여 실리카 겔 (바이오타지) 상에서 정제하여 1-(3-브로모페닐)부탄-1-온을 황갈색 고체로서 수득하였다 (2.1 g, 수율 75%).
단계 c) 1-브로모-3-부틸벤젠
1-(3-브로모페닐)부탄-1-온 (1.0 g, 4.4 mmol) 및 디글라임 (10 mL)의 혼합 물을 히드라진 (1.49 g, 44 mmol)으로 처리하고, 100 ℃에서 2시간 동안 교반하고, KOH (1.23 g, 22 mmol)로 처리하고, 150 ℃에서 6시간 동안 교반하고, 실온으로 냉각하고, 물에 붓고, 에틸 에테르로 추출하였다. 유기 추출물을 합하고, MgSO4로 건조하고, 진공하에 농축하였다. 얻어진 잔류물을, 용리 용매로서 헥산을 사용하여 실리카 겔 (ISCO) 상에서 정제하여 1-브로모-3-부틸벤젠을 투명 오일로서 수득하였다 (0.81 g, 수율 86%).
단계 d) 1-부틸-3-{[4-(디플루오로메톡시)페닐]에티닐}벤젠
본질적으로 상기 실시예 1, 단계 a에 기재된 동일한 절차를 이용하고, 1-브로모-3-부틸벤젠 및 1-(디플루오로메톡시)-4-에티닐벤젠을 사용하여 페닐에티닐벤젠 생성물을 수득하였다. 상기 생성물을, 용리 용매로서 헥산/EtOAc 50/1을 사용하여 실리카 겔 (바이오타지) 상에서 정제하여 1-부틸-3-{[4-(디플루오로메톡시)페닐]에티닐}벤젠을 무색 오일로서 수득하였다 (0.56 g, 수율 28%).
단계 e) 1-(3-부틸페닐)-2-[4-(디플루오로메톡시)페닐]에탄-1,2-디온
본질적으로 상기 실시예 1, 단계 b에 기재된 동일한 절차를 이용하고, 1-부틸-3-{[4-(디플루오로메톡시)페닐]에티닐}벤젠을 사용하여 디온 생성물을 수득하였다. 상기 생성물을, 용리 용매로서 헥산/EtOAc 30/1을 사용하여 실리카 겔 (ISCO) 상에서 정제하여 1-(3-부틸페닐)-2-[4-(디플루오로메톡시)페닐]-에탄-1,2-디온을 황색 오일로서 수득하였다 (0.39 g, 수율 92%).
단계 f) 2-아미노-5-(3-부틸페닐)-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온
본질적으로 상기 실시예 1, 단계 c에 기재된 동일한 절차를 이용하고, 1-(3-부틸페닐)-2-[4-(디플루오로메톡시)페닐]에탄-1,2-디온을 사용하여 히단토인 생성물을 수득하였다. 상기 생성물을, 용리 용매로서 EtOAc/MeOH 20/1을 사용하여 실리카 겔 상에서 정제하여 2-아미노-5-(3-부틸페닐)-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온을 백색 고체로서 수득하였다.
단계 g) (5R)-2-아미노-5-(3-부틸페닐)-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온 [A] 및 (5S)-2-아미노-5-(3-부틸페닐)-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온 [B]
2-아미노-5-(3-부틸페닐)-5-[4-(디플루오로메톡시)-페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 라세미 혼합물을 키랄 크로마토그래피 기술 [키랄셀 OJ, 0.46 x 10 cm, 이동상으로서 CO2 (100 bar) 중 20% 에탄올 및 디에틸아민 사용]로 분리하여 2종의 거울상이성질체를 생성하였다: [A] (5R)-2-아미노-5-(3-부틸페닐)- 5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온,
[B] (5S)-2-아미노-5-(3-부틸페닐)-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온,
실시예 6 내지 10
2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-(3-치환된-페닐)-3,5-디히드로-4H-이미다졸-4-온 화합물의 제조
본질적으로 상기 실시예 5, 단계 d 내지 f에 기재된 동일한 절차를 이용하고, 적합한 1-브로모-3-알킬벤젠 및 1-(디플루오로메톡시-4-에티닐벤젠)을 사용하여 하기에 나타낸 화합물들을 수득하고, HNMR 및 질량 스펙트럼 분석으로 확인하였다.
실시예 6: 2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-(3-펜틸페닐)-3,5-디히드로-4H-이미다졸-4-온
실시예 7: 2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-[3-(2-메틸부틸)페닐]-3,5-디히드로-4H-이미다졸-4-온
실시예 8: 2-아미노-5-(3-부트-3-엔-1-일페닐)-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온
실시예 9: 2-아미노-5-[3-(시클로프로필메틸)페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온
실시예 10: 3-(3-{2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}페닐)프로판니트릴
실시예 11
(5R)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-(3-펜트-4-엔-1-일페닐)-3,5-디히드로-4H-이미다졸-4-온 [A] 및 (5S)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-(3-펜트-4-엔-1-일페닐)-3,5-디히드로-4H-이미다졸-4-온 [B]의 제조
단계 a) 1-(3-브로모페닐)펜트-4-엔-1-온
THF 중 마그네슘 (0.48 g, 20.29 mmol)의 혼합물을 THF 중 (브로모메틸)시클로프로판 (2.49 g, 18.45 mmol)로 적가 처리하고, 환류 온도에서 1시간 동안 가열하고, 3-브로모-N-메톡시-N-메틸벤즈아미드 (2.5 g, 10.24 mmol)와 THF의 냉각 (0 ℃) 혼합물에 붓고, 실온이 되게 하고, 10분 동안 교반하고, 수성 NH4Cl로 켄칭하고, 에틸 에테르로 추출하였다. 유기 추출물을 합하고, MgSO4로 건조하고, 진공에서 농축하였다. 얻어진 잔류물을, 용리 용매로서 헥산/EtOAc 10/1을 사용하여 실리카 겔 (ISCO) 상에서 정제하여 투명 오일 (2.4 g, 수율 54%)을 수득하였다,
단계 b) 2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-(3-펜트-4-엔-1-일페닐)-3,5-디히드로-4H-이미다졸-4-온
본질적으로 상기 실시예 5, 단계 d 내지 f에 기재된 동일한 절차를 이용하고, 1-(3-브로모페닐)펜트-4-엔-1-온 및 1-(디플루오로메톡시)-4-에티닐벤젠을 사용하여 2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-(3-펜트-4-엔-1-일페닐)-3,5-디히드로-4H-이미다졸-4-온을 수득하였다.
단계 c) (5R)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-(3-펜트-4-엔-1-일페닐)-3,5-디히드로-4H-이미다졸-4-온 [A] 및 (5S)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-(3-펜트-4-엔-1-일페닐)-3,5-디히드로-4H-이미다졸-4-온 [B]
2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-페닐-3,5-디히드로-4H-이미다졸-4-온의 라세미 혼합물을 키랄 크로마토그래피 기술 (키랄팩(Chiralpak) AD, 0.46 x 25 cm, 이동상으로서 90% 헥산 중 10% 에탄올 및 디에틸아민 사용)로 분리하여 2종의 거울상이성질체를 생성하였다: [A] (5R)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-(3-펜트-4-엔-1-일페닐)-3,5-디히드로-4H-이미다졸-4-온,
[B] (5S)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-(3-펜트-4-엔-1-일페닐)-3,5-디히드로-4H-이미다졸-4-온,
실시예 12
N-(3-{(4R)-2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}페닐)-2-메톡시아세트아미드 [A] 및 N-(3-{(4S)-2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}페닐)-2-메톡시아세트아미드 [B]의 제조
단계 a) 3-{[4-(디플루오로메톡시)페닐]에티닐}아닐린
본질적으로 상기 실시예 1, 단계 a에 기재된 동일한 절차를 이용하고, 3-에티닐아닐린 및 1-(디플루오로메톡시)-4-요오도벤젠을 사용하여 페닐에티닐아닐린 생성물을 수득하였다. 상기 생성물을, 용리 용매로서 EtOAc/헥산 1/3을 사용하여 실리카 겔 (ISCO) 상에서 정제하여 3-{[4-(디플루오로-메톡시)페닐]에티닐}아닐린을 황색 고체로서 수득하였다 (수율 95%).
단계 b) N-(3-{[4-(디플루오로메톡시)페닐]에티닐}페닐)-2-메톡시아세트아미드
CH2Cl2 중 3-{[4-(디플루오로메톡시)페닐]에티닐}아닐린 (1 g, 3.86 mmol), 트리에틸아민 (0.65 mL, 4.63 mmol)의 냉각 (0 ℃) 용액을 메톡시아세틸 클로라이드 (0.5 g, 4.63 mmol)로 적가 처리하고, 실온이 되게 하고, 2시간 동안 교반하고, 물에 붓고, EtOAc/에틸 에테르 1/1로 추출하였다. 유기 추출물을 합하고, MgSO4로 건조하고, 진공에서 농축하였다. 얻어진 잔류물을, 용리 용매로서 헥산/EtOAc (1/1)를 사용하여 실리카 겔 (바이오타지) 상에서 정제하여 N-(3-{[4-(디플루오로메톡시)페닐]에티닐}페닐)-2-메톡시아세트아미드를 황색 고체로서 수득하였다 (1.25 g, 수율 94%).
단계 c) N-{3-[[4-(디플루오로메톡시)페닐](옥소)아세틸]페닐}-2-메톡시-아세트아미드
N-(3-{[4-(디플루오로메톡시)페닐]에티닐}페닐)-2-메톡시아세트아미드 (0.68 g, 2.05 mmol), 아세톤, H2O, NaHCO3 (0.1 g , 1.23 mmol) 및 MgSO4 (0.37 g, 3.07 mmol)의 혼합물을 KMnO4 (0.32 g, 2.05 mmol)로 처리하고, 실온에서 4시간 동안 교반하고, 여과하였다. 여액을 물로 희석하고, 에틸 에테르로 추출하였다. 유기 추출물을 합하고, MgSO4로 건조하고, 진공에서 농축하였다. 얻어진 잔류물을, 용리 용매로서 헥산/EtOAc (1/1)를 사용하여 실리카 겔 (바이오타지) 상에서 정제하여 N-{3-[[4-(디플루오로메톡시)페닐](옥소)아세틸]페닐}-2-메톡시아세트아미드를 황색 오일로서 수득하였다 (0.73 g, 수율 98%).
단계 d) N-(3-{2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}페닐)-2-메톡시아세트아미드
본질적으로 상기 실시예 1, 단계 c에 기재된 동일한 절차를 이용하고, N-{3-[[4-(디플루오로메톡시)페닐](옥소)아세틸]페닐}-2-메톡시아세트아미드를 사용하여 히단토인 생성물을 수득하였다. 상기 생성물을, 용리 용매로서 EtOAc/MeOH 10/1을 사용하여 실리카 겔 (ISCO) 상에서 정제하여 N-(3-{2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}페닐)-2-메톡시아세트아미 드를 백색 고체로서 수득하였다 (0.15 g, 수율 70%).
단계 e) N-(3-{(4R)-2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}페닐)-2-메톡시아세트아미드
N-(3-{2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}페닐)-2-메톡시아세트아미드의 라세미 혼합물을 키랄 크로마토그래피 기술 (키랄셀 AD, 2 x 25 cm, 이동상으로서 75% 헥산 중 25% 이소프로판올 및 디에틸아민 사용)로 분리하여 2종의 거울상이성질체를 백색 고체로서 생성하였다: [A] N-(3-{(4R)-2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}페닐)-2-메톡시아세트아미드,
[B] N-(3-{(4S)-2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}페닐)-2-메톡시아세트아미드,
실시예 13
2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-[3-(4,4,4-트리플루오로부 틸)페닐]-3,5-디히드로-4H-이미다졸-4-온의 제조
단계 a) 3-브로모-N-메톡시-N-메틸벤즈아미드
CH2Cl2 중 3-브로모벤질 클로라이드 (20 g, 91.1 mmol)의 용액을 CH2Cl2 중 N,O-디메틸히드록실아민 히드로클로라이드 (33.6 g, 319 mmol), 디이소프로필아민 (98 mL, 551 mmol)의 냉각 (0 ℃) 용액에 1시간에 걸쳐 적가하였다. 실온에서 30분 동안 교반을 계속하고, 이어서 진공하에 농축하였다. 얻어진 잔류물을 물에 분산시키고, 에틸 에테르로 추출하였다. 유기 추출물을 합하고, MgSO4로 건조하고, 진공에서 농축하였다. 상기 잔류물을, 용리 용매로서 헥산/EtOAc (4/1)를 사용하여 실리카 겔 (ISCO) 상에서 정제하여 3-브로모-N-메톡시-N-메틸벤즈아미드를 밝은 황색 고체로서 수득하였다 (20 g, 수율 89%).
단계 b) 1-(3-브로모-페닐)-4,4,4-트리플루오로-부탄-1-온
THF 중 트리플루오로메틸 에탄-마그네슘 브로마이드의 제조 용액 (2시간 동안 THF에서 1-브로모, 2-트리플루오로메틸 에탄과 함께 Mg를 환류하여 제조; 4.6 g = 25.82 mmol)을 THF 중 3-브로모-N-메톡시-N-메틸벤즈아미드 (3.5 g, 14.3 mmol)의 냉각 (0 ℃) 용액에 서서히 첨가하였다. 실온에서 1시간 동안 교반을 계속하고, 냉각 포화 수성 NH4Cl로 켄칭하고, 1 N HCl로 산성화하고, 에틸 에테르로 추출하였다. 유기 추출물을 합하고, MgSO4로 건조하고, 진공에서 농축하였다. 조 생성물을, 용리 용매로서 헥산/EtOAc (10/1)를 사용하여 실리카 겔 (ISCO) 상에서 정제하여 1-(3-브로모-페닐)-4,4,4-트리플루오로-부탄-1-온을 무색 오일로서 수득하였다 (3.1 g, 수율 77%).
단계 c) 1-브로모-3-(4,4,4-트리플루오로-부틸)-벤젠
1-(3-브로모-페닐)-4,4,4-트리플루오로-부탄-1-온 (3.1 g, 11 mmol) 및 디글라임의 혼합물을 히드라진 일수화물 (5.5 g, 110.3 mmol)로 처리하고, 100 ℃에서 2시간 동안 교반하고, 이어서 분말 KOH (3.1 g, 55.1 mmol)로 처리하였다. 150 ℃에서 6시간 동안 교반을 계속하였다. 상기 혼합물을 실온으로 냉각하고, 얼음/물의 혼합물에 붓고, 에틸 에테르로 추출하였다. 추출물을 합하고, MgSO4로 건조하고, 진공에서 농축하였다. 조 생성물을, 용리 용매로서 헥산을 사용하여 실리카 겔 (ISCO) 상에서 정제하여 1-브로모-3-(4,4,4-트리플루오로-부틸)-벤젠을 무색 오일로서 수득하였다 (2.4 g, 수율 88%).
단계 d) 1-디플루오로메톡시-4-[3-(4,4,4-트리플루오로부틸)페닐에티닐]벤젠
본질적으로 상기 실시예 1, 단계 a에 기재된 동일한 절차를 이용하여 1-디플루오로메톡시-4-[3-(4,4,4-트리플루오로부틸)페닐에티닐]벤젠을 무색 오일로서 수득하였다 (0.19 g, 수율 30%).
단계 e) 1-(4-디플루오로메톡시페닐)-2-[3-(4,4,4-트리플루오로부틸)페닐]에탄-1,2-디온
아세톤 중 1-디플루오로메톡시-4-[3-(4,4,4-트리플루오로부틸)페닐에티닐]-벤젠 (7.62 mmol)의 용액을 MgSO4 (1.83 g, 15.25 mmol), 및 이어서 H2O 중 NaHCO3 (0.38 g, 4.57 mmol)의 수용액 및 KMnO4 (2.41 g, 15.24 mmol)로 처리하였다. 현탁액을 20시간 동안 교반하고, H2O 및 에테르로 희석하고, 솔카 플록(solka floc) 패드를 통해 여과하였다. 여액을 에테르로 추출하였다. 상기 추출물을 염수로 세척하고, MgSO4로 건조하고, 진공에서 농축하여 1-(4-디플루오로메톡시페닐)-2-[3-(4,4,4-트리플루오로부틸)페닐]에탄-1,2-디온을 황색 오일로서 수득하였다.
단계 f) 2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-[3-(4,4,4-트리플루오로부틸)페닐]-3,5-디히드로-4H-이미다졸-4-온
본질적으로 상기 실시예 1, 단계 c에 기재된 동일한 절차를 이용하여 표제 화합물 0.11 g (수율 55%, mp 70 ℃)을 백색 고체로서 수득하였다.
실시예 14
5-(3-{2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}페닐)펜탄니트릴의 제조
단계 a) 4-(3-브로모페닐)-4-옥소-부티로니트릴
DMF 중 분말 시안화나트륨 (1.23 g, 25 mmol)의 혼합물을 DMF 중 3-브로모-벤즈알데히드의 용액으로 서서히 처리하고, 35 ℃에서 3시간 동안 교반하고, 실온으로 냉각하고, 냉각한 0.5 N HCl 용액에 붓고, 에틸 에테르로 추출하였다. 추출물을 합하고, 포화 수성 중탄산나트륨, 염수로 세척하고, MgSO4로 건조하고, 진공에서 농축하였다. 얻어진 잔류물 에틸 에테르로 처리하고, 여과하였다. 여과케이크를 건조하여 4-(3-브로모페닐)-4-옥소-부티로니트릴을 황색 고체로서 수득하였다 (4 g, 수율 58%).
단계 b) 4-(3-브로모페닐)부티르산
실질적으로 상기 실시예 3, 단계 c에 기재된 바와 동일한 방식으로 표제 화합물을 제조하여 밝은 갈색 오일로서 수득하였다 (2.85 g, 수율 93%).
단계 c) 4-(3-브로모페닐)부탄-1-올
THF 중 4-(3-브로모페닐)부티르산 (2.85 g, 11.7 mmol)의 냉각 (0 ℃) 용액을 B2H6-THF (35 mL)의 용액으로 서서히 처리하고, 실온에서 18시간 동안 교반하고, 얼음/물에 붓고, 2.5 N NaOH를 사용하여 pH 11로 염기화하하고, CH2Cl2로 추출하였다. 상기 추출물을 합하고, 염수로 세척하고, MgSO4로 건조하고, 진공에서 농축하였다. 얻어진 잔류물을, 용리 용매로서 헥산/CH2Cl2/MeOH (4/4.5/0.5)를 사용하여 칼럼 크로마토그래피로 정제하여 4-(3-브로모페닐)부탄-1-올을 무색 오일로서 수득하였다 (1.9 g, 수율 70%).
단계 d) 톨루엔-4-술폰산 4-(3-브로모-페닐)부틸 에스테르
THF 중 4-(3-브로모페닐)부탄-1-올 (1.08 g, 4.7 mmol) 및 p-톨루엔술포닐 클로라이드 (1.2 g, 6.3 mmol)의 냉각 (0 ℃) 용액을 트리에틸 아민 (1.8 mL, 12.3 mmol)으로 서서히 처리하고, 실온에서 4시간 동안 교반하고, 냉각한 포화 수성 NH4Cl에 붓고, 에테르로 추출하였다. 유기 추출물을 합하고, 염수로 세척하고, MgSO4로 건조하고, 진공에서 농축하였다. 얻어진 잔류물을, 용리 용매로서 헥산/EtOAC 9.5/0.5를 사용하여 실리카 겔 (ISCO) 상에서 정제하여 톨루엔-4-술폰산 4-(3-브로모페닐)-부틸 에스테르를 무색 오일로서 수득하였다 (2.4 g, 수율 76%).
단계 e) 5-(3-브로모페닐)펜탄니트릴
DMSO 중 톨루엔-4-술폰산 4-(3-브로모페닐)부틸 에스테르 (2.3 g, 6 mmol) 및 시안화나트륨 분말 (0.65 g, 13 mmol)의 혼합물을 80 ℃ 이하로 가열하고, 1.5시간 동안 교반하고, NMR로 모니터링하였다. 반응이 완료되었을 때, 상기 반응 혼합물을 실온으로 냉각하고, H2O로 희석하고, CH2Cl2로 추출하였다. 합한 유기 추출물을 염수로 세척하고, MgSO4로 건조하고, 진공에서 농축하였다. 상기 잔류물을, 용리 용매로서 헥산/EtOAC 9.5/0.5를 사용하여 실리카 겔 (ISCO) 상에서 정제하여 5-(3-브로모-페닐)펜탄니트릴을 무색 오일로서 수득하였다 (1.12 g, 수율 78%).
단계 f) 5-[3-(4-디플루오로메톡시페닐에티닐)페닐]펜탄니트릴
본질적으로 상기 실시예 1, 단계 a에 기재된 동일한 절차를 이용하여 5-[3- (4-디플루오로메톡시페닐에티닐)페닐]펜탄니트릴을 밝은 갈색 오일로서 수득하였다 (0.54 g, 수율 88%).
단계 g) 5-{3-[2-(4-디플루오로메톡시페닐)-2-옥소-아세틸]페닐}펜탄니트릴
본질적으로 상기 실시예 13, 단계 e에 기재된 동일한 절차를 이용하여 5-{3-[2-(4-디플루오로메톡시페닐)-2-옥소-아세틸]페닐}펜탄니트릴을 밝은 황색 오일로서 수득하였다 (0.46 g, 수율 77%).
단계 h) 5-(3-{2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}페닐)펜탄니트릴.
본질적으로 상기 실시예 1, 단계 c에 기재된 동일한 절차를 이용하여 표제 화합물 0.23 g (수율 43%, mp 65 ℃)을 백색 고체로서 수득하였다.
실시예 15
4-(3-{2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}페닐)부탄니트릴의 제조
본질적으로 상기 실시예 14에 기재된 동일한 절차를 이용하고, 3-(3-브로모페닐)프로판산을 사용하여 표제 생성물 0.23 g (수율 48%, mp 75 ℃)을 백색 고체로서 수득하였다.
실시예 16
2-아미노-5-[3-(1,4-디플루오로부틸)페닐]-5-[4-(디플루오로메톡시)-페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
단계 a) 4-(3-브로모페닐)부트-3-인-1-올
DMF 중 3-요오도-브로모벤젠 10.0 gm (35.3 mmol)의 용액을 4-부틴-1-올 2.95 mL (88 mmol), 요오드화구리(I) 0.2 gm (1.06 mmol), 디클로로비스(트리페닐포스핀)-팔라듐(II) 1.23 gm 및 트리에틸아민 49 mL (0.35 mol)로 처리하고, 실온에서 18시간 동안 교반하고, 물에 붓고, EtOAc로 추출하였다. 합한 추출물을 물 및 염수로 연속적으로 세척하고, Na2SO4로 건조하고, 감압하 농축하였다. 얻어진 농축물을 5% 내지 30% EtOAc-헥산 농도구배를 이용하여 실리카 겔 상에서 크로마토그래피하여 4-(3-브로모페닐)부트-3-인-1-올 7.3 gm (수율 92%)을 오렌지색 오일로서 수득하였다.
단계 b) 1-브로모-3-(4-플루오로-부트-1-이닐)벤젠
0 ℃에서 CH2Cl2 중 4-(3-브로모페닐)부트-3-인-1-올 1.5 gm (6.67 mmol)의 용액을 DAST 2.0 mL (15.3 mmol)로 처리하고, 0 ℃에서 1시간 동안 교반하고, 1시간 동안 실온으로 가온하고, 포화 중탄산나트륨에 붓고, EtOAc로 추출하였다. 합한 추출물을 물 및 염수로 연속적으로 세척하고, Na2SO4로 건조하고, 감압하 농축하였다. 얻어진 농축물을 0% 내지 24% EtOAc-헥산 농도구배를 이용하여 실리카 겔 상에서 크로마토그래피하여 1-브로모-3-(4-플루오로-부트-1-이닐)벤젠 0.96 gm (수율 64%)을 휘발성 액체로서 수득하였다.
단계 c) 1-(3-브로모페닐)-4-플루오로부탄-1-온
1-브로모-3-(4-플루오로부트-1-이닐)벤젠 0.2 gm (0.89 mmol), MeOH 2 mL, 메틸(트리페닐포스핀)금 (I) 1 mg, 진한 H2SO4 25 ㎕ 및 H2O 0.44 mL의 혼합물을 밀봉된 튜브에 두고, 아르곤으로 플러싱하고, 2시간 동안 72 ℃로 가열하고, 냉각하였다. 상기 반응 혼합물을 EtOAc로 희석하고, 물 및 염수로 연속적으로 세척하고, Na2SO4로 건조하고, 감압하 농축하였다. 상기 농축물을 0% 내지 20% EtOAc-헥산 농도구배를 이용하여 실리카 겔 상에서 크로마토그래피하여 1-(3-브로모페닐)-4-플루오로부탄-1-온 0.086 gm (수율 40%)을 오일로서 수득하였다.
단계 d) 1-브로모-3-(1,4-디플루오로-부틸)벤젠
0 ℃에서 THF 중 1-(3-브로모-페닐)-4-플루오로부탄-1-온 0.3 gm (1.22 mmol)의 용액을 고체 NaBH4 0.055 gm (1.47 mmol)으로 처리하고, 0 ℃에서 0.5시간 동안 교반하고, 실온으로 가온하고, 18시간 동안 교반하고, 수성 NH4Cl로 켄칭하고, EtOAC에 부었다. 상들을 분리하였다. 유기상을 물 및 염수로 연속적으로 세척하고, Na2SO4로 건조하고, 감압하에 농축하여 1-(3-브로모페닐)-4-플루오로부탄-1-올 0.29 gm (수율 96%)을 오일로서 수득하였다. 상기 오일을 CH2Cl2에 용해하고, 0 ℃로 냉각하고, DAST 0.23 mL (1.75 mmol)로 처리하고, 0 ℃에서 0.5시간 동안 교반하고, 실온으로 가온하고, 실온에서 18시간 동안 교반하고, 물로 켄칭하고, EtOAc에 부었다. 상들을 분리하였다. 유기상을 물 및 염수로 연속적으로 세척하고, Na2SO4로 건조하고, 감압하에 조심스럽게 농축하였다. 상기 농축물을 더이상 정제하지 않고 단계 e에서 사용하였다.
단계 e) 1-(3-{[4-(디플루오로메톡시)페닐]에티닐}페닐)-1,4-디플루오로부탄
디옥산 중 비스(벤조니트릴)디클로로팔라듐(II) 13 mg (0.034 mmol)의 탈기 용액에 헥산 중 10% (wt/wt) 트리-t-부틸포스핀 0.145 gm (0.072 mmol)을 첨가하였다. 상기 반응 혼합물을 실온에서 15분 동안 교반하고, 요오드화구리(I) 4.3 mg 및 이어서 디이소프로필아민 0.21 mL로 처리하고, 10분 동안 교반하고, 디옥산 2 mL에 용해된 1-브로모-3-(1,4-디플루오로-부틸)벤젠 0.28 gm (1.14 mmol) 및 1-디플루오로메톡시-4-에티닐-벤젠 0.25 gm (1.48 mmol)으로 처리하였다. 상기 반응 혼합물을 35 ℃로 0.5 시간 동안 교반하고, 실온으로 냉각하고, 실온에서 3시간 동안 교반하고, EtOAc에 부었다. 유기상을 분리하고, 물 및 염수로 연속적으로 세척하고, Na2SO4로 건조하고, 감압하 농축하였다. 상기 농축물을 0% 내지 25% EtOAc-헥산 농도구배를 이용하여 실리카 겔 상에서 크로마토그래피하여 1-(3-{[4-(디플루오로메톡시)페닐]에티닐}페닐)-1,4-디플루오로부탄 0.314 gm (수율 82%)을 오일로서 수득하였다.
단계 f) 2-아미노-5-[3-(1,4-디플루오로부틸)페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온
본질적으로 상기 실시예 13, 단계 e 및 실시예 1, 단계 c에 기재된 동일한 절차를 이용하고, 출발 물질로서 1-(3-{[4-(디플루오로메톡시)페닐]에티닐}페닐)-1,4-디플루오로부탄을 사용하여 표제 생성물을 포말성 고체로서 수득하였다. mp 54-57 ℃;
실시예 17
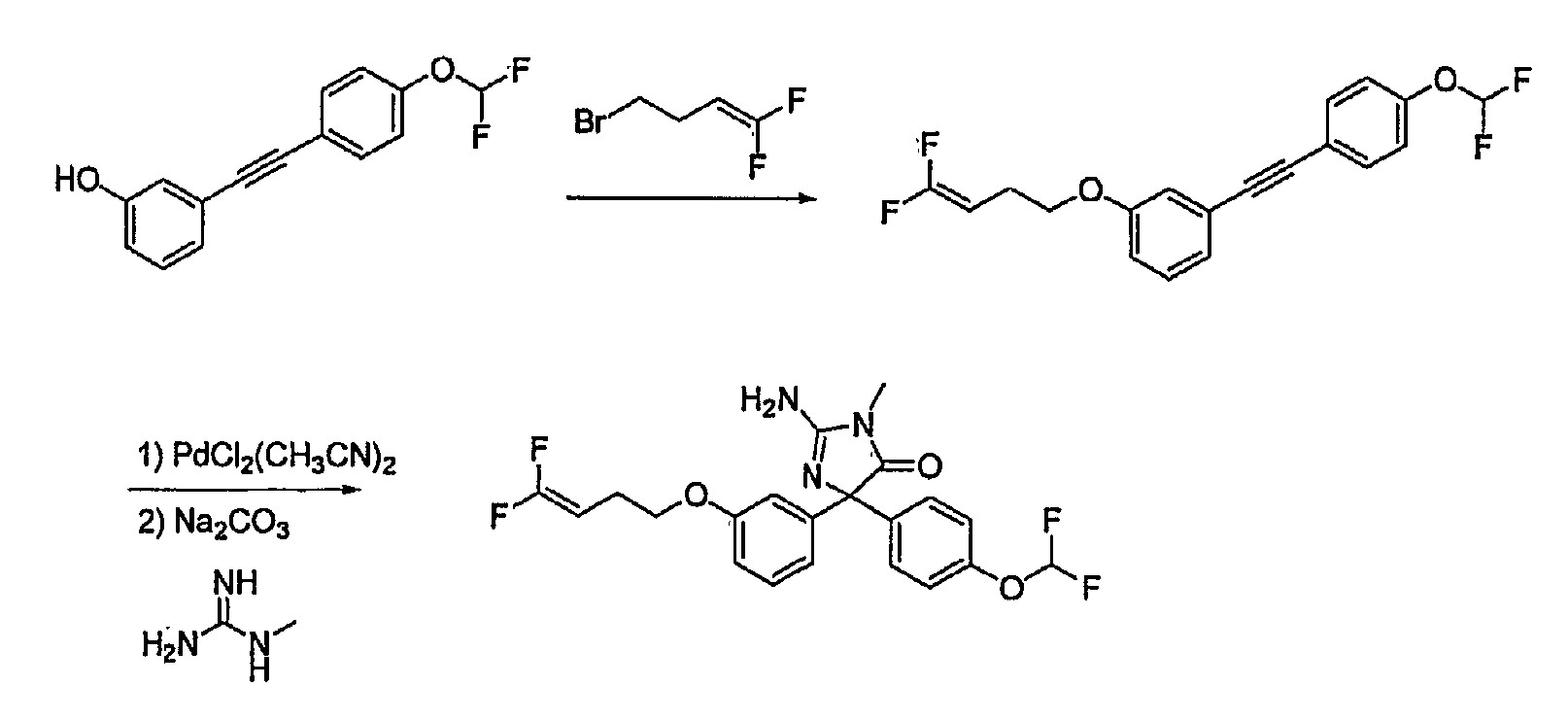
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(3-플루오로부트-3-엔-1-일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
단계 a) 1-브로모-3-부트-3-에닐벤젠
0 ℃에서 THF 중 메틸트리페닐포스포늄 브로마이드 1.34 gm (3.77 mmol)의 용액을 헥산 (3.77 mmol) 중 1.6 M n-BuLi 2.3 mL로 적가 처리하고, 0 ℃에서 0.25시간 동안 교반하고, -78 ℃로 냉각하고, THF 중 3-(3-브로모페닐)프로피온알데히드 (0.7 gm, 3.28 mmol) 용액으로 적가 처리하고, -78 ℃에서 1시간 동안 교반하고, 실온으로 가온하고, 수성 NH4Cl로 켄칭하고, 감압하 농축하였다. 얻어진 잔류물을 EtOAc에 용해하고, 물 및 염수로 연속적으로 세척하고, Na2SO4로 건조하고, 감압하 농축하였다. 상기 농축물을 0.5% EtOAc-헥산 내지 2.0% EtOAc-헥산의 농도구배를 이용하여 실리카 겔 상에서 크로마토그래피하여 1-브로모-3-부트-3-에닐벤젠 0.35 gm (수율 50%)을 오일로서 수득하였다.
단계 b) 1-브로모-3-(3-플루오로-4-요오도-부틸)-벤젠
0 ℃에서 CH2Cl2 중 1-브로모-3-부트-3-에닐벤젠 0.245 gm (1.16 mmol)의 용 액을 CH2Cl2 중 N-요오도숙신이미드 0.39 gm (1.74 mmol) 및 50% wt/wt 테트라부틸암모늄디히드로겐 트리플루오라이드 1.05 gm (1.74 mmol)로 처리하고, 0 ℃에서 2시간 동안 교반하고, 1시간에 걸쳐 실온으로 가온하고, CH2Cl2에 부었다. 얻어진 유기상을 물 및 염수로 연속적으로 세척하고, Na2SO4로 건조하고, 감압하 농축하였다. 상기 농축물을 헥산 내지 7.0% EtOAc-헥산의 농도구배를 이용하여 실리카 겔 상에서 크로마토그래피하여 1-브로모-3-(3-플루오로-4-요오도-부틸)-벤젠 0.40 gm (수율 50%)을 오일로서 수득하였다.
단계 c) 1-브로모-3-(3-플루오로부트-3-에닐)벤젠
CH2Cl2 중 1-브로모-3-(3-플루오로-4-요오도부틸)-벤젠 0.405 gm (1.1 mmol)의 용액을 실온에서 DBU 0.82 mL (5.5 mmol)로 처리하고, 실온에서 24시간 동안 교반하고, EtOAc에 부었다. 얻어진 유기상을 물 및 염수로 연속적으로 세척하고, Na2SO4로 건조하고, 감압하 농축하였다. 상기 농축물을 헥산 내지 7.0% EtOAc-헥산의 농도구배를 이용하여 실리카 겔 상에서 크로마토그래피하여 1-브로모-3-(3-플루오로부트-3-에닐)벤젠 0.20 gm (수율 80%)을 오일로서 수득하였다.
단계 d) 2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(3-플루오로부트-3-엔 -1-일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온
본질적으로 상기 실시예 1, 단계 a, b 및 c에 기재된 동일한 절차를 이용하고, 출발 물질로서 1-브로모-3-(3-플루오로부트-3-에닐)벤젠을 사용하여 표제 생성물을 황색-황갈색 포말성 고체로서 수득하였다. mp 58-60 ℃;
실시예 18
2-아미노-5-[3-(4,4-디플루오로부트-3-엔-1-일)페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
단계 a) 3-[3-(4-디플루오로메톡시페닐에티닐)페닐]프로피온알데히드
본질적으로 상기 실시예 16, 단계 e에 기재된 동일한 절차를 이용하고, 1-브로모-3-(1,4-디플루오로-부틸)벤젠 대신 3-(3-브로모페닐)프로피온알데히드를 사용하여 3-[3-(4-디플루오로메톡시-페닐에티닐)페닐]프로피온알데히드를 수율 42%로 오일로서 수득하였다. 상기 오일을 더이상 정제하지 않고 다음 단계에서 사용하였다.
단계 b) 1-(3-{[4-(디플루오로메톡시)페닐]에티닐}페닐)-4,4-디플루오로부트-3-엔
-78 ℃에서 THF 중 디이소프로필아민 0.122 mL (0.86 mmol)의 용액으로 헥산 중 1.6 M n-BuLI 0.54 mL (0.54 mmol)로 처리하고, -78 ℃에서 0.5시간 동안 교반하고, THF 중 디플루오로메틸디페닐포스핀 옥시드 0.22 gm (0.86 mmol)의 용액으로 적가 처리하고, -78 ℃에서 45분 동안 교반하고, THF 중 3-[3-(4-디플루오로메톡시페닐에티닐)페닐]프로피온알데히드 0.17 gm (0.58 mmol)의 용액으로 처리하고, -78 ℃에서 4시간 동안 교반하고, 실온으로 가온하고, 실온에서 18시간 동안 교반하고, CH2Cl2로 희석하였다. 유기상을 물 및 염수로 연속적으로 세척하고, Na2SO4로 건조하고, 감압하 농축하였다. 상기 농축물을 헥산 내지 10% EtOAc-헥산의 농도구배를 이용하여 실리카 겔 상에서 크로마토그래피하여 1-(3-{[4-(디플루오로메톡시)페닐]에티닐}-페닐)-4,4-디플루오로부트-3-엔 0.09 gm (수율 52%)을 오일로서 수득하였다.
단계 c) 2-아미노-5-[3-(4,4-디플루오로부트-3-엔-1-일)페닐]-5-[4-(디플루오로메톡시)-페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온
본질적으로 상기 실시예 1, 단계 b 및 c에 기재된 동일한 절차를 이용하고, 출발 물질로서 1-(3-{[4-(디플루오로메톡시)페닐]에티닐}페닐)-4,4-디플루오로부트-3-엔을 사용하여 표제 화합물을 밝은 황색 고체로서 수득하였다. mp 59-62 ℃;
실시예 19
2-아미노-5-[3-(4,4-디플루오로부틸)페닐]-5-[4-(디플루오로메톡시)-페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
단계 a) 1-브로모-3-(4,4-디플루오로부틸)벤젠
펜탄 중 4-(3-브로모페닐)부티르알데히드 (0.6 g, 2.6 mmol)의 용액을 펜탄 중 삼불화 디에틸아미노황 (DAST) 용액으로 처리하고, 실온에서 1시간 동안 교반하고, 물에 붓고, 에테르로 추출하였다. 추출물을 합하고, 염수로 세척하고, 황산마그네슘으로 건조하고, 진공에서 농축하였다. 얻어진 잔류물을 헥산 중 실리카 겔 상에서 플래시 크로마토그래피로 정제하여 1-브로모-3-(4,4-디플루오로부틸)-벤젠 0.36 g (수율 54%)을 투명 오일로서 수득하였다.
질량 스펙트럼 [(+)ESI] m/z = 248 [M-H]+.
단계 b) 2-아미노-5-[3-(4,4-디플루오로부틸)페닐]-5-[4-(디플루오로메톡시)-페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온
본질적으로 상기 실시예 18, 단계 a 및 c에 기재된 동일한 절차를 이용하고, 반응물로서 1-브로모-3-(4,4-디플루오로부틸)-벤젠 및 1-디플루오로메톡시-4-에티닐벤젠을 사용하여 표제 화합물 0.17 g (수율 42%)을 백색 고체로서 수득하였다.
실시예 20
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(4-히드록시부트-1-인-1-일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
아르곤하 요오드화구리 (8 mg, 0.04 mmol), 비스(벤조니트릴)디클로로 팔라듐(II) (23 mg, 0.06 mmol) 및 무수 디옥산의 혼합물을 3분 동안 교반하고, 트리-t-부틸 포스핀 (헥산 중 10%) (240 mg, 0.12 mmol)으로 처리하고, 5분 동안 교반 하고, 디이소프로필 아민 (0.33 mL, 2.4 mmol), 및 이어서 디옥산 중 2-아미노-5-(3-브로모페닐)-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온 (0.82 g, 2 mmol)의 용액 및 1-히드록시-2-프로판 (0.47 mL, 0.006 mmol)으로 처리하였다. 상기 반응 혼합물을 30분 동안 35 ℃로 가열하고, 물에 붓고, 에틸 아세테이트로 추출하였다. 추출물을 합하고, 염수로 세척하고, 황산나트륨으로 건조하고, 감압하 농축하였다. 얻어진 잔류물을 용리액으로서 먼저 에틸 아세테이트 및 이어서 5% 메탄올/에틸 아세테이트에서 실리카 겔 상의 플래시 크로마토그래피로 정제하여 표제 화합물 0.39 g (수율 48%, mp 90-93 ℃)을 백색 고체로서 수득하였다.
실시예 21
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(4-히드록시부틸)-페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
에탄올 중 2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(4-히드록시부트-1-인-1-일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온 (0.26 g, 0.65 mmol)의 용액 및 목탄 상 5% 팔라듐 (26 mg)의 혼합물을 8시간 동안 수소 40 psi에서 파 르(Paar) 수소첨가기에 두었다. 상기 반응 혼합물을 셀라이트 패드를 통해 여과하였다. 여액을 진공에서 농축하였다. 얻어진 잔류물을 용리액으로 5% 메탄올/에틸 아세테이트를 사용하여 실리카 겔 상에서 플래시 크로마토그래피로 정제하여 표제 화합물 0.16 g (수율 61%, mp 63-66 ℃)을 백색 고체로서 수득하였다.
실시예 22
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(3-메톡시프로프-1-인-1-일)-페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
피롤리딘 중 2-아미노-5-(3-브로모페닐)-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온 (0.65 g, 1.6 mmol)의 용액을 3-메톡시-프로핀 (0.27 mL, 3.2 mmol) 및 이어서 테트라키스(트리페닐포스핀) 팔라듐(0) (90 mg, 0.08 mmol)으로 처리하고, 4시간 동안 80 ℃로 가열하고, 물에 붓고, 에틸 아세테이트로 추출하였다. 추출물을 합하고, 물 및 염수로 연속적으로 세척하고, 황산나트륨으로 건조하고, 진공에서 농축하였다. 얻어진 잔류물을 에틸 아세테이트에서 실리카 겔 상의 플래시 크로마토그래피로 정제하여 표제 화합물 0.4 g (수율 63%) 을 갈색 왁스로서 수득하고, NMR 및 질량 스펙트럼 분석으로 확인하였다.
실시예 23
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[(1Z)-3-메톡시프로프-1-엔-1-일]페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
에탄올 (1.5 mL) 중 2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(3-메톡시프로프-1-인-1-일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온 (0.1 g, 0.25 mmol)의 용액, 퀴놀린 (1 방울) 및 린들라(Lindlar) 촉매 (24 mg. 10% mol)의 혼합물을 수소 충전된 벌룬하에 두고, 16시간 동안 교반하고, 셀라이트를 통해 여과하였다. 여액을 진공에서 농축하였다. 얻어진 잔류물을 용리액으로서 에틸 아세테이트를 사용하여 실리카 겔 상에서 플래시 크로마토그래피로 정제하여 표제 화합물 0.05 g (수율 50%, mp 41-44 ℃)을 백색 고체로서 수득하였다.
실시예 24
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(3-메톡시프로필)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(3-메톡시프로프-1-인-1-일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온 (0.1 g, 0.25 mmol)의 에탄올 용액 및 목탄 상 10% 팔라듐 (10 mg)의 혼합물을 수소 충전된 벌룬하에 16시간 동안 두고, 셀라이트를 통해 여과하였다. 여액을 진공에서 농축 건조하였다. 얻어진 잔류물을 용리액으로서 에틸 아세테이트를 사용하여 실리카 겔 상에서 플래시 크로마토그래피로 정제하여 표제 화합물 0.04 g (수율 40%, mp 48-50 ℃)을 백색 고체로서 수득하였다.
실시예 25
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(5-플루오로펜틸)-페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
단계 a) 5-(3-브로모페닐)펜탄-1-올
5-(3-브로모-페닐)-펜트-4-인-1-올 (실시예 3, 단계 a) (1 g, 4.2 mmol)의 에탄올 용액 및 산화백금 (24 mg, 10% mol)의 혼합물을 4시간 동안 수소 40 psi하 파르 진탕기에 두었다. 상기 반응 혼합물을 셀라이트를 통해 여과하였다. 여액을 진공에서 농축하였다. 얻어진 잔류물을 용리액으로서 먼저 10:1 헥산/에틸 아세테이트, 이어서 2:1 헥산/에틸 아세테이트를 사용하여 실리카 겔 상에서 플래시 크로마토그래피로 정제하여 5-(3-브로모페닐)펜탄-1-올 0.75 g (수율 74%)을 투명 오일으로서 수득하였다.
단계 b) 1-브로모-3-(5-플루오로펜틸)벤젠
-78 ℃에서 염화메틸렌 중 5-(3-브로모페닐)펜탄-1-올 (0.63 g, 2.6 mmol)의 용액을 염화메틸렌 중 삼불화 디에틸아미노황 (DAST) (0.7 mL, 5.2 mmol)의 용액으로 처리하고, 실온으로 가온하고, 실온에서 0.5시간 동안 교반하고, 물에 붓고, 에 테르로 추출하였다. 추출물을 합하고, 포화 중탄산나트륨 및 물로 연속적으로 세척하고, 황산마그네슘으로 건조하고, 감압하 농축하였다. 상기 농축물을 용리액으로서 40:1 헥산/에틸 아세테이트를 사용하여 실리카 겔 상에서 플래시 크로마토그래피로 정제하여 1-브로모-3-(5-플루오로펜틸)벤젠 0.4 g (수율 63%)을 담황색 오일로서 수득하였다.
단계 c) 2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(5-플루오로펜틸)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온
본질적으로 상기 실시예 18, 단계 a 및 c에 기재된 동일한 절차를 이용하고, 반응물로서 1-브로모-3-(5-플루오로펜틸)벤젠 및 1-디플루오로메톡시-4-에티닐벤젠을 사용하여 표제 화합물 0.04 g (수율 18%)을 백색 고체로서 수득하였다.
실시예 26
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(4-플루오로부틸)-페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
본질적으로 상기 실시예 25에 기재된 동일한 절차를 이용하고, 1-브로모-3- (4-플루오로부틸)벤젠을 사용하여 표제 화합물을 백색 고체로서 수득하였다.
실시예 27
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(6-플루오로헥실)-페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
본질적으로 상기 실시예 25에 기재된 동일한 절차를 이용하고, 1-브로모-3-(6-플루오로헥실)벤젠을 사용하여 표제 화합물을 백색 고체로서 수득하였다.
실시예 28
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(6-플루오로헥실)-페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
단계 a) 1-브로모-3-(4-메톡시부틸)벤젠
수소화나트륨 [오일 중 60%] (130, mg, 3.3 mmol) 및 THF의 혼합물을 -5 ℃로 냉각하고, 주사기를 통해 1분에 걸쳐 THF 중 4-(3-브로모페닐)부탄-1-올 (0.7 g, 3.0 mmol)의 용액으로 처리하고, 실온으로 가온하고, 실온에서 0.5시간 동안 교반하고, 요오드화메틸 (4.6 g, 35 mmol)로 처리하고, 2시간 동안 교반하고, 포화 염화암모늄에 붓고, 에테르로 추출하였다. 추출물을 합하고, 염수로 세척하고, 황산 마그네슘으로 건조하고, 진공에서 농축하였다. 얻어진 잔류물을 용리액으로서 40:1 헥산/에틸 아세테이트를 사용하여 실리카 겔 상에서 플래시 크로마토그래피로 정제하여 1-브로모-3-(4-메톡시부틸)벤젠 0.38 g (수율 51%)을 투명 오일로서 수득하였다.
단계 b) 2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(4-메톡시부틸)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온
본질적으로 상기 실시예 18, 단계 a 및 c에 기재된 동일한 절차를 이용하고, 반응물로서 1-브로모-3-(4-메톡시부틸)벤젠 및 1-디플루오로메톡시-4-에티닐벤젠을 사용하여 표제 화합물을 백색 고체로서 수득하였다. mp 36-39 ℃;
실시예 29
3-{2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}-N-프로필벤즈아미드의 제조
단계 a) 3-브로모-N-프로필-벤즈아미드
염화메틸렌 중 N-프로필 아민 (0.33 mL, 4.1 mmol) 및 트리에틸아민 (0.83 mL, 5.8 mmol)의 혼합물을 -5 ℃로 냉각하고, 3-브로모벤조일 클로라이드 (1 g, 4.5 mmol)로 처리하고, 실온으로 가온하고, 실온에서 1시간 동안 교반하고, 수성 중탄산나트륨에 붓고, 염화메틸렌으로 추출하였다. 추출물을 합하고, 물 및 염수로 연속적으로 세척하고, 황산마그네슘으로 건조하고, 감압하 농축하였다. 얻어진 잔류물을 용리액으로서 2:1 헥산/에틸 아세테이트를 사용하여 실리카 겔 상에서 플래시 크로마토그래피로 정제하여 3-브로모-N-프로필-벤즈아미드 0.74 g (수율 67%)을 백색 고체로서 수득하였다.
단계 b) 3-{2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}-N-프로필벤즈아미드
본질적으로 상기 실시예 18, 단계 a 및 c에 기재된 동일한 절차를 이용하고, 반응물로서 3-브로모-N-프로필-벤즈아미드 및 1-디플루오로메톡시-4-에티닐-벤젠을 사용하여 표제 화합물을 백색 고체로서 수득하였다. mp 93-96 ℃;
실시예 30
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[(2-플루오로에톡시)-메틸]페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
단계 a) 1-브로모-3-(2-플루오로에톡시메틸)벤젠
-5 ℃에서 수소화나트륨 [오일 중 60%] (343, mg, 8.6 mmol) 및 THF의 혼합물을 주사기를 통해 1분에 걸쳐 THF 중 2-플루오로에탄올의 용액으로 처리하고, 2분 동안 교반하고, 실온으로 가온하고, 실온에서 15분 동안 교반하고, 3-브로모벤질브로마이드 (2.5 g, 11.7 mmol)로 처리하고, 1시간 동안 교반하고, 포화 염화암모늄에 붓고, 에테르로 추출하였다. 추출물을 합하고, 물 및 염수로 연속적으로 세척하고, 황산마그네슘으로 건조하고, 감압하에 농축하였다. 잔류물을 용리액으로서 20:1 헥산/에틸 아세테이트를 사용하여 실리카 겔 상에서 플래시 크로마토그래피로 정제하여 1-브로모-3-(2-플루오로에톡시메틸)벤젠 1 g (수율 58%)을 황색 오일로서 수득하였다.
단계 b) 2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[(2-플루오로에톡시)메틸]-페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온
본질적으로 상기 실시예 18, 단계 a 및 c에 기재된 동일한 절차를 이용하고, 반응물로서 1-브로모-3-(2-플루오로에톡시메틸)벤젠 및 1-디플루오로메톡시-4-에티닐벤젠을 사용하여 표제 화합물을 백색 고체로서 수득하였다. mp 40-43 ℃;
실시예 31 내지 39
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(알콕시메틸)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
본질적으로 실시예 30에 기재된 동일한 절차를 이용하고, 단계 a에서 목적하는 알코올을 사용하여, 하기 표 I에 나타낸 화합물을 수득하고, NMR 및 질량 스펙트럼 분석으로 확인하였다.
실시예 40
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[(1E)-6-메톡시-헥스-1-엔-1-일]-페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
단계 a) (E)-6-메톡시-헥스-1-에닐보론산
메틸헥시닐 에테르 (7.2 mmol), THF 중 9-BBN 0.5 M (1.8 ml, 0.9 mmol) 및 카테콜보란 (1.21 g, 10.1 mmol)의 혼합물을 압력 튜브 내 100 ℃에서 16시간 동안 가열하고, pH 7 포스페이트 완충액으로 켄칭하고, 2시간 동안 교반하고, 에테르로 추출하였다. 합한 추출물을 MgSO4로 건조하고, 진공에서 농축하였다. 얻어진 잔류물을 플래시 크로마토그래피로 정제하여 (E)-6-메톡시-헥스-1-에닐보론산을 수득하고, NMR 및 질량 스펙트럼 분석으로 확인하였다.
단계 b) 2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[(1E)-6-메톡시-헥스-1-엔-1-일]-페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온
2 M K2CO3 1 ml 및 DME 2.5 ml 중 2-아미노-5-(3-브로모페닐)-5-[4-(디플루오로메톡시)-페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온 (200 mg, 0.488 mmol) 및 (E)-6-메톡시-헥스-1-에닐보론산 (0.537 mmol)의 탈기 용액을 Pd(CH3CN)2Cl2 (20 mg, 5%)로 처리하고, 상기 혼합물을 질소 분위기하 95 ℃에서 16시간 동안 가열하고, 물로 희석하고, CH2Cl2로 추출하였다. 추출물을 합하고, MgSO4로 건조하고, 진공에서 농축하였다. 얻어진 잔류물을 실리카 겔 카트리지 상에서 및 이이서 정제용 HPLC로 정제하여 표제 화합물 121 mg (수율 56%)을 수득하고, NMR 및 질량 스펙트럼 분석으로 확인하였다.
실시예 41
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[(1E)-5-히드록시-펜트-1-엔-1-일]-페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
단계 a) t-부틸펜트-4-이닐옥시 디페닐 실란
CH2Cl2 중 펜티놀 (8.0 g, 95 mmol), t-부틸디페닐실릴클로라이드 (28 g, 114 mmol) 및 Et3N (14 g, 138 mmol)의 혼합물을 실온에서 16시간 동안 교반하고, 1 M K2CO3으로 처리하고, CH2Cl2로 처리하였다. 합한 추출물을 MgSO4로 건조하고, 진공에서 농축하였다. 잔류물을 실리카 패드 상에서 여과 정제하여 t-부틸펜트-4-이닐옥시 디페닐 실란 30 g (수율 98%)을 수득하였다.
단계 b) 2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[(1E)-5-히드록시-펜트-1-엔-1-일]-페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온
본질적으로 상기 실시예 40에 기재된 동일한 절차를 이용하고, t-부틸펜트-4-이닐옥시 디페닐 실란을 사용하여 표제 화합물의 실릴 에테르를 수득하였다. THF 중 실릴 에테르 (635 mg, 0.97 mmol)의 용액을 THF (1 ml, 1 mmol) 중 1 M TBAF로 처리하고, 16시간 동안 교반하고, 물로 희석하고, CH2Cl2로 추출하였다. 합한 추출물을 MgSO4로 건조하고, 진공에서 농축하였다. 얻어진 잔류물을 실리카 카트리지, 정제용 HPLC 및 SCX 카트리지로 정제하여 (남은 TBAF 모두를 제거) 표제 화합물 59 mg (수율 15%)을 백색 고체로서 수득하고, NMR 및 질량 스펙트럼 분석으로 확인하였다.
실시예 42 내지 49
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-(3-알케닐페닐)-3-메틸-3,5-디히드로-4H-이미다졸-4-온 화합물의 제조
본질적으로 상기 실시예 40 및 41에 기재된 동일한 절차를 이용하고, 단계 a에서 목적하는 알킨을 사용하여 하기 표 II에 나타낸 화합물을 수득하고, NMR 및 질량 스펙트럼 분석으로 확인하였다.
실시예 50
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[2-(메톡시메틸)-시클로프로필]페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
0 ℃에서 건조 CH2Cl2 중 디에틸 아연 (4.92 ml, 4.92 mmol)의 1 M 용액을 건조 CH2Cl2 중 CF3CO2H (0.56 g, 4.92 mmol)의 용액으로 매우 서서히 처리하고, 20분 동안 교반하고, 건조 CH2Cl2 중 CH2I2 (0.66g, 2.46 mmol)의 용액으로 적가 처리하고, 20분 동안 교반하고, 건조 CH2Cl2 중 2-아미노-5-[4-(디플루오로메톡시)-페닐]-5-{3-[(1E)-3-메톡시프로프-1-엔-1-일]페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온 (197 mg, 0.492 mmol)의 용액으로 처리하고, 실온이 되게 하고, 실온에서 2시간 동안 교반하고, 수성 NH4Cl로 켄칭하고, CH2Cl2로 추출하였다. 합한 추출물을 MgSO4로 건조하고, 진공에서 농축하였다. 얻어진 잔류물을 SCX 카트리지 및 정제용 HPLC로 정제하여 표제 화합물 32 mg (수율 16%)을 백색 고체로서 수득하고, NMR 및 질량 스펙트럼 분석으로 확인하였다.
실시예 51
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[2-(2-메톡시에틸)-시클로프로필]페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
본질적으로 상기 실시예 50에 기재된 동일한 절차를 이용하고, 출발 물질로서 2-아미노-5-[4-(디플루오로메톡시)-페닐]-5-{3-[(1E)-4-메톡시부트-1-엔-1-일]페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온을 사용하여 표제 화합물을 백색 고체로서 수득하고, NMR 및 질량 스펙트럼 분석으로 확인하였다.
실시예 52
5-(3-아세틸페닐)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
DMF/물 (8 ml/0.8 ml) 중 2-아미노-5-(3-브로모페닐)-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온 (1.50 g, 3.66 mmol), 1,3-비스(디페닐포스피노)프로판 (DPPP) (0.377 g, 0.915 mmol), K2CO3 (0.606 g, 4.39 mmol), Pd(OAc)2 (82 mg, 0.37 mmol) 및 n-부틸비닐에테르 (1.47g, 14.6 mmol)의 혼합물을 마이크로파 오븐 내 120 ℃에서 1시간 동안 가열하고, 실온으로 냉각하고, 5% HCl 15 ml로 조심스럽게 처리하고, 실온에서 1시간 동안 교반하고, 물로 희석하고, 수성 K2CO3으로 염기화하고, 에틸 아세테이트로 추출하였다. 추출물을 합하고, MgSO4로 건조하고, 진공에서 농축하여 잔류물을 수득하였다. 상기 잔류물을 SCX 카트리지로 정제하여 표제 화합물 1.20 g (수율 88%)을 수득하고, NMR 및 질량 스펙트럼 분석으로 확인하였다.
실시예 53
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(3-히드록시헥스-4-인-1-일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
단계 a) 2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(3-히드록시프로프-1-인-1-일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온 (1)
피롤리딘 중 2-아미노-5-(3-브로모페닐)-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온 (2.4 g, 5.85 mmol), 3-히드록시-1-프로핀 (3.27 g, 58.5 mmol) 및 Pd(PPh3)4 (670 mg, 0.585 mmol)의 혼합물을 질소 분위기하 70 ℃에서 16시간 동안 가열하고, 물로 희석하고, CH2Cl2로 추출하였다. 추출물을 합하고, MgSO4로 건조하고, 진공에서 농축하여 잔류물을 수득하였다. 상기 잔류물을 실리카 카트리지 상에서 크로마토그래피로 정제하여 2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(3-히드록시프로프-1-인-1-일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온 1 g (수율 45%)을 수득하고, NMR 및 질량 스펙트럼 분석으로 확인하였다.
단계 b) 2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(3-히드록시프로필)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온 (2)
1 (1 g, 2.6 mmol) 및 PtO2 (50 mg, 10%)의 에탄올 용액의 혼합물을 파르 수소첨가기 상 15 psi에서 4시간 동안 수소화하고, 셀라이트를 통해 여과하였다. 여액을 감압하 농축 건조하여 2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(3-히드록시프로필)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온 830 mg을 수득하고, NMR 및 질량 스펙트럼 분석으로 확인하였다.
단계 c) 화합물 3
질소하 THF 중 2 (480 mg)의 용액을 DMAP (150 mg, 1.23 mmol) 및 Boc2O (938 mg, 4.3 mmol)로 처리하고, 2시간 동안 교반하고, 물로 희석하고, CH2Cl2로 추출하였다. 추출물을 합하고, MgSO4로 건조하고, 진공에서 농축하여 잔류물을 수득하였다. 상기 잔류물을 MeOH 10 ml 및 30% 수성 NaOH (400 ㎕, 3 당량)에 용해하고, 실온에서 16시간 동안 교반하고, 염수로 희석하고, CH2Cl2로 추출하였다. 추출물을 합하고, MgSO4로 건조하고, 진공에서 농축하여 잔류물을 수득하였다. 상기 잔류물을 플래시 크로마토그래피로 정제하여 보호된 2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(3-히드록시프로필)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온 화합물 265 mg (수율 44%)을 수득하였다. 상기 화합물 (265 mg, 0.542 mmol)을 건조 CH2Cl2에 용해하고, 데스-마틴(Dess-Martin) 페리오디난 (276 mg, 0.650 mmol)으로 처리하고, 2시간 동안 교반하고, 물 및 염수로 세척하고, MgSO4로 건조하고, 증발 건조하였다. 얻어진 잔류물을 실리카 카트리지 상에서 정제하여 화합물 3 170 mg (수율 64%)을 수득하고, NMR 및 질량 스펙트럼 분석으로 확인하였다.
단계 d) 2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(3-히드록시헥스-4-인-1-일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온
질소하 -70 ℃에서 건조 THF 중 3 (80 mg, 0.164 mmol)의 용액을 그리나드(Grignard) 시약 4 (65.6 ㎕, 0.328 mmol)로 처리하고, 실온에 되게 하고, 실온에서 2시간 동안 교반하고, 물로 희석하고, CH2Cl2로 추출하였다. 추출물을 합하고, MgSO4로 건조하고, 진공에서 농축하여 잔류물을 수득하였다. 상기 잔류물 (50 mg)을 CH2Cl2에 분산시키고, 트리플루오로아세트산 (215 mg, 1.9 mmol)으로 처리하고, 16시간 동안 교반하고, 수성 K2CO3로 세척하고, MgSO4로 건조하고, 감압하 증발시켰다. 얻어진 잔류물을 정제용 HPLC로 정제하여 표제 생성물 15 mg을 수득하고, NMR 및 질량 스펙트럼 분석으로 확인하였다.
실시예 54
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(3-플루오로프로프-1-인-1-일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
질소하 -40 ℃에서 건조 CH2Cl2 중 2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(3-히드록시프로프-1-인-1-일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온 (300 mg, 0.779 mmol)의 용액을 DAST (252 mg, 1.56 mmol)로 적가 처리하고, -40 ℃에서 1시간 동안 교반하고, 실온으로 가온하고, 실온에서 16시간 동안 교반하고, 물로 희석하고, 30분 동안 교반하고. CH2Cl2로 추출하였다. 추출물을 합하고, MgSO4로 건조하고, 진공에서 농축하여 잔류물을 수득하였다. 상기 잔류물을 정제용 HPLC로 반복적으로 정제하여 표제 생성물 23 mg (수율 8%, LC-MS 순도 98%)을 수득하고, NMR 및 질량 스펙트럼 분석으로 확인하였다.
실시예 55 내지 57
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(3-치환된)-페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온 화합물의 제조
본질적으로 상기 실시예 14, 단계 f, g 및 h에 기재된 동일한 절차를 이용하고, 목적하는 할로벤젠을 사용하여 하기 표 III에 나타낸 화합물을 수득하고, NMR 및 질량 스펙트럼 분석으로 확인하였다.
실시예 58
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-(3-히드록시페닐)-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
단계 a) 3-((4-(디플루오로메톡시)페닐)에티닐)페놀
탈산소화 디메틸포름아미드 중 4-(디플루오로메톡시)페닐 요오다이드 (4.70 g)의 용액을 트랜스-디클로로비스(트리페닐포스핀) 팔라듐(II) (244 mg) 및 요오드화구리(II) 66 mg 및 이어서 트리에틸아민 (7.52 mL)으로 처리하고, 질소 분위기하 5분 동안 교반하고, 3-히드록시페닐 아세틸렌 (2.467 g)으로 처리하고, 질소 분위기하 16시간 동안 교반하고, 에틸 아세테이트에 붓고, 0.05 N HCl 및 물로 세척하였다. 유기상을 MgSO4로 건조하고, 진공에서 농축하였다. 잔류물을 용리액으로서 40% 에틸 아세테이트/헥산을 사용하여 실리카 겔 상에서 크로마토그래피하여 3-((4-(디플루오로메톡시)페닐)에티닐)페놀 5.40 g을 황갈색 고체로서 수득하였다.
단계 b) 1-(4-(디플루오로메톡시)페닐)-2-(3-히드록시페닐)에탄-1,2-디온
3-((4-(디플루오로메톡시)페닐)에티닐)페놀 (5.0 g) 및 디클로로비스(아세토니트릴)팔라듐(II) (0.50 g) 및 디메틸술폭시드의 혼합물을 140 ℃에서 4시간 동안 가열하고, 실온으로 냉각하고, 물에 붓고, 10분 동안 교반하고, 클로로포름으로 추출하였다. 합한 추출물을 MgSO4로 건조하고, 증발시켜 진한 오일을 수득하였다. 상기 오일을 단계 농도구배 용리 (10% 에틸 아세테이트/헥산 내지 20% 에틸 아세테이트/헥산)를 이용하여 플래시 크로마토그래피 (실리카 겔)로 정제하여 1-(4-(디플루오로메톡시)페닐)-2-(3-히드록시페닐)에탄-1,2-디온 2.75 g을 밝은 황색 왁스 고체로서 수득하였다.
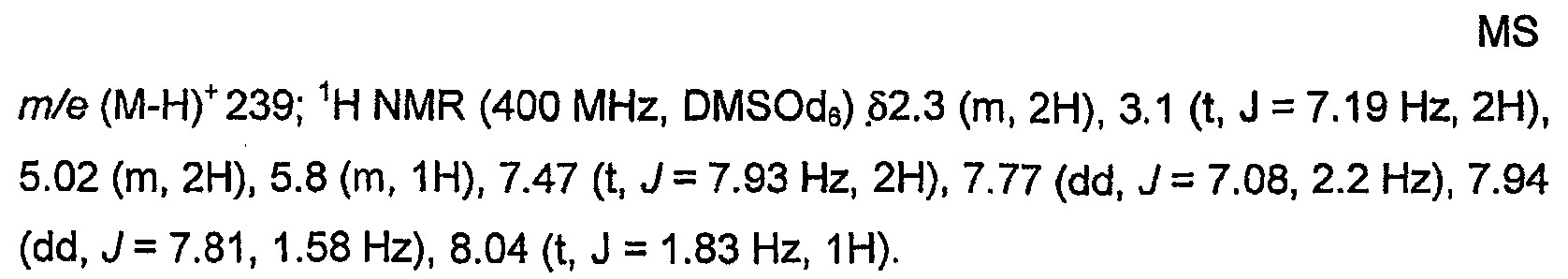
1H NMR (DMSO-d6): δ10.02 (s, 1H), 7.95 (d, J = 8.9 Hz, 2H), 7.41 (t, J = 73.0 Hz, 1H), 7.38 (m, 1H), 7.34 (d, J = 8.9 Hz, 2H), 7.25 (m, 2H), 및 7.12 (m, 1H); MS (ES neg) m/z 292.
단계 c) 2-아미노-5-[4-(디플루오로메톡시)페닐]-5-(3-히드록시페닐)-3-메틸-3,5-디히드로-4H-이미다졸-4-온
에탄올 중 1-(4-(디플루오로메톡시)페닐)-2-(3-히드록시페닐)에탄-1,2-디온 (2.75 g), N-메틸구아니딘 히드로클로라이드 (1.237 g) 및 탄산나트륨 (2.20 g)의 혼합물을 85 ℃에서 8시간 동안 가열하고, 실온으로 냉각하고, 진공에서 증발시켰다. 얻어진 잔류물을 물과 클로로포름 사이에 분배하였다. 유기상을 분리하고, Na2SO4로 건조하고, 증발시켜 밝은 갈색 오일을 수득하였다. 상기 오일을 단계 농도구배 용리 (100% 클로로포름 내지 15% 메탄올/클로로포름)를 이용하여 플래시 크로마토그래피 (실리카 겔)로 정제하여 표제 화합물 2.20 g을 백색 포말 유리로서 수득하였다.
실시예 59
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(3-플루오로프로폭스-1-일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
건조 DMF 중 2-아미노-5-[4-(디플루오로메톡시)페닐]-5-(3-히드록시페닐)-3-메틸-3,5-디히드로-4H-이미다졸-4-온 (197 mg), 1-요오도-3-플루오로프로판 (127 mg) 및 탄산세슘 (240 mg)의 혼합물을 질소 분위기하 실온에서 16시간 동안 교반하고, 클로로포름으로 희석하고, 5분 동안 교반하고, 유리 섬유 3.1 ㎛ 주사 여과기를 통해 여과하였다. 여액을 증발시켰다. 얻어진 잔류물을 농도구배 용리 (80%A/20%B 내지 20%A/80%B, A=헥산; B=(20% 메탄올/80% 디클로로메탄)를 이용하여 HPLC;CN 결합된 상 정제용 칼럼으로 정제하여 투명 오일을 수득하였다. 상기 오일을 가온한 에틸 아세테이트/헥산으로부터 결정화하여 표제 화합물을 백색 결정으로 수득하고 (mp 161-162 ℃), NMR 및 질량 스펙트럼 분석으로 확인하였다. MS (APPI) m/z 408.
실시예 60
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-(4-플루오로-3-히드록시-페닐)-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
본질적으로 상기 실시예 17, 단계 d에 기재된 동일한 절차를 이용하고, 출발 물질로서 5-브로모-2-플루오로페놀을 사용하여 표제 화합물을 수득하고, NMR 및 질량 스펙트럼 분석으로 확인하였다.
실시예 61 내지 78
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-(알콕시페닐)-3-메틸-3,5-디히드로-4H-이미다졸-4-온 화합물의 제조
본질적으로 상기 실시예 59에 기재된 동일한 절차를 이용하고, 목적하는 알킬 할라이드 및 적합한 2-아미노-5-[4-(디플루오로메톡시)페닐]-5-(히드록시페닐)-3-메틸-3,5-디히드로-4H-이미다졸-4-온 기질을 사용하여 하기 표 IV에 나타낸 화합물을 수득하고, NMR 및 질량 스펙트럼 분석으로 확인하였다.
실시예 79
(5R)-2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[4-플루오로-3-(3-플루오로프로폭스-1-일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온 (A) 및 (5S)-2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[4-플루오로-3-(3-플루오로프로폭스-1-일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온 (B)의 제조
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[4-플루오로-3-(3-플루오로프로폭스-1-일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 라세미 혼합물을 키랄 HPLC (칼럼 유형: 키랄셀 AD, 5 x 50 cm, 이동상: 95 mL/분에서 0.1% 디에틸아민을 갖는 헥산 중 14% 에탄올 사용)로 분리하여 표제의 R-이성질체 (A) 및 표제의 S-이성질체 (B)를 포움으로서 수득하고, NMR 및 질량 스펙트럼 분석으로 확인하였다. 표제의 R-이성질체 (A) [α]D25 = -14.00°(1% EtOH); MS (ES) m/z 424.1: 및 표제의 S-이성질체 (B) [α]D25 = +15.00°(1% EtOH); MS (ES) m/z 424.1.
실시예 80
(5R)-2-아미노-5-[3-(2,2-디플루오로에톡시)-4-플루오로페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온 (A) 및 (5S)-2-아미노-5-[3-(2,2-디플루오로에톡시)-4-플루오로페닐]-5-[4-(디플루오로메톡시)-페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온 (B)의 제조
2-아미노-5-[3-(2,2-디플루오로에톡시)-4-플루오로페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 라세미 혼합물을 키랄 HPLC (칼럼 유형: 키랄팩 AD-H, 2 x 25 cm, 이동상: 0.1% 디에틸아민을 갖는 헥산 중 15% 에탄올 사용)로 분리하여 표제의 R-이성질체 (A)를 유리로서 및 표제의 S-이성질체 (B)를 포움으로서 수득하고, NMR 및 질량 스펙트럼 분석으로 확인하였다. 표제의 R-이성질체 (A) MS (ES) m/z 428.1: 및 표제의 S-이성질체 (B) [α]D25 = +15.2°(1% EtOH); MS (ES) m/z 428.1.
실시예 81
2-아미노-5-{3-[(4,4-디플루오로부트-3-엔-1-일)옥시]페닐}-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
단계 a) 1-(4,4-디플루오로부트-3-에닐옥시)-3-((4-(디플루오로메톡시)페닐)에티닐)-벤젠
메틸 에틸 케톤 중 3-((4-(디플루오로메톡시)페닐)에티닐)페놀 (900 mg), 탄산칼륨 (636 mg), 앨리쿼트(Aliquat) 336 (4 방울), 요오드화나트륨 (촉매량) 및 4-브로모-1,1-디플루오로-1-부텐 (591 ㎕)의 혼합물을 압력 용기에 두고, 80 ℃에서 15시간 동안 가열하고, 실온으로 냉각하고, 디클로로메탄으로 희석하고, 여과하였다. 여액을 진공에서 농축하였다. 얻어진 잔류물을 플래시 크로마토그래피 (실리카 겔, 용리액: 2.5% 에틸 아세테이트/헥산)로 정제하여 1-(4,4-디플루오로부트-3-에닐옥시)-3-((4-(디플루오로메톡시)페닐)-에티닐)벤젠 560 mg (수율 46.2%)을 수득하였다.
단계 b) 2-아미노-5-{3-[(4,4-디플루오로부트-3-엔-1-일)옥시]페닐}-5-[4-(디플루오로-메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온
본질적으로 상기 실시예 1, 단계 b 및 c에 기재된 동일한 절차를 이용하고, 출발 물질로서 1-(4,4-디플루오로부트-3-에닐옥시)-3-((4-(디플루오로메톡시)페닐)에티닐)-벤젠을 사용하여 표제 화합물을 백색 고체로서 수득하고 (mp 127-128 ℃), NMR 및 질량 스펙트럼 분석으로 확인하였다. MS (ES) m/z 436.1.
실시예 82
2-아미노-5-{3-[(4,4-디플루오로부트-3-엔-1-일)옥시]-4-플루오로페닐}-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
단계 a) 4-브로모-2-(4,4-디플루오로부트-3-에닐옥시)-1-플루오로벤젠
메틸 에틸 케톤 중 2-플루오로-5-브로모페놀 (2.40 g), 탄산칼륨 (2.31 m), 앨리쿼트 336 (5 방울), 요오드화나트륨 (촉매량) 및 4-브로모-1,1-디플루오로-1-부텐 (1.79 mL)의 혼합물을 압력 용기에 두고, 82 ℃ 오일조에서 15시간 동안 가열하였다. 상기 반응 혼합물을 냉각하고, 디클로로메탄으로 희석하고, 여과하고, 진공에서 증발시켰다. 얻어진 잔류물을 플래시 크로마토그래피 (실리카 겔, 용리액: 2.5% 에틸 아세테이트/헥산)로 정제하여 4-브로모-2-(4,4-디플루오로부트-3-에닐옥시)-1-플루오로벤젠 2.23 g (수율 63%)을 수득하고, NMR 분석으로 확인하였다.
단계 b) 2-아미노-5-{3-[(4,4-디플루오로부트-3-엔-1-일)옥시]-4-플루오로페닐}-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온
본질적으로 상기 실시예 60에 기재된 동일한 절차를 이용하고, 출발 물질로서 4-브로모-2-(4,4-디플루오로부트-3-에닐옥시)-1-플루오로벤젠을 사용하여 표제 화합물 700 mg (수율 68%, mp 139-140 ℃)을 회백색 고체로서 수득하고, NMR 및 질량 스펙트럼 분석으로 확인하였다. MS (ES) m/z 456.1
실시예 83
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-(4-플루오로-3-펜트-4-엔-1-일)-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
단계 a) 1-플루오로-4-요오도-2-펜트-4-엔-1-일벤젠의 제조
질소하 -78 ℃에서 건조 THF 중 2-플루오로-5-요오도-벤즈알데히드 (0.714 g, 2.86 mmol)의 교반 용액을 10분에 걸쳐 THF (6.85 mL, 3.43 mmol) 중 0.5 M 3-부테닐 마그네슘 브로마이드로 처리하고, 0.5시간 동안 교반하고, 1시간에 걸쳐 -30 ℃로 가온하고, 포화 염화암모늄으로 켄칭하고, 물로 희석하고, 에틸 아세테이트로 추출하였다. 추출물을 합하고, MgSO4로 건조하고, 진공에서 농축하였다. 얻어진 잔류물을 플래시 크로마토그래피 (5% 내지 10% 에틸 아세테이트/석유 에테르)로 정제하여 1-(2-플루오로-5-요오도-페닐)펜트-4-엔-1-올 565 mg (수율 65%)을 투명 오일로서 수득하였다. 상기 오일의 일부 (0.25 g, 0.82 mmol)를 건조 염화메틸렌에 용해하고, 0 ℃로 냉각하고, 삼불화붕소 에테레이트 (0.1 mL, 0.81 mmol)로 처리하고, 질소 분위기하 15분 동안 교반하고, 1시간 동안 실온으로 가온하고, 포화 중탄산나트륨으로 켄칭하였다. 상기 반응 혼합물을 염화메킬렌과 H2O 사이에 분배하고, 수성상을 염화메틸렌으로 추출하였다. 유기상 및 추출물을 합하고, 염수로 세척하고, MgSO4로 건조하고, 진공에서 농축하여 1-플루오로-4-요오도-2-펜트-4-엔-1-일벤젠 0.18 g (수율 76%)을 투명 오일로서 수득하였다.
단계 b) 2-아미노-5-[4-(디플루오로메톡시)페닐]-5-(4-플루오로-3-펜트-4-엔-1-일)-3-메틸-3,5-디히드로-4H-이미다졸-4-온
본질적으로 상기 실시예 60에 기재된 동일한 절차를 이용하고, 출발 물질로서 1-플루오로-4-요오도-2-펜트-4-엔-1-일벤젠을 사용하여 표제 화합물을 다소 황색인 포움으로 수득하고 (mp 45-46 ℃), NMR 및 질량 스펙트럼 분석으로 확인하였다. MS (ES-): 416 (M-H)
실시예 84
2-아미노-5-(3-부트-3-엔-1-일-4-플루오로페닐)-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
본질적으로 상기 실시예 83에 기재된 동일한 절차를 이용하고, 단계 a에서 알릴 브롬화마그네슘을 사용하여 표제 화합물을 다소 황색인 포움으로 수득하고 (mp 55-58 ℃), NMR 및 질량 스펙트럼 분석으로 확인하였다. MS (ES+): 404 (M+H).
실시예 85
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(1-히드록시부트-2-인-1-일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
질소하 0 ℃에서 건조 DME 중 3-[2-(4-디플루오로메톡시페닐)-2-옥소-아세틸]-벤즈알데히드 (0.1 g, 0.33 mmol)의 교반 용액을 10분에 걸쳐 THF 중 0.5 M 1-프로피닐 브롬화마그네슘으로 처리하였다. 상기 반응물을 0.5시간 동안 교반하고, 포화 염화암모늄으로 켄칭하고, 물로 희석하고, 에틸 아세테이트로 추출하였다. 합한 추출물을 MgSO4로 건조하고, 진공에서 농축하였다. 얻어진 잔류물을 플래시 크로마토그래피 (20% 내지 40% 에틸 아세테이트/석유 에테르)로 정제하여 1-(4-디플루오로메톡시페닐)-2-[3-(1-히드록시부트-2-이닐)페닐]에탄-1,2-디온 55 mg (수율 49%)을 투명 오일로서 수득하였다. 본질적으로 상기 실시예 1, 단계 c에 기재된 동일한 절차를 이용하고, 1-(4-디플루오로메톡시페닐)-2-[3-(1-히드록시-부트-2-이닐)페닐]-에탄-1,2-디온 (0.055 g, 0.16 mmol)을 사용하여 표제 생성물 0.044 g (수율 69%)을 다소 황색인 포움으로 수득하고, NMR 및 질량 스펙트럼 분석으로 확인하였다. MS (ES+): 400 (M+H).
실시예 86
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(1,4-디히드록시부트-2-인-1-일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
질소하 -78 ℃에서 건조 THF 중 프로파르길 알코올 (0.1 g, 1.78 mmol)의 교반 용액을 1.9 M n-BuLi (1.88 mL, 3.57 mmol)로 10분에 걸쳐 적가 처리하고, 0.5시간 동안 교반하고, 0 ℃로 가온하였다. 상기 용액의 3 mL 분량을 질소하 0 ℃에서 건조 DME 중 3-[2-(4-디플루오로메톡시페닐)-2-옥소-아세틸]벤즈알데히드 (0.15 g, 0.49 mmol)의 교반 용액에 첨가하였다. 10분 후, 상기 반응 혼합물을 포화 염화암모늄으로 켄칭하고, 물로 희석하고, 에틸 아세테이트로 추출하였다. 합한 추출물을 MgSO4로 건조하고, 진공에서 농축하였다. 얻어진 잔류물을 플래시 크로마토그래피 (30% 내지 70% 에틸 아세테이트/석유 에테르)로 정제하여 1-[4-(디플루오로메톡시)페닐]-2-[3-(1,4-디히드록시부트-2-이닐)페닐]에탄-1,2-디온 52 mg (수율 29%)을 투명 오일로서 수득하였다. 본질적으로 상기 실시예 1, 단계 c에 기재된 동일한 절차를 이용하고, 1-[4-(디플루오로메톡시)페닐]-2-[3-(1,4-디히드록시부트-2-이닐)페닐]에탄-1,2-디온 (0.052 g, 0.14 mmol)을 사용하여 표제 화합물 0.031 g (수율 52%)을 다소 갈색인 포움으로 수득하고, NMR 및 질량 스펙트럼 분석으로 확인하였다. MS (ES+): 416 (M+H).
실시예 87
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(2,2-디메틸-3-옥소시클로부틸)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
단계 a) 3-(3-브로모-페닐)-2,2-디메틸-시클로부타논
-13 ℃에서 질소하 N,N,2-트리메틸프로피온아미드 (3.65 g, 31.7 mmol) 및 디클로로메탄의 용액을 주사기를 통해 트리플릭산 무수물 (Tf2O)로 처리하고, 10분 동안 교반하고, CH2Cl2 중 3-브로모스티렌 (5.04 g, 27.6 mmol) 및 2,4,6-콜리딘 (4.32 g, 35.7 mmol)의 용액으로 40분에 걸쳐 적가 처리하고, 환류 온도에서 20시간 동안 가열하고, 실온으로 냉각하고, 진공에서 농축하였다. 상기 농축물을 물 및 CH2Cl2로 희석하고, 89 ℃에서 7시간 동안 가열하였다. 실온으로 냉각한 후, 상들을 분리하고, 수성상을 CH2Cl2로 추출하였다. 유기상 및 상기 추출물을 합하고, Na2SO4로 건조하고, 진공에서 농축하였다. 얻어진 농축물을 실리카 겔 칼럼 크로마토그래피 (농도구배; 헥산 중 5% 내지 10% EtOAc)로 정제하여 3-(3-브로모페닐)-2,2-디메틸-시클로부타논 4.26 g (수율 61%)을 담황색 오일로서 수득하였다.
단계 b) 2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(2,2-디메틸-3-옥소시클로부틸)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온
본질적으로 상기 실시예 17, 단계 d에 기재된 동일한 절차를 이용하고, 출발 물질로서 3-(3-브로모페닐)-2,2-디메틸-시클로부타논을 사용하여 표제 화합물을 백색 고체로서 수득하였다.
실시예 88
2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-[3-(3-옥소시클로부틸)페닐]-3,5-디히드로-4H-이미다졸-4-온의 제조
본질적으로 상기 실시예 87에 기재된 동일한 절차를 이용하고, 단계 a에서 N,N-디메틸아세트아미드를 사용하여 표제 화합물을 백색 고체로서 수득하였다. mp 68-70 ℃(포움);
실시예 89
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(3-히드록시-시클로부틸)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
빙조 온도에서 2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-[3-(3-옥소시클로부틸)페닐]-3,5-디히드로-4H-이미다졸-4-온 (0.324 gm, 0.811 mmol)의 메탄올 용액을 NaBH4 (0.042 gm, 1.11 mmol)로 모두 한번에 처리하고, 0 ℃에서 45분 동안 교반하고, 진공에서 농축하였다. 고체 잔류물을 물과 클로로포름 사이에 분배하였다. 유기상을 분리하고, 황산마그네슘으로 건조하고, 증발시켜 포움을 수득하였다. 상기 포움을 클로로포름에 용해하고, 헥산으로 침전시켜 표제 화합물 0.307 g (수율 94%, mp 186-190 ℃)을 백색 고체로서 수득하였다.
실시예 90
에틸 [3-(3-{2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}페닐)시클로부틸리덴]아세테이트의 제조
단계 a) [3-(3-브로모페닐)시클로부틸리덴]아세트산 에틸 에스테르
3-(3-브로모페닐)시클로부타논 (2.03 g, 9.02 mmol) 및 트리페닐포스포르아닐리덴 아세트산 에틸 에스테르 (15.72 gm, 45.12 mmol) 디클로로메탄 용액을 CEM 디스커버(CEM Discover; 상표명) 마이크로파 기기에서 30 분 동안 120 ℃에서 조사하였다. 압력이 최대 180 PSI에 도달하였다. 표준 후처리 절차 및 이어서 칼럼 크로마토그래피 (등용매; 헥산 중 10% 디에틸 에테르)로 정제하여 [3-(3-브로모페닐)시클로부틸리덴]아세트산 에틸 에스테르 2.37 g (수율 89%)을 오일로서 수득하였다.
단계 b) 에틸 [3-(3-{2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}페닐)-1-메톡시시클로부틸리덴]아세테이트
본질적으로 상기 실시예 17, 단계 d에 기재된 동일한 절차를 이용하고, [3-(3-브로모페닐)시클로부틸리덴]아세트산 에틸 에스테르를 사용하여 표제 화합물을 백색 포말성 고체로서 수득하였다.
실시예 91
메틸 [3-(3-{2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}페닐)시클로부틸리덴]아세테이트의 제조
본질적으로 상기 실시예 90에 기재된 동일한 절차를 이용하고, 단계 a에서 트리페닐포스포르아닐리덴 아세트산 에틸 에스테르를 사용하여 표제 생성물을 포움으로서 수득하였다. NMR 분석 결과, 상기 포움은 메틸 및 에틸 에스테르의 7:3 혼합물인 것으로 나타났다.
실시예 92
메틸 [3-(3-{2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}페닐)시클로부틸]아세테이트의 제조
단계 a) (3-{3-[2-(4-디플루오로메톡시페닐)-1,2-디히드록시에틸]페닐}-시클로부틸)아세트산 메틸 에스테르
에탄올 중 10% Pd/C (0.092 g) 및 (3-{3-[2-(4-디플루오로메톡시페닐)-2-옥소아세틸]-헤닐}-시클로부틸리덴)아세트산 메틸 에스테르 (0.78 g, 1.95 mmol)의 혼합물을 3시간 동안 15 PSI 수소하 파르 수소첨가기에 두었다. 추가의 10% Pd/C (0.056 g)를 첨가하고, 진탕기를 30 PSI 수소 분위기하에 2시간 동안 두었다. 상기 반응 혼합물을 셀라이트를 통해 여과하였다. 여액을 진공에서 농축하여 (3-{3-[2-(4-디플루오로메톡시페닐)-1,2-디히드록시에틸]페닐}-시클로부틸)아세트산 메틸 에스테르 402 mg (수율 51%)을 오일로서 수득하였다.
단계 b) 1-(4-디플루오로메톡시페닐)-2-[3-(3-옥소시클로부틸)-페닐]에탄-1,2-디온
DMSO (0.90 mL) 중 o-요오독시벤조산 (IBX)의 1 M 용액 및 (3-{3-[2-(4-디플루오로메톡시페닐)-1,2-디히드록시에틸]페닐-시클로부틸)아세트산 메틸 에스테르 (0.144 g, 0.354 mmol)의 혼합물을 30분 동안 교반하고, 추가의 DMSO 중 1 M IBX 1.2 mL로 처리하고, 15분 동안 교반하고, 물과 디에틸 에테르 사이에 분배하였다. 유기상을 분리하고, Na2SO4로 건조하고, 진공에서 농축하였다. 얻어진 잔류물을 칼럼 크로마토그래피 (에틸 아세테이트 중 10% 헥산)로 정제하여 1-(4-디플루오로메톡시페닐)-2-[3-(3-옥소시클로부틸)페닐]에탄-1,2-디온 0.133 g (수율 93%)을 오일로서 수득하였다.
단계 c) 메틸 [3-(3-{2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}페닐)시클로부틸]아세테이트
본질적으로 상기 실시예 1, 단계 c에 기재된 동일한 절차를 이용하고, 출발 물질로서 1-(4-디플루오로메톡시페닐)-2-[3-(3-옥소시클로부틸)페닐]에탄-1,2-디온을 사용하여 표제 화합물을 백색 고체로서 수득하였다. mp 68-70 ℃ (포움)
실시예 93
2-아미노-5-[3-(디플루오로메톡시)페닐]-5-[4-(디플루오로메톡시)-페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
본질적으로 상기 실시예 18, 단계 d에 기재된 동일한 절차를 이용하고, 출발 물질로서 4-디플루오로메톡시브로모벤젠 및 1-디플루오로메톡시-3-에티닐-벤젠을 사용하여 표제 화합물을 백색 포움으로서 수득하였다. mp 52-54 ℃;
실시예 94
(5S)-2-아미노-5-[3-(디플루오로메톡시)페닐]-5-[4-(디플루오로-메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온 (A) 및 (5R)-2-아미노-5-[3-(디플루오로메톡시)페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온 (B)의 제조
2-아미노-5-[3-(디플루오로메톡시)페닐]-5-[4-(디플루오로-메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 라세미 혼합물을 키랄셀 OJ, 2 x 25 cm 칼럼 (22 mL/분의 유속에서 헥산/DEA 중 10% EtOH로 용리)에 두었다. 물질을 6.14분 (생성물 A) 및 7.42분 (생성물 B)에 수집하였다. 각각의 거울상이성질체 생성물을 개별적으로 회전증발기에서 농축하고, 에탄올로 희석하고, 다시 농축하여 오일성 잔류물을 수득하였다. 각각의 오일성 잔류물을 디에틸 에테르 및 동량의 헥산으로 희석하고, 농축하여 표제의 거울상이성질체 생성물을 백색 고체로서 수득하였다. A (118 mg) 및 B (96 mg). 생성물 A는 (+)-거울상이성질체로 확인되었다:
생성물 B는 (R)-거울상이성질체로 확인되었다:
실시예 95
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[(1R)-1-플루오로펜트-4-엔-1-일]페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
단계 a) (3-브로모페닐)아세트알데히드
0 ℃에서 납 테트라아세테이트 (3.6 g, 8.2 mmol) 및 트리플루오로아세트산 (8.25 mL)의 혼합물을 디클로로메탄 중 1-브로모-3-비닐벤젠 (1.5 g, 8.2 ml)의 용액으로 적가 처리하고, 실온으로 가온하고, 실온에서 2시간 동안 교반하고, 디클로로메탄으로 희석하고, 물에 붓고, 격렬히 교반하고, 셀라이트 패드를 통해 여과하였다. 여액을 분리하였다. 여과케이크를 추가 분량의 디클로로메탄으로 세정하였다. 합한 유기상을 물, NaHCO3 및 염수로 연속적으로 세척하고, MgSO4로 건조하고, 진공에서 농축하여 (3-브로모페닐)아세트알데히드를 수득하였다.
단계 b) (R)-2-플루오로-2-(3-브로모페닐)아세트알데히드 (참조 문헌 [MacMillan and Beeson, JACS 2005, 127, 8826])
실온에서 아세톤 및 이소프로판올의 9:1 혼합물 중 (5R)-5-벤질-2,2,3-트리메틸 이미다졸리딘-4-온 디클로로아세트산 염 (97 mg, 0.4 mmol) 및 N-플루오로벤젠술폰이미드 (3.15 g, 10 mmol)의 균질 혼합물을 (3-브로모페닐)아세트알데히드 (280 mg, 1.4 mmol)로 처리하고, 실온에서 1시간 동안 교반하고, -78 ℃로 냉각하고, 에테르로 희석하고, 셀라이트 패드를 통해 여과하였다. 여과케이크를 추가의 에테르로 세척하였다. 합한 여액을 메틸술피드 (5 mL)로 처리하고, 포화 NaHCO3 및 염수로 세척하고, MgSO4로 건조하고, 감압하 농축하여 (R)-2-플루오로-2-(3-브로모페닐)아세트알데히드를 수득하였다.
단계 c) 톨루엔-4-술폰산 (S)-2-(3-브로모페닐)-2-플루오로-에틸 에스테르
CH2Cl2 및 에탄올 중 (R)-2-플루오로-2-(3-브로모페닐)아세트알데히드의 용액을 NaBH4 (189 mg, 5 mmol)로 처리하고, 30분 동안 교반하고, 0 ℃로 냉각하고, 포화 NH4Cl로 처리하고, 실온으로 가온하고, 실온에서 1시간 동안 격렬히 교반하고, CH2Cl2로 희석하였다. 상들을 분리하였다. 수성상을 CH2Cl2로 추출하였다. 유기상 및 상기 추출물을 합하고, NaHCO3 및 염수로 세척하고, MgSO4로 건조하고, 진공에서 농축하였다. 얻어진 잔류물을 칼럼 크로마토그래피 (용리액으로서 5% EtOAc 및 헥산)로 정제하여 (R)-2-플루오로-2-(3-브로모페닐)-1-에탄올을 수득하였다.
빙조 온도에서 CH2Cl2 중 (R)-2-플루오로-2-(3-브로모페닐)-1-에탄올 (5 mmol) 및 p-톨루엔술포닐 클로라이드 (5.1 mmol)의 용액을 교반하면서 피리딘으로 처리하였다. 상기 반응 혼합물을 질소 분위기하 환류 온도에서 가열하고, 실온으로 냉각하고, 10% HCl, 포화 NaHCO3 및 염수로 세척하고, MgSO4로 건조하고, 진공에서 농축하여 톨루엔-4-술폰산 (S)-2-(3-브로모페닐)-2-플루오로-에틸 에스테르를 수득하였다.
단계 d) 1-브로모-(S)-3-(1-플루오로펜트-4-엔-1-일)벤젠
실온에서 THF 중 톨루엔-4-술폰산 (S)-2-(3-브로모페닐)-2-플루오로-에틸 에스테르 (5 mmol)의 용액을 브롬화알릴마그네슘 1 M 용액으로 적가 처리하고, 실온에서 5시간 동안 교반하고, 포화 NH4Cl로 켄칭하고, 에틸 아세테이트로 추출하였다. 추출물을 합하고, 물 및 염수로 연속적으로 세척하고, MgSO4로 건조하고, 진공에서 농축하여 1-브로모-(S)-3-(1-플루오로펜트-4-엔-1-일)벤젠을 수득하였다.
단계 e) 2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[(1R)-1-플루오로펜트-4-엔-1-일]페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온
본질적으로 상기 실시예 14, 단계 f, g 및 h에 기재된 동일한 절차를 이용하고, 출발 물질로서 1-브로모-(S)-3-(1-플루오로펜트-4-엔-1-일)벤젠을 사용하여 표제 생성물을 수득하고, NMR 및 질량 스펙트럼 분석으로 확인하였다.
실시예 96
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[(1R)-1-플루오로부트-3-엔-1-일]페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
본질적으로 상기 실시예 95에 기재된 동일한 절차를 이용하고, 단계 d에서 브롬화에테닐마그네슘을 사용하여 표제 화합물을 수득하고, NMR 및 질량 스펙트럼 분석으로 확인하였다.
실시예 97
N-(3-{2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}페닐)에탄술폰아미드의 제조
단계 a) N-(3-{[4-(디플루오로메톡시)페닐]에티닐}페닐)에탄술폰아미드
CH2Cl2 중 3-{[4-(디플루오로메톡시)페닐]에티닐}아닐린 (0.5 g, 1.93 mmol) 및 피리딘 (0.31 mL, 3.80 mmol)의 냉각 (0 ℃) 용액을 에틸술포닐 클로라이드 (0.27 mL, 2.89 mmol)로 적가 처리하였다. 상기 혼합물을 5시간 동안 교반하고, 물에 붓고, EtOAc/에틸 에테르 1/1로 추출하였다. 유기 추출물을 합하고, MgSO4로 건조하고, 진공에서 농축하였다. 얻어진 잔류물을, 용리 용매로서 헥산/EtOAc (3/1)를 사용하여 실리카 겔 (바이오타지) 상에서 정제하여 N-(3-{[4-(디플루오로메톡시)페닐]에티닐}페닐)에탄술폰아미드를 황색 오일로서 수득하였다 (0.62 g).
단계 b) N-(3-{2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}페닐)에탄술폰아미드
본질적으로 상기 실시예 12, 단계 c 및 d에 기재된 동일한 절차를 이용하고, 출발 물질로서 N-(3-{[4-(디플루오로메톡시)페닐]에티닐}페닐)에탄술폰아미드를 사용하여 표제 화합물을 백색 고체로서 수득하고, NMR 및 질량 스펙트럼 분석으로 확인하였다. [M+H]+ 439.1
실시예 98 내지 108
N-(3-{2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}페닐)술폰아미드 화합물의 제조
본질적으로 상기 실시예 97에 기재된 동일한 절차를 이용하고, 단계 a에서 목적하는 술포닐 클로라이드를 사용하여 하기 표 V에 나타낸 화합물을 수득하고, NMR 및 질량 스펙트럼 분석으로 확인하였다.
실시예 109 내지 112
N-(3-{2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}페닐)아세트아미드 화합물의 제조
본질적으로 상기 실시예 97에 기재된 동일한 절차를 이용하고, 단계 a에서 적합한 산 클로라이드를 사용하여 하기 표 VI에 나타낸 화합물을 수득하고, NMR 및 질량 스펙트럼 분석으로 확인하였다. 본질적으로 실시예 1, 단계 d에 기재된 동일한 절차를 이용하여 키랄 분리를 달성하였다.
실시예 113
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(5-히드록시펜트-1-인-1-일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
2-아미노-5-(3-브로모페닐)-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온 (1.15 g, 2.8 mmol), 디옥산, 비스(벤조니트릴)디클로로팔라듐(II) (32.2 mg, 0.084 mmol), 트리-tert-부틸 포스핀 (헥산 중 10% w/w, 339 mg, 0.17 mmol) 및 디이소프로필 아민 (340 mg, 3.36 mmol)의 혼합물을 아르곤하에 5분 동안 탈기하고, 펜트-4-인-1-올 (236 mg, 2.8 mmol)로 처리하고, 80 ℃에서 5시간 동안 교반하고, 물에 붓고, 에틸 아세테이트로 추출하였다. 유기 추출물을 합하고, MgSO4로 건조하고, 진공에서 농축하였다. 얻어진 잔류물을 ICSO (EtOAc/MeOH 10/1)로 정제하여 표제 화합물을 백색 고체로서 수득하고 (849 mg), NMR 및 질량 스펙트럼 분석으로 확인하였다. [M+H]+ 414.2
실시예 114 내지 173
2-아미노-5-[4-(디플루오로메톡시)페닐]-5-(3-알키닐페닐)-3-메틸-3,5-디히드로-4H-이미다졸-4-온 화합물의 제조
본질적으로 상기 실시예 113에 기재된 동일한 절차를 이용하고, 목적하는 알킨 시약을 사용하여 하기 표 VII에 나타낸 화합물을 수득하고, NMR 및 질량 스펙트럼 분석으로 확인하였다. 본질적으로 실시예 1, 단계 d에 기재된 동일한 절차를 이용하여 키랄 분리를 달성하였다.
실시예 174
2-아미노-5-{3-[(E)-2-시클로프로필비닐]페닐}-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온의 제조
2-아미노-5-(3-브로모페닐)-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온 (150 g, 0.36 mmol), 디메톡시에탄, 2-[(E)-2-시클로프로필비닐]-4,4,5,5-테트라메틸-1,3,2-디옥사보로란 (105 mg) 및 Na2CO3 (2 M, 2.5 mL)의 혼합물을 아르곤하에 5분 동안 탈기하고, 테트라키스(트리페닐포스핀) 팔라듐(0) (21 mg, 0.018 mmol)으로 처리하였다. 상기 반응 혼합물을 15시간 동안 교반하고, 물에 붓고, 에틸 아세테이트로 추출하였다. 추출물을 합하고, MgSO4로 건조하고, 진공에서 농축하였다. 얻어진 잔류물을 ICSO (EtOAc/MeOH 10/1)로 정제하여 표제 화합물을 백색 고체 (98 mg)로서 수득하고, NMR 및 질량 스펙트럼 분석으로 확인하였다.
실시예 175 내지 187
2-아미노-5-[3-(2-치환된-비닐)페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온 화합물의 제조
본질적으로 상기 실시예 174에 기재된 동일한 절차를 이용하고, 비닐디보로란 시약 또는 비닐 트리부틸주석 시약을 사용하여 하기 표 VIII에 나타낸 화합물을 수득하고, NMR 및 질량 스펙트럼 분석으로 확인하였다.
실시예 188
시험 화합물의 BACE-1 결합 친화성의 평가
형광 반응속도론 검정
최종 검정 조건: 10 nM 인간 BACE1 (또는 10 nM 쥐과 BACE1, 1.5 nM 인간 BACE2), 25 μM 기질 (WABC-6, MW 1549.6, 아나스펙(AnaSpec)으로부터 입수), 완충액: 50 mM Na-아세테이트, pH 4.5, 0.05% CHAPS, 25% PBS, 실온. Na-아세테이트는 알드리치(Aldrich)로부터 제품 번호 24,124-5로 입수하였고, CHAPS는 리서치 오가닉스(Research Organics)로부터 제품 번호 1304C 1X로 입수하였고, PBS는 미디어테크(Mediatech (Cellgro))로부터 제품 번호 21-031-CV로 입수하였고, 펩티드 기질 AbzSEVNLDAEFRDpa는 아나스펙으로부터 펩티드 명칭 WABC-6으로 입수하였다.
스톡 기질 ( AbzSEVNLDAEFRDpa ) 농도의 측정: 상기 펩티드 중량 및 MW를 이용하여 DMSO 중에서 대략 25 mM 원액을 제조하고, 1X PBS 중에서 대략 25 μM (1:1000)로 희석하였다. 18172 M-1cm-1의 흡광 계수 ε를 이용하여 354 nm에서의 흡광도에 의해 농도를 측정하고, 스톡 기질의 농도를 보정하고, 기질 스톡을 -80 ℃에서 적은 분취량으로 저장하였다.
[기질 스톡] = ABS 354 nm * 106 / 18172 (mM)
흡광 계수 ε354 nm를 동일한 켄처-형광발색단 쌍을 갖는 TACE 펩티드 기질로부터 적용하였다.
스톡 효소 농도의 측정: 각 효소의 스톡 농도를 6 M 구아니디늄 히드로클로라이드 (리서치 오가닉스로부터 제품 번호 5134G-2로 입수, 대략 pH 6) 중에서 hBACE1 및 MuBACE1의 경우 64150 M-1cm-1의 ε를 이용하고, hBACE2의 경우 62870 M-1cm-1의 ε를 이용하여 280 nm에서의 흡광도에 의해 측정하였다. 각 효소에 대한 흡광 계수 ε280 nm를 기존의 아미노산 조성물 및 Trp (5.69 M-1cm-1) 및 Tyr (1.28 M-1cm-1) 잔기에 대해 공개된 흡광 계수에 기초하여 계산하였다 (문헌 [Anal. Biochem. 182, 319-326]).
희석 및 혼합 단계: 전체 반응 부피: 100 ㎕
완충액 A (66.7 mM Na-아세테이트, pH 4.5, 0.0667% CHAPS) 중 2X 억제제 희석액을 제조하였다.
완충액 A (66.7 mM Na-아세테이트, pH 4.5, 0.0667% CHAPS) 중 4X 효소 희석액을 제조하였다.
1X PBS 중 100 μM 기질 희석액을 제조하였다.
50 ㎕ 2X 억제제, 25 ㎕ 100 μM 기질을 96-웰 플레이트 (디넥스 테크놀로지즈(DYNEX Technologies)로부터 입수, VWR #: 11311-046)의 각 웰에 첨가한 직후, 25 ㎕ 4X 효소를 첨가하고 (억제제 및 기질 혼합물에 첨가하고), 형광 판독을 개시하였다.
형광 판독: 실온에서 30 분 동안 매 40초 마다 λex 320 nm 및 λem 420 nm에서 판독하고, 기질 절단율 (vi)에 대한 선형 기울기를 측정하였다.
억제율%의 계산:
억제율% = 100 * (1- vi/v0)
vi: 억제제 존재하의 기질 절단율
v0: 억제제 부재하의 기질 절단율
IC 50 측정:
억제율% = ((B * IC50 n) + (100 * I0 n)) / (IC50 n + I0 n)
(엑셀의 LSW 툴 바로부터 모델 번호 39, 여기서, B는 효소 대조군(이는 0에 가까워야 함)으로부터의 억제율%임). 억제율%을 억제제 농도 (I0)에 대해 플롯하고, 데이타를 상기 수학식에 적용하여, 각 화합물에 대한 IC50 값 및 힐(Hill) 수 (n)를 수득하였다. 10개 이상의 상이한 억제제 농도에서 시험하는 것이 바람직하다. 결과를 하기 표 IX에 기재하였다. 표 IX에 있어서, A = ≤0.01 μM-0.10 μM, B = 0.11 μM-1.00 μM, C = 〉1.00 μM이다.
Claims (15)
- 하기 화학식 I의 화합물, 또는 그의 호변이성질체, 그의 입체이성질체 또는 그의 제약상 허용가능한 염.<화학식 I>식 중,R1 및 R2는 각각 독립적으로 H, 또는 각각 임의로 치환된 알킬, 시클로알킬, 시클로헤테로알킬, 아릴 또는 헤테로아릴 기이거나, 또는 R1 및 R2는 이들이 부착된 원자와 함께 O, N 또는 S로부터 선택된 추가의 헤테로원자를 임의로 함유하는 임의로 치환된 5- 내지 7-원 고리를 형성할 수 있고;R3은 H, 또는 각각 임의로 치환된 알킬, 시클로알킬, 시클로헤테로알킬, 아릴 또는 헤테로아릴 기이고;R4, R5 및 R6은 각각 독립적으로 H, 할로겐, NO2, CN, COR7, NR10CO2R11, NR15COR16, OR14, NR12R13, SOnR17, 또는 각각 임의로 치환된 알킬, 할로알킬, 알케닐, 할로알케닐, 알키닐, 시클로알킬 또는 시클로헤테로알킬 기이거나, 또는 인접 탄소 원자에 부착된 경우 R4 및 R5는 이들이 부착된 원자와 함께 O, N 또는 S로부터 선택된 1 또는 2개의 헤테로원자를 임의로 함유하는 임의로 치환된 5- 내지 7-원 고리를 형성할 수 있고;n은 0, 1 또는 2이고;R7 및 R17은 각각 독립적으로 H, NR8R9, 또는 각각 임의로 치환된 알킬, 할로알킬, 알콕시알킬, 알케닐, 알키닐, 시클로알킬 또는 아릴 기이고;R8 및 R9는 각각 독립적으로 H, 또는 각각 임의로 치환된 알킬, 알케닐, 알키닐 또는 시클로알킬 기이거나, 또는 R8 및 R9는 이들이 부착된 원자와 함께 O, N 또는 S로부터 선택된 추가의 헤테로원자를 임의로 함유하는 임의로 치환된 5- 내지 7-원 고리를 형성할 수 있고;R11, R14 및 R16은 각각 독립적으로 H, 또는 각각 임의로 치환된 알킬, 할로알킬, 알콕시알킬, 알케닐, 알키닐, 시클로알킬 또는 아릴 기이고;R10 및 R15는 각각 독립적으로 H 또는 임의로 치환된 알킬 기이며;R12 및 R13은 각각 독립적으로 H, 또는 각각 임의로 치환된 알킬 또는 시클로알킬 기이거나, 또는 R12 및 R13은 이들이 부착된 원자와 함께 O, N 또는 S로부터 선택된 추가의 헤테로원자를 임의로 함유하는 임의로 치환된 5- 내지 7-원 고리를 형성할 수 있다.
- 제1항에 있어서, R1 및 R2가 H인 화합물.
- 제1항 또는 제2항에 있어서, R3이 C1-C4알킬인 화합물.
- 제3항에 있어서, R3이 메틸인 화합물.
- 제1항 내지 제4항 중 어느 한 항에 있어서, R4, R5 및 R6이 각각 독립적으로 H, 할로겐, COR7, OR14, 또는 각각 임의로 치환된 알킬, 할로알킬, 알콕시, 할로알콕시, 알키닐 또는 시클로알킬 기인 화합물.
- 제5항에 있어서, R4가 H, COR7, OR14, 또는 각각 임의로 치환된 알킬, 할로알킬, 알콕시, 할로알콕시, 알키닐 또는 시클로알킬 기인 화합물.
- 제1항 내지 제6항 중 어느 한 항에 있어서, R5 및 R6이 H 또는 할로겐인 화합물.
- 제1항 내지 제7항 중 어느 한 항에 있어서, R4가 페닐 고리의 3-위치에 존재 하는 화합물.
- 제1항에 있어서,(5S)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-페닐-3,5-디히드로-4H-이미다졸-4-온;(5R)-2-아미노-5-[4-(디플루오로메톡시)-페닐]-3-메틸-5-페닐-3,5-디히드로-4H-이미다졸-4-온;(5R)-2-아미노-5-(3-브로모페닐)-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;(5S)-2-아미노-5-(3-브로모페닐)-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;(5R)-2-아미노-5-(3-브로모-4-플루오로페닐)-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;(5S)-2-아미노-5-(3-브로모-4-플루오로페닐)-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;(5R)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-(3-프로필페닐)-3,5-디히드로-4H-이미다졸-4-온;(5S)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-(3-프로필페닐)-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(3-플루오로프로필)페닐]-3-메 틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(3,3-디플루오로프로필)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(4-플루오로부틸)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[3-(4,4-디플루오로부틸)페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(2-플루오로에틸)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[3-(2,2-디플루오로에틸)페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-[3-(2,2,2-트리플루오로에틸)페닐]-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-[3-(3,3,3-트리플루오로프로필)페닐]-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-[3-(4,4,4-트리플루오로부틸)페닐]-3,5-디히드로-4H-이미다졸-4-온;(5R)-2-아미노-5-(3-부틸페닐)-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;(5S)-2-아미노-5-(3-부틸페닐)-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디 히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-(3-펜틸페닐)-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-[3-(2-메틸부틸)페닐]-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-(3-부트-3-엔-1-일페닐)-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[3-(시클로프로필메틸)페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;3-(3-{2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}페닐)프로판니트릴;(5R)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-(3-펜트-4-엔-1-일페닐)-3,5-디히드로-4H-이미다졸-4-온;(5S)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-(3-펜트-4-엔-1-일페닐)-3,5-디히드로-4H-이미다졸-4-온;N-(3-{(4R)-2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}페닐)-2-메톡시아세트아미드;N-(3-{(4S)-2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}페닐)-2-메톡시아세트아미드;(5S)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-페닐-3,5-디히드로- 4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(4-히드록시부트-1-인-1-일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(4-히드록시부틸)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(5-플루오로펜틸)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(4-플루오로부틸)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(6-플루오로헥실)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(4-메톡시부틸)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[(1Z)-3-메톡시프로프-1-엔-1-일]페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(3-메톡시프로필)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[3-(4,4-디플루오로부틸)페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;3-{2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H- 이미다졸-4-일}-N-프로필벤즈아미드;(1E)-3-클로로프로프-1-에닐 2,5-디클로로페닐 술폰;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[(2-플루오로에톡시)메틸]페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-{3-[(3,3,3-트리플루오로프로폭시)메틸]페닐}-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(메톡시메틸)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[3-(부톡시메틸)페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-{3-[(시클로프로필메톡시)메틸]페닐}-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(에톡시메틸)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-[3-(프로폭시메틸)페닐]-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-(3-{[2-플루오로-1-(플루오로메틸)에톡시]메틸}페닐)-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-{3-[(2,2,2-트리플루오로에톡시)메틸]페닐}-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-{3-[(2,2,3,3-테트라플루오로프로폭시)메틸]페닐}-3,5-디히드로-4H-이미다졸-4-온;4-[4-(디플루오로메톡시)페닐]-4-[3-(3-메톡시프로프-1-인-1-일)페닐]-1-메틸-4,5-디히드로-1H-이미다졸-2-아민;2-아미노-5-[3-(1,4-디플루오로부틸)페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(3-플루오로부트-3-엔-1-일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[3-(4,4-디플루오로부트-3-엔-1-일)페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-[3-(4,4,4-트리플루오로부틸)페닐]-3,5-디히드로-4H-이미다졸-4-온;5-(3-{2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}페닐)펜탄니트릴;4-(3-{2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}페닐)부탄니트릴;2-아미노-5-{3-[(1E)-4,4-디플루오로부트-1-엔-1-일]페닐}-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(3-히드록시헥스-4-인-1-일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[(1E)-6-메톡시헥스-1-엔-1-일]페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[(1E)-5-메톡시펜트-1-엔-1-일]페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[2-(메톡시메틸)시클로프로필]페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[(1E)-5-히드록시펜트-1-엔-1-일}페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[(1E)-3-메톡시프로프-1-엔-1-일]페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[(1E)-4-메톡시부트-1-엔-1-일]페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[(1E)-4-히드록시부트-1-엔-1-일]페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[2-(2-메톡시에틸)시클로프로필]페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[(1E)-4-플루오로부트-1-엔-1-일]페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{3-[(1E)-5-플루오로펜트-1-엔-1-일]페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온;5-(3-아세틸페닐)-2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-{4-플루오로-3-[(1E)-4-플루오로부트-1-엔-1-일]페닐}-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(3-플루오로프로프-1-인-1-일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-(3-히드록시페닐)-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(3-플루오로프로폭시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[3-(시클로프로필메톡시)페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-[3-(4,4,4-트리플루오로부톡시)페닐]-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[3-(2,2-디플루오로에톡시)페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(4-플루오로부톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-[3-(3-페녹시프로폭시)페닐]-3,5-디히드로-4H-이미다졸-4-온;4-(3-{2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}페녹시)부탄니트릴;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[4-플루오로-3-(3-플루오로프로폭시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[3-(부트-2-인-1-일옥시)-4-플루오로페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[4-플루오로-3-(4-플루오로부톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[3-(2,2-디플루오로에톡시)-4-플루오로페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;(5R)-2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[4-플루오로-3-(3-플루오로프로폭시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;(5S)-2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[4-플루오로-3-(3-플루오로프로폭시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-{3-[(4,4-디플루오로부트-3-엔-1-일)옥시]페닐}-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;(5S)-2-아미노-5-[3-(2,2-디플루오로에톡시)-4-플루오로페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;(5R)-2-아미노-5-[3-(2,2-디플루오로메톡시)-4-플루오로페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(2-플루오로에틸)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(5-플루오로펜타노일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(4-플루오로부타노일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[3-(부트-3-엔-1-일옥시)페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[3-(부트-3-엔-1-일옥시)-4-플루오로페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;(5R)-2-아미노-5-[3-(부트-3-엔-1-일옥시)페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;(5S)-2-아미노-5-[3-(부트-3-엔-1-일옥시)페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-{3-[(4,4-디플루오로부트-3-엔-1-일)옥시]-4-플루오로페닐}-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-(4-플루오로-3-펜트-4-엔-1-일페닐)-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-(3-부트-3-엔-1-일-4-플루오로페닐)-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;3-{2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}벤즈알데히드;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(1-히드록시부트-2-인-1-일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(1,4-디히드록시부트-2-인-1-일)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;(5R)-2-아미노-5-[3-(디플루오로메톡시)페닐]-5-[4-(디플루오로메톡시)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(2,2-디메틸-3-옥소시클로부틸)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-3-메틸-5-[3-(3-옥소시클로부틸)페닐]-3,5-디히드로-4H-이미다졸-4-온;2-아미노-5-[4-(디플루오로메톡시)페닐]-5-[3-(3-히드록시시클로부틸)페닐]-3-메틸-3,5-디히드로-4H-이미다졸-4-온;메틸 [3-(3-{2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}페닐)시클로부틸]아세테이트;메틸 [3-(3-{2-아미노-4-[4-(디플루오로메톡시)페닐]-1-메틸-5-옥소-4,5-디히드로-1H-이미다졸-4-일}페닐)시클로부틸리덴]아세테이트;이들의 호변이성질체;이들의 입체이성질체; 및이들의 제약상 허용가능한 염으로 이루어진 군으로부터 선택되는 것인 화합물.
- 치료 유효량의 제1항 내지 제9항 중 어느 한 항에 따른 화합물을 치료가 필요한 환자에게 투여하는 것을 포함하는, 상기 환자에서 과도한 BACE 활성과 관련된 질환 또는 장애의 치료 방법.
- 제10항에 있어서, 상기 질환 또는 장애가 알쯔하이머병, 인지 장애, 다운 증후군, 네덜란드형의 아밀로이드증성 유전성 뇌출혈 (HCHWA-D), 인지 저하, 노인성 치매, 대뇌 아밀로이드 맥관병증 및 신경퇴행성 장애로 이루어진 군으로부터 선택되는 것인 방법.
- 제10항에 있어서, 상기 질환 또는 장애가 β-아밀로이드 침착 또는 신경섬유 농축의 발생을 특징으로 하는 방법.
- 유효량의 제1항 내지 제9항 중 어느 한 항에 따른 화합물을 이들의 수용체와 접촉시키는 것을 포함하는, BACE 활성의 조정 방법.
- 유효량의 제1항 내지 제9항 중 어느 한 항에 따른 화합물을 치료가 필요한 환자에게 제공하는 것을 포함하는, 상기 환자에서 알쯔하이머병의 치료 방법.
- 유효량의 제1항 내지 제9항 중 어느 한 항에 따른 화합물 및 제약상 허용가능한 담체를 포함하는 제약 조성물.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US72058905P | 2005-09-26 | 2005-09-26 | |
| US60/720,589 | 2005-09-26 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20080050430A true KR20080050430A (ko) | 2008-06-05 |
Family
ID=37693581
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020087007179A KR20080050430A (ko) | 2005-09-26 | 2006-09-22 | 베타-세크레타제 (bace) 억제제로서아미노-5-[4-(디플루오로메톡시)페닐]-5-페닐이미다졸론화합물 |
Country Status (19)
| Country | Link |
|---|---|
| US (2) | US7423158B2 (ko) |
| EP (2) | EP1928841A1 (ko) |
| JP (1) | JP2009509957A (ko) |
| KR (1) | KR20080050430A (ko) |
| CN (1) | CN101273018A (ko) |
| AR (1) | AR056536A1 (ko) |
| AU (1) | AU2006294620A1 (ko) |
| BR (1) | BRPI0616757A2 (ko) |
| CA (1) | CA2623245A1 (ko) |
| CR (1) | CR9830A (ko) |
| EC (1) | ECSP088286A (ko) |
| GT (1) | GT200600432A (ko) |
| IL (1) | IL189650A0 (ko) |
| NO (1) | NO20080942L (ko) |
| PE (1) | PE20070461A1 (ko) |
| RU (1) | RU2008106936A (ko) |
| TW (1) | TW200808735A (ko) |
| WO (1) | WO2007038271A1 (ko) |
| ZA (1) | ZA200802636B (ko) |
Families Citing this family (67)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7592348B2 (en) | 2003-12-15 | 2009-09-22 | Schering Corporation | Heterocyclic aspartyl protease inhibitors |
| US7763609B2 (en) | 2003-12-15 | 2010-07-27 | Schering Corporation | Heterocyclic aspartyl protease inhibitors |
| US7700603B2 (en) | 2003-12-15 | 2010-04-20 | Schering Corporation | Heterocyclic aspartyl protease inhibitors |
| TW200602045A (en) * | 2004-06-16 | 2006-01-16 | Wyeth Corp | Amino-5, 5-diphenylimidazolone derivatives for the inhibition of β-secretase |
| PE20060299A1 (es) | 2004-06-16 | 2006-05-18 | Wyeth Corp | DIFENILIMIDAZOPIRIMIDINA E -IMIDAZOL AMINAS COMO INHIBIDORES DE ß-SECRETASA |
| ATE396990T1 (de) | 2004-07-28 | 2008-06-15 | Schering Corp | Makrocyclische inhibitoren der beta-sekretase |
| CN101103034A (zh) | 2005-01-14 | 2008-01-09 | 惠氏公司 | 抑制β-分泌酶的氨基-咪唑酮 |
| KR20070107062A (ko) * | 2005-02-01 | 2007-11-06 | 와이어쓰 | β-세크리타제의 억제제로서의 아미노-피리딘 |
| JP2008530103A (ja) | 2005-02-14 | 2008-08-07 | ワイス | β−セクレターゼ阻害剤としてのアゾリルアシルグアニジン |
| WO2006138265A2 (en) * | 2005-06-14 | 2006-12-28 | Schering Corporation | Heterocyclic aspartyl protease inhibitors, preparation and use thereof |
| TWI332005B (en) | 2005-06-14 | 2010-10-21 | Schering Corp | Aspartyl protease inhibitors |
| TW200738683A (en) * | 2005-06-30 | 2007-10-16 | Wyeth Corp | Amino-5-(5-membered)heteroarylimidazolone compounds and the use thereof for β-secretase modulation |
| MX2008000212A (es) * | 2005-06-30 | 2008-03-24 | Wyeth Corp | Compuestos amino-5-(6 miembros)heteroarilimidazolona y el uso de estos para la modulacion de la (-secretasa. |
| TW200730523A (en) * | 2005-07-29 | 2007-08-16 | Wyeth Corp | Cycloalkyl amino-hydantoin compounds and use thereof for β-secretase modulation |
| CA2620136A1 (en) * | 2005-09-05 | 2007-03-15 | Jun Fujita | Sequence capable of enhancing the expression of gene under moderately low temperature |
| WO2007049532A1 (ja) | 2005-10-25 | 2007-05-03 | Shionogi & Co., Ltd. | アミノジヒドロチアジン誘導体 |
| EP1966185A2 (en) * | 2005-12-19 | 2008-09-10 | Wyeth a Corporation of the State of Delaware | 2-AMINO-5-PIPERIDINYLIMIDAZOLONE COMPOUNDS AND USE THEREOF FOR ß-SECRETASE MODULATION |
| WO2007100536A1 (en) * | 2006-02-24 | 2007-09-07 | Wyeth | DIHYDROSPIRO[DIBENZO[A,D][7]ANNULENE-5,4'-IMIDAZOL] COMPOUNDS FOR THE INHIBITION OF β-SECRETASE |
| EP2032542A2 (en) * | 2006-06-12 | 2009-03-11 | Schering Corporation | Heterocyclic aspartyl protease inhibitors |
| US7700606B2 (en) * | 2006-08-17 | 2010-04-20 | Wyeth Llc | Imidazole amines as inhibitors of β-secretase |
| JP2010504326A (ja) * | 2006-09-21 | 2010-02-12 | ワイス エルエルシー | β−セクレターゼを阻害するためのインドリルアルキルピリジン−2−アミン |
| AU2007332750A1 (en) * | 2006-12-12 | 2008-06-19 | Schering Corporation | Aspartyl protease inhibitors containing a tricyclic ring system |
| AU2007332754A1 (en) | 2006-12-12 | 2008-06-19 | Schering Corporation | Aspartyl protease inhibitors |
| WO2008076044A1 (en) * | 2006-12-20 | 2008-06-26 | Astrazeneca Ab | Novel 2-amino-5, 5-diaryl-imidazol-4-ones |
| PE20090160A1 (es) * | 2007-03-20 | 2009-02-11 | Wyeth Corp | COMPUESTOS AMINO-5-[4-(DIFLUOROMETOXI)FENIL SUSTITUIDO]-5-FENILIMIDAZOLONA COMO INHIBIDORES DE ß-SECRETASA |
| CL2008000791A1 (es) * | 2007-03-23 | 2008-05-30 | Wyeth Corp | Compuestos derivados de 2-amino-5-(4-difluorometoxi-fenil)-5-fenil-imidazolidin-4-ona; composicion farmaceutica que comprende a dichos compuestos; y su uso en el tratamiento de una enfermedad asociada con la actividad bace excesiva, tales como enferm |
| JP5383483B2 (ja) | 2007-04-24 | 2014-01-08 | 塩野義製薬株式会社 | アルツハイマー症治療用医薬組成物 |
| EP2689780A1 (en) | 2007-04-24 | 2014-01-29 | Shionogi & Co., Ltd. | Intermediates for aminodihydrothiazine derivatives substituted with a cyclic group |
| AU2009239536C1 (en) | 2008-04-22 | 2012-12-13 | Merck Sharp & Dohme Corp. | Phenyl-substituted 2-imino-3-methyl pyrrolo pyrimidinone compounds as BACE-1 inhibitors, compositions, and their use |
| US8637504B2 (en) | 2008-06-13 | 2014-01-28 | Shionogi & Co., Ltd. | Sulfur-containing heterocyclic derivative having beta secretase inhibitory activity |
| EP2324032B1 (en) | 2008-08-19 | 2014-10-01 | Vitae Pharmaceuticals, Inc. | Inhibitors of beta-secretase |
| CN102209721A (zh) | 2008-09-11 | 2011-10-05 | 安姆根有限公司 | 作为β-分泌酶调节剂的螺四环化合物及其使用方法 |
| CN102186841A (zh) | 2008-10-22 | 2011-09-14 | 盐野义制药株式会社 | 具有bace1抑制活性的2-氨基嘧啶-4-酮及2-氨基吡啶衍生物 |
| PT2406240E (pt) | 2009-03-13 | 2016-02-24 | Boehringer Ingelheim Int | Inibidores de beta-secretase |
| UA108363C2 (uk) | 2009-10-08 | 2015-04-27 | Похідні імінотіадіазиндіоксиду як інгібітори bace, композиція на їх основі і їх застосування | |
| EP2485920B1 (en) | 2009-10-08 | 2016-04-27 | Merck Sharp & Dohme Corp. | Pentafluorosulfur imino heterocyclic compounds as bace-1 inhibitors, compositions, and their use |
| WO2011044184A1 (en) | 2009-10-08 | 2011-04-14 | Schering Corporation | Pentafluorosulfur imino heterocyclic compounds as bace-1 inhibitors, compositions, and their use |
| EP2485591B1 (en) | 2009-10-08 | 2016-03-23 | Merck Sharp & Dohme Corp. | Iminothiadiazine dioxide compounds as bace inhibitors, compositions, and their use |
| US8999980B2 (en) | 2009-12-11 | 2015-04-07 | Shionogi & Co., Ltd. | Oxazine derivatives |
| CN102812005B (zh) | 2010-02-24 | 2014-12-10 | 生命医药公司 | β-分泌酶抑制剂 |
| EP2547685A1 (en) | 2010-03-15 | 2013-01-23 | Amgen Inc. | Spiro-tetracyclic ring compounds as beta - secretase modulators |
| ES2450568T3 (es) | 2010-03-15 | 2014-03-25 | Amgen Inc. | Compuestos espiero de amino-dihidrooxazina y amino-dihidrotiazina como moduladores de beta-secretasa y su uso médico |
| WO2012019056A1 (en) | 2010-08-05 | 2012-02-09 | Amgen Inc. | Amino-iso-indole, amino-aza-iso-indole, amino-dihydroisoquinoline and amino-benzoxazine compounds as beta-secretase modulators and methods of use |
| JP5766198B2 (ja) | 2010-10-29 | 2015-08-19 | 塩野義製薬株式会社 | 縮合アミノジヒドロピリミジン誘導体 |
| WO2012057248A1 (ja) | 2010-10-29 | 2012-05-03 | 塩野義製薬株式会社 | ナフチリジン誘導体 |
| US8957083B2 (en) | 2010-11-23 | 2015-02-17 | Amgen Inc. | Spiro-amino-imidazolone and spiro-amino-dihydro-pyrimidinone compounds as beta-secretase modulators and methods of use |
| EP2673279A1 (en) | 2011-02-07 | 2013-12-18 | Amgen Inc. | 5-amino-oxazepine and 5-amino-thiazepane compounds as beta-secretase antagonists and methods of use |
| WO2012112462A1 (en) | 2011-02-15 | 2012-08-23 | Amgen Inc. | Spiro-amino-imidazo-fused heterocyclic compounds as beta-secretase modulators and methods of use |
| EP2694489B1 (en) | 2011-04-07 | 2017-09-06 | Merck Sharp & Dohme Corp. | C5-c6 oxacyclic-fused thiadiazine dioxide compounds as bace inhibitors, compositions, and their use |
| EP2694521B1 (en) | 2011-04-07 | 2015-11-25 | Merck Sharp & Dohme Corp. | Pyrrolidine-fused thiadiazine dioxide compounds as bace inhibitors, compositions, and their use |
| EP2703399A4 (en) | 2011-04-26 | 2014-10-15 | Shionogi & Co | OXAZINE DERIVATIVE AND BACE-1 HEMMER THEREOF |
| CA2844988A1 (en) | 2011-08-22 | 2013-02-28 | Merck Sharp & Dohme Corp. | 2-spiro-substituted iminothiazines and their mono- and dioxides as bace inhibitors, compositions, and their use |
| EP2758406A1 (en) | 2011-09-21 | 2014-07-30 | Amgen Inc. | Amino-oxazines and amino-dihydrothiazine compounds as beta-secretase modulators and methods of use |
| TWI557112B (zh) | 2012-03-05 | 2016-11-11 | 百靈佳殷格翰國際股份有限公司 | β-分泌酶抑制劑 |
| ES2745539T3 (es) | 2012-03-19 | 2020-03-02 | Buck Inst Res Aging | Inhibidores de BACE específicos de APP (ASBI) y uso de los mismos |
| TW201422592A (zh) | 2012-08-27 | 2014-06-16 | Boehringer Ingelheim Int | β-分泌酶抑制劑 |
| WO2014052398A1 (en) | 2012-09-28 | 2014-04-03 | Vitae Pharmaceuticals, Inc. | Inhibitor of beta-secretase |
| US9422277B2 (en) | 2012-10-17 | 2016-08-23 | Merck Sharp & Dohme Corp. | Tricyclic substituted thiadiazine dioxide compounds as BACE inhibitors, compositions and their use |
| EP2908824B1 (en) | 2012-10-17 | 2018-05-02 | Merck Sharp & Dohme Corp. | Tricyclic substituted thiadiazine dioxide compounds as bace inhibitors, compositions, and their use |
| JP2016501827A (ja) | 2012-10-24 | 2016-01-21 | 塩野義製薬株式会社 | Bace1阻害作用を有するジヒドロオキサジンまたはオキサゼピン誘導体 |
| US9725469B2 (en) | 2012-11-15 | 2017-08-08 | Amgen, Inc. | Amino-oxazine and amino-dihydrothiazine compounds as beta-secretase modulators and methods of use |
| EP3653609B1 (en) * | 2013-02-12 | 2024-04-03 | Buck Institute for Research on Aging | Hydantoins that modulate bace-mediated app processing |
| CN103408573B (zh) * | 2013-07-12 | 2015-12-23 | 上海工程技术大学 | 硼酸衍生物及其制备方法和应用 |
| EP3341362B1 (en) * | 2015-08-27 | 2023-07-05 | Nantneuro, LLC | Compositions for app-selective bace inhibition and uses therfor |
| CN106749033A (zh) * | 2015-11-25 | 2017-05-31 | 中国人民解放军军事医学科学院毒物药物研究所 | 乙内酰脲类化合物及其作为β-分泌酶抑制剂的用途 |
| CN113087667B (zh) * | 2021-03-24 | 2022-06-24 | 五邑大学 | 一种咪唑啉酮衍生物的合成方法 |
| WO2024201390A1 (en) * | 2023-03-29 | 2024-10-03 | Simon Fraser University | Methods and reagents for synthesizing haloaldehydes, and uses thereof |
Family Cites Families (32)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| IE45198B1 (en) | 1976-06-05 | 1982-07-14 | Wyeth John & Brother Ltd | Guanidine derivatives |
| DE2901362A1 (de) | 1978-01-25 | 1979-07-26 | Sandoz Ag | Guanidinderivate, ihre herstellung und verwendung |
| GB1588096A (en) | 1978-05-20 | 1981-04-15 | Wyeth & Bros Ltd John | Pyrrole derivatives |
| GB9511694D0 (en) | 1995-06-09 | 1995-08-02 | Fujisawa Pharmaceutical Co | Benzamide derivatives |
| ZA967800B (en) | 1995-09-20 | 1997-04-03 | Yamanouchi Pharma Co Ltd | Heteroaryllsubstituted acryloylguanidine derivatives and pharmaceutical compositions comprising them |
| GB9611046D0 (en) | 1996-05-25 | 1996-07-31 | Wivenhoe Techn Ltd | Pharmacological compounds |
| GB2323841A (en) | 1997-04-04 | 1998-10-07 | Ferring Bv Group Holdings | Pyridine derivatives with anti-tumor and anti-inflammatory activity |
| TW544448B (en) | 1997-07-11 | 2003-08-01 | Novartis Ag | Pyridine derivatives |
| US6492408B1 (en) | 1999-07-21 | 2002-12-10 | Boehringer Ingelheim Pharmaceuticals, Inc. | Small molecules useful in the treatment of inflammatory disease |
| DE10024319A1 (de) | 2000-05-17 | 2001-11-22 | Merck Patent Gmbh | Bisacylguanidine |
| DE10046993A1 (de) | 2000-09-22 | 2002-04-11 | Aventis Pharma Gmbh | Substituierte Zimtsäureguanidide, Verfahren zur ihrer Herstellung, ihre Verwendung als Medikament sowie sie enthaltendes Medikament |
| WO2003053938A1 (en) | 2001-12-20 | 2003-07-03 | Novo Nordisk A/S | Benzimidazols and indols as glucagon receptor antagonists/inverse agonisten |
| US7053220B2 (en) | 2002-02-01 | 2006-05-30 | Elan Pharmaceuticals, Inc. | Hydroxyalkanoyl aminopyrazoles and related compounds |
| US6974829B2 (en) | 2002-05-07 | 2005-12-13 | Elan Pharmaceuticals, Inc. | Succinoyl aminopyrazoles and related compounds |
| AU2003299791A1 (en) * | 2002-12-20 | 2004-07-22 | Bayer Pharmaceuticals Corporation | Substituted 3,5-dihydro-4h-imidazol-4-ones for the treatment of obesity |
| EP1644354A1 (en) | 2003-07-01 | 2006-04-12 | Bayer CropScience GmbH | 3-pyridylcarboxamide derivatives as pesticidal agents |
| US7700603B2 (en) | 2003-12-15 | 2010-04-20 | Schering Corporation | Heterocyclic aspartyl protease inhibitors |
| NZ547462A (en) * | 2003-12-15 | 2010-06-25 | Schering Corp | Heterocyclic aspartyl protease inhibitors |
| US7592348B2 (en) | 2003-12-15 | 2009-09-22 | Schering Corporation | Heterocyclic aspartyl protease inhibitors |
| PE20060299A1 (es) | 2004-06-16 | 2006-05-18 | Wyeth Corp | DIFENILIMIDAZOPIRIMIDINA E -IMIDAZOL AMINAS COMO INHIBIDORES DE ß-SECRETASA |
| TW200602045A (en) * | 2004-06-16 | 2006-01-16 | Wyeth Corp | Amino-5, 5-diphenylimidazolone derivatives for the inhibition of β-secretase |
| CN101103034A (zh) | 2005-01-14 | 2008-01-09 | 惠氏公司 | 抑制β-分泌酶的氨基-咪唑酮 |
| KR20070107062A (ko) | 2005-02-01 | 2007-11-06 | 와이어쓰 | β-세크리타제의 억제제로서의 아미노-피리딘 |
| WO2006088694A1 (en) | 2005-02-14 | 2006-08-24 | Wyeth | SUBSTITUTED THIENYL AND FURYL ACYLGUANIDINES AS β-SECRETASE MODULATORS |
| WO2006088705A1 (en) | 2005-02-14 | 2006-08-24 | Wyeth | Terphenyl guanidines as [beta symbol] -secretase inhibitors |
| JP2008530103A (ja) | 2005-02-14 | 2008-08-07 | ワイス | β−セクレターゼ阻害剤としてのアゾリルアシルグアニジン |
| TW200738683A (en) | 2005-06-30 | 2007-10-16 | Wyeth Corp | Amino-5-(5-membered)heteroarylimidazolone compounds and the use thereof for β-secretase modulation |
| MX2008000212A (es) | 2005-06-30 | 2008-03-24 | Wyeth Corp | Compuestos amino-5-(6 miembros)heteroarilimidazolona y el uso de estos para la modulacion de la (-secretasa. |
| TW200730523A (en) | 2005-07-29 | 2007-08-16 | Wyeth Corp | Cycloalkyl amino-hydantoin compounds and use thereof for β-secretase modulation |
| EP1966185A2 (en) | 2005-12-19 | 2008-09-10 | Wyeth a Corporation of the State of Delaware | 2-AMINO-5-PIPERIDINYLIMIDAZOLONE COMPOUNDS AND USE THEREOF FOR ß-SECRETASE MODULATION |
| WO2007100536A1 (en) | 2006-02-24 | 2007-09-07 | Wyeth | DIHYDROSPIRO[DIBENZO[A,D][7]ANNULENE-5,4'-IMIDAZOL] COMPOUNDS FOR THE INHIBITION OF β-SECRETASE |
| US7700606B2 (en) | 2006-08-17 | 2010-04-20 | Wyeth Llc | Imidazole amines as inhibitors of β-secretase |
-
2006
- 2006-09-22 AU AU2006294620A patent/AU2006294620A1/en not_active Abandoned
- 2006-09-22 RU RU2008106936/04A patent/RU2008106936A/ru not_active Application Discontinuation
- 2006-09-22 BR BRPI0616757-8A patent/BRPI0616757A2/pt not_active IP Right Cessation
- 2006-09-22 EP EP06815185A patent/EP1928841A1/en not_active Withdrawn
- 2006-09-22 CA CA002623245A patent/CA2623245A1/en not_active Abandoned
- 2006-09-22 WO PCT/US2006/036985 patent/WO2007038271A1/en active Application Filing
- 2006-09-22 EP EP10172623A patent/EP2256107A1/en not_active Withdrawn
- 2006-09-22 JP JP2008532416A patent/JP2009509957A/ja not_active Withdrawn
- 2006-09-22 PE PE2006001150A patent/PE20070461A1/es not_active Application Discontinuation
- 2006-09-22 KR KR1020087007179A patent/KR20080050430A/ko not_active Application Discontinuation
- 2006-09-22 CN CNA2006800353948A patent/CN101273018A/zh active Pending
- 2006-09-25 US US11/526,511 patent/US7423158B2/en not_active Expired - Fee Related
- 2006-09-26 AR ARP060104191A patent/AR056536A1/es unknown
- 2006-09-26 GT GT200600432A patent/GT200600432A/es unknown
- 2006-09-26 TW TW095135587A patent/TW200808735A/zh unknown
-
2008
- 2008-02-21 IL IL189650A patent/IL189650A0/en unknown
- 2008-02-25 NO NO20080942A patent/NO20080942L/no not_active Application Discontinuation
- 2008-03-17 EC EC2008008286A patent/ECSP088286A/es unknown
- 2008-03-25 ZA ZA200802636A patent/ZA200802636B/xx unknown
- 2008-03-26 CR CR9830A patent/CR9830A/es not_active Application Discontinuation
- 2008-08-29 US US12/201,026 patent/US20090012139A1/en not_active Abandoned
Also Published As
| Publication number | Publication date |
|---|---|
| US7423158B2 (en) | 2008-09-09 |
| ZA200802636B (en) | 2009-03-25 |
| TW200808735A (en) | 2008-02-16 |
| EP1928841A1 (en) | 2008-06-11 |
| WO2007038271A9 (en) | 2008-05-08 |
| GT200600432A (es) | 2007-05-28 |
| CN101273018A (zh) | 2008-09-24 |
| US20090012139A1 (en) | 2009-01-08 |
| AU2006294620A1 (en) | 2007-04-05 |
| IL189650A0 (en) | 2008-06-05 |
| WO2007038271A1 (en) | 2007-04-05 |
| AR056536A1 (es) | 2007-10-10 |
| CR9830A (es) | 2008-05-21 |
| BRPI0616757A2 (pt) | 2011-06-28 |
| NO20080942L (no) | 2008-04-07 |
| ECSP088286A (es) | 2008-04-28 |
| US20070072925A1 (en) | 2007-03-29 |
| RU2008106936A (ru) | 2009-11-10 |
| JP2009509957A (ja) | 2009-03-12 |
| CA2623245A1 (en) | 2007-04-05 |
| PE20070461A1 (es) | 2007-05-10 |
| EP2256107A1 (en) | 2010-12-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US7423158B2 (en) | Amino-5-[4-(difluoromethoxy)phenyl]-5-phenylimidazolone compounds for the inhibition of β-secretase | |
| US7417047B2 (en) | Amino-5-(5-membered)hetero-arylimidazolone compounds and the use thereof for β-secretase modulation | |
| US7723368B2 (en) | Amino-5-[4-(difluoromethoxy)phenyl]-5-phenylimidazolone compounds for the inhibition of beta-secretase | |
| US20070027199A1 (en) | Cycloalkyl amino-hydantoin compounds and use thereof for beta-secretase modulation | |
| US7452885B2 (en) | Amino-5-(6-membered)heteroarylimidazolone compounds and the use thereof for β-secretase modulation | |
| JP2010522235A (ja) | β−セクレターゼ阻害薬としてのアミノ−5−[置換−4−(ジフルオロメトキシ)フェニル]−5−フェニルイミダゾロン化合物 | |
| AU2006333049A1 (en) | 2-amino-5-piperidinylimidazolone compounds and use thereof for beta-secretase modulation | |
| WO2008036196A2 (en) | Indolylalkylpyridin-2-amines for the inhibition of beta-secretase | |
| MX2008001436A (en) | Cycloalkyl amino-hydantoin compounds and use thereof forî²-secretase modulation | |
| MX2008008011A (en) | 2-amino-5-piperidinylimidazolone compounds and use thereof forî²-secretase modulation |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WITN | Application deemed withdrawn, e.g. because no request for examination was filed or no examination fee was paid |