JP2004309798A - Electrolyte, and electrochemical display device using thesame - Google Patents
Electrolyte, and electrochemical display device using thesame Download PDFInfo
- Publication number
- JP2004309798A JP2004309798A JP2003103243A JP2003103243A JP2004309798A JP 2004309798 A JP2004309798 A JP 2004309798A JP 2003103243 A JP2003103243 A JP 2003103243A JP 2003103243 A JP2003103243 A JP 2003103243A JP 2004309798 A JP2004309798 A JP 2004309798A
- Authority
- JP
- Japan
- Prior art keywords
- dimethyl sulfoxide
- butyrolactone
- electrolyte
- solvent
- display device
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Landscapes
- Electrochromic Elements, Electrophoresis, Or Variable Reflection Or Absorption Elements (AREA)
Abstract
Description
【0001】
【発明の属する技術分野】
本発明は、溶媒を含む電解質およびそれを用いた電気化学表示装置に関する。
【0002】
【従来の技術】
近年、ネットワークの普及につれ、従来印刷物として配布されていた文書類が、いわゆる電子書類で配信されるようになってきた。更に、書籍や雑誌などもいわゆる電子出版の形で提供される場合が多くなりつつある。これらの情報を閲覧するために、従来より、コンピュータのCRT(Cathode−Ray Tube;ブラウン管)または液晶ディスプレイが用いられている。
【0003】
しかし、これら発光型のディスプレイでは、人間工学的理由から疲労が著しく、長時間の読書には耐えられないことが指摘されている。また、読む場所がコンピュータの設置場所に限られるという難点もある。
【0004】
最近では、ノート型コンピュータの普及により、携帯型のディスプレイとして使えるものもあるが、それらは主にバックライトによる発光型であることに加えて消費電力との関係で、これも数時間以上の読書に用いることが難しい。また、反射型液晶ディスプレイも開発され、これによれば低消費電力で駆動することができるが、液晶の無表示(白色表示)における反射率は30%であり、紙への印刷物に比べ著しく視認性が悪く、疲労が生じやすく、これも長時間の読書に耐えるものではない。
【0005】
これらの問題点を解決するために、最近、主に電気泳動法により着色粒子を電極間で移動させるか、あるいは二色性を有する粒子を電場で回転させることにより着色させたディスプレイが開発されつつある。しかし、このディスプレイでは、粒子間の隙間が光を吸収し、その結果としてコントラストが悪くなり、また駆動する電圧を100V以上にしなければ実用上の書き込み速度(1秒以内)が得られないという難点がある。
【0006】
一方、電圧の印加により色が変化することを利用したエレクトロクロミック表示装置(Electro Chromic Display ;ECD)も開発されている。このようなエレクトロクロミック表示装置としては、例えば、H+ などのイオンが入ることにより透明から青色に変化する酸化タングステン(WO3 )、または、酸化あるいは還元により発色する有機材料を用いたものが知られている。これらは、コントラストの高さという点では上記電気泳動方式のものなどに比べて優れているが、黒色の品位が悪い他、マトリクス駆動の必要性がない調光ガラスあるいは時計用ディスプレイの用途として開発が進められているため、現状では、ペーパーライクディスプレイ、あるいは電子ペーパーなどのマトリクス駆動の表示装置用としては用いることは難しい。なお、マトリクス駆動のもの(特許文献1参照)も知られるが、駆動素子は液晶表示装置との組み合わせでその一部を構成するに過ぎない。
【0007】
更に、有機材料は、一般的に、耐光性に乏しいので、用途上太陽光や室内光などの光に晒され続けることになる電子ペーパーに用いた場合、長時間使用すると褪色して黒色濃度が低下するという問題が生ずる。
【0008】
そこで、金属イオンを含む白く着色した電解質を介して電極を対向配置し、表示側の電極に金属を析出させることにより画像の書き込みを行い、その析出させた金属を電解質に溶解させることにより画像の消去を行うエレクトロデポジション型表示装置が提案されている(例えば、特許文献2参照。)。これによれば、マトリクス駆動が容易であり、かつコントラストおよび黒色濃度を高くすることが可能となる。
【0009】
【特許文献1】
特公平4−73764号公報
【特許文献2】
特開2002−258327号公報
【0010】
【発明が解決しようとする課題】
しかしながら、このエレクトロデポジション型表示装置でも、特性、特にサイクル特性が未だ不十分である。また、酸化還元反応を適切に制御することが十分にできず、表示切換の際の消え残り、すなわち残像が発生することがあり、これが画像品質の低下につながるという問題もあった。加えて、電気化学反応を利用した表示装置に多々見られる、応答速度が遅いという問題や、または、温度による依存性が大きく、特に低温において応答速度が低下してしまうという問題もあった。
【0011】
本発明はかかる問題点に鑑みてなされたもので、その目的は、高速応答性を得ることができ、かつ、応答速度の温度依存性を小さくすることができる電気化学表示装置、およびそれに用いる電解質を提供することにある。
【0012】
【課題を解決するための手段】
本発明による電解質は、スルホキシドと、環状カルボン酸エステルとを含有する溶媒を含むものである。
【0013】
本発明による電気化学表示装置は、第1電極と第2電極との間に電解質を備えたものであって、電解質は、スルホキシドと、環状カルボン酸エステルとを含有する溶媒を含むものである。
【0014】
本発明による電解質および電気化学表示装置では、スルホキシドと、環状カルボン酸エステルとを含んでいるので、高速応答性が得られ、かつ、応答速度の温度依存性が小さくなる。
【0015】
【発明の実施の形態】
以下、本発明の実施の形態について、図面を参照して詳細に説明する。
【0016】
図1は、本発明の一実施の形態に係る電気化学表示装置の概略構成を表すものである。この電気化学表示装置は、例えば、電気化学表示素子10と、この電気化学表示素子10を駆動させるための周辺回路部20とを備えている。
【0017】
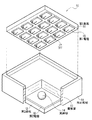
図2は、図1に示した電気化学表示素子10の概略構成を表すものである。電気化学表示素子10は、第1基板11と第2基板12とが電解質13および真絲球14を介して対向配置された構造を有している。第1基板11の第2基板12と対向する側の面には、画素に対応して複数の第1電極15がマトリクス状に配列され、第2基板12の第1基板11と対向する側の全面には第2電極16が形成されている。また、第1基板11の第2基板12と対向する側の面には、TFT(Thin Film transistor;薄膜トランジスタ)17が画素毎に設けられており、TFT17により第1電極15への通電が制御されるようになっている。すなわち、この電気化学表示装置は、アクティブマトリクス型の駆動機構を有している。更に、第1基板11および第2基板12の側面と電解質13とは封止部材18により封止されている。
【0018】
第1基板11は、透明性を有する材料、具体的には、石英ガラスなどにより構成されている。また、この他にも、例えば、合成樹脂、具体的には、ポリエチレンナフタレート,ポリエチレンテレフタレートあるいはポリカーボネートなどのエステル、または、酢酸セルロースなどのセルロースエステル、または、ポリフッ化ビニリデンあるいはポリテトラフルオロエチレンとヘキサフルオロプロピレンとの共重合体などのフッ素ポリマー、または、ポリオキシメチレンなどのポリエーテル、または、ポリアセタール,ポリスチレン,ポリエチレン,ポリプロピレンあるいはメチルペンテンポリマーなどのポリオレフィン、または、ポリアミドイミドあるいはポリエーテルイミドなどのポリイミド、または、ポリアミドにより構成してもよい。これら合成樹脂は、容易に曲がらないような剛性基板状であってもよく、また、可とう性を有するフィルム状の構造体であってもよい。
【0019】
第2基板12は、透明であっても、透明でなくてもよく、例えば、石英ガラス、白板ガラス、セラミックス、紙あるいは木材により構成することができる。また、この他にも、第1基板11で説明した合成樹脂により構成するようにしてもよい。なお、第2電極16が十分な剛性を有する場合には、第2基板12は設けなくてもよい。
【0020】
電解質13は、例えば、溶媒と、酸化還元反応により析出および溶解する析出溶解材料とを含んでいる。溶媒は、スルホキシドと環状カルボン酸エステルとを含んでいる。これにより、この電気化学表示装置では、高速応答性を得ることができ、かつ、応答速度の温度依存性を小さくすることができるようになっている。
【0021】
スルホキシドとしては、ジメチルスルホキシド((CH3 )2 S=O)が常温において液体状であるので好ましく、環状カルボン酸エステルとしては、例えば、化1に示したγ−ブチロラクトンあるいは化2に示したγ−バレロラクトンが好ましい。
【0022】
【化1】
【0023】
【化2】
【0024】
このうちジメチルスルホキシドとγ−ブチロラクトンとを含む場合、ジメチルスルホキシドとγ−ブチロラクトンとの割合は、ジメチルスルホキシド:γ−ブチロラクトン=7:3〜3:7の体積比であることが好ましく、ジメチルスルホキシド:γ−ブチロラクトン=6:4〜3:7の体積比であればより好ましい。この範囲内において、最も多く使用される環境である10℃〜30℃の温度領域において応答速度を速くし、かつ、低温において急速な応答速度の低下を防止することができるからである。
【0025】
また、ジメチルスルホキシドとγ−バレロラクトンとを含む場合、ジメチルスルホキシドとγ−バレロラクトンとの割合は、ジメチルスルホキシド:γ−バレロラクトン=8:2〜3:7の体積比であることが好ましく、ジメチルスルホキシド:γ−バレロラクトン=8:2〜5:5の体積比であればより好ましい。この範囲内において応答速度をより速くすることができるからである。
【0026】
溶媒は、また、スルホキシドと環状カルボン酸エステルとに加えて、化3に示したプロピレンカーボネートを含んでいることが好ましい。特に常温において応答速度を速くすることができるからである。
【0027】
【化3】
【0028】
この場合、より高い効果を得るには、溶媒は、特に、ジメチルスルホキシドを10体積%以上80体積%以下の範囲内、γ−ブチロラクトンを10体積%以上90体積%以下の範囲内、プロピレンカーボネートを60体積%以下の範囲内でそれぞれ含んでいることが好ましく、ジメチルスルホキシドを20体積%以上70体積%以下の範囲内、γ−ブチロラクトンを20体積%以上80体積%以下の範囲内、プロピレンカーボネートを50体積%以下の範囲内でそれぞれ含んでいればより好ましい。
【0029】
また、ジメチルスルホキシドとγ−ブチロラクトンとプロピレンカーボネートとの体積比による割合は、図3に示したように、それらを頂点とした三角図100において、ジメチルスルホキシドをx、γ−ブチロラクトンをy、プロピレンカーボネートをzとすると、数3に示したA,B,C,DおよびEの各点を結んだz=0を除く範囲内の値であることが好ましい。但し、x+y+z=1であり、A,B,C,DおよびEの各点を結んだ線上はz=0を除く範囲内に含まれる。図3では、A,B,C,DおよびEの各点を結んだ範囲内を右上斜線で示してあり、範囲内に含まれないz=0の部分は破線で示してある。
【0030】
【数3】
A(x,y,z)=(0.1,0.3,0.6)
B(x,y,z)=(0.3,0.1,0.6)
C(x,y,z)=(0.8,0.1,0.1)
D(x,y,z)=(0.8,0.2,0)
E(x,y,z)=(0.1,0.9,0)
【0031】
また、ジメチルスルホキシドとγ−ブチロラクトンとプロピレンカーボネートとの体積比による割合は、図4に示したように、数4に示したF,G,H,IおよびJの各点を結んだz=0を除く範囲内の値であることが好ましい。但し、x+y+z=1であり、F,G,H,IおよびJの各点を結んだ線上はz=0を除く範囲内に含まれる。図4では、F,G,H,IおよびJの各点を結んだ範囲内を左上斜線で示してあり、範囲内に含まれないz=0の部分は破線で示してある。
【0032】
【数4】
F(x,y,z)=(0.2,0.3,0.5)
G(x,y,z)=(0.3,0.2,0.5)
H(x,y,z)=(0.7,0.2,0.1)
I(x,y,z)=(0.7,0.3,0)
J(x,y,z)=(0.2,0.8,0)
【0033】
なお、溶媒は、これらスルホキシド,環状カルボン酸エステルおよびプロピレンカーボネートに加えて、目的に応じた特性を得るために、他の溶媒を含んでいてもよい。
【0034】
他の溶媒としては、例えば、ジメチルカーボネート、エチレンカーボネート、アセトニトリル、スルホラン、ジメトキシエタン、エチルアルコール、イソプロピルアルコール、ジメチルホルムアミド、ジメチルアセトアミドあるいはN−メチルピロリドンが挙げられ、これらのいずれか1種または2種以上を混合して用いてもよい。
【0035】
析出溶解材料は、析出した状態と溶解した状態とで色が変化することを利用して画素の表示を可能にするためのものである。析出溶解材料としては、還元により金属として析出する金属イオンが挙げられる。金属イオンとしては、特に限定されるものではないが、例えば、ビスマスイオン,銅イオン,銀イオン,ナトリウムイオン,リチウムイオン,鉄イオン,クロムイオン,ニッケルイオンあるいはカドミウムイオンが挙げられる。その中でも特に好ましい金属イオンはビスマスイオンあるいは銀イオンであり、更に好ましいのは銀イオンである。ビスマスイオンおよび銀イオンは、可逆的な反応を容易に進めることができると共に、析出時の変色度が高く、特に、銀イオンはイオン価数が通常1であるので、イオン価数が通常3であるビスマスイオンに比べて、1原子を還元させて金属にするのに必要な電荷量が3分の1となるからである。金属イオンは、例えば、金属塩として溶媒に添加されている。金属塩としては、銀塩であれば、例えば、硝酸銀、ホウフッ化銀、ハロゲン化銀、過塩素酸銀、シアン化銀あるいはチオシアン化銀が挙げられる。金属塩には、いずれか1種を用いてもよく、2種以上を混合して用いてもよい。
【0036】
この電解質13は、また、必要に応じて支持電解質塩と着色剤と各種添加剤とを含んでいてもよい。
【0037】
支持電解質塩は、電解質のイオン伝導性を高めることにより、析出溶解材料の析出溶解反応がより効果的に、かつ安定して行われるようにするためのものである。支持電解質塩としては、例えば、LiCl,LiBr,LiI,LiBF4 ,LiClO4 ,LiPF6 あるいはLiCF3 SO3 などのリチウム塩、または、KCl,KIあるいはKBrなどのカリウム塩、または、NaCl,NaIあるいはNaBrなどのナトリウム塩、または、ホウフッ化テトラエチルアンモニウム塩,過塩素酸テトラエチルアンモニウム塩,ホウフッ化テトラブチルアンモニウム塩,過塩素酸テトラブチルアンモニウム塩あるいはテトラブチルアンモニウムハライド塩などのテトラアルキル四級アンモニウム塩が挙げられる。支持電解質塩にはいずれか1種を用いてもよく、2種以上を混合して用いてもよい。
【0038】
着色剤は、コントラストを向上させるためのものである。着色剤としては、例えば、無機顔料あるいは有機顔料が挙げられ、これらを単独で用いてもよく、混合して用いてもよい。例えば、銀のように金属の発色が黒色の場合には、白色の隠蔽性の高い材料が好ましい。このような材料として、例えば、二酸化チタン、炭酸カルシウム、酸化ケイ素、酸化マグネシウムあるいは酸化アルミニウムなどの無機粒子を使用することができる。また、色素を用いることもできる。色素としては、油溶性染料を用いることが好ましい。
【0039】
着色剤の含有量は、無機粒子の場合、電解質13に対して、10質量%〜70質量%であることが好ましく、15質量%〜60質量%であればより好ましく、20質量%〜60質量%であれば更に好ましい。着色剤が少ないと所望の着色が得られず、逆に多いと、イオン量の低下、さらには電解質13の導電性の低下を来すからである。すなわち、この範囲内で着色剤を含有させることにより、これらの不具合を発生することなく、良好な着色状態を実現することが可能となる。
【0040】
一方、色素の場合には、電解質13に対して、50質量%程度でもよい。色素の発色効率は無機粒子に比べてはるかに高いためである。従って、電気化学的に安定した色素であれば、少ない量でもコントラストを向上させることが可能となる。
【0041】
添加剤としては、電気化学的な反応、特に金属の析出溶解反応を可逆的、かつ効率的に行うために、成長阻害剤、応力抑制剤、光沢剤、錯化剤あるいは還元剤のいずれか1種または2種以上を混合して含んでいることが好ましい。このような添加剤としては、酸素原子(O)または硫黄原子(S)を有する基を備えた有機化合物が好ましく、例えば、チオ尿素、1−アリル−2−チオ尿素、化4に示したメルカプトアルキルイミダゾール類、化5に示したクマリン、フタル酸、コハク酸、サリチル酸、グリコール酸、ジメチルアミンボラン、トリメチルアミンボラン、酒石酸、シュウ酸あるいはD−グルコノ−1,5−ラクトンが挙げられる。その中でも、化5に示したクマリン、メルカプトアルキルイミダゾールに準ずる化6に示した2−メルカプトベンゾイミダゾールは、金属の析出溶解反応の可逆性を向上させることができると共に、長期保存性および高温保存性においても優れた効果を得ることができるので好ましく、両者を同時に用いることで、より効果が増大するので好ましい。
【0042】
【化4】
式中、R1,R2およびR3は、水素原子またはCn H2n+1(nは1以上の整数である。)で表されるアルキル基をそれぞれ表す。
【0043】
【化5】
【0044】
【化6】
【0045】
また、アニオン種に起因した副反応に伴い、所望の発色以外の発色が生じる虞があるので、添加剤としては、アニオン種に起因した副反応を抑制するための還元剤または酸化剤のいずれか1種または2種以上を混合して含んでいることが好ましい。例えば、電解質13がハロゲン化物を含有している場合、ハロゲン化物は電位によっては化7、化8あるいは化9に示したような反応によりイオン状態から酸化される場合がある。
【0046】
【化7】
括弧内の数値は水溶液における標準水素電極(NHE)を基準電極とした標準電極電位である。
【0047】
【化8】
括弧内の数値は水溶液における標準水素電極(NHE)を基準電極とした標準電極電位である。
【0048】
【化9】
括弧内の数値は水溶液における標準水素電極(NHE)を基準電極とした標準電極電位である。
【0049】
このような還元剤としては、例えば、アスコルビン酸化合物あるいは化10に示したトリアルキルアルコールアミンなどが好ましい。中でも、トリアルキルアルコールアミン種であり、化11に示したトリエタノールアミンは、長期保存性および高温保存性においても優れた効果を得ることができるので好ましい。
【0050】
【化10】
式中、nは1以上の整数を表す。
【0051】
【化11】
【0052】
なお、この電解質13は、これら液状の溶媒,析出溶解材料および添加剤などからなる液状のいわゆる電解液とされていてもよいが、更に、これらを保持する高分子化合物を含み、ゲル状とされていてもよい。ゲル状とする場合、単層により構成してもよいが、複数層により構成してもよい。複数層にする場合、着色剤は複数層に含有させる必要はなく、少なくとも1層に含有させるようにすればよい。
【0053】
高分子化合物としては、例えば、主骨格単位、もしくは側鎖単位、もしくはその両方に、アルキレンオキサイド、アルキレンイミン、アルキレンスルフィドの繰り返し単位を有するもの、または、これらの異なる単位を複数含む共重合物、または、ポリメチルメタクリレート誘導体、ポリフッ化ビニリデン、ポリ塩化ビニリデン、ポリアクリロニトリルあるいはポリカーボネート誘導体が好ましい。高分子化合物には、いずれか1種を用いてもよいが、2種以上を混合して用いてもよい。
【0054】
電解質13の厚みは、無機粒子を着色剤として含む場合、20μm〜200μmであることが好ましく、30μm〜120μmであればより好ましく、30μm〜50μmであれば更に好ましい。薄い方が電極間の抵抗が小さくなり、発色・消色時間の低減や消費電力の低下を図ることができる一方、薄すぎると着色剤の含有量が少なくなるため、白色性(光学濃度)が十分でなく、特に、20μm以下であると、機械的強度が低下してピンホールや亀裂も生じるからである。
【0055】
なお、電解質13は、例えば、スルホキシドと環状カルボン酸エステルとを混合した溶媒に析出溶解材料を溶解させたのち、これに必要に応じて、支持電解質塩,着色剤および各種添加剤を添加することにより製造することができる。また、ゲル状とする場合には、この電解液と高分子化合物とを混合して乾燥させることにより製造することができる。また、この電解液を高分子化合物の出発原料であるモノマーあるいはオリゴマーと混合し、加熱法あるいはUV照射法により、重合あるいは架橋させることにより製造することもできる。なお、この場合、効率的にゲル化を促進させるために、架橋助剤や光増感剤などを併用してもよい。
【0056】
真絲球14は、例えば、絶縁性のプラスチックにより構成されている。なお、この真絲球14は設けなくてもよい。
【0057】
第1電極15は、画素として表示する金属を析出させるものであり、例えば、透明導電性膜により構成されている。具体的には、酸化インジウム(In2 O3 )、酸化スズ(SnO2 )、あるいはスズ(Sn)とインジウム(In)との酸化物であるITO(Indium Tin oxide)、または、これらにスズあるいはアンチモン(Sb)などをドーピングしたものにより構成されることが好ましい。また、酸化マグネシウム(MgO)あるいは酸化亜鉛(ZnO)などにより構成してもよい。
【0058】
第2電極16は、電気化学的に安定な金属により構成されていることが好ましく、中でも、金(Au),白金(Pt),クロム(Cr),アルミニウム(Al),コバルト(Co),パラジウム(Pd),ビスマス(Bi)および銀(Ag)からなる群のうちの少なくとも1種により構成されることが好ましい。また、析出させる金属と同じ金属により構成するようにすれば、電気化学的により安定な電極反応を実現できるのでより好ましい。この他にも、主反応に用いる金属を予めあるいは随時十分に補うことができれば、カーボンにより構成するようにしてもよい。カーボンを使用することで、第2電極16の低価格化を図ることができるからである。また、第1電極15と同じ透明導電性膜により構成するようにしてもよい。
【0059】
封止部材18は、例えば、変性ポリオレフィン,アクリル樹脂あるいはアイオノマにより構成されている。
【0060】
周辺回路部20は、図1に示したように、信号制御部21と、データ線駆動回路22A,22Bと、ゲート線駆動回路23とを有している。信号制御部21は、信号線24,25,26を介して、データ線駆動回路22A,22Bおよびゲート線駆動回路23とそれぞれ接続されている。データ線駆動回路22A,22Bおよびゲート線駆動回路23は、信号制御部21からの信号により、電気化学表示素子10の各画素を選択的に表示させるようになっている。
【0061】
このような構成を有する電気化学表示装置は例えば次のようにして製造することができる。
【0062】
図5は、本実施の形態に係る電気化学表示装置の製造方法を工程順に表すものである。まず、図5(A)に示したように、例えば、ガラスなどよりなる第1基板11上に、公知の半導体製造技術によりTFT17を形成したのち、蒸着あるいはスパッタリングによりITOなどよりなる第1電極15を形成する。このとき、第1電極15を形成するに先立って、第1基板11と第1電極15との結着性を向上させる処理を第1基板11に施してもよい。次いで、図5(B)に示したように、例えば、第1基板11にUVオゾン処理を施して第1基板11の洗浄および表面改質を行う。
【0063】
また、図5(C)に示したように、例えば、ガラスなどによりなる第2基板12上に、例えば、蒸着、スパッタリング、あるいはメッキにより銀よりなる第2電極16を形成する。このとき、第2電極16を形成するに先立って、予め第2基板12に第2電極16とは異なる金属薄膜を形成したのち第2電極16を形成するような、第2基板12と第2電極16との結着性を向上させるための処理を施してもよい。また、カーボンを例えば樹脂を用いてインク化し、第2基板12に印刷するか、もしくは、その他ドライプロセスによる成膜により、第2基板12上にカーボンよりなる第2電極16を形成するようにしてもよい。
【0064】
次いで、電解質13をゲル状とする場合には、図5(D)に示したように、例えば、第1基板11上に電解質13を形成する。そののち、図5(E)に示したように、例えば、第1基板11に電解質13を介して第2基板12を貼り合わせる。その際、第1電極15と第2電極16とを対向配置させる。続いて、図5(F)に示したように、例えば、第1基板11,第2基板12および電解質13などの側面を封止部材18により封止し、必要に応じて、電解質13を熱または紫外線などにより架橋させる。最後に、電気化学表示素子10の周辺に周辺回路部20を設ける。以上により、図1に示した電気化学表示装置が完成する。
【0065】
また、この電気化学表示装置は、次のようにして製造することもできる。
【0066】
図6は、本実施の形態に係る電気化学表示装置の他の製造方法を工程順に表すものである。まず、先の製造方法と同様に、第1基板11上にTFT17および第1電極15を順次形成したのち、第1基板11にUVオゾン処理を施す。また、第2基板12上に第2電極16を形成する。そののち、図6(A)に示したように、例えば、第1基板11上に真絲球14を散布したのち、第1基板11と第2基板12とを封止部材18を用いて所定の間隔で対向配置させる。続いて、図6(B)に示したように、例えば、図示しない注入口から、例えば、毛細管現象を利用した注入法により流動性のある電解質13を注入し、その後、図6(C)に示したように、例えば、注入口を接着剤31などにより封止し、必要に応じて、電解質13を熱または紫外線などにより架橋させる。最後に、電気化学表示素子10の周辺に周辺回路部20を設ける。以上により、図1に示した電気化学表示装置が完成する。
【0067】
この電気化学表示装置では、第1電極15と第2電極16との間に所定の電圧が印加されると、これら第1電極15と第2電極16との間に存在する電解質13中の金属イオンが第1電極15に移動し、第1電極15において金属イオンが還元されて第1電極15に金属が析出し、書き込みが行われる。析出した金属は第1基板11を通して画像として認識される。一方、第1電極15と第2電極16との間に所定の逆電圧が印加されると、第1電極15に析出した金属が酸化されて電解質13に金属イオンとなって溶解し、消去が行われる。その際、溶媒がスルホキシドと環状カルボン酸エステルとを含んでいるので、高速応答性が得られ、かつ、応答速度の温度依存性が小さくなる。
【0068】
このように本実施の形態では、スルホキシドと、環状カルボン酸エステルとを含有する溶媒を含むようにしたので、高速応答性を得ることができると共に、応答速度の温度依存性を小さくすることができる。よって、低温においても高速応答性を得ることができる。その結果、使用温度が変わっても、画素の色(着色濃度)を一定に保つことができ、優れた表示品位を得ることができる。
【0069】
特に、ジメチルスルホキシドとγ−ブチロラクトンとを、ジメチルスルホキシド:γ−ブチロラクトン=7:3〜3:7の体積比で含むようにすれば、最も多く使用される環境である10℃〜30℃の温度領域において応答速度を速くし、かつ低温において急速な応答速度の低下を防止することができる。
【0070】
更に、スルホキシドと環状カルボン酸エステルとに加えて、プロピレンカーボネートを含むようにすれば、特に常温において応答速度を速くすることができる。
【0071】
なお、本実施の形態に係る電気化学表示装置では、電気化学表示素子10を図2に示した以外の構成としてもよい。例えば、図7に示したように、第1電極15を第1基板11の全面に形成し、第2電極16をマトリクス状に複数形成すると共に、TFTを第2基板12上に画素に対応して形成し、第2電極16への通電を制御するようにしてもよい。この場合、第2電極16はTFT全体を覆うように形成することが好ましい。また、第1基板11の第2電極16と対向する部分を除いた領域に図示しない絶縁層を形成するようにしてもよい。なお、図7においては、電解質,TFTを省略して表している。
【0072】
また、図8に示したように、第1電極15を第1基板11にストライプ状に形成し、第2電極16を第2基板12にストライプ状に形成し、第1電極15と第2電極16とが互いに直交するように対向配置させるようにしてもよい。なお、図8では、電解質および封止部材を省略して表している。
【0073】
更に、図9に一例を示したように、金属の析出溶解反応の進み具合を第1電極15および第2電極16の影響を受けることなく正確に検知するための銀などよりなる第3電極19を設けるようにしてもよい。この場合、電気化学表示素子10の駆動を的確に制御し、信頼性を向上させることができるので好ましい。なお、第3電極19は、電気化学表示素子10の構造に応じて適宜の場所に形成するようにする。第3電極19は、例えば、蒸着,スパッタリングあるいはメッキにより形成することができる。
【0074】
なお、このように電気化学表示素子10を図2に示した以外の構成とした場合、周辺回路部20等の構成は電気化学表示素子10の構成に応じて適宜変更する。
【0075】
【実施例】
更に、本発明の具体的な実施例について詳細に説明する。
【0076】
(実施例1−1)
図8に示した電気化学表示素子10を備えた電気化学表示装置を作製した。まず、10cm×10cmの厚み1.5mmのガラスよりなる第1基板11上に、ITOよりなる第1電極15を形成した。その際、第1電極15のピッチは150μmとした。
【0077】
また、8cm×12cmの厚み1.5mmのガラスよりなる第2基板12上に、蒸着によりクロムよりなる層を成膜したのち、その層の上に、厚み1000nmの銀合金よりなる層を成膜し、第2電極16とした。
【0078】
更に、ジメチルスルホキシド(DMSO)とγ−ブチロラクトン(γBL)とを、ジメチルスルホキシド:γ−ブチロラクトン=6:4の体積比で混合した溶媒に、LiIおよびAgIをそれぞれ0.75mol/dm3 および0.50mol/dm3 となるように溶解させると共に、化5に示したクマリンと、化6に示した2−メルカプトベンゾイミダゾールと、化11に示したトリエタノールアミンとを5g/dm3 、5g/dm3 、10g/dm3 となるように添加し、電解液を作製した。次いで、この電解液5質量部と重量平均分子量約35万のポリエーテル1質量部とを混合し、80℃〜120℃に加熱したのち、更に、これに平均粒径0.5μmの二酸化チタン0.2質量部を添加し、ホモジナイザーで均一に分散させることにより前駆体溶液を作製した。
【0079】
続いて、第1基板11の第1電極15が形成された表面に、UVオゾン処理を施したのち、前駆体溶液をドクターブレードにより厚み100μmで塗布し、第2電極16が形成された第2基板12を直ちに貼り合わせた。そののち、前駆体溶液をゲル化させることにより電解質とした。次いで、貼り合わせの端面を接着剤よりなる封止部材18によって封止し、図8に示した電気化学表示素10を作製した。最後に、電気化学表示素子10の周辺に周辺回路部20を設けた。
【0080】
また、実施例1−1に対する比較例1−1,1−2として、ジメチルスルホキシドのみよりなる溶媒またはγ−ブチロラクトンのみよりなる溶媒を用いたことを除き、他は実施例1−1と同様にして電気化学表示装置を作製した。更に、実施例1−1に対する比較例1−3〜1−5として、γ−ブチロラクトンに代えてジメチルホルムアミド(DMF)、プロピレンカーボネート(PC)またはジエチルアセトアミド(DEA)をそれぞれ用いたことを除き、他は実施例1−1と同様にして電気化学表示装置を作製した。
【0081】
作製した実施例1−1および比較例1−1〜1−5の電気化学表示装置について、−20℃〜40℃の温度領域において、10℃おきに書き込みおよび消去を行い、駆動特性および表示特性を評価した。書き込みは、−2Vの電圧を必要濃度(絶対反射率10%、光学濃度(オプティカルデンシティ;OD)1.0)に達するまでの時間印加することにより行い、一方、消去は、+2Vの電圧を書込みに要した時間と同じ時間もしくは書き込みに要した電圧の時間に対する時間積分強度以上印加することにより行った。駆動特性としては、電圧印加後、必要濃度に達するまでの時間(応答時間)を調べた。また、表示特性としては、光学濃度が1.0となるのに要した電荷量を調べた。図10に駆動特性を示し、図11に表示特性を示す。
【0082】
図10および図11から分かるように、ジメチルスルホキシドのみよりなる溶媒を用いた比較例1−1およびジメチルスルホキシドとγ−ブチロラクトン以外の溶媒とを含む溶媒を用いた比較例1−3〜1−5では、10℃以上であれば、比較的良好な応答時間を示し、また、さほど温度変化が少ないものの、10℃以下では急激に応答時間が長くなり、特に比較例1−1では、その度合いが大きかった。また、γ−ブチロラクトンのみよりなる溶媒を用いた比較例1−2では、低温になるに従って、応答時間が長くなる他、光学濃度が1.0に達するのに要する電荷量も大きく、デバイスの低消費電力化という点からも極めて劣っていた。
【0083】
これに対して、ジメチルスルホキシドとγ−ブチロラクトンとを含む溶媒を用いた実施例1−1では、−15℃〜40℃の温度領域において、応答時間の変化が少なく、かつ0.1秒以下の応答時間を保持できた。
【0084】
すなわち、溶媒にジメチルスルホキシドとγ−ブチロラクトンとを含むようにすれば、高速応答性を得ることができると共に、応答速度の温度依存性を小さくし、低温においても高速応答性を得ることができることが分かった。
【0085】
(実施例1−2〜1−9)
ジメチルスルホキシドとγ−ブチロラクトンとの割合を表1に示したように変化させたことを除き、他は実施例1−1と同様にして電気化学表示装置を作製した。実施例1−2〜1−9の電気化学表示装置についても実施例1−1と同様にして、駆動特性および表示特性を調べた。図12に実施例1−2〜1−4の駆動特性を実施例1−1の結果と共に示し、図13に実施例1−5〜1−9の駆動特性を実施例1−1の結果と共に示す。また、図14に実施例1−2〜1−4の表示特性を実施例1−1の結果と共に示し、図15に実施例1−5〜1−9の表示特性を実施例1−1の結果と共に示す。
【0086】
【表1】
【0087】
図12〜図15から分かるように、ジメチルスルホキシドとγ−ブチロラクトンとを、ジメチルスルホキシド:γ−ブチロラクトン=8:2〜9:1または1:9〜2:8の体積比で含有する溶媒を用いた実施例1−2,1−3,1−8,1−9では、10℃〜40℃においては、極めて応答時間が短く、光学濃度が1.0に達するのに要する電荷量も小さく、デバイスの低消費電力を図ることができるので非常に好ましいものであった。但し、10℃未満では図10に示した比較例1−1ほどではないが、応答時間が急激に長くなってしまうという問題が見られた。10℃未満の低温環境での使用が見込まれないデバイスでは非常に優れているが、冬季に屋外等で使用するようなことが見込まれるモバイル系のデバイスには適しているとは言えない。
【0088】
一方、図12および図13から分かるように、ジメチルスルホキシドとγ−ブチロラクトンとを、ジメチルスルホキシド:γ−ブチロラクトン=7:3〜3:7の体積比で含有する溶媒を用いた実施例1−1,1−4〜1−7では、10℃〜40℃の温度領域においては実施例1−2,1−3ほど高速応答性を示さないものの、−15℃〜40℃の温度領域において、応答時間の変化が少なく、かつ0.1秒以下の応答時間を保持できた。
【0089】
すなわち、ジメチルスルホキシドとγ−ブチロラクトンとの割合を、体積比でジメチルスルホキシド:γ−ブチロラクトン=7:3〜3:7、更には、ジメチルスルホキシド:γ−ブチロラクトン=6:4〜3:7とすれば、最も多く使用される環境である10℃〜30℃の温度領域において応答速度を速くし、かつ低温において急速な応答速度の低下を防止することができることが分かった。
【0090】
(実施例2−1〜2−4)
γ−ブチロラクトンに代えてγ−バレロラクトン(γVL)を用いると共に、ジメチルスルホキシドとγ−バレロラクトンとの割合を表2に示したように変化させたことを除き、他は実施例1−1と同様にして電気化学表示装置を作製した。実施例2−1〜2−4の電気化学表示装置についても、実施例1−1と同様にして駆動特性を調べた。図16にその結果を実施例1−2,1−4,1−5,1−7および比較例1−1の結果と共に示す。
【0091】
【表2】
【0092】
図16から、ジメチルスルホキシドとγ−バレロラクトンとを含む溶媒を用いるようにすれば、ジメチルスルホキシドとγ−ブチロラクトンとを含む溶媒を用いたものと同様に、ジメチルスルホキシドのみよりなる溶媒を用いたものに比べて低温においての応答時間を短縮することができることが分かった。但し、γ−バレロラクトンの割合が70%以上になると電解液が淡黄色に変色し、更にその比率が増大するにつれて、変色も増大し、γ−バレロラクトンのみよりなる溶媒を用いたものでは電解液が赤色に変色した。表示装置としてはこのような着色は好ましくないので、γ−バレロラクトンの割合は70%未満とすることが好ましく、50%未満とすればより好ましいことが分かった。なお、この変色は、析出材料としてハロゲン化物を用いたことに起因すると考えられる。また、−20℃までの応答時間を1秒以内を必要とする場合にはγ−バレロラクトンの割合は10%よりも多く70%未満とすることが好ましいことが分かった。すなわち、ジメチルスルホキシドとγ−バレロラクトンとの割合は、体積比で、ジメチルスルホキシド:γ−バレロラクトン=8:2〜3:7であることが好ましいことが分かった。
【0093】
また、実施例2−1〜2−4と実施例1−2,1−4,1−5,1−7との比較から、10℃以上では、γ−バレロラクトンを用いたもの方が、γ−ブチロラクトンを用いたものに比べて応答時間を短くすることができ、0℃以下ではγ−ブチロラクトンを用いたものの方が、γ−バレロラクトンを用いたものに比べて、応答時間を短くすることができることが分かった。
【0094】
(実施例3−1〜3−18)
ジメチルスルホキシドとγ−ブチロラクトンとに加えて、プロピレンカーボネートを混合した溶媒を用いると共に、それらの割合を表3に示したように変化させたことを除き、他は実施例1−1と同様にして電気化学表示装置を作製した。また、実施例3−1〜3−18に対する比較例3−1〜3−6として、プロピレンカーボネートよりなる溶媒、または、γ−ブチロラクトンおよびプロピレンカーボネートよりなる溶媒、または、ジメチルスルホキシドおよびプロピレンカーボネートよりなる溶媒を用いると共に、それらの割合を表3に示したように変えたことを除き、他は実施例1−1と同様にして電気化学表示装置を作製した。
【0095】
【表3】
【0096】
実施例3−1〜3−18および比較例3−1〜3−6の電気化学表示装置について、−20℃〜30℃の温度領域において、実施例1−1と同様にして、10℃おきに書き込みおよび消去を行い、駆動特性を評価した。図17〜図22に、その結果を、実施例1−1〜1−9および比較例1−1,1−2の結果と共に示す。なお、図17は−20℃における駆動特性、図18は−10℃における駆動特性、図19は0℃における駆動特性、図20は10℃における駆動特性、図21は20℃における駆動特性、図22は30℃における駆動特性をそれぞれ示している。また、図17〜21の○は実施例、□は比較例をそれぞれ表し、その中の上段が実施例の番号、下段の数字が応答時間(sec)を表している。
【0097】
図17〜22から分かるように、ジメチルスルホキシドとγ−ブチロラクトンとプロピレンカーボネートとを含む溶媒を用いた実施例3−1〜3−18によれば、常温下では応答時間を極めて短くすることができ、更に−10℃の低温においても極度に応答時間が長くなることを抑制することができることが分かった。
【0098】
すなわち、溶媒がジメチルスルホキシドとγ−ブチロラクトンとプロピレンカーボネートとを含むようにすれば、高速応答性を得ることができると共に、応答速度の温度依存性を小さくすることができ、特に、常温において優れた高速応答性を得ることができることが分かった。
【0099】
また、溶媒が、ジメチルスルホキシドを10体積%以上80体積%以下の範囲内、γ−ブチロラクトンを10体積%以上90体積%以下の範囲内、プロピレンカーボネートを60体積%以下の範囲内でそれぞれ含むようにすれば、更には、ジメチルスルホキシドを20体積%以上70体積%以下の範囲内、γ−ブチロラクトンを20体積%以上80体積%以下の範囲内、プロピレンカーボネートを50体積%以下の範囲内でそれぞれ含むようにすれば、高速応答性を得ることができると共に、低温での応答速度の低下が少ないことが分かった。
【0100】
なお、上記実施例では、スルホキシドおよび環状カルボン酸エステルについて具体的に例を挙げて説明したが、上述した効果はその構造に起因するものと考えられる。よって、他のスルホキシドおよび他の環状カルボン酸エステルを用いても同様の結果を得ることができる。また、上記実施例では、ゲル状の電解質を用いる場合について説明したが、電解液を用いても同様の結果を得ることができる。
【0101】
以上、実施の形態および実施例を挙げて本発明を説明したが、本発明は上記実施の形態および実施例に限定されるものではなく、種々変形可能である。例えば、上記実施の形態および実施例では、電気化学表示素子の構造について具体的に例を挙げて説明したが、他の構造としてもよい。例えば、図示しないが、電解質を不織布や多孔質性のフィルムに含浸するようにしてもよい。
【0102】
また、本発明の電解質は、コンデンサ,キャパシタあるいは電池などの他の電気デバイスに用いることもできる。
【0103】
【発明の効果】
以上説明したように本発明による電解質および電気化学表示装置によれば、スルホキシドと、環状カルボン酸エステルとを含有する溶媒を含むようにしたので、高速応答性を得ることができると共に、応答速度の温度依存性を小さくすることができる。よって、低温においても高速応答性を得ることができる。その結果、使用温度が変わっても、画素の色(着色濃度)を一定に保つことができ、優れた表示品位を得ることができる。
【0104】
特に、ジメチルスルホキシドとγ−ブチロラクトンとを、ジメチルスルホキシド:γ−ブチロラクトン=7:3〜3:7の体積比で含むようにすれば、最も多く使用される環境である10℃〜30℃の温度領域において応答速度を速くし、かつ低温において急速な応答速度の低下を防止することができる。
【0105】
また、スルホキシドと環状カルボン酸エステルとに加えて、プロピレンカーボネートを含むようにすれば、特に常温において応答速度を速くすることができる。
【図面の簡単な説明】
【図1】本発明の一実施の形態に係る電気化学表示装置の構成を表すブロック図である。
【図2】図1に示した電気化学表示素子の構成を表す斜視図である。
【図3】図1に示した電解質の好ましい組成を表す三角図である。
【図4】図1に示した電解質の好ましい組成を表す他の三角図である。
【図5】図1に示した電気化学表示装置の製造工程を表す断面図である。
【図6】図1に示した電気化学表示装置の他の製造工程を表す断面図である。
【図7】図1に示した他の電気化学表示素子の構成を表す斜視図である。
【図8】図1に示した他の電気化学表示素子の構成を表す斜視図である。
【図9】図1に示した他の電気化学表示素子の構成を表す斜視図である。
【図10】本発明の実施例1−1に係る駆動特性を表す特性図である。
【図11】本発明の実施例1−1に係る表示特性を表す特性図である。
【図12】本発明の実施例1−2〜1−4に係る駆動特性を表す特性図である。
【図13】本発明の実施例1−5〜1−9に係る駆動特性を表す特性図である。
【図14】本発明の実施例1−2〜1−4に係る表示特性を表す特性図である。
【図15】本発明の実施例1−5〜1−9に係る表示特性を表す特性図である。
【図16】本発明の実施例2−1〜2−4に係る駆動特性を表す特性図である。
【図17】本発明の実施例3−1〜3−18に係る−20℃における駆動特性を表す特性図である。
【図18】本発明の実施例3−1〜3−18に係る−10℃における駆動特性を表す特性図である。
【図19】本発明の実施例3−1〜3−18に係る0℃における駆動特性を表す特性図である。
【図20】本発明の実施例3−1〜3−18に係る10℃における駆動特性を表す特性図である。
【図21】本発明の実施例3−1〜3−18に係る20℃における駆動特性を表す特性図である。
【図22】本発明の実施例3−1〜3−18に係る30℃における駆動特性を表す特性図である。
【符号の説明】
10…電気化学表示素子、11…第1基板、12…第2基板、13…電解質、14…真絲球、15…第1電極、16…第2電極、17…TFT、18…封止部材、19…第3電極、20…周辺回路部、21…信号制御部、22A,22B…データ線駆動回路、23…ゲート線駆動回路、24,25,26…信号線、31…接着剤。[0001]
TECHNICAL FIELD OF THE INVENTION
The present invention relates to an electrolyte containing a solvent and an electrochemical display using the same.
[0002]
[Prior art]
In recent years, as networks have become widespread, documents that have been conventionally distributed as printed matter have been distributed as so-called electronic documents. Further, books and magazines are often provided in a so-called electronic publishing form. Conventionally, a computer CRT (Cathode-Ray Tube; cathode ray tube) or a liquid crystal display has been used to browse such information.
[0003]
However, it has been pointed out that these light-emitting displays are extremely fatigued for ergonomic reasons and cannot withstand long-time reading. Another drawback is that the place to read is limited to the location of the computer.
[0004]
Recently, due to the spread of notebook computers, some of them can be used as portable displays, but they are mainly light-emitting by backlight and also because of power consumption, this also requires more than several hours of reading. Difficult to use. A reflective liquid crystal display has also been developed, which can be driven with low power consumption. However, the reflectivity of the liquid crystal in non-display (white display) is 30%, which is remarkably visible compared to printed matter on paper. It is poor in quality and prone to fatigue, which is not endurable for prolonged reading.
[0005]
In order to solve these problems, recently, a display in which colored particles are moved between electrodes mainly by an electrophoresis method or colored by rotating dichroic particles in an electric field is being developed. is there. However, in this display, gaps between particles absorb light, resulting in poor contrast, and a practical writing speed (within 1 second) cannot be obtained unless the driving voltage is set to 100 V or more. There is.
[0006]
On the other hand, an electrochromic display (ECD) utilizing the change of color by application of a voltage has also been developed. As such an electrochromic display device, for example, H + Tungsten oxide (WO) that changes from transparent to blue when ions such as 3 ) Or using an organic material that develops color by oxidation or reduction. These are superior in terms of high contrast to those of the electrophoresis method, etc., but have poor black quality and are developed for use as dimming glass or watch displays that do not require matrix driving. At present, it is difficult to use it for a matrix-driven display device such as a paper-like display or electronic paper. Note that a matrix drive (see Patent Document 1) is also known, but the drive element only constitutes a part thereof in combination with a liquid crystal display device.
[0007]
Furthermore, since organic materials generally have poor light resistance, when used in electronic paper that is to be continuously exposed to light such as sunlight or indoor light for use, when used for a long time, the color fades and the black density becomes low. The problem of lowering occurs.
[0008]
Therefore, the electrodes are arranged to face each other via a white-colored electrolyte containing metal ions, an image is written by depositing a metal on the display-side electrode, and the deposited metal is dissolved in the electrolyte to form an image. Electrodeposition type display devices that perform erasure have been proposed (for example, see Patent Document 2). According to this, matrix driving is easy, and the contrast and the black density can be increased.
[0009]
[Patent Document 1]
Japanese Patent Publication No. 4-73764
[Patent Document 2]
JP-A-2002-258327
[0010]
[Problems to be solved by the invention]
However, even with this electro-deposition type display device, the characteristics, particularly the cycle characteristics, are still insufficient. In addition, the oxidation-reduction reaction cannot be adequately controlled, and there is a problem that the image disappears at the time of display switching, that is, an afterimage occurs, which leads to a decrease in image quality. In addition, there is a problem that the response speed is slow, which is often seen in a display device using an electrochemical reaction, or that the response speed is greatly dependent on temperature, and the response speed is reduced particularly at a low temperature.
[0011]
The present invention has been made in view of the above problems, and an object of the present invention is to provide an electrochemical display device capable of obtaining a high-speed response and reducing the temperature dependence of a response speed, and an electrolyte used therefor. Is to provide.
[0012]
[Means for Solving the Problems]
The electrolyte according to the present invention contains a solvent containing a sulfoxide and a cyclic carboxylic acid ester.
[0013]
The electrochemical display device according to the present invention includes an electrolyte between the first electrode and the second electrode, and the electrolyte includes a solvent containing a sulfoxide and a cyclic carboxylate.
[0014]
Since the electrolyte and the electrochemical display device according to the present invention contain the sulfoxide and the cyclic carboxylate, a high-speed response is obtained and the temperature dependence of the response speed is reduced.
[0015]
BEST MODE FOR CARRYING OUT THE INVENTION
Hereinafter, embodiments of the present invention will be described in detail with reference to the drawings.
[0016]
FIG. 1 shows a schematic configuration of an electrochemical display device according to one embodiment of the present invention. The electrochemical display device includes, for example, an
[0017]
FIG. 2 shows a schematic configuration of the
[0018]
The
[0019]
The
[0020]
The
[0021]
As the sulfoxide, dimethyl sulfoxide ((CH 3 ) 2 S = O) is preferable because it is liquid at normal temperature. As the cyclic carboxylic acid ester, for example, γ-butyrolactone shown in
[0022]
Embedded image
[0023]
Embedded image
[0024]
When dimethyl sulfoxide and γ-butyrolactone are contained, the ratio of dimethyl sulfoxide to γ-butyrolactone is preferably a volume ratio of dimethyl sulfoxide: γ-butyrolactone = 7: 3 to 3: 7, and dimethyl sulfoxide: More preferably, the volume ratio of γ-butyrolactone is from 6: 4 to 3: 7. Within this range, the response speed can be increased in a temperature range of 10 ° C. to 30 ° C., which is the most frequently used environment, and a rapid decrease in response speed at low temperatures can be prevented.
[0025]
When dimethyl sulfoxide and γ-valerolactone are contained, the ratio of dimethyl sulfoxide to γ-valerolactone is preferably a volume ratio of dimethyl sulfoxide: γ-valerolactone = 8: 2 to 3: 7, More preferably, the volume ratio of dimethyl sulfoxide: γ-valerolactone = 8: 2 to 5: 5. This is because the response speed can be further increased within this range.
[0026]
It is preferable that the solvent contains propylene carbonate shown in
[0027]
Embedded image
[0028]
In this case, in order to obtain a higher effect, the solvent is, in particular, dimethyl sulfoxide in the range of 10% by volume to 80% by volume, γ-butyrolactone in the range of 10% by volume to 90% by volume, and propylene carbonate. It is preferable to contain dimethyl sulfoxide in the range of 20% by volume or more and 70% by volume or less, γ-butyrolactone in the range of 20% by volume or more and 80% by volume or less, and propylene carbonate. It is more preferable to contain each within the range of 50% by volume or less.
[0029]
Also, as shown in FIG. 3, the ratio by volume ratio of dimethyl sulfoxide, γ-butyrolactone, and propylene carbonate is x in dimethyl sulfoxide, y in γ-butyrolactone, propylene carbonate If z is z, it is preferable that the value be in a range excluding z = 0 connecting points A, B, C, D and E shown in
[0030]
[Equation 3]
A (x, y, z) = (0.1, 0.3, 0.6)
B (x, y, z) = (0.3, 0.1, 0.6)
C (x, y, z) = (0.8, 0.1, 0.1)
D (x, y, z) = (0.8, 0.2, 0)
E (x, y, z) = (0.1, 0.9, 0)
[0031]
Further, as shown in FIG. 4, the ratio of dimethyl sulfoxide, γ-butyrolactone, and propylene carbonate by volume ratio was z = 0 connecting the points of F, G, H, I, and J shown in
[0032]
(Equation 4)
F (x, y, z) = (0.2, 0.3, 0.5)
G (x, y, z) = (0.3, 0.2, 0.5)
H (x, y, z) = (0.7, 0.2, 0.1)
I (x, y, z) = (0.7, 0.3, 0)
J (x, y, z) = (0.2, 0.8, 0)
[0033]
The solvent may contain, in addition to the sulfoxide, the cyclic carboxylate, and the propylene carbonate, another solvent in order to obtain characteristics according to the purpose.
[0034]
Other solvents include, for example, dimethyl carbonate, ethylene carbonate, acetonitrile, sulfolane, dimethoxyethane, ethyl alcohol, isopropyl alcohol, dimethylformamide, dimethylacetamide or N-methylpyrrolidone, and any one or two of these may be used. The above may be used in combination.
[0035]
The deposited dissolving material is for enabling display of pixels by utilizing the fact that the color changes between the deposited state and the dissolved state. Examples of the precipitation dissolving material include metal ions that precipitate as a metal by reduction. Examples of the metal ion include, but are not particularly limited to, bismuth ion, copper ion, silver ion, sodium ion, lithium ion, iron ion, chromium ion, nickel ion, and cadmium ion. Among them, particularly preferred metal ions are bismuth ions and silver ions, and more preferred are silver ions. Bismuth ions and silver ions can easily promote a reversible reaction and have a high degree of discoloration at the time of deposition. In particular, silver ions usually have an ionic valence of 1 and thus have an ionic valence of usually 3. This is because, compared to a certain bismuth ion, the amount of charge required to reduce one atom to a metal is reduced to one third. The metal ion is added to the solvent as a metal salt, for example. As the metal salt, for example, silver salts include silver nitrate, silver borofluoride, silver halide, silver perchlorate, silver cyanide and silver thiocyanate. As the metal salt, any one kind may be used, or two or more kinds may be used in combination.
[0036]
The
[0037]
The supporting electrolyte salt is for increasing the ionic conductivity of the electrolyte so that the precipitation-dissolution reaction of the deposition-dissolved material is performed more effectively and stably. As the supporting electrolyte salt, for example, LiCl, LiBr, LiI, LiBF 4 , LiClO 4 , LiPF 6 Or LiCF 3 SO 3 Or potassium salt such as KCl, KI or KBr, or sodium salt such as NaCl, NaI or NaBr, or tetraethylammonium borofluoride, tetraethylammonium perchlorate, tetrabutylammonium borofluoride And tetraalkylammonium salts such as tetrabutylammonium perchlorate and tetrabutylammonium halide. Any one of the supporting electrolyte salts may be used, or two or more may be used in combination.
[0038]
The coloring agent is for improving the contrast. Examples of the coloring agent include inorganic pigments and organic pigments, and these may be used alone or in combination. For example, when the color of the metal is black, such as silver, a white material with high concealing properties is preferable. As such a material, for example, inorganic particles such as titanium dioxide, calcium carbonate, silicon oxide, magnesium oxide, and aluminum oxide can be used. Further, a dye can also be used. It is preferable to use an oil-soluble dye as the pigment.
[0039]
In the case of inorganic particles, the content of the coloring agent is preferably from 10% by mass to 70% by mass, more preferably from 15% by mass to 60% by mass, and more preferably from 20% by mass to 60% by mass, based on the
[0040]
On the other hand, in the case of a dye, it may be about 50% by mass with respect to the
[0041]
As an additive, any one of a growth inhibitor, a stress inhibitor, a brightener, a complexing agent, or a reducing agent is used in order to reversibly and efficiently perform an electrochemical reaction, particularly, a precipitation and dissolution reaction of a metal. It is preferable to contain the species or a mixture of two or more species. As such an additive, an organic compound having a group having an oxygen atom (O) or a sulfur atom (S) is preferable. For example, thiourea, 1-allyl-2-thiourea, mercapto shown in
[0042]
Embedded image
Wherein R1, R2 and R3 are hydrogen or C n H 2n + 1 (N is an integer of 1 or more).
[0043]
Embedded image
[0044]
Embedded image
[0045]
Further, since a coloration other than the desired coloration may occur with the side reaction caused by the anionic species, as an additive, any one of a reducing agent or an oxidizing agent for suppressing a side reaction caused by the anionic species is used. It is preferable that one or two or more of them are mixed and contained. For example, when the
[0046]
Embedded image
The numerical values in parentheses are the standard electrode potentials using the standard hydrogen electrode (NHE) in the aqueous solution as the reference electrode.
[0047]
Embedded image
The numerical values in parentheses are the standard electrode potentials using the standard hydrogen electrode (NHE) in the aqueous solution as the reference electrode.
[0048]
Embedded image
The numerical values in parentheses are the standard electrode potentials using the standard hydrogen electrode (NHE) in the aqueous solution as the reference electrode.
[0049]
As such a reducing agent, for example, an ascorbic acid compound or a trialkyl alcohol amine shown in
[0050]
Embedded image
In the formula, n represents an integer of 1 or more.
[0051]
Embedded image
[0052]
The
[0053]
Examples of the high molecular compound include, for example, a main skeleton unit, or a side chain unit, or both, having a repeating unit of alkylene oxide, alkylene imine, or alkylene sulfide, or a copolymer containing a plurality of these different units, Alternatively, a polymethyl methacrylate derivative, polyvinylidene fluoride, polyvinylidene chloride, polyacrylonitrile, or a polycarbonate derivative is preferable. Any one of the polymer compounds may be used, or a mixture of two or more thereof may be used.
[0054]
When the inorganic particles are included as a colorant, the thickness of the
[0055]
For the
[0056]
The
[0057]
The
[0058]
The
[0059]
The sealing
[0060]
As shown in FIG. 1, the
[0061]
The electrochemical display device having such a configuration can be manufactured, for example, as follows.
[0062]
FIG. 5 shows a method of manufacturing the electrochemical display device according to the present embodiment in the order of steps. First, as shown in FIG. 5A, a
[0063]
In addition, as shown in FIG. 5C, a
[0064]
Next, when the
[0065]
Further, the electrochemical display device can be manufactured as follows.
[0066]
FIG. 6 illustrates another method of manufacturing the electrochemical display device according to the present embodiment in the order of steps. First, after the
[0067]
In this electrochemical display device, when a predetermined voltage is applied between the
[0068]
As described above, in the present embodiment, since the solvent containing the sulfoxide and the cyclic carboxylic acid ester is included, high-speed response can be obtained and the temperature dependence of the response speed can be reduced. . Therefore, high-speed response can be obtained even at a low temperature. As a result, even if the use temperature changes, the color (color density) of the pixel can be kept constant, and excellent display quality can be obtained.
[0069]
In particular, if dimethyl sulfoxide and γ-butyrolactone are contained in a volume ratio of dimethyl sulfoxide: γ-butyrolactone = 7: 3 to 3: 7, the temperature of 10 ° C. to 30 ° C., which is the most frequently used environment, is used. It is possible to increase the response speed in the region and prevent a rapid decrease in the response speed at a low temperature.
[0070]
Furthermore, if propylene carbonate is contained in addition to the sulfoxide and the cyclic carboxylic acid ester, the response speed can be particularly increased at room temperature.
[0071]
In the electrochemical display device according to the present embodiment, the
[0072]
Also, as shown in FIG. 8, the
[0073]
Further, as shown in FIG. 9, a
[0074]
When the
[0075]
【Example】
Further, specific examples of the present invention will be described in detail.
[0076]
(Example 1-1)
An electrochemical display device including the
[0077]
Further, a layer made of chromium is formed by vapor deposition on the
[0078]
Furthermore, LiI and AgI were each added to a solvent in which dimethyl sulfoxide (DMSO) and γ-butyrolactone (γBL) were mixed at a volume ratio of dimethyl sulfoxide: γ-butyrolactone = 6: 4, and LiI and AgI were each 0.75 mol / dm. 3 And 0.50 mol / dm 3 5 g /
[0079]
Subsequently, after applying UV ozone treatment to the surface of the
[0080]
In addition, as Comparative Examples 1-1 and 1-2 with respect to Example 1-1, except that a solvent consisting only of dimethyl sulfoxide or a solvent consisting only of γ-butyrolactone was used, the other steps were the same as in Example 1-1. Thus, an electrochemical display device was manufactured. Furthermore, as Comparative Examples 1-3 to 1-5 with respect to Example 1-1, except that dimethylformamide (DMF), propylene carbonate (PC) or diethylacetamide (DEA) was used instead of γ-butyrolactone, respectively. Other than that produced the electrochemical display device like Example 1-1.
[0081]
With respect to the manufactured electrochemical display devices of Example 1-1 and Comparative Examples 1-1 to 1-5, writing and erasing were performed at intervals of 10 ° C. in a temperature range of −20 ° C. to 40 ° C., and drive characteristics and display characteristics Was evaluated. Writing is performed by applying a voltage of -2 V for a period until the required density (
[0082]
As can be seen from FIGS. 10 and 11, Comparative Example 1-1 using a solvent consisting of dimethyl sulfoxide alone and Comparative Examples 1-3 to 1-5 using a solvent containing dimethyl sulfoxide and a solvent other than γ-butyrolactone. At 10 ° C. or higher, a relatively good response time is shown. Further, although the temperature change is very small, the response time sharply increases at 10 ° C. or lower. It was big. In Comparative Example 1-2 using a solvent consisting of γ-butyrolactone alone, the response time becomes longer as the temperature becomes lower, and the amount of charge required for the optical density to reach 1.0 becomes larger. It was also inferior in terms of power consumption.
[0083]
On the other hand, in Example 1-1 using the solvent containing dimethyl sulfoxide and γ-butyrolactone, in the temperature range of −15 ° C. to 40 ° C., the change in the response time was small, and 0.1 second or less. Response time was maintained.
[0084]
That is, if dimethyl sulfoxide and γ-butyrolactone are contained in the solvent, high-speed response can be obtained, and the temperature dependence of the response speed can be reduced, so that high-speed response can be obtained even at low temperatures. Do you get it.
[0085]
(Examples 1-2 to 1-9)
An electrochemical display was produced in the same manner as in Example 1-1, except that the ratio between dimethyl sulfoxide and γ-butyrolactone was changed as shown in Table 1. The driving characteristics and the display characteristics of the electrochemical display devices of Examples 1-2 to 1-9 were examined in the same manner as in Example 1-1. FIG. 12 shows the driving characteristics of Examples 1-2 to 1-4 together with the results of Example 1-1, and FIG. 13 shows the driving characteristics of Examples 1-5 to 1-9 together with the results of Example 1-1. Show. FIG. 14 shows the display characteristics of Examples 1-2 to 1-4 together with the results of Example 1-1, and FIG. 15 shows the display characteristics of Examples 1-5 to 1-9 of Example 1-1. Shown together with the results.
[0086]
[Table 1]
[0087]
As can be seen from FIGS. 12 to 15, a solvent containing dimethyl sulfoxide and γ-butyrolactone in a volume ratio of dimethyl sulfoxide: γ-butyrolactone = 8: 2 to 9: 1 or 1: 9 to 2: 8 was used. In Examples 1-2, 1-3, 1-8, and 1-9, the response time was extremely short at 10 ° C. to 40 ° C., and the amount of charge required for the optical density to reach 1.0 was small. This is very preferable because the power consumption of the device can be reduced. However, when the temperature is lower than 10 ° C., although not as large as in Comparative Example 1-1 shown in FIG. A device that is not expected to be used in a low-temperature environment of less than 10 ° C. is excellent, but cannot be said to be suitable for a mobile device that is expected to be used outdoors or the like in winter.
[0088]
On the other hand, as can be seen from FIGS. 12 and 13, Example 1-1 using a solvent containing dimethyl sulfoxide and γ-butyrolactone in a volume ratio of dimethyl sulfoxide: γ-butyrolactone = 7: 3 to 3: 7. , 1-4 to 1-7 do not show the high-speed response as much as Examples 1-2 and 1-3 in the temperature range of 10 ° C. to 40 ° C., but respond in the temperature range of −15 ° C. to 40 ° C. The change in time was small, and a response time of 0.1 second or less could be maintained.
[0089]
That is, the ratio of dimethyl sulfoxide to γ-butyrolactone is set to be dimethyl sulfoxide: γ-butyrolactone = 7: 3 to 3: 7, and further dimethyl sulfoxide: γ-butyrolactone = 6: 4 to 3: 7 in volume ratio. For example, it has been found that the response speed can be increased in a temperature range of 10 ° C. to 30 ° C., which is the most frequently used environment, and a rapid decrease in response speed can be prevented at low temperatures.
[0090]
(Examples 2-1 to 2-4)
Except that γ-valerolactone (γVL) was used in place of γ-butyrolactone and the ratio of dimethyl sulfoxide to γ-valerolactone was changed as shown in Table 2, the others were the same as in Example 1-1. Similarly, an electrochemical display device was manufactured. The driving characteristics of the electrochemical display devices of Examples 2-1 to 2-4 were examined in the same manner as in Example 1-1. FIG. 16 shows the results together with the results of Examples 1-2, 1-4, 1-5, and 1-7 and Comparative Example 1-1.
[0091]
[Table 2]
[0092]
From FIG. 16, if a solvent containing dimethyl sulfoxide and γ-valerolactone is used, as in the case of using a solvent containing dimethyl sulfoxide and γ-butyrolactone, a solvent using only dimethyl sulfoxide is used. It was found that the response time at a low temperature can be shortened as compared with. However, when the ratio of γ-valerolactone is 70% or more, the electrolytic solution discolors to pale yellow. Further, as the ratio increases, the discoloration also increases. The liquid turned red. Since such coloring is not preferable for a display device, it was found that the ratio of γ-valerolactone is preferably less than 70%, and more preferably less than 50%. This discoloration is considered to be due to the use of a halide as a deposition material. In addition, it was found that when the response time up to -20 ° C requires within 1 second, the ratio of γ-valerolactone is preferably more than 10% and less than 70%. That is, it was found that the ratio of dimethyl sulfoxide and γ-valerolactone is preferably dimethylsulfoxide: γ-valerolactone = 8: 2 to 3: 7 by volume ratio.
[0093]
Further, from a comparison between Examples 2-1 to 2-4 and Examples 1-2, 1-4, 1-5, and 1-7, at 10 ° C. or higher, those using γ-valerolactone were: Response time can be shortened as compared with those using γ-butyrolactone, and at 0 ° C. or lower, those using γ-butyrolactone shorten the response time as compared with those using γ-valerolactone. I found that I could do it.
[0094]
(Examples 3-1 to 3-18)
Aside from using a solvent in which propylene carbonate was mixed in addition to dimethyl sulfoxide and γ-butyrolactone, and changing the proportions as shown in Table 3, the others were the same as in Example 1-1. An electrochemical display device was manufactured. Further, as Comparative Examples 3-1 to 3-6 with respect to Examples 3-1 to 3-18, a solvent composed of propylene carbonate, or a solvent composed of γ-butyrolactone and propylene carbonate, or composed of dimethyl sulfoxide and propylene carbonate An electrochemical display device was produced in the same manner as in Example 1-1, except that a solvent was used and the proportions were changed as shown in Table 3.
[0095]
[Table 3]
[0096]
Regarding the electrochemical display devices of Examples 3-1 to 3-18 and Comparative examples 3-1 to 3-6, every 10 ° C. in a temperature range of −20 ° C. to 30 ° C. in the same manner as in Example 1-1. Were written and erased, and the driving characteristics were evaluated. 17 to 22 show the results together with the results of Examples 1-1 to 1-9 and Comparative examples 1-1 and 1-2. 17 is a driving characteristic at −20 ° C., FIG. 18 is a driving characteristic at −10 ° C., FIG. 19 is a driving characteristic at 0 ° C., FIG. 20 is a driving characteristic at 10 ° C., FIG. Numeral 22 indicates the driving characteristics at 30 ° C., respectively. In FIGS. 17 to 21, ○ represents an example and □ represents a comparative example, in which the upper part represents the number of the example, and the lower part represents the response time (sec).
[0097]
As can be seen from FIGS. 17 to 22, according to Examples 3-1 to 3-18 using the solvent containing dimethyl sulfoxide, γ-butyrolactone, and propylene carbonate, the response time can be extremely shortened at room temperature. Further, it was found that the extremely long response time can be suppressed even at a low temperature of -10 ° C.
[0098]
That is, if the solvent contains dimethyl sulfoxide, γ-butyrolactone, and propylene carbonate, a high-speed response can be obtained, and the temperature dependence of the response speed can be reduced. It was found that high-speed response could be obtained.
[0099]
Further, the solvent may contain dimethyl sulfoxide in a range of 10% by volume to 80% by volume, γ-butyrolactone in a range of 10% by volume to 90% by volume, and propylene carbonate in a range of 60% by volume or less. In addition, dimethyl sulfoxide in the range of 20% by volume to 70% by volume, γ-butyrolactone in the range of 20% by volume to 80% by volume, and propylene carbonate in the range of 50% by volume or less, respectively. It has been found that, if it is included, a high-speed response can be obtained, and the decrease in the response speed at low temperatures is small.
[0100]
In addition, in the said Example, although the sulfoxide and the cyclic carboxylic acid ester were demonstrated concretely, the above-mentioned effect is considered to be derived from the structure. Therefore, similar results can be obtained by using other sulfoxides and other cyclic carboxylic acid esters. Further, in the above embodiment, the case where the gel electrolyte is used has been described, but the same result can be obtained by using the electrolyte.
[0101]
As described above, the present invention has been described with reference to the embodiment and the example. However, the present invention is not limited to the above-described embodiment and example, and can be variously modified. For example, in the above embodiments and examples, the structure of the electrochemical display element has been specifically described by way of example, but other structures may be used. For example, although not shown, the electrolyte may be impregnated into a nonwoven fabric or a porous film.
[0102]
Further, the electrolyte of the present invention can be used for other electric devices such as a capacitor, a capacitor and a battery.
[0103]
【The invention's effect】
As described above, according to the electrolyte and the electrochemical display device of the present invention, since the sulfoxide and the solvent containing the cyclic carboxylic acid ester are included, a high-speed response can be obtained and the response speed can be improved. Temperature dependency can be reduced. Therefore, high-speed response can be obtained even at a low temperature. As a result, even if the use temperature changes, the color (color density) of the pixel can be kept constant, and excellent display quality can be obtained.
[0104]
In particular, if dimethyl sulfoxide and γ-butyrolactone are contained in a volume ratio of dimethyl sulfoxide: γ-butyrolactone = 7: 3 to 3: 7, the temperature of 10 ° C. to 30 ° C., which is the most frequently used environment, is used. It is possible to increase the response speed in the region and prevent a rapid decrease in the response speed at a low temperature.
[0105]
In addition, when propylene carbonate is contained in addition to the sulfoxide and the cyclic carboxylic acid ester, the response speed can be increased particularly at room temperature.
[Brief description of the drawings]
FIG. 1 is a block diagram illustrating a configuration of an electrochemical display device according to an embodiment of the present invention.
FIG. 2 is a perspective view illustrating a configuration of the electrochemical display element illustrated in FIG.
FIG. 3 is a triangular diagram showing a preferred composition of the electrolyte shown in FIG.
FIG. 4 is another triangular diagram showing a preferred composition of the electrolyte shown in FIG.
FIG. 5 is a cross-sectional view illustrating a manufacturing process of the electrochemical display device illustrated in FIG.
FIG. 6 is a cross-sectional view illustrating another manufacturing process of the electrochemical display device illustrated in FIG.
FIG. 7 is a perspective view illustrating a configuration of another electrochemical display element illustrated in FIG.
8 is a perspective view illustrating a configuration of another electrochemical display element illustrated in FIG.
FIG. 9 is a perspective view illustrating a configuration of another electrochemical display element illustrated in FIG.
FIG. 10 is a characteristic diagram illustrating drive characteristics according to Example 1-1 of the present invention.
FIG. 11 is a characteristic diagram illustrating display characteristics according to Example 1-1 of the present invention.
FIG. 12 is a characteristic diagram illustrating drive characteristics according to Examples 1-2 to 1-4 of the present invention.
FIG. 13 is a characteristic diagram illustrating driving characteristics according to Examples 1-5 to 1-9 of the present invention.
FIG. 14 is a characteristic diagram illustrating display characteristics according to Examples 1-2 to 1-4 of the present invention.
FIG. 15 is a characteristic diagram illustrating display characteristics according to Examples 1-5 to 1-9 of the present invention.
FIG. 16 is a characteristic diagram illustrating drive characteristics according to Examples 2-1 to 2-4 of the present invention.
FIG. 17 is a characteristic diagram illustrating drive characteristics at −20 ° C. according to Examples 3-1 to 3-18 of the present invention.
FIG. 18 is a characteristic diagram illustrating driving characteristics at −10 ° C. according to Examples 3-1 to 3-18 of the present invention.
FIG. 19 is a characteristic diagram illustrating driving characteristics at 0 ° C. according to Examples 3-1 to 3-18 of the present invention.
FIG. 20 is a characteristic diagram illustrating drive characteristics at 10 ° C. according to Examples 3-1 to 3-18 of the present invention.
FIG. 21 is a characteristic diagram illustrating drive characteristics at 20 ° C. according to Examples 3-1 to 3-18 of the present invention.
FIG. 22 is a characteristic diagram illustrating driving characteristics at 30 ° C. according to Examples 3-1 to 3-18 of the present invention.
[Explanation of symbols]
DESCRIPTION OF
Claims (18)
前記電解質は、スルホキシドと、環状カルボン酸エステルとを含有する溶媒を含むことを特徴とする電気化学表示装置。An electrochemical display device including an electrolyte between a first electrode and a second electrode,
The electrochemical display device, wherein the electrolyte includes a solvent containing a sulfoxide and a cyclic carboxylate.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2003103243A JP4508544B2 (en) | 2003-04-07 | 2003-04-07 | Electrochemical display device |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2003103243A JP4508544B2 (en) | 2003-04-07 | 2003-04-07 | Electrochemical display device |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2004309798A true JP2004309798A (en) | 2004-11-04 |
| JP4508544B2 JP4508544B2 (en) | 2010-07-21 |
Family
ID=33466452
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2003103243A Expired - Fee Related JP4508544B2 (en) | 2003-04-07 | 2003-04-07 | Electrochemical display device |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP4508544B2 (en) |
Cited By (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2004309946A (en) * | 2003-04-10 | 2004-11-04 | Sony Corp | Electrochemical display device and its manufacturing method |
| WO2006061980A1 (en) * | 2004-12-09 | 2006-06-15 | Konica Minolta Holdings, Inc. | Display element |
| WO2006061987A1 (en) * | 2004-12-10 | 2006-06-15 | Konica Minolta Holdings, Inc. | Display element |
| JP2007072169A (en) * | 2005-09-07 | 2007-03-22 | Konica Minolta Holdings Inc | Display element |
| JP2007248835A (en) * | 2006-03-16 | 2007-09-27 | Konica Minolta Holdings Inc | Display element |
| WO2008029669A1 (en) | 2006-09-08 | 2008-03-13 | Konica Minolta Holdings, Inc. | Display element |
| JP4968061B2 (en) * | 2005-02-04 | 2012-07-04 | コニカミノルタホールディングス株式会社 | Display element and driving method thereof |
| CN114230378A (en) * | 2021-12-27 | 2022-03-25 | 复旦大学 | Preparation method of redox-driven super-assembly intelligent door control system |
Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH0992328A (en) * | 1995-09-20 | 1997-04-04 | Polytec Design:Kk | Gelled electrolyte |
| JPH10133236A (en) * | 1996-09-06 | 1998-05-22 | Sony Corp | Optical device and electrolyte |
| JPH11101994A (en) * | 1997-09-29 | 1999-04-13 | Sony Corp | Picture display device of electrodeposition type |
| JPH11142895A (en) * | 1997-09-08 | 1999-05-28 | Sony Corp | Optical device and electrolyte |
| JPH11142891A (en) * | 1997-11-05 | 1999-05-28 | Nippon Oil Co Ltd | Electrochromic mirror |
| JP2001115134A (en) * | 1999-10-14 | 2001-04-24 | Nippon Mitsubishi Oil Corp | Ion-conductive substance |
| JP2003005224A (en) * | 2001-06-26 | 2003-01-08 | Sony Corp | Display element and method for manufacturing the same |
-
2003
- 2003-04-07 JP JP2003103243A patent/JP4508544B2/en not_active Expired - Fee Related
Patent Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH0992328A (en) * | 1995-09-20 | 1997-04-04 | Polytec Design:Kk | Gelled electrolyte |
| JPH10133236A (en) * | 1996-09-06 | 1998-05-22 | Sony Corp | Optical device and electrolyte |
| JPH11142895A (en) * | 1997-09-08 | 1999-05-28 | Sony Corp | Optical device and electrolyte |
| JPH11101994A (en) * | 1997-09-29 | 1999-04-13 | Sony Corp | Picture display device of electrodeposition type |
| JPH11142891A (en) * | 1997-11-05 | 1999-05-28 | Nippon Oil Co Ltd | Electrochromic mirror |
| JP2001115134A (en) * | 1999-10-14 | 2001-04-24 | Nippon Mitsubishi Oil Corp | Ion-conductive substance |
| JP2003005224A (en) * | 2001-06-26 | 2003-01-08 | Sony Corp | Display element and method for manufacturing the same |
Cited By (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2004309946A (en) * | 2003-04-10 | 2004-11-04 | Sony Corp | Electrochemical display device and its manufacturing method |
| WO2006061980A1 (en) * | 2004-12-09 | 2006-06-15 | Konica Minolta Holdings, Inc. | Display element |
| JP4876921B2 (en) * | 2004-12-09 | 2012-02-15 | コニカミノルタホールディングス株式会社 | Display element |
| JPWO2006061980A1 (en) * | 2004-12-09 | 2008-06-05 | コニカミノルタホールディングス株式会社 | Display element |
| US7697189B2 (en) | 2004-12-10 | 2010-04-13 | Konica Minolta Holdings, Inc. | Display element |
| WO2006061987A1 (en) * | 2004-12-10 | 2006-06-15 | Konica Minolta Holdings, Inc. | Display element |
| JPWO2006061987A1 (en) * | 2004-12-10 | 2008-06-05 | コニカミノルタホールディングス株式会社 | Display element |
| JP4968061B2 (en) * | 2005-02-04 | 2012-07-04 | コニカミノルタホールディングス株式会社 | Display element and driving method thereof |
| JP2007072169A (en) * | 2005-09-07 | 2007-03-22 | Konica Minolta Holdings Inc | Display element |
| JP4569425B2 (en) * | 2005-09-07 | 2010-10-27 | コニカミノルタホールディングス株式会社 | Display element |
| JP2007248835A (en) * | 2006-03-16 | 2007-09-27 | Konica Minolta Holdings Inc | Display element |
| WO2008029669A1 (en) | 2006-09-08 | 2008-03-13 | Konica Minolta Holdings, Inc. | Display element |
| CN114230378A (en) * | 2021-12-27 | 2022-03-25 | 复旦大学 | Preparation method of redox-driven super-assembly intelligent door control system |
| CN114230378B (en) * | 2021-12-27 | 2022-11-15 | 复旦大学 | Preparation method of redox-driven super-assembly intelligent door control system |
Also Published As
| Publication number | Publication date |
|---|---|
| JP4508544B2 (en) | 2010-07-21 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2002258327A (en) | Electrochromic display element and electrodeposition type display element | |
| EP1475656A1 (en) | Electrochemical display element and electrochemical display | |
| JP3804822B2 (en) | Display element and manufacturing method thereof | |
| JPWO2002079868A1 (en) | Display device and driving method thereof | |
| US20080170288A1 (en) | Display Element and Driving Method Thereof | |
| JP4508544B2 (en) | Electrochemical display device | |
| US20080166590A1 (en) | Display Element | |
| JPWO2008023551A1 (en) | Display element | |
| JP4036045B2 (en) | Display device and driving method thereof | |
| JP4569110B2 (en) | Electrochemical display device and driving method thereof | |
| JP2005189299A (en) | Electrochemical display device | |
| JP4470451B2 (en) | Method for producing electrochemical dimmer and method for producing polymer electrolyte | |
| US20050087448A1 (en) | Electrochemical display element and electrochemical display | |
| JP2006195141A (en) | Method for driving electrodeposition type display device | |
| JP4506171B2 (en) | Electrochemical light control device and method for manufacturing the same | |
| JP2004294931A (en) | Electrochemical dimmer and its manufacturing method | |
| JP4998470B2 (en) | Display element | |
| JP4569140B2 (en) | Electrochemical display device and electrochemical display method | |
| JP2006146252A (en) | Electrodeposition-type display element, electrodeposition-type display device, and method for manufacturing electrodeposition-type display device | |
| JP2004177491A (en) | Electrodeposition type display device and method for driving the same | |
| JP2007248961A (en) | Display element | |
| JP2005189384A (en) | Electrochemical light controlling device and its driving method | |
| JP4497283B2 (en) | Electrochemical display device and manufacturing method thereof | |
| JP2004309946A (en) | Electrochemical display device and its manufacturing method | |
| JP2008065028A (en) | Display element |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20060316 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20090826 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20091015 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20091201 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100125 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20100217 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100324 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20100414 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130514 Year of fee payment: 3 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20100427 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130514 Year of fee payment: 3 |
|
| LAPS | Cancellation because of no payment of annual fees |