ES2719776T3 - Inhibidores de GSK3 y métodos de uso de los mismos - Google Patents
Inhibidores de GSK3 y métodos de uso de los mismos Download PDFInfo
- Publication number
- ES2719776T3 ES2719776T3 ES13780300T ES13780300T ES2719776T3 ES 2719776 T3 ES2719776 T3 ES 2719776T3 ES 13780300 T ES13780300 T ES 13780300T ES 13780300 T ES13780300 T ES 13780300T ES 2719776 T3 ES2719776 T3 ES 2719776T3
- Authority
- ES
- Spain
- Prior art keywords
- optionally substituted
- compound
- group
- certain embodiments
- pharmaceutically acceptable
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 0 CC1*C(C)CC1 Chemical compound CC1*C(C)CC1 0.000 description 12
- TYYMYGWTBNTQHZ-UHFFFAOYSA-N CC(C)(C1)CC(Nc2n[nH]c(C(F)(F)F)c2C2c3cc(F)ccc3F)=C2C1=O Chemical compound CC(C)(C1)CC(Nc2n[nH]c(C(F)(F)F)c2C2c3cc(F)ccc3F)=C2C1=O TYYMYGWTBNTQHZ-UHFFFAOYSA-N 0.000 description 1
- DCAIFVKDYWYHDP-UHFFFAOYSA-N CC(C)(C1)CC(Nc2n[nH]c(C)c2C2(C)c3cccc(C(N)=O)c3)=C2C1=O Chemical compound CC(C)(C1)CC(Nc2n[nH]c(C)c2C2(C)c3cccc(C(N)=O)c3)=C2C1=O DCAIFVKDYWYHDP-UHFFFAOYSA-N 0.000 description 1
- GQFUYSHWMLTFPZ-UHFFFAOYSA-N CC(C)(C1)CC(Nc2n[nH]c(C)c2C2c3ccc(C)cc3)=C2C1=O Chemical compound CC(C)(C1)CC(Nc2n[nH]c(C)c2C2c3ccc(C)cc3)=C2C1=O GQFUYSHWMLTFPZ-UHFFFAOYSA-N 0.000 description 1
- YCEJJWWUCHXBOX-UHFFFAOYSA-N CC(C)(C1)CC(Nc2n[nH]c(C)c2C2c3ccn[nH]3)=C2C1=O Chemical compound CC(C)(C1)CC(Nc2n[nH]c(C)c2C2c3ccn[nH]3)=C2C1=O YCEJJWWUCHXBOX-UHFFFAOYSA-N 0.000 description 1
- CNKCQXIXZDUWHE-QFIPXVFZSA-N CC(C)(C1)CC(Nc2n[nH]c(C3CC3)c2[C@@]2(C)c3cc(C(F)(F)F)ccc3)=C2C1=O Chemical compound CC(C)(C1)CC(Nc2n[nH]c(C3CC3)c2[C@@]2(C)c3cc(C(F)(F)F)ccc3)=C2C1=O CNKCQXIXZDUWHE-QFIPXVFZSA-N 0.000 description 1
- IMKJGRXMBFNOGA-UHFFFAOYSA-N CC(C)(C1)CC(Nc2n[nH]cc2C2(C)c3ccccc3)=C2C1=O Chemical compound CC(C)(C1)CC(Nc2n[nH]cc2C2(C)c3ccccc3)=C2C1=O IMKJGRXMBFNOGA-UHFFFAOYSA-N 0.000 description 1
- IMKJGRXMBFNOGA-LJQANCHMSA-N CC(C)(C1)CC(Nc2n[nH]cc2[C@@]2(C)c3ccccc3)=C2C1=O Chemical compound CC(C)(C1)CC(Nc2n[nH]cc2[C@@]2(C)c3ccccc3)=C2C1=O IMKJGRXMBFNOGA-LJQANCHMSA-N 0.000 description 1
- IMKJGRXMBFNOGA-IBGZPJMESA-N CC(C)(C1)CC(Nc2n[nH]cc2[C@]2(C)c3ccccc3)=C2C1=O Chemical compound CC(C)(C1)CC(Nc2n[nH]cc2[C@]2(C)c3ccccc3)=C2C1=O IMKJGRXMBFNOGA-IBGZPJMESA-N 0.000 description 1
- MIVPKTHOMGOFRR-LURJTMIESA-N CC[C@H](C)C[NH+](C)[O-] Chemical compound CC[C@H](C)C[NH+](C)[O-] MIVPKTHOMGOFRR-LURJTMIESA-N 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/4738—Quinolines; Isoquinolines ortho- or peri-condensed with heterocyclic ring systems
- A61K31/4745—Quinolines; Isoquinolines ortho- or peri-condensed with heterocyclic ring systems condensed with ring systems having nitrogen as a ring hetero atom, e.g. phenantrolines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/4747—Quinolines; Isoquinolines spiro-condensed
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/18—Drugs for disorders of the alimentary tract or the digestive system for pancreatic disorders, e.g. pancreatic enzymes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P21/00—Drugs for disorders of the muscular or neuromuscular system
- A61P21/02—Muscle relaxants, e.g. for tetanus or cramps
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/18—Antipsychotics, i.e. neuroleptics; Drugs for mania or schizophrenia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/24—Antidepressants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/10—Spiro-condensed systems
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- General Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Medicinal Chemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Biomedical Technology (AREA)
- Epidemiology (AREA)
- Diabetes (AREA)
- Hematology (AREA)
- Psychiatry (AREA)
- Pain & Pain Management (AREA)
- Obesity (AREA)
- Oncology (AREA)
- Emergency Medicine (AREA)
- Hospice & Palliative Care (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Physical Education & Sports Medicine (AREA)
- Endocrinology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Enzymes And Modification Thereof (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Oxygen Or Sulfur (AREA)
Abstract
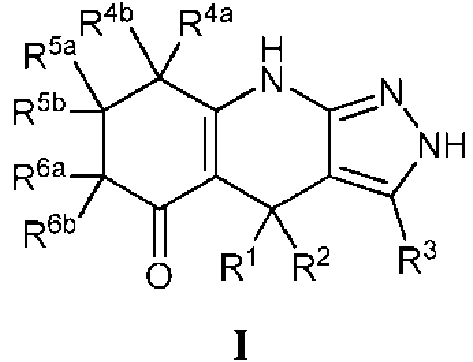
Un compuesto de fórmula I:**Fórmula** o una de sus sales farmacéuticamente aceptables, en la que: R1 y R2 se seleccionan independientemente del grupo que consiste en grupo alifático opcionalmente sustituido, arilo opcionalmente sustituido y heteroarilo opcionalmente sustituido; o R1 y R2 se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido, en el que el anillo formado por R1 y R2 está condensado opcionalmente a un anillo arilo o heteroarilo; R3 se selecciona del grupo que consiste en hidrógeno, halo, -CN, -NO2, grupo alifático opcionalmente sustituido, fenilo opcionalmente sustituido, heterociclilo opcionalmente sustituido, heteroarilo opcionalmente sustituido, -ORA, - N(RB)2, -SRA, -C(=O)RA, -C(=O)ORA, -C(=O)SRA, -C(=O)N(RB)2, -OC(=O)RA, -NRBC(=O)RA, -NRBC(=O)N(RB)2, - OC(=O)N(RB)2, -NRBC(=O)ORA, -SC(=O)RA, -C(=NRB)RA, -C(=NRB)N(RB)2, -NRBC(=NRB)RB, -C(=S)RA, - C(=S)N(RB)2, -NRBC(=S)RA, -S(=O)RA, -SO2RA, -NRBSO2RA y -SO2N(RB)2; cada RA se selecciona independientemente del grupo que consiste en hidrógeno, grupo alifático opcionalmente sustituido, carbociclilo opcionalmente sustituido, heterociclilo opcionalmente sustituido, arilo opcionalmente sustituido y heteroarilo opcionalmente sustituido; cada RB se selecciona independientemente del grupo que consiste en hidrógeno, grupo alifático opcionalmente sustituido, carbociclilo opcionalmente sustituido, heterociclilo opcionalmente sustituido, arilo opcionalmente sustituido y heteroarilo opcionalmente sustituido, o dos grupos RB se toman junto con sus átomos intermedios para formar un anillo heterocíclico opcionalmente sustituido; R4a y R4b se seleccionan independientemente del grupo que consiste en hidrógeno, halo, -CN, -ORA, -N(RB)2, y grupo alifático opcionalmente sustituido, o R4a y R4b se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido; R5a y R5b se seleccionan independientemente del grupo que consiste en hidrógeno, halo, -CN, -ORA, -N(RB)2, y grupo alifático opcionalmente sustituido, o R5a y R5b se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido; y R6a y R6b se seleccionan independientemente del grupo que consiste en hidrógeno, halo, -CN, -ORA, -N(RB)2, y grupo alifático opcionalmente sustituido, o R6a y R6b se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido; en los que cada ocasión de arilo tiene independientemente de 6 a 14 átomos de carbono en el anillo; y en los que cada ocasión de heteroarilo es independientemente de 5 a 10 miembros, y monocíclico o bicíclico, y tiene independientemente de 1 a 4 heteroátomos en el anillo seleccionados independientemente del grupo que consiste en nitrógeno, oxígeno y azufre; en los que los artículos "un/o", "una" y "el/la" pueden indicar uno o más de uno; y con la condición de que el compuesto no sea de ninguna de las fórmulas**Fórmula**
Description
DESCRIPCIÓN
Inhibidores de GSK3 y métodos de uso de los mismos
Solicitudes relacionadas
La presente solicitud reivindica prioridad según 35 U.S.C. § 119(e) a las solicitudes de patente provisionales de Estados Unidos, U.S.S.N. 61/713.314, presentada el 12 de octubre de 2012 y U.S.S.N. 61/779.394, presentada el 13 de marzo de 2013.
Antecedentes de la invención
La búsqueda de nuevos agentes terapéuticos ha estado ayudada enormemente en los últimos años por una mejor comprensión de la estructura de las enzimas y otras biomoléculas asociadas con enfermedades. Una clase importante de enzimas que ha sido objeto de considerable estudio es las proteína cinasas.
Las proteína cinasas constituyen una gran familia de enzimas estructuralmente relacionadas que son responsables del control de una diversidad de procesos de transducción de señales dentro de la célula. Se cree que las proteína cinasas han evolucionado desde un gen ancestral común debido a la conservación de su estructura y función catalítica. Casi todas las cinasas contienen un dominio catalítico de 250-300 aminoácidos similar. Las cinasas pueden clasificarse en familias por los sustratos que fosforilan (por ejemplo, proteína-tirosina, proteínaserina/treonina, lípidos, etc.).
En general, las proteína cinasas median la señalización intracelular logrando la transferencia de un fosforilo desde un nucleósido trifosfato a una proteína aceptadora que está implicada en una ruta de señalización. Estos eventos de actúan como activadores/desactivadores que pueden modular o regular la función biológica de la proteína diana. Estos eventos de fosforilación finalmente se desencadenan en respuesta a una diversidad de estímulos extracelulares y otros estímulos. Los ejemplos de dichos estímulos incluyen señales de sobrecarga ambiental y química (por ejemplo, choque osmótico, choque térmico, radiación ultravioleta, endotoxina bacteriana y H2O2), citocinas (por ejemplo, interleucina-1 (IL-I) y factor de necrosis tumoral a (TNF-a)), y factores de crecimiento (por ejemplo, factor estimulador de colonias de granulocitos macrófagos (GM-CSF), y factor de crecimiento de fibroblastos (FGF)). Un estímulo extracelular puede afectar a una o más respuestas celulares relacionadas con el crecimiento celular, la migración, la diferenciación, la secreción de hormonas, la activación de factores de transcripción, la contracción muscular, el metabolismo de la glucosa, el control de la síntesis de proteínas y la regulación del ciclo celular.
Muchas enfermedades están asociadas con respuestas celulares anómalas desencadenadas por eventos mediados por proteína cinasas, como se describe anteriormente. Estas enfermedades incluyen, aunque sin limitación, enfermedades autoinmunitarias, enfermedades inflamatorias, enfermedades óseas, enfermedades metabólicas, enfermedades neurológicas y neurodegenerativas, cáncer, enfermedades cardiovasculares, alergias y asma, enfermedad de Alzheimer, trastornos metabólicos (por ejemplo, diabetes) y enfermedades relacionadas con hormonas. Por consiguiente, sigue existiendo una necesidad de encontrar inhibidores de proteína cinasa, particularmente inhibidores de GSK3, útiles como agentes terapéuticos.
Quiroga J. et al., Tetrahedron, vol. 57, n.° 32, páginas 6947-6953 divulga la síntesis regioselectiva de 4,7,8,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-5(6H)-onas. Drizin I. et al., Bioorganica & Medicinal Chemistry Letters, vol. 12, páginas 1481-1484 divulga estudios de estructura-actividad para una serie de dihidropirimidinas tricíclicas como abridores de canales de KATP (KCO). La publicación internacional WO 2007/012972 divulga heterociclos de 1,4-dihidropiridina condensados, proceso para preparar los mismos, uso y composiciones que los contienen.
Compendio de la invención
Es importante identificar inhibidores de cinasa selectivos para reducir o eliminar efectos inespecíficos. En determinadas realizaciones, compuestos descritos en la presente memoria son inhibidores de cinasa selectivos.
En algunas realizaciones, la presente divulgación proporciona un compuesto de fórmula I:
definen en la presente memoria. En determinadas realizaciones, la presente divulgación proporciona un compuesto de fórmula II:
R , R y n son como se definen en la presente memoria. En determinadas realizaciones, la presente divulgación proporciona un compuesto de fórmula III:
o una de sus sales farmacéuticamente aceptables, en la que Anillo A, R2, R3, R5a, R5b, R7 y n son como se definen en la presente memoria.
En algunas realizaciones, un compuesto descrito en la presente memoria está enantioméricamente enriquecido. Por ejemplo, en determinadas realizaciones, un compuesto proporcionado es de fórmula II-a-i o II-a-ii:
o una de sus sales farmacéuticamente aceptables.
En algunas realizaciones, se proporcionan composiciones farmacéuticas que comprenden un compuesto descrito en la presente memoria (por ejemplo, un compuesto de fórmula I, II o III), o una de sus sales farmacéuticamente aceptables, y un excipiente farmacéuticamente aceptable.
En determinadas realizaciones, compuestos descritos en la presente memoria inhiben la actividad de una o más cinasas (por ejemplo, glucógeno sintasa cinasa 3 (GSK3), caseína cinasa 1 (CK1)). En determinadas realizaciones, se proporcionan compuestos para su uso en métodos de inhibición de una cinasa, que comprenden poner en contacto una cinasa, o mutante o variante de la misma, con una cantidad eficaz de un compuesto de fórmula I, II, o III, o una de sus sales farmacéuticamente aceptables. La cinasa puede estar purificada o en bruto, y puede estar presente en una célula, tejido o un sujeto. Por tanto, dichos métodos abarcan la inhibición tanto in vitro como in vivo de la actividad cinasa. En determinadas realizaciones, se proporcionan compuestos para su uso en la inhibición de GSK3, que comprenden poner en contacto GSK3, o un mutante o variante de la misma, con una cantidad eficaz de un compuesto descrito en la presente memoria (por ejemplo, un compuesto de fórmula I, II, o III), o una de sus sales farmacéuticamente aceptables. En determinadas realizaciones, la GSK3 es GSK3 de tipo silvestre. En determinadas realizaciones, la GSK3 es GSK3p. En determinadas realizaciones, la GSK3 es GSK3a. En determinadas realizaciones, la GSK3 está en una célula. En determinadas realizaciones, se proporcionan compuestos para su uso en la inhibición de CK1, que comprenden poner en contacto CK1, o un mutante o variante de la misma, con una cantidad eficaz de un compuesto descrito en la presente memoria (por ejemplo, un compuesto de fórmula I, II, o III),
o una de sus sales farmacéuticamente aceptables. En determinadas realizaciones, la CK1 está en una célula. En determinadas realizaciones, la CK1 es CK1 de tipo silvestre. En determinadas realizaciones, la CK1 es CK18. En determinadas realizaciones, la CK18 es CK18 de tipo silvestre. En determinadas realizaciones, la CK18 está en una célula. En algunas realizaciones, un compuesto proporcionado es selectivo para GSK3 sobre CK1.
En algunas realizaciones, se proporcionan compuestos para su uso en métodos de tratamiento de un trastorno mediado por cinasas, que comprenden administrar a un sujeto que padece un trastorno mediado por cinasas una cantidad eficaz de un compuesto descrito en la presente memoria (por ejemplo, un compuesto de fórmula I, II, o III), o una de sus sales farmacéuticamente aceptables. En determinadas realizaciones, se proporcionan compuestos para su uso en métodos de tratamiento de un trastorno mediado por GSK3, que comprenden administrar a un sujeto que padece un trastorno mediado por GSK3 una cantidad eficaz de un compuesto descrito en la presente memoria (por ejemplo, un compuesto de fórmula I, II, o III), o una de sus sales farmacéuticamente aceptables. En determinadas realizaciones, el trastorno mediado por GSK3 es un trastorno mediado por GSK3p, tal como enfermedad neurológica, trastorno psiquiátrico, cáncer (por ejemplo, glioma, cáncer pancreático) o un trastorno metabólico (por ejemplo, diabetes (por ejemplo, diabetes de tipo II)). En determinadas realizaciones, el trastorno mediado por GSK3 es un trastorno neurodegenerativo, tal como enfermedad de Alzheimer, demencia frontotemporal (incluyendo parálisis supranuclear progresiva, degeneración corticobasal) o esclerosis lateral amiotrófica (ALS). En determinadas realizaciones, el trastorno mediado por GSK3 es un trastorno psiquiátrico, tal como trastorno bipolar, esquizofrenia, autismo, síndrome del X frágil o depresión (por ejemplo, depresión insensible a litio). En determinadas realizaciones, el trastorno mediado por GSK3 es un trastorno mediado por GSK3a. En determinadas realizaciones, el trastorno mediado por GSK3a es cáncer. En determinadas realizaciones, el trastorno mediado por GSK3a es leucemia, tal como leucemia mieloide aguda. En determinadas realizaciones, el trastorno mediado por GSK3a es un trastorno metabólico (por ejemplo, diabetes (por ejemplo, diabetes de tipo II)). En determinadas realizaciones, se proporcionan compuestos para su uso en métodos de tratamiento de un trastorno mediado por CK1, que comprenden administrar a un sujeto que padece un trastorno mediado por CK1 una cantidad eficaz de un compuesto descrito en la presente memoria (por ejemplo, un compuesto de fórmula I, II, o III), o una de sus sales farmacéuticamente aceptables. En determinadas realizaciones, se proporcionan compuestos para su uso en métodos de tratamiento de un trastorno mediado por CK18, que comprenden administrar a un sujeto que padece un trastorno mediado por CK18 una cantidad eficaz de un compuesto descrito en la presente memoria (por ejemplo, un compuesto de fórmula I, II, o III), o una de sus sales farmacéuticamente aceptables. En determinadas realizaciones, el trastorno mediado por CK18 es un trastorno neuropsiquiátrico, tal como trastorno por déficit de atención con de hiperactividad (ADHD). En determinadas realizaciones, un compuesto proporcionado estimula la neurogénesis (por ejemplo, de neuronas humanas).
En algunas realizaciones, compuestos descritos en la presente memoria muestran potencia, selectividad y/o estabilidad mejoradas sobre inhibidores de cinasa divulgados previamente (por ejemplo, GSK3, CK18). En determinadas realizaciones, un compuesto proporcionado es potente para GSK (por ejemplo, <1 |jM). En determinadas realizaciones, un compuesto proporcionado es selectivo para GSK frente a la selectividad por otras cinasas (por ejemplo, CI50 > 10 veces). En determinadas realizaciones, un compuesto proporcionado inhibe la fosforilación de Tau (por ejemplo, CI50< 10 j M). En determinadas realizaciones, un compuesto proporcionado activa la señalización de Wnt (por ejemplo, CE50 <10 j M). En determinadas realizaciones, un compuesto proporcionado es potente para CK18 (por ejemplo, <1 j M). En determinadas realizaciones, un compuesto proporcionado es selectivo para CK18 frente a la selectividad por otras cinasas (por ejemplo, CI50 >10 veces). En determinadas realizaciones, compuestos descritos en la presente memoria muestran un perfil farmacocinético mejorado, tal como penetración cerebral potenciada.
En algunas realizaciones, compuestos descritos en la presente memoria son útiles como compuestos de sonda para investigar la función de la señalización de cinasas, por ejemplo, la señalización de GSK3, en la fisiopatología de diversos trastornos, por ejemplo, trastorno bipolar y otros trastornos psiquiátricos. En determinadas realizaciones, compuestos proporcionados son útiles como compuestos de sonda para modular la neurogénesis humana.
Esta solicitud se refiere a diversas patentes expedidas, solicitudes de patente publicadas, artículos de revista y otras publicaciones.
Definiciones
Definiciones químicas
Se describen definiciones de grupos funcionales específicos y términos químicos en más detalle a continuación. Los elementos químicos se identifican de acuerdo con la Tabla Periódica de los Elementos, versión CAS, Handbook of Chemistry and Physics, 75.a Ed., cubierta interior, y los grupos funcionales específicos en general se definen como se describe en ese documento. Además, se describen principios generales de química orgánica, así como restos funcionales específicos y reactividad, en Thomas Sorrell, Organic Chemistry, University Science Books, Sausalito, 1999; Smith y March, March's Advanced Organic Chemistry, 5.a edición, John Wiley & Sons, Inc., Nueva York, 2001; Larock, Comprehensive Organic Transformations, VCH Publishers, Inc., Nueva York, 1989; y Carruthers, Some Modern Methods of Organic Synthesis, 3.a edición, Cambridge University Press, Cambridge, 1987.
Compuestos descritos en la presente memoria pueden comprender uno o más centros asimétricos y, por tanto, pueden existir en diversas formas isoméricas, por ejemplo, enantiómeros y/o diastereómeros. Por ejemplo, los compuestos descritos en la presente memoria pueden estar en forma de un enantiómero, diastereómero o isómero geométrico individual, o pueden estar en forma de una mezcla de estereoisómeros, incluyendo mezclas racémicas y mezclas enriquecidas en uno o más estereoisómeros. Los isómeros pueden aislarse de mezclas por métodos conocidos por los expertos en la materia, incluyendo cromatografía de líquidos a alta presión (HPLC) quiral y la formación y cristalización de sales quirales; o pueden prepararse isómeros preferidos mediante síntesis asimétricas.
Véase, por ejemplo, Jacques et al., Enantiomers, Racemates and Resolutions (Wiley Interscience, Nueva York,
1981); Wilen et al., Tetrahedron 33:2725 (1977); Eliel, Stereochemistry of Carbon Compounds (McGraw-Hill, NY,
1962); y Wilen, Tables of Resolving Agents and Optical Resolutions pág. 268 (E.L. Eliel, Ed., Univ. of Notre Dame
Press, Notre Dame, IN 1972). La presente divulgación abarca adicionalmente compuestos descritos en la presente memoria como isómeros individuales sustancialmente libres de otros isómeros y, como alternativa, como mezclas de diversos isómeros.
Salvo que se indique otra cosa, se entiende que las estructuras representadas en la presente memoria también incluyen compuestos que difieren únicamente en la presencia de uno o más átomos enriquecidos isotópicamente.
Por ejemplo, compuestos descritos en la presente memoria donde los compuestos están enriquecidos con deuterio, tritio, 18F, 13C y/o 14C están dentro del alcance de la divulgación. Dichos compuestos son útiles, por ejemplo, como herramientas analíticas o sondas en ensayos biológicos.
El término "alifático" incluye hidrocarburos, de cadena lineal (es decir, no ramificados), ramificados, acíclicos y cíclicos (es decir, carbocíclicos), no aromáticos, tanto saturados como insaturados. En algunas realizaciones, un grupo alifático está opcionalmente sustituido con uno o más grupos funcionales (por ejemplo, halo, tal como flúor).
Como apreciara un experto en la materia, se pretende que "alifático", en la presente memoria, incluya restos alquilo, alquenilo, alquinilo, cicloalquilo, cicloalquenilo y cicloalquinilo.
Cuando se enumera un intervalo de valores, se pretende que abarque cada valor y subintervalo dentro del intervalo.
Por ejemplo, se pretende que "alquilo C-i-a" abarque alquilo C1, C2 , C3 , C4 , C5 , Ce, C1-6, C1-5, C1-4, 5 , C2-4, C2-3, C3-6, C3-5, C3-4, C4-6, C4-5 y C5-6.
"Alquilo" se refiere a un radical de un grupo hidrocarbonado saturado de cadena lineal o ramificado que tiene de 1 a
2 0 átomos de carbono ("alquilo C1-20"). En algunas realizaciones, un grupo alquilo tiene de 1 a 10 átomos de carbono ("alquilo C1-10"). En algunas realizaciones, un grupo alquilo tiene de 1 a 9 átomos de carbono ("alquilo C1-9"). En algunas realizaciones, un grupo alquilo tiene de 1 a 8 átomos de carbono ("alquilo C1-8"). En algunas realizaciones, un grupo alquilo tiene de 1 a 7 átomos de carbono ("alquilo C1-7"). En algunas realizaciones, un grupo alquilo tiene
de 1 a 6 átomos de carbono ("alquilo C1-6"). En algunas realizaciones, un grupo alquilo tiene de 1 a 5 átomos de carbono ("alquilo C1-5"). En algunas realizaciones, un grupo alquilo tiene de 1 a 4 átomos de carbono ("alquilo C1-4").
En algunas realizaciones, un grupo alquilo tiene de 1 a 3 átomos de carbono ("alquilo C1-3"). En algunas realizaciones, un grupo alquilo tiene de 1 a 2 átomos de carbono ("alquilo C1-2"). En algunas realizaciones, un grupo
alquilo tiene 1 átomo de carbono ("alquilo C1"). En algunas realizaciones, un grupo alquilo tiene de 2 a 6 átomos de carbono ("alquilo C2-6"). Los ejemplos de grupos alquilo C1-6 incluyen metilo (C1), etilo (C2), n-propilo (C3), isopropilo
(C3), n-butilo (C4), terc-butilo (C4), sec-butilo (C4), iso-butilo (C4), n-pentilo (C5), 3-pentanilo (C5), amilo (C5), neopentilo (C5), 3-metil-2-butanilo (C5), amilo terciario (C5) y n-hexilo (C6). Ejemplos adicionales de grupos alquilo incluyen n-heptilo (C7), n-octilo (C8) y similares. Salvo que se especifique otra cosa, cada ocasión de un grupo alquilo
está independientemente sustituido opcionalmente, por ejemplo, sin sustituir (un "alquilo sin sustituir") o sustituido
(un "alquilo sustituido") con uno o más sustituyentes. En determinadas realizaciones, el grupo alquilo es alquilo C1-10 sin sustituir (por ejemplo, -CH3). En determinadas realizaciones, el grupo alquilo es alquilo C1-10 sin sustituir.
En algunas realizaciones, un grupo alquilo está sustituido con uno o más halógenos. "Perhaloalquilo" es un grupo
alquilo sustituido como se define en la presente memoria, en el que todos los átomos de hidrógeno están remplazados independientemente por un halógeno, por ejemplo, flúor, bromo, cloro o yodo. En algunas realizaciones, el resto alquilo tiene de 1 a 8 átomos de carbono ("perhaloalquilo CW). En algunas realizaciones, el resto alquilo tiene de 1 a 6 átomos de carbono ("perhaloalquilo C1-6"). En algunas realizaciones, el resto alquilo tiene
de 1 a 4 átomos de carbono ("perhaloalquilo C1-4"). En algunas realizaciones, el resto alquilo tiene de 1 a 3 átomos de carbono ("perhaloalquilo C1-3"). En algunas realizaciones, el resto alquilo tiene de 1 a 2 átomos de carbono ("perhaloalquilo C1-2"). En algunas realizaciones, todos los átomos de hidrógeno están remplazados con flúor. En algunas realizaciones, todos los átomos de hidrógeno están remplazados con cloro. Los ejemplos de grupos perhaloalquilo incluyen -CF3 , -CF2CF3 , -CF2CF2CF3 , -CCl3, -CFCh, -CF2Cl y similares.
"Alquenilo" se refiere a un radical de un grupo hidrocarbonado de cadena lineal o ramificado que tiene de 2 a 20 átomos de carbono, uno o más dobles enlaces carbono-carbono y ningún triple enlace ("alquenilo C2-20"). En algunas realizaciones, un grupo alquenilo tiene de 2 a 10 átomos de carbono ("alquenilo C2-10"). En algunas realizaciones, un grupo alquenilo tiene de 2 a 9 átomos de carbono ("alquenilo C2-9"). En algunas realizaciones, un grupo alquenilo
tiene de 2 a 8 átomos de carbono ("alquenilo C2-8"). En algunas realizaciones, un grupo alquenilo tiene de 2 a 7 átomos de carbono ("alquenilo C2-7"). En algunas realizaciones, un grupo alquenilo tiene de 2 a 6 átomos de carbono ("alquenilo C2-6"). En algunas realizaciones, un grupo alquenilo tiene de 2 a 5 átomos de carbono ("alquenilo C2-5").
En algunas realizaciones, un grupo alquenilo tiene de 2 a 4 átomos de carbono ("alquenilo C2-4"). En algunas realizaciones, un grupo alquenilo tiene de 2 a 3 átomos de carbono ("alquenilo C2-3"). En algunas realizaciones, un
grupo alquenilo tiene 2 átomos de carbono ("alquenilo C2"). El uno o más dobles enlaces carbono-carbono pueden
ser internos (tal como en 2-butenilo) o terminales (tal como en 1 -butenilo). Los ejemplos de grupos alquenilo C2-4 incluyen etenilo (C2), 1 -propenilo (C3), 2 -propenilo (C3), 1 -butenilo (C4), 2 -butenilo (C4), butadienilo (C4) y similares.
Los ejemplos de grupos alquenilo C2-6 incluyen los grupos alquenilo C2-4 mencionados anteriormente, así como pentenilo (C5), pentadienilo (C5), hexenilo (Ca) y similares. Ejemplos adicionales de alquenilo incluyen heptenilo (C7), octenilo (C8), octatrienilo (C8) y similares. Salvo que se especifique otra cosa, cada ocasión de un grupo alquenilo
está independientemente sustituido opcionalmente, por ejemplo, sin sustituir (un "alquenilo sin sustituir") o sustituido
(un "alquenilo sustituido") con uno o más sustituyentes. En determinadas realizaciones, el grupo alquenilo es alquenilo C2-10 sin sustituir. En determinadas realizaciones, el grupo alquenilo es alquenilo C2-10 sustituido.
"Alquinilo" se refiere a un radical de un grupo hidrocarbonado de cadena lineal o ramificado que tiene de 2 a 20
átomos de carbono, uno o más triples enlaces carbono-carbono y opcionalmente uno o más dobles enlaces ("alquinilo C2-20"). En algunas realizaciones, un grupo alquinilo tiene de 2 a 10 átomos de carbono ("alquinilo C2-10").
En algunas realizaciones, un grupo alquinilo tiene de 2 a 9 átomos de carbono ("alquinilo C2-9"). En algunas realizaciones, un grupo alquinilo tiene de 2 a 8 átomos de carbono ("alquinilo C2-8"). En algunas realizaciones, un
grupo alquinilo tiene de 2 a 7 átomos de carbono ("alquinilo C2-7"). En algunas realizaciones, un grupo alquinilo tiene
de 2 a 6 átomos de carbono ("alquinilo C2-a"). En algunas realizaciones, un grupo alquinilo tiene de 2 a 5 átomos de carbono ("alquinilo C2-5"). En algunas realizaciones, un grupo alquinilo tiene de 2 a 4 átomos de carbono ("alquinilo
C2-4"). En algunas realizaciones, un grupo alquinilo tiene de 2 a 3 átomos de carbono ("alquinilo C2-3"). En algunas realizaciones, un grupo alquinilo tiene 2 átomos de carbono ("alquinilo C2"). El uno o más triples enlaces carbonocarbono pueden ser internos (tal como en 2-butinilo) o terminales (tal como en 1 -butinilo). Los ejemplos de grupos alquinilo C2-4 incluyen, sin limitación, etinilo (C2), 1 -propinilo (C3), 2 -propinilo (C3), 1 -butinilo (C4), 2 -butinilo (C4) y similares. Lo ejemplos de grupos alquenilo C2-a incluyen los grupos alquinilo C2-4 mencionados anteriormente, así como pentinilo (C5), hexinilo (Ca) y similares. Ejemplos adicionales de alquinilo incluyen heptinilo (C7), octinilo (C8) y similares. Salvo que se especifique otra cosa, cada ocasión de un grupo alquinilo está independientemente sustituido opcionalmente, por ejemplo, sin sustituir (un "alquinilo sin sustituir") o sustituido (un "alquinilo sustituido")
con uno o más sustituyentes. En determinadas realizaciones, el grupo alquinilo es alquinilo C2-10 sin sustituir. En determinadas realizaciones, el grupo alquinilo es alquinilo C2-10 sustituido.
"Carbociclilo" o "carbocíclico" se refiere a un radical de un grupo hidrocarbonado cíclico no aromático que tiene de 3
a 10 átomos de carbono en el anillo ("carbociclilo C3-10") y cero heteroátomos en el sistema cíclico no aro algunas realizaciones, un grupo carbociclilo tiene de 3 a 8 átomos de carbono en el algunas realizaciones, un grupo carbociclilo tiene de 3 a 6 átomos de carbono en el algunas realizaciones, un grupo carbociclilo tiene de 3 a 6 átomos de carbono en el algunas realizaciones, un grupo carbociclilo tiene de 5 a 10 átomos de carbono en el anillo ("carbociclilo C5-10"). Los
grupos carbociclilo C3-a ejemplares incluyen, sin limitación, ciclopropilo (C3), ciclopropenilo (C3), ciclobutilo (C4), ciclobutenilo (C4), ciclopentilo (C5), ciclopentenilo (C5), ciclohexilo (Ca), ciclohexenilo (Ca), ciclohexadieni similares. Los grupos carbociclilo C3-8 ejemplares incluyen, sin limitación, los grupos carbociclilo C3-a mencionados anteriormente, así como cicloheptilo (C7), cicloheptenilo (C7), cicloheptadienilo (C7), cicloheptatrienilo (C7), ciclooctilo
(C8), ciclooctenilo (C8), biciclo[2.2.1 ]heptanilo (C7), biciclo[2.2.2 ]octanilo (C8) y similares. Los grupos carbociclilo C3-10 ejemplares incluyen, sin limitación, los grupos carbociclilo C3-8 mencionados anteriormente, así como ciclononilo
(C9), ciclononenilo (C9), ciclodecilo (C10), ciclodecenilo (C10), octahidro-1 H-indenilo (C9), decahidronaftalenilo (C10), espiro[4.5]decanilo (C10) y similares. Como los ejemplos anteriores ilustran, en determinadas realizaciones, el grupo carbociclilo es monocíclico ("carbociclilo monocíclico") o contiene un sistema cíclico condensado, unido o espiro tal como un sistema bicíclico ("carbociclilo bicíclico"). El carbociclilo puede estar saturado, y carbociclilo saturado se menciona como "cicloalquilo". En algunas realizaciones, el carbociclilo es un grupo carbociclilo saturado monocíclico
que tiene de 3 a 10 átomos de carbono en el anillo ("cicloalquilo C3-10"). En algunas realizaciones, un grupo cicloalquilo tiene de 3 a 8 átomos de carbono en el anillo ("cicloalquilo C3-8"). En algunas realizaciones, un grupo cicloalquilo tiene de 3 a a átomos de carbono en el anillo ("cicloalquilo C3-a"). En algunas realizaciones, un grupo cicloalquilo tiene de 5 a a átomos de carbono en el anillo ("cicloalquilo C5-a"). En algunas realizaciones, un grupo cicloalquilo tiene de 5 a 10 átomos de carbono en el anillo ("cicloalquilo C5-10"). Los ejemplos de grupos cicloalquilo
C5-a incluyen ciclopentilo (C5) y ciclohexilo (C5). Los ejemplos de grupos cicloalquilo C3-a incluyen los grupos cicloalquilo C5-a mencionados anteriormente, así como ciclopropilo (C3) y ciclobutilo (C4). Los ejemplos de grupos cicloalquilo C3-8 incluyen los grupos cicloalquilo C3-a mencionados anteriormente, así como cicloheptilo (C7) y ciclooctilo (C8). Salvo que se especifique otra cosa, cada ocasión de un grupo cicloalquilo está independientemente
sin sustituir (un "cicloalquilo sin sustituir") o sustituido (un "cicloalquilo sustituido") con uno o más sustituyentes. En determinadas realizaciones, el grupo cicloalquilo es cicloalquilo C3-10 sin sustituir. En determinadas realizaciones, el grupo cicloalquilo es cicloalquilo C3-10 sustituido. El carbociclilo puede estar parcialmente insaturado. El carbociclilo
que incluye uno o más dobles enlaces C=C en el anillo carbocíclico se menciona como "cicloalquenilo". El carbociclilo que incluye uno o más triples enlaces CeC en el anillo carbocíclico se menciona como "cicloalquinilo". El carbociclilo incluye arilo. "Carbociclilo" también incluye sistemas cíclicos en los que el anillo carbociclilo, como se
define anteriormente, está condensado con uno o más grupos arilo o heteroarilo, en el que el punto de adhesión está
en el anillo carbociclilo y, en dichos casos, el número de carbonos sigue indicando el número de carbonos en el
a
sistema cíclico carbocíclico. Salvo que se especifique otra cosa, cada ocasión de un grupo carbociclilo está independientemente sustituido opcionalmente, por ejemplo, sin sustituir (un "carbociclilo sin sustituir") o sustituido (un "carbociclilo sustituido") con uno o más sustituyentes. En determinadas realizaciones, el grupo carbociclilo es carbociclilo C3-10 sin sustituir. En determinadas realizaciones, el grupo carbociclilo es un carbociclilo C3-10 sustituido.
En algunas realizaciones, el carbociclilo es un grupo carbociclilo saturado monocíclico que tiene de 3 a 10 átomos de carbono en el anillo ("cicloalquilo C3-10"). En algunas realizaciones, un grupo cicloalquilo tiene de 3 a 8 átomos de carbono en el anillo ("cicloalquilo C3-8"). En algunas realizaciones, un grupo cicloalquilo tiene de 3 a 6 átomos de carbono en el anillo ("cicloalquilo C3-6"). En algunas realizaciones, un grupo cicloalquilo tiene de 5 a 6 átomos de carbono en el anillo ("cicloalquilo C5-6"). En algunas realizaciones, un grupo cicloalquilo tiene de 5 a 10 átomos de carbono en el anillo ("cicloalquilo C5-10"). Los ejemplos de grupos cicloalquilo C5-6 incluyen ciclopentilo (C5) y ciclohexilo (C5). Los ejemplos de grupos cicloalquilo C3-6 incluyen los grupos cicloalquilo C5-6 mencionados anteriormente, así como ciclopropilo (C3) y ciclobutilo (C4). Los ejemplos de grupos cicloalquilo C3-8 incluyen los grupos cicloalquilo C3-6 mencionados anteriormente, así como cicloheptilo (C7) y ciclooctilo (C8). Salvo que se especifique otra cosa, cada ocasión de un grupo cicloalquilo está independientemente sin sustituir (un "cicloalquilo sin sustituir") o sustituido (un "cicloalquilo sustituido") con uno o más sustituyentes. En determinadas realizaciones, el grupo cicloalquilo es cicloalquilo C3-10 sin sustituir. En determinadas realizaciones, el grupo cicloalquilo es cicloalquilo C3-10 sustituido.
"Heterociclilo" o "heterocíclico" se refiere a un radical de un sistema cíclico no aromático de 3 a 10 miembros que tienen átomos de carbono en el anillo y de 1 a 4 heteroátomos en el anillo, en el que cada heteroátomo se selecciona independientemente de nitrógeno, oxígeno y azufre ("heterociclilo de 3-10 miembros"). En los grupos heterociclilo que contienen uno o más átomos de nitrógeno, el punto de adhesión puede ser un átomo de carbono o nitrógeno, según permita la valencia. Un grupo heterociclilo puede ser un monocíclico ("heterociclilo monocíclico") o un sistema cíclico condensado, unido o espiro, tal como un sistema bicíclico ("heterociclilo bicíclico"), y puede estar saturado o puede estar parcialmente insaturado. Los grupos heterociclilo parcialmente insaturados incluyen heteroarilo. Los sistemas cíclicos bicíclicos heterociclilo pueden incluir uno o más heteroátomos en uno o ambos anillos. "Heterociclilo" también incluye sistemas cíclicos, en los que el anillo heterociclilo, como se define anteriormente, está condensado con uno o más grupos carbociclilo, en los que el punto de adhesión es en el anillo carbociclilo o heterociclilo, o sistemas cíclicos, en los que el anillo heterociclilo, como se define anteriormente, está condensado con uno o más grupos arilo o heteroarilo, en los que el punto de adhesión está en el anillo heterociclilo y, en dichos casos, el número de miembros en el anillo sigue indicando los miembros del anillo en el sistema cíclico heterociclilo. Salvo que se especifique otra cosa, cada ocasión de heterociclilo está independientemente sustituido opcionalmente, por ejemplo, sin sustituir (un "heterociclilo sin sustituir") o sustituido (un "heterociclilo sustituido") con uno o más sustituyentes. En determinadas realizaciones, el grupo heterociclilo es heterociclilo de 3-10 miembros sin sustituir. En determinadas realizaciones, el grupo heterociclilo es heterociclilo de 3-10 miembros sustituido.
En algunas realizaciones, un grupo heterociclilo es un sistema cíclico no aromático de 5-10 miembros que tiene átomos de carbono en el anillo y 1-4 heteroátomos en el anillo, en el que cada heteroátomo se selecciona independientemente de nitrógeno, oxígeno y azufre ("heterociclilo de 5-10 miembros"). En algunas realizaciones, un grupo heterociclilo es un sistema cíclico no aromático de 5-8 miembros que tiene átomos de carbono en el anillo y 1 4 heteroátomos en el anillo, en el que cada heteroátomo se selecciona independientemente de nitrógeno, oxígeno y azufre ("heterociclilo de 5-8 miembros"). En algunas realizaciones, un grupo heterociclilo es un sistema cíclico no aromático de 5-6 miembros que tiene átomos de carbono en el anillo y 1-4 heteroátomos en el anillo, en el que cada heteroátomo se selecciona independientemente de nitrógeno, oxígeno y azufre ("heterociclilo de 5-6 miembros"). En algunas realizaciones, el heterociclilo de 5-6 miembros tiene 1-3 heteroátomos en el anillo seleccionados de nitrógeno, oxígeno y azufre. En algunas realizaciones, el heterociclilo de 5-6 miembros tiene 1-2 heteroátomos en el anillo seleccionados de nitrógeno, oxígeno y azufre. En algunas realizaciones, el heterociclilo de 5-6 miembros tiene un heteroátomo en el anillo seleccionado de nitrógeno, oxígeno y azufre.
Los grupos heterociclilo de 3 miembros ejemplares que contienen un heteroátomo incluyen, sin limitación, azirdinilo, oxiranilo, tiorenilo. Los grupos heterociclilo de 4 miembros ejemplares que contienen un heteroátomo incluyen, sin limitación, azetidinilo, oxetanilo y tietanilo. Los grupos heterociclilo de 5 miembros ejemplares que contienen un heteroátomo incluyen, sin limitación, tetrahidrofuranoílo, dihidrofuranilo, tetrahidrotiofenilo, dihidrotiofenilo, pirrolidinilo, dihidropirrolilo y pirrolil-2,5-diona. Los grupos heterociclilo de 5 miembros ejemplares que contienen dos heteroátomos incluyen, sin limitación, dioxolanilo, oxasulfuranilo, disulfuranilo y oxazolidin-2-ona. Los grupos heterociclilo de 5 miembros ejemplares que contienen tres heteroátomos incluyen, sin limitación, triazolinilo, oxadiazolinilo y tiadiazolinilo. Los grupos heterociclilo de 6 miembros ejemplares que contienen un heteroátomo incluyen, sin limitación, piperidinilo, tetrahidropiranilo, dihidropiridinilo y tianilo. Los grupos heterociclilo de 6 miembros ejemplares que contienen dos heteroátomos incluyen, sin limitación, piperazinilo, morfolinilo, ditianilo y dioxanilo. Los grupos heterociclilo de 6 miembros ejemplares que contienen dos heteroátomos incluyen, sin limitación, triazinanilo. Los grupos heterociclilo de 7 miembros ejemplares que contienen un heteroátomo incluyen, sin limitación, azepanilo, oxepanilo y tiepanilo. Los grupos heterociclilo de 8 miembros ejemplares que contienen un heteroátomo incluyen, sin limitación, azocanilo, oxecanilo y tiocanilo. Los grupos heterociclilo de 5 miembros ejemplares condensados a un anillo arilo C6 (también mencionado en la presente memoria como un anillo heterocíclico 5,6-bicíclico) incluyen, sin limitación, indolinilo, isoindolinilo, dihidrobenzofuranilo, dihidrobenzotienilo,
benzoxazolinonilo y similares. Los grupos heterociclilo de 6 miembros ejemplares condensados a un anillo arilo (también mencionado en la presente memoria como un anillo heterocíclico 6 ,6 -bicíclico) incluyen, sin limitación, tetrahidroquinolinilo, tetrahidroisoquinolinilo y similares.
"Arilo" se refiere a un radical de un sistema cíclico aromático monocíclico o policíclico (por ejemplo, bicíclico o tricíclico) 4n+2 (por ejemplo, que tiene 6 , 10 o 14 electrones n compartidos en una matriz cíclica) que tiene 6-14 átomos de carbono en el anillo y cero heteroátomos proporcionados en el sistema cíclico aromático ("arilo C6-14"). En algunas realizaciones, un grupo arilo tienen seis átomos de carbono en el anillo ("arilo C6"; por ejemplo, fenilo). En algunas realizaciones, un grupo arilo tiene diez átomos de carbono en el anillo ("arilo C10"; por ejemplo, naftilo tal como 1-naftilo y 2-naftilo). En algunas realizaciones, un grupo arilo tiene catorce átomos de carbono en el anillo ("arilo C14"; por ejemplo, antracilo). "Arilo" también incluye sistemas cíclicos en los que el anillo arilo, como se define anteriormente, está condensado con uno o más grupos carbociclilo o heterociclilo, en los que el radical o punto de adhesión está en el anillo arilo y, en dichos casos, el número de átomos de carbono sigue indicando el número de átomos de carbono en el sistema cíclico arilo. Salvo que se especifique otra cosa, cada ocasión de un grupo arilo está independientemente sustituido opcionalmente, por ejemplo, sin sustituir (un "arilo sin sustituir") o sustituido (un "arilo sustituido") con uno o más sustituyentes. En determinadas realizaciones, el grupo arilo es arilo C6-14 sin sustituir. En determinadas realizaciones, el grupo arilo es arilo C6-14 sustituido.
"Heteroarilo" se refiere a un radical de un sistema cíclico aromático monocíclico o bicíclico de 5-10 miembros 4n+2 (por ejemplo, que tiene 6 o 10 electrones n compartidos en una matriz cíclica) que tiene átomos de carbono en el anillo y 1-4 heteroátomos en el anillo proporcionados en el sistema cíclico aromático, en el que cada heteroátomo se selecciona independientemente de nitrógeno, oxígeno y azufre ("heteroarilo de 5-10 miembros"). En los grupos heteroarilo que contienen uno o más átomos de nitrógeno, el punto de adhesión puede ser un átomo de carbono o nitrógeno, según permita la valencia. Los sistemas cíclicos bicíclicos heteroarilo pueden incluir uno o más heteroátomos en uno o ambos anillos. "Heteroarilo" incluye sistemas cíclicos en los que el anillo heteroarilo, como se define anteriormente, está condensado con uno o más grupos carbociclilo o heterociclilo, en los que el punto de adhesión está en el anillo heteroarilo y, en dichos casos, el número de miembros en el anillo sigue indicando el número de miembros en el anillo en el sistema cíclico heteroarilo. "Heteroarilo" también incluye sistemas cíclicos en los que el anillo heteroarilo, como se define anteriormente, está condensado con uno o más grupos arilo, en el que el punto de adhesión está en el anillo arilo o heteroarilo y, en dichos casos, el número de miembros en el anillo indica el número de miembros en el anillo en el sistema cíclico condensado (arilo/heteroarilo). En grupos heteroarilo bicíclicos en los que un anillo no contiene un heteroátomo (por ejemplo, indolilo, quinolinilo, carbazolilo y similares), el punto de adhesión puede estar en cualquier anillo, por ejemplo, el anillo que alberga un heteroátomo (por ejemplo, 2-indolilo) o el anillo que no contiene un heteroátomo (por ejemplo, 5-indolilo).
En algunas realizaciones, un grupo heteroarilo es un sistema cíclico aromático de 5-10 miembros que tiene átomos de carbono en el anillo y 1-4 heteroátomos en el anillo proporcionados en el sistema cíclico aromático, en el que cada heteroátomo se selecciona independientemente de nitrógeno, oxígeno y azufre ("heteroarilo de 5-10 miembros"). En algunas realizaciones, un grupo heteroarilo es un sistema cíclico aromático de 5-8 miembros que tiene átomos de carbono en el anillo y 1-4 heteroátomos en el anillo proporcionados en el sistema cíclico aromático, en el que cada heteroátomo se selecciona independientemente de nitrógeno, oxígeno y azufre ("heteroarilo de 5-8 miembros"). En algunas realizaciones, un grupo heteroarilo es un sistema cíclico aromático de 5-6 miembros que tiene átomos de carbono en el anillo y 1-4 heteroátomos en el anillo proporcionados en el sistema cíclico aromático, en el que cada heteroátomo se selecciona independientemente de nitrógeno, oxígeno y azufre ("heteroarilo de 5-6 miembros"). En algunas realizaciones, el heteroarilo de 5-6 miembros tiene 1-3 heteroátomos en el anillo seleccionados de nitrógeno, oxígeno y azufre. En algunas realizaciones, el heteroarilo de 5-6 miembros tiene 1-2 heteroátomos en el anillo seleccionados de nitrógeno, oxígeno y azufre. En algunas realizaciones, el heteroarilo de 5-6 miembros tiene 1 heteroátomo en el anillo seleccionado de nitrógeno, oxígeno y azufre. Salvo que se especifique otra cosa, cada ocasión de un grupo heteroarilo está independientemente sustituido opcionalmente, por ejemplo, sin sustituir ("heteroarilo sin sustituir") o sustituido ("heteroarilo sustituido") con uno o más sustituyentes. En determinadas realizaciones, el grupo heteroarilo es heteroarilo de 5-14 miembros sin sustituir. En determinadas realizaciones, el grupo heteroarilo es heteroarilo de 5-14 miembros sustituido.
Los grupos heteroarilo de 5 miembros ejemplares que contienen un heteroátomo incluyen, sin limitación, pirrolilo, furanilo y tiofenilo. Los grupos heteroarilo de 5 miembros ejemplares que contienen dos heteroátomos incluyen, sin limitación, imidazolilo, pirazolilo, oxazolilo, isoxazolilo, tiazolilo e isotiazolilo. Los grupos heteroarilo de 5 miembros ejemplares que contienen tres heteroátomos incluyen, sin limitación, triazolilo, oxadiazolilo y tiadiazolilo. Los grupos heteroarilo de 5 miembros ejemplares que contienen cuatro heteroátomos incluyen, sin limitación, tetrazolilo. Los grupos heteroarilo de 6 miembros ejemplares que contienen un heteroátomo incluyen, sin limitación, piridinilo. Los grupos heteroarilo de 6 miembros ejemplares que contienen dos heteroátomos incluyen, sin limitación, piridazinilo, pirimidinilo y pirazinilo. Los grupos heteroarilo de 6 miembros ejemplares que contienen tres o cuatro heteroátomos incluyen, sin limitación, triazinilo y tetrazinilo, respectivamente. Los grupos heteroarilo de 7 miembros ejemplares que contienen un heteroátomo incluyen, sin limitación, azepinilo, oxepinilo y tiepinilo. Los grupos heteroarilo 5,6-bicíclicos ejemplares incluyen, sin limitación, indolilo, isoindolilo, indazolilo, benzotriazolilo, benzotiofenilo, isobenzotiofenilo, benzofuranilo, benzoisofuranilo, bencimidazolilo, benzoxazolilo, bencisoxazolilo, benzoxadiazolilo, benztiazolilo, bencisotiazolilo, benztiadiazolilo, indolizinilo y purinilo. Los grupos heteroarilo 6 ,6 -bicíclicos ejemplares incluyen, sin
limitación, naftiridinilo, pteridinilo, quinolinilo, isoquinolinilo, cinnolinilo, quinoxalinilo, ftalazinilo y quinazolinilo.
"Parcialmente insaturado" se refiere a un grupo que incluye al menos un doble o triple enlace. Se pretende que la expresión "parcialmente insaturado" abarque anillos que tienen múltiples sitios de insaturación, pero no se pretende que incluya grupos aromáticos (por ejemplo, grupos arilo o heteroarilo) como se define en la presente memoria. Asimismo, "saturado" se refiere a un grupo que no contiene un doble o triple enlace, es decir, contiene todos enlaces sencillos.
En algunas realizaciones, los grupos alifático, alquilo, alquenilo, alquinilo, carbociclilo, heterociclilo, arilo y heteroarilo, como se definen en la presente memoria, están opcionalmente sustituidos (por ejemplo, grupo alquilo "sustituido" o "sin sustituir", alquenilo "sustituido" o "sin sustituir", alquinilo "sustituido" o "sin sustituir", carbociclilo "sustituido" o "sin sustituir", heterociclilo "sustituido" o "sin sustituir", arilo "sustituido" o "sin sustituir" o heteroarilo "sustituido" o "sin sustituir"). En general, el término "sustituido", ya sea precedido por el término "opcionalmente" o no, significa que al menos un hidrógeno presente en un grupo (por ejemplo, un átomo de carbono o nitrógeno) está remplazado con un sustituyente permisible, por ejemplo, un sustituyente que, tras la sustitución, produce un compuesto estable, por ejemplo, un compuesto que no experimenta espontáneamente transformación, tal como por reordenamiento, ciclación, eliminación u otra reacción. Salvo que se indique otra cosa, un grupo "sustituido" tiene un sustituyente en una o más posiciones sustituibles del grupo y, cuando se sustituye más de una posición en cualquier estructura dada, el sustituyente es igual o diferente en cada posición. Se contempla que el término "sustituido" incluye sustitución con todos los sustituyentes permisibles de compuestos orgánicos, cualquiera de los sustituyentes descritos en la presente memoria que provoque la formación de un compuesto estable. La presente divulgación contempla todas y cada una de estas combinaciones para llegar a un compuesto estable. Para los fines de esta divulgación, los heteroátomos tales como nitrógeno pueden tener sustituyentes de hidrógeno y/o cualquier sustituyente adecuado como se describe en la presente memoria que satisfaga las valencias de los heteroátomos y provoque la formación de un resto estable.
Los sustituyentes de átomo de carbono ejemplares incluyen, aunque sin limitación, halógeno, -CN, -NO2, -N3 , -SO2H, -SO3H, -OH, -ORaa, -ON(Rbb)2 , -N(Rbb)2, -N(Rbb)3+X", -N(ORcc)Rbb, -SH, -SRaa, -SSRcc, -C(=O)Raa, -CO2H, -CHO, -C(ORcc)2 , -CO2Ra -OC(=O)Raa OCO2Raa, -C(=O)N(Rbb)2, -OC(=O)N(Rbbbb)2 NRbbC(=O)Raa, -NRbbCO2Raa, NR ’bbC ^ O(=O ) N)N (( RRbb) '2, -C(=NRbb)R -C(=NRbb)OR -OC(=NRbb)Raa, -OC(=NRbb)ORaa, -C(=NRbb)N(Rbb)2, OC(=NRbb)N(Rbb)2, -NRbbC(=NRbb)N(Rbb)2 C(=O)NRbbSO2Raa, -NRbbSO2Raa, -SO2N(Rbb)2, -SO2Raa, -SO2ORaa, OSO2Raa, -S(=O)R -OS(=O)R aaaa, -Si(Raa)3, -OSi(R aaaa)3, -C(=S)N(R bbbb)2, -C(=O)SR aaaa, -C(=S)SR aaaa, -SC(=S)SR aa SC(=O)SRaa, -OC(=O)SRaa, -SC(=O)ORaa, -SC(=O)Raa, -P(=O)2Raa, -OP(=O)2Raa, -P(=O)(Raa)2, -OP(=O)(Raa)2, -OP(=O)(ORcc)2, -P(=O)2N(Rbb)2, -OP(=O)2N(Rbb)2, -P(=O)(NRbb)2, -OP(=O)(NRbb)2, -NRbbP(=O)(ORcc)2, -NRbbP(=O)(NRbb)2, -P(Rcc)2, -P(Rcc)3, -OP(Rcc)2, -OP(Rcc)3, -B(Raa)2, -B(ORcc)2, -BRaa(ORcc), alquilo C1.10, perhaloalquilo C1-10, alquenilo C2-10, alquinilo C2-10, carbociclilo C3-10, heterociclilo de 3-14 miembros, arilo C6-14 y heteroarilo de 5-14 miembros, en los que cada alquilo, alquenilo, alquinilo, carbociclilo, heterociclilo, arilo y heteroarilo está sustituido independientemente con 0, 1, 2, 3, 4 o 5 grupos Rdd;
o dos hidrógenos geminales en un átomo de carbono se remplazan con el grupo =O, =S, =NN(Rbb)2, =NNRbbC(=O)Raa, =NNRbbC(=O)ORaa, =NNRbbS(=O)2Raa, =NRbb o =NORcc;
cada ocasión de Raa se selecciona, independientemente, de alquilo C1-10, perhaloalquilo C1-10, alquenilo C2-10, alquinilo C2-10, carbociclilo C3-10, heterociclilo de 3-14 miembros, arilo C6-14 y heteroarilo de 5-14 miembros, o dos grupos Raa se unen para formar un heterociclilo de 3-14 miembros o anillo heteroarilo de 5-14 miembros, en los que cada alquilo, alquenilo, alquinilo, carbociclilo, heterociclilo, arilo y heteroarilo está sustituido independientemente con 0, 1, 2, 3, 4 o 5 grupos Rdd;
cada ocasión de Rbb se selecciona, independientemente, de hidrógeno, -OH, -ORaa, -N(Rcc)2 , -CN, -C(=O)Raa, -C(=O)N(Rcc)2, -CO2Raa, -SO2Raa, -C(=NRcc)ORaa, -C(=NRcc)N(Rcc)2, -SO2N(Rcc)2, -SO2Rcc, -SO2ORcc, -SORaa, -C(=S)N(Rcc)2, -C(=O)SRcc, -C(=S)SRcc, -P(=O)2Raa, -P(=O)(Raa)2 , -P(=O)2N(Rcc)2 , -P(=O)(NRcc)2, alquilo C1-10, perhaloalquilo C1-10, alquenilo C2-10, alquinilo C2-10, carbociclilo C3-10, heterociclilo de 3-14 miembros, arilo C6-14 y heteroarilo de 5-14 miembros, o dos grupos Rbb se unen para formar un heterociclilo de 3-14 miembros o anillo heteroarilo de 5-14 miembros, en los que cada alquilo, alquenilo, alquinilo, carbociclilo, heterociclilo, arilo y heteroarilo está sustituido independientemente con 0, 1, 2, 3, 4 o 5 grupos Rdd;
cada ocasión de Rcc se selecciona, independientemente, de hidrógeno, alquilo C1-10, perhaloalquilo C1-10, alquenilo C2-10, alquinilo C2-10, carbociclilo C3-10, heterociclilo de 3-14 miembros, arilo C6-14 y heteroarilo de 5-14 miembros, o dos grupos Rcc se unen para formar un heterociclilo de 3-14 miembros o anillo heteroarilo de 5-14 miembros, en los que cada alquilo, alquenilo, alquinilo, carbociclilo, heterociclilo, arilo y heteroarilo está sustituido independientemente con 0, 1, 2, 3, 4 o 5 grupos Rdd;
cada ocasión de Rd se selecciona, independientemente, de halógeno, -CN, -NO2, -N3, -SO2H, -SO3H, -OH, -OR1 ee ON(Rff)2, -N(Rff)2, -N( /oR" f)f\3+ \ >X/~-, -N ni//**\r~(ORe >hhe)\r~R"ff, -S oH 11, -SRHH, -SSRHH, -C(=O)R' CO2H n, -CO2Ree, -OC(=O)Ree, -OCO2 OR 1ee C(=O)N(Rff)2, -OC(=O)N(Rf )2, NRffC(=O)Ree, -NRTTCO2Re -NRffC(=O)N(Rff)2, -C(=NRff)ORee, -OC(=NRff)Ree, OC(=NRff)ORee, -C(=NRff)N(Rff)2, OC(=NR")N(R")2, -NR"C(=NRff)N(Rff)2, -NRffSO2Ree, -SO2N(Rtt)2, -SO2Ree,
SO2ORee, -OSO2Ree, -S(=O)Ree, -Si(Ree)a, -OSi(Ree)a, -C(=S)N(Rff)2, -C(=O)SRee, -C(=S)SRee, -SC(=S)SRee, -P(=O)2Ree, -P(=O)(Ree)2 , -OP(=O)(Ree)2, -OP(=O)(ORee)2 , alquilo Ci-6, perhaloalquilo Ci-6, alquenilo C2-6, alquinilo C2-6, carbociclilo C3-10, heterociclilo de 3-10 miembros, arilo C6-10, heteroarilo de 5-10 miembros, en los que cada alquilo, alquenilo, alquinilo, carbociclilo, heterociclilo, arilo y heteroarilo está sustituido independientemente con 0, 1, 2, 3, 4 o 5 grupos Rgg, o dos sustituyentes Rdd geminales pueden unirse para formar =O o =S;
cada ocasión de Ree se selecciona, independientemente, de alquilo C1-6, perhaloalquilo C1-6, alquenilo C2-6, alquinilo C2-6, carbociclilo C3-10, arilo C6-10, heterociclilo de 3-10 miembros y heteroarilo de 3-10 miembros, en los que cada alquilo, alquenilo, alquinilo, carbociclilo, heterociclilo, arilo y heteroarilo está sustituido independientemente con 0, 1, 2, 3, 4 o 5 grupos Rgg;
cada ocasión de Rff se selecciona, independientemente, de hidrógeno, alquilo C1-6, perhaloalquilo C1-6, alquenilo C2-6, alquinilo C2-6, carbociclilo C3-10, heterociclilo de 3-10 miembros, arilo C6-10 y heteroarilo de 5-10 miembros, o dos grupos Rff se unen para formar un heterociclilo de 3-14 miembros o anillos heteroarilo de 5-14 miembros, en los que cada alquilo, alquenilo, alquinilo, carbociclilo, heterociclilo, arilo y heteroarilo está sustituido independientemente con 0, 1, 2, 3, 4 o 5 grupos Rgg; y
cada ocasión de Rgg es, independientemente, halógeno, -CN, -NO2, -N3, -SO2H, -SO3H, -OH, -Oalquilo C1-6, -ON(alquilo C ^ , -N(alquilo C ^ , -N(alquilo C^b+X', -NH(alquilo C^k+X', -NH2(alquilo C ^+ X ', -NH3+X', -N(Oalquil C1-6)(alquilo C1-6), -N(OH)(alquilo C1-6), -NH(OH), -SH, -Salquilo C1-6, -SS(alquilo C1-6), -C(=O)(alquilo C1-6), -CO2H, -CO2(alquilo C1.6), -OC(=O)(alquilo C1.6), -OCO2(alquilo C1.6), -C(=O)NH2 , -C(=O)N(alquilo C1-6)2,-OC(=O)NH(alquilo C1-6), -NHC(=O)(alquilo C1-6), -N(alquil C1-6)C(=O)(alquilo C1-6), -NHCO2(alquilo C1-6), -NHC(=O)N(alquilo C1-6)2, -NHC(=O)NH(alquilo C1.6), -NHC(=O)NH2, -C(=NH)O(alquilo C1-6),-OC(=NH)(alquilo C1.6), -OC(=NH)Oalquilo C1.6, -C(=NH)N(alquilo C1-6)2 , -C(=NH)NH(alquilo C1-6), -C(=NH)NH2 , -OC(=NH)N(alquilo C1-6)2, -OC(NH)NH(alquilo C1-6), -OC(NH)NH2 , -NHC(NH)N(alquilo C1-6)2, -NHC(=NH)NH2, -NHSO2(alquilo C1-6),-SO2N(alquilo C1-6)2, -SO2NH(alquilo C1.6), -SO2NH2, -SO2alquilo C1-6, -SO2Oalquilo C1.6, -OSO2alquilo C1-6, -SOalquilo C1.6, -Si(alquilo C1-6)3, -OSi(alquilo C1-6)3 -C(=S)N(alquilo C1-6)2 , C(=S)NH(alquilo C1-6), C(=S)NH2 , -C(=O)S(alquilo C1-6), -C(=S)Salquilo C1-6, -SC(=S)Salquilo C1.6, -P(=O)2(alquilo C1.6), -P(=O)(alquilo C1-6)2 , -OP(=O)(alquilo C1-6)2, -OP(=O)(Oalquilo C1-6)2 , alquilo C1.6, perhaloalquilo C1.6, alquenilo C2-6, alquinilo C2-6, carbociclilo C3-10, arilo C6-10, heterociclilo de 3-10 miembros, heteroarilo de 5-10 miembros; o dos sustituyentes Rgg geminales pueden unirse para formar =O o =S; en los que X- es un contraión.
Un "contraión" o "contraión aniónico" es un grupo cargado negativamente asociado con un grupo amino cuaternario catiónico para mantener la neutralidad electrónica. Los contraiones ejemplares incluyen iones de haluro (por ejemplo, F-, Cl-, Br-, I-), NO3", OO 4", OH-, H2PO4", HSO4", iones sulfonato (por ejemplo, metanosulfonato, trifluorometanosulfonato, p-toluenosulfonato, bencenosulfonato, 10-alcanforsulfonato, naftaleno-2-sulfonato, ácido naftaleno-1-sulfónico-5-sulfonato, ácido etan-1-sulfónico-2-sulfonato y similares), e iones carboxilato (por ejemplo, acetato, etanoato, propanoato, benzoato, glicerato, lactato, tartrato, glicolato y similares).
"Halo" o "halógeno" se refiere a flúor (fluoro, -F), cloro (cloro, -Cl), bromo (bromo, -Br), o yodo (yodo, -I).
Los átomos de nitrógeno pueden estar sustituidos o sin sustituir según permita la valencia, e incluyen átomos de nitrógeno primarios, secundarios, terciarios y cuaternarios. Los sustituyentes de átomo de nitrógeno ejemplares incluyen, aunque sin limitación, hidrógeno, -OH, -ORaa, -N(Rcc)2 , -CN,-C(=O)Raa, -C(=O)N(Rcc)2, -CO2Raa, -SO2Raa, -C(=NRbb)Raa, -C(=NRcc)ORaa, -C(=NRcc)N(Rcc)2, -SO2N(Rcc)2, -SO2Rcc, -SO2ORcc, -SORaa, -C(=S)N(Rcc)2, -C(=O)SRee, -C(=S)SRcc, -P(=O)2Raa, -P(=O)(Raa)2, -P(=O)2N(Rcc)2, -P(=O)(NRcc)2 , alquilo C1-10, perhaloalquilo C1-10, alquenilo C2-10, alquinilo C2-10, carbociclilo C3-10, heterociclilo de 3-14 miembros, arilo C6-14 y heteroarilo de 5-14 miembros o dos grupos Rcc adheridos a un átomo de nitrógeno se unen para formar un heterociclilo de 3-14 miembros o anillo heteroarilo de 5-14 miembros, en los que cada alquilo, alquenilo, alquinilo, carbociclilo, heterociclilo arilo y heteroarilo está sustituido independientemente con 0, 1, 2, 3, 4 o 5 grupos R y en los que R Rbb, Rcc y Rdd son como se definen anteriormente.
En determinadas realizaciones, el sustituyente presente en un átomo de nitrógeno es un grupo protector de nitrógeno (también mencionado como un grupo protector de amino). Los grupos protectores de nitrógeno incluyen, aunque sin limitación, -OH, -ORaa, -N(Rcc)2, -C(=O)Raa, -C(=O)N(Rcc)2, -CO2Raa, -SO2Raa, -C(=NRcc)Raa, -C(=NRcc)ORaa, -C(=NRcc)N(Rcc)2, -SO2N(Rcc)2, -SO2Rcc, -SO2ORcc, -SORaa, -C(=S)N(Rcc)2, -C(=O)SRee, -C(=S)SRcc, alquilo C1-10 (por ejemplo, aralquilo, heteroaralquilo), alquenilo C2-10, alquinilo C2-10, carbociclilo C3-10, heterociclilo de 3-14 miembros, arilo C6-14 y grupos heteroarilo de 5-14 miembros, en los que cada alquilo, alquenilo, alquinilo, carbociclilo, heterociclilo, aralquilo, arilo y heteroarilo está sustituido independientemente con 0, 1, 2, 3, 4 o 5 grupos Rdd, y en los que Raa Rbb, Rcc y Rdd son como se definen en la presente memoria. Los grupos protectores de nitrógeno son bien conocidos en la técnica e incluyen los descritos en detalle en Protecting Groups in Organic Synthesis, T. W. Greene y P. G. M. Wuts, 3.a edición, John Wiley & Sons, 1999.
Los grupos protectores de nitrógeno de amida (por ejemplo, -C(=O)Raa) incluyen, aunque sin limitación, formamida, acetamida, cloroacetamida, tricloroacetamida, trifluoroacetamida, fenilacetamida, 3-fenilpropanamida, picolinamida, 3-piridilcarboxamida, derivado de /V-benzoilfenilalanilo, benzamida, p-fenilbenzamida, o-nitrofenilacetamida, o-nitrofenoxiacetamida, acetoacetamida, (N'-ditiobenciloxiacilamino)acetamida, 3-(p-hidroxifenil)propanamida, 3-(onitrofenil)propanamida, 2-metil-2-(o-nitrofenoxi)propanamida, 2-metil-2-(o-fenilazofenoxi)propanamida, 4-clorobutanamida, 3-metil-3-nitrobutanamida, o-nitrocinamida, N-acetilmetionina, o-nitrobenzamida y o-(benzoiloximetil)benzamida.
Los grupos protectores de nitrógeno de carbamato (por ejemplo, -C(=O)ORaa) incluyen, aunque sin limitación, metil carbamato, etil carbamato, 9-fluorenilmetil carbamato (Fmoc), 9-(2-sulfo)fluorenilmetil carbamato, 9-(2,7-dibromo)fluoroenilmetil carbamato, 2,7-di-f-butil-[9-(10,10-dioxo-10,10,10,10-tetrahidrotioxanthil)]metil carbamato (DBD-Tmoc), 4-metoxifenacil carbamato (Phenoc), 2,2,2-tricloroetil carbamato (Troc), 2-trimetilsililetil carbamato (Teoc), 2-feniletil carbamato (hZ), 1-(1-adamantil)-1-metiletil carbamato (Adpoc), 1,1 -dimetil-2-haloetil carbamato, 1,1 -dimetil-2,2-dibromoetil carbamato (DB-f-BOc), 1,1-dimetil-2,2,2-tricloroetil carbamato (TCBOC), 1 -metil-1 -(4-bifenilil)etil carbamato (Bpoc), 1 -(3,5-di-f-butilfenil)-1 -metiletil carbamato (f-Bumeoc), 2-(2'- y 4'-piridil)etil carbamato (Pyoc), 2-(N,N-diciclohexilcarboxamido)etil carbamato, f-butil carbamato (BOC), 1-adamantil carbamato (Adoc), vinil carbamato (Voc), alil carbamato (Alloc), 1-isopropilalil carbamato (Ipaoc), cinamil carbamato (Coc), 4-nitrocinamil carbamato (Noc), 8-quinolil carbamato, N-hidroxipiperidinil carbamato, alquilditio carbamato, bencil carbamato (Cbz), p-metoxibencil carbamato (Moz), p-nitobencil carbamato, p-bromobencil carbamato, p-clorobencil carbamato, 2,4-diclorobencil carbamato, 4-metilsulfinilbencil carbamato (Msz), 9-antrilmetil carbamato, difenilmetil carbamato, 2-metiltioetil carbamato, 2-metilsulfoniletil carbamato, 2-(p-toluenosulfonil)etil carbamato, [2-(1,3-ditianil)]metil carbamato (Dmoc), 4-metiltiofenil carbamato (Mtpc), 2,4-dimetiltiofenil carbamato (Bmpc), 2-fosfonioetil carbamato (Peoc), 2-trifenilfosfonioisopropil carbamato (Ppoc), 1,1-dimetil-2-cianoetil carbamato, m-cloro-p-aciloxibencil carbamato, p-(dihidroxiboril)bencil carbamato, 5-bencisoxazolilmetil carbamato, 2-(trifluorometil)-6-cromonilmetil carbamato (Tcroc), m-nitrofenil carbamato, 3,5-dimetoxibencil carbamato, o-nitrobencil carbamato, 3,4-dimetoxi-6-nitrobencil carbamato, fenil(o-nitrofenil)metil carbamato, f-amil carbamato, S-bencil tiocarbamato, p-cianobencil carbamato, ciclobutil carbamato, ciclohexil carbamato, ciclopentil carbamato, ciclopropilmetil carbamato, p-deciloxibencil carbamato, 2,2-dimetoxiacilvinil carbamato, o-(N,N-dimetilcarboxamido)bencil carbamato, 1,1 -dimetil-3-(N,N-dimetilcarboxamido)propil carbamato, 1,1-dimetilpropinil carbamato, di(2-piridil)metil carbamato, 2-furanilmetil carbamato, 2-yodoetil carbamato, isobornil carbamato, isobutil carbamato, isonicotinil carbamato, p-(p '-metoxifenilazo)bencil carbamato, 1 -metilciclobutil carbamato, 1-metilciclohexil carbamato, 1 -metil-1 -ciclopropilmetil carbamato, 1-metil-1-(3,5-dimetoxifenil)etil carbamato, 1-metil-1-(p-fenilazofenil)etil carbamato, 1 -metil-1-feniletil carbamato, 1-metil-1-(4-piridil)etil carbamato, fenil carbamato, p-(fenilazo)bencil carbamato, 2,4,6-tri-f-butilfenil carbamato, 4-(trimetilamonio)bencil carbamato y 2,4,6-trimetilbencil carbamato.
Los grupos protectores de nitrógeno de sulfonamida (por ejemplo, -S(=O)2Raa) incluyen, aunque sin limitación, ptoluenosulfonamida (Ts), bencenosulfonamida, 2,3,6,-trimetil-4-metoxibencenosulfonamida (Mtr), 2,4,6-trimetoxibencenosulfonamida (Mtb), 2,6-dimetil-4-metoxibencenosulfonamida (Pme), 2,3,5,6-tetrametil-4-metoxibencenosulfonamida (Mte), 4-metoxibencenosulfonamida (Mbs), 2,4,6-trimetilbencenosulfonamida (Mts), 2,6-dimetoxi-4-metilbencenosulfonamida (iMds), 2,2,5,7,8-pentametilcroman-6-sulfonamida (Pmc), metanosulfonamida (Ms), p-trimetilsililetanosulfonamida (SES), 9-antracenosulfonamida, 4-(4',8'-dimetoxinaftilmetil)bencenosulfonamida (DNMBS), bencilsulfonamida, trifluorometilsulfonamida y fenacilsulfonamida.
Otros grupos protectores de nitrógeno incluyen, aunque sin limitación, derivado de fenotiazinil-(10)-acilo, derivado de N'-p-toluenosulfonilaminoacilo, derivado de N'-fenilaminotioacilo, derivado de N-benzoilfenilalanilo, derivado de N-acetilmetionina, 4,5-difenil-3-oxazolin-2-ona, N-ftalimida, N-ditiasuccinimida (Dts), N-2,3-difenilmaleimida, N-2,5-dimetilpirrol, aducto N-1,1,4,4-tetrametildisililazaciclopentano (STABASE), 1,3-dimetil-1,3,5-triazaciclohexan-2-ona 5-sustituida, 1,3-dibencil-1,3,5-triazaciclohexan-2-ona 5-sustituida, 3,5-dinitro-4-piridona 1 -sustituida, N-metilamina, N-alilamina, N-[2-(trimetilsilil)etoxi]metilamina (SEM), N-3-acetoxipropilamina, N-(1-isopropil-4-nitro-2-oxo-3-pirrolin-3-il)amina, sales de amonio cuaternario, N-bencilamina, N-di(4-metoxifenil)metilamina, N-5-dibenzosuberilamina, N-trifenilmetilamina (Tr), N-[(4-metoxifenil)difenilmetil]amina (MMTr), N-9-fenilfluorenilamina (PhF), N-2,7-dicloro-9-fluorenilmetilenamina, N-ferrocenilmetilamino (Fcm), N'-óxido de N-2-picolilamino, N-1,1-dimetiltiometilenamina, N-bencilidenamina, N-p-metoxibencilidenamina, N-difenilmetilenamina, N-[(2-piridil)mesitil]metilenamina, N-(N',N'-dimetilaminometilen)amina, N,N'-isopropilidendiamina, N-p-nitrobencilidenamina, N-salicilidenamina, N-5-clorosalicilidenamina, N-(5-cloro-2-hidroxifenil)fenilmetilenamina, N-ciclohexilidenamina, N-(5,5-dimetil-3-oxo-1-ciclohexenil)amina, derivado de N-borano, derivado de ácido N-difenilborínico, N-[fenil(pentaacilcromo- o tungsteno)acil]amina, quelato de N-cobre, quelato de N-cinc, N-nitroamina, N-nitrosoamina, N-óxido de amina, difenilfosfinamida (Dpp), dimetiltiofosfinamida (Mpt), difeniltiofosfinamida (Ppt), dialquil fosforamidatos, dibencil fosforamidato, difenil fosforamidato, bencenosulfenamida, o-nitrobencenosulfenamida (Nps), 2,4-dinitrobencenosulfenamida, pentaclorobencenosulfenamida, 2-nitro-4-metoxibencenosulfenamida, trifenilmetilsulfenamida y 3-nitropiridinsulfenamida (Npys).
En determinadas realizaciones, el sustituyente presente en un átomo de oxígeno es un grupo protector de oxígeno (también mencionado como un grupo protector de hidroxilo). Los grupos protectores de oxígeno incluyen, aunque sin limitación, -Raa, -N(Rbb)2, -C(=O)SRaa, -C(=O)Raa, -CO2Raa, -C(=O)N(Rbb)2, -C(=NRb1b)Raa, -C(=NRbb)ORaa, -C(=NRbb)N(Rbb)2 -S(=O)Ra SO2R -Si(Raa)3, -P(Rcc)2, -P(R)3, -P(=O)2R -P(=O)(Raa)2, -P(=O)(ORcc)2, -P(=O)2N(Rbb)2 y -P(=O)(NRbb)2 ; en los que Raa, Rbb y Rcc son como se definen en la presente memoria. Los grupos protectores de oxígeno son bien conocidos en la técnica e incluyen los descritos en detalle en Protecting Groups in Organic Synthesis, T. W. Greene y P. G. M. Wuts, 3.a edición, John Wiley & Sons, 1999.
Los grupos protectores de oxígeno ejemplares incluyen, aunque sin limitación, metilo, metoxilmetilo (MOM), metiltiometilo (MTM), f-butiltiometilo, (fenildimetilsilil)metoximetilo (SMOM), benciloximetilo (Bo M), p-metoxibenciloximetilo (PMBM), (4-metoxifenoxi)metilo (p-AOM), guaiacolmetilo (GUM), f-butoximetilo, 4-penteniloximetilo (POM), siloximetilo, 2-metoxietoximetilo (MEM), 2,2,2-tricloroetoximetilo, bis(2-cloroetoxi)metilo, 2-(trimetilsilil)etoximetilo (SEMOR), tetrahidropiranilo (THP), 3-bromotetrahidropiranilo, tetrahidrotiopiranilo, 1-metoxiciclohexilo, 4-metoxitetrahidropiranilo (MTHP), 4-metoxitetrahidrotiopiranilo, S,S-dióxido 4-metoxitetrahidrotiopiranilo, 1-[(2-cloro-4-metil)fenil]-4-metoxipiperidin-4-ilo (CTMP), 1,4-dioxan-2-ilo, tetrahidrofuranoílo, tetrahidrotiofuranilo, 2,3,3a,4,5,6,7,7a-octahidro-7,8,8-trimetil-4,7-metanobenzofuran-2-ilo, 1-etoxietilo, 1 -(2 -cloroetoxi)etilo, 1 -metil-1 -metoxietilo, 1 -metil-1 -benciloxietilo, 1 -metil-1 -benciloxi-2 -fluoroetilo, 2 ,2 ,2 -tricloroetilo, 2-trimetilsililetilo, 2-(fenilselenil)etilo, f-butilo, alilo, p-clorofenilo, p-metoxifenilo, 2,4-dinitrofenilo, bencilo (Bn), p-metoxibencilo, 3,4-dimetoxibencilo, o-nitrobencilo, p-nitrobencilo, p-halobencilo, 2,6-diclorobencilo, pcianobencilo, p-fenilbencilo, 2-picolilo, 4-picolilo, N-óxido de 3-metil-2-picolilo, difenilmetilo, p,p'-dinitrobenzhidrilo, 5-dibenzosuberilo, trifenilmetilo, a-naftildifenilmetilo, p-metoxifenildifenilmetilo, di(p-metoxifenil)fenilmetilo, tri(pmetoxifenil)metilo, 4-(4'-bromofenaciloxifenil)difenilmetilo, 4,4',4"-tris(4,5-dicloroftalimidofenil)metilo, 4,4',4''-tris(levulinoiloxifenil)metilo, 4,4',4''-tris(benzoiloxifenil)metilo, 3-(imidazol-1-il)bis(4',4''-dimetoxifenil)metilo, 1,1 -bis(4-metoxifenil)-1'-pirenilmetilo, 9-antrilo, 9-(9-fenil)xantenilo, 9-(9-fenil-10-oxo)antrilo, 1,3-benzodisulfuran-2-ilo, S,S-dióxido bencisotiazolilo, trimetilsililo (TMS), trietilsililo (TES), triisopropilsililo (TIPS), dimetilisopropilsililo (IPDMS), dietilisopropilsililo (DEIPS), dimetilthexilsililo, f-butildimetilsililo (TBDMS), f-butildifenilsililo (TBDPS), tribencilsililo, trip-xililsililo, trifenilsililo, difenilmetilsililo (DPMS), f-butilmetoxifenilsililo (TBMPS), formiato, benzoilformiato, acetato, cloroacetato, dicloroacetato, tricloroacetato, trifluoroacetato, metoxiacetato, trifenilmetoxiacetato, fenoxiacetato, pclorofenoxiacetato, 3-fenilpropionato, 4-oxopentanoato (levulinato), 4,4-(etilenditio)pentanoato (levulinoilditioacetal), pivaloato, adamantoato, crotonato, 4-metoxicrotonato, benzoato, p-fenilbenzoato, 2,4,6-trimetilbenzoato (mesitoato), alquil metil carbonato, 9-fluorenilmetil carbonato (Fmoc), alquilo etil carbonato, alquil 2,2,2-tricloroetil carbonato (Troc), 2-(trimetilsilil)etil carbonato (TMSEC), 2-(fenilsulfonil) etil carbonato (Psec), 2-(trifenilfosfonio) etil carbonato (Peoc), alquil isobutil carbonato, alquil vinil carbonato, alquil alil carbonato, alquil p-nitrofenil carbonato, alquil bencil carbonato, alquil p-metoxibencil carbonato, alquil 3,4-dimetoxibencil carbonato, alquil o-nitrobencil carbonato, alquil p-nitrobencil carbonato, alquil S-bencil tiocarbonato, 4-etoxi-1 -naptil carbonato, metil ditiocarbonato, 2-yodobenzoato, 4-azidobutirato, 4-nitro-4-metilpentanoato, o-(dibromometil)benzoato, 2-formilbencenosulfonato, 2-(metiltiometoxi)etilo, 4-(metiltiometoxi)butirato, 2-(metiltiometoximetil)benzoato, 2,6-dicloro-4-metilfenoxiacetato, 2,6-dicloro-4-(1,1,3,3-tetrametilbutil)fenoxiacetato, 2,4-bis(1,1-dimetilpropil)fenoxiacetato, clorodifenilacetato, isobutirato, monosuccinoato, (£)-2-metil-2-butenoato, o-(metoxiacil)benzoato, a-naftoato, nitrato, alquil N,N,N',N'-tetrametilfosforodiamidato, alquil N-fenilcarbamato, borato, dimetilfosfinotioilo, alquil 2,4-dinitrofenilsulfenato, sulfato, metanosulfonato (mesilato), bencilsulfonato y tosilato (Ts).
En determinadas realizaciones, el sustituyente presente en un átomo de azufre es un grupo protector de azufre (también mencionado como un grupo protector de tiol). Los grupos protectores de azufre incluyen, aunque sin limitación, -Raa, -N(Rbb)2 , -C(=O)SRaa, -C(=O)Raa, -CO2Raa,-C(=O)N(Rbb)2, -C(=NRbb)Raa, -C(=NRbb)ORaa, -C(=NRbb)N(Rbb)2, -S(=O)Raa, -SO2Raa, -Si(Raak -P(Rcc)2, -P(Rcc)a, -P(=O)2Raa, -P(=O)(Raa)2, -P(=O)(ORcc)2, -P(=O)2N(Rbb)2 y -P(=O)(NRbb)2 , en los que Raa, Rbb y Rcc son como se definen en la presente memoria. Los grupos protectores de azufre son bien conocidos en la técnica e incluyen los descritos en detalle en Protecting Groups in Organic Synthesis, T. W. Greene y P. G. M. Wuts, 3.a edición, John Wiley & Sons, 1999.
Estos y otros sustituyentes ejemplares se describen en más detalle en la descripción detallada, los ejemplos y las reivindicaciones. No se pretende que la presente divulgación esté limitada de ninguna manera por la lista ejemplar anterior de sustituyentes.
Ofras definiciones
"Sal farmacéuticamente aceptable" se refiere a aquellas sales que son, dentro del alcance del criterio médico sensato, adecuadas para su uso en contacto con los tejidos de seres humanos y otros animales sin toxicidad excesiva, irritación, respuesta alérgica y similares, y son proporcionales con una relación beneficio/riesgo razonable. Las sales farmacéuticamente aceptables son bien conocidas en la técnica. Por ejemplo, Berge ef al., describe sales farmacéuticamente aceptables en detalle en J. Pharmaceutical Sciences (1977) 66:1-19. Las sales farmacéuticamente aceptables de los compuestos descritos en la presente memoria incluyen las derivadas de bases y ácidos orgánicos e inorgánicos adecuados. Los ejemplos de sales de adición de ácido no tóxicas farmacéuticamente aceptables son sales de un grupo amino formado con ácidos inorgánicos tales como ácido clorhídrico, ácido bromhídrico, ácido fosfórico, ácido sulfúrico y ácido perclórico o con ácidos orgánicos tales como ácido acético, ácido oxálico, ácido maleico, ácido tartárico, ácido cítrico, ácido succínico o ácido malónico o usando otros métodos usados en la técnica tales como intercambio iónico. Otras sales farmacéuticamente aceptables incluyen sales adipato, alginato, ascorbato, aspartato, bencenosulfonato, benzoato, bisulfato, borato, butirato, alcanforato, alcanforsulfonato, citrato, ciclopentanopropionato, digluconato, dodecilsulfato, etanosulfonato, formiato, fumarato, glucoheptonato, glicerofosfato, gluconato, hemisulfato, heptanoato, hexanoato, hidroyoduro, 2 -hidroxi-etanosulfonato, lactobionato, lactato, laurato, lauril sulfato, malato, maleato, malonato, metanosulfonato, 2-naftalenosulfonato, nicotinato, nitrato, oleato, oxalato, palmitato, pamoato, pectinato, persulfato, 3-fenilpropionato, fosfato, picrato, pivalato, propionato, estearato, succinato, sulfato, tartrato, tiocianato, p-toluenosulfonato, undecanoato, valerato y similares. Las sales derivadas de bases apropiadas incluyen sales de metales alcalinos,
metales alcalinotérreos, amonio y N+(alquilo C-m )4. Las sales de metales alcalinos y alcalinotérreos representativas incluyen sodio, litio, potasio, calcio magnesio y similares. Las sales farmacéuticamente aceptables adicionales incluyen, cuando es apropiado, sales cuaternarias.
Un "sujeto" para el que se contempla la administración incluyen, aunque sin limitación seres humanos (por ejemplo, un hombre o mujer de cualquier grupo de edad, por ejemplo, un sujeto pediátrico (por ejemplo, bebé, niño, adolescente) o sujeto adulto (por ejemplo, adulto joven, adulto de mediana edad o adulto mayor)) y/u otros animales no humanos, por ejemplo, mamíferos (por ejemplo, primates (por ejemplo, macacos de la India, macacos cangrejeros); mamíferos comercialmente relevantes tales como ganado bovino, cerdos, caballos ovejas, cabras gatos y/o perros), aves (por ejemplo, aves comercialmente relevantes tales como pollos, patos, gansos y/o pavos), reptiles, anfibios y peces. En determinadas realizaciones, el animal no humano es un mamífero. El animal no humano puede ser un macho o hembra en cualquier fase del desarrollo. Un animal no humano puede ser un animal transgénico.
"Afección", "enfermedad" y "trastorno" se usan indistintamente en la presente memoria.
"Tratar", "que trata" y "tratamiento" abarca una acción que se produce mientras un sujeto está padeciendo una afección, que reduce la gravedad de la afección o retarda o ralentiza la progresión de la afección ("tratamiento terapéutico"). "Tratar", "que trata" y "tratamiento" también abarca una acción que se produce antes de que un sujeto empiece a padecer la afección y que inhibe o reduce la gravedad de la afección ("tratamiento profiláctico").
Una "cantidad eficaz" de un compuesto se refiere a una cantidad suficiente para provocar la respuesta biológica deseada, por ejemplo, tratar la afección. Como apreciarán los expertos en la materia, la cantidad eficaz de un compuesto descrito en la presente memoria puede variar dependiendo de factores tales como el criterio de valoración biológico deseado, la farmacocinética del compuesto, la afección que se está tratando, el modo de administración y la edad y salud del sujeto. Una cantidad eficaz abarca tratamiento terapéutico y profiláctico.
Una "cantidad terapéuticamente eficaz" de un compuesto es una cantidad suficiente para proporcionar un beneficio terapéutico en el tratamiento de una afección o para retardar o minimizar uno o más síntomas asociados con la afección. Una cantidad terapéuticamente eficaz de un compuesto significa una cantidad de agente terapéutico, en solitario o en combinación con otros tratamientos, que proporciona un beneficio terapéutico en el tratamiento de la afección. La expresión "cantidad terapéuticamente eficaz" puede abarcar una cantidad que mejora el tratamiento global, reduce o evita los síntomas o causas de la afección, o potencia la eficacia terapéutica de otro agente terapéutico.
Una "cantidad profilácticamente eficaz" de un compuesto es una cantidad suficiente para prevenir una afección, o uno o más síntomas asociados con la afección o prevenir su reaparición. Una cantidad profilácticamente eficaz de un compuesto significa una cantidad de un agente terapéutico, en solitario o en combinación con otros agentes, que proporciona un beneficio profiláctico en la prevención de la afección. La expresión "cantidad profilácticamente eficaz" puede abarcar una cantidad que mejora la profilaxis global o potencia la eficacia profiláctica de otro agente profiláctico.
El término "cinasa" representa enzimas de la clase transferasa que pueden transferir un grupo fosfato desde una molécula donadora hasta una molécula aceptadora, por ejemplo, un resto de aminoácido de una proteína o una molécula lipídica. Ejemplos no limitantes representativos de cinasas incluyen Abl, ACK, Akt1/PKBa, Akt2/PKBp, Akt3/PKBY, ALK1, ALK2, Alk4, AMPKa1/pify1, AMPKa1/pify2, AMPKa1/pi/Y3, AMPKa1/p2/Yl, AMPKa2/pi/Yl, AMPKa2/p2/Y2, Abl2, ARKS, Ask1, Aurora A, Aurora B, Aurora C, Axl, BARK1, Blk, Bmx, B-Raf, Brk, BrSKI, BrSK2, Btk, CaMKIa, CaMKip, CaMKlY, CaMK16, CAMK2a, CaMK2p, CAMK26, CAMK2y, CAMK4, CAMKK1, CAMKK2, CDK1, CDK2, CDK3, CDK4, CDK5, CDK6, CDK7, CDK9, CDKI/ciclina B, CDK2/ciclina A, CDK2/ciclina E, CDK3/ciclina E, CDK5/p25, CDK5/p35, CDK6/ciclina D3, CDK7/ciclina H/MAT1, CDK9/ciclina T1, CHK1, CHK2, CK1a, CK1y, CK15, CK1e, C K ip i, CK1y1, CK1y2, CK1y3, CK2a1, CK2a2, cKit, c-RAF, CLK1, CLK2, CLK3, COT, Csk, DAPK1, DAPK2, DAPK3, DCAMLK2, DDR2, DMPK, DRAK1, DYRK1A, DYRK2, DYRK3, eEF2K, EGFR, EPHA1, EPHA2, EPHA3, EPHA4, EPHA5, EPHA6, EPHA7, EPHA8, EphBI, EphB2, EphB3, EphB4, ErbB4, Erk1, Erk2, FAK, Fer, Fes, FGFR1, Flt2, Flt4, FLT3 D835Y, FGFR2, FGFR3, FGFR4, Fgr, Flt1, Flt3, Fms, FRK, FynA, GCK, GPRK5, GRK2, GRK4, GRK6, GRK7, GSK3a, GSK3p, Hck, HER2, HER4, HIPK1, HIPK2, HIPK3, HIPK4, IGF1R, IKKp, IKKa, IKKe, IR, InsR, IRR, IRAK1, IRAK2, IRAK4, Itk, JAK2, JAK3, JNK1, JNK2, JNK3, KDR, KHS1, Kit, Lck, LIMK1, LKB1, LOK, LRRK2, Lyn A, Lyn B, MAPK1, MAPK2, MAPK12, MAPKAP-K2, MAPKAP-K3, MAPKAPK2, MAPKAPK3, MAPKAPK5, MARK1, MARK2, MARK3, MARK4, MELK, MEK1, MEK2, MEKK2, MEKK3, Mer, Met, MET M1250T, MINK, MKK4, MKK6, MKK7p, MLCK, MLK1, MLK3, MNK1, MNK2, MRCKa, MRCKp, MSK1, MSK2, MSSK1, STK23, STK4, STK3, STK24, MST1, MST2, MST3, MST4, MUSK, mTOR, MYO3p, MYT1, NDR1, NEK11, NEK2, NEK3, NEK6, NEK7, NEK9, NLK, NUAK2, p38a, p38p, p385, p38Y, p70S6K, S6K, SRK, PAK1/CDC42, PAK2, PAK3, PAK4, PAK5, PAK6, PAR-1Ba, PASK, PBK, PDGFRa, PDGFRp, PDK1, PEK, PHKG2, PI3Ka, PI3Kp, PI3Ky, PI3K6, Pim1, Pim2, PKAca, PKAcp, PKAcy, PKA(b), PKA, PKBa, PKBp, PKBy, PKCa, PKCpi, PKCp2, P K C pil, PKC5, PKCe, PKCy, PKCp, PKCn, PKCi, PKC0, PKCZ, PKD1, PKD2, PKD3, PKG1a, PKG1B, PKN1, PKN2, PKR, PLK1, PLK2, PLK3, PLK4, Polo, PRAK, PRK2, PrKX, PTK5, PYK2, QIK, Raf1, Ret, RIPK2, RIPK5, ROCK1, ROCK2, RON, ROS, Rse, RSK1, RSK2, RSK3, RSK4, SAPK2a, SAPK2b, SAPK3, SAPK4, SGK1,
SGK2, SGK3, SIK, MLCK, SLK, Snk, Src, SRPK1, SRPK2, STK33, SYK, TAK1-TAB1, TAK1, TBK1, TAO1, TAO2, TAO3, TBK1, TEC, TESK1, TGFpR1, TGFpR2, Tie2, TLK2, TrkA, TrkB, TrkC, TSSK1, TSSK2, TTK, TXK, TYK2, TYRO3, ULK1, ULK2, WEE1, WNK2, WNK3, Yes1, YSK1, ZAK, ZAP70, ZC3 y ZIPK.
El término "mutante" se refiere a una secuencia (por ejemplo, una secuencia de proteína o una secuencia de ácido nucleico) que tiene al menos una mutación. El término "mutación", tal como se usa en la presente memoria, se refiere a una sustitución de un resto dentro de una secuencia, por ejemplo, una secuencia de ácido nucleico o de aminoácidos, con otro resto, o una eliminación o inserción de uno o más restos dentro de una secuencia.
El término "variante" se refiere a variaciones del ácido nucleico o secuencias de aminoácido de la biomolécula de interés. Están abarcadas dentro del término "variante" sustituciones, adiciones o eliminaciones de nucleótidos y aminoácidos. Además, están abarcadas dentro del término "variante" biomoléculas naturales y sintéticas modificadas químicamente. Por ejemplo, una variante puede referirse a polipéptidos que difieren de un polipéptido de referencia. En general, las diferencias entre el polipéptido que difiere en la secuencia de aminoácidos del polipéptido de referencia y el polipéptido de referencia están limitadas de modo que las secuencias de aminoácido de la referencia y la variante son globalmente muy similares y, en algunas regiones, idénticas. Un polipéptido variante y de referencia pueden diferir en la secuencia de aminoácidos en una o más sustituciones, eliminaciones, adiciones, fusiones y truncamientos que pueden ser conservativos o no conservativos y pueden estar presentes en cualquier combinación. Por ejemplo, las variantes pueden ser aquellas en que varios, por ejemplo, de 50 a 30, de 30 a 20, de 20 a 10, de 10 a 5, de 5 a 3, de 3 a 2, de 2 a 1 o 1 aminoácido se insertan, sustituyen o eliminan, en cualquier combinación. Adicionalmente, una variante puede ser un fragmento de un polipéptido que difiere de una secuencia de polipéptido de referencia en que es más corto que la secuencia de referencia, tal como por una eliminación terminal o interna. Una variante de un polipéptido también incluye un polipéptido que retiene esencialmente la misma función biológica o actividad que dicho polipéptido, por ejemplo, proteínas precursoras que pueden activarse por escisión de la parte precursora para producir un polipéptido maduro activo, estas variantes pueden ser variaciones alélicas caracterizadas por diferencias en las secuencia de nucleótidos del gen estructural que codifica la proteína, o pueden implicar corte y empalme diferencial o modificación postraduccional. Las variantes también incluyen una proteína relacionada que tiene sustancialmente la misma actividad biológica, pero se obtiene de una especie diferente. Los expertos en la materia pueden producir variantes que tienen sustituciones, eliminaciones, adiciones o remplazos de un aminoácido o múltiples aminoácidos. Estas variantes pueden incluir, entre otras cosas: (i) una en que uno o más de los restos de aminoácido se sustituyen con un resto de aminoácido conservado o no conservado (preferiblemente un resto de aminoácido conservado) y dicho resto de aminoácido sustituido puede estar codificado o no por el código genético, o (ii) una en que se elimina uno o más aminoácidos del péptido o proteína, o (iii) una en que se añade uno o más aminoácidos al polipéptido o proteína, o (iv) una en que uno o más de los restos de aminoácido incluyen un grupo sustituyente, o (v) una en que el polipéptido maduro se fusiona con otro compuesto, tal como un compuesto para aumentar la semivida del polipéptido (por ejemplo, polietilenglicol), o (vi) una en que los aminoácidos adicionales se fusionan al polipéptido maduro tal como una secuencia líder o de secreción o una secuencia que se emplea para la purificación del polipéptido maduro o una secuencia de proteína precursora. Una variante del polipéptido también puede ser una variante de origen natural tal como una variante alélica de origen natural, o puede ser una variante que se sabe que no se produce de forma natural.
El término "cáncer" se refiere a una clase de enfermedades caracterizas por el desarrollo de células anómalas que proliferan de forma incontrolable y tienen la capacidad de infiltrarse y destruir tejidos corporales normales. Véase, por ejemplo, Stedman's Medical Dictionary, 25.a ed.; Hensyl ed.; Williams & Wilkins: Philadelphia, 1990. Cánceres ejemplares incluyen, aunque sin limitación, neuroma acústico; adenocarcinoma; cáncer de glándula suprarrenal; cáncer anal; angiosarcoma (por ejemplo, linfangiosarcoma, linfangioendoteliosarcoma; hemangiosarcoma); cáncer de apéndice; gammopatía monoclonal benigna; cáncer biliar (por ejemplo, colangiocarcinoma); cáncer de vejiga; cáncer de mama (por ejemplo, adenocarcinoma de mama, carcinoma papilar de mama, cáncer mamario, carcinoma medular de mama); cáncer cerebral (por ejemplo, meningioma, glioblastomas, glioma (por ejemplo, astrocitoma, oligodendroglioma), meduloblastoma); cáncer de bronquios; tumor carcinoide; cáncer cervicouterino (por ejemplo, adenocarcinoma cervicouterino); coriocarcinoma; cordoma; craneofaringioma; cáncer colorrectal (por ejemplo, cáncer de colon, cáncer rectal, adenocarcinoma colorrectal); cáncer de tejido conjuntivo, carcinoma epitelial; ependimoma; endoteliosarcoma (por ejemplo, sarcoma de Kaposi, sarcoma hemorrágico idiopático múltiple); cáncer endometrial (por ejemplo, cáncer uterino, sarcoma uterino); cáncer esofágico (por ejemplo, adenocarcinoma del esófago, adenocarcinoma de Barrett); sarcoma de Ewing; cáncer ocular (por ejemplo, melanoma intraocular, retinoblastoma); hipereosinofilia familiar; cáncer de vesícula biliar; cáncer gástrico (por ejemplo, adenocarcinoma de estómago); tumor del estroma gastrointestinal (GIST); cáncer de células germinales; cáncer de cabeza y cuello (por ejemplo, carcinoma escamocelular de cabeza y cuello, cáncer bucal (por ejemplo, carcinoma escamocelular bucal), cáncer de garganta (por ejemplo, cáncer laríngeo, cáncer faríngeo, cáncer nasofaríngeo, cáncer orofaríngeo)); cánceres hematopoyéticos (por ejemplo, leucemia tal como leucemia linfocítica aguda (ALL) (por ejemplo, ALL de linfocitos B, ALL de linfocitos T),leucemia mielocítica aguda (AML) (por ejemplo, AML de linfocitos B, AML de linfocitos T), leucemia mielocítica crónica (CML) (por ejemplo, CML de linfocitos B, CML de linfocitos T) y leucemia linfocítica crónica (CLL) (por ejemplo, CLL de linfocitos B, CLL de linfocitos T); linfoma tal como linfoma de Hodgkin (HL) (por ejemplo, HL de linfocitos B, HL de linfocitos T) y linfoma no hodgkiniano (NHL) (por ejemplo, NHL de
linfocitos B tal como linfoma de células grandes difuso (DLCL) (por ejemplo, linfoma de linfocitos B grande difuso), linfoma folicular, leucemia linfocítica crónica/linfoma linfocítico pequeño (CLL/SLL), linfoma de células de manto (MCL), linfomas de linfocitos B de la zona marginal (por ejemplo, linfomas del tejido linfoide asociado a la mucosa (MALT), linfoma de linfocitos B de la zona marginal nodal, linfoma de linfocitos B de la zona marginal esplénica), linfoma de linfocitos B mediastinal primario, linfoma de Burkitt, linfoma linfoplasmacítico (es decir, macroglobulinemia de Waldenstrom), leucemia de células pilosas (HCL), linfoma de células grandes inmunoblástico, linfoma linfoblástico B precursor y linfoma primario del sistema nervioso central (SNC); NHL de linfocitos T tal como linfoma/leucemia linfoblástico T precursor, linfoma de linfocitos T periférico (PTCL) (por ejemplo, linfoma de linfocitos T cutáneo (CTCL) (por ejemplo, micosis fungoides, síndrome de Sezary), linfoma de linfocitos T angioinmunoblástico, linfoma de linfocitos T citolíticos naturales extranodal, linfoma de linfocitos T de tipo enteropático, linfoma de linfocitos T de tipo paniculitis subcutánea y linfoma de células grandes anaplásico); una mezcla de una o más leucemias/linfomas como se describe anteriormente; y mieloma múltiple (MM), enfermedad de la cadena pesada (por ejemplo, enfermedad de la cadena alfa, enfermedad de la cadena gamma, enfermedad de la cadena mu); hemangioblastoma; cáncer de hipofaringe; tumores miofibroblásticos inflamatorios; amiloidosis inmunocítica; cáncer de riñón (por ejemplo, nefroblastoma anteriormente conocido como tumor de Wilms, carcinoma de células renales); cáncer de hígado (por ejemplo, cáncer hepatocelular (HCC), hepatoma maligno); cáncer de pulmón (por ejemplo, carcinoma broncógeno, cáncer broncopulmonar microcítico (SCLC), cáncer broncopulmonar no microcítico (NSCLC), adenocarcinoma del pulmón); leiomiosarcoma (LMS); mastocitosis (por ejemplo, mastocitosis sistémica); cáncer de músculos, síndrome mielodisplásico (MDS); mesotelioma; trastorno mieloproliferativo (MPD) (por ejemplo, policitemia vera (PV), trombocitosis esencial (ET), metaplasia mieloide agnogénica (AMM) anteriormente conocida como mielofibrosis (MF), mielofibrosis idiopática crónica, leucemia mielocítica crónica (CML), leucemia neutrofílica crónica (CNL), síndrome hipereosinofílico (HES)); neuroblastoma; neurofibroma (por ejemplo, neurofibromatosis (NF) de tipo 1 o de tipo 2, schwannomatosis); cáncer neuroendocrino (por ejemplo, tumor neuroendocrino gatroenteropancreático (GEP-NET), tumor carcinoide); osteosarcoma (por ejemplo, cáncer de huesos); cáncer de ovario (por ejemplo, cistadenocarcinoma, carcinoma embrionario de ovario, adenocarcinoma de ovario); adenocarcinoma papilar; cáncer pancreático (por ejemplo, adenocarcinoma pancreático, (por ejemplo, neoplasia mucinosa papilar intraductal (IPMN), tumores de células de los islotes); cáncer de pene (por ejemplo, enfermedad de Paget del pene y el escroto); pinealoma; tumor neuroectodérmico primitivo (PNT); neoplasia de células plasmáticas; síndromes paraneoplásicos; neoplasias intraepiteliales; cáncer de próstata (por ejemplo, adenocarcinoma de próstata); cáncer rectal; rabdomiosarcoma; cáncer la glándula salival; cáncer de piel (por ejemplo, carcinoma escamocelular (SCC), queratoacantoma (KA), melanoma, carcinoma basocelular (BCC); cáncer del intestino delgado (por ejemplo, cáncer de apéndice); sarcoma de tejido blando (por ejemplo, histiocitoma fibroso maligno (MFH), liposarcoma, tumor de la vaina de los nervios periféricos maligno (MPNST), condrosarcoma, fibrosarcoma, mixosarcoma); carcinoma de glándulas sebáceas; cáncer del intestino delgado; carcinoma de glándulas sudoríparas; sinovioma; cáncer testicular (por ejemplo, seminoma, carcinoma embrionario testicular); cáncer tiroideo (por ejemplo, carcinoma papilar de la glándula tiroides, carcinoma tiroideo papilar (PTC), cáncer tiroideo medular); cáncer uretral; cáncer vaginal; y cáncer vulvar (por ejemplo, enfermedad de Paget de la vulva).
La expresión "trastorno metabólico" se refiere a cualquier trastorno que implique una alteración en el metabolismo normal de carbohidratos, lípidos, proteínas, ácidos nucleicos o una combinación de los mismos. Un trastorno metabólico está asociado con una deficiencia o un exceso en una ruta metabólica que provoca un desequilibrio en el metabolismo de ácidos nucleicos, proteínas, lípidos y/o carbohidratos. Los factores que afectan al metabolismo incluyen, y no se limitan a, el sistema del control endocrino (hormonal) (por ejemplo, la ruta de insulina, las hormonas enteroendocrinas incluyendo GLP-1, PYY o similares), el sistema de control neural (por ejemplo, GLP-1 en el cerebro) o similares. Los ejemplos de trastornos metabólicos incluyen, aunque sin limitación, diabetes (por ejemplo, diabetes de tipo 1, diabetes de tipo 2, diabetes gestacional), hiperglucemia, hiperinsulinemia, resistencia a la insulina y obesidad. En determinadas realizaciones, el trastorno metabólico es diabetes de tipo II.
Breve descripción de los dibujos
La figura 1 muestra los datos de estabilidad para el compuesto 54 en tampón PBS (pH 7,423 °C).
La figura 2 muestra una trayectoria ejemplar para el desarrollo de la sonda.
La figura 3 muestra la actividad dependiente de la dosis del compuesto 54 en la diana (GSK3p, parte superior) y antidiana (CDK5, parte inferior). Se muestran curvas representativas con datos duplicados (círculos y triángulos).
La figura 4 muestra a) un diagrama de cintas que representa la estructura cristalina de GSK3p unida al compuesto 22 en el bolsillo de unión a ATP y b) la representación superficial que muestra el sitio de unión, la orientación de unión y la configuración absoluta del compuesto 22 en la estructural cristalina.
La figura 5 muestra el porcentaje del cinoma (311 cinasas) inhibido por CHIR99021 y tres compuestos de la presente divulgación.
La figura 6 muestra inhibidores de GSK3 conocidos.
La figura 7 muestra el efecto de compuesto 22 en comparación con el vehículo para atenuar la hiperactividad
inducida por anfetamina a lo largo del tiempo después de inyección ICV intracerebroventricular.
La figura 8 muestra el efecto del compuesto 22 sobre la actividad total de actividad total de hiperactividad inducida por anfetamina, en comparación con un vehículo.
La figura 9 muestra un diagrama de Lineweaver-Burk de inhibición competitiva del compuesto 22 para GSK3p.
La figura 10 muestra que, en comparación con el compuesto CHIR99021, el compuesto 137 mostraba un perfil farmacocinético mejorado, tal como exposición sistémica y distribución cerebral, cuando se administraba a ratones C57BL/6 macho. Conc.: concentración. ABC: área bajo la curva. T1/2 : semivida. Cmáx: concentración máxima.
La figura 11A muestra el efecto del compuesto 70 en comparación con el vehículo para atenuar la hiperactividad inducida por anfetamina a lo largo del tiempo después de inyección intraperitoneal sistémica. La figura 11B muestra el efecto del compuesto 70 sobre la actividad total de la hiperactividad inducida por anfetamina, en comparación con un vehículo.
La figura 12 muestra que el inhibidor de GSK3 selectivo 70 induce evidencias morfológicas de diferenciación de AML (leucemia mieloide aguda). La tinción con Giemsa de May-Grunwald de líneas celulares de AML tres días después del tratamiento con el compuesto 70 demostró diferenciación celular en comparación con los controles tratados con vehículo.
Las figuras 13A a 13B muestran que el compuesto 70 induce diferenciación de AML (leucemia mieloide aguda) por GE-HTS característico. Se trataron células HL-60 y U937 durante tres días con compuesto 70 o vehículo. Se cuantificó una característica de diferenciación de 32 genes por la estrategia basada en LMA/microesferas y se determinó una puntuación de suma ponderada (puntuación de diferenciación) calculada para todos los genes para cada condición. Las barras de error indican la media ±DT de 8 réplicas y la significación estadística de las diferencias entre estas puntuaciones de diferenciación se obtuvo usando un ANOVA unidireccional con una corrección de Bonferroni.
La figura 14A a 14B muestra los resultados del compuesto 54 en un ensayo de ELISA SH-SY5Y de p-Tau y un ensayo de indicador TCF/LEF.
La figura 15 muestra los resultados del compuesto 22 en un ensayo de neurogénesis.
Descripción detallada de determinadas realizaciones
La presente divulgación proporciona compuestos que son útiles para inhibir cinasas, por ejemplo, GSK3 o CK1. La presente divulgación proporciona además composiciones farmacéuticas de compuestos descritos en la presente memoria y métodos de uso de los compuestos descritos en la presente memoria. En determinadas realizaciones, un compuesto proporcionado es un inhibidor de GSK3 (por ejemplo, un inhibidor de GSK3a, un inhibidor de GSK3p). En determinadas realizaciones, un compuesto proporcionado es un inhibidor de CK1 (por ejemplo, un inhibidor de CK18). En determinadas realizaciones, un compuesto proporcionado se usa para prevenir y/o tratar un trastorno mediado por cinasa (por ejemplo, un trastorno mediado por GSK o un trastorno mediado por CK1) en un sujeto.
La serina/treonina cinasa, glucógeno sintasa cinasa-3 beta (GSK3p) es un regulador principal conocido para varias rutas celulares que incluyen la señalización de insulina y la síntesis de glucógeno, la señalización del factor neurotrófico, la señalización de Wnt, la señalización de neurotransmisores y la dinámica de microtúbulos (Forde, et al. Cell Mol Life Sci, 2007, 64(15):1930-44; Phiel, et al. Nature, 2003, 423(6938):435-9; Beaulieu, et al. Trends Pharmacol Sci, 2007, 28(4):166-72). Por consiguiente, esta enzima tiene una función crítica en el metabolismo, la transcripción, el desarrollo, la supervivencia celular y las funciones neuronales y se ha implicado en múltiples trastornos humanos incluyendo enfermedades neurológicas (por ejemplo, enfermedad de Alzheimer), trastornos psiquiátricos (por ejemplos, trastorno bipolar), diabetes mellitus no insulinodependiente, hipertrofia cardíaca y cáncer (Gould, TD, et al. Curr Drug Targets, 2006, 7(11):1399-409; Matsuda, et al. Proc Natl Acad Sci UsA, 2008, 105(52):20900-5; Biechele, et al. Methods Mol Biol, 2008, 468:99-110; Woodgett, Curr Drug Targets Immune Endocr Metabol Disord, 2003, 3(4):281-90; Manoukian, et al. Adv Cancer Res, 2002, 84:203-29). Por ejemplo, la leucemia mieloide aguda (AML) es un cáncer caracterizado por múltiples desajustes celulares, incluyendo un bloqueo en la diferenciación de células mieloides. Y aunque el tratamiento actual para la mayoría de pacientes con AML utiliza quimioterapia citotóxica de dosis elevada, el subtipo más satisfactoriamente tratado de AML, leucemia promielocítica aguda, combina tratamiento de diferenciación con ácido todo-trans-retinoico con tratamiento citotóxico de dosis baja (Ades L, Guerci A, Raffoux E, Sanz M, Chevallier P, Lapusan S, Recher C, Thomas X, Rayon C, Castaigne S, Tournilhac O, de Botton S, Ifrah N, Cahn JY, Solary E, Gardin C, Fegeux N, Bordessoule D, Ferrant A, Meyer-Monard S, Vey N, Dombret H, Degos L, Chevret S, Fenaux P. Very long-term outcome of acute promyelocytic leukemia after treatment with all-trans retinoic acid and chemotherapy: the European APL Group experience. Blood.
115:1690-1696). Para identificar nuevas dianas de diferenciación de AML, se realizaron dos cribados de colecciones de moléculas pequeñas independientes y un cribado de ARNhp. La glucógeno sintasa cinasa-3a (GSK3a) surgió como una diana en la intersección de estos tres cribados (Banerji V, Frumm SM, Ross KN, Li LS, Schinzel AC, Hahn CK, Kakoza RM, Chow KT, Ross L, Alexe G, Tolliday N, Inguilizian H, Galinsky I, Stone RM, DeAngelo DJ, Roti G,
Aster JC, Hahn WC, Kung AL, Stegmaier K. The intersection of genetic and Chemical genomic screens identifies GSK-3alpha as a target in human acute myeloid leukemia. J Clin Invest. 2012; 122:935-947). Se demostró que la pérdida específica de alfa de GSK3 induce la diferenciación en AML por múltiples mediciones, incluyendo cambios morfológicos, expresión de marcador de superficie celular coherente con la maduración mieloide y la inducción de un programa de expresión génica coherente con la maduración mieloide. La supresión específica de GSK3a también da lugar a un crecimiento alterado y proliferación in vitro, inducción de la apoptosis, pérdida de formación de colonias en metilcelulosa y actividad anti-AML in vivo. De forma importante, la inhibición selectiva de GSK3a en AML no da lugar a la estabilización de p-catenina. La estabilización de p-catenina es indeseable en tratamiento de AML porque la p-catenina promueve la población de células madre de AML (Wang Y, Krivtsov AV, Sinha AU, North TE, Goessling W, Feng Z, Zon LI, Armstrong SA. The Wnt/beta-catenin pathway is required for the development of leukemia stem cells in AML. Science. 2010; 327:1650-1653). Aunque gran parte de la bibliografía se ha centrado en la función de la inhibición global de GSK3 en AML, ha habido datos que apoyan una función de los inhibidores de GSK3a selectivos en esta enfermedad (Wang Z, Smith KS, Murphy M, Piloto O, Somervaille TC, Cleary ML. Glycogen synthase kinase 3 in MLL leukaemia maintenance and targeted therapy. Nature. 2008; 455:1205-1209; Wang Z, Iwasaki M, Ficara F, Lin C, Matheny C, Wong SH, Smith KS, Cleary ML. GSK-3 promotes conditional association of CREB and its coactivators with MEIS1 to facilitate HOX-mediated transcription and oncogenesis. Cancer Cell. 2010; 17:597-608). Además, cada vez más documentos sugieren una función más amplia para perturbar GSK3a en cáncer (Piazza F, Manni S, Tubi LQ, Montini B, Pavan L, Colpo A, Gnoato M, Cabrelle A, Adami F, Zambello R, Trentin L, Gurrieri C, Semenzato G. Glycogen Synthase Kinase-3 regulates multiple myeloma cell growth and bortezomib-induced cell death. BMC Cancer. 2010; 10:526; Bang D, Wilson W, Ryan M, Yeh JJ, Baldwin AS. GSK-3alpha promotes oncogenic KRAS function in pancreatic cancer via TAK1-TAB stabilization and regulation of noncanonical NF-kappaB. Cancer discovery. 2013; 3:690-703).
El litio ha demostrado inhibir la actividad cinasa de GSK3 directamente, mediante competición con magnesio, e indirectamente, aumentando la fosforilación inhibidora de GSK3 (Beaulieu et al., 2004, 2008; Chalecka-Franaszek y Chuang, 1999; De Sarno et al., 2002; Klein y Melton, 1996). Además, los ratones GSK3a nulos o GSK3p aploinsuficientes fenocopian el efecto del litio de atenuación de los comportamientos aberrantes (Beaulieu et al., 2004; Kaidanovich-Beilin et al., 2009; O'Brien et al., 2004). A la inversa, los ratones que sobreexpresan GSK3p o que portan mutaciones que evitan la fosforilación inhibidora de GSk3a (Ser21) y GSK3p (Ser9) muestran comportamientos que modelan los síntomas psiquiátricos, como lo hacen los ratones con alteración dirigida de AKT1, que fosforila e inactiva GSK3a (Ser21) y GSK3p (Ser9) (Emamian et al., 2004; Lai et al., 2006; Polter et al., 2010; Prickaerts et al., 2006).
Pan et al. mostraron que los inhibidores de GSK3p son eficaces en modelos insensibles al litio (Pan et al., Neuropsychopharmacology, 2011, 36(7):1397-411). Por lo tanto, los inhibidores de GSK3p pueden ser eficaces en pacientes bipolares insensibles al litio.
La señalización de AKT/GSK3 se ha implicado en la fisiopatología de trastornos neuropsiquiátricos mediante estudios de asociación bioquímica y genética de pacientes (Emamian et al., 2004; Tan et al., 2008; Thiselton et al., 2008). Además del litio, los antidepresivos, los antipsicóticos y otros estabilizantes del estado de ánimo también modulan la actividad de GSK3 (Beaulieu et al., 2009), apoyando además su implicación en la enfermedad psiquiátrica. Diversas sondas farmacológicas de GSK3 se han usado para implicar la actividad cinasa de GSK3 en la regulación del comportamiento in vivo (Beaulieu et al., 2007a; Gould et al., 2004).
En Beurel et al. (Mol. Psych., 2011), la eliminación de la inhibición de GSK3p, demostró insensibilidad al modelo de tratamiento antidepresivo por quetamina. Además, recientemente la inhibición de GSK3p ha demostrado ser eficaz en modelos de síndrome del X frágil (Franklin et al., Biol. Psychiatry. 13 de sep. de 2013, Glycogen Synthase Kinase-3 Inhibitors Reverse Deficits in Long-term Potentiation and Cognition in Fragile X Mice). Por tanto, la inhibición de GSK3p puede dar lugar a múltiples indicaciones de tratamiento de enfermedad mental y trastornos del estado de ánimo.
En determinadas realizaciones, se necesitan moduladores de molécula pequeña altamente selectivos para ayudar a dilucidar la función de GSK3p y la regulación en trastornos del sistema nervioso central. Actualmente, no existe dicha molécula pequeña con la combinación correcta de selectividad y propiedades farmacocinéticas para alterar de forma precisa la función de GSK3p en modelos de roedor establecidos de memoria y el estado de ánimo.
Existen evidencias significativas de una función crítica para la señalización de GSK3 en la regulación de la neurogénesis, el neurodesarrollo y en la neuroplasticidad. La función de GSK3 se modula tanto por estabilizantes del estado de ánimo que tratan a pacientes con trastorno bipolar como con antipsicóticos para tratar la esquizofrenia. La señalización aberrante de GSK3 se ha implicado además en la etiología de trastornos neuropsiquiátricos, lo que demuestra una función para la inhibición de GSK3 por el gen asociado a esquizofrenia DISC1 (Mao Y, et al. Cell 2009, 136(6):1017-1031). Por consiguiente, las moléculas pequeñas que inhiben la señalización de GSK3 son útiles como compuestos de herramienta valiosa para sondear la función de la señalización de Wnt/GSK3 en fisiopatología del trastorno bipolar y otros trastornos neuropsiquiátricos y también como agentes terapéuticos para modular la neurogénesis humana.
En determinadas realizaciones, los compuestos descritos en la presente memoria son útiles como compuestos de sonda para investigar la función de la señalización de cinasas, por ejemplo, la señalización de GSK3, en la fisiopatología de diversos trastornos, por ejemplo, trastorno bipolar y otros trastornos neuropsiquiátricos. En determinadas realizaciones, un compuesto proporcionado es útil como herramienta para sondear las rutas moleculares de GSK/Wnt tanto en estudios in vitro con progenitores neurales humanos y de roedor, y/o in vivo. La señalización de Wnt/GSK3 ha demostrado desempeñar una función importante en la regulación de la neurogénesis y neurodesarrollo en mamíferos (Chen, et al. J Neurochem. 2000, 75(4):1729-34; Wexler, et al. Mol Psychiatry. 2008, 13(3):285-92). En determinadas realizaciones, un compuesto proporcionado es útil como una herramienta para sondear el efecto de disminuir la fosforilación de Tau. La fosforilación aberrante de Tau, incluyendo en sitios de GSK3, se ha implicado en la fisiopatología de varios trastornos neurodegenerativos humanos, incluyendo la enfermedad de Alzheimer y las taupatías primarias (por ejemplo, parálisis supranuclear progresiva y otras demencias frontotemporales). (Lee, et al. Cold Spring Harb Perspect Med. 2011, 1(1): a006437; Hooper, et al. J Neurochem. 2008, 104(6):1433-9) por tanto, disminuir la fosforilación de Tau con un inhibidor de GSK3 selectivo puede proporcionar visión de los mecanismos de enfermedad subyacentes y puede proporcionar un método de reversión de los síntomas de la enfermedad.
En determinadas realizaciones, un compuesto proporcionado es útil como una herramienta para evaluar si hay diferencias en la respuesta de células progenitoras neurales derivadas de células madre pluripotentes inducidas (iPSC) (iPSC-NPC) de pacientes con trastornos neuropsiquiátricos a moduladores de GSK3 diferentes a aquellos sin dichos trastornos. Por ejemplo, puede usarse un panel de modelos de iPSC desarrollados a partir de pacientes con trastorno bipolar, esquizofrenia y/o sindroma del X frágil; existe evidencia de que dichos trastornos están relacionados con la regulación incorrecta de la señalización de GSK3.
En determinadas realizaciones, un compuesto proporcionado es útil como una herramienta para sondear si la inhibición de GSK3 selectiva puede rescatar las deficiencias causadas por la variación genética en DISC1 humano/de ratón, incluyendo en ensayos de neurogénesis in vivo en ratones embrionarios y adultos. La función de la señalización de DISC1/GSK3 en la fisiopatología de los trastornos neuropsiquiátricos (Mao, et al. Cell. 2009, 136(6): 1017-1031) es un área de estudio en curso.
En determinadas realizaciones, un compuesto proporcionado modula la neurogénesis posnatal y/o adulta, proporcionando una vía terapéutica para múltiples trastornos neuropsiquiátricos y neurodegenerativos, incluyendo trastorno bipolar, depresión mayor, lesión cerebral traumática, enfermedad de Alzheimer, enfermedad de Parkinson y enfermedad de Huntington.
Compuestos
Como se describe en líneas generales anteriormente, en la presente memoria se proporcionan compuestos útiles como inhibidores de cinasa, por ejemplo, inhibidores de GSK3 o inhibidores de c K1. En algunas realizaciones, la presente divulgación proporciona un compuesto de fórmula I:
o una de sus sales farmacéuticamente aceptables,
en la que
R1 y R2 se seleccionan independientemente del grupo que consiste en grupo alifático opcionalmente sustituido, arilo opcionalmente sustituido y heteroarilo opcionalmente sustituido; o R1 y R2 se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido, en el que el anillo formado por R1 y R2 puede estar condensado opcionalmente a un anillo arilo o heteroarilo;
R3 se selecciona del grupo que consiste en hidrógeno, halo, -CN, -NO2, grupo alifático opcionalmente sustituido, fenilo opcionalmente sustituido, heterociclilo opcionalmente sustituido, heteroarilo opcionalmente sustituido, -ORA, -N(Rb)2, -SRa, -C(=O)Ra, -C(=O)ORa, -C(=O)SRa, -C(=O)N(Rb)2, -OC(=O)Ra, -NRbC(=O)Ra, -NRbC(=O)N(Rb)2, -OC(=O)N(Rb)2, -NRbC(=O)ORa, -SC(=O)Ra, -C(=NRb)Ra, -C(=NRb)N(Rb)2, -NRbC(=NRb)Rb, -C(=S)Ra, -C(=S)N(Rb)2, -NRbC(=S)Ra, -S(=O)Ra, -SO2Ra, -NRBSO2RAy -SO2N(Rb)2;
cada Ra es independientemente hidrógeno, grupo alifático opcionalmente sustituido, carbociclilo opcionalmente sustituido, heterociclilo opcionalmente sustituido, arilo opcionalmente sustituido o heteroarilo opcionalmente
sustituido;
cada Rb es independientemente hidrógeno, grupo alifático opcionalmente sustituido, carbociclilo opcionalmente sustituido, heterociclilo opcionalmente sustituido, arilo opcionalmente sustituido, heteroarilo opcionalmente sustituido, o dos grupos RB se toman junto con sus átomos intermedios para formar un anillo heterocíclico opcionalmente sustituido;
R4a y R4b son independientemente hidrógeno, halo, -CN, -ORA, -N(RB)2 o grupo alifático opcionalmente sustituido, o R4a y R4b se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido;
R5a y R5b son independientemente hidrógeno, halo, -CN, -OR , -N(RB)2 y grupo alifático opcionalmente sustituido, o R5a y R5b se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido; y
R6a y R6b son independientemente hidrógeno, halo, -CN, -ORA, -N(RB)2 o grupo alifático opcionalmente sustituido, o R6a y R6b se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido;
en los que cada ocasión de arilo tiene independientemente de 6 a 14 átomos de carbono en el anillo; y
en los que cada ocasión de heteroarilo es independientemente de 5 a 10 miembros, y monocíclico o bicíclico, y tiene independientemente de 1 a 4 heteroátomos en el anillo seleccionados independientemente del grupo que consiste en nitrógeno, oxígeno y azufre.
En determinados aspectos, la presente divulgación proporciona un compuesto de fórmula I-a:
o una de sus sales farmacéuticamente aceptables, en la que R3, R4a, R4b, R5a, R5b, R6a y R6b son como se definen para la fórmula I, y R1' y R2 se seleccionan independientemente del grupo que consiste en ¡ grupo alifático opcionalmente sustituido, arilo opcionalmente sustituido y heteroarilo opcionalmente sustituido; o R1 y R2 se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico de 3 a 7 miembros opcionalmente sustituido, en el que el anillo formado por R1 y R2 puede estar condensado opcionalmente a un anillo arilo o heteroarilo.
En determinadas realizaciones, un compuesto proporcionado es de fórmula II:
o una de sus sales farmacéuticamente aceptables, en la que R2, R3, R5a y R5b son como se definen para la fórmula I,
cada R7 se selecciona independientemente del grupo que consiste en hidrógeno, halo, -CN,-NO2 , grupo alifático opcionalmente sustituido, fenilo opcionalmente sustituido, heterociclilo opcionalmente sustituido, heteroarilo opcionalmente sustituido, -ORA, -N(RB)2 , -SRA -C(=O)RA, -C(=O)ORA, -C(=O)SRA, -C(=O)N(RB)2, -OC(=O)RA, -NRBC(=O)RA, -NRBC(=O)N(RB)2, -OC(=O)N(RB)2, -NRBC(=O)ORA, -SC(=O)RA, -C(=NRb)Ra, -C(=NRb)N(Rb)2, -NRbC(=NRb)Rb, -C(=S)RA, -C(=S)N(Rb)2, -NRbC(=S)Ra, -S(=O)RA, -SO2RA, -NRBSO2RA y -SO2N(RB)2; o dos grupos R7 adyacentes se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico, condensado opcionalmente sustituido; o R2 y R7 se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico, condensado opcionalmente sustituido; y
n es 0, 1, 2, 3, 4 o 5.
En determinadas realizaciones, un compuesto proporcionado es de fórmula II-a:
o una de sus sales farmacéuticamente aceptables, en la que R3, R5a, R5b, R7 y n son como se definen para la fórmula II, y R2 se selecciona del grupo que consiste en grupo alifático opcionalmente sustituido, arilo opcionalmente sustituido y heteroarilo opcionalmente sustituido; o R2 y R7 se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico, condensado opcionalmente sustituido; en la que arilo tiene de 6 a 14 átomos de carbono en el anillo; y en la que heteroarilo es de 5 a 10 miembros, y monocíclico o bicíclico, y tiene de 1 a 4 heteroátomos en el anillo seleccionados independientemente del grupo que consiste en nitrógeno, oxígeno y azufre.
En determinadas realizaciones, un compuesto proporcionado es de fórmula II-a-/ o W-a-ii:
o una de sus sales farmacéuticamente aceptables.
En determinadas realizaciones, un compuesto proporcionado es de fórmula III:
o una de sus sales farmacéuticamente aceptables, en la que R2, R3, R5a y R5b son como se definen para la fórmula I,
Anillo A es un heteroarilo de 5 a 6 miembros, un carbociclilo de 4 a 6 miembros, o un heterociclilo de 4 a 6 miembros;
cada R7 se selecciona independientemente del grupo que consiste en hidrógeno, halo, -CN,-NO2 , grupo alifático opcionalmente sustituido, fenilo opcionalmente sustituido, heterociclilo opcionalmente sustituido, heteroarilo opcionalmente sustituido, -ORA, -N(Rb)2, -SRA -C(=O)RA, -C(=O)ORa, -C(=O)SRa, -C(=O)N(Rb)2, -OC(=O)Ra, -NRbC(=O)Ra, -NRbC(=O)N(Rb)2, -OC(=O)N(RB)2, -NRbC(=O)ORA, -SC(=O)Ra -C(=NRb)Ra, -C(=NRb)N(Rb)2, -NRbC(=NRb)Rb, -C(=S)RA, -C(=S)N(Rb)2, -NRBC(=S)RA, -S(=O)Ra, -SO2RA, -NRbSO2Ra y -SO2N(Rb)2; o dos grupos R7 adyacentes se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico, condensado opcionalmente sustituido; o R2 y R7 se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico, condensado opcionalmente sustituido;
cada Ra es independientemente hidrógeno, grupo alifático opcionalmente sustituido, carbociclilo opcionalmente sustituido, heterociclilo opcionalmente sustituido, arilo opcionalmente sustituido o heteroarilo opcionalmente sustituido; y
cada Rb es independientemente hidrógeno, grupo alifático opcionalmente sustituido, carbociclilo opcionalmente sustituido, heterociclilo opcionalmente sustituido, arilo opcionalmente sustituido, heteroarilo opcionalmente sustituido, o dos grupos RB se toman junto con sus átomos intermedios para formar un anillo heterocíclico opcionalmente sustituido; y
n es 0, 1, 2, 3 o 4, según permita la valencia.
En algunas realizaciones, Anillo A es un heteroarilo de 5 a 6 miembros.
En determinadas realizaciones, un compuesto proporcionado es de fórmula IlI-a:
o una de sus sales farmacéuticamente aceptables en la que R3, R5a, y R5b, R7 y n son como se definen para la fórmula III, y R2 se selecciona del grupo que consiste en grupo alifático opcionalmente sustituido, arilo opcionalmente sustituido y heteroarilo opcionalmente sustituido; o R2' y R7 se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico, condensado opcionalmente sustituido; en la que arilo tiene de 6 a 14 átomos de carbono en el anillo; y en la que heteroarilo es de 5 a 10 miembros, y monocíclico o bicíclico, y tiene de 1 a 4 heteroátomos en el anillo seleccionados independientemente del grupo que consiste en nitrógeno, oxígeno y azufre.
En determinadas realizaciones, un compuesto proporcionado es de fórmula III-a-i o III-a-ii:
o una de sus sales farmacéuticamente aceptables.
Como se define en general anteriormente, R1 y R2 se seleccionan independientemente del grupo que consiste en grupo alifático opcionalmente sustituido, arilo opcionalmente sustituido y heteroarilo opcionalmente sustituido; o R1 y R2 se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido, en el que el anillo formado por R1 y R2 puede estar condensado opcionalmente a un anillo arilo o heteroarilo. Como se define en general anteriormente, R1 y R2 se seleccionan independientemente del grupo que consiste en grupo alifático opcionalmente sustituido, arilo opcionalmente sustituido y heteroarilo opcionalmente sustituido, o R1 y R2 se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido, en el que el anillo formado por R1 y R2 puede estar condensado opcionalmente a un anillo arilo o heteroarilo.
En algunas realizaciones, R1 o R1 es grupo alifático opcionalmente sustituido. En determinadas realizaciones, R1 o R1 es alquilo opcionalmente sustituido. En determinadas realizaciones, R1 o R1 es alquilo sin sustituir. En determinadas realizaciones, R1 o R1 es alquilo sustituido. En determinadas realizaciones, R1 o R1 es metilo, etilo o propilo. En determinadas realizaciones, R1 o R1 es metilo. En determinadas realizaciones, R1 o R1 es cicloalquilo opcionalmente sustituido. En determinadas realizaciones, R1 o R1 es ciclopropilo, ciclobutilo, ciclopentilo o ciclohexilo. En determinadas realizaciones, R1 o R1 es alquenilo opcionalmente sustituido. En determinadas realizaciones, R1 o R1 es alquenilo sin sustituir. En determinadas realizaciones, R1 o R1 es alquenilo sustituido. En determinadas realizaciones, R1 o R1 es alquinilo opcionalmente sustituido. En determinadas realizaciones, R1 o R1 es alquinilo sin sustituir. En determinadas realizaciones, R1 o R1 es alquinilo sustituido. En algunas realizaciones, R1 o R1 es arilo opcionalmente sustituido. En determinadas realizaciones, R1 o R1 es fenilo opcionalmente sustituido.
En determinadas realizaciones, R1 o R1 es fenilo sin sustituir. En determinadas realizaciones, R1 o R1 es fenilo sustituido. En algunas realizaciones, R1 o R1 es heteroarilo opcionalmente sustituido. En determinadas realizaciones, R1 o R1 es un heteroarilo de 5 a 6 miembros opcionalmente sustituido que tiene 1-3 heteroátomos seleccionados de nitrógeno, oxígeno y azufre. En determinadas realizaciones, R1 o R1 es heteroarilo sin ¡ sustituir. En determinadas realizaciones, R1 o R1 es heteroarilo sustituido. En determinadas realizaciones, R1 o R1 es tiofenilo opcionalmente sustituido. En determinadas realizaciones, R1 o R1 es tiofenilo sin sustituir. En determinadas realizaciones, R1 o R1 es tiofenilo sustituido. En determinadas realizaciones, R1 o R1 es 2-tiofenilo opcionalmente sustituido. En determinadas realizaciones, R1 o R1 es 3-tiofenilo opcionalmente sustituido. En algunas realizaciones, R1 o R1 es piridilo opcionalmente sustituido. En determinadas realizaciones, R1 o R1 es piridilo sin sustituir. En determinadas realizaciones, R1 o R1 es piridilo sustituido. En determinadas realizaciones, R1 o R1 es 2-piridilo opcionalmente sustituido. En determinadas realizaciones, R1 o R1 es 3-piridilo opcionalmente sustituido. En determinadas realizaciones, R1 o R1 es 4-piridilo opcionalmente sustituido. En determinadas realizaciones, R1 o R1 es heteroarilo de 9 a 10 miembros opcionalmente sustituido que tiene 1-4 heteroátomos seleccionados de nitrógeno, oxígeno y azufre. En determinadas realizaciones, R1 o R1 es benzoxadiazolilo opcionalmente sustituido.
En algunas realizaciones, R2 o R2 es grupo alifático opcionalmente sustituido. En determinadas realizaciones, R2 o R2 es alquilo opcionalmente sustituido. En determinadas realizaciones, R2 o R2 es alquilo sin sustituir. En determinadas realizaciones, R2 o R2 es alquilo sustituido. En determinadas realizaciones, R2 o R2 es metilo, etilo o propilo. En determinadas realizaciones, R2 o R2 es metilo. En determinadas realizaciones, R2 o R2 es etilo. En determinadas realizaciones, R2 o R2 es propilo. En determinadas realizaciones, R2 o R2 es cicloalquilo opcionalmente sustituido. En determinadas realizaciones, R2 o R2 es ciclopropilo, ciclobutilo, ciclopentilo o ciclohexilo. En determinadas realizaciones, R2 o R2 es alquenilo opcionalmente sustituido. En determinadas realizaciones, R2 o R2 es alquenilo sin sustituir. En determinadas realizaciones, R2 o R2 es alquenilo sustituido. En determinadas realizaciones, R2 o R2 es alquinilo opcionalmente sustituido. En determinadas realizaciones, R2 o R2 es alquinilo sin sustituir. En determinadas realizaciones, R2 o R2 es alquinilo sustituido. En algunas realizaciones, R2 o R2 es arilo opcionalmente sustituido. En determinadas realizaciones, R2 o R2 es fenilo opcionalmente sustituido. En determinadas realizaciones, R2 o R2 es fenilo sin sustituir. En determinadas realizaciones, R2 o R2 es fenilo sustituido. En algunas realizaciones, R2 o R2 es heteroarilo opcionalmente sustituido. En determinadas realizaciones, R2 o R2 es un heteroarilo de 5-6 miembros opcionalmente sustituido que tiene 1-3 heteroátomos seleccionados de nitrógeno, oxígeno y azufre. En determinadas realizaciones, R2 o R2 es heteroarilo sin sustituir. En determinadas realizaciones, R2 o R2 es heteroarilo sustituido. En determinadas realizaciones, R2 o R2 es heteroarilo sin sustituir. En determinadas realizaciones, R2 o R2 es heteroarilo sustituido. En determinadas realizaciones, R2 o R2 es tiofenilo opcionalmente sustituido. En determinadas realizaciones, R2 o R2 es tiofenilo sin sustituir. En determinadas realizaciones, R2 o R2 es tiofenilo sustituido. En determinadas realizaciones, R2 o R2 es 2-tiofenilo opcionalmente sustituido. En determinadas realizaciones, R2 o R2 es 3-tiofenilo opcionalmente sustituido. En algunas realizaciones, R2 o R2 es piridilo opcionalmente sustituido. En determinadas realizaciones, R2 o R2 es piridilo sin sustituir. En determinadas realizaciones, R2 o R2 es piridilo sustituido. En determinadas realizaciones, R2 o R2 es 2-piridilo opcionalmente sustituido. En determinadas realizaciones, R2 o R2 es 3-piridilo opcionalmente sustituido. En determinadas realizaciones, R2 o R2 es 4-piridilo opcionalmente sustituido. En determinadas realizaciones, R2 o R2 es heteroarilo de 9 a 10 miembros opcionalmente sustituido que tiene 1-4 heteroátomos seleccionados de nitrógeno, oxígeno y azufre. En determinadas realizaciones, R2 o R2 es benzoxadiazolilo opcionalmente sustituido.
En algunas realizaciones R1 es fenilo opcionalmente sustituido, y R2 es grupo alifático opcionalmente sustituido. En algunas realizaciones, R1 es heteroarilo opcionalmente sustituido, y R2 es grupo alifático opcionalmente sustituido. En algunas realizaciones, R1 es grupo alifático opcionalmente sustituido, y R2 es grupo alifático opcionalmente sustituido. En algunas realizaciones, R1 es fenilo opcionalmente sustituido, y R2 es metilo. En algunas realizaciones, R1 es heteroarilo opcionalmente sustituido, y R2 es metilo. En algunas realizaciones, R1 es grupo alifático opcionalmente sustituido, y R2 es metilo. En algunas realizaciones, R1 es fenilo opcionalmente sustituido, y R2 es grupo alifático opcionalmente sustituido. En algunas realizaciones, R1 es heteroarilo opcionalmente sustituido, y R2 es grupo alifático opcionalmente sustituido. En algunas realizaciones, R1 es grupo alifático opcionalmente sustituido, y R2 es grupo alifático opcionalmente sustituido. En algunas realizaciones, R1 es fenilo opcionalmente sustituido, y R2 es metilo. En algunas realizaciones, R1 es heteroarilo opcionalmente sustituido, y R2 es metilo. En algunas realizaciones, R1 es grupo alifático opcionalmente sustituido, y R2 es metilo. En determinadas realizaciones, al menos uno de R1, R , R2 y J R2 es etilo. En d 1'eterm 2'inadas realizaciones, al menos uno de R1 y J R2 es etilo. En determinadas realizaciones, al menos uno de R y R es etilo.
En determinadas realizaciones, R1 y R2 o R1 y R2 se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido. En determinadas realizaciones, R1 y R2 se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido, en el que el anillo está condensado a un anillo arilo o heteroarilo (por ejemplo, para formar un anillo indano).
Como se define en general anteriormente, R3 se selecciona del grupo que consiste en hidrógeno, halo, -CN, -NO2, grupo alifático opcionalmente sustituido, fenilo opcionalmente sustituido, heterociclilo opcionalmente sustituido, heteroarilo opcionalmente sustituido, -ORA, -N(RB)2, -SRA, -C(=O)RA,-C(=O)ORA, -C(=O)SRA, -C(=O)N(RB)2 , OC(=O)Ra, -NRBC(=O)RA, -NRBC(=O)N(RB)2, -OC(=O)N(RB)2, -NRbC(=O)ORa, -SC(=O)RA, -C(=NRb)Ra, -C(=NRb)N(Rb)2 , -NRbC(=NRb)Rb, -C(=S)Ra, -C(=S)N(RB)2, -NRbC(=S)RA, -S(=O)RA, -SO2RA, -NRBSO2RA y -s 02N(Rb)2, en los que RA y RB son como se describen en la presente memoria. En determinadas realizaciones, R3 es hidrógeno. En determinadas realizaciones, R3 no es hidrógeno. En determinadas realizaciones, R3 es -OH. En determinadas realizaciones, R3 no es -OH. En determinadas realizaciones, R3 es metilo. En determinadas realizaciones, R3 no es metilo. En algunas realizaciones, R3 es grupo alifático opcionalmente sustituido. En determinadas realizaciones, R3 es alquilo opcionalmente sustituido. En determinadas realizaciones, R3 es alquilo sin sustituir. En determinadas realizaciones, R3 es alquilo sustituido. En determinadas realizaciones, R3 es metilo, etilo, n-propilo, isopropilo o terc-butilo. En determinadas realizaciones, R es metilo. En determinadas realizaciones, R es isopropilo. En determinadas realizaciones, R3 es terc-butilo. En determinadas realizaciones, R3 es isobutilo. En determinadas realizaciones, R3 es haloalquilo. En determinadas realizaciones, R3 es trifluorometilo. En determinadas realizaciones, R3 es alquenilo opcionalmente sustituido. En determinadas realizaciones, R3 es alquenilo sin sustituir. En determinadas realizaciones, R3 es alquenilo sustituido. En determinadas realizaciones, R3 es alquinilo opcionalmente sustituido. En determinadas realizaciones, R3 es alquinilo sin sustituir. En determinadas realizaciones, R3 es alquinilo sustituido. En algunas realizaciones, R3 es halo. En determinadas realizaciones, R3 es flúor. En determinadas realizaciones, R3 es cloro. En determinadas realizaciones, R3 es bromo. En determinadas realizaciones, R3 es cicloalquilo sin sustituir. En determinadas realizaciones, R3 es ciclopropilo. En determinadas realizaciones, R3 es ciclobutilo. En determinadas realizaciones, R3 es ciclopentilo. En determinadas realizaciones, R3 es ciclohexilo. En determinadas realizaciones, R3 es cicloalquilo sustituido. En determinadas realizaciones, R3 es cicloalquilo sustituido con uno o más de flúor. En determinadas realizaciones, R3 es ciclopropilo sustituido con uno o más de flúor. En determinadas realizaciones, R3 es ciclobutilo sustituido con uno o más de flúor. En determinadas realizaciones, R3 es difluorociclobutilo. En determinadas realizaciones, R3 es ciclopentilo sustituido con uno o más de flúor. En determinadas realizaciones, R3 es ciclohexilo sustituido con uno o más de flúor. En algunas realizaciones, R3 es fenilo opcionalmente sustituido, heterociclilo opcionalmente sustituido o heteroarilo opcionalmente sustituido. En determinadas realizaciones, R3 es fenilo. En algunas realizaciones, R3 es -N(RB)2 o -SRA. En determinadas realizaciones, R es -OR . En determinadas realizaciones, R es -OR , en el que R no es hidrógeno. En algunas realizaciones, R3 es-C(=O)RA, -C(=O)ORA, -C(=O)SRA, -C(=O)N(RB)2 , -OC(=O)RA, -NRBC(=O)RA, -NRBC(=O)N(RB)2 , -OC(=O)N(RB)2 , -NRBC(=O)ORA, -SC(=O)RA, -C(=NRB)RA, -C(=NRB)N(RB)2, -NRBC(=NRB)RB, -C(=S)RA, -C(=S)N(Rb)2, -NRbC(=S)Ra, -S(=O)Ra, -SO2Ra, -NRbSO2Ra o -SO2N(Rb)2.
Como se define en general anteriormente, R se selecciona del grupo que consiste en halo, -CN, -NO2, alquilo C1 sustituido, alquilo C2-6 opcionalmente sustituido, alcoxi opcionalmente sustituido, alquenilo opcionalmente sustituido, alquinilo opcionalmente sustituido, carbociclilo opcionalmente sustituido, fenilo opcionalmente sustituido, heterociclilo opcionalmente sustituido, heteroarilo opcionalmente sustituido, -N(RB)2, -SRA, -C(=O)RA, -C(=O)ORA, -C(=O)SRA, -C(=O)N(Rb)2, -OC(=O)Ra, -NRbC(=O)Ra, -NRbC(=O)N(Rb)2, -OC(=O)N(Rb)2, -NRbC(=O)ORa, -SC(=O)Ra, -C(=NRb)r a7 -C(=NRb)N(Rb)2, -NRbC(=NRb)Rb, -C(=S)Ra, '-C(=S)N(Rb)2 ; -NRbC(=S)RA, -S(=O)RA, -SO2RA, NRbSO2Ra y -SO2N(Rb)2 , en los que RA y RB son como se describen en la presente memoria. En algunas realizaciones, R3 es grupo alifático C1 sustituido. En determinadas realizaciones, R3 es -CF3. En determinadas realizaciones, R3 es alquilo C2-6 opcionalmente sustituido. En determinadas realizaciones, R3 es alquilo C2-6 sin sustituir. En determinadas realizaciones, R3 es alquilo C2-6 sustituido. En determinadas realizaciones, R3 es metilo, etilo, n-propilo, isopropilo, terc-butilo o isobutilo. En determinadas realizaciones, R3 es haloalquilo. En determinadas realizaciones, R3 es trifluorometilo. En determinadas realizaciones, R3 es alquenilo opcionalmente sustituido. En determinadas realizaciones, R3 es alquenilo sin sustituir. En determinadas realizaciones, R3 es alquenilo sustituido. En determinadas realizaciones, R3 es alquinilo opcionalmente sustituido. En determinadas realizaciones, R3 es alquinilo sin sustituir. En determinadas realizaciones, R3 es alquinilo sustituido. En algunas realizaciones, R3 es alcoxi opcionalmente sustituido. En determinadas realizaciones, R3 es metoxi o etoxi. En algunas realizaciones, R3 es halo. En determinadas realizaciones, R3 es flúor. En determinadas realizaciones, R3 es cloro. En determinadas realizaciones, R3 es bromo. En determinadas realizaciones, R3 es carbociclilo sin sustituir. En determinadas realizaciones, R3 es cicloalquilo sin sustituir. En determinadas realizaciones, R3 es ciclopropilo. En determinadas realizaciones, R3 es ciclobutilo. En determinadas realizaciones, R3 es ciclopentilo. En determinadas realizaciones, R3 es ciclohexilo. En determinadas realizaciones, R3 es carbociclilo sustituido. En determinadas realizaciones, R3 es cicloalquilo sustituido. En determinadas realizaciones, R3 es carbociclilo sustituido con uno o más de flúor. En determinadas realizaciones, R3 es ciclobutilo sustituido con uno o más de flúor. En determinadas realizaciones, R3 es difluorociclobutilo. En determinadas realizaciones, R3 es cicloalquenilo opcionalmente sustituido. En determinadas realizaciones, R3 es cicloalquinilo opcionalmente sustituido. En algunas realizaciones, R3 es fenilo opcionalmente sustituido, heterociclilo opcionalmente sustituido o heteroarilo opcionalmente sustituido. En determinadas realizaciones, R3 es fenilo. En algunas realizaciones, R3 es -N(Rb)2 o -SRa. En algunas realizaciones, R3' es -C(=O)Ra, -C(=O)ORa, -C(=O)SRa, -C(=O)N(Rb)2 , -OC(=O)Ra, -NRbC(=O)Ra, -NRbC(=O)N(Rb)2 , -OC(=O)N(Rb)2, -NRbC(=O)ORa, -SC(=O)RA, -C(=NRb)Ra, -C(=NRB)N(Rb)2 , -NRbC(=NRb)Rb, -C(=S)Ra, -C(=S)N(Rb)2, -NRbC(=S)Ra, -S(=O)Ra, -SO2Ra, -NRbSO2RA o -SO2N(Rb)2.
En determinadas realizaciones, R3 o R3 es flúor. En determinadas realizaciones, R3 o R3 es grupo alifático opcionalmente sustituido. En determinadas realizaciones, R3 o R3' es metilo. En determinadas realizaciones, R3 o R3' es trifluorometilo. En determinadas realizaciones, R3 o R3 es ferc-butilo o isobutilo. En determinadas realizaciones, R3 o R3 es ciclopropilo. En determinadas realizaciones, R3 o R3 es difluorociclobutilo.
Como se define en general anteriormente, R4a y R4b se seleccionan independientemente del grupo que consiste en hidrógeno, halo, -CN, -ORA, -N(RB)2 y grupo alifático opcionalmente sustituido, o R4a y R4b se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido. En determinadas realizaciones, R4a es hidrógeno. En determinadas realizaciones, R4a no es hidrógeno. En algunas realizaciones, R4b es hidrógeno. En algunas realizaciones, R4b no es hidrógeno. En algunas realizaciones, R4a y R4b son ambos hidrógeno. En algunas realizaciones, R4a y R4b no son ambos hidrógeno. En determinadas realizaciones, R4a es hidrógeno y R4b no es hidrógeno. En determinadas realizaciones, R4a y R4b son ambos grupo alifático opcionalmente sustituido. En determinadas realizaciones, R4a y R4b son metilo.
Como se define en general anteriormente, R5a y R5b se seleccionan independientemente del grupo que consiste en hidrógeno, halo, -CN, -ORA, -N(RB)2 y grupo alifático opcionalmente sustituido, o R5a y R5b se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido. En determinadas realizaciones, R5a es hidrógeno. En determinadas realizaciones, R5a no es hidrógeno. En algunas realizaciones, R5b es hidrógeno. En algunas realizaciones, R5b no es hidrógeno. En algunas realizaciones, R5a y R5b son ambos hidrógeno. En algunas realizaciones, R5a y R5b no son ambos hidrógeno. En determinadas realizaciones, R5a es hidrógeno y R5b no es hidrógeno. En determinadas realizaciones, R5a y R5b son ambos grupo alifático opcionalmente sustituido. En determinadas realizaciones, R5a y R5b son metilo.
Como se define en general anteriormente, R6a y R6b se seleccionan independientemente del grupo que consiste en hidrógeno, halo, -CN, -ORA, -N(RB)2 y grupo alifático opcionalmente sustituido, o R6a y R6b se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido. En determinadas realizaciones, R6a es hidrógeno. En determinadas realizaciones, R6a no es hidrógeno. En algunas realizaciones, R6b es hidrógeno. En algunas realizaciones, R6b no es hidrógeno. En algunas realizaciones, R6a y R6b son ambos hidrógeno. En algunas realizaciones, R6a y R6b no son ambos hidrógeno. En determinadas realizaciones, R6a es hidrógeno y R6b no es hidrógeno. En determinadas realizaciones, R6a y R6b son ambos grupo alifático opcionalmente sustituido. En determinadas realizaciones, R6a y R6b son metilo.
En algunas realizaciones, R4a, R4b, R6a y R6b son hidrógeno, y R5a y R5b se seleccionan independientemente del grupo que consiste en hidrógeno, halo, -CN, -OR A , -N(R B )2 y grupo alifático opcionalmente sustituido, o R 5a y R 5b se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido. En determinadas realizaciones, R4a, R4b, R6a y R6b son hidrógeno, y R5a y R5b son metilo.
En algunas realizaciones, R4a, R4b, R5a y R5b son hidrógeno, y R6a y R6b se seleccionan independientemente del grupo que consiste en hidrógeno, halo, -Cn , -ORa, -N(Rb)2 y grupo alifático opcionalmente sustituido, o R6a y R6b se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido. En determinadas realizaciones, R4a, R4b, R5a y R5b son hidrógeno, y R6a y R6b son metilo.
En algunas realizaciones, R5a, R5b, R6a y R6b son hidrógeno, y R4a y R4b se seleccionan independientemente del grupo que consiste en hidrógeno, halo, -Cn , -ORa, -N(Rb)2 y grupo alifático opcionalmente sustituido, o R4a y R4b se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido. En determinadas realizaciones, R5a, R5b, R6a y R6b son hidrógeno, y R4a y R4b son metilo.
En algunas realizaciones, R4a, R4b, R5a, R5 R6a y R6b son hidrógeno.
Como se define en general anteriormente, cada R7 se selecciona independientemente del grupo que consiste en hidrógeno, halo, -CN,-NO2, grupo alifático opcionalmente sustituido, fenilo opcionalmente sustituido, heterociclilo opcionalmente sustituido, heteroarilo opcionalmente sustituido, -ORA, -N(RB)2 , -SRa, -C(=O)Ra, -C(=O)ORa, -C(=O)SRa, -C(=O)N(Rb)2 , -OC(=O)Ra, -NRbC(=O)Ra, -NRbC(=O)N(Rb)2, -OC(=O)N(RbJ2 , -NRbC(=O)ORa, -SC(=O)Ra, -C(=NRb)Ra, -C(=NRb)N(Rb)2, -NRbC(=NRb)Rb, -C(=S)Ra, -C(=S)N(Rb)2, -NRbC(=S)Ra, -S(=O)RA, -SO2Ra, -NRbSO2Ra y -SO2N(Rb)2; o dos grupos R7 adyacentes se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico, condensado opcionalmente sustituido; o R2 y R7 se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico, condensado opcionalmente sustituido.
En algunas realizaciones, R7 es halo. En determinadas realizaciones, R7 es flúor. En determinadas realizaciones, R7 es cloro. En determinadas realizaciones, R7 es bromo. En algunas realizaciones, R7 es grupo alifático opcionalmente sustituido. En determinadas realizaciones, R7 es alquilo opcionalmente sustituido. En determinadas realizaciones, R7 es alquilo sin sustituir. En determinadas realizaciones, R7 es metilo. En determinadas realizaciones, R7 es haloalquilo. En determinadas realizaciones, R7 es trifluorometilo. En algunas realizaciones, R7 es -ORA, -N(Rb)2 , -SRa. En determinadas realizaciones, R7 es -OCH3 o -SCH3. En determinadas realizaciones, R7 es -OCF3. En algunas realizaciones, R7 es -CN. En algunas realizaciones, un grupo R7 es orto. En algunas realizaciones, un grupo R7 es meta. En algunas realizaciones, un grupo R7 es para. En algunas realizaciones, dos grupos R7 adyacentes se toman junto con sus átomos intermedios para formar un anillo carbocíclico (por ejemplo, arilo o carbocíclico saturado) o heterocíclico (por ejemplo, heteroarilo o heterocíclico saturado) condensado opcionalmente sustituido.
Por ejemplo, en algunas realizaciones, dos grupos R7 se toman juntos para formar un grupo metilendioxi condensado. En algunas realizaciones, R2 y R7 se toman junto con sus átomos intermedios para formar un anillo carbocíclico (por ejemplo, arilo o carbocíclico saturado) o heterocíclico (por ejemplo, heteroarilo o heterocíclico saturado) condensado opcionalmente sustituido.
Como se define en general anteriormente, n es 0, 1, 2, 3, 4 o 5, según permita la valencia. En algunas realizaciones, n es 0. En algunas realizaciones, n es 1. En algunas realizaciones, n es 2. En algunas realizaciones, n es 3. En algunas realizaciones, n es 4. En algunas realizaciones, n es 5.
En determinadas realizaciones, un compuesto proporcionado es uno de los siguientes:
10
5
y sus sales farmacéuticamente aceptables.
En determinadas realizaciones, la presente invención proporciona compuestos de fórmula I, y sus sales farmacéuticamente aceptables, en la que:
R1 y R2 se seleccionan independientemente del grupo que consiste en grupo alifático opcionalmente sustituido, arilo opcionalmente sustituido y heteroarilo opcionalmente sustituido; o R1 y R2 se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido, en el que el anillo formado por R1 y R2 puede estar condensado opcionalmente a un anillo arilo o heteroarilo;
R3 es hidrógeno o flúor;
R4a y R4b se seleccionan independientemente del grupo que consiste en hidrógeno, halo, -CN, -ORA, -N(RB)2, y grupo alifático opcionalmente sustituido, o R4a y R4b se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido;
R y R se seleccionan independientemente del grupo que consiste en hidrógeno, halo, -CN, -OR , -N(R )2, y grupo alifático opcionalmente sustituido, o R5a y R5b se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido; y
R6a y R6b se seleccionan independientemente del grupo que consiste en hidrógeno, halo, -CN, -ORA, -N(RB)2 y grupo alifático opcionalmente sustituido, o R6a y R6b se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido;
en los que cada ocasión de arilo tiene independientemente de 6 a 14 átomos de carbono en el anillo; y
en los que cada ocasión de heteroarilo es independientemente de 5 a 10 miembros, y monocíclico o bicíclico, y tiene independientemente de 1 a 4 heteroátomos en el anillo seleccionados independientemente del grupo que consiste en nitrógeno, oxígeno y azufre.
En determinadas realizaciones, la presente invención proporciona compuestos de fórmula I, y sus sales farmacéuticamente aceptables, en la que:
R1 y R2 se seleccionan independientemente del grupo que consiste en grupo alifático opcionalmente sustituido, arilo opcionalmente sustituido, y heteroarilo opcionalmente sustituido, en la que al menos uno de R1 y R2 es etilo;
R3 se selecciona del grupo que consiste en hidrógeno, halo, -CN, -NO2, grupo alifático opcionalmente sustituido, fenilo opcionalmente sustituido, heterociclilo opcionalmente sustituido, heteroarilo opcionalmente sustituido, -ORA, -N(Rb)2, -SRa, -C(=O)RA, -C(=O)ORa, -C(=O)SRa, -C(=O)N(Rb)2, -OC(=O)RA -NRbC(=O)Ra, -NRbC(=O)N(Rb)2, -OC(=O)N(Rb)2, -NRBC(=0)ORa, -SC(=O)Ra, -C(=NRB)RA -C(=NRb)N(RB)2, -NRbC(=NRb)Rb, -C(=S)Ra, -C(=S)N(RB)2, -NRBC(=S)Ra, -S(=O)Ra, -SO2Ra, -NRBSO2RAy -SO2N(RB)2;
cada Ra se selecciona independientemente del grupo que consiste en hidrógeno, grupo alifático opcionalmente sustituido, carbociclilo opcionalmente sustituido, heterociclilo opcionalmente sustituido, arilo opcionalmente sustituido y heteroarilo opcionalmente sustituido;
cada RB se selecciona independientemente del grupo que consiste en hidrógeno, grupo alifático opcionalmente sustituido, carbociclilo opcionalmente sustituido, heterociclilo opcionalmente sustituido, arilo opcionalmente sustituido y heteroarilo opcionalmente sustituido, o dos grupos RB se toman junto con sus átomos intermedios para formar un anillo heterocíclico opcionalmente sustituido;
R4a y R4b se seleccionan independientemente del grupo que consiste en hidrógeno, halo, -CN, -ORa, -N(RB)2, y grupo alifático opcionalmente sustituido, o R4a y R4b se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido;
R y R se seleccionan independientemente del grupo que consiste en hidrógeno, halo, -CN, -OR , -N(R )2, y grupo alifático opcionalmente sustituido, o R5a y R5b se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido; y
R6a y R6b se seleccionan independientemente del grupo que consiste en hidrógeno, halo, -CN, -ORa, -N(RB)2 y grupo alifático opcionalmente sustituido, o R6a y R6b se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido;
en los que cada ocasión de arilo tiene independientemente de 6 a 14 átomos de carbono en el anillo; y
en los que cada ocasión de heteroarilo es independientemente de 5 a 10 miembros, y monocíclico o bicíclico, y tiene independientemente de 1 a 4 heteroátomos en el anillo seleccionados independientemente del grupo que consiste en nitrógeno, oxígeno y azufre.
En determinadas realizaciones, un compuesto proporcionado inhibe una cinasa, o un mutante o variante de la misma. En determinadas realizaciones, un compuesto proporcionado inhibe GSK3. En determinadas realizaciones, un compuesto proporcionado inhibe CK1. En determinadas realizaciones, un compuesto proporcionado inhibe una cinasa (por ejemplo, GSK3 o CK1), por ejemplo, como se mide en un ensayo descrito en la presente memoria. En determinadas realizaciones, un compuesto proporcionado inhibe la cinasa (por ejemplo, GSK3 o CK1) a una CI50 de menos de o igual a 30 pM. En determinadas realizaciones, un compuesto proporcionado inhibe la cinasa a una CI50 de menos de o igual a 5 pM. En determinadas realizaciones, un compuesto proporcionado inhibe la cinasa a una CI 50 de menos de o igual a 1 pM. En determinadas realizaciones, un compuesto proporcionado inhibe la cinasa a una CI50 de menos de o igual a 0,1 pM. En determinadas realizaciones, el compuesto es selectivo para GSK3 en comparación con otras cinasas. En determinadas realizaciones, el compuesto es selectivo para GSK3a y GSK3p en comparación con otras cinasas. En determinadas realizaciones, el compuesto es selectivo para GSK3a en comparación con otras cinasas. En determinadas realizaciones, el compuesto es selectivo para GSK3p en comparación con otras cinasas. En determinadas realizaciones, el compuesto es selectivo para GSK3 en comparación con CDK5. En determinadas realizaciones, el compuesto es al menos 10 veces más activo contra GSK3 que contra otras cinasas (por ejemplo, CDK5). En determinadas realizaciones, el compuesto es al menos 5 veces más activo contra GSK3 que contra otras cinasas (por ejemplo, CDK5). En determinadas realizaciones, el compuesto es al menos 2 veces más activo contra GSK3 que contra otras cinasas (por ejemplo, CDK5). En determinadas realizaciones, el compuesto es selectivo para CK1 en comparación con otras cinasas. En determinadas realizaciones, el compuesto es selectivo para CK1 en comparación con CDK5. En determinadas realizaciones, el compuesto es al menos 10 veces más activo contra CK1 que contra otras cinasas (por ejemplo, CDK5). En determinadas realizaciones, el compuesto es al menos 5 veces más activo contra CK1 que contra otras cinasas (por ejemplo, CDK5). En determinadas realizaciones, el compuesto es al menos 2 veces más activo contra CK1 que contra otras cinasas (por ejemplo, CDK5). En determinadas realizaciones, un inhibidor selectivo de GSK3a es ventajoso sobre un inhibidor de GSK3 global. En determinadas realizaciones, un inhibidor selectivo de GSK3p es
ventajoso sobre un inhibidor de GSK3 global.
Métodos de preparación de los compuestos
En un aspecto, la presente invención proporciona métodos de preparación de los compuestos descritos en la presente memoria (por ejemplo, compuestos de fórmula I, y sus sales). En determinadas realizaciones, los métodos de la invención incluyen poner en contacto un compuesto de fórmula A, o una de sus sales, con un compuesto de fórmula B, o una de sus sales, y un compuesto de fórmula C, o una de sus sales, en condiciones adecuadas para proporcionar el compuesto de fórmula I, o su sal:
en la que:
R1 y R2 se seleccionan independientemente del grupo que consiste en grupo alifático opcionalmente sustituido, arilo opcionalmente sustituido y heteroarilo opcionalmente sustituido; o R1 y R2 se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido, en el que el anillo formado por R1 y R2 puede estar condensado opcionalmente a un anillo arilo o heteroarilo;
R3 se selecciona del grupo que consiste en hidrógeno, halo, -CN, -NO2, grupo alifático opcionalmente sustituido, fenilo opcionalmente sustituido, heterociclilo opcionalmente sustituido, heteroarilo opcionalmente sustituido, -ORA, -N(Rb)2, -SRa, -C(=O)Ra, -C(=O)ORa, -C(=O)SRa, -C(=O)N(Rb)2, -OC(=O)Ra -NRbC(=O)Ra, -NRbC(=O)N(Rb)2, -OC(=O)N(Rb)2, -NRBC(=O)ORa, -SC(=O)Ra, -C(=NRb)RA, -C(=NRb)N(RB)2, -NRbC(=NRb)Rb, -C(=S)Ra, -C(=S)N(RB)2, -NRBC(=S)Ra, -S(=O)Ra, -SO2Ra, -NRBSO2RAy -SO2N(RB)2;
cada Ra se selecciona independientemente del grupo que consiste en hidrógeno, grupo alifático opcionalmente sustituido, carbociclilo opcionalmente sustituido, heterociclilo opcionalmente sustituido, arilo opcionalmente sustituido y heteroarilo opcionalmente sustituido;
cada RB se selecciona independientemente del grupo que consiste en hidrógeno, grupo alifático opcionalmente sustituido, carbociclilo opcionalmente sustituido, heterociclilo opcionalmente sustituido, arilo opcionalmente sustituido y heteroarilo opcionalmente sustituido, o dos grupos RB se toman junto con sus átomos intermedios para formar un anillo heterocíclico opcionalmente sustituido;
R4a y R4b se seleccionan independientemente del grupo que consiste en hidrógeno, halo, -CN, -ORa, -N(RB)2, y grupo alifático opcionalmente sustituido, o R4a y R4b se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido;
R y R se seleccionan independientemente del grupo que consiste en hidrógeno, halo, -CN, -OR , -N(R )2, y grupo alifático opcionalmente sustituido, o R5a y R5b se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido; y
r 6A y R6b se seleccionan independientemente del grupo que consiste en hidrógeno, halo, -CN, -ORa, -N(RB)2 y grupo alifático opcionalmente sustituido, o R6a y R6b se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido;
en los que cada ocasión de arilo tiene independientemente de 6 a 14 átomos de carbono en el anillo; y
en los que cada ocasión de heteroarilo es independientemente de 5 a 10 miembros, y monocíclico o bicíclico, y tiene independientemente de 1 a 4 heteroátomos en el anillo seleccionados independientemente del grupo que consiste en nitrógeno, oxígeno y azufre.
En otro aspecto, la presente invención proporciona métodos de preparación de un compuesto de fórmula I':
o una de sus sales, incluyendo el método:
poner en contacto un compuesto de fórmula C, o una de sus sales, con un compuesto de fórmula D, o una de sus sales, en condiciones adecuadas para proporcionar un compuesto de fórmula E, o una de sus sales:
conjugar el compuesto de fórmula E, o su sal, con un compuesto de fórmula A, o una de sus sales, en condiciones adecuadas para proporcionar un compuesto de fórmula F, o una de sus sales:
ciclar el compuesto de fórmula F, o su sal, en condiciones adecuadas para proporcionar el compuesto de fórmula I', o su sal, en la que:
R1a y R1b se seleccionan independientemente del grupo que consiste en hidrógeno y grupo alifático opcionalmente sustituido, o R1a y R1b se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado o insaturado de 3 a 7 miembros opcionalmente sustituido, en el que el anillo formado por R1a y R1b puede estar condensado be opcionalmente a un anillo arilo o heteroarilo;
R2 se selecciona del grupo que consiste en grupo alifático opcionalmente sustituido, arilo opcionalmente sustituido y heteroarilo opcionalmente sustituido, o R1a y R2 se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado o insaturado de 3 a 7 miembros opcionalmente sustituido, en el que el anillo formado por R1a y R2 puede estar condensado opcionalmente a un anillo arilo o heteroarilo;
R3 se selecciona del grupo que consiste en hidrógeno, halo, -CN, -NO2, grupo alifático opcionalmente sustituido, fenilo opcionalmente sustituido, heterociclilo opcionalmente sustituido, heteroarilo opcionalmente sustituido, -ORA, -N(Rb)2, -SRa, -C(=O)RA, -C(=O)ORA, -C(=O)SRA, -C( O)N(RB)2, -OC(=O)R AA -NRBC(=O)RA, -NRBC(=O)N(R ->BB)\2, OC(=O)N(RB)2, -NRBC(=O)ORA, -SC(=O)RA -C(=NRb)RA, -C(=NRb)N(RB)2, -NRbC(=NRb)Rb, -C(=S)Ra, C(=S)N(RB)2, -NRbC(=S)Ra, -S(=O)RA, -SO2RA, NRBSO2RAy -SO2N(RB)2;
cada RA se selecciona independientemente del grupo que consiste en hidrógeno, grupo alifático opcionalmente sustituido, carbociclilo opcionalmente sustituido, heterociclilo opcionalmente sustituido, arilo opcionalmente sustituido y heteroarilo opcionalmente sustituido;
cada Rb se selecciona independientemente del grupo que consiste en hidrógeno, grupo alifático opcionalmente sustituido, carbociclilo opcionalmente sustituido, heterociclilo opcionalmente sustituido, arilo opcionalmente sustituido y heteroarilo opcionalmente sustituido, o dos grupos RB se toman junto con sus átomos intermedios para formar un anillo heterocíclico opcionalmente sustituido;
R4a y R4b se seleccionan independientemente del grupo que consiste en hidrógeno, halo, -CN, -ORA, -N(RB)2, y grupo alifático opcionalmente sustituido, o R4a y R4b se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido;
R y R se seleccionan independientemente del grupo que consiste en hidrógeno, halo, -CN, -OR , -N(R )2, y grupo alifático opcionalmente sustituido, o R5a y R5b se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido;
R6a y R6b se seleccionan independientemente del grupo que consiste en hidrógeno, halo, -CN, -ORA, -N(RB)2 y grupo alifático opcionalmente sustituido, o R6a y R6b se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido;
R1a y R1b se seleccionan independientemente del grupo que consiste en hidrógeno y grupo alifático opcionalmente sustituido;
en los que cada ocasión de arilo tiene independientemente de 6 a 14 átomos de carbono en el anillo; y
en los que cada ocasión de heteroarilo es independientemente de 5 a 10 miembros, y monocíclico o bicíclico, y tiene independientemente de 1 a 4 heteroátomos en el anillo seleccionados independientemente del grupo que consiste en nitrógeno, oxígeno y azufre.
Otro aspecto de la presente invención se refiere a métodos de preparación de un compuesto de fórmula I':
o una de sus sales, comprendiendo el método:
proteger el grupo amino primario de un compuesto de fórmula C, o una de sus sales, para proporcionar un compuesto de fórmula G, o una de sus sales:
halogenar el compuesto de fórmula G, o su sal, para proporcionar un compuesto de fórmula H, o una de sus sales:
proteger el grupo amino secundario del compuesto de fórmula H, o su sal, para proporcionar un compuesto de fórmula J, o una de sus sales;
J;
acoplar el compuesto de fórmula J, o su sal, con un ácido borónico o éster de fórmula K, o una de sus sales, para proporcionar un compuesto de fórmula L, o una de sus sales:
desproteger el grupo amino primario del compuesto de fórmula L, o su sal, para proporcionar un compuesto de fórmula M, o una de sus sales:
conjugar el compuesto de fórmula M, o su sal, con un compuesto de fórmula A, o una de sus sales, para proporcionar un compuesto de fórmula N, o una de sus sales:
desproteger el grupo amino secundario del compuesto de fórmula N, o su sal, para proporcionar un compuesto de fórmula F, o una de sus sales:
ciclar el compuesto de fórmula F, o su sal, en condiciones adecuadas para proporcionar el compuesto de fórmula I', o su sal, en la que:
R1a y R1b se seleccionan independientemente del grupo que consiste en hidrógeno y grupo alifático opcionalmente sustituido, o R1a y R1b se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico
saturado o insaturado de 3 a 7 miembros opcionalmente sustituido, en el que el anillo formado por R1a y R1b puede estar condensado be opcionalmente a un anillo arilo o heteroarilo;
R2 se selecciona del grupo que consiste en grupo alifático opcionalmente sustituido, arilo opcionalmente sustituido y heteroarilo opcionalmente sustituido, o R1a y R2 se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado o insaturado de 3 a 7 miembros opcionalmente sustituido, en el que el anillo formado por R1a y R2 puede estar condensado opcionalmente a un anillo arilo o heteroarilo;
R3 se selecciona del grupo que consiste en hidrógeno, halo, -CN, -NO2, grupo alifático opcionalmente sustituido, fenilo opcionalmente sustituido, heterociclilo opcionalmente sustituido, heteroarilo opcionalmente sustituido, -ORA, -N(Rb)2, -SRa, -C(=O)RA, -C(=O)ORA, -C(=O)SRA, -C( O)N(RB)2, -OC(=O)R AA -NRBC(=O)RA, -NRBC(=O)N(R ->BB)\2, OC(=O)N(RB)2, -NRBC(=O)ORA, -SC(=O)RA -C(=NRb)RA, -C(=NRb)N(RB)2, -NRbC(=NRb)Rb, -C(=S)Ra, C(=S)N(RB)2, -NRbC(=S)Ra, -S(=O)RA, -SO2RA, NRBSO2RAy -SO2N(RB)2;
cada RA se selecciona independientemente del grupo que consiste en hidrógeno, grupo alifático opcionalmente sustituido, carbociclilo opcionalmente sustituido, heterociclilo opcionalmente sustituido, arilo opcionalmente sustituido y heteroarilo opcionalmente sustituido;
cada Rb se selecciona independientemente del grupo que consiste en hidrógeno, grupo alifático opcionalmente sustituido, carbociclilo opcionalmente sustituido, heterociclilo opcionalmente sustituido, arilo opcionalmente sustituido y heteroarilo opcionalmente sustituido, o dos grupos RB se toman junto con sus átomos intermedios para formar un anillo heterocíclico opcionalmente sustituido;
R4a y R4b se seleccionan independientemente del grupo que consiste en hidrógeno, halo, -CN, -ORA, -N(RB)2, y grupo alifático opcionalmente sustituido, o R4a y R4b se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido;
R 5a y R 5b se seleccionan independientemente del grupo que consiste en hidrógeno, halo, -CN, -OR A , -N(R B )2, y grupo alifático opcionalmente sustituido, o R5a y R5b se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido;
R6a y R6b se seleccionan independientemente del grupo que consiste en hidrógeno, halo, -CN, -ORA, -N(RB)2 y grupo alifático opcionalmente sustituido, o R6a y R6b se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido;
cada ocasión de P1 es independientemente un grupo protector de nitrógeno, o dos ocasiones de P1 se unen para formar un anillo heterocíclico opcionalmente sustituido;
X es halógeno;
P2 es un grupo protector de nitrógeno y es diferente de cualquier ocasión de P1;
R2a y R2b se seleccionan independientemente del grupo que consiste en hidrógeno y grupo alifático opcionalmente sustituido; y
cada ocasión de R8 es independientemente hidrógeno, acilo sustituido o sin sustituir, alquilo sustituido o sin sustituir, carbociclilo sustituido o sin sustituir, heterociclilo sustituido o sin sustituir, arilo sustituido o sin sustituir, o heteroarilo sustituido o sin sustituir, o dos ocasiones de R8 se unen para formar un anillo heterocíclico sustituido o sin sustituir;
en los que cada ocasión de arilo tiene independientemente de 6 a 14 átomos de carbono en el anillo; y
en los que cada ocasión de heteroarilo es independientemente de 5 a 10 miembros, y monocíclico o bicíclico, y tiene independientemente de 1 a 4 heteroátomos en el anillo seleccionados independientemente del grupo que consiste en nitrógeno, oxígeno y azufre.
En determinadas realizaciones, dos ocasiones de P1 se unen para formar ftalimido. En determinadas realizaciones, P2 es EtOCH(CH3)-. En determinadas realizaciones, R1a y R1b cada uno es hidrógeno. En determinadas realizaciones, R3 es hidrógeno, flúor, cloro o metilo. En determinadas realizaciones, R4a, R , R6a y R6b cada uno es hidrógeno. En determinadas realizaciones, X es yodo o bromo. En determinadas realizaciones, X es yodo. En determinadas realizaciones, dos ocasiones de R8 cada una es hidrógeno, o dos ocasiones de R8 se unen para formar un anillo heterocíclico de la fórmula:
En determinadas realizaciones, dos ocasiones de R8 cada una es hidrógeno. En determinadas realizaciones, las condiciones adecuadas comprenden la presencia de un ácido o una temperatura de al menos aproximadamente 25 °C, o una combinación de las mismos. En determinadas realizaciones, las condiciones adecuadas comprenden la presencia de un ácido (por ejemplo, ácido p-toluenosulfónico (PTSA) o ácido trifluoroacético (TFA)). En determinadas realizaciones, las condiciones adecuadas comprenden la presencia de un alcohol (por ejemplo, etanol o metanol). En determinadas realizaciones, las condiciones adecuadas comprenden una temperatura de al menos aproximadamente 25 °C (por ejemplo, al menos aproximadamente 40 °C, al menos aproximadamente 70 °C, al menos aproximadamente 110 °C o al menos aproximadamente 150 °C). En determinadas realizaciones, las condiciones adecuadas comprenden irradiación con microondas. En determinadas realizaciones, las condiciones adecuadas son una combinación de condiciones adecuadas descritas en la presente memoria.
Composiciones farmacéuticas y administración
La presente divulgación proporciona composiciones farmacéuticas que comprenden un compuesto descrito en la presente memoria, por ejemplo, un compuesto de fórmula I, II o III, o una sal farmacéuticamente aceptable del mismo, como se describe en la presente memoria, y opcionalmente un excipiente farmacéuticamente aceptable. Los expertos en la materia entenderán que los compuestos descritos en la presente memoria, o sales de los mismos, pueden estar presentes en diversas formas, por ejemplo, amorfos, hidratos, solvatos o polimorfos. En determinadas realizaciones, un compuesto descrito en la presente memoria se proporciona como un profármaco. En determinadas realizaciones, un compuesto descrito en la presente memoria, o una sal farmacéuticamente aceptable del mismo, se proporciona en una cantidad eficaz en la composición farmacéutica. En determinadas realizaciones, la cantidad eficaz es una cantidad terapéuticamente eficaz. En determinadas realizaciones, la cantidad eficaz es una cantidad eficaz para inhibir una cinasa (por ejemplo, GSK3 o CK1). En determinadas realizaciones, la cantidad eficaz es una cantidad eficaz para tratar un trastorno mediado por cinasas. En determinadas realizaciones, la cantidad eficaz es una cantidad profilácticamente eficaz. En determinadas realizaciones, la cantidad eficaz es una cantidad eficaz para prevenir un trastorno mediado por cinasas.
Los excipientes farmacéuticamente aceptables incluyen todos y cada uno de los disolventes, diluyentes u otros vehículos líquidos, dispersiones, auxiliares de suspensión, agentes tensioactivos, agentes isotónicos, agentes espesantes o emulsionantes, conservantes, aglutinantes sólidos, lubricantes y similares, que son adecuados para la forma galénica particular deseada. Pueden encontrarse consideraciones generales en la formulación y/o fabricación de composiciones farmacéuticas, por ejemplo, en Remington's Pharmaceutical Sciences, decimosexta edición, E. W. Martin (Mack Publishing Co., Easton, Pa., 1980), y Remington: The Science and Practice of Pharmacy, 21.a edición (Lippincott Williams y Wilkins, 2005).
Las composiciones farmacéuticas descritas en la presente memoria pueden prepararse por cualquier método conocido en la técnica de farmacología. En general, dichos métodos preparatorios incluyen las etapas de poner un compuesto descrito en la presente memoria (el "ingrediente activo") en asociación con un vehículo y/o uno o más ingredientes accesorios adicionales y, después, si fuera necesario y/o deseable, conformar y/o envasar el producto en una unidad monodosis o multidosis deseada.
Las composiciones farmacéuticas pueden prepararse, envasarse y/o venderse a granel, como una dosis unitaria y/o como una pluralidad de dosis unitarias. Una "dosis unitaria" es la cantidad concreta de la composición farmacéutica que comprende una cantidad predeterminada del ingrediente activo. La cantidad del ingrediente activo es generalmente igual a la dosificación del ingrediente activo que se administraría a un sujeto y/o una fracción conveniente de dicha dosificación tal como, por ejemplo, una mitad o una tercera parte de dicha dosificación.
Las cantidades relativas del ingrediente activo, el excipiente farmacéuticamente aceptable y/o cualquier ingrediente adicional en la composición farmacéutica de la presente divulgación variarán, dependiendo de la identidad, tamaño y/o afección del sujeto tratado y dependiendo además de la ruta por la que se tiene administrar la composición. A modo de ejemplo, la composición puede comprender entre un 0,1 % y un 100 % (p/p) de ingrediente activo.
Los excipientes farmacéuticamente aceptables usados en la fabricación de composiciones farmacéuticas proporcionadas incluyen diluyentes inertes, agentes dispersantes y/o de granulación, agentes tensioactivos y/o emulsionantes, agentes disgregantes, agentes aglutinantes, conservantes, agentes tamponantes, agentes lubricantes y/o aceites. También pueden estar presentes en la composición excipientes tales como mantea de cacao y ceras de supositorio, agentes colorantes, agentes de recubrimiento, agentes edulcorantes, aromatizantes y perfumantes.
Los diluyentes ejemplares incluyen carbonato de calcio, carbonato de sodio, fosfato de calcio, fosfato de dicalcio, sulfato de calcio, hidrogenofosfato de calcio, fosfato de sodio lactosa, sacarosa, celulosa, celulosa microcristalina, caolín, manitol, sorbitol, inositol, cloruro de sodio, almidón deshidratado, almidón de maíz, azúcar en polvo y mezclas de los mismos.
Los agentes de granulación y/o dispersión ejemplares incluyen almidón de patata, almidón de maíz, almidón de tapioca, almidón glicolato de sodio, arcillas, ácido algínico, goma guar, pulpa de cítrico, agar, bentonita, celulosa y productos de la madera, esponja natural, resinas de intercambio catiónico, carbonato de calcio, silicatos, carbonato de sodio, polivinilpirrolidona reticulada (crospovidona), carboximetilalmidón de sodio, (almidón glicolato de sodio), carboximetilcelulosa, carboximetilcelulosa de sodio reticulada (croscarmelosa), metilcelulosa, almidón pregelatinizado (almidón 1500), almidón microcristalino, almidón insoluble en agua, carboximetilcelulosa de calcio, silicato de magnesio y aluminio (Veegum), lauril sulfato de sodio, compuestos amonio cuaternario y mezclas de los mismos.
Los agentes tensioactivos y/o emulsionantes ejemplares incluyen emulsionantes naturales (por ejemplo, goma arábiga, agar, ácido algínico, alginato de sodio, tragacanto, chondrux, colesterol, goma xantana, pectina, gelatina, yema de huevo, caseína, lanolina, colesterol, cera y lecitina), arcillas coloidales (por ejemplo, bentonita (silicato de aluminio) y Veegum (silicato de magnesio y aluminio)), derivados de aminoácido de cadena larga, alcoholes de alto peso molecular (por ejemplo, alcohol estearílico, alcohol cetílico, alcohol oleílico, monoestearato de triacetina, diestearato de etilenglicol, monoestearato de glicerilo y monoestearato de propilenglicol, poli(alcohol vinílico)), carbómeros (por ejemplo, carboxipolimetileno, ácido poliacrílico, polímero de ácido acrílico y polímero de carboxivinilo), carragenina, derivados celulósicos (por ejemplo, carboximetilcelulosa de sodio, celulosa en polvo, hidroximetilcelulosa, hidroxipropilcelulosa, hidroxipropilmetilcelulosa, metilcelulosa), ésteres de ácido graso de sorbitano (por ejemplo, monolaurato de polioxietilensorbitano (Tween 20), polioxietilensorbitano (Tween 60), monooleato de polioxietilensorbitano (Tween 80), monopalmitato de sorbitano (Span 40), monoestearato de sorbitano (Span 60), triestearato de sorbitano (Span 65), monooleato de glicerilo, monooleato de sorbitano (Span 80), ésteres de polioxietileno (por ejemplo, monoestearato de polioxietileno (Myrj 45), aceite de ricino hidrogenado polioxietilenado, aceite de ricino polioxietilenado, estearato de polioximetileno y Solutol), ésteres de ácido graso de sacarosa, ésteres de ácido graso de polietilenglicol (por ejemplo Cremophor®), éteres de polioxietileno (por ejemplo, lauril éter de polioxietileno (Brij 30)), polivinilpirrolidona, monolaurato de dietilenglicol, oleato de trietanolamina, oleato de sodio, oleato de potasio, oleato de etilo, ácido oleico, laurato de etilo, lauril sulfato de sodio, Pluronic F68, Poloxamer 188, bromuro de cetrimonio, cloruro de cetilpiridinio, cloruro de benzalconio, docusato de sodio y/o mezclas de los mismos.
Los agentes aglutinantes ejemplares incluyen almidón (por ejemplo, almidón de maíz y pasta de almidón), gelatina, azúcares (por ejemplo, sacarosa, glucosa, dextrosa, dextrina, melazas, lactosa, lactitol, manitol, etc.), gomas naturales y sintéticas (por ejemplo, goma arábiga, alginato de sodio, extracto de musgo irlandés, goma panwar, goma ghatti, mucílago de cáscaras de isapol, carboximetilcelulosa, metilcelulosa, etilcelulosa, hidroxietilcelulosa, hidroxipropilcelulosa, hidroxipropilmetilcelulosa, celulosa microcristalina, acetato de celulosa, polivinilpirrolidona, silicato de magnesio y aluminio (Veegum) y arabogalactano de alerce), alginatos, óxido de polietileno, polietilenglicol, sales de calcio inorgánicas, ácido silícico, polimetacrilatos, ceras, agua, alcohol y/o mezclas de los mismos.
Los conservantes ejemplares incluyen antioxidantes, agentes quelantes, conservantes antimicrobianos, conservantes antifúngicos, conservantes alcohólicos, conservantes ácidos y otros conservantes.
Los antioxidantes ejemplares incluyen alfa tocoferol, ácido ascórbico, palmitato de ascorbilo, hidroxianisol butilado, hidroxitolueno butilado, monotioglicerol, metabisulfito de potasio, ácido propiónico, galato de propilo, ascorbato de sodio, bisulfito de sodio, metabisulfito de sodio y sulfito de sodio.
Los agentes quelantes ejemplares incluyen ácido etilendiaminatetraacético (EDTA) y sales e hidratos del mismo (por ejemplo, edetato de sodio, edetato de disodio, edetato de trisodio, edetato de calcio y disodio, edetato de dipotasio y similares), ácido cítrico y sales e hidratos del mismo (por ejemplo, ácido cítrico monohidratado), ácido fumárico y sales e hidratos del mismo, ácido málico y sales e hidratos del mismo, ácido fosfórico y sales e hidratos del mismo y ácido tartárico y sales e hidratos del mismo. Los conservantes antimicrobianos ejemplares incluyen cloruro de benzalconio, cloruro de bencetonio, alcohol bencílico, bronopol, cetrimida, cloruro de cetilpiridinio, clorhexidina, clorobutanol, clorocresol, cloroxilenol, cresol, alcohol etílico, glicerina, hexetidina, imidurea, fenol, fenoxietanol, alcohol feniletílico, nitrato fenilmercúrico, propilenglicol y timerosal.
Los conservantes antifúngicos ejemplares incluyen butilparabeno, metilparabeno, etilparabeno, propilparabeno, ácido benzoico, ácido hidroxibenzoico, benzoato de potasio, sorbato de potasio, benzoato de sodio, propionato de sodio y ácido sórbico.
Los conservantes alcohólicos ejemplares incluyen etanol, polietilenglicol, fenol, compuestos fenólicos, bisfenol, clorobutanol, hidroxibenzoato, y alcohol feniletílico.
Los conservantes ácidos ejemplares incluyen vitamina A, vitamina C, vitamina E, betacaroteno, ácido cítrico, ácido acético, ácido deshidroacético, ácido ascórbico, ácido sórbico y ácido fítico.
Otros conservantes incluyen tocoferol, acetato de tocoferol, mesilato de deteroxima, cetrimida, hidroxianisol butilado (BHA), hidroxitolueno butilado (BHT), etilendiamina, lauril sulfato de sodio (SLS), lauril éter sulfato de sodio (SLES), bisulfito de sodio, metabisulfito de sodio, sulfito de potasio, metabisulfito de potasio, Glydant Plus, Phenonip, metilparabeno, Germall 115, Germaben II, Neolone, Kathon y Euxyl. En determinadas realizaciones, el conservante es un antioxidante. En otras realizaciones, el conservante es un agente quelante.
Los agentes tamponantes ejemplares incluyen disoluciones de tampón citrato, disoluciones de tampón acetato, disoluciones de tampón fosfato, cloruro de amonio, carbonato de calcio, cloruro de calcio, citrato de calcio, glubionato de calcio, gluceptato de calcio, gluconato de calcio, ácido D-glucónico, glicerofosfato de calcio, lactato de calcio, ácido propanoico, levulinato de calcio, ácido pentanoico, fosfato de calcio dibásico, ácido fosfórico, fosfato de calcio tribásico, fosfato de hidróxido de calcio, acetato de potasio, cloruro de potasio, gluconato de potasio, mezclas de potasio, fosfato de potasio dibásico, fosfato de potasio monobásico, mezclas de fosfato de potasio, acetato de sodio, bicarbonato de sodio, cloruro de sodio, citrato de sodio, lactato de sodio, fosfato de sodio dibásico, fosfato de sodio monobásico, mezclas de fosfato de sodio, trometamina, hidróxido de magnesio, hidróxido de aluminio, ácido algínico, agua apirógena, disolución salina isotónica, disolución de Ringer, alcohol etílico y mezclas de los mismos.
Los agentes lubricantes ejemplares incluyen estearato de magnesio, estearato de calcio, ácido esteárico, sílice, talco, malta, behenato de glicerilo, aceites vegetales hidrogenados, polietilenglicol, benzoato de sodio, acetato de sodio, cloruro de sodio, leucina, lauril sulfato de magnesio, lauril sulfato de sodio y mezclas de los mismos.
Los aceites naturales ejemplares incluyen aceite de almendra, hueso de albaricoque, aguacate, babassu, bergamota, moras, borraja, enebro, manzanilla, canola, alcaravea, carnauba, ricino, canela, manteca de cacao, coco, hígado de bacalao, café, maíz, semilla de algodón, emú, eucalipto, onagra, pescado, linaza, geraniol, calabaza, semilla de uva, avellana, hisopo, miristato de isopropilo, jojoba, nuez de kukui, lavandina, lavanda, limón, litsea cubeba, nuez de macadamia, malva, semilla de mango, semilla de hierba de la pradera, visón, nuez moscada, oliva, naranja, reloj anaranjado, palma, palmiste, hueso de melocotón, cacahuete, semilla de amapola, semilla de calabaza, colza, salvado de arroz, romero, cártamo, sándalo, sasquana, sabroso, espino amarillo, sésamo, manteca de karité, silicona, soja, girasol, árbol del té, cardo, tsubaki, vetiver, nuez y germen de trigo. Los aceites sintéticos ejemplares incluyen, aunque sin limitación estearato de butilo, triglicérido caprílico, triglicérido cáprico, ciclometicona, sebacato de dietilo, dimeticona 360, miristato de isopropilo, aceite mineral, octildodecanol, alcohol oleílico, aceite de silicona y mezclas de los mismos.
Las formas galénicas líquidas para administración oral y parenteral incluyen emulsiones, microemulsiones, disoluciones, suspensiones, jarabes y elixires farmacéuticamente aceptables. Además de los ingredientes activos, las formas galénicas líquidas pueden comprender diluyentes inertes habitualmente usados en la técnica tales como, por ejemplo, agua u otros disolventes, agentes solubilizantes y emulsionantes tales como alcohol etílico, alcohol isopropílico, carbonato de etilo, acetato de etilo, alcohol bencílico, benzoato de bencilo, propilenglicol, 1.3- butilenglicol, dimetilformamida, aceites (por ejemplo, aceite de algodón, de maní, de maíz, de oliva, de ricino y de sésamo), glicerol, alcohol tetrahidrofurfurílico, polietilenglicoles y ésteres de ácido graso de sorbitano, y mezclas de los mismos. Además de los diluyentes inertes, las composiciones orales pueden incluir adyuvantes tales como agentes humectantes, agentes emulsionantes y de suspensión, agentes edulcorantes, aromatizantes y perfumantes. En determinadas realizaciones para administración parenteral, los compuestos descritos en la presente memoria se mezclan con agentes solubilizantes tales como Cremophor®, alcoholes, aceites, aceites modificados, glicoles, polisorbatos, ciclodextrinas, polímeros y mezclas de los mismos.
Las preparaciones inyectables, por ejemplo, suspensiones acuosas u oleaginosas inyectables estériles pueden formularse de acuerdo con la técnica conocida usando agentes dispersantes o humectantes adecuados y agentes de suspensión. La preparación inyectable estéril puede ser una disolución, suspensión o emulsión inyectable estéril en un diluyente o disolvente farmacéuticamente aceptable no tóxico, por ejemplo, como una disolución en 1.3- butanodiol. Entre los vehículos y disolventes aceptables que pueden emplearse están el agua, disolución de Ringer, U.S.P. y disolución de cloruro de sodio isotónica. Además, se emplean convencionalmente aceites fijos estériles como disolvente o medio de suspensión. Para este fin, puede emplearse cualquier aceite fijo blando incluyendo mono- o diglicéridos sintéticos. Además, se usan ácidos grasos tales como ácido oleico en la preparación de inyectables.
Las formulaciones inyectables pueden esterilizarse, por ejemplo, por filtración a través de un filtro de retención de bacterias, o incorporando agentes esterilizantes en forma de composiciones sólidas estériles que pueden disolverse o dispersarse en agua estéril u otro medio inyectable estéril antes de su uso.
Para prolongar el efecto de un fármaco, a menudo es deseable ralentizar la absorción del fármaco desde la inyección subcutánea o intramuscular. Esto puede conseguirse mediante el uso de una suspensión líquida de material cristalino a amorfo con poca solubilidad en agua. La tasa de absorción del fármaco entonces depende de su tasa de disolución que, a su vez, puede depender del tamaño del cristal y la forma cristalina. Como alternativa, la absorción retardada de un fármaco administrado por vía parenteral se consigue disolviendo o suspendiendo el fármaco en un vehículo oleoso.
Las composiciones para administración rectal o vaginal típicamente son supositorios que pueden prepararse mezclando los compuestos descritos en la presente memoria con excipientes o vehículos no irritantes adecuados tales como manteca de cacao, polietilenglicol o una cera de supositorio que son sólidos a temperatura ambiente, pero líquidos a temperatura corporal y, por lo tanto, se funden el recto o la cavidad vaginal y liberan el ingrediente activo.
Las formas galénicas sólidas para administración oral incluyen cápsulas, comprimidos, píldoras, polvos y gránulos. En dichas formas galénicas sólidas, el ingrediente activo se mezcla con al menos un excipiente o vehículo farmacéuticamente aceptable inerte, tal como citrato de sodio o fosfato de dicalcio y/o a) rellenos o diluyentes tales como almidones, lactosa, sacarosa, glucosa, manitol y ácido silícico, b) aglutinantes tales como, por ejemplo, carboximetilcelulosa, alginatos, gelatina, polivinilpirrolidona, sacarosa y goma arábiga, c) humectantes tales como glicerol, d) agentes disgregantes tales como agar, carbonato de calcio, almidón de patata o tapioca, ácido algínico, determinados silicatos y carbonato de sodio, e) agentes retardadores de la disolución tales como parafina, f) aceleradores de la absorción tales como compuestos de amonio cuaternario, g) agentes humectantes tales como, por ejemplo, alcohol cetílico y monoestearato de glicerol, h) absorbentes tales como caolín y arcilla bentonita e i) lubricantes tales como talco, estearato de calcio, estearato de magnesio, polietilenglicoles sólidos, lauril sulfato de sodio y mezclas de los mismos. En el caso de cápsulas, comprimidos y píldoras, la forma galénica puede comprender agentes tamponantes.
Pueden emplearse composiciones sólidas de un tipo similar como rellenos en cápsulas de gelatina rellenas blandas y duras usando excipientes tales como lactosa o azúcar de la leche, así como polietilenglicoles de alto peso molecular y similares. Las formas galénicas sólidas de comprimidos, grageas, cápsulas, píldoras y gránulos pueden prepararse con recubrimientos y cubiertas tales como recubrimientos entéricos y otros recubrimientos bien conocidos en la técnica de formulación farmacéutica. Pueden comprender opcionalmente agentes opacificantes y pueden ser de una composición que libera el ingrediente o ingredientes activos únicamente, o preferentemente, en una determinada parte del conducto intestinal, opcionalmente, de una manera retardada. Los ejemplos de composiciones de inclusión que pueden usarse incluyen sustancias poliméricas y ceras. Pueden emplearse composiciones sólidas de un tipo similar como rellenos en cápsulas de gelatina rellenas blandas y duras usando excipientes tales como lactosa o azúcar de la leche, así como polietilenglicoles de alto peso molecular y similares.
El ingrediente activo puede estar en forma microencapsulada con uno o más excipientes como se indica anteriormente. Las formas galénicas sólidas de comprimidos, grageas, cápsulas, píldoras y gránulos pueden prepararse con recubrimientos y cubiertas tales como recubrimientos entéricos, recubrimientos de control de la liberación y otros recubrimientos bien conocidos en la técnica de formulación farmacéutica. En dichas formas galénicas sólidas, el ingrediente activo puede mezclarse con al menos un diluyente inerte tal como sacarosa, lactosa o almidón. Dichas formas galénicas pueden comprender, como es práctica normal, sustancias adicionales diferentes a diluyentes inertes, por ejemplo, lubricantes de compresión y otros auxiliares de comprensión tales como estearato de magnesio y celulosa microcristalina. En el caso de cápsulas, comprimidos y píldoras, las formas galénicas pueden comprender agentes tamponantes. Pueden comprender opcionalmente agentes opacificantes y pueden ser de una composición que libera el ingrediente o ingredientes activos únicamente, o preferentemente, en una determinada parte del conducto intestinal, opcionalmente de una manera retardada. Los ejemplos de composiciones de inclusión que pueden usarse incluyen sustancias poliméricas y ceras.
Las formas galénicas para administración tópica y/o transdérmica de un compuesto proporcionado pueden incluir pomadas, pastas, cremas, lociones, geles, polvos, disoluciones, pulverizaciones, inhalantes y/o parches. Generalmente, el ingrediente activo se mezcla en condiciones estériles con un vehículo farmacéuticamente aceptable y/o cualquier conservante y/o tampón deseado según pueda requerirse. Adicionalmente, la presente divulgación abarca el uso de parches transdérmicos, que a menudo tienen la ventaja añadida de proporcionar suministro controlado de un ingrediente activo al organismo. Dichas formas galénicas pueden prepararse, por ejemplo, disolviendo y/o dispensando el ingrediente activo en el medio apropiado. Como alternativa o adicionalmente, la tasa puede controlarse proporcionando una membrana de control de tasa y/o dispersando el ingrediente activo en una matriz polimérica y/o gel.
Los dispositivos adecuados para su uso en el suministro de composiciones farmacéuticas intradérmicas descritas en la presente memoria incluyen dispositivos de aguja corta tales como los descritos en las patentes de Estados Unidos 4886499; 5190521; 5328483; 5527288; 4270537; 5015235; 5141496; y 5417662. Las composiciones intradérmicas pueden administrarse por dispositivos que limitan la longitud de penetración eficaz de una aguja en la piel, tal como los descritos en la publicación PCT WO 99/34850 y equivalentes funcionales de los mismos. Los dispositivos de inyección de chorro que suministran vacunas líquidas a la dermis mediante un inyector de chorro de líquido y/o mediante una aguja que perfora el estrato córneo y produce un chorro que alcanza la dermis son adecuados. Los dispositivos de inyección de chorro se describen, por ejemplo, en las patentes de Estados Unidos 5480381; 5599302; 5334144; 5993412; 5649912; 5569189; 5704911; 5383851; 5893397; 5466220; 5339163; 5312335; 5503627; 5064413; 5520639; 4596556; 4790824; 4941880; 4940460; y las publicaciones PCT WO 97/37705 y WO 97/13537. Los dispositivos de suministro balístico de polvo/partículas que usan gas comprimido para impulsar la vacuna en forma de polvo a través de las capas exteriores de la piel hasta la dermis son adecuados. Como alternativa o adicionalmente, pueden usarse jeringas convencionales en el método de Mantoux clásico de
administración intradérmica.
Las formulaciones adecuadas para administración tópica incluyen, aunque sin limitación, preparaciones líquidas y/o semilíquidas tales como linimentos, lociones, emulsiones de aceite en agua y/o agua en aceite tales como cremas, pomadas y/o pastas, y/o disoluciones y/o suspensiones. Las formulaciones administrables por vía tópica pueden comprender, por ejemplo, de aproximadamente un 1 % a aproximadamente un 10% (p/p) de ingrediente activo, aunque la concentración del ingrediente activo puede ser tan elevada como el límite de solubilidad del ingrediente en el disolvente. Las formulaciones para administración tópica pueden comprender además uno o más de los ingredientes adicionales descritos en la presente memoria.
Una composición farmacéutica proporcionada puede prepararse, envasarse y/o venderse en una formulación adecuada para administración pulmonar mediante la cavidad bucal. Dicha formulación puede comprender partículas deshidratadas que comprenden el ingrediente activo y que tienen un diámetro en el intervalo de aproximadamente 0,5 a aproximadamente 7 nanómetros o de aproximadamente 1 a aproximadamente 6 nanómetros. Dichas composiciones están convenientemente en forma de polvos deshidratados para su administración usando un dispositivo que comprende un depósito de polvo deshidratado al que puede dirigirse una corriente de propulsor para dispersar el polvo y/o usar un recipiente de distribución de disolvente/polvo autopropulsor tal como un dispositivo que comprende el ingrediente activo disuelto y/o suspendido en un propulsor de bajo punto de ebullición en un recipiente precintado. Dichos polvos comprenden partículas en las que al menos un 98 % de las partículas en peso tienen un diámetro mayor de 0,5 nanómetros y al menos un 95 % de las partículas en número tienen un diámetro de menos de 7 nanómetros. Como alternativa, al menos un 95 % de las partículas en peso tienen un diámetro mayor de 1 nanómetro y al menos un 90 % de las partículas en número tienen un diámetro de menos de 6 nanómetros. Las composiciones de polvo deshidratado pueden incluir un diluyente de polvo fino sólido tal como azúcar y se proporcionan convenientemente en una forma de dosis unitaria.
Los propulsores de bajo punto de ebullición generalmente incluyen propulsores líquidos que tienen un punto de ebullición por debajo de 18,33 °C (65 °F) a presión atmosférica. En general, el propulsor puede constituir de un 50 a un 99% (p/p) de la composición, y el ingrediente activo puede constituir de un 0,1 a un 20% (p/p) de la composición. El propulsor puede comprender además ingredientes adicionales tales como un tensioactivo no iónico líquido y/o aniónico sólido y/o un diluyente sólido (que puede tener un tamaño de partícula del mismo orden que las partículas que comprenden el ingrediente activo).
Las composiciones farmacéuticas formuladas para suministro pulmonar pueden proporcionar el ingrediente activo en forma de gotas de una disolución y/o suspensión. Dichas formulaciones pueden prepararse, envasarse y/o venderse como disoluciones acuosas y/o alcohólicas diluidas y/o suspensiones, opcionalmente estériles, que comprenden el ingrediente activo, y pueden administrarse convenientemente usando cualquier dispositivo de nebulización y/o atomización. Dichas formulaciones pueden comprender además uno o más ingredientes adicionales incluyendo, aunque sin limitación, un agente aromatizante tal como sacarina de sodio, un aceite volátil, un agente tamponante, un agente tensioactivo y/o un conservante tal como metilhidroxibenzoato. Las gotas proporcionadas por esta vía de administración pueden tener un promedio de diámetro en el intervalo de aproximadamente 0,1 a aproximadamente 200 nanómetros.
Las formulaciones descritas en la presente memoria que son útiles para suministro pulmonar son útiles para suministro intranasal de una composición farmacéutica. Otra formulación adecuada para administración intranasal es un polvo grueso que comprende el ingrediente activo que tiene un promedio de partícula de aproximadamente 0,2 a 500 micrómetros. Dicha formulación se administra por inhalación rápida a través de la fosa nasal desde un recipiente del polvo mantenido cerca de los orificios nasales.
Las formulaciones para administración nasal pueden comprender, por ejemplo, de aproximadamente tan poco como un 0,1 % (p/p) y tanto como un 100% (p/p) del ingrediente activo, y pueden comprender uno o más de los ingredientes adicionales descritos en la presente memoria. Una composición farmacéutica proporcionada puede prepararse, envasarse y/o venderse en una formulación para administración bucal. Dichas formulaciones pueden estar, por ejemplo, en forma de comprimidos y/o grageas hechas usando métodos convencionales, y pueden contener, por ejemplo, de un 0,1% a un 10% (p/p) de ingrediente activo, comprendiendo el equilibrio una composición que se puede disolver y/o degradable por vía oral y, opcionalmente, uno o más de los ingredientes adicionales descritos en la presente memoria. Como alternativa, las formulaciones para administración bucal pueden comprender un polvo y/o una disolución y/o suspensión en aerosol y/o atomizada que comprende el ingrediente activo. Dichas formulaciones en polvo, en aerosol y/o en aerosol, cuando se dispersan, pueden tener un promedio de partícula y/o un tamaño de gota en el intervalo de aproximadamente 0,1 a aproximadamente 200 nanómetros, y pueden comprender además uno o más de los ingredientes adicionales descritos en la presente memoria.
Una composición farmacéutica proporcionada puede prepararse, envasarse y/o venderse en una formulación para administración oftálmica. Dichas formulaciones pueden estar, por ejemplo, en forma de colirios, incluyendo, por ejemplo, una disolución y/o suspensión de un 0,1/1,0 % (p/p) del ingrediente activo en un vehículo líquido acuoso u oleoso. Dichas gotas pueden comprender además agenten tamponantes, sales y/o uno o más ingredientes adicionales diferentes descritos en la presente memoria. Otras formulaciones administrables por vía oftálmica que
son útiles incluyen aquellas que comprenden el ingrediente activo en forma microcristalina y/o en una preparación liposómica. Las gotas óticas y/o colirios se contemplan dentro del alcance de esta divulgación.
Aunque las descripciones de composiciones farmacéuticas proporcionadas en la presente memoria están dirigidas principalmente a composiciones farmacéuticas que son adecuadas para su administración a seres humanos, los expertos en la materia entenderán que dichas composiciones en general son adecuadas para su administración a animales de todo tipo. La modificación de composiciones farmacéuticas adecuadas para su administración a seres humanos para hacer que las composiciones sean adecuadas para su administración a diversos animales está bien comprendida, y el farmacólogo veterinario experto puede diseñar y/o realizar dicha modificación con experimentación habitual.
Los compuestos proporcionados en la rente memoria se formulan típicamente en forma galénica unitaria para facilitar la administración y la uniformidad de la dosificación. Se entenderá, sin embargo, que el uso diario total de las composiciones proporcionadas se decidirá por el médico a cargo dentro del alcance del criterio médico razonable. El nivel de dosis terapéuticamente eficaz específico para cualquier sujeto u organismo particular dependerá de una diversidad de factores, incluyendo la enfermedad, trastorno o afección que se está tratando y la gravedad del trastorno; la actividad del ingrediente activo específico empleado; la composición específica empleada; la edad, peso corporal, salud general, sexo y dieta del sujeto; el tiempo de administración, la vía de administración y la tasa de excreción del ingrediente activo específico empleado; la duración del tratamiento; los fármacos usados en combinación o coincidentes con el ingrediente activo específico empleado; y factores similares bien conocidos en la técnicas médicas.
Los compuestos y composiciones proporcionados en la presente memoria pueden administrarse por cualquier vía, incluyendo enteral (por ejemplo, oral), parenteral, intravenosa, intramuscular, intraarterial, intramedular, intratecal, subcutánea, intraventricular, transdérmica, interdérmica, rectal, intravaginal, intraperitoneal, tópica (como mediante polvos, pomadas, cremas y/o gotas), a la mucosa, nasal, bucal, sublingual; por instilación intratraqueal, instilación bronquial y/o inhalación; y/o como una pulverización oral, pulverización nasal y/o aerosol. Las vías específicamente contempladas son administración oral, administración intravenosa (por ejemplo, inyección intravenosa sistémica), administración regional mediante el suministro sanguíneo y/o linfático, y/o administración directa a un sitio afectado. En general, la vía más apropiada de administración dependerá de una diversidad de factores, incluyendo la naturaleza del agente (por ejemplo, su estabilidad en el entorno del conducto gastrointestinal) y/o el estado del sujeto (por ejemplo, si el sujeto puede tolerar la administración oral).
La cantidad exacta de un compuesto requerida para conseguir una cantidad eficaz variará de un sujeto a otro, dependiendo, por ejemplo, de la especie, la edad y el estado general de un sujeto, la gravedad de los efectos secundarios o el trastorno, la identidad del compuesto o compuestos particulares, el modo de administración y similares. La dosificación deseada puede suministrarse tres veces al día, dos veces al día una vez al día, en días alternos, cada dos días, cada semana, cada dos semanas, cada tres semanas o cada cuatro semanas. En determinadas realizaciones, la dosificación deseada puede suministrarse usando múltiples administraciones (por ejemplo, dos, tres, cuatro, cinco, seis, siete, ocho, nueve, diez, once, doce, trece, catorce o más administraciones).
En determinadas realizaciones, una cantidad eficaz de un compuesto para su administración una o más veces al día a un ser humano adulto de 70 kg puede comprender de aproximadamente 0,0001 mg a aproximadamente 3000 mg, de aproximadamente 0,0001 mg a aproximadamente 2000 mg, de aproximadamente 0,0001 mg a aproximadamente 1000 mg, de aproximadamente 0,001 mg a aproximadamente 1000 mg, de aproximadamente 0,01 mg a aproximadamente 1000 mg, de aproximadamente 0,1 mg a aproximadamente 1000 mg, de aproximadamente 1 mg a aproximadamente 1000 mg, de aproximadamente 1 mg a aproximadamente 100 mg, de aproximadamente 10 mg a aproximadamente 1000 mg o de aproximadamente 100 mg a aproximadamente 1000 mg de un compuesto por forma galénica unitaria.
En determinadas realizaciones, un compuesto descrito en la presente memoria puede administrarse a niveles de dosificación suficientes para suministrar de aproximadamente 0,001 mg/kg a aproximadamente 1000 mg/kg, de aproximadamente 0,01 mg/kg a aproximadamente mg/kg, de aproximadamente 0,1 mg/kg a aproximadamente 40 mg/kg, de aproximadamente 0,5 mg/kg a aproximadamente 30 mg/kg, de aproximadamente 0,01 mg/kg a aproximadamente 10 mg/kg, de aproximadamente 0,1 mg/kg a aproximadamente 10 mg/kg o de aproximadamente 1 mg/kg a aproximadamente 25 mg/kg de peso corporal del sujeto por día, una o más veces al día, para obtener el efecto terapéutico deseado.
En algunas realizaciones, un compuesto descrito en la presente memoria se administra una o más veces al día, durante múltiples días. En algunas realizaciones, la pauta posológica se continúa durante días, semanas, meses o años.
Se apreciará que los intervalos de dosis descritos en la presente memoria proporcionan directrices para la administración de composiciones farmacéuticas a un adulto. La cantidad a administrar a, por ejemplo, un niño o un adolescente puede determinarse por un facultativo médico o experto en la materia y puede ser inferior o igual a la administrada a un adulto.
Se apreciará que un compuesto o composición, como se describe en la presente memoria, puede administrarse en combinación con uno o más agentes terapéuticamente activos adicionales. Los compuestos o composiciones pueden administrarse en combinación con agentes terapéuticamente activos adicionales que mejoran su eficacia, potencia y/o biodisponibilidad, reducen y/o modifican su metabolismo, inhiben su excreción y/o modifican su distribución dentro del organismo. También se apreciará que el tratamiento empleado puede conseguir un efecto deseado para el mismo trastorno y/o puede conseguir efectos diferentes.
El compuesto o composición puede administrarse simultáneamente con, antes de o posterior a, uno o más agentes terapéuticamente activos adicionales. En general, cada agente se administrará a una dosis y/o un horario determinado para ese agente. Se apreciará además que el agente terapéuticamente activo adicional en esta combinación puede administrarse conjuntamente en una composición única o administrarse por separado en diferentes composiciones. La combinación particular a emplear en un régimen tendrá en cuenta la compatibilidad de un compuesto proporcionado con el agente terapéuticamente activo adicional y/o el efecto terapéutico deseado a conseguir. En general, se espera que los agentes terapéuticamente activos adicionales utilizados en combinación se utilicen a niveles que no excedan los niveles a los que se utilizan individualmente. En algunas realizaciones, los niveles utilizados en combinación serán inferiores a los utilizados individualmente.
Los agentes terapéuticamente activos adicionales ejemplares incluyen, aunque sin limitación, agentes antimicrobianos, agentes antifúngicos, agentes antiparasitarios, agentes antiinflamatorios y un agente analgésico. Los agentes terapéuticamente activos incluyen moléculas orgánicas pequeñas tales como compuestos farmacéuticos (por ejemplo, compuestos aprobados por la Food and Drug Administration estadounidense proporcionados en el Code of Federal Regulations (c Fr )), péptidos, proteínas, carbohidratos, monosacáridos, oligosacáridos, polisacáridos, nucleoproteínas, mucoproteínas, lipoproteínas, polipéptidos sintéticos o proteínas, moléculas pequeñas unidas a proteínas, glucoproteínas, esteroides, ácidos nucleicos, ADN, ARN, nucleótidos, nucleósidos, oligonucleótidos, oligonucleótidos de antisentido, lípidos, hormonas, vitaminas y células.
En determinadas realizaciones, un compuesto proporcionado se combina con un agente terapéuticamente activo adicional (por ejemplo, litio y/o quetamina) para su uso en el tratamiento de trastorno bipolar y/o depresión (por ejemplo, depresión insensible a litio). El litio ha sido desde hace mucho el tratamiento de elección para trastorno bipolar y síndromes maníacos, aunque el mecanismo exacto de acción ha sido difícil de discernir (J. A. Quiroz, T. D. Gould y H. K. Manji, Mol. Interv., 2004, 4, 259). Se sabe que el litio afecta a la función de una diversidad de enzimas, un efecto atribuido a la competición del litio por sitios de unión a magnesio esencial (W. J. Ryves y A. J. Harwood, Biochem. Biophys. Res. Commun., 2001, 280, 720). Las dosis terapéuticamente eficaces de Li+ (niveles en plasma de 0,6-1.2mM) se aproximan a su CI50 de GSK3 (CI50 = 2mM) (Annual Reports in Medicinal Chemistry, 2005, Volumen 40, página 137).
En determinadas realizaciones, un compuesto proporcionado se combina con un agente terapéuticamente activo adicional (por ejemplo, ácido todo-trans retinoico) para su uso en el tratamiento de AML. En determinadas realizaciones, una combinación de un compuesto proporcionado y un agente terapéuticamente activo adicional muestra efecto sinérgico en el tratamiento de una enfermedad neurológica, trastorno psiquiátrico (por ejemplo, trastorno bipolar o depresión (por ejemplo, depresión insensible a litio)), trastorno metabólico (por ejemplo, diabetes) y/o cáncer (por ejemplo, AML).
También se abarcan por la presente divulgación kits (por ejemplo, envases farmacéuticos). Los kits proporcionados pueden comprender una composición farmacéutica o compuesto proporcionado y un recipiente (por ejemplo, un vial, ampolla, frasco, jeringa y/o envase dispensador, u otro recipiente adecuado). En algunas realizaciones, los kits proporcionados pueden incluir además opcionalmente un segundo recipiente que comprende un excipiente farmacéutico para dilución o suspensión de una composición farmacéutica o compuesto proporcionado. En algunas realizaciones, una composición farmacéutica o compuesto proporcionado que se ha proporcionado en el recipiente y el segundo recipiente se combinan para formar una forma galénica unitaria.
Uso y tratamientos
Los compuestos y composiciones descritos en la presente memoria en general son útiles para la inhibición de una o más cinasas. En algunas realizaciones, los compuestos y composiciones descritos en la presente memoria son útiles para inhibir la actividad de GSK3. En algunas realizaciones los compuestos y composiciones descritos en la presente memoria son útiles para inhibir CK1. En algunas realizaciones, se proporcionan compuestos descritos en la presente memoria para su uso en métodos de tratamiento de un trastorno mediado por cinasas en un sujeto que comprenden administrar una cantidad eficaz de un compuesto descrito en la presente memoria (por ejemplo, un compuesto de fórmula I, II o III) o una de sus sales farmacéuticamente aceptables, a un sujeto que necesita tratamiento. En determinadas realizaciones, la cantidad eficaz es una cantidad terapéuticamente eficaz. En determinadas realizaciones, la cantidad eficaz es una cantidad profilácticamente eficaz. En determinadas realizaciones, el sujeto está padeciendo un trastorno mediado por cinasas. En determinadas realizaciones, el sujeto es susceptible a un trastorno mediado por cinasas. En determinadas realizaciones, el trastorno mediado por cinasas es un trastorno mediado por GSK3 (por ejemplo, un trastorno mediado por GSK3a, trastorno mediano por GSK3p). En determinadas realizaciones, el trastorno mediado por cinasas es un trastorno mediado por CK1 (por ejemplo, un
trastorno mediado por CK18).
La expresión "trastorno mediado por cinasas" (por ejemplo, trastorno mediado por GSK3, trastorno mediado por CK1) significa cualquier enfermedad, trastorno u otra afección perjudicial en que se sabe que una o más cinasas (por ejemplo, GSK3 o CK1) o un mutante de las mismas desempeñan una función. Por consiguiente, en algunas realizaciones, la presente divulgación se refiere al tratamiento o reducción de la gravedad de una o más enfermedades en que se sabe que una o más cinasas (por ejemplo, GSK3 o CK1) desempeñan una función.
En algunas realizaciones, la presente divulgación proporciona además un compuesto como se describe en la presente memoria para su uso en un método de inhibición de una cinasa, que comprende poner en contacto una cinasa con una cantidad eficaz de un compuesto descrito en la presente memoria (por ejemplo, un compuesto de fórmula I, II o III) o una de sus sales farmacéuticamente aceptables. En algunas realizaciones, la presente divulgación proporciona un compuesto como se describe en la presente memoria para su uso en un método de inhibición de GSK3, que comprende poner en contacto GSK3 con una cantidad eficaz de un compuesto descrito en la presente memoria (por ejemplo, un compuesto de fórmula I, II o III) o una de sus sales farmacéuticamente aceptables. En algunas realizaciones, la presente divulgación proporciona un compuesto como se describe en la presente memoria para su uso en un método de inhibición de CK1, que comprende poner en contacto CK1 con una cantidad eficaz de un compuesto descrito en la presente memoria (por ejemplo, un compuesto de fórmula I, II o III) o una de sus sales farmacéuticamente aceptables. La cinasa puede estar purificada o en bruto, y puede estar presente en una célula, tejido o sujeto. Por tanto, dichos métodos abarcan la inhibición de la actividad cinasa tanto in vitro como in vivo. En determinadas realizaciones, el método es un método in vitro, por ejemplo, tal como un método de ensayo útil como una herramienta de investigación.
En algunas realizaciones, se proporciona un compuesto como se describe en la presente memoria para su uso en un método de inhibición de la actividad cinasa en un sujeto que lo necesita (por ejemplo, que tiene una actividad cinasa mayor de la normal), que comprende administrar al sujeto una cantidad eficaz de un compuesto descrito en la presente memoria (por ejemplo, un compuesto de fórmula I, II o III) o una de sus sales farmacéuticamente aceptables. En algunas realizaciones, se proporciona un método de inhibición de la actividad de GSK3 en un sujeto que lo necesita, que comprende administrar al sujeto una cantidad eficaz de un compuesto descrito en la presente memoria (por ejemplo, un compuesto de fórmula I, II o III) o una de sus sales farmacéuticamente aceptables. En algunas realizaciones, se proporciona un compuesto como se describe en la presente memoria para su uso en un método de inhibición de la actividad de CK1 en un sujeto que lo necesita, que comprende administrar al sujeto una cantidad eficaz de un compuesto descrito en la presente memoria (por ejemplo, un compuesto de fórmula I, II o III) o una de sus sales farmacéuticamente aceptables.
En algunas realizaciones, la motivación para administrar un compuesto de acuerdo con algunas realizaciones es una intención de tratar una enfermedad neurológica o trastorno psiquiátrico en un sujeto. En determinadas realizaciones, un compuesto proporcionado es útil en el tratamiento de una enfermedad neurológica (por ejemplo, una enfermedad neurológica descrita en la presente memoria). La enfermedad neurológica que se trata por un compuesto proporcionado puede estar mediada por GSK3a y/o GSK3p. En determinadas realizaciones, un compuesto proporcionado es útil en el tratamiento de un trastorno psiquiátrico (por ejemplo, un trastorno psiquiátrico descrito en la presente memoria). El trastorno psiquiátrico que se trata por un compuesto proporcionado puede estar mediado por GSK3a y/o GSK3p.
La expresión "enfermedad neurológica" se refiere a una afección que tiene como un componente un mal funcionamiento del sistema nervioso central o periférico. Una enfermedad neurológica puede causar una alteración en la estructura o función del sistema nervioso como resultado de anomalías en el desarrollo y funcionales, enfermedad, defectos genéticos, lesión o toxinas. Estos trastornos pueden afectar al sistema nervioso central (por ejemplo, el cerebro, tronco cerebral y cerebelo), el sistema nervioso periférico (por ejemplo, los nervios craneales, los nervios espinales y los sistemas nerviosos simpáticos y parasimpáticos) y/o el sistema nervioso autónomo (por ejemplo, la parte del sistema nervioso que regula la acción involuntaria y que está dividido en los sistemas nerviosos simpático y parasimpático). Por consiguiente, una enfermedad neurodegenerativa es un ejemplo de una enfermedad neurológica.
La expresión "enfermedad neurodegenerativa" se refiere a una afección caracterizada por la pérdida de células neuronales y células de soporte de las células neuronales, que causa disfunción y/o discapacidades cognitivas y/o motoras. Por consiguiente, la expresión se refiere a cualquier enfermedad o trastorno que pudiera revertirse, detenerse, controlarse, tratarse, mejorarse o eliminarse con agentes que estimulan la generación de nuevas neuronas. Los ejemplos de enfermedades neurodegenerativas incluyen: (i) enfermedades neurodegenerativas crónicas tales como esclerosis lateral amiotrófica familiar y esporádica (FALS y ALS, respectivamente), enfermedad de Parkinson familiar y esporádica, enfermedad de Huntington, enfermedad de Alzheimer familiar y esporádica, síndrome del X frágil, esclerosis múltiple, atrofia olivopontocerebelar, atrofia multisistémica, parálisis supranuclear progresiva, enfermedad difusa con cuerpos de Lewy, degeneración corticodentatonigral, epilepsia mioclónica familiar progresiva, degeneración estrionigral, distonía por torsión, temblores familiares, síndrome de Down, síndrome de Gilles de la Tourette, enfermedad de Hallervorden-Spatz, demencia pugilística, demencia por SIDA, demencia senil, alteración de la memoria asociada con la edad y enfermedades neurodegenerativas relacionadas con amiloidosis
tales las causadas por la proteína de priones (PrP) que está asociada con la encefalopatía espongiforme transmisible (enfermedad de Creutzfeldt-Jakob, síndrome de Gerstmann-Straussler-Scheinker, prurigo lumbar y kuru) y las causadas por exceso de acumulación de cistatina C (angiopatía por cistatina C hereditaria); y (ii) trastornos neurodegenerativos agudos tales como lesión cerebral traumática (por ejemplo, lesión cerebral relacionada con cirugía), edema cerebral, daño de nervios periféricos, lesión de la médula espinal, enfermedad de Leigh, síndrome de Guillain-Barre, trastornos de almacenamiento lisosómico tales como lipofuccionosis, enfermedad de Alper, vértigo como resultado de degeneración del SNC; patologías que surgen con el abuso crónico de alcohol o fármacos incluyendo, por ejemplo, la degeneración de las neuronas en el locus coeruleus y el cerebelo; patologías que surgen con el envejecimiento incluyendo la degeneración de las neuronas cerebelares y las neuronas corticales, que dan lugar a alteraciones cognitivas y motoras; y patologías que surgen por el abuso crónico de anfetaminas, incluyendo la degeneración de las neuronas de los ganglios basales, que da lugar a alteraciones motoras; cambios patológicos como resultado de traumatismo focal tal como apoplejía, isquemia focal, insuficiencia vascular, encefalopatía hipóxica-isquémica, hiperglucemia, hipoglucemia o traumatismo directo; patologías que surgen como efecto secundario negativo de fármacos y tratamientos terapéuticos (por ejemplo, degeneración de neuronas del cingulado y la corteza entorrinal en respuesta a dosis anticonvulsivas de antagonistas de la clase NMDA del receptor de glutamato) y demencia relacionada con la enfermedad de Wernicke-Korsakoff. Las enfermedades neurodegenerativas que afectan a las neuronas sensitivas incluyen ataxia de Friedreich y degeneración neuronal de la retina. Otras enfermedades neurodegenerativas incluyen lesión o traumatismo de los nervios asociado con lesión de la médula espinal. Las enfermedades neurodegenerativas de los sistemas límbico y cortical incluyen amiloidosis cerebral, atrofia de Pick y síndrome de Rett. Los ejemplos anteriores no se entienden como exhaustivos, sino que sirve simplemente como una ilustración de la expresión "enfermedad degenerativa".
La enfermedad de Alzheimer es un trastorno cerebral degenerativo caracterizado por síntomas psiquiátricos cognitivos y no cognitivos. Los síntomas psiquiátricos son habituales en la enfermedad de Alzheimer, con psicosis (alucinaciones y delirios) presentes en aproximadamente un 50 % de los pacientes afectados. Similar a la esquizofrenia, los síntomas psicóticos positivos son habituales en la enfermedad de Alzheimer. Los delirios típicamente se producen más frecuentemente que las alucinaciones. Los pacientes con enfermedad de Alzheimer también muestran síntomas negativos, tales como desconexión, apatía, sensibilidad emocional disminuida, pérdida de voluntad e iniciativa disminuida. De hecho, los compuestos antipsicóticos que se usan para aliviar la psicosis de la esquizofrenia también son útiles en el alivio de las psicosis en pacientes con enfermedad de Alzheimer. El término "demencia" se refiere a la pérdida de funciones cognitivas e intelectuales sin alteración de la percepción o la conciencia. La demencia se caracteriza típicamente por desorientación, deterioro de la memoria, el juicio y el intelecto y un afecto inestable superficial.
El síndrome del X frágil, o síndrome de Martin-Bell. Es un síndrome genético, que produce un espectro de rasgos psíquicos, intelectuales emocionales y de comportamiento característicos que varían de manifestación grave a leve. El síndrome está asociado con la expansión de una única secuencia génica trinucleotídica (CGG) en el cromosoma X, y provoca un fallo para expresar la proteína FMRP que es necesaria para el desarrollo neural normal. Hay cuatro formas generalmente aceptadas de síndrome del X frágil que se refieren a la longitud de la secuencia CGG repetida en el gen FMR1; normal (29-31 repeticiones CGG), premutación (55-200 repeticiones CGG), mutación completa (más de 200 repeticiones CGG), y alelos intermedios o de zona gris (40-60 repeticiones). Normalmente, el gen FMR1 contiene entre 6 y 55 repeticiones del codón CGG (repeticiones trinucleotídicas). En personas con síndrome del X frágil, el alelo FMR1 tiene más de 230 repeticiones de este codón. La expansión del codón repetitivo CGG a dicho grado provoca una metilación de esa parte del ADN, silenciando de forma eficaz la expresión de la proteína FMR1. Esta metilación del locus FMR1 en la banda cromosómica Xq27.3 se cree que provoca la constricción del cromosoma X que parece "frágil" bajo el microscopio en ese punto, un fenómeno que dio su nombre al síndrome. La mutación del gen FMR1 da lugar al silenciamiento transcripcional de la proteína de retraso mental del X frágil, FMRP. En individuos normales, se cree que FMRP regula una población sustancial de ARNm: FMRP desempeña funciones importantes en el aprendizaje y la memoria, y también parece estar implicado en el desarrollo de los axones, la formación de sinapsis y el cableado y desarrollo de circuitos neurales.
La esclerosis lateral amiotrófica (ALS), también llamada enfermedad de Lou Gehrig es una enfermedad neurológica mortal progresiva. La ALS se produce cuando células nerviosas específicas en el cerebro y la médula espinal que controlan el movimiento voluntario se degeneran gradualmente y causa que los músculos bajo su control se debiliten y atrofien, dando lugar a parálisis. Actualmente, no hay cura para a LS; ni hay un tratamiento demostrado que prevenga o revierta el curso del trastorno.
La enfermedad de Parkinson es una alteración del movimiento voluntario en que los músculos quedan rígidos y lentos. Los síntomas de la enfermedad incluyen contracción rítmica difícil e incontrolable de grupos de músculos, que produce agitación o temblores. La enfermedad está causada por la degeneración de neuronas dopaminérgicas presinápticas en el cerebro y específicamente en el tronco cerebral. Como resultado de la degeneración, se produce una liberación inadecuada del transmisor químico dopamina durante la actividad neuronal. Actualmente, la enfermedad de Parkinson se trata con varios compuestos diferentes y combinaciones. Levodopa (L-dopa), que se convierte en dopamina en el cerebro, a menudo se administra para restaurar el control muscular. Perindopril, un inhibidor de ACE que cruza la barrera hematoencefálica, se usa para mejorar las respuestas motoras de los pacientes a L-dopa. Carbidopa se administra con L-dopa para retardar la conversión de L-dopa en dopamina hasta
que alcance el cerebro, y también reduce los efectos secundarios de L-dopa. Otros fármacos usados en el tratamiento de la enfermedad de Parkinson incluyen miméticos de dopamina Mirapex (dihidrocloruro de pramipexol) y Requip (hidrocloruro de ropinirol) y Tasmar (tolcapona), un inhibidor de COMt que bloquea un enzima clave responsable de la descomposición de levodopa antes de que alcance el cerebro.
La expresión "trastorno psiquiátrico" se refiere a una afección o trastorno que se refiere al funcionamiento del cerebro y los procesos cognitivos o el comportamiento. Los trastornos psiquiátricos pueden clasificarse además basándose en el tipo de alteración neurológica que afecta a las facultades mentales. Los trastornos psiquiátricos se expresan principalmente en anomalías de pensamiento, sentimiento, emoción y/o comportamiento, que producen angustia o alteración de la función (por ejemplo, alteración de la función mental tal como con demencia o senilidad). La expresión "trastorno psiquiátrico", por consiguiente, a veces se usa indistintamente con la expresión "trastorno mental" o la expresión "enfermedad mental".
Un trastorno psiquiátrico a menudo se caracteriza por un patrón psicológico o del comportamiento que se produce en un individuo y se cree que causa angustia o discapacidad que no se espera como parte del desarrollo normal o cultura. Las definiciones, evaluaciones y clasificaciones de los trastornos mentales pueden variar, pero los criterios enumerados en la International Classification of Diseases and Related Health Problems (ICD, publicado por la Organización Mundial de la Salud, OMS), o el Diagnostic and Statistical Manual of Mental Disorders (DSM publicado por la Asociación Psiquiátrica Americana, APA) y otros manuales están aceptados ampliamente por los profesionales de salud mental. Los individuos pueden evaluarse para diversos trastornos psiquiátricos usando criterios expuestos en estas y otras publicaciones aceptadas por los facultativos médicos en el campo y la manifestación y gravedad de un trastorno psiquiátrico puede determinarse en un individuo usando estas publicaciones.
Las categorías de diagnósticos en estos esquemas pueden incluir trastornos disociativos, trastornos del estado de ánimo, trastornos de ansiedad, trastornos psicóticos, trastornos de la alimentación, trastornos del desarrollo, trastornos de personalidad y otras categorías. Hay diferentes categorías de trastorno mental, y muchas facetas diferentes de comportamiento humano y personalidad que pueden quedar desordenadas.
Un grupo de trastornos psiquiátricos incluye trastornos del pensamiento y la cognición, tal como esquizofrenia y delirio. Un segundo grupo de trastornos psiquiátricos incluye trastorno del estado de ánimo, tales como trastornos afectivos y ansiedad. Un tercer grupo de trastornos psiquiátricos incluye trastornos de comportamiento social, tal como defectos del carácter y trastornos de personalidad. Y un cuarto grupo de trastornos psiquiátricos incluye trastornos del aprendizaje, la memoria y la inteligencia, tal como retraso mental y demencia. Por consiguiente, los trastornos psiquiátricos abarcan esquizofrenia, delirio, trastorno con déficit de atención (ADD), trastorno esquizoafectivo, depresión (por ejemplo, depresión insensible a litio), manía, trastornos con déficit de atención, adicción a fármacos, demencia, agitación, apatía, ansiedad, psicosis, trastornos de personalidad, trastornos bipolares, trastorno afectivo unipolar, trastornos obsesivo-compulsivos, trastornos de la alimentación, trastornos de estrés postraumático, irritabilidad, trastorno de conducta adolescente y desinhibición.
Algunas enfermedades clasificadas como enfermedades neurodegenerativas, por ejemplo, la enfermedad de Alzheimer, también muestran a veces aspectos de trastornos psiquiátricos que se enumeran en la presente memoria, por ejemplo, trastornos de memoria o demencia. Algunas enfermedades neurodegenerativas o manifestaciones de la mismas también pueden mencionarse, por consiguiente, como trastornos psiquiátricos. Estos términos, por lo tanto, no son mutuamente exclusivos.
El estado de ansiedad o temor puede quedar desordenado, de modo que inusualmente sea intenso o generalizado durante un periodo prolongado de tiempo. Las categorías habitualmente reconocidas de trastornos de ansiedad incluyen fobia específica, trastorno de ansiedad generalizada, trastorno de ansiedad social, trastorno de pánico, agorafobia, trastorno obsesivo-compulsivo, trastorno de estrés postraumático.
Los estados afectivos de duración relativamente larga también pueden quedar desordenados. El trastorno del estado de ánimo que implica tristeza inusualmente intensa y mantenida, melancolía o desesperación se conoce como depresión clínica (o depresión mayor) y más generalmente puede describirse como desregulación emocional. La depresión más leve, pero prolongada, puede diagnosticarse como distimia. Los trastornos bipolares implican estados del estado de ánimo anómalamente "elevados" o presionados, conocidos como manía o hipomanía, que alternan con un estado de ánimo normal o deprimido.
Los patrones de creencia, uso del lenguaje y percepción pueden quedar desordenados. Los trastornos psicóticos que implican de forma central este dominio incluyen esquizofrenia y trastorno delirante. El trastorno esquizoafectivo es una categoría usada para individuos que muestran aspectos tanto de esquizofrenia como de trastornos afectivos. La esquizotipia es una categoría usada para individuos que muestran algunos de los rasgos asociados con esquizofrenia, pero sin cumplir los criterios de valoración.
Las características fundamentales de una persona que influyen en sus cogniciones, motivaciones y comportamientos entre situaciones y el tiempo, pueden observarse como trastornos debido a que son anómalamente rígidas y de mala adaptación. Los esquemas de categorías enumeran varios trastornos de
personalidad diferentes, tales como los clasificados como excéntricos (por ejemplo, trastorno de personalidad paranoide, trastorno de personalidad esquizoide, trastorno de personalidad esquizotípica), los descritos como dramáticos o emocionales (trastorno de personalidad antisocial, trastorno de personalidad límite, trastorno de personalidad histriónica, trastorno de personalidad narcisista) o los observados como relacionados con temor (trastorno de personalidad evitativa, trastornos de personalidad dependiente, trastorno de personalidad obsesivo-compulsiva).
Otros trastornos pueden implicar otros atributos del funcionamiento humano. Las prácticas de alimentación pueden desordenarse, con alimentación excesiva o alimentación insuficiente compulsiva o atracones. Las categorías de trastorno en esta área incluyen anorexia nerviosa, bulimia nerviosa, bulimia por ejercicio o trastorno de alimentación por atracones. Los trastornos del sueño tales como insomnio también existen y pueden alterar los patrones de sueño normales. Los trastornos de identidad sexual y de género, tales como dispareunia o trastorno de identidad de género u homosexualidad egodistónica. Las personas que son anómalamente incapaces de resistir las urgencias o impulsos para realizar actos que pudieran ser dañinos para sí mismos u otros, pueden clasificarse con un trastorno de control de los impulsos, incluyendo diversos tipos de trastornos de tic tales como síndrome de Tourette y trastornos tales como cleptomanía (robar) o piromanía (incendiar). Los trastornos por uso de sustancias incluyen trastorno por abuso de sustancias. El juego adictivo puede clasificarse como un trastorno. La incapacidad de ajustar suficientemente las circunstancias de la vida puede clasificarse como un trastorno de ajuste. La categoría del trastorno de ajuste se reserva habitualmente para problemas que empiezan en tres meses desde el evento o situación y finalizan en seis meses después de que se detenga o elimine el factor estresante. Las personas que padecen alteraciones graves de su autoidentidad, memoria y conciencia general de sí mismos y su alrededor pueden clasificarse con un trastorno de identidad disociativa, tal como trastorno de despersonalización (que también se ha llamado trastorno de personalidad múltiple o "personalidad dividida"). Los trastornos facticios, tales como síndrome de Munchausen, también existen cuando los síntomas se experimentan y/o presentan para beneficio personal.
Los trastornos que parecen originarse en el organismo, pero que se cree que son mentales, se conocen como trastornos somatomorfos, incluyendo el trastorno de somatización. También hay trastornos de la percepción del organismo, incluyendo el trastorno dismórfico corporal. La neurastenia es una categoría que implica quejas somáticas, así como fatiga y falta de ánimo/depresión, que se reconoce oficialmente por el ICD (versión 10) pero no por el DSM (versión IV). Los trastornos de memoria o cognitivos, tales como amnesia o enfermedad de Alzheimer, también se clasifican a veces como trastornos psiquiátricos.
Otros trastornos propuestos incluyen: trastorno de personalidad autodestructivo, trastorno de personalidad sádica, trastorno de personalidad pasiva-agresiva, trastorno disfórico premenstrual, trastorno de adición a los videojuegos o de adicción a internet.
El trastorno bipolar es un diagnóstico psiquiátrico que describe una categoría de trastornos del estado de ánimo definidos por la presencia de uno o más episodios de estado de ánimo anómalamente elevado clínicamente mencionado como manía o, si es más leve, hipomanía. Los individuos que experimentan episodios maníacos también experimentan habitualmente episodios o síntomas depresivos, o episodios mixtos en que hay características tanto de manía como de depresión presentes al mismo tiempo. Estos episodios están separados habitualmente por periodos de estado de ánimo "normal", pero en algunos individuos la depresión y la manía pueden alternar rápidamente, conocido como ciclo rápido. Los episodios maníacos extremos a veces pueden dar lugar a síntomas psicóticos tales como delirios y alucinaciones. El trastorno se ha subdividido en bipolar I, bipolar II, ciclotimia y otros tipos, basándose en la naturaleza y gravedad de los episodios del estado de ánimo experimentados; el intervalo se describe a menudo como el espectro bipolar.
El autismo (también mencionado como trastorno de espectro autista, o ASD) es un trastorno que altera gravemente el funcionamiento de los individuos. Se caracteriza por autoabsorción, una capacidad reducida de comunicarse con o responder al mundo exterior, rituales y fenómenos compulsivos y retraso mental. Los individuos autistas también están en riesgo aumentado de desarrollar trastornos convulsivos, tales como epilepsia. Aunque la causa real del autismo es desconocida, parece que incluye uno o más factores genéticos, como se indica por el hecho de que la tasa de concordancia es mayor en gemelos monocigóticos que en gemelos dicigóticos y también puede implicar factores inmunitarios y ambiental, tales como la dieta, agentes químicos tóxicos e infecciones.
La esquizofrenia es un trastorno que afecta a aproximadamente un uno por ciento de la población mundial. A menudo se mencionan tres síntomas generales de esquizofrenia como síntomas positivos, síntomas negativos y síntomas desorganizados. Los síntomas positivos pueden incluir delirios (creencias anómalas), alucinaciones (percepciones anómalas) y pensamiento desorganizado. Las alucinaciones de la esquizofrenia pueden ser auditivas, visuales, olfativas o táctiles. El pensamiento desorganizado puede manifestarse por sí mismo en pacientes esquizofrénicos mediante habla inconexa y la incapacidad de mantener un proceso de pensamiento lógico. Los síntomas negativos pueden representar la ausencia de comportamiento normal. Los síntomas negativos incluyen aplanamiento emocional o ausencia de expresión y pueden caracterizarse por la retracción social, energía reducida, motivación reducida y actividad reducida. La catatonia también puede estar asociada con los síntomas negativos de la esquizofrenia. Los síntomas de la esquizofrenia deben persistir de forma continua durante un tiempo de aproximadamente seis meses para que el paciente se diagnostique como esquizofrénico. Basándose en los tipos de
síntomas que revela un paciente, la esquizofrenia puede clasificarse en subtipos incluyendo esquizofrenia catatónica, esquizofrenia paranoide y esquizofrenia desorganizada.
Los ejemplos de fármacos antipsicóticos que pueden usarse para tratar a los pacientes esquizofrénicos incluyen fenotiacinas, tales como clorpromazina y trifluopromazina; tioxantenos, tales como clorprotixeno; flufenazina; butiropenonas, tales como haloperidol; loxapina; mesoridazina; molindona; quetiapina; tiotixeno; trifluoperazina; perfenazina; tioridazina; risperidona; dibenzodiazepinas, tales como clozapina; y olanzapina. Aunque estos compuestos pueden aliviar los síntomas de la esquizofrenia, su administración puede provocar efectos secundarios indeseables incluyendo síntomas de tipo enfermedad de Parkinson (temblores, rigidez muscular, pérdida de expresión facial); distonía; inquietud; discinesia tardía; aumento de peso; problemas cutáneos; sequedad bucal; estreñimiento; visión borrosa, somnolencia; habla confusa y agranulocitosis.
Los trastornos del estado de ánimo se caracterizan típicamente por exageraciones generalizadas, prolongadas y discapacitantes del estado de ánimo y el afecto que están asociadas con disfunciones del comportamiento, psicológicas, cognitivas, neuroquímicas y psicomotoras. Los trastornos del estado de ánimo principales incluyen, aunque sin limitación, trastorno depresivo mayor (también conocido como trastorno unipolar), trastorno bipolar (también conocido como enfermedad depresiva maníaca o depresión bipolar), trastorno distímico.
El término "depresión", a veces se usa indistintamente con "trastorno depresivo" y se refiere a trastornos del estado de ánimo que se manifiestan en tristeza mórbida, abatimiento o melancolía. Los trastornos depresivos pueden implicar sistemas neuronales serotonérgicos o noradrenérgicos basados en las pautas terapéuticas actuales que abordan los receptores de serotonina y noradrenalina. La manía puede ser el resultado de un desequilibrio en determinados mensajeros químicos dentro del cerebro. Se ha informado de que la administración de fosfotidilcolina alivia los síntomas de manía. En determinadas realizaciones, la depresión descrita en la presente memoria es depresión insensible a litio.
La manía es una forma mantenida de euforia que afecta a millones de personas en los Estados Unidos que padecen depresión. Los episodios maníacos pueden caracterizarse por un estado de ánimo elevado, expansivo o irritable que dura varios días, y a menudo viene acompañado por otros síntomas, tales como hiperactividad, conversación excesiva, intrusión social, energía aumentada, presión de ideas, grandiosidad, distracción, disminución de la necesidad de dormir y temeridad. Los pacientes maníacos también pueden experimentar delirios y alucinaciones.
Los trastornos de ansiedad se caracterizan por aparición frecuente de síntomas de temor incluyendo excitación, inquietud, mayor capacidad de respuesta, sudoración, corazón acelerado, aumento de la presión arterial, sequedad bucal, un deseo de correr o escapar, y conducta de evitación. La ansiedad generalizada persiste durante varios meses, y está asociada con tensión motora (temblores, espasmos, dolores musculares, inquietud); hiperactividad autónoma (falta de aliento, palpitaciones, ritmo cardíaco aumentado, sudoración, manos frías) y vigilancia y exploración (sensación al límite, respuesta de sobresalto exagerada, dificultad en la concentración). Las benzodiazepinas, que potencian los efectos inhibidores del receptor de ácido gamma aminobutírico (GABA) de tipo A, se usan frecuentemente para tratar la ansiedad. Las buspirona es otro tratamiento para la ansiedad eficaz.
El trastorno esquizoafectivo describe una afección donde hay síntomas tanto de un trastorno del estado de ánimo como esquizofrenia, presentes. Una persona puede manifestar alteraciones en la percepción o la expresión de la realidad, más habitualmente en forma de alucinaciones auditivas, delirios paranoides o bizarros o habla y pensamiento desorganizado, así como episodios maníacos y/o depresivos concretos en el contexto de una disfunción social u ocupacional significativa.
En algunas realizaciones, un compuesto proporcionado es útil en el tratamiento del trastorno de hiperactividad con déficit de atención (ADHD). En algunas realizaciones, el tratamiento de ADHD se logra inhibiendo CK15 (véase, por ejemplo, Zhou, et al. Proc. Natl. Acad. Sci. USA 2010, 107:4401).
En determinadas realizaciones, un compuesto proporcionado estimula la neurogénesis. Por consiguiente, en algunas realizaciones, un compuesto proporcionado es útil en el tratamiento de enfermedades que están relacionadas con la neurogénesis. Por ejemplo, un compuesto proporcionado es útil para tratar un trastorno neurológico en un sujeto, que comprende administrar al sujeto una cantidad eficaz de un compuesto proporcionado o su sal farmacéuticamente aceptable. En algunas realizaciones, el trastorno neurológico es deterioro cognitivo asociado con envejecimiento normal, lesión cerebral traumática, enfermedad de Parkinson, depresión mayor, trastorno bipolar, epilepsia, ataxia espinocerebelar, enfermedad de Huntington, ALS, apoplejía, radioterapia, trastorno de estrés postraumático, síndrome de Down, estrés crónico, degeneración de la retina, lesión de la médula espinal, lesión de los nervios periféricos, pérdida de peso fisiológica asociada con diversas afecciones, abuso de un fármaco neuroactivo, lesión de la médula espinal o deterioro cognitivo asociado con quimioterapia.
En algunas realizaciones, un compuesto proporcionado es útil en la regulación de los ritmos circadianos en un sujeto que o necesita. En algunas realizaciones, la regulación de los ritmos circadianos anómalos se logra por inhibición de CK15.
En algunas realizaciones, un compuesto proporcionado es útil en el tratamiento de la alopecia.
En algunas realizaciones, un compuesto proporcionado es útil como inmunopotenciador.
En algunas realizaciones, un compuesto proporcionado es útil en el tratamiento del cáncer. El cáncer que se trata mediante un compuesto proporcionado puede estar mediado por GSK3a y/o GSK3p. En algunas realizaciones, un compuesto proporcionado es útil en el tratamiento de un cáncer descrito en la presente memoria, por ejemplo, en algunas realizaciones, un compuesto proporcionado es útil en el tratamiento de leucemia. En determinadas realizaciones, un compuesto proporcionado es útil en el tratamiento de leucemia mieloide aguda (AML). En determinadas realizaciones, un compuesto proporcionado es útil en el tratamiento de leucemia linfocítica aguda (ALL), leucemia mielocítica crónica (CML) y/o leucemia linfocítica crónica (CLL). En algunas realizaciones, el tratamiento de leucemia (por ejemplo, leucemia mieloide agua) se logra mediante inhibición de GSK3a. En algunas realizaciones, un compuesto proporcionado es útil en el tratamiento de mieloma múltiple. En algunas realizaciones, un compuesto proporcionado es útil en el tratamiento de glioma o cáncer pancreático. En algunas realizaciones, un compuesto proporcionado es útil en el tratamiento de cáncer de mama, carcinoma broncopulmonar no microcítico, cáncer tiroideo, leucemia de linfocitos T o linfocitos B o un tumor inducido por virus.
GSK3a y GSK3p también están implicadas en trastornos metabólicos, tales como diabetes (por ejemplo, diabetes de tipo II) (A. S. Wagman, K. W. Johnson y D. E. Bussiere, Curr. Pharm. Design, 2004, 10, 1105). La actividad de GSK3 está elevada en modelos humanos y de roedor de diabetes, y diversos inhibidores de GSK3 y mejoran la tolerancia a glucosa y la sensibilidad a la insulina en modelos de roedor de obesidad y diabetes. A diferencia de los mutantes de GSK3p, que mueren antes del nacimiento, los animales con silenciamiento de GSK3a (GSK3a KO) son viables, pero presentan sensibilidad potenciada a la glucosa y la insulina acompañada por una masa grasa reducida (Katrina et al., Cell Metabolism 6, 329-337, October 2007). El contenido de glucógeno hepático en ayunas y estimulado por glucosa se potenció en ratones GSK3a KO, mientras que el glucógeno muscular estuvo inalterado. La fosforilación de proteína cinasa B (PKB/Akt) y GSK3p estimulada por insulina fue mayor en hígados GSK3a KO en comparación con hermanos de la misma camada de tipo silvestre, y la expresión de IRS-1 estaba aumentada notablemente. Se concluyó que las isoformas de GSK3 muestran funciones fisiológicas específicas de tejido y que los ratones GSK3a KO son sensibles a insulina, lo que refuerza el potencial de GSK3 como diana terapéutica para diabetes de tipo II.
En algunas realizaciones, un compuesto proporcionado es útil en el tratamiento de un trastorno metabólico. En algunas realizaciones, un compuesto proporcionado es útil en el tratamiento de la diabetes (por ejemplo, diabetes de tipo 1, diabetes de tipo 2 o diabetes gestacional). En algunas realizaciones, un compuesto proporcionado es útil en el tratamiento de diabetes de tipo 2. En algunas realizaciones, un compuesto proporcionado es útil en el tratamiento de la obesidad.
Ejemplos
Para que la invención descrita en la presente memoria puede comprender más completamente, se exponen los siguientes ejemplos. Debe entenderse que estos ejemplos son con fines ilustrativos únicamente y no deben interpretarse como limitantes de esta invención de ninguna manera.
Se cribó una colección de más de trecientos veinte mil compuestos frente a GSK3p humana. Entre los inhibidores identificados, el compuesto 1 mostró potencia aceptable y selectividad excelente, inhibiendo únicamente otras cuatro cinasas de más de trescientas cinasas a 10 pM en más de un cincuenta por ciento. Las posteriores modificaciones químicas del compuesto 1, guiadas por una estructura cocristalina con GSK3p, y una batería de ensayos bioquímicos y basados en células, dieron lugar al compuesto 54 que inhibe GSK3p con una CI50 entre 10-30 nM. El compuesto 54 tiene un perfil de selectividad superior en todo el cinoma en comparación con CHIR99021. Además, el compuesto 54 demuestra actividad celular excelente en la inhibición de la fosforilación de Tau mediada por GSK3p en células de neuroblastoma SH-SY5Y (CI50 de 1 pM) y en el alivio de la regulación negativa por GSK3p en la degradación de p-catenina celular y actividades promotoras de TCF/LEF con CE50 de 5 pM en ambos ensayos. Al mismo tiempo, no se observó toxicidad celular por el compuesto 54 en células SH-SY5Y a la máxima concentración de ensayo de 30 pM. Tomados en conjunto, el compuesto 54 es una sonda molecular pequeña potente y altamente selectiva contra GSK3p, lo que permite una mejor investigación e interpretación de los inhibidores conocidos previamente de las funciones celulares de GSK3p. El armazón del compuesto 54 también trae la promesa de suministrar compuestos adicionales con propiedades bioquímicas, celulares y farmacocinéticas mejoradas adicionales adecuadas para investigar las funciones in vivo de GSK3p en fisiología y patología animal pertinentes.
Métodos sintéticos
Detalles generales. Todas las reacciones sensibles al oxígeno y/o la humedad se realizaron en atmósfera de nitrógeno (N2) en artículos de cristal que se habían secado al fuego al vacío (aproximadamente 0,5 mm de Hg) y se habían purgado con N2 antes de su uso. Todos los reactivos y disolventes se adquirieron de vendedores comerciales y se usaron como se recibieron, o se sintetizaron de acuerdo con métodos ya presentados. Los espectros de RMN se registraron en un espectrómetro Bruker 300 (300 MHz 1H, 75 MHz 13C) o Varian UNITY INOVA 500 (500 MHz 1H, 125 MHz 13C). Los desplazamientos químicos de protones y carbono se presentan en ppm (8) con referencia al disolvente de RMN. Los datos se presentan de la siguiente manera: desplazamientos químicos, multiplicidad (a = ancho, s = singulete, d = doblete, t = triplete, c = cuadruplete, m = multiplete; constante(s) de acoplamiento en Hz).
Salvo que se indique otra cosa, los datos de RMN se recogieron a 25 °C. Se realizó cromatografía ultrarrápida usando gel de sílice de 40-60 pm (malla de 60 A) en un Teledyne Isco Combiflash Rf Se realizó cromatografía de líquidos/espectrometría de masas en tándem (CL/EM) en un módulo de separaciones Waters 2795 y detector de masas 3100. Se realizó cromatografía en capa fina (CCF) analítica en placas 60-F de gel de sílice de 0,25 mm de EM Reagent. La visualización se consiguió con luz ultravioleta (UV) y tinte de permanganato de potasio (KMnO4) acuoso seguido de calentamiento. Los espectros de masas de alta resolución se obtuvieron en la instalación de espectrométrica de masas de MIT (Bruker Daltonics APEXIV 4.7 Tesla Fourier Transform Ion Ciclotron Resonance Mass Spectrometer).
En el protocolo de síntesis A (esquema 1a), se disolvieron 1,3-diona (1,0 equivalentes), aldehído (1,0 equivalentes) y amina (1,35 equivalentes) en etanol (0,4 M) y la mezcla se calentó a 150 °C en el microondas durante 15 minutos. La mezcla de reacción se enfrió y el etanol se evaporó. La mezcla de reacción en bruto se purificó por cromatografía en columna sobre sílice (ISCO).
4-(2-metoxifenM)-7,7-dimetN-3-(tN fluorometM)-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]qumolm-5(4H)-ona:
5,5-Dimetilcidohexano-1,3-diona (824 mg, 5,88 mmol), 2-metoxibenzaldehído (800 mg, 5,88 mmol) y 3-(trifluorometil)-1H-pirazol-5-amina (1199 mg, 7,93 mmol) se mezclaron juntos en un vial de microondas y se le añadió etanol (14,7 ml, 0,4 M). La mezcla de reacción se calentó en microondas durante 15 min a 150 °C. La mezcla se enfrió y el disolvente se evaporó. La mezcla resultante entonces se purificó por cromatografía en columna sobre gel de sílice (hexano/acetato de etilo: 100/0 a 20/80) para producir el producto deseado como un sólido blanco (372,0 mg). 1H NMR (300 MHz, MeOD) 87.19 (d, J= 7.4 Hz, 1H), 7.12 - 7.03 (m, 1H), 6.78 (dd, J= 13.8, 7.4 Hz, 2H), 5.39 (s, 1H), 3.67 (s, 3H), 2.56 (d, J = 16.8 Hz, 1H), 2.42 (d, J = 16.7 Hz, 1H), 2.24 (d, J = 16.5 Hz, 1H), 2.04 (d, J = 16.5 Hz, 1H), 1.08 (s, 3H), 0.97 (s, 3H). LRMS (ESI+) (M+): 391.82.
La mezcla racémica se separó por HPLC quiral para proporcionar (R)-4-(2-metoxifenil)-7,7-dimetil-3-(trifluorometil)-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-5(4H)-ona (compuesto 54) y (S)-4-(2-metoxifenil)-7,7-dimetil-3-(trifluorometil)-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-5(4H)-ona (compuesto 55).
En el protocolo de síntesis B, se disolvió 1,3-diona (1,0 equivalentes) en ácido trifluoroacético (0,45 M) seguido de la adición de cetona (10,0 equivalentes) en una porción. La reacción se calentó a reflujo durante 3 horas a 190 °C, seguido de la adición de amina (1,5 equivalentes) y se continuó el reflujo durante 2,5 horas adicionales a 190 °C. La mezcla de reacción se enfrió y se evaporó (para retirar el TFA). La mezcla de reacción en bruto se purificó por HPLC.
4,7,7-tnmetN-4-feml-3-(tnfluorometM)-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]qumolm-5(4H)-ona
En un matraz rb de 25 ml, se disolvió 5,5-dimetilciclohexano-1,3-diona (1402,0 mg, 10,0 mmol, 1,0 equivalente) en ácido trifluoroacético (10,0 ml, 0,47 molar), seguido de la adición de acetofenona (11,44 ml, 100,0 mmol, 10,0 equivalentes) en una porción. La reacción se calentó a reflujo durante 3 horas a 190 °C, seguido de la adición de 3-(trifluorometil)-1H-pirazol-5-amina (1511,0 mg, 10,0 mmol, 1,5 equivalentes) y se continuó el reflujo durante 2,5 horas adicionales a 190 °C. La mezcla de reacción se enfrió y se evaporó para retirar el TFA. La mezcla de reacción en bruto se purificó por HPLC para producir el producto deseado como un sólido blanco (17,0 mg). 1H NMR (300 MHz, DMSO) 87.24 (d, J = 7.6 Hz, 2H), 7.14 (t, J = 7.6 Hz, 2H), 6.99 (t, J = 7.1 Hz, 1H), 2.43 (d, J = 4.7 Hz, 2H), 2.01 (d, J = 15.8 Hz, 1H), 1.92 (s, 3H), 1.86 (d, J = 15.8 Hz, 1H), 0.99 (s, 3H), 0.92 (s, 3H). LRMS (ESI+) (M+H): 376.24, retention time 0.67 min.
La mezcla racémica se separó por HPLC quiral para proporcionar compuesto 70 o compuesto 71.
7,7-dimetN-4-feml-3-(trifluorometM)-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]qumolm-5(4W)-ona
1H NMR (300 MHz, d6-DMSO) 810.14 (s, 1H), 7.23 - 7.12 (m, 2H), 7.12 - 7.00 (m, 3H), 5.07 (s, 1H), 2.56 -2.35 (m, 2H), 2.15 - 2.09 (m, 1H), 1.95 - 1.90 (m, 1H), 1.01 (s, 3H), 0.88 (s, 3H).LRMS (ESI+): 362 ([M+H]+), retention time 0.62 min.
3,7,7-trimetil-4-(tiofen-2-il)-6,7,8,9-tetrahidro-1H-pirazolo[3,4-b]quinolin-5(4H)-ona
1H NMR (300 MHz, d6-DMSO) 811.63 (s, 1H), 9.54 (s, 1H), 6.9 (d, J = 3.0 Hz, 1H), 6.57 (t, J = 3.0, 6.0 Hz, 1H), 6.51 (d, J = 3.0 Hz, 1H), 5.07 (s, 1H), 2.18 - 2.08 (m, 2H), 1.95 - 1.76 (m, 2H), 1.90 (s, 3H), 0.77 (s, 3H), 0.75 (s, 3H). LRMS (ESI+): 314 ([M+H]+), retention time 0.57 min. La mezcla racémica se separó por HPLC quiral para proporcionar compuesto 6 y compuesto 7.
3,7,7-trimetil-4-(tiofen-3-il)-6,7,8,9-tetrahidro-1H-pirazolo[3,4-b]quinolin-5(4H)-ona
1H NMR (300 MHz, d6-DMSO) 811.77 (s, 1H), 9.68 (s, 1H), 7.26 (s, 1H), 6.95 (d, J = 3.0 Hz, 1H), 6.78 (d, J = 3.0 Hz, 1H), 5.09 (s, 1H), 2.49 - 2.33 (m, 2H), 2.17 - 2.08 (m, 2H), 2.0 (s, 3H), 1.00 (s, 3H), 0.94 (s, 3H). LRMS (ESI+): 314 ([M+H]+), retention time 0.57 min.
4-(5-clorotiofen-2-il)-3,7,7-trimetil-6,7,8,9-tetrahidro-1H-pirazolo[3,4-b]quinolin-5(4H)-ona.1
1H NMR (300 MHz, d6-DMSO) 811.71 (s, 1H), 9.62 (s, 1H), 6.54 (d, J = 3.0 Hz, 1H), 6.3 (d, J = 3.0 Hz, 1H), 4.99 (s, 1H), 2.3 - 2.07 (m, 2H), 1.9 (s, 3H), 1.95 - 1.81 (m, 2H), 0.75 (s, 3H), 0.73 (s, 3H). LRMS (ESI+): 348 ([M+H]+), retention time 0.64 min.
4-(2-fluorofenil)-3,7,7-trimetil-6,7,8,9-tetrahidro-1H-pirazolo[3,4-b]quinolin-5(4H)-ona
1H NMR (300 MHz, d6-DMSO) 8 11.77 (s, 1H), 9.76 (s, 1H), 7.10 - 7.01 (m, 4H), 5.18 (s, 1H), 2.45 - 2.32 (m, 2H), 2.15 -1.95 (m, 2H), 1.88 (s, 1H), 1.01 (s, 3H), 0.96 (s, 3H). LRMS (ESI+): 327 ([M+H]+), retention time 0.59 min. 4-(3-fluorofenil)-3,7,7-trimetil-6,7,8,9-tetrahidro-1H-pirazolo[3,4-b]quinolin-5(4H)-ona
1H NMR (300 MHz, d6-DMSO) 811.8 (s, 1H), 9.76 (s, 1H), 7.23 (m, 1H), 6.95 (d, J = 9.0 Hz, 1H), 6.90 -6.84 (m, 2H), 4.97 (s, 1H), 2.44 - 2.37 (m, 2H), 2.15 - 1.93 (m, 2H), 1.91 (s, 3H), 1.00 (s, 3H), 0.94 (s, 3H). LRMS (ESI+): 327 ([M+H]+), retention time 0.61 min.
4-(4-fluorofenil)-3,7,7-trimetil-6,7,8,9-tetrahidro-1H-pirazolo[3,4-b]quinolin-5(4H)-ona
1H NMR (300 MHz, d6-DMSO) 811.77 (s, 1H), 9.73 (s, 1H), 7.13 (d, J = 6.0 Hz, 2H), 6.99 (d, J = 6.0 Hz, 2H), 4.94 (s, 1H), 2.43 - 2.35 (m, 2H), 2.14 - 1.91 (m, 2H), 1.89 (s, 3H), 1.00 (s, 3H), 0.93 (s, 3H). LRMS (ESI+): 327 ([M+H]+), retention time 0.60 min.
4-(3-clorofenil)-3,7,7-trimetil-6,7,8,9-tetrahidro-1H-pirazolo[3,4-b]quinolin-5(4H)-ona
1H NMR (300 MHz, d6-DMSO) 811.57 (s, 1H), 9.54 (s, 1H), 7.00 -6.95 (m, 1H), 6.87 -6.83 (m, 3H) 4.7 (s, 1H), 2.25 - 2.12 (m, 2H), 1.91 - 1.69 (m, 2H), 1.66 (s, 3H), 0.76 (s, 3H), 0.69 (s, 3H). LRMS (ESI+): 342 ([M+H]+), retention time 0.62 min.
4-(4-clorofenil)-3,7,7-trimetil-6,7,8,9-tetrahidro-1H-pirazolo[3,4-b]quinolin-5(4H)-ona
1H NMR (300 MHz, d6-DMSO) 811.60 (s, 1H), 9.57 (s, 1H), 7.05 (d, J = 9.0 Hz, 2H), 6.95 (d, J = 9.0 Hz, 2H), 4.74 (s, 1H), 2.25 - 2.22 (m, 2H), 1.95 - 1.72 (m, 2H), 1.70 (s, 3H), 0.81 (s, 3H), 0.74 (s, 3H). LRMS (ESI+): 342 ([M+H]+), retention time 0.64 min.
3,7,7-trimetil-4-(p-tolil)-6,7,8,9-tetrahidro-1H-pirazolo[3,4-b]quinolin-5(4H)-ona
1H NMR (300 MHz, d6-DMSO) 811.65 (s, 1H), 9.61 (s, 1H), 6.99 (m, 4H), 4.89 (s, 1H), 2.44 - 2.30 (m, 2H), 2.25 (s, 3H), 2.24 -2.19 (m, 2H), 2.18 (s, 3H), 1.00 (s, 3H), 0.95 (s, 3H). LRMS (ESI+): 322 ([M+H]+), retention time 0.62 min.
4-(2-metoxifenil)-3,7,7-trimetil-6,7,8,9-tetrahidro-1H-pirazolo[3,4-b]quinolin-5(4H)-ona
1H NMR (300 MHz, DMSO) 811.39 (s, 1H), 9.38 (s, 1H), 6.79 (t, J = 6.0, 15.0 Hz, 1H), 6.70 (d, J = 6.0 Hz, 1H), 6.65 (d, J = 9.0 Hz, 1H), 6.52 (t, J = 6.0, 15.0 Hz, 1H), 5.08 (s, 1H), 3.6 (s, 3H), 2.22-2.14 (m, 2H), 1.90 - 1.71 (m, 2H), 1.67 (s, 3H), 0.78 (s, 3H), 0.75 (s, 3H). LRMS (ESI+): 339 ([M+H]+), retention time 0.58-0.59 min.
4-(3-metoxifenil)-3,7,7-trimetil-6,7,8,9-tetrahidro-1H-pirazolo[3,4-b]quinolin-5(4H)-ona
1H NMR (300 MHz, d6-DMSO) 811.5 (s, 1H), 9.45 (s, 1H), 6.85 (t, J = 6.0, 15.0 Hz, 1H), 6.48 -6.37 (m, 3H), 4.66 (s, 1H), 3.43 (s, 3H), 2.21 - 2.12 (m, 2H), 1.92 - 1.71 (m, 2H), 1.69 (s, 3H), 0.77 (s, 3H), 0.72 (s, 3H). LRMS (ESI+): 339 ([M+H]+), retention time 0.59 min.
4-(4-metoxifenil)-3,7,7-trimetil-6,7,8,9-tetrahidro-1H-pirazolo[3,4-b]quinolin-5(4H)-ona
1H NMR (300 MHz, d6-DMSO) 811.71(s, 1H), 9.65 (s, 1H), 7.2 (d, J = 9.0 Hz, 2H), 6.72 (d, J = 9.0 Hz, 2H), 4.87 (s, 1H), 3.66 (s, 3H), 2.42 - 2.34 (m, 2H), 2.13 - 1.96 (m, 2H), 1.89 (s, 3H), 1.00 (s, 3H), 0.93 (s, 3H). LRMS (ESI+): 339 ([M+H]+), retention time 0.58 min.
4-(benzo[d][1,3]dioxol-5-il)-3,7,7-trimetil-6,7,8,9-tetrahidro-1H-pirazolo[3,4-b]quinolin-5(4H)-ona
1H NMR (300 MHz, d6-DMSO) 8 11.75 (s, 1H), 9.68 (s, 1H), 6.70 (d, J = 9.0 Hz, 1H), 6.59 (m, 2H), 5.90 (d, J = 6.0 Hz, 2H), 4.86 (s, 1H), 2.42 - 2.35 (m, 2H), 2.14 - 1.95 (m, 2H), 1.92 (s, 3H), 1.00 (s, 3H), 0.94 (s, 3H). LRMS (ESI+): 352 ([M+H]+), retention time 0.57 min.
4-(2-cloro-4-fluoropheoil)-3,7,7-trimetil-6,7,8,9-tetrahidro-1H-pirazolo[3,4-b]quinolin-5(4H)-ona
1H NMR (300 MHz, d6-DMSO) 811.56 (s, 1H), 9.56 (s, 1H), 6.97 (m, 1H), 6.83 (m, 2H), 5.06 (s, 1H), 2.20 -2.11 (m, 2H), 1.88 - 1.69 (m, 2H), 1.63 (s, 3H), 0.76 (s, 3H), 0.70 (s, 3H). LRMS (ESI+): 360 ([M+H]+), retention time 0.64 min.
3,7,7-trimetil-4-(piridin-2-il)-6,7,8,9-tetrahidro-1H-pirazolo[3,4-b]quinolin-5(4H)-ona
1H NMR (300 MHz, d6-DMSO) 811.52 (s, 1H), 9.51 (s, 1H), 8.17 (d, J = 3.0 Hz, 1H), 7.41 (t, J = 6.0 Hz, 15.0 Hz, 1H), 6.95 (d, J = 9.0 Hz, 1H), 6.87 (t, J = 6.0, 12.0 Hz, 1H), 4.89 (s, 1H), 2.31 - 2.26 (m, 2H), 1.97 - 1.76 (m, 5H), 0.83 (s, 6H). LRMS (ESI+): 310 ([M+H]+), retention time 0.50 min.
3,7,7-trimetil-4-(piridin-3-il)-6,7,8,9-tetrahidro-1H-pirazolo[3,4-b]quinolin-5(4H)-ona
1H NMR (300 MHz, d6-DMSO) 811.64 (s, 1H), 9.62 (s, 1H), 8.20 (s, 1H), 8.06 (d, J = 6.0 Hz, 1H), 7.25 (d, J = 9.0 Hz, 1H), 7.01 (t, J = 6.0, 12.0 Hz, 1H), 5.57 (s, 1H), 2.26 - 2.22 (m, 2H), 1.96 - 1.73 (m, 2H), 1.69 (s, 3H), 0.81 (s, 3H), 0.73 (s, 3H). LRMS (ESI+): 310 ([M+H]+), retention time 0.49 min.
3,7,7-trimetil-4-(piridin-4-il)-6,7,8,9-tetrahidro-1H-pirazolo[3,4-b]quinolin-5(4H)-ona
1H NMR (300 MHz, d6-DMSO) 8 11.61 (s, 1H), 9.6 (s, 1H), 8.12 (d, J = 6.0 Hz, 2H), 6.88 (d, J= 6.0 Hz, 2H), 4.7 (s, 1H), 2.21 - 2.14 (m, 2H), 1.92 - 1.70 (m, 2H), 1.66 (s, 3H), 0.77 (s, 3H), 0.71 (s, 3H). LRMS (ESI+): 310 ([M+H]+), retention time 0.48 min.
4-(5-bromopiridin-2-il)-3,7,7-trimetil-6,7,8,9-tetrahidro-1H-pirazolo[3,4-b]quinolin-5(4H)-ona
1H NMR (300 MHz, d6-DMSO) 811.52 (s, 1H), 9.51 (s, 1H), 8.23 (s, 1H), 7.61 (d, J = 9.0 Hz, 1H), 6.92 (d, J = 9.0 Hz, 1H), 4.83 (s, 1H), 2.20 - 2.17 (m, 2H), 1.91 - 1.71 (m, 2H), 1.69 (s, 3H), 0.77 (s, 3H), 0.75 (s, 3H). LRMS (ESI+): 389 ([M+H]+), retention time 0.57 min.
3,7,7-trimetil-4-(1H-pirazol-5-il)-6,7,8,9-tetrahidro-1H-pirazolo[3,4-b]quinolin-5(4H)-ona 1
1H NMR (300 MHz, d6-DMSO) 8 12.20-11.40(m, 1H), 9.60-9.25 (m, 1H), 7.25-6.80(m, 1H), 5.70-5.30 (m, 1H), 4.90 4.75 (m, 1H), 2.20 (br s, 3H), 2.00-1.75 (m, 4H), 0.80-0.70 (br s, 6H), . LRMS (ESI+): 299 ([M+H]+), retention time 0.45 min.
4-(2-clorofenil)-3,7,7-trimetil-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-5(4H)-ona
1H NMR (300 MHz, d6-DMSO) 8 11.77 (s, 1H), 9.77 (s, 1H), 7.27 (d, J = 7.6, 1H), 7.19-7.02 (m, 3H), 5.34 (s, 1H), 2.48 - 2.23 (m, 2H), 2.17-2.04 (m, 1H), 1.88 (s, 3H), 1.96 - 1.81 (m, 1H), 1.01 (s, 3H), 0.95 (s, 3H); LRMS (ESI+): 342 ([M+H]+), retention time 0.61 min.
3,7,7-trimetil-4-(o-tolil)-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-5(4H)-ona
1H NMR (300 MHz, d6-DMSO) 8 11.70 (s, 1H), 9.69 (s, 1H), 86.98 (t, J = 6.9 Hz, 2H), 6.93 - 6.87 (m, 2H), 5.05 (s, 1H), 3.17 (d, J = 5.2, 3H), 2.49-2.31 (m, 2H), 2.15-2.03 (m, 1H), 1.96- 1.85 (m, 1H), 1.79 (s, 3H), 1.00 (s, 1H), 0.91 (s, 1H); LRMS (ESI+): 322 ([M+H]+), retention time 0.62 min.
3,7,7-trimetil-4-(4-(trifluorometil)fenil)-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-5(4H)-ona
1H NMR (300 MHz, d6-DMSO) 811.83 (s, 1H), 9.83 (s, 1H), 7.56 (d, J = 8.1, 2H), 7.34 (d, J = 8.0, 2H), 5.03 (s, 1H), 2.49-2.35 (m, 2H), 2.17-2.08 (m, 1H), 1.98-1.90 (m, 1H), 1.88 (s, 3H), 1.00 (s, 3H), 0.93 (s, 3H); LRMS (ESI+): 376 ([M+H]+), retention time 0.68 min.
3,4,7,7-tetrametil-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-5(4H)-ona
(d, J = 3.6 Hz, 2H), 1.03 (d, J = 6.4 Hz, 3H), 1.00 (s, 3H), 0.98 (s, 3H); LRMS (ESI+): 246 ([M+H]+), retention time 0.52 min.
4-ciclohexil-3,7,7-trimetil-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-5(4H)-ona
1H NMR (300 MHz, d6-DMSO) 811.72 (s, 1H), 9.40 (s, 1H), 3.76 (s, 1H), 82.37-2.38 (m, 2H), 2.20 - 2.04 (m, 5H), 1.71 - 1.39 (m, 6H), 1.39 - 1.20 (m, 2H), 1.02 (s, 3H), 0.99 (s, 3H), 0.63 - 0.46 (m, 2H); LRMS (ESI+): 314 ([M+H]+), retention time 0.65 min.
4-deutero-3,7,7-trimetil-4-fenil-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-5(4H)-ona
1H NMR (300 MHz, d6-DMSO) 811.73 (s, 1H), 9.70 (s, 1H), 87.21 - 7.09 (m, 4H), 7.03 (t, J= 6.9 Hz, 1H), 2.47-2.33 (m, 2H), 2.18-2.06 (m, 1H), 1.99-1.85 (m, 4H), 1.00 (s, 3H), 0.94 (s, 3H); LRMS (ESI+): 309 ([M+H]+), retention time 0.59 min.
4-ciclopropil-3,7,7-trimetil-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-5(4H)-ona
1H NMR (300 MHz, d6-DMSO) 811.80 (s, 1H), 9.44 (s, 1H), 83.91 (d, J = 5.6Hz, 1H), 2.35 -2.28 (m, 2H), 2.19 -2.06 (m, 5H), 1.03 (s, 3H), 0.99 (s, 3H), 0.96 - 0.87 (m, 1H), 0.20 - 0.02 (m, 3H), -0.12- -0.22 (m, 1H); LRMS (ESI+): 272 ([M+H]+), retention time 0.56 min.
3,7,7-trimetil-4-(m-tolil)-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-5(4H)-ona 1
1H NMR (300 MHz, d6-DMSO) 8 11.72 (s, 1H), 9.67 (s, 1H), 7.09 - 7.01 (m, 1H), 6.94-6.82 (m, 3H), 4.87 (s, 1H), 2.46-2.33 (m, 2H), 2.20 (s, 3H), 2.16-2.04 (m, 1H), 2.01-1.83 (m, 4H), 1.00 (s, 3H), 0.95 (s, 3H); LRMS (ESI+): 322 ([M+H]+), retention time 0.61 min.
4-(2-metoxifenil)-3,6,6-trimetil-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-5(4H)-ona
1H NMR (300 MHz, d6-DMSO) 811.60 (s, 1H), 9.54 (s, 1H), 7.05-6.98 (m, 1H), 6.92-6.84 (m, 2H), 6.77-6.69 (m, 1H), 5.31 (s, 1H), 3.82 (s, 3H), 2.30-2.24 (m, 2H), 1.91 (s, 3H), 1.79-1.70 (m, 2H), 0.94 (s, 3H), 0.85 (s, 3H); LRMS (ESI+): 338 ([M+H]+), retention time 0.62 min.
2-(3,7,7-trimetil-5-oxo-4,5,6,7,8,9-hexahidro-2H-pirazolo[3,4-b]quinolin-4-il)benzonitrilo
1H NMR (300 MHz, DMSO) 811.74 (s, 1H), 9.70 (s, 1H), 87.21 -6.99 (m, 4H), 4.91 (s, 1H), 2.46-2.33 (m, 2H), 2.16 -2.07 (m, 1H),1.98-1.85 (m, 4H), 1.00 (s, 1H), 0.94 (s, 1H) ; LRMS (ESI+): 333 ([M+H]+), retention time 0.57 min. 3-(3,7,7-trimetil-5-oxo-4,5,6,7,8,9-hexahidro-2H-pirazolo[3,4-b]quinolin-4-il)benzonitrilo
1H NMR (300 MHz, DMSO) 8 11.89 (s, 1H), 9.93 (s, 1H), 7.69-7.63 (m, 1H), 7.56-7.48 (m, 1H), 7.29-7.18 (m, 2H), 5.23 (s, 1H), 2.48-2.33 (m, 2H), 2.18-2.05 (m, 1H), 1.97 - 1.80 (m, 4H), 1.01 (s, 3H), 0.95 (s, 3H); LRMS (ESI+): 333 ([M+H]+), retention time 0.58 min.
4-(3,7,7-trimetil-5-oxo-4,5,6,7,8,9-hexahidro-2H-pirazolo[3,4-b]quinolin-4-il)benzonitrilo
1H NMR (300 MHz, DMSO) 811.84 (s, 1H), 9.84 (s, 1H), 7.66 (d, J = 8.2 Hz, 2H), 7.32 (d, J = 8.0 Hz, 2H), 5.05 (s, 1H), 2.44 (d, J = 6.3 Hz, 2H), 2.12 (d, J = 16.7 Hz, 1H), 1.94 (d, J = 16.0 Hz, 1H), 1.87 (s, 3H), 1.00 (s, 3H), 0.92 (s, 3H); LRMS (ESI+): 333 ([M+H]+), retention time 0.54 min.
3,4,7,7-tetrametil-4-fenil-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-5(4H)-ona
1H NMR (300 MHz, DMSO) 8 11.69 (s, 1H), 9.69 (s, 1H), 7.27-7.22 (m, 1H), 7.08-6.92 (m, 3H), 5.44 (s, 1H), 2.48 -2.32 (m, 2H), 2.16-2.04 (m, 1H), 1.95-1.84 (m, 4H), 1.00 (s, 3H), 0.95 (s, 3H).; LRMS (ESI+): 322 ([M+H]+), retention time 0.62 min.
4-(2-metoxifenil)-3-metil-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-5(4H)-ona
LRMS (ESI+): 310 ([M+H]+), retention time 0.51 min.
3,7,7-trimetil-4-(2-(trifluorometil)fenil)-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-5(4H)-ona
LRMS (ESI+): 376 ([M+H]+), retention time 0.64-0.66 min. La mezcla racémica se separó por HPLC quiral para proporcionar compuesto 28 y compuesto 29.
3,7,7-trimetil-4-(3-(trifluorometil)fenil)-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-5(4H)-ona
LRMS (ESI+): 376 ([M+H]+), retention time 0.66 min.
4-(2-metoxifenil)-7,7-dimetil-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-5(4H)-ona
LRMS (ESI+): 324 ([M+H]+), retention time 0.57 min.
3-isopropil-4-(2-metoxifenil)-7,7-dimetil-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-5(4H)-ona
LRMS (ESI+): 366 ([M+H]+), retention time 0.63 min.
4-(2-metoxifenil)-7,7-dimetil-3-fenil-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-5(4H)-ona
LRMS (ESI+): 400 ([M+H]+), retention time 0.67 min.
3-(terc-butil)-4-(2-metoxifenil)-7,7-dimetil-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-5(4H)-ona
LRMS (ESI+): 380 ([M+H]+), retention time 0.65 min.
3-etil-4-(2-metoxifenil)-7,7-dimetil-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-5(4H)-ona
LRMS (ESI+): 352 ([M+H]+), retention time 0.62 min.
3,7,7-trimetil-4-(2-(metiltio)fenil)-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-5(4H)-ona
LRMS (ESI+): 354 ([M+H]+), retention time 0.62 min.
4-(benzo[c][1,2,5]oxadiazol-4-il)-3,7,7-trimetil-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-5(4H)-ona
LRMS (ESI+): 350 ([M+H]+), retention time 0.54 min.
4'-(2-metoxifenM)-3'-metM-4',6',8',9'-tetrahidroespiro[cidohexano-1,7'-pirazolo[3,4-b]qumoMn]-5'(2'H)-ona
1H NMR (300 MHz, d6-DMSO) 9.57 (s, 1H), 7.06 -6.97 (m, 1H), 6.94 -6.83 (m, 2H), 6.78 -6.69 (m, 1H), 5.27 (s, 1H), 3.78 (s, 3H), 2.62 - 2.40 (m, 4H), 2.07 (s, 2H), 1.88 (s, 3H), 1.50-1.26 (m, 10H). LRMS (ESI+) ([M+H]+): 378, retention time 0.67 min.
4-(2-fluorofeml)-7,7-dimetN-3-(tnfluorometM)-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]qumolm-5(4H)-ona
1H NMR (300 MHz, d6-DMSO) 810.32 (s, 1H), 6.96 - 6.83 (m, 1H), 6.79 - 6.70 (m, 1H), 6.70 - 6.57 (m, 2H), 5.29 (s, 1H), 2.48 - 2.32 (m, 2H), 2.28 - 2.12 (m, 1H), 2.09 - 1.94 (m, 1H), 1.01 (s, 3H), 0.87 (s, 3H). LRMS (ESI+) ([M]+): 379, retention time 0.59 min.
4-(5-fluoro-2-(trifluorometN)feml)-7,7-dimetN-3-(tnfluorometM)-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]qumolm-5(4w)-ona
1H RMN (300 MHz, d6-DMSO) 810,29 (s, 1H), 7,66 - 7,61 (m, 1H), 7,22 - 7,09 (m, 1H), 6,93 - 6,86 (m, 1H), 5,68 (s, 1H), 2,51 - 2,40 (m, 2H), 2,19 - 2,09 (m, 1H), 2,01 - 1,91 (m, 1H), 1,01 (s, 3H), 0,89 (s, 3H). LRMS (ESI+) ([M+H]+): 448, retention time 0.55 min.
4-(3-fluoro-2-(trifluorometN)feml)-7,7-dimetN-3-(tnfluorometM)-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]qumolm-5(4H)-ona
1H NMR (300 MHz, d6-DMSO) 810.28 (s, 1H), 7.53 - 7.42 (m, 1H), 7.21 - 7.11 (m, 1H), 6.99 - 6.92 (m, 1H), 5.78 (s, 1H), 2.49 - 2.30 (m, 2H), 2.19 - 2.10 (m, 1H), 2.0 - 1.87 (m, 1H), 1.01 (s, 3H), 0.85 (s, 3H). LRMS (ESI+) ([M+H]+): 448, retention time 0.66 min.
4-(5-fluoro-2-(trifluorometoxi)fenil)-7,7-dimetil-3-(trifluorometil)-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-5(4H)-ona
1H NMR (300 MHz, d6-DMSO) 810.30 (s, 1H), 7.25 - 7.14 (m, 1H), 7.14 - 7.02 (m, 2H), 5.31 (s, 1H), 2.48 -2.34 (m, 2H), 2.18 - 2.07 (m, 1H), 2.01 - 1.92 (m, 1H), 1.01 (s, 3H), 0.92 (s, 3H). LRMS (ESI+) ([M+H]+): 464, retention time 0.58 min.
4-(2,5-difluorofenil)-7,7-dimetil-3-(trifluorometil)-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-5(4H)-ona 1
1H NMR (300 MHz, d6-DMSO) 810.35 (s, 1H), 6.81 - 6.69 (m, 2H), 6.69 - 6.60 (m, 2H), 6.55 - 6.43 (m, 2H), 5.25 (s, 2H), 2.48 - 2.34 (m, 2H), 2.25 - 2.13 (m, 1H), 2.08 - 1.96 (m, 1H), 1.01 (s, 3H), 0.89 (s, 3H). LRMS (ESI+) ([M]+): 397, retention time 0.48 min.
4-(2-fluorofenil)-4,7,7-trimetil-3-(trifluorometil)-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-5(4H)-ona
1H NMR (300 MHz, d4-MeOD) 87.63 - 7.52 (m, 1H), 7.17 - 7.01 (m, 2H), 6.88 - 6.74 (m, 1H), 2.46 (q, J = 16.5 Hz, 2H), 2.18 -2.01 (m, 2H), 1.99 (s, 3H), 1.07 (s, 3H), 1.01 (s, 3H). LRMS (ESI+) ([M+H]+): 394, retention time 0.67 min.
7,7-dimetN-3-(trifluorometM)-4-(2-(trifluorometN)feml)-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]qumolm-5(4H)-ona
1H NMR (300 MHz, d6-DMSO) 810.22 (s, 1H), 7.52 - 7.40 (m, 2H), 7.31 - 7.22 (m, 1H), 7.20 - 7.13 (m, 1H), 5.69 (s, 1H), 2.60 - 2.34 (m, 2H), 2.21 - 2.05 (m, 1H), 1.96 - 1.86 (m, 1H), 1.01 (s, 3H), 0.86 (s, 3H). LRMS (ESI+) ([M+H]+): 430, retention time 0.66 min. La mezcla racémica se separó por HPLC quiral para proporcionar compuesto 72 y compuesto 73.
4-(4-fluoro-2-(trifluorometN)feml)-7,7-dimetN-3-(tnfluorometM)-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]qumolm-5(4H)-ona
1H NMR (300 MHz, d6-DMSO) 810.28 (s, 1H), 7.41 - 7.30 (m, 2H), 7.25 - 7.15 (m, 1H), 5.66 (s, 1H), 2.59 -2.35 (m, 2H), 2.19 - 2.08 (m, 1H), 1.98 - 1.88 (m, 1H), 1.01 (s, 3H), 0.87 (s, 3H). LRMS (ESI+) ([M+H]+): 448, retention time 0.56 min.
4-(2,6-difluorofenil)-7,7-dimetil-3-(trifluorometil)-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-5(4H)-ona
1H NMR (300 MHz, d6-DMSO) 810.08 (s, 1H), 6.97 - 6.81 (m, 1H), 6.55 - 6.34 (m, 2H), 5.50 (s, 1H), 2.51 -2.41 (m, 1H), 2.39 - 2.24 (m, 1H), 2.12 - 2.08 (m, 1H), 2.03 - 1.88 (m, 1H), 1.01 (s, 3H), 0.91 (s, 3H). LRMS (ESI+): 397 ([M]+), retention time 0.50 min.
7,7-dimetil-4-(3-(trifluorometoxi)fenil)-3-(trifluorometil)-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-5(4H)-ona
1H NMR (300 MHz, MeOD) 87.31 - 7.23 (m, 1H), 7.18 - 7.12 (m, 1H), 7.08 - 6.96 (m, 2H), 5.24 (s, 1H), 2.63 - 2.42 (m, 2H), 2.32 -2.22 (m, 1H), 2.15 -2.03 (m, 1H), 1.09 (s, 3H), 0.95 (s, 3H). LRMS (ESI+) ([M+H]+): 446.
7,7-dimetil-3-(trifluorometil)-4-(4-(trifluorometil)piridin-3-il)-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-5(4H)-ona
LRMS (ESI+) ([M+H]+): 431.
3-bromo-7,7-dimetil-4-fenil-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-5(4H)-ona
1H NMR (400 MHz, d6-DMSO): 812.72 (s, 1H), 9.89 (s, 1H), 7.20-7.04 (m, 5H), 4.85 (s, 1H), 2.50-2.30 (m, 2H), 2.13 (d, J = 16.4 Hz, 1H), 1.96 (d, J = 16.0 Hz, 1H), 1.00 (s, 3H), 0.926 (s, 3H). ESI+ LCMS: m/z 372 ([M+H]+).
7,7-dietil-3-metil-4-fenil-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-5(4H)-ona 1
1H NMR (500 MHz, CD3OD): 87.18-7.15 (m, 4H), 7.06-7.04 (m, 1H), 5.00 (s, 1H), 2.58-2.47 (m, 2H), 2.22-2.11 (m, 2H), 1.93 (s, 3H), 1.46-1.37 (m, 4H), 0.85 (t, J = 7Hz, 3H), 0.78 (t, J = 7.5Hz, 3H). ESI+ LCMS: m/z 336 ([M+H]+). 7,7-dimetil-4-(piridin-3-il)-3-(trifluorometil)-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-5(4H)-ona
1H NMR (400 MHz, d6-DMSO): 8 13.63 (bs, 0.5H), 13.32 (bs, 0.5H), 10.27-10.20 (m, 1H), 8.31 (d, J= 22.0 Hz, 2H), 7.43-7.41 (m, 1H), 7.24-7.21 (m, 1H), 5.12-5.09 (m, 1H), 2.50-2.30 (m, 2H), 2.16 (d, J = 16.4 Hz, 1H), 1.97 (d, J = 16.4 Hz, 1H), 1.00 (s, 3H), 0.86 (s, 3H). ESI+ LCMS: m/z 363 ([M+H]+).
3'-metil-4'-fenil-4',6',8',9'-tetrahidroespiro[ciclopropano-1,7'-pirazolo[3,4-b]quinolin]-5'(2'H)-ona
1H NMR (500 MHz, d6-DMSO): 811.71 (bs, 1H), 9.68-9.66 (m, 1H), 7.20-7.16 (m, 4H), 7.04 (t, J = 7 Hz, 1H), 4.98 (s, 1H), 2.59 (d, J = 17 Hz, 1H), 2.35-2.25 (m, 2H), 1.93(s, 3H), 1.87 (d, J = 16.5 Hz, 1H), 0.41-0.27 (m, 4H). ESI+ LCMS: m/z 306 ([M+H]+).
3'-metM-4'-feml-4',6',8',9'-tetrahidroespiro[cidobutano-1,7'-pirazolo[3,4-b]qumoMn]-5'(2'H)-ona
1H NMR (500 MHz, d6-DMSO): 811.68 (s, 1H), 9.68 (s, 1H), 7.16-6.99 (m, 5H), 4.90 (s, 1H), 2.71-2.59 (m, 2H), 2.30 2.25 (m, 2H), 1.90 (s, 3H), 1.85-1.72 (m, 5H), 1.62-1.57 (m, 1H). ESI+ LCMS: m/z 320 ([M+H]+).
3'-metM-4'-feml-4',6',8',9'-tetrahidroespiro[cidopentano-1,7'-pirazolo[3,4-b]qumoMn]-5'(2'H)-ona
1H NMR (500 MHz, d6-DMSO): 811.69 (s, 1H), 9.64 (s, 1H), 7.19-7.10 (m, 4H), 7.03 (t, J = 7 Hz, 1H), 4.91 (s, 1H), 2.65-2.50 (m, 2H), 2.21 (d, J = 16 Hz, 1H), 2.06 (d, J = 16 Hz, 1H), 1.90 (s, 3H), 1.62-1.51 (m, 4H), 1.49-1.37 (m, 3H), 1.30-1.26 (m, 1H). ESI+ LCMS: m/z 334 ([M+H]+) .
4-(2-bromofenil)-3,7,7-trimetil-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-5(4H)-ona
1H NMR (300 MHz, DMSO) 811.78 (s, 1H), 9.77 (s, 1H), 7.44 (d, J = 6.95 Hz, 1H), 7.19 (t, J = 6.95 Hz, 1H), 7.10 -6.92 (m, 2H), 5.31 (s, 1H), 2.56 - 2.35 (m, 2H), 2.15 - 2.05 (m, 1H), 1.95 - 1.84 (m, 4H), 1.01 (s, 3H), 0.95 (s, 3H). LRMS (ESI+) ([M+H]+): 388. La mezcla racémica se separó por HPLC quiral para proporcionar compuesto 80 y compuesto 81.
3,7,7-trimetil-4-fenil-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-5(4H)-ona
LRMS (ESI+): 308 ([M+H]+). La mezcla racémica se separó por HPLC quiral para proporcionar compuesto 3 y compuesto 2.
Los compuestos descritos en la presente memoria también pueden prepararse de acuerdo con los protocolos de síntesis C a F como se muestra en el esquema 1c.
Esquema 1c. Protocolos de síntesis C a F.
En el protocolo de síntesis C (esquema 1c), la cetona (1,0 equivalente) y la amina (1,0 equivalente) se disolvieron en
tolueno (0,1-0,5 M). Se añadió ácido p-toluenosulfónico (0,1 equivalente), y la mezcla se calentó a 110 °C. La mezcla de reacción se enfrió y el tolueno se evaporó. La mezcla de reacción en bruto se purificó por cromatografía en columna sobre sílice para producir intermedio I1. El intermedio I1 resultante (1,0 equivalente) entonces se disolvió en tolueno, y se añadieron la 1,3-dicetona (1,0 equivalente) seguida de ácido p-toluenosulfónico (0,1 equivalente). La mezcla se calentó a 110 °C durante 30-60 minutos para producir el intermedio I2 sin ciclar cuantitativamente. El tolueno se evaporó para retirar el agua generada en la reacción de formación de enamina. Se añadió tolueno fresco y la mezcla se calentó a 110 °C. Después de la conversión completa del intermedio 12 sin ciclar, el tolueno se evaporó, y la mezcla en bruto se purificó por cromatografía en columna sobre sílice para producir el producto ciclado.
En el protocolo de síntesis D, el intermedio I2 sin ciclar se disolvió en tolueno y se añadió ácido trifluoroacético (1,0 equivalente). La mezcla se calentó a 150 °C en un reactor de microondas. Después de la conversión completa del intermedio sin ciclar, los volátiles se evaporaron, y la mezcla en bruto se purificó por cromatografía en columna sobre sílice para producir el producto ciclado.
En el protocolo de síntesis E, el intermedio I2 sin ciclar se disolvió en ácido trifluoroacético (0,5 M), y la mezcla se calentó a 73 °C. Después de la conversión completa del intermedio sin ciclar, los volátiles se evaporaron, y la mezcla en bruto se purificó por cromatografía en columna sobre sílice para producir el producto ciclado.
En el protocolo de síntesis F, el intermedio I2 sin ciclar se disolvió en ácido trifluoroacético (0,5 M), y la mezcla se calentó a 140 °C en un reactor de microondas. Después de la conversión completa del intermedio sin ciclar, los volátiles se evaporaron, y la mezcla en bruto se purificó por cromatografía en columna sobre sílice para producir el producto ciclado.
Los compuestos descritos en la presente memoria también pueden prepararse de acuerdo con el protocolo de síntesis G mostrado en el esquema 1d, donde R3 es -CF3 , isopropilo o un grupo más grande que -CF3 o isopropilo.
Esquema 1d. Protocolo de síntesis G.
A una disolución agitada de 5-trifluorometil-1H-pirazol-3-amina (compuesto G1) (2 g, 1,0 equiv.) en dioxano (30 ml) se le añadió anhídrido ftálico (2,15 g, 1,1 equiv.) en atmósfera de nitrógeno a temperatura ambiente. La mezcla de reacción se calentó a reflujo durante 24 h. Los volátiles se evaporaron a presión reducida para producir un residuo en bruto (compuesto G2). El compuesto en bruto G2 se usó en la siguiente etapa tal cual sin purificación adicional (rendimiento en bruto: 3 g, 81 % de rendimiento).
A una disolución agitada de compuesto G2 en bruto (3 g, 1,0 equiv.) en ACN (acetonitrilo, 50 ml) se le añadió N-yodosuccinimida (NIS, 5,04 g, 2 equiv.) en atmósfera de nitrógeno a temperatura ambiente. La mezcla de reacción se calentó a reflujo durante 16 h, y la mezcla de reacción se inactivó con una disolución saturada acuosa de sulfito de sodio y se extrajo con EtOAc. La capa orgánica se separó, se lavó con agua y salmuera, se secó sobre Na2SO4, se filtró y se concentró a presión reducida para dar compuesto G3 en bruto. El compuesto en bruto G3 se usó en la siguiente etapa tal cual sin purificación adicional (rendimiento en bruto: 3 g, 69 % de rendimiento).
A una disolución agitada de compuesto G3 en bruto (2 g, 1,0 equiv.) en tolueno (20 ml) se le añadieron éter etilvinílico (0,92 ml, 2 equiv.) y una cantidad catalítica de HCl concentrado (5 gotas) en atmósfera de nitrógeno a temperatura ambiente. La mezcla de reacción se agitó a 50 °C durante 30 min. Después de completarse la reacción, la mezcla de reacción se inactivó con disolución saturada acuosa de NaHCO3 y se extrajo con EtOAc. La capa orgánica se separó, se lavó con agua y salmuera, se secó sobre Na2SO4 , se filtró y se concentró a presión reducida para dar compuesto G4 en bruto. El compuesto G4 en bruto se purificó por cromatografía en columna sobre gel de sílice eluyendo con un 30 % de EtOAc en hexanos para producir compuesto G4 puro: 1,88 g, 80 % de rendimiento.
Una mezcla de compuesto G4 (500 mg, 1 equiv.), el ácido borónico que se muestra en el Esquema Id (230 mg, 1,5 equiv.), Pd(PPh3)4 (120 mg, 0,1 equiv.) y K2CO3 (288 mg, 2 equiv.) en una mezcla de disolvente [tolueno (3 ml), agua
(3 ml) y etanol (1 ml)] se desgasificó con argón y se calentó a 100 °C en un reactor de microondas durante 1 h. Después de completarse, la reacción se diluyó con agua y el producto se extrajo con EtOAc. La capa orgánica se separó, se lavó con agua y salmuera, se secó sobre Na2SO4 y se concentró a presión reducida para dar compuesto G5 en bruto. El compuesto G5 en bruto se purificó por cromatografía en columna eluyendo con un 20 % de EtOAc en hexanos para producir una mezcla de compuestos que contiene compuesto G5. Un análisis de CLEM de la mezcla aislada mostró un 56 % de la masa deseada de compuesto G5. El compuesto G5 en bruto se usó en la siguiente etapa tal cual sin purificación adicional.
A una disolución agitada de compuesto G5 en bruto (1 g, 1 equiv.) en metanol (20 ml) se le añadió N2H4 ■ H2O (0,5 ml, 2,8 equiv.). La mezcla de reacción se agitó a temperatura ambiente durante 5 h. Después de completarse, la mezcla de reacción se inactivó con agua y el producto se extrajo con EtOAc. La capa orgánica se lavó con agua y salmuera, se secó sobre Na2SO4 , se filtró y se concentró a presión reducida para dar compuesto G6 en bruto. El compuesto G6 en bruto se purificó por cromatografía en columna eluyendo con un 30 % EtOAc en hexanos para producir compuesto G6 puro: 0,6 g, 84 % de rendimiento.
A una disolución agitada de compuesto G6 (600 mg, 1,0 equiv.) en tolueno (20 ml) se le añadieron dimedona (388 mg, 1,5 equiv.), PTSA (ácido p-toluenosulfónico, 702 mg, 2 equiv.) en atmósfera de nitrógeno a temperatura ambiente. La mezcla de reacción se calentó a reflujo durante 2 h. Después de completarse (controlada por CCF), la reacción se interrumpió con una disolución saturada acuosa de NaHCO3 y se extrajo con EtOAc. La capa orgánica se separó, se lavó con agua y salmuera, se secó sobre Na2SO4 anhidro y se concentró a presión reducida para producir un residuo en bruto. El residuo en bruto se purificó por cromatografía en columna sobre gel de sílice eluyendo con un 2 % de MeOH en DCM (diclorometano) para producir una mezcla de compuestos que contiene compuesto G7 (62,8 % de la masa deseada de compuesto G7 y 23 % de una impureza de imina; rendimiento en bruto 240 mg, 34 % de rendimiento). El compuesto G7 en bruto se usó para la siguiente etapa tal cual sin purificación adicional.
A una disolución agitada de compuesto G7 en bruto (240 mg, 1,0 equiv.) en tolueno (10 ml) se le añadió PTSA (486 mg, 4 equiv.) en atmósfera de nitrógeno a temperatura ambiente. La mezcla de reacción se calentó a reflujo durante 12 h. Después de completarse (controlada por CCF), la reacción se interrumpió con disolución saturada acuosa de NaHCO3 y se extrajo con EtOAc. La capa orgánica se lavó con agua y salmuera, se secó sobre Na2SO4 anhidro y se concentró a presión reducida para producir un residuo en bruto. El residuo en bruto se purificó por cromatografía en columna eluyendo con un 2% de MeOH en DCM para producir compuesto final 68 puro: 120 mg (50% de rendimiento). Después de separación quiral, se obtuvieron 40 mg de cada uno de los dos enantiómeros, compuesto 70 y compuesto 71.
9-etil-1,6,6-trimetil-9-fenil-5,6,7,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-8(4H)-ona (89)
7.3Hz, 1H), 2.52 (s, 2H), 2.2-1.9 (m, 4H), 1.63 (s, 3H), 1.10 (s, 3H), 1.05 (s, 3H), 0.75 (t, J = 7.3Hz, 3H) ppm. La mezcla racémica se separó por HPLC quiral para proporcionar compuesto 125 y compuesto 126.
1,6,6-trimetil-9-fenil-9-(trifluorometil)-5,6,7,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-8(4H)-ona (92, 93 y 94)
J = 7.3Hz, 2H), 2.7-2.5 (m, 2H), 2.2-2.0 (m, 2H), 1.47 (s, 3H), 1.09 (s, 3H), 1.08 (s, 3H) ppm. La mezcla racémica se separó por HPLC quiral para proporcionar compuesto 93 y compuesto 94.
3-(1,6,6,9-tetrametil-8-oxo-4,5,6,7,8,9-hexahidro-2H-pirazolo[3,4-b]quinolin-9-il)benzonitrilo (95, 96 y 97)
1H), 7.48 (d, J = 7.5 Hz, 1H), 7.38 (t, J = 8.0 Hz, 1H), 2.42-2.35 (m, 2H), 1.98 (d, J = 30.0Hz, 1H), 1.89 (d, J = 30.0Hz, iH), 1.81 (s, 3H), 1.60 (s, 3H), 0.98 (s, 3H), 0.94 (s, 3H) ppm. La mezcla racémica se separó por HPLC quiral para proporcionar compuesto 96 y compuesto 97.
3-(3,4,7,7-tetrametil-5-oxo-4,5,6,7,8,9-hexahidro-2H-pirazolo[3,4-b]quinolin-4-il)benzamida (90)
LCMS: m/z 365 [M+H]+; 1H NMR (400 MHz, DMSO-d6): 6 11.62 (s, 1H), 9.64 (s, 1H), 7.87 (bs, 1H), 7.83 (bs, 1H), 7.53 (d, J = 7.6Hz, 1H), 7.39 (d, J = 8.4 Hz, 1H), 7.24-7.19 (m, 2H), 2.50-2.40 (m, 2H), 2.04-1.97 (m, 1H), 1.90-1.80 (m, 4H), 1.59 (s, 3H), 0.99 (s, 3H), 0.96 (s, 3H) ppm.
3',7',7'-trimetil-2,3,6',7',8',9'-hexahidroespiro[indeno-1,4'-pirazolo[3,4-b]quinolin]-5'(2'H)-ona (91)
LCMS: m/z 334 [M+H]+; 1H NMR (300 MHz, MeOD): 67.25-6.95 (m, 3H), 6.85-6.70 (m, 1H), 3.40-3.25 (m, 1H), 3.20 3.00 (m, 1H), 2.70-2.45 (m, 3H), 2.30-2.00 (m, 3H), 1.57 (s, 3H), 1.09 (s, 3H), 1.07 (s, 3H) ppm.
3',7',7'-trimetil-6',7',8',9'-tetrahidro-2H-espiro[benzofuran-3,4'-pirazolo[3,4-b]quinolin]-5'(2'H)-ona (98)
LCMS: m/z 334 [M-H]-; 1H NMR (300 MHz, MeOD): 67.03 (td, J = 7.1Hz, J = 1.6Hz, 1H), 7.80-7-65 (m, 3H), 4.81 (d, J = 8.2Hz, 1H), 4.36 (d, J = 8.2Hz, 1H), 2.65-2.45 (m, 2H), 2.25-2.05 (m, 2H), 1.71 (s, 3H), 1.09 (s, 6H) ppm.
3',7',7'-trimetil-3,4,6',7',8',9'-hexahidro-2H-espiro[naftaleno-1,4'-pirazolo[3,4-b]quinolin]-5'(2'H)-ona (99)
LCMS: m/z 346 [M-H]-; 1H NMR (300 MHz, MeOD): 67.0-6.9 (m, 4H), 3.1-2.9 (m, 1H), 2.85-2.75 (m, 1H), 2.6-2.4 (m, 2H), 2.3-2.0 (m, 4H), 1.90-1.80 (m, 2H), 1.48 (s, 3H), 1,10 (s, 3H), 1.08 (s, 3H) ppm.
Compuesto 100
LCMS: m/z 288 [M+H]+; 'H NMR (400 MHz, d6-DMSO): 6 11.61 (s, 1H), 9.24 (s, 1H), 2.55-2.50 (m, 2H), 2.31 (bs, 3H), 2.12-2.05 (m, 5H), 1.38-1.28 (m, 2H), 1.00 (s, 6H), 0.54 (t, J = 7.2Hz, 5H) ppm.
Compuesto 101
LCMS: m/z 316 [M+H]+; 1H NMR (300 MHz, CD3OD): 6 2.65-2.50 (m, 2H), 2.41-2.35 (m, 2H), 2.24-2.10 (m, 5H), 1.47-1.20 (m, 5H), 1.12-0.95 (m, 7H), 0.84-0.72 (m, 6H) ppm.
Compuesto 102
LCMS: m/z 286 [M+H]+; 'H NMR (400 MHz, d6-DMSO): 6 11.66 (s, 1H), 9.43 (s, 1H), 2.32-2.28 (m, 2H), 2.18-2.12 (m, 5H), 2.10-2.06 (m, 2H), 2.04-1.94 (m, 2H), 1.79 (d, J = 5.0 Hz, 2H), 1.64-1.54 (m, 2H), 0.98 (s, 6H) ppm.
Compuesto 103
LCMS: m/z 299 [M]+; 'H NMR (CD3OD, 300 MHz): 62.60-2.40 (m, 5H), 2.25-1.55 (m, 12H), 1.10-1.00 (m, 6H) ppm. Compuesto 104
ESI+ MS: m/z 366 [M+H]+.
Compuesto 105
ESI+ LCMS: m/z 319 (M+H); 1H NMR (400 MHz, da-DMSO): 813.62 (bs, 1H), 10.17 (s, 1H), 7.25-7.20 (m, 2H), 7.15 7.08 (m, 3H), 5.12 (s, 1H), 2.47-2.40 (m, 2H), 2.15 (d, J = 16.0 Hz, 1H), 2.00 (d, J = 16.0 Hz, 1H), 1.02 (s, 3H), 0.97 (s, 3H) ppm.
Compuestos 107, 108 y 109
J = 7.6Hz, 2H), 7.08 (s, 1H), 6.99 (t, J = 7.2 Hz, 1H), 2.44 (s, 2H), 2.05 (d, J = 15.6Hz, 1H), 1.97-1.95 (m, 1H), 1.92 (s, 3H), 1.01 (s, 3H), 0.99 (s, 3H) ppm. La mezcla racémica se separó por HPLC quiral para proporcionar compuesto 108 y compuesto 109.
Compuesto 106
LCMS: m/z 326 [M+H]+; 1H NMR (300 MHz, CD3OD): 87.36-7.25 (m, 2H), 7.25-7.13 (m, 2H), 7.12-7.00 (m, 1H), 2.50 (bs, 2H), 2.25-1.90 (m, 5H), 1.09 (s, 3H), 1.06 (s, 3H) ppm.
Compuesto 110
ESI+ MS: m/z 341 [M]+.
Compuesto 111
LCMS:m/z 386 [M]+ :1H NMR (400 MHz,DMSO-da): 812.57 (s, 1H), 9.80 (s, 1H), 7.26 (d, J = 7.6Hz, 2H), 7.16 (t, J = 7.6 Hz, 2H), 7.00 (t, J = 7.2 Hz, 1H), 2.45-2.35 (m, 2H),2.05-2.00 (m, 1H), 1.94 (s, 3H), 1.90-1.85 (m, 1H), 0.99 (s, 3H), 0.95 (s, 3H) ppm.
Compuestos 113, 114 y 115
(m, 1H), 2.52-2.48 (m, 2H), 2.25-2.00 (m, 2H), 2.01 (s, 3H), 1.25-1.00 (m, 1H), 1.08 (s, 3H), 1.08 (s, 3H), 1.04 (s, 3H), 0.80-0.73 (m, 1H), 0.60-0.46 (m, 1H), 0.46-0.26 (m, 1H), 0.26-0.15 (m, 1H) ppm. La mezcla racémica se separó por HPLC quiral para proporcionar compuesto 114 y compuesto 115.
Compuesto 112
ESI+ MS: m/z 402 [M+H]+.
Compuesto 116
ESI+ MS: m/z 366 ([M+H]+); 1H NMR (400 MHz, DMSO-d6): 8 11.37 (s, 1H), 9.59 (s, 1H), 7.57-7.51 (m, 1H), 7.11 7.03 (m, 2H), 6.89-6.83 (m, 1H), 2.42 (d, J = 16.0 Hz, 1H), 2.30 (d, J = 16.0Hz, 1H), 2.02 (d, J = 16.0 Hz, 1H) 1.92 (s, 3H), 1.85 (d, J = 16.0 Hz, 1H), 1.13-1.05 (m, 1H), 0.99 (s, 3H), 0.93 (s, 3H), 0.70-0.65 (m, 1H), 0.51-0.46 (m, 1H), 0.33-0.21 (m, 2H) ppm.
Compuestos 118, 130 y 131
CLEM: m/z 416 [M+H]+. La mezcla racémica se separó por HPLC quiral para proporcionar compuesto 130 y compuesto 131.
Compuestos 117, 132 y 133
(d, J = 8 Hz, 1H), 7.50 (d, J = 7.6Hz, 1H), 7.38 (t, J = 7.6 Hz, 1H), 2.45 (s, 2H), 2.00 (d, J = 15.6Hz, 1H), 1.93-1.88 (m, 1H), 1.93 (s, 3H), 1.18-1.10 (m, 1H), 0.99 (s, 3H), 0.95 (s, 3H), 0.75-0.68 (m, 1H), 0.60-0.52 (m, 1H), 0.37-0.28 (m, 1H), 0.15-0.08 (m, 1H) ppm. La mezcla racémica se separó por HPLC quiral para proporcionar compuesto 132 y compuesto 133.
Compuesto 119
CLEM: m/z 361 [M]+.
Compuesto 120, 127 y 128
Hz, 1H), 2.90-2.60 (m, 3H), 2.49 (s, 2H), 2.20-1.75 (m, 3H), 1.90 (s, 3H), 1.80-1.60 (m, 1H), 1.07 (s, 3H), 1.03 (s, 3H) ppm. La mezcla racémica se separó por HPLC quiral para proporcionar compuesto 127 y compuesto 128.
4,7,7-trimetil-3,4-difenil-6,7,8,9-tetrahidro-2H-pirazolo[3,4-b]quinolin-5(4H)-ona (121)
LCMS: m/z 384 [M+H]+, 1H NMR (300 MHz, CDCla): 87.40-7.25 (m, 3H), 7.26-7.02 (m, 5H), 6.59 (d, J = 9.0 Hz, 2H), 2.40-2.25 (m, 2H), 2.25-2.00 (m, 2H), 1.81 (s, 3H), 1.06 (s, 3H), 0.99 (s, 3H) ppm.
Compuesto 122
LCMS: m/z 321 [M]+ ; 1H NMR (300 MHz,DMSO-da): 811.58 (s, 1H), 9.39 (s, 1H), 7.22-7.10 (m, 3H), 6.88 (d, J = 6.0 Hz, 2H), 4.08 (dd, J = 3.0, 9.0 Hz, 1H), 2.80-2.60 (m, 1H), 2.50-2.13 (m, 5H), 1.41 (s, 3H), 0.99 (s, 3H), 0.98 (s, 3H) ppm.
ESI+ MS: m/z 322 ([M+H]+): 1H NMR (500 MHz, d6-DMSO): 8 11.91 (s, 1H), 9.63 (s, 1H), 7.28 (d, J = 7.5 Hz, 2H), 7.15 (t, J = 7.2Hz, 2H), 7.05 (s, 1H), 7.01-6.97 (m, 1H), 2.92-2.88 (m, 1H), 2.50-2.42 (m, 2H), 2.07-1.97 (m, 3H), 1.04 (s, 3H), 1.02 (s, 3H), 0.65 (t, J = 7.5Hz, 3H) ppm.
ESI+ MS: m/z 333 ([M+H]+): 1H NMR (400 MHz,CDaOD): 87.72-7.64 (m, 2H), 7.01 (s, 1H), 2.60-2.50 (m, 1H), 2.16 (d, J = 16.0Hz, 1H), 2.08 (d, J = 16.4 Hz, 1H), 1.98 (s, 3H), 1.10 (s, 3H), 1.07 (s, 3H) ppm.
ESI+ MS: m/z 376 ([M+H]+); 1H NMR (500 MHz, d6-DMSO): 812.01 (s, 1H), 9.81 (s, 1H), 7.60 (d, J = 8 Hz, 1H), 7.53 (s, 1H), 7.45-7.36 (m, 2H), 7.17 (s, 1H), 2.50-2.40 (m, 2H), 2.08(d, J = 15.5 Hz, 1H), 1.93 (s, 3H), 1.94-1.90 (m, 1H), 1.01 (s, 3H), 0.97 (s, 3H) ppm.
ESI+ MS: m/z 382 ([M+H]+); 1H NMR (400 MHz, d6-DMSO): 811.32 (s, 1H), 9.66 (s, 1H), 7.75 (dd, J = 1.2Hz, 7.6Hz, 1H), 7.27-7.21 (m, 1H), 7.17-7.13 (m, 1H), 7.11-7.05 (m, 1H), 2.42-2.26 (m, 2H), 2.01-1.84 (m, 5H), 0.99 (s, 3H), 0.98 (s, 3H), 0.95-0.87(m, 1H), 0.64-0.55 (m, 1H), 0.53-0.45 (m, 1H), 0.25-0.14 (m, 2H) ppm.
Otros compuestos. Cualquier otro compuesto descrito en la presente memoria puede prepararse de una manera similar a los métodos descritos anteriormente. Pueden analizarse por UPLC como se describe a continuación.
Método de UPLC del tiempo de retención
La pureza e identidad del compuesto se determinaron por UPLC-EM (Waters, Milford, MA). La pureza se midió por absorbancia UV a 210 nm. La identidad se determinó en un espectrómetro de masas SQ por ionización por electronebulización positiva y negativa. La fase móvil A consistía en hidróxido de amonio al 0,1 % o ácido trifluoroacético al 0,1 % en agua, mientras que la fase móvil B consistía en los mismos aditivos en acetonitrilo. El gradiente discurrió de un 5 % a un 95 % de fase móvil B durante 0,8 minutos a 0,45 ml/min. Se usó una columna Acquity BEH C18, 1,7 um, 1 ,0x50 mm con la temperatura de la columna mantenida a 65 °C. Los compuestos se disolvieron en DMSO a una concentración nominal de 1 mg/ml, y se inyectaron 0,25 pl de esta disolución.
Ensayos analíticos adicionales
Solubilidad. La solubilidad se determinó en disolución salina tamponada con fosfato (PBS) pH 7,4 con DMSO al 1 %. Cada compuesto se preparó por duplicado a 100 pM tanto en Dm SO al 100 % como en PBs con DMSO al 1 %. Se dejó que los compuestos se equilibraran a temperatura ambiente con una agitación orbital a 250 rpm durante 24 horas. Después del equilibrado, las muestras se analizaron por UPLC-EM (Waters, Milford, MA) con los compuestos detectados por detección de SIR en un espectrómetro de masas de cuadrupolo único. Las muestras de DMSO se usaron para crear una curva de calibrado de dos puntos a la que se ajustó la respuesta en PBS. Los resultados se muestran en la tabla 3.
Estabilidad en PBS. La estabilidad se determinó en presencia de PBS pH 7,4 con DMSO al 0,1 %. Cada compuesto se preparó por duplicado en seis placas diferentes y se dejó que se equilibraran a temperatura ambiente con una agitación orbital a 250 rpm durante 48 horas. Se retiró una placa en cada punto temporal (0, 2, 4, 8, 24 y 48 horas). Se retiró una alícuota de cada pocillo y se analizó por UPLC-EM (Waters, Milford, Ma ) con los compuestos detectados por detección de SIR en un espectrómetro de masas de cuadrupolo único. Además, al material restante en cada punto temporal, se le añadió acetonitrilo para forzar la disolución del compuesto (para ensayar la recuperación del compuesto). También se analizó una alícuota de esto por UPLC-EM.
Estabilidad en GSH. La estabilidad se determinó en presencia de PBS pH 7,4 pM y glutatión 50 pM con DMSO al 0,1 %. Cada compuesto se preparó por duplicado en seis placas diferentes y se dejó que se equilibraran a temperatura ambiente con una agitación orbital a 250 rpm durante 48 horas. Se retiró una placa en cada punto temporal (0, 2, 4, 8, 24 y 48 horas). Se retiró una alícuota de cada pocillo y se analizó por UPLC-EM (Waters, Milford, MA) con los compuestos detectados por detección de SIR en un espectrómetro de masas de cuadrupolo único. Además, al material restante en cada punto temporal, se le añadió acetonitrilo para forzar la disolución del compuesto (para ensayar la recuperación del compuesto). También se analizó una alícuota de esto por UPLC-EM.
Unión a proteína plasmática. La unión a proteína plasmática se determinó por diálisis en equilibrio usando el dispositivo de diálisis rápida en equilibrio (RED) (Pierce Biotechnology, Rockford, IL) tanto para plasma humano como para plasma de ratón. Cada compuesto se preparó por duplicado a 5 pM en plasma (acetonitrilo al 0,95%, DMSO al 0,05 %) y se añadió a un lado de la membrana (200 pl) con PBS pH 7,4 añadido al otro lado (350 pl). Los compuestos se incubaron a 37 °C durante 5 horas con una agitación orbital a 250 rpm. Después de la incubación, las muestras se analizaron por UPLC-EM (Waters, Milford, MA) con los compuestos detectados por detección de SIR en un espectrómetro de masas de cuadrupolo único. Los resultados se muestran en la tabla 3.
Estabilidad en plasma. La estabilidad en plasma se determinó a 37 °C a las 5 horas tanto en plasma humano como en plasma de ratón. Cada compuesto se preparó por duplicado a 5 pM en plasma diluido 50/50 (v/v) con PBS pH 7,4 (acetonitrilo al 0,95 %, DMSO al 0,05 %). Los compuestos se incubaron a 37 °C durante 5 horas con una agitación orbital a 250 rpm con puntos temporales tomados a 0 y 5 horas. Las muestras se analizaron por UPLC-EM (Waters, Milford, MA) con los compuestos detectados por detección de SIR en un espectrómetro de masas de cuadrupolo único. Los resultados se muestran en la tabla 3.
HTS primario
El cribado primario de GSK3p se realizó en placas de 1536 pocillos listas para ensayo (Aurora 29847) que contienen 2,5 nl/pocillo de compuesto 10 mM. La GSK3p humana como una fusión con GST expresada en sistema de baculovirus se adquirió de BPS Bioscience (San Diego, CA). El sustrato peptídico de GSK3p fue de American Peptide (Sunnyvale, CA; Cat. 311153). Se añadieron 1 pl/pocillo de CABPE (GSK3p 22,5 nM, péptido 8 pM en tampón Ab (DTT 12,5 mM, 0,25 mg/ml de BSA, 0,5 unidades/ml de heparina)), 0,5 pl/pocillo de ATP 125 pM y 1 pl/pocillo de control positivo, 50 pM de GW8510 (control positivo) o AB (control neutro de únicamente DMSO) en los pocillos respectivos de acuerdo con el diseño de placa usando BioRAPTR (Beckman, Brea, CA). Las reacciones se incubaron a temperatura ambiente durante 60 minutos. Se añadieron 2,5 pl/pocillo de ADP-Glo (Promega, V9103) con BioRAPTR, y se incubaron a temperatura ambiente durante 40 minutos seguido de la adición de 5 pl/pocillo de reactivo de detección ADP-Glo (Promega, V9103) con Combi nL (Thermo, Waltham, MA) e incubación a temperatura ambiente durante 30 minutos. Las placas se leyeron en un ViewLux (PerkinElmer, Waltham, MA) para la luminiscencia. Los datos se cambiaron de escala usando los controles positivo y neutro y se ajustaron para la CI50 como se describe a continuación.
Se distribuyeron 1 pl/pocillo de CABPE, 0,5 pl de ATP y 1 pl de control positivo GW8510 o AB en pocillos respectivos de acuerdo con el diseño de placa a placas listas para ensayo de 1536 pocillos (Aurora 29847) que
contienen 2,5 nl/pocillo de compuesto 10 mM usando BioRAPTR (Beckman) para empezar la reacción. Las placas se incubaron a temperatura ambiente durante 60 minutos. Se añadieron 2,5 pl/pocillo de ADP-Glo (Promega, V9103) con BioRAPTR, y las placas se incubaron a temperatura ambiente durante 40 minutos. Se añadieron 5 pl/pocillo de ADP-Glo (Promega, V9103) con Combi nL (Thermo), y las placas se incubaron a temperatura ambiente durante 30 minutos. Las placas se leyeron en ViewLux (PerkinElmer) para la luminiscencia.
Disoluciones:
AB:
GW8510 (en AB, Sigma G7791)
CABPE (en AB):
Péptido: Tyr-Arg-Arg-Ala-Ala-Val-Pro-Pro-Ser-Pro-Ser-Leu-Ser-Arg-His-Ser-Ser-Pro-His-Gln-Ser(PO3H2)-Glu-Asp-Glu-Glu-Glu (SEQ ID NO: 1)
ATP (en AB, Promega componente V9103):
Ensayo de confirmación
El ensayo de confirmación fue un nuevo ensayo de los compuestos activos en el HTS primario anterior y junto con algunos de sus análogos negativos. El ensayo se realizó de la misma manera que el cribado primario excepto que los compuestos se ensayaron en dosis y con réplicas.
Se distribuyeron 1 pl/pocillo de CABPE, 0,5 pl de ATP y 1 pl de control positivo GW8510 o AB en pocillos respectivos de acuerdo con el diseño de placa a placas listas para ensayo de 1536 pocillos (Aurora 29847) que contienen 2,5 nl/pocillo de compuesto 10 mM usando BioRAPTR (Beckman) para empezar la reacción. Las placas se incubaron a temperatura ambiente durante 60 minutos. Se añadieron 2,5 pl/pocillo de ADP-Glo (Promega, V9103) con BioRAPTR, y las placas se incubaron a temperatura ambiente durante 40 minutos. Se añadieron 5 pl/pocillo de ADP-Glo (Promega, V9103) con Combi nL (Thermo), y las placas se incubaron a temperatura ambiente durante 30 minutos. Las placas se leyeron en ViewLux (PerkinElmer) para la luminiscencia.
Disoluciones:
AB:
GW8510 (en AB, Sigma G7791)
CABPE (en AB):
Péptido: Tyr-Arg-Arg-Ala-Ala-Val-Pro-Pro-Ser-Pro-Ser-Leu-Ser-Arg-His-Ser-Ser-Pro-His-Gln-Ser(PO3H2)-Glu-Asp-Glu-Glu-Glu (SEQ ID NO: 1)
ATP (en AB, Promega componente V9103):
Contracribado de reactivos ADP-Glo
El contracribado de reactivo ADP-Glo es para identificar positivos falsos debido a la inhibición del sistema de detección de ADP-Glo. Se incubaron 2,5 j l de ADP 5 μM directamente con compuestos en dosis a temperatura ambiente durante 60 minutos. Se añadieron 2,5 jl/pocillo de ADP-Glo (Promega, V9103) con BioRAPTR, y se incubaron a temperatura ambiente durante 40 minutos seguido de la adición de 5 jl/pocillo de reactivo de detección ADP-Glo (Promega, V9103) con Combi nL (Thermo, Waltham, MA) e incubación a temperatura ambiente durante 30 minutos. Las placas se leyeron en un ViewLux (PerkinElmer, Waltham, MA) para la luminiscencia. Los datos se cambiaron de escala usando los controles positivo y neutro y se ajustaron para la CI50 como se describe a continuación.
Se distribuyeron 2,5 j l de ADP 5 μM o tampón AB en pocillo en placas listas para ensayo de 1536 pocillos de acuerdo con el diseño de placa (Aurora 29847) generado por transferencia acústica usando Labcyte Echo que contiene 7,5 nl/pocillo de compuesto en dosis. Se añadieron 2,5 jl/pocillo de ADP-Glo (Promega, V9103) con Combi nL (Thermo), y las placas se incubaron a temperatura ambiente durante 40 minutos. Se añadieron 5 jl/pocillo de ADP-Glo (Promega, V9103) con Combi nL (Thermo), y las placas se incubaron a temperatura ambiente durante 35 minutos. Las placas se leyeron en ViewLux (PerkinElmer) para la luminiscencia.
Disoluciones:
AB: TrisCl 25 mM pH 7,5, MgCh 10 mM
ADP: ADP 5 μM (en AB, Promega componente V9103)
Análisis de inhibición de un punto de compuestos seleccionados (Carna Biosciences)
En resumen, se cribó una selección de compuestos frente a un panel de cinasas a una concentración única de 10 μM . Las cinasas se seleccionaron de todas las familias del cinoma y en todas representaban un 60 % del cinoma completo para un total de 311 cinasas cribadas. Esto se completó utilizando uno de dos ensayos dependiendo de la cinasa que se está examinando.
Los compuestos de ensayo se disolvieron en y se diluyeron con dimetilsulfóxido (DMSO) para generar una disolución de muestra 100X. Estos entonces se diluyeron hasta disoluciones de muestra 4X en tampón de ensayo para preparar las disoluciones de compuesto de ensayo finales. Los compuestos de referencia para el control de ensayo se prepararon de forma similar.
Ensayo de IMAP. Una disolución de inhibidor 4X (5 jl), disolución de sustrato/ATP/metal 4X (5 j l ) y disolución de cinasa 2X (10 j l ) se preparó con tampón de ensayo (HEPES 20 mM, Tween-20 al 0,01 %, Dt T 2 mM, pH 7,4) y se mezcló/incubó en placas negras de 384 pocillos durante 1 hora a temperatura ambiente. Se añadió una disolución de reactivo de unión de IMAP (kit IMAP Screening Express; Molecular Devices) (60 j l ) a cada pocillo y se incubó
durante 30 minutos. Entonces se evaluó el nivel de actividad cinasa por polarización de la fluorescencia a 485 nM (exc.) y 530 nM (emi.) de cada pocillo.
Ensayo de desplazamiento de movilidad fuera de chip (MSA). Se preparó una disolución de inhibidor 4X (5 jl), disolución de sustrato ATP-metal 4X (5 j l ) y disolución de cinasa 2X (10 j l ) con tampón de ensayo (HEPES 20 nM, Triton X-100 al 0,01 %, DTT 2 mM, pH 7,5) y se mezclaron/incubaron en placas de 384 pocillos durante 1 o 5 horas dependiendo de la cinasa que se esté examinando, a temperatura ambiente. Se añadió una disolución de tampón de terminación (QuickScout Screening assist MSA; Carna Biosciences) (60 j l ) a cada pocillo. La mezcla de reacción completa entonces se aplicó a un sistema LabChip3000 (Caliper Life Science) y se separaron y cuantificaron los picos de péptido de producto y sustrato. La evaluación de la actividad cinasa entonces se determinó basándose en la relación de las alturas de pico calculadas de péptidos de producto (P) y sustrato (S) (P/(P+S)).
Determinación de la CI50 de respuesta a dosis de compuestos seleccionados contra cinasas seleccionadas
Se cribó una selección de compuestos frente a un panel seleccionado de cinasas basándose en la capacidad inhibidora en un único punto para determinar la actividad inhibidora absoluta, que da lugar a mediciones de selectividad. El ensayo utilizado fue idéntico al de la determinación de actividad inhibidora de un único punto (MSA), pero se procesó en respuesta a dosis. Se preparó una disolución de inhibidor 4X (5 jl), disolución de sustrato/ATP metal 4X (5 j l ) y disolución de cinasa a 2 X (10 j l ) con tampón de ensayo (HEPES 20 nM, Triton X-100 al 0,01 %, DTT 2 mM, pH 7,5) y se mezclaron/incubaron en placas de 384 pocillos durante 1 o 5 horas dependiendo de la cinasa, a temperatura ambiente. Se añadió una disolución de tampón de terminación (QuickScout Screening assist MSA; Carna Biosciences) (60 j l ) a cada pocillo. La mezcla de reacción completa entonces se aplicó a un sistema LabChip3000 (Caliper Life Science) y se separaron y cuantificaron los picos de péptido de producto y sustrato. La evaluación de la actividad cinasa entonces se determinó basándose en la relación de las alturas de pico calculadas de péptidos de producto (P) y sustrato (S) (P/(P+S)).
Ensayo de fosforilación de Tau y de Tau total
Células SH-SY5Y se mantuvieron en DMEN complementado con FBS inactivado por calor al 10% y penicilina-estreptomicina al 1 % (Invitrogen) salvo que se indique de otro modo. Se adquirieron kits de ELISA para la detección de fosfo-Tau (Ser199) y Tau total de Invitrogen (KHB0041 y KHB7041, respectivamente). En resumen, se sembraron células SH-SY5Y a 50000 células/200 jl/pocillo en placas de 96 pocillos y después de incubación durante una noche, se trataron con diversas dosis de compuestos químicos a 0,2 jl/pocillo. El siguiente día, las células se lavaron con PBS dos veces antes de lisarse en 100 j l de tampón de lisis/pocillo. Se transfirieron 50 j l de lisado celular de cada muestra a un vial de ELISA recubierto con el anticuerpo de captura, y la mezcla se incubó a temperatura ambiente durante 2 horas, antes de que aspirara el sobrenadante, y cada vial se lavó cuatro veces. Entonces se añadieron 100 j l de anticuerpo de detección a cada pocillo, se incubaron durante 1 hora y después se lavaron cuatro veces. La cantidad fosfo-Tau y Tau total se midió añadiendo 100 j l de disolución de trabajo anti-IgG de conejo con peroxidasa de rábano rusticano a cada pocillo, y se leyó la absorbancia de cada pocillo a 450 nM en EnVision (PerkinElmer, Valtham, MA). Los datos se cambiaron de escala usando los controles positivos y neutros y se ajustaron para la CI50.
Se empleó un protocolo convencional usando un kit de inmunoensayo para cuantificar la proteína Tau total y la proteína fosfo-Tau (Ser199) en células de neuroblastoma humano SH-SY5Y. El kit de ELISA de Tau humana (total) (n.° KHB0041) y el kit de e L iSA de fosfo-Tau humana (Ser199) se adquirieron de Invitrogen (n.° KHB7041).
Se sembraron 50000 células en 200 j l por pocillo en medio de cultivo celular (250000 células/ml). Las células se incubaron durante una noche a 37 °C. Las células se indujeron con dosis apropiadas de inhibidores y se incubaron durante aproximadamente 24 h a 37 °C. Los lisados celulares se recogieron lavando las células una vez con PBS frio y añadiendo 100 j l de tampón de lisis frio y pipeteando arriba y abajo vigorosamente. El lisado se transfirió a una placa de PCR de 96 pocillos y se centrifugó a 4000 r.p.m. durante 20 minutos a 4 °C.
El patrón de Tau humana (total) se reconstituyó con 1300 j l de tampón diluyente de patrón. Se hicieron diluciones en serie del patrón de acuerdo con la siguiente tabla:
El patrón de pTau humana (Ser199) se reconstituyó con 1730 |jl de tampón diluyente de patrón, se mezcló suavemente y se permitió que reposara durante 10 minutos. Se hicieron diluciones en serie del patrón de acuerdo con la siguiente tabla:
Se diluyó anticuerpo anti-IgG de conejo con HRP tanto para Tau human (total) como para pTau humana (Ser199) permitiendo que alcanzara temperatura ambiente, después se usa la siguiente tabla:
Se diluyó tampón de lavado a partir de concentrado 25X de acuerdo con lo siguiente: Cantidad de tampón de lavado = (x)*(8)*(400)*(4)*(3), donde x = número de tiras de placa de ELISA
Se diluyeron 24 volúmenes con agua desionizada (es decir, 5 ml de concentrado en 120 ml de agua).
Las tiras de pocillos se calentaron y se insertaron en la estructura. Se cargaron 100 j de tampón diluyente de patrón en células ZERO, y se cargaron 100 ul de cada concentración de patrón (tanto Tau total como pTau) en pocillos por duplicado. Las muestras se cargaron a cada pocillo que se analizaría para Tau total, se añadieron 85 j l de tampón diluyente de patrón y 15 j l de lisado celular. A cada pocillo que se analizará para pTau (Ser199), se añadieron 50 j l de tampón diluyente de patrón 50 j l de lisado celular. Las placas se golpearon suavemente en el lateral para mezclarlas. Determinados pocillos se dejaron vacíos para el blanco de cromógeno. Las placas se cubrieron y se incubaron durante 2 horas a temperatura ambiente. Los pocillos se aspiraron 4 veces (400 j l de tampón de lavado diluido, dejado durante 30 segundos, aspirando todos los pocillos; como alternativa se usó un lavador de placas automatizado y se programó en un mantenimiento de 30 segundos entre cada ciclo). Se añadieron 100 j l de disolución de anticuerpo de detección a cada pocillo excepto los blancos de cromógeno. Se añadió anticuerpo anti-Tau total a los pocillos que se están analizando para Tau total, se añadió anticuerpo anti-pTau (Ser199) a los pocillos que se están analizando para pTau (Ser199) y las placas se golpearon suavemente en el lateral para mezclarlas. Las placas se cubrieron y se incubaron durante 1 hora a temperatura ambiente, después los pocillos se aspiraron y se lavaron 4 veces como se describe anteriormente. Se añadieron 100 j l de disolución de trabajo anti-IgG de conejo con HRP (preparada de antemano) a cada pocillo excepto los blancos de cromógeno, y las placas se cubrieron y se incubaron durante 30 minutos a temperatura ambiente, después los pocillos se aspiraron y
se lavaron 4 veces como se describe anteriormente. Se añadieron 100 |jl de cromógeno estabilizado a cada pocilio (el líquido se volvió azul). Las placas se incubaron durante 30 minutos a temperatura ambiente en la oscuridad, después se añadieron 100 j l de disolución de parada a cada pocillo y las placas se golpearon suavemente en el lateral para mezclarlas. Se leyó la absorbancia de cada pocillo a 450 nm (en 2 horas desde la adición de la disolución de parada).
Ensayo de localización nuclear de p-catenina
Células U2-OS que expresan de forma estable dos fragmentos de p-galactosidasa complementarios (una parte en p-catenina y la otra expresada constitutivamente en el núcleo celular) se mantuvieron en DMEN F12 complementado con FBS al 10%. Cuando la p-catenina se trasloca al núcleo, los fragmentos complementarios forman una p-galactosidasa completa, cuya cantidad entonces se cuantifica por la actividad p-galactosidasa (DiscoveRx). Las células se sembraron en CulturPlate de 384 pocillos (Perkin Elmer, Boston, MA) con 10000 por célula en 20 j l de DMEN F12 que contenía FCS al 10 %, 100 U/ml de penicilina y 100 jg/m l de estreptomicina. Después de incubación durante una noche a 37 °C, las células se estimularon con 100 nl de compuesto de ensayo/pocillo y después se devolvieron a la incubadora durante 6 h. Las células se alteraron usando 12 j l de tampón de lisis que contiene sustrato del kit de detección PathHunter en la formulación especificada por el proveedor (DiscoveRx). Las placas se incubaron en la oscuridad durante 1 h a temperatura ambiente antes de la medición de la actividad p-galactosidasa (luminiscencia) en un lector de placa EnVision (PerkinElmer, Waltham, MA). La distancia entre la placa y el detector era de 0,2 mm. Tiempo de medición(s) = 0,1; factor de corrección de brillo (CT2) = 0.
Ensayo indicador de TCF/LEF
Se obtuvieron células HEK293-pBARL a partir de células HEK293 y expresaban de forma estable un gen indicador de luciferasa de luciérnaga dirigido por un promotor que contenía 12 copias de las secuencias de unión de TCF/LEF. Estas células se mantuvieron en DMEN y se complementaron con FBS al 10 % y penicilina-estreptomicina al 1 % (Invitrogen). Los ensayos de gen indicados se realizaron en medio sin antibiótico. La actividad del gen indicador de TCF/LEF se ensayó como se describe previamente (Pan et al., 2011, Neuropsychopharmacology). Estas células también contenían un gen indicador de luciferasa de Renilla dirigido por el promotor EF1a ubicuo como control. Las líneas celulares de indicador HEK293 se sembraron en placas de cultivo de 384 pocillos (Corning) a 6000 células/pocillo. A las 24 horas después de la siembra, las células se trataron durante una noche con compuestos pertinentes y se ensayaron usando el kit de ensayo DualGlo (Promega). Las intensidades luminiscentes se leyeron por EnVision (PerkinElmer, Waltham, MA). La intensidad de luciferasa de luciérnaga se normaliza por la intensidad de luciferasa de Renilla. El protocolo detallado se analiza a continuación.
Reactivos: Reactivo de ensayo de luciferasa Dual-Glo de Promega (E2940) (tampón de luciferasa, sustrato de luciferasa, tampón de luciferasa Stop & Glo, sustrato de luciferasa Stop & Glo); Tipo de placa: Placas de cultivo tratadas con TC, blancas de 384 pocillos Corning (3707)
Las células se cultivaron en placas de 384 pocillos hasta una densidad apropiada (40 j l de volumen de siembra total). A las 24 horas después de la siembra, las células se trataron con 100 nl de compuestos. A las 24 horas después de incubación con los compuestos (48 horas después de la siembra), se prepararon los reactivos de ensayo mezclando la disolución de ensayo de luciferasa con sustrato de luciferasa y disolución Stop & Glo con sustrato Stop & Glo (los reactivos adicionales pueden dividirse en alícuotas y congelarse para uso futuro y son estables durante al menos un ciclo de congelación/descongelación). Se añadió un volumen de reactivo de luciferasa igual a % el volumen del medio a cada pocillo (por ejemplo, en una placa de 384 pocillos con 40 j l en cada pocillo, se añadieron 10 j l para dar un volumen final de 50 jl). La placa se centrifugó y se permitieron 10 minutos para la estabilización de la señal. La señal de luciferasa en el Perkin Elmer EnVision usando los siguientes parámetros: Distancia entre la placa y el detector (mm) = 0,2; tiempo de medición(s) = 0,1; factor de corrección de brillo (CT2) = 0. Una vez fijados los datos iniciales, se añadió un volumen de Stop & Glo igual a cada pocillo igual al volumen de reactivo de luciferasa añadido anteriormente (si se añadían 10 j l de reactivo de luciferasa, también se añadían 10 j l de Stop & Glo). La placa se centrifugó y se permitieron 10 minutos para la estabilización de la señal. La placa se leyó en el EnVision usando los mismos parámetros detallados anteriormente.
Determinación de afinidad por resonancia de plasmones superficiales secundaria
Se inmovilizaron aproximadamente 20000 unidades de respuesta (UR) de anticuerpo anti-GST (GE Healthcare Life Sciences) en la celda de flujo (FC) 1 y FC2 de un nuevo chip detector CM5 recién acondicionado (GE Healthcare Life Sciences) en un instrumento Biacore T100 utilizando el asistente de inmovilización del paquete de programas informáticos T100. Entonces se capturaron aproximadamente 1200 UR de GST recombinante (GE Healthcare Life Sciences) en FC1 utilizando el protocolo del asistente de captura del paquete de programas informáticos T100. FC1 se usa como punto de sustracción de referencia para este y todos ensayos de SPR. Entonces se capturaron aproximadamente 2500 UR de GST-GSK3p recombinante en FC2 utilizando el protocolo del asistente de captura del paquete de programas informáticos T100. FC2 se usa como celda de flujo activa para este y todos los ensayos de SPR. La placa de analito se genera de un modo de respuesta a dosis en tampón TBS que contenía una concentración final de DMSO al 2%, con una concentración de analito final de 10 μM a 10 nM con un factor de
dilución 2X. Se determina un valor cero procesando inyecciones de tampón que contenían únicamente DMSO al 2 % y sin analito. Todas las inyecciones se procesaron por duplicado y se sustrajo la referencia de FC1. Se desarrolló un método que consistía en un tiempo de contacto de 60 segundos y un tiempo de lavado de 60 segundos con un caudal de 30 pl/min. La curva de patrón interno para los valores de DMSO se generó con siete inyecciones de DMSO que consistían en DMSO al 1, 1,25, 1,5, 2, 2,25, 2,5 y 3 % en tampón de procesamiento TBS. El análisis de los compuestos se hizo usando el modelo de unión 1:1 y mediciones de afinidad en el paquete de programas informáticos de evaluación Biacore T100.
Generación de tampón:
PBS: Se mezclaron 900 ml de agua DI filtrada con 100 ml de disolución de tampón PBS 10X (Invitrogen)
TBS propio: Se añadieron 1,21 g de Tris y 8,7 g de NaCl a 950 ml de agua DI filtrada. El pH se ajustó usando HCl 6 M hasta 7,35. Se rellenaron hasta la marca de 1000 ml. Se filtraron y se recogieron 900 ml en un frasco, y se filtraron y se recogieron 100 ml en un segundo frasco. Se añadieron 450 pl de detergente P20 (GE Healthcare Life Sciences) al frasco 1, se añadieron 50 pl de detergente P20 al frasco 2 y se mezclaron minuciosamente. Se transfirieron 18 ml de tampón del frasco 1 al frasco 2 para general el tampón de procesamiento TBS. Se añadieron 18 ml de DMSO (Aldrich) al frasco 1 para general un tampón de procesamiento de DMSO al 2 %.
Generación del chip detector CM5 de GSK3p: Acondicionamiento del nuevo chip: Se cargó tampón de inmovilización PBS en el estante de tampón y se inserta tampón en la línea A. El chip detector CM5 sin usar se cargó en el instrumento según el manual del usuario. El chip se cebó con 6 minutos de inyección de tampón a 30 pl/min. El procesamiento manual se inició y se inyectó sobre la celda de flujo (FC) 1 y 2 inyecciones alternas de tampón de lisina (GE Healthcare Life Sciences) y tampón de hidróxido de sodio (GE Healthcare Life Sciences) a un caudal de 30 pl/min durante 30 segundos por inyección. Inmovilización de anticuerpo anti-GST: El chip se cebó de nuevo como describe anteriormente. Se generó disolución de anticuerpo anti-GST mezclando 4,5 pl de anticuerpo anti-GST (GE Healthcare Life Sciences, kit de captura de GST) con 95,5 pl de tampón de inmovilización (Ge Healthcare Life Sciences, kit de captura de GST). La disolución se puso en un vial pequeño de 700 pl y se tapó. Se repitió. Ambos viales se colocaron en la gradilla de reactivo 1 del instrumento Biacore T100 y se insertaron en la máquina según el manual del usuario. Se inició la inmovilización del anticuerpo anti-GST utilizando el protocolo del asistente de inmovilización del programa informático Biacore T100. Se inmovilizaron aproximadamente 20000 unidades de respuesta (UR) de anticuerpo anti-GST en FC1 y FC2. Se capturan las proteínas de referencia y activa en FC1 y FC2, respectivamente: Se retiró el tampón de inmovilización PBS de la gradilla de tampón y se remplazó con tampón de procesamiento DMSO al 2 % con TBS. Se insertó tampón en la línea A. Se repitió el procedimiento de cebado. Se generó la disolución de proteína GST mezclando 2 pl de GST recombinante (GE Healthcare Life Sciences, kit de captura de GST) con 98 pl de tampón DMSO al 2 % con TBS. Se generó la disolución de proteína GST-GSK3p mezclando 5 pl de GST-GSK3p recombinante con 95 pl de tampón de procesamiento DMSO al 2 % con TBS. Se colocó la disolución de proteína GST en la posición B1 en la gradilla de reactivo 1. Se colocó la disolución de proteína GST-GSK3p en la posición C1 en la gradilla de reactivo 1. Se inició un procesamiento de inyección manual y se inyectó durante 30 segundos a 5 pl/min de disolución de proteína GST en FC1 para generar la celda de flujo de referencia. Se inició un procesamiento de inyección manual y se inyectó durante 30 segundos a 5 pl/min de disolución de proteína GST-GSK3p en FC2 para generar la celda de flujo activa. Se capturaron aproximadamente 1000 UR de proteína GST en FC1. Se capturaron aproximadamente 2500 UR de proteína GST-GSK3p en FC2.
Análisis de inhibidores de GSK3p de molécula pequeña: Se generó una placa de analito para el ensayo. Usando una placa de 384 pocillos de volumen de profundidad convencional, se colocaron 100 pl de una disolución de DMSO al 2 % con TBS 10 pM de analito deseado en los pocillos A1 y A2. Se colocaron 100 pl de una disolución de DMSO al 2 % con TBS 5 pM de analito deseado en los pocillos A3 y A4. Se colocaron 100 pl de una disolución de DMSO al 2 % con TBS 2,5 pM de analito deseado en los pocillos A5 y A6. Se repitieron estas etapas con analitos diluidos en serie hasta 10 nM en los pocillos A21 y A22. Se colocaron 100 pl de tampón de procesamiento DMSO al 2 % con TBS en los pocillos A23 y A24. Se repitieron las etapas para los posteriores analitos. La placa de analitos se colocó en Biacore T100 según el manual del usuario. Se generó el método que consiste en lo siguiente: Inyección de analito sobre FC1 y FC2 con sustracción de referencia; caudal de 30 pl/min de analito, 60 segundos de tiempo de contacto de analito; 60 segundos de tiempo de lavado de tampón de procesamiento; generación de la curva patrón de DMSO usando DMSO al 1, 1,5, 1,75, 2, 2,5, 2,75 y 3% en tampón de procesamiento TBS. El análisis de los compuestos se procesó, y los compuestos se clasificaron de acuerdo con la determinación de KD utilizando la opción de medición de afinidad en el programa informático Biacore T100.
Generación del chip detector CM5 de CK15: Se inmovilizaron aproximadamente 20000 unidades de respuesta (UR) de anticuerpo anti-GST (GE Healthcare Life Sciences) en la celda de flujo (FC) 1 y FC2 de un nuevo chip detector CM5 recién acondicionado (GE Healthcare Life Sciences) en un instrumento Biacore T100 utilizando el asistente de inmovilización del paquete de programas informáticos T100. Entonces se capturaron aproximadamente 1500 UR de GST recombinante (GE Healthcare Life Sciences) en FC1 utilizando el protocolo del asistente de captura del paquete de programas informáticos T100. FC1 se usa como punto de sustracción de referencia para este y todos ensayos de SPR. Entonces se capturaron aproximadamente 2700 UR de GST-CK15 recombinante en
FC2 utilizando el protocolo del asistente de captura del paquete de programas informáticos T100. FC2 se usa como celda de flujo activa para este y todos los ensayos de SPR. La placa de analito se genera de un modo de respuesta a dosis en tampón TBS que contenía una concentración final de DMSO al 2 %, con una concentración de analito final de 10 μM , 100 nM y 10 nM. Se determina un valor cero procesando inyecciones de tampón que contenían únicamente DMSO al 2% y sin analito. Todas las inyecciones se procesaron por duplicado y se sustrajo la referencia de FC1. Se empleó un método que consistía en un tiempo de contacto de 60 segundos y un tiempo de lavado de 60 segundos con un caudal de 30 jl/m in. La curva de patrón interno para los valores de DMSO se generó con siete inyecciones de DMSO que consistían en DMSO al 1, 1,25, 1,5, 2, 2,25, 2,5 y 3% en tampón de procesamiento TBS. El análisis de los compuestos se hizo usando el modelo de unión 1:1 y mediciones de afinidad en el paquete de programas informáticos de evaluación Biacore T100.
Generación del chip detector CM5 de CK15: Acondicionamiento del nuevo chip: Se cargó tampón de inmovilización PBS en el estante de tampón y se inserta tampón en la línea A. El chip detector CM5 no usado se cargó en el instrumento según el manual del usuario. El chip se cebó con 6 minutos de inyección de tampón a 30 jl/min. El procesamiento manual se inició y se inyectó sobre la celda de flujo (FC) 1 y 2 inyecciones alternas de tampón de lisina (GE Healthcare Life Sciences) y tampón de hidróxido de sodio (GE Healthcare Life Sciences) a un caudal de 30 jl/m in durante 30 segundos por inyección.
Inmovilización de anticuerpo anti-GST: El chip se cebó de nuevo como describe anteriormente. Se generó disolución de anticuerpo anti-GST mezclando 4,5 j l de anticuerpo anti-GST (GE Healthcare Life Sciences, kit de captura de GST) con 95,5 j l de tampón de inmovilización (GE Healthcare Life Sciences, kit de captura de GST). La disolución se puso en un vial pequeño de 700 j l y se tapó. Se repitió. Ambos viales se colocaron en la gradilla de reactivo 1 del instrumento Biacore T100 y se insertaron en la máquina según el manual del usuario. Se inició la inmovilización del anticuerpo anti-GST utilizando el protocolo del asistente de inmovilización del programa informático Biacore T100. Se inmovilizaron aproximadamente 20000 unidades de respuesta (UR) de anticuerpo anti-GST en FC1 y FC2. Se capturan las proteínas de referencia y activa en FC1 y FC2, respectivamente: Se retiró el tampón de inmovilización PBS de la gradilla de tampón y se remplazó con tampón de procesamiento DMSO al 2 % con TBS. Se insertó tampón en la línea A. Se repitió el procedimiento de cebado. Se generó la disolución de proteína GST mezclando 2 j l de GST recombinante (Ge Healthcare Life Sciences, kit de captura de GST) con 98 j l de tampón DMSO al 2 % con TBS. Se generó la disolución de proteína GST-GK18 mezclando 5 j l de GST-GK18 recombinante con 95 j l de tampón de procesamiento DMSO al 2 % con TBS. Se colocó la disolución de proteína GST en la posición B1 en la gradilla de reactivo 1. Se colocó la disolución de proteína GST-GK18 en la posición C1 en la gradilla de reactivo 1. Se inició un procesamiento de inyección manual y se inyectó durante 30 segundos a 5 jl/m in de disolución de proteína GST en FC1 para generar la celda de flujo de referencia. Se inició un procesamiento de inyección manual y se inyectó durante 30 segundos a 5 jl/m in de disolución de proteína GST-GK15 en FC2 para generar la celda de flujo activa. Se capturaron aproximadamente 1500 UR de proteína GST en FC1. Se capturaron aproximadamente 2700 UR de proteína GST-GK15 en FC2.
Análisis de ligandos de CK15 de molécula pequeña: Se generó una placa de analito para el ensayo. Usando una placa de 384 pocillos de un volumen de profundidad convencional, se colocaron 100 j l de un analito 10 μM en disolución de DMSO al 2 % con TBS en los pocillos A1 y A2. Se colocaron 100 j l de un analito 50 nM en disolución de DMSO al 2 % con TBS en los pocillos A3 y A4. Se colocaron 100 j l de un analito 10 nM en disolución de DMSO al 2 % con TBS en los pocillos A5 y A6. Se colocaron 100 j l de tampón de procesamiento de DMSO al 2 % con TBS en los pocillos A7 y A8. Se repitieron las etapas para los posteriores analitos. La placa de analitos se colocó en Biacore T100 según el manual del usuario. Se generó el método que consiste en lo siguiente: Inyección de analito sobre FC1 y FC2 con sustracción de referencia; caudal de 30 jl/m in de analito, 60 segundos de tiempo de contacto de analito; 60 segundos de tiempo de lavado de tampón de procesamiento; generación de la curva patrón de DMSO usando DMSO al 1, 1,5, 1,75, 2, 2,5, 2,75 y 3 % en tampón de procesamiento TBS. El análisis de los compuestos se procesó, y los compuestos se clasificaron de acuerdo con la determinación de KD utilizando la opción de medición de afinidad en el programa informático Biacore T100.
Ensayo de desplazamiento de movilidad de m icrofluidos de GSK3p
Se incubó GSK3p purificada con compuestos ensayados en dosis en presencia de 4,3 μM de ATP y 1,5 μM de sustrato peptídico (péptido 15 de Caliper) durante 60 minutos a temperatura ambiente en placas de 384 pocillos (Seahorse Bioscience, MA), en tampón de ensayo que contenía h Ep ES 100 mM (pH 7,5), MgCh 10 mM, DTT 2,5 mM, Tween-20 al 0,004 % y Briji-35 al 0,003 %. Las reacciones se terminaron mediante la adición de EDTA 10 nM. El sustrato y el producto se separaron electroforéticamente y se determinó la intensidad de fluorescencia del sustrato y el producto por el Lector II Labchip EZ (Caliper Life Sciences, MA). La actividad cinasa se midió como el porcentaje de conversión. Las reacciones se realizaron por duplicado para cada muestra. El control positivo (GW8510 a 20 μM ; CID 6539118) se incluyó en cada placa y se usó para cambiar de escala los datos junto con los controles de DMSO en la placa. Los resultados se analizaron por el analizador de ensayo Genedata. El porcentaje de inhibición se representó frente a la concentración de compuesto y se determinó el valor de CI50 a partir del ajuste de curva de respuesta a dosis logística.
Protocolo de ensayo de ADP Glo (ATP 10 pM) en formato de 384 pocillos
Se distribuyeron 20 pl/pocillo de GSK3p 4,7 nM y péptido 7 pM en KBA (HEPES 250 mM (pH 7,5), MgCl2 50 mM, EGTA 5 mM, BRIJ-35 al 0,05 %) en placa de 384 pocilios opaca blanca. Se fijaron 100 nl/pocillo de los compuestos. Se distribuyó 1 pl/pocillo de ATP 140 pM en k Ba . Se incubó a temperatura ambiente durante 60 minutos. Se añadieron 20 pl/pocillo de ADP-glo (Promega, V9103) con Combi, y se incubaron a temperatura ambiente durante 40 minutos. Se añadieron 40 pl/pocillo de ADP-glo (Promega, V9103) con Combi, se incubó a temperatura ambiente durante 30 minutos. Se leyó en Envision para la luminiscencia.
Protocolo in vivo de AIH
Se realizó hiperactividad inducida por anfetamina como se describe en Pan et al. Neuropsychopharmacology, 2011).
Cirugía: A los ratones que recibieron infusiones intracraneales se les implantó una cánula de guía de acero inoxidable (Plastics One, Roanoke, VA) dirigida al tercer ventrículo dorsal. Los ratones se anestesiaron con quetamina/xilacina (150 mg/kg y 10 mg/kg, respectivamente; 5 ml/kg de volumen de inyección). Usando un aparato estereotáxico, la cánula de guía (C232GC, calibre 26, Plastics One) con cánula simulada insertada (C232DC) se dirigió hacia el tercer ventrículo dorsal (-0,5 mm posterior a la Bregma, ±0,0 lateral a la línea media y -3.0 (sitio de inyección) ventral a la superficie del cráneo), (Paxinos, 2001). Los ratones se recuperaron durante al menos 5 días antes del ensayo. Durante las infusiones, los ratones se restringieron suavemente. La cánula simulada se remplazó con la cánula de inyección (calibre 26; que se prolonga 1,0 mm más allá de la punta de la guía de 2,0 mm; C2321) adherida al tubo de polietileno (PE50) conectado a una jeringa Hamilton de 10 pl. Las infusiones se controlaron mediante una bomba de microinfusión (KDS 100, KD Scientific; New Hope, PA).
Procedimientos de comportamiento respecto a los ratones a los que se ha dosificado compuesto 22:
Se examinó la hiperactividad inducida por anfetamina (AIH) en ocho cámaras de campo abierto idénticas (41,91 x 40.64 x 30,48 cm (16,5" x 16" x 12"); AccuScan Instruments, Columbus, OH). La actividad se detectó por interrupciones del rayo infrarrojo y se registraron automáticamente por el programa informático VersaMax (AccuScan). Las sesiones diarias se almacenaron automáticamente en intervalos de 5 minutos (VersaDat; AccuSacn) para el análisis estadístico. La AIH se procesó durante tres días consecutivos de la siguiente manera:
Día 1: los ratones se aclimataron al procedimiento de infusión limitándolos suavemente y retirando la cánula simulada. Los ratones se restringieron durante tres minutos en cuyo punto se remplazó la cánula simulada. Entonces los ratones se colocaron en el campo abierto durante 20 minutos y después se retiraron para una inyección de disolución salina. Los ratones se colocaron de nuevo en el campo abierto durante 30 minutos adicionales, en cuyo punto los ratones se devolvieron a su jaula de hogar.
El día 2 se procesó de forma idéntica al día 1, con la excepción de que el segundo día duró una hora (20 minutos ^ inyección ^ 40 minutos) y la aclimatación restringida incluía una infusión ICV de disolución salina (2 minutos de infusión seguida de un minuto para la difusión del fármaco desde la cánula de inyección).
El día 3 fue el día de exposición a anfetamina. Los ratones se pretrataron con una infusión de compuesto 22 o vehículo 40 minutos antes de colocarse en el campo abierto. Después de 20 minutos, los ratones se retiraron y expusieron a anfetamina, y se colocaron de nuevo en el campo abierto durante 80 minutos.
Dosificación: 3 mg/kg, 10 mg/kg o 30 mg/kg. Vehículo: PEG400 al 45 %, disolución salina al 45 %; DMSO al 10 %. Los resultados se muestran en las figuras 7 y 8.
Procedimientos de comportamiento respecto a ratones a los que se ha dosificado compuesto 70
Se examinó la hiperactividad inducida por anfetamina (AIH) en ocho cámaras de campo abierto idénticas (41,91 x 40.64 x 30,48 cm (16,5" x 16" x 12"); AccuScan Instruments). La actividad se detectó por interrupciones del rayo infrarrojo y se registraron automáticamente por el programa informático VersaMax (AccuScan). Las sesiones diarias se almacenaron automáticamente en intervalos de 5 minutos (VersaDat; AccuSacn) para el análisis estadístico. La AIH se procesó durante tres días consecutivos de la siguiente manera:
• Día 1: Los ratones se colocaron en el campo abierto durante 20 minutos antes de retirarlos para una inyección de disolución salina. Los ratones entonces se colocaron de nuevo en el campo abierto durante 30 minutos adicionales, en cuyo punto los ratones se devolvieron a su jaula de hogar.
• El día 2 se procesó de forma idéntica al día 1, con la excepción de que, en el día 2 el tiempo total fue una hora (20 minutos antes de la inyección seguido de 40 minutos de control de la actividad).
• El día 3 fue el día de exposición a anfetamina. Los ratones se pretrataron con compuesto 137 (i.p. (intraperitoneal)) 30 minutos antes de colocarse en los campos abiertos. Después de 20 minutos, los ratones se retiraron, se expusieron a anfetamina y se colocaron de nuevo en el campo abierto durante 80 minutos.
Dosificación: 3 mg/kg, 10 mg/kg o 30 mg/kg. Vehículo: PEG400 al 45 %, disolución salina al 45 %; DMSO al 10 %.
Los resultados se muestran en la figura 11.
Resultados
Resumen de los resultados de cribado
La figura 2 presenta una ruta ejemplar para el desarrollo de sonda.
Se completó un cribado de alto rendimiento de aproximadamente 320000 compuestos frente a GSK3p humana en formato de placa de 1536 pocillos. El cribado caracterizó un promedio de Z' > 0,8. Aproximadamente 1000 compuestos que mostraron más de un 25 % de inhibición se seleccionaron como activos.
Estos compuestos activos, junto con aproximadamente 1000 de sus análogos negativos en la colección, se escogieron y se evaluaron sus potencias (CI50) frente a GSK3p en dosis en un nuevo ensayo de confirmación. En paralelo, también se completó un contracribado para descartar los positivos falsos debido a inhibición de reactivos de detección. Los compuestos con potencia prometedora (CI50 < 10 pM frente a GSK3p en esta fase), pero sin inhibición de reactivos de detección, se evaluaron adicionalmente para las características estructurales que probablemente los hacen novedosos, selectivos y maleables.
Se deseaban inhibidores de GSK3p altamente selectivos y potentes. Dado que se ha hecho una gran cantidad de trabajo sobre la diana GSK3p, el foco fue las series estructurales que no poseían armazones comunes a inhibidores de cinasa conocidos. Este filtro inicial permitió la selección de un número limitado de armazones de la colección original de más de 320000 moléculas pequeñas cribadas. La selección del armazón de pirazolodihidropiridina (esquema 1) como punto de partida de sonda inicial se hizo basándose en los resultados de experimentos de ADP-Glo (véase más adelante, tabla 2, entrada 1) que indicaron una potencia frente a GSK3p en el intervalo submicromolar. Basándose en una búsqueda de PubChem, este armazón se había analizado en una gran selección de ensayos (>600), pero se confirmó como activo en únicamente un ensayo diferente a los ensayos descritos en la presente memoria, que no pertenecían a la inhibición de cinasa. En segundo lugar, como se ilustra en el esquema 1a y b, la síntesis de este armazón le permitió la rápida introducción de diversidad química. Esta maleabilidad sintética elevada generó una diana atractiva desde un punto de ventaja químico. Se hizo un análisis de selectividad inicial para determinar el porcentaje del cinoma inhibido por nuestro acierto de HTS inicial (compuesto 1) usando un perfil de todo el cinoma (Carna Biosciences). El ensayo de selectividad descrito anteriormente examinó la capacidad inhibidora del compuesto 1 de pirazolodihidropiridina frente a 311 cinasas (que representan un 60% del cinoma existente) a una concentración mantenida de 10 pM. Capturados en la tabla 1 a continuación están los resultados de las únicas cinasas inhibidas a más de un 50 % por el tratamiento con compuesto 1 a 10 pM.
Tabla 1. Porcentaje de inhibición de cinasas seleccionadas por el acierto de HTS (compuesto I) a 10 pM.
CHIR99021 (o CHIR 99021) es un inhibidor de GSK3p del estado de vanguardia. Cuando este compuesto se comparaba para la selectividad con los mismos criterios que el acierto de HTS, CHIR99021 inhibía 21 cinasas a más de un 50% a 10 pM. Este análisis de selectividad inicial, combinado con la excelente potencia dio lugar a la conclusión de que el armazón de pirazolodihidropiridina sería una excelente elección para análisis adicional como candidato de sonda o como un agente terapéutico potencial. El compuesto 3, un enantiómero del compuesto 1, se examinó para la actividad frente a la lista de cinasas previamente determinadas (tabla 1), que ilustra que el compuesto 3 era selectivo para GSK3p y no inhibía ninguno de la familia de CK1 como se observa cuando se examina la mezcla racémica.
Examen de resonancia de plasmones superficiales
Entonces se utilizó un ensayo de unión directa como un análisis secundario de la actividad del compuesto. Se empleó resonancia de plasmones superficiales (SPR) para examinar una pequeña colección de derivados pirazolodihidropiridina descritos en la presente memoria. Tras el examen usando este ensayo, se descubrió que la sustitución del anillo arilo en la posición 2 daba lugar a un aumento de dos veces en la afinidad de estas moléculas por GSK3p. El acierto de HTS (compuesto 1) tiene una Kd determinada de forma experimental de 130 nM. El compuesto 20 tiene una Kd determinada de forma experimental de 60 nM.
Separación de enantiómeros
La separación de los dos enantiómeros de compuesto 20 se completó para llegar a un compuesto individual. El compuesto 22, el enantiómero R del compuesto 20, inhibía 8 cinasas a más de un 50% a l0 j M, y fue selectivo para GSK3 en más de 22 veces (22 veces respecto a la siguiente cinasa más cercana, CDK5) (véase la tabla 5). La estequiometría absoluta del enantiómero se determinó mediante cocristalización del compuesto 22 con GSK3p (véase la figura 4). La estructura cristalina también confirmó que el compuesto se une al sitio de unión de ATP. Para generar cocristales de GSK3p/compuesto 22, se usó el siguiente procedimiento: (1) se añadió un exceso molar de 5 veces de compuesto 22 (en DMSO al 100%) a una GSK3p diluida y después se mezcló suavemente; y (2) el complejo de GSK3p/compuesto 22 se incubó en hielo durante 30 minutos, se concentró hasta 5 mg/ml y después se cribó con los métodos descritos anteriormente. Los cristales se nuclearon en cuatro días y crecieron hasta un tamaño máximo después de una semana. Los cristales para GSK3p/compuesto 22 se transportaron a la instalación de sincrotrón de NSLs en Brookhaven National Laboratory y se evaluaron usando la línea de luz X29.
Se diseñaron y sintetizaron compuestos para explorar SAR en diferentes restos químicos del armazón de pirazolodihidropiridina, potenciar las propiedades deseadas incluyendo la potencia, selectividad, solubilidad y, en algunos casos, estabilidad microsómica, y disminuir las inestabilidades. Se separaron mezclas racémicas de determinados análogos y se midieron las actividades de los enantiómeros (tabla 2).
La caracterización bioquímica de estos compuestos sintetizados se evaluó frente a GSK3p y CDK5/p25, sirviendo CDK5/p25 como contradiana de la selectividad de GSK3p. También se realizó una caracterización bioquímica adicional para la potencia y la selectividad en Carna Biosciences. También se realizó una batería de ensayos basados en células para evaluar la actividad celular de un subconjunto de estos compuestos. Estos ensayos basados en células incluyen la fosforilación de Tau en células de fisiopatología humana SH-SY5Y, translocación nuclear de beta-catenina y el ensayo indicador de TCF/LEF que controla la ruta de señalización de Wnt en células HEK293. También se controlaron los efectos de estos compuestos sobre la supervivencia de células de fisiopatología SH-SY5Y. El compuesto 54 demuestra coherentemente una potencia de 10-20 nM frente a GSK3p, una selectividad de 150-380 veces respecto a CDK5/p25, un perfil selectivo de cinoma superior en comparación con CHIR99021 y potente actividad celular.
Una búsqueda de PubChem para el compuesto del acierto para el cribado primario (compuesto 1) reveló que se había ensayado en 652 bioensayos y se confirmó como activo únicamente en un ensayo diferente a los ensayos descritos en la presente memoria. El ensayo fue un cribado de inhibidores de hidroxiesteroide (17-beta) deshidrogenasa 4 (HSD17B4) con una potencia de 25,1 j M. Basándose en esta información, el compuesto no parece ser un inhibidor promiscuo, además el armazón no contiene ninguna inestabilidad química obvia.
Análisis de SAR
Los resultados se describen en la tabla 2.
Tabla 2. Resultados de ensayo ejemplares.
Para la tabla 2, "A" indica una CI50 o Kd de < 0,100 j M, "B" indica una CI50 o Kd de 0,101-1,000 j M, "C" indica una CI50 o Kd de 1,001-5,000 j M, "D" indica una CI50 o Kd de 5,001-30,000 j M y "E" indica una CI50 o Kd >30 j M.
Aunque se mantiene R3 como un grupo metilo, se exploraron diversas sustituciones en el anillo fenilo. La naturaleza del sustituyente tiene poco efecto sobre la potencia del compuesto, fluoro, cloro, trifluorometilo, metilo, metoxi y ciano produjeron todos compuestos con potencia similar. La posición del sustituyente, sin embargo, tuvo un impacto más profundo en la actividad. La sustitución en la posición orto produjo los compuestos más potentes, aunque en general, la selectividad más baja frente a CDK5. Los compuestos sustituidos en la posición meta fueron ligeramente menos potentes, pero presentaron mayor selectividad sobre CDK5. Los compuestos que se sustituyeron en la posición para produjeron una bajada significativa en la actividad de GSK3 que puede predecirse basándose en la unión observada en la estructura cristalina (figura 4). La estructura cristalina muestra que, aunque hay bolsillos para los sustituyentes en la posición 2 y 3, la unión en la posición 4 del anillo fenilo es demasiado estrecha para tolerar grupos más grandes que el hidrógeno. Los compuestos que eran particularmente interesantes debido a su actividad en el ensayo primario y los ensayos celulares fueron el compuesto 2-fluoro, 2-trifluorometilo, 2-metoxi, 2-metiltio, 3-trifluorometilo y 3-ciano.
En casos donde R3 se mantenía constante como un grupo metilo, se exploró el remplazo del grupo fenilo con heteroaromáticos. El remplazo del grupo fenilo con tiofenos produjo una bajada en la potencia contra GSK3 y ningún aumento en la actividad celular. El remplazo con imidazol también dio lugar a una bajada en la potencia contra GSK3. El remplazo con un grupo 3-piridilo produjo un compuesto que era equipotente con el compuesto del acierto y solubilidad aumentada, sin embargo, no tenía actividad celular apreciable. Otros remplazos con piridilo produjeron una bajada en la potencia en comparación con el compuesto del acierto.
Habiendo investigado una gama de remplazos comunes y sustituciones para el grupo fenilo, se eligió el 2-metoxi fenilo por su potencia, selectividad y propiedades físicas para su uso como el compuesto básico para estudios de SAR adicionales. El movimiento del grupo dimetilo geminal hasta la posición a del carbonilo produjo un compuesto que tenía una bajada en la potencia en el ensayo primario y una pérdida de actividad en los ensayos celulares. La eliminación del grupo dimetilo geminal provocó una pérdida moderada de actividad. El remplazo del anillo de seis miembros con un anillo de cinco miembros proporcionó el compuesto aromatizado, que no tenía actividad contra GSK3. La eliminación del anillo que ceto produjo una bajada significativa en la actividad. El remplazo del dimetilo geminal con un grupo ciclohexilo proporcionó un compuesto que era potente de forma similar al compuesto principal, sin embargo, perdió actividad en los ensayos celulares.
Se exploraron compuestos para los que se ha remplazado o sustituido el pirazol en el grupo metilo. La eliminación del grupo metilo del pirazol produce un compuesto que tiene potencia comparable al compuesto principal, lo que indica que el grupo metilo no es vital para la actividad. El remplazo del metilo con grupos alquilo más grandes, tales como etilo, isopropilo y tercbutilo presentan una tendencia de disminución de la actividad según aumenta el tamaño del grupo. Esto puede explicarse por la estructura cristalina ya que hay pequeño bolsillo en esta posición que puede
explotarse para la sustitución, que permite el aumento en el tamaño hasta etilo, sin embargo, aumentos adicionales provocan interacciones negativas. El remplazo con fenilo provoca una bajada en la potencia y una disminución en la actividad en los ensayos celulares. El pirazol que contiene trifluorometilo, aunque es potente de forma similar al compuesto principal en el ensayo primario, muestra una mejora significativa en los ensayos celulares, presumiblemente debido al aumento de la permeabilidad. El remplazo del pirazol con un oxazol o fenilo proporciona compuestos con actividad limitada.
La estabilidad microsómica de determinados compuestos es escasa. Principalmente, parece que la posición bencílica es propensa a oxidación. Como se menciona previamente, el análogo aromatizado del compuesto del acierto es inactivo. Como nuestro modo de metabolismo produce presumiblemente productos aromatizados, se sintetizaron compuestos para bloquear este sitio de metabolismo. Para ensayar si la hidroxilación mediada por P450 de la posición bencílica era clave para el perfil de estabilidad metabólica escasa de la serie, se sintetizó un compuesto en que el hidrógeno en la posición bencílica estaba remplazado con un deuterio en un esfuerzo por aprovechar potencialmente un efecto de isótopo secundario y proporcionar un análogo con estabilidad metabólica mejorada. El remplazo con deuterio proporcionó un compuesto que tenía actividad similar al compuesto del acierto, sin embargo, no hubo mejora en la estabilidad microsómica. La estructura cristalina indicó que la sustitución en la posición bencílica con un grupo metilo puede tolerarse, por ejemplo, el compuesto 67 presentaba estabilidad microsómica mejorada (de un 6 % a un 32 %) y tampoco producía una pérdida en la potencia contra GSK3, sin embargo, este compuesto no presentaba actividad en los ensayos celulares. Los esfuerzos futuros estarán dirigidos a compuestos que tienen un metilo en la posición bencílica con actividad celular mejorada.
Basándose en los resultados de la sustitución del fenilo y el pirazol mostrada en la tabla 2, se sintetizaron varios compuestos híbridos. El remplazo del metilo en el pirazol del compuesto del acierto con un trifluorometilo provoca un aumento en la potencia en el ensayo primario y la actividad en los ensayos celulares, lo que indica que el trifluorometilo es beneficioso para la permeabilidad celular. La mono o disustitución del fenilo con grupos fluoro y trifluorometilo, da lugar a compuesto que, aunque son potentes en el ensayo primario, pierden actividad en los ensayos basados en células.
Los resultados de la tabla 2 indicaron que un enantiómero en las mezclas racémicas de los compuestos era responsable de la actividad observada que entonces se explicaba por la unión del enantiómero activo en la estructura cristalina, por lo tanto, se realizó la separación de los enantiómeros de varios compuestos. Para estos compuestos, se descubrió que el enantiómero en el que el grupo arilo estaba "caído", como se muestra en las estructuras a continuación, era típicamente más potente para GSK3p.
Caracterización química del compuesto 54
El compuesto 54 se analizó por UPLC, espectroscopia de RMN de 1H y 13C, y espectrometría de masas de alta resolución. Los datos obtenidos de RMN y espectroscopia de masas fueron coherentes con la estructura del compuesto 54 (datos no mostrados) y la UPLC indicó una pureza aislada de >95 %.
La solubilidad del compuesto 54 se determinó experimentalmente en 85 pM en disolución salina tamponada con fosfato (PBS, pH 7,4, 23 °C). La unión a proteína plasmática (PPB) se determinó en un 93 % unida en plasma humano. El compuesto 54 es estable en plasma humano, con aproximadamente un 97 % restante después de un
periodo de incubación de 5 horas. Se descubrió que el compuesto era estable en glutatión (GSH) con un 99 % restante después de 48 horas.
La estabilidad del compuesto 54 en PBS (DMSO al 0,1 %) se midió durante 48 horas. La concentración del compuesto 54 permaneció constante durante 48 horas a aproximadamente un 200 % (datos no mostrados). Sin el deseo de limitarse a teoría alguna, se cree que el aumento gradual en la concentración es el resultado directo de la disolución de más compuesto en PBS a lo largo del tiempo. En otras palabras, el ensayo de estabilidad en PBS se realizó en las condiciones recomendadas, la solubilidad cinética del compuesto 54 se midió en PBS y no su estabilidad. Por tanto, la cantidad total de compuesto 54 presente en el pocillo después de que el compuesto se tratara con PBS en solitario se determinó para una longitud de tiempo dada. Se añadió acetonitrilo en diversos puntos temporales a los pocillos que contenían compuesto 54 en PBS y se midió la cantidad total del compuesto. Este resultado se muestra en la figura 1. A partir de estos resultados, parece que el compuesto 54 es estable en PBS ya que más de un 95 % está aún presente después de 48 horas de incubación.
Análisis analítico adicional
Se descubrió que el compuesto 54 estaba un 93 % y un 91 % unido a plasma humano y de ratón respectivamente y era estable en plasma humano y de ratón con un 97 % y un 99 % restante después de 5 horas. El compuesto del acierto, la sonda racémica y siete análogos se sometieron a microsomas de ratón para el análisis de estabilidad (tabla 3). Se descubrió que la sonda racémica era inestable a los microsomas de ratón con <1 % restante después de 1 hora. Todos los demás análogos que estaban sin sustituir en la posición bencílica tenían <7% restante después de 1 hora, lo que indica que la responsabilidad metabólica principal es la posición bencílica. La sustitución en la posición bencílica con un grupo metilo produjo un 32 % de compuesto restante después de 1 hora. Compuestos adicionales con sustitución en la posición bencílica pueden producir potencia aumentada manteniendo al mismo tiempo o mejorando este aumento de estabilidad metabólica.
Tabla 3: Solubilidad, unión a proteína, estabilidad en plasma y estabilidad microsómica de compuestos selectos.
Todos los valores son el promedio de al menos dos réplicas
Actividad celular
GSK3p es constitutivamente activa y a menudo sirve como regulador negativo de la señalización celular. La inhibición de GSK3p elimina esta regulación negativa, que provoca la activación de diversas rutas celulares. Muchas proteínas, incluyendo beta-catenina en la ruta de señalización de Wnt y la proteína Tau en la dinámica de microtúbulos, se someten a fosforilación por GSK3p. Específicamente, GSK3p fosforila directamente la proteína Tau en Ser199 y modula el autoensamblaje de Tau. La hiperfosforilación de Tau está implicada en la fisiopatología del trastorno de Alzheimer. La beta-catenina se fosforila por GSK3p en la región del extremo N y esta fosforilación marca la proteína para su degradación. La acumulación de beta-catenina después de la inhibición de GSK3p se transloca al núcleo y activa los genes dirigidos por el promotor de TCF/LEF en la ruta de Wnt canónica. Tau y pcatenina se eligen como dos sustratos independientes para evaluar la inhibición de GSK3p en tres ensayos celulares:
1) Evaluar la cantidad de fosforilación de Tau (Ser199) en células SH-SY5Y tras la inhibición de GSK3p (AID 624057);
2) Evaluar la cantidad de acumulación nuclear de beta-catenina después de la inhibición de GSK3p en células U2OS (AID 624086) y la posterior activación de TCF/LEF por beta-catenina nuclear aumentada en células HEK293 (AID 624088).
Se exploró la monosustitución en el grupo fenilo, y se evaluaron adicionalmente algunos de los compuestos enzimáticamente activos en ensayos celulares. La sustitución con cloro, metoxi y trifluorometilo en la posición 2 del grupo fenilo generaron compuestos con una CI50 <1 pM en ensayos enzimáticos, y eran activos en la inhibición de la fosforilación de Tau (CI50 <10 pM) por GSK3p. Una 3-sustitución con un grupo trifluorometilo en el anillo fenilo también fue activa en el ensayo de fosfo-Tau. Estos compuestos eran activos de forma similar en el ensayo de translocación nuclear de beta-catenina y el ensayo indicador de TCF/LEF con CE50 entre 5 y 25 pM.
Basándose en el 2-metoxi en el anillo fenilo, se exploraron sustituciones en el pirazol. La trifluorosustitución en el pirazol obtuvo la mejor actividad celular en la serie, con una CI50 submicromolar (0,48 pM) en el ELISA de p-Tau, y una CE50 en el ensayo indicador de TCF/LEF de <10 pM.
La trifluorosustitución en el pirazol se fijó y la sustitución en el anillo fenilo se evaluó adicionalmente en ensayos enzimáticos y celulares, y se descubrió que 2-metoxi en el anillo fenilo tiene un perfil de actividad celular superior.
Como se esperaba, también se descubrió que enantiómeros enzimáticamente activos eran activos en las células. Aunque el compuesto 47, el compuesto 50 y el compuesto 51 tienen actividades enzimáticas similares, el compuesto 50 demostró una selectividad reducida contra CDK5. El compuesto 54 se eligió como una sonda debido a su excelente potencia y selectividad.
Los resultados de los ensayos de Tau, p-catenina y TCF/LEF se muestran en la tabla 4 y las figuras 14A a 14B.
Tabla 4. Resultados de los ensayos ejemplares de Tau, p-catenina y TCF/LEF.
Ensayos de perfilado
Selectividad amplia de cinoma. Un componente clave para generar una sonda útil para determinar la función de GSK3p en el SNC es la selectividad de acción en solidificación. En la figura 5 se ilustran gráficos que representan el porcentaje del cinoma que se inhibe por cada compuesto investigado. Como se muestra, CHIR99021 es de muy baja selectividad en comparación con las pirazolodihidropiridinas descritas en la presente memoria. El acierto de HTS (compuesto 1) muestra excelente selectividad funcional contra este panel de 311 cinasas, inhibiendo únicamente 5 cinasas como se describe previamente. Otros dos compuestos examinados de este modo (compuesto 22 y compuesto 54) mostraron marcas de selectividad notables, inhibiendo únicamente un 2,3 y un 2,6 del cinoma (311 cinasas) respectivamente, con potencias notablemente mejoradas analizadas en la siguiente sección.
Determinación de selectividad absoluta. Un segundo delimitador utilizado para llegar al compuesto 54 fue la selectividad absoluta en CI50 de cada compuesto contra la cinasa diana (por ejemplo, GSK3p) y la siguiente antidiana más cercana. En los tres casos anteriores (compuesto 1, compuesto 22 y compuesto 54), la elección del compuesto a perseguir llegó a estar muy clara al observar estos valores. A continuación (tabla 5) se ilustran las determinaciones de CI50 para dos de estos compuestos contra cinasas seleccionadas que se inhibieron más de un 50 % a una concentración de 10 pM.
Tabla 5. Selectividad absoluta de compuestos seleccionados.
Utilizar una medición absoluta en lugar de un perfil de selectividad general permite la conclusión de que el compuesto 54 es mucho más selectivo que el compuesto 22 (factor de selectividad de 150 en comparación con 23 contra CDK5, la cinasa inhibida por el máximo % a 10 pM). El factor de selectividad en este caso se determina comparando la CI50 del compuesto contra GSK3p, con aquella contra las otras cinasas competidoras. La cuestión de selectividad se analiza en más detalle en la sección de discusión.
Farmacocinética y d istribución cerebral del compuesto 70
Se administró una única dosis intraperitoneal de compuesto 70 (estructura mostrada en la figura 10) o CHIR99021 a ratones C57BL/6 macho a 30 mg/kg o 12,5 mg/kg, respectivamente. La farmacocinética (por ejemplo, concentración en plasma y distribución cerebral) del compuesto 70 y CHIR99021 se midió después de la dosis en diferentes puntos temporales (hasta aproximadamente 8 horas). Los resultados (mostrados en la figura 10) indican que, en comparación con el compuesto CHIR99021, el compuesto 70 mostraba un perfil farmacocinético mejorado, tal como exposición sistémica y distribución cerebral.
El compuesto 70 induce cambios m orfo lógicos en líneas celulares de AML coherentes con la diferenciación mieloide
En el día tres tras el tratamiento químico, se realizaron preparaciones de Cytospin. Se evaluaron los cambios en la morfología por tinción con Giemsa de May-Grunwald (Sigma Aldrich). Se adquirieron imágenes por microscopia óptica a 400x aumentos. Los resultados mostraron que la tinción con Giemsa de May-Grunwald de las líneas celulares de AML tres días después del tratamiento con el compuesto 70 demostraban diferenciación celular en comparación con los controles tratados con vehículo (figura 12).
El compuesto 70 induce una característica de expresión génica en líneas celulares de AML coherente con la diferenciación mieloide
Se realizó GE-HTS usando métodos previamente descritos para evaluar una característica de expresión compuesta de genes que distinguen AML del estado diferenciado de neutrófilos o monocitos (Banerji V, Frumm SM, Ross KN, Li LS, Schinzel AC, Hahn CK, Kakoza RM, Chow KT, Ross L, Alexe G, Tolliday N, Inguilizian H, Galinsky I, Stone RM, DeAngelo DJ, Roti G, Aster JC, Hahn WC, Kung AL, Stegmaier K. The intersection of genetic and chemical genomic screens identifies GSK-3alpha as a target in human acute myeloid leukemia. J Clin Invest. 2012; 122:935-947; Hahn CK, Berchuck JE, Ross k N, Kakoza RM, Clauser K, Schinzel AC, Ross L, Galinsky I, Davis TN, Silver SJ, Root DE, Stone RM, DeAngelo DJ, Carroll M, Hahn WC, Carr SA, Golub TR, Kung AL, Stegmaier K. Proteomic and genetic approaches identify Syk as an AML target. Cancer Cell. 2009; 16:281-294). Los 32 genes marcadores para diferenciación mieloide se eligieron usando los conjuntos de datos relacionados con AML de Affymetrix publicados previamente (Stegmaier K, Ross KN, Colavito SA, O'Malley S, Stockwell BR, Golub TR. Gene expression-based high-throughput screening(GE-HTS) and application to leukemia differentiation. Nat Genet. 2004; 36:257-263). Estos genes han demostrado distinguir AML de neutrófilos o monocitos con p < 0,05 por ensayo de la t y distinguir indiferenciados frente a diferenciados de HL-60 con ATRA, 12-miristato 13-acetato de forbol o 1,25-dihidroxivitamina D3 con p < 0,05 por ensayo de la t. Este ensayo usa amplificación mediada por ligamiento con un sistema de detección basado en microesferas fluorescentes para cuantificar la expresión de hasta 500 genes en un único pocillo. Se usan dos métodos de puntuación principales para cuantificar la inducción de la característica de diferenciación mieloide de 32 genes. La suma de la puntuación combina las relaciones de expresión (gen
marcador/gen de control) sumándolas con un signo determinado por la dirección esperada de regulación de los controles positivos tratados con ATRA. La suma de la puntuación ponderada combina las relaciones de expresión sumándolas con un peso y signo determinados por la relación de señal a ruido de cada relación de expresión para las muestras de control positivo (tratado con ATRA) y de control negativo (tratadas con DMSO). Para evaluar la significación estadística de las diferencias entre estas puntuaciones de diferenciación, se empleó un ANOVA unidireccional con una corrección de Bonferroni en un ensayo post-hoc. Estos resultados muestran que el compuesto 70 inducía una característica de expresión génica en líneas celulares de AML coherente con diferenciación mieloide (figura 13A y 13B).
Discusión
Partiendo del acierto de HTS, se investigó el SAR de cuatro regiones de la molécula mediante la síntesis de múltiples compuestos, la posición bencílica, el resto pirazol, el anillo fenilo y la dicetona derivados del anillo en la parte occidental de la molécula guiada por análisis de estructura cristalina (véase la figura 4). La sustitución en la posición bencílica con un grupo metilo se toleró. La oxidación del anillo central dio lugar a una pérdida en la actividad. Las modificaciones en el pirazol se toleraron, tales como sustitución con un grupo trifluorometilo. Mediante SAR del anillo fenilo, se descubrió que compuestos que tienen sustitución en la posición 2 o 3 eran particularmente activos. La sustitución con heteroaromáticos se toleró. Se descubrió que compuestos con sustitución en la posición 4 presentan alguna actividad. Se descubrió que el compuesto que tiene sustitución de trifluorometilo o metoxi en la posición 2 o 3 era particularmente activo en células. El compuesto 54 se identificó como mucho más potente que el compuesto del acierto, especialmente en ensayos celulares en que el compuesto del acierto era débilmente activo.
Globalmente, los datos apoyan la identificación de una sonda potente (por ejemplo, CI50 = 0,02 j M) (compuesto 54) que inhibe GSK3 y es selectivo contra 309 otras cinasas con selectividad mayor de 150 veces (vide infra). Se descubrió que el compuesto 54 era activo en tres ensayos celulares diferentes que presentan la capacidad del compuesto de inhibir GSK3 en diferentes contextos celulares.
Ventajas sobre los inhibidores divulgados previamente
Existen otros inhibidores de GSK3p; sin embargo, se ha descubierto que estos compuestos que se han ensayado contra otras cinasas carecen de selectividad (Leclerc, et al., J Biol Chem, 2001; 276: 251-260; Meijer, et al., Chem Biol, 2003; 10:1255-1266; Polychronopoulos, et al., J Med Chem, 2004; 47:935-946; Leost, et al., Eur J Biochem, 2000; 267:5983-5994; Chang, et al., Chem Biol, 1999; 7:51-63). Las cinasas que los compuestos inhiben más a menudo son las cinasas dependientes de ciclina (CDK), con las que GSK3 es la que está más estrechamente relacionada. Los perfiles de selectividad se compararon con los inhibidores de GSK3 existentes previamente tales como CHIR 99021 (figura 6). CHIR 99021 se ensayó en un cribado frente a >300 cinasas, que confirma que el compuesto inhibe CDK2 junto con muchas otras cinasas, incluyendo CDK5, CDK9, LIMK1, c Lk 1, PLK1, e Rk 5 a más de un 50 % a 10 j M. Una comparación de la actividad y las propiedades físicas del compuesto 54 y CHIR 99021 se muestra en la tabla 6 y una comparación de la actividad del compuesto 54 para el perfil de cinasa de CHIR 99021 se muestra en la tabla 7. Como puede observarse en las tablas siguientes, el compuesto 54 presenta potencia comparable con CHIR 99021 en todos los ensayos, mientras que presenta selectividad significativamente mayor contra el cinoma. Además, basándose en los datos microsómicos de la tabla 3, resulta prometedor desarrollar un inhibidor de GSK3 de esta clase con estabilidad microsómica y potencia, permitiendo estudios in vivo que no son posibles con CHIR 99021 debido a sus escasas propiedades físicas. En comparación con los inhibidores de GSK3 conocidos en la técnica, los compuestos descritos son más estables en los microsomas y muestran farmacocinética y/o perfiles de selectividad mejorados.
Tabla 6. Comparación de la actividad y las propiedades físicas de CHIR99021 y el compuesto 54.
Tabla 7. Comparación del perfil de cinasa de CHIR 99021 y el compuesto 54 (% de inhibición a 10 |j M).
Estudios del mecanismo de acción
El compuesto 54 demuestra características inhibidoras coherentes con ser un inhibidor competitivo de ATP. Las CI50 se midieron contra GSK3p a dos concentraciones de ATP diferentes. En comparación con una CI50 de 24 nM en ATP 7 j M, la CI50 del compuesto 54 en 100 j M de ATP aumentó hasta 143 nM, lo que sugiere inhibición competitiva de ATP.
De forma celular, la inhibición de GSK3p por compuesto 54 elimina la regulación negativa de dos rutas de señalización importantes en la dinámica de microtúbulos y la señalización de Wnt. La beta-catenina en la ruta de Wnt y la proteína Tau en la dinámica de microtúbulos se someten a fosforilación por GSK3p. GSK3p es constitutivamente activa y a menudo sirve como regulador negativo de la señalización celular. Específicamente, la inhibición de GSK3p inhibe la fosforilación de la proteína Tau, y la inhibición de la fosforilación de beta-catenina evita la degradación de b-catenina, promueve su translocación nuclear y posteriormente activa el indicador TCF/LEF. Por tanto, este compuesto y otros descritos en la presente memoria serían herramientas excelentes para investigar la ruta de Wnt, así como para sondear la dinámica de microtúbulos en células y potencialmente en animales.
Los compuestos 22 y 54 se ensayaron en ensayos celulares, incluyendo como una herramienta para sondear las rutas moleculares de GSK/Wnt in vitro mediante el uso de células progenitoras neurales humanas y de roedor para determinar su capacidad de promover la neurogénesis. Mediante el uso de células madre pluripotentes inducidascélulas progenitoras neurales (iPSC-NPC) de pacientes con trastornos neuropsiquiátricos, tal como trastorno bipolar y esquizofrenia, se exploró la cuestión de si hay diferencias en la respuesta a moduladores de GSK3. Esto permitió
la determinación de la función de la señalización de GSK3 mal regulada en las patologías subyacentes. Lo que se determinó es el efecto de la inhibición de GSK3 selectiva en células que tienen una variación genética en DISC1 para ayudar a comprender la función de la señalización de DISC1/ GSK3 en la fisiopatología de trastornos neuropsiquiátricos.
Ensayos de neurogénesis
Se generaron células neuroprogenitoras humanas y se derivaron de acuerdo con métodos conocidos en la técnica. Véase, por ejemplo, Zhao et al., J Biomol Screen. Octubre de 2012;17(9):1252-63. Se prepararon suspensiones de células individuales a partir de iPSC-NPC humanas, se integraron de forma estable con el indicador de luciferasa TCF/LEF y se distribuyeron en placas de 96 o 384 pocillos a las densidades de siembra de 20000 o 6000 por pocillo, respectivamente, usando un dispensador de microplaca Matrix WellMate (Thermo Scientific). Se usó el formato de placa de 96 pocillos para medir los efectos de respuesta a dosis de Wnt3a y litio (disolución de cloruro de litio, 10 M; Fluka, St. Louis, MO), mientras que se usó un formato de placa de 384 pocillos para todos los tratamientos con sonda de molécula pequeña y cribado químico. El siguiente día, las células se sometieron a diversos tratamientos de 24 h. Justo antes de la lectura de luminiscencia, las placas se recogieron de una incubadora a 37 °C y se equilibraron a temperatura ambiente durante 30 min antes de distribuir el reactivo SteadyGlo (Promega, Madison, WI) (volumen equitativo 1:1 SteadyGlo:medio de cultivo). La luminiscencia se midió después de una incubación de 10 min usando un lector de placa de múltiples marcadores EnVision (PerkinElmer, Waltham, MA). Los resultados ejemplares se muestran en la figura 15, que indica que el compuesto 22 promovía la neurogénesis.
Los compuestos descritos en la presente memoria también pueden ensayarse in vivo, tal como ensayando el efecto de inhibidores de GSK3 selectivos en modelos de ratón para trastornos neuropsiquiátricos, tales como el modelo de hiperactividad inducida por anfetamina (AIH) para manía y el ensayo de natación forzada y ensayos de impotencia aprendida para depresión.
Equivalentes y alcance
En las reivindicaciones, artículos tales como "un/o", "una" y "el/la" pueden indicar uno o más de uno. Las reivindicaciones o descripciones que incluyen "o" entre uno o más miembros de un grupo, se consideran satisfechas si uno, más de uno o todos los miembros del grupo están presentes en, se emplean en o son pertinentes de otro modo para un producto o proceso dado salvo que se indique lo contrario o sea evidente de otro modo a partir del contexto. La invención incluye realizaciones en que exactamente un miembro del grupo está presente en, se emplea en o es pertinente de otro modo para un producto o proceso dado. La invención incluye realizaciones en que más de uno o todos los miembros del grupo están presentes, se emplean en o son pertinentes de otro modo para un producto o proceso dado.
Esta solicitud se refiere a diversas patentes emitidas, solicitudes de patente publicadas, artículos de revista y otras publicaciones. Si hay un conflicto entre cualquiera de las referencias y la presente solicitud, prevalecerá la memoria descriptiva. Además, cualquier realización particular de la presente invención que esté dentro de la técnica anterior puede excluirse de forma explícita de una cualquiera o más de las reivindicaciones. Como se consideran que dichas realizaciones son conocidas para un experto en la materia, pueden excluirse incluso si la exclusión no se expone explícitamente en la presente memoria. Cualquier realización particular de la invención puede excluirse de cualquier reivindicación, por cualquier razón, esté relacionada o no con la existencia de técnica anterior.
Claims (26)
1. Un compuesto de fórmula I:
o una de sus sales farmacéuticamente aceptables,
en la que:
R1 y R2 se seleccionan independientemente del grupo que consiste en grupo alifático opcionalmente sustituido, arilo opcionalmente sustituido y heteroarilo opcionalmente sustituido; o R1 y R2 se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido, en el que el anillo formado por R1 y R2 está condensado opcionalmente a un anillo arilo o heteroarilo;
R3 se selecciona del grupo que consiste en hidrógeno, halo, -CN, -NO2, grupo alifático opcionalmente sustituido, fenilo opcionalmente sustituido, heterociclilo opcionalmente sustituido, heteroarilo opcionalmente sustituido, -ORA, -N(Rb)2, -SRa, -C(=O)RA, -C(=O)ORa, -C(=O)SRa, -C( O)N(Rb)2, -OC(=O)R AA -NRbC(=O)Ra, -NRbC(=O)N(R ->bB)\2, OC(=O)N(Rb)2, -NRBC(=O)ORa, -SC(=O)Ra -C(=NRb)RA, -C(=NRb)N(RB)2, -NRbC(=NRb)Rb, -C(=S)Ra, C(=S)N(RB)2, -NRbC(=S)Ra, -S(=O)Ra, -SO2Ra, NRBSO2RAy -SO2N(Rb)2;
cada Ra se selecciona independientemente del grupo que consiste en hidrógeno, grupo alifático opcionalmente sustituido, carbociclilo opcionalmente sustituido, heterociclilo opcionalmente sustituido, arilo opcionalmente sustituido y heteroarilo opcionalmente sustituido;
cada Rb se selecciona independientemente del grupo que consiste en hidrógeno, grupo alifático opcionalmente sustituido, carbociclilo opcionalmente sustituido, heterociclilo opcionalmente sustituido, arilo opcionalmente sustituido y heteroarilo opcionalmente sustituido, o dos grupos Rb se toman junto con sus átomos intermedios para formar un anillo heterocíclico opcionalmente sustituido;
R4a y R4b se seleccionan independientemente del grupo que consiste en hidrógeno, halo, -CN, -ORa, -N(Rb)2, y grupo alifático opcionalmente sustituido, o R4a y R4b se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido;
R 5a y R 5b se seleccionan independientemente del grupo que consiste en hidrógeno, halo, -CN, -OR A , -N(R B )2, y grupo alifático opcionalmente sustituido, o R5a y R5b se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido; y
R6a y R6b se seleccionan independientemente del grupo que consiste en hidrógeno, halo, -CN, -ORa, -N(Rb)2, y grupo alifático opcionalmente sustituido, o R6a y R6b se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico saturado de 3 a 7 miembros opcionalmente sustituido;
en los que cada ocasión de arilo tiene independientemente de 6 a 14 átomos de carbono en el anillo; y
en los que cada ocasión de heteroarilo es independientemente de 5 a 10 miembros, y monocíclico o bicíclico, y tiene independientemente de 1 a 4 heteroátomos en el anillo seleccionados independientemente del grupo que consiste en nitrógeno, oxígeno y azufre;
en los que los artículos "un/o", "una" y "el/la" pueden indicar uno o más de uno; y
con la condición de que el compuesto no sea de ninguna de las fórmulas:
2. El compuesto de la reivindicación 1, en el que el compuesto es de fórmula II:
o una de sus sales farmacéuticamente aceptables,
en el que en la fórmula II:
R2, R3, R5a y R5b son como se definen en la reivindicación 1;
cada R se selecciona independientemente del grupo que consiste en hidrógeno, halo, -CN,-NO2 , grupo alifático opcionalmente sustituido, fenilo opcionalmente sustituido, heterociclilo opcionalmente sustituido, heteroarilo opcionalmente sustituido, -ORA, -N(RB)2 , -SRA -C(=O)RA, -C(=O)ORA, -C(=O)SRA, -C(=O)N(RB)2, -OC(=O)RA, -NRbC(=O)Ra, -NRbC(=O)N(Rb)2, -OC(=O)N(RB)2, -NRBC(=O)ORA, -SC(=O)RA, -C(=NRb)Ra, -C(=NRb)N(Rb)2, -NRBC(=NRB)RB, -C(=S)RA, -C(=S)N(RB)2, -NRBC(=S)RA, -S(=O)RA, -SO2RA, -NRBSO2RA y -SO2N(RB)2; o dos grupos R7 adyacentes se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico, condensado opcionalmente sustituido; o R2 y R7 se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico, condensado opcionalmente sustituido; y
n es 0, 1, 2, 3, 4 o 5; o
en el que el compuesto es de fórmula NI:
o una de sus sales farmacéuticamente aceptables,
en el que en la fórmula III:
R2, R3, R5a y R5b son como se definen en la reivindicación 1;
Anillo A es heteroarilo de 5 a 6 miembros, carbociclilo de 4 a 6 miembros, o heterociclilo de 4 a 6 miembros; cada R se selecciona independientemente del grupo que consiste en hidrógeno, halo, -CN,-NO2 , grupo alifático opcionalmente sustituido, fenilo opcionalmente sustituido, heterociclilo opcionalmente sustituido, heteroarilo opcionalmente sustituido, -ORA, -N(RB)2 , -SRA, -C(=O)RA, -C(=O)ORA, -C(=O)SRA, -C(=O)N(RB)2, -OC(=O)RA, -NRBC(=O)RA, -NRBC(=O)N(RB)2, -OC(=O)N(RB)2, -NRBC(=O)ORA, -SC(=O)RA, -C(=NRb)Ra, -C(=NRb)N(Rb)2,
NRbC(=NRb)Rb, -C(=S)Ra, -C(=S)N(Rb)2, -NRbC(=S)Ra, -S(=O)RA, -SO2RA, -NRBSO2RA y -SO2N(RB)2; o dos grupos R7 adyacentes se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico, condensado opcionalmente sustituido; o R2 y R7 se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico, condensado opcionalmente sustituido; y
n es 0, 1, 2, 3 o 4, según permita la valencia.
3. El compuesto de la reivindicación 2, en el que el compuesto es de fórmula II-a:
o una de sus sales farmacéuticamente aceptables,
en el que en la fórmula II-a:
R3, R5a, R5b, R7 y n son como se definen en la reivindicación 2; y
R2 se selecciona del grupo que consiste en grupo alifático opcionalmente sustituido, arilo opcionalmente sustituido y heteroarilo opcionalmente sustituido; o R2 y R7 se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico, condensado opcionalmente sustituido; en la que arilo tiene de 6 a 14 átomos de carbono en el anillo; y en la que heteroarilo es de 5 a 10 miembros, y monocíclico o bicíclico, y tiene de 1 a 4 heteroátomos en el anillo seleccionados independientemente del grupo que consiste en nitrógeno, oxígeno y azufre;
por ejemplo, en el que el compuesto de fórmula II-a es un compuesto de fórmula II-a-/ o II-a-//:
o una de sus sales farmacéuticamente aceptables.
4. El compuesto de la reivindicación 2, en el que el compuesto de fórmula III es de fórmula III-a:
o una de sus sales farmacéuticamente aceptables,
en el que en la fórmula III-a:
Anillo A, R3, R5a, R5b, R7 y n son como se definen en la reivindicación 2; y
R2 se selecciona del grupo que consiste en grupo alifático opcionalmente sustituido, arilo opcionalmente sustituido y heteroarilo opcionalmente sustituido; o R2 y R7 se toman junto con sus átomos intermedios para formar un anillo carbocíclico o heterocíclico condensado opcionalmente sustituido;
en el que arilo tiene de 6 a 14 átomos de carbono en el anillo; y en el que heteroarilo es de 5 a 10 miembros, y monocíclico o bicíclico, y tiene de 1 a 4 heteroátomos en el anillo seleccionados independientemente del grupo que consiste en nitrógeno, oxígeno y azufre;
por ejemplo, en el que el compuesto de fórmula IlI-a es un compuesto de fórmula III-a-/ o Ml-a-//:
o una de sus sales farmacéuticamente aceptables.
5. El compuesto de una cualquiera de las reivindicaciones 1-4 o una de sus sales farmacéuticamente aceptables, en el que R3 es hidrógeno o flúor.
6. El compuesto de una cualquiera de las reivindicaciones 1-4 o una de sus sales farmacéuticamente aceptables, en el que R3 es grupo alifático opcionalmente sustituido.
7. El compuesto de la reivindicación 6 o una de sus sales farmacéuticamente aceptables, en el que R3 es metilo; o en el que R3 es trifluorometilo.
8. El compuesto de la reivindicación 6 o una de sus sales farmacéuticamente aceptables, en el que R3 es etilo, npropilo, isopropilo o ferc-butilo.
9. El compuesto de una cualquiera de las reivindicaciones 1-8 o una de sus sales farmacéuticamente aceptables, en el que R2 o R2 es grupo alifático opcionalmente sustituido.
10. El compuesto de la reivindicación 9 o una de sus sales farmacéuticamente aceptables, en el que R2 o R2 es metilo.
11. El compuesto de la reivindicación 9 o una de sus sales farmacéuticamente aceptables, en el que R2 o R2 es etilo o propilo.
12. El compuesto de una cualquiera de las reivindicaciones 1-11 o una de sus sales farmacéuticamente aceptables, en el que R5a y R5b son metilo.
16. Una composición que comprende uno o más compuestos de una cualquiera de las reivindicaciones 1-14, o una o más de sus sales farmacéuticamente aceptables, y uno o más excipientes farmacéuticamente aceptables.
17. Un compuesto de acuerdo con una cualquiera de las reivindicaciones 1 a 14, o su sal farmacéuticamente aceptable, o una composición de acuerdo con la reivindicación 16 para su uso en la inhibición de la glucógeno sintasa cinasa 3 (GSK3) o caseína cinasa 1 (CK1), preferiblemente en el que la GSK3 está en una célula; o preferiblemente en el que la CK1 está en una célula; o preferiblemente en el que la CK1 es CK18.
18. Un compuesto de acuerdo con una cualquiera de las reivindicaciones 1 a 14, o su sal farmacéuticamente aceptable, o una composición de acuerdo con la reivindicación 16 para su uso en el tratamiento de un trastorno mediado por la glucógeno sintasa cinasa 3 (GSK3) o un trastorno mediado por la caseína cinasa 1 (CK1).
19. El compuesto para su uso, sal farmacéuticamente aceptable para su uso, o composición para su uso de acuerdo con la reivindicación 17 o 18, en el que la GSK3 es glucógeno sintasa cinasa 3a (GSK3a).
20. El compuesto para su uso, sal farmacéuticamente aceptable para su uso, o composición para su uso de acuerdo con la reivindicación 17 o 18, en el que la GSK3 es glucógeno sintasa cinasa 3p (GSK3p).
21. El compuesto para su uso, sal farmacéuticamente aceptable para su uso, o composición para su uso de acuerdo con la reivindicación 18, en el que el trastorno mediado por GSK3 es:
- un trastorno mediado por la glucógeno sintasa cinasa 3p (GSK3p); o
- una enfermedad neurológica, por ejemplo, una enfermedad neurodegenerativa, tal como lesión cerebral traumática, enfermedad de Parkinson, enfermedad de Huntington, enfermedad de Alzheimer, demencia frontotemporal, esclerosis lateral amiotrófica (ALS), parálisis supranuclear progresiva o degeneración corticobasal; o
- un trastorno psiquiátrico; por ejemplo, trastorno bipolar, esquizofrenia, depresión o trastorno de estrés postraumático; o
- un trastorno del estado de ánimo; o
- diabetes de tipo II.
22. El compuesto para su uso, sal farmacéuticamente aceptable para su uso, o composición para su uso de acuerdo con la reivindicación 18, en el que el trastorno mediado por GSK3 es:
- un trastorno mediado por la glucógeno sintasa cinasa 3a (GSK3a); o
- un trastorno psiquiátrico; por ejemplo, autismo o síndrome del X frágil; o
- cáncer; o
- leucemia; o
- leucemia mieloide aguda; o
- glioma o cáncer pancreático; o
- diabetes de tipo II;
o en el que la CK1 es CK15, preferiblemente en el que el trastorno mediado por CK15 es trastorno por déficit de atención con hiperactividad (ADHD).
23. El compuesto para su uso, sal farmacéuticamente aceptable para su uso, o composición para su uso de acuerdo con la reivindicación 18, en el que el trastorno mediado por GSK3 es leucemia linfocítica aguda, leucemia mielocítica crónica, leucemia linfocítica crónica o mieloma múltiple.
24. Una composición que comprende al menos un compuesto de la reivindicación 15, o al menos una de sus sales farmacéuticamente aceptables, y al menos un excipiente farmacéuticamente aceptable.
25. Un compuesto de acuerdo con la reivindicación 15, o su sal farmacéuticamente aceptable, o una composición de acuerdo con la reivindicación 24 para su uso en el tratamiento de un trastorno mediado por la glucógeno sintasa cinasa 3 (GSK3) o un trastorno mediado por la caseína cinasa 1 (CK1).
26. El compuesto para su uso, sal farmacéuticamente aceptable para su uso, o composición para su uso de acuerdo con la reivindicación 25, en el que:
la GSK3 es glucógeno sintasa cinasa 3a (GSK3a); o
la GSK3 es glucógeno sintasa cinasa 3p (GSK3p); o
el trastorno mediado por GSK3 es:
- un trastorno mediado por la glucógeno sintasa cinasa 3p (GSK3p); o
- una enfermedad neurológica, por ejemplo, una enfermedad neurodegenerativa, tal como lesión cerebral traumática, enfermedad de Parkinson, enfermedad de Huntington, enfermedad de Alzheimer, demencia frontotemporal, esclerosis lateral amiotrófica (ALS), parálisis supranuclear progresiva o degeneración corticobasal; o
- un trastorno psiquiátrico; por ejemplo, trastorno bipolar, esquizofrenia, depresión, trastorno de estrés postraumático, autismo o síndrome del X frágil; o
- un trastorno del estado de ánimo; o
- diabetes de tipo II; o
- un trastorno mediado por la glucógeno sintasa cinasa 3a (GSK3a); o
- cáncer; o
- leucemia; o
- leucemia mieloide aguda; o
- glioma o cáncer pancreático; o
- leucemia linfocítica aguda, leucemia mielocítica crónica, leucemia linfocítica crónica o mieloma múltiple; o la CK1 es CK15, preferiblemente en el que el trastorno mediado por CK15 es trastorno por déficit de atención con hiperactividad (ADHD).
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201261713314P | 2012-10-12 | 2012-10-12 | |
| US201361779394P | 2013-03-13 | 2013-03-13 | |
| PCT/US2013/064716 WO2014059383A1 (en) | 2012-10-12 | 2013-10-11 | Gsk3 inhibitors and methods of use thereof |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2719776T3 true ES2719776T3 (es) | 2019-07-16 |
Family
ID=49474737
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES13780300T Active ES2719776T3 (es) | 2012-10-12 | 2013-10-11 | Inhibidores de GSK3 y métodos de uso de los mismos |
Country Status (15)
| Country | Link |
|---|---|
| US (4) | US9096594B2 (es) |
| EP (1) | EP2909204B1 (es) |
| JP (2) | JP6321662B2 (es) |
| CA (1) | CA2887701C (es) |
| CY (1) | CY1122601T1 (es) |
| DK (1) | DK2909204T3 (es) |
| ES (1) | ES2719776T3 (es) |
| HR (1) | HRP20190406T1 (es) |
| HU (1) | HUE043853T2 (es) |
| LT (1) | LT2909204T (es) |
| PL (1) | PL2909204T3 (es) |
| PT (1) | PT2909204T (es) |
| RS (1) | RS58700B1 (es) |
| SI (1) | SI2909204T1 (es) |
| WO (1) | WO2014059383A1 (es) |
Families Citing this family (21)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ES2719776T3 (es) | 2012-10-12 | 2019-07-16 | Broad Inst Inc | Inhibidores de GSK3 y métodos de uso de los mismos |
| PT3702443T (pt) | 2013-03-14 | 2022-02-17 | Massachusetts Inst Technology | Composições e métodos para expansão e cultura de células estaminais epiteliais |
| WO2016007540A2 (en) | 2014-07-10 | 2016-01-14 | The J. David Gladstone Institutes | Compositions and methods for treating dengue virus infection |
| US10568883B2 (en) | 2014-09-03 | 2020-02-25 | Massachusetts Institute Of Technology | Compositions, systems, and methods for generating inner ear hair cells for treatment of hearing loss |
| WO2016061344A1 (en) * | 2014-10-15 | 2016-04-21 | Mirx Pharmaceuticals Llc | Gsk3 inhibitors and their uses |
| EP3400286A1 (en) | 2016-01-08 | 2018-11-14 | Massachusetts Institute Of Technology | Production of differentiated enteroendocrine cells and insulin producing cells |
| US10201540B2 (en) | 2016-03-02 | 2019-02-12 | Frequency Therapeutics, Inc. | Solubilized compositions for controlled proliferation of stem cells / generating inner ear hair cells using GSK3 inhibitors: I |
| US11260130B2 (en) | 2016-03-02 | 2022-03-01 | Frequency Therapeutics, Inc. | Solubilized compositions for controlled proliferation of stem cells / generating inner ear hair cells using a GSK3 inhibitor: IV |
| US10213511B2 (en) | 2016-03-02 | 2019-02-26 | Frequency Therapeutics, Inc. | Thermoreversible compositions for administration of therapeutic agents |
| AU2017386417B2 (en) | 2016-12-30 | 2022-07-14 | Frequency Therapeutics, Inc. | 1H-pyrrole-2,5-dione compounds and methods of using them to induce self-renewal of stem/progenitor supporting cells |
| CN110958882B (zh) * | 2017-04-05 | 2023-08-29 | 布罗德研究所股份有限公司 | 作为糖原合酶激酶3(gsk3)抑制剂的三环化合物及其用途 |
| WO2018217766A1 (en) * | 2017-05-22 | 2018-11-29 | Whitehead Institute For Biomedical Research | Kcc2 expression enhancing compounds and uses thereof |
| CN110407769B (zh) * | 2018-04-27 | 2022-11-08 | 复旦大学 | 3,4-二氢-苯并[f][1,4]硫氮杂䓬-5(2H)-酮类化合物及其药物用途 |
| EP3801768A4 (en) | 2018-06-05 | 2022-04-20 | Actuate Therapeutics Inc. | METHODS OF TREATING MALIGNANT HYPERPROLIFERATIVE DISORDERS |
| US20210299233A1 (en) * | 2018-07-12 | 2021-09-30 | The Children's Medical Center Corporation | Method for treating cancer |
| EP3837352A1 (en) | 2018-08-17 | 2021-06-23 | Frequency Therapeutics, Inc. | Compositions and methods for generating hair cells by upregulating jag-1 |
| EP3837351A1 (en) | 2018-08-17 | 2021-06-23 | Frequency Therapeutics, Inc. | Compositions and methods for generating hair cells by downregulating foxo |
| JP2022520671A (ja) | 2019-02-08 | 2022-03-31 | フリークエンシー・セラピューティクス・インコーポレイテッド | 耳障害を治療するためのバルプロ酸化合物及びwnt作動薬 |
| US20230014430A1 (en) * | 2019-11-20 | 2023-01-19 | Washington University | Methods and Compositions for Generating Functionally Mature Beta Cells and Uses Thereof |
| WO2023056463A1 (en) * | 2021-09-30 | 2023-04-06 | Trustees Of Tufts College | Glycogen synthase kinase 3 (gsk3) inhibitors for treating ctnnb1 syndrome |
| WO2024081939A2 (en) * | 2022-10-13 | 2024-04-18 | The Broad Institute, Inc. | Glycogen synthase kinase 3 inhibitors and uses thereof |
Family Cites Families (52)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE2722416A1 (de) | 1977-05-18 | 1978-11-30 | Thomae Gmbh Dr K | Neue thiazolo-pyridine |
| US4270537A (en) | 1979-11-19 | 1981-06-02 | Romaine Richard A | Automatic hypodermic syringe |
| US4596556A (en) | 1985-03-25 | 1986-06-24 | Bioject, Inc. | Hypodermic injection apparatus |
| US4886499A (en) | 1986-12-18 | 1989-12-12 | Hoffmann-La Roche Inc. | Portable injection appliance |
| GB8704027D0 (en) | 1987-02-20 | 1987-03-25 | Owen Mumford Ltd | Syringe needle combination |
| US4790824A (en) | 1987-06-19 | 1988-12-13 | Bioject, Inc. | Non-invasive hypodermic injection device |
| US4941880A (en) | 1987-06-19 | 1990-07-17 | Bioject, Inc. | Pre-filled ampule and non-invasive hypodermic injection device assembly |
| US4940460A (en) | 1987-06-19 | 1990-07-10 | Bioject, Inc. | Patient-fillable and non-invasive hypodermic injection device assembly |
| US5339163A (en) | 1988-03-16 | 1994-08-16 | Canon Kabushiki Kaisha | Automatic exposure control device using plural image plane detection areas |
| FR2638359A1 (fr) | 1988-11-03 | 1990-05-04 | Tino Dalto | Guide de seringue avec reglage de la profondeur de penetration de l'aiguille dans la peau |
| US5312335A (en) | 1989-11-09 | 1994-05-17 | Bioject Inc. | Needleless hypodermic injection device |
| US5064413A (en) | 1989-11-09 | 1991-11-12 | Bioject, Inc. | Needleless hypodermic injection device |
| US5190521A (en) | 1990-08-22 | 1993-03-02 | Tecnol Medical Products, Inc. | Apparatus and method for raising a skin wheal and anesthetizing skin |
| US5527288A (en) | 1990-12-13 | 1996-06-18 | Elan Medical Technologies Limited | Intradermal drug delivery device and method for intradermal delivery of drugs |
| GB9118204D0 (en) | 1991-08-23 | 1991-10-09 | Weston Terence E | Needle-less injector |
| SE9102652D0 (sv) | 1991-09-13 | 1991-09-13 | Kabi Pharmacia Ab | Injection needle arrangement |
| JPH05157164A (ja) | 1991-12-03 | 1993-06-22 | Aisin Aw Co Ltd | 車両用自動変速機のサーボ油圧制御装置 |
| US5328483A (en) | 1992-02-27 | 1994-07-12 | Jacoby Richard M | Intradermal injection device with medication and needle guard |
| US5383851A (en) | 1992-07-24 | 1995-01-24 | Bioject Inc. | Needleless hypodermic injection device |
| US5569189A (en) | 1992-09-28 | 1996-10-29 | Equidyne Systems, Inc. | hypodermic jet injector |
| US5334144A (en) | 1992-10-30 | 1994-08-02 | Becton, Dickinson And Company | Single use disposable needleless injector |
| CZ251995A3 (en) | 1993-04-08 | 1996-01-17 | Du Pont Merck Pharma | Disubstituted polycyclic compounds and their derivatives per se and for therapy as well as pharmaceutical compositions based thereon |
| WO1995024176A1 (en) | 1994-03-07 | 1995-09-14 | Bioject, Inc. | Ampule filling device |
| US5466220A (en) | 1994-03-08 | 1995-11-14 | Bioject, Inc. | Drug vial mixing and transfer device |
| US5599302A (en) | 1995-01-09 | 1997-02-04 | Medi-Ject Corporation | Medical injection system and method, gas spring thereof and launching device using gas spring |
| US5750528A (en) | 1995-02-01 | 1998-05-12 | The Dupont Merck Pharmaceutical Company | Blockade of neuronal m-channels as a therapeutic approach to the treatment of neurological disease |
| US5730723A (en) | 1995-10-10 | 1998-03-24 | Visionary Medical Products Corporation, Inc. | Gas pressured needle-less injection device and method |
| US5893397A (en) | 1996-01-12 | 1999-04-13 | Bioject Inc. | Medication vial/syringe liquid-transfer apparatus |
| GB9607549D0 (en) | 1996-04-11 | 1996-06-12 | Weston Medical Ltd | Spring-powered dispensing device |
| US5993412A (en) | 1997-05-19 | 1999-11-30 | Bioject, Inc. | Injection apparatus |
| IT1298087B1 (it) | 1998-01-08 | 1999-12-20 | Fiderm S R L | Dispositivo per il controllo della profondita' di penetrazione di un ago, in particolare applicabile ad una siringa per iniezioni |
| TW526202B (en) | 1998-11-27 | 2003-04-01 | Shionogi & Amp Co | Broad spectrum cephem having benzo[4,5-b]pyridium methyl group of antibiotic activity |
| US6977262B2 (en) | 2001-02-02 | 2005-12-20 | Mitsubishi Pharma Corporation | Dihydropyrazolopyridine compounds and pharmaceutical use thereof |
| JP2005501800A (ja) * | 2001-02-02 | 2005-01-20 | 三菱ウェルファーマ株式会社 | ジヒドロピラゾロピリジン化合物およびその医薬用途 |
| DE10121217A1 (de) | 2001-04-30 | 2002-10-31 | Merck Patent Gmbh | 6H-Oxazolo[4,5-e]indol-Derivate als nikotinische Acetylcholinrezeptor Liganden und/oder serotonerge Liganden |
| EP1395257A1 (en) | 2001-06-12 | 2004-03-10 | Elan Pharmaceuticals, Inc. | Macrocycles useful in the treatment of alzheimer's disease |
| KR20060070486A (ko) * | 2003-06-13 | 2006-06-23 | 젠타리스 게엠베하 | 포스파티딜이노시톨 3-키나제의 억제 활성을 갖는 화합물및 이의 사용 방법 |
| ES2339676T3 (es) * | 2005-07-20 | 2010-05-24 | Aventis Pharma S.A. | Heterociclicos condensados con 1,4-dihidropiridina, procedimiento par a prepararlos, uso y composiciones que los contienen. |
| US8492378B2 (en) | 2006-08-03 | 2013-07-23 | Takeda Pharmaceutical Company Limited | GSK-3β inhibitor |
| US8778986B1 (en) | 2007-01-25 | 2014-07-15 | University Of South Florida | Treatment of glycogen synthase kinase-based disease |
| US20090181986A1 (en) | 2007-07-05 | 2009-07-16 | Matthew Abelman | Substituted heterocyclic compounds |
| WO2010098888A1 (en) | 2009-02-27 | 2010-09-02 | Massachusetts Institute Of Technology | Uses of chemicals to modulate gsk-3 signaling for treatment of bipolar disorder and other brain disorders |
| FR2945535B1 (fr) * | 2009-05-18 | 2011-06-10 | Sanofi Aventis | Compose anticancereux et composition pharmaceutique le contenant |
| DE102011106990B3 (de) | 2011-07-08 | 2013-01-03 | Technische Universität Darmstadt | Verbindungen als Glykogen Synthase Kinase 3 (GSK-3) Inhibitoren für die Behandlung von GSK-3-vermittelten Erkrankungen |
| TW201406758A (zh) | 2012-06-28 | 2014-02-16 | Daiichi Sankyo Co Ltd | 三環性化合物 |
| US20160375006A1 (en) | 2012-10-12 | 2016-12-29 | The Broad Institute, Inc. | Uses of paralog-selective inhibitors of gsk3 kinases |
| ES2719776T3 (es) * | 2012-10-12 | 2019-07-16 | Broad Inst Inc | Inhibidores de GSK3 y métodos de uso de los mismos |
| JP2014139870A (ja) * | 2013-01-21 | 2014-07-31 | Hitachi Consumer Electronics Co Ltd | 照明装置およびこれを用いた映像表示装置 |
| WO2015087996A1 (ja) | 2013-12-13 | 2015-06-18 | 第一三共株式会社 | イミダゾピリジン誘導体 |
| KR101602559B1 (ko) | 2014-04-29 | 2016-03-10 | 경북대학교 산학협력단 | 2,5,6,7-사중치환 티아졸로[4,5-b]피리딘 유도체 및 이의 용도 |
| US10437707B2 (en) * | 2015-03-19 | 2019-10-08 | Teachers Insurance And Annuity Association Of America | Evaluating and presenting software testing project status indicators |
| CN110958882B (zh) | 2017-04-05 | 2023-08-29 | 布罗德研究所股份有限公司 | 作为糖原合酶激酶3(gsk3)抑制剂的三环化合物及其用途 |
-
2013
- 2013-10-11 ES ES13780300T patent/ES2719776T3/es active Active
- 2013-10-11 JP JP2015536972A patent/JP6321662B2/ja active Active
- 2013-10-11 SI SI201331368T patent/SI2909204T1/sl unknown
- 2013-10-11 PL PL13780300T patent/PL2909204T3/pl unknown
- 2013-10-11 PT PT13780300T patent/PT2909204T/pt unknown
- 2013-10-11 LT LTEP13780300.3T patent/LT2909204T/lt unknown
- 2013-10-11 CA CA2887701A patent/CA2887701C/en active Active
- 2013-10-11 DK DK13780300.3T patent/DK2909204T3/en active
- 2013-10-11 WO PCT/US2013/064716 patent/WO2014059383A1/en active Application Filing
- 2013-10-11 HU HUE13780300A patent/HUE043853T2/hu unknown
- 2013-10-11 EP EP13780300.3A patent/EP2909204B1/en active Active
- 2013-10-11 US US14/052,661 patent/US9096594B2/en active Active
- 2013-10-11 RS RS20190292A patent/RS58700B1/sr unknown
-
2015
- 2015-07-14 US US14/799,281 patent/US10137122B2/en active Active
-
2018
- 2018-04-05 JP JP2018072831A patent/JP6606691B2/ja active Active
- 2018-11-21 US US16/198,589 patent/US11052080B2/en active Active
-
2019
- 2019-03-01 HR HRP20190406TT patent/HRP20190406T1/hr unknown
- 2019-03-05 CY CY20191100268T patent/CY1122601T1/el unknown
-
2021
- 2021-06-10 US US17/344,830 patent/US20220160702A1/en active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| PL2909204T3 (pl) | 2019-07-31 |
| PT2909204T (pt) | 2019-03-21 |
| HRP20190406T1 (hr) | 2019-05-31 |
| JP2018150302A (ja) | 2018-09-27 |
| US11052080B2 (en) | 2021-07-06 |
| US20140107141A1 (en) | 2014-04-17 |
| RS58700B1 (sr) | 2019-06-28 |
| US9096594B2 (en) | 2015-08-04 |
| JP2015536307A (ja) | 2015-12-21 |
| WO2014059383A1 (en) | 2014-04-17 |
| SI2909204T1 (sl) | 2019-06-28 |
| CA2887701A1 (en) | 2014-04-17 |
| EP2909204A1 (en) | 2015-08-26 |
| EP2909204B1 (en) | 2018-12-05 |
| LT2909204T (lt) | 2019-05-10 |
| US20220160702A1 (en) | 2022-05-26 |
| JP6321662B2 (ja) | 2018-05-09 |
| US10137122B2 (en) | 2018-11-27 |
| CA2887701C (en) | 2020-12-15 |
| US20190175584A1 (en) | 2019-06-13 |
| CY1122601T1 (el) | 2021-03-12 |
| JP6606691B2 (ja) | 2019-11-20 |
| DK2909204T3 (en) | 2019-04-01 |
| US20200061050A9 (en) | 2020-02-27 |
| US20150313890A1 (en) | 2015-11-05 |
| HUE043853T2 (hu) | 2019-09-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2719776T3 (es) | Inhibidores de GSK3 y métodos de uso de los mismos | |
| JP7200282B2 (ja) | サイクリン依存性キナーゼの阻害剤 | |
| CN104350055B (zh) | 作为mnk1和mnk2调节剂的二环杂芳基衍生物及其用途 | |
| US20160375006A1 (en) | Uses of paralog-selective inhibitors of gsk3 kinases | |
| KR20160111520A (ko) | 디히드로프테리디논 유도체 및 그의 용도 | |
| KR20190075043A (ko) | 비시클릭 우레아 키나제 억제제 및 그의 용도 | |
| JP2016505597A (ja) | Prmt5阻害剤およびその使用 | |
| JP2018522866A (ja) | 4,6−ピリミジニレン誘導体およびこれらの使用 | |
| WO2015108490A2 (en) | Heteroaryl alkyne derivatives and uses thereof | |
| JP2018522867A (ja) | 縮合二環式ピリミジン誘導体およびこれらの使用 | |
| KR20180051576A (ko) | 아세트아미드 티에노트리아졸로디아제핀 및 그의 용도 | |
| US20220112216A1 (en) | Tricyclic compounds as glycogen synthase kinase 3 (gsk3) inhibitors and uses thereof | |
| KR20180049058A (ko) | 시아노 티에노트리아졸로디아제핀 및 그의 용도 | |
| KR20140105598A (ko) | [1,2,4]트리아졸로피리딘 및 포스포디에스테라제 억제제로서의 이의 용도 |