CN1284064A - 作为环加氧酶-2抑制剂的2,3-取代的吲哚化合物 - Google Patents
作为环加氧酶-2抑制剂的2,3-取代的吲哚化合物 Download PDFInfo
- Publication number
- CN1284064A CN1284064A CN98813530A CN98813530A CN1284064A CN 1284064 A CN1284064 A CN 1284064A CN 98813530 A CN98813530 A CN 98813530A CN 98813530 A CN98813530 A CN 98813530A CN 1284064 A CN1284064 A CN 1284064A
- Authority
- CN
- China
- Prior art keywords
- indol
- chloro
- acetic acid
- carbonyl
- alkyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/06—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/04—Centrally acting analgesics, e.g. opioids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/02—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom condensed with one carbocyclic ring
- C07D209/04—Indoles; Hydrogenated indoles
- C07D209/10—Indoles; Hydrogenated indoles with substituted hydrocarbon radicals attached to carbon atoms of the hetero ring
- C07D209/18—Radicals substituted by carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/10—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/06—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/06—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/10—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings
- C07D409/06—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings
- C07D409/10—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/06—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/06—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/10—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a carbon chain containing aromatic rings
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Life Sciences & Earth Sciences (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Pain & Pain Management (AREA)
- Rheumatology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Immunology (AREA)
- Physical Education & Sports Medicine (AREA)
- Biomedical Technology (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
- Indole Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
Abstract
本发明提供一种式(Ⅰ)的化合物或其药学上可接受的盐,其中Z为OH、C1-6烷氧基、-NR2R3或杂环;Q选自下列基团:(a)任选取代的苯基,(b)任选取代的含有1、2、3或4个N的6-员单环芳基,(c)任选取代的含有一个选自O、S和N的杂原子并且除所说的杂原子外还任选地含有1、2或3个N的5-员单环芳基,(d)任选取代的C3-7环烷基,和(e)任选取代的苯并稠合的杂环;R1为H、C1-4烷基或卤素;R2和R3独立地为H、OH、C1-4烷氧基、C1-4烷基或者是被卤素、OH、C1-4烷氧基或CN取代的C1-4烷基;X独立地选自H、卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-C4烷硫基、NO2、NH2、二(C1-4烷基)氨基和CN;而n为0、1、2、3和4。本发明还提供一种可用于治疗与前列腺素(作为病原)关联的医学病症的药物组合物。
Description
技术领域
本发明涉及新的2,3-取代的吲哚药物。本发明具体地涉及用于治疗或减轻疼痛和炎症及其它与炎症有关的疾病(如关节炎)的化合物、组合物及其方法。
背景技术
非甾族消炎药(NSAID)因为有止痛和消炎活性而广泛地用于治疗疼痛和关节炎的症状。公认通常的NSAID的作用是阻断环加氧酶(COX)(也已知作为前列腺素G/H合成酶(PGHS),即把二十碳四烯酸转变为前列腺素类的酶)的活性。前列腺素特别是前列腺素E2(PGE2)作为在炎症条件下检测到的主要的类二十烷酸,是疼痛、发烧和其它与炎症有关的症状的介体。抑制前列腺素的生物合成一直是发现消炎药物的治疗目标。然而,由于与药物有关的副作用包括危及生命的溃疡和肾毒性,常规NSAID的治疗用途是有限的。NSAID的替代品是使用皮质类固醇,然而,长期治疗也会产生严重的副作用。
最近,鉴定了两种COX,一种是结构性同工型(COX-1),一种是诱导性同工型(COX-2),它的表达在发炎部位是正调节的(Vane,J.R.、Mitchell,J.A.、Appleton,I.、Tomlinson,A.、Bishop-Bailey,D.、Croxtoll,J.、Willoughby,D.A.Proc.Natl.Acad.Sci.USA,1994,91,2046)。COX-1被认为发挥一定的生理作用并负责胃肠和肾保护。另一方面,COX-2似乎发挥着致病作用,并且是炎症条件下存在的主要同工型。前列腺素的致病作用与多种人类病症包括类风湿和骨关节炎、发热、哮喘、骨吸收、心血管疾病、肾毒症、动脉粥样硬化、高血压、休克、疼痛、癌症和早老性痴呆症有关。当前市场上的NSAIDs同时抑制两种COX同工型,任选变化很少,这就解释了它们的好的作用(抑制COX-2)和坏的作用(抑制COX-1)。相信能通过干涉可诱导酶环加氧酶-2的诱导期和/或通过干涉对二十碳四烯酸发生作用的酶环加氧酶-2的活性,能够任选地抑制前列腺素的生物合成的化合物将提供一种除使用NSAID和皮质类固醇之外的另一种治疗方法,其中这些化合物将发挥消炎作用,没有与抑制COX-1有关的副作用。
有多种吲哚化合物是已知的并且已经在几个专利申请中公开了。国际专利申请号WO96/32379中公开了N-取代的吲哚化合物作为cGMP-PDE抑制剂。国际专利申请号WO96/37467、WO96/37469、英国专利公开号GB2283745A和US5510368公开了2-甲基-N-取代的吲哚化合物作为环加氧酶-2抑制剂。Konya,Kazumi等人在欧洲专利公开号0556949A2中还公开了多种吲哚化合物作为控制水下发霉微生物的试剂。具体地,国际专利公开号WO97/09308中公开了吲哚化合物作为神经肽拮抗剂。另外,在Sci.Pharm.64,577(1996)中公开了一种制备2-酯取代的吲哚的方法。
本发明的简要公开
本发明提供一种下式的化合物:或其药学上可接受的盐,其中Z为OH、C1-6烷氧基、-NR2R3或一种式(II)或(III)的基团:其中r为1、2、3或4,Y是一条直接键、O、S或NR4,而W是OH或-NR2R3;Q选自下列基团:
(a)任选地被1、2或3个独立地选自下列基团的取代基取代的苯基:
(a-1)卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基,
(a-2)芳基或-O-(CH2)n-芳基,而该芳基或芳基部分任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代,
(a-3)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的5-员单环芳基,
(a-4)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的6-员单环芳基,
(b)含有1、2、3或4个N的6-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述基团(a-1)、(a-2)、(a-3)或(a-4)的取代基取代;
(c)含有一个选自O、S和N的杂原子并且除所说的杂原子外还任选地含有1、2或3个N的5-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(d)任选地被1或2个独立地选自OH、C1-4烷基、卤素和卤素取代的C1-4烷基的取代基取代的C3-7环烷基;和
(e)任选地被1、2或3个独立地选自上述(a-1)的基团的取代基取代的苯并稠合的杂环;R1为H、C1-4烷基或卤素;R2和R3独立地为H、OH、C1-4烷氧基、C1-4烷基或者是被卤素、OH、C1-4烷氧基、NH2或CN取代的C1-4烷基;R4为H或C1-4烷基;X独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-C4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基;而n为0、1、2、3或4。
本发明的吲哚化合物能抑制COX的活性。本发明的优选化合物具有抑制COX-2的活性,更优选具有COX-2选择性的化合物。
因此,本发明还提供一种可用于治疗其中前列腺素作为病原的医学病症的药物组合物,包括一种式(I)的化合物和其药学上可接受的盐。
本发明还提供一种治疗哺乳动物受治者中前列腺素作为病原的医学病症的方法,包括给所说的受治者给药治疗有效量的所说的药物组合物。
其中前列腺素作为病原的医学病症包括减轻疼痛、包括风湿性发烧在内的发烧和多种炎症、与流行性感冒或其它病毒性感染有关的症状、感冒、下背和颈痛、痛经、头痛、牙痛、扭伤和劳损、肌炎、神经痛、滑膜炎、关节炎包括风湿性关节炎、退化性关节病(骨关节炎)痛风、关节强硬、脊椎炎、全身性肿块红斑狼疮和青少年关节炎、滑囊炎、烧伤、外科和牙科手术后产生的伤。
本发明的化合物和药物组合物可以抑制细胞致瘤性转化和转移性肿瘤的生长,因此可用于治疗和/或预防结肠、乳腺、皮肤、食道、胃、膀胱、肺和肝脏中的癌。本发明的化合物和药物组合物用于治疗和/或预防环加氧酶介导的增生病例如发生在糖尿病性视网膜病和肿瘤血管生成中的增生病。
本发明的化合物和药物组合物通过防止收缩性前列腺素类的合成而抑制前列腺素诱导的平滑肌收缩,因此可用于治疗痛经、早产、哮喘和与嗜酸性细胞有关的疾病以及用于治疗神经变性疾病例如早老性痴呆症和帕金森氏病,用于治疗骨损失病(骨关节炎)、中风、癫痫发作、偏头痛、多发性硬化、艾滋病和脑病。
就COX-2的活性和/或对COX-2相对于COX-1的特异性来说,这些化合物将证明可替代常规的NSAID特别是当该NSAID是禁忌的时,例如有溃疡(例如消化性溃疡和胃溃疡)、胃炎、局部性肠炎、溃疡性结肠炎、憩室炎或有GI损伤、GI出血、包括贫血例如低凝血酶原血症、血友病和其它出血问题在内的凝结病的复发史、肾病的病人;给药抗凝血剂的外科手术前。
(a)任选地被1、2或3个独立地选自下列基团的取代基取代的苯基:
(a-1)卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基,
(a-2)芳基或-O-(CH2)n-芳基,且该芳基或芳基部分任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代,
(a-3)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的5-员单环芳基,
(a-4)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的6-员单环芳基,
(b)含有1、2、3或4个N的6-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(c)含有一个选自O、S和N的杂原子并且除所说的杂原子外还任选地含有1、2或3个N的5-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(d)任选地被1或2个独立地选自OH、C1-4烷基、卤素和卤素取代的C1-4烷基的取代基取代的C3-7环烷基;和
(e)任选地被1、2或3个独立地选自上述(a-1)的基团的取代基取代的苯并稠合的杂环;R2和R3独立地为H、OH、C1-4烷氧基、C1-4烷基或者是被卤素、OH、C1-4烷氧基、NH2或CN取代的C1-4烷基;X独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-C4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基;R5是C1-6烷基;而n为0、1、2、3和4。
本发明还提供一种式7-V的化合物:其中B为一种合适的保护基;Q选自下列基团:
(a)任选地被1、2或3个独立地选自下列基团的取代基取代的苯基:
(a-1)卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基,
(a-2)芳基或-O-(CH2)n-芳基,且该芳基或芳基部分任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代,
(a-3)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的5-员单环芳基,
(a-4)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的6-员单环芳基,
(b)含有1、2、3或4个N的6-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(c)含有一个选自O、S和N的杂原子并且除所说的杂原子外还任选地含有1、2或3个N的5-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(d)任选地被1或2个独立地选自OH、C1-4烷基、卤素和卤素取代的C1-4烷基的取代基取代的C3-7环烷基;和
(e)任选地被1、2或3个独立地选自上述(a-1)的基团的取代基取代的苯并稠合的杂环;R2和R3独立地为H、OH、C1-4烷氧基、C1-4烷基或者是被卤素、OH、C1-4烷氧基、NH2或CN取代的C1-4烷基;X独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-C4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基;R5是C1-C6烷基;而n为0、1、2、3或4。
本发明的详细公开
这里所用的“卤素”是氟、氯、溴或碘。
这里所用的术语“C1-4烷基”是指含有1-4个碳原子的直链或支链饱和基,包括但是不限于甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基等。
这里所用的“丙基”的例子为正丙基和异丙基。
这里所用的“丁基”的例子为正丁基、异丁基、仲丁基和叔丁基。
这里所用的“烷氧基”的例子为甲氧基、乙氧基、正丙氧基、异丙氧基、正丁氧基、异丁氧基、仲丁氧基、叔丁氧基等。
这里所用的“烷硫基”的例子为甲硫基、乙硫基、正丙硫基、异丙硫基、正丁硫基、异丁硫基、仲丁硫基、叔丁硫基等。
这里所用的“二-(C1-4烷基)氨基”的例子为二甲基氨基、二乙基氨基、二丙基氨基、N-甲基-N-乙基氨基、N-甲基-N-丙基氨基、N-甲基-N-丁基氨基、N-乙基-N-丙基氨基等。
这里所用的“C1-4烷基氨基”的例子为甲基氨基、乙基氨基、正丙基氨基、异丙基氨基、正丁基氨基、异丁基氨基、仲丁基氨基、叔丁基氨基等。
这里所用的“HO-C1-4烷基氨基”的例子为羟甲基、羟乙基(例如1-羟基乙基和2-羟基乙基)、羟丙基(例如1-羟基丙基、2-羟基丙基和3-羟基丙基)。
这里所用的“C1-4烷氧基-C1-4烷基”的例子为甲氧基甲基、甲氧基乙基、甲氧基丙基、甲氧基丁基、乙氧基甲基、乙氧基乙基、乙氧基丙基等。
这里所用的术语“卤素取代的烷基”是指被1个或多个卤素取代的上述烷基,包括但是不限于氯甲基、二氯甲基、氟甲基、二氟甲基、三氟甲基、2,2,2-三氯乙基等。
这里所用的“卤素取代的烷氧基”的例子为氯代甲氧基、二氯代甲氧基、氟代甲氧基、二氟代甲氧基、三氟代甲氧基、2,2,2-三氯乙氧基等。
这里所用的术语“C3-7环烷基”是指含有3-7个碳原子的碳环基团,包括但是不限于环丙基、环丁基、环戊基、环己基、环庚基等。
这里所用的“芳基”的例子为苯基和萘基。
这里所用的5-员单环芳基通常在其环中含有一个选自O、S和N的杂原子。除了所说的杂原子外,该单环芳基还任选地在其环中含有至多3个N原子。例如,5-员单环芳基包括噻吩基、呋喃基、噻唑基(例如1,3-噻唑基、1,2-噻唑基)、咪唑基、吡咯基、噁唑基(例如1,3噁唑基、1,2噁唑基、异噁唑基)、吡唑基、四唑基、三唑基(例如1,2,3-三唑基、1,2,4-三唑基)、噁二唑基(例如1,2,3-噁二唑基)、噻二唑基(例如1,3,4-噻二唑基、1,2,3-噻二唑基)等。
这里所用的6-员单环芳基包括吡啶基、吡嗪基、嘧啶基、哒嗪基、三嗪基(例如1,3,5-三嗪基)、四嗪基等。
这里所用的苯并稠合的杂环基的例子包括喹啉基、异喹啉基、1,2-二氮杂萘基、喹喔啉基、苯并咪唑基、苯并噻唑基、苯并噁唑基、苯并呋喃基、苯并噻吩基、吲哚基、异吲哚基、1H-吲唑基、喹唑啉基、2,3-二氮杂萘基等。
这里所用的(乙基)(乙氧基)吡啶基的例子包括3-乙氧基-4-乙基-2-吡啶基、4-乙氧基-3-乙基-2-吡啶基等。
这里所用的(氯)(乙基)吡啶基的例子包括3-氯-4-乙基-2-吡啶基、4-氯-3-乙基-2-吡啶基等。
这里所用的(氟)(乙基)吡啶基(phenyl)的例子包括3-氟-4-乙基-2-吡啶基、4-氟-3-乙基-2-吡啶基等。
本发明的优选化合物是式(I)中Z为OH、C1-6烷氧基、二甲基氨基、甲基氨基、氨基、N-甲氧基-N-甲基氨基、2-氰基乙基氨基、2-羟基乙基氨基、吡咯烷基、哌啶子基、哌嗪基、N-甲基哌嗪基、吗啉代、甲氧基氨基、哌嗪基(piperazynyl)、氨基吡咯烷基或氨基乙基氨基。
本发明的更优选的化合物是式(I)中Z为OH或C1-6烷氧基,而Q选自下列基团的化合物:
(a)任选地被1、2或3个独立地选自下列基团的取代基取代的苯基:
(a-1)卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基,
(a-2)芳基或-O-(CH2)n-芳基,且该芳基或芳基部分任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代,
(a-3)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的5-员单环芳基,
(a-4)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的6-员单环芳基,
(b)含有1、2、3或4个N的6-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(c)含有一个选自O、S和N的杂原子并且除所说的杂原子外还任选地含有1、2或3个N的5-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(d)选自环丙基、环丁基、环戊基和环己基的C3-7环烷基,并且所说的环烷基任选地被1个选自OH、甲基、乙基、丙基、F、Cl和CF3的取代基取代;和
(e)选自喹啉基、异喹啉基、1,2-二氮杂萘基、喹喔啉基、苯并咪唑基、苯并噻唑基、苯并噁唑基、苯并呋喃基、苯并噻吩基和吲哚基的苯并稠合的杂环,并且所说的苯并稠合的杂环任选地被1、2或3个独立地选自上述(a-1)的基团的取代基取代。
本发明的更优选的化合物是式(I)中Q选自下列基团的化合物:
(a)任选地被1、2或3个独立地选自下列基团的取代基取代的苯基:
(a-1)卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基,
(a-2)芳基或-O-(CH2)n-芳基,且该芳基或芳基部分任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代,
(a-3)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的5-员单环芳基,
(a-4)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的6-员单环芳基,
(b)含有1、2、3或4个N的6-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(c)含有一个选自O、S和N的杂原子并且除所说的杂原子外还任选地含有1、2或3个N的5-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(d)环丙基、环丁基和环己基;和
(e)喹啉基或异喹啉基,并且所说的喹啉基或异喹啉基任选地被1个选自卤素、C1-4烷基、NH2、OH、C1-4烷氧基和C1-4卤代烷基的取代基取代。
本发明的更优选的化合物是式(I)中Z为OH或C1-6烷氧基,而Q选自下列基团的化合物:
(a)任选地被1、2或3个独立地选自下列基团的取代基取代的苯基:
(a-1)卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4烷基)、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基,
(a-2)芳基或-O-(CH2)n-芳基,且该芳基或芳基部分任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代,
(a-3)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的5-员单环芳基,
(a-4)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的6-员单环芳基,
(b)含有1、2、3或4个N的6-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(c)含有一个选自O、S和N的杂原子并且除所说的杂原子外还任选地含有1、2或3个N的5-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;和
(e)异喹啉基;R1是H或C1-4烷基;R2和R3独立地为H或甲基;X独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-C4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOR4、C1-4烷基磺酰基氨基和C3-7环烷基;而n为0、1、2或3。
本发明的更优选的化合物是式(I)中Z为OH、甲氧基、乙氧基、正丙氧基、异丙氧基、正丁氧基、异丁氧基或叔丁氧基;Q选自下列基团的化合物:
(a)任选地被1或2个独立地选自下列基团的取代基取代的苯基:
(a-1)卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、-COOH、C1-4烷基磺酰基氨基、NO2、C1-4烷基磺酰基和CN,
(a-2)苯基或苄氧基,并且苯基或苄氧基的苯基基团任选地被1个选自C1-4烷基、卤素取代的C1-4烷基、卤素、OH、C1-4烷氧基、卤素取代的C1-4烷氧基和NH2的取代基取代,
(a-3)选自咪唑基、噻唑基、呋喃基、噻吩基、吡咯基、四唑基、三唑基、噁唑基、异噁唑基、噻二唑基和吡唑基的5-员单环芳基,并且该5-员单环芳基任选地被1个选自C1-4烷基、卤素取代的C1-4烷基、卤素、OH、C1-4烷氧基、卤素取代的C1-4烷氧基和NH2的取代基取代,
(a-4)选自吡啶基、吡嗪基、嘧啶基和哒嗪基的6-员单环芳基,并且该6-员单环芳基任选地被1个选自C1-4烷基、卤素取代的C1-4烷基、卤素、OH、C1-4烷氧基、卤素取代的C1-4烷氧基和NH2的取代基取代,
(b)选自吡啶基、吡嗪基、嘧啶基和哒嗪基的6-员单环芳基,并且所说的单环芳基任选地被1或2个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代,
(c)选自咪唑基、噻唑基、呋喃基、噻吩基、吡咯基、四唑基、三唑基、噁唑基、异噁唑基、噻二唑基和吡唑基的5-员单环芳基,并且所说的单环芳基任选地被1或2个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;R1是H、甲基、乙基、正丙基、异丙基、正丁基、异丁基或叔丁基;X独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-C4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基和氨基磺酰基;而n为0、1、2或3。
本发明的更优选的化合物是式(I)的化合物中Z为OH、甲氧基、乙氧基、正丙氧基、异丙氧基、正丁氧基、异丁氧基或叔丁氧基;Q选自下列基团:
(a)任选地被1或2个独立地选自下列基团的取代基取代的苯基:
(a-1)氟、氯、溴、碘、甲基、乙基、丙基、丁基、CH2F、CHF2、CF3、甲氧基、乙氧基、正丙氧基、正丁氧基、异丙氧基、CH2F-O-、CHF2-O-、CF3-O-、甲硫基、乙硫基、羟甲基、甲氧基甲基、甲氧基乙基、乙氧基甲基、OH、NO2、甲磺酰基、CN、(HO)(H3C)2C-、乙酰基和甲磺酰基氨基,
(a-2)苯基或苄氧基,并且苯基或苄氧基的苯基部分任选地被1个选自甲基、乙基、丙基、CF3、F、Cl、OH、甲氧基、乙氧基和NH2的取代基取代,
(a-3)选自呋喃基、噻吩基和吡咯基的5-员单环芳基,并且该5-员单环芳基任选地被1个选自甲基、乙基、丙基、CF3、F、Cl、OH、甲氧基、乙氧基和NH2的取代基取代,
(a-4)任选地被1个选自甲基、乙基、丙基、CF3、F、Cl、OH、甲氧基、乙氧基和NH2的取代基取代的吡啶基,
(b)任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代的吡啶基,
(c)咪唑基、噻唑基、呋喃基、噻吩基、异噁唑基、1,2,3-噻二唑基或吡咯基,并且所说的咪唑基、噻唑基、呋喃基、噻吩基、异噁唑基、1,2,3-噻二唑基或吡咯基任选地被1或2个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;R1是H、甲基、乙基、正丙基、异丙基;X独立地选自F、Cl、Br、甲基、乙基、丙基、丁基、CH2F、CHF2、CF3、甲氧基、CF3-O-或乙氧基;而n为0、1或2。
本发明的更优选的化合物是式(I)的化合物,其中:Z为OH、乙氧基或甲氧基;Q为苯基、氯代苯基、氟代苯基、溴代苯基、甲苯基、甲氧基苯基、(呋喃基)苯基、三氟甲基苯基、三氟甲氧基苯基、吡啶基、甲基吡啶基、乙基吡啶基、丙基吡啶基、二甲基吡啶基、氯代吡啶基、氟代吡啶基、三氟甲基吡啶基、甲氧基吡啶基、(乙基)(乙氧基)吡啶基、(氯)(乙基)吡啶基、噻唑基、甲基噻唑基、呋喃基、甲氧基甲基呋喃基、异喹啉基、环己基、甲氧基苯基、(氟)(乙基)吡啶基、二甲基吡啶基或(乙氧基)(乙基)吡啶基;R1为H;X为F、Cl、甲基、乙基、异丙基、叔丁基、CF3或甲氧基;而n为1或2。
本发明的更优选的化合物是式(I)的化合物,其中:Z为OH、乙氧基或甲氧基;Q为苯基、氯代苯基、吡啶基、甲基吡啶基、乙基吡啶基、丙基吡啶基或氯代吡啶基;R1为H;X为F、Cl、甲基或CF3;而n为1或2。
优选的本发明的单个化合物是:(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸乙酯、(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸、(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸,钠盐[6-氯-2-(2-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-氟苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氟苯甲酰基)-1H-吲哚-3-基]乙酸、[2-(3-溴苯甲酰基)-6-氯-1H-吲哚-3-基]乙酸、[2-(4-溴苯甲酰基)-6-氯-1H-吲哚-3-基]乙酸、[6-氯-2-(3-三氟甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-三氟甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3,4-二氯苯甲酰基)-1H-吲哚-3-基]乙酸、(2-苯甲酰基-4-氯-1H-吲哚-3-基)乙酸、[5-氯-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、[2-(3-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、[5-甲氧基-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、(2-苯甲酰基-7-氯-1H-吲哚-3-基)乙酸、(2-苯甲酰基-4,5-二氯-1H-吲哚-3-基)乙酸、(2-苯甲酰基-4,6-二氯-1H-吲哚-3-基)乙酸、(2-苯甲酰基-5,6-二氯-1H-吲哚-3-基)乙酸、dl-2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)丙酸、极性较小的对映体2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)丙酸、极性较大的对映体2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)丙酸、[6-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(1-甲基咪唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(噻唑-2-羰基)-1H-吲哚-3-基]乙酸、(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸甲酯、(2-苯甲酰基-6-氯-1H-吲哚-3-基)-N,N-二甲基乙酰胺、(2-苯甲酰基-6-氯-1H-吲哚-3-基)-N-甲基乙酰胺、(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酰胺、(2-苯甲酰基-6-氯-1H-吲哚-3-基)-N-甲氧基-N-甲基乙酰胺、2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)-1-哌啶子基-1-乙酮、2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)-1-(4-甲基-1-哌嗪基)-1-乙酮、(2-苯甲酰基-6-氯-1H-吲哚-3-基)-N-(2-氰基乙基)乙酰胺、(2-苯甲酰基-6-氯-1H-吲哚-3-基)-N-(2-羟基乙基)乙酰胺、2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)-1-吗啉代-1-乙酮、[2-(4-氯苯甲酰基)-1H-吲哚-3-基)乙酸、[6-氯-2-(2-呋喃基羰基)-1H-吲哚-3-基)乙酸、[6-氯-2-(环己烷羰基)-1H-吲哚-3-基)乙酸、[6-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-叔丁基吡啶-2-羰基)-6-氯-1H-吲哚-3-基]乙酸甲酯、[2-(4-叔丁基吡啶-2-羰基)-6-氯-1H-吲哚-3-基]乙酸、[2-(4-叔丁基吡啶-2-羰基)-5-氯-1H-吲哚-3-基]乙酸甲酯、[2-(4-叔丁基吡啶-2-羰基)-5-氯-1H-吲哚-3-基]乙酸、[6-氯-2-(3-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(3-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(3-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(3-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[5-(三氟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[5-(三氟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[5-氯-2-[5-(三氟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-[5-(三氟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[5-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(吡啶-3-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(吡啶-3-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(吡啶-4-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(吡啶-4-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(羟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[4-(羟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[5-氯-2-[4-(羟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-[4-(羟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[5-氯-2-(3,4-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(3,4-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(3,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(3-乙氧基-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-氯-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(3-氯-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(3-氯-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(3-氯-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5,6-二氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5,6-二氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-甲氧基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-甲氧基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-甲氧基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-甲氧基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-乙基-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-乙基-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-异丙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-异丙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基吡啶-2-羰基)-6-三氟甲基-1H-吲哚-3-基]乙酸甲酯、[2-(4-甲基吡啶-2-羰基)-6-三氟甲基-1H-吲哚-3-基]乙酸、[5-叔丁基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-叔丁基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基吡啶-2-羰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸甲酯、[2-(4-甲基-2-吡啶-2-羰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸、[2-(4-乙基吡啶-2-羰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸甲酯、[2-(4-乙基吡啶-2-羰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸、[6-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸甲酯、[2-(4-甲基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[2-(4-乙基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸甲酯、[2-(4-乙基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、(2-苯甲酰基-1H-吲哚-3-基]乙酸甲酯、(2-苯甲酰基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-6-甲基-1H-吲哚-3-基]乙酸甲酯、[2-(4-氯苯甲酰基)-6-甲基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-甲基-1H-吲哚-3-基]乙酸、[6-甲氧基-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-甲氧基-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-6-三氟甲基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-乙基-1H-吲哚-3-基]乙酸甲酯、[2-(4-氯苯甲酰基)-5-乙基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-甲氧基-1H-吲哚-3-基]乙酸甲酯、[2-(4-氯苯甲酰基)-5-甲氧基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-异丙基-1H-吲哚-3-基]乙酸甲酯、[2-(4-氯苯甲酰基)-5-异丙基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-三氟甲基-1H-吲哚-3-基]乙酸甲酯、[2-(4-氯苯甲酰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸甲酯、[2-(4-氯苯甲酰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸、[6-氯-2-(2-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(2-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(3-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-苄氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(3-苄氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-羟基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(3-羟基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-苄氧基苯甲酰基(benzoxybenzyloyl))-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-苄氧基苯甲酰基(benzyloxybenzoyl))-1H-吲哚-3-基]乙酸、[6-氯-2-(4-羟基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-羟基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-异丙氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-异丙氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-苯基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-苯基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-硝基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-硝基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[(4-甲磺酰基)苯甲酰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[(4-甲磺酰基)苯甲酰基]-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(甲磺酰基氨基)苯甲酰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[4-(甲磺酰基氨基)苯甲酰基]-1H-吲哚-3-基]乙酸、[6-氯-2-2-(氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(2,4-二氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯-3-氟苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-氯-3-氟苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氰基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[4-溴代苯甲酰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[4-(2-噻吩基)苯甲酰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[4-(2-噻吩基)苯甲酰基]-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(2-呋喃基)苯甲酰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[4-(2-呋喃基)苯甲酰基]-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(3-吡啶基)苯甲酰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[4-(3-吡啶基)苯甲酰基]-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(2-噻唑基)苯甲酰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[4-(2-噻唑基)苯甲酰基]-1H-吲哚-3-基]乙酸、[6-氯-2-(3-溴代苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[3-(2-呋喃基)苯甲酰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[3-(2-呋喃基)苯甲酰基]-1H-吲哚-3-基]乙酸、dl-2-[6-氯-2-(4-氯代苯甲酰基)-1H-吲哚-3-基]丙酸甲酯、dl-2-[2-(4-氯代苯甲酰基)-6-氯-1H-吲哚-3-基]丙酸、[5-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(5-甲基异噁唑-3-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(5-甲基异噁唑-3-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-甲基异噁唑-3-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(5-甲基异噁唑-3-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲基-1,2,3-噻二唑-5-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-甲基-1,2,3-噻二唑-5-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲基-1,2,3-噻二唑-5-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-甲基-1,2,3-噻二唑-5-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(5-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(5-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(5-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(2-噻吩基)羰基吲哚-3-基]乙酸、[6-氯-2-[3-(1-羟基-1-甲基乙基)-2-呋喃甲酰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[3-(1-羟基-1-甲基乙基)-2-呋喃甲酰基]-1H-吲哚-3-基]乙酸、[6-氯-2-[3-甲氧基甲基-2-呋喃甲酰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[3-甲氧基甲基-2-呋喃甲酰基]-1H-吲哚-3-基]乙酸、[6-氯-2-(1-甲基咪唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(1-甲基咪唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(1-甲基咪唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(1-甲基咪唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(咪唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(咪唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(咪唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(咪唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(1-甲基吡咯-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(1-甲基吡咯-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(2-甲基咪唑-4-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(2-甲基咪唑-4-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(噻唑-5-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(噻唑-5-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-[3-(乙氧基羰基)异噁唑-5-羰基]-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-[3-(羧基)异噁唑-5-羰基]-1H-吲哚-3-基]乙酸、[6-氯-2-环丙烷羰基-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-环丙烷羰基-1H-吲哚-3-基]乙酸、[6-氯-2-环丁烷羰基-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-环丁烷羰基-1H-吲哚-3-基]乙酸、[5-(叔丁基)-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[5-(叔丁基)-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]-N,N-二甲基乙酰胺、[6-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]-N-甲基乙酰胺、[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]-N-(2-羟乙基)乙酰胺、[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]-N-甲氧基乙酰胺、2-[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]-1-哌嗪基-1-乙酮、[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]-N-(2-氨基乙基)乙酰胺、2-[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]-1-(3-氨基-1-吡咯烷基)-1-乙酮、[6-氯-2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、[6-氯-5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(1-羟乙基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[4-(1-羟乙基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[6-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(2-硝基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(2,4-二甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-二氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(2,5-二甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-乙酰基-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[5-乙酰基-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸甲酯、[6-氟-2-(4-甲基吡啶-2-羰基)-H-吲哚-3-基]乙酸甲酯、[6-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氟-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氟-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基吡啶-2-羰基)-5-甲硫基-1H-吲哚-3-基]乙酸、[2-(4-甲基吡啶-2-羰基)-5-甲硫基-1H-吲哚-3-基]乙酸,及其盐。
优选的本发明的单个化合物是:(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸乙酯、(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸、(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸,钠盐、[6-氯-2-(2-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-氟苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氟苯甲酰基)-1H-吲哚-3-基]乙酸、[2-(3-溴苯甲酰基)-6-氯-1H-吲哚-3-基]乙酸、[2-(4-溴苯甲酰基)-6-氯-1H-吲哚-3-基]乙酸、[6-氯-2-(3-三氟甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-三氟甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3,4-二氯苯甲酰基)-1H-吲哚-3-基]乙酸、(2-苯甲酰基-4-氯-1H-吲哚-3-基)乙酸、[5-氯-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、[2-(3-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、[5-甲氧基-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、(2-苯甲酰基-7-氯-1H-吲哚-3-基)乙酸、(2-苯甲酰基-4,5-二氯-1H-吲哚-3-基)乙酸、(2-苯甲酰基-4,6-二氯-1H-吲哚-3-基)乙酸、(2-苯甲酰基-5,6-二氯-1H-吲哚-3-基)乙酸、dl-2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)丙酸、极性较小的对映体2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)丙酸、极性较大的对映体2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)丙酸、[6-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(1-甲基咪唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(噻唑-2-羰基)-1H-吲哚-3-基]乙酸、(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸甲酯、[2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(2-呋喃基羰基)-1H-吲哚-3-基)乙酸、[6-氯-2-(环己烷羰基)-1H-吲哚-3-基)乙酸、[6-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-叔丁基吡啶-2-羰基)-6-氯-1H-吲哚-3-基]乙酸、[2-(4-叔丁基吡啶-2-羰基)-5-氯-1H-吲哚-3-基]乙酸、[6-氯-2-(3-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(3-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[5-(三氟甲基)吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-[5-(三氟甲基)吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(吡啶-3-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(吡啶-4-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(羟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[5-氯-2-[4-(羟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[5-氯-2-(3,4-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-乙氧基-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-氯-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(3-氯-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5,6-二氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-甲氧基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-甲氧基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-乙基-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-异丙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基吡啶-2-羰基)-6-三氟甲基-1H-吲哚-3-基]乙酸、[5-叔丁基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基-2-吡啶-2-羰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸、[2-(4-乙基吡啶-2-羰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸、[6-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[2-(4-乙基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、(2-苯甲酰基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-6-甲基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-甲基-1H-吲哚-3-基]乙酸、[6-甲氧基-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-6-三氟甲基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-乙基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-甲氧基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-异丙基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸、[6-氯-2-(2-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-苄氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-羟基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-苄氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-羟基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-异丙氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-苯基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-硝基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[(4-甲磺酰基)苯甲酰基]-1H-吲哚-3-基]乙酸、[6-氯-2-[(4-甲磺酰基氨基)苯甲酰基]-1H-吲哚-3-基]乙酸、[6-氯-2-(2-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(2,4-二氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯-3-氟苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氰基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[4-溴代苯甲酰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[4-(2-噻吩基)苯甲酰基]-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(2-呋喃基)苯甲酰基]-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(3-吡啶基)苯甲酰基]-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(2-噻唑基)苯甲酰基]-1H-吲哚-3-基]乙酸、[6-氯-2-(3-溴代苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[3-(2-呋喃基)苯甲酰基]-1H-吲哚-3-基]乙酸、dl-2-[2-(4-氯代苯甲酰基)-6-氯-1H-吲哚-3-基]丙酸、[5-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(5-甲基异噁唑-3-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-甲基异噁唑-3-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲基-1,2,3-噻二唑-5-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲基-1,2,3-噻二唑-5-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(5-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(2-噻吩基)羰基吲哚-3-基]乙酸、[6-氯-2-[3-(1-羟基-1-甲基乙基)-2-呋喃甲酰基]-1H-吲哚-3-基]乙酸、[6-氯-2-[3-甲氧基甲基-2-呋喃甲酰基]-1H-吲哚-3-基]乙酸、[6-氯-2-(1-甲基咪唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(1-甲基咪唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(1-甲基咪唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(咪唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(咪唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(1-甲基吡咯-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(2-甲基咪唑-4-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(噻唑-5-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-[3-(羧基)异噁唑-5-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-环丙烷羰基-1H-吲哚-3-基]乙酸、[6-氯-2-环丁烷羰基-1H-吲哚-3-基]乙酸、[5-(叔丁基)-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、[6-氯-5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(1-羟乙基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[4-(1-羟乙基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[6-氯-2-[4-乙基-3-氟吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[6-氯-2-(2-硝基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(2,4-二甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-二氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(2,5-二甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-乙酰基-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸及其盐。
优选的本发明的单个化合物是:(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸乙酯、(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸、[6-氯-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-氟苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氟苯甲酰基)-1H-吲哚-3-基]乙酸、[2-(3-溴苯甲酰基)-6-氯-1H-吲哚-3-基]乙酸、[2-(4-溴苯甲酰基)-6-氯-1H-吲哚-3-基]乙酸、[6-氯-2-(3-三氟甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-三氟甲基苯甲酰基)-1H-吲哚-3-基]乙酸、(2-苯甲酰基-4-氯-1H-吲哚-3-基)乙酸、[5-氯-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、[2-(3-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、(2-苯甲酰基-4,5-二氯-1H-吲哚-3-基)乙酸、(2-苯甲酰基-4,6-二氯-1H-吲哚-3-基)乙酸、(2-苯甲酰基-5,6-二氯-1H-吲哚-3-基)乙酸、dl-2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)丙酸、极性较小的对映体2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)丙酸、极性较大的对映体2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)丙酸、[6-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(1-甲基咪唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(噻唑-2-羰基)-1H-吲哚-3-基]乙酸、(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸甲酯、[6-氯-2-(2-呋喃基羰基)-1H-吲哚-3-基)乙酸、[6-氯-2-(环己烷羰基)-1H-吲哚-3-基)乙酸、[6-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-叔丁基吡啶-2-羰基)-6-氯-1H-吲哚-3-基]乙酸甲酯、[2-(4-叔丁基吡啶-2-羰基)-6-氯-1H-吲哚-3-基]乙酸、[6-氯-2-(3-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(3-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基乙酸、[5-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[5-(三氟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[5-(三氟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[5-氯-2-[5-(三氟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-[5-(三氟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[5-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-[4-(羟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-[4-(羟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[5-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(3,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(3-乙氧基-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-氯-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(3-氯-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(3-氯-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(3-氯-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5,6-二氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5,6-二氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-甲氧基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-甲氧基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-甲氧基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-甲氧基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-乙基-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-乙基-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-异丙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-异丙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基吡啶-2-羰基)-6-三氟甲基-1H-吲哚-3-基]乙酸甲酯、[2-(4-甲基吡啶-2-羰基)-6-三氟甲基-1H-吲哚-3-基]乙酸、[5-叔丁基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-叔丁基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基吡啶-2-羰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸甲酯、[2-(4-甲基-2-吡啶-2-羰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸、[6-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸甲酯、[2-(4-甲基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[2-(4-乙基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸甲酯、[2-(4-乙基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-6-甲基-1H-吲哚-3-基]乙酸甲酯、[2-(4-氯苯甲酰基)-6-甲基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-甲基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-三氟甲基-1H-吲哚-3-基]乙酸甲酯、[2-(4-氯苯甲酰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸甲酯、[2-(4-氯苯甲酰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸、[6-氯-2-(3-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(3-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(2-呋喃基)苯甲酰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[4-(2-呋喃基)苯甲酰基]-1H-吲哚-3-基]乙酸、[5-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-甲基异噁唑-3-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(5-甲基异噁唑-3-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(5-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(5-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(5-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[3-甲氧基甲基-2-呋喃甲酰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[3-甲氧基甲基-2-呋喃甲酰基]-1H-吲哚-3-基]乙酸、[6-氯-2-(1-甲基咪唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(2-甲基咪唑-4-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(2-甲基咪唑-4-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(1-羟乙基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[4-(1-羟乙基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[6-氯-2-[4-乙基-3-氟吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸甲酯及其盐。
优选的本发明的单个化合物是:(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸乙酯、(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸、[6-氯-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-氟苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氟苯甲酰基)-1H-吲哚-3-基]乙酸、[2-(3-溴苯甲酰基)-6-氯-1H-吲哚-3-基]乙酸、[2-(4-溴苯甲酰基)-6-氯-1H-吲哚-3-基]乙酸、[6-氯-2-(3-三氟甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-三氟甲基苯甲酰基)-1H-吲哚-3-基]乙酸、(2-苯甲酰基-4-氯-1H-吲哚-3-基)乙酸、[5-氯-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、[2-(3-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、(2-苯甲酰基-4,5-二氯-1H-吲哚-3-基)乙酸、(2-苯甲酰基-4,6-二氯-1H-吲哚-3-基)乙酸、(2-苯甲酰基-5,6-二氯-1H-吲哚-3-基)乙酸、dl-2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)丙酸、极性较小的对映体2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)丙酸、极性较大的对映体2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)丙酸、[6-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(1-甲基咪唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(噻唑-2-羰基)-1H-吲哚-3-基]乙酸、(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸甲酯、[6-氯-2-(2-呋喃基羰基)-1H-吲哚-3-基)乙酸、[6-氯-2-(环己烷羰基)-1H-吲哚-3-基)乙酸、[6-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-叔丁基吡啶-2-羰基)-6-氯-1H-吲哚-3-基]乙酸、[6-氯-2-(3-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[5-(三氟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[5-氯-2-[5-(三氟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[5-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-[4-(羟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[5-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-乙氧基-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-氯-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(3-氯-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5,6-二氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-甲氧基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-甲氧基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-乙基-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-异丙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基吡啶-2-羰基)-6-三氟甲基-1H-吲哚-3-基]乙酸、[5-叔丁基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基-2-吡啶-2-羰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸、[6-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[2-(4-乙基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-6-甲基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-甲基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸、[6-氯-2-(3-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(2-呋喃基)苯甲酰基]-1H-吲哚-3-基]乙酸、[5-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-甲基异噁唑-3-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(5-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[3-甲氧基甲基-2-呋喃甲酰基]-1H-吲哚-3-基]乙酸、[6-氯-2-(1-甲基咪唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(2-甲基咪唑-4-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(1-羟乙基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[4-(1-羟乙基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、2-{6-氯-2-[4-乙基-3-氟-2-吡啶基)羰基]-1H-吲哚-3-基}乙酸、[6-氯-2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸甲酯及其盐。
优选的本发明的单个化合物是:(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸、[6-氯-2-(4-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-氟苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氟苯甲酰基)-1H-吲哚-3-基]乙酸、[2-(3-溴苯甲酰基)-6-氯-1H-吲哚-3-基]乙酸、[2-(4-溴苯甲酰基)-6-氯-1H-吲哚-3-基]乙酸、[6-氯-2-(4-三氟甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、[2-(3-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、(2-苯甲酰基-4,5-二氯-1H-吲哚-3-基)乙酸、(2-苯甲酰基-4,6-二氯-1H-吲哚-3-基)乙酸、(2-苯甲酰基-5,6-二氯-1H-吲哚-3-基)乙酸、[6-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(噻唑-2-羰基)-1H-吲哚-3-基]乙酸、(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸甲酯、[6-氯-2-(环己烷羰基)-1H-吲哚-3-基)乙酸、[6-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[5-(三氟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[5-(三氟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[5-氯-2-[5-(三氟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-[5-(三氟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[5-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(3-乙氧基-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-氯-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(3-氯-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5,6-二氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5,6-二氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-异丙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-异丙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基吡啶-2-羰基)-6-三氟甲基-1H-吲哚-3-基]乙酸甲酯、[2-(4-甲基吡啶-2-羰基)-6-三氟甲基-1H-吲哚-3-基]乙酸、[5-叔丁基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-叔丁基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基吡啶-2-羰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸甲酯、[2-(4-甲基-2-吡啶-2-羰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸、[6-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸甲酯、[2-(4-甲基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[2-(4-乙基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸甲酯、[2-(4-乙基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-甲基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-三氟甲基-1H-吲哚-3-基]乙酸甲酯、[2-(4-氯苯甲酰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[6-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(2-呋喃基)苯甲酰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[4-(2-呋喃基)苯甲酰基]-1H-吲哚-3-基]乙酸、[5-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(5-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(5-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(5-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[3-甲氧基甲基-2-呋喃甲酰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[3-甲氧基甲基-2-呋喃甲酰基]-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(2-甲基咪唑-4-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(2-甲基咪唑-4-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、[6-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸甲酯及其盐。
优选的本发明的单个化合物是:(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸、[6-氯-2-(4-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-氟苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氟苯甲酰基)-1H-吲哚-3-基]乙酸、[2-(3-溴苯甲酰基)-6-氯-1H-吲哚-3-基]乙酸、[2-(4-溴苯甲酰基)-6-氯-1H-吲哚-3-基]乙酸、[6-氯-2-(4-三氟甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、[2-(3-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、(2-苯甲酰基-4,5-二氯-1H-吲哚-3-基)乙酸、(2-苯甲酰基-4,6-二氯-1H-吲哚-3-基)乙酸、(2-苯甲酰基-5,6-二氯-1H-吲哚-3-基)乙酸、[6-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(噻唑-2-羰基)-1H-吲哚-3-基]乙酸、(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸甲酯、[6-氯-2-(环己烷羰基)-1H-吲哚-3-基)乙酸、[6-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[5-(三氟甲基)吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-[5-(三氟甲基)吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-乙氧基-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-氯-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5,6-二氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-异丙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基吡啶-2-羰基)-6-三氟甲基-1H-吲哚-3-基]乙酸、[5-叔丁基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基-2-吡啶-2-羰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸、[6-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[2-(4-乙基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[6-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(2-呋喃基)苯甲酰基]-1H-吲哚-3-基]乙酸、[5-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(5-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(5-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[3-甲氧基甲基-2-呋喃甲酰基]-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(2-甲基咪唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、[6-氯-2-(4-乙基-3-氟吡啶-2-羰基]-1H-吲哚-3-基)乙酸、[6-氯-2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸甲酯、[6-氯-5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(1-羟乙基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸,及其盐。
优选的本发明的单个化合物是:(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸、[6-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、(2-苯甲酰基-5,6-二氯-1H-吲哚-3-基)乙酸、[6-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-乙基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸甲酯、[2-(4-乙基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸[5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸、[6-氯-5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(1-羟乙基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[4-(1-羟乙基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[6-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸(cj-020,099)、[6-氯-5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸,及其盐。
最优选的单个化合物是:(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸、[6-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、(2-苯甲酰基-5,6-二氯-1H-吲哚-3-基)乙酸、[6-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-乙基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(1-羟乙基)吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸,及其盐。
优选的本发明的药物组合物含有上述定义的式(I)化合物。
药物组合物中包含的最优选的单个化合物是:(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸、[6-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、(2-苯甲酰基-5,6-二氯-1H-吲哚-3-基)乙酸、[6-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-乙基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(1-羟乙基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[6-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸,及其盐。
(a)任选地被1、2或3个独立地选自下列基团的取代基取代的苯基:
(a-1)卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基,
(a-2)芳基或-O-(CH2)n-芳基,且该芳基或芳基部分任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代,
(a-3)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的5-员单环芳基,
(a-4)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的6-员单环芳基,
(b)含有1、2、3或4个N的6-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(c)含有一个选自O、S和N的杂原子并且除所说的杂原子外还任选地含有1、2或3个N的5-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(d)任选地被1或2个独立地选自OH、C1-4烷基、卤素和卤素取代的C1-4烷基的取代基取代的C3-7环烷基;和
(e)任选地被1、2或3个独立地选自上述(a-1)的基团的取代基取代的苯并稠合的杂环;R2和R3独立地为H、OH、C1-4烷氧基、C1-4烷基或者是被卤素、OH、C1-4烷氧基、NH2或CN取代的C1-4烷基;X独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-C4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基;而n为0、1、2、3和4,该方法包括下列步骤:
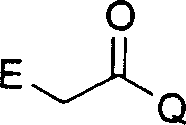
其中E为卤素,Q如上所定义;
ii)使步骤i)的产物与第二种碱反应;
iii)使步骤ii)的产物与一种酸反应。
优选的上述方法是其中所说的第一种碱是碳酸钾、碳酸氢钾、碳酸钠、碳酸氢钠或碳酸铯。
优选的上述方法是其中所说的第一种碱是碳酸钾。
优选的上述方法是其中所说的第二种碱是氢氧化钠、氢氧化钾、碳酸钠、碳酸钾、戊醇钠(然后是水)、甲醇钠(然后是水)或叔丁醇钾水溶液(然后是水)。
优选的上述方法是其中所说的第二种碱是氢氧化钠。
优选的上述方法是其中所说的酸是盐酸、氢溴酸、硫酸或氯化铵水溶液。
优选的上述方法是其中所说的酸是盐酸水溶液。
优选的上述方法是其中所说的溶剂是N,N-二甲基乙酰胺、N,N-二甲基甲酰胺、甲乙酮、丙酮或四氢呋喃。
优选的上述方法是其中所说的溶剂是N,N-二甲基乙酰胺。
(a)任选地被1、2或3个独立地选自下列基团的取代基取代的苯基:
(a-1)卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基,
(a-2)芳基或-O-(CH2)n-芳基,且该芳基或芳基部分任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代,
(a-3)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的5-员单环芳基,
(a-4)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的6-员单环芳基,
(b)含有1、2、3或4个N的6-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(c)含有一个选自O、S和N的杂原子并且除所说的杂原子外还任选地含有1、2或3个N的5-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(d)任选地被1或2个独立地选自OH、C1-4烷基、卤素和卤素取代的C1-4烷基的取代基取代的C3-7环烷基;和
(e)任选地被1、2或3个独立地选自上述(a-1)的基团的取代基取代的苯并稠合的杂环;R2和R3独立地为H、OH、C1-4烷氧基、C1-4烷基或者是被卤素、OH、C1-4烷氧基、NH2或CN取代的C1-4烷基;X独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-C4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基;而n为0、1、2、3和4,该方法包括使下式的化合物:
其中R5为C1-6烷基,X和n如前面所定义,与一种碱在一种合适的溶剂中反应。
优选的上述方法是其中所说的碱是氢氧化钠、氢氧化钾、碳酸钠、碳酸钾、碳酸氢钠、碳酸氢钾、叔戊醇钠、甲醇钠、乙醇钠或叔丁醇钾。
优选的上述方法是其中所说的碱是氢氧化钠。
优选的上述方法是其中所说的溶剂是甲醇、乙醇、异丙醇或四氢呋喃与水的混合物。
优选的上述方法是其中所说的溶剂是含有水的甲醇。
(a)任选地被1、2或3个独立地选自下列基团的取代基取代的苯基:
(a-1)卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基,
(a-2)芳基或-O-(CH2)n-芳基,且该芳基或芳基部分任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代,
(a-3)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的5-员单环芳基,
(a-4)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的6-员单环芳基,
(b)含有1、2、3或4个N的6-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(c)含有一个选自O、S和N的杂原子并且除所说的杂原子外还任选地含有1、2或3个N的5-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(d)任选地被1或2个独立地选自OH、C1-4烷基、卤素和卤素取代的C1-4烷基的取代基取代的C3-7环烷基;和
(e)任选地被1、2或3个独立地选自上述(a-1)的基团的取代基取代的苯并稠合的杂环;R2和R3独立地为H、OH、C1-4烷氧基、C1-4烷基或者是被卤素、OH、C1-4烷氧基、NH2或CN取代的C1-4烷基;X独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-C4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基;R5为C1-6烷基;而n为0、1、2、3或4,该方法包括使下式的化合物:
其中B、Q、X、n和R5如前面所定义,与一种碱在一种合适的溶剂中反应。
优选的上述方法是其中所说的碱是1,8-二氮杂双环[5.4.0]十一碳-7-烯、1,5-二氮杂双环[4.3.0]壬-5-烯、1,1,3,3-四甲基胍、叔戊醇钠、甲醇钠或叔丁醇钾。
优选的上述方法是其中所说的碱是1,8-二氮杂双环[5.4.0]十一碳-7-烯或叔丁醇钾。
优选的上述方法是其中所说的溶剂是N,N-二甲基乙酰胺、N,N-二甲基甲酰胺、甲乙酮、丙酮或四氢呋喃。
优选的上述方法是其中所说的溶剂是N,N-二甲基乙酰胺。
本发明还提供一种制备下式化合物的方法:
其中B是合适的保护基;
其中Q选自下列基团:
(a)任选地被1、2或3个独立地选自下列基团的取代基取代的苯基:
(a-1)卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基,
(a-2)芳基或-O-(CH2)n-芳基,而该芳基或芳基部分任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代,
(a-3)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的5-员单环芳基,
(a-4)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的6-员单环芳基,
(b)含有1、2、3或4个N的6-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(c)含有一个选自O、S和N的杂原子并且除所说的杂原子外还任选地含有1、2或3个N的5-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(d)任选地被1或2个独立地选自OH、C1-4烷基、卤素和卤素取代的C1-4烷基的取代基取代的C3-7环烷基;和
(e)任选地被1、2或3个独立地选自上述(a-1)的基团的取代基取代的苯并稠合的杂环;R2和R3独立地为H、OH、C1-4烷氧基、C1-4烷基或者是被卤素、OH、C1-4烷氧基、NH2或CN取代的C1-4烷基;X独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-C4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基;R5为C1-6烷基;而n为0、1、2、3和4,该方法包括使下式的化合物:
其中B、Q、X、n和R5如前面所定义,与一种碱在一种溶剂存在下反应。
优选的上述方法是其中所说的碱是碳酸钾、碳酸氢钾、碳酸氢钠、碳酸钠或碳酸铯。
优选的上述方法是其中所说的碱是碳酸钾。
优选的上述方法是其中所说的溶剂是N,N-二甲基乙酰胺、N,N-二甲基甲酰胺、甲乙酮、丙酮或四氢呋喃。
优选的上述方法是其中所说的溶剂是N,N-二甲基乙酰胺。
(a)任选地被1、2或3个独立地选自下列基团的取代基取代的苯基:
(a-1)卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基,
(a-2)芳基或-O-(CH2)n-芳基,而该芳基或芳基部分任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代,
(a-3)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的5-员单环芳基,
(a-4)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的6-员单环芳基,
(b)含有1、2、3或4个N的6-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(c)含有一个选自O、S和N的杂原子并且除所说的杂原子外还任选地含有1、2或3个N的5-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(d)任选地被1或2个独立地选自OH、C1-4烷基、卤素和卤素取代的C1-4烷基的取代基取代的C3-7环烷基;和
(e)任选地被1、2或3个独立地选自上述(a-1)的基团的取代基取代的苯并稠合的杂环;R2和R3独立地为H、OH、C1-4烷氧基、C1-4烷基或者是被卤素、OH、C1-4烷氧基、NH2或CN取代的C1-4烷基;X独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-C4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基;R5为C1-6烷基;而n为0、1、2、3或4,该方法包括使下式的化合物:
其中E为卤素,Q如上所定义。
优选的上述方法是其中所说的碱是碳酸钾、碳酸氢钾、碳酸氢钠、碳酸钠或碳酸铯。
优选的上述方法是其中所说的碱是碳酸钾。
优选的上述方法是其中所说的溶剂是N,N-二甲基乙酰胺、N,N-二甲基甲酰胺、甲乙酮、丙酮或四氢呋喃。
优选的上述方法是其中所说的溶剂是N,N-二甲基乙酰胺。
(a)任选地被1、2或3个独立地选自下列基团的取代基取代的苯基:
(a-1)卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基,
(a-2)芳基或-O-(CH2)n-芳基,而该芳基或芳基部分任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代,
(a-3)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的5-员单环芳基,
(a-4)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的6-员单环芳基,
(b)含有1、2、3或4个N的6-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(c)含有一个选自O、S和N的杂原子并且除所说的杂原子外还任选地含有1、2或3个N的5-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(d)任选地被1或2个独立地选自OH、C1-4烷基、卤素和卤素取代的C1-4烷基的取代基取代的C3-7环烷基;和
(e)任选地被1、2或3个独立地选自上述(a-1)的基团的取代基取代的苯并稠合的杂环;R1为H、C1-4烷基或卤素;R2和R3独立地为H、OH、C1-4烷氧基、C1-4烷基或者是被卤素、OH、C1-4烷氧基、NH2或CN取代的C1-4烷基;R5为C1-6烷基;X独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-C4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基;而n为0、1、2、3或4,该方法包括在一种合适的碱存在下处理下式(X)的化合物:
其中R1、R5、X、Q和n如前面所定义,而B为合适的保护基团,得到式(XII)的化合物。
(a)任选地被1、2或3个独立地选自下列基团的取代基取代的苯基:
(a-1)卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基,
(a-2)芳基或-O-(CH2)n-芳基,而该芳基或芳基部分任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代,
(a-3)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的5-员单环芳基,
(a-4)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的6-员单环芳基,
(b)含有1、2、3或4个N的6-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(c)含有一个选自O、S和N的杂原子并且除所说的杂原子外还任选地含有1、2或3个N的5-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(d)任选地被1或2个独立地选自OH、C1-4烷基、卤素和卤素取代的C1-4烷基的取代基取代的C3-7环烷基;和
(e)任选地被1、2或3个独立地选自上述(a-1)的基团的取代基取代的苯并稠合的杂环;R1为H、C1-4烷基或卤素;R2和R3独立地为H、OH、C1-4烷氧基、C1-4烷基或者是被卤素、OH、C1-4烷氧基、NH2或CN取代的C1-4烷基;R5为C1-6烷基;X独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-C4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基;而n为0、1、2、3或4,该方法包括使下式(IX)的化合物:
其中E为卤素,而Q如上所定义,得到式(XII)的化合物。
优选的上述方法是其中反应在0-100℃的温度下进行。
优选的上述方法是其中合适的碱是碳酸钾、碳酸铯、碳酸钠、叔丁醇钠、叔丁醇钾、氢化钠、氢化钾或氟化钾。
优选的上述方法是其中反应先在碱存在下进行2分钟至1天,然后向反应混合物中加入另一种碱。
优选的上述方法是其中反应先进行30分钟至8小时。
优选的上述方法是其中合适的保护基团是甲氧基羰基、乙氧基羰基、叔丁氧基羰基、苄氧基羰基、苯磺酰基、对甲苯磺酰基、甲磺酰基或三氟甲磺酰基。
优选的上述方法是其中合适的保护基团是苯磺酰基、对甲苯磺酰基、甲磺酰基或三氟甲磺酰基。
优选的上述方法是其中第一种碱选自叔丁醇钠、叔丁醇钾、碳酸钠、碳酸钾、碳酸铯、氢化钠、氢化钾、碳酸钠、碳酸钾、碳酸铯、氟化钾、1,8-二氮杂双环[5.4.0]十一碳-7-烯、1,5-二氮杂双环[4.3.0]壬-5-烯、1,4-二氮杂双环[2.2.2]辛烷、吡啶、吡咯烷、三乙胺、二异丙基胺、二异丙基乙胺和二乙基异丙胺;而第二种碱选自叔丁醇钠、叔丁醇钾、碳酸钠、碳酸钾、碳酸铯、氢化钠、氢化钾、碳酸钠、碳酸钾、碳酸铯、氟化钾、1,8-二氮杂双环[5.4.0]十一碳-7-烯、1,5-二氮杂双环[4.3.0]壬-5-烯、1,4-二氮杂双环[2.2.2]辛烷、吡啶、吡咯烷、三乙胺、二异丙基胺、二异丙基乙胺和二乙基异丙胺。
优选的上述方法是其中第一种碱选自碳酸钾、碳酸铯、氢化钠和氟化钾;而第二种碱选自1,8-二氮杂双环[5.4.0]十一碳-7-烯、碳酸铯、吡咯烷、二异丙基胺、三乙胺、二乙基异丙胺和二异丙基乙胺。
优选的上述方法是其中第一种碱是碳酸钾、碳酸铯或氟化钾;而第二种碱是1,8-二氮杂双环[5.4.0]十一碳-7-烯、叔丁醇钾或碳酸铯。
优选的上述方法是其中第一种碱和第二种碱的组合(第一种碱/第二种碱)选自碳酸钾/1,8-二氮杂双环[5.4.0]十一碳-7-烯、碳酸钾/碳酸铯、碳酸铯/叔丁醇钾、碳酸铯/1,8-二氮杂双环[5.4.0]十一碳-7-烯和氟化钾/1,8-二氮杂双环[5.4.0]十一碳-7-烯以及氟化钾/碳酸铯。
优选的上述方法是其中第一种碱和第二种碱的组合(第一种碱/第二种碱)选自碳酸钾/1,8-二氮杂双环[5.4.0]十一碳-7-烯、碳酸钾/碳酸铯和碳酸铯/叔丁醇钾。
(a)任选地被1、2或3个独立地选自下列基团的取代基取代的苯基:
(a-1)卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基,
(a-2)芳基或-O-(CH2)n-芳基,而该芳基或芳基部分任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代,
(a-3)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的5-员单环芳基,
(a-4)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的6-员单环芳基,
(b)含有1、2、3或4个N的6-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(c)含有一个选自O、S和N的杂原子并且除所说的杂原子外还任选地含有1、2或3个N的5-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(d)任选地被1或2个独立地选自OH、C1-4烷基、卤素和卤素取代的C1-4烷基的取代基取代的C3-7环烷基;和
(e)任选地被1、2或3个独立地选自上述(a-1)的基团的取代基取代的苯并稠合的杂环;R1为H、C1-4烷基或卤素;R2和R3独立地为H、OH、C1-4烷氧基、C1-4烷基或者是被卤素、OH、C1-4烷氧基、NH2或CN取代的C1-4烷基;X独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-C4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基;而n为0、1、2、3或4,该方法包括用一种合适的碱在水解条件下处理下式(X)的化合物:
其中R1、R5、X、Q和n如前面所定义,得到式(VIII)的化合物。
本发明还提供一种制备式(VIII)化合物的方法:其中Q选自下列基团:
(a)任选地被1、2或3个独立地选自下列基团的取代基取代的苯基:
(a-1)卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基,
(a-2)芳基或-O-(CH2)n-芳基,而该芳基或芳基部分任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代,
(a-3)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的5-员单环芳基,
(a-4)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的6-员单环芳基,
(b)含有1、2、3或4个N原子的6-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(c)含有一个选自O、S和N的杂原子并且除所说的杂原子外还任选地含有1、2或3个N的5-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(d)任选地被1或2个独立地选自OH、C1-4烷基、卤素和卤素取代的C1-4烷基的取代基取代的C3-7环烷基;和
(e)任选地被1、2或3个独立地选自上述(a-1)的基团的取代基取代的苯并稠合的杂环;R1为H、C1-4烷基或卤素;R2和R3独立地为H、OH、C1-4烷氧基、C1-4烷基或者是被卤素、OH、C1-4烷氧基、NH2或CN取代的C1-4烷基;X独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-C4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基;而n为0、1、2、3或4,该方法包括水解下式(XII)的化合物:
其中R5为C1-6烷基,R1、X、Q和n如前面所定义。
一般合成
[R4=H或卤素] [R5=C1-6烷基]
方案1
简单地说,使式(III)化合物发生氧化性均裂性丙二酰化(主要参考文献参见J.M.Muchowski等人的Can.J.Chem.,70,1838,
1992和E.Baciocchi等人的J.Org.Chem.,58,7610,
1993)。在一种实施例中,使式(III)的化合物与从式C(R4)H(CO2R5)中R4为H或卤素,优选氯,且R5为C1-6烷基的化合物得到的合适的丙二酰基和锰(III)试剂优选三乙酸锰(III)反应。锰(III)试剂的用量通常为化学计量,但是通过使用合适的再氧化剂例如过硫酸钠还可以使其用量变为催化量,而且通常在一种助催化剂例如银(I)盐如硝酸银存在下使用。优选的反应溶剂是乙酸,但是可以使用乙酸-乙酸酐或其它质子性溶剂例如丙酸。反应优选在乙酸钠或乙酸钾存在下进行,但是可以单独在溶剂中进行。反应温度一般在室温(例如25℃)至溶剂的回流温度的范围内,优选在60-100℃下进行,但是如果必要的话,可以使用更高或更低的温度。反应时间一般为1小时-1天,优选为4-16小时,然而,如果必要的话,可以用更长或更短的时间。在中间体的情况中,式(IV)的α-乙酸基化合物通常作为主要产物得到。通过用合适的还原剂例如三烷基硅烷、α-(二甲基氨基)萘基钠、在液态氨中的锂、萘基钠(sodium naphtalenide),优选于合适的质子性溶剂如三氟乙酸中三乙基硅烷还原,可以容易地把式(IV)的化合物转变为式(V)的化合物。另外,反应可以在反应惰性的助溶剂例如二氯甲烷或1,2-二氯乙烷中进行。反应温度一般在室温至溶剂的回流温度的范围内,优选在15-100℃下进行,但是如果必要的话,可以使用更高或更低的温度。反应时间一般为几分钟至1天,优选为20分钟-5小时,然而,如果必要的话,可以用更长或更短的时间。另外,式(V)的化合物可以直接从式(III)的化合物,(i)通过三烷基硼烷例如三乙基硼烷的空气氧化的介导,从合适的一卤代丙二酸酯优选溴代丙二酸酯产生的丙二酰基得到(参见B.Giese的Radicals in organic synthesis:formation of carbon-carbon bonds.Pergamon Press,Oxford.pp.86-89,
1986,及P.G.Allies和P.B.Brindley的J.Chem.Soc.(B),1126,
1960),或者(ii)在铈(IV)盐例如硝酸铈(IV)铵存在下,从丙二酸酯产生的丙二酰基得到(例如参见E.Baciocchi等人的Tetrahedron Lett.,2763,
1986)。通过对式(V)的化合物进行标准的皂化/脱羧条件,可以容易地把它转变为式(VI)的化合物。方案2
或者,如方案2所示,按照与式(VI)化合物的制备方法相似的方式,使用如上所述的合适的反应条件,可以从合适的一烷基丙二酸酯,其中R1为C1-4烷基,W为H或卤素,优选溴,而R5为C1-6烷基,从式(III)化合物制备式(VIII)中R1为C1-4烷基的化合物(其中Z为OH的化合物(I))。
方案2
在方案2中,例如氧化剂是锰(III)试剂如三乙酸锰(III)或铈(IV)试剂例如硝酸铈(IV)铵或硫酸铈(IV)。方案3:
在另一种实施方式中,式(VIII)的化合物容易地从合适的2-氨基肉桂酸酯(IX)得到,式(IX)中B为合适的保护基团,例如甲氧基羰基、乙氧基羰基、叔丁氧基羰基(Boc)、苄氧基羰基、苯磺酰基、对甲苯磺酰基、甲磺酰基、三氟甲磺酰基、甲磺酰基或三氟甲磺酰基(优选苯磺酰基、对甲苯磺酰基、甲磺酰基或三氟甲磺酰基)。
方案3
在方案3中,使必要的2-氨基肉桂酸酯(IX)与式(XI)中Q如上所定义,而E为卤素(优选碘、溴或氯)的化合物在一种合适的碱存在下反应。合适的碱例如为碱金属或碱土金属的醇盐、碳酸盐、氟化物或氢化物,例如叔丁醇钠、叔丁醇钾、碳酸钠、碳酸钾、碳酸铯、氢化钠、氟化钾或氢化钾。优选的反应惰性的溶剂包括但是不限于丙酮、甲乙酮、乙腈、N,N-二甲基甲酰胺(DMF)、N,N-二甲基乙酰胺(DMA)、二甲基亚砜(DMSO)、二噁烷或四氢呋喃(THF)。反应温度优选为-40℃-溶剂的回流温度(例如200℃),通常在0-100℃的范围,但是如果必要的话,可以使用更高或更低的温度。反应时间一般为2分钟-1天,优选为30分钟-8小时,但是可以用更长或更短的时间。例如,当反应在室温下(例如25℃)进行时,可以分离出中间体二氢吲哚(X)。在更高的温度下(例如40-100℃)进行反应可以形成吲哚(XII)。通常不把中间体二氢吲哚(X)分离出来,而是(i)在本领域技术人员已知的标准条件下把伴随形成的吲哚环直接水解为式(VIII)的化合物,或者(ii)通过使用合适的碱例如碱金属或碱土金属碳酸盐如碳酸钠、碳酸钾或碳酸铯,或有机碱例如1,8-二氮杂双环[5.4.0]十一碳-7-烯(DBU)、1,5-二氮杂双环[4.3.0]壬-5-烯(DBN)、1,4-二氮杂双环[2.2.2]辛烷(DABCO)、吡啶、吡咯烷、三乙胺、二异丙基胺、二异丙基乙胺、二乙基异丙胺、Hunig碱、叔丁醇钾、叔丁醇钠或类似物,或合适的氧化剂例如硝酸铈(IV)铵(CAN)、氧化锰(IV)、三乙酸锰(III)、乙酸铜(II)/空气、四氯苯醌、2,3-二氯-5,6-二氰基-1,4-苯并醌(DDQ)、N-甲基吗啉-N-氧化物或类似物把它转变为式(XII)的化合物(例如参见H.Dumoulin等人的J.Heterocycl.Chem.,32,1703,
1995;H.Rapoport等人的Tetrahedron Lett.,5053,
1991;P.Martin等人的Helv.Chim.Acta,77,111,
1994;Y.Kikugawa等人的J.Chem.Soc.Perkins Trans 1,7,1401,
1984;A.Goti等人的Tetrahedron Lett.,6567,
1996;L.S.Liebeskind等人的J.Org.Chem.,61,2594,
1996)。优选的反应惰性的溶剂包括但是不限于丙酮、甲乙酮、乙腈、二噁烷或四氢呋喃(THF)。反应温度优选在0℃-溶剂的回流温度,通常在15-60℃的范围内,但是如果必要的话,可以使用更高或更低的温度。反应时间一般为几分钟-1天,优选为30分钟-8小时,但是如果必要的话,可以用更长或更短的时间。在标准条件下,式(XII)的化合物可以容易地水解为式(VIII)的化合物。反应式4:
方案4
例如,按照T.Fukuyama在J.Am.Chem.Soc.,116,3127,(1994)中所描述的方法,用三烷基氢化锡例如三丁基氢化锡通常在自由基引发剂例如2,2’-氮杂双异丁腈(AIBN)存在下处理式(XIII)中R1、R5、X和n如上所定义的化合物,通过一种分子内自由基环化,得到中间体2-甲锡烷基吲哚(XIV)。随后按照Stille的方法(例如参见J.K.Stille等人的J.Am.Chem.Soc.,109,813,5478,(1987)和J.Am.Chem.Soc.,106,813,4833,(1984)),用其中Q和E如上所定义的酰卤在一种合适的钯催化剂存在下处理原位产生的中间体(XIV),得到吲哚(XII),用常规方法可以把该吲哚水解为式(VIII)的化合物。
钯催化剂的例子为四(三苯基膦)钯(O)、二氯化双(三苯基膦)钯(II)、双(二亚苄基丙酮)钯(O)、苄基(氯)双(三苯基膦)钯(II)、双(乙腈)二氯化钯(II)。方氨5:
方案5
例如,使式(XV)中R1、X和n如上所定义的化合物与式Q-C(O)-A的化合物反应,得到式(VIII)的化合物或式(XVI)的化合物(例如参见U.Pindur等人的Liebigs Ann.Chem.,601(1991)和C.J.Moody等人的J.Chem.Soc.Perkin Trans.1,3249(1988)),用常规方法可以把该化合物水解为式(VIII)的化合物(例如参见E.B.Fray等人的Tetrahedron,49,439(1993)和U.Pindur等人的J.Heterocycl.Chem.,29,145(1992))。在式A-C(O)-Q的化合物中,定义A使得A-C(O)-Q的化合物例如为酰卤、羧酸、羧酸酐、混合羧酸磺酸酸酐或类似物。反应可以在有或没有催化剂存在下进行,优选在诸如三氟化硼-乙醚、氯化锡(IV)、氯化铝、氯化铁、氯化锌、碘、铁或类似物的催化剂存在下进行。优选的反应惰性的溶剂包括但是不限于乙醚、二氯甲烷、1,2-二氯乙烷、二硫化碳、硝基苯或硝基甲烷。反应温度优选在-78-210℃的范围内,通常在-10℃-溶剂的回流温度的范围内,但是如果必要的话,可以使用更高或更低的温度。反应时间一般为几分钟-1天,优选为30分钟-8小时,但是如果必要的话,可以用更长或更短的时间。方案6:
按照本领域技术人员已知的常规方法,可以容易地把上述方案中所述的式(VI)和(VII)的乙酸化合物转变为相应的酰胺,式(XVII)和(XVIII)化合物或酯,式(XII)化合物。
方案6
如方案6所示,通过用其中R2、R3、Y和r如前面所定义的合适的胺在合适的偶合剂存在下处理必要的式(VI)和(VIII)乙酸化合物,可以容易地制备式(XVII)和(XVIII)的化合物,偶合剂的例子为但是不限于1-(二甲基氨基丙基)-3-乙基碳化二亚胺(WSC)、N,N’-二环己基碳化二咪唑(DCC)、碳酰二咪唑、二乙基磷酰氰酸酯(DEPC)等。优选的反应惰性的溶剂包括但是不限于丙酮、乙腈、二氯甲烷、1,2-二氯乙烷、N,N-二甲基甲酰胺(DMF)、N,N-二甲基乙酰胺(DMA)、二甲基亚砜(DMSO)、二噁烷、四氢呋喃(THF)或吡啶。反应温度优选在-40-150℃的范围内,通常在15℃-溶剂的回流温度的范围内,但是如果必要的话,可以使用更高或更低的温度。反应时间一般为几分钟-1天,优选为30分钟-8小时,但是如果必要的话,可以用更长或更短的时间。也可以用常规方法容易地把式(VI)和(VIII)的化合物转变为相应的酯。方案7 (其中B为合适的保护基团,R5为C1-6烷基,E为卤素,Q、X和n如上所定义)。
在方案7中,式7-I的反应原料可以按照本领域技术人员熟知的方法制备,包括R.W.Carling、P.D.Leeson、K.Moore、J.D.Smith、C.R.Moyes在
J.Med.Chem.,1993,p3397-3408中描述的一个或多个合成方法。
通过用一种碱和一种亲电子试剂在合适的溶剂中处理式7-I的化合物可以制备式7-II的化合物。合适的碱包括例如三乙胺、二异丙基乙胺或任选地被1-3个(C1-C4)烷基取代的吡啶,优选吡啶。合适的亲电子试剂包括甲磺酰氯或甲磺酸酐,或苯磺酰氯,其中所说的苯磺酰基中的苯基任选地包含1或2个选自卤素、硝基和(C1-C4)烷基取代基。合适的溶剂包括二氯甲烷、二氯乙烷、甲基叔丁基醚、二异丙基醚或甲苯,优选二氯甲烷。上说反应的温度可以为0-50℃,优选在大约室温(20-25℃)下反应大约1-30小时,优选18小时。
通过用第一种碱和式7-III的烷基化剂在一种溶剂存在下处理,然后与第二种碱反应,再与一种酸反应,可以从式7-II的化合物制备式7-IV的化合物。合适的第一种碱包括碳酸钾、碳酸氢钾、碳酸氢钠、碳酸钠或碳酸铯,优选碳酸钾。合适的溶剂包括N,N-二甲基乙酰胺、N,N-二甲基甲酰胺、甲乙酮、丙酮或四氢呋喃(THF),优选N,N-二甲基乙酰胺。上述所说的反应在大约0-100℃的温度下,优选在室温下(20-25℃)下进行大约10分钟-5小时,典型地进行15分钟的时间。合适的第二种碱包括一种碱例如氢氧化钠、氢氧化钾、碳酸钠、碳酸钾、叔戊醇钠(然后是水)、甲醇钠(然后是水)或叔丁醇钾(然后是水)的水溶液,优选氢氧化钠的水溶液。与第二种碱的反应在大约20-120℃,优选100℃的温度下进行大约1小时-24小时,典型地进行8小时的时间。合适的酸包括盐酸、氢溴酸、硫酸或氯化铵水溶液,优选盐酸水溶液。与酸的反应在大约0-50℃,优选大约20-25℃的温度下进行大约1/2小时-6小时,典型地进行大约1小时的时间。
或者,可以分步把式7-II的化合物转变为式7-IV的化合物。通过用一种碱和式7-III的烷基化剂在一种溶剂存在下处理,可以从式7-II的化合物制备式7-V的化合物。合适的碱包括碳酸钾、碳酸氢钾、碳酸氢钠、碳酸钠或碳酸铯,优选碳酸钾。合适的溶剂包括N,N-二甲基乙酰胺、N,N-二甲基甲酰胺、甲乙酮、丙酮或四氢呋喃,优选N,N-二甲基乙酰胺。上述所说的反应可以在大约0-50℃的温度下,优选在室温下(20-25℃)下进行大约10分钟-40分钟,典型地进行30分钟的时间。
通过与一种碱在一种溶剂的存在下反应,可以从式7-V的化合物制备式7-VI的化合物。合适的碱包括碳酸钾、碳酸氢钾、碳酸氢钠、碳酸钠或碳酸铯,优选碳酸钾。合适的溶剂包括N,N-二甲基乙酰胺(DMA)、N,N-二甲基甲酰胺、甲乙酮、丙酮或四氢呋喃,优选N,N-二甲基乙酰胺。上述所说的反应可以在大约0-50℃的温度下,优选在室温下(20-25℃)下进行大约1小时-6小时,优选进行4小时的时间。
通过与一种碱在一种合适的溶剂中反应,可以从式7-VI的化合物制备式7-VII的化合物。合适的碱包括1,8-二氮杂双环[5.4.0]十一碳-7-烯、1,5-二氮杂双环[4.3.0]壬-5-烯、1,1,3,3-四甲基胍、叔戊醇钠、甲醇钠或叔丁醇钾,优选1,8-二氮杂双环[5.4.0]十一碳-7-烯、甲醇钠或叔丁醇钾。合适的溶剂包括N,N-二甲基甲酰胺、N,N-二甲基乙酰胺、甲乙酮、丙酮或四氢呋喃,优选N,N-二甲基乙酰胺。上述所说的反应可以在大约0-100℃的温度下,优选在室温下(20-25℃)下进行大约30分钟-5小时,优选进行1小时的时间。
通过用一种碱在一种合适的溶剂中处理,可以从式7-VII的化合物制备式7-IV的化合物。合适的碱包括氢氧化钠、氢氧化钾、碳酸钠、碳酸钾、碳酸氢钠、碳酸氢钾、叔戊醇钠、甲醇钠、乙醇钠或叔丁醇钾,优选氢氧化钠。合适的溶剂包括甲醇、乙醇、异丙醇或四氢呋喃与水的混合物,优选含有水的甲醇。上述所说的反应可以在大约10-100℃的温度下,优选在室温下(20-25℃)下进行大约12-48小时,优选进行24小时的时间,得到式7-IV化合物的羧酸盐,然后用一种酸处理,得到式7-IV的化合物。
式7-VI的化合物含有不对称原子,因此以不同的对映体和非对映体形式存在。根据非对映体的物理化学性质的不同,用本领域技术人员熟知的方法例如通过色谱或分步结晶可以把非对映体的混合物分离成单个的非对映体。所有这些异构体包括非对映体混合物和纯粹的对映体的用途被认为是本发明的一部分。
上述一般合成中所用的原料可以通过本领域技术人员已知的常规方法得到。在附加的非限定性的实施例中描述了制备这些原料的方法,提供这些实施例只是为了说明。另外,必要的原料可以通过与后面所述类似的方法或其改进方法得到。
上述一般合成中所记载的和在后面的试验实施例中所描述的产品可以通过标准方法分离,并且可以用本领域技术人员已知的常规手段例如蒸馏、结晶或色谱技术纯化。
其中所述的某些化合物含有一个或多个不对称中心,并且能以各种立体异构体形式存在。本发明考虑了所有这些可能的立体异构体及其外消旋体和经过拆分的对映体纯的形式及其药学上可接受的盐。
本发明的某些化合物能与无机酸或有机酸形成加成盐。式(I)化合物的药学上可接受的酸盐是那些形成无毒的加成盐的酸加成盐,这样的盐包括但是不限于盐酸盐、氢溴酸盐、硫酸盐或硫酸氢盐、乙酸盐、苯甲酸盐、苯磺酸盐、柠檬酸盐、富马酸盐、葡糖醛酸盐、马尿酸盐、乳酸盐、酒石酸盐、糖二酸盐、丁二酸盐、顺丁烯二酸盐、甲磺酸盐、对甲苯磺酸盐、磷酸盐和双羟萘酸盐(即4,4’-亚甲基-双(3-羟基-2-萘甲酸盐))。药学上可接受的酸盐可以按照常规技术制备。
本发明的某些化合物能形成药学上可接受的无毒的阳离子。式(I)化合物的药学上可接受的无毒的阳离子可以按照常规技术制备,例如使所说的化合物与化学计量的合适的碱金属或碱土金属(钠、钾、钙和镁)氢氧化物或醇盐在水中或合适的有机溶剂例如乙醇、异丙醇或其混合物中接触。
本发明的保护范围还包括式(I)化合物的生物前体(也称为前体药物)。式(I)化合物的生物前体是式(I)化合物的一种化学衍生物,它在生物体系中容易回变为式(I)的母体化合物。特别地,当一种式(I)化合物的生物前体对哺乳动物受治者例如人给药并被其吸收后,它回变为式(I)的母体化合物。当本发明的式(I)化合物可以形成溶剂化物例如水合物时,这样的溶剂化物包括在本发明的保护范围内。
式(I)化合物的药物前体的一个例子是式(I)中吲哚环的1位被一个选自羟甲基、-C(O)-C1-4烷基、-C(O)-(NH2)CH-(C1-4烷基)、-C(O)-苯基、-CH2NHC(O)-芳基、-CH2-C1-4烷基-O-C(O)-C1-4烷基、-C1-4烷基-吡啶基、-C(O)CH2NR2和-CH2N(C1-4烷基)2的基团取代的化合物。
式(I)化合物的药物前体的另一个例子是式(I)中羧基被一个选自C1-4烷基、-CH2-C1-4烷基-O-C(O)-C1-4烷基、-CH2-C1-4烷基-O-C(O)-N(C1-4烷基)2、-CH2C(O)N(C1-4烷基)2、-CH2-C1-4烷基-O-C(O)-O-C1-4烷基、乙基-OH和CH2CO2H的基团取代的化合物。
本发明的式(I)化合物可以通过口服、非肠胃给药或局部给药方式向哺乳动物给药。一般来说,最希望以0.01mg-100mg/kg体重/天的剂量给人给药这些化合物,尽管必要时将根据接受治疗的受治者的体重、性别和身体状况、被治疗疾病的状况和选定的给药方式而改变剂量。但是为了治疗上述疾病,0.01mg-10mg/kg体重/天的剂量水平,一次性或分多次剂量是最希望的。
本发明的化合物可以通过上述的任何一种给药途径单独给药或与药学上可接受的载体或稀释剂组合给药,且这种给药可以一次性或分多次完成。更具体地,本发明的新治疗试剂可以以多种不同的剂型给药,即它们可以与各种药学上可接受的惰性载体组合成片剂、胶囊、锭剂、糖锭、硬糖、粉末、喷雾剂、霜剂、油膏、栓剂、凝胶、冻胶、糊剂、洗液、软膏、水性悬浮液、注射液、酏剂、浆等。这样的载体包括固体稀释剂或填料、无菌的水介质和各种无毒的有机溶剂等。而且,口服的药物组合物可以适当地增甜和/或矫味。一般来说,这种剂型的治疗有效的本发明的化合物以5%-70%重量,优选10%-50%重量范围内的浓度水平存在。
用于口服时,可以把含有各种赋形剂例如微晶纤维素、柠檬酸钠、碳酸钙、磷酸氢二钾和甘氨酸的片剂与各种崩解剂例如淀粉(优选玉米、马铃薯或木薯淀粉)、藻酸和某些复合硅酸盐以及颗粒粘合剂如聚乙烯基吡咯烷酮、蔗糖、明胶和阿拉伯胶一起使用。另外,润滑剂例如硬脂酸镁、月桂基硫酸钠和滑石经常用于制造片剂。在明胶胶囊中也可以使用类似的固体组合物作为填料,优选的这种材料也包括乳糖或奶糖以及高分子量的聚乙二醇。当要把水性悬浮液和/或酏剂用于口服时,可以把活性组分与各种甜味剂或调味剂、着色物质或染料以及(如果需要的话)乳化剂和/或悬浮剂、连同稀释剂(如水、乙醇、丙二醇、甘油及其各种组合)一起混合。
用于非肠胃给药时,可以使用本发明的化合物在芝麻油或花生油中的溶液或者在丙二醇水溶液中的溶液。如果需要的话,水性溶液应当合适地缓冲(优选pH>8),并且先使液体稀释剂成为等渗的。这些水性溶液适于静脉内注射。油性溶液适于动脉内注射、肌肉内注射和皮下注射。按照本领域技术人员熟知的标准制药技术容易在无菌条件下制备所有这些溶液。另外,当治疗皮肤炎症时,本发明的这些化合物也可以局部给药,并且优选以乳膏、冻胶、凝胶、糊剂、油膏等方式按照标准的药学操作给药。
式(I)的化合物也可以以用于直肠或阴道给药的活性组分的栓剂形式给药。通过把活性组分与一种在室温下为固体(例如10-32℃)但是在直肠温度下为液体并且在直肠或阴道中会融化而释放出活性组分的合适的非刺激性的赋形剂混合。这样的材料是聚乙二醇、可可油、栓剂和蜡。
用于颊给药时,组合物可以采取按照常规方式配制的片剂或锭剂形式。与其它药物组合:
式I的化合物可用于但是不限于治疗受治者的炎症,用于治疗其它与炎症相关的疾病例如用作止痛剂用于治疗疼痛和头痛,或者用作退烧药用于治疗发烧。例如,本发明的组合可用于治疗关节炎,包括但是不限于类风湿性关节炎、脊椎关节病、痛风性关节炎、骨关节炎、全身性红斑狼疮和青少年关节炎。本发明的这些组合将可用于治疗哮喘、支气管炎、经期痉挛性疼痛、腱炎、滑囊炎和皮肤病例如牛皮癣、湿疹、烧伤和皮炎。本发明的组合还可用于治疗肠胃病例如炎症性肠病、节段性回肠病、胃炎、过敏性肠综合症和溃疡性结肠炎,用于预防结肠直肠癌。本发明的组合可用于治疗这些疾病如血管病、偏头痛、结节性动脉周炎、甲状腺炎、再生障碍性贫血、何杰金氏病、硬皮病、风湿性发烧、I型糖尿病、重症肌无力、多发性硬化、肉瘤病、肾病综合症、贝赫切特综合症、多肌炎、龈炎、过敏、结膜炎、伤后肿胀、心肌缺血等中的炎症。本发明的组合可用于治疗某些中枢神经系统疾病例如早老性痴呆症和痴呆症。本发明的组合可用作消炎药例如用于治疗关节炎,并且还具有有害的副作用显著小的附加的优点。这些组合也用于治疗过敏性鼻炎、呼吸窘迫综合症、内毒素休克综合症、动脉粥样硬化以及由中风、局部缺血和创伤引起的中枢神经系统损伤。
式(I)的化合物将可用于部分或完全替代制剂中常用的NSAID’s,其中把它们与其它试剂或组份同时给药。因此,本发明包括用于治疗上述COX-2介导的疾病的药物组合物,该组合物包括无毒的治疗有效量的式(I)化合物和一种或多种组份例如另一种去痛剂,包括对乙酰氨基酚和菲那西丁;增效剂,包括咖啡因;H2-拮抗剂、氢氧化铝或镁、二甲硅油、一种减充血剂包括苯福林、苯丙醇胺、伪麻黄碱、苯甲唑啉、肾上腺素、萘甲唑啉、赛洛唑啉、丙己君或左旋氧化肾上腺素;一种镇咳剂包括可待因、氢可酮、卡拉美芬、咳必清或右旋甲吗喃;一种前列腺素包括米索前列醇、恩前列素、利奥前列素、奥诺前列醇或罗沙前列醇;一种利尿剂;一种有或没有镇静作用的抗组胺药;一种抗癌剂例如血管抑制素和内抑制剂;抗早老性痴呆剂例如Doepezil和他克林盐酸盐;和TNF-α抑制剂例如Etanercept。
这些环加氧酶抑制剂还可以与WO96/28145中公开的一种氧化氮抑制剂组合使用。
本发明还包括用于治疗上述COX-2介导的疾病的药物组合物,包含一种无毒的治疗有效量的式(I)化合物和WO97/11701中公开的一种或多种抗溃疡剂和/或前列腺素。
可以使用的前列腺素包括米索前列醇、加-减11α,16-二羟基-16-甲基-9-氧代前列腺素-13E-烯-1-酸甲酯;enisoprost和7-[2B-[6-(1-环戊烯-1-基)-4-羟基-4-甲基-1E,5E-己二烯]-3α-羟基-5-氧代1R,1α-环戊基]-4Z-庚烯酸甲酯。属于本发明保护范围的前列腺素还包括阿巴前列素、恩前列素、利奥前列素、诺氯前列素、美昔前列素、奥诺前列醇、地莫前列素、替前列胺和罗沙前列醇。
本发明的化合物还可用于共治疗,部分或完全替代其它常用的消炎药,例如与类固醇、5-脂氧化酶抑制剂、LTB4拮抗剂和LTA4水解酶抑制剂一起使用。
WO97/29774中公开了LTB4的例子。合适的LTB4抑制剂的例子中包括依布西啉、Bayer Bay-x-1005、Ciba Geigy化合物CGS-25019C、LeoDenmark化合物ETH-615、Lilly化合物LY-293111、Ono化合物ONO-4057、Terumo化合物TMK-688、Lilly化合物LY-213024,264086和292728、Ono化合物ONO-LB457、Searle化合物SC-S3228、钙三醇、Lilly化合物LY-210073,LY-223982,LY233469和LY255283、Ono化合物ONO-LB-448、Searle化合物SC-41930,SC-50605和SC-51146以及SK&F化合物SKF-104493。优选地,LTB4抑制剂选自依布西啉、BayerBay-x-1005、Ciba Geigy化合物CGS-25019C、Leo Denmark化合物ETH-615、Lilly化合物LY-293111、Ono化合物ONO-4057和Terumo化合物TMK-688。
WO97/29776中公开了5-LO抑制剂的例子。合适的5-LO抑制剂的例子中包括马索丙考、替尼达帕、弃白通、pranlukast、替波沙林、利洛吡司、flezelastine盐酸盐、enazadrem磷酸盐和bunaprolast。
WO97/29774中公开了LTA4水解酶抑制剂的例子,合适的LTA4水解酶抑制剂中包括Rhone-Poulene Rorer RP-64966。
给药本发明的化合物可用于预防或治疗的目的。这里所用的方法和组合物可以单独使用或与本领域技术人员已知的用于预防或治疗血管发生的其它治疗方法一起使用。另外,这里所说的方法和组合物可以用作辅助治疗。例如,环加氧酶-2抑制剂可以单独给药或与其它抗肿瘤剂或其它生长抑制剂或其它药物或营养物一起给药。
已有大量的抗肿瘤剂进入商业、临床评价和临床前开发中,从中可以选出与药物化学治疗一起使用、用于治疗血管发生的药剂。这样的抗肿瘤剂分为几大类,即抗生素型药剂、烷基化剂、抗代谢药剂、激素、免疫制剂、干扰素型药剂和混杂制剂类。另外可以使用其它抗肿瘤剂例如金属-基质蛋白酶抑制剂(MMP),如MMP-13抑制剂包括batiastat、marimastat、Agouron Pharmaceuticals AG-3340和Roche R0-32-3555或α,β,抑制剂。
可以与一种任选的环加氧酶-2抑制剂组合使用的第一族抗肿瘤剂由抗代谢型抗肿瘤剂组成。合适的抗代谢型抗肿瘤剂可以选自5-Fu-纤维蛋白原、棘叶酸、氨基噻二唑、brequinar钠、卡莫氟、Ciba-GeityCGP-30694、环戊基胞嘧啶、阿糖胞苷磷酸硬脂酸酯、阿糖胞苷缀合物、Lilly DATHF、Merrel Dow DDFC、地扎呱宁、二脱氧胞苷、二脱氧鸟苷、didox、Yoshitomi DMDC、去氧氟尿苷、Wellcome EHNA、Merck&Co.EX-015、法扎拉滨、氟尿苷、氟达拉宾磷酸酯、5-氟尿嘧啶、N-(2’-呋喃基)-5-氟尿嘧啶、Daiichi Seiyaku F0-152、ispropyl pyrrolizine、LillyLY-188011、Lilly LY-264618、methobenzaprim、甲氨喋呤、WellcomeMZPES、降精脒、NCI NSC-127716、NCI NSC-264880、NCI NSC-39661、NCI NSC-612567、Warner-Lambert PALA、喷司他丁、吡曲克辛、普卡霉素、Asahi Chemical PL-AC、Takeda TAC-788、硫代鸟嘌呤、噻唑呋啉、Erbamont TIF、三甲曲沙、酪氨酸激酶抑制剂、酪氨酸蛋白激酶抑制剂、Taiho UFT和uricytin。
可以与一种任选的环加氧酶-2抑制剂组合使用的第二族抗肿瘤剂由烷基化型抗肿瘤剂组成。合适的烷基化型抗肿瘤剂可以选自Shionogi254-S、氧代磷酰胺类似物、六甲密胺、阿那昔酮、Boehringer MannheimBBR-2207、bestrabucil、布多替钛、Wakunaga CA-102、卡铂、卡莫司汀、Chinoin-139、Chinoin-153、苯丁酸氮芥、顺铂、环磷酰胺、AmericanCyanamid CL-286558、Sanofi CY-233、cyplatate、Degussa D-19-384、Sumimoto DACHP(Myr)2、二苯基螺莫司汀、二铂合细胞生长抑制剂、Erba司替霉素衍生物、Chugai DWA-2114R、ITI E09、依莫司汀、ErbamontFCE-24517、雌莫司汀磷酸钠、福莫司汀、Unimed G-6-M、ChinoinGYKI-17230、hepsul-fam、异环磷酰胺、异丙铂、iomustine、马磷酰胺、二溴卫矛醇、Nippon Kayaku NK-121、NCI NSC-264395、NCI NSC-342215、奥沙利铂、Upjohn PCNU、泼尼莫司汀、Proter PTT-II9、雷莫司汀、司莫司汀、SmithKline SK&F-101772、Yakult Honsha SN-22、螺莫司汀、Tanabe Seiyaku TA-077、牛黄莫司汀、替莫唑胺、替罗昔隆、四铂和trimelamol。
可以与一种任选的环加氧酶-2抑制剂组合使用的第三族抗肿瘤剂由抗生素型抗肿瘤剂组成。合适的抗生素型抗肿瘤剂可以选自Taiho4181-A、阿柔比辛、放线菌素D、actinoplanone、Erbamont ADR-456、aeroplysinin衍生物、Ajinomoto AN-201-II、Ajinomoto AN-3、NipponSoda茴香霉素、蒽环素、连氮基霉素-A、bisucaberin、Bristol-MyersBL-6859、Bristol-Myers BMY-25067、Bristol-Myers BMy-25551、Bristol-Myers BMY-26605、Bristol-Myers BMY-27557、Bristol-MyersBMY-28438、硫酸博来霉素、泻根静止素-1、Taiho C-1-2、Kyowa HakkoDC-79、Kyowa Hakko DC-88A、Kyowa Hakko DC-89A1、Kyowa Hakko DC92-B、ditrisarubicin B、Shionogi DOB-41、阿霉素、阿霉素-纤维蛋白原、elsamicin-A、表柔比星、erbstatin、esperamicin-Al、esperamicin-Alb、Erbamont FCE-21954、Fujisawa FK-973、磷曲星、Fujisawa FR-900482、glidobactin、gregatin-A、grincamycin、杀草霉素、伊达比星、隐杯伞素、kazusamycin、kesarirhodins、Kyowa HakkoKM-5539、Kirin Brewery KRN-8602、Kyowa Hakko KT-5432、Kyowa HakkoKT-5594、Kyowa Hakko KT-6149、American Cyanamid LL-D49194、MeijiSeika ME 2303、美诺立尔、丝裂霉素、米托蒽醌、SmithKline M-TAG、neoenactin、Nippon Kayaku NK-313、Nippon Kayaku NKT-O1、SRIInternational NSC-357704、氧代溶菌素、oxaunomycin、培洛霉素、pilatin、吡柔比星、porothramycin A、Tobishi RA-I、雷帕霉素、rhizoxin、罗多比星、sibanomicin、siwenmycin、Sumitomo SM-5887、Snow Brand SN-706、Snow Brand SN-07、sorangicin-A、司帕霉素、SSPharmaceutical SS-21020、SS Pharmaceutical SS-7313B、SSPharmaceutical SS-9816B、司替霉素B、Taiho 4181-2、他利霉素、TakedaTAN-868A、terpentecin、thrazine、tricrozarin A、Upjohn U-73975、Kyowa Hakko UCN-10028A、Fujisawa WF-3405、Yoshitomi Y-2S024和佐柔比星。
可以与任选的环加氧酶-2抑制剂组合使用的第四族抗肿瘤剂由一混杂族抗肿瘤剂组成,选自α-胡萝卜素、α-二氟甲基-精氨酸、阿维A、Biotec AD-5、Kyorin AHC-52、鸡骨常山碱、氨萘非特、amphethinile、安吖啶、血管静止素、ankinomycin、抗肿瘤素AIO、抗肿瘤素A2、抗肿瘤素A3、抗肿瘤素A5、抗肿瘤素AS2-1、Henkel APD、阿非迪霉素、甘氨酸盐、门冬酰胺酶、avarol、燕茜素、batracylin、benfluron、氯苯酰色氨酸、Ipsen-Beaufour BIM-23015、比生群、Bristo-MyersBMY-40481、Vestar硼-IO、溴硫磷酰胺、Wellcome BW-502、WellcomeBW-773、caracemide、carmethizole盐酸盐、Ajinomoto CDAF、氯磺胺喹噁酮、Chemes CHX-2052、Chemes CHX-i00、Warner-Lambert CI-921、Warner-Lambert CI-937、Warner-Lambert CI-941、Warner-LambertCI-958、clanfenur、claviridenone、ICN化合物1259、ICH化合物4711、Contracan、Yakult Honsha CPT-11、crisnatol、curaderm、细胞松弛素B、阿糖胞苷、cytocytin、Merz D-609、DABIS马来酸盐、达卡巴嗪、达替氯胺、didemnin-B、二血卟啉醚、二氢lenperone、地那啉、司替霉素、Toyo Pharmar DM-75、Daiichi Seiyaku DN-9693、elliprabin、依利醋铵、Tsumura EPMTC、麦角胺、依托泊甙、阿维A酯、芬维A胺、Fujisawa FR-57704、硝酸镓、12-苯甲酰瑞香毒素、Chugai GLA-43、GlaxoGR-63178、grifolan NMF-5N、十六碳烷基胆碱磷酸、Green Cross H0-221、高三尖杉酯碱、羟基脲、BTG ICRF-187、伊莫福新、异谷酰胺、异维A酸、Otsuka JI-36、Ramot K-477、Otsuak K-76COONa、Kureha ChemicalK-AM、MECT Corp KI-8110、American Cyanamid L-623、leukoregulin、Ionidamine、Lundbeck LU-23-112、Lilly LY-186641、NCI(US)MAP、marycin、Merrel Dow MDL-27048、Medco MEDR-340、merbarone、merocyanine衍生物、甲基苯胺基吖啶、Molecular Genetics MGI-136、minactivin、米托萘胺、米托喹酮、莫哌达醇、莫维A胺、Zenyaku KogyoMST-16、N-(视黄酰基)氨基酸、Nisshin Flour Milling N-021、N-酰化的-脱氢丙氨酸、nafazatrom、Taisho NCU-190、诺考达唑衍生物、Normosang、NCI NSC-145813、NCI NSC-361456、NCI NSC-604782、NCINSC-95580、奥曲肽、Ono ONO-112、oquizanocine、Akzo Org-10172、胰酶静止素、帕折普汀、Warner-Lambert PD-111707、Warner-LambertPD-115934、Warner-Lambert PD-131141、Pierre Fabre PE-1001、ICRT多肽D、piroxantrone、多聚血卟啉、polypreic酸、苯氧丙酚胺卟啉、probimane、丙卡巴肼、proglurnide、Invitron蛋白酶nexin I、TobishiRA-700、雷佐生、Sapporo Breweries RBS、局限曲菌素-P、retelliptine、视黄酸、Rhone-Poulenc RP-49532、Rhone-Poulenc RP-56976、SmithKline SK&F-104864、Sumitomo SM-108、Kuraray SMANCS、SeaPharmSP-10094、spatol、螺环丙烷衍生物、锗螺胺、Unimed、SS PharmaceuticalSS-554、strypoldinone、Stypoldione、Suntory SUN 0237、Suntory SUN2071、超氧化物歧化酶、Toyama T-506、Toyama T-680、紫杉酚、TeijinTEI-0303、替尼泊甙、thaliblastine、Eastman Kodak TJB-29、生育三烯酚、Topostin、Teijin TT-82、Kyowa Hakko UCN-O1、Kyowa HakkoUCN-1028、ukrain、Eastman Kodak USB-006、硫酸长春碱、长春新碱、长春地辛、vinestramide、长春瑞宾、长春曲醇、长春利定、醉茄内酯和Yamanouchi YM-534。
可以与本发明的化学治疗一起使用的放射性保护剂的例子是AD-5、adchnon、氨磷汀类似物、骨胺苷肽、dimesna、1-102、MN-159、N-酰化的-脱氢丙氨酸、TGF-Genentech、噻丙莫特、氨磷汀、WR-151327、FUT-187、透皮酮洛芬、萘丁美酮、超氧化物歧化酶(Chiron)和超氧化物歧化酶Enzon。
可以在文献中找到制备上述抗肿瘤剂的方法。例如在USP3,590,028和US4,012,448中描述了制备阿霉素的方法;在EP780386、WO97/20824、WO96/15096中描述了制备金属-基质蛋白酶抑制剂的方法;在EP524,101中描述了制备SOD模拟物的方法;在WO97/08174中描述了制备α,β,抑制剂的方法。
另外,为了最安全最有效地进行治疗,可以把选择性的COX-2抑制剂与其它消炎药一起给药。这些消炎药包括:NSAID’s、COX-1的选择性的抑制剂和白三烯途径的抑制剂,包括5-脂氧化酶抑制剂。NSAID’s的例子包括吲哚美辛、萘普生、布洛芬、水杨酸衍生物例如阿斯匹灵、双氯芬酸、酮咯酸、吡罗西康、美洛西康、甲芬那酸、舒林酸、托美汀钠、佐美酸、苯氧苯丙酸、保太松、羟布宗、尼美舒利、zaltoprofen和letodolac。
评价生物活性的方法:
本发明的式(I)化合物的活性通过下列试验证明。体外试验基于人体细胞的COX-1试验
用3.8%的柠檬酸钠溶液把从健康的志愿者得到的人周围血稀释到1/10体积。用含有12mM Tris-HCl(pH7.4)和1.2mM EDTA的0.14M氯化钠洗涤刚刚得到的富含血小板的血浆。然后用血小板缓冲液(含有0.2%BSA和20mM Hepes的Hanks缓冲液(不含Ca))洗涤血小板。最后把洗涤后的人血小板(HWP)悬浮于浓度为2.85×108个细胞/ml的血小板缓冲液中,在室温下储存备用。把HWP悬浮液(每份70μl,最终浓度2.0×107个细胞/ml)置于一个96-孔的U形底培养皿中,每份加入10μl 12.6mMCaCl2,在37℃,把血小板与A23187(最终浓度10μM,Sigma)和溶于DMSO(最终浓度小于0.01%)中的试验化合物(0.1-100μM)一起培养15分钟。加入EDTA(最终浓度7.7mM)使反应停止,使用放射免疫试剂盒(Amersham)按照生产商的程序定量测定上清液中的TxB2。基于人体细胞的COX-2试验用hIL-1β诱导COX-2后COX-2活性的抑制
按照以前所述的方式(Moore等人,Inflam.Res,45,54,1996)进行基于人体细胞的COX-2试验。把96-孔的U形底培养皿中的铺满的人脐静脉内皮细胞(HUVECs,Morinaga)用100μl含有2%FCS的RPMI1640洗涤,在37℃与hIL-1β(最终浓度300单位/ml,R&D Systems)一起温育24小时。洗涤后,在37℃用溶于Hanks缓冲液中的A23187(最终浓度30μM)刺激活化后的HUVECs 15分钟,Hanks缓冲液含有0.2%BSA、20mM Hepes和试验化合物(0.1nM-100μM)的DMSO溶液(最终浓度小于0.01%)。充分稀释后,使用放射免疫试剂盒(Amersham)按照生产商的程序定量测定上清液中6-酮-PGF1α-一种PGI2的稳定代谢物。诱导期间对COX-2的抑制
把96-孔的U形底培养皿中的铺满的人脐静脉内皮细胞(HUVECs,Morinaga)用100μl含有2%FCS和试验化合物(0.1nM-100μM)的DMSO溶液(最终浓度小于0.01%)的RPMI1640洗涤,在37℃与hIL-1β(最终浓度300单位/ml,R&D Systems)一起温育24小时。洗涤后,在37℃用溶于Hanks缓冲液中的A23187(最终浓度30μM)激发HUVECs 15分钟,Hanks缓冲液含有0.2%BSA和20mM Hepes。充分稀释后,使用放射免疫试剂盒(Amersham)按照生产商的程序定量测定上清液中6-酮-PGF1α-一种PGI2的稳定代谢物。体内试验角叉菜聚糖诱导的大鼠足浮肿
把雄性Sprague-Dawley大鼠(年龄5星期,Charles River Japan)禁食过夜。用记号笔在右后爪的踝以上画一条线,用体积测定计(Muromachi)通过排水法测定爪体积(V0)。给动物口服载体(0.1%甲基纤维素或5%Tween80)或试验化合物(2.5ml/100g体重)。1小时之后,给动物的右后爪皮下注射λ-角叉菜聚糖(0.1ml 1%w/v的盐水悬浮液,Zushikagaku)(Winter等人,Proc.Soc.Exp.Biol.Med.,111,544,1962;Lombardino等人,Arzneim.Forsch.,25,1629,1975),3小时之后测定爪体积(V3),计算体积增加值(V3-V0)。由于用经典的NSAIDs得到的最大抑制是60-70%,因此计算了ED30值。大鼠的胃溃疡
用修正的常规方法评价试验化合物引起胃溃疡的作用(Ezer等人,J.Pharm.Pharmacol.,28,655,1976;Cashin等人J.Pharm.Pharmacol.,29,330-336,1977)。给禁食过夜后的雄性Sprague-Dawley大鼠(年龄5星期,Charles River Japan)口服载体(0.1%甲基纤维素或5%Tween80)或试验化合物(1ml/100g体重)。6小时后,通过引颈法杀死动物。取出胃,用福尔马林溶液(10ml)膨胀。沿着胃大湾切开胃。根据至少有一个胃溃疡或出血性糜烂(包括淤斑)的大鼠数量计算溃疡的发生率。在试验期间不让动物进食或水。数据分析
使用用于Macintosh的统计程序包SYSTAT(SYSTAT,INC.)和StatView(Abacus Cencepts,Inc.)。使用ANOVA测试接受了试验化合物处理的组与对照组之间的差别。从浓度(剂量)的对数线性回归线的与抑制百分数的方程计算IC50(ED30)。
通过这些方法试验了后面所述的工作实施例中制备的一些化合物,表明抑制COX-2的IC50值为0.001μM-10μM。
通过这些方法还试验了上述的最优选化合物,表明抑制COX-2的IC50值为0.001μM-0.5μM。
用抑制COX-1的IC50值与抑制COX-2的IC50值的比可以确定对COX-2的任选。总之,可以这样说,COX-1/COX-2抑制比大于2的化合物具有好的COX-2任选。
实施例中制备的一些化合物的COX-1/COX-2抑制比大于10。
下列实施例中包含对式(I)化合物制备方法的详细描述。这些详细描述落在本发明的保护范围之内,用于例举上述的一般合成方法,构成了本发明的一部分。提供这些详细描述仅仅是为了说明,其目的不是为了限制本发明的保护范围。
实施例
在下列非限定性的实施例中说明本发明,除非另有指明,所有的操作在室温或环境温度即18-25℃的范围内进行;溶剂的蒸发在减压下在最高达60℃的浴温下用旋转蒸发器进行;通过薄层色谱(tlc)监测反应,给出的反应时间仅仅是为了说明;给出的熔点(m.p.)没有进行校正(多晶现象会产生不同的熔点);通过下列技术中的至少一种确认所有分离出的化合物的结构和纯度:tlc(Merck硅胶60 F-254预涂层板)、质谱、核磁共振(NMR)或微量分析。给出的产率仅仅是为了说明。使用Merck硅胶60(230-400目ASTM)进行闪蒸柱色谱。在Automass 120(JEOL)质谱仪上得到低分辨率质谱数据(EI)。在Quattro II(Micromass)质谱仪上得到低分辨率质谱数据(ESI)。除非另有指明,NMR数据是在270MHz(JEOLJNM-LA 270光谱仪)处、使用氘代的氯仿(99.8%D)或二甲基亚砜(99.9%D)作为溶剂测定的,相对于作为内标的四甲基硅烷(TMS),以百万分数(ppm)表示,常用的缩写有:s=单峰,d=二重峰,t=三重峰,q=四重峰,m=多重峰,br=宽峰等。实施例1 (2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸乙酯 步骤1.反式-4-氯-2-硝基肉桂酸乙酯
在室温下,向氢化钠(60%w/w矿物油分散液,4.4g,0.11mol)的THF(150ml)悬浮液中滴加膦酰乙酸三乙酯(25.0g,0.11mol)的THF(50ml)溶液。搅拌1小时后,加入4-氯-2-硝基苯甲醛(19.0g,0.10mol)的THF(50ml)溶液。再搅拌1小时后,加入饱和氯化铵水溶液(50ml),所得的混合物用乙酸乙酯(300ml×2)萃取。干燥(硫酸镁)合并后的有机萃取液并且浓缩,得到27g(定量的)棕色固体的标题化合物。1H-NMR(CDCl3)δ:8.04(1H,d,J=15.8Hz),8.03(1H,d,J=1.8Hz),7.64-7.58(2H,m),6.36(1H,d,J=15.8Hz),4.30(2H,q,J=7.0Hz),1.35(3H,t,J=7.0Hz).步骤2.反式-2-氨基-4-氯肉桂酸乙酯
在室温下,搅拌反式-4-氯-2-硝基肉桂酸乙酯(步骤1,27.0g,0.11mol)和硫氢化钠(92g,0.53mol)的THF-H2O(1∶1,500ml)溶液1小时。然后加入饱和的碳酸氢钠水溶液(300ml),用乙酸乙酯(300ml×2)萃取混合物。干燥(硫酸镁)合并后的有机萃取液并且浓缩,得到16.7g(67%)黄色固体的标题化合物。1H-NMR(CDCl3)δ:7.72(1H,d,J=15.8Hz),7.27(1H,d,J=8.4Hz),6.78-6.68(2H,m),6.31(1H,d,J=15.8Hz),4.27(2H,q,J=7.0Hz),1.33(3H,t,J=7.0Hz).步骤3.反式-4-氯-2-甲酰氨基肉桂酸乙酯
在60℃下加热乙酸酐(20ml)和甲酸(10ml)的混合物2小时。冷却到0℃后,小心地加入反式-2-氨基-4-氯肉桂酸乙酯(步骤2,15.5g,0.069mol)的THF(80ml)溶液。让所得的混合物温热到室温。搅拌过夜后,浓缩混合物,过滤收集沉淀,用己烷洗涤固体,得到9.6%(55%)的标题化合物。1H-NMR(CDCl3)δ:9.40-9.15(1H,m),8.51-8.40(1H,m),8.10-7.80(2H,m),7.60-7.47(1H,m),7.28-7.12(1H,m),6.40(1H,d,J=15.8Hz),4.25(2H,q,J=7.3Hz),1.34(3H,t,J=7.3Hz).步骤4.反式-4-氯-2-异氰基肉桂酸乙酯
向冷却到0℃的三苯基膦(5.3g,20mmol)的二氯甲烷(80ml)溶液中滴加三光气(2.0g,6.7mmol)的二氯甲烷(20ml)溶液。移去冰浴,在室温下搅拌所得的混合物10分钟。然后把混合物冷却到0℃,加入反式-4-氯-2-甲酰胺基肉桂酸乙酯(步骤3,5.2g,0.020mol)的二氯甲烷(80ml)溶液。让混合物过夜温热到室温,然后浓缩。残留物在水(80ml)与乙酸乙酯(100ml)之间分配,分离出水层,用乙酸乙酯(100ml)萃取。干燥(硫酸镁)合并后的有机萃取液,蒸去溶剂,粗产物通过闪蒸柱色谱纯化,用乙酸乙酯/己烷(1∶6)洗脱,得到3.9g(83%)白色固体的标题化合物。1H-NMR(CDCl3)δ:7.89(1H,d,J=16.1Hz),7.60(1H,d,J=8.8Hz),7.45(1H,d,J=1.8Hz),7.42(1H,dd,J=1.8,8.8Hz),6.52(1H,d,J=16.1Hz),4.30(2H,q,J=7.0Hz),1.35(3H,t,J=7.0Hz).步骤5.(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸乙酯
在100℃下加热反式-4-氯-2-异氰基肉桂酸乙酯(步骤4,1.2g,5.1mmol)、三丁基氢化锡(1.6g,5.6mmol)和AIBN(43mg,0.26mmol)在乙腈(30ml)中的混合物。1小时后,加入四(三苯基膦)钯(580mg,0.50mmol)和苯甲酰氯(0.65ml,5.6mmol),再加热混合物17小时。冷却混合物,倒入2N HCl(50ml)水溶液中,用乙醚(80ml×2)萃取。合并后的有机萃取液用饱和的氟化钾水溶液(50ml)萃取并干燥(硫酸镁)。除去溶剂后,粗产物通过闪蒸柱色谱纯化,用乙酸乙酯/己烷(1∶5)洗脱,得到0.43g(25%)白色固体的标题化合物。熔点:160-163℃。1H-NMR(CDCl3)δ:8.94(1H,br s),7.82-7.75(2H,m),7.67-7.47(4H,m),7.37(1H,d,J=1.8 Hz),7.13(1H,dd,J=1.8,8.4Hz),4.11(2H,q,J=7.3Hz),3.78(2H,s),1.22(3H,t,J=7.3Hz).实施例2 (2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸方法A
向(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸乙酯(实施例1,380mg,0.11mmol)的乙醇(15ml)溶液中加入2N KOH(5ml)。在80℃加热1小时后,冷却混合物并浓缩,然后小心地加入2N HCl水溶液(15ml),混合物用乙醚(50ml×2)萃取,干燥(硫酸镁)合并后的有机萃取液并且浓缩。残留的固体在乙酸乙酯/己烷中重结晶,得到60mg(17%)淡黄色固体的标题化合物。m.p.:183-186℃.1R(KBr)ν:1700,1610,1520,1425,1330,1000cm-1.1H-NMR(DMSO-d6)δ:12.26(1H,br s),11.76(1H,s),7.77-7.66(4H,m),7.62-7.54(2H,m),7.48(1H,d,J=1.8Hz),7.13(1H,dd,J=1.8,8.7Hz),3.80(2H,s).方法B步骤1.6-氯-1-(苯磺酰基)吲哚
在室温下搅拌6-氯吲哚(Y.Watanabe等人,J.Org.Chem.,1990,55,580,36.2g,0.24mol)、四丁基硫氢化铵(8.1g,0.024mol)和50%KOH(160ml)的水溶液在苯(500ml)中的混合物10分钟,然后把混合物冷却到0℃,加入苯磺酰氯的苯(20ml)溶液。在室温搅拌3小时后,把混合物倒入水(200ml)中,分离出有机层,水层用乙醚(200ml×2)萃取。合并后的有机萃取液用盐水(200ml)洗涤,干燥(硫酸镁)并且浓缩。残留的固体用乙醇(100ml×3)洗涤,得到58g(83%)浅白色固体的标题化合物。1H-NMR(CDCl3)δ:8.02(1H,s),7.92-7.85(2H,m),7.60-7.40(5H,m),7.21(1H,dd,J=1.8,8.4Hz),6.62(1H,d,J=3.6Hz).步骤2. 6-氯-2-苯甲酰基-1-(苯磺酰基)吲哚
在搅拌下,向冷却到-78℃的6-氯-1-(苯磺酰基)吲哚(步骤1,12.58g,43.0mmol)的THF(270ml)溶液中滴加叔丁基锂(32ml,52.0mmol,1.64M的正戊烷溶液),并且保持内部温度低于-65℃。在-78℃搅拌30分钟后,通过套管把溶液转入冷却到-78℃的苯甲酰氯(6.0ml,52.0mmol)的THF(30ml)溶液中。搅拌混合物1.5小时,然后用冷却到-78℃的饱和的氯化铵溶液(200ml)骤冷,把混合物温热到室温。分离出水层,用碳酸氢钠水溶液中和,然后用乙酸乙酯(50ml×2)萃取。合并后的有机萃取液用盐水(50ml)洗涤,干燥(硫酸镁)并且浓缩。残留物在乙醚/己烷(1∶3)中结晶,得到白色固体的标题化合物(14.4g,85%)。1H-NMR(CDCl3)δ:8.20-8.16(1H,m),8.14-8.06(2H,m),8.01-7.93(2H,m),7.66-7.47(7H,m),7.29(1H,dd,J=1.7,8.5Hz),6.89(1H,J=0.7Hz).步骤3. 2-苯甲酰基-6-氯吲哚
把2-苯甲酰基-6-氯-1-(苯磺酰基)吲哚(步骤2,48g,0.12mol)和碳酸钾(80g,0.58mol)在THF-MeOH-H2O(4∶2∶1,1100ml)中的混合物加热回流过夜。除去溶剂后,残留物用乙醚(300ml×2)萃取并且干燥(硫酸镁)。除去溶剂,得到淡棕色固体的粗产物。在乙酸乙酯中重结晶后,得到20g(65%)白色固体的标题化合物。m.p.:206-207℃.1H-NMR(CDCl3)δ:9.31(1H,br s),8.01-7.95(2H m),7.68-7.47(5H,m),7.17-7.12(2H,m).步骤4.α-乙酰氧-(2-苯甲酰基-6-氯-1H-吲哚-3-基)丙二酸二乙酯
在80℃加热搅拌2-苯甲酰基-6-氯吲哚(步骤3,4.0g,16mmol)、乙酸锰(III)二水合物(13g,48mmol)、丙二酸二乙酯(14g,80mmol)和乙酸钠(6.6g,80mmol)在乙酸(150ml)中的混合物2小时。加入乙酸锰(III)二水合物(3g,11mmol),再继续加热2小时。冷却混合物,加入盐水(200ml)。所得的混合物用乙醚(200ml×2)萃取,干燥(硫酸镁)合并后的有机萃取液并且浓缩。残留物通过闪蒸柱色谱纯化,用乙酸乙酯/己烷(1∶3)洗脱,得到5.2g(69%)黄色固体的标题化合物。m.p.:141-144℃.1H-NMR(CDCl3)δ:8.84(1H,br s),7.90-7.81(3H,m),7.66-7.58(1H,m),7.51-7.42(2H,m),7.38(1H,d,J=1.3Hz),7.15(1H,dd,J=2.0,8.7Hz),4.30-4.06(4H,m),1.70(3H,s),1.30-1.58 (6H,m).步骤5.(2-苯甲酰基-6-氯-1H-吲哚-3-基)丙二酸二乙酯
把α-乙酰氧基-(2-苯甲酰基-6-氯-1H-吲哚-3-基)丙二酸二乙酯(步骤4,5.0g,11mmol)、三氟乙酸(3.3ml,44mmol)和三乙基硅烷(2.1ml,13mmol)在二氯甲烷(80ml)中的混合物加热回流12小时,然后冷却并浓缩。所得的残留物在饱和的碳酸氢钠水溶液(50ml)与二氯甲烷(80ml)之间分配。分离出水层,用二氯甲烷(80ml)萃取。干燥(硫酸镁)合并后的有机萃取液,除去溶剂。粗产物通过闪蒸柱色谱纯化,用乙酸乙酯/己烷(1∶4)洗脱,得到4.0g(87%)白色固体的标题化合物。1H-NMR(CDCl3)δ:8.93(1H,br s),7.81-7.70(3H,m),7.68-7.60(1H,m),7.55-7.48(2H,m),7.32(1H,s),7.12(1H,dd,J=1.8,8.8Hz),5.29(1H,s),4.26-4.09(4H,m),1.21(6H,t,J=7.1Hz).步骤6.(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸
加热回流(2-苯甲酰基-6-氯-1H-吲哚-3-基)丙二酸二乙酯(步骤5,4.4g,11mmol)在乙醇(120ml)和2N NaOH水溶液(15ml)混合物中的溶液1小时。冷却混合物并且浓缩,小心地用2N HCl水溶液(30ml)酸化残留物。混合物用乙醚(150ml×3)萃取,干燥(硫酸镁)合并后的萃取液并且浓缩。残留的固体在乙酸乙酯/己烷中重结晶,得到1.1g(30%)淡黄色固体的标题化合物。m.p.:183-186℃.IR(KBr)ν:1700,1610,1520,1425,1330,1000cm-1.1H-NMR(DMSO-d6)δ:12.26(1H,br s),11.76(1H,s),7.77-7.66(4H,m),7.62-7.54(2H,m),7.48(1H,d,J=1.8Hz),7.13(1H,dd,J=1.8,8.7Hz),3.80(2H,s).实施例3 (2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸,钠盐
在室温下,用2N NaOH水溶液(0.7ml,1.4mmol)处理(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸(实施例2,480mg,1.5mmol)的乙醇(10ml)溶液30分钟,然后浓缩。把残留物溶于水(10ml)中,用乙醚(15ml×2)洗涤,浓缩水层,得到350mg(68%)淡棕色固体的标题化合物。m.p.:185-189℃.IR(KBr)ν:1523,1380,1230,1060,1004,918cm-1.1H-NMR(DMSO-d6)δ:11.46(1H,br s),7.88-7.84(2H,m),7.66(1H,d,J=8.4Hz),7.64-7.46(3H,m),7.39(1H,d,J=1.8Hz),7.00(1H,dd,J=1.8,8.4Hz),3.32(2H,s).实施例4 [6-氯-2-(2-甲基苯甲酰基)-1H-吲哚-3-基]乙酸 步骤1. 6-氯-2-(2-甲基苯甲酰基)-1-(苯磺酰基)吲哚
按照实施例2(方法B)的步骤2中描述的方法,从6-氯-1-(苯磺酰基)吲哚(实施例2方法B的步骤1)和邻甲基苯甲酰氯制备标题化合物。tlc∶Rf=0.3(乙酸乙酯/己烷=1∶10)步骤2. 6-氯-2-(2-甲基苯甲酰基)吲哚
按照实施例2(方法B)的步骤3中描述的方法,从6-氯-2-(2-甲基苯甲酰基)-1-(苯磺酰基)吲哚(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:9.37(1H,br s),7.58(2H,d,J=8.91Hz),7.48(1H,s),7.42(1H,dd,J=1.49,7.75Hz),7.34-7.27(2H,m),7.12(2H,dd,J=1.81,8.56Hz),2.44(3H,s).步骤3.α-乙酰氧基-[6-氯-2-(2-甲基苯甲酰基)-1H-吲哚-3-基]丙二酸 二乙酯
按照实施例2(方法B)的步骤4中描述的方法,从6-氯-2-(2-甲基苯甲酰基)吲哚(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:8.52(1H,br s),7.78(1H,d,J=8.88Hz),7.48-7.13(6H,m),4.31-4.16(4H,m),2.52(3H,s),1.96(3H,s),1.22(6H,t,7.26Hz).步骤4.[6-氯-2-(2-甲基苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯
按照实施例2(方法B)的步骤5中描述的方法,从α-乙酰氧基-[6-氯-2-(2-甲基苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯(步骤3)制备标题化合物。1H-NMR(CDCl3)δ:9.0(1H,br s),7.73(1H,d,J=8.88Hz),7.73-7.09(5H,m),7.11(1H,dd,J=1.97,8.75Hz),4.89(1H,s),4.20-4.08(4H,m),2.35(3H,s),1.19(6H,t,J=7.1Hz).步骤5.[6-氯-2-(2-甲基苯甲酰基)-1H-吲哚-3-基]乙酸
按照实施例2(方法B)的步骤6中描述的方法,从[6-氯-2-(2-甲基苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯(步骤4)制备标题化合物。m.p.:150-152℃.IR(KBr)ν:3321,1717,1624,1602,1568,1531,1431,1319,1249,1230cm-1.1H-NMR(DMSO-d6)δ:11.70(1H,s),7.69(2H,d,8.72Hz),7.51-7.31(3H,m),7.10(2H,dd,J=1.97,8.56Hz),3.57(2H,s),2.24(3H,s).实施例5 [6-氯-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]乙酸 步骤1. 6-氯-2-(3-甲基苯甲酰基)-1-(苯磺酰基)吲哚
按照实施例2(方法B)的步骤2中描述的方法,从6-氯-1-(苯磺酰基)吲哚(实施例2方法B的步骤1)和间甲基苯甲酰氯制备标题化合物。tlc∶Rf=0.3(乙酸乙酯/己烷=1∶10)步骤2. 6-氯-2-(2-甲基苯甲酰基)吲哚
按照实施例2(方法B)的步骤3中描述的方法,从6-氯-2-(3-甲基苯甲酰基)-1-(苯磺酰基)吲哚(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:9.37(1H,s),7.77(2H,br s),7.64(1H,d,J=8.56Hz),7.47-7.12(5H,m),2.47(3H,s).步骤3.α-乙酰氧基-[6-氯-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]丙二酸 二乙酯
按照实施例2(方法B)的步骤4中描述的方法,从6-氯-2-(3-甲基苯甲酰基)吲哚(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:8.80(1H,br s),7.83(1H,d,J=8.88Hz),7.67-7.32(5H,m),7.16(1H,dd,J=1.81,8.88Hz),4.27-4.15(4H,m),2.39(3H,s),1.72(3H,s),1.29(6H,t,J=7.26Hz).步骤4.[6-氯-2-(3-甲基苯甲酰基)-1H-吲哚-3-基)丙二酸二乙酯
按照实施例2(方法B)的步骤5中描述的方法,从α-乙酰氧基-[6-氯-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯(步骤3)制备标题化合物。1H-NMR(CDCl3)δ:9.21(1H,br s),7.71(1H,d,J=8.51Hz),7.59-7.28(5H,m),7.10(1H,dd,J=1.97,8.72Hz),5.27(1H,s),4.23-4.07(4H,m),2.40(3H,s),1.21(6H,t,J=7.1Hz).步骤5.[6-氯-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]乙酸
按照实施例2(方法B)的步骤6中描述的方法,从[6-氯-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯(步骤4)制备标题化合物。m.p.:182-184℃.IR(KBr)ν:3313,1699,1616,1568,1533,1408,1325,1265,1203cm-1.1H-NMR(DMSO-d6)δ:11.75(1H,s),7.70(1H,d,J=8.75),7.55-7.46(5H,m),7.12(1H,dd,J=1.97,8.72Hz),3.75(2H,s),2.39(3H,s).实施例6 [6-氯-2-(4-甲基苯甲酰基)-1H-吲哚-3-基]乙酸 步骤1. 6-氯-2-(4-甲基苯甲酰基)-1-(苯磺酰基)吲哚
按照实施例2(方法B)的步骤2中描述的方法,从6-氯-1-(苯磺酰基)吲哚(实施例2方法B的步骤1)和对甲基苯甲酰氯制备标题化合物。tlc∶Rf=0.3(乙酸乙酯/己烷=1∶10)步骤2. 6-氯2-(4-甲基苯甲酰基)吲哚
按照实施例2(方法B)的步骤3中描述的方法,从6-氯-2-(4-甲基苯甲酰基)-1-(苯磺酰基)吲哚(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:9.37(1H,br s),7.90(2H,d,J=8.6Hz),7.63(1H,d,J=8.9Hz),7.48(1H,s),7.34(2H,d,J=8.6Hz),7.16-7.10(2H,m),2.47(3H,s).步骤3.α-乙酰氧基-[6-氯-2-(4-甲基苯甲酰基)-1H-吲哚-3-基]丙二酸 二乙酯
按照实施例2(方法B)的步骤4中描述的方法,从6-氯-2-(4-甲基苯甲酰基)吲哚(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:8.65(1H,br s),7.84(1H,d,J=8.9Hz),7.76(2H,d,J=8.2Hz),7.39-7.37(1H,m),7.27(2H,d,J=8.2Hz),7.16(1H,dd,J=1.8,8.2Hz),4.36-4.16(4H,m),2.44(3H,s),1.72(3H,s),1.34-1.22(6H,m).步骤4.[6-氯-2-(4-甲基苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯
按照实施例2(方法B)的步骤5中描述的方法,从α-乙酰氧基-[6-氯-2-(4-甲基苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯(步骤3)制备标题化合物。1H-NMR(CDCl3)δ:8.83(1H,br s),7.76(1H,d,J=8.7Hz),7.71(2H,d,J=8.2Hz),7.39-7.36(1H,m),7.32(2H,d,J=8.2Hz),7.14(1H,dd,J=2.0,8.7Hz),5.30(1H,s),4.26-4.14(4H,m),2.47(3H,s),1.22(6H,t,J=7.1Hz).步骤5.[6-氯-2-(4-甲基苯甲酰基)-1H-吲哚-3-基]乙酸
按照实施例2(方法B)的步骤6中描述的方法,从[6-氯-2-(4-甲基苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯(步骤4)制备标题化合物。m.p.:182-184℃.IR(KBr)ν:3321,1705,1616,1602,1566,1529,1431,1323,1257,1230cm-1.1H-NMR(DMSO-d6)δ:11.72(1H,s),7.74-7.64(3H,m),7.49-7.45(1H,m),7.39(2H,d,J=8.1Hz),7.16-7.09(1H,m),3.g1(2H,s),2.43(3H,s).实施例7 [6-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]乙酸 步骤1. 6-氯-2-[(N-甲氧基-N-甲基氨基)羰基]吲哚
在搅拌下,向6-氯吲哚-2-甲酸(H.N.Rydon和J.C.Tweddle,J.Chem.Soc.,1955,,3499.,7.0g,36mmol)的亚硫酰氯(30ml)悬浮液中滴加DMF(1ml)。搅拌30分钟后,浓缩混合物,把残留物溶于二氯甲烷(100ml)中,冷却到0℃。向混合物中加入N,O-二甲基羟基胺盐酸盐(7.0g,72mmol)和吡啶(15ml)。搅拌2小时后,用水(100ml)骤冷混合物,用二氯甲烷(150ml×2)萃取。合并后的有机萃取液用2N HCl水溶液(100ml)、饱和碳酸氢钠水溶液(100ml)、盐水(100ml)洗涤,干燥(硫酸镁)。除去溶剂,得到8.2g(96%)黄色固体的标题化合物。1H-NMR(CDCl3)δ:9.48(1H,br s),7.60(1H,d,J=8.6Hz),7.46-7.41(1H,m),7.22-7.18(1H,m),7.11(1H,dd,J=8.6,1.8Hz),3.85(3H,s),3.44(3H,s).步骤2. 6-氯-2-(3-氯苯甲酰基)吲哚
在-78℃和搅拌下,向6-氯-2-[(N-甲氧基-N-甲基氨基)羰基]吲哚(步骤1,610mg,2.56mmol)和3-溴氯苯(1.47g,7.67mmol)的THF(20ml)溶液中滴加正丁基锂(1.54M的己烷溶液,4.90ml,7.67mmol)。搅拌1小时后,用饱和的氯化铵溶液(20ml)骤冷混合物,用乙酸乙酯(50ml×2)萃取。合并后的有机萃取液用2N HCl水溶液(50ml)、饱和的碳酸氢钠水溶液(50ml)、盐水(50ml)洗涤,干燥(硫酸镁)。除去溶剂,粗产物通过闪蒸柱色谱纯化,用乙酸乙酯/己烷(1∶10)洗脱,得到565mg(76%)淡棕色固体的标题化合物。1H-NMR(CDCl3)δ:9.31(1H,br s),7.94(1H,t,J=1.9Hz),7.85(1H,dt,J=1.9,7.6Hz),7.65(1H,d,J=8.4Hz),7.63-7.58(1H,m),7.52-7.45(2H,m),7.18-7.12(2H,m).步骤3.α-乙酰氧基-[6-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]丙二酸二 乙酯
按照实施例2(方法B)的步骤4中描述的方法,从6-氯-2-(3-氯苯甲酰基)吲哚(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:8.88(1H,br s),7.87-7.74(3H,m),7.61-7.56(1H,m),7.43(1H,d,J=7.6Hz),7.41-7.38(1H,m),7.20-7.14(1H,m),4.30-4.14(4H,m),1.74(3H,s),1.20(6H,t,J=8.2Hz).步骤4.[6-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯
按照实施例2(方法B)的步骤5中描述的方法,从α-乙酰氧基-[6-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯(步骤3)制备标题化合物。1H-NMR(CDCl3)δ:8.87(1H,br s),7.79-7.74(2H,m),7.70-7.58(2H,m),7.47(1H,t,J=8.1Hz),7.39-7.37(1H,m),7.15(1H,dd,J=1.8,8.7Hz),5.19(1H,s),4.27-4.10(4H,m),1.22(6H,t,J=7.1Hz).步骤5.[6-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基)乙酸
按照实施例2(方法B)的步骤6中描述的方法,从[6-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯(步骤4)制备标题化合物。m.p.:199-201℃.1H-NMR(DMSO-d6)δ:12.25(1H,br s),11.81(1H,s),7.79-7.57(5H,m),7.48(1H,d,J=1.8Hz),7.14(1H,dd,J=1.8,8.7Hz),3.81(2H,s).实施例8 [6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸甲酯方法A步骤1.反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯
向反式-2-氨基-4-氯肉桂酸甲酯(R.W.Carling等人,J.Med.Chem.,1993,
36,3397.,30.7g,0.15mol)和吡啶(36ml,0.45mol)的二氯甲烷(500ml)溶液中加入苯磺酰氯(20ml,0.16mol)。搅拌20小时后,加入甲醇(50ml),浓缩混合物。把残留的固体溶于二氯甲烷(700ml)中,用2N HCl水溶液(150ml)、盐水(150ml)洗涤,干燥(硫酸镁)。除去溶剂后,残留的固体在乙醇中重结晶,得到40g(76%)淡黄色固体的标题化合物。1H-NMR(CDCl3)δ:7.77-7.71(2H,m),7.59-7.52(1H,m),7.48-7.35(5H,m),7.20(1H,dd,J=2.0,8.4Hz),6.85(1H,br s),6.15(1H,d,J=15.8Hz),3.78(3H,s).步骤2.[6-氯-2-(4-氯苯甲酰基)-1-(苯磺酰基)二氢吲哚-3-基]乙酸甲 酯
在室温下搅拌反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(步骤1,1.1g,3.1mmol)、4-氯苯甲酰甲基溴(1.1g,4.6mmol)和碳酸钾(2.1g,15.4mmol)在丙酮(10ml)中的混合物1.5小时。过滤混合物,浓缩滤液。残留的固体在乙酸乙酯/己烷中重结晶,得到0.91g(59%)淡黄色固体的标题化合物。1H-NMR(CDCl3)δ:7.97-7.94(2H,m),7.86-7.81(2H,m),7.65-7.58(1H,m),7.55-7.46(5H,m),7.02(1H,dd,J=2.0,8.2Hz),6.90(1H,d,J=8.2Hz),5.99(1H,d,J=9.7Hz),4.00-3.87(1H,m),3.41(3H,s),2.63(1H,dd,J=6.3,17.6Hz),2.51(1H,dd,J=6.3,17.6Hz).步骤3.[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基)乙酸甲酯
在搅拌下,向[6-氯-2-(4-氯苯甲酰基)-1-(苯磺酰基)二氢吲哚-3-基]乙酸甲酯(步骤2,50mg,0.10mmol)d THF溶液中加入1,8-二氮杂双环[5.4.0]十一碳-7-烯(DBU,30μl,0.20mmol)。搅拌15小时后,用水(30ml)骤冷混合物,用乙酸乙酯(50ml)萃取混合物。萃取液用2N HCl水溶液(30ml)、饱和的碳酸氢钠水溶液(30ml)、盐水(30ml)洗涤,干燥(硫酸镁)。除去溶剂后,得到34mg(93%)黄色固体的标题化合物。MS(EI)m/z:361(M+).1H-NMR(CDCl3)δ:8.90(1H,br s),7.74(2H,d,J=8.6Hz),7.56(1H,d,J=8.6Hz),7.49(2H,d,J=8.6Hz),7.36(1H,d,J=1.6Hz),7.16(1H,dd,J=1.6,8.6Hz),3.81(2H,s),3.66(3H,s).方法B
在室温下搅拌反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(方法A的步骤1,0.70g,2.0mmol)、4-氯苯甲酰甲基溴(0.51g,2.2mmol)和碳酸钾(0.83g,6.0mmol)在丙酮(10ml)中的混合物。搅拌2小时后,加入碳酸铯(2.0g,6.0mmol),再继续搅拌4小时。浓缩混合物,用水(100ml0稀释残留物,用乙酸乙酯(100ml×2)萃取水性混合物。合并后的有机萃取液用2NHCl水溶液(100ml)、饱和的碳酸氢钠水溶液(100ml)、盐水(100ml)洗涤,干燥(硫酸镁)。除去溶剂后,固体在乙醇中重结晶,得到0.44g(61%)标题化合物。MS和NMR光谱与步骤3中制备的化合物的光谱一样。实施例9 [6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基)乙酸方法A步骤1. 6-氯-2-(4-氯苯甲酰基)吲哚
按照实施例7的步骤2中描述的方法,从6-氯-2-[(N-甲氧基-N-甲基氨基)羰基]吲哚(实施例7的步骤1)和4-溴氯苯制备标题化合物。1H-NMR(DMSO-d6)δ:12.14(1H,br s),7.97(2H,d,J=8.4Hz),7.76(1H,d,J=8.6Hz),7.66(2H,d,J=8.4Hz),7.54-7.50(1H,m),7.20(1H,s),7.14(1H,dd,J=2.0,8.6Hz).步骤2.α-乙酰氧基-[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]丙二酸二 乙酯
按照实施例2(方法B)的步骤4中描述的方法,从6-氯-2-(4-氯苯甲酰基)吲哚(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:8.83(1H,br s),7.87-7.77(3H,m),7.48-7.36(3H,m),7.17(1H,dd,J=2.0,8.9Hz),4.28-4.14(4H,m),1.73(3H,s),1.20(6H,t,J=7.1Hz).步骤3.[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯
按照实施例2(方法B)的步骤5中描述的方法,从α-乙酰氧基-[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:8.91(1H,br s),7.75(2H,d,J=8.6Hz),7.75-7.69(1H,m),7.50(2H,d,J=8.6Hz),7.29(1H,d,J=1.8Hz),7.13(1H,dd,J=1.8,8.7Hz),5.23(1H,s),4.28-4.07(4H,m),1.23(6H,t,J=7.2Hz).步骤4.[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸
按照实施例2(方法B)的步骤6中描述的方法,从[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯(步骤3)制备标题化合物。m.p.:189-190℃.IR(KBr)ν:3309,1699,1616,1525,1431,1325,1255,1226,1091cm-1.1H-NMR(DMSO-d6)δ:11.78(1H,s),7.80-7.72(3H,m),7.65(2H,d,J=8.6Hz),7.47(1H,d,J=1.8Hz),7.13(1H,dd,J=1.8,8.7Hz),3.83(2H,s).方法B[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸
在80℃下,搅拌[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸甲酯(实施例8,1.80g)和2N NaOH水溶液(7.5ml)在MeOH-THF(10ml-10ml)中的混合物1小时。冷却混合物并浓缩。把残留物溶于水(150ml)中,用乙醚(50ml)洗涤。水层用2N HCl水溶液(10ml)酸化,用乙酸乙酯(100ml×2)萃取。合并后的有机萃取液用盐水(50ml)洗涤,干燥(硫酸镁)并且浓缩。残留的固体在甲苯中重结晶,得到1.58g(91%)标题化合物。MS和NMR光谱与方法A制备的化合物的光谱一样。实施例10 [6-氯-2-(3-氟苯甲酰基)-1H-吲哚-3-基]乙酸 步骤1. 6-氯-2-(3-氟苯甲酰基)-1H-吲哚
按照实施例7的步骤2中描述的方法,从6-氯-2-[(N-甲氧基-N-甲基氨基)羰基]吲哚(实施例7的步骤1)和3-溴氟苯制备标题化合物。1H-NMR(CDCl3)δ:9.28(1H,br s),7.79-7.75(1H,m),7.68-7.63(2H,m),7.56-7.48(2H,m),7.36-7.30(1H,m),7.17-7.14(2H,m).步骤2.α-乙酰氧基-[6-氯-2-(3-氟苯甲酰基)-1H-吲哚-3-基]丙二酸二 乙酯
按照实施例2(方法B)的步骤4中描述的方法,从6-氯-2-(3-氟苯甲酰基)吲哚(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:9.15(1H,br s),8.83(1H,d,J=8.72Hz),7.66-7.27(5H,m),7.17(1H,dd,J=2.00,8.72Hz),4.25-4.13(4H,m),1.75(3H,s),1.19(6H,t,J=7.07Hz).步骤3.[6-氯-2-(3-氟苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯
按照实施例2(方法B)的步骤5中描述的方法,从α-乙酰氧基-[6-氯-2-(3-氟苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:8.91(1H,br s),7.77-7.12(7H,m),5.21(1H,s),4.25-4.11(4H,m),1.22(6H,t,J=7.07Hz).步骤4.[6-氯-2-(3-氟苯甲酰基)-1H-吲哚-3-基]乙酸
按照实施例2(方法B)的步骤6中描述的方法,从[6-氯-2-(3-氟苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯(步骤3)制备标题化合物。m.p.:278-281℃.IR(KBr)ν:3385,1697,1638,1583,1541,1508,1420,1400,1315,1261,1236cm-1.1H-NMR(DMSO-d6)δ:11.79(1H,s),7.76-7.48(7H,m),7.13(1H,dd,J=1.97,8.56Hz),3.80(2H,s).实施例11 [6-氯-2-(4-氟苯甲酰基)-1H-吲哚-3-基]乙酸 步骤1. 6-氯-2-(4-氟苯甲酰基)-1H-吲哚
按照实施例7的步骤2中描述的方法,从6-氯-2-[(N-甲氧基-N-甲基氨基)羰基]吲哚(实施例7的步骤1)和4-溴氟苯制备标题化合物。1H-NMR(CDCl3)δ:9.29(1H,br s),8.05-8.00(2H,m),7.64(1H,d,8.72Hz),7.48-7.11(5H,m).步骤2.α-乙酰氧基-[6-氯-2-(4-氟苯甲酰基)-1H-吲哚-3-基]丙二酸二 乙酯
按照实施例2(方法B)的步骤4中描述的方法,从6-氯-2-(4-氟苯甲酰基)吲哚(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:9.20(1H,br s),7.92-7.11(7H,m),4.25-4.14(4H,m),1.73(3H,s),1.20(6H,t,J=7.10Hz).步骤3.[6-氯-2-(4-氟苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯
按照实施例2(方法B)的步骤5中描述的方法,从α-乙酰氧基-[6-氯-2-(4-氟苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:9.01(1H,br s),7.87-7.69(2H,m),7.71(2H,d,J=8.91Hz),7.27-7.10(4H,m),5.25(1H,s),4.26-4.11(4H,m),1.22(6H,t,J=7.07Hz).步骤4.[6-氯-2-(4-氟苯甲酰基)-1H-吲哚-3-基]乙酸
按照实施例2(方法B)的步骤6中描述的方法,从[6-氯-2-(4-氟苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯(步骤3)制备标题化合物。m.p.:181-183℃.IR(KBr)ν:3309,1701,1616,1601,1566,1527,1508,1419,1323,1257,1229cm-1.1H-NMR(DMSO-d6)δ:11.75(1H,s),7.87-7.82(2H,m),7.73(1H,d,J=8.72),7.47-7.36(3H,m),7.12(1H,dd,J=1.84,8.72Hz),3.78(2H,s).实施例12 [2-(3-溴苯甲酰基)-6-氯-1H-吲哚-3-基]乙酸 步骤1. 2-(3-溴苯甲酰基)-6-氯吲哚
按照实施例7的步骤2中描述的方法,从6-氯-2-[(N-甲氧基-N-甲基氨基)羰基]吲哚(实施例7的步骤1)和3-溴碘苯制备标题化合物。1H-NMR(CDCl3)δ:9.28(1H,br s),8.11-8.08(1H,m),7.93-7.87(1H,m),7.79-7.73(1H,m),7.65(1H,d,J=8.6Hz),7.50-7.38(2H,m),7.19-7.01(2H,m).步骤2.α-乙酰氧基-[2-(3-溴苯甲酰基)-6-氯-1H-吲哚-3-基]丙二酸二 乙酯
按照实施例2(方法B)的步骤4中描述的方法,从2-(3-溴苯甲酰基)-6-氯吲哚(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:8.73(1H,br s),7.93(1H,t,J=1.8Hz),7.85(1H,d,J=8.6Hz),7.82-7.72(2H,m),7.42-7.32(2H,m),7.18(1H,dd,J=2.0,8.6Hz),4.32-4.16(4H,m),1.75(3H,s),1.20(6H,t,J=7.1Hz).步骤3.[2-(3-溴苯甲酰基)-6-氯-1H-吲哚-3-基]丙二酸二乙酯
按照实施例2(方法B)的步骤5中描述的方法,从α-乙酰氧基-[2-(3-溴苯甲酰基)-6-氯-1H-吲哚-3-基]丙二酸二乙酯(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:8.88(1H,br s),7.92-7.90(1H,m),7.80-7.68(3H,m),7.45-7.36(2H,m),7.15(1H,dd,J=1.8,8.7Hz).5.20(1H,s),4.30-4.10(4H,m),1.23(6H,t,J=7.2Hz).步骤4.[2-(3-溴苯甲酰基)-6-氯-1H-吲哚-3-基]乙酸
按照实施例2(方法B)的步骤6中描述的方法,从[2-(3-溴苯甲酰基)-6-氯-1H-吲哚-3-基]丙二酸二乙酯(步骤3)制备标题化合物。m.p.:215-218℃.IR(KBr)ν:3369,1710,1604,1558,1533,1423,1319,1253,1228cm-1.1H-NMR(DMSO-d6)δ:11.81(1H,s),7.92-7.83(2H,m),7.78-7.70(2H,m),7.54(1H,t,J=7.8Hz),7.48(1H,d,J=2.0Hz),7.13(1H,dd,J=2.0,8.7Hz),3.80(2H,s).实施例13 [2-(4-溴苯甲酰基)-6-氯-1H-吲哚-3-基]乙酸 步骤1. 2-(4-溴苯甲酰基)-6-氯吲哚
按照实施例7的步骤2中描述的方法,从6-氯-2-[(N-甲氧基-N-甲基氨基)羰基]吲哚(实施例7的步骤1)和3-溴碘苯制备标题化合物。1H-NMR(DMSO-d6)δ:12.28(1H,br s),7.88(2H,d,J=8.7Hz),7.80(2H,d,J=8.7Hz).7.76(1H,d,J=8.7Hz),7.53-7.50(1H,m),7.22-7.19(1H,m),7.13(1H,dd,J=2.0,8.7Hz).步骤2.α-乙酰氧基-[2-(4-溴苯甲酰基)-6-氯-1H-吲哚-3-基]丙二酸二 乙酯
按照实施例2(方法B)的步骤4中描述的方法,从2-(4-溴苯甲酰基)-6-氯吲哚(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:8.72(1H,br s),7.84(1H,d,J=8.7Hz),7.73(2H,d,J=8.4Hz),7.62(2H,d,J=8.4Hz),7.38(1H,d,J=1.8Hz),7.18(1H,dd,J=1.8,8.7Hz),4.28-4.14(4H,m),1.73(3H,s),1.20(6H,t,J=7.1Hz).步骤3.[2-(4-溴苯甲酰基)-6-氯-1H-吲哚-3-基]丙二酸二乙酯
按照实施例2(方法B)的步骤5中描述的方法,从α-乙酰氧基-[2-(4-溴苯甲酰基)-6-氯-1H-吲哚-3-基]丙二酸二乙酯(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:8.86(1H,br s),7.75(1H,d,J=8.4Hz),7.67(4H,s),7.37-7.32(1H,m),7.18-7.12(1H,m),5.22(1H,s),4.26-4.10(4H,m),1.23(6H,t,J=7.1Hz).步骤4.[2-(4-溴苯甲酰基)-6-氯-1H-吲哚-3-基]乙酸
按照实施例2(方法B)的步骤6中描述的方法,从[2-(4-溴苯甲酰基)-6-氯-1H-吲哚-3-基]丙二酸二乙酯(步骤3)制备标题化合物。m.p.:199-201℃.IR(KBr)ν:3300,1699,1618,1587,1525,1433,1406,1325,1255,1226cm-1.1H-NMR(DMSO-d6)δ:11.78(1H,s),7.80(2H,d,J=8.4Hz),7.75(1H,d,J=8.6Hz),7.69(2H,d,J=8.4Hz),7.47(1H,d,J=1.8Hz),7.13(1H,dd,J=1.8,8.6Hz),3.84(2H,s).实施例14 [6-氯-2-(3-三氟甲基苯甲酰基)-1H-吲哚-3-基]乙酸 步骤1. 6-氯-2-(3-三氟甲基苯甲酰基)-1H-吲哚
按照实施例7的步骤2中描述的方法,从6-氯-2-[(N-甲氧基-N-甲基氨基)羰基]吲哚(实施例7的步骤1)和3-溴苯基三氟甲烷制备标题化合物。1H-NMR(DMSO-d6)δ:12.23(1H,br s),8.28-8.04(3H,m),7.89-7.75(2H,m),7.55-7.51(1H,m),7.22-7.12(2H,m).步骤2.α-乙酰氧基-[6-氯-2-(3-三氟甲基苯甲酰基)-1H-吲哚-3-基]丙 二酸二乙酯
按照实施例2(方法B)的步骤4中描述的方法,从6-氯-2-(3-三氟甲基苯甲酰基)吲哚(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:8.82(1H,br s),8.25-7.80(4H,m),7.68-7.57(1H,m),7.43-7.41(1H,m),7.22-7.16(1H,m),4.36-4.20(4H,m),1.67(3H,s),1.20(6H,t,J=7.1Hz).步骤3.[6-氯-2-(3-三氟甲基苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯
按照实施例2(方法B)的步骤5中描述的方法,从α-乙酰氧基-[6-氯-2-(3-三氟甲基苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:8.91(1H,br s),8.08-8.03(1H,m),8.02-7.87(2H,m),7.76(1H,d,J=9.0Hz),7.73-7.64(1H,m),7.39-7.36(1H,m),7.15(1H,dd,J=1.8,9.0Hz).5.15(1H,s),4.26-4.10(4H,m),1.22(6H,t,J=7.2Hz).步骤4.[6-氯-2-(3-三氟甲基苯甲酰基)-1H-吲哚-3-基]乙酸
按照实施例2(方法B)的步骤6中描述的方法,从[6-氯-2-(3-三氟甲基苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯(步骤3)制备标题化合物。m.p.:194-196℃.IR(KBr)ν:3371,1705,1631,1421,1307,1228,1168,1122,1072cm-1.1H-NMR(DMSO-d6)δ:11.86(1H,s),8.10-7.98(3H,m),7.83(1H,t,J=7.7Hz),7.75(1H,d,J=8.6Hz),7.49(1H,d,J=2.0Hz),7.15(1H,dd,J=2.0,8.6Hz),3.80(2H,s).实施例15 [6-氯-2-(4-三氟甲基苯甲酰基)-1H-吲哚-3-基]乙酸 步骤1. 6-氯-1-(苯磺酰基)-2-(3-三氟甲基苯甲酰基)吲哚
按照实施例2的步骤2中描述的方法,从6-氯-1-(苯磺酰基)吲哚(实施例2方法B的步骤1)和4-三氟甲基苯甲酰氯制备标题化合物。tlc∶Rf=0.2(乙酸乙酯/己烷=1∶4)。
按照实施例2(方法B)的步骤3中描述的方法,从6-氯-1-苯磺酰基-2-(4-三氟甲基苯甲酰基)吲哚(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:9.53(1H,br s),7.94(4H,dd,J=8.24,69.1Hz),7.63(1H,d,J=8.56Hz),7.49-7.11(3H,m).步骤3.α-乙酰氧基-[6-氯-2-(4-三氟甲基苯甲酰基)-1H-吲哚-3-基]丙 二酸二乙酯
按照实施例2(方法B)的步骤4中描述的方法,从6-氯-2-(4-三氟甲基苯甲酰基)吲哚(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:8.66(1H,br s),7.98(2H,d,J=8.24Hz),7.87(1H,d,J=8.91Hz),7.75(2H,d,J=8.07Hz),7.39(1H,d,J=1.81Hz),7.19(1H,dd,J=1.81,7.10Hz)4.36-4.16(4H,m),1.70(3H,s),1.34-1.22(6H,m).步骤4.[6-氯-2-(4-三氟甲基苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯
按照实施例2(方法B)的步骤5中描述的方法,从α-乙酰氧基-[6-氯-2-(4-三氟甲基苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯(步骤3)制备标题化合物。1H-NMR(CDCl3)δ:9.24(1H,br s),7.84(4H,dd,J=7.91,25.7Hz),7.69-7.09(3H,m),5.24(1H,s),4.21-4.06(4H,m),1.21(6H,t,J=7.07Hz).步骤5.[6-氯-2-(4-三氟甲基苯甲酰基)-1H-吲哚-3-基]乙酸
按照实施例2(方法B)的步骤6中描述的方法,从[6-氯-2-(4-三氟甲基苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯(步骤4)制备标题化合物。1H-NMR(DMSO-d6)δ:11.78(1H,s),7.94(4H,s),7.76(1H,d,J=8.72Hz),7.47(1H,m),7.14(1H,d,J=1.81,8.72),3.81(2H,s).实施例16 [6-氯-2-(3,4-二氯苯甲酰基)-1H-吲哚-3-基)乙酸 步骤1. 6-氯-2-(3,4-二氯苯甲酰基)吲哚
按照实施例7的步骤2中描述的方法,从6-氯-2-[(N-甲氧基-N-甲基氨基)羰基]吲哚(实施例7的步骤1)和1-溴-3,4-二氯苯制备标题化合物。tlc∶Rf=0.7(乙酸乙酯/己烷=1∶3)步骤2.α-乙酰氧基-[6-氯-2-(3,4-二氯苯甲酰基)-1H-吲哚-3-基]丙二 酸二乙酯
按照实施例2(方法B)的步骤4中描述的方法,从6-氯-2-(3,4-二氯苯甲酰基)吲哚(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:8.80(1H,br s),7.90-7.79(2H,m),7.71(1H,dd,J=2.0,8.4Hz),7.57(1H,d,J=8.4Hz),7.40-7.35(1H,m),7.18(1H,dd,J=1.8,8.8Hz),4.30-4.14(4H,m),1.77(3H,s),1.20(6H,t,J=7.1Hz).步骤3.[6-氯-2-(3,4-二氯苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯
按照实施例2(方法B)的步骤5中描述的方法,从α-乙酰氧基-[6-氯-2-(3,4-二氯苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:8.95(1H,br s),7.88(1H,d,J=1.6Hz),7.72(1H,d,J=8.7Hz),7.68-7.58(2H,m),7.28(1H,d,J=1.6Hz),7.14(1H,dd,J=1.6,8.7Hz).5.18(1H,s),4.28-4.10(4H,m),1.23(6H,t,J=7.1Hz).步骤4.[6-氯-2-(3,4-二氯苯甲酰基)-1H-吲哚-3-基]乙酸
按照实施例2(方法B)的步骤6中描述的方法,从[6-氯-2-(3,4-二氯苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯(步骤3)制备标题化合物。m.p.:206-209℃.IR(KBr)ν:3435,1708,1620,1583,1525,1423,1384,1301,1263,1228cm-1.1H-NMR(DMSO-d6)δ:11.62(1H,br s),7.95-7.75(3H,m),7.68(1H,d,J=8.7Hz),7.42(1H,d,J=2.0Hz),7.02(1H,dd,J=2.0,8.7Hz),3.50(2H,s).实施例17 [2-苯甲酰基-4-氯-1H-吲哚-3-基)乙酸 步骤1. 4-氯-2-[(N-甲氧基-N-甲基氨基)羰基]吲哚
按照实施例7的步骤1中描述的方法,使用4-氯吲哚-2-甲酸制备标题化合物(F.C.Uhle,J.Amer.Chem.Soc.,1949,
71,761)。1H-NMR(CDCl3)δ:9.56(1H,br s),7.36-7.29(2H,m),7.24-7.12(2H,m),3.88(3H,s),3.45(3H,s).步骤2. 2-苯甲酰基-4-氯吲哚
向冷却到-78℃的4-氯-2-[(N-甲氧基-N-甲基氨基)羰基]吲哚(步骤1,3.4g,0.014mol)的THF(60ml)溶液中滴加苯基锂(1.8M的环己烷/乙醚(7∶3)溶液,30ml,0.070mol)。搅拌1小时后,把混合物倒入水(80ml)中,用乙酸乙酯(80ml×2)萃取。干燥并除去溶剂后,粗产物用闪蒸柱色谱纯化,用乙酸乙酯/己烷(1∶10)洗脱,得到3.6g(100%)白色固体的标题化合物。1H-NMR(CDCl3)δ:9.46(1H,br s),8.05-8.00(2H,m),7.73-7.51(3H,m),7.40(1H,dd,J=1.0,8.3Hz),7.33-7.24(2H,m),7.18(1H,d,J=7.6Hz).步骤3.α-乙酰氧基-(2-苯甲酰基-4-氯-1H-吲哚-3-基]丙二酸二乙酯
按照实施例2(方法B)的步骤4中描述的方法,从2-苯甲酰基-4-氯吲哚(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:9.49(1H,br s),7.98-7.92(2H,m),7.66-7.57(1H,m),7.53-7.44(2H,m),7.34(1H,dd,J=2.0,7.1Hz),7.21-7.15(2H,m),4.30-3.90(4H,m),2.08(3H,s),1.15(6H,t,J=7.3Hz).步骤4.(2-苯甲酰基-4-氯-1H-吲哚-3-基]丙二酸二乙酯
按照实施例2(方法B)的步骤5中描述的方法,从α-乙酰氧基-(2-苯甲酰基-4-氯-1H-吲哚-3-基]丙二酸二乙酯(步骤3)制备标题化合物。1H-NMR(CDCl3)δ:8.88(1H,br s),7.83-7.77(2H,m),7.64-7.58(1H,m),7.55-7.46(2H,m),7.25-7.05(3H,m),5.86(1H,s),4.25-4.08(4H,m),1.23(6H,t,J=7.3Hz).步骤5.(2-苯甲酰基-4-氯-1H-吲哚-3-基]乙酸
按照实施例2(方法B)的步骤6中描述的方法,从(2-苯甲酰基-4-氯-1H-吲哚-3-基]丙二酸二乙酯(步骤3)制备标题化合物。熔点:206-209℃(在乙酸乙酯/己烷中重结晶)。IR(KBr)ν:1700,1575,1245cm-1.1H-NMR(DMSO-d6)δ:12.20(1H,br s),11.98(1H,s),7.85-7.67(3H,m),7.63-7.55(2H,m),7.45(1H,d,J=8.2Hz),7.25(1H,t,J=8.2Hz),7.12(1H,d,J=7.6Hz),4.02(2H,s).实施例18 [5-氯-2-(3-甲基苯甲酰基)-1H-吲哚-3-基)乙酸 步骤1. 5-氯-2-[(N-甲氧基-N-甲基氨基)羰基]吲哚
按照实施例7的步骤1中描述的方法,从5-氯吲哚-2-甲酸制备标题化合物。1H-NMR(CDCl3)δ:9.68(1H,br s),7.68-7.65(1H,m),7.37(1H,d,J=8.7Hz),7.23(1H,d,J=1.6Hz),7.18-7.15(1H,m),3.85(3H,s),2.05(3H,s).步骤2. 5-氯-2-(3-甲基苯甲酰基)吲哚
按照实施例17的步骤2中描述的方法,从5-氯-2-[(N-甲氧基-N-甲基氨基)羰基]吲哚(步骤1)和3-甲基苯基锂制备标题化合物。熔点:197.5-198℃(在乙酸乙酯/己烷中重结晶)。IR(KBr)ν:3310,1626,1603,1583,1516,1406,1377,1337,1269,1178,1134cm-1.1H-NMR(CDCl3)δ:9.39(1H,br s),7.28-7.76(2H,m),7.71-7.68(1H,m),7.46-7.38(3H,m),7.32(1H,dd,J=8.7,2.0Hz),7.08(1H,dd,J=2.0,0.8Hz),2.47(3H,s).步骤3.α-乙酰氧基-[5-氯-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]两二酸 二乙酯
按照实施例2(方法B)的步骤4中描述的方法,从5-氯-2-(3-甲基苯甲酰基)吲哚(步骤2)制备标题化合物。熔点:173-174℃(在乙酸乙酯/己烷中重结晶)。1H-NMR(CDCl3)δ:8.64(1H,br s),7.91(1H,br s),7.69-7.61(2H,m),7.46-7.22(4H,m),4.30-4.16(4H,m),2.39(3H,s),1.72(3H,s),1.23(3H,t,J=7.2Hz).步骤4.[5-氯-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯
按照实施例2(方法B)的步骤5中描述的方法,从α-乙酰氧基-[5-氯-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯(步骤3)制备标题化合物。熔点:143-144℃(在乙酸乙酯/己烷中重结晶)。1H-NMR(CDCl3)δ:8.88(1H,br s),7.84-7.80(1H,m),7.62-7.55(2H,m),7.48-7.36(2H,m),7.32-7.28(2H,m),5.27(1H,s),4.30-4.10(4H,m),2.42(3H,s),1.24(3H,t,J=7.1Hz).步骤5.[5-氯-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]乙酸
按照实施例2(方法B)的步骤6中描述的方法,从[5-氯-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯制备标题化合物。熔点:241-242℃(在乙酸乙酯/己烷中重结晶)。IR(KBr)ν:3321,1703,1618,1535,1431,1335,1232,1016,808,758cm-1.1H-NMR(DMSO-d6)δ:11.7(1H,br s),7.62(1H,d,J=1.8Hz),7.45-7.30(6H,m),7.19(1H,dd,J=8.6,1.8Hz),3.63(2H,s),2.27(3H,s).实施例19 [5-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基)乙酸 步骤1. 5-氯-2-(4-氯苯甲酰基)吲哚
按照实施例7的步骤2中描述的方法,从5-氯-2-[(N-甲氧基-N-甲基氨基)羰基]吲哚(实施例18的步骤1)和4-溴氯苯制备标题化合物。1H-NMR(CDCl3)δ:9.32(1H,br s),7.94(2H,d,J=8.4Hz),7.70(1H,s),7.53(2H,d,J=8,4Hz),7.42(1H,d,J=8.9Hz),7.34(1H,dd,J=2.0,8.9Hz),7.07(1H,s).步骤2.α-乙酰氧基-[5-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]丙二酸二 乙酯
按照实施例2(方法B)的步骤4中描述的方法,从5-氯-2-(4-氯苯甲酰基)吲哚(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:9.11(1H,br s),7.87(1H,s),7.76(2H,d,J=8.6Hz),7.41(2H,d,J=8.6Hz),7.27(1H,d,J=8.7Hz),7.22(1H,dd,J=1.8,8.7Hz),4.25-4.14(4H,m),1.72(3H,s),1.24-1.19(6H,m).步骤3.[5-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯
按照实施例2(方法B)的步骤5中描述的方法,从α-乙酰氧基-[5-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:9.13(1H,br s),7.73(2H,d,J=8.4Hz),7.68(1H,d,J=2.0Hz),7.48(2H,d,J=8.4Hz),7.11(1H,dd,J=2.0,8.9Hz),7.02(1H,d,J=8.9Hz),5.28(1H,s),4.24-4.03(4H,m),1.27-1.21(6H,m).步骤4.[5-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸
按照实施例2(方法B)的步骤6中描述的方法,从[5-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯(步骤3)制备标题化合物。熔点:220-224℃(在乙酸乙酯/己烷中重结晶)。IR(KBr)ν:3321,1618,1535,1379,1339,1263,1130,1090,1057,1007cm-1.1H-NMR(DMSO-d6)δ:11.83(1H,s),7.80-7.75(3H,m),7.67-7.62(2H,m),7.48(1H,d,J=8.7Hz),7.31(1H,dd,J=2.0,8.7Hz),3.84(2H,s).实施例20 [5-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基)乙酸 步骤1. 5-氯-2-(3-氯苯甲酰基)吲哚
按照实施例7的步骤2中描述的方法,从5-氯-2-[(N-甲氧基-N-甲基氨基)羰基]吲哚(实施例18的步骤1)和3-溴氯苯制备标题化合物。1H-NMR(CDCl3)δ:9.28(1H,br s),7.95(1H,t,J=1.7Hz),7.88-7.84(1H,m),7.71(1H,d,J=2.0Hz),7.63-7.59(1H,m),7.49(1H,t,J=7.7Hz),7.42(1H,d,J=8.7Hz),7.34(1H,dd,J=2.0,8.7Hz),7.10-7.09(1H,m).步骤2.α-乙酰氧基-[5-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]丙二酸二 乙酯
按照实施例2(方法B)的步骤4中描述的方法,从5-氯-2-(3-氯苯甲酰基)吲哚(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:8.94(1H,br s),7.91(1H,d,J=1.8Hz),7.79-7.76(1H,m),7.74(1H,d,J=7.7Hz),7.60-7.56(1H,m),7.42(1H,t,J=7.7Hz),7.33(1H,d,J=8.7Hz),7.27(1H,dd,J=1.8,8.7Hz),4.37-4.19(4H,m),1.75(3H,s),1.26-1.20(6H,m).步骤3.[5-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯
按照实施例2(方法B)的步骤5中描述的方法,从α-乙酰氧基-[5-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:9.04(1H,br,s),7.77-7.75(2H,m),7.68-7.58(2H,m),7.46(1H,t,J=7.7Hz),7.24-7.20(2H,m),5.23(1H,s),4.27-4.14(4H,m),1.27-1.22(6H,m).步骤4.[5-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]乙酸
按照实施例2(方法B)的步骤6中描述的方法,从[5-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯(步骤3)制备标题化合物。熔点:243-247℃(在乙酸乙酯/己烷中重结晶)。IR(KBr)ν:3329,1707,1618,1535,1431,1406,1375,1333,1279,1232,1053cm-1.1H-NMR(DMSO-d6)δ:11.87(1H,s),7.81-7.68(4H,m),7.64-7.58(1H,m),7.49(1H,d,J=8.9Hz),7.32(1H,dd,J=2.0,8.9Hz),3.82(2H,s).实施例21 [2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基)乙酸 步骤1. 5-氟-2-[(N-甲氧基-N-甲基氨基)羰基]吲哚
按照实施例7的步骤1中描述的方法,从5-氟吲哚-2-甲酸制备标题化合物。1H-NMR(CDCl3)δ:10.15(1H,br s),7.41-7.36(1H,m),7.32(1H,dd,J=2.5,9.1Hz),7.20-7.19(1H,m),7.09-7.01(1H,m),3.84(3H,s),3.47(3H,s).步骤2. 2-(4-氯苯甲酰基)-5-氟-吲哚
按照实施例7的步骤2中描述的方法,从5-氟-2-[(N-甲氧基-N-甲基氨基)羰基]吲哚(步骤1)和4-溴氯苯制备标题化合物。1H-NMR(CDCl3)δ:9.27(1H,br s),7.94(2H,d,J=8.4Hz),7.52(2H,d,J=8.4Hz),7.45-7.40(1H,m),7.37-7.33(1H,m),7.21-7.12(1H,m),7.10-7.09(1H,m).步骤3.α-乙酰氧基-[2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]丙二酸二 乙酯
按照实施例2(方法B)的步骤4中描述的方法,从2-(4-氯苯甲酰基)-5-氟-吲哚(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:9.01(1H,br s),7.80-7.77(2H,m),7.58-7.54(1H,m),7.45-7.41(2H,m),7.36-7.27(1H,m),7.12-7.01(1H,m),4.29-4.15(4H,m),1.74(3H,s),1.28-1.17(6H,m).步骤4.[2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]丙二酸二乙酯
按照实施例2(方法B)的步骤5中描述的方法,从α-乙酰氧基-[2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]丙二酸二乙酯(步骤3)制备标题化合物。1H-NMR(CDCl3)δ:8.98(1H,br s),7.77-7.72(2H,m),7.51-7.46(2H,m),7.40(1H,dd,J=2.5,9.7Hz),7.18-7.13(1H,m),7.04-6.96(1H,m),5.28(1H,s),4.26-4.07(4H,m),1.30-1.18(6H,m).步骤5.[2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸
按照实施例2(方法B)的步骤6中描述的方法,从[2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]丙二酸二乙酯(步骤4)制备标题化合物。熔点:233-238℃(在乙酸乙酯/己烷中重结晶)。IR(KBr)ν:3317,1707,1624,1609,1587,1526,1458,1408,1344,1263,1242cm-1.1H-NMR(DMSO-d6)δ:11.73(1H,s),7.77(2H,d,J=8.6Hz),7.65(2H,d,J=8.6Hz),7.52-7.44(2H,m),7.22-7.15(1H,m),3.84(2H,s).实施例22 [2-(3-氯苯甲酰基)-5-氟-1H-吲哚-3-基)乙酸 步骤1. 2-(3-氯苯甲酰基)-5-氟吲哚
按照实施例7的步骤2中描述的方法,从5-氟-2-[(N-甲氧基-N-甲基氨基)羰基]吲哚(实施例21的步骤1)和3-溴氯苯制备标题化合物。1H-NMR(CDCl3)δ:9.29(1H,m),7.96-7.94(1H,m),7.88-7.84(1H,m),7.63-7,59(1H,m),7.48(1H,t,J=8.0Hz),7.45-7.40(1H,m),7.36(1H,dd,J=2.6,8.6Hz),7.20-7.11(2H,m).步骤2.α-乙酰氧基-[2-(3-氯苯甲酰基)-5-氟-1H-吲哚-3-基]丙二酸二 乙酯
按照实施例2(方法B)的步骤4中描述的方法,从2-(3-氯苯甲酰基)-5-氟吲哚(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:8.73(1H,br s),7.79-7.74(2H,m),7.61-7.56(2H,m),7.43(1H,t,J=7.6Hz),7.37-7.32(1H,m),7.13-7.06(1H,m),4.34-4.20(4 H,m),1.76(3H,s),1.33-1.20(6H,m).步骤3.[2-(3-氯苯甲酰基)-5-氟-1H-吲哚-3-基]丙二酸二乙酯
按照实施例2(方法B)的步骤5中描述的方法,从α-乙酰氧基-[2-(3-氯苯甲酰基)-5-氟-1H-吲哚-3-基]丙二酸二乙酯(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:9.05(1H,br s),7.76-7.75(1H,m),7.68-7.64(1H,m),7.61-7.56(1H,m),7.48-7.40(2H,m),7.24-7.19(1H,m),7.08-7.00(1H,m),5.25(1H,s),4.28-4.07(4H,m),1.33-1.21(6H,m).步骤4.[2-(3-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸
按照实施例2(方法B)的步骤6中描述的方法,从[2-(3-氯苯甲酰基)-5-氟-1H-吲哚-3-基]丙二酸二乙酯(步骤3)制备标题化合物。熔点:208-212℃(在乙酸乙酯/己烷中重结晶)。IR(KBr)ν:3337,1709,1618,1560,1529,1477,1458,1427,1408,1335,1304cm-1.1H-NMR(DMSO-d6)δ:11.78(1H,s),7.77-7.58(4H,m),7.52-7.46(2H,m),7.24-7.16(1H,m),3.82(2H,s).实施例23 [5-甲氧基-2-(3-甲基苯甲酰基)-1H-吲哚-3-基)乙酸 步骤1. 5-甲氧基-2-[(N-甲氧基-N-甲基氨基)羰基]吲哚
按照实施例7的步骤1中描述的方法,从5-甲氧基吲哚-2-甲酸制备标题化合物。1H-NMR(CDCl3)δ:9.29-9.13(1H,br),7.33(1H,d,J=8.9Hz),7.19-7.14(1H,m),7.10(1H,d,J=2.3Hz),6.98(1H,dd,J=8.9,2.3Hz),3.86(3H,s),3.84(3H,s),3.42(3H,s).步骤2. 5-甲氧基-2-(3-甲基苯甲酰基)吲哚
按照实施例17的步骤2中描述的方法,从5-甲氧基-2-[(N-甲氧基-N-甲基氨基)羰基]吲哚(步骤1)和3-甲基苯基锂制备标题化合物。1H-NMR(CDCl3)δ:9.65-9.45(1H,br),7.84-7.75(2H,m),7.46-7.35(3H,m),7.12-7.01(3H,m),3.85(3H,s),2.46(3H,s).步骤3.α-乙酰氧基-[5-甲氧基-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]丙 二酸二乙酯
按照实施例2(方法B)的步骤4中描述的方法,从5-甲氧基-2-(3-甲基苯甲酰基)吲哚(步骤2)制备标题化合物。tlc∶Rf=0.45(乙酸乙酯/己烷=1∶3)步骤4.[5-甲氧基-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯
按照实施例2(方法B)的步骤5中描述的方法,从α-乙酰氧基-[5-甲氧基-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯(步骤3)制备标题化合物。1H-NMR(CDCl3)δ:9.52-9.13(0.5H,m),8.81-8.71(0.5H,m),7.80-7.72(1H,m),7.63-7.55(1H,m),7.47-7.00(5H,m),5.41(0.5H,s),5.37(0.5H,s),4.27-4.15(4H,m),3.89(1.5H,s),3.84(1.5H,s),2.45(1.5H,s),2.43(1.5H,s),1.29-1.19(6H,m).步骤5.[5-甲氧基-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]乙酸
按照实施例2(方法B)的步骤6中描述的方法,从[5-甲氧基-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯(步骤4)制备标题化合物。熔点:230.4-232.0℃(分解)(在乙酸乙酯中重结晶)。IR(KBr)ν:3310,1705,1614,1583cm-1.1H-NMR(DMSO-d6)δ:11.47(1H,br s),7.60-7.34(5H,m),7.16-7.09(1H,m),6.98(1H,dd,J=9.0,2.4Hz),3.78(5H,s),2.40(3H,s).13C-NMR(DMSO-d6)δ:188.1,172.1,153.8,138.9,137.9,132.7,132.3,132.0,129.2,128.5,128.0,125.8,117.0,115.6,113.6,100.7,55.3,30.6,20.8.实施例24 (2-苯甲酰基-7-氯-1H-吲哚-3-基)乙酸 步骤1. 7-氯-2-[(N-甲氧基-N-甲基氨基)羰基]吲哚
按照实施例7的步骤1中描述的方法,从7-氯吲哚-2-甲酸制备标题化合物(H.N.Rydon和J.C.Tweddle,J.Chem.Soc.,1955,3499)。1H-NMR(CDCl3)δ:9.40(1H,br s),7.59(1H,d,J=8.1Hz),7.32-7.25(2H,m),7.08(1H,t,J=8.1Hz),3.85(3H,s),3.43(3H,s).步骤2. 2-苯甲酰基-7-氯吲哚
按照实施例17的步骤2中描述的方法,从7-氯-2-[(N-甲氧基-N-甲基氨基)羰基]吲哚(步骤1)和苯基锂制备标题化合物。1H-NMR(CDCl3)δ:9.40(1H,br s),8.01-7.96(2H,m),7.70-7.50(4H,m),7.38(1H,d,J=7.6Hz),7.18(1H,d,J=2.0Hz),7.11(1H,t,J=7.6Hz).步骤3.α-乙酰氧基-(2-苯甲酰基-7-氯-1H-吲哚-3-基)丙二酸二乙酯
按照实施例2(方法B)的步骤4中描述的方法,从2-苯甲酰基-7-氯-吲哚(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:8.76(1H,br s),7.92-7.81(3H,m),7.68-7.60(1H,m),7.53-7.45(2H,m),7.33(1H,d,J=7.6Hz),7.1 5(1H,t,J=8.2Hz),4.60-4.20(4H,m),1.71(3H,s),1.98(6H,t,J=7.1Hz).步骤4.(2-苯甲酰基-7-氯-1H-吲哚-3-基)丙二酸二乙酯
按照实施例2(方法B)的步骤5中描述的方法,从α-乙酰氧基-(2-苯甲酰基-7-氯-1H-吲哚-3-基)丙二酸二乙酯(步骤3)制备标题化合物。1H-NMR(CDCl3)δ:8.94(1H,br s),7.86-7.80(2H,m),7.75(1H,d,J=8.1Hz),7.70-7.62(1H,m),7.55-7.50(2H,m),7.36(1H,d,J=7.6Hz),7.13(1H,t,J=7.6Hz),5.29(1H,s),4.25-4.11(4H,m),1.22(6H,t,J=7.3Hz).步骤5.(2-苯甲酰基-7-氯-1H-吲哚-3-基)乙酸
按照实施例2(方法B)的步骤6中描述的方法,从(2-苯甲酰基-7-氯-1H-吲哚-3-基)丙二酸二乙酯(步骤4)制备标题化合物。熔点:190-193℃(在乙酸乙酯/己烷中重结晶)。IR(KBr)ν:1691,1627,1598,1323,1260 1199,1010cm-1.1H-NMR(DMSO-d6)δ:11.90(1H,br s),7.82(2H,m),7.74-7.65(2H,m),7.62-7.38(2H,m),7.40(1H,d,J=7.6Hz),7.13(1H,t,J=7.6Hz),3.75(2H,s).实施例25 (2-苯甲酰基-4,5-二氯-1H-吲哚-3-基)乙酸 步骤1. 4,5-二氯-吲哚-3-基)乙酸
向4,5-二氯吲哚-2-甲酸乙酯(Ishii等人,Chem.Pharm. Bull,1974,
22,1981.,1.8g,7.0mmol)的乙醇(40ml)悬浮液中加入2N NaOH水溶液(10ml),加热回流反应混合物2小时。把混合物冷却到室温并浓缩。残留的固体用2N HCl水溶液(30ml)酸化,用乙醚(80ml×2)萃取。干燥(硫酸镁)有机萃取液并且浓缩,得到1.5g(94%)黄色固体的标题化合物。1H-NMR(DMSO-d6)δ:12.34(1H,br s),7.47-7.39(2H,m),7.08(1H,d,J=1.8Hz).步骤2. 4,5-二氯-2-[(N-甲氧基-N-甲基氨基)羰基]吲哚
按照实施例7的步骤1中描述的方法,从4,5-二氯吲哚-2-甲酸(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:9.62(1H,br s),7.40-7.05(3H,m),3.88(3H,s),3.45(3H,s).步骤3. 2-苯甲酰基-4,5-二氯吲哚
按照实施例17的步骤2中描述的方法,从4,5-二氯-2-[(N-甲氧基-N-甲基氨基)羰基]吲哚(步骤2)和苯基锂制备标题化合物。熔点:206-210℃(在乙酸乙酯/己烷中重结晶)。1H-NMR(CDCl3)δ:9.58(1H,br s),8.05-7.98(2H,m),7.71-7.53(3H,m),7.42(1H,d,J=8.9Hz),7.35(1H,d,J=8.9Hz),7.22(1H,s).步骤4.α-乙酰氧基-(2-苯甲酰基-4,5-二氯-1H-吲哚-3-基)丙二酸二乙 酯
按照实施例2(方法B)的步骤4中描述的方法,从2-苯甲酰基-4,5-二氯-吲哚(步骤3)制备标题化合物。1H-NMR(CDCl3)δ:8.85(1H,br s),7.91-7.86(2H,m),7.66-7.58(1H,m),7.52-7.44(2H,m),7.36(1H,d,J=8.7Hz),7.21(1H,d,J=8.7Hz),4.20-3.98(4H,m),2.07(3H,s),1.15(6H,t,J=7.3Hz).步骤5.(2-苯甲酰基-4,5-二氯-1H-吲哚-3-基)丙二酸二乙酯
按照实施例2(方法B)的步骤5中描述的方法,从α-乙酰氧基-(2-苯甲酰基-4,5二氯-1H-吲哚-3-基)丙二酸二乙酯(步骤4)制备标题化合物。1H-NMR(CDCl3)δ:9.24(1H,br s),7.82-7.76(2H,m),7.65-7.58(1H,m),7.55-7.44(2H,m),7.20(1H,d,J=8.7Hz),7.03(1H,d,J=8.7Hz),5.89(1H,s),4.16-4.02(4H,m),1.20(6H,t,J=7.3Hz).步骤6.(2-苯甲酰基-4,5-二氯-1H-吲哚-3-基)乙酸
按照实施例2(方法B)的步骤6中描述的方法,从(2-苯甲酰基-4,5-二氯-1H-吲哚-3-基)丙二酸二乙酯(步骤5)制备标题化合物。熔点:249-252℃(在乙酸乙酯/己烷中重结晶)。IR(KBr)ν:1701,1625,1523,1450,1330,1257,1012cm-1.1H-NMR(CDCl3)δ:9.92(1H,br s),7.85-7.81(2H,m),7.66-7.42(3H,m),7.36(1H,d,J=8.8Hz),7.29(1H,d,J=8.8Hz),4.09(2H,s).实施例26 (2-苯甲酰基-4,6-二氯-1H-吲哚-3-基)乙酸 步骤1. 4,6-二氯-2-(N-甲氧基-N-甲基氨基)羰基]吲哚
按照实施例7的步骤1中描述的方法,从4,6-二氯吲哚-2-甲酸(Salituro,Francesco G.等人,J.Med.Chem.,1990,
33,2944)制备标题化合物。1H-NMR(DMSO-d6)δ:12.09(1H,br s),7.48(1H,dd,J=1.0,1.6Hz),7.25(1H,d,J=1.6Hz),7.11(1H,s),3.82(3H,s),3.63(3H,s).步骤2. 2-苯甲酰基-4,6-二氯吲哚
按照实施例17的步骤2中描述的方法,从4,6-二氯-2-[(N-甲氧基-N-甲基氨基)羰基]吲哚(步骤1)和苯基锂制备标题化合物。熔点:214-218℃。1H-NMR(CDCl3)δ:9.45(1H,br s),8.02-7.95(2H,m),7.70-7.52(3H,m),7.40(1H,d,J=1.6Hz),7.25(1H,s),7.20(1H,d,J=1.6Hz).步骤3.α-乙酰氧基-(2-苯甲酰基-4,6-二氯-1H-吲哚-3-基)丙二酸二乙 酯
按照实施例2(方法B)的步骤4中描述的方法,从2-苯甲酰基-4,6-二氯-吲哚(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:8.92(1H,br s),7.95-7.86(2H,m),7.68-7.43(3H,m),7.29(1H,d,J=1.8Hz),7.23(1H,d,J=1.8Hz),4.60-4.00(4H,m),2.04(3H,s),1.30-1.10(6H,m)步骤4.(2-苯甲酰基-4,6-二氯-1H-吲哚-3-基)丙二酸二乙酯
按照实施例2(方法B)的步骤5中描述的方法,从α-乙酰氧基-(2-苯甲酰基-4,6二氯-1H-吲哚-3-基)丙二酸二乙酯(步骤3)制备标题化合物。熔点:170-172℃。1H-NMR(CDCl3)δ:9.15(1H,br s),7.84-7.75(2H,m),7.66-7.45(3H,m),7.26(1H,s),7.12(1H,s),5.79(1H,s),4.20-4.00(4H,m),1.20(6H,t,J=7.3Hz).步骤5.(2-苯甲酰基-4,6-二氯-1H-吲哚-3-基)乙酸
按照实施例2(方法B)的步骤6中描述的方法,从(2-苯甲酰基-4,6-二氯-1H-吲哚-3-基)丙二酸二乙酯(步骤4)制备标题化合物。熔点:239-243℃(在乙酸乙酯/己烷中重结晶)。IR(KBr)ν:1725,1555,1525,1330,1287,1250,1005cm-1.1H-NMR(DMSO-d6)δ:12.40(1H,br s),12.12(1H,br s),7.80-7.67(3H,m),7.64-7.54(2H,m),7.48(1H,d,J=1.8Hz),7.23(1H,d,J=1.8Hz),3.99(2H,s).实施例27 (2-苯甲酰基-5,6-二氯-1H-吲哚-3-基)乙酸 步骤1. 5,6-二氯-吲哚-3-基)乙酸
按照实施例25的步骤1中描述的方法,从5,6-二氯吲哚-2-甲酸制备标题化合物(Ishii等人,Chem.Pharm.Bull.,1974,
22,1981)。1H-NMR(DMSO-d6)δ:12.06(1H,br s),7.95(1H,s),7.62(1H,s),7.09(1H,s).步骤2. 5,6-二氯-2-[N-甲氧基-N-甲基氨基)羰基]吲哚
按照实施例7的步骤1中描述的方法,从5,6-二氯吲哚-2-甲酸(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:11.86(1H,br s),7.96(1H,s),7.66(1H,s),7.16(1H,s),3.80(3H,s),3.34(3H,s).步骤3. 2-苯甲酰基-5,6-二氯吲哚
按照实施例17的步骤2中描述的方法,从5,6-二氯-2-[(N-甲氧基-N-甲基氨基)羰基]吲哚(步骤2)和苯基锂制备标题化合物。熔点:206-210℃(在乙酸乙酯/己烷中重结晶)。1H-NMR(CDCl3)δ:9.35(1H,br s),8.00-7.93(2H,m),7.81(1H,s),7.69-7.51(3H,m),7.26(1H,s),7.08(1H,s).步骤4.α-乙酰氧基-(2-苯甲酰基-5,6-二氯-1H-吲哚-3-基)丙二酸二乙 酯
按照实施例2(方法B)的步骤4中描述的方法,从2-苯甲酰基-5,6-二氯吲哚(步骤3)制备标题化合物。1H-NMR(CDCl3)δ:8.76(1H,br s),8.05(1H,s),7.90-7.82(2H,m),7.67-7.59(1H,m),7.54-7.44(3H,m),4.30-4.10(4H,m),1.69(3H,s),1.35-1.20(6H,m).步骤5.(2-苯甲酰基-5,6-二氯-1H-吲哚-3-基)丙二酸二乙酯
按照实施例2(方法B)的步骤5中描述的方法,从α-乙酰氧基-(2-苯甲酰基-5,6二氯-1H-吲哚-3-基)丙二酸二乙酯(步骤4)制备标题化合物。1H-NMR(CDCl3)δ:8.90(1H,br s),7.95(1H,s),7.82-7.76(2H,m),7.70-7.61(1H,m),7.58-7.46(3H,m),5.26(1H,s),4.30-4.05(4H,m),1.24(6H,t,J=7.1Hz).步骤6.(2-苯甲酰基-5,65-二氯-1H-吲哚-3-基)乙酸
按照实施例2(方法B)的步骤6中描述的方法,从(2-苯甲酰基-4,5-二氯-1H-吲哚-3-基)丙二酸二乙酯(步骤5)制备标题化合物。熔点:208-210℃(在乙酸乙酯/己烷中重结晶)。1H-NMR(DMSO-d6)δ:11.91(1H,br s),8.04(1H,s),7.77-7.50(6H,m),3.81(2H,s).实施例28 dl-2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)丙酸 步骤1.α-甲基-(2-苯甲酰基-6-氯-1H-吲哚-3-基)丙二酸二乙酯
按照实施例2(方法B)的步骤4中描述的方法,从2-苯甲酰基-6-氯吲哚(实施例2方法B的步骤3)和甲基丙二酸二乙酯制备标题化合物。m.p.:193-196℃.1H-NMR(CDCl3)δ:8.42(1H,br s),7.87(2H,m),7.66-7.48(3H,m),7.42(1H,d,J=8.8Hz),7.35(1H,d,J=1.8Hz),7.11(1H,dd,J=1.8,8.8Hz),4.30-4.02(4H,m),1.98(3H,s),1.15(6H,t,J=7.1Hz).步骤2.dl-2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)丙酸
按照实施例2(方法B)的步骤6中描述的方法,从α-甲基-(2-苯甲酰基-6-氯-1H-吲哚-3-基)丙二酸二乙酯(步骤1)制备标题化合物。熔点:204-208℃(在乙酸乙酯/己烷中重结晶)。IR(KBr)ν:1720,1620,1475,1260,1230cm-1.1H-NMR(DMSO-d6)δ:12.29(1H,br s),11.72(1H,br s),7.82-7.76(2H,m),7.75-7.68(2H,m),7.65-7.57(2H,m),7.48(1H,d,J=1.8Hz),7.12(1H,dd,J=1.8,8.4Hz),4.15(1H,q,J=7.1Hz),1.44(3H,d,J=7.1Hz).实施例29和实施例30 极性较小的对映体2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)丙酸(实施例29) 和极性较大的对映体2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)丙酸(实施例 30)
用DAICEL CHIRALCEL OJ对dl-2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)丙酸进行手性分离(4.6×250mm,洗脱剂:己烷/异丙醇/三氟乙酸=85∶15∶0.1,流速:1.0ml/分钟),得到极性较小的化合物(保留时间:17分钟)和极性较大的化合物(保留时间:27分钟)。实施例31 [6-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸 步骤1.反式-4-氯-2-(乙氧基羰基氨基)肉桂酸甲酯
在室温和搅拌下,向反式-2-氨基-4-氯肉桂酸甲酯(R.W.Carling等人,J.Med.Chem.,1993,
36,3397.,32.6g,0.15mol)、吡啶(14.9ml,0.17mol)和4-二甲基氨基吡啶(0.5g)的二氯甲烷(500ml)溶液中滴加氯代甲酸乙酯(16.2ml,0.17mol)。搅拌2小时后,浓缩混合物。残留物在乙酸乙酯(1000ml)中稀释,用10%柠檬酸水溶液(500ml)洗涤。有机层依次用水(500ml)、饱和的碳酸氢钠(500ml)、水(500ml)、盐水(500ml)洗涤。干燥(硫酸镁)并除去溶剂后,残留的固体在乙酸乙酯/己烷中重结晶,得到39.13g(92%)的标题化合物。1H-NMR(CDCl3)δ:7.95(1H,br s),7.76(1H,d,J=15.8Hz),7.42(1H,d,J=8.6Hz),7.22(1H,dd,J=2.1,8.5Hz),6.69(1H,br),6.37(1H,d,J=15.7Hz),4.26(2H,q,J=7.3Hz),3.82(3H,s),1.34(3H,t,J=7.25Hz).步骤2.[6-氯-1-乙氧基羰基-2-(4-甲基吡啶-2-羰基)二氢吲哚-3-基] 乙酸甲酯
加热回流反式-4-氯-2-(乙氧基羰基氨基)肉桂酸甲酯(步骤1,1.5g,5.3mmol)、2-溴乙酰基-4-甲基吡啶氢溴酸盐*、碳酸钾(7.3g,53mmol)和乙腈(50ml)的混合物17小时。然后冷却混合物并且浓缩。残留物在乙酸乙酯(200ml)中稀释,用水(200ml)和盐水(200ml)洗涤。干燥(硫酸镁)并除去溶剂后,粗产物通过闪蒸柱色谱纯化,用乙酸乙酯/己烷(1∶5)洗脱,得到433mg(20%)的标题化合物。MS(EI)m/z:416(M+)。*2-溴乙酰基-4-甲基吡啶氢溴酸盐按照下列方法制备:
在冰冷却和搅拌下,向2-乙酰基-4-甲基吡啶(F.H.Case等人,J.Am.Chem.Soc.,1956,
78,5842.,7.8g,57.7mmol)在25%HBr-AcOH(40ml)中的溶液中滴加溴(10.1g,63.5mmol)的AcOH(10ml)溶液。搅拌1小时后,加入乙醚(100ml),过滤收集沉淀,得到10.8g(63%)的标题化合物。1H-NMR(DMSO-d6)d:8.71(1H,d,J=5.1Hz),8.14(1H,s),7.75(1H,d,J=5.1Hz),5.07(2H,s),2.52(3H,s).步骤3.[6-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
在搅拌下,加热回流[6-氯-1-乙氧基羰基-2-(4-甲基吡啶-2-羰基)吲哚-3-基]乙酸甲酯(步骤2,930mg,2.2mmol)的乙醇(20ml)溶液和2NNaOH水溶液(10ml)72小时。冷却到室温后,用2N HCl水溶液(10ml)中和所得的混合物,并且浓缩。残留物在二氯甲烷/甲醇(10∶1,300ml)中稀释,并且干燥(硫酸镁)。除去溶剂后,粗产物通过闪蒸柱色谱纯化,用乙酸乙酯/甲醇(20∶1)洗脱,然后用异丙醇(大约20ml)洗涤,得到120mg(17%)黄色粉末状的标题化合物。熔点:223℃(分解)。IR(KBr)ν:1707,1647,1595,1533,1487,1429,1276,1289,1196cm-1.1H-NMR(DMSO-d6)δ:12.30(1H,s),8.70(1H,d,J=4.9Hz),7.96(1H.br s),7.85-7.70(2H,m),7.65-7.55(1H,m),7.17-7.07(1H,m),4.08(2H,s),2.47(3H,s).实施例32 [6-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸 步骤1.[6-氯-1-乙氧基羰基-2-(5-甲基吡啶-2-羰基)二氢吲哚-3-基] 乙酸甲酯
按照实施例31的步骤2中描述的方法,从反式-4-氯-2-(乙氧基羰基氨基)肉桂酸甲酯(实施例31的步骤l)和2-溴乙酰基-5-甲基吡啶*制备标题化合物的两种非对映体。极性较小的产物:tlc∶Rf=0.30(乙酸乙酯/己烷=1/2),MS(EI)m/z∶416(M+);极性较大的产物:tlc∶Rf=0.25(乙酸乙酯/己烷=1/2),MS(EI)m/z:416(M+)。*2-溴乙酰基-5-甲基吡啶按照下列方法制备:
加热回流2-溴-5-甲基吡啶(5.00g,29.06mmol)、三丁基(1-乙氧基乙烯基)锡(10.49g,29.07mmol)和四(三苯基膦)钯(3.36g,2.91mmol)在甲苯(40ml)中的混合物18小时。冷却混合物,通过硅藻土过滤垫过滤,然后浓缩。把残留物(大约10g)溶于THF(100ml)和水(20ml)的混合物中,冷却到0℃,用20分钟的时间加入N-溴代丁二酰亚胺(5.43g,30.52mmol)。在该温度下搅拌所得的混合物0.5小时,然后浓缩到大约20ml。混合物在乙酸乙酯(300ml)中稀释,用水(200ml×3)洗涤,干燥(硫酸镁)。除去溶剂后,粗产物通过闪蒸柱色谱纯化,用乙酸乙酯/己烷(1∶15-1∶10)洗脱,得到2.30g(37%)油状的标题化合物。1H-NMR(CDCl3)δ:8.49(1H,br s),8.01(1H,d,J=8.1Hz),7.68-7.64(1H,m),4.84(2H,s),2.44(3H,s).步骤2.[6-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例31的步骤3中描述的方法,分别把[6-氯-1-乙氧基羰基-2-(5-甲基吡啶-2-羰基)二氢吲哚-3-基]乙酸甲酯(步骤2)的两种非对映体转变为标题化合物。MS(EI)m/z:328(M+)熔点:235-238℃(在乙酸乙酯中重结晶)。IR(KBr)ν:3281,1699,1638,1529,1310,1150,797,702cm-1.1H-NMR(DMSO-d6)δ:12.26(1H,br s),8.68(1H,br s),8.04(1H,d,J=8.1Hz),7.94(1H,br d,J=9.1Hz),7.79(1H,d,J=8.7Hz),7.74(1H,br s),7.11(1H,br d,J=8.6Hz),4.10(2H,s),2.47(3H,s).没有观察到NH或COOH的信号。实施例33 [6-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
加热回流反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1,675mg,1.92mmol)、2-溴乙酰基-4-氯吡啶氢溴酸盐*(907mg,2.88mol)和碳酸钾(2.65g,19.18mmol)在丙酮(20ml)中的混合物4小时。冷却混合物并且浓缩。残留物在乙酸乙酯(1500ml)中稀释,用水(70ml×6)洗涤。干燥(硫酸镁)并除去溶剂后,粗产物通过闪蒸柱色谱纯化,用乙酸乙酯/己烷(1∶6-1∶3)洗脱,得到195mg(28%)的标题化合物(黄色固体)和264mg(27%)[6-氯-2-(4-氯吡啶-2-羰基)-1-(苯磺酰基)二氢吲哚-3-基]乙酸甲酯(棕色结晶)。[6-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯:MS(EI)m/z:362(M+)。1H-NMR(CDCl3)δ:12.09(1H,br s),8.62(1H,d,J=5.3Hz),8.28(1H,d,J=2.1Hz),7.57(1H,d,J=8.6Hz),7.52(1H,dd,J=2.0 and 5.3Hz),7.45(1H,d,J=1.8Hz),7.08(1H,dd,J=1.8 and 8.7Hz),4.27(2H,s),3.75(3H,s).[6-氯-2-(4-氯吡啶-2-羰基)-1-(苯磺酰基)二氢吲哚-3-基]乙酸甲酯:tlc∶Rf=0.35(乙酸乙酯/己烷=1∶2)。MS(EI)m/z(强度):504(M+,0.1),363(90),335(30),304(100),275(10),223(15)。*2-溴乙酰基-4-氯吡啶氢溴酸盐按照下列方法制备:4-氯-2-吡啶甲腈:向冷却到0℃的4-氯吡啶-N-氧化物(5.00g,38.6mmol)和三甲基甲氰化硅(4.84g,46.3mmol)在二氯甲烷(60ml)中的混合物中滴加N,N-二甲基氨基甲酰氯(3.8ml,40.5mmol)。让混合物温热到环境温度,并搅拌16小时。把混合物冷却到0℃,加入30%碳酸钾的水溶液(100ml)。粗产物用二氯甲烷(100ml×2)萃取,干燥(硫酸镁)有机萃取液并且蒸馏,得到4-氯-2-吡啶甲腈(5.35g,100%)。1H-NMR(CDCl3)δ:8.63(1H,d,J=4.8Hz),7.72(1H,d,J=2.6Hz),7.55(1H,dd,J=1.8,5.1Hz).2-乙酰基-4-氯吡啶:用20分钟时间向冷却到0℃的4-氯-2-吡啶甲腈(5.35g,38.6mmol)的苯(50ml)和乙醚(50ml)溶液中滴加2M MeMgI的乙醚溶液(23ml,46.3mmol)。0.5小时后,让混合物温热到环境温度,并且继续搅拌2小时。把混合物冷却到0℃,加入2M HCl水溶液(100ml)。用饱和的碳酸氢钠水溶液(大约80ml)把混合物变成碱性,分离出有机层,并且干燥(硫酸镁)。除去溶剂后,残留物通过闪蒸色谱纯化,用乙酸乙酯/己烷(1∶5)洗脱,得到3.60g(60%)的2-乙酰基-4-氯吡啶。1H-NMR(DMSO-d6)δ:8.59(1H,d,J=5.1Hz),8.04(1H,d,J=1.8Hz),7.47(1H,dd,J=1.8,5.1Hz),2.72(3H,s).2-溴代乙酰基-4-氯吡啶氢溴酸盐:2-溴代乙酰基-4-氯吡啶氢溴酸盐按照H.McKennis,Jr.,L.B.Turnbull,E.R.Bowman,和E.Tamaki等人的方法(见J.Org.Chem.,1963,
28,383-387),从2-乙酰基-4-氯吡啶制备。1H-NMR(DMSO-d6)δ:8.74(1H,d,J=5.5Hz),8.05(1H,d,J=1.8Hz),7.88(1H,dd,J=2.2 and 5.5Hz),5.02(2H,s).实施例34 [6-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸
在50℃下,加热[6-氯-2-[4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例33,195mg,0.537mmol)在乙醇(20ml)溶液和2N NaOH水溶液(4ml)中的悬浮液1小时。冷却到室温后,加入2N HCl(4ml),并且浓缩混合物。残留物在乙酸乙酯(100ml)中稀释,用水(50ml×2)洗涤并且干燥(硫酸镁)。除去溶剂后,结晶状残留物在乙酸乙酯中重结晶,得到175mg(94%)标题化合物。m.p.:233-234℃.IR(KBr)ν:3306,1709,1641,1531,1254,1236,741cm-1.1H-NMR(DMSO-d6)δ:12.20(1H,br s),12.16(1H,br s),8.80(1H,d,J=5.4Hz),8.12(1H,d,J=2.1Hz),7.90(1H,dd,J=2.1,5.3Hz),7.81(1H,d,J=8.7Hz),7.70(1H,d,J=1.8Hz),7.13(1H,dd,J=2.0,8.7Hz),4.07(2H.s).实施例35 [6-氯-2-(吡啶-2-羰基)-1H-吲哚-3-基]乙酸 步骤1.步骤1.[6-氯-1-乙氧基羰基-2-(吡啶-2-羰基)二氢吲哚-3-基] 乙酸甲酯
按照实施例31的步骤2中描述的方法,从反式-4-氯-2-(乙氧基羰基氨基)肉桂酸甲酯(实施例31的步骤1)和2-溴乙酰基吡啶氢溴酸盐(H.McKennis等人,J.Org.Chem.,1963,387)制备标题化合物。tlc∶Rf=0.3(乙酸乙酯/己烷=1∶3)。步骤2.[6-氯-2-(吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例31的步骤3中描述的方法,分别从[6-氯-1-乙氧基羰基-2-(吡啶-2-羰基)二氢吲哚-3-基]乙酸甲酯(步骤1)制备标题化合物。熔点:210℃(分解)。IR(KBr)ν:3280,1697,1643,1531,1234,1150cm-1.1H-NMR(DMSO-d6)δ:12.22(1H,s),8.84(1H,d,J=4.9Hz),8.15-8.05(2H,m),7.85-7.65(3H,m),7.11(1H,dd,J=1.9,8.7Hz),4.04(2H,s).实施例36 [5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸 步骤1.反式-5-氯-2-硝基肉桂酸甲酯
加热回流5-氯-2-硝基苯甲醛(9.68g,52.16mmol)和(三苯基亚正膦基)乙酸甲酯(18.31g,54.77mmol)在甲苯(200ml)中的混合物2小时,浓缩混合物,结晶状残留物通过闪蒸柱色谱纯化,用乙酸乙酯/己烷(1∶5)洗脱,得到结晶。在乙酸乙酯/己烷中重结晶,得到7.54g(60%)淡黄色固体的标题化合物。1H-NMR(CDCl3)δ:8.09(1H,d,J=15.8Hz),8.04(1H,d,J=8.7Hz),7.60(1H,d,J=2.1Hz),7.51(1H,dd,J=2.1,8.7Hz),6.36(1H,d,J=15.8Hz),3.84(3H,s).步骤2.反式-2-氨基-5-氯肉桂酸甲酯
加热回流反式-5-氯-2-硝基肉桂酸甲酯(步骤1,3.00g,12.42mmol)、铁粉(3.65g,62.08mmol)、氯化铵(332mg,6.21mmol)、乙醇(60ml)和水(10ml)的混合物2小时,冷却混合物,通过硅藻土过滤垫过滤,浓缩滤液。残留物用乙酸乙酯(200ml)稀释,用水(100ml×2)洗涤。干燥(硫酸镁)后,除去溶剂,得到2.57g(98%)结晶状的标题化合物。1H-NMR(CDCl3)δ:7.73(1H,d,J=15.8Hz),7.34(1H,d,J=2.5Hz),7.12(1H,dd,J=2.3,8.6Hz),6.64(1H,d,J=8.6Hz),6.35(1H,d,J=15.8Hz),3.95(2H,br s),3.81(3H,s).步骤3.反式-5-氯-2-(苯磺酰基氨基)肉桂酸甲酯
按照实施例8(方法A)的步骤1中描述的方法,从反式-2-氨基-5-氯肉桂酸甲酯(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:7.72-7.67(2H,m),7.58-7.51(1H,m),7.47-7.40(4H,m),7.36(1H,d,J=8.6Hz),7.31(1H,dd,J=2.1,8.6Hz),6.14(1H,d,J=15.8Hz),3.78(3H.s).没有观察到NH的信号。步骤4.[5-氯-2-(4-甲基吡啶-2-羰基)-1-(苯磺酰基氨基)二氢吲哚-3- 基]乙酸甲酯
按照实施例8(方法A)的步骤2中描述的方法,从反式-5-氯-2-(苯磺酰基氨基)肉桂酸甲酯(步骤3)和2-溴代乙酰基-4-甲基吡啶氢溴酸盐(F.H.Case等人,J.Am.Chem.Soc.,1956,
78,5842)制备标题化合物。tlc∶Rf=0.32(乙酸乙酯/己烷=1∶2)步骤5.[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例31的步骤3中描述的方法,从[5-氯-2-(4-甲基吡啶-2-羰基)-1-(苯磺酰基氨基)二氢吲哚-3-基]乙酸甲酯(步骤4)制备标题化合物。MS(EI)m/z:328(M+)熔点:230-231℃(在乙酸乙酯中重结晶)。IR(KBr)ν:3292,1699,1597,1533,1282,1198,1059,802,704cm-1.1H-NMR(DMSO-d6)δ:12.26(1H,br s),8.69(1H,d,J=5.1Hz),7.93(1H,br s),7.82(1H,d,J=2.0Hz),7.66(1H,d,J=8.7Hz),7.56(1H,br d,J=4.9Hz),7.31(1H,dd,J=2.0,8.7Hz),4.02(2H,s),2.46(3H,s).没有观察到NH或COOH的信号。实施例37 [5-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯 步骤1.[5-氯-2-(6-甲基吡啶-2-羰基)-1-(苯磺酰基氨基)二氢吲哚-3- 基]乙酸甲酯
按照实施例8(方法A)的步骤2中描述的方法,从反式-5-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例36的步骤3)和2-溴代乙酰基-6-甲基吡啶氢溴酸盐(H.Erlenmeyer,J.Jenni和B.Prijs,J.Med.Pharm.Chem.,1961,
3,561-566)制备标题化合物。tlc∶Rf=0.39(乙酸乙酯/己烷=2∶3)步骤2.[5-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例8(方法A)的步骤3中描述的方法,从[5-氯-2-(6-甲基吡啶-2-羰基)-1-(苯磺酰基氨基)二氢吲哚-3-基]乙酸甲酯(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:12.62(1H,br s),8.15(1H,d,J=7.9Hz),7.84(1H,t,J=7.7Hz),7.67(1H,d,J=1.8Hz),7.43(1H,d,J=8.9Hz),7.40(1H,d,J=7.7Hz),7.32(1H,dd,J=2.0,8.7Hz),4.28(2H,s),3.73(3H,s),2.76(3H,s).实施例38 [5-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例34中描述的方法,从[5-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸制备标题化合物。MS(EI)m/z:328(M+)熔点:225-226℃(在乙酸乙酯中重结晶)。IR(KBr)ν:1705,1636,1529,1333,1236,1180,1061,669cm-1.1H-NMR(DMSO-d6)δ:12.13(1H,br s),12.09(1H,br s),7.99(1H,t,J=7.7Hz),7.87(1H,d,J=7.7Hz),7.84(1H,d,J=2.0Hz),7.66(1H,d,J=8.9Hz),7.59(1H,d,J=7.6Hz),7.33(1h,dd,J=2.0,8.9Hz),4.03(2H,s),2.69(3H,s).实施例39 [6-氯-2-(1-甲基咪唑-2-羰基)-1H-吲哚-3-基]乙酸 步骤1.[6-氯-1-乙氧基羰基-2-(1-甲基咪唑-2-羰基)二氢吲哚-3-基] 乙酸甲酯
按照实施例31的步骤2中描述的方法,从反式-4-氯-2-(乙氧基羰基氨基)肉桂酸甲酯(实施例31的步骤1)和2-溴代乙酰基-1-甲基咪唑氢溴酸盐*制备标题化合物。MS(EI)m/z:405(M+)。*2-溴代乙酰基-1-甲基咪唑氢溴酸盐按照下列方法制备:
在冰冷却和搅拌下,向2-乙酰基-1-甲基咪唑(D.H.Davis,J.Hall和E.H.Smith,J.Chem.Soc.Perkin Trans.1,1991,2691.,3.0g,26.8mmol)在25%HBr-AcOH中的悬浮液中滴加溴(4.7g,29.5mmol)的溶液。搅拌0.5小时后,把混合物温热到室温,并且再继续搅拌1小时。向混合物中加入乙醚(150ml),用冰浴冷却混合物。过滤收集沉淀,得到5.2g(66%)淡黄色粉末状的标题化合物。1H-NMR(DMSO-d6)d:7.61(1H,s),7.27(1H,s),4.68(2H,s),3.81(3H,s).步骤2.[6-氯-2-(1-甲基咪唑-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例31的步骤3中描述的方法,从[6-氯-1-乙氧基羰基-2-(1-甲基咪唑-2-羰基)二氢吲哚-3-基]乙酸(步骤1)制备标题化合物。熔点:236℃(分解)。MS(EI)m/z:317(M+).IR(KBr)ν:3238,1695,1630,1537,1402,1229,1146cm-1.1H-NMR(CDCl3+DMSO-d6)δ:12.30(1H,s),7.65(1H,d,J=8.7Hz),7.50(1H,d,J=1.8Hz),7.42(1H,s),7.28-7.23(1H,m),7.16(1H,s),7.09(1H,dd,J=1.8,8.6Hz),4.25(2H,s),4.13(3H,s).实施例40 [5-氯-2-(噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯 步骤1.[5-氯-1-苯磺酰基-2-(噻唑-2-羰基)二氢吲哚-3-基]乙酸甲酯
按照实施例8(方法A)的步骤2中描述的方法,从反式-5-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例36的步骤3)和2-溴代乙酰基噻唑氢溴酸盐(A.Dondoni,A.Marra和P.Merino,J.Am.Chem.Soc.,1994,116,3324)制备标题化合物。tlc:Rf=0.07(乙酸乙酯/己烷=1∶2)。步骤2.[5-氯-2-(噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例8(方法A)的步骤3中描述的方法,从[5-氯-1-苯磺酰基-2-(噻唑-2-羰基)二氢吲哚-3-基]乙酸甲酯(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:11.78(1H,br s),8.12(1H,d,J=3.1Hz),7.75(1H,d,J=3.1Hz),7.68(1H,d,J=1.8Hz),7.44(1H,d,J=8.7Hz),7.34(1H,dd,J=2.0,8.9Hz),4.29(2H,s),3.74(3H,s).实施例41 [5-氯-2-(噻唑-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例9中描述的方法,从[5-氯-1-苯磺酰基-2-(噻唑-2-羰基)二氢吲哚-3-基]乙酸甲酯(步骤2)制备标题化合物。MS(EI)m/z:320(M+)熔点:230-231℃(在乙酸乙酯中重结晶)。IR(KBr)ν:3302,1703,1636,1541,1387,1335,1267,1232,1186,1003,766cm-1.1H-NMR(DMSO-d6)δ:12.23(1H,br s),12.10(1H,br s),8.33(1H,d,J=3.1Hz),8.31(1H,d,J=3.1Hz),7.89(1H,d,J=2.0Hz),7.77(1H,d,J=8.9Hz),7.36(1H,dd,J=2.0,8.7Hz),4.17(2H,s).实施例42 (2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸甲酯
在室温下搅拌(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸(实施例2,50mg,0.16mmol)和10%HCl的甲醇(3ml)溶液的混合物3小时。浓缩混合物,残留物通过闪蒸柱色谱纯化,用乙酸乙酯/己烷(1∶5)洗脱,得到23mg(44%)白色固体的标题化合物。m.p.:134-137℃.IR(KBr)ν:1735,1620,1529,1434,1325,1147,1013,945cm-1.1H-NMR(CDCl3)δ:8.96(1H,br s),7.85-7.74(2H,m),7.66-7.47(4H,m),7.38(1H,d,J=1.8Hz),7.15(1H,dd,J=1.8,8.6Hz),3.18(2H,s),3.65(3H,s).实施例43 (2-苯甲酰基-6-氯-1H-吲哚-3-基)-N,N-二甲基乙酰胺
在0℃下,向(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸(实施例2,140mg,0.45mmol)、二甲基胺盐酸盐(45mg,0.54mmol)和三乙胺(0.1ml,0.54mmol)的DMF(2ml)溶液中加入氰基磷酸二乙酯(DEPC,0.1ml,0.54mmol)。然后在室温下搅拌混合物1小时,把混合物倒入水(20ml)中,用乙醚(50ml×2)萃取。有机萃取液用水(30ml×2)洗涤,干燥(硫酸镁)并且浓缩。残留的固体在乙酸乙酯/己烷中重结晶,得到50mg(33%)标题化合物。熔点:190-193℃(在乙酸乙酯/己烷中重结晶)。IR(KBr)ν:1631,1232,1007,908cm-1.1H-NMR(CDCl3)δ:11.72(1H,br s),7.72-7.64(4H,m),7.60-7.52(2H,m),7.45(1H,d,J=1.2Hz),7.08(1H,d,J=8.6Hz),3.32(2H,s),2.80(3H,s),2.76(3H,s).实施例44 (2-苯甲酰基-6-氯-1H-吲哚-3-基)-N-甲基乙酰胺
按照实施例43中描述的方法,从(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸(实施例2)和甲胺盐酸盐制备标题化合物。熔点:242-246℃(在乙酸乙酯/己烷中重结晶)。IR(KBr)ν:1618,1527,1409,1325cm-1.1H-NMR(CDCl3)δ:11.71(1H,br s),7.82-7.75(2H,m),7.62-7.52(5H,m),7.49-7.46(1H,m),7.15-7.08(1H,m),3.64(2H,s),3.31(3H,s).实施例45 (2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酰胺
按照实施例43中描述的方法,从(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸(实施例2)和氨的THF溶液制备标题化合物。m.p.:234-237℃.IR(KBr)ν:1665,1618,1566,1523,1325.1259,943cm-1.1H-NMR(CDCl3)δ:11.66(1H,br s),7.82-7.75(2H,m),7.74-7.65(2H,m),7.62-7.53(2H,m),7.46(1H,d,J=1.8Hz),7.27(1H,br s),7.12(1H,dd,J=1.8,8.6Hz),6.85(1H,br s),3.63(2H,s).实施例46 (2-苯甲酰基-6-氯-1H-吲哚-3-基)-N-甲氧基-N-甲基乙酰胺
按照实施例43中描述的方法,从(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸(实施例2)和N,O-二甲基羟胺盐酸盐制备标题化合物。熔点:109.9-112.2℃(分解)。IR(KBr)ν:3179,2970,2937,1634,1599,1570cm-1.1H-NMR(CDCl3)δ:9.20-8.90(1H,m),7.84-7.75(2H,m),7.66-7.45(4H,m),7.33(1H,d,J=1.3Hz),7.12(1H,dd,J=8.6,1.8Hz),3.94(2H,s),3.51(3H,s),3.13(3H,s).实施例47 2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)-1-哌啶子基-1-乙酮 步骤1.7-氯-1-苯基-9H-吡喃并[3,4-b]吲哚-3-酮
在室温下搅拌(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸(实施例2,200mg,0.64mmol)、氰基磷酸二乙酯(DEPC,0.12ml,0.76mmol)和三乙胺(0.11ml,0.76mmol)的DMF(3.0ml)溶液5分钟。然后把混合物倒入水(20ml)中,过滤收集橙色沉淀,得到20mg(11%)橙色固体的标题化合物。1H-NMR(CDCl3)δ:10.79(1H,br s),8.10(1H,d,J=8.4Hz),7.93-7.84(2H,m),7.67-7.50(3H,m),7.29(1H,s),7.13(1H,d,J=8.4Hz),6.87(1H,s).步骤2.2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)-1-哌啶子基-1-乙酮
加热回流7-氯-1-苯基-9H-吡喃并[3,4-b]吲哚-3-酮(步骤1,0.30g,1.0mmol)和哌啶(1.0ml,10mmol)的甲醇(20ml)溶液2小时。冷却到室温后,浓缩黄色的混合物,残留的固体在甲醇/己烷中重结晶,得到0.12g(32%)标题化合物。m.p.:223-224℃.IR(KBr)ν:3310,2928,1655,1570,1533,1447,1323,1256,1225,1059,945,858,737,700cm-1.1H-NMR(DMSO-d6)δ:11.7(1H,br s),7.74-7.63(4H,m).7.55(2H,t,J=8.7Hz).7.46(1H,d,J=1.8Hz),7.09(1H,dd,J=8.7,1.8Hz),3.80(2H,s),3.45-3.20(4H,m),1.55-1.20(6H,m)实施例48 2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)-N-(4-甲基-1-哌嗪基)-1-乙酮
按照实施例43中描述的方法,从(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸(实施例2)和1-甲基哌嗪制备标题化合物。熔点:184-185℃(在甲醇/己烷中重结晶)。IR(KBr)ν:2939,2795,1634,1531,1435,1325,1229,1144,1001,737,700cm-1 1H-NMR(CDCl3)δ:9.37(1H,br s),7.78-7.75(1H,m),7.73(1H,d,J=1.5Hz),7.62-7.52(2H,m),7.52-7.43(2H,m),7.18-7.10(1H,m),7.10-7.02(1H,m),3.81(2H,s),3.54(2H,br s),3.36(2H,t,J=4.8Hz),2.36-2.22(4H,m).2.28(3H,s).实施例49 (2-苯甲酰基-6-氯-1H-吲哚-3-基)-N-(2-氰基乙基)乙酰胺
按照实施例43中描述的方法,从(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸(实施例2)和氨基丙腈制备标题化合物。熔点:233-233.5℃(在甲醇/己烷中重结晶)。1H-NMR(DMSO-d6)δ:11.7(1H,br s),8.16(1H,t,J=6.3Hz),7.81-7.75(2H,m),7.72-7.64(2H,m),7.62-7.53(2H,m),7.47(1H,d,J=1.9Hz),7.10(1H,dd,J=8.7,1.9Hz),3.67(2H,s),3.23(2H,q,J=6.3Hz),2.58(2H,t,J=6.3Hz)实施例50 (2-苯甲酰基-6-氯-1H-吲哚-3-基)-N-(2-羟基乙基)乙酰胺
按照实施例43中描述的方法,从(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸(实施例2)和2-氨基乙醇制备标题化合物。熔点:178-179.5℃(在甲醇/己烷中重结晶)。1H-NMR(DMSO-d6)δ:11.7(1H,br s),7.84-7.75(3H,m),7.72-7.64(2H,m),7.61-7.52(2H,m),7.46(1H,d,J=2.0Hz),7.11(1H,dd,J=8.6,2.0Hz),3.64(2H,s),3.38-3.30(3H,m),3.06(2H,q,J=5.9Hz).实施例51 2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)-1-吗啉代-1-乙酮
按照实施例43中描述的方法,从(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸(实施例2)和吗啉制备标题化合物。m.p.:187.7-189.5℃.IR(KBr)ν:3339,2964,2849,1653,1612,1568cm-1.1H-NMR(CDCl3)δ:9.08-8.92(1H,m),7.81-7.72(2H,m),7.69-7.58(2H,m),7.56-7.47(2H,m),7.29(1H,d,J=1.8Hz),7.12(1H,dd,J=8.6,1.8Hz),3.87(2H,s),3.67-3.46(6H,m),3.41-3.31(2H,m).实施例52 [2-(4-氯苯甲酰基)-1H-吲哚-3-基)乙酸 步骤1.2-(4-氯苯甲酰基)-1-(苯磺酰基)吲哚
在氮气气氛和-78℃下,向1-(苯磺酰基)吲哚(500mg,1.94mmol)的THF(5ml)溶液中滴加叔丁基锂(1.4ml,2.33mmol)。把黄色溶液直接倒入冷却到-78℃的对氯苯甲酰氯(0.3ml,2.33mmol)的THF(3ml)溶液中,在-78℃下搅拌反应混合物2小时。用饱和的氯化铵溶液骤冷混合物,用乙酸乙酯萃取(100ml)。有机层用水(50ml)、盐水(50ml)洗涤,干燥(硫酸镁)。除去溶剂后,粗产物通过闪蒸柱色谱纯化,用己烷/乙酸乙酯(10∶1)洗脱,得到339mg(44.1%)黄色无定形的标题化合物。1H-NMR(CDCl3)δ:8.13(1H,d,J=8.4Hz),8.04-8.00(2H,m),7.93-7.90(2H,m),7.58-7.44(7H,m),7.30(1H,t,J=7.4Hz),6.95(1H,s).步骤2.2-(4-氯苯甲酰基)吲哚
加热回流2-(4-氯苯甲酰基)-1-(苯磺酰基)吲哚(步骤1,334mg,0.84mmol)和2N氢氧化钠(1.5ml,2.78mmol)在乙醇(5ml)中的混合物15分钟。浓缩混合物,用乙酸乙酯(100ml)稀释残留物。有机层用水洗涤,干燥(硫酸镁),浓缩,得到211mg(98.2%)黄色固体的标题化合物。1H-NMR(CDCl3)δ:9.45(1H,br.s),7.97-7.92(2H,m),7.74-7.70(1H,m),7.54-7.47(3H,m),7.42-7.36(1H,m),7.21-7.13(2H,m).步骤3.α-乙酰氧基-[2-(4-氯苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯
按照实施例2(方法B)的步骤4中描述的方法,使用2-(4-氯苯甲酰基)吲哚(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:8.94(1H,br.s),7.90(1H,d,J=8.4Hz),7.81-7.77(2H,m),7.43-7.36(3H,m),7.32-7.26(1H,m),7.22-7.16(1H,m),4.27-4.14(4H,m),1.75(3H,s),1.29-1.16(6H,m).步骤4.[2-(4-氯苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯
按照实施例2(方法B)的步骤5中描述的方法,使用α-乙酰氧基-[2-(4-氯苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯(步骤3)制备标题化合物。1H-NMR(CDCl3)δ:8.73(1H,br.s),7.85-7.82(1H,m),7.79-7.76(2H,m),7.52-7.46(2H,m),7.39-7.37(1H,m),7.26-7.19(2H,m),5.27(1H,s),4.26-4.16(4H,m),1.26-1.21(6H,m)步骤5.[2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸
按照实施例2(方法B)的步骤6中描述的方法,使用[2-(4-氯苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯(步骤4)制备标题化合物。熔点:221-224℃(在乙酸乙酯/己烷中重结晶)。IR(KBr)ν:3321,1697,1607,1576,1529,1433,1408,1339,1263,1223,1202cm-1.1H-NMR(DMSO-d6)δ:11.62(1H,s),7.79-7.75(2H,m),7.71-7.63(3H,m),7.46(1H,d,J=8.2Hz),7.35-7.29(1H,m),7.14-7.08(1H,m),3.84(2H,s)实施例53 [6-氯-2-(2-呋喃基羰基)-1H-吲哚-3-基]乙酸 步骤1.6-氯-2-(2-呋喃基羰基)-1-(苯磺酰基)吲哚
按照实施例2(方法B)的步骤2中描述的方法,从6-氯-1-(苯磺酰基)吲哚(实施例2方法B的步骤1)和2-呋喃甲酰氯制备标题化合物。1H-NMR(CDCl3)δ:8.11-8.19(3H,m),7.73-7.74(1H,m),7.51-7.65(4H,m),7.27-7.31(2H,m),7.10(1H,s),6.62-6.64(1H,m).步骤2.6-氯-2-(2-呋喃基羰基)吲哚
按照实施例2(方法B)的步骤3中描述的方法,从6-氯-2-(2-呋喃基羰基)-1-(苯磺酰基)吲哚(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:9.33(1H,br s),7.65-7.73(3H,m),7.46-7.48(2H,m),7.12-7.16(1H,m),6.64-6.66(1H,m).步骤3.α-乙酰氧基-[6-氯-2-(2-呋喃基羰基)吲哚-3-基]丙二酸二乙酯
按照实施例2(方法B)的步骤4中描述的方法,从6-氯-2-(2-呋喃基羰基)吲哚(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:9.60(1H,br s),7.76(1H,d,J=8.9Hz),7.62-7.63(1H,m),7.43(1H,d,J=1.3Hz),7.28-7.29(1H,m),7.13(1H,dd,J=1.8Hz,8.7Hz),6.59(1H,dd,J=1.6Hz,3.5Hz),4.18-4.32(4H,m),1.88(3H,s),1.18-1.28(6H,m).步骤4.[6-氯-2-(2-呋喃基羰基)吲哚-3-基]丙二酸二乙酯
按照实施例2(方法B)的步骤5中描述的方法,从α-乙酰氧基-[6-氯-2-(2-呋喃基羰基)吲哚-3-基]丙二酸二乙酯(步骤3)制备标题化合物。1H-NMR(CDCl3)δ:9.83(1H,br s),7.67(1H,t,J=0.8Hz),7.63(1H,d,J=8.9Hz),7.40(1H,d,J=3.6Hz),7.30(1H,d,J=1.8Hz),7.01(1H,dd,J=1.8Hz,8.9Hz),6.62(1H,dd,J=1.6Hz,2.1Hz),6.19(1H,s),4.20-4.32(4H,m),1.27(6H,t,J=7.3Hz).步骤5.[6-氯-2-(2-呋喃基羰基)吲哚-3-基]乙酸
按照实施例2(方法B)的步骤6中描述的方法,从[6-氯-2-(2-呋喃基羰基)吲哚-3-基]丙二酸二乙酯(步骤4)制备标题化合物。1H-NMR(DMSO-d6)δ:12.22(1H,br s),11.76(1H,br s),8.13(1H,d,J=1.0Hz),7.75(1H,d,J=8.6Hz),7.56(1H,d,J=1.8Hz),7.48(1H,d,J=3.6Hz),7.14(1H,dd,J=1.8Hz,8.6Hz),6.85(1H,dd,J=1.8Hz,3.6Hz),4.02(2H,s).实施例54 [6-氯-2-(环己烷羰基)-1H-吲哚-3-基]乙酸 步骤1.6-氯-2-环己烷羰基-1-(苯磺酰基)吲哚
按照实施例2(方法B)的步骤2中描述的方法,从6-氯-1-(苯磺酰基)吲哚(实施例2方法B的步骤1)和环己烷甲酰氯制备标题化合物。tlc:Rf=0.4(乙酸乙酯/己烷=1∶4)步骤2.6-氯-2-(环己烷羰基)吲哚
按照实施例2(方法B)的步骤3中描述的方法,从6-氯-2-环己烷羰基-1-(苯磺酰基)吲哚(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:10.08(1H,br s),8.08-7.04(4H.m),2.28-1.20(11H,m).步骤3.α-乙酰氧基-[6-氯-2-(环己烷羰基)吲哚-3-基]丙二酸二乙酯
按照实施例2(方法B)的步骤4中描述的方法,从6-氯-2-(环己烷羰基)吲哚(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:8.94(1H,br s),8.12-7.09(3H,m),4.34-4.21(4H,m),2.20(3H,s),1.81-1.20(17H,m).步骤4.[6-氯-2-(环己烷羰基)-1H-吲哚-3-基]丙二酸二乙酯
按照实施例2(方法B)的步骤5中描述的方法,从α-乙酰氧基-[6-氯-2-(环己烷羰基)吲哚-3-基]丙二酸二乙酯(步骤3)制备标题化合物。1H-NMR(CDCl3)δ:8.90(1H,br s),7.72(1H,d,J=8.72Hz),7.36-7.09(2H,m),5.70(1H,s),4.28-4.19(4H,m),1.91-1.22(17H,m).步骤5.[6-氯-2-(环己烷羰基)-1H-吲哚-3-基]乙酸
按照实施例2(方法B)的步骤6中描述的方法,从[6-氯-2-(环己烷羰基)-1H-吲哚-3-基]丙二酸二乙酯(步骤4)制备标题化合物。m.p.:206-209℃IR(KBr)ν:3314,2924,2856,1734,1650,1537,1396,1248,cm-1 1H-NMR(DMSO-d6)δ:11.78(1H,s),7.71(1H,d,J=8.64Hz),7.46-7.07(2H,m),4.01(2H,s),1.78-1.16(11H).实施例55 [6-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例8中描述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8的步骤1)和4-甲氧基苯甲酰甲基溴制备标题化合物。1H-NMR(CDCl3)δ:8.85(1H,s),7.82(2H,d,J=8.9Hz),7.56(1H,d,J=8.6Hz),7.40(1H,d,J=1.8Hz),7.15(1H,dd,J=1.8,8.6Hz),6.99(2H,d,J=8.6Hz),3.90(3H,s),3.86(2H,s),3.67(3H,s).实施例56 [6-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸
按照实施例9(方法B)中描述的方法,从[6-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯(步骤1)制备标题化合物。m.p.:187-190℃1H-NMR(DMSO-d6)δ:11.72(1H,s),7.78(2H,d,J=8.7Hz),7.70(1H,d,J=8.6Hz),7.49-7.45(1H,m),7.15-7.07(3H,m),3.87(3H,s),3.81(2H,s).实施例57 [6-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
在室温下搅拌反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1,700mg,1.99mmol)、2-溴代乙酰基-4-乙基吡啶*(545mg,2.39mmol)、碳酸钾(1.37g,13.9mmol)和丙酮(20ml)的混合物。搅拌3小时后,加入1,8-二氮杂双环[5.4.0]十一碳-7-烯(DBU,0.6ml,3.98mmol)。再搅拌所得的混合物19小时,然后浓缩。残留物用二氯甲烷(200ml)稀释,用水(100ml×2)洗涤。干燥(硫酸镁)有机层,并且浓缩。残留物通过闪蒸柱色谱纯化,用乙酸乙酯/己烷/二氯甲烷(1∶4∶1)洗脱,得到含有杂质的标题化合物。粗产物用乙酸乙酯洗涤,得到297mg(42%)黄色固体的标题化合物。1H-NMR(CDCl3)δ:12.52(1H,br s),8.64(1H,d,J=4.9Hz),8.21(1H,br s),7.62(1H,d,J=8.7Hz),7.52(1H,d,J=1.8Hz),7.39-7.35(1H,m),7.13(1H,dd,J=1.8,8.6Hz),4.31(2H,s),3.73(3H,s),2.78(2H,q,J=7.6Hz),1.32(3H,t,J=7.6Hz).*2-溴代乙酰基-4-乙基吡啶按照下列方法制备:
在冰冷却下,向2-乙酰基-4-乙基吡啶(E.C.Constable等人,J.Am.Chem.Soc.,1997,
119,5606.,8.37g,56.1mmol)在25%氢溴酸-乙酸(150ml)中的溶液中滴加溴(9.86g,61.7mmol)的乙酸(30ml)溶液。把混合物温热到室温并搅拌2小时。向混合物中加入乙醚(500ml),用冰浴冷却所得的混合物。通过倾滗而收集从溶液中析出的棕色油状物。用饱和的碳酸氢钠水溶液(50ml)处理该油状物,用乙醚(300ml)萃取。干燥(硫酸镁)有机层并且浓缩,得到15.3g(88%)标题化合物。1H-NMR(CDCl3)δ:8.56(1H,d,J=5.1Hz),7.95(1H,br s),7.36-7.34(1H,m),4.86(2H,s),2.74(2H,q,J=7.7Hz),1.29(3H,t.J=7.6Hz).实施例58 [6-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
加热回流[6-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例57,297mg,0.83mmol)在2N氢氧化钠水溶液(2.5ml)和乙醇(20ml)中的黄色悬浮液3小时。把混合物冷却到室温后,用2N盐酸水溶液(2.5ml)中和,浓缩。残留物用THF(150ml)稀释,干燥(硫酸镁),浓缩。残留的固体在乙酸乙酯中重结晶,得到251mg(88%)黄色固体的标题化合物。MS(EI)m/z:342(M+)。熔点:215-216℃(分解)。IR(KBr)ν:3206,1707,1643,1595,1535,1421,1227,1192,1140,912,777cm-1.1H-NMR(DMSO-d6)δ:12.30(1H,br s),12.18(1H,br s),8.73(1H,d,J=4.9Hz),7.98(1H,br s),7.79(1H,d,J=8.7Hz),7.74(1H,d,J=1.8Hz),7.62(1H,br d,J=5.1Hz),7.12(1H,dd,J=1.8,8.6Hz),4.08(2H,s),2.78(2H.q,J=7.7Hz),1.26(3H,t,J=7.7Hz).实施例59 [5-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-5-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例36的步骤3)和2-溴代乙酰基-4-乙基吡啶(其制备方法见实施例57)制备标题化合物。1H-NMR(CDCl3)δ:12.57(1H,br s),8.65(1H,d,J=5.1Hz),8.21(1H,br s),7.68(1H,br s),7.45(1H,d,J=8.9Hz),7.40-7.36(1H,m),7.31(1H,dd,J=2.0,8.7Hz),4.28(2H,s),3.74(3H,s),2.78(2H,q,J=7.7Hz),1.32(3H,t,J=7.7Hz).实施例60 [5-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例57中描述的方法,从[5-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例59)制备标题化合物。MS(EI)m/z:342(M+).m.p.:217-218℃IR(KBr)ν:3269,1705,1643,1595,1533,1418,1335,1225,1200,1059,779cm-1.1H-NMR(DMSO-d6)δ:12.33(1H,br s),8.73(1H,d,J=4.9Hz),7.98(1H,br s),7.86(1H,d,J=2.0Hz),7.69(1H,d,J=8.9Hz),7.61(1H,dd,J=4.8,1.6Hz),7.33(1H,dd,J=2.0,8.7Hz),4.07(2H,s),2.78(2H,q,J=7.6Hz),1.26(3H,t,J=7.6Hz).实施例61 [6-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和2-溴代乙酰基-4-异丙基吡啶*制备标题化合物。1H-NMR(CDCl3)δ:12.53(1H,br s),8.65(1H,d,J=4.9Hz),8.24(1H,d,J=1.6Hz),7.62(1H,d,J=8.7Hz),7.52(1H,d,J=1.6Hz),7.40(1H,dd,J=1.8,4.9Hz),7.13(1H,dd,J=1.8,8.7Hz),4.30(2H,s),3.73(3H,s),2.97-3.07(1H,m),1.32(6H,d,J=6.9Hz).*2-溴代乙酰基-4-异丙基吡啶是按照实施例57中所述的制备2-溴代乙酰基-4-乙基吡啶的方法,从2-乙酰基-4-异丙基吡啶(K.Ishihama等人,J.Agric.Food Chem.,1992,
40,1647)制备的。1H-NMR(CDCl3)δ:8.57(1H,d,J=5.8Hz),7.97-7.98(1H,m),7.36-7.38(1H,m),4.86(2H,s),2.94-3.04(1H,m),1.27-1.32(6H,m).实施例62 [6-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[6-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例61)制备标题化合物。m.p.:194-196℃.IR(KBr)ν:3244,2965,1692,1647,1597,1537,1254,1200,1178,1150,764cm-1.1H-NMR(DMSO-d6)δ:12.28(1H,br s),8.74(1H,d,J=5.3Hz),8.01(1H,s),7.80(1H,d,J=8.9Hz),7.74(1H,d,J=1.6Hz),7.64-7.66(1H,m),7.12(1H,dd,J=1.8,8.6Hz),4.08(2H,s),3.02-3.13(1H,m),1.28(6H,d,J=6.9Hz).实施例63 [5-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-5-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例36的步骤3)和2-溴代乙酰基-4-异丙基吡啶*(其制备方法见实施例61)制备标题化合物。1H-NMR(CDCl3)δ:12.57(1H,br s),8.65(1H,d,J=5.1Hz),8.24(1H,d,J=1.6Hz),7.67(1H,d,J=2.0Hz),7.44(1H,d,J=8.2Hz),7.40(1H,dd,J=1.8,4.9Hz),7.31(1H,dd,J=2.0,8.7Hz),4.28(2H,s),3.74(3H,s),2.97-3.07(1H,m),1.32(6H,d,J=6.9Hz).实施例64 [5-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[5-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例63)制备标题化合物。MS(EI)m/z:356(M+).m.p.:227-228℃.IR(KBr)ν:2964,1703,1643,1595,1537,1202,1059,768cm-1.1H-NMR(DMSO-d6)δ:12.32(1H,br s),12.15(1H,br s),8.74(1H,d,J=4.9Hz),8.00(1H,s),7.86(1H,s),7.64-7.71(2H,m),7.31-7.35(1H,m),4.08(2H,s),3.03-3.13(1H,m),1.28(6H,d,J=6.9Hz).实施例65 [6-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和2-溴代乙酰基-4-丙基吡啶氢溴酸盐*制备标题化合物。1H-NMR(CDCl3)δ:12.53(1H,br s),8.64(1H,d,J=4.9Hz),8.19(1H,s),7.62(1H,d,J=8.7Hz),7.53(1H,d,J=1.6Hz),7.35-7.37(1H,m),7.13(1H,dd,J=1.8,8.7Hz),4.31(2H,s),3.73(3H,s),2.71(2H,t,J=7.3Hz),1.69-1.77(2H,m),0.98(3H,t,J=7.3Hz).*2-溴代乙酰基-4-丙基吡啶氢溴酸盐按照下列方法制备:4-丙基-2-吡啶甲腈:
按照实施例33中描述的制备4-氯-2-吡啶甲腈的方法,从4-丙基吡啶-N-氧化物(S.Ghersetti等人,J.Heterocycl.Chem.,1969,
6,859)制备标题化合物。1H-NMR(CDCl3)δ:8.59(1H,d,J=5.1Hz),7.53(1H,s),7.32-7.34(1H,m),2.66(2H,t,J=7.3Hz),1.62-1.76(2H,m),0.97(3H,t,J=7.3Hz).2-乙酰基-4-丙基吡啶:
按照实施例33中描述的制备2-乙酰基-4-氯吡啶的方法,从4-丙基-2-吡啶甲腈制备标题化合物。1H-NMR(CDCl3)δ:8.56(1H,d,J=4.9Hz),7.88(1H,s),7.27-7.30(1H,m),2.72(3H,s),2.66(2H,t,J=7.4Hz),1.62-1.76(2H,m),0.95(3H,t,J=7.4Hz).2-溴代乙酰基-4-丙基吡啶氢溴酸盐:
按照实施例31的步骤2中所述的制备2-溴代乙酰基-4-甲基吡啶氢溴酸盐的方法,从2-乙酰基-4-丙基吡啶制备标题化合物。1H-NMR(DMSO-d6)δ:8.64(1H,d,J=4.9Hz),7.90(1H,d,J=1.0Hz),7.59(1H,dd,J=16,4.9Hz),5.02(2H,s),2.70(2H,t,J=7.4Hz),1.57-1.71(2H,m),0.89(3H,t,J=7.3Hz).实施例66 [6-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从2-[6-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸(实施例65)制备标题化合物。m.p.:189-191℃.IR(KBr)ν:2964,2928,1711,1645,1595,1533,1281,1225,1192,799cm-1.1H-NMR(DMSO-d6)δ:12.28(1H,br s),8.73(1H,d,J=5.1Hz),7.96(1H,s),7.73-7.81(2H,m),7.59(1H,d,J=4.9Hz),7.10-7.13(1H,m),4.08(2H,s),2.73(2H,t,J=7.1Hz),1.63-1.72(2H,m),0.92(3H,t,J=7.3Hz).实施例67 [5-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-5-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例36的步骤3)和2-溴代乙酰基-4-丙基吡啶氢溴酸盐(其制备方法见实施例65)制备标题化合物。1H-NMR(CDCl3)δ:12.56(1H,br s),8.64(1H,d,J=4.9Hz),8.18(1H,s),7.67(1H,d,J=2.0Hz),7.45(1H,d,J=8.7Hz),7.29-7.37(2H,m),4.28(2H,s),3.74(3H,s),2.71(2H,t,J=7.4Hz),1.80-1.66(2H,m),0.97(3H,t,J=7.3Hz).实施例68 [5-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[5-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例67)制备标题化合物。m.p.:208-209℃.IR(KBr)ν:3296,2957,1705,1645,1595,1535,1329,1273,1204,1057,795cm-1 1H-NMR(DMSO-d6)δ:12.33(1H,br s),12.15(1H,br s),8.73(1H,d,J=4.9Hz),7.95(1H,s),7.86(1H,s),7.69(1H,d,J=8.7Hz),7.58-7.61(1H,m),7.31-7.35(1H,m),4.08(2H,s),2.73(2H,t,J=7.4Hz),1.64-1.72(2H,m),0.92(3H,t,J=7.4Hz).实施例69 [2-(4-叔丁基吡啶-2-羰基)-6-氯-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和2-溴代乙酰基-4-叔丁基吡啶*制备标题化合物。1H-NMR(CDCl3)δ:12.55(1H,br s),8.67(1H,d,J=5.3Hz),8.39(1H,d,J=2.1Hz),7.63(1H,d,J=8.7Hz),7.53-7.55(2H,m),7.13(1H,dd,J=1.8,8.7Hz),4.31(2H,s),3.73(3H,s),1.38(9H,s).*2-溴代乙酰基-4-叔丁基吡啶是按照实施例57中所述的制备2-溴代乙酰基-4-乙基吡啶的方法,从2-乙酰基-4-叔丁基吡啶(E.C.Constable等人,J.Am.Chem.Soc.,1997,
119,5606)制备的。1H-NMR(CDCl3)δ:8.58(1H,d,J=4.8Hz),8.11(1H,d,J=1.6Hz),7.51(1H,dd,J=1.8,5.1Hz),4.86(2H,s),1.35(9H,s).实施例70 [2-(4-叔丁基吡啶-2-羰基)-6-氯-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[2-(4-叔丁基吡啶-2-羰基)-6-氯-1H-吲哚-3-基]乙酸甲酯(实施例69)制备标题化合物。MS(EI)m/z:370(M+).m.p.:203-205℃.IR(KBr)ν:2966,1699,1647,1591,1535,1229cm-1.1H-NMR(DMSO-d6)δ:12.29(1H,br s),8.76(1H,d,J=5.3Hz),8.10(1H,d,J=2.0Hz),7.74-7.81(3H,m),7.12(1H,dd,J=1.8,8.6Hz),4.08(2H,s),1.36(9H,s).实施例71 [2-(4-叔丁基吡啶-2-羰基)-5-氯-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-5-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例36的步骤3)和2-溴代乙酰基-4-叔丁基吡啶(其制备方法见实施例69)制备标题化合物。1H-NMR(CDCl3)δ:12.59(1H,br s),8.67(1H,d,J=5.3Hz),8.38(1H,d,J=2.0Hz),7.68(1H,d,J=2.0Hz),7.54(2H,dd,2.0,5.3Hz),7.45(1H,d,J=8.9Hz),7.32(1H,dd,J=2.0,8.9Hz),4.29(2H,s),3.74(3H,s),1.38(9H,s).实施例72 [2-(4-叔丁基吡啶-2-羰基)-5-氯-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[2-(4-叔丁基吡啶-2-羰基)-5-氯-1H-吲哚-3-基]乙酸甲酯(实施例71)制备标题化合物。MS(EI)m/z:370(M+).m.p:209-211℃.IR(KBr)ν:3269,2968,1746,1705,1589,1531,1236,1207,1177,1150,1059,737cm-1.1H-NMR(DMSO-d6)δ:12.33(1H,br s),8.76(1H,d,J=5.3Hz),8.10(1H,d,J=2.0Hz),7.86(1H,d,J=2.0Hz),7.78(1H,dd,J=2.0,5.1Hz),7.69(1H,d,J=8.7Hz),7.33(1H,dd,J=2.0,8.7Hz),4.08(2H,s),1.36(9H,s).实施例73 [6-氯-2-(3-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和2-溴代乙酰基-3-甲基吡啶氢溴酸盐*制备标题化合物。1H-NMR(CDCl3)δ:11.19(1H,br s),8.54(1H,d,J=4.6Hz),7.65(1H,d,J=7.7Hz),7.55(1H,d,J=8.6Hz),7.33-7.38(2H,m),7.06(1H,dd,J=1.8,8.7Hz),4.15(2H,s),3.69(3H,s),2.59(3H,s).*2-溴代乙酰基-3-甲基吡啶是按照实施例31的步骤2中所述的制备2-溴代乙酰基-4-甲基吡啶氢溴酸盐的方法,从2-乙酰基-3-甲基吡啶(T.A.Crabb等人,Org.Magn.Reson.,1982,
20,242)制备的。1H-NMR(DMSO-d6)δ:8.56(1H,d,J=3.6Hz),7.84(1H,d,J=7.7Hz),7.56-7.60(1H,m),5.01(2H,s),4.01(3H,s).实施例74 [6-氯-2-(3-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[6-氯-2-(3-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例73)制备标题化合物。MS(EI)m/z:328(M+).m.p.:195-196℃.IR(KBr)ν:3314,1703,1636,1526,1418,1396,1231,1196,1150,1109cm-1.1H-NMR(DMSO-d6)δ:12.14(1H,br s),11.76(1H,br s),8.53(1H,d,J=3.8Hz),7.85(1H,d,J=7.9Hz),7.74(1H,d,J=8.6Hz),7.52-7.56(2H,m),7.10(1H,dd,J=1.8,8.6Hz),3.66(2H,s),2.33(3H,s).实施例75 [5-氯-2-(3-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-5-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例36的步骤3)和2-溴代乙酰基-3-甲基吡啶氢溴酸盐(其制备方法见实施例73)制备标题化合物。1H-NMR(CDCl3)δ:11.28(1H,br s),8.56(1H,d,J=3.1Hz),7.61-7.69(2H,m),7.23-7.41(3H,m),4.15(2H,s),3.70(3H,s),2.61(3H,s).实施例76 [5-氯-2-(3-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从2-[5-氯-2-(3-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例75)制备标题化合物。熔点:209-211℃(分解)。IR(KBr)ν:3379,3271,1728,1649,1638,1528,1231,1195,1182,1165,1015cm-1.1H-NMR(DMSO-d6)δ:11.81(1H,br s),8.53(1H,d,J=4.4Hz),7.85(1H,d,J=7.7Hz),7.80(1H,d,J=2.0Hz),7.49-7.56(2H,m),7.31(1H,dd,J=2.1,8.7Hz),3.66(2H,s).2.33(3H,s).实施例77 [6-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤13)和2-溴代乙酰基-6-甲基吡啶氢溴酸盐(H.Erlenmeyer,J.Jenni和B.Prijs,J.Med.Pharm Chem.,1961,3,561-566)制备标题化合物。1H-NMR(CDCl3)δ:12.58(1H,br s),8.15(1H,d,J=7.9Hz),7.83(1H,t,J=7.7Hz),7.62(1H,d,J=8.7Hz),7.51(1H,d,J=1.8Hz),7.40(1H,d.J=7.7Hz),7.13(1H,dd,J=1.8,8.7Hz),4.31(2H,s),3.72(3H,s),2.76(3H,s).实施例78 [6-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[6-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例77)制备标题化合物。MS(EI)m/z:328(M+).m.p.:230-231℃.IR(KBr)ν:3273,1697,1643,1535,1308,1227,1183,1150,797,760,671cm-1.1H-NMR(DMSO-d6)δ:12.06(1H,br s),7.99(1H,t,J=7.7Hz),7.87(1H,d,J=7.6Hz),7.78(1H,d,J=8.9Hz),7.74(1H,d,J=2.0Hz),7.59(1H,d,J=7.6Hz),7.13(1H,dd,J=2.0,8.7Hz),4.04(2H,s),2.69(3H,s).实施例79 [5-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-5-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例36的步骤3)和2-溴代乙酰基-5-甲基吡啶(其制备方法见实施例32的步骤1)制备标题化合物。1H-NMR(CDCl3)δ:12.48(1H,br s),8.59(1H,d,J=2.1Hz),8.24(1H,d,J=8.1Hz),7.75(1H,dd,J=2.1,8.1Hz),7.67(1H,d,J=2.0Hz),7.44(1H,d,J=8.7Hz),7.31(1H,dd,J=2.0,8.9Hz),4.29(2H,s),3.74(3H,s),2.48(3H,s).实施例80 [5-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[5-氯-2-(5-甲基吡啶-2-羰基)--1H-吲哚-3-基]乙酸甲酯(实施例79)制备标题化合物。MS(EI)m/z:328(M+).m.p.:247-248℃.IR(KBr)ν:3288,1699,1638,1531,1427,1329,1285,1246,1209,1177,1059,1016,800,700cm-1.1H-NMR(DMSO-d6)δ:12.30(1H,br s),12.15(1H,br s),8.68(1H,br s),8.04(1H,d,J=7.9Hz),7.93(1H,br d,J=8.9Hz),7.84(1H,br s),7.69(1H,d,J=8.9Hz),7.33(1H,dd,J=2.0,8.9Hz),4.09(2H,s),2.46(3H,s).实施例81 [6-氯-2-[5-(三氟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和2-溴代乙酰基-5-(三氟甲基)吡啶*制备标题化合物。1H-NMR(CDCl3)δ:11.97(1H,br s),9.07(1H,br s),8.48(1H,d,J=8.4Hz),8.23(1H,dd,J=2.1,8.4Hz),7.63(1H,d,J=8.6Hz),7.52(1H,d,J=1.8Hz),7.15(1H,dd,J=1.8,8.6Hz),4.31(2H,s),3.74(3H,s).*2-溴代乙酰基-5-(三氟甲基)吡啶是按照实施例32的步骤1中所述的制备2-溴代乙酰基-5-甲基吡啶的方法,从2-氯-5-(三氟甲基)吡啶制备的。1H-NMR(CDCl3)δ:8.96(1H,br s),8.23(1H,br d.J=8.2Hz),8.13(1H,dd,J=2.1,8.1Hz),4.83(2H,s).实施例82 [6-氯-2-[5-(三氟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[6-氯-2-(5-三氟甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例81)制备标题化合物。MS(EI)m/z:382(M+).m.p.:228-229℃.IR(KBr)ν:3325,1707,1636,1529,1333,1310,1138,1078,1020cm-1.1H-NMR(DMSO-d6)δ:12.05(1H,br s),9.17(1H,br s),8.54(1H,dd,J=2.0,8.4Hz),8.24(1H,d,J=8.2Hz),7.82(1H,d,J=8.6Hz),7.64(1H,d,J=1.8Hz),7.14(1H,dd,J=2.0,8.7Hz),4.06(2H,s).实施例83 [5-氯-2-[5-(三氟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-5-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例36的步骤3)和2-溴代乙酰基-5-(三氟甲基)吡啶(其制备方法见实施例81)制备标题化合物。1H-NMR(CDCl3)δ:12.01(1H,br s),9.05(1H,br s),8.45(1H,d,J=8.2Hz),8.21(1H,dd,J=2.3,8.4Hz),7.65(1H,br s),7.43(1H,d,J=8.7Hz),7.32(1H,dd,J=2.0,8.7Hz),4.27(2H,s),3.76(3H,s).实施例84 [5-氯-2-[5-(三氟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[5-氯-2-(5-三氟甲基吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯(实施例83)制备标题化合物。MS(EI)m/z:382(M+).m.p.:230-231℃.IR(KBr)ν:3300,1720,1701,1641,1531,1327,1235,1163,1130,1078,1020,864cm-1.1H-NMR(DMSO-d6)δ:12.09(1H,br s),9.17(1H,br s),8.54(1H,dd,J=2.0,8.2Hz),8.23(1H,d,J=8.2Hz),7.89(1H,d,J=1.8Hz),7.62(1H,d,J=8.9Hz),7.36(1H,dd,J=1.8,8.9Hz),4.06(2H,s).实施例85 [5-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-5-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例36的步骤3)和2-溴代乙酰基-5-氯吡啶*制备标题化合物。1H-NMR(CDCl3)δ:12.01(1H,br s),8.72(1H,d,J=2.5Hz),8.29(1H,d,J=8.6Hz),7.93(1H,dd,J=2.5,8.6Hz),7.65(1H,d,J=2.0Hz),7.43(1H,d,J=8.7Hz),7.31(1H,dd,J=2.0,8.7Hz),4.27(2H,s),3.75(3H,s).*2-溴代乙酰基-5-氯吡啶是按照实施例32的步骤1中所述的制备2-溴代乙酰基-5-甲基吡啶的方法,从2-溴-5-氯吡啶(Case,J.Am.Chem.Soc.,1946,
68,2574)制备的。1H-NMR(CDCl3)δ:8.63(1H,dd,J=0.6,2.5Hz),8.06(1H,dd,J=0.6,8.4Hz),7.85(1H,dd,J=2.3,8.4Hz),4.79(2H,s).实施例86 [5-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[5-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例85)制备标题化合物。MS(EI)m/z:348(M+).m.p.:259-260℃.IR(KBr)ν:3314,1703,1632,1528,1331,1236,1178,1111,1059,1015,806,698cm-1.1H-NMR(DMSO-d6)δ:12.18(1H,br s),12.08(1H,br s),8.84(1H,d,J=2.5Hz),8.25(1H,dd,J=2.5,8.4Hz),8.10(1H,d,J=8.6Hz),7.87(1H,d,J=2.0Hz),7.63(1H,d,J=8.7Hz),7.34(1H,dd,J=2.1,8.9Hz),4.06(2H,s).实施例87 [6-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和2-溴代乙酰基-5-氯吡啶(其制备方法见实施例85)制备标题化合物。1H-NMR(CDCl3)δ:11.98(1H,br s),8.74(1H,dd,J=0.7 and 2.3Hz),8.31(1H,dd,J=0.7,8.6Hz),7.94(1H,dd,J=2.3,8.4Hz),7.63(1H,d,J=8.7Hz),7.52(1H,d,J=1.6Hz),7.14(1H,dd,J=1.8,8.7Hz),4.30(2H,s),3.73(3H,s).实施例88 [6-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[6-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例87)制备标题化合物。MS(EI)m/z:348(M+).m.p.:242-244℃.IR(KBr)ν:3306,1703,1636,1529,1308,1234,1151,1109,698cm-1.1H-NMR(DMSO-d6)δ:12.05(1H,br s),8.84(1H,d,J=2.3Hz),8.26(1H,dd,J=2.3,8.4Hz),8.10(1H,d,J=8.4Hz),7.80(1H,d,J=8.7Hz),7.67(1H,d,J=1.8Hz),7.13(1H,dd,J=1.8,8.7Hz),4.06(2H,s).实施例89 [5-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-5-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例36的步骤3)和2-溴代乙酰基-4-氯吡啶(其制备方法见实施例33)制备标题化合物。1H-NMR(CDCl3)δ:12.20(1H,br s),8.67(1H,d,J=5.3Hz),8.33(1H,d,J=2.1Hz),7.66(1H,d,J=2.0Hz),7.56(1H,dd,J=2.1,5.3Hz),7.43(1H,d,J=8.7Hz),7.32(1H,dd,J=2.0,8.9Hz),4.27(2H,s),3.75(3H,s).实施例90 [5-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[5-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例89)制备标题化合物。MS(EI)m/z:348(M+).m.p.:243-244℃.IR(KBr)ν:3000,1719,1643,1528,1242,1202,741cm-1.1H-NMR(DMSO-d6)δ:12.20(1H,br s),8.80(1H,d,J=5.3Hz),8.12(1H,d,J=2.1Hz),7.90(1H,dd,J=2.1,5.4Hz),7.66(1H,d,J=8.9Hz),7.34(1H,dd,J=2.0,8.7Hz),4.06(2H,s).实施例91 [6-氯-2-(吡啶-3-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和3-溴代乙酰基吡啶氢溴酸盐(G.B.Barlin,L.P.Davies,S.J.Ireland,M.M.L.Ngu,Aust.J.Chem.,1989,42,1735)制备标题化合物。1H-NMR(CDCl3)δ:9.26(1H,br s),9.00(1H,dd,J=0.8,2.1Hz),8.80(1H,dd,J=1.6,4.8Hz),8.10(1H,dt,J=2.0,2.0,7.9Hz),7.58(1H,d,J=8.7Hz),7.47(1H,ddd,J=0.8,4.9,7.9Hz),7.37(1H,d,J=1.8Hz),7.16(1H,dd,J=1.8,8.6Hz),3.84(2H,s),3.65(3H,s).实施例92 [6-氯-2-(吡啶-3-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[6-氯-2-(吡啶-3-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例91)制备标题化合物。MS(EI)m/z:314(M+).m.p.:267-268℃.IR(KBr)ν:3346,1705,1609,1566,1528,1433,1418,1327,1267,1215,943,761cm-1.1H-NMR(DMSO-d6)δ:12.28(1H,br s),11.86(1H,br s),8.90(1H,br s),8.85(1H,brd,J=4.9Hz),8.12(1H,dt,J=2.0,2.0,7.9Hz),7.77(1H,t,J=8.6Hz),7.62(1H,dd,J=4.9,8.0Hz),7.49(1H,d,J=2.0Hz),7.15(1H,dd,J=1.6,8.4Hz),3.85(2H,s).实施例93 [6-氯-2-(吡啶-4-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和4-溴代乙酰基吡啶氢溴酸盐(L.W.Deady,M.S.Stanborough,Aust.J.Chem.,1981,
34,1295)制备标题化合物。1H-NMR(CDCl3)δ:9.21(1H,br s),8.82-8.79(2H,m),7.59-7.57(2H,m),7.56(1H,d,J=8.7Hz),7.33(1H,d,J=1.8Hz),7.16(1H,dd,J=1.8,8.7Hz),3.80(2H,s),3.65(3H,s).实施例94 [6-氯-2-(吡啶-4-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[6-氯-2-(吡啶-4-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例93)制备标题化合物。MS(EI)m/z:314(M+).m.p.:256-257℃.IR(KBr)ν:3352,1709,1607,1528,1431,1329,1259,1202,772,687cm-1.1H-NMR(DMSO-d6)δ:11.82(1H,br s),8.82(2H,d,J=5.8Hz),7.77(1H,d,J=8.6Hz),7.64-7.62(2H,m),7.48(1H,d,J=1.8Hz),7.15(1H,dd,J=2.0,8.7Hz),3.83(2H,s).实施例95 [6-氯-2-[4-(羟甲基)吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯 步骤1.[6-氯-2-[4-(叔丁基二甲基甲硅烷氧基甲基)吡啶-2-羰基]-1H- 吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和2-溴代乙酰基-4-(叔丁基二甲基甲硅烷氧基甲基)吡啶*制备标题化合物。1H-NMR(CDCl3)δ:12.47(1H,br s),8.70(1H,d,J=4.9Hz),8.21-8.22(1H,m),7.55-7.58(2H,m),7.50-7.51(1H,m),7.10(1H,dd,J=1.8,8.7Hz),4.83(2H,s),4.31(2H,s),3.72(3H,s),0.98(9H,s),0.15(6H,s).*2-溴代乙酰基-4-(叔丁基二甲基甲硅烷氧基甲基)吡啶是按照下列方法制备的:2-乙酰基-4-(叔丁基二甲基甲硅烷氧基甲基)吡啶:
按照实施例33中所述的制备2-乙酰基-4-氯吡啶的方法,从4-(叔丁基二甲基甲硅烷氧基甲基)吡啶甲腈(A.Hadri等人,J.Heterocycl.Chem.,1993,
30,631)制备标题化合物。1H-NMR(CDCl3)δ:8.64(1H,d,J=4.8Hz),7.96(1H,s),7.50(1H,d,J=4.8Hz),4.80(2H,s),2.73(3H,s),0.96(9H,s),0.12(6H,s).2-溴代乙酰基-4-(叔丁基二甲基甲硅烷氧基甲基)吡啶:
在-78℃下,向2-溴代乙酰基-4-(叔丁基二甲基甲硅烷氧基甲基)吡啶(1.84g,6.932mmol)的THF(50ml)溶液中滴加二(三甲基甲硅烷基)氨基锂溶液(1M的THF溶液,8.3ml,8.3mmol)。搅拌1小时后,在-78℃下向混合物中加入三乙基氯硅烷(1.7ml,10.4mmol),在该温度下搅拌混合物1小时,然后温热到0℃。搅拌1小时后,加入饱和的氯化铵(50ml)水溶液。用乙醚(100ml)萃取混合物,有机层用水(50ml)洗涤,干燥(硫酸镁)并浓缩。把残留物溶于THF(20ml)中,然后在0℃下加入水(4ml)和NBS。搅拌1小时后,混合物用乙醚(200ml)稀释,用水(50ml)洗涤,干燥(硫酸镁)。除去溶剂后,得到粗产物。粗产物通过闪蒸柱色谱纯化,用乙酸乙酯/己烷(1∶20)洗脱,得到0.74g(31%)结晶状的标题化合物。1H-NMR(CDCl3)δ:8.63(1H,d,J=4.8Hz),8.02(1H,q,J=0.8Hz),7.53(1H,dt, J=0.8,4.9Hz),4.87(2H,s),4.81(2H,s),0.96(9H,s),0.13(3H,s).步骤2.[6-氯-2-[4-(羟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯
在室温下,向[6-氯-2-[4-(叔丁基二甲基甲硅烷氧基甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯(步骤1,171.5mg,0.3625mmol)的THF(5ml)溶液中加入四丁基氟化铵(1M的THF溶液,0.54ml,0.54mmol)溶液。搅拌1小时后,浓缩混合物。残留物用乙酸乙酯(100ml)稀释,用水(20ml×2)洗涤,干燥(硫酸镁)。除去溶剂后,得到粗产物。通过闪蒸柱色谱纯化粗产物,用乙酸乙酯/己烷/二氯甲烷(1∶1∶1)洗脱,得到69.6mg(54%)结晶状的标题化合物。1H-NMR(CDCl3)δ:12.43(1H,br s),8.74(1H,d,J=5.1Hz),8.29(1H,s),7.59-7.64(2H,m),7.52(1H,d,J=1.5Hz),7.13(1H,dd,J=1.6,8.6Hz),4.86(2H,d,J=5.1Hz),4.31(2H,s),3.73(3H,s).实施例96 [6-氯-2-[4-(羟甲基)吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[6-氯-2-[4-(羟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯(实施例95)制备标题化合物。MS(EI)m/z:344(M+).m.p:210-212℃.IR(KBr)ν:3304,1728,1713,1622,1583,1526,1194cm-1.1H-NMR(DMSO-d6)δ:12.3I(1H,br s),8.78(1H,d,J=4.8Hz),8.08(1H,s),7.80(1H,d,J=8.6Hz),7.74(1H,d,J=1.8Hz),7.67(1H,d,J=4.9Hz),7.12(1H,dd,J=1.8,8.7Hz),4.69(2H,s),4.09(2H,s).实施例97 [5-氯-2-[4-(羟甲基)吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯 步骤1.[5-氯-2-[4-(叔丁基二甲基甲硅烷氧基甲基)吡啶-2-羰基]-1H- 吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-5-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例36的步骤3)和2-溴代乙酰基-4-(叔丁基二甲基甲硅烷氧基甲基)吡啶(其制备方法见实施例95的步骤1)制备标题化合物。1H-NMR(CDCl3)δ:12.47(1H,br s),8.66(1H,d,J=4.9Hz),8.18(1H,s),7.60-7.61(1H,m),7.54-7.57(1H,m),7.39(1H,d,J=8.9Hz),7.25(1H,dd,J=2.0,8.9Hz),4.82(2H,s),4.27(2H,s),3.74(3H,s),0.98(9H,s),0.14(6H,s).步骤2.[5-氯-2-[4-(羟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯
按照实施例95的步骤2中描述的方法,从[5-氯-2-[4-(叔丁基二甲基甲硅烷氧基甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:12.48(1H,br s),8.75(1H,d,J=4.9Hz),8.31(1H,s),7.68(1H,s),7.60-7.62(1H,m),7.45(1H,d,J=8.91Hz),7.32(1H,dd,J=2.0,8.9Hz),4.87(2H,d,J=5.4Hz),4.28(2H,s),3.74(3H,s).实施例98 [5-氯-2-[4-(羟甲基)吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[5-氯-2-[4-(羟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯(实施例97)制备标题化合物。MS(EI)m/z:344(M+).m.p.:218-219℃.IR(KBr)ν:3263,1705,1641,1595,1528,1327,1198.1061cm-1.1H-NMR(DMSO-d6)δ:12.34(1H,br s),8.77(1H,d,J=4.9Hz),8.08(1H,s),7.85(1H,s),7.66-7.71(2H,m),7.33(1H,dd,J=1.8,8.9Hz),5.63(1H,br s),4.68(2H,s),4.09(2H,s).实施例99 [5-氯-2-(3,4-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-5-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例36的步骤3)和2-溴代乙酰基-3,4-二甲基吡啶氢溴酸盐*制备标题化合物。1H-NMR(CDCl3)δ:12.20(1H,br s),8.67(1H,d,J=5.3Hz),8.33(1H,d,J=2.1Hz),7.66(1H,d,J=2.0Hz),7.56(1H,dd,J=2.1,5.3Hz),7.43(1H,d,J=8.7Hz),7.32(1H,dd,J=2.0,8.9Hz),4.27(2H,s),3.75(3H,s).*2-溴代乙酰基-3,4-二甲基吡啶氢溴酸盐是按照下列方法制备的:3,4-二甲基吡啶-2-甲腈:
按照实施例33中所述的制备4-氯-2-吡啶甲腈的方法,从3,4-二甲基吡啶-N-氧化物(Abramovitch等人,J.Org.Chem.,1972,
37,1690),制得包含4,5-二甲基吡啶-2-甲腈的标题化合物,其比例为5∶1。2-乙酰基-3,4-二甲基吡啶:
按照实施例33中所述的制备2-乙酰基-4-氯吡啶的方法,从包含4,5-二甲基吡啶-2-甲腈的3,4-二甲基吡啶-2-甲腈制得标题化合物和2-乙酰基-4,5-二甲基吡啶,其比例为5.5∶1。2-乙酰基-3,4-二甲基吡啶:1H-NMR(CDCl3)δ:8.34(1H,d,J=4.6Hz),7.19(1H,d,J=4.8Hz),2.69(3H,s),2.43(3H,s),2.34(3H,s).2-乙酰基-4,5-二甲基吡啶:1H-NMR(CDCl3)δ:8.39(1H,s),7.83(1H,s),2.70(3H,s),2.33(3H,s),2.32(3H,s).2-溴代乙酰基-3,4-二甲基吡啶氢溴酸盐:
按照H.McKennis,Jr.,L.B.Turnbull,E.R.Bowman和E.Tamaki在J.Org.Chem.,1963,
23,383-387中描述的方法,从2-乙酰基-3,4-二甲基吡啶制备标题化合物。1H-NMR(DMSO-d6)δ:8.39(1H,d,J=4.8Hz),7.46(1H,d,J=4.8Hz),4.96(2H,s),2.38(3H,s),2.35(3H,s).实施例100 [5-氯-2-(3,4-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[5-氯-2-(3,4-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例99)制备标题化合物。MS(EI)m/z:342(M+).m.p.:236-237℃.IR(KBr)ν:3395,1710,1641,1526,1339,1281,1196,1053,1007cm-1.1H-NMR(DMSO-d6)δ:11.76(1H,br s),8.37(1H,d,J=4.9Hz),7.79(1H,d,J=2.0Hz),7.48(1H,d,J=8.7Hz),7.41(1H,d,J=4.9Hz),7.31(1H,dd,J=2.0,8.7Hz),3.56(2H,s),2.35(3H,s),2.16(3H,s).实施例101 [5-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-5-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例36的步骤3)和2-溴代乙酰基-4,5-二甲基吡啶*制备标题化合物。1H-NMR(CDCl3)δ:12.59(1H,br s),8.47(1H,s),8.12(1H,s),7.67(1H,d,J=1.8Hz),7.44(1H,d,J=9.4Hz),7.30(1H,dd,J=2.0,8.7Hz),4.28(2H,s),3.73(3H,s),2.38(6H,s).*2-溴代乙酰基-4,5-二甲基吡啶是按照实施例57中所述的制备2-溴代乙酰基-4-乙基吡啶的方法,从2-乙酰基-4,5-二甲基吡啶(其制备方法见实施例99)制备的。1H-NMR(CDCl3)δ:8.39(1H,s),7.87(1H,s),4.83(2H,s),2.35(3H.s),2.34(3H,s).实施例102 [5-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[5-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例101)制备标题化合物。MS(EI)m/z:342(M+).m.p:245-246℃.IR(KBr)ν:3281,1697,1638,1589,1535,1254,1232,1188,1060,802cm-1.1H-NMR(DMSO-d6)δ:12.34(1H,br s),12.15(1H,br s),8.57(1H,s),7.93(1H,s),7.84(1H,d,J=1.8Hz),7.69(1H,d,J=8.7Hz),7.32(1H,dd,J=2.0,8.7Hz),4.09(2H,s),2.39(3H,s),2.38(3H,s).实施例103 [6-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和2-溴代乙酰基-4,5-二甲基吡啶(其制备方法见实施例99)制备标题化合物。1H-NMR(CDCl3)δ:12.55(1H,br s),8.47(1H,s),8.12(1H,s),7.62(1H,d,J=8.6Hz),7.52(1H,d,J=1.8Hz),7.13(1H,dd,J=1.8,8.6Hz),4.31(2H,s),3.72(3H,s),2.39(6H,s).实施例104 [6-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[6-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例103)制备标题化合物。MS(EI)m/z:342(M+).m.p.226-228℃.IR(KBr)ν:3275,1697,1638,1537,1258,1188,799cm-1.1H-NMR(DMSO-d6)δ:12.30(1H,br s),8.57(1H,s),7.94(1H,s),7.78(1H,d,J=8.7Hz),7.74(1H,d,J=1.8Hz),7.11(1H,dd,J=2.0,8.6Hz),4.09(2H,s),2.39(3H,s),2.38(3H,s).实施例105 [6-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和2-溴代乙酰基-4-甲氧基吡啶氢溴酸盐*制备标题化合物。1H-NMR(CDCl3)δ:12.61(1H,br s),8.57(1H,d,J=5.9Hz),7.89(1H,d,J=2.6Hz),7.63(1H,d,J=8.6Hz),7.52(1H,d,J=1.8Hz),7.13(1H,dd,J=1.8,8.7Hz),7.04(1H,dd,J=2.6,5.8Hz),4.30(2H,s),3.96(3H,s),3.73(3H,s).*2-溴代乙酰基-4-甲氧基吡啶氢溴酸盐是按照实施例31的步骤2中所述的制备2-溴代乙酰基-4-甲基吡啶氢溴酸盐方法,从2-乙酰基-4-甲氧基吡啶(B.Case等人,J.Org.Chem.,1961,
26,4415)制得的。1H-NMR(DMSO-d6)δ:8.59-8.62(1H,m),7.63-7.65(1H,m),7.33-7.37(1H,m),5.03(2H,s),3.96(3H,s).实施例106 [6-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[6-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例105)制备标题化合物。MS(EI)m/z:344(M+)熔点:213℃(分解)。IR(KBr)ν:3200,1709,1645,1589,1533,1225,1207cm-1.1H-NMR(DMSO-d6)δ:12.35(1H,br s),12.18(1H,br s),8.66(1H,d,J=5.6Hz),7.80(1H,d,J=8.9Hz),7.74(1H,d,J=1.8Hz),7.63(1H,d,J=2.6Hz),7.31(1H,dd,J=2.9,5.1Hz),7.12(1H,dd,J=1.3,8.7Hz),4.09(2H,s),3.96(3H.s).实施例107 [5-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-5-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例36的步骤3)和2-溴代乙酰基-4-甲氧基吡啶氢溴酸盐(其制备方法见实施例105)制备标题化合物。1H-NMR(CDCl3)δ:12.65(1H,br s),8.57(1H,d,J=5.8Hz),7.88(1H,d,J=2.5Hz),7.68(1H,d,J=2.0Hz),7.45(1H,dd,J=0.5,8.7Hz),7.32(1H,dd,J=1.8,8.7Hz),7.05(1H,dd,J=2.8,5.8Hz),4.28(2H,s),3.96(3H,s),3.74(3H,s).实施例108 [5-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[5-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例107)制备标题化合物。熔点:228℃(分解)。IR(KBr)ν:3230,1707,1647,1595,1566,1533,1477,1331,1300,1219,1180,1038,1013cm-1.1H-NMR(DMSO-d6)δ:12.39(1H,br s),12.16(1H,br s),8.66(1H,d,J=5.8Hz),7.86(1H,d,J=1.5Hz),7.70(1H,d,J=8.7Hz),7.63(1H,d,J=2.5Hz),7.29-7.35(2H,m),4.09(2H,s),3.96(3H,s).实施例109 [6-氯-2-(3,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和2-溴代乙酰基-3,5-二甲基吡啶氢溴酸盐*制备标题化合物。1H-NMR(CDCl3)δ:11.43(1H,br s),8.43(1H,s),7.60(1H,d,J=8.7Hz),7.51(1H,s),7.45(1H,d,J=1.8Hz),7.12(1H,dd,J=1.8,8.7Hz),4.22(2H,s),3.69(3H,s),2.62(3H,s),2.43(3H,s).*2-溴代乙酰基-3,5-二甲基吡啶氢溴酸盐按照下列方法制备:2-乙酰基-3,5-二甲基吡啶:
按照实施例33中所述的制备2-乙酰基-4-氯吡啶的方法,从3,5-二甲基吡啶-甲腈(K.Takahashi等人,J.Heterocycl.Chem.,1978,
15,893)制得标题化合物。1H-NMR(CDCl3)δ:8.32(1H,s),7.37(1H,s),2.69(3H,s),2.56(3H,s),2.36(3H,s).2-溴代乙酰基-3,5-二甲基吡啶氢溴酸盐:
按照H.McKennis,Jr.,L.B.Turnbull,E.R.Bowman和E.Tamaki在J.Org.Chem.,1963,
23,383-387中描述的方法,从2-乙酰基-3,5-二甲基吡啶制备标题化合物。1H-NMR(DMSO-d6)δ:8.43(1H,s),7.69(1H,s),5.00(2H,s),2.52(3H,s),2.39(3H,s).实施例110 [6-氯-2-(3,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[6-氯-2-(3,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例109)制备标题化合物。MS(EI)m/z:342(M+).m.p.:199-200℃.IR(KBr)ν:3279,1705,1639,1526,1238,1177,827,797cm-1.1H-NMR(DMSO-d6)δ:12.12(1H,br s),11.72(1H,br s),8.38(1H,s),7.74(1H,d,J=8.6Hz),7.68(1H,s),7.52(1H,d,J=2.0Hz),7.10(1H,dd,J=1.8,8.6Hz),3.72(2H,s),2.38(3H,s),2.33(3H,s).实施例111 [5-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-5-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例36的步骤3)和2-溴代乙酰基-4-乙基-3-氟吡啶*制备标题化合物。1H-NMR(CDCl3)δ:11.29(1H,br s),8.45(1H,d,J=4.8Hz),7.64(1H,d,J=1.8Hz),7.44(1H,t,J=4.8Hz),7.38(1H,d,J=8.9Hz),7.29(1H,dd,J=2.0,8.7Hz),4.21(2H,s),3.72(3H,s),2.81(2H,q,J=7.6Hz),1.31(3H,t,J=7.6Hz).*2-溴代乙酰基-4-乙基-3-氟吡啶按照下列方法制备:4-乙基-3-氟吡啶-N-氧化物:
把4-乙基-3-氟吡啶(R.P.Dikinson等人,Bioorg.Med.Chem.Lett.,1996,
6,2031,28.51g,205.9mmol)和30%过氧化氢(30ml)在乙酸(300ml)中的混合物加热回流3小时。冷却到室温后,浓缩所得的混合物。残留物在二氯甲烷(300ml)中稀释,干燥(硫酸镁)。除去溶剂后,得到32.30g(100%)油状的标题化合物。1H-NMR(DMSO-d6)d:8.43-8.46(1H,m),8.08(1H,d,J=6.1Hz),7.38(1H,dd,J=6.6,9.7Hz),2.61(2H,q,J=7.6Hz),1.17(3H,t,J=7.6Hz).4-乙基-3-氟-2-吡啶甲腈:
按照实施例33中所述的制备4-氯-2-吡啶甲腈的方法,从4-乙基-3-氟吡啶-N-氧化物制备标题化合物。1H-NMR(CDCl3)d:8.42(1H,d,J=4.8Hz),7.43(1H,t,J=5.1Hz),2.78(2H,q,J=7.6Hz),1.30(3H,t,J=7.6Hz).2-乙酰基-4-乙基-3-氟吡啶:
按照实施例33中所述的制备2-乙酰基-4-氯吡啶的方法,从4-乙基-3-氟-2-吡啶甲腈制备标题化合物。1H-NMR(CDCl3)d:8.376(1H,d,J=4.6Hz),7.36(1H,t,J=4.8Hz),2.76(2H,q,J=7.6Hz),2.71(3H,s),1.28(3H,t,J=7.6Hz).2-溴代乙酰基-4-乙基-3-氟吡啶:
按照实施例57中所述的制备2-溴代乙酰基-4-乙基吡啶的方法,从2-乙酰基-4-乙基-3-氟吡啶制备标题化合物。1H-NMR(CDCl3)d:8.38(1H,d,J=4.6Hz),7.43(1H,d,J=4.6Hz),4.75(2H,s),2.78(2H,q,J=7.6Hz),1.29(3H,t,J=7.6Hz).实施例112 [5-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸
在搅拌下,加热回流[5-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例111,391.2mg,1.044mmol)在乙酸(12ml)和2NHCl水溶液(4ml)中的溶液24小时。冷却到室温后,浓缩所得的混合物。残留物在THF(100ml)中稀释,干燥(硫酸镁),浓缩。通过重结晶来纯化粗产物,得到349.2mg(93%)的标题化合物。MS(EI)m/z:361(M+).m.p.208℃.IR(KBr)ν:3217,1720,1632,1516,1429,1234,1180,1057cm-1.1H-NMR(DMSO-d6)δ:11.78(1H,br s),8.35(1H,d,J=4.8Hz),7.73(1H,d,J=2.0Hz),7.56(1H,t,J=5.1Hz),7.39(1H,d,J=8.9Hz),7.22(1H,dd,J=2.0,8.9Hz),3.65(2H,s),2.65(2H,q,J=7.6Hz),1.14(3H,t,J=7.6Hz).实施例113 [6-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)制备标题化合物。1H-NMR(CDCl3)δ:11.23(1H,br s),8.46(1H,d,J=4.8Hz),7.60(1H,d,J=9.2Hz),7.42-7.46(2H,m),7.10-7.14(1H,m),4.23(2H,s),3.71(3H,s),2.81(2H,q,J=7.7Hz),1.31(3H,t,J=7.7Hz).实施例114 [6-氯-2-(3-乙氧基-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[6-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例113)制备标题化合物。m.p.:165℃.IR(KBr)ν:3300,2974,705,1645,1529,1339,1178cm-1.1H-NMR(DMSO-d6)δ:11.65(1H,br s),8.32(1H,d,J=4.6Hz),7.73(1H,d,J=8.9Hz),7.47-7.52(2H,m),7.10(1H,dd,J=1.8,8.6Hz),3.89(2H,q,J=6.9Hz),3.70(2H,s),2.72(2H,q,J=7.6Hz),1.13-1.26(6H,m).实施例115 [6-氯-2-(3-氯-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和2-溴代乙酰基-3-氯-4-乙基吡啶氢溴酸盐*制备标题化合物。1H-NMR(CDCl3)δ:10.05(1H,br s),8.47(1H,d,J=4.9Hz),7.53(1H,d,J=8.7Hz),7.32-7.34(2H,m),7.05(1H,dd,J=1.8,8.7Hz),3.79(2H,s),3.61(3H,s),2.83(2H,q,J=7.6Hz),1.28(3H,t,J=7.6Hz).*2-溴代乙酰基-3-氯-4-乙基吡啶氢溴酸盐按照下列方法制备:3-氯-4-乙基吡啶-N-氧化物:
按照实施例111中所述的制备4-乙基-3-氟吡啶-N-氧化物方法,从3-氯-4-乙基吡啶(F.Marsais等人,J.Organomet.Chem,1981,216,139)制得标题化合物。1H-NMR(DMSO-d6)δ:8.46(1H,d,J=1.8Hz),8.16(1H,d,J=6.6Hz),7.40(1H,dd,J=1.8,6.6Hz),2.67(2H,q,J=7.6Hz),1.14-1.19(3H,m).3-氯-4-乙基-2-吡啶甲腈:
按照实施例33中所述的制备4-氯-2-吡啶甲腈的方法,从3-氯-4-乙基吡啶-N-氧化物制备标题化合物。1H-NMR(CDCl3)δ:8.50(1H,d,J=4.9Hz),7.41(1H,t,J=4.9Hz),2.84(2H,q,J=7.4Hz),1.30(3H,t,J=7.6Hz).2-乙酰基-3-氯-4-乙基吡啶:
按照实施例33中所述的制备2-乙酰基-4-氯吡啶的方法,从3-氯-4-乙基吡啶-2-吡啶甲腈制备标题化合物。1H-NMR(CDCl3)δ:8.41(1H,d,J=4.8Hz),7.29(1H,d,J=4.8Hz),2.83(2H,q,J=7.6Hz),2.67(3H,s),1.27(3H,t,J=7.6Hz).2-溴代乙酰基-3-氯-4-乙基吡啶氢溴酸盐:
按照实施例31的步骤2中所述的制备2-溴-4-甲基吡啶的方法,从2-乙酰基-3-氯-4-乙基吡啶制备标题化合物。1H-NMR(DMSO-d6)δ:8.55(1H,d,J=4.9Hz),7.66(1H,d,J=4.8Hz),4.93(2H,s),2.82(2H,q,J=7.3Hz),1.21(3H,t,J=7.4Hz).实施例116 [6-氯-2-(3-氯-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[6-氯-2-(3-氯-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例115)制备标题化合物。m.p.:158℃.IR(KBr)ν:3335,1730,1630,1529,1325,1200cm-1.1H-NMR(DMSO-d6)δ:11.83(1H,br s),8.54(1H,d,J=4.8Hz),7.75(1H,d,J=8.7Hz),7.63(1H,d,J=4.9Hz),7.46(1H,s),7.12(1H,dd,J=1.8,8.7Hz),3.57(2H,s),2.82(2H,q,J=7.4Hz),1.25(3H,t,J=7.4Hz).实施例117 [5-氯-2-(3-氯-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-5-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例36的步骤3)和2-溴代乙酰基-3-氯-4-乙基吡啶氢溴酸盐(其制备方法见实施例115)制备标题化合物。1H-NMR(CDCl3)δ:9.87(1H,br s),8.50(1H,d,J=4.9Hz),7.64(1H,s),7.29-7.40(3H,m),3.86(2H,s),3.63(3H,s),2.88(2H,q,J=7.6Hz),1.32(3H,t,J=7.6Hz).实施例118 [5-氯-2-(3-氯-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[5-氯-2-(3-氯-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例117)制备标题化合物。m.p.:220℃.IR(KBr)ν:3341,1695,1626,1533,1458,1429,1229cm-1.1H-NMR(DMSO-d6)δ:11.88(1H,br s),8.54(1H,d,J=4.9Hz),7.82(1H,s),7.63(1H,d,J=4.9Hz),7.46(1H,d,J=8.9Hz),7.34(1H,dd,J=2.0,8.9Hz),3.60(2H,s),2.82(2H,q,J=7.4Hz),1.25(3H,t,J=7.4Hz).实施例119 [5-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-5-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例36的步骤3)和2-溴代乙酰基-4,6-二甲基吡啶*制备标题化合物。1H-NMR(CDCl3)δ:12.73(1H,br s),7.98(1H,s),7.67(1H,br s),7.42(1H,d,J=8.9Hz),7.30(1H,dd,J=1.8 and 8.7Hz),7.22(1H,s),4.27(2H,s),3.73(3H,s),2.70(3H,s),2.43(3H,s).*2-溴代乙酰基-4,6-二甲基吡啶是按照实施例57中所述的制备2-溴代乙酰基-4-乙基吡啶的方法,从2-乙酰基-4,6-二甲基吡啶(Sundberg等人,J.Am.Chem.Soc.,1969,
91,658)制备的。1H-NMR(CDCl3)δ:7.72(1H,s),7.19(1H,s),5.13(2H,s),2.55(3H,s),2.38(3H,s).实施例120 [5-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[5-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例119)制备标题化合物。MS(EI)m/z:342(M+).m.p.:233-235℃.IR(KBr)ν:3288,2919,1742,1630,1599,1529,1333,1232,1180,1067,772cm-1.1H-NMR(DMSO-d6)δ:11.99(1H,br s),7.69(1H,s),7.57(1H,s),7.52(1H,d,J=8.9Hz),7.28(1H,s),7.18(1H,dd,J=2.1,8.9Hz),3.87(2H,s),2.49(3H,s),2.27(3H,s).实施例121 [6-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和2-溴代乙酰基-4,6-二甲基吡啶(其制备方法见实施例119)制备标题化合物。1H-NMR(CDCl3)δ:12.69(1H,br s),7.98(1H,s),7.62(1H,d,J=8.7Hz),7.50(1H,d,J=0.7Hz),7.22(1H,s),7.12(1H,dd,J=1.6,8.6Hz),4.30(2H,s),3.72(3H,s),2.70(3H,s),2.43(3H,s).实施例122 [6-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[6-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例121)制备标题化合物。MS(EI)m/z:342(M+).m.p.:219-220℃.IR(KBr)ν:3300,1701,1639,1603,1535,1225,1180cm-1.1H-NMR(DMSO-d6)δ:11.95(1H,br s),7.62(1H,d,J=8.7Hz),7.58(1H,d,J=1.3Hz),7.56(1H,s),7.27(1H,s),6.96(1H,dd,J=2.0,8.7Hz),3.87(2H,s),2.49(3H,s),2.26(3H,s).实施例123 [5,6-二氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯 步骤1.反式-4,5-二氯-2-硝基肉桂酸甲酯
按照实施例36的步骤1中所述的方法,从4,5-二氯-2-硝基苯甲醛(J.Kenneth等人,J.Med.Chem.,1968,
11,946)制备标题化合物。1H-NMR(CDCl3)δ:8.20(1H,s),8.04(1H,d,J=15.8Hz),7.72(1H,s),6.36(1H,d,J=15.8Hz).步骤2.反式-2-氨基-4,5-二氯肉桂酸甲酯
按照实施例36的步骤2中描述的方法,从反式-4,5-二氯-2-硝基肉桂酸甲酯(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:7.65(1H,d,J=15.8Hz),7.42(1H,s),7.26(1H,s),6.81(1H,s),6.28(1H,d,J=15.8Hz).步骤3.反式-4,5-二氯-2-(苯磺酰基氨基)肉桂酸甲酯
按照实施例8方法A的步骤1中所述的方法,从反式-2-氨基-4,5-二氯肉桂酸甲酯(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:7.80-7.70(2H,m),7.60-7.40(6H,m),7.02(1H,br s),6.13(1H,d,J=16.1Hz),3.79(3H,s).步骤4.[(5,6-二氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中所述的方法,从反式-4,5-二氯-2-(苯磺酰基氨基)肉桂酸甲酯(步骤3)和2-溴代乙酰基-4-甲基吡啶氢溴酸盐(其制备方法见实施例31的步骤2)制备标题化合物。1H-NMR(DMSO-d6)δ:12.45(1H,br s),8.69(1H,d,J=5.1Hz),8.14(1H,s),8.00-7.93(2H,m),7.59(1H,d,J=4.3Hz),4.16(2H,s),3.59(3H,s),3.32(3H,s).实施例124 [5,6-二氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[5,6-二氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例123)制备标题化合物。m.p.:220-224℃.1H-NMR(DMSO-d6)δ:12.41(1H,s),12.20(1H,br s),8.69(1H,d,J=5.1Hz),8.11(1H,s),7.96-7.58(2H,m),7.58(1H,d,J=4.8Hz),4.08(2H,s),2.47(3H,s).实施例125 [5-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯 步骤1.反式-2-氨基-5-甲基肉桂酸甲酯
按照实施例36的步骤2中描述的方法,从反式-5-甲基-2-硝基肉桂酸甲酯(C.Venkatasubban,J.Annamalai Univ.,1933,
2,227)制备标题化合物。1H-NMR(CDCl3)δ:7.82(1H,d,J=15.8Hz),7.20-7.19(1H,m),7.01-6.98(1H,m),6.63(1H,d,J=8.2Hz),6.35(1H,d,J=15.8Hz),3.83(2H,m),3.80(3H,s),2.24(3H,s).步骤2.反式-5-甲基-2-(苯磺酰基氨基)肉桂酸甲酯
按照实施例8方法A的步骤1中所述的方法,从反式-2-氨基-5-甲基肉桂酸甲酯(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:7.70-7.67(2H,m),7.55-7.38(4H,m),7.26-7.14(3H,m),6.55(1H,br s),6.14(1H,d,J=16.0Hz),3.77(3H,s),2.33(3H,s)步骤3.[5-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中所述的方法,从反式-5-甲基-2-(苯磺酰基氨基)肉桂酸甲酯(步骤2)和2-溴代乙酰基-4-甲基吡啶氢溴酸盐(其制备方法见实施例31的步骤2)制备标题化合物。1H-NMR(CDCl3)δ:12.32(1H,br s),8.61(1H,d,J=5.0Hz),8.17(1H,s),7.46(1H,s),7.40(1H,d,J=8.6Hz),7.33-7.32(1H,m),7.22-7.19(1H,m),4.31(2H,s),3.72(3H,s),2.46(6H.m)实施例126 [5-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[5-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例125)制备标题化合物。m.p.:220-226℃.IR(KBr)ν:3736,3649,1697,1533,1508,1398,1194,802cm-1.1H-NMR(DMSO-d6)δ:12.08(1H,br s),8.69(1H,d,J=4.8Hz),7.94(1H,s),7.56-7.49(3H,m),7.17(1H,dd,J=8.4Hz),4.05(2H,s),2.46(3H,s),2.40(3H,s).实施例127 [5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯 步骤1.反式-5-氟-2-硝基肉桂酸甲酯
按照实施例36的步骤1中所述的方法,从5-氟-2-硝基苯甲醛制备标题化合物。1H-NMR(CDCl3)δ:8.17-8.10(2H,m),7.32-7.19(2H,m),6.36(1H,d,J=15.8Hz),3.84(3H,s).步骤2.反式-5-氟-2-氨基肉桂酸甲酯
按照实施例36的步骤2中描述的方法,从反式-5-氟-2-硝基肉桂酸甲酯(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:7.77(1H,dd,J=15.8,1.5Hz),7.10-7.06(1H,m),6.94-6.87(1H,m),6.68-6.63(1H,m),6.33(1H,d,J=15.8Hz),3.85(2H,m),3.81(3H,s).步骤3.反式-5-氟-2-(苯磺酰基氨基)肉桂酸甲酯
按照实施例8方法A的步骤1中所述的方法,从反式-5-氟-2-氨基肉桂酸甲酯(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:7.68-7.65(2H,m),7.55-7.49(2H,m),7.44-7.33(3H,m),7.18-7.13(1H,m),7.10-7.04(1H,m),6.10(1H,d,J=15.8Hz),3.78(3H,s).步骤4.[5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中所述的方法,从反式-5-氟-2-(苯磺酰基氨基)肉桂酸甲酯(步骤3)制备标题化合物。1H-NMR(CDCl3)δ:12.46(1H,br s),8.58-8.56(1H,m),8.12(1H,s),7.43-7.39(1H,m),7.33-7.26(2H,m),7.14-7.06(1H,m),4.26(2H,s),3.74(3H,s),2.45(3H,s).实施例128 [5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例127)制备标题化合物。熔点:223℃(分解)。IR(KBr)ν:1705,1643,1570,1277,1227,1204,1186cm-1.1H-NMR(DMSO-d6)δ:12.28(1H,br s),8.70(1H,d.J=4.9Hz),7.95(1H,s),7.71-7.66(1H,m),7.58-7.52(2H,m),7.25-7.17(1H,m),4.06(2H,s),2.47(3H,s).实施例129 [5-甲氧基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯 步骤1.反式-5-甲氧基-2-硝基肉桂酸甲酯
按照实施例36的步骤1中所述的方法,从5-甲氧基-2-硝基苯甲醛制备标题化合物。1H-NMR(CDCl3)δ:8.21(1H,d,J=15.8Hz),8.16-8.12(1H,m),7.00-6.96(2H,m),6.30(1H,d,J=15.8Hz),3.93(3H,s),3.83(3H,s).步骤2.反式-5-甲氧基-2-氨基肉桂酸甲酯
按照实施例36的步骤2中描述的方法,从反式-5-甲氧基-2-硝基肉桂酸甲酯(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:7.83(1H,d,J=15.8Hz),6.92-6.91(1H,m),6.82(1H,dd,J=8.7,2.8Hz),6.66(1H,d,J=8.7Hz),6.35(1H,d,J=15.8Hz),3.80(3H,s),3.76(3H,s).步骤3.反式-5-甲氧基-2-(苯磺酰基氨基)肉桂酸甲酯
按照实施例8方法A的步骤1中所述的方法,从反式-5-甲氧基-2-氨基肉桂酸甲酯(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:7.67-7.64(2H,m),7.54-7.37(4H,m),7.24(1H,d,J=8.7Hz),6.95(1H,d,J=2.8Hz),6.89(1H,dd,J=8.7,2.8Hz),6.82(1H,br s),6.10(1H,d,J=15.8Hz),3.81(3H,s),3.77(3H,s).步骤4.[5-甲氧基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中所述的方法,从反式-5-甲氧基-2-(苯磺酰基氨基)肉桂酸甲酯(步骤3)制备标题化合物。1H-NMR(CDCl3)δ:12.38(1H,br s),8.61(1H,d,J=4.9Hz),8.17(1H,s),7.40(1H,d,J=8.7Hz),7.34-7.32(1H,m),7.08-7.03(2H,m),4.31(2H,s),3.88(3H,s),3.73(3H,s),2.47(3H,s).实施例130 [5-甲氧基-2-(4甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[5-甲氧基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例129)制备标题化合物。熔点:235℃(分解)。IR(KBr)ν:1701,1638,1595,1528,1448,1423,1340,1279,1263,1234,1223,1192,1111cm-1.1H-NMR(DMSO-d6)δ:12.11(1H,br s),8.69(1H,d,J=4.9Hz),7.95(1H,s),7.58-7.55(2H,m),7.18(1H,m),7.02-6.98(1H,m),4.07(2H,s),3.79(3H,s),2.46(3H,s).实施例131 [6-甲氧基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯 步骤1.反式-(4-甲氧基-2-硝基)肉桂酸甲酯
在130℃下搅拌4-溴-3-硝基苯甲醚(4.177g,18.0mmol)、丙烯酸甲酯(3.24ml,36.0mmol)、乙酸钯(II)(606.1mg,2.7mmol)、三苯基膦(1.416g,5.4mmol)、三乙胺(3.76ml,27.0mmol)在DMF(45.0ml)中的混合物4小时。冷却到室温后,浓缩混合物。向残留物中加入水(30ml),然后用乙酸乙酯-甲苯(3∶1,40ml)萃取混合物。水层进一步用乙酸乙酯(2×30ml)萃取,干燥(硫酸镁)合并后的有机层,并且浓缩,得到6.42g(定量的)棕色油状的标题化合物。1H-NMR(CDCl3)δ:8.07-6.97(4H,m),6.31(1Hd,15.8Hz),3.90(3H,s),3.82(3H,s).步骤2.反式-2-氨基-4-甲氧基肉桂酸甲酯
按照实施例36的步骤2中描述的方法,从反式-(4-甲氧基-2-硝基)肉桂酸甲酯(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:7.80-6.21(5H,m),4.03(2H,brs),3.79(6H,s).步骤3.反式-4-甲氧基-2-(对甲苯磺酰基氨基)肉桂酸甲酯
按照实施例8方法A的步骤1中所述的方法,从反式-4-甲氧基-2-氨基肉桂酸甲酯(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:7.62-6.73(9H,m),6.07(1H,d,15.8Hz),3.80(3H,s),3.77(3H,s),2.37(3H,s).步骤4.[6-甲氧基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中所述的方法,从反式-4-甲氧基-2-(对甲苯磺酰基氨基)肉桂酸甲酯(步骤3)和2-溴代乙酰基-4-甲基吡啶氢溴酸盐(其制备方法见实施例31的步骤2)制备标题化合物。1H-NMR(CDCl3)δ:12.32(1H,br s),8.61(1H,d,4.94Hz),8.19-7.55(2H,m),7.34-6.82(3H,m),4.31(2H,s),3.89(3H,s),3.72(3H,s),2.47(3H,s).实施例132 [6-甲氧基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例9方法B中描述的方法,从[6-甲氧基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例131)制备标题化合物。m.p.:204_C.IR(KBr)ν:3198,1709,1630,1593,1531,1460,1423,1334,1275,1213,1161,1136,1039,1001cm-1.1H-NMR(DMSO-d6)δ:12.11(1H,br s),8.68(1H,d,4.94Hz),7.94(1H,m),7.62(1H,d,8.88Hz),7.56-7.52(1H,m),7.14(1H,d,2.30Hz),6.76(1H,dd, 8,88Hz,2.30Hz),4.05(2H,s),3.82(3H,s),2.47(3H,s).实施例133 [5-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯 步骤1.反式-5-乙基-2-氨基肉桂酸甲酯
在110℃下加热2-溴-4-乙基苯胺(1.0g,5.10mmol)、丙烯酸甲酯(1.15ml,12.74mmol)、乙酸钯(II)(137mg,0.61mmol)、三-邻-甲苯基-膦(745mg,2.45mmol)和三乙胺(2.5ml)在乙腈(10ml)中的混合物。甲苯2小时后,加入丙烯酸甲酯(0.6ml,6.37mmol)、乙酸钯(II)(68mg,0.30mmol)、三(邻甲苯基)膦(372mg,1.22mmol)和三乙胺(1.3ml),在110℃下搅拌混合物7小时。除去溶剂后,残留物用乙酸乙酯(100ml)稀释,用水(100ml)洗涤,干燥(硫酸镁),浓缩。残留物通过闪蒸柱色谱纯化,用乙酸乙酯/己烷(1∶5/1∶4)洗脱,得到793mg(75.8%)黄色固体的标题化合物。1H-NMR(CDCl3)δ:7.83(1H,d,J=15.8Hz),7.21(1H,m),7.04-7.01(1H,m),6.64(1H,d,J=8.2Hz),6.36(1H,d,J=15.8Hz),3.87(2H,m),3.80(3H,s),2.51(2H,q,J=7.6Hz),1.19(3H,t,J=7.6Hz).步骤2.反式-5-乙基-2-(苯横酰基氨基)肉桂酸甲酯
按照实施例8方法A的步骤1中所述的方法,从反式-5-乙基-2-氨基肉桂酸甲酯(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:7.70-7.48(4H,m),7.42-7.36(2H,m),7.29-7.26(2H,m),7.20-7.17(2H,m),6.14(1H,d,J=15.8Hz),3.76(3H,s),2.62(2H,q,J=7.6Hz),1.21(3H,t,J=7.6Hz).步骤3.[5-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中所述的方法,从反式-5-乙基-2-(苯磺酰基氨基)肉桂酸甲酯(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:12.32(1H,br s),8.59-8.57(1H,m),8.14(1H,m),7.47-7.39(2H,m),7.30-7.21(2H,m),4.32(2H,s),3.73(3H,s),2.75(2H,q,J=7.6Hz),2.43(3H,s),1.27(3H,t,J=7.6Hz)实施例134 [5-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[5-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例133)制备标题化合物。熔点:215℃(分解)。IR(KBr)ν:1701,1638,1597,1535,1443,1420,1398,1331,1279,1236,1205cm-1.1H-NMR(DMSO)δ:12.09(1H,br s),8.69(1H,d,J=4.9Hz),7.94(1H,m),7.58-7.51(3H,m),7.23-7.20(1H,m),4.06(2H,s),2.69(2H,q,J=7.6Hz),2.46(3H,s),1.23(3H,t,J=7.6Hz).实施例135 [5-乙基-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯)
按照实施例57中描述的方法,从反式-5-乙基-2-(苯磺酰基氨基)肉桂酸甲酯(实施例133步骤2)和2-溴代乙酰基-4-乙基吡啶(其制备方法见实施例57)制备标题化合物。1H-NMR(CDCl3)δ:12.35(1H,br s),8.63(1H,d,J=5.1Hz),8.20(1H,m),7.48(1H,s),742(1H,d,J=8.6Hz),7.34(1H,dd,J=5.1,1.8Hz),7.26-7.22(1H,m),4.32(2H,s),3.73(3H,s),2.76(4H,q,J=7.6Hz),1.30(6H,t,J=7.6Hz)实施例136 [5-乙基-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[5-乙基-2-(4-乙基基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例135)制备标题化合物。m.p.:206.2℃.IR(KBr)ν:1703,1636,1595,1533,1431,1333,1283,1236,1188,1117cm-1.1H-NMR(DMSO-d6)δ:12.09(1H,br s),8.73(1H,d,J=4.9Hz),7.97(1H,s),7.60-7.52(3H,m),7.22(1H,d,J=8.6Hz),4.06(2H,s),2.82-2.65(4H,m),1.28-1.21(6H,m).实施例137 [6-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯 步骤1.反式-(4-乙酰基-2-硝基)肉桂酸甲酯
按照实施例131中所述的方法,从4-溴-3-硝基苯乙酮和丙烯酸甲酯制备标题化合物。1H-NMR(CDCl3)δ:8.58-8.10(3H,m),7.77-7.74(1H,m),6.48-6.42(1H,m),3.85(3H,s),2.68(3H,s).步骤2.反式-4-(1-羟乙基)-2-硝基肉桂酸甲酯
在室温下,向反式-4-乙酰基-2-硝基肉桂酸甲酯(462.2mg,1.854mmol)的甲醇(55ml)溶液中加入硼氢化钠(176.3mg,4.66mol)。搅拌10分钟后,浓缩混合物。残留物用二氯甲烷(20ml)稀释,用盐水(20ml)洗涤。水层用二氯甲烷(20ml×2)萃取。干燥(硫酸镁)合并后的有机层并且浓缩,得到442mg(定量的)标题化合物。1H-NMR(CDCl3)δ:8.12-6.33(5H,m),5.0(1H,m),3.83(3H,s),1.54(3H,d,9.56Hz).步骤3.反式-(4-乙基-2-硝基)肉桂酸甲酯
在室温下,向碘化钠(1.668g,11.1mmol)和乙腈(581μl,11.1mmol)的混合物中加入三甲基氯硅烷(1.41ml,11.1mmol)。搅拌10分钟后,加入反式-4-(1-羟乙基)-2-硝基肉桂酸甲酯(563.6mg,步骤1)的己烷-甲苯-乙腈(1∶1∶1,6.0ml)溶液,再搅拌混合物48小时。用甲苯-乙酸乙酯(2∶3,25ml)稀释反应混合物,然后倒入水(25ml)中。分离出有机层,用5%硫代硫酸钠溶液(30ml)、盐水(30ml)洗涤,干燥(硫酸镁)。除去溶剂后,得到460mg(定量的)棕色油状的标题化合物。1H-NMR(CDCl3)δ:8.12-6.32(5H,m),3.83(3H,s),2.76(2H,q,7.59Hz),1.29(3H,t,7.59Hz).步骤4.反式-2-氨基-4-乙基肉桂酸甲酯
按照实施例36的步骤2中描述的方法,从反式-4-乙基-2-硝基肉桂酸甲酯(步骤3)制备标题化合物。1H-NMR(CDCl3)δ:7.84-6.29(5H,m),3.80(3H,s),2.57(2H,m),1.21(3H,t,7.59Hz).步骤5.反式-4-乙基-2-(对甲苯磺酰基氨基)肉桂酸甲酯
按照实施例8方法A的步骤1中所述的方法,从反式-2-氨基-4-乙基肉桂酸甲酯(步骤4)制备标题化合物。1H-NMR(CDCl3)δ:7.57(2H,d,8.40Hz),7.46(1H,d,15.8Hz),7.39-7.08(5H,m),6.43(1H,s),6.43(1H,d,15.8Hz),3.78(3H,s),2.61(2H,m),2.37(3H,s),1.18(3H,t,7.75Hz).步骤6.[6-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中所述的方法,从反式-4-乙基-2-(对甲苯磺酰基氨基)肉桂酸甲酯(步骤5)和2-溴代乙酰基-4-甲基吡啶氢溴酸盐(其制备方法见实施例31的步骤2)制备标题化合物。1H-NMR(CDCl3)δ:12.30(1H,br s),8.62(1H,d,4.94Hz),8.18-7.32(4H,m),7.05-7.02(2H,m),4.33(2H,s),3.72(3H,s),2.79(2H,q,7.59Hz),2.48(3H,s),1.31(3H,t,7.59Hz).实施例138 [6-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例9方法B中描述的方法,从[6-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例137)制备标题化合物。m.p.:204-207℃.IR(KBr)ν:3240,1709,1636,1593,1531,1394,1204,1144,1001cm-1.1H-NMR(CDCl3)δ:12.07(1H,br s),8.69(1H,d,4.94Hz),7.93(1H,m),7.63(1H,d,8.40Hz),7.55(1H,m),7.45(1H,s),7.00-6.96(1H,m),4.05(2H,s),2.73(2H,q,7.56Hz),2.46(3H,s),1.24(3H,t,7.56Hz).实施例139 [5-异丙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯 步骤1.反式-5-异丙基-2-氨基肉桂酸甲酯
按照实施例133的步骤1中所述的方法,从2-溴-4-异丙基苯胺制备标题化合物。1H-NMR(CDCl3)δ:7.83(1H,d,J=15.8Hz),7.23(1H,m),7.08-7.05(1H,m),6.66(1H,d,J=8.4Hz),6.37(1H,d,J=15.8Hz),3.85(2H,m),3.81(3H,s),2.84-2.76(1H,m),1.21(6H,m).步骤2.反式-5-异丙基-2-(苯磺酰基氨基)肉桂酸甲酯
按照实施例8方法A的步骤1中所述的方法,从反式-5-异丙基-2-氨基肉桂酸甲酯(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:7.71-7.68(2H,m),7.58(1H,d,J=15.8Hz),7.51-7.20(6H,m),7.09(1H,br.s),6.16(1H,d,J=15.8Hz),4.11(3H,s),2.94-2.83(1H,m),1.24-1.21(6H,m).步骤3.[5-异丙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中所述的方法,从反式-5-异丙基-2-(苯磺酰基氨基)肉桂酸甲酯(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:12.33(1H,br s),8.61(1H,d,J=5.1Hz),8.17-8.16(1H,m),7.50-7.42(2H,m),7.33-7.26(2H,m),4.32(2H,s),3.73(3H,s),3.08-2.97(1H,m),2.46(3H,s),1.33-1.30(6H,m).实施例140 [5-异丙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[5-异丙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例139)制备标题化合物。熔点:213℃(分解)。IR(KBr)ν:1717,1641,1597,1537,1327,1273,1196cm-1.1H-NMR(DMSO-d6)δ:12.10(1H,br s),8.70(1H,d,J=4.9Hz),7.95-7.94(1H,m),7.59-7.54(2H,m),7.27(1H,dd,J=8.6,1.7Hz),4.07(2H,s),3.03(1H,m),2.46(3H,s),1.27-1.25(6H,m).实施例141 [2-(4-甲基吡啶-2-羰基)-6-三氟甲基-1H-吲哚-3-基]乙酸甲酯 步骤1.反式-2-氨基-4-(三氟甲基)肉桂酸甲酯
按照实施例133的步骤1中所述的方法,从2-溴-5-(三氟甲基)苯胺制备标题化合物。1H-NMR(CDCl3)δ:7.79(1H,d,J=15.8Hz),7.46-7.43(1H,m),7.00-6.94(2H,m),6.41(1H,d,J=15.8Hz),4.18(2H,m),3.82(3H,m).步骤2.反式-2-苯磺酰基氨基-4-(三氟甲基)肉桂酸甲酯
按照实施例8方法A的步骤1中所述的方法,从反式-2-氨基-4-(三氟甲基)肉桂酸甲酯(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:7.77-7.68(2H,m),7.65-7.53(4H,m),7.47-7.41(3H,m),6.24(1H,d,J=15.8Hz),3.80(3H,s).步骤3.[2-(4-甲基吡啶-2-羰基)-6-三氟甲基-1H-吲哚-3-基]乙酸甲酯
按照实施例57中所述的方法,从反式-2-苯磺酰基氨基-4-(三氟甲基)肉桂酸甲酯(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:12.74(1H,br s),8.58(1H,d,J=4.9Hz),8.12(1H,s),7.81-7.74(2H,m),7.35-7.32(2H,m),4.32(2H,s),3.75(3H,s),2.46(3H,s).实施例142 [2-(4-甲基吡啶-2-羰基)-6-三氟甲基-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[2-(4-甲基吡啶-2-羰基)-6-三氟甲基-1H-吲哚-3-基]乙酸甲酯(实施例141)制备标题化合物。m.p.:210-220℃.IR(KBr)ν:1697,1651,1599,1537,1506,1339,1283,1196,1103,1055cm-1.1H-NMR(DMSO)δ:12.62(1H,br s),8.71(1H,d,J=4.9Hz),8.10(1H,s),7.99-7.97(2H,m),7.61-7.59(1H,m),7.39-7.36(1H,m),4.14(2H,s),2.48(3H,s).实施例143 [5-叔丁基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯 步骤1.反式-5-叔丁基-2-氨基肉桂酸甲酯
按照实施例133的步骤1中所述的方法,从2-溴-4-叔丁基苯胺制备标题化合物。1H-NMR(CDCl3)δ:7.85(1H,d,15.8Hz),7.38(1H,d,2.30Hz),7.23(1H,dd,8.56Hz,2.30Hz),6.67(1H,d,8.56Hz),6.37(1H,d,15.8Hz).3.87(2H,br s),3.81(3H,s),1.28(9H,s).步骤2.反式-5-叔丁基-2-(对甲苯磺酰基氨基)肉桂酸甲酯
按照实施例8方法A的步骤1中所述的方法,从反式-5-叔丁基-2-氨基肉桂酸甲酯和对甲苯磺酰氯制备标题化合物。1H-NMR(CDCl3)δ:7.60-7.20(8H,m),6.53(1H,s),6.17(1H,d,15.8Hz),3.79(3H,s),2.46(3H,s),1.29(s,9H).步骤3.[5-叔丁基基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中所述的方法,从反式-5-叔丁基-2-(对甲苯磺酰基氨基)肉桂酸甲酯(步骤2)和2-溴代乙酰基-4-甲基吡啶氢溴酸盐(其制备方法见实施例31的步骤2)制备标题化合物。1H-NMR(CDCl3)δ:12.33(1H,br s),8.63(1H,d,4.94Hz),8.18(1H,m),7.62-7.32(4H,m),4.43(2H,s),3.74(3H,s),2.47(3H,s),1.40(s,9H).实施例144 [5-叔丁基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例9方法B中描述的方法,从[5-叔丁基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例143)制备标题化合物。熔点:191℃。IR(KBr)ν:2963,1717,1645,1597,1533,1437,1281,1211,1080,1032,1003cm-1.1H-NMR(DMSO-d6)δ:12.10(1H,br s),7.70(1H,d,5.1Hz),7.95-7.44(6H,m),4.09(2H,s),2.46(3H,s),1.35(9H,s).实施例145 [2-(4-甲基吡啶-2-羰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸甲酯 步骤1.反式-2-氨基-5-(三氟甲氧基)肉桂酸甲酯
按照实施例133的步骤1中所述的方法,从2-溴-4-(三氟甲氧基)苯胺制备标题化合物。1H-NMR(CDCl3)δ:7.74(1H,d,15.8Hz),7.23-7.02(2H,m),6.68(1H,d,8.72Hz),6.36(1H,d,15.8Hz),4.00(2H,br s),3.81(3H,s).步骤2.反式-2-对-甲苯磺酰基氨基-5-(三氟甲氧基)肉桂酸甲酯
按照实施例8方法A的步骤1中所述的方法,从反式-2-氨基-4-三氟甲氧基肉桂酸甲酯(步骤1)和对甲苯磺酰氯制备标题化合物。1H-NMR(CDCl3)δ:7.59-7.19(8H,m),6.76(1H,s),6.15(1H,d,15.8Hz),3.80(3H,s),2.39(3H,s).步骤3.[2-(4-甲基吡啶-2-羰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸甲 酯
按照实施例57中所述的方法,从反式-2-对甲苯磺酰基氨基-5-(三氟甲氧基)肉桂酸甲酯(步骤2)和2-溴代乙酰基-4-甲基吡啶氢溴酸盐(其制备方法见实施例31的步骤2)制备标题化合物。1H-NMR(CDCl3)δ:12.7(1H,br s),8.64(1H,d,5.10Hz),8.19(1H,m),7.55-7.23(4H,m),4.30(2H,s),3.74(3H,s),2.49(3H,s).实施例146 [2-(4-甲基-2-吡啶-2-羰基)-5-三氟甲氧基苯基-1H-吲哚-3-基]乙酸
按照实施例9方法B中描述的方法,从[2-(4-甲基吡啶-2-羰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸甲酯(实施例145)制备标题化合物。熔点:235-238℃。IR(KBr)ν:3248,1701,1645,1597,1537,1447,1420,1333,1259,1203,1115,1034,1003cm-1.1H-NMR(DMSO-d6)δ:12.40(1H,br s),8.71(1H,d,4.94Hz),7.97-7.96(1H,m),7.80-7.30(4H,m),4.09(2H,s),2.47(3H,s).实施例147 [2-(4-乙基吡啶-2-羰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸甲酯
按照实施例57中所述的方法,从反式-2-(对甲苯磺酰基氨基)-5-(三氟甲氧基)肉桂酸甲酯(实施例145的步骤2)和2-溴代乙酰基-4-乙基吡啶(其制备方法见实施例57)制备标题化合物。1H-NMR(CDCl3)δ:8.66(1H,d,4.97Hz),8.22(1H,br s),7.55-7.26(4H,m),4.30(2H,s),3.74(3H,s),2.79(2H,q,7.59Hz),1.32(3H,t,7.59Hz).实施例148 [2-(4-乙基吡啶-2-羰基)-5-三氟甲氧基苯基-1H-吲哚-3-基]乙酸
按照实施例9方法B中描述的方法,从[2-(4-乙基吡啶-2-羰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸甲酯(实施例147)制备标题化合物。熔点:223℃。R(KBr)ν:3271,1697,1645,1597,1539,1423,1400,1337,1258,1198,1117,1028,1003cm-1.1H-NMR(DMSO-d6)δ:12.41(1H,br s),8.74(1H,d,4.94Hz),7.99(1H,m),7.80-7.75(2H,m),7.63-7.30(2H,m),4.10(2H,s),2.78(2H,q,7.59Hz),1.26(3H,t,7.59Hz).实施例149 [6-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯 步骤1.反式-2-氨基-4-甲基肉桂酸甲酯
按照实施例36的步骤2中所述的方法,从反式-4-甲基-2-硝基肉桂酸甲酯制备标题化合物。1H-NMR(CDCl3)δ:7.81(1H,d,J=15.8Hz),7.30-7.26(1H,m),6.60-6.57(1H,m),6.52(1H,m),6.31(1H,d,J=15.8Hz),3.92(2H,br s),3.79(3H,s),2.26(2H,s).步骤2.反式-4-甲基-2-(苯磺酰基氨基)肉桂酸甲酯
按照实施例8方法A的步骤1中所述的方法,从反式-2-氨基-4-甲基肉桂酸甲酯(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:7.72-7.68(2H,m),7.55-7.49(1H,m),7.44-7.34(4H,m),7.26-722(1H,m),7.07-7.04(1H,m),6.62(1H,br s),6.12(1H,d,J=15.8Hz),3.76(3H,s),2.34(3H,s).步骤3.[6-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中所述的方法,从反式-4-甲基-2-(对甲苯磺酰基氨基)肉桂酸甲酯(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:12.26(1H,br s),8.61(1H,d,J=4.9Hz),8.17(1H,m),7.58(1H,d,J=8.4Hz),7.34-7.29(2H,m),7.01-6.98(1H,m),4.32(2H,s),3.72(3H,s),2.49(3H,s),2.47(3H,s).实施例150 [6-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[6-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例149)制备标题化合物。熔点:208℃(分解)。IR(KBr)ν:1707,1638,1593,1531,1277,1205,1142cm-1.1H-NMR(DMSO-d6)δ:12.02(1H,br s),8.68(1H,d,J=4.9Hz),7.93(1H,s),7.61(1H,d,J=8.2Hz),7.56-7.54(1H,m),7.42(1H,s),6.96-6.93(1H,m),4.04(2H,s),2.46(3H,s),2.43(3H,s).实施例151 [2-(4-甲基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸甲酯 步骤1.反式-2-氨基-5-(三氟甲基)肉桂酸甲酯
按照实施例133的步骤1中所述的方法,从2-溴-4-(三氟甲基)苯胺制备标题化合物。1H-NMR(CDCl3)δ:7.77(1H,d,J=15.8Hz),7.61(1H,s),7.39(1H,d,J=8.4Hz),6.74(1H,d,J=8.4Hz),6.41(1H,dd,J=15.8,1.5Hz),4.29(2H,m),3.82(3H,m).步骤2.反式-2-苯磺酰基氨基-5-(三氟甲基)肉桂酸甲酯
按照实施例8方法A的步骤1中所述的方法,从反式-2-氨基-5-(三氟甲基)肉桂酸甲酯(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:7.79-7.76(2H,m),7.66(1H,m),7.60-7.44(6H,m),7.06(1H,brs),6.26(1H,d,J=15.8Hz),3.81(3H,s).步骤3.[2-(4-甲基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸甲酯
按照实施例57中所述的方法,从反式-2-苯磺酰基氨基-5-(三氟甲基)肉桂酸甲酯(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:12.70(1H,br s),8.62(1H,d,J=4.9Hz),8.17(1H,s),8.00(1H,s),7.61-7.54(2H,m),7.38-7.36(1H,m),4.34(2H,s),3.75(3H,s),2.48(3H,s).实施例152 [2-(4-甲基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[2-(4-甲基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸甲酯(实施例151)制备标题化合物。m.p.:218-225℃.IR(KBr)ν:1697,1645,1599,1541,1337,1277,1202,1161,1111,1053cm-1.1H-NMR(DMSO-d6)δ:12.52(1H,br s),8.71(1H,d,J=4.9Hz),8.23(1H,s),7.97(1H,m),7.85(1H,d,J=8.9Hz),7.62-7.58(2H,m),4.16(2H,s),2.48(3H,s).实施例153 [2-(4-乙基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸甲酯
按照实施例57中所述的方法,从反式-2-苯磺酰基氨基-5-(三氟甲基)肉桂酸甲酯(实施例151的步骤2)和2-溴代乙酰基-4-乙基吡啶(其制备方法见实施例57)制备标题化合物。1H-NMR(CDCl3)δ:12.65(1H,br s),8.64(1H,d,J=5.1Hz),8.21(1H,m),8.01(1H,s),7.61-7.52(2H,m),7.40-7.37(1H,m),4.34(2H,s),3.76(3H,s),2.78(2H,q,J=7.6Hz),1.31(3H,t,J=7.6Hz).实施例154 [2-(4-乙基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[2-(4-乙基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸甲酯(实施例153)制备标题化合物。m.p.:203.6℃.IR(KBr)ν:1703,1647,1599,1537,1340,1202,1105,1051cm-1.1H-NMR(DMSO-d6)δ:12.52(1H,br s),8.74(1H,d,J=5.1Hz),8.24(1H,s),8.00-7.99(1H,m),7.86(1H,d,J=8.7Hz),7.64-7.58(2H,m),4.16(2H,s),2.79(2H,q,J=7.6Hz),1.26(3H,t,J=7.6Hz).实施例155 (2-苯甲酰基-1H-吲哚-3-基)乙酸甲酯 步骤1.反式-2-(苯磺酰基氨基)-肉桂酸甲酯
按照实施例8方法A的步骤1中所述的方法,从反式-2-氨基肉桂酸甲酯制备标题化合物。1H-NMR(CDCl3)δ:7.71-7.67(2H,m),7.58(1H,d,J=15.8Hz),7.52-7.32(6H,m),7.28-7.22(1H,m),7.08(1H,br s),6.15(1H,d,J=15.8Hz),3.78(3H,s).步骤2.(2-苯甲酰基-1H-吲哚-3-基)乙酸甲酯
按照实施例57中所述的方法,从反式-2-(苯磺酰基氨基)肉桂酸甲酯(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:8.91(1H,br s),7.80-7.77(2H,m),7.67-7.58(2H,m),7.53-7.48(2H,m),7.43-7.34(2H,m),7.21-7.15(1H,m),3.86(2H,s),3.65(3H,s).实施例156 (2-苯甲酰基-1H-吲哚-3-基)乙酸
按照实施例9方法B中描述的方法,从(2-苯甲酰基-1H-吲哚-3-基)乙酸甲酯(实施例155)制备标题化合物。m.p.:194-196℃.IR(KBr)ν:1713,1597,1541,1450,1402,1267,1180,729cm-1.1H-NMR(DMSO-d6)δ:11.62(1H,br s),7.77-7.74(2H,m),7.69-7.66(2H,m),7.60-7.55(2H,m),7.48-7.45(1H,m),7.34-7.28(1H,m),7.13-7.08(1H,m),3.80(2H,s).实施例157 [2-(4-氯苯甲酰基)-6-甲基-1H-吲哚-3-基]乙酸甲酯
按照实施例57中所述的方法,从反式-4-甲基-2-(苯磺酰基氨基)肉桂酸甲酯(实施例149的步骤2)和4-氯苯甲酰甲基溴制备标题化合物。1H-NMR(CDCl3)δ:8.84(1H,br s),7.74-7.71(2H,m),7.53-7.45(3H,m),7.14(1H,m),7.03-7.00(1H,m),3.81(2H,s),3.65(3H,s),2.46(3H,s).实施例158 [2-(4-氯苯甲酰基)-6-甲基-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[2-(4-氯苯甲酰基)-6-甲基-1H-吲哚-3-基]乙酸甲酯(实施例157)制备标题化合物。m.p.:193-195℃.IR(KBr)ν:3302,1697,1587,1335,1263,1090,999,770cm-1.1H-NMR(DMSO-d6)δ:11.47(1H,br s),7.76-7.73(2H,m),7.65-7.61(2H,m),7.57(1H,d,J=8.4Hz),7.23(1H,s),6.96-6.93(1H,m),3.79(2H,s),2.42(3H,s).实施例159 [2-(4-氯苯甲酰基)-5-甲基-1H-吲哚-3-基]乙酸甲酯 步骤1.[2-(4-氯苯甲酰基)-5-甲基-1-(苯磺酰基)吲哚
按照实施例2方法B的步骤2中所述的方法,从5-甲基-1-(苯磺酰基)吲哚(E.Wenkert,P.Moeller和S.Piettre,J.Am. Chem.Soc.,1988,110,7188-7194)和4-氯苯甲酰氯制备标题化合物。1H-NMR(CDCl3)δ:8.02-7.96(3H,m),7.96-7.88(2H,m),7.57-7.43(5H,m),7.33-7.25(2H,m),6.88(1H,s),2.41(3H,s).步骤2.2-(4-氯苯甲酰基)-5-甲基吲哚
按照实施例2方法B的步骤3中所述的方法,从2-(4-氯苯甲酰基)--5-甲基-1-(苯磺酰基)吲哚(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:9.43(1H,br s),7.94-7.91(2H,m),7.51-7.47(3H,m),7.37(1H,d,J=8.4Hz),7.21(1H,dd,J=8.4,1.5Hz),7.04-7.03(1H,m),2.44(3H,s).步骤3.α-乙酰氧基-[2-(4-氯苯甲酰基)-5-甲基-1H-吲哚-3-基]丙二酸 二乙酯
按照实施例2方法B的步骤4中所述的方法,从2-(4-氯苯甲酰基)-5-甲基吲哚(步骤3)制备标题化合物。1H-NMR(CDCl3)δ:8.74(1H,br s),7.79(2H,d,J=8.4Hz),7.67(1H,s),7.42(2H,d,J=8.4Hz),7.27-7.24(1H,m),7.14-7.11(1H,m),4.24-4.16(4H,m),2,45(3H,s),1.28-1.18(6H,m).步骤4.[2-(4-氯苯甲酰基)-5-甲基-1H-吲哚-3-基]丙二酸二乙酯
按照实施例2方法B的步骤5中所述的方法,从α-乙酰氧基-[2-(4-氯苯甲酰基)-5-甲基-1H-吲哚-3-基]丙二酸二乙酯(步骤3)制备标题化合物。1H-NMR(CDCl3)δ:8.80(1H,br s),7.73(2H,d,J=8.4Hz),7.54(1H,s),7.47(2H,d,J=8.4Hz),7.21-7.18(1H,m),7.13-7.10(1H,m),4.25-4.13(4H,m),2.42(3H,s),1.28-1.21(6H,m).步骤5.[2-(4-氯苯甲酰基)-5-甲基-1H-吲哚-3-基]乙酸
按照实施例2方法B的步骤6中所述的方法,从[2-(4-氯苯甲酰基)-5-甲基-1H-吲哚-3-基]丙二酸二乙酯(步骤4)制备标题化合物。m.p.:194-197℃.IR(KBr)ν:3308,1695,1609,1529,1402,1263,1223,1088.1015cm-1.1H-NMR(DMSO-d6)δ:12.18(1H,br s),11.49(1H,s),7.77-7.73(2H,m),7.66-7.62(2H,m),7.45(1H,s),7.35(1H,d,J=8.6Hz),7.15(1H,dd,J=8.6,1.5Hz),3.81(2H,s),2.39(3H,s).实施例160 [6-甲氧基-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中所述的方法,从反式-4-甲氧基-3-(对甲苯磺酰基氨基)肉桂酸甲酯(实施例131的步骤3)和4-氯苯甲酰基甲基溴制备标题化合物。1H-NMR(CDCl3)δ:8.89(1H,br s),7.74-7.43(5H,m),6.86-6.77(m,2H),3.85(3H,s),3.79(3H,s),3.65(3H,s).实施例161 [6-甲氧基-2-(4-氯苯甲酰基)-1H-吲哚-3-基)乙酸
按照实施例9方法B中描述的方法,从[6-甲氧基-2-(4-氯苯甲酰基)-1H-吲哚-3-基)乙酸甲酯(实施例160)制备标题化合物。m.p.:193℃.IR(KBr)ν:3308,1701,1628,1603,1526,1427,1335,1271,1205,1148,1092,1032,999cm-1.1H-NMR(DMSO-d6)δ:11.43(1H,brs),7.75-7.56(5H,m),6.87(1H,d,2.13Hz),7.76(1H,dd,8.88Hz,2.13Hz),3.80(3H,s),3.79(2H,s).实施例162 [2-(4-氯苯甲酰基)-6-三氟甲基-1H-吲哚-3-基]乙酸 步骤1.1-苯磺酰基-6-(三氟甲基)吲哚
在室温和搅拌下,向6-(三氟甲基)吲哚(500mg,2.70mmol)、50%氢氧化钠水溶液(5ml)、水(7ml)和四丁基溴化铵(87mg,0,27mmol)的混合物中加入苯磺酰氯(379μl,2.97mmol)的甲苯(5ml)溶液。搅拌1小时后,分离出有机层,水层用乙酸乙酯(50ml)萃取。合并后的有机层用饱和的碳酸氢钠溶液(30ml)、水(30ml)、盐水(30ml)洗涤,干燥(硫酸镁),浓缩,得到835mg(95%)标题化合物。1H-NMR(CDCl3)δ:8.29(1H,s),7.91-7.88(2H,m),7.71(1H,d,J=3.6Hz),7.64-7.54(2H,m),7.49-7.44(3H,m),6.72(1H,d,J=3.6Hz).步骤2.2-(4-氯苯甲酰基)-1-苯磺酰基-6-(三氟甲基)吲哚
按照实施例2方法B的步骤2中所述的方法,从1-苯磺酰基-6-(三氟甲基)吲哚(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:8.42(1H,s),8.05-8.01(2H,m),7.92-7.89(2H,m),7.71-7.47(7H,m),6.95(1H,s).步骤3.2-(4-氯苯甲酰基)-6-(三氟甲基)吲哚
按照实施例2方法B的步骤3中所述的方法,从2-(4-氯苯甲酰基)-1-苯磺酰基-6-(三氟甲基)吲哚(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:9.53(1H,br s),7.99-7.95(2H,m),7.85-7.79(2H,m),7.56-7.53(2H,m),7.42-7.39(1H,m),7.19-7.18(1H,m).步骤4.α-乙酰氧基-[2-(4-氯苯甲酰基)-6-(三氟甲基)-1H-吲哚-3-基] 丙二酸二乙酯
按照实施例2方法B的步骤4中所述的方法,从2-(4-氯苯甲酰基)-6-(三氟甲基)吲哚(步骤3)制备标题化合物。1H-NMR(CDCl3)δ:9.27(1H,br s),8.00(1H,d,J=8.7Hz),7.78(2H,d,J=8.6Hz),7.68(1H,s),7.45-7.39(3H,m),4.24-4.12(4H,m),1.74(3H,s),1.21-1.14(6H,m).步骤5.[2-(4-氯苯甲酰基)-6-(三氟甲基)O-1H-吲哚-3-基]丙二酸二 乙酯
按照实施例2方法B的步骤5中所述的方法,从α-乙酰氧基-[2-(4-氯苯甲酰基)-6-(三氟甲基)-1H-吲哚-3-基]丙二酸二乙酯(步骤4)制备标题化合物。1H-NMR(CDCl3)δ:9.37(1H,br s),7.83(1H,d,J=8.6Hz),7.77-7.73(2H,m),7.51-7.48(3H,m),7.33-7.30(1H,m),5.27(1H,s),4.25-4.06(4H,m),1.31-1.15(6H,m).步骤6.[2-(4-氯苯甲酰基)-5-甲基-1H-吲哚-3-基]乙酸
按照实施例2方法B的步骤6中所述的方法,从[2-(4-氯苯甲酰基)-6-(三氟甲基)-1H-吲哚-3-基]丙二酸二乙酯(步骤5)制备标题化合物。m.p.:155-160℃.IR(KBr)ν:3379,1705,1611,1589,1516,1337,1229,1119,1092,1055cm-1 1H-NMR(DMSO-d6)δ:12.09(1H,br s),7.96-7.93(1H,m),7,82-7.78(3H,m),7.68-7.64(2H,m),7.41-7.37(1H,m),3.86(2H,s).实施例163 [2-(4-氯苯甲酰基)-5-乙基-1H-吲哚-3-基]乙酸甲酯
按照实施例57中所述的方法,从反式-5-乙基-2-(苯磺酰基氨基)肉桂酸甲酯(实施例133的步骤2)制备标题化合物。1H-NMR(CDCl3)δ:8.86(1H,br s),7.74-7.71(2H,m),7.48-7.41(3H,m),7.32-7.21(2H,m),3.85(2H,s),3.66(3H,s),2.75(2H,q,J=7.6Hz),1.28(3H,t,J=7.6Hz)实施例164 [2-(4-氯苯甲酰基)-5-乙基-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[2-(4-氯苯甲酰基)-5-乙基-1H-吲哚-3-基]乙酸甲酯(实施例163)制备标题化合物。m.p.:165-168℃.IR(KBr):3321,1693,1605,1531,1221,1088,1011cm-1.1H-NMR(DMSO-d6)δ:11.49(1H,br s),7.76-7.72(2H,m),7.65-7.61(2H,m),7.46(1H,m),7.36(1H,d,J=8.6Hz),7.18(1H,dd,J=8.6,1.5Hz),3.81(2H,s),2.67(2H,q,J=7.6Hz),1.21(3H,t,J=7.6Hz).实施例165 [2-(4-氯苯甲酰基)-5-甲氧基-1H-吲哚-3-基]乙酸甲酯
按照实施例57中所述的方法,从反式-5-甲氧基-2-(苯磺酰基氨基)肉桂酸甲酯(实施例129的步骤3)制备标题化合物。1H-NMR(CDCl3)δ:8.81(1H,br s),7.75-7.72(2H,m),7.49-7.46(2H,m),7.29(1H,d,J=8.9Hz),7.04(1H,dd,J=8.9,2.5Hz),6.98(1H,d,J=2.5Hz),3.86(3H,s),3.85(2H,s),3.67(3H,s)实施例166 [2-(4-氯苯甲酰基)-5-甲氧基-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[2-(4-氯苯甲酰基)-5-甲氧基-1H-吲哚-3-基]乙酸甲酯(实施例165)制备标题化合物。m.p.:200-204℃.IR(KBr)ν:3325,1724,1607,1526,1429,1356,1265,1229,1092,1011cm-1.1H-NMR(DMSO-d6)δ:11.46(1H,br s),7.74(2H,d,J=8.6Hz),7.63(2H,d,J=8.6Hz),7.35(1H,d,J=8.9Hz),7.13(1H,d,J=2.5Hz),6.96(1H,dd,J=8.9,2.5Hz),3.83(2H,s),3.77(3H,s).实施例167 [2-(4-氯苯甲酰基)-5-异丙基-1H-吲哚-3-基]乙酸甲酯
按照实施例57中所述的方法,从反式-5-异丙基-2-(苯磺酰基氨基)肉桂酸甲酯(实施例139的步骤2)制备标题化合物。1H-NMR(CDCl3)δ:8.87(1H,br s),7.74-7.70(2H,m),7.49-7.44(3H,m),7.33-7.25(2H,m),3.85(2H,s),3.66(3H,s),3.07-2.96(1H,m),1.32-1.29(6H,m)实施例168 [2-(4-氯苯甲酰基)-5-异丙基-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[2-(4-氯苯甲酰基)-5-异丙基-1H-吲哚-3-基]乙酸甲酯(实施例169)制备标题化合物。m.p.:197-200℃.IR(KBr)ν:1697,1609,1533,1429,1348,1265,1090,1011cm-1.1H-NMR(DMSO-d6)δ:12.18(1H,br s),11.50(1H,br s),7.77-7.74(2H,m),7.65-7.62(2H,m),7.50(1H,m),7.40-7.37(1H,m),7.26-7.23(1H,m),3.83(2H,s),3.03-2.92(1H,m),1.26-1.24(6H,m).实施例169 [2-(4-氯苯甲酰基)-5-三氟甲基-1H-吲哚-3-基]乙酸甲酯
按照实施例57中所述的方法,从反式-2-苯磺酰基氨基-5-(三氟甲基)肉桂酸甲酯(实施例151的步骤2)制备标题化合物。1H-NMR(CDCl3)δ:9.34(1H,br s),7.90(1H,s),7.77-7.70(2H,m),7.51-7.43(3H,m),7.33(1H,d,J=8.7Hz),3.85(2H,s),3.66(3H,s)实施例170 [2-(4-氯苯甲酰基)-5-三氟甲基-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[2-(4-氯苯甲酰基)-5-三氟甲基-1H-吲哚-3-基]乙酸甲酯(实施例169)制备标题化合物。m.p.:198-200℃.IR(KBr)ν:3317,1697,1611,1333,1271,1113,1051,1007cm-1.1H-NMR(DMSO-d6)δ:12.08(1H,br s),8.18(1H,s),7.80-7.77(2H,m),7.68-7.57(4H,m),3.92(2H,s).实施例171 [2-(4-氯苯甲酰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸甲酯
按照实施例57中所述的方法,从反式-3-P-苯磺酰基氨基-5-(三氟甲氧基)肉桂酸甲酯(实施例145的步骤2)和4-氯苯甲酰甲基溴制备标题化合物。1H-NMR(CDCl3)δ:8.93(1H,br s),7.76(2H,d,8.75Hz),7.52-7.40(5H,m),3.82(2H,s),3.68(3H,s).实施例172 [2-(4-氯苯甲酰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸
按照实施例9方法B中描述的方法,从[2-(4-氯苯甲酰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸甲酯(实施例171)制备标题化合物。m.p.:195℃.IR(KBr)ν:3339,1705,1622,1589,1533,1435,1342,1256,1225,1177,1092,1013cm-1.1H-NMR(DMSO-d6)δ:11.91(1H,br s),7.80-7.64(5H,m),7.55(1H,d,8.91Hz).7.32-7.24(m,IH),3.87(2H,s).实施例173 [6-氯-2-(2-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯 步骤1.2-[6-氯-2(2-甲氧苯甲酰基)-1H-吲哚-3-基(乙酸 甲酯
按照实施例57中所述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和2-甲氧基苯甲酰甲基溴制备标题化合物。1H-NMR(CDCl3)δ:9.02(1H,br s),7.60-7.46(2H,m),7.42-7.34(2H,m),7.15-6.99(3H,m),3.78(3H,s),3.66(2H,s),3.60(3H,m).实施例174 [6-氯-2-(2-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸
按照实施例9方法B中描述的方法,从[6-氯-2-(2-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯(实施例172)制备标题化合物。m.p.:214-217℃.IR(KBr)ν:3398,2939,2642,1711,1680,1624,1537,1461,1315,1230,937cm-1.1H-NMR(DMSO-d6)δ:11.61(1H,s),7.67(1H,d,J=8.7Hz),7.60-7.51(1H,m),7.45(1H,d,J=2.0Hz),7.28(1H,dd,J=7.4,1.6Hz),7.18(1H,d,J=8.2Hz),7.12-7.04(2H,m),3.70(3H,s),3.60(2H,s).实施例175 [6-氯-2-(3-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中所述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和3-甲氧基苯甲酰甲基溴制备标题化合物。1H-NMR(CDCl3)δ:8.86(1H,s),7.57(1H,d,J=8.7Hz),7.46-7.26(4H,m),7.19-7.12(2H,m),3.86(3H,s),3.83(2H,s).3.67(3H,s).实施例176 [6-氯-2-(3-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸
按照实施例9方法B中描述的方法,从[6-氯-2-(3-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯(实施例175)制备标题化合物。m.p.:227-231℃.IR(KBr)ν:3354,2933,2636,1709,1607,1569,1427,1321,1269,1218,1049cm-1.1H-NMR(DMSO-d6)δ:11.76(1H,s),7.72(1H,d,J=8.6Hz),7.54-7.45(2H,m),7.35-7.22(3H,m),7.16-7.10(1H,m),3.83(3H,s),3.79(2H,s).实施例177 [6-氯-2-(3-苄氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中所述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和3-苄氧基苯甲酰甲基溴(A.Hernandez等人,J.Org.Chem.,1994,
59,1058)制备标题化合物。1H-NMR(CDCl3)δ:8.79(1H,s),7.56(1H,d,J=8.6Hz),7.46-7.33(9H,m),7.26-7.19(1H,m),7.16(1H,dd,J=8.6,1.8Hz),5.12(2H,s),3.82(2H,s),3.64(3H,s).实施例178 [6-氯-2-(3-苄氧基苯甲酰基)-1H-吲哚-3-基]乙酸
按照实施例9方法B中描述的方法,从[6-氯-2-(3-苄氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯(实施例177)制备标题化合物。m.p.:174-177℃.IR(KBr)ν:3308,3028,2897,1697,1612,1566,1444,1328,1269,1223,732cm-1.1H-NMR(DMSO-d6)δ:11.76(1H,s),7.71(1H,d,J=8.6Hz),7.54-7.30(10H,m),7.13(1H,dd,J=8.6,1.6Hz),5.18(2H,s),3.78(2H,s).实施例179 [6-氯-2-(3-羟基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯
在氢气气氛下,搅拌[6-氯-2-(3-苄氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯(实施例177,0.37g,0.85mmol)和10%钯/活性炭(80mg)在乙酸乙酯-甲醇(5∶1,30ml)中的混合物2.5小时。通过硅藻土过滤垫过滤混合物,浓缩滤液。固体用二氯甲烷(10ml)洗涤,得到70mg(24%)白色固体的标题化合物。1H-NMR(CDCl3)δ:10.36(1H,br s),9.06(1H,s),7.55(1H,d,J=8.7Hz),7.50-7.46(1H,m),7.36-7.22(3H,m),7.15-7.05(2H,m),3.89(2H,s),3.65(3H,s).实施例180 [6-氯-2-(3-羟基苯甲酰基)-1H-吲哚-3-基]乙酸
按照实施例9方法B中描述的方法,从[6-氯-2-(3-羟基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯(实施例179)制备标题化合物。m.p.:213-215℃.IR(KBr)ν:3311,3069,1715,1624,1583,1529,1448,1325,1278,1220,761cm-1.1H-NMR(DMSO-d6)δ:11.71(1H,s),9.86(1H,br s),7.71(1H,d,J=8.6Hz),7.47(1H,d,J=1.5Hz),7.41-7.32(1H,m),7.20-7.02(4H,m),3.82(2H,s).实施例181 [6-氯-2-(4-苄氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中所述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和4-苄氧基苯甲酰甲基溴(A.Brossi等人,J.Heterocycl.Chem.,1965,
2,310)制备标题化合物。1H-NMR(CDCl3)δ:8.87(1H,br s),7.81(2H,d,J=8.6Hz),7.55(1H,d,J=8.7Hz),7.48-7.32(6H,m),7.14(1H,dd,J=8.7,1.8Hz),7.06(2H,d,J=8.6Hz),5.16(2H,s),3.86(2H,s),3.65(3H,s).实施例182 [6-氯-2-(4-苄氧基苯甲酰基)-1H-吲哚-3-基]乙酸
按照实施例9方法B中描述的方法,从[6-氯-2-(4-苄氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯(实施例181)制备标题化合物。m.p.:220-222℃.IR(KBr)ν:3331,3013,2914,1717,1699,1599,1564,1508,1253,1167,941cm-1.1H-NMR(DMSO-d6)δ:11.72(1H,s),7.76(2H,d,J=8.9Hz),7.69(1H,d,J=8.4Hz),7.52-7.32(6H,m),7.17(2H,d,J=8.9Hz),7.11(1H,dd,J=8.4,2.2Hz),5.23(2H,s),3.81(2H,s).实施例183 [6-氯-2-(4-羟基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例179中所述的方法,从[6-氯-2-(4-苄氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯(实施例181)制备标题化合物。1H-NMR(丙酮-d6)δ:10.82(1H,br s),9.21(1H,br s),7.75(2H,d,J=8.7Hz),7.71(1H,d,J=8.7Hz),7.56(1H,d,J=2.0Hz),7.13(1H,dd,J=8.7,2.0Hz),6.97(2H,d,J=8.7Hz),3.95(2H,s),3.59(3H,s).实施例184 [6-氯-2-(4-羟基苯甲酰基)-1H-吲哚-3-基]乙酸
按照实施例9方法B中描述的方法,从[6-氯-2-(4-羟基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯(实施例183)制备标题化合物。m.p.:231-234℃.IR(KBr)ν:3250,3120,2822,1734,1618,1539,1456,1321,1236,1120,1060cm-1.1H-NMR(DMSO-d6)δ:11.58(1H,br s),7.63-7.53(3H,m),7.35(1H,d,J=1.9Hz),7.00(1H,dd,J=8.6,1.9Hz),6.80(2H,d,J=8.9Hz),3.69(2H,s).实施例185 [6-氯-2-(4-异丙氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯
在室温、氮气气氛和搅拌下,向[6-氯-2-(4-羟基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯(实施例183,0.15g,0.44mmol)的DMF(5ml)溶液中加入氢化钠(15mg,0.46mmol)。5分钟后,加入2-碘丙烷(78mg),搅拌混合物7小时。用2N HCl水溶液(20ml)骤冷混合物,用乙酸乙酯(50ml)萃取。萃取液用水(30ml)和盐水(30ml)洗涤,干燥(硫酸镁),浓缩。残留物通过闪蒸柱色谱纯化,用乙酸乙酯-己烷(1∶2)洗脱,得到72mg(43%)白色固体的标题化合物。1H-NMR(CDCl3)δ:8.81(1H,br s),7.80(2H,d,J=8.9Hz),7.56(1H,d,J=8.7Hz),7.41(1H,d,J=1.8Hz),7.15(1H,dd,J=8.7,1.8Hz),6.95(2H,d,J=8.9Hz),4.67(1H,七重峰,J=6.1Hz),3.87(2H,s),3.67(3H,s)1.39(6H,d,J=6.1Hz).实施例186 [6-氯-2-(4-异丙氧基苯甲酰基)-1H-吲哚-3-基]乙酸
按照实施例9方法B中描述的方法,从[6-氯-2-(4-异丙氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯(实施例185)制备标题化合物。m.p.:216-218℃.IR(KBr)ν:3304,2972,2881,1707,1614,1596,1560,1508,1311,1261,1163cm-1.1H-NMR(DMSO-d6)δ:11.71(1H,br s),7.75(2H,d,J=8.9Hz),7.69(1H,d,J=8.6Hz),7.46(1H,d,J=2.0Hz),7.12(1H,dd,J=8.6,2.0Hz),7.07(2H,d,J=8.9Hz),4.78(1H,七重峰,J=5.9Hz),3.82(2H,s)1.32(6H,d,J=5.9Hz).实施例187 [6-氯-2-(4-苯基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中所述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和4-苯基苯甲酰甲基溴制备标题化合物。1H-NMR(CDCl3)δ:8.91(1H,br s),7.88(2H,d,J=8.1Hz),7.73(2H,d,J=8.1Hz),7.68-7.38(7H,m),7.16(1H,dd,J=8.1,1.8Hz),3.89(2H,s),3.66(3H,s).实施例188 [6-氯-2-(4-苯基苯甲酰基)-1H-吲哚-3-基]乙酸
按照实施例9方法B中描述的方法,从[6-氯-2-(4-苯基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯(实施例187)制备标题化合物。m.p.:228-231℃.IR(KBr)ν:3317,3030,2868,1707,1620,1600,1527,1431,1323,1256,1194cm-1.1H-NMR(DMSO-d6)δ:11.81(1H,s),7.89(2H,d,J=8.6Hz),7.87(2H,d,J=8.6Hz),7.82-7.72(3H,m),7.58-7.40(4H,m),7.14(1H,dd,J=8.6,1.8Hz),3.87(2H,s).实施例189 [6-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中所述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和4-(三氟甲氧基)苯甲酰甲基溴*制备标题化合物。1H-NMR(CDCl3)δ:8.85(1H,br s),7.85(2H,d,J=8.9Hz),7.57(1H,d,J=8.6Hz),7.40(1H,d,J=1.8Hz),7.35(2H,d,J=8.9Hz),7.16(1H,dd,J=8.6,1.8Hz),3.80(2H,s),3.65(3H,s).*4-(三氟甲氧基)苯甲酰甲基溴按照下列方法制备:
搅拌4-(三氟甲氧基)苯乙酮(0.52g,2.55mmol)和四丁基溴化铵(1.35g,2.80mmol)在二氯甲烷-甲醇(1∶1,8ml)中的混合物18小时,然后浓缩。残留物用乙酸乙酯(50ml)稀释,用水(50ml)、盐水(50ml)洗涤,干燥(硫酸镁)。除去溶剂后,得到0.36g(50%)黄色油状的标题化合物。tlc:Rf=0.47(己烷-乙酸乙酯=10∶1)。实施例190 [6-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸
按照实施例9方法B中描述的方法,从[6-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯(实施例189)制备标题化合物。m.p.:166-168℃.IR(KBr)ν:3315,3219,1719,1699,1616,1527,1508,1254,1221,1167,943cm-1.1H-NMR(DMSO-d6)δ:11.79(1H,s),7.88(2H,d,J=8.6Hz),7.75(1H,d,J=8.9Hz),7.56(2H,d,J=8.6Hz),7.47(1H,d,J=1.8Hz),7.14(1H,dd,J=8.9,1.8Hz),3.85(2H,s).实施例191 [5-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例8方法B中所述的方法,从反式-5-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例36的步骤3)和4-(三氟甲氧基)苯甲酰甲基溴(其制备方法见实施例189)制备标题化合物。1H-NMR(CDCl3)δ:8.92(1H,br s),7.85(2H,d,J=8.7Hz),7.61(1H,br s),7.38-7.28(4H,m),3.79(2H,s),3.67(3H,s).实施例192 [5-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸
按照实施例9方法B中描述的方法,从[5-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯(实施例191)制备标题化合物。m.p.:186.7℃.IR(KBr)ν:3332,3086,2925,1697,1610,1408,1259,1217,1161,1007,941cm-1.1H-NMR(DMSO-d6)δ:11.85(1H,br s),7.89(2H,d,J=8.7Hz),7.81(1H,d,J=2.1Hz),7.60-7.53(2H,m),7.48(1H,d,J=8.7Hz),7.32(1H,dd,J=8.7,2.1Hz),3.86(2H,s).实施例193 [5-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中所述的方法,从反式-5-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例36的步骤3)和4-甲氧基苯甲酰甲基溴制备标题化合物。1H-NMR(CDCl3)δ:8.86(1H,s),7.82(2H,d,J=8.9Hz),7.63-7.60(1H,m),7.37-7.26(2H,m),6.99(2H,d,J=8.9Hz),3.90(3H,s),3.84(2H,s),3.69(3H,s).实施例194 [5-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸
按照实施例9方法B中描述的方法,从[5-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯(实施例193)制备标题化合物。m.p.:232-235℃.IR(KBr)ν:3312,2833,2621,1701,1599,1510,1454,1263,1167,1001,777cm-1.1H-NMR(DMSO-d6)δ:11.78(1H,s),7.78(2H,d,J=8.9Hz),7.75(1H,d,J=2.0Hz),7.47(1H,d,J=8.7Hz),7.29(1H,dd,J=8.7,2.0Hz),7.11(2H,d,J=8.9Hz),3.88(3H,s),3.82(2H,s).实施例195 [6-氯-2-(4-硝基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中所述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和4-硝基苯甲酰甲基溴制备标题化合物。1H-NMR(CDCl3)δ:8.92(1H,br s),8.37(2H,d,J=8.9Hz),7.93(2H,d,J=8.9Hz),7.57(1H,d,J=8.7Hz),7.40(1H,d,J=1.8Hz),7.18(1H,dd,J=8.7,1.8Hz),3.73(2H,s),3.65(3H,s).实施例196 [6-氯-2-(4-硝基苯甲酰基)-1H-吲哚-3-基]乙酸
按照实施例9方法B中描述的方法,从[6-氯-2-(4-硝基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯(实施例195)制备标题化合物。熔点:218.9℃(分解)。IR(KBr)ν:3365,3101,2846,1718,1699,1647,1537,1348,1255,1227,852m-1.1H-NMR(DMSO-d6)δ:11.84(1H,s),8.38(2H,d,J=8.9Hz),7.97(2H,d,J=8.9Hz),7.78(1H,d,J=8.6Hz),7.48(1H,d,J=2.0Hz),7.15(1H,dd,J=8.6,2.0Hz),3.83(2H,s).实施例197 [6-氯-2-[(4-甲磺酰基)苯甲酰基])-1H-吲哚-3-基]乙酸甲酯
按照实施例57中所述的方法,从4-(甲磺酰基)苯甲酰甲基溴制备标题化合物。1H-NMR(CDCl3)δ:9.10(1H,br s),8.08(2H,d,J=8.6Hz),7.93(2H,d,J=8.3Hz),7.57(1H,d,J=8.7Hz),7.37(1H,br),7.20-7.10m(1H,m),3.78(2H,s),3.64(3H,s),3.12(3H,s).实施例198 [6-氯-2-[(4-甲磺酰基)苯甲酰基]-1H-吲哚-3-基]乙酸
按照实施例9方法B中描述的方法,从[6-氯-2-(4-甲磺酰基)苯甲酰基]-1H-吲哚-3-基]乙酸甲酯(实施例197)制备标题化合物。熔点:241℃(分解)。IR(KBr)ν:3330,1713,1614,1524,1230,1150,941,781cm-1.1H-NMR(DMSO-d6)δ:11..83(IH,s),8.12(2H.d,J=8.3Hz),7.96(2H,d,J=8.3Hz),7.78(1H,d,J=8.7Hz),7.48(1H,d,J=1.8Hz),7.15(1H,dd,J=1.8,8.7Hz),3.85(2H,s),3.33(3H,s).实施例199 [6-氯-2-[4-(甲磺酰基氨基)苯甲酰基]-1H-吲哚-3-基]乙酸甲酯
按照实施例8方法B中所述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和4-(甲磺酰基氨基)苯甲酰甲基溴*制备标题化合物。1H-NMR(CDCl3)δ:8.86(1H,br s),7.82(2H,d,J=8.72Hz),7.58(1H,d,J=8.72Hz),7.42-7.15(4H,m),6.80(1H,br s),3.83(2H,s),3.67(3H,s),3.13(3H,s).*4-(甲磺酰基氨基)苯甲酰甲基溴是按照实施例189中所述的制备4-(三氟甲氧基)苯甲酰甲基溴的方法,从(4-乙酰基苯基)甲磺酰胺(R.Lis等,J.Org.Chem.,1987,
52,4377)制备的。1H-NMR(CDCl3)δ:8.01(2H,d,8.72Hz),7.28(2H,d,8.72Hz),4.40(2H,s),3.13(2H,s)实施例200 [6-氯-2-[4-(甲磺酰基氨基)苯甲酰基]-1H-吲哚-3-基]乙酸
按照实施例9方法B中描述的方法,从[6-氯-2-(4-甲磺酰基氨基)苯甲酰基]-1H-吲哚-3-基]乙酸甲酯(实施例199)制备标题化合物。m.p.:207-210℃.IR(KBr)ν:3333,3248,1715,1603,1570,1529,1508,1394,1323,1259,1231,1159,1061cm-1.1H-NMR(DMSO-d6)δ:11.6(1H,br s),7.76(2H,d,J=8.88Hz),7.71(1H,d,J=8.56Hz),7.46(1H,1.65Hz),7.12(1H,dd,J=8.56Hz,1.65Hz),3.81(2H,s),3.13(3H,s).实施例201 [6-氯-2-(2-氯苯甲酰基)-1H-吲哚-3-基]乙酸 步骤1.6-氯-2-(2-氯苯甲酰基)-1-(苯磺酰基)吲哚
按照实施例1方法B的步骤2中所述的方法,从6-氯-1-(苯磺酰基)吲哚(实施例1方法B的步骤1)和2-氯苯甲酰氯制备标题化合物。粗产物不需要纯化直接用于下步。tlc:Rf=0.25(己烷-乙酸乙酯=4∶1)。步骤2.6-氯-2-(2-氯苯甲酰基)吲哚
按照实施例1方法B的步骤3中所述的方法,从6-氯-2-(2-氯苯甲酰基)-1-(苯磺酰基)吲哚(步骤1)制备标题化合物。粗产物不需要纯化直接用于下一步。tlc:Rf=0.37(己烷-乙酸乙酯=4∶1)。步骤3.α-乙酰氧基-2-[6-氯-2-(2-氯苯甲酰基)-1H-吲哚-3-基]丙二 酸二乙酯
按照实施例1方法B的步骤4中所述的方法,从6-氯-2-(2-氯苯甲酰基)吲哚(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:8.61(1H,br s),7.79(1H,d,J=8.88Hz),7.52-7.33(5H,m),7.15(1H,dd,J=1.97Hz,8.88Hz),4.26(4H,m),2.02(3H,s),1.22(6H,t,J=7.07Hz).步骤4.[6-氯-2-(2-氯苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯
按照实施例1方法B的步骤5中所述的方法,从α-乙酰氧基-[6-氯-2-(2-氯苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯(步骤3)制备标题化合物。1H-NMR(CDCl3)δ:8.95(1H,br s),7.75(1H,d,J=8.88Hz),7.53-7.39(5H,m),4.83(1H,s),4.15(4H,m),1.20(6H,t,J=7.26Hz).步骤5.2-[6-氯-2-(2-氯苯甲酰基)-1H-吲哚-3-基]乙酸
按照实施例1方法B的步骤6中所述的方法,从[6-氯-2-(2-氯苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯(步骤4)制备标题化合物。m.p.:138-140_C.IR(KBr)ν:3315,1713,1632,1564,1526,1435,1325,1254,1215,1151,1061cm-1.1H-NMR(DMSO-d6)δ:11.67(1H,s),7.61(1H,d,J=8.72),7.51-7.34(5H,m),7.50(1H,dd,J=1.97,8.72Hz),3.75(2H,s).实施例202 [6-氯-2-(2,4-二氯苯甲酰基)-1H-吲哚-3-基]乙酸 步骤1.6-氯-2-(2,4-二氯苯甲酰基)-1-(苯磺酰基)吲哚
按照实施例1方法B的步骤2中所述的方法,从6-氯-1-(苯磺酰基)吲哚(实施例1方法B的步骤1)和2,4-二氯苯甲酰氯制备标题化合物。粗产物不需要纯化直接用于下一步。tlc:Rf=0.34(己烷-乙酸乙酯=4∶1)。步骤2.6-氯-2-(2,4-二氯苯甲酰基)吲哚
按照实施例1方法B的步骤3中所述的方法,从6-氯-2-(2,4-二氯苯甲酰基)-1-(苯磺酰基)吲哚(步骤1)制备标题化合物。粗产物不需要纯化直接用于下一步。tlc:Rf=0.45(己烷-乙酸乙酯=4∶1)。步骤3.α-乙酰氧基-[6-氯-2-(2,4-二氯苯甲酰基)-1H-吲哚-3-基]丙二 酸二乙酯
按照实施例1的步骤4中所述的方法,从6-氯-2-(2,4-二氯苯甲酰基)吲哚(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:8.92(1H,br s),7.79-7.11(6H,m),4.24(4H,m),2.02(3H,s),1.22(6H,t,J=7.10Hz).步骤4.[6-氯-2-(2,4-二氯苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯
按照实施例1方法B的步骤5中所述的方法,从α-乙酰氧基-[6-氯-2-(2,4-二氯苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯(步骤3)制备标题化合物。1H-NMR(CDCl3)δ:8.92(1H,br s),7.75(1H,d,J=8.92Hz),7.55-7.36(4H,m),7.13(1H,dd,8.92Hz,1.81Hz),4.85(1H,s),4.17(4H,m),1.21(6H,t,J=7.10Hz).步骤5.[6-氯-2-(2,4-二氯苯甲酰基)-1H-吲哚-3-基]乙酸
按照实施例1方法B的步骤6中所述的方法,从2-[6-氯-2-(2,4-二氯苯甲酰基)-1H-吲哚-3-基]丙二酸二乙酯(步骤4)制备标题化合物。m.p.:190-192℃.IR(KBr)ν:3304,1709,1630,1589,1526,1427,1321,1231,1150,1061cm-1.1H-NMR(DMSO-d6)δ:11.66(1H,s),7.72(1H,d,J=2.00Hz),7.64(1H,d,8.91Hz),751-7.33(3H,m),7.01(1H,dd,J=2.00,8.91Hz),3.61(2H,s).实施例203 [6-氯-2-(4-氯-3-氟苯甲酰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和4-氯-3-氟苯甲酰甲基溴*制备标题化合物。1H-NMR(CDCl3)δ:8.87(1H,br s),7.65-7.36(4H,m),7.17(1H,dd,J=8.72Hz,1.81Hz),3.80(2H,s),3.68(3H,s).*4-氯-3-氟苯甲酰甲基溴按照下列方法制备:4-乙酰基-1-氯-2-氟苯:
在-78℃和氮气气氛下,向1-溴-4-氯-3-氟苯(2.09g,10mmol)在干燥的乙醚(12.0ml)中的溶液中加入正丁基锂(1.55M的己烷溶液,6.77ml,10.5mmol)溶液。把混合物温热到-20℃,搅拌45分钟。加入N,N-二甲基乙酰胺(1.04ml,11.2mmol)的乙醚(1.5ml)溶液,再搅拌混合物1小时,然后把混合物温热到室温。搅拌3小时后,把反应混合物倒入饱和的氯化铵水溶液(20ml)中,用乙醚(30ml×3)萃取。合并后的有机层用2N HCl水溶液(20ml)、饱和的碳酸氢钠水溶液(20ml)、盐水(20ml)洗涤,干燥(硫酸镁)。除去溶剂后,得到黄色油状的标题化合物(定量的)。1H-NMR(CDCl3)δ:7.75-7.09(3H,m),2.59(3H,s).4-氯-3-氟苯甲酰甲基溴:
按照实施例189中所述的制备4-(三氟甲氧基)苯甲酰甲基溴的方法,从4-乙酰基-1-氯-2-氟苯制备标题化合物。1H-NMR(CDCl3)δ:7.79-7.71(2H,m),7.58-7.52(1H,m),4.38(2H,s).实施例204 [6-氯-2-(4-氯-3-氟苯甲酰基)-1H-吲哚-3-基]乙酸
按照实施例9方法B中描述的方法,从[6-氯-2-(4-甲磺酰基氨基苯甲酰甲基)-1H-吲哚-3-基]乙酸甲酯(实施例203)制备标题化合物。m.p.:179-182℃.MS(EI)m/z:365(M+).1H-NMR(DMSO-d6)δ:11.80(1H,br s),7.85-7.48(5H,m),7.14(1H,dd,J=8.72Hz,1.97Hz),3.84(2H,s).实施例205 [6-氯-2-(4-氰基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例8方法B中所述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和4-氰基苯甲酰甲基溴制备标题化合物。1H-NMR(CDCl3)δ:8.88(1H,br s),7.89-7.80(4H,m),7.58(1H,d,J=8.75Hz),7.41(1H,d,1.65Hz),7.18(1H,dd,8.75Hz,1.65Hz),3.74(2H,s),3.36(3H,s).实施例206 [6-氯-2-(4-(溴)苯甲酰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和4-溴苯甲酰甲基溴制备标题化合物。1H-NMR(CDCl3)δ:8.89(1H,br s),7.66(4H,s),7.55(1H,d,J=8.6Hz),7.36(1H,d,J=1.6Hz),7.15(1H,dd,J=8.6,1.6Hz),3.81(2H,s),3.66(3H,s).实施例207 [6-氯-2-[4-(2-噻吩基)苯甲酰基]-1H-吲哚-3-基]乙酸甲酯
回流[6-氯-2-(4-溴苯甲酰基)-1H-吲哚-3-基]乙酸甲酯(实施例206,0.40g,0.98mmol)、噻吩-2-硼酸(0.14g,1.08mmol)、饱和的碳酸氢钠水溶液(4ml)和二氯化双(三苯基膦)钯(II)(70mg,0.098mmol)在DME(15ml)中的混合物3小时。把混合物倒入水(30ml)中,用乙酸乙酯(50ml×2)萃取。合并后的萃取液用盐水(50ml)洗涤,干燥(硫酸镁),浓缩。残留物通过闪蒸柱色谱纯化,用乙酸乙酯-己烷(1∶6)洗脱,得到0.33g(83%)黄色固体的标题化合物。1H-NMR(CDCl3)δ:8.88(1H,br s),7.83(2H,d,J=8.2Hz),7.75(2H,d,J=8.2Hz),7.58(1H,d,J=8.6Hz),7.46(1H,dd,J=3.6,1.2Hz),7.42-7.38(2H,m),7.19-7.12(2H,m),3.87(2H,s),3.67(3H,s).实施例208 [6-氯-2-[4-(2-噻吩基)苯甲酰基]-1H-吲哚-3-基]乙酸
按照实施例9方法B中描述的方法,从[6-氯-2-[4-(2-噻吩基)苯甲酰基]-1H-吲哚-3-基]乙酸甲酯(实施例207)制备标题化合物。m.p.:246-249℃.IR(KBr)ν:3319,3068,2628,1705,1610,1593,1427,1323,1257,1186,941cm-1.1H-NMR(DMSO-d6)δ:11.79(1H,s),7.87(2H,d,J=8.6Hz),7.82(2H,d,J=8.6Hz),7.77-7.68(3H,m),7.48(1H,d,J=1.5Hz),7.26-7.20(1H,m),7.13(1H,dd,J=8.6,2.0Hz),3.86(2H,s).实施例209 [6-氯-2-[4-(2-呋喃基)苯甲酰基]-1H-吲哚-3-基]乙酸甲酯
按照实施例207中描述的方法,从[6-氯-2-(4-溴苯甲酰基)-1H-吲哚-3-基]乙酸甲酯(实施例206)和呋喃-2-硼酸制备标题化合物。1H-NMR(CDCl3)δ:8.90(1H,br s),7.83(2H,d,J=8.7Hz),7.80(2H,d,J=8.7Hz),7.60-7.54(2H,m),7.40(1H,d,J=1.8Hz),7.15(1H,dd,J=8.6,1.8Hz),6.83(1H,d,J=3.5Hz),6.57-6.52(1H,m),3.86(2H,s),3.66(3H,s).实施例210 [6-氯-2-[4-(2-呋喃基)苯甲酰基]-1H-吲哚-3-基]乙酸
按照实施例9方法B中所述的方法,从[6-氯-2-[4-(2-呋喃基)苯甲酰基]-1H-吲哚-3-基]乙酸甲酯(实施例209)制备标题化合物。m.p.:230-232℃.IR(KBr)ν:3315,2873,2630,1709,1616,1597,1527,1431,1321,1257,1232cm-1.1H-NMR(DMSO-d6)δ:11.80(1H,s),7.93-7.79(3H,m),7.83(2H,d,J=8.1Hz),7.73(1H,d,J=8.6Hz),7.48(1H,d,J=1.8Hz),7.21(1H,d,J=3.5Hz),7.14(1H,dd,J=8.6,1.8Hz),6.72-6.66(1H,m),3.84(2H,s).实施例211 [6-氯-2-[4-(3-吡啶基)苯甲酰基]-1H-吲哚-3-基]乙酸甲酯
按照实施例207中描述的方法,从[6-氯-2-(4-溴苯甲酰基)-1H-吲哚-3-基]乙酸甲酯(实施例206)和吡啶-3-硼酸制备标题化合物。1H-NMR(CDC13)δ:8.95(1H,br s),8.90(1H,d,J=2.5Hz),8.69-8.65(1H,m),7.98-7.92(1H,m),7.92(2H,d,J=8.6Hz),7.73(2H,d,J=8.6Hz),7.59(1H,d,J=8.7Hz),7.48-7.40(2H,m),7.17(1H,dd,J=8.7,1.8Hz),3.88(2H,s),3.67(3H,s).实施例212 [6-氯-2-[4-(3-吡啶基)苯甲酰基]-1H-吲哚-3-基]乙酸
按照实施例9方法B中所述的方法,从[6-氯-2-[4-(3-吡啶基)苯甲酰基]-1H-吲哚-3-基]乙酸甲酯(实施例211)制备标题化合物。m.p.:194.8℃.IR(KBr)ν:3224,2960,1604,1568,1527,1382,1321,1259,1004,920cm-1.1H-NMR(CD3OD)δ:8.93-8.89(1H,m),8.57(1H,dd,J=4.8,1.5Hz),8.24-8.17(1H,m),7.98(2H,d,J=8.6Hz),7.85(2H,d,J=8.6Hz),7.68(1H,d,J=8.6Hz),7.60-7.53(1H,m),7.46-7.42(1H,m),7.04(1H,dd,J=8.6,1.8Hz),3.67(2H,s).实施例213 [6-氯-2-[4-(2-噻唑基)苯甲酰基]-1H-吲哚-3-基]乙酸甲酯
在-78℃、氮气气氛和搅拌下,向噻唑(0.11g,1.23mmol)的乙醚(4ml)溶液中加入正丁基锂(1.55M的己烷溶液,0.79ml)。搅拌30分钟后,加入氯化锌(1.0M的乙醚溶液,3.7ml,3.7mmol),在0℃下搅拌混合物30分钟。向所得的混合物中加入钯催化剂,该催化剂是通过在THF(5ml)中用正丁基锂(1.55M的己烷溶液,0.39ml)处理二氯化双(三苯基膦)钯(II)(0.22g,0.31mmol)而配制的。向混合物中加入[6-氯-2-(4-溴苯甲酰基)-1H-吲哚-3-基]乙酸甲酯(实施例206,0.25g,0.61mmol)。加热回流反应混合物4小时,把混合物倒入水(50ml)中,用乙酸乙酯(50ml)萃取。合并后的萃取液用盐水(50ml)洗涤,干燥(硫酸镁),浓缩。粗产物通过闪蒸柱色谱纯化,用乙酸乙酯-己烷(1∶3)洗脱,得到0.18g(72%)黄色固体的标题化合物。1H-NMR(DMSO-d6)δ:11.87(1H,br s),8.16(2H,d,J=8.4Hz),8.04(1H,d,J=3.1Hz),7.93(1H,d,J=3.1Hz),7.86(2H,d,J=8.4Hz),7.77(1H,d,J=8.6Hz),7.49(1H,d,J=1.6Hz),7.15(1H,dd,J=8.6,1.6Hz),3.97(2H,s),3.54(3H,s).实施例214 [6-氯-2-[4-(2-噻唑基)苯甲酰基]-1H-吲哚-3-基]乙酸
按照实施例9方法B中所述的方法,从[6-氯-2-[4-(2-噻唑基)苯甲酰基]-1H-吲哚-3-基]乙酸甲酯(实施例213)制备标题化合物。m.p.:230-233℃.IR(KBr)ν:3331,3126,2546,1693,1635,1535,1350,1313,1213,1150,912cm-1.1H-NMR(DMSO-d6)δ:11.82(1H,s),8.15(2H,d,J=8.6Hz),8.04(1H,d,J=3.3Hz),7.93(1H,d,J=3.3Hz),7.88(2H,d,J=8.6Hz),7.75(1H,d,J=8.7Hz),7.49(1H,d,J=2.0Hz),7.14(1H,dd,J=8.7,2.0Hz),3.86(2H,s).实施例215 [6-氯-2-(3-溴苯甲酰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和3-溴苯甲酰甲基溴制备标题化合物。1H-NMR(CDCl3)δ:8.91(1H,br s),7.93-7.87(1H,m),7.77-7.67(2H,m),7.57(1H,d,J=8.7Hz),7.43-7.35(2H,m),7.19-7.13(1H,m),3.78(2H,s),3.69(3H,s).实施例216 [6-氯-2-[3-(2-呋喃基)苯甲酰基]-1H-吲哚-3-基]乙酸甲酯
按照实施例207中描述的方法,从[6-氯-2-(3-溴苯甲酰基)-1H-吲哚-3-基]乙酸甲酯(实施例215)和呋喃-2-硼酸制备标题化合物。1H-NMR(CDCl3)δ:8.93(1H,br s),8.05-8.01(1H,m),7.94-7.88(1H,m),7.68-7.62(1H,m),7.60-7.47(3H,m),7.45-7.41(1H,m),7.16(1H,dd,J=8.6,1.6Hz),6.74(1H,d,J=3.3Hz),6.52-6.47(1H,m),3.80(2H,s),3.57(3H,s).实施例217 [6-氯-2-[3-(2-呋喃基)苯甲酰基]-1H-吲哚-3-基]乙酸
按照实施例9方法B中所述的方法,从[6-氯-2-[3-(2-呋喃基)苯甲酰基]-1H-吲哚-3-基]乙酸甲酯(实施例216)制备标题化合物。m.p.:246-249℃.IR(KBr)ν:3310,2984,2632,1695,1624,1568,1327,1227,1062,806,739cm-1.1H-NMR(DMSO-d6)δ:11.81(1H,s),8.05-7.96(2H,m),7.82-7.77(1H,m),7.74(1H,d,J=8.7Hz),7.68-7.61(2H,m),7.49(1H,d,J=2.0Hz),7.14(1H,dd,J=8.7,2.0Hz),7.09(1H,d,J=3.3Hz),6.66-6.61(1H,m),3.83(2H,s).实施例218 dl-2-[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]丙酸甲酯 步骤1.[1-叔丁氧羰基-2-(4-氯苯甲酰基)-6-甲基-1H-吲哚-3-基]乙 酸甲酯
在室温和搅拌下,向[2-(4-氯苯甲酰基)-6-甲基-1H-吲哚-3-基]乙酸甲酯(实施例8方法B,2.0g,5.5mmol)的二氯甲烷(20ml)悬浮液中加入碳酸二叔丁基酯(2.4g,11mmol)和4-二甲基氨基吡啶(670mg,5.5mmol)。搅拌5分钟后,把混合物倒入10%柠檬酸(200ml)中,用二氯甲烷(200ml)萃取。萃取液用水(200ml)、盐水(200ml)洗涤,干燥(硫酸镁),浓缩。残留物通过闪蒸柱色谱纯化,用乙酸乙酯-己烷(1∶4)洗脱,得到2.3g(90%)黄色固体的标题化合物。1H-NMR(CDCl3)δ:8.26(1H,d,J=2.2Hz),7.74(2H,d,J=8.6Hz),7.53(1H,d,J=8.6Hz),7.44(2H,d,J=8.6Hz),7.32(1H,dd,J=1.6,8.4Hz),3.72(2H,s),3.56(3H,s),1.30(9H,s).步骤2.[1-叔丁氧羰基-2-(4-氯苯甲酰基)-6-甲基-1H-吲哚-3-基]丙 酸甲酯
在-78℃和搅拌下,向[1-叔丁氧羰基-2-(4-氯苯甲酰基)-6-甲基-1H-吲哚-3-基]乙酸甲酯(步骤1,200mg,0.43mmol)的THF(3ml)溶液中加入双(三甲基甲硅烷基)氨基锂的THF溶液(1M,0.5ml)。搅拌0.5小时后,在同样的温度下加入碘甲烷(0.14ml,2.2mmol)。把混合物温热到-10℃,再搅拌0.5小时。把所得的混合物倒入饱和的氯化铵水溶液(50ml)中,用乙醚(50ml)萃取。萃取液用水(50ml)、盐水(50ml)洗涤,干燥(硫酸镁),浓缩。残留物通过TLC纯化,用乙酸乙酯-己烷(1∶4)展开,得到146mg(71%)无色油状的标题化合物。1H-NMR(CDCl3)δ:8.28(1H,d,J=1.9Hz),7.75(2H.d,J=8.4Hz),7.59(1H,d,J=8.4Hz),7.44(2H,d,J=8.6Hz),7.28(1H,dd,J=1.9,8.4Hz),3.86(1H,q,J=7.3Hz),3.54(3H,s),1.54(3H,d,J=7.3Hz),1.30(9H,s).步骤3.dl-[2-(4-氯苯甲酰基)-6-甲基-1H-吲哚-3-基]丙酸甲酯
把[1-叔丁氧羰基-2-(4-氯苯甲酰基)-1H-吲哚-3-基]丙酸甲酯(步骤2,270mg,0.72mmol)溶于三氟乙酸(5ml)中。搅拌10分钟后,浓缩混合物。向残留物中加入饱和的碳酸氢钠水溶液(30ml),然后用乙酸乙酯(100ml)萃取混合物。萃取液用水(50ml)、盐水(50ml)洗涤,干燥(硫酸镁),浓缩。残留物通过闪蒸柱色谱纯化,用乙酸乙酯-己烷(1∶3)洗脱,得到210mg(78%)黄色固体的标题化合物。1H-NMR(CDCl3)δ:8.89(1H,br),7.78(2H,d,J=8.7Hz),7.67(1H,d,J=8.7Hz),7.50(2H,d,J=8.6Hz),7.40-7.37(1H,m),7.11(1H,dd,J=1.8,8.7Hz),4.20(1H,q,J=7.2Hz),3.64(3H,s),1.54(3H,d,J=7.2Hz).实施例219 dl-2-[2-(4-氯苯甲酰基)-6-氯-1H-吲哚-3-基]丙酸
按照实施例9方法B中描述的方法,从dl-2-[2-(4-氯苯甲酰基)-6-甲基-1H-吲哚-3-基]丙酸甲酯(实施例218)制备标题化合物。1H-NMR(CDCl3)δ:8.77(1H,br s),7.82(2H,d,J=8.6Hz),7.75(1H,d,J=8.7Hz),7.53(2H,d,J=8.6Hz),7.40(1H,br),7.13(1H,dd,J=1.8,8.7Hz),4.29(1H,q,J=7.2Hz),1.61(3H,d,J=7.2Hz).实施例220 [5-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中所述的方法,从反式-5-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例36的步骤3)和3-溴乙酰基异喹啉氢溴酸盐*制备标题化合物。1H-NMR(CDCl3)δ:12.72(1H,br s),9.37(1H,s),8.80(1H,s),8.15-8.02(2H,m),7.87-7.76(2H,m),7.69(1H,d,J=2.0Hz),7.48(1H,d,J=8.9Hz),7.32(1H,dd,J=2.0,8.7Hz),4.33(2H,s),3.76(3H,s).*3-溴乙酰基异喹啉氢溴酸盐是按照H.Mckennis,Jr.,L.B.Turnbull,E.R.Bowman和E.Tamaki的方法(见J.Org.Chem.,1963,
28,383-387),从3-乙酰基异喹啉(D.L.Klayman等人,Arzneim.Forsch.,1986,
36,10)制备的。1H-NMR(DMSO-d6)δ:9.49(1H,s),8.68(1H,s),8.34-8.26(2H,m),7.99-7.88(2H,m),5.14(2H,s).实施例221 [5-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中所述的方法,从[5-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例219)制备标题化合物。MS(EI)m/z:364(M+).m.p.:239-240℃.IR(KBr)ν:3277,1699,1641,1531,1329,1202,1059,961,787cm-1.1H-NMR(DMSO-d6)δ:12.46(1H,br s),9.56(1H,s),8.69(1H,s),8.39-8.26(2H,m),7.99-7.90(2H,m),7.87(1H,d,J=2.1Hz),7.72(1H,d,J=8.7Hz),7.35(1H,dd,J=2.1,8.9Hz),4.13(2H,s)..实施例222 [6-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和3-溴代乙酰基异喹啉(其制备方法见实施例220)制备标题化合物。1H-NMR(CDCl3)δ:12.69(1H,br s),9.38(1H,s),8.81(1H,s),8.16-8.04(2H,m),7.88-7.77(2H,m),7.65(1H,d,J=8.9Hz),7.57(1H,d,J=2.0Hz),7.15(1H,dd,J=2.0and 8.7Hz),4.36(2H,s),3.75(3H,s).实施例223 [6-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中所述的方法,从[6-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例222)制备标题化合物。MS(EI)m/z:364(M+).m.p.:236-237℃.IR(KBr)ν:3229,1709,1641,1618,1531,1198,793cm-1.1H-NMR(DMSO-d6)δ:12.43(1H,br s),9.56(1H,s),8.70(1H,s),8.41-8.26(2H,m),7.99-7.87(2H,m),7.82(1H,d,J=8.7Hz),7.77(1H,d,J=1.5Hz),7.14(1H,dd,J=2.0,8.6Hz),4.14(2H,s).实施例224 [5-氯-2-(5-甲基异噁唑-3-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-5-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例36的步骤3)和3-溴代乙酰基-5-甲基异噁唑(M.D.Amici等人,J.Org.Chem.,1989,
54,2646)制备标题化合物。1H-NMR(CDCl3)δ:10.75(1H,br s),7.68(1H,br s),7.42(1H,d,J=8.2Hz),7.34(1H,dd,J=1.8,9.1Hz),6.60(1H,s),4.25(2H,s),3.74(3H,s),2.56(3H,s).实施例225 [5-氯-2-(5-甲基异噁唑-3-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中所述的方法,从[5-氯-2-(5-甲基异噁唑-3-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例224)制备标题化合物。MS(EI)m/z:318(M+).m.p.:253-255℃.IR(KBr)ν:3379,1699,1639,1539,1425,1259,1207,1059,804cm-1.1H-NMR(DMSO-d6)δ:11.76(1H,br s),7.81(1H,d,J=2.0Hz),7.59(1H,d,J=8.9Hz),7.29(1H,dd,J=2.0,8.7Hz),6.67(1H,s),4.00(2H,s),2.49(3H,s).实施例226 [6-氯-2-(5-甲基异噁唑-3-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和3-溴代乙酰基-5-甲基异噁唑(M.D.Amici等人,J.Org.Chem.,1989,
54,2646)制备标题化合物。1H-NMR(CDCl3)δ:10.70(1H,br s),7.62(1H,d,J=8.7Hz),7.49(1H,d,J=1.8Hz),7.15(1H,dd,J=1.8 and 8.7Hz),6.60(1H,br s),4.27(2H,s),3.72(3H,s),2.56(3H,s).实施例227 [6-氯-2-(5-甲基异噁唑-3-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中所述的方法,从[6-氯-2-(5-甲基异噁唑-3-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例226)制备标题化合物。MS(EI)m/z:318(M+).m.p.:227-229℃.IR(KBr)ν:3331,1713,1645,1543,1404,1259,1202,891,804cm-1.1H-NMR(DMSO-d6)δ:11.70(1H,br s),7.74(1H,d,J=8.7Hz),7.62(1H,d,J=1.3Hz),7.07(1H,dd,J=1.8,8.6Hz),6.67(1H,br s),4.01(2H,s),2.49(3H,s).实施例228 [5-氯-2-(4-甲基-1,2,3-噻二唑-5-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-5-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例36的步骤3)和5-溴代乙酰基-4-甲基-1,2,3-噻二唑氢溴酸盐*制备标题化合物。1H-NMR(CDCl3)δ:9.00(1H,br s),7.63(1H,br s),7.34(1H,dd,J=1.8,8.9Hz),7.28(1H,d,J=8.9Hz),3.81(2H,s),3.66(3H,s),2.78(3H,s).*5-溴代乙酰基-4-甲基-1,2,3-噻二唑氢溴酸盐按照下列方法制备:N-甲氧基-N-甲基-4-甲基-1,2,3-噻二唑-5-甲酰胺:
在0℃下,向1,2,3-噻二唑-5-甲酰氯(10.00g,61.5mmol)和N,O-二甲基羟基胺盐酸盐(7.20g,73.8mmol)的二氯甲烷(200ml0溶液中加入三乙胺(20.6ml,147.6mmol)。在室温下搅拌混合物2小时后,用二氯甲烷(300ml)稀释,用水(200ml×2)洗涤,干燥(硫酸镁)。除去溶剂后,得到11.31g(98%)棕色结晶的标题化合物。1H-NMR(CDCl3)δ:3.75(3H,s),3.40(3H,s),3.01(3H,s).5-乙酰基-4-甲基-1,2,3-噻二唑:
在0℃下,用0.5小时向N-甲氧基-N-甲基-4-甲基-1,2,3-噻二唑-5-甲酰胺(11.31g,60.4mmol)的THF(100ml)溶液中加入2M甲基碘化镁的乙醚溶液(45.3ml,90.6mmol)。把混合物温热到室温并搅拌3小时。混合物用饱和的氯化铵水溶液(100ml)骤冷,然后用乙醚(200ml×2)萃取。干燥(硫酸镁)并浓缩萃取液,得到7.49g(87%)淡棕色油状的标题化合物。1H-NMR(CDCl3)δ:2.96(3H,s),2.67(3H,s).5-溴代乙酰基-4-甲基-1,2,3-噻二唑:
在室温下,用0.5小时向5-乙酰基-4-甲基-1,2,3-噻二唑(1.00g,7.03mmol)的氯仿(20ml)溶液中滴加溴(1.24g,7.73mmol)的氯仿(10ml)溶液。加热回流混合物2小时。冷却到室温后,用饱和的碳酸氢钠水溶液把混合物变为碱性的,用二氯甲烷(100ml×2)萃取。干燥(硫酸镁)并且浓缩萃取液,得到1.55g(100%)棕色油状的标题化合物。1H-NMR(CDCl3)δ:4.28(2H,s),2.98(3H,s).实施例229 [5-氯-2-(4-甲基-1,2,3-噻二唑-5-羰基)-1H-吲哚-3-基]乙酸
加热回流[5-氯-2-(4-甲基-1,2,3-噻二唑-5-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例228,190mg,0.54mmol)、2N HCl水溶液(4ml)和乙酸(20ml)的混合物2小时。把混合物冷却到室温,然后浓缩。结晶状残留物用THF(100ml)稀释,干燥(硫酸镁),浓缩。残留的固体用乙酸乙酯洗涤,得到145mg(79%)黄色固体的标题化合物。MS(EI)m/z:335(M+).m.p.:229-230℃.IR(KBr)ν:3300,1715,1622,1526,1329,1261,1204,1063,1009,822cm-1.1H-NMR(DMSO-d6)δ:11.92(1H,br s),7.89(1H,d,J=2.0Hz),7.48(1H,d,J=8.9Hz),7.36(1H,dd,J=2.0,8.9Hz),3.95(2H,s),2.63(3H,s).实施例230 [6-氯-2-(4-甲基-1,2,3-噻二唑-5-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和5-溴代乙酰基-4-甲基-1,2,3-噻二唑(其制备方法见实施例228)制备标题化合物。tlc:Rf=0.56(乙酸乙酯/己烷=1∶2)。实施例231 [6-氯-2-(4-甲基-1,2,3-噻二唑-5-羰基)-1H-吲哚-3-基]乙酸
按照实施例229中描述的方法,从[6-氯-2-(4-甲基-1,2,3-噻二唑-5-羰基)-1H-吲哚-3-基]乙酸(实施例230)制备标题化合物。MS(EI)m/z:335(M+).m.p.:215-216℃.IR(KBr)ν:3300,1709,1645,1531,1327,1211,1065,922,789cm-1.1H-NMR(DMSO-d6)δ:12.35(1H,br s),11.86(1H,br s),7.82(1H,d,J=8.7Hz),7.47(1H,d,J=1.8Hz),7.17(1H,dd,J=1.8,8.6Hz),3.93(2H,s),2.63(3H,s).实施例232 [5-氯-2-(5-甲基-噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-5-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例36的步骤3)和2-溴代乙酰基-5-甲基噻唑氢溴酸盐*制备标题化合物。1H-NMR(CDCl3)δ:11.74(1H,br s),7.76(1H,d,J=1.1Hz),7.67(1H,d,J=1.8),7.43(1H,d,J=8.7Hz),7.32(1H,dd,J=2.0,8.7Hz),4.28(2H,s),3.73(3H,s),2.62(3H,d,J=1.0Hz).*2-溴代乙酰基-5-甲基噻唑是按照H.Mckennis,Jr.,L.B.Turnbull,E.R.Bowman和E.Tamaki的方法(见J.Org.Chem.,1963,
28,383-387),从2-乙酰基5-甲基噻唑(Metzger等人,Bu7.Soc.Chim.Fr,1953,
702)制备的。1H-NMR(DMSO-d6)δ:7.91(1H,d,J=1.2Hz),4.87(2H,s),2.58(3H,d,J=0.8Hz).实施例233 [5-氯-2-(5-甲基-噻唑-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中所述的方法,从[5-氯-2-(5-甲基-噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例232)制备标题化合物。MS(EI)m/z:334(M+).m.p.:231-233℃.IR(KBr)ν:3348,1699,1630,1541,1404,1333,1271,1057,1003,804cm-1.1H-NMR(DMSO-d6)δ:12.05(1H,br s),8.04(1H,s),7.88(1H,br s),7.77(1H,d,J=8.7Hz),7.35(1H,brd,J=8.9Hz),4.15(2H,s),2.63(3H,s).实施例234 [6-氯-2-(5-甲基-噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和2-溴代乙酰基-5-甲基-噻唑(其制备方法见实施例232)制备标题化合物。1H-NMR(CDCl3)δ:11.73(1H,br s),7.77(1H,s),7.62(1H,d,J=8.2Hz),7.51(1H,brs),7.14(1H,br d,J=8.7Hz),4.31(2H,s),3.72(3H,s),2.62(3H,s).实施例235 [6-氯-2-(5-甲基-噻唑-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中所述的方法,从[6-氯-2-(5-甲基-噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例234)制备标题化合物。MS(EI)m/z:334(M+).m.p.:225-226℃.IR(KBr)ν:3277,1707,1630,1541,1398,1350,1231,1219,1138,878,800cm-1.1H-NMR(DMSO-d6)δ:12.25(1H,br s),11.99(1H,br s),8.04(1H,s),7.82(1H,s),7.81(1H,d,J=9.0Hz),7.13(1H,br d,J=8.7Hz),4.15(2H,s),2.63(3H,s).实施例236 [6-氯-2-(2-噻吩基)羰基吲哚-3-基]乙酸 步骤1.6-氯-2-(2-噻吩基羰基)-1-苯磺酰基吲哚
按照实施例2方法B的步骤2中所述的方法,从6-氯-1-(苯磺酰基)吲哚(实施例2方法B的步骤1)和2-噻吩甲酰氯制备标题化合物。1H-NMR(CDCl3)δ:8.13-8.16(3H,m),7.77-7.80(2H,m),7.50-7.63(4H,m),7.29(1H,dd,J=1.8,8.4Hz),7.19(1H,t,J=5.4Hz),7.03(1H,s).步骤2.6-氯-2-(2-噻吩羰基)吲哚
按照实施例2方法B的步骤3中所述的方法,从6-氯-2-(2-噻吩羰基)-1-苯磺酰基吲哚(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:10.96(1H,br s),8.01(1H,dd,J=1.2,3.8Hz),7.73(1H,dd,J=1.2,4.9Hz),7.64(1H,d,J=8.6Hz),7.54-7.55(1H,m),7.35-7.37(1H,m),7.23(1H,dd,J=3.8,4.9Hz),7.10(1H,dd,J=1.8,8.6Hz).步骤3.α-乙酰氧基-[6-氯-2-(2-噻吩羰基)-1H-吲哚-3-基]丙二酸二乙 酯
按照实施例2方法B的步骤4中所述的方法,从6-氯-2-(2-噻吩羰基)吲哚(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:8.93(1H,br s),7.82(1H,d,J=8.9Hz),7.76(1H,d,J=4.9Hz),7.55(1H,d,J=3.8Hz),7.39(1H,d,J=1.8Hz),7.11-7.18(2H,m),4.16-4.31(4H,m),1.87(3H,s),1.17-1.32(6H,m).步骤4.[6-氯-2-(2-噻吩羰基)-1H-吲哚-3-基]丙二酸二乙酯
按照实施例2方法B的步骤5中所述的方法,从α-乙酰氧基-[6-氯-2-(2-噻吩羰基)-1H-吲哚-3-基]丙二酸二乙酯(步骤3)制备标题化合物。1H-NMR(CDCl3)δ:9.27(1H,br s),7.71-7.75(2H,m),7.60-7.66(1H,m),7.05-7.17(3H,m),5.56(1H,s),4.07-4.26(4H,m),1.20-1.28(6H,m).步骤5.[6-氯-2-(2-噻吩羰基)-1H-吲哚-3-基]乙酸
按照实施例2方法B的步骤6中所述的方法,从[6-氯-2-(2-噻吩羰基)-1H-吲哚-3-基]丙二酸二乙酯(步骤4)制备标题化合物。MS(EI)m/z:319(M+).m.p.:177-178℃.IR(KBr)ν:3323,1701,1593,1568,1524,1435,1412,1323,1258,1229,920cm-1.1H-NMR(DMSO-d6)δ:12.25(1H,br s),11.85(1H,br s),8.13(1H,d,J=4.9Hz),7.89(1H,d,J=3.6Hz),7.74(1H,d,J=8.7Hz),7.51(1H,d,J=1.8Hz),7.34(1H,t,J=4.8Hz),7.15(1H,dd,J=1.8,8.7Hz),3.96(2H,s).实施例237 [6-氯-2-[3-(1-羟基-1-甲基乙基)-2-呋喃甲酰基]-1H-吲哚-3-基]乙酸 甲酯
按照实施例57中描述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和2-氯代乙酰基-3-(1-羟基-1-甲基乙基)呋喃*制备标题化合物。1H-NMR(CDCl3)δ:9.89(1H,br s),7.59(1H,d,J=1.6Hz),7.53(1H,d,J=8.7Hz),7.34(1H,d,J=1.5Hz),7.08(1H,dd,J=1.6,8.7Hz),6.57(1H,d,J=1.8Hz),6.39(1H,brs),4.22(2H,s),3.73(3H,s),1.57(6H,s).*2-氯代乙酰基-3-(1-羟基-1-甲基乙基)呋喃按照下列方法制备:
在-78℃下,向2-(3-呋喃基)-2-丙醇(T.M.Bargar等人,J.Med.Chem.,1986,
29,315.,2.0g,15.85mmol)的THF(100ml)溶液中加入正丁基锂的己烷溶液(1.55M,30.7ml,47.55mmol)溶液。搅拌1小时后,在0℃下加入2-氯-N-甲氧基-N-甲基乙酰胺(6.54g,47.55mmol)。向混合物中加入饱和的氯化铵水溶液(100ml),分离出有机层。用水(100ml×2)和盐水(50ml)洗涤有机层,并且干燥(硫酸镁)。除去溶剂后,残留物通过闪蒸柱色谱纯化,用乙酸乙酯/己烷(1∶4)洗脱,得到1.03g(32%)油状的标题化合物。1H-NMR(CDCl3)δ:7.52(1H,d,J=1.8Hz),6.56(1H,d,J=1.8Hz),5.51(1H,s),4.74(2H,s),1.56(6H,s).实施例238 [6-氯-2-[3-(1-羟基-1-甲基乙基)-2-呋喃甲酰基]-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[6-氯-2-[3-(1-羟基-1-甲基乙基)-2-呋喃甲酰基]-1H-吲哚-3-基]乙酸甲酯(实施例237)制备标题化合物。MS(EI)m/z:361(M+).m.p.:229-230℃.IR(KBr)ν:3270,2980,1270,1591,1564,1522,1398,1302,1263,1200,785cm-1.1H-NMR(DMSO-d6)δ:11.78(1H,br s),7.97(1H,d,J=1.6Hz),7.77(1H,d,J=8.6Hz),7.56(1H,d,J=1.5Hz),7.13(1H,dd,J=1.8,8.6Hz),6.87(1H,d,J=1.6Hz),5.69(1H,brs),3.96(2H,s),1.53(6H,s).实施例239 [6-氯-2-[3-甲氧基甲基-2-呋喃甲酰基]-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和2-氯代乙酰基-3-(甲氧基甲基)呋喃*制备标题化合物。1H-NMR(CDCl3)δ:9.81(1H,br s),7.60(1H,d,J=1.6Hz),7.56(1H,d,J=8.7Hz),7.40(1H,d,J=1.5Hz),7.10(1H,dd,J=1.8,8.7Hz),6.79(1H,d,J=1.6Hz),4.81(2H,s),4.26(2H,s),3.74(3H,s),3.48(3H,s).*2-氯代乙酰基-3-(甲氧基甲基)呋喃是按照实施例37中所述的制备2-氯代乙酰基-3-(1-羟基-1-甲基乙基)呋喃的方法,从3-(甲氧基甲基)呋喃(N.Greeves等人,Synthesis,1993,1109)制备的。1H-NMR(CDCl3)δ:7.52(1H,d,J=1.8Hz),6.74(1H,d,J=1.8Hz).4.73(2H,s),4.62(2H,s),3.44(3H,s).实施例240 [6-氯-2-[3-甲氧基甲基-2-呋喃甲酰基]-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[6-氯-2-(3-甲氧基甲基-2-呋喃甲酰基)-1H-吲哚-3-基]乙酸甲酯(实施例239)制备标题化合物。MS(EI)m/z:347(M+).m.p.:212-213℃.IR(KBr)ν:3373,3221,1720,1601,1576,1529,1205,1173,1115,1088cm-1.1H-NMR(DMSO-d6)δ:11.72(1H,br s),8.04(1H,d,J=1.6Hz),7.76(1H,d,J=8.7Hz),7.59(1H,d,J=1.5Hz),7.12(1H,dd,J=1.8,8.7Hz),6.86(1H,d,J=1.6Hz),4.70(2H,s),4.02(2H,s),3.36(3H,s).实施例241 [6-氯-2-(1-甲基咪唑-2-羰基)-1H-吲哚-3-基]乙酸 步骤1.[6-氯-1-乙氧基羰基-2-(1-甲基咪唑-2-羰基)二氢吲哚-3-基] 乙酸甲酯
按照实施例31的步骤2中描述的方法,从反式-4-氯-2-(乙氧基羰基)肉桂酸甲酯(实施例31的步骤1)和2-溴代乙酰基-1-甲基咪唑氢溴酸盐*制备标题化合物。MS(EI)m/z:405(M+)。*2-溴代乙酰基-1-甲基咪唑氢溴酸盐是按照实施例31的步骤2中所述的制备2-溴代乙酰基-4-甲基吡啶氢溴酸盐的方法,从2-乙酰基-1-甲基咪唑制备的。1H-NMR(DMSO-d6)δ:7.69(1H,s),7.27(1H,s),4.68(2H,s),3.81(3H,s).步骤2.[6-氯-1-乙氧基羰基-2-(1-甲基咪唑-2-羰基)吲哚-3-基]乙酸
按照实施例31的步骤3中所述的方法,从[6-氯-1-乙氧基羰基-2-(1-甲基咪唑-2-羰基)二氢吲哚-3-基]乙酸甲酯(步骤1)制备标题化合物。m.p.:235.5℃.IR(KBr)ν:3238,1695,1630,1538,1402,1229,1146cm-1.1H-NMR(CDCl3)δ:12.3(1H,br s),7.64(1H,d,J=8.7Hz),7.50(1H,d,J=1.8Hz),7.41(1H,s),7.16(1H,s),7.09(1H,dd,J=1.8,8.6Hz),4.25(2H,s),4.13(3H,s).实施例242 [6-氯-2-(1-甲基咪唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯
在室温和搅拌下,向[6-氯-2-(1-甲基咪唑-2-羰基)-1H-吲哚-3-基]乙酸(实施例241,65mg,0.21mmol)的甲醇(10ml)溶液中加入(三甲基甲硅烷基)重氮甲烷(1.0M的己烷溶液,1.05ml,2.1mmol)。搅拌19小时后,浓缩混合物。残留物通过TLC纯化,用乙酸乙酯-己烷(1∶2)展开,得到20mg(23%)黄色固体的标题化合物。1H-NMR(CDCl3)δ:12.35(1H,br s),7.59(1H,d,J=8.0Hz),7.49(1H,d,J=1.5Hz),7.24(1H,s),7.11(1H,dd,J=1.7,8.1Hz),7.08(1H,s),4.30(2H,s),4.12(3H,s),3.71(3H,s).实施例243 [5-氯-2-(1-甲基咪唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-5-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例36的步骤3)和2-溴代乙酰基-1-甲基咪唑氢溴酸盐(其制备方法见实施例241)制备标题化合物。1H-NMR(DMSO-d6)δ:12.28(1H,br s),7.85(1H,s),7.77(1H,d,J=8.7Hz),7.66(1H,s),7.33-7.29(2H,m),4.21(2H,s),4.03(3H,s),3.60(3H,s).实施例244 [5-氯-2-(1-甲基咪唑-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[5-氯-2-(1-甲基咪唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例243)制备标题化合物。m.p.:230-233℃.1H-NMR(DMSO-d6)d:12.50(1H,br s),7.84(1H,s),7.76(1H,d,J=13.2Hz),7.66(1H,s),7.35-7.7.28(2H,m).4.15(2H,s),4.06(3H,s).实施例245 [5-氯-2-(咪唑-2-羰基)-1H-吲哚-3-基] 步骤1.[5-氯-2-[1-[2-(三甲基甲硅烷基)乙氧基甲基]咪唑-2-羰 基]-1H-吲哚-3-基]乙酸甲酯
按照实施例57描述的方法,从反式-5-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例36的步骤3)和2-氯代乙酰基-1-[2-(三甲基甲硅烷基)乙氧基甲基]咪唑*制备标题化合物。1H-NMR(CDCl3)d:12.38(1H,br s),7.66(1H,s),7.46-7.38(2H,m),7.34-7.29(2H,m),5.95(2H,s),4.29(2H,s),3.73(3H,s),3.66(2H,t,J=8.0Hz),0.98(2H,t,J=8.0Hz),0.03(9H,s).*2-氯代乙酰基-1-[2-(三甲基甲硅烷基)乙氧基甲基]咪唑按照下列方法制备:
在-78℃和搅拌下,向1-[2-(三甲基甲硅烷基)乙氧基甲基]咪唑(Jeffrey P.Whitten等人,J.Org.Chem.,51,1891(1986),3.0g,15mmol)的THF(30ml)溶液中滴加正丁基锂(1.55M的己烷溶液,11.0ml,17mmol),搅拌混合物1小时。在该温度下,向所得的混合物中加入2-氯-N-甲氧基-N-甲基乙酰胺(2.4g,17mol),把混合物温热到0℃,再搅拌2小时。把混合物倒入水(50ml)中,用乙酸乙酯(80ml)萃取,干燥(硫酸镁),浓缩。通过闪蒸柱色谱纯化残留的棕色油状物,用乙酸乙酯/己烷(1∶4)洗脱,得到1.2g(32%)黄色油状的标题化合物。1H-NMR(CDCl3)d:7.39(1H,s),7.25(1H,s),5.81(2H,s),4.96(2H,s),3.60(2H,t,J=8.2Hz),0.95(2H,t,J=8.2Hz),0.02(9H,s).步骤2.[5-氯-2-(咪唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯
向[5-氯-2-[1-[2-(三甲基甲硅烷基)乙氧基甲基]咪唑-2-羰基]-1H-吲哚-3-基]乙酸甲酯(步骤1,300mg,0.67mmol)的甲醇(10ml)溶液中加入2N HCl水溶液(7ml),回流混合物1.5小时。把混合物冷却到室温,然后浓缩。向残留物中加入饱和的碳酸氢钠水溶液(10ml),然后浓缩混合物。把残留的黄色固体溶于THF(100ml)中并且干燥(硫酸镁)。除去溶剂后,得到220mg(100%)黄色固体的标题化合物。1H-NMR(CDCl3)d:12.16(1H,br s),10.80(1H,br s),7.68(1H,s),7.50-7.28(5H,m),4.29(2H,s),3.70(3H,s).实施例246 [5-氯-2-(咪唑-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[5-氯-2-(咪唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例245)制备标题化合物。m.p.:253-254℃.1H-NMR(DMSO-d6)δ:12.28(1H,br s),7.84(1H,d,J=2.0Hz),7.80(1H,d,J=9.1Hz),7.32(1H,dd,J=2.0,9.1Hz),4.17(2H,s).实施例247 [6-氯-2-(咪唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯 步骤1.[6-氯-2-[1-[2-(三甲基甲硅烷基)乙氧基甲基]咪唑-2-羰 基]-1H-吲哚-3-基]乙酸甲酯
按照实施例57描述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和2-氯代乙酰基-1-[2-(三甲基甲硅烷基)乙氧基甲基]咪唑(其制备方法见实施例245的步骤1)制备标题化合物。1H-NMR(CDCl3)δ:12.34,(1H,br s),7.61(1H,d,J=8.6Hz),7.52(1H,d,J=1.6Hz),7.40(1H,d,J=1.4Hz),7.31(1H,d,J=1.4Hz),7.13(1H,dd,J=1.6,8.6Hz),5.95(2H,s),4.32(2H,s),3.72(3H,s),3.67(2H,t,J=8.0Hz),1.00(2H,t,J=8.0Hz),0.02(9H,s).步骤2.[5-氯-2-(咪唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例245的步骤2中描述的方法,从[6-氯-2-[1-[2-(三甲基甲硅烷基)乙氧基甲基]咪唑-2-羰基]-1H-吲哚-3-基]乙酸甲酯(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:12.50(1H,br s),7.68-7.48(2H,m),7.40-7.30(1H,m),7.19-7.06(1H,m),6.97-6.92(1H,m),4.30(2H,s),3.67(3H,s).实施例248 [6-氯-2-(咪唑-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[6-氯-2-(咪唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例247)制备标题化合物。m.p.:252-253℃.1H-NMR(DMSO-d6)δ:13.63(1H,br s),12.40-12.15(2H,br),7.88(1H,d,J=1.8Hz),7.78(1H,d,J=8.6Hz),7.59(1H,s),7.40(1H,s),7.11(1H dd,J=1.8,8.6Hz),4.18(2H,实施例249 [5-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57描述的方法,从反式-5-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例36的步骤3)和2-溴代乙酰基-4-甲基噻唑氢溴酸盐(Cowden,William B.等人,Aust.J.Chem.,1985,
38,1257)制备标题化合物。1H-NMR(DMSO-d6)δ:12.02(1H,br s),7.93-7.85(2H,m),7.75(1H,d,J=8.9Hz),7.38(1H,dd,J=2.0,8.9Hz),4.23(2H,s),3.60(3H,s),2.61(3H,s).实施例250 [5-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[5-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例249)制备标题化合物。m.p.:218-220℃.1H-NMR(DMSO-d6)δ:11.97(1H,br s),7.89(1H,d,J=2.0Hz),7.75(1H,d,J=8.7Hz),7.37(1H,dd,J=2.0,8.7Hz),4.13(2H,s),2.62(3H,s).实施例251 [5-氯-2-(1-甲基吡咯-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例8方法B中描述的方法,从反式-5-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例36的步骤3)和2-氯代乙酰基-1-甲基吡咯(P.D.Croce等人,Synthesis,1990,212)制备标题化合物。1H-NMR(DMSO-d6)δ:11.8(1H,br s),7.80(1H,br s),7.55(1H,d,J=8.6Hz),7.40-7.32(2H,m),6.95-6.90(1H,m),6.35-6.26(1H,m),4.00(2H,s),3.43(3H,s),2.50(3H,s).实施例252 [5-氯-2-(1-甲基吡咯-2-羰基)-1H-吲哚-3-基]乙酸
加热回流[5-氯-2-(1-甲基吡咯-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例251,250mg,0.79mmol)和碳酸钾(900mg,6.4mmol)在甲醇-水(1∶1,40ml)中的混合物1小时。把混合物冷却到室温,然后浓缩。残留物用2N HCl水溶液中和,用乙酸乙酯(50ml×2)萃取。干燥(硫酸镁)并浓缩合并后的有机萃取液。残留物的固体在乙酸乙酯/己烷中重结晶,得到40mg(23%)淡黄色固体的标题化合物。mp:203-205℃.1H-NMR(DMSO-d6)δ:11.56(1H,br s),7.57(1H,s),7.33(1H,d,J=8.6Hz),7.20-7.10(2H,m),6.72(1H,s),6.10(1H,s),3.81(2H,s),2.52(3H,s).实施例253 [5-氯-2-(2-甲基咪唑-4-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例8方法B中描述的方法,从反式-5-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例36的步骤3)和4-溴代乙酰基-2-甲基咪唑(Deady,Leslie W.等人,Aust.J.Chem.,1981,
34,1295)制备标题化合物。1H-NMR(DMSO-d6)δ:12.04(1H br s),8.51(1H,s),7.86(1H,d,J=2.0Hz),7.71(1H,d,J=8.9Hz),7.34(1H,dd,J=2.0,8.9Hz),4.17(2H,s),3.59(3H,s),2.71(3H,s).实施例254 [5-氯-2-(2-甲基咪唑-4-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中所述的方法,从[5-氯-2-(2-甲基咪唑-4-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例253)制备标题化合物。m.p.:237-238℃.1H-NMR(DMSO-d6)δ:12.03(1H,br),12.00(1H,s),8.49(1H,s),7.83(1H,d,J=2.0Hz),7.70(1H,d,J=8.9Hz),7.34(1H,dd,J=2.0,8.9Hz),4.09(2H,s),2.87(3H,s).实施例255 [5-氯-2-(噻唑-5-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-5-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例36的步骤3)和5-溴代乙酰基噻唑氢溴酸盐*制备标题化合物。1H-NMR(CDCl3)d:12.05(1H,br s),9.51(1H,s),8.62(1H,s),7.85(1H,d,J=1.9Hz),7.55(1H,d,J=8.7Hz),7.35(1H,dd,J=1.9,8.7Hz),4.09(2H,s),3.59(3H,s).*5-溴代乙酰基噻唑氢溴酸盐是按照实施例31的步骤2中描述的制备2-溴代乙酰基-4-甲基吡啶氢溴酸盐方法,从5-乙酰基噻唑制备的。1H-NMR(DMSO-d6)δ:9.49(1H,s),8.34(1H,s)4.91(2H,s).实施例256 [5-氯-2-(噻唑-5-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中所述的方法,从[5-氯-2-(噻唑-5-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例255)制备标题化合物。m.p.:175-180℃.1H-NMR(DMSO-d6)δ:11.80(1H,br s),9.48(1H,s),8.74(1H,s),7.78(1H,s),7.48(1H,d,J=8.7Hz),7.30(1H,d,J=8.9Hz),3.81(2H,s).实施例257 [6-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例8方法B中描述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和2-溴代乙酰基-4-甲基噻唑氢溴酸盐(Cowden,William B.等人,Aust,J.Chem.,1985,
38,1257)制备标题化合物。1H-NMR(DMSO-d6)δ:11.95(1H,br s),7.90(1H,s),7.84(1H,d,J=8.7Hz),7.84(1H,d,J=2.0Hz),7.15(1H,d,J=2.0Hz),4.24(2H,s),3.60(3H,s),2.62(3H,s).实施例258 [6-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中所述的方法,从[6-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例257)制备标题化合物。m.p.:239-240℃.1H-NMR(DMSO-d6)δ:11.80(1H,br s),7.75(1H,s),7.68(1H,d,J=8.4Hz),7.67(1H,d,J=2.0Hz),7.02(1H,dd,J=2.0,8.4Hz),4.03(2H,s),2.49(3H,s).实施例259 [5-氯-2-[3-(乙氧基羰基)异噁唑-5-羰基]-1H-吲哚-3-基]乙酸甲酯
按照实施例8方法B中描述的方法,从反式-5-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例36的步骤3)和5-(溴代乙酰基)异噁唑-3-甲酸乙酯制备标题化合物。1H-NMR(DMSO-d6)δ:12.07(1H,br s),7.93(1H,d,J=1.9Hz),7.70(1H,s),7.39(1H,dd,J=1.9,12.8Hz).7.62(1H,d.J=12.8Hz),4.44(2H,q,J=7.1Hz),4.15(2H,s),3.60(3H,s),1.37(3H,t,J=7.1Hz).实施例260 [5-氯-2-[3-(羧基)异噁唑-5-羰基])-1H-吲哚-3-基]乙酸
向[5-氯-2-[3-(乙氧基羰基)异噁唑-5-羰基]-1H-吲哚-3-基]乙酸甲酯(实施例259,314mg,0.80mmol)的乙酸(20ml)溶液中加入2N HCl水溶液(6.0ml),在110℃加热混合物5小时,然后把混合物冷却到室温,并且浓缩。残留的黄色固体用乙酸乙酯洗涤,在乙酸乙酯/己烷中重结晶,得到120mg(43%)淡黄色固体的标题化合物。m.p.:200-205℃.1H-NMR(DMSO-d6)δ:12.01(1H,s),7.91(1H,s),7.65-7.56(2H,m),7.39(1H,d,J=8.9Hz),4.06(2H,s).实施例261 [6-氯-2-环丙烷羰基-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和溴代甲基环丙基酮*制备标题化合物。1H-NMR(CDCl3)δ:9.55(1H,br s),7.58(1H,d,J=8.56Hz),7.26(1H,d,J=1.97Hz)7.10(1H,dd,J=8.56Hz,1.97Hz),4.17(2H,s),3.73(3H,s),2.58-2.49(1H,m),1.30-1.25(2H,m),1.09-1.02(2H,m).*溴代甲基环丙基酮是按照实施例189中描述的制备4-(三氟甲氧基)苯甲酰甲基溴的方法,从环丙基甲基酮制备的。1H-NMR(CDCl3)δ:3.91(2H,s),2.65(1H,t,6.94Hz),1.20-0.98(4H,m).实施例262 [6-氯-2-环丙烷羰基-1H-吲哚-3-基]乙酸
按照实施例9中方法B中描述的方法,从2-(6-氯-2-环丙烷羰基-1H-吲哚-3-基]乙酸甲酯(实施例261)制备标题化合物。m.p.:207-210_C.IR(KBr)ν:3304,3013,1709,1624,1566,1443,1414,1387,1340,1286,1248,1217,1200,1157,1057,1045,1022cm-1.1H-NMR(DMSO-d6)δ:11.98(1H,br s),7.75(1H,d,J=8.75Hz),7.48(1H,d,J=1.81Hz)7.11(1H,dd,J=8.75Hz,1.81Hz),4.08(2H,s),2.73(1H,quintet,6.24Hz),1.07(4H,d,6.24Hz).实施例263 [6-氯-2-环丁烷羰基-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和溴代甲基环丁基酮*制备标题化合物。1H-NMR(CDCl3)δ:9.35(1H,br s),7.53(1H,d,J=8.72Hz),7.18(1H,d,J=1.65Hz)7.07(1H,dd,J=8.72Hz,1.65Hz),4.10(2H,s),3.77(3H,s),3.72(1H,m),2.44-1.86(6H,m).*溴代甲基环丁基酮是按照实施例189中描述的制备4-(三氟甲氧基)苯甲酰甲基溴的方法,从环丁基甲基酮制备的。1H-NMR(CDCl3)δ:3.88(2H,s),3.60(1H,m),2.33-1.80(6H,m)实施例264 [6-氯-2-环丁烷羰基-1H-吲哚-3-基]乙酸
按照实施例9中方法B中描述的方法,从2-(6-氯-2-环丁烷羰基-1H-吲哚-3-基]乙酸甲酯(实施例263)制备标题化合物。m.p.:225-228℃.IR(KBr)ν:3303,2954,1705,1632,1564,1529,1437,1412,1335,1242,1213,1188,1157,1056,1024cm-1.1H-NMR(DMSO-d6)δ:11.63(1H,br s),7.71(1H,d,J=8.72Hz),7.46(1H,d,J=1.81Hz),7.09(1H,dd,J=8.72Hz,1.81Hz),4.04(2H,s),2.30-1.78(7H,m).实施例265 [5-(叔丁基)-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-5-叔丁基-2-(对甲苯磺酰基氨基)肉桂酸甲酯(实施例143的步骤2)和4-氯苯甲酰甲基溴制备标题化合物。1H-NMR(CDCl3)δ:8.82(1H,br s),7,8-7.31(7H,m),3.87(2H,s),3.67(3H,s),1.38(9H,s).实施例266 [5-(叔丁基)-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸
按照实施例9中方法B中描述的方法,从[5-叔丁基-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸甲酯(实施例265)制备标题化合物。m.p.:171C.IR(KBr)ν:3241,2963,1699,1634,1589/1541,1394,1331,1222,1091,1011cm-1 1H-NMR(DMSO-d6)δ:11.48(1H,br s),7.78-7.37(7H,m),3.85(2H,s),1.34(9H,s).实施例267 [6-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]-N,N-二甲基乙酰胺
按照实施例43中描述的方法,从[6-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基](实施例31)制备标题化合物。熔点:208℃(分解)。IR(KBr):3233,1655,1638,1524,1398,1200,1134cm-1.1H-NMR(CDCl3)δ:12.54(1H,br s),8.62(1H,d,J=5.0Hz),8.15(1H,br),7.79(1H,d,J=8.7Hz),7.49(1H,d,J=1.8Hz),7.40-7.30(1H,m),7.09(1H,dd,J=1.8,8.7Hz),4.43(2H,s),3.16(3H,s),2.98(3H,s),2.48(3H,s).实施例268 [6-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]-N-甲基乙酰胺
按照实施例43中描述的方法,从[6-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸(实施例31)和甲胺盐酸盐制备标题化合物。m.p.:231℃.IR(KBr)ν:3306,1643,1595,1560,1526,1277,1202,797cm-1.1H-NMR(CDCl3)δ:12.45(1H,br),8.64(1H,d,J=4.9Hz),8.19(1H,br),7.85(1H,d,J=8.6Hz),7.50(1H,br),7.40(1H,br d,J=4.6Hz),7.15(1H,dd,J=1.6,8.9Hz),6.67(1H,br),4.14(2H,s),2.73(3H,d,J=4.8Hz),2.51(3H,s).实施例269 [5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]-N-(2-羟基乙基)乙酰胺
按照实施例43中描述的方法,从[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸(实施例36)和2-氨基乙醇制备标题化合物。MS(EI)m/z:371(M+).m.p.:195.9℃.1H-NMR(DMSO-d6)δ:12.28(1H,br s),8.69(1H,d,J=4.9Hz),7.94(1H,br s),7.78(2H,m),7.66(1H,d,J=8.7Hz),7.56(1H,m),7.31(1H,dd,J=2.0Hz,8.7Hz),3.94(2H,s),3.09(2H,dd,J=5.93Hz,11.86Hz),2.47(3H,s).实施例270 [5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]-N-甲氧基乙酰胺
按照实施例43中描述的方法,从[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸(实施例36)和O-甲基羟胺盐酸盐制备标题化合物。MS(EI)m/z:357(M+).1H-NMR(CDCl3)δ:12.53(1H,br s),9.54(1H,br s),8.65(1H,d,J=5.1Hz),8.19(1H,br s),7.92(1H,br s),7.42(2H,m),7.34(1H,dd,J=1.7Hz,8.9Hz),4.01(2H,s),3.74(3H,s),2.52(3H,s).实施例271 2-[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]-1-(1-哌嗪基)-1-乙 酮 步骤1.2-[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]-1-(4-叔丁氧 基羰基-1-哌嗪基)-1-乙酮
按照实施例43中描述的方法,从[5-氯-2-(4-甲基吡啶)-1H-吲哚-3-基]乙酸(实施例36)和1-哌嗪甲酸叔丁基酯制备标题化合物。1H-NMR(CDCl3)δ:12.61(1H,br s),8.62(1H,d,J=5.1Hz),8.14(1H,br s),7.84(1H,s),7.42(1H,d,J=8.7Hz),7.37(br d,1H,J=4.9Hz),7.30(1H,dd,J=2.0Hz,8.9Hz),4.42(2H,s),3.66(4H,m),2.50(3H,s),1.64(4H,m),1.46(9H,s).步骤2.2-[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]-1-(1-哌嗪 基)-1-乙酮
在0℃下,向[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]-N-(4-叔丁氧基羰基-1-哌嗪基(piperadino))乙酰胺(步骤1,152.6mg,0.042mmol)的IHF(1ml)溶液中滴加三氟乙酸(2ml)。在室温下搅拌混合物1.5小时,然后浓缩。残留物用二氯甲烷(25ml)稀释,用饱和的碳酸氢钠水溶液(25ml)洗涤。水层用二氯甲烷(25ml×2)萃取。干燥(硫酸镁)并且浓缩合并后的有机层。残留物通过闪蒸柱色谱纯化,用甲醇/二氯甲烷(1∶10)洗脱,得到80.8mg黄色结晶状的标题化合物。MS(EI)m/z:396(M+).m.p.:.205.0C.IR(KBr)ν:3244,1647,1595,1525,1429,1205cm-1.1H-NMR(DMSO-d6)δ:12.28(1H,br s),8.68(1H,d,J=4.9Hz),7.90(1H,br s),7.81(1H,br s),7.65(1H,d,J=8.9Hz),7.56(br d,1H,J=4.1Hz),7.31(1H,dd,J=1.8Hz,8.9Hz),4.15(2H,br s),3.50-3.15(4H,m),2.70-2.55(4H,m),2.46(3H,s).实施例272 [5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]-N-(2-氨基乙基)乙酰胺 步骤1.[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]-N-(2-叔丁氧基 羰基氨基乙基)乙酰胺
按照实施例43中所述的方法,从[5-氯-2-(4-甲基吡啶)-1H-吲哚-3-基]乙酸(实施例36)和N-(2-氨基乙基)氨基甲酸叔丁基酯。1H-NMR(CDCl3)δ:12.29(1H,br s),8.68(1H,d,J=4.9Hz),7.94(1H,br s),7.78(2H,m),7.67(1H,d,J=8.9Hz),7.57(1H,br d,J=4.9Hz),7.32(dd,1H,J=2.0Hz,8.7Hz),6.73(1H,m),3.94(2H,s),3.05-2.95(4H,m),2.47(3H,s),1.35(9H,s).步骤2.[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]-N-(2-氨基乙基) 乙酰胺
按照实施例273的步骤2中描述的方法,从[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]-N-(2-叔丁氧基羰基氨基乙基)乙酰胺(步骤1)制备标题化合物。MS(EI)m/z:370(M+).m.p.:165.7℃.IR(KBr)ν:3346,2927,1665,1627,1593,1515,1435,1267,1207cm-1.1H-NMR(DMSO-d6)δ:12.28(1H,br s),8.69(1H,d,J=4.9Hz),7.93(1H,br s),7.80-7.76(2H,m),7.66(1H,d,J=8.9Hz),7.57(1H,m),7.31(dd,1H,J=2.0Hz,8.9Hz),3.94(2H,s),3.01(2H,q,J=5.77Hz),2.55-2.45(2H,m),2.47(3H,s).实施例273 2-[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]-1-(3-氨基-1-吡咯烷 基)-1-乙酮 步骤1.2-[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]-1-[3-(叔丁 氧基羰基氨基)-1-吡咯烷基]-1-乙酮
按照实施例43中所述的方法,从[5-氯-2-(4-甲基吡啶)-1H-吲哚-3-基]乙酸(实施例36)和3-(叔丁氧基羰基氨基)吡咯烷。1H-NMR(CDCl3)δ:12.56(1H,br s),8.62(1H,d,J=4.9Hz),8.18(1H,br s),7.78(1H,br s),7.42(1H,d,J=8.9Hz),7.35(1H,br d,J=4.9Hz),7.29(2H,m),4.89(1H,br d,J=25.05),4.36-3.45(7H,m),2.48(3H,s),2.35-1.80(2H,m),1.46(9H,s).步骤2.2-[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]-1-(3-氨基 -1-吡咯烷基)-1-乙酮
按照实施例271的步骤2中描述的方法,从2-[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]-1-[3-(叔丁氧基羰基氨基)-1-吡咯烷基]-1-乙酮(步骤1)制备标题化合物。MS(EI)m/z:396(M+).m.p.:179.2℃.IR(KBr)ν:3238,2876,1638,1595,1526,1423,1203cm-1.1H-NMR(DMSO-d6)δ:12.26(1H,br s),8.68(1H,d,J=4.9Hz),7.89(1H,br s),7.81(1H,d,J=1.81Hz),7.65(1H,d,J=8.9Hz),7.55(1H,br d,J=5.1Hz),7.31(dd,1H,J=2.0Hz,8.7Hz),4.07(1H,s).4.05(1H,s),3.70-2.90(5H,m),2.46(3H,s),2.10-1.80(1H,m),1.75-1.45(1H,m).实施例274 [6-氯-2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸甲酯 步骤1.反式-2-氨基-4-氯-5-氟肉桂酸甲酯
按照实施例133的步骤1中描述的方法,从2-溴-5-氯-4-氟苯胺(JP01311056 A2,Nippon Kayaku Co.,Ltd.,Japan)制备标题化合物。1H-NMR(CDCl3)δ:7.69(1H,d,J=15.8Hz),7.15(1H,d,J=9.7Hz),6.74(1H,d,J=6.4Hz),6.31(1H,d,J=15.8Hz),3.81(3H,s).步骤2.反式-4-氯-5-氟-2-(苯磺酰基氨基)肉桂酸甲酯
按照实施例8方法A的步骤1中描述的方法,从反式-2-氨基-4-氯-5-氟肉桂酸甲酯(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:7.71-7.68(1H,m),7.57-7.40(6H,m),7.23(1H,d,J=9.4Hz),6.09(1H,d,J=15.8Hz),3.77(3H,s).步骤3.[6-氯-2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-4-氯-5-氟2-(苯磺酰基氨基)肉桂酸甲酯(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:9.05(1H,br.s),7.74(2H,d,J=8.7Hz),7.49(2H,d,J=8.7Hz),7.35-7.32(2H,m),3.77(2H,s),3.66(3H,s)实施例275 [6-氯-2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[6-氯-2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸甲酯制备标题化合物。m.p.:215-220℃.IR(KBr)ν:1709,1626,1585,1529,1456,1439,1279,1250cm-1.1H-NMR(DMSO-d6)δ:11.85(1H,br.s),7.79-7.75(3H,m),7.67-7.63(2H,m),7.60-7.58(1H,m),3.83(2H,s).实施例276 [6-氯-5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-4-氯-5-氟-2-(苯磺酰基氨基)肉桂酸甲酯(实施例274的步骤2)制备标题化合物。1H-NMR(CDCl3)δ:12.54(1H,br.s),8.58(1H,d,J=4.9Hz),8.14(1H,m),7.56-7.53(1H,m),7.39-7.34(2H,m),4.25(2H,s),3.75(3H,s),2.48(3H,s).实施例277 [6-氯-5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[6-氯-5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例276)制备标题化合物。mp:219.5℃.IR(KBr)ν:1732,1709,1647,1597,1529,1279,1252,1204cm-1.1H-NMR(DMSO-d6)δ:12.35(1H,br.s),8.70(1H,d,J=5.1Hz),7.96(1H,s),7.87(1H,d,J=6.6Hz),7.81(1H,d,J=10.1Hz),7.59-7.58(1H,m),4.05(2H,s),2.47(3H,s).实施例278 [6-氯-2-[4-(1-羟基乙基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯 步骤1.[6-氯-2-[4-[1-(叔丁基二甲基甲硅烷氧基)乙基]吡啶-2-羰 基]-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-4-氯-2-(苯磺酰基氨基)肉桂酸甲酯(实施例8方法A的步骤1)和2-溴代乙酰基-4-[1-(叔丁基二甲基甲硅烷氧基)乙基]吡啶*制备标题化合物。1H-NMR(CDCl3)δ:12.49(1H,br s),8.71(1H,d,J=4.9Hz),8.24(1H,d,J=1.5Hz),7.61-7.63(2H,m),7.53(1H,d,J=1.8Hz),7.13(1H,dd,J=1.8,8.7Hz),4.96(1H,q,J=6.4Hz),4.32(2H,s),3.73(3H,s),1.45(3H,d,J=6.4Hz),0.93(9H,s),0.10(3H,s),0.03(3H,s).*2-溴代乙酰基-4-[1-(叔丁基二甲基甲硅烷氧基)乙基]吡啶按照下列方法制备:4-[1-(三甲基甲硅烷氧基)乙基]-2-吡啶甲腈:
按照实施例33中所述的制备4-氯-2-吡啶甲腈的方法,从4-(1-羟基乙基)吡啶-N-氧化物(C.W.Muth等人,J.heterocycl.Chem.,1972,
9,1299)制备标题化合物。1H-NMR(CDCl3)δ:8.64(1H,d,J=5.1Hz),7.69-7.70(1H,m),7.45-7.48(1H,m),4.88(2H,q,J=6.4Hz),1.43(3H,d,J=6.6Hz),0.14(9H,s).4-[1-(叔丁基二甲基甲硅烷氧基)乙基]-2-吡啶甲腈:
在室温下,向4-[1-(三甲基甲硅烷氧基)乙基]-2-吡啶甲腈(39.04g,0.1624mol)的THF(200ml)溶液中加入四丁基氟化铵的THF溶液(1M,178.6ml,0.1786mol)。搅拌混合物0.5小时,然后浓缩。残留物用乙酸乙酯(300ml)稀释,用水(200ml)洗涤。然后用二氯甲烷(200ml×2)萃取水层。干燥(硫酸镁)并且浓缩合并后的有机层。把残留的油状物溶于DMF(200ml)中。在室温下,向溶液中加入叔丁基二甲基氯化硅(36.72g,0.2436mol)和咪唑(22.11g,0.3248mol)。搅拌混合物19小时后,加入乙醚(500ml)和水(200ml),分离出有机层。有机层用水(100ml×2)洗涤,干燥(硫酸镁),浓缩。残留物通过闪蒸柱色谱纯化,用乙酸乙酯/己烷(1∶20)洗脱,得到39.23g(92%)油状的标题化合物。1H-NMR(CDCl3)δ:8.64(1H.d,J=5.1Hz),7.67-7.68(1H,m),7.46-7.48(1H,m),4.89(1H,q,J=6.4Hz),1.42(3H,d,J=6.4Hz),0.92(9H,s),0.10(6H,s).2-乙酰基-4-[1-(叔丁基二甲基甲硅烷氧基)乙基]吡啶:
按照实施例33中描述的制备2-乙酰基-4-氯吡啶的方法,从4-[1-(叔丁基二甲基甲硅烷氧基)乙基]-2-吡啶甲腈制备标题化合物。1H-NMR(CDCl3)δ:8.62(1H,d,J=4.9Hz),7.95-7.96(1H,m),7.49-7.52(1H,m),4.91(1H,q,J=6.4Hz),2.73(3H,s),1.41(3H,d,J=6.4Hz),0.91(9H,s),0.10(6H,s).2-溴代乙酰基-4-[1-(叔丁基二甲基甲硅烷氧基)乙基]吡啶:
按照实施例95中描述的制备2-溴代乙酰基-4-(叔丁基二甲基甲硅烷氧基甲基)吡啶的方法,从2-乙酰基-4-[1-(叔丁基二甲基甲硅烷氧基)乙基]吡啶制备标题化合物。步骤2.[6-氯-2-[4-(1-羟基乙基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲 酯
按照实施例95的步骤2中描述的方法,从[6-氯-2-[4-[1-(叔丁基二甲基甲硅烷氧基)乙基]吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯(步骤1)制备标题化合物。1H-NMR(DMSO-d6)δ:12.34(1H,br s),8.77(1H,d,J=5.1Hz),8.11(1H,s),7.81(1H,d,J=8.7Hz),7.75(1H,d,J=1.6Hz),7.70(1H,dd,J=1.2,4.9Hz),7.13(1H,dd,J=1.8,8.6Hz),5.61(1H,d,J=4.6Hz),4.84-4.93(1H,m),4.17(2H,s),3.59(3H,s),1.39(3H,d,J=6.4Hz).实施例279 [6-氯-2-[4-(1-羟基乙基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸
按照实施例58中描述的方法,从[6-氯-2-[4-(1-羟基乙基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯(实施例278)制备标题化合物。m.p.:193-194℃.IR(KBr)ν:3464,1707,1632,1591,1526,1250,1225,1192,1144,914cm-1.1H-NMR(DMSO-d6)δ:12.30(1H,br s),8.78(1H,d,J=5.1Hz),8.11(1H,s),7.79(1H,d,J=8.6Hz),7.74(1H,d,J=1.6Hz),7.71(1H,d,J=5.3Hz),7.12(1H,dd,J=1.8、8.7Hz),5.60(1H,d,J=4.4Hz),4.84-4.93(1H,m),4.09(2H,s),1.39(3H,d,J=6.6Hz).实施例280 [6-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例112中描述的方法,从[6-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例113)制备标题化合物。m.p.;193-194℃.IR(KBr)ν:3256,1707,1645,1529,1420,1227,1180,1159,1153cm-1.MS(EI)m/z:360(M+).1H-NMR(DMSO-d6)δ:11.84(1H,br s),8.46(1H,d,J=5.3Hz),7.77(1H,d,J=8.7Hz),7.67(1H,t,J=5.1Hz),7.51(1H,d,J=1.8Hz),7.12(1H,dd,J=1.8,8.6Hz),3.74(2H,s),2.76(2H,q,J=7.6Hz),1.25(3H,t,J=7.6Hz).实施例281 [6-氯-2-(2-硝基苯甲酰基)-1H-吲哚-3-基]乙酸 步骤1.连接在聚合物上的反式-4-氯-2-(苯磺酰基氨基)肉桂酸
向王树脂(200-400目,1.37g,大约0.89mmol)和反式-4-氯-2-(苯磺酰基氨基)肉桂酸(600mg,1.77mmol)的混合物中加入二氯甲烷(10ml)和N,N-二异丙基乙胺(1.86ml,10.7mmol)。静置混合物1小时,然后加入4-二甲基氨基吡啶(22mg,0.18mmol)和WSC(339mg,1.77mmol)。搅拌混合物18小时,过滤。残留物用水(20ml×3)、甲醇(20ml×3)、丙酮(20ml×3)、二氯甲烷(20ml×3)洗涤,干燥,得到1.65g标题化合物。步骤2.[6-氯-2-(2-硝基苯甲酰基)-1H-吲哚-3-基]乙酸
向连接在聚合物上的反式-4-氯-2-(苯磺酰基氨基)肉桂酸(步骤1,100mg,53mmol)和2-硝基苯甲酰甲基溴(39mg,0.16mmol)在丙酮(3ml)中的混合物中加入碳酸钾(37mg,0.27mmol)。搅拌混合物18小时,过滤。残留的树脂用水(20ml×3)、丙酮(20ml×3)、二氯甲烷(20ml×3)和THF(20ml×2)洗涤,干燥。用THF(4ml)稀释树脂,然后加入DBU(40μl,0.27mmol)。搅拌16小时后,把树脂过滤出来,用THF(20ml×3)、丙酮(20ml×3)和二氯甲烷(20ml×3)洗涤。向树脂中加入95%三氟乙酸的二氯甲烷(5ml)溶液,搅拌混合物3小时。过滤混合物,残留物用二氯甲烷(20ml×5)洗涤。浓缩滤液,残留物通过HPLC纯化(MeOH/AcONH4水溶液=60/40-90/10),得到3.2mg(17%)的标题化合物。MS(ESI)m/z:359(MH+)。实施例282 [6-氯-2-(2,4-二甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸
按照实施例281中所述的方法,从4-氯-2-(苯磺酰基氨基)肉桂酸制备标题化合物。MS(ESI)m/z:374(MH+)。实施例283 [6-氯-2-(4-二氟代甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸
按照实施例289中所述的方法,从4-氯-2-(苯磺酰基氨基)肉桂酸制备标题化合物。MS(ESI)m/z:380(MH+)。实施例284 [6-氯-2-(2,5-二甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸
按照实施例281中所述的方法,从4-氯-2-(苯磺酰基氨基)肉桂酸制备标题化合物。MS(ESI)m/z:374(MH+)。实施例285 [5-乙酰基-2-(4-氯代苯甲酰基)-1H-吲哚-3-基]乙酸甲酯 步骤1.4-乙酰基-2-溴代苯胺
在0℃和搅拌下,向4-乙酰胺基-3-溴代苯乙酮的乙醇(12ml)悬浮液中滴加盐酸(3ml)。搅拌回流反应混合物4.5小时,冷却并浓缩混合物。残留的固体在饱和的碳酸氢钠水溶液(50ml)和乙醚(50ml)之间分配。水层用乙酸乙酯(50ml×2)萃取。干燥(硫酸镁)合并后的有机层并且浓缩,得到1.79g(定量的)棕色油状的标题化合物。1H-NMR(CDCl3)δ:8.06(1H,d,1.97Hz),7.76-7.72(1H,m),6.74(1H,d,8.40Hz),4.60(1H,br s),2.50(s,3H)步骤2.反式-(5-乙酰基-2-氨基)肉桂酸甲酯
按照实施例133的步骤1中描述的方法,从4-乙酰基-2-溴代苯胺(步骤1)和丙烯酸甲酯制备标题化合物。1H-NMR(CDCl3)δ:8.02(1H,d,2.13Hz),7.81-7.75(2H,m),6.70(1H,d,8.56Hz),6.44(1H,d,15.8Hz),4.55(2H,br s),3.81(3H,s),2.53(3H,s).步骤3.反式-5-乙酰基-2-(对甲苯磺酰基氨基)肉桂酸甲酯
按照实施例8方法A的步骤1中描述的方法,从反式-(5-乙酰基-2-氨基)肉桂酸甲酯(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:8.01(1H,d,2.00Hz),7.89(1H,dd,8.59Hz,1.97Hz),7.68-7.22(7H,m),6.30(1H,s),6.15(1H,d,15.8Hz),3.81(3H,s),2.57(3H,s),2.38(3H,s).步骤4.[5-乙酰基-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-5-乙酰基-2-(对甲苯磺酰基氨基)肉桂酸甲酯(步骤3)和4-氯苯甲酰甲基溴制备标题化合物。1H-NMR(CDCl3)δ:9.2(1H,br s),8.34-7.75(4H,m),7.52-7.45(3H,m),3.89(2H,s),3.69(3H,s),2.68(3H,s).实施例286 [5-乙酰基-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸
按照实施例9的方法B中描述的方法,从[5-乙酰基-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸甲酯(实施例285)制备标题化合物。m.p.:225℃.IR(KBr)ν:3281,1703,1666,1643,1614,1574,1539,1452,1425,1402,1364,1263,1240,1178,1092,1011,959cm-1 1H-NMR(DMSO-d6)δ:12.01(1H,br s),8.49(1H,br s),7.93-7.89(1H,m),7.78(2H,d,8.56Hz),7.65(d,2H,8.56Hz),7.52(1H,d,8.72Hz),3.93(2H,s),2.63(3H,s).实施例287 [6-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯 步骤1.反式-(4-氟-2-硝基)肉桂酸甲酯
按照实施例133的步骤1中描述的方法,从3-氟-6-碘硝基苯和丙烯酸甲酯制备标题化合物。1H-NMR(CDCl3)δ:8.67(1H,d,15.8Hz),7.78(1H,dd,8.07Hz,2.65Hz),7.68-7.63(2H,m),6.34(1H,d,15.8Hz),3.84(3H,s).步骤2.反式-(2-氨基-4-氟)肉桂酸甲酯
按照实施例36的步骤2中描述的方法,从反式-(4-氟-2-硝基)肉桂酸甲酯(步骤1)制备标题化合物。1H-NMR(CDCl3)δ:7.75(1H,d,15.8Hz),7.37-7.31(1H,m),6.50-6.37(2H,m),6.32-6.26(1H,m),4.13(2H,br s),3.80(3H,s).步骤3.反式-4-氟-2-(对甲苯磺酰基氨基)肉桂酸甲酯
按照实施例8方法A的步骤1中描述的方法,从反式-(2-氨基-4-氟)肉桂酸甲酯(步骤2)制备标题化合物。1H-NMR(CDCl3)δ:7.64(1H,d,8.40Hz),7.46-7.19(4H,m),6.94-6.87(1H,m),6.77(1H,s),6.16-6.10(1H,m),3.79(3H,s),2.38(3H,s).步骤4.[6-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-4-氟-2-(对甲苯磺酰基氨基)肉桂酸甲酯(步骤3)制备标题化合物。1H-NMR(CDCl3)δ:12.49(1H,br s),8.61(1H,d,4.94Hz),8.17-7.61(2H,m),7.36-7.14(2H,m),6.98-6.90(1H,m),4.31(2H,s),3.73(3H,s),2.47(3H,s).实施例288 [6-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸
按照实施例9的方法B中描述的方法,从[6-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯(实施例287)制备标题化合物。m.p.:208℃.IR(KBr)ν:3238,1701,1638,1597,1533,1398,1281,1211,1132,1003cm-1.1H-NMR(CDCl3)δ:12.28(1H,br s),8.70(1H,d,4.94Hz),7.96(1H,s),7.83-7.77(1H,m),7.57(1H,d,4.94Hz),7.42(1H,dd,10.2Hz,2.13Hz),7.03-6.95(1H,m),4.09(2H,s),2.47(3H,s).实施例289 [6-氟-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸甲酯
按照实施例57中描述的方法,从反式-4-氟-3-(对甲苯磺酰基氨基)肉桂酸甲酯(实施例287的步骤3)和4-氯苯甲酰甲基溴制备标题化合物。1H-NMR(CDCl3)δ:9.10(1H,br s),7.76-7.71(2H,m),7.60-7.54(2H,m),7.50-7.45(2H,m),7.04-6.90(2H,m),3.81(2H,s),3.66(3H,s).实施例290 [6-氟-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸
按照实施例9的方法B中描述的方法,从[6-氟-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸甲酯(实施例289)制备标题化合物。m.p.:214℃.IR(KBr)ν:3335,1699,1618,1605,1587,1531,1425,1327,1267,1231,1134,1094,1001cm-1.1H-NMR(DMSO-d6)δ:11.73(1H,br s),7.78-7.63(5H,m),7.17(1H,dd,9.72Hz,2.13Hz),7.04-6.96(1H,m),3.84(2H,s).实施例291 [2-(4-甲基吡啶-2-羰基)-5-甲硫基-1H-吲哚-3-基]乙酸 步骤1.反式-(2-氨基-5-甲硫基)肉桂酸甲酯
按照实施例133的步骤1中描述的方法,从2-溴-4-甲硫基氧苯胺(JP80-122756)和丙烯酸甲酯制备标题化合物。1H-NMR(CDCl3)δ:7.77(1H,d,15.8Hz),7.38(1H,d,2.13Hz),7.19(1H,dd,8.40Hz,2.13Hz),6.66(1H,d,8.40Hz),6.36(1H,d,15.8Hz),3.97(1H,br s),3.80(3H,s),2.43(3H,s).步骤2.反式-2-对甲苯磺酰基氨基-5-甲硫基肉桂酸甲酯
按照实施例8的步骤1中描述的方法,从反式-(2-氨基-4-甲硫基)肉桂酸甲酯(步骤1)和对甲苯磺酰氯制备标题化合物。1H-NMR(CDCl3)δ:7.81(2H,d,8.40Hz),7.56-6.91(8H,m),6.13(1H,d,156Hz),3.79(3H,s),2.46(3H,s),2.39(3H,s).步骤3.反式-[2-(4-甲基吡啶-2-羰基)-5-甲硫基-1H-吲哚-3-基]乙酸 甲酯
按照实施例57中描述的方法,从反式-2-对甲苯磺酰基氨基-5-甲硫基肉桂酸甲酯(步骤2)和2-溴代乙酰基-4-甲基吡啶氢溴酸盐(其制备方法见实施例31的步骤2)制备标题化合物。1H-NMR(CDCl3)δ:12.47(1H,br s),8.62(1H,d,4.78Hz),8.19-8.17(1H,m),7.65-7.62(1H,m),7.47-7.30(3H,m),4.31(2H,s),3.73(3H,s),2.48(3H,s).实施例292 [2-(4-甲基吡啶-2-羰基)-5-甲硫基-1H-吲哚-3-基]乙酸
按照实施例9的方法B中描述的方法,从[2-(4-甲基吡啶-2-羰基)-5-甲硫基-1H-吲哚-3-基]乙酸甲酯(实施例)制备标题化合物。1H-NMR(DMSO-d6)δ:12.22(1H,br s),8.70(1H,d,4.62Hz),7.95-7.17(4H,m),4.08(2H,s),2.47(3H,s),2.35(3H,s).MS(EI)m/z:340(M+).实施例293 3-[4-氯-2-(甲苯-4-磺酰氨基)-苯基]-丙烯酸乙酯
向3-(2-氨基-4-氯-苯基)丙烯酸乙酯(18.0g,79.8mmol)的二氯甲烷(144ml)溶液中加入吡啶(9.04ml,112mmol)和对甲苯磺酰氯(16.0g,83.9mmol)。在室温下搅拌反应混合物18小时,然后把混合物倒入1N盐酸(150ml)中。分层,有机层通过硫酸镁干燥,过滤,浓缩。所得的固体在己烷中制成浆液,过滤,得到3-[4-氯-2-(甲苯-4-磺酰胺基)-苯基]-丙烯酸乙酯(28.3g,93%)。mp=124-127℃.1H NMR(300MHz,CDCl3)d 1.35(t,3,J=7.2),2.40(s,3),4.27(q,2,J=7.2),6.12(dd,1,J=15.9,0.9),7.20-7.39(m,4),7.39(d,1,J=8.6),7.48-7.53(m,2),7.62(d,2,J=8.3).13C NMR(75MHz,CDCl3)d 15.50,22.79,62.24,122.48.127.98,128.49,129.34,129.50,131.05,136.82,137.00,137.73,138.93,145.55,167.59.IR 3214,1694,1631,1318,1167cm-1.C18H18ClNO4S的分析:
计算值:C,56.91;H,4.78;N,3.69
测定值:C,57.10;H,5.08;N,3.70实施例294 [6-氯-2-(4-氯-苯甲酰基)-1H-吲哚-3-基]乙酸
向3-[4-氯-2-(甲苯-4-磺酰胺基)-苯基]-丙烯酸乙酯(13.0g,34.2mmol)的N,N-二甲基乙酰胺(120ml)溶液中加入碳酸钾(9.45g,68.4mmol)和2-溴-4’-氯苯乙酮(8.78g,37.6mmol),在室温下搅拌反应混合物15分钟。加入1N氢氧化钠(130ml),在100℃加热反应混合物8小时。把反应混合物冷却到室温,倒入分液漏斗中,用甲基叔丁基醚(2×200ml)洗涤。用6N盐酸把水层酸化到pH1,用乙酸乙酯(150ml)萃取。在减压下除去溶剂,向所得的油状物中加入异丙醇(24ml)和水(48ml)。搅拌沉淀出的固体和浆液12小时。过滤出沉淀,用水洗涤,干燥,得到[6-氯-2-(4-氯-苯甲酰基)-1H-吲哚-3-基]乙酸(9.73g,82%)。mp 181-183℃.1H NMR(400MHz,d6-DMSO)d 3.79(s,2),7.08(dd,1,J=8.5,1.9),7.42(d,1,J=1.9),7.60(d,2,J=8.5),7.62-7.73(m,3),11.74(bs,1),12.22(bs,1).13C NMR(75 MHz,d6-DMSO)d 31.74,113.25,118.00,121.93,123.96,127.69,130.10,131.30,132.02,133.59,138.02,138.37,138.58,173.20,188.29.IR 3314,1710,1700,1618,1522,1323,1227,1093,941cm-1.C17H11Cl2NO3的分析:
计算值:C,58.64;H,3.18;N,4.02
测定值:C,58.58;H,3.22;N,3.93实施例295 3-{4-氯-2-[[2-(4-氯-苯基)-2-氧代-乙基]-(甲苯-4-磺酰基)-氨基]- 苯基}-丙烯酸乙酯
向3-[4-氯-2-(甲苯-4-磺酰胺基)-苯基]-丙烯酸乙酯(3.00g,7.90mmol)的N,N-二甲基乙酰胺(15.0ml)溶液中加入碳酸钾(2.18g,15.8mmol)和2-溴-4’-氯苯乙酮(2.03g,8.69mmol),搅拌反应混合物30分钟。倒入1N盐酸(30ml)中,用甲基叔丁基醚(2×30ml)萃取。有机萃取液通过硫酸镁干燥,过滤,浓缩到很小的体积。加入己烷,沉淀出固体。过滤出沉淀,得到3-{4-氯-2-[[2-(4-氯-苯基)-2-氧代-乙基]-(甲苯-4-磺酰基)-氨基]-苯基}-丙烯酸乙酯(3.19g,76%)。mp=162-165℃.1H NMR(300MHz,CDCl3)d 1.38(t,3,J=7.2),2.47(s,3),4.28(q,2,J=7.2),5.00(bs,2),6.23(d,1,J=16.0),7.29-7.36(m,4),7.47(d,2,J=8.7),7.54(d,1,J-8.4),7.59(d,2,J=8.3),7.74(d,1,J=16.0),7.88(d,2,J=8.7).13C NMR(75MHz,CDCl3)d 14.33,21.62,57.72,60.66,112.49,120.69,128.07,129.21,129.58,129.70,131.22,132.80,133.83,134.80,135.84,138.55,139.28,140.38,144.46,166.02,191.70.IR 1720,1698,1590,1338,1313,1179,1161,1089cm-1.C26H23Cl2NO5S的分析:
计算值:C,58.65;H,4.35;N,2.63
测定值:C,58.74;H,4.56;N,2.72实施例296 顺式-和反式-[6-氯-2-(4-氯-苯甲酰基)-1-(甲苯-4-磺酰基)-2,3-二氢 -1H-吲哚-3-基]乙酸乙酯
向3-{4-氯-2-[[2-(4-氯-苯基)-2-氧代-乙基]-(甲苯-4-磺酰基)-氨基]-苯基}-丙烯酸乙酯(1.00g,1.88mmol)的N,N-二甲基乙酰胺(5.0ml)溶液中加入碳酸钾(0.520g,3.76mmol),搅拌反应混合物4小时。倒入1N盐酸(30ml)中,用甲基叔丁基醚(2×30ml)萃取。有机萃取液通过硫酸镁干燥,过滤,浓缩。所得的固体通过硅胶色谱(乙酸乙酯/己烷20/80)纯化,得到顺式-和反式-[6-氯-2-(4-氯-苯甲酰基)-1-(甲苯-4-磺酰基)-2,3-二氢-1H-吲哚-3-基]乙酸乙酯异构体的1-9混合物(0.488g,49%)。一些重要的1NMR(300MHz,CDCl3)信号为:d 1.0)9(t,J=7.2),1.19(t,J=7.2),2.44(s),5.40(d,J=4.0),5.99(d,J=9.7),6.92(dd,J=8.1,1.1),7.04(dd,J=8.1,1.9),7.52(d,J=8.4),7.57(d,J=1.9),7.73(d,J=8.3),7.99(d,J=8.6).对非对映异构体混合物进行的Lc-MS分析表明,这些产物具有相同的质量531(M+H+)。实施例297 [6-氯-2-(4-氯-苯甲酰基)-1H-吲哚-3-基]乙酸乙酯
向3-[4-氯-2-(甲苯-4-磺酰胺基)-苯基]-丙烯酸乙酯(3.00g,7.90mmol)的N,N-二甲基乙酰胺(15.0ml)溶液中加入碳酸钾(2.18g,15.8mmol)和2-溴-4’-氯苯乙酮(2.03g,8.69mmol),搅拌反应混合物30分钟。加入1,8-二氮杂双环[5.4.0]十一碳-7-烯(3.54ml,23.7mmol),搅拌反应混合物1小时,倒入1N盐酸(30ml)中,用甲基叔丁基醚(2×30ml)萃取。有机萃取液用硫酸镁干燥,过滤,浓缩,得到一固体。把该固体在甲基叔丁基醚和己烷的混合物中制成浆液,得到[6-氯-2-(4-氯-苯甲酰基)-1H-吲哚-3-基]乙酸乙酯(2.42g,81%)。mp=186-188℃.1H NMR(300MHz,CDCl3)d 1.27(t,2,J=7.1),3.80(s,2),4.11(q,2,J=7.1),7.15(ddd,1,J=8.5,1.7,0.5),7.28-7.30(m,1),7.48(d,J=8.3),7.54-7.57(m,1),7.77(d,2,J=8.3),9.16(bs,1).13C NMR(75MHz,CDCl3)d 15.42,32.29,62.45,113.27,117.60,122.99,123.23,127.85,130.12,131.77,133.61,137.86,138.13,140.10,172.45,188.25.IR 3305,1732,1618,1323cm-1.C19H15Cl2NO3的分析:
计算值:C,60.65;H,4.02;N,3.72
测定值:C,60.70;H,3.97;N,3.71实施例298 [6-氯-2-(4-氯-苯甲酰基)-1H-吲哚-3-基]乙酸
向[6-氯-2-(4-氯-苯甲酰基)-1H-吲哚-3-基]乙酸乙酯(200mg,0.532mmol)的甲醇(2ml)和水(0.8ml)溶液中加入氢氧化钠(137mg,3.43mmol)。搅拌反应混合物24小时,浓缩到很小的体积。加入水(4ml),把混合物转移到分液漏斗中,用二氯甲烷(5ml)洗涤。用1N盐酸把水层酸化到pH1,用乙酸乙酯(15ml)萃取。有机层通过硫酸镁干燥,过滤,浓缩,得到[6-氯-2-(4-氯-苯甲酰基)-1H-吲哚-3-基]乙酸乙酯(150mg,81%)。1NMR光谱与按照实施例2中所述方法得到的化合物相同。
实施例1-292中制备的化合物的化学结构概括在下表中。
表
| 实施例序号 | (X)n | R1 | Z | Q |
| 1 | 6-Cl | H | 乙氧基 | 苯基 |
| 2 | 6-Cl | H | OH | 苯基 |
| 3 | 6-Cl | H | ONa | 苯基 |
| 4 | 6-Cl | H | OH | 2-甲基苯基 |
| 5 | 6-Cl | H | OH | 3-甲基苯基 |
| 6 | 6-Cl | H | OH | 4-甲基苯基 |
| 7 | 6-Cl | H | OH | 3-氯苯基 |
| 8 | 6-Cl | H | 甲氧基 | 4-氯苯基 |
| 9 | 6-Cl | H | OH | 4-氯苯基 |
| 10 | 6-Cl | H | OH | 3-氟苯基 |
| 11 | 6-Cl | H | OH | 4-氟苯基 |
| 12 | 6-Cl | H | OH | 3-溴苯基 |
| 13 | 6-Cl | H | OH | 4-溴苯基 |
| 14 | 6-Cl | H | OH | 3-CF3-苯基 |
| 15 | 6-Cl | H | OH | 4-CF3-苯基 |
| 16 | 6-Cl | H | OH | 3,4-二氯苯基 |
| 17 | 4-Cl | H | OH | 苯基 |
| 18 | 5-Cl | H | OH | 3-甲基苯基 |
| 19 | 5-Cl | H | OH | 4-氯苯基 |
| 20 | 5-Cl | H | OH | 3-氯苯基 |
| 21 | 5-F | H | OH | 4-氯苯基 |
| 22 | 5-F | H | OH | 3-氯苯基 |
| 23 | 5-甲氧基 | H | OH | 3-甲基苯基 |
| 24 | 7-Cl | H | OH | 苯基 |
| 25 | 4,5-二氯 | H | OH | 苯基 |
| 26 | 4,6-二氯 | H | OH | 苯基 |
| 27 | 5,6-二氯 | H | OH | 苯基 |
| 28(外消旋的) | 6-Cl | 甲基 | OH | 苯基 |
| 29(极性较小的对映体) | 6-Cl | 甲基 | OH | 苯基 |
| 30(极性较大的对映体) | 6-Cl | 甲基 | OH | 苯基 |
| 31 | 6-Cl | H | OH | 4-甲基-2-吡啶基 |
| 32 | 6-Cl | H | OH | 5-甲基-2-吡啶基 |
| 33 | 6-Cl | H | 甲氧基 | 4-氯-2-吡啶基 |
| 34 | 6-Cl | H | OH | 4-氯-2-吡啶基 |
| 35 | 6-Cl | H | OH | 2-吡啶基 |
| 36 | 5-Cl | H | OH | 4-甲基-2-吡啶基 |
| 37 | 5-Cl | H | 甲氧基 | 6-甲基-2-吡啶基 |
| 38 | 5-Cl | H | OH | 6-甲基-2-吡啶基 |
| 39 | 6-Cl | H | OH | 1-甲基-2-咪唑基 |
| 40 | 5-Cl | H | 甲氧基 | 2-噻唑基 |
| 41 | 5-Cl | H | OH | 2-噻唑基 |
| 42 | 6-Cl | H | 甲氧基 | 苯基 |
| 43 | 6-Cl | H | 二甲基氨基 | 苯基 |
| 44 | 6-Cl | H | 甲胺基 | 苯基 |
| 45 | 6-Cl | H | 氨基 | 苯基 |
| 46 | 6-Cl | H | N-甲氧基-N-甲基氨基 | 苯基 |
| 47 | 6-Cl | H | 哌啶子基 | 苯基 |
| 48 | 6-Cl | H | 4-甲基-1-哌嗪基 | 苯基 |
| 49 | 6-Cl | H | 2-氰基乙氨基 | 苯基 |
| 50 | 6-Cl | H | 2-HO-乙氨基 | 苯基 |
| 51 | 6-Cl | H | 吗啉代 | 苯基 |
| 52 | H | H | OH | 4-氯苯基 |
| 53 | 6-Cl | H | OH | 2-呋喃基 |
| 54 | 6-Cl | H | OH | 环己基 |
| 55 | 6-Cl | H | OH | 4-甲氧基苯基 |
| 56 | 6-Cl | H | 甲氧基 | 4-甲氧基苯基 |
| 57 | 6-Cl | H | 甲氧基 | 4-乙基-2-吡啶基 |
| 58 | 6-Cl | H | OH | 4-乙基-2-吡啶基 |
| 59 | 5-Cl | H | 甲氧基 | 4-乙基-2-吡啶基 |
| 60 | 5-Cl | H | OH | 4-乙基-2-吡啶基 |
| 61 | 6-Cl | H | 甲氧基 | 4-异丙基-2-吡啶基 |
| 62 | 6-Cl | H | OH | 4-异丙基-2-吡啶基 |
| 63 | 5-Cl | H | 甲氧基 | 4-异丙基-2-吡啶基 |
| 64 | 5-Cl | H | OH | 4-异丙基-2-吡啶基 |
| 65 | 6-Cl | H | 甲氧基 | 4-正丙基-2-吡啶基 |
| 66 | 6-Cl | H | OH | 4-正丙基-2-吡啶基 |
| 67 | 5-Cl | H | 甲氧基 | 4-正丙基-2-比啶基 |
| 68 | 5-Cl | H | OH | 4-正丙基-2-吡啶基 |
| 69 | 6-Cl | H | 甲氧基 | 4-叔丁基-2-吡啶基 |
| 70 | 6-Cl | H | OH | 4-叔丁基-2-吡啶基 |
| 71 | 5-Cl | H | 甲氧基 | 4-叔丁基-2-吡啶基 |
| 72 | 5-Cl | H | OH | 4-叔丁基-2-吡啶基 |
| 73 | 6-Cl | H | 甲氧基 | 3-甲基-2-吡啶基 |
| 74 | 6-Cl | H | OH | 3-甲基-2-吡啶基 |
| 75 | 5-Cl | H | 甲氧基 | 3-甲基-2-吡啶基 |
| 76 | 5-Cl | H | OH | 3-甲基-2-吡啶基 |
| 77 | 6-Cl | H | 甲氧基 | 6-甲基-2-吡啶基 |
| 78 | 6-Cl | H | OH | 6-甲基-2-吡啶基 |
| 79 | 5-Cl | H | 甲氧基 | 5-甲基-2-吡啶基 |
| 80 | 5-Cl | H | OH | 5-甲基-2-吡啶基 |
| 81 | 6-Cl | H | 甲氧基 | 5-三氟甲基-2-吡啶基 |
| 82 | 6-Cl | H | OH | 5-三氟甲基-2-吡啶基 |
| 83 | 5-Cl | H | 甲氧基 | 5-三氟甲基-2-吡啶基 |
| 84 | 5-Cl | H | OH | 5-三氟甲基-2-吡啶基 |
| 85 | 5-Cl | H | 甲氧基 | 5-氯-2-吡啶基 |
| 86 | 5-Cl | H | OH | 5-氯-2-吡啶基 |
| 87 | 6-Cl | H | 甲氧基 | 5-氯-2-吡啶基 |
| 88 | 6-Cl | H | OH | 5-氯-2-吡啶基 |
| 89 | 5-Cl | H | 甲氧基 | 4-氯-2-吡啶基 |
| 90 | 5-Cl | H | OH | 4-氯-2-吡啶基 |
| 91 | 6-Cl | H | 甲氧基 | 3-吡啶基 |
| 92 | 6-Cl | H | OH | 3-吡啶基 |
| 93 | 6-Cl | H | 甲氧基 | 4-吡啶基 |
| 94 | 6-Cl | H | OH | 4-吡啶基 |
| 95 | 6-Cl | H | 甲氧基 | 4-羟甲基-2-吡啶基 |
| 96 | 6-Cl | H | OH | 4-羟甲基-2-吡啶基 |
| 97 | 5-Cl | H | 甲氧基 | 4-羟甲基-2-吡啶基 |
| 98 | 5-Cl | H | OH | 4-羟甲基-2-吡啶基 |
| 99 | 5-Cl | H | 甲氧基 | 3,4-二甲基-2-吡啶基 |
| 100 | 5-Cl | H | OH | 3,4-二甲基-2-吡啶基 |
| 101 | 5-Cl | H | 甲氧基 | 4,5-二甲基-2-吡啶基 |
| 102 | 5-Cl | H | OH | 4,5-二甲基-2-吡啶基 |
| 103 | 6-Cl | H | 甲氧基 | 4,5-二甲基-2-吡啶基 |
| 104 | 6-Cl | H | OH | 4,5-二甲基-2-吡啶基 |
| 105 | 6-Cl | H | 甲氧基 | 4-甲氧基-2-吡啶基 |
| 106 | 6-Cl | H | OH | 4-甲氧基-2-吡啶基 |
| 107 | 5-Cl | H | 甲氧基 | 4-甲氧基-2-吡啶基 |
| 108 | 5-Cl | H | OH | 4-甲氧基-2-吡啶基 |
| 109 | 6-Cl | H | 甲氧基 | 3,5-二甲基-2-吡啶基 |
| 110 | 6-Cl | H | OH | 3,5-二甲基-2-吡啶基 |
| 111 | 5-Cl | H | 甲氧基 | 3-氟-4-乙基-2-吡啶基 |
| 112 | 5-Cl | H | OH | 3-氟-4-乙基-2-吡啶基 |
| 113 | 6-Cl | H | 甲氧基 | 3-氟-4-乙基-2-吡啶基 |
| 114 | 6-Cl | H | OH | 3-乙氧基-4-乙基-2-吡啶基 |
| 115 | 6-Cl | H | 甲氧基 | 3-氯-4-乙基-2-吡啶基 |
| 116 | 6-Cl | H | OH | 3-氯-4-乙基-2-吡啶基 |
| 117 | 5-Cl | H | 甲氧基 | 3-氯-4-乙基-2-吡啶基 |
| 118 | 5-Cl | H | OH | 3-氯-4-乙基-2-吡啶基 |
| 119 | 5-Cl | H | 甲氧基 | 4,6-二甲基-2-吡啶基 |
| 120 | 5-Cl | H | OH | 4,6-二甲基-2-吡啶基 |
| 121 | 6-Cl | H | 甲氧基 | 4,6-二甲基-2-吡啶基 |
| 122 | 6-Cl | H | OH | 4,6-二甲基-2-吡啶基 |
| 123 | 5,6-二氯 | H | 甲氧基 | 4-甲基-2-吡啶基 |
| 124 | 5,6-二氯 | H | OH | 4-甲基-2-吡啶基 |
| 125 | 5-甲基 | H | 甲氧基 | 4-甲基-2-吡啶基 |
| 126 | 5-甲基 | H | OH | 4-甲基-2-吡啶基 |
| 127 | 5-F | H | 甲氧基 | 4-甲基-2-吡啶基 |
| 128 | 5-F | H | OH | 4-甲基-2-吡啶基 |
| 129 | 5-甲氧基 | H | 甲氧基 | 4-甲基-2-吡啶基 |
| 130 | 5-甲氧基 | H | OH | 4-甲基-2-吡啶基 |
| 131 | 6-甲氧基 | H | 甲氧基 | 4-甲基-2-吡啶基 |
| 132 | 6-甲氧基 | H | OH | 4-甲基-2-吡啶基 |
| 133 | 5-乙基 | H | 甲氧基 | 4-甲基-2-吡啶基 |
| 134 | 5-乙基 | H | OH | 4-甲基-2-吡啶基 |
| 135 | 5-乙基 | H | 甲氧基 | 4-乙基-2-吡啶基 |
| 136 | 5-乙基 | H | OH | 4-乙基-2-吡啶基 |
| 137 | 6-乙基 | H | 甲氧基 | 4-甲基-2-吡啶基 |
| 138 | 6-乙基 | H | OH | 4-甲基-2-吡啶基 |
| 139 | 5-异丙基 | H | 甲氧基 | 4-乙基-2-吡啶基 |
| 140 | 5-异丙基 | H | OH | 4-甲基-2-吡啶基 |
| 141 | 6-CF3 | H | 甲氧基 | 4-甲基-2-吡啶基 |
| 142 | 6-CF3 | H | OH | 4-甲基-2-吡啶基 |
| 143 | 5-叔丁基 | H | 甲氧基 | 4-甲基-2-吡啶基 |
| 144 | 5-叔丁基 | H | OH | 4-甲基-2-吡啶基 |
| 145 | 5-CF3O | H | 甲氧基 | 4-甲基-2-吡啶基 |
| 146 | 5-CF3O | H | OH | 4-甲基-2-吡啶基 |
| 147 | 5-CF3O | H | 甲氧基 | 4-乙基-2-吡啶基 |
| 148 | 5-CF3O | H | OH | 4-乙基-2-吡啶基 |
| 149 | 6-甲基 | H | 甲氧基 | 4-甲基-2-吡啶基 |
| 150 | 6-甲基 | H | OH | 4-甲基-2-吡啶基 |
| 151 | 5-CF3 | H | 甲氧基 | 4-甲基-2-吡啶基 |
| 152 | 5-CF3 | H | OH | 4-甲基-2-吡啶基 |
| 153 | 5-CF3 | H | 甲氧基 | 4-乙基-2-吡啶基 |
| 154 | 5-CF3 | H | OH | 4-乙基-2-吡啶基 |
| 155 | H | H | 甲氧基 | 苯基 |
| 156 | H | H | OH | 苯基 |
| 157 | 6-甲基 | H | 甲氧基 | 4-氯苯基 |
| 158 | 6-甲基 | H | OH | 4-氯苯基 |
| 159 | 5-甲基 | H | OH | 4-氯苯基 |
| 160 | 6-甲氧基 | H | 甲氧基 | 4-氯苯基 |
| 161 | 6-甲氧基 | H | OH | 4-氯苯基 |
| 162 | 6-CF3 | H | OH | 4-氯苯基 |
| 163 | 5-乙基 | H | 甲氧基 | 4-氯苯基 |
| 164 | 5-乙基 | H | OH | 4-氯苯基 |
| 165 | 5-甲氧基 | H | 甲氧基 | 4-氯苯基 |
| 166 | 5-甲氧基 | H | OH | 4-氯苯基 |
| 167 | 5-异丙基 | H | 甲氧基 | 4-氯苯基 |
| 168 | 5-异丙基 | H | OH | 4-氯苯基 |
| 169 | 5-CF3 | H | 甲氧基 | 4-氯苯基 |
| 170 | 5-CF3 | H | OH | 4-氯苯基 |
| 171 | 5-CF3O | H | 甲氧基 | 4-氯苯基 |
| 172 | 5-CF3O | H | OH | 4-氯苯基 |
| 173 | 6-Cl | H | 甲氧基 | 2-甲氧基苯基 |
| 174 | 6-Cl | H | OH | 2-甲氧基苯基 |
| 175 | 6-Cl | H | 甲氧基 | 3-甲氧基苯基 |
| 176 | 6-Cl | H | OH | 3-甲氧基苯基 |
| 177 | 6-Cl | H | 甲氧基 | 3-苄氧基苯基 |
| 178 | 6-Cl | H | OH | 3-苄氧基苯基 |
| 179 | 6-Cl | H | 甲氧基 | 3-羟基苯基 |
| 180 | 6-Cl | H | OH | 3-羟基苯基 |
| 181 | 6-Cl | H | 甲氧基 | 4-苄氧基苯基 |
| 182 | 6-Cl | H | OH | 4-苄氧基苯基 |
| 183 | 6-Cl | H | 甲氧基 | 4-羟基苯基 |
| 184 | 6-Cl | H | OH | 4-羟基苯基 |
| 185 | 6-Cl | H | 甲氧基 | 4-异丙氧基苯基 |
| 186 | 6-Cl | H | OH | 4-异丙氧基苯基 |
| 187 | 6-Cl | H | 甲氧基 | 4-联苯基 |
| 188 | 6-Cl | H | OH | 4-联苯基 |
| 189 | 6-Cl | H | 甲氧基 | 4-CF3O-苯基 |
| 190 | 6-Cl | H | OH | 4-CF3O-苯基 |
| 191 | 5-Cl | H | 甲氧基 | 4-CF3O-苯基 |
| 192 | 5-Cl | H | OH | 4-CF3O-苯基 |
| 193 | 5-Cl | H | 甲氧基 | 4-甲氧基苯基 |
| 194 | 5-Cl | H | OH | 4-甲氧基苯基 |
| 195 | 6-Cl | H | 甲氧基 | 4-硝基苯基 |
| 196 | 6-Cl | H | OH | 4-硝基苯基 |
| 197 | 6-Cl | H | 甲氧基 | 4-甲基-S(O)2-苯基 |
| 198 | 6-Cl | H | OH | 4-甲基-S(O)2-苯基 |
| 199 | 6-Cl | H | 甲氧基 | 4-甲基-S(O)2-NH-苯基 |
| 200 | 6-Cl | H | OH | 4-甲基-S(O)2-NH-苯基 |
| 201 | 6-Cl | H | OH | 2-氯苯基 |
| 202 | 6-Cl | H | OH | 2,4-二氯苯基 |
| 203 | 6-Cl | H | 甲氧基 | 3-氟-4-氯苯基 |
| 204 | 6-Cl | H | OH | 3-氟-4-氯苯基 |
| 205 | 6-Cl | H | 甲氧基 | 4-氰基苯基 |
| 206 | 6-Cl | H | 甲氧基 | 4-溴苯基 |
| 207 | 6-Cl | H | 甲氧基 | 4-(2-噻吩基)苯基 |
| 208 | 6-Cl | H | OH | 4-(2-噻吩基)苯基 |
| 209 | 6-Cl | H | 甲氧基 | 4-(2-呋喃基)苯基 |
| 210 | 6-Cl | H | OH | 4-(2-呋喃基)苯基 |
| 211 | 6-Cl | H | 甲氧基 | 4-(3-吡啶基)苯基 |
| 212 | 6-Cl | H | OH | 4-(3-吡啶基)苯基 |
| 213 | 6-Cl | H | 甲氧基 | 4-(2-噻唑基)苯基 |
| 214 | 6-Cl | H | OH | 4-(2-噻唑基)苯基 |
| 215 | 6-Cl | H | 甲氧基 | 3-溴苯基 |
| 216 | 6-Cl | H | 甲氧基 | 3-(2-呋喃基)苯基 |
| 217 | 6-Cl | H | OH | 3-(2-呋喃基)苯基 |
| 218 | 6-Cl | 甲基 | 甲氧基 | 4-氯苯基 |
| 219 | 6-Cl | 甲基 | OH | 4-氯苯基 |
| 220 | 5-Cl | H | 甲氧基 | 异喹啉-3-基 |
| 221 | 5-Cl | H | OH | 异喹啉-3-基 |
| 222 | 6-Cl | H | 甲氧基 | 异喹啉-3-基 |
| 223 | 6-Cl | H | OH | 异喹啉-3-基 |
| 224 | 5-Cl | H | 甲氧基 | 5-甲基-3-异噁唑基 |
| 225 | 5-Cl | H | OH | 5-甲基-3-异噁唑基 |
| 226 | 6-Cl | H | 甲氧基 | 5-甲基-3-异噁唑基 |
| 227 | 6-Cl | H | OH | 5-甲基-3-异噁唑基 |
| 228 | 5-Cl | H | 甲氧基 | 4-甲基-5-(1,2,3-噻二唑基) |
| 229 | 5-Cl | H | OH | 4-甲基-5-(1,2,3-噻二唑基) |
| 230 | 6-Cl | H | 甲氧基 | 4-甲基-5-(1,2,3-噻二唑基) |
| 231 | 6-Cl | H | OH | 4-甲基-5-(1,2,3-噻二唑基) |
| 232 | 5-Cl | H | 甲氧基 | 5-甲基-2-噻唑基 |
| 233 | 5-Cl | H | OH | 5-甲基-2-噻唑基 |
| 234 | 6-Cl | H | 甲氧基 | 5-甲基-2-噻唑基 |
| 235 | 6-Cl | H | OH | 5-甲基-2-噻唑基 |
| 236 | 6-Cl | H | OH | 2-噻吩基 |
| 237 | 6-Cl | H | 甲氧基 | 3-(HO)(CH3)2C-2-呋喃基 |
| 238 | 6-Cl | H | OH | 3-(HO)(CH3)2C-2-呋喃基 |
| 239 | 6-Cl | H | 甲氧基 | 3-甲氧基甲基-2-呋喃基 |
| 240 | 6-Cl | H | OH | 3-甲氧基甲基-2-呋喃基 |
| 241 | 6-Cl | H | OH | 1-甲基-2-咪唑基 |
| 242 | 6-Cl | H | 甲氧基 | 1-甲基-2-咪唑基 |
| 243 | 5-Cl | H | 甲氧基 | 1-甲基-2-咪唑基 |
| 244 | 5-Cl | H | OH | 1-甲基-2-咪唑基 |
| 245 | 5-Cl | H | 甲氧基 | 2-咪唑基 |
| 246 | 5-Cl | H | OH | 2-咪唑基 |
| 247 | 6-Cl | H | 甲氧基 | 2-咪唑基 |
| 248 | 6-Cl | H | OH | 2-咪唑基 |
| 249 | 5-Cl | H | 甲氧基 | 4-甲基-2-噻唑基 |
| 250 | 5-Cl | H | OH | 4-甲基-2-噻唑基 |
| 251 | 5-Cl | H | 甲氧基 | 1-甲基-2-吡咯基 |
| 252 | 5-Cl | H | OH | 1-甲基-2-吡咯基 |
| 253 | 5-Cl | H | 甲氧基 | 2-甲基-4-噻唑基 |
| 254 | 5-Cl | H | OH | 2-甲基-4-噻唑基 |
| 255 | 5-Cl | H | 甲氧基 | 5-噻唑基 |
| 256 | 5-Cl | H | OH | 5-噻唑基 |
| 257 | 6-Cl | H | 甲氧基 | 4-甲基-2-噻唑基 |
| 258 | 6-Cl | H | OH | 4-甲基-2-噻唑基 |
| 259 | 5-Cl | H | 甲氧基 | 3-羧基-5-异噁唑基 |
| 260 | 5-Cl | H | OH | 3-羧基-5-异噁唑基 |
| 261 | 6-Cl | H | 甲氧基 | 环丙基 |
| 262 | 6-Cl | H | OH | 环丙基 |
| 263 | 6-Cl | H | 甲氧基 | 环丁基 |
| 264 | 6-Cl | H | OH | 环丁基 |
| 265 | 5-叔丁基 | H | 甲氧基 | 4-氯苯基 |
| 266 | 5-叔丁基 | H | OH | 4-氯苯基 |
| 267 | 6-Cl | H | 二甲基氨基 | 4-甲基-2-吡啶基 |
| 268 | 6-Cl | H | 甲氨基 | 4-甲基-2-吡啶基 |
| 269 | 5-Cl | H | HO-(CH2)2-NH- | 4-甲基-2-吡啶基 |
| 270 | 5-Cl | H | 甲氧基氨基 | 4-甲基-2-吡啶基 |
| 271 | 5-Cl | H | 1-哌嗪基 | 4-甲基-2-吡啶基 |
| 272 | 5-Cl | H | H2N-(CH2)2-NH- | 4-甲基-2-吡啶基 |
| 273 | 5-Cl | H | 3-氨基-1-吡咯烷基 | 4-甲基-2-吡啶基 |
| 274 | 5-F,6-Cl | H | 甲氧基 | 4-氯苯基 |
| 275 | 5-F,6-Cl | H | OH | 4-氯苯基 |
| 276 | 5-F,6-Cl | H | 甲氧基 | 4-甲基-2-吡啶基 |
| 277 | 5-F,6-Cl | H | OH | 4-甲基-2-吡啶基 |
| 278 | 6-Cl | H | 甲氧基 | 4-(HO)(H3C)CH-2-吡啶基 |
| 279 | 6-Cl | H | OH | 4-(HO)(H3C)CH-2-吡啶基 |
| 280 | 6-Cl | H | OH | 4-乙基-3-氟-2-吡啶基 |
| 281 | 6-Cl | H | OH | 2-硝基苯基 |
| 282 | 6-Cl | H | OH | 2,4-二甲氧基苯基 |
| 283 | 6-Cl | H | OH | 4-CHF2O-苯基 |
| 284 | 6-Cl | H | OH | 2,5-二甲氧基苯基 |
| 285 | 5-乙酰基 | H | 甲氧基 | 4-氯苯基 |
| 286 | 5-乙酰基 | H | OH | 4-氯苯基 |
| 287 | 6-F | H | 甲氧基 | 4-甲基-2-苯基 |
| 288 | 6-F | H | OH | 4-甲基-2-苯基 |
| 289 | 6-F | H | 甲氧基 | 4-氯苯基 |
| 290 | 6-F | H | OH | 4-氯苯基 |
| 291 | 5-甲硫基 | H | 甲氧基 | 4-甲基-2-苯基 |
| 292 | 5-甲硫基 | H | OH | 4-甲基-2-苯基 |
Claims (81)
1.一种下式的化合物:或其药学上可接受的盐,其中Z为OH、C1-6烷氧基、-NR2R3或一种式(II)或(III)的基团:其中r为1、2、3或4,Y是一条直接键、O、S或NR4,而W是OH或-NR2R3;Q选自下列基团:
(a)任选地被1、2或3个独立地选自下列基团的取代基取代的苯基:
(a-1)卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基,
(a-2)芳基或-O-(CH2)n-芳基,且该芳基或芳基部分任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代,
(a-3)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的5-员单环芳基,
(a-4)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的6-员单环芳基,
(b)含有1、2、3或4个N的6-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述基团(a-1)、(a-2)、(a-3)或(a-4)的取代基取代;
(c)含有一个选自O、S和N的杂原子并且除所说的杂原子外还任选地含有1、2或3个N的5-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(d)任选地被1或2个独立地选自OH、C1-4烷基、卤素和卤素取代的C1-4烷基的取代基取代的C3-7环烷基;和
(e)任选地被1、2或3个独立地选自上述(a-1)的基团的取代基取代的苯并稠合的杂环;R1为H、C1-4烷基或卤素;R2和R3独立地为H、OH、C1-4烷氧基、C1-4烷基或者是被卤素、OH、C1-4烷氧基、NH2或CN取代的C1-4烷基;R4为H或C1-4烷基;X独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-C4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基;而n为0、1、2、3或4。
2.权利要求1的化合物,其中Z为OH、C1-6烷氧基、二甲基氨基、甲氨基、氨基、N-甲氧基-N-甲基氨基、2-氰基乙氨基、2-羟基乙氨基、吡咯烷基、哌啶子基、哌嗪基、N-甲基哌嗪基、吗啉代、甲氧基氨基、哌嗪基、氨基吡咯烷基或氨基乙氨基。
3.权利要求2的化合物,其中Z是OH或C1-6烷氧基;而Q选自下列基团:
(a)任选地被1、2或3个独立地选自下列基团的取代基取代的苯基:
(a-1)卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基,
(a-2)芳基或-O-(CH2)n-芳基,且该芳基或芳基部分任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代,
(a-3)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的5-员单环芳基,
(a-4)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的6-员单环芳基,
(b)含有1、2、3或4个N的6-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(c)含有一个选自O、S和N的杂原子并且除所说的杂原子外还任选地含有1、2或3个N的5-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(d)选自环丙基、环丁基、环戊基和环己基的C3-7环烷基,并且所说的环烷基任选地被1个选自OH、甲基、乙基、丙基、F、Cl和CF3的取代基取代;和
(e)选自喹啉基、异喹啉基、1,2-二氮杂萘基、喹喔啉基、苯并咪唑基、苯并噻唑基、苯并噁唑基、苯并呋喃基、苯并噻吩基和吲哚基的苯并稠合的杂环,该苯并稠合的杂环任选地被1、2或3个独立地选自上述(a-1)的基团的取代基取代。
4.权利要求3的化合物,其中Q选自下列基团:
(a)任选地被1、2或3个独立地选自下列基团的取代基取代的苯基:
(a-1)卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基,
(a-2)芳基或-O-(CH2)n-芳基,且该芳基或芳基部分任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代,
(a-3)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的5-员单环芳基,
(a-4)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的6-员单环芳基,
(b)含有1、2、3或4个N的6-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(c)含有一个选自O、S和N的杂原子并且除所说的杂原子外还任选地含有1、2或3个N的5-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(d)选自环丙基、环丁基和环己基;和
(e)喹啉基或异喹啉基,并且所说的喹啉基或异喹啉基任选地被1个选自卤素、C1-4烷基、NH2、OH、C1-4烷氧基和C1-4卤代的烷基的取代基取代。
5.权利要求4的化合物,其中Z为OH、C1-5烷氧基;Q选自下列基团:
(a)任选地被1、2或3个独立地选自下列基团的取代基取代的苯基:
(a-1)卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基,
(a-2)芳基或-O-(CH2)n-芳基,而该芳基或芳基部分任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代,
(a-3)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的5-员单环芳基,
(a-4)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的6-员单环芳基,
(b)含有1、2、3或4个N的6-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(c)含有一个选自O、S和N的杂原子并且除所说的杂原子外还任选地含有1、2或3个N的5-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;和
(e)异喹啉基;R1为H、C1-4烷基;R2和R3独立地为H或甲基;X独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-C4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOR4、C1-4烷基磺酰基氨基和C3-7环烷基;而n为0、1、2或3。
6.权利要求5的化合物,其中Z为OH、甲氧基、乙氧基、正丙氧基、异丙氧基、正丁氧基、异丁氧基或叔丁氧基;Q选自下列基团:
(a)任选地被1或2个独立地选自下列基团的取代基取代的苯基:
(a-1)卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、-COOH、C1-4烷基磺酰基氨基、硝基、C1-4烷基磺酰基和氰基,
(a-2)苯基或苄氧基,并且苯基或苄氧基的苯基部分任选地被1个选自C1-4烷基、卤素取代的C1-4烷基、卤素、OH、C1-4烷氧基、卤素取代的C1-4烷氧基和NH2的取代基取代,
(a-3)选自咪唑基、噻唑基、呋喃基、噻吩基、吡咯基、四唑基、三唑基、噁唑基、异噁唑基、噻二唑基和吡唑基的5-员单环芳基,并且该5-员单环芳基任选地被1个选自C1-4烷基、卤素取代的C1-4烷基、卤素、OH、C1-4烷氧基、卤素取代的C1-4烷氧基和NH2的取代基取代,
(a-4)选自吡啶基、吡嗪基、嘧啶基和哒嗪基的6-员单环芳基,并且该6-员单环芳基任选地被1个选自C1-4烷基、卤素取代的C1-4烷基、卤素、OH、C1-4烷氧基、卤素取代的C1-4烷氧基和NH2的取代基取代,
(b)选自吡啶基、吡嗪基、嘧啶基和哒嗪基的6-员单环芳基,并且所说的单环芳基任选地被1或2个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代,
(c)选自咪唑基、噻唑基、呋喃基、噻吩基、吡咯基、四唑基、三唑基、噁唑基、异噁唑基、噻二唑基和吡唑基的5-员单环芳基,并且所说的单环芳基任选地被1或2个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;R1是H、甲基、乙基、正丙基、异丙基、正丁基、异丁基或叔丁基;X独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-C4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基和氨基磺酰基;而n为0、1、2或3。
7.权利要求6的化合物,其中Z为OH、甲氧基、乙氧基、正丙氧基、异丙氧基、正丁氧基、异丁氧基或叔丁氧基;Q选自下列基团:
(a)任选地被1或2个独立地选自下列基团的取代基取代的苯基:
(a-1)氟、氯、溴、碘、甲基、乙基、丙基、丁基、CH2F、CHF2、CF3、甲氧基、乙氧基、正丙氧基、正丁氧基、异丙氧基、CH2F-O-、CHF2-O-、CF3-O-、甲硫基、乙硫基、羟甲基、甲氧基甲基、甲氧基乙基、乙氧基甲基、OH、NO2、甲磺酰基、CN、(HO)(H3C)2C-、乙酰基和甲磺酰基氨基,
(a-2)苯基或苄氧基,并且苯基或苄氧基的苯基部分任选地被1个选自甲基、乙基、丙基、CF3、F、Cl、OH、甲氧基、乙氧基和NH2的取代基取代,
(a-3)选自呋喃基、噻吩基和吡咯基的5-员单环芳基,并且该5-员单环芳基任选地被1个选自甲基、乙基、丙基、CF3、F、Cl、OH、甲氧基、乙氧基和NH2的取代基取代,
(a-4)任选地被1个选自甲基、乙基、丙基、CF3、F、Cl、OH、甲氧基、乙氧基和NH2的取代基取代的吡啶基,
(b)任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代的吡啶基,
(c)咪唑基、噻唑基、呋喃基、噻吩基、异噁唑基、1,2,3-噻二唑基或吡咯基,并且所说的咪唑基、噻唑基、呋喃基、噻吩基、异噁唑基、1,2,3-噻二唑基或吡咯基任选地被1或2个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;R1是H、甲基、乙基、正丙基、异丙基;X独立地选自F、Cl、Br、甲基、乙基、丙基、丁基、CH2F、CHF2、CF3、甲氧基、CF3-O-或乙氧基;而n为0、1或2。
8.权利要求7的化合物,其中Z为OH、乙氧基或甲氧基;Q为苯基、氯代苯基、氟代苯基、溴代苯基、甲苯基、甲氧基苯基、(呋喃基)苯基、三氟甲基苯基、三氟甲氧基苯基、吡啶基、甲基吡啶基、乙基吡啶基、丙基吡啶基、二甲基吡啶基、氯代吡啶基、氟代吡啶基、三氟甲基吡啶基、甲氧基吡啶基、(乙基)(乙氧基)吡啶基、(氯)(乙基)吡啶基、噻唑基、甲基噻唑基、呋喃基、甲氧基甲基呋喃基、异喹啉基、环己基、甲氧基苯基、(氟)(乙基)吡啶基、二甲基吡啶基或(乙氧基)(乙基)吡啶基;R1为H;X为F、Cl、甲基、乙基、异丙基、叔丁基、CF3或甲氧基;而n为1或2。
9.权利要求8的化合物,其中Z为OH、乙氧基或甲氧基;Q为苯基、氯代苯基、吡啶基、甲基吡啶基、乙基吡啶基、丙基吡啶基或氯代吡啶基;R1为H;X为F、Cl、甲基或CF3;而n为1或2。
10.权利要求1的化合物选自:(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸乙酯、(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸、(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸,钠盐、[6-氯-2-(2-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-氟苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氟苯甲酰基)-1H-吲哚-3-基]乙酸、[2-(3-溴苯甲酰基)-6-氯-1H-吲哚-3-基]乙酸、[2-(4-溴苯甲酰基)-6-氯-1H-吲哚-3-基]乙酸、[6-氯-2-(3-三氟甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-三氟甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3,4-二氯苯甲酰基)-1H-吲哚-3-基]乙酸、(2-苯甲酰基-4-氯-1H-吲哚-3-基)乙酸、[5-氯-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、[2-(3-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、[5-甲氧基-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、(2-苯甲酰基-7-氯-1H-吲哚-3-基)乙酸、(2-苯甲酰基-4,5-二氯-1H-吲哚-3-基)乙酸、(2-苯甲酰基-4,6-二氯-1H-吲哚-3-基)乙酸、(2-苯甲酰基-5,6-二氯-1H-吲哚-3-基)乙酸、dl-2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)丙酸、极性较小的对映体2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)丙酸、极性较大的对映体2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)丙酸、[6-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(1-甲基咪唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(噻唑-2-羰基)-1H-吲哚-3-基]乙酸、(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸甲酯、(2-苯甲酰基-6-氯-1H-吲哚-3-基)-N,N-二甲基乙酰胺、(2-苯甲酰基-6-氯-1H-吲哚-3-基)-N-甲基乙酰胺、(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酰胺、(2-苯甲酰基-6-氯-1H-吲哚-3-基)-N-甲氧基-N-甲基乙酰胺、2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)-1-哌啶子基-1-乙酮、2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)-1-(4-甲基-1-哌嗪基)-1-乙酮、(2-苯甲酰基-6-氯-1H-吲哚-3-基)-N-(2-氰基乙基)乙酰胺、(2-苯甲酰基-6-氯-1H-吲哚-3-基)-N-(2-羟基乙基)乙酰胺、2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)-1-吗啉代-1-乙酮、[2-(4-氯苯甲酰基)-1H-吲哚-3-基)乙酸、[6-氯-2-(2-呋喃基羰基)-1H-吲哚-3-基)乙酸、[6-氯-2-(环己烷羰基)-1H-吲哚-3-基)乙酸、[6-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-叔丁基吡啶-2-羰基)-6-氯-1H-吲哚-3-基]乙酸甲酯、[2-(4-叔丁基吡啶-2-羰基)-6-氯-1H-吲哚-3-基]乙酸、[2-(4-叔丁基吡啶-2-羰基)-5-氯-1H-吲哚-3-基]乙酸甲酯、[2-(4-叔丁基吡啶-2-羰基)-5-氯-1H-吲哚-3-基]乙酸、[6-氯-2-(3-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(3-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(3-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(3-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[5-(三氟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[5-(三氟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[5-氯-2-[5-(三氟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-[5-(三氟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[5-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(吡啶-3-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(吡啶-3-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(吡啶-4-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(吡啶-4-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(羟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[4-(羟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[5-氯-2-[4-(羟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-[4-(羟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[5-氯-2-(3,4-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(3,4-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(3,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(3-乙氧基-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-氯-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(3-氯-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(3-氯-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(3-氯-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5,6-二氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5,6-二氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-甲氧基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-甲氧基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-甲氧基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-甲氧基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-乙基-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-乙基-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-异丙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-异丙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基吡啶-2-羰基)-6-三氟甲基-1H-吲哚-3-基]乙酸甲酯、[2-(4-甲基吡啶-2-羰基)-6-三氟甲基-1H-吲哚-3-基]乙酸、[5-叔丁基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-叔丁基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基吡啶-2-羰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸甲酯、[2-(4-甲基-2-吡啶-2-羰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸、[2-(4-乙基吡啶-2-羰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸甲酯、[2-(4-乙基吡啶-2-羰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸、[6-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸甲酯、[2-(4-甲基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[2-(4-乙基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸甲酯、[2-(4-乙基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、(2-苯甲酰基-1H-吲哚-3-基]乙酸甲酯、(2-苯甲酰基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-6-甲基-1H-吲哚-3-基]乙酸甲酯、[2-(4-氯苯甲酰基)-6-甲基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-甲基-1H-吲哚-3-基]乙酸、[6-甲氧基-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-甲氧基-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-6-三氟甲基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-乙基-1H-吲哚-3-基]乙酸甲酯、[2-(4-氯苯甲酰基)-5-乙基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-甲氧基-1H-吲哚-3-基]乙酸甲酯、[2-(4-氯苯甲酰基)-5-甲氧基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-异丙基-1H-吲哚-3-基]乙酸甲酯、[2-(4-氯苯甲酰基)-5-异丙基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-三氟甲基-1H-吲哚-3-基]乙酸甲酯、[2-(4-氯苯甲酰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸甲酯、[2-(4-氯苯甲酰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸、[6-氯-2-(2-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(2-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(3-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-苄氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(3-苄氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-羟基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(3-羟基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-苄氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-苄氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-羟基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-羟基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-异丙氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-异丙氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-苯基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-苯基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-硝基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-硝基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[(4-甲磺酰基)苯甲酰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[(4-甲磺酰基)苯甲酰基]-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(甲磺酰基氨基)苯甲酰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[4-(甲磺酰基氨基)苯甲酰基]-1H-吲哚-3-基]乙酸、[6-氯-2-(2-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(2,4-二氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯-3-氟苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-氯-3-氟苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氰基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[4-溴代苯甲酰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[4-(2-噻吩基)苯甲酰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[4-(2-噻吩基)苯甲酰基]-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(2-呋喃基)苯甲酰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[4-(2-呋喃基)苯甲酰基]-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(3-吡啶基)苯甲酰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[4-(3-吡啶基)苯甲酰基]-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(2-噻唑基)苯甲酰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[4-(2-噻唑基)苯甲酰基]-1H-吲哚-3-基]乙酸、[6-氯-2-(3-溴代苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[3-(2-呋喃基)苯甲酰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[3-(2-呋喃基)苯甲酰基]-1H-吲哚-3-基]乙酸、dl-2-[6-氯-2-(4-氯代苯甲酰基)-1H-吲哚-3-基]丙酸甲酯、dl-2-[2-(4-氯代苯甲酰基)-6-氯-1H-吲哚-3-基]丙酸、[5-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(5-甲基异噁唑-3-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(5-甲基异噁唑-3-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-甲基异噁唑-3-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(5-甲基异噁唑-3-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲基-1,2,3-噻二唑-5-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-甲基-1,2,3-噻二唑-5-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲基-1,2,3-噻二唑-5-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-甲基-1,2,3-噻二唑-5-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(5-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(5-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(5-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(2-噻吩基)羰基吲哚-3-基]乙酸、[6-氯-2-[3-(1-羟基-1-甲基乙基)-2-呋喃甲酰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[3-(1-羟基-1-甲基乙基)-2-呋喃甲酰基]-1H-吲哚-3-基]乙酸、[6-氯-2-[3-甲氧基甲基-2-呋喃甲酰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[3-甲氧基甲基-2-呋喃甲酰基]-1H-吲哚-3-基]乙酸、[6-氯-2-(1-甲基咪唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(1-甲基咪唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(1-甲基咪唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(1-甲基咪唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(咪唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(咪唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(咪唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(咪唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(1-甲基吡咯-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(1-甲基吡咯-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(2-甲基咪唑-4-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(2-甲基咪唑-4-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(噻唑-5-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(噻唑-5-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-[3-(乙氧基羰基)异噁唑-5-羰基]-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-[3-(羧基)异噁唑-5-羰基]-1H-吲哚-3-基]乙酸、[6-氯-2-环丙烷羰基-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-环丙烷羰基-1H-吲哚-3-基]乙酸、[6-氯-2-环丁烷羰基-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-环丁烷羰基-1H-吲哚-3-基]乙酸、[5-(叔丁基)-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[5-(叔丁基)-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]-N,N-二甲基乙酰胺、[6-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]-N-甲基乙酰胺、[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]-N-(2-羟乙基)乙酰胺、[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]-N-甲氧基乙酰胺、2-[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]-1-哌嗪基-1-乙酮、[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]-N-(2-氨基乙基)乙酰胺、2-[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]-1-(3-氨基-1-吡咯烷基)-1-乙酮、[6-氯-2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、[6-氯-5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(1-羟乙基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[4-(1-羟乙基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[6-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(2-硝基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(2,4-二甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-二氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(2,5-二甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-乙酰基-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[5-乙酰基-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸甲酯、[6-氟-2-(4-甲基吡啶-2-羰基)-H-吲哚-3-基]乙酸甲酯、[6-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氟-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氟-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基吡啶-2-羰基)-5-甲硫基-1H-吲哚-3-基]乙酸、[2-(4-甲基吡啶-2-羰基)-5-甲硫基-1H-吲哚-3-基]乙酸及其盐。
11.权利要求10的化合物,选自:(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸乙酯、(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸、(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸,钠盐、[6-氯-2-(2-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-氟苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氟苯甲酰基)-1H-吲哚-3-基]乙酸、[2-(3-溴苯甲酰基)-6-氯-1H-吲哚-3-基]乙酸、[2-(4-溴苯甲酰基)-6-氯-1H-吲哚-3-基]乙酸、[6-氯-2-(3-三氟甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-三氟甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3,4-二氯苯甲酰基)-1H-吲哚-3-基]乙酸、(2-苯甲酰基-4-氯-1H-吲哚-3-基)乙酸、[5-氯-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、[2-(3-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、[5-甲氧基-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、(2-苯甲酰基-7-氯-1H-吲哚-3-基)乙酸、(2-苯甲酰基-4,5-二氯-1H-吲哚-3-基)乙酸、(2-苯甲酰基-4,6-二氯-1H-吲哚-3-基)乙酸、(2-苯甲酰基-5,6-二氯-1H-吲哚-3-基)乙酸、dl-2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)丙酸、极性较小的对映体2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)丙酸、极性较大的对映体2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)丙酸、[6-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(1-甲基咪唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(噻唑-2-羰基)-1H-吲哚-3-基]乙酸、(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸甲酯、[2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(2-呋喃基羰基)-1H-吲哚-3-基)乙酸、[6-氯-2-(环己烷羰基)-1H-吲哚-3-基)乙酸、[6-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-叔丁基吡啶-2-羰基)-6-氯-1H-吲哚-3-基]乙酸、[2-(4-叔丁基吡啶-2-羰基)-5-氯-1H-吲哚-3-基]乙酸、[6-氯-2-(3-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(3-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[5-(三氟甲基)吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-[5-(三氟甲基)吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(吡啶-3-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(吡啶-4-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(羟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[5-氯-2-[4-(羟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[5-氯-2-(3,4-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-乙氧基-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-氯-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(3-氯-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5,6-二氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-甲氧基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-甲氧基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-乙基-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-异丙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基吡啶-2-羰基)-6-三氟甲基-1H-吲哚-3-基]乙酸、[5-叔丁基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基-2-吡啶-2-羰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸、[2-(4-乙基吡啶-2-羰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸、[6-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[2-(4-乙基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、(2-苯甲酰基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-6-甲基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-甲基-1H-吲哚-3-基]乙酸、[6-甲氧基-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-6-三氟甲基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-乙基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-甲氧基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-异丙基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸、[6-氯-2-(2-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-苄氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-羟基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-苄氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-羟基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-异丙氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-苯基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-硝基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[(4-甲磺酰基)苯甲酰基]-1H-吲哚-3-基]乙酸、[6-氯-2-[(4-甲磺酰基氨基)苯甲酰基]-1H-吲哚-3-基]乙酸、[6-氯-2-(2-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(2,4-二氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯-3-氟苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氰基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[4-溴代苯甲酰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[4-(2-噻吩基)苯甲酰基]-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(2-呋喃基)苯甲酰基]-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(3-吡啶基)苯甲酰基]-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(2-噻唑基)苯甲酰基]-1H-吲哚-3-基]乙酸、[6-氯-2-(3-溴代苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[3-(2-呋喃基)苯甲酰基]-1H-吲哚-3-基]乙酸、dl-2-[2-(4-氯代苯甲酰基)-6-氯-1H-吲哚-3-基]丙酸、[5-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(5-甲基异噁唑-3-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-甲基异噁唑-3-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲基-1,2,3-噻二唑-5-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲基-1,2,3-噻二唑-5-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(5-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(2-噻吩基)羰基吲哚-3-基]乙酸、[6-氯-2-[3-(1-羟基-1-甲基乙基)-2-呋喃甲酰基]-1H-吲哚-3-基]乙酸、[6-氯-2-[3-甲氧基甲基-2-呋喃甲酰基]-1H-吲哚-3-基]乙酸、[6-氯-2-(1-甲基咪唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(1-甲基咪唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(1-甲基咪唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(咪唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(咪唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(1-甲基吡咯-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(2-甲基咪唑-4-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(噻唑-5-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-[3-(羧基)异噁唑-5-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-环丙烷羰基-1H-吲哚-3-基]乙酸、[6-氯-2-环丁烷羰基-1H-吲哚-3-基]乙酸、[5-(叔丁基)-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、[6-氯-5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(1-羟乙基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[4-(1-羟乙基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[6-氯-2-[4-乙基-3-氟吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[6-氯-2-(2-硝基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(2,4-二甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-二氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(2,5-二甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-乙酰基-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸及其盐。
12.权利要求10的化合物选自:(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸乙酯、(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸、[6-氯-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-氟苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氟苯甲酰基)-1H-吲哚-3-基]乙酸、[2-(3-溴苯甲酰基)-6-氯-1H-吲哚-3-基]乙酸、[2-(4-溴苯甲酰基)-6-氯-1H-吲哚-3-基]乙酸、[6-氯-2-(3-三氟甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-三氟甲基苯甲酰基)-1H-吲哚-3-基]乙酸、(2-苯甲酰基-4-氯-1H-吲哚-3-基)乙酸、[5-氯-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、[2-(3-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、(2-苯甲酰基-4,5-二氯-1H-吲哚-3-基)乙酸、(2-苯甲酰基-4,6-二氯-1H-吲哚-3-基)乙酸、(2-苯甲酰基-5,6-二氯-1H-吲哚-3-基)乙酸、dl-2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)丙酸、极性较小的对映体2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)丙酸、极性较大的对映体2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)丙酸、[6-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(1-甲基咪唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(噻唑-2-羰基)-1H-吲哚-3-基]乙酸、(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸甲酯、[6-氯-2-(2-呋喃基羰基)-1H-吲哚-3-基)乙酸、[6-氯-2-(环己烷羰基)-1H-吲哚-3-基)乙酸、[6-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-叔丁基吡啶-2-羰基)-6-氯-1H-吲哚-3-基]乙酸甲酯、[2-(4-叔丁基吡啶-2-羰基)-6-氯-1H-吲哚-3-基]乙酸、[6-氯-2-(3-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(3-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[5-(三氟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[5-(三氟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[5-氯-2-[5-(三氟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-[5-(三氟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[5-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-[4-(羟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-[4-(羟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[5-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(3,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(3-乙氧基-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-氯-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(3-氯-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(3-氯-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(3-氯-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5,6-二氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5,6-二氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-甲氧基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-甲氧基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-甲氧基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-甲氧基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-乙基-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-乙基-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-异丙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-异丙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基吡啶-2-羰基)-6-三氟甲基-1H-吲哚-3-基]乙酸甲酯、[2-(4-甲基吡啶-2-羰基)-6-三氟甲基-1H-吲哚-3-基]乙酸、[5-叔丁基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-叔丁基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基吡啶-2-羰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸甲酯、[2-(4-甲基-2-吡啶-2-羰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸、[6-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸甲酯、[2-(4-甲基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[2-(4-乙基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸甲酯、[2-(4-乙基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-6-甲基-1H-吲哚-3-基]乙酸甲酯、[2-(4-氯苯甲酰基)-6-甲基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-甲基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-三氟甲基-1H-吲哚-3-基]乙酸甲酯、[2-(4-氯苯甲酰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸甲酯、[2-(4-氯苯甲酰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸、[6-氯-2-(3-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(3-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(2-呋喃基)苯甲酰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[4-(2-呋喃基)苯甲酰基]-1H-吲哚-3-基]乙酸、[5-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-甲基异噁唑-3-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(5-甲基异噁唑-3-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(5-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(5-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(5-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[3-甲氧基甲基-2-呋喃甲酰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[3-甲氧基甲基-2-呋喃甲酰基]-1H-吲哚-3-基]乙酸、[6-氯-2-(1-甲基咪唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(2-甲基咪唑-4-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(2-甲基咪唑-4-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(1-羟乙基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[4-(1-羟乙基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[6-氯-2-[4-乙基-3-氟吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸甲酯,及其盐。
13.权利要求10的化合物选自:(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸乙酯、(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸、[6-氯-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-氟苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氟苯甲酰基)-1H-吲哚-3-基]乙酸、[2-(3-溴苯甲酰基)-6-氯-1H-吲哚-3-基]乙酸、[2-(4-溴苯甲酰基)-6-氯-1H-吲哚-3-基]乙酸、[6-氯-2-(3-三氟甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-三氟甲基苯甲酰基)-1H-吲哚-3-基]乙酸、(2-苯甲酰基-4-氯-1H-吲哚-3-基)乙酸、[5-氯-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、[2-(3-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、(2-苯甲酰基-4,5-二氯-1H-吲哚-3-基)乙酸、(2-苯甲酰基-4,6-二氯-1H-吲哚-3-基)乙酸、(2-苯甲酰基-5,6-二氯-1H-吲哚-3-基)乙酸、dl-2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)丙酸、极性较小的对映体2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)丙酸、极性较大的对映体2-(2-苯甲酰基-6-氯-1H-吲哚-3-基)丙酸、[6-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(1-甲基咪唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(噻唑-2-羰基)-1H-吲哚-3-基]乙酸、(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸甲酯、[6-氯-2-(2-呋喃基羰基)-1H-吲哚-3-基)乙酸、[6-氯-2-(环己烷羰基)-1H-吲哚-3-基)乙酸、[6-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-叔丁基吡啶-2-羰基)-6-氯-1H-吲哚-3-基]乙酸、[6-氯-2-(3-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[5-(三氟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[5-氯-2-[5-(三氟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[5-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-[4-(羟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[5-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-乙氧基-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-氯-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(3-氯-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5,6-二氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-甲氧基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-甲氧基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-乙基-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-异丙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基吡啶-2-羰基)-6-三氟甲基-1H-吲哚-3-基]乙酸、[5-叔丁基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基-2-吡啶-2-羰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸、[6-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[2-(4-乙基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-6-甲基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-甲基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸、[6-氯-2-(3-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(2-呋喃基)苯甲酰基]-1H-吲哚-3-基]乙酸、[5-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-甲基异噁唑-3-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(5-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[3-甲氧基甲基-2-呋喃甲酰基]-1H-吲哚-3-基]乙酸、[6-氯-2-(1-甲基咪唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(2-甲基咪唑-4-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(1-羟乙基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[4-(1-羟乙基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、2-{6-氯-2-[4-乙基-3-氟-2-吡啶基]羰基}-1H-吲哚-3-基}乙酸、[6-氯-2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸甲酯,及其盐。
14.权利要求10的化合物选自:(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸、[6-氯-2-(4-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-氟苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氟苯甲酰基)-1H-吲哚-3-基]乙酸、[2-(3-溴苯甲酰基)-6-氯-1H-吲哚-3-基]乙酸、[2-(4-溴苯甲酰基)-6-氯-1H-吲哚-3-基]乙酸、[6-氯-2-(4-三氟甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、[2-(3-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、(2-苯甲酰基-4,5-二氯-1H-吲哚-3-基)乙酸、(2-苯甲酰基-4,6-二氯-1H-吲哚-3-基)乙酸、(2-苯甲酰基-5,6-二氯-1H-吲哚-3-基)乙酸、[6-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(噻唑-2-羰基)-1H-吲哚-3-基]乙酸、(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸甲酯、[6-氯-2-(环己烷羰基)-1H-吲哚-3-基)乙酸、[6-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[5-(三氟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[5-(三氟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[5-氯-2-[5-(三氟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-[5-(三氟甲基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[5-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(3-乙氧基-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-氯-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(3-氯-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5,6-二氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5,6-二氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-异丙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-异丙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基吡啶-2-羰基)-6-三氟甲基-1H-吲哚-3-基]乙酸甲酯、[2-(4-甲基吡啶-2-羰基)-6-三氟甲基-1H-吲哚-3-基]乙酸、[5-叔丁基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-叔丁基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基吡啶-2-羰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸甲酯、[2-(4-甲基-2-吡啶-2-羰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸、[6-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸甲酯、[2-(4-甲基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[2-(4-乙基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸甲酯、[2-(4-乙基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-甲基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-三氟甲基-1H-吲哚-3-基]乙酸甲酯、[2-(4-氯苯甲酰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[6-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(2-呋喃基)苯甲酰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[4-(2-呋喃基)苯甲酰基]-1H-吲哚-3-基]乙酸、[5-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(5-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(5-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(5-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[3-甲氧基甲基-2-呋喃甲酰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[3-甲氧基甲基-2-呋喃甲酰基]-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(2-甲基咪唑-4-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(2-甲基咪唑-4-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、[6-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸甲酯及其盐。
15.权利要求10的化合物选自:(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸、[6-氯-2-(4-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-氟苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氟苯甲酰基)-1H-吲哚-3-基]乙酸、[2-(3-溴苯甲酰基)-6-氯-1H-吲哚-3-基]乙酸、[2-(4-溴苯甲酰基)-6-氯-1H-吲哚-3-基]乙酸、[6-氯-2-(4-三氟甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(3-甲基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、[2-(3-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、(2-苯甲酰基-4,5-二氯-1H-吲哚-3-基)乙酸、(2-苯甲酰基-4,6-二氯-1H-吲哚-3-基)乙酸、(2-苯甲酰基-5,6-二氯-1H-吲哚-3-基)乙酸、[6-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(噻唑-2-羰基)-1H-吲哚-3-基]乙酸、(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸甲酯、[6-氯-2-(环己烷羰基)-1H-吲哚-3-基)乙酸、[6-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(6-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[5-(三氟甲基)吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-[5-(三氟甲基)吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4,5-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-乙氧基-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(3-氯-4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4,6-二甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5,6-二氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-乙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-异丙基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基吡啶-2-羰基)-6-三氟甲基-1H-吲哚-3-基]乙酸、[5-叔丁基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基-2-吡啶-2-羰基)-5-三氟甲氧基-1H-吲哚-3-基]乙酸、[6-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-甲基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[2-(4-乙基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[6-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-三氟甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(2-呋喃基)苯甲酰基]-1H-吲哚-3-基]乙酸、[5-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(5-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(5-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[3-甲氧基甲基-2-呋喃甲酰基]-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(2-甲基咪唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲基噻唑-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、[6-氯-2-(4-乙基-3-氟吡啶-2-羰基]-1H-吲哚-3-基)乙酸、[6-氯-2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸甲酯、[6-氯-5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(1-羟乙基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸,及其盐。
16.权利要求1的化合物选自:(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸、[6-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、(2-苯甲酰基-5,6-二氯-1H-吲哚-3-基)乙酸、[6-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-乙基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸甲酯、[2-(4-乙基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸[5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸、[6-氯-5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(1-羟乙基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-[4-(1-羟乙基)吡啶-2-羰基]-1H-吲哚-3-基]乙酸、[6-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯、[6-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸甲酯、[5-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸(cj-020,099)、[6-氯-5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸甲酯,及其盐。
17.权利要求10的化合物选自:(2-苯甲酰基-6-氯-1H-吲哚-3-基)乙酸、[6-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(3-氯苯甲酰基)-1H-吲哚-3-基]乙酸、[2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸、(2-苯甲酰基-5,6-二氯-1H-吲哚-3-基)乙酸、[6-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-乙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-异丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-丙基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[2-(4-乙基吡啶-2-羰基)-5-三氟甲基-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-甲氧基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氟-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(4-甲氧基苯甲酰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-[4-(1-羟乙基)吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-乙基-3-氟吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(5-氯吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[6-甲基-2-(4-甲基吡啶-2-羰基)-1H-吲哚-3-基]乙酸、[5-氯-2-(异喹啉-3-羰基)-1H-吲哚-3-基]乙酸、[6-氯-2-(4-氯苯甲酰基)-5-氟-1H-吲哚-3-基]乙酸,及其盐。
18.一种用于治疗与作为病原的前列腺素关联的医学病症的药物组合物,包括权利要求1的式(I)化合物和一种药学惰性的载体。
19.权利要求18的药物组合物,其中式(I)化合物如权利要求2所定义。
20.权利要求19的药物组合物,其中式(I)化合物如权利要求3所定义。
21.权利要求20的药物组合物,其中式(I)化合物如权利要求4所定义。
22.权利要求21的药物组合物,其中式(I)化合物如权利要求5所定义。
23.权利要求22的药物组合物,其中式(I)化合物如权利要求6所定义。
24.权利要求23的药物组合物,其中化合物如权利要求7所定义。
25.权利要求24的药物组合物,其中化合物如权利要求8所定义。
26.权利要求25的药物组合物,其中化合物如权利要求9所定义。
27.权利要求26的药物组合物,其中化合物如权利要求10所定义。
28.权利要求27的药物组合物,其中化合物如权利要求11所定义。
29.权利要求28的药物组合物,其中化合物如权利要求12所定义。
30.权利要求29的药物组合物,其中化合物如权利要求13所定义。
31.权利要求30的药物组合物,其中化合物如权利要求14所定义。
32.权利要求31的药物组合物,其中化合物如权利要求15所定义。
33.权利要求32的药物组合物,其中化合物如权利要求16所定义。
34.权利要求33的药物组合物,其中化合物如权利要求17所定义。
35.一种治疗哺乳动物受治者中与作为病原的前列腺素关联的医学病症的方法,包括给药权利要求1所说的药物组合物。
36.一种下式的化合物:其中B为合适的保护基团:Q选自下列基团:
(a)任选地被1、2或3个独立地选自下列基团的取代基取代的苯基:
(a-1)卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基,
(a-2)芳基或-O-(CH2)n-芳基,而该芳基或芳基部分任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代,
(a-3)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的5-员单环芳基,
(a-4)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的6-员单环芳基,
(b)含有1、2、3或4个N的6-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(c)含有一个选自O、S和N的杂原子并且除所说的杂原子外还任选地含有1、2或3个N的5-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(d)任选地被1或2个独立地选自OH、C1-4烷基、卤素和卤素取代的C1-4烷基的取代基取代的C3-7环烷基;和
(e)任选地被1、2或3个独立地选自上述(a-1)的基团的取代基取代的苯并稠合的杂环;R2和R3独立地为H、OH、C1-4烷氧基、C1-4烷基或者是被卤素、OH、C1-4烷氧基、NH2或CN取代的C1-4烷基;X独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-C4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基;R5是C1-C6烷基;而n为0、1、2、3或4。
(a)任选地被1、2或3个独立地选自下列基团的取代基取代的苯基:
(a-1)卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基,
(a-2)芳基或-O-(CH2)n-芳基,而该芳基或芳基部分任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代,
(a-3)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的5-员单环芳基,
(a-4)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的6-员单环芳基,
(b)含有1、2、3或4个N的6-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(c)含有一个选自O、S和N的杂原子并且除所说的杂原子外还任选地含有1、2或3个N的5-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(d)任选地被1或2个独立地选自OH、C1-4烷基、卤素和卤素取代的C1-4烷基的取代基取代的C3-7环烷基;和
(e)任选地被1、2或3个独立地选自上述(a-1)的基团的取代基取代的苯并稠合的杂环;R2和R3独立地为H、OH、C1-4烷氧基、C1-4烷基或者是被卤素、OH、C1-4烷氧基、NH2或CN取代的C1-4烷基;X独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-C4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基;R5是C1-C6烷基;而n为0、1、2、3或4。
38.一种制备下式的化合物的方法:其中Q选自下列基团:
(a)任选地被1、2或3个独立地选自下列基团的取代基取代的苯基:
(a-1)卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基,
(a-2)芳基或-O-(CH2)n-芳基,且该芳基或芳基部分任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代,
(a-3)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的5-员单环芳基,
(a-4)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的6-员单环芳基,
(b)含有1、2、3或4个N的6-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(c)含有一个选自O、S和N的杂原子并且除所说的杂原子外还任选地含有1、2或3个N的5-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(d)任选地被1或2个独立地选自OH、C1-4烷基、卤素和卤素取代的C1-4烷基的取代基取代的C3-7环烷基;和
(e)任选地被1、2或3个独立地选自上述(a-1)的基团的取代基取代的苯并稠合的杂环;R2和R3独立地为H、OH、C1-4烷氧基、C1-4烷基或者是被卤素、OH、C1-4烷氧基、NH2或CN取代的C1-4烷基;X独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-C4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基;而n为0、1、2、3或4,该方法包括下列步骤:
其中E为卤素,Q如上所定义;
ii)使步骤i)的产物与第二种碱反应;
iii)使步骤ii)的产物与一种酸反应。
39.权利要求38的方法,其中所说的第一种碱是碳酸钾、碳酸氢钾、碳酸钠、碳酸氢钠或碳酸铯。
40.权利要求38的方法,其中所说的第一种碱是碳酸钾。
41.权利要求38的方法,其中所说的第二种碱是氢氧化钠、氢氧化钾、碳酸钠、碳酸钾、戊醇钠(然后是水)、甲醇钠(然后是水)或叔丁醇钾水溶液(然后是水)。
42.权利要求38的方法,其中所说的第二种碱是氢氧化钠。
43.权利要求38的方法,其中所说的酸是盐酸、氢溴酸、硫酸或氯化铵水溶液。
44.权利要求38的方法,其中所说的酸是盐酸水溶液。
45.权利要求38的方法,其中所说的溶剂是N,N-二甲基乙酰胺、N,N-二甲基甲酰胺、甲乙酮、丙酮或四氢呋喃。
46.权利要求38的方法,其中所说的溶剂是N,N-二甲基乙酰胺。
(a)任选地被1、2或3个独立地选自下列基团的取代基取代的苯基:
(a-1)卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基,
(a-2)芳基或-O-(CH2)n-芳基,且该芳基或芳基部分任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代,
(a-3)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的5-员单环芳基,
(a-4)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的6-员单环芳基,
(b)含有1、2、3或4个N的6-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(c)含有一个选自O、S和N的杂原子并且除所说的杂原子外还任选地含有1、2或3个N的5-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(d)任选地被1或2个独立地选自OH、C1-4烷基、卤素和卤素取代的C1-4烷基的取代基取代的C3-7环烷基;和
(e)任选地被1、2或3个独立地选自上述(a-1)的基团的取代基取代的苯并稠合的杂环;R2和R3独立地为H、OH、C1-4烷氧基、C1-4烷基或者是被卤素、OH、C1-4烷氧基、NH2或CN取代的C1-4烷基;X独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-C4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基;而n为0、1、2、3或4,该方法包括使下式的化合物:
其中R5为C1-6烷基,Q、X和n如前面所定义,与一种碱在一种合适的溶剂中反应。
48.权利要求47的方法,其中所说的碱是氢氧化钠、氢氧化钾、碳酸钠、碳酸钾、碳酸氢钠、碳酸氢钾、叔戊醇钠、甲醇钠、乙醇钠或叔丁醇钾。
49.权利要求47的方法,其中所说的碱是氢氧化钠。
50.权利要求47的方法,其中所说的溶剂是甲醇、乙醇、异丙醇或四氢呋喃与水的混合物。
51.权利要求47的方法,其中所说的溶剂是含有水的甲醇。
(a)任选地被1、2或3个独立地选自下列基团的取代基取代的苯基:
(a-1)卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基,
(a-2)芳基或-O-(CH2)n-芳基,而该芳基或芳基部分任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代,
(a-3)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的5-员单环芳基,
(a-4)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的6-员单环芳基,
(b)含有1、2、3或4个N的6-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(c)含有一个选自O、S和N的杂原子并且除所说的杂原子外还任选地含有1、2或3个N的5-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(d)任选地被1或2个独立地选自OH、C1-4烷基、卤素和卤素取代的C1-4烷基的取代基取代的C3-7环烷基;和
(e)任选地被1、2或3个独立地选自上述(a-1)的基团的取代基取代的苯并稠合的杂环;R2和R3独立地为H、OH、C1-4烷氧基、C1-4烷基或者是被卤素、OH、C1-4烷氧基、NH2或CN取代的C1-4烷基;X独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-C4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基;R5为C1-6烷基;而n为0、1、2、3或4,该方法包括使下式的化合物:
其中B、Q、X、n和R5如前面所定义,与一种碱在一种合适的溶剂中反应。
53.权利要求52的方法,其中所说的碱是1,8-二氮杂双环[5.4.0]十一碳-7-烯、1,5-二氮杂双环[4.3.0]壬-5-烯、1,1,3,3-四甲基胍、叔戊醇钠、甲醇钠或叔丁醇钾。
54.权利要求52的方法,其中所说的碱是1,8-二氮杂双环[5.4.0]十一碳-7-烯或叔丁醇钾。
55.权利要求52的方法,其中所说的溶剂是N,N-二甲基乙酰胺、N,N-二甲基甲酰胺、甲乙酮、丙酮或四氢呋喃。
56.权利要求52的方法,其中所说的溶剂是N,N-二甲基乙酰胺。
(a)任选地被1、2或3个独立地选自下列基团的取代基取代的苯基:
(a-1)卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基,
(a-2)芳基或-O-(CH2)n-芳基,而该芳基或芳基部分任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代,
(a-3)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的5-员单环芳基,
(a-4)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的6-员单环芳基,
(b)含有1、2、3或4个N的6-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(c)含有一个选自O、S和N的杂原子并且除所说的杂原子外还任选地含有1、2或3个N的5-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(d)任选地被1或2个独立地选自OH、C1-4烷基、卤素和卤素取代的C1-4烷基的取代基取代的C3-7环烷基;和
(e)任选地被1、2或3个独立地选自上述(a-1)的基团的取代基取代的苯并稠合的杂环;R2和R3独立地为H、OH、C1-4烷氧基、C1-4烷基或者是被卤素、OH、C1-4烷氧基、NH2或CN取代的C1-4烷基;X独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-C4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基;R5为C1-6烷基;而n为0、1、2、3或4,该方法包括使下式的化合物:
其中B、Q、X、n和R5如前面所定义,与一种碱在一种溶剂存在下反应。
58.权利要求57的方法,其中所说的碱是碳酸钾、碳酸氢钾、碳酸氢钠、碳酸钠或碳酸铯。
59.权利要求57的方法,其中所说的碱是碳酸钾。
60.权利要求57的方法,其中所说的溶剂是N,N-二甲基乙酰胺、N,N-二甲基甲酰胺、甲乙酮、丙酮或四氢呋喃。
61.权利要求57的方法,其中所说的溶剂是N,N-二甲基乙酰胺。
62.一种制备下式化合物的方法:其中B是合适的保护基团;Q选自下列基团:
(a)任选地被1、2或3个独立地选自下列基团的取代基取代的苯基:
(a-1)卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基,
(a-2)芳基或-O-(CH2)n-芳基,而该芳基或芳基部分任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代,
(a-3)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的5-员单环芳基,
(a-4)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的6-员单环芳基,
(b)含有1、2、3或4个N的6-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(c)含有一个选自O、S和N的杂原子并且除所说的杂原子外还任选地含有1、2或3个N的5-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(d)任选地被1或2个独立地选自OH、C1-4烷基、卤素和卤素取代的C1-4烷基的取代基取代的C3-7环烷基;和
(e)任选地被1、2或3个独立地选自上述(a-1)的基团的取代基取代的苯并稠合的杂环;R2和R3独立地为H、OH、C1-4烷氧基、C1-4烷基或者是被卤素、OH、C1-4烷氧基、NH2或CN取代的C1-4烷基;X独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-C4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基;R5为C1-6烷基;而n为0、1、2、3或4,该方法包括使下式的化合物:
其中B、X、n和R5如前面所定义,与一种下式的化合物和一种碱在一种溶剂存在下反应:
其中E为卤素,Q如上所定义。
63.权利要求62的方法,其中所说的碱是碳酸钾、碳酸氢钾、碳酸氢钠、碳酸钠或碳酸铯。
64.权利要求62的方法,其中所说的碱是碳酸钾。
65.权利要求62的方法,其中所说的溶剂是N,N-二甲基乙酰胺、N,N-二甲基甲酰胺、甲乙酮、丙酮或四氢呋喃。
66.权利要求62的方法,其中所说的溶剂是N,N-二甲基乙酰胺。
(a)任选地被1、2或3个独立地选自下列基团的取代基取代的苯基:
(a-1)卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基,
(a-2)芳基或-O-(CH2)n-芳基,而该芳基或芳基部分任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代,
(a-3)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的5-员单环芳基,
(a-4)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的6-员单环芳基,
(b)含有1、2、3或4个N的6-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(c)含有一个选自O、S和N的杂原子并且除所说的杂原子外还任选地含有1、2或3个N的5-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团取代;
(d)任选地被1或2个独立地选自OH、C1-4烷基、卤素和卤素取代的C1-4烷基的取代基取代的C3-7环烷基;和
(e)任选地被1、2或3个独立地选自上述(a-1)的基团取代的苯并稠合的杂环;R1为H、C1-4烷基或卤素;R2和R3独立地为H、OH、C1-4烷氧基、C1-4烷基或者是被卤素、OH、C1-4烷氧基、NH2或CN取代的C1-4烷基;R5为C1-6烷基;X独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-C4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基;而n为0、1、2、3或4,该方法包括在一种合适的碱存在下处理下式(X)的化合物:
其中R1、R5、X、Q和n如前面所定义,而B为合适的保护基团,得到式(XII)的化合物。
(a)任选地被1、2或3个独立地选自下列基团的取代基取代的苯基:
(a-1)卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基,
(a-2)芳基或-O-(CH2)n-芳基,而该芳基或芳基部分任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代,
(a-3)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的5-员单环芳基,
(a-4)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的6-员单环芳基,
(b)含有1、2、3或4个N的6-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(c)含有一个选自O、S和N的杂原子并且除所说的杂原子外还任选地含有1、2或3个N的5-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(d)任选地被1或2个独立地选自OH、C1-4烷基、卤素和卤素取代的C1-4烷基的取代基取代的C3-7环烷基;和
(e)任选地被1、2或3个独立地选自上述(a-1)的基团的取代基取代的苯并稠合的杂环;R1为H、C1-4烷基或卤素;R2和R3独立地为H、OH、C1-4烷氧基、C1-4烷基或者是被卤素、OH、C1-4烷氧基、NH2或CN取代的C1-4烷基;R5为C1-6烷基;X独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-C4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基;而n为0、1、2、3或4,该方法包括使下式(IX)的化合物:
其中R1、R5、X和n如上所定义,而B为合适的保护基团,与下式的化合物(XI)在一种合适的碱存在下在-40℃-200℃的温度下反应:
其中E为卤素,而Q如上所定义,得到式(XII)的化合物。
69.权利要求68的方法,其中反应在0-100℃的温度下进行。
70.权利要求68的方法,其中合适的碱是碳酸钾、碳酸铯、碳酸钠、叔丁醇钠、叔丁醇钾、氢化钠、氢化钾或氟化钾。
71.权利要求68的方法,其中反应先在碱存在下进行2分钟至1天,然后向反应混合物中加入另一种碱。
72.权利要求71的方法,其中反应先进行30分钟至8小时。
73.权利要求67-68的方法,其中合适的保护基团是甲氧基羰基、乙氧基羰基、叔丁氧基羰基、苄氧基羰基、苯磺酰基、对甲苯磺酰基、甲磺酰基或三氟甲磺酰基。
74.权利要求73的方法,其中合适的保护基团是苯磺酰基、对甲苯磺酰基、甲磺酰基或三氟甲磺酰基。
75.权利要求71的方法,其中第一种碱选自叔丁醇钠、叔丁醇钾、碳酸钠、碳酸钾、碳酸铯、氢化钠、氢化钾、碳酸钠、碳酸钾、碳酸铯、氟化钾、1,8-二氮杂双环[5.4.0]十一碳-7-烯、1,5-二氮杂双环[4.3.0]壬-5-烯、1,4-二氮杂双环[2.2.2]辛烷、吡啶、吡咯烷、三乙胺、二异丙基胺、二异丙基乙胺和二乙基异丙胺,而第二种碱选自叔丁醇钠、叔丁醇钾、碳酸钠、碳酸钾、碳酸铯、氢化钠、氢化钾、碳酸钠、碳酸钾、碳酸铯、氟化钾、1,8-二氮杂双环[5.4.0]十一碳-7-烯、1,5-二氮杂双环[4.3.0]壬-5-烯、1,4-二氮杂双环[2.2.2]辛烷、吡啶、吡咯烷、三乙胺、二异丙基胺、二异丙基乙胺和二乙基异丙胺。
76.权利要求75的方法,其中第一种碱选自碳酸钾、碳酸铯、氢化钠和氟化钾,而第二种碱选自1,8-二氮杂双环[5.4.0]十一碳-7-烯、碳酸铯、吡咯烷、二异丙基胺、三乙胺、二乙基异丙胺和二异丙基乙胺。
77.权利要求75的方法,其中第一种碱是碳酸钾、碳酸铯或氟化钾,而第二种碱是1,8-二氮杂双环[5.4.0]十一碳-7-烯、叔丁醇钾或碳酸铯。
78.权利要求77的方法,其中第一种碱和第二种碱的组合(第一种碱/第二种碱)选自碳酸钾/1,8-二氮杂双环[5.4.0]十一碳-7-烯、碳酸钾/碳酸铯、碳酸铯/叔丁醇钾、碳酸铯/1,8-二氮杂双环[5.4.0]十一碳-7-烯和氟化钾/1,8-二氮杂双环[5.4.0]十一碳-7-烯以及氟化钾/碳酸铯。
79.权利要求78的方法,其中第一种碱和第二种碱的组合(第一种碱/第二种碱)选自碳酸钾/1,8-二氮杂双环[5.4.0]十一碳-7-烯、碳酸钾/碳酸铯和碳酸铯/叔丁醇钾。
(a)任选地被1、2或3个独立地选自下列基团的取代基取代的苯基:
(a-1)卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基,
(a-2)芳基或-O-(CH2)n-芳基,而该芳基或芳基部分任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代,
(a-3)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的5-员单环芳基,
(a-4)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的6-员单环芳基,
(b)含有1、2、3或4个N的6-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(c)含有一个选自O、S和N的杂原子并且除所说的杂原子外还任选地含有1、2或3个N的5-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(d)任选地被1或2个独立地选自OH、C1-4烷基、卤素和卤素取代的C1-4烷基的取代基取代的C3-7环烷基;和
(e)任选地被1、2或3个独立地选自上述(a-1)的基团的取代基取代的苯并稠合的杂环;R1为H、C1-4烷基或卤素;R2和R3独立地为H、OH、C1-4烷氧基、C1-4烷基或者是被卤素、OH、C1-4烷氧基、NH2或CN取代的C1-4烷基;X独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-C4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基;而n为0、1、2、3或4,该方法包括用一种合适的碱在水解条件下处理下式(X)的化合物:
其中R1、R5、X、Q和n如前面所定义,得到式(VIII)的化合物。
(a)任选地被1、2或3个独立地选自下列基团的取代基取代的苯基:
(a-1)卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基,
(a-2)芳基或-O-(CH2)n-芳基,而该芳基或芳基部分任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代,
(a-3)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的5-员单环芳基,
(a-4)任选地被1、2或3个独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基和CN的取代基取代的6-员单环芳基,
(b)含有1、2、3或4个N原子的6-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(c)含有一个选自O、S和N的杂原子并且除所说的杂原子外还任选地含有1、2或3个N的5-员单环芳基,并且所说的单环芳基任选地被1、2或3个独立地选自上述(a-1)、(a-2)、(a-3)或(a-4)的基团的取代基取代;
(d)任选地被1或2个独立地选自OH、C1-4烷基、卤素和卤素取代的C1-4烷基的取代基取代的C3-7环烷基;和
(e)任选地被1、2或3个独立地选自上述(a-1)的基团的取代基取代的苯并稠合的杂环;R1为H、C1-4烷基或卤素;R2和R3独立地为H、OH、C1-4烷氧基、C1-4烷基或者是被卤素、OH、C1-4烷氧基、NH2或CN取代的C1-4烷基;X独立地选自卤素、C1-4烷基、卤素取代的C1-4烷基、OH、C1-4烷氧基、卤素取代的C1-4烷氧基、C1-C4烷硫基、NO2、NH2、二(C1-4烷基)氨基、C1-4烷基氨基、CN、HO-(C1-4)烷基、C1-4烷氧基-C1-4烷基、C1-4烷基磺酰基、氨基磺酰基、-NH2S(O)2NR2R3、乙酰基、-COOH、-C(O)O-C1-4烷基、C1-4烷基磺酰基氨基和C3-7环烷基;而n为0、1、2、3或4,该方法包括水解下式(XII)的化合物:
其中R5为C1-6烷基,R1、X、Q和n如前面所定义。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| IB9800003 | 1998-01-05 | ||
| CAPCT/IB98/00003 | 1998-01-05 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN1284064A true CN1284064A (zh) | 2001-02-14 |
Family
ID=11004645
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN98813530A Pending CN1284064A (zh) | 1998-01-05 | 1998-12-18 | 作为环加氧酶-2抑制剂的2,3-取代的吲哚化合物 |
Country Status (39)
| Country | Link |
|---|---|
| US (1) | US6608070B1 (zh) |
| EP (1) | EP1045833B1 (zh) |
| JP (1) | JP3347136B2 (zh) |
| KR (1) | KR100404054B1 (zh) |
| CN (1) | CN1284064A (zh) |
| AP (1) | AP869A (zh) |
| AR (1) | AR016977A1 (zh) |
| AT (1) | ATE308519T1 (zh) |
| AU (1) | AU748107B2 (zh) |
| BG (1) | BG104643A (zh) |
| BR (1) | BR9813124A (zh) |
| CA (1) | CA2316863A1 (zh) |
| CO (1) | CO4970807A1 (zh) |
| DE (1) | DE69832200T2 (zh) |
| DZ (1) | DZ2700A1 (zh) |
| EA (1) | EA200000614A1 (zh) |
| ES (1) | ES2255190T3 (zh) |
| GT (1) | GT199800205A (zh) |
| HN (1) | HN1997000098A (zh) |
| HR (1) | HRP20000454A2 (zh) |
| HU (1) | HUP0102922A3 (zh) |
| ID (1) | ID24876A (zh) |
| IL (1) | IL136885A0 (zh) |
| IS (1) | IS5532A (zh) |
| MA (1) | MA24736A1 (zh) |
| NO (1) | NO20003451L (zh) |
| OA (1) | OA11441A (zh) |
| PA (1) | PA8466201A1 (zh) |
| PE (1) | PE20000055A1 (zh) |
| PL (1) | PL341696A1 (zh) |
| SA (1) | SA99191299A (zh) |
| SK (1) | SK9912000A3 (zh) |
| TN (1) | TNSN99001A1 (zh) |
| TR (1) | TR200001906T2 (zh) |
| TW (1) | TW436482B (zh) |
| UY (2) | UY25332A1 (zh) |
| WO (1) | WO1999035130A1 (zh) |
| YU (1) | YU41600A (zh) |
| ZA (1) | ZA9911B (zh) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN111004121A (zh) * | 2019-12-09 | 2020-04-14 | 南京杰运医药科技有限公司 | 一种4-烷氧基乙酰乙酸酯类化合物的制备方法 |
Families Citing this family (21)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6555540B1 (en) * | 1999-06-30 | 2003-04-29 | Pfizer Inc | Combinations of aldose reductase inhibitors and selective cyclooxygenase-2 inhibitors |
| EP1065206B1 (en) * | 1999-07-02 | 2002-10-09 | Pfizer Inc. | Tetrazolylalkyl indole compounds as anti-inflammatory and analgesic agents |
| MXPA00006605A (es) * | 1999-07-02 | 2004-12-09 | Pfizer | Compuestos de carbonil-indol biciclicos como agentes antiinflamatorios/analgesicos. |
| CA2509881A1 (en) * | 2002-12-19 | 2004-07-08 | Elan Pharmaceuticals, Inc. | Substituted n-phenyl sulfonamide bradykinin antagonists |
| US7223785B2 (en) | 2003-01-22 | 2007-05-29 | Boehringer Ingelheim International Gmbh | Viral polymerase inhibitors |
| US7098231B2 (en) | 2003-01-22 | 2006-08-29 | Boehringer Ingelheim International Gmbh | Viral polymerase inhibitors |
| PL1534305T3 (pl) | 2003-05-07 | 2007-03-30 | Osteologix As | Leczenie zaburzeń chrząstek i kości solami strontu rozpuszczalnymi w wodzie |
| KR100795462B1 (ko) * | 2006-09-27 | 2008-01-16 | 한국생명공학연구원 | 인돌 유도체, 이의 제조방법 및 이를 유효성분으로함유하는 대사성 질환 예방 및 치료용 약학적 조성물 |
| CA2667053C (en) * | 2006-10-17 | 2015-04-28 | Stiefel Laboratories, Inc. | Talarazole metabolites |
| US20120022121A1 (en) * | 2007-11-29 | 2012-01-26 | Dalton James T | Indoles, derivatives and analogs thereof and uses therefor |
| JP2013525355A (ja) * | 2010-04-19 | 2013-06-20 | メタボリック ソリューションズ ディベロップメント カンパニー, エルエルシー | チアゾリジンジオン化合物の新規合成 |
| WO2012054110A2 (en) | 2010-07-07 | 2012-04-26 | Ardelyx, Inc. | Compounds and methods for inhibiting phosphate transport |
| WO2012006474A2 (en) | 2010-07-07 | 2012-01-12 | Ardelyx, Inc. | Compounds and methods for inhibiting phosphate transport |
| JP5827326B2 (ja) | 2010-07-07 | 2015-12-02 | アーデリクス,インコーポレーテッド | リン酸輸送を阻害する化合物及び方法 |
| WO2012006477A1 (en) * | 2010-07-07 | 2012-01-12 | Ardelyx, Inc. | Compounds and methods for inhibiting phosphate transport |
| EP2603507B1 (en) | 2010-08-10 | 2016-06-29 | Metabolic Solutions Development Company LLC | Synthesis for thiazolidinedione compounds |
| HUE031424T2 (en) | 2010-08-10 | 2017-07-28 | Octeta Therapeutics Llc | New synthesis of thiazolidinedione compounds |
| WO2013138600A1 (en) * | 2012-03-16 | 2013-09-19 | Rosen Eliot M | Radioprotector compounds |
| US9808443B1 (en) | 2016-11-28 | 2017-11-07 | King Saud University | Cyclooxygenase inhibitors |
| CN112409281B (zh) * | 2020-08-20 | 2022-11-18 | 上海大学 | (e)-3-(3-氯-2-氟-6-(1h-四氮唑-1-基)苯基)丙烯酸的合成方法 |
| US20240165148A1 (en) | 2021-03-15 | 2024-05-23 | Saul Yedgar | Hyaluronic acid-conjugated dipalmitoyl phosphatidyl ethanolamine in combination with non-steroidal anti-inflammatory drugs (nsaids) for treating or alleviating inflammatory diseases |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5604253A (en) * | 1995-05-22 | 1997-02-18 | Merck Frosst Canada, Inc. | N-benzylindol-3-yl propanoic acid derivatives as cyclooxygenase inhibitors |
| US5510368A (en) * | 1995-05-22 | 1996-04-23 | Merck Frosst Canada, Inc. | N-benzyl-3-indoleacetic acids as antiinflammatory drugs |
| CO5190664A1 (es) * | 1999-06-30 | 2002-08-29 | Pfizer Prod Inc | Terapia de combinacion para el tratamiento de migrana administracion de un receptor 5ht, cafeina y un inhibidor de ciclooxigenasa-2 |
-
1998
- 1998-12-17 AP APAP/P/1998/001423A patent/AP869A/en active
- 1998-12-18 EA EA200000614A patent/EA200000614A1/ru unknown
- 1998-12-18 YU YU41600A patent/YU41600A/sh unknown
- 1998-12-18 AT AT98959082T patent/ATE308519T1/de not_active IP Right Cessation
- 1998-12-18 DE DE69832200T patent/DE69832200T2/de not_active Expired - Fee Related
- 1998-12-18 IL IL13688598A patent/IL136885A0/xx unknown
- 1998-12-18 PL PL98341696A patent/PL341696A1/xx unknown
- 1998-12-18 TR TR2000/01906T patent/TR200001906T2/xx unknown
- 1998-12-18 EP EP98959082A patent/EP1045833B1/en not_active Expired - Lifetime
- 1998-12-18 KR KR10-2000-7007419A patent/KR100404054B1/ko not_active IP Right Cessation
- 1998-12-18 US US09/355,494 patent/US6608070B1/en not_active Expired - Fee Related
- 1998-12-18 CA CA002316863A patent/CA2316863A1/en not_active Abandoned
- 1998-12-18 ID IDW20001286A patent/ID24876A/id unknown
- 1998-12-18 CN CN98813530A patent/CN1284064A/zh active Pending
- 1998-12-18 BR BR9813124-9A patent/BR9813124A/pt not_active IP Right Cessation
- 1998-12-18 JP JP2000527531A patent/JP3347136B2/ja not_active Expired - Fee Related
- 1998-12-18 WO PCT/IB1998/002065 patent/WO1999035130A1/en active IP Right Grant
- 1998-12-18 AU AU15005/99A patent/AU748107B2/en not_active Ceased
- 1998-12-18 ES ES98959082T patent/ES2255190T3/es not_active Expired - Lifetime
- 1998-12-18 HU HU0102922A patent/HUP0102922A3/hu unknown
- 1998-12-18 SK SK991-2000A patent/SK9912000A3/sk unknown
- 1998-12-22 TW TW087120865A patent/TW436482B/zh active
- 1998-12-28 HN HN1997000098A patent/HN1997000098A/es unknown
- 1998-12-28 PE PE1998001288A patent/PE20000055A1/es not_active Application Discontinuation
- 1998-12-29 GT GT199800205A patent/GT199800205A/es unknown
- 1998-12-30 CO CO98077588A patent/CO4970807A1/es unknown
- 1998-12-31 UY UY25332A patent/UY25332A1/es not_active IP Right Cessation
-
1999
- 1999-01-04 TN TNTNSN99001A patent/TNSN99001A1/fr unknown
- 1999-01-04 MA MA25414A patent/MA24736A1/fr unknown
- 1999-01-04 ZA ZA9900011A patent/ZA9911B/xx unknown
- 1999-01-04 AR ARP990100010A patent/AR016977A1/es not_active Application Discontinuation
- 1999-01-04 DZ DZ990001A patent/DZ2700A1/xx active
- 1999-01-05 PA PA19998466201A patent/PA8466201A1/es unknown
- 1999-04-13 SA SA99191299A patent/SA99191299A/ar unknown
- 1999-06-28 UY UY25590A patent/UY25590A1/es not_active Application Discontinuation
-
2000
- 2000-06-13 IS IS5532A patent/IS5532A/is unknown
- 2000-06-30 OA OA1200000195A patent/OA11441A/en unknown
- 2000-07-04 NO NO20003451A patent/NO20003451L/no unknown
- 2000-07-05 HR HR20000454A patent/HRP20000454A2/hr not_active Application Discontinuation
- 2000-07-28 BG BG104643A patent/BG104643A/bg unknown
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN111004121A (zh) * | 2019-12-09 | 2020-04-14 | 南京杰运医药科技有限公司 | 一种4-烷氧基乙酰乙酸酯类化合物的制备方法 |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN1284064A (zh) | 作为环加氧酶-2抑制剂的2,3-取代的吲哚化合物 | |
| CN1196692C (zh) | 用于治疗发炎的取代的苯并吡喃衍生物 | |
| CN1150181C (zh) | 用于治疗炎症的取代的苯并吡喃类似物 | |
| EP1104760B1 (en) | Sulfamoylheteroaryl pyrazole compounds as anti-inflammatory/analgesic agents | |
| CN1217936C (zh) | 含有磺酰胺的杂环化合物 | |
| CA2313122C (en) | Bicycliccarbonyl indole compounds as anti-inflammatory/analgesic agents | |
| CA2281426C (en) | Substituted indole compounds as anti-inflammatory and analgesic agents | |
| CN1829709A (zh) | 对抗黄病毒的双环咪唑衍生物 | |
| CN1441783A (zh) | 含二氰基吡啶衍生物的药物 | |
| CN101061092A (zh) | 烟酸受体激动剂、含有这样化合物的组合物和治疗方法 | |
| WO2005105777A1 (en) | Substituted thiophene amide compounds for the treatment of inflammation | |
| CZ20002455A3 (cs) | 2,3-Substituované indoly, farmaceutické kompozice na jejich bázi, způsob léčení a způsoby výroby | |
| CA2313106C (en) | Tetrazolylalkyl indole compounds as anti-inflammatory and analgesic agents |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C02 | Deemed withdrawal of patent application after publication (patent law 2001) | ||
| WD01 | Invention patent application deemed withdrawn after publication | ||
| REG | Reference to a national code |
Ref country code: HK Ref legal event code: WD Ref document number: 1033670 Country of ref document: HK |