本申请要求在2019年10月24日提交的美国专利申请第62/925,596号;以及在2020年6月26日提交的美国专利申请第63/044,898号的利益,所述美国专利申请两者均通过引用以它们的整体并入本文中。
具体实施方式
如在本文中和在所附权利要求书中所用的,单数形式“一种”、“一个”和“所述”包括复数指代物,除非上下文另有明确说明。因此,例如,提及“一种药剂”包括多种这样的药剂,而提及“所述细胞”包括提及一种或多种细胞(或多个细胞)和本领域技术人员已知的其等同物,等等。当本文中针对物理性质例如分子量或化学性质例如化学式使用范围时,旨在包括范围和其中具体实施方案的所有组合和子组合。当提及数字或数值范围时术语“约”是指所提及的数字或数值范围为在实验可变性内(或者在统计实验误差内)的近似值,因此在一些情况下,该数字或数值范围将在所述数字或数值范围的1%至15%之间变化。术语“包含”(以及相关的术语,例如“包括”或“具有”或“含有”)并非旨在排除,在其他某些实施方案中,例如,本文描述的任何物质组成、组合物、方法或过程等的实施方案中,“由所述特征组成”或“基本上由所述特征组成”。
定义
如在本说明书及所附权利要求书中所使用的,除非相反地指出,否则下列术语具有以下所述的含义。
“氨基”是指–NH2基团。
“氰基”是指-CN基团。
“硝基”是指-NO2基团。
“氧杂”是指-O-基团。
“氧代”是指=O基团。
“硫代”是指=S基团。
“亚氨基”是指=N-H基团。
“肟基”是指=N-OH基团。
“肼基”是指=N-NH2基团。
“烷基”是指仅由碳原子和氢原子组成、不含不饱和度、具有1-15个碳原子(例如,C1-C15烷基)的直链或支链的烃链基团。在某些实施方案中,烷基包含1至13个碳原子(例如,C1-C13烷基)。在某些实施方案中,烷基包含1至8个碳原子(例如,C1-C8烷基)。在其他实施方案中,烷基包含1至5个碳原子(例如,C1-C5烷基)。在其他实施方案中,烷基包含1至4个碳原子(例如,C1-C4烷基)。在其他实施方案中,烷基包含1至3个碳原子(例如,C1-C3烷基)。在其他实施方案中,烷基包含1至2个碳原子(例如,C1-C2烷基)。在其他实施方案中,烷基包含一个碳原子(例如,C1烷基)。在其他实施方案中,烷基包含5至15个碳原子(例如,C5-C15烷基)。在其他实施方案中,烷基包含5至8个碳原子(例如,C5-C8烷基)。在其他实施方案中,烷基包含2至5碳原子(例如,C2-C5烷基)。在其他实施方案中,烷基包含3至5个碳原子(例如,C3-C5烷基)。在其他实施方案中,烷基选自甲基、乙基、1-丙基(正丙基)、1-甲基乙基(异丙基)、1-丁基(正丁基)、1-甲基丙基(仲丁基)、2-甲基丙基(异丁基)、1,1-二甲基乙基(叔丁基)、1-戊基(正戊基)。该烷基通过单键而与分子的其余部分连接。除非在说明书中另有明确规定,否则烷基任选地被一个或多个下列取代基取代:卤代、氰基、硝基、氧代、硫代、亚氨基、肟基、三甲基甲硅烷基、-ORa、-SRa、-OC(O)-Ra、-N(Ra)2、-C(O)Ra、-C(O)ORa、-C(O)N(Ra)2、-N(Ra)C(O)ORa、-OC(O)-N(Ra)2、-N(Ra)C(O)Ra、-N(Ra)S(O)tRa(其中t为1或2)、-S(O)tORa(其中t为1或2)、-S(O)tRa(其中t为1或2)和-S(O)tN(Ra)2(其中t为1或2),其中每个Ra独立地为氢、烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、氟烷基、碳环基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、碳环基烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、芳基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、芳烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、杂环基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、杂环基烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、杂芳基(任选地被卤素、羟基、甲氧基或三氟甲基取代)或杂芳基烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)。
“烷氧基”是指通过式-O-烷基的氧原子键合的基团,其中烷基为如上定义的烷基链。
“烯基”是指仅由碳原子和氢原子组成、含有至少一个碳碳双键且具有2-12个碳原子的直链或支链的烃链基团。在某些实施方案中,烯基包含2至8个碳原子。在其他实施方案中,烯基包含2至4个碳原子。烯基通过单键而与分子的其余部分连接,例如,乙烯基、丙-1-烯基(即烯丙基)、丁-1-烯基、戊-1-烯基、戊-1,4-二烯基等。除非在说明书中另有明确规定,否则烯基任选地被一个或多个下列取代基取代:卤代、氰基、硝基、氧代、硫代、亚氨基、肟基、三甲基甲硅烷基、-ORa、-SRa、-OC(O)-Ra、-N(Ra)2、-C(O)Ra、-C(O)ORa、-C(O)N(Ra)2、-N(Ra)C(O)ORa、-OC(O)-N(Ra)2、-N(Ra)C(O)Ra、-N(Ra)S(O)tRa(其中t为1或2)、-S(O)tORa(其中t为1或2)、-S(O)tRa(其中t为1或2)和-S(O)tN(Ra)2(其中t为1或2),其中每个Ra独立地为氢、烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、氟烷基、碳环基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、碳环基烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、芳基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、芳烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、杂环基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、杂环基烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、杂芳基(任选地被卤素、羟基、甲氧基或三氟甲基取代)或杂芳基烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)。
“炔基”是指仅由碳原子和氢原子组成、含有至少一个碳碳三键、具有2-12个碳原子的直链或支链的烃链基团。在某些实施方案中,炔基包含2至8个碳原子。在其他实施方案中,炔基包含2至6个碳原子。在其他实施方案中,炔基包含2至4个碳原子。炔基通过单键而与分子的其余部分连接,例如,乙炔基、丙炔基、丁炔基、戊炔基、己炔基等。除非在说明书中另有明确规定,否则炔基任选地被一个或多个下列取代基取代:卤代、氰基、硝基、氧代、硫代、亚氨基、肟基、三甲基甲硅烷基、-ORa、-SRa、-OC(O)-Ra、-N(Ra)2、-C(O)Ra、-C(O)ORa、-C(O)N(Ra)2、-N(Ra)C(O)ORa、-OC(O)-N(Ra)2、-N(Ra)C(O)Ra、-N(Ra)S(O)tRa(其中t为1或2)、-S(O)tORa(其中t为1或2)、-S(O)tRa(其中t为1或2)和-S(O)tN(Ra)2(其中t为1或2),其中每个Ra独立地为氢、烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、氟烷基、碳环基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、碳环基烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、芳基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、芳烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、杂环基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、杂环基烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、杂芳基(任选地被卤素、羟基、甲氧基或三氟甲基取代)或杂芳基烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)。
“亚烷基”或“亚烷基链”指将分子的其余部分与基团连接的直链或支链二价烃链,其仅由碳和氢组成,不包含不饱和度并具有1-12个碳原子,例如,亚甲基、亚乙基、亚丙基、亚正丁基等。亚烷基链通过单键而与该分子的其余部分连接并通过单键而与该基团连接。亚烷基链与分子的其余部分以及与基团的连接点是通过亚烷基链中的一个碳或通过该链内的任何两个碳。在某些实施方案中,亚烷基包含1至8个碳原子(例如,C1-C8亚烷基)。在其他实施方案中,亚烷基包含1至5个碳原子(例如,C1-C5亚烷基)。在其他实施方案中,亚烷基包含1至4个碳原子(例如,C1-C4亚烷基)。在其他实施方案中,亚烷基包含1至3个碳原子(例如,C1-C3亚烷基)。在其他实施方案中,亚烷基包含1至2个碳原子(例如,C1-C2亚烷基)。在其他实施方案中,亚烷基包含1个碳原子(例如,C1亚烷基)。在其他实施方案中,亚烷基包含5至8个碳原子(例如,C5-C8亚烷基)。在其他实施方案中,亚烷基包含2至5个碳原子(例如,C2-C5亚烷基)。在其他实施方案中,亚烷基包含3至5个碳原子(例如,C3-C5亚烷基)。除非在说明书中另有明确规定,否则亚烷基链任选地被一个或多个下列取代基取代:卤代、氰基、硝基、氧代、硫代、亚氨基、肟基、三甲基甲硅烷基、-ORa、-SRa、-OC(O)-Ra、-N(Ra)2、-C(O)Ra、-C(O)ORa、-C(O)N(Ra)2、-N(Ra)C(O)ORa、-OC(O)-N(Ra)2、-N(Ra)C(O)Ra、-N(Ra)S(O)tRa(其中t为1或2)、-S(O)tORa(其中t为1或2)、-S(O)tRa(其中t为1或2)和-S(O)tN(Ra)2(其中t为1或2),其中每个Ra独立地为氢、烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、氟烷基、碳环基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、碳环基烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、芳基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、芳烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、杂环基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、杂环基烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、杂芳基(任选地被卤素、羟基、甲氧基或三氟甲基取代)或杂芳基烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)。
“亚烯基”或“亚烯基链”是指将分子的其余部分与基团连接的直链或支链二价烃链,其仅由碳和氢组成,含有至少一个碳碳双键,并且具有2至12个碳原子。亚烯基链通过单键连接至分子的其余部分,并且通过单键连接至基团。在某些实施方案中,亚烯基包含2至8个碳原子(例如,C2-C8亚烯基)。在其他实施方案中,亚烯基包含2至5个碳原子(例如,C2-C5亚烯基)。在其他实施方案中,亚烯基包含2至4个碳原子(例如,C2-C4亚烯基)。在其他实施方案中,亚烯基包含2至3个碳原子(例如,C2-C3亚烯基)。在其他实施方案中,亚烯基包含2个碳原子(例如,C2亚烯基)。在其他实施方案中,亚烯基包含5至8个碳原子(例如,C5-C8亚烯基)。在其他实施方案中,亚烯基包含3至5个碳原子(例如,C3-C5亚烯基)。除非在说明书中另有明确规定,否则亚烯基链任选地被一个或多个下列取代基取代:卤代、氰基、硝基、氧代、硫代、亚氨基、肟基、三甲基甲硅烷基、-ORa、-SRa、-OC(O)-Ra、-N(Ra)2、-C(O)Ra、-C(O)ORa、-C(O)N(Ra)2、-N(Ra)C(O)ORa、-OC(O)-N(Ra)2、-N(Ra)C(O)Ra、-N(Ra)S(O)tRa(其中t为1或2)、-S(O)tORa(其中t为1或2)、-S(O)tRa(其中t为1或2)和-S(O)tN(Ra)2(其中t为1或2),其中每个Ra独立地为氢、烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、氟烷基、碳环基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、碳环基烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、芳基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、芳烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、杂环基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、杂环基烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、杂芳基(任选地被卤素、羟基、甲氧基或三氟甲基取代)或杂芳基烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)。
“亚炔基”或“亚炔基链”是指将分子的其余部分与基团连接的直链或支链二价烃链,其仅由碳和氢组成,含有至少一个碳碳三键,并且具有2至12个碳原子。亚炔基链通过单键连接至分子的其余部分,并且通过单键连接至基团。在某些实施方案中,亚炔基包含2至8个碳原子(例如,C2-C8亚炔基)。在其他实施方案中,亚炔基包含2至5个碳原子(例如,C2-C5亚炔基)。在其他实施方案中,亚炔基包含2至4个碳原子(例如,C2-C4亚炔基)。在其他实施方案中,亚炔基包含2至3个碳原子(例如,C2-C3亚炔基)。在其他实施方案中,亚炔基包含2个碳原子(例如,C2亚炔基)。在其他实施方案中,亚炔基包含5至8个碳原子(例如,C5-C8亚炔基)。在其他实施方案中,亚炔基包含3至5个碳原子(例如,C3-C5亚炔基)。除非在说明书中另有明确规定,否则亚炔基链任选地被一个或多个下列取代基取代:卤代、氰基、硝基、氧代、硫代、亚氨基、肟基、三甲基甲硅烷基、-ORa、-SRa、-OC(O)-Ra、-N(Ra)2、-C(O)Ra、-C(O)ORa、-C(O)N(Ra)2、-N(Ra)C(O)ORa、-OC(O)-N(Ra)2、-N(Ra)C(O)Ra、-N(Ra)S(O)tRa(其中t为1或2)、-S(O)tORa(其中t为1或2)、-S(O)tRa(其中t为1或2)和-S(O)tN(Ra)2(其中t为1或2),其中每个Ra独立地为氢、烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、氟烷基、碳环基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、碳环基烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、芳基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、芳烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、杂环基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、杂环基烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、杂芳基(任选地被卤素、羟基、甲氧基或三氟甲基取代)或杂芳基烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)。
“芳基”是指通过从环碳原子上去除氢原子而由芳族单环或多环烃环体系衍生的基团。芳族单环或多环烃环体系仅包含氢和5-18个碳原子的碳,其中该环体系中的至少一个环是完全不饱和的,即,其根据休克尔(Hückel)理论包含环状、离域的(4n+2)π-电子体系。衍生出芳基的环体系包括但不限于基团诸如苯、芴、茚满、茚、四氢化萘和萘。除非在说明书中另有明确说明,否则术语“芳基”或前缀“芳”(例如在“芳烷基”中)意在包括任选地被独立地选自以下各项中的一个或多个取代基取代的芳基基团:烷基、烯基、炔基、卤代、氟烷基、氰基、硝基、任选取代的芳基、任选取代的芳烷基、任选取代的芳烯基、任选取代的芳炔基、任选取代的碳环基、任选取代的碳环基烷基、任选取代的杂环基、任选取代的杂环基烷基、任选取代的杂芳基、任选取代的杂芳基烷基、-Rb-ORa、-Rb-OC(O)-Ra、-Rb-OC(O)-ORa、-Rb-OC(O)-N(Ra)2、-Rb-N(Ra)2、-Rb-C(O)Ra、-Rb-C(O)ORa、-Rb-C(O)N(Ra)2、-Rb-O-Rc-C(O)N(Ra)2、-Rb-N(Ra)C(O)ORa、-Rb-N(Ra)C(O)Ra、-Rb-N(Ra)S(O)tRa(其中t为1或2)、-Rb-S(O)tRa(其中t为1或2)、-Rb-S(O)tORa(其中t为1或2)和-Rb-S(O)tN(Ra)2(其中t为1或2),其中每个Ra独立地为氢、烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、氟烷基、环烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、环烷基烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、芳基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、芳烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、杂环基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、杂环基烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、杂芳基(任选地被卤素、羟基、甲氧基或三氟甲基取代)或杂芳基烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代),每个Rb独立地为直接键或直链或支链亚烷基或亚烯基链,且Rc为直链或支链亚烷基或亚烯基链,并且其中除非另有说明,否则上述取代基中的每一个为未取代的。
“芳烷基”是指式-Rc-芳基的基团,其中Rc为如上文所定义的亚烷基链,例如,亚甲基、亚乙基等。芳烷基基团的亚烷基链部分任选地被取代,如上文针对亚烷基链所述。芳烷基基团的芳基部分任选地被取代,如上文针对芳基所述。
“芳烯基”是指式-Rd-芳基的基团,其中Rd为如上文所定义的亚烯基链。芳烯基基团的芳基部分任选地被取代,如上文针对芳基所述。芳烯基基团的亚烯基链部分任选地被取代,如上文针对亚烯基所述。
“芳炔基”是指式-Re-芳基的基团,其中Re为如上文所定义的亚炔基链。芳炔基基团的芳基部分任选地被取代,如上文针对芳基所述。芳炔基基团的亚炔基链部分任选地被取代,如上文针对亚炔基链所述。
“芳烷氧基”是指通过式-O-Rc-芳基的氧原子键合的基团,其中Rc为如上文所定义的亚烷基链,例如,亚甲基、亚乙基等。芳烷基基团的亚烷基链部分任选地被取代,如上文针对亚烷基链所述。芳烷基基团的芳基部分任选地被取代,如上文针对芳基所述。
“碳环基”是指仅由碳原子和氢原子组成的稳定的非芳族单环或多环烃基团,其包括稠环或桥环体系,具有3至15个碳原子。在某些实施方案中,碳环基包含3至10个碳原子。在其他实施方案中,碳环基包含5至7个碳原子。该碳环基通过单键而与分子的其余部分连接。碳环基是饱和的(即仅包含C-C单键)或不饱和的(即含有一个或多个双键或三键)。完全饱和的碳环基基团还被称为“环烷基”。单环环烷基的实例包括,例如,环丙基、环丁基、环戊基、环己基、环庚基和环辛基。不饱和的碳环基还被称为“环烯基”。单环环烯基的实例包括,例如,环戊烯基、环己烯基、环庚烯基和环辛烯基。多环碳环基基团包括,例如,金刚烷基、降冰片基(即,双环[2.2.1]庚烷基)、降冰片烯基、十氢萘基、7,7-二甲基-双环[2.2.1]庚烷基等。除非在说明书中另有明确说明,否则术语“碳环基”意在包括任选地被独立地选自以下各项中的一个或多个取代基取代的碳环基基团:烷基、烯基、炔基、卤代、氟烷基、氧代、硫代、氰基、硝基、任选取代的芳基、任选取代的芳烷基、任选取代的芳烯基、任选取代的芳炔基、任选取代的碳环基、任选取代的碳环基烷基、任选取代的杂环基、任选取代的杂环基烷基、任选取代的杂芳基、任选取代的杂芳基烷基、-Rb-ORa、-Rb-OC(O)-Ra、-Rb-OC(O)-ORa、-Rb-OC(O)-N(Ra)2、-Rb-N(Ra)2、-Rb-C(O)Ra、-Rb-C(O)ORa、-Rb-C(O)N(Ra)2、-Rb-O-Rc-C(O)N(Ra)2、-Rb-N(Ra)C(O)ORa、-Rb-N(Ra)C(O)Ra、-Rb-N(Ra)S(O)tRa(其中t为1或2)、-Rb-S(O)tRa(其中t为1或2)、-Rb-S(O)tORa(其中t为1或2)和-Rb-S(O)tN(Ra)2(其中t为1或2),其中每个Ra独立地为氢、烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、氟烷基、环烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、环烷基烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、芳基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、芳烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、杂环基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、杂环基烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、杂芳基(任选地被卤素、羟基、甲氧基或三氟甲基取代)或杂芳基烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代),每个Rb独立地为直接键或直链或支链亚烷基或亚烯基链,且Rc为直链或支链亚烷基或亚烯基链,并且除非另有说明,否则其中上述取代基中的每一个为未取代的。
“碳环基烷基”是指式-Rc-碳环基的基团,其中Rc为如上文所定义的亚烷基链。亚烷基链和碳环基基团任选地被取代,如上文所述。
“碳环基炔基”是指式-Rc-碳环基的基团,其中Rc为如上文所定义的亚炔基链。亚炔基链和碳环基基团任选地被取代,如上文所述。
“碳环基烷氧基”是指通过式-O-Rc-碳环基的氧原子键合的基团,其中Rc为如上所定义的亚烷基链。亚烷基链和碳环基基团任选地被取代,如上文所述。
如本文所用的,“羧酸生物电子等排体”是指表现出与羧酸部分类似的物理、生物和/或化学性质的官能团或部分。羧酸生物电子等排体的实例包括但不限于:
“卤代”或“卤素”是指溴代、氯代、氟代或碘代取代基。
“氟烷基”是指被如上定义的一个或多个氟代基团取代的如上定义的烷基基团,例如,三氟甲基、二氟甲基、氟甲基、2,2,2-三氟乙基、1-氟甲基-2-氟乙基等。在一些实施方案中,氟烷基的烷基部分任选地被取代,如以上针对烷基所述。
“杂环基”是指稳定的3至18元非芳族环基团,其包含2至12个碳原子和1至6个选自氮、氧和硫中的杂原子。除非在说明书中另有明确说明,否则杂环基基团是单环、双环、三环或四环的环体系,其任选地包括稠环或桥环体系。杂环基基团中的杂原子任选地被氧化。如果存在一个或多个氮原子,则其任选地被季铵化。杂环基是部分或完全饱和的。杂环基通过环中的任何原子连接至分子的其余部分。这类杂环基基团的实例包括但不限于二氧杂环戊基、噻吩基[1,3]二噻烷基、十氢异喹啉基、咪唑啉基、咪唑烷基、异噻唑烷基、异噁唑烷基、吗啉基、八氢吲哚基、八氢异吲哚基、2-氧代哌嗪基、2-氧代哌啶基、2-氧代吡咯烷基、噁唑烷基、哌啶基、哌嗪基、4-哌啶酮基、吡咯烷基、吡唑烷基、奎宁环基、噻唑烷基、四氢呋喃基、三噻烷基、四氢吡喃基、硫代吗啉基(thiomorpholinyl)、硫杂吗啉基(thiamorpholinyl)、1-氧代-硫代吗啉基和1,1-二氧代-硫代吗啉基。除非在说明书中另有明确说明,否则术语“杂环基”意在包括任选地被选自以下各项中的一个或多个取代基取代的如上定义的杂环基基团:烷基、烯基、炔基、卤代、氟烷基、氧代、硫代、氰基、硝基、任选取代的芳基、任选取代的芳烷基、任选取代的芳烯基、任选取代的芳炔基、任选取代的碳环基、任选取代的碳环基烷基、任选取代的杂环基、任选取代的杂环基烷基、任选取代的杂芳基、任选取代的杂芳基烷基、-Rb-ORa、-Rb-OC(O)-Ra、-Rb-OC(O)-ORa、-Rb-OC(O)-N(Ra)2、-Rb-N(Ra)2、-Rb-C(O)Ra、-Rb-C(O)ORa、-Rb-C(O)N(Ra)2、-Rb-O-Rc-C(O)N(Ra)2、-Rb-N(Ra)C(O)ORa、-Rb-N(Ra)C(O)Ra、-Rb-N(Ra)S(O)tRa(其中t为1或2)、-Rb-S(O)tRa(其中t为1或2)、-Rb-S(O)tORa(其中t为1或2)和-Rb-S(O)tN(Ra)2(其中t为1或2),其中每个Ra独立地为氢、烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、氟烷基、环烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、环烷基烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、芳基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、芳烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、杂环基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、杂环基烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、杂芳基(任选地被卤素、羟基、甲氧基或三氟甲基取代)或杂芳基烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代),每个Rb独立地为直接键或直链或支链亚烷基或亚烯基链,且Rc为直链或支链亚烷基或亚烯基链,并且除非另有说明,否则其中上述取代基中的每一个为未取代的。
“N-杂环基”或“N-连接的杂环基”是指含有至少一个氮的如上定义的杂环基基团,并且其中该杂环基基团与该分子的其余部分的连接点是通过该杂环基基团中的氮原子。N-杂环基基团任选地被取代,如上文针对杂环基基团所述。这样的N-杂环基基团的实例包括但不限于1-吗啉基、1-哌啶基、1-哌嗪基、1-吡咯烷基、吡唑烷基、咪唑啉基和咪唑烷基。
“C-杂环基”或“C-连接的杂环基”是指含有至少一个杂原子的如上定义的杂环基基团,并且其中该杂环基基团与该分子的其余部分的连接点是通过该杂环基基团中的碳原子。C-杂环基基团任选地被取代,如上文针对杂环基基团所述。这样的C-杂环基基团的实例包括但不限于2-吗啉基、2-或3-或4-哌啶基、2-哌嗪基、2-或3-吡咯烷基等。
“杂环基烷基”是指式-Rc-杂环基的基团,其中Rc为如上所定义的亚烷基链。如果杂环基为含氮的杂环基,则该杂环基任选地在该氮原子处连接至烷基基团。杂环基烷基基团的亚烷基链任选地被取代,如上文针对亚烷基链所述。杂环基烷基基团的杂环基部分任选地被取代,如上文针对杂环基所述。
“杂环基烷氧基”是指通过式-O-Rc-杂环基的氧原子键合的基团,其中Rc为如上所定义的亚烷基链。如果杂环基为含氮的杂环基,则该杂环基任选地在该氮原子处连接至烷基基团。杂环基烷氧基基团的亚烷基链任选地被取代,如上文针对亚烷基链所述。杂环基烷氧基基团的杂环基部分任选地被取代,如上文针对杂环基所述。
“杂芳基”是指由包含2至17个碳原子以及选自氮、氧和硫中的1至6个杂原子的3至18元芳族环基团衍生的基团。如本文所用的,杂芳基基团是单环、双环、三环或四环环体系,其中该环体系中的至少一个环是完全不饱和的,即,其根据休克尔理论包含环状、离域的(4n+2)π–电子体系。杂芳基包括稠环或桥环体系。杂芳基基团中的杂原子任选地被氧化。如果存在一个或多个氮原子,则其任选地被季铵化。杂芳基通过环中的任何原子而与分子的其余部分连接。杂芳基的实例包括但不限于氮杂
基、吖啶基、苯并咪唑基、苯并吲哚基、1,3-苯并二氧杂环戊基、苯并呋喃基、苯并噁唑基、苯并[d]噻唑基、苯并噻二唑基、苯并[b][1,4]二氧杂
基、苯并[b][1,4]噁嗪基、1,4-苯并二噁烷基、苯并萘并呋喃基(benzonaphthofuranyl)、苯并噁唑基、苯并二氧杂环戊基、苯并二噁英基(benzodioxinyl)、苯并吡喃基、苯并吡喃酮基(benzopyranonyl)、苯并呋喃基、苯并呋喃酮基(benzofuranonyl)、苯并噻吩基(benzothienyl)(benzothiophenyl)、苯并噻吩并[3,2-d]嘧啶基、苯并三唑基、苯并[4,6]咪唑并[1,2-a]吡啶基、咔唑基、噌啉基、环戊并[d]嘧啶基、6,7-二氢-5H-环戊并[4,5]噻吩并[2,3-d]嘧啶基、5,6-二氢苯并[h]喹唑啉基、5,6-二氢苯并[h]噌啉基、6,7-二氢-5H-苯并[6,7]环庚并[1,2-c]哒嗪基、二苯并呋喃基、二苯并噻吩基、呋喃基、呋喃酮基、呋喃并[3,2-c]吡啶基、5,6,7,8,9,10-六氢环辛并[d]嘧啶基、5,6,7,8,9,10-六氢环辛并[d]哒嗪基、5,6,7,8,9,10-六氢环辛并[d]吡啶基、异噻唑基、咪唑基、吲唑基、吲哚基、吲唑基、异吲哚基、吲哚啉基、异吲哚啉基、异喹啉基、吲嗪基、异噁唑基、5,8-甲桥-5,6,7,8-四氢喹唑啉基、萘啶基、1,6-萘啶酮基(1,6-naphthyridinonyl)、噁二唑基、2-氧代氮杂

基、噁唑基、环氧乙烷基、5,6,6a,7,8,9,10,10a-八氢苯并[h]喹唑啉基、1-苯基-1H-吡咯基、吩嗪基、吩噻嗪基、吩噁嗪基、酞嗪基、蝶啶基、嘌呤基、吡咯基、吡唑基、吡唑并[3,4-d]嘧啶基、吡啶基、吡啶并[3,2-d]嘧啶基、吡啶并[3,4-d]嘧啶基、吡嗪基、嘧啶基、哒嗪基、吡咯基、喹唑啉基、喹喔啉基、喹啉基、异喹啉基、四氢喹啉基、5,6,7,8-四氢喹唑啉基、5,6,7,8-四氢苯并[4,5]噻吩并[2,3-d]嘧啶基、6,7,8,9-四氢-5H-环庚并[4,5]噻吩并[2,3-d]嘧啶基、5,6,7,8-四氢吡啶并[4,5-c]哒嗪基、噻唑基、噻二唑基、三唑基、四唑基、三嗪基、噻吩并[2,3-d]嘧啶基、噻吩并[3,2-d]嘧啶基、噻吩并[2,3-c]吡啶基和噻吩基(thiophenyl)(即噻吩基(thienyl))。除非在说明书中另有明确说明,否则术语“杂芳基”意在包括任选地被选自以下各项中的一个或多个取代基取代的如上所定义的杂芳基基团:烷基、烯基、炔基、卤代、氟烷基、卤代烯基、卤代炔基、氧代、硫代、氰基、硝基、任选取代的芳基、任选取代的芳烷基、任选取代的芳烯基、任选取代的芳炔基、任选取代的碳环基、任选取代的碳环基烷基、任选取代的杂环基、任选取代的杂环基烷基、任选取代的杂芳基、任选取代的杂芳基烷基、-R
b-OR
a、-R
b-OC(O)-R
a、-R
b-OC(O)-OR
a、-R
b-OC(O)-N(R
a)
2、-R
b-N(R
a)
2、-R
b-C(O)R
a、-R
b-C(O)OR
a、-R
b-C(O)N(R
a)
2、-R
b-O-R
c-C(O)N(R
a)
2、-R
b-N(R
a)C(O)OR
a、-R
b-N(R
a)C(O)R
a、-R
b-N(R
a)S(O)
tR
a(其中t为1或2)、-R
b-S(O)
tR
a(其中t为1或2)、-R
b-S(O)
tOR
a(其中t为1或2)和-R
b-S(O)
tN(R
a)
2(其中t为1或2),其中每个R
a独立地为氢、烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、氟烷基、环烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、环烷基烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、芳基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、芳烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、杂环基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、杂环基烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代)、杂芳基(任选地被卤素、羟基、甲氧基或三氟甲基取代)或杂芳基烷基(任选地被卤素、羟基、甲氧基或三氟甲基取代),每个R
b独立地为直接键或直链或支链亚烷基或亚烯基链,且R
c为直链或支链的亚烷基或亚烯基链,并且除非另有说明,否则其中上述取代基中的每一个为未取代的。
“N-杂芳基”是指含有至少一个氮的如上定义的杂芳基基团,并且其中该杂芳基基团与该分子的其余部分的连接点是通过该杂芳基基团中的氮原子。N-杂芳基基团任选地被取代,如上文针对杂芳基基团所述。
“C-杂芳基”是指如上所定义的杂芳基,其中该杂芳基基团与该分子的其余部分的连接点是通过该杂芳基基团中的碳原子。C-杂芳基基团任选地被取代,如上文针对杂芳基基团所述。
“杂芳基烷基”是指式–Rc-杂芳基的基团,其中Rc为如上所定义的亚烷基链。如果杂芳基为含氮的杂芳基,则该杂芳基任选地在该氮原子处与烷基基团连接。杂芳基烷基基团的亚烷基链任选地被取代,如上文针对亚烷基链所定义的。杂芳基烷基基团的杂芳基部分任选地被取代,如上文针对杂芳基所定义的。
“杂芳基烷氧基”是指通过式–O-Rc-杂芳基的氧原子键合的基团,其中Rc为如上所定义的亚烷基链。如果杂芳基为含氮的杂芳基,则该杂芳基任选地在该氮原子处与烷基基团连接。杂芳基烷氧基基团的亚烷基链任选地被取代,如上文针对亚烷基链所定义的。杂芳基烷氧基基团的杂芳基部分任选地被取代,如上文针对杂芳基所定义的。
在一些实施方案中,本文公开的化合物含有一个或多个不对称中心,因此产生了对映异构体、非对映异构体以及根据绝对立体化学被定义为(R)-或(S)-的其他立体异构形式。除非另有说明,否则本公开意在涉及本文公开的化合物的所有立体异构形式。当本文所述的化合物含有烯烃双键时,除非另有说明,否则本公开意在同时包括E和Z几何异构体(例如,顺式或反式)。同样,还意在包括所有可能的异构体,以及其外消旋形式和光学纯形式,和所有互变异构形式。术语“几何异构体”是指烯烃双键的E或Z几何异构体(例如顺式或反式)。术语“位置异构体”是指围绕中心环的结构异构体,如围绕苯环的邻位、间位和对位异构体。
“互变异构体”是指这样的分子,其中质子从分子的一个原子移动到同一分子的另一原子是可能的。在某些实施方案中,本文提出的化合物作为互变异构体存在。在可能发生互变异构的情形下,将存在互变异构体的化学平衡。互变异构体的确切比例取决于若干因素,包括物理状态、温度、溶剂和pH。互变异构平衡的一些实例包括:
在一些实施方案中,本文公开的化合物以不同的富集同位素形式使用,例如,富含2H、3H、11C、13C和/或14C含量的形式。在一个特定实施方案中,所述化合物在至少一个位置处被氘化。这类氘化形式可通过美国专利号5,846,514和6,334,997所述的程序制备。如美国专利号5,846,514和6,334,997所述,氘化可改善代谢稳定性和/或功效,从而增加药物作用的持续时间。
除非另有说明,否则本文所示的结构旨在包括仅在是否存在一个或多个同位素富集的原子方面不同的化合物。例如,除了氢被氘或氚替代或者碳被13C-或14C-富集的碳替代之外具有本结构的化合物也在本公开的范围内。
本公开的化合物任选地在构成此类化合物的一个或多个原子处含有非天然比例的原子同位素。例如,可使用同位素如氘(2H)、氚(3H)、碘-125(125I)或碳-14(14C)来标记化合物。用2H、11C、13C、14C、15C、12N、13N、15N、16N、16O、17O、14F、15F、16F、17F、18F、33S、34S、35S、36S、35Cl、37Cl、79Br、81Br、125I进行的同位素取代均在设想之内。在一些实施方案中,考虑用18F进行同位素取代。本发明化合物的所有同位素变化,无论是否为放射性的,均包括在本发明的范围内。
在某些实施方案中,本文公开的化合物的一些或全部1H原子被2H原子替代。含氘化合物的合成方法是本领域已知的,仅作为非限制性实例,包括以下合成方法。
使用各种方法来合成氘取代的化合物,所述方法例如描述于:Dean,Dennis C.编.Recent Advances in the Synthesis and Applications of Radiolabeled Compoundsfor Drug Discovery and Development.[Curr.,Pharm.Des.,2000;6(10)]2000,110 pp;George W.;Varma,Rajender S.The Synthesis of Radiolabeled Compounds viaOrganometallic Intermediates,Tetrahedron,1989,45(21),6601-21;以及Evans,E.Anthony.Synthesis of radiolabeled compounds,J.Radioanal.Chem.,1981,64(1-2),9-32。
氘化的起始材料容易获得,并且经受本文所述的合成方法以提供含氘化合物的合成。大量的含氘试剂和结构单元可以从化学供应商如Aldrich Chemical Co.商购获得。
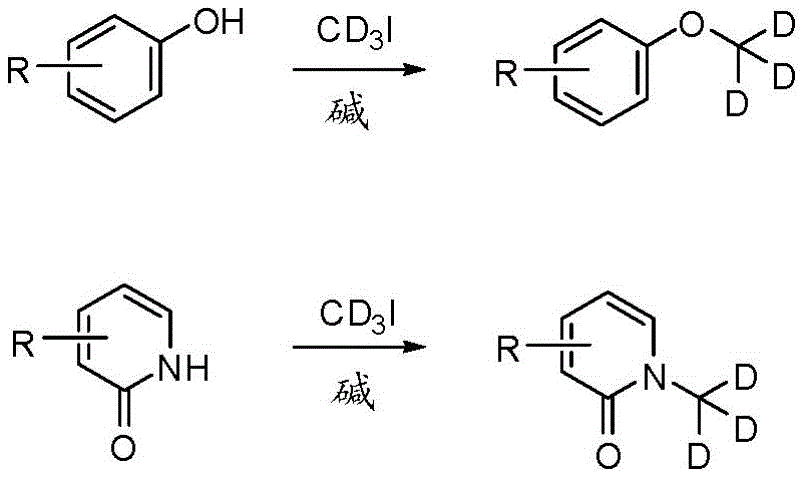
适用于亲核取代反应的氘转移试剂如碘甲烷-d3(CD3I)易于获得,并且可用于在亲核取代反应条件下将氘取代的碳原子转移至反应底物。
仅举例而言,CD3I的使用在以下的反应流程中示出。
使用氘转移试剂如氘化铝锂(LiAlD4)在还原条件下将氘转移至反应底物。仅举例而言,LiAlD4的使用在以下的反应流程中示出。
仅举例而言,如以下的反应方案所示,使用氘气和钯催化剂来还原不饱和的碳-碳键,并进行芳基碳-卤键的还原性取代。
在一个实施方案中,本文公开的化合物含有一个氘原子。在另一个实施方案中,本文公开的化合物含有两个氘原子。在另一个实施方案中,本文公开的化合物含有三个氘原子。在另一个实施方案中,本文公开的化合物含有四个氘原子。在另一个实施方案中,本文公开的化合物含有五个氘原子。在另一个实施方案中,本文公开的化合物含有六个氘原子。在另一个实施方案中,本文公开的化合物含有多于六个氘原子。在另一个实施方案中,本文公开的化合物完全被氘原子取代,并且不含不可交换的1H氢原子。在一个实施方案中,氘并入的水平由使用氘化合成结构单元作为起始材料的合成方法决定。
“药学上可接受的盐”包括酸加成盐和碱加成盐。任一种本文所述的杂芳族RAF抑制性化合物的药学上可接受的盐均意在包括任何和所有药学上合适的盐形式。本文所述化合物的优选的药学上可接受的盐是药学上可接受的酸加成盐和药学上可接受的碱加成盐。
“药学上可接受的酸加成盐”是指保留了游离碱的生物有效性和性质的那些盐,其在生物学上或其他方面不是不合需要的,并且其是用无机酸诸如盐酸、氢溴酸、硫酸、硝酸、磷酸、氢碘酸、氢氟酸、亚磷酸等形成的。还包括用如下有机酸形成的盐:诸如脂肪族单羧酸和二羧酸、苯基取代的链烷酸、羟基链烷酸、链烷二酸、芳族酸、脂肪族和芳香族磺酸等,并且包括例如乙酸、三氟乙酸、丙酸、羟基乙酸、丙酮酸、草酸、马来酸、丙二酸、琥珀酸、富马酸、酒石酸、柠檬酸、苯甲酸、肉桂酸、扁桃酸、甲磺酸、乙磺酸、对甲苯磺酸、水杨酸等。因此,示例性的盐包括硫酸盐、焦硫酸盐、硫酸氢盐、亚硫酸盐、亚硫酸氢盐、硝酸盐、磷酸盐、磷酸一氢盐、磷酸二氢盐、偏磷酸盐、焦磷酸盐、氯化物、溴化物、碘化物、乙酸盐、三氟乙酸盐、丙酸盐、辛酸盐、异丁酸盐、草酸盐、丙二酸盐、琥珀酸盐、辛二酸盐、癸二酸盐、富马酸盐、马来酸盐、扁桃酸盐、苯甲酸盐、氯苯甲酸盐、甲基苯甲酸盐、二硝基苯甲酸盐、邻苯二甲酸盐、苯磺酸盐、甲苯磺酸盐、苯乙酸盐、柠檬酸盐、乳酸盐、苹果酸盐、酒石酸盐、甲磺酸盐等。还设想到氨基酸的盐如精氨酸盐、葡糖酸盐和半乳糖醛酸盐(参见,例如,Berge S.M等人,"Pharmaceutical Salts,"Journal of Pharmaceutical Science,66:1-19(1997))。在一些实施方案中,碱性化合物的酸加成盐通过按照熟练技术人员熟悉的方法和技术使其游离碱形式与足量的所需酸接触以产生盐而制备。
“药学上可接受的碱加成盐”是指保留了游离酸的生物有效性和性质的那些盐,其在生物学上或其他方面不是不合需要的。这些盐是通过向游离酸中加入无机碱或有机碱而制备的。在一些实施方案中,药学上可接受的碱加成盐用金属或胺如碱金属和碱土金属或有机胺形成。衍生自无机碱的盐包括但不限于钠盐、钾盐、锂盐、铵盐、钙盐、镁盐、铁盐、锌盐、铜盐、锰盐、铝盐等。衍生自有机碱的盐包括但不限于下列有机碱的盐:伯胺、仲胺和叔胺,取代胺(包括天然存在的取代胺),环胺和碱性离子交换树脂,例如,异丙胺、三甲胺、二乙胺、三乙胺、三丙胺、乙醇胺、二乙醇胺、2-二甲基氨基乙醇、2-二乙基氨基乙醇、二环己基胺、赖氨酸、精氨酸、组氨酸、咖啡因、普鲁卡因、N,N-二苄基乙二胺、氯普鲁卡因、海巴明(hydrabamine)、胆碱、甜菜碱、乙二胺、亚乙基二苯胺、N-甲基葡糖胺、葡糖胺、甲基葡糖胺、可可碱(theobromine)、嘌呤、哌嗪、哌啶、N-乙基哌啶、聚胺树脂等。参见Berge等人,同上。
“药学上可接受的溶剂化物”是指作为溶剂加成形式的物质的组成物。在一些实施方案中,溶剂化物含有化学计量或非化学计量的量的溶剂,并且在与药学上可接受的溶剂如水、乙醇等制备的过程中形成。当溶剂为水时形成水合物,或者当溶剂为醇时形成醇化物。本文所述化合物的溶剂化物在本文所述的过程中方便地制备或形成。本文提供的化合物任选地以非溶剂化形式以及溶剂化形式存在。
术语“受试者”或“患者”包括哺乳动物。哺乳动物的实例包括但不限于哺乳纲的任何成员:人,非人灵长类动物,如黑猩猩以及其他猿和猴物种;农畜,如牛、马、绵羊、山羊、猪;家畜,如兔、狗和猫;实验动物,包括啮齿动物,如大鼠、小鼠和豚鼠,等等。在一方面,该哺乳动物是人。
如本文所用的,“治疗”或“处理”或“减轻”或“改善”可互换使用。这些术语是指获得有益的或期望的结果(包括但不限于治疗性益处和/或预防性益处)的途径。所谓“治疗性益处”是指所治疗的潜在病症的消除或改善。另外,治疗性益处也如下实现:与该潜在病症相关的一种或多种生理学症状得到根除或改善,从而在患者中观察到改善,虽然该患者仍受该潜在病症的折磨。对于预防性益处,在一些实施方案中,将所述组合物施用于处于发生特定疾病的风险中的患者,或报告疾病的一种或多种生理学症状的患者,即便尚未作出该疾病的诊断。
RAF激酶家族
RAF激酶是丝氨酸/苏氨酸蛋白激酶家族,其构成RAS–RAF–MEK–ERK促分裂原激活的蛋白激酶(MAPK)信号传导级联(也称为MAPK/ERK途径)的核心组分,该途径介导信号从细胞表面受体传递到细胞核,以调节细胞生长、分化和存活。RAF蛋白与逆转录病毒癌基因相关,并且从后生动物到哺乳动物在结构上是保守的,如同MAPK/ERK途径一样。它们的失调导致不受控制的细胞增殖、存活和去分化。因此,在大多数癌症中,RAF激酶被改变或被不适当地激活。
MAPK/ERK信号传导途径是细胞中的蛋白质网络,它将信号从细胞表面的受体传递到细胞核中的DNA。当信号分子与细胞表面的受体结合时,信号开始,而当细胞核中的DNA表达蛋白质并在细胞中产生某种变化例如细胞分裂时,信号结束。该途径包括许多蛋白质,它们通过向邻近的蛋白质添加磷酸基团来进行传递,该蛋白质作为分子“开”或“关”开关,总体而言,该途径可分为3个步骤:(I)Ras激活,(ii)激酶信号转导级联,以及(iii)翻译和转录的调节。简言之,细胞外促分裂原或信号分子与膜受体结合。这允许Ras(一种小GTP酶)将其GDP换成GTP,并变得具有活性。活化的Ras激活RAF激酶的蛋白激酶活性。RAF激酶磷酸化并激活MEK(MEK1和MEK2)。然后MEK磷酸化并激活MAPK(也称为ERK)。MAPK激活调节数种转录因子的活性,并且还改变mRNA向蛋白质的翻译。通过改变转录因子的水平和活性,MAPK导致对细胞周期而言重要的基因的转录发生改变。
存在三种已知的哺乳动物RAF同种型:C-RAF(也称为RAF-1或c-RAF-1)、B-RAF和A-RAF。所有RAF激酶共有共同的模块结构,该模块结构由3个具有不同功能的保守区域(CR1、CR2和CR3)组成。CR1包含(i)Ras结合域(RBD),其对于与Ras和与膜募集所需的膜磷脂的相互作用是必需的,以及(ii)富含半胱氨酸的结构域(CRD),它是次级Ras-结合位点,对于CR1与激酶结构域相互作用以实现RAF自动抑制也是必需的。CR2包含重要的抑制性磷酸化位点,这些位点参与对Ras结合和RAF激活的负调节。CR3的特征是激酶结构域,包括激活区段,其磷酸化对于激酶激活至关重要。
在功能上,RAF结构可以分成调节性N末端区域和催化性C末端区域,所述调节性N末端区域包含对激活至关重要的RBD以及抑制性磷酸化位点,所述催化性C末端区域包含激酶激活所必需的磷酸化位点。调节性结构域抑制激酶结构域的活性,其去除导致组成型致癌性激活。然而,分离的C-RAF激酶结构域的活性受到进一步调节,并且可以被佛波酯、v-Src和磷酸化刺激。
所有3种RAF激酶同种型的激活中的共同和关键步骤是Ras家族蛋白的膜募集。RAF激酶当与14-3-3蛋白结合时以其非活性状态位于胞质溶胶中。在活性Ras的存在下,它们易位到质膜。膜易位触发进一步的激活事件,例如PP2A的结合使RAF-1中的抑制性pS259位点(以及A-RAF和B-RAF中可能的相应位点)去磷酸化,以及与负责多重激活磷酸化的激酶的共定位。形成结合界面的序列在RAF以及Ras家族中非常保守,表明Ras家族的几个成员具有结合RAF激酶的能力。H-Ras、N-Ras和K-Ras刺激所有3种RAF同种型,并且是唯一激活B-RAF的Ras蛋白。相比之下,A-RAF也被R-Ras3激活,而C-RAF对R-Ras3、Rit和TC21的响应也弱。但是,所有RAF激酶都共享MEK1/2激酶作为底物。MEK1/2继而激活ERK1/2,该途径调节许多细胞功能,如细胞增殖、分化、迁移或凋亡。
C-RAF
C-RAF最早被鉴定出来,是一种普遍表达的同种型。在人类中,C-RAF由RAF1基因编码。C-RAF还有优先在肌肉和大脑中表达的已知的剪接变体。C-RAF在介导生长因子信号的细胞效应中起关键作用。在非活性状态下,C-RAF以闭合构象存在,其中N末端调节性区域折叠并阻塞催化性区域。这种构象通过与N末端位点磷酸-S259(pS259)和C末端位点pS621结合的14-3-3二聚体来稳定。特定磷酸酶(PP2A、PP1)在细胞膜处对pS259的去磷酸化从其在C-RAF中的N末端结合位点释放14-3-3,从而允许发生构象变化,所述构象变化揭开CR1区域中的RBD和CRD结构域,使得能够发生Ras结合和膜募集。
B-RAF
B-RAF在人类中由BRAF基因编码,该基因也被称为原癌基因B-RAF和v-RAF鼠肉瘤病毒癌基因同源物B。可变性剪接产生多种B-RAF同种型,它们在各种组织中差异表达。A-RAF和C-RAF的激活需要某些残基的磷酸化和去磷酸化以及与其他蛋白质的结合,而B-RAF在易位到质膜后立即被激活。B-RAF表现出比A-RAF和C-RAF更高的基础激酶活性。B-RAF需要Ras和14-3-3结合以便其激活,并根据14-3-3表达的水平而被PKA抑制或激活,需要高表达水平以允许激活。B-RAF活性也通过剪接来调节。含有外显子8b的B-RAF同种型在抑制性S365位点上磷酸化程度更高,导致与14-3-3的相互作用增加,并且加强N末端调节性结构域与激酶结构域之间的抑制性相互作用,从而一起导致较低的激酶活性。
A-RAF
丝氨酸/苏氨酸-蛋白激酶A-RAF或A-RAF在人类中是由ARAF基因编码的酶。A-RAF有2种已知的剪接同种型——DA-RAF1和D-RAF2。它们缺乏激酶结构域,并充当Ras和ARFGTP酶的显性抑制性突变体。DA-RAF1通过介导对分化所需的ERK途径的抑制,是生肌分化的正调节剂。A-RAF与其他RAF激酶有若干不同之处。A-RAF是唯一受类固醇激素调节的Raf同种型。另外,A-RAF蛋白在激酶结构域(N区)上游带负电荷的区域具有氨基酸置换,这导致其低基础活性。A-RAF也仅被致癌性H-Ras和Src微弱激活,并且还表现出对MEK的低激酶活性(在Raf激酶家族中对MEK蛋白的激酶活性最低)。除了对MEK进行磷酸化外,A-RAF还抑制MST2——一种在MAPK途径中未发现的肿瘤抑制物和促凋亡激酶。通过抑制MST2,A-RAF阻止凋亡的发生。然而,这种抑制仅在剪接因子核内不均一核糖核蛋白H(hnRNP H)维持全长A-RAF蛋白的表达时发生。肿瘤细胞通常过度表达hnRNP H,这导致A-Raf的全长表达,A-Raf然后抑制凋亡,使原本应该被破坏的癌细胞保持存活。A-RAF还与丙酮酸激酶M2(PKM2)结合,同样在MAPK途径之外。PKM2是丙酮酸激酶的同工酶,是癌细胞中的Warburg效应的原因。A-RAF通过促进PKM2的构象变化来上调PKM2的活性。这导致PKM2从其低活性二聚体形式转变为高活性四聚体形式。这导致更多的葡萄糖碳转化为丙酮酸和乳酸,为细胞产生能量,将A-Raf与能量代谢调节和细胞转化相关联,这两者在肿瘤发生中非常重要。
RAF激酶抑制剂
MAPK/ERK途径的异常激活在各种癌症中经常发现,并且是癌症治疗的靶点。特别是,B-RAF已成为癌症治疗中最具吸引力的分子靶点之一,因为已在人类肿瘤中经常发现B-RAF的体细胞突变。迄今为止测试的所有癌症样品中约有20%携带B-RAF突变。B-RAF-V600E是由第600位谷氨酸被置换为缬氨酸而生成的激酶结构域中的错义突变,是最常见的B-RAF突变。在测试的各种肿瘤类型中约有1%发生C-RAF突变,而A-RAF的突变率甚至更低。B-RAF和C-RAF形成同源和异源二聚体,作为其激活机制的部分,而A-RAF使B-RAF:C-RAF复合物稳定化以维持信号传导效率。此外,C-RAF将信号从致癌性RAS传递到MEK,而B-RAF则不能。因此,在不同的情况下,每个RAF同种型都充当潜在的治疗靶点。
索拉非尼是第一个进入临床试验的RAF抑制剂。索拉非尼是一种宽特异性药物,其抑制其他激酶,包括血管内皮生长因子受体家族(VEGFR-2和VEGFR-3)、血小板衍生生长因子受体家族(PDGFR-b和KIT)和FLT3。临床试验显示,临床响应与B-RAF突变状态之间没有相关性,表明它是B-RAF的不良抑制剂。这导致了新一代B-RAF抑制剂的开发,包括但不限于维罗非尼(vemurafenib)、SB-590885和达拉非尼(GSK2118436)。尽管B-RAF突变型黑素瘤的临床研究的初步结果令人鼓舞,但随着其他B-RAF突变型癌症(如甲状腺癌和结直肠癌)的临床试验开始,显然携带B-RAF突变的不同细胞类型的肿瘤对选择性B-RAF抑制具有不同的响应。此外,对RAF抑制的原发性和继发性抗性的存在是RAF激酶抑制剂治疗进展的最大挑战之一。抗性机制分为两大类。大约50%的患者表现出固有/原发性抗性。其他50%的患者最初对RAF抑制剂有响应(>30%肿瘤缩小),但随后发展为与对RAF抑制剂的获得性/继发性抗性相关的进行性疾病。这两类并不相互排斥,因为几乎所有的应答者都患有其余的疾病,因此可能表现出固有抗性。原发性RAF抑制剂抗性的决定因素似乎因肿瘤类型而异,也涉及RTK信号传导的改变。继发性B-RAF抑制剂抗性的潜在机制包括但不限于ERK1/2途径的再激活、RTK信号传导的上调、受体酪氨酸激酶的上调、RAS的突变和COT的上调。B-RAF-V600E的B-Raf可变性剪接和扩增也已分别涉及约30%和20%的患者。此外,RAF激酶抑制剂引起MAPK途径的反常激活,在一些情况下,这导致继发性RAS突变驱动的恶性病的发展。因此,本领域需要能克服现有抑制剂的现有缺陷和所带来的挑战的新型RAF激酶抑制剂。
杂芳族RAF抑制性化合物
在一方面,本文提供了杂芳族RAF抑制性化合物。
一个实施方案提供了一种化合物,或其药学上可接受的盐或溶剂化物,其具有式(I)的结构:
其中,
环A为5或6元任选取代的杂芳基或5或6元任选取代的杂环基;
W为NH、NR7或O;
X为N、C-H、C-F或C-CN;
Y为N、C-F或C-H;
R为H、C1-C8任选取代的烷基、(C1-C8任选取代的亚烷基)-OPO(OH)2、C3-C6任选取代的环烷基、(C3-C6任选取代的亚环烷基)-OPO(OH)2、C4-C8任选取代的环烷基烷基、(C3-C6任选取代的环烷基亚烷基)-OPO(OH)2、C3-C6任选取代的杂环基、(C3-C6任选取代的杂环基)-OPO(OH)2、C3-C6任选取代的杂环基烷基、(C3-C6任选取代的杂环基烷基)-OPO(OH)2或C1-C8任选取代的烷基-CO-;
R2为H、D或F;
R4为卤素、任选取代的C1-C3烷基、-CD3或任选取代的C1-C3烷氧基;
R6为H、D、Cl或F;
R7为C1-C8任选取代的烷基;或R不为H,且R和R7任选地连接以形成任选取代的杂环基环;
Z为:
(a)
其中m为0、1、2或3;p为0、1、2、3或4;且
每个R11独立地选自氨基、烷基氨基、二烷基氨基、-OH、卤素、任选取代的C1-C6烷基、任选取代的C3-C6环烷基、任选取代的C1-C6烷氧基、任选取代的C2-C6炔基、任选取代的-S-烷基、任选取代的-SO2烷基、任选取代的C3-C6环烷基烷基、任选取代的杂环基或任选取代的杂环基烷基;或者两个R11基团一起形成氧代;或
(b)
其中m为0、1、2或3;n为0、1、2或3;p为0、1、2、3或4;且每个R
11独立地选自氨基、烷基氨基、二烷基氨基、-OH、卤素、任选取代的C1-C6烷基、任选取代的C3-C6环烷基、任选取代的C1-C6烷氧基、任选取代的C2-C6炔基、任选取代的-S-烷基、任选取代的-SO
2烷基、任选取代的C3-C6环烷基烷基、任选取代的杂环基或任选取代的杂环基烷基;或者两个R
11基团一起形成氧代。
另一实施方案提供了式(I)化合物,或其药学上可接受的盐或溶剂化物,其中环A为5或6元任选取代的杂芳基。
另一实施方案提供了式(I)化合物,或其药学上可接受的盐或溶剂化物,其中环A为任选取代的吡啶或任选取代的吡唑。另一实施方案提供了式(I)化合物,或其药学上可接受的盐或溶剂化物,其中环A为任选取代的4-吡啶基或任选取代的3-吡唑。
另一实施方案提供了式(I)化合物,或其药学上可接受的盐或溶剂化物,其中环A为5或6元任选取代的杂环基。
另一实施方案提供了式(I)化合物,或其药学上可接受的盐或溶剂化物,其中环A为任选取代的二氢吡喃、任选取代的四氢吡喃、任选取代的二氢呋喃或任选取代的四氢呋喃。另一实施方案提供了式(I)化合物,或其药学上可接受的盐或溶剂化物,其中环A为任选取代的二氢-2H-吡喃-4-基、任选取代的四氢吡喃-4-基、任选取代的2,5-二氢呋喃-3-基、任选取代的四氢呋喃-3-基、3-氧杂双环[3.1.0]己烷-1-基或3-氧杂双环[4.1.0]庚烷-6-基。
另一实施方案提供了式(I)化合物,或其药学上可接受的盐或溶剂化物,其中环A为任选取代的吗啉。
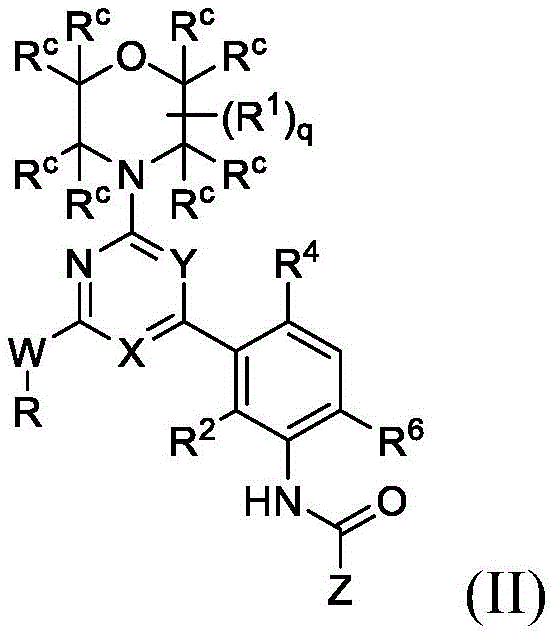
另一实施方案提供了式(I)化合物,或其药学上可接受的盐或溶剂化物,其具有式(II)的结构:
其中,
W为NH、NR7或O;
X为N、C-H、C-F或C-CN;
Y为N、C-F或C-H;
R为H、C1-C8任选取代的烷基、(C1-C8任选取代的亚烷基)-OPO(OH)2、C3-C6任选取代的环烷基、(C3-C6任选取代的亚环烷基)-OPO(OH)2、C4-C8任选取代的环烷基烷基、(C3-C6任选取代的环烷基亚烷基)-OPO(OH)2、C3-C6任选取代的杂环基、(C3-C6任选取代的杂环基)-OPO(OH)2、C3-C6任选取代的杂环基烷基、(C3-C6任选取代的杂环基烷基)-OPO(OH)2或C1-C8任选取代的烷基-CO-;
R1为C1-C3任选取代的烷基,且q为0、1或2;
R2为H、D或F;
R4为卤素、任选取代的C1-C3烷基、-CD3或任选取代的C1-C3烷氧基;
R6为H、D、Cl或F;
R7为C1-C8任选取代的烷基;或R不为H,且R和R7任选地连接以形成任选取代的杂环基环;
Rc为H或D;
Z为(a)
其中m为0、1、2或3;p为0、1、2、3或4;且
每个R11独立地选自氨基、烷基氨基、二烷基氨基、-OH、卤素、任选取代的C1-C6烷基、任选取代的C3-C6环烷基、任选取代的C1-C6烷氧基、任选取代的C2-C6炔基、任选取代的-S-烷基、任选取代的-SO2烷基、任选取代的C3-C6环烷基烷基、任选取代的杂环基或任选取代的杂环基烷基;或者两个R11基团一起形成氧代;或
(b)
其中n为1、2或3;m为1、2或3;p为0、1、2、3或4;且每个R
11独立地选自氨基、烷基氨基、二烷基氨基、-OH、卤素、任选取代的C1-C6烷基、任选取代的C3-C6环烷基、任选取代的C1-C6烷氧基、任选取代的C2-C6炔基、任选取代的-S-烷基、任选取代的-SO
2烷基、任选取代的C3-C6环烷基烷基、任选取代的杂环基或任选取代的杂环基烷基;或者两个R
11基团一起形成氧代。
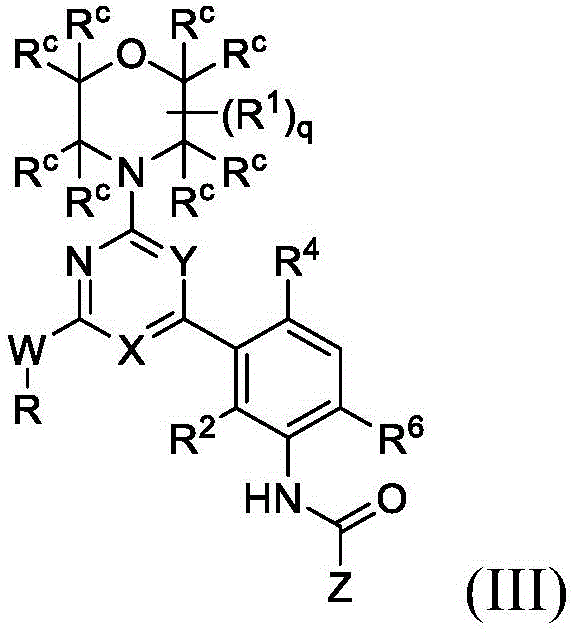
另一实施方案提供了式(I)化合物,或其药学上可接受的盐或溶剂化物,其具有式(III)的结构:
其中,
W为NH或O;
X为N、C-H或C-CN;
Y为N或C-H;
R为C1-C8任选取代的烷基、-(C1-C8任选取代的亚烷基)-OPO(OH)2、C3-C6任选取代的环烷基、-(C3-C6任选取代的亚环烷基)-OPO(OH)2、C4-C6任选取代的环烷基烷基、-(C3-C6任选取代的环烷基亚烷基)-OPO(OH)2、C3-C6任选取代的杂环基、-(C3-C6任选取代的杂环基)-OPO(OH)2、C3-C6任选取代的杂环基烷基、-(C3-C6任选取代的杂环基烷基)-OPO(OH)2;
R1为C1-C3任选取代的烷基,且q为0、1或2;
R2为H、D或F;
R4为卤素、任选取代的C1-C3烷基、-CD3或任选取代的C1-C3烷氧基;
R6为H、D、Cl或F;
Rc为H或D;
Z为
其中m为0、1、2或3;p为0、1、2、3或4;且
每个R11独立地选自氨基、烷基氨基、二烷基氨基、-OH、卤素、任选取代的C1-C6烷基、任选取代的C3-C6环烷基、任选取代的C1-C6烷氧基、任选取代的C2-C6炔基、任选取代的-S-烷基、任选取代的-SO2烷基、任选取代的C3-C6环烷基烷基、任选取代的杂环基或任选取代的杂环基烷基;或者两个R11基团一起形成氧代。
另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中W为NH。
另一实施方案提供了式(I)或(II)的化合物,或其药学上可接受的盐或溶剂化物,其中W为NR7。另一实施方案提供了式(I)或(II)的化合物,或其药学上可接受的盐或溶剂化物,其中R7为任选取代的C1烷基。
另一实施方案提供了式(I)或(II)的化合物,或其药学上可接受的盐或溶剂化物,其中W为NR7,R不为H,且R和R7连接以形成任选取代的杂环基环。另一实施方案提供了式(I)或(II)的化合物,或其药学上可接受的盐或溶剂化物,其中任选取代的杂环基环为1-氮杂环丁烷基、1-吡咯烷基或1-哌啶基环。另一实施方案提供了式(I)或(II)的化合物,或其药学上可接受的盐或溶剂化物,其中任选取代的杂环基环被选自-OH、卤素、任选取代的C1-C6烷基或任选取代的C1-C6烷氧基中的至少一个取代基取代。
另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中R为C1-C8任选取代的烷基、C3-C6任选取代的环烷基、C4-C8任选取代的环烷基烷基、C3-C6任选取代的杂环基或C3-C6任选取代的杂环基烷基。另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中R为C1-C8任选取代的烷基、C3-C6任选取代的环烷基、C4-C6任选取代的环烷基烷基、C3-C6任选取代的杂环基或C3-C6任选取代的杂环基烷基。另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中R为C1-C8任选取代的烷基。另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中R为C1-C6任选取代的烷基。另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中R为C1-C4任选取代的烷基。另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中R为C1-C3任选取代的烷基。另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中R为C1-C2任选取代的烷基。另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中R为C1-C6任选取代的烷基,且所述烷基被至少一个羟基取代。
另一实施方案提供了式(I)或(II)的化合物,或其药学上可接受的盐或溶剂化物,其中R为H。
另一实施方案提供了式(I)或(II)的化合物,或其药学上可接受的盐或溶剂化物,其中R为C1-C8任选取代的烷基-CO-。
另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中R为C3-C6任选取代的环烷基。
另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中R为C4-C6任选取代的环烷基烷基。
另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中R为C3-C6任选取代的杂环基。
另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中R为C3-C6任选取代的杂环基烷基。
另一实施方案提供了式(II)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中R1为C1任选取代的烷基。另一实施方案提供了式(II)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中q为0。另一实施方案提供了式(II)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中q为1。
另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中Z为
另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中m为0。另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中m为1。另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中m为2。另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中p为1。另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中p为2。
另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中R11为任选取代的C1-C6烷基。另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中R11为任选取代的C1-C4烷基。另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中R11为任选取代的C1-C3烷基。另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中R11为任选取代的C1-C2烷基。另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中R11为任选取代的C1-C4氟烷基。另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中R11为-CH2CF3。另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中R11为任选取代的C3-C6环烷基。
另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中Z为
另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中m为0。另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中m为1。另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中m为2。另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中n为1。另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中n为2。另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中p为1。另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中p为2。
另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中R11为任选取代的C1-C6烷基。另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中R11为任选取代的C1-C4烷基。另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中R11为任选取代的C1-C3烷基。另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中R11为任选取代的C1-C2烷基。另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中R11为任选取代的C1-C4氟烷基。另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中R11为-CH2CF3。另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中R11为任选取代的C3-C6环烷基。
另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中W为NH,且环A为任选取代的吗啉。
另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中W为NH,且Z为3-(2,2,2-三氟乙基)吡咯烷。
另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中环A为任选取代的吗啉,且Z为3-(2,2,2-三氟乙基)吡咯烷。
另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中W为NH,环A为任选取代的吗啉,且Z为3-(2,2,2-三氟乙基)吡咯烷。
另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中R为C1-C4任选取代的烷基,W为NH,且环A为任选取代的吗啉。
另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中R为C1-C4任选取代的烷基,W为NH,且Z为3-(2,2,2-三氟乙基)吡咯烷。
另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中R为C1-C4任选取代的烷基,环A为任选取代的吗啉,且Z为3-(2,2,2-三氟乙基)吡咯烷。
另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中R为C1-C4任选取代的烷基,W为NH,环A为任选取代的吗啉,且Z为3-(2,2,2-三氟乙基)吡咯烷。
另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中X为C-H,Y为C-H,W为NH,且环A为任选取代的吗啉。
另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中X为C-H,Y为C-H,W为NH,且Z为3-(2,2,2-三氟乙基)吡咯烷。
另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中X为C-H,Y为C-H,环A为任选取代的吗啉,且Z为3-(2,2,2-三氟乙基)吡咯烷。
另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中X为C-H,Y为C-H,W为NH,环A为任选取代的吗啉,且Z为3-(2,2,2-三氟乙基)吡咯烷。
另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中X为C-H,Y为C-H,R为C1-C4任选取代的烷基,W为NH,且环A为任选取代的吗啉。
另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中X为C-H,Y为C-H,R为C1-C4任选取代的烷基,W为NH,且Z为3-(2,2,2-三氟乙基)吡咯烷。
另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中X为C-H,Y为C-H,R为C1-C4任选取代的烷基,环A为任选取代的吗啉,且Z为3-(2,2,2-三氟乙基)吡咯烷。
另一实施方案提供了式(I)-(III)的化合物,或其药学上可接受的盐或溶剂化物,其中X为C-H,Y为C-H,R为C1-C4任选取代的烷基,W为NH,环A为任选取代的吗啉,且Z为3-(2,2,2-三氟乙基)吡咯烷。
一个实施方案提供了一种化合物,或其药学上可接受的盐或溶剂化物,其具有式(IV)的结构:
其中,
环A为5或6元任选取代的杂芳基或5或6元任选取代的杂环基;
W为NH或NR7;
X为N、C-H、C-F或C-CN;
Y为N、C-F或C-H;
R为-SO2-(C1-C8任选取代的烷基)、-SO2-(C3-C6任选取代的环烷基)、-SO2-(C4-C8任选取代的环烷基烷基)、-SO2-(C3-C6任选取代的杂环基)、-SO2-(C3-C6任选取代的杂环基烷基)、-SO2-N(R8)R9-C1-C8任选取代的烷基、-CO2-C1-C8任选取代的烷基或-CO-N(R8)R9-C1-C8任选取代的烷基;
R2为H、D或F;
R4为卤素、任选取代的C1-C3烷基、-CD3或任选取代的C1-C3烷氧基;
R6为H、D、Cl或F;
R7为C1-C8任选取代的烷基;或R和R7任选地连接以形成任选取代的杂环基环;
每个R8和R9独立地选自H或C1-C8任选取代的烷基;
Z为(a)
其中m为0、1、2或3;p为0、1、2、3或4;且
每个R11独立地选自氨基、烷基氨基、二烷基氨基、-OH、卤素、任选取代的C1-C6烷基、任选取代的C3-C6环烷基、任选取代的C1-C6烷氧基、任选取代的C2-C6炔基、任选取代的-S-烷基、任选取代的-SO2烷基、任选取代的C3-C6环烷基烷基、任选取代的杂环基或任选取代的杂环基烷基;或者两个R11基团一起形成氧代;或
(b)
其中m为0、1、2或3;n为0、1、2或3;p为0、1、2、3或4;且每个R
11独立地选自氨基、烷基氨基、二烷基氨基、-OH、卤素、任选取代的C1-C6烷基、任选取代的C3-C6环烷基、任选取代的C1-C6烷氧基、任选取代的C2-C6炔基、任选取代的-S-烷基、任选取代的-SO
2烷基、任选取代的C3-C6环烷基烷基、任选取代的杂环基或任选取代的杂环基烷基;或者两个R
11基团一起形成氧代。
另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中环A为5或6元任选取代的杂芳基。
另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中环A为任选取代的吡啶或任选取代的吡唑。另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中环A为任选取代的4-吡啶基或任选取代的3-吡唑。
另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中环A为5或6元任选取代的杂环基。
另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中环A为任选取代的二氢吡喃、任选取代的四氢吡喃、任选取代的二氢呋喃或任选取代的四氢呋喃。另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中环A为任选取代的二氢-2H-吡喃-4-基、任选取代的四氢吡喃-4-基、任选取代的2,5-二氢呋喃-3-基、任选取代的四氢呋喃-3-基、3-氧杂双环[3.1.0]己烷-1-基或3-氧杂双环[4.1.0]庚烷-6-基。
另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中环A为任选取代的吗啉。
另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中W为NH。
另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中W为NR7。另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中R7为C1-C8任选取代的烷基。另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中R和R7任选地连接以形成任选取代的杂环基环。
另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中R为-SO2-(C1-C8任选取代的烷基)。
另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中R为-SO2-(C3-C6任选取代的环烷基)。
另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中R为-SO2-(C4-C8任选取代的环烷基烷基)。
另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中R为-SO2-(C3-C6任选取代的杂环基)。
另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中R为-SO2-(C3-C6任选取代的杂环基烷基)。
另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中R为-SO2-N(R8)R9-C1-C8任选取代的烷基。另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中每个R8和R9独立地选自H或C1-C8任选取代的烷基。
另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中R为-CO2-C1-C8任选取代的烷基。
另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中R为-CO-N(R8)R9-C1-C8任选取代的烷基。另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中每个R8和R9独立地选自H或C1-C8任选取代的烷基。
另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中Z为
另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中m为0。另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中m为1。另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中m为2。另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中p为1。另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中p为2。
另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中Z为
另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中m为0。另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中m为1。另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中m为2。另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中n为1。另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中n为2。另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中p为1。另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中p为2。
另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中R11为任选取代的C1-C6烷基。另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中R11为任选取代的C1-C4烷基。另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中R11为任选取代的C1-C3烷基。另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中R11为任选取代的C1-C2烷基。另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中R11为任选取代的C1-C4氟烷基。另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中R11为-CH2CF3。另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中R11为任选取代的C3-C6环烷基。
另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中W为NH,且环A为任选取代的吗啉。
另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中W为NH,且Z为3-(2,2,2-三氟乙基)吡咯烷。
另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中环A为任选取代的吗啉,且Z为3-(2,2,2-三氟乙基)吡咯烷。
另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中W为NH,环A为任选取代的吗啉,且Z为3-(2,2,2-三氟乙基)吡咯烷。
另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中X为C-H,Y为C-H,W为NH,且环A为任选取代的吗啉。
另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中X为C-H,Y为C-H,W为NH,且Z为3-(2,2,2-三氟乙基)吡咯烷。
另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中X为C-H,Y为C-H,环A为任选取代的吗啉,且Z为3-(2,2,2-三氟乙基)吡咯烷。
另一实施方案提供了式(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中X为C-H,Y为C-H,W为NH,环A为任选取代的吗啉,且Z为3-(2,2,2-三氟乙基)吡咯烷。
另一实施方案提供了式(I)-(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中X为N;且Y为C-H。
另一实施方案提供了式(I)-(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中X为N;且Y为N。
另一实施方案提供了式(I)-(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中X为C-H;且Y为C-H。
另一实施方案提供了式(I)-(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中X为C-H;且Y为N。
另一实施方案提供了式(I)-(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中X为C-F;且Y为C-H。
另一实施方案提供了式(I)-(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中X为C-H;且Y为C-F。
另一实施方案提供了式(I)-(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中R2为H。
另一实施方案提供了式(I)-(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中R4为任选取代的C1-C3烷基。
另一实施方案提供了式(I)-(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中R4为任选取代的C1烷基。
另一实施方案提供了式(I)-(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中R4为CH3。
另一实施方案提供了式(I)-(IV)的化合物,或其药学上可接受的盐或溶剂化物,其中R6为H。
在一些实施方案中,如本文所述的杂芳族RAF激酶抑制性化合物具有表1中提供的结构。
表1
化合物的制备
在本文所述的反应中使用的化合物根据本领域技术人员已知的有机合成技术,从可商购获得的化学品和/或从化学文献中描述的化合物开始进行制备。“可商购获得的化学品”从标准商业来源获得,该商业来源包括Acros Organics(Pittsburgh,PA)、AldrichChemical(Milwaukee,WI,包括Sigma Chemical和Fluka)、Apin Chemicals Ltd.(MiltonPark,UK)、Avocado Research(Lancashire,U.K.)、BDH Inc.(Toronto,Canada)、Bionet(Cornwall,U.K.)、Chemservice Inc.(West Chester,PA)、Crescent Chemical Co.(Hauppauge,NY)、Eastman Organic Chemicals、Eastman Kodak Company(Rochester,NY)、Fisher Scientific Co.(Pittsburgh,PA)、Fisons Chemicals(Leicestershire,UK)、Frontier Scientific(Logan,UT)、ICN Biomedicals,Inc.(Costa Mesa,CA)、KeyOrganics(Cornwall,U.K.)、Lancaster Synthesis(Windham,NH)、Maybridge ChemicalCo.Ltd.(Cornwall,U.K.)、Parish Chemical Co.(Orem,UT)、Pfaltz&Bauer,Inc.(Waterbury,CN)、Polyorganix(Houston,TX)、Pierce Chemical Co.(Rockford,IL)、Riedel de Haen AG(Hanover,Germany)、Spectrum Quality Product,Inc.(NewBrunswick,NJ)、TCI America(Portland,OR)、Trans World Chemicals,Inc.(Rockville,MD)和Wako Chemicals USA,Inc.(Richmond,VA)。
详述了在本文所述化合物的制备中有用的反应物的合成或对描述该制备的文章提供参考的合适的参考书籍和论文包括,例如,"Synthetic Organic Chemistry",JohnWiley&Sons,Inc.,New York;S.R.Sandler等人,"Organic Functional GroupPreparations,"第2版,Academic Press,New York,1983;H.O.House,"Modern SyntheticReactions",第2版,W.A.Benjamin,Inc.Menlo Park,Calif.1972;T.L.Gilchrist,"Heterocyclic Chemistry",第2版,John Wiley&Sons,New York,1992;J.March,"AdvancedOrganic Chemistry:Reactions,Mechanisms and Structure",第4版,Wiley-Interscience,New York,1992。详述了在本文所述化合物的制备中有用的反应物的合成或对描述该制备的文章提供参考的其他合适的参考书籍和论文包括,例如,Fuhrhop,J.和Penzlin G."Organic Synthesis:Concepts,Methods,Starting Materials",第二次修订增补版(Second,Revised and Enlarged Edition)(1994)John Wiley&Sons ISBN:3-527-29074-5;Hoffman,R.V."Organic Chemistry,An Intermediate Text"(1996)OxfordUniversity Press,ISBN 0-19-509618-5;Larock,R.C."Comprehensive OrganicTransformations:A Guide to Functional Group Preparations"第2版(1999)Wiley-VCH,ISBN:0-471-19031-4;March,J."Advanced Organic Chemistry:Reactions,Mechanisms,and Structure"第4版(1992)John Wiley&Sons,ISBN:0-471-60180-2;Otera,J.(编著)"Modern Carbonyl Chemistry"(2000)Wiley-VCH,ISBN:3-527-29871-1;Patai,S."Patai's 1992 Guide to the Chemistry of Functional Groups"(1992)Interscience ISBN:0-471-93022-9;Solomons,T.W.G."Organic Chemistry"第7版(2000)John Wiley&Sons,ISBN:0-471-19095-0;Stowell,J.C.,"Intermediate OrganicChemistry"第2版(1993)Wiley-Interscience,ISBN:0-471-57456-2;"IndustrialOrganic Chemicals:Starting Materials and Intermediates:An Ullmann'sEncyclopedia"(1999)John Wiley&Sons,ISBN:3-527-29645-X,8卷;"Organic Reactions"(1942-2000)John Wiley&Sons,超过55卷;以及"Chemistry of Functional Groups"JohnWiley&Sons,73卷。
特定的和类似的反应物任选地通过由美国化学学会(American ChemicalSociety)的化学文摘服务(Chemical Abstract Service)编制的已知化学品索引来确定,该索引可从大多数公共图书馆和大学图书馆以及通过在线数据库(联系美国化学学会,Washington,D.C.获得更多细节)获得。目录中的已知但不可商购获得的化学品任选地由定制化学合成公司制备,其中许多标准化学供应公司(例如,上文列出的那些)提供定制合成服务。对于本文所述化合物的药用盐的制备和选择有用的参考文献是P.H.Stahl和C.G.Wermuth"Handbook of Pharmaceutical Salts",Verlag Helvetica Chimica Acta,Zurich,2002。
药物组合物
在某些实施方案中,本文所述的杂芳族RAF激酶抑制性化合物作为纯化学品施用。在其他实施方案中,本文所述的杂芳族RAF激酶抑制性化合物与药学上合适的或可接受的载体(本文中也称为药学上合适的(或可接受的)赋形剂,生理学上合适的(或可接受的)赋形剂,或生理学上合适的(或可接受的)载体)组合,该载体是基于选定的给药途径和例如在Remington:The Science and Practice of Pharmacy(Gennaro,第21版.Mack Pub.Co.,Easton,PA(2005))中描述的标准药学实践而选择的。
本文提供了一种药物组合物,其包含至少一种本文所述的杂芳族RAF激酶抑制性化合物,或其立体异构体、药学上可接受的盐、水合物或溶剂化物,以及一种或多种药学上可接受的载体。如果该载体与该组合物的其他成分相容并且对该组合物的接受者(即,受试者或患者)无害,则该载体(或赋形剂)是可接受的或合适的。
一个实施方案提供了一种药物组合物,所述药物组合物包含药学上可接受的赋形剂和式(I)-(VI)的化合物或其药学上可接受的盐或溶剂化物。
一个实施方案提供了一种制备药物组合物的方法,所述方法包括将式(I)-(VI)的化合物或其药学上可接受的盐或溶剂化物与药学上可接受的载体混合。
在某些实施方案中,如式(I)-(VI)描述的杂芳族RAF激酶抑制性化合物或其药学上可接受的盐或溶剂化物是基本上纯的,因为其含有少于约5%,或少于约1%,或少于约0.1%的其他有机小分子,例如在合成方法的一个或多个步骤中产生的未反应的中间体或合成副产物。
合适的口服剂型包括,例如,片剂、丸剂、囊剂,或硬或软明胶、甲基纤维素或在消化道中易于溶解的另一合适材料的胶囊。在一些实施方案中,使用合适的无毒性固体载体,其包括例如药物级的甘露醇、乳糖、淀粉、硬脂酸镁、糖精钠、滑石、纤维素、葡萄糖、蔗糖、碳酸镁等。(参见,例如,Remington:The Science and Practice of Pharmacy(Gennaro,第21版.Mack Pub.Co.,Easton,PA(2005))。
在一些实施方案中,将式(I)-(VI)描述的杂芳族RAF激酶抑制性化合物或其药学上可接受的盐或溶剂化物配制成用于通过注射给药。在一些情况下,该注射制剂是水性制剂。在一些情况下,该注射制剂是非水性制剂。在一些情况下,该注射制剂是基于油诸如芝麻油等的制剂。
包含至少一种本文所述的杂芳族RAF激酶抑制性化合物的组合物的剂量根据受试者或患者(例如,人)的状况而不同。在一些实施方案中,这类因素包括总体健康状况、年龄和其他因素。
药物组合物以适合于待治疗(或预防)的疾病的方式施用。适当的剂量和合适的给药持续时间和频率将取决于这种因素诸如患者的状况、患者疾病的类型和严重程度、活性成分的特定形式和给药方法等。通常,适当的剂量和治疗方案以足以提供治疗性和/或预防性益处(例如,改善的临床结果,例如更频繁的完全或部分缓解,或更长的无病和/或总体存活期,或症状严重程度的减轻)的量提供组合物。通常使用实验模型和/或临床试验来确定最佳剂量。最佳剂量取决于患者的身体质量、体重或血容量。
口服剂量一般在约1.0mg至约1000mg的范围内,每天一至四次或更多次。
治疗方法
一个实施方案提供了式(I)-(IV)的化合物,或其药学上可接受的盐或溶剂化物,用于治疗人或动物体的方法中。
一个实施方案提供了式(I)-(IV)的化合物,或其药学上可接受的盐或溶剂化物,用于治疗癌症或赘生性疾病(neoplastic disease)的方法中。
一个实施方案提供了式(I)-(IV)的化合物或其药学上可接受的盐或溶剂化物在制备用于治疗癌症或赘生性疾病的药物中的用途。
在一些实施方案中,本文描述了一种治疗有需要的患者的癌症的方法,其包括向所述患者施用式(I)-(IV)的化合物,或其药学上可接受的盐或溶剂化物。在一些实施方案中,本文描述了一种治疗有需要的患者的癌症的方法,其包括向所述患者施用药物组合物,所述药物组合物包含式(I)-(IV)的化合物或其药学上可接受的盐或溶剂化物以及药学上可接受的赋形剂。
本文提供了所述方法,其中所述药物组合物经口服施用。本文提供了所述方法,其中所述药物组合物通过注射施用。
根据本公开,其他实施方案和用途对于本领域技术人员将是明显的。以下实施例仅仅提供作为对各种实施方案的说明,而不应解释为以任何方式限制本发明。
实施例
I.化学合成
在一些实施方案中,本文公开的杂芳族RAF激酶抑制性化合物按照以下实施例来合成。如以下所用的,在本发明的整篇说明书中,除非另有说明,否则下列缩写应理解为具有以下含义:
℃ 摄氏度
δH 从四甲基硅烷向低场(downfield)的化学位移,百万分比
DCM 二氯甲烷(CH2Cl2)
DMF 二甲基甲酰胺
DMSO 二甲基亚砜
EA 乙酸乙酯
ESI 电喷雾电离
Et 乙基
g 克
h 小时
HPLC 高效液相色谱法
Hz 赫兹
J 耦合常数(在NMR光谱分析中)
LCMS 液相色谱质谱法
μ 微
m 多重峰(光谱);米;毫
M 摩尔
M+ 母分子离子
Me 甲基
Mhz 兆赫兹
min 分钟
mol 摩尔;分子(如在mol wt中)
mL 毫升
MS 质谱法
nm 纳米
NMR 核磁共振
pH 酸碱度;水溶液的酸性或碱性的量度
PE 石油醚
RT 室温
s 单峰(光谱)
t 三重峰(光谱)
T 温度
TFA 三氟乙酸
THF 四氢呋喃
实施例1:(3S)-N-(3-[6-[(3,3-二氟环戊基)氨基]-2-(吗啉-4-基)嘧啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
合成方案
制备例1A:(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在环境温度和氮气氛下,向4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯胺(11.0g,47.186mmol,1.00当量)在THF(1000mL)中的搅拌溶液中加入DIEA(30.5g,235.930mmol,5.00当量)和三光气(5.6g,18.874mmol,0.40当量)。将所得混合物在环境温度下搅拌30min。向这个混合物中加入(3S)-3-(2,2,2-三氟乙基)吡咯烷盐酸盐(8.95g,47.186mmol,1.00当量)在THF(100mL)中的溶液。将所得混合物在环境温度下搅拌3h。将反应混合物减压浓缩。将残余物通过硅胶柱色谱法纯化,用含EtOAc的PE(5%-45%)洗脱,得到呈白色固体的(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(16.3g,84%)。MS ESI:C20H28BF3N2O3[M+H]+的计算值:413.21,实测值:413.25。1H NMR(300MHz,氯仿-d)δ7.75(dd,J=8.4,2.7Hz,1H),7.44(d,J=2.7Hz,1H),7.14(d,J=8.4Hz,1H),6.14(s,1H),3.86-3.74(m,1H),3.69-3.56(m,1H),3.43(td,J=9.6,6.6Hz,1H),3.11(t,J=9.6Hz,1H),2.58(dd,J=16.5,8.4Hz,1H),2.50(s,3H),2.37-2.18(m,3H),1.82-1.75(m,1H),1.36(s,12H)。19F NMR(282MHz,氯仿-d)δ-64.95。
制备例1B:N-(3,3-二甲基环戊基)-6-甲基-2-(吗啉-4-基)嘧啶-4-胺
在0℃和氮气氛下,向4-(4,6-二氯嘧啶-2-基)吗啉(140mg,0.598mmol)和3,3-二氟环戊-1-胺盐酸盐(104mg,0.658mmol)在DMSO(1mL)中的搅拌溶液中逐滴加入DIEA(386mg,2.990mmol)。将所得混合物在室温和氮气氛下搅拌16。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用饱和盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/(EA/EtOH=3:1)(3:1)洗脱,得到呈灰白色固体的N-(3,3-二甲基环戊基)-6-甲基-2-(吗啉-4-基)嘧啶-4-胺(160mg,92%)。MS ESI:C13H17ClF2N4O[M+H]+的计算值:319.11,实测值:319.15。1H NMR(400MHz,DMSO-d6)δ7.55(s,1H),5.81(s,1H),4.36(s,1H),3.61(s,8H),3.42(s,2H),2.62-2.55(m,1H),2.28-1.92(m,2H),1.73-1.63(m,1H)。19F NMR(376MHz,DMSO-d6)δ-87.90(2F)。
实施例1:(3S)-N-(3-[6-[(3,3-二氟环戊基)氨基]-2-(吗啉-4-基)嘧啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在室温和氮气氛下,向6-氯-N-(3,3-二氟环戊基)-2-(吗啉-4-基)嘧啶-4-胺(140mg,0.439mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(181mg,0.439mmol)和K
3PO
4(186mg,0.878mmol,)在二噁烷:H
2O=2:1(2mL)中的搅拌溶液中加入Pd(DtBPF)Cl
2(29mg,0.044mmol)。将所得混合物在60℃和氮气氛下搅拌16h。通过LCMS监测反应。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用饱和盐水(3x50mL)洗涤,经无水Na
2SO
4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/(EA/EtOH=3:1)(2:1)洗脱,得到150mg粗产物。将残余物通过反相快速色谱法采用以下条件纯化:柱:XBridge C18 OBD制备柱,
10μm,19mm X 250mm;流动相A:水(10MMOL/L NH
4HCO
3),流动相B:CH
3CN;流速:20mL/min;梯度:在5.8min内40%B至80%B;210/254nm,得到呈灰白色固体的(3S)-N-(3-[6-[(3,3-二氟环戊基)氨基]-2-(吗啉-4-基)嘧啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(130mg,52%)。MS ESI:C
27H
33F
5N
6O
2[M+H]
+的计算值:569.26,实测值:569.25。
1H NMR(400MHz,DMSO-d
6)δ8.13(s,1H),7.52(m,1H),7.42-7.41(m,1H),7.30-7.28(m,1H),7.09-7.06(m,1H),5.86(s,1H),4.40(s,1H),3.69-3.64(m,9H),3.55-3.50(m,1H),3.31-3.28(m,1H),3.05-3.00(m,1H),2.59-2.51(m,1H),2.49-2.40(m,3H),2.26-2.13(m,5H),2.13-2.03(m,3H),1.75-1.66(m,2H)。
19F NMR(376MHz,DMSO-d
6)δ-63.36(3F),-87.70-87.80(2F)。
实施例2和3:(3S)-N-[3-(6-[[(1R)-3,3-二氟环戊基]氨基]-2-(吗啉-4-基)嘧啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺,(3S)-N-[3-(6-[[(1S)-3,3-二氟环戊基]氨基]-2-(吗啉-4-基)嘧啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
(3S)-N-(3-[6-[(3,3-二氟环戊基)氨基]-2-(吗啉-4-基)嘧啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(130mg)通过手性制备型HPLC采用以下条件纯化:(柱:CHIRALPAK AD-H,2.0cm*25cm;流动相A:Hex(8mmol/L NH3.MeOH),流动相B:EtOH;流速:20mL/min;梯度:在18min内20B至20B;220/254nm),得到呈灰白色固体的(3S)-N-[3-(6-[[(1R)-3,3-二氟环戊基]氨基]-2-(吗啉-4-基)嘧啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(41mg,32%),MS ESI:C27H33F5N6O2[M+H]+的计算值:569.26,实测值:569.25。1H NMR(400MHz,DMSO-d6)δ8.14(s,1H),7.52(m,1H),7.43-7.41(m,1H),7.30(s,1H),7.09-7.07(m,1H),5.86(s,1H),4.40(s,1H),3.69-3.64(m,9H),3.55-3.50(m,1H),3.31-3.28(m,1H),3.05-3.00(m,1H),2.61-2.55(m,1H),2.46-2.38(m,3H),2.26-2.13(m,5H),2.13-1.91(m,3H),1.78-1.61(m,2H)。19F NMR(376MHz,DMSO-d6)δ-63.33(3F),-87.67(2F)。
还得到呈灰白色固体的(3S)-N-[3-(6-[[(1S)-3,3-二氟环戊基]氨基]-2-(吗啉-4-基)嘧啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(44mg,34%)。MSESI:C27H33F5N6O2[M+H]+的计算值:569.26,实测值:569.25。1H NMR(400MHz,DMSO-d6)δ8.14(s,1H),7.52(m,1H),7.43-7.40(m,1H),7.30(s,1H),7.09-7.06(m,1H),5.86(s,1H),4.40(s,1H),3.69-3.64(m,9H),3.55-3.50(m,1H),3.31-3.28(m,1H),3.05-3.00(m,1H),2.61-2.55(m,1H),2.46-2.38(m,3H),2.26-2.13(m,5H),2.13-1.91(m,3H),1.78-1.61(m,2H)。19FNMR(376MHz,DMSO-d6)δ-63.36(3F),-87.68(2F)。
实施例4和5:(3S)-N-[3-(2-[[(1S,3S)-3-羟基环戊基]氨基]-6-(吗啉-4-基)嘧啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺,(3S)-N-[3-(2-[[(1R,3R)-3-羟基环戊基]氨基]-6-(吗啉-4-基)嘧啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例4A:4-[6-氯-2-(甲基硫烷基)嘧啶-4-基]吗啉
在室温和氮气氛下,向4,6-二氯-2-(甲基硫烷基)嘧啶(2.20g,11.28mmol)在THF(29mL)中的搅拌溶液中逐滴加入DIPEA(1.60g,12.41mmol)、吗啉(1.08g,12.40mmol)。将所得混合物在60℃和氮气氛下搅拌过夜。使混合物冷却至室温。将所得混合物用水(50mL)稀释。通过过滤来收集沉淀的固体,得到呈浅黄色固体的4-[6-氯-2-(甲基硫烷基)嘧啶-4-基]吗啉(2.7g,97%)。MS ESI:C9H12ClN3OS[M+H]+的计算值:246.04;实测值:245.95。1H NMR(400MHz,DMSO-d6)δ6.68(s,1H),3.68-3.64(m,8H),2.45(s,3H)。
制备例4B:4-(6-氯-2-甲烷磺酰基嘧啶-4-基)吗啉
在室温和氮气氛下,向4-[6-氯-2-(甲基硫烷基)嘧啶-4-基]吗啉(12.33g,50.18mmol)和m-CPBA(23.43g,115.41mmol,85%)在DCM(172.6mL)中的搅拌溶液中。将所得混合物在室温和氮气氛下搅拌2h。将所得混合物减压浓缩。在0℃下通过添加NaHCO3水溶液(200mL)来猝灭反应。将所得混合物用EtOAc(3x150mL)萃取。将合并的有机层用NaHCO3水溶液(200mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用己烷/EtOAc(1:1)洗脱,得到呈白色固体的4-(6-氯-2-甲烷磺酰基嘧啶-4-基)吗啉(13.3g,95%)。MS ESI:C9H12ClN3O3S[M+H]+的计算值:278.03;实测值:277.95。1H NMR(300MHz,氯仿-d)δ6.62(s,1H),3.82-3.75(m,8H),3.36-3.31(m,3H)。
制备例4C:反式-3-[[4-氯-6-(吗啉-4-基)嘧啶-2-基]氨基]环戊-1-醇
将4-(6-氯-2-甲烷磺酰基嘧啶-4-基)吗啉(1.00g,3.60mmol)、(反式)-3-氨基环戊-1-醇盐酸盐(0.55g,4.00mmol)和DIEA(1.40g,10.80mmol)在DMSO(10mL)中的混合物在60℃和氮气氛下搅拌过夜。将所得混合物用水(10mL)稀释。将所得混合物用EtOAc(3x10mL)萃取。将合并的有机层用盐水(10mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/(EtOAc:EtOH=3:1)(1:1)洗脱,得到呈灰白色固体的反式-3-[[4-氯-6-(吗啉-4-基)嘧啶-2-基]氨基]环戊-1-醇(0.38g,33%)。MS ESI:C13H19ClN4O2[M+H]+的计算值:299.77,实测值:299.10。1H NMR(300MHz,DMSO-d6)δ6.07(s,1H),4.29(m,1H),4.18(m,1H),3.64(m,4H),3.54(m,4H),3.40(m,2H),2.05(m,1H),1.86(m,2H),1.64-1.58(m,1H),1.41(m,2H)。
制备例4D:(3S)-N-[3-(2-[[反式-3-羟基环戊基]氨基]-6-(吗啉-4-基)嘧啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将反式-3-[[4-氯-6-(吗啉-4-基)嘧啶-2-基]氨基]环戊-1-醇(200mg,0.669mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(276mg,0.669mmol)、Pd(DtBPF)Cl
2(44mg,0.067mmol)和K
3PO
4(284mg,1.339mmol)在1,4-二噁烷(3.6mL)和H
2O(0.9mL)中的混合物在80℃和氮气氛下搅拌过夜。将所得混合物真空浓缩。将残余物通过硅胶柱色谱法纯化,用PE/((EtOAc:EtOH=3:1):NH
4OH=20:1)(1:1)洗脱。将粗产物通过反相快速色谱法采用以下条件纯化:柱:XBridge C
18 OBD制备柱,
10μm,19mm x 250mm;流动相A:水(10mmol/L NH
4HCO
3),流动相B:CH
3CN;流速:20mL/min;梯度:在5.8min内35B至70B;210/254nm,得到呈灰白色固体的(3S)-N-[3-(2-[[(反式)-3-羟基环戊基]氨基]-6-(吗啉-4-基)嘧啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(180mg,29%)。MSESI:C
27H
35F
3N
6O
3[M+H]
+的计算值:549.27;实测值:549.30。
实施例4:(3S)-N-[3-(2-[[(1S,3S)-3-羟基环戊基]氨基]-6-(吗啉-4-基)嘧啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
实施例4和5:(3S)-N-[3-(2-[[(1R,3R)-3-羟基环戊基]氨基]-6-(吗啉-4-基)嘧啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
(3S)-N-[3-(2-[[(反式)-3-羟基环戊基]氨基]-6-(吗啉-4-基)嘧啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(180mg)通过手性HPLC采用以下条件进行拆分:(柱:Reg-AD,30x250mm,5um;流动相A:Hex(8mmol/L NH3.MeOH),流动相B:IPA;流速:45mL/min;梯度:在25min内20B至20B;220/254nm),得到75mg(44%),呈灰白色固体。MSESI:C27H35F3N6O3[M+H]+的计算值:549.61;实测值:549.30。1H NMR(300MHz,DMSO-d6)δ8.11(s,1H),7.46-7.43(m,2H),7.09-7.06(m,1H),6.52-6.50(m,1H),5.99(s,1H),4.41-4.36(m,2H),4.18-4.17(m,1H),3.70-3.43(m,10H),3.35-3.28(m,1H),3.05-2.99(m,1H),2.50-2.32(m,3H),2.25-2.16(m,3H),2.08-1.91(m,2H),1.90-1.75(m,2H),1.74-1.65(m,2H),1.64-1.30(m,2H)。19F NMR(282MHz,DMSO-d6)δ-63.39-63.45(3F),以及呈灰白色固体的(3S)-N-[3-(2-[[(1R,3R)-3-羟基环戊基]氨基]-6-(吗啉-4-基)嘧啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(77mg,45%)。MS ESI:C27H35F3N6O3[M+H]+的计算值:549.61;实测值:549.30。1H NMR(300MHz,DMSO-d6)δ8.11(s,1H),7.46-7.43(m,2H),7.09-7.06(m,1H),6.52(m,1H),5.99(s,1H),4.41-4.32(m,2H),4.17(m,1H),3.69-3.64(m,5H),3.55-3.50(m,5H),3.35-3.26(m,1H),3.05-2.99(m,1H),2.51-2.40(m,3H),2.25(s,3H),2.07-1.99(m,2H),1.93-1.85(m,2H),1.70-1.55(m,2H),1.54-1.25(m,2H)。19F NMR(376MHz,DMSO-d6)δ-63.35(3F)。
实施例6:(3S)-N-[3-(2-[[(3-羟基氧杂环丁烷-3-基)甲基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例6A:3-([[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]甲基)氧杂环丁烷-3-醇
将4-(6-氟-4-碘吡啶-2-基)吗啉(500mg,1.623mmol)、3-(氨基甲基)氧杂环丁烷-3-醇(251mg,2.434mmol)和K2CO3(449mg,3.246mmol)在NMP(15mL)中的混合物在150℃和氩气氛下搅拌过夜。将所得混合物减压浓缩。将残余物通过硅胶柱色谱法纯化,用DCM/MeOH(20/1)洗脱,得到粗产物。将残余物通过反相快速色谱法采用以下条件纯化:柱,C18硅胶;流动相,含MeCN的水,在30min内20%至50%梯度;检测器,UV 254nm,得到呈浅棕色固体的3-([[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]甲基)氧杂环丁烷-3-醇(148mg,23%)。MSESI:C13H18IN3O3[M+H]+的计算值:392.04,实测值:392.00。1H NMR(400MHz,DMSO-d6)δ6.56-6.53(m,1H),6.33(m,1H),6.23(m,1H),5.90(s,1H),4.41-4.36(m,4H),3.66-3.63(m,4H),3.54-3.53(m,2H),3.36-3.34(m,4H)。
实施例6:(3S)-N-[3-(2-[[(3-羟基氧杂环丁烷-3-基)甲基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在25℃和氮气氛下,向3-([[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]甲基)氧杂环丁烷-3-醇(140mg,0.358mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(162mg,0.394mmol)和Na2CO3(114mg,1.074mmol)在二噁烷:H2O=4:1(2.00mL)中的搅拌溶液中加入Pd(dppf)Cl2.CH2Cl2(29mg,0.036mmol)。将所得混合物在60℃和氮气氛下搅拌16h。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用饱和盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/(EA/EtOH=3:1)(2:1)洗脱,得到150mg粗产物。将残余物通过反相快速色谱法采用以下条件纯化:柱:XBridge Shield RP18 OBD柱,5um,19*150mm;流动相A:水(10MMOL/L NH4HCO3),流动相B:CH3CN;流速:20mL/min;梯度:在4.5min内45B至60B;254/210nm,得到呈灰白色固体的(3S)-N-[3-(2-[[(3-羟基氧杂环丁烷-3-基)甲基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(100mg,51%)。MS ESI:C27H34F3N5O4[M+H]+的计算值:550.26,实测值:550.25。1H NMR(300MHz,DMSO-d6)δ8.11(s,1H),7.44-7.35(m,2H),7.11-7.09(m,1H),6.45-6.42(m,1H),6.05(s,1H),5.86-5.81(m,2H),4.46-4.39(m,4H),3.69-3.64(m,5H),3.61-3.59(m,2H),3.55-3.50(m,1H),3.39-3.34(m,4H),3.30-3.27(m,1H),3.05-3.00(m,1H),2.48-2.36(m,3H),2.16(s,3H),2.10-2.07(m,1H),1.71-1.61(m,1H)。19F NMR(376MHz,DMSO-d6)δ-63.38(3F)。
实施例7:(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例7A:4-氯-N-(3,3-二氟环戊基)-6-(吗啉-4-基)嘧啶-2-胺
在室温和氮气氛下,向4-(6-氯-2-甲烷磺酰基嘧啶-4-基)吗啉(200mg,0.720mmol)和3,3-二氟环戊-1-胺盐酸盐(125mg,0.79mmol)在DMSO(4mL)中的搅拌溶液中逐滴加入DIEA(279mg,2.16mmol)。将所得混合物在60℃和氮气氛下搅拌过夜。将所得混合物用水(15mL)稀释。将所得混合物用EtOAc(3x20mL)萃取。将合并的有机层用盐水(15mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用己烷/EtOAc(1:1)洗脱,得到呈白色固体的4-氯-N-(3,3-二氟环戊基)-6-(吗啉-4-基)嘧啶-2-胺(84mg,37%)。MS ESI:C13H17ClF2N4O[M+H]+的计算值:319.11;实测值:319.15。1H NMR(300MHz,DMSO-d6)δ5.93(s,1H),5.16(s,1H),4.47-4.42(m,1H),3.79-3.76(m,4H),3.60-3.57(m,4H),2.70-2.53(m,1H),2.32-1.82(m,4H),1.79-1.73(m,1H)。
实施例7:(3S)-N-(3-[2-[(3,3-二氟环戊基)氨基]-6-(吗啉-4-基)嘧啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在室温和氮气氛下,向4-氯-N-(3,3-二氟环戊基)-6-(吗啉-4-基)嘧啶-2-胺(160mg,0.502mmol)和(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(248mg,0.602mmol)、K3PO4(213mg,1.004mmol)在二噁烷(3.2mL)、H2O(0.8mL)中的搅拌溶液中加入Pd(DtBPF)Cl2(33mg,0.050mmol)。将所得混合物在80℃和氮气氛下搅拌2h。将所得混合物真空浓缩。将残余物通过硅胶柱色谱法纯化,用己烷/(EtOAc:EtOH=3:1)(1:1)洗脱,得到粗物质。将粗产物(150mg)通过制备型HPLC采用以下条件纯化:(柱:XSelect CSH制备型C18 OBD柱,19x250mm,5um;流动相A:水(0.1%FA),流动相B:CH3CN;流速:20mL/min;梯度:在6.5min内30B至40B;254/210nm,得到呈白色固体的(3S)-N-(3-[2-[(3,3-二氟环戊基)氨基]-6-(吗啉-4-基)嘧啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(85mg,30%)。MS ESI:C27H33F5N6O2[M+H]+的计算值:569.26,实测值:569.20。1H NMR(400MHz,DMSO-d6)δ8.14(s,1H),7.47-7.45(m,2H),7.11-7.09(m,2H),6.07(s,1H),4.37-4.35(m,1H),3.67-3.51(m,10H),3.05-3.00(m,1H),2.44-2.42(m,6H),2.34-2.21(m,3H),2.09-2.08(m,4H),1.79-1.63(m,2H)。19F NMR(376MHz,DMSO-d6)δ-63.37(3F),-87.50(2F)。
实施例8和9:(3S)-N-[3-(2-[[(1R)-3,3-二氟环戊基]氨基]-6-(吗啉-4-基)嘧啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺,(3S)-N-[3-(2-[[(1S)-3,3-二氟环戊基]氨基]-6-(吗啉-4-基)嘧啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
(3S)-N-(3-[2-[(3,3-二氟环戊基)氨基]-6-(吗啉-4-基)嘧啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(80mg)通过制备型手性HPLC采用以下条件进行拆分:(柱:CHIRALPAK ADH,2x25cm,5um;流动相A:Hex(8mmol/L NH3.MeOH)--HPLC,流动相B:IPA--HPLC;流速:20mL/min;梯度:在35min内20B至20B;220/254nm),得到33mg(41%),呈白色固体。MS ESI:C27H33F5N6O2[M+H]+的计算值:569.26,实测值:569.25。1H NMR(400MHz,DMSO-d6)δ8.13(s,1H),7.47-7.44(m,2H),7.10-7.08(m,2H),6.06(s,1H),4.36-4.34(m,1H),3.69-3.51(m,11H),3.05-3.00(m,1H),2.47-2.27(m,7H),2.11-2.08(m,5H),1.75-1.66(m,2H)。19F NMR(376MHz,DMSO-d6)δ-63.37(3F),-87.50(2F),以及33mg(41%),呈白色固体。MS ESI:C27H33F5N6O2[M+H]+的计算值:569.26,实测值:569.25。1H NMR(400MHz,DMSO-d6)δ8.13(s,1H),7.47-7.44(m,2H),7.10-7.08(m,1H),6.93-6.82(m,1H),6.06(s,1H),4.39-4.27(m,1H),3.66-3.55(m,11H),3.05-3.00(m,1H),2.47-2.27(m,7H),2.19-2.03(m,5H),1.79-1.66(m,2H)。19F NMR(376MHz,DMSO-d6)δ-63.37(3F),-87.51(2F)。
实施例10:(3S)-N-[3-(2-[[(顺式-3-羟基环戊基]氨基]-6-(吗啉-4-基)嘧啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
合成方案
制备例10A:顺式-3-[[4-氯-6-(吗啉-4-基)嘧啶-2-基]氨基]环戊-1-醇
在室温和氮气氛下,向4-(6-氯-2-甲烷磺酰基嘧啶-4-基)吗啉(500mg,1.800mmol)和顺式-3-氨基环戊-1-醇盐酸盐(273mg,1.980mmol)在DMSO(9mL)中的搅拌溶液中逐滴加入DIEA(698mg,5.401mmol)。将所得混合物在60℃和氮气氛下搅拌过夜。将所得混合物用水(30mL)稀释。将所得混合物用EtOEt(4x30mL)萃取。将合并的有机层用盐水(30mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用己烷/(EtOAc:EtOH=3:1)(1:1)洗脱,得到呈白色固体的(顺式)-3-[[4-氯-6-(吗啉-4-基)嘧啶-2-基]氨基]环戊-1-醇(221mg,42%)。MS ESI:C13H19ClN4O2[M+H]+的计算值:299.12;实测值:299.151H NMR(300MHz,氯仿-d)δ5.88-5.87(m,1H),5.57(m,1H),5.34-5.32(m,1H)。4.43-4.35(m,2H),3.78-3.75(m,4H),3.60-3.56(m,4H),2.23-2.07(m,2H),1.94-1.80(m,4H)。
实施例10:(3S)-N-[3-(2-[[(顺式-3-羟基环戊基]氨基]-6-(吗啉-4-基)嘧啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在室温和氮气氛下,向(顺式)-3-[[4-氯-6-(吗啉-4-基)嘧啶-2-基]氨基]环戊-1-醇(270mg,0.904mmol)和(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(447mg,1.084mmol)、K3PO4(384mg,1.807mmol)在二噁烷(5.4mL)、H2O(1.35mL)中的搅拌混合物中加入Pd(DtBPF)Cl2(59mg,0.090mmol)。将所得混合物在80℃和氮气氛下搅拌2h。将所得混合物真空浓缩。将残余物通过硅胶柱色谱法纯化,用己烷/(EtOAc:EtOH=3:1)(1:1)洗脱,得到粗物质。将粗产物(277mg)通过制备型HPLC采用以下条件纯化:(柱:XBridge Shield RP18 OBD柱,5um,19x150mm;流动相A:水(10MMOL/L NH4HCO3),流动相B:CH3CN;流速:20mL/min;梯度:在4.3min内28B至40B;254/210nm,得到呈白色固体的(3S)-N-[3-(2-[[(顺式)-3-羟基环戊基]氨基]-6-(吗啉-4-基)嘧啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(165mg,33%)。MS ESI:C27H35F3N6O3[M+H]+的计算值:549.27;实测值:549.30。1H NMR(300MHz,DMSO-d6)δ8.12(s,1H),7.44-7.42(m,2H),7.08-7.06(m,1H),6.41-6.39(m,1H),6.00(s,1H),4.60-5.59(m,1H),4.17-4.08(m,2H),3.69-3.42(m,10H),3.05-2.99(m,1H),2.46-2.39(m,3H),2.24-2.15(m,3H),2.10-2.07(m,3H),1.88-1.85(m,1H),1.82-1.77(m,5H)。19F NMR(282MHz,DMSO-d6)δ-63.35(3F)。
实施例11和12:(3S)-N-[3-(2-[[(1S,3R)-3-羟基环戊基]氨基]-6-(吗啉-4-基)嘧啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺,(3S)-N-[3-(2-[[(1R,3S)-3-羟基环戊基]氨基]-6-(吗啉-4-基)嘧啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
(3S)-N-[3-(2-[[(顺式)-3-羟基环戊基]氨基]-6-(吗啉-4-基)嘧啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(160mg)通过制备型手性HPLC采用以下条件进行拆分:(柱:CHIRALPAK ADH,2x25cm,5um;流动相A:Hex(8mmol/L NH3.MeOH)--HPLC,流动相B:IPA--HPLC;流速:20mL/min;梯度:在15min内30B至30B;220/254nm),得到66mg(41%),呈白色固体。MS ESI:C27H35F3N6O3[M+H]+的计算值:549.27;实测值:549.30。1H NMR(400MHz,DMSO-d6)δ8.15-8.13(m,1H),7.49-7.46(m,2H),7.11-7.08(m,1H),6.52-6.33(m,1H),6.01(s,1H),4.63-4.61(m,1H),4.23-4.02(m,2H),3.79-3.52(m,11H),3.13-3.02(m,1H),2.46-2.44(m,3H),2.39-2.12(m,3H),2.17-2.05(m,2H),1.93-1.86(m,1H),1.73-1.46(m,5H)。19F NMR(376MHz,DMSO-d6)δ-63.37(3F),以及67mg(42%),呈白色固体。MS ESI:C27H35F3N6O3[M+H]+的计算值:549.27;实测值:549.30。1H NMR(400MHz,DMSO-d6)δ8.15-8.13(m,1H),7.57-7.40(m,2H),7.11-7.08(m,1H),6.52-6.43(m,1H),6.10-5.96(m,1H),4.63-5.61(m,1H),4.17-4.10(m,2H),3.82-3.41(m,11H),3.10-3.02(m,1H),2.46-2.39(m,3H),2.24-2.19(m,3H),2.17-2.07(m,2H),1.88-1.68(m,1H),1.65-1.46(m,5H)。19F NMR(376MHz,DMSO-d6)δ-63.34-63.37(3F)。
实施例13:(3S)-N-[3-(2-[[(2R)-2-羟基丙基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例13A:(2R)-1-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丙-2-醇
在室温和氮气氛下,向4-(6-氟-4-碘吡啶-2-基)吗啉(400mg,1.298mmol)和K2CO3(359mg,2.597mmol)在NMP(4mL)中的搅拌溶液中加入(R)-1-氨基-2-丙醇(146mg,1.947mmol)。将所得混合物在150℃和氮气氛下搅拌16h。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用饱和盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(2:1)洗脱,得到呈灰白色固体的(2R)-1-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丙-2-醇(200mg,42%)。MS ESI:C12H18IN3O2[M+H]+的计算值:364.04,实测值:363.90。1H NMR(400MHz,DMSO-d6)δ6.37(m,1H),6.25(m,1H),6.19(m,1H),4.64-4.63(m,1H),3.77-3.71(m,1H),3.66-3.63(m,4H),3.34-3.33(m,4H),3.17-3.06(m,2H),1.06-1.04(m,3H)。
实施例13:(3S)-N-[3-(2-[[(2R)-2-羟基丙基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在室温和氮气氛下,向(2R)-1-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丙-2-醇(50mg,0.138mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(60mg,0.145mmol)和Na2CO3(44mg,0.413mmol)在二噁烷(0.8mL)和H2O(0.2mL)中的搅拌溶液中加入Pd(dppf)Cl2.CH2Cl2(11mg,0.014mmol)。将所得混合物在60℃和氮气氛下搅拌16h。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用饱和盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EA/EtOH(8/3/1)洗脱,得到50mg粗产物。将残余物通过反相快速色谱法采用以下条件纯化:柱:XBridge制备型酰胺OBD柱,19×150mm 5um 13nm;流动相A:水(10mmol/L NH4HCO3),流动相B:CH3CN;流速:20mL/min;梯度:在4.3min内40B至70B;210/254nm。这产生呈灰白色固体的(3S)-N-[3-(2-[[(2R)-2-羟基丙基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(38mg,53%)。MS ESI:C26H34F3N5O3[M+H]+的计算值:522.26,实测值:522.15。1H NMR(400MHz,DMSO-d6)δ8.11(s,1H),7.43-7.40(m,1H),7.34-7.33(m,1H),7.10-7.08(m,1H),6.22-6.19(m,1H),5.78-5.76(m,2H),4.70-4.69(m,1H),3.83-3.77(m,1H),3.69-3.55(m,5H),3.53-3.50(m,1H),3.38-3.36(m,4H),3.31-3.27(m,1H),3.22-3.13(m,2H),3.04-3.00(m,1H),2.48-2.38(m,3H),2.16(s,3H),2.11-2.07(m,1H),1.68-1.63(m,1H),1.09-1.07(m,3H)。19F NMR(376MHz,DMSO-d6)δ-63.36(3F)。
实施例14:(3S)-N-[3-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例14A:(2R)-2-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丙-1-醇
在室温和氮气氛下,向4-(6-氟-4-碘吡啶-2-基)吗啉(300mg,0.974mmol)和K2CO3(269mg,1.947mmol)在NMP(3mL)中的搅拌溶液中加入(R)-(-)-2-氨基-1-丙醇(110mg,1.461mmol)。将所得混合物在150℃和氮气氛下搅拌16h。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用饱和盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(2:1)洗脱,得到呈灰白色固体的(2R)-2-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丙-1-醇(85mg,24%)。MS ESI:C12H18IN3O2[M+H]+的计算值:364.04,实测值:364.10。1H NMR(400MHz,DMSO-d6)δ6.23(s,1H),6.18-6.13(m,2H),4.63-4.60(m,1H),3.86-3.80(m,1H),3.66-3.63(m,4H),3.45-3.41(m,1H),3.38-3.34(m,4H),3.28-3.22(m,1H),1.09-1.07(m,3H)。
实施例14:(3S)-N-[3-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在室温和氮气氛下,向(2R)-2-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丙-1-醇(50mg,0.138mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(57mg,0.138mmol)和Na2CO3(44mg,0.413mmol)在二噁烷(0.8mL)和H2O(0.2mL)中的搅拌溶液中加入Pd(dppf)Cl2.CH2Cl2(11mg,0.014mmol)。将所得混合物在60℃和氮气氛下搅拌16h。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用饱和盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EA/EtOH(8/3/1)洗脱,得到50mg粗产物。将残余物通过反相快速色谱法采用以下条件纯化:柱:XBridge Shield RP18 OBD柱,30*150mm,5um;流动相A:水(10mmol/l NH4HCO3),流动相B:CH3CN;流速:20mL/min;梯度:在8min内35B至65B;210/254nm。这产生呈灰白色固体的(3S)-N-[3-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(31mg,43%)。MS ESI:C26H34F3N5O3[M+H]+的计算值:522.26,实测值:522.10。1H NMR(400MHz,DMSO-d6)δ8.11(s,1H),7.42-7.40(m,1H),7.34(m,1H),7.10-7.08(m,1H),5.98-5.96(m,1H),5.75(m,2H),4.66-4.64(m,1H),3.91-3.87(m,1H),3.69-3.65(m,5H),3.52-3.47(m,2H),3.38-3.36(m,4H),3.32-3.26(m,2H),3.04-3.00(m,1H),2.48-2.38(m,3H),2.16(s,3H),2.10-2.07(m,1H),1.71-1.61(m,1H),1.13-1.12(m,3H)。19F NMR(376MHz,DMSO-d6)δ-63.36(3F)。
实施例15:(3S)-N-[3-[2-(3-羟基氮杂环丁烷-1-基)-6-(吗啉-4-基)嘧啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例15A:1-[4-氯-6-(吗啉-4-基)嘧啶-2-基]氮杂环丁烷-3-醇
将4-(6-氯-2-甲烷磺酰基嘧啶-4-基)吗啉(200mg,0.720mmol)、氮杂环丁烷-3-醇盐酸盐(87mg,0.792mmol)和2,6-二甲基吡啶(232mg,2.160mmol)在DMSO(2mL)中的混合物在60℃和氮气氛下搅拌16h。在室温下通过添加水(20mL)来猝灭反应。将所得混合物用EtOAc(5x20mL)萃取。将合并的有机层经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc/EtOH(4/3/1)洗脱,得到呈灰白色固体的1-[4-氯-6-(吗啉-4-基)嘧啶-2-基]氮杂环丁烷-3-醇(110mg,48%)。MS ESI:C11H15ClN4O2[M+H]+的计算值:271.09,实测值:271.05。1H NMR(400MHz,DMSO-d6)δ6.15(s,1H),5.64(d,J=6.4Hz,1H),4.51-4.44(m,1H),4.15-4.11(m,2H),3.70-3.66(m,2H),3.61-3.59(m,4H),3.52-3.50(m,4H)。
实施例15:(3S)-N-[3-[2-(3-羟基氮杂环丁烷-1-基)-6-(吗啉-4-基)嘧啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将1-[4-氯-6-(吗啉-4-基)嘧啶-2-基]氮杂环丁烷-3-醇(50mg,0.185mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(76mg,0.185mmol)、Pd(DtBPF)Cl2(12mg,0.018mmol)和K3PO4(78mg,0.369mmol)在二噁烷(0.9mL)和H2O(0.2mL)中的混合物在80℃和氮气氛下搅拌16h。将所得混合物真空浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc/EtOH(4/3/1)洗脱,粗产物(50mg)通过制备型HPLC采用以下条件纯化:(柱:XBridge制备型C18 OBD柱,19×150mm 5um;流动相A:水(10mmol/L NH4HCO3),流动相B:CH3CN;流速:20mL/min;梯度:在4.3min内40B至75B;210/254nm),得到呈灰白色固体的(3S)-N-[3-[2-(3-羟基氮杂环丁烷-1-基)-6-(吗啉-4-基)嘧啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(38mg,39%)。MS ESI:C25H31F3N6O3[M+H]+的计算值:521.24,实测值:521.25。1H NMR(400MHz,DMSO-d6)δ8.15(s,1H),7.48-7.45(m,2H),7.10-7.08(m,1H),6.10(s,1H),5.60-5.58(m,1H),4.52-4.50(m,1H),4.18-4.14(m,2H),3.83(m,2H),3.74-3.64(m,5H),3.56-3.51(m,5H),3.31-3.30(m,1H),3.05-3.00(m,1H),2.51-2.41(m,3H),2.24(s,3H),2.08(m,1H),1.75-1.55(m,1H)。19F NMR(376MHz,DMSO-d6)δ-63.36(3F)。
实施例16:(3S)-N-[3-[2-(3-羟基氮杂环丁烷-1-基)-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例16A:1-[4-碘-6-(吗啉-4-基)吡啶-2-基]氮杂环丁烷-3-醇
在室温和氮气氛下,向4-(6-氟-4-碘吡啶-2-基)吗啉(300mg,0.974mmol)和K2CO3(269mg,1.947mmol)在NMP(3mL)中的搅拌溶液中加入氮杂环丁烷-3-醇盐酸盐(160mg,1.461mmol)。将所得混合物在150℃和氮气氛下搅拌16h。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用饱和盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(2:1)洗脱,得到呈灰白色固体的1-[4-碘-6-(吗啉-4-基)吡啶-2-基]氮杂环丁烷-3-醇(90mg,26%)。MS ESI:C12H16IN3O2[M+H]+的计算值:361.03,实测值:361.90。1H NMR(400MHz,DMSO-d6)δ6.37(m,1H),6.06-6.05(m,1H),5.61-5.59(m,1H),4.53-4.43(m,1H),4.09-4.03(m,2H),3.65-3.58(m,6H),3.37-3.35(m,4H)。
实施例16:(3S)-N-[3-[2-(3-羟基氮杂环丁烷-1-基)-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在室温和氮气氛下,向1-[4-碘-6-(吗啉-4-基)吡啶-2-基]氮杂环丁烷-3-醇(50mg,0.138mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(60mg,0.145mmol)和Na2CO3(44mg,0.415mmol)在二噁烷(0.8mL)和H2O(0.2mL)中的搅拌溶液中加入Pd(dppf)Cl2.CH2Cl2(11mg,0.014mmol)。将所得混合物在60℃和氮气氛下搅拌16h。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用饱和盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EA/EtOH(8/3/1)洗脱,得到50mg粗产物。将残余物通过反相快速色谱法采用以下条件纯化:柱:XBridge制备型C18 OBD柱,30*100mm,5um;流动相A:水(10mmol/l NH4HCO3),流动相B:CH3CN;流速:20mL/min;梯度:在8min内35B至65B;210/254nm。这产生呈灰白色固体的(3S)-N-[3-[2-(3-羟基氮杂环丁烷-1-基)-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(33mg,46%)。MS ESI:C26H32F3N5O3[M+H]+的计算值:519.25,实测值:520.15。1H NMR(400MHz,DMSO-d6)δ8.12(s,1H),7.45-7.42(m,1H),7.34-7.33(m,1H),7.12-7.10(m,1H),5.93(s,1H),5.61-5.57(m,2H),4.56-4.52(m,1H),4.12-4.08(m,2H),3.69-3.61(m,7H),3.59-3.50(m,1H),3.41-3.39(m,4H),3.31-3.27(m,1H),3.04-3.00(m,1H),2.47-2.38(m,2H),2.16(s,3H),2.10-2.08(m,1H),1.71-1.63(m,1H),1.24(m,1H)。19FNMR(376MHz,DMSO-d6)δ-63.36(3F)。
实施例17:(3R)-N-[3-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(三氟甲氧基)吡咯烷-1-甲酰胺
制备例17A:(3R)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(三氟甲氧基)吡咯烷-1-甲酰胺
在室温下,向(3R)-3-(三氟甲氧基)吡咯烷盐酸盐(150mg,0.64mmol)和DIEA(415.80mg,3.22mmol)在THF(5mL)中的搅拌溶液中加入三光气(76mg,0.26mmol,)。将所得混合物在室温下搅拌30min。向这个混合物中加入(3R)-3-(三氟甲氧基)吡咯烷盐酸盐(136mg,0.708mmol)。将溶液在室温下搅拌1h。将所得混合物真空浓缩。将残余物通过硅胶柱色谱法纯化,用EA/PE(0~60%)洗脱,得到呈灰白色固体的(3R)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(三氟甲氧基)吡咯烷-1-甲酰胺(250mg,94%)。MS ESI:C19H26BF3N2O4[M+H]+的计算值:415.19,实测值:415.25。1H NMR(400MHz,氯仿-d)δ7.73-7.71(m,1H),7.46-7.45(m,1H),7.16-7.14(m,1H),6.14(s,1H),4.95-4.92(m,1H),3.80-3.71(m,2H),3.64-3.61(m,2H),2.51(s,3H),2.37-2.20(m,2H),1.37(s,12H)。19F NMR(376MHz,氯仿-d)δ-58.70(3F)。
实施例17:(3R)-N-[3-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(三氟甲氧基)吡咯烷-1-甲酰胺
在室温和氮气氛下,向(2R)-2-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丙-1-醇(109mg,0.300mmol)在二噁烷(2mL)和H2O(0.2mL)中的搅拌溶液中加入(3R)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(三氟甲氧基)吡咯烷-1-甲酰胺(149mg,0.360mmol)、Na2CO3(191mg,0.900mmol)和Pd(dppf)Cl2 CH2Cl2(25mg,0.030mmol)。将所得混合物在80℃和氮气氛下搅拌1h。过滤所得混合物,将滤饼用EtOAc(3x10mL)洗涤。将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用含EtOAc的PE(0-82%)洗脱,得到呈棕色固体的粗产物。将粗产物(201mg)通过制备型HPLC采用以下条件纯化:柱:Atlantis制备型T3 OBD柱,19*250mm 10u;流动相A:水(0.1%FA),流动相B:CH3CN;流速:20mL/min;梯度:在6min内25B至50B;210/254nm,得到呈灰白色固体的(3R)-N-[3-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(三氟甲氧基)吡咯烷-1-甲酰胺(83mg,53%)。MS ESI:C25H33F3N5O4[M+H]+的计算值:524.25,526.25,实测值:524.10.526.10。1H NMR(300MHz,DMSO-d6)δ8.24(s,1H),7.47–7.34(m,2H),7.12(d,J=8.4Hz,1H),5.98(d,J=7.7Hz,1H),5.77(s,2H),5.16(s,1H),4.65(s,1H),3.90(t,J=6.5Hz,1H),3.82–3.59(m,7H),3.55–3.37(m,6H),2.18(s,6H),1.14(d,J=6.6Hz,3H)。
实施例18:N-[3-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)-2,5-二氢吡咯-1-甲酰胺
制备例18A:N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)-2,5-二氢吡咯-1-甲酰胺
在室温下,向4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯胺(68mg,0.292mmol,1.00当量)在THF(4mL)中的搅拌混合物中加入DIEA(188mg,1.458mmol)、三光气(35mg,0.117mmol)。将所得混合物在室温下搅拌0.5h。在室温下,向这个混合物中逐滴加入含3-(2,2,2-三氟乙基)-2,5-二氢-1H-吡咯盐酸盐(60mg,0.321mmol)的THF(3mL)。将所得混合物在室温下搅拌2h。将所得混合物用MeOH(10mL)稀释,并且真空浓缩。将残余物通过硅胶柱色谱法纯化,用己烷/(EtOAc:EtOH=3:1)(1:1)洗脱,得到呈浅棕色油状物的N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)-2,5-二氢吡咯-1-甲酰胺(100mg,84%)。MS ESI:C20H26BF3N2O3[M+H]+的计算值:411.20,实测值:411.20。1H NMR(300MHz,DMSO-d6)δ8.22(s,1H),7.69(d,J=2.4Hz,1H),7.64(d,J=8.4Hz,1H),7.06(d,J=8.4Hz,1H),5.95(s,1H),4.21(s,4H),3.32(q,J=11.7Hz,2H),2.40(s,3H),1.31(s,12H)。
实施例18:N-[3-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)-2,5-二氢吡咯-1-甲酰胺
向(2R)-2-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丙-1-醇(132mg,0.36mmol)和N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)-2,5-二氢吡咯-1-甲酰胺(149mg,0.363mmol)在1,4-二噁烷(2mL)和H2O(0.2mL)中的溶液中加入Pd(dppf)Cl2·CH2Cl2(30mg,0.030mmol)和K3PO4(231mg,1.090mmol)。在80℃和氮气氛下搅拌1h后,将所得混合物减压浓缩。将残余物通过硅胶柱色谱法纯化,用含EtOAc的PE(0-50%)洗脱,得到粗产物。粗产物通过制备型HPLC采用以下条件纯化:柱:球形C18,19x150mm 5um;流动相A:水(0.1%FA),流动相B:CH3CN;流速:20mL/min;梯度:在4.3min内30%B至60%B;检测器:UV 210和254nm,得到呈浅粉红色固体的N-[3-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)-2,5-二氢吡咯-1-甲酰胺(82mg,44%)。MS ESI:C26H34F3N5O3[M+H]+的计算值:520.25,实测值:520.10。1HNMR(400MHz,DMSO-d6)δ8.19(s,1H),7.43(dd,J=8.2,2.3Hz,1H),7.35(d,J=2.3Hz,1H),7.11(d,J=8.3Hz,1H),6.00–5.91(m,2H),5.76(d,J=1.6Hz,2H),4.64(t,J=5.5Hz,1H),4.18(S,4H)3.89(p,J=6.5Hz,1H),3.72–3.64(m,4H),3.50(dt,J=10.0,5.0Hz,1H),3.37(t,J=4.9Hz,4H),3.32–3.25(m,2H),2.17(s,3H),1.13(d,J=6.5Hz,3H)。19F NMR(376MHz,DMSO-d6)δ-63.28(3F)
实施例19:(3S)-N-(3-[2-[(2-羟基乙基)氨基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例19A:2-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]乙醇
在室温下,向4-(6-氟-4-碘吡啶-2-基)吗啉(2.00g,6.492mmol)和K2CO3(1.79g,12.983mmol)在NMP(20mL)中的搅拌混合物中加入乙醇胺(595mg,9.737mmol)。将所得混合物在150℃下搅拌16h。使混合物冷却至室温。在室温下用水(20mL)猝灭反应。将所得混合物用EtOAc(3x20mL)萃取。将合并的有机层用盐水(1x20mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1:1)洗脱,得到呈黄色油状物的2-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]乙醇(2g,88%)。MS ESI:C15H20BrN3O2[M+H]+的计算值:350.03,实测值:350.00。1H NMR(300MHz,DMSO-d6)δ6.23(m,2H),4.64(m,1H),3.66(t,J=4.6Hz,4H),2.72(d,J=1.2Hz,8H)。
实施例19:(3S)-N-(3-[2-[(2-羟基乙基)氨基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在60℃和氮气氛下,分数份向2-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]乙醇(150mg,0.430mmol)和(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(142mg,0.344mmol)在二噁烷(4mL)和H2O(1mL)中的搅拌混合物中加入Na2CO3(137mg,1.289mmol)和Pd(dppf)Cl2 CH2Cl2(35mg,0.043mmol)。在室温下用水(20mL)猝灭反应。将所得混合物用EtOAc(3x60mL)萃取。将合并的有机层用盐水(3x10mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1:1)洗脱,得到呈浅绿色固体的(3S)-N-(3-[2-[(2-羟基乙基)氨基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(95mg,43%)。MS ESI:C15H20BrN3O2[M+H]+的计算值:508.25,实测值:508.00。1H NMR(400MHz,DMSO-d6)δ8.11(s,1H),7.49–7.27(m,2H),7.09(d,J=8.4Hz,1H),6.21(s,1H),5.76(s,2H),4.66(t,J=5.5Hz,1H),3.68(s,3H),3.53(d,J=7.4Hz,3H),3.38(s,9H),3.02(t,J=9.4Hz,1H),2.44(s,3H),2.12(d,J=29.5Hz,4H),1.66(t,J=10.6Hz,1H)。
实施例20:N-(3-[2-[(2-羟基乙基)氨基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)-2,5-二氢吡咯-1-甲酰胺
在60℃和氮气氛下,分数份向2-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]乙醇(150mg,0.430mmol)和N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)-2,5-二氢吡咯-1-甲酰胺(141mg,0.344mmol)在二噁烷(4mL)和H2O(1mL)中的搅拌混合物中加入Na2CO3(137mg,1.289mmol)和Pd(dppf)Cl2 CH2Cl2(35mg,0.043mmol)。在室温下通过添加水(20mL)来猝灭反应。将所得混合物用EtOAc(3x60mL)萃取。将合并的有机层用盐水(3x10mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1:1)洗脱,得到呈浅绿色固体的N-(3-[2-[(2-羟基乙基)氨基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)-2,5-二氢吡咯-1-甲酰胺(97mg,44%)。MS ESI:C25H30F3N5O3[M+H]+的计算值:506.23,实测值:506.00。1H NMR(400MHz,DMSO-d6)δ8.20(s,1H),7.49-7.30(m,2H),7.11(d,J=8.4Hz,1H),6.23(s,1H),5.94(s,1H),5.77(s,2H),4.66(s,1H),4.20(s,4H),3.68(s,4H),3.54(s,2H),3.36(d,J=18.2Hz,8H),2.17(s,3H)。
实施例21:(3S)-N-[3-[2-(3-羟基氮杂环丁烷-1-基)-6-(吗啉-4-基)嘧啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例21A:2-[[4-碘-6-(吗啉-4-基)吡啶-2-基](甲基)氨基]乙醇
在室温下,向4-(6-氟-4-碘吡啶-2-基)吗啉(500mg,1.623mmol)和K2CO3(449mg,3.246mmol)在NMP(5mL)中的搅拌混合物中加入甲基乙醇胺(183mg,2.434mmol)。将所得混合物在150℃下搅拌16h。使混合物冷却至室温。在室温下用水(20mL)猝灭反应。将所得混合物用EtOAc(3x20mL)萃取。将合并的有机层用盐水(20mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈黄色油状物的2-[[4-碘-6-(吗啉-4-基)吡啶-2-基](甲基)氨基]乙醇(480mg,81%)。MS ESI:C12H18IN3O2[M+H]+的计算值:363.95,实测值:363.95。1H NMR(300MHz,氯仿-d)δ6.34-6.26(m,2H),3.80(m,6H),3.70(dd,J=5.5,4.4Hz,2H),3.47-3.36(m,4H),3.02(s,3H)。
实施例21:(3S)-N-[3-[2-(3-羟基氮杂环丁烷-1-基)-6-(吗啉-4-基)嘧啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在室温和氮气氛下,向2-[[4-碘-6-(吗啉-4-基)吡啶-2-基](甲基)氨基]乙醇(200mg,0.551mmol)和(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(227mg,0.551mmol)在1,4-二噁烷(2mL)和H2O(0.5mL)中的搅拌溶液中加入Na2CO3(175mg,1.652mmol)和Pd(dppf)Cl2 CH2Cl2(40mg,0.055mmol)。将所得混合物在70℃和氮气氛下搅拌16h。使混合物冷却至室温。在室温下通过添加水(10mL)来猝灭反应。将所得混合物用EtOAc(3x10mL)萃取。将合并的有机层用盐水(10mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc/EtOH(4/3/1)洗脱,得到呈浅棕色固体的(3S)-N-(3-[2-[(2-羟基乙基)(甲基)氨基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(172mg,60%)。MS ESI:C26H34F3N5O3[M+H]+的计算值:522.15,实测值:522.15。1H NMR(400MHz,DMSO-d6)δ8.12(s,1H),7.44(dd,J=8.3,2.3Hz,1H),7.34(d,J=2.3Hz,1H),7.11(d,J=8.4Hz,1H),5.84(d,J=13.6Hz,2H),4.68-4.59(m,1H),3.69(d,J=5.2Hz,5H),3.61-3.48(m,5H),3.40(t,J=4.7Hz,4H),3.03(s,4H),2.44(t,J=10.4Hz,3H),2.17(s,3H),2.09(s,1H),2.01(s,1H),1.73-1.60(m,1H)。19F NMR(376MHz,DMSO-d6)δ-63.36(3F)。
实施例22:(3R)-N-(3-[2-[(2-羟基乙基)氨基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(三氟甲氧基)吡咯烷-1-甲酰胺
在60℃和氮气氛下,分数份向2-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]乙醇(150mg,0.430mmol)和(3R)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(三氟甲氧基)吡咯烷-1-甲酰胺(142mg,0.344mmol)在二噁烷(4ml)和H2O(1mL)中的搅拌混合物中加入Na2CO3(137mg,1.289mmol)和Pd(dppf)Cl2 CH2Cl2(35mg,0.043mmol)。在室温下通过添加水(20mL)来猝灭反应。将所得混合物用EtOAc(3x60mL)萃取。将合并的有机层用盐水(3x10mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈浅绿色固体的(3R)-N-(3-[2-[(2-羟基乙基)氨基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(三氟甲氧基)吡咯烷-1-甲酰胺(74.3mg,34%)。MS ESI:C24H30F3N5O4[M+H]+的计算值:510.22,实测值:510.00。1HNMR(400MHz,DMSO-d6)δ8.24(s,1H),7.53–7.24(m,2H),7.11(d,J=8.3Hz,1H),6.22(t,J=5.9Hz,1H),5.77(s,2H),5.15(s,1H),4.66(t,J=5.5Hz,1H),3.78–3.62(m,5H),3.56(dd,J=14.2,8.1Hz,3H),3.46(d,J=8.9Hz,1H),3.38(s,3H),3.34(s,3H),3.31(d,J=5.9Hz,1H),2.20-2.00(m,5H)。
实施例23:(3R)-N-[3-(2-[[(2R)-2-羟基丙基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(三氟甲氧基)吡咯烷-1-甲酰胺
在室温和氮气氛下,向(2R)-1-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丙-2-醇(132mg,0.363mmol)、(3R)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(三氟甲氧基)吡咯烷-1-甲酰胺(151mg,0.363mmol)和Na2CO3(116mg,1.090mmol)在二噁烷(0.8mL)和水(0.2mL)中的搅拌溶液中加入Pd(dppf)Cl2.CH2Cl2(30mg,0.036mmol)。将所得混合物在60℃和氮气氛下搅拌16h。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用饱和盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EA/EtOH(8/3/1)洗脱,得到125mg粗产物。将残余物通过反相快速色谱法采用以下条件纯化:柱:XBridge制备型C18 OBD柱,19×150mm 5um;流动相A:水(10mmol/l NH4HCO3),流动相B:CH3CN;流速:20mL/min;梯度:在4.3min内40B至75B;210/254nm。这产生呈浅绿色固体的(3R)-N-[3-(2-[[(2R)-2-羟基丙基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(三氟甲氧基)吡咯烷-1-甲酰胺(102mg,54%)。MS ESI:C25H32F3N5O4[M+H]+的计算值:524.24,实测值:524.15。1H NMR(400MHz,DMSO-d6)δ8.22(s,1H),7.42-7.33(m,2H),7.12-7.09(m,1H),6.20-6.15(m,1H),5.83-5.76(m,2H),5.14(s,1H),4.69-4.67(m,1H),3.83-3.76(m,1H),3.67-3.55(m,7H),3.48-3.37(m,5H),3.20-3.14(m,2H),2.24-2.16(m,5H),1.09-1.07(m,3H)。19F NMR(376MHz,DMSO-d6)δ-56.69(3F)。
实施例24:N-[3-(2-[[(2R)-2-羟基丙基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)-2,5-二氢吡咯-1-甲酰胺
将(2R)-1-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丙-2-醇(133mg,0.366mmol)、N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)-2,5-二氢吡咯-1-甲酰胺(150mg,0.370mmol)、Pd(dppf)Cl2.CH2Cl2(30mg,0.040mmol)和K3PO4(233mg,1.100mmol)在二噁烷(3mL)和H2O(0.3mL)中的混合物在80℃和N2氛下搅拌2小时。将混合物冷却。向所得混合物中加入水(5mL),并且用EtOAc(3x10mL)萃取。将合并的有机层用水(2x10mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(50-100%)洗脱,得到粗产物。将残余物通过制备型HPLC采用以下条件纯化:柱:X-Bridge制备型C18 OBD柱,19x150mm 5um;流动相A:水(10mmol/LNH4HCO3),流动相B:ACN;流速:20mL/min;梯度:在4.3min内20B至55B;210/254nm,得到呈白色固体的N-[3-(2-[[(2R)-2-羟基丙基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)-2,5-二氢吡咯-1-甲酰胺(97mg,51%)。MS ESI:C19H25BrN4O3[M+H]+的计算值:437.11,实测值:437.00。1H NMR(400MHz,CDCL3)δ7.37(dd,J=8.2,2.4Hz,1H),7.24(d,J=2.4Hz,1H),7.18(d,J=8.2Hz,1H),6.13(s,1H),5.88-5.82(m,3H),4.70(brs,1H),4.32-4.30(m,4H),4.06-3.98(m,1H),3.84-3.81(m,4H),3.54-3.43(m,5H),3.31-3.28(m,1H),3.05-2.98(m,2H),2.24(s,3H),1.25(d,J=6.3Hz,3H)。
实施例25:(3S)-N-[3-(2-[[(2R)-2-羟基丙基](甲基)氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例25A:(2R)-1-[[4-碘-6-(吗啉-4-基)吡啶-2-基](甲基)氨基]丙-2-醇
在0℃和氮气氛下,向(2R)-1-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丙-2-醇(500mg,1.377mmol)和K2CO3(571mg,4.130mmol)在丙酮(10mL)中的搅拌溶液中加入碘代甲烷(234mg,1.652mmol)。将所得混合物在60℃和氮气氛下搅拌48h。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用饱和盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(2/1)洗脱,得到呈灰白色固体的(2R)-1-[[4-碘-6-(吗啉-4-基)吡啶-2-基](甲基)氨基]丙-2-醇(150mg,29%)。MS ESI:C13H20IN3O2[M+H]+的计算值:378.06,实测值:378.10。1H NMR(400MHz,CDCL3)δ6.33-6.30(m,2H),4.16-4.09(m,1H),3.81-3.79(m,4H),1.66-1.61(m,1H),3.48-3.42(m,5H),3.04(s,3H),1.23-1.22(m,3H)。
实施例25:(3S)-N-[3-(2-[[(2R)-2-羟基丙基](甲基)氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在室温和氮气氛下,向(2R)-1-[[4-碘-6-(吗啉-4-基)吡啶-2-基](甲基)氨基]丙-2-醇(200mg,0.530mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(219mg,0.530mmol)和Na2CO3(169mg,1.591mmol)在二噁烷(1.6mL)和H2O(0.4mL)中的搅拌溶液中加入Pd(dppf)Cl2.CH2Cl2(43mg,0.053mmol)。将所得混合物在60℃和氮气氛下搅拌16h。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用饱和盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EA/EtOH(8/3/1)洗脱,得到70mg粗产物。将残余物通过反相快速色谱法采用以下条件纯化:柱:XBridge制备型C18 OBD柱,19×150mm 5um;流动相A:水(10mmol/l NH4HCO3),流动相B:CH3CN;流速:20mL/min;梯度:在4.3min内40B至70B;210/254nm。这产生呈浅绿色固体的(3S)-N-[3-(2-[[(2R)-2-羟基丙基](甲基)氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(144mg,51%)。MS ESI:C27H36F3N5O3[M+H]+的计算值:536.28,实测值:536.20。1H NMR(400MHz,DMSO-d6)δ8.11(s,1H),7.44-7.40(m,1H),7.33-7.32(m,1H),7.11-7.08(m,1H),5.84-5.79(m,2H),4.66-4.65(m,1H),3.92-3.86(m,1H),3.69-3.63(m,5H),3.55-3.44(m,2H),3.40-3.37(m,4H),3.29-3.26(m,2H),3.02-2.98(m,4H),2.46-2.39(m,3H),2.15-2.06(m,4H),1.71-1.61(m,1H),1.06-1.04(m,3H)。19FNMR(376MHz,DMSO-d6)δ-63.35(3F)。
实施例26:(3S)-N-[3-[2-(3,6-二氢-2H-吡喃-4-基)-6-[[(2R)-2-羟基丙基]氨基]吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例26A:(2R)-1-[(6-氯-4-碘吡啶-2-基)氨基]丙-2-醇
在室温下,向2,6-二氯-4-碘吡啶(1g,3.651mmol)和K2CO3(1g,7.302mmol)在NMP(20mL)中的搅拌溶液中加入(R)-1-氨基-2-丙醇(274mg,3.651mmol)。将所得混合物的部分在100℃下搅拌16h。通过添加水(70mL)来猝灭反应。将所得混合物用EtOAc(3x150mL)萃取。将合并的有机层用饱和盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(2/1)洗脱,得到呈黄色油状物的(2R)-1-[(6-氯-4-碘吡啶-2-基)氨基]丙-2-醇(410mg,36%)。MS ESI:C8H10ClIN2O[M+H]+的计算值:312.54,实测值:312.95。1H NMR(300MHz,氯仿-d)δ6.96(d,J=1.0Hz,1H),6.74(d,J=1.1Hz,1H),5.31(s,1H),3.46(dd,J=13.7,3.1Hz,2H),3.19(dd,J=13.7,7.7Hz,1H),1.26(d,J=6.2Hz,3H)。
制备例26B:(3S)-N-[3-(2-氯-6-[[(2R)-2-羟基丙基]氨基]吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在室温和氮气氛下,分数份向(2R)-1-[(6-氯-4-碘吡啶-2-基)氨基]丙-2-醇(380mg,1.216mmol)和(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(501mg,1.216mmol)、K3PO4(774mg,3.648mmol)在二噁烷(4mL)、H2O(0.4mL)中的搅拌混合物中加入Pd(dppf)Cl2 CH2Cl2(99mg,0.122mmol)。将所得混合物在50℃和氮气氛下搅拌1h。将所得混合物用水(100mL)猝灭,并且用EtOAc(3x300mL)萃取。将合并的有机层用盐水(2x70mL)洗涤,经无水Na2SO4干燥,并且减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE中的0%至50%EtOAc洗脱,得到呈黄色固体的(3S)-N-[3-(2-氯-6-[[(2R)-2-羟基丙基]氨基]吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(510mg,89%)。MS ESI:C22H26ClF3N4O2[M+H]+的计算值:471.17,实测值:471.20。1H NMR(300MHz,DMSO-d6)δ8.19(s,1H),7.49(s,1H),7.41(s,1H),7.15(s,1H),7.00(s,1H),6.44(d,J=1.1Hz,2H),4.75(s,1H),4.05-3.98(m,1H),3.69-3.60(m,1H),3.55-3.51(m,1H),3.33-3.29(m,2H),3.21-3.18(m,2H),2.19(s,1H),2.16-2.05(m,2H),2.01(d,J=1.1Hz,1H),1.67-1.61(m,2H),1.07(s,3H)。
实施例26:(3S)-N-[3-[2-(3,6-二氢-2H-吡喃-4-基)-6-[[(2R)-2-羟基丙基]氨基]吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在室温和氮气氛下,分数份向(3S)-N-[3-(2-氯-6-[[(2R)-2-羟基丙基]氨基]吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(430mg,0.913mmol)和2-(3,6-二氢-2H-吡喃-4-基)-4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷(384mg,1.826mmol)、Cs2CO3(893mg,2.739mmol)在二噁烷(5mL)、H2O(0.5mL)中的搅拌混合物中加入Pd(dppf)Cl2 CH2Cl2(75mg,0.091mmol)。将所得混合物在100℃和氮气氛下搅拌1h。将所得混合物用水(50mL)猝灭,并且用EtOAc(3x100mL)萃取。将合并的有机层用盐水(2x30mL)洗涤,经无水Na2SO4干燥,并且减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE中的0%至90%EtOAc洗脱,得到呈黄色固体的(3S)-N-[3-[2-(3,6-二氢-2H-吡喃-4-基)-6-[[(2R)-2-羟基丙基]氨基]吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(310mg,65%)。MS ESI:C27H33F3N4O3[M+H]+的计算值:519.25,实测值:519.15。1H NMR(300MHz,DMSO-d6)δ8.17(s,1H),7.47-7.45(m,2H),7.40(s,1H),7.16-7.13(m,1H),6.73(s,1H),6.53(s,1H),6.36(s,1H),4.84-4.83(m,1H),4.27(s,2H),3.81(s,3H),3.71-3.69(m,2H),3.57-3.31(m,4H),3.07-3.01(m,1H),2.52-2.42(m,4H),2.18-2.10(m,4H),1.70-1.64(m,1H),1.12-1.10(m,3H)。
实施例27:(3S)-N-[3-(2-[[(2R)-2-羟基丙基]氨基]-6-(氧杂环己烷-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在氮气氛下,向(3S)-N-[3-[2-(3,6-二氢-2H-吡喃-4-基)-6-[[(2R)-2-羟基丙基]氨基]吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(150mg,0.289mmol)在MeOH(2mL)、CH3COOH(0.1mL)中的溶液中加入Pd/C(92mg,0.868mmol)。在室温下,使用氢气气球在氢气氛下使混合物氢化2h,经硅藻土垫过滤,并且减压浓缩。将粗产物(200mg)通过制备型HPLC采用以下条件纯化:(柱:XBridge制备型C18 OBD柱,150mm 5um;流动相A:水(10mmol/L NH4HCO3),流动相B:CH3CN;流速:20mL/min;梯度:在4.3min内20B至50B;210/254nm),得到呈白色固体的(3S)-N-[3-(2-[[(2R)-2-羟基丙基]氨基]-6-(氧杂环己烷-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(115mg,76%)。MS ESI:C27H35F3N4O3[M+H]+的计算值:521.27,实测值:521.15。1H NMR(300MHz,DMSO-d6)δ8.14(s,1H),7.41(s,2H),7.36-7.35(m,1H),7.13-7.10(m,1H),6.29-6.27(m,2H),4.84(s,1H),3.95(s,2H),3.91(s,1H),3.41(s,1H),3.37-3.33(m,3H),3.27-3.25(m,2H),3.10-2.98(m,1H),2.78(s,1H),2.50-2.42(m,4H),2.15-2.10(m,4H),1.75-1.71(m,5H),1.09-1.07(m,3H)。
实施例28:N-[3-(2-[[(2R)-2-羟基丙基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(三氟甲基)-2,5-二氢吡咯-1-甲酰胺
制备例28A:N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(三氟甲基)-2,5-二氢吡咯-1-甲酰胺
在室温和氮气氛下,向4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯胺(435mg,1.867mmol)和三光气(246mg,0.830mmol)在THF(40mL)中的溶液中加入DIEA(1.81mL,13.977mmol)。将混合物在室温下搅拌30min。向这个混合物中加入3-(三氟甲基)-2,5-二氢-1H-吡咯盐酸盐(180mg,1.037mmol),并且将混合物在室温下搅拌3h。将所得混合物减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(2/1)洗脱,得到呈黄色油状物的N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(三氟甲基)-2,5-二氢吡咯-1-甲酰胺(500mg,61%)。MS ESI:C19H24F3N2O3[M+H]+的计算值:397.25,实测值:397.25。1H NMR(400MHz,CDCl3-d)δ7.71(dd,J=8.3,2.5Hz,1H),7.48(d,J=2.6Hz,1H),7.15(d,J=8.3Hz,1H),6.45-6.40(m,1H),6.16(s,1H),4.44(s,4H),2.50(s,3H),1.36(s,12H)。19F NMR(376MHz,CDCl3-d)δ-65.69(3F)。
实施例28:N-[3-(2-[[(2R)-2-羟基丙基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(三氟甲基)-2,5-二氢吡咯-1-甲酰胺
向(2R)-1-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丙-2-醇(160mg,0.441mmol)和N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(三氟甲基)-2,5-二氢吡咯-1-甲酰胺(174mg,0.441mmol)在1,4-二噁烷(2mL)和H2O(0.5mL)中的搅拌溶液中加入Pd(dppf)Cl2·CH2Cl2(36mg,0.044mmol)和Na2CO3(140mg,1.322mmol)。将所得混合物在60℃和氮气氛下搅拌16h。使混合物冷却至室温。在室温下通过添加水(10mL)来猝灭反应。将所得混合物用EtOAc(3x10mL)萃取。将合并的有机层用盐水(10mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/2)洗脱,得到呈浅绿色固体的N-[3-(2-[[(2R)-2-羟基丙基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(三氟甲基)-2,5-二氢吡咯-1-甲酰胺(116mg,44%)。MS ESI:C25H30F3N5O3[M+H]+的计算值:506.05,实测值:506.05。1H NMR(300MHz,DMSO-d6)δ8.31(s,1H),7.45(dd,J=8.2,2.3Hz,1H),7.37(d,J=2.3Hz,1H),7.14(d,J=8.3Hz,1H),6.75(d,J=2.6Hz,1H),6.23(s,1H),5.79(d,J=6.5Hz,2H),4.70(s,1H),4.41(s,4H),3.81(s,1H),3.70(t,J=4.8Hz,4H),3.39(t,J=4.8Hz,4H),3.23-3.09(m,2H),2.19(s,3H),1.10(d,J=6.2Hz,3H)。19FNMR(282MHz,DMSO-d6)δ-63.98(3F)。
实施例29:N-[3-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(三氟甲基)-2,5-二氢吡咯-1-甲酰胺
向(2R)-2-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丙-1-醇(150mg,0.413mmol)和N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(三氟甲基)-2,5-二氢吡咯-1-甲酰胺(164mg,0.413mmol)在1,4-二噁烷(2mL)和H2O(0.4mL)中的搅拌溶液中加入Na2CO3(131mg,1.239mmol)和Pd(dppf)Cl2.CH2Cl2(34mg,0.041mmol)。将所得混合物在60℃和氮气氛下搅拌16h。使混合物冷却至室温。在室温下通过添加水(10mL)来猝灭反应。将所得混合物用EtOAc(3x10mL)萃取。将合并的有机层用盐水(10mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/2)洗脱,得到呈浅黄色固体的N-[3-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(三氟甲基)-2,5-二氢吡咯-1-甲酰胺(116mg,56%)。MS ESI:C25H30F3N5O3[M+H]+的计算值:506.10,实测值:506.10。1H NMR(400MHz,DMSO-d6)δ8.29(s,1H),7.45-7.40(m,1H),7.36(d,J=2.3Hz,1H),7.13(d,J=8.4Hz,1H),6.76-672(m,1H),5.99(s,1H),5.76(s,2H),4.65(s,1H),4.39(s,4H),3.93-3.85(m,1H),3.71-3.64(m,4H),3.49(dd,J=10.3,4.9Hz,1H),3.37(t,J=4.8Hz,4H),3.34-3.33(m,1H),2.17(s,3H),1.13(d,J=6.5Hz,3H)。19F NMR(376MHz,DMSO-d6)δ-63.99(3F)。
实施例30:(3S)-N-[3-(2-[[(2S)-1-羟基丙烷-2-基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例30A:(2S)-2-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丙-1-醇
在室温和氮气氛下,向4-(6-氟-4-碘吡啶-2-基)吗啉(300mg,0.974mmol)和K2CO3(269mg,1.947mmol)在NMP(3mL)中的搅拌溶液中加入(2S)-2-氨基丙-1-醇(110mg,1.461mmol)。将所得混合物在150℃和氮气氛下搅拌16h。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈灰白色固体的(2S)-2-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丙-1-醇(198mg,55%)。MS ESI:C12H18IN3O2[M+H]+的计算值:364.04,实测值:364.10。1H NMR(400MHz,CDCL3)δ6.29-6.25(m,2H),4.32-4.28(m,1H),4.02(s,1H),3.81-3.72(m,5H),3.58-3.54(m,1H),3.45-3.43(m,4H),1.23-1.22(m,3H)。
实施例30:(3S)-N-[3-(2-[[(2S)-1-羟基丙烷-2-基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将(2S)-2-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丙-1-醇(200mg,0.551mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(227mg,0.551mmol)、Na2CO3(175mg,1.652mmol)、1,4-二噁烷(1.6mL)、H2O(0.4mL)和Pd(dppf)Cl2.CH2Cl2(45mg,0.055mmol)的混合物在60℃和氮气氛下搅拌16h。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用饱和盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc/EtOH=(8/3/1)洗脱,随后进行采用以下条件的反相快速色谱法:柱:SunFire制备型C18 OBD柱,19×150mm 5um 10nm;流动相A:水(0.05%TFA),流动相B:CH3CN;流速:20mL/min;梯度:在5.3min内25B至65B;254/210nm。这产生呈灰白色固体的(3S)-N-[3-(2-[[(2S)-1-羟基丙烷-2-基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(111mg,37%)。MS ESI:C26H34F3N5O3[M+H]+的计算值:522.26,实测值:522.30。1H NMR(400MHz,DMSO-d6)δ8.11(s,1H),7.42-7.40(m,1H),7.34-7.33(m,1H),7.10-7.08(m,1H),5.98-5.96(m,1H),5.75(m,2H),4.65(s,1H),3.90-3.87(m,1H),3.69-3.65(m,5H),3.55-3.48(m,2H),3.38-3.34(m,5H),3.04-2.99(m,1H),2.48-2.41(m,3H),2.16(s,3H),2.10-2.07(m,1H),1.70-1.60(m,1H),1.13-1.12(m,3H)。19F NMR(376MHz,DMSO-d6)δ-63.37(3F)。
实施例31:(3S)-N-[3-(2-[[(2R)-2-羟基丙基](甲基)氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例31A:(2R)-1-[[4-碘-6-(吗啉-4-基)吡啶-2-基](甲基)氨基]丙-2-醇
将4-(6-氟-4-碘吡啶-2-基)吗啉(300mg,0.974mmol)、K2CO3(269mg,1.947mmol)、NMP(3mL)和(2S)-1-氨基丙-2-醇(110mg,1.461mmol)的混合物在150℃和氮气氛下搅拌16h。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用饱和盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈灰白色固体的(2S)-1-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丙-2-醇(222mg,63%)。MS ESI:C12H18IN3O2[M+H]+的计算值:364.04,实测值:364.10。1H NMR(400MHz,氯仿-d)δ6.29-6.25(m,2H),4.65(s,1H),4.05-3.97(m,1H),3.81-3.78(m,4H),3.47-3.41(m,5H),3.25-3.18(m,1H),1.25-1.23(m,3H)。
实施例31:(3S)-N-[3-(2-[[(2R)-2-羟基丙基](甲基)氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将(2S)-1-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丙-2-醇(200mg,0.551mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(227mg,0.551mmol)、Na2CO3(175mg,1.652mmol)、二噁烷:H2O=4:1(2mL)和Pd(dppf)Cl2.CH2Cl2(45mg,0.055mmol)的混合物在60℃和氮气氛下搅拌16h。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用饱和盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EA/EtOH=(8/3/1)洗脱,随后进行采用以下条件的反相快速色谱法:柱:SunFire制备型C18 OBD柱,19×150mm 5um 10nm;流动相A:水(0.1%FA),流动相B:CH3CN;流速:20mL/min;梯度:在5.3min内25B至65B;254/210nm。这产生呈灰白色固体的(3S)-N-[3-(2-[[(2S)-2-羟基丙基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(145mg,49%)。MS ESI:C26H34F3N5O3[M+H]+的计算值:522.26,实测值:522.25。1H NMR(400MHz,DMSO-d6)δ8.11(s,1H),7.43-7.40(m,1H),7.34-7.33(m,1H),7.10-7.08(m,1H),6.22-6.19(m,1H),5.78-5.76(m,2H),4.70(s,1H),3.82-3.77(m,1H),3.69-3.65(m,5H),3.55-3.50(m,1H),3.38-3.36(m,4H),3.23-3.11(m,2H),3.04-2.99(m,1H),2.48-2.36(m,3H),2.16(s,3H),2.11-2.07(m,1H),1.70-1.60(m,1H),1.09-1.07(m,3H)。19F NMR(376MHz,DMSO-d6)δ-63.37(3F)。
实施例32:(3S)-N-[3-[2-(3,6-二氢-2H-吡喃-4-基)-6-[[(2R)-1-羟基丙烷-2-基]氨基]吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例32A:(2R)-2-[(6-氯-4-碘吡啶-2-基)氨基]丙-1-醇
在室温下,向2,6-二氯-4-碘吡啶(1g,3.651mmol)和K2CO3(1g,7.302mmol)在NMP(20mL)中的搅拌溶液中加入(R)-(-)-2-氨基-1-丙醇(274mg,3.651mmol)。将所得混合物的部分在100℃下搅拌16h。通过添加水(70mL)来猝灭反应。将所得混合物用EtOAc(3x150mL)萃取。将合并的有机层用饱和盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(2/1)洗脱,得到呈黄色油状物的(2R)-2-[(6-氯-4-碘吡啶-2-基)氨基]丙-1-醇(240mg,21%)。MS ESI:C8H10ClIN2O[M+H]+的计算值:312.95,实测值:312.95。1H NMR(300MHz,氯仿-d)δ6.97(d,J=1.0Hz,1H),6.77(d,J=1.1Hz,1H),4.90(s,1H),3.76(dd,J=13.7,3.1Hz,2H),3.61(dd,J=13.7,7.7Hz,1H),1.28(d,J=6.2Hz,3H)。
制备例32B:(3S)-N-[3-(2-氯-6-[[(2R)-1-羟基丙烷-2-基]氨基]吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在室温和氮气氛下,分数份向(2R)-2-[(6-氯-4-碘吡啶-2-基)氨基]丙-1-醇(230mg,0.736mmol)和(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(303mg,0.736mmol)、K3PO4(469mg,2.208mmol)在二噁烷(3mL)、H2O(0.3mL)中的搅拌混合物中加入Pd(dppf)Cl2 CH2Cl2(60mg,0.074mmol)。将所得混合物在50℃和氮气氛下搅拌1h。将所得混合物用水(50mL)猝灭,并且用EtOAc(3x100mL)萃取。将合并的有机层用盐水(2x30mL)洗涤,经无水Na2SO4干燥,并且减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE中的0%至90%EtOAc洗脱,得到呈黄色固体的(3S)-N-[3-(2-氯-6-[[(2R)-1-羟基丙烷-2-基]氨基]吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(310mg,89%)。MS ESI:C22H26ClF3N4O2[M+H]+的计算值:471.17,实测值:471.05。1H NMR(300MHz,DMSO-d6)δ8.17(s,1H),7.48-7.45(m,1H),7.40-7.34(m,1H),7.15-7.12(m,1H),6.87-6.81(m,1H),6.41(s,1H),7.41(s,1H),6.36(s,1H),4.04-4.02(m,1H),3.90(s,1H),3.67(s,1H),3.52(s,2H),3.36-3.25(m,2H),3.03(s,1H),2.51-2.34(m,3H),2.17(s,3H),2.13-2.05(m,1H),1.73-1.59(m,1H),1.26-1.10(m,4H)。
实施例32:(3S)-N-[3-[2-(3,6-二氢-2H-吡喃-4-基)-6-[[(2R)-1-羟基丙烷-2-基]氨基]吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在室温和氮气氛下,分数份向(3S)-N-[3-(2-氯-6-[[(2R)-1-羟基丙烷-2-基]氨基]吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(310mg,0.658mmol)和2-(3,6-二氢-2H-吡喃-4-基)-4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷(277mg,1.317mmol)、Cs2CO3(643mg,1.975mmol)在二噁烷(4mL)、H2O(0.4mL)中的搅拌混合物中加入Pd(dppf)Cl2CH2Cl2(54mg,0.066mmol)。将所得混合物在100℃和氮气氛下搅拌12h。将所得混合物用水(50mL)猝灭,并且用EtOAc(3x100mL)萃取。将合并的有机层用盐水(2x30mL)洗涤,经无水Na2SO4干燥,并且减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE中的0%至90%EtOAc洗脱,得到呈黄色固体的(3S)-N-[3-[2-(3,6-二氢-2H-吡喃-4-基)-6-[[(2R)-1-羟基丙烷-2-基]氨基]吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(130mg,38%)。MS ESI:C27H33F3N4O3[M+H]+的计算值:519.25,实测值:519.15。1H NMR(300MHz,DMSO-d6)δ8.15(s,1H),7.45-7.39(m,2H),7.14-7.12(m,1H),6.71(s,1H),6.50(s,1H),6.31(s,2H),4.85-4.83(m,1H),4.25-4.24(m,2H),4.07(s,1H),3.81(s,2H),3.67-3.66(m,1H),3.52-3.50(m,2H),3.33-3.29(m,2H),3.02(s,1H),2.51-2.43(m,5H),2.41-2.17(m,4H),1.75-1.70(m,1H),1.16-1.14(m,3H)。
实施例33:(3S)-N-[3-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-(氧杂环己烷-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在氮气氛下,向(3S)-N-[3-[2-(3,6-二氢-2H-吡喃-4-基)-6-[[(2R)-1-羟基丙烷-2-基]氨基]吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(130mg,0.251mmol)在MeOH(2mL)、CH3COOH(0.1mL)中的溶液中加入Pd/C(80mg,0.752mmol)。在室温下,使用氢气气球在氢气氛下使混合物氢化2h。将反应混合物经硅藻土垫过滤,并且减压浓缩。粗产物(200mg)通过制备型HPLC采用以下条件纯化:(柱:XBridge制备型C18 OBD柱,150mm 5um;流动相A:水(10mmoL/L NH4HCO3),流动相B:CH3CN;流速:20mL/min;梯度:在4.3min内20B至50B;210/254nm),得到呈白色固体的(3S)-N-[3-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-(氧杂环己烷-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(63mg,48%)。MS ESI:C27H35F3N4O3[M+H]+的计算值:521.27,实测值:521.15。1HNMR(300MHz,DMSO-d6)δ8.13(s,1H),7.43-7.41(m,2H),7.36(s,1H),6.26-6.19(m,3H),4.77(s,1H),3.95-3.91(m,3H),3.63(s,1H),3.55-3.25(m,5H),3.04-2.98(m,1H),2.76(s,1H),2.50-2.39(m,4H),2.27-2.06(m,4H),1.78-1.61(m,5H),1.23-1.13(m,3H)。
实施例34:(S)-N-(3-(2-(((1S,3R)-3-羟基-3-甲基环丁基)氨基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例34A:(1S,3S)-3-((4-碘-6-吗啉基吡啶-2-基)氨基)-1-甲基环丁-1-醇
将4-(6-氟-4-碘吡啶-2-基)吗啉(300mg,0.974mmol)和(1S,3S)-3-氨基-1-甲基环丁-1-醇盐酸盐(134mg,0.974mmol)、K2CO3(269mg,1.947mmol)在NMP(3mL)中的混合物在150℃和氮气氛下搅拌16h。在室温下用水(2x8mL)猝灭反应。将所得混合物用EtOAc(2x8mL)萃取。将合并的有机层用盐水(10mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc/EtOH(4/3/1)洗脱,得到呈灰白色固体的(1S,3S)-3-((4-碘-6-吗啉基吡啶-2-基)氨基)-1-甲基环丁-1-醇(270mg,64%)。MS ESI:C14H20IN3O2[M+H]+的计算值:390.06,实测值:390.05。1H NMR(300MHz,CDCL3)δ6.32(s,1H),6.11(s,1H),4.48(m,1H),3.81-3.78(m,4H),3.73-3.66(m,1H),3.46-3.42(m,4H),2.65-2.58(m,1H),2.01-1.95(m,2H),1.45(s,3H),1.31-1.26(m,1H),0.91-0.86(m,1H)。
实施例34:(S)-N-(3-(2-(((1S,3R)-3-羟基-3-甲基环丁基)氨基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将(1S,3S)-3-((4-碘-6-吗啉基吡啶-2-基)氨基)-1-甲基环丁-1-醇(142mg,0.364mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(150mg,0.364mmol)、Pd(dppf)Cl2.CH2Cl2(30mg,0.036mmol)和Na2CO3(116mg,1.092mmol)在二噁烷(1.2mL)和H2O(0.3mL)中的混合物在60℃和氮气氛下搅拌16h。在室温下通过添加水(3mL)来猝灭反应。将所得混合物用EtOAc(2x10mL)萃取。将合并的有机层用盐水(5mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc/EtOH(4/3/1)洗脱,将粗产物通过反相快速色谱法采用以下条件纯化:柱:SunFire制备型C18 OBD柱,19×150mm 5um 10nm;流动相A:水(0.1%FA),流动相B:CH3CN;流速:20mL/min;梯度:在4.3min内35B至70B;210/254nm。这产生呈灰白色固体的(S)-N-(3-(2-(((1S,3R)-3-羟基-3-甲基环丁基)氨基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(117mg,58%)。MSESI:C28H36F3N5O3[M+H]+的计算值:548.28,实测值:548.20。1H NMR(300MHz,DMSO-d6)δ8.13-8.11(m,1H),7.42-7.40(m,1H),7.33(s,1H),7.10-7.07(m,1H),6.44-6.32(m,1H),5.77-5.69(m,2H),4.90-4.87(m,1H),3.89-3.60(m,6H),3.55-3.49(m,1H),3.37-3.29(m,5H),3.07-2.99(m,1H),2.51-2.34(m,5H),2.20-1.94(m,4H),1.90-1.81(m,2H),1.80-1.50(m,1H),1.45-1.05(m,3H)。19F NMR(282MHz,DMSO-d6)δ-63.35(3F)。
实施例35:(S)-N-(3-(2-(((1R,3S)-3-羟基-3-甲基环丁基)氨基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例35A:(1R,3R)-3-((4-碘-6-吗啉基吡啶-2-基)氨基)-1-甲基环丁-1-醇
将4-(6-氟-4-碘吡啶-2-基)吗啉(300mg,0.974mmol)和(反式)-3-氨基-1-甲基环丁-1-醇盐酸盐(201mg,1.461mmol)、K2CO3(269mg,1.947mmol)在NMP(3mL)中的混合物在150℃和氮气氛下搅拌16h。在室温下通过添加水(30mL)来猝灭反应。将所得混合物用EtOAc(2x20mL)萃取。将合并的有机层用盐水(10mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc/EtOH=(4/3/1)洗脱,得到呈灰白色固体的(1R,3R)-3-((4-碘-6-吗啉基吡啶-2-基)氨基)-1-甲基环丁-1-醇(370mg,88%)。MSESI:C14H20IN3O2[M+H]+的计算值:390.06,实测值:390.05。1H NMR(300MHz,氯仿-d)δ6.33-6.32(m,1H),6.11-6.10(s,1H),4.47-4.45(m,1H),4.23-4.11(m,1H),3.80-3.77(m,4H),3.45-3.42(m,4H),2.60-2.53(m,1H),2.00-1.93(m,2H),1.46(s,3H),1.31-1.26(m,1H),0.91-0.88(m,1H)。
实施例35:(S)-N-(3-(2-(((1R,3S)-3-羟基-3-甲基环丁基)氨基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将(1R,3R)-3-((4-碘-6-吗啉基吡啶-2-基)氨基)-1-甲基环丁-1-醇(142mg,0.364mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(150mg,0.364mmol)、Pd(dppf)Cl2.CH2Cl2(30mg,0.036mmol)和Na2CO3(116mg,1.092mmol)在二噁烷(1.2mL)和H2O(0.3mL)中的混合物在60℃和氢气氛下搅拌16h。在室温下通过添加水(5mL)来猝灭反应。将所得混合物用EtOAc(2x10mL)萃取。将合并的有机层用盐水(5mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc/EtOH=(4/3/1)洗脱,将粗产物通过反相快速色谱法采用以下条件纯化:柱:SunFire制备型C18 OBD柱,19×150mm 5um 10nm;流动相A:水(0.1%FA),流动相B:CH3CN;流速:20mL/min;梯度:在4.3min内35B至70B;210/254nm。这产生呈灰白色固体的(S)-N-(3-(2-(((1R,3S)-3-羟基-3-甲基环丁基)氨基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(114mg,56%)。MSESI:C28H36F3N5O3[M+H]+的计算值:548.28,实测值:548.15。1H NMR(300MHz,DMSO-d6)δ8.13-8.11(m,1H),7.43-7.40(m,1H),7.33(s,1H),7.10-7.08(m,1H),6.42(m,1H),5.77(s,1H),5.64(s,1H),4.83-4.23(m,1H),4.45-4.05(m,1H),3.80-3.67(m,5H),3.57-3.55(m,1H),3.52-3.38(m,5H),3.10-2.99(m,1H),2.46-2.32(m,5H),2.29-2.08(m,4H),1.94-1.84(m,2H),1.72-1.62(m,1H),1.27-1.06(m,3H)。19F NMR(282MHz,DMSO-d6)δ-63.35-63.42(3F)。
实施例36:(S)-N-(3-(2-(((1S,4R)-4-羟基-4-甲基环己基)氨基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例36A:(1S,4S)-4-((4-碘-6-吗啉基吡啶-2-基)氨基)-1-甲基环己-1-醇
在室温下,向4-(6-氟-4-碘吡啶-2-基)吗啉(300mg,0.974mmol)和K2CO3(407mg,2.921mmol)在NMP(3mL)中的搅拌混合物中加入(顺式)-4-氨基-1-甲基环己-1-醇(189mg,1.461mmol)。将所得混合物在150℃下搅拌16h。使混合物冷却至室温。将残余物通过反相快速色谱法采用以下条件纯化:柱,C18硅胶;流动相,含CH3CN的水,在20min内30%至70%梯度;检测器,UV 254nm,得到呈浅棕色固体的(1S,4S)-4-((4-碘-6-吗啉基吡啶-2-基)氨基)-1-甲基环己-1-醇(290mg,71%)。MS ESI:C16H24IN3O2的计算值:418.09,实测值:417.95。1H NMR(300MHz,氯仿-d)δ6.26(s,1H),6.16(s,1H),4.24(d,J=8.0Hz,1H),3.84-3.75(m,4H),3.45-3.42(m,5H),2.00-1.40(m,8H),1.29(s,3H),1.13(s,1H)。
实施例36:(S)-N-(3-(2-(((1S,4R)-4-羟基-4-甲基环己基)氨基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在70℃和氮气氛下,向(1S,4S)-4-((4-碘-6-吗啉基吡啶-2-基)氨基)-1-甲基环己-1-醇(150mg,0.359mmol)和(3S)-N-[4-甲基-3-(4,4,5-三甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(143mg,0.359mmol)在1,4-二噁烷(4mL)和H2O(1mL)中的搅拌混合物中加入Na2CO3(114mg,1.078mmol)和Pd(dppf)Cl2.DCM(29mg,0.036mmol)。在室温下通过添加水(20mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用盐水(2x5mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1:1)洗脱,得到呈浅绿色固体的(S)-N-(3-(2-(((1S,4R)-4-羟基-4-甲基环己基)氨基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(98mg,47%)。MS ESI:C30H40F3N5O3的计算值:576.31,实测值:576.20。1H NMR(300MHz,DMSO-d6)δ8.12(s,1H),7.41(dd,J=8.2,2.3Hz,1H),7.33(d,J=2.3Hz,1H),7.09(d,J=8.4Hz,1H),6.07(d,J=7.4Hz,1H),5.73(s,2H),4.02(s,1H),3.68(dd,J=5.9,3.7Hz,5H),3.52(td,J=9.4,8.3,5.3Hz,2H),3.37(s,3H),3.02(t,J=9.4Hz,1H),2.44(dd,J=12.6,8.1Hz,3H),2.16(s,3H),2.09(d,J=11.9Hz,1H),1.69(t,J=7.9Hz,3H),1.56(p,J=9.9,8.8Hz,5H),1.43-1.28(m,3H),1.24(s,1H),1.12(s,3H)。
实施例37:(S)-N-(3-(2-(((1R,4S)-4-羟基-4-甲基环己基)氨基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例37A:(1R,4R)-4-((4-碘-6-吗啉基吡啶-2-基)氨基)-1-甲基环己-1-醇
在室温下,向4-(6-氟-4-碘吡啶-2-基)吗啉(300mg,0.974mmol)和K2CO3(404mg,2.921mmol)在NMP(3mL)中的搅拌混合物中加入(1R,4R)-4-氨基-1-甲基环己-1-醇(189mg,1.461mmol)。将所得混合物在150℃下搅拌16h。使混合物冷却至室温。将残余物通过反相快速色谱法采用以下条件纯化:柱,C18硅胶;流动相,含CH3CN的水,在20min内30%至70%梯度;检测器,UV 254nm,得到呈浅棕色固体的(1R,4R)-4-((4-碘-6-吗啉基吡啶-2-基)氨基)-1-甲基环己-1-醇(320mg,79%)。MS ESI:C16H24IN3O2[M+H]+的计算值:418.09,实测值:418.00。1H NMR(300MHz,氯仿-d)δ6.28(s,1H),6.18(s,1H),4.27(s,1H),3.84-3.75(m,4H),3.63-3.39(m,5H),2.02-1.36(m,8H),1.31(s,3H),1.27(s,1H)。
实施例37:(S)-N-(3-(2-(((1R,4S)-4-羟基-4-甲基环己基)氨基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将(1R,4R)-4-((4-碘-6-吗啉基吡啶-2-基)氨基)-1-甲基环己-1-醇(220mg,0.527mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(217mg,0.527mmol)、1,4-二噁烷(5.3mL)、H2O(1.3mL)、Na2CO3(168mg,1.582mmol)和Pd(dppf)Cl2.DCM(43mg,0.053mmol)的混合物在70℃和氮气氛下搅拌2h。在室温下通过添加水(20mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用盐水(2x5mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈浅绿色固体的(S)-N-(3-(2-(((1R,4S)-4-羟基-4-甲基环己基)氨基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(153mg,50%)。MS ESI:C30H40F3N5O3[M+H]+的计算值:576.31,实测值:576.15。1H NMR(300MHz,DMSO-d6)δ8.12(s,1H),7.41(dd,J=8.3,2.3Hz,1H),7.34(d,J=2.3Hz,1H),7.09(d,J=8.4Hz,1H),6.08(d,J=7.3Hz,1H),5.74(d,J=4.4Hz,2H),4.20(s,1H),3.67(q,J=8.3,6.4Hz,6H),3.57-3.50(m,1H),3.44-3.27(m,5H),3.02(t,J=9.4Hz,1H),2.47(d,J=19.5Hz,3H),2.18-2.16(m,4H),1.93-1.81(m,2H),1.75-1.53(m,3H),1.41(h,J=10.4Hz,4H),1.14(s,3H)。
实施例38:(3S)-N-[3-[2-(3-羟基-3-甲基氮杂环丁烷-1-基)-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例38A:1-[4-碘-6-(吗啉-4-基)吡啶-2-基]-3-甲基氮杂环丁烷-3-醇
在室温下,向4-(6-氟-4-碘吡啶-2-基)吗啉(300mg,0.974mmol)和3-甲基氮杂环丁烷-3-醇(127mg,1.461mmol)在NMP(3mL)中的搅拌溶液/混合物中加入K2CO3(404mg,3.00当量)。将所得混合物在150℃下搅拌16h。将残余物通过反相快速色谱法采用以下条件纯化:柱,C18硅胶;流动相,含MeOH的水,在30min内10%至50%梯度;检测器,UV 254nm,得到呈灰白色固体的1-[4-碘-6-(吗啉-4-基)吡啶-2-基]-3-甲基氮杂环丁烷-3-醇(270mg,74%)。MS ESI:C13H18IN3O2,[M+H]+的计算值:376.21,实测值:376.00。1H NMR(300MHz,氯仿-d)δ6.32(s,1H),6.10(s,1H),3.89(q,J=8.6Hz,4H),3.83-3.75(m,4H),3.50-3.41(m,4H),1.60(s,3H)
实施例38:(3S)-N-[3-[2-(3-羟基-3-甲基氮杂环丁烷-1-基)-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在室温和N2氛下,1-[4-碘-6-(吗啉-4-基)吡啶-2-基]-3-甲基氮杂环丁烷-3-醇(150mg,0.400mmol)和(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(181mg,0.440mmol)、1,4-二噁烷(1.6mL)、H2O(0.4mL)、K3PO4(255mg,1.199mmol)和Pd(dppf)Cl2.DCM(43mg,0.053mmol)的混合物。将所得混合物在80℃和N2氛下搅拌1h。将所得混合物减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈灰白色固体的(3S)-N-[3-[2-(3-羟基-3-甲基氮杂环丁烷-1-基)-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(79mg,37%)。MS ESI:C27H34F3N5O3[M+H]+的计算值:534.26,实测值:534.15。1HNMR(400MHz,DMSO-d6)δ8.12(s,1H),7.43(dd,J=8.3,2.3Hz,1H),7.33(d,J=2.4Hz,1H),7.10(d,J=8.4Hz,1H),5.93(d,J=1.0Hz,1H),5.61(d,J=0.9Hz,1H),5.49(s,1H),3.80-3.62(m,9H),3.52(ddd,J=10.4,8.3,2.3Hz,1H),3.40(t,J=4.9Hz,4H),3.32(d,J=2.5Hz,1H),3.02(t,J=9.5Hz,1H),2.45(d,J=11.3Hz,1H),2.41(s,2H),2.15(s,3H),2.12-2.00(m,1H),1.65(p,J=9.9Hz,1H),1.43(s,3H)。19F NMR(376MHz,DMSO-d6)δ-63.12。
实施例39:(3S)-N-[3-[2-(异丙基氨基)-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例39A:4-碘-N-异丙基-6-(吗啉-4-基)吡啶-2-胺
将4-(6-氟-4-碘吡啶-2-基)吗啉(300mg,0.974mmol)、异丙胺(86mg,1.461mmol)、NMP(3mL)和K2CO3(404mg,2.921mmol)的混合物在150℃下搅拌16h。将所得混合物减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(0-50%)洗脱,得到呈白色固体的4-碘-N-异丙基-6-(吗啉-4-基)吡啶-2-胺(210mg,62%)。MS ESI:C12H18IN3O[M+H]+的计算值:348.05,实测值:348.10。1H NMR(300MHz,氯仿-d)δ6.27(s,1H),6.16(s,1H),4.17(d,J=7.7Hz,1H),3.92-3.74(m,5H),3.48-3.39(m,4H),1.22(d,J=6.4Hz,6H)。
实施例39:(3S)-N-[3-[2-(异丙基氨基)-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将4-碘-N-异丙基-6-(吗啉-4-基)吡啶-2-胺(150mg,0.432mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(196mg,0.475mmol)、1,4-二噁烷(2mL)、H2O(0.5mL)、K3PO4(275mg,1.296mmol)和Pd(dppf)Cl2.DCM(43mg,0.053mmol)的混合物在80℃和N2氛下搅拌1h。将所得混合物减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈灰白色固体的(3S)-N-[3-[2-(异丙基氨基)-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(86mg,40%)。MS ESI:C26H34F3N5O2[M+H]+的计算值:506.27,实测值:506.15。1H NMR(400MHz,DMSO-d6)δ8.13(d,J=17.1Hz,1H),7.41(dd,J=8.3,2.3Hz,1H),7.33(d,J=2.4Hz,1H),7.09(d,J=8.4Hz,1H),6.05(d,J=7.5Hz,1H),5.72(dd,J=8.5,1.0Hz,2H),3.96(h,J=6.6Hz,1H),3.71-3.62(m,5H),3.57-3.47(m,1H),3.36-3.30(m,5H),3.02(t,J=9.4Hz,1H),2.50-2.42(m,1H),2.41-2.39(m,2H),2.16(s,3H),2.08(s,1H),1.67(q,J=10.5,10.1Hz,1H),1.15(d,J=6.5Hz,6H)。
实施例40:(3S)-N-[3-[2-(叔丁基氨基)-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例40A:N-叔丁基-4-碘-6-(吗啉-4-基)吡啶-2-胺
将4-(6-氟-4-碘吡啶-2-基)吗啉(300mg,0.974mmol)、3-甲基氮杂环丁烷-3-醇(127mg,1.461mmol)、NMP(3mL)和K2CO3(404mg,2.921mmol)的混合物在150℃下搅拌16h。通过LCMS监测反应。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈白色固体的N-叔丁基-4-碘-6-(吗啉-4-基)吡啶-2-胺(120mg,34%)。MS ESI:C13H20IN3O[M+H]+的计算值:362.07,实测值:362.05。1H NMR(400MHz,DMSO-d6)δ6.28(d,J=1.0Hz,1H),6.19-6.11(m,2H),3.66(t,J=4.9Hz,4H),3.44-3.29(m,4H),1.34(s,9H)。
实施例40:(3S)-N-[3-[2-(叔丁基氨基)-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在室温和N2氛下,分数份向N-叔丁基-4-碘-6-(吗啉-4-基)吡啶-2-胺(100mg,0.277mmol)和(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(126mg,0.305mmol)在二噁烷(1mL)H2O(0.2mL)中的搅拌混合物中加入K3PO4(176mg,0.831mmol)和Pd(dppf)Cl2.CH2Cl2(23mg,0.028mmol)。将所得混合物在80℃和N2氛下搅拌1h。将所得混合物减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1:1)洗脱。将残余物通过反相快速色谱法采用以下条件纯化:柱:XBridge制备型苯基OBD柱,19×150mm 5um 13nm;流动相A:水(10mmol/l NH4HCO3),流动相B:CH3CN;流速:20mL/min;梯度:在4.2min内30B至70B;254/210nm。将含有所需产物的级分合并,并且浓缩,得到呈白色固体的(3S)-N-[3-[2-(叔丁基氨基)-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(86mg,60%)。MS ESI:C27H36F3N5O2[M+H]+的计算值:520.28,实测值:520.15。1H NMR(400MHz,DMSO-d6)δ8.10(s,1H),7.40(dd,J=8.2,2.3Hz,1H),7.34(d,J=2.3Hz,1H),7.09(d,J=8.3Hz,1H),5.98(s,1H),5.81(s,1H),5.73(s,1H),3.69(q,J=8.0,6.3Hz,5H),3.57-3.48(m,1H),3.37(s,1H),3.32(s,1H),3.02(t,J=9.4Hz,1H),2.45(d,J=11.3Hz,1H),2.41(s,2H),2.16(s,3H),2.12-2.05(m,1H),1.70-1.61(m,1H),1.40(s,9H)。19F NMR(376MHz,DMSO-d6)δ-63.37(3F)。
实施例41:(3S)-N-(3-[2-[(1-羟基-2-甲基丙烷-2-基)氨基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例41A:2-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]-2-甲基丙-1-醇
在室温下,分数份向4-(6-氟-4-碘吡啶-2-基)吗啉(300mg,0.974mmol)和2-氨基-2-甲基-1-丙醇(130mg,1.461mmol)在NMP(3mL)中的搅拌溶液中加入K2CO3(404mg,2.922mmol)。将所得混合物在150℃下搅拌16h。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(0-50%)洗脱,得到呈浅蓝色固体的2-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]-2-甲基丙-1-醇(160mg,44%)。MS ESI:C13H20IN3O2[M+H]+的计算值:378.06,实测值:378.10。1HNMR(400MHz,DMSO-d6)δ6.67(s,1H),6.49(s,1H),3.87(s,2H),3.67(t,J=4.7Hz,4H),3.42(t,J=4.8Hz,4H),1.57(s,2H),1.05(s,6H)。
实施例41:(3S)-N-(3-[2-[(1-羟基-2-甲基丙烷-2-基)氨基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在室温和N2氛下,分数份向2-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]-2-甲基丙-1-醇(100mg,0.265mmol)和(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(120mg,0.292mmol)在二噁烷(2mL)、H2O(0.5mL)中的搅拌混合物中加入K3PO4(169mg,0.795mmol)和Pd(dppf)Cl2.CH2Cl2(22mg,0.027mmol)。将所得混合物在80℃和N2氛下搅拌1h。将所得混合物减压浓缩。将残余物通过硅胶柱色谱法纯化,用EA洗脱。将残余物通过反相快速色谱法采用以下条件纯化:柱:XBridge制备型苯基OBD柱,19×150mm 5um 13nm;流动相A:水(10mmol/l NH4HCO3),流动相B:CH3CN;流速:20mL/min;梯度:在4.3min内40B至75B;254/210nm。将含有所需产物的级分合并,并且浓缩,得到呈浅蓝色固体的(3S)-N-(3-[2-[(1-羟基-2-甲基丙烷-2-基)氨基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(31mg,22%)。MS ESI:C27H36F3N5O2[M+H]+的计算值:536.28,实测值:536.15。1H NMR(400MHz,DMSO-d6)δ8.11(s,1H),7.40(dd,J=8.2,2.4Hz,1H),7.35(d,J=2.3Hz,1H),7.09(d,J=8.3Hz,1H),5.82(d,J=14.0Hz,2H),5.75(s,1H),4.90(t,J=5.7Hz,1H),3.73-3.62(m,5H),3.58-3.48(m,3H),3.32(dd,J=16.9,10.3Hz,3H),3.02(t,J=9.4Hz,1H),2.51-2.34(m,2H),2.17(s,3H),2.08(t,J=5.8Hz,1H),1.67(q,J=10.0Hz,1H),1.32(s,6H)。19F-NMR(376MHz,DMSO-d6)δ-63.37(3F)。
实施例42:(3S)-N-[4-甲基-3-[2-(吗啉-4-基)-6-(氧杂环丁烷-3-基氨基)吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例42A:6-氟-4-碘-N-(氧杂环丁烷-3-基)吡啶-2-胺
在室温和氮气氛下,向2,6-二氟-4-碘吡啶(300mg,1.245mmol)和氧杂环丁烷-3-胺盐酸盐(150mg,1.369mmol)、DIEA(354mg,2.739mmol)在DMSO(4mL)中的搅拌混合物中。将所得混合物在70℃和氮气氛下搅拌3h。不进一步后处理,并且直接用于下一步骤中。MSESI:C8H8FIN2O[M+H]+的计算值:294.97,实测值:295.05。
制备例42B:4-碘-6-(吗啉-4-基)-N-(氧杂环丁烷-3-基)吡啶-2-胺
在室温和氮气氛下,向6-氟-4-碘-N-(氧杂环丁烷-3-基)吡啶-2-胺(300mg,1.020mmol)和吗啉(444mg,5.101mmol)、DIEA(145mg,1.122mmol)在DMSO(4.5mL)中的搅拌混合物中。将所得混合物在70℃和氮气氛下搅拌16h。将所得混合物用水(50mL)稀释。将所得混合物用EtOAc(3x60mL)萃取。将合并的有机层用盐水(2x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc/EtOH=(4/3/1)洗脱,得到呈灰白色固体的4-碘-6-(吗啉-4-基)-N-(氧杂环丁烷-3-基)吡啶-2-胺(395mg,90%)。MS ESI:C12H16IN3O2[M+H]+的计算值:362.03,实测值:362.00。1H NMR(400MHz,氯仿-d)δ6.35-6.34(m,1H),6.15(s,1H),4.99-4.95(m,2H),4.57-4.55(m,2H),3.81-3.87(m,4H),3.86-3.43(m,5H)。
实施例42:(3S)-N-[4-甲基-3-[2-(吗啉-4-基)-6-(氧杂环丁烷-3-基氨基)吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将4-碘-6-(吗啉-4-基)-N-(氧杂环丁烷-3-基)吡啶-2-胺(200mg,0.554mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(228mg,0.554mmol)、Na2CO3(176mg,1.661mmol)、二噁烷(1.6mL)、H2O(0.4mL)和Pd(dppf)Cl2.CH2Cl2(45mg,0.055mmol)的混合物在60℃下搅拌16h。将所得混合物用H2O(20mL)稀释。将所得混合物用EtOAc(3x20mL)萃取。将合并的有机层用盐水(2x15mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc/EtOH=(4/3/1)洗脱,随后进行采用以下条件的制备型HPLC:(柱:SunFire制备型C18 OBD柱,19×150mm 5um 10nm;流动相A:水(0.1%FA),流动相B:CH3CN;流速:20mL/min;梯度:在4.3min内20B至50B;210/254nm,得到呈白色固体的(3S)-N-[4-甲基-3-[2-(吗啉-4-基)-6-(氧杂环丁烷-3-基氨基)吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(160mg,55%)。MS ESI:C26H32F3N5O3[M+H]+的计算值:520.25,实测值:520.15。1H NMR(400MHz,DMSO-d6)δ8.13(s,1H),7.54-7.34(m,2H),7.11-7.01(m,2H),5.83-5.74(m,2H),4.87-4.77(m,3H),4.48-4.32(m,2H),3.76-3.60(m,6H),3.54-3.21(m,5H),3.04-2.99(m,1H),2.45-2.41(m,3H),2.34-2.07(m,4H),1.68-1.63(m,1H)。19F NMR(376MHz,DMSO-d6)δ-63.36(3F)。
实施例43:(3S)-N-[4-甲基-3-[2-(吗啉-4-基)-6-[(3R)-氧杂环戊烷-3-基氨基]吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例43A:4-碘-6-(吗啉-4-基)-N-[(3R)-氧杂环戊烷-3-基]吡啶-2-胺
在室温下,向4-(6-氟-4-碘吡啶-2-基)吗啉(300mg,0.974mmol)和K2CO3(404mg,2.921mmol)在NMP(3mL)中的搅拌混合物中加入(3R)-氧杂环戊烷-3-胺(127mg,1.461mmol)。将所得混合物在150℃下搅拌16h。使混合物冷却至室温。将残余物通过反相快速色谱法采用以下条件纯化:柱,C18硅胶;流动相,含CH3CN的水,在20min内30%至70%梯度;检测器,UV 254nm,得到呈棕色固体的4-碘-6-(吗啉-4-基)-N-[(3R)-氧杂环戊烷-3-基]吡啶-2-胺(230mg,63%)。MS ESI:C13H18IN3O2[M+H]+的计算值:376.04,实测值:375.90。1H NMR(300MHz,氯仿-d)δ6.32(d,J=1.0Hz,1H),6.20(d,J=1.0Hz,1H),4.47-4.28(m,2H),4.04-3.91(m,2H),3.91-3.81(m,1H),3.85-3.75(m,4H),3.68(dd,J=9.2,3.3Hz,1H),3.56-3.40(m,4H),2.38-2.20(m,1H),1.92-1.79(m,1H)。
实施例43:(3S)-N-[4-甲基-3-[2-(吗啉-4-基)-6-[(3R)-氧杂环戊烷-3-基氨基]吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在70℃和氮气氛下,向4-碘-6-(吗啉-4-基)-N-[(3R)-氧杂环戊烷-3-基]吡啶-2-胺(130mg,0.346mmol,)和(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(142.84mg,0.346mmol,)在1,4-二噁烷(4mL)和H2O(1mL)中的搅拌混合物中加入Na2CO3(110mg,1.039mmol)和Pd(dppf)Cl2.CH2Cl2(29mg,0.035mmol)。在室温下通过添加水(10mL)来猝灭反应。将所得混合物用EtOAc(3x40mL)萃取。将合并的有机层用盐水(2x4mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1:1)洗脱,得到呈浅绿色固体的(3S)-N-[4-甲基-3-[2-(吗啉-4-基)-6-[(3R)-氧杂环戊烷-3-基氨基]吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(55mg,30%)。MS ESI:C27H34F3N5O4[M+H]+的计算值:534.26,实测值:534.10。1H NMR(300MHz,DMSO-d6)δ8.12(s,1H),7.49-7.30(m,2H),7.10(d,J=8.3Hz,1H),6.53(s,1H),5.79(d,J=6.6Hz,2H),4.33(s,1H),3.92(dd,J=8.7,6.0Hz,1H),3.84(dd,J=8.3,7.0Hz,1H),3.77-3.64(m,6H),3.59-3.46(m,2H),3.39(d,J=4.8Hz,4H),3.29(dd,J=10.1,6.7Hz,1H),3.02(t,J=9.3Hz,1H),2.44(dd,J=12.8,7.7Hz,3H),2.36-1.94(m,5H),1.89-1.74(m,1H),1.67(q,J=9.8Hz,1H)。
实施例44:(3S)-N-[4-甲基-3-[2-(吗啉-4-基)-6-[(3S)-氧杂环戊烷-3-基氨基]吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(FT002912 PH-FNT-KIN-04-1601-0)
制备例44A:4-碘-6-(吗啉-4-基)-N-[(3S)-氧杂环戊烷-3-基]吡啶-2-胺
在室温下,向4-(6-氟-4-碘吡啶-2-基)吗啉(300mg,0.974mmol)和K2CO3(404mg,2.921mmol)在NMP(3mL)中的搅拌混合物中加入(3S)-氧杂环戊烷-3-胺(127mg,1.461mmol)。将所得混合物在150℃下搅拌16h。在室温下通过添加水(20mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用盐水(2x5mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈浅绿色固体的4-碘-6-(吗啉-4-基)-N-[(3S)-氧杂环戊烷-3-基]吡啶-2-胺(304mg,83%)。MS ESI:C13H18IN3O2的计算值:376.04,实测值:375.95。1H NMR(400MHz,氯仿-d)δ6.32(d,J=1.1Hz,1H),6.20(d,J=1.0Hz,1H),4.42(s,1H),3.98(dd,J=9.0,5.7Hz,2H),3.86(td,J=8.4,5.6Hz,1H),3.80(t,J=4.9Hz,4H),3.69(dd,J=9.1,3.2Hz,1H),3.45(s,4H),2.36-2.22(m,1H),1.60(s,1H),1.28(s,1H)。
实施例44:(3S)-N-[4-甲基-3-[2-(吗啉-4-基)-6-[(3S)-氧杂环戊烷-3-基氨基]吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在150℃和氮气氛下,向4-碘-6-(吗啉-4-基)-N-[(3S)-氧杂环戊烷-3-基]吡啶-2-胺(150mg,0.400mmol)和(3R)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)环戊烷-1-甲酰胺(132mg,0.321mmol)在1,4-二噁烷(4mL)和H2O(1mL)中的搅拌混合物中加入Na2CO3(127mg,1.199mmol)和Pd(dppf)Cl2.CH2Cl2(33mg,0.040mmol)。在室温下通过添加水(20mL)来猝灭反应。将所得混合物用EtOAc(3x60mL)萃取。将合并的有机层用盐水(2x20mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。残余物通过制备型HPLC采用以下条件纯化:柱:SunFire制备型C18 OBD柱,19×150mm 5um 10nm;流动相A:水(0.1%FA),流动相B:CH3CN;流速:20mL/min;梯度:在5.3min内35B至70B;254/210nm,得到呈浅绿色固体的(3S)-N-[4-甲基-3-[2-(吗啉-4-基)-6-[(3S)-氧杂环戊烷-3-基氨基]吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(61mg,29%)。MS ESI:计算值:534.26,实测值:534.15。1H NMR(400MHz,DMSO-d6)δ8.11(s,1H),7.51-7.25(m,2H),7.10(d,J=8.3Hz,1H),6.51(d,J=5.8Hz,1H),5.88-5.64(m,2H),4.33(s,1H),3.92(dd,J=8.7,6.0Hz,1H),3.82(q,J=7.5Hz,1H),3.68(t,J=4.9Hz,6H),3.51(dd,J=8.7,3.9Hz,3H),3.39(d,J=5.4Hz,5H),3.02(t,J=9.4Hz,1H),2.44(t,J=10.9Hz,2H),2.16(s,4H),2.12-2.04(m,1H),1.80(dq,J=12.3,6.0Hz,1H),1.67(q,J=10.0Hz,1H)。
实施例45:(3S)-N-[4-甲基-3-[2-(吗啉-4-基)-6-[(3R)-氧杂环己烷-3-基氨基]吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例45A:4-碘-6-(吗啉-4-基)-N-[(3R)-氧杂环己烷-3-基]吡啶-2-胺
在室温和氮气氛下,向4-(6-氟-4-碘吡啶-2-基)吗啉(300mg,0.974mmol)和K2CO3(673mg,4.869mmol)、(3R)-氧杂环己烷-3-胺盐酸盐(670mg,4.869mmol)在NMP(3mL)中的搅拌混合物中。将所得混合物在150℃和氮气氛下搅拌16h。将所得混合物用水(50mL)稀释。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用盐水(2x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用己烷/EtOAc/EtOH(4/3/1)洗脱,得到呈白色固体的4-碘-6-(吗啉-4-基)-N-[(3R)-氧杂环己烷-3-基]吡啶-2-胺(322mg,85%)。MS ESI:C14H20IN3O2[M+H]+的计算值:390.06,实测值:389.95。
实施例45:(3S)-N-[4-甲基-3-[2-(吗啉-4-基)-6-[(3R)-氧杂环己烷-3-基氨基]吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在150℃和氮气氛下,向4-碘-6-(吗啉-4-基)-N-[(3R)-氧杂环己烷-3-基]吡啶-2-胺(150mg,0.385mmol)和(3R)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)环戊烷-1-甲酰胺(127mg,0.308mmol)在1,4-二噁烷(4mL)和H2O(1mL)中的搅拌混合物中加入Na2CO3(122mg,1.156mmol)和Pd(dppf)Cl2.CH2Cl2(31mg,0.039mmol),搅拌2h。在室温下通过添加水(20mL)来猝灭反应。将所得混合物用EtOAc(3x60mL)萃取。将合并的有机层用盐水(2x10mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1:1)洗脱,得到呈浅绿色固体的(3S)-N-[4-甲基-3-[2-(吗啉-4-基)-6-[(3R)-氧杂环己烷-3-基氨基]吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(25mg,12%)。MS ESI:C28H36F3N5O3[M+H]+的计算值:547.28,实测值:548.15。1H NMR(400MHz,DMSO-d6)δ8.13(s,1H),7.49-7.29(m,2H),7.10(d,J=8.3Hz,1H),6.20(brs,1H),5.81(s,2H),3.92(s,1H),3.81(s,1H),3.73-3.62(m,6H),3.52(ddd,J=10.3,8.3,2.3Hz,1H),3.36-3.30(m,8H),2.48-2.32(m,3H),2.16(s,3H),2.11-2.06(m,1H),1.92-1.90(m,1H),1.76-1.59(m,4H)。
实施例46:(3S)-N-[4-甲基-3-[2-(吗啉-4-基)-6-(氧杂环己烷-4-基氨基)吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例46A:4-碘-6-(吗啉-4-基)-N-(氧杂环己烷-4-基)吡啶-2-胺
在60℃和氮气氛下,向4-(6-氟-4-碘吡啶-2-基)吗啉(300mg,0.974mmol)和氧杂环己烷-4-胺(541.70mg,5.355mmol)在NMP(3mL)中的搅拌混合物中加入K2CO3(269.15mg,1.947mmol)。在室温下通过添加水(10mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用盐水(2x5mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1:1)洗脱,得到呈浅绿色固体的4-碘-6-(吗啉-4-基)-N-(氧杂环己烷-4-基)吡啶-2-胺(150mg,40%)。MS ESI:C14H20IN3O2[M+H]+的计算值:390.06,实测值:389.95 1H NMR(400MHz,DMSO-d6)δ6.38(d,J=7.3Hz,1H),6.23(d,J=1.0Hz,1H),6.20(d,J=1.0Hz,1H),3.84(dt,J=11.7,3.7Hz,2H),3.68-3.61(m,4H),3.44-3.30(m,4H),1.84(d,J=12.2Hz,2H),1.49-1.30(m,2H),1.24(s,1H),0.89(dd,J=29.8,6.5Hz,2H)。
实施例46:(3S)-N-[4-甲基-3-[2-(吗啉-4-基)-6-(氧杂环己烷-4-基氨基)吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在150℃和氮气氛下,向4-碘-6-(吗啉-4-基)-N-(氧杂环己烷-4-基)吡啶-2-胺(150mg,0.385mmol)和(3R)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)环戊烷-1-甲酰胺(127mg,0.308mmol)在1,4-二噁烷(4mL)和H2O(1mL)中的搅拌混合物中加入Na2CO3(122mg,1.156mmol)和Pd(dppf)Cl2.CH2Cl2(31mg,0.039mmol)。在室温下通过添加水(20mL)来猝灭反应。将所得混合物用EtOAc(3x60mL)萃取。将合并的有机层用盐水(2x20mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。残余物通过制备型HPLC采用以下条件纯化:柱:SunFire制备型C18 OBD柱,19×150mm 5um10nm;流动相A:水(0.1%FA),流动相B:CH3CN;流速:20mL/min;梯度:在5.5min内30B至75B;254/210nm,得到呈浅绿色固体的(3S)-N-[4-甲基-3-[2-(吗啉-4-基)-6-(氧杂环己烷-4-基氨基)吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(89mg,42%)。MS ESI:C28H36F3N5O3[M+H]+的计算值:548.28,实测值:548.15。1H NMR(400MHz,DMSO-d6)δ8.13(d,J=14.5Hz,1H),7.41(dd,J=8.3,2.4Hz,1H),7.34(d,J=2.3Hz,1H),7.09(d,J=8.4Hz,1H),6.21(d,J=7.4Hz,1H),5.76(s,2H),3.95-3.76(m,4H),3.76-3.59(m,6H),3.52(t,J=8.8Hz,1H),3.45-3.39(m,5H),3.02(t,J=9.5Hz,1H),2.44(t,J=11.0Hz,3H),2.16(s,3H),2.08(s,1H),1.90(d,J=13.2Hz,2H),1.66(p,J=10.1Hz,1H),1.52-1.32(m,2H)。
实施例47:(S)-N-(3-(2-(((1S,3R)-3-羟基环丁基)氨基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例47A:(1S,3S)-3-((4-碘-6-吗啉基吡啶-2-基)氨基)环丁-1-醇
将4-(6-氟-4-碘吡啶-2-基)吗啉(300mg,0.974mmol)、(顺式)-3-氨基环丁-1-醇盐酸盐(181mg,1.461mmol)和K2CO3(404mg,2.921mmol)在NMP(5mL)中的混合物在150℃和氮气氛下搅拌16h。使混合物冷却至室温。在室温下通过添加水(50mL)来猝灭反应。将所得混合物用EtOAc(3x30mL)萃取。将合并的有机层用盐水(50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用含EtOAc的PE(80%)洗脱,得到呈灰白色固体的(1S,3S)-3-((4-碘-6-吗啉基吡啶-2-基)氨基)环丁-1-醇(300mg,80%)。MSESI:C13H18IN3O2[M+H]+的计算值:376.04,实测值:375.95。1H NMR(400MHz,氯仿-d)δ6.31(s,1H),6.12(s,1H),4.45-4.44(m,1H),4.17-4.10(m,1H),3.80-3.78(m,4H),3.68-3.62(m,1H),3.46-3.43(m,4H),2.92-2.85(m,1H),1.83-1.81(m,4H)。
实施例47:(S)-N-(3-(2-(((1S,3R)-3-羟基环丁基)氨基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将(1S,3S)-3-((4-碘-6-吗啉基吡啶-2-基)氨基)环丁-1-醇(200mg,0.533mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(242mg,0.586mmol)、Pd(dppf)Cl2.CH2Cl2(43mg,0.053mmol)、Na2CO3(169mg,1.599mmol)、1,4-二噁烷(6mL)和水(1.5mL)的混合物在60℃和氮气氛下搅拌16h。将反应混合物冷却至室温,并且减压浓缩。将残余物通过硅胶柱色谱法纯化,用含EA/EtOH(3/1)的PE(65%)洗脱,随后用DCM/己烷(1/5)湿磨,得到呈浅黄色固体的(S)-N-(3-(2-(((1S,3R)-3-羟基环丁基)氨基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(214mg,74%)。MS ESI:C27H34F3N5O3[M+H]+的计算值:534.26,实测值:534.20。1H NMR(400MHz,DMSO-d6)δ8.12(s,1H),7.42-7.40(m,1H),7.40(s,1H),7.33-7.32(m,1H),7.10-7.08(m,1H),5.76(s,1H),5.68(s,1H),5.00(s,1H),3.86-3.84(m,1H),3.69-3.65(m,6H),3.52-3.50(m,1H),3.38-3.29(m,5H),3.04-2.99(m,1H),2.63-2.41(m,5H),2.15-2.07(m,4H),1.74-1.66(m,3H)。19F NMR(376MHz,DMSO-d6)δ-63.37(3F)。
实施例48:(S)-N-(3-(2-(((1R,3S)-3-羟基环丁基)氨基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例48A:(1R,3R)-3-((4-碘-6-吗啉基吡啶-2-基)氨基)环丁-1-醇
将4-(6-氟-4-碘吡啶-2-基)吗啉(300mg,0.974mmol)、(1R,3R)-3-氨基环丁-1-醇盐酸盐(181mg,1.461mmol)和K2CO3(404mg,2.921mmol)在NMP(5mL)中的混合物在150℃和氮气氛下搅拌16h。使混合物冷却至室温。在室温下通过添加水(50mL)来猝灭反应。将所得混合物用EtOAc(3x30mL)萃取。将合并的有机层用盐水(50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用含EtOAc的PE(80%)洗脱,得到呈浅黄色固体的(1R,3R)-3-((4-碘-6-吗啉基吡啶-2-基)氨基)环丁-1-醇(270mg,74%)。MSESI:C13H18IN3O2[M+H]+的计算值:376.04,实测值:375.90。1H NMR(400MHz,DMSO-d6)δ6.63-6.60(m,1H),6.22(s,1H),6.11(s,1H),4.96(s,1H),4.29-4.13(m,2H),3.65-3.63(m,4H),3.41-3.33(m,4H),2.16-2.06(m,4H)。
实施例48:(S)-N-(3-(2-(((1R,3S)-3-羟基环丁基)氨基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
(1R,3R)-3-((4-碘-6-吗啉基吡啶-2-基)氨基)环丁-1-醇(200mg,0.533mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(242mg,0.586mmol)、Pd(dppf)Cl2.CH2Cl2(43mg,0.053mmol)、Na2CO3(169mg,1.599mmol)、1,4-二噁烷(6mL)和水(1.5mL)的混合物。将所得混合物在60℃和氮气氛下搅拌16h。将反应混合物冷却至室温,并且减压浓缩。将残余物通过硅胶柱色谱法纯化,用含EA/EtOH(3/1)的PE(65%)洗脱,随后用DCM/己烷(1/5)湿磨,得到呈棕黄色固体的(S)-N-(3-(2-(((1R,3S)-3-羟基环丁基)氨基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(190mg,65%)。MS ESI:C27H34F3N5O3[M+H]+的计算值:534.26,实测值:534.30。1H NMR(400MHz,DMSO-d6)δ8.12(s,1H),7.42-7.41(m,1H),7.40(s,1H),7.33-7.32(m,1H),7.10-7.08(m,1H),5.78(s,1H),5.63(s,1H),4.97-4.95(m,1H),4.31-4.18(m,2H),3.69-3.50(m,6H),3.39-3.29(m,5H),3.04-2.99(m,1H),2.50-2.41(m,3H),2.16-2.08(m,8H),1.68-1.66(m,1H)。19F NMR(376MHz,DMSO-d6)δ-63.37(3F)。
实施例49:(3S)-N-[3-(2-[[(2R)-1-羟基丁烷-2-基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例49A:(2R)-2-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丁-1-醇
将4-(6-氟-4-碘吡啶-2-基)吗啉(300mg,0.974mmol)和K2CO3(269mg,1.947mmol)、NMP(3mL)和(2R)-2-氨基丁-1-醇(130mg,1.461mmol)的混合物在150℃和氮气氛下搅拌16h。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用饱和盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(2/1)洗脱,得到呈灰白色固体的(2R)-2-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丁-1-醇(90mg,24%)。MS ESI:C13H20IN3O2[M+H]+的计算值:378.06,实测值:377.90。1H NMR(300MHz,CDCL3)δ6.29-6.26(m,2H),4.23(s,1H),3.81-3.76(m,6H),3.62-3.55(m,1H),3.45-3.42(m,4H),3.14(s,1H),1.77-1.63(m,1H),1.57-1.43(m,1H),1.03-0.96(m,3H)。
实施例49:(3S)-N-[3-(2-[[(2R)-1-羟基丁烷-2-基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将(2R)-2-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丁-1-醇(90mg,0.239mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(98mg,0.239mmol)、Na2CO3(76mg,0.716mmol)、二噁烷:H2O=4:1(1mL)和Pd(dppf)Cl2.CH2Cl2(19mg,0.024mmol)的混合物在60℃和氮气氛下搅拌16h。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用饱和盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EA/EtOH(8/3/1)洗脱,得到70mg粗产物。将残余物通过反相快速色谱法采用以下条件纯化:柱:SunFire制备型C18 OBD柱,19×150mm5um 10nm;流动相A:水(0.1%FA),流动相B:CH3CN;流速:20mL/min;梯度:在5.1min内25B至65B;254/210nm。这产生呈灰白色固体的(3S)-N-[3-(2-[[(2R)-1-羟基丁烷-2-基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(59mg,46%)。MS ESI:C27H36F3N5O3[M+H]+的计算值:536.28,实测值:536.15。1H NMR(400MHz,DMSO-d6)δ8.11(s,1H),7.42-7.40(m,1H),7.34-7.33(m,1H),7.10-7.08(m,1H),5.95-5.93(m,1H),5.78-5.73(m,2H),4.59(s,1H),3.75-3.64(m,6H),3.55-3.48(m,2H),3.38-3.36(m,4H),3.31-3.27(m,2H),3.04-2.99(m,1H),2.48-2.38(m,3H),2.16(s,3H),2.12-2.07(m,1H),1.70-1.60(m,2H),1.48-1.37(m,1H),0.91-0.88(m,3H)。19F NMR(376MHz,DMSO-d6)δ-63.37(3F)。
实施例50:(3S)-N-[3-(2-[[(2R)-1-甲氧基丙烷-2-基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例50A:4-碘-N-[(2R)-1-甲氧基丙烷-2-基]-6-(吗啉-4-基)吡啶-2-胺
将4-(6-氟-4-碘吡啶-2-基)吗啉(300mg,0.974mmol)和K2CO3(269mg,1.947mmol)、NMP(3mL)和(2R)-1-甲氧基丙-2-胺(434mg,4.869mmol)的混合物在150℃和氮气氛下搅拌16h。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用饱和盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(2:1)洗脱,得到呈灰白色固体的4-碘-N-[(2R)-1-甲氧基丙烷-2-基]-6-(吗啉-4-基)吡啶-2-胺(150mg,41%)。MS ESI:C13H20IN3O2[M+H]+的计算值:378.06,实测值:377.95。1H NMR(400MHz,CDCL3)δ6.27(m,1H),6.20(s,1H),4.45-4.43(m,1H),4.00-3.97(m,1H),3.84-3.78(m,4H),3.53-3.27(m,8H),1.28-1.23(m,3H)。
实施例50:(3S)-N-[3-(2-[[(2R)-1-甲氧基丙烷-2-基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在60℃和氮气氛下,向4-碘-N-[(2R)-1-甲氧基丙烷-2-基]-6-(吗啉-4-基)吡啶-2-胺(150mg,0.398mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(172mg,0.418mmol)、Na2CO3(126mg,1.193mmol)、二噁烷:H2O=4:1(2mL)的混合物中加入Pd(dppf)Cl2.CH2Cl2(32mg,0.040mmol),搅拌16h。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用饱和盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EA/EtOH(8/3/1)洗脱,得到70mg粗产物。将残余物通过反相快速色谱法采用以下条件纯化:柱:Welch Xtimate C18,21.2*250mm,5um;流动相A:水(0.1%FA),流动相B:CH3CN;流速:20mL/min;梯度:在5.5min内20B至60B;254/210nm;这产生呈灰白色固体的(3S)-N-[3-(2-[[(2R)-1-甲氧基丙烷-2-基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(41mg,19%)。MS ESI:C27H36F3N5O3[M+H]+的计算值:536.28,实测值:536.20。1H NMR(400MHz,DMSO-d6)δ8.13(s,1H),7.44-7.36(m,2H),7.12-7.09(m,1H),6.12-6.09(m,1H),5.77(s,2H),4.14-4.10(m,1H),3.77-3.69(m,6H),3.57-3.36(m,5H),3.29(s,4H),3.27-3.22(m,1H),3.07-3.00(m,1H),32.48-2.41(m,3H),2.17(s,3H),2.08-2.03(m,1H),1.71-1.64(m,1H),1.16-1.14(m,3H)。19F NMR(376MHz,DMSO-d6)δ-63.36(3F)。
实施例51:(3S)-N-[3-(2-[[(2S)-2-甲氧基丙基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例51A:4-碘-N-[(2S)-2-甲氧基丙基]-6-(吗啉-4-基)吡啶-2-胺
将4-(6-氟-4-碘吡啶-2-基)吗啉(300mg,0.974mmol)和(2S)-2-甲氧基丙-1-胺(87mg,0.974mmol)、NMP(3mL)和K2CO3(269mg,1.947mmol)的混合物在60℃和氮气氛下搅拌16h。在室温下通过添加水(15mL)来猝灭反应。将所得混合物用EtOAc(3x30mL)萃取。将合并的有机层用盐水(2x8mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈浅绿色固体的4-碘-N-[(2S)-2-甲氧基丙基]-6-(吗啉-4-基)吡啶-2-胺(120mg,粗物质),其不经进一步纯化即用于下一步骤。MSESI:C13H20IN3O2的计算值:378.06,实测值:378.00。
实施例51:(3S)-N-[3-(2-[[(2S)-2-甲氧基丙基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在70℃和氮气氛下搅拌4-碘-N-[(2S)-2-甲氧基丙基]-6-(吗啉-4-基)吡啶-2-胺(112mg,0.297mmol)、(3R)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)环戊烷-1-甲酰胺(98mg,0.238mmol)、1,4-二噁烷(4mL)、H2O(1mL)、Na2CO3(94mg,0.891mmol)和Pd(dppf)Cl2.CH2Cl2(24mg,0.030mmol)的混合物。在室温下通过添加水(10mL)来猝灭反应。将所得混合物用EtOAc(3x30mL)萃取。将合并的有机层用盐水(2x8mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈浅绿色固体的(3S)-N-[3-(2-[[(2S)-2-甲氧基丙基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(22mg,%)。MS ESI:C27H36F3N5O3的计算值:536.28,实测值:536.00。1H NMR(400MHz,DMSO-d6)δ8.12(s,1H),7.42(dd,J=8.3,2.3Hz,1H),7.33(d,J=2.4Hz,1H),7.09(d,J=8.4Hz,1H),6.29(t,J=5.9Hz,1H),5.78(d,J=15.3Hz,2H),3.71-3.62(m,5H),3.57-3.45(m,2H),3.38(t,J=4.9Hz,4H),3.32(s,6H),3.02(t,J=9.4Hz,1H),2.50(s,3H),2.16(s,3H),2.12-2.05(m,1H),1.64(q,J=10.2Hz,1H),1.10(d,J=6.2Hz,3H)。
实施例52:(3S)-N-[4-甲基-3-[2-(吗啉-4-基)-6-[(3S)-氧杂环己烷-3-基氨基]吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例52A:4-碘-6-(吗啉-4-基)-N-[(3S)-氧杂环己烷-3-基]吡啶-2-胺
在室温和氮气氛下,向4-(6-氟-4-碘吡啶-2-基)吗啉(300mg,0.974mmol)和K2CO3(673mg,4.869mmol)、(3S)-氧杂环己烷-3-胺盐酸盐(670mg,4.869mmol)在NMP(3mL)中的搅拌混合物中。将所得混合物在150℃和氮气氛下搅拌16h。将所得混合物用水(50mL)稀释。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用盐水(2x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用己烷/EtOAc/EtOH(4/3/1)洗脱,得到呈白色固体的4-碘-6-(吗啉-4-基)-N-[(3S)-氧杂环己烷-3-基]吡啶-2-胺(260mg,69%)。MS ESI:C14H20IN3O2[M+H]+的计算值:390.06,实测值:389.95。1H NMR(300MHz,氯仿-d)δ6.33-6.32(m,1H),6.11-6.10(s,1H),4.47-4.45(m,1H),4.23-4.11(m,1H),3.80-3.77(m,4H),3.45-3.42(m,4H),2.60-2.53(m,1H),2.00-1.93(m,2H),1.46(s,3H),1.31-1.26(m,1H),0.91-0.88(m,1H)。
实施例52:(3S)-N-[4-甲基-3-[2-(吗啉-4-基)-6-[(3S)-氧杂环己烷-3-基氨基]吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将4-碘-6-(吗啉-4-基)-N-[(3S)-氧杂环己烷-3-基]吡啶-2-胺(200mg,0.514mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(212mg,0.514mmol)、二噁烷(2mL)、H2O(0.5mL)、Pd(dppf)Cl2.CH2Cl2(42mg,0.051mmol)和Na2CO3(163mg,1.541mmol)的混合物在80℃和氮气氛下搅拌3h。使混合物冷却至室温。将所得混合物真空浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(0%至80%)洗脱,随后进行采用以下条件的制备型HPLC:柱:SunFire制备型C18 OBD柱,19?150mm 5um 10nm;流动相A:水(0.1%FA),流动相B:CH3CN;流速:20mL/min;梯度:在5.3min内25B至65B;254/210nm,得到呈灰白色固体的(3S)-N-[4-甲基-3-[2-(吗啉-4-基)-6-[(3S)-氧杂环己烷-3-基氨基]吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(120mg,43%)。MS ESI:C28H36F3N5O3[M+H]+的计算值:548.28,实测值:548.10。1H NMR(400MHz,DMSO-d6)δ8.11(s,1H),7.41(dd,J=8.3,2.3Hz,1H),7.34(d,J=2.4Hz,1H),7.09(d,J=8.3Hz,1H),6.19(s,1H),5.78(d,J=4.9Hz,2H),3.94(dd,J=10.8,4.0Hz,1H),3.82(dt,J=13.4,6.3Hz,1H),3.77-3.62(m,6H),3.52(ddd,J=10.5,8.3,2.3Hz,1H),3.41-3.25(m,6H),3.05(dt,J=24.7,9.5Hz,2H),2.51-2.34(m,3H),2.16(s,3H),2.08(dd,J=9.6,3.5Hz,1H),1.99-1.90(m,1H),1.75-1.50(m,4H)。
实施例53:(3S)-N-(4-甲基-3-[2-[(3-甲基氧杂环戊烷-3-基)氨基]-6-(吗啉-4-基)吡啶-4-基]苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例53A:4-碘-N-(3-甲基氧杂环戊烷-3-基)-6-(吗啉-4-基)吡啶-2-胺
将2,6-二氟-4-碘吡啶(300mg,1.245mmol)、3-甲基氧杂环戊烷-3-胺(138mg,1.369mmol)、DMSO(3mL)和DIEA(0.48mL,3.691mmol)的混合物在110℃下搅拌4h。在室温下,向以上混合物中加入吗啉(361mg,4.150mmol)。将所得混合物在110℃下搅拌16h。使混合物冷却至室温,并且用水(50mL)猝灭。将所得混合物用EtOAc(3x10mL)萃取。将合并的有机层用盐水(10mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(4:1)洗脱,得到呈黄色固体的4-碘-N-(3-甲基氧杂环戊烷-3-基)-6-(吗啉-4-基)吡啶-2-胺(230mg,47%)。MS ESI:C14H20IN3O2[M+H]+的计算值:390.05,实测值:390.05。1H NMR(300MHz,氯仿-d)δ6.28(d,J=1.0Hz,1H),6.20(d,J=1.0Hz,1H),4.39(s,1H),4.00-3.91(m,3H),3.82-3.76(m,5H),3.51-3.37(m,4H),2.41-2.31(m,1H),2.03-1.93(m,1H),1.57(s,3H)。
实施例53:(3S)-N-(4-甲基-3-[2-[(3-甲基氧杂环戊烷-3-基)氨基]-6-(吗啉-4-基)吡啶-4-基]苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将4-碘-N-(3-甲基氧杂环戊烷-3-基)-6-(吗啉-4-基)吡啶-2-胺(230mg,0.591mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(244mg,0.591mmol)、1,4-二噁烷(3mL)、H2O(0.6mL)、Na2CO3(188mg,1.773mmol)和Pd(dppf)Cl2.CH2Cl2(48mg,0.059mmol)的混合物在60℃和氮气氛下搅拌16h。使混合物冷却至室温。在室温下通过添加水(10mL)来猝灭反应。将所得混合物用EtOAc(3x10mL)萃取。将合并的有机层用盐水(10mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1:2)洗脱,得到呈浅粉红色固体的(3S)-N-(4-甲基-3-[2-[(3-甲基氧杂环戊烷-3-基)氨基]-6-(吗啉-4-基)吡啶-4-基]苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(200mg,62%)。MS ESI:C28H36F3N5O3[M+H]+的计算值:548.15,实测值:548.15。1H NMR(400MHz,DMSO-d6)δ8.11(s,1H),7.40(dd,J=8.3,2.3Hz,1H),7.35(d,J=2.3Hz,1H),7.09(d,J=8.4Hz,1H),6.45(s,1H),5.80(dd,J=10.3,1.0Hz,2H),3.95(d,J=8.5Hz,1H),3.86-3.74(m,2H),3.73-3.67(m,6H),3.57-3.44(m,1H),3.39-3.22(m,5H),3.02(t,J=9.4Hz,1H),2.49-2.36(m,3H),2.33-2.22(m,1H),2.16(s,3H),2.08(d,J=11.2Hz,1H),1.95-1.86(m,1H),1.70-1.61(m,1H),1.50(s,3H)。19F NMR(376MHz,DMSO-d6)δ-63.61(3F)。
实施例54:(3S)-N-[3-(2-[[1-(羟基甲基)环丁基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例54A:[1-[(6-氟-4-碘吡啶-2-基)氨基]环丁基]甲醇
在0℃和氮气氛下,向2,6-二氟-4-碘吡啶(550mg,2.282mmol)、(1-氨基环丁基)甲醇盐酸盐(345mg,2.511mmol)和DMSO(6mL)的混合物中加入DIEA(944mg,7.304mmol)。将所得混合物在70℃和氮气氛下搅拌3h。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用饱和盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(2/1)洗脱,得到呈灰白色固体的[1-[(6-氟-4-碘吡啶-2-基)氨基]环丁基]甲醇(320mg,43%)。MS ESI:C10H12FIN2O[M+H]+的计算值:323.00,实测值:322.85。1H NMR(300MHz,氯仿-d)δ6.60-6.55(m,2H),3.86(s,2H),2.35-2.25(m,2H),2.17-2.07(m,2H),2.06-1.83(m,2H)。
制备例54B:(1-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]环丁基)甲醇
在0℃和氮气氛下,向[1-[(6-氟-4-碘吡啶-2-基)氨基]环丁基]甲醇(210mg,0.652mmol)和吗啉(125mg,1.434mmol)在DMSO(2.1mL)中的搅拌溶液中加入DIEA(185mg,1.434mmol)。将所得混合物在110℃和氮气氛下搅拌16h。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用饱和盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(2/1)洗脱,得到呈浅黄色油状物的(1-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]环丁基)甲醇(195mg,77%)。MS ESI:C14H20IN3O2[M+H]+的计算值:390.06,实测值:389.95。1H NMR(300MHz,DMSO-d6)δ6.45(s,1H),6.24-6.18(m,2H),4.71(s,1H),3.66-3.63(m,6H),3.32-3.29(m,4H),2.13-2.08(m,4H),1.84-1.66(m,2H)。
实施例54:(3S)-N-[3-(2-[[1-(羟基甲基)环丁基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将(1-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]环丁基)甲醇(190mg,0.488mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(201mg,0.488mmol)、Na2CO3(155.21mg,1.464mmol)、二噁烷:H2O=4:1(2mL)和Pd(dppf)Cl2.CH2Cl2(40mg,0.049mmol)的混合物在60℃和氮气氛下搅拌16h。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用饱和盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EA/EtOH(8/3/1)洗脱,得到200mg粗产物,随后进行采用以下条件的反相快速色谱法:柱,C18硅胶;流动相,含CH3CN的水(10mmol/lNH4HCO3),在30min内10%至80%梯度;检测器,UV 254nm。这产生呈灰白色固体的(3S)-N-[3-(2-[[1-(羟基甲基)环丁基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(160mg,60%)。MS ESI:C28H36F3N5O3[M+H]+的计算值:548.28,实测值:548.15。1H NMR(400MHz,DMSO-d6)δ8.11(s,1H),7.41-7.35(m,2H),7.11-7.08(m,1H),6.29(s,1H),5.75(s,2H),4.86-4.82(m,1H),3.69-3.67(m,8H),3.56-3.50(m,1H),3.32(s,3H),3.05-2.99(m,1H),2.47-2.40(m,3H),2.16-2.13(m,9H),1.83-1.59(m,3H)。19F NMR(376MHz,DMSO-d6)δ-63.36(3F)。
实施例55:(3S)-N-[3-(2-[[3-(羟基甲基)氧杂环丁烷-3-基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例55A:[3-[(6-氟-4-碘吡啶-2-基)氨基]氧杂环丁烷-3-基]甲醇
在室温和氮气氛下,分数份向2,6-二氟-4-碘吡啶(1.00g,4.150mmol)和(3-氨基氧杂环丁烷-3-基)甲醇(0.51g,4.980mmol)在DMSO(8mL)中的搅拌混合物中加入DIEA(1.34g,10.374mmol)。将所得混合物在100℃和氮气氛下搅拌16h。将所得混合物用EtOAc(100mL)稀释。将合并的有机层用盐水(2x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩,得到呈浅黄色油状物的(3-((6-氟-4-碘吡啶-2-基)氨基)氧杂环丁烷-3-基)甲醇(1g,粗物质)。粗产物不经进一步纯化即用于下一步骤。MS ESI:C9H10FIN2O2[M+H]+的计算值:324.98,实测值:324.95。
制备例55B:(3-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]氧杂环丁烷-3-基)甲醇
在室温和氮气氛下,分数份向[3-[(6-氟-4-碘吡啶-2-基)氨基]氧杂环丁烷-3-基]甲醇(600mg,1.851mmol,1.00当量)和吗啉(177mg,2.036mmol)在DMSO(4mL)中的搅拌混合物中加入DIEA(526mg,4.073mmol)。将所得混合物在100℃和氮气氛下搅拌16h。将所得混合物用EtOAc(3x300mL)萃取。将合并的有机层用盐水(2x500mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(2:1)洗脱,得到呈白色固体的(3-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]氧杂环丁烷-3-基)甲醇(300mg,41.42%)。MS ESI:C13H18IN3O3[M+H]+的计算值:392.04,实测值:392.04。1H NMR(400MHz,氯仿-d)δ7.28(s,1H),6.34(d,J=1.0Hz,1H),6.28(s,1H),4.73(d,J=6.4Hz,1H),4.63(d,J=6.5Hz,2H),4.14(s,1H),3.81-3.77(m,2H),3.37(s,2H),3.13(s,1H),1.59(s,2H),1.34-1.23(m,2H),0.93-0.81(m,2H)。
实施例55:(3S)-N-[3-(2-[[3-(羟基甲基)氧杂环丁烷-3-基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将(3-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]氧杂环丁烷-3-基)甲醇(250mg,0.639mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(263mg,0.639mmol)、H2O(0.75mL)和1,4-二噁烷(3mL)、Pd(dppf)Cl2.CH2Cl2(52mg,0.064mmol)和Na2CO3(203mg,1.917mmol)的混合物在60℃和氮气氛下搅拌2h。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用饱和盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用EtOAc洗脱,随后采用以下条件进行反相快速色谱法:柱:球形C18,20-40um,40g;流动相A:水(5mM NH4HCO3);流动相B:CH3CN;流速:60mL/min;梯度:5%-5%B,10min,5%-40%B,35min,在10min内40%B-98%B梯度;检测器:220nm,得到呈浅蓝色固体的(3S)-N-[3-(2-[[3-(羟基甲基)氧杂环丁烷-3-基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(186mg,53%)。MSESI:C27H34F3N5O4[M+H]+的计算值:550.26,实测值:550.3。1H NMR(400MHz,DMSO-d6)δ8.12(s,1H),7.43-7.33(m,2H),7.10(d,J=8.3Hz,1H),6.81(s,1H),5.87-5.73(m,2H),5.03(t,J=5.7Hz,1H),4.56(q,J=6.1Hz,4H),3.81(d,J=5.8Hz,2H),3.66(dd,J=5.9,3.9Hz,5H),3.52(ddd,J=10.4,8.4,2.3Hz,1H),3.32(s,5H),3.02(t,J=9.4Hz,1H),2.44(t,J=10.8Hz,3H),2.16(s,3H),2.09(q,J=5.3,4.7Hz,1H),1.65(p,J=10.0Hz,1H)。
实施例56:(3S)-N-(4-甲基-3-[2-[(3-甲基氧杂环丁烷-3-基)氨基]-6-(吗啉-4-基)吡啶-4-基]苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例56A:6-氟-4-碘-N-(3-甲基氧杂环丁烷-3-基)吡啶-2-胺
将2,6-二氟-4-碘吡啶(500mg,2.075mmol)、3-甲基氧杂环丁烷-3-胺(181mg,2.075mmol)和DIEA(295mg,2.282mmol)在DMSO(5mL)中的溶液在70℃和氮气氛下搅拌16h。将所得混合物冷却至室温,并且用水(50mL)稀释并用EtOAc(3x30mL)萃取。将合并的有机层用盐水(100mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用含EtOAc的PE(50%)洗脱,得到呈灰白色固体的6-氟-4-碘-N-(3-甲基氧杂环丁烷-3-基)吡啶-2-胺(450mg,70%)。MS ESI:C9H10FIN2O[M+H]+的计算值:309.09,实测值:308.85。1H NMR(400MHz,DMSO-d6)δ7.62(s,1H),6.74-6.73(m,1H),6.59-6.58(m,1H),4.59-4.58(m,2H),4.39-4.38(m,2H),1.58(s,3H)。19F NMR(376MHz,DMSO-d6)δ-69.76(1F)。
制备例56B:4-碘-N-(3-甲基氧杂环丁烷-3-基)-6-(吗啉-4-基)吡啶-2-胺
将6-氟-4-碘-N-(3-甲基氧杂环丁烷-3-基)吡啶-2-胺(400mg,1.298mmol)、吗啉(124mg,1.428mmol)和DIEA(335mg,2.597mmol)在DMSO(4mL)中的溶液在100℃和氮气氛下搅拌16h。将所得混合物冷却至室温,并且用水(50mL)稀释并用EtOAc(3x30mL)萃取。将合并的有机层用盐水(100mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用含EtOAc的PE(50%)洗脱,得到呈浅黄色固体的4-碘-N-(3-甲基氧杂环丁烷-3-基)-6-(吗啉-4-基)吡啶-2-胺(270mg,55%)。MS ESI:C13H18IN3O2[M+H]+的计算值:376.21,实测值:375.90。1H NMR(400MHz,DMSO-d6)δ6.90(s,1H),6.25(s,1H),6.20(s,1H),4.63-4.60(m,2H),4.36-4.34(m,2H),3.65-3.62(m,4H),3.31-3.28(m,4H),1.59(s,3H)。
实施例56:(3S)-N-(4-甲基-3-[2-[(3-甲基氧杂环丁烷-3-基)氨基]-6-(吗啉-4-基)吡啶-4-基]苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将4-碘-N-(3-甲基氧杂环丁烷-3-基)-6-(吗啉-4-基)吡啶-2-胺(200mg,0.533mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(242mg,0.586mmol)、Pd(dppf)Cl2.CH2Cl2(43mg,0.053mmol)、Na2CO3(169mg,1.599mmol)、1,4-二噁烷(6mL)和H2O(1.5mL)的混合物在60℃和氮气氛下搅拌16h。将反应混合物冷却至室温,并且减压浓缩。将残余物通过硅胶柱色谱法纯化,用含EA/EtOH(3/1)的PE(58%)洗脱,随后进行采用以下条件的制备型HPLC:柱:XBridge制备型苯基OBD柱,19×150mm 5um 13nm;流动相A:水(10mmol/L NH4HCO3),流动相B:乙腈;流速:20mL/min;梯度:在5.5min内40B至65B;254/210nm,得到呈灰白色固体的(3S)-N-(4-甲基-3-[2-[(3-甲基氧杂环丁烷-3-基)氨基]-6-(吗啉-4-基)吡啶-4-基]苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(97mg,33%)。MS ESI:C27H34F3N5O3[M+H]+的计算值:534.26,实测值:534.25。1H NMR(400MHz,DMSO-d6)δ8.12(s,1H),7.42-7.35(m,2H),7.11-7.09(m,1H),6.77(s,1H),5.81(s,1H),5.73(s,1H),4.70-4.69(m,2H),4.40-4.38(m,2H),3.68-3.64(m,5H),3.52-3.50(m,1H),3.35-3.29(m,5H),3.04-2.99(m,1H),2.52-2.41(m,3H),2.16(s,3H),2.06-2.04(m,1H),1.75-1.60(m,4H)。19F NMR(376MHz,DMSO-d6)δ-63.37(3F)。
实施例57:(3S)-N-(4-甲基-3-[2-[(4-甲基氧杂环己烷-4-基)氨基]-6-(吗啉-4-基)吡啶-4-基]苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例57A:4-碘-N-(4-甲基氧杂环己烷-4-基)-6-(吗啉-4-基)吡啶-2-胺
将2,6-二氟-4-碘吡啶(200mg,0.830mmol)、4-甲基氧杂环己烷-4-胺(105mg,0.913mmol)、DMSO(2mL)和DIEA(0.32mL,2.461mmol)的溶液在110℃下搅拌4h。向这个溶液中加入吗啉(361mg,4.150mmol)。将所得混合物在110℃下搅拌16h。使混合物冷却至室温,并且用水(10mL)猝灭。将所得混合物用EtOAc(3x10mL)萃取。将合并的有机层用盐水(10mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(4:1)洗脱,得到呈黄色固体的4-碘-N-(4-甲基氧杂环己烷-4-基)-6-(吗啉-4-基)吡啶-2-胺(220mg,66%)。MS ESI:C15H22IN3O2[M+H]+的计算值:404.10,实测值:404.10。1H NMR(300MHz,CDCl3-d)δ6.23(dd,J=10.0,1.0Hz,2H),4.05(s,1H),3.86-3.67(m,11H),3.43-3.35(m,5H),2.10(t,J=12.3Hz,3H)。
实施例57:(3S)-N-(4-甲基-3-[2-[(4-甲基氧杂环己烷-4-基)氨基]-6-(吗啉-4-基)吡啶-4-基]苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将4-碘-N-(4-甲基氧杂环己烷-4-基)-6-(吗啉-4-基)吡啶-2-胺(220mg,0.546mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(225mg,0.546mmol)、1,4-二噁烷(2mL)、H2O(0.4mL)、Na2CO3(173mg,1.637mmol)和Pd(dppf)Cl2.CH2Cl2(44mg,0.055mmol)的混合物在60℃和氮气氛下搅拌16h。使混合物冷却至室温。在室温下通过添加水(10mL)来猝灭反应。将所得混合物用EtOAc(3x10mL)萃取。将合并的有机层用盐水(10mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/2)洗脱,得到呈浅黄色固体的(3S)-N-(4-甲基-3-[2-[(4-甲基氧杂环己烷-4-基)氨基]-6-(吗啉-4-基)吡啶-4-基]苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(158mg,52%)。MS ESI:C29H38F3N5O3[M+H]+的计算值:562.15,实测值:562.15。1H NMR(400MHz,DMSO-d6)δ8.11(s,1H),7.42(dd,J=8.3,2.4Hz,1H),7.35(d,J=2.3Hz,1H),7.09(d,J=8.4Hz,1H),5.97(s,1H),5.91(d,J=0.9Hz,1H),5.75(d,J=1.0Hz,1H),3.72-3.54(m,9H),3.52-3.49(m,1H),3.36-3.32(m,5H),3.02(t,J=9.5Hz,1H),2.47-2.35(m,3H),2.21(s,1H),2.17(s,4H),2.09(dd,J=12.4,6.2Hz,1H),1.73-1.53(m,3H),1.46(s,3H)。19F NMR(376MHz,DMSO-d6)δ-63.36(3F)。
实施例58:(3S)-N-[3-(2-[[1-(羟基甲基)环丙基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例58A:[1-[(6-氟-4-碘吡啶-2-基)氨基]环丙基]甲醇
将2,6-二氟-4-碘吡啶(500mg,2.075mmol)、(1-氨基环丙基)甲醇盐酸盐(282mg,2.282mmol)和NaHCO3(523mg,6.225mmol)在DMSO(5mL)中的混合物在100℃和氮气氛下搅拌3h。将所得混合物冷却至室温,并且用水(50mL)稀释并用EtOAc(3x30mL)萃取。将合并的有机层用盐水(100mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用含EtOAc的PE(58%)洗脱,得到呈浅黄色油状物的[1-[(6-氟-4-碘吡啶-2-基)氨基]环丙基]甲醇(575mg,90%)。MS ESI:C9H10FIN2O[M+H]+的计算值:309.09,实测值:308.90。1H NMR(400MHz,DMSO-d6)δ7.42(s,1H),6.84(s,1H),6.59(s,1H),4.77(brs,1H),3.48-3.42(m,2H),0.80-0.74(m,2H),0.61-0.55(m,2H)。19F NMR(376MHz,DMSO-d6)δ-70.00(1F)。
制备例58B:(1-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]环丙基)甲醇
将[1-[(6-氟-4-碘吡啶-2-基)氨基]环丙基]甲醇(575mg,1.866mmol)、吗啉(179mg,2.053mmol)和DIEA(482mg,3.733mmol)在DMSO(6mL)中的溶液在100℃和氮气氛下搅拌16h。将所得混合物冷却至室温,并且用水(60mL)猝灭并用EtOAc(3x30mL)萃取。将合并的有机层用盐水(100mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用含EtOAc的PE(76%)洗脱,得到呈浅黄色固体的(1-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]环丙基)甲醇(315mg,45%)。MS ESI:C13H18IN3O2[M+H]+的计算值:376.21,实测值:375.90。1H NMR(400MHz,DMSO-d6)δ6.60(s,1H),6.29-6.27(m,2H),4.68(brs,1H),3.64-3.62(m,4H),3.50-3.41(m,2H),3.33-3.30(m,4H),0.75-0.72(m,2H),0.57-0.55(m,2H)。
实施例58:(3S)-N-[3-(2-[[1-(羟基甲基)环丙基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将(1-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]环丙基)甲醇(200mg,0.533mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(242mg,0.586mmol)、Pd(dppf)Cl2.CH2Cl2(43mg,0.053mmol)、Na2CO3(169mg,1.599mmol)、1,4-二噁烷(6mL)和水(1.5mL)的混合物在60℃和氮气氛下搅拌16h。将反应混合物冷却至室温,并且减压浓缩。将残余物通过硅胶柱色谱法纯化,用含EA/EtOH(3/1)的PE(60%)洗脱,随后进行采用以下条件的制备型HPLC:柱:XBridge制备型苯基OBD柱,19×150mm 5um 13nm;流动相A:水(10mmol/L NH4HCO3),流动相B:乙腈;流速:20mL/min;梯度:在5.5min内45B至65B;254/210nm,得到呈灰白色固体的(3S)-N-[3-(2-[[1-(羟基甲基)环丙基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(151mg,51%)。MS ESI:C27H34F3N5O3[M+H]+的计算值:534.59,实测值:534.25。1H NMR(400MHz,DMSO-d6)δ8.12(s,1H),7.43-7.33(m,2H),7.11-7.09(m,1H),6.43(s,1H),5.85-5.83(m,2H),4.75-4.74(m,1H),3.68-3.66(m,5H),3.52-3.49(m,3H),3.38-3.30(m,5H),3.03-3.02(m,1H),2.52-2.44(m,3H),2.16(s,3H),2.08-2.06(m,1H),1.78-1.65(m,1H),0.76-0.75(m,2H),0.63-0.62(m,2H)。19F NMR(376MHz,DMSO-d6)δ-63.36(3F)。
实施例59和60:(S)-N-(3-(2-(((1R,3S)-3-羟基-1-甲基环丁基)氨基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺,(S)-N-(3-(2-(((1S,3R)-3-羟基-1-甲基环丁基)氨基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例59A:(3-羟基-1-甲基环丁基)氨基甲酸叔丁酯
在0℃和氮气氛下,向N-(1-甲基-3-氧代环丁基)氨基甲酸叔丁酯(2.00g,10.04mmol)在THF(20mL)中的溶液中逐滴加入NaBH4(0.76g,20.07mmol)。将所得混合物在室温下搅拌16h。在0℃下用饱和NH4Cl(100mL)猝灭反应。将所得混合物用EtOAc(3x100mL)萃取。将合并的有机层用盐水(50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。所得混合物不经进一步纯化即直接用于下一步骤中。1H NMR(400MHz,氯仿-d)δ4.72(s,1H),4.17-4.10(m,2H),1.99-1.86(m,2H),1.30(d,J=20.8Hz,9H)。
制备例59B:3-氨基-3-甲基环丁-1-醇盐酸盐
在0℃下,向(3-羟基-1-甲基环丁基)氨基甲酸叔丁酯(1.50g,7.46mmol)在DCM(4mL)中的溶液中加入含HCl(气体)的1,4-二噁烷(2mL,65.82mmol,4M)。将所得混合物在室温下搅拌1h。将所得混合物减压浓缩。所得混合物不经进一步纯化即直接用于下一步骤中。1HNMR(400MHz,DMSO-d6)δ8.37(s,2H),4.43-4.35(m,1H),4.04(p,J=7.1Hz,1H),2.26(ddt,J=9.3,7.1,2.3Hz,2H),2.17-2.08(m,2H),1.33(s,3H)。
制备例59C:3-((6-氟吡啶-2-基)氨基)-3-甲基环丁-1-醇
在室温下,向3-氨基-3-甲基环丁-1-醇盐酸盐(1.3g,9.489mmol)在DMSO(13mL)中的溶液中加入2,6-二氟-4-碘吡啶(1.37g,5.67mmol)和DIEA(6.10g,47.23mmol)。将所得混合物在110℃下搅拌16h。在室温下通过添加水(130mL)来猝灭反应。将所得混合物用EtOAc(3x100mL)萃取。将合并的有机层用盐水(200mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(3:1)洗脱,得到呈浅黄色油状物的3-((6-氟吡啶-2-基)氨基)-3-甲基环丁-1-醇(800mg,26%)。MS ESI:C10H13FN2O[M+H]+的计算值:323.00,实测值:323.05。1H NMR(400MHz,氯仿-d)δ6.55-6.45(m,2H),4.63(d,J=53.3Hz,1H),4.23(p,J=6.9Hz,1H),4.13-4.03(m,1H),2.51-2.43(m,2H),2.37-2.25(m,2H),1.34-1.22(m,3H)。
制备例59D:3-((4-碘-6-吗啉基吡啶-2-基)氨基)-3-甲基环丁-1-醇
在室温下,向3-((6-氟-4-碘吡啶-2-基)氨基)-3-甲基环丁-1-醇(980mg,3.043mmol)在DMSO(10mL)中的溶液中加入DIEA(786mg,6.085mmol)。将所得混合物在110℃下搅拌16h。将反应用水(100mL)猝灭。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用盐水(100mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1:1)洗脱,得到呈浅黄色油状物的3-((4-碘-6-吗啉基吡啶-2-基)氨基)-3-甲基环丁-1-醇(200mg,17%)。MS ESI:C14H20IN3O2[M+H]+的计算值:390.06,实测值:389.95。1H NMR(400MHz,DMSO-d6)δ6.17(d,J=1.1Hz,1H),6.14(d,J=1.0Hz,1H),4.03(q,J=7.1Hz,3H),3.90(t,J=7.3Hz,1H),3.64(dd,J=5.8,3.9Hz,4H),2.39(ddd,J=12.0,6.0,2.6Hz,2H),2.23-2.20(m,2H),1.21(s,3H)。
实施例59和60:(S)-N-(3-(2-(((1R,3S)-3-羟基-1-甲基环丁基)氨基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺,(S)-N-(3-(2-(((1S,3R)-3-羟基-1-甲基环丁基)氨基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将3-((4-碘-6-吗啉基吡啶-2-基)氨基)-3-甲基环丁-1-醇(200mg,0.514mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(212mg,0.514mmol)、Pd(dppf)Cl2.CH2Cl2(42mg,0.051mmol)和Na2CO3(163mg,1.541mmol)在二噁烷(2mL)和H2O(0.2mL)中的混合物在80℃和氮气氛下搅拌3h。将反应混合物减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/2)洗脱。将所得混合物通过手性HPLC采用以下条件进行拆分:柱:CHIRALPAK IE,2*25cm,5um;流动相A:Hex(0.5%2M NH3-MeOH),流动相B:EtOH;流速:18mL/min;A:B=70:30;220/254nm,得到14.7mg(9%),呈浅蓝色固体。MS ESI:C28H36F3N5O3[M+H]+的计算值:548.28,实测值:548.25。1HNMR(400MHz,DMSO-d6)δ8.10(s,1H),7.48-7.32(m,2H),7.09(d,J=8.3Hz,1H),6.24(s,1H),5.73(d,J=28.8Hz,2H),4.91(d,J=5.8Hz,1H),4.16(h,J=6.7Hz,1H),3.75-3.60(m,5H),3.53(ddd,J=10.4,8.2,2.3Hz,1H),3.36(d,J=9.6Hz,4H),3.32-3.25(m,1H),3.02(t,J=9.4Hz,1H),2.63(ddd,J=10.0,7.3,2.6Hz,2H),2.43(dd,J=15.0,7.1Hz,3H),2.17(s,4H),1.89-1.77(m,2H),1.77-1.59(m,1H),1.49(s,3H)。19F NMR(376MHz,DMSO-d6)δ-63.36,以及50.5mg(30%),呈浅蓝色固体。MS ESI:C28H36F3N5O3[M+H]+的计算值:548.28,实测值:548.25。1H NMR(300MHz,DMSO-d6)δ8.11(s,1H),7.49-7.30(m,2H),7.09(d,J=8.3Hz,1H),6.42(s,1H),5.72(d,J=19.3Hz,2H),4.93(d,J=6.2Hz,1H),4.03(h,J=7.1Hz,1H),3.80-3.62(m,5H),3.53(ddd,J=10.5,8.3,2.4Hz,1H),3.39(s,1H),3.37-3.21(m,3H),3.03(t,J=9.3Hz,1H),2.50-2.34(m,5H),2.17(s,3H),2.05(t,J=10.2Hz,3H),1.85-1.55(m,1H),1.42(s,3H)。19F NMR(282MHz,DMSO-d6)δ-63.36,-63.43。
实施例61:(3S)-N-[3-(2-[[(2R,3R)-3-羟基丁烷-2-基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例61A:(2R,3R)-3-[(6-氟-4-碘吡啶-2-基)氨基]丁-2-醇
将2,6-二氟-4-碘吡啶(300mg,1.245mmol)、DMSO(3mL)、(2R,3R)-3-氨基丁-2-醇(133mg,1.494mmol)和DIEA(804mg,6.225mmol)的溶液在70℃下搅拌2h。将所得混合物用H2O(100mL)猝灭,并且用EtOAc(4x50mL)萃取。将合并的有机层用盐水(4x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1:1)洗脱,得到呈浅黄色油状物的(2R,3R)-3-[(6-氟-4-碘吡啶-2-基)氨基]丁-2-醇(172mg,44%)。MS ESI:C9H12FIN2O[M+H]+的计算值:311.11,实测值:310.90。1H NMR(400MHz,氯仿-d)δ6.65(s,1H),6.52(m,1H),4.78(s,1H),3.80(m,2H),2.19(s,1H),1.32-1.19(m,6H)。
制备例61B:(2R,3R)-3-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丁-2-醇
将(2R,3R)-3-[(6-氟-4-碘吡啶-2-基)氨基]丁-2-醇(110mg,0.355mmol)、DMSO(2mL)、吗啉(102mg,1.171mmol)和DIEA(55mg,0.426mmol)的混合物在70℃下搅拌16h。将所得混合物用H2O(100mL)猝灭,并且用EtOAc(4x50mL)萃取。将合并的有机层用盐水(4x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE中的39%EtOAc洗脱,得到呈暗黄色油状物的(2R,3R)-3-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丁-2-醇(110mg,67%)。MS ESI:C13H20IN3O2[M+H]+的计算值:379.06,实测值:379.00。C13H20IN3O2:1H NMR(400MHz,氯仿-d)δ7.28(s,1H),6.28(s,1H),6.24(s,1H),4.44-4.20(m,1H),3.79(s,4H),3.72(m,1H),3.43(s,4H),2.07(s,1H),1.29-1.20(m,6H)。
实施例61:(3S)-N-[3-(2-[[(2R,3R)-3-羟基丁烷-2-基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将(2R,3R)-3-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丁-2-醇(110mg,0.292mmol)和(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(120mg,0.292mmol)、1,4-二噁烷(2mL)、H2O(0.5mL)、Na2CO3(93mg,0.875mmol)和Pd(dppf)Cl2.CH2Cl2(24mg,0.029mmol)的混合物在80℃和氮气氛下搅拌2h。将所得混合物减压浓缩。将残余物通过硅胶柱色谱法纯化,用EtOAc洗脱,随后进行采用以下条件的反相快速色谱法:(柱,C18硅胶;流动相,含MeCN的水,在10min内5%至95%梯度;检测器,UV 254nm),得到呈白色固体的(3S)-N-[3-(2-[[(2R,3R)-3-羟基丁烷-2-基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(59mg,38%)。MS ESI:C27H36F3N5O3[M+H]+的计算值:536.61,实测值:536.15。1H NMR(300MHz,DMSO-d6)δ8.11(s,1H),7.41(m,1H),7.33(s,1H),7.09(s,1H),5.86(s,1H),5.79(s,1H),5.73(s,1H),4.59(s,1H),3.87(s,1H),3.78-3.62(m,6H),3.57-3.47(m,1H),3.37(sz,4H),3.31-3.25(m,1H),3.02(m,1H),2.50(s,3H),2.16(s,3H),2.12-1.97(m,1H),1.66(m,1H),1.06(m,6H)。19F NMR(376MHz,DMSO-d6)δ-63.4(3F)。
实施例62:(3S)-N-(3-[2-[(1-氰基丙烷-2-基)氨基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例62A:3-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丁腈
将2,6-二氟-4-碘吡啶(300mg,1.245mmol)、DMSO(4mL)、3-氨基丁腈盐酸盐(165mg,1.369mmol)和DIEA(354mg,2.739mmol)的溶液在70℃下搅拌3h。向以上搅拌混合物中加入吗啉(357mg,4.097mmol)。将所得混合物在100℃下搅拌16h。将所得混合物用水(50mL)稀释。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用盐水(2x30mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc/EtOH=(4/3/1)洗脱,得到呈灰白色固体的3-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丁腈(351mg,75%)。MS ESI:C13H17IN4O[M+H]+的计算值:373.04,实测值:372.90。1H NMR(300MHz,氯仿-d)δ6.45-6.40(m,1H),6.23-6.22(m,1H),4.25-4.22(m,1H),3.84-3.78(m,5H),3.54-3.37(m,4H),2.84-2.64(m,2H),1.47-1.42(m,3H)。
实施例62:(3S)-N-(3-[2-[(1-氰基丙烷-2-基)氨基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将3-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丁腈(150mg,0.403mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(166mg,0.403mmol)、Na2CO3(128mg,1.209mmol)、二噁烷(4mL)、H2O(1mL)和Pd(dppf)Cl2.CH2Cl2(33mg,0.040mmol)的混合物在60℃和氮气氛下搅拌16h。将所得混合物用水(50mL)稀释,并且用EtOAc(3x50mL)萃取。将合并的有机层用盐水(2x40mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用己烷/EtOAc/EtOH=4/3/1洗脱,随后进行采用以下条件的反相快速色谱法:柱,C18硅胶;流动相,含MeCN的水,在10min内5%至95%梯度;检测器,UV 254nm,得到呈白色固体的(3S)-N-(3-[2-[(1-氰基丙烷-2-基)氨基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(149mg,69%)。MS ESI:C27H33F3N6O2[M+H]+的计算值:531.26,实测值:531.15。1H NMR(300MHz,DMSO-d6)δ8.01(s,1H),7.43-7.33(m,2H),7.11-7.08(m,1H),6.53-6.51(m,1H),5.82-5.81(m,2H),4.16-4.15(m,1H),3.68-3.49(m,5H),3.52-3.49(m,1H),3.39-3.33(m,4H),3.04-3.02(m,1H),2.98-2.72(m,2H),2.50-2.42(m,3H),2.18-2.01(m,5H),2.71-2.59(m,1H),1.29-1.22(m,3H)。19F NMR(282MHz,DMSO-d6)δ-63.36(3F)。
实施例63和64:(S)-N-(3-(2-(((1S,4R)-4-羟基-1-甲基环己基)氨基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺,(S)-N-(3-(2-(((1R,4S)-4-羟基-1-甲基环己基)氨基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例63A:N-(4-羟基-1-甲基环己基)氨基甲酸叔丁酯
在室温下,分数份向N-(1-甲基-4-氧代环己基)氨基甲酸叔丁酯(700mg,3.080mmol)在MeOH(10mL)中的溶液中加入NaBH4(174mg,4.619mmol)。将混合物在室温下搅拌2h。在0℃下通过添加水(50mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。这产生呈无色油状物的N-(4-羟基-1-甲基环己基)氨基甲酸叔丁酯(600mg,85%)。MS ESI:C12H23NO3[M+H]+的计算值:230.17,实测值:N/A。1H NMR(400MHz,氯仿-d)δ3.65(td,J=10.1,4.8Hz,1H),1.47(s,3H),1.46-1.40(m,8H),1.44(s,9H)。
制备例63B:4-氨基-4-甲基环己-1-醇盐酸盐
在室温下,向N-(4-羟基-1-甲基环己基)氨基甲酸叔丁酯(600mg,2.616mmol)在EtOAc(5mL)中的溶液中加入含HCl(气体)的EtOAc(10mL)。将混合物在室温下搅拌2h。将所得混合物减压浓缩。这产生呈白色固体的4-氨基-4-甲基环己-1-醇盐酸盐(400mg,92%)。粗产物不经进一步纯化即直接用于下一步骤中。MS ESI:C7H15NO[M+H]+的计算值:130.12,实测值:N/A。1H NMR(400MHz,甲醇-d4)δ3.84(td,J=6.1,3.1Hz,1H),1.93-1.66(m,8H),1.37(s,3H)。
制备例63C:4-[(6-氟-4-碘吡啶-2-基)氨基]-4-甲基环己-1-醇
在室温下,向4-(6-氟-4-碘吡啶-2-基)吗啉(744mg,2.415mmol)和4-氨基-4-甲基环己-1-醇盐酸盐(500mg,3.018mmol)在DMSO(10mL)中的溶液中加入DIEA(1.95g,15.091mmol)。将混合物在100℃下搅拌3h。使混合物冷却至室温。在室温下通过添加水(50mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。MS ESI:C12H16FIN2O[M+H]+的计算值:351.03,实测值:350.95。1H NMR(400MHz,氯仿-d)δ6.67-6.61(m,1H),6.51(dd,J=2.9,1.0Hz,1H),3.69(td,J=9.3,4.2Hz,1H),2.33-2.25(m,2H),1.94-1.78(m,3H),1.49(d,J=20.6Hz,3H),1.44(s,3H)。
制备例63D:4-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]-4-甲基环己-1-醇
在室温下,向4-[(6-氟-4-碘吡啶-2-基)氨基]-4-甲基环己-1-醇(130mg,0.371mmol)和吗啉(48mg,0.557mmol)在DMSO(5mL)中的溶液中加入DIEA(96mg,0.742mmol)。将混合物在110℃下搅拌16h。将所得溶液通过制备型HPLC采用以下条件纯化:(柱:XBridge Shield RP18 OBD柱,30*150mm,5um;流动相A:水(10mmoL/L NH4HCO3),流动相B:CH3CN;流速:60mL/min;梯度:在25min内35B至75B),得到呈浅黄色固体的4-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]-4-甲基环己-1-醇(80mg,52%)。MS ESI:C16H24IN3O2[M+H]+的计算值:418.09,实测值:418.00。1H NMR(400MHz,氯仿-d)δ6.60-6.44(m,1H),6.32(dd,J=9.8,1.2Hz,1H),3.85(q,J=3.9,2.7Hz,5H),3.54(dd,J=5.7,3.8Hz,4H),2.18(d,J=13.6Hz,1H),1.99-1.76(m,3H),1.70-1.44(m,2H),1.42(s,3H),1.32-1.30(m,2H)。
实施例63和64:(S)-N-(3-(2-(((1S,4R)-4-羟基-1-甲基环己基)氨基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺,(S)-N-(3-(2-(((1R,4S)-4-羟基-1-甲基环己基)氨基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在室温下,向4-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]-4-甲基环己-1-醇(130mg,0.312mmol)和(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(128mg,0.312mmol)在1,4-二噁烷(10mL)和H2O(1mL)中的溶液中加入Pd(dppf)Cl2.CH2Cl2(25mg,0.031mmol)和K2CO3(129mg,0.935mmol)。将混合物在80℃和氮气氛下搅拌2h。将所得混合物真空浓缩。将粗产物通过制备型HPLC采用以下条件纯化:(柱:XBridge Shield RP18 OBD柱,30*150mm,5um;流动相A:水(10mmoL/L NH4HCO3),流动相B:CH3CN;流速:60mL/min;梯度:在25min内35B至75B;),得到呈白色固体的外消旋物(40mg)。将混合物(40mg)通过手性HPLC采用以下条件进行分离:柱:CHIRALPAK IH,2.0*25cm,5um;流动相A:MeOH(0.1%DEA),流动相B:CO2;流速:50mL/min;梯度:50%B。第一峰提供了8mg(4%),呈白色固体。MS ESI:C30H40F3N5O3[M+H]+的计算值:576.31,实测值:576.15。1H NMR(400MHz,甲醇-d4)δ7.27(dt,J=4.1,2.4Hz,2H),7.14(d,J=8.9Hz,1H),5.87(d,J=16.9Hz,2H),3.84-3.75(m,6H),3.63(ddd,J=10.5,8.4,2.3Hz,1H),3.44(h,J=6.5Hz,5H),3.18–3.09(m,1H),2.55(s,1H),2.47-2.32(m,2H),2.23(s,4H),2.05(t,J=9.4Hz,2H),1.97-1.67(m,5H),1.54(q,J=8.4,7.1Hz,2H),1.49(s,3H)。19FNMR(376MHz,氯仿-d)δ-66.49(3F)。第二峰提供了33mg(18%),呈白色固体。MS ESI:C30H40F3N5O3[M+H]+的计算值:576.31,实测值:576.15。1H NMR(400MHz,甲醇-d4)δ7.31-7.25(m,2H),7.15(d,J=9.0Hz,1H),5.93(s,1H),5.84(s,1H),3.84-3.75(m,5H),3.68-3.53(m,2H),3.49-3.38(m,5H),3.13(t,J=9.7Hz,1H),2.65-2.30(m,5H),2.24(s,4H),1.97-1.67(m,3H),1.68-1.53(m,2H),1.46(s,3H),1.44-1.29(m,2H)。19F NMR(376MHz,氯仿-d)δ-66.48(3F)。
实施例65:(3S)-N-(3-[2-[(1,3-二羟基丙烷-2-基)氨基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例65A:2-((4-碘-6-吗啉基吡啶-2-基)氨基)丙烷-1,3-二醇
在室温下,向4-(6-氟-4-碘吡啶-2-基)吗啉(300mg,0.974mmol)和K2CO3(404mg,2.921mmol)在NMP(4mL)中的搅拌混合物中加入2-氨基丙烷-1,3-二醇(443mg,4.869mmol)。将反应混合物在150℃下搅拌16h。将所得混合物用水(50mL)稀释。将所得混合物用EtOAc(3x20mL)萃取。将合并的有机层用盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。残余物通过反相色谱法纯化,用水(含0.5%NH4HCO3)中的55%CH3CN洗脱。收集含有所需产物的级分,并且减压浓缩,得到呈粉红色固体的2-((4-碘-6-吗啉基吡啶-2-基)氨基)丙烷-1,3-二醇(110mg,25%)。MS ESI:C12H18IN3O3[M+H]+的计算值:380.04,实测值:380.05。1H NMR(400MHz,DMSO-d6)δ6.29(d,J=1.0Hz,1H),6.19(d,J=1.0Hz,1H),4.55(t,J=5.5Hz,2H),3.64(t,J=4.9Hz,4H),3.52-3.40(m,4H),3.34(d,J=4.9Hz,4H),1.06(t,J=7.0Hz,1H)。
实施例65:(3S)-N-(3-[2-[(1,3-二羟基丙烷-2-基)氨基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在室温下,向2-((4-碘-6-吗啉基吡啶-2-基)氨基)丙烷-1,3-二醇(80mg,0.211mmol)、K2CO3(87mg,0.633mmol)和(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(104mg,0.253mmol)在二噁烷(2mL)和H2O(0.5mL)中的搅拌混合物中加入Pd(dppf)Cl2.CH2Cl2(17mg,0.021mmol)。T将反应混合物在80℃和N2氛下搅拌2h。将所得混合物用水(10mL)稀释。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用盐水(2x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用EA中的50%PE洗脱。收集含有所需产物的级分,并且减压浓缩。粗物质通过反相色谱法纯化,用水(含10mmol/mL NH4HCO3)中的50%CH3CN洗脱。收集含有所需产物的级分,并且减压浓缩,得到呈灰白色固体的(3S)-N-(3-[2-[(1,3-二羟基丙烷-2-基)氨基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(105mg,98%)。MS ESI:C26H34F3N5O4[M+H]+的计算值:538.26,实测值:538.35。1H NMR(400MHz,DMSO-d6)δ8.11(s,1H),7.41(dd,J=8.3,2.3Hz,1H),7.34(d,J=2.3Hz,1H),7.09(d,J=8.4Hz,1H),5.86(d,J=7.6Hz,1H),5.81(d,J=0.9Hz,1H),5.76(d,J=1.1Hz,1H),4.58(t,J=5.5Hz,2H),3.82(d,J=6.7Hz,1H),3.67(q,J=8.3,6.4Hz,5H),3.58-3.45(m,5H),3.37(d,J=9.6Hz,4H),3.30(d,J=10.0Hz,1H),3.02(t,J=9.4Hz,1H),2.44(t,J=10.7Hz,3H),2.16(s,3H),2.08(d,J=3.7Hz,1H),1.66(p,J=9.9Hz,1H)。
实施例66:(3S)-N-[3-[2-氨基-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例66A:4-碘-6-(吗啉-4-基)吡啶-2-胺
将4-(6-氟-4-碘吡啶-2-基)吗啉(2.00g,6.492mmol)和NH4OH(140mL)在n-BuOH(20mL)中的溶液在120℃下搅拌16h。使混合物冷却至室温。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈浅黄色油状物的4-碘-6-(吗啉-4-基)吡啶-2-胺(0.70g,35%)。MS ESI:C9H12IN3O[M+H]+的计算值:306.00,实测值:305.95。1H NMR(300MHz,氯仿-d)δ6.32(dd,J=15.3,1.0Hz,2H),4.21(s,2H),3.82-3.73(m,4H),3.48-3.39(m,4H)。
实施例66:(3S)-N-[3-[2-氨基-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在室温下,向4-碘-6-(吗啉-4-基)吡啶-2-胺(100mg,0.328mmol)和(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(135mg,0.328mmol)在1,4-二噁烷(1mL)和H2O(0.2mL)中的搅拌溶液中加入Na2CO3(104mg,0.983mmol)和Pd(dppf)Cl2.CH2Cl2(27mg,0.033mmol)。将所得混合物在80℃和氮气氛下搅拌2h。使混合物冷却至室温。在室温下通过添加水(50mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈浅黄色固体的(3S)-N-[3-[2-氨基-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(73mg,48%)。MS ESI:C23H28F3N5O2[M+H]+的计算值:464.22,实测值:464.10。1H NMR(400MHz,DMSO-d6)δ8.11(s,1H),7.42(dd,J=8.3,2.4Hz,1H),7.34(d,J=2.4Hz,1H),7.09(d,J=8.4Hz,1H),5.77(dd,J=17.6,1.0Hz,2H),5.64(s,2H),3.71-3.63(m,5H),3.55-3.49(m,1H),3.41-3.35(m,3H),3.32-3.26(m,2H),3.02(t,J=9.4Hz,1H),2.51-2.36(m,3H),2.16(s,3H),2.08(d,J=10.6Hz,1H),1.67(q,J=10.4,10.0Hz,1H)。19FNMR(376MHz,DMSO-d6)δ-63.37(3F)。
实施例67:(3S)-N-[4-甲基-3-[2-(甲基氨基)-6-(吗啉-4-基)吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例67A:4-碘-N-[(4-甲氧基苯基)甲基]-N-甲基-6-(吗啉-4-基)吡啶-2-胺
在室温下,分数份向4-(6-氟-4-碘吡啶-2-基)吗啉(320mg,0.974mmol)和[(4-甲氧基苯基)甲基](甲基)胺(740mg,4.869mmol)在NMP(3mL)中的搅拌混合物中加入K2CO3(670mg,4.869mmol)。将所得混合物在150℃下搅拌16h。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(5/1)洗脱,得到呈黄色固体的4-碘-N-[(4-甲氧基苯基)甲基]-N-甲基-6-(吗啉-4-基)吡啶-2-胺(170mg,39%)。MS ESI:C18H22IN3O2[M+H]+的计算值:440.08,实测值:440.05。1H NMR(300MHz,甲醇-d4)δ7.16(d,J=8.5Hz,2H),6.86(d,J=8.5Hz,2H),6.35(s,1H),4.70(s,2H),3.81(d,J=5.0Hz,7H),3.46(t,J=4.9Hz,3H),2.96(s,3H)。
制备例67B:(3S)-N-[3-(2-[[(4-甲氧基苯基)甲基](甲基)氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
向4-碘-N-[(4-甲氧基苯基)甲基]-N-甲基-6-(吗啉-4-基)吡啶-2-胺(170mg,0.387mmol)和(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(160mg,0.387mmol)和K2CO3(160mg,1.161mmol)在二噁烷(1.6mL)和H2O(0.4mL)中的搅拌混合物中加入Pd(dppf)Cl2.CH2Cl2(31mg,0.039mmol)。将所得混合物在80℃和氮气氛下搅拌2h。将所得混合物减压浓缩。残余物通过制备型TLC(PE/EtOAc=1/1)纯化,得到呈浅黄色固体的(3S)-N-[3-(2-[[(4-甲氧基苯基)甲基](甲基)氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(240mg,93%)。MS ESI:C32H38F3N5O3[M+H]+的计算值:598.29,实测值:598.30。1H NMR(400MHz,氯仿-d)δ7.37(d,J=8.3Hz,1H),7.19(dd,J=15.4,8.2Hz,3H),6.87(d,J=8.5Hz,2H),6.10(s,1H),5.97(s,1H),4.77(s,2H),3.84(d,J=19.9Hz,7H),3.64(t,J=8.9Hz,1H),3.57-3.40(m,4H),3.06(s,2H),2.28(t,J=9.5Hz,3H),1.81-1.73(m,1H)。
实施例67:(3S)-N-[4-甲基-3-[2-(甲基氨基)-6-(吗啉-4-基)吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将(3S)-N-[3-(2-[[(4-甲氧基苯基)甲基](甲基)氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(190mg,0.318mmol)和TFA(1.5mL)在DCM(1.5mL)中的混合物在室温下搅拌16h。将所得混合物减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈灰白色固体的(3S)-N-[4-甲基-3-[2-(甲基氨基)-6-(吗啉-4-基)吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(90mg,59%)。MS ESI:C24H30F3N5O2[M+H]+的计算值:478.24,实测值:478.05。1H NMR(300MHz,甲醇-d4)δ7.34-7.25(m,2H),7.15(d,J=8.6Hz,1H),5.89(d,J=1.3Hz,1H),5.82(d,J=1.2Hz,1H),3.84-3.75(m,5H),3.64(t,J=9.8Hz,1H),3.50-3.39(m,5H),3.20-3.07(m,1H),2.91-2.84(m,3H),2.55(s,1H),2.48-2.29(m,2H),2.23(s,4H),1.77(p,J=10.9,10.2Hz,1H)。19F NMR(376MHz,甲醇-d4)δ-63.36(3F)。
实施例68:(3S)-N-[3-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-(3-氧代吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例68A:4-(6-氟-4-碘吡啶-2-基)吗啉-3-酮
在0℃和氮气氛下,向吗啉-3-酮(0.92g,9.13mmol)在甲苯(20mL)中的溶液中逐滴加入含t-BuOK的THF(8.3mL,8.30mmol,1M)。在室温下,向以上混合物中加入2,6-二氟-4-碘吡啶(2.00g,8.30mmol)。将所得混合物在80℃下搅拌5h。在0℃下用水(20mL)猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用己烷/EtOAc(1/1)洗脱,得到呈白色固体的4-(6-氟-4-碘吡啶-2-基)吗啉-3-酮(2.00g,74%)。MS ESI:C9H8FIN2O2[M+H]+的计算值:322.96,实测值:323.00。1H NMR(400MHz,氯仿-d)δ8.63(t,J=1.2Hz,1H),7.15(dd,J=3.3,1.0Hz,1H),4.36(s,2H),4.03(s,4H)。
制备例68B:4-(6-[[(2R)-1-羟基丙烷-2-基]氨基]-4-碘吡啶-2-基)吗啉-3-酮
向4-(6-氟-4-碘吡啶-2-基)吗啉-3-酮(1.00g,3.10mmol)和(R)-(-)-2-氨基-1-丙醇(0.35g,4.66mmol)在NMP(10mL)中的溶液中加入K2CO3(0.86g,6.21mmol)。将所得混合物在100℃下搅拌16h。在室温下通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x60mL)萃取。将合并的有机层用盐水(3x100mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈黄色油状物的4-(6-[[(2R)-1-羟基丙烷-2-基]氨基]-4-碘吡啶-2-基)吗啉-3-酮(0.40g,粗物质)。MSESI:C12H16IN3O3[M+H]+的计算值:378.02;实测值:378.00。
实施例68:(3S)-N-[3-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-(3-氧代吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
4-(6-[[(2R)-1-羟基丙烷-2-基]氨基]-4-碘吡啶-2-基)吗啉-3-酮(150mg,0.398mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(164mg,0.398mmol)、Pd(dppf)Cl2.CH2Cl2(32mg,0.040mmol)、Na2CO3(126mg,1.193mmol)、二噁烷(2mL)和H2O(0.2mL)的混合物。将混合物在80℃和氮气氛下搅拌2h。将反应混合物减压浓缩。将残余物通过反相色谱法采用以下条件纯化:(柱:球形C18,20-40um,40g;流动相A:水(10mmol/mL NH4HCO3),流动相B:CH3CN;流速:40mL/min;在20min内30%~60%)。将收集的级分合并,并且减压浓缩,得到呈白色固体的(3S)-N-[3-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-(3-氧代吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(45mg,21%)。MS ESI:C26H32F3N5O4[M+H]+的计算值:536.25,实测值:536.24。1H NMR(300MHz,DMSO-d6)δ8.17(s,1H),7.49-7.33(m,2H),7.17-7.06(m,2H),6.44(d,J=7.6Hz,1H),6.26(d,J=1.2Hz,1H),4.69(t,J=5.6Hz,1H),4.21(s,2H),3.97(s,5H),3.68(dd,J=10.3,6.7Hz,1H),3.59-3.46(m,2H),3.32-3.25(m,2H),3.03(t,J=9.3Hz,1H),2.45(q,J=9.5,7.6Hz,3H),2.18(s,4H),1.73-1.56(m,1H),1.16(d,J=6.5Hz,3H)。19F NMR(276MHz,DMSO-d6)δ-63.37(3F)。
实施例69:(3S)-N-[3-[2-乙酰胺基-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例69A:N-[4-碘-6-(吗啉-4-基)吡啶-2-基]乙酰胺
在室温下,向4-碘-6-(吗啉-4-基)吡啶-2-胺(200mg,0.655mmol)在DCM(2mL)中的搅拌溶液中加入4-碘-6-(吗啉-4-基)吡啶-2-胺(200mg,0.655mmol)。将所得混合物在室温下搅拌2h。在室温下通过添加MeOH(1mL)来猝灭反应。将所得混合物减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1至0/1)洗脱,得到呈白色固体的N-[4-碘-6-(吗啉-4-基)吡啶-2-基]乙酰胺(210mg,92%)。MS ESI:C11H14IN3O2[M+H]+的计算值:348.01,实测值:348.00。1H NMR(300MHz,氯仿-d)δ7.93(s,1H),7.53(s,1H),6.75(d,J=1.1Hz,1H),3.83-3.73(m,4H),3.48-3.39(m,4H),2.18(s,3H)。
实施例69:(3S)-N-[3-[2-乙酰胺基-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
向N-[4-碘-6-(吗啉-4-基)吡啶-2-基]乙酰胺(200mg,0.576mmol)和(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(237mg,0.576mmol)、1,4-二噁烷(2mL)和H2O(0.4mL)的搅拌溶液中加入Na2CO3(183mg,1.728mmol)和Pd(dppf)Cl2.CH2Cl2(47mg,0.058mmol)。将所得混合物在80℃和氮气氛下搅拌2h。使混合物冷却至室温。在室温下通过添加水(50mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/2)洗脱,得到呈浅粉红色固体的(3S)-N-[3-[2-乙酰胺基-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(89mg,31%)。MS ESI:C25H30F3N5O3[M+H]+的计算值:506.23,实测值:506.10。1H NMR(400MHz,DMSO-d6)δ10.04(s,1H),8.16(s,1H),7.47(dd,J=8.3,2.4Hz,1H),7.37(d,J=2.4Hz,2H),7.14(d,J=8.4Hz,1H),6.40(d,J=1.1Hz,1H),3.73-3.63(m,5H),3.58-3.44(m,5H),3.35-3.25(m,1H),3.02(t,J=9.5Hz,1H),2.51-2.36(m,3H),2.16(s,3H),2.08(s,4H),1.72-1.60(m,1H)。19F NMR(376MHz,DMSO-d6)δ-66.37(3F)。
实施例70:(S)-N-(3-(3-氟-2-(((R)-1-羟基丙烷-2-基)氨基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例70A:4-(5,6-二氟-4-碘吡啶-2-基)吗啉和4-(3,6-二氟-4-碘吡啶-2-基)吗啉
在室氛下,分数份向4-(6-氟-4-碘吡啶-2-基)吗啉(6.00g,19.475mmol)在MeCN(240mL)中的溶液中加入selectfluor(6.9g,19.475mmol)。将混合物在室氛下搅拌16h。将所得混合物用水(300mL)猝灭,并且用EtOAc(3x500mL)萃取。将合并的有机层用盐水(2x150mL)洗涤,经无水Na2SO4干燥,并且减压浓缩。将残余物通过硅胶柱色谱法纯化,用含EtOAc的PE(0~90%)洗脱,得到呈白色固体的4-(5,6-二氟-4-碘吡啶-2-基)吗啉(700mg,11%)。MS ESI:C9H9F2IN2O[M+H]+的计算值:326.97,实测值:326.90。1H NMR(400MHz,氯仿-d)δ6.75(t,J=1.8Hz,1H),3.84-3.76(m,4H),3.43(dd,J=5.8,4.1Hz,4H)。还得到呈白色固体的4-(3,6-二氟-4-碘吡啶-2-基)吗啉(3.2g,50%)。MS ESI:C9H9F2IN2O[M+H]+的计算值:326.97,实测值:326.95。1H NMR(400MHz,氯仿-d)δ6.68(dd,J=4.2,2.3Hz,1H),3.82-3.80(m,4H),3.59-3.56(m,4H)。
制备例70B:(R)-2-((3-氟-4-碘-6-吗啉基吡啶-2-基)氨基)丙-1-醇
在室温下,4-(5,6-二氟-4-碘吡啶-2-基)吗啉(300mg,0.920mmol)、(R)-(-)-2-氨基-1-丙醇(138mg,1.840mmol)和K2CO3(254mg,1.840mmol)在NMP(5mL)中的混合物,将混合物在70℃下搅拌16h。使混合物冷却至室温。在室温下用水(50mL)猝灭反应。将所得混合物用EtOAc(50mL)萃取。将合并的有机层用盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。残余物通过制备型TLC(PE/EtOAc/EtOH=12/3/1)纯化,得到呈黄色油状物的(2R)-2-[[3-氟-4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丙-1-醇(224mg,64%)。MS ESI:C12H17FIN3O2[M+H]+的计算值:382.03,实测值:381.95。1H NMR(400MHz,氯仿-d)δ6.17(d,J=2.4Hz,1H),4.28-4.20(m,1H),3.84-3.80(m,4H),3.80-3.75(m,1H),3.62(dd,J=10.7,7.0Hz,1H),3.37(dd,J=5.9,3.9Hz,4H),1.31-1.28(m,3H)。
实施例70:(S)-N-(3-(3-氟-2-(((R)-1-羟基丙烷-2-基)氨基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将(2R)-2-[[3-氟-4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丙-1-醇(200mg,0.525mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(238mg,0.577mmol)、Pd(dppf)Cl2.CH2Cl2(43mg,0.052mmol)和K2CO3(217mg,1.574mmol)在二噁烷(8mL)和H2O(2mL)中的混合物在80℃下搅拌2h。使混合物冷却至室温。将所得混合物减压浓缩。混合物通过制备型TLC(PE/EtOAc/EtOH=4:3:1)纯化,随后进行采用以下条件的反相快速色谱法:柱:C18柱120g;流动相A:水(10mmoL NH4HCO3),流动相B:CH3CN;流速:60mL/min;梯度:在30min内40%至65%B;254/220nm。在55%B下收集含有所需产物的级分,并且减压浓缩,得到呈白色固体的(3S)-N-[3-(3-氟-2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(128mg,45%)。MS ESI:C26H33F4N5O3[M+H]+的计算值:540.58,实测值:540.30。1H NMR(400MHz,DMSO-d6)δ8.15(s,1H),7.45(dd,J=8.3,2.4Hz,1H),7.37(d,J=2.3Hz,1H),7.14(d,J=8.4Hz,1H),5.89(dd,J=7.7,1.8Hz,1H),5.63(d,J=3.0Hz,1H),4.67(t,J=5.7Hz,1H),4.07(p,J=6.4Hz,1H),3.71-3.66(m,4H),3.64(s,1H),3.57-3.46(m,2H),3.41-3.35(m,1H),3.32-3.23(m,4H),3.02(t,J=9.4Hz,1H),2.50-2.35(m,4H),2.09(s,4H),1.66(p,J=9.9Hz,1H),1.16(d,J=6.6Hz,3H)。19F NMR(376MHz,DMSO-d6)δ-63.37(3F),-158.76(1F)。
实施例71:(3S)-N-[3-(3-氟-6-[[(2R)-1-羟基丙烷-2-基]氨基]-2-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例71A:(2R)-2-[[5-氟-4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丙-1-醇
在室温下,向4-(3,6-二氟-4-碘吡啶-2-基)吗啉(900mg,2.760mmol)和(R)-(-)-2-氨基-1-丙醇(829mg,11.040mmol)在NMP(15mL)中的搅拌溶液中加入K2CO3(763mg,5.520mmol)。将所得混合物在150℃下搅拌16h。使混合物冷却至室温。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用水(3x100mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过反相快速色谱法采用以下条件纯化:柱:球形C18,20-40um,330g;流动相A:水(10mM NH4HCO3);流动相B:乙腈;流速:80mL/min;梯度:在20min内50%-65%B;检测器:254nm。在55%B下收集含有所需产物的级分,并且减压浓缩,得到呈浅黄色固体的(2R)-2-[[5-氟-4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丙-1-醇(175mg,16%)。MSESI:C12H16FIN2O3[M+H]+的计算值:382.04;实测值:381.95。1H NMR(300MHz,氯仿-d)δ6.27(d,1H),4.11(s,1H),3.90(s,1H),3.85-3.75(m,4H),3.54(m,1H),3.47-3.39(m,3H),1.21(d,3H)。19F NMR(376MHz,氯仿-d)δ-127.54。
实施例71:(3S)-N-[3-(3-氟-6-[[(2R)-1-羟基丙烷-2-基]氨基]-2-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
向(2R)-2-[[5-氟-4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丙-1-醇(230mg,0.603mmol)和(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(298mg,0.724mmol)、Na2CO3(191mg,1.810mmol)在二噁烷(4mL)、H2O(1mL)中的搅拌混合物中加入Pd(dppf)Cl2.CH2Cl2(49mg,0.060mmol)。将所得混合物在100℃和氮气氛下搅拌16h。将所得混合物用水(20mL)猝灭,并且用EtOAc(3x100mL)萃取。将合并的有机层用盐水(3x50mL)洗涤,经无水Na2SO4干燥,并且减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE中的0%至50%EtOAc洗脱,得到呈黄色固体的(3S)-N-[3-(3-氟-6-[[(2R)-1-羟基丙烷-2-基]氨基]-2-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(84mg,25%)。MS ESI:C26H33F4N5O3[M+H]+的计算值:540.26;实测值:540.25。1H NMR(300MHz,DMSO-d6)δ8.15(s,1H),7.49-7.34(m,2H),7.13(m,1H),5.99(m,1H),5.78(m,1H),4.64(m,1H),3.99-3.59(m,7H),3.58-3.45(m,2H),3.32-3.22(m,5H),3.03(m,1H),2.44(m,3H),2.08(s,4H),1.66(m,1H),1.12(m,3H)。19F NMR(282MHz,DMSO-d6)δ-63.36(3F),-151.86(1F)。
实施例72:(S)-N-(3-(2-(反式-3-羟基-2-甲基氮杂环丁烷-1-基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
实施例73:(S)-N-(3-(2-(顺式-3-羟基-2-甲基氮杂环丁烷-1-基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
合成方案
制备例72A:2-甲基氮杂环丁烷-3-醇盐酸盐
在室温下,向3-羟基-2-甲基氮杂环丁烷-1-甲酸叔丁酯(450mg,2.403mmol)在1,4-二噁烷(4.5mL)中的搅拌溶液中逐滴加入含HCl(气体)的1,4-二噁烷(4.5mL)。将所得溶液在室温下搅拌16h。将反应混合物减压浓缩,得到呈黄色油状物的2-甲基氮杂环丁烷-3-醇盐酸盐(400mg,粗物质)。粗产物不经任何其他纯化即直接用于下一步骤。
制备例72B:1-(6-氟-4-碘吡啶-2-基)-2-甲基氮杂环丁烷-3-醇
将2,6-二氟-4-碘吡啶(690mg,2.863mmol)、2-甲基氮杂环丁烷-3-醇盐酸盐(389mg,3.150mmol)和NaHCO3(721mg,8.590mmol)在DMSO(7mL)中的混合物在100℃下搅拌3h。将所得混合物冷却至室温,并且用水(100mL)稀释并用EtOAc(3x50mL)萃取。将合并的有机层用盐水(3x100mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用含EtOAc的PE(40%至50%)洗脱,得到呈灰白色半固体的1-(6-氟-4-碘吡啶-2-基)-2-甲基氮杂环丁烷-3-醇(270mg,33%)(顺式和反式的混合物)。MS ESI:C9H10FIN2O[M+H]+的计算值:308.98,实测值:308.85。1H NMR(400MHz,DMSO-d6)δ6.93-6.68(m,0.5H),6.62(ddt,J=4.2,2.6,1.4Hz,1H),6.57(t,J=1.4Hz,0.5H),5.59(dd,J=57.6,6.2Hz,1H),4.69-4.35(m,2H),4.18-3.89(m,1H),3.79-3.42(m,1H),1.48-1.23(m,3H)。
制备例72C:1-[4-碘-6-(吗啉-4-基)吡啶-2-基]-2-甲基氮杂环丁烷-3-醇
将1-(6-氟-4-碘吡啶-2-基)-2-甲基氮杂环丁烷-3-醇(275mg,0.893mmol)、吗啉(85mg,0.982mmol)和DIEA(230mg,1.785mmol)在DMSO(3mL)中的溶液在100℃下搅拌16h。将所得混合物冷却至室温。将所得溶液用水(50mL)猝灭,并且用EtOAc(3x30mL)萃取。将合并的有机层用盐水(1x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用含EtOAc的PE(48%至60%)洗脱,得到呈浅黄色固体的1-[4-碘-6-(吗啉-4-基)吡啶-2-基]-2-甲基氮杂环丁烷-3-醇(170mg,36%)(顺式和反式的混合物)。MS ESI:C13H18IN3O2[M+H]+的计算值:376.04,实测值:375.95。1H NMR(400MHz,氯仿-d)δ6.34(dd,J=17.3,1.2Hz,1H),6.09(dd,J=17.7,1.0Hz,1H),4.62(t,J=5.4Hz,1H),4.53-4.34(m,1H),4.25-4.03(m,1H),3.80(q,J=5.2Hz,5H),3.54-3.36(m,4H),1.49(dd,J=29.7,6.5Hz,3H)。
实施例72:(S)-N-(3-(2-(反式-3-羟基-2-甲基氮杂环丁烷-1-基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
实施例73:(S)-N-(3-(2-(顺式-3-羟基-2-甲基氮杂环丁烷-1-基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将1-[4-碘-6-(吗啉-4-基)吡啶-2-基]-2-甲基氮杂环丁烷-3-醇(170mg,0.453mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(205mg,0.498mmol)、Pd(dppf)Cl2.CH2Cl2(37mg,0.045mmol)、Na2CO3(144mg,1.359mmol)、1,4-二噁烷(4mL)和H2O(1mL)的混合物在60℃下搅拌16h。将反应混合物冷却至室温,并且减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EA/EtOH(12/3/1)洗脱。将粗产物通过制备型HPLC采用以下条件纯化:柱:制备型C18OBD柱,19×150mm 5um 10nm;流动相A:水(0.5%TFA),流动相B:乙腈;流速:20mL/min;梯度:在4.3min内35%-50%B;得到呈浅黄色固体的(S)-N-(3-(2-(反式-3-羟基-2-甲基氮杂环丁烷-1-基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(73mg,30%)。MS ESI:C27H34F3N5O3[M+H]+的计算值:534.26,实测值:534.25。1H NMR(400MHz,DMSO-d6)δ8.12(s,1H),7.43-7.41(m,1H),7.32-7.31(m,1H),7.11-7.09(m,1H),5.90(s,1H),5.54(s,1H),5.38-5.37(m,1H),4.47-4.45(m,1H),4.32-4.29(m,1H),4.00-3.96(m,1H),3.69-3.63(m,6H),3.52-3.50(m,1H),3.40-3.30(m,5H),3.04-2.99(m,1H),2.52-2.41(m,3H),2.15-2.08(m,4H),1.66-1.65(m,1H),1.32(d,J=6.8Hz,3H)。19F NMR(376MHz,DMSO-d6)δ-63.36(3F)。
还得到呈浅黄色固体的(S)-N-(3-(2-(顺式-3-羟基-2-甲基氮杂环丁烷-1-基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(24mg,10%)。MS ESI:C27H34F3N5O3[M+H]+的计算值:534.26,实测值:534.25。1H NMR(300MHz,DMSO-d6)δ8.10(s,1H),7.44-7.40(m,1H),7.32-7.31(m,1H),7.11-7.08(m,1H),5.96(s,1H),5.60(s,1H),5.38-5.37(m,1H),4.08-3.94(m,2H),3.89-3.85(m,1H),3.76-3.65(m,5H),3.54-3.49(m,2H),3.39-3.25(m,5H),3.04-3.00(m,1H),2.49-2.42(m,3H),2.15-2.05(m,4H),1.71-1.61(m,1H),1.42(d,J=6.3Hz,3H)。19F NMR(376MHz,DMSO-d6)δ-63.12(3F)。
实施例74:(3S)-N-[4-甲基-3-[2-(吗啉-4-基)-6-[[(2S)-1,1,1-三氟-3-羟基丙烷-2-基]氨基]吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例74A:(2S)-3,3,3-三氟-2-[(6-氟-4-碘吡啶-2-基)氨基]丙-1-醇
在室温下,向2,6-二氟-4-碘吡啶(300mg,1.245mmol)和(2S)-2-氨基-3,3,3-三氟丙-1-醇(209mg,1.618mmol)在DMSO(4mL)中的搅拌混合物中加入K2CO3(516mg,3.735mmol)。将所得混合物在70℃下搅拌2h。将所得混合物用EtOAc(3x100mL)萃取。将合并的有机层用盐水(3x100mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用含EtOAc的PE(0%至30%)洗脱,得到呈白色固体的(2S)-3,3,3-三氟-2-[(6-氟-4-碘吡啶-2-基)氨基]丙-1-醇(20mg,5%)。MS ESI:C8H7F4IN2O[M+H]+的计算值:350.95,实测值:350.95。1H NMR(300MHz,氯仿-d)δ6.80(s,1H),6.68(d,J=2.7Hz,1H),5.15(d,J=9.5Hz,1H),4.90-4.74(m,1H),4.07(dd,J=12.0,3.7Hz,1H)。
制备例74B:(2S)-3,3,3-三氟-2-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丙-1-醇
在室温下,向(2S)-3,3,3-三氟-2-[(6-氟-4-碘吡啶-2-基)氨基]丙-1-醇(20mg,0.057mmol)和吗啉(5mg,0.063mmol)在DMSO(2mL)中的搅拌溶液中加入K2CO3(24mg,0.171mmol)。将所得混合物在70℃下搅拌16h。使混合物冷却至室温。将所得混合物用水(20mL)稀释,并且用EtOAc(3x30mL)萃取。将合并的有机层用盐水(3x30mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。残余物通过制备型TLC(PE/EtOAc=2/1)纯化,得到呈白色固体的(2S)-3,3,3-三氟-2-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丙-1-醇(10mg,17%)。MS ESI:C12H15F3IN3O2[M+H]+的计算值:418.02,实测值:417.85。1H NMR(300MHz,氯仿-d)δ6.55(d,J=8.9Hz,2H),4.54(dd,J=11.2,3.9Hz,1H),4.36-4.25(m,1H),3.88-3.74(m,4H),3.66(d,J=3.9Hz,1H),3.54-3.38(m,4H)。
实施例74:(3S)-N-[4-甲基-3-[2-(吗啉-4-基)-6-[[(2S)-1,1,1-三氟-3-羟基丙烷-2-基]氨基]吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在室温下,向(2S)-3,3,3-三氟-2-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丙-1-醇(20mg,0.048mmol)和(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(21mg,0.053mmol)、二噁烷(1mL)和H2O(0.25mL)的搅拌混合物中加入Pd(dppf)Cl2.CH2Cl2(4mg,0.005mmol)和Na2CO3(15mg,0.144mmol)。将所得混合物在60℃和氮气氛下搅拌16h。将所得混合物真空浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱。残余物通过制备型TLC(PE/EA/EtOH=8/3/1)纯化,得到呈白色固体的(3S)-N-[4-甲基-3-[2-(吗啉-4-基)-6-[[(2S)-1,1,1-三氟-3-羟基丙烷-2-基]氨基]吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(7mg,15%)。MS ESI:C26H31F6N5O3[M+H]+的计算值:575.23,实测值:575.56。1H NMR(400MHz,DMSO-d6)δ8.12(s,1H),7.42(dd,J=8.2,2.4Hz,1H),7.36(d,J=2.3Hz,1H),7.10(d,J=8.4Hz,1H),6.70(d,J=9.0Hz,1H),5.94(d,J=1.0Hz,1H),5.88(d,J=1.0Hz,1H),5.12(t,J=5.7Hz,1H),4.99-4.88(m,1H),3.77-3.62(m,J=6.2Hz,7H),3.52(t,J=2.1Hz,1H),3.47-3.34(m,5H),3.02(t,J=9.4Hz,1H),2.49-2.34(m,3H),2.16(s,3H),2.12-2.05(m,1H),1.73-1.59(m,1H)。19F NMR(376MHz,DMSO-d6)δ-64.96(3F),-73.37(3F)。
实施例75:(3S)-N-[3-[2-(2-羟基-2-甲基丙酰胺基)-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例75A:乙酸1-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基甲酰基]-1-甲基乙酯
在室温下,向4-碘-6-(吗啉-4-基)吡啶-2-胺(250mg,0.819mmol)和乙酸1-氯-2-甲基-1-氧代丙烷-2-基酯(202mg,1.229mmol)在DCM(3mL)中的搅拌混合物中加入TEA(248mg,2.458mmol)。将反应混合物在室温下搅拌6h。将所得混合物用水(20mL)稀释。将所得混合物用EtOAc(3x20mL)萃取。将合并的有机层用盐水(2x30mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩,得到呈黄色固体的乙酸1-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基甲酰基]-1-甲基乙酯(400mg,粗物质)。MS ESI:的计算值:C15H20IN3O4[M+H]+,434.05,实测值:434.00.
制备例75B:2-羟基-N-[4-碘-6-(吗啉-4-基)吡啶-2-基]-2-甲基丙酰胺
在室温下,向乙酸1-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基甲酰基]-1-甲基乙酯(370mg,0.854mmol)在MeOH(4mL)中的搅拌混合物中加入K2CO3(354mg,2.562mmol)。将反应混合物在室温下搅拌16h。将所得混合物用水(30mL)稀释。将所得混合物用EtOAc(3x40mL)萃取。将合并的有机层用盐水(3x40mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。残余物通过反相色谱法纯化,用含65%至80%CH3CN的水(含0.5%NH4HCO3)洗脱。收集含有所需产物的级分,并且减压浓缩,得到呈灰白色固体的2-羟基-N-[4-碘-6-(吗啉-4-基)吡啶-2-基]-2-甲基丙酰胺(180mg,53%)。MS ESI:C13H18IN3O3[M+H]+的计算值:392.04,实测值:391.95;1H NMR(400MHz,DMSO-d6)δ9.09(s,1H),7.81(d,J=1.0Hz,1H),6.96(d,J=1.1Hz,1H),6.03(s,1H),3.66(dd,J=5.8,3.9Hz,4H),3.43(dd,J=5.7,3.9Hz,4H),1.34(s,6H)。
实施例75:(3S)-N-[3-[2-(2-羟基-2-甲基丙酰胺基)-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
向2-羟基-N-[4-碘-6-(吗啉-4-基)吡啶-2-基]-2-甲基丙酰胺(130mg,0.332mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(164mg,0.399mmol)和K2CO3(137mg,0.997mmol)在二噁烷(2mL)和H2O(0.5mL)中的搅拌混合物中加入Pd(dppf)Cl2.CH2Cl2(27mg,0.033mmol)。将反应混合物在80℃和N2氛下搅拌2h。将所得混合物用水(20mL)稀释。将所得混合物用EtOAc(3x30mL)萃取。将合并的有机层用盐水(2x30mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用EA中的45%PE洗脱。收集含有所需产物的级分,并且减压浓缩。粗物质通过反相色谱法纯化,用含CH3CN的水(含10mmol/mL NH4HCO3)洗脱。收集含有所需产物的级分,并且减压浓缩,得到呈白色固体的(3S)-N-[3-[2-(2-羟基-2-甲基丙酰胺基)-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(138mg,73%)。MS ESI:C27H34F3N5O4[M+H]+的计算值:550.26,实测值:550.25;1H NMR(400MHz,DMSO-d6)δ9.16(s,1H),8.18(s,1H),7.49(dd,J=8.3,2.3Hz,1H),7.40(dd,J=6.3,1.6Hz,2H),7.15(d,J=8.4Hz,1H),6.49(d,J=1.1Hz,1H),6.03(s,1H),3.73-3.63(m,5H),3.58-3.43(m,5H),3.33-3.26(m,1H),3.03(t,J=9.4Hz,1H),2.49-2.33(m,3H),2.18(s,3H),2.08(q,J=4.5,3.8Hz,1H),1.66(dq,J=11.9,9.7Hz,1H),1.35(s,6H)。
实施例76:(3S)-N-[2-氟-5-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例76A:2-氟-4-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯胺
将5-溴-2-氟-4-甲基苯胺(50g,245.048mmol)、4,4,5,5-四甲基-2-(四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)-1,3,2-二氧杂硼杂环戊烷(75g,294.057mmol)、KOAc(72g,735.143mmol,)和Pd(dppf)Cl2.CH2Cl2(10g,12.252mmol)在1,4-二噁烷(600mL)中的混合物在100℃和氩气氛下搅拌16h。将所得混合物减压浓缩。将残余物通过硅胶柱色谱法纯化,用含EtOAc的PE(0~30%)洗脱,得到呈灰白色固体的2-氟-4-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯胺(57g,93%)。MS ESI:C13H19BFNO2[M+H]+的计算值:252.15,实测值:252.10。
制备例76B:(3S)-N-[2-氟-4-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在室温和氮气氛下,将2-氟-4-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯胺(2.00g,7.965mmol,1.00当量)、DIEA(5.15g,0.040mmol,5当量)和三光气(0.95g,0.003mmol,0.4当量)在THF(19mL)中的混合物搅拌30min。向以上混合物中加入(3S)-3-(2,2,2-三氟乙基)吡咯烷盐酸盐(1.51g,0.008mmol,1.00当量)。将所得混合物在室温下再搅拌3h。将所得混合物真空浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc/EtOH(4/3/1)洗脱,得到呈灰白色固体的(3S)-N-[2-氟-4-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(3.2g,75%)。MSESI:C20H27BF4N2O3[M+H]+的计算值:431.21,实测值:431.25。1H NMR(400MHz,氯仿-d)δ8.38(d,J=9.3Hz,1H),6.88(dd,J=12.3,0.8Hz,1H),6.20(d,J=3.2Hz,1H),3.83(dd,J=9.9,7.5Hz,1H),3.67-3.63(m,1H),3.46(td,J=9.7,6.8Hz,1H),3.13(t,J=9.5Hz,1H),2.66-2.51(m,1H),2.46(s,3H),2.35-2.17(m,3H),1.78-1.74(m,1H),1.33(s,12H)。
实施例76:(3S)-N-[2-氟-5-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在室温和氮气氛下,向(2R)-2-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丙-1-醇(130mg,0.358mmol)和(3S)-N-[2-氟-4-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(154mg,0.358mmol)在1,4-二噁烷(2mL)和H2O(0.4mL)中的搅拌溶液中加入Na2CO3(113mg,1.074mmol)和Pd(dppf)Cl2.CH2Cl2(29mg,0.036mmol)。将所得混合物在60℃和氮气氛下搅拌16h。使混合物冷却至室温。在室温下通过添加水(20mL)来猝灭反应。将所得混合物用EtOAc(3x20mL)萃取。将合并的有机层用盐水(3x20mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈浅黄色固体的(3S)-N-[2-氟-5-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(105mg,54%)。MS ESI:C26H33F4N5O3[M+H]+的计算值:540.25,实测值:540.15。1H NMR(400MHz,DMSO-d6)δ7.86(s,1H),7.29(d,J=8.3Hz,1H),7.10(d,J=11.7Hz,1H),5.99(d,J=7.5Hz,1H),5.77-5.71(m,2H),4.64(t,J=5.6Hz,1H),3.92-3.84(m,1H),3.67(dd,J=5.7,3.9Hz,5H),3.57-3.44(m,2H),3.41-3.32(m,5H),3.03(t,J=9.4Hz,1H),2.51-2.35(m,3H),2.20(s,3H),2.13-2.05(m,1H),1.74-1.62(m,1H),1.24(s,1H),1.12(d,J=6.6Hz,3H)。19F NMR(376MHz,DMSO-d6)δ-63.39(3F),-125.64(1F)。
实施例77:N-[2-氟-5-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)-2,5-二氢吡咯-1-甲酰胺
制备例77A:(2R)-2-[[4-(5-氨基-4-氟-2-甲基苯基)-6-(吗啉-4-基)吡啶-2-基]氨基]丙-1-醇
在室温和氮气氛下,向(2R)-2-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丙-1-醇(200mg,0.551mmol)和2-氟-4-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯胺(138mg,0.551mmol)在1,4-二噁烷(2mL)和H2O(0.4mL)中的搅拌溶液中加入Na2CO3(175mg,1.652mmol)和Pd(dppf)Cl2CH2Cl2(45mg,0.055mmol)。将所得混合物在80℃和氮气氛下搅拌1h。使混合物冷却至室温。在室温下通过添加水(20mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc/EtOH(6/3/1)洗脱,得到呈灰白色固体的(2R)-2-[[4-(5-氨基-4-氟-2-甲基苯基)-6-(吗啉-4-基)吡啶-2-基]氨基]丙-1-醇(140mg,38%)。MS ESI:C19H25FN4O2[M+H]+的计算值:361.20,实测值:361.15。1H NMR(300MHz,氯仿-d)δ6.88(d,J=11.9Hz,1H),6.64(d,J=9.2Hz,1H),5.81(d,J=14.5Hz,2H),4.08(s,1H),3.88-3.73(m,5H),3.68-3.53(m,3H),3.49(s,4H),2.17(s,3H),1.25(d,J=6.7Hz,3H)。19F NMR(282MHz,氯仿-d)δ-136.65。
实施例77:N-[2-氟-5-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)-2,5-二氢吡咯-1-甲酰胺
将(2R)-2-[[4-(5-氨基-4-氟-2-甲基苯基)-6-(吗啉-4-基)吡啶-2-基]氨基]丙-1-醇(60mg,0.166mmol)、DIEA(0.14mL,1.084mmol)和三光气(20mg,0.067mmol)在THF(6mL)中的混合物在室温下搅拌30min。在室温下,向以上混合物中加入3-(2,2,2-三氟乙基)-2,5-二氢-1H-吡咯盐酸盐(31mg,0.166mmol)。将所得混合物在室温下再搅拌3h。将所得混合物真空浓缩。将残余物通过硅胶柱色谱法纯化,用(PE/EtOAc/EtOH=8/3/1)洗脱,得到混合物。将残余物通过反相快速色谱法采用以下条件纯化:柱,C18硅胶;流动相,含CH3CN的水(0.1%NH4HCO3),在20min内10%至50%梯度;检测器,UV 254nm,得到呈白色固体的N-[2-氟-5-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)-2,5-二氢吡咯-1-甲酰胺(5mg,6%)。MS ESI:C26H31F4N5O3[M+H]+的计算值:538.24,实测值:538.05。1H NMR(400MHz,DMSO-d6)δ7.97(s,1H),7.31(d,J=8.3Hz,1H),7.11(d,J=11.7Hz,1H),5.99(d,J=7.5Hz,1H),5.93(s,1H),5.77-5.72(m,2H),4.64(t,J=5.5Hz,1H),4.20(s,4H),3.94-3.85(m,1H),3.67(t,J=4.7Hz,4H),3.53-3.45(m,1H),3.37(t,J=4.9Hz,4H),3.28(d,J=13.8Hz,3H),2.21(s,3H),1.12(d,J=6.6Hz,3H)。19FNMR(376MHz,DMSO-d6)δ-66.30(3F),-125.50(1F)。
实施例78:(3S)-N-[3-[2-(2,5-二氢呋喃-3-基)-6-[[(2R)-1-羟基丙烷-2-基]氨基]吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
向(3S)-N-[3-(2-氯-6-[[(2R)-1-羟基丙烷-2-基]氨基]吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(500mg,1.062mmol)和2-(2,5-二氢呋喃-3-基)-4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷(416mg,2.124mmol)在1,4-二噁烷(6mL)和H2O(0.6mL)中的搅拌混合物中加入Pd(dppf)Cl2.CH2Cl2(87mg,0.106mmol)和Na2CO3(338mg,3.185mmol)。将所得混合物在80℃和氮气氛下搅拌2h。将所得混合物减压浓缩。将残余物通过硅胶柱色谱法纯化,用(PE/EtOAc/EtOH=12/3/1)洗脱。将残余物通过反相快速色谱法采用以下条件纯化:柱:球形C18,20-40um,120g;流动相A:水(5mM NH4HCO3);流动相B:CH3CN;流速:50mL/min;梯度:在30min内35%-55%B;检测器:220nm。在46%B下收集含有所需产物的级分,并且减压浓缩,得到呈白色固体的(3S)-N-[3-[2-(2,5-二氢呋喃-3-基)-6-[[(2R)-1-羟基丙烷-2-基]氨基]吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(320mg,60%)。MS ESI:C26H31F3N4O3[M+H]+的计算值:505.23,实测值:505.25。1HNMR(300MHz,DMSO-d6)δ8.16(s,1H),7.54-7.33(m,2H),7.14(d,J=8.4Hz,1H),6.67-6.56(m,2H),6.32(t,J=2.0Hz,2H),4.91(td,J=5.0,2.1Hz,2H),4.75(td,J=5.1,2.1Hz,3H),4.05-3.86(m,1H),3.75-3.61(m,1H),3.52(dt,J=8.8,2.5Hz,2H),3.36(s,2H),3.03(t,J=9.3Hz,1H),2.49-2.31(m,3H),2.17(s,3H),2.14-2.03(m,1H),1.68(d,J=10.4Hz,1H),1.15(d,J=6.6Hz,3H)。19F NMR(376MHz,DMSO-d6)δ-63.363(3F)。
实施例79:(3S)-N-[3-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-(氧杂环戊烷-3-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
向(3S)-N-[3-[2-(2,5-二氢呋喃-3-基)-6-[[(2R)-1-羟基丙烷-2-基]氨基]吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(100mg,0.198mmol)在MeOH(5mL)中的搅拌混合物中加入Pd/C(21mg,0.198mmol)。将所得混合物在室温和氢气氛下搅拌16h。过滤所得混合物。将滤饼用MeOH(3x20mL)洗涤。将滤液减压浓缩。将残余物通过反相快速色谱法采用以下条件纯化:柱:球形C18,20-40um,120g;流动相A:水(加5mmol/mLNH4HCO3);流动相B:CH3CN;流速:60mL/min;梯度:在25min内35%-55%B;检测器:220nm。在48%B下收集含有所需产物的级分,并且减压浓缩,得到呈白色固体的(3S)-N-[3-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-(氧杂环戊烷-3-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(79mg,79%)。MS ESI:C26H33F3N4O3[M+H]+的计算值:507.25,实测值:507.30。1H NMR(300MHz,DMSO-d6)δ8.13(s,1H),7.44(dd,J=8.3,2.3Hz,1H),7.37(d,J=2.3Hz,1H),7.12(d,J=8.3Hz,1H),6.33(d,J=1.3Hz,1H),6.30-6.17(m,2H),4.73(t,J=5.5Hz,1H),4.03(t,J=7.8Hz,1H),3.99-3.61(m,5H),3.60-3.43(m,2H),3.40-3.34(m,3H),3.03(t,J=9.3Hz,1H),2.44(t,J=10.1Hz,3H),2.25-2.00(m,6H),1.66(p,J=9.8Hz,1H),1.15(d,J=6.5Hz,3H)。19F NMR(376MHz,DMSO-d6)δ-63.360(3F)。
实施例80:(3S)-N-[3-(2-[[(2S)-1-羟基丙烷-2-基]氨基]-6-(1H-吡唑-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例80A:(2S)-2-[(6-氯-4-碘吡啶-2-基)氨基]丙-1-醇
在室温下,向2,6-二氯-4-碘吡啶(5.00g,18.256mmol)和K2CO3(5.05g,36.540mmol)在NMP(100mL)中的搅拌溶液中加入(2S)-2-氨基丙-1-醇(1.37g,18.256mmol)。将所得混合物在150℃下搅拌2h。通过添加水(1200mL)来猝灭反应。将所得混合物用EtOAc(3x1000mL)萃取。将合并的有机层用饱和盐水(2x500mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(2/1)洗脱,得到呈黄色油状物的(2S)-2-[(6-氯-4-碘吡啶-2-基)氨基]丙-1-醇(1.3g,23%)。MS ESI:C8H10ClIN2O[M+H]+的计算值:312.95,实测值:313.05。1H NMR(400MHz,氯仿-d)δ7.05(s,1H),6.97(s,1H),4.02-3.94(m,1H),3.78-3.74(m,1H),3.63-3.58(m,1H),1.26(d,J=10.8Hz,3H)。
制备例80B:(3S)-N-[3-(2-氯-6-[[(2S)-1-羟基丙烷-2-基]氨基]吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将(2S)-2-[(6-氯-4-碘吡啶-2-基)氨基]丙-1-醇(300mg,0.960mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(395mg,0.960mmol)、Pd(dppf)Cl2.CH2Cl2(78mg,0.096mmol)和Na2CO3(305mg,2.880mmol)在二噁烷(3mL)和H2O(0.75mL)中的混合物在60℃和氮气氛下搅拌16h。在室温下通过添加水(50mL)来猝灭反应。将所得混合物用EtOAc(2x100mL)萃取。将合并的有机层用盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用(PE/EtOAc/EtOH=8/3/1)洗脱,得到呈棕色固体的(3S)-N-[3-(2-氯-6-[[(2S)-1-羟基丙烷-2-基]氨基]吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(410mg,85%)。.MS ESI:C22H26ClF3N4O2[M+H]+的计算值:471.17,实测值:471.20。1H NMR(400MHz,氯仿-d)δ7.31-7.30(m,1H),7.19-7.16(m,1H),6.57(s,1H),6.27-6.23(m,2H),4.77(s,1H),4.13-3.81(m,1H),3.79-3.74(m,2H),3.67-3.58(m,2H),3.49-3.40(m,1H),3.15-3.09(m,1H),2.57-2.55(m,1H),2.34-2.24(m,5H),1.82-1.72(m,1H),1.31-1.25(m,3H)。
制备例80C:(3S)-N-[3-(2-氯-6-[[(2S)-1-羟基丙烷-2-基]氨基]吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将(3S)-N-[3-(2-氯-6-[[(2S)-1-羟基丙烷-2-基]氨基]吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(300mg,0.637mmol)、1-(氧杂环己烷-2-基)-4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)吡唑(354mg,1.274mmol)、Pd(dppf)Cl2.CH2Cl2(52mg,0.064mmol)和Cs2CO3(622mg,1.911mmol)在二噁烷(3mL)和H2O(0.3mL)中的混合物在80℃和氮气氛下搅拌2h。在室温下通过添加水(50mL)来猝灭反应。将所得混合物用EtOAc(3x100mL)萃取。将合并的有机层用盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用(PE/EtOAc/EtOH=8/3/1)洗脱,得到呈浅棕色固体的(3S)-N-[3-(2-[[(2S)-1-羟基丙烷-2-基]氨基]-6-[1-(氧杂环己烷-2-基)吡唑-4-基]吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(330mg,79%)。MS ESI:C30H37F3N6O3[M+H]+的计算值:587.29,实测值:587.30。1H NMR(300MHz,氯仿-d)δ8.22(s,1H),7.95(s,1H),7.40-7.36(m,2H),7.21-7.19(m,1H),6.79(s,1H),6.28-6.26(m,2H),5.43-5.39(m,1H),4.18-4.07(m,2H),3.85-3.84(m,1H),3.81-3.62(m,5H),3.50-3.41(m,1H),3.16-3.10(m,1H),2.57(m,1H),2.34-2.26(m,3H),2.10-2.07(m,2H),1.82-1.62(m,6H),1.31-1.26(m,3H)。19F NMR(282MHz,氯仿-d)δ-64.58-65.56(3F)。
实施例80:(3S)-N-[3-(2-[[(2S)-1-羟基丙烷-2-基]氨基]-6-(1H-吡唑-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在0℃下,向(3S)-N-[3-(2-[[(2S)-1-羟基丙烷-2-基]氨基]-6-[1-(氧杂环己烷-2-基)吡唑-4-基]吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(330mg,0.563mmol)在MeOH(3mL)和THF(4mL)中的搅拌混合物中逐滴加入含HCl(气体)的1,4-二噁烷(1mL)。将所得混合物在室温下搅拌30min。在0℃下通过添加饱和NaHCO3(水性)(10mL)来猝灭反应。将所得混合物用EtOAc(2x20mL)萃取。将合并的有机层用盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过反相快速色谱法采用以下条件纯化:流动相A:水(10mmol/L NH4HCO3),流动相B:CH3CN;流速:20mL/min;梯度:在20min内40B至65B。这产生呈灰白色固体的(3S)-N-[3-(2-[[(2S)-1-羟基丙烷-2-基]氨基]-6-(1H-吡唑-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(168mg,59%)。MS ESI:C25H29F3N6O2[M+H]+的计算值:503.23;实测值:503.30。1H NMR(400MHz,DMSO-d6)δ12.91(s,1H),8.19-8.15(m,2H),7.98(s,1H),7.48-7.40(m,2H),7.15-7.13(m,1H),6.75(s,1H),6.23-6.21(m,2H),4.89-4.86(m,1H),4.03-4.00(m,1H),3.70-3.65(m,1H),3.58-3.51(m,2H),3.38-3.28(m,3H),3.05-3.00(m,1H),2.53-2.50(m,2H),2.20(s,3H),2.15-2.05(m,1H),1.75-1.55(m,1H),1.20(s,3H)。19F NMR(282MHz,DMSO-d6)δ-63.36(3F)。
实施例81:(3S)-N-[3-(6-[[(2R)-1-羟基丙烷-2-基]氨基]-[2,4'-联吡啶]-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在室温下,向(3S)-N-[3-(2-氯-6-[[(2R)-1-羟基丙烷-2-基]氨基]吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(150mg,0.319mmol)、吡啶-4-基硼酸(58mg,0.478mmol)和K2CO3(88mg,0.637mmol)在二噁烷(2mL)和H2O(0.5mL)中的搅拌混合物中加入Pd(PPh3)4(37mg,0.032mmol)。将反应混合物在80℃和氮气氛下搅拌2h。将所得混合物用水(50mL)稀释。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用盐水(2x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用(EA/PE/EtOH=12/3/1)洗脱。收集含有所需产物的级分,并且减压浓缩。残余物通过反相色谱法纯化,用含CH3CN的水(含10mmol/mL NH4HCO3)洗脱。收集含有所需产物的级分,并且减压浓缩,得到呈白色固体的(3S)-N-[3-(6-[[(2R)-1-羟基丙烷-2-基]氨基]-[2,4'-联吡啶]-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(141mg,86%)。MS ESI:C27H30F3N5O2[M+H]+的计算值:514.24,实测值:514.20;1H NMR(400MHz,DMSO-d6)δ8.67-8.61(m,2H),8.18(s,1H),8.06-8.00(m,2H),7.52-7.43(m,2H),7.20-7.13(m,2H),6.60(d,J=7.6Hz,1H),6.51(d,J=1.1Hz,1H),4.76(t,J=5.6Hz,1H),4.16(p,J=6.4Hz,1H),3.67(dd,J=10.2,6.9Hz,1H),3.63-3.48(m,2H),3.40(dt,J=10.4,6.0Hz,1H),3.32-3.27(m,1H),3.03(t,J=9.4Hz,1H),2.48-2.36(m,3H),2.22(s,3H),2.09(h,J=6.3Hz,1H),1.66(p,J=9.8Hz,1H),1.21(d,J=6.6Hz,3H)。19F NMR(282MHz,DMSO-d6)δ-63.37(3F)。
实施例82:(3S)-N-[3-(2'-氨基-6-[[(2R)-1-羟基丙烷-2-基]氨基]-[2,4'-联吡啶]-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
向(3S)-N-[3-(2-氯-6-[[(2R)-1-羟基丙烷-2-基]氨基]吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(150mg,0.319mmol)、4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)吡啶-2-胺(84mg,0.382mmol)和K2CO3(88mg,0.637mmol)在二噁烷(2ml)和H2O(0.5ml)中的搅拌混合物中加入Pd(PPh3)4(37mg,0.032mmol)。将反应混合物在80℃和N2氛下搅拌2h。将所得混合物用水(40mL)稀释。将所得混合物用EtOAc(3x40mL)萃取。将合并的有机层用盐水(3x40mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用(EA/PE/EtOH=12/3/1)洗脱。收集含有所需产物的级分,并且减压浓缩。残余物通过反相色谱法纯化,用含CH3CN的水(含10mmol/mL NH4HCO3)洗脱。收集含有所需产物的级分,并且减压浓缩,得到呈白色固体的(3S)-N-[3-(2'-氨基-6-[[(2R)-1-羟基丙烷-2-基]氨基]-[2,4'-联吡啶]-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(101mg,58%)。MS ESI:C27H31F3N6O2[M+H]+的计算值:529.25,实测值:529.30;1H NMR(400MHz,DMSO-d6)δ8.17(s,1H),7.95(dd,J=5.2,0.8Hz,1H),7.51-7.42(m,2H),7.19-7.07(m,3H),6.90(d,J=1.2Hz,1H),6.51-6.44(m,2H),5.91(s,2H),4.75(t,J=5.5Hz,1H),4.14(p,J=6.4Hz,1H),3.67(dd,J=10.2,6.9Hz,1H),3.59-3.50(m,2H),3.40(dt,J=10.4,5.9Hz,1H),3.29(d,J=6.7Hz,1H),3.03(t,J=9.4Hz,1H),2.49-2.36(m,3H),2.21(s,3H),2.13-2.05(m,1H),1.66(p,J=10.1Hz,1H),1.20(d,J=6.6Hz,3H)。
实施例83:(3S)-N-[3-(2'-氰基-6-[[(2R)-1-羟基丙烷-2-基]氨基]-[2,4'-联吡啶]-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
向4-氯吡啶-2-甲腈(0.50g,3.61mmol)和双(频哪醇合)二硼(1.83g,7.21mmol)在1,4-二噁烷(10mL)中的溶液中加入AcOK(1.06g,10.83mmol)和Pd(dppf)Cl2(0.53g,0.72mmol)。在100℃和氮气氛下搅拌2h之后。在室温和氮气氛下,向以上溶液中加入(3S)-N-[3-(2-氯-6-[[(2R)-1-羟基丙烷-2-基]氨基]吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(0.30g,0.65mmol)、4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)吡啶-2-甲腈(0.30g,1.30mmol)、H2O(0.4mL)、Pd(PPh3)4(0.07mg,0.06mmol)和K2CO3(0.18g,1.30mmol)。在80℃下搅拌2h之后。将所得混合物减压浓缩。残余物通过制备型TLC纯化,用(PE/EtOAc/EtOH=12/3/1)洗脱。将残余物通过反相快速色谱法采用以下条件纯化:柱:球形C18,20-40um,120g;流动相A:水(加5mmol/mL NH4HCO3);流动相B:CH3CN;流速:80mL/min;梯度:在25min内38%-60%B梯度;检测器:220nm。在54%B下收集含有所需产物的级分,得到呈浅黄色固体的(3S)-N-[3-(2-氰基-6-[[(2R)-1-羟基丙烷-2-基]氨基]-[2,4-联吡啶]-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(0.12g,33%)。MS ESI:C28H29F3N6O2[M+H]+的计算值:539.23,实测值:539.10。1H NMR(400MHz,DMSO-d6)δ8.81(dd,J=5.2,0.8Hz,1H),8.67(dd,J=1.8,0.8Hz,1H),8.40(dd,J=5.2,1.8Hz,1H),8.19(s,1H),7.52-7.44(m,2H),7.34(d,J=1.1Hz,1H),7.18(d,J=8.2Hz,1H),6.71(d,J=7.6Hz,1H),6.57(d,J=1.1Hz,1H),4.76(t,J=5.6Hz,1H),4.18(p,J=6.4Hz,1H),3.68(dd,J=10.2,6.9Hz,1H),3.63-3.48(m,2H),3.39(dt,J=10.4,6.1Hz,1H),3.30(dd,J=10.0,6.7Hz,1H),3.03(t,J=9.4Hz,1H),2.51-2.34(m,3H),2.22(s,3H),2.09(d,J=10.3Hz,1H),1.66(p,J=9.7Hz,1H),1.22(d,J=6.6Hz,3H)。19F NMR(376MHz,DMSO-d6)δ-63.367(3F)。
实施例84和85:(3S)-N-[3-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-[(1R,6S)-3-氧杂双环[4.1.0]庚烷-6-基]吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺,(3S)-N-[3-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-[(1S,6R)-3-氧杂双环[4.1.0]庚烷-6-基]吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例84A:2,4-二氯-6-(3,6-二氢-2H-吡喃-4-基)吡啶
在室温和氮气氛下,向2,4,6-三氯吡啶(5.00g,27.41mmol)、2-(3,6-二氢-2H-吡喃-4-基)-4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷(5.76g,27.41mmol)和K2CO3(7.58g,54.82mmol)在DME/EtOH/H2O=2/1/2(50mL)中的搅拌溶液中加入Pd(PPh3)2Cl2(0.96g,1.37mmol)。将所得混合物在80℃和氮气氛下搅拌16h。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用饱和盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(2/1)洗脱,得到呈灰白色固体的2,4-二氯-6-(3,6-二氢-2H-吡喃-4-基)吡啶(2.77g,44%)。MSESI:C10H9Cl2NO[M+H]+的计算值:230.01,实测值:229.90。1H NMR(300MHz,氯仿-d)δ7.26-7.25(m,1H),7.23-7.22(m,1H),6.86-6.82(m,1H),4.40-4.37(m,2H),3.95-3.91(m,2H),2.60-2.54(m,2H)。
制备例84B:2,4-二氯-6-[3-氧杂双环[4.1.0]庚烷-6-基]吡啶
在0℃和氮气氛下,分数份向三甲基碘化亚砜(7.65g,34.77mmol)在DMSO(20mL)中的搅拌溶液中加入NaH(1.40g,35.03mmol,60%)。将所得混合物在室温和氮气氛下搅拌30min。在室温下,向以上混合物中加入2,4-二氯-6-(3,6-二氢-2H-吡喃-4-基)吡啶(2.00g,8.69mmol)。将所得混合物在60℃下再搅拌16h。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用饱和盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(4/1)洗脱,得到呈灰白色固体的2,4-二氯-6-[3-氧杂双环[4.1.0]庚烷-6-基]吡啶(1.7g,80%)。MS ESI:C11H11Cl2NO[M+H]+的计算值:244.02,实测值:243.95。1H NMR(300MHz,氯仿-d)δ7.14-7.13(m,2H),4.04-3.93(m,2H),3.68-3.61(m,1H),3.50-3.41(m,1H),2.49-2.41(m,1H),2.15-2.06(m,1H),1.82-1.75(m.1H),1.36-1.32(m,1H),1.15-1.11(m,1H)。
制备例84C:(2R)-2-[(4-氯-6-[3-氧杂双环[4.1.0]庚烷-6-基]吡啶-2-基)氨基]丙-1-醇
在室温和氮气氛下,向2,4-二氯-6-[3-氧杂双环[4.1.0]庚烷-6-基]吡啶(1.40g,5.73mmol)和(R)-(-)-2-氨基-1-丙醇(0.86g,11.47mmol)在DMSO(15mL)中的搅拌溶液中逐滴加入DIEA(1.48g,11.47mmol)。将所得混合物在130℃和氮气氛下搅拌16h。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用饱和盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过反相快速色谱法采用以下条件纯化:柱,C18硅胶;流动相,含CH3CN的水(0.1%TFA),在40min内5%至95%梯度;检测器,UV 254nm;得到呈灰白色固体的(2R)-2-[(4-氯-6-[3-氧杂双环[4.1.0]庚烷-6-基]吡啶-2-基)氨基]丙-1-醇(0.21g,13%)。MS ESI:C14H19ClN2O2[M+H]+的计算值:283.11,实测值:283.20。1H NMR(300MHz,DMSO-d6)δ6.44-6.42(m,2H),6.31(m,1H),4.65(s,1H),3.91-3.74(m,3H),3.50-3.36(m,3H),3.29-3.22(m,1H),2.42-2.34(m,1H),1.92-1.83(m,1H),1.67-1.61(m,1H),1.22-1.19(m,1H),1.09-1.07(m,3H),0.90-0.85(m,1H)。
制备例84D:(3S)-N-[3-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-[3-氧杂双环[4.1.0]庚烷-6-基]吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在室温和氮气氛下,向(2R)-2-[(4-氯-6-[3-氧杂双环[4.1.0]庚烷-6-基]吡啶-2-基)氨基]丙-1-醇(310mg,1.096mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(452mg,1.096mmol)和K3PO4(465mg,2.193mmol)在THF/H2O=10/1(4mL)中的搅拌溶液中加入XPhos Pd G2(86mg,0.110mmol)。将所得混合物在80℃和氮气氛下搅拌16h。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用饱和盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用(PE/EA/EtOH=8/3:1)洗脱,得到呈浅黄色固体的(3S)-N-[3-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-[3-氧杂双环[4.1.0]庚烷-6-基]吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(350mg,60%)。MS ESI:C28H35F3N4O3[M+H]+的计算值:533.27,实测值:533.15。1H NMR(300MHz,DMSO-d6)δ8.14(s,1H),7.46-7.43(m,1H),7.37-7.36(m,1H),7.14-7.11(m,1H),6.34(s,1H),6.19(m,2H),4.70(m,1H),3.97-3.92(m,2H),3.82-3.78(m,1H),3.71-3.65(m,1H),3.57-3.47(m,3H),3.42-3.35(m,2H),3.31-3.28(m,1H),3.06-3.00(m,1H),2.24(m,3H),2.17-2.10(m,4H),2.00-1.89(m,1H),1.74-1.63(m,3H),1.28-1.27(m,1H),1.15-1.12(m,3H),0.93-0.88(m,1H)。19F NMR(282MHz,DMSO-d6)δ-63.36(3F)。
实施例84和85:(3S)-N-[3-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-[(1R,6S)-3-氧杂双环[4.1.0]庚烷-6-基]吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺,(3S)-N-[3-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-[(1S,6R)-3-氧杂双环[4.1.0]庚烷-6-基]吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
粗产物((3S)-N-[3-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-[3-氧杂双环[4.1.0]庚烷-6-基]吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(350mg,0.657mmol)通过手性制备型HPLC采用以下条件进行拆分:(柱:CHIRAL ART纤维素-SB,2*25cm,5um;流动相A:Hex(0.5%2M NH3-MeOH)--HPLC,流动相B:EtOH--HPLC;流速:20mL/min;梯度:在19min内20B至20B;254/220nm)。第一峰提供了呈灰白色固体的(3S)-N-[3-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-[(1R,6S)-3-氧杂双环[4.1.0]庚烷-6-基]吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(139mg,40%)。MS ESI:C28H35F3N4O3[M+H]+的计算值:533.27,实测值:533.20。1H NMR(400MHz,DMSO-d6)δ8.12(s,1H),7.45-7.35(m,2H),7.12-7.10(m,1H),6.33-6.32(m,1H),6.17-6.14(m,2H),4.69-4.65(m,1H),3.95-3.90(m,2H),3.80-3.77(m,1H),3.69-3.63(m,1H),3.52-3.45(m,3H),3.38-3.34(m,2H),3.31-3.25(m,1H),3.04-2.99(m,1H),2.46-2.40(m,3H),2.15-2.05(m,4H),1.96-1.87(m,1H),1.73-1.63(m,3H),1.26-1.22(m,1H),1.13-1.10(m,3H),0.90-0.88(m,1H)。19F NMR(376MHz,DMSO-d6)δ-63.36(3F)。
第二峰提供了呈灰白色固体的(3S)-N-[3-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-[(1S,6R)-3-氧杂双环[4.1.0]庚烷-6-基]吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(150mg,43%)。MS ESI:C28H35F3N4O3[M+H]+的计算值:533.27,实测值:533.20。1H NMR(400MHz,DMSO-d6)δ8.12(s,1H),7.44-7.35(m,2H),7.12-7.10(m,1H),6.33(m,1H),6.17-6.15(m,2H),4.70-4.66(m,1H),3.95-3.90(m,2H),3.80-3.77(m,1H),3.69-3.63(m,1H),3.52-3.45(m,3H),3.38-3.35(m,2H),3.31-3.28(m,1H),3.04-2.99(m,1H),2.46-2.40(m,3H),2.15-2.07(m,4H),1.96-1.87(m,1H),1.73-1.63(m,3H),1.26-1.22(m,1H),1.13-1.11(m,3H),0.90-0.87(m,1H)。19F NMR(376MHz,DMSO-d6)δ-63.35(3F)。
实施例86:(3S)-N-[3-(2-[[(2R)-2,3-二羟基丙基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例86A:(2R)-3-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丙烷-1,2-二醇
在氮气氛下,向4-(6-氟-4-碘吡啶-2-基)吗啉(600mg,1.947mmol)和(2R)-3-氨基丙烷-1,2-二醇(266mg,2.921mmol)在DMSO(6mL)中的搅拌溶液中加入DIEA(1mL,7.874mmol)。将所得混合物在80℃和氮气氛下搅拌16h。将所得混合物减压浓缩。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用(EA/PE/EtOH=12/3/1)洗脱,得到呈浅黄色固体的(2R)-3-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丙烷-1,2-二醇(350mg,47%)。MS ESI:C12H18IN3O3[M+H]+的计算值:380.19,实测值:380.00。1H NMR(400MHz,氯仿-d)δ6.258-6.21(m,2H),4.70(s,1H),3.89-3.80(m,1H),3.80-3.74(m,4H),3.67-3.55(m,2H),3.67-3.55(m,2H),3.42-3.36(m,4H)。
实施例86:(3S)-N-[3-(2-[[(2R)-2,3-二羟基丙基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
向(2R)-3-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丙烷-1,2-二醇(200mg,0.527mmol)和(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(217mg,0.527mmol)在1,4-二噁烷(2mL)和H2O(0.4mL)中的搅拌溶液中加入Na2CO3(167mg,1.582mmol)和Pd(dppf)Cl2.CH2Cl2(43mg,0.053mmol)。将所得混合物在60℃和氮气氛下搅拌16h。使混合物冷却至室温。在室温下通过添加水(50mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用(EtOAc/PE/EtOH=12/3/1)洗脱,得到呈灰白色固体的(3S)-N-[3-(2-[[(2R)-2,3-二羟基丙基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(186mg,66%)。MS ESI:C26H34F3N5O4[M+H]+的计算值:537.26,实测值:537.26。1HNMR(400MHz,DMSO-d6)δ8.11(s,1H),7.45-7.38(m,1H),7.33(d,J=2.4Hz,1H),7.09(d,J=8.4Hz,1H),6.17(d,J=6.1Hz,1H),5.81-5.74(m,2H),4.80(d,J=4.8Hz,1H),4.53(t,J=5.7Hz,1H),3.71-3.58(m,6H),3.57-3.48(m,1H),3.44-3.25(m,8H),3.19-3.08(m,1H),3.02(t,J=9.4Hz,1H),2.51-2.34(m,3H),2.16(s,3H),2.08(d,J=6.9Hz,1H),1.73-1.58(m,1H)。19F NMR(376MHz,DMSO-d6)δ-63.24(3F)。
实施例87:(3S)-N-[3-(2-[[(2S)-2,3-二羟基丙基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例87A:(2S)-3-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丙烷-1,2-二醇
向4-(6-氟-4-碘吡啶-2-基)吗啉(600mg,1.947mmol)和3-氨基丙烷-1,2-二醇(266mg,2.921mmol)在DMSO(6mL)中的搅拌溶液中加入DIEA(1mL,5.841mmol)。将所得混合物在80℃下搅拌16h。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈浅黄色固体的(2S)-3-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丙烷-1,2-二醇(400mg,54%)。MS ESI:C12H18IN3O3[M+H]+的计算值:380.19,实测值:380.05。1H NMR(400MHz,氯仿-d)δ6.30-6.23(m,2H),4.72(t,J=6.1Hz,1H),3.91-3.82(m,1H),3.82-3.75(m,4H),3.69-3.57(m,2H),3.57-3.45(m,2H),3.45-3.38(m,4H)。
实施例87:(3S)-N-[3-(2-[[(2S)-2,3-二羟基丙基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在室温和氮气氛下,向(2S)-3-[[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基]丙烷-1,2-二醇(200mg,0.527mmol)和(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(217mg,0.527mmol)在1,4-二噁烷(2mL)和H2O(0.4mL)中的搅拌溶液中加入Na2CO3(168mg,1.582mmol)和Pd(dppf)Cl2.CH2Cl2(43mg,0.053mmol)。将所得混合物在60℃和氮气氛下搅拌16h。使混合物冷却至室温。在室温下通过添加水(50mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用(PE/EtOAc/EtOH=12/3/1)洗脱,得到呈浅粉红色固体的(3S)-N-[3-(2-[[(2S)-2,3-二羟基丙基]氨基]-6-(吗啉-4-基)吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(178mg,63%)。MS ESI:C26H34F3N5O4[M+H]+的计算值:538.26,实测值:538.10。1H NMR(400MHz,DMSO-d6)δ8.10(s,1H),7.44-7.37(m,1H),7.33(d,J=2.4Hz,1H),7.09(d,J=8.6Hz,1H),6.17(s,1H),5.81-5.74(m,2H),4.79(d,J=4.7Hz,1H),4.52(t,J=5.7Hz,1H),3.70-3.59(m,6H),3.52(t,J=8.5Hz,1H),3.43-3.33(m,7H),3.18-3.07(m,1H),3.01(t,J=9.4Hz,1H),2.44(d,J=11.2Hz,1H),2.40(s,3H),2.15(s,3H),2.12-2.04(m,1H),1.72-1.58(m,1H)。19F NMR(376MHz,DMSO-d6)δ-63.36(3F)。
实施例88和89:(3S)-N-[3-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-[(1S,5R)-3-氧杂双环[3.1.0]己烷-1-基]吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺,(3S)-N-[3-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-[(1R,5S)-3-氧杂双环[3.1.0]己烷-1-基]吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例88A:2,4-二氯-6-(2,5-二氢呋喃-3-基)吡啶
向2,4,6-三氯吡啶(5.50g,30.15mmol)、2-(2,5-二氢呋喃-3-基)-4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷(5.91g,30.15mmol)和K2CO3(8.38g,60.60mmol)在DME/EtOH/H2O=2/1/2(60mL)中的搅拌溶液中加入Pd(PPh3)2Cl2(1.06g,1.51mmol)。将所得混合物在80℃和氮气氛下搅拌16h。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用饱和盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(2/1)洗脱,得到呈灰白色固体的2,4-二氯-6-(2,5-二氢呋喃-3-基)吡啶(2.55g,39%)。MS ESI:C9H7Cl2NO[M+H]+的计算值:215.99,实测值:215.95。1H NMR(300MHz,氯仿-d)δ7.26-7.23(m,2H),6.74-6.71(m,1H),5.07-5.03(m,2H),3.93-3.89(m,2H)。
制备例88B:2,4-二氯-6-[3-氧杂双环[3.1.0]己烷-1-基]吡啶
在0℃下,分数份向三甲基碘化亚砜(10.39g,47.21mmol)在DMSO(30mL)中的搅拌溶液中加入NaH(1.89g,47.25mmol)。将所得混合物在室温和氮气氛下搅拌30min。向以上混合物中加入2,4-二氯-6-(2,5-二氢呋喃-3-基)吡啶(2.55g,11.80mmol)。将所得混合物在60℃下再搅拌16h。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用饱和盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(4/1)洗脱,得到呈灰白色固体的2,4-二氯-6-[3-氧杂双环[3.1.0]己烷-1-基]吡啶(2.28g,84%)。MS ESI:C10H9Cl2NO[M+H]+的计算值:230.01,实测值:229.95。1H NMR(300MHz,氯仿-d)δ7.18-7.17(m,1H),6.97-6.96(m,1H),4.14(s,2H),3.95-3.86(m,2H),2.21-2.16(m,1H),1.46-1.42(m,1H),1.28-1.19(m,1H)。
制备例88C:(2R)-2-[(4-氯-6-[3-氧杂双环[3.1.0]己烷-1-基]吡啶-2-基)氨基]丙-1-醇
在室温下,向2,4-二氯-6-[3-氧杂双环[3.1.0]己烷-1-基]吡啶(2.28g,9.91mmol)和(R)-(-)-2-氨基-1-丙醇(1.49g,19.82mmol)在DMSO(25mL)中的搅拌溶液中逐滴加入DIEA(2.56g,19.82mmol)。将所得混合物在130℃下搅拌16h。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用饱和盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过反相快速色谱法采用以下条件纯化:柱,C18硅胶;流动相,含CH3CN的水(0.1%TFA),在40min内5%至95%梯度;检测器,UV 254nm;得到呈灰白色固体的(2R)-2-[(4-氯-6-[3-氧杂双环[3.1.0]己烷-1-基]吡啶-2-基)氨基]丙-1-醇(0.38g,14%)。MS ESI:C13H17ClN2O2[M+H]+的计算值:269.10,实测值:269.00。1H NMR(300MHz,氯仿-d)δ6.38-6.36(m,1H),6.31-6.30(m,1H),4.72(s,1H),4.09(s,2H),4.04-3.84(m,3H),3.78-3.73(m,1H),3.61-3.54(m,1H),2.14-2.07(m,1H),1.38-1.31(m,1H),1.28-1.24(m,4H),1.11-1.07(m,1H)。
制备例88D:(3S)-N-[3-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-[3-氧杂双环[3.1.0]己烷-1-基]吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在室温和氮气氛下,向(2R)-2-[(4-氯-6-[3-氧杂双环[3.1.0]己烷-1-基]吡啶-2-基)氨基]丙-1-醇(380mg,1.414mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(583mg,1.414mmol)和K3PO4(600mg,2.828mmol)在THF/H2O=10/1(4mL)中的搅拌溶液中加入XPhos Pd G2(111mg,0.141mmol)。将所得混合物在80℃和氮气氛下搅拌16h。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用饱和盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用(EA/PE/EtOH=8/3/1)洗脱,得到呈浅黄色固体的(3S)-N-[3-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-[3-氧杂双环[3.1.0]己烷-1-基]吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(420mg,57%)。MS ESI:C27H33F3N4O3[M+H]+的计算值:519.25,实测值:519.25。1H NMR(300MHz,氯仿-d)δ7.31-7.29(m,1H),7.19-7.16(m,1H),6.34-6.32(m,1H),6.24-6.22(m,2H),4.59(s,1H),4.18-4.04(m,3H),3.93-3.75(m,4H),3.67-3.55(m,2H),3.49-3.40(m,1H),3.15-3.08(m,1H),2.62-2.49(m,1H),2.34-2.11(m,7H),1.81-1.68(m,2H),1.40-1.30(m,1H),1.27-1.24(m,3H),1.09-1.05(m,1H)。19F NMR(282MHz,氯仿-d)δ-64.94(3F)。
实施例88和89:(3S)-N-[3-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-[(1S,5R)-3-氧杂双环[3.1.0]己烷-1-基]吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺,(3S)-N-[3-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-[(1R,5S)-3-氧杂双环[3.1.0]己烷-1-基]吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
粗产物((3S)-N-[3-(2-[[(2R)-1-羟基丙烷-2-基]氨基]-6-[3-氧杂双环[3.1.0]己烷-1-基]吡啶-4-基)-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(420mg,0.810mmol)通过手性制备型HPLC采用以下条件纯化:(柱:CHIRAL ART纤维素-SB,30*250mm,5um;流动相A:CO2,流动相B:IPA(0.5%2M NH3-MeOH);流速:80mL/min;梯度:40%B;220nm)。第一峰提供了169mg(40%),呈灰白色固体。MS ESI:C27H33F3N4O3[M+H]+的计算值:519.25,实测值:519.10。1H NMR(400MHz,氯仿-d)δ7.28(m,1H),7.17-7.14(m,1H),6.31-6.30(m,1H),6.21-6.19(m,2H),4.99-4.56(m,2H),4.09-4.02(m,3H),3.91-3.73(m,4H),3.62-3.53(m,2H),3.44-3.40(m,1H),3.13-3.07(m,1H),2.60-2.49(m,1H),2.32-2.09(m,7H),1.80-1.67(m,2H),1.39-1.35(m,1H),1.24-1.22(m,3H),1.08-1.05(m,1H)。19F NMR(376MHz,氯仿-d)δ-64.95(3F)。
第二峰提供了119mg(28%),呈灰白色固体。MS ESI:C27H33F3N4O3[M+H]+的计算值:519.25,实测值:519.10。1H NMR(400MHz,氯仿-d)δ7.31-7.30(m,1H),7.20-7.17(m,1H),6.35(m,1H),6.25-6.19(m,2H),4.63(m,2H),4.11-4.04(m,3H),3.94-3.75(m,4H),3.64-3.56(m,2H),3.47-3.43(m,1H),3.19-3.10(m,1H),2.58-2.55(m,1H),2.32-2.14(m,7H),1.83-1.72(m,2H),1.35-1.31(m,1H),1.28-1.24(m,3H),1.09-1.06(m,1H)。19F NMR(376MHz,氯仿-d)δ-64.95(3F)。
实施例90和91:(S)-N-(3-(6-(((R)-2-羟基丙基)氨基)-2-吗啉基嘧啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺和(R)-N-(3-(6-(((R)-2-羟基丙基)氨基)-2-吗啉基嘧啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
步骤1:在-20℃下,向2,4,6-三氯嘧啶(4.00g,21.85mmol)在EtOH(70mL)中的搅拌溶液中加入(R)-1-氨基丙-2-醇(1.63g,21.85mmol)和DIEA(2.82g,21.85mmol)。将反应混合物在-20℃下搅拌20min。将所得混合物用水(150mL)稀释,并且用EA(300mL x 3)萃取。将合并的有机层用盐水(100mL x 4)洗涤,经无水Na2SO4干燥并过滤。将滤液减压浓缩。残余物通过FCC(PE:EA=5:1)纯化,得到呈灰白色固体的(R)-1-((2,6-二氯嘧啶-4-基)氨基)丙-2-醇(2.30g,48%)。MS计算值:221,MS实测值:222([M+H]+)。
步骤2:在室温下,向(R)-1-((2,6-二氯嘧啶-4-基)氨基)丙-2-醇(1.00g,4.52mmol)在DMSO(5mL)中的搅拌溶液中加入吗啉(396mg,4.52mmol)和DIEA(875mg,6.78mmol)。将反应混合物在50℃下搅拌16h。将所得混合物冷却至室温,用水(10mL)稀释并用EA(10mL x 3)萃取。将合并的有机层用盐水(5mL x 4)洗涤,经无水Na2SO4干燥并过滤。将滤液减压浓缩。残余物通过FCC(PE:EA=1:2)纯化,得到呈白色固体的(R)-1-((6-氯-2-吗啉基嘧啶-4-基)氨基)丙-2-醇(1.07g,86%)。MS计算值:272,MS实测值:273([M+H]+)。
步骤3:在室温和氮气氛下,向(R)-1-((6-氯-2-吗啉基嘧啶-4-基)氨基)丙-2-醇(600mg,2.20mmol)、N-(4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(996mg,2.42mmol)和Cs2CO3(1.79g,2.49mmol)在二噁烷(40mL)和水(4mL)中的溶液中加入Pd(dppf)Cl2(80mg,0.11mmol)。将反应混合物在100℃下搅拌过夜。将混合物冷却至室温,过滤并浓缩。残余物通过手性制备型SFC(柱:Chiralpak IG 5μm*20*250mm;流动相:CO2:EtOH=70:30,在50g/min下;温度:40℃;波长:214nm,背压:100bar)纯化,得到183.8mg(16%),RT=7.13min,ee>98%),1H NMR(400MHz,DMSO-d6):δ8.13(s,1H),7.49(d,J=2.4Hz,1H),7.42(dd,J=2.0,8.4Hz,1H),7.07(d,J=8.4Hz,2H),5.90(s,1H),4.71(br s,1H),3.80-3.79(m,1H),3.69-3.63(m,9H),3.55-3.50(m,1H),3.34-3.20(m,3H),3.02(t,J=9.2Hz,1H),2.49-2.38(m,3H),2.25(s,3H),2.09-2.07(m,1H),1.68-1.63(m,1H),1.08(d,J=6.4Hz,3H),以及196.7mg,(17%),RT=6.31min,ee>98%),1H NMR(400MHz,DMSO-d6):δ8.13(s,1H),7.49(d,J=2.4Hz,1H),7.42(dd,J=2.4,8.4Hz,1H),7.08-7.03(m,2H),5.90(s,1H),4.71(d,J=4.0Hz,1H),3.81-3.78(m,1H),3.69-3.63(m,9H),3.55-3.50(m,1H),3.34-3.20(m,3H),3.02(t,J=9.2Hz,1H),2.49-2.38(m,3H),2.25(s,3H),2.09-2.07(m,1H),1.68-1.63(m,1H),1.08(d,J=6.4Hz,3H)。MS计算值:522,MS实测值:523([M+H]+)。
实施例92:(S)-N-(3-(2-(((R)-2-羟基丙基)氨基)-6-吗啉基嘧啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
步骤1:在-50℃和氮气氛下,向4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯胺(3.80g,16.31mmol)和DIEA(10.5g,81.50mmol)在THF(100mL)中的溶液中加入BTC(1.9g,6.40mmol)。将混合物在-50℃下搅拌30min。接着将(S)-3-(2,2,2-三氟乙基)吡咯烷盐酸盐(3.1g,16.40mmol)加入至混合物中,在-50℃下再搅拌1h。将残余物浓缩,并且通过FCC(PE:EA=1:1)纯化,得到呈白色固体的(S)-N-(4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(3.85g,57%)。MS计算值:412,MS实测值:413([M+H]+)。
步骤2:在-20℃下,向2,4,6-三氯嘧啶(5.00g,27.47mmol)在EtOH(70mL)中的搅拌溶液中加入吗啉(2.39g,27.47mmol)和DIEA(3.51g,27.47mmol)。将反应混合物在-20℃下搅拌0.5h。将所得混合物用水(150mL)稀释,并且用EA(300mL x 3)萃取。将合并的有机层用盐水(100mL x 4)洗涤,经无水Na2SO4干燥并过滤。将滤液减压浓缩。残余物通过FCC(PE:EA=10:1)纯化,得到呈灰白色固体的4-(4,6-二氯嘧啶-2-基)吗啉(1.13g,17%)和4-(2,6-二氯嘧啶-4-基)吗啉(3.58g,54%)。MS计算值:233,MS实测值:234([M+H]+)。
步骤3:在室温下,向4-(2,6-二氯嘧啶-2-基)吗啉(600mg,2.36mmol)在DMSO(5mL)中的搅拌溶液中加入(R)-1-氨基丙-2-醇(250mg,3.33mmol)和DIEA(496mg,3.84mmol)。将反应混合物在70℃下搅拌16h。将所得混合物冷却至室温,用水(10mL)稀释并用EA(10mL x3)萃取。将合并的有机层用盐水(5mL x 4)洗涤,经无水Na2SO4干燥并过滤。将滤液减压浓缩。残余物通过FCC(PE:EA=1:1)纯化,得到呈白色固体的(R)-1-((4-氯-6-吗啉基嘧啶-2-基)氨基)丙-2-醇(400mg,57%)。MS计算值:272,MS实测值:273([M+H]+)。
步骤4:在室温和氮气氛下,向(R)-1-((4-氯-6-吗啉基嘧啶-2-基)氨基)丙-2-醇(33mg,0.12mmol)、(S)-N-(4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(50mg,0.12mmol)和Cs2CO3(98mg,0.30mmol)在二噁烷(10mL)和水(2mL)中的溶液中加入Pd(dppf)Cl2(9mg,0.012mmol)。将反应混合物在100℃下搅拌16h。将混合物冷却至室温,过滤并浓缩。残余物通过制备型HPLC纯化,得到呈白色固体的(S)-N-(3-(2-(((R)-2-羟基丙基)氨基)-6-吗啉基嘧啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(21mg,33%)。1H NMR(400MHz,DMSO-d6):δ8.12(s,1H),7.45-7.43(m,2H),7.07(dd,J=3.6,4.8Hz,1H),6.40(s,1H),6.02(s,1H),4.76-4.71(m,1H),3.76-3.50(m,12H),3.29-3.14(m,2H),3.02(t,J=9.2Hz,1H),2.46-2.33(m,3H),2.24(s,3H),2.11-2.07(m,1H),1.70-1.63(m,1H),1.04(d,J=6.0Hz,3H)。MS计算值:522,MS实测值:523([M+H]+)。
实施例93:(S)-N-(3-(6-(((S)-2-羟基丙基)氨基)-2-吗啉基嘧啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
步骤1:在室温下,向4-(4,6-二氯嘧啶-2-基)吗啉(300mg,1.28mmol)在DMSO(5mL)中的搅拌溶液中加入(S)-1-氨基丙-2-醇(96mg,1.28mmol)和DIEA(248mg,1.92mmol)。将反应混合物在70℃下搅拌16h。将所得混合物冷却至室温,用水(10mL)稀释并用EA(10mL x 3)萃取。将合并的有机层用盐水(5mL x 4)洗涤,经无水Na2SO4干燥并过滤。将滤液减压浓缩。残余物通过FCC(PE:EA=1:1)纯化,得到呈白色固体的(S)-1-((6-氯-2-吗啉基嘧啶-4-基)氨基)丙-2-醇(200mg,57%)。MS计算值:272,MS实测值:273([M+H]+)。
步骤2:在室温和氮气氛下,向(S)-1-((6-氯-2-吗啉基嘧啶-4-基)氨基)丙-2-醇(33mg,0.12mmol)、(S)-N-(4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(50mg,0.12mmol)和Cs2CO3(98mg,0.30mmol)在二噁烷(10mL)和水(2mL)中的溶液中加入Pd(dppf)Cl2(4mg,0.006mmol)。将反应混合物在100℃下搅拌16h。将混合物冷却至室温,过滤并浓缩。残余物通过制备型HPLC纯化,得到呈白色固体的(S)-N-(3-(6-(((S)-2-羟基丙基)氨基)-2-吗啉基嘧啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(15.7mg,24%)。1H NMR(400MHz,DMSO-d6):δ8.13(d,J=1.6Hz,1H),7.49(d,J=2.4Hz,1H),7.42(dd,J=2.0,8.0Hz,1H),7.08-7.05(m,2H),5.90(s,1H),4.70(d,J=4.4Hz,1H),3.81-3.78(m,1H),3.69-3.63(m,9H),3.55-3.50(m,1H),3.29-3.24(m,3H),3.02(t,J=9.2Hz,1H),2.49-2.38(m,3H),2.25(s,3H),2.10-2.07(m,1H),1.68-1.63(m,1H),1.07(d,J=6.0Hz,3H)。MS计算值:522,MS实测值:523([M+H]+)。
实施例94:(S)-N-(3-(6-((2-羟基乙基)氨基)-2-吗啉基嘧啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
步骤1:在室温下,向4-(4,6-二氯嘧啶-2-基)吗啉(300mg,1.28mmol)在DMSO(5mL)中的搅拌溶液中加入2-氨基乙醇(102mg,1.17mmol)和DIEA(248mg,1.92mmol)。将反应混合物在70℃下搅拌16h。将所得混合物冷却至室温,用水(10mL)稀释并用EA(10mL x 3)萃取。将合并的有机层用盐水(5mL x 4)洗涤,经无水Na2SO4干燥并过滤。将滤液减压浓缩。残余物通过FCC(PE:EA=1:1)纯化,得到呈白色固体的2-((6-氯-2-吗啉基嘧啶-4-基)氨基)乙醇(325mg,98%)。MS计算值:258,MS实测值:259([M+H]+)。
步骤2:在室温和氮气氛下,向2-((6-氯-2-吗啉基嘧啶-4-基)氨基)乙醇(31mg,0.12mmol)、(S)-N-(4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(50mg,0.12mmol)和Cs2CO3(98mg,0.30mmol)在二噁烷(10mL)和水(2mL)中的溶液中加入Pd(dppf)Cl2(9mg,0.012mmol)。将反应混合物在100℃下搅拌16h。将混合物冷却至室温,过滤并浓缩。残余物通过制备型HPLC纯化,得到呈白色固体的(S)-N-(3-(6-((2-羟基乙基)氨基)-2-吗啉基嘧啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(17mg,27.4%)。1H NMR(400MHz,DMSO-d6):δ8.13(s,1H),7.49(d,J=2.4Hz,1H),7.42(dd,J=2.0,8.8Hz,1H),7.07(d,J=8.4Hz,1H),5.88(s,1H),4.69(t,J=5.2Hz,1H),3.69-3.63(m,9H),3.55-3.51(m,3H),3.36-3.27(m,3H),3.02(t,J=9.6Hz,1H),2.49-2.38(m,3H),2.25(s,3H),2.09-2.07(m,1H),1.68-1.63(m,1H)。MS计算值:508,MS实测值:509([M+H]+)。
实施例95:(S)-N-(3-(6-(((S)-1-羟基丙烷-2-基)氨基)-2-吗啉基嘧啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
步骤1:在室温下,向4-(4,6-二氯嘧啶-2-基)吗啉(300mg,1.28mmol)在DMSO(5mL)中的搅拌溶液中加入(S)-2-氨基丙-1-醇(125mg,1.66mmol)和DIEA(248mg,1.92mmol)。将反应混合物在70℃下搅拌16h。将所得混合物用水(10mL)稀释,并且用EA(10mL x 3)萃取。将合并的有机层用盐水(5mL x 4)洗涤,经无水Na2SO4干燥并过滤。将滤液减压浓缩。残余物通过FCC(PE:EA=1:1)纯化,得到呈白色固体的(S)-2-((6-氯-2-吗啉基嘧啶-4-基)氨基)丙-1-醇(270mg,77%)。MS计算值:272,MS实测值:273([M+H]+)。
步骤2:在室温和氮气氛下,向(S)-2-((6-氯-2-吗啉基嘧啶-4-基)氨基)丙-1-醇(33mg,0.12mmol)、(S)-N-(4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(50mg,0.12mmol)和Cs2CO3(98mg,0.30mmol)在二噁烷(10mL)和水(2mL)中的溶液中加入Pd(dppf)Cl2(4mg,0.006mmol)。将反应混合物在100℃下搅拌16h。将混合物冷却至室温,过滤并浓缩。残余物通过制备型HPLC纯化,得到呈白色固体的(S)-N-(3-(6-(((S)-1-羟基丙烷-2-基)氨基)-2-吗啉基嘧啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(11.4mg,18%)。1H NMR(400MHz,DMSO-d6):δ8.12(s,1H),7.50(s,1H),7.41(d,J=8.4Hz,1H),7.08-6.81(m,2H),5.85(s,1H),4.70-4.69(m,1H),4.03(br s,1H),3.69-3.63(m,9H),3.55-3.45(m,1H),3.38-3.27(m,3H),3.02(t,J=9.2Hz,1H),2.49-2.38(m,3H),2.26(s,3H),2.10-2.07(m,1H),1.68-1.63(m,1H),1.13(d,J=6.8Hz,3H)。MS计算值:522,MS实测值:523([M+H]+)。
实施例96:(S)-N-(3-(6-((2-羟基-2-甲基丙基)氨基)-2-吗啉基嘧啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
步骤1:在室温下,向4-(4,6-二氯嘧啶-2-基)吗啉(200mg,0.85mmol)在DMSO(5mL)中的搅拌溶液中加入1-氨基-2-甲基丙-2-醇(91mg,1.03mmol)和DIEA(165mg,1.28mmol)。将反应混合物在70℃下搅拌16h。将所得混合物用水(10mL)稀释,并且用EA(10mL x 3)萃取。将合并的有机层用盐水(5mL x 4)洗涤,经无水Na2SO4干燥并过滤。将滤液减压浓缩。残余物通过FCC(PE:EA=2:1)纯化,得到呈白色固体的1-((6-氯-2-吗啉基嘧啶-4-基)氨基)-2-甲基丙-2-醇(150mg,61%)。MS计算值:286,MS实测值:287([M+H]+)。
步骤2:在室温和氮气氛下,向1-((6-氯-2-吗啉基嘧啶-4-基)氨基)-2-甲基丙-2-醇(35mg,0.12mmol)、(S)-N-(4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(50mg,0.12mmol)和Cs2CO3(98mg,0.30mmol)在二噁烷(10mL)和水(2mL)中的溶液中加入Pd(dppf)Cl2(4mg,0.006mmol)。将反应混合物在100℃下搅拌16h。将混合物冷却至室温,过滤并浓缩。残余物通过制备型HPLC纯化,得到呈白色固体的(S)-N-(3-(6-((2-羟基-2-甲基丙基)氨基)-2-吗啉基嘧啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(7.9mg,12%)。1H NMR(400MHz,DMSO-d6):δ8.13(s,1H),7.50(d,J=2.0Hz,1H),7.43(dd,J=2.4,8.4Hz,1H),7.08-6.64(m,2H),5.98(s,1H),4.53(s,1H),3.69-3.50(m,10H),3.37-3.23(m,3H),3.02(t,J=9.2Hz,1H),2.46-2.33(m,3H),2.26(s,3H),2.11-2.07(m,1H),1.70-1.60(m,1H),1.07(s,6H)。MS计算值:536,MS实测值:537([M+H]+)。
实施例97:(S)-N-(3-(2-((2-羟基乙基)氨基)-6-吗啉基嘧啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺甲酸盐
步骤1:在室温下,向4-(2,6-二氯嘧啶-4-基)吗啉(500mg,2.14mmol)在DMSO(5mL)中的搅拌溶液中加入2-氨基乙醇(170mg,2.78mmol)和DIEA(415mg,3.21mmol)。将反应混合物在70℃下搅拌12h。将所得混合物用水(10mL)稀释,并且用EA(10mL x 3)萃取。将合并的有机层用盐水(5mL x 4)洗涤,经无水Na2SO4干燥并过滤。将滤液减压浓缩。残余物通过FCC(PE:EA=2:1)纯化,得到呈白色固体的2-((4-氯-6-吗啉基嘧啶-2-基)氨基)乙醇(360mg,65%)。MS计算值:258,MS实测值:259([M+H]+)。
步骤2:在室温和氮气氛下,向2-((4-氯-6-吗啉基嘧啶-2-基)氨基)乙醇(32mg,0.12mmol)、(S)-N-(4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(50mg,0.12mmol)和Cs2CO3(98mg,0.30mmol)在二噁烷(10mL)和水(2mL)中的溶液中加入Pd(dppf)Cl2(9mg,0.012mmol)。将反应混合物在100℃下搅拌16h。将混合物冷却至室温,过滤并浓缩。残余物通过制备型HPLC纯化,得到呈黄色固体的(S)-N-(3-(2-((2-羟基乙基)氨基)-6-吗啉基嘧啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺甲酸盐(15.8mg,25%)。1H NMR(400MHz,DMSO-d6):δ8.17(s,1H),8.12(s,1H),7.45-7.43(m,2H),7.07(d,J=9.2Hz,1H),6.43(br s,1H),6.02(s,1H),4.62(br,0.5H),3.69-3.64(m,5H),3.54-3.46(m,7H),3.41-3.30(m,3H),3.02(t,J=9.2Hz,1H),2.46-2.36(m,3H),2.24(s,3H),2.10-2.07(m,1H),1.68-1.63(m,1H)。MS计算值:508,MS实测值:509([M+H]+)。
实施例98:(S)-N-(3-(2-(((R)-1-羟基丙烷-2-基)氨基)-6-吗啉基嘧啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
步骤1:在室温下,向4-(2,6-二氯嘧啶-4-基)吗啉(500mg,2.14mmol)在DMSO(5mL)中的搅拌溶液中加入(R)-2-氨基丙-1-醇(210mg,2.78mmol)和DIEA(415mg,3.21mmol)。将反应混合物在70℃下搅拌12h。将所得混合物冷却至室温,用水(10mL)稀释并用EA(10mL x3)萃取。将合并的有机层用盐水(5mL x 4)洗涤,经无水Na2SO4干燥并过滤。将滤液减压浓缩。残余物通过FCC(PE:EA=1:1)纯化,得到呈黄色固体的(R)-2-((4-氯-6-吗啉基嘧啶-2-基)氨基)丙-1-醇(180mg,31%)。MS计算值:272,MS实测值:273([M+H]+)。
步骤2:在室温和氮气氛下,向(R)-2-((4-氯-6-吗啉基嘧啶-2-基)氨基)丙-1-醇(32mg,0.12mmol)、(S)-N-(4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(50mg,0.12mmol)和Cs2CO3(98mg,0.30mmol)在二噁烷(10mL)和水(2mL)中的溶液中加入Pd(dppf)Cl2(9mg,0.012mmol)。将反应混合物在100℃下搅拌16h。将混合物冷却至室温,过滤并浓缩。残余物通过制备型HPLC纯化,得到呈粉红色固体的(S)-N-(3-(2-(((R)-1-羟基丙烷-2-基)氨基)-6-吗啉基嘧啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(4.18mg,6%)。1H NMR(400MHz,DMSO-d6):δ8.12(s,1H),7.46-7.43(m,2H),7.08(d,J=8.0Hz,1H),6.17-6.15(m,1H),6.02(s,1H),4.64(br s,1H),3.98-3.91(m,1H),3.69-3.59(m,5H),3.54-3.43(m,6H),3.31-3.29(m,2H),3.04-2.98(m,1H),2.46-2.32(m,3H),2.25(s,3H),2.10-2.07(m,1H),1.68-1.63(m,1H),1.11(d,J=6.8Hz,3H)。MS计算值:522,MS实测值:523([M+H]+)。
实施例99:(S)-N-(3-(2-((2-羟基-2-甲基丙基)氨基)-6-吗啉基嘧啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
步骤1:在室温下,向4-(2,6-二氯嘧啶-4-基)吗啉(500mg,2.14mmol)在DMSO(5mL)中的搅拌溶液中加入1-氨基-2-甲基丙-2-醇(250mg,2.78mmol)和DIEA(415mg,3.21mmol)。将反应混合物在70℃下搅拌12h。将所得混合物用水(10mL)稀释,并且用EA(10mL x 3)萃取。将合并的有机层用盐水(5mL x 4)洗涤,经无水Na2SO4干燥并过滤。将滤液减压浓缩。残余物通过FCC(PE:EA=1:1)纯化,得到呈黄色固体的1-((4-氯-6-吗啉基嘧啶-2-基)氨基)-2-甲基丙-2-醇(280mg,46%)。MS计算值:286,MS实测值:287([M+H]+)。
步骤2:在室温和氮气氛下,向1-((4-氯-6-吗啉基嘧啶-2-基)氨基)-2-甲基丙-2-醇(39mg,0.12mmol)、(S)-N-(4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(50mg,0.12mmol)和Cs2CO3(98mg,0.30mmol)在二噁烷(10mL)和水(2mL)中的溶液中加入Pd(dppf)Cl2(9mg,0.012mmol)。将反应混合物在100℃下搅拌16h。将混合物冷却至室温,过滤并浓缩。残余物通过制备型HPLC纯化,得到呈黄色固体的(S)-N-(3-(2-((2-羟基-2-甲基丙基)氨基)-6-吗啉基嘧啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(14.3mg,22%)。1H NMR(400MHz,DMSO-d6):δ8.13(s,1H),7.46-7.44(m,2H),7.08(d,J=9.2Hz,1H),6.26(br s,1H),6.03(s,1H),3.69-3.64(m,5H),3.55-3.50(m,5H),3.30-3.25(m,3H),3.02(t,J=9.2Hz,1H),2.48-2.38(m,3H),2.24(s,3H),2.10-2.07(m,1H),1.68-1.65(m,1H),1.04(s,6H)。MS计算值:536,MS实测值:537([M+H]+)。
实施例100:(S)-N-(3-(6-(((R)-1-羟基丙烷-2-基)氨基)-2-吗啉基嘧啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺甲酸盐
步骤1:在室温下,向4-(4,6-二氯嘧啶-2-基)吗啉(300mg,1.28mmol)在DMSO(5mL)中的搅拌溶液中加入(R)-2-氨基丙-1-醇(125mg,1.66mmol)和DIEA(248mg,1.92mmol)。将反应混合物在70℃下搅拌16h。将所得混合物用水(10mL)稀释,并且用EA(10mL x 3)萃取。将合并的有机层用盐水(5mL x 4)洗涤,经无水Na2SO4干燥并过滤。将滤液减压浓缩。残余物通过FCC(PE:EA=1:1)纯化,得到呈白色固体的(R)-2-((6-氯-2-吗啉基嘧啶-4-基)氨基)丙-1-醇(270mg,77%)。MS计算值:272,MS实测值:273([M+H]+)。
步骤2:在室温和氮气氛下,向(R)-2-((6-氯-2-吗啉基嘧啶-4-基)氨基)丙-1-醇(66mg,0.24mmol)、(S)-N-(4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(100mg,0.24mmol)和Cs2CO3(198mg,0.61mmol)在二噁烷(10mL)和水(2mL)中的溶液中加入Pd(dppf)Cl2(9mg,0.012mmol)。将反应混合物在100℃下搅拌16h。将混合物冷却至室温,过滤并浓缩。残余物通过制备型HPLC纯化,得到呈白色固体的(S)-N-(3-(6-(((R)-1-羟基丙烷-2-基)氨基)-2-吗啉基嘧啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺甲酸盐(29.4mg,23%)。1H NMR(400MHz,DMSO-d6):δ8.21(s,0.3H),8.12(s,1H),7.50(d,J=2.4Hz,1H),7.41(dd,J=2.0,8.0Hz,1H),7.06(d,J=4.4Hz,1H),6.82(br s,1H),5.86(s,1H),4.70(br s,1H),3.98(brs,1H),3.69-3.63(m,9H),3.55-3.46(m,2H),3.34-3.27(m,2H),3.02(t,J=9.2Hz,1H),2.49-2.41(m,3H),2.26(s,3H),2.10-2.07(m,1H),1.68-1.63(m,1H),1.13(d,J=6.8Hz,3H)。MS计算值:522,MS实测值:523([M+H]+)。
实施例101:(S)-N-(3-(2-(((S)-1-羟基丙烷-2-基)氨基)-6-吗啉基嘧啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
步骤1:在室温下,向4-(2,6-二氯嘧啶-4-基)吗啉(1.0g,4.28mmol)在DMSO(15mL)中的搅拌溶液中加入(S)-2-氨基丙-1-醇(420mg,5.56mmol)和DIEA(830mg,6.42mmol)。将反应混合物在70℃下搅拌12h。将所得混合物冷却至室温,用水(30mL)稀释并用EA(15mL x3)萃取。将合并的有机层用盐水(15mL x 4)洗涤,经无水Na2SO4干燥并过滤。将滤液减压浓缩。残余物通过FCC(PE:EA=1:1)纯化,得到呈白色固体的(S)-2-((4-氯-6-吗啉基嘧啶-2-基)氨基)丙-1-醇(580mg,50%)。MS计算值:272,MS实测值:273([M+H]+)。
步骤2:在室温和氮气氛下,向(S)-2-((4-氯-6-吗啉基嘧啶-2-基)氨基)丙-1-醇(50mg,0.18mmol)、(S)-N-(4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(75mg,0.18mmol)和Cs2CO3(150mg,0.46mmol)在二噁烷(10mL)和水(2mL)中的溶液中加入Pd(dppf)Cl2(27mg,0.036mmol)。将反应混合物在100℃下搅拌9h。将混合物冷却至室温,过滤并浓缩。残余物通过制备型HPLC纯化,得到呈白色固体的(S)-N-(3-(2-(((R)-1-羟基丙烷-2-基)氨基)-6-吗啉基嘧啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(7.3mg,7.6%)。1H NMR(400MHz,DMSO-d6):δ8.12(s,1H),7.46-7.43(m,2H),7.07(d,J=8.4Hz,1H),6.16(br s,1H),6.01(s,1H),4.63-4.62(m,1H),3.92-3.91(m,1H),3.69-3.64(m,5H),3.59-3.43(m,6H),3.31-3.24(m,2H),3.02(t,J=9.2Hz,1H),2.46-2.32(m,3H),2.25(s,3H),2.11-2.07(m,1H),1.70-1.60(m,1H),1.11(d,J=6.4Hz,3H)。MS计算值:522,MS实测值:523([M+H]+)。
实施例102和103:(R)-N-(3-(2-((S)-3-羟基吡咯烷-1-基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺和(S)-N-(3-(2-((S)-3-羟基吡咯烷-1-基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
步骤1:在室温和氮气氛下,向2,6-二氟-4-碘吡啶(16.00g,66.40mmol)在DMSO(240mL)中的搅拌溶液中加入吗啉(5.49mL,63.04mmol)和DIEA(12.07mL,93.40mmol)。将反应混合物在70℃下搅拌3h。将所得混合物冷却至室温,用水(150mL)稀释并用EA(300mL x3)萃取。将合并的有机层用盐水(100mL x 4)洗涤,经无水Na2SO4干燥,过滤并减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE中的30%EA洗脱,得到呈灰白色固体的4-(6-氟-4-碘吡啶-2-基)吗啉(17.60g,86%)。MS计算值:308,MS实测值:309([M+H]+)。
步骤2:在室温下,向4-(6-氟-4-碘吡啶-2-基)吗啉(600mg,1.95mmol)在DMSO(15mL)中的搅拌溶液中加入(S)-吡咯烷-3-醇(254mg,2.92mmol)和K2CO3(538mg,3.89mmol)。将反应混合物在130℃下搅拌12h。将所得混合物冷却至室温,用水(30mL)稀释并用EA(15mL x 3)萃取。将合并的有机层用盐水(15mL x 4)洗涤,经无水Na2SO4干燥并过滤。将滤液减压浓缩。残余物通过FCC(PE:EA=5:1)纯化,得到呈白色固体的(S)-1-(4-碘-6-吗啉基吡啶-2-基)吡咯烷-3-醇(500mg,68%)。MS计算值:375,MS实测值:376([M+H]+)。
步骤3:在室温和氮气氛下,向(S)-1-(4-碘-6-吗啉基吡啶-2-基)吡咯烷-3-醇(300mg,0.80mmol)、N-(4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(330mg,0.80mmol)和Cs2CO3(650mg,1.99mmol)在二噁烷(40mL)和水(4mL)中的溶液中加入Pd(dppf)Cl2(60mg,0.08mmol)。将反应混合物在80℃下搅拌12h。将混合物冷却至室温,过滤并浓缩。残余物通过手性制备型SFC(柱:Chiralpak IC 5μm*20*250mm;流动相:CO2:MeOH=65:35;温度:40℃;波长:214nm,背压:100bar)纯化,得到呈白色固体的(R)-N-(3-(2-((S)-3-羟基吡咯烷-1-基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(111.4mg,26%,RT=7.31min,ee>98%)和(S)-N-(3-(2-((S)-3-羟基吡咯烷-1-基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(114.6mg,27%,RT=6.45min,ee>98%)。(R)-N-(3-(2-((S)-3-羟基吡咯烷-1-基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺:1H NMR(400MHz,DMSO-d6):δ8.10(s,1H),7.42(dd,J=2.4,8.4Hz,1H),7.33(d,J=2.0Hz,1H),7.10(d,J=8.4Hz,1H),5.83(s,1H),5.63(s,1H),4.88(d,J=4.0Hz,1H),4.35(br s,1H),3.68-3.64(m,5H),3.54-3.39(m,8H),3.29-3.27(m,2H),3.02(t,J=9.2Hz,1H),2.49-2.36(m,3H),2.16(s,3H),2.09-1.95(m,2H),1.87-1.85(m,1H),1.68-1.63(m,1H)。(S)-N-(3-(2-((S)-3-羟基吡咯烷-1-基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺:1H NMR(400MHz,DMSO-d6):δ8.10(s,1H),7.42(dd,J=2.4,8.4Hz,1H),7.33(d,J=2.4Hz,1H),7.10(d,J=8.4Hz,1H),5.83(s,1H),5.63(s,1H),4.88(d,J=3.6Hz,1H),4.35(br s,1H),3.69-3.64(m,5H),3.54-3.39(m,8H),3.29-3.27(m,2H),3.02(t,J=9.2Hz,1H),2.49-2.37(m,3H),2.16(s,3H),2.11-1.96(m,2H),1.87-1.85(m,1H),1.68-1.62(m,1H)。MS计算值:533,MS实测值:534([M+H]+)。
实施例104:(S)-N-(3-(2-(((S)-2-羟基丙基)氨基)-6-吗啉基嘧啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
步骤1:在室温下,向4-(2,6-二氯嘧啶-4-基)吗啉(500mg,2.14mmol)在DMSO(15mL)中的搅拌溶液中加入(S)-1-氨基丙-2-醇(210mg,2.78mmol)和DIEA(400mg,3.21mmol)。将反应混合物在70℃下搅拌12h。将所得混合物冷却至室温,用水(30mL)稀释并用EA(15mL x 3)萃取。将合并的有机层用盐水(15mL x 4)洗涤,经无水Na2SO4干燥并过滤。将滤液减压浓缩。残余物通过FCC(PE:EA=1:1)纯化,得到呈白色固体的(S)-1-((4-氯-6-吗啉基嘧啶-2-基)氨基)丙-2-醇(260mg,45%)。MS计算值:272,MS实测值:273([M+H]+)。
步骤2:在室温和氮气氛下,向(S)-1-((4-氯-6-吗啉基嘧啶-2-基)氨基)丙-2-醇(50mg,0.18mmol)、(S)-N-(4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(75mg,0.18mmol)和Cs2CO3(150mg,0.46mmol)在二噁烷(10mL)和水(2mL)中的溶液中加入Pd(dppf)Cl2(27mg,0.036mmol)。将反应混合物在100℃下搅拌9h。将混合物冷却至室温,过滤并浓缩。残余物通过制备型HPLC纯化,得到呈白色固体的(S)-N-(3-(2-(((S)-2-羟基丙基)氨基)-6-吗啉基嘧啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(7.6mg,8%)。1H NMR(400MHz,DMSO-d6):δ8.12(s,1H),7.45-7.43(m,2H),7.09-7.06(m,1H),6.40-6.37(m,1H),6.02(s,1H),4.74-4.70(m,1H),3.78-3.76(m,1H),3.69-3.64(m,5H),3.55-3.50(m,5H),3.26-3.14(m,3H),3.02(t,J=9.2Hz,1H),2.46-2.38(m,3H),2.24(s,3H),2.10-2.04(m,1H),1.70-1.60(m,1H),1.04(d,J=6.0Hz,3H)。MS计算值:522,MS实测值:523([M+H]+)。
实施例105:(3S)-N-(3-[2-[(3R)-3-氨基吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例105A:N-[(3R)-1-[4-碘-6-(吗啉-4-基)吡啶-2-基]吡咯烷-3-基]氨基甲酸叔丁酯
将4-(6-氟-4-碘吡啶-2-基)吗啉(500mg,1.623mmol)、N-[(3R)-吡咯烷-3-基]氨基甲酸叔丁酯(453mg,2.434mmol)和K2CO3(449mg,3.246mmol)在NMP(5mL)中的混合物在150℃下搅拌2h。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用盐水(3x20mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(5/1)洗脱,得到呈白色固体的N-[(3R)-1-[4-碘-6-(吗啉-4-基)吡啶-2-基]吡咯烷-3-基]氨基甲酸叔丁酯(588mg,76%)。MS ESI:C18H27IN4O3[M+H]+的计算值:475.11;实测值:475.10。1H NMR(400MHz,氯仿-d)δ6.28(d,J=1.2Hz,1H),6.16(d,J=1.2Hz,1H),4.71-4.67(m,1H),4.35-4.25(m,1H),3.82-3.76(m,4H),3.70-3.68(m,1H),3.55-3.44(m,6H),3.34-3.24(m,1H),2.24-2.20(m,1H),1.93-1.91(m,1H),1.47(s,9H)。
制备例105B:N-[(3S)-1-(4-[2-甲基-5-[(3S)-3-(2,2,2-三氟乙基)吡咯烷-1-羰基氨基]苯基]-6-(吗啉-4-基)吡啶-2-基)吡咯烷-3-基]氨基甲酸叔丁酯
将N-[(3S)-1-[4-碘-6-(吗啉-4-基)吡啶-2-基]吡咯烷-3-基]氨基甲酸叔丁酯(173mg,0.364mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(150mg,0.364mmol)、Pd(dppf)Cl2.CH2Cl2(30mg,0.036mmol)和Na2CO3(116mg,1.092mmol)在二噁烷(4mL)和H2O(1mL)中的混合物在60℃和氮气氛下搅拌16h。使混合物冷却至室温。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用盐水(3x20mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。残余物通过采用PE/EtOAc(1/1)的制备型TLC纯化,得到呈浅黄色固体的N-[(3S)-1-(4-[2-甲基-5-[(3S)-3-(2,2,2-三氟乙基)吡咯烷-1-羰基氨基]苯基]-6-(吗啉-4-基)吡啶-2-基)吡咯烷-3-基]氨基甲酸叔丁酯(200mg,87%)。MS ESI:C32H43F3N6O4[M+H]+的计算值:633.33,实测值:633.10。1H NMR(400MHz,氯仿-d)δ7.42-7.41(m,1H),7.19-7.17(m,2H),6.14(s,1H),5.87(s,1H),5.73(s,1H),4.77-4.73(m,1H),4.34-4.32(m,1H),3.85-3.80(m,5H),3.74-3.72(m,1H),3.66-3.63(m,1H),3.57-3.45(m,7H),3.38-3.36(m,1H),3.13-3.11(m,1H),2.56-2.52(m,1H),2.31-2.21(m,7H),1.95-1.93m,1H),1.79-1.71(m,1H),1.47(s,9H)。
实施例105:(3S)-N-(3-[2-[(3R)-3-氨基吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将N-[(3R)-1-(4-[2-甲基-5-[(3S)-3-(2,2,2-三氟乙基)吡咯烷-1-羰基氨基]苯基]-6-(吗啉-4-基)吡啶-2-基)吡咯烷-3-基]氨基甲酸叔丁酯(233mg,0.368mmol)和TFA(1mL)在DCM(5mL)中的混合物在室温下搅拌1h。将反应混合物减压浓缩,并且用饱和NaHCO3碱化至pH 8。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用盐水(3x20mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过反相快速色谱法采用以下条件纯化:柱:C18柱120g;流动相A:水(10mmol/L NH4HCO3),流动相B:CH3CN;流速:60mL/min;梯度:30%B至50%B;254/220nm,得到呈白色固体的(3S)-N-(3-[2-[(3R)-3-氨基吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(94mg,48%)。MS ESI:C27H35F3N6O2[M+H]+的计算值:533.28,实测值:533.40。1H NMR(400MHz,DMSO-d6)δ8.12(s,1H),7.43(dd,J=8.4,2.4Hz,1H),7.34(d,J=2.4Hz,1H),7.10(d,J=8.4Hz,1H),5.83(s,1H),5.61(s,1H),3.72-3.63(m,5H),3.57-3.45(m,4H),3.42-3.26(m,6H),3.03-3.00(m,2H),2.48-2.35(m,3H),2.17(s,3H),2.05-2.00(m,2H),1.84-1.58(m,4H)。19F NMR(376MHz,DMSO-d6)δ-63.37(3F)。
实施例106:(3S)-N-(3-[2-[(3S)-3-氨基吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例106A:N-[(3S)-1-[4-碘-6-(吗啉-4-基)吡啶-2-基]吡咯烷-3-基]氨基甲酸叔丁酯
将4-(6-氟-4-碘吡啶-2-基)吗啉(500mg,1.623mmol)、N-[(3S)-吡咯烷-3-基]氨基甲酸叔丁酯(453mg,2.434mmol)和K2CO3(449mg,3.246mmol)在NMP(5mL)中的混合物在150℃下搅拌2h。在室温下通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用盐水(3x20mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(5/1)洗脱,得到呈白色固体的N-[(3S)-1-[4-碘-6-(吗啉-4-基)吡啶-2-基]吡咯烷-3-基]氨基甲酸叔丁酯(577mg,75%)。MS ESI:C18H27IN4O3[M+H]+的计算值:475.11,实测值:475.15。1H NMR(400MHz,氯仿-d)δ6.28(d,J=1.2Hz,1H),6.16(d,J=1.2Hz,1H),4.71-4.67(s,1H),4.35-4.25(m,1H),3.82-3.76(m,4H),3.70-3.68(m,1H),3.55-3.48(m,1H),3.48-3.44(m,4H),3.34-3.24(m,1H),2.24-2.20(m,1H),1.93-1.91(m,1H),1.47(s,9H)。
制备例106B:N-[(3S)-1-(4-[2-甲基-5-[(3S)-3-(2,2,2-三氟乙基)吡咯烷-1-羰基氨基]苯基]-6-(吗啉-4-基)吡啶-2-基)吡咯烷-3-基]氨基甲酸叔丁酯
将N-[(3S)-1-[4-碘-6-(吗啉-4-基)吡啶-2-基]吡咯烷-3-基]氨基甲酸叔丁酯(173mg,0.364mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(150mg,0.364mmol)、Pd(dppf)Cl2.CH2Cl2(30mg,0.036mmol)和Na2CO3(116mg,1.092mmol)在二噁烷(4mL)和H2O(1mL)中的混合物在60℃和氮气氛下搅拌3h。将所得混合物减压浓缩。残余物通过采用PE/EtOAc(1/1)的制备型TLC纯化,得到呈浅黄色固体的N-[(3S)-1-(4-[2-甲基-5-[(3S)-3-(2,2,2-三氟乙基)吡咯烷-1-羰基氨基]苯基]-6-(吗啉-4-基)吡啶-2-基)吡咯烷-3-基]氨基甲酸叔丁酯(200mg,87%)。MS ESI:C32H43F3N6O4[M+H]+的计算值:633.33,实测值:633.10。1H NMR(400MHz,氯仿-d)δ7.42-7.41(m,1H),7.19-7.17(m,2H),6.14(s,1H),5.87(s,1H),5.73(s,1H),4.77-4.73(m,1H),4.34-4.32(m,1H),3.85-3.80(m,5H),3.74-3.72(m,1H),3.66-3.63(m,1H),3.57-3.45(m,6H),3.38-3.36(m,2H),3.13-3.11(m,1H),2.56-2.52(m,1H),2.31-2.21(m,7H),1.95-1.93m,1H),1.79-1.71(m,1H),1.47(s,9H)。
实施例106:(3S)-N-(3-[2-[(3S)-3-氨基吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将N-[(3S)-1-(4-[2-甲基-5-[(3S)-3-(2,2,2-三氟乙基)吡咯烷-1-羰基氨基]苯基]-6-(吗啉-4-基)吡啶-2-基)吡咯烷-3-基]氨基甲酸叔丁酯(223mg,0.368mmol)和TFA(1mL)在DCM(5mL)中的混合物在室温下搅拌1h。将反应混合物减压浓缩,并且用饱和NaHCO3碱化至pH 8。将所得混合物用EtOAc(50mL)萃取。将合并的有机层用盐水(3x20mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过反相快速色谱法采用以下条件纯化:柱:C18柱120g;流动相A:水(10mmol/L NH4HCO3),流动相B:CH3CN;流速:60mL/min;梯度:在25min内30%B至50%B;254/220nm,得到呈白色固体的(3S)-N-(3-[2-[(3S)-3-氨基吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(81mg,48%)。MS ESI:C27H35F3N6O2[M+H]+的计算值:533.28,实测值:533.15。1H NMR(400MHz,DMSO-d6)δ8.12(s,1H),7.43(dd,J=8.4,2.4Hz,1H),7.34(d,J=2.4Hz,1H),7.10(d,J=8.4Hz,1H),5.83(s,1H),5.61(s,1H),3.72-3.63(m,5H),3.57-3.45(m,4H),3.42-3.26(m,6H),3.03-3.00(m,2H),2.48-2.35(m,3H),2.17(s,3H),2.05-2.00(m,2H),1.94-1.60(m,4H)。19F NMR(376MHz,DMSO-d6)δ-63.37(3F)。
实施例107:(3S)-N-(3-[2-[(3R)-3-氨基哌啶-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例107A:N-[(3R)-1-[4-碘-6-(吗啉-4-基)吡啶-2-基]哌啶-3-基]氨基甲酸叔丁酯
将4-(6-氟-4-碘吡啶-2-基)吗啉(500mg,1.623mmol)、N-[(3R)-哌啶-3-基]氨基甲酸叔丁酯(486mg,2.435mmol)在NMP(5mL)和K2CO3(449mg,3.246mmol)中的混合物在150℃下搅拌2h。通过添加水(30mL)来猝灭反应。将所得混合物用EtOAc(3x40mL)萃取。将合并的有机层用盐水(30mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(3/1)洗脱,得到呈白色固体的N-[(3R)-1-[4-碘-6-(吗啉-4-基)吡啶-2-基]哌啶-3-基]氨基甲酸叔丁酯(450mg,57%)。MS ESI:C19H29IN4O3[M+H]+的计算值:489.13;实测值:488.95。
制备例107B:N-[(3R)-1-(4-[2-甲基-5-[(3S)-3-(2,2,2-三氟乙基)吡咯烷-1-羰基氨基]苯基]-6-(吗啉-4-基)吡啶-2-基)哌啶-3-基]氨基甲酸叔丁酯
将N-[(3R)-1-[4-碘-6-(吗啉-4-基)吡啶-2-基]哌啶-3-基]氨基甲酸叔丁酯(200mg,0.410mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(169mg,0.410mmol)、1,4-二噁烷(2mL)、H2O(0.4mL)、Na2CO3(130mg,1.229mmol)和Pd(dppf)Cl2.CH2Cl2(39mg,0.041mmol)的混合物在80℃和氮气氛下搅拌16h。在室温下通过添加水(25mL)来猝灭反应。将所得混合物用EtOAc(3x25mL)萃取。将合并的有机层用盐水(15mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈浅棕色固体的N-[(3R)-1-(4-[2-甲基-5-[(3S)-3-(2,2,2-三氟乙基)吡咯烷-1-羰基氨基]苯基]-6-(吗啉-4-基)吡啶-2-基)哌啶-3-基]氨基甲酸叔丁酯(200mg,76%)。MS ESI:C33H45F3N6O4[M+H]+的计算值:647.35,实测值:647.40。
实施例107:(3S)-N-(3-[2-[(3R)-3-氨基哌啶-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在室温下,向N-[(3R)-1-(4-[2-甲基-5-[(3S)-3-(2,2,2-三氟乙基)吡咯烷-1-羰基氨基]苯基]-6-(吗啉-4-基)吡啶-2-基)哌啶-3-基]氨基甲酸叔丁酯(200mg,0.309mmol)在DCM(3mL)中的搅拌溶液中加入TFA(1mL)。将所得混合物在室温下搅拌1h。将所得混合物减压浓缩。将混合物用饱和NaHCO3碱化至pH 8。将所得混合物用DCM(3x20mL)萃取。将合并的有机层用盐水(2x10mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用CH2Cl2/MeOH(10/1)洗脱,得到呈浅黄色固体的(3S)-N-(3-[2-[(3R)-3-氨基哌啶-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(94mg,55%)。MS ESI:C28H37F3N6O2[M+H]+的计算值:547.29,实测值:547.15。1HNMR(400MHz,DMSO-d6)δ8.14(s,1H),7.43(dd,J=8.4,2.4Hz,1H),7.35(d,J=2.4Hz,1H),7.11(d,J=8.4Hz,1H),6.00(s,1H),5.92(s,1H),4.15-4.12(m,1H),4.07-4.03(m,1H),3.72-3.63(m,4H),3.53-3.50(m,2H),3.44-3.37(m,4H),3.31-3.30(m,1H),3.02-3.00(m,1H),2.85-2.75(m,2H),2.79-2.71(m,1H),2.51-2.34(m,3H),2.16(s,3H),2.14-2.03(m,1H),1.88-1.86(m,1H),1.74-1.58(m,2H),1.53-1.37(m,1H),1.37-1.24(m,3H)。19F NMR(282MHz,氯仿-d)δ-64.92(3F)。
实施例108:(3S)-N-(3-[2-[(3S)-3-氨基哌啶-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例108A:N-[(3S)-1-[4-碘-6-(吗啉-4-基)吡啶-2-基]哌啶-3-基]氨基甲酸叔丁酯
将4-(6-氟-4-碘吡啶-2-基)吗啉(500mg,1.623mmol)、N-[(3S)-哌啶-3-基]氨基甲酸叔丁酯(486mg,2.435mmol)在NMP(5mL)和K2CO3(449mg,3.246mmol)中的混合物在150℃下搅拌2h。通过添加水(30mL)来猝灭反应。将所得混合物用EtOAc(3x40mL)萃取。将合并的有机层用盐水(30mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(3/1)洗脱,得到呈白色固体的N-[(3S)-1-[4-碘-6-(吗啉-4-基)吡啶-2-基]哌啶-3-基]氨基甲酸叔丁酯(480mg,61%)。MS ESI:C19H29IN4O3[M+H]+的计算值:489.13;实测值:488.95。1H NMR(300MHz,氯仿-d)δ6.42(s,1H),6.31(s,1H),4.86-4.83(m,1H),3.80-3.75(m,4H),3.62-3.56(m,2H),3.46-3.42(m,6H),1.85-1.63(m,4H),1.46(s,9H)。
制备例108B:N-[(3S)-1-(4-[2-甲基-5-[(3S)-3-(2,2,2-三氟乙基)吡咯烷-1-羰基氨基]苯基]-6-(吗啉-4-基)吡啶-2-基)哌啶-3-基]氨基甲酸叔丁酯
将N-[(3S)-1-[4-碘-6-(吗啉-4-基)吡啶-2-基]哌啶-3-基]氨基甲酸叔丁酯(200mg,0.410mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(169mg,0.410mmol)、1,4-二噁烷(2mL)、H2O(0.4mL)、Na2CO3(130mg,1.229mmol)和Pd(dppf)Cl2.CH2Cl2(39mg,0.041mmol)的混合物在80℃和氮气氛下搅拌16h。通过添加水(25mL)来猝灭反应。将所得混合物用EtOAc(3x25mL)萃取。将合并的有机层用盐水(15mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc/EtOH(8/3/1)洗脱,得到呈浅棕色固体的N-[(3S)-1-(4-[2-甲基-5-[(3S)-3-(2,2,2-三氟乙基)吡咯烷-1-羰基氨基]苯基]-6-(吗啉-4-基)吡啶-2-基)哌啶-3-基]氨基甲酸叔丁酯(210mg,79%)。MS ESI:C33H45F3N6O4[M+H]+的计算值:647.35,实测值:647.45。1H NMR(400MHz,氯仿-d)δ7.43-7.40(m,1H),7.21-7.14(m,2H),6.12(s,1H),6.02(s,1H),5.92(s,1H),4.99-4.94(m,1H),3.85-3.77(m,6H),3.64-3.62(m,2H),3.56-3.39(m,8H),3.15-3.10(m,1H),2.56-2.53(m,1H),2.37-2.22(m,5H),1.85-1.58(m,5H),1.45(s,9H)。
实施例108:(3S)-N-(3-[2-[(3S)-3-氨基哌啶-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
向N-[(3S)-1-(4-[2-甲基-5-[(3S)-3-(2,2,2-三氟乙基)吡咯烷-1-羰基氨基]苯基]-6-(吗啉-4-基)吡啶-2-基)哌啶-3-基]氨基甲酸叔丁酯(200mg,0.309mmol)在DCM(3mL)中的搅拌溶液中加入TFA(1mL)。将所得混合物在室温下搅拌1h。将所得混合物减压浓缩。将混合物用饱和NaHCO3碱化至pH 8。将所得混合物用DCM(3x20mL)萃取。将合并的有机层用盐水(2x10mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用CH2Cl2/MeOH(10/1)洗脱,得到呈浅黄色固体的(3S)-N-(3-[2-[(3S)-3-氨基哌啶-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(107mg,63%)。MS ESI:C28H37F3N6O2[M+H]+的计算值:547.29,实测值:547.15。1H NMR(400MHz,DMSO-d6)δ8.14(s,1H),7.43(dd,J=8.4,2.0Hz,1H),7.35(d,J=2.0Hz,1H),7.11(d,J=8.4Hz,1H),5.99(s,1H),5.91(s,1H),4.15-4.05(m,2H),3.72-3.63(m,5H),3.53-3.50(m,1H),3.44-3.37(m,4H),3.31-3.29(m,1H),3.02-3.00(m,1H),2.85-2.75(m,2H),2.79-2.71(m,1H),2.51-2.34(m,3H),2.16(s,3H),2.14-2.03(m,1H),1.88-1.86(m,1H),1.74-1.58(m,2H),1.53-1.37(m,1H),1.37-1.24(m,2H)。19F NMR(282MHz,氯仿-d)δ-64.93(3F)。
实施例109:(3S)-N-[4-甲基-3-[2-(吗啉-4-基)-6-(2-氧代吡咯烷-1-基)吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例109A:1-[4-氯-6-(吗啉-4-基)吡啶-2-基]吡咯烷-2-酮
将4-(4,6-二氯吡啶-2-基)吗啉(1.00g,4.29mmol)和吡咯烷酮(0.55g,6.435mmol)、1,4-二噁烷(20mL)、Na2CO3(0.91g,8.58mmol)、XantPhos(0.50g,0.86mmol)和Pd2(dba)3.CHCl3(0.44g,0.43mmol)的混合物在100℃和氮气氛下搅拌16h。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x100mL)萃取。将合并的有机层用盐水(2x100mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc/EtOH(9/3/1)洗脱,得到呈浅黄色固体的1-[4-氯-6-(吗啉-4-基)吡啶-2-基]吡咯烷-2-酮(690mg,57%)。MS ESI:C13H16ClN3O2[M+H]+的计算值:282.09,实测值:282.15。1H NMR(400MHz,氯仿-d)δ7.86(d,J=1.2Hz,1H),6.38(d,J=1.2Hz,1H),4.10-4.02(m,2H),3.86-3.79(m,4H),3.52-3.45(m,4H),2.66-2.64(m,2H),2.17-2.05(m,2H)。
实施例109:(3S)-N-[4-甲基-3-[2-(吗啉-4-基)-6-(2-氧代吡咯烷-1-基)吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将1-[4-氯-6-(吗啉-4-基)吡啶-2-基]吡咯烷-2-酮(150mg,0.532mmol,)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(219mg,0.532mmol)、1,4-二噁烷(2mL)、H2O(0.4mL)、K3PO4(38mg,0.355mmol)和第2代XPhos预催化剂(14mg,0.018mmol)的混合物在80℃和氮气氛下搅拌16h。使混合物冷却至室温。通过添加水(10mL)来猝灭反应。将所得混合物用EtOAc(3x20mL)萃取。将合并的有机层用盐水(20mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc/EtOH(4/3/1)洗脱,得到呈白色固体的(3S)-N-[4-甲基-3-[2-(吗啉-4-基)-6-(2-氧代吡咯烷-1-基)吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(117.7mg,42%)。MS ESI:C27H32F3N5O3[M+H]+的计算值:532.25,实测值:532.20。1H NMR(400MHz,DMSO-d6)δ8.17(s,1H),7.58(s,1H),7.47(dd,J=8.4,2.4Hz,1H),7.38(d,J=2.4Hz,1H),7.14(d,J=8.4Hz,1H),6.44(s,1H),4.02(t,J=7.2Hz,2H),3.74-3.63(m,5H),3.58-3.43(m,5H),3.34-3.32(m,1H),3.04-3.02(m,1H),2.61-2.51(m,2H),2.50-2.30(m,3H),2.16(s,3H),2.13-1.95(m,3H),1.66-1.64(m,1H)。19F NMR(376MHz,DMSO-d6)δ-63.37(3F)。
实施例110:(3S)-N-(3-[2-[(3R)-3-羟基吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例110A:(3R)-1-[4-碘-6-(吗啉-4-基)吡啶-2-基]吡咯烷-3-醇
将4-(6-氟-4-碘吡啶-2-基)吗啉(500mg,1.623mmol)和(3R)-吡咯烷-3-醇(212mg,2.434mmol)在NMP(6mL)和K2CO3(448mg,3.246mmol)中的混合物在150℃和氮气氛下搅拌2h。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x300mL)萃取。将合并的有机层用盐水(3x200mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈灰白色固体的(3R)-1-[4-碘-6-(吗啉-4-基)吡啶-2-基]吡咯烷-3-醇(572mg,94%)。MS ESI:C13H18IN3O2[M+H]+的计算值:376.04,实测值:376.00。1H NMR(400MHz,DMSO-d6)δ6.30(s,1H),6.10(s,1H),4.90(d,J=3.6Hz,1H),4.38-4.28(m,1H),3.65-3.63(m,4H),3.45-3.33(m,7H),3.23-3.21(m,1H),2.00-1.95(m,1H),1.89-1.78(m,1H)。
实施例110:(3S)-N-(3-[2-[(3R)-3-羟基吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将(3R)-1-[4-碘-6-(吗啉-4-基)吡啶-2-基]吡咯烷-3-醇(120mg,0.320mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(105mg,0.256mmol)在二噁烷(4mL)和H2O(1mL)、Pd(dppf)Cl2.CH2Cl2(26mg,0.032mmol)和Na2CO3(102mg,0.959mmol)中的混合物在60℃和氮气氛下搅拌2h。将反应混合物减压浓缩。残余物通过采用PE/EtOAc(1/1)的制备型TLC纯化。将粗产物通过制备型HPLC采用以下条件纯化:(柱:XBridge制备型苯基OBD柱,19×150mm,5um,13nm;流动相A:水(10mmoL/L NH4HCO3),流动相B:CH3CN;流速:20mL/min;梯度:在4.3min内40%B至60%B;254/210nm,得到呈浅蓝色固体的(3S)-N-(3-[2-[(3R)-3-羟基吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(53.7mg,31%)。MS ESI:C27H34F3N5O3[M+H]+的计算值:534.26,实测值:534.20。1H NMR(400MHz,DMSO-d6)δ8.12(s,1H),7.43(dd,J=8.4,2.4Hz,1H),7.34(d,J=2.4Hz,1H),7.10(d,J=8.4Hz,1H),5.84(s,1H),5.64(s,1H),4.90(d,J=3.6Hz,1H),4.36-4.34(m,1H),3.72-3.63(m,5H),3.53-3.42(m,8H),3.33-3.30(m,2H),3.04-3.00(m,1H),2.50-2.34(m,3H),2.17(s,3H),2.10-1.94(m 2H),1.88-1.82(m,1H),1.73-1.58(m,1H)。19F NMR(376MHz,DMSO-d6)δ-63.37(3F)。
实施例111:(3S)-N-[4-甲基-3-[2-(3-甲基-2-氧代咪唑烷-1-基)-6-(吗啉-4-基)吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例111A:1-[4-氯-6-(吗啉-4-基)吡啶-2-基]-3-甲基咪唑烷-2-酮
在氮气氛下,向4-(4,6-二氯吡啶-2-基)吗啉(500mg,2.145mmol)和1-甲基咪唑烷-2-酮(322mg,3.218mmol)在1,4-二噁烷(5mL)中的搅拌溶液中加入Na2CO3(682mg,6.435mmol)、XantPhos(248mg,0.429mmol)和Pd2(dba)3CHCl3(222mg,0.215mmol)。将所得混合物在100℃和氮气氛下搅拌16h。通过添加水(20mL)来猝灭反应。将所得混合物用EtOAc(3x20mL)萃取。将合并的有机层用盐水(20mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈浅黄色固体的1-[4-氯-6-(吗啉-4-基)吡啶-2-基]-3-甲基咪唑烷-2-酮(500mg,79%)。MS ESI:C13H17ClN4O2[M+H]+的计算值:297.10;实测值:297.15。1H NMR(400MHz,氯仿-d)δ7.74(d,J=1.2Hz,1H),6.23(d,J=1.2Hz,1H),4.03-3.99(m,2H),3.83-3.80(m,4H),3.48-3.43(m,6H),2.92(s,3H)。
实施例111:(3S)-N-[4-甲基-3-[2-(3-甲基-2-氧代咪唑烷-1-基)-6-(吗啉-4-基)吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在氮气氛下,向1-[4-氯-6-(吗啉-4-基)吡啶-2-基]吡咯烷-2-酮(150mg,0.532mmol,)和(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(219mg,0.532mmol)在1,4-二噁烷(2mL)和H2O(0.4mL)中的搅拌溶液中加入K3PO4(38mg,0.355mmol)和第2代XPhos预催化剂(14mg,0.018mmol)。将所得混合物在80℃和氮气氛下搅拌16h。通过添加水(10mL)来猝灭反应。将所得混合物用EtOAc(3x20mL)萃取。将合并的有机层用盐水(20mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc/EtOH(4/3/1)洗脱,得到呈白色固体的(3S)-N-[4-甲基-3-[2-(吗啉-4-基)-6-(2-氧代吡咯烷-1-基)吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(113.5mg,41%)。MS ESI:C27H33F3N6O3[M+H]+的计算值:547.26,实测值:547.15。1H NMR(400MHz,DMSO-d6)δ8.16(s,1H),7.47-7.44(m,2H),7.37(s,1H),7.13(d,J=8.8Hz,1H),6.28(s,1H),3.99-3.91(m,2H),3.72-3.63(m,5H),3.56-3.38(m,7H),3.34-3.25(m,1H),3.03(t,J=9.6Hz,1H),2.77(s,3H),2.51-2.34(m,3H),2.16(s,3H),2.11-2.07(m,1H),1.70-1.60(m,1H)。19F NMR(282MHz,DMSO-d6)δ-69.69(3F)。
实施例112:(3S)-N-[4-甲基-3-[2-(N-甲基乙酰胺基)-6-(吗啉-4-基)吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例112A:N-[4-氯-6-(吗啉-4-基)吡啶-2-基]乙酰胺
在0℃下,向4-氯-6-(吗啉-4-基)吡啶-2-胺(300mg,1.404mmol)和吡啶(222mg,2.808mmol)在DCM(5mL)中的搅拌混合物中加入乙酰氯(220mg,2.808mmol)。将所得混合物在室温下搅拌2h。通过添加水(10mL)来猝灭反应。将所得混合物用EtOAc(3x10mL)萃取。将合并的有机层用盐水(2x5mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈灰白色固体的N-[4-氯-6-(吗啉-4-基)吡啶-2-基]乙酰胺(224mg,62%)。MS ESI:C11H14ClN3O2[M+H]+的计算值:256.08,实测值:256.10。1H NMR(400MHz,DMSO-d6)δ7.41(s,1H),6.59(s,1H),3.66(m,4H),3.47(m,4H),2.06(s,3H)。
制备例112B:N-[4-氯-6-(吗啉-4-基)吡啶-2-基]-N-甲基乙酰胺
在0℃下,向N-[4-氯-6-(吗啉-4-基)吡啶-2-基]乙酰胺(200mg,0.782mmol)和NaH(28mg,1.173mmol)在DMF(8mL)中的搅拌混合物中逐滴加入MeI(167mg,1.173mmol)。将所得混合物在室温和氮气氛下搅拌5h。将所得混合物用水(20mL)稀释。将所得混合物用EtOAc(3x10mL)萃取。将合并的有机层用盐水(2x10mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈灰白色固体的N-[4-氯-6-(吗啉-4-基)吡啶-2-基]-N-甲基乙酰胺(166mg,79%)。MS ESI:C12H16ClN3O2[M+H]+的计算值:270.09,实测值:270.20。1H NMR(300MHz,氯仿-d)δ6.63(s,1H),6.49(s,1H),3.87-3.78(m,4H),3.57-3.47(m,4H),3.33(s,3H),2.16(s,3H)。
实施例112:(3S)-N-[4-甲基-3-[2-(N-甲基乙酰胺基)-6-(吗啉-4-基)吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
向N-[4-氯-6-(吗啉-4-基)吡啶-2-基]-N-甲基乙酰胺(140mg,0.519mmol)和(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(148mg,0.519mmol)在THF(5mL)和H2O(0.5mL)中的搅拌溶液中加入第2代XPhos预催化剂(41mg,0.052mmol)和K3PO4(220mg,1.038mmol)。将所得混合物在50℃和氮气氛下搅拌1h。将所得混合物用水(30mL)稀释。将所得混合物用EtOAc(3x10mL)萃取。将合并的有机层用盐水(2x10mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。残余物通过采用PE/EtOAc(1/1)的制备型TLC纯化,得到呈灰白色固体的(3S)-N-[4-甲基-3-[2-(N-甲基乙酰胺基)-6-(吗啉-4-基)吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(113mg,41%)。MS ESI:C26H32F3N5O3[M+H]+的计算值:520.25,实测值:520.15。1H NMR(400MHz,氯仿-d)δ7.54(s,1H),7.42-7.41(m,1H),7.28-7.02(m,1H),6.53(s,1H),6.48(s,1H),6.17(s,1H),3.86-3.80(m,5H),3.67-3.65(m,1H),3.63-3.54(m,4H),3.49-3.43(m,1H),3.36(s,3H),3.14(t,J=9.6Hz,1H),2.63-2.54(m,1H),2.35-2.28(m,2H),2.24(s,3H),2.16(s,3H),1.90-1.77(m,2H)。19F NMR(376MHz,氯仿-d)δ-64.96(3F)。
实施例113:(3S)-N-[3-[2-甲烷磺酰胺基-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例113A:N-[4-氯-6-(吗啉-4-基)吡啶-2-基]甲烷磺酰胺
将4-氯-6-(吗啉-4-基)吡啶-2-胺(300mg,1.404mmol)、MsCl(209mg,1.8mmol)在吡啶(5mL)中的混合物在80℃下搅拌2h。将所得混合物减压浓缩。将残余物通过硅胶柱色谱法纯化,用含EtOAc/EtOH(3/1)的石油醚(70%)洗脱,得到呈浅粉红色固体的N-[4-氯-6-(吗啉-4-基)吡啶-2-基]甲烷磺酰胺(350mg,85%)。MS ESI:C10H14ClN3O3S[M+H]+的计算值:292.04,实测值:291.95。1H NMR(400MHz,氯仿-d)δ6.51(d,J=1.2Hz,1H),6.35(d,J=1.2Hz,1H),3.85-3.78(m,4H),3.54-3.47(m,4H),3.25(s,3H)。
实施例113:(3S)-N-[3-[2-甲烷磺酰胺基-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将N-[4-氯-6-(吗啉-4-基)吡啶-2-基]甲烷磺酰胺(170mg,0.6mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(192mg,0.5mmol)、K3PO4(371mg,1.8mmol)和第2代XPhos预催化剂(46mg,0.06mmol)在H2O(0.4mL)和THF(4mL)中的混合物在80℃和氮气氛下搅拌2h。将所得混合物减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc/EtOH(6/3/1)洗脱。将粗产物通过制备型HPLC采用以下条件纯化:柱:SunFire制备型C18 OBD柱,19×150mm,5μm;流动相A:水(0.05%FA),流动相B:CH3CN;流速:20mL/min;梯度:55%B至75%B,得到呈灰白色固体的(3S)-N-[3-[2-甲烷磺酰胺基-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(129mg,46%)。MS ESI:C24H30F3N5O4S[M+H]+的计算值:542.20,实测值:542.20。1H NMR(400MHz,氯仿-d)δ7.31-7.28(m,2H),7.18-7.16(m,1H),7.09(s,1H),6.37(s,1H),6.28(s,1H),6.23(s,1H),3.84-3.79(m,5H),3.67-3.62(m,1H),3.52-3.48(m,4H),3.47-3.42(m,1H),3.27(s,3H),3.13(t,J=9.6Hz,1H),2.57-2.55(m,1H),2.31-2.21(m,6H),1.78-1.73(m,1H)。19F NMR(376MHz,氯仿-d)δ-64.94(3F)。
实施例114:(3S)-N-[3-[2-(3-羟基-2-氧代吡咯烷-1-基)-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例114A:1-[4-氯-6-(吗啉-4-基)吡啶-2-基]-3-羟基吡咯烷-2-酮
在氮气氛下,向4-(4,6-二氯吡啶-2-基)吗啉(600mg,2.574mmol)、Na2CO3(546mg,5.148mmol)和3-羟基吡咯烷-2-酮(390mg,3.861mmol)在1,4-二噁烷(5mL)中的搅拌混合物中加入XantPhos(298mg,0.515mmol)和Pd2(dba)3CHCl3(266mg,0.257mmol)。将所得混合物在100℃和氮气氛下搅拌16h。将所得混合物用H2O(100mL)稀释。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用盐水(2x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(3/1)洗脱,得到呈棕色固体的1-[4-氯-6-(吗啉-4-基)吡啶-2-基]-3-羟基吡咯烷-2-酮(440mg,57%)。MS ESI:C13H16ClN3O3[M+H]+的计算值:298.09;实测值:298.05。1H NMR(400MHz,氯仿-d)δ7.81(s,1H),6.40-6.39(m,1H),4.55-4.50(m,1H),4.23-4.18(m,1H),3.88-3.68(m,5H),3.57-3.47(m,5H),2.60-2.53(m,1H),2.10-1.76(m,1H)。
实施例114:(3S)-N-[3-[2-(3-羟基-2-氧代吡咯烷-1-基)-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将1-[4-氯-6-(吗啉-4-基)吡啶-2-基]-3-羟基吡咯烷-2-酮(100mg,0.336mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(111mg,0.269mmol)、第2代XPhos预催化剂(26mg,0.034mmol)、K3PO4(143mg,0.672mmol)、THF(2mL)和H2O(0.2mL)的混合物在80℃和氮气氛下搅拌2h。将所得混合物用H2O(100mL)稀释。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用盐水(2x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。不纯的产物通过采用PE/EtOAc/EtOH(8/3/1)的制备型TLC纯化,得到呈灰白色固体的(3S)-N-[3-[2-(3-羟基-2-氧代吡咯烷-1-基)-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(76mg,41%)。MS ESI:C27H32F3N5O4[M+H]+的计算值:548.24;实测值:548.30。1HNMR(300MHz,氯仿-d)δ7.73(s,1H),7.40-7.39(m,1H),7.29-7.26(m,1H),7.21-7.18(m,1H),6.40(s,1H),6.20(s,1H),4.54-4.47(m,1H),4.34-4.26(m,1H),3.87-3.79(m,6H),3.65-3.61(m,1H),3.54-3.43(m,5H),3.16-3.10(m,1H),2.61-2.55(m,2H),2.34-2.25(m,6H),2.09-2.02(m,1H),1.80-1.69(m,1H)。19F NMR(282MHz,氯仿-d)δ-64.95(3F)。
实施例115:(3S)-N-[4-甲基-3-[2-(吗啉-4-基)-6-(2-氧代-1,3-噁唑烷-3-基)吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例115A:3-[4-氯-6-(吗啉-4-基)吡啶-2-基]-1,3-噁唑烷-2-酮
在氮气氛下,向4-(4,6-二氯吡啶-2-基)吗啉(200mg,0.858mmol)、Na2CO3(182mg,1.716mmol)和噁唑烷酮(112mg,1.287mmol)在1,4-二噁烷(2mL)中的搅拌溶液中加入Pd2(dba)3.CHCl3(89mg,0.086mmol)和XantPhos(99mg,0.172mmol)。将所得混合物在100℃和氮气氛下搅拌16h。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用饱和盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈棕色固体的3-[4-氯-6-(吗啉-4-基)吡啶-2-基]-1,3-噁唑烷-2-酮(130mg,53%)。MS ESI:C12H14ClN3O3[M+H]+的计算值:284.07,实测值:284.05。1H NMR(400MHz,氯仿-d)δ7.62(d,J=1.2Hz,1H),6.34d,J=1.2Hz,1H),4.49-4.45(m,2H),4.25-4.21(m,2H),3.83-3.80(m,4H),3.49-3.47(m,4H)。
实施例115:(3S)-N-[4-甲基-3-[2-(吗啉-4-基)-6-(2-氧代-1,3-噁唑烷-3-基)吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在氮气氛下,向3-[4-氯-6-(吗啉-4-基)吡啶-2-基]-1,3-噁唑烷-2-酮(130mg,0.458mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(189mg,0.458mmol)和K3PO4(195mg,0.916mmol)在THF(2mL)和H2O(0.2mL)中的搅拌溶液中加入第2代XPhos预催化剂(36mg,0.046mmol)。将所得混合物在80℃和氮气氛下搅拌2h。通过添加水(100mL)来猝灭反应。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用饱和盐水(3x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱。将粗产物通过反相快速色谱法采用以下条件纯化:柱,C18硅胶;流动相,含CH3CN的水(10mmol/LNH4HCO3),5%至95%梯度;检测器,UV 254nm,得到呈灰白色固体的(3S)-N-[4-甲基-3-[2-(吗啉-4-基)-6-(2-氧代-1,3-噁唑烷-3-基)吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(122mg,50%)。MS ESI:C26H30F3N5O4[M+H]+的计算值:534.22,实测值:534.30。1H NMR(300MHz,氯仿-d)δ7.52(s,1H),7.38(dd,J=2.4,8.4Hz,1H),7.22(d,J=2.1Hz,1H),7.16(d,J=8.4Hz,1H),6.32(s,1H),6.18(s,1H),4.49-4.44(m,2H),4.31-4.26(m,2H),3.84-3.76(m,5H),3.65-3.59(m,1H),3.50-3.38(m,5H),3.13-3.07(m,1H),2.60-2.50(m,1H),2.31-2.18(m,6H),1.77-1.73(m,1H)。19F NMR(282MHz,氯仿-d)δ-64.95(3F)。
实施例116:(3S)-N-(3-[2-[5-羟基-2-氧代哌啶-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例116A:1-[4-氯-6-(吗啉-4-基)吡啶-2-基]-5-羟基哌啶-2-酮
向4-(4,6-二氯吡啶-2-基)吗啉(500mg,2.145mmol)和5-羟基哌啶-2-酮(370mg,3.218mmol)在二噁烷(7mL)中的混合物中加入XantPhos(248mg,0.429mmol)和Na2CO3(455mg,4.290mmol)和Pd2(dba)3·CHCl3(222mg,0.215mmol)。将所得混合物在100℃和氮气氛下搅拌16h。将所得混合物用水(15mL)稀释。将所得混合物用EtOAc(3x15mL)萃取。将合并的有机层用盐水(2x10mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈灰白色固体的1-[4-氯-6-(吗啉-4-基)吡啶-2-基]-5-羟基哌啶-2-酮(498mg,74%)。MS ESI:C14H18ClN3O3[M+H]+的计算值:312.10,实测值:312.05。1H NMR(300MHz,DMSO-d6)δ7.29(d,J=1.2Hz,1H),6.70(d,J=1.5Hz,1H),5.09(d,J=3.6Hz,1H),4.09(s,1H),3.90-3.81(m,1H),3.79-3.75(m,1H),3.71-3.68(m,4H),3.48-3.45(m,4H),2.62-2.40(m,2H),1.98-1.97(m,1H),1.80-1.73(m,1H)。
实施例116:(3S)-N-[3-[2-(5-羟基-2-氧代哌啶-1-基)-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
向1-[4-氯-6-(吗啉-4-基)吡啶-2-基]-5-羟基哌啶-2-酮(250mg,0.802mmol)和(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(264mg,0.641mmol)在THF(8mL)和H2O(0.8mL)中的搅拌混合物中加入K3PO4(340mg,1.604mmol)和第2代XPhos预催化剂(63mg,0.080mmol)。将所得混合物在80℃和氮气氛下搅拌2h。将所得混合物用水(30mL)稀释。将所得混合物用EtOAc(3x20mL)萃取。将合并的有机层用盐水(2x10mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈灰白色固体的(3S)-N-[3-[2-(5-羟基-2-氧代哌啶-1-基)-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(274mg,61%)。MS ESI:C28H34F3N5O4[M+H]+的计算值:562.26,实测值:562.20。
实施例117:(3S)-N-(4-甲基-3-(2-吗啉基-6-(2-氧代-3-氮杂双环[3.1.0]己烷-3-基)吡啶-4-基)苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例117A:3-[4-氯-6-(吗啉-4-基)吡啶-2-基]-3-氮杂双环[3.1.0]己-2-酮
将4-(4,6-二氯吡啶-2-基)吗啉(500mg,2.145mmol)、3-氮杂双环[3.1.0]己-2-酮(187mg,1.931mmol)、Pd2(dba)3.CHCl3(222mg,0.215mmol)、XantPhos(248mg,0.429mmol)和Na2CO3(455mg,4.290mmol)在二噁烷(5mL)中的混合物在100℃和氮气氛下搅拌3h。将所得混合物减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈红色固体的3-[4-氯-6-(吗啉-4-基)吡啶-2-基]-3-氮杂双环[3.1.0]己-2-酮(810mg,86%)。MSESI:C14H16ClN3O2[M+H]+的计算值:294.09,实测值:294.05。1H NMR(400MHz,氯仿-d)δ7.74(s,1H),6.32(s,1H),4.07-4.03(m,2H),3.82-3.80(m,4H),3.47-3.45(m,4H),2.15-2.11(m,1H),2.01-1.95(m,1H),1.24-1.19(m,1H),0.80-0.77(m,1H)。
实施例117:(3S)-N-[4-甲基-3-[2-(吗啉-4-基)-6-[2-氧代-3-氮杂双环[3.1.0]己烷-3-基]吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将3-[4-氯-6-(吗啉-4-基)吡啶-2-基]-3-氮杂双环[3.1.0]己-2-酮(200mg,0.681mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(225mg,0.545mmol)、第2代XPhos预催化剂(54mg,0.068mmol)和K3PO4(289mg,1.362mmol)在THF(2mL)和H2O(0.2mL)中的混合物在80℃和氮气氛下搅拌2h。通过添加水(10mL)来猝灭反应。将所得混合物用EtOAc(2x5mL)萃取。将合并的有机层用盐水(5mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈灰白色固体的(3S)-N-[4-甲基-3-[2-(吗啉-4-基)-6-[2-氧代-3-氮杂双环[3.1.0]己烷-3-基]吡啶-4-基]苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(109mg,29%)。MS ESI:C28H32F3N5O3[M+H]+的计算值:544.25,实测值:544.35。1H NMR(300MHz,氯仿-d)δ7.63(s,1H),7.40(dd,J=2.1,8.1Hz,1H),7.26-7.14(m,2H),6.27(s,1H),6.18(s,1H),4.13(s,1H),4.11(s,1H),3.83-3.76(m,5H),3.61-3.58(m,1H),3.48-3.38(m,5H),3.13-3.07(m,1H),2.31-2.28(m,1H),2.25-2.22(m,6H),2.18-2.06(m,1H),1.98-1.95(m,1H),1.76-1.73(m,1H),1.21-1.15(m,1H),0.81-0.77(m,1H)。19FNMR(282MHz,氯仿-d)δ-64.94(3F)。
实施例118:(3S)-N-(3-[2-[(3S,4S)-3,4-二羟基吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例118A:(3S,4S)-1-[4-碘-6-(吗啉-4-基)吡啶-2-基]吡咯烷-3,4-二醇
将4-(6-氟-4-碘吡啶-2-基)吗啉(200mg,0.649mmol)、K2CO3(358mg,2.597mmol)和(3S,4S)-吡咯烷-3,4-二醇盐酸盐(181mg,1.298mmol)在NMP(1.6mL)中的混合物在100℃和氮气氛下搅拌16h。将所得混合物用水(100mL)稀释。将所得混合物用EtOAc(3x100mL)萃取。将合并的有机层用盐水(2x100mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用己烷/EtOAc/EtOH(4/3/1)洗脱,得到呈白色固体的(3S,4S)-1-[4-碘-6-(吗啉-4-基)吡啶-2-基]吡咯烷-3,4-二醇(237mg,93%)。MS ESI:C13H18IN3O3[M+H]+的计算值:392.04,实测值:391.95。1H NMR(300MHz,DMSO-d6)δ6.31(s,1H),6.10(s,1H),5.06(s,2H),3.99-3.98(m,2H),3.68-3.65(m,4H),3.50-3.49(m,2H),3.46-3.45(m,4H),3.27-3.23(m,2H)。
实施例118:(3S)-N-(3-[2-[(3S,4S)-3,4-二羟基吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将(3S,4S)-1-[4-碘-6-(吗啉-4-基)吡啶-2-基]吡咯烷-3,4-二醇(120mg,0.307mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(113mg,0.276mmol)、Na2CO3(98mg,0.920mmol)、二噁烷(3mL)、H2O(0.75mL)和Pd(dppf)Cl2·CH2Cl2(25mg,0.031mmol)的混合物在60℃和氮气氛下搅拌3h。将所得混合物用水(50mL)稀释。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用盐水(2x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。残余物通过采用CH2Cl2/CH3OH(10:1)的制备型TLC纯化,得到呈灰白色固体的(3S)-N-(3-[2-[(3S,4S)-3,4-二羟基吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(76.3mg,45%)。MS ESI:C27H34F3N5O4[M+H]+的计算值:550.26,实测值:550.30。1H NMR(400MHz,DMSO-d6)δ8.12(s,1H),7.43(dd,J=2.0,8.4Hz,1H),7.34(d,J=2.0Hz,1H),7.10(d,J=8.4Hz,1H),5.84(s,1H),5.62(s,1H),5.04(d,J=3.2Hz,2H),4.01(s,2H),3.70-3.65(m,5H),3.54-3.51(m,3H),3.42-3.40(m,4H),3.30-3.29(m,3H),3.05-3.00(m,1H),2.48-2.41(m,3H),2.17(s,3H),2.10-2.07(m,1H),1.69-1.62(m,1H)。19F NMR(376MHz,DMSO-d6)δ-63.36(3F)。
实施例119:(3S)-N-(3-[2-[(3S,4S)-3-氟-4-羟基吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例119A:(3S,4S)-4-氟-1-[4-碘-6-(吗啉-4-基)吡啶-2-基]吡咯烷-3-醇
在130℃和氮气氛下,分数份向4-(6-氟-4-碘吡啶-2-基)吗啉(300mg,0.974mmol)和(3S,4S)-4-氟吡咯烷-3-醇盐酸盐(165mg,1.168mmol)在NMP(3mL)中的搅拌混合物中加入Cs2CO3(635mg,1.947mmol),搅拌2h。在室温下通过添加水(20mL)来猝灭反应。将所得混合物用EtOAc(3x20mL)萃取。将合并的有机层用盐水(2x5mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(5/1)洗脱,得到呈浅黄色固体的(3S,4S)-4-氟-1-[4-碘-6-(吗啉-4-基)吡啶-2-基]吡咯烷-3-醇(113mg,29%)。MSESI:C13H17FIN3O2[M+H]+的计算值:394.04,实测值:394.00。1H NMR(400MHz,氯仿-d)δ6.32(s,1H),6.19(s,1H),5.06(d,J=51.2Hz,1H),4.55-4.51(m,1H),3.85-3.66(m,7H),3.62-3.58(m,1H),3.52-3.44(m,4H)。
实施例119:(3S)-N-(3-[2-[(3S,4S)-3-氟-4-羟基吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将(3S,4S)-4-氟-1-[4-碘-6-(吗啉-4-基)吡啶-2-基]吡咯烷-3-醇(90mg,0.218mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(90mg,0.218mmol)、1,4-二噁烷(1.8mL)、H2O(0.45mL)、Na2CO3(69mg,0.653mmol)和Pd(dppf)Cl2·CH2Cl2(18mg,0.022mmol)的混合物在60℃和氮气氛下搅拌16h。通过添加水(5mL)来猝灭反应。将所得混合物用EtOAc(3x20mL)萃取。将合并的有机层用盐水(3x4mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(5/1)洗脱,得到呈灰白色固体的(3S)-N-(3-[2-[(3S,4S)-3-氟-4-羟基吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(74.9mg,62%)。MS ESI:C27H33F4N5O3[M+H]+的计算值:552.25,实测值:552.35。1H NMR(400MHz,氯仿-d)δ7.37(dd,J=2.4,8.4Hz,1H),7.23(d,J=2.4Hz,1H),7.18(d,J=8.4Hz,1H),6.21(s,1H),5.90(s,1H),5.74(s,1H),5.07(d,J=50.8Hz,1H),4.52-4.50(m,1H),3.92-3.71(m,8H),3.65-3.61(m,2H),3.52-3.50(m,4H),3.46-3.41(m,1H),3.11-3.07(m,1H),2.61-2.49(m,1H),2.33-2.20(m,6H),1.78-1.70(m,1H),1.70-1.66(m,1H)。19F NMR(376MHz,氯仿-d)δ-63.93(3F),-182.75(1F)。
实施例120:(3S)-N-[3-[2-环丙烷磺酰胺基-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2三氟乙基)吡咯烷-1-甲酰胺
制备例120A:N-[4-氯-6-(吗啉-4-基)吡啶-2-基]环丙烷磺酰胺
将4-氯-6-(吗啉-4-基)吡啶-2-胺(200mg,0.936mmol)在吡啶(6mL)和环丙烷磺酰氯(197mg,1.404mmol)中的混合物在室温下搅拌48h。将反应混合物减压浓缩。将残余物通过反相快速色谱法采用以下条件纯化:柱,C18硅胶;流动相,含CH3CN的水(含10mmol/LNH4HCO3),10%至95%梯度;检测器,UV 254nm,得到呈灰白色固体的N-[4-氯-6-(吗啉-4-基)吡啶-2-基]环丙烷磺酰胺(127mg,17%)。MS ESI:C12H16ClN3O3S[M+H]+的计算值:318.06,实测值:318.10。1H NMR(400MHz,氯仿-d)δ6.65(s,1H),6.34(s,1H),3.91-3.71(m,4H),3.59-3.39(m,4H),2.80-2.76m,1H),1.41-1.23(m,2H),1.19-0.97(m,2H)。
实施例120:(3S)-N-[3-[2-环丙烷磺酰胺基-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2三氟乙基)吡咯烷-1-甲酰胺
将N-[4-氯-6-(吗啉-4-基)吡啶-2-基]环丙烷磺酰胺(100mg,0.300mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(116.8mg,0.300mmol)、第2代XPhos预催化剂(24mg,0.030mmol)和K3PO4(135mg,0.640mmol)在THF(5mL)和H2O(0.5mL)中的混合物在80℃和氮气氛下搅拌2h。将所得混合物减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈灰白色固体的(3S)-N-[3-[2-环丙烷磺酰胺基-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2三氟乙基)吡咯烷-1-甲酰胺(69mg,38%)。MS ESI:C26H32F3N5O4S[M+H]+的计算值:568.21,实测值:568.15。1H NMR(400MHz,DMSO-d6)δ10.29(s,1H),8.17(s,1H),7.46(dd,J=8.4,2.4Hz,1H),7.37(d,J=2.4Hz,1H),7.14(d,J=8.4Hz,1H),6.32(s,1H),6.18(s,1H),3.86-3.62(m,5H),3.60-3.41(m,5H),3.32-3.27(m,1H),3.17-2.93(m,2H),2.50-2.29(m,3H),2.16(s,3H),2.09-2.07(m,1H),1.74-1.55(m,1H),1.04-1.02(m,4H)。19F NMR(282MHz,DMSO-d6)δ-63.36(3F)。
实施例121:(3S)-N-(3-[2-[(3S)-3-氨基-2-氧代吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例121A:N-[(3S)-1-[4-氯-6-(吗啉-4-基)吡啶-2-基]-2-氧代吡咯烷-3-基]氨基甲酸叔丁酯
将4-(4,6-二氯吡啶-2-基)吗啉(500mg,2.145mmol)、N-[(3S)-2-氧代吡咯烷-3-基]氨基甲酸叔丁酯(644mg,3.218mmol)、二噁烷(5mL)、Pd2(dba)3.CHCl3(222mg,0.215mmol)、XantPhos(248mg,0.429mmol)和Na2CO3(682mg,6.435mmol)的混合物在100℃和氮气氛下搅拌2h。将所得混合物用水(50mL)猝灭。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用盐水(50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈黄色固体的N-[(3S)-1-[4-氯-6-(吗啉-4-基)吡啶-2-基]-2-氧代吡咯烷-3-基]氨基甲酸叔丁酯(740mg,86%)。MS ESI:C18H25ClN4O4[M+H]+的计算值:397.16,实测值:397.25。1H NMR(400MHz,氯仿-d)δ7.80(d,J=1.2Hz,1H),6.38(d,J=1.2Hz,1H),5.22(s,1H),4.43-4.40(m,1H),4.26-4.16(m,1H),3.85-3.78(m,4H),3.75-3.71(m,1H),3.55-3.42(m,4H),2.74-2.70(m,1H),1.93-1.90(m,1H),1.49(s,9H)。
制备例121B:N-[(3S)-1-(4-[2-甲基-5-[(3S)-3-(2,2,2-三氟乙基)吡咯烷-1-羰基氨基]苯基]-6-(吗啉-4-基)吡啶-2-基)-2-氧代吡咯烷-3-基]氨基甲酸叔丁酯
将N-[(3S)-1-[4-氯-6-(吗啉-4-基)吡啶-2-基]-2-氧代吡咯烷-3-基]氨基甲酸叔丁酯(200mg,0.504mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(228mg,0.554mmol)、THF(5mL)、H2O(0.5mL)、第2代XPhos预催化剂(39mg,0.050mmol)和K3PO4(213mg,1.008mmol)的混合物在80℃和氮气氛下搅拌2h。将所得混合物减压浓缩。残余物通过采用PE/EtOAc/EtOH(4/3/1)的制备型TLC纯化,得到呈黄色油状物的N-[(3S)-1-(4-[2-甲基-5-[(3S)-3-(2,2,2-三氟乙基)吡咯烷-1-羰基氨基]苯基]-6-(吗啉-4-基)吡啶-2-基)-2-氧代吡咯烷-3-基]氨基甲酸叔丁酯(300mg,92%)。MS ESI:C32H41F3N6O5[M+H]+的计算值:647.31,实测值:647.35。
实施例121:(3S)-N-(3-[2-[(3S)-3-氨基-2-氧代吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将N-[(3S)-1-(4-[2-甲基-5-[(3S)-3-(2,2,2-三氟乙基)吡咯烷-1-羰基氨基]苯基]-6-(吗啉-4-基)吡啶-2-基)-2-氧代吡咯烷-3-基]氨基甲酸叔丁酯(200mg,0.309mmol)和TFA(1mL)在DCM(5mL)中的溶液在室温下搅拌1h。将所得混合物减压浓缩。将粗产物通过反相快速色谱法采用以下条件纯化:柱:球形C18,20~40μm,120g;流动相A:水(加0.05%FA);流动相B:CH3CN;流速:60mL/min;梯度:35%B至75%,检测器:220nm。将所得混合物用Na2CO3(1M,10mL)稀释。将所得混合物用EtOAc(2x15mL)萃取。将合并的有机层用盐水(15mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩,得到呈灰白色固体的(3S)-N-(3-[2-[(3S)-3-氨基-2-氧代吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(129mg,76%)。MS ESI:C27H33F3N6O3[M+H]+的计算值:547.26,实测值:547.25。1H NMR(400MHz,DMSO-d6)δ8.19(s,1H),7.62(s,1H),7.47(dd,J=2.0,8.4Hz,1H),7.39(d,J=2.0Hz,1H),7.15(d,J=8.4Hz,1H),6.45(s,1H),4.13-4.04(m,1H),3.77-3.65(m,6H),3.61-3.46(m,6H),3.31-3.27(m,1H),3.05-3.00(m,1H),2.51-2.40(m,3H),2.35-2.31(m,1H),2.17(s,3H),2.12-2.05(m,1H),1.91(s,2H),1.78-1.56(m,2H)。19F NMR(376MHz,DMSO-d6)δ-63.37(3F)。
实施例122:(3S)-N-(3-[2-[(4S)-4-氨基-2-氧代吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例122A:N-[(3S)-1-[4-氯-6-(吗啉-4-基)吡啶-2-基]-5-氧代吡咯烷-3-基]氨基甲酸叔丁酯
将4-(4,6-二氯吡啶-2-基)吗啉(500mg,2.145mmol)、N-[(3S)-5-氧代吡咯烷-3-基]氨基甲酸叔丁酯(644mg,3.218mmol)、Pd2(dba)3.CHCl3(222mg,0.215mmol)、Na2CO3(682mg,6.435mmol)和XantPhos(248mg,0.429mmol)在二噁烷(5mL)中的混合物在100℃和氮气氛下搅拌2h。将所得混合物用水(30mL)稀释。将所得混合物用EtOAc(3x30mL)萃取。将合并的有机层用盐水(30mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈浅黄色固体的N-[(3S)-1-[4-氯-6-(吗啉-4-基)吡啶-2-基]-5-氧代吡咯烷-3-基]氨基甲酸叔丁酯(750mg,88%)。MS ESI:C18H25ClN4O4[M+H]+的计算值:397.16,实测值:397.20。1H NMR(400MHz,氯仿-d)δ7.80(d,J=1.2Hz,1H),6.40(d,J=1.2Hz,1H),4.85-4.83(m,1H),4.40-4.38(m,1H),4.31-4.27(m,1H),4.01-3.93(m,1H),3.86-3.79(m,4H),3.54-3.45(m,4H),3.04-3.01(m,1H),2.58-2.54(m,1H),1.47(s,9H)。
制备例122B:N-[(3S)-1-(4-[2-甲基-5-[(3S)-3-(2,2,2-三氟乙基)吡咯烷-1-羰基氨基]苯基]-6-(吗啉-4-基)吡啶-2-基)-5-氧代吡咯烷-3-基]氨基甲酸叔丁酯
向N-[(3S)-1-[4-氯-6-(吗啉-4-基)吡啶-2-基]-5-氧代吡咯烷-3-基]氨基甲酸叔丁酯(200mg,0.504mmol)和(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(249mg,0.605mmol)在THF(6mL)和H2O(0.6mL)中的搅拌混合物中加入第2代XPhos预催化剂(39mg,0.050mmol)和K3PO4(213mg,1.008mmol)。将所得混合物在80℃和氮气氛下搅拌2h。将所得混合物减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc/EtOH(4/3/1)洗脱,得到呈浅黄色固体的N-[(3S)-1-(4-[2-甲基-5-[(3S)-3-(2,2,2-三氟乙基)吡咯烷-1-羰基氨基]苯基]-6-(吗啉-4-基)吡啶-2-基)-5-氧代吡咯烷-3-基]氨基甲酸叔丁酯(300mg,92%)。MS ESI:C32H41F3N6O5[M+H]+的计算值:647.31,实测值:647.15。
实施例122:(3S)-N-(3-[2-[(4S)-4-氨基-2-氧代吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在室温下,向N-[(3S)-1-(4-[2-甲基-5-[(3S)-3-(2,2,2-三氟乙基)吡咯烷-1-羰基氨基]苯基]-6-(吗啉-4-基)吡啶-2-基)-5-氧代吡咯烷-3-基]氨基甲酸叔丁酯(200mg,0.309mmol)在DCM(4mL)中的搅拌溶液中加入TFA(0.8mL)。将所得混合物在室温下搅拌1h。将所得混合物减压浓缩。将粗产物通过反相快速色谱法采用以下条件纯化:柱:球形C18,20~40μm,120g;流动相A:水(加0.05%FA);流动相B:CH3CN;流速:60mL/min;梯度:25%B至55%B,检测器:220nm,得到呈灰白色固体的(3S)-N-(3-[2-[(4S)-4-氨基-2-氧代吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(66mg,39%)。MS ESI:C27H33F3N6O3[M+H]+的计算值:547.26,实测值:547.30。1H NMR(400MHz,DMSO-d6)δ8.17(s,1H),7.59(s,1H),7.47(dd,J=2.4,8.4Hz,1H),7.38(d,J=2.4Hz,1H),7.14(d,J=8.8Hz,1H),6.43(s,1H),4.08-4.04(m,1H),3.76-3.59(m,6H),3.63-3.53(m,1H),3.56-3.43(m,5H),3.03(t,J=9.6Hz,1H),2.78-2.74(m,1H),2.48-2.36(m,3H),2.25-2.22(m,1H),2.16(s,3H),2.10-2.06(m,1H),1.85(brs,2H),1.66-1.55(m,1H)。19F NMR(282MHz,氯仿-d)δ-64.94(3F)。
实施例123:(3S)-N-(3-[2-[(3S)-3-氨基-3-甲基吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例123A:N-[(3S)-1-[4-碘-6-(吗啉-4-基)吡啶-2-基]-3-甲基吡咯烷-3-基]氨基甲酸叔丁酯
向4-(6-氟-4-碘吡啶-2-基)吗啉(693mg,2.249mmol)和N-[(3S)-3-甲基吡咯烷-3-基]氨基甲酸叔丁酯(450mg,2.249mmol)在NMP(15mL)中的搅拌溶液中加入K2CO3(932mg,6.748mmol)。将所得混合物在150℃和氮气氛下搅拌2h。将所得混合物用EtOAc(50mL)稀释。将合并的有机层用盐水(3x20mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(3/1)洗脱,得到呈白色固体的N-[(3S)-1-[4-碘-6-(吗啉-4-基)吡啶-2-基]-3-甲基吡咯烷-3-基]氨基甲酸叔丁酯(700mg,63%)。MS ESI:C19H29IN4O3[M+H]+的计算值:489.13,实测值:489.05。1H NMR(400MHz,氯仿-d)δ6.26(d,J=0.8Hz,1H),6.15(d,J=0.8Hz,1H),4.66(s,1H),3.85-3.76(m,4H),3.64(d,J=10.8Hz,1H),3.54-3.43(m,6H),3.39(d,J=10.8Hz,1H),2.43-2.33(m,1H),1.95-1.88(m,1H),1.51(s,3H),1.45(s,9H)。
制备例123B:N-[(3S)-3-甲基-1-(4-[2-甲基-5-[(3S)-3-(2,2,2-三氟乙基)吡咯烷-1-羰基氨基]苯基]-6-(吗啉-4-基)吡啶-2-基)吡咯烷-3-基]氨基甲酸叔丁酯
在室温下,向N-[(3S)-1-[4-碘-6-(吗啉-4-基)吡啶-2-基]-3-甲基吡咯烷-3-基]氨基甲酸叔丁酯(200mg,0.410mmol)和(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(185mg,0.450mmo)在二噁烷(6mL)和H2O(1.5mL)中的搅拌溶液中加入Pd(dppf)Cl2.CH2Cl2(33mg,0.041mmol)和Na2CO3(130mg,1.230mmol)。将所得混合物在60℃和氮气氛下搅拌2h。残余物通过制备型TLC(PE/EtOAc=1/1)纯化,得到呈浅棕色固体的N-[(3S)-3-甲基-1-(4-[2-甲基-5-[(3S)-3-(2,2,2-三氟乙基)吡咯烷-1-羰基氨基]苯基]-6-(吗啉-4-基)吡啶-2-基)吡咯烷-3-基]氨基甲酸叔丁酯(220mg,83%)。MS ESI:C33H45F3N6O4[M+H]+的计算值:647.35,实测值:647.30。
实施例123:(3S)-N-(3-[2-[(3S)-3-氨基-3-甲基吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将N-[(3S)-3-甲基-1-(4-[2-甲基-5-[(3S)-3-(2,2,2-三氟乙基)吡咯烷-1-羰基氨基]苯基]-6-(吗啉-4-基)吡啶-2-基)吡咯烷-3-基]氨基甲酸叔丁酯(200mg,0.309mmol)和TFA(1mL)在DCM(5mL)中的溶液在室温下搅拌1h。将所得混合物减压浓缩。将所得混合物用EtOAc(30mL)稀释。将合并的有机层用盐水(10mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将粗产物通过反相快速色谱法采用以下条件纯化:柱:球形C18,20~40μm,120g;流动相A:水(加10mM NH4CO3);流动相B:CH3CN;流速:60mL/min;梯度:25%B至55%B,检测器:220nm,得到呈浅绿色固体的(3S)-N-(3-[2-[(3S)-3-氨基-3-甲基吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(88mg,52%)。MS ESI:C28H37F3N6O2[M+H]+的计算值:547.29,实测值:547.30。1H NMR(300MHz,DMSO-d6)δ8.13(s,1H),7.44(dd,J=2.4,8.4Hz,1H),7.35(d,J=2.4Hz,1H),7.11(d,J=8.4Hz,1H),5.84(s,1H),5.61(s,1H),3.72-3.68(m,5H),3.55-3.23(m,10H),3.04(t,J=9.3Hz,1H),2.49-2.37(m,3H),2.18(s,3H),2.11-2.07(m,1H),1.81-1.60(m,5H),1.25(s,3H)。19FNMR(282MHz,DMSO-d6)δ-63.35(3F)。
实施例124:(3S)-N-(3-[2-[(3S)-3-氨基-3-甲基哌啶-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例124A:N-[(3S)-1-[4-碘-6-(吗啉-4-基)吡啶-2-基]-3-甲基哌啶-3-基]氨基甲酸叔丁酯
向4-(6-氟-4-碘吡啶-2-基)吗啉(646mg,2.100mmol)和N-[(3S)-3-甲基哌啶-3-基]氨基甲酸叔丁酯(450mg,2.100mmol)在NMP(5mL)中的搅拌溶液中加入K2CO3(870mg,6.299mmol)。将所得混合物在150℃和氮气氛下搅拌2h。将所得混合物用EtOAc(30mL)稀释。将合并的有机层用盐水(10mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc/EtOH(12/3/1)洗脱,得到呈浅黄色固体的N-[(3S)-1-[4-碘-6-(吗啉-4-基)吡啶-2-基]-3-甲基哌啶-3-基]氨基甲酸叔丁酯(270mg,25%)。MSESI:C20H31IN4O3[M+H]+的计算值:503.14,实测值:503.00。1H NMR(400MHz,氯仿-d)δ6.46(s,1H),6.31(s,1H),5.07(s,1H),4.20(d,J=13.2Hz,1H),3.97(d,J=12.9Hz,1H),3.83-3.79(m,4H),3.48-3.42(m,4H),3.03-2.82(m,1H),2.77(d,J=13.2Hz,1H),2.40-2.32(m,1H),1.75-1.55(m,3H),1.43(s,9H),1.39(s,3H)。
制备例124B:N-[(3S)-3-甲基-1-(4-[2-甲基-5-[(3S)-3-(2,2,2-三氟乙基)吡咯烷-1-羰基氨基]苯基]-6-(吗啉-4-基)吡啶-2-基)哌啶-3-基]氨基甲酸叔丁酯
向N-[(3S)-1-[4-碘-6-(吗啉-4-基)吡啶-2-基]-3-甲基哌啶-3-基]氨基甲酸叔丁酯(200mg,0.398mmol)和(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(180mg,0.438mmol)在1,4-二噁烷(2mL)和H2O(0.5mL)中的搅拌溶液中加入Pd(dppf)Cl2.CH2Cl2(32mg,0.040mmol)和Na2CO3(126.58mg,1.194mmol)。将所得混合物在60℃和氮气氛下搅拌2h。将所得混合物减压浓缩。残余物通过采用PE/EtOAc(1/1)的制备型TLC纯化,得到呈浅棕色固体的N-[(3S)-3-甲基-1-(4-[2-甲基-5-[(3S)-3-(2,2,2-三氟乙基)吡咯烷-1-羰基氨基]苯基]-6-(吗啉-4-基)吡啶-2-基)哌啶-3-基]氨基甲酸叔丁酯(230mg,87%)。MS ESI:C34H47F3N6O4[M+H]+的计算值:661.36,实测值:661.40。
实施例124:(3S)-N-(3-[2-[(3S)-3-氨基-3-甲基哌啶-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将N-[(3S)-3-甲基-1-(4-[2-甲基-5-[(3S)-3-(2,2,2-三氟乙基)吡咯烷-1-羰基氨基]苯基]-6-(吗啉-4-基)吡啶-2-基)哌啶-3-基]氨基甲酸叔丁酯(200mg,0.303mmol)和TFA(0.4mL)在DCM(2mL)中的溶液在室温下搅拌1h。将所得混合物减压浓缩。将残余物通过硅胶柱色谱法纯化,用CH2Cl2/MeOH(8/1)洗脱。将粗产物通过制备型HPLC采用以下条件纯化:柱:XBridge制备型苯基OBD柱,19×150mm,5μm;流动相A:水(10mmol/L NH4HCO3),流动相B:CH3CN;流速:20mL/min;梯度:40%B至50%B;254/210nm,得到呈白色固体的(3S)-N-(3-[2-[(3S)-3-氨基-3-甲基哌啶-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(29mg,17%)。MS ESI:C29H39F3N6O2[M+H]+的计算值:560.31,实测值:561.30。1H NMR(400MHz,DMSO-d6)δ8.13(s,1H),7.43(dd,J=8.4,2.4Hz,1H),7.34(d,J=2.4Hz,1H),7.11(d,J=8.4Hz,1H),6.01(s,1H),5.91(s,1H),3.73-3.62(m,5H),3.54-3.52(m,2H),3.42-3.38(m,5H),3.30-3.25(m,3H),3.02(t,J=9.6Hz,1H),2.50-2.42(m,4H),2.16(s,3H),2.10-2.06(m,1H),1.67-1.60(m,2H),1.55-1.50(m,3H),1.07(s,3H)。19FNMR(376MHz,DMSO-d6)δ-63.37(3F)。
实施例125:(3S)-N-(3-[2-[(4R)-4-羟基-2-氧代吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例125A:(4R)-1-[4-氯-6-(吗啉-4-基)吡啶-2-基]-4-羟基吡咯烷-2-酮
将4-(4,6-二氯吡啶-2-基)吗啉(500mg,2.145mmol)、(4R)-4-羟基吡咯烷-2-酮(195mg,1.931mmol)、Pd2(dba)3·CHCl3(222mg,0.215mmol)、XantPhos(248mg,0.429mmol)和Na2CO3(455mg,4.290mmol)在二噁烷(5mL)中的混合物在100℃和氮气氛下搅拌2h。将所得混合物减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈棕色固体的(4R)-1-[4-氯-6-(吗啉-4-基)吡啶-2-基]-4-羟基吡咯烷-2-酮(550mg,78%)。MSESI:C13H16ClN3O3[M+H]+的计算值:298.09,实测值:298.05。1H NMR(400MHz,氯仿-d)δ7.83(s,1H),6.36(s,1H),4.60(s,1H),4.19(dd,J=12.4,5.2Hz,1H),4.14-4.09(m,1H),3.87-3.79(m,4H),3.52-3.45(m,4H),2.97(dd,J=17.6,6.3Hz,1H),2.68-2.62(m,1H),2.10(s,1H)。
实施例125:(3S)-N-(3-[2-[(4R)-4-羟基-2-氧代吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将(4R)-1-[4-氯-6-(吗啉-4-基)吡啶-2-基]-4-羟基吡咯烷-2-酮(150mg,0.504mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(166mg,0.403mmol)、第2代XPhos预催化剂(40mg,0.050mmol)和K3PO4(214mg,1.008mmol)在THF(1.5mL)和H2O(0.2mL)中的混合物在80℃和氮气氛下搅拌2h。通过添加水(10mL)来猝灭反应。将所得混合物用EtOAc(2x20mL)萃取。将合并的有机层用盐水(10mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。残余物通过采用PE/EtOAc/EtOH(8/3/1)的制备型TLC纯化,得到呈灰白色固体的(3S)-N-(3-[2-[(4R)-4-羟基-2-氧代吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(126mg,45%)。MS ESI:C27H32F3N5O4[M+H]+的计算值:548.24,实测值:548.25。1H NMR(400MHz,DMSO-d6)δ8.18(s,1H),7.60(s,1H),7.48(dd,J=8.4,2.4Hz,1H),7.38(d,J=2.4Hz,1H),7.14(d,J=8.4Hz,1H),6.44(s,1H),5.27(s,1H),4.37-4.35(m,1H),4.09-4.05(m,1H),4.00-3.97(m,1H),3.73-3.70(m,5H),3.68-3.46(m,5H),3.33-3.28(m,1H),3.05-2.91(m,1H),2.89-2.87(m,1H),2.53-2.32(m,4H),2.16(s,3H),2.10-2.07(m,1H),1.68-1.63(m,1H)。19F NMR(376MHz,DMSO-d6)δ-63.37(3F)。
实施例126:(3S)-N-[3-[2-(1,1-二氧代-1λ6,2-噻唑烷-2-基)-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例126A:2-[6-(吗啉-4-基)吡啶-2-基]-1λ6,2-噻唑烷-1,1-二酮
在0℃下,向4-氯-6-(吗啉-4-基)吡啶-2-胺(250mg,1.200mmol)、吡啶(0.5mL)和DIEA(756mg,6.000mmol)在DCE(5mL)中的搅拌混合物中逐滴加入3-氯丙烷-1-磺酰氯(414mg,2.300mmol)。将反应混合物搅拌3h,并且用饱和Na2CO3(50mL)猝灭。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用盐水(50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈灰白色固体的2-[6-(吗啉-4-基)吡啶-2-基]-1λ6,2-噻唑烷-1,1-二酮(200mg,34%)。MS ESI:C12H16ClN3O3S[M+H]+的计算值:318.06,实测值:318.05。1H NMR(300MHz,氯仿-d)δ6.52(d,J=1.2Hz,1H),6.29(d,J=1.2Hz,1H),3.94(t,J=6.8Hz,2H),3.86-3.74(m,4H),3.51-3.49(m,4H),3.41(t,J=7.2Hz,2H),2.51-2.46(m,2H)。
实施例126:(3S)-N-[3-[2-(1,1-二氧代-1λ6,2-噻唑烷-2-基)-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将2-[4-氯-6-(吗啉-4-基)吡啶-2-基]-1λ6,2-噻唑烷-1,1-二酮(200mg,0.630mmol)、(3S)-N-[4-甲基-3-(4,4,5-三甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(200mg,0.500mmol)、K3PO4(267mg,0.130mmol)和第2代XPhos预催化剂(53mg,0.006mmol)在THF(2mL)和H2O(0.2mL)中的混合物在80℃和氮气氛下搅拌2h。将所得混合物减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈灰白色固体的(3S)-N-[3-[2-(1,1-二氧代-1λ6,2-噻唑烷-2-基)-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(115mg,32%)。MSESI:C26H32F3N5O4S[M+H]+的计算值:568.21,实测值:568.15。1H NMR(400MHz,氯仿-d)δ7.43(dd,J=8.0,2.4Hz,1H),7.24-7.12(m,2H),6.48(s,1H),6.25(s,1H),6.18(s,1H),4.00(t,J=6.8Hz,2H),3.93-3.69(m,5H),3.67-3.62(m,1H),3.58-3.48(m,4H),3.48-3.37(m,3H),3.15-3.10(m,1H),2.62-2.47(m,3H),2.34-2.21(m,6H),1.81-1.70(m,1H)。19F NMR(376MHz,氯仿-d)δ-64.95(3F)。
实施例127:(S)-N-(3-(2-((R)-4-氨基-2-氧代吡咯烷-1-基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例127A:(R)-(1-(4-氯-6-吗啉基吡啶-2-基)-5-氧代吡咯烷-3-基)氨基甲酸叔丁酯
将4-(4,6-二氯吡啶-2-基)吗啉(500mg,2.160mmol)和(R)-(5-氧代吡咯烷-3-基)氨基甲酸叔丁酯(648mg,3.240mmol)、二噁烷(5mL)、Pd2(dba)3.CHCl3(228mg,0.220mmol)、Xantphos(254mg,0.440mmol)和Na2CO3(687mg,6.480mmol)的混合物在100℃和氮气氛下搅拌2h。将所得混合物减压浓缩。将残余物通过硅胶柱色谱法纯化,用EtOAc/PE(1/4)洗脱,得到呈黄色固体的(R)-(1-(4-氯-6-吗啉基吡啶-2-基)-5-氧代吡咯烷-3-基)氨基甲酸叔丁酯(567.8mg,67%)。MS ESI:C18H25ClN4O4[M+H]+的计算值:397.16,实测值:397.10。1H NMR(400MHz,氯仿-d6)δ7.76(s,1H),6.35(s,1H),4.92(s,1H),4.37(s,1H),4.26(dd,J=12.0,6.4Hz,1H),3.94(dd,J=12.0,3.2Hz,1H),3.82-3.76(m,4H),3.48-3.41(m,4H),3.03-2.97(m,1H),2.56-2.51(m,1H),1.45(s,9H)。
制备例127B:((R)-1-(4-(2-甲基-5-((S)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺基)苯基)-6-吗啉基吡啶-2-基)-5-氧代吡咯烷-3-基)氨基甲酸叔丁酯
将(R)-(1-(4-氯-6-吗啉基吡啶-2-基)-5-氧代吡咯烷-3-基)氨基甲酸叔丁酯(200mg,0.505mmol)和(S)-N-(4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(250mg,0.606mmol)、第2代XPhos预催化剂(40mg,0.051mmol)和K3PO4(212mg,1.010mmol)在THF(5mL)和H2O(0.5mL)中的混合物在80℃和氮气氛下搅拌3h。将所得混合物减压浓缩。将残余物通过硅胶柱色谱法纯化,用EtOAc/PE(1/1)洗脱,得到呈浅黄色固体的((R)-1-(4-(2-甲基-5-((S)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺基)苯基)-6-吗啉基吡啶-2-基)-5-氧代吡咯烷-3-基)氨基甲酸叔丁酯(293mg,90%)。MS ESI:C32H41F3N6O5 +[M+H]+的计算值:647.31,实测值:647.20。
实施例127:(S)-N-(3-(2-((R)-4-氨基-2-氧代吡咯烷-1-基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将((R)-1-(4-(2-甲基-5-((S)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺基)苯基)-6-吗啉基吡啶-2-基)-5-氧代吡咯烷-3-基)氨基甲酸叔丁酯(200mg,0.309mmol)、DCM(5.0mL)和TFA(0.5mL)的混合物在室温下搅拌30min。将所得混合物减压浓缩。将残余物通过制备型HPLC采用以下条件纯化:柱:球形C18,20~40μm,120g;流动相A:水(加10mMNH4CO3);流动相B:CH3CN;流速:60mL/min;梯度:35%B至65%B;检测器:220nm,得到呈白色固体的(S)-N-(3-(2-((R)-4-氨基-2-氧代吡咯烷-1-基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(90.5mg,53%)。MS ESI:C27H33F3N6O3[M+H]+的计算值:547.26,实测值:547.30。1H NMR(400MHz,氯仿-d6)δ7.75(s,1H),7.36(dd,J=8.4,2.4Hz,1H),7.22(d,J=2.4Hz,1H),7.16(d,J=8.4Hz,1H),6.31(s,1H),6.20(s,1H),4.32-4.27(m,1H),3.93-3.87(m,1H),3.82-3.78(m,6H),3.63-3.60(m,1H),3.49-3.37(m,5H),3.12-3.08(m,1H),2.94-2.90(m,1H),2.60-2.43(m,2H),2.29-2.20(m,6H),1.76-1.63(m,3H)。19F NMR(376MHz,氯仿-d6)δ-64.94(3F)。
实施例128和129:(3S)-N-(3-{2-[(4R)-3,3-二氟-4-羟基吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基}-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺和(3S)-N-(3-{2-[(4S)-3,3-二氟-4-羟基吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基}-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例128A:4,4-二氟吡咯烷-3-醇盐酸盐
在0℃下,向3,3-二氟-4-羟基吡咯烷-1-甲酸叔丁酯(300mg,1.344mmol)在DCM(5mL)中的搅拌溶液中逐滴加入含HCl的二噁烷(1mL,1M)。将所得混合物在室温下搅拌2h。将所得混合物减压浓缩,得到呈黄色油状物的4,4-二氟吡咯烷-3-醇盐酸盐(350mg,粗物质)。C4H8ClF2NO,1H NMR(400MHz,DMSO-d6)δ4.33-4.31(m,1H),3.59-3.52(m,2H),3.51-3.45(m,1H),3.29-3.26(m,1H)。
制备例128B:4-碘-N-(4-甲基氧杂环己烷-4-基)-6-(吗啉-4-基)吡啶-2-胺
在室温下,向2,6-二氟-4-碘吡啶(350mg,1.452mmol)和4,4-二氟吡咯烷-3-醇盐酸盐(214mg,1.742mmol)在DMSO(5mL)中的搅拌溶液中加入DIEA(412mg,3.194mmol)。将所得混合物在80℃下搅拌4h。向这个混合物中加入吗啉(632mg,7.260mmol)。将所得混合物在80℃下搅拌16h。使混合物冷却至室温。将所得混合物用H2O(50mL)稀释,并且用EtOAc(3x50mL)萃取。将合并的有机层用盐水(50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(4/1)洗脱,得到呈黄色固体的4-碘-N-(4-甲基氧杂环己烷-4-基)-6-(吗啉-4-基)吡啶-2-胺(240mg,40%)。MS ESI:C13H16F2IN3O2[M+H]+的计算值:412.03,实测值:412.05。1H NMR(400MHz,氯仿-d)δ6.36(s,1H),6.14(s,1H),4.40-4.36(m,1H),3.88-3.74(m,7H),3.55-3.53(m,1H),3.50-3.42(m,4H)。
制备例128C:(3S)-N-[3-[2-(3,3-二氟-4-羟基吡咯烷-1-基)-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将4,4-二氟-1-[4-碘-6-(吗啉-4-基)吡啶-2-基]吡咯烷-3-醇(240mg,0.584mmol)和(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(240mg,0.582mmol)、1,4-二噁烷(2.4mL)、H2O(0.6mL)、Pd(dppf)Cl2.CH2Cl2(47mg,0.058mmol)和Na2CO3(185mg,1.752mmol)的混合物在60℃和氮气氛下搅拌2h。将反应用水(50mL)猝灭。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用盐水(30mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc/EtOH(2/3/1)洗脱,得到呈白色固体的(3S)-N-[3-[2-(3,3-二氟-4-羟基吡咯烷-1-基)-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(265mg,79%)。MS ESI:C27H32F5N5O3[M+H]+的计算值:570.24,实测值:570.30。
实施例128和129:(3S)-N-(3-{2-[(4R)-3,3-二氟-4-羟基吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基}-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺和(3S)-N-(3-{2-[(4S)-3,3-二氟-4-羟基吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基}-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
(3S)-N-{3-[2-(3,3-二氟-4-羟基吡咯烷-1-基)-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基}-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(265mg,0.465mmol)通过手性制备型HPLC采用以下条件进行拆分:柱:(R,R)-WHELK-O1-Kromasil,2.11*25cm,5μm;流动相A:Hex(0.5%2M NH3-MeOH),流动相B:EtOH;A:B=50:50;220/254nm。
RT1:29.71min产生了55mg(20%)的白色固体。MS ESI:C27H32F5N5O3[M+H]+的计算值:570.24,实测值:570.20。1H NMR(400MHz,DMSO-d6)δ8.12(s,1H),7.43(dd,J=8.4,2.4Hz,1H),7.33(d,J=2.0Hz,1H),7.11(d,J=8.4Hz,1H),6.05(d,J=5.2Hz,1H),5.95(s,1H),5.73(s,1H),4.35-4.31(m,1H),3.95-3.61(m,9H),3.52-3.49(m,1H),3.43-3.3.30(m,5H),3.02(t,J=9.6Hz,1H),2.42-2.30(m,3H),2.17(s,3H),2.10-2.06(m,1H),1.66-1.55(m,1H)。19F NMR(376MHz,DMSO-d6)δ-66.36(3F),-109.20(d,J=230.5Hz,1F),-120.58(d,J=230.5Hz,1F)。
RT2:39.58min产生了55mg(20%),呈白色固体。MS ESI:C27H32F5N5O3[M+H]+的计算值:570.24,实测值:570.20。1H NMR(400MHz,DMSO-d6)δ8.12(s,1H),7.43(dd,J=8.4,2.4Hz,1H),7.33(d,J=2.0Hz,1H),7.11(d,J=8.4Hz,1H),5.95(s,1H),5.73(s,1H),4.35-4.31(m,1H),3.95-3.61(m,9H),3.53-3.51(m,1H),3.41-3.29(m,5H),3.02(t,J=9.6Hz,1H),2.42-2.37(m,3H),2.17(s,3H),2.12-2.07(m,1H),1.66-1.62(m,1H)。19F NMR(376MHz,DMSO-d6)δ-58.61(3F),-104.46(d,J=230.5Hz,1F),-115.83(d,J=230.5Hz,1F)。
实施例130和131:(3S)-N-(3-{2-[(1R)-1-氨基-3-氮杂双环[3.1.0]己烷-3-基]-6-(吗啉-4-基)吡啶-4-基}-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺和(3S)-N-(3-{2-[(1S)-1-氨基-3-氮杂双环[3.1.0]己烷-3-基]-6-(吗啉-4-基)吡啶-4-基}-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例130A:N-[3-[4-碘-6-(吗啉-4-基)吡啶-2-基]-3-氮杂双环[3.1.0]己烷-1-基]氨基甲酸叔丁酯
向4-(6-氟-4-碘吡啶-2-基)吗啉(400mg,1.298mmol)和N-[3-氮杂双环[3.1.0]己烷-1-基]氨基甲酸叔丁酯(309mg,1.558mmol)在NMP(4mL)中的搅拌混合物中加入Cs2CO3(1.27g,3.895mmol)。将反应混合物在130℃和氮气氛下搅拌2h。将反应用水(20mL)猝灭。将所得混合物用EtOAc(3x20mL)萃取。将合并的有机层用盐水(20mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(5/1)洗脱,得到呈浅黄色固体的N-[3-[4-碘-6-(吗啉-4-基)吡啶-2-基]-3-氮杂双环[3.1.0]己烷-1-基]氨基甲酸叔丁酯(100mg,16%)。MS ESI:C19H27IN4O3[M+H]+的计算值:487.11;实测值:487.05。1H NMR(400MHz,氯仿-d)δ6.30(s,1H),6.15(s,1H),5.05(brs,1H),3.93-3.91(m,1H),3.85-3.78(m,4H),3.62-3.60(m,2H),3.45-3.41(m,5H),1.81-1.79(m,1H),1.47(s,9H),1.10-1.08(m,1H),0.76-0.74(m,1H)。
制备例130B:N-[3-(4-[2-甲基-5-[(3S)-3-(2,2,2-三氟乙基)吡咯烷-1-羰基氨基]苯基]-6-(吗啉-4-基)吡啶-2-基)-3-氮杂双环[3.1.0]己烷-1-基]氨基甲酸叔丁酯
在60℃和氮气氛下,分数份向(3-(4-碘-6-吗啉基吡啶-2-基)-3-氮杂双环[3.1.0]己烷-1-基)氨基甲酸叔丁酯(150mg,0.316mmol)和(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(130mg,0.316mmol)在1,4-二噁烷(2mL)和H2O(0.5mL)中的搅拌混合物中加入Na2CO3(100mg,0.949mmol)和Pd(dppf)Cl2.CH2Cl2(26mg,0.032mmol),搅拌16h。在室温下用水(10mL)猝灭反应。将所得混合物用EtOAc(3x20mL)萃取。将合并的有机层用盐水(10mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。残余物通过采用PE/EtOAc(1/1)的制备型TLC纯化,得到呈灰白色固体的N-[3-(4-[2-甲基-5-[(3S)-3-(2,2,2-三氟乙基)吡咯烷-1-羰基氨基]苯基]-6-(吗啉-4-基)吡啶-2-基)-3-氮杂双环[3.1.0]己烷-1-基]氨基甲酸叔丁酯(144mg,71%)。MS ESI:C33H43F3N6O4[M+H]+的计算值:645.33;实测值:645.25。
制备例130C/131C:N-[(1R)-3-(4-{2-甲基-5-[(3S)-3-(2,2,2-三氟乙基)吡咯烷-1-羰基氨基]苯基}-6-(吗啉-4-基)吡啶-2-基)-3-氮杂双环[3.1.0]己烷-1-基]氨基甲酸叔丁酯和N-[(1S)-3-(4-{2-甲基-5-[(3S)-3-(2,2,2-三氟乙基)吡咯烷-1-羰基氨基]苯基}-6-(吗啉-4-基)吡啶-2-基)-3-氮杂双环[3.1.0]己烷-1-基]氨基甲酸叔丁酯
N-[3-(4-{2-甲基-5-[(3S)-3-(2,2,2-三氟乙基)吡咯烷-1-羰基氨基]苯基}-6-(吗啉-4-基)吡啶-2-基)-3-氮杂双环[3.1.0]己烷-1-基]氨基甲酸叔丁酯(144mg,0.223mmol)通过手性制备型HPLC采用以下条件进行拆分:柱:(R,R)-WHELK-O1-Kromasil,2.11x25cm,5μm;流动相A:MTBE(0.5%2M NH3-MeOH),流动相B:EtOH;流速:20mL/min;梯度:10%B;220/254nm。RT1:20.89min产生了67mg(46%)的制备例130C。RT2:24.627min产生了76mg(53%)的呈灰白色固体的制备例131C。
实施例130/131:(3S)-N-(3-{2-[(1R)-1-氨基-3-氮杂双环[3.1.0]己烷-3-基]-6-(吗啉-4-基)吡啶-4-基}-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺以及(3S)-N-(3-{2-[(1S)-1-氨基-3-氮杂双环[3.1.0]己烷-3-基]-6-(吗啉-4-基)吡啶-4-基}-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将制备例130C(60mg,0.093mmol)在DCM(1.5mL)和TFA(0.3mL)中的混合物在室温下搅拌1h。将所得混合物减压浓缩。将残余物通过反相快速色谱法采用以下条件纯化:柱,C18柱;流动相,含CH3CN的水,10%至50%;检测器,UV 254nm,得到呈灰白色固体的实施例130(34.2mg,67%)。MS ESI:C28H35F3N6O2[M+H]+的计算值:545.28;实测值:545.20。1H NMR(300MHz,氯仿-d)δ7.40-7.38(m,1H),7.28-7.17(m,2H),6.11(s,1H),5.85(s,1H),5.68(s,1H),3.95(d,J=9.6Hz,1H),3.85-3.82(m,5H),3.79-3.70(m,2H),3.69-3.43(m,6H),3.34(d,J=9.6Hz,1H),3.12(t,J=9.6Hz,1H),2.65-2.50(m,1H),2.30-2.23(m,6H),1.57-1.53(m,2H),1.06-1.01(m,1H),0.69-0.66(m,1H)。19F NMR(282MHz,氯仿-d)δ-64.95(3F)。
将制备例131C在DCM(1.5mL)和TFA(0.3mL)中的混合物在室温和空气氛下搅拌1h。将所得混合物减压浓缩。将残余物通过反相快速色谱法采用以下条件纯化:柱,硅胶;流动相,含MeCN的水,在10min内10%至50%梯度;检测器,UV 254nm,得到呈灰白色固体的实施例131(40.3mg,68%)。MS ESI:C28H35F3N6O2[M+H]+的计算值:545.28;实测值:545.25。1H NMR(400MHz,氯仿-d)δ7.40-7.38(m,1H),7.28-7.17(m,2H),6.11(s,1H),5.83(s,1H),5.66(s,1H),3.93(d,J=9.6Hz,1H),3.84-3.78(m,5H),3.68-3.52(m,2H),3.50-3.40(m,6H),3.33(d,J=10.0Hz,1H),3.12(t,J=9.6Hz,1H),2.58-2.50(m,1H),2.28-2.18(m,6H),1.57-1.53(m,1H),1.06-1.01(m,1H),0.69-0.66(m,1H)。19F NMR(376MHz,氯仿-d)δ-64.95(3F)。
实施例132:(S)-N-(3-(2-((R)-4-氨基-2-氧代吡咯烷-1-基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺甲酸盐
制备例132A:(R)-(1-(4-氯-6-吗啉基吡啶-2-基)-2-氧代吡咯烷-3-基)氨基甲酸叔丁酯
将4-(4,6-二氯吡啶-2-基)吗啉(500mg,2.160mmol)和(R)-(2-氧代吡咯烷-3-基)氨基甲酸叔丁酯(648mg,3.240mmol)、Pd2(dba)3.CHCl3(228mg,0.220mmol)、Xantphos(254mg,0.440mmol)和Na2CO3(687mg,6.480mmol)在二噁烷(5mL)中的混合物在100℃和氮气氛下搅拌2h。将所得混合物减压浓缩。将残余物通过硅胶柱色谱法纯化,用EtOAc/PE(1/4)洗脱,得到呈黄色固体的(R)-(1-(4-氯-6-吗啉基吡啶-2-基)-2-氧代吡咯烷-3-基)氨基甲酸叔丁酯(680mg,80%)。MS ESI:C18H25ClN4O4[M+H]+的计算值:397.16,实测值:397.05。1HNMR(400MHz,氯仿-d)δ7.79(s,1H),6.37(s,1H),5.19(s,1H),4.39-4.37(m,1H),4.20-4.17(m,1H),3.82-3.78(m,4H),3.76-3.69(m,1H),3.47-3.45(m,4H),2.73-2.70(m,1H),1.94-1.90(m,1H),1.47(s,9H)。
制备例132B:((R)-1-(4-(2-甲基-5-((S)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺基)苯基)-6-吗啉基吡啶-2-基)-2-氧代吡咯烷-3-基)氨基甲酸叔丁酯
将(R)-(1-(4-氯-6-吗啉基吡啶-2-基)-2-氧代吡咯烷-3-基)氨基甲酸叔丁酯(200mg,0.505mmol)、(S)-N-(4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(250mg,0.606mmol)、第2代XPhos预催化剂(40mg,0.051mmol)和K3PO4(212mg,1.010mmol)在THF(5.0mL)和H2O(0.5mL)中的混合物在80℃和氮气氛下搅拌3h。将所得混合物减压浓缩。将残余物通过硅胶柱色谱法纯化,用EtOAc/PE(1/1)洗脱,得到呈浅黄色固体的((R)-1-(4-(2-甲基-5-((S)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺基)苯基)-6-吗啉基吡啶-2-基)-2-氧代吡咯烷-3-基)氨基甲酸叔丁酯(309mg,96%)。MS ESI:C32H41F3N6O5[M+H]+的计算值:647.31,实测值:647.20。
实施例132:(S)-N-(3-(2-((R)-4-氨基-2-氧代吡咯烷-1-基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺甲酸盐
将((R)-1-(4-(2-甲基-5-((S)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺基)苯基)-6-吗啉基吡啶-2-基)-2-氧代吡咯烷-3-基)氨基甲酸叔丁酯(200mg,0.309mmol)、DCM(5mL)和TFA(0.5mL)的混合物在室温下搅拌30min。将所得混合物减压浓缩。将残余物通过制备型HPLC采用以下条件纯化:柱:球形C18,20~40μm,120g;流动相A:水(加10mM FA);流动相B:CH3CN;流速:60mL/min;梯度:35%B至65%B;检测器:220nm,得到呈白色固体的(S)-N-(3-(2-((R)-4-氨基-2-氧代吡咯烷-1-基)-6-吗啉基吡啶-4-基)-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺甲酸盐(100.2mg,59%)。MS ESI:C28H35F3N6O5[M–HCOO]+的计算值:547.26,实测值:547.30。1H NMR(400MHz,氯仿-d)δ8.18(s,1H),7.68(s,1H),7.36(dd,J=8.4,2.4Hz,1H),7.22(d,J=2.4Hz,1H),7.14(d,J=8.4Hz,1H),6.47(s,1H),6.34(s,1H),4.26-4.15(m,1H),3.95-3.68(m,7H),3.65-3.56(m,1H),3.49-3.46(m,4H),3.42-3.20(m,3H),3.09-3.06(m,1H),2.55-2.50(m,2H),2.32-2.10(m,6H),1.97-1.86(m,1H),1.73-1.61(m,1H)。19F NMR(376MHz,氯仿-d6)δ-64.92(3F)。
实施例133和134:(3S)-N-(3-{2-[(4R)-4-氨基-3,3-二氟吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基}-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺和(3S)-N-(3-{2-[(4S)-4-氨基-3,3-二氟吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基}-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例133A:4-{[(苯甲基氧基)羰基]氨基}-3,3-二氟吡咯烷-1-甲酸叔丁酯
在0℃下,向4-氨基-3,3-二氟吡咯烷-1-甲酸叔丁酯(200mg,0.900mmol)和Na2CO3(114mg,1.080mmol)在1,4-二噁烷(2mL)和H2O(2mL)中的搅拌溶液中加入Cbz-Cl(184mg,1.080mmol)。将所得混合物在室温下搅拌4h。将反应混合物用水(30mL)稀释。将所得混合物用EtOAc(3x30mL)萃取。将合并的有机层用盐水(30mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩,得到呈黄色油状物的4-{[(苯甲基氧基)羰基]氨基}-3,3-二氟吡咯烷-1-甲酸叔丁酯(700mg,粗物质)。MS ESI:C17H22F2N2O4[M–Boc+H]+的计算值:257.15;实测值:257.10。
制备例133B:N-(4,4-二氟吡咯烷-3-基)氨基甲酸苯甲酯2,2,2-三氟乙酸盐
在0℃下,向4-{[(苯甲基氧基)羰基]氨基}-3,3-二氟吡咯烷-1-甲酸叔丁酯(700mg,1.964mmol)在DCM(10mL)中的搅拌溶液中逐滴加入TFA(2mL)。将所得混合物在室温下搅拌2h。将所得混合物减压浓缩,得到呈黄色油状物的N-(4,4-二氟吡咯烷-3-基)氨基甲酸苯甲酯2,2,2-三氟乙酸盐(750mg,粗物质)。MS ESI:C14H15F5N2O4[M–CF3COO]+的计算值:257.10,实测值:257.10。
制备例133C:6-氟-4-碘-N-(4-甲基氧杂环己烷-4-基)吡啶-2-胺
将2,6-二氟-4-碘吡啶(700mg,2.905mmol)、N-(4,4-二氟吡咯烷-3-基)氨基甲酸苯甲酯2,2,2-三氟乙酸盐(893mg,3.486mmol)在DMSO(7mL)和DIEA(825mg,6.391mmol)中的溶液在80℃下搅拌4h。将所得混合物用H2O(50mL)稀释,并且用EtOAc(3x50mL)萃取。将合并的有机层用盐水(15mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(4/1)洗脱,得到呈黄色固体的6-氟-4-碘-N-(4-甲基氧杂环己烷-4-基)吡啶-2-胺(550mg,56%)。MS ESI:C17H15F3IN3O2[M+H]+的计算值:478.02,实测值:477.90。
制备例133D:N-[4,4-二氟-1-[4-碘-6-(吗啉-4-基)吡啶-2-基]吡咯烷-3-基]氨基甲酸苯甲酯
在室温下,向N-[4,4-二氟-1-(6-氟-4-碘吡啶-2-基)吡咯烷-3-基]氨基甲酸苯甲酯(500mg,1.048mmol)和吗啉(109mg,1.257mmol)在DMSO(5.00mL)中的搅拌溶液中加入DIEA(203mg,1.572mmol)。将所得混合物在80℃下搅拌16h。将反应用水(50mL)猝灭。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用盐水(2x30mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EA(2/1)洗脱,得到呈白色固体的N-[4,4-二氟-1-[4-碘-6-(吗啉-4-基)吡啶-2-基]吡咯烷-3-基]氨基甲酸苯甲酯(480mg,84%)。MS ESI:C21H23F2IN4O3[M+H]+的计算值:545.08,实测值:545.10。1H NMR(400MHz,氯仿-d)δ7.40-7.30(m,5H),6.36(s,1H),6.10(s,1H),5.15(s,2H),4.66-4.62(m,1H),4.04-3.98(m,1H),3.90-3.67(m,7H),3.49-3.40(m,4H),3.24-3.20(m,1H)。
制备例133E:N-[4,4-二氟-1-(4-{2-甲基-5-[(3S)-3-(2,2,2-三氟乙基)吡咯烷-1-羰基氨基]苯基}-6-(吗啉-4-基)吡啶-2-基)吡咯烷-3-基]氨基甲酸苯甲酯
将N-{4,4-二氟-1-[4-碘-6-(吗啉-4-基)吡啶-2-基]吡咯烷-3-基}氨基甲酸苯甲酯(300mg,0.551mmol)、N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-2-(三氟甲基)吡啶-4-甲酰胺(223mg,0.551mmol)、1,4-二噁烷(3mL)、H2O(0.7mL)、Pd(dppf)Cl2.CH2Cl2(45mg,0.055mmol)和K2CO3(152mg,1.101mmol)的混合物在80℃和氮气氛下搅拌2h。将反应用水(50mL)猝灭。将所得混合物用EtOAc(3x50mL)萃取。将合并的有机层用盐水(2x30mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc/EtOH(2/3/1)洗脱,得到呈黄色油状物的N-[4,4-二氟-1-(4-{2-甲基-5-[(3S)-3-(2,2,2-三氟乙基)吡咯烷-1-羰基氨基]苯基}-6-(吗啉-4-基)吡啶-2-基)吡咯烷-3-基]氨基甲酸苯甲酯(300mg,77%)。MS ESI:C35H39F5N6O4[M+H]+的计算值:703.30,实测值:703.15。1H NMR(400MHz,氯仿-d)δ7.42-7.35(m,6H),7.23(d,J=2.4Hz,1H),7.18(d,J=8.4Hz,1H),6.14(s,1H),5.99(s,1H),5.71(s,1H),5.21-5.17(m,3H),4.74-4.68(m,1H),4.12-4.07(m,1H),3.98-3.77(m,7H),3.64(t,J=8.8Hz,1H),3.50-3.42(m,5H),3.31(t,J=9.2Hz,1H),3.12(t,J=9.2Hz,1H),2.56-2.53(m,1H),2.31-2.20(m,5H),1.77-1.71(m,1H)。
制备例133F/134F:N-[(3R)-4,4-二氟-1-(4-{2-甲基-5-[(3S)-3-(2,2,2-三氟乙基)吡咯烷-1-羰基氨基]苯基}-6-(吗啉-4-基)吡啶-2-基)吡咯烷-3-基]氨基甲酸苯甲酯和N-[(3S)-4,4-二氟-1-(4-{2-甲基-5-[(3S)-3-(2,2,2-三氟乙基)吡咯烷-1-羰基氨基]苯基}-6-(吗啉-4-基)吡啶-2-基)吡咯烷-3-基]氨基甲酸苯甲酯
N-[4,4-二氟-1-(4-{2-甲基-5-[(3S)-3-(2,2,2-三氟乙基)吡咯烷-1-羰基氨基]苯基}-6-(吗啉-4-基)吡啶-2-基)吡咯烷-3-基]氨基甲酸苯甲酯(330mg,0.470mmol)通过手性制备型HPLC采用以下条件进行拆分:柱:CHIRALPAK IE,2*25cm,5μm;流动相A:Hex(0.5%2M NH3-MeOH),流动相B:EtOH;流速:20mL/min;梯度:A:B=70:30;220/254nm。RT1:16.88min产生了100mg(30%)的呈白色固体的制备例133F。MS ESI:的计算值:C35H39F5N6O4[M+H]+,703.30,实测值:703.35。并且RT2:22.22min产生了110mg(33%)的呈白色固体的制备例134F。MS ESI:C35H39F5N6O4[M+H]+的计算值:703.30,实测值:703.40。
实施例133和134:(3S)-N-(3-{2-[(4R)-4-氨基-3,3-二氟吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基}-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺和(3S)-N-(3-{2-[(4S)-4-氨基-3,3-二氟吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基}-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将制备例133F(110mg,0.157mmol)在MeOH(3mL)和Pd/C(50mg)中的混合物在室温和氢气氛下搅拌30min。过滤所得混合物,并且用MeOH(3x10mL)洗涤。将滤液减压浓缩,得到呈白色固体的实施例133(70mg,78%)。MS ESI:C27H33F5N6O2[M+H]+的计算值:569.26,实测值:569.25。1H NMR(400MHz,DMSO-d6)δ8.12(s,1H),7.43(dd,J=2.4,8.4Hz,1H),7.33(d,J=2.4Hz,1H),7.11(d,J=8.4Hz,1H),5.95(s,1H),5.70(s,1H),3.90-3.73(m,3H),3.72-3.63(m,6H),3.52(t,J=9.2Hz,1H),3.42-3.40(m,4H),3.31-3.29(m,1H)3.15(t,J=8.8Hz,1H),3.02(t,J=9.6Hz,1H),2.45-2.52(m,3H),2.17(s,3H),2.10-2.07(m,1H),1.94(s,1H),1.70-1.62(m,1H)。19F NMR(376MHz,DMSO-d6)δ-66.37(3F),-110.15(d,J=224.8Hz,1F),-117.55(d,J=224.8Hz,1F)。
将制备例134F(110mg,0.157mmol)、MeOH(3mL)和Pd/C(50mg)的混合物在室温和氢气氛下搅拌30min。过滤所得混合物,并且用MeOH(3x10mL)洗涤。将所得混合物减压浓缩,得到呈白色固体的实施例134(72mg,88%)。MS ESI:C27H33F5N6O2[M+H]+的计算值:569.26,实测值:569.20。1H NMR(400MHz,DMSO-d6)δ8.12(s,1H),7.43(dd,J=2.4,8.4Hz,1H),7.34(d,J=2.4Hz,1H),7.11(d,J=8.4Hz,1H),5.95(s,1H),5.70(s,1H),3.90-3.73(m,3H),3.72-3.63(m,6H),3.52(t,J=9.2Hz,1H),3.42-3.40(m,4H),3.31-3.29(m,1H)3.15(t,J=8.8Hz,1H),3.02(t,J=9.6Hz,1H),2.45-2.52(m,3H),2.17(s,3H),2.10-2.05(m,1H),1.94(s,1H),1.69-1.63(m,1H)。19F NMR(376MHz,DMSO-d6)δ-63.36(3F),-110.13(d,J=224.8Hz,1F),-117.54(d,J=224.8Hz,1F)。
实施例135和136:(3S)-N-(3-{2-[(3R,4R)-3-氨基-4-羟基吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基}-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺和(3S)-N-(3-{2-[(3S,4S)-3-氨基-4-羟基吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基}-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例135A:反式-3-[[(苯甲基氧基)羰基]氨基]-4-羟基吡咯烷-1-甲酸叔丁酯
在0℃下,向反式-3-氨基-4-羟基吡咯烷-1-甲酸叔丁酯(5g,24.721mmol)和Na2CO3(3g,29.666mmol)在二噁烷(57mL)和H2O(57mL)中的搅拌混合物中逐滴加入Cbz-Cl(5g,29.661mmol)。将所得混合物在室温下搅拌3h。将反应混合物用水(100mL)稀释。将所得混合物用EtOAc(2x200mL)萃取。将合并的有机层用盐水(50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc/EtOH(4/3/1)洗脱,得到呈灰白色固体的反式-3-[[(苯甲基氧基)羰基]氨基]-4-羟基吡咯烷-1-甲酸叔丁酯(7.2g,78%)。MS ESI:C17H24N2O5[M–Boc+H]+的计算值:237.17,实测值:237.10。1H NMR(300MHz,氯仿-d)δ7.40-7.33(m,5H),5.11(s,2H),4.27-4.23(m,1H),4.02-3.98(m,1H),3.79(m,1H),3.65(m,1H),3.33-3.24(m,2H),1.46(s,9H)。
制备例135B:反式-(4-羟基吡咯烷-3-基)氨基甲酸苯甲酯2,2,2-三氟乙酸盐
在0℃下,向反式-3-[[(苯甲基氧基)羰基]氨基]-4-羟基吡咯烷-1-甲酸叔丁酯(2g,5.946mmol)在DCM(20mL)中的搅拌混合物中逐滴加入TFA(4mL,53.852mmol)。将所得混合物在室温下搅拌30min。将所得混合物减压浓缩,得到呈浅棕色油状物的反式-(4-羟基吡咯烷-3-基)氨基甲酸苯甲酯2,2,2-三氟乙酸盐(3g,粗物质)。MS ESI:C14H17F3N2O5[M–CF3COO]+的计算值:237.12,实测值:237.10。
制备例135C:反式-[1-(6-氟-4-碘吡啶-2-基)-4-羟基吡咯烷-3-基]氨基甲酸苯甲酯
将2,6-二氟-4-碘吡啶(1.5g,6.225mmol)、反式-(4-羟基吡咯烷-3-基)氨基甲酸苯甲酯2,2,2-三氟乙酸盐(2.2g,6.223mmol)和DIEA(4g,31.104mmol)在DMSO(15mL)中的混合物在80℃和氮气氛下搅拌16h。将反应用水(80mL)猝灭。将所得混合物用EtOAc(2x30mL)萃取。将合并的有机层用盐水(10mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈灰白色固体的反式-[1-(6-氟-4-碘吡啶-2-基)-4-羟基吡咯烷-3-基]氨基甲酸苯甲酯(2.1g,66%)。MS ESI:C17H17FIN3O3[M+H]+的计算值:458.03,实测值:458.10。1H NMR(300MHz,氯仿-d)δ7.40-7.36(m,5H),6.58-6.56(m,2H),5.15(s,2H),4.95-4.91(m,1H),4.45-4.43(m,1H),4.18-4.11(m,1H),3.96-3.90(m,1H),3.79-3.74(m,1H),3.43-3.35(m,2H)。
制备例135D:反式-(4-羟基-1-(4-碘-6-吗啉基吡啶-2-基)吡咯烷-3-基)氨基甲酸苯甲酯
将反式-[1-(6-氟-4-碘吡啶-2-基)-4-羟基吡咯烷-3-基]氨基甲酸苯甲酯(1g,2.187mmol)、吗啉(1.9g,21.914mmol)和DIEA(0.85g,6.577mmol)在DMSO(10mL)中的混合物在80℃和氮气氛下搅拌16h。将混合物用水(50mL)猝灭。将所得混合物用EtOAc(2x30mL)萃取。将合并的有机层用盐水(10mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物在乙酸乙酯(20mL)中湿磨,得到呈灰白色固体的反式-(4-羟基-1-(4-碘-6-吗啉基吡啶-2-基)吡咯烷-3-基)氨基甲酸苯甲酯(760mg,60%)。MS ESI:C21H25IN4O4[M+H]+的计算值:525.09,实测值:525.25。1H NMR(400MHz,DMSO-d6)δ7.39-7.30(m,5H),6.32(s,1H),6.09(s,1H),5.03(s,2H),4.10-4.04(m,1H),3.90-3.87(m,1H),3.65-3.58(m,4H),3.57-3.52(m,1H),3.37-3.35(m,5H),3.25-3.17(m,2H)。
制备例135E:反式-(4-羟基-1-(4-(2-甲基-5-((S)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺基)苯基)-6-吗啉基吡啶-2-基)吡咯烷-3-基)氨基甲酸苯甲酯
将反式-(4-羟基-1-(4-碘-6-吗啉基吡啶-2-基)吡咯烷-3-基)氨基甲酸苯甲酯(300mg,0.572mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(236mg,0.572mmol)、K2CO3(237mg,1.716mmol)和Pd(dppf)Cl2.CH2Cl2(47mg,0.057mmol)在二噁烷(3mL)和H2O(0.75mL)中的混合物在80℃和氮气氛下搅拌16h。将所得混合物减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc/EtOH(8/3/1)洗脱,得到呈灰白色固体的反式-(4-羟基-1-(4-(2-甲基-5-((S)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺基)苯基)-6-吗啉基吡啶-2-基)吡咯烷-3-基)氨基甲酸苯甲酯(270mg,66%)。MS ESI:C35H41F3N6O5[M+H]+的计算值:683.31,实测值:683.70。1H NMR(300MHz,氯仿-d)δ7.40-7.35(m,5H),7.22-7.17(m,2H),6.16(s,1H),5.90(s,1H),5.74(s,1H),5.14(s,2H),4.40-4.30(m,1H),3.99-3.94(m,1H),3.83-3.68(m,7H),3.67-3.62(m,1H),3.51-3.43(m,7H),3.23-3.09(m,2H),2.56-2.50(m,1H),2.30-2.23(m,5H),1.77-1.73(m,2H)。
制备例135F/136F:((3R,4R)-4-羟基-1-(4-(2-甲基-5-((S)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺基)苯基)-6-吗啉基吡啶-2-基)吡咯烷-3-基)氨基甲酸苯甲酯和((3S,4S)-4-羟基-1-(4-(2-甲基-5-((S)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺基)苯基)-6-吗啉基吡啶-2-基)吡咯烷-3-基)氨基甲酸苯甲酯
反式-(4-羟基-1-(4-(2-甲基-5-((S)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺基)苯基)-6-吗啉基吡啶-2-基)吡咯烷-3-基)氨基甲酸苯甲酯(270mg)通过手性制备型HPLC采用以下条件进行拆分:柱:(R,R)-WHELK-O1-Kromasil,2.12x25cm,5μm;流动相A:MTBE(0.5%2M NH3-MeOH),流动相B:EtOH;流速:20mL/min;梯度:A:B=70:30;220/254nm。RT1:13.7min产生了100mg(35%)的呈灰白色固体的制备例135F,MS ESI:C35H41F3N6O5[M+H]+的计算值:683.31,实测值:683.35。
并且RT2:18.3min产生了70mg(24%)的呈灰白色固体的制备例136F。MS ESI:C35H41F3N6O5[M+H]+的计算值:683.31,实测值:683.35。
实施例135和136:(3S)-N-(3-{2-[(3R,4R)-3-氨基-4-羟基吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基}-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺和(3S)-N-(3-{2-[(3S,4S)-3-氨基-4-羟基吡咯烷-1-基]-6-(吗啉-4-基)吡啶-4-基}-4-甲基苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将制备例135F(100mg,0.146mmol)和Pd/C(50mg,0.470mmol)在MeOH(2mL)中的混合物在室温和H2氛下搅拌30min。过滤所得混合物,并且用MeOH(3x5mL)洗涤。将滤液减压浓缩,得到呈灰白色固体的实施例135(27mg,32%)。MS ESI:C27H35F3N6O3[M+H]+的计算值:549.27,实测值:549.25。1H NMR(300MHz,DMSO-d6)δ8.12(s,1H),7.51-7.35(m,2H),7.16-7.10(m,1H),5.89-5.84(m,1H),5.66-5.61(m,1H),5.00(s,1H),3.90-3.86(m,1H),3.69-3.51(m,8H),3.42-3.33(m,4H),3.28-3.13(m,3H),3.09-2.94(m,2H),2.74-2.47(m,3H),2.29(s,3H),2.18-2.02(m,1H),1.72-1.58(m,2H)。19F NMR(282MHz,DMSO-d6)δ-63.35(3F)。
将制备例136F(75mg,0.110mmol)和Pd/C(50mg,0.470mmol)在MeOH(2mL)中的混合物在室温和H2氛下搅拌30min。过滤所得混合物,并且用MeOH(3x5mL)洗涤。将滤液减压浓缩,得到呈灰白色固体的实施例136(29mg,46%)。MS ESI:C27H35F3N6O3[M+H]+的计算值:549.27,实测值:549.25。1H NMR(400MHz,DMSO-d6)δ8.11(s,1H),7.42(dd,J=2.4,8.4Hz,1H),7.33(d,J=2.0Hz,1H),7.09(d,J=8.4Hz,1H),5.82(s,1H),5.60(s,1H),4.99(s,1H),3.86(s,1H),3.68-3.60(m,6H),3.59-3.53(m,2H),3.50-3.39(m,4H),3.32-3.29(m,1H),3.25-3.19(m,2H),3.12-2.99(m,2H),2.52-2.43(m,3H),2.16(s,3H),2.09-2.08(m,1H),1.75-1.55(m,2H)。19F NMR(376MHz,DMSO-d6)δ-63.37(3F)。
实施例137:(S)-N-(4-甲基-3-(2-(((R)-1-(甲基氨基)-1-氧代丙烷-2-基)氨基)-6-吗啉基吡啶-4-基)苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例137A:N-[(1R)-1-(甲基氨基甲酰基)乙基]氨基甲酸叔丁酯
在0℃下,向(叔丁氧基羰基)-D-丙氨酸(3.00g,15.86mmol)在THF(30mL)中的搅拌溶液中加入氯甲酸异丁酯(2.26mL,17.45mmol)和N-甲基吗啉(1.9mL,17.45mmol)。将所得混合物在0℃下搅拌1h。向这个混合物中加入甲胺(16.8mL,79.30mmol)。将所得混合物在0℃和氮气氛下搅拌1h。通过添加水(30mL)来猝灭反应。将所得混合物减压浓缩,得到呈浅黄色固体的N-[(1R)-1-(甲基氨基甲酰基)乙基]氨基甲酸叔丁酯(3g,粗物质)。C9H18N2O3,1HNMR(400MHz,氯仿-d)δ3.74-3.70(m,1H),3.23-3.19(m,1H),2.80(s,3H),1.44(s,9H),1.35(d,J=7.2Hz,3H)。
制备例137B:(R)-2-氨基-N-甲基丙酰胺盐酸盐
向N-[(1R)-1-(甲基氨基甲酰基)乙基]氨基甲酸叔丁酯(680mg,3.360mmol)在1,4-二噁烷(15mL)中的溶液中加入HCl(4M,在二噁烷中,4mL)。将反应混合物在室温下搅拌1h。通过过滤来收集沉淀的固体,并且用乙醚(3x50mL)洗涤,得到(R)-2-氨基-N-甲基丙酰胺盐酸盐(630mg,95%)。C4H11ClN2O,1H NMR(300MHz,DMSO-d6)δ8.57(brs,1H),8.29(brs,3H),3.82-3.76(m,1H),2.67-3.73(m,3H),1.35(d,J=7.2Hz,3H)。
制备例137C:(2R)-2-{[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基}-N-甲基丙酰胺
将(R)-2-氨基-N-甲基丙酰胺盐酸盐(315mg,2.270mmol)、4-(6-氟-4-碘吡啶-2-基)吗啉(350mg,1.140mmol)、NMP(5mL)和DIEA(0.86mL,4.45mmol)的溶液在160℃下搅拌16h。将反应用水(30mL)猝灭。将残余物用EtOAc(3x30mL)萃取。将所得混合物减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈棕色固体的(2R)-2-{[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基}-N-甲基丙酰胺(151mg,34%)。MS ESI:C13H19IN4O2[M+H]+的计算值:391.06,实测值:391.00。1H NMR(300MHz,氯仿-d)δ6.42(brs,1H),6.35(s,1H),6.21(s,1H),4.44-4.40(m,1H),4.19-4.15(m,1H),3.79-3.75(m,4H),3.43-3.40(m,4H),2.78(d,J=4.8Hz,3H),1.46(d,J=7.2Hz,3H)。
实施例137:(S)-N-(4-甲基-3-(2-(((R)-1-(甲基氨基)-1-氧代丙烷-2-基)氨基)-6-吗啉基吡啶-4-基)苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将(2R)-2-{[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基}-N-甲基丙酰胺(100mg,0.260mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(127mg,0.310mmol)、1,4-二噁烷(2mL)、H2O(0.5mL)、Pd(dppf)Cl2.CH2Cl2(31mg,0.026mmol)和K2CO3(106mg,0.770mmol)的混合物在80℃和氮气氛下搅拌2h。通过添加水(10mL)来猝灭反应。将所得混合物减压浓缩。将残余物通过硅胶柱色谱法纯化,用EtOAc洗脱。将粗产物通过手性制备型HPLC采用以下条件进行拆分:(柱:CHIRALPAK AD-H,2x25cm,5μm;流动相A:Hex(0.5%2M NH3-MeOH),流动相B:IPA;流速:20mL/min;梯度:A:B=70:30;220/254nm;RT1:12.12min;得到呈白色固体的(S)-N-(4-甲基-3-(2-(((S)-1-(甲基氨基)-1-氧代丙烷-2-基)氨基)-6-吗啉基吡啶-4-基)苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(13.9mg,9%),并且RT2:18.73min提供了呈白色固体的(S)-N-(4-甲基-3-(2-(((R)-1-(甲基氨基)-1-氧代丙烷-2-基)氨基)-6-吗啉基吡啶-4-基)苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(124.7mg,87%)。MS ESI:C27H35F3N6O3[M+H]+的计算值:549.27,实测值:549.35。1H NMR(400MHz,DMSO-d6)δ8.11(s,1H),7.74-7.72(m,1H),7.40-7.38(m,2H),7.09(d,J=8.4Hz,1H),6.43(d,J=6.4Hz,1H),5.82(s,1H),5.79(s,1H),4.23-4.17(m,1H),3.66-3.55(m,5H),3.52-3.50(m,1H),3.36-3.30(m,4H),3.04-3.01(m,1H),2.58-2.50(m,3H),2.45-2.40(m,3H),2.15(s,3H),2.14-2.10(m,1H),1.70-1.65(m,1H),1.26(d,J=7.2Hz,3H)。19F NMR(282MHz,DMSO-d6)δ-63.35(3F)。
实施例138:(S)-N-(4-甲基-3-(2-(((S)-1-(甲基氨基)-1-氧代丙烷-2-基)氨基)-6-吗啉基吡啶-4-基)苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例138A:N-[(S)-1-(甲基氨基甲酰基)乙基]氨基甲酸叔丁酯
在0℃下,向(叔丁氧基羰基)-L-丙氨酸(2.00g,10.58mmol)在THF(20mL)中的搅拌溶液中加入氯甲酸异丁酯(1.51mL,11.64mmol)和N-甲基吗啉(1.28mL,11.64mmol),持续1h。添加甲胺(6.56mL,52.9mmol)后将所得混合物在0℃和氮气氛下搅拌1.0h。在室温下通过添加水(30mL)来猝灭反应。将所得混合物减压浓缩,得到呈浅黄色固体的N-[(S)-1-(甲基氨基甲酰基)乙基]氨基甲酸叔丁酯(2g粗物质)。
制备例138B:(S)-2-氨基-N-甲基丙酰胺盐酸盐
在室温和空气氛下,向N-[(S)-1-(甲基氨基甲酰基)乙基]氨基甲酸叔丁酯(1.00g,4.94mmol)在1,4-二噁烷中的搅拌溶液中逐滴加入HCl(4M,在二噁烷中,5mL)。通过过滤来收集沉淀的固体,并且用乙醚(3x50mL)洗涤,得到呈白色固体的(S)-2-氨基-N-甲基丙酰胺盐酸盐(920mg,95%)。
制备例138C:(S)-2-{[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基}-N-甲基丙酰胺
向(S)-2-氨基-N-甲基丙酰胺盐酸盐(450mg,3.246mmol)和4-(6-氟-4-碘吡啶-2-基)吗啉(500mg,1.623mmol)在NMP中的搅拌溶液中加入DIEA(839mg,6.492mmol)。将所得混合物在170℃下搅拌24h。将反应用水(30mL)猝灭。将残余物用乙酸乙酯(3x30mL)洗涤。将所得混合物减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈棕色固体的(S)-2-{[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基}-N-甲基丙酰胺(204mg,32%)。MSESI:C13H19IN4O2[M+H]+的计算值:391.06,实测值:391.00。
实施例138:(S)-N-(4-甲基-3-(2-(((S)-1-(甲基氨基)-1-氧代丙烷-2-基)氨基)-6-吗啉基吡啶-4-基)苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
向(2S)-2-{[4-碘-6-(吗啉-4-基)吡啶-2-基]氨基}-N-甲基丙酰胺(117mg,0.300mmol)和(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(123.61mg,0.300mmol)在1,4-二噁烷和H2O中的搅拌溶液/混合物中加入Pd(dppf)Cl2.CH2Cl2(26.3mg,0.032mmol)和K2CO3(124.31mg,0.900mmol)。将所得混合物在80℃和氮气氛下搅拌2h。将所得混合物减压浓缩。将残余物通过硅胶柱色谱法纯化,用EtOAc洗脱。将粗物质通过手性制备型HPLC采用以下条件进行拆分:(柱:CHIRALPAK AD-H,2x25cm,5μm;流动相A:己烷(0.5%2M NH3-MeOH),流动相B:IPA;流速:20mL/min;梯度:A:B=70:30;220/254nm;RT1:12.12min,得到呈白色固体的(S)-N-(4-甲基-3-(2-(((S)-1-(甲基氨基)-1-氧代丙烷-2-基)氨基)-6-吗啉基吡啶-4-基)苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(51mg,31%)。MS ESI:C27H35F3N6O3[M+H]+的计算值:549.27,实测值:549.20。1H NMR(400MHz,DMSO-d6)δ8.11(s,1H),7.74-7.72(m,1H),7.40-7.38(m,2H),7.09(d,J=8.4Hz,1H),6.43(d,J=6.0Hz,1H),5.82(s,1H),5.79(s,1H),4.23-4.17(m,1H),3.66-3.55(m,5H),3.52-3.50(m,1H),3.36-3.28(m,4H),3.04-3.01(m,1H),2.58-2.50(m,3H),2.45-2.40(m,4H),2.15(s,3H),2.14-2.10(m,1H),1.70-1.65(m,1H),1.26(d,J=7.2Hz,3H)。19F NMR(282MHz,DMSO-d6)δ-63.35(3F)。并且RT2:18.73min提供了呈白色固体的(S)-N-(4-甲基-3-(2-(((R)-1-(甲基氨基)-1-氧代丙烷-2-基)氨基)-6-吗啉基吡啶-4-基)苯基)-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(5.7mg,4%)。
实施例139:(3S)-N-{3-[2-乙烷磺酰胺基-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基}-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例139A:N-[4-氯-6-(吗啉-4-基)吡啶-2-基]乙烷磺酰胺
将4-氯-6-(吗啉-4-基)吡啶-2-胺(500mg,2.340mmol)和乙烷磺酰氯(451mg,3.510mmol)在吡啶(7.5mL)中的混合物在80℃下搅拌16h。将所得混合物减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到呈棕色固体的N-[4-氯-6-(吗啉-4-基)吡啶-2-基]乙烷磺酰胺(120mg,15%)。MS ESI:C11H16ClN3O3S[M+H]+的计算值:306.06,实测值:306.10。1H NMR(400MHz,氯仿-d)δ6.84(brs,1H),6.51(s,1H),6.31(s,1H),3.80-3.77(m,4H),3.48-3.46(m,4H),3.35(q,J=7.2Hz,2H),1.41(t,J=7.2Hz,3H)。
实施例139:(3S)-N-{3-[2-乙烷磺酰胺基-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基}-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将N-[4-氯-6-(吗啉-4-基)吡啶-2-基]乙烷磺酰胺(100mg,0.327mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(108mg,0.262mmol)、K3PO4(139mg,0.654mmol)和第2代XPhos预催化剂(26mg,0.033mmol)在THF(1mL)和H2O(0.1mL)中的混合物在80℃和氮气氛下搅拌2h。将所得混合物减压浓缩。将残余物通过制备型TLC采用PE/EtOAc/EtOH(8/3/1)纯化,得到呈灰白色固体的(3S)-N-{3-[2-乙烷磺酰胺基-6-(吗啉-4-基)吡啶-4-基]-4-甲基苯基}-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(87mg,46%)。MS ESI:C25H32F3N5O4S[M+H]+的计算值:556.21,实测值:556.30。1H NMR(400MHz,DMSO-d6)δ10.25(brs,1H),8.16(s,1H),7.46(dd,J=2.4,8.4Hz,1H),7.36(d,J=2.4Hz,1H),7.14(d,J=8.4Hz,1H),6.32(s,1H),6.15(s,1H),3.71-3.65(m,5H),3.53-3.43(m,7H),3.32-3.30(m,1H),3.02-3.00(m,1H),2.53-2.33(m,3H),2.20(s,3H),2.12-2.00(m,1H),2.75-2.65(m,1H),1.26(t,J=7.2Hz,3H)。19F NMR(376MHz,DMSO-d6)δ-63.37(3F)。
实施例140:(3S)-N-{4-甲基-3-[2-(吗啉-4-基)-6-(丙烷-2-磺酰胺基)吡啶-4-基]苯基}-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例140A:N-[4-氯-6-(吗啉-4-基)吡啶-2-基]丙烷-2-磺酰胺
在-30℃下,向4-氯-6-(吗啉-4-基)吡啶-2-胺(500mg,2.340mmol)和DBU(1.43g,9.393mmol)在DCM(7mL)中的搅拌混合物中逐滴加入丙烷-2-磺酰氯(350mg,9.360mmol)。将反应混合物在-30℃下搅拌3h。将所得混合物用水(30mL)稀释。将所得混合物用DCM(3x20mL)萃取。将合并的有机层用盐水(2x20mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过反相色谱法纯化,用水(加0.5%TFA)中的40%CH3CN洗脱,得到呈浅黄色固体的N-[4-氯-6-(吗啉-4-基)吡啶-2-基]丙烷-2-磺酰胺(350mg,47%)。MS ESI:C12H18ClN3O3S[M+H]+的计算值:320.08;实测值:320.10。1H NMR(400MHz,氯仿-d)δ6.62(d,J=1.2Hz,1H),6.33(d,J=1.2Hz,1H),3.84-3.77(m,4H),3.62-3.45(m,5H),1.45(d,J=6.8Hz,6H)。
实施例140:(3S)-N-{4-甲基-3-[2-(吗啉-4-基)-6-(丙烷-2-磺酰胺基)吡啶-4-基]苯基}-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
在80℃和氮气氛下,向N-[4-氯-6-(吗啉-4-基)吡啶-2-基]丙烷-2-磺酰胺(120mg,0.375mmol)、K3PO4(239mg,1.125mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(155mg,0.375mmol)在THF(2mL)和H2O(0.2mL)中的混合物中加入第2代XPhos预催化剂(29mg,0.038mmol),搅拌2h。将所得混合物减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(2/3)洗脱,并且通过反相色谱法纯化,用水(0.05%NH4HCO3)中的45%CH3CN洗脱,得到呈白色固体的(3S)-N-{4-甲基-3-[2-(吗啉-4-基)-6-(丙烷-2-磺酰胺基)吡啶-4-基]苯基}-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(145.2mg,66%)。MS ESI:C26H34F3N5O4S[M+H]+的计算值:570.23;实测值:570.30。1H NMR(300MHz,氯仿-d)δ7.33-7.30(m,2H),7.19(d,J=8.4Hz,1H),6.58(brs,1H),6.30(s,1H),6.17(s,1H),3.85-3.80(m,5H),3.68-3.43(m,7H),3.14-3.11(m,1H),2.64-2.53(m,1H),2.35-2.15(m,6H),1.84-1.66(m,1H),1.46(d,J=6.9Hz,6H)。19F NMR(282MHz,氯仿-d)δ-64.95(3F)。
实施例141:(3S)-N-{4-甲基-3-[2-(1-甲基环丙烷磺酰胺基)-6-(吗啉-4-基)吡啶-4-基]苯基}-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
制备例141A:N-[4-氯-6-(吗啉-4-基)吡啶-2-基]-1-甲基环丙烷-1-磺酰胺
将4-(4,6-二氯吡啶-2-基)吗啉(1.00g,4.29mmol)、1-甲基环丙烷-1-磺酰胺(0.58g,4.29mmol)、二噁烷(12mL)、XantPhos(0.25g,0.43mmol)、Cs2CO3(4.2g,12.87mmol)和Pd(OAc)2(0.10g,0.43mmol)的混合物在100℃和氮气氛下搅拌16h。将所得混合物用水(50mL)稀释。将所得混合物用EtOAc(3x30mL)萃取。将合并的有机层用盐水(2x50mL)洗涤,经无水Na2SO4干燥。过滤后,将滤液减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc(1/1)洗脱,得到N-[4-氯-6-(吗啉-4-基)吡啶-2-基]-1-甲基环丙烷-1-磺酰胺(1.00g,70%)。MS ESI:C13H18ClN3O3S[M+H]+的计算值:332.08;实测值:332.10。1H NMR(400MHz,甲醇-d4)δ11.11(s,1H),7.34(s,1H),7.20(s,1H),4.49-4.47(m,4H),4.29-4.27(m,4H),2.23(s,3H),2.14-2.03(m,2H),1.71-1.63(m,2H)。
实施例141:(3S)-N-{4-甲基-3-[2-(1-甲基环丙烷磺酰胺基)-6-(吗啉-4-基)吡啶-4-基]苯基}-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺
将N-[4-氯-6-(吗啉-4-基)吡啶-2-基]-1-甲基环丙烷-1-磺酰胺(150mg,0.452mmol)、(3S)-N-[4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯基]-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(186mg,0.452mmol)、THF(2mL)、H2O(0.2mL)、K3PO4(288mg,1.356mmol)和第2代XPhos预催化剂(35mg,0.045mmol)的混合物在80℃和氮气氛下搅拌2h。将所得混合物减压浓缩。将残余物通过硅胶柱色谱法纯化,用PE/EtOAc/EtOH(4/3/1)洗脱,并且通过反相色谱法纯化,用水(0.05%NH4HCO3)中的55%CH3CN洗脱,得到呈白色固体的(3S)-N-{4-甲基-3-[2-(1-甲基环丙烷磺酰胺基)-6-(吗啉-4-基)吡啶-4-基]苯基}-3-(2,2,2-三氟乙基)吡咯烷-1-甲酰胺(71mg,27%)。MS ESI:C27H34F3N5O4S[M+H]+的计算值:582.23;实测值:582.30。1H NMR(300MHz,氯仿-d)δ7.35-7.29(m,2H),7.19(d,J=8.4Hz,1H),6.71(brs,2H),6.31(s,1H),6.16(s,1H),3.85-3.82(m,5H),3.68-3.63(m,1H),3.60-3.40(m,5H),3.17-3.11(m,1H),2.64-2.53(m,1H),2.39-2.18(m,6H),1.84-1.77(m,1H),1.58(s,3H),1.48-1.46(m,2H),0.84-0.82(m,2H)。19F NMR(282MHz,氯仿-d)δ-64.95(3F)。
II.生物学评估
酶促RAF1激酶活性测定:
使用ADP-Glo测定来测量小分子对RAF1激酶的抑制。在测定中,ADP在测试激酶和底物存在下转化成ATP,从而产生荧光素酶反应和发光读数,其中产生的光与相对激酶活性成比例。在DMSO中稀释的化合物以10点3倍剂量曲线用于两个测定。将最终浓度3nM RAF1(CarnaBio,目录号09-125)和30nM MEK1底物(Millipore,目录号14-420)与3μM ATP、10mMMgCl2、0.003%Brij-35、2mM DTT、0.05%BSA、1mM EGTA和50mM HEPES一起在室温下孵育90分钟,随后添加ADP-Glo试剂(Promega,目录号V9102)孵育40分钟,并且添加检测试剂,孵育45分钟。在Envision板读取器(PerkinElmer)上读取发光,并且采用Dotmatics KnowledgeSolutions Studies曲线拟合(Dotmatics,Bishops Stortford,UK,CM23),利用四参数拟合模型,使用剩余活性百分比来计算IC50。示例性化合物的代表性数据呈现在表2中。
表2
注意:生化试验IC50数据被指定在以下范围内:
A:≤0.010μM B:>0.010μM至≤0.100μM
C:>0.100μM至<1μM
III.药物剂型的制备
实施例1:口服胶囊
活性成分是表1的化合物,或其药学上可接受的盐或溶剂化物。通过将1-1000mg活性成分与淀粉或其他合适的粉末掺合物混合来制备用于口服给药的胶囊。将该混合物掺入适合于口服给药的口服剂量单元例如硬明胶胶囊中。
实施例2:用于注射的溶液
活性成分是表1的化合物或其药学上可接受的盐,并且在芝麻油中以50mg-eq/mL的浓度被配制为溶液。
本文所述的实施例和实施方案仅用于说明性目的,并且向本领域技术人员提示的各种修改或变化都将被包含在本申请的精神和范围以及所附权利要求书的范围内。