CN114649570A - 一种可聚合电解质及其制备方法和应用 - Google Patents
一种可聚合电解质及其制备方法和应用 Download PDFInfo
- Publication number
- CN114649570A CN114649570A CN202011491494.XA CN202011491494A CN114649570A CN 114649570 A CN114649570 A CN 114649570A CN 202011491494 A CN202011491494 A CN 202011491494A CN 114649570 A CN114649570 A CN 114649570A
- Authority
- CN
- China
- Prior art keywords
- group
- membered ring
- cyclic
- electrolyte
- substituent
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 239000003792 electrolyte Substances 0.000 title claims abstract description 62
- 238000002360 preparation method Methods 0.000 title abstract description 26
- WTEOIRVLGSZEPR-UHFFFAOYSA-N boron trifluoride Chemical class FB(F)F WTEOIRVLGSZEPR-UHFFFAOYSA-N 0.000 claims abstract description 38
- 150000003839 salts Chemical class 0.000 claims abstract description 34
- 125000001424 substituent group Chemical group 0.000 claims description 60
- -1 cyclic acetals Chemical class 0.000 claims description 47
- 239000011244 liquid electrolyte Substances 0.000 claims description 40
- 239000000654 additive Substances 0.000 claims description 32
- 239000007787 solid Substances 0.000 claims description 25
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 claims description 19
- 230000000996 additive effect Effects 0.000 claims description 18
- 125000004122 cyclic group Chemical group 0.000 claims description 17
- 239000007788 liquid Substances 0.000 claims description 17
- 239000000178 monomer Substances 0.000 claims description 14
- 239000007784 solid electrolyte Substances 0.000 claims description 12
- 238000000034 method Methods 0.000 claims description 11
- 125000004432 carbon atom Chemical group C* 0.000 claims description 10
- 125000005843 halogen group Chemical group 0.000 claims description 10
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 10
- 229910015900 BF3 Inorganic materials 0.000 claims description 9
- 239000010416 ion conductor Substances 0.000 claims description 8
- 229910052751 metal Inorganic materials 0.000 claims description 8
- 239000002184 metal Substances 0.000 claims description 8
- 125000004429 atom Chemical group 0.000 claims description 7
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 7
- 150000005676 cyclic carbonates Chemical class 0.000 claims description 6
- 150000001925 cycloalkenes Chemical class 0.000 claims description 6
- 125000005842 heteroatom Chemical group 0.000 claims description 6
- 229910001416 lithium ion Inorganic materials 0.000 claims description 6
- 229910052760 oxygen Inorganic materials 0.000 claims description 6
- 239000001301 oxygen Substances 0.000 claims description 5
- 238000006116 polymerization reaction Methods 0.000 claims description 5
- HBBGRARXTFLTSG-UHFFFAOYSA-N Lithium ion Chemical compound [Li+] HBBGRARXTFLTSG-UHFFFAOYSA-N 0.000 claims description 4
- FKNQFGJONOIPTF-UHFFFAOYSA-N Sodium cation Chemical compound [Na+] FKNQFGJONOIPTF-UHFFFAOYSA-N 0.000 claims description 4
- 125000003342 alkenyl group Chemical group 0.000 claims description 4
- 125000000217 alkyl group Chemical group 0.000 claims description 4
- 125000000304 alkynyl group Chemical group 0.000 claims description 4
- 125000002837 carbocyclic group Chemical group 0.000 claims description 4
- 150000001768 cations Chemical class 0.000 claims description 4
- 150000003950 cyclic amides Chemical class 0.000 claims description 4
- 150000004292 cyclic ethers Chemical class 0.000 claims description 4
- 150000004294 cyclic thioethers Chemical class 0.000 claims description 4
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 claims description 4
- 125000001153 fluoro group Chemical group F* 0.000 claims description 4
- 239000011245 gel electrolyte Substances 0.000 claims description 4
- 125000004404 heteroalkyl group Chemical group 0.000 claims description 4
- 125000000623 heterocyclic group Chemical group 0.000 claims description 4
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 claims description 4
- 229910001415 sodium ion Inorganic materials 0.000 claims description 4
- 229910052717 sulfur Inorganic materials 0.000 claims description 4
- 239000011593 sulfur Substances 0.000 claims description 4
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 claims description 3
- 229910052731 fluorine Inorganic materials 0.000 claims description 3
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 3
- 125000003548 sec-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 claims description 3
- 125000003229 2-methylhexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 claims description 2
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical group [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 claims description 2
- LSNNMFCWUKXFEE-UHFFFAOYSA-M Bisulfite Chemical compound OS([O-])=O LSNNMFCWUKXFEE-UHFFFAOYSA-M 0.000 claims description 2
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical group [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 claims description 2
- NPYPAHLBTDXSSS-UHFFFAOYSA-N Potassium ion Chemical compound [K+] NPYPAHLBTDXSSS-UHFFFAOYSA-N 0.000 claims description 2
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 claims description 2
- 125000004414 alkyl thio group Chemical group 0.000 claims description 2
- 125000003368 amide group Chemical group 0.000 claims description 2
- 150000001408 amides Chemical class 0.000 claims description 2
- 125000004369 butenyl group Chemical group C(=CCC)* 0.000 claims description 2
- 125000000480 butynyl group Chemical group [*]C#CC([H])([H])C([H])([H])[H] 0.000 claims description 2
- 229910052801 chlorine Inorganic materials 0.000 claims description 2
- 125000001309 chloro group Chemical group Cl* 0.000 claims description 2
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 claims description 2
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 claims description 2
- 150000002148 esters Chemical class 0.000 claims description 2
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 claims description 2
- 125000002485 formyl group Chemical class [H]C(*)=O 0.000 claims description 2
- 125000006038 hexenyl group Chemical group 0.000 claims description 2
- 125000005980 hexynyl group Chemical group 0.000 claims description 2
- 229910052740 iodine Inorganic materials 0.000 claims description 2
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 claims description 2
- 125000004491 isohexyl group Chemical group C(CCC(C)C)* 0.000 claims description 2
- 125000001972 isopentyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])C([H])([H])* 0.000 claims description 2
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 claims description 2
- 125000001160 methoxycarbonyl group Chemical group [H]C([H])([H])OC(*)=O 0.000 claims description 2
- 125000002816 methylsulfanyl group Chemical group [H]C([H])([H])S[*] 0.000 claims description 2
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 claims description 2
- 125000003136 n-heptyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 claims description 2
- 125000001280 n-hexyl group Chemical group C(CCCCC)* 0.000 claims description 2
- 125000000740 n-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 claims description 2
- 125000005244 neohexyl group Chemical group [H]C([H])([H])C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])C([H])([H])* 0.000 claims description 2
- 125000001971 neopentyl group Chemical group [H]C([*])([H])C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])[H] 0.000 claims description 2
- 125000002255 pentenyl group Chemical group C(=CCCC)* 0.000 claims description 2
- 125000005981 pentynyl group Chemical group 0.000 claims description 2
- 229920000642 polymer Polymers 0.000 claims description 2
- 229910001414 potassium ion Inorganic materials 0.000 claims description 2
- 125000004368 propenyl group Chemical group C(=CC)* 0.000 claims description 2
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 claims description 2
- 125000002568 propynyl group Chemical group [*]C#CC([H])([H])[H] 0.000 claims description 2
- 229920006395 saturated elastomer Polymers 0.000 claims description 2
- 125000000020 sulfo group Chemical group O=S(=O)([*])O[H] 0.000 claims description 2
- 229940124530 sulfonamide Drugs 0.000 claims description 2
- 125000000565 sulfonamide group Chemical group 0.000 claims description 2
- 150000003456 sulfonamides Chemical class 0.000 claims description 2
- 125000000472 sulfonyl group Chemical group *S(*)(=O)=O 0.000 claims description 2
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 claims description 2
- 125000006193 alkinyl group Chemical group 0.000 claims 1
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 claims 1
- HXJUTPCZVOIRIF-UHFFFAOYSA-N sulfolane Chemical compound O=S1(=O)CCCC1 HXJUTPCZVOIRIF-UHFFFAOYSA-N 0.000 claims 1
- 239000002994 raw material Substances 0.000 abstract description 28
- 150000002500 ions Chemical class 0.000 abstract description 14
- 239000005518 polymer electrolyte Substances 0.000 abstract description 12
- 238000002161 passivation Methods 0.000 abstract description 10
- 230000008901 benefit Effects 0.000 abstract description 5
- 239000013538 functional additive Substances 0.000 abstract description 4
- 238000011065 in-situ storage Methods 0.000 abstract description 4
- 239000004020 conductor Substances 0.000 abstract 1
- 238000011066 ex-situ storage Methods 0.000 abstract 1
- 125000000524 functional group Chemical group 0.000 abstract 1
- 239000002904 solvent Substances 0.000 description 30
- 238000012360 testing method Methods 0.000 description 28
- 239000011259 mixed solution Substances 0.000 description 21
- 239000000243 solution Substances 0.000 description 20
- 238000001035 drying Methods 0.000 description 19
- 229910052744 lithium Inorganic materials 0.000 description 19
- KZMGYPLQYOPHEL-UHFFFAOYSA-N Boron trifluoride etherate Chemical compound FB(F)F.CCOCC KZMGYPLQYOPHEL-UHFFFAOYSA-N 0.000 description 18
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 18
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 18
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 18
- 230000000694 effects Effects 0.000 description 18
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 17
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 17
- 208000028659 discharge Diseases 0.000 description 15
- 239000000047 product Substances 0.000 description 15
- WMFOQBRAJBCJND-UHFFFAOYSA-M lithium hydroxide Inorganic materials [Li+].[OH-] WMFOQBRAJBCJND-UHFFFAOYSA-M 0.000 description 14
- 238000006243 chemical reaction Methods 0.000 description 12
- 230000000052 comparative effect Effects 0.000 description 12
- 239000012043 crude product Substances 0.000 description 12
- 230000005415 magnetization Effects 0.000 description 12
- 239000000203 mixture Substances 0.000 description 12
- MZRVEZGGRBJDDB-UHFFFAOYSA-N N-Butyllithium Chemical compound [Li]CCCC MZRVEZGGRBJDDB-UHFFFAOYSA-N 0.000 description 10
- 230000014759 maintenance of location Effects 0.000 description 10
- ZOXJGFHDIHLPTG-UHFFFAOYSA-N Boron Chemical compound [B] ZOXJGFHDIHLPTG-UHFFFAOYSA-N 0.000 description 9
- 229910052796 boron Inorganic materials 0.000 description 9
- XTHFKEDIFFGKHM-UHFFFAOYSA-N Dimethoxyethane Chemical compound COCCOC XTHFKEDIFFGKHM-UHFFFAOYSA-N 0.000 description 8
- 238000001914 filtration Methods 0.000 description 8
- 150000002894 organic compounds Chemical class 0.000 description 8
- 239000007858 starting material Substances 0.000 description 8
- 238000003756 stirring Methods 0.000 description 8
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 7
- 239000012300 argon atmosphere Substances 0.000 description 7
- 239000000463 material Substances 0.000 description 7
- 239000012299 nitrogen atmosphere Substances 0.000 description 7
- OZAIFHULBGXAKX-UHFFFAOYSA-N 2-(2-cyanopropan-2-yldiazenyl)-2-methylpropanenitrile Chemical compound N#CC(C)(C)N=NC(C)(C)C#N OZAIFHULBGXAKX-UHFFFAOYSA-N 0.000 description 6
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 6
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 6
- 239000010410 layer Substances 0.000 description 6
- 239000002243 precursor Substances 0.000 description 6
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 6
- 238000005406 washing Methods 0.000 description 6
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 5
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 description 5
- 239000011230 binding agent Substances 0.000 description 5
- 150000001875 compounds Chemical class 0.000 description 5
- 229910052593 corundum Inorganic materials 0.000 description 5
- 238000002156 mixing Methods 0.000 description 5
- 239000003960 organic solvent Substances 0.000 description 5
- 229910001845 yogo sapphire Inorganic materials 0.000 description 5
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 4
- 239000002033 PVDF binder Substances 0.000 description 4
- 239000013543 active substance Substances 0.000 description 4
- 230000005540 biological transmission Effects 0.000 description 4
- 239000002041 carbon nanotube Substances 0.000 description 4
- 229910021393 carbon nanotube Inorganic materials 0.000 description 4
- 239000011248 coating agent Substances 0.000 description 4
- 238000000576 coating method Methods 0.000 description 4
- 238000010586 diagram Methods 0.000 description 4
- USIUVYZYUHIAEV-UHFFFAOYSA-N diphenyl ether Chemical compound C=1C=CC=CC=1OC1=CC=CC=C1 USIUVYZYUHIAEV-UHFFFAOYSA-N 0.000 description 4
- 229920002981 polyvinylidene fluoride Polymers 0.000 description 4
- 230000008569 process Effects 0.000 description 4
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 3
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 3
- OIFBSDVPJOWBCH-UHFFFAOYSA-N Diethyl carbonate Chemical compound CCOC(=O)OCC OIFBSDVPJOWBCH-UHFFFAOYSA-N 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 3
- KMTRUDSVKNLOMY-UHFFFAOYSA-N Ethylene carbonate Chemical compound O=C1OCCO1 KMTRUDSVKNLOMY-UHFFFAOYSA-N 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 229910052782 aluminium Inorganic materials 0.000 description 3
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 3
- 230000015572 biosynthetic process Effects 0.000 description 3
- 239000002482 conductive additive Substances 0.000 description 3
- JBTWLSYIZRCDFO-UHFFFAOYSA-N ethyl methyl carbonate Chemical compound CCOC(=O)OC JBTWLSYIZRCDFO-UHFFFAOYSA-N 0.000 description 3
- 239000011888 foil Substances 0.000 description 3
- 239000003999 initiator Substances 0.000 description 3
- CHNLPLHJUPMEOI-UHFFFAOYSA-N oxolane;trifluoroborane Chemical compound FB(F)F.C1CCOC1 CHNLPLHJUPMEOI-UHFFFAOYSA-N 0.000 description 3
- 239000007774 positive electrode material Substances 0.000 description 3
- 239000002002 slurry Substances 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 3
- VAYTZRYEBVHVLE-UHFFFAOYSA-N 1,3-dioxol-2-one Chemical compound O=C1OC=CO1 VAYTZRYEBVHVLE-UHFFFAOYSA-N 0.000 description 2
- DURPTKYDGMDSBL-UHFFFAOYSA-N 1-butoxybutane Chemical compound CCCCOCCCC DURPTKYDGMDSBL-UHFFFAOYSA-N 0.000 description 2
- SBLRHMKNNHXPHG-UHFFFAOYSA-N 4-fluoro-1,3-dioxolan-2-one Chemical compound FC1COC(=O)O1 SBLRHMKNNHXPHG-UHFFFAOYSA-N 0.000 description 2
- 239000004342 Benzoyl peroxide Substances 0.000 description 2
- OMPJBNCRMGITSC-UHFFFAOYSA-N Benzoylperoxide Chemical compound C=1C=CC=CC=1C(=O)OOC(=O)C1=CC=CC=C1 OMPJBNCRMGITSC-UHFFFAOYSA-N 0.000 description 2
- BTBUEUYNUDRHOZ-UHFFFAOYSA-N Borate Chemical compound [O-]B([O-])[O-] BTBUEUYNUDRHOZ-UHFFFAOYSA-N 0.000 description 2
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 2
- 229910013716 LiNi Inorganic materials 0.000 description 2
- 229910000572 Lithium Nickel Cobalt Manganese Oxide (NCM) Inorganic materials 0.000 description 2
- WQDUMFSSJAZKTM-UHFFFAOYSA-N Sodium methoxide Chemical compound [Na+].[O-]C WQDUMFSSJAZKTM-UHFFFAOYSA-N 0.000 description 2
- UCKMPCXJQFINFW-UHFFFAOYSA-N Sulphide Chemical compound [S-2] UCKMPCXJQFINFW-UHFFFAOYSA-N 0.000 description 2
- LVZGQWKTUCVPBQ-UHFFFAOYSA-N acetic acid;trifluoroborane Chemical compound CC(O)=O.FB(F)F LVZGQWKTUCVPBQ-UHFFFAOYSA-N 0.000 description 2
- 239000011149 active material Substances 0.000 description 2
- 239000006256 anode slurry Substances 0.000 description 2
- 229910052786 argon Inorganic materials 0.000 description 2
- 235000019400 benzoyl peroxide Nutrition 0.000 description 2
- JHRWWRDRBPCWTF-OLQVQODUSA-N captafol Chemical compound C1C=CC[C@H]2C(=O)N(SC(Cl)(Cl)C(Cl)Cl)C(=O)[C@H]21 JHRWWRDRBPCWTF-OLQVQODUSA-N 0.000 description 2
- 239000006258 conductive agent Substances 0.000 description 2
- 238000000354 decomposition reaction Methods 0.000 description 2
- 230000007547 defect Effects 0.000 description 2
- 239000012467 final product Substances 0.000 description 2
- 238000009472 formulation Methods 0.000 description 2
- 230000006872 improvement Effects 0.000 description 2
- FRMOHNDAXZZWQI-UHFFFAOYSA-N lithium manganese(2+) nickel(2+) oxygen(2-) Chemical compound [O-2].[Mn+2].[Ni+2].[Li+] FRMOHNDAXZZWQI-UHFFFAOYSA-N 0.000 description 2
- JILPJDVXYVTZDQ-UHFFFAOYSA-N lithium methoxide Chemical compound [Li+].[O-]C JILPJDVXYVTZDQ-UHFFFAOYSA-N 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 239000012528 membrane Substances 0.000 description 2
- 229910052757 nitrogen Inorganic materials 0.000 description 2
- LKWKIVHUCKVYOA-UHFFFAOYSA-N phosphoric acid;trifluoroborane Chemical compound FB(F)F.OP(O)(O)=O LKWKIVHUCKVYOA-UHFFFAOYSA-N 0.000 description 2
- 238000011160 research Methods 0.000 description 2
- 229910052708 sodium Inorganic materials 0.000 description 2
- 239000011734 sodium Substances 0.000 description 2
- 229910001220 stainless steel Inorganic materials 0.000 description 2
- 239000010935 stainless steel Substances 0.000 description 2
- 238000003786 synthesis reaction Methods 0.000 description 2
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 description 2
- WVLBCYQITXONBZ-UHFFFAOYSA-N trimethyl phosphate Chemical compound COP(=O)(OC)OC WVLBCYQITXONBZ-UHFFFAOYSA-N 0.000 description 2
- 238000001291 vacuum drying Methods 0.000 description 2
- ZPFAVCIQZKRBGF-UHFFFAOYSA-N 1,3,2-dioxathiolane 2,2-dioxide Chemical compound O=S1(=O)OCCO1 ZPFAVCIQZKRBGF-UHFFFAOYSA-N 0.000 description 1
- SFXNZFATUMWBHR-UHFFFAOYSA-N 2-morpholin-4-yl-2-pyridin-3-ylacetonitrile Chemical compound C=1C=CN=CC=1C(C#N)N1CCOCC1 SFXNZFATUMWBHR-UHFFFAOYSA-N 0.000 description 1
- OEOIWYCWCDBOPA-UHFFFAOYSA-N 6-methyl-heptanoic acid Chemical compound CC(C)CCCCC(O)=O OEOIWYCWCDBOPA-UHFFFAOYSA-N 0.000 description 1
- 229910018632 Al0.05O2 Inorganic materials 0.000 description 1
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 1
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- GSNUFIFRDBKVIE-UHFFFAOYSA-N DMF Natural products CC1=CC=C(C)O1 GSNUFIFRDBKVIE-UHFFFAOYSA-N 0.000 description 1
- RWSOTUBLDIXVET-UHFFFAOYSA-N Dihydrogen sulfide Chemical compound S RWSOTUBLDIXVET-UHFFFAOYSA-N 0.000 description 1
- ZAFNJMIOTHYJRJ-UHFFFAOYSA-N Diisopropyl ether Chemical compound CC(C)OC(C)C ZAFNJMIOTHYJRJ-UHFFFAOYSA-N 0.000 description 1
- 239000002000 Electrolyte additive Substances 0.000 description 1
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 1
- 229910013075 LiBF Inorganic materials 0.000 description 1
- 229910012820 LiCoO Inorganic materials 0.000 description 1
- 229910013872 LiPF Inorganic materials 0.000 description 1
- 101150058243 Lipf gene Proteins 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- KEAYESYHFKHZAL-UHFFFAOYSA-N Sodium Chemical compound [Na] KEAYESYHFKHZAL-UHFFFAOYSA-N 0.000 description 1
- VMHLLURERBWHNL-UHFFFAOYSA-M Sodium acetate Chemical compound [Na+].CC([O-])=O VMHLLURERBWHNL-UHFFFAOYSA-M 0.000 description 1
- ADKPKEZZYOUGBZ-UHFFFAOYSA-N [C].[O].[Si] Chemical compound [C].[O].[Si] ADKPKEZZYOUGBZ-UHFFFAOYSA-N 0.000 description 1
- PFYQFCKUASLJLL-UHFFFAOYSA-N [Co].[Ni].[Li] Chemical compound [Co].[Ni].[Li] PFYQFCKUASLJLL-UHFFFAOYSA-N 0.000 description 1
- FBDMTTNVIIVBKI-UHFFFAOYSA-N [O-2].[Mn+2].[Co+2].[Ni+2].[Li+] Chemical compound [O-2].[Mn+2].[Co+2].[Ni+2].[Li+] FBDMTTNVIIVBKI-UHFFFAOYSA-N 0.000 description 1
- 239000006230 acetylene black Substances 0.000 description 1
- 238000007605 air drying Methods 0.000 description 1
- 125000003158 alcohol group Chemical group 0.000 description 1
- 239000010405 anode material Substances 0.000 description 1
- 239000003125 aqueous solvent Substances 0.000 description 1
- 239000012298 atmosphere Substances 0.000 description 1
- 238000009835 boiling Methods 0.000 description 1
- 238000003421 catalytic decomposition reaction Methods 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 239000011889 copper foil Substances 0.000 description 1
- 238000005520 cutting process Methods 0.000 description 1
- 230000001351 cycling effect Effects 0.000 description 1
- QKWQJULHSYOWGC-UHFFFAOYSA-N cyclobuten-1-ylmethanol Chemical compound OCC1=CCC1 QKWQJULHSYOWGC-UHFFFAOYSA-N 0.000 description 1
- 239000008367 deionised water Substances 0.000 description 1
- 229910021641 deionized water Inorganic materials 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- IEJIGPNLZYLLBP-UHFFFAOYSA-N dimethyl carbonate Chemical compound COC(=O)OC IEJIGPNLZYLLBP-UHFFFAOYSA-N 0.000 description 1
- 239000011267 electrode slurry Substances 0.000 description 1
- JDVIRCVIXCMTPU-UHFFFAOYSA-N ethanamine;trifluoroborane Chemical compound CCN.FB(F)F JDVIRCVIXCMTPU-UHFFFAOYSA-N 0.000 description 1
- 238000004880 explosion Methods 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 239000010439 graphite Substances 0.000 description 1
- 229910002804 graphite Inorganic materials 0.000 description 1
- 238000000227 grinding Methods 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 229910052739 hydrogen Inorganic materials 0.000 description 1
- 229910000037 hydrogen sulfide Inorganic materials 0.000 description 1
- 150000003949 imides Chemical class 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 238000003475 lamination Methods 0.000 description 1
- XIXADJRWDQXREU-UHFFFAOYSA-M lithium acetate Chemical compound [Li+].CC([O-])=O XIXADJRWDQXREU-UHFFFAOYSA-M 0.000 description 1
- MHCFAGZWMAWTNR-UHFFFAOYSA-M lithium perchlorate Chemical compound [Li+].[O-]Cl(=O)(=O)=O MHCFAGZWMAWTNR-UHFFFAOYSA-M 0.000 description 1
- 229910001486 lithium perchlorate Inorganic materials 0.000 description 1
- 229910001496 lithium tetrafluoroborate Inorganic materials 0.000 description 1
- AZVCGYPLLBEUNV-UHFFFAOYSA-N lithium;ethanolate Chemical compound [Li+].CC[O-] AZVCGYPLLBEUNV-UHFFFAOYSA-N 0.000 description 1
- 239000011572 manganese Substances 0.000 description 1
- 230000003446 memory effect Effects 0.000 description 1
- 238000013508 migration Methods 0.000 description 1
- 230000005012 migration Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 239000007773 negative electrode material Substances 0.000 description 1
- 239000005416 organic matter Substances 0.000 description 1
- 230000002093 peripheral effect Effects 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- 239000004014 plasticizer Substances 0.000 description 1
- 239000002798 polar solvent Substances 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 239000011241 protective layer Substances 0.000 description 1
- 238000012827 research and development Methods 0.000 description 1
- 238000005096 rolling process Methods 0.000 description 1
- 238000007789 sealing Methods 0.000 description 1
- 238000007086 side reaction Methods 0.000 description 1
- 150000003384 small molecules Chemical class 0.000 description 1
- 239000001632 sodium acetate Substances 0.000 description 1
- 235000017281 sodium acetate Nutrition 0.000 description 1
- QDRKDTQENPPHOJ-UHFFFAOYSA-N sodium ethoxide Chemical compound [Na+].CC[O-] QDRKDTQENPPHOJ-UHFFFAOYSA-N 0.000 description 1
- 238000001228 spectrum Methods 0.000 description 1
- 229920003048 styrene butadiene rubber Polymers 0.000 description 1
- 238000006467 substitution reaction Methods 0.000 description 1
- 125000000542 sulfonic acid group Chemical group 0.000 description 1
- 239000013589 supplement Substances 0.000 description 1
Images
Classifications
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0564—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of organic materials only
- H01M10/0565—Polymeric materials, e.g. gel-type or solid-type
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0564—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of organic materials only
- H01M10/0566—Liquid materials
- H01M10/0567—Liquid materials characterised by the additives
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0564—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of organic materials only
- H01M10/0566—Liquid materials
- H01M10/0568—Liquid materials characterised by the solutes
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0564—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of organic materials only
- H01M10/0566—Liquid materials
- H01M10/0569—Liquid materials characterised by the solvents
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/42—Methods or arrangements for servicing or maintenance of secondary cells or secondary half-cells
- H01M10/4235—Safety or regulating additives or arrangements in electrodes, separators or electrolyte
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2300/00—Electrolytes
- H01M2300/0017—Non-aqueous electrolytes
- H01M2300/0025—Organic electrolyte
Landscapes
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Manufacturing & Machinery (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Electrochemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Physics & Mathematics (AREA)
- Condensed Matter Physics & Semiconductors (AREA)
- General Physics & Mathematics (AREA)
- Inorganic Chemistry (AREA)
- Dispersion Chemistry (AREA)
- Secondary Cells (AREA)
Abstract
Description
技术领域
本申请涉及电池技术领域,特别涉及一种可聚合电解质及其制备方法和应用。
背景技术
二次电池由于具有高能量密度、长寿命、无记忆效应等优点,因而得到迅猛发展,应用范围也越来越广。目前,二次电池主要以液态电池为主,但液态电池能量密度较低、安全性差。主要是由于目前使用的液态电解质电化学窗口较窄,不能匹配高电压正极材料(如高电压钴酸锂、镍锰酸锂等)使用;有机溶剂沸点较低,容易漏液、发生起火爆炸等危险;常规盐高温易分解(如六氟磷酸锂)、易腐蚀铝箔(如双(三氟甲基)磺酰亚胺锂、双氟磺酰亚胺锂)、易产气(如二氟草酸磷酸锂),影响电池寿命。
目前解决方法主要有两种,一是在液态电解质中加入一些功能添加剂,该功能添加剂可以在电极表面形成一层钝化膜,有效缓解液态电解质被电极催化分解,但常规功能添加剂经分解在电极表面形成的钝化层并不致密,且在形成钝化层过程中消耗了来自于正极的离子,因而首周效率、放电比容较低。二是发展固态电池,即将传输离子的液态电解质替换成固态电解质,固态电解质大大提高了电池的安全性,不易发生热失控,高温稳定性好。目前常用的固态电解质包括氧化物电解质、硫化物电解质、聚合物电解质,其中,氧化物电解质电化学窗口较宽,但刚性太强;硫化物电解质有可塑性,但电化学窗口窄且极易产生硫化氢气体;聚合物电解质机械性能好,但离子电导率较低、离子迁移数低。世界范围内,全固态电池均处于起步阶段,依然无法兼顾高能量密度、长循环、本质安全。目前发展较多的是混合固液、凝胶电池,可以兼顾液态电池和全固态电池的优点,然而液态电解质的缺点依然决定着电池的性能。因此急需开发热稳定性好、钝化层稳定、自身提供离子的添加剂,开发新的稳定性好、电导率高的盐,开发离子电导率高、迁移数高的单离子导体。
发明内容
有鉴于此,本申请实施例提供了一种可聚合电解质及其制备方法和应用,以解决现有技术中存在的技术缺陷。
本申请提供一种可聚合电解质,所述电解质包括三氟化硼盐,所述三氟化硼盐的结构如通式Ⅰ所示:
其中,R+选自正一价的金属阳离子的中的任意一种,R1选自空白、含有取代基或不含有取代基的第一环或链中的任意一种,R2选自含有取代基或不含有取代基的能够发生聚合的第二环;
所述第一环包括由碳原子构成的环和含有至少一个杂原子的环,所述链包括仅由碳原子构成的链和含有至少一个杂原子的链,所述取代基包括环状取代基、链状取代基和卤素原子。
进一步地,R+选自钠离子、锂离子、钾离子中的任意一种;
所述第一环为三元环-十六元环,所述第一环包括饱和碳环、不饱和碳环、饱和杂环、不饱和杂环,所述链为1-20个原子组成的链,所述仅由碳原子构成的链和含有至少一个杂原子的链均包括饱和链和含有不饱和键的不饱和链,所述不饱和键包括双键和/或三键;
所述第二环为三元环-十元环,所述第二环选自环烯、环醚、环缩醛、环酯、环酸酐、环碳酸酯、环酰胺、环胺、环硫醚、环二硫、环硅氧烷、环磷氮烯中的任意一种;
所述环状取代基包括取代或未取代的三元环-二十元环、同时含有两个或两个以上环结构的多环取代基;
所述链状取代基包括取代或未取代的烷基、杂烷基、烯基、杂烯基、炔基、烯炔基、烷硫基、含C=O取代基、=O、=S。
进一步地,在R2选自环烯的情况下,R2为含有取代基或不含有取代基的四元环、五元环、七元环、八元环、九元环或十元环;
在R2选自环醚的情况下,R2为含有取代基或不含有取代基的三元环、四元环、五元环或七元环;
在R2选自环缩醛的情况下,R2为含有取代基或不含有取代基的六元环或八元环;
在R2选自环酯的情况下,R2为含有取代基或不含有取代基的四元环、六元环、七元环或八元环;
在R2选自环酸酐的情况下,R2为含有取代基或不含有取代基的五元环、七元环或八元环;
在R2选自环碳酸酯的情况下,R2为含有取代基或不含有取代基的六元-八元环;
在R2选自环酰胺的情况下,R2为含有取代基或不含有取代基的四元-八元环;
在R2选自环胺的情况下,R2为含有取代基或不含有取代基的三元环、四元环或七元环;
在R2选自环硫醚的情况下,R2为含有取代基或不含有取代基的三元环或四元环;
在R2选自环二硫的情况下,R2为含有取代基或不含有取代基的四元-八元环;
在R2选自环硅氧烷的情况下,R2为含有取代基或不含有取代基的六元环、八元环或十元环;
在R2选自环磷氮烯的情况下,R2为含有取代基或不含有取代基的六元环。
进一步地,在R2选自环烯的情况下,通式Ⅰ的结构包括:
在R2选自环醚的情况下,通式Ⅰ的结构包括:
在R2选自环缩醛的情况下,通式Ⅰ的结构包括:
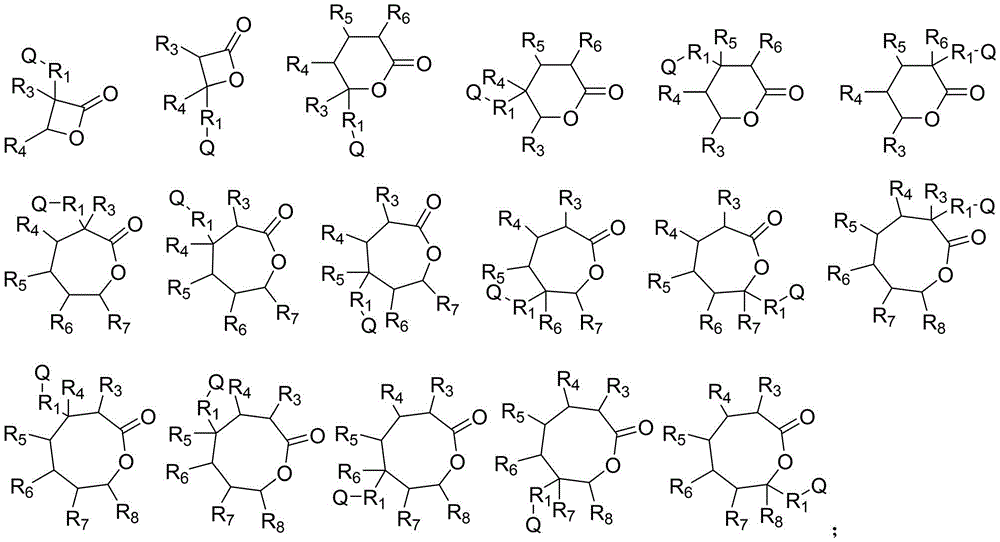
在R2选自环酯的情况下,通式Ⅰ的结构包括:
在R2选自环酸酐的情况下,通式Ⅰ的结构包括:
在R2选自环碳酸酯的情况下,通式Ⅰ的结构包括:
在R2选自环酰胺的情况下,通式Ⅰ的结构包括:
在R2选自环胺的情况下,通式Ⅰ的结构包括:
在R2选自环硫醚的情况下,通式Ⅰ的结构包括:
在R2选自环二硫的情况下,通式Ⅰ的结构包括:
在R2选自环硅氧烷的情况下,通式Ⅰ的结构包括:
在R2选自环磷氮烯的情况下,通式Ⅰ的结构包括:
R3、R4、R5、R6、R7、R8、R9、R10均选自氢原子、含有取代基或不含有取代基的环或链、卤素原子、金属阳离子中的任意一种或几种的组合。
进一步地,所述链状取代基包括氢原子、卤素原子、醚氧键/基、醚硫键/基、硝基、酰胺、磺酰胺基、磺基、磺酸基、盐类取代基、含C=O取代基、含N取代基、烷基、杂烷基、烯基、杂烯基、炔基、烯炔基、=O、=S;
所述环状取代基包括三元环、四元环、五元环、六元环、七元环、八元环和同时含有两个或两个以上环结构的多环取代基;
所述卤素原子包括氯原子、溴原子、碘原子、氟原子。
进一步地,所述取代基包括:
氢原子、甲基、乙基、丙基、异丙基、正丁基、异丁基、正戊基、异戊基、仲戊基、新戊基、正己基、异己基、仲己基、新己基、正庚基、异庚基、仲庚基、新庚基、正辛基、异辛基、仲辛基、新辛基、乙烯基、丙烯基、丁烯基、戊烯基、己烯基、庚烯基、乙炔基、丙炔基、丁炔基、戊炔基、己炔基、庚炔基、环己基、环戊基、苯基、酯基、磺基烷、酰胺基、磺酰胺基、磺酰基、磺酸基、醛基、醚氧键/基、醚硫键/基、硝基、-COOCH3、COOCH2CH3、-SCH3、=O、-N(CH3)2、-CO-N(CH3)2、-S-、-O-、
进一步地,任意一种通式Ⅰ中所有碳原子上的全部或部分氢原子独立地被卤素原子取代;
优选地,任意一种通式Ⅰ中所有碳原子上的全部或部分氢原子独立地被氟原子取代。
本申请还提供一种根据如上任意一段所述的可聚合电解质在二次电池中的应用,所述应用为:所述三氟化硼盐既能够作为电解质的添加剂应用,也能够作为盐应用,含有可聚合基团的单体聚合之后还能够作为单离子导体兼高分子框架应用。
进一步地,所述应用包括在液态电解质、凝胶电解质、混合固液电解质、准固态电解质、全固态电解质中的应用,所述液态电解质、凝胶电解质、混合固液电解质、准固态电解质、全固态电解质均独立地包括如上任意一段所述的电解质;
优选地,所述应用还包括作为电池或电池组的应用,所述电池包括如上任意一段所述的电解质以及正极、负极和封装外壳;所述液态电解质、凝胶电解质、混合固液电解质、准固态电解质、全固态电解质可应用于液态电池、混合固液电池、半固态电池、凝胶电池、准固态电池和全固态电池,所述电池组包括所述电池。
技术效果:
本申请提供的含硼有机化合物可作为电池中的添加剂,其能够在电池的电极表面形成稳定、致密的钝化膜,阻碍电解质与电极活性物质直接接触,抑制电解质各组分的分解,扩宽了整个电解质体系的电化学窗口,可显著提高电池的放电比容量、库伦效率和循环性能;此外,该含硼有机化合物本身是一种离子导体,作为添加剂,其在电极表面形成钝化层的同时较少消耗从正极脱出的活性离子,能够对电池的首次库伦效率、首周放电比容量有明显的提升。且含有该含硼有机化合物的电解质和现有的高电压高比容的正极材料及低电压高比容负极材料复配成电池时,电池的电化学性能均有改善。此外,本申请结构还能与常规添加剂混合使用,即双添加剂或多添加剂,使用双添加剂或多添加剂的电池显示出更优异的电化学性能。
本申请提供的含硼有机化合物可作为电池中的主盐,含有的离子较容易被解离,因而离子电导率较高,组装的电池电化学性能优异。
本申请提供的含硼有机化合物若含有可聚合的基团,还可以聚合之后形成单离子导体兼高分子骨架,不仅可以提供良好的离子电导,还可以提供良好的机械性能,电池综合性能佳。
此外,本申请中的三氟化硼盐的原料来源丰富,原料选择性广,成本低,制备过程简单,反应简单条件温和,具有极佳的工业应用前景。
另外,本申请还能采用钠、钾等除了传统锂以外的金属来形成盐,这为本申请后期的应用、成本控制或原料选择等提供了更多可能性,意义较大。
所以,本申请提供的可聚合电解质可以应用于液态电池、混合固液电池、凝胶电池、准固态电池、全固态电池中,可以改善电池的电化学性能,包括提高电池的能量密度、提升循环稳定性、延长电池的使用寿命,并且合成工艺简单、原料价格低廉,具有良好的经济效益。
附图说明
图1~12是实施例1~12所示产物的核磁氢谱图;
图13~图16分别为实施例1/6/9/14作为液态电解质添加剂所制成的电池1/6/9/14与对应的不含有本发明实施例的对比电池1/4/7/11的效果对比图;
图17~18分别为实施例1/7作为液态电解质盐所制成的电池1/7与对应的不含有本发明实施例的对比电池1/7的效果对比图;
图19为实施例2中的单体作为聚合单体所制成的聚合物电解质电池2的效果图;
图20为实施例10中的单体作为聚合单体所制成的聚合物电解质电池10的效果图。
具体实施方式
下面结合附图对本申请的具体实施方式进行描述。
在本发明中,除非另有说明,否则本文中使用的科学和技术名词具有本领域技术人员所通常理解的含义。并且,本文中所用的试剂、材料和操作步骤均为相应领域内广泛使用的试剂、材料和常规步骤。同时,为了更好地理解本发明,下面提供相关术语的定义和解释。
在本发明中,若某一个基团需要与两部分结构相连,故其有两个待连接的连接键,若没有明确指出是哪两个原子与被连接部分连接,则任意一个含有H的原子均可进行连接。
在本发明中,若一个C上含有多个H,则这多个H中的任意一个或几个H可被取代基取代,也可以全部H均被取代基取代,在两个及两个以上H被取代基取代的情况下,取代基可相同也可不同。比如R01和R02均表示其所连接的C既可以被一个取代基取代,也可以被两个取代基取代,例如若R01为甲基,R02为F,则上述结构可为若R01为H,R02为甲基和F,则上述结构可为
在本发明中,若化学键没有画在原子上,而是画在了与键相交的位置上,如代表环己烷上任意一个H都可以被取代基R04取代,且可取代一个H也可以取代两个或多个H,取代基可相同也可不同。若环己烷的某一个C上含有两个H,则这两个氢H可全部被取代基取代,也可以仅取代1个,如两个H可都被甲基取代,也可以一个被甲基取代,一个被乙基取代。此外,取代基还可通过双键与环连接。例如,在该结构中,若R04为甲基、=O、F,则上述结构可为
所述“Et”为乙基,“Ph”为苯基。
所述“三氟化硼类化合物”指三氟化硼、含有三氟化硼的化合物或三氟化硼络合物等等。
本发明的发明点为提供一种可作为电解质添加剂、电解质盐和可聚合单体的一元有机三氟化硼盐,即在该有机物中含有基团,其中,R+可以为Li+、Na+等。该三氟化硼盐可应用于液态电池、混合固液电池、半固态电池、凝胶电池、准固态电池和全固态电池中。该化合物的制备方法简单、巧妙,得率高。即将原料、三氟化硼类化合物和R+源进行反应所得,具体为原料中的-OH参与反应,其他结构不参与反应。具体的制备方法主要包括两种:
一、氮气/氩气气氛下,R+源与原料加入到溶剂中,混合,在5-60℃反应3-24小时,所得混合溶液于20-80℃、真空度约-0.1MPa的条件下减压干燥除去溶剂,得到中间体;然后加三氟化硼类化合物,5-60℃搅拌反应6-24小时,将所得混合液于20-80℃、真空度约-0.1MPa的条件下减压干燥,得到粗产物,将粗产物洗涤、过滤、干燥,得终产物一元有机三氟化硼盐,得率为70~95%。
二、氮气/氩气气氛下,原料与三氟化硼类化合物加入到溶剂中,混合均匀,在5-60℃下反应6-24小时,所得混合溶液于20-80℃、真空度约-0.1MPa的条件下减压干燥除去溶剂,反应得中间体;将R+源加入至溶剂中,然后将含有R+源的溶剂加入到中间体中,5-60℃搅拌反应3-24小时,即得粗产物,将粗产物直接洗涤或减压干燥后洗涤,然后过滤、干燥,得终产物一元有机三氟化硼盐,得率为70~95%。
以上两种具体的制备方法中,三氟化硼类化合物可包括三氟化硼乙醚络合物、三氟化硼四氢呋喃络合物、三氟化硼丁醚络合物、三氟化硼乙酸络合物、三氟化硼单乙胺络合物、三氟化硼磷酸络合物等等。R+源包括金属锂/钠、甲醇锂/钠、氢氧化锂/钠、乙醇锂/钠、丁基锂/钠、乙酸锂/钠等。每一处所述的溶剂独立地为醇类(有些液体醇类的原料也可同时为溶剂)、乙酸乙酯、DMF、丙酮、己烷、二氯甲烷、四氢呋喃、乙二醇二甲醚等。洗涤可用小极性溶剂,如乙醚、正丁醚、正己烷、二苯醚等。
实施例1
制备方法:氮气气氛下,将原料(0.88g,0.01mol)和氢氧化锂(0.24g,0.01mol)用10ml甲醇溶液混合均匀,15℃反应8小时。所得混合溶液于30℃、真空度约-0.1MPa的条件下减压干燥除去溶剂,得到中间体。将三氟化硼乙醚络合物(1.45g,0.01mol)和15mlTHF(四氢呋喃)加入到中间体中,40℃搅拌反应6小时,将所得混合液于30℃、真空度约-0.1MPa的条件下减压干燥,得到的粗产物经二氯甲烷过滤、干燥,得到产物A1。产率为86%,核磁如图1所示。
实施例2
制备方法:氮气气氛下,将原料(0.90g,0.01mol)和三氟化硼四氢呋喃络合物(1.40g,0.01mol)在15ml乙二醇二甲醚中混合均匀,室温反应10小时。所得混合溶液于40℃、真空度约-0.1MPa的条件下减压干燥除去溶剂,得到中间体。将乙醇锂(0.52g,0.01mol)溶解在10ml的乙醇中缓慢加入到中间体中,45℃搅拌反应8小时,将所得混合液于45℃、真空度约-0.1MPa的条件下减压干燥,得到的固体用正丁醚洗涤三次,经过滤、干燥,得到产物A2。产率为80%,核磁如图2所示。
实施例3
制备方法:氩气气氛下,将原料(1.15g,0.01mol)和三氟化硼乙醚络合物(1.49g,0.0105mol)在15mlTHF(四氢呋喃)中混合均匀,室温反应12小时。所得混合溶液于30℃、真空度约-0.1MPa的条件下减压干燥除去溶剂,得到中间体。将6.25ml丁基锂的己烷溶液(c=1.6mol/L)加入到中间体中,室温搅拌反应7小时,将所得混合液于30℃、真空度约-0.1MPa的条件下减压干燥,得到的粗产物用环己烷洗涤3次,过滤、干燥,得到产物A3。产率为89%,核磁如图3所示。
实施例4
制备方法:氮气气氛下,取一定量的原料(0.74g,0.01mol)和甲醇锂(0.38g,0.01mol),用20ml甲醇混合均匀,室温反应10小时。所得混合溶液于40℃、真空度约-0.1MPa的条件下减压干燥除去溶剂,得到中间体。将三氟化硼四氢呋喃络合物(1.40g,0.01mol)和15mlTHF(四氢呋喃)加入到中间体中,室温搅拌反应6小时,将所得混合液于40℃、真空度约-0.1MPa的条件下减压干燥,得到的固体用异丙醚洗涤三次、经过滤、干燥,得到产物A4。产率81%,核磁如图4所示。
实施例5
制备方法:氮气气氛下,将原料(0.91g,0.01mol)和氢氧化锂(0.24g,0.01mol)用10ml甲醇溶液混合均匀,室温反应8小时。所得混合溶液于40℃、真空度约-0.1MPa的条件下减压干燥除去溶剂,得到中间体。将三氟化硼磷酸络合物(1.66g,0.01mol)和15mlTHF加入到中间体中,45℃搅拌反应6小时,将所得混合液于60℃、真空度约-0.1MPa的条件下减压干燥,得到的粗产物经二氯甲烷过滤、干燥,得到产物A5。产率为85%,核磁如图5所示。
实施例6
制备方法:氩气气氛下,将原料(0.88g,0.01mol)和三氟化硼乙酸络合物(1.92g,0.0102mol)在15mlTHF(四氢呋喃)中混合均匀,室温反应12小时,所得混合溶液于40℃、真空度约-0.1MPa的条件下减压干燥除去溶剂,得到中间体。将乙酸锂(0.68g,0.0102mol)溶解在10ml的N,N-二甲基甲酰胺中并加入到中间体中,50℃搅拌反应8小时,将所得混合液于80℃、真空度约-0.1MPa的条件下减压干燥,得到的固体用二苯醚洗涤三次、经过滤、干燥,得到产物A6。产率为78%,核磁如图6所示。
实施例7
制备方法:氩气气氛下,将甲醇锂(0.38g,0.01mol)溶解在15ml的甲醇中,混合均匀后,加入到原料(1.04g,0.01mol)混合均匀,45℃反应12小时,所得混合溶液于45℃、真空度约-0.1MPa的条件下减压干燥除去溶剂,得到中间体。将三氟化硼乙醚络合物(1.45g,0.01mol)和15mlTHF加入到中间体中,室温搅拌24小时,将所得混合液于40℃、真空度约-0.1MPa的条件下减压干燥,得到的固体用二氯甲烷洗涤三次、经过滤、干燥,得到产物A7。产率为75%,核磁如图7所示。
实施例8
制备方法:氮气气氛下,将原料(1.04g,0.01mol)和氢氧化锂(0.24g,0.01mol)用10ml甲醇溶液混合均匀,10℃反应8小时。所得混合溶液于40℃、真空度约-0.1MPa的条件下减压干燥除去溶剂,得到中间体。将三氟化硼乙醚络合物(1.45g,0.01mol)加入到中间体中,加入10ml的乙二醇二甲醚溶剂,室温搅拌24小时,将所得混合液于40℃、真空度约-0.1MPa的条件下减压干燥,得到的固体用二氯甲烷洗涤三次、经过滤、干燥,得到产物A8。产率为82%,核磁如图8所示。
实施例9
制备方法:氩气气氛下,将原料(1.36g,0.01mol)和三氟化硼乙醚络合物(1.45g,0.01mol)在15mlTHF(四氢呋喃)中混合均匀,室温反应12小时。所得混合溶液于30℃、真空度约-0.1MPa的条件下减压干燥除去溶剂,得到中间体。将6.25ml丁基锂的己烷溶液(c=1.6mol/L)加入到中间体中,室温搅拌反应6小时,将所得混合液于40℃、真空度约-0.1MPa的条件下减压干燥,得到的粗产物用环己烷洗涤3次,过滤、干燥,得到产物A9。产率为85%,核磁如图9所示。
实施例10
制备方法:氩气气氛下,将10mlTHF加到原料(0.84g,0.01mol)中,将6.25ml丁基锂的己烷溶液(c=1.6mol/L)缓慢滴加到1-环丁烯-1-甲醇的THF溶液中,室温搅拌反应6小时,将所得混合液于40℃、真空度约-0.1MPa的条件下减压干燥,得到中间体。将三氟化硼乙醚络合物(1.45g,0.01mol)和15mlTHF加入中间体中,室温反应12小时。将所得混合液于30℃、真空度约-0.1MPa的条件下减压干燥除去溶剂。得到的粗产物用环己烷洗涤3次,过滤、干燥,得到产物A10。产率为85%,核磁如图10所示。
实施例11
制备方法:氮气气氛下,将原料(1.12g,0.01mol)和氢氧化锂(0.24g,0.01mol)用10ml甲醇溶液混合均匀,10℃反应8小时。所得混合溶液于40℃、真空度约-0.1MPa的条件下减压干燥除去溶剂,得到中间体。将三氟化硼乙醚络合物(1.45g,0.01mol)加入到中间体中,加入10ml的乙二醇二甲醚溶剂,室温搅拌24小时,将所得混合液于40℃、真空度约-0.1MPa的条件下减压干燥,得到的固体用二氯甲烷洗涤三次、经过滤、干燥,得到产物A11。产率为79%,核磁如图11所示。
实施例12
制备方法:氩气气氛下,将原料(1.30g,0.01mol)和三氟化硼乙醚络合物(1.45g,0.01mol)在15mlTHF(四氢呋喃)中混合均匀,室温反应12小时。所得混合溶液于30℃、真空度约-0.1MPa的条件下减压干燥除去溶剂,得到中间体。将6.25ml丁基锂的己烷溶液(c=1.6mol/L)加入到中间体中,室温搅拌反应6小时,将所得混合液于40℃、真空度约-0.1MPa的条件下减压干燥,得到的粗产物用环己烷洗涤3次,过滤、干燥,得到产物A12。产率为83%,核磁如图12所示。
试验例1
本发明所保护的三氟化硼有机盐主要起三个方面的作用:1、在电解质(包括液态和固态)中用作添加剂,主要起到生成钝化层的作用,并且由于本身可以解离离子,起到补充所消耗的离子作用,因此对于电池的首周效率、首周放电比容量、长循环稳定性、倍率性能均有很大提升;2、在电解质(包括液态和固态)中作为盐,主要起到提供离子传输兼顾钝化电极的作用,其单独作为盐或与传统的盐配合作为双盐应用,效果好;3、聚合后作为单离子导体聚合物电解质,应用于凝胶电池和全固态电池。下面以试验的方式来说明本申请的性能。
一、作为液态电解质中的添加剂
首先,在水分含量小于10ppm的手套箱中,依次加入有机溶剂、盐、常规添加剂充分混合均匀,即可配制基础液态电解质L1~L10。
需要说明的是,在本试验例中用到的有机溶剂包括碳酸甲乙酯(EMC)、碳酸二甲酯(DMC)、碳酸二乙酯(DEC)、碳酸乙烯酯(EC),常规添加剂包括氟代碳酸乙烯酯(FEC)、碳酸亚乙烯酯(VC)、磷酸三甲酯(TMP)、硫酸乙烯酯(DTD),盐包括双草酸硼酸锂(LiBOB)、二氟草酸硼酸锂(LiODFB)、双氟磺酰亚胺锂(LiFSI)、六氟磷酸锂(LiPF6)、双(三氟甲基)磺酰亚胺锂(LiTFSI)、四氟硼酸锂(LiBF4)、高氯酸锂(LiClO4)。具体如表1所示。
表1基础液态电解质配方
将实施例1~12获得的有机物A1~A12和基础液态电解质L1~L10充分混合均匀得到系列液态电解质E1~E15,具体成分、配比等如表2所示。
表2实施例1~12的有机物配制的液态电解质E1~E15
| 液态电解质 | 基础液态电解质 | 添加剂 | 添加剂占比 |
| E1 | L1 | A1 | 0.5% |
| E2 | L1 | A1 | 1% |
| E3 | L1 | A1 | 2% |
| E4 | L1 | A2 | 1% |
| E5 | L2 | A3 | 1% |
| E6 | L3 | A4 | 1% |
| E7 | L4 | A5 | 1% |
| E8 | L5 | A6 | 1% |
| E9 | L6 | A7 | 1% |
| E10 | L7 | A7 | 1% |
| E11 | L8 | A8 | 1% |
| E12 | L9 | A9 | 2% |
| E13 | L10 | A10 | 1% |
| E14 | L10 | A11 | 1% |
| E15 | L10 | A12 | 1% |
将上述获得的基础液态电解质L1~L10和系列液态电解质E1~E15分别组装成扣式电池,具体如下:负极壳、负极极片、PE/Al2O3隔膜、电解质、正极极片、不锈钢片、弹簧片、正极壳装配成扣式电池,室温进行长循环测试,其中循环方式0.1C/0.1C1周、0.2C/0.2C5周、1C/1C44周(C代表倍率),所述正极极片是直径为12mm的圆片,所述负极极片是直径为14mm的圆片,所述隔膜是直径为16.2mm的圆片,为商用Al2O3/PE多孔隔膜,具体如表4和表5所示。
其中,电池正负极极片制备过程如下:
(1)正极极片
将正极主材活性物质、导电添加剂、粘结剂按照95:2:3加入到溶剂中,溶剂占总浆料的68%,混合搅拌均匀得到具有一定流动性的正极浆料;将正极浆料涂布在铝箔上,烘干、压实后,得到可用的正极极片。这里活性物质选择使用钴酸锂(LiCoO2,简写LCO)、镍钴锰酸锂(选用NCM811)、镍钴铝酸锂(LiNi0.8Co0.15Al0.05O2,简写NCA)、镍锰酸锂(LiNi0.5Mn1.5O4,简写LNMO),导电添加剂均选择使用碳纳米管(CNT)和SuperP,粘结剂使用聚偏氟乙烯(PVDF),溶剂使用N-甲基吡咯烷酮(NMP)。
(2)负极极片
将负极主材活性物质(金属锂除外)、导电添加剂、粘结剂按照95:2:3加入到溶剂去离子水中,溶剂占总浆料的45%,混合搅拌均匀得到具有一定流动性的负极浆料;将负极浆料涂布在铜箔上,烘干、压实后得到可用的负极极片。这里活性物质选择使用石墨(C)、硅氧碳(SiOC450)、金属锂(Li),导电剂为碳纳米管(CNT)和SuperP,粘结剂为羧甲基纤维素(CMC)和丁苯橡胶(SBR)。
选用的正负极体系如表3所示:
表3正负极体系
| 电池正负极体系 | 正极主材 | 负极主材 |
| X1 | LCO | SiOC450 |
| X2 | NCM811 | SiOC450 |
| X3 | NCA | C |
| X4 | NCM811 | Li |
| X5 | LNMO | C |
将电池1~16和对比电池1~12室温下的首周效率、首周放电比容量、循环50周容量保持率进行测试,实施例和对比例电池的配置和测试方式如表4所示,测试结果如表5所示。
表4实施例和对比例电池的配置和测试方式
表5首周效率、首周放电比容量、循环50周容量保持率测试结果对比
可以看出,加入了本申请提供的材料作为添加剂的电池相对于未加入的对比电池其首周放电比容量更高、首周效率更高、循环50周的容量保持率也更高,且性能优于目前的常规添加剂。此外,在有常规添加剂存在的情况下,使用含硼盐添加剂的电池显示出更优异的电化学性能。
二、作为液态电解质中的盐
(1)配制液态电解质
A1、A5、A6、A7、A12与有机溶剂、常规添加剂、常规盐混合均匀得到系列液态电解质R1、R5、R6、R7、R12,常规盐、有机溶剂、常规添加剂混合均匀得到系列常规液态电解质Q1、Q5、Q6、Q7、Q12,使用的溶剂和常规添加剂均包含在本试验例“一”中所述的溶剂和常规添加剂。液态电解质具体成分、配比等如表6所示。
表6合成的含硼有机物作为盐配制的液态电解质
注:1M指1mol/L。
(2)电池装配
获得的系列液态电解质R(表6所示)和常规液态电解质Q(表6所示)组装成扣式电池,正负极、隔膜大小、装配方法、电池的循环方式同本试验例“一”中所示的扣式电池,分别为电池(即实施例)1、5、6、7、12以及对应的对比电池。电池具体配置、循环方式和电压范围如表7所示,电池(即表7或8中的实施例)和对比电池(即表7或8中的对比例)室温下的首周放电比容量、首周效率、循环50周容量保持率结果如表8所示。
表7实施例和对比例扣式电池的配置和测试方式
表8表7所示的实施例和对比例扣式电池测试结果对比
综上,本发明所提供的三氟化硼盐单独作为传输离子的盐或与常规盐形成双盐在非水溶剂中,离子容易被溶剂化,为电池提供较高的离子电导率,且稳定性高,具有较优异的综合性能,在LCO、NCM811为正极,SiOC450、Li为负极的液态电池体系中,均显示出非常优异的电化学性能,首周效率、首周放电比容量、容量保持率均比较高,且性能与传统盐对应的电池相当或略优于传统盐对应的电池。
三、单离子导体聚合物电解质
(1)配制电解质
将单体(本申请实施例中的化合物A1、A2、A4、A5、A9、A10、A11、A12)、塑化剂、电池添加剂、盐、引发剂搅拌均匀后,形成前驱体溶液,获得前驱体S1、S2、S4、S5、S9、S10、S11、S12,具体配比如表9。使用的引发剂为偶氮二异丁腈(AIBN)、过氧化苯甲酰(BPO)、异辛酸亚锡(Sn(Oct)2)。
表9前驱体溶液组成
(2)电池装配
由表9获得的电解质前驱体溶液S1、S2、S4、S5、S9、S10、S11、S12,由这些前驱体分别组装成软包电池,即为电池1、2、4、5、9、10、11、12;具体如下:将尺寸为64mm×45mm的正极极片、65mm×46mm的负极极片、隔膜装配成2Ah软包电芯,经叠片、烘烤、注液、化成过程,得到二次电池,电池装配体系为表3中的X2,隔膜使用商业PE/Al2O3多孔膜。
(3)电池测试
电解质前驱体溶液S1、S2、S4、S5、S9、S10、S11、S12制备的二次电池原位固化完全后,室温下对电池的首周放电容量、首周效率、循环50周容量保持率进行测试,测试电压范围为3.0~4.2V,其中循环方式0.1C/0.1C2周、0.3C/0.3C48周(C代表倍率),测试结果如表10所示。
表10实施例电池的测试结果
| 电池 | 首周放电容量(Ah) | 首周效率(%) | 循环50周容量保持率(%) |
| 电池1 | 1.74 | 86.8 | 79.6 |
| 电池2 | 1.90 | 94.6 | 89.8 |
| 电池4 | 1.94 | 96.5 | 90.3 |
| 电池5 | 1.92 | 95.8 | 90.1 |
| 电池9 | 1.88 | 93.3 | 89.9 |
| 电池10 | 1.73 | 86.0 | 79.1 |
| 电池11 | 1.76 | 87.4 | 80.0 |
| 电池12 | 1.89 | 94.2 | 90.4 |
如表10,通过实施例中的测试数据发现可聚合的单体A1、A2、A4、A5、A9、A10、A11、A12构成的前驱体溶液经过原位固化之后作为聚合物电解质,在NCM811/SiOC450的固态电池体系中,显示出非常优异的电化学性能,首周效率、首周放电容量、容量保持率均比较高。由实施例1、10、11(如表10所示,体系中均没有加入常规盐)聚合之后可得到性能优异的固态电解质;当额外匹配常规盐使用时,由于提高了解离的离子数量,因而电池展现出更加优异的电化学性能。
此外,本申请还展示了一些实施例作为添加剂、盐和聚合物电解质的效果图。图13~图16分别为实施例1/6/9/14作为液态电解质添加剂所制成的电池1/6/9/14与对应的不含有本发明实施例的对比电池1/4/7/11的效果对比图。图17~18分别为实施例1/7作为液态电解质盐所制成的电池1/7与对应的不含有本发明实施例的对比电池1/7的效果对比图。图19为实施例2中的单体作为聚合单体所制成的聚合物电解质电池2的效果图;图20为实施例10中的单体作为聚合单体所制成的聚合物电解质电池10的效果图。
综上,首周效率、首周放电比容量、首周放电容量、容量保持率等性能对于电池的整体性能具有直接且显著的影响,其直接决定着电池能否应用。因此,提高这些性能是众多本领域研究者的目标或方向,但在本领域中,这些性能的提高是非常不易的,一般能提高3-5%左右便是较大的进展。本申请在前期试验数据中,很惊喜的发现,这些数据与常规的数据相比,具有很大的提高。作为液态电解质添加剂时,电池性能提高了5-35%左右,且本申请中的添加剂与常规添加剂联合应用也表现出了较佳的效果;本发明提供的材料作为电解质中的盐效果非常好,与常规盐匹配具备效果更佳,还可以使用更高的浓度(如1.5M、2M),获得高盐体系电解质,对电池的电化学性能也有非常突出的效果,这里不再赘述;本发明提供的材料还可以引发聚合成为单离子导体聚合物电解质,应用于凝胶电池、准固态电池和全固态电池。且本申请的结构类型也与常规的结构具有巨大的区别,这为本领域的研发提供了一种新的方向和思路,也为进一步的研究带来了很大的空间,且该本申请中的物质还能一种结构多种用途;意义极大。
试验例2
本试验例设置试验组1-3、对照组1-3。其中,试验组1采用上述实施例1提供的电解质,试验组2采用上述实施例2提供的电解质,试验组3采用上述实施例3提供的电解质。
对照组1采用如下所示结构的电解质:
对照组2采用如下所示结构的电解质:
对照组3采用如下所示结构的电解质:
试验组1-3、对照组1-3均采用如下方法制备电池:
(1)正极片的制备:正极活性物质、导电剂乙炔黑、粘结剂聚偏二氟乙烯(PVDF)按80:10:10的质量比混合均匀后,加入一定量溶剂N-甲基-2-吡咯烷酮(NMP),在混料机中充分研磨1小时,然后通过自动涂覆机在集流体铝箔上涂上一定厚度的薄膜,置于80℃鼓风干燥箱中烘30min,再放入120℃真空干燥箱烘干12小时。将烘干的极片经过对辊机滚压,使活性物质与集流体紧密结合。将压好的极片裁成Φ12mm的圆片后,再次进行真空干燥,储存备用。
(2)负极片、液态电解质、隔膜的制备:负极极片采用厚度为1.5mm直径为14mm的锂金属薄片;液态电解质为各组所述电解质溶于EC:DEC:EMC=1:1:1(体积比)的溶液中(各组电解质的固含量为20%)并加入1%的AIBN或Sn(Oct)2引发剂制备得到;隔膜为商用Al2O3/PE多孔隔膜,将隔膜通过切片机裁剪成为Φ16mm的圆片。
(3)电池的组装:在充满氩气的手套箱中进行电池组装,手套箱中氧含量、水含量均须低于1ppm,干燥的正负极片移入手套箱后,将负极壳、负极极片、PE/Al2O3隔膜、液态电解质、正极极片、不锈钢片、弹簧片、正极壳按顺序装配成扣式电池,用封口机压封。然后将扣式电池在60℃烘箱中加热12h。电池装配体系为表3中的X4,隔膜使用商业PE/Al2O3多孔膜。分别测试并记录试验组1-3、对照组1-3电池的首周放电比容量、首周效率、循环50周容量保持率,结果如表11所示。
表11试验组及对照组电池测试结果对比
可以看出,对照组1-3的首周放电比容量、首周效率和50周容量保持率均低于试验组1-3,可能是由于当电解质固含量相同时,对照组1中锂离子相对数量较低,且对锂离子的传输较差;对照组2的单体虽然可以自由基聚合,但对Li的稳定性稍差;对照组3是不可聚合的小分子,无法在金属锂表面形成一层稳定的钝化保护层,因此无法阻止金属锂与电解液的副反应,且黏度稍大,离子传输性能略低。综上,本申请提供的电解质通过其在电池中原位聚合,可以有效改善电池性能,延长电池使用寿命,提高电池的安全性。
在本发明中,选择了实施例1-12中的结构作为代表来说明本申请的制备方法和效果。其他没有列举的结构均可采用实施例1-12中任意一个中所记载的方法来进行制备。其制备方法均为由原料、三氟化硼类化合物以及R+源反应得到产物三氟化硼有机物盐,即原料中的-OH变为R+可为Li+、Na+等,其它结构不变。另外,还有很多结构本申请人的研究团队已经做了系列化效果试验,效果都很不错,与上述实施例中的效果类似,但由于篇幅关系,只记载了部分结构。
实施例中所用到的原料均可以购买得到或经过简单制备得到,制备工艺也均为现有技术,故在说明书中未进行详细描述。
还需要说明的是,本申请人对该系列结构做了极大量的试验,有时候为了更好的与现有体系进行对比,存在同一个结构和体系,做了不止一次试验的情况,因此,不同次的试验可能会存在一定的误差。
最后应说明的是:以上所述的各实施例仅用于说明本发明的技术方案,而非对其限制;尽管参照前述实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述实施例所记载的技术方案进行修改,或者对其中部分或全部技术特征进行等同替换;而这些修改或替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围。
Claims (10)
2.根据权利要求1所述的可聚合电解质,其特征在于,
R+选自钠离子、锂离子、钾离子中的任意一种;
所述第一环为三元环-十六元环,所述第一环包括饱和碳环、不饱和碳环、饱和杂环、不饱和杂环,所述链为1-20个原子组成的链,所述仅由碳原子构成的链和含有至少一个杂原子的链均包括饱和链和含有不饱和键的不饱和链,所述不饱和键包括双键和/或三键;
所述第二环为三元环-十元环,所述第二环选自环烯、环醚、环缩醛、环酯、环酸酐、环碳酸酯、环酰胺、环胺、环硫醚、环二硫、环硅氧烷、环磷氮烯中的任意一种;
所述环状取代基包括取代或未取代的三元环-二十元环、同时含有两个或两个以上环结构的多环取代基;
所述链状取代基包括取代或未取代的烷基、杂烷基、烯基、杂烯基、炔基、烯炔基、烷硫基、含C=O取代基、=O、=S。
3.根据权利要求2所述的可聚合电解质,其特征在于,
在R2选自环烯的情况下,R2为含有取代基或不含有取代基的四元环、五元环、七元环、八元环、九元环或十元环;
在R2选自环醚的情况下,R2为含有取代基或不含有取代基的三元环、四元环、五元环或七元环;
在R2选自环缩醛的情况下,R2为含有取代基或不含有取代基的六元环或八元环;
在R2选自环酯的情况下,R2为含有取代基或不含有取代基的四元环、六元环、七元环或八元环;
在R2选自环酸酐的情况下,R2为含有取代基或不含有取代基的五元环、七元环或八元环;
在R2选自环碳酸酯的情况下,R2为含有取代基或不含有取代基的六元-八元环;
在R2选自环酰胺的情况下,R2为含有取代基或不含有取代基的四元-八元环;
在R2选自环胺的情况下,R2为含有取代基或不含有取代基的三元环、四元环或七元环;
在R2选自环硫醚的情况下,R2为含有取代基或不含有取代基的三元环或四元环;
在R2选自环二硫的情况下,R2为含有取代基或不含有取代基的四元-八元环;
在R2选自环硅氧烷的情况下,R2为含有取代基或不含有取代基的六元环、八元环或十元环;
在R2选自环磷氮烯的情况下,R2为含有取代基或不含有取代基的六元环。
4.根据权利要求3所述的可聚合电解质,其特征在于,
在R2选自环烯的情况下,通式Ⅰ的结构包括:
在R2选自环醚的情况下,通式Ⅰ的结构包括:
在R2选自环缩醛的情况下,通式Ⅰ的结构包括:
在R2选自环酯的情况下,通式Ⅰ的结构包括:
在R2选自环酸酐的情况下,通式Ⅰ的结构包括:
在R2选自环碳酸酯的情况下,通式Ⅰ的结构包括:
在R2选自环酰胺的情况下,通式Ⅰ的结构包括:
在R2选自环胺的情况下,通式Ⅰ的结构包括:
在R2选自环硫醚的情况下,通式Ⅰ的结构包括:
在R2选自环二硫的情况下,通式Ⅰ的结构包括:
在R2选自环硅氧烷的情况下,通式Ⅰ的结构包括:
在R2选自环磷氮烯的情况下,通式Ⅰ的结构包括:
R3、R4、R5、R6、R7、R8、R9、R10均选自氢原子、含有取代基或不含有取代基的环或链、卤素原子、金属阳离子中的任意一种或几种的组合。
5.根据权利要求4所述的可聚合电解质,其特征在于,
所述链状取代基包括氢原子、卤素原子、醚氧键/基、醚硫键/基、硝基、酰胺、磺酰胺基、磺基、磺酸基、盐类取代基、含C=O取代基、含N取代基、烷基、杂烷基、烯基、杂烯基、炔基、烯炔基、=O、=S;
所述环状取代基包括三元环、四元环、五元环、六元环、七元环、八元环和同时含有两个或两个以上环结构的多环取代基;
所述卤素原子包括氯原子、溴原子、碘原子、氟原子。
7.根据权利要求1-6任意一项所述的可聚合电解质,其特征在于,任意一种通式Ⅰ中所有碳原子上的全部或部分氢原子独立地被卤素原子取代;
优选地,任意一种通式Ⅰ中所有碳原子上的全部或部分氢原子独立地被氟原子取代。
9.一种根据权利要求1-7中任意一项所述的可聚合电解质在二次电池中的应用,其特征在于,所述应用为:所述三氟化硼盐既能够作为电解质的添加剂应用,也能够作为盐应用,含有可聚合基团的单体聚合之后还能够作为单离子导体兼高分子框架应用。
10.根据权利要求9所述的应用,其特征在于,所述应用包括在液态电解质、凝胶电解质、混合固液电解质、准固态电解质、全固态电解质中的应用,所述液态电解质、凝胶电解质、混合固液电解质、准固态电解质、全固态电解质均独立地包括权利要求1-7中任意一项所述的电解质;
优选地,所述应用还包括作为电池或电池组的应用,所述电池包括权利要求1-7中任意一项所述的电解质以及正极、负极和封装外壳;所述液态电解质、凝胶电解质、混合固液电解质、准固态电解质、全固态电解质可应用于液态电池、混合固液电池、半固态电池、凝胶电池、准固态电池和全固态电池,所述电池组包括所述电池。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN202011491494.XA CN114649570A (zh) | 2020-12-17 | 2020-12-17 | 一种可聚合电解质及其制备方法和应用 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN202011491494.XA CN114649570A (zh) | 2020-12-17 | 2020-12-17 | 一种可聚合电解质及其制备方法和应用 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN114649570A true CN114649570A (zh) | 2022-06-21 |
Family
ID=81990731
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202011491494.XA Pending CN114649570A (zh) | 2020-12-17 | 2020-12-17 | 一种可聚合电解质及其制备方法和应用 |
Country Status (1)
| Country | Link |
|---|---|
| CN (1) | CN114649570A (zh) |
Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4596644A (en) * | 1984-07-14 | 1986-06-24 | Ciba-Geigy Corporation | Method of polymerization |
| US20030108800A1 (en) * | 2001-11-09 | 2003-06-12 | Barbarich Thomas J. | Non-aqueous electrolytes for lithium electrochemical cells |
| JP2005285332A (ja) * | 2004-03-01 | 2005-10-13 | Nippon Soda Co Ltd | 高分子固体電解質電池 |
| WO2015185660A1 (de) * | 2014-06-06 | 2015-12-10 | Westfälische Wilhelms-Universität Münster | Trifluorborat-substituierte lithium pyrazole und deren verwendung als leitsalz für lithium-basierte energiespeicher |
| CN105489934A (zh) * | 2016-01-11 | 2016-04-13 | 东莞新能源科技有限公司 | 电解液以及包括该电解液的锂离子电池 |
| CN106946925A (zh) * | 2017-03-31 | 2017-07-14 | 中国科学院青岛生物能源与过程研究所 | 氟代烷氧基三氟硼酸锂盐及其制备方法和应用 |
| CN108258307A (zh) * | 2016-12-29 | 2018-07-06 | 罗伯特·博世有限公司 | 用于锂-电池和/或锂-电池组的具有改善的接触性的保护层 |
| WO2019180945A1 (ja) * | 2018-03-23 | 2019-09-26 | 富山薬品工業株式会社 | 蓄電デバイス用電解質及び非水電解液 |
| CN212380457U (zh) * | 2020-06-16 | 2021-01-19 | 比亚迪股份有限公司 | 电池系统和车辆 |
-
2020
- 2020-12-17 CN CN202011491494.XA patent/CN114649570A/zh active Pending
Patent Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4596644A (en) * | 1984-07-14 | 1986-06-24 | Ciba-Geigy Corporation | Method of polymerization |
| US20030108800A1 (en) * | 2001-11-09 | 2003-06-12 | Barbarich Thomas J. | Non-aqueous electrolytes for lithium electrochemical cells |
| JP2005285332A (ja) * | 2004-03-01 | 2005-10-13 | Nippon Soda Co Ltd | 高分子固体電解質電池 |
| WO2015185660A1 (de) * | 2014-06-06 | 2015-12-10 | Westfälische Wilhelms-Universität Münster | Trifluorborat-substituierte lithium pyrazole und deren verwendung als leitsalz für lithium-basierte energiespeicher |
| CN105489934A (zh) * | 2016-01-11 | 2016-04-13 | 东莞新能源科技有限公司 | 电解液以及包括该电解液的锂离子电池 |
| CN108258307A (zh) * | 2016-12-29 | 2018-07-06 | 罗伯特·博世有限公司 | 用于锂-电池和/或锂-电池组的具有改善的接触性的保护层 |
| CN106946925A (zh) * | 2017-03-31 | 2017-07-14 | 中国科学院青岛生物能源与过程研究所 | 氟代烷氧基三氟硼酸锂盐及其制备方法和应用 |
| WO2019180945A1 (ja) * | 2018-03-23 | 2019-09-26 | 富山薬品工業株式会社 | 蓄電デバイス用電解質及び非水電解液 |
| CN212380457U (zh) * | 2020-06-16 | 2021-01-19 | 比亚迪股份有限公司 | 电池系统和车辆 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP3972030B1 (en) | Electrolyte, lithium-ion battery comprising said electrolyte, battery module, battery pack and device | |
| CN113571771B (zh) | 锂离子电池用电解液及其制备方法和锂离子电池 | |
| EP4265622A1 (en) | Electrolyte containing nitrogen-based salt structure, preparation method therefor and use thereof | |
| KR20230137437A (ko) | 이미다졸 구조 그룹의 이소시아네이트계 전해액 첨가제 및 이의 응용 | |
| CN114507257A (zh) | 一种氟代环状含磷分子及其应用 | |
| CN112786964A (zh) | 一种高电压高能量密度电解液及其锂电池 | |
| CN112366354B (zh) | 一种电解液及锂离子电池 | |
| CN114695960A (zh) | 一种兼具高低温性能的新型添加剂、其制备方法及应用 | |
| CN114566712B (zh) | 含有二氟磷酸锂的高电压锂离子电池电解液及其制备方法和锂离子电池 | |
| CN113889667B (zh) | 一种适配可快充钴酸锂电池的高电压电解液及其应用 | |
| CN114649581B (zh) | 含有五元环状氮基盐结构的电解质及其制备方法和应用 | |
| CN114649570A (zh) | 一种可聚合电解质及其制备方法和应用 | |
| CN114649582A (zh) | 含有六元环状氮基盐结构的电解质及其制备方法和应用 | |
| CN114649579A (zh) | 一种不饱和碳链类硫基电解质及其制备方法和应用 | |
| CN114605447A (zh) | 一种含有不饱和碳链结构的电解质及其制备方法和应用 | |
| CN118645698B (zh) | 一种基于1,3,5,7-四氧环辛烷及其衍生物的复合溶剂、电解液及锂金属电池 | |
| CN114605448A (zh) | 一种含有不饱和杂链结构的电解质及其制备方法和应用 | |
| CN114243107A (zh) | 一种不饱和碳链类电解质及其制备和应用 | |
| CN114649580A (zh) | 一种硫基类不饱和杂链三氟化硼盐电解质及其制备方法和应用 | |
| CN114621263A (zh) | 一种含有不饱和碳环结构的电解质及其制备方法和应用 | |
| CN114621266A (zh) | 一种含有饱和杂链结构的电解质及其制备方法和应用 | |
| CN114621264A (zh) | 一种含有饱和碳链结构的电解质及其制备方法和应用 | |
| CN114230592A (zh) | 一种饱和碳链类电解质及其制备和应用 | |
| CN114230593A (zh) | 一种不饱和杂链类电解质及其制备和应用 | |
| CN114573613A (zh) | 一种饱和碳链类的三元电解质及其制备和应用 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| CB02 | Change of applicant information |
Country or region after: China Address after: 108, 1st Floor, Building 4, No. 91 Pu'an Road, Doudian, Fangshan District, Beijing 102402 Applicant after: Beijing Weilan New Energy Technology Co.,Ltd. Address before: No.1 Qihang West Street, Doudian Town, Fangshan District, Beijing Applicant before: BEIJING WELION NEW ENERGY TECHNOLOGY Co.,Ltd. Country or region before: China |
|
| CB02 | Change of applicant information |