CN114642686B - 一种复合益生菌及其延缓衰老和抗氧化的作用 - Google Patents
一种复合益生菌及其延缓衰老和抗氧化的作用 Download PDFInfo
- Publication number
- CN114642686B CN114642686B CN202210475556.0A CN202210475556A CN114642686B CN 114642686 B CN114642686 B CN 114642686B CN 202210475556 A CN202210475556 A CN 202210475556A CN 114642686 B CN114642686 B CN 114642686B
- Authority
- CN
- China
- Prior art keywords
- parts
- lactobacillus
- powder
- bacillus coagulans
- lactobacillus fermentum
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 239000006041 probiotic Substances 0.000 title claims abstract description 33
- 235000018291 probiotics Nutrition 0.000 title claims abstract description 33
- 239000002131 composite material Substances 0.000 title claims abstract description 26
- 230000003647 oxidation Effects 0.000 title claims abstract description 18
- 238000007254 oxidation reaction Methods 0.000 title claims abstract description 18
- 230000006870 function Effects 0.000 title claims abstract description 11
- 241000186840 Lactobacillus fermentum Species 0.000 claims abstract description 43
- 229940012969 lactobacillus fermentum Drugs 0.000 claims abstract description 43
- 241000186606 Lactobacillus gasseri Species 0.000 claims abstract description 32
- 241000193749 Bacillus coagulans Species 0.000 claims abstract description 31
- 229940054340 bacillus coagulans Drugs 0.000 claims abstract description 30
- 238000000855 fermentation Methods 0.000 claims abstract description 29
- 230000004151 fermentation Effects 0.000 claims abstract description 27
- 230000000813 microbial effect Effects 0.000 claims abstract description 21
- 238000004321 preservation Methods 0.000 claims abstract description 15
- 230000000529 probiotic effect Effects 0.000 claims abstract description 12
- 101001076687 Lactobacillus gasseri Inulosucrase Proteins 0.000 claims abstract description 5
- 239000000843 powder Substances 0.000 claims description 35
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 claims description 22
- 239000003795 chemical substances by application Substances 0.000 claims description 16
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 15
- 238000002156 mixing Methods 0.000 claims description 13
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 claims description 11
- 229940041514 candida albicans extract Drugs 0.000 claims description 11
- ZPWVASYFFYYZEW-UHFFFAOYSA-L dipotassium hydrogen phosphate Chemical compound [K+].[K+].OP([O-])([O-])=O ZPWVASYFFYYZEW-UHFFFAOYSA-L 0.000 claims description 11
- 239000008103 glucose Substances 0.000 claims description 11
- 229910052943 magnesium sulfate Inorganic materials 0.000 claims description 11
- 235000019341 magnesium sulphate Nutrition 0.000 claims description 11
- 229940099596 manganese sulfate Drugs 0.000 claims description 11
- 239000011702 manganese sulphate Substances 0.000 claims description 11
- 235000007079 manganese sulphate Nutrition 0.000 claims description 11
- SQQMAOCOWKFBNP-UHFFFAOYSA-L manganese(II) sulfate Chemical compound [Mn+2].[O-]S([O-])(=O)=O SQQMAOCOWKFBNP-UHFFFAOYSA-L 0.000 claims description 11
- 239000012138 yeast extract Substances 0.000 claims description 11
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical compound [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 claims description 8
- 239000012153 distilled water Substances 0.000 claims description 8
- 239000001888 Peptone Substances 0.000 claims description 7
- 108010080698 Peptones Proteins 0.000 claims description 7
- VMHLLURERBWHNL-UHFFFAOYSA-M Sodium acetate Chemical compound [Na+].CC([O-])=O VMHLLURERBWHNL-UHFFFAOYSA-M 0.000 claims description 7
- 239000003963 antioxidant agent Substances 0.000 claims description 7
- 230000003078 antioxidant effect Effects 0.000 claims description 7
- 235000006708 antioxidants Nutrition 0.000 claims description 7
- -1 diamine citrate Chemical class 0.000 claims description 7
- 235000019319 peptone Nutrition 0.000 claims description 7
- 239000001632 sodium acetate Substances 0.000 claims description 7
- 235000017281 sodium acetate Nutrition 0.000 claims description 7
- UQZIYBXSHAGNOE-USOSMYMVSA-N Stachyose Natural products O(C[C@H]1[C@@H](O)[C@H](O)[C@H](O)[C@@H](O[C@@]2(CO)[C@H](O)[C@@H](O)[C@@H](CO)O2)O1)[C@@H]1[C@H](O)[C@@H](O)[C@@H](O)[C@H](CO[C@@H]2[C@@H](O)[C@@H](O)[C@@H](O)[C@H](CO)O2)O1 UQZIYBXSHAGNOE-USOSMYMVSA-N 0.000 claims description 6
- 229910000396 dipotassium phosphate Inorganic materials 0.000 claims description 6
- 235000019797 dipotassium phosphate Nutrition 0.000 claims description 6
- LWIHDJKSTIGBAC-UHFFFAOYSA-K potassium phosphate Substances [K+].[K+].[K+].[O-]P([O-])([O-])=O LWIHDJKSTIGBAC-UHFFFAOYSA-K 0.000 claims description 6
- UQZIYBXSHAGNOE-XNSRJBNMSA-N stachyose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO[C@@H]2[C@@H]([C@@H](O)[C@@H](O)[C@@H](CO[C@@H]3[C@@H]([C@@H](O)[C@@H](O)[C@@H](CO)O3)O)O2)O)O1 UQZIYBXSHAGNOE-XNSRJBNMSA-N 0.000 claims description 6
- 238000002360 preparation method Methods 0.000 claims description 5
- 235000015278 beef Nutrition 0.000 claims description 4
- 229910000019 calcium carbonate Inorganic materials 0.000 claims description 4
- 239000000284 extract Substances 0.000 claims description 4
- 239000012137 tryptone Substances 0.000 claims description 4
- 241001052560 Thallis Species 0.000 claims description 3
- 230000003712 anti-aging effect Effects 0.000 claims description 3
- 238000001035 drying Methods 0.000 claims description 3
- 238000007710 freezing Methods 0.000 claims description 3
- 230000008014 freezing Effects 0.000 claims description 3
- 235000013305 food Nutrition 0.000 claims description 2
- 239000002417 nutraceutical Substances 0.000 claims description 2
- 235000021436 nutraceutical agent Nutrition 0.000 claims description 2
- 239000002054 inoculum Substances 0.000 claims 2
- 241000894006 Bacteria Species 0.000 abstract description 18
- 238000013329 compounding Methods 0.000 abstract description 10
- 230000009758 senescence Effects 0.000 abstract description 4
- 239000000243 solution Substances 0.000 description 16
- 238000012360 testing method Methods 0.000 description 15
- 230000000694 effects Effects 0.000 description 12
- 239000007788 liquid Substances 0.000 description 11
- 239000002609 medium Substances 0.000 description 11
- 239000000523 sample Substances 0.000 description 10
- HHEAADYXPMHMCT-UHFFFAOYSA-N dpph Chemical compound [O-][N+](=O)C1=CC([N+](=O)[O-])=CC([N+]([O-])=O)=C1[N]N(C=1C=CC=CC=1)C1=CC=CC=C1 HHEAADYXPMHMCT-UHFFFAOYSA-N 0.000 description 9
- 239000001963 growth medium Substances 0.000 description 9
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 8
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 7
- 241000186660 Lactobacillus Species 0.000 description 7
- 230000001580 bacterial effect Effects 0.000 description 7
- 230000000968 intestinal effect Effects 0.000 description 7
- 229940039696 lactobacillus Drugs 0.000 description 7
- XUJNEKJLAYXESH-REOHCLBHSA-N L-Cysteine Chemical compound SC[C@H](N)C(O)=O XUJNEKJLAYXESH-REOHCLBHSA-N 0.000 description 6
- 238000000034 method Methods 0.000 description 6
- WQGWDDDVZFFDIG-UHFFFAOYSA-N pyrogallol Chemical compound OC1=CC=CC(O)=C1O WQGWDDDVZFFDIG-UHFFFAOYSA-N 0.000 description 6
- 230000032683 aging Effects 0.000 description 5
- 201000010099 disease Diseases 0.000 description 5
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 5
- 239000000047 product Substances 0.000 description 5
- 102000019197 Superoxide Dismutase Human genes 0.000 description 4
- 108010012715 Superoxide dismutase Proteins 0.000 description 4
- 238000002835 absorbance Methods 0.000 description 4
- 230000004913 activation Effects 0.000 description 4
- 210000004027 cell Anatomy 0.000 description 4
- 150000001875 compounds Chemical class 0.000 description 4
- 238000010790 dilution Methods 0.000 description 4
- 239000012895 dilution Substances 0.000 description 4
- 210000001035 gastrointestinal tract Anatomy 0.000 description 4
- 239000004310 lactic acid Substances 0.000 description 4
- 235000014655 lactic acid Nutrition 0.000 description 4
- 238000009630 liquid culture Methods 0.000 description 4
- 239000000463 material Substances 0.000 description 4
- 239000004201 L-cysteine Substances 0.000 description 3
- 235000013878 L-cysteine Nutrition 0.000 description 3
- 230000003213 activating effect Effects 0.000 description 3
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 3
- 210000004369 blood Anatomy 0.000 description 3
- 239000008280 blood Substances 0.000 description 3
- 230000036541 health Effects 0.000 description 3
- 210000004251 human milk Anatomy 0.000 description 3
- 235000020256 human milk Nutrition 0.000 description 3
- 238000001727 in vivo Methods 0.000 description 3
- 238000011081 inoculation Methods 0.000 description 3
- 239000001301 oxygen Substances 0.000 description 3
- 229910052760 oxygen Inorganic materials 0.000 description 3
- 229940079877 pyrogallol Drugs 0.000 description 3
- 238000011160 research Methods 0.000 description 3
- 210000002966 serum Anatomy 0.000 description 3
- 239000007787 solid Substances 0.000 description 3
- WQZGKKKJIJFFOK-SVZMEOIVSA-N (+)-Galactose Chemical compound OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@H]1O WQZGKKKJIJFFOK-SVZMEOIVSA-N 0.000 description 2
- 108020004465 16S ribosomal RNA Proteins 0.000 description 2
- 241000193830 Bacillus <bacterium> Species 0.000 description 2
- 108020004414 DNA Proteins 0.000 description 2
- 238000007400 DNA extraction Methods 0.000 description 2
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 2
- MHAJPDPJQMAIIY-UHFFFAOYSA-N Hydrogen peroxide Chemical compound OO MHAJPDPJQMAIIY-UHFFFAOYSA-N 0.000 description 2
- 210000000683 abdominal cavity Anatomy 0.000 description 2
- 230000003064 anti-oxidating effect Effects 0.000 description 2
- 210000000170 cell membrane Anatomy 0.000 description 2
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Natural products OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 230000018109 developmental process Effects 0.000 description 2
- 238000009472 formulation Methods 0.000 description 2
- 230000012010 growth Effects 0.000 description 2
- 230000003859 lipid peroxidation Effects 0.000 description 2
- 238000009629 microbiological culture Methods 0.000 description 2
- 239000000203 mixture Substances 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 238000005502 peroxidation Methods 0.000 description 2
- 238000000746 purification Methods 0.000 description 2
- 230000001105 regulatory effect Effects 0.000 description 2
- 238000012216 screening Methods 0.000 description 2
- 239000006228 supernatant Substances 0.000 description 2
- QKNYBSVHEMOAJP-UHFFFAOYSA-N 2-amino-2-(hydroxymethyl)propane-1,3-diol;hydron;chloride Chemical compound Cl.OCC(N)(CO)CO QKNYBSVHEMOAJP-UHFFFAOYSA-N 0.000 description 1
- 229920001817 Agar Polymers 0.000 description 1
- 244000153158 Ammi visnaga Species 0.000 description 1
- 235000010585 Ammi visnaga Nutrition 0.000 description 1
- 208000023275 Autoimmune disease Diseases 0.000 description 1
- 108020000946 Bacterial DNA Proteins 0.000 description 1
- 241000194032 Enterococcus faecalis Species 0.000 description 1
- 102000006587 Glutathione peroxidase Human genes 0.000 description 1
- 108700016172 Glutathione peroxidases Proteins 0.000 description 1
- 241000581650 Ivesia Species 0.000 description 1
- 208000008589 Obesity Diseases 0.000 description 1
- 241000589517 Pseudomonas aeruginosa Species 0.000 description 1
- 241000607142 Salmonella Species 0.000 description 1
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical class [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 1
- DGEZNRSVGBDHLK-UHFFFAOYSA-N [1,10]phenanthroline Chemical compound C1=CN=C2C3=NC=CC=C3C=CC2=C1 DGEZNRSVGBDHLK-UHFFFAOYSA-N 0.000 description 1
- 239000008272 agar Substances 0.000 description 1
- 208000026935 allergic disease Diseases 0.000 description 1
- 230000003321 amplification Effects 0.000 description 1
- 244000052616 bacterial pathogen Species 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 239000007853 buffer solution Substances 0.000 description 1
- 210000005252 bulbus oculi Anatomy 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 230000001276 controlling effect Effects 0.000 description 1
- 238000012258 culturing Methods 0.000 description 1
- 238000007865 diluting Methods 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- 239000012154 double-distilled water Substances 0.000 description 1
- 239000003814 drug Substances 0.000 description 1
- 230000037149 energy metabolism Effects 0.000 description 1
- 229940032049 enterococcus faecalis Drugs 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 230000002496 gastric effect Effects 0.000 description 1
- 238000003304 gavage Methods 0.000 description 1
- 235000011187 glycerol Nutrition 0.000 description 1
- 208000019622 heart disease Diseases 0.000 description 1
- TUJKJAMUKRIRHC-UHFFFAOYSA-N hydroxyl Chemical compound [OH] TUJKJAMUKRIRHC-UHFFFAOYSA-N 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 230000002401 inhibitory effect Effects 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 238000001746 injection moulding Methods 0.000 description 1
- 230000007413 intestinal health Effects 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 238000002372 labelling Methods 0.000 description 1
- 230000031700 light absorption Effects 0.000 description 1
- 230000004060 metabolic process Effects 0.000 description 1
- 239000002207 metabolite Substances 0.000 description 1
- 239000011259 mixed solution Substances 0.000 description 1
- DDHVILIIHBIMQU-YJGQQKNPSA-L mupirocin calcium hydrate Chemical class O.O.[Ca+2].C[C@H](O)[C@H](C)[C@@H]1O[C@H]1C[C@@H]1[C@@H](O)[C@@H](O)[C@H](C\C(C)=C\C(=O)OCCCCCCCCC([O-])=O)OC1.C[C@H](O)[C@H](C)[C@@H]1O[C@H]1C[C@@H]1[C@@H](O)[C@@H](O)[C@H](C\C(C)=C\C(=O)OCCCCCCCCC([O-])=O)OC1 DDHVILIIHBIMQU-YJGQQKNPSA-L 0.000 description 1
- 238000003199 nucleic acid amplification method Methods 0.000 description 1
- 235000015097 nutrients Nutrition 0.000 description 1
- 235000016709 nutrition Nutrition 0.000 description 1
- 230000035764 nutrition Effects 0.000 description 1
- 235000020824 obesity Nutrition 0.000 description 1
- 238000005457 optimization Methods 0.000 description 1
- 238000005192 partition Methods 0.000 description 1
- 230000035790 physiological processes and functions Effects 0.000 description 1
- 239000002504 physiological saline solution Substances 0.000 description 1
- 238000007747 plating Methods 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 108090000623 proteins and genes Proteins 0.000 description 1
- 102000004169 proteins and genes Human genes 0.000 description 1
- 239000012488 sample solution Substances 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 238000012163 sequencing technique Methods 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 230000035882 stress Effects 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 230000008961 swelling Effects 0.000 description 1
- 238000012353 t test Methods 0.000 description 1
- 238000010998 test method Methods 0.000 description 1
- YNJBWRMUSHSURL-UHFFFAOYSA-N trichloroacetic acid Chemical compound OC(=O)C(Cl)(Cl)Cl YNJBWRMUSHSURL-UHFFFAOYSA-N 0.000 description 1
- 238000012795 verification Methods 0.000 description 1
- 238000005303 weighing Methods 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/66—Microorganisms or materials therefrom
- A61K35/74—Bacteria
- A61K35/741—Probiotics
- A61K35/744—Lactic acid bacteria, e.g. enterococci, pediococci, lactococci, streptococci or leuconostocs
- A61K35/747—Lactobacilli, e.g. L. acidophilus or L. brevis
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L33/00—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof
- A23L33/10—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof using additives
- A23L33/135—Bacteria or derivatives thereof, e.g. probiotics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/66—Microorganisms or materials therefrom
- A61K35/74—Bacteria
- A61K35/741—Probiotics
- A61K35/742—Spore-forming bacteria, e.g. Bacillus coagulans, Bacillus subtilis, clostridium or Lactobacillus sporogenes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P39/00—General protective or antinoxious agents
- A61P39/06—Free radical scavengers or antioxidants
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N1/00—Microorganisms, e.g. protozoa; Compositions thereof; Processes of propagating, maintaining or preserving microorganisms or compositions thereof; Processes of preparing or isolating a composition containing a microorganism; Culture media therefor
- C12N1/20—Bacteria; Culture media therefor
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23V—INDEXING SCHEME RELATING TO FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES AND LACTIC OR PROPIONIC ACID BACTERIA USED IN FOODSTUFFS OR FOOD PREPARATION
- A23V2002/00—Food compositions, function of food ingredients or processes for food or foodstuffs
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23V—INDEXING SCHEME RELATING TO FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES AND LACTIC OR PROPIONIC ACID BACTERIA USED IN FOODSTUFFS OR FOOD PREPARATION
- A23V2400/00—Lactic or propionic acid bacteria
- A23V2400/11—Lactobacillus
- A23V2400/143—Fermentum
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23V—INDEXING SCHEME RELATING TO FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES AND LACTIC OR PROPIONIC ACID BACTERIA USED IN FOODSTUFFS OR FOOD PREPARATION
- A23V2400/00—Lactic or propionic acid bacteria
- A23V2400/11—Lactobacillus
- A23V2400/145—Gasseri
Landscapes
- Life Sciences & Earth Sciences (AREA)
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Mycology (AREA)
- Microbiology (AREA)
- Engineering & Computer Science (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Zoology (AREA)
- Pharmacology & Pharmacy (AREA)
- Organic Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Biotechnology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Wood Science & Technology (AREA)
- Genetics & Genomics (AREA)
- Biochemistry (AREA)
- Molecular Biology (AREA)
- Epidemiology (AREA)
- Nutrition Science (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Toxicology (AREA)
- Tropical Medicine & Parasitology (AREA)
- Virology (AREA)
- General Chemical & Material Sciences (AREA)
- Biomedical Technology (AREA)
- Polymers & Plastics (AREA)
- Food Science & Technology (AREA)
- General Engineering & Computer Science (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Abstract
本发明公开了一种复合益生菌及其延缓衰老和抗氧化的作用,属于微生物发酵技术领域。本发明公开了一种具有延缓衰老和抗氧化功能的复合益生菌,所述复合益生菌包括发酵乳杆菌、凝结芽孢杆菌和格氏乳杆菌;所述发酵乳杆菌的保藏编号为CGMCC NO.14493;所述凝结芽孢杆菌保藏编号为CCTCC NO:M2017813;所述格氏乳杆菌保藏编号为CGMCC No.23187。本发明通过三种菌的复配可以实现清除自由基达到抗氧化和延缓衰老的目的,这对于制备抗氧化和延缓衰老的产品提供了新的菌株和科学指导。
Description
技术领域
本发明涉及微生物发酵技术领域,特别是涉及一种复合益生菌及其延缓衰老和抗氧化的作用。
背景技术
人体健康是追求物质、精神和文化的基础,而肠道菌群影响着人体的生长发育、营养与健康,甚至与疾病密切相关,菌群失衡可能引发肥胖、自身免疫性疾病、过敏性疾病、心脏病等,可见,肠道菌群与人体健康乃至生命长短紧密相关。
目前,用于调控肠道菌群的菌种具有多种,而乳酸菌是最常见的一种,乳酸菌可以通过平衡肠道内菌群,促使肠道健康,减少疾病的发生,而相反,肠道菌群紊乱不仅会增加疾病的发生,还能引起体内物质和能量代谢的失衡,从而使得机体代谢过程中,会因各种内因和外因而产生的各种活性氧和自由基,过多的自由基会损伤人的机体,不断的攻击细胞膜等细胞组织,造成脂质过氧化反应,而脂质过氧化产物又再分解成更多自由基,进而引起自由基的连锁反应。由于细胞膜遭到破坏,引起细胞结构、遗传物质等损伤,让细胞失去正常的生理功能,进而导致疾病的产生。另外,相关研究表明多种自由基和人体衰老直接相关,所以,保证肠道菌群免受破坏,保证体内自由基的正常运行状态,才能更好的防止疾病的发生,细胞的衰老以及避免过氧化。而目前,用于调节肠道菌群或者抗氧化的菌种多都是单一的乳酸菌菌种,但是由于单一菌种功能单一,对于肠道一个复杂的体内环境而言,并不能保证能够最高限度的发挥菌种优势,而目前没有多种菌种复配方式应用到延缓衰老和抗氧化中。
发明内容
本发明的目的是提供一种复合益生菌及其延缓衰老和抗氧化的作用,以解决上述现有技术存在的问题,通过三种菌种的复配可以实现清除自由基达到抗氧化和延缓衰老的目的,这对于制备抗氧化和延缓衰老的产品提供了新的菌株和科学指导。
为实现上述目的,本发明提供了如下方案:
本发明提供一种具有延缓衰老和抗氧化功能的复合益生菌,所述复合益生菌包括发酵乳杆菌(Lactobacillus fermentum)、凝结芽孢杆菌(Bacillus coagulans)和格氏乳杆菌(Lactobacillus gasseri);
所述发酵乳杆菌的保藏编号为CGMCC NO.14493,保藏时间:2017年8月4日,保藏单位:中国微生物菌种保藏管理委员会普通微生物中心,保藏地址:北京市朝阳区北辰西路1号院3号;所述凝结芽孢杆菌保藏编号为CCTCC NO:M2017813,保藏时间:2017年12月21日,保藏单位:中国典型培养物保藏中心,保藏地址:中国武汉大学;所述格氏乳杆菌保藏编号为CGMCC No.23187,保藏时间2021年08月24日,保藏单位:中国微生物菌种保藏管理委员会普通微生物中心,保藏地址:北京市朝阳区北辰西路1号院3号。
本发明还提供一种微生物菌剂,包括所述的复合益生菌。
优选的是,所述发酵乳杆菌、凝结芽孢杆菌和格氏乳杆菌分别接种发酵培养基后,获取发酵液;然后将所得发酵液离心,收集菌体,冷冻、干燥,分别得到发酵乳杆菌菌粉、凝结芽孢杆菌菌粉和格氏乳杆菌菌粉。
优选的是,所述微生物菌剂还包括水苏糖,将所述发酵乳杆菌菌粉、凝结芽孢杆菌菌粉、格氏乳杆菌菌粉和所述水苏糖按照质量比(0.5-2):(0.5-2):(0.5-2):(1-5)混合制备得到所述微生物菌剂。
优选的是,所述发酵乳杆菌的发酵培养基包括以下重量份的组分:蛋白胨10份、牛肉浸膏5份、酵母浸粉3份、葡萄糖20份、醋酸钠5份、柠檬酸二胺2份、磷酸氢二钾0.2份、硫酸镁0.35份、硫酸锰0.01份、碳酸钙5份和水1000份;
所述凝结芽孢杆菌的发酵培养基包括以下重量份组分:胰蛋白胨5份、酵母浸粉15份、葡萄糖5份、磷酸氢二钾3份、硫酸镁0.3份、硫酸锰0.01份和蒸馏水1000份;
所述格氏乳杆菌的发酵培养基包括以下重量份组分:蛋白胨10份、酵母浸粉8份、葡萄糖20份、磷酸氢二钾3份、硫酸镁0.2份、醋酸钠3份、硫酸锰0.01份和水1000份。
本发明还提供一种所述的复合益生菌或其代谢物,或所述的微生物菌剂在制备具有延缓衰老和抗氧化功能的产品中的应用。
优选的是,所述产品包括药物、食品或保健食品。
本发明公开了以下技术效果:
本发明公开的复合益生菌中包含发酵乳杆菌、凝结芽孢杆菌和格氏乳杆菌组合而成,发明人在前期的研究中发现发酵乳杆菌具有抗氧化能力,但是单一菌株的抗氧化能力有限,然后将其与其他菌株进行复配,新发现的格氏乳杆菌自身的抗氧化能力几乎没有,但是经过不断的调整优化试验条件,发现在发酵乳杆菌中添加格氏乳杆菌进行复配后,能提高抗氧化能力,而凝结芽孢杆菌自身芽孢萌发速度快,在肠道内快速生长为营养体,定植性较强,有助于营造肠道内乳酸菌繁殖做需要的厌氧环境,并且抑制多种致病菌比如粪肠球菌、沙门氏菌、绿脓杆菌等效果显著,所以,考虑到复配之后要用于肠道菌群平衡中,于是经过筛选和优化将凝结芽孢杆菌和另外两种菌进行复配,并且进行不断的优化后,发现发酵乳杆菌菌粉、凝结芽孢杆菌菌粉和格氏乳杆菌菌粉的质量比为2:0.5:0.5,所制备的微生物菌剂含菌量最高,并且显著增强发酵乳杆菌的抗氧化能力,延缓衰老。可见,本发明将两种本身不具有抗氧化能力的菌株和发酵乳杆菌复配后,经过不断的条件优化,显著提高了发酵乳杆菌的抗氧化能力,这对于将该复合益生菌应用到延缓衰老和抗氧化的产品中具有重要意义,提供科学依据。
具体实施方式
现详细说明本发明的多种示例性实施方式,该详细说明不应认为是对本发明的限制,而应理解为是对本发明的某些方面、特性和实施方案的更详细的描述。
应理解本发明中所述的术语仅仅是为描述特别的实施方式,并非用于限制本发明。另外,对于本发明中的数值范围,应理解为还具体公开了该范围的上限和下限之间的每个中间值。在任何陈述值或陈述范围内的中间值以及任何其他陈述值或在所述范围内的中间值之间的每个较小的范围也包括在本发明内。这些较小范围的上限和下限可独立地包括或排除在范围内。
除非另有说明,否则本文使用的所有技术和科学术语具有本发明所述领域的常规技术人员通常理解的相同含义。虽然本发明仅描述了优选的方法和材料,但是在本发明的实施或测试中也可以使用与本文所述相似或等同的任何方法和材料。本说明书中提到的所有文献通过引用并入,用以公开和描述与所述文献相关的方法和/或材料。在与任何并入的文献冲突时,以本说明书的内容为准。
在不背离本发明的范围或精神的情况下,可对本发明说明书的具体实施方式做多种改进和变化,这对本领域技术人员而言是显而易见的。由本发明的说明书得到的其他实施方式对技术人员而言是显而易见的。本申请说明书和实施例仅是示例性的。
关于本文中所使用的“包含”、“包括”、“具有”、“含有”等等,均为开放性的用语,即意指包含但不限于。
本发明以下实施例所用的发酵乳杆菌、凝结芽孢杆菌和格氏乳杆菌均保藏于善恩康生物科技(苏州)有限公司。
实施例1格氏乳杆菌的分离与鉴定
1、样品来源
江苏省昆山市中医院母乳样本,无菌取样运送至善恩康生物科技有限公司实验室。
2、母乳中乳酸菌的筛选
2.1分离纯化
富集培养:取3-5ml母乳样品于50ml已灭菌的MRS液体培养基(1LMRS液体培养基+0.5%L-半胱氨酸)/TPY液体培养基中,将其置于37℃无氧条件下培养24-48h,进行稀释后涂板。
2.2培养方案
2.2.1.稀释液
改良的生理盐水稀释液:1L 0.9%生理盐水+0.05%L-半胱氨酸。
2.2.2.稀释涂板法
吸取上述繁殖好的细菌培养液1ml,至9ml稀释液中,得到10-1,依次做五个梯度,而后依次接种到预先准备好的的固体培养皿中,涂布均匀。对每个培养皿进行相对应的稀释度标记,每个稀释度做2个平行,并留空白培养皿作对照,后将其置于37℃厌氧条件下倒置培养72h。
2.2.3培养基的配制
(1)改良的MRS液体(1L)配制,如表1:
表1
(2)改良的MRS固体培养基(1L)配制,如表2:
表2
注:L-半胱氨酸溶液过滤除菌后,在培养基灭菌后,倒平板前加入。
(3)改良TPY琼脂(莫匹罗星里盐添加量为50mg/L)
2.2.4纯化
将37℃厌氧培养72h后的平板取出,观察固体培养基上的菌落形态,包括形状、颜色、大小、表面、边缘、隆起度、透明度等,挑选不同菌落形态的单菌进行分区划线,37℃培养48h。
2.2.5镜检
2.2.6液体培养
用已灭好的牙签挑取已纯化好的菌落接于液体中,置于37℃条件下厌氧培养48h。
2.2.6菌种保藏
将培养48h后的液体试管接入到2mL甘油管中,于-80℃下进行保藏。
2.3菌株DNA提取
采用细菌DNA提试剂盒提取DNA,经16S rRNA扩增测序,鉴定为格氏乳杆菌。
16S rRNA序列如下:
TATCATGCAGTCGAGCGAGCTTGCCTAGATGAATTTGGTGCTTGCACCAAATGAAACTAGATACAAGCGAGCGGCGGACGGGTGAGTAACACGTGGGTAACCTGCCCAAGAGACTGGGATAACACCTGGAAACAGATGCTAATACCGGATAACAACACTAGACGCATGTCTAGAGTTTAAAAGATGGTTCTGCTATCACTCTTGGATGGACCTGCGGTGCATTAGCTAGTTGGTAAGGTAACGGCTTACCAAGGCAATGATGCATAGCCGAGTTGAGAGACTGATCGGCCACATTGGGACTGAGACACGGCCCAAACTCCTACGGGAGGCAGCAGTAGGGAATCTTCCACAATGGACGCAAGTCTGATGGAGCAACGCCGCGTGAGTGAAGAAGGGTTTCGGCTCGTAAAGCTCTGTTGGTAGTGAAGAAAGATAGAGGTAGTAACTGGCCTTTATTTGACGGTAATTACTTAGAAAGTCACGGCTAACTACGTGCCAGCAGCCGCGGTAATACGTAGGTGGCAAGCGTTGTCCGGATTTATTGGGCGTAAAGCGAGTGCAGGCGGTTCAATAAGTCTGATGTGAAAGCCTTCGGCTCAACCGGAGAATTGCATCAGAAACTGTTGAACTTGAGTGCAGAAGAGGAGAGTGGAACTCCATGTGTAGCGGTGGAATGCGTAGATATATGGAAGAACACCAGTGGCGAAGGCGGCTCTCTGGTCTGCAACTGACGCTGAGGCTCGAAAGCATGGGTAGCGAACAGGATTAGATACCCTGGTAGTCCATGCCGTAAACGATGAGTGCTAAGTGTTGGGAGGTTTCCGCCTCTCAGTGCTGCAGCTAACGCATTAAGCACTCCGCCTGGGGAGTACGACCGCAAGGTTGAAACTCAAAGGAATTGACGGGGGCCCGCACAAGCGGTGGAGCATGTGGTTTAATTCGAAGCAACGCGAAGAACCTTACCAGGTCTTGACATCCAGTGCAAACCTAAGAGATTAGGTGTTCCCTTCGGGGACGCTGAGACAGGTGGTGCATGGCTGTCGTCAGCTCGTGTCGTGAGATGTTGGGTTAAGTCCCGCAACGAGCGCAACCCTTGTCATTAGTTGCCATCATTAAGTTGGGCACTCTAATGAGACTGCCGGTGACAAACCGGAGGAAGGTGGGGATGACGTCAAGTCATCATGCCCCTTATGACCTGGGCTACACACGTGCTACAATGGACGGTACAACGAGAAGCGAACCTGCGAAGGCAAGCGGATCTCTGAAAGCCGTTCTCAGTTCGGACTGTAGGCTGCAACTCGCCTACACGAAGCTGGAATCGCTAGTAATCGCGGATCAGCACGCCGCGGTGAATACGTTCCCGGGCCTTGTACACACCGCCCGTCACACCATGAGAGTCTGTAACACCCAAAGCCGGTGGGATAACCTTTATAGGAGTCAGCCGTCTAAGGTAGGACAGATGATTAGGGTGAAG。
实施例2一种微生物菌剂的制备
(1)发酵乳杆菌的发酵
先将保存的发酵乳杆菌进行活化,活化培养基包括以下重量份组分:蛋白胨15份、牛肉浸膏8份、酵母浸粉3份、葡萄糖25份、醋酸钠5份、柠檬酸二胺2份、磷酸氢二钾0.2份、硫酸镁0.35份、硫酸锰0.01份、碳酸钙5份和水1000份。活化条件37℃,厌氧活化18h,获得发酵乳杆菌活化菌液。
将所得发酵乳杆菌活化菌液按照接种量4.5%接种于发酵培养基中,37℃,厌氧发酵24h,得到发酵乳杆菌发酵液。发酵培养基包括以下重量份组分:蛋白胨10份、牛肉浸膏5份、酵母浸粉3份、葡萄糖20份、醋酸钠5份、柠檬酸二胺2份、磷酸氢二钾0.2份、硫酸镁0.35份、硫酸锰0.01份、碳酸钙5份和水1000份。
(2)先将保存的凝结芽孢杆菌活化,活化培养基为胰蛋白胨8份、酵母浸粉15份、葡萄糖10份、磷酸氢二钾3份、硫酸镁0.3份、硫酸锰0.01份和蒸馏水1L;活化条件为40℃,250rpm活化12h,获得凝结芽孢杆菌活化菌液。
将所得的凝结芽孢杆菌活化菌液按照接种量3.5%接种于发酵培养基中,37℃,250rpm发酵24h,得到凝结芽孢杆菌发酵液。发酵培养基包括以下重量份组分:胰蛋白胨5份、酵母浸粉15份、葡萄糖5份、磷酸氢二钾3份、硫酸镁0.3份、硫酸锰0.01份和蒸馏水1000份。
(3)将实施例1分离纯化后的格氏乳杆菌按照接种量4.5%接种于发酵培养基中,37℃,厌氧发酵24h,获得格氏乳杆菌发酵液。发酵培养基包括以下重量份组分:蛋白胨10份、酵母浸粉8份、葡萄糖20份、磷酸氢二钾3份、硫酸镁0.2份、醋酸钠3份、硫酸锰0.01份和水1000份。
(4)将所得的发酵乳杆菌发酵液、凝结芽孢杆菌发酵液和格氏乳杆菌发酵液分别离心后,收集菌体,冷冻、干燥,得到发酵乳杆菌菌粉、凝结芽孢杆菌菌粉以及格氏乳杆菌菌粉。将三种菌粉按照不同配比组合,发现各种菌随着添加量的不同发生变化,但是在发酵乳杆菌菌粉、凝结芽孢杆菌菌粉、格氏乳杆菌菌粉的质量比为2:0.5:0.5时,制备的复合益生菌中,各菌种的含菌量最低,分别为发酵乳杆菌的活菌量2.85×1010cfu/g,凝结芽孢杆菌的活菌量3.10×1010cfu/g,格氏芽孢杆菌的活菌量2.50×1010cfu/g,见表2。将三种菌粉和水苏糖混合,为了保证最低含量量仍然存在技术效果的基础上,后续功能验证过程中按照如下用量称量:发酵乳杆菌菌粉200g、凝结芽孢杆菌菌粉50g、格氏乳杆菌菌粉50g和水苏糖350g,制备的微生物菌剂。
表2
实施例3具有延缓衰老和抗氧化功能的复合益生菌的应用
本实施例主要是研究复合益生菌在抗氧化和延缓衰老方面的应用。
(1)复合益生菌对氧胁迫的耐受性
根据实施例2制备微生物菌剂的方法,先混合制备复合益生菌,然后在MRS培养基添加0.50mmol/L H2O2,37℃发酵4h,分别测定0h和4h的OD600,检测复合益生菌对H2O2的耐受性。通过分别以发酵乳杆菌和凝结芽孢乳杆菌、发酵乳杆菌和格氏乳杆菌、格氏乳杆菌和凝结芽孢杆菌、以及单独的发酵乳杆菌、凝结芽孢乳杆菌和格氏乳杆菌作为对照。结果如表3所示。
表3
从表4可以看出,当三种菌株混合复配时表现出相比单一菌种或任意两种菌株复配时对氧的耐受性。
(2)复合益生菌清除DPPH自由基的能力
按照实施例2最优条件制备的微生物菌剂,取1.0mg加入1mL DPPH无水乙醇溶液(0.2mmol/L)混合均匀,室温避光反应20min,2000rpm离心15min,取上清液于517nm处测定吸光度值Ai,空白组以等体积无水乙醇替代DPPH无水乙醇溶液A0,对照组以等体积空白溶剂代替样品溶液Aj,并以等体积蒸馏水和乙醇混合液空白调零。清除率(%)=100-(Ai-A0)/Aj×100%。
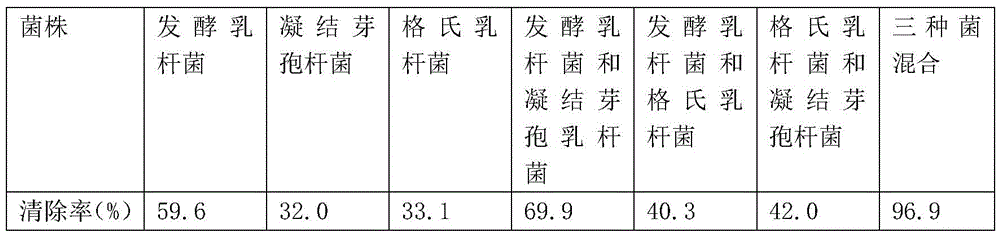
同时,用发酵乳杆菌、凝结芽孢乳杆菌和格氏乳杆菌单独一种以及任意两种组合,替代上述三种菌株混合复配制备的微生物菌剂,作为对照试验。结果如表4所示。
表4
从表5中可以看出,单独的凝结芽孢杆菌和格氏乳杆菌几乎无清除DPPH的能力,发酵乳杆菌具有明显清除DPPH的能力;而任意两种菌种复配时,除了发酵乳杆菌与其他两种菌分别复配时,仍具有清除DPPH的能力,但是效果不明显,惊奇的是,凝结芽孢杆菌和格氏乳杆菌单独使用虽然几乎无清除DPPH能力,但是两种复配不但没降低,反而稍有增强,但是增强并不是很明显。而将三种菌复配后发现,能够显著的提高对DPPH的清除率,具体原理尚不清楚。
(3)复合益生菌清除羟基自由基的能力
0.5mL的邻二氮菲(6mmol/L),0.5mL的FeSO4溶液(6mmol/L)与1.0mL的PBS溶液(pH7.2)混匀。再向此体系中加入0.5mL样品和0.5mL 0.1%过氧化氢,用双蒸水将总体积定容至4.0mL。混匀后在37℃下孵育1h,于536nm下读取吸光度。羟自由基的清除率按下式计算:清除率(%)=[(As-A0)/(A-A0)]×100%
As:样品的吸光度值;A0:用H2O替代样品;A:用H2O替代H2O2和样品。
用发酵乳杆菌、凝结芽孢乳杆菌和格氏乳杆菌单独一种以及任意两种组合,替代上述三种菌株混合复配制备的微生物菌剂,作为对照试验。结果如表5所示,复合益生菌清除羟基自由基能力最强。
表5
(4)复合益生菌清除超氧阴离子的能力
Ai组:2mL Tris-HCl缓冲液(150mM pH8.0)中加入1mL邻苯三酚溶液,再加入0.5mL样品;Aj组:用1mL蒸馏水取代邻苯三酚溶液;A0组:用0.5mL蒸馏水取代样品;A1组:用1.5mL蒸馏水取代1mL邻苯三酚和0.5mL样品;混匀,室温反应30min后于325nm处测定吸光值;记录数据并计算清除率:清除率(%)=[1-(Ai-Aj)/(A0-A1)]×100%
用发酵乳杆菌、凝结芽孢乳杆菌和格氏乳杆菌单独一种以及任意两种组合,替代上述三种菌株混合复配制备的微生物菌剂,作为对照试验。结果如表6所示,复合益生菌清除超氧阴离子的能力最强。
表6
(5)复合益生菌总还原力测定
0.5mL 0.2M PBS溶液(pH6.6)中加入0.5mL 0.1%的铁氰化钾溶液和0.5mL样品;充分混匀,50℃保温20min;加入等体积的10%三氯乙酸,3000g离心10min;取1mL上清,加入0.175mL 0.1%FeCl3溶液,混合均匀,反应10min;700nm处测定吸光值。
用发酵乳杆菌、凝结芽孢乳杆菌和格氏乳杆菌单独一种以及任意两种组合,替代上述三种菌株混合复配制备的微生物菌剂,作为对照试验。结果如表7所示,复合益生菌总还原力最强。
表7
(6)复合益生菌模拟体内抗氧化作用
用D-半乳糖腹空注射小鼠(SPF级昆明种雄性12月龄)建造衰老模型,腹空注射造模同时灌胃治疗,连续六周。分组如下表8:
表8
实验前小鼠尾尖上采血测定MAD含量;6周最后一天,小鼠尾尖上采血测定MDA的含量,并摘眼球采血,离心,取血清,测定血清超氧化物歧化酶(SOD)活力和谷胱甘肽过氧化物酶(GSH-PX)活力,结果检验方法采用组间t检验。
结果如表9所示,与对照相比,本发明试验1组即本发明的复合益生菌相差较明显,而其他单一菌株或者两种菌株复配和对照相比无明显差异,说明本发明的复合益生菌治疗效果更明显,优于对照以及其他单一菌株或者两种菌株复配的治疗效果。
表9
如表10所示,经过灌胃治疗不同菌株制备的样品后,试验1组即复合益生菌组中血清SOD活力明显高于对照组以及其他单一菌株或者两种菌株复配组,而单一菌株或者两种菌株复配组与对照组差异并不明显,说明本发明的复合益生菌的治疗效果更优。
表10
| 分组 | 重复次数 | SOD活力(U/mL) |
| 对照1 | 5 | 150.02±40.89 |
| 对照2 | 5 | 164.64±45.66 |
| 试验1 | 5 | 210.23±50.35 |
| 试验2 | 5 | 175.23±43.23 |
| 试验3 | 5 | 163.21±45.03 |
| 试验4 | 5 | 160.56±44.01 |
| 试验5 | 5 | 179.30±46.02 |
| 试验6 | 5 | 179.02±45.20 |
| 试验7 | 5 | 168.01±45.23 |
以上所述的实施例仅是对本发明的优选方式进行描述,并非对本发明的范围进行限定,在不脱离本发明设计精神的前提下,本领域普通技术人员对本发明的技术方案做出的各种变形和改进,均应落入本发明权利要求书确定的保护范围内。
Claims (7)
1.一种具有延缓衰老和抗氧化功能的复合益生菌,其特征在于,所述复合益生菌包括发酵乳杆菌(Lactobacillus fermentum)、凝结芽孢杆菌(Bacillus coagulans)和格氏乳杆菌(Lactobacillus gasseri);
所述发酵乳杆菌的保藏编号为CGMCC NO.14493;所述凝结芽孢杆菌保藏编号为CCTCCNO:M2017813;所述格氏乳杆菌保藏编号为CGMCC No.23187。
2.一种微生物菌剂,其特征在于,包括权利要求1所述的复合益生菌。
3.如权利要求2所述的微生物菌剂,其特征在于,所述发酵乳杆菌、凝结芽孢杆菌和格氏乳杆菌分别接种发酵培养基后,获取发酵液;然后将所得发酵液离心,收集菌体,冷冻、干燥,分别得到发酵乳杆菌菌粉、凝结芽孢杆菌菌粉和格氏乳杆菌菌粉。
4.如权利要求3所述的微生物菌剂,其特征在于,所述微生物菌剂还包括水苏糖,将所述发酵乳杆菌菌粉、凝结芽孢杆菌菌粉、格氏乳杆菌菌粉和所述水苏糖按照质量比(0.5-2):(0.5-2):(0.5-2):(1-5)混合制备得到所述微生物菌剂。
5.如权利要求3所述的微生物菌剂,其特征在于,所述发酵乳杆菌的发酵培养基包括以下重量份的组分:蛋白胨10份、牛肉浸膏5份、酵母浸粉3份、葡萄糖20份、醋酸钠5份、柠檬酸二胺2份、磷酸氢二钾0.2份、硫酸镁0.35份、硫酸锰0.01份、碳酸钙5份和水1000份;
所述凝结芽孢杆菌的发酵培养基包括以下重量份组分:胰蛋白胨5份、酵母浸粉15份、葡萄糖5份、磷酸氢二钾3份、硫酸镁0.3份、硫酸锰0.01份和蒸馏水1000份;
所述格氏乳杆菌的发酵培养基包括以下重量份组分:蛋白胨10份、酵母浸粉8份、葡萄糖20份、磷酸氢二钾3份、硫酸镁0.2份、醋酸钠3份、硫酸锰0.01份和水1000份。
6.一种如权利要求1所述的复合益生菌或权利要求2-5任一项所述的微生物菌剂在制备具有延缓衰老和抗氧化功能的产品中的应用。
7.如权利要求6所述的应用,其特征在于,所述产品包括药物、食品或保健食品。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN202210475556.0A CN114642686B (zh) | 2022-04-29 | 2022-04-29 | 一种复合益生菌及其延缓衰老和抗氧化的作用 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN202210475556.0A CN114642686B (zh) | 2022-04-29 | 2022-04-29 | 一种复合益生菌及其延缓衰老和抗氧化的作用 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN114642686A CN114642686A (zh) | 2022-06-21 |
| CN114642686B true CN114642686B (zh) | 2023-02-10 |
Family
ID=81997618
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202210475556.0A Active CN114642686B (zh) | 2022-04-29 | 2022-04-29 | 一种复合益生菌及其延缓衰老和抗氧化的作用 |
Country Status (1)
| Country | Link |
|---|---|
| CN (1) | CN114642686B (zh) |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN115317399A (zh) * | 2022-07-07 | 2022-11-11 | 湖北真福医药有限公司 | 一种抗衰老组合物及其制备方法和应用 |
| CN116622584A (zh) * | 2023-06-16 | 2023-08-22 | 广东南芯医疗科技有限公司 | 格氏乳杆菌ls03在制备抗氧化和抗衰老产品中的应用 |
| CN117660262B (zh) * | 2023-12-14 | 2024-06-21 | 善恩康生物科技(苏州)有限公司 | 一种用于低/零乳糖乳制品生产的乳酸菌组合及其应用 |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN106399163B (zh) * | 2016-09-08 | 2019-09-27 | 江苏微康生物科技有限公司 | 一种抗衰老益生菌制剂及制备方法 |
| CN110577912B (zh) * | 2019-09-24 | 2022-03-29 | 华南理工大学 | 一种格氏乳杆菌及其在制备发酵乳中的应用 |
| CN114191490A (zh) * | 2022-01-28 | 2022-03-18 | 善恩康生物科技(苏州)有限公司 | 一种发酵乳杆菌及其产物在抗氧化和抗肿瘤中的应用 |
| CN114703105B (zh) * | 2022-04-29 | 2022-12-27 | 善恩康生物科技(苏州)有限公司 | 一种复合益生菌在降血脂或缓解肥胖中的应用 |
-
2022
- 2022-04-29 CN CN202210475556.0A patent/CN114642686B/zh active Active
Also Published As
| Publication number | Publication date |
|---|---|
| CN114642686A (zh) | 2022-06-21 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN114642686B (zh) | 一种复合益生菌及其延缓衰老和抗氧化的作用 | |
| CN116024130B (zh) | 一株降血尿酸发酵乳杆菌a21215及其应用 | |
| CN110106119B (zh) | 一株分离自母乳的鼠李糖乳杆菌m9及其应用 | |
| CN111925961B (zh) | 一株植物乳杆菌Lp2及其应用 | |
| CN110564638A (zh) | 一株具有益生特性的罗伊氏乳杆菌及其用途 | |
| CN111849836B (zh) | 一种具有抗氧化的鼠李糖乳杆菌及其应用 | |
| CN110577912A (zh) | 一种格氏乳杆菌及其在制备发酵乳中的应用 | |
| CN110023486B (zh) | 一种嗜酸乳杆菌及其培养方法和应用 | |
| CN115820498A (zh) | 一株植物乳杆菌yj2406及其应用 | |
| CN108018248B (zh) | 一种具有调节抗生素引起的菌群结构紊乱的干酪乳杆菌 | |
| CN111944712B (zh) | 一株具有优良酒精耐受能力的植物乳杆菌和应用 | |
| CN115895966B (zh) | 一株辅助缓解痛风的两歧双歧杆菌bl002及其应用 | |
| CN115322932B (zh) | 一株具有解酒醒酒能力的植物乳植杆菌和应用 | |
| CN114836349A (zh) | 拮抗幽门螺旋杆菌的嗜酸乳杆菌la16及其应用 | |
| CN113444656B (zh) | 一种具有抗衰老功能的菌株及其应用 | |
| CN113249244B (zh) | 一种拮抗咽炎致病菌乙型溶血性链球菌的副干酪乳杆菌 | |
| CN117683670A (zh) | 一种植物乳植杆菌fmbl l23036 cnn、酸奶发酵剂、酸奶及其应用 | |
| CN117660253A (zh) | 一种鼠李糖乳酪杆菌fmbl l23004 cnn、酸奶发酵剂、酸奶及其应用 | |
| CN116987645A (zh) | 一种植物乳植杆菌(Lactiplantibacillus plantarum)HEPRO-185及其应用 | |
| CN117327616A (zh) | Lactiplantibacillus plantarum ZN1及其应用 | |
| CN116987626A (zh) | 一种副干酪乳杆菌ap14及其在肠道调节与尿酸代谢的应用 | |
| CN116656542A (zh) | 一株具有缓解酒精性肝损伤功能的发酵粘液乳杆菌及其应用 | |
| CN111004735A (zh) | 一株发酵乳杆菌及其在改善肠道健康方面的应用 | |
| CN113215067A (zh) | Vbnc状态短乳杆菌cshrr5-3菌株及其应用 | |
| CN113508907A (zh) | 一株耐热型发酵乳杆菌在制备促排便食品或药品中的应用 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| GR01 | Patent grant | ||
| GR01 | Patent grant |