CN112292380A - 作为用于治疗癌症的hpk1抑制剂的n-(苯基)-2-(苯基)嘧啶-4-甲酰胺衍生物及相关化合物 - Google Patents
作为用于治疗癌症的hpk1抑制剂的n-(苯基)-2-(苯基)嘧啶-4-甲酰胺衍生物及相关化合物 Download PDFInfo
- Publication number
- CN112292380A CN112292380A CN201980020899.4A CN201980020899A CN112292380A CN 112292380 A CN112292380 A CN 112292380A CN 201980020899 A CN201980020899 A CN 201980020899A CN 112292380 A CN112292380 A CN 112292380A
- Authority
- CN
- China
- Prior art keywords
- independently selected
- radical
- alkyl
- substituted
- membered heterocycloalkyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- 150000001875 compounds Chemical class 0.000 title claims abstract description 208
- 206010028980 Neoplasm Diseases 0.000 title claims abstract description 50
- 102100028199 Mitogen-activated protein kinase kinase kinase kinase 1 Human genes 0.000 title claims abstract description 44
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 title claims abstract description 39
- 101001059991 Homo sapiens Mitogen-activated protein kinase kinase kinase kinase 1 Proteins 0.000 title claims description 40
- 201000011510 cancer Diseases 0.000 title claims description 19
- 239000003112 inhibitor Substances 0.000 title abstract description 70
- 238000011282 treatment Methods 0.000 title abstract description 10
- -1 5-fluoro-2- (2- (pyridin-2-yl) pyrrolidin-1-yl) phenyl Chemical group 0.000 claims abstract description 1049
- 208000020816 lung neoplasm Diseases 0.000 claims abstract description 9
- 206010061902 Pancreatic neoplasm Diseases 0.000 claims abstract description 6
- 206010006187 Breast cancer Diseases 0.000 claims abstract description 5
- 208000026310 Breast neoplasm Diseases 0.000 claims abstract description 5
- 206010061535 Ovarian neoplasm Diseases 0.000 claims abstract description 5
- 208000001333 Colorectal Neoplasms Diseases 0.000 claims abstract description 4
- 150000003254 radicals Chemical class 0.000 claims description 700
- 125000000592 heterocycloalkyl group Chemical group 0.000 claims description 539
- 125000001424 substituent group Chemical group 0.000 claims description 504
- 125000001313 C5-C10 heteroaryl group Chemical group 0.000 claims description 463
- 125000003601 C2-C6 alkynyl group Chemical group 0.000 claims description 426
- 125000006376 (C3-C10) cycloalkyl group Chemical group 0.000 claims description 352
- 125000000171 (C1-C6) haloalkyl group Chemical group 0.000 claims description 294
- 125000005843 halogen group Chemical group 0.000 claims description 185
- 125000000475 sulfinyl group Chemical group [*:2]S([*:1])=O 0.000 claims description 163
- 150000003839 salts Chemical class 0.000 claims description 135
- 229910052739 hydrogen Inorganic materials 0.000 claims description 114
- 125000001188 haloalkyl group Chemical group 0.000 claims description 97
- 125000000217 alkyl group Chemical group 0.000 claims description 95
- 125000004432 carbon atom Chemical group C* 0.000 claims description 93
- 229910052717 sulfur Inorganic materials 0.000 claims description 93
- 229910052799 carbon Inorganic materials 0.000 claims description 81
- 125000000304 alkynyl group Chemical group 0.000 claims description 80
- 125000004397 aminosulfonyl group Chemical group NS(=O)(=O)* 0.000 claims description 80
- 125000003917 carbamoyl group Chemical group [H]N([H])C(*)=O 0.000 claims description 80
- 125000004429 atom Chemical group 0.000 claims description 79
- 125000000882 C2-C6 alkenyl group Chemical group 0.000 claims description 74
- 229910052805 deuterium Inorganic materials 0.000 claims description 74
- 125000004433 nitrogen atom Chemical group N* 0.000 claims description 74
- 125000004750 (C1-C6) alkylaminosulfonyl group Chemical group 0.000 claims description 73
- 125000005842 heteroatom Chemical group 0.000 claims description 66
- 229910052760 oxygen Inorganic materials 0.000 claims description 63
- 125000003545 alkoxy group Chemical group 0.000 claims description 60
- 125000006582 (C5-C6) heterocycloalkyl group Chemical group 0.000 claims description 57
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 claims description 52
- 125000002947 alkylene group Chemical group 0.000 claims description 45
- 125000004916 (C1-C6) alkylcarbonyl group Chemical group 0.000 claims description 40
- 125000006568 (C4-C7) heterocycloalkyl group Chemical group 0.000 claims description 40
- 125000001072 heteroaryl group Chemical group 0.000 claims description 40
- 229910052757 nitrogen Inorganic materials 0.000 claims description 36
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 34
- 125000000753 cycloalkyl group Chemical group 0.000 claims description 28
- 125000005913 (C3-C6) cycloalkyl group Chemical group 0.000 claims description 25
- 125000006570 (C5-C6) heteroaryl group Chemical group 0.000 claims description 25
- 238000000034 method Methods 0.000 claims description 24
- 125000003118 aryl group Chemical group 0.000 claims description 23
- 201000010099 disease Diseases 0.000 claims description 22
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 19
- 125000006652 (C3-C12) cycloalkyl group Chemical group 0.000 claims description 13
- 229910052731 fluorine Inorganic materials 0.000 claims description 13
- 208000035475 disorder Diseases 0.000 claims description 12
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 claims description 12
- 238000006467 substitution reaction Methods 0.000 claims description 12
- 125000004737 (C1-C6) haloalkoxy group Chemical group 0.000 claims description 11
- 230000000694 effects Effects 0.000 claims description 11
- 125000004573 morpholin-4-yl group Chemical group N1(CCOCC1)* 0.000 claims description 10
- 125000004029 hydroxymethyl group Chemical group [H]OC([H])([H])* 0.000 claims description 9
- 125000004076 pyridyl group Chemical group 0.000 claims description 9
- HKSQZEGSMBFHGC-UHFFFAOYSA-N pyrimidine-4-carboxamide Chemical compound NC(=O)C1=CC=NC=N1 HKSQZEGSMBFHGC-UHFFFAOYSA-N 0.000 claims description 9
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 claims description 8
- 125000004390 alkyl sulfonyl group Chemical group 0.000 claims description 7
- 229910052801 chlorine Inorganic materials 0.000 claims description 7
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 claims description 7
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 claims description 7
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 claims description 7
- 230000002401 inhibitory effect Effects 0.000 claims description 7
- 101100177670 Caenorhabditis elegans hpk-1 gene Proteins 0.000 claims description 6
- 229910052794 bromium Inorganic materials 0.000 claims description 6
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 claims description 6
- 125000004454 (C1-C6) alkoxycarbonyl group Chemical group 0.000 claims description 5
- 125000004739 (C1-C6) alkylsulfonyl group Chemical group 0.000 claims description 5
- 125000004845 (C1-C6) alkylsulfonylamino group Chemical group 0.000 claims description 5
- 125000006598 aminocarbonylamino group Chemical group 0.000 claims description 5
- 125000004566 azetidin-1-yl group Chemical group N1(CCC1)* 0.000 claims description 5
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 claims description 5
- 206010058467 Lung neoplasm malignant Diseases 0.000 claims description 4
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 claims description 4
- 201000005202 lung cancer Diseases 0.000 claims description 4
- 206010009944 Colon cancer Diseases 0.000 claims description 3
- 206010033128 Ovarian cancer Diseases 0.000 claims description 3
- 125000006311 cyclobutyl amino group Chemical group [H]N(*)C1([H])C([H])([H])C([H])([H])C1([H])[H] 0.000 claims description 3
- 230000005764 inhibitory process Effects 0.000 claims description 3
- 208000015486 malignant pancreatic neoplasm Diseases 0.000 claims description 3
- 201000002528 pancreatic cancer Diseases 0.000 claims description 3
- 208000008443 pancreatic carcinoma Diseases 0.000 claims description 3
- ABTDMVCVUKSZKX-QZTJIDSGSA-N (1R,4R)-5-[4-fluoro-2-[[2-(2-fluoro-6-methoxyphenyl)pyrimidine-4-carbonyl]amino]phenyl]-N-propyl-2,5-diazabicyclo[2.2.1]heptane-2-carboxamide Chemical compound FC1=CC(=C(C=C1)N1[C@H]2CN([C@@H](C1)C2)C(=O)NCCC)NC(=O)C1=NC(=NC=C1)C1=C(C=CC=C1OC)F ABTDMVCVUKSZKX-QZTJIDSGSA-N 0.000 claims description 2
- 125000004890 (C1-C6) alkylamino group Chemical group 0.000 claims description 2
- ZVWJPRNAWADZOO-UHFFFAOYSA-N 2-(2-fluoro-6-methoxyphenyl)pyrimidine-4-carboxamide Chemical compound FC1=C(C(=CC=C1)OC)C1=NC=CC(=N1)C(=O)N ZVWJPRNAWADZOO-UHFFFAOYSA-N 0.000 claims description 2
- 125000003349 3-pyridyl group Chemical group N1=C([H])C([*])=C([H])C([H])=C1[H] 0.000 claims description 2
- 125000004195 4-methylpiperazin-1-yl group Chemical group [H]C([H])([H])N1C([H])([H])C([H])([H])N(*)C([H])([H])C1([H])[H] 0.000 claims description 2
- GAWIXWVDTYZWAW-UHFFFAOYSA-N C[CH]O Chemical group C[CH]O GAWIXWVDTYZWAW-UHFFFAOYSA-N 0.000 claims description 2
- GQAGJQNVOPGUCQ-UHFFFAOYSA-N N-[2-(3-aminocyclohexyl)phenyl]-2-(2-fluoro-6-methoxyphenyl)pyrimidine-4-carboxamide Chemical compound N(C1=C(C2CC(CCC2)N)C=CC=C1)C(=O)C1=CC=NC(=N1)C1=C(OC)C=CC=C1F GQAGJQNVOPGUCQ-UHFFFAOYSA-N 0.000 claims description 2
- LLFCXYBVJBKXHH-UHFFFAOYSA-N N-[2-(3-aminocyclopentyl)phenyl]-2-(2-fluoro-6-methoxyphenyl)pyrimidine-4-carboxamide Chemical compound N(C1=C(C2CCC(N)C2)C=CC=C1)C(=O)C1=CC=NC(=N1)C1=C(OC)C=CC=C1F LLFCXYBVJBKXHH-UHFFFAOYSA-N 0.000 claims description 2
- NRYRSQRRSBLVER-IRXDYDNUSA-N N-[2-[(2S,4S)-4-(dimethylamino)-2-(hydroxymethyl)pyrrolidin-1-yl]-5-fluorophenyl]-2-(2-fluoro-6-methoxyphenyl)pyrimidine-4-carboxamide Chemical compound C1=C(F)C=CC(=C1NC(=O)C1=CC=NC(=N1)C1=C(F)C=CC=C1OC)N1C[C@@H](N(C)C)C[C@H]1CO NRYRSQRRSBLVER-IRXDYDNUSA-N 0.000 claims description 2
- WXKLVVXNBFIYSG-DCFHFQCYSA-N N-[2-[(2S,4S)-4-amino-2-(1-hydroxycyclopropyl)pyrrolidin-1-yl]-4-(4-cyanopyridin-3-yl)phenyl]-2-(2-fluoro-6-methoxyphenyl)pyrimidine-4-carboxamide Chemical compound N[C@H]1C[C@H](N(C1)C1=C(C=CC(=C1)C=1C=NC=CC=1C#N)NC(=O)C1=NC(=NC=C1)C1=C(C=CC=C1OC)F)C1(CC1)O WXKLVVXNBFIYSG-DCFHFQCYSA-N 0.000 claims description 2
- YTYIKQGGIQKXKW-DCFHFQCYSA-N N-[2-[(2S,4S)-4-amino-2-(2-hydroxypropan-2-yl)pyrrolidin-1-yl]-4-(4-cyanopyridin-3-yl)phenyl]-2-(2-fluoro-6-methoxyphenyl)pyrimidine-4-carboxamide Chemical compound N[C@H]1C[C@H](N(C1)C1=C(C=CC(=C1)C=1C=NC=CC=1C#N)NC(=O)C1=NC(=NC=C1)C1=C(C=CC=C1OC)F)C(C)(C)O YTYIKQGGIQKXKW-DCFHFQCYSA-N 0.000 claims description 2
- WJEPQBUJWFNXPG-IRXDYDNUSA-N N-[2-[(2S,4S)-4-amino-2-(hydroxymethyl)pyrrolidin-1-yl]-4-(1-cyanocyclopropyl)phenyl]-2-(2,6-difluorophenyl)pyrimidine-4-carboxamide Chemical compound N[C@H]1C[C@H](N(C1)C1=C(C=CC(=C1)C1(CC1)C#N)NC(=O)C1=NC(=NC=C1)C1=C(C=CC=C1F)F)CO WJEPQBUJWFNXPG-IRXDYDNUSA-N 0.000 claims description 2
- BLLJUCXNHUVEHL-PMACEKPBSA-N N-[2-[(2S,4S)-4-amino-2-(hydroxymethyl)pyrrolidin-1-yl]-4-(2-methylpyridin-3-yl)phenyl]-2-(2-fluoro-6-methoxyphenyl)pyrimidine-4-carboxamide Chemical compound C=1(C=CC=NC=1C)C1=CC=C(NC(=O)C2=CC=NC(=N2)C2=C(F)C=CC=C2OC)C(N2C[C@@H](N)C[C@H]2CO)=C1 BLLJUCXNHUVEHL-PMACEKPBSA-N 0.000 claims description 2
- HENRITOGWFFGGA-PMACEKPBSA-N N-[2-[(2S,4S)-4-amino-2-(hydroxymethyl)pyrrolidin-1-yl]-4-(3-cyanopyridin-2-yl)phenyl]-2-(2-fluoro-6-methoxyphenyl)pyrimidine-4-carboxamide Chemical compound N[C@H]1C[C@H](N(C1)C1=C(C=CC(=C1)C1=NC=CC=C1C#N)NC(=O)C1=NC(=NC=C1)C1=C(C=CC=C1OC)F)CO HENRITOGWFFGGA-PMACEKPBSA-N 0.000 claims description 2
- MRLPZQXQFOPDDQ-PMACEKPBSA-N N-[2-[(2S,4S)-4-amino-2-(hydroxymethyl)pyrrolidin-1-yl]-4-(3-cyanopyridin-4-yl)phenyl]-2-(2-fluoro-6-methoxyphenyl)pyrimidine-4-carboxamide Chemical compound N[C@H]1C[C@H](N(C1)C1=C(C=CC(=C1)C1=C(C=NC=C1)C#N)NC(=O)C1=NC(=NC=C1)C1=C(C=CC=C1OC)F)CO MRLPZQXQFOPDDQ-PMACEKPBSA-N 0.000 claims description 2
- ZMSBSUWREUXWEU-OALUTQOASA-N N-[2-[(2S,4S)-4-amino-2-(hydroxymethyl)pyrrolidin-1-yl]-4-(3-methoxypyridin-4-yl)phenyl]-2-(2-fluoro-6-methoxyphenyl)pyrimidine-4-carboxamide Chemical compound C1(C=2C(OC)=CN=CC=2)=CC=C(NC(=O)C2=CC=NC(=N2)C2=C(F)C=CC=C2OC)C(N2[C@@H](C[C@H](N)C2)CO)=C1 ZMSBSUWREUXWEU-OALUTQOASA-N 0.000 claims description 2
- SEKQICVALVTKMV-OALUTQOASA-N N-[2-[(2S,4S)-4-amino-2-(hydroxymethyl)pyrrolidin-1-yl]-4-(4-cyanopyridin-3-yl)phenyl]-2-(2,3-difluoro-6-methoxyphenyl)pyrimidine-4-carboxamide Chemical compound C1(C#N)=C(C2=CC=C(NC(=O)C3=CC=NC(=N3)C3=C(OC)C=CC(F)=C3F)C(N3C[C@@H](N)C[C@H]3CO)=C2)C=NC=C1 SEKQICVALVTKMV-OALUTQOASA-N 0.000 claims description 2
- LDCDYMPNMGJUDB-OALUTQOASA-N N-[2-[(2S,4S)-4-amino-2-(hydroxymethyl)pyrrolidin-1-yl]-4-(4-cyanopyridin-3-yl)phenyl]-2-(2,6-difluorophenyl)pyrimidine-4-carboxamide Chemical compound N[C@H]1C[C@H](N(C1)C1=C(C=CC(=C1)C=1C=NC=CC=1C#N)NC(=O)C1=NC(=NC=C1)C1=C(C=CC=C1F)F)CO LDCDYMPNMGJUDB-OALUTQOASA-N 0.000 claims description 2
- PJPVNRZDRDNSLL-OALUTQOASA-N N-[2-[(2S,4S)-4-amino-2-(hydroxymethyl)pyrrolidin-1-yl]-4-(4-cyanopyridin-3-yl)phenyl]-2-(2-chloro-6-fluorophenyl)pyrimidine-4-carboxamide Chemical compound C1(C#N)=C(C2=CC=C(NC(=O)C3=CC=NC(=N3)C3=C(Cl)C=CC=C3F)C(N3C[C@@H](N)C[C@H]3CO)=C2)C=NC=C1 PJPVNRZDRDNSLL-OALUTQOASA-N 0.000 claims description 2
- KZPWAZPBJQZJGY-VXKWHMMOSA-N N-[2-[(2S,4S)-4-amino-2-(hydroxymethyl)pyrrolidin-1-yl]-4-(4-cyanopyridin-3-yl)phenyl]-2-(2-cyclopropyl-6-fluorophenyl)pyrimidine-4-carboxamide Chemical compound C=1(C=NC=CC=1C#N)C1=CC=C(NC(=O)C2=CC=NC(=N2)C2=C(C3CC3)C=CC=C2F)C(N2C[C@@H](N)C[C@H]2CO)=C1 KZPWAZPBJQZJGY-VXKWHMMOSA-N 0.000 claims description 2
- RQXLMBLSWQYUNA-SFTDATJTSA-N N-[2-[(2S,4S)-4-amino-2-(hydroxymethyl)pyrrolidin-1-yl]-4-(4-cyanopyridin-3-yl)phenyl]-2-(2-ethoxy-6-fluorophenyl)pyrimidine-4-carboxamide Chemical compound C=1(C=NC=CC=1C#N)C1=CC=C(NC(=O)C2=CC=NC(=N2)C2=C(OCC)C=CC=C2F)C(N2[C@H](CO)C[C@H](N)C2)=C1 RQXLMBLSWQYUNA-SFTDATJTSA-N 0.000 claims description 2
- BZUQIMZNTIMOAJ-SFTDATJTSA-N N-[2-[(2S,4S)-4-amino-2-(hydroxymethyl)pyrrolidin-1-yl]-4-(4-cyanopyridin-3-yl)phenyl]-2-(2-fluoro-6-methoxy-4-methylphenyl)pyrimidine-4-carboxamide Chemical compound N[C@H]1C[C@H](N(C1)C1=C(C=CC(=C1)C=1C=NC=CC=1C#N)NC(=O)C1=NC(=NC=C1)C1=C(C=C(C=C1OC)C)F)CO BZUQIMZNTIMOAJ-SFTDATJTSA-N 0.000 claims description 2
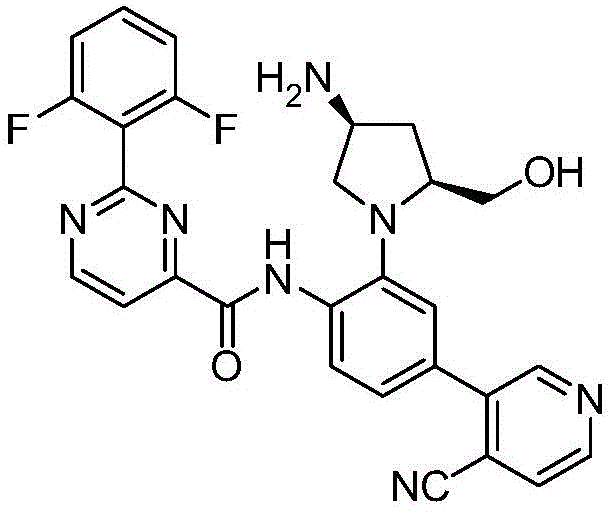
- XCAXLCSQKKQKHA-PMACEKPBSA-N N-[2-[(2S,4S)-4-amino-2-(hydroxymethyl)pyrrolidin-1-yl]-4-(4-cyanopyridin-3-yl)phenyl]-2-(2-fluoro-6-methoxyphenyl)pyrimidine-4-carboxamide Chemical compound N[C@H]1C[C@H](N(C1)C1=C(C=CC(=C1)C=1C=NC=CC=1C#N)NC(=O)C1=NC(=NC=C1)C1=C(C=CC=C1OC)F)CO XCAXLCSQKKQKHA-PMACEKPBSA-N 0.000 claims description 2
- SOVOQANEIZCLPU-SFTDATJTSA-N N-[2-[(2S,4S)-4-amino-2-(hydroxymethyl)pyrrolidin-1-yl]-4-(4-cyanopyridin-3-yl)phenyl]-2-(2-fluoro-6-methylphenyl)pyrimidine-4-carboxamide Chemical compound C(#N)C1=C(C2=CC=C(NC(=O)C3=CC=NC(=N3)C3=C(C)C=CC=C3F)C(N3[C@@H](C[C@H](N)C3)CO)=C2)C=NC=C1 SOVOQANEIZCLPU-SFTDATJTSA-N 0.000 claims description 2
- YAOFYZWYGQFFGQ-OALUTQOASA-N N-[2-[(2S,4S)-4-amino-2-(hydroxymethyl)pyrrolidin-1-yl]-4-(4-cyanopyridin-3-yl)phenyl]-2-(3,6-difluoro-2-methoxyphenyl)pyrimidine-4-carboxamide Chemical compound C1(C#N)=C(C2=CC=C(NC(=O)C3=CC=NC(=N3)C3=C(OC)C(F)=CC=C3F)C(N3C[C@@H](N)C[C@H]3CO)=C2)C=NC=C1 YAOFYZWYGQFFGQ-OALUTQOASA-N 0.000 claims description 2
- GNAQOVDYXBQJML-PMACEKPBSA-N N-[2-[(2S,4S)-4-amino-2-(hydroxymethyl)pyrrolidin-1-yl]-4-(4-cyanopyridin-3-yl)phenyl]-2-(3,6-difluoro-2-methylphenyl)pyrimidine-4-carboxamide Chemical compound C(#N)C1=C(C2=CC=C(NC(=O)C3=CC=NC(=N3)C3=C(C)C(F)=CC=C3F)C(N3[C@@H](C[C@H](N)C3)CO)=C2)C=NC=C1 GNAQOVDYXBQJML-PMACEKPBSA-N 0.000 claims description 2
- FMVORWLTJBNIRP-OALUTQOASA-N N-[2-[(2S,4S)-4-amino-2-(hydroxymethyl)pyrrolidin-1-yl]-4-(4-cyanopyridin-3-yl)phenyl]-2-[2-(difluoromethoxy)-6-fluorophenyl]pyrimidine-4-carboxamide Chemical compound N[C@H]1C[C@H](N(C1)C1=C(C=CC(=C1)C=1C=NC=CC=1C#N)NC(=O)C1=NC(=NC=C1)C1=C(C=CC=C1F)OC(F)F)CO FMVORWLTJBNIRP-OALUTQOASA-N 0.000 claims description 2
- LYYVVXSDOBKXQQ-GJZGRUSLSA-N N-[2-[(2S,4S)-4-amino-2-(hydroxymethyl)pyrrolidin-1-yl]-4-chlorophenyl]-2-(2-fluoro-6-methoxyphenyl)pyrimidine-4-carboxamide Chemical compound C1(=CC=C(C=C1N1[C@@H](C[C@H](N)C1)CO)Cl)NC(=O)C1=CC=NC(=N1)C1=C(OC)C=CC=C1F LYYVVXSDOBKXQQ-GJZGRUSLSA-N 0.000 claims description 2
- ATUJAUVLSRXUKR-GJZGRUSLSA-N N-[2-[(2S,4S)-4-amino-2-(hydroxymethyl)pyrrolidin-1-yl]-4-fluorophenyl]-2-(2-fluoro-6-methoxyphenyl)pyrimidine-4-carboxamide Chemical compound C1(=CC=C(C=C1N1[C@@H](C[C@H](N)C1)CO)F)NC(=O)C1=CC=NC(=N1)C1=C(OC)C=CC=C1F ATUJAUVLSRXUKR-GJZGRUSLSA-N 0.000 claims description 2
- NDNBINPLTHGVKS-KBPBESRZSA-N N-[2-[(2S,4S)-4-amino-2-(hydroxymethyl)pyrrolidin-1-yl]-5-fluorophenyl]-2-(2,3-difluoro-6-methoxyphenyl)pyrimidine-4-carboxamide Chemical compound C1=C(C=CC(=C1NC(=O)C1=CC=NC(=N1)C1=C(OC)C=CC(F)=C1F)N1C[C@@H](N)C[C@H]1CO)F NDNBINPLTHGVKS-KBPBESRZSA-N 0.000 claims description 2
- AJBJISUUCJXQBM-KBPBESRZSA-N N-[2-[(2S,4S)-4-amino-2-(hydroxymethyl)pyrrolidin-1-yl]-5-fluorophenyl]-2-(2,6-difluorophenyl)pyrimidine-4-carboxamide Chemical compound N[C@H]1C[C@H](N(C1)C1=C(C=C(C=C1)F)NC(=O)C1=NC(=NC=C1)C1=C(C=CC=C1F)F)CO AJBJISUUCJXQBM-KBPBESRZSA-N 0.000 claims description 2
- SUBYPZBREZXPCW-GJZGRUSLSA-N N-[2-[(2S,4S)-4-amino-2-(hydroxymethyl)pyrrolidin-1-yl]-5-fluorophenyl]-2-(2-fluoro-6-methoxyphenyl)pyrimidine-4-carboxamide Chemical compound N[C@H]1C[C@H](N(C1)C1=C(C=C(C=C1)F)NC(=O)C1=NC(=NC=C1)C1=C(C=CC=C1OC)F)CO SUBYPZBREZXPCW-GJZGRUSLSA-N 0.000 claims description 2
- VCJUDPLLCXBMCM-HOTGVXAUSA-N N-[2-[(2S,4S)-4-amino-2-(hydroxymethyl)pyrrolidin-1-yl]-5-fluorophenyl]-2-(3-cyano-2-fluoro-6-methoxyphenyl)pyrimidine-4-carboxamide Chemical compound N[C@H]1C[C@H](N(C1)C1=C(C=C(C=C1)F)NC(=O)C1=NC(=NC=C1)C1=C(C(=CC=C1OC)C#N)F)CO VCJUDPLLCXBMCM-HOTGVXAUSA-N 0.000 claims description 2
- FEHHLVAMJBTESK-GJZGRUSLSA-N N-[2-[(2S,4S)-4-amino-2-(hydroxymethyl)pyrrolidin-1-yl]phenyl]-2-(2-fluoro-6-methoxyphenyl)pyrimidine-4-carboxamide Chemical compound N[C@H]1C[C@H](N(C1)C1=C(C=CC=C1)NC(=O)C1=NC(=NC=C1)C1=C(C=CC=C1OC)F)CO FEHHLVAMJBTESK-GJZGRUSLSA-N 0.000 claims description 2
- ZXFVDANYDFDDRY-RXVVDRJESA-N N-[2-[(2S,4S)-4-amino-2-methylpiperidin-1-yl]-4-(4-cyanopyridin-3-yl)phenyl]-2-(2-fluoro-6-methoxyphenyl)pyrimidine-4-carboxamide Chemical compound N[C@@H]1C[C@@H](N(CC1)C1=C(C=CC(=C1)C=1C=NC=CC=1C#N)NC(=O)C1=NC(=NC=C1)C1=C(C=CC=C1OC)F)C ZXFVDANYDFDDRY-RXVVDRJESA-N 0.000 claims description 2
- QLSPHCRQKIJNFU-WRGVRERRSA-N N-[4-(4-cyanopyridin-3-yl)-2-[(1S,4S)-1-(hydroxymethyl)-2,5-diazabicyclo[2.2.1]heptan-2-yl]phenyl]-2-(2-fluoro-6-methoxyphenyl)pyrimidine-4-carboxamide Chemical compound C(#N)C1=C(C=NC=C1)C1=CC(=C(C=C1)NC(=O)C1=NC(=NC=C1)C1=C(C=CC=C1OC)F)N1[C@@]2(CN[C@H](C1)C2)CO QLSPHCRQKIJNFU-WRGVRERRSA-N 0.000 claims description 2
- SMOFRAIZAKBEKX-UHFFFAOYSA-N N-[4-(4-cyanopyridin-3-yl)-2-[3-(methoxymethyl)azetidin-1-yl]phenyl]-2-(2-fluoro-6-methoxyphenyl)pyrimidine-4-carboxamide Chemical compound C1=C(C=C(C(NC(=O)C2=CC=NC(=N2)C2=C(F)C=CC=C2OC)=C1)N1CC(COC)C1)C1=CN=CC=C1C#N SMOFRAIZAKBEKX-UHFFFAOYSA-N 0.000 claims description 2
- RFRULRQBRDHJSB-UHFFFAOYSA-N N-[4-(4-cyanopyridin-3-yl)-2-[4-(2-hydroxyethyl)piperazin-1-yl]phenyl]-2-(2-fluoro-6-methoxyphenyl)pyrimidine-4-carboxamide Chemical compound C1=C(C=C(C(=C1)NC(=O)C1=CC=NC(=N1)C1=C(F)C=CC=C1OC)N1CCN(CC1)CCO)C1=CN=CC=C1C#N RFRULRQBRDHJSB-UHFFFAOYSA-N 0.000 claims description 2
- JOXBUECBAXTYRH-ZFWWWQNUSA-N N-[5-fluoro-2-[(2S,4S)-4-hydroxy-2-methylpyrrolidin-1-yl]phenyl]-2-(2-fluoro-6-methoxyphenyl)pyrimidine-4-carboxamide Chemical compound C1=C(C=CC(=C1NC(=O)C1=CC=NC(=N1)C1=C(F)C=CC=C1OC)N1C[C@@H](O)C[C@@H]1C)F JOXBUECBAXTYRH-ZFWWWQNUSA-N 0.000 claims description 2
- 239000003937 drug carrier Substances 0.000 claims description 2
- 230000003993 interaction Effects 0.000 claims description 2
- 125000004184 methoxymethyl group Chemical group [H]C([H])([H])OC([H])([H])* 0.000 claims description 2
- DXASQZJWWGZNSF-UHFFFAOYSA-N n,n-dimethylmethanamine;sulfur trioxide Chemical group CN(C)C.O=S(=O)=O DXASQZJWWGZNSF-UHFFFAOYSA-N 0.000 claims description 2
- 239000008194 pharmaceutical composition Substances 0.000 claims description 2
- 239000000546 pharmaceutical excipient Substances 0.000 claims description 2
- 125000004482 piperidin-4-yl group Chemical group N1CCC(CC1)* 0.000 claims description 2
- 125000004214 1-pyrrolidinyl group Chemical group [H]C1([H])N(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 claims 1
- 108010002838 hematopoietic progenitor kinase 1 Proteins 0.000 abstract description 4
- 210000000481 breast Anatomy 0.000 abstract description 3
- 210000004072 lung Anatomy 0.000 abstract description 3
- 230000002611 ovarian Effects 0.000 abstract description 2
- 150000001721 carbon Chemical group 0.000 description 36
- 125000004043 oxo group Chemical group O=* 0.000 description 36
- 102000037982 Immune checkpoint proteins Human genes 0.000 description 18
- 108091008036 Immune checkpoint proteins Proteins 0.000 description 18
- 210000001744 T-lymphocyte Anatomy 0.000 description 16
- 229940126546 immune checkpoint molecule Drugs 0.000 description 15
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 13
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 13
- 239000000203 mixture Substances 0.000 description 12
- 238000006243 chemical reaction Methods 0.000 description 11
- 125000002950 monocyclic group Chemical group 0.000 description 10
- 208000009956 adenocarcinoma Diseases 0.000 description 9
- 125000003342 alkenyl group Chemical group 0.000 description 9
- 239000002904 solvent Substances 0.000 description 9
- 206010025323 Lymphomas Diseases 0.000 description 8
- 208000015914 Non-Hodgkin lymphomas Diseases 0.000 description 8
- 239000002253 acid Substances 0.000 description 8
- 230000001404 mediated effect Effects 0.000 description 8
- 206010041823 squamous cell carcinoma Diseases 0.000 description 8
- 229940045513 CTLA4 antagonist Drugs 0.000 description 7
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 7
- 108091008874 T cell receptors Proteins 0.000 description 7
- 102000016266 T-Cell Antigen Receptors Human genes 0.000 description 7
- 230000004913 activation Effects 0.000 description 7
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 7
- 239000003795 chemical substances by application Substances 0.000 description 7
- 125000004122 cyclic group Chemical group 0.000 description 7
- 239000001301 oxygen Substances 0.000 description 7
- 125000006413 ring segment Chemical group 0.000 description 7
- 239000011593 sulfur Substances 0.000 description 7
- 108010074708 B7-H1 Antigen Proteins 0.000 description 6
- 201000009030 Carcinoma Diseases 0.000 description 6
- 102100024216 Programmed cell death 1 ligand 1 Human genes 0.000 description 6
- 206010039491 Sarcoma Diseases 0.000 description 6
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 6
- 239000002585 base Substances 0.000 description 6
- 210000004027 cell Anatomy 0.000 description 6
- 201000001441 melanoma Diseases 0.000 description 6
- 230000037361 pathway Effects 0.000 description 6
- 125000006239 protecting group Chemical group 0.000 description 6
- 230000011664 signaling Effects 0.000 description 6
- 125000001544 thienyl group Chemical group 0.000 description 6
- 108091008875 B cell receptors Proteins 0.000 description 5
- 101000801234 Homo sapiens Tumor necrosis factor receptor superfamily member 18 Proteins 0.000 description 5
- 101000851370 Homo sapiens Tumor necrosis factor receptor superfamily member 9 Proteins 0.000 description 5
- 101710089372 Programmed cell death protein 1 Proteins 0.000 description 5
- 102100033728 Tumor necrosis factor receptor superfamily member 18 Human genes 0.000 description 5
- 102100022153 Tumor necrosis factor receptor superfamily member 4 Human genes 0.000 description 5
- 101710165473 Tumor necrosis factor receptor superfamily member 4 Proteins 0.000 description 5
- 102100036856 Tumor necrosis factor receptor superfamily member 9 Human genes 0.000 description 5
- 230000002950 deficient Effects 0.000 description 5
- 125000005647 linker group Chemical group 0.000 description 5
- 230000002503 metabolic effect Effects 0.000 description 5
- 230000007170 pathology Effects 0.000 description 5
- 108090000623 proteins and genes Proteins 0.000 description 5
- 102100022464 5'-nucleotidase Human genes 0.000 description 4
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 4
- 208000031261 Acute myeloid leukaemia Diseases 0.000 description 4
- 102100035634 B-cell linker protein Human genes 0.000 description 4
- 208000032791 BCR-ABL1 positive chronic myelogenous leukemia Diseases 0.000 description 4
- 208000018084 Bone neoplasm Diseases 0.000 description 4
- 108010021064 CTLA-4 Antigen Proteins 0.000 description 4
- 102100039498 Cytotoxic T-lymphocyte protein 4 Human genes 0.000 description 4
- YZCKVEUIGOORGS-OUBTZVSYSA-N Deuterium Chemical compound [2H] YZCKVEUIGOORGS-OUBTZVSYSA-N 0.000 description 4
- 102100034458 Hepatitis A virus cellular receptor 2 Human genes 0.000 description 4
- 101000678236 Homo sapiens 5'-nucleotidase Proteins 0.000 description 4
- 101000803266 Homo sapiens B-cell linker protein Proteins 0.000 description 4
- 101001068133 Homo sapiens Hepatitis A virus cellular receptor 2 Proteins 0.000 description 4
- 101001137987 Homo sapiens Lymphocyte activation gene 3 protein Proteins 0.000 description 4
- 101001090688 Homo sapiens Lymphocyte cytosolic protein 2 Proteins 0.000 description 4
- 102000017578 LAG3 Human genes 0.000 description 4
- 206010024612 Lipoma Diseases 0.000 description 4
- 102100034709 Lymphocyte cytosolic protein 2 Human genes 0.000 description 4
- 208000000453 Skin Neoplasms Diseases 0.000 description 4
- 210000003719 b-lymphocyte Anatomy 0.000 description 4
- 238000006880 cross-coupling reaction Methods 0.000 description 4
- 206010012818 diffuse large B-cell lymphoma Diseases 0.000 description 4
- 206010016629 fibroma Diseases 0.000 description 4
- 230000006870 function Effects 0.000 description 4
- 230000014509 gene expression Effects 0.000 description 4
- 125000004438 haloalkoxy group Chemical group 0.000 description 4
- 201000011066 hemangioma Diseases 0.000 description 4
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 4
- 230000036039 immunity Effects 0.000 description 4
- 238000011813 knockout mouse model Methods 0.000 description 4
- 201000008968 osteosarcoma Diseases 0.000 description 4
- 229910052763 palladium Inorganic materials 0.000 description 4
- 229960002621 pembrolizumab Drugs 0.000 description 4
- ZAHRKKWIAAJSAO-UHFFFAOYSA-N rapamycin Natural products COCC(O)C(=C/C(C)C(=O)CC(OC(=O)C1CCCCN1C(=O)C(=O)C2(O)OC(CC(OC)C(=CC=CC=CC(C)CC(C)C(=O)C)C)CCC2C)C(C)CC3CCC(O)C(C3)OC)C ZAHRKKWIAAJSAO-UHFFFAOYSA-N 0.000 description 4
- 102000005962 receptors Human genes 0.000 description 4
- 108020003175 receptors Proteins 0.000 description 4
- QFJCIRLUMZQUOT-HPLJOQBZSA-N sirolimus Chemical compound C1C[C@@H](O)[C@H](OC)C[C@@H]1C[C@@H](C)[C@H]1OC(=O)[C@@H]2CCCCN2C(=O)C(=O)[C@](O)(O2)[C@H](C)CC[C@H]2C[C@H](OC)/C(C)=C/C=C/C=C/[C@@H](C)C[C@@H](C)C(=O)[C@H](OC)[C@H](O)/C(C)=C/[C@@H](C)C(=O)C1 QFJCIRLUMZQUOT-HPLJOQBZSA-N 0.000 description 4
- 229960002930 sirolimus Drugs 0.000 description 4
- 238000003786 synthesis reaction Methods 0.000 description 4
- 238000002560 therapeutic procedure Methods 0.000 description 4
- 108010002164 tyrosine receptor Proteins 0.000 description 4
- 102100023990 60S ribosomal protein L17 Human genes 0.000 description 3
- 208000024893 Acute lymphoblastic leukemia Diseases 0.000 description 3
- 208000036762 Acute promyelocytic leukaemia Diseases 0.000 description 3
- 208000010839 B-cell chronic lymphocytic leukemia Diseases 0.000 description 3
- 206010005949 Bone cancer Diseases 0.000 description 3
- 208000010833 Chronic myeloid leukaemia Diseases 0.000 description 3
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 3
- 102100031968 Ephrin type-B receptor 2 Human genes 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 3
- 201000008808 Fibrosarcoma Diseases 0.000 description 3
- 208000032612 Glial tumor Diseases 0.000 description 3
- 206010018338 Glioma Diseases 0.000 description 3
- 208000002927 Hamartoma Diseases 0.000 description 3
- 208000017604 Hodgkin disease Diseases 0.000 description 3
- 208000010747 Hodgkins lymphoma Diseases 0.000 description 3
- 241000282414 Homo sapiens Species 0.000 description 3
- 101001037256 Homo sapiens Indoleamine 2,3-dioxygenase 1 Proteins 0.000 description 3
- 101000831007 Homo sapiens T-cell immunoreceptor with Ig and ITIM domains Proteins 0.000 description 3
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 3
- 229940076838 Immune checkpoint inhibitor Drugs 0.000 description 3
- 102100040061 Indoleamine 2,3-dioxygenase 1 Human genes 0.000 description 3
- 102000037984 Inhibitory immune checkpoint proteins Human genes 0.000 description 3
- 108091008026 Inhibitory immune checkpoint proteins Proteins 0.000 description 3
- 208000007766 Kaposi sarcoma Diseases 0.000 description 3
- 208000031671 Large B-Cell Diffuse Lymphoma Diseases 0.000 description 3
- 108091054455 MAP kinase family Proteins 0.000 description 3
- 102000043136 MAP kinase family Human genes 0.000 description 3
- 241001465754 Metazoa Species 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- 208000034578 Multiple myelomas Diseases 0.000 description 3
- 201000003793 Myelodysplastic syndrome Diseases 0.000 description 3
- 208000033761 Myelogenous Chronic BCR-ABL Positive Leukemia Diseases 0.000 description 3
- 208000033776 Myeloid Acute Leukemia Diseases 0.000 description 3
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 3
- 238000005481 NMR spectroscopy Methods 0.000 description 3
- 206010035226 Plasma cell myeloma Diseases 0.000 description 3
- 208000033826 Promyelocytic Acute Leukemia Diseases 0.000 description 3
- 102100024834 T-cell immunoreceptor with Ig and ITIM domains Human genes 0.000 description 3
- 206010043276 Teratoma Diseases 0.000 description 3
- 208000003721 Triple Negative Breast Neoplasms Diseases 0.000 description 3
- 208000002495 Uterine Neoplasms Diseases 0.000 description 3
- 102100033177 Vascular endothelial growth factor receptor 2 Human genes 0.000 description 3
- 239000000556 agonist Substances 0.000 description 3
- 230000005809 anti-tumor immunity Effects 0.000 description 3
- 125000002393 azetidinyl group Chemical group 0.000 description 3
- 125000002619 bicyclic group Chemical group 0.000 description 3
- 230000015572 biosynthetic process Effects 0.000 description 3
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 3
- 210000004443 dendritic cell Anatomy 0.000 description 3
- XEYBRNLFEZDVAW-ARSRFYASSA-N dinoprostone Chemical compound CCCCC[C@H](O)\C=C\[C@H]1[C@H](O)CC(=O)[C@@H]1C\C=C/CCCC(O)=O XEYBRNLFEZDVAW-ARSRFYASSA-N 0.000 description 3
- 229960002986 dinoprostone Drugs 0.000 description 3
- 239000002552 dosage form Substances 0.000 description 3
- 208000005017 glioblastoma Diseases 0.000 description 3
- 230000002489 hematologic effect Effects 0.000 description 3
- 125000000623 heterocyclic group Chemical group 0.000 description 3
- 150000002430 hydrocarbons Chemical group 0.000 description 3
- 239000001257 hydrogen Substances 0.000 description 3
- 210000002865 immune cell Anatomy 0.000 description 3
- 239000012274 immune-checkpoint protein inhibitor Substances 0.000 description 3
- 238000000338 in vitro Methods 0.000 description 3
- 238000001727 in vivo Methods 0.000 description 3
- 201000010260 leiomyoma Diseases 0.000 description 3
- 238000004519 manufacturing process Methods 0.000 description 3
- 229960003301 nivolumab Drugs 0.000 description 3
- 208000002154 non-small cell lung carcinoma Diseases 0.000 description 3
- 125000002971 oxazolyl group Chemical group 0.000 description 3
- 125000003367 polycyclic group Chemical group 0.000 description 3
- 239000012041 precatalyst Substances 0.000 description 3
- 238000002360 preparation method Methods 0.000 description 3
- 230000008569 process Effects 0.000 description 3
- XEYBRNLFEZDVAW-UHFFFAOYSA-N prostaglandin E2 Natural products CCCCCC(O)C=CC1C(O)CC(=O)C1CC=CCCCC(O)=O XEYBRNLFEZDVAW-UHFFFAOYSA-N 0.000 description 3
- 125000003226 pyrazolyl group Chemical group 0.000 description 3
- 230000001105 regulatory effect Effects 0.000 description 3
- 201000009410 rhabdomyosarcoma Diseases 0.000 description 3
- 230000019491 signal transduction Effects 0.000 description 3
- 239000007787 solid Substances 0.000 description 3
- 239000012453 solvate Substances 0.000 description 3
- 230000001225 therapeutic effect Effects 0.000 description 3
- 125000000335 thiazolyl group Chemical group 0.000 description 3
- 208000022679 triple-negative breast carcinoma Diseases 0.000 description 3
- 208000029729 tumor suppressor gene on chromosome 11 Diseases 0.000 description 3
- 206010046766 uterine cancer Diseases 0.000 description 3
- KWGRBVOPPLSCSI-WPRPVWTQSA-N (-)-ephedrine Chemical compound CN[C@@H](C)[C@H](O)C1=CC=CC=C1 KWGRBVOPPLSCSI-WPRPVWTQSA-N 0.000 description 2
- YPBKTZBXSBLTDK-PKNBQFBNSA-N (3e)-3-[(3-bromo-4-fluoroanilino)-nitrosomethylidene]-4-[2-(sulfamoylamino)ethylamino]-1,2,5-oxadiazole Chemical compound NS(=O)(=O)NCCNC1=NON\C1=C(N=O)/NC1=CC=C(F)C(Br)=C1 YPBKTZBXSBLTDK-PKNBQFBNSA-N 0.000 description 2
- NSPMIYGKQJPBQR-UHFFFAOYSA-N 4H-1,2,4-triazole Chemical compound C=1N=CNN=1 NSPMIYGKQJPBQR-UHFFFAOYSA-N 0.000 description 2
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 2
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonia chloride Chemical compound [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 2
- 201000003076 Angiosarcoma Diseases 0.000 description 2
- 102000004452 Arginase Human genes 0.000 description 2
- 108700024123 Arginases Proteins 0.000 description 2
- 102100029822 B- and T-lymphocyte attenuator Human genes 0.000 description 2
- 230000003844 B-cell-activation Effects 0.000 description 2
- 102100022005 B-lymphocyte antigen CD20 Human genes 0.000 description 2
- 208000011691 Burkitt lymphomas Diseases 0.000 description 2
- 102100027207 CD27 antigen Human genes 0.000 description 2
- 102100038078 CD276 antigen Human genes 0.000 description 2
- 101710185679 CD276 antigen Proteins 0.000 description 2
- 101150013553 CD40 gene Proteins 0.000 description 2
- 101150071146 COX2 gene Proteins 0.000 description 2
- 101100114534 Caenorhabditis elegans ctc-2 gene Proteins 0.000 description 2
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 2
- 206010007275 Carcinoid tumour Diseases 0.000 description 2
- ZEOWTGPWHLSLOG-UHFFFAOYSA-N Cc1ccc(cc1-c1ccc2c(n[nH]c2c1)-c1cnn(c1)C1CC1)C(=O)Nc1cccc(c1)C(F)(F)F Chemical compound Cc1ccc(cc1-c1ccc2c(n[nH]c2c1)-c1cnn(c1)C1CC1)C(=O)Nc1cccc(c1)C(F)(F)F ZEOWTGPWHLSLOG-UHFFFAOYSA-N 0.000 description 2
- 206010008342 Cervix carcinoma Diseases 0.000 description 2
- 201000005262 Chondroma Diseases 0.000 description 2
- 208000005243 Chondrosarcoma Diseases 0.000 description 2
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 2
- 102100029722 Ectonucleoside triphosphate diphosphohydrolase 1 Human genes 0.000 description 2
- 201000009051 Embryonal Carcinoma Diseases 0.000 description 2
- 206010014733 Endometrial cancer Diseases 0.000 description 2
- 206010014759 Endometrial neoplasm Diseases 0.000 description 2
- 102000004190 Enzymes Human genes 0.000 description 2
- 108090000790 Enzymes Proteins 0.000 description 2
- 208000000461 Esophageal Neoplasms Diseases 0.000 description 2
- HKVAMNSJSFKALM-GKUWKFKPSA-N Everolimus Chemical compound C1C[C@@H](OCCO)[C@H](OC)C[C@@H]1C[C@@H](C)[C@H]1OC(=O)[C@@H]2CCCCN2C(=O)C(=O)[C@](O)(O2)[C@H](C)CC[C@H]2C[C@H](OC)/C(C)=C/C=C/C=C/[C@@H](C)C[C@@H](C)C(=O)[C@H](OC)[C@H](O)/C(C)=C/[C@@H](C)C(=O)C1 HKVAMNSJSFKALM-GKUWKFKPSA-N 0.000 description 2
- 208000006168 Ewing Sarcoma Diseases 0.000 description 2
- 102100023593 Fibroblast growth factor receptor 1 Human genes 0.000 description 2
- 101710182386 Fibroblast growth factor receptor 1 Proteins 0.000 description 2
- 102100023600 Fibroblast growth factor receptor 2 Human genes 0.000 description 2
- 101710182389 Fibroblast growth factor receptor 2 Proteins 0.000 description 2
- 102100027842 Fibroblast growth factor receptor 3 Human genes 0.000 description 2
- 101710182396 Fibroblast growth factor receptor 3 Proteins 0.000 description 2
- 102100027844 Fibroblast growth factor receptor 4 Human genes 0.000 description 2
- 108091007911 GSKs Proteins 0.000 description 2
- 102000038624 GSKs Human genes 0.000 description 2
- 206010017993 Gastrointestinal neoplasms Diseases 0.000 description 2
- 208000001258 Hemangiosarcoma Diseases 0.000 description 2
- 208000021519 Hodgkin lymphoma Diseases 0.000 description 2
- 241000282412 Homo Species 0.000 description 2
- 101000864344 Homo sapiens B- and T-lymphocyte attenuator Proteins 0.000 description 2
- 101000897405 Homo sapiens B-lymphocyte antigen CD20 Proteins 0.000 description 2
- 101000914511 Homo sapiens CD27 antigen Proteins 0.000 description 2
- 101001012447 Homo sapiens Ectonucleoside triphosphate diphosphohydrolase 1 Proteins 0.000 description 2
- 101000917134 Homo sapiens Fibroblast growth factor receptor 4 Proteins 0.000 description 2
- 101000916644 Homo sapiens Macrophage colony-stimulating factor 1 receptor Proteins 0.000 description 2
- 101000573441 Homo sapiens Misshapen-like kinase 1 Proteins 0.000 description 2
- 101001059984 Homo sapiens Mitogen-activated protein kinase kinase kinase kinase 4 Proteins 0.000 description 2
- 101001059982 Homo sapiens Mitogen-activated protein kinase kinase kinase kinase 5 Proteins 0.000 description 2
- 101000914514 Homo sapiens T-cell-specific surface glycoprotein CD28 Proteins 0.000 description 2
- 101000666896 Homo sapiens V-type immunoglobulin domain-containing suppressor of T-cell activation Proteins 0.000 description 2
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 2
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 2
- 208000008839 Kidney Neoplasms Diseases 0.000 description 2
- 239000002177 L01XE27 - Ibrutinib Substances 0.000 description 2
- 208000018142 Leiomyosarcoma Diseases 0.000 description 2
- 208000031422 Lymphocytic Chronic B-Cell Leukemia Diseases 0.000 description 2
- 102100028198 Macrophage colony-stimulating factor 1 receptor Human genes 0.000 description 2
- 208000025205 Mantle-Cell Lymphoma Diseases 0.000 description 2
- 206010027476 Metastases Diseases 0.000 description 2
- 102100026287 Misshapen-like kinase 1 Human genes 0.000 description 2
- 102100028192 Mitogen-activated protein kinase kinase kinase kinase 2 Human genes 0.000 description 2
- 102100028193 Mitogen-activated protein kinase kinase kinase kinase 3 Human genes 0.000 description 2
- 102100028194 Mitogen-activated protein kinase kinase kinase kinase 4 Human genes 0.000 description 2
- 102100028195 Mitogen-activated protein kinase kinase kinase kinase 5 Human genes 0.000 description 2
- YNAVUWVOSKDBBP-UHFFFAOYSA-N Morpholine Chemical compound C1COCCN1 YNAVUWVOSKDBBP-UHFFFAOYSA-N 0.000 description 2
- 241000699670 Mus sp. Species 0.000 description 2
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 2
- LRHPLDYGYMQRHN-UHFFFAOYSA-N N-Butanol Chemical compound CCCCO LRHPLDYGYMQRHN-UHFFFAOYSA-N 0.000 description 2
- 125000000815 N-oxide group Chemical group 0.000 description 2
- 150000001204 N-oxides Chemical class 0.000 description 2
- 201000004404 Neurofibroma Diseases 0.000 description 2
- 102000004473 OX40 Ligand Human genes 0.000 description 2
- 108010042215 OX40 Ligand Proteins 0.000 description 2
- 206010030155 Oesophageal carcinoma Diseases 0.000 description 2
- 102000038030 PI3Ks Human genes 0.000 description 2
- 108091007960 PI3Ks Proteins 0.000 description 2
- 101150000187 PTGS2 gene Proteins 0.000 description 2
- 108091000080 Phosphotransferase Proteins 0.000 description 2
- 208000006664 Precursor Cell Lymphoblastic Leukemia-Lymphoma Diseases 0.000 description 2
- 206010038389 Renal cancer Diseases 0.000 description 2
- 102100023085 Serine/threonine-protein kinase mTOR Human genes 0.000 description 2
- 206010041067 Small cell lung cancer Diseases 0.000 description 2
- 208000005718 Stomach Neoplasms Diseases 0.000 description 2
- 230000006044 T cell activation Effects 0.000 description 2
- 230000006052 T cell proliferation Effects 0.000 description 2
- 102100027213 T-cell-specific surface glycoprotein CD28 Human genes 0.000 description 2
- 108010065917 TOR Serine-Threonine Kinases Proteins 0.000 description 2
- CBPNZQVSJQDFBE-FUXHJELOSA-N Temsirolimus Chemical compound C1C[C@@H](OC(=O)C(C)(CO)CO)[C@H](OC)C[C@@H]1C[C@@H](C)[C@H]1OC(=O)[C@@H]2CCCCN2C(=O)C(=O)[C@](O)(O2)[C@H](C)CC[C@H]2C[C@H](OC)/C(C)=C/C=C/C=C/[C@@H](C)C[C@@H](C)C(=O)[C@H](OC)[C@H](O)/C(C)=C/[C@@H](C)C(=O)C1 CBPNZQVSJQDFBE-FUXHJELOSA-N 0.000 description 2
- 208000024313 Testicular Neoplasms Diseases 0.000 description 2
- 206010057644 Testis cancer Diseases 0.000 description 2
- 102100040653 Tryptophan 2,3-dioxygenase Human genes 0.000 description 2
- 102100040245 Tumor necrosis factor receptor superfamily member 5 Human genes 0.000 description 2
- 208000006105 Uterine Cervical Neoplasms Diseases 0.000 description 2
- 108010079206 V-Set Domain-Containing T-Cell Activation Inhibitor 1 Proteins 0.000 description 2
- 102100038929 V-set domain-containing T-cell activation inhibitor 1 Human genes 0.000 description 2
- 102100038282 V-type immunoglobulin domain-containing suppressor of T-cell activation Human genes 0.000 description 2
- 108010053099 Vascular Endothelial Growth Factor Receptor-2 Proteins 0.000 description 2
- 208000008383 Wilms tumor Diseases 0.000 description 2
- 230000002378 acidificating effect Effects 0.000 description 2
- 208000017733 acquired polycythemia vera Diseases 0.000 description 2
- OIRDTQYFTABQOQ-KQYNXXCUSA-N adenosine Chemical compound C1=NC=2C(N)=NC=NC=2N1[C@@H]1O[C@H](CO)[C@@H](O)[C@H]1O OIRDTQYFTABQOQ-KQYNXXCUSA-N 0.000 description 2
- 239000002671 adjuvant Substances 0.000 description 2
- 150000001335 aliphatic alkanes Chemical class 0.000 description 2
- 150000001336 alkenes Chemical class 0.000 description 2
- 150000001412 amines Chemical class 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- 125000005605 benzo group Chemical group 0.000 description 2
- 239000011203 carbon fibre reinforced carbon Substances 0.000 description 2
- 208000002458 carcinoid tumor Diseases 0.000 description 2
- 239000003054 catalyst Substances 0.000 description 2
- 238000006555 catalytic reaction Methods 0.000 description 2
- 210000003169 central nervous system Anatomy 0.000 description 2
- 201000010881 cervical cancer Diseases 0.000 description 2
- 125000003636 chemical group Chemical group 0.000 description 2
- 230000001684 chronic effect Effects 0.000 description 2
- 208000009060 clear cell adenocarcinoma Diseases 0.000 description 2
- 210000001072 colon Anatomy 0.000 description 2
- 208000029742 colonic neoplasm Diseases 0.000 description 2
- 238000010168 coupling process Methods 0.000 description 2
- 238000005859 coupling reaction Methods 0.000 description 2
- 208000035250 cutaneous malignant susceptibility to 1 melanoma Diseases 0.000 description 2
- 125000004093 cyano group Chemical group *C#N 0.000 description 2
- 229960002465 dabrafenib Drugs 0.000 description 2
- BFSMGDJOXZAERB-UHFFFAOYSA-N dabrafenib Chemical compound S1C(C(C)(C)C)=NC(C=2C(=C(NS(=O)(=O)C=3C(=CC=CC=3F)F)C=CC=2)F)=C1C1=CC=NC(N)=N1 BFSMGDJOXZAERB-UHFFFAOYSA-N 0.000 description 2
- 230000001419 dependent effect Effects 0.000 description 2
- 238000010511 deprotection reaction Methods 0.000 description 2
- 125000004431 deuterium atom Chemical group 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 230000003828 downregulation Effects 0.000 description 2
- 229950009791 durvalumab Drugs 0.000 description 2
- 229940088598 enzyme Drugs 0.000 description 2
- 239000002532 enzyme inhibitor Substances 0.000 description 2
- 229950006370 epacadostat Drugs 0.000 description 2
- 201000004101 esophageal cancer Diseases 0.000 description 2
- 229960005167 everolimus Drugs 0.000 description 2
- 230000001747 exhibiting effect Effects 0.000 description 2
- 125000001153 fluoro group Chemical group F* 0.000 description 2
- IJJVMEJXYNJXOJ-UHFFFAOYSA-N fluquinconazole Chemical compound C=1C=C(Cl)C=C(Cl)C=1N1C(=O)C2=CC(F)=CC=C2N=C1N1C=NC=N1 IJJVMEJXYNJXOJ-UHFFFAOYSA-N 0.000 description 2
- 201000003444 follicular lymphoma Diseases 0.000 description 2
- 238000010575 fractional recrystallization Methods 0.000 description 2
- 125000002541 furyl group Chemical group 0.000 description 2
- 108020001507 fusion proteins Proteins 0.000 description 2
- 102000037865 fusion proteins Human genes 0.000 description 2
- 206010017758 gastric cancer Diseases 0.000 description 2
- 229910052736 halogen Inorganic materials 0.000 description 2
- 201000010536 head and neck cancer Diseases 0.000 description 2
- 208000014829 head and neck neoplasm Diseases 0.000 description 2
- 201000005787 hematologic cancer Diseases 0.000 description 2
- 210000003958 hematopoietic stem cell Anatomy 0.000 description 2
- 206010073071 hepatocellular carcinoma Diseases 0.000 description 2
- 150000004677 hydrates Chemical class 0.000 description 2
- 229960001507 ibrutinib Drugs 0.000 description 2
- XYFPWWZEPKGCCK-GOSISDBHSA-N ibrutinib Chemical compound C1=2C(N)=NC=NC=2N([C@H]2CN(CCC2)C(=O)C=C)N=C1C(C=C1)=CC=C1OC1=CC=CC=C1 XYFPWWZEPKGCCK-GOSISDBHSA-N 0.000 description 2
- 125000002883 imidazolyl group Chemical group 0.000 description 2
- 239000000543 intermediate Substances 0.000 description 2
- 229960005386 ipilimumab Drugs 0.000 description 2
- 125000000904 isoindolyl group Chemical group C=1(NC=C2C=CC=CC12)* 0.000 description 2
- 125000000842 isoxazolyl group Chemical group 0.000 description 2
- 201000010982 kidney cancer Diseases 0.000 description 2
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 2
- 208000032839 leukemia Diseases 0.000 description 2
- 208000014018 liver neoplasm Diseases 0.000 description 2
- 239000000463 material Substances 0.000 description 2
- 206010027191 meningioma Diseases 0.000 description 2
- 230000009401 metastasis Effects 0.000 description 2
- 150000007522 mineralic acids Chemical class 0.000 description 2
- 206010028537 myelofibrosis Diseases 0.000 description 2
- 125000001624 naphthyl group Chemical group 0.000 description 2
- 201000011682 nervous system cancer Diseases 0.000 description 2
- 231100000252 nontoxic Toxicity 0.000 description 2
- 230000003000 nontoxic effect Effects 0.000 description 2
- 229960003347 obinutuzumab Drugs 0.000 description 2
- 150000007524 organic acids Chemical class 0.000 description 2
- 230000002018 overexpression Effects 0.000 description 2
- 125000004430 oxygen atom Chemical group O* 0.000 description 2
- 229960005184 panobinostat Drugs 0.000 description 2
- FWZRWHZDXBDTFK-ZHACJKMWSA-N panobinostat Chemical compound CC1=NC2=CC=C[CH]C2=C1CCNCC1=CC=C(\C=C\C(=O)NO)C=C1 FWZRWHZDXBDTFK-ZHACJKMWSA-N 0.000 description 2
- 102000020233 phosphotransferase Human genes 0.000 description 2
- 125000004193 piperazinyl group Chemical group 0.000 description 2
- 208000037244 polycythemia vera Diseases 0.000 description 2
- 208000003476 primary myelofibrosis Diseases 0.000 description 2
- 239000000047 product Substances 0.000 description 2
- 210000002307 prostate Anatomy 0.000 description 2
- 102000004169 proteins and genes Human genes 0.000 description 2
- 125000003373 pyrazinyl group Chemical group 0.000 description 2
- 125000002098 pyridazinyl group Chemical group 0.000 description 2
- 125000000714 pyrimidinyl group Chemical group 0.000 description 2
- 125000000719 pyrrolidinyl group Chemical group 0.000 description 2
- 125000000168 pyrrolyl group Chemical group 0.000 description 2
- 108091006082 receptor inhibitors Proteins 0.000 description 2
- 230000009467 reduction Effects 0.000 description 2
- 210000003289 regulatory T cell Anatomy 0.000 description 2
- 229960004641 rituximab Drugs 0.000 description 2
- 238000000926 separation method Methods 0.000 description 2
- 208000007056 sickle cell anemia Diseases 0.000 description 2
- 201000000849 skin cancer Diseases 0.000 description 2
- 208000000587 small cell lung carcinoma Diseases 0.000 description 2
- 229950007213 spartalizumab Drugs 0.000 description 2
- 239000007858 starting material Substances 0.000 description 2
- 201000011549 stomach cancer Diseases 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- 125000004434 sulfur atom Chemical group 0.000 description 2
- 230000004083 survival effect Effects 0.000 description 2
- 208000024891 symptom Diseases 0.000 description 2
- 201000000596 systemic lupus erythematosus Diseases 0.000 description 2
- 229960000235 temsirolimus Drugs 0.000 description 2
- QFJCIRLUMZQUOT-UHFFFAOYSA-N temsirolimus Natural products C1CC(O)C(OC)CC1CC(C)C1OC(=O)C2CCCCN2C(=O)C(=O)C(O)(O2)C(C)CCC2CC(OC)C(C)=CC=CC=CC(C)CC(C)C(=O)C(OC)C(O)C(C)=CC(C)C(=O)C1 QFJCIRLUMZQUOT-UHFFFAOYSA-N 0.000 description 2
- 201000003120 testicular cancer Diseases 0.000 description 2
- CXWXQJXEFPUFDZ-UHFFFAOYSA-N tetralin Chemical compound C1=CC=C2CCCCC2=C1 CXWXQJXEFPUFDZ-UHFFFAOYSA-N 0.000 description 2
- 238000004809 thin layer chromatography Methods 0.000 description 2
- 125000000101 thioether group Chemical group 0.000 description 2
- 210000001519 tissue Anatomy 0.000 description 2
- 231100000419 toxicity Toxicity 0.000 description 2
- 230000001988 toxicity Effects 0.000 description 2
- 229960004066 trametinib Drugs 0.000 description 2
- LIRYPHYGHXZJBZ-UHFFFAOYSA-N trametinib Chemical compound CC(=O)NC1=CC=CC(N2C(N(C3CC3)C(=O)C3=C(NC=4C(=CC(I)=CC=4)F)N(C)C(=O)C(C)=C32)=O)=C1 LIRYPHYGHXZJBZ-UHFFFAOYSA-N 0.000 description 2
- 206010044412 transitional cell carcinoma Diseases 0.000 description 2
- 229950007217 tremelimumab Drugs 0.000 description 2
- 229960003862 vemurafenib Drugs 0.000 description 2
- GPXBXXGIAQBQNI-UHFFFAOYSA-N vemurafenib Chemical compound CCCS(=O)(=O)NC1=CC=C(F)C(C(=O)C=2C3=CC(=CN=C3NC=2)C=2C=CC(Cl)=CC=2)=C1F GPXBXXGIAQBQNI-UHFFFAOYSA-N 0.000 description 2
- WAEXFXRVDQXREF-UHFFFAOYSA-N vorinostat Chemical compound ONC(=O)CCCCCCC(=O)NC1=CC=CC=C1 WAEXFXRVDQXREF-UHFFFAOYSA-N 0.000 description 2
- 229960000237 vorinostat Drugs 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 2
- 229910001868 water Inorganic materials 0.000 description 2
- UGOMMVLRQDMAQQ-UHFFFAOYSA-N xphos Chemical compound CC(C)C1=CC(C(C)C)=CC(C(C)C)=C1C1=CC=CC=C1P(C1CCCCC1)C1CCCCC1 UGOMMVLRQDMAQQ-UHFFFAOYSA-N 0.000 description 2
- XYLPKCDRAAYATL-OAHLLOKOSA-N (11S)-7-(3,5-dimethyl-1,2-oxazol-4-yl)-11-pyridin-2-yl-9-oxa-1,3-diazatricyclo[6.3.1.04,12]dodeca-4(12),5,7-trien-2-one Chemical compound CC1=NOC(C)=C1C1=CC=C2C3=C1OC[C@H](C=1N=CC=CC=1)N3C(=O)N2 XYLPKCDRAAYATL-OAHLLOKOSA-N 0.000 description 1
- FMCGSUUBYTWNDP-ONGXEEELSA-N (1R,2S)-2-(dimethylamino)-1-phenyl-1-propanol Chemical compound CN(C)[C@@H](C)[C@H](O)C1=CC=CC=C1 FMCGSUUBYTWNDP-ONGXEEELSA-N 0.000 description 1
- QBYIENPQHBMVBV-HFEGYEGKSA-N (2R)-2-hydroxy-2-phenylacetic acid Chemical compound O[C@@H](C(O)=O)c1ccccc1.O[C@@H](C(O)=O)c1ccccc1 QBYIENPQHBMVBV-HFEGYEGKSA-N 0.000 description 1
- DNISEZBAYYIQFB-PHDIDXHHSA-N (2r,3r)-2,3-diacetyloxybutanedioic acid Chemical compound CC(=O)O[C@@H](C(O)=O)[C@H](C(O)=O)OC(C)=O DNISEZBAYYIQFB-PHDIDXHHSA-N 0.000 description 1
- KCOYQXZDFIIGCY-CZIZESTLSA-N (3e)-4-amino-5-fluoro-3-[5-(4-methylpiperazin-1-yl)-1,3-dihydrobenzimidazol-2-ylidene]quinolin-2-one Chemical compound C1CN(C)CCN1C1=CC=C(N\C(N2)=C/3C(=C4C(F)=CC=CC4=NC\3=O)N)C2=C1 KCOYQXZDFIIGCY-CZIZESTLSA-N 0.000 description 1
- KPJDVVCDVBFRMU-AREMUKBSSA-N (6r)-6-(2-fluorophenyl)-n-[3-[2-(2-methoxyethylamino)ethyl]phenyl]-5,6-dihydrobenzo[h]quinazolin-2-amine Chemical compound COCCNCCC1=CC=CC(NC=2N=C3C4=CC=CC=C4[C@H](C=4C(=CC=CC=4)F)CC3=CN=2)=C1 KPJDVVCDVBFRMU-AREMUKBSSA-N 0.000 description 1
- 125000006700 (C1-C6) alkylthio group Chemical group 0.000 description 1
- BJEPYKJPYRNKOW-REOHCLBHSA-N (S)-malic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O BJEPYKJPYRNKOW-REOHCLBHSA-N 0.000 description 1
- 125000005919 1,2,2-trimethylpropyl group Chemical group 0.000 description 1
- 125000004502 1,2,3-oxadiazolyl group Chemical group 0.000 description 1
- 125000004511 1,2,3-thiadiazolyl group Chemical group 0.000 description 1
- 125000001399 1,2,3-triazolyl group Chemical group N1N=NC(=C1)* 0.000 description 1
- 125000004504 1,2,4-oxadiazolyl group Chemical group 0.000 description 1
- 125000004514 1,2,4-thiadiazolyl group Chemical group 0.000 description 1
- 125000001376 1,2,4-triazolyl group Chemical group N1N=C(N=C1)* 0.000 description 1
- MMWRGWQTAMNAFC-UHFFFAOYSA-N 1,2-dihydropyridine Chemical group C1NC=CC=C1 MMWRGWQTAMNAFC-UHFFFAOYSA-N 0.000 description 1
- 125000001781 1,3,4-oxadiazolyl group Chemical group 0.000 description 1
- 125000004520 1,3,4-thiadiazolyl group Chemical group 0.000 description 1
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 1
- KEIPNCCJPRMIAX-HNNXBMFYSA-N 1-[(3s)-3-[4-amino-3-[2-(3,5-dimethoxyphenyl)ethynyl]pyrazolo[3,4-d]pyrimidin-1-yl]pyrrolidin-1-yl]prop-2-en-1-one Chemical compound COC1=CC(OC)=CC(C#CC=2C3=C(N)N=CN=C3N([C@@H]3CN(CC3)C(=O)C=C)N=2)=C1 KEIPNCCJPRMIAX-HNNXBMFYSA-N 0.000 description 1
- RQEUFEKYXDPUSK-UHFFFAOYSA-N 1-phenylethylamine Chemical compound CC(N)C1=CC=CC=C1 RQEUFEKYXDPUSK-UHFFFAOYSA-N 0.000 description 1
- QWENRTYMTSOGBR-UHFFFAOYSA-N 1H-1,2,3-Triazole Chemical compound C=1C=NNN=1 QWENRTYMTSOGBR-UHFFFAOYSA-N 0.000 description 1
- RAXXELZNTBOGNW-UHFFFAOYSA-N 1H-imidazole Chemical class C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 1
- KGRVJHAUYBGFFP-UHFFFAOYSA-N 2,2'-Methylenebis(4-methyl-6-tert-butylphenol) Chemical compound CC(C)(C)C1=CC(C)=CC(CC=2C(=C(C=C(C)C=2)C(C)(C)C)O)=C1O KGRVJHAUYBGFFP-UHFFFAOYSA-N 0.000 description 1
- SSNMISUJOQAFRR-UHFFFAOYSA-N 2,6-naphthyridine Chemical compound N1=CC=C2C=NC=CC2=C1 SSNMISUJOQAFRR-UHFFFAOYSA-N 0.000 description 1
- UZYQSNQJLWTICD-UHFFFAOYSA-N 2-(n-benzoylanilino)-2,2-dinitroacetic acid Chemical compound C=1C=CC=CC=1N(C(C(=O)O)([N+]([O-])=O)[N+]([O-])=O)C(=O)C1=CC=CC=C1 UZYQSNQJLWTICD-UHFFFAOYSA-N 0.000 description 1
- LXMGXMQQJNULPR-NTISSMGPSA-N 2-[(4S)-6-(4-chlorophenyl)-1-methyl-4H-[1,2]oxazolo[5,4-d][2]benzazepin-4-yl]acetamide hydrate Chemical compound O.Cc1noc2[C@H](CC(N)=O)N=C(c3ccc(Cl)cc3)c3ccccc3-c12 LXMGXMQQJNULPR-NTISSMGPSA-N 0.000 description 1
- KTBSXLIQKWEBRB-UHFFFAOYSA-N 2-[1-[1-[3-fluoro-2-(trifluoromethyl)pyridine-4-carbonyl]piperidin-4-yl]-3-[4-(7h-pyrrolo[2,3-d]pyrimidin-4-yl)pyrazol-1-yl]azetidin-3-yl]acetonitrile Chemical compound C1=CN=C(C(F)(F)F)C(F)=C1C(=O)N1CCC(N2CC(CC#N)(C2)N2N=CC(=C2)C=2C=3C=CNC=3N=CN=2)CC1 KTBSXLIQKWEBRB-UHFFFAOYSA-N 0.000 description 1
- KMGUEILFFWDGFV-UHFFFAOYSA-N 2-benzoyl-2-benzoyloxy-3-hydroxybutanedioic acid Chemical compound C=1C=CC=CC=1C(=O)C(C(C(O)=O)O)(C(O)=O)OC(=O)C1=CC=CC=C1 KMGUEILFFWDGFV-UHFFFAOYSA-N 0.000 description 1
- LIOLIMKSCNQPLV-UHFFFAOYSA-N 2-fluoro-n-methyl-4-[7-(quinolin-6-ylmethyl)imidazo[1,2-b][1,2,4]triazin-2-yl]benzamide Chemical compound C1=C(F)C(C(=O)NC)=CC=C1C1=NN2C(CC=3C=C4C=CC=NC4=CC=3)=CN=C2N=C1 LIOLIMKSCNQPLV-UHFFFAOYSA-N 0.000 description 1
- 125000004493 2-methylbut-1-yl group Chemical group CC(C*)CC 0.000 description 1
- VHMICKWLTGFITH-UHFFFAOYSA-N 2H-isoindole Chemical class C1=CC=CC2=CNC=C21 VHMICKWLTGFITH-UHFFFAOYSA-N 0.000 description 1
- HCDMJFOHIXMBOV-UHFFFAOYSA-N 3-(2,6-difluoro-3,5-dimethoxyphenyl)-1-ethyl-8-(morpholin-4-ylmethyl)-4,7-dihydropyrrolo[4,5]pyrido[1,2-d]pyrimidin-2-one Chemical compound C=1C2=C3N(CC)C(=O)N(C=4C(=C(OC)C=C(OC)C=4F)F)CC3=CN=C2NC=1CN1CCOCC1 HCDMJFOHIXMBOV-UHFFFAOYSA-N 0.000 description 1
- MXKLDYKORJEOPR-UHFFFAOYSA-N 3-(5-fluoro-1h-indol-3-yl)pyrrolidine-2,5-dione Chemical compound C12=CC(F)=CC=C2NC=C1C1CC(=O)NC1=O MXKLDYKORJEOPR-UHFFFAOYSA-N 0.000 description 1
- 125000006163 5-membered heteroaryl group Chemical group 0.000 description 1
- GOZMBJCYMQQACI-UHFFFAOYSA-N 6,7-dimethyl-3-[[methyl-[2-[methyl-[[1-[3-(trifluoromethyl)phenyl]indol-3-yl]methyl]amino]ethyl]amino]methyl]chromen-4-one;dihydrochloride Chemical compound Cl.Cl.C=1OC2=CC(C)=C(C)C=C2C(=O)C=1CN(C)CCN(C)CC(C1=CC=CC=C11)=CN1C1=CC=CC(C(F)(F)F)=C1 GOZMBJCYMQQACI-UHFFFAOYSA-N 0.000 description 1
- GNMUEVRJHCWKTO-FQEVSTJZSA-N 6h-thieno[3,2-f][1,2,4]triazolo[4,3-a][1,4]diazepine-6-acetamide, 4-(4-chlorophenyl)-n-(4-hydroxyphenyl)-2,3,9-trimethyl-, (6s)- Chemical compound C([C@@H]1N=C(C2=C(N3C(C)=NN=C31)SC(=C2C)C)C=1C=CC(Cl)=CC=1)C(=O)NC1=CC=C(O)C=C1 GNMUEVRJHCWKTO-FQEVSTJZSA-N 0.000 description 1
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 1
- 101150107888 AKT2 gene Proteins 0.000 description 1
- VRQMAABPASPXMW-HDICACEKSA-N AZD4547 Chemical compound COC1=CC(OC)=CC(CCC=2NN=C(NC(=O)C=3C=CC(=CC=3)N3C[C@@H](C)N[C@@H](C)C3)C=2)=C1 VRQMAABPASPXMW-HDICACEKSA-N 0.000 description 1
- 206010000830 Acute leukaemia Diseases 0.000 description 1
- 208000014697 Acute lymphocytic leukaemia Diseases 0.000 description 1
- 206010001233 Adenoma benign Diseases 0.000 description 1
- 101150051155 Akt3 gene Proteins 0.000 description 1
- 229940080328 Arginase inhibitor Drugs 0.000 description 1
- 206010003571 Astrocytoma Diseases 0.000 description 1
- 208000032116 Autoimmune Experimental Encephalomyelitis Diseases 0.000 description 1
- 208000023275 Autoimmune disease Diseases 0.000 description 1
- 102100035080 BDNF/NT-3 growth factors receptor Human genes 0.000 description 1
- QADPYRIHXKWUSV-UHFFFAOYSA-N BGJ-398 Chemical compound C1CN(CC)CCN1C(C=C1)=CC=C1NC1=CC(N(C)C(=O)NC=2C(=C(OC)C=C(OC)C=2Cl)Cl)=NC=N1 QADPYRIHXKWUSV-UHFFFAOYSA-N 0.000 description 1
- 229940125565 BMS-986016 Drugs 0.000 description 1
- 101000840545 Bacillus thuringiensis L-isoleucine-4-hydroxylase Proteins 0.000 description 1
- 206010004146 Basal cell carcinoma Diseases 0.000 description 1
- 102000015735 Beta-catenin Human genes 0.000 description 1
- 108060000903 Beta-catenin Proteins 0.000 description 1
- 206010005969 Bone giant cell tumour Diseases 0.000 description 1
- 206010073106 Bone giant cell tumour malignant Diseases 0.000 description 1
- 241000283690 Bos taurus Species 0.000 description 1
- 108700031361 Brachyury Proteins 0.000 description 1
- 208000003174 Brain Neoplasms Diseases 0.000 description 1
- 206010006143 Brain stem glioma Diseases 0.000 description 1
- 102000001805 Bromodomains Human genes 0.000 description 1
- 108050009021 Bromodomains Proteins 0.000 description 1
- 206010006417 Bronchial carcinoma Diseases 0.000 description 1
- 239000002126 C01EB10 - Adenosine Substances 0.000 description 1
- 108091007914 CDKs Proteins 0.000 description 1
- 101100322915 Caenorhabditis elegans akt-1 gene Proteins 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- 208000009458 Carcinoma in Situ Diseases 0.000 description 1
- 208000017897 Carcinoma of esophagus Diseases 0.000 description 1
- 206010007953 Central nervous system lymphoma Diseases 0.000 description 1
- 206010008263 Cervical dysplasia Diseases 0.000 description 1
- 201000009047 Chordoma Diseases 0.000 description 1
- 208000006332 Choriocarcinoma Diseases 0.000 description 1
- 206010048832 Colon adenoma Diseases 0.000 description 1
- 206010010356 Congenital anomaly Diseases 0.000 description 1
- 108090000266 Cyclin-dependent kinases Proteins 0.000 description 1
- 102000003903 Cyclin-dependent kinases Human genes 0.000 description 1
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 1
- 241000527994 Cyclotella gamma Species 0.000 description 1
- 102000004127 Cytokines Human genes 0.000 description 1
- 108090000695 Cytokines Proteins 0.000 description 1
- 101100481408 Danio rerio tie2 gene Proteins 0.000 description 1
- RWSOTUBLDIXVET-UHFFFAOYSA-N Dihydrogen sulfide Chemical compound S RWSOTUBLDIXVET-UHFFFAOYSA-N 0.000 description 1
- 206010059866 Drug resistance Diseases 0.000 description 1
- 208000007033 Dysgerminoma Diseases 0.000 description 1
- 208000000471 Dysplastic Nevus Syndrome Diseases 0.000 description 1
- CUDVHEFYRIWYQD-UHFFFAOYSA-N E-3810 free base Chemical compound C=1C=C2C(C(=O)NC)=CC=CC2=CC=1OC(C1=CC=2OC)=CC=NC1=CC=2OCC1(N)CC1 CUDVHEFYRIWYQD-UHFFFAOYSA-N 0.000 description 1
- 206010014967 Ependymoma Diseases 0.000 description 1
- 108010055196 EphA2 Receptor Proteins 0.000 description 1
- 108010055191 EphA3 Receptor Proteins 0.000 description 1
- 108010055334 EphB2 Receptor Proteins 0.000 description 1
- 102100030322 Ephrin type-A receptor 1 Human genes 0.000 description 1
- 102100030340 Ephrin type-A receptor 2 Human genes 0.000 description 1
- 102100030324 Ephrin type-A receptor 3 Human genes 0.000 description 1
- 102100031983 Ephrin type-B receptor 4 Human genes 0.000 description 1
- 241000283086 Equidae Species 0.000 description 1
- 208000032027 Essential Thrombocythemia Diseases 0.000 description 1
- 108010007457 Extracellular Signal-Regulated MAP Kinases Proteins 0.000 description 1
- 108091008794 FGF receptors Proteins 0.000 description 1
- 101150009958 FLT4 gene Proteins 0.000 description 1
- JNCMHMUGTWEVOZ-UHFFFAOYSA-N F[CH]F Chemical compound F[CH]F JNCMHMUGTWEVOZ-UHFFFAOYSA-N 0.000 description 1
- 201000001342 Fallopian tube cancer Diseases 0.000 description 1
- 208000013452 Fallopian tube neoplasm Diseases 0.000 description 1
- 241000282326 Felis catus Species 0.000 description 1
- 208000007659 Fibroadenoma Diseases 0.000 description 1
- 206010053717 Fibrous histiocytoma Diseases 0.000 description 1
- 201000010915 Glioblastoma multiforme Diseases 0.000 description 1
- 206010018404 Glucagonoma Diseases 0.000 description 1
- 101710155270 Glycerate 2-kinase Proteins 0.000 description 1
- 244000060234 Gmelina philippensis Species 0.000 description 1
- 206010018691 Granuloma Diseases 0.000 description 1
- 239000007821 HATU Substances 0.000 description 1
- 102100034051 Heat shock protein HSP 90-alpha Human genes 0.000 description 1
- 206010019629 Hepatic adenoma Diseases 0.000 description 1
- 102100035108 High affinity nerve growth factor receptor Human genes 0.000 description 1
- 108090000353 Histone deacetylase Proteins 0.000 description 1
- 102100038720 Histone deacetylase 9 Human genes 0.000 description 1
- 101000596896 Homo sapiens BDNF/NT-3 growth factors receptor Proteins 0.000 description 1
- 101000938354 Homo sapiens Ephrin type-A receptor 1 Proteins 0.000 description 1
- 101001016865 Homo sapiens Heat shock protein HSP 90-alpha Proteins 0.000 description 1
- 101000596894 Homo sapiens High affinity nerve growth factor receptor Proteins 0.000 description 1
- 101001055145 Homo sapiens Interleukin-2 receptor subunit beta Proteins 0.000 description 1
- 101000868279 Homo sapiens Leukocyte surface antigen CD47 Proteins 0.000 description 1
- 101001138062 Homo sapiens Leukocyte-associated immunoglobulin-like receptor 1 Proteins 0.000 description 1
- 101001059990 Homo sapiens Mitogen-activated protein kinase kinase kinase kinase 2 Proteins 0.000 description 1
- 101001059989 Homo sapiens Mitogen-activated protein kinase kinase kinase kinase 3 Proteins 0.000 description 1
- 101001012157 Homo sapiens Receptor tyrosine-protein kinase erbB-2 Proteins 0.000 description 1
- 101000932478 Homo sapiens Receptor-type tyrosine-protein kinase FLT3 Proteins 0.000 description 1
- 101000596234 Homo sapiens T-cell surface protein tactile Proteins 0.000 description 1
- 101000914484 Homo sapiens T-lymphocyte activation antigen CD80 Proteins 0.000 description 1
- 101000997835 Homo sapiens Tyrosine-protein kinase JAK1 Proteins 0.000 description 1
- 101000997832 Homo sapiens Tyrosine-protein kinase JAK2 Proteins 0.000 description 1
- 101000818543 Homo sapiens Tyrosine-protein kinase ZAP-70 Proteins 0.000 description 1
- 229940043367 IDO1 inhibitor Drugs 0.000 description 1
- 238000004566 IR spectroscopy Methods 0.000 description 1
- 108010002350 Interleukin-2 Proteins 0.000 description 1
- 102000000588 Interleukin-2 Human genes 0.000 description 1
- 102100026879 Interleukin-2 receptor subunit beta Human genes 0.000 description 1
- 102000042838 JAK family Human genes 0.000 description 1
- 108091082332 JAK family Proteins 0.000 description 1
- 230000004163 JAK-STAT signaling pathway Effects 0.000 description 1
- 229940122245 Janus kinase inhibitor Drugs 0.000 description 1
- 102000002698 KIR Receptors Human genes 0.000 description 1
- 108010043610 KIR Receptors Proteins 0.000 description 1
- 208000002260 Keloid Diseases 0.000 description 1
- 206010023330 Keloid scar Diseases 0.000 description 1
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 description 1
- 239000002144 L01XE18 - Ruxolitinib Substances 0.000 description 1
- 206010023825 Laryngeal cancer Diseases 0.000 description 1
- 102100032913 Leukocyte surface antigen CD47 Human genes 0.000 description 1
- 102100020943 Leukocyte-associated immunoglobulin-like receptor 1 Human genes 0.000 description 1
- 208000002404 Liver Cell Adenoma Diseases 0.000 description 1
- 102000001291 MAP Kinase Kinase Kinase Human genes 0.000 description 1
- 108060006687 MAP kinase kinase kinase Proteins 0.000 description 1
- 208000006644 Malignant Fibrous Histiocytoma Diseases 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 208000000172 Medulloblastoma Diseases 0.000 description 1
- 208000015021 Meningeal Neoplasms Diseases 0.000 description 1
- 206010027406 Mesothelioma Diseases 0.000 description 1
- 206010027480 Metastatic malignant melanoma Diseases 0.000 description 1
- 101710144533 Mitogen-activated protein kinase kinase kinase kinase 2 Proteins 0.000 description 1
- 101710144521 Mitogen-activated protein kinase kinase kinase kinase 3 Proteins 0.000 description 1
- 108010006519 Molecular Chaperones Proteins 0.000 description 1
- 208000003445 Mouth Neoplasms Diseases 0.000 description 1
- 101100120552 Mus musculus Foxp3 gene Proteins 0.000 description 1
- 101100407308 Mus musculus Pdcd1lg2 gene Proteins 0.000 description 1
- 101100481410 Mus musculus Tek gene Proteins 0.000 description 1
- 208000014767 Myeloproliferative disease Diseases 0.000 description 1
- FMCGSUUBYTWNDP-UHFFFAOYSA-N N-Methylephedrine Natural products CN(C)C(C)C(O)C1=CC=CC=C1 FMCGSUUBYTWNDP-UHFFFAOYSA-N 0.000 description 1
- ADUXEIHMPHRMBP-HOTGVXAUSA-N N-[2-[(2S,4S)-4-amino-2-(hydroxymethyl)pyrrolidin-1-yl]-5-methylphenyl]-2-(2-fluoro-6-methoxyphenyl)pyrimidine-4-carboxamide Chemical compound C1(=CC(=CC=C1N1C[C@@H](N)C[C@H]1CO)C)NC(=O)C1=CC=NC(=N1)C1=C(F)C=CC=C1OC ADUXEIHMPHRMBP-HOTGVXAUSA-N 0.000 description 1
- 102100029166 NT-3 growth factor receptor Human genes 0.000 description 1
- 101150117329 NTRK3 gene Proteins 0.000 description 1
- 208000001894 Nasopharyngeal Neoplasms Diseases 0.000 description 1
- 206010061306 Nasopharyngeal cancer Diseases 0.000 description 1
- 238000006411 Negishi coupling reaction Methods 0.000 description 1
- 206010029113 Neovascularisation Diseases 0.000 description 1
- 241000772415 Neovison vison Species 0.000 description 1
- 206010029260 Neuroblastoma Diseases 0.000 description 1
- 102000014736 Notch Human genes 0.000 description 1
- 108010070047 Notch Receptors Proteins 0.000 description 1
- YGACXVRLDHEXKY-WXRXAMBDSA-N O[C@H](C[C@H]1c2c(cccc2F)-c2cncn12)[C@H]1CC[C@H](O)CC1 Chemical compound O[C@H](C[C@H]1c2c(cccc2F)-c2cncn12)[C@H]1CC[C@H](O)CC1 YGACXVRLDHEXKY-WXRXAMBDSA-N 0.000 description 1
- 201000010133 Oligodendroglioma Diseases 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 208000010191 Osteitis Deformans Diseases 0.000 description 1
- 208000027067 Paget disease of bone Diseases 0.000 description 1
- 208000000821 Parathyroid Neoplasms Diseases 0.000 description 1
- 229910002666 PdCl2 Inorganic materials 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 1
- 102000014750 Phosphorylase Kinase Human genes 0.000 description 1
- 108010064071 Phosphorylase Kinase Proteins 0.000 description 1
- 208000007641 Pinealoma Diseases 0.000 description 1
- 208000007913 Pituitary Neoplasms Diseases 0.000 description 1
- 201000005746 Pituitary adenoma Diseases 0.000 description 1
- 206010061538 Pituitary tumour benign Diseases 0.000 description 1
- 229920000776 Poly(Adenosine diphosphate-ribose) polymerase Polymers 0.000 description 1
- 241000288906 Primates Species 0.000 description 1
- 108700030875 Programmed Cell Death 1 Ligand 2 Proteins 0.000 description 1
- 102100024213 Programmed cell death 1 ligand 2 Human genes 0.000 description 1
- 102100038280 Prostaglandin G/H synthase 2 Human genes 0.000 description 1
- 108050003267 Prostaglandin G/H synthase 2 Proteins 0.000 description 1
- 206010060862 Prostate cancer Diseases 0.000 description 1
- 208000000236 Prostatic Neoplasms Diseases 0.000 description 1
- 102000001253 Protein Kinase Human genes 0.000 description 1
- 201000001263 Psoriatic Arthritis Diseases 0.000 description 1
- 208000036824 Psoriatic arthropathy Diseases 0.000 description 1
- WTKZEGDFNFYCGP-UHFFFAOYSA-N Pyrazole Chemical class C=1C=NNC=1 WTKZEGDFNFYCGP-UHFFFAOYSA-N 0.000 description 1
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical group C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 1
- IWYDHOAUDWTVEP-UHFFFAOYSA-N R-2-phenyl-2-hydroxyacetic acid Natural products OC(=O)C(O)C1=CC=CC=C1 IWYDHOAUDWTVEP-UHFFFAOYSA-N 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- 102100030086 Receptor tyrosine-protein kinase erbB-2 Human genes 0.000 description 1
- 101710100969 Receptor tyrosine-protein kinase erbB-3 Proteins 0.000 description 1
- 102100029986 Receptor tyrosine-protein kinase erbB-3 Human genes 0.000 description 1
- 102100029981 Receptor tyrosine-protein kinase erbB-4 Human genes 0.000 description 1
- 101710100963 Receptor tyrosine-protein kinase erbB-4 Proteins 0.000 description 1
- 102100020718 Receptor-type tyrosine-protein kinase FLT3 Human genes 0.000 description 1
- 208000015634 Rectal Neoplasms Diseases 0.000 description 1
- 201000000582 Retinoblastoma Diseases 0.000 description 1
- 208000005678 Rhabdomyoma Diseases 0.000 description 1
- 241000283984 Rodentia Species 0.000 description 1
- 101001037255 Saccharomyces cerevisiae (strain ATCC 204508 / S288c) Indoleamine 2,3-dioxygenase Proteins 0.000 description 1
- 201000010208 Seminoma Diseases 0.000 description 1
- 208000000097 Sertoli-Leydig cell tumor Diseases 0.000 description 1
- 206010054184 Small intestine carcinoma Diseases 0.000 description 1
- 208000021712 Soft tissue sarcoma Diseases 0.000 description 1
- 241000282887 Suidae Species 0.000 description 1
- 101100215487 Sus scrofa ADRA2A gene Proteins 0.000 description 1
- 238000006069 Suzuki reaction reaction Methods 0.000 description 1
- 230000005867 T cell response Effects 0.000 description 1
- 208000031673 T-Cell Cutaneous Lymphoma Diseases 0.000 description 1
- 206010042971 T-cell lymphoma Diseases 0.000 description 1
- 208000027585 T-cell non-Hodgkin lymphoma Diseases 0.000 description 1
- 102100035268 T-cell surface protein tactile Human genes 0.000 description 1
- 102100027222 T-lymphocyte activation antigen CD80 Human genes 0.000 description 1
- 229940125828 TAS-120 Drugs 0.000 description 1
- 108091005735 TGF-beta receptors Proteins 0.000 description 1
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 1
- 208000024770 Thyroid neoplasm Diseases 0.000 description 1
- 102000016715 Transforming Growth Factor beta Receptors Human genes 0.000 description 1
- 102000009618 Transforming Growth Factors Human genes 0.000 description 1
- 108010009583 Transforming Growth Factors Proteins 0.000 description 1
- YZCKVEUIGOORGS-NJFSPNSNSA-N Tritium Chemical compound [3H] YZCKVEUIGOORGS-NJFSPNSNSA-N 0.000 description 1
- 101710136122 Tryptophan 2,3-dioxygenase Proteins 0.000 description 1
- 102000014384 Type C Phospholipases Human genes 0.000 description 1
- 108010079194 Type C Phospholipases Proteins 0.000 description 1
- 102100033438 Tyrosine-protein kinase JAK1 Human genes 0.000 description 1
- 102100033444 Tyrosine-protein kinase JAK2 Human genes 0.000 description 1
- 102100021125 Tyrosine-protein kinase ZAP-70 Human genes 0.000 description 1
- 208000015778 Undifferentiated pleomorphic sarcoma Diseases 0.000 description 1
- 208000007097 Urinary Bladder Neoplasms Diseases 0.000 description 1
- 208000006593 Urologic Neoplasms Diseases 0.000 description 1
- 206010046798 Uterine leiomyoma Diseases 0.000 description 1
- 108091008605 VEGF receptors Proteins 0.000 description 1
- 201000003761 Vaginal carcinoma Diseases 0.000 description 1
- 108010053096 Vascular Endothelial Growth Factor Receptor-1 Proteins 0.000 description 1
- 102000016663 Vascular Endothelial Growth Factor Receptor-3 Human genes 0.000 description 1
- 102100033178 Vascular endothelial growth factor receptor 1 Human genes 0.000 description 1
- 206010047741 Vulval cancer Diseases 0.000 description 1
- 208000004354 Vulvar Neoplasms Diseases 0.000 description 1
- 208000033559 Waldenström macroglobulinemia Diseases 0.000 description 1
- 206010048214 Xanthoma Diseases 0.000 description 1
- 206010048215 Xanthomatosis Diseases 0.000 description 1
- BEMNJULZEQTDJY-UHFFFAOYSA-N [5-amino-1-(2-methyl-3h-benzimidazol-5-yl)pyrazol-4-yl]-(1h-indol-2-yl)methanone Chemical compound C1=CC=C2NC(C(=O)C=3C=NN(C=3N)C=3C=C4N=C(NC4=CC=3)C)=CC2=C1 BEMNJULZEQTDJY-UHFFFAOYSA-N 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 230000001154 acute effect Effects 0.000 description 1
- 102000035181 adaptor proteins Human genes 0.000 description 1
- 108091005764 adaptor proteins Proteins 0.000 description 1
- 208000002718 adenomatoid tumor Diseases 0.000 description 1
- 229960005305 adenosine Drugs 0.000 description 1
- 229940121359 adenosine receptor antagonist Drugs 0.000 description 1
- 201000005179 adrenal carcinoma Diseases 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 239000003513 alkali Substances 0.000 description 1
- 125000004450 alkenylene group Chemical group 0.000 description 1
- 150000001345 alkine derivatives Chemical class 0.000 description 1
- 125000004414 alkyl thio group Chemical group 0.000 description 1
- 208000026935 allergic disease Diseases 0.000 description 1
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 1
- BJEPYKJPYRNKOW-UHFFFAOYSA-N alpha-hydroxysuccinic acid Natural products OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 1
- 238000010976 amide bond formation reaction Methods 0.000 description 1
- 229910021529 ammonia Inorganic materials 0.000 description 1
- 235000019270 ammonium chloride Nutrition 0.000 description 1
- 229940124691 antibody therapeutics Drugs 0.000 description 1
- 125000002029 aromatic hydrocarbon group Chemical group 0.000 description 1
- 150000004945 aromatic hydrocarbons Chemical group 0.000 description 1
- 125000000732 arylene group Chemical group 0.000 description 1
- 239000010425 asbestos Substances 0.000 description 1
- 238000003556 assay Methods 0.000 description 1
- 230000005784 autoimmunity Effects 0.000 description 1
- ZSIQJIWKELUFRJ-UHFFFAOYSA-N azepane Chemical compound C1CCCNCC1 ZSIQJIWKELUFRJ-UHFFFAOYSA-N 0.000 description 1
- 125000004567 azetidin-3-yl group Chemical group N1CC(C1)* 0.000 description 1
- 125000003943 azolyl group Chemical group 0.000 description 1
- 229950000971 baricitinib Drugs 0.000 description 1
- XUZMWHLSFXCVMG-UHFFFAOYSA-N baricitinib Chemical compound C1N(S(=O)(=O)CC)CC1(CC#N)N1N=CC(C=2C=3C=CNC=3N=CN=2)=C1 XUZMWHLSFXCVMG-UHFFFAOYSA-N 0.000 description 1
- 208000001119 benign fibrous histiocytoma Diseases 0.000 description 1
- 125000004603 benzisoxazolyl group Chemical group O1N=C(C2=C1C=CC=C2)* 0.000 description 1
- 125000000499 benzofuranyl group Chemical group O1C(=CC2=C1C=CC=C2)* 0.000 description 1
- 125000004196 benzothienyl group Chemical group S1C(=CC2=C1C=CC=C2)* 0.000 description 1
- 201000009036 biliary tract cancer Diseases 0.000 description 1
- 208000020790 biliary tract neoplasm Diseases 0.000 description 1
- 230000031018 biological processes and functions Effects 0.000 description 1
- 229950000080 birabresib Drugs 0.000 description 1
- 210000003969 blast cell Anatomy 0.000 description 1
- 238000009835 boiling Methods 0.000 description 1
- 208000016738 bone Paget disease Diseases 0.000 description 1
- 201000011143 bone giant cell tumor Diseases 0.000 description 1
- 210000001185 bone marrow Anatomy 0.000 description 1
- 201000009480 botryoid rhabdomyosarcoma Diseases 0.000 description 1
- 201000003149 breast fibroadenoma Diseases 0.000 description 1
- 125000001246 bromo group Chemical group Br* 0.000 description 1
- 208000003362 bronchogenic carcinoma Diseases 0.000 description 1
- 201000002143 bronchus adenoma Diseases 0.000 description 1
- 230000003185 calcium uptake Effects 0.000 description 1
- MIOPJNTWMNEORI-UHFFFAOYSA-N camphorsulfonic acid Chemical class C1CC2(CS(O)(=O)=O)C(=O)CC1C2(C)C MIOPJNTWMNEORI-UHFFFAOYSA-N 0.000 description 1
- 125000002837 carbocyclic group Chemical group 0.000 description 1
- 150000001720 carbohydrates Chemical class 0.000 description 1
- 235000014633 carbohydrates Nutrition 0.000 description 1
- 150000001735 carboxylic acids Chemical class 0.000 description 1
- 208000022033 carcinoma of urethra Diseases 0.000 description 1
- 230000015556 catabolic process Effects 0.000 description 1
- 230000020411 cell activation Effects 0.000 description 1
- 230000006369 cell cycle progression Effects 0.000 description 1
- 230000010261 cell growth Effects 0.000 description 1
- 208000019065 cervical carcinoma Diseases 0.000 description 1
- PIQCTGMSNWUMAF-UHFFFAOYSA-N chembl522892 Chemical compound C1CN(C)CCN1C1=CC=C(NC(=N2)C=3C(NC4=CC=CC(F)=C4C=3N)=O)C2=C1 PIQCTGMSNWUMAF-UHFFFAOYSA-N 0.000 description 1
- 239000003638 chemical reducing agent Substances 0.000 description 1
- 125000001309 chloro group Chemical group Cl* 0.000 description 1
- 208000006990 cholangiocarcinoma Diseases 0.000 description 1
- 201000005217 chondroblastoma Diseases 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- 208000024207 chronic leukemia Diseases 0.000 description 1
- 208000032852 chronic lymphocytic leukemia Diseases 0.000 description 1
- 229960002271 cobimetinib Drugs 0.000 description 1
- BSMCAPRUBJMWDF-KRWDZBQOSA-N cobimetinib Chemical compound C1C(O)([C@H]2NCCCC2)CN1C(=O)C1=CC=C(F)C(F)=C1NC1=CC=C(I)C=C1F BSMCAPRUBJMWDF-KRWDZBQOSA-N 0.000 description 1
- 238000002648 combination therapy Methods 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 230000001276 controlling effect Effects 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 201000007241 cutaneous T cell lymphoma Diseases 0.000 description 1
- 201000010305 cutaneous fibrous histiocytoma Diseases 0.000 description 1
- 125000002993 cycloalkylene group Chemical group 0.000 description 1
- 125000002188 cycloheptatrienyl group Chemical group C1(=CC=CC=CC1)* 0.000 description 1
- 125000000582 cycloheptyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000003678 cyclohexadienyl group Chemical group C1(=CC=CCC1)* 0.000 description 1
- SSJXIUAHEKJCMH-UHFFFAOYSA-N cyclohexane-1,2-diamine Chemical compound NC1CCCCC1N SSJXIUAHEKJCMH-UHFFFAOYSA-N 0.000 description 1
- 125000000596 cyclohexenyl group Chemical group C1(=CCCCC1)* 0.000 description 1
- 125000002433 cyclopentenyl group Chemical group C1(=CCCC1)* 0.000 description 1
- KWGRBVOPPLSCSI-UHFFFAOYSA-N d-ephedrine Natural products CNC(C)C(O)C1=CC=CC=C1 KWGRBVOPPLSCSI-UHFFFAOYSA-N 0.000 description 1
- 238000006731 degradation reaction Methods 0.000 description 1
- 150000001975 deuterium Chemical group 0.000 description 1
- ZJULYDCRWUEPTK-UHFFFAOYSA-N dichloromethyl Chemical compound Cl[CH]Cl ZJULYDCRWUEPTK-UHFFFAOYSA-N 0.000 description 1
- DLNKOYKMWOXYQA-UHFFFAOYSA-N dl-pseudophenylpropanolamine Natural products CC(N)C(O)C1=CC=CC=C1 DLNKOYKMWOXYQA-UHFFFAOYSA-N 0.000 description 1
- 229950005778 dovitinib Drugs 0.000 description 1
- 239000003814 drug Substances 0.000 description 1
- 239000003596 drug target Substances 0.000 description 1
- 210000003162 effector t lymphocyte Anatomy 0.000 description 1
- 229940056913 eftilagimod alfa Drugs 0.000 description 1
- 238000010828 elution Methods 0.000 description 1
- 239000012156 elution solvent Substances 0.000 description 1
- 201000009409 embryonal rhabdomyosarcoma Diseases 0.000 description 1
- 201000002491 encephalomyelitis Diseases 0.000 description 1
- 210000000750 endocrine system Anatomy 0.000 description 1
- 201000003914 endometrial carcinoma Diseases 0.000 description 1
- 230000002357 endometrial effect Effects 0.000 description 1
- 230000002708 enhancing effect Effects 0.000 description 1
- 230000002255 enzymatic effect Effects 0.000 description 1
- 229940125532 enzyme inhibitor Drugs 0.000 description 1
- 229960002179 ephedrine Drugs 0.000 description 1
- 102000052116 epidermal growth factor receptor activity proteins Human genes 0.000 description 1
- 108700015053 epidermal growth factor receptor activity proteins Proteins 0.000 description 1
- 229950004444 erdafitinib Drugs 0.000 description 1
- 235000019439 ethyl acetate Nutrition 0.000 description 1
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 1
- 208000012997 experimental autoimmune encephalomyelitis Diseases 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 201000001343 fallopian tube carcinoma Diseases 0.000 description 1
- 230000008713 feedback mechanism Effects 0.000 description 1
- 102000052178 fibroblast growth factor receptor activity proteins Human genes 0.000 description 1
- 125000003709 fluoroalkyl group Chemical group 0.000 description 1
- VUWZPRWSIVNGKG-UHFFFAOYSA-N fluoromethane Chemical compound F[CH2] VUWZPRWSIVNGKG-UHFFFAOYSA-N 0.000 description 1
- 238000001640 fractional crystallisation Methods 0.000 description 1
- 238000007710 freezing Methods 0.000 description 1
- 230000008014 freezing Effects 0.000 description 1
- 230000002496 gastric effect Effects 0.000 description 1
- 208000015419 gastrin-producing neuroendocrine tumor Diseases 0.000 description 1
- 201000000052 gastrinoma Diseases 0.000 description 1
- 230000012010 growth Effects 0.000 description 1
- 230000003394 haemopoietic effect Effects 0.000 description 1
- 150000002367 halogens Chemical class 0.000 description 1
- 210000003128 head Anatomy 0.000 description 1
- 208000024200 hematopoietic and lymphoid system neoplasm Diseases 0.000 description 1
- 230000002440 hepatic effect Effects 0.000 description 1
- 208000006359 hepatoblastoma Diseases 0.000 description 1
- 201000002735 hepatocellular adenoma Diseases 0.000 description 1
- 231100000844 hepatocellular carcinoma Toxicity 0.000 description 1
- DMEGYFMYUHOHGS-UHFFFAOYSA-N heptamethylene Natural products C1CCCCCC1 DMEGYFMYUHOHGS-UHFFFAOYSA-N 0.000 description 1
- 125000003187 heptyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 238000004128 high performance liquid chromatography Methods 0.000 description 1
- 210000003630 histaminocyte Anatomy 0.000 description 1
- 229940088597 hormone Drugs 0.000 description 1
- 239000005556 hormone Substances 0.000 description 1
- 229940121569 ieramilimab Drugs 0.000 description 1
- 230000028993 immune response Effects 0.000 description 1
- 230000003053 immunization Effects 0.000 description 1
- 238000002649 immunization Methods 0.000 description 1
- 201000004933 in situ carcinoma Diseases 0.000 description 1
- 125000001041 indolyl group Chemical group 0.000 description 1
- 230000006698 induction Effects 0.000 description 1
- 206010022498 insulinoma Diseases 0.000 description 1
- 230000004073 interleukin-2 production Effects 0.000 description 1
- 210000002570 interstitial cell Anatomy 0.000 description 1
- 201000010985 invasive ductal carcinoma Diseases 0.000 description 1
- 125000002346 iodo group Chemical group I* 0.000 description 1
- 229910052742 iron Inorganic materials 0.000 description 1
- 230000007794 irritation Effects 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000000555 isopropenyl group Chemical group [H]\C([H])=C(\*)C([H])([H])[H] 0.000 description 1
- 125000003253 isopropoxy group Chemical group [H]C([H])([H])C([H])(O*)C([H])([H])[H] 0.000 description 1
- 125000002183 isoquinolinyl group Chemical group C1(=NC=CC2=CC=CC=C12)* 0.000 description 1
- 125000001786 isothiazolyl group Chemical group 0.000 description 1
- 210000001117 keloid Anatomy 0.000 description 1
- 208000022013 kidney Wilms tumor Diseases 0.000 description 1
- 239000004310 lactic acid Substances 0.000 description 1
- 235000014655 lactic acid Nutrition 0.000 description 1
- 201000011061 large intestine cancer Diseases 0.000 description 1
- 206010023841 laryngeal neoplasm Diseases 0.000 description 1
- KRTIYQIPSAGSBP-KLAILNCOSA-N linrodostat Chemical compound C1(CCC(CC1)C1=C2C=C(F)C=CC2=NC=C1)[C@@H](C)C(=O)NC1=CC=C(Cl)C=C1 KRTIYQIPSAGSBP-KLAILNCOSA-N 0.000 description 1
- 208000012987 lip and oral cavity carcinoma Diseases 0.000 description 1
- 206010024627 liposarcoma Diseases 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 229950004231 lucitanib Drugs 0.000 description 1
- 201000011649 lymphoblastic lymphoma Diseases 0.000 description 1
- 208000025036 lymphosarcoma Diseases 0.000 description 1
- 201000000564 macroglobulinemia Diseases 0.000 description 1
- 210000002540 macrophage Anatomy 0.000 description 1
- 239000001630 malic acid Substances 0.000 description 1
- 235000011090 malic acid Nutrition 0.000 description 1
- 230000036210 malignancy Effects 0.000 description 1
- 201000004593 malignant giant cell tumor Diseases 0.000 description 1
- 208000020984 malignant renal pelvis neoplasm Diseases 0.000 description 1
- 201000000289 malignant teratoma Diseases 0.000 description 1
- 208000022006 malignant tumor of meninges Diseases 0.000 description 1
- 208000026045 malignant tumor of parathyroid gland Diseases 0.000 description 1
- 229960002510 mandelic acid Drugs 0.000 description 1
- 238000004949 mass spectrometry Methods 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 210000000716 merkel cell Anatomy 0.000 description 1
- LVWZTYCIRDMTEY-UHFFFAOYSA-N metamizole Chemical compound O=C1C(N(CS(O)(=O)=O)C)=C(C)N(C)N1C1=CC=CC=C1 LVWZTYCIRDMTEY-UHFFFAOYSA-N 0.000 description 1
- 208000021039 metastatic melanoma Diseases 0.000 description 1
- 230000005012 migration Effects 0.000 description 1
- 238000013508 migration Methods 0.000 description 1
- 125000002757 morpholinyl group Chemical group 0.000 description 1
- 208000010492 mucinous cystadenocarcinoma Diseases 0.000 description 1
- 201000005962 mycosis fungoides Diseases 0.000 description 1
- 208000009091 myxoma Diseases 0.000 description 1
- OLAHOMJCDNXHFI-UHFFFAOYSA-N n'-(3,5-dimethoxyphenyl)-n'-[3-(1-methylpyrazol-4-yl)quinoxalin-6-yl]-n-propan-2-ylethane-1,2-diamine Chemical compound COC1=CC(OC)=CC(N(CCNC(C)C)C=2C=C3N=C(C=NC3=CC=2)C2=CN(C)N=C2)=C1 OLAHOMJCDNXHFI-UHFFFAOYSA-N 0.000 description 1
- PTORCEYGCGXHDH-OVMXCRKPSA-N n-[(7r)-4-[(3r,4r,5s)-3-amino-4-hydroxy-5-methylpiperidin-1-yl]-7-hydroxy-6,7-dihydro-5h-cyclopenta[b]pyridin-3-yl]-6-(2,6-difluorophenyl)-5-fluoropyridine-2-carboxamide Chemical compound C1[C@@H](N)[C@H](O)[C@@H](C)CN1C1=C(CC[C@H]2O)C2=NC=C1NC(=O)C1=CC=C(F)C(C=2C(=CC=CC=2F)F)=N1 PTORCEYGCGXHDH-OVMXCRKPSA-N 0.000 description 1
- YOHYSYJDKVYCJI-UHFFFAOYSA-N n-[3-[[6-[3-(trifluoromethyl)anilino]pyrimidin-4-yl]amino]phenyl]cyclopropanecarboxamide Chemical compound FC(F)(F)C1=CC=CC(NC=2N=CN=C(NC=3C=C(NC(=O)C4CC4)C=CC=3)C=2)=C1 YOHYSYJDKVYCJI-UHFFFAOYSA-N 0.000 description 1
- SYSQUGFVNFXIIT-UHFFFAOYSA-N n-[4-(1,3-benzoxazol-2-yl)phenyl]-4-nitrobenzenesulfonamide Chemical class C1=CC([N+](=O)[O-])=CC=C1S(=O)(=O)NC1=CC=C(C=2OC3=CC=CC=C3N=2)C=C1 SYSQUGFVNFXIIT-UHFFFAOYSA-N 0.000 description 1
- VRQXRVAKPDCRCI-ZNMIVQPWSA-N n-[4-[(1r,3s,5s)-3-amino-5-methylcyclohexyl]pyridin-3-yl]-6-(2,6-difluorophenyl)-5-fluoropyridine-2-carboxamide Chemical compound C1[C@H](C)C[C@H](N)C[C@@H]1C1=CC=NC=C1NC(=O)C1=CC=C(F)C(C=2C(=CC=CC=2F)F)=N1 VRQXRVAKPDCRCI-ZNMIVQPWSA-N 0.000 description 1
- 125000004370 n-butenyl group Chemical group [H]\C([H])=C(/[H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- AGVKXDPPPSLISR-UHFFFAOYSA-N n-ethylcyclohexanamine Chemical compound CCNC1CCCCC1 AGVKXDPPPSLISR-UHFFFAOYSA-N 0.000 description 1
- 125000001280 n-hexyl group Chemical group C(CCCCC)* 0.000 description 1
- 229940073569 n-methylephedrine Drugs 0.000 description 1
- 125000000740 n-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000003506 n-propoxy group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])O* 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000004593 naphthyridinyl group Chemical group N1=C(C=CC2=CC=CN=C12)* 0.000 description 1
- 210000003739 neck Anatomy 0.000 description 1
- 201000008026 nephroblastoma Diseases 0.000 description 1
- 208000007538 neurilemmoma Diseases 0.000 description 1
- 210000000440 neutrophil Anatomy 0.000 description 1
- 208000004649 neutrophil actin dysfunction Diseases 0.000 description 1
- 229960004378 nintedanib Drugs 0.000 description 1
- XZXHXSATPCNXJR-ZIADKAODSA-N nintedanib Chemical compound O=C1NC2=CC(C(=O)OC)=CC=C2\C1=C(C=1C=CC=CC=1)\NC(C=C1)=CC=C1N(C)C(=O)CN1CCN(C)CC1 XZXHXSATPCNXJR-ZIADKAODSA-N 0.000 description 1
- 150000002825 nitriles Chemical class 0.000 description 1
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 1
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 1
- 125000006574 non-aromatic ring group Chemical group 0.000 description 1
- 239000012457 nonaqueous media Substances 0.000 description 1
- 125000002868 norbornyl group Chemical group C12(CCC(CC1)C2)* 0.000 description 1
- 125000005482 norpinyl group Chemical group 0.000 description 1
- 239000012038 nucleophile Substances 0.000 description 1
- 230000000269 nucleophilic effect Effects 0.000 description 1
- 229960000572 olaparib Drugs 0.000 description 1
- FAQDUNYVKQKNLD-UHFFFAOYSA-N olaparib Chemical compound FC1=CC=C(CC2=C3[CH]C=CC=C3C(=O)N=N2)C=C1C(=O)N(CC1)CCN1C(=O)C1CC1 FAQDUNYVKQKNLD-UHFFFAOYSA-N 0.000 description 1
- 238000011275 oncology therapy Methods 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 150000002894 organic compounds Chemical class 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- 230000002188 osteogenic effect Effects 0.000 description 1
- 208000008798 osteoma Diseases 0.000 description 1
- 229940127084 other anti-cancer agent Drugs 0.000 description 1
- 230000001590 oxidative effect Effects 0.000 description 1
- 229960004390 palbociclib Drugs 0.000 description 1
- AHJRHEGDXFFMBM-UHFFFAOYSA-N palbociclib Chemical compound N1=C2N(C3CCCC3)C(=O)C(C(=O)C)=C(C)C2=CN=C1NC(N=C1)=CC=C1N1CCNCC1 AHJRHEGDXFFMBM-UHFFFAOYSA-N 0.000 description 1
- 208000021255 pancreatic insulinoma Diseases 0.000 description 1
- 208000017954 parathyroid gland carcinoma Diseases 0.000 description 1
- 230000036961 partial effect Effects 0.000 description 1
- 208000030940 penile carcinoma Diseases 0.000 description 1
- RGSFGYAAUTVSQA-UHFFFAOYSA-N pentamethylene Natural products C1CCCC1 RGSFGYAAUTVSQA-UHFFFAOYSA-N 0.000 description 1
- 125000003538 pentan-3-yl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])[H] 0.000 description 1
- 210000003819 peripheral blood mononuclear cell Anatomy 0.000 description 1
- 230000002093 peripheral effect Effects 0.000 description 1
- 239000008177 pharmaceutical agent Substances 0.000 description 1
- 229950006768 phenylethanolamine Drugs 0.000 description 1
- DLNKOYKMWOXYQA-APPZFPTMSA-N phenylpropanolamine Chemical compound C[C@@H](N)[C@H](O)C1=CC=CC=C1 DLNKOYKMWOXYQA-APPZFPTMSA-N 0.000 description 1
- 229960000395 phenylpropanolamine Drugs 0.000 description 1
- 229910052698 phosphorus Inorganic materials 0.000 description 1
- 239000011574 phosphorus Substances 0.000 description 1
- 230000026731 phosphorylation Effects 0.000 description 1
- 238000006366 phosphorylation reaction Methods 0.000 description 1
- 229950010773 pidilizumab Drugs 0.000 description 1
- 208000024724 pineal body neoplasm Diseases 0.000 description 1
- 125000003386 piperidinyl group Chemical group 0.000 description 1
- 208000021310 pituitary gland adenoma Diseases 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 238000010837 poor prognosis Methods 0.000 description 1
- 230000001855 preneoplastic effect Effects 0.000 description 1
- 208000016800 primary central nervous system lymphoma Diseases 0.000 description 1
- 208000025638 primary cutaneous T-cell non-Hodgkin lymphoma Diseases 0.000 description 1
- 230000000770 proinflammatory effect Effects 0.000 description 1
- 230000035755 proliferation Effects 0.000 description 1
- 201000005825 prostate adenocarcinoma Diseases 0.000 description 1
- 108060006633 protein kinase Proteins 0.000 description 1
- 239000000296 purinergic P1 receptor antagonist Substances 0.000 description 1
- 125000000561 purinyl group Chemical group N1=C(N=C2N=CNC2=C1)* 0.000 description 1
- UBQKCCHYAOITMY-UHFFFAOYSA-N pyridin-2-ol Chemical compound OC1=CC=CC=N1 UBQKCCHYAOITMY-UHFFFAOYSA-N 0.000 description 1
- 125000002943 quinolinyl group Chemical group N1=C(C=CC2=CC=CC=C12)* 0.000 description 1
- 239000000376 reactant Substances 0.000 description 1
- 230000007115 recruitment Effects 0.000 description 1
- 206010038038 rectal cancer Diseases 0.000 description 1
- 201000001275 rectum cancer Diseases 0.000 description 1
- 230000000306 recurrent effect Effects 0.000 description 1
- 230000002829 reductive effect Effects 0.000 description 1
- 201000007444 renal pelvis carcinoma Diseases 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 201000006845 reticulosarcoma Diseases 0.000 description 1
- 208000029922 reticulum cell sarcoma Diseases 0.000 description 1
- 229910052895 riebeckite Inorganic materials 0.000 description 1
- HFNKQEVNSGCOJV-OAHLLOKOSA-N ruxolitinib Chemical compound C1([C@@H](CC#N)N2N=CC(=C2)C=2C=3C=CNC=3N=CN=2)CCCC1 HFNKQEVNSGCOJV-OAHLLOKOSA-N 0.000 description 1
- 229960000215 ruxolitinib Drugs 0.000 description 1
- 229930195734 saturated hydrocarbon Natural products 0.000 description 1
- 206010039667 schwannoma Diseases 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- CYOHGALHFOKKQC-UHFFFAOYSA-N selumetinib Chemical compound OCCONC(=O)C=1C=C2N(C)C=NC2=C(F)C=1NC1=CC=C(Br)C=C1Cl CYOHGALHFOKKQC-UHFFFAOYSA-N 0.000 description 1
- 229950010746 selumetinib Drugs 0.000 description 1
- 208000004548 serous cystadenocarcinoma Diseases 0.000 description 1
- 230000007727 signaling mechanism Effects 0.000 description 1
- 201000002314 small intestine cancer Diseases 0.000 description 1
- 238000002798 spectrophotometry method Methods 0.000 description 1
- 201000011096 spinal cancer Diseases 0.000 description 1
- 208000014618 spinal cord cancer Diseases 0.000 description 1
- 230000000707 stereoselective effect Effects 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 125000001174 sulfone group Chemical group 0.000 description 1
- 125000000472 sulfonyl group Chemical group *S(*)(=O)=O 0.000 description 1
- 150000003462 sulfoxides Chemical class 0.000 description 1
- 230000009469 supplementation Effects 0.000 description 1
- 238000010189 synthetic method Methods 0.000 description 1
- 230000008685 targeting Effects 0.000 description 1
- 235000002906 tartaric acid Nutrition 0.000 description 1
- 239000011975 tartaric acid Substances 0.000 description 1
- 229940126625 tavolimab Drugs 0.000 description 1
- 208000001608 teratocarcinoma Diseases 0.000 description 1
- UXAWXZDXVOYLII-UHFFFAOYSA-N tert-butyl 2,5-diazabicyclo[2.2.1]heptane-2-carboxylate Chemical compound C1C2N(C(=O)OC(C)(C)C)CC1NC2 UXAWXZDXVOYLII-UHFFFAOYSA-N 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 230000002381 testicular Effects 0.000 description 1
- NQRYJNQNLNOLGT-UHFFFAOYSA-N tetrahydropyridine hydrochloride Natural products C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 1
- 125000003831 tetrazolyl group Chemical group 0.000 description 1
- 125000002813 thiocarbonyl group Chemical group *C(*)=S 0.000 description 1
- 201000002510 thyroid cancer Diseases 0.000 description 1
- 210000001685 thyroid gland Anatomy 0.000 description 1
- 208000013077 thyroid gland carcinoma Diseases 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 125000004306 triazinyl group Chemical group 0.000 description 1
- ZBZJXHCVGLJWFG-UHFFFAOYSA-N trichloromethyl(.) Chemical compound Cl[C](Cl)Cl ZBZJXHCVGLJWFG-UHFFFAOYSA-N 0.000 description 1
- 125000000876 trifluoromethoxy group Chemical group FC(F)(F)O* 0.000 description 1
- 229910052722 tritium Inorganic materials 0.000 description 1
- 208000022271 tubular adenoma Diseases 0.000 description 1
- 230000005747 tumor angiogenesis Effects 0.000 description 1
- 230000004614 tumor growth Effects 0.000 description 1
- OUYCCCASQSFEME-UHFFFAOYSA-N tyrosine Natural products OC(=O)C(N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-UHFFFAOYSA-N 0.000 description 1
- 238000010798 ubiquitination Methods 0.000 description 1
- 230000034512 ubiquitination Effects 0.000 description 1
- 208000010576 undifferentiated carcinoma Diseases 0.000 description 1
- 230000002485 urinary effect Effects 0.000 description 1
- 206010046885 vaginal cancer Diseases 0.000 description 1
- 208000013139 vaginal neoplasm Diseases 0.000 description 1
- 230000002792 vascular Effects 0.000 description 1
- 208000009540 villous adenoma Diseases 0.000 description 1
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 1
- 201000005102 vulva cancer Diseases 0.000 description 1
- 208000013013 vulvar carcinoma Diseases 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing three or more hetero rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/4995—Pyrazines or piperazines forming part of bridged ring systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/506—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim not condensed and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
- A61K31/5375—1,4-Oxazines, e.g. morpholine
- A61K31/5377—1,4-Oxazines, e.g. morpholine not condensed and containing further heterocyclic rings, e.g. timolol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D239/00—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings
- C07D239/02—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings
- C07D239/24—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members
- C07D239/26—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D239/00—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings
- C07D239/02—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings
- C07D239/24—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members
- C07D239/28—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, directly attached to ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/08—Bridged systems
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Epidemiology (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Plural Heterocyclic Compounds (AREA)
- Nitrogen And Oxygen Or Sulfur-Condensed Heterocyclic Ring Systems (AREA)
Abstract
Description
技术领域
本公开提供化合物以及它们的组合物和使用方法。所述化合物调节造血祖细胞激酶1(HPK1)活性,并且可用于治疗各种疾病,包括癌症。
背景技术
最初克隆自造血祖细胞的造血祖细胞激酶1(HPK1)是MAP激酶激酶激酶激酶(MAP4K)家族的成员,该家族包括MAP4K1/HPK1、MAP4K2/GCK、MAP4K3/GLK、MAP4K4/HGK、MAP4K5/KHS和MAP4K6/MINK(Hu,M.C.等人,Genes Dev,1996.10(18):第2251-64页)。HPK1特别受关注,因为其主要在造血细胞如T细胞、B细胞、巨噬细胞、树突细胞、嗜中性粒细胞和肥大细胞中表达(Hu,M.C.等人,Genes Dev,1996.10(18):第2251-64页;Kiefer,F.等人,EMBOJ,1996.15(24):第7013-25页)。已证明HPK1激酶活性经T细胞受体(TCR)(Liou,J.等人,Immunity,2000.12(4):第399-408页)、B细胞受体(BCR)(Liou,J.等人,Immunity,2000.12(4):第399-408页)、转化生长因子受体(TGF-βR)(Wang,W.等人,J Biol Chem,1997.272(36):第22771-5页;Zhou,G.等人,J Biol Chem,1999.274(19):第13133-8页)或Gs偶联PGE2受体(EP2和EP4)(Ikegami,R.等人,J Immunol,2001.166(7):第4689-96页)的激活诱导。因而,HPK1调控各种免疫细胞的各种功能。
HPK1在调控各种免疫细胞的功能方面具有重要作用,并且其与自身免疫性疾病和抗肿瘤免疫力有关(Shui,J.W.等人,Nat Immunol,2007.8(1):第84-91页;Wang,X.等人,JBiol Chem,2012.287(14):第11037-48页)。HPK1敲除小鼠更易诱发实验性自身免疫性脑脊髓炎(EAE)(Shui,J.W.等人,Nat Immunol,2007.8(1):第84-91页)。在人类中,HPK1在银屑病关节炎患者的外周血单核细胞或全身性红斑狼疮(SLE)患者的T细胞中被下调(Batliwalla,F.M.等人,Mol Med,2005.11(1-12):第21-9页)。这些观察结果表明,HPK1活性的减弱可有助于患者的自身免疫。此外,HPK1也可经由T细胞依赖性机制控制抗肿瘤免疫力。在产生PGE2的Lewis肺癌肿瘤模型中,与野生型小鼠相比,肿瘤在HPK1敲除小鼠中发展得更缓慢(参见US2007/0087988)。此外,研究表明HPK1缺陷型T细胞的过继转移在控制肿瘤生长和转移方面比野生型T细胞更有效(Alzabin,S.等人,Cancer Immunol Immunother,2010.59(3):第419-29页)。类似地,与野生型BMDC相比,来自HPK1敲除小鼠的BMDC更有效地启动T细胞应答以根除Lewis肺癌(Alzabin,S.等人,J Immunol,2009.182(10):第6187-94页)。这些数据连同HPK1在造血细胞中的限制表达以及对免疫细胞正常发育缺乏效应表明,HPK1是增强抗肿瘤免疫力的药物靶标。因此,需要调节HPK1活性的新化合物。
发明内容
本公开尤其提供式(I’)的化合物:
或其药学上可接受的盐,其中组成变量定义在本文中。
本公开进一步提供包含本公开的化合物或其药学上可接受的盐和至少一种药学上可接受的载体或赋形剂的药物组合物。
本公开进一步提供抑制HPK1活性的方法,其包括对个体施用本公开的化合物或其药学上可接受的盐。本公开还提供本文所述的化合物在制造供治疗用的药物中的用途。本公开还提供本文所述的供治疗用的化合物。
本公开进一步提供治疗患者的疾病或病症的方法,包括对患者施用治疗有效量的本公开的化合物或其药学上可接受的盐。
具体实施方式
化合物
本公开提供式(I’)的化合物:
或其药学上可接受的盐,其中:
CyA是C3-12环烷基或4-12元杂环烷基;其中所述4-12元杂环烷基具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中所述N和S任选被氧化;其中所述4-12元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述C3-12环烷基和4-12元杂环烷基各自任选被1、2、3或4个独立地选自RA的取代基取代;
A是N或CR16;
R16选自H、D、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、卤代基、CN、NO2、ORa16、SRa16、C(O)Rb16、C(O)NRc16Rd16、C(O)ORa16、OC(O)Rb16、OC(O)NRc16Rd16、NRc16Rd16、NRc16C(O)Rb16、NRc16C(O)ORa16、NRc16C(O)NRc16Rd16、NRc16S(O)Rb16、NRc16S(O)2Rb16、NRc16S(O)2NRc16Rd16、S(O)Rb16、S(O)NRc16Rd16、S(O)2Rb16、S(O)2NRc16Rd16和BRh16Ri16;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
R1选自H、D、卤代基、CN、C1-6烷基、ORa15和NRc15Rd15;其中所述C1-6烷基任选被1、2或3个独立地选自Rg的取代基取代;
R2选自H、D、Cy2、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、卤代基、CN、NO2、ORa、SRa、C(O)Rb、C(O)NRcRd、C(O)ORa、OC(O)Rb、OC(O)NRcRd、NRcRd、NRcC(O)Rb、NRcC(O)ORa、NRcC(O)NRcRd、C(=NRe)Rb、C(=NORa)Rb、C(=NRe)NRcRd、NRcC(=NRe)NRcRd、NRcS(O)Rb、NRcS(O)2Rb、NRcS(O)2NRcRd、S(O)Rb、S(O)NRcRd、S(O)2Rb、S(O)2NRcRd和BRhRi;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自R10的取代基取代;
Cy2选自C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述4-10元杂环烷基和5-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中所述N和S任选被氧化;其中5-10元杂芳基和4-10元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R10的取代基取代;
Z是N或CR3;
R3选自H、D、Cy3、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、卤代基、CN、NO2、ORa4、SRa4、C(O)Rb4、C(O)NRc4Rd4、C(O)ORa4、OC(O)Rb4、OC(O)NRc4Rd4、NRc4Rd4、NRc4C(O)Rb4、NRc4C(O)ORa4、NRc4C(O)NRc4Rd4、C(=NRe4)Rb4、C(=NORa4)Rb4、C(=NRe4)NRc4Rd4、NRc4C(=NRe4)NRc4Rd4、NRc4S(O)Rb4、NRc4S(O)2Rb4、NRc4S(O)2NRc4Rd4、S(O)Rb4、S(O)NRc4Rd4、S(O)2Rb4、S(O)2NRc4Rd4和BRh4Ri4;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自R13的取代基取代;
Cy3选自C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述4-10元杂环烷基和5-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中所述N和S任选被氧化;其中5-10元杂芳基和4-10元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R13的取代基取代;
每个R4独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、NO2、ORa8、SRa8、C(O)Rb8、C(O)NRc8Rd8、C(O)ORa8、OC(O)Rb8、OC(O)NRc8Rd8、NRc8Rd8、NRc8C(O)Rb8、NRc8C(O)ORa8、NRc8C(O)NRc8Rd8、C(=NRe8)Rb8、C(=NORa8)Rb8、C(=NRe8)NRc8Rd8、NRc8C(=NRe8)NRc8Rd8、NRc8S(O)Rb8、NRc8S(O)2Rb8、NRc8S(O)2NRc8Rd8、S(O)Rb8、S(O)NRc8Rd8、S(O)2Rb8、S(O)2NRc8Rd8和BRh8Ri8;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R5的取代基取代;
每个R5独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、ORa9、SRa9、C(O)Rb9、C(O)NRc9Rd9、C(O)ORa9、NRc9Rd9、NRc9C(O)Rb9、NRc9C(O)ORa9、NRc9S(O)Rb9、NRc9S(O)2Rb9、NRc9S(O)2NRc9Rd9、S(O)Rb9、S(O)NRc9Rd9、S(O)2Rb9、S(O)2NRc9Rd9和BRh9Ri9;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R6的取代基取代;
每个R6独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-6环烷基、苯基、5-6元杂芳基、4-7元杂环烷基、卤代基、D、CN、ORa10、SRa10、C(O)Rb10、C(O)NRc10Rd10、C(O)ORa10、NRc10Rd10、NRc10C(O)Rb10、NRc10C(O)ORa10、NRc10S(O)Rb10、NRc10S(O)2Rb10、NRc10S(O)2NRc10Rd10、S(O)Rb10、S(O)NRc10Rd10、S(O)2Rb10和S(O)2NRc10Rd10;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-6环烷基、苯基、5-6元杂芳基和4-7元杂环烷基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个RA选自H、D、Cy1、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、卤代基、CN、NO2、ORa11、SRa11、C(O)Rb11、C(O)NRc11Rd11、C(O)ORa11、OC(O)Rb11、OC(O)NRc11Rd11、NRc11Rd11、NRc11C(O)Rb11、NRc11C(O)ORa11、NRc11C(O)NRc11Rd11、C(=NRe11)Rb11、C(=NORa11)Rb11、C(=NRe11)NRc11Rd11、NRc11C(=NRe11)NRc11Rd11、NRc11S(O)Rb11、NRc11S(O)2Rb11、NRc11S(O)2NRc11Rd11、S(O)Rb11、S(O)NRc11Rd11、S(O)2Rb11、S(O)2NRc11Rd11和BRh11Ri11;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自R7的取代基取代;
Cy1选自C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述4-10元杂环烷基和5-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中所述N和S任选被氧化;其中5-10元杂芳基和4-10元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R7的取代基取代;
每个R7独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、NO2、ORa12、SRa12、C(O)Rb12、C(O)NRc12Rd12、C(O)ORa12、OC(O)Rb12、OC(O)NRc12Rd12、NRc12Rd12、NRc12C(O)Rb12、NRc12C(O)ORa12、NRc12C(O)NRc12Rd12、C(=NRe12)Rb12、C(=NORa12)Rb12、C(=NRe12)NRc12Rd12、NRc12C(=NRe12)NRc12Rd12、NRc12S(O)Rb12、NRc12S(O)2Rb12、NRc12S(O)2NRc12Rd12、S(O)Rb12、S(O)NRc12Rd12、S(O)2Rb12、S(O)2NRc12Rd12和BRh12Ri12;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R8的取代基取代;
每个R8独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、ORa13、SRa13、C(O)Rb13、C(O)NRc13Rd13、C(O)ORa13、NRc13Rd13、NRc13C(O)Rb13、NRc13C(O)ORa13、NRc13S(O)Rb13、NRc13S(O)2Rb13、NRc13S(O)2NRc13Rd13、S(O)Rb13、S(O)NRc13Rd13、S(O)2Rb13S(O)2NRc13Rd13和BRh13Ri13;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R9的取代基取代;
每个R9独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-6环烷基、苯基、5-6元杂芳基、4-7元杂环烷基、卤代基、D、CN、ORa14、SRa14、C(O)Rb14、C(O)NRc14Rd14、C(O)ORa14、NRc14Rd14、NRc14C(O)Rb14、NRc14C(O)ORa14、NRc14S(O)Rb14、NRc14S(O)2Rb14、NRc14S(O)2NRc14Rd14、S(O)Rb14、S(O)NRc14Rd14、S(O)2Rb14和S(O)2NRc14Rd14;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-6环烷基、C6-10芳基、5-10元杂芳基和4-7元杂环烷基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个R10独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、NRc1C(O)NRc1Rd1、C(=NRe1)Rb1、C(=NORa1)Rb1、C(=NRe1)NRc1Rd1、NRc1C(=NRe1)NRc1Rd1、NRc1S(O)Rb1、NRc1S(O)2Rb1、NRc1S(O)2NRc1Rd1、S(O)Rb1、S(O)NRc1Rd1、S(O)2Rb1、S(O)2NRc1Rd1和BRh1Ri1;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R11的取代基取代;
每个R11独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、ORa2、SRa2、C(O)Rb2、C(O)NRc2Rd2、C(O)ORa2、NRc2Rd2、NRc2C(O)Rb2、NRc2C(O)ORa2、NRc2S(O)Rb2、NRc2S(O)2Rb2、NRc2S(O)2NRc2Rd2、S(O)Rb2、S(O)NRc2Rd2、S(O)2Rb2S(O)2NRc2Rd2和BRh2Ri2;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R12的取代基取代;
每个R12独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-6环烷基、苯基、5-6元杂芳基、4-7元杂环烷基、卤代基、D、CN、ORa3、SRa3、C(O)Rb3、C(O)NRc3Rd3、C(O)ORa3、NRc3Rd3、NRc3C(O)Rb3、NRc3C(O)ORa3、NRc3S(O)Rb3、NRc3S(O)2Rb3、NRc3S(O)2NRc3Rd3、S(O)Rb3、S(O)NRc3Rd3、S(O)2Rb3和S(O)2NRc3Rd3;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-6环烷基、C6-10芳基、5-10元杂芳基和4-7元杂环烷基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个R13独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、NO2、ORa5、SRa5、C(O)Rb5、C(O)NRc5Rd5、C(O)ORa5、OC(O)Rb5、OC(O)NRc5Rd5、NRc5Rd5、NRc5C(O)Rb5、NRc5C(O)ORa5、NRc5C(O)NRc5Rd5、C(=NRe5)Rb5、C(=NORa5)Rb5、C(=NRe5)NRc5Rd5、NRc5C(=NRe5)NRc5Rd5、NRc5S(O)Rb5、NRc5S(O)2Rb5、NRc5S(O)2NRc5Rd5、S(O)Rb5、S(O)NRc5Rd5、S(O)2Rb5、S(O)2NRc5Rd5和BRh5Ri5;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R14的取代基取代;
每个R14独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、ORa6、SRa6、C(O)Rb6、C(O)NRc6Rd6、C(O)ORa6、NRc6Rd6、NRc6C(O)Rb6、NRc6C(O)ORa6、NRc6S(O)Rb6、NRc6S(O)2Rb6、NRc6S(O)2NRc6Rd6、S(O)Rb6、S(O)NRc6Rd6、S(O)2Rb6S(O)2NRc6Rd6和BRh6Ri6;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R15的取代基取代;
每个R15独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-6环烷基、苯基、5-6元杂芳基、4-7元杂环烷基、卤代基、D、CN、ORa7、SRa7、C(O)Rb7、C(O)NRc7Rd7、C(O)ORa7、NRc7Rd7、NRc7C(O)Rb7、NRc7C(O)ORa7、NRc7S(O)Rb7、NRc7S(O)2Rb7、NRc7S(O)2NRc7Rd7、S(O)Rb7、S(O)NRc7Rd7、S(O)2Rb7和S(O)2NRc7Rd7;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-6环烷基、C6-10芳基、5-10元杂芳基和4-7元杂环烷基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Ra、Rc和Rd独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R10的取代基取代;
或者与同一N原子连接的任何Rc和Rd与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R10的取代基取代的4、5、6或7元杂环烷基;
每个Rb独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R10的取代基取代;
每个Re独立地选自H、CN、C1-6烷基、C1-6卤代烷基、C1-6烷硫基、C1-6烷基磺酰基、C1-6烷基羰基、C1-6烷基氨基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、氨基磺酰基、C1-6烷基氨基磺酰基和二(C1-6烷基)氨基磺酰基;
每个Rh和Ri独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh和Ri均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra1、Rc1和Rd1独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R11的取代基取代;
或者与同一N原子连接的任何Rc1和Rd1与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R11的取代基取代的4、5、6或7元杂环烷基;
每个Rb1独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R11的取代基取代;
每个Re1独立地选自H、CN、C1-6烷基、C1-6卤代烷基、C1-6烷硫基、C1-6烷基磺酰基、C1-6烷基羰基、C1-6烷基氨基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、氨基磺酰基、C1-6烷基氨基磺酰基和二(C1-6烷基)氨基磺酰基;
每个Rh1和Ri1独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh1和Ri1均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra2、Rc2和Rd2独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R12的取代基取代;
或者与同一N原子连接的任何Rc2和Rd2与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R12的取代基取代的4、5、6或7元杂环烷基;
每个Rb2独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R12的取代基取代;
每个Rh2和Ri2独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh2和Ri2均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra3、Rc3和Rd3独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Rb3独立地选自C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Ra4、Rc4和Rd4独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R13的取代基取代;
或者与同一N原子连接的任何Rc4和Rd4与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R13的取代基取代的4、5、6或7元杂环烷基;
每个Rb4独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R13的取代基取代;
每个Re4独立地选自H、CN、C1-6烷基、C1-6卤代烷基、C1-6烷硫基、C1-6烷基磺酰基、C1-6烷基羰基、C1-6烷基氨基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、氨基磺酰基、C1-6烷基氨基磺酰基和二(C1-6烷基)氨基磺酰基;
每个Rh4和Ri4独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh4和Ri4均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra5、Rc5和Rd5独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R14的取代基取代;
或者与同一N原子连接的任何Rc5和Rd5与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R14的取代基取代的4、5、6或7元杂环烷基;
每个Rb5独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R14的取代基取代;
每个Re5独立地选自H、CN、C1-6烷基、C1-6卤代烷基、C1-6烷硫基、C1-6烷基磺酰基、C1-6烷基羰基、C1-6烷基氨基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、氨基磺酰基、C1-6烷基氨基磺酰基和二(C1-6烷基)氨基磺酰基;
每个Rh5和Ri5独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh5和Ri5均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra6、Rc6和Rd6独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R15的取代基取代;
或者与同一N原子连接的任何Rc6和Rd6与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R15的取代基取代的4、5、6或7元杂环烷基;
每个Rb6独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R15的取代基取代;
每个Rh6和Ri6独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh6和Ri6均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra7、Rc7和Rd7独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Rb7独立地选自C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Ra8、Rc8和Rd8独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R5的取代基取代;
或者与同一N原子连接的任何Rc8和Rd8与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R5的取代基取代的4、5、6或7元杂环烷基;
每个Rb8独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R5的取代基取代;
每个Re8独立地选自H、CN、C1-6烷基、C1-6卤代烷基、C1-6烷硫基、C1-6烷基磺酰基、C1-6烷基羰基、C1-6烷基氨基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、氨基磺酰基、C1-6烷基氨基磺酰基和二(C1-6烷基)氨基磺酰基;
每个Rh8和Ri8独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh8和Ri8均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra9、Rc9和Rd9独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R6的取代基取代;
或者与同一N原子连接的任何Rc9和Rd9与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R6的取代基取代的4、5、6或7元杂环烷基;
每个Rb9独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R6的取代基取代;
每个Rh9和Ri9独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh9和Ri9均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra10、Rc10和Rd10独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Rb10独立地选自C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Ra11、Rc11和Rd11独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R7的取代基取代;
或者与同一N原子连接的任何Rc11和Rd11与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R7的取代基取代的4、5、6或7元杂环烷基;
每个Rb11独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R7的取代基取代;
每个Re11独立地选自H、CN、C1-6烷基、C1-6卤代烷基、C1-6烷硫基、C1-6烷基磺酰基、C1-6烷基羰基、C1-6烷基氨基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、氨基磺酰基、C1-6烷基氨基磺酰基和二(C1-6烷基)氨基磺酰基;
每个Rh11和Ri11独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh11和Ri11均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra12、Rc12和Rd12独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R8的取代基取代;
或者与同一N原子连接的任何Rc12和Rd12与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R8的取代基取代的4、5、6或7元杂环烷基;
每个Rb12独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R8的取代基取代;
每个Re12独立地选自H、CN、C1-6烷基、C1-6卤代烷基、C1-6烷硫基、C1-6烷基磺酰基、C1-6烷基羰基、C1-6烷基氨基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、氨基磺酰基、C1-6烷基氨基磺酰基和二(C1-6烷基)氨基磺酰基;
每个Rh12和Ri12独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh12和Ri12均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra13、Rc13和Rd13独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R9的取代基取代;
或者与同一N原子连接的任何Rc13和Rd13与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R9的取代基取代的4、5、6或7元杂环烷基;
每个Rb13独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R9的取代基取代;
每个Rh13和Ri13独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh13和Ri13均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra14、Rc14和Rd14独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Rb14独立地选自C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Ra15、Rc15和Rd15独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Ra16、Rc16和Rd16独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Rb16独立地选自C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Rh16和Ri16独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh16和Ri16均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;且
每个Rg独立地选自OH、NO2、CN、卤代基、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-6环烷基、C3-6环烷基-C1-2亚烷基、C1-6烷氧基、C1-6卤代烷氧基、C1-3烷氧基-C1-3烷基、C1-3烷氧基-C1-3烷氧基、HO-C1-3烷氧基、HO-C1-3烷基、氰基-C1-3烷基、H2N-C1-3烷基、氨基、C1-6烷基氨基、二(C1-6烷基)氨基、硫代基、C1-6烷硫基、C1-6烷基亚磺酰基、C1-6烷基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、羧基、C1-6烷基羰基、C1-6烷氧基羰基、C1-6烷基羰基氨基、C1-6烷基磺酰基氨基、氨基磺酰基、C1-6烷基氨基磺酰基、二(C1-6烷基)氨基磺酰基、氨基磺酰基氨基、C1-6烷基氨基磺酰基氨基、二(C1-6烷基)氨基磺酰基氨基、氨基羰基氨基、C1-6烷基氨基羰基氨基和二(C1-6烷基)氨基羰基氨基;且
n是0、1、2、3或4。
本公开提供式(I’)的化合物或其药学上可接受的盐,其中:
CyA是C3-12环烷基或4-12元杂环烷基;其中所述4-12元杂环烷基具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中所述N和S任选被氧化;其中所述4-12元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述C3-12环烷基和4-12元杂环烷基各自任选被1、2、3或4个独立地选自RA的取代基取代;
A是N或CR16;
R16选自H、D、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、卤代基、CN、NO2、ORa16、SRa16、C(O)Rb16、C(O)NRc16Rd16、C(O)ORa16、OC(O)Rb16、OC(O)NRc16Rd16、NRc16Rd16、NRc16C(O)Rb16、NRc16C(O)ORa16、NRc16C(O)NRc16Rd16、NRc16S(O)Rb16、NRc16S(O)2Rb16、NRc16S(O)2NRc16Rd16、S(O)Rb16、S(O)NRc16Rd16、S(O)2Rb16、S(O)2NRc16Rd16和BRh16Ri16;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
R1选自H、D、卤代基、CN、C1-6烷基和ORa15;其中所述C1-6烷基任选被1、2或3个独立地选自Rg的取代基取代;
R2选自H、D、Cy2、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、卤代基、CN和NO2;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自R10的取代基取代;
Cy2选自4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述4-10元杂环烷基和5-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中5-10元杂芳基和4-10元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述4-10元杂环烷基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R10的取代基取代;
Z是N或CR3;
R3选自H、D、Cy3、卤代基和CN;
Cy3是6-10元杂芳基;其中所述6-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;
每个R4独立地选自C1-6烷基、C1-6卤代烷基、卤代基、D、CN和ORa8;
RA选自H、D、Cy1、C1-6烷基、C1-6卤代烷基、卤代基、CN、ORa11、C(O)NRc11Rd11和NRc11Rd11;其中所述C1-6烷基任选被1、2、3或4个独立地选自R7的取代基取代;
Cy1选自C3-10环烷基和5-10元杂芳基;其中所述5-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中5-10元杂芳基的成环碳原子任选被氧代基取代以形成羰基;且其中所述C3-10环烷基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R7的取代基取代;
每个R7独立地选自C1-6烷基、卤代基、D、CN、ORa12和NRc12Rd12;
每个R10独立地选自C1-6烷基、C1-6卤代烷基、4-10元杂环烷基、卤代基、D、CN、ORa1、C(O)NRc1Rd1和NRc1Rd1;其中所述C1-6烷基和4-10元杂环烷基各自任选被1、2、3或4个独立地选自R11的取代基取代;
每个R11独立地选自C1-6烷基、C1-6卤代烷基、卤代基、D、CN和ORa2;
每个Ra1、Rc1和Rd1独立地选自H、C1-6烷基、C1-6卤代烷基和C3-10环烷基;其中所述C1-6烷基和C3-10环烷基各自任选被1、2、3或4个独立地选自R11的取代基取代;
每个Ra2、Rc2和Rd2独立地选自H、C1-6烷基和C1-6卤代烷基;
每个Ra8、Rc8和Rd8独立地选自H、C1-6烷基和C1-6卤代烷基;
每个Ra11、Rc11和Rd11独立地选自H、C1-6烷基和C1-6卤代烷基;其中所述C1-6烷基任选被1、2、3或4个独立地选自R7的取代基取代;
每个Ra12、Rc12和Rd12独立地选自H、C1-6烷基和C1-6卤代烷基;
每个Ra15、Rc15和Rd15独立地选自H、C1-6烷基和C1-6卤代烷基;其中所述C1-6烷基任选被1、2、3或4个独立地选自Rg的取代基取代;
Ra16独立地选自H和C1-6烷基;
每个Rg独立地选自OH、CN、卤代基、C1-6烷基、C1-6卤代烷基、C1-6烷氧基、C1-6卤代烷氧基、氨基、C1-6烷硫基、C1-6烷基磺酰基;且
n是0、1、2或3。
本公开提供式(I’)的化合物或其药学上可接受的盐,其中:
CyA是4-12元杂环烷基;其中所述4-12元杂环烷基具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中所述4-12元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述4-12元杂环烷基各自任选被1、2、3或4个独立地选自RA的取代基取代;
A是N或CR16;
R16选自H、D、C1-6烷基、卤代基、CN和ORa16;
R1选自H、D、卤代基、CN、C1-6烷基和ORa15;其中所述C1-6烷基任选被1、2或3个独立地选自Rg的取代基取代;
R2选自H、D、Cy2、C1-6烷基、C1-6卤代烷基、卤代基、CN;其中所述C1-6烷基任选被1、2、3或4个独立地选自R10的取代基取代;
Cy2选自4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述4-10元杂环烷基和5-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中5-10元杂芳基和4-10元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述4-10元杂环烷基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R10的取代基取代;
Z是N或CR3;
R3选自H、D、Cy3、卤代基和CN;
Cy3是6-10元杂芳基;其中所述6-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;
每个R4独立地选自C1-6烷基、C1-6卤代烷基、卤代基、D、CN和ORa8;
RA选自H、D、Cy1、C1-6烷基、C1-6卤代烷基、卤代基、CN、ORa11、C(O)NRc11Rd11和NRc11Rd11;其中所述C1-6烷基任选被1、2、3或4个独立地选自R7的取代基取代;
Cy1选自C3-10环烷基和5-10元杂芳基;其中所述5-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中5-10元杂芳基的成环碳原子任选被氧代基取代以形成羰基;且其中所述C3-10环烷基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R7的取代基取代;
每个R7独立地选自C1-6烷基、卤代基、D、CN、ORa12和NRc12Rd12;
每个R10独立地选自C1-6烷基、C1-6卤代烷基、4-10元杂环烷基、卤代基、D、CN、ORa1、C(O)NRc1Rd1和NRc1Rd1;其中所述C1-6烷基和4-10元杂环烷基各自任选被1、2、3或4个独立地选自R11的取代基取代;
每个R11独立地选自C1-6烷基、C1-6卤代烷基、卤代基、D、CN和ORa2;
每个Ra1、Rc1和Rd1独立地选自H、C1-6烷基、C1-6卤代烷基和C3-10环烷基;其中所述C1-6烷基和C3-10环烷基各自任选被1、2、3或4个独立地选自R11的取代基取代;
每个Ra2、Rc2和Rd2独立地选自H、C1-6烷基和C1-6卤代烷基;
每个Ra8、Rc8和Rd8独立地选自H、C1-6烷基和C1-6卤代烷基;
每个Ra11、Rc11和Rd11独立地选自H、C1-6烷基和C1-6卤代烷基;其中所述C1-6烷基任选被1、2、3或4个独立地选自R7的取代基取代;
每个Ra12、Rc12和Rd12独立地选自H、C1-6烷基和C1-6卤代烷基;
每个Ra15、Rc15和Rd15独立地选自H、C1-6烷基和C1-6卤代烷基;其中所述C1-6烷基任选被1、2、3或4个独立地选自Rg的取代基取代;
Ra16独立地选自H和C1-6烷基;
每个Rg独立地选自OH、CN、卤代基、C1-6烷基、C1-6卤代烷基、C1-6烷氧基、C1-6卤代烷氧基、氨基、C1-6烷硫基、C1-6烷基磺酰基;且
n是0、1、2或3。
本公开提供式(I)的化合物:
或其药学上可接受的盐,其中:
CyA是C3-12环烷基或4-12元杂环烷基;其中所述4-12元杂环烷基具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中所述N和S任选被氧化;其中所述4-12元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述C3-12环烷基和4-12元杂环烷基各自任选被1、2、3或4个独立地选自RA的取代基取代;
A是N或CF;
R1选自H、D、卤代基、CN、C1-6烷基、ORa15和NRc15Rd15;其中所述C1-6烷基任选被1、2或3个独立地选自Rg的取代基取代;
R2选自H、D、Cy2、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、卤代基、CN、NO2、ORa、SRa、C(O)Rb、C(O)NRcRd、C(O)ORa、OC(O)Rb、OC(O)NRcRd、NRcRd、NRcC(O)Rb、NRcC(O)ORa、NRcC(O)NRcRd、C(=NRe)Rb、C(=NORa)Rb、C(=NRe)NRcRd、NRcC(=NRe)NRcRd、NRcS(O)Rb、NRcS(O)2Rb、NRcS(O)2NRcRd、S(O)Rb、S(O)NRcRd、S(O)2Rb、S(O)2NRcRd和BRhRi;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自R10的取代基取代;
Cy2选自C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述4-10元杂环烷基和5-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中所述N和S任选被氧化;其中5-10元杂芳基和4-10元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R10的取代基取代;
R3选自H、D、Cy3、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、卤代基、CN、NO2、ORa4、SRa4、C(O)Rb4、C(O)NRc4Rd4、C(O)ORa4、OC(O)Rb4、OC(O)NRc4Rd4、NRc4Rd4、NRc4C(O)Rb4、NRc4C(O)ORa4、NRc4C(O)NRc4Rd4、C(=NRe4)Rb4、C(=NORa4)Rb4、C(=NRe4)NRc4Rd4、NRc4C(=NRe4)NRc4Rd4、NRc4S(O)Rb4、NRc4S(O)2Rb4、NRc4S(O)2NRc4Rd4、S(O)Rb4、S(O)NRc4Rd4、S(O)2Rb4、S(O)2NRc4Rd4和BRh4Ri4;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自R13的取代基取代;
Cy3选自C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述4-10元杂环烷基和5-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中所述N和S任选被氧化;其中5-10元杂芳基和4-10元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R13的取代基取代;
每个R4独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、NO2、ORa8、SRa8、C(O)Rb8、C(O)NRc8Rd8、C(O)ORa8、OC(O)Rb8、OC(O)NRc8Rd8、NRc8Rd8、NRc8C(O)Rb8、NRc8C(O)ORa8、NRc8C(O)NRc8Rd8、C(=NRe8)Rb8、C(=NORa8)Rb8、C(=NRe8)NRc8Rd8、NRc8C(=NRe8)NRc8Rd8、NRc8S(O)Rb8、NRc8S(O)2Rb8、NRc8S(O)2NRc8Rd8、S(O)Rb8、S(O)NRc8Rd8、S(O)2Rb8、S(O)2NRc8Rd8和BRh8Ri8;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R5的取代基取代;
每个R5独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、ORa9、SRa9、C(O)Rb9、C(O)NRc9Rd9、C(O)ORa9、NRc9Rd9、NRc9C(O)Rb9、NRc9C(O)ORa9、NRc9S(O)Rb9、NRc9S(O)2Rb9、NRc9S(O)2NRc9Rd9、S(O)Rb9、S(O)NRc9Rd9、S(O)2Rb9、S(O)2NRc9Rd9和BRh9Ri9;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R6的取代基取代;
每个R6独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-6环烷基、苯基、5-6元杂芳基、4-7元杂环烷基、卤代基、D、CN、ORa10、SRa10、C(O)Rb10、C(O)NRc10Rd10、C(O)ORa10、NRc10Rd10、NRc10C(O)Rb10、NRc10C(O)ORa10、NRc10S(O)Rb10、NRc10S(O)2Rb10、NRc10S(O)2NRc10Rd10、S(O)Rb10、S(O)NRc10Rd10、S(O)2Rb10和S(O)2NRc10Rd10;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-6环烷基、苯基、5-6元杂芳基和4-7元杂环烷基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
RA选自H、D、Cy1、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、卤代基、CN、NO2、ORa11、SRa11、C(O)Rb11、C(O)NRc11Rd11、C(O)ORa11、OC(O)Rb11、OC(O)NRc11Rd11、NRc11Rd11、NRc11C(O)Rb11、NRc11C(O)ORa11、NRc11C(O)NRc11Rd11、C(=NRe11)Rb11、C(=NORa11)Rb11、C(=NRe11)NRc11Rd11、NRc11C(=NRe11)NRc11Rd11、NRc11S(O)Rb11、NRc11S(O)2Rb11、NRc11S(O)2NRc11Rd11、S(O)Rb11、S(O)NRc11Rd11、S(O)2Rb11、S(O)2NRc11Rd11和BRh11Ri11;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自R7的取代基取代;
Cy1选自C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述4-10元杂环烷基和5-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中所述N和S任选被氧化;其中5-10元杂芳基和4-10元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R7的取代基取代;
每个R7独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、NO2、ORa12、SRa12、C(O)Rb12、C(O)NRc12Rd12、C(O)ORa12、OC(O)Rb12、OC(O)NRc12Rd12、NRc12Rd12、NRc12C(O)Rb12、NRc12C(O)ORa12、NRc12C(O)NRc12Rd12、C(=NRe12)Rb12、C(=NORa12)Rb12、C(=NRe12)NRc12Rd12、NRc12C(=NRe12)NRc12Rd12、NRc12S(O)Rb12、NRc12S(O)2Rb12、NRc12S(O)2NRc12Rd12、S(O)Rb12、S(O)NRc12Rd12、S(O)2Rb12、S(O)2NRc12Rd12和BRh12Ri12;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R8的取代基取代;
每个R8独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、ORa13、SRa13、C(O)Rb13、C(O)NRc13Rd13、C(O)ORa13、NRc13Rd13、NRc13C(O)Rb13、NRc13C(O)ORa13、NRc13S(O)Rb13、NRc13S(O)2Rb13、NRc13S(O)2NRc13Rd13、S(O)Rb13、S(O)NRc13Rd13、S(O)2Rb13S(O)2NRc13Rd13和BRh13Ri13;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R9的取代基取代;
每个R9独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-6环烷基、苯基、5-6元杂芳基、4-7元杂环烷基、卤代基、D、CN、ORa14、SRa14、C(O)Rb14、C(O)NRc14Rd14、C(O)ORa14、NRc14Rd14、NRc14C(O)Rb14、NRc14C(O)ORa14、NRc14S(O)Rb14、NRc14S(O)2Rb14、NRc14S(O)2NRc14Rd14、S(O)Rb14、S(O)NRc14Rd14、S(O)2Rb14和S(O)2NRc14Rd14;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-6环烷基、C6-10芳基、5-10元杂芳基和4-7元杂环烷基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个R10独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、NRc1C(O)NRc1Rd1、C(=NRe1)Rb1、C(=NORa1)Rb1、C(=NRe1)NRc1Rd1、NRc1C(=NRe1)NRc1Rd1、NRc1S(O)Rb1、NRc1S(O)2Rb1、NRc1S(O)2NRc1Rd1、S(O)Rb1、S(O)NRc1Rd1、S(O)2Rb1、S(O)2NRc1Rd1和BRh1Ri1;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R11的取代基取代;
每个R11独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、ORa2、SRa2、C(O)Rb2、C(O)NRc2Rd2、C(O)ORa2、NRc2Rd2、NRc2C(O)Rb2、NRc2C(O)ORa2、NRc2S(O)Rb2、NRc2S(O)2Rb2、NRc2S(O)2NRc2Rd2、S(O)Rb2、S(O)NRc2Rd2、S(O)2Rb2S(O)2NRc2Rd2和BRh2Ri2;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R12的取代基取代;
每个R12独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-6环烷基、苯基、5-6元杂芳基、4-7元杂环烷基、卤代基、D、CN、ORa3、SRa3、C(O)Rb3、C(O)NRc3Rd3、C(O)ORa3、NRc3Rd3、NRc3C(O)Rb3、NRc3C(O)ORa3、NRc3S(O)Rb3、NRc3S(O)2Rb3、NRc3S(O)2NRc3Rd3、S(O)Rb3、S(O)NRc3Rd3、S(O)2Rb3和S(O)2NRc3Rd3;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-6环烷基、C6-10芳基、5-10元杂芳基和4-7元杂环烷基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个R13独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、NO2、ORa5、SRa5、C(O)Rb5、C(O)NRc5Rd5、C(O)ORa5、OC(O)Rb5、OC(O)NRc5Rd5、NRc5Rd5、NRc5C(O)Rb5、NRc5C(O)ORa5、NRc5C(O)NRc5Rd5、C(=NRe5)Rb5、C(=NORa5)Rb5、C(=NRe5)NRc5Rd5、NRc5C(=NRe5)NRc5Rd5、NRc5S(O)Rb5、NRc5S(O)2Rb5、NRc5S(O)2NRc5Rd5、S(O)Rb5、S(O)NRc5Rd5、S(O)2Rb5、S(O)2NRc5Rd5和BRh5Ri5;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R14的取代基取代;
每个R14独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、ORa6、SRa6、C(O)Rb6、C(O)NRc6Rd6、C(O)ORa6、NRc6Rd6、NRc6C(O)Rb6、NRc6C(O)ORa6、NRc6S(O)Rb6、NRc6S(O)2Rb6、NRc6S(O)2NRc6Rd6、S(O)Rb6、S(O)NRc6Rd6、S(O)2Rb6S(O)2NRc6Rd6和BRh6Ri6;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R15的取代基取代;
每个R15独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-6环烷基、苯基、5-6元杂芳基、4-7元杂环烷基、卤代基、D、CN、ORa7、SRa7、C(O)Rb7、C(O)NRc7Rd7、C(O)ORa7、NRc7Rd7、NRc7C(O)Rb7、NRc7C(O)ORa7、NRc7S(O)Rb7、NRc7S(O)2Rb7、NRc7S(O)2NRc7Rd7、S(O)Rb7、S(O)NRc7Rd7、S(O)2Rb7和S(O)2NRc7Rd7;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-6环烷基、C6-10芳基、5-10元杂芳基和4-7元杂环烷基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Ra、Rc和Rd独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R10的取代基取代;
或者与同一N原子连接的任何Rc和Rd与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R10的取代基取代的4、5、6或7元杂环烷基;
每个Rb独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R10的取代基取代;
每个Re独立地选自H、CN、C1-6烷基、C1-6卤代烷基、C1-6烷硫基、C1-6烷基磺酰基、C1-6烷基羰基、C1-6烷基氨基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、氨基磺酰基、C1-6烷基氨基磺酰基和二(C1-6烷基)氨基磺酰基;
每个Rh和Ri独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh和Ri均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra1、Rc1和Rd1独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R11的取代基取代;
或者与同一N原子连接的任何Rc1和Rd1与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R11的取代基取代的4、5、6或7元杂环烷基;
每个Rb1独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R11的取代基取代;
每个Re1独立地选自H、CN、C1-6烷基、C1-6卤代烷基、C1-6烷硫基、C1-6烷基磺酰基、C1-6烷基羰基、C1-6烷基氨基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、氨基磺酰基、C1-6烷基氨基磺酰基和二(C1-6烷基)氨基磺酰基;
每个Rh1和Ri1独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh1和Ri1均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra2、Rc2和Rd2独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R12的取代基取代;
或者与同一N原子连接的任何Rc2和Rd2与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R12的取代基取代的4、5、6或7元杂环烷基;
每个Rb2独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R12的取代基取代;
每个Rh2和Ri2独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh2和Ri2均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra3、Rc3和Rd3独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Rb3独立地选自C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Ra4、Rc4和Rd4独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R13的取代基取代;
或者与同一N原子连接的任何Rc4和Rd4与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R13的取代基取代的4、5、6或7元杂环烷基;
每个Rb4独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R13的取代基取代;
每个Re4独立地选自H、CN、C1-6烷基、C1-6卤代烷基、C1-6烷硫基、C1-6烷基磺酰基、C1-6烷基羰基、C1-6烷基氨基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、氨基磺酰基、C1-6烷基氨基磺酰基和二(C1-6烷基)氨基磺酰基;
每个Rh4和Ri4独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh4和Ri4均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra5、Rc5和Rd5独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R14的取代基取代;
或者与同一N原子连接的任何Rc5和Rd5与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R14的取代基取代的4、5、6或7元杂环烷基;
每个Rb5独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R14的取代基取代;
每个Re5独立地选自H、CN、C1-6烷基、C1-6卤代烷基、C1-6烷硫基、C1-6烷基磺酰基、C1-6烷基羰基、C1-6烷基氨基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、氨基磺酰基、C1-6烷基氨基磺酰基和二(C1-6烷基)氨基磺酰基;
每个Rh5和Ri5独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh5和Ri5均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra6、Rc6和Rd6独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R15的取代基取代;
或者与同一N原子连接的任何Rc6和Rd6与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R15的取代基取代的4、5、6或7元杂环烷基;
每个Rb6独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R15的取代基取代;
每个Rh6和Ri6独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh6和Ri6均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra7、Rc7和Rd7独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Rb7独立地选自C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Ra8、Rc8和Rd8独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R5的取代基取代;
或者与同一N原子连接的任何Rc8和Rd8与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R5的取代基取代的4、5、6或7元杂环烷基;
每个Rb8独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R5的取代基取代;
每个Re8独立地选自H、CN、C1-6烷基、C1-6卤代烷基、C1-6烷硫基、C1-6烷基磺酰基、C1-6烷基羰基、C1-6烷基氨基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、氨基磺酰基、C1-6烷基氨基磺酰基和二(C1-6烷基)氨基磺酰基;
每个Rh8和Ri8独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh8和Ri8均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra9、Rc9和Rd9独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R6的取代基取代;
或者与同一N原子连接的任何Rc9和Rd9与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R6的取代基取代的4、5、6或7元杂环烷基;
每个Rb9独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R6的取代基取代;
每个Rh9和Ri9独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh9和Ri9均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra10、Rc10和Rd10独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Rb10独立地选自C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Ra11、Rc11和Rd11独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R7的取代基取代;
或者与同一N原子连接的任何Rc11和Rd11与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R7的取代基取代的4、5、6或7元杂环烷基;
每个Rb11独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R7的取代基取代;
每个Re11独立地选自H、CN、C1-6烷基、C1-6卤代烷基、C1-6烷硫基、C1-6烷基磺酰基、C1-6烷基羰基、C1-6烷基氨基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、氨基磺酰基、C1-6烷基氨基磺酰基和二(C1-6烷基)氨基磺酰基;
每个Rh11和Ri11独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh11和Ri11均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra12、Rc12和Rd12独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R8的取代基取代;
或者与同一N原子连接的任何Rc12和Rd12与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R8的取代基取代的4、5、6或7元杂环烷基;
每个Rb12独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R8的取代基取代;
每个Re12独立地选自H、CN、C1-6烷基、C1-6卤代烷基、C1-6烷硫基、C1-6烷基磺酰基、C1-6烷基羰基、C1-6烷基氨基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、氨基磺酰基、C1-6烷基氨基磺酰基和二(C1-6烷基)氨基磺酰基;
每个Rh12和Ri12独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh12和Ri12均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra13、Rc13和Rd13独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R9的取代基取代;
或者与同一N原子连接的任何Rc13和Rd13与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R9的取代基取代的4、5、6或7元杂环烷基;
每个Rb13独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R9的取代基取代;
每个Rh13和Ri13独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh13和Ri13均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra14、Rc14和Rd14独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Rb14独立地选自C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Ra15、Rc15和Rd15独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Rg独立地选自OH、NO2、CN、卤代基、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-6环烷基、C3-6环烷基-C1-2亚烷基、C1-6烷氧基、C1-6卤代烷氧基、C1-3烷氧基-C1-3烷基、C1-3烷氧基-C1-3烷氧基、HO-C1-3烷氧基、HO-C1-3烷基、氰基-C1-3烷基、H2N-C1-3烷基、氨基、C1-6烷基氨基、二(C1-6烷基)氨基、硫代基、C1-6烷硫基、C1-6烷基亚磺酰基、C1-6烷基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、羧基、C1-6烷基羰基、C1-6烷氧基羰基、C1-6烷基羰基氨基、C1-6烷基磺酰基氨基、氨基磺酰基、C1-6烷基氨基磺酰基、二(C1-6烷基)氨基磺酰基、氨基磺酰基氨基、C1-6烷基氨基磺酰基氨基、二(C1-6烷基)氨基磺酰基氨基、氨基羰基氨基、C1-6烷基氨基羰基氨基和二(C1-6烷基)氨基羰基氨基;且
n是0、1、2、3或4;
条件为R4不是未取代或取代的4-吗啉基、4-硫代吗啉基、1-氧负离子基-4-硫代吗啉基和1,1-二氧负离子基-4-硫代吗啉基。
在一些实施方案中,本文提供式(I)的化合物或其药学上可接受的盐,其中:
CyA是C3-12环烷基或4-12元杂环烷基;其中所述4-12元杂环烷基具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中所述N和S任选被氧化;其中所述4-12元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述C3-12环烷基和4-12元杂环烷基各自任选被1、2、3或4个独立地选自RA的取代基取代;
A是N或CF;
R1选自H、D、卤代基、CN、C1-6烷基、ORa15和NRc15Rd15;其中所述C1-6烷基任选被1、2或3个独立地选自Rg的取代基取代;
R2选自H、D、Cy2、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、卤代基、CN、NO2、ORa、SRa、C(O)Rb、C(O)NRcRd、C(O)ORa、OC(O)Rb、OC(O)NRcRd、NRcRd、NRcC(O)Rb、NRcC(O)ORa、NRcC(O)NRcRd、C(=NRe)Rb、C(=NORa)Rb、C(=NRe)NRcRd、NRcC(=NRe)NRcRd、NRcS(O)Rb、NRcS(O)2Rb、NRcS(O)2NRcRd、S(O)Rb、S(O)NRcRd、S(O)2Rb、S(O)2NRcRd和BRhRi;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自R10的取代基取代;
Cy2选自C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述4-10元杂环烷基和5-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中所述N和S任选被氧化;其中5-10元杂芳基和4-10元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R10的取代基取代;
R3选自H、D、Cy3、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、卤代基、CN、NO2、ORa4、SRa4、C(O)Rb4、C(O)NRc4Rd4、C(O)ORa4、OC(O)Rb4、OC(O)NRc4Rd4、NRc4Rd4、NRc4C(O)Rb4、NRc4C(O)ORa4、NRc4C(O)NRc4Rd4、C(=NRe4)Rb4、C(=NORa4)Rb4、C(=NRe4)NRc4Rd4、NRc4C(=NRe4)NRc4Rd4、NRc4S(O)Rb4、NRc4S(O)2Rb4、NRc4S(O)2NRc4Rd4、S(O)Rb4、S(O)NRc4Rd4、S(O)2Rb4、S(O)2NRc4Rd4和BRh4Ri4;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自R13的取代基取代;
Cy3选自C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述4-10元杂环烷基和5-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中所述N和S任选被氧化;其中5-10元杂芳基和4-10元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R13的取代基取代;
每个R4独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、NO2、ORa8、SRa8、C(O)Rb8、C(O)NRc8Rd8、C(O)ORa8、OC(O)Rb8、OC(O)NRc8Rd8、NRc8Rd8、NRc8C(O)Rb8、NRc8C(O)ORa8、NRc8C(O)NRc8Rd8、C(=NRe8)Rb8、C(=NORa8)Rb8、C(=NRe8)NRc8Rd8、NRc8C(=NRe8)NRc8Rd8、NRc8S(O)Rb8、NRc8S(O)2Rb8、NRc8S(O)2NRc8Rd8、S(O)Rb8、S(O)NRc8Rd8、S(O)2Rb8、S(O)2NRc8Rd8和BRh8Ri8;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R5的取代基取代;
每个R5独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、ORa9、SRa9、C(O)Rb9、C(O)NRc9Rd9、C(O)ORa9、NRc9Rd9、NRc9C(O)Rb9、NRc9C(O)ORa9、NRc9S(O)Rb9、NRc9S(O)2Rb9、NRc9S(O)2NRc9Rd9、S(O)Rb9、S(O)NRc9Rd9、S(O)2Rb9、S(O)2NRc9Rd9和BRh9Ri9;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R6的取代基取代;
每个R6独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-6环烷基、苯基、5-6元杂芳基、4-7元杂环烷基、卤代基、D、CN、ORa10、SRa10、C(O)Rb10、C(O)NRc10Rd10、C(O)ORa10、NRc10Rd10、NRc10C(O)Rb10、NRc10C(O)ORa10、NRc10S(O)Rb10、NRc10S(O)2Rb10、NRc10S(O)2NRc10Rd10、S(O)Rb10、S(O)NRc10Rd10、S(O)2Rb10和S(O)2NRc10Rd10;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-6环烷基、苯基、5-6元杂芳基和4-7元杂环烷基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
RA选自H、D、Cy1、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、卤代基、CN、NO2、ORa11、SRa11、C(O)Rb11、C(O)NRc11Rd11、C(O)ORa11、OC(O)Rb11、OC(O)NRc11Rd11、NRc11Rd11、NRc11C(O)Rb11、NRc11C(O)ORa11、NRc11C(O)NRc11Rd11、C(=NRe11)Rb11、C(=NORa11)Rb11、C(=NRe11)NRc11Rd11、NRc11C(=NRe11)NRc11Rd11、NRc11S(O)Rb11、NRc11S(O)2Rb11、NRc11S(O)2NRc11Rd11、S(O)Rb11、S(O)NRc11Rd11、S(O)2Rb11、S(O)2NRc11Rd11和BRh11Ri11;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自R7的取代基取代;
Cy1选自C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述4-10元杂环烷基和5-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中所述N和S任选被氧化;其中5-10元杂芳基和4-10元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R7的取代基取代;
每个R7独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、NO2、ORa12、SRa12、C(O)Rb12、C(O)NRc12Rd12、C(O)ORa12、OC(O)Rb12、OC(O)NRc12Rd12、NRc12Rd12、NRc12C(O)Rb12、NRc12C(O)ORa12、NRc12C(O)NRc12Rd12、C(=NRe12)Rb12、C(=NORa12)Rb12、C(=NRe12)NRc12Rd12、NRc12C(=NRe12)NRc12Rd12、NRc12S(O)Rb12、NRc12S(O)2Rb12、NRc12S(O)2NRc12Rd12、S(O)Rb12、S(O)NRc12Rd12、S(O)2Rb12、S(O)2NRc12Rd12和BRh12Ri12;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R8的取代基取代;
每个R8独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、ORa13、SRa13、C(O)Rb13、C(O)NRc13Rd13、C(O)ORa13、NRc13Rd13、NRc13C(O)Rb13、NRc13C(O)ORa13、NRc13S(O)Rb13、NRc13S(O)2Rb13、NRc13S(O)2NRc13Rd13、S(O)Rb13、S(O)NRc13Rd13、S(O)2Rb13S(O)2NRc13Rd13和BRh13Ri13;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R9的取代基取代;
每个R9独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-6环烷基、苯基、5-6元杂芳基、4-7元杂环烷基、卤代基、D、CN、ORa14、SRa14、C(O)Rb14、C(O)NRc14Rd14、C(O)ORa14、NRc14Rd14、NRc14C(O)Rb14、NRc14C(O)ORa14、NRc14S(O)Rb14、NRc14S(O)2Rb14、NRc14S(O)2NRc14Rd14、S(O)Rb14、S(O)NRc14Rd14、S(O)2Rb14和S(O)2NRc14Rd14;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-6环烷基、C6-10芳基、5-10元杂芳基和4-7元杂环烷基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个R10独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、NRc1C(O)NRc1Rd1、C(=NRe1)Rb1、C(=NORa1)Rb1、C(=NRe1)NRc1Rd1、NRc1C(=NRe1)NRc1Rd1、NRc1S(O)Rb1、NRc1S(O)2Rb1、NRc1S(O)2NRc1Rd1、S(O)Rb1、S(O)NRc1Rd1、S(O)2Rb1、S(O)2NRc1Rd1和BRh1Ri1;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R11的取代基取代;
每个R11独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、ORa2、SRa2、C(O)Rb2、C(O)NRc2Rd2、C(O)ORa2、NRc2Rd2、NRc2C(O)Rb2、NRc2C(O)ORa2、NRc2S(O)Rb2、NRc2S(O)2Rb2、NRc2S(O)2NRc2Rd2、S(O)Rb2、S(O)NRc2Rd2、S(O)2Rb2S(O)2NRc2Rd2和BRh2Ri2;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R12的取代基取代;
每个R12独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-6环烷基、苯基、5-6元杂芳基、4-7元杂环烷基、卤代基、D、CN、ORa3、SRa3、C(O)Rb3、C(O)NRc3Rd3、C(O)ORa3、NRc3Rd3、NRc3C(O)Rb3、NRc3C(O)ORa3、NRc3S(O)Rb3、NRc3S(O)2Rb3、NRc3S(O)2NRc3Rd3、S(O)Rb3、S(O)NRc3Rd3、S(O)2Rb3和S(O)2NRc3Rd3;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-6环烷基、C6-10芳基、5-10元杂芳基和4-7元杂环烷基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个R13独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、NO2、ORa5、SRa5、C(O)Rb5、C(O)NRc5Rd5、C(O)ORa5、OC(O)Rb5、OC(O)NRc5Rd5、NRc5Rd5、NRc5C(O)Rb5、NRc5C(O)ORa5、NRc5C(O)NRc5Rd5、C(=NRe5)Rb5、C(=NORa5)Rb5、C(=NRe5)NRc5Rd5、NRc5C(=NRe5)NRc5Rd5、NRc5S(O)Rb5、NRc5S(O)2Rb5、NRc5S(O)2NRc5Rd5、S(O)Rb5、S(O)NRc5Rd5、S(O)2Rb5、S(O)2NRc5Rd5和BRh5Ri5;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R14的取代基取代;
每个R14独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、ORa6、SRa6、C(O)Rb6、C(O)NRc6Rd6、C(O)ORa6、NRc6Rd6、NRc6C(O)Rb6、NRc6C(O)ORa6、NRc6S(O)Rb6、NRc6S(O)2Rb6、NRc6S(O)2NRc6Rd6、S(O)Rb6、S(O)NRc6Rd6、S(O)2Rb6S(O)2NRc6Rd6和BRh6Ri6;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R15的取代基取代;
每个R15独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-6环烷基、苯基、5-6元杂芳基、4-7元杂环烷基、卤代基、D、CN、ORa7、SRa7、C(O)Rb7、C(O)NRc7Rd7、C(O)ORa7、NRc7Rd7、NRc7C(O)Rb7、NRc7C(O)ORa7、NRc7S(O)Rb7、NRc7S(O)2Rb7、NRc7S(O)2NRc7Rd7、S(O)Rb7、S(O)NRc7Rd7、S(O)2Rb7和S(O)2NRc7Rd7;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-6环烷基、C6-10芳基、5-10元杂芳基和4-7元杂环烷基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Ra、Rc和Rd独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R10的取代基取代;
或者与同一N原子连接的任何Rc和Rd与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R10的取代基取代的4、5、6或7元杂环烷基;
每个Rb独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R10的取代基取代;
每个Re独立地选自H、CN、C1-6烷基、C1-6卤代烷基、C1-6烷硫基、C1-6烷基磺酰基、C1-6烷基羰基、C1-6烷基氨基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、氨基磺酰基、C1-6烷基氨基磺酰基和二(C1-6烷基)氨基磺酰基;
每个Rh和Ri独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh和Ri均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra1、Rc1和Rd1独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R11的取代基取代;
或者与同一N原子连接的任何Rc1和Rd1与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R11的取代基取代的4、5、6或7元杂环烷基;
每个Rb1独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R11的取代基取代;
每个Re1独立地选自H、CN、C1-6烷基、C1-6卤代烷基、C1-6烷硫基、C1-6烷基磺酰基、C1-6烷基羰基、C1-6烷基氨基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、氨基磺酰基、C1-6烷基氨基磺酰基和二(C1-6烷基)氨基磺酰基;
每个Rh1和Ri1独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh1和Ri1均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra2、Rc2和Rd2独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R12的取代基取代;
或者与同一N原子连接的任何Rc2和Rd2与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R12的取代基取代的4、5、6或7元杂环烷基;
每个Rb2独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R12的取代基取代;
每个Rh2和Ri2独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh2和Ri2均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra3、Rc3和Rd3独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Rb3独立地选自C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Ra4、Rc4和Rd4独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R13的取代基取代;
或者与同一N原子连接的任何Rc4和Rd4与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R13的取代基取代的4、5、6或7元杂环烷基;
每个Rb4独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R13的取代基取代;
每个Re4独立地选自H、CN、C1-6烷基、C1-6卤代烷基、C1-6烷硫基、C1-6烷基磺酰基、C1-6烷基羰基、C1-6烷基氨基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、氨基磺酰基、C1-6烷基氨基磺酰基和二(C1-6烷基)氨基磺酰基;
每个Rh4和Ri4独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh4和Ri4均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra5、Rc5和Rd5独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R14的取代基取代;
或者与同一N原子连接的任何Rc5和Rd5与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R14的取代基取代的4、5、6或7元杂环烷基;
每个Rb5独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R14的取代基取代;
每个Re5独立地选自H、CN、C1-6烷基、C1-6卤代烷基、C1-6烷硫基、C1-6烷基磺酰基、C1-6烷基羰基、C1-6烷基氨基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、氨基磺酰基、C1-6烷基氨基磺酰基和二(C1-6烷基)氨基磺酰基;
每个Rh5和Ri5独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh5和Ri5均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra6、Rc6和Rd6独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R15的取代基取代;
或者与同一N原子连接的任何Rc6和Rd6与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R15的取代基取代的4、5、6或7元杂环烷基;
每个Rb6独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R15的取代基取代;
每个Rh6和Ri6独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh6和Ri6均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra7、Rc7和Rd7独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Rb7独立地选自C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Ra8、Rc8和Rd8独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R5的取代基取代;
或者与同一N原子连接的任何Rc8和Rd8与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R5的取代基取代的4、5、6或7元杂环烷基;
每个Rb8独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R5的取代基取代;
每个Re8独立地选自H、CN、C1-6烷基、C1-6卤代烷基、C1-6烷硫基、C1-6烷基磺酰基、C1-6烷基羰基、C1-6烷基氨基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、氨基磺酰基、C1-6烷基氨基磺酰基和二(C1-6烷基)氨基磺酰基;
每个Rh8和Ri8独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh8和Ri8均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra9、Rc9和Rd9独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R6的取代基取代;
或者与同一N原子连接的任何Rc9和Rd9与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R6的取代基取代的4、5、6或7元杂环烷基;
每个Rb9独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R6的取代基取代;
每个Rh9和Ri9独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh9和Ri9均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra10、Rc10和Rd10独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Rb10独立地选自C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Ra11、Rc11和Rd11独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R7的取代基取代;
或者与同一N原子连接的任何Rc11和Rd11与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R7的取代基取代的4、5、6或7元杂环烷基;
每个Rb11独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R7的取代基取代;
每个Re11独立地选自H、CN、C1-6烷基、C1-6卤代烷基、C1-6烷硫基、C1-6烷基磺酰基、C1-6烷基羰基、C1-6烷基氨基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、氨基磺酰基、C1-6烷基氨基磺酰基和二(C1-6烷基)氨基磺酰基;
每个Rh11和Ri11独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh11和Ri11均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra12、Rc12和Rd12独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R8的取代基取代;
或者与同一N原子连接的任何Rc12和Rd12与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R8的取代基取代的4、5、6或7元杂环烷基;
每个Rb12独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R8的取代基取代;
每个Re12独立地选自H、CN、C1-6烷基、C1-6卤代烷基、C1-6烷硫基、C1-6烷基磺酰基、C1-6烷基羰基、C1-6烷基氨基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、氨基磺酰基、C1-6烷基氨基磺酰基和二(C1-6烷基)氨基磺酰基;
每个Rh12和Ri12独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh12和Ri12均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra13、Rc13和Rd13独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R9的取代基取代;
或者与同一N原子连接的任何Rc13和Rd13与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R9的取代基取代的4、5、6或7元杂环烷基;
每个Rb13独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R9的取代基取代;
每个Rh13和Ri13独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh13和Ri13均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra14、Rc14和Rd14独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Rb14独立地选自C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Ra15、Rc15和Rd15独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Rg独立地选自OH、NO2、CN、卤代基、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-6环烷基、C3-6环烷基-C1-2亚烷基、C1-6烷氧基、C1-6卤代烷氧基、C1-3烷氧基-C1-3烷基、C1-3烷氧基-C1-3烷氧基、HO-C1-3烷氧基、HO-C1-3烷基、氰基-C1-3烷基、H2N-C1-3烷基、氨基、C1-6烷基氨基、二(C1-6烷基)氨基、硫代基、C1-6烷硫基、C1-6烷基亚磺酰基、C1-6烷基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、羧基、C1-6烷基羰基、C1-6烷氧基羰基、C1-6烷基羰基氨基、C1-6烷基磺酰基氨基、氨基磺酰基、C1-6烷基氨基磺酰基、二(C1-6烷基)氨基磺酰基、氨基磺酰基氨基、C1-6烷基氨基磺酰基氨基、二(C1-6烷基)氨基磺酰基氨基、氨基羰基氨基、C1-6烷基氨基羰基氨基和二(C1-6烷基)氨基羰基氨基;且
n是0、1、2、3或4。
在一些实施方案中,本文提供式(I)的化合物或其药学上可接受的盐,其中
CyA是4-12元杂环烷基;其中所述4-12元杂环烷基具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中所述4-12元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述4-12元杂环烷基各自任选被1、2、3或4个独立地选自RA的取代基取代;
A是N;
R1选自H、D、卤代基、CN、C1-6烷基和ORa15;其中所述C1-6烷基任选被1、2或3个独立地选自Rg的取代基取代;
R2选自H、D、Cy2、C1-6烷基、C1-6卤代烷基、卤代基、CN;其中所述C1-6烷基任选被1、2、3或4个独立地选自R10的取代基取代;
Cy2选自4-10元杂环烷基和5-10元杂芳基;其中所述4-10元杂环烷基和5-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中5-10元杂芳基和4-10元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述4-10元杂环烷基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R10的取代基取代;
R3选自H、D、Cy3、卤代基和CN;
Cy3是5-10元杂芳基;其中所述5-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中5-10元杂芳基的成环碳原子任选被氧代基取代以形成羰基;且其中所述5-10元杂芳基任选被1、2、3或4个独立地选自R13的取代基取代;
每个R4独立地选自C1-6烷基、C1-6卤代烷基、卤代基、D、CN和ORa8;其中所述C1-6烷基任选被1、2、3或4个独立地选自R5的取代基取代;
每个R5独立地选自C1-6烷基、C1-6卤代烷基、卤代基、D、CN、ORa9和NRc9Rd9;
RA选自H、D、Cy1、C1-6烷基、C1-6卤代烷基、卤代基、CN、ORa11、C(O)NRc11Rd11和NRc11Rd11;其中所述C1-6烷基任选被1、2、3或4个独立地选自R7的取代基取代;
Cy1是5-10元杂芳基;其中所述5-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中5-10元杂芳基的成环碳原子任选被氧代基取代以形成羰基;且其中所述5-10元杂芳基各自任选被1、2、3或4个独立地选自R7的取代基取代;
每个R7独立地选自C1-6烷基、卤代基、D、CN、ORa12和NRc12Rd12;
每个R10独立地选自C1-6烷基、C1-6卤代烷基、4-10元杂环烷基、卤代基、D、CN、ORa1、C(O)NRc1Rd1和NRc1Rd1;其中所述C1-6烷基和4-10元杂环烷基各自任选被1、2、3或4个独立地选自R11的取代基取代;
每个R11独立地选自C1-6烷基、C1-6卤代烷基、卤代基、D、CN和ORa2;
每个R13独立地选自C1-6烷基和C1-6卤代烷基;
每个Ra1、Rc1和Rd1独立地选自H、C1-6烷基、C1-6卤代烷基和C3-10环烷基;其中所述C1-6烷基和C3-10环烷基各自任选被1、2、3或4个独立地选自R11的取代基取代;
每个Ra2、Rc2和Rd2独立地选自H、C1-6烷基和C1-6卤代烷基;
每个Ra8、Rc8和Rd8独立地选自H、C1-6烷基和C1-6卤代烷基;
每个Ra9、Rc9和Rd9独立地选自H、C1-6烷基和C1-6卤代烷基;
每个Ra11、Rc11和Rd11独立地选自H、C1-6烷基和C1-6卤代烷基;其中所述C1-6烷基任选被1、2、3或4个独立地选自R7的取代基取代;
每个Ra12、Rc12和Rd12独立地选自H、C1-6烷基和C1-6卤代烷基;
每个Ra15、Rc15和Rd15独立地选自H、C1-6烷基和C1-6卤代烷基;其中所述C1-6烷基任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Rg独立地选自OH、CN、卤代基、C1-6烷基、C1-6卤代烷基、C1-6烷氧基、C1-6卤代烷氧基、氨基、C1-6烷硫基、C1-6烷基磺酰基;且
n是0、1、2或3。
在一些实施方案中,本文提供式(I)的化合物或其药学上可接受的盐,其中:
CyA是C3-12环烷基或4-12元杂环烷基;其中所述4-12元杂环烷基具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中所述N和S任选被氧化;其中所述4-12元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述C3-12环烷基和4-12元杂环烷基各自任选被1、2、3或4个独立地选自RA的取代基取代;
A是N或CR16;
R16选自H、D、C1-6烷基、卤代基、CN和ORa16;
R1选自H、D、卤代基、CN、C1-6烷基和ORa15;其中所述C1-6烷基任选被1、2或3个独立地选自Rg的取代基取代;
R2选自H、D、Cy2、C1-6烷基、C1-6卤代烷基、卤代基、CN和S(O)2Rb;其中所述C1-6烷基任选被1、2、3或4个独立地选自R10的取代基取代;
Cy2选自C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述4-10元杂环烷基和5-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中所述N和S任选被氧化;其中5-10元杂芳基和4-10元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R10的取代基取代;
R3选自H、D、Cy3、卤代基和CN;
Cy3是6-10元杂芳基;其中所述6-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;
每个R4独立地选自C1-6烷基、C1-6卤代烷基、C3-10环烷基、卤代基、D、CN和ORa8;
每个R5独立地选自卤代基、D和CN;
RA选自H、D、Cy1、C1-6烷基、C1-6卤代烷基、卤代基、CN、ORa11、C(O)NRc11Rd11和NRc11Rd11;其中所述C1-6烷基任选被1、2、3或4个独立地选自R7的取代基取代;
Cy1选自C3-10环烷基和5-10元杂芳基;其中所述5-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中5-10元杂芳基的成环碳原子任选被氧代基取代以形成羰基;且其中所述C3-10环烷基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R7的取代基取代;
每个R7独立地选自C1-6烷基、卤代基、D、CN、ORa12和NRc12Rd12;
每个R10独立地选自C1-6烷基、C1-6卤代烷基、4-10元杂环烷基、卤代基、D、CN、ORa1、C(O)NRc1Rd1和NRc1Rd1;其中所述C1-6烷基和4-10元杂环烷基各自任选被1、2、3或4个独立地选自R11的取代基取代;
每个R11独立地选自C1-6烷基、C1-6卤代烷基、卤代基、D、CN和ORa2;
每个R13独立地选自C1-6烷基;
每个Rb独立地为C1-6烷基;
每个Ra1、Rc1和Rd1独立地选自H、C1-6烷基、C1-6卤代烷基和C3-10环烷基;其中所述C1-6烷基和C3-10环烷基各自任选被1、2、3或4个独立地选自R11的取代基取代;
每个Ra2、Rc2和Rd2独立地选自H、C1-6烷基和C1-6卤代烷基;
每个Ra8、Rc8和Rd8独立地选自H、C1-6烷基和C1-6卤代烷基;
每个Ra11、Rc11和Rd11独立地选自H、C1-6烷基和C1-6卤代烷基;其中所述C1-6烷基任选被1、2、3或4个独立地选自R7的取代基取代;
每个Ra12、Rc12和Rd12独立地选自H、C1-6烷基和C1-6卤代烷基;
每个Ra15、Rc15和Rd15独立地选自H、C1-6烷基和C1-6卤代烷基;其中所述C1-6烷基任选被1、2、3或4个独立地选自Rg的取代基取代;
Ra16独立地选自H和C1-6烷基;
每个Rg独立地选自OH、CN、卤代基、C1-6烷基、C1-6卤代烷基、C1-6烷氧基、C1-6卤代烷氧基、氨基、C1-6烷硫基、C1-6烷基磺酰基;且
n是0、1、2或3。
在一些实施方案中,CyA是4-12元杂环烷基;其中所述4-12元杂环烷基具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中所述4-12元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述4-12元杂环烷基各自任选被1、2、3或4个独立地选自RA的取代基取代。
在一些实施方案中,CyA选自2,5-二氮杂双环[2.2.1]庚-2-基;3-氨基吡咯烷-1-基;2-(氨甲基)吡咯烷-1-基;2-(羟甲基)吡咯烷-1-基;2-(甲氧基甲基)吡咯烷-1-基;4-氨基-2-(羟甲基)吡咯烷-1-基;4-羟基-2-甲基吡咯烷-1-基;2-(吡啶-2-基)吡咯烷-1-基;六氢吡咯并[3,4-b]吡咯-1(2H)-基;2-甲基哌嗪-1-基;2-(羟甲基)哌嗪-1-基;3-(羟甲基)吗啉代;5-乙基-2,5-二氮杂双环[2.2.1]庚-2-基;(2-羟乙基)-2,5-二氮杂双环[2.2.1]庚-2-基);5-(丙基氨甲酰基)-2,5-二氮杂双环[2.2.1]庚-2-基;4-羟基-2-(羟甲基)吡咯烷-1-基;2-(羟甲基)-5-甲基哌嗪-1-基;6-(羟甲基)-4,7-二氮杂螺[2.5]辛-7-基;4-氨基-2-(1-羟基环丙基)吡咯烷-1-基;4-氨基-2-(2-羟基丙-2-基)吡咯烷-1-基;4-氨基-2-(羟甲基-d2)吡咯烷-1-基;3-(羟甲基)-2,5-二氮杂双环[2.2.1]庚-2-基;4-氨基-2-甲基哌啶-1-基;哌啶-4-基;4-(二甲氨基)-2-(羟甲基)吡咯烷-1-基;2-(羟甲基)-4-(异丙基氨基)吡咯烷-1-基;4-(羟甲基)-5-甲基-2,5-二氮杂双环[2.2.1]庚-2-基;2-(羟甲基)吗啉代;2-(2-((二甲氨基)甲基)吗啉代;2-(氰甲基)吗啉代;3-氧代四氢-3H-噁唑并[3,4-a]吡嗪-7(1H)-基;3-(羟甲基)哌嗪-1-基;3-(甲氧基甲基)氮杂环丁-1-基;2-(羟甲基)氮杂环丁-1-基;2-((二甲氨基)甲基)氮杂环丁-1-基;4-甲基哌嗪-1-基;和4-(2-羟乙基)哌嗪-1-基。
在一些实施方案中,CyA选自2,5-二氮杂双环[2.2.1]庚-2-基;3-氨基吡咯烷-1-基;2-(氨甲基)吡咯烷-1-基;2-(羟甲基)吡咯烷-1-基;2-(甲氧基甲基)吡咯烷-1-基;4-氨基-2-(羟甲基)吡咯烷-1-基;4-羟基-2-甲基吡咯烷-1-基;2-(吡啶-2-基)吡咯烷-1-基;六氢吡咯并[3,4-b]吡咯-1(2H)-基;2-甲基哌嗪-1-基;2-(羟甲基)哌嗪-1-基;3-(羟甲基)吗啉代;5-乙基-2,5-二氮杂双环[2.2.1]庚-2-基;(2-羟乙基)-2,5-二氮杂双环[2.2.1]庚-2-基);5-(丙基氨甲酰基)-2,5-二氮杂双环[2.2.1]庚-2-基;4-羟基-2-(羟甲基)吡咯烷-1-基;2-(羟甲基)-5-甲基哌嗪-1-基;6-(羟甲基)-4,7-二氮杂螺[2.5]辛-7-基;4-氨基-2-(1-羟基环丙基)吡咯烷-1-基;4-氨基-2-(2-羟基丙-2-基)吡咯烷-1-基;4-氨基-2-(羟甲基-d2)吡咯烷-1-基;3-(羟甲基)-2,5-二氮杂双环[2.2.1]庚-2-基;和4-氨基-2-甲基哌啶-1-基。
在一些实施方案中,CyA选自2,5-二氮杂双环[2.2.1]庚-2-基;3-氨基吡咯烷-1-基;2-(氨甲基)吡咯烷-1-基;2-(羟甲基)吡咯烷-1-基;2-(甲氧基甲基)吡咯烷-1-基;4-氨基-2-(羟甲基)吡咯烷-1-基;4-羟基-2-甲基吡咯烷-1-基;2-(吡啶-2-基)吡咯烷-1-基;六氢吡咯并[3,4-b]吡咯-1(2H)-基;2-甲基哌嗪-1-基;2-(羟甲基)哌嗪-1-基;3-(羟甲基)吗啉代;5-乙基-2,5-二氮杂双环[2.2.1]庚-2-基;(2-羟乙基)-2,5-二氮杂双环[2.2.1]庚-2-基);和5-(丙基氨甲酰基)-2,5-二氮杂双环[2.2.1]庚-2-基。
在一些实施方案中,CyA选自4-羟基-2-(羟甲基)吡咯烷-1-基;2-(羟甲基)-5-甲基哌嗪-1-基;6-(羟甲基)-4,7-二氮杂螺[2.5]辛-7-基;4-氨基-2-(1-羟基环丙基)吡咯烷-1-基;4-氨基-2-(2-羟基丙-2-基)吡咯烷-1-基;4-氨基-2-(羟甲基-d2)吡咯烷-1-基;3-(羟甲基)-2,5-二氮杂双环[2.2.1]庚-2-基;和4-氨基-2-甲基哌啶-1-基。
在一些实施方案中,CyA是4-氨基-2-(羟甲基)吡咯烷-1-基。
在一些实施方案中,CyA是5元杂环烷基。
在一些实施方案中,CyA选自2,5-二氮杂双环[2.2.1]庚基、吡咯烷基、六氢吡咯并[3,4-b]吡咯-1(2H)-基和哌嗪基,其每一者任选被1、2、3或4个独立地选自RA的取代基取代。
在一些实施方案中,CyA是C3-10环烷基,其中所述C3-10环烷基任选被1、2或3个独立地选自RA的取代基取代。在一些实施方案中,CyA选自环戊基和环己基,其中所述环戊基和环己基任选被NH2取代。
在一些实施方案中,A是N。
在一些实施方案中,A是CF。
在一些实施方案中,A是CR16。
在一些实施方案中,R16是H、CN或ORa16。
在一些实施方案中,Ra16独立地选自H和C1-6烷基。在一些实施方案中,Ra16是甲基。
在一些实施方案中,R1选自H、D、卤代基、CN、C1-6烷基和ORa15;其中所述C1-6烷基任选被1、2或3个独立地选自Rg的取代基取代。
在一些实施方案中,R1选自H、D、F、CN、甲基、羟甲基和甲氧基。
在一些实施方案中,R1是H或D。在一些实施方案中,R1是H。在一些实施方案中,R1是D。
在一些实施方案中,R1是卤代基。
在一些实施方案中,R1是F。
在一些实施方案中,R1是ORa15。
在一些实施方案中,R1是甲氧基。
在一些实施方案中,R1是C1-6烷基;其中所述C1-6烷基任选被1、2或3个独立地选自Rg的取代基取代。
在一些实施方案中,R1是羟甲基。
在一些实施方案中,R1是CN。
在一些实施方案中,R1是甲基。
在一些实施方案中,R2选自H、D、Cy2、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、卤代基、CN、NO2、ORa、SRa、C(O)Rb、C(O)NRcRd、C(O)ORa、NRcRd、NRcC(O)Rb、NRcC(O)ORa和S(O)2Rb;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自R10的取代基取代。
在一些实施方案中,R2选自H、D、Cy2、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、卤代基、CN、NO2、ORa、SRa、C(O)Rb、C(O)NRcRd、C(O)ORa、NRcRd、NRcC(O)Rb和NRcC(O)ORa;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自R10的取代基取代。
在一些实施方案中,R2选自H、D、Cy2、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、卤代基、CN和ORa;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自R10的取代基取代。
在一些实施方案中,R2选自H、D、Cy2、C1-6烷基、C1-6卤代烷基、卤代基、CN;其中所述C1-6烷基任选被1、2、3或4个独立地选自R10的取代基取代。
在一些实施方案中,R2选自H、D、Cy2、C1-6烷基、卤代基和S(O)2Rb;其中所述C1-6烷基任选被1、2、3或4个独立地选自R10的取代基取代。
在一些实施方案中,R2选自H、D、Cy2、C1-6烷基和卤代基;其中所述C1-6烷基任选被1、2、3或4个独立地选自R10的取代基取代。
在一些实施方案中,R2是H或D。在一些实施方案中,R2是H。在一些实施方案中,R2是D。
在一些实施方案中,R2是C1-6烷基;其中所述C1-6烷基任选被1、2、3或4个独立地选自R10的取代基取代。
在一些实施方案中,R2选自异丙基、F、Cl、Br和S(O)2CH3。
在一些实施方案中,R2是异丙基。
在一些实施方案中,R2是卤代基。
在一些实施方案中,R2选自Br、Cl和F。
在一些实施方案中,R2是Br。
在一些实施方案中,R2是S(O)2CH3。
在一些实施方案中,R2是Cy2。
在一些实施方案中,Cy2选自4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述4-10元杂环烷基和5-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中所述N和S任选被氧化;其中5-10元杂芳基和4-10元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R10的取代基取代。
在一些实施方案中,Cy2选自4-10元杂环烷基和5-10元杂芳基;其中所述4-10元杂环烷基和5-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中5-10元杂芳基和4-10元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述4-10元杂环烷基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R10的取代基取代。
在一些实施方案中,Cy2是任选被1、2、3或4个独立地选自R10的取代基取代的C6-10芳基。
Cy2选自1-甲基-1H-吡唑-4-基;6-(羟甲基)吡啶-3-基;6-(甲基氨甲酰基)吡啶-3-基;1-甲基-6-氧代-1,6-二氢吡啶-3-基;2-甲基吡啶-3-基;4-甲氧基吡啶-3-基;4-氰基吡啶-3-基;1,3,5-三甲基-1H-吡唑-4-基;吗啉代;氮杂环丁-1-基;2-(甲氧基甲基)氮杂环丁-1-基);3-氰基吡啶-4-基;3-甲氧基吡啶-4-基;2-氰基-6-氟苯基;3-氰基吡啶-2-基;4-氰基-1-甲基-1H-吡唑-5-基;四氢-2H-吡喃-4-基;5-氰基-2-(吡咯烷-1-基)吡啶-4-基;和1-氰基环丙基。在一些实施方案中,Cy2选自1-甲基-1H-吡唑-4-基;6-(羟甲基)吡啶-3-基;6-(甲基氨甲酰基)吡啶-3-基;1-甲基-6-氧代-1,6-二氢吡啶-3-基;2-甲基吡啶-3-基;4-甲氧基吡啶-3-基;4-氰基吡啶-3-基;1,3,5-三甲基-1H-吡唑-4-基;吗啉代;氮杂环丁-1-基;2-(甲氧基甲基)氮杂环丁-1-基);3-氰基吡啶-4-基;3-甲氧基吡啶-4-基;2-氰基-6-氟苯基;3-氰基吡啶-2-基;和4-氰基-1-甲基-1H-吡唑-5-基。
在一些实施方案中,Cy2选自1-甲基-1H-吡唑-4-基;6-(羟甲基)吡啶-3-基;6-(甲基氨甲酰基)吡啶-3-基;1-甲基-6-氧代-1,6-二氢吡啶-3-基;2-甲基吡啶-3-基;4-甲氧基吡啶-3-基;4-氰基吡啶-3-基;1,3,5-三甲基-1H-吡唑-4-基;吗啉代;和氮杂环丁-1-基。
在一些实施方案中,Cy2选自2-(甲氧基甲基)氮杂环丁-1-基);3-氰基吡啶-4-基;3-甲氧基吡啶-4-基;2-氰基-6-氟苯基;3-氰基吡啶-2-基;和4-氰基-1-甲基-1H-吡唑-5-基。
在一些实施方案中,Cy2选自3-氰基吡啶-4-基;4-氰基吡啶-3-基;和3-氰基吡啶-2-基。在一些实施方案中,Cy2是4-氰基吡啶-3-基。
在一些实施方案中,Z是N。
在一些实施方案中,Z是CR3。
在一些实施方案中,R3选自H、D、Cy3、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、卤代基、CN、NO2、ORa4、SRa4、C(O)Rb4、C(O)NRc4Rd4、C(O)ORa4、OC(O)Rb4、OC(O)NRc4Rd4、NRc4Rd4、NRc4C(O)Rb4、NRc4C(O)ORa4、NRc4C(O)NRc4Rd4、NRc4S(O)Rb4、NRc4S(O)2Rb4、NRc4S(O)2NRc4Rd4、S(O)Rb4、S(O)NRc4Rd4、S(O)2Rb4、S(O)2NRc4Rd4和BRh4Ri4;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自R13的取代基取代。
在一些实施方案中,R3选自H、D、Cy3、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、卤代基、CN、NO2、ORa4、SRa4、C(O)Rb4、NRc4Rd4和NRc4C(O)Rb4;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自R13的取代基取代。
在一些实施方案中,R3选自H、D、Cy3、卤代基和CN。在一些实施方案中,R3选自H、D、F、Br和CN。
在一些实施方案中,R3是H或D。在一些实施方案中,R3是H。在一些实施方案中,R3是D。
在一些实施方案中,R3是卤代基。
在一些实施方案中,R3是Br。
在一些实施方案中,R3是F。
在一些实施方案中,R3是CN。
在一些实施方案中,R3是Cy3。
在一些实施方案中,Cy3是5-10元杂芳基;其中所述5-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中5-10元杂芳基的成环碳原子任选被氧代基取代以形成羰基;且其中所述5-10元杂芳基任选被1、2、3或4个独立地选自R13的取代基取代。
在一些实施方案中,Cy3是6-10元杂芳基;其中所述6-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中6-10元杂芳基的成环碳原子任选被氧代基取代以形成羰基;且其中所述6-10元杂芳基任选被1、2、3或4个独立地选自R13的取代基取代。
在一些实施方案中,Cy3选自吡啶-3-基和1-甲基-1H-吡唑-4-基。
在一些实施方案中,R4独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、NO2、ORa8、SRa8、C(O)Rb8、C(O)NRc8Rd8、C(O)ORa8、OC(O)Rb8、OC(O)NRc8Rd8、NRc8Rd8、NRc8C(O)Rb8、NRc8C(O)ORa8、NRc8C(O)NRc8Rd8、C(=NRe8)Rb8、C(=NORa8)Rb8、C(=NRe8)NRc8Rd8、NRc8C(=NRe8)NRc8Rd8、NRc8S(O)Rb8、NRc8S(O)2Rb8、NRc8S(O)2NRc8Rd8、S(O)Rb8、S(O)NRc8Rd8、S(O)2Rb8、S(O)2NRc8Rd8和BRh8Ri8;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R5的取代基取代。
在一些实施方案中,R4独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、卤代基、D、CN、NO2、ORa8、SRa8、C(O)Rb8、C(O)NRc8Rd8、C(O)ORa8、NRc8Rd8、NRc8C(O)Rb8、NRc8C(O)ORa8、S(O)Rb8、S(O)NRc8Rd8、S(O)2Rb8和S(O)2NRc8Rd8;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1或2个独立地选自R5的取代基取代。
在一些实施方案中,R4独立地选自C1-6烷基、C1-6卤代烷基、C3-10环烷基、卤代基、D、CN和ORa8;其中所述C1-6烷基任选被1、2、3或4个独立地选自R5的取代基取代。
在一些实施方案中,每个R4独立地选自C1-6烷基、C1-6卤代烷基、卤代基、D、CN和ORa8;其中所述C1-6烷基任选被1、2、3或4个独立地选自R5的取代基取代。
在一些实施方案中,每个R4独立地选自C1-6烷基、C1-6卤代烷基、卤代基、D、CN和ORa8。
在一些实施方案中,每个R4独立地选自D、甲基、F、Cl、CN、甲氧基、甲氧基-d3、乙氧基、二氟甲氧基和环丙基。
在一些实施方案中,每个R4独立地选自卤代基和ORa8。
在一些实施方案中,每个R4独立地选自F和甲氧基。
在一些实施方案中,每个R4独立地选自卤代基。
在一些实施方案中,每个R4独立地选自F和Cl。
在一些实施方案中,每个R4独立地选自F和甲基。
在一些实施方案中,每个R4是F。
在一些实施方案中,R4不是未取代或取代的4-吗啉基、未取代或取代的4-硫代吗啉基、未取代或取代的1-氧负离子基-4-硫代吗啉基或者未取代或取代的1,1-二氧负离子基-4-硫代吗啉基。
在一些实施方案中,每个R5独立地选自C1-6烷基、C1-6卤代烷基、卤代基、D、CN、ORa9和NRc9Rd9。
在一些实施方案中,每个R5独立地选自F和D。
在一些实施方案中,每个RA选自H、D、Cy1、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、卤代基、CN、NO2、ORa11、SRa11、C(O)Rb11、C(O)NRc11Rd11、C(O)ORa11和NRc11Rd11;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自R7的取代基取代。
在一些实施方案中,RA选自H、D、Cy1、C1-6烷基、C1-6卤代烷基、卤代基、CN、ORa11、C(O)NRc11Rd11和NRc11Rd11;其中所述C1-6烷基任选被1、2、3或4个独立地选自R7的取代基取代。
在一些实施方案中,RA选自Cy1、C1-6烷基、ORa11、C(O)NRc11Rd11和NRc11Rd11;其中所述C1-6烷基任选被1、2、3或4个独立地选自R7的取代基取代。
在一些实施方案中,RA是C1-6烷基;其中所述C1-6烷基任选被1、2、3或4个独立地选自R7的取代基取代。
在一些实施方案中,RA选自甲基和乙基;其中所述甲基和乙基各自任选被1、2或3个独立地选自R7的取代基取代。
在一些实施方案中,RA是Cy1。
在一些实施方案中,RA选自OH、NH2、氨甲基、羟甲基、甲氧基甲基、OH、吡啶基、乙基、羟乙基和丙基氨甲酰基。
在一些实施方案中,Cy1选自C3-10环烷基和5-10元杂芳基;其中所述5-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中所述N和S任选被氧化;其中5-10元杂芳基的成环碳原子任选被氧代基取代以形成羰基;且其中所述C3-10环烷基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R7的取代基取代。
在一些实施方案中,Cy1是5-10元杂芳基;其中所述5-10元杂芳基具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;且其中所述5-10元杂芳基任选被1、2、3或4个独立地选自R7的取代基取代。
在一些实施方案中,Cy1选自任选被1、2、3或4个独立地选自R7的取代基取代的C3-10环烷基。
在一些实施方案中,Cy1是吡啶基。在一些实施方案中,Cy1是环丙基。
在一些实施方案中,每个R7独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、卤代基、D、CN、NO2、ORa12、SRa12、C(O)Rb12、C(O)NRc12Rd12、C(O)ORa12、OC(O)Rb12和NRc12Rd12;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自R8的取代基取代。
在一些实施方案中,每个R7独立地选自C1-6烷基、卤代基、D、CN、ORa12和NRc12Rd12。
在一些实施方案中,每个R7独立地选自CN、ORa12、NRc12Rd12和D。
在一些实施方案中,每个R7独立地选自ORa12、D和NRc12Rd12。
在一些实施方案中,每个R7独立地选自D、CN、NH2和甲氧基。
在一些实施方案中,每个R7独立地选自OH、D、NH2和甲氧基。
在一些实施方案中,每个R10独立地选自C1-6烷基、C1-6卤代烷基、4-10元杂环烷基、卤代基、D、CN、ORa1、C(O)NRc1Rd1和NRc1Rd1;其中所述C1-6烷基和4-10元杂环烷基各自任选被1、2、3或4个独立地选自R11的取代基取代。
在一些实施方案中,每个R10独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、4-10元杂环烷基、卤代基、D、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1和NRc1C(O)NRc1Rd1;其中所述C1-6烷基、C2-6烯基、C2-6炔基和4-10元杂环烷基各自任选被1、2、3或4个独立地选自R11的取代基取代。
在一些实施方案中,每个R10独立地选自C1-6烷基、4-10元杂环烷基、CN、OH、ORa1、C(O)NRc1Rd1和NRc1Rd1;其中所述C1-6烷基和4-10元杂环烷基各自任选被1、2、3或4个独立地选自R11的取代基取代。
在一些实施方案中,每个R10独立地选自C1-6烷基、4-10元杂环烷基、卤代基、CN、OH、ORa1、C(O)NRc1Rd1和NRc1Rd1;其中所述C1-6烷基和4-10元杂环烷基各自任选被1、2、3或4个独立地选自R11的取代基取代。
在一些实施方案中,每个R10独立地选自OH、CN、甲基、羟甲基、甲基氨甲酰基、甲氧基、吗啉代和环丁基氨基。
在一些实施方案中,每个R10独立地选自OH、F、CN、甲基、羟甲基、甲基氨甲酰基、甲氧基、吗啉代和环丁基氨基。
在一些实施方案中,每个R11独立地选自C1-6烷基、C1-6卤代烷基、卤代基、D、CN和ORa2。
在一些实施方案中,每个R11是ORa2。在一些实施方案中,每个R11是OH。
在一些实施方案中,每个R13独立地选自C1-6烷基和C1-6卤代烷基。
在一些实施方案中,每个R13独立地为C1-6烷基。
在一些实施方案中,R13是甲基。
在一些实施方案中,每个Ra1、Rc1和Rd1独立地选自H、C1-6烷基、C1-6卤代烷基和C3-10环烷基;其中所述C1-6烷基和C3-10环烷基各自任选被1、2、3或4个独立地选自R11的取代基取代。
在一些实施方案中,每个Ra1、Rc1和Rd1独立地选自H、C1-6烷基和C3-10环烷基;其中所述C1-6烷基和C3-10环烷基各自任选被1、2、3或4个独立地选自R11的取代基取代。
在一些实施方案中,每个Ra2、Rc2和Rd2独立地选自H、C1-6烷基和C1-6卤代烷基。在一些实施方案中,每个Ra2、Rc2和Rd2独立地为H。
在一些实施方案中,每个Ra8、Rc8和Rd8独立地选自H、C1-6烷基和C1-6卤代烷基。在一些实施方案中,每个Ra8、Rc8和Rd8独立地选自H和C1-6烷基。
在一些实施方案中,每个Ra9、Rc9和Rd9独立地选自H、C1-6烷基和C1-6卤代烷基。在一些实施方案中,每个Ra9、Rc9和Rd9独立地选自H和C1-6烷基。
在一些实施方案中,每个Ra11、Rc11和Rd11独立地选自H、C1-6烷基和C1-6卤代烷基;其中所述C1-6烷基任选被1、2、3或4个独立地选自R7的取代基取代。在一些实施方案中,每个Ra11、Rc11和Rd11独立地选自H和C1-6烷基;其中所述C1-6烷基任选被1、2、3或4个独立地选自R7的取代基取代。
在一些实施方案中,每个Ra12、Rc12和Rd12独立地选自H、C1-6烷基和C1-6卤代烷基。
在一些实施方案中,Ra12是H。
在一些实施方案中,Rc12和Rd12各自是H。
在一些实施方案中,每个Ra15、Rc15和Rd15独立地选自H、C1-6烷基和C1-6卤代烷基;其中所述C1-6烷基任选被1、2、3或4个独立地选自Rg的取代基取代。在一些实施方案中,每个Ra15、Rc15和Rd15独立地选自H和C1-6烷基;其中所述C1-6烷基任选被1、2、3或4个独立地选自Rg的取代基取代。
在一些实施方案中,每个Rg独立地选自OH、CN、卤代基、C1-6烷基、C1-6卤代烷基、C1-6烷氧基、C1-6卤代烷氧基、氨基、C1-6烷硫基、C1-6烷基磺酰基。在一些实施方案中,每个Rg是OH。
在一些实施方案中,n是0、1、2、3或4。在一些实施方案中,n是0、1、2或3。在一些实施方案中,n是0。在一些实施方案中,n是1。在一些实施方案中,n是2。在一些实施方案中,n是3。在一些实施方案中,n是4。
在一些实施方案中,本文提供了具有式IA的化合物:
或其药学上可接受的盐。
在一些实施方案中,本文提供了具有式IB的化合物:
或其药学上可接受的盐。
在一些实施方案中,本文提供了具有式IC的化合物:
或其药学上可接受的盐。
在一些实施方案中,本文提供了具有式IIA的化合物:
或其药学上可接受的盐。
在一些实施方案中,本文提供了具有式IIB的化合物:
或其药学上可接受的盐。
在一些实施方案中,本文提供了具有式IIC的化合物:
或其药学上可接受的盐。
在一些实施方案中,本文提供了具有式IID的化合物:
或其药学上可接受的盐。
在一些实施方案中,本文提供了具有式III的化合物:
或其药学上可接受的盐。
在一些实施方案中,本文提供了具有式IV的化合物:
或其药学上可接受的盐。
在一些实施方案中,本文提供了具有式V的化合物:
或其药学上可接受的盐。
在一些实施方案中,本文提供了具有式VI的化合物:
或其药学上可接受的盐。
在一些实施方案中,本文提供选自以下的化合物:
N-(2-((1R,4R)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
(S)-N-(2-(3-氨基吡咯烷-1-基)-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
(R)-N-(2-(2-(氨甲基)吡咯烷-1-基)-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
(R)-N-(5-氟-2-(2-(羟甲基)吡咯烷-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
(R)-N-(5-氟-2-(2-(甲氧基甲基)吡咯烷-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(5-氟-2-((2S,4S)-4-羟基-2-甲基吡咯烷-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(5-氟-2-(2-(吡啶-2-基)吡咯烷-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(5-氟-2-(六氢吡咯并[3,4-b]吡咯-1(2H)-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
(R)-N-(5-氟-2-(2-甲基哌嗪-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
(R)-N-(5-氟-2-(2-(羟甲基)哌嗪-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(5-氟-2-(3-(羟甲基)吗啉代)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1R,4R)-2,5-二氮杂双环[2.2.1]庚-2-基)-3-溴-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1R,4R)-2,5-二氮杂双环[2.2.1]庚-2-基)-3-氰基苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1R,4R)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟-3-(吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1R,4R)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟-3-(1-甲基-1H-吡唑-4-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟-4-(羟甲基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-4-溴-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟-4-(1-甲基-1H-吡唑-4-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟-4-(6-(羟甲基)吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟-4-(6-(甲基氨甲酰基)吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟-4-(1-甲基-6-氧代-1,6-二氢吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟-4-(2-甲基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-4-(2-甲基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-4-(4-甲氧基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-4-(1,3,5-三甲基-1H-吡唑-4-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟-4-吗啉代苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(4-(氮杂环丁-1-基)-2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟-4-(吗啉代甲基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-4-((环丁基氨基)甲基)-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1R,4R)-5-乙基-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(5-氟-2-((1R,4R)-5-(2-羟乙基)-2,5-二氮杂双环[2.2.1]庚-2-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
(1R,4R)-5-(4-氟-2-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)苯基)-N-丙基-2,5-二氮杂双环[2.2.1]庚烷-2-甲酰胺;
N-(2-((1R,4R)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-甲氧基苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1R,4R)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-(羟甲基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;和
N-(2-((1R,4R)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氰基苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
或其药学上可接受的盐。
在一些实施方案中,本文提供选自以下的化合物:
N-(4-(氮杂环丁-1-基)-2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-4-((S)-2-(甲氧基甲基)氮杂环丁-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-4-(3-氰基吡啶-4-基)-3-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(3-氰基吡啶-4-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(2-甲基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(3-甲氧基吡啶-4-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(3-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-2'-氰基-6'-氟联苯-4-基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(3-氰基吡啶-2-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基-1-甲基-1H-吡唑-5-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-异丙基苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(4-(3-氰基吡啶-4-基)-2-((2S,4S)-4-羟基-2-(羟甲基)吡咯烷-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(4-(4-氰基吡啶-3-基)-2-((2S,5R)-2-(羟甲基)-5-甲基哌嗪-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(4-(4-氰基吡啶-3-基)-2-((2S,5S)-2-(羟甲基)-5-甲基哌嗪-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
(S)-N-(4-(4-氰基吡啶-3-基)-2-(6-(羟甲基)-4,7-二氮杂螺[2.5]辛-7-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(1-羟基环丙基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(2-羟基丙-2-基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基-d2)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(4-(4-氰基吡啶-3-基)-2-((1S,3R,4S)-3-(羟甲基)-2,5-二氮杂双环[2.2.1]庚-2-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(4-(4-氰基吡啶-3-基)-2-((1S,4S)-1-(羟甲基)-2,5-二氮杂双环[2.2.1]庚-2-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-甲基哌啶-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-6-(2-氟-6-甲氧基苯基)吡啶酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-5-氰基-6-(2-氟-6-甲氧基苯基)吡啶酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-6-(2-氟-6-甲氧基苯基)-5-甲氧基吡啶酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2,6-二氟苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氯-6-氟苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-6-(1,3,5-三甲基-1H-吡唑-4-基)吡啶-3-基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-5-氟苯基)-2-(2,6-二氟苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-5-氟苯基)-2-(3-氰基-2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-5-氟苯基)-2-(2,3-二氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-5-氟苯基)-2-(2-氟-6-(甲氧基-d3)-3-甲基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基-4-甲基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(3,6-二氟-2-甲基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2,3-二氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(3,6-二氟-2-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(3-氰基-2-氟-6-(甲氧基-d3)苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(3,6-二氟-2-(甲氧基-d3)苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2,3-二氟-6-(甲氧基-d3)苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-(甲氧基-d3)苯基-5-d)嘧啶-4-甲酰胺;
2-(2-氟-6-甲氧基苯基)-N-(2-(哌啶-4-基)苯基)嘧啶-4-甲酰胺;
N-(2-(顺)4-氨基环己基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-(反)4-氨基环己基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-(3-氨基环己基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-(3-氨基环戊基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((顺)-4-氨基环己基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((反)-4-氨基环己基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((顺)-4-氨基环己基)-4-(4-氰基-1-甲基-1H-吡唑-5-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((反)-4-氨基环己基)-4-(4-氰基-1-甲基-1H-吡唑-5-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((顺)-4-氨基环己基)-4-(1,3,5-三甲基-1H-吡唑-4-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(甲基磺酰基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-5-甲基苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-(二甲氨基)-2-(羟甲基)吡咯烷-1-基)-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(5-氟-2-((2S,4S)-2-(羟甲基)-4-(异丙基氨基)吡咯烷-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(四氢-2H-吡喃-4-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-氯苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(5-氰基-2-(吡咯烷-1-基)吡啶-4-基)苯基)-2-(2,6-二氟苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(1-氰基环丙基)苯基)-2-(2,6-二氟苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-(二氟甲氧基)-6-氟苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-(甲氧基-d3)苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-环丙基-6-氟苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-乙氧基-6-氟苯基)嘧啶-4-甲酰胺;
N-(4-(4-氰基吡啶-3-基)-2-((1S,4S)-4-(羟甲基)-5-甲基-2,5-二氮杂双环[2.2.1]庚-2-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
(S)-N-(4-(4-氰基吡啶-3-基)-2-(2-(羟甲基)吗啉代)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
(S)-N-(4-(4-氰基吡啶-3-基)-2-(2-((二甲氨基)甲基)吗啉代)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
(R)-N-(2-(2-(氰甲基)吗啉代)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
(R)-N-(4-(4-氰基吡啶-3-基)-2-(3-氧代四氢-3H-噁唑并[3,4-a]吡嗪-7(1H)-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
(S)-N-(5-氟-2-(3-(羟甲基)哌嗪-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(4-(4-氰基吡啶-3-基)-2-(3-(甲氧基甲基)氮杂环丁-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
(S)-N-(4-(4-氰基吡啶-3-基)-2-(2-(羟甲基)氮杂环丁-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
(R)-N-(4-(4-氰基吡啶-3-基)-2-(2-((二甲氨基)甲基)氮杂环丁-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(4-(4-氰基吡啶-3-基)-2-(4-甲基哌嗪-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(4-(4-氰基吡啶-3-基)-2-(4-(2-羟乙基)哌嗪-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;和
(S)-N-(5-氟-2-(3-(羟甲基)哌嗪-1-基)-4-异丙基苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
或其药学上可接受的盐。
进一步要了解的是,为了清楚起见,在分开的实施方案的背景中描述的本发明的某些特征也可在单个实施方案中组合提供(尽管意图将这些实施方案组合,如同以多项从属形式书写一样)。相反,为了简洁起见,在单个实施方案的背景中描述的本发明的各种特征也可分开或者以任意合适的子组合形式提供。因此,预期描述为式(I)和(I’)的化合物的实施方案的特征能以任意合适的组合来组合。
在本说明书各处以组或范围的形式公开了化合物的某些特征。这种公开特别是意图包括这类组和范围的成元的每一种单独的子组合。例如,术语“C1-6烷基”特别是意图单独公开(但不限于)甲基、乙基、C3烷基、C4烷基、C5烷基和C6烷基。
术语“n元”(其中n是整数)通常描述部分中的成环原子的数目,其中成环原子的数目是n。例如,哌啶基是6元杂环烷基环的实例,吡唑基是5元杂芳基环的实例,吡啶基是6元杂芳基环的实例,且1,2,3,4-四氢-萘是10元环烷基的实例。
在本说明书各处可描述定义二价连接基团的变量。每个连接取代基特别是意图包括连接取代基的前向和后向形式两者。例如,-NR(CR'R”)n-包括-NR(CR'R”)n-和-(CR'R”)nNR-两者,并且意图单独公开每种形式。在结构需要连接基团的情况下,为该基团所列出的马库什变量(Markush variable)被理解为是连接基团。例如,如果结构需要连接基团,并且该变量的马库什基团定义列出了“烷基”或“芳基”,则要理解“烷基”或“芳基”分别代表连接亚烷基或亚芳基。
术语“取代的”意指原子或原子团作为与另一基团连接的“取代基”在形式上置换氢。除另指出外,术语“取代的”是指任何水平的取代,例如单取代、二取代、三取代、四取代或五取代,只要这种取代被允许。取代基是独立选择的,并且取代可位于任何化学上可及的位置上。要理解的是,给定原子上的取代受价态限制。要理解的是,给定原子上的取代产生化学上稳定的分子。短语“任选取代的”意指未取代的或取代的。术语“取代的”意指氢原子被取代基移除和置换。单个二价取代基例如氧代基可置换两个氢原子。
术语“Cn-m”指示包括端点的范围,其中n和m是整数,并且指示碳的数目。实例包括C1-4、C1-6等。
单独或与其它术语组合使用的术语“烷基”是指可以是直链或支链的饱和烃基团。术语“Cn-m烷基”是指具有n至m个碳原子的烷基。烷基在形式上对应于烷烃,其中一个C-H键通过烷基与化合物的其余部分的连接点被置换。在一些实施方案中,烷基含有1至6个碳原子、1至4个碳原子、1至3个碳原子或1至2个碳原子。烷基部分的实例包括但不限于化学基团如甲基、乙基、正丙基、异丙基、正丁基、叔丁基、异丁基、仲丁基;高级同系物如2-甲基-1-丁基、正戊基、3-戊基、正己基、1,2,2-三甲基丙基等。
单独或与其它术语组合使用的术语“烯基”是指对应于具有一个或多个碳-碳双键的烷基的直链或支链烃基团。烯基在形式上对应于烯烃,其中一个C-H键通过烯基与化合物的其余部分的连接点被置换。术语“Cn-m烯基”是指具有n至m个碳的烯基。在一些实施方案中,烯基部分含有2至6、2至4或2至3个碳原子。示例烯基包括但不限于乙烯基、正丙烯基、异丙烯基、正丁烯基、仲丁烯基等。
单独或与其它术语组合使用的术语“炔基”是指对应于具有一个或多个碳-碳三键的烷基的直链或支链烃基团。炔基在形式上对应于炔烃,其中一个C-H键通过烷基与化合物的其余部分的连接点被置换。术语“Cn-m炔基”是指具有n至m个碳的炔基。示例炔基包括但不限于乙炔基、丙炔-1-基、丙炔-2-基等。在一些实施方案中,炔基部分含有2至6个、2至4个或2至3个碳原子。
单独或与其它术语组合使用的术语“亚烷基”是指二价烷基连接基团。亚烷基在形式上对应于烷烃,其中两个C-H键通过亚烷基与化合物的其余部分的连接点被置换。术语“Cn-m亚烷基”是指具有n至m个碳原子的亚烷基。亚烷基的实例包括但不限于乙-1,2-二基、乙-1,1-二基、丙-1,3-二基、丙-1,2-二基、丙-1,1-二基、丁-1,4-二基、丁-1,3-二基、丁-1,2-二基、2-甲基-丙-1,3-二基等。
单独或与其它术语组合使用的术语“烷氧基”是指式-O-烷基的基团,其中所述烷基定义如上。术语“Cn-m烷氧基”是指这样的烷氧基,其烷基具有n至m个碳。示例烷氧基包括甲氧基、乙氧基、丙氧基(例如,正丙氧基和异丙氧基)、叔丁氧基等。在一些实施方案中,烷基具有1至6、1至4或1至3个碳原子。术语“Cn-m二烷氧基”是指式-O-(Cn-m烷基)-O-的连接基团,其烷基具有n至m个碳。示例二烷氧基包括-OCH2CH2O-和OCH2CH2CH2O-。在一些实施方案中,Cn-m二烷氧基的两个O原子可与同一B原子连接以形成5或6元杂环烷基。
术语“氨基”是指式-NH2的基团。
单独或与其它术语组合使用的术语“羰基”是指-C(=O)-基团,其也可书写为C(O)。
术语“氰基”或“腈”是指式-C≡N的基团,其也可书写为-CN。
单独或与其它术语组合使用的术语“卤代基”或“卤素”是指氟代基、氯代基、溴代基和碘代基。在一些实施方案中,“卤代基”是指选自F、Cl或Br的卤素原子。在一些实施方案中,卤代基是F。
如本文所用的术语“卤代烷基”是指其中一个或多个氢原子已被卤素原子置换的烷基。术语“Cn-m卤代烷基”是指具有n至m个碳原子和至少一个至最多{2(n至m)+1}个卤素原子的Cn-m烷基,卤素原子可以是相同的或不同的。在一些实施方案中,卤素原子是氟原子。在一些实施方案中,卤代烷基具有1至6或1至4个碳原子。示例卤代烷基包括CF3、C2F5、CHF2、CH2F、CCl3、CHCl2、C2Cl5等。在一些实施方案中,卤代烷基是氟烷基。
单独或与其它术语组合使用的术语“卤代烷氧基”是指式-O-卤代烷基的基团,其中卤代烷基定义如上。术语“Cn-m卤代烷氧基”是指这样的卤代烷氧基,其卤代烷基具有n至m个碳。示例卤代烷氧基包括三氟甲氧基等。在一些实施方案中,卤代烷氧基具有1至6、1至4或1至3个碳原子。
术语“氧代基”是指这样的氧原子,其作为二价取代基当与碳连接时形成羰基,或者与杂原子连接形成亚砜或砜基团或N-氧化物基团。在一些实施方案中,杂环基团可任选被1或2个氧代基(=O)取代基取代。
术语“硫离子基(sulfido)”是指这样的硫原子,其作为二价取代基当与碳连接时形成硫代羰基(C=S)。
关于成环N原子的术语“氧化的”是指成环N-氧化物。
关于成环S原子的术语“氧化的”是指成环磺酰基或成环亚磺酰基。
术语“芳族”是指具有一个或多个具有芳族特征(即,具有(4n+2)个离域π(pi)电子,其中n是整数)的多不饱和环的碳环或杂环。
单独或与其它术语组合使用的术语“芳基”是指芳族烃基团,其可以是单环或多环的(例如,具有2个稠环)。术语“Cn-m芳基”是指具有n至m个环碳原子的芳基。芳基包括例如苯基、萘基等。在一些实施方案中,芳基具有6至约10个碳原子。在一些实施方案中,芳基具有6个碳原子。在一些实施方案中,芳基具有10个碳原子。在一些实施方案中,芳基是苯基。在一些实施方案中,芳基是萘基。
单独或与其它术语组合使用的术语“杂芳基”或“杂芳族”是指具有至少一个选自硫、氧和氮的杂原子环成员的单环或多环芳族杂环。在一些实施方案中,杂芳基环具有1、2、3或4个独立地选自氮、硫和氧的杂原子环成员。在一些实施方案中,杂芳基部分中的任何成环N均可以是N-氧化物。在一些实施方案中,杂芳基具有5-14个包括碳原子在内的环原子和1、2、3或4个独立地选自氮、硫和氧的杂原子环成员。在一些实施方案中,杂芳基具有5-10个包括碳原子在内的环原子和1、2、3或4个独立地选自氮、硫和氧的杂原子环成员。在一些实施方案中,杂芳基具有5-6个环原子和1或2个独立地选自氮、硫和氧的杂原子环成员。在一些实施方案中,杂芳基是五元或六元杂芳基环。在其它实施方案中,杂芳基是八元、九元或十元稠合双环杂芳基环。示例杂芳基包括但不限于吡啶基(pyridinyl/pyridyl)、嘧啶基、吡嗪基、哒嗪基、吡咯基、吡唑基、唑基(azolyl)、噁唑基、异噁唑基、噻唑基、咪唑基、呋喃基、噻吩基(thiophenyl)、喹啉基、异喹啉基、萘啶基(包括1,2-、1,3-、1,4-、1,5-、1,6-、1,7-、1,8-、2,3-和2,6-萘啶)、吲哚基、异吲哚基、苯并噻吩基、苯并呋喃基、苯并异噁唑基、咪唑并[1,2-b]噻唑基、嘌呤基等。在一些实施方案中,杂芳基是吡啶酮(例如,2-吡啶酮)。
五元杂芳基环是具有五个环原子的杂芳基,其中一个或多个(例如1、2或3个)环原子独立地选自N、O和S。示例性五元环杂芳基包括噻吩基(thienyl)、呋喃基、吡咯基、咪唑基、噻唑基、噁唑基、吡唑基、异噻唑基、异噁唑基、1,2,3-三唑基、四唑基、1,2,3-噻二唑基、1,2,3-噁二唑基、1,2,4-三唑基、1,2,4-噻二唑基、1,2,4-噁二唑基、1,3,4-三唑基、1,3,4-噻二唑基和1,3,4-噁二唑基。
六元杂芳基环是具有六个环原子的杂芳基,其中一个或多个(例如1、2或3个)环原子独立地选自N、O和S。示例性六元环杂芳基有吡啶基、吡嗪基、嘧啶基、三嗪基、异吲哚基和哒嗪基。
单独或与其它术语组合使用的术语“环烷基”是指非芳族烃环体系(单环、双环或多环),包括环化的烷基和烯基。术语“Cn-m环烷基”是指具有n至m个环成员碳原子的环烷基。环烷基可包括单环或多环(例如,具有2、3或4个稠环)基团和螺环。环烷基可具有3、4、5、6或7个成环碳(C3-7)。在一些实施方案中,环烷基具有3至6个环成员、3至5个环成员或3至4个环成员。在一些实施方案中,环烷基是单环的。在一些实施方案中,环烷基是单环的或双环的。在一些实施方案中,环烷基是C3-6单环状环烷基。环烷基的成环碳原子可任选被氧化以形成氧代基或硫离子基。环烷基也包括亚环烷基。在一些实施方案中,环烷基是环丙基、环丁基、环戊基或环己基。环烷基的定义中还包括具有一个或多个与环烷基环稠合(即,具有共同的键)的芳族环的部分,例如环戊烷、环己烷等的苯并或噻吩基衍生物。含有稠合芳族环的环烷基可通过任何成环原子(包括稠合芳族环的成环原子)连接。环烷基的实例包括环丙基、环丁基、环戊基、环己基、环庚基、环戊烯基、环己烯基、环已二烯基、环庚三烯基、降莰基、降蒎基、降蒈基、双环[1.1.1]戊烷基、双环[2.1.1]己烷基等。在一些实施方案中,环烷基是环丙基、环丁基、环戊基或环己基。
单独或与其它术语组合使用的术语“杂环烷基”是指非芳族环或环体系,其可任选含有一个或多个亚烯基作为环结构的一部分,其具有至少一个独立地选自氮、硫、氧和磷的杂原子环成员,并且其具有4-10个环成员、4-7个环成员或4-6个环成员。术语“杂环烷基”内包括单环4、5、6和7元杂环烷基。杂环烷基可包括单环或双环(例如,具有两个稠环或桥环)或螺环状环体系。在一些实施方案中,杂环烷基是具有1、2或3个独立地选自氮、硫和氧的杂原子的单环基团。杂环烷基的成环碳原子和杂原子可任选被氧化以形成氧代基或硫离子基或其它氧化连键(例如C(O)、S(O)、C(S)或S(O)2、N-氧化物等),或者氮原子可以被季铵化。杂环烷基可通过成环碳原子或成环杂原子连接。在一些实施方案中,杂环烷基含有0至3个双键。在一些实施方案中,杂环烷基含有0至2个双键。杂环烷基的定义中也包括具有一个或多个与杂环烷基环稠合(即,具有共同键)的芳族环的部分,例如哌啶、吗啉、氮杂环庚三烯等的苯并或噻吩基衍生物。含有稠合芳族环的杂环烷基可通过任何成环原子(包括稠合芳族环的成环原子)连接。杂环烷基的实例包括2,5-二氮杂双环[2.2.1]庚基;吡咯烷基;六氢吡咯并[3,4-b]吡咯-1(2H)-基;1,6-二氢吡啶基;吗啉基;氮杂环丁基;哌嗪基;和4,7-二氮杂螺[2.5]辛-7-基。
在某些地方,定义或实施方案是指特定的环(例如氮杂环丁烷环、吡啶环等)。除另指出外,这些环可与任何环成员连接,条件为不超过原子的价态。例如,氮杂环丁烷环可在环的任何位置连接,而氮杂环丁-3-基环在位置3连接。
本文所述的化合物可以是不对称的(例如,具有一个或多个立体中心)。除另指出外,意图涵盖所有立体异构体,如对映异构体和非对映异构体。可以光学活性或外消旋形式分离含有不对称取代的碳原子的本发明的化合物。本领域中已知如何由非光学活性起始物制备光学活性形式的方法,如通过外消旋混合物的拆分或通过立体选择性合成。烯烃、C=N双键等的许多几何异构体也可存在于本文所述的化合物中,并且本发明涵盖所有这类稳定的异构体。描述了本发明的化合物的顺式和反式几何异构体,并且可将它们分离为异构体的混合物或分开的异构体形式。
可通过本领域中已知的多种方法中的任何一种来进行化合物的外消旋混合物的拆分。一种方法包括使用作为光学活性的成盐有机酸的手性拆分酸进行分级重结晶。用于分级重结晶方法的合适拆分剂有例如光学活性的酸,如D和L形式的酒石酸、二乙酰基酒石酸、二苯甲酰基酒石酸、扁桃酸、苹果酸、乳酸或各种光学活性的樟脑磺酸,如β-樟脑磺酸。适合分级结晶方法的其它拆分剂包括立体异构纯形式的α-甲基苄胺(例如,S和R形式,或非对映异构纯形式)、2-苯基乙醇胺、降麻黄碱、麻黄碱、N-甲基麻黄碱、环己基乙胺、1,2-二氨基环己烷等。
也可通过在填充有光学活性拆分剂(例如二硝基苯甲酰基苯基甘氨酸)的柱上洗脱来进行外消旋混合物的拆分。本领域技术人员可以确定合适的洗脱溶剂组成。
在一些实施方案中,本发明的化合物具有(R)-构型。在其它实施方案中,化合物具有(S)-构形。在具有不只一个手性中心的化合物中,除另指出外,化合物中的每个手性中心可独立地呈(R)或(S)。
本发明的化合物也包括互变异构形式。互变异构形式是由单键与相邻双键的交换连同伴随的质子迁移产生的。互变异构形式包括呈具有相同经验式和总电荷的异构质子化状态的质子移变互变异构体。示例质子移变互变异构体包括酮-烯醇对、酰胺-酰亚胺酸对、内酰胺-内酰亚胺对、烯胺-亚胺对和其中质子可占据杂环体系的两个或更多个位置的环状形式,例如1H-和3H-咪唑;1H-、2H-和4H-1,2,4-三唑;1H-和2H-异吲哚;以及1H-和2H-吡唑。互变异构形式可处于平衡状态,或者通过适当的取代在空间上锁定于一种形式。
本发明的化合物还可包括中间体或最终化合物中存在的原子的所有同位素。同位素包括原子数相同但质量数不同的原子。例如,氢的同位素包括氚和氘。本发明的化合物的一个或多个组成原子可以被天然或非天然丰度的原子的同位素置换或取代。在一些实施方案中,化合物包括至少一个氘原子。例如,本公开的化合物中的一个或多个氢原子可以被氘置换或取代。在一些实施方案中,化合物包括两个或更多个氘原子。在一些实施方案中,化合物包括1、2、3、4、5、6、7、8、9、10、11或12个氘原子。将同位素包括到有机化合物中的合成方法是本领域中已知的(Deuterium Labeling in Organic Chemistry,Alan F.Thomas(New York,N.Y.,Appleton-Century-Crofts,1971;The Renaissance of H/D Exchange,Jens Atzrodt,Volker Derdau,Thorsten Fey和Jochen Zimmermann,Angew.Chem.Int.Ed.2007,7744-7765;The Organic Chemistry of Isotopic Labelling,James R.Hanson,Royal Society of Chemistry,2011)。同位素标记的化合物可用于各种研究,如NMR光谱、代谢实验和/或测定。
用较重的同位素如氘进行取代由于代谢稳定性更高而可以提供某些治疗优点,例如体内半衰期增加或剂量需求减少,因此在一些情况下可能是优选的。(A.Kerekes等人,J.Med.Chem.2011,54,201-210;R.Xu等人,J.Label Compd.Radiopharm.2015,58,308-312)。
如本文所用的术语“化合物”旨在包括所描述的结构的所有立体异构体、几何异构体、互变异构体和同位素。该术语也意指本发明的化合物,不管它们是例如以合成方式、通过生物过程(例如,代谢或酶转化)还是其组合制备的。
所有化合物及其药学上可接受的盐都可与其它物质如水和溶剂(例如,水合物和溶剂合物)一起存在,或者可以被分离出来。当处于固态时,本文所述的化合物及其盐可以各种形式存在,并且可例如呈溶剂合物的形式,包括水合物。化合物可呈任何固态形式,如多晶型物或溶剂合物,因此除另有明确指示外,说明书中提到化合物及其盐应被理解为涵盖该化合物的任何固态形式。
在一些实施方案中,本发明的化合物或其盐是基本上分离的。所谓“基本上分离的”意指该化合物至少部分地或基本上自其形成或检测到的环境分开。部分分离可包括例如富含本发明的化合物的组合物。基本上分离可包括按重量计含有至少约50%、至少约60%、至少约70%、至少约80%、至少约90%、至少约95%、至少约97%或至少约99%的本发明的化合物或其盐的组合物。
短语“药学上可接受的”在本文中用来指在合理的医学判断范围内适合与人和动物的组织接触而没有过度的毒性、刺激性、过敏反应或其它问题或并发症、与合理的利益/风险比相称的化合物、物质、组合物和/或剂型。
如本文所用的表述“环境温度”和“室温”是本领域中所理解的,并且通常是指大约为进行反应的室内温度的温度,例如反应温度,例如约20℃至约30℃的温度。
本发明还包括本文所述的化合物的药学上可接受的盐。术语“药学上可接受的盐”是指所公开的化合物的衍生物,其中通过将现有的酸或碱部分转化为其盐形式而对母体化合物进行改性。药学上可接受的盐的实例包括但不限于碱性残基(如胺)的无机酸盐或有机酸盐;酸性残基(如羧酸)的碱盐或有机盐;等等。本发明的药学上可接受的盐包括例如由无毒的无机酸或有机酸形成的母体化合物的无毒盐。可通过常规的化学方法由含有碱性或酸性部分的母体化合物合成本发明的药学上可接受的盐。一般地,这类盐可通过使这些化合物的游离酸或碱形式与化学计算量的适当碱或酸在水中或在有机溶剂中或在两者的混合物中反应来制备;一般地,非水介质如醚、乙酸乙酯、醇(例如甲醇、乙醇、异丙醇或丁醇)或乙腈(MeCN)是优选的。合适的盐的一览表可见于Remington's Pharmaceutical Sciences,第17版,(Mack Publishing Company,Easton,1985),第1418页;Berge等人,J.Pharm.Sci.,1977,66(1),1-19;和Stahl等人,Handbook of Pharmaceutical Salts:Properties,Selection,and Use,(Wiley,2002)。在一些实施方案中,本文所述的化合物包括N-氧化物形式。
合成
本发明的化合物(包括其盐)可采用已知的有机合成技术来制备,并且可根据多种可能的合成路线中的任一种来合成,如下面的方案中的合成路线。
制备本发明的化合物的反应可在合适的溶剂中进行,有机合成领域的技术人员可以很容易地选择溶剂。合适的溶剂在反应进行的温度下(例如温度范围可以是从溶剂的冻结温度到溶剂的沸点温度)可基本上不与起始物(反应物)、中间体或产物反应。可在一种溶剂或不只一种溶剂的混合物中进行给定的反应。根据特定的反应步骤,可由技术人员选择用于特定反应步骤的合适溶剂。
本发明的化合物的制备可涉及各种化学基团的保护和脱保护。本领域技术人员可以很容易确定需要进行保护和脱保护以及选择适当的保护基团。在例如以下文献中有保护基团的化学描述:Kocienski,Protecting Groups,(Thieme,2007);Robertson,ProtectingGroup Chemistry,(Oxford University Press,2000);Smith等人,March's AdvancedOrganic Chemistry:Reactions,Mechanisms,and Structure,第6版(Wiley,2007);Peturssion等人,"Protecting Groups in Carbohydrate Chemistry,"J.Chem.Educ.,1997,74(11),1297;和Wuts等人,Protective Groups in Organic Synthesis,第4版(Wiley,2006)。
可根据本领域中已知的任意合适的方法来监测反应。例如,可通过光谱手段监测产物形成,如核磁共振光谱法(例如1H或13C)、红外光谱法、分光光度法(例如UV-可见光)、质谱法,或者通过色谱方法,如高效液相色谱法(HPLC)或薄层色谱法(TLC)。
下面的方案提供关于制备本发明的化合物的一般指导。本领域技术人员将要理解的是,可采用有机化学的一般知识来改动或优化方案中所示的制备方法,以制备本发明的各种化合物。
可例如采用如下面的方案中所示的制程来制备式(I)和(I’)的化合物。
可采用如方案1中所示的制程来制备式(I)和(I’)的化合物。在方案1中描述的制程中,式1-1的化合物的卤代基取代基可用于通过多种方法来安置CyA取代基,例如通过用适当的胺亲核试剂与合适的碱(例如,三乙胺或DIPEA)在合适的溶剂(例如,DMF、DMSO、二噁烷)中进行亲核置换,或者通过合适的交叉偶联反应,得到式1-2的化合物。合适的交叉偶联反应包括但不限于Buchwald偶联(例如,在环钯配合物预催化剂如RuPhod Pd G2存在下)和Negishi或Suzuki偶联(例如,在环钯配合物预催化剂如Xphos Pd G2存在下)。不同交叉偶联程序的实例包括Stille(ACS Catalysis 2015,5,3040-3053)、Suzuki(Tetrahedron2002,58,9633-9695)、Sonogashira(Chem.Soc.Rev.2011,40,5084-5121)、Negishi(ACSCatalysis 2016,6,1540-1552)、Buchwald–Hartwig胺化(Chem.Sci.2011,2,27-50)和Cu催化胺化(Org.React.2014,85,1-688)等等。
用适当的还原剂(例如,在氯化铵存在下的铁或在Pd/C催化剂存在下的氢气)还原硝基,得到式1-3的化合物。用式1-5的酸(例如使用HATU和碱如Hunig碱)进行酰胺键形成,得到所需的式(I)或(I’)的化合物。
方案1
可采用交叉偶联如Suzuki(例如,在环钯配合物预催化剂如Xphos Pd G2存在下)或Stille(例如,在钯催化剂如(PPh3)2PdCl2和碱如三乙胺存在下)由式1-4的化合物来制备式1-5的酸。
方案2
HPK1激酶
研究已确定HPK1是T细胞和B细胞激活的负调控子(Hu,M.C.等人,Genes Dev,1996.10(18):第2251-64页;Kiefer,F.等人,EMBO J,1996.15(24):第7013-25页)。在体外经抗CD3刺激,HPK1缺陷小鼠T细胞显示出显著增加的TCR近端信号传导激活、增强的IL-2产生和过度增殖(Shui,J.W.等人,Nat Immunol,2007.8(1):第84-91页)。与T细胞类似,HPK1敲除B细胞在KLH免疫后产生水平高得多的IgM和IgG亚型,并且可能由于BCR信号传导增强而表现出过度增殖。Wang,X.等人,J Biol Chem,2012.287(14):第11037-48页。从机理上讲,在TCR或BCR信号传导期间,HPK1由LCK/ZAP70(T细胞)或SYK/LYN(B细胞)介导的Tyr379磷酸化及其随后与衔接蛋白SLP-76(T细胞)或BLNK(B细胞)的结合所激活(Wang,X.等人,JBiol Chem,2012.287(14):第11037-48页)。激活的HPK1使Ser376上的SLP-76或Thr152上的BLNK磷酸化,导致信号传导分子14-3-3的募集和最终泛素化介导的SLP-76或BLNK的降解(Liou,J.等人,Immunity,2000.12(4):第399-408页;Di Bartolo,V.等人,J Exp Med,2007.204(3):第681-91页)。由于SLP-76和BLNK对TCR/BCR介导的信号传导激活(例如ERK、磷脂酶Cγ1、钙通量和NFAT激活)至关重要,因此HPK1介导的这些衔接蛋白的下调提供了一种负反馈机制,以在T细胞或B细胞激活期间减弱信号传导强度(Wang,X.等人,J BiolChem,2012.287(14):第11037-48页)。
与野生型DC相比,来自HPK1敲除小鼠的骨髓来源的树突细胞(BDMC)显示共刺激分子(例如CD80/CD86)的表达更高,且促炎性细胞因子(IL-12、TNF-α等)的产生增强,并且表现出在体外和体内刺激T细胞增殖的优越能力(Alzabin,S.等人,J Immunol,2009.182(10):第6187-94页)。这些数据表明HPK1也是树突细胞激活的重要负调控子(Alzabin,S.等人,J Immunol,2009.182(10):第6187-94页)。然而,作为HPK-1介导的DC激活的负调控的信号传导机制仍有待阐明。
相比之下,HPK1似乎是调控T细胞(Treg)的抑制功能的正调控子(Sawasdikosol,S.等人,The journal of immunology,2012.188(补编1):第163页)。HPK1缺陷小鼠Foxp3+Treg在抑制TCR诱导的效应T细胞增殖方面有缺陷,而在TCR结合之后反常地获得产生IL-2的能力(Sawasdikosol,S.等人,The Journal of Immunology,2012.188(补编1):第163页)。这些数据表明HPK1是Treg功能和外周自我耐受性的重要调控子。
HPK1还参与PGE2介导的CD4+ T细胞激活的抑制(Ikegami,R.等人,J Immunol,2001.166(7):第4689-96页)。US 2007/0087988中公布的研究表明,暴露于CD4+ T细胞中的生理浓度的PGE2增加了HPK1激酶活性,并且这种效应是通过PEG2诱导的PKA激活来介导。HPK1缺陷T细胞的增殖对PGE2的抑制效应具有抗性(参见US2007/0087988)。因此,PGE2介导的HPK1的激活可能代表调节免疫应答的新新颖调控途径。
本公开提供通过使HPK1与本发明的化合物或其药学上可接受的盐接触来调节(例如,抑制)HPK1活性的方法。在一些实施方案中,接触可以是对患者施用本文提供的化合物或其药学上可接受的盐。在某些实施方案中,本公开的化合物或其药学上可接受的盐可用于治疗性施用以在癌症中增强、刺激和/或增加免疫力。例如,治疗与抑制HPK1相互作用相关的疾病或病症的方法可包括对有需要的患者施用治疗有效量的本文提供的化合物或其药学上可接受的盐。本公开的化合物可单独使用,与其它药剂或疗法组合使用,或者作为佐剂或新佐剂用于治疗包括癌症在内的疾病或病症。对于本文所述的用途,可使用本公开的任何化合物,包括其任何实施方案。
可使用本公开的化合物治疗的癌症的实例包括但不限于骨癌、胰腺癌、皮肤癌、头颈癌、皮肤或眼内恶性黑色素瘤、子宫癌、卵巢癌、直肠癌、肛区癌、胃癌、睾丸癌、子宫癌、输卵管癌、子宫内膜癌(carcinoma of the endometrium)、子宫内膜癌(endometrialcancer)、宫颈癌、阴道癌、外阴癌、霍奇金病(Hodgkin's Disease)、非霍奇金淋巴瘤、食道癌、小肠癌、内分泌系统癌、甲状腺癌、甲状旁腺癌、肾上腺癌、软组织肉瘤、尿道癌、阴茎癌、慢性或急性白血病(包括急性骨髓样白血病、慢性骨髓样白血病、急性成淋巴细胞性白血病、慢性淋巴细胞性白血病)、儿童期实体肿瘤、淋巴细胞性淋巴瘤、膀胱癌、肾癌或尿道癌、肾盂癌、中枢神经系统(CNS)肿瘤、原发性CNS淋巴瘤、肿瘤血管生成、脊椎轴肿瘤、脑干神经胶质瘤、垂体腺瘤、卡波西氏肉瘤(Kaposi's sarcoma)、表皮样癌、鳞状细胞癌、T细胞淋巴瘤、环境诱发的癌症(包括由石棉诱发的癌症))以及所述癌症的组合。
在一些实施方案中,可用本公开的化合物治疗的癌症包括黑色素瘤(例如,转移性恶性黑色素瘤)、肾癌(例如透明细胞癌)、前列腺癌(例如激素难治性前列腺腺癌)、乳腺癌、三阴性乳腺癌、结肠癌和肺癌(例如非小细胞肺癌和小细胞肺癌)。另外,本公开包括可使用本公开的化合物抑制其生长的难治性或复发性恶性肿瘤。
在一些实施方案中,可使用本公开的化合物治疗的癌症包括但不限于实体肿瘤(例如,前列腺癌、结肠癌、食道癌、子宫内膜癌、卵巢癌、子宫癌、肾癌、肝癌、胰腺癌、胃癌、乳腺癌、肺癌、头颈癌、甲状腺癌、成胶质细胞瘤、肉瘤、膀胱癌等)、血液学癌症(例如,淋巴瘤、白血病,如急性成淋巴细胞性白血病(ALL)、急性骨髓性白血病(AML)、慢性淋巴细胞性白血病(CLL)、慢性骨髓性白血病(CML)、DLBCL、套细胞淋巴瘤、非霍奇金淋巴瘤(包括复发或难治性NHL和复发性滤泡性淋巴瘤)、霍奇金淋巴瘤或多发性骨髓瘤)以及所述癌症的组合。
在一些实施方案中,可使用本公开的化合物治疗的疾病和适应症包括但不限于血液学癌症、肉瘤、肺癌、胃肠癌、泌尿生殖道癌、肝癌、骨癌、神经系统癌症、妇科癌症和皮肤癌。
示例性血液学癌症包括淋巴瘤和白血病,如急性成淋巴细胞性白血病(ALL)、急性骨髓性白血病(AML)、急性早幼粒细胞性白血病(APL)、慢性淋巴细胞性白血病(CLL)、慢性骨髓性白血病(CML)、弥漫性大B细胞淋巴瘤(DLBCL)、套细胞淋巴瘤、非霍奇金淋巴瘤(包括复发或难治性NHL和复发性滤泡性淋巴瘤)、霍奇金淋巴瘤、骨髓增殖性疾病(例如,原发性骨髓纤维化(PMF)、真性红细胞增多症(PV)、原发性血小板增多症(ET))、骨髓增生异常综合征(MDS)、T细胞急性成淋巴细胞性淋巴瘤(T-ALL)、多发性骨髓瘤、皮肤T细胞淋巴瘤、华氏巨球蛋白血症(Waldenstrom's Macroglubulinemia)、毛细胞淋巴瘤、慢性骨髓性淋巴瘤和伯基特淋巴瘤(Burkitt's lymphoma)。
示例性肉瘤包括软骨肉瘤、尤文氏肉瘤(Ewing’s sarcoma)、骨肉瘤、横纹肌肉瘤、血管肉瘤、纤维肉瘤、脂肪肉瘤、粘液瘤、横纹肌瘤、横纹肌肉瘤、纤维瘤、脂肪瘤、错构瘤和畸胎瘤。
示例性肺癌包括非小细胞肺癌(NSCLC)、小细胞肺癌、支气管癌(鳞状细胞、未分化小细胞、未分化大细胞、腺癌)、肺泡(细支气管)癌、支气管腺瘤、软骨瘤样错构瘤和间皮瘤。
示例性胃肠癌包括食道癌(鳞状细胞癌、腺癌、平滑肌肉瘤、淋巴瘤)、胃癌(癌(carcinoma)、淋巴瘤、平滑肌肉瘤)、胰腺癌(导管腺癌、胰岛素瘤、胰高血糖素瘤、胃泌素瘤、类癌肿瘤、舒血管肠肽瘤)、小肠癌(腺癌、淋巴瘤、类癌肿瘤、卡波西氏肉瘤、平滑肌瘤、血管瘤、脂肪瘤、神经纤维瘤、纤维瘤)、大肠癌(腺癌、管状腺瘤、绒毛状腺瘤、错构瘤、平滑肌瘤)和结肠直肠癌。
示例性泌尿生殖道癌包括肾癌(腺癌、威尔姆氏肿瘤(Wilm's tumor)[肾母细胞瘤])、膀胱和尿道癌(鳞状细胞癌、移行细胞癌、腺癌)、前列腺癌(腺癌、肉瘤)和睾丸癌(精原细胞瘤、畸胎瘤、胚胎癌、畸胎癌、绒毛膜癌、肉瘤、间质细胞癌、纤维瘤、纤维腺瘤、腺瘤样肿瘤、脂肪瘤)。
示例性肝癌包括肝细胞瘤(肝细胞癌)、胆管癌、肝母细胞瘤、血管肉瘤、肝细胞腺瘤和血管瘤。
示例性骨癌包括例如骨原性肉瘤(骨肉瘤)、纤维肉瘤、恶性纤维组织细胞瘤、软骨肉瘤、尤因氏肉瘤、恶性淋巴瘤(网状细胞肉瘤)、多发性骨髓瘤、恶性巨细胞瘤脊索瘤、骨软骨纤维瘤(骨软骨性外生骨疣)、良性软骨瘤、软骨母细胞瘤、软骨粘液纤维瘤、骨样骨瘤和巨细胞瘤
示例性神经系统癌症包括颅骨癌(骨瘤、血管瘤、肉芽肿、黄瘤、变形性骨炎)、脑膜癌(脑膜瘤、脑膜肉瘤、神经胶质瘤病)、脑癌(星形细胞瘤、成神经管细胞瘤、神经胶质瘤、室管膜瘤、胚组织瘤(松果体瘤)、胶质母细胞瘤、多形性胶质母细胞瘤、少突胶质细胞瘤、许旺氏细胞瘤、视网膜母细胞瘤、先天性肿瘤)和脊髓癌(神经纤维瘤、脑膜瘤、神经胶质瘤、肉瘤)以及神经母细胞瘤和Lhermitte-Duclos病。
示例性妇科癌症包括子宫癌(子宫内膜癌)、宫颈癌(宫颈癌、肿瘤前宫颈发育不良)、卵巢癌(卵巢癌(浆液性囊腺癌、粘液性囊腺癌、未分类癌)、粒层-膜细胞肿瘤、Sertoli-Leydig细胞肿瘤、无性细胞瘤、恶性畸胎瘤)、外阴癌(鳞状细胞癌、上皮内癌、腺癌、纤维肉瘤、黑色素瘤)、阴道癌(透明细胞癌、鳞状细胞癌、葡萄样肉瘤(胚胎横纹肌肉瘤)和输卵管癌(癌(carcinoma))。
示例性皮肤癌包括黑色素瘤、基底细胞癌、鳞状细胞癌、卡波西氏肉瘤、梅克尔细胞皮肤癌、发育不良痣、脂肪瘤、血管瘤、皮肤纤维瘤和瘢痕瘤。在一些实施方案中,可使用本公开的化合物治疗的疾病和适应症包括但不限于镰状细胞病(例如,镰状细胞贫血)、三阴性乳腺癌(TNBC)、骨髓增生异常综合征、睾丸癌、胆道癌、食道癌和尿路上皮癌。
示例性头颈癌包括成胶质细胞瘤、黑色素瘤、横纹肌肉瘤、淋巴肉瘤、骨肉瘤、鳞状细胞癌、腺癌、口腔癌、喉癌、鼻咽癌、鼻癌和鼻侧癌、甲状腺癌和甲状旁腺癌。
在一些实施方案中,HPK1抑制剂可用于治疗产生PGE2的肿瘤(例如Cox-2过表达肿瘤)和/或产生腺苷的肿瘤(CD73和CD39过表达肿瘤)。已在诸如结肠直肠癌、乳腺癌、胰腺癌和肺癌的许多肿瘤中检测到Cox-2的过表达,其中其与不良预后相关联。已在诸如RAJI(伯基特淋巴瘤)和U937(急性前单核细胞白血病)的血液学癌症模型中以及在患者的母细胞中报道了COX-2的过表达。CD73在包括结肠癌、肺癌、胰腺癌和卵巢癌在内的各种人类癌中上调。重要的是,CD73的较高表达水平与肿瘤新血管形成、侵袭性和转移以及与乳腺癌患者的存活时间较短相关。
如本文所用,术语“接触”是指使体外系统或体内系统中的指定部分集合到一起,使得它们在物理上足够接近以相互作用。
可互换使用的术语“个体”或“患者”是指任何动物,包括哺乳动物,优选小鼠、大鼠、其它啮齿动物、兔、狗、猫、猪、牛、绵羊、马或灵长类动物,最优选人。
短语“治疗有效量”是指研究人员、兽医、医生或其他临床医师所寻求的在组织、系统、动物、个体或人体中引发生物学反应或药物反应的活性化合物或药剂的量。
如本文所用,术语“治疗(treating/treatment)”是指以下各项中的一者或多者:(1)抑制疾病;例如在正经历疾病、疾患或病症或显示出疾病、疾患或病症的病理或症状的个体中抑制所述疾病、疾患或病症(即阻止病理和/或症状的进一步发展);和(2)减轻疾病;例如在正经历疾病、疾患或病症或显示出疾病、疾患或病症的病理或症状的个体中减轻所述疾病、疾患或病症(即逆转病理和/或症状),如降低疾病的严重程度。
在一些实施方案中,本发明的化合物可用于预防或降低发生本文中提到的任何疾病的风险;例如,在可能易患疾病、疾患或病症但尚未经历或表现出所述疾病的病理或症状的个体中预防或降低发生所述疾病、疾患或病症的风险。
组合疗法
I.免疫检查点疗法
在一些实施方案中,本文提供的HPK1抑制剂可与一种或多种免疫检查点抑制剂组合,用于治疗如本文所述的癌症。本公开的化合物可与一种或多种免疫检查点抑制剂组合使用。示例性免疫检查点抑制剂包括针对免疫检查点分子如CD20、CD28、CD39、CD40、CD122、CD96、CD73、CD47、GITR、CSF1R、JAK、PI3Kδ、PI3Kγ、TAM、精氨酸酶、CD137(也称为4-1BB)、ICOS、B7-H3、B7-H4、BTLA、CTLA-4、LAG3、TIM3、VISTA、TIGIT、PD-1、PD-L1和PD-L2的抑制剂。在一些实施方案中,免疫检查点分子是选自CD27、CD28、CD40、ICOS、OX40、GITR和CD137的刺激性检查点分子。在一些实施方案中,免疫检查点分子是选自A2AR、B7-H3、B7-H4、BTLA、CTLA-4、IDO、KIR、LAG3、PD-1、TIM3、TIGIT和VISTA的抑制性检查点分子。在一些实施方案中,本文提供的本公开的化合物可与选自KIR抑制剂、TIGIT抑制剂、LAIR1抑制剂、CD160抑制剂、2B4抑制剂和TGFRβ抑制剂的一种或多种药剂组合使用。
在一些实施方案中,本文提供的化合物可与免疫检查点分子例如OX40、CD27、GITR和CD137(也称为4-1BB)的一种或多种激动剂组合使用。
在一些实施方案中,免疫检查点分子的抑制剂是抗PD1抗体、抗PD-L1抗体或抗CTLA-4抗体。
在一些实施方案中,免疫检查点分子的抑制剂是PD-1的抑制剂,例如抗PD-1单克隆抗体。在一些实施方案中,抗-PD-1单克隆抗体是纳武单抗(nivolumab)、派姆单抗(pembrolizumab)(也称为MK-3475)、度伐单抗皮地珠单抗(pidilizumab)、SHR-1210、PDR001、MGA012、PDR001、AB122或AMP-224。在一些实施方案中,抗PD-1单克隆抗体是纳武单抗或派姆单抗。在一些实施方案中,抗PD1抗体是派姆单抗。在一些实施方案中,抗PD-1单克隆抗体是MGA012。在一些实施方案中,抗PD1抗体是SHR-1210。其它抗癌剂包括抗体治疗剂,如4-1BB(例如乌瑞鲁单抗(urelumab)、乌托米鲁单抗(utomilumab))。
在一些实施方案中,免疫检查点分子的抑制剂是PD-L1的抑制剂,例如抗PD-L1单克隆抗体。在一些实施方案中,抗PD-L1单克隆抗体是BMS-935559、MEDI4736、MPDL3280A(也称为RG7446)或MSB0010718C。在一些实施方案中,抗PD-L1单克隆抗体是MPDL3280A或MEDI4736。
在一些实施方案中,免疫检查点分子的抑制剂是PD-1和PD-L1的抑制剂,例如抗PD-1/PD-L1单克隆抗体。在一些实施方案中,抗PD-1/PD-L1是MCLA-136。
在一些实施方案中,所述抑制剂是MCLA-145。
在一些实施方案中,免疫检查点分子的抑制剂是CTLA-4的抑制剂,例如抗CTLA-4抗体。在一些实施方案中,抗CTLA-4抗体是伊匹单抗(ipilimumab)、曲美目单抗(tremelimumab)、AGEN1884或CP-675,206。
在一些实施方案中,免疫检查点分子的抑制剂是CSF1R的抑制剂,例如抗CSF1R抗体。在一些实施方案中,抗CSF1R抗体是IMC-CS4或RG7155。
在一些实施方案中,免疫检查点分子的抑制剂是LAG3的抑制剂,例如抗LAG3抗体。在一些实施方案中,抗LAG3抗体是BMS-986016、LAG525、IMP321、GSK2831781或INCAGN2385。
在一些实施方案中,免疫检查点分子的抑制剂是TIM3的抑制剂,例如抗TIM3抗体。在一些实施方案中,抗TIM3抗体是INCAGN2390、MBG453或TSR-022。
在一些实施方案中,免疫检查点分子的抑制剂是GITR抑制剂,例如抗GITR抗体。在一些实施方案中,抗GITR抗体是TRX518、MK-4166、INCAGN1876、MK-1248、AMG228、BMS-986156、GWN323或MEDI1873。
在一些实施方案中,免疫检查点分子的抑制剂是OX40的激动剂,例如OX40激动剂抗体或OX40L融合蛋白。在一些实施方案中,抗OX40抗体是INCAGN01949、MEDI0562、MEDI6469、MOXR-0916、PF-04518600、GSK3174998或BMS-986178。在一些实施方案中,OX40L融合蛋白是MEDI6383。
在一些实施方案中,免疫检查点分子的抑制剂是CD20的抑制剂,例如抗CD20抗体。在一些实施方案中,抗CD20抗体是奥比妥珠单抗(obinutuzumab)或利妥昔单抗(rituximab)。
本公开的化合物可与双特异性抗体组合使用。在一些实施方案中,双特异性抗体的结构域之一靶向PD-1、PD-L1、CTLA-4、GITR、OX40、TIM3、LAG3、CD137、ICOS、CD3或TGFβ受体。
在一些实施方案中,本公开的化合物可与一种或多种代谢酶抑制剂组合使用。在一些实施方案中,代谢酶抑制剂是IDO1、TDO或精氨酸酶的抑制剂。IDO1抑制剂的实例包括依帕卡司他(epacadostat)、NLG919、BMS-986205、PF-06840003、IOM2983、RG-70099和LY338196。精氨酸酶抑制剂的实例是CB-1158。
如全文所提供,另外的化合物、抑制剂、药剂等可与本发明化合物组合在单一或连续剂型中,或者它们可作为单独的剂型同时或顺序施用。
II.癌症疗法
癌细胞生长和存活可受多个信号传导途径影响。因此,将不同的酶/蛋白质/受体抑制剂组合起来治疗这类疾患是有用的,这些抑制剂对它们调节活性的靶标表现出不同的偏好。可与本公开的化合物组合的药剂的实例包括PI3K-AKT-mTOR途径的抑制剂、Raf-MAPK途径的抑制剂、JAK-STAT途径的抑制剂、β连环蛋白途径的抑制剂、notch途径的抑制剂、hedgehog途径的抑制剂、Pim激酶的抑制剂以及蛋白质伴侣和细胞周期进展的抑制剂。靶向不止一个信号传导途径(或不止一种参与给定信号传导途径的生物分子)可降低在细胞群体中产生抗药性的可能性和/或减少治疗的毒性。
本公开的化合物可与一种或多种其它的酶/蛋白质/受体抑制剂组合使用,用于治疗诸如癌症的疾病。癌症的实例包括实体肿瘤和液体肿瘤,如血癌。例如,本公开的化合物可与以下激酶的一种或多种抑制剂组合用于治疗癌症:Akt1、Akt2、Akt3、TGF-bR、PKA、PKG、PKC、CaM-激酶、磷酸化酶激酶、MEKK、ERK、MAPK、mTOR、EGFR、HER2、HER3、HER4、INS-R、IGF-1R、IR-R、PDGFaR、PDGFbR、CSFIR、KIT、FLK-II、KDR/FLK-1、FLK-4、flt-1、FGFR1、FGFR2、FGFR3、FGFR4、c-Met、Ron、Sea、TRKA、TRKB、TRKC、FLT3、VEGFR/Flt2、Flt4、EphA1、EphA2、EphA3、EphB2、EphB4、Tie2、Src、Fyn、Lck、Fgr、Btk、Fak、SYK、FRK、JAK、ABL、ALK和B-Raf。在一些实施方案中,本公开的化合物可与以下抑制剂中的一种或多种组合用于治疗癌症。可与本公开的化合物组合用于治疗癌症的抑制剂的非限制性实例包括FGFR抑制剂(FGFR1、FGFR2、FGFR3或FGFR4,例如AZD4547、BAY1187982、ARQ087、BGJ398、BIBF1120、TKI258、德立替尼(lucitanib)、多韦替尼(dovitinib)、TAS-120、JNJ-42756493、Debio1347、INCB54828、INCB62079和INCB63904)、JAK抑制剂(JAK1和/或JAK2,例如鲁索替尼(ruxolitinib)、巴瑞替尼(baricitinib)或INCB39110)、IDO抑制剂(例如,依帕卡司他和NLG919)、LSD1抑制剂(例如,GSK2979552、INCB59872和INCB60003)、TDO抑制剂、PI3K-δ抑制剂(例如,INCB50797和INCB50465)、PI3K-γ抑制剂如PI3K-γ选择性抑制剂、CSF1R抑制剂(例如,PLX3397和LY3022855)、TAM受体酪氨酸激酶(Tyro-3、Axl和Mer)、血管生成抑制剂、白介素受体抑制剂、溴区和额外末端家族成员抑制剂(例如,溴区结构域抑制剂或BET抑制剂,如OTX015、CPI-0610、INCB54329和INCB57643)和腺苷受体拮抗剂或其组合。HDAC的抑制剂,如帕比司他(panobinostat)和伏立诺他(vorinostat)。c-Met的抑制剂,如奥纳珠单抗(onartumzumab)、替伐尼布(tivantnib)和INC-280。BTK的抑制剂,如依鲁替尼(ibrutinib)。mTOR的抑制剂,如雷帕霉素(rapamycin)、西罗莫司(sirolimus)、替西罗莫司(temsirolimus)和依维莫司(everolimus)。Raf的抑制剂,如维莫非尼(vemurafenib)和达拉非尼(dabrafenib)。MEK的抑制剂,如曲美替尼(trametinib)、司美替尼(selumetinib)和GDC-0973。Hsp90的抑制剂(例如,坦螺旋霉素(tanespimycin))、细胞周期蛋白依赖性激酶的抑制剂(例如,帕博西尼(palbociclib))、PARP的抑制剂(例如,奥拉帕尼(olaparib))和Pim激酶的抑制剂(LGH447、INCB053914和SGI-1776)也可与本公开的化合物组合。
本公开的化合物可与一种或多种用于治疗疾病如癌症的剂组合使用。在一些实施方案中,所述剂是烷化剂、蛋白酶体抑制剂、皮质类固醇或免疫调节剂。烷化剂的实例包括苯达莫司汀(bendamustine)、氮芥类、乙烯亚胺衍生物、磺酸烷基酯、亚硝基脲和三氮烯、尿嘧啶氮芥、氯甲川(chlormethine)、环磷酰胺(CytoxanTM)、异环磷酰胺、美法仑(melphalan)、苯丁酸氮芥、哌泊溴烷(pipobroman)、三亚乙基-三聚氰胺、三亚乙基硫代磷胺、白消安(busulfan)、卡莫司汀(carmustine)、洛莫司汀(lomustine)、链脲佐菌素(streptozocin)、达卡巴嗪(dacarbazine)和替莫唑胺(temozolomide)。在一些实施方案中,蛋白酶体抑制剂是卡非佐米(carfilzomib)。在一些实施方案中,皮质类固醇是地塞米松(dexamethasone,DEX)。在一些实施方案中,免疫调节剂是来那度胺(lenalidomide,LEN)或泊马度胺(pomalidomide,POM)。
本公开的化合物可进一步与例如通过化学疗法、放射疗法、肿瘤靶向疗法、辅助疗法、免疫疗法或外科手术治疗癌症的其它方法组合使用。免疫疗法的实例包括细胞因子治疗(例如,干扰素、GM-CSF、G-CSF、IL-2)、CRS-207免疫疗法、癌症疫苗、单克隆抗体、过继性T细胞转移、作为T细胞激活促进剂的CAR(嵌合抗原受体)T细胞治疗、溶瘤病毒疗法和免疫调节小分子,包括沙利度胺(thalidomide)或JAK1/2抑制剂等。所述化合物可与一种或多种抗癌药物如化学治疗剂组合施用。示例化学治疗剂包括以下中的任何一种:阿巴瑞克(abarelix)、阿比特龙(abiraterone)、阿法替尼(afatinib)、阿柏西普(aflibercept)、阿地白介素(aldesleukin)、阿仑单抗(alemtuzumab)、阿利维甲酸(alitretinoin)、别嘌呤醇、六甲蜜胺、安吖啶、阿那曲唑(anastrozole)、阿非迪霉素(aphidicolon)、三氧化二砷、天冬酰胺酶、阿西替尼(axitinib)、阿扎胞苷、贝伐单抗(bevacizumab)、贝沙罗汀(bexarotene)、巴瑞替尼、比卡鲁胺(bicalutamide)、博莱霉素(bleomycin)、硼替佐必(bortezombi)、硼替佐米(bortezomib)、布立尼布(brivanib)、布帕尼西(buparlisib)、静脉注射用白消安、口服白消安、卡鲁睾酮(calusterone)、抗癌妥(camptosar)、卡培他滨(capecitabine)、卡铂(carboplatin)、卡莫司汀、西地尼布(cediranib)、西妥昔单抗(cetuximab)、苯丁酸氮芥、顺铂(cisplatin)、克拉屈滨(cladribine)、氯法拉滨(clofarabine)、克唑替尼(crizotinib)、环磷酰胺、阿糖胞苷、达卡巴嗪(dacarbazine)、达克替尼(dacomitinib)、放线菌素D(dactinomycin)、达肝素钠(dalteparin sodium)、达沙替尼(dasatinib)、放线菌素D、道诺霉素(daunorubicin)、地西他滨(decitabine)、地加瑞克(degarelix)、地尼白介素(denileukin)、地尼白介素2(denileukin diftitox)、脱氧助间型霉素(deoxycoformycin)、右雷佐生(dexrazoxane)、多西他赛(docetaxel)、多柔比星(doxorubicin)、屈洛昔芬(droloxafine)、丙酸屈他雄酮(dromostanolone propionate)、依库丽单抗(eculizumab)、恩扎鲁胺(enzalutamide)、表鬼臼毒素(epidophyllotoxin)、表柔比星(epirubicin)、埃博霉素(epothilones)、埃罗替尼(erlotinib)、雌莫司汀(estramustine)、磷酸依托泊苷(etoposide phosphate)、依托泊苷、依西美坦(exemestane)、柠檬酸芬太尼(fentanyl citrate)、非格司亭(filgrastim)、氟尿苷、氟达拉滨(fludarabine)、氟尿嘧啶、氟他胺(flutamide)、氟维司群(fulvestrant)、吉非替尼(gefitinib)、吉西他滨(gemcitabine)、吉妥珠单抗奥唑米星(gemtuzumab ozogamicin)、醋酸戈舍瑞林(goserelin acetate)、醋酸组胺瑞林(histrelin acetate)、替伊莫单抗(ibritumomab tiuxetan)、伊达比星(idarubicin)、艾代拉里斯(idelalisib)、异环磷酰胺、甲磺酸伊马替尼(imatinib mesylate)、干扰素α-2a、伊立替康(irinotecan)、二甲苯磺酸拉帕替尼(lapatinib ditosylate)、来那度胺、来曲唑(letrozole)、亚叶酸、醋酸亮丙瑞林(leuprolide acetate)、左旋咪唑、洛莫司汀、麦克劳胺(meclorethamine)、醋酸甲地孕酮(megestrol acetate)、美法仑、巯嘌呤、甲氨蝶呤(methotrexate)、甲氧沙林(methoxsalen)、光神霉素(mithramycin)、丝裂霉素C(mitomycin C)、米托坦(mitotane)、米托蒽醌(mitoxantrone)、苯丙酸诺龙(nandrolone phenpropionate)、诺维本(navelbene)、耐昔妥珠单抗(necitumumab)、奈拉滨(nelarabine)、来那替尼(neratinib)、尼罗替尼(nilotinib)、尼鲁米特(nilutamide)、诺非单抗(nofetumomab)、奥舍瑞林(oserelin)、奥沙利铂(oxaliplatin)、紫杉醇(paclitaxel)、帕米膦酸盐(pamidronate)、帕尼单抗(panitumumab)、帕唑帕尼(pazopanib)、培门冬酶(pegaspargase)、培非格司亭(pegfilgrastim)、培美曲塞二钠(pemetrexed disodium)、喷司他丁(pentostatin)、匹拉利塞(pilaralisib)、哌泊溴烷、普卡霉素(plicamycin)、普纳替尼(ponatinib)、卟菲尔钠(porfimer)、泼尼松(prednisone)、丙卡巴肼(procarbazine)、奎纳克林(quinacrine)、兰尼单抗(ranibizumab)、拉布立酶(rasburicase)、瑞格拉非尼(regorafenib)、雷洛昔芬(reloxafine)、雷利米得(revlimid)、利妥昔单抗、鲁索替尼、索拉非尼(sorafenib)、链脲菌素(streptozocin)、舒尼替尼(sunitinib)、马来酸舒尼替尼、他莫西芬(tamoxifen)、替加氟(tegafur)、替莫唑胺(temozolomide)、替尼泊苷(teniposide)、睪内酯、沙利度胺、硫鸟嘌呤、噻替派(thiotepa)、拓扑替康(topotecan)、托瑞米芬(toremifene)、托西莫单抗(tositumomab)、曲妥珠单抗(trastuzumab)、维甲酸(tretinoin)、曲普瑞林(triptorelin)、尿嘧啶氮芥、戊柔比星(valrubicin)、凡德他尼(vandetanib)、长春花碱(vinblastine)、长春新碱(vincristine)、长春地辛(vindesine)、长春瑞滨(vinorelbine)、伏立诺他(vorinostat)和唑来膦酸盐(zoledronate)。
其它抗癌剂包括抗体治疗剂如曲妥珠单抗(赫赛汀(Herceptin))、针对共刺激分子如CTLA-4的抗体(例如,伊匹单抗或曲美目单抗)、针对4-1BB的抗体、针对PD-1和PD-L1的抗体或针对细胞因子(IL-10、TGF-β等)的抗体。可与本公开的化合物组合用于治疗癌症或感染如病毒感染、细菌感染、真菌感染和寄生虫感染的针对PD-1和/或PD-L1的抗体的实例包括但不限于纳武单抗、派姆单抗、MPDL3280A、MEDI-4736和SHR-1210。
其它抗癌剂包括与细胞增殖病症相关的激酶的抑制剂。这些激酶包括但不限于Aurora-A、CDK1、CDK2、CDK3、CDK5、CDK7、CDK8、CDK9、肝配蛋白受体激酶、CHK1、CHK2、SRC、Yes、Fyn、Lck、Fer、Fes、Syk、Itk、Bmx、GSK3、JNK、PAK1、PAK2、PAK3、PAK4、PDK1、PKA、PKC、Rsk和SGK。
其它抗癌剂还包括阻断免疫细胞迁移的抗癌剂,如包括CCR2和CCR4的趋化因子受体的拮抗剂。
本公开的化合物可进一步与一种或多种抗炎剂、类固醇、免疫抑制剂或治疗性抗体组合使用。类固醇包括但不限于17α-乙炔雌二醇、己烯雌酚、睾酮、泼尼松、氟羟甲睪酮、甲基泼尼松龙(methylprednisolone)、甲基睾酮、泼尼松龙、曲安西龙(triamcinolone)、氯烯雌醚、羟孕酮、氨鲁米特(aminoglutethimide)和乙酸甲羟孕酮。
本公开的化合物也可与洛那法尼(lonafarnib)(SCH6636)、替吡法尼(tipifarnib)(R115777)、L778123、BMS 214662、替扎他滨(tezacitabine)(MDL 101731)、Sml1、三氮平(triapine)、地多西(didox)、屈米多西(trimidox)和艾米多西(amidox)组合使用。
式(I)、(I’)或如本文所述的任何式的化合物、如任何权利要求中叙述和本文所述的化合物或其盐可与另一种免疫原性剂组合,如癌细胞、纯化的肿瘤抗原(包括重组蛋白质、肽和碳水化合物分子)、细胞和用编码免疫刺激细胞因子的基因转染的细胞。可以使用的肿瘤疫苗的非限制性实例包括黑色素瘤抗原的肽,如gp100、MAGE抗原、Trp-2、MARTI和/或酪氨酸酶的肽,或经转染以表达细胞因子GM-CSF的肿瘤细胞。
式(I)、(I’)或如本文所述的任何式的化合物、如任何权利要求中叙述和本文所述的化合物或其盐可与用于治疗癌症的疫苗接种方案组合使用。在一些实施方案中,肿瘤细胞被转导以表达GM-CSF。在一些实施方案中,肿瘤疫苗包括来自牵涉于人类癌症的病毒如人类乳头瘤病毒(HPV)、肝炎病毒(HBV和HCV)和卡波西氏疱疹肉瘤病毒(KHSV)的蛋白质。在一些实施方案中,本公开的化合物可与肿瘤特异性抗原组合使用,如分离自肿瘤组织本身的热休克蛋白。在一些实施方案中,式(I)、(I’)或如本文所述的任何式的化合物、如任何权利要求中叙述和本文所述的化合物或其盐可与树突细胞免疫组合以激活高效的抗肿瘤反应。
本公开的化合物可与将表达Feα或Feγ受体的效应细胞靶向肿瘤细胞的双特异性大环肽组合使用。本公开的化合物也可与激活宿主免疫反应性的大环肽组合。
本公开的化合物可与骨髓移植组合使用,用于治疗多种造血源性肿瘤。
预期与本公开的化合物组合使用的合适抗病毒剂可包括核苷和核苷酸逆转录酶抑制剂(NRTI)、非核苷逆转录酶抑制剂(NNRTI)、蛋白酶抑制剂及其它抗病毒药物。
示例的合适NRTI包括齐多夫定(zidovudine)(AZT);地达诺新(didanosine)(ddl);扎西他滨(zalcitabine)(ddC);司他夫定(stavudine)(d4T);拉米夫定(lamivudine)(3TC);阿巴卡韦(abacavir)(1592U89);阿德福韦酯(adefovir dipivoxil)[双(POM)-PMEA];洛布卡韦(lobucavir)(BMS-180194);BCH-10652;恩曲他滨(emitricitabine)[(-)-FTC];β-L-FD4(也称为β-L-D4C,且命名为β-L-2',3'-二脱氧-5-氟-胞苷);DAPD((-)-β-D-2,6,-二氨基-嘌呤二氧戊环);和洛德腺苷(lodenosine)(FddA)。典型的合适NNRTI包括奈韦拉平(nevirapine)(BI-RG-587);地拉韦啶(delaviradine)(BHAP,U-90152);依法韦仑(efavirenz)(DMP-266);PNU-142721;AG-1549;MKC-442(1-(乙氧基-甲基)-5-(1-甲基乙基)-6-(苯基甲基)-(2,4(1H,3H)-嘧啶二酮);以及(+)-胡桐内酯A(NSC-675451)和B。典型的合适蛋白酶抑制剂包括沙奎那韦(saquinavir)(Ro 31-8959);利托那韦(ritonavir)(ABT-538);茚地那韦(indinavir)(MK-639);奈非那韦(nelfnavir)(AG-1343);安普那韦(amprenavir)(141W94);拉西那韦(lasinavir)(BMS-234475);DMP-450;BMS-2322623;ABT-378;和AG-1549。其它抗病毒剂包括羟基脲、利巴韦林(ribavirin)、IL-2、IL-12、喷他夫西(pentafuside)和伊萨姆(Yissum)项目第11607号。
当对患者施用不止一种药剂时,它们可以同时、分开、顺序或组合施用(例如,对于不止两种剂)。
在一些实施方案中,本公开的化合物可与INCB086550组合使用。
制剂、剂型和施用
本公开的化合物当用作药物时可以药物组合物的形式施用。因此本公开提供了一种组合物,其包含式(I)、(I’)或如本文所述的任何式的化合物、如任何权利要求中叙述和本文所述的化合物或其药学上可接受的盐或其任何实施方案和至少一种药学上可接受的载体或赋形剂。这些组合物可以药学领域中熟知的方式制备,并且可通过多种途径施用,这取决于是指示要局部治疗还是全身治疗以及要治疗的区域。施用可以是外用(包括透皮施用、表皮施用、经眼施用和对粘膜施用,包括鼻内递送、阴道递送和直肠递送)、肺部施用(例如,通过吸入或吹入粉剂或气雾剂,包括通过喷雾器;气管内施用或鼻内施用)、口服或肠胃外施用。肠胃外施用包括静脉内、动脉内、皮下、腹膜内、肌内注射或输注;或颅内施用,例如鞘内或脑室内施用。肠胃外施用可以单次推注剂量的形式进行,或者可例如通过连续灌注泵进行。用于外用施用的药物组合物和制剂可包括透皮贴剂、软膏、洗剂、乳膏、凝胶、滴剂、栓剂、喷雾剂、液体和粉剂。常规的药物载体、水溶液、粉剂或油性基质、增稠剂等可能是必要的或可取的。
本发明还包括药物组合物,其含有作为活性成分的本公开的化合物或其药学上可接受的盐与一种或多种药学上可接受的载体或赋形剂相组合。在一些实施方案中,所述组合物适合外用施用。在制备本发明的组合物时,通常将活性成分与赋形剂混合,用赋形剂进行稀释,或者封闭在例如胶囊、小袋、纸或其它容器形式这样的载体中。当赋形剂充当稀释剂时,其可以是充当活性成分的媒介物、载体或介质的固体、半固体或液体物质。因此,组合物的形式可以是片剂、丸剂、粉剂、菱形锭剂、小袋、扁囊剂、酏剂、混悬液、乳液、溶液、糖浆、气雾剂(作为固体或在液体介质中)、含有例如最多10重量%活性化合物的软膏、软明胶胶囊和硬明胶胶囊、栓剂、无菌可注射溶液和无菌包装粉剂。
在制备制剂时,可将活性化合物研磨以提供适当的粒度,之后才与其它成分组合。如果活性化合物基本上不溶,则可将其研磨至粒度小于200目。如果活性化合物基本上是水溶性的,则可通过研磨来调节粒度,以提供在制剂中基本上均匀的分布,例如约40目。
可采用已知的研磨程序对本发明的化合物进行研磨,如湿法研磨,以获得适于片剂形成和适于其它制剂类型的粒度。可通过本领域中已知的制程制备本发明的化合物的细碎(纳米颗粒)制剂,参见例如WO 2002/000196。
合适的赋形剂的一些实例包括乳糖、右旋糖、蔗糖、山梨糖醇、甘露糖醇、淀粉、阿拉伯胶、磷酸钙、海藻酸盐、黄蓍胶、明胶、硅酸钙、微晶纤维素、聚乙烯吡咯烷酮、纤维素、水、糖浆和甲基纤维素。制剂可另外包括:润滑剂,如滑石、硬脂酸镁和矿物油;润湿剂;乳化剂和悬浮剂;防腐剂,如羟基苯甲酸甲酯和羟基苯甲酸丙酯;甜味剂;和调味剂。可通过采用本领域中已知的程序配制本发明的组合物,以便在对患者施用后提供活性成分的快速、持续或延迟释放。
在一些实施方案中,药物组合物包含硅化微晶纤维素(SMCC)和至少一种本文所述的化合物或其药学上可接受的盐。在一些实施方案中,硅化微晶纤维素包含约98%的微晶纤维素和约2%的二氧化硅w/w。
在一些实施方案中,组合物是包含至少一种本文所述的化合物或其药学上可接受的盐和至少一种药学上可接受的载体或赋形剂的持续释放组合物。在一些实施方案中,组合物包含至少一种本文所述的化合物或其药学上可接受的盐以及至少一种选自微晶纤维素、乳糖一水合物、羟丙基甲基纤维素和聚环氧乙烷的组分。在一些实施方案中,组合物包含至少一种本文所述的化合物或其药学上可接受的盐以及微晶纤维素、乳糖一水合物和羟丙基甲基纤维素。在一些实施方案中,组合物包含至少一种本文所述的化合物或其药学上可接受的盐以及微晶纤维素、乳糖一水合物和聚环氧乙烷。在一些实施方案中,组合物进一步包含硬脂酸镁或二氧化硅。在一些实施方案中,微晶纤维素是Avicel PH102TM。在一些实施方案中,乳糖一水合物是Fast-flo 316TM。在一些实施方案中,羟丙基甲基纤维素是羟丙基甲基纤维素2208K4M(例如,Methocel K4 M PremierTM)和/或羟丙基甲基纤维素2208K100LV(例如,Methocel K00LVTM)。在一些实施方案中,聚环氧乙烷是聚环氧乙烷WSR1105(例如,Polyox WSR 1105TM)。
在一些实施方案中,采用湿法制粒制程制备组合物。在一些实施方案中,采用干法制粒制程制备组合物。
可将组合物配制成单位剂型,每个剂型含有约5至约1,000mg(1g)、更通常为约100mg至约500mg活性成分。在一些实施方案中,每一剂量含有约10mg活性成分。在一些实施方案中,每一剂量含有约50mg活性成分。在一些实施方案中,每一剂量含有约25mg活性成分。术语“单位剂型”是指适合作为单一剂量用于人受试者及其他哺乳动物的物理上分立的单位,每个单位含有经计算产生所需治疗效果的预定量的活性物质与合适的药物赋形剂的联合。
用于配制药物组合物的组分是高纯度的,并且基本上不含可能有害的污染物(例如,至少是国家食品级的,通常至少是分析级的,更典型至少是药物级的)。特别是对于人服用,优选按照如美国食品与药物管理局的适用规章中限定的良好生产规范标准来生产或配制组合物。例如,合适的制剂可以是无菌的和/或基本上等渗的和/或完全符合美国食品与药物管理局的所有良好生产规范章程。
活性化合物可在宽剂量范围内有效,并且通常以治疗有效量施用。然而要理解的是,实际施用的化合物量通常由医师根据相关情况进行确定,包括要治疗的疾患、选择的施用途径、实际施用的化合物、个体患者的年龄、体重和反应、患者症状的严重程度等。
本发明的化合物的治疗剂量可根据例如进行治疗的特定用途、化合物的施用方式、患者的健康状况和病状以及处方医师的判断而变化。本发明的化合物在药物组合物中的比例或浓度可根据许多因素而变化,包括剂量、化学特性(例如,疏水性)和施用途径。例如,本发明的化合物可提供在用于肠胃外施用的含有约0.1至约10%w/v化合物的生理缓冲水溶液中。一些典型的剂量范围是每天约1μg/kg体重至约1g/kg体重。在一些实施方案中,剂量范围是每天约0.01mg/kg体重至约100mg/kg体重。剂量有可能取决于诸如以下的变量:疾病或病症的类型和进展程度、特定患者的总体健康状态、选定化合物的相对生物学功效、赋形剂的配方及其施用途径。可由得自体外或动物模型测试系统的剂量反应曲线外推出有效剂量。
为制备固体组合物如片剂,将主要活性成分与药物赋形剂混合以形成含有本发明的化合物的均匀混合物的固体预制剂组合物。当提到这些预制剂组合物均匀时,活性成分通常均匀分散遍布于组合物中,使得组合物可以很容易地被细分成同等有效的单位剂型,如片剂、丸剂和胶囊。然后将此固体预制剂细分成含有例如约0.1至约1000mg本发明的活性成分的上述类型的单位剂型。
本发明的片剂或丸剂可经包衣或以其它方式混配以获得能提供延长作用的优点的剂型。例如,片剂或丸剂可包含内剂量和外剂量组分,后者呈在前者之上的包膜形式。这两种组分可由肠溶层隔开,该肠溶层用来抵抗在胃中崩解,并允许内部组分完整地进入十二指肠或延迟释放。多种物质可用于这类肠溶层或包衣,这类物质包括许多聚合酸以及聚合酸与诸如虫胶、鲸蜡醇和醋酸纤维素的物质的混合物。
可掺入本发明的化合物和组合物以用于口服或通过注射施用的液体形式包括水溶液、适当调味的糖浆、水性或油混悬液和含食用油如棉籽油、芝麻油、椰子油或花生油的调味乳液以及酏剂和类似的药物媒介物。
用于吸入或吹入的组合物包括在药学上可接受的水性或有机溶剂或其混合物中的溶液和混悬液以及粉剂。液体或固体组合物可含有如上文所述的合适的药学上可接受的赋形剂。在一些实施方案中,通过口服或鼻呼吸途径施用组合物以获得局部或全身效果。可通过使用惰性气体将组合物雾化。可直接呼吸来自雾化装置的雾化溶液,或者可将雾化装置附接于面罩、帐幕或间歇正压呼吸机。可由以适当方式递送制剂的装置口服或经鼻施用溶液、混悬液或粉剂组合物。
外用制剂可含有一种或多种常规载体。在一些实施方案中,软膏可含有水和选自例如液体石蜡、聚氧乙烯烷基醚、丙二醇、白凡士林等的一种或多种疏水载体。乳膏的载体组合物可基于水与甘油和一种或多种其它组分例如单硬脂酸甘油酯、PEG-单硬脂酸甘油酯及鲸蜡硬脂醇组合。可使用异丙醇和水合适地与其它组分举例如甘油、羟乙基纤维素等组合来配制凝胶。在一些实施方案中,外用制剂含有至少约0.1重量%、至少约0.25重量%、至少约0.5重量%、至少约1重量%、至少约2重量%或至少约5重量%的本发明的化合物。可合适地将外用制剂包装在例如100g的管中,所述管任选关联有治疗选定适应症例如银屑病或其它皮肤病状的说明书。
对患者施用的化合物或组合物的量将根据所施用的药物、施用的目的如预防或治疗、患者的状态、施用方式等而变化。在治疗应用中,对已经罹患疾病的患者施用足以治愈或至少部分地遏制所述疾病及其并发症的症状的量的组合物。有效剂量将取决于所治疗的疾病状况以及通过主治医师根据诸如疾病的严重程度、患者的年龄、体重和一般状况等因素进行判断。
对患者施用的组合物可呈上述药物组合物的形式。这些组合物可通过常规的灭菌技术进行灭菌,或者可以进行无菌过滤。可将水溶液包装供原样使用,或者冻干,在施用之前将冻干的制剂与无菌水性载体组合。化合物制剂的pH通常将在3与11之间,更优选为5至9,且最优选为7至8。将要理解的是,使用某些前述赋形剂、载体或稳定剂将导致药物盐的形成。
本发明化合物的治疗剂量可根据例如进行治疗的特定用途、化合物的施用方式、患者的健康状况和病状以及处方医师的判断而变化。本发明的化合物在药物组合物中的比例或浓度可根据许多因素而变化,包括剂量、化学特性(例如,疏水性)和施用途径。例如,本发明的化合物可提供在用于肠胃外施用的含有约0.1至约10%w/v化合物的生理缓冲水溶液中。一些典型的剂量范围是每天约1μg/kg体重至约1g/kg体重。在一些实施方案中,剂量范围是每天约0.01mg/kg体重至约100mg/kg体重。剂量有可能取决于诸如以下的变量:疾病或病症的类型和进展程度、特定患者的总体健康状态、选定化合物的相对生物学功效、赋形剂的配方及其施用途径。可由得自体外或动物模型测试系统的剂量反应曲线外推出有效剂量。
标记化合物和测定方法
本发明的另一方面涉及本公开的标记化合物(放射标记、荧光标记等),它们不仅可用于成像技术,而且也可用于体外和体内测定,用于定位和定量包括人在内的组织样本中的HPK1蛋白,以及通过抑制标记化合物的结合来鉴别HPK1配体。取代本公开的化合物的一个或多个原子也可用于产生有差别的ADME(吸附、分布、代谢和排泄)。因此,本发明包括含有这类标记或取代化合物的HPK1结合测定。
本公开进一步包括本公开的同位素标记化合物。“同位素”或“放射标记”化合物是本公开的化合物,其中一个或多个原子被原子质量或质量数不同于通常存在于自然界中的(即,天然存在的)原子质量或质量数的原子置换或取代。可结合到本公开的化合物中的合适放射性核素包括但不限于2H(氘,也写成D)、3H(氚,也写成T)、11C、13C、14C、13N、15N、15O、17O、18O、18F、35S、36Cl、82Br、75Br、76Br、77Br、123I、124I、125I和131I。例如,本公开的化合物中的一个或多个氢原子可以被氘原子置换(例如,式(I)或(I’)的C1-6烷基的一个或多个氢原子可任选被氘原子取代,如–CD3取代–CH3)。在一些实施方案中,式(I)或(I’)中的烷基可以是全氘化的。
本文提供的化合物的一个或多个组成原子可以被天然或非天然丰度的原子的同位素置换或取代。在一些实施方案中,所述化合物包括至少一个氘原子。在一些实施方案中,所述化合物包括两个或更多个氘原子。在一些实施方案中,所述化合物包括1-2、1-3、1-4、1-5或1-6个氘原子。在一些实施方案中,化合物中的所有氢原子均可被氘原子置换或取代。
将同位素包括到有机化合物中的合成方法是本领域中已知的(DeuteriumLabeling in Organic Chemistry,Alan F.Thomas(New York,N.Y.,Appleton-Century-Crofts,1971);The Renaissance of H/D Exchange,Jens Atzrodt、Volker Derdau、Thorsten Fey和Jochen Zimmermann,Angew.Chem.Int.Ed.2007,7744-7765;The OrganicChemistry of Isotopic Labelling,James R.Hanson,Royal Society of Chemistry,2011)。同位素标记化合物可用于各种研究,如NMR光谱、代谢实验和/或测定。
用较重的同位素如氘进行取代可由于代谢稳定性更高而提供某些治疗优点,例如体内半衰期增加或剂量需求减少,且因此在一些情况下可能是优选的。(参见例如A.Kerekes等人,J.Med.Chem.2011,54,201-210;R.Xu等人,J.LabelCompd.Radiopharm.2015,58,308-312)。特别地,在一个或多个代谢位点进行取代可提供一种或多种治疗优点。
结合到本发明放射标记化合物中的放射性核素将取决于该放射标记化合物的具体应用。例如,对于体外腺苷受体标记和竞争测定,结合3H、14C、82Br、125I、131I或35S的化合物可能是有用的。对于放射成像应用,11C、18F、125I、123I、124I、131I、75Br、76Br或77Br可能是有用的。
要理解的是,“放射标记”或“标记化合物”是已结合至少一种放射性核素的化合物。在一些实施方案中,放射性核素选自由3H、14C、125I、35S和82Br组成的组。
本公开可进一步包括将放射性同位素结合到本公开的化合物中的合成方法。将放射性同位素结合到有机化合物中的合成方法是本领域中熟知的,并且本领域普通技术人员将会很容易确认适用于本公开的化合物的方法。
本发明的标记化合物可用于鉴别和/或评估化合物的筛选测定。例如,经标记的新合成或鉴别的化合物(即,测试化合物)可通过经由跟踪标记监测其与HPK1接触时的浓度变化来评估其结合HPK1蛋白的能力。例如,可对测试化合物(标记的)评估其减少结合另一种已知与HPK1蛋白结合的化合物(即,标准化合物)的能力。因此,测试化合物与标准化合物竞争与HPK1蛋白结合的能力直接与其结合亲和力相关。相反,在一些其它筛选测定中,标准化合物被标记,而测试化合物未被标记。因此,监测标记的标准化合物的浓度,以便评估标准化合物与测试化合物之间的竞争性,从而确定测试化合物的相对结合亲和力。
试剂盒
本公开还包括可用于例如治疗或预防与HPK1的活性相关的疾病或病症如癌症或感染的药物试剂盒,其包括一个或多个容器,所述容器含有包含治疗有效量的式(I)、(I’)或其任何实施方案的化合物的药物组合物。如对于本领域技术人员而言显而易见的那样,这类试剂盒可进一步包括各种常规药物试剂盒组分中的一种或多种,举例如含一种或多种药学上可接受的载体的容器、另外的容器等。试剂盒中还可以包括插页或标签形式的说明书,其指示要施用的组分的量、关于施用的指导和/或关于混合组分的指导。
将借助于具体实施例对本发明进行更详细的描述。提供以下实施例是用于说明的目的,并不意图以任何方式限制本发明。本领域技术人员将容易认识到可以对各种非关键参数进行变动或修改以产生基本上相同的结果。根据本文描述的至少一种测定已发现,实施例的化合物抑制HPK1的活性。
实施例
以下提供本发明的化合物的实验程序。制备的一些化合物的制备型LC-MS纯化在Waters质量指导型分级系统上进行。文献中已经详细描述了操作这些系统的基本设备设置、方案和控制软件。参见例如“Two-Pump At Column Dilution Configuration forPreparative LC-MS”,K.Blom,J.Combi.Chem.,4,295(2002);“Optimizing PreparativeLC-MS Configurations and Methods for Parallel Synthesis Purification”,K.Blom、R.Sparks、J.Doughty、G.Everlof、T.Haque、A.Combs,J.Combi.Chem.,5,670(2003);和“Preparative LC-MS Purification:Improved Compound Specific MethodOptimization”,K.Blom、B.Glass、R.Sparks、A.Combs,J.Combi.Chem.,6,874-883(2004)。通常使分离的化合物经受分析液相色谱质谱(LCMS)以进行纯度检查。
通常在以下条件下使分离的化合物经受分析液相色谱质谱(LCMS)以进行纯度检查:仪器;Agilent 1100系列,LC/MSD;柱:Waters SunfireTM C18 5μm粒度,2.1x 5.0mm;缓冲液:流动相A:在水中0.025%TFA,以及流动相B:乙腈;梯度为在3分钟内2%至80%的B,流速为2.0mL/分钟。
如实施例中所示,也通过具有MS检测器的反相高效液相色谱法(RP-HPLC)或快速色谱法(硅胶)在制备规模上分离一些制备的化合物。典型的制备型反相高效液相色谱法(RP-HPLC)柱条件如下:
pH=2纯化:Waters SunfireTM C18 5μm粒度,19x 100mm柱,用流动相A:在水中0.1%TFA(三氟乙酸)和流动相B:乙腈进行洗脱;流速为30mL/分钟,采用如文献中描述的化合物特异性方法优化方案对每种化合物优化分离梯度[参见“Preparative LCMSPurification:Improved Compound Specific Method Optimization”,K.Blom、B.Glass、R.Sparks、A.Combs,J.Comb.Chem.,6,874-883(2004)]。典型地,30x 100mm柱所用的流速为60mL/分钟。
pH=10纯化:Waters XBridge C18 5μm粒度,19x 100mm柱,用流动相A:在水中0.15%NH4OH和流动相B:乙腈进行洗脱;流速为30mL/分钟,采用如文献中描述的化合物特异性方法优化方案对每种化合物优化分离梯度[参见“Preparative LCMS Purification:Improved Compound Specific Method Optimization”,K.Blom、B.Glass、R.Sparks、A.Combs,J.Comb.Chem.,6,874-883(2004)]。典型地,30x 100mm柱所用的流速为60mL/分钟。
本文可使用以下缩写:AcOH(乙酸);Ac2O(乙酸酐);aq.(水溶液);atm.(大气压);Boc(叔丁氧羰基);BOP((苯并三唑-1-基氧基)三(二甲氨基)鏻六氟磷酸盐);br(宽);Cbz(羧基苄基);calc.(计算);d(双重峰);dd(双重双重峰);DBU(1,8-二氮杂双环[5.4.0]十一碳-7-烯);DCM(二氯甲烷);DIAD(叠氮二甲酸N,N'-二异丙酯);DIEA(N,N-二异丙基乙胺);DIPEA(N,N-二异丙基乙胺);DIBAL(二异丁基氢化铝);DMF(N,N-二甲基甲酰胺);Et(乙基);EtOAc(乙酸乙酯);FCC(快速柱色谱法);g(克);h(小时);HATU(N,N,N',N'-四甲基-O-(7-氮杂苯并三唑-1-基)脲鎓六氟磷酸盐);HCl(盐酸);HPLC(高效液相色谱法);Hz(赫兹);J(耦合常数);LCMS(液相色谱-质谱法);LDA(二异丙基氨基锂);m(多重峰);M(摩尔);mCPBA(3-氯过氧苯甲酸);MS(质谱法);Me(甲基);MeCN(乙腈);MeOH(甲醇);mg(毫克);min.(分钟);mL(毫升);mmol(毫摩尔);N(正);nM(纳摩尔);NMP(N-甲基吡咯烷酮);NMR(核磁共振谱);OTf(三氟甲磺酸酯);Ph(苯基);pM(皮摩尔);RP-HPLC(反相高效液相色谱法);r.t.(室温)、s(单重峰);t(三重峰或叔);TBS(叔丁基二甲基甲硅烷基);tert(叔);tt(三重三重峰);TFA(三氟乙酸);THF(四氢呋喃);μg(微克);μL(微升);μM(微摩尔);wt%(重量百分比)。盐水是饱和氯化钠水溶液。真空是在真空下。
实施例1.N-(2-((1R,4R)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
步骤1. 2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酸
将2-氯嘧啶-4-甲酸(9.0g,56.8mmol)、(2-氟-6-甲氧基苯基)硼酸(11.58g,68.1mmol)、XPhosPd G2(1.340g,1.703mmol)和磷酸三钾(24.10g,114mmol)的混合物与1,4-二噁烷(100mL)和水(20.00mL)合并。将反应烧瓶抽真空,用氮气回填,然后加热到80℃保持2h。然后将反应混合物冷却到室温,用水处理并用乙酸乙酯稀释。将水相分离,并用1NHCl酸化。过滤收集所得固体并用水洗涤。风干后,将其不经进一步纯化在步骤4中使用。C12H10FN2O3(M+H)+的LCMS计算值:m/z=249.2;实测值249.2。
步骤2.(1R,4R)-5-(4-氟-2-硝基苯基)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯
用三乙胺(338μl,2.4mmol)处理1,4-二氟-2-硝基苯(257mg,1.6mmol)和(1R,4R)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯(320mg,1.6mmol)在DMSO(2.5mL)中的溶液。将反应混合物加热到80℃保持3h。冷却到室温后,将反应混合物用二氯甲烷稀释,并用盐水洗涤。将分离的有机相经硫酸钠干燥并浓缩。粗产物不经进一步纯化用于下一步。C12H13FN3O4(M+H-C4H8)+的LCMS计算值:m/z=282.1;实测值282.1。
步骤3.(1R,4R)-5-(2-氨基-4-氟苯基)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯
将(1R,4R)-5-(4-氟-2-硝基苯基)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯(545mg,1.6mmol)、铁(451mg,8.1mmol)和氯化铵(518mg,9.7mmol)在THF(2mL)、水(2mL)和甲醇(2mL)中的混合物在60℃下搅拌3h。冷却到室温后,将反应混合物通过硅藻土塞过滤,并用二氯甲烷稀释。将有机相分离,用盐水洗涤,经硫酸钠干燥,并真空蒸发溶剂。粗产物不经进一步纯化用于下一步。C16H23FN3O2(M+H)+的LCMS计算值:m/z=308.2;实测值:308.2。
步骤4.N-(2-((1R,4R)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
将HATU(178mg,0.468mmol)添加到(1R,4R)-5-(2-氨基-4-氟苯基)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯(96mg,0.312mmol)、2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酸(来自步骤1;78mg,0.312mmol)和DIPEA(109μl,0.625mmol)在DMF(2mL)中的溶液中。将反应混合物在室温下搅拌30分钟,然后用水处理。过滤收集沉淀产物,用水洗涤并风干。然后将固体残留物重新溶解在TFA中,并将溶液在室温下搅拌10分钟。然后将混合物用乙腈稀释,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化,以分离标题化合物,为TFA盐。C23H22F2N5O2(M+H)+的LCMS计算值:m/z=438.2;实测值:438.2。
实施例2.(S)-N-(2-(3-氨基吡咯烷-1-基)-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例1中所述的程序,使用(S)-吡咯烷-3-胺代替(1R,4R)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯作为起始物质制备标题化合物的TFA盐。C22H22F2N5O2(M+H)+的LCMS计算值:m/z=426.2;实测值:426.3。
实施例3.(R)-N-(2-(2-(氨甲基)吡咯烷-1-基)-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例1中所述的程序,使用(R)-吡咯烷-2-基甲基氨基甲酸叔丁酯代替(1R,4R)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯作为起始物质制备标题化合物的TFA盐。C23H24F2N5O2(M+H)+的LCMS计算值:m/z=440.2;实测值:440.1。
实施例4.(R)-N-(5-氟-2-(2-(羟甲基)吡咯烷-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例1中所述的程序,使用(R)-吡咯烷-2-基甲醇代替(1R,4R)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯作为起始物质制备标题化合物的TFA盐。C23H23F2N4O3(M+H)+的LCMS计算值:m/z=441.2;实测值:441.1。
实施例5.(R)-N-(5-氟-2-(2-(甲氧基甲基)吡咯烷-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例1中所述的程序,使用(R)-2-(甲氧基甲基)吡咯烷代替(1R,4R)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯作为起始物质制备标题化合物的TFA盐。C24H25F2N4O3(M+H)+的LCMS计算值:m/z=455.2;实测值:455.3。
实施例6.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例1中所述的程序(且在下文详述),使用(3S,5S)-5-(羟甲基)-吡咯烷-3-基氨基甲酸叔丁酯代替(1R,4R)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯作为起始物质制备标题化合物的游离碱和TFA盐。
步骤1.((3S,5S)-1-(4-氟-2-硝基苯基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯
用三乙胺(131μL,0.943mmol)处理1,4-二氟-2-硝基苯(68.2μL,0.629mmol)和((3S,5S)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯(136mg,0.629mmol)在DMSO(2.5mL)中的溶液,并将反应混合物加热到80℃保持3小时。冷却到室温后,将反应混合物用DCM稀释,用盐水洗涤,经硫酸钠干燥,并在真空下蒸发溶剂。得到的粗产物不经进一步纯化用于下一步。C12H15FN3O5(M+H-C4H8)+的LCMS计算值:m/z=300.1;实测值:300.1。
步骤2.((3S,5S)-1-(2-氨基-4-氟苯基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯
将((3S,5S)-1-(4-氟-2-硝基苯基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯(100mg,0.281mmol)、铁(79mg,1.407mmol)和氯化铵(90mg,1.7mmol)在THF(2mL)、水(2mL)和甲醇(2mL)中的混合物在60℃下搅拌3小时。冷却到室温后,将混合物通过硅藻土塞过滤,并用DCM稀释。将有机相分离,用盐水洗涤,经硫酸钠干燥,并在真空下蒸发溶剂。得到的粗产物不经进一步纯化用于下一步。C16H25FN3O3(M+H)+的LCMS计算值:m/z=326.2;实测值:326.2。
步骤3.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
将HATU(175mg,0.461mmol)添加到((3S,5S)-1-(2-氨基-4-氟苯基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯(100mg,0.307mmol)、2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酸(实施例1步骤1的产物,76mg,0.307mmol)和DIPEA(107μL,0.615mmol)在DMF(2mL)中的溶液中。将反应混合物在室温下搅拌30分钟,然后添加水,并过滤收集沉淀产物,用水洗涤并风干。将固体溶解在TFA中,并将所得溶液在室温下搅拌10分钟。然后将溶液用乙腈稀释,并用制备型LCMS纯化。C23H24F2N5O3(M+H)+的LCMS计算值:m/z=456.2;实测值:456.3。制备型LCMS(XBridge C18柱,以含有0.1%NH4OH的乙腈/水的梯度洗脱,流速为60mL/分钟)。游离碱:1HNMR(600MHz,DMSO-d6)δ9.34–9.18(m,1H),8.25–8.19(m,1H),8.18–8.14(m,1H),7.60–7.49(q,J=7.7Hz,1H),7.49–7.43(m,1H),7.08–7.02(d,J=8.4Hz,1H),7.02–6.94(m,2H),3.78–3.71(s,3H),3.38–3.30(t,J=6.4Hz,1H),3.30–3.23(m,1H),3.23–3.17(m,1H),3.17–3.10(dd,J=11.1,6.1Hz,1H),2.95–2.88(t,J=7.4Hz,1H),2.88–2.80(m,1H),2.35–2.25(dt,J=14.1,8.0Hz,1H),1.25–1.12(m,1H)ppm。制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)TFA盐:1H NMR(600MHz,DMSO-d6)δ10.78–10.58(s,1H),9.32–9.20(d,J=5.0Hz,1H),8.24–8.08(m,2H),7.93–7.77(br,J=5.7Hz,2H),7.62–7.53(td,J=8.4,6.8Hz,1H),7.53–7.46(dd,J=8.8,5.7Hz,1H),7.10–7.02(m,2H),7.02–6.93(t,J=8.8Hz,1H),3.82–3.73(s,3H),3.75–3.67(m,1H),3.59–3.51(m,1H),3.30–3.15(m,4H),2.44–2.35(ddd,J=13.6,9.1,7.2Hz,1H),1.81–1.71(dt,J=13.5,4.3Hz,1H)ppm。
实施例7.N-(5-氟-2-((2S,4S)-4-羟基-2-甲基吡咯烷-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例1中所述的程序,使用(3S,5S)-5-甲基吡咯烷-3-醇代替(1R,4R)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯作为起始物质制备标题化合物的TFA盐。C23H23F2N4O3(M+H)+的LCMS计算值:m/z=441.2;实测值:441.3。
实施例8.N-(5-氟-2-(2-(吡啶-2-基)吡咯烷-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例1中所述的程序,使用2-(吡咯烷-2-基)吡啶代替(1R,4R)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯作为起始物质制备标题化合物的TFA盐。C27H24F2N5O2(M+H)+的LCMS计算值:m/z=488.2;实测值:488.1。
实施例9.N-(5-氟-2-(六氢吡咯并[3,4-b]吡咯-1(2H)-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例1中所述的程序,使用六氢吡咯并[3,4-b]吡咯-5(1H)-甲酸叔丁酯代替(1R,4R)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯作为起始物质制备标题化合物的TFA盐。C24H24F2N5O2(M+H)+的LCMS计算值:m/z=452.2;实测值:452.2。
实施例10.(R)-N-(5-氟-2-(2-甲基哌嗪-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例1中所述的程序,使用(R)-3-甲基哌嗪-1-甲酸叔丁酯代替(1R,4R)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯作为起始物质制备标题化合物的TFA盐。C23H24F2N5O2(M+H)+的LCMS计算值:m/z=440.2;实测值:440.2。
实施例11.(R)-N-(5-氟-2-(2-(羟甲基)哌嗪-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例1中所述的程序,使用(R)-3-(羟甲基)哌嗪-1-甲酸叔丁酯代替(1R,4R)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯作为起始物质制备标题化合物的TFA盐。C23H24F2N5O3(M+H)+的LCMS计算值:m/z=456.2;实测值:456.2。
实施例12.N-(5-氟-2-(3-(羟甲基)吗啉代)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例1中所述的程序,使用吗啉-3-基甲醇代替(1R,4R)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯作为起始物质制备标题化合物的TFA盐。C23H23F2N4O4(M+H)+的LCMS计算值:m/z=457.2;实测值:457.2。
实施例13.N-(2-((1R,4R)-2,5-二氮杂双环[2.2.1]庚-2-基)-3-溴-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例1中所述的程序,使用1-溴-2,5-二氟-3-硝基苯代替1,4-二氟-2-硝基苯作为起始物质制备标题化合物的TFA盐。C23H21BrF2N5O2(M+H)+的LCMS计算值:m/z=516.1;实测值:516.1。
实施例14.N-(2-((1R,4R)-2,5-二氮杂双环[2.2.1]庚-2-基)-3-氰基苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例1中所述的程序,使用2-氟-3-硝基苄腈代替1,4-二氟-2-硝基苯作为起始物质制备标题化合物的TFA盐。C24H22FN6O2(M+H)+的LCMS计算值:m/z=445.2;实测值:445.2。
实施例15.N-(2-((1R,4R)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟-3-(吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
将(1R,4R)-5-(2-溴-4-氟-6-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)苯基)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯(来自实施例13;10mg,0.016mmol)、吡啶-3-基硼酸(4mg,0.032mmol)、XPhosPd G2(1.3mg,1.6μmol)和磷酸三钾(6.7mg,0.032mmol)的混合物与1,4-二噁烷(1mL)和水(0.1mL)合并。将反应烧瓶抽真空,用氮气回填,并将混合物在80℃下搅拌1h。将反应混合物冷却到室温并真空蒸发溶剂。将残留物与TFA(1mL)合并,并在室温下搅拌10分钟。将反应混合物用CH3CN和水稀释,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化,得到标题化合物的TFA盐。C28H25F2N6O2(M+H)+的LCMS计算值:m/z=515.2;实测值:515.3。
实施例16.N-(2-((1R,4R)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟-3-(1-甲基-1H-吡唑-4-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例15中所述的程序,使用1-甲基-4-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)-1H-吡唑代替吡啶-3-基硼酸作为起始物质制备标题化合物的TFA盐。C27H26F2N7O2(M+H)+的LCMS计算值:m/z=518.2;实测值:518.3。
实施例17.N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟-4-(羟甲基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例1中所述的程序,使用(2,5-二氟-4-硝基苯基)甲醇代替1,4-二氟-2-硝基苯,并使用(1S,4S)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯代替(1R,4R)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯作为起始物质制备标题化合物的TFA盐。C24H24F2N5O3(M+H)+的LCMS计算值:m/z=468.2;实测值:468.2。1H NMR(600MHz,DMSO-d6)δ10.81–10.70(s,1H),9.33–9.25(d,J=5.0Hz,1H),8.19–8.12(d,J=5.0Hz,1H),8.12–8.04(d,J=11.4Hz,1H),7.63–7.52(q,J=7.9Hz,1H),7.38–7.28(d,J=7.2Hz,1H),7.13–7.06(d,J=8.5Hz,1H),7.05–6.95(t,J=8.8Hz,1H),5.28–5.16(s,1H),4.57–4.42(s,2H),3.82–3.71(s,3H),3.70–3.60(s,1H),3.54–3.46(s,1H),3.26–3.17(d,J=9.0Hz,1H),3.12–3.04(d,J=9.0Hz,1H),2.92–2.86(d,J=10.0Hz,1H),2.67–2.59(d,J=9.7Hz,1H),1.65–1.59(d,J=9.3Hz,1H),1.54–1.38(d,J=9.1Hz,1H)ppm。
实施例18.N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-4-溴-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例1中所述的程序,使用1-溴-2,5-二氟-4-硝基苯代替1,4-二氟-2-硝基苯,并使用(1S,4S)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯代替(1R,4R)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯作为起始物质制备标题化合物的TFA盐。C23H21BrF2N5O2(M+H)+的LCMS计算值:m/z=516.1;实测值:516.1。
实施例19.N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟-4-(1-甲基-1H-吡唑-4-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
将(1S,4S)-5-(5-溴-4-氟-2-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)苯基)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯(来自实施例18;10mg,0.016mmol)、1-甲基-4-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)-1H-吡唑(6.8mg,0.032mmol)、XPhosPd G2(1.3mg,1.6μmol)和磷酸三钾(6.7mg,0.032mmol)的混合物与1,4-二噁烷(1mL)和水(0.1mL)合并。将反应烧瓶抽真空,用氮气回填,然后在80℃下搅拌1h。将反应混合物冷却到室温,将溶剂真空蒸发并添加TFA(1mL)。将反应混合物在室温下搅拌10分钟,然后用CH3CN和水稀释,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化,得到标题化合物的TFA盐。C27H26F2N7O2(M+H)+的LCMS计算值:m/z=518.2;实测值:518.3。1H NMR(600MHz,DMSO-d6)δ10.58(s,1H),9.30(d,J=4.9Hz,1H),8.94(br,2H),8.20–8.15(m,2H),8.14(s,1H),7.94(s,1H),7.67–7.53(m,2H),7.09(d,J=8.5Hz,1H),7.02(t,J=8.7Hz,1H),4.41(s,1H),4.04(s,1H),3.91(s,3H),3.78(s,3H),3.51(d,J=11.0Hz,1H),3.42(d,J=11.2Hz,1H),3.34–3.20(m,1H),3.03(s,1H),1.91(d,J=10.6Hz,1H),1.77(d,J=10.7Hz,1H)ppm。
实施例20.N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟-4-(6-(羟甲基)吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例19中所述的程序,使用(5-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)吡啶-2-基)甲醇代替1-甲基-4-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)-1H-吡唑作为起始物质制备标题化合物的TFA盐。C29H27F2N6O3(M+H)+的LCMS计算值:m/z=545.2;实测值:545.3。
实施例21.N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟-4-(6-(甲基氨甲酰基)吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例19中所述的程序,使用N-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)吡啶酰胺代替1-甲基-4-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)-1H-吡唑作为起始物质制备标题化合物的TFA盐。C30H28F2N7O3(M+H)+的LCMS计算值:m/z=572.2;实测值:572.3。
实施例22.N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟-4-(1-甲基-6-氧代-1,6-二氢吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例19中所述的程序,使用1-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)吡啶-2(1H)-酮代替1-甲基-4-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)-1H-吡唑作为起始物质制备标题化合物的TFA盐。C29H27F2N6O3(M+H)+的LCMS计算值:m/z=545.2;实测值:545.3。
实施例23.N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟-4-(2-甲基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例19中所述的程序,使用2-甲基吡啶-3-基硼酸代替1-甲基-4-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)-1H-吡唑作为起始物质制备标题化合物的TFA盐。C29H27F2N6O2(M+H)+的LCMS计算值:m/z=529.2;实测值:529.3。
实施例24.N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-4-(2-甲基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
步骤1.(1S,4S)-5-(5-溴-2-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)苯基)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯
根据实施例18中所述的程序,使用4-溴-2-氟-1-硝基苯代替1-溴-2,5-二氟-4-硝基苯作为起始物质制备此化合物。C28H30BrFN5O4(M+H)+的LCMS计算值:m/z=598.2;实测值:598.2。
步骤2.N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-4-(2-甲基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
将(1S,4S)-5-(5-溴-2-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)苯基)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯(10mg,0.017mmol)、(2-甲基吡啶-3-基)硼酸(4.6mg,0.033mmol)、XPhosPd G2(1.3mg,1.6μmol)和磷酸三钾(6.7mg,0.032mmol)的混合物与1,4-二噁烷(1mL)和水(0.1mL)合并。将反应烧瓶抽真空,用氮气回填,然后在80℃下搅拌1h。将反应混合物冷却到室温,将溶剂真空蒸发并添加TFA(1mL)。将反应混合物在室温下搅拌10分钟,然后用CH3CN和水稀释,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化,得到标题化合物的TFA盐。C29H28FN6O2(M+H)+的LCMS计算值:m/z=511.2;实测值:511.2。1H NMR(600MHz,DMSO-d6)δ10.54–10.46(s,1H),9.33–9.18(d,J=5.0Hz,1H),9.06–8.91(s,1H),8.80–8.74(s,1H),8.67–8.63(dd,J=5.2,1.8Hz,1H),8.20–8.14(d,J=5.0Hz,1H),8.14–8.09(d,J=8.2Hz,1H),8.09–7.98(d,J=8.1Hz,1H),7.70–7.61(m,1H),7.61–7.55(td,J=8.4,6.8Hz,1H),7.31–7.27(d,J=1.9Hz,1H),7.21–7.15(dd,J=8.2,1.8Hz,1H),7.12–7.06(d,J=8.5Hz,1H),7.06–6.96(t,J=8.8Hz,1H),4.39–4.30(s,1H),4.28–4.17(s,1H),3.84–3.71(s,3H),3.62–3.52(m,1H),3.39–3.34(d,J=11.2Hz,1H),3.34–3.28(m,1H),3.15–3.04(m,1H),2.63–2.58(s,3H),1.97–1.90(dd,J=10.8,2.5Hz,1H),1.84–1.67(m,1H)。
实施例25.N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-4-(4-甲氧基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例24中所述的程序,使用4-甲氧基吡啶-3-基硼酸代替(2-甲基吡啶-3-基)硼酸作为起始物质制备标题化合物的TFA盐。C29H28FN6O3(M+H)+的LCMS计算值:m/z=527.2;实测值:527.2。
实施例26.N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例24中所述的程序(且在下文详述),使用3-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)异烟腈代替(2-甲基吡啶-3-基)硼酸作为起始物质制备标题化合物的TFA盐。
步骤1.(1S,4S)-5-(5-溴-2-硝基苯基)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯
向4-溴-2-氟-1-硝基苯(500mg,2.3mmol)和(1S,4S)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯(451mg,2.3mmol)在DMSO(8mL)中的溶液中添加三乙胺(475μl,3.41mmol),并将反应混合物加热到80℃保持2小时。冷却到室温后,添加水并过滤收集沉淀产物,用水洗涤并风干。其不经进一步纯化用于下一步。C16H21BrN3O4(M+H)+的LCMS计算值:m/z=398.1/400.1;实测值398.1/400.1。
步骤2.(1S,4S)-5-(2-氨基-5-溴苯基)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯
将(1S,4S)-5-(5-溴-2-硝基苯基)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯(914mg,2.295mmol)、铁(684mg,12.25mmol)和氯化铵(786mg,14.70mmol)在THF(5mL)、水(5mL)和甲醇(5mL)中的混合物在60℃下搅拌3小时。冷却到室温后,将其通过硅藻土塞过滤,并用DCM稀释。将有机相分离,用盐水洗涤,经硫酸钠干燥并真空蒸发溶剂。得到的粗产物不经进一步纯化用于下一步。C16H23BrN3O2(M+H)+的LCMS计算值:m/z=368.1/370.1;实测值:368.1/370.1。
步骤3.(1S,4S)-5-(5-溴-2-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)苯基)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯
用HATU(1.3g,3.4mmol)处理(1S,4S)-5-(2-氨基-5-溴苯基)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯(845mg,2.294mmol)、2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酸(实施例1步骤1的产物,570mg,2.3mmol)和DIPEA(800μl,4.6mmol)在DMF(5mL)中的溶液。将反应混合物在室温下搅拌30分钟,然后添加水并过滤收集沉淀产物,用水洗涤并风干。粗产物不经进一步纯化用于下一步。C28H30BrFN5O4(M+H)+的LCMS计算值:m/z=598.2/600.2;实测值:598.2/600.2。
步骤4.N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
通过抽真空将(1S,4S)-5-(5-溴-2-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)苯基)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯(10mg,0.017mmol)、3-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)异烟腈(9.8mg,0.043mmol)、Xphos Pd G2(1.3mg,1.6μmol)和磷酸三钾(6.7mg,0.032mmol)在1,4-二噁烷(1mL)和水(0.1mL)中的混合物脱气,并用氮气回填。将反应混合物在80℃下搅拌1小时,冷却到室温并真空蒸发溶剂。将TFA(1mL)添加到残留物中,并将反应混合物在室温下搅拌10分钟,然后用CH3CN和水稀释,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化。C29H25FN7O2(M+H)+的LCMS计算值:m/z=522.2;实测值:522.3。1H NMR(600MHz,DMSO-d6)δ10.60–10.51(s,1H),9.33–9.22(d,J=4.9Hz,1H),9.08–9.00(m,1H),9.01–8.95(s,1H),8.88–8.80(d,J=4.9Hz,1H),8.81–8.70(m,1H),8.21–8.15(d,J=4.9Hz,1H),8.15–8.10(d,J=8.2Hz,1H),8.06–8.00(d,J=5.0Hz,1H),7.60–7.53(q,J=7.9Hz,1H),7.53–7.49(s,1H),7.40–7.32(d,J=8.1Hz,1H),7.13–7.07(d,J=8.5Hz,1H),7.05–6.95(t,J=8.8Hz,1H),4.42–4.35(s,1H),4.32–4.24(s,1H),3.84–3.76(s,3H),3.67–3.58(d,J=11.0Hz,1H),3.46–3.35(d,J=10.9Hz,2H),3.15–3.04(dd,J=11.6,8.2Hz,1H),1.99–1.92(d,J=10.8Hz,1H),1.89–1.75(d,J=10.7Hz,1H)。
实施例27.N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-4-(1,3,5-三甲基-1H-吡唑-4-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例24中所述的程序,使用1,3,5-三甲基-4-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)-1H-吡唑代替(2-甲基吡啶-3-基)硼酸作为起始物质制备标题化合物的TFA盐。C29H31FN7O2(M+H)+的LCMS计算值:m/z=528.2;实测值:528.2。
实施例28.N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟-4-吗啉代苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
将(1S,4S)-5-(5-溴-4-氟-2-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)苯基)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯(来自实施例18,10mg,0.016mmol)、吗啉(1.4mg,0.016mmol)、RuPhosPd G2(1.2mg,1.6μmol)和碳酸铯(10.6mg,0.032mmol)的混合物与1,4-二噁烷(1mL)合并。将反应烧瓶抽真空,用氮气回填,并在100℃下搅拌3h。将反应混合物冷却到室温,将溶剂真空蒸发并添加TFA(1mL)。将反应混合物在室温下搅拌10分钟,然后用CH3CN和水稀释,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化,得到标题化合物的TFA盐。C27H29F2N6O3(M+H)+的LCMS计算值:m/z=523.2;实测值:523.2。
实施例29.N-(4-(氮杂环丁-1-基)-2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例28中所述的程序,使用氮杂环丁烷代替吗啉作为起始物质制备标题化合物的TFA盐。C26H27F2N6O2(M+H)+的LCMS计算值:m/z=493.2;实测值:493.2。
实施例30.N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟-4-(吗啉代甲基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
步骤1.(1S,4S)-5-(4-氟-2-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)-5-甲酰基苯基)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯
将戴斯-马丁过碘烷(Dess-Martin periodinane)(269mg,0.634mmol)添加到(1S,4S)-5-(4-氟-2-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)-5-(羟甲基)苯基)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯(实施例17,300mg,0.529mmol)和吡啶(51.0μl,0.63mmol)在二氯甲烷(5mL)中的溶液中。在室温下搅拌1h后,将溶剂真空蒸发,并通过BiotageIsoleraTM纯化粗产物。C29H30F2N5O5(M+H)+的LCMS计算值m/z=566.2;实测值:566.3。
步骤2.N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟-4-(吗啉代甲基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
将三乙酰氧基硼氢化钠(7.5mg,0.035mmol)添加到吗啉(1.5mg,0.018mmol)、乙酸(2μl,0.035mmol)和(1S,4S)-5-(4-氟-2-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)-5-甲酰基苯基)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯(10mg,0.018mmol)在二氯乙烷(1mL)中的溶液中。将反应混合物在室温下搅拌2h,然后用水处理。用乙酸乙酯萃取水相,并将合并的有机相用盐水洗涤,经硫酸钠干燥并浓缩。将粗残留物吸收在TFA(1mL)中,并在室温下搅拌反应30分钟。然后将反应混合物用乙腈稀释,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化,得到标题化合物的TFA盐。C28H31F2N6O3(M+H)+的LCMS计算值:m/z=537.2;实测值:537.3。
实施例31.N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-4-((环丁基氨基)甲基)-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例30中所述的程序,使用环丁胺代替吗啉作为起始物质制备标题化合物的TFA盐。C28H31F2N6O2(M+H)+的LCMS计算值:m/z=521.2;实测值:521.2。
实施例32.N-(2-((1R,4R)-5-乙基-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
将三乙酰氧基硼氢化钠(10mg,0.046mmol)添加到乙醛(1mg,0.023mmol)、乙酸(2μl,0.035mmol)和N-(2-((1R,4R)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺(来自实施例1;10mg,0.023mmol)在二氯乙烷(1mL)中的溶液中。将反应混合物在室温下搅拌2h后,将其用乙腈稀释,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化,得到标题化合物的TFA盐。C25H26F2N5O2(M+H)+的LCMS计算值:m/z=466.2;实测值:466.3。
实施例33.N-(5-氟-2-((1R,4R)-5-(2-羟乙基)-2,5-二氮杂双环[2.2.1]庚-2-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
将三乙酰氧基硼氢化钠(10mg,0.046mmol)添加到2-((叔丁基二甲基甲硅烷基)氧基)乙醛(3.98mg,0.023mmol)、乙酸(2μl,0.035mmol)和N-(2-((1R,4R)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺(来自实施例1;10mg,0.023mmol)在二氯乙烷(1mL)中的溶液中。将反应混合物在室温下搅拌2h后,将溶剂真空蒸发,并将在二噁烷中的4M HCl溶液(1mL)添加到残留物中。在室温下再搅拌1h后,将反应混合物用乙腈稀释,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化,得到标题化合物的TFA盐。C25H26F2N5O3(M+H)+的LCMS计算值:m/z=482.2;实测值:482.2。
实施例34.(1R,4R)-5-(4-氟-2-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)苯基)-N-丙基-2,5-二氮杂双环[2.2.1]庚烷-2-甲酰胺
将三光气(4.1mg,0.014mmol)添加到N-(2-((1R,4R)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺(来自实施例1,6mg,0.014mmol)和三乙胺(4μl,0.027mmol)在THF(1mL)中的溶液中。将反应混合物在室温下搅拌30分钟后,添加丙-1-胺(1.2mg,0.021mmol),并将混合物在室温下再搅拌30分钟。然后将反应混合物用乙腈稀释,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化,得到标题化合物的TFA盐。C27H29F2N6O3(M+H)+的LCMS计算值:m/z=523.2;实测值:523.3。
实施例35.N-(2-((1R,4R)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-甲氧基苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例1中所述的程序,使用1-氟-4-甲氧基-2-硝基苯代替1,4-二氟-2-硝基苯作为起始物质制备标题化合物的TFA盐。C24H25FN5O3(M+H)+的LCMS计算值:m/z=450.2;实测值:450.3。
实施例36.N-(2-((1R,4R)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-(羟甲基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例1中所述的程序,使用(4-氟-3-硝基苯基)甲醇代替1,4-二氟-2-硝基苯作为起始物质制备标题化合物的TFA盐。C24H25FN5O3(M+H)+的LCMS计算值:m/z=450.2;实测值:450.3。
实施例37.N-(2-((1R,4R)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氰基苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例1中所述的程序,使用4-氟-3-硝基苄腈代替1,4-二氟-2-硝基苯作为起始物质制备标题化合物的TFA盐。C24H22FN6O2(M+H)+的LCMS计算值:m/z=445.2;实测值:445.1。
实施例38.N-(4-(氮杂环丁-1-基)-2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例28和29中所述的程序,使用N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-4-溴苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺代替N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-4-溴-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺作为起始物质制备此化合物。C26H28FN6O2(M+H)+的LCMS计算值:m/z=475.2;实测值:475.2。1HNMR(500MHz,DMSO-d6)δ10.17–10.04(s,1H),9.27–9.16(d,J=5.0Hz,1H),8.15–8.04(d,J=5.1Hz,1H),7.83–7.71(d,J=8.3Hz,1H),7.59–7.48(td,J=8.4,6.6Hz,1H),7.10–7.02(d,J=8.5Hz,1H),7.02–6.96(t,J=8.8Hz,1H),6.07–5.95(m,2H),3.89–3.83(s,1H),3.81–3.72(m,7H),3.49–3.44(s,1H),3.38–3.25(m,1H),3.00–2.89(m,2H),2.71–2.63(d,J=9.7Hz,1H),2.34–2.23(q,J=7.1Hz,2H),1.64–1.57(d,J=9.1Hz,1H),1.52–1.38(d,J=9.0Hz,1H)ppm。
实施例39.N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-4-((S)-2-(甲氧基甲基)氮杂环丁-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例38中所述的程序,使用(S)-2-(甲氧基甲基)氮杂环丁烷代替氮杂环丁烷作为起始物质制备此化合物。C28H32FN6O3(M+H)+的LCMS计算值:m/z=519.2;实测值:519.3。1H NMR(500MHz,DMSO-d6)δ10.18–9.96(s,1H),9.28–9.11(d,J=5.0Hz,1H),8.15–8.01(d,J=5.0Hz,1H),7.79–7.67(d,J=8.5Hz,1H),7.60–7.37(td,J=8.4,6.8Hz,1H),7.10–7.02(d,J=8.4Hz,1H),7.02–6.91(m,1H),6.41–6.27(d,J=2.4Hz,1H),6.19–6.04(dd,J=8.7,2.4Hz,1H),4.14–4.05(dd,J=7.6,3.6Hz,1H),3.87–3.79(m,3H),3.79–3.74(s,3H),3.67–3.58(dd,J=10.3,6.7Hz,1H),3.58–3.46(m,3H),3.40–3.27(m,4H),3.04–2.90(m,2H),2.74–2.60(dd,J=9.7,2.2Hz,1H),2.32–2.21(m,1H),2.17–2.05(dq,J=10.8,8.3Hz,1H),1.68–1.57(d,J=9.1Hz,1H),1.56–1.47(m,1H)ppm。
实施例40.N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-4-(3-氰基吡啶-4-基)-3-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
步骤1.(1S,4S)-5-(3-溴-2-氟-6-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)苯基)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯
根据实施例18中所述的程序,使用1-溴-2,3-二氟-4-硝基苯代替1-溴-2,5-二氟-4-硝基苯作为起始物质制备此化合物。C28H29BrF2N5O4(M+H)+的LCMS计算值:m/z=616.1;实测值:616.1。
步骤2.N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-4-(3-氰基吡啶-4-基)-3-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
将(1S,4S)-5-(3-溴-2-氟-6-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)苯基)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯(10mg,0.016mmol)、4-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)烟腈(10mg,0.043mmol)、Xphos Pd G2(1.3mg,1.6μmol)和磷酸三钾(6.7mg,0.032mmol)的混合物与1,4-二噁烷(1ml)和水(0.1ml)合并。将反应混合物在真空下脱气,用氮气回填,然后在80℃下搅拌1h。将反应混合物冷却到室温,将溶剂浓缩并添加TFA(1mL)。将反应混合物在室温下搅拌10分钟,然后用CH3CN和水稀释,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化。C29H24F2N7O2(M+H)+的LCMS计算值:m/z=540.2;实测值:540.1。1H NMR(500MHz,DMSO-d6)δ10.94–10.84(s,1H),9.37–9.27(d,J=5.0Hz,1H),9.20–9.11(s,1H),9.07–8.99(br,1H),8.98–8.94(d,J=5.2Hz,1H),8.81–8.72(br,1H),8.44–8.37(d,J=8.6Hz,1H),8.27–8.16(d,J=5.0Hz,1H),7.79–7.75(d,J=5.2Hz,1H),7.62–7.56(td,J=8.5,6.9Hz,1H),7.56–7.51(t,J=8.1Hz,1H),7.12–7.06(d,J=8.5Hz,1H),7.05–6.97(m,1H),4.46–4.34(m,1H),4.15–4.08(s,1H),3.82–3.74(s,3H),3.62–3.54(d,J=10.7Hz,1H),3.49–3.41(m,1H),3.41–3.33(n,1H),3.17–3.07(m,1H),1.95–1.88(d,J=10.6Hz,1H),1.68–1.58(m,1H)ppm。
实施例41.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(3-氰基吡啶-4-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
步骤1.(3S,5S)-1-(5-溴-2-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)苯基)-5-(羟甲基)吡咯烷-3-基氨基甲酸叔丁酯
根据实施例22和1中所述的程序,使用(3S,5S)-5-(羟甲基)吡咯烷-3-基氨基甲酸叔丁酯代替(1S,4S)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯作为起始物质制备此化合物。C28H32BrFN5O5(M+H)+的LCMS计算值:m/z=616.2;实测值:616.2。
步骤2.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(3-氰基吡啶-4-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
将((3S,5S)-1-(5-溴-2-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)苯基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯(10mg,0.016mmol)、4-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)烟腈(9.8mg,0.043mmol)、Xphos Pd G2(1.3mg,1.6μmol)和磷酸三钾(6.7mg,0.032mmol)的混合物与1,4-二噁烷(1ml)和水(0.1ml)合并。将反应混合物在真空下脱气,用氮气回填,然后在80℃下搅拌1h。将反应混合物冷却到室温,将溶剂浓缩并添加TFA(1mL)。将反应混合物在室温下搅拌10分钟,然后用CH3CN和水稀释,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化。C29H27FN7O3(M+H)+的LCMS计算值:m/z=540.2;实测值:540.1。1H NMR(600MHz,DMSO-d6)δ10.69–10.61(s,1H),9.32–9.25(d,J=5.0Hz,1H),9.14–9.04(s,1H),8.94–8.86(d,J=5.3Hz,1H),8.35–8.28(d,J=8.4Hz,1H),8.22–8.13(d,J=5.0Hz,1H),7.97–7.85(d,J=5.5Hz,2H),7.81–7.75(d,J=5.4Hz,1H),7.73–7.68(d,J=2.1Hz,1H),7.60–7.53(td,J=8.4,6.8Hz,1H),7.53–7.47(dd,J=8.4,2.0Hz,1H),7.11–7.05(d,J=8.5Hz,1H),7.04–6.96(t,J=8.8Hz,1H),3.89–3.81(m,1H),3.79–3.76(s,3H),3.76–3.68(m,1H),3.44–3.29(m,3H),3.27–3.22(dd,J=11.1,2.6Hz,1H),2.43–2.33(m,1H),1.90–1.80(m,1H)ppm。
实施例42.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例41中所述的程序(且在下文详述),使用3-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)异烟腈代替4-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)烟腈作为起始物质制备此化合物(游离碱和TFA盐)。
步骤1.((3S,5S)-1-(5-溴-2-硝基苯基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯
用三乙胺(506μL,3.63mmol)处理4-溴-2-氟-1-硝基苯(532mg,2.42mmol)和((3S,5S)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯(523mg,2.42mmol)在DMSO(8mL)中的溶液,并将反应混合物加热到80℃保持2小时。冷却到室温后,添加水并过滤收集沉淀产物,用水洗涤并风干。其不经进一步纯化用于下一步。C12H15BrN3O5(M+H-C4H8)+的LCMS计算值:m/z=360.0/362.0;实测值:360.0/362.0。
步骤2.((3S,5S)-1-(2-氨基-5-溴苯基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯
将((3S,5S)-1-(5-溴-2-硝基苯基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯(1g,2.45mmol)、铁(684mg,12.25mmol)和氯化铵(786mg,14.70mmol)在THF(5mL)、水(5mL)和甲醇(5mL)中的混合物在60℃下搅拌3小时。冷却到室温后,将其通过硅藻土塞过滤,并用DCM稀释。将有机相分离,用饱和氯化钠水溶液洗涤,经硫酸钠干燥并真空蒸发溶剂。得到的粗产物不经进一步纯化用于下一步。C16H25BrN3O3(M+H)+的LCMS计算值:m/z=386.1/388.1;实测值:386.1/388.1。
步骤3.((3S,5S)-1-(5-溴-2-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)苯基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯
将HATU(1196mg,3.15mmol)添加到((3S,5S)-1-(2-氨基-5-溴苯基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯(810mg,2.097mmol)、2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酸(实施例1步骤1的产物,520mg,2.097mmol)和DIPEA(732μl,4.19mmol)在DMF(5mL)中的溶液中。将反应混合物在室温下搅拌30分钟,然后添加水并过滤收集沉淀产物,用水洗涤并风干。固体不经进一步纯化用于下一步。C28H32BrFN5O5(M+H)+的LCMS计算值:m/z=616.2/618.2;实测值:616.2/618.2。
步骤4.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
将((3S,5S)-1-(5-溴-2-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)苯基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯(10mg,0.016mmol)、3-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)异烟腈(9.8mg,0.043mmol)、Xphos Pd G2(1.3mg,1.6μmol)和磷酸三钾(6.7mg,0.032mmol)的混合物与1,4-二噁烷(1mL)和水(0.1mL)合并,并将反应烧瓶抽真空,用氮气回填,然后在80℃下搅拌1小时。将反应混合物冷却到室温,将溶剂真空蒸发并添加TFA(1mL)。将反应混合物在室温下搅拌10分钟,然后用CH3CN和水稀释,并用制备型LCMS纯化。C29H27FN7O3(M+H)+的LCMS计算值:m/z=540.2;实测值:540.1。制备型LCMS(XBridge C18柱,以含有0.1%NH4OH的乙腈/水的梯度洗脱,流速为60mL/分钟)。游离碱:1H NMR(500MHz,DMSO-d6)δ9.33–9.25(d,J=5.0Hz,1H),8.98–8.93(s,1H),8.84–8.78(d,J=5.0Hz,1H),8.46–8.39(d,J=8.4Hz,1H),8.22–8.18(d,J=5.0Hz,1H),8.00–7.92(dd,J=5.1,0.7Hz,1H),7.67–7.64(m,1H),7.59–7.52(td,J=8.4,6.8Hz,1H),7.48–7.43(dd,J=8.3,2.1Hz,1H),7.11–7.04(d,J=8.5Hz,1H),7.03–6.90(t,J=8.8Hz,1H),3.85–3.73(s,3H),3.68–3.56(m,1H),3.39–3.29(m,3H),3.28–3.22(d,J=4.8Hz,1H),3.06–2.97(d,J=5.4Hz,1H),2.31–2.18(dt,J=12.6,7.5Hz,1H),1.40–1.29(dt,J=12.7,6.2Hz,1H)ppm。制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)。TFA盐:1HNMR(500MHz,DMSO-d6)δ10.66–10.59(s,1H),9.31–9.24(d,J=5.0Hz,1H),9.03–8.94(d,J=0.8Hz,1H),8.88–8.78(d,J=5.0Hz,1H),8.34–8.24(d,J=8.4Hz,1H),8.24–8.17(d,J=5.0Hz,1H),8.04–7.95(dd,J=5.1,0.8Hz,1H),7.92–7.82(br,J=5.5Hz,2H),7.73–7.65(d,J=2.0Hz,1H),7.61–7.54(td,J=8.5,6.9Hz,1H),7.50–7.45(dd,J=8.4,2.0Hz,1H),7.11–7.05(d,J=8.5Hz,1H),7.05–6.98(t,J=8.8Hz,1H),3.89–3.82(m,1H),3.81–3.77(s,3H),3.76–3.69(m,1H),3.42–3.21(m,4H),2.43–2.31(m,1H),1.90–1.77(dt,J=13.2,5.3Hz,1H)ppm。
实施例43.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(2-甲基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例41中所述的程序,使用(2-甲基吡啶-3-基)硼酸代替4-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)烟腈作为起始物质制备此化合物。C29H30FN6O3(M+H)+的LCMS计算值:m/z=529.2;实测值:529.2。1H NMR(500MHz,DMSO-d6)δ10.69–10.55(s,1H),9.33–9.17(d,J=5.0Hz,1H),8.72–8.62(dd,J=5.4,1.7Hz,1H),8.31–8.20(d,J=8.3Hz,1H),8.23–8.15(d,J=5.0Hz,1H),8.14–8.05(d,J=7.6Hz,1H),8.05–7.86(br,J=5.4Hz,2H),7.75–7.64(dd,J=7.7,5.4Hz,1H),7.62–7.52(td,J=8.4,6.8Hz,1H),7.47–7.41(d,J=2.0Hz,1H),7.31–7.23(dd,J=8.3,1.9Hz,1H),7.11–7.05(d,J=8.5Hz,1H),7.05–6.95(t,J=8.8Hz,1H),3.87–3.76(m,4H),3.76–3.66(m,1H),3.42–3.20(m,4H),2.65–2.57(s,3H),2.43–2.32(dt,J=13.2,7.9Hz,1H),1.91–1.65(dt,J=13.3,5.5Hz,1H)ppm。
实施例44.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(3-甲氧基吡啶-4-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例41中所述的程序,使用(3-甲氧基吡啶-4-基)硼酸代替4-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)烟腈作为起始物质制备此化合物。C29H30FN6O4(M+H)+的LCMS计算值:m/z=545.2;实测值:545.3。1H NMR(500MHz,DMSO-d6)δ10.66–10.59(s,1H),9.30–9.25(d,J=5.0Hz,1H),8.55–8.48(s,1H),8.39–8.33(d,J=5.0Hz,1H),8.28–8.21(d,J=8.4Hz,1H),8.21–8.16(d,J=5.0Hz,1H),7.92–7.81(br,2H),7.63–7.59(m,1H),7.59–7.55(m,1H),7.55–7.51(m,1H),7.48–7.44(dd,J=8.4,1.9Hz,1H),7.14–7.11(s,1H),7.09–7.05(d,J=8.5Hz,1H),7.01–6.96(d,J=8.8Hz,1H),3.99–3.90(s,3H),3.83–3.73(m,4H),3.73–3.67(m,1H),3.40–3.19(m,4H),2.44–2.35(m,1H),1.88–1.79(dt,J=13.3,5.2Hz,1H)ppm。
实施例45.N-(3-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-2'-氰基-6'-氟联苯-4-基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例41中所述的程序,使用3-氟-2-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)苄腈代替4-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)烟腈作为起始物质制备此化合物。C30H27F2N6O3(M+H)+的LCMS计算值:m/z=557.2;实测值:557.1。
实施例46.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(3-氰基吡啶-2-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
步骤1.(3S,5S)-1-(2-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)苯基)-5-(羟甲基)吡咯烷-3-基氨基甲酸叔丁酯
将1,4-二噁烷(10ml)添加到4,4,5,5,4',4',5',5'-八甲基-[2,2']双[[1,3,2]二氧杂硼戊环基](412mg,1.6mmol)、乙酸钾(159mg,1.6mmol)、与二氯甲烷络合的[1,1'-双(二苯基膦基)二茂铁]二氯钯(II)(1:1)(66.2mg,0.081mmol)和((3S,5S)-1-(5-溴-2-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)苯基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯(500mg,0.811mmol)的混合物中。将反应混合物在真空下脱气,用氮气回填,并在100℃下搅拌过夜。然后将反应混合物冷却到室温,通过硅藻土塞过滤,并在真空下浓缩溶剂。通过Biotage Isolera纯化粗物质,得到黄色固体(300mg,56%)。C34H44BFN5O7(M+H)+的LCMS计算值:m/z=664.3;实测值:664.3。
步骤2.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(3-氰基吡啶-2-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
将((3S,5S)-1-(2-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)苯基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯(10mg,0.015mmol)、2-溴烟腈(5.52mg,0.030mmol)、Xphos Pd G2(1.3mg,1.6μmol)和磷酸三钾(6.7mg,0.032mmol)的混合物与1,4-二噁烷(1ml)和水(0.1ml)合并。将反应混合物在真空下脱气,用氮气回填,然后在80℃下搅拌1h。将反应混合物冷却到室温,将溶剂浓缩并添加TFA(1mL)。将反应混合物在室温下搅拌10分钟,然后用CH3CN和水稀释,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化。C29H27FN7O3(M+H)+的LCMS计算值:m/z=540.2;实测值:540.1。1H NMR(500MHz,DMSO-d6)δ10.71–10.58(s,1H),9.35–9.21(d,J=5.0Hz,1H),8.97–8.91(dd,J=4.8,1.7Hz,1H),8.49–8.40(dd,J=7.9,1.7Hz,1H),8.39–8.30(d,J=8.4Hz,1H),8.26–8.16(d,J=5.0Hz,1H),7.96–7.82(m,3H),7.75–7.70(dd,J=8.4,2.0Hz,1H),7.66–7.60(dd,J=7.9,4.9Hz,1H),7.60–7.52(td,J=8.4,6.8Hz,1H),7.11–7.05(d,J=8.5Hz,1H),7.04–6.97(t,J=8.8Hz,1H),3.87–3.76(m,4H),3.75–3.69(m,1H),3.46–3.15(m,4H),2.44–2.33(m,1H),1.91–1.76(m,1H)ppm。
实施例47.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基-1-甲基-1H-吡唑-5-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例46中所述的程序,使用5-溴-1-甲基-1H-吡唑-4-甲腈代替2-溴烟腈作为起始物质制备此化合物。C28H28FN8O3(M+H)+的LCMS计算值:m/z=543.2;实测值:543.2。
实施例48.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-异丙基苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
步骤1.(3S,5S)-1-(2-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)-5-(丙-1-烯-2-基)苯基)-5-(羟甲基)吡咯烷-3-基氨基甲酸叔丁酯
根据实施例41中所述的程序,使用4,4,5,5-四甲基-2-(丙-1-烯-2-基)-1,3,2-二氧杂硼戊环代替4-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)烟腈作为起始物质制备此化合物。C31H37FN5O5(M+H)+的LCMS计算值:m/z=578.3;实测值:578.3。
步骤2.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-异丙基苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
将钯/碳(10w%,18.42mg,0.017mmol)添加到((3S,5S)-1-(2-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)-5-(丙-1-烯-2-基)苯基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯(100mg,0.173mmol)在甲醇(6ml)中的溶液中。将反应混合物在室温和氢气氛下搅拌5h。将催化剂滤出,将溶剂浓缩并添加TFA(1mL)。将反应混合物在室温下搅拌10分钟,然后用CH3CN和水稀释,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化。C26H31FN5O3(M+H)+的LCMS计算值:m/z=480.2;实测值:480.2。1HNMR(500MHz,DMSO-d6)δ10.50–10.37(s,1H),9.33–9.20(d,J=5.0Hz,1H),8.18–8.07(d,J=5.0Hz,1H),8.07–8.02(d,J=8.3Hz,1H),7.88–7.73(br,J=5.7Hz,2H),7.61–7.47(td,J=8.4,6.8Hz,1H),7.27–7.18(s,1H),7.14–7.03(dd,J=8.4,1.9Hz,2H),7.03–6.94(t,J=8.8Hz,1H),3.81–3.73(s,3H),3.75–3.66(m,1H),3.33–3.12(m,4H),2.95–2.81(p,J=6.9Hz,1H),2.45–2.33(m,1H),1.87–1.67(dt,J=13.2,5.0Hz,1H),1.24–1.17(d,J=6.9Hz,6H)ppm。
实施例49.N-(4-(3-氰基吡啶-4-基)-2-((2S,4S)-4-羟基-2-(羟甲基)吡咯烷-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例41所述的程序,使用(3S,5S)-5-(羟甲基)吡咯烷-3-醇代替(3S,5S)-5-(羟甲基)吡咯烷-3-基氨基甲酸叔丁酯作为起始物质制备此化合物。C29H26FN6O4(M+H)+的LCMS计算值:m/z=541.2;实测值:541.2。
中间体1. 3-(3-氟-4-硝基苯基)异烟腈
将3-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)异烟腈(1g,4.34mmol)、4-溴-2-氟-1-硝基苯(637mg,2.90mmol)、XPhos Pd G2(228mg,0.29mmol)和磷酸三钾(1.23g,5.79mmol)的混合物与二噁烷(88mL)和水(8.8mL)合并。将反应混合物在真空下脱气,用氮气回填,然后在80℃下搅拌16h。冷却到室温后,将混合物通过硅藻土过滤,并用乙酸乙酯洗涤,接着在真空下浓缩。然后通过Biotage Isolera纯化残留物,得到3-(3-氟-4-硝基苯基)异烟腈,为褐色固体(550mg,78%收率)。C12H7FN3O2(M+H)+的LCMS计算值:m/z=244.0;实测值244.0。
实施例50.N-(4-(4-氰基吡啶-3-基)-2-((2S,5R)-2-(羟甲基)-5-甲基哌嗪-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
步骤1.(2R,5S)-4-(5-(4-氰基吡啶-3-基)-2-硝基苯基)-5-(羟甲基)-2-甲基哌嗪-1-甲酸叔丁酯
用三乙胺(45.4μL,0.33mmol)处理3-(3-氟-4-硝基苯基)异烟腈(中间体1,52.8mg,0.22mmol)和(2R,5S)-5-(羟甲基)-2-甲基哌嗪-1-甲酸叔丁酯(50mg,0.22mmol;通过改动Chessari,G.等人,J.Med.Chem.2015,58,6574-6588中所述的程序制备)在DMSO(724μL)中的溶液,并将反应混合物加热到100℃保持16h。冷却到室温后,将反应混合物用CH2Cl2稀释,用盐水洗涤,经MgSO4干燥,过滤并在真空下浓缩。将粗产物不经纯化用于下一反应。C23H28N5O5(M+H)+的LCMS计算值:m/z=454.2;实测值454.2。
步骤2.(2R,5S)-4-(2-氨基-5-(4-氰基吡啶-3-基)苯基)-5-(羟甲基)-2-甲基哌嗪-1-甲酸叔丁酯
将(2R,5S)-4-(5-(4-氰基吡啶-3-基)-2-硝基苯基)-5-(羟甲基)-2-甲基哌嗪-1-甲酸叔丁酯(98mg,0.22mmol)、铁(60mg,1.08mmol)和氯化铵(69mg,1.30mmol)在THF(2mL)、水(2mL)和甲醇(2mL)中的混合物在60℃下搅拌1h。冷却到室温后,将反应混合物通过硅藻土塞过滤,并用CH2Cl2稀释。将有机相分离,用盐水洗涤,经MgSO4干燥,过滤并在真空下浓缩。粗产物不经进一步纯化用于下一步。C23H30N5O3(M+H)+的LCMS计算值:m/z=424.2;实测值:424.2。
步骤3.N-(4-(4-氰基吡啶-3-基)-2-((2S,5R)-2-(羟甲基)-5-甲基哌嗪-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
将HATU(124mg,0.326mmol)添加到(2R,5S)-4-(2-氨基-5-(4-氰基吡啶-3-基)苯基)-5-(羟甲基)-2-甲基哌嗪-1-甲酸叔丁酯(92mg,0.22mmol)、2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酸(54mg,0.22mmol)和DIPEA(76μL,0.43mmol)在DMF(510μL)中的溶液中。将反应混合物在60℃下搅拌30分钟,然后用水处理。过滤收集沉淀产物,用水洗涤并风干。然后将其重新溶解在TFA中,并将溶液在60℃下搅拌10分钟。冷却后,在真空下浓缩溶剂,并将粗残留物溶解在THF(1mL)、MeOH(1mL)和NH4OH水溶液(1mL)中。在密封容器中将反应混合物在60℃下搅拌30分钟。将混合物冷却,在真空下浓缩溶剂,并将所得到的残留物用乙腈稀释,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化。C30H29FN7O3(M+H)+:m/z=554.2;实测值554.3。
实施例51.N-(4-(4-氰基吡啶-3-基)-2-((2S,5S)-2-(羟甲基)-5-甲基哌嗪-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例50中所述的程序,使用(2S,5S)-5-(羟甲基)-2-甲基哌嗪-1-甲酸叔丁酯代替(2R,5S)-5-(羟甲基)-2-甲基哌嗪-1-甲酸叔丁酯作为起始物质制备此化合物。C30H29FN7O3(M+H)+的LCMS计算值:m/z=554.2;实测值:554.1。
实施例52.(S)-N-(4-(4-氰基吡啶-3-基)-2-(6-(羟甲基)-4,7-二氮杂螺[2.5]辛-7-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例50中所述的程序,使用(S)-6-(羟甲基)-4,7-二氮杂螺[2.5]辛烷-4-甲酸叔丁酯代替(2R,5S)-5-(羟甲基)-2-甲基哌嗪-1-甲酸叔丁酯作为起始物质制备此化合物。C31H29FN7O3(M+H)+的LCMS计算值:m/z=566.2;实测值:566.2。
实施例53.N-(2-((2S,4S)-4-氨基-2-(1-羟基环丙基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
步骤1.(2S,4S)-4-(叔丁氧羰基氨基)吡咯烷-1,2-二甲酸1-苄酯2-甲酯
在0℃下用氯甲酸苄酯(175μL,1.23mmol)处理(2S,4S)-4-(叔丁氧羰基氨基)吡咯烷-2-甲酸甲酯(250mg,1.02mmol)和DIPEA(536μL,3.07mmol)在CH2Cl2(6.4mL)中的溶液,并将反应混合物搁置搅拌1h。将反应混合物用饱和NaHCO3水溶液处理,并用CH2Cl2稀释,用盐水洗涤,经MgSO4干燥,过滤并浓缩。粗产物不经纯化用于下一反应。C19H27N2O6(M+H)+的LCMS计算值:m/z=379.2;实测值:379.1。
步骤2.(2S,4S)-4-(叔丁氧羰基氨基)-2-(1-羟基环丙基)吡咯烷-1-甲酸苄酯
在0℃下用乙基溴化镁(在THF中1M,1.06mL,1.06mmol)处理(2S,4S)-4-(叔丁氧羰基氨基)吡咯烷-1,2-二甲酸1-苄酯2-甲酯(100mg,0.26mmol)和异丙醇钛(16μL,0.053mmol)在THF(755μL)中的溶液,并将反应混合物在室温下搅拌1h。然后将反应混合物用饱和NH4Cl水溶液处理,并用EtOAc稀释。将分离的有机相用盐水洗涤,经MgSO4干燥,过滤并浓缩。粗产物不经纯化用于下一反应。C20H29N2O5(M+H)+的LCMS计算值:m/z=377.2;实测值:377.1。
步骤3.(3S,5S)-5-(1-羟基环丙基)吡咯烷-3-基氨基甲酸叔丁酯
向帕尔反应容器(Parr reaction vessel)中装入(2S,4S)-4-(叔丁氧羰基氨基)-2-(1-羟基环丙基)吡咯烷-1-甲酸苄酯(99mg,0.26mmol)、Pd/C(10%润湿,Degussa型,28mg),接着是MeOH(10.5mL)。将反应混合物抽真空,并用氮气回填3x,接着进行另一抽真空循环,然后用氢气加压至25psi。将反应容器搅动过夜。然后将反应混合物经硅藻土过滤,并在真空下浓缩溶剂。粗产物不经纯化用于下一反应。C12H23N2O3(M+H)+的LCMS计算值:m/z=243.2;实测值243.3。
步骤4.(3S,5S)-1-(5-(4-氰基吡啶-3-基)-2-硝基苯基)-5-(1-羟基环丙基)吡咯烷-3-基氨基甲酸叔丁酯
用三乙胺(55μL,0.40mmol)处理3-(3-氟-4-硝基苯基)异烟腈(中间体1,64mg,0.26mmol)和(3S,5S)-5-(1-羟基环丙基)吡咯烷-3-基氨基甲酸叔丁酯(64mg,0.26mmol)在DMSO(880μL)中的溶液,并将反应混合物加热到100℃保持16h。冷却到室温后,将反应混合物用CH2Cl2稀释,用盐水洗涤,经MgSO4干燥,过滤并在真空下浓缩溶剂。粗产物不经纯化用于下一反应。C24H28N5O5(M+H)+的LCMS计算值:m/z=466.2;实测值466.3。
步骤5.(3S,5S)-1-(2-氨基-5-(4-氰基吡啶-3-基)苯基)-5-(1-羟基环丙基)吡咯烷-3-基氨基甲酸叔丁酯
将(3S,5S)-5-(1-羟基环丙基)吡咯烷-3-基氨基甲酸叔丁酯(123mg,0.26mmol)、铁(74mg,1.32mmol)和氯化铵(85mg,1.58mmol)在THF(2mL)、水(2mL)和甲醇(2mL)中的混合物在60℃下搅拌1h。冷却到室温后,将混合物通过硅藻土塞过滤,并用CH2Cl2稀释。将有机相分离,用盐水洗涤,经MgSO4干燥,过滤并在真空下浓缩溶剂。粗产物不经进一步纯化用于下一步。C24H30N5O3(M+H)+的LCMS计算值:m/z=436.1;实测值:436.2。
步骤6.N-(2-((2S,4S)-4-氨基-2-(1-羟基环丙基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
将HATU(151mg,0.40mmol)添加到(3S,5S)-1-(2-氨基-5-(4-氰基吡啶-3-基)苯基)-5-(1-羟基环丙基)吡咯烷-3-基氨基甲酸叔丁酯(115mg,0.26mmol)、2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酸(65mg,0.26mmol)和DIPEA(92μL,0.53mmol)在DMF(620μL)中的溶液中。将反应混合物在60℃下搅拌30分钟,然后用水处理。过滤收集沉淀产物,用水洗涤并风干。将其重新溶解在TFA中,并将溶液在60℃下搅拌10分钟。冷却后,将溶剂浓缩,然后用CH3CN稀释粗产物,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化。C31H29FN7O3(M+H)+的LCMS计算值:m/z=566.2;实测值:566.3。
实施例54.N-(2-((2S,4S)-4-氨基-2-(2-羟基丙-2-基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
步骤1.(3S,5S)-5-(2-羟基丙-2-基)吡咯烷-3-基氨基甲酸叔丁酯
在0℃下用甲基溴化镁(在THF中3M,546μL,1.64mmol)处理(2S,4S)-4-(叔丁氧羰基氨基)吡咯烷-2-甲酸甲酯(100mg,0.41mmol)在THF(4.1mL)中溶液,并将反应混合物在室温下搅拌1h。将反应混合物用饱和NH4Cl水溶液处理,并用EtOAc稀释。将分离的有机相用盐水洗涤,经MgSO4干燥,过滤并在真空下浓缩。粗产物不经纯化用于下一反应。C12H25N2O3(M+H)+的LCMS计算值:m/z=245.2;实测值:245.2。
步骤2.(3S,5S)-1-(5-(4-氰基吡啶-3-基)-2-硝基苯基)-5-(2-羟基丙-2-基)吡咯烷-3-基氨基甲酸叔丁酯
用三乙胺(43μL,0.31mmol)处理3-(3-氟-4-硝基苯基)异烟腈(中间体1,50mg,0.20mmol)和(3S,5S)-5-(2-羟基丙-2-基)吡咯烷-3-基氨基甲酸叔丁酯(50mg,0.20mmol)在DMSO(680μL)中的溶液,并将反应混合物加热到100℃保持16h。冷却到室温后,将反应混合物用CH2Cl2稀释,用盐水洗涤,经MgSO4干燥,过滤并在真空下浓缩。粗产物不经纯化用于下一反应。C24H30N5O5(M+H)+的LCMS计算值:m/z=468.2;实测值:468.1。
步骤3.(3S,5S)-1-(2-氨基-5-(4-氰基吡啶-3-基)苯基)-5-(2-羟基丙-2-基)吡咯烷-3-基氨基甲酸叔丁酯
将(3S,5S)-1-(5-(4-氰基吡啶-3-基)-2-硝基苯基)-5-(2-羟基丙-2-基)吡咯烷-3-基氨基甲酸叔丁酯(96mg,0.20mmol)、铁(57mg,1.03mmol)和氯化铵(66mg,1.23mmol)在THF(2mL)、水(2mL)和甲醇(2mL)中的混合物在60℃下搅拌1h。冷却到室温后,将混合物通过硅藻土塞过滤,并用CH2Cl2稀释。将有机相分离,用盐水洗涤,经MgSO4干燥,过滤并将溶剂在真空下浓缩。粗产物不经进一步纯化用于下一步。C24H32N5O3(M+H)+的LCMS计算值:m/z=438.2;实测值:438.1。
步骤4.N-(2-((2S,4S)-4-氨基-2-(2-羟基丙-2-基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
将HATU(117mg,0.31mmol)添加到(3S,5S)-1-(2-氨基-5-(4-氰基吡啶-3-基)苯基)-5-(2-羟基丙-2-基)吡咯烷-3-基氨基甲酸叔丁酯(90mg,0.21mmol)、2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酸(51mg,0.21mmol)和DIPEA(72μL,0.41mmol)在DMF(480μL)中的溶液中。将反应混合物在60℃下搅拌30分钟,然后用水处理。过滤收集沉淀产物,用水洗涤并风干。将固体溶解在TFA中,并将所得到的溶液在60℃下搅拌10分钟。将溶液冷却,浓缩,用CH3CN稀释粗产物,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化。C31H31FN7O3(M+H)+的LCMS计算值:m/z=568.2;实测值:568.3
实施例55.N-(2-((2S,4S)-4-氨基-2-(羟甲基-d2)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
步骤1.(3S,5S)-5-(羟甲基-d2)吡咯烷-3-基氨基甲酸叔丁酯
在0℃下用氘化锂铝(17mg,0.41mmol)处理(2S,4S)-4-(叔丁氧羰基氨基)吡咯烷-2-甲酸甲酯(100mg,0.41mmol)在THF(4.1mL)中的溶液,并将反应混合物搅拌1h,然后升温至室温,并再搅拌30分钟。将反应混合物用Et2O、水和15%的LiOH水溶液稀释。将分离的有机相经MgSO4干燥,过滤并在真空下浓缩溶剂。粗产物不经纯化用于下一反应。C10H19D2N2O3(M+H)+的LCMS计算值:m/z=219.2;实测值219.1。
步骤2.(3S,5S)-1-(5-(4-氰基吡啶-3-基)-2-硝基苯基)-5-(羟甲基-d2)吡咯烷-3-基氨基甲酸叔丁酯
用三乙胺(85μL,0.61mmol)处理3-(3-氟-4-硝基苯基)异烟腈(中间体1,99mg,0.41mmol)和(3S,5S)-5-(羟甲基-d2)吡咯烷-3-基氨基甲酸叔丁酯(89mg,0.41mmol)在DMSO(1.36mL)中的溶液,并将反应混合物加热到100℃保持16小时。冷却到室温后,将反应混合物用CH2Cl2稀释,用盐水洗涤,经MgSO4干燥,过滤并将溶剂浓缩。粗产物不经纯化用于下一反应。C22H24D2N5O5(M+H)+的LCMS计算值:m/z=442.2;实测值:442.1。
步骤3.(3S,5S)-1-(2-氨基-5-(4-氰基吡啶-3-基)苯基)-5-(羟基双氘甲基)吡咯烷-3-基氨基甲酸叔丁酯
将(3S,5S)-1-(5-(4-氰基吡啶-3-基)-2-硝基苯基)-5-(羟甲基-d2)吡咯烷-3-基氨基甲酸叔丁酯(180mg,2.04mmol)、铁(114mg,1.03mmol)和氯化铵(131mg,2.45mmol)在THF(2mL)、水(2mL)和甲醇(2mL)中的混合物在60℃下搅拌1h。冷却到室温后,将混合物通过硅藻土塞过滤,并用CH2Cl2稀释。将有机相分离,用盐水洗涤,经MgSO4干燥,过滤并浓缩溶剂。粗产物不经进一步纯化用于下一步。C22H26D2N5O3(M+H)+的LCMS计算值:m/z=412.2;实测值:412.2。
步骤4.N-(2-((2S,4S)-4-氨基-2-(羟甲基-d2)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
将HATU(233mg,0.61mmol)添加到(3S,5S)-1-(2-氨基-5-(4-氰基吡啶-3-基)苯基)-5-(羟甲基-d2)吡咯烷-3-基氨基甲酸叔丁酯(168mg,0.41mmol)、2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酸(101mg,0.41mmol)和DIPEA(143μL,0.82mmol)在DMF(956μL)中的溶液中。将反应混合物在60℃下搅拌30分钟,然后用水处理。过滤收集沉淀产物,用水洗涤并风干。然后将固体溶解在TFA中,并将溶液在60℃下搅拌10分钟。冷却后将溶液浓缩,并将粗残留物溶解在THF(1mL)、MeOH(1mL)和NH4OH水溶液(1mL)中。在密封容器中将混合物在60℃下搅拌30分钟。将混合物冷却,在真空下浓缩,将粗产物用CH3CN稀释,并用制备型LCMS(XBridgeC18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化。C29H25D2FN7O3(M+H)+的LCMS计算值:m/z=542.2;实测值:542.4。1H NMR(500MHz,DMSO-d6)δ10.64(s,1H),9.28(d,J=5.0Hz,1H),8.97(s,1H),8.82(d,J=5.0Hz,1H),8.29(d,J=8.4Hz,1H),8.18(d,J=5.0Hz,1H),7.99(d,J=5.0Hz,1H),7.96–7.84(m,3H),7.67(s,1H),7.56(td,J=8.4,6.8Hz,1H),7.47(dd,J=8.4,2.0Hz,1H),7.06(d,J=8.5Hz,1H),7.00(t,J=8.8Hz,1H),4.96(s,1H),3.83(dd,J=8.6,5.3Hz,1H),3.78(s,3H),3.74–3.65(m,1H),3.38–3.35(m,1H),3.32–3.29(m,1H),2.38(dt,J=13.2,7.8Hz,1H),1.84(dt,J=13.3,5.4Hz,1H)ppm。
实施例56.N-(4-(4-氰基吡啶-3-基)-2-((1S,3R,4S)-3-(羟甲基)-2,5-二氮杂双环[2.2.1]庚-2-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例50中所述的程序,使用(1S,4S,6R)-6-(羟甲基)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯(通过改动Balog,A.等人,Bioorg.Med.Chem.Lett.2004,14,6107-6111中所述的程序制备)代替(2R,5S)-5-(羟甲基)-2-甲基哌嗪-1-甲酸叔丁酯作为起始物质制备此化合物。C30H27FN7O3(M+H)+的LCMS计算值:m/z=552.2;实测值:552.2。
实施例57.N-(4-(4-氰基吡啶-3-基)-2-((1S,4S)-1-(羟甲基)-2,5-二氮杂双环[2.2.1]庚-2-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例50中所述的程序,使用(1S,4S)-4-(羟甲基)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯(通过改动Ivon,Y.等人,Synthesis 2015,47,1123-1130中所述的程序制备)代替(2R,5S)-5-(羟甲基)-2-甲基哌嗪-1-甲酸叔丁酯作为起始物质制备此化合物。C30H27FN7O3(M+H)+的LCMS计算值:m/z=552.2;实测值:552.3。
实施例58.N-(2-((2S,4S)-4-氨基-2-甲基哌啶-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
步骤1. 2-((2S,4S)-2-甲基哌啶-4-基)异吲哚啉-1,3-二酮
用DIAD(83μL,0.43mmol)处理(2S,4R)-4-羟基-2-甲基哌啶-1-甲酸叔丁酯(75mg,0.35mmol)、邻苯二甲酰亚胺(62mg,0.43mmoL)和三苯基膦(111mg,0.43mmol)在THF(1.7mL)中的溶液,并将混合物在室温下搅拌1h。将反应混合物用MeOH和EtOAc稀释,用盐水洗涤,经MgSO4干燥,过滤并将溶剂浓缩。然后用HCl(在二噁烷中4M,1mL)处理粗产物,并在室温下搅拌1h。在真空下浓缩溶剂,并且粗产物不经纯化用于下一反应。C14H17N2O2(M+H)+的LCMS计算值:m/z=245.1;实测值:245.1。
步骤2. 3-(3-((2S,4S)-4-(1,3-二氧代异吲哚啉-2-基)-2-甲基哌啶-1-基)-4-硝基苯基)异烟腈
用三乙胺(73μL,0.52mmol)处理3-(3-氟-4-硝基苯基)异烟腈(中间体1,85mg,0.35mmol)和2-((2S,4S)-2-甲基哌啶-4-基)异吲哚啉-1,3-二酮(85mg,0.35mmol)在DMSO(1.2mL)中的溶液,并将反应混合物加热到100℃保持16h。冷却到室温后,将反应混合物用CH2Cl2稀释,用盐水洗涤,经MgSO4干燥,过滤并在真空下浓缩溶剂。粗产物不经纯化用于下一反应。C26H22N5O4(M+H)+的LCMS计算值:m/z=468.2;实测值:468.1。
步骤3. 3-(4-氨基-3-((2S,4S)-4-(1,3-二氧代异吲哚啉-2-基)-2-甲基哌啶-1-基)苯基)异烟腈
将3-(3-((2S,4S)-4-(1,3-二氧代异吲哚啉-2-基)-2-甲基哌啶-1-基)-4-硝基苯基)异烟腈(163mg,0.35mmol)、铁(97mg,1.70mmol)和氯化铵(112mg,2.10mmol)在THF(2mL)、水(2mL)和甲醇(2mL)中的混合物在60℃下搅拌1h。冷却到室温后,将混合物通过硅藻土塞过滤,并用CH2Cl2稀释。将有机相分离,用盐水洗涤,经MgSO4干燥,过滤并将溶剂浓缩。粗产物不经进一步纯化用于下一步。C26H24N5O2(M+H)+的LCMS计算值:m/z=438.2;实测值:438.1。
步骤4.N-(2-((2S,4S)-4-氨基-2-甲基哌啶-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
将HATU(99mg,0.26mmol)添加到3-(4-氨基-3-((2S,4S)-4-(1,3-二氧代异吲哚啉-2-基)-2-甲基哌啶-1-基)苯基)异烟腈(76mg,0.17mmol)、2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酸(43mg,0.17mmol)和DIPEA(61μL,0.35mmol)在DMF(400μL)中的溶液中。将反应混合物在60℃下搅拌30分钟,然后用水处理。过滤收集沉淀产物,用水洗涤并风干。然后将固体溶解在EtOH(2mL)中,并用水合肼(50-60%水溶液,1mL)处理。将溶液在60℃下搅拌16h,冷却并浓缩。然后将残留物用乙腈稀释,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化。C30H29FN7O2(M+H)+的LCMS计算值:m/z=538.2;实测值:538.4。
实施例59.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-6-(2-氟-6-甲氧基苯基)吡啶酰胺
步骤1.(3S,5S)-1-(2-氨基-5-(4-氰基吡啶-3-基)苯基)-5-(羟甲基)吡咯烷-3-基氨基甲酸叔丁酯
根据实施例50步骤2中所述的程序,使用(3S,5S)-5-(羟甲基)吡咯烷-3-基氨基甲酸叔丁酯代替(2R,5S)-5-(羟甲基)-2-甲基哌嗪-1-甲酸叔丁酯作为起始物质制备此化合物。C22H28N5O3(M+H)+的LCMS计算值:m/z=410.2;实测值:410.1。
步骤2.(3S,5S)-1-(2-(6-氯吡啶酰胺基)-5-(4-氰基吡啶-3-基)苯基)-5-(羟甲基)吡咯烷-3-基氨基甲酸叔丁酯
将HATU(320mg,0.843mmol)添加到((3S,5S)-1-(2-氨基-5-(4-氰基吡啶-3-基)苯基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯(230mg,0.562mmol)、6-氯吡啶甲酸(88mg,0.562mmol)和DIPEA(0.196ml,1.123mmol)在DMF(1ml)中的溶液中。在室温下搅拌30分钟,添加水(3mL)。过滤收集所需产物,用水洗涤并干燥过夜。C28H30ClN6O4(M+H)+的LCMS计算值:m/z=549.2;实测值:549.2。
步骤3.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-6-(2-氟-6-甲氧基苯基)吡啶酰胺
将(3S,5S)-1-(2-(6-氯吡啶酰胺基)-5-(4-氰基吡啶-3-基)苯基)-5-(羟甲基)吡咯烷-3-基氨基甲酸叔丁酯(20mg,0.036mmol)、(2-氟-6-甲氧基苯基)硼酸(6.20mg,0.036mmol)、磷酸三钾(15.49mg,0.073mmol)、XPhos Pd G2(3.03mg,3.65μmol)在对二噁烷(1mL)和水(0.2mL)中的混合物在70℃下搅拌2h。将混合物在真空下浓缩,并溶解在DCM(1mL)和TFA(1mL)中。将所得混合物在室温下搅拌15分钟。在真空下浓缩溶剂,将残留物用乙腈稀释,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化。C30H28FN6O3(M+H)+的LCMS计算值:m/z=539.2;实测值:539.1。
实施例60.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-5-氰基-6-(2-氟-6-甲氧基苯基)吡啶酰胺
根据实施例59中所述的程序,使用6-氯-5-氰基吡啶甲酸代替6-氯吡啶甲酸作为起始物质制备此化合物。C31H27FN7O3(M+H)+的LCMS计算值:m/z=564.2;实测值:564.2。
实施例61.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-6-(2-氟-6-甲氧基苯基)-5-甲氧基吡啶酰胺
根据实施例59中所述的程序,使用6-氯-5-甲氧基吡啶甲酸代替6-氯吡啶甲酸作为起始物质制备此化合物。C31H30FN6O4(M+H)+的LCMS计算值:m/z=569.2;实测值:569.2。
实施例62.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2,6-二氟苯基)嘧啶-4-甲酰胺
步骤1.(3S,5S)-1-(2-(2-氯嘧啶-4-甲酰胺基)-5-(4-氰基吡啶-3-基)苯基)-5-(羟甲基)吡咯烷-3-基氨基甲酸叔丁酯
根据实施例59步骤2中所述的程序,使用2-氯嘧啶-4-甲酸代替6-氯吡啶甲酸作为起始物质制备此化合物。C27H29ClN7O4(M+H)+的LCMS计算值:m/z=550.2;实测值:550.1。
步骤2.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2,6-二氟苯基)嘧啶-4-甲酰胺
将(3S,5S)-1-(2-(2-氯嘧啶-4-甲酰胺基)-5-(4-氰基吡啶-3-基)苯基)-5-(羟甲基)吡咯烷-3-基氨基甲酸叔丁酯(20mg,0.036mmol)、(2,6-二氟苯基)硼酸(5.75mg,0.036mmol)、磷酸三钾(15.46mg,0.073mmol)、XPhos Pd G2(3.02mg,3.64μmol)在对二噁烷(1mL)和水(0.2mL)中的混合物在70℃下搅拌2h。将混合物在真空下浓缩,并溶解在DCM(1mL)和TFA(1mL)中。将所得混合物在室温下搅拌15分钟,然后将溶剂浓缩。将残留物用乙腈稀释,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化。C28H24F2N7O2(M+H)+的LCMS计算值:m/z=528.2;实测值:528.4。
实施例63.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲基苯基)嘧啶-4-甲酰胺
根据实施例62中所述的程序,使用(2-氟-6-甲基苯基)硼酸代替(2,6-二氟苯基)硼酸作为起始物质制备此化合物。C29H27FN7O2(M+H)+的LCMS计算值:m/z=524.2;实测值:524.1。
实施例64.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氯-6-氟苯基)嘧啶-4-甲酰胺
根据实施例62中所述的程序,使用(2-氯-6-氟苯基)硼酸代替(2,6-二氟苯基)硼酸作为起始物质制备此化合物。C28H24ClFN7O2(M+H)+的LCMS计算值:m/z=544.2;实测值:544.2。
实施例65.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-6-(1,3,5-三甲基-1H-吡唑-4-基)吡啶-3-基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
步骤1.(3S,5S)-1-(6-溴-3-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)吡啶-2-基)-5-(羟甲基)吡咯烷-3-基氨基甲酸叔丁酯
根据实施例41和1中所述的程序,使用6-溴-2-氯-3-硝基吡啶代替4-溴-2-氟-1-硝基苯作为起始物质制备此化合物。C27H31BrFN6O5(M+H)+的LCMS计算值:m/z=617.2;实测值:617.2。
步骤2.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-6-(1,3,5-三甲基-1H-吡唑-4-基)吡啶-3-基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
将((3S,5S)-1-(6-溴-3-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)吡啶-2-基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯(35mg,0.057mmol)、1,3,5-三甲基-4-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)-1H-吡唑(0.020g,0.085mmol)、Xphos Pd G2(13mg,16μmol)和磷酸三钾(67mg,0.32mmol)的混合物与1,4-二噁烷(1ml)和水(0.1ml)合并。将反应烧瓶抽真空,用氮气回填,然后在80℃下搅拌1h。将反应混合物冷却到室温,在真空下浓缩溶剂并添加TFA(1mL)。将反应混合物在室温下搅拌10分钟,然后用CH3CN和水稀释,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化。C28H32FN8O3(M+H)+的LCMS计算值:m/z=547.3;实测值:547.3。
实施例66.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-5-氟苯基)-2-(2,6-二氟苯基)嘧啶-4-甲酰胺
步骤1.((3S,5S)-1-(2-氨基-4-氟苯基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯
用Hunig碱(274μl,1.57mmol)处理1,4-二氟-2-硝基苯(250mg,1.57mmol)和((3S,5S)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯(340mg,1.57mmol)在DMSO(5ml)中的溶液,并将反应混合物加热到90℃保持1小时。用水处理反应混合物,并用乙酸乙酯萃取产物。将有机相用水和饱和氯化钠水溶液洗涤,经硫酸钠干燥并浓缩。将粗产物溶解在THF/水/MeOH的1:1:1混合物(9mL)中,并用铁(351mg,6.29mmol)和氯化铵(504mg,9.43mmol)处理。将反应混合物加热到60℃保持1小时,然后用乙酸乙酯稀释,并通过硅藻土塞过滤。将滤液用水和饱和氯化钠水溶液洗涤,经硫酸钠干燥并浓缩。通过Biotage IsoleraTM(在己烷中30-100%乙酸乙酯)纯化粗产物,得到所需产物,为黄色固体(226mg,46%)。C16H25FN3O3(M+H)+的LCMS计算值:m/z=326.2;实测值:326.2。
步骤2.((3S,5S)-1-(2-(2-氯嘧啶-4-甲酰胺基)-4-氟苯基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯
用Hunig碱(192μl,1.100mmol)处理2-氯嘧啶-4-甲酸(87mg,0.550mmol)、HATU(230mg,0.605mmol)和((3S,5S)-1-(2-氨基-4-氟苯基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯(179mg,0.550mmol)在DMF(1834μl)中的溶液,并将反应混合物在室温下搅拌30分钟,然后用水处理,并用乙酸乙酯萃取产物。将有机相用水和盐水洗涤,经硫酸钠干燥并浓缩。通过Biotage IsoleraTM(在己烷中25-100%乙酸乙酯)纯化粗产物,得到所需产物(107mg,42%)。C21H26ClFN5O4(M+H)+的LCMS计算值:m/z=466.2;实测值:466.2。
步骤3.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-5-氟苯基)-2-(2,6-二氟苯基)嘧啶-4-甲酰胺
向(2,6-二氟苯基)硼酸(15mg,0.097mmol)、XPhos Pd G2(5.07mg,6.44μmol)、磷酸钾(27.5mg,0.129mmol)和((3S,5S)-1-(2-(2-氯嘧啶-4-甲酰胺基)-4-氟苯基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯(30mg,0.064mmol)的混合物中添加1,4-二噁烷(530μl)和水(100μl),并将烧瓶抽真空,用氮气回填,然后在90℃下搅拌过夜。用DCM/水稀释反应物并分离各相。浓缩有机相,将残留物溶解在TFA(1mL)中,并允许在室温下静置30分钟,然后用MeOH稀释,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化。C22H21F3N5O2(M+H)+的LCMS计算值:m/z=444.2;实测值:444.2。
实施例67.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-5-氟苯基)-2-(3-氰基-2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
以类似于实施例66步骤3的方式,使用2-氟-4-甲氧基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)苄腈代替(2,6-二氟苯基)硼酸制备此化合物。C24H23F2N6O3(M+H)+的LCMS计算值:m/z=481.2;实测值:481.2。
实施例68.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-5-氟苯基)-2-(2,3-二氟-6-甲氧基苯基)嘧啶-4-甲酰胺
以类似于实施例66步骤3的方式,使用(2,3-二氟-6-甲氧基苯基)硼酸代替(2,6-二氟苯基)硼酸制备此化合物。C23H23F3N5O3(M+H)+的LCMS计算值:474.2;实测值:474.2。1HNMR(500MHz,DMSO-d6)δ10.69(s,1H),9.30(s,1H),8.21(d,J=5.0Hz,1H),8.18(d,J=3.0Hz,1H),7.81(s,2H),7.60(q,J=9.5Hz,1H),7.53(dd,J=8.9,5.8Hz,1H),7.13–6.96(m,2H),5.19(s,1H),3.75(s,4H),3.56(dd,J=8.2,3.6Hz,1H),3.26–3.17(m,4H),2.46–2.35(m,1H),1.77(dt,J=13.6,4.1Hz,1H)ppm。
实施例69.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-5-氟苯基)-2-(2-氟-6-(甲氧基-d3)-3-甲基苯基)嘧啶-4-甲酰胺
步骤1. 2-氟-4-(甲氧基-d3)-1-甲基苯
用碳酸钾(1.644g,11.89mmol)和碘甲烷-d3(0.592ml,9.51mmol)处理3-氟-4-甲基苯酚(1.0g,7.93mmol)在DMF(26.4ml)中的溶液,并将反应混合物加热到80℃保持1小时。将反应混合物用水处理,并用二乙醚萃取。将有机相用水和盐水洗涤,经硫酸钠干燥并浓缩。粗产物不经进一步纯化用于下一步。C8H7D3FO(M+H)+的LCMS计算值:m/z=144.2;实测值:144.2。
步骤2. 2-(2-氟-6-(甲氧基-d3)-3-甲基苯基)-4,4,5,5-四甲基-1,3,2-二氧杂硼戊环
在-78℃下用n-BuLi(在己烷中2.5M,3.35ml,8.38mmol)逐滴处理2-氟-4-(甲氧基-d3)-1-甲基苯(1.0g,6.98mmol)和HMPA(1.823ml,10.48mmol)在THF(34.9ml)中的溶液,并将反应混合物在此温度下搅拌1小时。然后添加2-异丙氧基-4,4,5,5-四甲基-1,3,2-二氧杂硼戊环(2.166ml,10.48mmol),并将反应混合物在-78℃下搅拌10分钟,然后通过移除冷却浴升温至室温。用1N HCl水溶液处理反应物,并用乙酸乙酯萃取。将有机相用水和盐水洗涤,经硫酸钠干燥并浓缩。粗产物不经进一步纯化用于下一步。
步骤3.甲基2-(2-氟-6-(甲氧基-d3)-3-甲基苯基)嘧啶-4-甲酸
用2-氯嘧啶-4-甲酸甲酯(500mg,2.90mmol)和((t-Bu)3P)2Pd(74.0mg,0.145mmol)处理2-(2-氟-6-(甲氧基-d3)-3-甲基苯基)-4,4,5,5-四甲基-1,3,2-二氧杂硼戊环(1.56g,5.79mmol)和Hunig碱(1ml,5.79mmol)在水(1333μl)和1,4-二噁烷(12mL)中的溶液。将反应烧瓶抽真空,用氮气回填,并在80℃下搅拌过夜。然后将反应混合物用DCM稀释,并通过硅藻土塞过滤。将滤液浓缩,并通过Biotage IsoleraTM(在己烷中0-100%乙酸乙酯)纯化残留物,得到所需中间体。C14H11D3FN2O3(M+H)+的LCMS计算值:m/z=280.2;实测值:280.2。
步骤4. 2-(2-氟-6-(甲氧基-d3)-3-甲基苯基)嘧啶-4-甲酸
将来自先前步骤的产物溶解在THF/水的1:1混合物(4mL)中。添加氢氧化锂(238mg,5.79mmol),并将反应混合物加热到60℃保持1小时,然后用1N HCl酸化至pH 1,并用乙酸乙酯萃取。将有机相用盐水洗涤,经硫酸钠干燥并浓缩。粗产物不经进一步纯化用于下一步。C13H9D3FN2O3(M+H)+的LCMS计算值:m/z=266.2;实测值:266.2。
步骤5.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-5-氟苯基)-2-(2-氟-6-(甲氧基-d3)-3-甲基苯基)嘧啶-4-甲酰胺
用Hunig碱(16.10μl,0.092mmol)处理2-(2-氟-6-(甲氧基-d3)-3-甲基苯基)嘧啶-4-甲酸(12.27mg,0.046mmol)、HATU(21.03mg,0.055mmol)和((3S,5S)-1-(2-氨基-4-氟苯基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯(实施例66步骤2;15mg,0.046mmol)在DMF(461μl)中的溶液,并将反应混合物在室温下搅拌30分钟。将反应混合物用水处理,并用乙酸乙酯萃取。将有机相用水和盐水洗涤,经硫酸钠干燥并浓缩。将粗产物溶解在TFA(1mL)中,在室温下保持30分钟,然后用MeOH稀释,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化。C24H23D3F2N5O3(M+H)+的LCMS计算值:m/z=473.2;实测值:473.2。
实施例70.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基-4-甲基苯基)嘧啶-4-甲酰胺
步骤1. 2-(2-氟-6-甲氧基-4-甲基苯基)-4,4,5,5-四甲基-1,3,2-二氧杂硼戊环
以类似于实施例69步骤1-2的方式,使用3-氟-5-甲基苯酚代替3-氟-4-甲基苯酚制备此化合物。
步骤2.((3S,5S)-1-(2-氨基-5-溴苯基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯
用Hunig碱(1.588ml,9.09mmol)处理4-溴-2-氟-1-硝基苯(1.0g,4.55mmol)和((3S,5S)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯(0.983g,4.55mmol)在DMF(15.15ml)中的溶液,并将反应混合物加热到80℃保持1小时。将反应混合物倒入水/乙酸乙酯中,分离各相,并将有机相用水和盐水洗涤,经硫酸钠干燥并浓缩。将残留物溶解在THF/MeOH/水的1:1:1混合物(15mL)中,并用铁(1.015g,18.18mmol)和氯化铵(1.46g,27.3mmol)处理。将反应混合物加热到60℃过夜,然后用乙酸乙酯稀释,并通过硅藻土塞过滤。将滤液用水和盐水洗涤,经硫酸钠干燥并浓缩。粗产物(1.61g,92%)不经进一步纯化用于下一步。C16H25BrN3O3(M+H)+的LCMS计算值:m/z=386.0/388.0;实测值:386.0/388.0。
步骤3.((3S,5S)-1-(2-氨基-5-(4-氰基吡啶-3-基)苯基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯
向((3S,5S)-1-(2-氨基-5-溴苯基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯(200mg,0.518mmol)、XPhos Pd G2(20.37mg,0.026mmol)、3-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)异烟腈(155mg,0.673mmol)和磷酸钾(220mg,1.035mmol)的混合物中添加1,4-二噁烷(1438μl)和水(288μl),并将反应烧瓶抽真空,用氮气回填,然后在90℃下搅拌1小时。将混合物用乙酸乙酯稀释,并通过硅藻土塞过滤。将滤液浓缩,并通过BiotageIsoleraTM纯化残留物(在己烷中30-100%乙酸乙酯,然后在乙酸乙酯中5-20%甲醇),得到所需产物,为棕色固体(175mg,83%)。C22H28N5O3(M+H)+的LCMS计算值:m/z=410.2;实测值:410.2。
步骤4.((3S,5S)-1-(2-(2-氯嘧啶-4-甲酰胺基)-5-(4-氰基吡啶-3-基)苯基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯
用Hunig碱(262μl,1.502mmol)处理2-氯嘧啶-4-甲酸(119mg,0.751mmol)、HATU(314mg,0.826mmol)和((3S,5S)-1-(2-氨基-5-(4-氰基吡啶-3-基)苯基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯(307mg,0.751mmol)在DMF(3800μl)中的溶液,并允许在室温下搅拌30分钟。将反应混合物用水处理,并用乙酸乙酯萃取。将有机相用水和盐水洗涤,经硫酸钠干燥并浓缩。通过Biotage IsoleraTM(在己烷中40-100%乙酸乙酯)纯化粗产物,得到所需产物,为橙色固体(310mg,75%)。C27H29ClN7O4(M+H)+的LCMS计算值:m/z=550.2;实测值:550.2。
步骤5.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基-4-甲基苯基)嘧啶-4-甲酰胺
向((3S,5S)-1-(2-(2-氯嘧啶-4-甲酰胺基)-5-(4-氰基吡啶-3-基)苯基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯(15mg,0.027mmol)、2-(2-氟-6-甲氧基-4-甲基苯基)-4,4,5,5-四甲基-1,3,2-二氧杂硼戊环(10.89mg,0.041mmol)、XPhos Pd G2(2.145mg,2.73μmol)和磷酸钾(12mg,0.055mmol)的混合物中添加水(54.5μl)和1,4-二噁烷(218μl),并将反应烧瓶抽真空,用氮气回填,然后在90℃下搅拌过夜。将混合物在DCM/水之间分配,并将有机相浓缩。在室温下允许残留物在TFA(1mL)中静置30分钟,然后用MeOH稀释,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化。C30H29F2N7O3(M+H)+的LCMS计算值:m/z=573.2;实测值:573.2。
实施例71.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(3,6-二氟-2-甲基苯基)嘧啶-4-甲酰胺
以类似于实施例70步骤5的方式,使用(3,6-二氟-2-甲基苯基)硼酸代替2-(2-氟-6-甲氧基-4-甲基苯基)-4,4,5,5-四甲基-1,3,2-二氧杂硼戊环制备此化合物。C29H26F2N7O2(M+H)+的LCMS计算值:m/z=542.2;实测值:542.2。
实施例72.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2,3-二氟-6-甲氧基苯基)嘧啶-4-甲酰胺
以类似于实施例70步骤5的方式,使用(2,3-二氟-6-甲氧基苯基)硼酸代替2-(2-氟-6-甲氧基-4-甲基苯基)-4,4,5,5-四甲基-1,3,2-二氧杂硼戊环制备此化合物。C29H26F2N7O3(M+H)+的LCMS计算值:m/z=558.2;实测值:558.2。
实施例73.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(3,6-二氟-2-甲氧基苯基)嘧啶-4-甲酰胺
以类似于实施例70步骤5的方式,使用(3,6-二氟-2-甲氧基苯基)硼酸代替2-(2-氟-6-甲氧基-4-甲基苯基)-4,4,5,5-四甲基-1,3,2-二氧杂硼戊环制备此化合物。C29H26F2N7O3(M+H)+的LCMS计算值:m/z=558.2;实测值:558.2。
实施例74.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(3-氰基-2-氟-6-(甲氧基-d3)苯基)嘧啶-4-甲酰胺
步骤1. 2-(3-氰基-2-氟-6-(甲氧基-d3)苯基)嘧啶-4-甲酸
以类似于实施例69步骤1-4的方式,以3-氟-4-氰基苯酚代替3-氟-4-甲基苯酚制备此化合物。C13H6D3FN3O3(M+H)+的LCMS计算值:m/z=277.2;实测值:277.2。
步骤2.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(3-氰基-2-氟-6-(甲氧基-d3)苯基)嘧啶-4-甲酰胺
用Hunig碱(12.80μl,0.073mmol)处理2-(3-氰基-2-氟-6-(甲氧基-d3)苯基)嘧啶-4-甲酸(9.72mg,0.037mmol)、HATU(16.71mg,0.044mmol)和((3S,5S)-1-(2-氨基-5-(4-氰基吡啶-3-基)苯基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯(实施例70步骤4,15mg,0.037mmol)在DMF(366μl)中的溶液,并允许将反应混合物在室温下搅拌30分钟。将反应混合物用水处理,并用乙酸乙酯萃取。将有机相用水和盐水洗涤,经硫酸钠干燥并浓缩。将粗产物溶解在TFA(1mL)中,并允许在室温下静置30分钟,然后用MeOH稀释,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化。C30H23D3FN8O3(M+H)+的LCMS计算值:m/z=568.2;实测值:568.2。
实施例75.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(3,6-二氟-2-(甲氧基-d3)苯基)嘧啶-4-甲酰胺
步骤1. 2-(3,6-二氟-2-(甲氧基-d3)苯基)嘧啶-4-甲酸
以类似于实施例69步骤1-4的方式,以2,5-二氟苯酚代替3-氟-4-甲基苯酚为起始物制备此化合物。C12H6D3F2N2O3(M+H)+的LCMS计算值:m/z=270.2;实测值:270.2。
步骤2.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(3,6-二氟-2-(甲氧基-d3)苯基)嘧啶-4-甲酰胺
以类似于实施例74步骤2的方式,使用2-(3,6-二氟-2-(甲氧基-d3)苯基)嘧啶-4-甲酸作为偶联伴侣制备此化合物。C29H23D3F2N7O3(M+H)+的LCMS计算值:m/z=561.2;实测值:561.2。
实施例76.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2,3-二氟-6-(甲氧基-d3)苯基)嘧啶-4-甲酰胺
以类似于实施例75步骤1-2的方式,使用4,5-二氟苯酚作为起始物质制备此化合物。C29H23D3F2N7O3(M+H)+的LCMS计算值:m/z=561.2;实测值:561.2。
实施例77.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-(甲氧基-d3)苯基-5-d)嘧啶-4-甲酰胺
步骤1. 1-溴-4-氟-2-(甲氧基-d3)苯
用碳酸钾(1.085g,7.85mmol)和碘甲烷-d3(0.414ml,6.28mmol)处理2-溴-5-氟苯酚(1.0g,5.24mmol)在DMF(17.45ml)中的溶液。将反应混合物加热到60℃过夜,然后用水处理,并用乙酸乙酯萃取。将有机相用水和盐水洗涤,经硫酸钠干燥并浓缩。粗产物不经进一步纯化用于下一步。C7H4D3BrFO(M+H)+的LCMS计算值:m/z=208.0/210.0;实测值:208.0/210.0。
步骤2. 2-(2-氟-6-(甲氧基-d3)苯基-5-d)-4,4,5,5-四甲基-1,3,2-二氧杂硼戊环
用碘(23.97mg,0.094mmol)、接着用1-溴-4-氟-2-(甲氧基-d3)苯(393mg,1.889mmol)在THF(8mL)中的溶液逐滴处理在THF(2mL)中的镁(92mg,3.78mmol)。将混合物加热到60℃保持1小时,然后将反应混合物冷却到室温,并通过添加甲醇-d4(382μl,9.45mmol)进行处理。在室温下搅拌15分钟后,用1N HCl进一步处理混合物以破坏剩余的镁。然后用二乙醚萃取混合物。将有机相用水和盐水洗涤,经硫酸钠干燥并浓缩。向粗中间体中添加THF(10mL),并将混合物冷却到-78℃。滴加n-BuLi(在己烷中1.6M,907μl,2.267mmol),并将反应混合物在-78℃下搅拌1小时。添加2-异丙氧基-4,4,5,5-四甲基-1,3,2-二氧杂硼戊环(586μl,2.83mmol)。将混合物在-78℃下搅拌10分钟,然后升温至室温。1小时后,用饱和氯化铵水溶液处理反应物,并用乙酸乙酯萃取。将有机相用水和盐水洗涤,经硫酸钠干燥并浓缩。粗产物不经进一步纯化用于下一步。
步骤3.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-(甲氧基-d3)苯基-5-d)嘧啶-4-甲酰胺
以类似于实施例70步骤5的方式,使用步骤2中制备的频哪醇硼酸酯代替2-(2-氟-6-甲氧基-4-甲基苯基)-4,4,5,5-四甲基-1,3,2-二氧杂硼戊环制备此化合物。C29H23D4FN7O3(M+H)+的LCMS计算值:m/z=544.2;实测值:544.2。1H NMR(600MHz,DMSO-d6)δ10.65(s,1H),9.29(d,J=5.0Hz,1H),8.98(s,1H),8.83(d,J=5.0Hz,1H),8.30(d,J=8.4Hz,1H),8.19(d,J=5.0Hz,1H),7.99(d,J=5.0Hz,1H),7.93(s,2H),7.68(s,1H),7.60–7.53(m,1H),7.48(d,J=9.9Hz,1H),7.01(t,J=8.8Hz,1H),3.88–3.80(m,1H),3.73–3.68(m,1H),3.41–3.29(m,3H),3.26(d,J=8.9Hz,1H),2.39(dt,J=15.7,8.0Hz,1H),1.86(dt,J=11.2,5.4Hz,1H)ppm。
实施例78. 2-(2-氟-6-甲氧基苯基)-N-(2-(哌啶-4-基)苯基)嘧啶-4-甲酰胺
步骤1. 4-(2-氨基苯基)哌啶-1-甲酸叔丁酯
向4-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)-3,6-二氢吡啶-1(2H)-甲酸叔丁酯(230mg,0.743mmol)、1-溴-2-硝基苯(100mg,0.495mmol)、XPhos Pd G2(38.9mg,0.050mmol)和磷酸三钾(210mg,0.990mmol)的混合物中添加1,4-二噁烷(1320μl)和水(330μl),并将反应混合物抽真空,用氮气回填,然后加热到90℃保持1小时。将混合物用DCM稀释,并通过硅藻土塞过滤。将滤液浓缩,并通过Biotage IsoleraTM(在己烷中0-70%乙酸乙酯)纯化残留物。向纯化的产物中添加MeOH(4mL),接着是氢氧化钯/碳(20%w/w,69.5mg,0.099mmol)。将反应烧瓶抽真空,用来自气球的氢气回填,然后加热到60℃过夜。然后将混合物通过硅藻土塞过滤并浓缩滤液。粗产物(130mg,95%)不经进一步纯化用于下一步。C16H25N2O2(M+H)+的LCMS计算值:m/z=277.2;实测值:277.2。
步骤2.2-(2-氟-6-甲氧基苯基)-N-(2-(哌啶-4-基)苯基)嘧啶-4-甲酰胺
用Hunig碱(164μl,0.941mmol)处理2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酸(93mg,0.376mmol)、HATU(215mg,0.564mmol)和4-(2-氨基苯基)哌啶-1-甲酸叔丁酯(130mg,0.470mmol)在DMF(2352μl)中的溶液,并将反应混合物在室温下搅拌30分钟。将反应混合物用水处理,并用乙酸乙酯萃取。将有机相用水和盐水洗涤,经硫酸钠干燥并浓缩。将残留物溶解在TFA(1mL)中,并允许静置30分钟,然后用甲醇稀释,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化。C23H24FN4O2(M+H)+的LCMS计算值:m/z=407.2;实测值:407.2。
实施例79.N-(2-(顺)4-氨基环己基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺和N-(2-(反)4-氨基环己基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
以类似于实施例78步骤1-2的方式,以(4-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)环己-3-烯-1-基)氨基甲酸叔丁酯为起始物制备这些化合物。通过制备型LCMS进行纯化,得到顺式和反式异构体。C24H26FN4O2(M+H)+的LCMS计算值:m/z=421.2;实测值:421.2。
实施例80.N-(2-(3-氨基环己基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
以类似于实施例78步骤1-2的方式,以(3-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)环己-2-烯-1-基)氨基甲酸叔丁酯为起始物制备此化合物。C24H26FN4O2(M+H)+的LCMS计算值:m/z=421.2;实测值:421.2。
实施例81.N-(2-(3-氨基环戊基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
以类似于实施例78步骤1-2的方式,以(3-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)环戊-3-烯-1-基)氨基甲酸叔丁酯为起始物制备此化合物。C23H24FN4O2(M+H)+的LCMS计算值:m/z=407.2;实测值:407.2。
实施例82.N-(2-((顺)-4-氨基环己基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺和N-(2-((反)-4-氨基环己基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
步骤1.(4-(2-氨基-5-羟苯基)环己基)氨基甲酸叔丁酯
向(4-(4,4,5,5-四甲基-1,3-二氧戊环-2-基)环己-3-烯-1-基)氨基甲酸叔丁酯(308mg,0.947mmol)、4-氯-2-碘苯胺(200mg,0.789mmol)、DPPF-PdCl2(64.4mg,0.079mmol)和碳酸钾(218mg,1.578mmol)的混合物中添加1,4-二噁烷(3156μl)和水(789μl)。将反应烧瓶抽真空,用氮气回填,然后在90℃下搅拌2小时。将混合物用DCM稀释,并通过硅藻土塞过滤。将滤液浓缩,并通过Biotage IsoleraTM(在己烷中0-100%乙酸乙酯)纯化残留物。将粗物质溶解在EtOH(4mL)中,并添加氢氧化钯/碳(20%w/w,111mg,0.158mmol)。将反应烧瓶抽真空,用来自气球的氢气回填,然后在60℃下搅拌2小时。然后将反应混合物用乙酸乙酯稀释,并通过硅藻土塞过滤。将滤液浓缩,并且粗产物不经进一步纯化用于下一步。C17H27N2O3(M+H)+的LCMS计算值:m/z=307.2;实测值:307.2。
步骤2.三氟甲磺酸3-(4-((叔丁氧羰基)氨基)环己基)-4-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)苯酯
用Hunig碱(90μl,0.516mmol)处理2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酸(64.0mg,0.258mmol)、HATU(118mg,0.309mmol)和(4-(2-氨基-5-羟苯基)环己基)氨基甲酸叔丁酯(79mg,0.258mmol)在DMF(1289μl)中的溶液,并将反应混合物在室温下搅拌30分钟。将反应混合物用水稀释,并用乙酸乙酯萃取。将有机相用水和盐水洗涤,经硫酸钠干燥并浓缩。通过Biotage IsoleraTM(在己烷中20-100%乙酸乙酯)纯化粗产物。将中间体溶解在DCM(3mL)中,并添加三乙胺(71.9μl,0.516mmol)。将反应混合物冷却到0℃,并滴加在DCM(0.5mL)中的N-苯基三氟甲磺酰亚胺(92mg,0.258mmol)。然后将反应混合物升温至室温并搅拌2小时,然后用饱和碳酸氢钠处理。分离各相,并将有机相经硫酸钠干燥并浓缩。通过BiotageIsoleraTM(在己烷中20-100%乙酸乙酯)纯化粗产物,得到所需产物,为白色固体(68mg,40%)。C30H33F4N4O7S(M+H)+的LCMS计算值:m/z=669.2;实测值:669.2。
步骤3.N-(2-((顺)-4-氨基环己基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺和N-(2-((反)-4-氨基环己基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
向3-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)异烟腈(35.1mg,0.153mmol)、DPPF-PdCl2(8.30mg,10.17μmol)、碳酸铯(66.3mg,0.203mmol)和三氟甲磺酸3-(4-((叔丁氧羰基)氨基)环己基)-4-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)苯酯(68mg,0.102mmol)的溶液中添加1,4-二噁烷(915μl)和水(102μl),并将反应烧瓶抽真空,用氮气回填,然后加热到90℃过夜。然后将混合物用水和DCM稀释,并分离各相。浓缩有机相。在室温下允许残留物在TFA(1mL)中静置30分钟,然后用MeOH稀释,并用制备型LCMS(XBridgeC18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化。通过制备型LCMS成功地将两种异构体分离。C30H28FN6O2(M+H)+的LCMS计算值:m/z=523.2;实测值:523.2。
实施例83.N-(2-((顺)-4-氨基环己基)-4-(4-氰基-1-甲基-1H-吡唑-5-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺和N-(2-((反)-4-氨基环己基)-4-(4-氰基-1-甲基-1H-吡唑-5-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
以类似于实施例82步骤2的方式,使用1-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)-1H-吡唑-4-甲腈作为偶联伴侣制备此化合物。C29H29FN7O2(M+H)+的LCMS计算值:m/z=526.2;实测值:526.2。
实施例84.N-(2-((顺)-4-氨基环己基)-4-(1,3,5-三甲基-1H-吡唑-4-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
以类似于实施例82步骤2的方式,使用1,3,5-三甲基-4-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)-1H-吡唑作为偶联伴侣制备此化合物。C30H34FN6O2(M+H)+的LCMS计算值:m/z=529.2;实测值:529.2。1H NMR(500MHz,DMSO-d6)δ10.42(s,1H),9.25(d,J=5.0Hz,1H),8.13(d,J=5.0Hz,1H),7.75(s,2H),7.54(q,J=8.1Hz,1H),7.47(d,J=8.1Hz,1H),7.20(s,1H),7.15(d,J=8.2Hz,1H),7.07(d,J=8.5Hz,3H),7.01(t,J=8.8Hz,1H),3.80(s,3H),3.71(s,3H),3.08(s,1H),2.64(t,J=11.9Hz,1H),2.25(s,3H),2.16(s,3H),1.98(d,J=11.6Hz,2H),1.87(d,J=12.3Hz,2H),1.56(q,J=12.5Hz,2H),1.30(q,J=12.0,11.4Hz,2H)ppm。
实施例85.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(甲基磺酰基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
步骤1.((3S,5S)-1-(2-氨基-5-(甲基磺酰基)苯基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯
用Hunig碱(159μl,0.912mmol)处理2-氟-4-(甲基磺酰基)-1-硝基苯(100mg,0.456mmol)和((3S,5S)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯(118mg,0.547mmol)在DMSO(1521μl)中的混合物,并将反应混合物在90℃下搅拌1小时,然后用水处理,并用乙酸乙酯萃取。将有机相用水和盐水洗涤,经硫酸钠干燥并浓缩。将残留物溶解在THF/水/MeOH的1:1:1混合物(3mL)中,并用铁(102mg,1.825mmol)和氯化铵(146mg,2.74mmol)处理。将反应混合物在60℃下搅拌1小时,然后用乙酸乙酯稀释,并通过硅藻土塞过滤。将滤液用水和盐水洗涤,经硫酸钠干燥并浓缩。粗固体不经进一步纯化用于下一步。C17H28N3O5S(M+H)+的LCMS计算值:m/z=386.2;实测值:386.2。
步骤2.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(甲基磺酰基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
用2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酸(31.9mg,0.128mmol)、HATU(65.1mg,0.171mmol)和Hunig碱(49.8μl,0.285mmol)处理((3S,5S)-1-(2-氨基-5-(甲基磺酰基)苯基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯(55mg,0.143mmol)在DMF(476μl)中的溶液。将反应混合物在室温下搅拌30分钟,然后用水处理,并用乙酸乙酯萃取。将有机相用水和盐水洗涤,经硫酸钠干燥并浓缩。向粗残留物中添加在二噁烷和MeOH中的4N HCl(2mL,1:1),并将反应混合物加热到60℃保持1小时,然后用MeOH稀释,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化。C24H27FN5O5S(M+H)+的LCMS计算值:m/z=516.2;实测值:516.2。
实施例86.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
步骤1.((3S,5S)-5-(羟甲基)-1-(2-硝基苯基)吡咯烷-3-基)氨基甲酸叔丁酯
用三乙胺(59.3μl,0.425mmol)处理1-氟-2-硝基苯(30μl,0.283mmol)和((3S,5S)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯(61.3mg,0.283mmol)在DMSO(1.5ml)中的溶液,并将反应混合物加热到80℃保持3小时。冷却到室温后,将反应混合物用DCM稀释,用盐水洗涤,经硫酸钠干燥,并将溶剂真空蒸发。得到的粗产物不经进一步纯化用于下一步。C12H16N3O5(M+H-C4H8)+的LCMS计算值:m/z=282.1;实测值:282.2。
步骤2.((3S,5S)-1-(2-氨基苯基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯
将((3S,5S)-5-(羟甲基)-1-(2-硝基苯基)吡咯烷-3-基)氨基甲酸叔丁酯(70mg,0.207mmol)、铁(57.9mg,1.037mmol)和氯化铵(67mg,1.25mmol)在THF(2ml)、水(2ml)和甲醇(2ml)中的混合物在60℃下搅拌3小时。冷却到室温后,将其通过硅藻土塞过滤,并用DCM稀释。将有机相分离,用盐水洗涤,经硫酸钠干燥,并真空蒸发溶剂。得到的粗产物不经进一步纯化用于下一步。C16H26N3O3(M+H)+的LCMS计算值:m/z=308.2;实测值:308.2。
步骤3.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
将HATU(74.2mg,0.195mmol)添加到((3S,5S)-1-(2-氨基苯基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯(40mg,0.130mmol)、2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酸(实施例1步骤1的产物,32.3mg,0.130mmol)和DIPEA(45.5μl,0.260mmol)在DMF(1ml)中的溶液中。将反应混合物在室温下搅拌30分钟,然后添加水并过滤收集沉淀产物,用水洗涤并风干。将固体溶解在TFA中,并将所得到的溶液在室温下搅拌10分钟。然后将其用乙腈稀释,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化。C23H25FN5O3(M+H)+的LCMS计算值:m/z=438.2;实测值:438.2。1H NMR(500MHz,DMSO-d6)δ10.61–10.48(s,1H),9.34–9.19(d,J=5.0Hz,1H),8.21–8.11(m,2H),7.95–7.80(br,2H),7.60–7.49(td,J=8.4,6.8Hz,1H),7.41–7.33(dd,J=6.7,2.5Hz,1H),7.25–7.15(m,2H),7.11–7.03(d,J=8.5Hz,1H),7.03–6.93(t,J=8.8Hz,1H),3.79–3.74(s,3H),3.75–3.62(m,2H),3.37–3.16(m,4H),2.43–2.31(m,1H),1.87–1.74(dt,J=13.4,5.1Hz,1H)ppm。
实施例87.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-5-甲基苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例6中所述的程序,使用1-氟-4-甲基-2-硝基苯代替1,4-二氟-2-硝基苯作为起始物质制备此化合物。C24H27FN5O3(M+H)+的LCMS计算值:m/z=452.2;实测值:452.2。
实施例88.N-(2-((2S,4S)-4-(二甲氨基)-2-(羟甲基)吡咯烷-1-基)-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
将三乙酰氧基硼氢化钠(9mg,0.044mmol)添加到甲醛(1.4mg,0.044mmol)、乙酸(2.51μl,0.044mmol)和N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺(实施例6,10mg,0.022mmol)在DCM(1ml)中的溶液中。在室温下搅拌1h后,蒸发溶剂,将反应混合物用CH3CN稀释,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化。C25H28F2N5O3(M+H)+的LCMS计算值:m/z=484.2;实测值:484.2。
实施例89.N-(5-氟-2-((2S,4S)-2-(羟甲基)-4-(异丙基氨基)吡咯烷-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例88中所述的程序,使用丙酮代替甲醛作为起始物质制备此化合物。C26H30F2N5O3(M+H)+的LCMS计算值:m/z=498.2;实测值:498.1。
实施例90.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(四氢-2H-吡喃-4-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例49中所述的程序,使用2-(3,6-二氢-2H-吡喃-4-基)-4,4,5,5-四甲基-1,3,2-二氧杂硼戊环代替4,4,5,5-四甲基-2-(丙-1-烯-2-基)-1,3,2-二氧杂硼戊环作为起始物质制备此化合物。C28H33FN5O4(M+H)+的LCMS计算值:m/z=522.2;实测值:522.2。
实施例91.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-氯苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例6中所述的程序,使用4-氯-2-氟-1-硝基苯代替1,4-二氟-2-硝基苯作为起始物质制备此化合物。C23H24ClFN5O3(M+H)+的LCMS计算值:m/z=472.2;实测值:472.3。
实施例92.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例6中所述的程序,使用2,4-二氟-1-硝基苯代替1,4-二氟-2-硝基苯作为起始物质制备此化合物。C23H24F2N5O3(M+H)+的LCMS计算值:456.2;实测值:456.3。
实施例93.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(5-氰基-2-(吡咯烷-1-基)吡啶-4-基)苯基)-2-(2,6-二氟苯基)嘧啶-4-甲酰胺
步骤1. 4-溴-6-(吡咯烷-1-基)烟腈
将4-溴-6-氯烟腈(200mg,0.920mmol)和吡咯烷(327mg,4.60mmol)在2-丙醇(2mL)中的溶液在100℃下搅拌12h。然后将溶剂真空蒸发。得到的粗产物不经进一步纯化用于下一步。C10H11BrN3(M+H)+的LCMS计算值:m/z=252.0;实测值:252.0。
步骤2.((3S,5S)-1-(2-(2-(2,6-二氟苯基)嘧啶-4-甲酰胺基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)苯基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯
根据实施例46和41中所述的程序,使用(2,6-二氟苯基)硼酸代替(2-氟-6-甲氧基苯基)硼酸作为起始物质制备此化合物。C33H41BF2N5O6(M+H)+的LCMS计算值:m/z=652.3;实测值:652.2。
步骤3.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(5-氰基-2-(吡咯烷-1-基)吡啶-4-基)苯基)-2-(2,6-二氟苯基)嘧啶-4-甲酰胺
根据实施例46步骤2中所述的程序,使用4-溴-6-(吡咯烷-1-基)烟腈代替2-溴烟腈,并使用((3S,5S)-1-(2-(2-(2,6-二氟苯基)嘧啶-4-甲酰胺基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)苯基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯代替((3S,5S)-1-(2-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼戊环-2-基)苯基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯作为起始物质制备此化合物。C32H31F2N8O2(M+H)+的LCMS计算值:m/z=597.3;实测值:597.2。
实施例94.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(1-氰基环丙基)苯基)-2-(2,6-二氟苯基)嘧啶-4-甲酰胺
步骤1.((3S,5S)-1-(5-(氰甲基)-2-硝基苯基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯
根据实施例6中所述的程序,使用2-(3-氟-4-硝基苯基)乙腈代替1,4-二氟-2-硝基苯作为起始物质制备此化合物。C14H17N4O5(M-C4H8+H)+的LCMS计算值:m/z=321.1;实测值:321.1。
步骤2.((3S,5S)-5-(((叔丁基二甲基甲硅烷基)氧基)甲基)-1-(5-(氰甲基)-2-硝基苯基)吡咯烷-3-基)氨基甲酸叔丁酯
将叔丁基氯二甲基硅烷(0.054g,0.359mmol)添加到1H-咪唑(0.024g,0.359mmol)和((3S,5S)-1-(5-(氰甲基)-2-硝基苯基)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯(0.090g,0.239mmol)在1mL DCM中的溶液中。在室温下将反应混合物搅拌2h后,添加水,并用DCM萃取产物。将合并的有机相用水和盐水洗涤,经硫酸钠干燥,并将溶剂真空蒸发。得到的粗产物不经进一步纯化用于下一步。C20H31N4O5Si(M-C4H8+H)+的LCMS计算值:m/z=435.2;实测值:435.2。
步骤3.((3S,5S)-5-(((叔丁基二甲基甲硅烷基)氧基)甲基)-1-(5-(1-氰基环丙基)-2-硝基苯基)吡咯烷-3-基)氨基甲酸叔丁酯
用1,2-二溴乙烷(0.046g,0.245mmol)处理((3S,5S)-5-(((叔丁基二甲基甲硅烷基)氧基)甲基)-1-(5-(氰甲基)-2-硝基苯基)吡咯烷-3-基)氨基甲酸叔丁酯(0.120g,0.245mmol)在1mL DMF中的溶液。在室温下搅拌混合物,然后用氢化钠(0.120g,5.00mmol)处理。将混合物进一步在室温下搅拌过夜。然后添加水,并过滤收集沉淀产物,用水洗涤并风干。其不经进一步纯化用于下一步。C22H33N4O5Si(M-C4H8+H)+的LCMS计算值:m/z=461.2;实测值:461.2。
步骤4.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(1-氰基环丙基)苯基)-2-(2,6-二氟苯基)嘧啶-4-甲酰胺
根据实施例1中所述的程序,使用(2,6-二氟苯基)硼酸代替(2-氟-6-甲氧基苯基)硼酸,并使用((3S,5S)-5-(((叔丁基二甲基甲硅烷基)氧基)甲基)-1-(5-(1-氰基环丙基)-2-硝基苯基)吡咯烷-3-基)氨基甲酸叔丁酯代替(1R,4R)-5-(4-氟-2-硝基苯基)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯作为起始物质制备此化合物。C26H25F2N6O2(M+H)+的LCMS计算值:m/z=491.2;实测值:491.1。
实施例95.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-(二氟甲氧基)-6-氟苯基)嘧啶-4-甲酰胺
步骤1. 2-溴-1-(二氟甲氧基)-3-氟苯
将2-溴-3-氟苯酚(0.865g,4.53mmol)、氯二氟乙酸钠(4.14g,27.2mmol)和碳酸铯(4.43g,13.59mmol)在DMF(10mL)中的混合物在100℃下搅拌4h。冷却到室温后,将混合物真空浓缩。通过Biotage IsoleraTM纯化得到的粗产物,得到所需产物。
步骤2. 2-(2-(二氟甲氧基)-6-氟苯基)-4,4,5,5-四甲基-1,3,2-二氧杂硼戊环
在-78℃下用nBuLi 1.6M(1.72mL,4.32mmol)处理2-溴-1-(二氟甲氧基)-3-氟苯(400mg,1.660mmol)在THF(10mL)中的溶液。搅拌1h后,添加2-异丙氧基-4,4,5,5-四甲基-1,3,2-二氧杂硼戊环(1.02mL,4.98mmol),然后经6h将混合物缓慢升温至室温。向混合物中添加EtOAc(50mL)和水(30mL)。将有机相分离,用盐水洗涤,经MgSO4干燥,过滤并真空蒸发溶剂。得到的粗产物不经进一步纯化用于下一步。
步骤3.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-(二氟甲氧基)-6-氟苯基)嘧啶-4-甲酰胺
根据实施例63中所述的程序,使用2-(2-(二氟甲氧基)-6-氟苯基)-4,4,5,5-四甲基-1,3,2-二氧杂硼戊环代替(2,6-二氟苯基)硼酸作为起始物质制备此化合物。C29H25F3N7O3(M+H)+的LCMS计算值:m/z=576.2;实测值:576.3。
实施例96.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-(甲氧基-d3)苯基)嘧啶-4-甲酰胺
步骤1. 2-(2-氟-6-(甲氧基-d3)苯基)-4,4,5,5-四甲基-1,3,2-二氧杂硼戊环
以类似于实施例69的方式,以3-氟苯酚代替3-氟-4-甲基苯酚为起始物制备此化合物。C13H16D3BFO3(M+H)+的LCMS计算值:m/z=256.2;实测值:256.2。
步骤2.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-(甲氧基-d3)苯基)嘧啶-4-甲酰胺
根据实施例63中所述的程序,使用2-(2-氟-6-(甲氧基-d3)苯基)-4,4,5,5-四甲基-1,3,2-二氧杂硼戊环代替(2,6-二氟苯基)硼酸作为起始物质制备此化合物。C29H24D3FN7O3(M+H)+的LCMS计算值:m/z=543.2;实测值:543.3。
实施例97.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-环丙基-6-氟苯基)嘧啶-4-甲酰胺
根据实施例63中所述的程序,使用2-(2-环丙基-6-氟苯基)-4,4,5,5-四甲基-1,3,2-二氧杂硼戊环代替(2,6-二氟苯基)硼酸作为起始物质制备此化合物。C31H29FN7O2(M+H)+的LCMS计算值:m/z=550.2;实测值:550.3。
实施例98.N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-乙氧基-6-氟苯基)嘧啶-4-甲酰胺
根据实施例63中所述的程序,使用(2-乙氧基-6-氟苯基)硼酸代替(2,6-二氟苯基)硼酸作为起始物质制备此化合物。C30H29FN7O3(M+H)+的LCMS计算值:m/z=554.2;实测值:554.3。
实施例99.N-(4-(4-氰基吡啶-3-基)-2-((1S,4S)-4-(羟甲基)-5-甲基-2,5-二氮杂双环[2.2.1]庚-2-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
步骤1.(1S,4S)-4-(羟甲基)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯
向帕尔反应容器中装入(1S,4S)-4-(羟甲基)-5-(4-甲氧基苄基)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯(通过改动Ivon,Y.等人,Synthesis 2015,47,1123-1130中所述的程序制备)(25mg,0.072mmol)、Pd/C(10%润湿,Degussa型,7.7mg),接着是MeOH(7.2mL),将反应混合物抽真空,并用氮气回填3次,接着进行另一抽真空循环,然后用氢气加压至25psi。将容器在氢气压力下摇动6小时,此时经硅藻土过滤溶液,并将溶剂真空蒸发。得到的粗产物不经纯化用于下一反应。C11H21N2O3(M+H)+的LCMS计算值:m/z=229.2;实测值229.2。
步骤2.(1S,4S)-4-(羟甲基)-5-甲基-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯
用甲醛(在H2O中37重量%,16.1μL,0.217mmol)和三乙酰氧基硼氢化钠(31mg,0.145mmol)处理(1S,4S)-4-(羟甲基)-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯(16.5mg,0.072mmol)在CH3CN(200μL)和H2O(50μL)中的溶液,并将反应混合物在室温下搅拌2小时。然后将反应混合物用CH2Cl2稀释,用饱和NaHCO3水溶液洗涤,经MgSO4干燥,过滤并将溶剂真空蒸发。得到的粗产物不经纯化用于下一反应。C12H23N2O3(M+H)+的LCMS计算值:m/z=243.2;实测值:243.2。
步骤3. 3-(3-((1S,4S)-4-(羟甲基)-5-甲基-2,5-二氮杂双环[2.2.1]庚-2-基)-4-硝基苯基)异烟腈
将(1S,4S)-4-(羟甲基)-5-甲基-2,5-二氮杂双环[2.2.1]庚烷-2-甲酸叔丁酯(17mg,0.070mmol)和4M HCl/二噁烷(1mL)的混合物在室温下搅拌1小时,之后将溶剂真空蒸发。然后用3-(3-氟-4-硝基苯基)异烟腈(实施例49与50之间描述的中间体1,17.1mg,0.070mmol)、DMSO(300μL)、三乙胺(14.7μL,0.943mmol)处理残留物,并将反应混合物加热到100℃过夜。冷却到室温后,将反应混合物用DCM稀释,用盐水洗涤,经硫酸钠干燥,并将溶剂真空蒸发。得到的粗产物不经进一步纯化用于下一步。C19H20N5O3(M+H)+的LCMS计算值:m/z=366.2;实测值:366.1。
步骤4. 3-(4-氨基-3-((1S,4S)-4-(羟甲基)-5-甲基-2,5-二氮杂双环[2.2.1]庚-2-基)苯基)异烟腈
将3-(3-((1S,4S)-4-(羟甲基)-5-甲基-2,5-二氮杂双环[2.2.1]庚-2-基)-4-硝基苯基)异烟腈(26mg,0.071mmol)、铁(20.0mg,0.356mmol)和氯化铵(22.9mg,0.427mmol)在THF(1mL)、H2O(1mL)和甲醇(1mL)中的混合物在60℃下搅拌1小时。冷却到室温后,将其通过硅藻土塞过滤,并用CH2Cl2稀释。将有机相分离,用盐水洗涤,经MgSO4干燥,过滤并真空蒸发溶剂。得到的粗产物不经进一步纯化用于下一步。C19H22N5O(M+H)+的LCMS计算值:m/z=336.2;实测值:336.2。
步骤5.N-(4-(4-氰基吡啶-3-基)-2-((1S,4S)-4-(羟甲基)-5-甲基-2,5-二氮杂双环[2.2.1]庚-2-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
将HATU(20.4mg,0.054mmol)添加到3-(4-氨基-3-((1S,4S)-4-(羟甲基)-5-甲基-2,5-二氮杂双环[2.2.1]庚-2-基)苯基)异烟腈(13mg,0.036mmol)、2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酸(8.9mg,0.036mmol)和DIPEA(12.5μL,0.072mmol)在DMF(300μL)中的溶液中。将反应混合物在60℃下搅拌30分钟,然后添加水,并过滤收集沉淀产物,用水洗涤并风干。将固体溶解在TFA中,并将所得到的溶液在60℃下搅拌10分钟,之后真空蒸发溶剂。然后将粗残留物溶解在THF(1mL)、MeOH(1mL)和NH4OH水溶液(1mL)中,密封,并将溶液在60℃下搅拌30分钟,之后真空蒸发溶剂。然后将得到的粗产物用CH3CN稀释,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化。C31H29FN7O3(M+H)+的LCMS计算值:m/z=566.2;实测值:566.2。
实施例100.(S)-N-(4-(4-氰基吡啶-3-基)-2-(2-(羟甲基)吗啉代)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
根据实施例51中所述的程序,使用(S)-吗啉-2-基甲醇代替(2R,5S)-5-(羟甲基)-2-甲基哌嗪-1-甲酸叔丁酯作为起始物质制备此化合物。C29H26FN6O4(M+H)+的LCMS计算值:m/z=541.2;实测值:541.3。
实施例101.(S)-N-(4-(4-氰基吡啶-3-基)-2-(2-((二甲氨基)甲基)吗啉代)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
步骤1.(R)-N-(4-(4-氰基吡啶-3-基)-2-(2-(羟甲基)吗啉代)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
以类似于实施例51步骤1-3的方式,以(R)-吗啉-2-基甲醇代替(2R,5S)-5-(羟甲基)-2-甲基哌嗪-1-甲酸叔丁酯作为起始物质来制备此化合物。C29H26FN6O4(M+H)+的LCMS计算值:m/z=541.2;实测值:541.3。
步骤2.(R)-4-甲基苯磺酸(4-(5-(4-氰基吡啶-3-基)-2-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)苯基)吗啉-2-基)甲酯
用DMAP(2.3mg,0.018mmol)、三乙胺(77μL,0.555mmol)和TsCl(42.3mg,0.222mmol)处理(R)-N-(4-(4-氰基吡啶-3-基)-2-(2-(羟甲基)吗啉代)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺(100mg,0.185mmol)在CH2Cl2(740μL)中的溶液,并将反应混合物在室温下搅拌过夜。然后将反应混合物用EtOAc稀释,用10%柠檬酸水溶液、饱和NaHCO3水溶液洗涤,经MgSO4干燥,过滤并将溶剂真空蒸发。得到的粗产物不经纯化用于下一反应。C36H32FN6O6S(M+H)+的LCMS计算值:m/z=695.2;实测值:695.3。
步骤3.(S)-N-(4-(4-氰基吡啶-3-基)-2-(2-((二甲氨基)甲基)吗啉代)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
用二甲胺(461μL,0.921mmol)处理(R)-4-甲基苯磺酸(4-(5-(4-氰基吡啶-3-基)-2-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)苯基)吗啉-2-基)甲酯(20mg,0.029mmol)在EtOH(480μL)中的溶液。将反应混合物在100℃下搅拌过夜。将溶剂真空蒸发,并将所得残留物用乙腈稀释,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化。C31H31FN7O3(M+H)+:m/z=568.2;实测值568.3。
实施例102.(R)-N-(2-(2-(氰甲基)吗啉代)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
用氰化钾(5.6mg,0.086mmol)处理(R)-4-甲基苯磺酸(4-(5-(4-氰基吡啶-3-基)-2-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)苯基)吗啉-2-基)甲酯(20mg,0.029mmol)在EtOH(480μL)中的溶液。将反应混合物在100℃下搅拌6小时。将溶剂真空蒸发,将所得残留物用乙腈稀释,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化。C30H25FN7O3(M+H)+:m/z=550.2;实测值550.2。
实施例103.(R)-N-(4-(4-氰基吡啶-3-基)-2-(3-氧代四氢-3H-噁唑并[3,4-a]吡嗪-7(1H)-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
步骤1.(R)-4-(5-(4-氰基吡啶-3-基)-2-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)苯基)-2-(羟甲基)哌嗪-1-甲酸叔丁酯
以类似于实施例51步骤1-3的方式,以(R)-2-(羟甲基)哌嗪-1-甲酸叔丁酯代替(2R,5S)-5-(羟甲基)-2-甲基哌嗪-1-甲酸叔丁酯作为起始物质来制备此化合物。C34H35FN7O5(M+H)+的LCMS计算值:m/z=640.3;实测值:640.2。
步骤2.(R)-4-(5-(4-氰基吡啶-3-基)-2-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)苯基)-2-(((甲基磺酰基)氧基)甲基)哌嗪-1-甲酸叔丁酯
用三乙胺(13.1μL,0.094mmol)和MsCl(5.5μL,0.070mmol)处理(R)-4-(5-(4-氰基吡啶-3-基)-2-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)苯基)-2-(羟甲基)哌嗪-1-甲酸叔丁酯(30mg,0.047mmol)在CH2Cl2(470μL)中的溶液,并将反应混合物在室温下搅拌1小时。将溶剂真空蒸发。得到的粗产物不经纯化用于下一反应。C35H37FN7O7S(M+H)+的LCMS计算值:m/z=718.2;实测值718.2。
步骤3.(R)-N-(4-(4-氰基吡啶-3-基)-2-(3-氧代四氢-3H-噁唑并[3,4-a]吡嗪-7(1H)-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
将氰化钾(9.2mg,0.142mmol)添加到(R)-4-(5-(4-氰基吡啶-3-基)-2-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)苯基)-2-(((甲基磺酰基)氧基)甲基)哌嗪-1-甲酸叔丁酯(34mg,0.047mmol)在DMSO(475μL)中的溶液中。将反应混合物在80℃下搅拌1小时。冷却到室温后,将所得溶液用乙腈稀释,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化。C30H25FN7O4(M+H)+:m/z=566.2;实测值566.3。
实施例104.(S)-N-(5-氟-2-(3-(羟甲基)哌嗪-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
以类似于实施例6的方式,以(S)-2-(羟甲基)哌嗪-1-甲酸叔丁酯代替((3S,5S)-5-(羟甲基)吡咯烷-3-基)氨基甲酸叔丁酯作为起始物质来制备此化合物。C23H24F2N5O3(M+H)+的LCMS计算值:m/z=456.2;实测值:456.3。1H NMR(400MHz,DMSO)δ11.03–10.69(s,1H),9.48–9.26(d,J=5.0Hz,1H),8.38–8.21(dd,J=10.8,3.0Hz,1H),8.20–8.09(d,J=5.0Hz,1H),7.68–7.51(td,J=8.4,6.9Hz,1H),7.42–7.31(dd,J=8.8,5.6Hz,1H),7.13–6.96(m,3H),3.83–3.71(s,3H),3.59–3.18(m,6H),3.15–2.79(m,4H),2.81–2.69(s,1H)。
实施例105.N-(4-(4-氰基吡啶-3-基)-2-(3-(甲氧基甲基)氮杂环丁-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
以类似于实施例51的方式,以3-(甲氧基甲基)氮杂环丁烷代替(2R,5S)-5-(羟甲基)-2-甲基哌嗪-1-甲酸叔丁酯作为起始物质来制备此化合物。C29H26FN6O3(M+H)+的LCMS计算值:m/z=525.2;实测值:525.2。
实施例106.(S)-N-(4-(4-氰基吡啶-3-基)-2-(2-(羟甲基)氮杂环丁-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
以类似于实施例51的方式,以(S)-氮杂环丁-2-基甲醇代替(2R,5S)-5-(羟甲基)-2-甲基哌嗪-1-甲酸叔丁酯作为起始物质来制备此化合物。C28H24FN6O3(M+H)+的LCMS计算值:m/z=511.2;实测值:511.2。
实施例107.(R)-N-(4-(4-氰基吡啶-3-基)-2-(2-((二甲氨基)甲基)氮杂环丁-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
步骤1.(R)-N-(4-(4-氰基吡啶-3-基)-2-(2-(羟甲基)氮杂环丁-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
以类似于实施例51的方式,以(R)-氮杂环丁-2-基甲醇代替(2R,5S)-5-(羟甲基)-2-甲基哌嗪-1-甲酸叔丁酯作为起始物质来制备此化合物。C28H24FN6O3(M+H)+的LCMS计算值:m/z=511.2;实测值:511.2。
步骤2.(R)-甲磺酸(1-(5-(4-氰基吡啶-3-基)-2-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)苯基)氮杂环丁-2-基)甲酯
用三乙胺(27μL,0.196mmol)和MsCl(11.4μL,0.147mmol)处理(R)-N-(4-(4-氰基吡啶-3-基)-2-(2-(羟甲基)氮杂环丁-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺(50mg,0.098mmol)在CH2Cl2(980μL)中的溶液,并将反应混合物在室温下搅拌2小时。将溶剂真空蒸发。得到的粗产物不经纯化用于下一反应。C29H26FN6O5S(M+H)+的LCMS计算值:m/z=589.2;实测值589.3。
步骤3.(R)-N-(4-(4-氰基吡啶-3-基)-2-(2-((二甲氨基)甲基)氮杂环丁-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
用二甲胺(544μL,1.09mmol)处理(R)-甲磺酸(1-(5-(4-氰基吡啶-3-基)-2-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)苯基)氮杂环丁-2-基)甲酯(20mg,0.034mmol)在EtOH(570μL)中的溶液。将反应混合物在100℃下搅拌过夜。冷却到室温后,将溶剂真空蒸发,将所得残留物用乙腈稀释,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化。C30H29FN7O2(M+H)+:m/z=538.2;实测值538.2。
实施例108.N-(4-(4-氰基吡啶-3-基)-2-(4-甲基哌嗪-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
步骤1.N-(4-(4-氰基吡啶-3-基)-2-(哌嗪-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
以类似于实施例51的方式,以哌嗪-1-甲酸叔丁酯代替(2R,5S)-5-(羟甲基)-2-甲基哌嗪-1-甲酸叔丁酯作为起始物质来制备此化合物。C28H25FN7O2(M+H)+的LCMS计算值:m/z=510.2;实测值:510.2。
步骤2.N-(4-(4-氰基吡啶-3-基)-2-(4-甲基哌嗪-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
用甲醛(在H2O中37重量%,110μL,1.47mmol)、乙酸(8.4μL,0.147mmol)和三乙酰氧基硼氢化钠(12.5mg,0.059mmol)处理N-(4-(4-氰基吡啶-3-基)-2-(哌嗪-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺(15mg,0.029mmol)在THF(980μL)中的溶液,并将反应混合物在室温下搅拌1h。然后将溶剂真空蒸发,将所得残留物用乙腈稀释,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化。C29H27FN7O2(M+H)+:m/z=524.2;实测值524.2。
实施例109.N-(4-(4-氰基吡啶-3-基)-2-(4-(2-羟乙基)哌嗪-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
用2-((叔丁基二甲基甲硅烷基)氧基)乙醛(34μL,0.177mmol)、乙酸(5.0μL,0.088mmol)和三乙酰氧基硼氢化钠(12.5mg,0.059mmol)处理N-(4-(4-氰基吡啶-3-基)-2-(哌嗪-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺(15mg,0.029mmol)在THF(980μL)中的溶液,并将反应混合物在室温下搅拌1h。完成后,添加4M HCl/二噁烷(1mL),并将反应物搁置搅拌30分钟。然后真空蒸发溶剂,将所得残留物用乙腈稀释,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化。C30H29FN7O3(M+H)+:m/z=554.2;实测值554.4。
实施例110.(S)-N-(5-氟-2-(3-(羟甲基)哌嗪-1-基)-4-异丙基苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
步骤1.(S)-4-(5-氯-4-氟-2-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)苯基)-2-(羟甲基)哌嗪-1-甲酸叔丁酯
根据实施例41中所述的程序,使用1-氯-2,5-二氟-4-硝基苯代替3-(3-氟-4-硝基苯基)异烟腈作为起始物质制备此化合物。C28H31ClF2N5O5(M+H)+的LCMS计算值:m/z=590.2;实测值:590.2。
步骤2.(S)-4-(4-氟-2-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)-5-(丙-1-烯-2-基)苯基)-2-(羟甲基)哌嗪-1-甲酸叔丁酯
向(S)-4-(5-氯-4-氟-2-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)苯基)-2-(羟甲基)哌嗪-1-甲酸叔丁酯(20mg,0.034mmol)、4,4,5,5-四甲基-2-(丙-1-烯-2-基)-1,3,2-二氧杂硼戊环(9.6μL,0.051mmol)、Xphos Pd G2(2.7mg,3.4μmol)和磷酸三钾(14.4mg,0.068mmol)的混合物中添加1,4-二噁烷(500μL)和H2O(100μL),并将反应烧瓶抽真空,用氮气回填,然后在80℃下搅拌1小时。将反应混合物冷却到室温,将溶剂真空蒸发,并通过Biotage IsoleraTM(在己烷中0-100%乙酸乙酯)纯化粗产物,得到所需产物。C31H36F2N5O5(M+H)+的LCMS计算值:m/z=596.3;实测值:596.3。
步骤3.(S)-N-(5-氟-2-(3-(羟甲基)哌嗪-1-基)-4-异丙基苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺
将钯/碳(10%润湿,Degussa型,3.6mg)添加到(S)-4-(4-氟-2-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)-5-(丙-1-烯-2-基)苯基)-2-(羟甲基)哌嗪-1-甲酸叔丁酯(20mg,0.034mmol)在甲醇(1.1ml)中的溶液中。将反应烧瓶与含氢气的气球连接,并将反应混合物在室温下搅拌2小时。然后将催化剂滤出,将溶剂真空蒸发,并添加TFA(2mL)。将反应混合物在室温下搅拌15分钟,然后用CH3CN和水稀释,并用制备型LCMS(XBridge C18柱,以含有0.1%TFA的乙腈/水的梯度洗脱,流速为60mL/分钟)纯化。C26H30F2N5O3(M+H)+的LCMS计算值:m/z=498.2;实测值:498.3。
实施例A.HPK1激酶结合测定
在DMSO中制备1mM测试化合物的储备溶液。通过3倍和11点连续稀释准备化合物板。将0.1μL在DMSO中的化合物从化合物板转移到白色384孔聚苯乙烯板上。测定缓冲液含有50mM HEPES(pH 7.5)、0.01%Tween-20、5mM MgCl2、0.01%BSA和5mM DTT。将5μL在缓冲液中制备的4nM活性HPK1(SignalChem M23-11G)添加到板中。给定的酶浓度基于供应商报告的给定储备液浓度。添加5μl的18nM示踪剂222(ThermoFisher PV6121)和4nMLanthaScreen Eu-抗GST抗体(ThermoFisher PV5595)。在25℃下温育一小时后,在PHERAstar FS读板器(BMG Labtech)上读板。测定Ki值。
如实施例中所例示的本公开的化合物显示在以下范围内的Ki值:+=Ki≤100nM;++=100nM<Ki≤500nM;+++=500nM<Ki≤5000nM。
表1.
实施例B.p-SLP76S376 HTRF测定
可采用如下所述的p-SLP76S376 HTRF测定来测试一种或多种本发明化合物。收集Jurkat细胞(在含10%FBS的RPMI1640培养基中培养)并离心,接着按3x106个细胞/mL重悬于适当的培养基中。将Jurkat细胞(35μL)分配到384孔板中的每个孔中。用细胞培养基将测试化合物稀释达40倍稀释度(将39μL细胞培养基添加到1μL化合物中)。在37℃、5%CO2下用各种浓度的测试化合物将孔板中的Jurkat细胞处理(将5ul稀释的化合物添加到35μLJurkat细胞中,且从3uM开始以1:3稀释度进行)1小时,接着用抗CD3(5μg/mL,OKT3克隆)处理30分钟。制备100x阻断试剂(来自p-SLP76 ser376HTRF试剂盒)与4x裂解缓冲液(LB)的1:25稀释液,并将15μL含阻断试剂的4xLB缓冲液添加到每个孔中,并伴随轻轻摇动在室温下温育45分钟。将细胞裂解物(16μL)添加到Greiner白板中,用p-SLP76 ser376HTRF试剂(2μL供体、2ul受体)处理,并在4℃下温育过夜。次日在PHERAstar读板器上测量均相时间分辨荧光(HTRF)。使用GraphPad Prism 5.0软件,通过拟合抑制百分比与抑制剂浓度对数的曲线来进行IC50测定。
实施例C.CD4+或CD8+ T细胞的分离和细胞因子测量
收集来自健康供体的血液样本。使用CD4+或CD8+富集试剂盒(lifetech,USA)通过阴性选择来分离CD4+或CD8+ T细胞。分离的CD4+或CD8+ T细胞的纯度通过流式细胞术测定,且常规上>80%。在补充有10%FCS、谷氨酰胺和抗生素的RPMI 1640(Invitrogen LifeTechnologies,USA)中培养细胞。对于细胞因子测量,将Jurkat细胞或原代CD4+或CD8+ T细胞以200k个细胞/孔进行铺板,并在存在或不存在各种浓度的测试化合物的情况下用抗CD3/抗CD28珠刺激24h。然后将16μL上清液转移到白检测板上,并使用人IL2或IFNγ测定试剂盒(Cisbio)进行分析。
实施例D.Treg测定
可采用如下所述的调控T细胞增殖测定法测试一种或多种化合物。使用来自Thermo Fisher Scientific(11363D)的分离试剂盒,自人供给的外周血单核细胞分离原代CD4+/CD25-T细胞和CD4+/CD25+调控T细胞。按照供应商提供的方案,将CD4+/CD25-T细胞用CFSE(Thermo Fisher Scientific,C34554)标记。将CFSE标记的T细胞和CD4+/CD25+调控T细胞以1X106个细胞/mL的浓度重悬在RPMI-1640培养基中。将100μL CFSE标记的T细胞与或不与50μL CD4+/CD25+调控T细胞混合,用5μl抗CD3/CD28珠(Thermo Fisher Scientific,11132D)和稀释在50μl RPMI-1640培养基中的各种浓度的化合物进行处理。将混合的细胞群培养5天(37℃,5%CO2),并在第5天使用FITC通道通过BD LSRFortessa X-20分析CFSE标记的T细胞的增殖。
本领域技术人员根据前面的描述可显而易见除本文描述的内容以外对本发明的各种修改。这类修改也旨在落入所附权利要求的范围内。本申请中引用的每一参考文献,包括但不限于所有专利、专利申请和出版物,均以引用的方式整体并入本文。
Claims (93)
1.一种式(I’)的化合物:
或其药学上可接受的盐,其中:
CyA是C3-12环烷基或4-12元杂环烷基;其中所述4-12元杂环烷基具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中所述N和S任选被氧化;其中所述4-12元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述C3-12环烷基和4-12元杂环烷基各自任选被1、2、3或4个独立地选自RA的取代基取代;
A是N或CR16;
R16选自H、D、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、卤代基、CN、NO2、ORa16、SRa16、C(O)Rb16、C(O)NRc16Rd16、C(O)ORa16、OC(O)Rb16、OC(O)NRc16Rd16、NRc16Rd16、NRc16C(O)Rb16、NRc16C(O)ORa16、NRc16C(O)NRc16Rd16、NRc16S(O)Rb16、NRc16S(O)2Rb16、NRc16S(O)2NRc16Rd16、S(O)Rb16、S(O)NRc16Rd16、S(O)2Rb16、S(O)2NRc16Rd16和BRh16Ri16;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
R1选自H、D、卤代基、CN、C1-6烷基、ORa15和NRc15Rd15;其中所述C1-6烷基任选被1、2或3个独立地选自Rg的取代基取代;
R2选自H、D、Cy2、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、卤代基、CN、NO2、ORa、SRa、C(O)Rb、C(O)NRcRd、C(O)ORa、OC(O)Rb、OC(O)NRcRd、NRcRd、NRcC(O)Rb、NRcC(O)ORa、NRcC(O)NRcRd、C(=NRe)Rb、C(=NORa)Rb、C(=NRe)NRcRd、NRcC(=NRe)NRcRd、NRcS(O)Rb、NRcS(O)2Rb、NRcS(O)2NRcRd、S(O)Rb、S(O)NRcRd、S(O)2Rb、S(O)2NRcRd和BRhRi;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自R10的取代基取代;
Cy2选自C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述4-10元杂环烷基和5-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中所述N和S任选被氧化;其中5-10元杂芳基和4-10元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R10的取代基取代;
Z是N或CR3;
R3选自H、D、Cy3、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、卤代基、CN、NO2、ORa4、SRa4、C(O)Rb4、C(O)NRc4Rd4、C(O)ORa4、OC(O)Rb4、OC(O)NRc4Rd4、NRc4Rd4、NRc4C(O)Rb4、NRc4C(O)ORa4、NRc4C(O)NRc4Rd4、C(=NRe4)Rb4、C(=NORa4)Rb4、C(=NRe4)NRc4Rd4、NRc4C(=NRe4)NRc4Rd4、NRc4S(O)Rb4、NRc4S(O)2Rb4、NRc4S(O)2NRc4Rd4、S(O)Rb4、S(O)NRc4Rd4、S(O)2Rb4、S(O)2NRc4Rd4和BRh4Ri4;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自R13的取代基取代;
Cy3选自C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述4-10元杂环烷基和5-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中所述N和S任选被氧化;其中5-10元杂芳基和4-10元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R13的取代基取代;
每个R4独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、NO2、ORa8、SRa8、C(O)Rb8、C(O)NRc8Rd8、C(O)ORa8、OC(O)Rb8、OC(O)NRc8Rd8、NRc8Rd8、NRc8C(O)Rb8、NRc8C(O)ORa8、NRc8C(O)NRc8Rd8、C(=NRe8)Rb8、C(=NORa8)Rb8、C(=NRe8)NRc8Rd8、NRc8C(=NRe8)NRc8Rd8、NRc8S(O)Rb8、NRc8S(O)2Rb8、NRc8S(O)2NRc8Rd8、S(O)Rb8、S(O)NRc8Rd8、S(O)2Rb8、S(O)2NRc8Rd8和BRh8Ri8;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R5的取代基取代;
每个R5独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、ORa9、SRa9、C(O)Rb9、C(O)NRc9Rd9、C(O)ORa9、NRc9Rd9、NRc9C(O)Rb9、NRc9C(O)ORa9、NRc9S(O)Rb9、NRc9S(O)2Rb9、NRc9S(O)2NRc9Rd9、S(O)Rb9、S(O)NRc9Rd9、S(O)2Rb9、S(O)2NRc9Rd9和BRh9Ri9;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R6的取代基取代;
每个R6独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-6环烷基、苯基、5-6元杂芳基、4-7元杂环烷基、卤代基、D、CN、ORa10、SRa10、C(O)Rb10、C(O)NRc10Rd10、C(O)ORa10、NRc10Rd10、NRc10C(O)Rb10、NRc10C(O)ORa10、NRc10S(O)Rb10、NRc10S(O)2Rb10、NRc10S(O)2NRc10Rd10、S(O)Rb10、S(O)NRc10Rd10、S(O)2Rb10和S(O)2NRc10Rd10;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-6环烷基、苯基、5-6元杂芳基和4-7元杂环烷基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个RA选自H、D、Cy1、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、卤代基、CN、NO2、ORa11、SRa11、C(O)Rb11、C(O)NRc11Rd11、C(O)ORa11、OC(O)Rb11、OC(O)NRc11Rd11、NRc11Rd11、NRc11C(O)Rb11、NRc11C(O)ORa11、NRc11C(O)NRc11Rd11、C(=NRe11)Rb11、C(=NORa11)Rb11、C(=NRe11)NRc11Rd11、NRc11C(=NRe11)NRc11Rd11、NRc11S(O)Rb11、NRc11S(O)2Rb11、NRc11S(O)2NRc11Rd11、S(O)Rb11、S(O)NRc11Rd11、S(O)2Rb11、S(O)2NRc11Rd11和BRh11Ri11;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自R7的取代基取代;
Cy1选自C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述4-10元杂环烷基和5-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中所述N和S任选被氧化;其中5-10元杂芳基和4-10元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R7的取代基取代;
每个R7独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、NO2、ORa12、SRa12、C(O)Rb12、C(O)NRc12Rd12、C(O)ORa12、OC(O)Rb12、OC(O)NRc12Rd12、NRc12Rd12、NRc12C(O)Rb12、NRc12C(O)ORa12、NRc12C(O)NRc12Rd12、C(=NRe12)Rb12、C(=NORa12)Rb12、C(=NRe12)NRc12Rd12、NRc12C(=NRe12)NRc12Rd12、NRc12S(O)Rb12、NRc12S(O)2Rb12、NRc12S(O)2NRc12Rd12、S(O)Rb12、S(O)NRc12Rd12、S(O)2Rb12、S(O)2NRc12Rd12和BRh12Ri12;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R8的取代基取代;
每个R8独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、ORa13、SRa13、C(O)Rb13、C(O)NRc13Rd13、C(O)ORa13、NRc13Rd13、NRc13C(O)Rb13、NRc13C(O)ORa13、NRc13S(O)Rb13、NRc13S(O)2Rb13、NRc13S(O)2NRc13Rd13、S(O)Rb13、S(O)NRc13Rd13、S(O)2Rb13S(O)2NRc13Rd13和BRh13Ri13;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R9的取代基取代;
每个R9独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-6环烷基、苯基、5-6元杂芳基、4-7元杂环烷基、卤代基、D、CN、ORa14、SRa14、C(O)Rb14、C(O)NRc14Rd14、C(O)ORa14、NRc14Rd14、NRc14C(O)Rb14、NRc14C(O)ORa14、NRc14S(O)Rb14、NRc14S(O)2Rb14、NRc14S(O)2NRc14Rd14、S(O)Rb14、S(O)NRc14Rd14、S(O)2Rb14和S(O)2NRc14Rd14;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-6环烷基、C6-10芳基、5-10元杂芳基和4-7元杂环烷基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个R10独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、NRc1C(O)NRc1Rd1、C(=NRe1)Rb1、C(=NORa1)Rb1、C(=NRe1)NRc1Rd1、NRc1C(=NRe1)NRc1Rd1、NRc1S(O)Rb1、NRc1S(O)2Rb1、NRc1S(O)2NRc1Rd1、S(O)Rb1、S(O)NRc1Rd1、S(O)2Rb1、S(O)2NRc1Rd1和BRh1Ri1;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R11的取代基取代;
每个R11独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、ORa2、SRa2、C(O)Rb2、C(O)NRc2Rd2、C(O)ORa2、NRc2Rd2、NRc2C(O)Rb2、NRc2C(O)ORa2、NRc2S(O)Rb2、NRc2S(O)2Rb2、NRc2S(O)2NRc2Rd2、S(O)Rb2、S(O)NRc2Rd2、S(O)2Rb2S(O)2NRc2Rd2和BRh2Ri2;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R12的取代基取代;
每个R12独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-6环烷基、苯基、5-6元杂芳基、4-7元杂环烷基、卤代基、D、CN、ORa3、SRa3、C(O)Rb3、C(O)NRc3Rd3、C(O)ORa3、NRc3Rd3、NRc3C(O)Rb3、NRc3C(O)ORa3、NRc3S(O)Rb3、NRc3S(O)2Rb3、NRc3S(O)2NRc3Rd3、S(O)Rb3、S(O)NRc3Rd3、S(O)2Rb3和S(O)2NRc3Rd3;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-6环烷基、C6-10芳基、5-10元杂芳基和4-7元杂环烷基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个R13独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、NO2、ORa5、SRa5、C(O)Rb5、C(O)NRc5Rd5、C(O)ORa5、OC(O)Rb5、OC(O)NRc5Rd5、NRc5Rd5、NRc5C(O)Rb5、NRc5C(O)ORa5、NRc5C(O)NRc5Rd5、C(=NRe5)Rb5、C(=NORa5)Rb5、C(=NRe5)NRc5Rd5、NRc5C(=NRe5)NRc5Rd5、NRc5S(O)Rb5、NRc5S(O)2Rb5、NRc5S(O)2NRc5Rd5、S(O)Rb5、S(O)NRc5Rd5、S(O)2Rb5、S(O)2NRc5Rd5和BRh5Ri5;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R14的取代基取代;
每个R14独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、ORa6、SRa6、C(O)Rb6、C(O)NRc6Rd6、C(O)ORa6、NRc6Rd6、NRc6C(O)Rb6、NRc6C(O)ORa6、NRc6S(O)Rb6、NRc6S(O)2Rb6、NRc6S(O)2NRc6Rd6、S(O)Rb6、S(O)NRc6Rd6、S(O)2Rb6S(O)2NRc6Rd6和BRh6Ri6;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R15的取代基取代;
每个R15独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-6环烷基、苯基、5-6元杂芳基、4-7元杂环烷基、卤代基、D、CN、ORa7、SRa7、C(O)Rb7、C(O)NRc7Rd7、C(O)ORa7、NRc7Rd7、NRc7C(O)Rb7、NRc7C(O)ORa7、NRc7S(O)Rb7、NRc7S(O)2Rb7、NRc7S(O)2NRc7Rd7、S(O)Rb7、S(O)NRc7Rd7、S(O)2Rb7和S(O)2NRc7Rd7;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-6环烷基、C6-10芳基、5-10元杂芳基和4-7元杂环烷基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Ra、Rc和Rd独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R10的取代基取代;
或者与同一N原子连接的任何Rc和Rd与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R10的取代基取代的4、5、6或7元杂环烷基;
每个Rb独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R10的取代基取代;
每个Re独立地选自H、CN、C1-6烷基、C1-6卤代烷基、C1-6烷硫基、C1-6烷基磺酰基、C1-6烷基羰基、C1-6烷基氨基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、氨基磺酰基、C1-6烷基氨基磺酰基和二(C1-6烷基)氨基磺酰基;
每个Rh和Ri独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh和Ri均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra1、Rc1和Rd1独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R11的取代基取代;
或者与同一N原子连接的任何Rc1和Rd1与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R11的取代基取代的4、5、6或7元杂环烷基;
每个Rb1独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R11的取代基取代;
每个Re1独立地选自H、CN、C1-6烷基、C1-6卤代烷基、C1-6烷硫基、C1-6烷基磺酰基、C1-6烷基羰基、C1-6烷基氨基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、氨基磺酰基、C1-6烷基氨基磺酰基和二(C1-6烷基)氨基磺酰基;
每个Rh1和Ri1独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh1和Ri1均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra2、Rc2和Rd2独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R12的取代基取代;
或者与同一N原子连接的任何Rc2和Rd2与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R12的取代基取代的4、5、6或7元杂环烷基;
每个Rb2独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R12的取代基取代;
每个Rh2和Ri2独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh2和Ri2均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra3、Rc3和Rd3独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Rb3独立地选自C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Ra4、Rc4和Rd4独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R13的取代基取代;
或者与同一N原子连接的任何Rc4和Rd4与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R13的取代基取代的4、5、6或7元杂环烷基;
每个Rb4独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R13的取代基取代;
每个Re4独立地选自H、CN、C1-6烷基、C1-6卤代烷基、C1-6烷硫基、C1-6烷基磺酰基、C1-6烷基羰基、C1-6烷基氨基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、氨基磺酰基、C1-6烷基氨基磺酰基和二(C1-6烷基)氨基磺酰基;
每个Rh4和Ri4独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh4和Ri4均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra5、Rc5和Rd5独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R14的取代基取代;
或者与同一N原子连接的任何Rc5和Rd5与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R14的取代基取代的4、5、6或7元杂环烷基;
每个Rb5独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R14的取代基取代;
每个Re5独立地选自H、CN、C1-6烷基、C1-6卤代烷基、C1-6烷硫基、C1-6烷基磺酰基、C1-6烷基羰基、C1-6烷基氨基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、氨基磺酰基、C1-6烷基氨基磺酰基和二(C1-6烷基)氨基磺酰基;
每个Rh5和Ri5独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh5和Ri5均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra6、Rc6和Rd6独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R15的取代基取代;
或者与同一N原子连接的任何Rc6和Rd6与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R15的取代基取代的4、5、6或7元杂环烷基;
每个Rb6独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R15的取代基取代;
每个Rh6和Ri6独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh6和Ri6均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra7、Rc7和Rd7独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Rb7独立地选自C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Ra8、Rc8和Rd8独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R5的取代基取代;
或者与同一N原子连接的任何Rc8和Rd8与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R5的取代基取代的4、5、6或7元杂环烷基;
每个Rb8独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R5的取代基取代;
每个Re8独立地选自H、CN、C1-6烷基、C1-6卤代烷基、C1-6烷硫基、C1-6烷基磺酰基、C1-6烷基羰基、C1-6烷基氨基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、氨基磺酰基、C1-6烷基氨基磺酰基和二(C1-6烷基)氨基磺酰基;
每个Rh8和Ri8独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh8和Ri8均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra9、Rc9和Rd9独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R6的取代基取代;
或者与同一N原子连接的任何Rc9和Rd9与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R6的取代基取代的4、5、6或7元杂环烷基;
每个Rb9独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R6的取代基取代;
每个Rh9和Ri9独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh9和Ri9均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra10、Rc10和Rd10独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Rb10独立地选自C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Ra11、Rc11和Rd11独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R7的取代基取代;
或者与同一N原子连接的任何Rc11和Rd11与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R7的取代基取代的4、5、6或7元杂环烷基;
每个Rb11独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R7的取代基取代;
每个Re11独立地选自H、CN、C1-6烷基、C1-6卤代烷基、C1-6烷硫基、C1-6烷基磺酰基、C1-6烷基羰基、C1-6烷基氨基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、氨基磺酰基、C1-6烷基氨基磺酰基和二(C1-6烷基)氨基磺酰基;
每个Rh11和Ri11独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh11和Ri11均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra12、Rc12和Rd12独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R8的取代基取代;
或者与同一N原子连接的任何Rc12和Rd12与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R8的取代基取代的4、5、6或7元杂环烷基;
每个Rb12独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R8的取代基取代;
每个Re12独立地选自H、CN、C1-6烷基、C1-6卤代烷基、C1-6烷硫基、C1-6烷基磺酰基、C1-6烷基羰基、C1-6烷基氨基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、氨基磺酰基、C1-6烷基氨基磺酰基和二(C1-6烷基)氨基磺酰基;
每个Rh12和Ri12独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh12和Ri12均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra13、Rc13和Rd13独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R9的取代基取代;
或者与同一N原子连接的任何Rc13和Rd13与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R9的取代基取代的4、5、6或7元杂环烷基;
每个Rb13独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R9的取代基取代;
每个Rh13和Ri13独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh13和Ri13均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra14、Rc14和Rd14独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Rb14独立地选自C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Ra15、Rc15和Rd15独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Ra16、Rc16和Rd16独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Rb16独立地选自C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Rh16和Ri16独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh16和Ri16均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;且
每个Rg独立地选自OH、NO2、CN、卤代基、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-6环烷基、C3-6环烷基-C1-2亚烷基、C1-6烷氧基、C1-6卤代烷氧基、C1-3烷氧基-C1-3烷基、C1-3烷氧基-C1-3烷氧基、HO-C1-3烷氧基、HO-C1-3烷基、氰基-C1-3烷基、H2N-C1-3烷基、氨基、C1-6烷基氨基、二(C1-6烷基)氨基、硫代基、C1-6烷硫基、C1-6烷基亚磺酰基、C1-6烷基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、羧基、C1-6烷基羰基、C1-6烷氧基羰基、C1-6烷基羰基氨基、C1-6烷基磺酰基氨基、氨基磺酰基、C1-6烷基氨基磺酰基、二(C1-6烷基)氨基磺酰基、氨基磺酰基氨基、C1-6烷基氨基磺酰基氨基、二(C1-6烷基)氨基磺酰基氨基、氨基羰基氨基、C1-6烷基氨基羰基氨基和二(C1-6烷基)氨基羰基氨基;并且
n是0、1、2、3或4。
2.一种式(I’)的化合物:
或其药学上可接受的盐,其中:
CyA是4-12元杂环烷基;其中所述4-12元杂环烷基具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中所述4-12元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述4-12元杂环烷基任选被1、2、3或4个独立地选自RA的取代基取代;
A是N或CR16;
R16选自H、D、C1-6烷基、卤代基、CN和ORa16;
R1选自H、D、卤代基、CN、C1-6烷基和ORa15;其中所述C1-6烷基任选被1、2或3个独立地选自Rg的取代基取代;
R2选自H、D、Cy2、C1-6烷基、C1-6卤代烷基、卤代基、CN;其中所述C1-6烷基任选被1、2、3或4个独立地选自R10的取代基取代;
Cy2选自4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述4-10元杂环烷基和5-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中5-10元杂芳基和4-10元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述4-10元杂环烷基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R10的取代基取代;
Z是N或CR3;
R3选自H、D、Cy3、卤代基和CN;
Cy3是6-10元杂芳基;其中所述6-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;
每个R4独立地选自C1-6烷基、C1-6卤代烷基、卤代基、D、CN和ORa8;
RA选自H、D、Cy1、C1-6烷基、C1-6卤代烷基、卤代基、CN、ORa11、C(O)NRc11Rd11和NRc11Rd11;其中所述C1-6烷基任选被1、2、3或4个独立地选自R7的取代基取代;
Cy1选自C3-10环烷基和5-10元杂芳基;其中所述5-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中5-10元杂芳基的成环碳原子任选被氧代基取代以形成羰基;且其中所述C3-10环烷基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R7的取代基取代;
每个R7独立地选自C1-6烷基、卤代基、D、CN、ORa12和NRc12Rd12;
每个R10独立地选自C1-6烷基、C1-6卤代烷基、4-10元杂环烷基、卤代基、D、CN、ORa1、C(O)NRc1Rd1和NRc1Rd1;其中所述C1-6烷基和4-10元杂环烷基各自任选被1、2、3或4个独立地选自R11的取代基取代;
每个R11独立地选自C1-6烷基、C1-6卤代烷基、卤代基、D、CN和ORa2;
每个Ra1、Rc1和Rd1独立地选自H、C1-6烷基、C1-6卤代烷基和C3-10环烷基;其中所述C1-6烷基和C3-10环烷基各自任选被1、2、3或4个独立地选自R11的取代基取代;
每个Ra2、Rc2和Rd2独立地选自H、C1-6烷基和C1-6卤代烷基;
每个Ra8、Rc8和Rd8独立地选自H、C1-6烷基和C1-6卤代烷基;
每个Ra11、Rc11和Rd11独立地选自H、C1-6烷基和C1-6卤代烷基;其中所述C1-6烷基任选被1、2、3或4个独立地选自R7的取代基取代;
每个Ra12、Rc12和Rd12独立地选自H、C1-6烷基和C1-6卤代烷基;
每个Ra15、Rc15和Rd15独立地选自H、C1-6烷基和C1-6卤代烷基;其中所述C1-6烷基任选被1、2、3或4个独立地选自Rg的取代基取代;
Ra16独立地选自H和C1-6烷基;
每个Rg独立地选自OH、CN、卤代基、C1-6烷基、C1-6卤代烷基、C1-6烷氧基、C1-6卤代烷氧基、氨基、C1-6烷硫基、C1-6烷基磺酰基;且
n是0、1、2或3。
3.一种式I的化合物:
或其药学上可接受的盐,其中:
CyA是C3-12环烷基或4-12元杂环烷基;其中所述4-12元杂环烷基具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中所述N和S任选被氧化;其中所述4-12元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述C3-12环烷基和4-12元杂环烷基各自任选被1、2、3或4个独立地选自RA的取代基取代;
A是N或CF;
R1选自H、D、卤代基、CN、C1-6烷基、ORa15和NRc15Rd15;其中所述C1-6烷基任选被1、2或3个独立地选自Rg的取代基取代;
R2选自H、D、Cy2、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、卤代基、CN、NO2、ORa、SRa、C(O)Rb、C(O)NRcRd、C(O)ORa、OC(O)Rb、OC(O)NRcRd、NRcRd、NRcC(O)Rb、NRcC(O)ORa、NRcC(O)NRcRd、C(=NRe)Rb、C(=NORa)Rb、C(=NRe)NRcRd、NRcC(=NRe)NRcRd、NRcS(O)Rb、NRcS(O)2Rb、NRcS(O)2NRcRd、S(O)Rb、S(O)NRcRd、S(O)2Rb、S(O)2NRcRd和BRhRi;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自R10的取代基取代;
Cy2选自C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述4-10元杂环烷基和5-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中所述N和S任选被氧化;其中5-10元杂芳基和4-10元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R10的取代基取代;
R3选自H、D、Cy3、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、卤代基、CN、NO2、ORa4、SRa4、C(O)Rb4、C(O)NRc4Rd4、C(O)ORa4、OC(O)Rb4、OC(O)NRc4Rd4、NRc4Rd4、NRc4C(O)Rb4、NRc4C(O)ORa4、NRc4C(O)NRc4Rd4、C(=NRe4)Rb4、C(=NORa4)Rb4、C(=NRe4)NRc4Rd4、NRc4C(=NRe4)NRc4Rd4、NRc4S(O)Rb4、NRc4S(O)2Rb4、NRc4S(O)2NRc4Rd4、S(O)Rb4、S(O)NRc4Rd4、S(O)2Rb4、S(O)2NRc4Rd4和BRh4Ri4;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自R13的取代基取代;
Cy3选自C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述4-10元杂环烷基和5-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中所述N和S任选被氧化;其中5-10元杂芳基和4-10元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R13的取代基取代;
每个R4独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、NO2、ORa8、SRa8、C(O)Rb8、C(O)NRc8Rd8、C(O)ORa8、OC(O)Rb8、OC(O)NRc8Rd8、NRc8Rd8、NRc8C(O)Rb8、NRc8C(O)ORa8、NRc8C(O)NRc8Rd8、C(=NRe8)Rb8、C(=NORa8)Rb8、C(=NRe8)NRc8Rd8、NRc8C(=NRe8)NRc8Rd8、NRc8S(O)Rb8、NRc8S(O)2Rb8、NRc8S(O)2NRc8Rd8、S(O)Rb8、S(O)NRc8Rd8、S(O)2Rb8、S(O)2NRc8Rd8和BRh8Ri8;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R5的取代基取代;
每个R5独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、ORa9、SRa9、C(O)Rb9、C(O)NRc9Rd9、C(O)ORa9、NRc9Rd9、NRc9C(O)Rb9、NRc9C(O)ORa9、NRc9S(O)Rb9、NRc9S(O)2Rb9、NRc9S(O)2NRc9Rd9、S(O)Rb9、S(O)NRc9Rd9、S(O)2Rb9、S(O)2NRc9Rd9和BRh9Ri9;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R6的取代基取代;
每个R6独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-6环烷基、苯基、5-6元杂芳基、4-7元杂环烷基、卤代基、D、CN、ORa10、SRa10、C(O)Rb10、C(O)NRc10Rd10、C(O)ORa10、NRc10Rd10、NRc10C(O)Rb10、NRc10C(O)ORa10、NRc10S(O)Rb10、NRc10S(O)2Rb10、NRc10S(O)2NRc10Rd10、S(O)Rb10、S(O)NRc10Rd10、S(O)2Rb10和S(O)2NRc10Rd10;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-6环烷基、苯基、5-6元杂芳基和4-7元杂环烷基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
RA选自H、D、Cy1、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、卤代基、CN、NO2、ORa11、SRa11、C(O)Rb11、C(O)NRc11Rd11、C(O)ORa11、OC(O)Rb11、OC(O)NRc11Rd11、NRc11Rd11、NRc11C(O)Rb11、NRc11C(O)ORa11、NRc11C(O)NRc11Rd11、C(=NRe11)Rb11、C(=NORa11)Rb11、C(=NRe11)NRc11Rd11、NRc11C(=NRe11)NRc11Rd11、NRc11S(O)Rb11、NRc11S(O)2Rb11、NRc11S(O)2NRc11Rd11、S(O)Rb11、S(O)NRc11Rd11、S(O)2Rb11、S(O)2NRc11Rd11和BRh11Ri11;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自R7的取代基取代;
Cy1选自C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述4-10元杂环烷基和5-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中所述N和S任选被氧化;其中5-10元杂芳基和4-10元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R7的取代基取代;
每个R7独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、NO2、ORa12、SRa12、C(O)Rb12、C(O)NRc12Rd12、C(O)ORa12、OC(O)Rb12、OC(O)NRc12Rd12、NRc12Rd12、NRc12C(O)Rb12、NRc12C(O)ORa12、NRc12C(O)NRc12Rd12、C(=NRe12)Rb12、C(=NORa12)Rb12、C(=NRe12)NRc12Rd12、NRc12C(=NRe12)NRc12Rd12、NRc12S(O)Rb12、NRc12S(O)2Rb12、NRc12S(O)2NRc12Rd12、S(O)Rb12、S(O)NRc12Rd12、S(O)2Rb12、S(O)2NRc12Rd12和BRh12Ri12;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R8的取代基取代;
每个R8独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、ORa13、SRa13、C(O)Rb13、C(O)NRc13Rd13、C(O)ORa13、NRc13Rd13、NRc13C(O)Rb13、NRc13C(O)ORa13、NRc13S(O)Rb13、NRc13S(O)2Rb13、NRc13S(O)2NRc13Rd13、S(O)Rb13、S(O)NRc13Rd13、S(O)2Rb13S(O)2NRc13Rd13和BRh13Ri13;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R9的取代基取代;
每个R9独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-6环烷基、苯基、5-6元杂芳基、4-7元杂环烷基、卤代基、D、CN、ORa14、SRa14、C(O)Rb14、C(O)NRc14Rd14、C(O)ORa14、NRc14Rd14、NRc14C(O)Rb14、NRc14C(O)ORa14、NRc14S(O)Rb14、NRc14S(O)2Rb14、NRc14S(O)2NRc14Rd14、S(O)Rb14、S(O)NRc14Rd14、S(O)2Rb14和S(O)2NRc14Rd14;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-6环烷基、C6-10芳基、5-10元杂芳基和4-7元杂环烷基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个R10独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、NRc1C(O)NRc1Rd1、C(=NRe1)Rb1、C(=NORa1)Rb1、C(=NRe1)NRc1Rd1、NRc1C(=NRe1)NRc1Rd1、NRc1S(O)Rb1、NRc1S(O)2Rb1、NRc1S(O)2NRc1Rd1、S(O)Rb1、S(O)NRc1Rd1、S(O)2Rb1、S(O)2NRc1Rd1和BRh1Ri1;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R11的取代基取代;
每个R11独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、ORa2、SRa2、C(O)Rb2、C(O)NRc2Rd2、C(O)ORa2、NRc2Rd2、NRc2C(O)Rb2、NRc2C(O)ORa2、NRc2S(O)Rb2、NRc2S(O)2Rb2、NRc2S(O)2NRc2Rd2、S(O)Rb2、S(O)NRc2Rd2、S(O)2Rb2S(O)2NRc2Rd2和BRh2Ri2;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R12的取代基取代;
每个R12独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-6环烷基、苯基、5-6元杂芳基、4-7元杂环烷基、卤代基、D、CN、ORa3、SRa3、C(O)Rb3、C(O)NRc3Rd3、C(O)ORa3、NRc3Rd3、NRc3C(O)Rb3、NRc3C(O)ORa3、NRc3S(O)Rb3、NRc3S(O)2Rb3、NRc3S(O)2NRc3Rd3、S(O)Rb3、S(O)NRc3Rd3、S(O)2Rb3和S(O)2NRc3Rd3;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-6环烷基、C6-10芳基、5-10元杂芳基和4-7元杂环烷基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个R13独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、NO2、ORa5、SRa5、C(O)Rb5、C(O)NRc5Rd5、C(O)ORa5、OC(O)Rb5、OC(O)NRc5Rd5、NRc5Rd5、NRc5C(O)Rb5、NRc5C(O)ORa5、NRc5C(O)NRc5Rd5、C(=NRe5)Rb5、C(=NORa5)Rb5、C(=NRe5)NRc5Rd5、NRc5C(=NRe5)NRc5Rd5、NRc5S(O)Rb5、NRc5S(O)2Rb5、NRc5S(O)2NRc5Rd5、S(O)Rb5、S(O)NRc5Rd5、S(O)2Rb5、S(O)2NRc5Rd5和BRh5Ri5;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R14的取代基取代;
每个R14独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基、5-10元杂芳基-C1-3亚烷基、卤代基、D、CN、ORa6、SRa6、C(O)Rb6、C(O)NRc6Rd6、C(O)ORa6、NRc6Rd6、NRc6C(O)Rb6、NRc6C(O)ORa6、NRc6S(O)Rb6、NRc6S(O)2Rb6、NRc6S(O)2NRc6Rd6、S(O)Rb6、S(O)NRc6Rd6、S(O)2Rb6S(O)2NRc6Rd6和BRh6Ri6;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基、5-10元杂芳基、C3-10环烷基-C1-3亚烷基、4-10元杂环烷基-C1-3亚烷基、C6-10芳基-C1-3亚烷基和5-10元杂芳基-C1-3亚烷基各自任选被1、2、3或4个独立地选自R15的取代基取代;
每个R15独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-6环烷基、苯基、5-6元杂芳基、4-7元杂环烷基、卤代基、D、CN、ORa7、SRa7、C(O)Rb7、C(O)NRc7Rd7、C(O)ORa7、NRc7Rd7、NRc7C(O)Rb7、NRc7C(O)ORa7、NRc7S(O)Rb7、NRc7S(O)2Rb7、NRc7S(O)2NRc7Rd7、S(O)Rb7、S(O)NRc7Rd7、S(O)2Rb7和S(O)2NRc7Rd7;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-6环烷基、C6-10芳基、5-10元杂芳基和4-7元杂环烷基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Ra、Rc和Rd独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R10的取代基取代;
或者与同一N原子连接的任何Rc和Rd与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R10的取代基取代的4、5、6或7元杂环烷基;
每个Rb独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R10的取代基取代;
每个Re独立地选自H、CN、C1-6烷基、C1-6卤代烷基、C1-6烷硫基、C1-6烷基磺酰基、C1-6烷基羰基、C1-6烷基氨基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、氨基磺酰基、C1-6烷基氨基磺酰基和二(C1-6烷基)氨基磺酰基;
每个Rh和Ri独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh和Ri均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra1、Rc1和Rd1独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R11的取代基取代;
或者与同一N原子连接的任何Rc1和Rd1与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R11的取代基取代的4、5、6或7元杂环烷基;
每个Rb1独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R11的取代基取代;
每个Re1独立地选自H、CN、C1-6烷基、C1-6卤代烷基、C1-6烷硫基、C1-6烷基磺酰基、C1-6烷基羰基、C1-6烷基氨基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、氨基磺酰基、C1-6烷基氨基磺酰基和二(C1-6烷基)氨基磺酰基;
每个Rh1和Ri1独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh1和Ri1均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra2、Rc2和Rd2独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R12的取代基取代;
或者与同一N原子连接的任何Rc2和Rd2与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R12的取代基取代的4、5、6或7元杂环烷基;
每个Rb2独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R12的取代基取代;
每个Rh2和Ri2独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh2和Ri2均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra3、Rc3和Rd3独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Rb3独立地选自C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Ra4、Rc4和Rd4独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R13的取代基取代;
或者与同一N原子连接的任何Rc4和Rd4与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R13的取代基取代的4、5、6或7元杂环烷基;
每个Rb4独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R13的取代基取代;
每个Re4独立地选自H、CN、C1-6烷基、C1-6卤代烷基、C1-6烷硫基、C1-6烷基磺酰基、C1-6烷基羰基、C1-6烷基氨基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、氨基磺酰基、C1-6烷基氨基磺酰基和二(C1-6烷基)氨基磺酰基;
每个Rh4和Ri4独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh4和Ri4均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra5、Rc5和Rd5独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R14的取代基取代;
或者与同一N原子连接的任何Rc5和Rd5与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R14的取代基取代的4、5、6或7元杂环烷基;
每个Rb5独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R14的取代基取代;
每个Re5独立地选自H、CN、C1-6烷基、C1-6卤代烷基、C1-6烷硫基、C1-6烷基磺酰基、C1-6烷基羰基、C1-6烷基氨基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、氨基磺酰基、C1-6烷基氨基磺酰基和二(C1-6烷基)氨基磺酰基;
每个Rh5和Ri5独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh5和Ri5均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra6、Rc6和Rd6独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R15的取代基取代;
或者与同一N原子连接的任何Rc6和Rd6与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R15的取代基取代的4、5、6或7元杂环烷基;
每个Rb6独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R15的取代基取代;
每个Rh6和Ri6独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh6和Ri6均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra7、Rc7和Rd7独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Rb7独立地选自C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Ra8、Rc8和Rd8独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R5的取代基取代;
或者与同一N原子连接的任何Rc8和Rd8与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R5的取代基取代的4、5、6或7元杂环烷基;
每个Rb8独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R5的取代基取代;
每个Re8独立地选自H、CN、C1-6烷基、C1-6卤代烷基、C1-6烷硫基、C1-6烷基磺酰基、C1-6烷基羰基、C1-6烷基氨基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、氨基磺酰基、C1-6烷基氨基磺酰基和二(C1-6烷基)氨基磺酰基;
每个Rh8和Ri8独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh8和Ri8均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra9、Rc9和Rd9独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R6的取代基取代;
或者与同一N原子连接的任何Rc9和Rd9与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R6的取代基取代的4、5、6或7元杂环烷基;
每个Rb9独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R6的取代基取代;
每个Rh9和Ri9独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh9和Ri9均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra10、Rc10和Rd10独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Rb10独立地选自C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Ra11、Rc11和Rd11独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R7的取代基取代;
或者与同一N原子连接的任何Rc11和Rd11与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R7的取代基取代的4、5、6或7元杂环烷基;
每个Rb11独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R7的取代基取代;
每个Re11独立地选自H、CN、C1-6烷基、C1-6卤代烷基、C1-6烷硫基、C1-6烷基磺酰基、C1-6烷基羰基、C1-6烷基氨基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、氨基磺酰基、C1-6烷基氨基磺酰基和二(C1-6烷基)氨基磺酰基;
每个Rh11和Ri11独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh11和Ri11均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra12、Rc12和Rd12独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R8的取代基取代;
或者与同一N原子连接的任何Rc12和Rd12与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R8的取代基取代的4、5、6或7元杂环烷基;
每个Rb12独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R8的取代基取代;
每个Re12独立地选自H、CN、C1-6烷基、C1-6卤代烷基、C1-6烷硫基、C1-6烷基磺酰基、C1-6烷基羰基、C1-6烷基氨基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、氨基磺酰基、C1-6烷基氨基磺酰基和二(C1-6烷基)氨基磺酰基;
每个Rh12和Ri12独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh12和Ri12均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra13、Rc13和Rd13独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R9的取代基取代;
或者与同一N原子连接的任何Rc13和Rd13与它们所连接的N原子一起形成任选被1、2、3或4个独立地选自R9的取代基取代的4、5、6或7元杂环烷基;
每个Rb13独立地选自C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基;其中所述C1-6烷基、C2-6烯基、C2-6炔基、C3-10环烷基、4-10元杂环烷基、C6-10芳基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R9的取代基取代;
每个Rh13和Ri13独立地选自OH和C1-6烷氧基;
或者与同一B原子连接的任何Rh13和Ri13均为C2-3二烷氧基,并与它们所连接的B原子一起形成任选被1、2、3或4个独立地选自C1-6烷基的取代基取代的5或6元杂环烷基;
每个Ra14、Rc14和Rd14独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Rb14独立地选自C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Ra15、Rc15和Rd15独立地选自H、C1-6烷基、C2-6烯基、C2-6炔基和C1-6卤代烷基;其中所述C1-6烷基、C2-6烯基和C2-6炔基各自任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Rg独立地选自OH、NO2、CN、卤代基、C1-6烷基、C2-6烯基、C2-6炔基、C1-6卤代烷基、C3-6环烷基、C3-6环烷基-C1-2亚烷基、C1-6烷氧基、C1-6卤代烷氧基、C1-3烷氧基-C1-3烷基、C1-3烷氧基-C1-3烷氧基、HO-C1-3烷氧基、HO-C1-3烷基、氰基-C1-3烷基、H2N-C1-3烷基、氨基、C1-6烷基氨基、二(C1-6烷基)氨基、硫代基、C1-6烷硫基、C1-6烷基亚磺酰基、C1-6烷基磺酰基、氨甲酰基、C1-6烷基氨甲酰基、二(C1-6烷基)氨甲酰基、羧基、C1-6烷基羰基、C1-6烷氧基羰基、C1-6烷基羰基氨基、C1-6烷基磺酰基氨基、氨基磺酰基、C1-6烷基氨基磺酰基、二(C1-6烷基)氨基磺酰基、氨基磺酰基氨基、C1-6烷基氨基磺酰基氨基、二(C1-6烷基)氨基磺酰基氨基、氨基羰基氨基、C1-6烷基氨基羰基氨基和二(C1-6烷基)氨基羰基氨基;且
n是0、1、2、3或4。
4.一种式I的化合物:
或其药学上可接受的盐,其中:
CyA是4-12元杂环烷基;其中所述4-12元杂环烷基具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中所述4-12元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述4-12元杂环烷基任选被1、2、3或4个独立地选自RA的取代基取代;
A是N;
R1选自H、D、卤代基、CN、C1-6烷基和ORa15;其中所述C1-6烷基任选被1、2或3个独立地选自Rg的取代基取代;
R2选自H、D、Cy2、C1-6烷基、C1-6卤代烷基、卤代基、CN;其中所述C1-6烷基任选被1、2、3或4个独立地选自R10的取代基取代;
Cy2选自4-10元杂环烷基和5-10元杂芳基;其中所述4-10元杂环烷基和5-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中5-10元杂芳基和4-10元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述4-10元杂环烷基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R10的取代基取代;
R3选自H、D、Cy3、卤代基和CN;
Cy3是5-10元杂芳基;其中所述5-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中5-10元杂芳基的成环碳原子任选被氧代基取代以形成羰基;且其中所述5-10元杂芳基任选被1、2、3或4个独立地选自R13的取代基取代;
每个R4独立地选自C1-6烷基、C1-6卤代烷基、卤代基、D、CN和ORa8;其中所述C1-6烷基任选被1、2、3或4个独立地选自R5的取代基取代;
每个R5独立地选自C1-6烷基、C1-6卤代烷基、卤代基、D、CN、ORa9和NRc9Rd9;
RA选自H、D、Cy1、C1-6烷基、C1-6卤代烷基、卤代基、CN、ORa11、C(O)NRc11Rd11和NRc11Rd11;其中所述C1-6烷基任选被1、2、3或4个独立地选自R7的取代基取代;
Cy1是5-10元杂芳基;其中所述5-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中5-10元杂芳基的成环碳原子任选被氧代基取代以形成羰基;且其中所述5-10元杂芳基各自任选被1、2、3或4个独立地选自R7的取代基取代;
每个R7独立地选自C1-6烷基、卤代基、D、CN、ORa12和NRc12Rd12;
每个R10独立地选自C1-6烷基、C1-6卤代烷基、4-10元杂环烷基、卤代基、D、CN、ORa1、C(O)NRc1Rd1和NRc1Rd1;其中所述C1-6烷基和4-10元杂环烷基各自任选被1、2、3或4个独立地选自R11的取代基取代;
每个R11独立地选自C1-6烷基、C1-6卤代烷基、卤代基、D、CN和ORa2;
每个R13独立地选自C1-6烷基和C1-6卤代烷基;
每个Ra1、Rc1和Rd1独立地选自H、C1-6烷基、C1-6卤代烷基和
C3-10环烷基;其中所述C1-6烷基和C3-10环烷基各自任选被1、2、3或4个独立地选自R11的取代基取代;
每个Ra2、Rc2和Rd2独立地选自H、C1-6烷基和C1-6卤代烷基;
每个Ra8、Rc8和Rd8独立地选自H、C1-6烷基和C1-6卤代烷基;
每个Ra9、Rc9和Rd9独立地选自H、C1-6烷基和C1-6卤代烷基;
每个Ra11、Rc11和Rd11独立地选自H、C1-6烷基和C1-6卤代烷基;其中所述C1-6烷基任选被1、2、3或4个独立地选自R7的取代基取代;
每个Ra12、Rc12和Rd12独立地选自H、C1-6烷基和C1-6卤代烷基;
每个Ra15、Rc15和Rd15独立地选自H、C1-6烷基和C1-6卤代烷基;其中所述C1-6烷基任选被1、2、3或4个独立地选自Rg的取代基取代;
每个Rg独立地选自OH、CN、卤代基、C1-6烷基、C1-6卤代烷基、C1-6烷氧基、C1-6卤代烷氧基、氨基、C1-6烷硫基、C1-6烷基磺酰基;且
n是0、1、2或3。
5.如权利要求1和3中任一项所述的化合物或其药学上可接受的盐,其中CyA是4-12元杂环烷基;其中所述4-12元杂环烷基具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中所述4-12元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述4-12元杂环烷基任选被1、2、3或4个独立地选自RA的取代基取代。
6.如权利要求1和3中任一项所述的化合物或其药学上可接受的盐,其中CyA是C3-10环烷基,其中所述C3-10环烷基任选被1、2或3个独立地选自RA的取代基取代。
7.如权利要求1-6中任一项所述的化合物或其药学上可接受的盐,其中每个RA独立地选自Cy1、C1-6烷基、ORa11、C(O)NRc11Rd11和NRc11Rd11;其中所述C1-6烷基任选被1、2、3或4个独立地选自R7的取代基取代。
8.如权利要求1-6中任一项所述的化合物或其药学上可接受的盐,其中每个RA独立地为C1-6烷基;其中所述C1-6烷基任选被1、2、3或4个独立地选自R7的取代基取代。
9.如权利要求1-6中任一项所述的化合物或其药学上可接受的盐,其中每个RA独立地选自甲基和乙基;其中所述甲基和乙基各自任选被1、2或3个独立地选自R7的取代基取代。
10.如权利要求1-6中任一项所述的化合物或其药学上可接受的盐,其中每个RA独立地选自OH、NH2、氨甲基、羟甲基、甲氧基甲基、吡啶基、乙基、羟乙基和丙基氨甲酰基。
11.如权利要求1-6中任一项所述的化合物或其药学上可接受的盐,其中每个RA独立地为Cy1。
12.如权利要求1-7和11中任一项所述的化合物或其药学上可接受的盐,其中Cy1选自C3-10环烷基和5-10元杂芳基;其中所述5-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中所述N和S任选被氧化;其中5-10元杂芳基的成环碳原子任选被氧代基取代以形成羰基;且其中所述C3-10环烷基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R7的取代基取代。
13.如权利要求1-7和11中任一项所述的化合物或其药学上可接受的盐,其中Cy1选自任选被1、2、3或4个独立地选自R7的取代基取代的C3-10环烷基。
14.如权利要求1-7和11中任一项所述的化合物或其药学上可接受的盐,其中Cy1是5-10元杂芳基;其中所述5-10元杂芳基具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;且其中所述5-10元杂芳基任选被1、2、3或4个独立地选自R7的取代基取代。
15.如权利要求1-7和11中任一项所述的化合物或其药学上可接受的盐,其中Cy1是吡啶基。
16.如权利要求1-7和11中任一项所述的化合物或其药学上可接受的盐,其中Cy1是环丙基。
17.如权利要求1-9和11-14中任一项所述的化合物或其药学上可接受的盐,其中每个R7独立地选自C1-6烷基、卤代基、D、CN、ORa12和NRc12Rd12。
18.如权利要求1-9和11-14中任一项所述的化合物或其药学上可接受的盐,其中每个R7独立地选自CN、ORa12、NRc12Rd12和D。
19.如权利要求1-9和11-14中任一项所述的化合物或其药学上可接受的盐,其中每个R7独立地选自D、CN、OH、NH2和甲氧基。
20.如权利要求1-9、11-14、17和18中任一项所述的化合物或其药学上可接受的盐,其中Ra12是H。
21.如权利要求1-9、11-14、17和18中任一项所述的化合物或其药学上可接受的盐,其中Rc12和Rd12各自是H。
22.如权利要求1-4中任一项所述的化合物或其药学上可接受的盐,其中CyA选自2,5-二氮杂双环[2.2.1]庚-2-基;3-氨基吡咯烷-1-基;2-(氨甲基)吡咯烷-1-基;2-(羟甲基)吡咯烷-1-基;2-(甲氧基甲基)吡咯烷-1-基;4-氨基-2-(羟甲基)吡咯烷-1-基;4-羟基-2-甲基吡咯烷-1-基;2-(吡啶-2-基)吡咯烷-1-基;六氢吡咯并[3,4-b]吡咯-1(2H)-基;2-甲基哌嗪-1-基;2-(羟甲基)哌嗪-1-基;3-(羟甲基)吗啉代;5-乙基-2,5-二氮杂双环[2.2.1]庚-2-基;(2-羟乙基)-2,5-二氮杂双环[2.2.1]庚-2-基);5-(丙基氨甲酰基)-2,5-二氮杂双环[2.2.1]庚-2-基;4-羟基-2-(羟甲基)吡咯烷-1-基;2-(羟甲基)-5-甲基哌嗪-1-基;6-(羟甲基)-4,7-二氮杂螺[2.5]辛-7-基;4-氨基-2-(1-羟基环丙基)吡咯烷-1-基;4-氨基-2-(2-羟基丙-2-基)吡咯烷-1-基;4-氨基-2-(羟甲基-d2)吡咯烷-1-基;3-(羟甲基)-2,5-二氮杂双环[2.2.1]庚-2-基;4-氨基-2-甲基哌啶-1-基;哌啶-4-基;4-(二甲氨基)-2-(羟甲基)吡咯烷-1-基;2-(羟甲基)-4-(异丙基氨基)吡咯烷-1-基;4-(羟甲基)-5-甲基-2,5-二氮杂双环[2.2.1]庚-2-基;2-(羟甲基)吗啉代;2-(2-((二甲氨基)甲基)吗啉代;2-(氰甲基)吗啉代;3-氧代四氢-3H-噁唑并[3,4-a]吡嗪-7(1H)-基;3-(羟甲基)哌嗪-1-基;3-(甲氧基甲基)氮杂环丁-1-基;2-(羟甲基)氮杂环丁-1-基;2-((二甲氨基)甲基)氮杂环丁-1-基;4-甲基哌嗪-1-基;和4-(2-羟乙基)哌嗪-1-基。
23.如权利要求1-4中任一项所述的化合物或其药学上可接受的盐,其中CyA选自2,5-二氮杂双环[2.2.1]庚-2-基;3-氨基吡咯烷-1-基;2-(氨甲基)吡咯烷-1-基;2-(羟甲基)吡咯烷-1-基;2-(甲氧基甲基)吡咯烷-1-基;4-氨基-2-(羟甲基)吡咯烷-1-基;4-羟基-2-甲基吡咯烷-1-基;2-(吡啶-2-基)吡咯烷-1-基;六氢吡咯并[3,4-b]吡咯-1(2H)-基;2-甲基哌嗪-1-基;2-(羟甲基)哌嗪-1-基;3-(羟甲基)吗啉代;5-乙基-2,5-二氮杂双环[2.2.1]庚-2-基;(2-羟乙基)-2,5-二氮杂双环[2.2.1]庚-2-基);和5-(丙基氨甲酰基)-2,5-二氮杂双环[2.2.1]庚-2-基。
24.如权利要求1-4中任一项所述的化合物或其药学上可接受的盐,其中CyA是4-氨基-2-(羟甲基)吡咯烷-1-基。
25.如权利要求1和3中任一项所述的化合物,其中CyA选自环戊基和环己基,其中所述环戊基和环己基任选被NH2取代。
26.如权利要求1-25中任一项所述的化合物或其药学上可接受的盐,其中R1选自H、D、卤代基、CN、C1-6烷基和ORa15;其中所述C1-6烷基任选被1、2或3个独立地选自Rg的取代基取代。
27.如权利要求1-25中任一项所述的化合物或其药学上可接受的盐,其中R1选自H、D、F、CN、甲基、羟甲基和甲氧基。
28.如权利要求1-25中任一项所述的化合物或其药学上可接受的盐,其中R1是H。
29.如权利要求1-26中任一项所述的化合物或其药学上可接受的盐,其中R1是F。
30.如权利要求1-29中任一项所述的化合物或其药学上可接受的盐,其中R2选自H、D、Cy2、C1-6烷基、卤代基和S(O)2Rb;其中所述C1-6烷基任选被1、2、3或4个独立地选自R10的取代基取代。
31.如权利要求1-30中任一项所述的化合物或其药学上可接受的盐,其中R2选自异丙基、F、Cl、Br和S(O)2CH3。
32.如权利要求1-30中任一项所述的化合物或其药学上可接受的盐,其中R2是Cy2。
33.如权利要求1-30和32中任一项所述的化合物或其药学上可接受的盐,其中Cy2选自4-10元杂环烷基和5-10元杂芳基;其中所述4-10元杂环烷基和5-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中5-10元杂芳基和4-10元杂环烷基的成环碳原子任选被氧代基取代以形成羰基;且其中所述4-10元杂环烷基和5-10元杂芳基各自任选被1、2、3或4个独立地选自R10的取代基取代。
34.如权利要求1-30和32中任一项所述的化合物或其药学上可接受的盐,其中Cy2是任选被1、2、3或4个独立地选自R10的取代基取代的C6-10芳基。
35.如权利要求1-30和32-34中任一项所述的化合物或其药学上可接受的盐,其中每个R10独立地选自C1-6烷基、4-10元杂环烷基、卤代基、CN、OH、ORa1、C(O)NRc1Rd1和NRc1Rd1;其中所述C1-6烷基和4-10元杂环烷基各自任选被1、2、3或4个独立地选自R11的取代基取代。
36.如权利要求1-30和32-34中任一项所述的化合物或其药学上可接受的盐,其中每个R10独立地选自OH、F、CN、甲基、羟甲基、甲基氨甲酰基、甲氧基、吗啉代和环丁基氨基。
37.如权利要求1-30和32-35中任一项所述的化合物或其药学上可接受的盐,其中每个Ra1、Rc1和Rd1独立地选自H、C1-6烷基和C3-10环烷基;其中所述C1-6烷基和C3-10环烷基各自任选被1、2、3或4个独立地选自R11的取代基取代。
38.如权利要求1-30、32-35和37中任一项所述的化合物或其药学上可接受的盐,其中每个R11是ORa2。
39.如权利要求1-30、32-35、37和38中任一项所述的化合物或其药学上可接受的盐,其中每个R11是OH。
40.如权利要求1-29中任一项所述的化合物或其药学上可接受的盐,其中Cy2选自1-甲基-1H-吡唑-4-基;6-(羟甲基)吡啶-3-基;6-(甲基氨甲酰基)吡啶-3-基;1-甲基-6-氧代-1,6-二氢吡啶-3-基;2-甲基吡啶-3-基;4-甲氧基吡啶-3-基;4-氰基吡啶-3-基;1,3,5-三甲基-1H-吡唑-4-基;吗啉代;氮杂环丁-1-基;2-(甲氧基甲基)氮杂环丁-1-基);3-氰基吡啶-4-基;3-甲氧基吡啶-4-基;2-氰基-6-氟苯基;3-氰基吡啶-2-基;4-氰基-1-甲基-1H-吡唑-5-基;四氢-2H-吡喃-4-基;5-氰基-2-(吡咯烷-1-基)吡啶-4-基;和1-氰基环丙基。
41.如权利要求1-29中任一项所述的化合物或其药学上可接受的盐,其中Cy2选自1-甲基-1H-吡唑-4-基;6-(羟甲基)吡啶-3-基;6-(甲基氨甲酰基)吡啶-3-基;1-甲基-6-氧代-1,6-二氢吡啶-3-基;2-甲基吡啶-3-基;4-甲氧基吡啶-3-基;4-氰基吡啶-3-基;1,3,5-三甲基-1H-吡唑-4-基;吗啉代;和氮杂环丁-1-基。
42.如权利要求1-29中任一项所述的化合物或其药学上可接受的盐,其中Cy2选自3-氰基吡啶-4-基;4-氰基吡啶-3-基;和3-氰基吡啶-2-基。
43.如权利要求1和2中任一项所述的化合物或其药学上可接受的盐,其中Z是CR3。
44.如权利要求1和2中任一项所述的化合物或其药学上可接受的盐,其中Z是N。
45.如权利要求1-43中任一项所述的化合物或其药学上可接受的盐,其中R3选自H、D、Cy3、卤代基和CN。
46.如权利要求1-43中任一项所述的化合物或其药学上可接受的盐,其中R3选自H、D、F、Br和CN。
47.如权利要求1-43中任一项所述的化合物或其药学上可接受的盐,其中R3是H。
48.如权利要求1-43中任一项所述的化合物或其药学上可接受的盐,其中R3是Cy3。
49.如权利要求1-43、45和48中任一项所述的化合物或其药学上可接受的盐,其中Cy3是5-10元杂芳基;其中所述5-10元杂芳基各自具有至少一个成环碳原子和1、2、3或4个独立地选自N、O和S的成环杂原子;其中5-10元杂芳基的成环碳原子任选被氧代基取代以形成羰基;且其中所述5-10元杂芳基任选被1、2、3或4个独立地选自R13的取代基取代。
50.如权利要求1-43、45、48和49中任一项所述的化合物或其药学上可接受的盐,其中每个R13独立地为C1-6烷基。
51.如权利要求1-43、45和49中任一项所述的化合物或其药学上可接受的盐,其中R13是甲基。
52.如权利要求1-43和45中任一项所述的化合物或其药学上可接受的盐,其中Cy3选自吡啶-3-基和1-甲基-1H-吡唑-4-基。
53.如权利要求1-52中任一项所述的化合物或其药学上可接受的盐,其中每个R4独立地选自C1-6烷基、C1-6卤代烷基、C3-10环烷基、卤代基、D、CN和ORa8;其中所述C1-6烷基任选被1、2、3或4个独立地选自R5的取代基取代。
54.如权利要求1-52中任一项所述的化合物或其药学上可接受的盐,其中每个R4独立地选自C1-6烷基、C1-6卤代烷基、卤代基、D、CN和ORa8。
55.如权利要求1-52中任一项所述的化合物或其药学上可接受的盐,其中每个R4独立地选自卤代基和ORa8。
56.如权利要求1-52中任一项所述的化合物或其药学上可接受的盐,其中每个R4独立地选自卤代基。
57.如权利要求1-52中任一项所述的化合物或其药学上可接受的盐,其中每个R4独立地选自F和Cl。
58.如权利要求1-52中任一项所述的化合物或其药学上可接受的盐,其中每个R4独立地选自F和甲氧基。
59.如权利要求1-52中任一项所述的化合物或其药学上可接受的盐,其中每个R4独立地选自F和甲基。
60.如权利要求1-52中任一项所述的化合物或其药学上可接受的盐,其中每个R4是F。
61.如权利要求1-55中任一项所述的化合物或其药学上可接受的盐,其中每个R5独立地选自C1-6烷基、C1-6卤代烷基、卤代基、D、CN、ORa9和NRc9Rd9。
62.如权利要求1-55中任一项所述的化合物或其药学上可接受的盐,其中每个R5独立地选自D和F。
63.如权利要求1-30和32-38中任一项所述的化合物或其药学上可接受的盐,其中每个Ra2、Rc2和Rd2独立地为H。
64.如权利要求1-53中任一项所述的化合物或其药学上可接受的盐,其中每个Ra8、Rc8和Rd8独立地选自H、C1-6烷基和C1-6卤代烷基。
65.如权利要求1-7中任一项所述的化合物或其药学上可接受的盐,其中每个Ra11、Rc11和Rd11独立地选自H和C1-6烷基;其中所述C1-6烷基任选被1、2、3或4个独立地选自R7的取代基取代。
66.如权利要求1-26中任一项所述的化合物或其药学上可接受的盐,其中每个Ra15、Rc15和Rd15独立地选自H和C1-6烷基;其中所述C1-6烷基任选被1、2、3或4个独立地选自Rg的取代基取代。
67.如权利要求1-66中任一项所述的化合物或其药学上可接受的盐,其中每个Rg是OH。
68.如权利要求1-67中任一项所述的化合物或其药学上可接受的盐,其中n是2。
69.如权利要求1-3和5-68中任一项所述的化合物或其药学上可接受的盐,其中A是N。
70.如权利要求1、2和5-68中任一项所述的化合物或其药学上可接受的盐,其中A是CR16。
71.如权利要求1、2、5-68和70中任一项所述的化合物或其药学上可接受的盐,其中R16是H、CN或ORa16。
72.如权利要求1、2、5-68、70和71中任一项所述的化合物或其药学上可接受的盐,其中Ra16选自H和C1-6烷基。
73.如权利要求1、2、5-68和70-72中任一项所述的化合物或其药学上可接受的盐,其中Ra16是甲基。
85.如权利要求1所述的化合物,其选自:
N-(2-((1R,4R)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
(S)-N-(2-(3-氨基吡咯烷-1-基)-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
(R)-N-(2-(2-(氨甲基)吡咯烷-1-基)-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
(R)-N-(5-氟-2-(2-(羟甲基)吡咯烷-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
(R)-N-(5-氟-2-(2-(甲氧基甲基)吡咯烷-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(5-氟-2-((2S,4S)-4-羟基-2-甲基吡咯烷-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(5-氟-2-(2-(吡啶-2-基)吡咯烷-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(5-氟-2-(六氢吡咯并[3,4-b]吡咯-1(2H)-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
(R)-N-(5-氟-2-(2-甲基哌嗪-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
(R)-N-(5-氟-2-(2-(羟甲基)哌嗪-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(5-氟-2-(3-(羟甲基)吗啉代)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1R,4R)-2,5-二氮杂双环[2.2.1]庚-2-基)-3-溴-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1R,4R)-2,5-二氮杂双环[2.2.1]庚-2-基)-3-氰基苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1R,4R)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟-3-(吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1R,4R)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟-3-(1-甲基-1H-吡唑-4-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟-4-(羟甲基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-4-溴-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟-4-(1-甲基-1H-吡唑-4-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟-4-(6-(羟甲基)吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟-4-(6-(甲基氨甲酰基)吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟-4-(1-甲基-6-氧代-1,6-二氢吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟-4-(2-甲基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-4-(2-甲基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-4-(4-甲氧基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-4-(1,3,5-三甲基-1H-吡唑-4-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟-4-吗啉代苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(4-(氮杂环丁-1-基)-2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟-4-(吗啉代甲基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-4-((环丁基氨基)甲基)-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1R,4R)-5-乙基-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(5-氟-2-((1R,4R)-5-(2-羟乙基)-2,5-二氮杂双环[2.2.1]庚-2-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
(1R,4R)-5-(4-氟-2-(2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺基)苯基)-N-丙基-2,5-二氮杂双环[2.2.1]庚烷-2-甲酰胺;
N-(2-((1R,4R)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-甲氧基苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1R,4R)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-(羟甲基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;和
N-(2-((1R,4R)-2,5-二氮杂双环[2.2.1]庚-2-基)-5-氰基苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
或其药学上可接受的盐。
86.如权利要求1所述的化合物,其选自:
N-(4-(氮杂环丁-1-基)-2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-4-((S)-2-(甲氧基甲基)氮杂环丁-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((1S,4S)-2,5-二氮杂双环[2.2.1]庚-2-基)-4-(3-氰基吡啶-4-基)-3-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(3-氰基吡啶-4-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(2-甲基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(3-甲氧基吡啶-4-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(3-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-2'-氰基-6'-氟联苯-4-基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(3-氰基吡啶-2-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基-1-甲基-1H-吡唑-5-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-异丙基苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(4-(3-氰基吡啶-4-基)-2-((2S,4S)-4-羟基-2-(羟甲基)吡咯烷-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(4-(4-氰基吡啶-3-基)-2-((2S,5R)-2-(羟甲基)-5-甲基哌嗪-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(4-(4-氰基吡啶-3-基)-2-((2S,5S)-2-(羟甲基)-5-甲基哌嗪-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
(S)-N-(4-(4-氰基吡啶-3-基)-2-(6-(羟甲基)-4,7-二氮杂螺[2.5]辛-7-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(1-羟基环丙基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(2-羟基丙-2-基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基-d2)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(4-(4-氰基吡啶-3-基)-2-((1S,3R,4S)-3-(羟甲基)-2,5-二氮杂双环[2.2.1]庚-2-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(4-(4-氰基吡啶-3-基)-2-((1S,4S)-1-(羟甲基)-2,5-二氮杂双环[2.2.1]庚-2-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-甲基哌啶-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-6-(2-氟-6-甲氧基苯基)吡啶酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-5-氰基-6-(2-氟-6-甲氧基苯基)吡啶酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-6-(2-氟-6-甲氧基苯基)-5-甲氧基吡啶酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2,6-二氟苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氯-6-氟苯基)嘧啶-4-甲酰胺;和
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-6-(1,3,5-三甲基-1H-吡唑-4-基)吡啶-3-基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
或其药学上可接受的盐。
87.如权利要求1所述的化合物,其选自:
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-5-氟苯基)-2-(2,6-二氟苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-5-氟苯基)-2-(3-氰基-2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-5-氟苯基)-2-(2,3-二氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-5-氟苯基)-2-(2-氟-6-(甲氧基-d3)-3-甲基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基-4-甲基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(3,6-二氟-2-甲基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2,3-二氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(3,6-二氟-2-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(3-氰基-2-氟-6-(甲氧基-d3)苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(3,6-二氟-2-(甲氧基-d3)苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2,3-二氟-6-(甲氧基-d3)苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-(甲氧基-d3)苯基-5-d)嘧啶-4-甲酰胺;
2-(2-氟-6-甲氧基苯基)-N-(2-(哌啶-4-基)苯基)嘧啶-4-甲酰胺;
N-(2-(顺)4-氨基环己基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-(反)4-氨基环己基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-(3-氨基环己基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-(3-氨基环戊基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((顺)-4-氨基环己基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((反)-4-氨基环己基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((顺)-4-氨基环己基)-4-(4-氰基-1-甲基-1H-吡唑-5-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((反)-4-氨基环己基)-4-(4-氰基-1-甲基-1H-吡唑-5-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((顺)-4-氨基环己基)-4-(1,3,5-三甲基-1H-吡唑-4-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(甲基磺酰基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-5-甲基苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-(二甲氨基)-2-(羟甲基)吡咯烷-1-基)-5-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(5-氟-2-((2S,4S)-2-(羟甲基)-4-(异丙基氨基)吡咯烷-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(四氢-2H-吡喃-4-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-氯苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-氟苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(5-氰基-2-(吡咯烷-1-基)吡啶-4-基)苯基)-2-(2,6-二氟苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(1-氰基环丙基)苯基)-2-(2,6-二氟苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-(二氟甲氧基)-6-氟苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-(甲氧基-d3)苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-环丙基-6-氟苯基)嘧啶-4-甲酰胺;
N-(2-((2S,4S)-4-氨基-2-(羟甲基)吡咯烷-1-基)-4-(4-氰基吡啶-3-基)苯基)-2-(2-乙氧基-6-氟苯基)嘧啶-4-甲酰胺;
N-(4-(4-氰基吡啶-3-基)-2-((1S,4S)-4-(羟甲基)-5-甲基-2,5-二氮杂双环[2.2.1]庚-2-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
(S)-N-(4-(4-氰基吡啶-3-基)-2-(2-(羟甲基)吗啉代)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
(S)-N-(4-(4-氰基吡啶-3-基)-2-(2-((二甲氨基)甲基)吗啉代)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
(R)-N-(2-(2-(氰甲基)吗啉代)-4-(4-氰基吡啶-3-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
(R)-N-(4-(4-氰基吡啶-3-基)-2-(3-氧代四氢-3H-噁唑并[3,4-a]吡嗪-7(1H)-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
(S)-N-(5-氟-2-(3-(羟甲基)哌嗪-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(4-(4-氰基吡啶-3-基)-2-(3-(甲氧基甲基)氮杂环丁-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
(S)-N-(4-(4-氰基吡啶-3-基)-2-(2-(羟甲基)氮杂环丁-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
(R)-N-(4-(4-氰基吡啶-3-基)-2-(2-((二甲氨基)甲基)氮杂环丁-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(4-(4-氰基吡啶-3-基)-2-(4-甲基哌嗪-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
N-(4-(4-氰基吡啶-3-基)-2-(4-(2-羟乙基)哌嗪-1-基)苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;和
(S)-N-(5-氟-2-(3-(羟甲基)哌嗪-1-基)-4-异丙基苯基)-2-(2-氟-6-甲氧基苯基)嘧啶-4-甲酰胺;
或其药学上可接受的盐。
88.一种药物组合物,其包含权利要求1-87中任一项的化合物或其药学上可接受的盐和至少一种药学上可接受的载体或赋形剂。
89.一种抑制HPK1活性的方法,所述方法包括使权利要求1-87中任一项的化合物或其药学上可接受的盐与HPK1接触。
90.如权利要求89所述的方法,其中所述接触包括对患者施用所述化合物。
91.一种治疗与HPK1相互作用的抑制相关的疾病或病症的方法,所述方法包括对有需要的患者施用治疗有效量的权利要求1-87中任一项的化合物或其药学上可接受的盐。
92.一种治疗患者的癌症的方法,所述方法包括:对所述患者施用治疗有效量的权利要求1-87中任一项的化合物或其药学上可接受的盐。
93.如权利要求92所述的方法,其中所述癌症选自乳腺癌、结肠直肠癌、肺癌、卵巢癌和胰腺癌。
Applications Claiming Priority (7)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201862632702P | 2018-02-20 | 2018-02-20 | |
| US62/632,702 | 2018-02-20 | ||
| US201862672772P | 2018-05-17 | 2018-05-17 | |
| US62/672,772 | 2018-05-17 | ||
| US201862750371P | 2018-10-25 | 2018-10-25 | |
| US62/750,371 | 2018-10-25 | ||
| PCT/US2019/018608 WO2019164846A1 (en) | 2018-02-20 | 2019-02-19 | N-(phenyl)-2-(phenyl)pyrimidine-4-carboxamide derivatives and related compounds as hpk1 inhibitors for treating cancer |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN112292380A true CN112292380A (zh) | 2021-01-29 |
| CN112292380B CN112292380B (zh) | 2024-04-05 |
Family
ID=65635851
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201980020899.4A Active CN112292380B (zh) | 2018-02-20 | 2019-02-19 | 作为用于治疗癌症的hpk1抑制剂的n-(苯基)-2-(苯基)嘧啶-4-甲酰胺衍生物及相关化合物 |
Country Status (30)
| Country | Link |
|---|---|
| US (3) | US10800761B2 (zh) |
| EP (1) | EP3755703B1 (zh) |
| JP (1) | JP7526673B2 (zh) |
| KR (1) | KR20200133747A (zh) |
| CN (1) | CN112292380B (zh) |
| AU (1) | AU2019223955B2 (zh) |
| BR (1) | BR112020016927A2 (zh) |
| CA (1) | CA3091517A1 (zh) |
| CL (1) | CL2020002146A1 (zh) |
| CO (1) | CO2020011530A2 (zh) |
| CR (1) | CR20200421A (zh) |
| DK (1) | DK3755703T3 (zh) |
| EC (1) | ECSP20058964A (zh) |
| ES (1) | ES2922237T3 (zh) |
| HR (1) | HRP20220833T1 (zh) |
| HU (1) | HUE059624T2 (zh) |
| IL (1) | IL276779B2 (zh) |
| LT (1) | LT3755703T (zh) |
| MD (1) | MD3755703T2 (zh) |
| MX (1) | MX2020008656A (zh) |
| PE (1) | PE20210397A1 (zh) |
| PH (1) | PH12020551278A1 (zh) |
| PL (1) | PL3755703T3 (zh) |
| PT (1) | PT3755703T (zh) |
| RS (1) | RS63659B1 (zh) |
| SG (1) | SG11202007917VA (zh) |
| SI (1) | SI3755703T1 (zh) |
| TW (1) | TWI828653B (zh) |
| UA (1) | UA128286C2 (zh) |
| WO (1) | WO2019164846A1 (zh) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN114450276A (zh) * | 2019-08-06 | 2022-05-06 | 因赛特公司 | Hpk1抑制剂的固体形式 |
Families Citing this family (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| MA46191A (fr) | 2016-09-09 | 2021-04-21 | Incyte Corp | Dérivés de pyrazolopyridine comme modulateurs de hpk1 et leurs utilisations pour le traitement du cancer |
| WO2018049152A1 (en) | 2016-09-09 | 2018-03-15 | Incyte Corporation | Pyrazolopyrimidine derivatives as hpk1 modulators and uses thereof for the treatment of cancer |
| US20180072718A1 (en) | 2016-09-09 | 2018-03-15 | Incyte Corporation | Pyrazolopyridine compounds and uses thereof |
| US20180228786A1 (en) | 2017-02-15 | 2018-08-16 | Incyte Corporation | Pyrazolopyridine compounds and uses thereof |
| WO2019051199A1 (en) | 2017-09-08 | 2019-03-14 | Incyte Corporation | 6-CYANO-INDAZOLE COMPOUNDS AS HEMATOPOIETIC PROGENITOR KINASE 1 (HPK1) MODULATORS |
| US10745388B2 (en) | 2018-02-20 | 2020-08-18 | Incyte Corporation | Indazole compounds and uses thereof |
| DK3755703T3 (da) | 2018-02-20 | 2022-06-27 | Incyte Corp | N-(phenyl)-2-(phenyl)pyrimidin-4-carboxamidderivater og relaterede forbindelser som hpk1-inhibitorer til behandling af kræft |
| WO2019164847A1 (en) | 2018-02-20 | 2019-08-29 | Incyte Corporation | Indazole compounds and uses thereof |
| US11299473B2 (en) | 2018-04-13 | 2022-04-12 | Incyte Corporation | Benzimidazole and indole compounds and uses thereof |
| US10899755B2 (en) | 2018-08-08 | 2021-01-26 | Incyte Corporation | Benzothiazole compounds and uses thereof |
| TW202028207A (zh) | 2018-09-25 | 2020-08-01 | 美商英塞特公司 | 吡唑并嘧啶化合物及其用途 |
| MX2021005047A (es) | 2018-10-31 | 2021-09-08 | Gilead Sciences Inc | Compuestos de 6-azabenzimidazol sustituidos como inhibidores de hpk1. |
| TW202136261A (zh) | 2018-10-31 | 2021-10-01 | 美商基利科學股份有限公司 | 經取代之6-氮雜苯并咪唑化合物 |
| MA54546A (fr) * | 2018-12-20 | 2022-03-30 | Amgen Inc | Amides d'hétéroaryle utiles en tant qu'inhibiteurs de kif18a |
| WO2020237025A1 (en) | 2019-05-23 | 2020-11-26 | Gilead Sciences, Inc. | Substituted exo-methylene-oxindoles which are hpk1/map4k1 inhibitors |
| WO2021249913A1 (en) | 2020-06-09 | 2021-12-16 | Bayer Aktiengesellschaft | 2'-(quinolin-3-yl)-5',6'-dihydrospiro[azetidine-3,4'-pyrrolo[1,2-b]pyrazole]-1-carboxylate derivatives and related compounds as map4k1 (hpk1) inhibitors for the treatment of cancer |
| CN114181257A (zh) * | 2020-09-14 | 2022-03-15 | 四川科伦博泰生物医药股份有限公司 | 吡啶类化合物,包含其的药物组合物,其制备方法及其用途 |
| US20240174683A1 (en) | 2021-02-05 | 2024-05-30 | Bayer Aktiengesellschaft | Map4k1 inhibitors |
| EP4373817A1 (en) | 2021-07-20 | 2024-05-29 | Astrazeneca AB | Substituted pyrazine-2-carboxamides as hpk1 inhibitors for the treatment of cancer |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN101801981A (zh) * | 2007-06-20 | 2010-08-11 | 西特里斯药业公司 | 瑟土因调节性噻唑并吡啶化合物 |
| CN101918371A (zh) * | 2007-11-01 | 2010-12-15 | 西特里斯药业公司 | 作为瑟土因调节剂的酰胺衍生物 |
| WO2016205942A1 (en) * | 2015-06-25 | 2016-12-29 | University Health Network | Hpk1 inhibitors and methods of using same |
Family Cites Families (239)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SE8800613D0 (sv) | 1988-02-23 | 1988-02-23 | Wallac Oy | A novel spectrofluorometric method and compounds that are of value for the method |
| JPH03287584A (ja) | 1990-04-05 | 1991-12-18 | Banyu Pharmaceut Co Ltd | 置換アリルアミン誘導体 |
| US5250534A (en) | 1990-06-20 | 1993-10-05 | Pfizer Inc. | Pyrazolopyrimidinone antianginal agents |
| US6200980B1 (en) | 1995-06-07 | 2001-03-13 | Cell Pathways, Inc. | Method of treating a patient having precancerous lesions with phenyl purinone derivatives |
| CN1281588C (zh) | 1997-04-25 | 2006-10-25 | 美国辉瑞有限公司 | 制备吡唑并嘧啶酮类化合物的新型中间体 |
| US6251904B1 (en) | 1998-04-20 | 2001-06-26 | Pfizer Inc. | Pyrazolopyrimidinone cGMP PDE5 inhibitors for the treatment of sexual dysfunction |
| JP2000038350A (ja) | 1998-05-18 | 2000-02-08 | Yoshitomi Pharmaceut Ind Ltd | 糖尿病治療薬 |
| GB9823101D0 (en) | 1998-10-23 | 1998-12-16 | Pfizer Ltd | Pharmaceutically active compounds |
| GB9823102D0 (en) | 1998-10-23 | 1998-12-16 | Pfizer Ltd | Pharmaceutically active compounds |
| CZ27399A3 (cs) | 1999-01-26 | 2000-08-16 | Ústav Experimentální Botaniky Av Čr | Substituované dusíkaté heterocyklické deriváty, způsob jejich přípravy, tyto deriváty pro použití jako léčiva, farmaceutická kompozice a kombinovaný farmaceutický přípravek tyto deriváty obsahující a použití těchto derivátů pro výrobu léčiv |
| IN187433B (zh) | 1999-09-10 | 2002-04-27 | Cipla Ltd | |
| WO2001019827A1 (en) | 1999-09-13 | 2001-03-22 | Cipla Ltd. | A novel process for the synthesis of sildenafil citrate |
| MXPA02002938A (es) | 1999-09-17 | 2004-12-06 | Abbott Gmbh & Co Kg | Inhibidores de cinasa como agentes agentes terapeuticos. |
| IL148814A0 (en) | 1999-09-24 | 2002-09-12 | Nihon Nohyaku Co Ltd | Aromatic diamine derivatives or salts thereof, agricultural/horticultural chemicals and method of using the same |
| EA200200240A1 (ru) | 1999-10-11 | 2002-10-31 | Пфайзер Инк. | 5-(2-ЗАМЕЩЕННЫЕ-5-ГЕТЕРОЦИКЛИЛСУЛЬФОНИЛПИРИД-3-ИЛ)-ДИГИДРОПИРАЗОЛО[4,3-d]ПИРИМИДИН-7-ОНЫ В КАЧЕСТВЕ ИНГИБИТОРОВ ФОСФОДИЭСТЕРАЗЫ |
| TWI265925B (en) | 1999-10-11 | 2006-11-11 | Pfizer | Pyrazolo[4,3-d]pyrimidin-7-ones useful in inhibiting type 5 cyclic guanosine 3',5'-monophosphate phosphodiesterases(cGMP PDE5), process and intermediates for their preparation, their uses and composition comprising them |
| IL152925A (en) | 1999-10-21 | 2010-04-15 | Pfizer | Pharmaceutical preparations for the treatment of neurological disease containing an inhibitor of ring guanizine '3', 5 '- monophosphate phosphodiesterase 5 and one of gabapentin or pregabalin |
| HUP0204412A3 (en) | 1999-12-22 | 2003-05-28 | Nihon Nohyaku Co Ltd | Insecticidal aromatic diamide derivatives, compositions containing them and use thereof |
| CO5271697A1 (es) | 2000-01-12 | 2003-04-30 | Pfizer Prod Inc | Composiciones y procedimientos para el tratamiento de afecciones que responden a un aumento de testosterona |
| US20020013327A1 (en) | 2000-04-18 | 2002-01-31 | Lee Andrew G. | Compositions and methods for treating female sexual dysfunction |
| US20040089753A1 (en) | 2000-06-28 | 2004-05-13 | Holland Simon Joseph | Wet milling process |
| WO2002016348A1 (en) | 2000-08-09 | 2002-02-28 | Astrazeneca Ab | Antiangiogenic bicyclic derivatives |
| WO2002019975A1 (fr) | 2000-09-05 | 2002-03-14 | Taisho Pharmaceutical Co., Ltd. | Stimulants de la croissance des cheveux |
| US6548508B2 (en) | 2000-10-20 | 2003-04-15 | Pfizer, Inc. | Use of PDE V inhibitors for improved fecundity in mammals |
| BR0115995A (pt) | 2000-12-19 | 2004-01-13 | Merck Patent Gmbh | Formulação farmacêutica compreendendo pirazolo[4,3-d]pirimidinas e antitrombóticos, antagonistas de cálcio, prostaglandinas ou derivados de prostaglandina |
| AU2002222293A1 (en) | 2000-12-19 | 2002-07-01 | Smithkline Beecham P.L.C. | Pyrazolo(3,4-c)pyridines as gsk-3 inhibitors |
| US6784185B2 (en) | 2001-03-16 | 2004-08-31 | Pfizer Inc. | Pharmaceutically active compounds |
| US6770645B2 (en) | 2001-03-16 | 2004-08-03 | Pfizer Inc. | Pharmaceutically active compounds |
| US7902179B2 (en) | 2001-04-26 | 2011-03-08 | Ajinomoto Co., Inc. | Heterocyclic compounds |
| EP1383760A1 (en) | 2001-04-30 | 2004-01-28 | Fujisawa Pharmaceutical Co., Ltd. | Biarylcarboxamide compounds as apolipoprotein b inhibitors |
| FR2825706B1 (fr) | 2001-06-06 | 2003-12-12 | Pf Medicament | Nouveaux derives de benzothienyle ou d'indole, leur preparation et leur utilisation comme inhibiteurs de proteines prenyl transferase |
| MXPA04004170A (es) | 2001-11-02 | 2004-09-06 | Pfizer Prod Inc | Tratamiento del sindrome de resitencia a la insulina y diabetes de tipo 2 con inhibidores de pde9. |
| TW200738672A (en) | 2001-12-10 | 2007-10-16 | Bristol Myers Squibb Co | Intermediated for the preparation of 4,5-dihydro-pyrazolo [3,4-c] pyrid-2-ones |
| US7166293B2 (en) | 2002-03-29 | 2007-01-23 | Carlsbad Technology, Inc. | Angiogenesis inhibitors |
| US20050119278A1 (en) | 2002-05-16 | 2005-06-02 | Che-Ming Teng | Anti-angiogenesis methods |
| IL164209A0 (en) | 2002-05-31 | 2005-12-18 | Eisai Co Ltd | Pyrazole derivatives and pharmaceutical compositions containing the same |
| ES2337254T3 (es) | 2003-02-14 | 2010-04-22 | Glaxo Group Limited | Derivados de carboxamida. |
| BRPI0407493A (pt) | 2003-02-14 | 2006-02-14 | Wyeth Corp | derivados heterociclil-3-sulfinilazaindol ou -azaindazol como ligantes de 5-hidroxitriptamina-6 |
| WO2004087906A1 (en) | 2003-03-31 | 2004-10-14 | Pfizer Products Inc. | Crystal structure of 3',5'-cyclic nucleotide phosphodiesterase 1b (pde1b) and uses thereof |
| OA13050A (en) | 2003-04-29 | 2006-11-10 | Pfizer Ltd | 5,7-diaminopyrazolo [4,3-D] pyrimidines useful in the treatment of hypertension. |
| JP2006526660A (ja) | 2003-06-05 | 2006-11-24 | バーテックス ファーマシューティカルズ インコーポレイテッド | Vr1レセプターのモジュレーター |
| US7183267B2 (en) | 2003-06-10 | 2007-02-27 | The Johns Hopkins University | β-lactamase inhibitors and methods of use thereof |
| JP2007500700A (ja) | 2003-07-29 | 2007-01-18 | スミスクライン ビーチャム コーポレーション | 化合物 |
| AR045595A1 (es) | 2003-09-04 | 2005-11-02 | Vertex Pharma | Composiciones utiles como inhibidores de proteinas quinasas |
| RU2351593C2 (ru) | 2003-11-19 | 2009-04-10 | Эррэй Биофарма Инк. | Гетероциклические ингибиторы мек и способы их применения |
| US20050137398A1 (en) | 2003-12-22 | 2005-06-23 | Jianguo Ji | 3-Quinuclidinyl heteroatom bridged biaryl derivatives |
| US7241773B2 (en) | 2003-12-22 | 2007-07-10 | Abbott Laboratories | 3-quinuclidinyl heteroatom bridged biaryl derivatives |
| GB0402137D0 (en) | 2004-01-30 | 2004-03-03 | Smithkline Beecham Corp | Novel compounds |
| DE102004005172A1 (de) | 2004-02-02 | 2005-08-18 | Aventis Pharma Deutschland Gmbh | Indazolderivate als Inhibitoren der Hormon Sensitiven Lipase |
| JP2007523938A (ja) | 2004-02-27 | 2007-08-23 | エフ.ホフマン−ラ ロシュ アーゲー | ピラゾールの縮合誘導体 |
| CA2558109A1 (en) | 2004-02-27 | 2005-09-15 | F. Hoffmann-La Roche Ag | Heteroaryl-fused pyrazolo derivatives |
| WO2005085227A1 (en) | 2004-03-02 | 2005-09-15 | Smithkline Beecham Corporation | Inhibitors of akt activity |
| AR050188A1 (es) | 2004-08-03 | 2006-10-04 | Uriach Y Compania S A J | Compuestos heterociclicos condensados utiles en terapia como inhibidores de quinasas p38 y composiciones farmaceuticas que los contienen |
| KR20200118909A (ko) | 2004-09-02 | 2020-10-16 | 제넨테크, 인크. | 헤지호그 신호전달에 대한 피리딜 억제제 |
| WO2006038001A1 (en) | 2004-10-06 | 2006-04-13 | Celltech R & D Limited | Aminopyrimidine derivatives as jnk inhibitors |
| CA2584485C (en) | 2004-10-20 | 2013-12-31 | Resverlogix Corp. | Stilbenes and chalcones for the prevention and treatment of cardiovascular diseases |
| AR051596A1 (es) | 2004-10-26 | 2007-01-24 | Irm Llc | Compuestos heterociclicos condensados nitrogenados como inhibidores de la actividad del receptor canabinoide 1; composiciones farmaceuticas que los contienen y su empleo en la preparacion de medicamentos para el tratamiento de trastornos alimentarios |
| CA2585555A1 (en) | 2004-10-28 | 2006-05-11 | The Institutes For Pharmaceutical Discovery, Llc | Substituted phenylalkanoic acids |
| MX2007005643A (es) | 2004-11-10 | 2008-03-13 | Cgi Pharmaceuticals Inc | Ciertas imidazo [1,2-a] pirazin-8-ilaminas, metodo para su elaboracion y metodo de uso de las mismas. |
| WO2006053227A2 (en) | 2004-11-10 | 2006-05-18 | Synta Pharmaceuticals Corp. | Il-12 modulatory compounds |
| TW200628463A (en) | 2004-11-10 | 2006-08-16 | Synta Pharmaceuticals Corp | Heteroaryl compounds |
| DE102004054666A1 (de) | 2004-11-12 | 2006-05-18 | Bayer Cropscience Gmbh | Substituierte Pyrazol-3-carboxamide, Verfahren zur Herstellung und Verwendung als Herbizide und Pflanzenwachstumsregulatoren |
| CN100516049C (zh) | 2004-11-16 | 2009-07-22 | 永信药品工业股份有限公司 | 抗血管生成药n2-(取代的芳基甲基)-3-(取代的苯基)吲唑的合成 |
| JP5038905B2 (ja) | 2005-01-07 | 2012-10-03 | エモリー・ユニバーシテイ | 医学的障害の治療用のcxcr4拮抗薬 |
| CN101184487B (zh) | 2005-03-31 | 2010-11-03 | 詹森药业有限公司 | 作为抗菌剂的二环吡唑化合物 |
| WO2006128172A2 (en) | 2005-05-26 | 2006-11-30 | Synta Pharmaceuticals Corp. | Method for treating b cell regulated autoimmune disorders |
| WO2007013673A1 (en) | 2005-07-29 | 2007-02-01 | Astellas Pharma Inc. | Fused heterocycles as lck inhibitors |
| JP5203196B2 (ja) | 2005-08-04 | 2013-06-05 | サートリス ファーマシューティカルズ, インコーポレイテッド | サーチュインモジュレーターとしてのオキサゾロピリジン誘導体 |
| GB0516703D0 (en) | 2005-08-15 | 2005-09-21 | Syngenta Participations Ag | Novel insecticides |
| JP2007055940A (ja) | 2005-08-24 | 2007-03-08 | Astellas Pharma Inc | ピラゾロピリミジン誘導体 |
| MX2008002587A (es) | 2005-08-25 | 2008-03-18 | Hoffmann La Roche | Inhibidores de la p38-map-cinasa y metodos para el uso de los mismos. |
| CA2620254A1 (en) | 2005-08-25 | 2007-03-01 | F. Hoffmann-La Roche Ag | P38 map kinase inhibitors and methods for using the same |
| BRPI0615442A2 (pt) | 2005-08-25 | 2011-05-17 | Hoffmann La Roche | inibidores de p38 map cinase e métodos para uso dos mesmos |
| CN101277939A (zh) | 2005-09-09 | 2008-10-01 | 布里斯托尔-迈尔斯斯奎布公司 | 无环ikur抑制剂 |
| US20070087988A1 (en) | 2005-09-30 | 2007-04-19 | New York University | Hematopoietic progenitor kinase 1 for modulation of an immune response |
| EP1940296A2 (en) | 2005-10-25 | 2008-07-09 | SmithKline Beecham Corporation | Chemical compounds |
| JP2009515837A (ja) | 2005-11-03 | 2009-04-16 | イリプサ, インコーポレイテッド | C4−酸性置換基を有するインドール化合物およびホスホリパーゼa2インヒビターとしてのその使用 |
| RU2008126228A (ru) | 2005-11-30 | 2010-01-10 | Астеллас Фарма Инк. (Jp) | 2-аминобензамидное производное |
| GB0525143D0 (en) | 2005-12-09 | 2006-01-18 | Novartis Ag | Organic compounds |
| AU2007204208A1 (en) | 2006-01-11 | 2007-07-19 | Astrazeneca Ab | Morpholino pyrimidine derivatives and their use in therapy |
| DE602007001870D1 (de) | 2006-02-16 | 2009-09-17 | Syngenta Ltd | Eine bicyclische bisamidstruktur enthaltende pestizide |
| US8163777B2 (en) | 2006-03-23 | 2012-04-24 | Synta Pharmaceuticals Corp. | Benzimidazolyl-pyridine compounds for inflammation and immune-related uses |
| CA2645967C (en) | 2006-03-30 | 2011-05-24 | Irm Llc | Compounds and compositions as inhibitors of cannabinoid receptor 1 activity |
| UA92083C2 (ru) | 2006-05-19 | 2010-09-27 | Эбботт Леборетриз | Азабициклические алкановые производные, замещенные конденсированным бициклогетероциклом |
| US20080280891A1 (en) | 2006-06-27 | 2008-11-13 | Locus Pharmaceuticals, Inc. | Anti-cancer agents and uses thereof |
| WO2008008059A1 (en) | 2006-07-12 | 2008-01-17 | Locus Pharmaceuticals, Inc. | Anti-cancer agents ans uses thereof |
| PE20121506A1 (es) | 2006-07-14 | 2012-11-26 | Amgen Inc | Compuestos triazolopiridinas como inhibidores de c-met |
| GB0614691D0 (en) | 2006-07-24 | 2006-08-30 | Syngenta Participations Ag | Insecticidal compounds |
| CN101522026A (zh) | 2006-10-06 | 2009-09-02 | Irm责任有限公司 | 蛋白激酶抑制剂及其应用方法 |
| MX2009003941A (es) | 2006-10-20 | 2009-04-24 | Concert Pharmaceuticals Inc | Derivados de 3-(dihidro-1h-pirazolo[4,3-d]pirimidin-5-il)-4-propox ibencenosulfonamida y metodos de uso. |
| WO2008089310A2 (en) | 2007-01-18 | 2008-07-24 | Lexicon Pharmaceuticals, Inc. | Delta 5 desaturase inhibitors for the treatment of obesity |
| US20080194557A1 (en) | 2007-01-18 | 2008-08-14 | Joseph Barbosa | Methods and compositions for the treatment of pain, inflammation and cancer |
| US20140249135A1 (en) * | 2007-03-01 | 2014-09-04 | Novartis Ag | Pim kinase inhibitors and methods of their use |
| MX2009009304A (es) | 2007-03-01 | 2009-11-18 | Novartis Ag | Inhibidores de cinasa pim y metodos para su uso. |
| EP2002835A1 (en) | 2007-06-04 | 2008-12-17 | GenKyo Tex | Pyrazolo pyridine derivatives as NADPH oxidase inhibitors |
| BRPI0814441A2 (pt) | 2007-07-19 | 2015-07-14 | Schering Corp | Compostos de amida heterocíclica como inibidores de proteína cinase |
| MY146643A (en) | 2007-07-30 | 2012-09-14 | Dae Woong Pharma | Novel benzoimidazole derivatives and pharmaceutical composition comprising the same |
| WO2009019167A1 (en) | 2007-08-08 | 2009-02-12 | Merck Serono S.A. | 6-amino-pyrimidine-4-carboxamide derivatives and related compounds which bind to the sphingosine 1-phosphate (s1p) receptor for the treatment of multiple sclerosis |
| GB0716414D0 (en) | 2007-08-22 | 2007-10-03 | Syngenta Participations Ag | Novel insecticides |
| WO2009032651A1 (en) | 2007-08-31 | 2009-03-12 | Smithkline Beecham Corporation | Inhibitors of akt activity |
| US8314131B2 (en) | 2007-09-21 | 2012-11-20 | Amgen Inc. | Triazole fused heteroaryl compounds and methods of use thereof |
| KR100963644B1 (ko) | 2007-11-23 | 2010-06-15 | 한국과학기술연구원 | 피라졸로피리미딘온 유도체 및 그의 제조방법 |
| KR20100115789A (ko) | 2008-02-04 | 2010-10-28 | 머큐리 테라퓨틱스, 인코포레이티드 | Ampk 조절자 |
| WO2009139834A1 (en) | 2008-05-13 | 2009-11-19 | Poniard Pharmaceuticals, Inc. | Bioactive compounds for treatment of cancer and neurodegenerative diseases |
| EA201001847A1 (ru) | 2008-06-11 | 2011-08-30 | Айрм Ллк | Соединения и композиции, применяемые для лечения малярии |
| SG10201510696RA (en) | 2008-06-27 | 2016-01-28 | Celgene Avilomics Res Inc | Heteroaryl compounds and uses thereof |
| WO2010029300A1 (en) | 2008-09-12 | 2010-03-18 | Biolipox Ab | Bis aromatic compounds for use in the treatment of inflammation |
| EP2166008A1 (en) | 2008-09-23 | 2010-03-24 | Genkyo Tex Sa | Pyrazolo pyridine derivatives as NADPH oxidase inhibitors |
| EP2166010A1 (en) | 2008-09-23 | 2010-03-24 | Genkyo Tex Sa | Pyrazolo pyridine derivatives as NADPH oxidase inhibitors |
| EP2165707A1 (en) | 2008-09-23 | 2010-03-24 | Genkyo Tex Sa | Pyrazolo pyridine derivatives as NADPH oxidase inhibitors |
| WO2010046780A2 (en) | 2008-10-22 | 2010-04-29 | Institut Pasteur Korea | Anti viral compounds |
| JP2010111624A (ja) | 2008-11-06 | 2010-05-20 | Shionogi & Co Ltd | Ttk阻害作用を有するインダゾール誘導体 |
| RU2525116C2 (ru) | 2008-12-19 | 2014-08-10 | Дженентек, Инк. | Гетероциклические соединения и способы применения |
| KR20100101055A (ko) | 2009-03-07 | 2010-09-16 | 주식회사 메디젠텍 | 세포핵에서 세포질로의 gsk3의 이동을 억제하는 화합물을 함유하는 세포핵에서 세포질로의 gsk3 이동 관련 질환의 치료 또는 예방용 약학적 조성물 |
| JP2012520887A (ja) | 2009-03-18 | 2012-09-10 | シェーリング コーポレイション | ジアシルグリセロールアシルトランスフェラーゼの阻害剤としての二環式化合物 |
| WO2010111624A1 (en) | 2009-03-26 | 2010-09-30 | Northeastern University | Carbon nanostructures from pyrolysis of organic materials |
| WO2010118367A2 (en) | 2009-04-10 | 2010-10-14 | Progenics Pharmaceuticals, Inc. | Antiviral pyrimidines |
| EP2464647B1 (en) | 2009-08-11 | 2016-09-21 | Bristol-Myers Squibb Company | Azaindazoles as btk kinase modulators and use thereof |
| WO2011031628A1 (en) | 2009-09-14 | 2011-03-17 | Schering Corporation | Inhibitors of diacylglycerol acyltransferase |
| WO2011050245A1 (en) | 2009-10-23 | 2011-04-28 | Yangbo Feng | Bicyclic heteroaryls as kinase inhibitors |
| ES2360333B1 (es) | 2009-10-29 | 2012-05-04 | Consejo Superior De Investigaciones Cientificas (Csic) (70%) | Derivados de bis (aralquil) amino y sistemas (hetero) aromaticos de seis miembros y su uso en el tratamiento de patologias neurodegenerativas, incluida la enfermedad de alzheimer |
| JP2013032290A (ja) | 2009-11-20 | 2013-02-14 | Dainippon Sumitomo Pharma Co Ltd | 新規縮合ピリミジン誘導体 |
| WO2011078143A1 (ja) | 2009-12-22 | 2011-06-30 | 塩野義製薬株式会社 | ピリミジン誘導体およびそれらを含有する医薬組成物 |
| EP2937345B1 (en) | 2009-12-29 | 2018-03-21 | Dana-Farber Cancer Institute, Inc. | Type ii raf kinase inhibitors |
| WO2011082400A2 (en) | 2010-01-04 | 2011-07-07 | President And Fellows Of Harvard College | Modulators of immunoinhibitory receptor pd-1, and methods of use thereof |
| WO2011082488A1 (en) | 2010-01-06 | 2011-07-14 | British Columbia Cancer Agency Branch | Bisphenol derivative therapeutics and methods for their use |
| DE102010009903A1 (de) | 2010-03-02 | 2011-09-08 | Merck Patent Gmbh | Verbindungen für elektronische Vorrichtungen |
| CN102206172B (zh) | 2010-03-30 | 2015-02-25 | 中国医学科学院医药生物技术研究所 | 一组取代双芳基化合物及其制备方法和抗病毒应用 |
| WO2011133920A1 (en) | 2010-04-23 | 2011-10-27 | Cytokinetics, Inc. | Certain amino-pyridines and amino-triazines, compositions thereof, and methods for their use |
| DK2563776T3 (en) | 2010-04-27 | 2016-09-19 | Calcimedica Inc | Relations that modulate intracellular calcium |
| GB201008134D0 (en) | 2010-05-14 | 2010-06-30 | Medical Res Council Technology | Compounds |
| JP2011246389A (ja) | 2010-05-26 | 2011-12-08 | Oncotherapy Science Ltd | Ttk阻害作用を有する縮環ピラゾール誘導体 |
| ES2660611T3 (es) | 2010-05-27 | 2018-03-23 | Bayer Cropscience Ag | Derivados de ácido piridinilcarboxílico como fungicidas |
| WO2011153553A2 (en) | 2010-06-04 | 2011-12-08 | The Regents Of The University Of California | Methods and compositions for kinase inhibition |
| BR112012032247A2 (pt) | 2010-06-15 | 2015-09-15 | Bayer Ip Gmbh | derivados de ácido antranílico |
| US9212139B2 (en) | 2010-06-16 | 2015-12-15 | Purdue Pharma, L.P. | Aryl substituted indoles and their use as blockers of sodium channels |
| JP5926727B2 (ja) | 2010-07-28 | 2016-05-25 | バイエル・インテレクチュアル・プロパティ・ゲゼルシャフト・ミット・ベシュレンクテル・ハフツングBayer Intellectual Property GmbH | 置換イミダゾ[1,2−b]ピリダジン |
| US10005750B2 (en) | 2010-10-06 | 2018-06-26 | J-Pharma Co., Ltd. | Developing potent urate transporter inhibitors: compounds designed for their uricosuric action |
| GB201017345D0 (en) | 2010-10-14 | 2010-11-24 | Proximagen Ltd | Receptor antagonists |
| US9090593B2 (en) | 2010-12-09 | 2015-07-28 | Amgen Inc. | Bicyclic compounds as Pim inhibitors |
| WO2012080376A1 (en) | 2010-12-17 | 2012-06-21 | Syngenta Participations Ag | Insecticidal compounds |
| WO2012093101A1 (en) | 2011-01-04 | 2012-07-12 | Novartis Ag | Indole compounds or analogues thereof useful for the treatment of age-related macular degeneration (amd) |
| EP2672820B1 (en) | 2011-02-07 | 2019-04-17 | The Washington University | Mannoside compounds and methods of use thereof |
| JP6001048B2 (ja) | 2011-03-28 | 2016-10-05 | エフ.ホフマン−ラ ロシュ アーゲーF. Hoffmann−La Roche Aktiengesellschaft | チアゾロピリミジン化合物 |
| PT2697207T (pt) | 2011-04-12 | 2017-02-14 | Chong Kun Dang Pharmaceutical Corp | Derivados de 3-(2-aril-cicloalcenilmetil)-oxazolidin-2-ona como inibidores da proteína de transferência de ésteres de colesterol (cetp) |
| WO2012143144A1 (en) | 2011-04-21 | 2012-10-26 | Origenis Gmbh | Pyrazolo [4, 3-d] pyrimidines useful as kinase inhibitors |
| WO2012151567A1 (en) | 2011-05-05 | 2012-11-08 | St. Jude Children's Research Hospital | Pyrimidinone compounds and methods for preventing and treating influenza |
| US20140107151A1 (en) | 2011-05-17 | 2014-04-17 | Principia Biophama Inc. | Tyrosine kinase inhibitors |
| EP2710004A1 (en) | 2011-05-17 | 2014-03-26 | Bayer Intellectual Property GmbH | Amino-substituted imidazopyridazines as mknk1 kinase inhibitors |
| TW201311677A (zh) | 2011-05-31 | 2013-03-16 | Syngenta Participations Ag | 殺蟲化合物 |
| WO2012163942A1 (en) | 2011-06-01 | 2012-12-06 | Bayer Intellectual Property Gmbh | Substituted aminoimidazopyridazines |
| CN103764656A (zh) | 2011-06-22 | 2014-04-30 | 拜耳知识产权有限责任公司 | 杂环基氨基咪唑并哒嗪 |
| EP2543372A1 (en) | 2011-07-08 | 2013-01-09 | Helmholtz-Zentrum für Infektionsforschung GmbH | Medicament for the treatment of liver cancer |
| ES2627120T3 (es) | 2011-07-08 | 2017-07-26 | Helmholtz-Zentrum für Infektionsforschung GmbH | Medicamento para el tratamiento del cáncer de hígado |
| WO2013021276A1 (en) | 2011-08-10 | 2013-02-14 | Purdue Pharma L.P. | Trpv1 antagonists including dihydroxy substituent and uses thereof |
| BR112014003237A2 (pt) | 2011-08-12 | 2017-04-25 | Hoffmann La Roche | compostos de indazol, composições e métodos de uso |
| CA2838784A1 (en) | 2011-08-12 | 2013-02-21 | F. Hoffmann-La Roche Ag | Pyrazolo[3,4-c]pyridine compounds and methods of use |
| WO2013042137A1 (en) | 2011-09-19 | 2013-03-28 | Aurigene Discovery Technologies Limited | Bicyclic heterocycles as irak4 inhibitors |
| WO2013041634A1 (en) | 2011-09-23 | 2013-03-28 | Bayer Intellectual Property Gmbh | Substituted imidazopyridazines |
| CN102516263B (zh) | 2011-10-25 | 2015-04-08 | 南方医科大学 | 一种螺三环类化合物及其制备方法、以及含该类化合物的药物组合物及其应用 |
| CN102503959B (zh) | 2011-10-25 | 2015-04-08 | 南方医科大学 | 一种稠三环类化合物及其制备方法、以及含该类化合物的药物组合物及其应用 |
| JP6173327B2 (ja) | 2011-11-01 | 2017-08-02 | エフ・ホフマン−ラ・ロシュ・アクチェンゲゼルシャフト | イミダゾピリダジン化合物 |
| CA2864484C (en) | 2012-02-17 | 2019-07-02 | Siga Technologies, Inc. | Antiviral drugs for treatment of arenavirus infection |
| TW201348231A (zh) | 2012-02-29 | 2013-12-01 | Amgen Inc | 雜雙環化合物 |
| KR20140131955A (ko) | 2012-03-09 | 2014-11-14 | 카나 바이오사이언스 인코포레이션 | 신규 트리아진 유도체 |
| WO2013146942A1 (ja) | 2012-03-28 | 2013-10-03 | 出光興産株式会社 | 新規化合物、有機エレクトロルミネッセンス素子用材料および有機エレクトロルミネッセンス素子 |
| TWI540134B (zh) | 2012-04-20 | 2016-07-01 | 吉李德科學股份有限公司 | 醫療性化合物 |
| WO2014003405A1 (ko) | 2012-06-26 | 2014-01-03 | 주식회사 제이앤드제이 캐미칼 | 신규한 화합물 및 이를 포함하는 발광소자 |
| MX2014015738A (es) | 2012-06-28 | 2015-08-06 | Novartis Ag | Derivados de pirrolidina y su uso como moduladores de la senda del complemento. |
| KR101936851B1 (ko) | 2012-07-16 | 2019-01-11 | 한국과학기술연구원 | 단백질 키나아제 저해제인 신규 피라졸로피리딘 유도체 또는 인다졸 유도체 |
| WO2014024125A1 (en) | 2012-08-08 | 2014-02-13 | Celon Pharma S.A. | Pyrazolo[4,3-d]pyrimidin-7(6h)-one derivatives as pde9 inhibitors |
| BR112015003380A2 (pt) | 2012-08-23 | 2017-07-04 | Mitsubishi Tanabe Pharma Corp | composto de pirazolopirimidina |
| KR102124227B1 (ko) | 2012-09-24 | 2020-06-17 | 아리조나 보드 오브 리젠츠 온 비하프 오브 아리조나 스테이트 유니버시티 | 금속 화합물, 방법, 및 이의 용도 |
| BR112015007182A2 (pt) | 2012-10-05 | 2017-07-04 | Rigel Pharmaceuticals Inc | inibidores de gdf-8 |
| KR102137472B1 (ko) | 2013-02-08 | 2020-07-27 | 삼성디스플레이 주식회사 | 유기 발광 소자 |
| WO2014152013A1 (en) | 2013-03-14 | 2014-09-25 | The Trustees Of Columbia University In The City Of New York | 4-phenylpiperidines, their preparation and use |
| US9242969B2 (en) | 2013-03-14 | 2016-01-26 | Novartis Ag | Biaryl amide compounds as kinase inhibitors |
| UY35464A (es) | 2013-03-15 | 2014-10-31 | Araxes Pharma Llc | Inhibidores covalentes de kras g12c. |
| US9034927B2 (en) | 2013-05-22 | 2015-05-19 | Curza Global, Llc | Methods of use for compositions comprising a biocidal polyamine |
| CN104232076B (zh) | 2013-06-10 | 2019-01-15 | 代表亚利桑那大学的亚利桑那校董会 | 具有改进的发射光谱的磷光四齿金属络合物 |
| EP3035800B1 (en) | 2013-08-22 | 2019-10-09 | Merck Sharp & Dohme Corp. | Compounds inhibiting leucine-rich repeat kinase enzyme activity |
| TWI652014B (zh) | 2013-09-13 | 2019-03-01 | 美商艾佛艾姆希公司 | 雜環取代之雙環唑殺蟲劑 |
| WO2015037965A1 (en) | 2013-09-16 | 2015-03-19 | Rohm And Haas Electronic Materials Korea Ltd. | Novel organic electroluminescent compounds and organic electroluminescent device comprising the same |
| AU2014337067B2 (en) | 2013-10-18 | 2019-01-24 | Syros Pharmaceuticals, Inc. | Heteroaromatic compounds useful for the treatment of proliferative diseases |
| DK3060550T3 (da) | 2013-10-21 | 2019-07-22 | Merck Patent Gmbh | Heteroarylforbindelser som btk-inhibitorer og anvendelser deraf |
| WO2015089327A1 (en) | 2013-12-11 | 2015-06-18 | Biogen Idec Ma Inc. | Biaryl compounds useful for the treatment of human diseases in oncology, neurology and immunology |
| EP3079683A4 (en) | 2013-12-13 | 2017-12-20 | Dana-Farber Cancer Institute, Inc. | Methods to treat lymphoplasmacytic lymphoma |
| TWI667233B (zh) | 2013-12-19 | 2019-08-01 | 德商拜耳製藥公司 | 新穎吲唑羧醯胺,其製備方法、含彼等之醫藥製劑及其製造醫藥之用途 |
| EP3083589B1 (en) | 2013-12-20 | 2019-12-18 | Sunshine Lake Pharma Co., Ltd. | Substituted piperazine compounds and methods of use thereof |
| MX2016009011A (es) | 2014-01-10 | 2017-01-23 | Aurigene Discovery Tech Ltd | Compuestos de indazol como inhibidores de cinasa-4 asociada al receptor de interleucina-1 (irak4). |
| US11393988B2 (en) | 2014-02-05 | 2022-07-19 | Merck Patent Gmbh | Metal complexes |
| US9643986B2 (en) | 2014-02-25 | 2017-05-09 | Achillion Pharmaceuticals, Inc. | Factor D inhibitors useful for treating inflammatory disorders |
| US9871208B2 (en) | 2014-02-26 | 2018-01-16 | Samsung Display Co., Ltd. | Condensed cyclic compound and organic light-emitting device including the same |
| WO2015164956A1 (en) | 2014-04-29 | 2015-11-05 | The University Of British Columbia | Benzisothiazole derivative compounds as therapeutics and methods for their use |
| US20150328188A1 (en) | 2014-05-19 | 2015-11-19 | Everardus O. Orlemans | Combination Therapies for the Treatment of Proliferative Disorders |
| US11107994B2 (en) | 2014-06-18 | 2021-08-31 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| CU20160188A7 (es) | 2014-06-20 | 2017-06-05 | Aurigene Discovery Tech Ltd | Compuestos de indazole substituidos como inhibidores de irak4 |
| JP2017518339A (ja) | 2014-06-20 | 2017-07-06 | インスティチュート パスツール コリア | 抗感染化合物 |
| WO2015200682A1 (en) | 2014-06-25 | 2015-12-30 | Vanderbilt University | Substituted 4-alkoxypicolinamide analogs ds mglur5 negative allosteric modulators |
| KR20160007967A (ko) | 2014-07-10 | 2016-01-21 | 삼성디스플레이 주식회사 | 유기 발광 소자 |
| WO2016040184A1 (en) | 2014-09-08 | 2016-03-17 | Samumed, Llc | 3-(3h-imidazo[4,5-b]pyridin-2-yl)-1h-pyrazolo[3,4-c]pyridine and therapeutic uses thereof |
| WO2016040181A1 (en) | 2014-09-08 | 2016-03-17 | Samumed, Llc | 3-(1h-imidazo[4,5-c]pyridin-2-yl)-1h-pyrazolo[3,4-c]pyridine and therapeutic uses thereof |
| WO2016040180A1 (en) | 2014-09-08 | 2016-03-17 | Samumed, Llc | 3-(1h-benzo[d]imidazol-2-yl)-1h-pyrazolo[3,4-c]pyridine and therapeutic uses thereof |
| WO2016040188A1 (en) | 2014-09-08 | 2016-03-17 | Samumed, Llc | 3-(3h-imidazo[4,5-c]pyridin-2-yl)-1h-pyrazolo[3,4-c]pyridine and therapeutic uses thereof |
| WO2016041618A1 (en) | 2014-09-15 | 2016-03-24 | Merck Patent Gmbh | Substituted indazoles and related heterocycles |
| US10253023B2 (en) | 2014-10-06 | 2019-04-09 | Merck Patent Gmbh | Heteroaryl compounds as BTK inhibitors and uses thereof |
| JO3705B1 (ar) | 2014-11-26 | 2021-01-31 | Bayer Pharma AG | إندازولات مستبدلة جديدة، عمليات لتحضيرها، مستحضرات دوائية تحتوي عليها واستخدامها في إنتاج أدوية |
| EP3227337A1 (en) | 2014-12-05 | 2017-10-11 | F. Hoffmann-La Roche AG | Methods and compositions for treating cancer using pd-1 axis antagonists and hpk1 antagonists |
| KR102554987B1 (ko) | 2015-02-03 | 2023-07-12 | 메르크 파텐트 게엠베하 | 금속 착물 |
| EP3265445B1 (en) | 2015-03-06 | 2021-05-05 | Pharmakea, Inc. | Lysyl oxidase-like 2 inhibitors and uses thereof |
| CN112608300B (zh) | 2015-03-11 | 2024-04-26 | Fmc公司 | 杂环取代的二环唑杀有害生物剂 |
| WO2016161571A1 (en) | 2015-04-08 | 2016-10-13 | Merck Sharp & Dohme Corp. | Indazole and azaindazole btk inhibitors |
| TW201701879A (zh) | 2015-04-30 | 2017-01-16 | 拜耳製藥公司 | Irak4抑制劑組合 |
| MX2018000512A (es) | 2015-07-15 | 2018-04-13 | Aurigene Discovery Tech Ltd | Compuestos de indazaol y azaindazol como inhibidores de la cinasa 4 asociada al receptor de interlucina 1 (irak-4). |
| US20180208605A1 (en) | 2015-07-15 | 2018-07-26 | Aurigene Discovery Technologies Limited | Substituted Aza Compounds as IRAK-4 Inhibitors |
| EP3331530A4 (en) | 2015-08-03 | 2018-12-19 | Raze Therapeutics Inc. | Mthfd2 inhibitors and uses thereof |
| WO2017023972A1 (en) | 2015-08-03 | 2017-02-09 | Samumed, Llc. | 3-(1h-imidazo[4,5-c]pyridin-2-yl)-1h-pyrazolo[4,3-b]pyridines and therapeutic uses thereof |
| WO2017027400A1 (en) | 2015-08-07 | 2017-02-16 | Calcimedica, Inc. | Use of crac channel inhibitors for the treatment of stroke and traumatic brain injury |
| WO2017045955A1 (en) | 2015-09-14 | 2017-03-23 | Basf Se | Heterobicyclic compounds |
| US10975071B2 (en) | 2015-09-28 | 2021-04-13 | Araxes Pharma Llc | Inhibitors of KRAS G12C mutant proteins |
| WO2017108744A1 (de) | 2015-12-22 | 2017-06-29 | Bayer Pharma Aktiengesellschaft | Neue substituierte indazole, verfahren zu ihrer herstellung, pharmazeutische präparate die diese enthalten, sowie deren verwendung zur herstellung von arzneimitteln |
| KR20180105161A (ko) | 2016-01-07 | 2018-09-27 | 씨에스 파마테크 리미티드 | Egfr 티로신 키나제의 임상적으로 중요한 돌연변이체의 선택적 억제제 |
| WO2018015255A1 (en) | 2016-07-19 | 2018-01-25 | CUMMINGS, Arthur Bernard | Artificial accommodating lens complex |
| CN108602802B (zh) | 2016-07-26 | 2020-01-21 | 深圳市塔吉瑞生物医药有限公司 | 用于抑制蛋白酪氨酸激酶活性的氨基嘧啶类化合物 |
| WO2018049152A1 (en) | 2016-09-09 | 2018-03-15 | Incyte Corporation | Pyrazolopyrimidine derivatives as hpk1 modulators and uses thereof for the treatment of cancer |
| US20180072718A1 (en) | 2016-09-09 | 2018-03-15 | Incyte Corporation | Pyrazolopyridine compounds and uses thereof |
| MA46191A (fr) * | 2016-09-09 | 2021-04-21 | Incyte Corp | Dérivés de pyrazolopyridine comme modulateurs de hpk1 et leurs utilisations pour le traitement du cancer |
| WO2018049191A1 (en) | 2016-09-09 | 2018-03-15 | Incyte Corporation | Pyrazolopyridone derivatives as hpk1 modulators and uses thereof for the treatment of cancer |
| US20180228786A1 (en) | 2017-02-15 | 2018-08-16 | Incyte Corporation | Pyrazolopyridine compounds and uses thereof |
| WO2019051199A1 (en) | 2017-09-08 | 2019-03-14 | Incyte Corporation | 6-CYANO-INDAZOLE COMPOUNDS AS HEMATOPOIETIC PROGENITOR KINASE 1 (HPK1) MODULATORS |
| DK3755703T3 (da) | 2018-02-20 | 2022-06-27 | Incyte Corp | N-(phenyl)-2-(phenyl)pyrimidin-4-carboxamidderivater og relaterede forbindelser som hpk1-inhibitorer til behandling af kræft |
| US10745388B2 (en) | 2018-02-20 | 2020-08-18 | Incyte Corporation | Indazole compounds and uses thereof |
| WO2019164847A1 (en) | 2018-02-20 | 2019-08-29 | Incyte Corporation | Indazole compounds and uses thereof |
| US11299473B2 (en) | 2018-04-13 | 2022-04-12 | Incyte Corporation | Benzimidazole and indole compounds and uses thereof |
| CU20200070A7 (es) | 2018-04-26 | 2021-05-12 | Pfizer | Derivados de 2-amino-piridina o 2-amino-pirimidina como inhibidores de quinasa dependientes de ciclina |
| AU2019263674B2 (en) | 2018-05-04 | 2023-03-02 | Novo Nordisk A/S | GIP derivatives and uses thereof |
| JOP20200294A1 (ar) | 2018-05-17 | 2020-11-17 | Bayer Ag | مشتقات ثنائي هيدروبيرازولو بيرازين كربوكساميد تحمل بدائل |
| US10899755B2 (en) | 2018-08-08 | 2021-01-26 | Incyte Corporation | Benzothiazole compounds and uses thereof |
| AU2020326703A1 (en) | 2019-08-06 | 2022-02-17 | Incyte Corporation | Solid forms of an HPK1 inhibitor |
-
2019
- 2019-02-19 DK DK19708757.0T patent/DK3755703T3/da active
- 2019-02-19 RS RS20220715A patent/RS63659B1/sr unknown
- 2019-02-19 EP EP19708757.0A patent/EP3755703B1/en active Active
- 2019-02-19 JP JP2020566534A patent/JP7526673B2/ja active Active
- 2019-02-19 CR CR20200421A patent/CR20200421A/es unknown
- 2019-02-19 SG SG11202007917VA patent/SG11202007917VA/en unknown
- 2019-02-19 US US16/278,865 patent/US10800761B2/en active Active
- 2019-02-19 CN CN201980020899.4A patent/CN112292380B/zh active Active
- 2019-02-19 IL IL276779A patent/IL276779B2/en unknown
- 2019-02-19 BR BR112020016927-7A patent/BR112020016927A2/pt unknown
- 2019-02-19 AU AU2019223955A patent/AU2019223955B2/en active Active
- 2019-02-19 MX MX2020008656A patent/MX2020008656A/es unknown
- 2019-02-19 PL PL19708757.0T patent/PL3755703T3/pl unknown
- 2019-02-19 KR KR1020207027017A patent/KR20200133747A/ko not_active Application Discontinuation
- 2019-02-19 CA CA3091517A patent/CA3091517A1/en active Pending
- 2019-02-19 MD MDE20210010T patent/MD3755703T2/ro unknown
- 2019-02-19 LT LTEPPCT/US2019/018608T patent/LT3755703T/lt unknown
- 2019-02-19 PE PE2020001252A patent/PE20210397A1/es unknown
- 2019-02-19 UA UAA202005974A patent/UA128286C2/uk unknown
- 2019-02-19 PT PT197087570T patent/PT3755703T/pt unknown
- 2019-02-19 WO PCT/US2019/018608 patent/WO2019164846A1/en active Application Filing
- 2019-02-19 HR HRP20220833TT patent/HRP20220833T1/hr unknown
- 2019-02-19 SI SI201930287T patent/SI3755703T1/sl unknown
- 2019-02-19 ES ES19708757T patent/ES2922237T3/es active Active
- 2019-02-19 HU HUE19708757A patent/HUE059624T2/hu unknown
- 2019-02-20 TW TW108105529A patent/TWI828653B/zh active
-
2020
- 2020-08-19 CL CL2020002146A patent/CL2020002146A1/es unknown
- 2020-08-19 PH PH12020551278A patent/PH12020551278A1/en unknown
- 2020-09-09 US US17/015,797 patent/US11731958B2/en active Active
- 2020-09-18 EC ECSENADI202058964A patent/ECSP20058964A/es unknown
- 2020-09-18 CO CONC2020/0011530A patent/CO2020011530A2/es unknown
-
2023
- 2023-06-21 US US18/212,444 patent/US20240150326A1/en active Pending
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN101801981A (zh) * | 2007-06-20 | 2010-08-11 | 西特里斯药业公司 | 瑟土因调节性噻唑并吡啶化合物 |
| CN101918371A (zh) * | 2007-11-01 | 2010-12-15 | 西特里斯药业公司 | 作为瑟土因调节剂的酰胺衍生物 |
| WO2016205942A1 (en) * | 2015-06-25 | 2016-12-29 | University Health Network | Hpk1 inhibitors and methods of using same |
| CN107922431A (zh) * | 2015-06-25 | 2018-04-17 | 大学健康网络 | Hpk1抑制剂及其使用方法 |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN114450276A (zh) * | 2019-08-06 | 2022-05-06 | 因赛特公司 | Hpk1抑制剂的固体形式 |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN112292380B (zh) | 作为用于治疗癌症的hpk1抑制剂的n-(苯基)-2-(苯基)嘧啶-4-甲酰胺衍生物及相关化合物 | |
| US11492354B2 (en) | Indazole compounds and uses thereof | |
| US11891388B2 (en) | Pyrazolopyridine compounds and uses thereof | |
| EP3510032B1 (en) | Pyrazolopyridine derivatives as hpk1 modulators and uses thereof for the treatment of cancer | |
| US11299473B2 (en) | Benzimidazole and indole compounds and uses thereof | |
| US11866426B2 (en) | Benzothiazole compounds and uses thereof | |
| US10745388B2 (en) | Indazole compounds and uses thereof | |
| US10722495B2 (en) | Cyanoindazole compounds and uses thereof | |
| CN115835908A (zh) | 作为fgfr抑制剂的双环杂环 | |
| CN114456175A (zh) | 作为tam抑制剂的吡咯并三嗪化合物 | |
| CN114787160A (zh) | 作为活化素受体样激酶-2的抑制剂的咪唑并哒嗪和咪唑并吡啶化合物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| GR01 | Patent grant | ||
| GR01 | Patent grant |