Heksametilbenzena
| |
| |

| |
| Nama | |
|---|---|
| Nama IUPAC (preferensi)
Heksametilbenzena | |
| Nama lain
1,2,3,4,5,6-Heksametilbenzena
Melitena | |
| Penanda | |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| ChEBI | |
| ChemSpider | |
| Nomor EC | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| C12H18 | |
| Massa molar | 162,28 g·mol−1 |
| Penampilan | Bubuk kristal putih |
| Densitas | 1,0630 g cm−3 |
| Titik lebur | 165,6 ± 0.7 °C |
| Titik didih | 265,2 °C (509,4 °F; 538,3 K) |
| tidak larut | |
| Kelarutan | asam asetat, aseton, benzena, kloroform, dietil eter, etanol |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
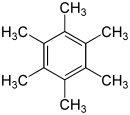
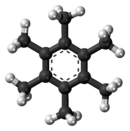
Heksametilbenzena (Inggris: Hexamethylbenzene), juga dikenal sebagai mellitene, adalah hidrokarbon dengan rumus molekul C12H18 dan formula struktural terkondensasi C6(CH3)6. Ini adalah senyawa aromatik dan turunan dari benzena, di mana enam atom hidrogen benzena masing-masing telah digantikan oleh gugus metil. Pada tahun 1929 Kathleen Lonsdale melaporkan struktur kristal hexamethylbenzene, menunjukkan bahwa cincin pusat adalah heksagonal dan datar dan dengan demikian mengakhiri perdebatan yang sedang berlangsung tentang 'parameter fisik sistem benzena'.[1] Ini adalah hasil yang signifikan secara historis, baik untuk bidang kristalografi sinar-X dan untuk memahami aromatisitas.
Produksi
[sunting | sunting sumber]Senyawa Heksametilbenzena dapat dibuat dengan mereaksikan fenol dengan metanol pada suhu tinggi melalui katalis padat yang sesuai seperti alumina. Mekanisme proses ini telah dipelajari secara luas, dengan beberapa perantara telah diidentifikasi. Trimerisasi alkuna dari dimethylacetylene juga menghasilkan hexamethylbenzene dengan adanya catalis yang sesuai. Hexamethylbenzene dapat dioksidasi menjadi asam mellitic, yang ditemukan di alam sebagai garam aluminium dalam mineral langka mellite. Hexamethylbenzene dapat digunakan sebagai ligan dalam senyawa organologam. Contoh dari kimia organoruthenium menunjukkan perubahan struktural pada ligan yang terkait dengan perubahan keadaan oksidasi dari pusat logam, meskipun perubahan yang sama tidak diamati dalam sistem organoiron analog.
Pada tahun 2016 struktur kristal dikasi hexamethylbenzene dilaporkan dalam Angewandte Chemie International Edition, menunjukkan struktur piramidal di mana atom karbon tunggal memiliki interaksi ikatan dengan enam atom karbon lainnya. Struktur ini "belum pernah terjadi sebelumnya", karena valensi karbon maksimum yang biasa adalah empat, dan menarik perhatian dari Ilmuwan Baru, Berita Kimia & Teknik, dan Berita Sains. Struktur ini tidak melanggar aturan oktet karena ikatan karbon-karbon yang terbentuk bukanlah ikatan dua elektron, dan secara pedagogis berharga untuk menggambarkan bahwa atom karbon "dapat [secara langsung mengikat] dengan lebih dari empat atom".[2] Steven Bachrach telah menunjukkan bahwa senyawa tersebut sangat terkoordinasi tetapi tidak hipervalen, dan juga menjelaskan aromatisitasnya. setelah :
C 6 (CH 3) 2 + 6
pertama kali diamati,[3] Diadakan gagasan untuk menggambarkan ikatan pada spesies seperti ini melalui lensa kimia organologam diusulkan pada tahun 1975.
Referensi
[sunting | sunting sumber]- ^ "Salinan arsip". Diarsipkan dari versi asli tanggal 2023-08-17. Diakses tanggal 2020-01-26.
- ^ "Salinan arsip". Diarsipkan dari versi asli tanggal 2017-01-09. Diakses tanggal 2020-01-26.
- ^ "Salinan arsip". Diarsipkan dari versi asli tanggal 2023-04-07. Diakses tanggal 2020-01-26.
