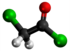
Etila kloroacetato
Aspekto
| Etila kloroetanato | |||||
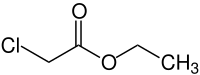 | |||||
| Plata kemia strukturo de la Etila kloroacetato | |||||
 | |||||
| Tridimensia kemia strukturo de la Etila kloroacetato | |||||
| Alternativa(j) nomo(j) | |||||
| |||||
| Kemia formulo | |||||
| CAS-numero-kodo | 105-39-5 | ||||
| ChemSpider kodo | 7465 | ||||
| PubChem-kodo | 7751 | ||||
| Merck Index | 15,2112 | ||||
| Fizikaj proprecoj | |||||
| Aspekto | senkolora likvaĵo kun tranĉa odoro | ||||
| Molmaso | 122.548 g·mol−1 | ||||
| Denseco | 1.145g cm−3 | ||||
| Fandpunkto | -26 °C | ||||
| Bolpunkto | 143 °C | ||||
| Refrakta indico | 1,4217 | ||||
| Ekflama temperaturo | 65.5 °C | ||||
| Memsparka temperaturo | 452 °C | ||||
| Acideco (pKa) | 2.86 | ||||
| Solvebleco | Akvo:12.3 g/L | ||||
| Mortiga dozo (LD50) | 180 mg/kg (buŝe) | ||||
| GHS etikedigo de kemiaĵoj | |||||
| GHS Damaĝo-piktogramo |
| ||||
| GHS Signalvorto | Damaĝo | ||||
| GHS Deklaroj pri damaĝoj | H226, H301, H310, H311, H315, H317, H318, H331, H400[1] | ||||
| GHS Deklaroj pri antaŭgardoj | P210, P233, P240, P241, P242, P243, P261, P262, P264, P270, P271, P272, P273, P280, P301+310, P302+352, P303+361+353, P304+340, P305+351+338, P310, P311, P312, P321, P330, P332+313, P333+313, P361, P362, P363, P370+378 | ||||
(25 °C kaj 100 kPa) | |||||
Etila kloroacetato estas etila estero de la kloroacetata acido, senkolora brulema substanco kun akra odoro, uzata kiel solvanto en kemiaj sintezoj, kiel larmiga gaso en militaplikoj, kaj en la produktado de pesticidoj. Etil-kloroacetato estas stabila kemiaĵo, neakordigebla kun acidoj, bazoj, oksidigaj agentoj kaj reduktagentoj.
Ĝi kaŭzas iriton per inhalado en la mukozaj membranoj, kapdolorojn kaj naŭzon. Kontakto kun la okuloj kaŭzas iriton kaj konjunktivito. Ingestado produktas iriton en la buŝo kaj stomako. Kiam hejtata ĝis malkomponiĝo ĝi eligas alte toksajn fumojn.
Sintezoj
[redakti | redakti fonton]Sintezo 1
[redakti | redakti fonton]- Preparado per interagado de kloroacetata acido kaj etanolo:
Sintezo 2
[redakti | redakti fonton]- Preparado ekde la kloroacetila klorido kaj etanolo:
Sintezo 3
[redakti | redakti fonton]- Preparado per traktado de kloroacetata acido kaj kloroetano:
Sintezo 4
[redakti | redakti fonton]- Preparado inter natria kloroacetato kaj kloroetano:
Sintezo 5
[redakti | redakti fonton]- Preparado per interagado de propila kloroacetato kaj etila formiato:
Sintezo 6
[redakti | redakti fonton]- Preparado per acida transesterigo inter kloroacetata acido kaj etila benzoato:
Sintezo 7
[redakti | redakti fonton]- Preparado per alkohola transesterigo inter alila kloroacetato kaj etanolo:
Reakcioj
[redakti | redakti fonton]Reakcio 1
[redakti | redakti fonton]- Hidrolizo de la etila kloroacetato:
Reakcio 2
[redakti | redakti fonton]- Sapigo de la etila kloroacetato:
Reakcio 3
[redakti | redakti fonton]- Preparado per acida transesterigo inter etila kloroacetat kaj formiata acido:
Reakcio 4
[redakti | redakti fonton]- Preparado per alkohola transesterigo inter "etila kloroacetato" kaj metanolo:
Reakcio 5
[redakti | redakti fonton]- Transesterigo inter "etila kloroacetato" kaj fenila acetato:
Reakcio 6
[redakti | redakti fonton]- Reakcio kun NH3:
Reakcio 7
[redakti | redakti fonton]- Reakcio kun HCl:
Literaturo
[redakti | redakti fonton]- New Jersey Department of Health and Senior Services
- Hamilton and Hardy's Industrial Toxicology, Raymond D. Harbison, Marie M. Bourgeois, Giffe T. Johnson
- Alpha Chemika
- ThermoFisher[rompita ligilo]
- Handbook of Industrial Toxicology and Hazardous Materials, Nicholas P. Cheremisinoff
- EPA United States Environmental Protection Agency
Vidu ankaŭ
[redakti | redakti fonton]- Fluoroacetata acido
- Natria fluoroacetato
- Kalia fluoroacetato
- Etila bromoacetato
- Metila kloroacetato
- Metila bromoacetato
- Metila jodoacetato
- Etila jodoacetato






![{\displaystyle {\mathsf {{\xrightarrow[{}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/af21b07e9e503bdbbee6814c136975f68f374663)